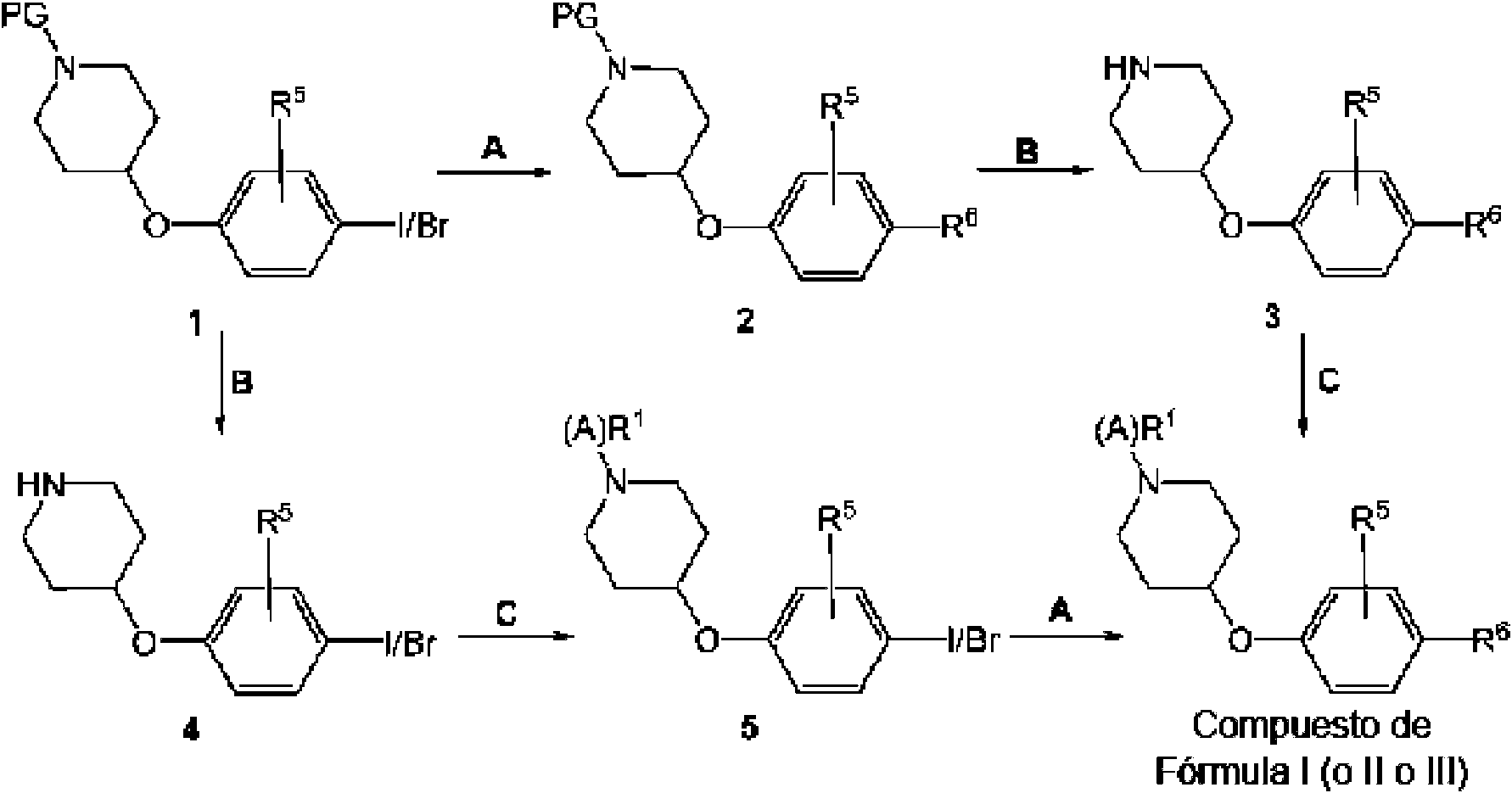
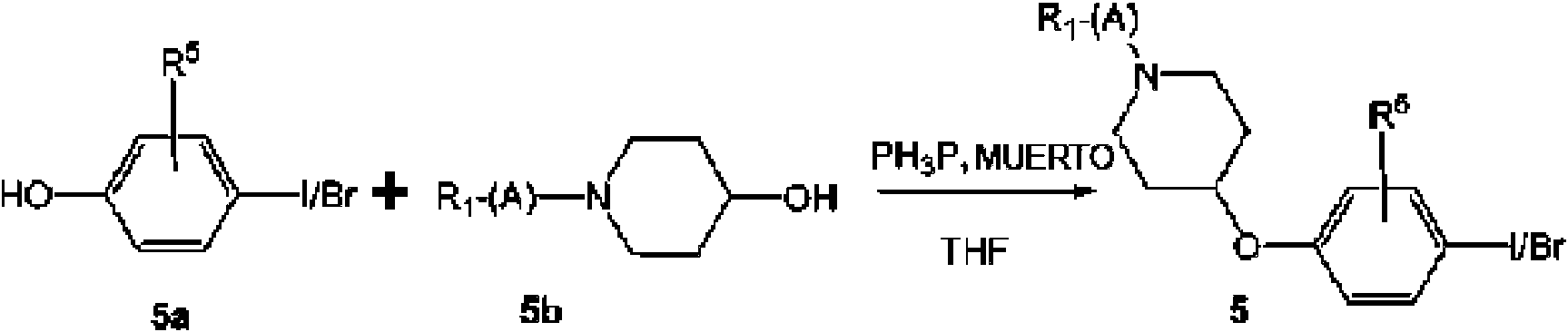
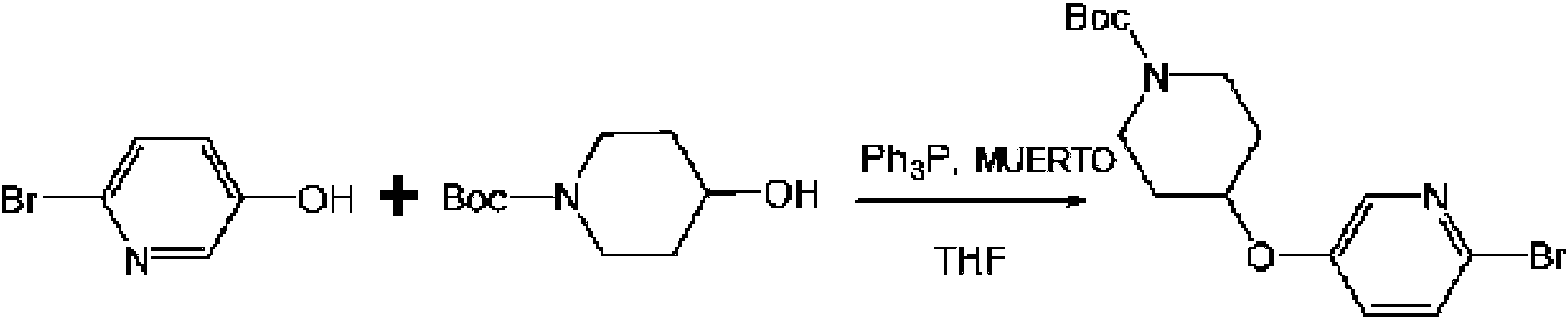
ES2821049T3 - Derivados de piperidina 1,4 sustituidos - Google Patents
Derivados de piperidina 1,4 sustituidos Download PDFInfo
- Publication number
- ES2821049T3 ES2821049T3 ES16736649T ES16736649T ES2821049T3 ES 2821049 T3 ES2821049 T3 ES 2821049T3 ES 16736649 T ES16736649 T ES 16736649T ES 16736649 T ES16736649 T ES 16736649T ES 2821049 T3 ES2821049 T3 ES 2821049T3
- Authority
- ES
- Spain
- Prior art keywords
- phenoxy
- piperidin
- methanone
- methyl
- propan
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 C*1C(*)(**)N(**)*(C)C(*)(*)*C(CC2*C(*)=*C(*)=C(*)*=*)[C@@]2C1* Chemical compound C*1C(*)(**)N(**)*(C)C(*)(*)*C(CC2*C(*)=*C(*)=C(*)*=*)[C@@]2C1* 0.000 description 8
- MDRARUQTUUWLFR-UHFFFAOYSA-N CC(C)C(N(CC1)CCC1Oc(c(OC)c1)ccc1-c1cnc(C=CCC2)c2c1)=O Chemical compound CC(C)C(N(CC1)CCC1Oc(c(OC)c1)ccc1-c1cnc(C=CCC2)c2c1)=O MDRARUQTUUWLFR-UHFFFAOYSA-N 0.000 description 1
- RHKFOKXEBJSTTI-UHFFFAOYSA-N CC(C)C(N(CC1)CCC1Oc(cc1)cnc1-c1cc2ccccc2nc1)=O Chemical compound CC(C)C(N(CC1)CCC1Oc(cc1)cnc1-c1cc2ccccc2nc1)=O RHKFOKXEBJSTTI-UHFFFAOYSA-N 0.000 description 1
- QLVHOFNLKQRKMO-UHFFFAOYSA-N CC(C)C(N(CC1)CCC1Oc1ccc(-c2cnc(cccc3)c3c2)c(F)c1)=O Chemical compound CC(C)C(N(CC1)CCC1Oc1ccc(-c2cnc(cccc3)c3c2)c(F)c1)=O QLVHOFNLKQRKMO-UHFFFAOYSA-N 0.000 description 1
- YNAQVJYQNPJHDO-UHFFFAOYSA-N CC(C)C(N(CC1)CCC1S(c(cc1)ccc1-c1cc(nccc2)c2cc1)(=O)=O)=O Chemical compound CC(C)C(N(CC1)CCC1S(c(cc1)ccc1-c1cc(nccc2)c2cc1)(=O)=O)=O YNAQVJYQNPJHDO-UHFFFAOYSA-N 0.000 description 1
- UHGLOMYKNSDITR-UHFFFAOYSA-N CC(C)C(N(CC1)CCC1S(c(cc1)ccc1-c1ccc(cncc2)c2c1)(=O)=O)=O Chemical compound CC(C)C(N(CC1)CCC1S(c(cc1)ccc1-c1ccc(cncc2)c2c1)(=O)=O)=O UHGLOMYKNSDITR-UHFFFAOYSA-N 0.000 description 1
- LDWSNHIOEIUQKW-UHFFFAOYSA-N CC(C)C(N(CC1)CCC1Sc(cc1)ccc1-c1cnc(cccc2)c2c1)=O Chemical compound CC(C)C(N(CC1)CCC1Sc(cc1)ccc1-c1cnc(cccc2)c2c1)=O LDWSNHIOEIUQKW-UHFFFAOYSA-N 0.000 description 1
- LEVPUPZEAWAANM-UHFFFAOYSA-N CC(C)CNC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1C)=O Chemical compound CC(C)CNC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1C)=O LEVPUPZEAWAANM-UHFFFAOYSA-N 0.000 description 1
- NYMHQVJAMRRZIO-UHFFFAOYSA-N CC(C)CONC(N(CC1)CCC1Oc(cc1)ccc1-c1c(C)c(nccc2)c2cc1)=O Chemical compound CC(C)CONC(N(CC1)CCC1Oc(cc1)ccc1-c1c(C)c(nccc2)c2cc1)=O NYMHQVJAMRRZIO-UHFFFAOYSA-N 0.000 description 1
- HONVUYYLSIORSW-UHFFFAOYSA-N CC(C)ONC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1C)=O Chemical compound CC(C)ONC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1C)=O HONVUYYLSIORSW-UHFFFAOYSA-N 0.000 description 1
- MDYGUHJVKHNLAC-RUZDIDTESA-N CC(C)Oc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O Chemical compound CC(C)Oc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O MDYGUHJVKHNLAC-RUZDIDTESA-N 0.000 description 1
- YUMFIMUNEHPBNF-UHFFFAOYSA-N CC1(C(N(CC2)CCC2Oc(cc2)ccc2-c2cc(cccc3)c3nc2)=O)OCCC1 Chemical compound CC1(C(N(CC2)CCC2Oc(cc2)ccc2-c2cc(cccc3)c3nc2)=O)OCCC1 YUMFIMUNEHPBNF-UHFFFAOYSA-N 0.000 description 1
- SWQUECXZVPBRAW-UHFFFAOYSA-N CCC(N(CC1)CCC1OC1C=CC(c2cc(C)cc3ncccc23)=CC1)=O Chemical compound CCC(N(CC1)CCC1OC1C=CC(c2cc(C)cc3ncccc23)=CC1)=O SWQUECXZVPBRAW-UHFFFAOYSA-N 0.000 description 1
- PAGUFFHUUNSYGJ-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c(cn1)ccc1Oc1ccccc1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c(cn1)ccc1Oc1ccccc1)=O PAGUFFHUUNSYGJ-UHFFFAOYSA-N 0.000 description 1
- KZZCTVGILPEDTL-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1c[n]2nccc2c(O)c1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1c[n]2nccc2c(O)c1)=O KZZCTVGILPEDTL-UHFFFAOYSA-N 0.000 description 1
- XICYUGYEGJLUEO-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1c[n]2nccc2c(OC)c1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1c[n]2nccc2c(OC)c1)=O XICYUGYEGJLUEO-UHFFFAOYSA-N 0.000 description 1
- JAUALCSFZGDVQX-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cc(c(C)ccc2)c2nc1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cc(c(C)ccc2)c2nc1)=O JAUALCSFZGDVQX-UHFFFAOYSA-N 0.000 description 1
- FHEYKLRAYUPGEI-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cc(ccc(F)c2)c2nc1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cc(ccc(F)c2)c2nc1)=O FHEYKLRAYUPGEI-UHFFFAOYSA-N 0.000 description 1
- WGVHEWPHCOSKOH-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1ccc(-c2ccccc2)nc1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1ccc(-c2ccccc2)nc1)=O WGVHEWPHCOSKOH-UHFFFAOYSA-N 0.000 description 1
- XTARAMFKFHUUAR-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1ccc2[o]ccc2c1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1ccc2[o]ccc2c1)=O XTARAMFKFHUUAR-UHFFFAOYSA-N 0.000 description 1
- SUMKLUADOASUGQ-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cc(c(C)c2)OC)c2c1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cc(c(C)c2)OC)c2c1)=O SUMKLUADOASUGQ-UHFFFAOYSA-N 0.000 description 1
- DHQXMEWKZJMMNP-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cc(cc2)OC)c2c1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cc(cc2)OC)c2c1)=O DHQXMEWKZJMMNP-UHFFFAOYSA-N 0.000 description 1
- UCLGLUWURWRTAL-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1Cl)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1Cl)=O UCLGLUWURWRTAL-UHFFFAOYSA-N 0.000 description 1
- DVFQUOVPODVDIQ-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2F)c2c1)=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2F)c2c1)=O DVFQUOVPODVDIQ-UHFFFAOYSA-N 0.000 description 1
- LBHHOUNEMAXFFY-UHFFFAOYSA-O CCC(N(CC1)CCC1Oc(cc1)ccc1C(C=C1)=CC(C2)C1=CN=C2[NH3+])=O Chemical compound CCC(N(CC1)CCC1Oc(cc1)ccc1C(C=C1)=CC(C2)C1=CN=C2[NH3+])=O LBHHOUNEMAXFFY-UHFFFAOYSA-O 0.000 description 1
- DMCMWLJOTHIWIR-UHFFFAOYSA-N CCC(N(CC1)CCC1Oc1ccc(-c2cnc(cccc3)c3c2)c(OC)c1)=O Chemical compound CCC(N(CC1)CCC1Oc1ccc(-c2cnc(cccc3)c3c2)c(OC)c1)=O DMCMWLJOTHIWIR-UHFFFAOYSA-N 0.000 description 1
- RXNHGTHHOIJDJV-UHFFFAOYSA-N CCCNC(N(CC1)CCC1Oc(cc1)ccc1-c(cc1)c(C)[n]2c1ncc2)=O Chemical compound CCCNC(N(CC1)CCC1Oc(cc1)ccc1-c(cc1)c(C)[n]2c1ncc2)=O RXNHGTHHOIJDJV-UHFFFAOYSA-N 0.000 description 1
- XQCCOXGOMSMNSJ-UHFFFAOYSA-N CCCNC(N(CC1)CCC1Oc(cc1)ccc1-c(cc1)cc2c1c(C)ncc2)=O Chemical compound CCCNC(N(CC1)CCC1Oc(cc1)ccc1-c(cc1)cc2c1c(C)ncc2)=O XQCCOXGOMSMNSJ-UHFFFAOYSA-N 0.000 description 1
- KNVAVBQXFINYTE-UHFFFAOYSA-N CCCNC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1C)=O Chemical compound CCCNC(N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1C)=O KNVAVBQXFINYTE-UHFFFAOYSA-N 0.000 description 1
- IAGHPKPZSXYKQH-UHFFFAOYSA-N CCNC(N(CC1)CCC1Oc(cc1)ccc1-c1cc2ccnc(C)c2cc1)=O Chemical compound CCNC(N(CC1)CCC1Oc(cc1)ccc1-c1cc2ccnc(C)c2cc1)=O IAGHPKPZSXYKQH-UHFFFAOYSA-N 0.000 description 1
- PWDGTOKIVFAYDN-XMMPIXPASA-N CN(C)c(c1ncccc1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O Chemical compound CN(C)c(c1ncccc1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O PWDGTOKIVFAYDN-XMMPIXPASA-N 0.000 description 1
- RJLDUCQETOCGEO-MUUNZHRXSA-N CN(CC1)CCN1c1nccc2c1ccc(-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O)c2 Chemical compound CN(CC1)CCN1c1nccc2c1ccc(-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O)c2 RJLDUCQETOCGEO-MUUNZHRXSA-N 0.000 description 1
- PURNKJJABPTRFK-UHFFFAOYSA-N COCCNC(N(CC1)CCC1Oc(cc1)ccc1-c(ccc1ncc[n]11)c1Cl)=O Chemical compound COCCNC(N(CC1)CCC1Oc(cc1)ccc1-c(ccc1ncc[n]11)c1Cl)=O PURNKJJABPTRFK-UHFFFAOYSA-N 0.000 description 1
- ZGDILYLLISHPPD-RUZDIDTESA-N COCCOc(c1ncccc1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O Chemical compound COCCOc(c1ncccc1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O ZGDILYLLISHPPD-RUZDIDTESA-N 0.000 description 1
- QCNRRFPFZVVINS-HSZRJFAPSA-N COc(c(nccc1)c1cc1)c1-c(cc1)cc(F)c1OC(CC1)CCN1C([C@@H]1OCCC1)=O Chemical compound COc(c(nccc1)c1cc1)c1-c(cc1)cc(F)c1OC(CC1)CCN1C([C@@H]1OCCC1)=O QCNRRFPFZVVINS-HSZRJFAPSA-N 0.000 description 1
- LSJVGHYRAHUWGK-UHFFFAOYSA-N COc1cccc(nc2)c1cc2-c(cc1)ccc1OC(CC1)CCN1C(C1CC1)=O Chemical compound COc1cccc(nc2)c1cc2-c(cc1)ccc1OC(CC1)CCN1C(C1CC1)=O LSJVGHYRAHUWGK-UHFFFAOYSA-N 0.000 description 1
- AEKCDGPYOSWFSS-QGZVFWFLSA-N C[C@H](C(N(CC1)CCC1Oc(cc1)ccc1-c1ccc(cccn2)c2c1C)=O)N Chemical compound C[C@H](C(N(CC1)CCC1Oc(cc1)ccc1-c1ccc(cccn2)c2c1C)=O)N AEKCDGPYOSWFSS-QGZVFWFLSA-N 0.000 description 1
- JRIXAOZKVKWLNY-UHFFFAOYSA-N Cc(c(-c(cc1)ccc1OC(CC1)CCN1C(C1C=C1)=O)ccc1)c1-c1ccccn1 Chemical compound Cc(c(-c(cc1)ccc1OC(CC1)CCN1C(C1C=C1)=O)ccc1)c1-c1ccccn1 JRIXAOZKVKWLNY-UHFFFAOYSA-N 0.000 description 1
- MNEJAJJHVVWGLP-UHFFFAOYSA-N Cc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(CO)=O Chemical compound Cc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(CO)=O MNEJAJJHVVWGLP-UHFFFAOYSA-N 0.000 description 1
- GUKAWGVWTHRNFO-UHFFFAOYSA-N Cc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(N1CCCCCC1)=O Chemical compound Cc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(N1CCCCCC1)=O GUKAWGVWTHRNFO-UHFFFAOYSA-N 0.000 description 1
- ILQFQKDCCKVVFK-UHFFFAOYSA-N Cc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(OCCN1CCCC1)=O Chemical compound Cc(c(nccc1)c1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(OCCN1CCCC1)=O ILQFQKDCCKVVFK-UHFFFAOYSA-N 0.000 description 1
- IKZLZQAGMCJQPY-RUZDIDTESA-N Cc(cc1)cc(nc2)c1cc2-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O Chemical compound Cc(cc1)cc(nc2)c1cc2-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)=O IKZLZQAGMCJQPY-RUZDIDTESA-N 0.000 description 1
- CRFJXHOGBCZQOE-UHFFFAOYSA-N Cc1c(cccc2)c2ncc1-c(cc1)ccc1OC(CC1)CCN1C(N(C)OC)=O Chemical compound Cc1c(cccc2)c2ncc1-c(cc1)ccc1OC(CC1)CCN1C(N(C)OC)=O CRFJXHOGBCZQOE-UHFFFAOYSA-N 0.000 description 1
- WPGMQOPWUVCLMQ-UHFFFAOYSA-N Cc1c(cccc2)c2ncc1-c(cc1)ccc1OC(CC1)CCN1C(NO)=O Chemical compound Cc1c(cccc2)c2ncc1-c(cc1)ccc1OC(CC1)CCN1C(NO)=O WPGMQOPWUVCLMQ-UHFFFAOYSA-N 0.000 description 1
- FQQMYVYQMRZVIR-UHFFFAOYSA-N Cc1c2NCC=Cc2ccc1-c(cc1)ccc1OC(CC1)CCN1C(NCCN1CCCC1)=O Chemical compound Cc1c2NCC=Cc2ccc1-c(cc1)ccc1OC(CC1)CCN1C(NCCN1CCCC1)=O FQQMYVYQMRZVIR-UHFFFAOYSA-N 0.000 description 1
- OBTAVFDHMMZOJU-UHFFFAOYSA-N Cc1c2ncccc2ccc1-c(cc1)ccc1OC(CC1)CCN1C(N1OCCC1)=O Chemical compound Cc1c2ncccc2ccc1-c(cc1)ccc1OC(CC1)CCN1C(N1OCCC1)=O OBTAVFDHMMZOJU-UHFFFAOYSA-N 0.000 description 1
- QQKZCIURZDFPKQ-UHFFFAOYSA-N Cc1cc(-c(cc2)ccc2OC(CC2)CCN2C(C2CC2)=O)c[n]2c1ncc2 Chemical compound Cc1cc(-c(cc2)ccc2OC(CC2)CCN2C(C2CC2)=O)c[n]2c1ncc2 QQKZCIURZDFPKQ-UHFFFAOYSA-N 0.000 description 1
- GFIARYZWQOWIGB-UHFFFAOYSA-N Cc1ccc(C)c(C(N(CC2)CCC2Oc(cc2)ccc2-c2cc3ccccc3nc2)=O)c1 Chemical compound Cc1ccc(C)c(C(N(CC2)CCC2Oc(cc2)ccc2-c2cc3ccccc3nc2)=O)c1 GFIARYZWQOWIGB-UHFFFAOYSA-N 0.000 description 1
- RPSPEKAHFJNHKB-UHFFFAOYSA-N Cc1ccc2ncccc2c1-c(cc1)ccc1OC(CC1)CCN1C(C1CC1)=O Chemical compound Cc1ccc2ncccc2c1-c(cc1)ccc1OC(CC1)CCN1C(C1CC1)=O RPSPEKAHFJNHKB-UHFFFAOYSA-N 0.000 description 1
- WEIIEANKJWWZKJ-XQZUBTRRSA-N Nc1nccc2c1ccc(-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)O)c2 Chemical compound Nc1nccc2c1ccc(-c(cc1)ccc1OC(CC1)CCN1C([C@@H]1OCCC1)O)c2 WEIIEANKJWWZKJ-XQZUBTRRSA-N 0.000 description 1
- LEPAPHCNDYGELI-UHFFFAOYSA-N O=C(C1CC1)N(CC1)CCC1Oc(cc(c(-c1cnc(cccc2)c2c1)c1)F)c1F Chemical compound O=C(C1CC1)N(CC1)CCC1Oc(cc(c(-c1cnc(cccc2)c2c1)c1)F)c1F LEPAPHCNDYGELI-UHFFFAOYSA-N 0.000 description 1
- DSMWMUVPPWFSRS-UHFFFAOYSA-N O=C(C1CC1)N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2F)c2c1 Chemical compound O=C(C1CC1)N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2F)c2c1 DSMWMUVPPWFSRS-UHFFFAOYSA-N 0.000 description 1
- KBEPAXGENRMUPO-UHFFFAOYSA-N O=C(C1CC1)N(CC1)CCC1Oc(cc1)ccc1-c1nc(cccc2)c2cc1 Chemical compound O=C(C1CC1)N(CC1)CCC1Oc(cc1)ccc1-c1nc(cccc2)c2cc1 KBEPAXGENRMUPO-UHFFFAOYSA-N 0.000 description 1
- VEJCNUMRNIPMDS-UHFFFAOYSA-N O=C(C1CC1)N(CC1)CCC1Oc(cc1)ccc1-c1ncc(cccc2)c2c1 Chemical compound O=C(C1CC1)N(CC1)CCC1Oc(cc1)ccc1-c1ncc(cccc2)c2c1 VEJCNUMRNIPMDS-UHFFFAOYSA-N 0.000 description 1
- UZIFVIDLXZYEIG-UHFFFAOYSA-N O=C(C1OCCC1)N(CC1)CCC1Oc(cc1)ccc1-c(cc1)cc2c1cncc2 Chemical compound O=C(C1OCCC1)N(CC1)CCC1Oc(cc1)ccc1-c(cc1)cc2c1cncc2 UZIFVIDLXZYEIG-UHFFFAOYSA-N 0.000 description 1
- RECBGPTYGJPTAZ-UHFFFAOYSA-N O=C(N1OCCC1)N(CC1)CCC1Oc(cc1)ccc1-c1ncc(cccc2)c2c1 Chemical compound O=C(N1OCCC1)N(CC1)CCC1Oc(cc1)ccc1-c1ncc(cccc2)c2c1 RECBGPTYGJPTAZ-UHFFFAOYSA-N 0.000 description 1
- PGFOJOMSLRORFT-UHFFFAOYSA-N O=C(c1cc(-c2ncc[nH]2)ccc1)N(CC1)CCC1Oc(cc1)ccc1-c1cc(cccc2)c2nc1 Chemical compound O=C(c1cc(-c2ncc[nH]2)ccc1)N(CC1)CCC1Oc(cc1)ccc1-c1cc(cccc2)c2nc1 PGFOJOMSLRORFT-UHFFFAOYSA-N 0.000 description 1
- ZOJHBECRCFVODG-UHFFFAOYSA-N O=C(c1ccc[o]1)N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1 Chemical compound O=C(c1ccc[o]1)N(CC1)CCC1Oc(cc1)ccc1-c1cnc(cccc2)c2c1 ZOJHBECRCFVODG-UHFFFAOYSA-N 0.000 description 1
- WSHICMCGZRQBPA-IKOFQBKESA-N OC([C@@H]1OCCC1)N(CC1)CCC1Oc(cc1)ccc1-c1cc(cccc2)c2nc1 Chemical compound OC([C@@H]1OCCC1)N(CC1)CCC1Oc(cc1)ccc1-c1cc(cccc2)c2nc1 WSHICMCGZRQBPA-IKOFQBKESA-N 0.000 description 1
- VPCJFPJAXDLZMY-UHFFFAOYSA-N Oc(c1ncccc1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(C1CC1)=O Chemical compound Oc(c1ncccc1cc1)c1-c(cc1)ccc1OC(CC1)CCN1C(C1CC1)=O VPCJFPJAXDLZMY-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/40—Oxygen atoms
- C07D211/44—Oxygen atoms attached in position 4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4545—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring hetero atom, e.g. pipamperone, anabasine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/472—Non-condensed isoquinolines, e.g. papaverine
- A61K31/4725—Non-condensed isoquinolines, e.g. papaverine containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/54—Sulfur atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/56—Nitrogen atoms
- C07D211/58—Nitrogen atoms attached in position 4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Obesity (AREA)
- Child & Adolescent Psychology (AREA)
- Virology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Dermatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Hydrogenated Pyridines (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
Abstract
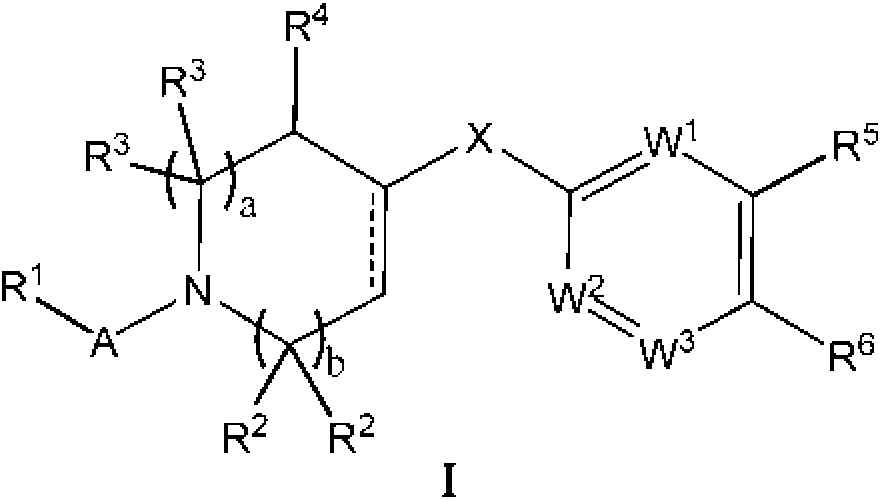
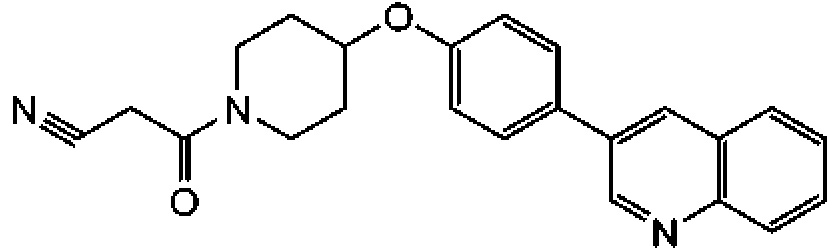
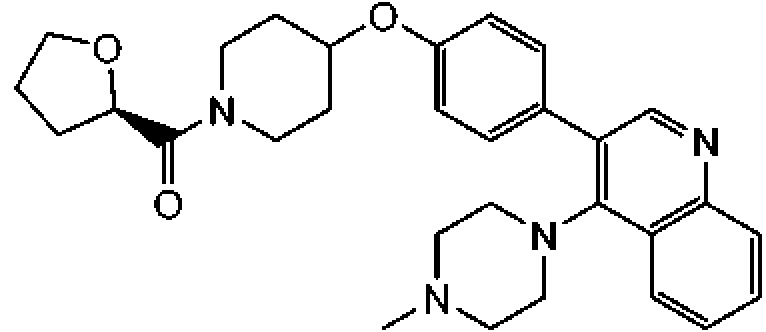
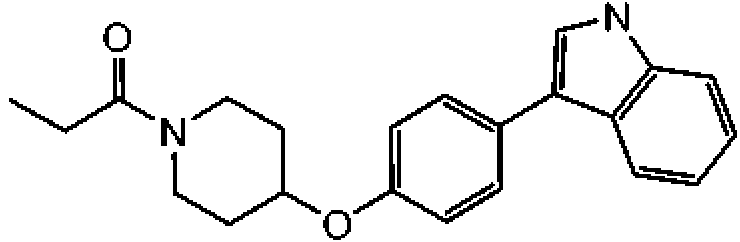
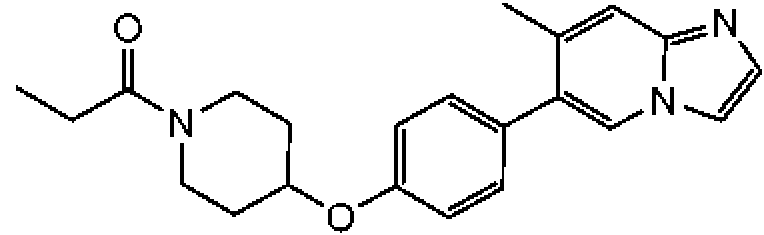
Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de -C(=O)- y -SO2-; R1 se selecciona de -H, -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -OR7, -SR7, -N(OR8)R7, -N(SR8)R7 y -C(=O)-(C1-C6) alquilo; a y b se seleccionan independientemente de 0 y 1; cada R2 se selecciona independientemente de -H y -(C1-C4) alquilo; cada R3 se selecciona independientemente de -H y -(C1-C4) alquilo R4 se selecciona de -H, (C1-C6) alquilo, =O, -OH, -O(C1-C6) alquilo, halógeno y -CN; en donde uno de los grupos R3 puede opcionalmente conectarse estructuralmente a uno de los grupos R2 para formar un puente alquileno para producir un anillo bicíclico; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R1 para formar un anillo heterociclilo de 5 a 7 miembros fusionado a la cara 1-2 del anillo de piperidina; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 a 7 miembros fusionado a la cara 2-3 del anillo de piperidina; indica que el enlace designado es un simple enlace carbono-carbono o un doble enlace carbono-carbono; X se selecciona de -O-, -S-, -SO-, -SO2-, -NH- y -NR9-; W1, W2 y W3 se seleccionan independientemente de N, CH y C-R10; siempre que W2 y W3 no sean N; R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3) haloalquilo, -OR7a, -CN-NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a-C(=O)OR7a, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, heteroarilo bicíclico de 8 a 10 miembros y heteroarilo bicíclico sustituido de 8 a 10 miembros; n es un número entero seleccionado de 1, 2, 3 y 4; R6 se selecciona de: **(Ver fórmula)** en donde, cuando R6 es (i), Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12; cuando R6 es (ii), Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sean N, y el resto de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sea C-R12; cuando R6 es (iii), Q8 se selecciona de O, S y N-R12n, Q9, Q10 y Q11 se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12; cuando R6 es (iv), Q8a se selecciona de O, S y N-R12n, Q9a, Q10a y Q11a se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9a, Q10a y Q11a sean N, y el resto de Q9a, Q10a y Q11a sea C-R12; cuando R6 es (v), Q12, Q13 y Q14 se seleccionan independientemente de N y C-R12; y cuando R6 es (vi), Q12a, Q13a y Q14a se seleccionan independientemente de N y C-R12; cuando R6 es (vii), Q15 se selecciona de N-R12n y C-R12 y Q16 se selecciona de N y C-R12; siempre que Q15 y Q16 no sean C-R12; en donde los átomos del anillo de carbono del anillo que no son cabeza de puente en (i), (ii), (iii), (iv), (v), (vi) y (vii) que no se designan como Q1, Q2, Q3, Q4, Q5, Q6, Q7, Q8, Q9, Q10, Q11, Q12, Q13, Q14, Q15, Q16, Q1a, Q2a, Q3a, Q4a, Q5a, Q6a, Q7a, Q8a, Q9a, Q10a, Q11a Q12a, Q13a o Q14a están sustituidos o no sustituidos; R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, -(C1-C6) heteroalquilo, arilo de 5 a 6 miembros, heteroarilo de 5 a 6 miembros y heterociclilo de 5 a 6 miembros; R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros; R7a se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo; R8a se selecciona de -H y -(C1-C6) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros; R9 se selecciona de -(C1-C7) hidrocarbilo, en donde R9 puede opcionalmente conectarse estructuralmente a R4 para formar un anillo heterociclilo de 5 a 7 miembros; cada R10 se selecciona independientemente de -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, halógeno, -C(=O)(C1-C7)hidrocarbilo, -C(=O)NH2, -C(=O)NH(C1-C7)hidrocarbilo, -C(=O)N((C1-C7)hidrocarbilo)2, -OH, -O(C1-C7) hidrocarbilo, -O(C1-C7) hidrocarbilo sustituido, -(C3-C6)heterociclilo, -(C3-C6)heterociclilo sustituido, -CN, -NH2, -NH(C1-C6)alquilo, -N(C1-C6 alquilo)2, -NH(CH2)m-R11, -N(C1-C6 alquilo)(CH2)m-R11, -O-(CH2)m-R11 y -(C1-C6) heteroalquilo; m es un número entero seleccionado independientemente de 1, 2, 3 y 4; y R11 se selecciona de -O(C1-C6) alquilo, -N(C1-C6 alquilo)2, -(C3-C6) heterociclilo y -(C3-C6) heterociclilo sustituido; y en donde cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1- C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo y -C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado independientemente de 1, 2, 3 y 4; y cada R12n se selecciona independientemente de -H, -(C1-C7) hidrocarbilo y -(C1-C7) hidrocarbilo sustituido.
Description
DESCRIPCIÓN
Derivados de piperidina 1,4 sustituidos
Campo de la invención
La presente invención se refiere a compuestos de acuerdo con la Fórmula I, así como a las composiciones farmacéuticas que contienen estos compuestos y a un compuesto de acuerdo con la Fórmula I, o una sal farmacéuticamente aceptable del mismo, o una composición farmacéutica que comprende al menos un compuesto de acuerdo con la Fórmula I o un una sal farmacéuticamente aceptable del mismo, y al menos un excipiente farmacéuticamente aceptable para usar en métodos de tratamiento del cáncer, y un compuesto de acuerdo con la Fórmula I, o una sal farmacéuticamente aceptable del mismo, o una composición farmacéutica que comprende al menos un compuesto de acuerdo con la Fórmula I o una sal farmacéuticamente aceptable del mismo, y al menos un excipiente farmacéuticamente aceptable para su uso en métodos de tratamiento del aumento de peso asociado con la terapia farmacológica con antipsicóticos, comprendiendo los métodos administrar una dosis terapéuticamente eficaz de uno o más de los compuestos de Fórmula I, o una composición farmacéutica que comprende uno o más de los compuestos de Fórmula I, a un paciente que necesite dicha terapia.
Antecedentes
La sintasa de ácidos grasos (FASN) es un complejo proteico multienzimático que cataliza la síntesis de ácidos grasos implicados en la producción y almacenamiento de energía, la estructura celular y la formación de intermediarios en la biosíntesis de hormonas y otras moléculas biológicamente significativas (Nature Reviews Cancer, 2007, pág. 7, 763 777). La FASN está compuesta por dos polipéptidos multifuncionales idénticos de 272 kDa. Como función principal, cataliza la síntesis de palmitato a partir de acetil-CoA y malonil-CoA, en presencia de nicotinamida adenina dinucleótido fosfato (NADPH). En los tejidos humanos normales (a excepción del hígado y el tejido adiposo), los ácidos grasos se obtienen preferentemente de la dieta y la expresión de los niveles de FASN es baja. Por el contrario, la expresión y actividad de FASN es muy elevada en varios estados patológicos que incluyen cáncer, enfermedades inflamatorias y metabólicas. En particular, la evidencia muestra que el aumento de la síntesis de ácidos grasos endógenos es fundamental para la tumorigénesis.
El cáncer es una enfermedad de crecimiento y proliferación celular acelerados. Las células cancerosas se adaptan metabólicamente para aumentar los niveles de lípidos para respaldar sus requisitos anabólicos. El aumento de la síntesis de ácidos grasos representa una adaptación metabólica fundamental de las células cancerosas y se facilita por los altos niveles de expresión de FASN. El aumento de la expresión de FASN es un evento temprano en la tumorigénesis y se encuentra en numerosos tipos de tumores, con frecuencia se correlaciona con un mal pronóstico (Nature Reviews Cancer, 2007, 7, 763-777). Se observó amplificación del gen FASN y sobreexpresión de proteínas en cánceres de mama, ovario, próstata, colon, pulmón, vejiga, estómago y riñón humanos, lo que sugiere que FASN es un objetivo farmacológico potencial y un marcador de mal pronóstico (Nature Reviews Cancer, 2007, 7, 763-777); Anticancer Res. 2007, 27, 27-34; Cancer Res., 2006, 66, 5977-5980, Nutrition, 2000, 16, 202-208).
Además de las células tumorales, las células inmunitarias se adaptan, proliferan y diferencian metabólicamente en distintas clases funcionales en respuesta a estímulos inmunogénicos. Los estudios han demostrado que la lipogénesis juega un papel fundamental en las respuestas inmunitarias y la adaptación metabólica de las células inmunitarias activadas. La inhibición de la síntesis de ácidos grasos durante la diferenciación de células T resulta en un cambio de células Th17 a células Treg, lo que sugiere un enfoque novedoso para el tratamiento de enfermedades autoinmunes, como la esclerosis múltiple, y para modular las respuestas inmunitarias (Nature Medicine, 2014, 20, 1327-1333). De manera similar, la síntesis de novo de ácidos grasos es fundamental para la expansión de las células T CD8+ y la activación de las células dendríticas (Nature Immunology, 2014, 15, 323-332). Estos resultados demuestran que la modulación de la vía de síntesis de ácidos grasos podría representar una estrategia para controlar las respuestas inmunitarias y para tratar una amplia gama de enfermedades autoinmunes.
Se ha implicado a FASN como una enzima importante que promueve un ciclo de vida de múltiples virus y
microorganismos. Se ha demostrado que la biosíntesis de lípidos de novo es necesaria para la replicación de la familia Flaviviridae, incluidos el virus de la hepatitis C, el virus del dengue, el virus de la fiebre amarilla, el virus del Nilo occidental y otros (Chemistry and Biology, 2013, 570-582). La inhibición de FASN por inhibidores de moléculas pequeñas como Cerulenin y Orlistat resultó en una fuerte inhibición de la replicación viral. Otros virus también dependen de la actividad de FASN, incluido el citomegalovirus humano (HCMV), influenza A, virus del Epstein Barr (EBV) y coxsackievirus B3 (CVB3). Numerosas pantallas de todo el genoma identificaron múltiples genes del huésped implicados en el metabolismo de los lípidos que son cruciales para la replicación de virus, y con frecuencia se requiere una mayor expresión de FASN para una replicación viral eficaz (Nature Biotechnology, 2008, 26, 179-186). En conjunto, estos resultados proporcionan un fundamento sólido para seleccionar a FASN para la terapia antiviral.
La acumulación de ácidos grasos se asocia con una variedad de enfermedades metabólicas y se ha demostrado que contribuye a su patogénesis. La esteatosis hepática no alcohólica (EHNA), también llamada enfermedad del hígado graso engloba un espectro de enfermedades hepáticas (esteatosis, esteatosis con inflamación, cirrosis) caracterizadas por una acumulación de ácidos grasos en los hepatocitos. Actualmente, la EHNA es la enfermedad hepática más común en los países desarrollados y se asocia con la obesidad, la resistencia a la insulina y la diabetes tipo 2. Los estudios en modelos animales demostraron que la inhibición farmacológica de FASN mejoró la función hepática y disminuyó la acumulación de grasa hepática (PloS One, 2013, 9, 1-8).
La FASN se expresa en gran medida en tejidos con alta actividad metabólica (hígado, tejido adiposo y cerebro) y es una enzima crítica para la lipogénesis endógena y la modulación de intermediarios claves del metabolismo celular de lípidos y carbohidratos. Se ha propuesto un inhibidor de FASN para el tratamiento de la obesidad, y la inhibición de FASN en el hipotálamo puede resultar en una reducción de la ingestión de alimentos. Se ha informado que los inhibidores irreversibles no específicos de FASN como cerulenina y C-75 disminuyen los niveles cerebrales de neuropéptidos orexigénicos y disminuyen la ingestión de alimentos. Por lo tanto, la inhibición de FASN representa un objetivo terapéutico en un amplio espectro de patologías que incluyen cáncer, enfermedades antivirales, hepáticas y cardiovasculares y el tratamiento de la obesidad, diabetes y aumento de peso corporal inducido por fármacos; por ejemplo, antipsicóticos.
Los avances recientes en el tratamiento y el manejo del cáncer muestran que muchas terapias contra el cáncer generan cambios profundos en el metabolismo tumoral. La inhibición de la señalización de BRAF por vemurafenib y la inhibición de BCR-ABL por imatinib genera un aumento de la fosforilación oxidativa (Pollak M, (2013) Targeting Oxidative Phosphorylation: Why, When and How; Cancer Cell 18, 263-63). Tal reprogramación del metabolismo celular inducida por fármacos desde la glucólisis a la fosforilación oxidativa podría crear una dependencia de los lípidos que podría aprovecharse terapéuticamente mediante el uso de inhibidores de FASN. En otro ejemplo más, se demostró que el cese de la terapia anti-angiogénica por sunitinib y sorafenib resultó un rápido crecimiento de los tumores y un aumento de la metástasis que fueron mediadas por un rápido cambio metabólico de las células tumorales y estromales a la lipogénesis de novo. La inhibición farmacológica de FASN fue suficiente para revertir el recrecimiento del tumor y la diseminación metastásica, lo que confirma aún más el papel del metabolismo de los lípidos en la adaptación del tumor a las terapias contra el cáncer (Sounni NE, Cimino J, Blacher S, Primac I, Truong A, Mazucchelli G, Paye A, calligaris D, Debois D, mari B, de pauw E, Noel A (2014) Blocking Lipid Synthesis Overcomes Tumor Regrowth and Metastasis after Angiogenic Therapy Withdrawal; Cell Metabolism 20, 1-15) y proporciona una justificación para los tratamientos combinatorios con inhibidores de FASN.
El documento WO 2015/084606 A1 describe "derivados de benzamida, composiciones farmacéuticas que los contienen y su uso como inhibidores de FASN, por ejemplo, en el tratamiento de cáncer, trastornos relacionados con la obesidad, trastornos relacionados con el hígado e infecciones virales".
Resumen
Las modalidades de la presente invención se exponen en las reivindicaciones adjuntas. En una modalidad, la presente invención proporciona un compuesto de acuerdo con la Fórmula I:
a sal farmacéuticamente aceptable del mismo, en donde:
A se selecciona de -C(=O)- y -SO2-;
R1 se selecciona de -H, -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -OR7, -SR7, -N(OR8)R7, -N(SR8)R7 y -C(=O)(C1-C6) alquilo; a y b se seleccionan independientemente de 0 y 1;
cada R2 se selecciona independientemente de -H y -(C1-C4) alquilo;
cada R3 se selecciona independientemente de -H y -(C1-C4) alquilo
R4 se selecciona de -H, -(C1-C6) alquilo, =O, -OH, -O(C1-C6) alquilo, halógeno y -CN; en donde uno de los grupos R3 puede opcionalmente conectarse estructuralmente a uno de los grupos R2 para formar un puente alquileno para producir un anillo bicíclico; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R1 para formar un anillo heterociclilo de 5 a 7 miembros fusionado a la cara 1-2 del anillo de piperidina; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 a 7 miembros fusionado a la cara 2-3 del anillo de piperidina;
----------indica que el enlace designado es un simple enlace carbono-carbono o un doble enlace carbono-carbono; X se selecciona de -O-, -S-, -SO-, -SO2-, -NH- y -NR9-;
W1, W2 y W3 se seleccionan independientemente de N, CH y C-R10; siempre que W2 y W3 no sean N;
R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a, -C(=O)OR7a, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, heteroarilo bicíclico de 8 a 10 miembros y heteroarilo bicíclico sustituido de 8 a 10 miembros;
n es un número entero seleccionado de 1, 2, 3 y 4;
R6 se selecciona de:
en donde, cuando R6 es (i), Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan independientemente de N y C-R12, siempre que 1,2 o 3 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12; cuando R6 es (ii), Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sean N, y el resto de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sea C-R12; cuando R6 es (iii), Q8 se selecciona de O, S y N-R12n, Q9, Q10 y Q11 se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;
cuando R6 es (iv), Q8a se selecciona de O, S y N-R12n, Q9a, Q10a y Q11a se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9a, Q10a y Q11a sean N, y el resto de Q9a, Q10a y Q11a sea C-R12;
cuando R6 es (v), Q12, Q13 y Q14 se seleccionan independientemente de N y C-R12; y
cuando R6 es (vi), Q12a, Q13a y Q14a se seleccionan independientemente de N y C-R12;
cuando R6 es (vii), Q15 se selecciona de N-R12n y C-R12 y Q16 se selecciona de N y C-R12; siempre que Q15 y Q16 no sean C-R12;
en donde los átomos del anillo de carbono del anillo que no son cabeza de puente en (i), (ii), (iii), (iv), (v), (vi) y (vii) que no se designan como Q1, Q2, Q3, Q4, Q5, Q6, Q7, Q8, Q9, Q10, Q11, Q12, Q13, Q14, Q15, Q16, Q1a, Q2a, Q3a, Q4a, Q5a, Q6a, Q7a, Q8a, Q9a, Q10a, Q11a, Q12a, Q13a o Q14a están sustituidos o no sustituidos; R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, -(C1-C6) heteroalquilo, arilo de 5 a 6 miembros, heteroarilo de 5 a 6 miembros y heterociclilo de 5 a 6 miembros;
R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;
R7a se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo, -C(=O)R8, y -(C1-C6) heteroalquilo sustituido; R8a se selecciona de -H y -(C1-C6) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros;
R9 se selecciona de -(C1-C7) hidrocarbilo, en donde R9 puede opcionalmente conectarse estructuralmente a R4 para formar un anillo heterociclilo de 5 a 7 miembros;
cada R10 se selecciona independientemente de (C1-C7) hidrocarbilo, (C1-C7) hidrocarbilo sustituido, halógeno, -C(=O)(C1-C7) hidrocarbilo, -C(=O)NH2, -C(=O)NH(C1-C7) hidrocarbilo, -C(=O)N((C1-C7)hidrocarbilo)2, -OH, -O(C1-C7) hidrocarbilo, -O(C1-C7) hidrocarbilo sustituido, -(C3-C6) heterociclilo, -(C3-C6)heterociclilo sustituido, -CN, -NH2, -NH(C1-C6)alquilo, -N(C1-C6 alquilo)2, -NH(CH2)m-R11, -N(C1-C6 alquilo)(CH2)m-R11, -O-(CH2)m-R11, y heteroalquilo -(Ci-Ce);
m es un número entero seleccionado independientemente de 1,2, 3 y 4; y
R11 se selecciona de -O(C1-C6) alquilo, -N(C1-C6 alquilo)2, -(C3-C6) heterociclilo y -(C3-C6) heterociclilo sustituido; y en donde cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=o )n H(C1-C6) alquilo y -C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado independientemente de 1, 2, 3 y 4; y
cada R12n se selecciona independientemente de -H, -(C1-C7) hidrocarbilo y -(C1-C7) hidrocarbilo sustituido.
En otra modalidad, la presente invención proporciona un compuesto de acuerdo con la Fórmula I, o una sal farmacéuticamente aceptable del mismo, para uso en el tratamiento de un sujeto que padece un trastorno mediado por la sintasa de ácidos grasos.
En otra modalidad, la presente invención proporciona una composición farmacéutica que comprende al menos un compuesto de acuerdo con la Fórmula I o una sal farmacéuticamente aceptable del mismo, y al menos un excipiente farmacéuticamente aceptable para su uso en el tratamiento de un sujeto que padece un trastorno mediado por la sintasa de ácidos grasos.
En otra modalidad, la presente invención proporciona un compuesto de acuerdo con la Fórmula I, o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento de un sujeto que padece un aumento de peso asociado con la terapia farmacológica con un agente antipsicótico.
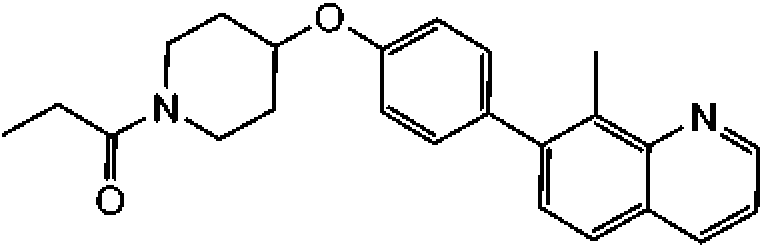
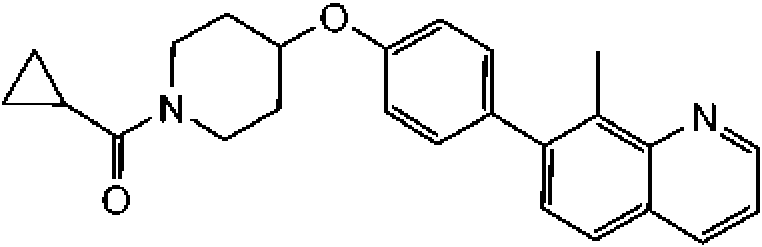
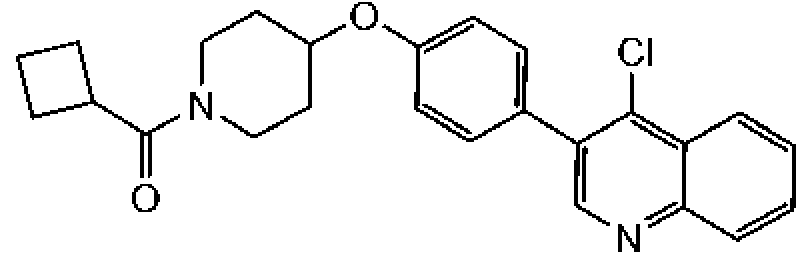
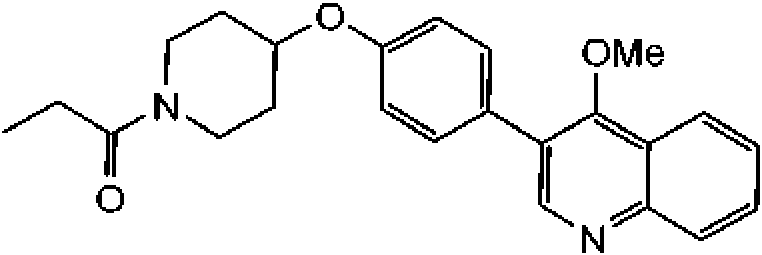
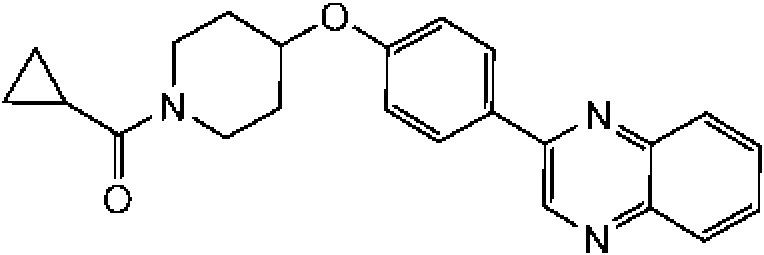
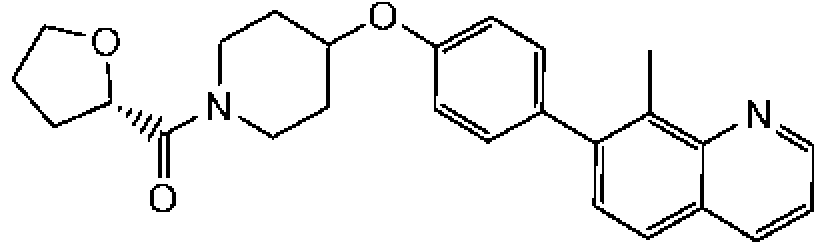
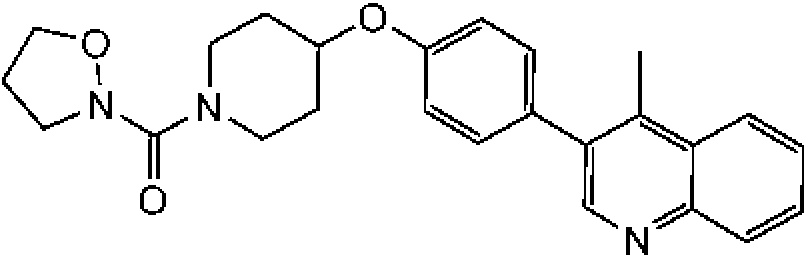
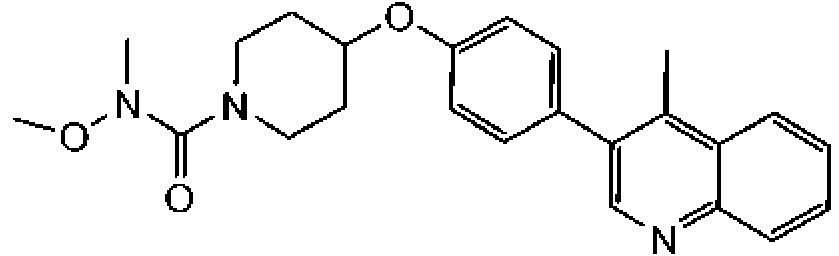
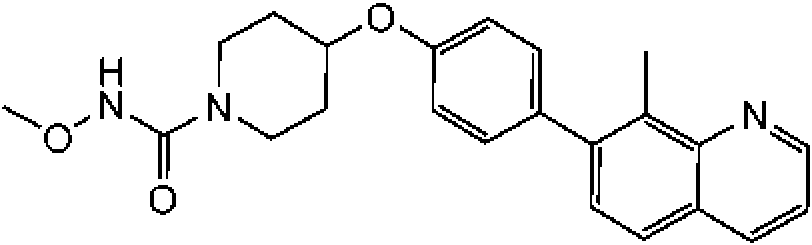
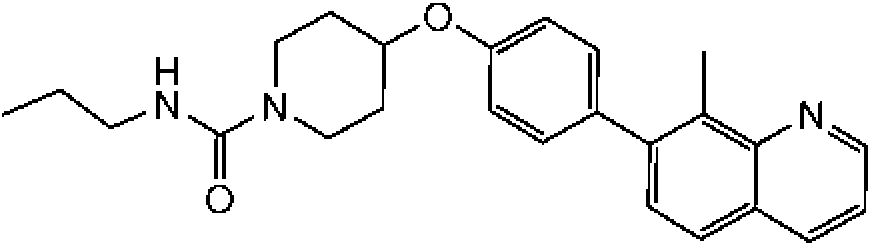
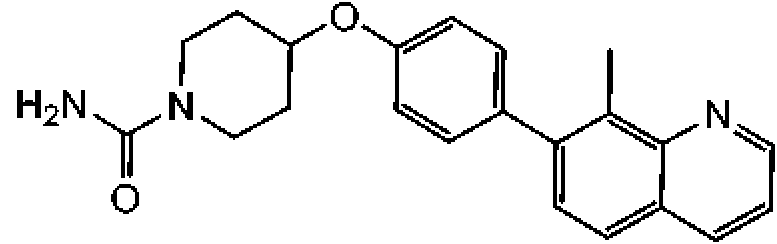
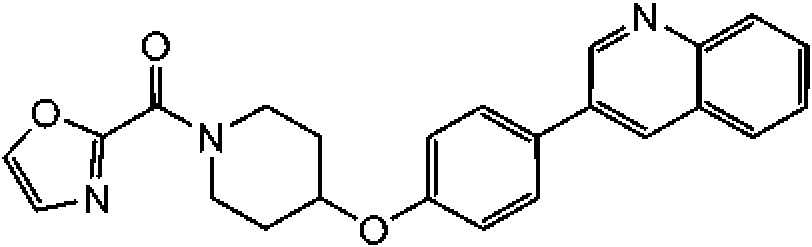
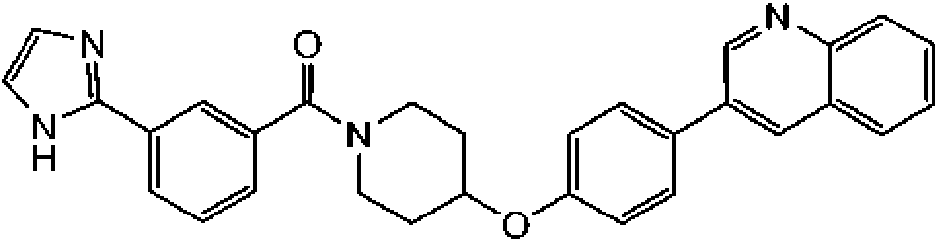
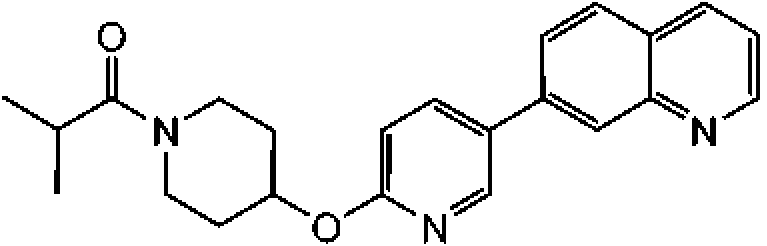
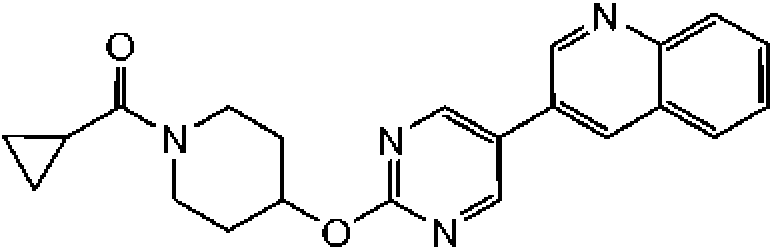
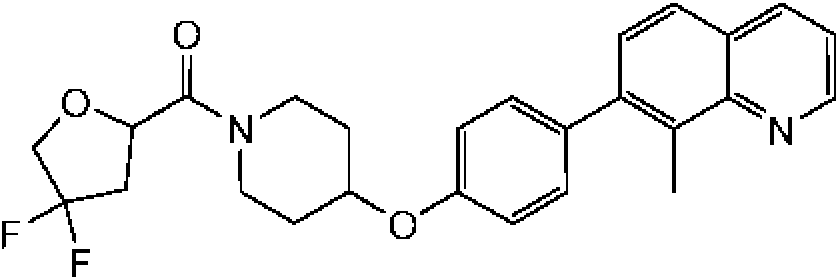
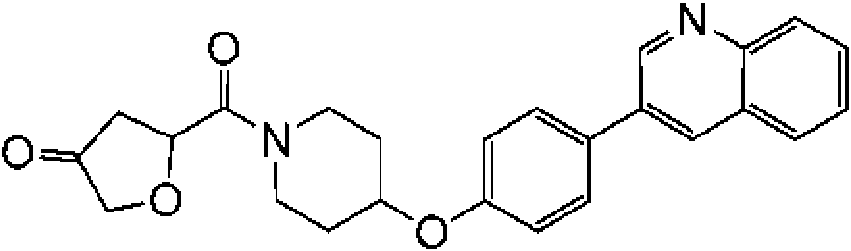
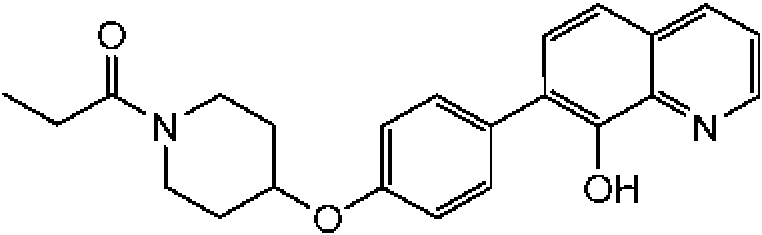
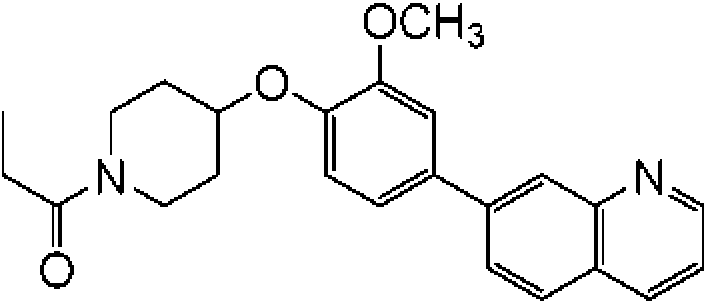
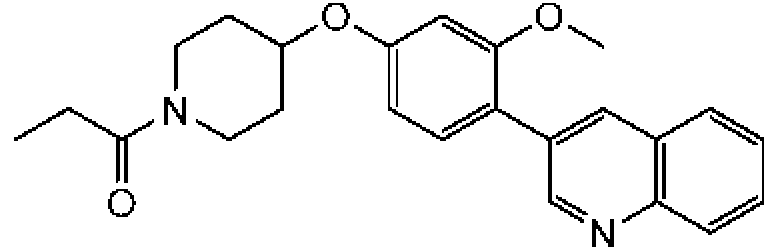
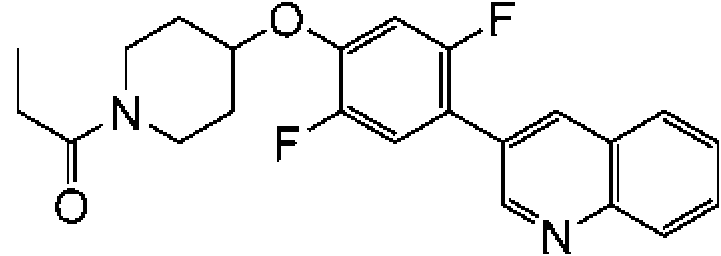
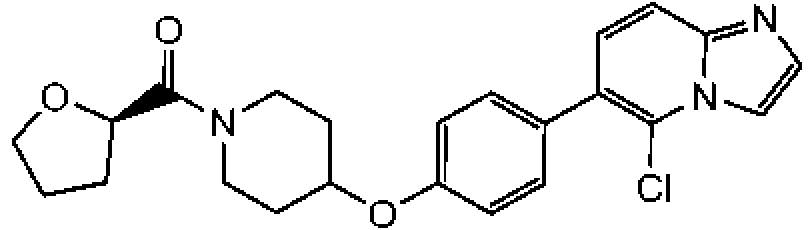
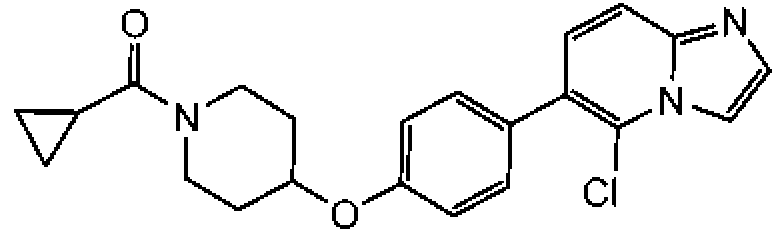
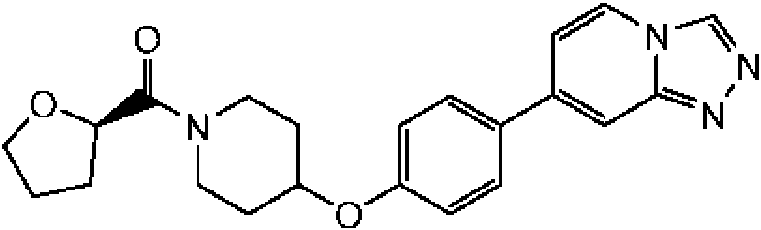
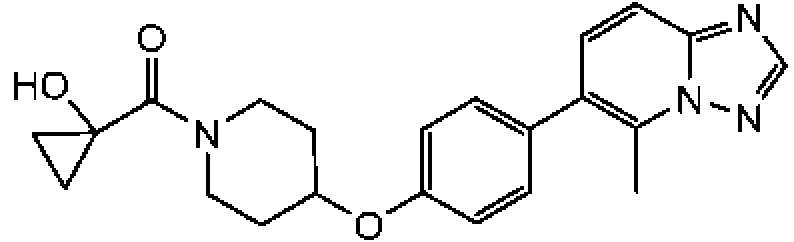
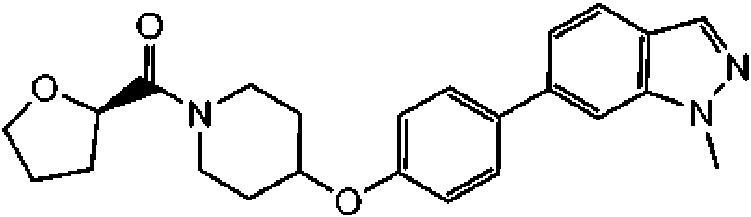
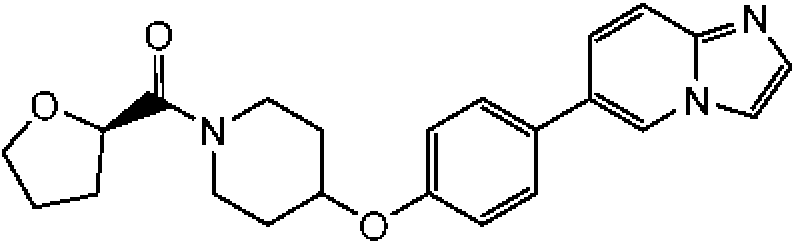
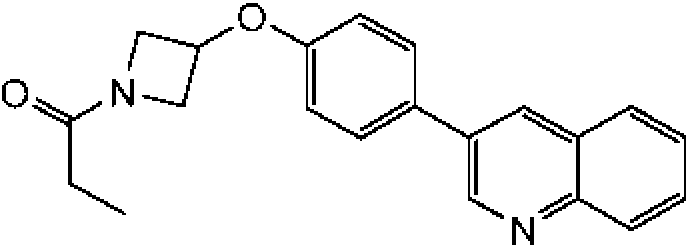
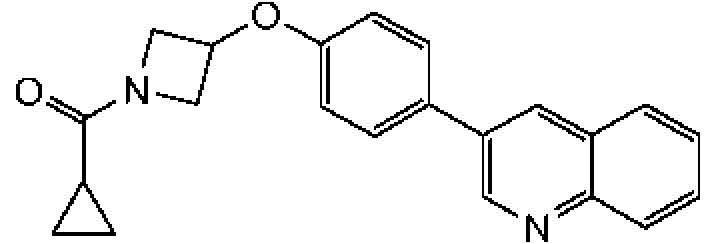
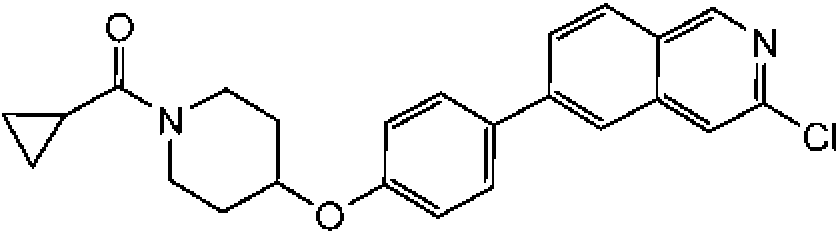
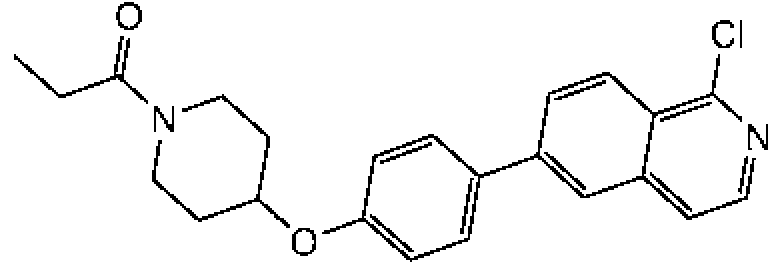
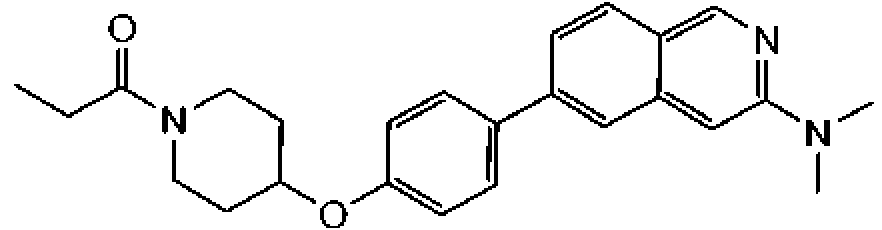
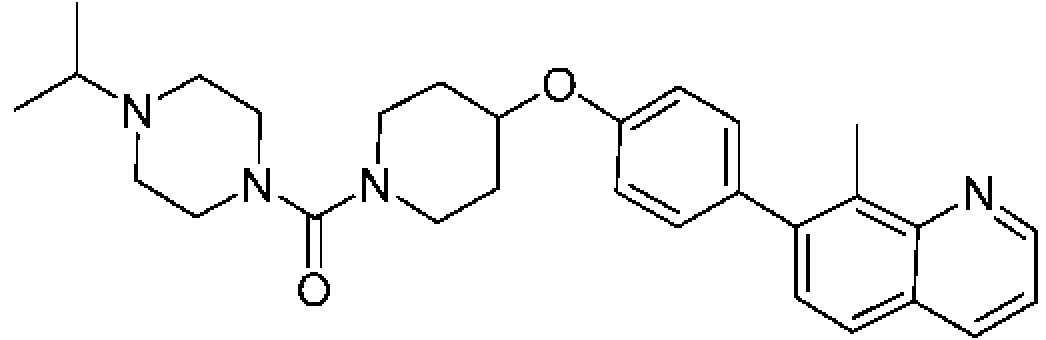
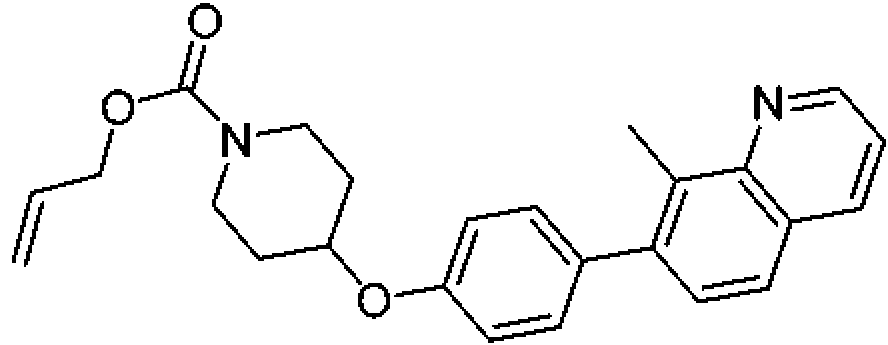
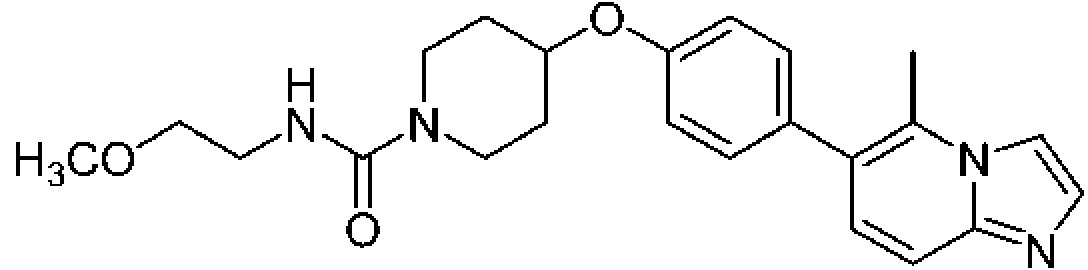
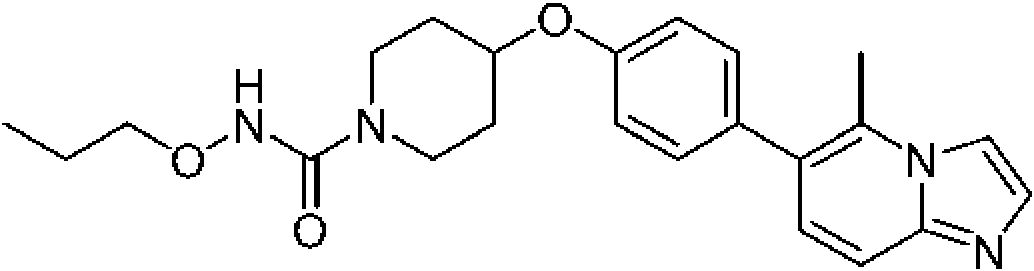
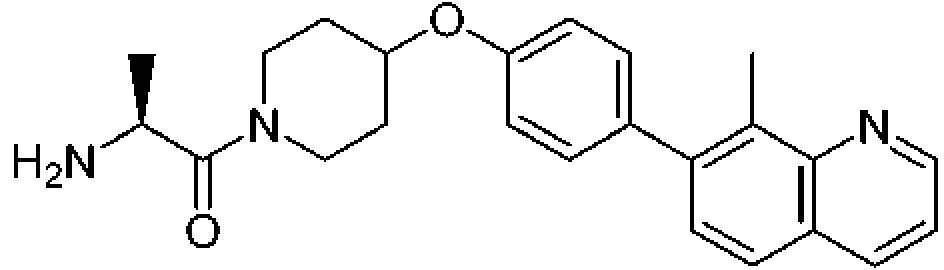
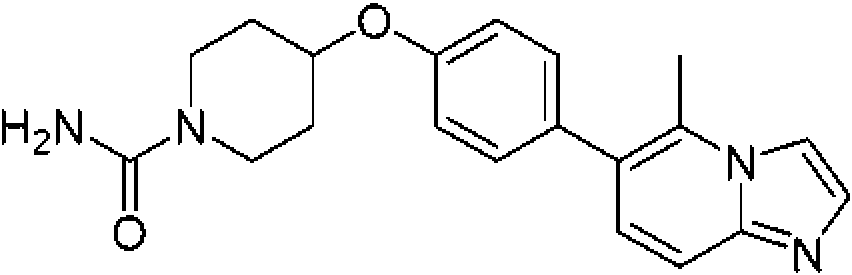
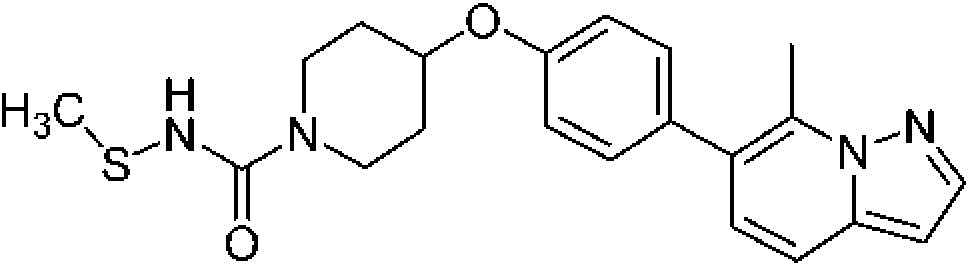
En otra modalidad de la presente invención proporciona un compuesto seleccionado del grupo que consiste en:
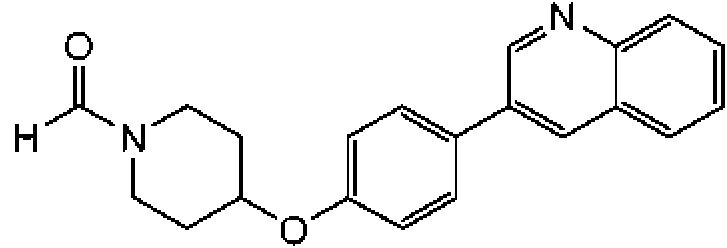
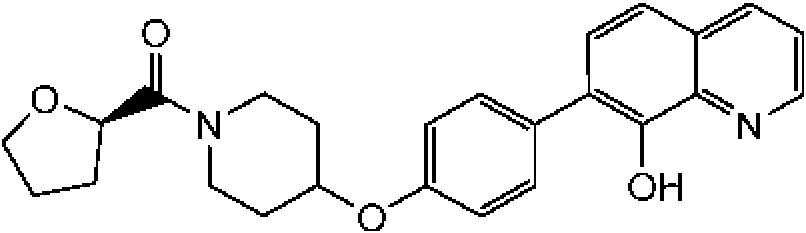
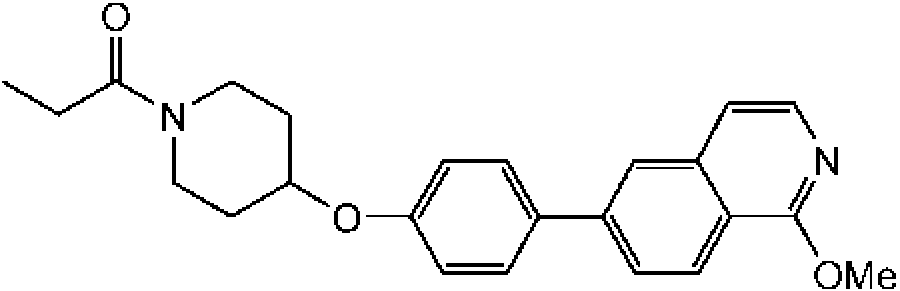
1-[4-(4-benzo[b]tiofen-5-il-fenoxi)-piperidin-1-il]-propan-1-ona;
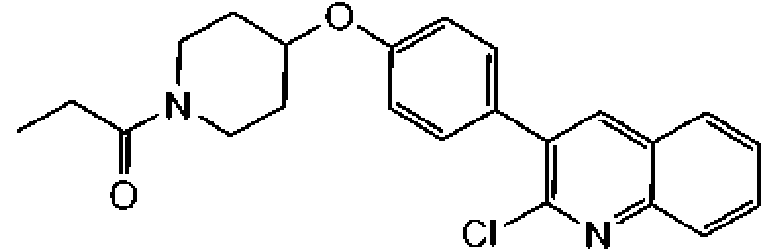
1-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;
ciclopropil-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;
1-[4-(4-benzofuran-5-il-fenoxi)-piperidin-1-il]-propan-1-ona;
1-[4-(4-benzofuran-5-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;
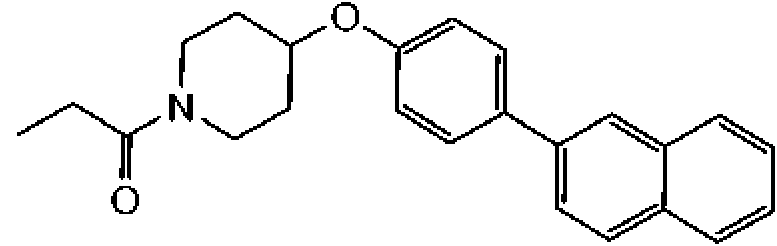
1- [4-(4-naftalen-2-il-fenoxi)-piperidin-1-il]-propan-1-ona;
2- metil-1-[4-(4-naftalen-2-il-fenoxi)-piperidin-1-il]-propan-1-ona;
ciclopropil-{4-[4-(5,6,7,8-tetrahidro-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;
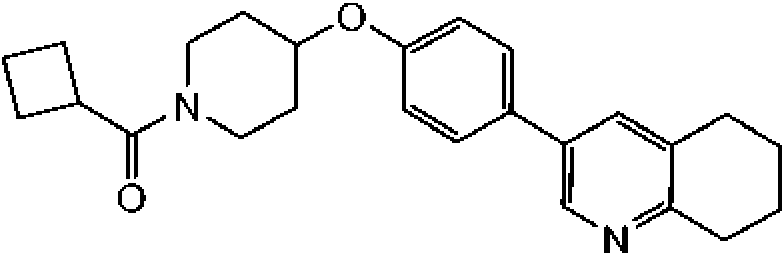
ciclobutil-{4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;
1-{4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
1-{4-[4-(1H-pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(1H-pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-1-il}-metanona;
ácido 1 -propionil-piperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)-amida;
ácido 1-propionil-piperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida;
ácido 1-propionilpiperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida;
2-fluoro-4-isoquinolin-6-il-N-metil-N-(1-propionil-piperidin-4-il)-benzamida;
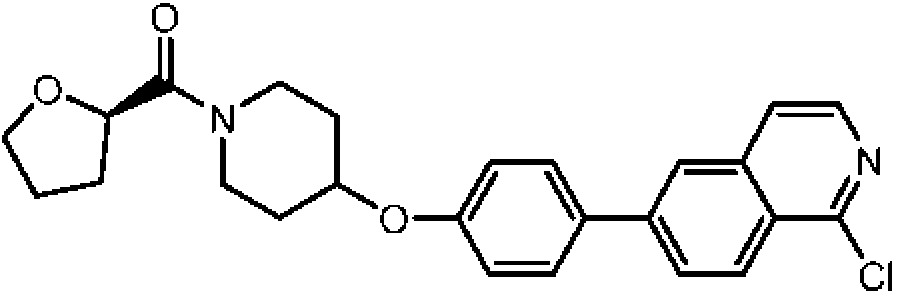
1-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1 -il}-metanona;
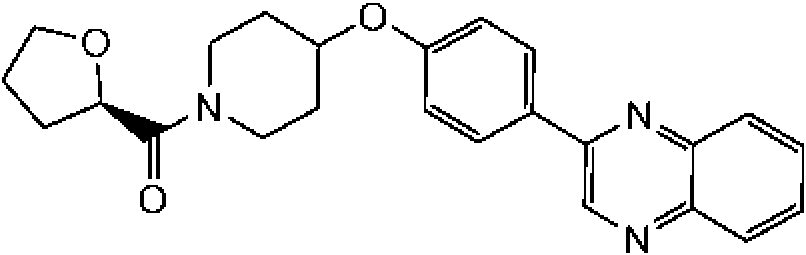
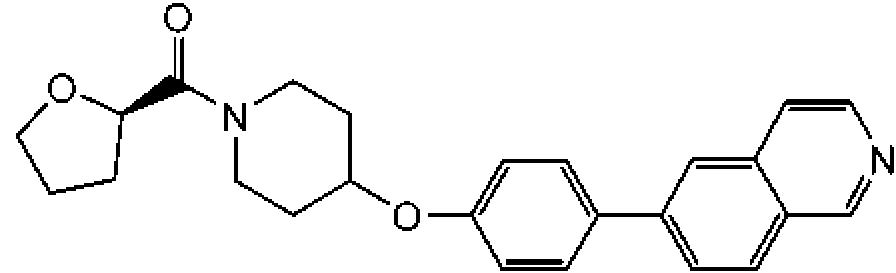
(R)-tetrahidrofuran-2-il-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; 4'-[1-((R)-tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-bifenil-4-carbonitrilo;
1-[4-(4-benzofuran-2-il-fenoxi)-piperidin-1-il]-propan-1-ona;
1-{4-[4-(1H-indol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
1-{4-[4-(1H-indazol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
1-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-propan-1-ona;
(R)-tetrahidrofuran-2-il-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona;
ciclopropil-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona;
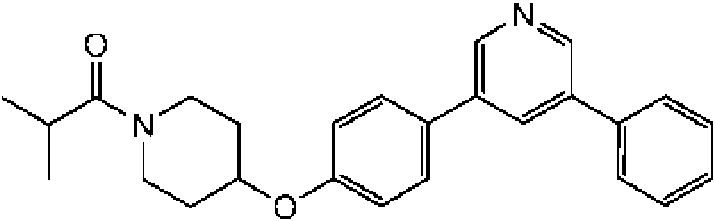
1- {4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
2- metil-1-{4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
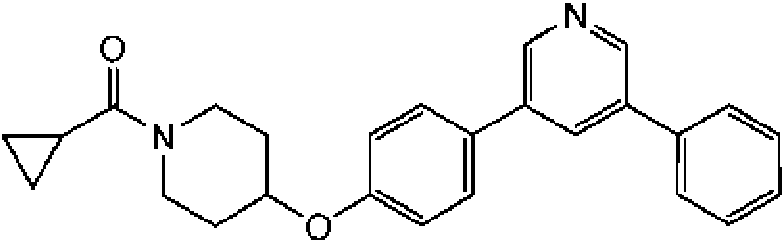
ciclopropil-{4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
ciclobutil-{4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
1- {4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
2- metil-1-{4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(5-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
ciclobutil-{4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
1-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
ciclobutil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
1-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
ciclobutil-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
1-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
ciclobutil-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
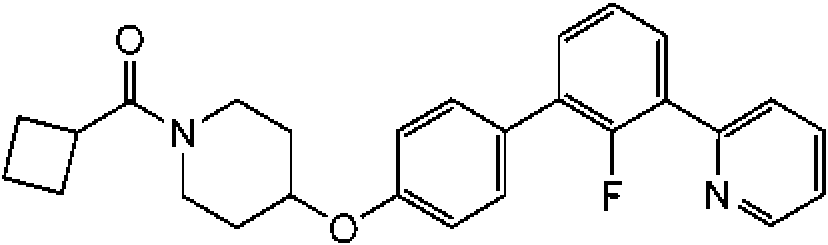
1-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
ciclopropil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;
1-{4-[4-(5-fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclobutil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;
ciclopropil-{4-[4-(5-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
ciclobutil-{4-[4-(5-fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
1-{4-[4-(5-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
1-{4-[4-(2-fenilpiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(2-fenilpiridin-4-il)-fenoxi]-piperidin-1-il}-metanona;
1-{4-[4-(2-fenilaminopiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(2-fenilaminopiridin-4-il)-fenoxi]-piperidin-1-il}-metanona;
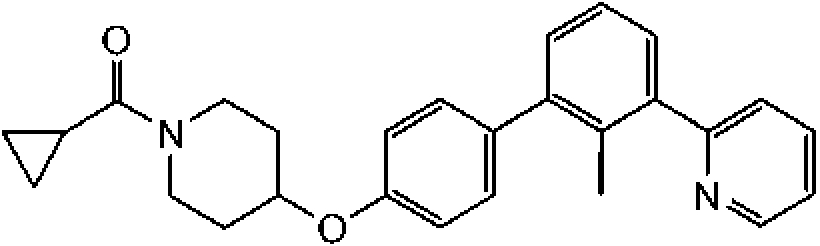
1-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
ciclopropil-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;
ciclobutil-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;
1-{4-[4-(2-fenoxipiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
t-butil éster del ácido 4-(3',4'-dimetoxibifenil-4-iloxi)-piperidina-1-carboxílico;
t-butil éster del ácido 4-(4'-ciano-bifenil-4-iloxi)-piperidina-1 -carboxílico;
1-[4-(3',4'-dimetoxi-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
1-[4-(3',4'-dimetoxibifenil-4-iloxi)-piperidin-1-il]-2-metil-propan-11-ona;
4'-(1-propionil-piperidin-4-iloxi)-bifenil-4-carbonitrilo;
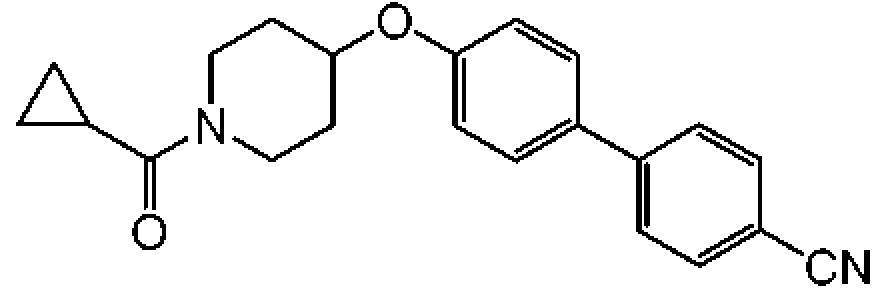
4'-(1-isobutirilpiperidin-4-iloxi)-bifenil-4-carbonitrilo;
4'-(1-ciclopropanocarbonil-piperidin-4-iloxi)-bifenil-4-carbonitrilo;
1-{4-[4-(5,6-dimetoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
ciclopropil-{4-[4-(5,6-dimetoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;
1-[4-(3',4'-diclorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
ciclopropil-[4-(3',4'-diclorobifenil-4-iloxi)-piperidin-1-il]-metanona;
1-{4-[4-(2,3-dihidro-1,4-benzodioxin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;
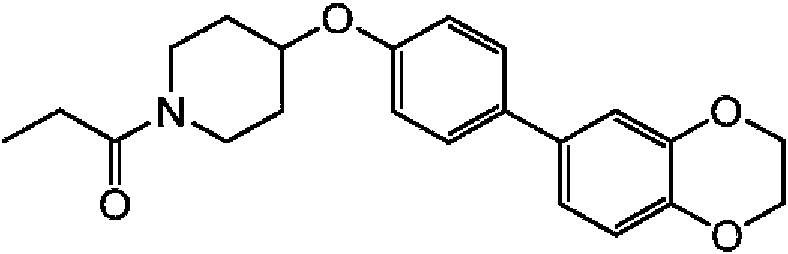
ciclopropil-{4-[4-(2,3-dihidro-1,4-benzodioxin-6-il)-fenoxi]-piperidin-1-il}-metanona;
1-[4-(4'-benziloxi-2'-fluoro-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
[4-(4'-benziloxi-2'-fluorobifenil-4-iloxi)-piperidin-1-il]-ciclopropil-metanona;
1-[4-(5'-benziloxi-3'-fluorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
[4-(5'-benziloxi-3'-fluorobifenil-4-iloxi)-piperidin-1-il]-ciclopropil-metanona;
1-[4-(4'-fenoxibifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
ciclopropil-[4-(4'-fenoxibifenil-4-iloxi)-piperidin-1-il]-metanona;
1-[4-(3'-fenoxibifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;
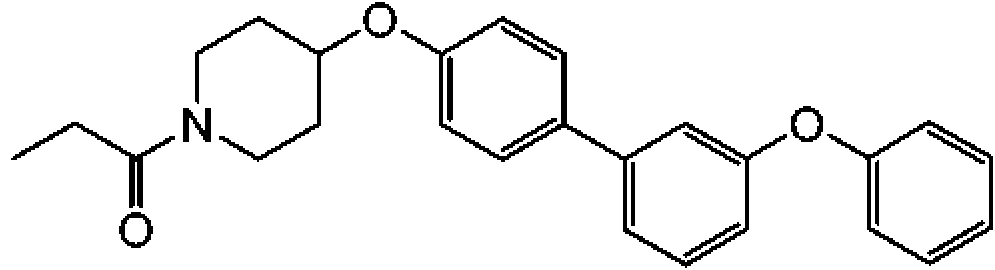
ciclopropil-[4-(3'-fenoxibifenil-4-iloxi)-piperidin-1-il]-metanona;
1-[4-(4-benzofuran-5-il-bencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona;
y sales farmacéuticamente aceptables de los mismos.
Esta solicitud se refiere a compuestos de Fórmula I:
incluyendo todas las formas estereoisoméricas y mezclas de formas estereoisoméricas de estos compuestos. La solicitud se refiere además a sales de compuestos de acuerdo con la Fórmula I, por ejemplo, sales farmacéuticamente aceptables, y sus composiciones, por ejemplo, composiciones farmacéuticas, que contienen compuestos de acuerdo con la Fórmula I, o sales de los mismos.
Los compuestos de Fórmula I y /o sus sales farmacéuticamente aceptables son útiles para tratar afecciones, trastornos y enfermedades que están controladas, mediadas, afectadas o influenciadas directa o indirectamente, por la expresión de FASN. Los compuestos de Fórmula I son inhibidores de FASN y, por lo tanto, son útiles en el tratamiento de diversas afecciones, trastornos o enfermedades mediados por la expresión de FASN, incluidas afecciones relacionadas con el cáncer, trastornos metabólicos y el sistema nervioso central (SNC).
Descripción detallada
A continuación, se proporcionan detalles adicionales no limitantes de los compuestos de Fórmula I, así como diversas especies y modalidades más específicas de los mismos, intermediarios y procesos de síntesis.
Un aspecto de esta solicitud se dirige a compuestos de Fórmula I:
y sales del mismo, por ejemplo, sales farmacéuticamente aceptables del mismo, en donde:
A se selecciona de -C(=O)- y -SO2-;
R1 se selecciona de -H, -(C1-C10) hidrocarbilo, (C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -OR7, -SR7, -N(OR8)R7, -N(SR8)R7 y -C(=O)-(C1-C6) alquilo; a y b se seleccionan independientemente de 0 y 1;
cada R2 se selecciona independientemente de -H y -(C1-C4) alquilo;
cada R3 se selecciona independientemente de -H y -(C1-C4) alquilo
R4 se selecciona de -H, -(C1-C6) alquilo, =O, -OH, -O(C1-C6) alquilo, halógeno y -CN; en donde uno de los grupos R3 puede opcionalmente conectarse estructuralmente a uno de los grupos R2 para formar un puente alquileno para producir un anillo bicíclico; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R1 para formar un anillo heterociclilo de 5 a 7 miembros fusionado a la cara 1-2 del anillo de piperidina; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 a 7 miembros fusionado a la cara 2-3 del anillo de piperidina;
........— indica que el enlace designado es un simple enlace carbono-carbono o un doble enlace carbono-carbono; X se selecciona de -O-, -S-, -SO-, -SO2-, -NH- y -NR9-;
W1, W2 y W3 se seleccionan independientemente de N, CH y C-R10; siempre que W2 y W3 no sean N;
R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2n)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a, -C(=O)OR7a, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, heteroarilo bicíclico de 8 a 10 miembros y heteroarilo bicíclico sustituido de 8 a 10 miembros;
n es un número entero seleccionado de 1,2, 3 y 4;
R6 se selecciona de heteroarilo de 6 miembros, heteroarilo sustituido de 6 miembros, heteroarilo bicíclico de 9 a 10 miembros, y heteroarilo bicíclico sustituido de 9 a 10 miembros;
R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, -(C1-C6) heteroalquilo, arilo de 6 miembros, heteroarilo de 5 a 6 miembros y heterociclilo de 5 a 6 miembros;
R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;
R7a se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo, -C(=O)R8, y -(C1-C6) heteroalquilo sustituido; R8a se selecciona de -H y -(C1-C6) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros;
R9 se selecciona de -(C1-C7) hidrocarbilo, en donde R9 puede opcionalmente conectarse estructuralmente a R4 para formar un anillo heterociclilo de 5 a 7 miembros;
cada R10 se selecciona independientemente de -(C1-C7) hidrocarbilo, (C1-C7) hidrocarbilo sustituido, halógeno, -C(=O)(C1-C7) hidrocarbilo, -C(=O)NH2, -C(=O)NH(C1-C7) hidrocarbilo, -C(=O)N(C1-C7)hidrocarbilo)2, -OH, -O(C1-C7) hidrocarbilo, -O(C1-C7) hidrocarbilo sustituido, -(C3-C6) heterociclilo, -(C3-C6) heterociclilo sustituido, -CN, -NH2, -NH(C1-C6)alquilo, -N(C1-C6 alquilo)2, -NH(CH2)m-R11, -N(C1-C6 alquilo)(CH2)m-R11, -O-(CH2)m-R11, y -(C1-C6) heteroalquilo;
m es un número entero seleccionado independientemente de 1, 2, 3 y 4; y
R11 se selecciona de -O(C1-C6) alquilo, -N(C1-C6 alquilo)2, -(C3-C6)heterociclilo y -(C3-C6) heterociclilo sustituido.
De acuerdo con algunas modalidades, A es -C(=O)-.
De acuerdo con algunas modalidades, R1 se selecciona de -H, -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -OR7, -N(OR8)R7 y -C(=O)-(C1-C6) alquilo.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -SR7, -Nr 7R8, -N(OR8)R7, -N(Sr 8)R7 y -C(=O)-(C1-C6) alquilo.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C10) hidrocarbilo, (C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -N(OR8)R7 y C(=O)-(C1-C6) alquilo.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C3-C6) cicloalquilo, -(C3-C6)cicloalquilo sustituido, -(C2-C6) alquenilo, -(C2-C6)alquenilo sustituido, bencilo, bencilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -SR7, -NR7R8 y -C(=O)-(C1-C6) alquilo.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C3-C6) cicloalquilo, -(C3-C6) cicloalquilo sustituido, -(C2-C6) alquenilo, -(C2-C6) alquenilo sustituido, bencilo, bencilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8 y -C(=O)-(C1-C6) alquilo.
De acuerdo con algunas modalidades, a es 1 y b es 0. De acuerdo con algunas modalidades, a es 0 y b es 1. De acuerdo con algunas modalidades, a y b son ambos 1.
De acuerdo con algunas modalidades, R2 es -H.
De acuerdo con algunas modalidades, R3 es -H.
De acuerdo con algunas modalidades, R4 se selecciona de -H, -(C1-C6) alquilo y halógeno.
De acuerdo con algunas modalidades, uno de los grupos R3 está conectado estructuralmente a uno de los grupos R2 para formar un puente alquileno -C H 2-CH2- para producir un anillo bicíclico; por ejemplo:
De acuerdo con algunas modalidades, uno de los grupos R3 puede conectarse estructuralmente al grupo R1 para formar un heterociclo de 5 o 6 miembros, por ejemplo, un anillo de lactama o imidazol, fusionado a la cara 1-2 del anillo de piperidina; por ejemplo:
en donde el resto R1a representa el residuo del sustituyente R1 enlazado covalentemente al átomo de carbono que es alfa del grupo carbonilo de resto A, por ejemplo, -H, -(C1-C9) hidrocarbilo, o -(C1-C9) hidrocarbilo sustituido. Ejemplos de sistemas de anillo que pueden formarse conectando estructuralmente los grupos R1 y R3 incluyen anillos de indolizin-3-ona, quinolizin-4-ona, octahidro-1H-pirido[1,2-c]pirimidina y octahidroimidazo[1,5-a]piridina.
De acuerdo con algunas modalidades, uno de los grupos R3 puede conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 o 6 miembros unido a la cara 2-3 del anillo de piperidina; por ejemplo:
De acuerdo con algunas modalidades,......— es un simple enlace carbono-carbono.
De acuerdo con algunas modalidades, X es -O-.
De acuerdo con algunas modalidades, W1, W2 y W3 se seleccionan independientemente de CH y C-R10. De acuerdo con algunas modalidades, W1, W2 y W3 son CH.
De acuerdo con algunas modalidades, R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a, -C(=O)OR7a, heteroarilo de 5 a 6 miembros y heteroarilo sustituido de 5 a 6 miembros. De acuerdo con algunas modalidades, R5 se selecciona de -H, -C1-C6 alquilo y halógeno. De acuerdo con algunas modalidades, R5 es -H.
De acuerdo con algunas modalidades, R6 se selecciona de un heteroarilo bicíclico de 9 a 10 miembros, y un heteroarilo bicíclico sustituido de 9 a 10 miembros De acuerdo con algunas modalidades, R6 se selecciona de:
en donde, cuando R6 es (i), Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan independientemente de N y C-R12, siempre que 1,2 o 3 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12; cuando R6 es (ii), Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sean N, y el resto de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sea C-R12; cuando R6 es (iii), Q8 se selecciona de O, S y N-R12n, Q9, Q10 y Q11 se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;
cuando R6 es (iv), Q8a se selecciona de O, S y N-R12n, Q9a, Q10a y Q11a se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;
cuando R6 es (v), Q12, Q13 y Q14 se seleccionan independientemente de N y C-R12; y
cuando R6 es (vi), Q12a, Q13a y Q14a se seleccionan independientemente de N y C-R12;
cuando R6 es (vii), Q15 se selecciona de N-R12n y C-R12 y Q16 se selecciona de N y C-R12;
siempre que Q15 y Q16 no sean C-R12;
y en donde cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, -(C1-C3) haloalquilo, -O(C1-C3) haloalquilo, heterociclilo de 5 a 6 miembros, -OH, - O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -O(CH2)r-NH(C1-C6 alquilo)2, -NH2, Cn , -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo y -C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado independientemente de 1, 2, 3 y 4; y
cada R12n se selecciona independientemente de -H, -(C1-C7) hidrocarbilo y -(C1-C7) hidrocarbilo sustituido.
Se entenderá que los átomos del anillo de carbono del anillo que no son cabeza de puente en (i), (ii), (iii), (iv), (v), (vi) y (vii) anteriores (es decir, los átomos del anillo que no son cabeza de puente que no se designan como Q) pueden estar opcionalmente sustituidos. De acuerdo con algunas modalidades, ninguno de estos átomos del anillo de carbono del anillo está sustituido. De acuerdo con algunas modalidades, uno o dos de estos átomos de carbono del anillo están sustituidos. De acuerdo con algunas modalidades, uno o dos de estos átomos de carbono del anillo están sustituidos con un sustituyente seleccionado entre -OH, -(C1-C3) alquilo, -O(C1-C3) alquilo y halógeno. De acuerdo con algunas modalidades, uno de estos átomos de anillo de carbono del anillo está sustituido con un sustituyente seleccionado de -OH, -CH3, -OCH3, -F y -Cl.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo y -C(=O)N(C1-C6 alquilo)2.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -CF3, -OCF3, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1 -ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1 -ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2,-NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1 -ilo y piperidin-1-ilo.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1 -ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo),-O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1 -ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo.
De acuerdo con algunas modalidades, cada R12n se selecciona independientemente de -H, bencilo y -(C1-C6) alquilo. De acuerdo con algunas modalidades, R6 es:
en donde 1 o 2 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 son N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), uno de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q2 es N y el resto de Q1, Q3, Q4, Q5, Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q6 es N y Q1, Q2, Q3, Q5, Q5 y Q7 son C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q6 es N, Q2, Q3, Q5, Q5 y Q7 son CH, y Q1 es C-R12, en donde -R12 es distinto de -H.
De acuerdo con algunas modalidades, R6 se selecciona de heteroarilo bicíclico de 9 a 10 miembros y heteroarilo bicíclico sustituido de 9 a 10 miembros; siempre que, cuando R6 sea un heteroarilo bicíclico de 9 miembros o un heteroarilo bicíclico sustituido de 9 miembros, el punto de unión de R6 al anillo aromático que contiene W1, W2 y W3 está en una porción de anillo de 6 miembros del heteroarilo bicíclico de 9 miembros o el heteroarilo bicíclico sustituido de 9 miembros.
De acuerdo con algunas modalidades, R6 es:
en donde uno de Q2 y Q6 es N, y el otro de Q2 y Q6 es C-R12, y q es un número entero seleccionado de 0, 1,2 y 3. De acuerdo con algunas modalidades de i2, Q2 es N y Q6 es C-R12. De acuerdo con algunas modalidades, Q6 es N y Q2 es C-R12. De acuerdo con algunas modalidades, q se selecciona de 0, 1 y 2. De acuerdo con algunas modalidades de i2, q es 0 o 1. Se entenderá que un valor de q de 0 es el equivalente a designar todos los R12 que se unen al heteroarilo bicíclico i2 en un lugar distinto de Q2 y Q6 como -H.
De acuerdo con algunas modalidades de i2, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1 -ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-il),
O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo. De acuerdo con algunas modalidades de i2, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3 y -OCH2CH3.
De acuerdo con algunas modalidades de i2, cada R12n se selecciona independientemente de -H, bencilo y -C1-C6 alquilo.
De acuerdo con algunas modalidades, R6 es:
en donde uno o dos de Q2, Q4 y Q6 es N, y el resto de Q2, Q4 y Q6 es C-R12, y q es un número entero seleccionado de 0, 1, 2 y 3.
De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo,-O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6 alquilo) y -C(=O)N(C1-C6 alquilo))2; en donde r es un número entero seleccionado de 1, 2, 3 y 4; o una sal del mismo.
De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1 -ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1 -ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo. De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3 y -OCH2CH3.
De acuerdo con algunas modalidades de i3, q es 0, 1 o 2. De acuerdo con algunas modalidades, q es 0 o 1. Se entenderá que un valor de q de 0 es el equivalente a designar todos los R12 que están unidos al resto heteroarilo bicíclico en un lugar distinto de Q2, Q4 o Q6 como -H.
De acuerdo con algunas modalidades de i3, Q2 es N y Q4 y Q6 son C-R12. De acuerdo con algunas modalidades de i3, Q6 es N y Q2 y Q4 son C-R12. De acuerdo con algunas modalidades de i3, Q4 es N y Q2 y Q6 son C-R12. De acuerdo con algunas modalidades de i3, Q2 es C-R12, y Q4 y Q6 son N. De acuerdo con algunas modalidades de i3, Q6 es C-R12 y Q2 y Q4 son N. De acuerdo con algunas modalidades de i3, Q4 es C-R12, y Q2 y Q6 son N.
De acuerdo con algunas modalidades, R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo.
De acuerdo con algunas modalidades, R7 se selecciona de -H, -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C3-C6) cicloalquilo, -(C3-C6) cicloalquilo sustituido, -(C2-C6) alquenilo, -(C2-C6) alquenilo sustituido, bencilo, bencilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo. De acuerdo con algunas modalidades, R7 se selecciona de -H y -(C1-C6) alquilo.
De acuerdo con algunas modalidades, R7a se selecciona de -H, -(C1-C6) alquilo, -(C1-C6)alquilo sustituido, -(C3-C6) cicloalquilo, -(C3-C6) cicloalquilo sustituido, -(C2-C6) alquenilo, -(C2-C6)alquenilo sustituido, bencilo, bencilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo. De acuerdo con algunas modalidades, R7a se selecciona de -H y -(C1-C6) alquilo.
De acuerdo con algunas modalidades, R8 se selecciona de -H, y -(C1-C6) alquilo. De acuerdo con algunas modalidades, R8 se selecciona de -H, -CH3 y -CH2CH3.
De acuerdo con algunas modalidades, R8a se selecciona de -H, y -(C1-C6) alquilo. De acuerdo con algunas modalidades, R8a se selecciona de -H, -CH3 y -CH2CH3.
Otro aspecto de esta solicitud está dirigido a compuestos de Fórmula II:
y sales del mismo, por ejemplo, sales farmacéuticamente aceptables del mismo, en donde:
A se selecciona de -C(=O)- y -SO2-;
R1 se selecciona de -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -N(OR8)R7, -N(SR8)R7, -SR7, -C(=O)-(C1-C6) alquilo, y -(C1-C6) heteroalquilo;
a y b se seleccionan independientemente de 0 y 1;
cada R2 se selecciona independientemente de -H y -(C1-C4) alquilo;
cada R3 se selecciona independientemente de -H y -(C1-C4) alquilo
R4 se selecciona de -H, -(C1-C6) alquilo, =O, -OH, -O(C1-C6) alquilo, halógeno y -CN; en donde uno de los grupos R3 puede opcionalmente conectarse estructuralmente a uno de los grupos R2 para formar un puente alquileno para producir un anillo bicíclico; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R1 para formar un anillo heterociclilo de 5 a 7 miembros fusionado a la cara 1-2 del anillo de piperidina; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un 5to anillo carbocíclico o heterocíclico de 7 miembros fusionado a la cara 2-3 del anillo de piperidina;
X se selecciona de -O-, -S-, -SO-, -SO2-, -NH- y -NR9-;
W1, W2 y W3 se seleccionan independientemente de N, CH y C-R10; siempre que W2 y W 3 no sean N;
R5 se selecciona de -H, (C1-C7) hidrocarbilo, (C3-C6) heterociclilo; halógeno, (C1-C3) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a, y -C(=O)OR7a, heteroarilo de 5 a 6 miembros y heteroarilo sustituido de 5 a 6 miembros;
n es un número entero seleccionado independientemente de 1, 2, 3 y 4;
R6 se selecciona de:
en donde, cuando R6 es (i), Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan independientemente de N y C-R12, siempre que 1,2 o 3 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12; cuando R6 es (ii), Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sean N, y el resto de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sea C-R12; cuando R6 es (iii), Q8 se selecciona de O, S y N-R12n, Q9, Q10 y Q11 se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;
cuando R6 es (iv), Q8a se selecciona de O, S y N-R12n, Q9a, Q10a y Q11a se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;
cuando R6 es (v), Q12, Q13 y Q14 se seleccionan independientemente de N y C-R12; y
cuando R6 es (vi), Q12a, Q13a y Q14a se seleccionan independientemente de N y C-R12;
cuando R6 es (vii), Q15 se selecciona de N-R12n y C-R12 y Q16 se selecciona de N y C-R12; siempre que uno de Q15 y Q16 no sea C-R12;
R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, -(C1-C6) heteroalquilo, arilo de 6 miembros, heteroarilo de 5 a 6 miembros y heterociclilo de 5 a 6 miembros;
R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;
R7a se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo, -C(=O)R8, y -(C1-C6) heteroalquilo sustituido; R8a se selecciona de -H y -(C1-C6) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros;
R9 se selecciona de -(C1-C7) hidrocarbilo, en donde R9 puede opcionalmente conectarse estructuralmente a R4 para formar un anillo heterociclilo de 5 a 7 miembros;
R10 se selecciona de -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, halógeno, -C(=O)-(C1-C7) hidrocarbilo, -C(=O)NH2, -C(=O)NH-(C1-C7) hidrocarbilo, -C(=O)N(C1-C7) hidrocarbilo)2, -OH, -O(C1-C7) hidrocarbilo, -O(C1-C7) hidrocarbilo sustituido, -(C3-C6) heterociclilo, -(C3-C6) heterociclilo sustituido -CN, -NH2, -NH(C1-C6) alquilo,-N(C1-C6 alquilo)2, -NH(CH2)m-R11, -N(C1-C6 alquilo)(CH2)m-R11, -O-(CH2)m-R11, y -(C1-C6) heteroalquilo;
m es un número entero seleccionado independientemente de 1, 2, 3 y 4;
R11 se selecciona de -O(C1-C6)alquilo, -N((C1-C6)alquilo)2 -(C3-C6)heterociclilo y -(C3-C6) heterociclilo sustituido;
cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, -(C1-C3) haloalquilo, -O(C1-C3) haloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -O(CH2)r-N(C1-C6 alquilo)2, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado independientemente de 1, 2, 3 y 4; y cada R12n se selecciona independientemente de -H, -(C1-C7) hidrocarbilo y -(C1-C7) hidrocarbilo sustituido.
De acuerdo con algunas modalidades, A es -C(=O)-. De acuerdo con otras modalidades, A es -SO2-.
De acuerdo con algunas modalidades, a y b son ambos 0, por lo que el anillo que contiene estos elementos es un anillo de 4 miembros. De acuerdo con otras modalidades, a es 0 y b es 1, o a es 1 y b es 0, lo que hace que el anillo que contiene estos elementos sea un anillo de 5 miembros. De acuerdo con algunas modalidades, a y b son ambos 1, lo que hace que el anillo que contiene estos elementos sea un anillo de 6 miembros.
De acuerdo con algunas modalidades, cada R2 es -H o -CH3. De acuerdo con otras modalidades, cada R2 es -H.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo,-O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2,-C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -N(OR8)R7, y -C(=O)-(C1-C6) alquilo y -(C1-C6) heteroalquilo.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C1-C6) cicloalquilo, -(C1-C6) cicloalquilo sustituido, -C(=O)-(C1-C6) alquilo, -S(C1-C6) alquilo, -S(C1-C6) alquilo sustituido, heterociclilo de 5 a 6 miembros, heterociclilo sustituido de 5 a 6 miembros, NH2, -NH(C1-C6) alquilo, -N((C1-C6) alquilo)2, -NH-O(C1-C6) alquilo,-(CH2)nO(C1-C6) alquilo, -(CH2)nOH, -(CH2)nSO2(C1-C6)alquilo, -(C6-C10) arilo, -(C6-C10) arilo sustituido y -(CH2)n-CN.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C1-C6) cicloalquilo, -(C1-C6) cicloalquilo sustituido, -C(=O)-(C1-C6) alquilo, heterociclilo de 5 a 6 miembros, heterociclilo sustituido de 5 a 6 miembros, NH2, -NH(C1-C6) alquilo, -N((C1-C6)alquilo)2, -NH-O(C1-C6) alquilo, -(CH2)nO(C1-C6) alquilo, -(CH2)nOH, -(CH2)nSO2(C1-C6)alquilo, -(C6-C10) arilo, -(C6-C10) arilo sustituido y -(CH2)n-CN.
De acuerdo con otras modalidades, R1 se selecciona de -CH3, -CH2CH3, -(CH2)2CH3, -(CH2)3CH3, -(CH2)4CH3, -CH(CH3)3, -C(CH3)3, ciclopropilo, ciclopropilo sustituido, ciclobutilo, ciclobutilo sustituido, ciclopentilo, -C(=O)CH3, -C(=O)CH2CH3, -NH-OH, -NH-OCH3, -NH-OCH2CH3, -N(CH3)-OCH3, -NH2, -NHCH3, -NH-CH2CH3, -NH(CH2)2-CH3, -NH(CH2)3-CH3, -NH(CH2)4-CH3, -NH(CH2)5-CH3, -N(CH3)2, -N(Et)2, -NH-CH(CH3)2, -NH-OCH2CH3, -NHSCH3, -NHSCH2CH3, -SCH3, -SCH2CH3, -SCH(CH3)2, tetrahidrofuranilo, tetrahidrofuranilo sustituido, furanilo, furanilo sustituido, dioxolanilo, dioxolanilo sustituido, tetrahidropirrolilo, piperidinilo, morfolinilo, tetrahidropiranilo, tiofenilo, tetrahidrotiofenilo, sulfolanilo, tetrahidroisoxazolidinilo, oxazolilo, isoxazolilo, tiazolilo, imidazolilo, fenoxazolilo, tiazolilo, imidazolilo sustituido, piperidinilo, piperidinilo sustituido, -CH2-OCH3, -(CH2)2-OCH3, y -(CH2)3-OCH3.
De acuerdo con otras modalidades, R1 se selecciona de -CH3, -CH2CH3, -(CH2)2CH3, -(CH2)3CH3, -(CH2)4CH3, -CH(CH3)3, -C(CH3)3, ciclopropilo, ciclopropilo sustituido, ciclobutilo, ciclobutilo sustituido, ciclopentilo, -C(=O)CH3, -C(=O)CH2CH3, -NH-OH, -NH-OCH3, -NH-OCH2CH3, -N(CH3)-OCH3, -NH2, -NHCH3, -NH-CH2CH3, -NH(CH2)2-CH3, -NH(CH2)3-CH3, -NH(CH2)4-CH3, -NH(CH2)5-CH3, -N(CH3)2, -N(Et)2, -NH-CH(CH3)2, -NH-OCH2CH3, tetrahidrofuranilo, tetrahidrofuranilo sustituido, furanilo, furanilo sustituido, dioxolanilo, dioxolanilo sustituido, tetrahidropirrolilo, piperidinilo, morfolinilo, tetrahidropiranilo, tiofenilo, tetrahidrotiofenilo, sulfolanilo, tetrahidroisoxazolidinilo, oxazolilo, isoxazolilo, tiazolilo, isotiazolilo, imidazol, piridilo, piridilo sustituido, quinolilo, quinolilo sustituido, fenilo, fenilo sustituido, -CH2-OCH3,-(CH2)2-OCH3, y -(CH2)3-OCH3.
De acuerdo con algunas modalidades, cuando R1 es ciclopropilo sustituido, el anillo de ciclopropilo está sustituido con 1 o dos sustituyentes seleccionados entre -OH, -CH2, -OH, -C(=O)NH2, -NH2, -CH3, -CN y -CF3.
De acuerdo con algunas modalidades, cuando R1 es tetrahidrofuranilo, es tetrahidrofuran-2-ilo o tetrahidrofuran-3-ilo. De acuerdo con algunas modalidades, cuando R1 es tetrahidrofuranilo sustituido es 2-metiltetrahidrofuran-2-ilo, 5-metiltetrahidrofuran-2-ilo, 2,5-dimetiltetrahidrofuran-2-ilo o tetrahidrofuran-4-ona-2-ilo, o 4,4-difluorotetrahidrofuran-2-ilo.
De acuerdo con algunas modalidades, cuando R1 es furanilo, es 2-furanilo o 3-furanilo.
De acuerdo con algunas modalidades, cuando R1 es furanilo sustituido, es 2-metilfuran-2-ilo, 5-metilfuran-2-ilo, o 2,5dimetilfu ran-2-ilo.
De acuerdo con algunas modalidades, cuando R1 es dioxolanilo, es 1,3-dioxolan-2-ilo. De acuerdo con algunas modalidades, cuando R1 es dioxolanilo sustituido es 2-metil-1,3-dioxolan-2-ilo.
De acuerdo con algunas modalidades, cuando R1 es tetrahidroisoxazolidina, es tetra-hidroisoxazolidin-2-ilo. De acuerdo con algunas modalidades, cuando R1 es tetrahidropirrolilo, es tetrahidropirrol-1 -ilo. De acuerdo con algunas modalidades, cuando R1 es morfolinilo, es morfolin-1-ilo. De acuerdo con algunas modalidades, cuando R1 es piperidinilo, es piperidin-1-ilo. De acuerdo con algunas modalidades, cuando R1 es furanilo, es 2-furanilo o 3-furanilo. De acuerdo con algunas modalidades, cuando R1 es tiofenilo, es 2-tiofenilo o 2-tiofenilo. De acuerdo con algunas modalidades, cuando R1 es tetrahidrotiofenilo, es 2-tetrahidrotiofenilo o 2-tetrahidrotiofenilo. De acuerdo con algunas modalidades, cuando R1 es sulfolanilo, es sulfolano-2-ilo o sulfolano-3-ilo. De acuerdo con algunas modalidades, cuando R1 es oxazolilo, es oxazol-1-ilo, oxazol-2-ona-1-il oxazol-2-ilo u oxazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es isoxazolilo, es isoxazol-1-ilo, isoxazol-3-ilo o isoxazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es imidazolilo, es imidazol-2-ilo o imidazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es tiazolilo, es tiazol-2-ilo o tiazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es isotiazolilo, es isotiazol-3-ilo o isotiazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es piridilo, que es 2-piridilo, 3-piridilo o 4-piridilo. De acuerdo con algunas modalidades, cuando R1 es quinolilo sustituido, es quinolin-1-ilo, quinolin-2-ilo o quinolin-3-ilo. De acuerdo con algunas modalidades, cuando R1 es fenilo sustituido, es 2-metilfenilo, 3-metilfenilo, 4-metilfenilo, o 2,5-dimetilfenilo. De acuerdo con algunas modalidades, R1 se selecciona de entre los restos representados en la Tabla 1 y la Tabla 1a a continuación.
Tabla 1: Una selección de algunos restos R1 adecuados.
Continuación
Tabla 1a. Una selección de algunos restos R1 adecuados adicionales.
De acuerdo con algunas modalidades, cada R3 es -H o -CH3. De acuerdo con otras modalidades, cada R3 es -H. De acuerdo con algunas modalidades, R4 se selecciona de -H, -(C1-C6) alquilo, -OH, -O(C1-C6) alquilo, -CN y halógeno. De acuerdo con otras modalidades, R4 se selecciona de -H, -CH3, -OH, -OCH3, -F, -Cl, y -CN. De acuerdo con algunas modalidades, R4 es halógeno o -H. De acuerdo con algunas modalidades, R4 es -F o -H. De acuerdo con algunas modalidades, R4 es-H.
De acuerdo con algunas modalidades, uno de los grupos R3 puede opcionalmente conectarse estructuralmente a uno de los grupos R2 para formar un puente C2-C3 alquileno para producir un anillo bicíclico. De acuerdo con algunas modalidades, uno de los grupos R3 está conectado estructuralmente a uno de los grupos R2 para formar un puente -CH2-CH2 para producir un anillo bicíclico; por ejemplo:
De acuerdo con algunas modalidades, uno de los grupos R3, puede opcionalmente conectarse estructuralmente al grupo R1 para formar un anillo heterociclilo de 5 a 7 miembros fusionado a la cara 1-2 del anillo de piperidina. De acuerdo con algunas modalidades, uno de los grupos R3 está conectado estructuralmente al grupo R1 para formar un heterociclo de 5 o 6 miembros, por ejemplo, un anillo de lactama o imidazol fusionado a la cara 1-2 del anillo de piperidina; por ejemplo:
en donde el resto R1a representa el residuo del sustituyente R1 enlazado covalentemente al átomo de carbono que es alfa del grupo carbonilo de resto A, por ejemplo, -H, -(C1-C9) hidrocarbilo, o -(C1-C9) hidrocarbilo sustituido. Ejemplos de sistemas de anillo que pueden formarse conectando estructuralmente los grupos R1 y R3 incluyen anillos de indolizin-3-ona, quinolizin-4-ona, octahidro-1H-pirido[1,2-c]pirimidina y octahidroimidazo[1,5-a]piridina.
De acuerdo con algunas modalidades, uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 a 7 miembros fusionado a la cara 2-3 del anillo de piperidina. De acuerdo con algunas modalidades, uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico de 5 miembros, un anillo carbocíclico de 6 miembros o un anillo carbocíclico de 7 miembros fusionado a la cara 2-3 del anillo de piperidina. De acuerdo con algunas modalidades, uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo heterocíclico de 5 miembros, un anillo heterocíclico de 6 miembros o un anillo heterocíclico de 7 miembros fusionado a la cara 2-3 del anillo de piperidina. De acuerdo con algunas modalidades, uno de los grupos R3 está conectado estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 miembros fusionado a la cara 2-3 del anillo de piperidina; por ejemplo:
De acuerdo con algunas modalidades, X se selecciona de -O-, -S-, -SO- y -SO2-. De acuerdo con algunas modalidades, X se selecciona de -O-, -S- y -SO2-. De acuerdo con algunas modalidades, X se selecciona de -O- y -S-. De acuerdo con algunas modalidades, X es -O-. De acuerdo con algunas modalidades, X es -S-. De acuerdo con algunas modalidades, X es -SO-. De acuerdo con algunas modalidades, X es -SO2-. De acuerdo con algunas modalidades, X es -NR9-. De acuerdo con algunas modalidades, X es -NH-.
De acuerdo con algunas modalidades, R9 es -(C1-C6) alquilo. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo heterociclilo de 5 a 7 miembros. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo heterociclilo de 5 miembros. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo heterociclilo de 6 miembros. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo de heterociclilo de 7 miembros.
De acuerdo con algunas modalidades, W1, W2 y W3 se seleccionan independientemente de CH y C-R10. De acuerdo con algunas modalidades, W1, W2 y W3 son todos CH. De acuerdo con algunas modalidades, uno de W1 y W2 es N, y W3 y el otro de W1 y W2 es CH o C-R10. De acuerdo con algunas modalidades, W1 es N y W2 y W3 son CH o C-R10. De acuerdo con algunas modalidades, W1 es N y W2 y W3 son CH. De acuerdo con algunas modalidades, W1 y W2 son N y W3 es CH o C-R10. De acuerdo con algunas modalidades, W1 y W2 son N y W3 es CH. De acuerdo con algunas modalidades, W1 y W2 son CH o C-R10, y W3 es N. De acuerdo con algunas modalidades, W1 y W2 son CH y W3 es N. De acuerdo con algunas modalidades, cada R10 se selecciona independientemente de -F, -Cl, -CN, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, -C(=O)-(C1-C6) alquilo, -C(=O)-(C3-C6) cicloalquilo, C(=O)NH2, -C(=O)NH-C1-C6 alquilo, -C(=O)N(C1-C6 alquilo)2, -O(C1-C6)alquilo, -(C1-C6)alquilo, -OH, -(C5-C6) heterociclilo, -(C5-C6) heterociclilo sustituido, -O-(CH2)m-O(C1-C6)alquilo, -O(CH2)n-(Cs-C6) heterociclilo, O-(CH2)m-(Cs-C6) heterociclilo sustituido, -NH2, -N((C1-C6)alquilo)2, -NH-(CH2)m-O-(C1-C6)alquilo, y -NH-(CH2)m- N((C1-C6)alquilo)2.
De acuerdo con algunas modalidades, cada R10 se selecciona independientemente de -F, -Cl, -CN, -(C1-C6)alquilo, -(C3-C6)cicloalquilo, -OH, -O(C1-C6)alquilo, NH2, -NH(C1-C6)alquilo, -N((C1-C6)alquilo)2, -C(=O)(C1-C6)alquilo, -C(=O)-(C3-C6) cicloalquilo, -C(=O)Nh2, -CF3, -O(CH2)m-morfolin-1-ilo, -O(CH2)m-pirrolidin-1-ilo, -O(CH2)m-4-metilpiperidin-1-ilo, -O(CH2)m-OCH3, morfolin-1 -ilo, 4-metilpiperidin-1-ilo, -NH(CH2)m-OCH3, y -NH(CH2)m-N(CH3)2,
De acuerdo con algunas modalidades, cada R10 se selecciona independientemente de -F, -Cl, -CN, -CH3, -CH2CH3, -OCH3 y -OCH2CH3.
De acuerdo con algunas modalidades, R5 se selecciona de -H, -(C1-C6) alquilo, -(C3-C6) cicloalquilo y halógeno. De acuerdo con algunas modalidades, R5 es -H.
De acuerdo con algunas modalidades, R6 puede seleccionarse de los sistemas de anillos bicíclicos mostrados en la Tabla 1b, en donde R12n es como se define en la presente, y los átomos de carbono que no son cabeza de puente en los sistemas de anillos bicíclicos pueden estar opcionalmente sustituidos. De acuerdo con algunas modalidades, 0, 1, 2 o 3 de los átomos de carbono que no son cabeza de puente en los sistemas de anillo mostrados en la Tabla 1b pueden estar sustituidos por sustituyentes R12 como se define en la presente R12.
Tabla 1b: Una selección de algunos restos R6 adecuados
Continuación
)
De acuerdo con algunas modalidades, R6 es:
en donde 1 o 2 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 son N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), uno de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es N, y el resto de Q1, Q2, Q3, Q4, Q5,
Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q2 es N y el resto de Q1, Q3, Q4, Q5, Q6 y
Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q6 es N y Q1, Q2, Q3, Q5, Q5 y Q7 son acuerdo con algunas modalidades, cuando R6 es (i), Q6 es N, Q2, Q3, Q5, Q5 y Q7 son CH, y Q1 es C-R12, en donde -R12 es distinto de -H.
Se entenderá que, cuando R6 es (iii), (iv), (v), (vi) o (vii), los no cabeza de puente de átomos de anillo de carbono del anillo (es decir, átomos de anillo no cabeza de puente que no se designan como Q) pueden estar opcionalmente sustituidos. De acuerdo con algunas modalidades, ninguno de estos átomos del anillo de carbono del anillo está sustituido. De acuerdo con algunas modalidades, uno o dos de estos átomos del anillo de carbono del anillo pueden estar sustituidos con un sustituyente seleccionado de -OH, -(C1-C3) alquilo, -O(C1-C3) alquilo y halógeno. De acuerdo con algunas modalidades, uno de estos átomos de anillo de carbono del anillo está sustituido con un sustituyente seleccionado de -OH, -CH3, -OCH3, -F y -Cl.
De acuerdo con algunas modalidades, R6 es:
en donde uno de Q2 y Q6 es N, y el otro de Q2 y Q6 es C-R12, y q es un número entero seleccionado de 0, 1, 2 y 3. De acuerdo con algunas modalidades de i2, Q2 es N y Q6 es C-R12. De acuerdo con algunas modalidades, Q6 es N y Q2 es C-R12. De acuerdo con algunas modalidades, q se selecciona de 0, 1 y 2. De acuerdo con algunas modalidades de i2, q es 0 o 1. Se entenderá que un valor de q de 0 es el equivalente a designar todos los R12 que se unen al heteroarilo bicíclico i2 en un lugar distinto de Q2 y Q6 como -H.
De acuerdo con algunas modalidades de i2, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo. De acuerdo con algunas modalidades de i2, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3 y -OCH(CH3)2.
De acuerdo con algunas modalidades de i2, cada R12n se selecciona independientemente de -H, bencilo y -C1-C6 alquilo.
De acuerdo con algunas modalidades, R6 es:
en donde uno o dos de Q2, Q4 y Q6 es N, y el resto de Q2, Q4 y Q6 es C-R12, y q es un número entero seleccionado de 0, 1, 2 y 3.
De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2,-C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado de 1, 2, 3 y 4; o una sal del mismo.
De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo. De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3 y -OCH2CH3.
De acuerdo con algunas modalidades de i3, q es 0, 1 o 2. De acuerdo con algunas modalidades, q es 0 o 1. Se entenderá que un valor de q de 0 es el equivalente a designar todos los R12 que están unidos al resto heteroarilo bicíclico en un lugar distinto de Q2, Q4 o Q6 como -H.
De acuerdo con algunas modalidades de i3, Q2 es N y Q4 y Q6 son C-R12. De acuerdo con algunas modalidades de i3, Q6 es N y Q2 y Q4 son C-R12. De acuerdo con algunas modalidades de i3, Q4 es N, y Q2 y Q6 son C-R12. De acuerdo con algunas modalidades de i3, Q2 es C-R12, y Q4 y Q6 son N. De acuerdo con algunas modalidades de i3, Q6 es C-R12, y Q2 y Q4 son N. De acuerdo con algunas modalidades de i3, Q4 es C-R12, y Q2 y Q6 son N.
De acuerdo con algunas modalidades, R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H,-Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2,-O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo, piperidin-1-ilo, -CF3, -OCF3, ciclopropilo, -OH, -C(=O)NH2, -NH(CH2)2 pirrolidin-1-ilo, -NH(CH2)2N(CH3)2, -NH(CH2)2OCH3 y -CN.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H,-Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2,-O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo.
De acuerdo con algunas modalidades, R12 se selecciona de -F, -Cl, -CH3, y -OCH3.
De acuerdo con algunas modalidades, R12n se selecciona de -H, bencilo y -(C1-C6) alquilo.
Otro aspecto de esta solicitud está dirigido a compuestos de Fórmula III:
y sales del mismo, por ejemplo, sales farmacéuticamente aceptables del mismo, en donde:
R1 se selecciona de -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -N(OR8)R7, -N(SR8)R7, -S-R7 y -C(=O)-(C1-C6) alquilo y -(C1-C6) heteroalquilo;
X se selecciona de -O-, -S-, -SO-, -SO2- y -NR9-;
W1 es CH o C-R10;
R4 es halógeno o -H;
R5 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C3-C6) heterociclilo; halógeno, -(C1-C3) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a, -C(=O)OR7a, heteroarilo de 5 a 6 miembros y heteroarilo sustituido de 5 a 6 miembros;
n es un número entero seleccionado independientemente de 1, 2, 3 y 4;
Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12;
R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, -(C1-C6) heteroalquilo, arilo de 6 miembros, heteroarilo de 5 a 6 miembros y heterociclilo de 5 a 6 miembros;
R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;
R7a se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo; R8a se selecciona de -H y -(C1-C6) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros;
R9 se selecciona de -(C1-C6) alquilo, en donde R9 puede opcionalmente conectarse estructuralmente a R4 para formar un anillo heterociclilo de 5 a 7 miembros;
R10 se selecciona de -F, -Cl, -CN, -(C1-C6)alquilo, -(C3-C6)cicloalquilo, -OH, -O-(C1-C6)alquilo, NH2, -NH(C1-C6)alquilo, N((C1-C6) alquilo)2, -C(=O)(C1-C6)alquilo, -C(=o )-(C3-C6) cicloalquilo, -C(=o )n H2, -CF3, -O(CH2)mmorfolin-1-ilo, -O(CH2)m-pirrolidin-1-ilo, -O(CH2)m-4-metilpiperidin-1-ilo, -O(CH2)m-OCH3, morfolin-1-ilo, 4-metilpiperidin-1-ilo, -NH(CH2)m-OCH3, y -NH(CH2)m-N(CH3)2;
m es un número entero seleccionado independientemente de 1, 2, 3 y 4;
R11 se selecciona de -O(C1-C6)alquilo, -N((C1-C6)alquilo)2, -(C3-C6)heterociclilo y -(C3-C6) heterociclilo sustituido; y
cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, -(C1-C3) haloalquilo, -O(C1-C3) haloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)p-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -O(CH2)r-N(C1-C6 alquilo)2, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado independientemente de 1, 2, 3 y 4.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -N(OR8)R7, y -C(=O)-(C1-C6) alquilo y -(C1-C6) heteroalquilo.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C1-C6) cicloalquilo, -(C1-C6) cicloalquilo sustituido, -C(=O)-(C1-C6) alquilo, heterociclilo de 5 a 6 miembros, heterociclilo sustituido de 5 a 6 miembros, -NH2, -NH(C1-C6) alquilo,-N((C1-C6) alquilo)2, -NH-O(C1-C6) alquilo, -NH-S(C1-C6) alquilo, -S(C1-C6) alquilo, -(CH2)nO(C1-C6) alquilo, -(CH2)nOH, -(CH2)nSO2(C1-C6)alquilo, -(C6-C10) arilo, -(C6-C10) arilo sustituido, y -(CH2)n-CN.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C1-C6) cicloalquilo, -(C1-C6) cicloalquilo sustituido, -C(=O)-(C1-C6) alquilo, heterociclilo de 5 a 6 miembros, heterociclilo sustituido de 5 a 6 miembros, -NH2, -NH(C1-C6) alquilo, -N((C1-C6)alquilo)2, -NH-O(C1-C6)alquilo, -(CH2)nO(C1-C6) alquilo, -(CH2)nOH, -(CH2)nSO2(C1-C6)alquilo, -(C6-C10) arilo, -(C6-C10) arilo sustituido y -(CH2)n-CN.
De acuerdo con otras modalidades, R1 se selecciona de -CH3, -CH2CH3, -(CH2)2CH3, -(CH2)3CH3, -(CH2)4CH3, -CH(CH3)3, -C(CH3)3, ciclopropilo, ciclopropilo sustituido, ciclobutilo, ciclobutilo sustituido, ciclopentilo, -C(=O)CH3, -C(=O)CH2CH3, -NH-OH, -NH-OCH3, -NH-OCH2CH3, -N(CH3)-OCH3, -NH2, -NHCH3, -NH-CH2CH3, -NH(CH2)2-CH3, -NH(CH2)3-CH3, -NH(CH2)4-CH3, -NH(CH2)5-CH3, -N(CH3)2, -N(Et)2, -NH-CH(CH3)2, -NH-OCH2CH3, tetrahidrofuranilo, tetrahidrofuranilo sustituido, furanilo, furanilo sustituido, dioxolanilo, dioxolanilo sustituido, tetrahidropirrolilo, piperidinilo, morfolinilo, tetrahidropiranilo, tiofenilo, tetrahidrotiofenilo, sulfolanilo, tetrahidroisoxazolidinilo, oxazolilo, isoxazolilo, tiazolilo, isotiazolilo, imidazol, piridilo, piridilo sustituido, quinolilo, quinolilo sustituido, fenilo, fenilo sustituido, -CH2-OCH3,-(CH2)2-OCH3, y -(CH2)3-OCH3.
De acuerdo con otras modalidades, R1 se selecciona de -CH3, -CH2CH3, -(CH2)2CH3, -(CH2)3CH3, -(CH2)4CH3, -CH(CH3)3, -ciclopropilo, ciclopropilo sustituido, ciclobutilo, ciclobutilo sustituido, ciclopentilo, -C(=O)CH3, -C(=O)CH2CH3, -NH-OH, -NH-OCH3, -NH-OCH2CH3, -N(CH3)-OCH3, -NH2, -NHCH3, -NH-CH2CH3, -NH(CH2)2-CH3, -NH(CH2)3-CH3, -NH(CH2)4-CH3, -NH(CH2)5-CH3, -N(CH3)2, -N(Et)2, -NH-CH(CH3)2, -NH-OCH2CH3, -NH-SCH2CH3, -NH-SCH3, -SCH3, -SCH2CH3, -SCH(CH3)2, tetrahidrofuranilo, tetrahidrofuranilo sustituido, furanilo, furanilo sustituido, dioxolanilo, dioxolanilo sustituido, tetrahidropirrolilo, piperidinilo, morfolinilo, tetrahidropiranilo, tiofenilo, tetrahidrotiofenilo, sulfolanilo, tetrahidroisoxazolidinilo, oxazolilo, isoxazolilo, tiazolilo, isotiazolilo, imidazol, piridilo, piridilo sustituido, quinolilo, quinolilo sustituido, fenilo, fenilo sustituido, -CH2-OCH3, -(CH2)2-OCH3, and -(CH2)3-OCH3.
De acuerdo con algunas modalidades, cuando R1 es ciclopropilo sustituido, el anillo de ciclopropilo está sustituido con
1 o 2 sustituyentes seleccionados de -OH, -CH3, -OH, -C(=o )n H2, -NH2, -CH3, -CN y -CF3.
De acuerdo con algunas modalidades, cuando R1 es tetrahidrofuranilo, es tetrahidrofuran-2-ilo o tetrahidrofuran-3-ilo.
De acuerdo con algunas modalidades, cuando R1 es tetrahidrofuranilo sustituido, es 2-metiltetrahidrofuran-2-ilo, 5-metiltetrahidrofuran-2-ilo, 2,5-dimetiltetrahidrofuran-2-ilo o tetrahidrofuran-4-ona-2-ilo, 4,4-difluorotetrahidrofuran-2-ilo.
De acuerdo con algunas modalidades, cuando R1 es furanilo, es 2-furanilo o 3-furanilo.
De acuerdo con algunas modalidades, cuando R1 es furanilo sustituido es 2-metilfuran-2-ilo, 5-metilfuran-2-ilo, o 2,5-dimetilfuran-2-ilo.
De acuerdo con algunas modalidades, cuando R1 es dioxolanilo, es 1,3-dioxolan-2-ilo. De acuerdo con algunas modalidades, cuando R1 es dioxolanilo sustituido es 2-metil-1,3-dioxolan-2-ilo.
De acuerdo con algunas modalidades, cuando R1 es tetrahidroisoxazolidina, es tetrahidroisoxazolidin-2-ilo. De acuerdo con algunas modalidades, cuando R1 es tetrahidropirrolilo, es tetrahidropirrol-1-ilo. De acuerdo con algunas modalidades, cuando R1 es morfolinilo, es morfolin-1-ilo. De acuerdo con algunas modalidades, cuando R1 es piperidinilo, es piperidin-1-ilo. De acuerdo con algunas modalidades, cuando R1 es furanilo, es 2-furanilo o 3-furanilo.
De acuerdo con algunas modalidades, cuando R1 es tiofenilo, es 2-tiofenilo o 2-tiofenilo. De acuerdo con algunas modalidades, cuando R1 es tetrahidrotiofenilo, es 2-tetrahidrotiofenilo o 2-tetrahidrotiofenilo. De acuerdo con algunas modalidades, cuando R1 es sulfolanilo, es sulfolano-2-ilo o sulfolano-3-ilo. De acuerdo con algunas modalidades, cuando R1 es oxazolilo, es oxazol-1-ilo, oxazol-2-ona-1-ilo, oxazol-2-ilo u oxazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es isoxazolilo, es isoxazol-1-ilo, isoxazol-3-ilo o isoxazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es imidazolilo, es imidazol-2-ilo o imidazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es tiazolilo, es tiazol-2-ilo o tiazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es isotiazolilo, es isotiazol-3-ilo o isotiazol-5-ilo. De acuerdo con algunas modalidades, cuando R1 es piridilo, que es 2-piridilo, 3-piridilo
o 4-piridilo. De acuerdo con algunas modalidades, cuando R1 es quinolilo sustituido, es quinolin-1-ilo, quinolin-2-ilo o quinolin-3-ilo. De acuerdo con algunas modalidades, cuando R1 es fenilo sustituido, es 2-metilfenilo, 3-metilfenilo, 4-metilfenilo, o 2,5-dimetilfenilo. De acuerdo con algunas modalidades, R1 se selecciona de los restos representados en la Tabla 1 y la Tabla 1a (infra).
De acuerdo con algunas modalidades, X se selecciona de -O-, -S-, -SO-, y-SO2-. De acuerdo con algunas modalidades, X se selecciona de -O-, -S- y -SO2-. De acuerdo con algunas modalidades, X se selecciona de -O- y -S-. De acuerdo con algunas modalidades, X es -O-. De acuerdo con algunas modalidades, X es -S-. De acuerdo con algunas modalidades, X es -SO-. De acuerdo con algunas modalidades, X es -SO2-. De acuerdo con algunas modalidades, X es -NR9-.
De acuerdo con algunas modalidades, R9 es -(C1-C6) alquilo. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo heterociclilo de 5 a 7 miembros. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo heterociclilo de 5 miembros. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo heterociclilo de 6 miembros. De acuerdo con algunas modalidades, el grupo R9 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo de heterociclilo de 7 miembros.
De acuerdo con algunas modalidades, R4 es -F o -H. De acuerdo con algunas modalidades, R4 es -H.
De acuerdo con algunas modalidades, R5 se selecciona de -H, -C1-C6 alquilo, -C3-C6 alquilo y halógeno. De acuerdo con algunas modalidades, R5 es -H.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo,
-(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo,-O(CH2)p-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2,-C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2,-O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1 -ilo, piperidin-1-ilo, -CF3, -OCF3, ciclopropilo, -OH, -C(=O)NH2, -NH(CH2)2 pirrolidin-1-ilo, -NH(CH2)2N(CH3)2, -NH(CH2)2OCH3 y -CN.
De acuerdo con algunas modalidades, R6 es:
en donde 1 o 2 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 son N, y el resto de Q1, Q2, Q3, Q4, con algunas modalidades, uno de Q2, Q3, Q4, Q5, Q6 y Q7 es N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, Q2 es N, y el resto de Q1, Q3, Q4, Q5, Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, Q6 es N, y Q1, Q2, Q3, Q4, Q5 y Q7 son C-R12. De acuerdo con algunas modalidades, Q6 es N; Q2, Q3,
Q4, Q5 y Q7 son CH, y Q1 es C-R12, en donde -R12 es distinto de -H. De acuerdo con algunas modalidades, Q6 es N;
Q2, Q3, Q4, Q5 y Q7 son CH, y Q1 es C-R12, en donde cada -R12 se selecciona independientemente de halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a
6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r- O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2,-C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y-C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado independientemente de 1, 2, 3 y 4.
De acuerdo con algunas modalidades, R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo.
Otro aspecto de esta solicitud está dirigido a compuestos de Fórmula IV:
y sales del mismo, por ejemplo, sales farmacéuticamente aceptables del mismo, en donde:
R1 se selecciona de -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -N(OR8)R7, -N(SR8)R7, -SR7, -C(=O)-(C1-C6) alquilo, y -(C1-C6) heteroalquilo;
W1 es CH o C-R10;
R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C (= O HC1-C7) hidrocarbilo, -(C1-C6) heteroalquilo, arilo de 6 miembros, heteroarilo de 5 a 6 miembros y heterociclilo de 5 a 6 miembros;
R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;
R10 se selecciona de -F, -Cl, -CN, -(C1-C6)alquilo, -(C3-C6)cicloalquilo, -OH, -O(C1-C6)alquilo, NH2, -NH(C1-C6)alquilo, -N((C1-C6)alquilo)2, -C(=O)(C1-C6)alquilo, -C(=O)-(C3-C6) cicloalquilo,-C(=O)NH2, -CF3; y
cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C1-C3) haloalquilo, -O(C1-C3)haloalquilo, -(C3-C6)cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -O(CH2),-N(C1-C6 alquilo)2, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)rO(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2; en donde R12 puede estar en cualquier posición en el anillo de quinolina al que está unido, y en donde r es un número entero seleccionado independientemente de 1, 2, 3 y 4; y q es un número entero seleccionado de 0, 1,2 y 3. De acuerdo con algunas modalidades, q es 0 o 1. De acuerdo con algunas modalidades, q es 1. Se entenderá que un valor de 0 para q es el equivalente de que todos los restos R12 sean -H.
De acuerdo con algunas modalidades, R1 se selecciona de -(C1-C10) hidrocarbilo, -(C1-C10) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10) arilo, -(C6-C10) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -N(OR8)R7, -C(=O)-(C1-C6) alquilo, y -(C1-C6) heteroalquilo;
De acuerdo con algunas modalidades, R1 se selecciona de -NR7R8-SR7, -N(SR8)R7 y -N(OR8)R7. De acuerdo con algunas modalidades, R1 se selecciona de -NR7R8 y -N(OR8)R7.
De acuerdo con algunas modalidades, W1 es CH.
De acuerdo con algunas modalidades, R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)-(C1-C7) hidrocarbilo, y -(C1-C6)heteroalquilo.
De acuerdo con algunas modalidades, R7 se selecciona de -H, -(C1-C6)alquilo, -(C1-C6)alquilo sustituido,-C(=O)-(C1-C6) alquilo, y -(C1-C6) heteroalquilo;
De acuerdo con algunas modalidades, R8 se selecciona de -H, y -(C1-C6) alquilo.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo,-O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)rO(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2,-C(=O)NH2, -C(=O)NH(C1-C6) alquilo y -C(=O)N(C1-C6 alquilo)2.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6)alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2.
Otro aspecto de esta solicitud está dirigido a compuestos de Fórmula V:
y sales del mismo, por ejemplo, sales farmacéuticamente aceptables del mismo, en donde:
R1b se selecciona de -NR7R8 y -N(OR8)R7;
a y b se seleccionan independientemente de 0 y 1;
cada R2 se selecciona independientemente de -H y -(C1-C4) alquilo;
cada R3 se selecciona independientemente de -H y -(C1-C4) alquilo
R4 se selecciona de -H, -(C1-C6) alquilo, =O, -OH, -O(C1-C6) alquilo, halógeno y -CN; en donde uno de los grupos R3 puede opcionalmente conectarse estructuralmente a uno de los grupos R2 para formar un puente alquileno para producir un anillo bicíclico; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R1 para formar un anillo heterociclilo de 5 a 7 miembros fusionado a la cara 1-2 del anillo de piperidina; o uno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 a 7 miembros fusionado a la cara 2-3 del anillo de piperidina;
---------- significa que el enlace designado es un simple enlace carbono-carbono o un doble enlace carbonocarbono;
X se selecciona de -O-, -S-, -SO-, -SO2- y -NR9-;
W1, W2 y W3 se seleccionan independientemente de N, CH y C-R10; siempre que W2 y W 3 no sean N;
R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C (=O)NR7aR8a, -C(=O)OR7a, heteroarilo de 5 a 6 miembros y heteroarilo sustituido de 5 a 6 miembros;
n es un número entero seleccionado de 1, 2, 3 y 4;
R6 se selecciona de heteroarilo de 6 miembros, heteroarilo sustituido de 6 miembros, heteroarilo bicíclico de 9 a 10 miembros, y heteroarilo bicíclico sustituido de 9 a 10 miembros;
R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo; R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;
R7a se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo; R8a se selecciona de -H y -(C1-C6) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros;
R9 se selecciona de -(C1-C7) hidrocarbilo, en donde R9 puede opcionalmente conectarse estructuralmente a R4 para formar un anillo heterociclilo de 5 a 7 miembros;
cada R10 se selecciona independientemente de -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, halógeno, -C(=O)-(C1-C7) hidrocarbilo, -C(=O)NH2, -C(=O)NH-(C1-C7) hidrocarbilo, -C(=O)N(C1-C7 hidrocarbilo)2, -OH, -O(C1-C7) hidrocarbilo, -O(C1-C7) hidrocarbilo sustituido, -(C3-C6) heterociclilo, -(C3-C6) heterociclilo sustituido -CN, -NH2, -NH(C1-C6)alquilo, -N(C1-C6 alquilo)2, -NH(CH2)m-R11, -N(C1-C6 alquilo)(CH2)m-R11, -O-(CH2)m-R11, y-(C1-C6) heteroalquilo; m es un número entero seleccionado independientemente de 1,2, 3 y 4; y
R11 se selecciona de -O-(C1-C6)alquilo, -N-(C1-C6 alquilo)2, -(C3-C6) heterociclilo y -(C3-C6) heterociclilo sustituido.
De acuerdo con algunas modalidades, a y b son ambos 1.
De acuerdo con algunas modalidades, R2 es -H.
De acuerdo con algunas modalidades, R3 es -H.
De acuerdo con algunas modalidades, R4 se selecciona de -H, -(C1-C6) alquilo y halógeno.
De acuerdo con algunas modalidades, uno de los grupos R3 está conectado estructuralmente a uno de los grupos R2 para formar un puente -CH2-CH2- para producir un anillo bicíclico; por ejemplo:
De acuerdo con algunas modalidades, uno de los grupos R3 está conectado estructuralmente al grupo R1b para formar un anillo heterocíclico de 5 o 6 miembros fusionado a la cara 1-2 del anillo de piperidina; por ejemplo:
De acuerdo con algunas modalidades, uno de los grupos R3 está conectado estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 miembros fusionado a la cara 2-3 del anillo de piperidina; por ejemplo:
De acuerdo con algunas modalidades,--------- es un simple enlace carbono-carbono.
De acuerdo con algunas modalidades, X es -O-.
De acuerdo con algunas modalidades, W1, W2 y W3 se seleccionan independientemente de CH y C-R10. De acuerdo con algunas modalidades, W1, W2 y W3 son CH.
De acuerdo con algunas modalidades, R5 se selecciona de -H, -C1-C6 alquilo y halógeno. De acuerdo con algunas modalidades, R5 es -H.
De acuerdo con algunas modalidades, R9 es -(C1-C6) alquilo.
De acuerdo con algunas modalidades, R6 se selecciona de heteroarilo bicíclico de 9 a 10 miembros, y heteroarilo bicíclico sustituido de 9 a 10 miembros; siempre que, cuando R6 sea un heteroarilo bicíclico de 9 miembros o un heteroarilo bicíclico sustituido de 9 miembros, el punto de unión de R6 al anillo aromático que contiene W1, W2 y W3 esté en una porción de anillo de 6 miembros del heteroarilo bicíclico de 9 miembros o el heteroarilo bicíclico sustituido de 9 miembros. De acuerdo con algunas modalidades, R6 se selecciona de:
donde, cuando R6 es (i), Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan ind que 1,2 o 3 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12; cuando R6 es (ii), Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de
Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sean N, y el resto de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sea C-R12;
cuando R6 es (iii), Q8 se selecciona de O, S y N-R12n, Q9, Q10 y Q11 se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;
cuando R6 es (iv), Q8a se selecciona de O, S y N-R12n, Q9a, Q10a y Q11a se seleccionan independientemente de N y
C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;
cuando R6 es (v), Q12, Q13 y Q14 se seleccionan independientemente de N y C-R12; y
cuando R6 es (vi), Q12a, Q13a y Q14a se seleccionan independientemente de N y C-R12;
cuando R6 es (vii), Q15 se selecciona de N-R12n y C-R12 y Q16 se selecciona de N y C-R12; siempre que uno de Q15 y Q16 no sea C-R12;
y en donde cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, -(C1-C3) haloalquilo, -O(C1-C3) haloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -O(CH2)r-N(C1-C6 alquilo)2, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2; en donde r es un número entero seleccionado independientemente de 1, 2, 3 y
4; y
cada R12n se selecciona de -H, -(C1-C7) hidrocarbilo y -(C1-C7) hidrocarbilo sustituido.
Se entenderá que los átomos del anillo de carbono del anillo en (i), (ii), (iii), (iv), (v), (vi) y (vii) anteriores (es decir, los átomos del anillo que no se designan como N o Q) pueden estar opcionalmente sustituidos. De acuerdo con algunas modalidades, ninguno de estos átomos del anillo de carbono del anillo está sustituido. De acuerdo con algunas modalidades, uno o dos de estos átomos de carbono del anillo están sustituidos con un sustituyente seleccionado entre -OH, -(C1-C3) alquilo, -O(C1-C3) alquilo y halógeno. De acuerdo con algunas modalidades, uno de estos átomos de anillo de carbono del anillo está sustituido con un sustituyente seleccionado de -OH, -CH3, -OCH3, -F y -Cl.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo,
-(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo,-O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2,-C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3,
OCH3, -OCH2CH3, -OCH(CH3)2, -CF3, -OCF3, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O (CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3 -N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1 -ilo y piperidin-1-ilo.
De acuerdo con algunas modalidades, R12n se selecciona de -H, bencilo y -C1-C6 alquilo.
De acuerdo con algunas modalidades, R6 se selecciona de los sistemas de anillos aromáticos descritos en la Tabla
1b (infra).
De acuerdo con algunas modalidades, R6 es:
en donde 1 o 2 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 son N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), uno de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es N, y el resto de Q1, Q2, Q3, Q4, Q5,
Q6 y Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q2 es N y el resto de Q1, Q3, Q4, Q5, Q6 y
Q7 es C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q6 es N y Q1, Q2, Q3, Q5, Q5 y Q7 son C-R12. De acuerdo con algunas modalidades, cuando R6 es (i), Q6 es N, Q2, Q3, Q5, Q5 y Q7 son CH, y Q1 es C-R12 es distinto de -H.
De acuerdo con algunas modalidades, R6 es:
en donde uno de Q2 y Q6 es N, y el otro de Q2 y Q6 es C-R12, y q es un número entero seleccionado de 0, 1,2 y 3. De acuerdo con algunas modalidades de i2, Q2 es N y Q6 es C-R12. De acuerdo con algunas modalidades, Q6 es N y Q2 es C-R12. De acuerdo con algunas modalidades, q se selecciona de 0, 1 y 2. De acuerdo con algunas modalidades de
i2, q es 0 o 1. Se entenderá que un valor de q de 0 es el equivalente a designar todos los R12 que se unen al heteroarilo bicíclico i2 en un lugar distinto de Q2 y Q6 como -H.
De acuerdo con algunas modalidades de i2, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1 -ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1 -ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo.
De acuerdo con algunas modalidades de i2, cada R12n se selecciona independientemente de -H, bencilo y -C1-C6 alquilo.
De acuerdo con algunas modalidades, R6 es:
en donde uno o dos de Q2, Q4 y Q6 es N, y el resto de Q2, Q4 y Q6 es C-R12, y q es un número entero seleccionado de 0, 1, 2 y 3.
De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O (CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6 alquilo) y -C(=O)N(C1-C6 alquilo)2; donde r es un número entero seleccionado de 1, 2, 3 y 4; o una sal del mismo.
De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1 -ilo), -O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N-metilpiperazin-1-ilo), O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2, -O(CH2)3-N(CH3)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1 -ilo y piperidin-1-ilo. De acuerdo con algunas modalidades de i3, cada R12 se selecciona independientemente de -H, -Cl, -F, -CH3, -CH2CH3, -OCH3 y -OCH2CH3.
De acuerdo con algunas modalidades de i3, q es 0, 1 o 2. De acuerdo con algunas modalidades, q es 0 o 1. Se entenderá que un valor de q de 0 es el equivalente a designar todos los R12 que están unidos al resto heteroarilo bicíclico en un lugar distinto de Q2, Q4 o Q6 como -H.
De acuerdo con algunas modalidades de i3, Q2 es N y Q4 y Q6 son C-R12. De acuerdo con algunas modalidades de i3, Q6 es N y Q2 y Q4 son C-R12. De acuerdo con algunas modalidades de i3, Q4 es N y Q2 y Q6 son C-R12. De acuerdo con algunas modalidades de i3, Q2 es C-R12, y Q4 y Q6 son N. De acuerdo con algunas modalidades de i3, Q6 es C-R12 y Q2 y Q4 son N. De acuerdo con algunas modalidades de i3, Q4 es C-R12, y Q2 y Q6 son N.
De acuerdo con algunas modalidades, R7 se selecciona de -H, -(C1-C6) alquilo, -(C1-C6) alquilo sustituido, -(C3-C6) cicloalquilo, -(C3-C6) cicloalquilo sustituido, -(C2-C6) alquenilo, -(C2-C6) alquenilo sustituido, bencilo, bencilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo. De acuerdo con algunas modalidades, R7 se selecciona de -H y -(C1-C6) alquilo.
De acuerdo con algunas modalidades, R7a se selecciona de -H, -(C1-C6) alquilo, -(C1-C6)alquilo sustituido, -(C3-C6) cicloalquilo, -(C3-C6) cicloalquilo sustituido, -(C2-C6) alquenilo, -(C2-C6)alquenilo sustituido, bencilo, bencilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo. De acuerdo con algunas modalidades, R7a se selecciona de -H y -(C1-C6) alquilo.
De acuerdo con algunas modalidades, R8 se selecciona de -H, y -(C1-C6) alquilo. De acuerdo con algunas modalidades, R8 se selecciona de -H, -CH3 y -CH2CH3.
De acuerdo con algunas modalidades, R8a se selecciona de -H, y -(C1-C6) alquilo. De acuerdo con algunas modalidades, R8a se selecciona de -H, -CH3 y -CH2CH3.
Otro aspecto de esta solicitud está dirigido a compuestos de Fórmula V(a), (que es un subconjunto de compuestos de acuerdo con la Fórmula V):
y sales del mismo, por ejemplo, sales farmacéuticamente aceptables del mismo, en donde:
R1b se selecciona de -NR7R8 y -N(OR8)R7;
R4 se selecciona de -H, -(C1-C6) alquilo, =O, -OH, -O(C1-C6) alquilo, halógeno y -CN;
X se selecciona de -O- y -S-;
R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a, -C(=O)OR7a, heteroarilo de 5 a 6 miembros y heteroarilo sustituido de 5 a 6 miembros;
n es un número entero seleccionado de 1, 2, 3 y 4;
R7 se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo; R8 se selecciona de -H, y -(C1-C6) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;
R7a se selecciona de -H, -(C1-C7) hidrocarbilo, -(C1-C7) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6) heteroalquilo; R8a se selecciona de -H y -(C1-C6) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros;
Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12;
cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C1-C3) haloalquilo,-O(C1-C3) haloalquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo, -O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -O(CH2)r-N(C1-C6 alquilo)2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2, -C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2 y r es un número entero seleccionado independientemente de 1, 2, 3 y 4.
De acuerdo con algunas modalidades, R4 se selecciona de -H, -(C1-C6) alquilo y halógeno.
De acuerdo con algunas modalidades, X es -O-.
De acuerdo con algunas modalidades, R5 se selecciona de -H, -C1-C6 alquilo y halógeno. De acuerdo con algunas modalidades, R5 es -H.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6) alquilo,-O(CH2)r-(heterociclilo de 5 a 6 miembros), -O(CH2)r-O(C1-C6) alquilo, -NH2, -CN, -NH(C1-C6) alquilo, -N(C1-C6 alquilo)2, -NH(CH2)r-O(C1-C6) alquilo, -NH(CH2)r-N(C1-C6 alquilo)2,-C(=O)NH2, -C(=O)NH(C1-C6) alquilo, y -C(=O)N(C1-C6 alquilo)2.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -Cl, -F, -CH3, -CH2CH3, -CF3, -OCF3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo),-O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N- metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2,-O(CH2)3-N(CHa)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo.
De acuerdo con algunas modalidades, cada R12 se selecciona independientemente de -Cl, -F, -CH3, -CH2CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -O(CH2)2(pirrolidin-1-ilo),-O(CH2)3(pirrolidin-1-ilo), -O(CH2)2(morfolin-1-ilo), -O(CH2)3(morfolin-1-ilo), -O(CH2)2(piperidin-1-ilo), -O(CH2)3(piperidin-1-ilo), -O(CH2)2(N-metilpiperazin-1-ilo), -O(CH2)3(N- metilpiperazin-1-ilo), -O(CH2)2-OCH3, -O(CH2)3-OCH3, -O(CH2)2-N(CH3)2,-O(CH2)3-N(CHa)2, -NH2, NHCH3, N(CH3)2, N-metilpiperazin-1-ilo, pirrolidin-1-ilo, morfolin-1-ilo y piperidin-1-ilo.
Los compuestos de acuerdo con la Fórmula I pueden incluir, por ejemplo: 1-[4-(4-isoquinolin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; terc-butil éster del ácido 4-(2-fluoro-4-quinolin-3-il-fenox)piperidina-1-carboxílico; 1-[4-(2-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]propan-1-ona; 1-[4-(2-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; 1-[4-(4-benzofuran-5-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(4-benzofuran-5-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; 1-[4-(4-naftalen-2-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(4-naftalen-2-il-fenoxi)-piperidin-1-il]-propan-1-ona; na; {4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona; 1-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-[4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-meti l-1 -[4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-metanona; éster metílico del ácido 4-(2-fluoro-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico; 1-{4-[4-(2-cloro-quinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; {4-[4-(2-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(2-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxi]-piperidin-l-il}-metanona; ciclobutil-{4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(8-fluoro-quinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-fluoro-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8
fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(1H-pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(1H-pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-l-il}-metanona; ciclopropil-{4-[4-(7-metoxi-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(4-quinolin-2-ilfenoxi)-piperidin-1-il]-propan-1-ona; ciclobutil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinolin-2-ilfenoxi)-piperldin-1-il]-(R)-tetrahidrofuran-2-il-metanona; 1-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ciclobutil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclobutilmetanona; 1-{4-[4-(4-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-[4-(4-furo[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-furo[3,2-b]piridin-6-ilfenoxi)-piperidin-1-il]-metanona;1-{4-[4-(6-metoxi-quinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-metoxi-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(6,7-dimetoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6,7-dimetoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-metoxiquinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(8-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metano{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-[4-(4-quinoxalin-2-ilfenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(S)-tetrahidrofuran-2-il-metanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1 -{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1 -il}-propano-1,2-diona; isoxazolidin-2-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona; {4-[4-(8-cloro-quinolin-7-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoxiamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoximetil-amida; ácido 4-[4-(4-metil-quinolin-3-il)-fenoxi]-piperidina-1-carboxílico etilamida; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico metilamida; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico etilamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico hidroxiamida; N-etil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N,N-dimetil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; etil 4-[4-(8-metil-7-quinolil)-fenoxi]piperidina-1-carboxilato; N-metoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-pirrolidin-1 -il-metanona; N-metil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propilpiperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(1-piperidil)metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-morfolinometanona; ciclopropil-[4-(4-quinolin-3-ilfenoxi)-piperidin-1-il]-metanona; ciclobutil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ciclopentil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(S)-tetrahidrofuran-2-il-metanona; 2-metoxi-1-[4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona; [4-(4-quinolin-3-il-fenoxil)-piperidin-1-il]-(tetrahidrofuran-3-il)-metanona; (R)-2-metoxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; (S)-2-metoxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-hidroxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona;
[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona; 1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona; 2-metil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; 2,2-dimetil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; (2-metil-1,3-dioxolan-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 2-metanosulfonil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona; (1,1 -dioxidotetrahidrotiofen-2-il)(4-(4-(quinolin-3-il)fenoxi)piperidin-1-il)metanona; (3,3-difluoro-ciclobutil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (R)-5-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-dihidro-furan-2-ona; (3-metilfu ran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1 -il]-metanona; (3,5-dimetilfuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; oxazol-2-il-[4-(4-quinolin-3-ilfenoxi)-piperidin-1-il]-metanona; isoxazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; isotiazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidrofuran-2-il)-metanona; fenil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (2,5-dimetil-fenil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1 -il]-metanona; [3-(1H-imidazol-2-il)-fenil]-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [3-(1H-bencimidazol-2-il)-fenil]-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; N-metoxi-4-[4-(8-metoxi-7-quinolil)fenoxi]piperidina-1-carboxamida; 1-[4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1 -il]-propan-1 -ona; ciclopropil-[4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-metanona; 1-[4-(5-quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(5-quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(5-quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-metanona; 2-metil-1-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1 -il]-propan-1 -ona; ciclopropil-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-metanona; 1-[4-(6-quinolin-3il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(6-quinolin-3-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(6-quinolin-3-il-piridin-3-iloxi)-piperidin-1-il]-metanona; 1-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-propan-1-ona; 1-[4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-metanona;1-[4-(6-isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; 1-[4-(6-isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-2-metilpropan-1-ona; ciclopropil-[4-(6-isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-metanona; ácido 1 -propionilpiperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)-amida; ácido 1-propionil-piperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida; oxo-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-acetaldehído; 4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbaldehído; ((2R,3S)/(2S,3R)-3-metiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;
((2R,3S,5R)/(2S,3R,5S)-3,5-dimetil-tetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ((2R,3S, 5R)/(2S,3R,5S)-3,5-dimetiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ácido 1 -propionilpiperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida; 2-fluoro-4-isoquinolin-6-il-N-metil-N-(1-propionil-piperidin-4-il)-benzamida; 1-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; (R)-tetrahidrofuran-2-il-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; 3-[4-(1-metanosulfonil-piperidin-4-iloxi)-fenil]-quinolina; (4,4-difluorotetrahidro-furan-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (4,4-difluorotetrahidrofuran-2-il)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (4,4-difluorotetrahidrofuran-2-il)-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; 5-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-dihidrofuran-3-ona; 1-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-l-il}-metanona; 1-{4-[4-(8-iso-propoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-propan-1 -ona; ciclopropil-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxil}-piperidin-1-il)-metanona; 1-(4-{4-[8-(2-pirrolidin-1-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; ciclopro-pil-(4-{4-[8-(2-pirrolidin-1-iletoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona; 1-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; ciclopropil-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona; 1-[4-[4-[8-[2-(4-metilpiperazin-1-il)etoxi]-7-quinolil]fenoxi]-1-piperidil]propan-1-ona; 1-[4-[4-[8-(2-metoxietoxi)-7-quinolil]fenoxi]-1 -piperidil]propan-1 -ona; 1-[4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona; {4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; (4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-(R)-tetrahidrofuran-2-il-metanona; (4-{4-[8-(2-pirrolidin-1-il-etoxi)quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-ilmetanona; (4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-ilmetanona; [4-[4-[8-[2-(4-metilpiperazin-1-il)etoxi]-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-[8-(2-metoxietoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il} -(R)-tetrahidrofuran-2-il-metanona; 1-[4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1 -il]-2-metil-propan-1 -ona; [4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-ciclopropilmetanona; 1-[4-(2-cloro-4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-cloro-4-quinolin-7-ilfenoxi)-piperidin-1-il]-2-metil-propan-1-ona;1-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metilpropan-1-ona; ciclopropil-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(2-metoxi-4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(3-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; 1-[4-(3-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; ciclopropil-[4-(3-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; [4-(3-cloro-4-quinolin-3-ilfenoxi)-piperidin-1-il]-ciclopropilmetanona; 2-metil-1-[4-(3-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(3-metil-4-quinolin-3-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; éster metílico del ácido 4-(3-metil-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico; 1-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1 -il]-2-metil-propan-1 -ona; ciclopropil-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(2,5-difluoro-4-quinolin-3-ilfenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2,5-difluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; ciclopropil-[4-(2,5-difluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 3-oxo-3-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propionitrilo; 1-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-cloroquinolin-7-il)-2-fluoro-fenoxi]-piperidin-1-il}-ciclo-propilmetanona; {4-[4-(8-cloroquinolin-7-il)-2-fluorofenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-cloroquinolin-7-il)-2-fluorofenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il} -propan-1-ona; ciclopropil-{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[2-fluoro-4-(4-metil-quinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(4-aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(4-dimetilamino-quinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-dimetilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(4-amino-quinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-metilamino-quinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-metilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-morfolin-4-il-quinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-morfolin-4-il-quinolin-3-il)-fenoxi]-piperidin-l-il}-(R)-tetrahidrofuran-2-ilmetanona;1-(4-{4-[4-(4-metilpiperazin-1-il)-quinolin-3-il]-fenoxi}-piperidin-1-il)-propan-1-ona; (4-{4-[4-(4-metilpiperazin-1-il)-quinolin-3-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 3-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]oxazolidin-2-ona; 1 -[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-butano-1,3-diona; 1-[4-(4-quinolin-3-il-fenoxi)-piperidina-1 -carbonil]-pirrolidin-2-ona; 4'-[1-((R)-tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-bifenil-4-carbonitrilo; 1-[4-(4-benzofuran-2-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-{4-[4-(1H-indol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-[4-(4-benzo[b]tiofen-5-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-{4-[4-(1H-indazol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-{4-[4-(2-metil-2H-indazol-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-[4-(4-[1,8]naftiridin-3-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; 1-{4-[4-(2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; (R)-tetrahidrofuran-2-il-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona; ciclopropil-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona;1-[4-(4-imidazo[1,2-a]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona; {4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona; {4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il} -(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; (R)-tetrahidrofuran-2-il-[4-(4-tieno[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(4-tieno[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona; {4-[4-(3-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(3-cloroquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; [4-(4-benzotiazol-5-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; [4-(4-benzo-tiazol-5-il-fenoxi)-piperidin-1-il]-ciclopropilmetanona; 1-[4-(4-benzotiazol-5-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo; 7-{4-[1-((R)-tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-fenil}-quinolina-3-carbonitrilo; 7-[4-(1-ciclopropanocarbonilpiperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo; 1-{4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona; ciclopropil-{4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il} -(R)-tetrahidrofuran-2-ilmetanona; 1-{4-[4-(8-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-{4-[4-(8-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(2,3-dimetilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran 2-il-metanona; 1-{4-[4-(2,3-dimetil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(2,3-dimetilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(7-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(7-metilinudazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona; [4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; 1-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-metanona; ácido 1-[4-(4-imidazo[1,5-a]piridin-6-ilfenoxi)-piperidina-1-carbonil]-ciclopropanocarboxílico amida; (1-hidroxiciclopropil)-[4-(4-imidazo[1,5-a]piridin-6-ilfenoxi)-piperidin-1-il]-metanona; (1-hidroxiciclopropil)-{4-[4-(8-metoxi-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (1-hidroximetilciclopropil)-{4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; (1-amino-ciclopropil)-{4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; (1 -hidroxiciclopropil)-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona; (R)-tetrahidrofuran-2-il-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona; ciclopropil-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-ilfenoxi)-piperidin-1-il]-metanona; (1-hidroxiciclopropil)-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; 2-hidroxi-2-metil-1-{4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; (1-hidroxiciclo-propil)-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(1-trifluorometil-ciclopropil)-metanona; (1-aminociclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-ilmetanona; [4-(4-imidazo[1,2-a]piridin-6-il-fenoxi)-piperidin-1-il]-(R)-tetrahidro-furan-2-il-metanona; 1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidina-1-carbonil}-ciclopropanocarbonitrilo; (1-metilciclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ((S)-2,2-dimetilciclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (2,2-dimetilciclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; [4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]-fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-(8-amino-7-quinolil)-fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; {4-[4-(8-metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-metilamino-quinolin-7-il)fenoxi]-piperidin-1-il}-propan-1-ona; (4-{4-[8-(2-metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; (4-{4-[8-(2-di-metilaminoetilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-ilmetanona; 7-[4-(1-propionilpiperidin-4-iloxi)-fenil]-quinolina-8-carbonitrilo; [4-[4-[8-(dimetilamino)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-{4-[4-(8-dimetilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-dimetilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (4-{4-[8-(2-pirrolidin-1 -il-etilamino)quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-pirrolidin-1-il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; 7-[4-[[1-[(2R)-tetrahidrofuran-2-carbonil]-4 piperidil]oxi]fenil]quinolina-8-carboxamida; ácido 7-[4-(1-propionilpiperidin-4-iloxi)-fenil]-quinolina-8-carboxílico amida; 1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona; 2-metil-1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona; ciclopropil(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)metanona; 3-metil-1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)butan-1-ona; (S)-1-(3-(4-(quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona; (S)-1-(3-(4-(quinolin-3-il)fenoxi)pirrolidin-1-il)propan-1-ona; (R)-1-(3-(4-(quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona; (R)-1-(3-(4-(quinolin-3-il)fenoxi)pirrolidin-1-il)propan-1-ona; 1-(4-(4-(5-metilquinolin-7-il)fenoxi)-piperidin-1-il)propan-1-ona; ciclopropil(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)-metanona; 1-(4-(4-(7-metilquinolin-5-il)fenoxi)piperidin-1-il)propan-1-ona; ciclopropil-{4-[4-(7-metilquinolin-5-il)-fenoxi]-piperidin-1-il}-metanona; 1-(4-(4-(6-metilquinolin-5-il)fenoxi)piperidin-1-il)propan-1-ona; ciclopropil(4-(4-(6-metilquinolin-5-il)fenoxi)-piperidin-1-il)metanona; (R)-(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona; (R)-(4-(4-(7-metilquinolin-5-il)fenoxi)piperidin-1-il)-(tetrahidrofuran-2-il)metanona; (R)-(4-(4-(6-metilquinolin-5-il)fenoxi)piperidin-1-il)-(tetrahidrofuran-2-il)metanona; (±)-(7S,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidro-indolizin-3 (2H)-ona; (±)-(7R,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona; 2,2,2-trifluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-etanona; 2,2-difluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 2-fluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {exo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{exo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-propan-1-ona; {2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-ilmetanona; 1-{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{endo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-propan-1-ona; ciclopropil-{endo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-metanona; {endo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-(R)-tetrahidrofuran-2-il-metanona; {(trans)-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{trans-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{trans-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 2-metil-1-{4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidin-l-il}-metanona; ciclobutil-{4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(5-fenilpiridin-3-il)-fenoxi]piperidin-1-il}-propan-1-ona; 2-metil-1-{4-[4-(5-fenilpiridin-3-il)-fenoxi]piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5-fenilpiridin-3-il)-fenoxi]piperidin-1-il}-metanona; ciclobutil-{4-[4-(5-fenilpiridin-3-il)-fe-noxi]-piperidin-1-il}-metanona; 1-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(6-din-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(6-fenoxipiridin-3-il)-fenoxi]-piperidin-l-il}-metanona; ciclobutil-{4-[4-(6-fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(6-fenil-aminopiridin-3-il)fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-fenilaminopiridin-3-il)fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(6-fenilamino-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona; 1-{4-[4-(5-fenoxipirldin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclobutil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona; ciclopropil-{4-[4-(5-fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(5-fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(5-fenilamino-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(2-fenilpiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(2-fenil-piridin-4-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(2-fenilaminopiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(2-fenilaminopiridin-4-il)-fenoxi]-piperidin-1-il}-metanona; 1-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona; ciclobutil-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona; 1-{4-[4-(2-fenoxipiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(3-metoxi-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(3-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(3-amino-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(3-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; {4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(4-hidroxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclobutil-{4-[4-(4-hidroxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclobutilmetanona; {4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1 -{4-[4-(3-metil i soqu inol in-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofu ran-2-ilmetanona; {4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclobutil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(3-aminoisoquinolin-6il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(3-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-etil-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(1-ciclo-propilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-l-il}-metanona; {4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidinl-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il} -(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; {4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(3-isopropoxiisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-morfolin-4-il-isoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofu ran-2-ilmetanona; {4-[4-(1-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetra-hidrofuran-2-il-metananona; {4-[4-(1-amino-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-metilaminoisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(4-metilisoquinolin-6-il)-fe-noxi]-piperidin-1-il}-metanona; {4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2- il-metanona; 1-{4-[4-(5-metoxiquino¡in-3-il)-fenoxi']-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(5-metoxiquinolin-3-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofu ran-2-ilmetanona; ciclopropil-[4-(4-isoquinolin-6-il-fenoxi)-piperidin-1-il]-metanona; [4-[4-(6-isoquinolil)fenoxi]-1 -piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; {4-[4-(5-metilisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofu ran-2-ilmetanona; 1-[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1-piperidil]propan-1-ona; ciclopropil-[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1-piperidil]metanona; [4-[4-(1,4-dimetil-6-isoquinolil)-fenoxi]-1 -piperidil]-[(2R)-tetrahidrofu ran-2-il]metanona; 1-[4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]propan-1-ona; ciclopropil-[4-[4-(1,5-dimetil-6-isoquinolil)-fenoxi]-1-piperidil]metanona; [4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-(8-cidopropil-7-quino¡il)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; {4-[4-(3-etilisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofu ran-2-il-metanona; ciclopropil-{4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(3-ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetra-hidrofuran-2-il-metanona; ciclopropil-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-metanona; {4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-metilquinolin-3- il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(8-metil-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; terc-butil éster del ácido 4-(3',4'-dimetoxibifenil-4-iloxi)-piperidina-1 -carboxílico; terc-butil éster del ácido 4-(4'-cianobifenil-4-iloxi)-piperidina-1 -carboxílico; 1-[4-(3',4'-dimetoxi-bifenil-4-iloxi)-piperidin-1 -il]-propan-1 -ona; 1-[4-(3',4'-dimetoxibifenil-4-iloxi)-piperidin-1-il]-2-metil-propan-1-ona; 4'-(1-propionilpiperidin-4-iloxi)-bifenil-4-carbonitrilo; 4'-(1-isobutirilpiperidin-4-iloxi)-bifenil-4-carbonitrilo; 4'-(1-ciclopropanocarbonil-piperidin-4-iloxi)-bifenil-4-carbonitrilo; 1-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 1-{4-[4-(5,6-dimetoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5,6-dimetoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-[4-(3',4'-diclorobifenil-4-iloxi)-piperidin-1 -il]-propan-1 -ona; ciclopropil-[4-(3',4'-diclorobifenil-4-iloxi)-piperidin-1 -il]-metanona; 1-{4-[4-(2,3-dihidro-1,4-benzo-dioxin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(2,3-dihidro-1,4-benzodioxin-6-il)-fenoxi]-piperidin-1-il}-metanona; 1-[4-(4'-benziloxi-2'-fluorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona; [4-(4'-benziloxi-2'-fluorobifenil-4-iloxi)-piperidin-1-il]-ciclopropilmetanona; 1-[4-(5'-benziloxi-3'-fluorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona; [4-(5'-benziloxi-3'-fluorobifenil-4-iloxi)-piperidin-1-il]-ciclopropilmetanona; 1-[4-(4'-fenoxibifenil-4-iloxi)-piperidin-1 -il]-propan-1 -ona; ciclopropil-[4-(4'-fenoxibifenil-4-iloxi)-piperidin-1-il]-metanona; 1-[4-(3'-fenoxibifenil-4-iloxi)-piperidin-1 -il]-propan-1 -ona; ciclopropil-[4-(3'-fenoxi-bifenil-4-iloxi)-piperidin-1-il]-metanona; 2-metil-1-(4-((4-(quinolin-7-il)fenil)sulfonil)piperidin-1-il)propan-1-ona; 1-[4-(4-isoquinolin-7-il-bencenosulfonil)-piperidin-1-il]-2-metilpropan-1-ona; 1-[4-(4-isoquinolin-6-il-bencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona; 1-[4-(4-benzofuran-5-il-bencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona; 1-(4-((4-(quinolin-7-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-4-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-6-il)-fenil)tio)piperidin-1-il)propan-1-ona; 1 -(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1 -il)-2-metilpropan-1 -ona; 2-metil-1-(4-((4-(quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-4-il)fenil)tio)piperidin-1-il)-2-metilpropan-1-ona; 1-{4-[metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-propan-1-ona; cidopropil-{4-[metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-metanona; 1-[4-(4-quinolin-3-il-fenilamino)-piperidin-1-il]-propan-1-ona; cidopropil-[4-(4-quinolin-3-il-fenilamino)-piperidin-1-il]-metanona; {4-[metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona y sales de dichos compuestos, por ejemplo, sales farmacéuticamente aceptables.
Los compuestos adicionales de acuerdo con la Fórmula I pueden incluir, por ejemplo: N-etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-pirrolidin-1-iletil)piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-morfolinoetil)piperidina-1-carboxamida; (4-isopropil-piperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; (4-metil-piperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1piperidil]metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperidil)metanona; (4-etil lpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; N-etil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-etoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-metoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-(2-metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-Isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-(2-dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 2-morfolinoetil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; 2-pirrolidin-1-iletil 1-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; N-[2-(1H-imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-tetrahidropiran-4-il-piperidina-1-carboxamida; isobutil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; alil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; N-ciclobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ciclopropilmetil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; ácido 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbohidroxámico; 2-metoxietil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; tetrahidropiran-4-il 4-[4-(8-metil-7-quinolil)-fenoxi]piperidina-1-carboxilato; tetrahidropiran-3-il 4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxilato;
[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)-metanona; tetrahidrofuran-3-il 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; N-(ciclobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ciclobutil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; N-butil-4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-etil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isobutil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-propilpiperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-(2-metoxietil)-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-(ciclopropilmetil)piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopropoxi-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopropil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isobutoxi-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopentil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-N-etoxi-piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida; ácido 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carbohidroxámico; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxipiperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-etil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propil-piperidina-1-carboxamida; N-isobutil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propoxipiperidina-1-carboxamida; ácido 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carbohidroxámico; N-etoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida; N-isobutil-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propilpiperidina-1-carboxamida; N-etil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(3-piridil)-piperidina-1-carboxamida; N-(2-metoxietil)-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; [4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-1-piperidil]-(4-metilpiperazin-1-il)metanona; N,N-dimetil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isobutoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; isobutil 4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato; N-isopropil-4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(1-metilpirazol-4-il)piperidina-1-carboxamida; terc-butil 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(2,2,2-trifluoro-etil)piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxi-piperidina-1-carboxamida; N-etoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamidal 2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona 2HCl; (2R)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona 2HCl; N-metoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; (2S)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona 2HCl; ácido 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carbohidroxámico; 2-(dimetilamino)-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; [(2R)-1-metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; [(2S)-1-metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; S-isopropil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbotioato; 2-amino-2-metil-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-propan-1-ona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-pirrolidin-2-il]metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-[(2S)-pirrolidin-2-il]metanona; [1-(metilamino)ciclopropil]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; 3-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona; 2-isopropoxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; [2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil] acetato; 2-hidroxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; (1-aminociclobutil)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-metanona; N-etil-4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxamida; N-etil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)-fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metilimidazo[1,2-a]piridin-7il)fenoxi]-N-propilpiperidina-1-carboxamida; N-isobutil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; ácido 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)-fenoxi]piperidina-1-carbohidroxámico; N,N-dimetil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; [4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]-pirrolidin-1 -il-metanona; [(3S)-3-fluoropirrolidin-1 -il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1 -piperidil]metanona; [(3R)-3-fluoropirrolidin-1-il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]metanona; 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida; N-etilsulfanil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-etilsulfanil-piperidina-1-carboxamida; 1-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona; 1-[4-[4-(4-metil-3-quinolil)-fenoxi]piperidina-1-carbonil]pirrolidin-2-ona; 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)-fenoxi]-N-propil-piperidina-1-carboxamida; N-etil-4-[4-(2-fluoro-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida y sales de dichos compuestos, por ejemplo, sales farmacéuticamente aceptables.
Los compuestos de acuerdo con la Fórmula III pueden incluir, por ejemplo: 1-[4-(4-isoquinolin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1- il]-propan-1-ona; 1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-fluoro-4-quinolin-3-ilfenoxi)piperidin-1-il]propan-1-ona; 1-[4-(2-fluoro-4-quinolin-3-ilfenoxi)-piperidin-1-il]-2-metilpropan-1-ona; 1-[4-(4-1,5-naftiridin-3-il-fenoxi)piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(4-1,5-naftiridin-3-il-fenoxi)piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-1,5-naftiridin-3-il-fenoxi)piperidin-1-il]-metanona; 1-{4-[4-(2-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(2-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(2-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropi l-{4-[4-(8-fluoro-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi-il}-propan-1-ona; ciclopropil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-{4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(4-quinolin-2-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; ciclobutil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; 1-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ciclobutil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclobutilmetanona; 1-{4-[4-(4-metoxiquinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; 1-{4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(6,7-dimetoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6,7-dimetoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-metoxiquinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(8-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-cloroquinolin-7-il)-fenoxi]piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(4-metilquinolin-3-il)-fenoxi]piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(4-metilquinolin-3-il)-fenoxi]piperidin-1-il}-metanona; ciclobutil-{4-[4-(4-metilquinolin-3-il)-fenoxi]piperidin-1-il}-metanona; 1-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2- il-metanona; 1-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(S)-tetrahidrofuran-2-il-metanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-ilmetanona; 1 -{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1 -il}-propano-1,2-diona; isoxazolidin-2-il-[4-(4-quinolin-2-ilfenoxi)-piperidin-1-il]-metanona; [4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]piperidin-1 -il}-isoxazolidin-2-il-metanona; {4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona; ácido 3-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoxiamida; ácido 4-[4-(4-metil-quinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoxi-metil-amida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1 -carboxílico etilamida; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico metilamida; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico etilamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico hidroxiamida; N-etil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N,N-dimetil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; etil 4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxilato; N-metoxi-4-[4-(8-metil-7quinolil)fenoxi]piperidina-1-carboxamida; N-isopropil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1 -piperidil]-pirrolidin-1 -il-metanona; N-metil-4-[4-(8-metil-7-quinolil)fenoxi] piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propilpiperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(1-piperidil)metanona; [4-[4-(8metil-7-quinolil)fenoxi]-1-piperidil]-morfolinometanona; ciclopropil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ciclobutil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ciclopentil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(S)-tetrahidrofuran-2-il-metanona; 2-metoxi-1-[4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona; [4-(4-quinolin-3-il-fenoxil)-piperidin-1-il]-(tetrahidrofuran-3-il)-metanona; (R)-2-metoxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; (S)-2-metoxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-hidroxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona; 1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona; 2-metil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2,2-dimetil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; (2-metiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (2-metil-1,3-dioxolan-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 2-metanosulfonil-1-[4-(4-quinolin-3-ilfenoxi)piperidin-1-il]-etanona; (1,1-dioxidotetrahidro-tiofen-2-il)(4-(4-(quinolin-3-il)fenoxi)piperidin-1-il)metanona; (3,3-difluorociclobutil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (R)-5-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-dihidrofuran-2-ona; (3-metilfuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (3,5-dimetilfuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; oxazol-2-il-[4-(4-quinolin-3-il-fenoxi)piperidin-1-il]-metanona; isoxazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; isotiazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidrofuran-2-il)-metanona; fenil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (2,5-dimetilfenil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [3-(1 H-imidazol-2-il)-fenil]-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; [3-(1H-bencimidazol-2-il)-fenil]-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; N-metoxi-4-[4-(8-metoxi-7-quinolil)fenoxi]piperidina-1-carboxamida; ácido 1-propionilpiperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)-amida; ácido 1-propionilpiperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida; oxo-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-acetaldehído; ((2R,3S)/(2S,3R)-3-metiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)piperidin-1-il]-metanona; ((2R,3S,5R) /(2S,3R,5S)-3,5-dimetiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ((2R,3S,5R)/(2S,3R,5S)-3,5-dimetiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 3-[4-(1-metanosulfonil-piperidin-4-iloxi)-fenil]-quinolina; (4,4-difluorotetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (4,4-diiluorotetrahidrofuran-2-il)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (4,4-difluorotetrahidrofuran-2-il)-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; 5-[4-(4-quinolin-3-il-fenoxi)-piperidina-1 -carbonil]-dihidrofuran-3-ona; 1-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-isopropoxi-quinolin-7-il)-fenoxi-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-isopropoxi-quinolin-7-il)-fenoxi]-pipendin-1-il}-metanona; 1-(4-{4-[8-(2-morfolin-4-il-etoxi)quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; ciclopropil-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxil}-piperidin-1-il)-metanona; 1-(4-{4-[8-(2-pirrolidin-1 -il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-propan-1 -ona; ciclopropil-(4-{4-[8-(2-pirrolidin-1 -il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona; 1-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)propan-1-ona; ciclopropil-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona; 1-[4-[4-[8-[2-(4-metilpiperazin-1-il)etoxi]-7-quinolil]fenoxi]-1-piperidil]-propan-1-ona; 1-[4-[4-[8-(2-metoxietoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona; 1-[4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona; {4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; (4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-(R)-tetrahidrofuran-2-il-metanona; (4-{4-[8-(2-pirrolidin-1-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-ilmetanona; (4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-ilmetanona; [4-[4-[8-[2-(4-metilpiperazin-1-il)etoxi]-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-[8-(2-metoxi-etoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-hidroxiquinolin-7-il)-fenoxi-il}-(R)-tetrahidrofuran-2-il-metanona; 1-[4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; [4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-ciclopropil-metanona; 1-[4-(2-cloro-4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-cloro-4-quinolin-7-ilfenoxi)-piperidin-1-il]-2-metilpropan-1-ona; 1-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; ciclopropil-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(2-metoxi-4-quinolin-7-il-fenoxi)piperidin-1-il]-propan-1-ona; 1-[4-(3-fluoro-4-quinolin-3-ilfenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(3-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metilpropan-1-ona; ciclopropil-[4-(3-fluoro-4-quinolin-3-ilfenoxi)-piperidin-1-il]-metanona; 1-[4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metilpropan-1-ona; [4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-ciclopropil-metanona; 2-metil-1-[4-(3-metil-4-quinolin-3-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; 1-[4-(3-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; éster metílico del ácido 4-(3-metil-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico; 1-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona; ciclopropil-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 1-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 2-metil-1-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 3-oxo-3-[4-(4-quinolin-3-il-fenoxi)-piperidin-1 -il]-propionitrilo; 1-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[2-fluoro-4-(8-metoxi-quinolin-7-il)-fenoxi]piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-cloroquinolin-7-il)-2-fluoro-fenoxi]-piperidin-1-il}-ciclopropilmetanona; {4-[4-(8-cloroquinolin-7-il)-2-fluoro-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-cloroquinolin-7-il)-2-fluorofenoxi]-piperidin-1 -il}-propan-1 -ona; 1-{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[2-fluoro4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-(4-(4-(4-(dimetilamino)quinolin-3-il)fenoxi)piperidin-1-il)propan-1-ona; {4-[4-(4-dimetilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(4-amino-quinolin-3-il)-fenoxi]-piperldin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-metilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-metil-aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-morfolin-4-ilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-morfolin-4-il-quinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[4-(4-metilpiperazin-1-il)-quinolin-3-il]-fenoxi}-piperidin-1-il)-propan-1-ona; (4-{4-[4-(4-metilpiperazin-1-il)-quinolin-3-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 3-[4-(4-quinolin-3-ilfenoxi)-piperidina-1-carbon-il]-oxazolidin-2-ona; 1 -[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-butano-1,3-diona; 1-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-pirrolidin-2-ona; 1-[4-(4-[1,8]naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-{4-[4-(2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il} -(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(3-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(3-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo; 7-{4-[1-((R)-tetrahidrofu ran-2-carbonil)-piperidin-4-iloxi]-fenil}-quinolina-3-carbonitrilo; 7-[4-(1-ciclopropanocarbonil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo; 1 -{4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; {4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (1-hidroxiciclopro-pil)-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(1-trifluorometilciclopropil)-metanona; (1-aminociclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidina-1-carbonil}ciclopropano-carbonitrilo; (1-metilciclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ((S)-2,2-dimetilciclopro-pil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (2,2-dimetilciclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; [4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]fenoxi]-1-piperi-dil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-(8-amino-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; {4-[4-(8-metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; (4-{4-[8-(2-metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-metoxi-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; (4-{4-[8-(2-dimetilamino-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 7-[4-(1-propionilpiperidin-4-iloxi)-fenil]-quinolina-8-carbonitrilo;[4-[4-[8-(dimetilamino)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-{4-[4-(8-dimetilamino-quinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-dimetilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (4-{4-[8-(2-pirrolidin-1 -il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-pirrolidin-1-il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-propan-1 -ona; 7-[4-[[1-[(2R)-tetrahidrofuran-2-carbonil]-4 piperidil]oxi]fenil]quinolina-8-carboxamida; ácido 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carboxílico amida; ciclopropil(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)metanona; 1-(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)propan-1-ona; ciclopropil(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)metanona; (R)-(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona; 2,2,2-trifluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-etanona; 2,2-difluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; 2-fluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona; 1-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofu ran-2-ilmetanona; 1-{4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; 1-{4-[4-(3-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 1-{4-[4-(3-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(3-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona; 1-{4-[4-(1-metil-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclobutil-metanona; {4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona; 1-{4-[4-(3-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona; {4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclobutil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(3-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(3-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1 -eti lisoquinol in-6-i l )-fe n oxi ]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(1-ciclopropil-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-fluoro-7-metoxiquinolin-3-il)fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-ilmetanona; 1-{4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; {4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(3-isopropoxi-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-morfolin-4-ilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metananona; {4-[4-(1 -aminoisoquinolin-6-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-dimetilamino-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-ilmetanona; {4-[4-(1-metilamino-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(4-metilisoquinolin-6-il)-fenoxi-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-metoxiquinolin-3-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(5-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(5-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-[4-(4-isoquinolin-6-il-fenoxi)-piperidin-1-il]-metanona; [4-[4-(6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; {4-[4-(5-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1- piperidil]propan-1-ona; ciclopropil-[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1-piperidil]metanona; [4-[4-(1,4-dimetil-6-isoquinolil)-fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-[4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]propan-1-ona; ciclopropil-[4-[4-(1,5-dimetil-6-isoquinolil)-fenoxi]-1-piperidil]metanona; [4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-(8-ciclopropil-7-quinolil)fenoxi]-1 -piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; {4-[4-(3-etilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-ilmetanona; ciclopropil-{4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; 1 -{4-[4-(7-fl u o roq uinol in-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-ilmetanona; {4-[4-(3-ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-metil-quinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-metil-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2- il-metanona; 1-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(3-quinolin-3-il-fenoxi)-piperidin-1- il]-metanona; 1-(4-((4-(quinolin-7-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)-2-metilpropan-1-ona; y 2-metil-1-(4-((4-(quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona; y sales de los mismos, por ejemplo, sales farmacéuticamente aceptables de los mismos.
Los compuestos adicionales de acuerdo con la Fórmula III pueden incluir, por ejemplo: N-etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-pirrolidin-1-iletil)piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-morfolinoetil)piperidina-1-carboxamida; (4-isopropilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; (4-metilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperidil)metanona; (4-etilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxamida; N-(2-metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-2-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-(2-dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-[2-(1H-imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-tetrahidropiran-4-il-piperidina-1-carboxamida; N-ciclobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ácido 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbohidroxámico; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)metanona; N-(ciclobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxamida; azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-metanona; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida; N-etil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;3-[4-(1-metil-6-isoquinolil)-fenoxi]-N-propil-piperidina-1-carboxamida; N-isobutil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propoxipiperidina-1-carboxamida; ácido 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carbohidroxámico; N-etoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(4-metil-3-quinolil)-fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida; N-isobutil-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida; 2- amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; (2R)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona 2HCl; (2S)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona 2HCl; 2-(dimetilamino)-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-etanona; [(2R)-1-metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; [(2S)-1-metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; S-isopropil 4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carbotioato; 2-amino-2-metil-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-propan-1-ona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-pirrolidin-2-il]metanona; [4-[4-(8-metil-7quinolil)fenoxi]-1-piperidil]-[(2S)-pirrolidin-2-il]metanona; [1-(metilamino)ciclopropil]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidiljmetanona; 3-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona; 2-isopropoxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; [2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil] acetato; 2-hidroxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; (1-aminociclobutil)-[4-[4-(8-metil-7-quinolil)-fenoxi]-1-piperidil]metanona; 4-[4-(4-metil-3-quinolil)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-etilsulfanilpiperidina-1-carboxamida; 1-[4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona; N-etil-4-[4-(2-fluoro-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida y sales de los mismos, por ejemplo, sales farmacéuticamente aceptables.
Los compuestos de acuerdo con la Fórmula IV pueden incluir, por ejemplo: 2-metil-1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; 1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-fluoro-2-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(S)-tetrahidrofuran-2-il-metanona; isoxazolidin-2-il-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico metilamida; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico etilamida; N-etil-4-[4-(8-metil-7-quinolil)-fenoxi]piperidina-1-carboxamida; N,N-dimetil-4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxamida; etil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; N-metoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(8-metil-7-quinolil)fe-noxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-pirrolidin-1-il-metanona; N-metil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(1-piperidil)metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-morfolino-metanona; N-metoxi-4-[4-(8-metoxi-7-quinolil)fenoxi]piperidina-1-carboxamida; (4,4-difluorotetrahidrofuran-2-il)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; ciclopropil-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; ciclopropil-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxil}-piperidin-1-il)-metanona; 1-(4-{4-[8-(2-pirrolidin-1 -il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-propan-1 -ona; ciclopropil-(4-{4-[8-(2-pirrolidin-1 -il-etoxi)-quinolin-7-il]-fenoxi}-pipendin-1-il)-metanona; 1-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-pipendin-1-il)-propan-1-ona; ciclopropil-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona; 1-[4-[4-[8-[2-(4-metilpiperazin-1 -il)etoxi]-7-quinolil]fenoxi]-1 -piperidil]propan-1 -ona; 1-[4-[4-[8-(2-metoxietoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona; 1-[4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona; {4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-etoxi-quinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; (4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-(R)-tetrahidrofuran-2-il-metanona; (4-{4-[8-(2-pirrolidin-1-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; (4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-ilmetanona; [4-[4-[8-[2-(4-metilpiperazin-1-il)etoxi]-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-[8-(2-metoxi-etoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; [4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-[4-(2-cloro-4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona; 1-[4-(2-cloro-4-quinolin-7-il-fenoxi)-piperidin-1-il]-2-metilpropan-1-ona; 1-[4-(2-metoxi-4-quinolin-7-il-fenoxi)-piperidin-1 -il]-propan-1 -ona; 1-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-cloroquinolin-7-il)-2-fluorofenoxi]-piperidin-1-il}-ciclopropilmetanona; {4-[4-(8-cloroquinolin-7-il)-2-fluoro-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-cloroquinolin-7-il)-2-fluoro-fenoxi]piperidin-1-il}-propan-1-ona; 1-{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(2-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(4-cloroquinolin-7-il)-fenoxi]piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}ciclopropilmetanona; 1-{4-[4-(4-cloro-quinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; {4-[4-(3-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(3-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; 7-[4-(1-propionilpiperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo; 7-{4-[1 -((R)-tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-fenil}-quinolina-3-carbonitrilo; 7-[4-(1-ciclopropanocarbonil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo; 1-{4-[4-(3metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (1-hidroxiciclopropil)-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-(1-trifluorometilciclopropil)-metanona; (1-aminociclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidina-1-carbonil}-ciclopropanocarbonitrilo; (1-metilciclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ((S)-2,2-dimetil-ciclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; (2,2-dimetilciclopropil)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; [4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]-metanona; [4-[4-(8-amino-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; {4-[4-(8-metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(8-metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; (4-{4-[8-(2-metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona; (4-{4-[8-(2-dimetilaminoetilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R) -tetrahidrofuran-2-il-metanona; 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carbonitrilo; [4-[4-[8-(dimetilamino)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-{4-[4-(8-dimetilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-dimetilaminoquinolin-7-il)-fe-noxi]-piperidin-1-il}-metanona; (4-{4-[8-(2-pirrolidin-1-il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-pirrolidin-1 -il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1 -ona; 7-[4-[[1-[(2R)-tetrahidrofuran-2-carbonil]-4 piperidil]oxi]fenil]quinolina-8-carboxamida; ácido 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carboxílico amida; (S) -1-(3-(4-(quinolin-7-il)fenoxi)-pirrolidin-1-il)propan-1-ona; (R)-1-(3-(4-(quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona; 1-(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)propan-1-ona; ciclopropil(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)metanona; (R)-(4-(4-(5-metilquinolin-7-il)-fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona; (±)-(7S,8aS)-7-(4-(8-metilquinolin-7-ii)fe-noxi)hexahidroindolizin-3(2H)-ona; (±)-(7R,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona;2,2,2-trifluoro-1-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-etanona; 2,2-difluoro-1 -{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; 2-fluoro-1-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; {cis-3-fluoro-4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-ilmetanona; 1-{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {(trans)-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-(R)-tetrahidrofuran-2-il-metanona; 1-{trans-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{trans-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; 1-{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona; cidopropil-{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; [4-[4-(8-ciclopropil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona; 1-(4-((4-(quinolin-7-il)fenil)tio)piperidin-1-il)propan-1-ona; 1-(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona; y sales de los mismos, por ejemplo, sales farmacéuticamente aceptables.
Los compuestos adicionales de acuerdo con Formula IV pueden incluir por ejemplo: N-etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-pirrolidin-1-iletil)piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-morfolinoetil)piperidina-1-carboxamida; (4-isopropilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; (4-metilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperidil)metanona; (4-etilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona tosilato; N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxamida; N-(2-metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-(2-dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-[2-(1 H-imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-tetrahidropiran-4-il-piperidina-1-carboxamida; N-ciclobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ácido 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbohidroxámico; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)metanona; N-(ciclobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida; 2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; (2R)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona; (2S)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona; 2-(dimetilamino)-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-etanona; [(2R)-1-metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; [(2S)-1-metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; S-isopropil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbotioato; 2-amino-2-metil-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-propan-1-ona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-pirrolidin-2-il]metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-[(2S)-pirrolidin-2-il]metanona; [1-(metilamino)ciclopropil]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; 3-amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona; 2-isopropoxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; [2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil] acetato; 2-hidroxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona; (1-aminociclobutil)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-metanona; N-etil-4-[4-(2-fluoro-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida y sales de los mismos, por ejemplo, sales farmacéuticamente aceptables de los mismos.
Los compuestos de acuerdo con la Fórmula V o V(a) pueden incluir por ejemplo: isoxazolidin-2-il-[4-(4-quinolin-3-ilfenoxi)-piperidin-1-il]-metanona; [4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(4-cloro-quinolin-3-il)-fenoxi]-piperidin-1-il}isoxazolidin-2-il-metanona; {4-[4-(8-cloro-quinolin-7-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoxiamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoximetilamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]piperidina-1-carboxílico etilamida; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico metilamida; ácido 4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico etilamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]piperidina-1-carboxílico hidroxi amida; N-etil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N,N-dimetil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-metoxi-4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxamida; N-isopropil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-pirrolidin-1-ilmetanona; N-metil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propilpiperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(1-piperidil)metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-morfolinometanona; N-metoxi-4-[4-(8-metoxi-7-quinolil)fenoxi]piperidina-1-carboxamida; 3-[4-(4-quinolin-3-il-fenoxi)-piperidina-1 -carbonil]-oxazolidin-2-ona; 1-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-pirrolidin-2-ona; y sales de los mismos, por ejemplo, sales farmacéuticamente aceptables de los mismos.
Los compuestos adicionales de acuerdo con Formula V pueden incluir por ejemplo: N-etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-pirrolidin-1-iletil)piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-morfolinoetil)piperidina-1-carboxamida; (4-iso-propilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; (4-metil-piperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperi-dil)metanona; (4-etilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; N-etil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-etoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-metoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(8-metil-7-qui-nolil)fenoxi]piperidina-1-carboxamida; N-(2-metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-(2-dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-[2-(1H-imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-tetrahidropiran-4-il-piperidina-1-carboxamida; N-ciclobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ácido 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbohidroxámico; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)-metanona; N-(ciclobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; N-butil-4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-etilpiperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isobutil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-(2-metoxietil)-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-(ciclopropil-metil)piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopropoxi-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopropil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isobutoxi-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopentil-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-etoxi-piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carbohidroxámico ácido; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxi-piperidina-1-carboxamida; 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-etil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propil-piperidina-1-carboxamida; N-isobutil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propoxipiperidina-1-carboxamida; ácido 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carbohidroxámico; N-etoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(4-metil-3-quinolil)-fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propoxipiperidina-1-carboxamida; N-isobutil-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida; N-etil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(3-piridil)-piperidina-1-carboxamida; N-(2-metoxietil)-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-piperidina-1-carboxamida; [4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-1-piperidil]-(4-metilpiperazin-1-il)metanona; N,N-dimetil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isobutoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-isopropil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-piperidina-1-carboxamida; 4-[4-(5-metilimida-zo[1,2-a]piridin-6-il)fenoxi]-N-(1-metilpirazol-4-il)piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]-piridin-6-il)fenoxi]-N-(2,2,2-trifluoroetil)piperidina-1-carboxamida; 4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxi-piperidina-1-carboxamida; N-etoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-metoxi-4-[4-(5-metilimidazo[1,2a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carbohidroxámico; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; N-etil-4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxamida; N-etil-4-[4-(8-metil-imidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]-N-propil-piperidina-1-carboxamida; N-isobutil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(7-metil-pirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; ácido 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carbohidroxámico; N,N-dimetil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-piperidina-1-carboxamida; [4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]-pirrolidin-1 -il-metanona; [(3S)-3-fluoropirrolidin-1 -il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1 -piperidil]metanona; [(3R)-3-fluoropirrolidin-1-il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]metanona; 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida; N-etilsulfanil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-etilsulfanil-piperidina-1-carboxamida; 1-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona; 1-[4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona; 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-N-propilpiperidina-1-carboxamida; N-etil-4-[4-(2-fluoro-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida y sales de los mismos, por ejemplo, sales farmacéuticamente aceptables de los mismos.
Los compuestos adicionales de acuerdo con Formula V(a) pueden incluir, por ejemplo: N-etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-pirrolidin-1-iletil)piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-morfolinoetil)piperidina-1-carboxamida; (4-iso-propilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; (4-metil-piperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperidil)metanona; (4-etilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-(2-metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-(2-dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; N-[2-(1H-imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxi]-N-tetrahidropiran-4-il-piperidina-1-carboxamida; N-ciclobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ácido 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbohidroxámico; [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)metanona; N-(ciclobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; 4-[4-(8-metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida; N-etil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propil-piperidina-1-carboxamida; N-isobutil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-(ciclopropilmetil)-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propoxipiperidina-1-carboxamida; ácido 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carbohidroxámico; N-etoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida; N-etoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; N-isopropoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propoxipiperidina-1-carboxamida; N-isobutil-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida; 4-[4-(4-metil-3-quinolil)fenoxi]-N-etilsulfanil-piperidina-1-carboxamida, 1-[4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona; N-etil-4-[4-(2-fluoro-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida y sales de los mismos, por ejemplo, sales farmacéuticamente aceptables de los mismos.
Los siguientes términos y expresiones tienen los significados que se describen a continuación.
Como se usa en la presente memoria, el término "aproximadamente" se refiere a un intervalo de valores de ± 10 % de un valor especificado. Por ejemplo, se entenderá que la frase "aproximadamente 50" incluye ± 10 % de 50, o de 45 a 55. La frase "de aproximadamente 10 a 100" incluye ± 10 % de 10 y ± 10 % de 100, o de 9 a 110.
Como se usa en la presente memoria, un rango de valores enteros en la forma "x-y" o "x a y" o "x hasta y", incluye los números enteros x e y, e incluye todos los números enteros entre x e y. Por ejemplo, las expresiones "1-6" o "1 a 6" o "1 hasta 6" pretenden incluir los números enteros 1, 2, 3, 4, 5 y 6. Las modalidades preferidas incluyen cada número entero individual en el intervalo, así como cualquier subcombinación de números enteros. Por ejemplo, los números enteros preferidos para la expresión "1-6" pueden incluir 1,2, 3, 4, 5, 6, 1-2, 1-3, 1-4, 1-5, 2-3, 2-4, 2-5, 2-6, etc.
El término "acilo" significa un radical de fórmula general -C(=O)R, en donde -R es hidrógeno o hidrocarbilo. Los ejemplos incluyen, acetilo (-C(=O)CH3), propionilo (-C(=O) CH2 CH3 ), benzoílo (-C(=O)C6Hs) y fenilacetilo (-C(=O)CH2C6H5).
El término "alquilo", por sí mismo o como parte de otro sustituyente significa, un radical hidrocarbonado de cadena lineal, ramificada o cíclica, que incluye radicales di y multirradicales, que tiene el número de átomos de carbono designado (es decir, C1-C6 designa un grupo alquilo que tiene de uno a seis carbonos), e incluye grupos de cadena lineal, ramificada o cíclicos. Los ejemplos de grupos alquilo incluyen: metilo, etilo, propilo, isopropilo, butilo, isobutilo,
terc-butilo, pentilo, neopentilo, hexilo, ciclohexilo y ciclopropilmetilo.
El término "alquileno", por sí mismo o como parte de otro sustituyente, significa un radical hidrocarbonado divalente de cadena lineal, ramificada o cíclica que tiene el número indicado de átomos de carbono. Por ejemplo, -(C1-C3 )-alquileno-CO2 H, incluiría, por ejemplo, CH2 CH2 CH2-CO2 H, -CH2CH(CH3)-CO2H, -C(CH3)2-CO2H, -ciclopropil-CO2 H, y -CH(CH3)-CH2-CO2H.
El término "alcoxi", empleado solo o en combinación con otros términos, significa un grupo alquilo que tiene el número designado de átomos de carbono, como se definió anteriormente, conectado al resto de la molécula a través de un átomo de oxígeno, tal como, por ejemplo, metoxi, etoxi, 1-propoxi, 2-propoxi (isopropoxi) y los homólogos e isómeros superiores.
El término "alquenilo", empleado solo o en combinación con otros términos, significa un radical hidrocarbonado estable monoinsaturado o diinsaturado de cadena lineal, cadena ramificada o grupo hidrocarbonado cíclico que tiene el número indicado de átomos de carbono. Los ejemplos incluyen vinilo, propenilo(alilo), crotilo, isopentenilo, butadienilo, 1,3-pentadienilo, 1,4-pentadienilo, ciclopentenilo, ciclopentadienilo y los homólogos e isómeros superiores. Un radical divalente derivado de un alqueno se ejemplifica mediante -CH=CH-CH2-.
El término "amina" o "amino" se refiere a radicales de fórmula general -NRR', en donde R y R' se seleccionan independientemente de hidrógeno y un radical hidrocarbilo, o en donde R y R' combinados forman un heterociclo. Ejemplos de grupos amino incluyen:
-NH2 , metilamino, dietilamino, anilino, bencilamino, piperidin-1-ilo, piperazin-1-ilo y indolin-1-ilo.
El término "carbamilo" significa el grupo -C(=O)NRR', en donde R y R' se seleccionan independientemente de hidrógeno y un radical hidrocarbilo, o en donde R y R 'combinados forman un heterocilo. Los ejemplos de grupos carbamilo incluyen: -C(=O)NH2 y -C(=O) N(CH3 )2.
El término "cicloalquilo" se refiere a radicales alquilo que contienen uno o más anillos, por ejemplo, grupos cicloalquilo C3 a C10 , por ejemplo, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, cicloheptilo, norbornilo, y octahidro-1H-indenilo.
El término "heteroalquilo" por sí mismo o en combinación con otro término, significa un radical de cadena lineal o ramificada estable que consiste en el número indicado de átomos de carbono y uno o dos heteroátomos seleccionados entre O, N y S, y en donde los átomos de nitrógeno y azufre pueden oxidarse opcionalmente y el heteroátomo de nitrógeno puede cuaternizarse opcionalmente. El(Los) heteroátomo(s) puede colocarse en cualquier posición del grupo heteroalquilo, incluso entre el resto del grupo heteroalquilo y el fragmento al que está unido, así como también unido al átomo de carbono más distal del grupo heteroalquilo. Los ejemplos incluyen: -O-CH2-CH2-CH3 , -CH2-CH2 CH2-OH, -CH2-CH2 -NH-CH3 , -CH2 -S-CH2-CH3 , y-CH2CH2-S(=O)-CH3. Hasta dos heteroátomos pueden ser consecutivos, como, por ejemplo, -CH2 -NH-OCH3 (en donde uno o los dos heteroátomos consecutivos también pueden ser S (SO o SO2 ) oxidado o N (NO) oxidado).
El término "heteroalquenilo", por sí mismo o en combinación con otro término, significa un radical hidrocarbonado mono o diinsaturado de cadena lineal o ramificada estable que consta del número indicado de átomos de carbono y uno o dos heteroátomos seleccionados de O, N y S, y en donde los átomos de nitrógeno y azufre pueden opcionalmente oxidarse y el heteroátomo de nitrógeno opcionalmente puede estar cuaternizado. Pueden colocarse hasta dos heteroátomos consecutivamente. Los ejemplos incluyen - c H=CH-O-CH3, -CH=CH-CH2-OH, -CH2 -CH=N-OCH3 , -CH=CH-N(CH3 )-CH3 , y -CH2 -CH=CH-CH2-SH.
El término "hidroxialquilo" se refiere a un subconjunto de grupos heteroalquilo que es un radical alquilo en donde uno o más de los átomos de carbono está sustituido con hidroxi. Los ejemplos incluyen -CH2CH(OH)CH3 y -CH2 CH2 OH.
Los términos "halo" o "halógeno" por sí mismos o como parte de otro sustituyente significan un átomo de flúor, cloro, bromo o yodo.
El término "haloalquilo" se refiere a un grupo C 1-C6 alquilo en donde uno o más de los átomos de carbono está sustituido con uno o más átomos de halógeno. Los grupos haloalquilo preferidos son los grupos C 1-C4 alquilo en los que uno o más de los átomos de carbono está sustituido con uno o más átomos de halógeno. El grupo alquilo puede ser un grupo alquilo lineal, ramificado o cíclico. El átomo de halógeno es uno o más de flúor, cloro, bromo y yodo. Ejemplos de grupos haloalquilo incluyen trifluorometilo, 2,2,2-trifluoroetilo, 2,2,2-tricloroetilo y 2-cloroetilo.
El término "sulfamilo" significa el grupo -SO2 NRR', en donde R y R' se seleccionan independientemente de hidrógeno o un radical hidrocarbilo, o en donde R y R' combinados forman un heterociclo. Los ejemplos de grupos sulfamilo incluyen: -SO2 NH2 , -SO2N(CH3)2, -SO2(pirrol-1-ilo) y -SO2 NH(C6 Hs).
El término "aromático" se refiere a un carbociclo o heterociclo que tiene uno o más anillos poliinsaturados que tienen un carácter aromático (electrones (pi) n deslocalizados (4n 2)).
El término "arilo", empleado solo o en combinación con otros términos, significa un sistema aromático carbocíclico que contiene uno o más anillos (típicamente uno, dos o tres anillos) en donde dichos anillos pueden unirse de manera colgante, como un bifenilo, o pueden fundirse, como naftaleno. Los ejemplos incluyen fenilo; antracilo; y naftilo.
El término "heterociclo" o "heterociclilo" o "heterocíclico", por sí mismo o como parte de otro sustituyente significa, un sistema de anillo heterocíclico mono o multicíclico, estable, no sustituido o sustituido que consiste en átomos de carbono y al menos un heteroátomo seleccionado de N, O y S, y en donde los heteroátomos de nitrógeno y azufre pueden oxidarse opcionalmente, y el átomo de nitrógeno puede estar opcionalmente cuaternizado. El sistema heterocíclico puede estar unido, a menos que se indique lo contrario, en cualquier heteroátomo o átomo de carbono que proporcione una estructura estable.
Como se usa en la presente memoria, "estructura estable" o "compuesto estable" se refiere a un compuesto que es suficientemente robusto para sobrevivir al aislamiento hasta un grado útil de pureza de una mezcla de reacción. Los compuestos de acuerdo con la presente invención son compuestos estables.
El término "heteroarilo" o "heteroaromático" se refiere a un heterociclo que tiene carácter aromático.
Ejemplos de heterociclos no aromáticos incluyen grupos monocíclicos tales como: aziridina, oxirano, tiirano, azetidina, oxetano, tietano, pirrolidina, pirrolina, imidazolina, pirazolidina, dioxolano, sulfolano, 2,3-dihidrofurano, 2,5-dihidrofurano, tetrahidrofurano, tiofano, piperidina, 1,2,3,6-tetrahidropiridina, 1,4-dihidropiridina, piperazina, morfolina, tiomorfolina, pirano, 2,3-dihidropirano, tetrahidropirano, 1,4-dioxano, 1,3-dioxano, homopiperazina, homopiperidina, 1,3-dioxepano, 4,7-dihidro-1,3-dioxepina y óxido de hexametileno.
Los ejemplos de grupos heteroarilo incluyen: piridilo, pirazinilo, pirimidinilo, particularmente 2- y 4-pirimidilo, piridazinilo, tienilo, furilo, pirrolilo, particularmente 2-pirrolilo, imidazolilo, tiazolilo, oxazolilo, pirazolilo, particularmente 3- y 5-pirazolilo, isotiazolilo, 1,2,3-traizolilo, 1,2,4-triazolilo, 1,3,4-triazolilo, tetrazolilo, 1,2,3-tiadiazolilo, 1,2,3-oxadiazolilo, 1,3,4-tiadiazolilo y 1,3,4-oxadiazolilo.
Los ejemplos de heterociclos policíclicos incluyen: heterociclos bicíclicos, tales como, Indolilo, particularmente 3-, 4-, 5-, 6- y 7-indolilo, indolinilo, quinolilo, tetrahidroquinolilo, isoquinolilo, particularmente 1- y 5-isoquinolilo, tetrahidroisoquinolilo, cinolinilo, quinoxalinilo, particularmente 2- y 5-quinoxalinilo, quinazolinilo, 1,4-benzodioxanilo, cumarina, dihidrocumarina, benzofurilo, particularmente 3-, 4-, 5-, 6- y 7-benzofurilo, 2,3-dihidrobenzofurilo, 1, 2-benzoisoxazolilo, benzotienilo, particularmente 3-, 4-, 5-, 6- y 7-benzotienilo, benzoxazolilo, benzotiazolilo, particularmente 2-benzotiazolilo y 5-benzotiazolilo, purinilo, bencimidazolilo, particularmente 2-bencimidazolilo, benzotriazolilo, tioxantinilo, carbazolilo, carbolinilo, acridinilo, pirrolizidinilo y quinolizidinilo. Los heterociclos policíclicos también incluyen heterociclos tricíclicos y otros heterociclos policíclicos tales como dibenzofurano y benzofuro[2,3-b]piridina.
Se pretende que la lista antes mencionada de restos de heterociclilos y heteroarilos sea representativa, no limitante.
El término "hidrocarbilo" se refiere a cualquier resto que comprenda solo átomos de hidrógeno y carbono. Por ejemplo, el término (C1-C7 ) hidrocarbilo incluiría grupos hidrocarbonados, tales como grupos alquilo y cicloalquilo(C1-C7), grupos alquenilo y cicloalquenilo (C1-C7 ), grupos alquinilo y cicloalquinilo (C1-C7 ), y arilo, por ejemplo, grupos bencilo y tolilo.
Como se usa en la presente memoria, el término "sustituido" se refiere en general a uno o más átomos de hidrógeno en el átomo indicado (preferentemente un átomo de carbono) que se reemplaza con un grupo seleccionado al que se hace referencia en la presente memoria como un "sustituyente", siempre que la valencia del átomo sustituido no se exceda, y que la sustitución de como resultado un compuesto estable. Un grupo sustituido tiene de 1 a 5, preferentemente de 1 a 3, y con mayor preferencia 1 sustituyentes seleccionados independientemente. Los posibles sustituyentes incluyen, pero no se limitan a, halógenos, -OH, -OR, -NR2 , -NHOH, -NO2 , -CN, -CF3 , -CF2 CF3 , -C1-C7 hidrocarbilo, -C1-C6 alcoxi, heterociclilo de 3 a 7 miembros, heteroarilo de 3 a 7 miembros, =O, =S, -C(=O)R, -COOH, -CO2 R, -OC(=O)R, -C(=O)NRR', -NRC(=O)R', -NRCO2 R', -OC(=O)NRR', -NRC(=O)NRR', -NRC(=S)NRR' y -SO2 NRR', en donde R y R' son cada uno independientemente -H, -C1-C7 hidrocarbilo (por ejemplo, -C1-C6 alquilo, -C2 -C6 alquenilo, -C3 -C6 cicloalquilo, bencilo o fenilo) o (C1-C7 ) acilo.
Cuando un sustituyente es un grupo alquilo o alcoxi, la cadena de carbono puede ser ramificada, lineal o cíclica, prefiriéndose la lineal.
Por consiguiente, el término "hidrocarbilo sustituido" se refiere a: un grupo hidrocarbilo como se define anteriormente, que tiene 1,2, 3, 4 o 5 sustituyentes, seleccionados independientemente de la selección proporcionada en la definición del término "sustituyente" en la presente memoria. De manera similar, las expresiones "alquilo sustituido", "cicloalquilo sustituido", "alquenilo sustituido", "alquinilo sustituido", "arilo sustituido", "bencilo sustituido", etc. se refieren al grupo especificado (por ejemplo, alquilo) como se define en la presente memoria que tiene 1, 2, 3, 4 o 5 sustituyentes, seleccionados independientemente de la selección proporcionada en la definición del término "sustituyente" en la presente memoria.
Como se usa en la presente memoria, el término "sujeto" se refiere a un animal de sangre caliente tal como un mamífero, preferentemente un ser humano, que está afectado o tiene el potencial de estar afectado por una o más enfermedades y afecciones descritas en la presente memoria.
Como se usa en la presente memoria, una "cantidad terapéuticamente eficaz" se refiere a una cantidad de un compuesto de la presente invención que es eficaz para tratar o prevenir los síntomas de un trastorno particular. Dichos trastornos incluyen, pero no se limitan a; aquellos trastornos patológicos y neurológicos asociados con la actividad aberrante de los receptores descritos en la presente memoria, en los que el tratamiento o la prevención comprenden inhibir la actividad de los mismos poniendo en contacto el receptor con un compuesto de la presente invención.
Como se usa en la presente memoria, el término "farmacéuticamente aceptable" se refiere a aquellos compuestos, materiales, composiciones y /o formas de administración que, dentro del alcance del juicio médico, son adecuadas para el contacto con los tejidos de seres humanos y animales sin una toxicidad, irritación, respuesta alérgica u otras complicaciones excesivas acordes del problema con una relación beneficio /riesgo razonable. El término "sal farmacéuticamente aceptable" se refiere a sales de compuestos de la presente invención que pueden derivarse de la combinación de dichos compuestos con sales de adición de ácidos o bases no tóxicas.
Las sales de adición de ácido incluyen ácidos inorgánicos tales como ácido clorhídrico, bromhídrico, yodhídrico, sulfúrico, nítrico y fosfórico, así como ácidos orgánicos tales como acético, cítrico, propiónico, trifluoroacético, tartárico, glutámico, salicílico, oxálico, metanosulfónico, bencenosulfónico, ácido paratoluensulfónico, succínico y benzoico, y ácidos orgánicos e inorgánicos relacionados.
Las sales de adición de bases incluyen aquellas derivadas de bases inorgánicas tales como hidróxidos, carbonatos y bicarbonatos de amonio y de metales alcalinos y alcalinotérreos, así como sales derivadas de aminas orgánicas básicas tales como aminas alifáticas y aromáticas, diaminas alifáticas e hidroxiaminas. Tales bases útiles para preparar las sales de esta invención incluyen, por ejemplo, hidróxido de amonio, carbonato de potasio, bicarbonato de sodio, hidróxido de calcio, metilamina, dietilamina, etilendiamina, ciclohexilamina, diisopropiletilamina (DIPEA), etanolamina.
Además de las sales farmacéuticamente aceptables, se incluyen otras sales en la invención. Pueden servir como productos intermedios en la purificación de los compuestos, en la preparación de otras sales o en la identificación y caracterización de los compuestos o productos intermedios.
Las sales farmacéuticamente aceptables de los compuestos de la presente invención también pueden existir como varios solvatos, tales como agua, metanol, etanol, dimetilformamida, acetato de etilo y THF. También pueden prepararse mezclas de tales solvatos. La fuente de tal solvato puede ser del disolvente de cristalización, inherente al disolvente de preparación o cristalización, o accidental a tal disolvente. Dichos solvatos están dentro del alcance de la presente invención.
Se entenderá que los compuestos de la presente invención pueden existir en diversas formas estereoisoméricas. Como tales, los compuestos de la presente invención incluyen tanto diastereómeros como enantiómeros. Los compuestos pueden prepararse como racematos y pueden usarse convenientemente como tales. Sin embargo, los enantiómeros individuales pueden aislarse mediante resolución o separación quiral de un racemato, o pueden sintetizarse mediante técnicas convencionales si así se desea. Dichos racematos y enantiómeros individuales y mezclas de los mismos forman parte de la presente invención.
Se conoce en la técnica cómo preparar y aislar tales formas ópticamente activas. Los estereoisómeros específicos pueden prepararse mediante síntesis estereoespecífica usando materiales de partida puros o enriquecidos enantioméricamente. Los estereoisómeros específicos de los materiales de partida o de los productos pueden resolverse y recuperar mediante técnicas conocidas en la técnica, tales como resolución de formas racémicas, cromatografía normal, de fase inversa, quiral, recristalización, resolución enzimática o recristalización fraccionada de sales de adición formadas por reactivos usados para tal fin. Métodos útiles para resolver y recuperar estereoisómeros específicos descritos en Eliel, E. L.; Wilen, S. H. Stereochemistry of Organic Compounds; Wiley: New York, 1994, and Jacques, J, et al. Enantiomers, Racemates, and Resolutions; Wiley: New York, 1981.
Se reconoce además que los grupos funcionales presentes en los intermedios usados para la síntesis de los compuestos de Fórmula I pueden contener grupos protectores. Por ejemplo, los sustituyentes de la cadena lateral de aminoácidos de los compuestos de Fórmula I pueden estar sustituidos con grupos protectores tales como grupos benciloxicarbonilo o t-butoxicarbonilo. Los grupos protectores se conocen per se como grupos funcionales químicos que pueden unirse selectivamente y eliminar de funcionalidades, tales como grupos hidroxilo y grupos carboxilo. Estos grupos están presentes en un compuesto químico para convertir dicha funcionalidad en inerte a las condiciones de reacción química a las que está expuesto el compuesto. Puede emplearse cualquiera de una variedad de grupos protectores con la presente invención. Los grupos preferidos para proteger lactamas incluyen grupos sililo tales como los grupos t-butildimetilsililo ("TBDMS"), dimetoxibenzhidrilo ("DMB"), acilo, bencilo ("Bn"), metoxibencilo y dimetoxi (por ejemplo, 2-4-dimetoxi) bencilo. Los grupos preferidos para proteger grupos hidroxi incluyen TBS, acilo, bencilo, benciloxicarbonilo ("CBZ"), t-butiloxicarbonilo ("Boc") y metoximetilo. Muchos otros grupos protectores estándar
empleados por un experto en la técnica pueden encontrarse en Greene, TW y Wuts, PGM, "Protective Groups in Organic Synthesis" 2da Edición, Wiley & Sons, 1991.
Los compuestos descritos en la presente memoria también pretenden incluir compuestos en los que las estructuras moleculares incluyen isótopos de átomos en la estructura química, por ejemplo, carbono, hidrógeno, nitrógeno, azufre y otros átomos que se encuentran en esas estructuras. Los isótopos incluyen aquellos átomos que tienen el mismo número atómico pero diferentes números de masa. Por ejemplo, los isótopos de hidrógeno incluyen deuterio; los isótopos de carbono incluyen 13C; los isótopos de nitrógeno incluyen 15N; e isótopos de azufre incluyen 33S.
En consecuencia, dentro de la estructura química de cualquier compuesto que se enseña en esta aplicación:
• cualquier átomo de hidrógeno o grupo de átomos de hidrógeno, por ejemplo, en un grupo hidrocarbilo, heteroalquilo, arilo, heteroarilo, heterociclilo o carbociclilo, podría sustituirse adecuadamente por un isótopo de hidrógeno, es decir, deuterio;
• cualquier átomo de carbono o grupo de átomos de carbono, por ejemplo, en un grupo hidrocarbilo, heteroalquilo, arilo, heteroarilo, heterociclilo o carbociclilo, podría sustituirse adecuadamente por un isótopo de carbono, por ejemplo, 13C;
• cualquier átomo de nitrógeno o grupo de átomos de nitrógeno, por ejemplo, en un grupo heteroalquilo, heteroarilo o heterociclilo, podría sustituirse adecuadamente por un isótopo de nitrógeno, por ejemplo, 15N; y • cualquier átomo de azufre o grupo de átomos de azufre, por ejemplo, en un grupo heteroalquilo, heteroarilo o heterociclilo, podría sustituirse adecuadamente por un isótopo de azufre, por ejemplo, 33S.
Como se usa en la presente memoria, un compuesto que se denomina "enriquecido isotópicamente" significa que la abundancia, por ejemplo, de deuterio, 13C, 15N o 33S en cualquier sitio relevante del compuesto es sustancialmente mayor que la abundancia de deuterio, 13C, o 15N o 33S que se encuentran naturalmente en ese sitio en una cantidad del compuesto. Un sitio relevante en un compuesto como se usó anteriormente es un sitio que se designaría como "H" o "C" o "N" o "S" en una representación de la estructura química del compuesto cuando no está enriquecido. Los sitios relevantes en la estructura química de los compuestos enseñados en la presente memoria para el reemplazo isotópico de un átomo o átomos pueden incluir cualquier sitio que sea sintéticamente accesible para dicho reemplazo isotópico. La expresión "de origen natural", como se usa anteriormente, se refiere a la abundancia del átomo particular que estaría presente en un sitio relevante en un compuesto si el compuesto se preparara sin ninguna etapa de síntesis afirmativa para enriquecer la abundancia de un isótopo diferente.
Así, por ejemplo, en un compuesto "enriquecido con deuterio", la abundancia de deuterio en cualquier sitio relevante en la estructura química puede variar desde una cantidad que es sustancialmente mayor que la abundancia natural de deuterio (aproximadamente 0,0115%) hasta el 100%, por ejemplo, desde aproximadamente el 1% hasta aproximadamente el 100%, o desde aproximadamente el 10% hasta aproximadamente el 100%, o desde aproximadamente el 50% hasta aproximadamente el 100%, o desde aproximadamente el 90% hasta aproximadamente el 100%.
De manera similar, para un compuesto "enriquecido con 13C", la abundancia de 13C en cualquier sitio relevante en la estructura química del compuesto puede variar desde una cantidad que es sustancialmente más que la abundancia natural de 13C (aproximadamente 1,109%) o todavía mayor hasta el 100%, por ejemplo, desde aproximadamente el 5% hasta aproximadamente el 100%, o desde aproximadamente el 10% hasta aproximadamente el 100%, o desde aproximadamente el 50% hasta aproximadamente el 100%, o desde aproximadamente el 90% hasta aproximadamente el 100%. De manera similar, para un compuesto "enriquecido con 15N", la abundancia de 15N en cualquier sitio relevante en la estructura química del compuesto puede variar desde una cantidad que es sustancialmente mayor que la abundancia natural de 15N (aproximadamente 0,364%) o todavía mayor hasta el 100%, por ejemplo, desde aproximadamente el 1% hasta aproximadamente el 100%, o desde aproximadamente el 10% hasta aproximadamente el 100%, o desde aproximadamente el 50% hasta aproximadamente el 100%, o desde aproximadamente el 90% hasta aproximadamente el 100%.
Los compuestos enriquecidos isotópicamente pueden prepararse generalmente mediante técnicas convencionales conocidas por los expertos en la técnica. Dichos compuestos enriquecidos isotópicamente también pueden prepararse adaptando procesos convencionales como se describe en la literatura científica para la síntesis de compuestos descritos en la presente memoria, y usando un reactivo (o reactivos) isotópicamente sustituido apropiado en lugar del correspondiente reactivo no isotópicamente sustituido(s) empleado en la síntesis convencional de los compuestos no enriquecidos isotópicamente. Los ejemplos de formas de obtener un compuesto enriquecido en deuterio incluyen intercambiar hidrógeno con deuterio o sintetizar el compuesto con materiales de partida enriquecidos en deuterio.
Como se usa en la presente memoria, el término "dosis unitaria" se refiere a una dosis única que es capaz de administrarse a un paciente, y que puede manipularse y empaquetarse fácilmente, permaneciendo como una dosis unitaria física y químicamente estable que comprende el compuesto activo en sí, o como una composición farmacéuticamente aceptable, como se describe en la presente memoria.
Se entenderá que todos los demás términos que se usan aquí en la descripción de la presente invención tienen significados que se entenderían y aceptarían en la técnica.
Con fines terapéuticos, los compuestos que se describen en la presente memoria pueden administrarse a un sujeto por cualquier medio que dé como resultado el contacto del agente activo con el sitio de acción del agente en el cuerpo del sujeto. Los compuestos pueden administrarse mediante cualquier medio convencional disponible para su uso junto con productos farmacéuticos, ya sea como agentes terapéuticos individuales o en combinación con otros agentes terapéuticos. Los compuestos se administran preferentemente en cantidades terapéuticamente eficaces para el tratamiento de las enfermedades y trastornos descritos en la presente memoria a un sujeto que lo necesite.
Una cantidad terapéuticamente eficaz de un compuesto como se describe en la presente memoria puede determinarse fácilmente por un diagnosticador asistente, como un experto en la técnica, mediante el uso de técnicas convencionales. La dosis eficaz variará dependiendo de varios factores, incluido el tipo de enfermedad o trastorno tratado, el grado de progresión de la enfermedad o trastorno, el estado general de salud del sujeto a tratar, la eficacia biológica relativa del compuesto seleccionado, la formulación del agente activo y la vía de administración usada en el tratamiento. Normalmente, los compuestos se administran inicialmente a niveles de administración más bajos, con un aumento gradual hasta que se obtiene el efecto terapéutico deseado.
Los intervalos de dosis típicos pueden ser de aproximadamente 0,01 mg /kg a aproximadamente 100 mg /kg de peso corporal por día, o de aproximadamente 0,01 mg /kg a 10 mg /kg de peso corporal por día. Las dosis diarias para humanos adultos pueden incluir aproximadamente 25, 50, 100 y 200 mg, y una dosis equivalente en un niño humano. Los compuestos pueden administrarse en una o más formas de dosis unitarias. La dosis unitaria puede variar de aproximadamente 1 a aproximadamente 500 mg administrados de una a cuatro veces al día, por ejemplo, de aproximadamente 10 mg a aproximadamente 300 mg, administrados dos veces al día. En un método alternativo para describir una dosis eficaz, una dosis unitaria oral es aquella que es necesaria para lograr un nivel terapéutico en suero sanguíneo, por ejemplo, un nivel en suero sanguíneo de aproximadamente 0,05 a 20 microgramos /ml en un sujeto, o aproximadamente 1 a 20 microgramos /ml. Los compuestos descritos en la presente memoria pueden administrarse como productos químicos puros; sin embargo, es preferible administrar el ingrediente activo como una composición farmacéutica.
Generalmente, los compuestos descritos en la presente memoria pueden administrarse a un paciente solos o en combinación con un portador farmacéuticamente aceptable. En consecuencia, los compuestos de la invención, por ejemplo, los compuestos de Fórmula I-V(a), se combinan preferentemente con un portador farmacéutico seleccionado sobre la base de la vía de administración elegida y la práctica farmacéutica estándar, como se describe, por ejemplo, en Remington's Pharmaceutical Sciences (Mack Publishing Co., Easton, Pensilvania, 1980). El (los) portador(s) deben ser aceptables en el sentido de ser compatibles con los otros ingredientes de la composición y no perjudiciales para el sujeto. Las proporciones relativas de ingrediente activo y portador pueden determinarse, por ejemplo, por la solubilidad y la naturaleza química de los compuestos, la vía de administración elegida y la práctica farmacéutica estándar.
Los compuestos descritos en la presente memoria pueden formularse en composiciones farmacéuticas mezclándolos con uno o más excipientes farmacéuticamente aceptables. Los excipientes pueden seleccionarse basándose en la vía de administración elegida y la práctica farmacéutica estándar, como se describe, por ejemplo, en Remington: The Science and Practice of Pharmacy, 20a Edición; Gennaro, AR, Ed.; Lippincott Williams y Wilkins: Filadelfia, Pensilvania, 2000. Las composiciones pueden formularse para controlar y /o retrasar la liberación del agente o agentes activos, como en formulaciones de disolución rápida, liberación modificada o liberación sostenida.
De acuerdo con algunas modalidades de la invención, una composición farmacéutica de la presente memoria puede contener tanto una cantidad de un inhibidor de FASN que tiene una estructura química como se describe en la presente memoria, como una cantidad de un agente antipsicótico. Los agentes antipsicóticos adecuados para tal composición farmacéutica de doble API incluyen, por ejemplo, clozapina, risperidona, aripiprazol, olanzapina, quetiapina y ziprasidona. Una composición farmacéutica de API dual de este tipo puede contener, por ejemplo, por unidad de administración, de aproximadamente 5 a aproximadamente 1000 mg, o más, de un inhibidor de FASN que tiene una estructura química como se describe en la presente memoria, y de aproximadamente 5 a aproximadamente 1000 mg de un agente antipsicótico. En tal modalidad, no es necesario que cada unidad de administración individual incluya una cantidad eficaz siempre que la cantidad total de fármaco administrada a un paciente sea una cantidad eficaz de cada una. Por tanto, por ejemplo, un paciente puede necesitar dos o más unidades de administración únicas para recibir cantidades eficaces de ambos agentes. La dosis puede ajustarse de manera apropiada para lograr los niveles de fármaco deseados, local o sistémicamente de ambos fármacos.
Las composiciones pueden prepararse para su administración por vía oral; medios parenterales, incluidas las vías intravenosa, intramuscular y subcutánea; medios tópicos o transdérmicos; medios transmucosos, incluidas las vías rectal, vaginal, sublingual y bucal; medios oftálmicos; o medios de inhalación. Preferentemente, las composiciones se preparan para administración oral, particularmente en forma de comprimidos, cápsulas o jarabes; para administración parenteral, particularmente en forma de soluciones, suspensiones o emulsiones líquidas; para administración intranasal, particularmente en forma de polvos, gotas nasales o aerosoles; o para administración tópica, como cremas,
ungüentos, soluciones, suspensiones, aerosoles, polvos.
Para la administración oral, por ejemplo, tabletas, píldoras, polvos, cápsulas y trociscos, las formulaciones pueden contener uno o más de los siguientes: diluyentes o cargas tales como almidón o celulosa; aglutinantes tales como celulosa microcristalina, gelatinas o polivinilpirrolidonas; desintegrantes tales como almidón o derivados de celulosa; lubricantes como talco o estearato de magnesio; deslizantes tales como dióxido de silicio coloidal; agentes edulcorantes como sacarosa o sacarina; y agentes aromatizantes tales como aroma de menta o cereza. Las cápsulas pueden contener cualquiera de los excipientes enumerados anteriormente y, además, pueden contener un portador semisólido o líquido, como un polietilenglicol. Las formas sólidas de administración oral pueden tener revestimientos de azúcar, goma laca o agentes entéricos. Las preparaciones líquidas pueden estar en forma de suspensiones, soluciones, emulsiones, jarabes, elixires, etc. acuosas u oleosas, o pueden presentarse como un producto seco para reconstituir con agua u otro portador adecuado antes de su uso. Tales preparaciones líquidas pueden contener aditivos convencionales tales como tensioactivos, agentes de suspensión, agentes emulsionantes, diluyentes, agentes edulcorantes y aromatizantes, colorantes y conservantes.
Las composiciones también pueden administrarse por vía parenteral. Las formas farmacéuticas aceptables para uso inyectable incluyen, por ejemplo, soluciones o suspensiones acuosas estériles. Los portadores acuosos incluyen, por ejemplo, mezclas de alcoholes y agua y medios tamponados. Los disolventes no acuosos incluyen, por ejemplo, alcoholes y glicoles, tales como etanol y polietilenglicoles; aceites, como aceites vegetales; ácidos grasos y ésteres de ácidos grasos. Pueden añadirse otros componentes, incluidos tensioactivos; como hidroxipropilcelulosa; agentes isotónicos, como cloruro de sodio; reabastecedores de fluidos y nutrientes; rellenadores de electrolitos; agentes que controlan la liberación de los compuestos activos, tales como monoestearato de aluminio y varios copolímeros; y agentes antibacterianos, como clorobutanol o fenol; tampones. Las preparaciones parenterales pueden incluirse en ampollas, jeringas desechables o viales de dosis múltiples. Otros sistemas de administración parenteral potencialmente útiles para los compuestos activos incluyen partículas de copolímero de etileno-acetato de vinilo, bombas osmóticas, sistemas de infusión implantables y liposomas.
Otros posibles modos de administración incluyen formulaciones para inhalación, que incluyen medios tales como polvo seco, aerosol o gotas. Las formulaciones para uso tópico se encuentran en forma de pomada, crema o gel. Normalmente, estas formas incluyen un portador, como vaselina, lanolina, alcohol estearílico, polietilenglicoles o sus combinaciones, y un agente emulsionante, como lauril sulfato de sodio, o un agente gelificante, como tragacanto. Las formulaciones adecuadas para la administración transdérmica pueden presentarse como parches discretos, como en un sistema de reservorio o microdepósito, sistema de difusión controlada de adhesivo o un sistema de tipo dispersión de matriz. Las formulaciones para administración bucal incluyen, por ejemplo, grageas o pastillas y también pueden incluir una base aromatizada, como sacarosa o goma arábiga, y otros excipientes como glicocolato. Las formulaciones adecuadas para administración rectal se presentan preferentemente como supositorios de dosis unitaria, con un portador de base sólida, tal como manteca de cacao, y pueden incluir un salicilato.
Los estuches farmacéuticos pueden comprender una cantidad terapéuticamente eficaz de un compuesto terapéutico como se describe en la presente memoria, en uno o más recipientes estériles que también están dentro del ámbito de la presente divulgación. La esterilización del recipiente puede llevar a cabo usando una metodología de esterilización convencional bien conocida por los expertos en la técnica. Los recipientes estériles de materiales pueden comprender recipientes separados o uno o más recipientes de varias partes. El compuesto como se describe en la presente memoria puede estar separado o puede combinarse en una única forma de administración como se describe anteriormente. Dichos estuches pueden incluir, además, si se desea, uno o más de varios componentes de kits farmacéuticos convencionales, por ejemplo, uno o más portadores farmacéuticamente aceptables, viales adicionales para mezclar los componentes, etc., como será fácilmente evidente para los expertos en la técnica. En dicho estuche también pueden incluirse instrucciones, ya sea en forma de encartes o etiquetas, que indiquen las cantidades de los componentes a administrar, las pautas para la administración y /o las pautas para mezclar los componentes.
Los compuestos de la presente invención pueden usarse en métodos para tratar una afección o trastorno asociado con una mayor expresión y /o actividad de FASN.
Tales trastornos incluyen, por ejemplo:
• obesidad,
• trastornos de la alimentación
• aumento de peso corporal inducido por fármacos; por ejemplo, aumento de peso atípico inducido por antipsicóticos
• enfermedades cardiovasculares,
• desórdenes gastrointestinales,
• trastornos dermatológicos,
enfermedades metabólicas (porejemplo, esteatosis hepática no alcohólica (NASH)) y diabetes tipo 2. (La EHNA es una enfermedad hepática grave cuya patogenia y pronóstico no se han determinado con claridad. En general, se cree que el metabolismo anormal de los ácidos grasos puede estar involucrado en la patogénesis de la EHNA, y es probable que los triacilgliceroles y sus precursores de ácidos grasos se acumulen en el
hepatocito).
• trastornos virales en los que la inhibición de FASN se correlaciona con la inhibición de la replicación viral, y • cánceres y /o metástasis de cáncer (por ejemplo, cánceres de mama, ovario, próstata, colon, pulmón, vejiga, estómago y riñón humanos).
Los métodos de tratamiento descritos en la presente memoria comprenden administrar a un sujeto que necesite dicho tratamiento una cantidad terapéuticamente eficaz de un compuesto de la invención, preferentemente un compuesto de Fórmula I-V(a). La invención incluye un compuesto de acuerdo con la Fórmula I, o una sal farmacéuticamente aceptable del mismo, o una composición farmacéutica que comprende al menos un compuesto de acuerdo con la Fórmula I o una sal farmacéuticamente aceptable del mismo, y al menos un excipiente farmacéuticamente aceptable para su uso en un método de tratamiento de un sujeto que padece un trastorno mediado por la sintasa de ácidos grasos, que comprende administrar al sujeto una cantidad terapéuticamente eficaz de un compuesto de acuerdo con la Fórmula I; o una cantidad terapéuticamente eficaz de una composición farmacéutica que comprende un compuesto de acuerdo con la Fórmula I. La invención también incluye un compuesto de acuerdo con la Fórmula I, o una sal farmacéuticamente aceptable del mismo, o una composición farmacéutica que comprende al menos un compuesto de acuerdo con la Fórmula I o una sal farmacéuticamente aceptable del mismo, y al menos un excipiente farmacéuticamente aceptable para usar en un método de tratamiento de un sujeto que padece obesidad, aumento de peso o aumento de peso, o aumento de peso asociado con la terapia farmacológica, por ejemplo, terapia farmacológica con un agente antipsicótico, por ejemplo, clozapina, risperidona, aripiprazol, olanzapina, quetiapina y ziprasidona. El método comprende administrar al sujeto una cantidad terapéuticamente eficaz de un compuesto de acuerdo con la Fórmula I; o una cantidad terapéuticamente eficaz de una composición farmacéutica que comprende un compuesto de acuerdo con la Fórmula I.
Los compuestos de la presente invención pueden sintetizarse usando los métodos que se describen en general en la presente memoria, y mediante métodos que se describen en los ejemplos de trabajo que se proporcionan en la presente memoria, o variaciones de los mismos. Los compuestos de la invención también pueden ser preparado usando otros métodos sintéticos conocidos, o variaciones de los mismos. A menos que se indique lo contrario, los compuestos de partida de los métodos sintéticos descritos en la presente memoria están disponibles comercialmente o pueden sintetizarse fácilmente mediante métodos conocidos. Las reacciones se realizan generalmente en disolventes que son apropiados para los reactivos y las condiciones de reacción. Se entiende que los materiales empleados en las reacciones son adecuados para las transformaciones que se están efectuando, y los materiales y métodos empleados en el aislamiento del producto se entienden adecuados para los compuestos del producto. Además, en la descripción de los métodos sintéticos en la presente memoria, debe entenderse que todas las condiciones de reacción propuestas, incluida la elección del disolvente, la atmósfera de reacción, la temperatura de reacción, la duración del experimento y los procedimientos de tratamiento, se eligen para que sean las condiciones apropiadas para esa reacción, como lo haría ser entendido por un experto en la técnica de síntesis orgánica. Se entiende que los ejemplos y modalidades descritos en la presente memoria se proporcionan solo con fines ilustrativos, y que se entenderá claramente que se incluyen varias modificaciones o cambios a la luz de los mismos dentro del alcance de esta solicitud y el alcance de las reivindicaciones adjuntas. Las transformaciones químicas específicas se enumeran en los esquemas y ejemplos de trabajo proporcionados en la presente memoria, y el experto en la materia apreciará fácilmente que puede usarse una variedad de reactivos diferentes en lugar de los enumerados. Pueden encontrarse reemplazos comunes para tales reactivos, por ejemplo, en textos como "Encyclopedia of Reagents for Organic Synthesis" Leo A. Paquette, John Wiley & Son Ltd (1995) o "Comprehensive 5 Organic Transformations: A Guide to Functional Group Preparations"Richard C. Larock. Wiley-VCH y "Strategic Applications of Named Reactions in Organic Synthesis" Kurti y Czako, Elsevier, 2005 y referencias allí.
Los compuestos de acuerdo con la Fórmula I-V(a) pueden prepararse mediante síntesis orgánica usando reacciones orgánicas conocidas. Por ejemplo, el Esquema 1 a continuación, describe una de las rutas generales que se usó para sintetizar numerosos ejemplos X = O de la invención. En el esquema 1, comenzando con un compuesto de fórmula 1 (por ejemplo, el terc-butil éster 1 del ácido 4-(4-yodofenoxi)-piperidin-1-carboxílico conocido, o terc-butil éster del ácido 4-(4-bromofenoxi) piperidin-1-carboxílico), un metal de transición (por ejemplo., paladio) reacción de acoplamiento catalizada con un ácido borónico apropiado R 6 o R 6 organoestannano reactivo puede usarse para producir un intermedio de fórmula 2. El intermedio de fórmula 2 puede desprotegerse luego para eliminar el grupo protector, PG (por ejemplo, en condiciones ácidas si el PG es un grupo Boc) para dar una amina intermedia de fórmula 3. La amina intermedia de fórmula 3_puede hacerse reaccionar luego con reactivos tales como ácidos carboxílicos, haluros de ácido carboxílico, anhídridos de ácido carboxílico, isocianatos o haluros de sulfonilo para producir compuestos de acuerdo con las fórmulas I - V(a).
Alternativamente, el orden anterior de las etapas puede invertirse, es decir, el compuesto de partida de fórmula 1 puede desprotegerse para producir una amina intermedia de fórmula 4. La amina intermedia de fórmula 4_puede hacerse reaccionar luego con reactivos tales como ácidos carboxílicos, haluros de ácido carboxílico, anhídridos de ácido carboxílico, isocianatos o haluros de sulfonilo para producir un intermedio de fórmula 5. La amina intermedia de fórmula 5_puede hacerse reaccionar luego con un ácido borónico R6 apropiado o un reactivo de organostanano R6 con catálisis de metal de transición (por ejemplo, paladio) para producir compuestos de Fórmula IV (a).
Esquema 1: Método de síntesis general A
PG = grupo protector; A = etapa de acoplamiento catalizada por metales de transición; B = etapa de desprotección de nitrógeno de piperidina; C = etapa de acilación (o sulfonilación) de nitrógeno de piperidina. También puede emplear otra metodología sintética. Por ejemplo, los intermedios de fórmula 5 en el esquema 1 también pueden sintetizarse usando una reacción de Mitsunobu entre un R 5 sustituido N-sustituido-hidroxipiperidina yodo- o de bromofenol y, como en el Esquema 1a.
Esquema 1a: Síntesis de Mitsunobu del intermedio de fórmula 5 del esquema 1
PH 3 P - trifenilfosfina; DEAD = azodicarboxilato de dietilo; THF = tetrahidrofurano
Los compuestos de Fórmula IV (a) también pueden sintetizarse (como se muestra en el Esquema 2 a continuación) invirtiendo los grupos funcionales en los socios de acoplamiento mostrados en el Esquema 1, por ejemplo, comenzando con un intermedio de boronato de Fórmula 1a (por ejemplo, terc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidin-1-carboxílico). El acoplamiento catalizado por paladio de un compuesto de fórmula 1 con bis (pinacolatato) diboron proporcionaría tal intermedio de boronato de fórmula la . El intermedio de boronato 1a puede convertirse fácilmente en compuestos sustituidos con R6 de acuerdo con la Fórmula I (o II-V (a)) acoplando un haluro o triflato de heteroarilo apropiado; seguido de la desprotección del nitrógeno de la piperidina y la acilación (o sulfonación) del nitrógeno de la piperidina, similar a los pasos de síntesis descritos en el Esquema 1.
Esquema 2: Síntesis a partir de intermedios de boronato de acuerdo con la fórmula la
La química de Mitsunobu también podría ser usado para producir compuestos intermedios de fórmula 1a, por ejemplo, mediante reacción entre un boronato de fenol sustituido R 5 y un hidroxipiperidina protegida N-(o N-sustituido), como en el Esquema 2a, a continuación.
Esquema 2a: Síntesis de Mitsunobu del intermedio de fórmula la del esquema 2
El intermedio de boronato la también podría sintetizarse de otras formas, por ejemplo, empleando una reacción SNAr entre un 4-fluoroyodobenceno y una 4-hidroxipiperidina protegida de Fórmula 5d.
Los compuestos de acuerdo con las fórmulas IV (a), en los que el anillo aromático contiene uno o dos átomos de nitrógeno del anillo (por ejemplo, Anillo de piridinilo y pirimidinilo) pueden sintetizarse a partir de intermedios de fórmula 1H (análogos de heteroarilo de compuestos de fórmula 1) como se describe en el esquema. 3 a continuación usando las condiciones de reacción de Mitsunobu.
Esquema 3: Síntesis de Mitsunobu y uso de intermedios de Fórmula 1H
Fórmula I, II o III
W1, W2 y W3 son N o C sustituido
Por ejemplo, la reacción de Mitsunobu para producir un intermedio piridilo de Fórmula 1H podría llevarse a cabo entre un 6-bromo-piridin-3-ol y una 4-hidroxipiperidina N-protegida (por i MUE ', protegida con Boc) como en el Esquema 3a a continuación.
Esquema 3a: reacción de Mitsunobu de 6 -3-ol con 4-hidroxipiperldina-1-carboxilato de terc-butilo-bromopiridina
La preparación de un intermedio heteroarilo (p. Ej., Piridilo o pirimidilo) de Fórmula 1H puede realizarse, por supuesto, de otras formas, por ejemplo, empleando una reacción de SnAr entre un intermedio de 2-cloropiridina o 2-cloropirimidina y un N-protegido-4 -hidroxipiperidina (por ejemplo, protegida con Boc) como en el Esquema 3b siguiente. La finalización de la síntesis de un compuesto de Fórmulas I - V (a) puede hacerse mediante la instalación de un grupo arilo o heteroarilo R6 (por ejemplo, mediante una reacción de Suzuki), seguido de la desprotección del nitrógeno de la piperidina, y la acilación (o sulfonilación) del nitrógeno de piperidina, como se describió anteriormente.
Esquema 3b: SnAR Reacción de una 2-cloropiridina o 2-cloropirimidina con una 4-hidroxipiperidina N-protegida
W 1 = N, y W2 = N o C (sustituido o no sustituido) Un comPuesto de
formula 1HJ
Los ejemplos de compuestos de Fórmula I, II o III, donde X = SO2 , X = NR9 y X = S pueden sintetizarse usando los mismos tipos de química que se han descrito anteriormente para:
• desprotección del nitrógeno piperidínico;
• acilación o sulfonación del nitrógeno de piperidina desprotegido; y
• metal de transición (por ejemplo, Pd) acoplamiento catalizado para instalar el aromático (o heteroaromático) grupo R6.
Para los compuestos de Fórmula I, II o III, donde X = SO2 , un material de partida adecuado para usar en lugar del intermedio de Fórmula 1 (en el Esquema 1) sería una 4-(4-bromobencenosulfonil) piperidina N-protegida (o 4-(4-yodobencenosulfonil) piperidina). De manera similar, para compuestos de Fórmula I, II o II, en donde X = NR9, un material de partida adecuado para usar en lugar del intermedio de Fórmula 1 (en el Esquema 1) incluiría, por ejemplo, 4-(4-bromofenilamino) -piperidina (o compuestos de 4-(4-yodofenilamino) -piperidina).
Para compuestos de Fórmula I, II o III, donde X = S, un material de partida adecuado para usar en lugar del intermedio de Fórmula 1 (en el Esquema 1) sería una 4-(4-bromofenilsulfanil) -piperidina N-protegida apropiadamente o 4-(4-yodofenilsulfanil) -piperidina. Dichos intermedios de sulfanilo se podrían preparar, por ejemplo, convirtiendo el grupo hidroxilo de un intermedio de 4-hidroxipiperidina N-protegido de fórmula 5d en un grupo saliente (porejemplo, mesilato, tosilato, triflato, etc.) y reaccionando con un 4 -bromo- o 4-yodotiofenol, como se muestra en el Esquema 4 a continuación.
Esquema 4: preparación de compuestos de fórmulas I, II y III a través de intermedios sintéticos de fórmula 1S
PG - grupo protector; A - etapa de acoplamien catalizada por metales de transición; B = etapa desprotección de nitrógeno de piperidina; C = etapa
acilación (o sulfonilación) de nitrógeno de piperidina.
La actividad enzimática de FASN puede determinarse detectando la coenzima A (CoA), un producto de la síntesis catalizada por FASN de palmitato a partir de acetil-CoA y malonil-CoA con NADPH como cofactor. El ensayo se basa en fluorescencia y mide la interacción de CoA libre con 7-dietilamino-3-(4-malemimidilfenil) -4-metilcumarina (CPM; Life Technologies, CA) como se describe en Chung et al (2008). El derivado de cumarina CPM contiene una maleimida reactiva con tiol que se vuelve fluorescente al interactuar con el grupo sulfhidrilo de CoA.
Para los compuestos de ejemplo descritos en la presente memoria, la reacción se realizó en placas sin unión de 384 pocillos de bajo volumen (Corning, NY) usando FASN etiquetado con GST expresado en baculovirus humano recombinante. La mezcla de ensayo de 20 pL contenía HEPe S 50 mM (pH 7,5), Fa Sn 5 nM, NADPH 150 pM (Sigma, St. Louis, MO), acetil-CoA (Sigma) 10 pM, malonil-CoA (Sigma) 25 pM y compuesto de prueba [diluido en dimetilsulfóxido (DMSO); DMSO final al 0,5% en el ensayo después de la adición de 100 nL]. Ver, Chung y otros "A fluorescence-based thiol quantification assay for ultra-high-throughput screening for inhibitors of coenzyme A production," Assay Drug Dev Tech 2008; 6: 361-374.
La reacción se inició añadiendo malonil-CoA, seguido de incubación durante 90 minutos a 250 ° C. Se preparó una solución madre del reactivo CPM en DMSO a 66 pM y se almacenó a -200 ° C. Para detectar la CoA producida en la reacción de FASN, la solución madre de CPM se diluyó hasta 50 pM en etanol al 70% y se añadió a 4 pL /pocillo a la placa de ensayo. Después, la mezcla de reacción se incubó durante 30 minutos. La fluorescencia se midió usando el lector de placas de etiquetas múltiples EnVision™ 2102 (PerkinElmer, Waltham, MA) usando un espejo doble general, un filtro de excitación de 390 nM y un filtro de emisión de 530 nM. El análisis de datos se realizó usando ActivityBase (IDBS, Guilford, Reino Unido). Los valores de CI50 se calcularon trazando la inhibición porcentual frente al log 10 de la concentración del compuesto, y ajustando a la regresión no lineal sigmoidal dosis-respuesta (pendiente variable) ecuación en XLFit (IDBS). Los datos de IC50 para los ejemplos descritos en la presente memoria se proporcionan en las Tablas 2 y 2a más abajo (A = 1 a 99 nM; B = de 100 a 999 nM; C = 1000 - 10000 nM).
Tabla 2 - datos IC50 para compuestos de las Fórmulas I-V/V(a)
Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad
1 A 25 C 49 A 73 A
2 A 26 C 50 B 74 A
3 B 27 c 51 C 75 A
4 A 28 A 52 C 76 A
5 C 29 A 53 C 77 A
6 A 30 A 54 B 78 A
7 A 31 A 55 C 79 A
8 B 32 B 56 C 80 A
9 C 33 B 57 B 81 A
10 A 34 A 58 B 82 A
11 C 35 A 59 A 83 A
12 C 36 A 60 A 84 A
13 c 37 A 61 A 85 B
Continuación
Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad 14 c 38 A 62 A 86 A 15 c 39 B 63 B 87 C 16 c 40 B 64 B 88 A 17 c 41 B 65 A 89 A 18 B 42 A 66 B 90 B 19 C 43 A 67 B 91 A 20 C 44 A 68 A 92 C 21 C 45 A 69 A 93 A 22 A 46 A 70 A 94 A 23 A 47 A 71 A 95 A 24 A 48 A 72 A 96 A
Tabla 2 (continuación) - datos IC50 para los compuestos de las Fórmulas I-V/V(a) Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad 97 B 133 C 169 B 205 A 98 A 134 C 170 B 206 C 99 B 135 B 171 C 207 B 100 A 136 C 172 C 208 C 101 A 137 B 173 C 209 C 102 B 138 C 174 C 210 C 103 A 139 C 175 C 211 C 104 A 140 C 176 C 212 C 105 A 141 C 177 C 213 C 106 B 142 C 178 B 214 C 107 C 143 C 179 B 215 B 108 B 144 C 180 A 216 C 109 C 145 C 181 A 217 B 110 C 146 C 182 B 218 C 111 C 147 C 183 C 219 A 112 B 148 C 184 B 220 A 113 B 149 C 185 B 221 A 114 B 150 B 186 A 222 A 115 B 151 B 187 A 223 A 116 A 152 A 188 B 224 A 117 C 153 C 189 B 225 A 118 C 154 A 190 A 226 A 119 c 155 C 191 C 227 A 120 A 156 B 192 C 228 B 121 c 157 C 193 c 229 B 122 c 158 C 194 c 230 A 123 c 159 C 195 c 231 C 124 c 160 C 196 c 232 C 125 c 161 C 197 c 233 c 126 A 162 C 198 c 234 B
Continuación
Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad 127 c 163 B 199 c 235 C 128 c 164 B 200 A 236 B 129 c 165 B 201 NT 237 C 130 c 166 C 202 A 238 B 131 A 167 A 203 A 239 C 132 c 168 B 204 B 240 C
Tabla 2 (continuación) - datos IC50 para los compuestos de las Fórmulas I--V/V(a) Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad 241 C TH B 313 C 349 A 242 C 278 A 314 C 350 B 243 c 279 B 315 c 351 B 244 A 280 A 316 A 352 A 245 B 281 C 317 A 353 A 246 C 282 C 318 A 354 A 247 B 283 A 319 C 355 C 248 B 284 C 320 A 356 C 249 B 285 A 321 B 357 c 250 A 286 C 322 A 358 B 251 B 287 B 323 C 359 A 252 B 288 B 324 A 360 B 253 C 289 C 325 A 361 C 254 A 290 C 326 B 362 A 255 A 291 C 327 A 363 B 256 B 292 B 328 B 364 B 257 A 293 C 329 A 365 C 258 B 294 C 330 B 366 A 259 B 295 A 331 A 367 C 260 A 296 B 332 C 368 C 261 A 297 B 333 C 369 B 262 A 298 A 334 B 370 B 263 A 299 C 335 C 371 A 264 C 300 C 336 B 372 A 265 A 301 c 337 C 373 B 266 B 302 A 338 B 374 B 267 A 303 A 339 C 375 A 268 C 304 C 340 C 376 A 269 B 305 B 341 C 377 A 270 B 306 C 342 C 378 C 271 B 307 B 343 C 379 C
Continuación
Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad 72 A 308 C 344 B 380 c 73 A 309 A 345 C 381 B 74 A 310 C 346 B 382 C 75 B 311 A 347 B 383 C 76 C 312 B 348 A 384 C
Tabla 2 (continuación) - datos IC50 para los compuestos de las Fórmulas I-V/V(a) Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad 385 C 421 C 457 A 493 C 386 C 422 B 458 A 494 C 387 c 423 B 459 A 495 B 388 c 424 A 460 B 496 C 389 c 425 A 461 B 497 C 390 c 426 C 462 A 498 C 391 c 427 C 463 C 499 C 392 c 428 B 464 C 500 C 393 c 429 A 465 B 501 C 394 c 430 C 466 A 502 C 395 c 431 A 467 A 503 C 396 c 432 A 468 A 504 C 397 c 433 B 469 B 505 C 398 c 434 B 470 B 506 c 399 c 435 B 471 A 507 c 400 c 436 A 472 B 508 c 401 c 437 A 473 B 509 c 402 c 438 A 474 A 510 c 403 c 439 C 475 A 511 c 404 c 440 A 476 A 512 c 405 c 441 C 477 A 513 c 406 c 442 C 478 A 514 c 407 c 443 c 479 A 515 c 408 c 444 c 480 A 516 A 409 c 445 c 481 A 517 A 410 B 446 c 482 A 518 A 411 B 447 c 483 A 519 c 412 A 448 c 484 B 520 A 413 c 449 c 485 A 521 B 414 c 450 A 486 A 522 C 415 c 451 A 487 A 523 C
Continuación
Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad 16 B 452 A 488 A 524 B 17 B 453 B 489 C 525 B 18 A 454 A 490 C 526 C 19 B 455 C 491 B 527 C 20 B 456 A 492 C 528 B
Tabla 2a - datos IC50 para los compuestos de las Fórmulas I-V(a) Ej# Actividad Ej# Actividad Ej# Actividad Ej# Actividad
529 C 559 A 589 A 619 C
530 A 560 B 590 A 620 C
531 C 561 C 591 A 621 C
532 C 562 C 592 A 622 C
533 C 563 A 593 C 623 C
534 C 564 C 594 A 624 C
535 C 565 B 595 B 625 A
536 C 566 A 596 A 626 A
537 A 567 B 597 C 627 C
538 A 568 C 598 B 628 A
539 A 569 B 599 C 629 C
540 A 570 A 600 B 630 B
541 A 571 C 601 A 631 A
542 A 572 C 602 C 632 A
543 C 573 C 603 C 633 A
544 A 574 A 604 C 634 NT
545 A 575 A 605 C 635 NT
546 C 576 C 606 C 636 NT
547 C 577 B 607 C 637 NT
548 C 578 C 608 B 638 NT
549 C 579 B 609 A 639 NT
550 C 580 A 610 C 640 NT
551 C 581 A 611 C 641 NT
552 C 582 C 612 A 642 NT
553 C 583 A 613 C 643 NT
554 C 584 A 614 C 644 NT
555 C 585 B 615 C 645 NT
556 C 586 C 616 C 646 NT
557 C 587 A 617 C 647 NT
558 C 588 A 618 C
Ejemplos
Cualquier compuesto no cubierto por la descripción de las reivindicaciones adjuntas es un ejemplo de referencia.
Ejemplo 1. 1-[4-(4-Isoquinolin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Etapa 1. 1-[4-(4-Bromofenoxi)-piperidin-1-il]-propan-1-ona.
4-(4-Bromofenoxi)piperidina (1,0 g, 3,9 mmol) y N,N-diisopropiletilamina (DIPEA) (2,72 mL, 15,6 mmol) en tetrahidrofurano (THF) (10 mL) se añadió cloruro de propanoilo (0,679 mL, 7,81 mmol). Después de 2 h de agitación a temperatura ambiente, la mezcla se concentró, el producto se suspendió en EtOAc, y se lavó con 1N Na2 CO3 , agua y salmuera y luego se secó (MgSO4 ). El producto se sometió a cromatografía en ISCO (columna de 80 g de gel de sílice, 30-90% EtOAc/hexanos) para dar un aceite viscoso. LCMS m/z = 313 (M 1); 1H Nm R (CDCb) ó: 7,37 (d, 2H, J = 7 Hz), 6,79 (d, 2H, J = 7 Hz), 4,49 (q, 1H, J = 3 Hz), 3,74-3,80 (m, 1H), 3,59 - 3,71 (m, 2H), 3,36-3,42 (m, 1H), 2,36 (q, 2H, J = 7,5 Hz), 1,87-1,94 (m, 2H), 1,73-1,84 (m, 2H), 1,16 (t, 3H, J = 7,5 Hz).
Etapa 2. 1-[4-(4-Isoquinolin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Acetato de paladio (0,00719 g, 0,0320 mmol) y trifenilfosfina (0,0336 g, 0,128 mmol) en dioxano (5 mL) se agitaron 15 min bajo una atmósfera de nitrógeno. 1-[4-(4-bromofenoxi)piperidin-1-il]propan-1-ona (0,20 g, 0,646mmol), ácido isoquinolina-6-borónico (0,122 g, 0,705 mmol), N,N-dimetilformamida (d Mf ) (3 mL) y 1M carbonato de sodio (2,56 mL) se añadieron y se calentaron a 80 °C por 17 h. La mezcla se concentró, se disolvió en EtOAc, se lavó con 1N Na2CO3, agua y salmuera, luego se secó sobre MgSO4. El producto se purificó por ISCO (columna de 12 g de gel de sílice, 5% MeOH/EtOAc) para dar un aceite. La sal de HCl se sintetizó añadiendo 0,25 mL de 1M solución de HCl-éter a una solución de diclorometano (DCM) de base. La sal se cristalizó nuevamente a partir de DCM-éter y se secó para dar un sólido amarillo claro (125 mg, 54%). Análisis: LCMS m/z = 361 (M 1); 1H NMR (DMSO-d6 (dimetilsulfóxido deuterado)) ó: 9,72 (s, 1H), 8,63 (d, 1H, J=6,5 Hz), 8,56 (s, 1H), 8,52 (d, 1H, J=8 Hz), 8,39 (d, 1H, J=6,5 Hz), 8,33 (dd, 1H, J=2, 8 Hz), 7,92 (d, 2H, J=8Hz), 7,21 (d, 2H, J=8 Hz), 4,76 (q, 1H, J=4 Hz), 3,89 (m, 1H), 3,72 (m, 1H), 3,34-3,40 (m, 1H), 3,25-3,31 (m, 1H), 2,35 (q, 2H, J=7,5 Hz), 1,99 (b, 2H), 1,63-1,67 (m, 1H), 1,54 (m, 1H), 1,00 (t, 3H, J=7,5 Hz).
Ejemplo 2. 1-[4-(4-Quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Este compuesto se sintetizó usando el método anterior con 1-[4-(4-bromofenoxi)-piperidin-1-il]propan-1-ona (0,150 g, 0,480 mmol), y ácido 3-quinolinaborónico (0,1247 g, 0,7207 mmol) (120 mg, 69%). Análisis: lCm S m/z = 361 (m 1); 1H NMR (CDCb) ó: 9,16 (s, 1H), 8,24 (d, 1H, J = 2 Hz), 8,10 (d, 1H, J = 8 Hz), 7,86 (d, 1H, J =8 Hz), 7,68-7,73 (m, 1H), 7,66 (d, 2H, J = 8 Hz), 7,55-7,59 (m, 1H), 7,07 (d, 2H, J = 8 Hz), 4,63 (q, 1H, J = 4 Hz), 3,79-3,85 (m, 1H), 3,65-3,76 (m, 2H), 3,41-3,47 (m, 1H), 2,38 (q, 2H, J = 7,5 Hz), 1,95-1,98 (b, 2H), 1,84-1,90 (b, 2H), 1,17 (t, 3H, J = 7,5 Hz).
Ejemplo 3. 2-Metil-1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Etapa 1. 7-[4-(Piperidin-4-iloxi)-fenil]-quinolina dihidrocloruro.
Acetato de paladio (0,0278 g, 0,124 mmol) y trifenilfosfina (0,130 g, 0,496 mmol) en dioxano (10 mL) se agitaron 15 min bajo una atmósfera de nitrógeno. terc-butil éster del ácido 4-(4-yodofenoxi)piperidina-1-carboxílico (1,00 g, 2,48 mmol), ácido quinolina-7-borónico (0,5147 g, 2,976 mmol), DMF (10 mL) y carbonato de sodio 1 M (9,92 mL) se añadieron y se calentaron a 80 °C por 18 h. La mezcla se concentró, se disolvió en EtOAc, se lavó con 1N Na2CO3 , agua y salmuera, y luego se secó (MgSO4 ). El producto intermedio Boc se purificó por ISCO (gel de sílice, 80g; 40-80% EtOAc/hex) para dar un sólido blanco. Este material se añadió 6 M HCl (10 mL) y se calentó a 65 °C por 4 h, luego se concentró. La sal de HCl se trituró con éter, se secó y se recogió para dar un sólido amarillo. LCMS m/z = 305 (M 1).
Etapa 2. 2-Metil-1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona.
7-[4-(Piperidin-4-iloxi)-fenil]-quinolina dihidrocloruro (0,042 g, 0,14 mmol) y DIPEA (0,097 mL, 0,55 mmol) en THF (2 mL) se añadió cloruro de isobutirilo (0,029 mL, 0,28 mmol). Después de 4 h de agitación a temperatura ambiente, la mezcla se concentró, se diluyó con EtOAc y se lavó con 1N Na2CO3, agua y salmuera, luego se secó (MgSO4). El producto se purificó por ISCO (4g de gel de sílice, 0-5% MeOH/DCM). La sal de HCl se obtuvo a partir de 2N HCl éter y se cristalizó nuevamente a partir de DCM-éter para dar un sólido blanco (40 mg, 77%). Análisis: LCMS m/z = 375 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,21 (d, 1H, J = 4 Hz), 8,96 (d, 1H, J=8 Hz), 8,45 (s, 1H), 8,32 (d, 1H, J=8,3 Hz), 8,21 (d, 1H, J = 8,3 Hz),7,89-7,92 (m, 1H), 7,83 (d, 2H, J=8 Hz), 7,20 (d, 2H, J = 8 Hz), 4,75 (m, 1H), 3,89 (b, 1H), 3,78 (b, 1H), 3,39 (b, 1H), 3,27 (b, 1H), 3,90 (q, 1H, J=7 Hz), 1,95-2,01 (b, 2H), 1,63 (b, 1H), 1,55 (b, 1H), 1,01 (d, 6H, J=7 Hz).
Ejemplo 4. 1-[4-(4-Quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Este compuesto se sintetizó usando el método del ejemplo 3. Análisis: LCMS m/z = 361 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,17 (m, 1H), 8,92 (d, 1H, J = 8 Hz), 8,40 (s, 1H), 8,30 (d, 1H, J = 9 Hz), 8,20 (dd, 1H, J = 2, 8,5 Hz), 8,86-8,90 (m, 1H), 8,63 (d, 1H, J = 8,5 Hz), 7,20 (d, 2H, J = 8,5 Hz), 4,74 (q, 1H, J = 4 Hz), 3,89 (m, 1H), 3,73 (m, 1H), 3,33-3,39 (m, 1H), 3,24-3,29 (m, 1H), 2,34 (q, 2H, J = 7,5 Hz), 1,90-2,03 (b, 2H), 1,61-1,65 (m, 1H), 1,53-1,57 (m, 1H), 1,00 (t, 3H, J = 7,5 Hz).
Ejemplo 5. t-butil éster del ácido 4-(2-Fluoro-4-quinolin-3-il-fenox)piperidina-1-carboxílico.
Etapa a. terc-butil éster del ácido 4-(4-Bromo-2-fluorofenoxi)piperidina-1- carboxílico.
Trifenilfosfina (4,12 g, 15,71 mmol) en THF se añadió 6 M de dietil azodicarboxilato (DEAD) en tolueno (2,62 mL, 15,71 mmol) a 0 °C. Después de 0,5 h, ácido 4-bromo-2-fluorofenol (1,13 mL, 10,5 mmol) y terc-butil éster del ácido 4-hidroxipiperidina-1-carboxílico (2,63 g, 13,09 mmol) en THF (10 mL) se añadió en forma de gotas y se agitó por 18 h a temperatura ambiente. La mezcla se filtró y se concentró. El producto se disolvió en Et2 O (ca. 100 mL) y hexano (ca.
25 mL) y filtró. El éter se concentró y el producto se purificó por Cromatografía ISCO de gel de sílice (columna de 120 g; 15-20% EtOAc/hexanos) para dar un sólido (11 g, 82%). Análisis: LCMS m/z = 375 (M 1); 1H NMR (CDCla) 67,23 7,26 (m, 1H), 7,11-7,21 (m, 1H), 6,84-6,92 (m, 1H), 4,41 (tt, J = 7,0, 3,5 Hz, 1H), 3,65-3,75 (m, 2H), 3,33 (ddd, J = 13,5, 7,6, 4,0 Hz, 2H), 1,86-1,95 (m, 2H), 1,69-1,82 (m, 3H), 1,44-1,48 (m, 9H).
Etapa b. terc-butil éster del ácido 4-(2-fluoro-4-quinolin-3-il-fenox)piperidina-1-carboxílico.
Este compuesto se sintetizó por el método del ejemplo 3 usando terc-butil éster del ácido 4-(4-bromo-2-fluorofenoxi)piperidina-1-carboxílico (0,50 g, 1,34 mmol), y ácido 3-quinolinaborónico (0,28 g, 1,60 mmol). Análisis: LCMS m/z = 423 (M 1); 1H NMR (CDCla) 9,13 (d, 1H, J=2 Hz), 8,12 (d, 1H, J=8,4 Hz), 7,87 (d, 1H, J=8,4 Hz), 7,64-7,74 (m, 2H), 7,56-7,60 (m, 1H), 7,44-7,48 (m, 2H), 7,40-7,43 (m, 1H), 7,14 (t, 1H, J=8 Hz), 4,54 (q, 1H, J=4,5 Hz), 3,72-3,79
(m, 2H), 3,33-3,40 (m, 2H), 1,94-2,00 (m, 2H), 1,79-1,87 (m, 2H), 1,48 (s, 9H).
Ejemplo 6. 1-[4-(2-Fluoro-4-quinolin-3-il-fenoxi)piperidin-1-il]propan-1-ona.
Etapa 1. 3-[3-Fluoro-4-(piperidin-4-iloxi)-fenil]-quinolina.
terc-butil éster del ácido 4-(2-fluoro-4-quinolin-3-il-fenox)piperidina-1-carboxílico (0,5 g) se añadió 6M HCl (10 mL) y se calentó a 65 °C, luego se concentró y el residuo se trituró con éter para dar un sólido amarillo claro (350 mg, 82%). Análisis: LCMS m/z = 323 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,49 (s, 1H), 9,11 (b, 3H), 8,25 (d, 1H, J = 8 Hz), 8,20 (d, 1H, J = 8 Hz), 7,94-7,98 (m, 2H), 7,79-7,84 (m, 2H), 7,50 (t, 1H, J = 8,5 Hz), 4,81 (b, 1H), 3,23 (b, 2H), 3,11 (b, 2H), 2,16 (b, 2H), 1,92 (b, 2H).
Etapa 2. 1-[4-(2-Fluoro-4-quinolin-3-il-fenoxi)piperidin-1-il]propan-1-ona.
A 3-[3-Fluoro-4-(piperidin-4-iloxi)fenil]quinolina (0,070 g, 0,22 mmol) y DIPEA (0,113 mL, 0,651 mmol) en DCM (3 mL) se añadió cloruro de propanoilo (0,0377 mL, 0,434 mmol). Después de 2 h de agitación a temperatura ambiente la mezcla se concentró, se disolvió en EtOAc y se lavó con 1N Na2CO3 y salmuera, luego se secó sobre MgSO4. El producto se purificó por ISCO (columna de 4g de gel de sílice, 0-5% MeOH/DCM) para dar un aceite. La sal de HCl se obtuvo añadiendo 0,25 mL en HCl-éter a una solución de DCM de la base para dar un sólido amarillo (60 mg, 73%). Análisis: LCMS m/z = 379 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,45 (s, 1H), 9,03 (s, 1H), 8,18 (t, 2H, J=7Hz), 7,91-7,94 (m, 2H), 7,75-7,81 (m, 2H), 7,48 (t, 1H, J=8 Hz), 4,77 (q, 1H, J=4Hz), 3,78 (b, 1H), 3,70 (b, 1H), 3,27-3,39 (m, 2H), 2,34 (q, 2H, J=7Hz),1,93-1,99 (b, 2H), 1,66 (b, 1H),1,57 (b, 1H), 1,00 (t, 3H, J=7Hz).
Ejemplo 7. 1-[4-(2-Fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z = 393 (M 1); 1H NMR (sal de HCl, DMSO) 6: 9,49 (s, 1H), 9,09 (s, 1H), 9,19-9,24 (m, 2H), 7,92 7,97 (m, 2H), 7,77-7,84 (m, 2H), 7,49 (t, 1H, J = 8 Hz), 4,79 (q, 1H, J = 4 Hz), 3,87 (b, 1H), 3,78 (b, 1H), 3,40 (b, 1H), 3,29 (b, 1H), 2,91 (q, 1H, J = 7 Hz), 2,00 (b, 1H), 1,96 (b, 1H),1,66 (b, 1H),1,58 (b, 1H),1,00 (d, 6H, J = 7 Hz).
Los siguientes ejemplos se sintetizaron comenzando con t-butil éster del ácido 4-(4-bromofenoxi)-piperidina-1-carboxílico o t-butil éster del ácido 4-(4-yodofenoxi)piperidina-1-carboxílico y un ácido borónico apropiado usando los métodos descritos para los ejemplos anteriores.
Ejemplo 8. 1-[4-(4-Benzofuran-5-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 350 (M 1); 1H NMR (CDCla) 6: 7,70 (d, 1H, J = 2 Hz), 7,64 (d, 1H, J=2 Hz), 7,51-7,54 (m, 3H), 7,46 (dd, 1H, J=2, 8 Hz), 7,00 (d, 2H, J=8,5 Hz), 6,80 (d, 1H, J=2 Hz), 4,58 (q, 1H, J=4 Hz), 3,79-3,85 (m, 1H), 3,63 3,74 (m, 2H), 3,39-3,46 (m, 1H), 2,38 (q, 2H, J=7,5 Hz), 1,94 (b, 2H), 1,84 (b, 2H), 1,17 (t, 3H, J=7,5 Hz).
Ejemplo 9. 1-[4-(4-Benzofuran-5-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z = 364 (M 1); 1H NMR (CDCls) 6: 7,73 (d, 1H, J = 2Hz), 7,64 (d, 1H, J = 2 Hz), 7,52-7,54 (m, 3H), 7,48 (d, 1H, J = 2, 8 Hz), 7,00 (d, 2H, J = 8,5 Hz), 6,80 (m, 1H), 4,59 (q, 1H, J = 4 Hz), 3,75-3,85 (m, 2H), 3,64-3,68 (m, 1H), 3,47 (b, 1H), 2,84 (q, 1H, J = 7 Hz), 1,96 (b, 2H), 1,86 (b, 2H), 1,15 (d, 6H, J = 7 Hz).
Ejemplo 10. 1 -[4-(4-Naftalen-2-il-fenoxi)-piperidin-1 -il]-propan-1 -ona.
Análisis: LCMS m/z = 360 (M 1); 1H NMR (CDCb) 6: 7,98 (s, 1H), 7,83-7,98 (m, 3H),7,70 (dd, 1H, J = 2, 8,5 Hz), 7,64-7,67 (m, 2H), 7,44-7,51 (m, 2H), 7,02-7,04 (m, 2H), 4,61 (q, 1H, J = 4 Hz), 3,79-3,85 (m, 1H), 3,64-3,76 (m, 2H), 3,40-3,46 (m, 1H), 2,37 (q, 2H, J = 7 Hz), 1,92-1,97 (m, 2H), 1,82-1,91 (m, 2H), 1,17 (t, 3H, J = 7 Hz).
Ejemplo 11. 2-Metil-1-[4-(4-naftalen-2-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 374 (M 1); 1H NMR (CDCla) 7,98 (s, 1H), 7,84-7,90 (m, 3H), 7,70 (dd, 1H, J = 2, 8 Hz), 7,64 7,67 (m, 2H), 7,44-7,51 (m, 2H), 7,02-7,05 (m, 2H), 4,61 (q, 1H, J = 4 Hz), 3,75-3,85 (m, 2H), 1,65-1,72 (m, 1H), 3,48 (b, 1H), 2,84 (q, 1H, J = 7 Hz), 1,96 (b, 2H), 1,87 (b, 2H), 1,15 (d, 6H, J = 7 Hz).
Ejemplo 12. 1-[4-(4-1,5-Naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 362 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,42 (d, 1H, J = 2Hz), 9,10 (dd, 1H, J = 2, 4 Hz), 8,67 (d, 1H, J = 2 Hz), 8,57 (d, 1H, J = 8,6 Hz), 7,91 (d, 2H, J = 8,5 Hz), 7,85 (dd, 1H, J = 2, 8 Hz), 7,20 (d, 2H, J = 8,5 Hz), 4,75 (q, 1H, J = 4 Hz), 3,89 (m, 1H), 3,71 (m, 1H), 3,33-3,39 (m, 1H), 3,24-3,30 (m, 1H), 2,34 (q, 2H, J = 7 Hz), 1,98 (b, 2H), 1,61-1,65 (m, 1H), 1,53-1,58 (m, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 13.2-Metil-1-[4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 376 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,47 (d, 1H, J = 2Hz), 9,10 (dd, 1H, J = 2, 4 Hz), 8,73 (d, 1H, J =2 Hz), 8,64 (d, 1H, J = 8,5 Hz), 7,94 (d, 2H, J = 8 Hz), 7,89-7,93 (m, 1H), 7,20 (d, 2H, J = 8 Hz), 4,76 (q, 1H, J = 4 Hz), 3,89 (b, 1H), 3,78 (b, 1H), 3,35-3,44 (m, 1H), 3,25-3,33 (m, 1H), 2,90 (q, 1H, J = 6 Hz), 1,98 (b, 2H), 1,63 (b, 1H), 1,55 (b, 1H), 1,00 (d, 6H, J = 6 Hz).
Ejemplo 14. Ciclopropil-[4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 374 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6:9,40 (d, 1H, J = 2 Hz), 9,06 (m, 1H), 9,63 (d, 1H, J = 2 Hz), 8,51 (d, 1H, J = 8,5 Hz), 7,91 9d, 2H, J = 8 Hz), 7,80-7,84 (dd, 1H, J = 2, 4 Hz), 7,19 (d, 2H, J = 8 Hz), 4,77 (q, 1H, J = 4 Hz), 4,00 (b, 1H), 3,90 (b, 1H), 3,57 (b, 1H), 3,29 (b, 1H), 1,91-2,10 (m, 3H), 1,66 (b, 1H), 1,56 (b, 1H), 0,69-0,74 (m, 4H).
Ejemplo 15. Éster metílico del ácido 4-(2-Fluoro-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico.
Análisis: LCMS m/z = 381 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,36 (s, 1H), 8,86 (s, 1H), 8,10 (d, 2H, J = 8 Hz), 7,83-7,90 (m, 2H), 7,71 (m, 2H), 7,45 (t, 1H, J = 9 Hz), 4,73 (m, 1H), 3,69-3,73 (m, 2H), 3,61 (s, 3H), 3,27-3,32 (m, 2H), 1,96 (m, 2H), 1,59-1,65 (m, 2H).
Ejemplo 16. 1-{4-[4-(2-Cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 395 (M 1); 1H NMR (CDCla) 6: 8,09 (s, 1H), 8,05 (d, 1H, J=8 Hz), 7,82 (d, 1H, J=8 Hz), 7,74 (t, 1H, J=7,5 Hz), 7,58 (t, 1H, J=7,5 Hz), 7,46 (d, 2H, J=8 Hz), 7,02 (d, 2H, J=8Hz), 4,63 (m, 1H), 3,81-3,85 (m, 1H), 3,67 3,76 (m, 2H), 3,43-3,47 (m,1H), 2,40 (d, 2H, J=7,5Hz), 1,97 (b, 2H), 1,88 (b, 2H), 1,18 (t, 3H, J=7,5 Hz).
Ejemplo 17. {4-[4-(2-Cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona.
Análisis: LCMS m/z = 407 (M 1); 1H NMR (CDCla) 6: 8,09 (s,1H), 8,05 (d, 1H, J = 8 Hz), 7,82 (d, 1H, J = 8 Hz), 7,74 (t, 1H, J = 7,5 Hz), 7,58 (t, 1H, J = 7,5 Hz), 7,47 (d, 2H, J = 8 Hz), 7,02 (d, 2H, J = 8Hz), 4,64 (q, 1H, J=4Hz), 3,95 (b, 1H), 3,82 (b, 1H), 3,65-3,71 (m, 2H), 1,88-2,00 (b, 4H), 1,76-1,82 (m, 1H), 0,99-1,02 (m, 2H), 0,76-0,79 (m, 2H).
E je m p lo 18. 1 - {4 -[4 -(2 -M e to x iq u in o lin -3 - i l) - fe n o x i] -p ip e r id in -1 - i l} -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 391 (M 1); 1H NMR (CDCla) 6: 7,95 (s, 1H), 7,86 (d, 1H, J = 8 Hz), 7,73 (d, 1H, J = 8 Hz), 7,57 7,63 (m, 3H), 7,38 (t, 1H, J = 7,5 Hz), 7,00 (d, 2H, J = 8 Hz), 4,61 (q, 1H, J=4Hz), 4,10 (s, 3H),3,78-3,83 (m, 1H),3,65-3,75 (m, 2H),3,40-3,46 (m, 1H), 2,37 (q, 2H, J=7,5Hz), 1,95 (b, 2H),1,87 (b, 2H), 1,17 (t, 3H, J=7,5Hz).
Ejemplo 19. Ciclopropil-{4-[4-(5,6,7,8-tetrahidro-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 377 (M 1); 1H NMR (DMSO-d6 - Sal de HCl) 6: 8,88 (s, 1H), 8,47 (s, 1H),7,78 (d, 2H, J = 8 Hz),7,16 (d, 1H, J = 8 Hz), 4,76 (q, 1H, J = 4Hz), 3,97 (b, 1H), 3,87 (b, 1H), 3,29 (b, 2H), 3,02 (m, 2H), 2,93 (m, 2H), 1,97-2,03 (m, 2H), 1,89 (m, 3H), 1,81 (m, 2H), 1,64 (b, 1H), 1,53 (b, 1H), 0,70-0,74 (m, 4H).
Ejemplo 20. Ciclobutil-{4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 391 (M 1): 1H NMR (DMSO-d6 - Sal de HCl) 6: 8,89 (s, 1H),8,53 (s, 1H), 7,79 (d, 2H, J = 8 Hz), 7,14 (d, 2H, J = 8 Hz),4,73 (m, 1H),3,84 (m, 1H),3,36 (m, 2H), 3,26 (m, 2H),3,05 (m, 2H), 2,94 (m, 2H), 2,09-2,19 (m, 4H), 3,17-3,92 (m, 8H), 1,53 (m, 2H).
Ejemplo 21. 1-{4-[4-(5,6,7,8-Tetrahidroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 365 (M 1); 1H NMR (DMSO-d6 - Sal de HCl) 6: 8,90 (s, 1H),8,54 (s, 1H),7,79 (d, 2H, J = 8 Hz),7,15 (d, 2H, J = 8 Hz), 4,74 (m, 1H), 3,87 (m, 1H), 3,68 (m, 1H), 3,24-3,37 (m, 2H), 3,05 (m, 2H), 2,94 (m, 2H), 2,33 (q, 2H, J = 7 Hz), 1,81-1,90 (m, 6H), 1,61 (m, 1H), 1,52 (m, 1H), 0,98 (t, 3H, J = 7 Hz).
Ejemplo 22. 1-{4-[4-(8-Fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 379 (M 1); 1H NMR (DMSO-d6) 6: 8,97 (d, 1H, J=4Hz), 8,44 (d, 1H, J=8Hz), 7,87 (d, H, J=8Hz), 7,74 (t, 1H, J=7,5Hz), 7,61-7,66 (m, 3H),7,15 (d, 2H, J=8Hz), 4,72 (q, 1H,j=4Hz), 3,89 (b, 1H), 3,70 (b, 1H), 3,38 (m, 1H), 3,26 (m, 1 H),2,34 (q, 2H, J=7,5Hz), 1,98 (b, 2H), 1,63 (m, 1H), 1,54 (m, 1H), 1,00 (t,3H, J=7,5Hz).
Ejemplo 23. Ciclopropil-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (DMSO-d6) 6: 8,97 (m, 1H), 8,44 (d, 1H, J = 8 Hz), 7,87 (d, 1H, J = 8Hz), 7,75 (t, 1H, J = 7,5 Hz), 7,61-7,67 (m, 3H), 7,16 (d, 2H, J = 8 Hz), 4,75 (q, 1H, J = 4 Hz), 4,00 (b, 1H), 3,91 (b, 1H), 3,56 (b, 1H), 3,26-3,34 (m, 2H), 1,98-2,04 (m, 3H), 1,67 (b, 1H), 1,56 (b, 1H), 0,70-0,74 (m, 4H).
Ejemplo 24. Ciclobutil-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 405 (M 1); 1H NMR (DMSO-d6) 6: 8,97 (m, 1H), 8,44 (d, 1H, J = 8Hz), 7,87 (d, 2H, J = 8 Hz), 7,73 (m, 1H), 7,61-7,66 (m, 3H), 7,14 (d, 2H, J = 8Hz), 4,70 (q, 1H, J=4Hz), 3,85-3,90 (m, 1H), 3,57-3,60 (m, 1H), 3,34 3,39 (m, 1H), 3,22-3,29 (m, 2H), 2,06-2,20 (m, 4H), 1,86-1,95 (m, 3H), 1,72-1,77 (m, 1H), 1,52-1,60 (m, 2H).
Ejemplo 25. 1-{4-[4-(8-Fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 393 (M 1); 1H NMR (DMSO-d6) 6: 8,57 (d, 1H, J = 7 Hz), 7,92 (d, 1H, J = 8 Hz), 7,78 (m, 1H), 7,65-7,69 (m, 3H), 7,18 (d, 2H, J = 8 Hz), 4,8 (m, 1H), 3,95 (b, 1H), 3,70 (b, 1H), 3,33-3,39 (m, 1H), 3,24-3,29 (m, 1H), 2,80 (s, 3H), 2,34 (q, 2H, J = 7 Hz), 1,94 (b, 2H), 1,63 (b, 1H), 1,53 (b, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 26. Ciclopropil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 405 (M 1); 1H NMR (DMSO-d6) 6: 8,45 (d, 1H, J = 7 Hz), 7,87 (d, 1H, J = 7Hz), 7,72 (m, 1H), 7,65 (d, 1H, J = 8 Hz), 7,60 (d, 1H, J = 8,5 Hz), 7,16 (d, 2H, J = 8 Hz), 4,74 (m, 1H), 4,00 (b, 1H), 3,90 (b, 1H), 3,56 (b, 1H), 3,28 (b, 1H), 2,76 (s, 3H), 1,98-2,04 (m, 3H), 1,66 (b, 1H), 1,56 (b, 1H), 0,70-0,74 (m, 4H).
E je m p lo 27. C ic lo b u t il- {4 -[4 -(8 - f lu o ro -2 -m e t i lq u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 419 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 8,36 (d, 1H, J = 7 Hz), 7,82 (d, 1H, J = 7 Hz), 7,62-7,68 (m, 3H), 7,53 (d, 1H, J = 7,5 Hz), 7,14 (d, 2H, J = 8 Hz), 4,70 (m, 1H), 3,8 (b, 1H), 3,57 (m, 1H), 3,35 (m, 1H), 3,22 (m, 2H), 2,72 (s, 3H), 2,09-2,20 (m, 4H), 1,86-1,95 (m,3H), 1,75 (m, 1H), 1,52-1,57 (m, 2H).
Ejemplo 28. {4-[4-(5-Fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 421 (M 1); 1H NMR (DMSO-d6) 6: 9,19 (s, 1H), 8,72 (d, 0,5H, J = 5 Hz), 8,46 (d, 0,5H, J = 2, 5 Hz), 8,28 (b, 1H), 7,64 (d, 2H, J = 8 Hz), 7,48-7,53 (m, 1H), 7,36-7,41 (m, 1H), 7,06 (d, 2H, J = 8 Hz), 4,65 (m, 2H), 3,84-3,98 (m, 3H), 2,31 (m, 1H), 1,89-2,10 (m, 8H), 1,44-1,55 (m, 4H).
Ejemplo 29. 1-{4-[4-(5-Fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 379 (M 1); 1H NMR (DMSO-d6) 6: 9,28 (s, 1H), 8,66 (s, 1H), 7,84 (m, 3H), 7,55-7,62 (m,2H), 7,17 (d, 2H, J = 8 Hz), 4,72 (m, 1H), 3,88 (m, 1H), 3,70 (m, 1H), 3,28-3,38 (m, 2H), 2,34 (q, 2H, J = 7Hz), 1,93-1,99 (m, 2H), 1,53-1,64 (m, 2H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 30. Ciclopropil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (sal de HCl, DMSO) 6: 9,29 (s, 1H), 8,68 (s, 1H), 7,86 (m, 3H), 7,54-7,64 (m, 2H), 7,18 (d, 2H, J = 8 Hz), 4,75 (m, 1H), 3,99 (b, 1H), 3,90 (b, 1H), 3,56 (b, 1H), 3,29 (b, 1H), 1,98-2,03 (m, 3H), 1,66 (b, 1H), 1,56 (b, 1H), 0,70-0,74 (m, 4H).
Ejemplo 31. Ciclobutil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
A n á lis is : L C M S m /z = 405 (M 1); 1H N M R (D M S O -d 6 ) 6: 9 ,28 (s, 1H ), 8 ,66 (s, 1H ), 7 ,85 (m , 3 H ), 7 ,53 -7 ,64 (m , 2 H ), 7 ,16 (d, 2 H , J = 8 H z), 4 ,72 (q, 1H , J = 4 H z ), 3 ,85 -3 ,89 (m , 1 H ), 3 ,57 -3 ,60 (m , 1H ), 3 ,34 -3 ,39 (m , 1H ), 3 ,23 -3 ,29 (m , 2 H ), 2 ,05 -2 ,20 (m , 4 H ), 1 ,86 -1 ,95 (m , 3 H ), 1 ,72 -1 ,77 (m , 1 H ), 1 ,52 -1 ,60 (m , 2 H ).
Ejemplo 32. 1-{4-[4-(1H-Pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. ferc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico.
Trifenilfosfina (9,53 g, 36,4 mmol), y DEAD (40% p/p DEAD en tolueno, 16,1 mL, 40,9 mmol) en THF (80 mL) se enfrió a 0 °C y se agitó bajo una atmósfera de nitrógeno. Una mezcla de 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenol (5,0 g, 22,7 mmol) y terc-butil éster del ácido 4-hidroxipiperidina-1-carboxílico (5,72 g, 28,4 mmol) en THF (10 mL) se añadió en forma de gotas a la reacción. El baño de enfriamiento se retiró y se agitó adicionalmente a temperatura ambiente por 20 h. La reacción se evaporó bajo vacío, se agitó con éter, y el sólido blanco se filtró. El filtrado se evaporó bajo vacío y se purificó por cromatografía ISCO de gel de sílice (0-20% EtOAc/hexanos) para obtener tercbutil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (6,3 g, 69%). LCMS m/z = 404 (M 1). Etapa 2. t-butil éster del ácido 4-[4-(1 H-pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidina-1 -carboxílico.
Acetato de paladio (0,0111 g, 0,0496 mmol) y trifenilfosfina (0,0520 g, 0,198 mmol) se agitaron por 15 min bajo una atmósfera de nitrógeno. terc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,40 g, 0,99 mmol), 5-bromo-1H-pirrolo[2,3-b]piridina (0,235 g, 1,19 mmol), DMF (4 mL) y 1 M Na2CO3 (4 mL) se añadieron y se calentaron a 80 °C por 18 h. La mezcla se concentró, se disolvió en EtOAc, se lavó con en Na2CO3, agua y salmuera, luego se secó (MgSO4). El producto se purificó por ISCO (gel de sílice, columna de 80g; 40-80% EtOAc/hexanos) para dar un sólido blanco (0,25 g, 64%). Análisis: LCMS m/z = 394 (M 1): 1H NMR (CDCb) 6 9,16 (br. s., 1H), 8,51 (d, J = 2,0 Hz, 1H), 8,07 (d, J = 2,0 Hz, 1H), 7,47-7,61 (m, 2H), 7,30-7,38 (m, 1H), 6,99-7,10 (m, 2H), 6,55(dd, J = 3,4, 1,9 Hz, 1H), 4,52 (dt, J = 7,1, 3,6 Hz, 1H), 3,69-3,80 (m, 2H), 3,31-3,46 (m, 2H), 1,93-2,00 (m, 2H), 1,76-1,84 (m, 2H), 1,48 (s, 9H).
Etapa 3. 5-[4-(Piperidin-4-iloxi)-fenil]-1H-pirrolo[2,3-b]piridina.
terc-butil éster del ácido 4-[4-(1 H-Pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidina-1 -carboxílico (200 mg, 0,51 mmol) se añadió 6M HCl en dioxano (4 mL, 20 mmol) y se agitó a temperatura ambiente por 6 h. La mezcla se concentró, y se trituró con éter para dar un sólido amarillo claro (150 mg, 98%). Análisis: LCMS m/z = 294 (M 1); 1H NMR (DMSO-d6) 612,25 (br. s., 1H), 9,19 (br. s., 2H), 8,43-8,65 (m, 2H), 7,59-7,73 (m, 3H), 7,15 (d, J = 8,5 Hz, 2H), 6,64 (d, J = 1,3 Hz, 1H), 4,74 (br. s., 1H), 3,23 (br. s., 2H), 3,09 (d, J = 4,3 Hz, 2H), 2,14 (d, J = 3,5 Hz, 2H), 1,90 (d, J = 9,3 Hz, 2H)
Etapa 4. 1-{4-[4-(1H-Pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
5-[4-(Piperidin-4-iloxi)fenil]-1H-pirrolo[2,3-b]piridina (0,043 g, 0,15 mmol) y DIPEA (0,0771 mL, 0,443 mmol) en DCM (2 mL) se añadió cloruro de propanoilo (0,026 mL, 0,295 mmol). Después de 2 h de agitación a temperatura ambiente la mezcla se concentró, se disolvió en EtOAc y se lavó con 1N Na2CO3 y salmuera, luego se secó sobre MgSO4. El producto se purificó por ISCO (columna de 4g de gel de sílice, 0-5% MeOH/DCM) para dar un aceite. La sal de HCl se sintetizó añadiendo 1N éter de HCl a una solución de base, dCM dio un sólido blanco (32 mg, 62%). Análisis: LCMS m/z = 350 (M 1): 1H NMR (DMSO, Sal de HCl) 6: 11,89 (s, 1H), 8,51 (s, 1H), 8,29 (s, 1H), 7,63 (d, 2H, J = 8 Hz), 7,54 (m, 1H), 7,09 (d, 2H, J = 8 Hz), 6,55 (s, 1H), 4,67 (m, 1H), 3,87 (b, 1H), 3,69 (b, 1H), 3,34 (m, 1H), 3,26 (m, 1H), 2,33 (q, 2H, J = 7Hz), 1,91-1,97 (b, 2H), 1,61 (m, 1H), 1,51 (m, 1H), 0,99 (t, 3H J =7 Hz).
Los siguientes ejemplos se sintetizaron a partir de terc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico usando el procedimiento general.
Ejemplo 33. Ciclopropil-{4-[4-(1H-pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-1-il}-metanona.
A n á lis is : L C M S m /z = 362 (M 1); 1H N M R (D M S O -d 6 , S a l d e H C l) 6: 11 ,92 (s, 1H ), 8 ,51 (s, 1H ), 8 ,30 (s, 1 H ), 7 ,65 (d, 2 H , J = 8 H z), 7 ,56 (m , 1H ), 7 ,10 (d, 2 H , J = 8 H z), 6 ,55 (m , 1 H ), 4 ,70 (m , 1 H ), 3 ,98 (b , 1H ), 3 ,89 (b, 1H ), 3 ,56 (b, 1H ), 3 ,28 (b, 1 H ), 1 ,93 -2 ,03 (m , 3 H ) ,1 ,64 (b, 1H ), 1 ,54 (b , 1 H ), 0 ,69 -0 ,74 (m , 4 H ).
Ejemplo 34. Ciclopropil-{4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 403 (M 1): 1H NMR (CDCla) 6: 9,07 (s, 1H), 8,18 (s, 1H), 7,73 (s, 1H, J = 8 Hz), 7,62 (d, 2H, J = 8 Hz), 7,44 (s, 1H), 7,22 (dd, 1H, J = 2, 8 Hz), 7,05 (d, 2H, J = 8 Hz), 4,64 (m, 1H), 3,97 (s, 3H), 3,83 (b, 2H), 3,64 3,70 (m, 2H), 1,87-2,00 (b, 4H), 1,75-1,81 (m, 1H), 1,00 (m, 2H), 0,77-0,79 (m, 2H).
Ejemplo 35. 1-{4-[4-(7-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (CDCla) 6: 9,06 (d, 1H, J = 2 Hz), 8,17 (d, 1H, J = 2 Hz), 7,73 (d, 1H, J=9 Hz), 7,61 (d, 2H, J=8 Hz), 7,44 (d, 1H, J=2 Hz), 7,22 (dd, 1H, J = 2, 8 Hz), 7,04 (d, 2H, J = 8 Hz), 4,62 (q, 1H, J=4 Hz), 3,97 (s, 3H), 3,80-3,84 (m, 1H), 3,67-3,75 (m, 2H), 3,42-3,48 (m, 1H), 2,38 (q, 2H, J = 7,5 Hz), 1,96 (b, 2H), 1,87 (b, 2H), 1,17 (t, 3H, J = 7,5 Hz).
Ejemplo 36. 1-{4-[4-(8-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 375 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,13 (m, 1H), 8,83 (s, 1H), 8,07 (d, 1H, J = 8 Hz), 7,86 (m, 1H), 7,67 (d, 1H, J = 8 Hz), 7,40 (d, 2H, J = 8 Hz), 7,13 (d, 2H, J = 8 Hz), 4,70 (q, 1H, J = 4 Hz), 3,90-393 (m, 1H), 3,71-3,74 (m, 1H), 3,33-3,39 (m, 1H), 3,24-3,28 (m, 1H), 2,72 (s, 3H), 2,34 (q, 2H, J = 7 Hz), 1,95 (b, 2H), 1,64 (b, 1H), 1,53 (b, 1H), 1,00 (t, 3H, J = 7Hz).
Ejemplo 37. Ciclopropil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 387 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,06 (s, 1H), 8,63 (s, 1H), 7,97 (m, 1H), 7,72 (m, 1H), 7,59 (m, 1H), 7,40 (d, 2H, J = 7 Hz), 7,14 (d, 2H, J = 7 Hz), 4,73 (m, 1H), 4,12 (b, 1H), 3,91 (b, 1H), 3,71 (b, 1H), 3,28 (b, 1H), 2,70 (s, 3H), 1,98-2,04 (m, 3H), 1,67 (b, 1H), 1,56 (b, 1H), 0,70-0,74 (m, 4H).
E je m p lo 38. C ic lo b u t il- {4 -[4 -(8 -m e t i lq u in o l in -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 401 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,08 (m, 1H), 8,73 (s, 1H), 8,01 (d, 1H, J = 8Hz), 7,79 (s, 1H), 7,62 (d, 1H, J = 8 Hz), 7,39 (d, 2H, J = 7 Hz), 7,12 (d, 2H,J = 7 Hz), 4,68 (m, 1H), 3,88-3,91 (m, 1H), 3,58 3,61 (m, 1H), 3,35-3,39 (m, 1H), 3,23-3,28 (m, 2H), 2,70 (s, 3H), 2,08-2,23 (m, 4H), 1,86-1,95 (m, 3H), 1,72-1,77 (m, 1H), 1,53-1,59 (m, 2H).
Ejemplo 39. Ciclopropil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 373 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 8,66 (s, 1H), 8,18-8,26 (m, 4H), 8,08 (d, 1H, J = 8 Hz), 7,88 (t, 1H, J = 7 Hz), 7,68 (t, 1H, J = 7 Hz), 7,22 (d, 2H, J = 7 Hz), 4,81 (q, 1H, J = 4 Hz), 4,01 (b, 1H), 3,90 (b, 1H), 3,58 (b, 1H), 3,30 (b, 1H), 1,98-2,04 (m, 3H), 1,66 (b, 1H), 1,57 (b, 1H), 0,70-0,74 (m, 4H).
Ejemplo 40. 1-[4-(4-Quinolin-2-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 361 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 8,74 (s, 1H), 8,25 (m, 4H), 8,14 (d, 1H, J = 8 Hz), 7,93 (m, 1H), 7,72 (m, 1H), 7,23 (d, 2H, J = 8 Hz), 4,80 (m, 1H), 3,90 (m, 1H), 3,74 (m, 1H), 3,34-3,39 (m, 1H), 3,25-3,30 (m, 1H), 2,34 (q, 2H, J = 7 Hz), 1,95-2,01 (b, 2H), 1,65(b, 1H), 1,54 (b, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 41. Ciclobutil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 387 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 8,73 (s, 1H), 8,26 (m, 4H), 8,12 (d, 1H, J = 8 Hz), 7,92 (m, 1H), 7,72 (m, 1H), 7,22 (d, 2H, J = 8 Hz), 4,79 (m, 1H), 3,87-3,90 (m, 1H), 3,57-3,61 (m, 1H), 3,35-3,39 (m, 1H), 3,23-3,30 (m, 2H), 2,05-2,22 (m, 4H), 1,86-1,96 (m, 3H), 1,70-1,78 (m, 1H), 1,50-1,63 (m, 2H).
Ejemplo 42. [4-(4-Quinolin-2-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona.
A n á lis is : L C M S m /z = 403 (M 1); 1H N M R (D M S O -d 6 , S a l d e H C l) 6: 8 ,65 (s, 1H ), 8 ,17 -8 ,25 (m , 4 H ), 8 ,08 (d , 1H , J = 8 H z ), 7 ,89 (m , 1H ), 7 ,68 (m , 1H ), 7 ,21 (d, 2 H , J = 8 H z ), 4 ,80 (m , 1H ), 4 ,69 (m , 1H ), 3 ,71 -3 ,92 (m , 3 H ), 3 ,23 -3 ,49 (m , 2 H ), 1 ,98 -2 ,08 (m , 3 H ), 1 ,79 -1 ,89 (m , 2 H ), 1 ,53 -1 ,67 (m , 2 H ), 1 ,24 -1 ,28 (m , 2 H ).
Ejemplo 43. 1-[4-(4-Isoquinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 361 (M 1); 1H NMR (DMSO-d6) 6: 9,36 (s, 1H), 8,32 (s, 1H), 8,15 (d, 2H, J = 8 Hz), 8,10 (d, 1H, J = 7,5 Hz), 7,98 (d, 1H, J = 7,5 Hz), 7,77 (m, 1H), 7,63 (m, 1H), 7,11 (d, 2H, J = 8 Hz), 4,71 (q, 1H, J = 4Hz), 3,24 3,35 (m, 3H), 3,19 (b, 1H), 3,70 (b, 1H), 2,34 (q, 2H, J = 7 Hz), 1,93-1,98 (b, 2H), 1,63 (b, 1H), 1,53 (b, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 44. Ciclopropil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 373 (M 1); 1H NMR (DMSO-d6) 6: 9,36 (s, 1H), 8,32 (s, 1H), 8,16 (d, 2H, J = 8,8 Hz), 8,10 (d, 1H, J = 8Hz), 7,98 (d, 1H, J = 8 Hz), 7,77 (m, 1H), 7,63 (m, 1H), 7,12 (d, 2H, J=8,8Hz), 4,74 (q, 1H, J=4Hz), 3,99 (b, 1H), 3,90 (b, 1H), 3,56 (b, 1H), 3,29 (m, 1H), 1,92-2,10 (m, 3H), 1,66 (b, 1H), 1,55 (b, 1H), 0,69-0,75 (m, 4H).
Ejemplo 45. Ciclobutil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 387 (M 1); 1H NMR (DMSO-d6) 6: 9,36 (s, 1H), 8,32 (s, 1H), 8,15 (d, 2H, J = 9 Hz) 8,09 (d, 1H, J = 8 Hz), 7,98 (d, 1H, J=8Hz), 7,77 (m, 1H), 7,63 (m, 1H), 7,14 (d, 2H, J=9Hz), 4,70 (m, 1H), 3,86-3,89 (m, 1H), 3,56 3,60 (m, 1H), 3,23-3,38 (m, 3H), 2,07-2,22 (m, 4H), 1,85-1,94 (m, 3H), 1,70-1,77 (m, 1H), 1,52-1,56 (m, 2H).
Ejemplo 46. [4-(4-Isoquinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 403 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,51 (s, 1H), 8,47 (s, 1H), 8,23 (d, 1H, J=8 Hz), 8,12 (d, 2H, J=9 Hz), 8,08 (d, 1H, J=8 Hz), 7,89 (m, 1H), 7,73 (m, 1H), 7,16 (d, 2H, J=9 Hz), 4,75 (m, 1H), 4,70 (m, 1H), 3,70-3,90 (m, 2H), 3,57-3,64 (m, 1H), 3,10-3,16 (m, 1H), 1,94-2,08 (m, 2H), 1,77-1,89 (m, 2H), 1,52-1,66 (b, 2H), 1,23-1,28 (m, 4H).
E je m p lo 47. 1 - {4 -[4 -(4 -C lo ro q u in o lin -3 - i l) - fe n o x i]-p ip e r id in -1 - i l } -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 395 (M 1); 1H NMR (DMSO HCl) 6: 8,91 (s, 1H), 8,32 (d, 1H, J = 8 Hz), 8,14 (d, 1H, J = 8 Hz), 7,89-7,93 (m, 1H), 7,81-7,88 (m, 1H), 7,56 (d, 2H, J = 8 Hz), 7,16 (d, 2H, J = 8 Hz), 4,73 (q, 1H, J = 4 Hz), 3,91 (b, 1H), 3,71 (b, 1H), 3,33-3,39 (m, 1H), 3,24-3,28 (m, 1H), 2,34 (q, 2H, J = 7 Hz), 1,94-2,00 (b, 2H), 1,63 (b, 1H), 1,55 (b, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 48. {4-[4-(4-Cloroquinolin-3-il)-fenoxi]-pipendin-1-il}-ciclopropil-metanona.
Análisis: LCMS m/z = 407 (M 1); 1H NMR (DMSO HCl) 6: 8,90 (s, 1H), 8,32 (d, 1H, J = 8 Hz), 8,13 (m, 1H), 7,90 (t, 1H, J = 8 Hz), 7,83 (m, 1H), 7,56 (d, 2H, J = 8 Hz), 7,17 (d, 2H, J = 8 Hz), 4,75 (q, 1H, J = 4 Hz), 3,93 (b, 2H), 3,56(b, 1H), 3,28 (b, 1H), 1,96-2,04 (m, 3H), 1,67 (b, 1H), 1,56 (b, 1H), 0,70-0,74 (m, 4H).
Ejemplo 49. {4-[4-(4-Cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclobutil-metanona.
Análisis: LCMS m/z = 421 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 8,92 (s, 1H), 8,32 (d, 1H, J = 8 Hz), 8,14 (d, 1H), 7,91 (m, 1H), 7,84 (m, 1H), 7,56 (d, 2H, J = 8 Hz), 7,15 (d, 2H, J = 8 Hz), 4,72 (m, 1H), 3,89 (b, 1H), 3,60 (b, 1H), 3,33 3,39 (m, 1H), 3,22-3,29 (m, 2H), 2,08-2,20 (m, 4H), 1,86-1,96 (m, 3H), 1,72-1,77 (m, 1H), 1,53-1,60 (m, 2H).
Ejemplo 50. 1-{4-[4-(4-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (CDCla) 6: 8,84 (s, 1H), 8,20 (d, 1H, J = 8 Hz), 8,03 (d, 1H, J = 8 Hz), 7,78 (t, 1H, J = 8,5 Hz), 7,60-7,68 (m,3H), 7,14 (d, 2H, J = 8 Hz), 4,70 (q, 1H, J = 4 Hz), 3,90 (b, 1H), 3,70 (b, 1H), 3,68 (s, 3H), 3,43-3,48 (m, 2H), 2,34 (q, 2H, J=7Hz), 1,97 (b, 2H), 1,65 (b, 1H), 155 (b, 1H), 1,00 (t, 3H, J=7Hz).
Ejemplo 51. 1-[4-(4-Furo[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 351 (M 1); 1H NMR (DMSO-d6) 6: 8,81 (d, 1H, J = 2 Hz), 8,31 (d, 1H, J = 2,3 Hz), 8,27 (m, 1H), 7,71 (d, 2H, J = 8 Hz), 7,15 (m, 1H), 7,13 (d, 2H, J = 8 Hz), 4,70 (q, 1H, J = 4 Hz), 3,88 (m, 1H), 3,70 (m, 1H), 3,37 (m, 1H), 3,26 (m, 1H), 2,33 (q, 2H, J = 7 Hz), 1,97 (b, 2H), 1,62 (m, 1H), 1,52 (m, 1H), 0,99 (t, 3H, J=7Hz).
Ejemplo 52. Ciclopropil-[4-(4-furo[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 363 (M 1); 1H NMR (DMSO-d6) 6: 8,82 (s, 1H), 8,31 (d, 1H, J = 2 Hz), 8,27 (s, 1H), 7,72 (d, 2H, J = 8 Hz), 7,15 (s, 1H), 7,12 (d, 2H, J = 8 Hz), 4,72 (q, 1H, J = 4 Hz), 3,98 (b, 1H), 3,88 (b, 1H), 3,55 (b, 1H), 3,28 (m, 1H), 1,93-2,01 (m, 3H), 1,64 (b, 1H), 1,51 (b, 1H), 0,69-0,73 (m, 4H).
Ejemplo 53. 1-{4-[4-(6-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,36 (s, 1H), 9,08 (s, 1H), 8,22 (d, 1H, J = 9 Hz), 7,89 (d, 2H, J = 8 Hz), 7,66 (m, 2H), 7,20 (d, 2H, J = 8 Hz), 4,76 (q, 1H, J = 4 Hz), 3,97 (s, 3H), 3,89 (m, 1H), 3,71 (m, 1H), 3,34-3,39 (m, 1H), 3,25-3,30 (m, 1H), 2,34 (q, 2H, J = 7 Hz), 1,97 (b, 2H), 1,64 (m, 1H), 1,54 (m, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 54. Ciclopropil-{4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 403 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,23 (s, 1H), 9,04 (s, 1H), 8,19 (d, 1H, J = 9 Hz), 7,89 (d, 2H, J = 8 Hz), 7,46 (m, 2H), 7,21 (d, 2H, J = 8 Hz), 4,78 (q, 1H, J = 4 Hz), 4,05 (b, 1H), 3,97 (s, 3H), 3,91 (b, 1H), 3,57(b, 1H), 3,29 (b, 1H), 1,96-2,04 (m, 3H), 1,65 (b, 1H), 1,56 (b, 1H), 0,69-0,75 (m, 4H).
Ejemplo 55. 1-{4-[4-(6,7-Dimetoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 421 (M 1); 1H NMR (sal de HCl, DMSO) 6: 9,30 (s, 1H), 9,10 (s, 1H), 7,86 (d, 2H, J = 8 Hz), 7,66 (d, 2H, J = 7 Hz), 7,20 (d, 2H, J = 8 Hz), 4,75 (q, 1H, J=4Hz), 4,03 (s, 3H), 3,99 (s, 3H), 3,89 (m, 1H), 3,71 (m, 1H), 3,37 (m, 1H), 3,27 (m, 1H), 2,34 (q, 2H, J=7Hz), 1,99 (b, 2H), 1,63 (m, 1H), 1,53 (m, 1H), 1,00 (t, 3H, J=7Hz).
E je m p lo 56. C ic lo p ro p il- {4 -[4 -(6 ,7 -d im e to x iq u in o lin -3 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 433 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,26 (s, 1H), 9,01 (s, 1H), 7,86 (d, 2H, J = 8Hz), 7,64 (s, 1H), 7,56 (s, 1H), 7,20 (d, 2H, J = 8 Hz), 4,77 (q, 1H, J = 4 Hz), 4,02 (s, 3H), 3,98 (s, 3H), 3,90 (b, 1H), 2,57(b, 2H), 3,29 (m, 1H), 1,96-2,03 (m, 3H), 1,66 (b, 1H), 1,53 (br, 1H), 0,70-0,75 (m, 4H).
Ejemplo 57. 1-{4-[4-(8-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (base, DMSO-d6) 6: 9,14 (d, 1H, J = 2 Hz), 8,51 (d, 1H, J = 2 Hz), 7,08 (d, 2H, J = 8 Hz), 7,54 (m, 2H), 7,16 (m, 3H), 4,72 (q, 1H, J = 4 Hz), 3,98 (s, 3H), 3,99 (m, 1H), 3,70 (m, 1H), 3,38 (m, 1H), 3,25 (m, 1H), 2,34 (q, 2H, J = 7 Hz), 1,98 (b, 2H), 1,62 (b, 1H), 1,53 (b, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 58. Ciclopropil-{4-[4-(8-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 403 (M 1); 1H NMR (base, DMSO-d6) 6: 9,14 (d, 1H, J = 2Hz), 8,51 (d, 1H, J = 2 Hz), 7,81 (d, 2H, J = 8 Hz), 7,54 (m, 2H), 7,16 (m, 3H), 4,74 (q, 1H, J = 4 Hz), 4,02 (b, 1H), 3,98 (s, 3H), 3,89 (b, 1H), 3,57 (b, 1H), 3,29 (m, 1H), 1,94-2,04 (m, 3H), 1,66 (b, 1H), 1,55 (b, 1H), 0,69-0,74 (m, 4H).
Ejemplo 59. {4-[4-(8-Cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona.
Análisis: LCMS m/z = 407 (M 1); 1H NMR (DMSO-d6) 6: 9,05 (d, 1H, J = 4 Hz), 8,48 (d, 1H, J = 8 Hz), 8,01 (d, 1H, J = 8 Hz), 7,62-7,68 (m, 2H), 7,50 (d, 2H, J = 8 Hz), 7,1(d, 2H, J = 8 Hz), 4,73 (q, 1H, J = 4 Hz), 4,01 (b, 1H), 3,92 (b, 1H), 3,56 (b, 1H), 3,22 (b, 1H), 1,98-2,04 (m, 3H), 1,68 (b, 1H), 1,56 (b, 1H), 0,70-0,74 (m, 4H).
E je m p lo 60. 1 - {4 -[4 -(4 -M e t i lq u in o lin -3 - i l) - fe n o x i]-p ip e r id in -1 - i l} -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 375 (M 1); 1H NMR (DMSO-d6) 6: 9,13 (s, 1H), 8,47 (d, 1H, J = 8,5 Hz), 8,33 (d, 1H, J = 9 Hz), 8,09 (t, 1H, J = 7,5 Hz), 7,95 (t, 1H, J = 7,5 Hz), 7,49 (d, 2H, J = 8 Hz), 7,20 (d, 2H, J = 8 Hz), 4,74 (q, 1H, J = 4 Hz), 3,91 (b, 1H), 3,71 (b, 1H), 3,34-3,39 (m, 1H), 3,24-3,29 (m, 1H), 2,83 (s, 3H), 2,34 (q, 2H, J = 7 Hz), 1,94 (b, 2H), 1,65 (b, 1H), 1,55 (b, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 61. Ciclopropil-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 387 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 1H NMR 9,06 (s, 1H), 8,42 (d, J = 8,3 Hz, 1H), 8,24 (d, J = 8,3 Hz, 1H), 8,02 (t, J = 7,7 Hz, 1H), 7,83-7,96 (m, 1H), 7,41-7,58 (m, 2H), 7,20 (d, J = 8,5 Hz, 2H), 4,76 (dt, J = 7,8, 3,9 Hz, 1H), 4,01-4,09 (m, 1H), 3,89-3,96 (m, 1H), 3,58 (br. s., 1H), 3,25-3,33 (m, 1H), 1,94-2,13 (m, 3H), 1,68 (br. s., 1H), 1,57 (br. s., 1H), 0,67-0,81 (m, 4H).
Ejemplo 62. Ciclobutil-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 401 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,09 (s, 1H), 8,45 (d, J = 8,5 Hz, 1H), 8,31 (d, J = 8,3 Hz, 1H), 7,86-8,13 (m, 2H), 7,49 (d, J = 8,5 Hz, 2H), 7,19 (d, J = 8,8 Hz, 2H), 4,61-4,81 (m, 1H), 3,84-3,97 (m, 1H), 3,60 (d, J = 13,8 Hz, 1H), 3,32-3,43 (m, 1H), 3,18-3,32 (m, 2H), 2,81 (s, 3H), 2,04-2,23 (m, 4H), 1,92 (dd, J = 19,4, 8,9 Hz, 4H), 1,70-1,82 (m, 1H), 1,50-1,68 (m, 3H).
Ejemplo 63. 1-{4-[4-(7-Metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 375 (M 1): 1H NMR (DMSO-d6) 6: 9,29 (d, J = 2,3 Hz, 1H), 8,79 (br. s., 1H), 7,95 (d, J = 8,0 Hz, 1H), 7,87 (d, J = 8,8 Hz, 2H), 7,69 (d, J = 7,0 Hz, 1H), 7,56-7,65 (m, 1H), 7,19 (d, J = 8,8 Hz, 2H), 4,74 (dt, J = 7,7, 4,0 Hz, 1H), 3,83-4,00 (m, 1H), 3,64-3,80 (m, 1H), 3,19-3,52 (m, 2H), 2,78 (s, 3H), 2,31-2,42 (m, 2H), 2,35 (q, J = 7,5 Hz, 2H), 1,86-2,10 (m, 2H), 1,64 (d, J = 8,5 Hz, 1H), 1,54 (d, J = 8,3 Hz, 1H), 1,00 (t, J = 7,4 Hz, 3H).
E je m p lo 64. C ic lo p ro p il- {4 -[4 -(7 -m e t i lq u in o lin -3 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 387 (M 1); 1H NMR (DMSO-d6) 6: 9,27 (d, J = 2,3 Hz, 1H), 8,67 (br. s., 1H), 7,81-8,01 (m, 3H), 7,65 (d, J = 6,8 Hz, 1H), 7,49-7,61 (m, 1H), 7,19 (d, J = 8,5 Hz, 2H), 4,76 (br. s., 1H), 4,01 (br. s., 1H), 3,90 (br. s., 1H), 3,57 (br. s., 1H), 3,30 (br. s., 1H), 2,73-2,82 (m, 3H), 2,01 (d, J = 5,3 Hz, 3H), 1,68 (br. s., 1H), 1,57 (br. s., 1H), 0,48 0,81 (m, 4H).
Ejemplo 65. {4-[4-(4-Metilquinolin-3-il)-fenoxi]-piperidin-1-il}-®-tetrahidro-furan-2-il-metanona.
Análisis: LCMS m/z = 417 (M 1): 1H NMR (DMSO-d6) 6: 9,13 (1 H, s), 8,47 (1 H, d, J=8,3 Hz), 8,32 (1 H, d, J=8,3 Hz), 8,08 (1 H, t, J=7,7 Hz), 7,90 - 8,00 (1 H, m), 7,50 (2 H, d, J= 8,8 Hz), 7,20 (2 H, d, J=8,5 Hz), 4,76 (1 H, d, J=3,5 Hz), 4,70 (1 H, t, J=6,1 Hz), 3,69-4,00 (4 H, m), 3,20-3,52 (2 H, m), 2,82 (3 H, s), 1,93-2,12 (4 H, m), 1,78-1,91 (2 H, m), 1,49-1,73 (2 H, m).
Ejemplo 66. 1-[4-(4-Quinoxalin-2-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 362 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,55 (s, 1H), 8,31 (d, 1H, J = 8Hz), 8,08 (d, 1H, J = 8 Hz), 7,79-7,87 (m, 2H), 7,19 (d, 2H, J = 8 Hz), 4,79 (m, 1H), 3,89 (m, 1H), 3,70 (m, 1H), 3,37 (m, 1H), 3,25 (m, 1H), 2,34 (q, 2H, J = 7 Hz), 1,99 (b, 2H), 1,63 (b, 1H), 1,53 (b, 1H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 67. Ciclopropil-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 374 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,55 (s, 1H), 8,31 (d, 2H, J = 9Hz), 8,08-8,11 (m, 2H), 7,79-7,88 (m, 2H), 7,20 (d, 2H, J = 8 Hz), 4,80 (q, 1H, J = 4 Hz), 3,99 (b, 1H), 3,91 (b, 1H), 3,56 (b, 1H), 3,28 (b, 1H), 1,98-2,08 (m, 3H), 1,67 (b, 1H), 1,57 (b, 1H), 0,70-0,74 (m, 4H).
E je m p lo 68. [4 -(4 -Q u in o x a lin -2 - i l- fe n o x i) -p ip e r id in -1 - i l ] -(R ) - te tra h id ro fu ra n -2 - i l-m e ta n o n a .
Análisis: LCMS m/z = 404 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,55 (s, 1H), 8,30 (d, 2H, J = 8 Hz), 8,08-8,11 (m, 2H), 7,80-7,88 (m, 2H), 7,20 (d, 2H, J = 8 Hz), 4,79 (m, 1H), 4,69 (m, 1H), 3,71-3,81 (m, 4H), 3,26-3,46 (m, 2H), 1,95-2,01 (m, 4H), 1,78-1,89 (m, 2H), 1,54-1,68 (m, 2H).
Ejemplo 69. {4-[4-(8-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Análisis: LCMS m/z = 417 (M 1); 1H NMR (DMSO-d6) 69,05-9,21 (m, 1H), 8,75 (br. s., 1H), 8,05 (d, J = 8,5 Hz, 1H), 7,76-7,89 (m, 1H), 7,66 (d, J = 8,3 Hz, 1H), 7,35-7,49 (m, 2H), 7,14 (d, J = 8,5 Hz, 2H), 4,65-4,81 (m, 3H), 3,70-3,98 (m, 5H), 3,15-3,50 (m, 3H), 2,71 (s, 3H), 1,91-2,19 (m, 4H), 1,75-1,91 (m, 2H), 1,45-1,73 (m, 2H).
Ejemplo 70. {4-[4-(8-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(S)-tetrahidro-furan-2-il-metanona.
Análisis: LCMS m/z = 417 (M 1); 1H NMR (DMSO-d6) 6: 8,97 (d, J = 2,5 Hz, 1H), 8,37 (d, J = 8,0 Hz, 1H), 7,85 (d, J = 8,5 Hz, 1H), 7,55 (dd, J = 8,3, 4,3 Hz, 1H), 7,48 (d, J = 8,5 Hz, 1H), 7,38 (d, J = 8,3 Hz, 2H), 7,11 (d, J = 8,5 Hz, 2H), 4,70 (d, J = 5,3 Hz, 2H), 3,69-4,03 (m, 4H), 3,38-3,58 (m, 1H), 3,25 (br. s., 1H), 2,68 (s, 3H), 1,91-2,13 (m, 4H), 1,85 (dt, J = 13,9, 6,7 Hz, 2H), 1,53-1,73 (m, 2H)
Ejemplo 71. {4-[4-(4-Cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Análisis: LCMS m/z = 437 (M 1); 1H NMR (DMSO-d6) 6: 8,88 (s, 1H), 8,31 (d, 1H, J = 8 Hz), 8,12 (d, 1H, J = 8 Hz), 7,89 (t, 1H, J = 7 Hz), 7,82 (t, 1H, J = 7 Hz), 7,55 (d, 2H, J = 8 Hz), 7,16 (d, 2H, J = 8 Hz), 4,68-4,74 (m, 2H), 3,72-3,93 (m, 4H), 3,39-3,48 (m, 1H), 3,23-3,28 (m, 1H), 1,96-2,08 (m, 4H), 1,80-1,87 (m, 2H), 1,66 (b, 1H), 1,56 (b, 1H).
Ejemplo 72. 1 -{4-[4-(4-Metilquinolin-3-il)-fenoxi]-piperidin-1 -il}-propano-1,2-diona.
Análisis: LCMS m/z = 389 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,09 (1 H, s), 8,45 (1 H, d, J=8,5 Hz), 8,29 (1 H, d, J=8,5 Hz), 8,05 (1 H, t, J = 7,7 Hz), 7,86 - 7,98 (1 H, m), 7,50 (2 H, d, J = 8,5 Hz), 7,21 (2 H, d, J = 8,5 Hz), 4,73 -4,87 (1H, m), 3,77-3,90 (2H, m), 3,53-3,65 (2H, m), 3,29-3,47 (3H, m), 2,40 (3H, s), 1,95-2,10 (2H, m), 1,55-1,78 (2H, m).
Ejemplo 73. Isoxazolidin-2-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
Método A: A 3-[4-(Piperidin-4-iloxi)-fenil]-quinolina • 2 HCl (0,180 g, 0,477 mmol) en DCM (3 mL) se añadió trifosgeno (0,0708 g, 0,238 mmol) en un baño de hielo. La mezcla se calentó hasta la temperatura ambiente, se agitó 4 h, y luego se concentró. A este material en DCM (4 mL) se añadió DIPEA (0,166 mL, 0,954 mmol) y isoxazolidina • HCl (0,0627 g, 0,572 mmol) y se agitó a temperatura ambiente por 2 h. La reacción se concentró, se disolvió en EtOAc y se lavó con 1N Na2CO3 y salmuera y luego se secó (MgSO4). El producto se sometió a cromatografía en ISCO (12 g de gel de sílice, 0-5% MeOH/DCM) para dar un aceite. La sal de HCl se preparó añadiendo 0,5 mL 1N HCl-éter a una solución de DCM de base, se cristalizó nuevamente a partir de DCM-éter y se secó para dar un sólido amarillo (140 mg, 72%). Análisis: LCMS m/z = 404 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,48 (s, 1H), 9,09 (s, 1H), 8,23 (d, 2H, J = 7Hz), 7,90-7,97 (m, 3H), 7,82 (t, 1H, J = 7,8 Hz), 7,20 (d, 2H, J = 8 Hz), 4,75 (q, 1H, J = 4 Hz), 3,76-3,83 (m, 4H), 3,43 (t, 2H, J = 7,5 Hz), 3,30 - 3,37 (m, 2H), 2,13 (q, 2H, J = 7 Hz), 1,98 - 2,02 (m, 2H), 1,58 - 1,66 (m, 2H).
Los siguientes ejemplos se sintetizaron usando el procedimiento anterior.
Ejemplo 74. [4-(4-Isoquinolin-3-il-fenoxi)-piperidin-1-il]-isoxazolidin-2-il-metanona.
Análisis: LCMS m/z = 404 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,61 (s, 1H), 8,56 (s, 1H), 8,31 (d, 1H, J = 8,5 Hz), 8,11 (m, 3H), 7,97 (7, 1H, J = 7 Hz), 7,79 (t, 1H, J = 7 Hz), 7,20 (d, 2H, J = 8 Hz), 4,75 (q, 1H, J = 4 Hz), 3,81 (m, 4H), 4,43 (t, 2H, J = 7 Hz), 3,31-3,36 (m, 2H), 2,13 (q, 2H, J = 7 Hz), 2,00 (b, 2H), 1,61 - 1,65 (m, 2H).
Ejemplo 75. Isoxazolidin-2-il-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 418 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 8,98 (s, 1H), 8,35 (d, 1H, J = 7,7Hz), 7,84 (d, 1H, J = 8 Hz), 7,53-7,56 (m, 1H), 7,46 (d, 1H, J = 8,5Hz), 7,36 (d, 2H, J = 8 Hz), 7,09 (d, 2H, J = 8 Hz), 4,68 (b, 1H), 3,81 (m, 4H), 3,43 (t, 2H, J=7Hz), 3,3 (m, 2H), 2,67 (s, 3H), 2,09-2,17 (m, 2H), 1,99 (b, 2H), 1,58-1,70 (m, 2H).
Ejemplo 76. {4-[4-(4-Cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona.
Análisis: LCMS m/z = 438 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,13 (d, 1H, J = 4 Hz), 8,85 (d, 1H, J = 7 Hz), 8,08 (d, 1H, J = 8 Hz),7,85-7,89 (m, 1H), 7,68 (d, 1H, J = 8 Hz), 7,42 (d, 2H, J = 8 Hz), 7,16 (d, 2H, J = 8 Hz), 4,69 4,73 (m, 2H), 3,78-3,83 (m, 4H), 3,43 (t, 2H, J = 7 Hz), 3,29-3,36 (m, 2H), 2,13 (q, 2H, J = 7,2 Hz), 1,98-2,03 (m, 2H), 1,58-1,66 (m, 2H),
Ejemplo 77. {4-[4-(8-Cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona.
Análisis: LCMS m/z = 438 (M 1); 1H NMR (DMSO-d6) 6: 9,05 (d, 1H, J = 5 Hz), 8,48 (d, 1H, J = 8 Hz), 8,01 (d, 1H, J = 8,5 Hz), 7,64-7,67 (m, 1H), 7,61 (d, 1H, J = 8 Hz), 7,49 (d, 2H, J = 8 Hz), 7,12 (d, 2H, J = 8 Hz), 4,70 (q, 1H, J = 4 Hz), 3,78-3,83 (m, 4H), 3,43 (t, 2H, J = 7,5 Hz), 3,30-3,35 (m, 2H), 2,13 (q, 2H, J =7,3 Hz), 1,98,2,03 (m, 2H), 1,58 1,66 (m, 2H).
Ejemplo 78. Isoxazolidin-2-il-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 418 (M 1); 1H NMR (DMSO-d6) 6: 8,74 (s, 1H), 8,20 (d, 1H, J = 8 Hz), 8,03 (d, 1H, J = 8 Hz), 7,78 (t, 1H, J = 7,2 Hz), 7,68 (t, 1H, J = 7,2 Hz), 7,42 (d, 2H, J = 8 Hz), 7,14 (d, 2H, J=8Hz), 4,70 (q, 1H, J=4Hz), 3,79 3,83 (m, 4H), 3,43 (t, 2H, J=7,2Hz), 3,29-3,36 (m, 4H), 2,63 (s, 3H), 2,13 (q, 2H, J=8Hz), 1,99-2,02 (m, 2H).
Ejemplo 79. Isoxazolidin-2-il-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 434 (M 1); 1H NMR (DMSO-d6) 6: 8,94 (m, 1H), 8,38 (d, 1H, J = 8 Hz), 7,75 (d, 1H, J = 8,5 Hz), 7,53-7,60 (m, 4H), 7,10 (d, 2H, J = 8 Hz), 4,68 (q, 1H, J = 4 Hz), 3,91 (s, 3H), 3,81 (m, 4H), 3,3 (m, 2H), 3,43 (t, 2H, J = 7 Hz), 2,14 (q, 2H, J = 7 Hz), 2,10 (m, 2H), 1,57 - 1,66 (m, 2H).
Ejemplo 80. Isoxazolidin-2-il-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 418 (M 1); 1H NMR (DMSO-d6) 6: 9,24 (d, 1H, J = 2 Hz), 8,52 (d, 1H, J = 2 Hz), 7,81-7,86 (m, 3H), 7,58 (d, 1H, J = 7 Hz), 7,51 (t, 1H, J = 7 Hz), 7,15 (d, 2H, J = 8 Hz), 4,70 (q, 1H, J=4Hz), 3,77-3,83 (m, 4H), 3,43 (t, 2H, J=7,5Hz), 3,30-3,36 (m, 2H), 2,75 (s, 3H), 2,13 (q, 2H, J=7Hz), 1,99 (m, 2H), 1,59-1,65 (m, 2H).
E je m p lo 81. Is o x a z o lid in -2 - il-[4 -(4 -q u in o x a lin -2 - i l- fe n o x i) -p ip e r id in -1 - i l ] -m e ta n o n a .
Análisis: LCMS m/z = 405 (M 1); 1H NMR (DMSO-d6) 6: 9,55 (s, 1H), 8,30 (d, 2H, J = 8 Hz), 8,09 (m, 2H) 7,78-7,88 (m, 2H), 7,20 (d, 2H, J = 8 Hz), 4,77 (q, 1H, J = 4 Hz), 3,77-3,83 (m, 4H), 3,43 (t, 2H, J = 7 Hz), 3,34 (m, 2H) 2,14 (q, 2H, J = 7 Hz), 2,00 (m, 2H), 1,58-1,67 (m, 2H).
Ejemplo 82. ácido 4-[4-(4-Metilquinolin-3-il)-fenoxi]-piperidina-1 -carboxílico metoxiamida.
Análisis: LCMS m/z=392 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,8 (s, 1H, D2 O exch), 8,99 (1 H, br. s.), 8,43 (1 H, d, J = 8,3 Hz), 8,20 (1 H, d, J = 8,3 Hz), 8,05 (1 H, t, J = 7,4 Hz), 7,88 - 7,99 (1 H, m), 7,49 (2 H, d, J = 8,0 Hz), 7,19 (2 H, d, J = 8,0 Hz), 4,70 (1 H, br. s.), 3,63 (2 H, d, J = 12,8 Hz), 3,56 (2 H, s), 3,19 (2 H, t, J = 9,9 Hz), 2,80 (3 H, s), I , 98 (2 H, br. s.), 1,60 (2 H, d, J = 8,3 Hz).
Ejemplo 83. ácido 4-[4-(4-Metilquinolin-3-il)-fenoxi]-piperidina-1 -carboxílico metoximetil-amida.
Análisis: LCMS m/z = 406 (M 1); 1H NMR (DMSO-d6 HCl) 6: 9,05 (1 H, s), 8,40 (1 H, d, J= 8,5 Hz), 8,17 - 8,27 (1 H, m), 7,95 - 8,03 (1 H, m), 7,83 - 7,94 (1 H, m), 7,42-7,55 (2 H, m), 7,13-7,26 (2 H, m), 4,65-4,83 (1 H, m), 3,68-3,77 (2 H, m), 3,55 (3 H, s), 3,23-3,34 (2 H, m), 2,84 (3 H, s), 2,78 (3 H, s), 1,98-2,08 (2 H, m), 1,59-1,71 (2 H, m).
Ejemplo 84. ácido 4-[4-(4-Metilquinolin-3-il)-fenoxi]-piperidina-1 -carboxílico etilamida.
Método A Ejemplo 73 usando etil amina. Análisis: LCMS m/z = 390 (M 1); 1H NMR (DMSO-d6) 6: 10,26 (1 H, m; D2 O exch), 8,73 (1 H, s), 8,19 (1 H, d, J = 8,3 Hz), 8,04 (1 H, d, J=8,3 Hz), 7,77 (1 H, td, J=7,5, 1,3 Hz), 7,63 - 7,71 (1 H, m), 7,40 (2 H, d, J=8,8 Hz), 7,13 (2 H, d, J=8,8 Hz), 6,51 (1 H, t, J = 5,3 Hz), 4,63 (1 H, dt, J = 8,0, 4,2 Hz), 3,65- 3,79 (2 H, m), 2,99 - 3,18 (4 H, m), 2,63 (3 H, s), 1,88 - 2,02 (2 H, m), 1,45 - 1,62 (2 H, m), 1,02 (3 H, t, J = 7,2 Hz).
E je m p lo 85. á c id o 4 -[4 -(8 -M e to x iq u in o lin -7 - i l) - fe n o x i] -p ip e r id in a -1 -c a rb o x í l ic o m e tila m id a .
Método A Ejemplo 73 usando metil amina en metanol. Análisis: LCMS m/z = 392 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,14 (1 H, d, J=3,8 Hz), 8,96 (1 H, br. s.), 8,05 (1 H, d, J=8,5 Hz), 7,92 (1 H, d, J = 7,8 Hz), 7,87 (1 H, d, J = 8,5 Hz), 7,69 (2 H, d, J = 8,8 Hz), 7,16 (2 H, d, J = 8,8 Hz), 4,61 - 4,70 (1 H, m), 3,74 (3 H, s), 3,70 (2 H, d, J = 4,8 Hz), 3,13 (2 H, ddd, J = 13,2, 9,7, 3,0 Hz), 2,58 (3 H, s), 1,90 - 2,00 (2 H, m), 1,47 - 1,59 (2 H, m).
Ejemplo 86. ácido 4-[4-(8-Metoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico etilamida.
Método A Ejemplo 73 usando etil amina HCl. Análisis: LCMS m/z = 406 9M 1): 1H NMR (DMSO-d6, Sal de HCl) 6: 9,17 (1 H, d, J = 4,0 Hz), 9,02 (1 H, d, J = 7,8 Hz), 8,09 (1 H, d, J = 8,5 Hz), 7,94 - 8,03 (1 H, m), 7,91 (1 H, d, J = 8,3 Hz), 7,70 (2 H, d, J = 8,8 Hz), 7,17 (2 H, d, J = 8,8 Hz), 4,66 (1 H, dt, J = 8,2, 4,2 Hz), 3,72 (5 H, s), 3,01 - 3,21 (4 H, m), 1,86 - 2,04 (2 H, m), 1,45 - 1,61 (2 H, m), 0,98 -1,05 (3 H, m).
Ejemplo 87. ácido 4-[4-(4-Metilquinolin-3-il)-fenoxi]-piperidina-1 -carboxílico hidroxiamida.
Análisis: LCMS m/z = 378 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 8,71 (1 H, s), 8,21 (1 H, d, J = 8,3 Hz), 8,05 (1 H, d, J = 8,5 Hz), 7,81 (1 H, t, J = 7,5 Hz), 7,66 - 7,76 (1 H, m), 7,41 (2 H, d, J = 8,3 Hz), 7,10 - 7,21 (2 H, m), 4,66(1 H, br. s.), 3,66 (2 H, d, J = 13,8 Hz), 3,17 (2 H, t, J = 9,9 Hz), 2,64 (3 H, s), 1,89 - 2,05 (2 H, m), 1,49 - 1,69 (2 H, m).
Ejemplo 88. N-etil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida.
Método A Ejemplo 73 usando etil amina HCl. Análisis: LCMS m/z = 390 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,13 (d, J = 3,8 Hz, 1H), 8,83 (br. s., 1H), 8,07 (d, J = 8,3 Hz, 1H), 7,85 (br. s., 1H), 7,68 (d, J = 8,3 Hz, 1H), 7,40 (d, J = 8,3 Hz, 2H), 7,13 (d, J = 8,5 Hz, 2H), 4,64 (d, J = 3,8 Hz, 1H), 3,72 (d, J = 13,6 Hz, 2H), 3,02-3,20 (m, 4H), 2,72 (s, 3H), 1,95 (d, J = 9,5 Hz, 2H), 1,47-1,65 (m, 2H), 1,02 (t, J = 7,2 Hz, 3H).
Método B. A 8-Metil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina dihidrocloruro (0,1 g, 0,31 mmol) y DIEA (0,16 mL, 0,94 mmol) en DCM (2 mL) se añadió isocianatoetano (0,27 g, 0,30 mL, 3,8 mmol) luego se agitó a 70 °C por 2 h. La reacción se concentró, se disolvió en EtOAc y se lavó con 1N Na2CO3 y salmuera y se secó (MgSO4). El producto se sometió a cromatografía en ISCO (24g de gel de sílice, 50-100% EtOAC-hexanos) para dar un aceite. La sal de HCl (sintetizado a partir de 1N HCl-éter y DCM) se cristalizó a partir de DCM-éter para dar un sólido amarillo (69%).
E je m p lo 89 N ,N -d im e t il-4 -[4 -(8 -m e t i l- 7 -q u in o li l) fe n o x i]p ip e r id in a -1 -c a rb o x a m id a .
A 8-metil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina dihidrocloruro (0,150 g, 0,383 mmol) en DCM (4 mL) se añadió TEA (0,214 mL, 1,53 mmol) y N,N-dimetilcarbamoil cloruro (0,0824 g, 0,767 mmol). Después de agitar a temperatura ambiente por 2h, la mezcla se concentró, se lavó con 1N Na2CO3 y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (12 g de gel de sílice, EtOAc/hexanos 40-80%) para dar un aceite. La sal de HCl se sintetizó añadiendo 0,5 mL de a 2M HCl éter solución a una solución de DCM de base. La sal se cristalizó a partir de DCM-éter para dar un sólido amarillo (87%). Análisis: LCMS m/z = 390 (M 1); 1H NMR (DMSO-d6) 6: 9,15 (d, J=3,5Hz, 1H), 8,89 (d, J=7,3Hz, 1H), 8,11 (d, J=8,5Hz, 1H), 7,90 (dd, J=7,8, 4,5Hz, 1H), 7,71 (d, J=8,3Hz, 1H), 7,41 (d, J=8,5Hz, 2H), 7,14 (d, J=8,5Hz, 2H), 4,66(dt, J=8,0, 4,2 Hz, 1H), 3,30-3,62 (m, 2H), 3,04 (ddd, J=12,9, 9,5, 2,9 Hz, 2H), 2,75 (s, 6H), 2,73 (s, 3H), 1,91-2,07 (m, 2H), 1,52-1,78 (m, 2H).
Ejemplo 90. Etil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato.
A 8-metil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina 2HCl (0,150 g, 0,383 mmol) en DCM (4 mL) se añadió TEA (0,214 mL, 1,53 mmol) y etil cloroformato (0,0832 g, 0,767 mmol). Después de agitar a temperatura ambiente por 2 h, la mezcla se concentró, se lavó con 1N Na2CO3 y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (12 g de gel de sílice, EtOAc/hexanos 40-80%) para dar aceite. La sal de HCl (sintetizado a partir de 2N HCl-éter y DCM) se cristalizó a partir de DCM-éter-hexanos para dar un sólido amarillo claro (73%). Análisis: LCMS m/z = 391 (M 1); 1H NMR (DMSO-d6) 6: 9,14 (d, J = 4,3 Hz, 1H), 8,87 (br. s., 1H), 8,09 (d, J = 8,3 Hz, 1H), 7,88 (d, J = 4,8 Hz, 1H), 7,70 (d, J = 8,5 Hz, 1H), 7,41 (d, J = 8,8 Hz, 2H), 7,14 (d, J = 8,5 Hz, 2H), 4,64-4,78 (m, 1H), 4,06 (q, J = 7,1 Hz, 2H), 3,68 3,84 (m, 2H), 3,28 (t, J = 9,5 Hz, 2H), 2,67-2,80 (m, 3H), 1,98 (d, J = 7,3 Hz, 2H), 1,60 (dtd, J = 12,7, 8,6, 3,9 Hz, 2H), 1,20 (t, J = 7,0 Hz, 3H).
Ejemplo 91. N-metoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida.
A 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina 2HCl (0,15 g, 0,3833 mmol) en DCM (4 mL) se añadió TEA (0,214 mL, 1,533 mmol) y trifosgeno (0,1138 g, 0,3833 mmol) en un baño de hielo, se agitó por 1 h luego se concentró. El residuo en DCM (4 mL) se añadió TEA (0,214 mL, 1,533 mmol) y O-metilhidroxilamina HCl (0,06403 g, 0,7667 mmol) luego se calentó a 70 °C por 2 h. La mezcla se concentró, se lavó con 1N Na2CO3 y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (12 g de gel de sílice, EtOAc/hexanos 40-90% sobre 5 min) para dar y aceite. La sal de HCl (0,5 mL 2N HCl-éter se añadió a la solución de DCM de base) se cristalizó a partir de DCM-éter para dar un sólido amarillo claro (67%). Análisis: LCMS m/z = 392 (M 1); 1H NMR (DMSO-d6) 6: 9,75 (br. s., 1H), 9,08 (d, J = 3,8 Hz, 1H), 8,70 (br. s., 1H), 8,02 (d, J = 8,0 Hz, 1H), 7,77 (br. s., 1H), 7,63 (d, J = 8,5 Hz, 1H), 7,40 (d, J = 8,8 Hz, 2H), 7,12 (d, J = 8,8 Hz, 2H), 4,60-4,71 (m, 1H), 3,59-3,72 (m, 2H), 3,54 (s, 3H), 3,06-3,21 (m, 2H), 2,67-2,76 (m, 3H), 1,96 (d, J = 10,3 Hz, 2H), 1,47-1,64 (m, 2H)
E je m p lo 92. N - Is o p ro p il-4 -[4 -(8 -m e t i l- 7 -q u in o li l) fe n o x i]p ip e r id in a -1 -c a rb o x a m id a .
Este ejemplo se sintetizó usando isopropil amina por el procedimiento del ejemplo 91. Análisis: LCMS m/z = 404 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,08 (d, J = 3,3 Hz, 1H), 8,70 (br. s., 1H), 8,01 (d, J = 8,3 Hz, 1H), 7,77 (br. s., 1H), 7,63 (d, J = 8,3 Hz, 1H), 7,39 (d, J = 8,8 Hz, 2H), 7,12 (d, J = 8,5 Hz, 2H), 6,20 (br. s., 1H), 4,63 (dt, J = 7,7, 4,0 Hz, 2H), 3,69-3,81 (m, 3H), 3,11 (t, J = 9,8 Hz, 2H), 2,70 (s, 3H), 1,95 (d, J = 10,3 Hz, 2H), 1,46-1,59 (m, 2H), 1,07 (d, J = 6,5 Hz, 6H).
Ejemplo 93. N-etoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida.
Este ejemplo se sintetizó usando O-etilhidroxilamina HCl. Análisis: LCMS m/z = 406 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,66 (br. s., 1H), 9,07 (d, J = 3,3 Hz, 1H), 8,67 (br. s., 1H), 8,00 (d, J = 8,3 Hz, 1H), 7,76 (br. s., 1H), 7,61 (d, J = 8,5 Hz, 1H), 7,39 (d, J = 8,5 Hz, 2H), 7,12 (d, J = 8,5 Hz, 2H), 4,65 (dt, J = 8,0, 3,9 Hz, 1H), 3,75 (q, J = 7,0 Hz, 2H), 3,69-3,58 (m, 2H), 3,22-3,06 (m, 2H), 2,72-2,68 (m, 3H), 1,96 (d, J = 12,5 Hz, 2H), 1,62-1,50 (m, 2H), 1,13 (t, J = 7,0 Hz, 3H).
Ejemplo 94. [4-[4-(8-metil-7-quinolil)fenoxi]-1 -piperidil]-pirrolidin-1 -il-metanona.
Este ejemplo se sintetizó usando pirrolidina-1-carbonil cloruro. Análisis: LCMS m/z = 390 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,15 (d, J = 3,5 Hz, 1H), 8,89 (d, J = 7,3 Hz, 1H), 8,11 (d, J = 8,5 Hz, 1H), 7,90 (dd, J = 7,8, 4,5 Hz, 1H), 7,71 (d, J = 8,3 Hz, 1H), 7,41 (d, J=8,5 Hz, 2H), 7,14 (d, J=8,5 Hz, 2H), 4,66 (dt, J = 8,0, 4,2 Hz, 1H), 3,30-3,62 (m, 2H), 3,04 (ddd, J=12,9, 9,5, 2,9 Hz, 2H), 2,75 (s, 6H), 2,73 (s, 3H), 1,91-2,07 (m, 2H), 1,52-1,78 (m, 2H).
Ejemplo 95. N-metil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida.
Este ejemplo se sintetizó usando metilamina acuosa y trifosgeno. Análisis: LCMS m/z = 376 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,10 (d, J = 3,3 Hz, 1H), 8,74 (br. s., 1H), 8,03 (d, J = 8,8 Hz, 1H), 7,79 (br. s., 1H), 7,64 (d, J = 8,5 Hz, 1H), 7,40 (d, J = 8,8 Hz, 2H), 7,12 (d, J = 8,5 Hz, 2H), 4,63 (dd, J = 7,8, 4,3 Hz, 2H), 3,71 (d, J = 13,6 Hz, 2H), 3,20-3,04 (m, 2H), 2,71 (s, 3H), 2,58 (s, 3H), 2,04-1,88 (m, 2H), 1,61-1,48 (m, 2H).
Ejemplo 96. 4-[4-(8-metil-7-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida.
Este ejemplo se sintetizó usando n-propilamina y trifosgeno. Análisis: LCMS m/z = 404 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,13 (d, J = 3,5 Hz, 1H), 8,85 (br. s., 1H), 8,08 (d, J = 8,3 Hz, 1H), 7,87 (br. s., 1H), 7,69 (d, J = 8,5 Hz, 1H), 7,41 (d, J = 8,8 Hz, 2H), 7,13 (d, J = 8,5 Hz, 2H), 4,64 (dt, J = 8,3, 4,1 Hz, 1H), 3,80-3,66 (m, 2H), 3,23-3,07 (m, 2H), 2,99 (t, J = 7,2 Hz, 2H), 2,72 (s, 3H), 1,95 (d, J = 9,8 Hz, 2H), 1,60-1,49 (m, 2H), 1,46-1,37 (m, 2H), 0,84 (t, J = 7,4 Hz, 3H).
Ejemplo 97. 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida.
Este ejemplo se sintetizó usando amoníaco en metanol y trifosgeno. Análisis: LCMS m/z = 362 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 8,97 (dd, J = 4,1, 1,9 Hz, 1H), 8,36 (dd, J = 8,2, 1,6 Hz, 1H), 7,85 (d, J=8,3 Hz, 1H), 7,55 (dd, J=8,3, 4,3 Hz, 1H), 7,48 (d, J=8,5 Hz, 1H), 7,37 (d, J=8,5 Hz, 2H), 7,10 (d, J=8,8 Hz, 2H), 5,96 (s, 2H, D2 O exch), 4,67-4,59 (m, 1H), 3,71 (d, J = 14,3 Hz, 2H), 3,29 (s, 1H), 3,18-3,07 (m, 2H), 2,68 (s, 3H), 1,95 (d, J = 9,0 Hz, 2H).
Ejemplo 98. [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(1-piperidil)metanona.
Este ejemplo se sintetizó usando piperidina-1-carbonil cloruro. Análisis: LCMS m/z = 430 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,08 (d, J = 3,3 Hz, 1H), 8,69 (br. s., 1H), 8,01 (d, J = 8,5 Hz, 1H), 7,77 (br. s., 1H), 7,62 (d, J = 8,5 Hz, 1H), 7,39 (d, J = 8,5 Hz, 2H), 7,19-7,08 (m, 2H), 4,64 (dt, J = 8,1, 4,1 Hz, 1H), 3,49-3,40 (m, 2H), 3,15-3,10 (m, 4H), 3,05 (ddd, J = 12,9, 9,5, 3,1 Hz, 2H), 2,70 (s, 3H), 2,06-1,93 (m, 2H), 1,70-1,58 (m, 2H), 1,57-1,46 (m, 6H).
Ejemplo 99. [4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-morfolino-metanona.
Este ejemplo se sintetizó usando morfolina-4-carbonil cloruro. Análisis: LCMS m/z = 432 (M 1); 1H NMR (DMSO-d6; Sal de HCl) 6: 9,13 (d, J = 3,5 Hz, 1H), 8,82 (d, J = 5,8 Hz, 1H), 8,07 (d, J = 8,3 Hz, 1H), 7,92-7,79 (m, 1H), 7,68 (d, J = 8,5 Hz, 1H), 7,41 (d, J = 8,5 Hz, 2H), 7,14 (d, J = 8,8 Hz, 2H), 4,67 (dt, J = 7,9, 4,1 Hz, 1H), 3,61-3,54 (m, 4H), 3,53 - 3,45 (m, 2H), 3,20-3,04 (m, 6H), 2,72 (s, 3H), 2,00 (d, J = 12,0 Hz, 2H), 1,73 - 1,57 (m, 2H).
Los siguientes ejemplos se sintetizaron usando los procedimientos representativos descritos anteriormente para el ejemplo 3 o ejemplo 33.
E je m p lo 100. C ic lo p ro p il-[4 -(4 -q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] -m e ta n o n a ,H C l.
El producto se aisló como un sólido amarillo. Análisis: mp: 170-173 °C; LCMS m/z = 373 (M+1); 1H NMR (DMSO- d6) 6: 9,51 (d, J = 2Hz, 1H), 9,15 (s, 1H), 8,29-8,24 (m, 2H), 8,00-7,95 (m, 3H), 7,87-7,83 (m, 1H), 7,23 (m, 2H), 4,79 (m, 1H), 4,08-3,82 (m, 2H), 3,66-3,49 (m, 1H), 3,39-3,22 (m, 1H), 2,13-1,87 (m, 3H), 1,75-1,46 (m, 2H), 0,79-0,65 (m, 4H). Ejemplo 101. Ciclobutil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: mp: 164-166 °C; LCMS m/z = 387 (M+1); 1H NMR (DMSO- d6) 6: 9,53 (d, J = 2Hz, 1H), 9,17 (s, 1H), 8,31-8,24 (m, 2H), 8,01-7,84 (m, 4H), 7,21 (m, 2H), 4,75 (m, 1H), 3,94-3,82 (m, 1H), 3,66-3,53 (m, 1H), 3,44-3,21 (m, 3H), 2,25-2,03 (m, 4H), 2,02-1,83 (m, 3H), 1,80-1,68 (m, 1H), 1,64-1,47 (m, 2H). Ejemplo 102. Ciclopentil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 145-147 °C; LCMS m/z = 401 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,52 (m, 1H), 9,16 (s, 1H), 8,27 (m, 2H), 8,02-7,82 (m, 4H), 7,22 (m, 2H), 4,77 (m, 1H), 3,97-3,74 (m, 2H), 3,48-3,21 (m, 2H), 3,02 (m, 1H), 2,08-1,88 (m, 2H), 1,84-1,45 (m, 10H).
Ejemplo 103. [4-(4-Quinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona, HCl.
El producto se aisló como un sólido marrón claro. Análisis: LCMS m/z = 403 (M+1); 1H NMR (400 MHz, DMSO- d6) 6: 9,52 (m, 1H), 9,16 (s, 1H), 8,26 (m, 2H), 7,99 (m, 1H), 7,93 (m, 2H), 7,85 (m, 1H), 7,22 (m, 2H), 4,78 (m, 1H), 4,70 (m, 1H), 3,95-3,70 (m, 4H), 3,66-3,07 (m, 2H), 2,12-1,75 (m, 4H), 1,73-1,45 (m, 2H), 1,33-1,21 (m, 2H).
Ejemplo 104. [4-(4-Quinolin-3-il-fenoxi)-piperidin-1-il]-(S)-tetrahidrofuran-2-il-metanona, HCl.
El producto se aisló como un sólido marrón claro. Análisis: LCMS m/z = 403 (M+1); 1H NMR (400 MHz, DMSO- d6) ó: 9,53 (m, 1H), 9,19 (s, 1H), 8,28 (m, 2H), 8,00 (m, 1H), 7,94 (m, 2H), 7,86 (m, 1H), 7,22 (m, 2H), 4,78 (m, 1H), 4,70 (m, 1H), 3,95-3,70 (m, 4H), 3,53-3,22 (m, 2H), 2,12-1,74 (m, 4H), 1,72-1,48 (m, 2H), 1,33-1,15 (m, 2H).
Ejemplo 105. 2-Metoxi-1-[4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona, 2HCl.
El producto se aisló como un sólido canela. Análisis: LCMS m/z = 377 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,53 (m, 1H), 9,20 (s, 1H), 8,29 (m, 2H), 8,00 (m, 1H), 7,94 (m, 2H), 7,87 (m, 1H), 7,22 (m, 2H), 4,78 (m, 1H), 4,11 (m, 2H), 3,87 (m, 1H), 3,66 (m, 1H), 3,32 (m, 2H), 3,30 (s, 3H), 1,99 (m, 2H), 1,62 (m, 2H).
Ejemplo 106. [4-(4-Quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona, 2HCl.
El producto se aisló como un sólido canela. Análisis: LCMS m/z = 417 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,54 -9,58 (1 H, m), 9,22 - 9,26 (1 H, m), 8,25 - 8,33 (2 H, m), 7,99 - 8,06 (1H, m), 7,93-7,97 (2H, m), 7,85-7,91 (1H, m), 7,20-7,25 (2H, m), 4,74-4,83 (1H, m), 4,12-4,19 (1H, m), 3,76-3,92 (3H, m), 3,56-3,65 (1H, m), 3,42-3,53 (2H, m), 3,08 3,16 (1H, m), 1,88-2,08 (2H, m), 1,79-1,86 (1H, m), 1,43-1,66 (7H, m), 1,24-1,32 (12H, m).
Ejemplo 107. [4-(4-Quinolin-3-il-fenoxil)-piperidin-1-il]-(tetrahidrofuran-3-il)-metanona, 2HCl.
Análisis: LCMS m/z = 403 (M+1); 1HNMR (400 MHz, DMSO-d6) ó: 9,53 (m, 1H), 9,19 (s, 1H), 8,28 (m, 2H), 8,00 (m, 1H), 7,94 (m, 2H), 7,86 (m, 1H), 7,22 (m, 2H), 4,78 (m, 1H), 3,96-3,55 (m, 4H), 3,50-3,27 (m, 3H), 2,10-1,89 (m, 4H), 1,70-1,50 (m, 2H), 1,33-1,22 (m, 2H).
Ejemplo 108. (R)-2-Metoxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona, 2HCl.
Análisis: LCMS m/z = 391 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,22 - 9,25 (1 H, m), 8,57 - 8,59 (1 H, m), 8,01 -8,06 (2 H, m), 7,81 - 7,86 (2 H, m), 7,72 - 7,78 (1 H, m), 7,60 - 7,67 (1 H, m), 7,15 - 7,20 (2 H, m), 4,70 - 4,79 (1 H, m), 4,20 - 4,29 (1 H, m), 3,80 - 3,98 (2 H, m), 3,38 - 3,50 (1 H, m), 3,33 - 3,38 (1 H, m), 3,22 (3 H, s), 1,92 - 2,07 (2 H, m), 1,51 - 1,73 (2 H, m), 1,23 (3 H, d, J=6,8 Hz).
E je m p lo 109. (S ) -2 -M e to x i-1 -[4 -(4 -q u in o lin -3 - i l - fe n o x i) -p ip e r id in -1 - i l ] - p ro p a n -1 -o n a , 2 H C l.
Análisis: LCMS m/z = 391 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,22 - 9,25 (1 H, m), 8,57 - 8,60 (1 H, m), 8,01 -8,06 (2 H, m), 7,81 - 7,86 (2 H, m), 7,72 - 7,78 (1 H, m), 7,60 - 7,66 (1 H, m), 7,15 - 7,20 (2 H, m), 4,71 - 4,79 (1 H, m), 4,20 - 4,28 (1 H, m), 3,81 - 3,97 (2 H, m), 3,39 - 3,50 (1 H, m), 3,33 - 3,38 (1 H, m), 3,22 (3 H, s), 1,93 - 2,08 (2 H, m), 1,51 - 1,71 (2 H, m), 1,23 (3 H, d, J=6,5 Hz).
Ejemplo 110. 2-Hidroxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona, 2HCl.
El producto se aisló como un sólido marrón claro. Análisis: LCMS m/z = 363 (M+1); 1H NMR (400 MHz, DMSO- d6) 6: 9,23 (1 H, d, J=2,5 Hz), 8,58 (1 H, d, J=2,3 Hz), 8,03 (2 H, d, J=8,1 Hz), 7,84 (2 H, d, J=8,8 Hz), 7,70 - 7,78 (1 H, m), 7,60 - 7,67 (1 H, m), 7,17 (2 H, d, J=7,9 Hz), 4,70 - 4,79 (1 H, m), 4,53 (1 H, t, J=5,4 Hz), 4,12 (2 H, d, J=5,5 Hz), 3,83 - 3,94 (1 H, m), 3,55 - 3,67 (1 H, m), 3,34 - 3,39 (1 H, m), 3,24 - 3,31 (1 H, m), 1,92 - 2,07 (2 H, m), 1,52 - 1,72 (2 H, m).
Ejemplo 111. [4-(4-Quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 399 (M+1); 1HNMR (400 MHz, DMSO-d6) 6: 9,53 (s, 1H), 9,18 (s, 1H), 8,27 (m, 2H), 8,06-7,81 (m, 5H), 7,23 (m, 2H), 7,01 (m, 1H), 6,64 (m, 1H), 4,84 (m, 1H), 3,99 (m, 2H), 3,58 (m, 2H), 2,06 (m, 2H), 1,70 (m, 2H).
Ejemplo 112. 1-[4-(4-Quinolin-3-il-fenoxi)-piperidin-1-il]-etanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 347 (M+1); 1HNMR (400 MHz, DMSO-d6) 6: 9,57 (m, 1H), 9,26 (s, 1H), 8,32 (m, 2H), 8,03 (m, 1H), 7,95 (m, 2H), 7,89 (m, 1H), 7,23 (m, 2H), 4,77 (m, 1H), 3,92-3,82 (m, 1H), 3,76-3,66 (m, 1H), 3,44-3,34 (m, 1H), 3,32-3,23 (m, 1H), 2,03 (s, 3H), 2,07-1,87 (m, 2H), 1,72-1,48 (m, 2H).
E je m p lo 113. 2 -M e t il- 1 -[4 -(4 -q u in o lin -3 - i l - fe n o x i) -p ip e r id in -1 - i l ] - p ro p a n -1 -o n a , H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 375 (M+1); 1HNMR (400 MHz, DMSO-d6) 6: 9,51 (m, 1H), 9,14 (s, 1H), 8,26 (m, 2H), 8,02-7,80 (m, 4H), 7,21 (m, 2H), 4,77 (m, 1H), 3,97-3,73 (m, 2H), 3,49-3,21 (m, 2H), 2,91 (m, 1H), 2,09-1,89 (m, 2H), 1,71-1,46 (m, 2H), 1,01 (d, J=6,7 Hz, 6H).
Ejemplo 114. 2,2-Dimetil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 389 (M+1); 1HNMR (400 MHz, DMSO-d6) 6: 9,55 (m, 1H), 9,15 (s, 1H), 8,26 (m, 2H), 7,98 (m, 1H), 7,94 (m, 2H), 7,85 (m, 1H), 7,21 (m, 2H), 4,78 (m, 1H), 3,98-3,86 (m, 2H), 3,45-3,34 (m, 2H), 2,05-1,94 (m, 2H), 1,65-1,53 (m, 2H), 1,22 (s, 9H).
Ejemplo 115. (2-Metiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 417 (M+1); 1HNMR (400 MHz, DMSO-d6) 6: 9,52 (m, 1H), 9,17 (s, 1H), 8,26 (m, 2H), 7,99 (m, 1H), 7,94 (m, 2H), 7,85 (m, 1H), 7,21 (m, 2H), 4,77 (m, 1H), 4,41-3,11 (m, 6H), 2,72-2,61 (m, 1H), 2,08-1,47 (m, 7H), 1,40 (s, 3H).
Ejemplo 116. (2-Metil-1,3-dioxolan-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido canela. Análisis: LCMS m/z = 419 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,22 -9,26 (1 H, m), 8,56 - 8,60 (1 H, m), 8,01 - 8,07 (2 H, m), 7,80 - 7,88 (2 H, m), 7,72 - 7,79 (1 H, m), 7,60 - 7,67 (1 H, m), 7,14 - 7,22 (2 H, m), 4,70 - 4,84 (1 H, m), 3,98 - 4,04 (1 H, m), 3,92 - 3,98 (2 H, m), 3,77 - 3,86 (2 H, m), 3,48-3,65 (1H, m), 3,35-3,48 (2H, m), 3,33 (3H, s), 1,95-2,08 (2H, m), 1,55-1,76 (2H, m).
Ejemplo 117. 2-Metanosulfonil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona, HCl.
El producto se aisló como un sólido canela. Análisis: LCMS m/z = 425 (M+1); 1HNMR (400 MHz, DMSO-d6) ó: 9,51 (m, 1H), 9,15 (s, 1H), 8,26 (m, 2H), 7,98 (m, 1H), 7,94 (m, 2H), 7,85 (m, 1H), 7,23 (m, 2H), 4,80 (m, 1H), 4,51 (s, 2H), 3,96-3,77 (m, 2H), 3,57-3,34 (m, 2H), 3,12 (s, 3H), 2,11-1,92 (m, 2H), 1,79-1,52 (m, 2H).
Ejemplo 118. (1,1-Dioxidotetrahidrotiofen-2-il)(4-(4-(quinolin-3-il)fenoxi)piperidin-1-il)metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 451 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,51 (s, 1H), 9,15 (s, 1H), 8,26 (m, 2H), 7,98 (m, 1H), 7,94 (m, 2H), 7,85 (m, 1H), 7,23 (m, 2H), 4,82 (m, 1H), 4,67 (m, 1H), 4,08-3,79 (m, 2H), 3,64-3,44 (m, 2H), 3,39-3,19 (m, 2H), 3,14-3,00 (m, 1H), 2,26-1,46 (m, 7H).
Ejemplo 119. (3,3-Difluorociclobutil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
El producto se aisló como un sólido blancuzco. Análisis: LCMS m/z = 423 (M+1); 1H NMR (400 MHz, DMSO- d6) ó: 9,21 - 9,25 (1 H, m), 8,56 - 8,60 (1 H, m), 8,01 - 8,06 (2 H, m), 7,81 - 7,86 (2 H, m), 7,72 - 7,78 (1 H, m), 7,60 - 7,67 (1 H, m), 7,14 - 7,20 (2 H, m), 4,69 - 4,78 (1 H, m), 3,84 - 3,93 (1 H, m), 3,60 - 3,70 (1 H, m), 3,33 - 3,39 (2 H, m), 3,23 -3,31 (1 H, m), 2,73 - 2,86 (4 H, m), 1,91 - 2,04 (2 H, m), 1,53 - 1,69 (2 H, m).
Ejemplo 120. (R)-5-[4-(4-Quinolin-3-il-fenoxi)-piperidina-1-carbonil]-dihidrofuran-2-ona, HCl.
LCMS m/z = sólido canela. Análisis: LCMS m/z = 417 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,48 - 9,51 (1 H, m), 9,08 - 9,13 (1 H, m), 8,20 - 8,28 (2 H, m), 7,90 - 8,00 (3 H, m), 7,80 - 7,86 (1 H, m), 7,20 - 7,26 (2 H, m), 5,51 - 5,57 (1 H, m), 4,75 - 4,86 (1 H, m), 3,68 - 3,97 (2 H, m), 3,28 - 3,52 (2 H, m), 2,39 - 2,49 (3 H, m), 2,14 - 2,26 (1 H, m), 1,92 -2,11 (2 H, m), 1,56 - 1,78 (2 H, m).
Ejemplo 121. (3-Metilfuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 413 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,51 - 9,55 (1 H, m), 9,14 - 9,20 (1 H, m), 8,23 - 8,32 (2 H, m), 7,92 - 8,04 (3 H, m), 7,82 - 7,89 (1 H, m), 7,67 - 7,72 (1 H, m), 7,20 - 7,27 (2 H, m), 6,48 - 6,53 (1 H, m), 4,78 - 4,88 (1 H, m), 3,83 - 3,96 (2 H, m), 3,43 - 3,55 (2 H, m), 2,16 (3 H, s), 2,00 - 2,11 (2 H, m), 1,62 - 1,75 (2 H, m).
E je m p lo 122. (3 ,5 -D im e ti lfu ra n -2 - i l) -[4 -(4 -q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] -m e ta n o n a , H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 427 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,51 - 9,56 (1 H, m), 9,15 - 9,21 (1 H, m), 8,22 - 8,34 (2 H, m), 7,92 - 8,04 (3 H, m), 7,82 - 7,90 (1 H, m), 7,20 - 7,27 (2 H, m), 6,10 - 6,14 (1 H, m), 4,78 - 4,87 (1 H, m), 3,86 - 3,96 (2 H, m), 3,42 - 3,53 (2 H, m), 2,27 (3 H, s), 2,11 (3 H, s), 2,00 - 2,09 (2 H, m), 1,61 - 1,73 (2 H, m).
Ejemplo 123. Oxazol-2-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 400 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,50 - 9,56 (1 H, m), 9,14 - 9,21 (1 H, m), 8,22 - 8,35 (3 H, m), 7,91 - 8,03 (3 H, m), 7,82 - 7,89 (1 H, m), 7,44 - 7,49 (1 H, m), 7,20 - 7,28 (2 H, m), 4,81 - 4,90 (1 H, m), 4,21 - 4,32 (1 H, m), 3,94 - 4,04 (1 H, m), 3,81 - 3,91 (1 H, m), 3,54 - 3,63 (1 H, m), 2,03 - 2,13 (2 H, m), 1,67 - 1,81 (2 H, m).
Ejemplo 124. Isoxazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 400 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,51 - 9,55 (1 H, m), 9,16 - 9,20 (1 H, m), 9,09 - 9,12 (1 H, m), 8,23 - 8,33 (2 H, m), 7,92 - 8,03 (3 H, m), 7,83 - 7,89 (1 H, m), 7,21 - 7,27 (2 H, m), 6,85 - 6,88 (1 H, m), 4,82 - 4,90 (1 H, m), 3,96 - 4,06 (1 H, m), 3,74 - 3,83 (1 H, m), 3,47 - 3,63 (2 H, m), 1,99 - 2,13 (2 H, m), 1,65 - 1,79 (2 H, m).
Ejemplo 125. Isotiazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 416 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,51 - 9,55 (1 H, m), 9,14 - 9,20 (2 H, m), 8,23 - 8,32 (2 H, m), 7,91 - 8,03 (3 H, m), 7,82 - 7,89 (1 H, m), 7,60 - 7,64 (1 H, m), 7,21 - 7,27 (2 H, m), 4,80 - 4,89 (1 H, m), 3,98 - 4,07 (1 H, m), 3,80 - 3,89 (1 H, m), 3,48 - 3,61 (2 H, m), 1,99 - 2,14 (2 H, m), 1,64 - 1,78 (2 H, m).
E je m p lo 126. [4 -(4 -Q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] -( te t ra h id ro fu ra n -2 - i l) -m e ta n o n a , H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 403 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,47 - 9,51 (1 H, m), 9,08 - 9,12 (1 H, m), 8,20 - 8,27 (2 H, m), 7,89 - 8,00 (3 H, m), 7,80 - 7,86 (1 H, m), 7,19 - 7,25 (2 H, m), 4,73 - 4,82 (1 H, m), 4,66 - 4,73 (1 H, m), 4,27 - 4,32 (1 H, m), 3,75 - 3,82 (4 H, m), 1,96 - 2,06 (3 H, m), 1,80 - 1,87 (4 H, m), 1,53 - 1,68 (2 H, m).
Ejemplo 127. Fenil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 409 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,46 - 9,51 (1 H, m), 9,05 - 9,10 (1 H, m), 8,18 - 8,27 (2 H, m), 7,89 - 7,99 (3 H, m), 7,78 - 7,85 (1 H, m), 7,40 - 7,49 (5 H, m), 7,19 - 7,25 (2 H, m), 4,77 -4,85 (1 H, m), 3,91 - 4,11 (1 H, m), 3,43 - 3,64 (2 H, m), 3,26 - 3,43 (1 H, m), 1,90 - 2,14 (2 H, m), 1,60 - 1,78 (2 H, m).
Ejemplo 128. (2,5-Dimetilfenil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 437 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,46 - 9,51 (1 H, m), 9,07 - 9,12 (1 H, m), 8,20 - 8,28 (2 H, m), 7,89 - 8,00 (3 H, m), 7,80 - 7,86 (1 H, m), 7,18 - 7,24 (2 H, m), 7,03 - 7,12 (3 H, m), 4,75 - 4,84 (1 H, m), 3,95 - 4,16 (1 H, m), 3,32 - 3,62 (2 H, m), 3,13 - 3,24 (1H, m), 2,29 (3H, s), 2,20 (3H, s), 2,02-2,13 (1H, m), 1,85-1,97 (1H, m), 1,64-1,77 (1H, m), 1,48-1,62 (1H, m).
Ejemplo 129. [3-(1H-Imidazol-2-il)-fenil]-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 475 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 15,02 - 15,51 (1 H, m), 9,44 - 9,48 (1 H, m), 9,01 - 9,06 (1 H, m), 8,18 - 8,31 (4 H, m), 7,89 - 7,97 (3 H, m), 7,84 (3 H, s), 7,68 - 7,76 (2 H, m), 7,20 - 7,26 (2 H, m), 4,80 - 4,89 (1 H, m), 3,96 - 4,13 (1 H, m), 3,48 - 3,66 (2 H, m), 3,31 - 3,48 (1 H, m), 2,00 - 2,18 (2 H, m), 1,66 - 1,81 (2 H, m).
E je m p lo 130. [3 -(1 H -B e n c im id a z o l-2 - i l ) - fe n il ] -[4 -(4 -q u in o lin -3 - i l - fe n o x i) -p ip e r id in -1 - i l ] -m e ta n o n a , H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 525 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,48 - 9,51 (1 H, m), 9,09 - 9,13 (1 H, m), 8,44 - 8,51 (2 H, m), 8,21 - 8,30 (2 H, m), 7,91 - 8,00 (3 H, m), 7,78 - 7,89 (5 H, m), 7,54 - 7,61 (2 H, m), 7,21 - 7,27 (2 H, m), 4,83 - 4,91 (1 H, m), 4,00 - 4,14 (2 H, m), 3,51 - 3,69 (2 H, m), 3,34 - 3,50 (1 H, m), 2,00 - 2,18 (2 H, m), 1,70 - 1,83 (2 H, m).
Ejemplo 131. N-Metoxi-4-[4-(8-metoxi-7-quinolil)fenoxi]piperidina-1-carboxamida, HCl.
Este ejemplo se sintetizó usando el procedimiento para el ejemplo 91 comenzando con 8-metoxi-7-[4-(4-piperidiloxi)fenil]quinolina 2HCl para dar un sólido amarillo. Análisis: LCm S m/z = 408 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,68 - 9,86 (1 H, m), 9,11 - 9,18 (1 H, m), 8,90 - 9,02 (1 H, m), 8,02 - 8,12 (1 H, m), 7,83 - 7,98 (2 H, m), 7,69 (2 H, d, J=8,5 Hz), 7,17 (2 H, d, J=8,8 Hz), 4,61 - 4,73 (1 H, m), 3,74 (3 H, s), 3,59 - 3,70 (2 H, m), 3,55 (3 H, s), 3,08 - 3,22 (2 H, m), 1,92 - 1,99 (2 H, m), 1,49-1,64 (2H, m).
Ejemplo 132. 1-[4-(5-Quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona, HCl.
Etapa 1. terc-butil éster del ácido 4-(5-Bromopiridin-2-iloxi)-piperidina-1-carboxílico.
A una solución de terc-butil éster del ácido 4-hidroxi-piperidina-1-carboxílico (5,75 g, 28,6 mmol) en DMF (50 mL) se añadió hidruro de sodio, 60% disp. en aceite mineral (1,35 g, 33,8 mmol) en forma de porciones. Después se agitó por 10 min, a la reacción se añadió 5-bromo-2-cloro-piridina (5,00 g, 26,0 mmol) seguido por K2 CO3 (3,59 g, 26,0 mmol). La reacción se calentó a 105 °C por 16 h y se enfrió hasta la temperatura ambiente. Se apagó cuidadosamente con H2 O (100 mL), se extrajo con EtOAc (3 x 300 mL). Las capas orgánicas combinadas se lavaron con H2 O, salmuera, se secaron (Na2SO4) y se concentraron. El residuo se sometió a cromatografía en gel de sílice (0-20% EtOAc/Hexanos) para dar un sólido blanco 8,30 g (89%).
Etapa 2. terc-butil éster del ácido 4-(5-Quinolin-3-il-piridin-2-iloxi)-piperidina-1 -carboxílico.
Un frasco cargado con terc-butil éster del ácido 4-(5-bromopiridin-2-iloxi)-piperidina-1-carboxílico (750 mg, 2,1 mmol), ácido 3-quinolinaborónico (540 mg, 3,1 mmol), acetato de paladio (47 mg, 0,21 mmol), trifenilfosfina (110 mg, 0,42 mmol), 1,0 M de carbonato de sodio en agua (8,4 mL, 8,4 mmol), 1,4-dioxano (5 mL), y DMF (10 mL) se enjuagó con N2 por 15 min. Después de agitarse a 85 °C por 16 h, la reacción se enfrió hasta la temperatura ambiente y se añadió EtOAc (100 mL), se lavó con solución 1M Na2CO3 (30 mL), H2 O, salmuera, se secó (Na2SO4), y se concentró. El residuo se sometió a cromatografía en gel de sílice (0-70% EtOAc/Hexanos) para dar un sólido grisáceo 723 mg (85%).
Etapa 3. 3-[6-(Piperidin-4-iloxi)-piridin-3-il]-quinolina, 2HCl.
A una solución de terc-butil éster del ácido 4-(5-quinolin-3-il-piridin-2-iloxi)-piperidina-1 -carboxílico (701 mg, 1,73 mmol) en DCM (25 mL) se añadió 4,0 M de HCl en 1,4-dioxano (4,32 mL, 17,3 mmol) y se agitó a temperatura ambiente por 24 h. El precipitado blanco resultante se recogió por filtración, se lavó con DCM, se secó para dar un sólido blanco
626 mg (96%).
Etapa 4.
A una solución de 3-[6-(piperidin-4-iloxi)-piridin-3-il]-quinolina, 2HCl (100 mg, 0,3 mmol) y Et3N en DCM (8 mL) se añadió cloruro de propanoilo (50 pL, 0,6 mmol). Después de 15 min, la reacción se diluyó con DCM (50 mL), se lavó con H2 O (2 x 20 mL), NaHCÜ3 saturado, salmuera, se secó (Na2SÜ4), y se concentró. El residuo se purificó por cromatografía en gel de sílice (0-100 EtOAc/Hexanos) y el producto aislado se disolvió en un disolvente mezclado MeOH-DCM (1:1), se trató con 1,2 eq. de solución 2 M HCl Et2 O, y se concentró. Se trató con una pequeña cantidad de MeOH-DCM (1:1) varias veces, se secó para dar un sólido canela 88 mg (80%). Análisis: LCMS m/z = 362 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,63 (1 H, d, J=2,3 Hz), 9,35 (1 H, s), 8,81 (1 H, d, J=2,8 Hz), 8,27 - 8,45 (3 H, m), 8,07 (1 H, ddd, J=8,5, 7,1, 1,3 Hz), 7,87- 7,96 (1 H, m), 7,05 (1 H, d, J=8,8 Hz), 5,33 (1 H, tt, J=8,2, 3,9 Hz), 3,89 - 4,01 (1 H, m), 3,69 - 3,81 (1 H, m), 3,32 - 3,44 (1 H, m), 3,20 - 3,32 (1 H, m), 2,36 (2 H, q, J=7,4 Hz), 1,94 - 2,12 (2 H, m), 1,52 - 1,76 (2 H, m), 1,01 (3 H, t, J=7,4 Hz).
Los siguientes compuestos se sintetizaron usando los procedimientos empleados en Ejemplo 132 anterior.
Ejemplo 133. 2-Metil-1-[4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona, HCl.
El producto se aisló como un sólido blancuzco. Análisis: LCMS m/z = 376 (M+1); 1H NMR (400 MHz, DMSO- d6) ó: 9,62 (1 H, d, J=2,0 Hz), 9,33 (1 H, s), 8,81 (1 H, d, J=2,3 Hz), 8,26 - 8,42 (3 H, m), 8,09 - 8,10 (1 H, m), 7,89 - 7,95 (1 H, m), 7,05 (1 H, d, J=8,5 Hz), 5,34 (1 H, tt, J=8,2, 3,9 Hz), 3,91 - 4,02 (1 H, m), 3,78 - 3,88 (1 H, m), 3,37 - 3,50 (1 H, m), 3,20 - 3,32 (1 H, m), 2,92 (1 H, quin, J=6,8 Hz), 1,94-2,15 (2 H, m), 1,52-1,76 (2 H, m), 0,97-1,06 (6 H, m).
Ejemplo 134. Ciclopropil-[4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido canela. Análisis: LCMS m/z = 374 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,57 (1H, d, J=2,3Hz), 9,22 (1H, s), 8,80 (1H, d, J=2,0Hz), 8,31-8,36 (2H, m), 8,25 (1H, d, J=7,8Hz), 8,02 (1 H, t, J=7,7Hz), 7,87(1H, t, J=7,5Hz), 7,05 (1 H, d, J=8,5Hz), 5,35 (1 H, tt, J=8,2, 3,9Hz), 3,90-4,12 (2H, m), 3,50-3,65 (1H, m), 3,20 3,35 (1H, m), 1,93-2,16 (3H, m), 1,52-1,79 (2 H, m), 0,67-0,80 (4H, m).
Ejemplo 135. 1-[4-(5-Quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona, HCl.
El producto se aisló como un sólido blancuzco. Análisis: LCMS m/z = 362 (M+1); 1H NMR (400 MHz, DMSO- d6) ó: 9.30 (1 H, dd, J=5,1, 1,4 Hz), 9,14 (1 H, d, J=8,0 Hz), 8,72 (1 H, d, J=2,3 Hz), 8,62 (1 H, s), 8,44 (1 H, d, J=8,8 Hz), 8.31 (1 H, d, J=8,7 Hz), 8,24 (1 H, dd, J=8,7, 2,6 Hz), 8,04 (1 H, dd, J=8,3, 5,3 Hz), 7,05 (1 H, d, J=8,5 Hz), 5,29 - 5,37 (1 H, m), 3,91 - 4,00 (1 H, m), 3,70 - 3,81 (1 H, m), 3,30 - 3,42 (1 H, m), 3,19 - 3,30 (1 H, m), 2,36 (2 H, q, J=7,4 Hz), 1,95 - 2,12 (2 H, m), 1,52 - 1,75 (2 H, m), 1,01 (3 H, t, J=7,4 Hz).
E je m p lo 136. 2 -M e t il-1 -[4 -(5 -q u in o lin -7 - i l -p ir id in -2 - i lo x i) -p ip e r id in -1 - i l ] -p ro p a n -1 -o n a , H C l.
El producto se aisló como un sólido canela. Análisis: LCMS m/z = 376 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,30 (1 H, dd, J=5,3, 1,3 Hz), 9,15 (1 H, d, J=8,3 Hz), 8,73 (1 H, d, J=2,3 Hz), 8,63 (1 H, s), 8,45 (1 H, d, J=8,8 Hz), 8,31 (1 H, dd, J=8,7, 1,6 Hz), 8,24 (1 H, dd, J=8,7, 2,6 Hz), 8,05 (1 H, dd, J=8,3, 5,3 Hz), 7,05 (1 H, d, J=8,5 Hz), 5,31 - 5,38 (1 H, m), 3,92 - 4,01 (1 H, m), 3,78 - 3,89 (1 H, m), 3,36 - 3,48 (1 H, m), 3,19 - 3,31 (1 H, m), 2,92 (1 H, quin, J=6,7 Hz), 1,95 - 2,15 (2H, m), 1,52-1,77 (2H, m), 1,02 (6H, d, J=6,8 Hz).
Ejemplo 137. Ciclopropil-[4-(5-quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido canela. Análisis: LCMS m/z = 374 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,29 (1 H, dd, J=5,3, 1,5 Hz), 9,12 (1 H, d, J=8,3 Hz), 8,73 (1 H, d, J=2,3 Hz), 8,60 (1 H, s), 8,44 (1 H, d, J=8,8 Hz), 8,23 -8,32 (2 H, m), 8,03 (1 H, t, J=6,4 Hz), 7,05 (1 H, d, J=8,8 Hz), 5,32 - 5,40 (1 H, m), 3,91 - 4,12 (2 H, m), 3,57 - 3,62 (1 H, m), 3,20 - 3,34 (1 H, m), 1,95 - 2,16 (3 H, m), 1,53-1,79 (2H, m), 0,67-0,79 (4H, m).
Ejemplo 138. 2-Metil-1-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-propan-1-ona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 124-130 °C; LCMS m/z = 377 (M+1); 1H NMR (DMSO-d6) 6: 9,62 (m, 1H), 9,29 (m, 1H), 9,23 (s, 2H), 8,36 (d, J = 8 Hz, 2H), 8,25 (d, J = 8 Hz, 1H), 8,08-8,01 (m, 1H), 7,93 7,85 (m, 1H), 5,31 (m, 1H), 4,01-3,77 (m, 2H), 3,52-3,38 (m, 1H), 3,36-3,23 (m, 1H), 2,92 (m, 1H), 2,17-1,97 (m, 2H), 1,81-1,56 (m, 2H), 1,02 (d, J = 7 Hz, 6H).
Ejemplo 139. Ciclopropil-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-metanona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 150-153 °C; LCMS m/z 375 (M+1); 1H NMR (DMSO-d6) 6: 9,65 (m, 1H), 9,35 (m, 1H), 9,24 (s, 2H), 8,39 (m, 1H), 8,27 (m, 1H), 8,10-8,04 (m, 1H), 7,95-7,88 (m, 1H), 5,33 (m, 1H), 4,15-3,85 (m, 2H), 3,71-3,51 (m, 1H), 3,39-3,23 (m, 1H), 2,22-1,92 (m, 3H), 1,86-1,54 (m, 2H), 0,83-0,62 (m, 4H).
E je m p lo 140. 1 -[4 -(6 -Q u in o lin -3 - i l- p ir id in -3 - i lo x i) -p ip e r id in -1 - i l ] - p ro p a n -1 -o n a , 2 H C l.
El producto se aisló como un sólido blancuzco. Análisis: mp: 207-212 °C; LCMS m/z = 362 (M+1); 1H NMR (DMSO-d6) 6: 9,82 (m, 1H), 9,59 (m, 1H), 8,54 (m, 1H), 8,41-8,30 (m, 3H), 8,11-8,03 (m, 1H), 7,95-7,88 (m, 1H), 7,80-7,74 (m, 1H), 4,87 (m, 1H), 3,97-3,86 (m, 1H), 3,80-3,68 (m, 1H), 3,44-3,21 (m, 2H), 2,36 (q, J = 7 Hz, 2H), 2,09-1,91 (m, 2H), 1,74-1,48 (m, 2H), 1,00 (t, J = 7 Hz, 3H).
Ejemplo 141. 2-Metil-1-[4-(6-quinolin-3-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 99-102 °C; LCMS m/z = 376 (M+1); 1H NMR (DMSO-d6) 6: 9,84 (m, 1H), 9,68 (m, 1H), 8,55 (m, 1H), 8,44-8,33 (m, 3H), 8,15-8,07 (m, 1H), 7,99-7,91 (m, 1H), 7,83-7,75 (m, 1H), 4,89 (m, 1H), 3,99-3,75 (m, 2H), 3,49-3,21 (m, 2H), 2,98-2,85 (m, 1H), 2,12-1,91 (m, 2H), 1,72-1,49 (m, 2H), 1,02 (d, J = 7Hz, 6H).
Ejemplo 142. Ciclopropil-[4-(6-quinolin-3-il-piridin-3-iloxi)-piperidin-1-il]-metanona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 230-234 °C; LCMS m/z = 374 (M+1); 1H NMR (DMSO-d6) 6: 9,84 (d, J = 2 Hz, 1H), 9,67 (m, 1H), 8,55 (d, J = 3 Hz, 1H), 8,42-8,35 (m, 3H), 8,12-8,08 (m, 1H), 7,96-7,92 (m, 1H), 7,81-7,78 (m, 1H), 4,90 (m, 1H), 4,12-3,85 (m, 2H), 3,66-3,50 (m, 1H), 3,38-3,23 (m, 1H), 2,16-1,92 (m, 3H), 1,77 1,51 (m, 2H), 0,79-0,66 (m, 4H).
Ejemplo 143. 1-[4-(5-Quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-propan-1-ona.
El producto se aisló como un sólido blanco. Análisis: mp: 162-166 °C; LCMS m/z = 363 (M 1); 1H NMR (DMSO- d6) 6: 9,29 (d, J = 2 Hz, 1H), 9,15 (s, 2H), 8,75 (d, J = 2 Hz, 1H), 8,06-8,03 (m, 2H), 7,83-7,79 (m, 1H), 7,70-7,66 (m, 1H), 5,28 (m, 1H), 4,00-3,88 (m, 1H), 3,81-3,70 (m, 1H), 3,44-3,20 (m, 2H), 2,37 (q, J = 8 Hz, 2H), 2,14-1,95 (m, 2H), 1,80 1,55 (m, 2H), 1,01 (t, J = 8 Hz, 3H).
E je m p lo 144. 1 -[4 -(6 -Q u in o lin -7 - i l- p ir id in -3 - i lo x i) -p ip e r id in -1 - i l ] - p ro p a n -1 -o n a , 2 H C l.
El producto se aisló como un sólido blancuzco. Análisis: mp: 90-96 °C; LCMS m/z = 362 (M+1); 1H NMR (DMSO-d6) 6: 9,31 (m, 1H), 9,18 (m, 1H), 9,05 (s, 1H), 8,63 (m, 1H), 8,57 (m, 1H), 8,45 (d, J = 9Hz, 1H), 8,22 (d, J=9Hz, 1H), 8,10 8,04 (m, 1H), 7,76-7,70 (m, 1H), 4,86 (m, 1H), 3,99-3,87 (m, 1H), 3,80-3,68 (m, 1H), 3,43-3,32 (m, 1H), 3,32-3,21 (m, 1H), 2,36 (q, J=7, 7Hz, 2H), 2,11-1,92 (m, 2H), 1,73-1,51 (m, 2H), 1,00 (t, J=7Hz, 3H).
Ejemplo 145. 2-Metil-1-[4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 170-179 °C; LCMS m/z = 376 (M+1); 1H NMR (DMSO-d6) 6: 9,30 (m, 1H), 9,17 (m, 1H), 9,02 (s, 1H), 8,63-8,57 (m, 2H), 8,44 (d, J = 9 Hz, 1H), 8,22 (d, J = 9 Hz, 1H), 8,07 8,04 (m, 1H), 7,74-7,71 (m, 1H), 4,87 (m, 1H), 3,98-3,88 (m, 1H), 3,88-3,76 (m, 1H), 3,49-3,36 (m, 1H), 3,34-3,20 (m, 1H), 2,92 (m, 1H), 2,14-1,91 (m, 2H), 1,74-1,46 (m, 2H), 1,02 (d, J = 7 Hz, 6H).
Ejemplo 146. Ciclopropil-[4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-metanona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 170-175 °C; LCMS m/z = 374 (M+1); 1HNMR (DMSO-d6) 6: 9,31 (m, 1H), 9,19 (m, 1H), 9,05 (s, 1H), 8,64-8,58 (m, 2H), 8,46 (d, J = 9 Hz, 1H), 8,23 (d, J = 9 Hz, 1H), 8,09-8,05 (m, 1H), 7,76-7,73 (m, 1H), 4,89 (m, 1H), 4,11-3,98 (m, 1H), 3,98-3,85 (m, 1H), 3,65-3,48 (m, 1H), 3,37-3,19 (m, 1H), 2,16-1,92 (m, 3H), 1,77-1,50 (m, 2H), 0,77-0,66 (m, 4H).
Ejemplo 147. 1-[4-(6-Isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 236-245 °C; LCMS m/z = 362 (M+1); 1HNMR (DMSO-d6) 6: 9,92 (s, 1H), 9,00 (s, 1H), 8,74-8,68 (m, 2H), 8,64-8,55 (m, 3H), 8,30 (d, J = 9 Hz, 1H), 7,76-7,73 (m, 1H), 4,88(m, 1H), 3,98-3,86 (m, 1H), 3,80-3,68 (m, 1H), 3,44-3,21 (m, 2H), 2,36 (q, J = 8 Hz, 2H), 2,11-1,92 (m, 2H), 1,74-1,50 (m, 2H), 1,00 (t, J = 7 Hz, 3H).
E je m p lo 148. 1 -[4 -(6 - Is o q u in o lin -6 - i l-p ir id in -3 - i lo x i) -p ip e r id in -1 - i l ] -2 -m e t i l- p ro p a n -1 -o n a , 2 H C l.
El producto se aisló como un sólido blancuzco. Análisis: mp: 236-241°C; LCMS m/z = 376 (M+1); 1HNMR (DMSO-d6) 6: 9,92 (s, 1H), 9,00 (s, 1H), 8,74 - 8,55 (m, 5H), 8,31 (d, J = 9 Hz, 1H), 7,76 - 7,73 (m, 1H), 4,89 (m, 1H), 3,98 - 3,88 (m, 1H), 3,88 - 3,76 (m, 1H), 3,49 - 3,37 (m, 1H), 3,33 - 3,22 (m, 1H), 2,92 (m, 1H), 2,11 - 1,93 (m, 2H), 1,72 -1,50 (m, 2H), 1,02 (d, J = 7 Hz, 6H).
Ejemplo 149. Ciclopropil-[4-(6-isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-metanona, 2HCl.
El producto se aisló como un sólido blancuzco. Análisis: mp: 136-146 °C; LCMS m/z = 374 (M+1); 1HNMR (DMSO-d6) 6: 9,91 (s, 1H), 9,00 (s, 1H), 8,75-8,56 (m, 5H), 8,31 (d, J = 9 Hz, 1H), 7,77-7,74 (m, 1H), 4,90 (m, 1H), 4,11-3,98 (m, 1H), 3,98-3,86 (m, 1H), 3,66-3,50 (m, 1H), 3,38-3,22 (m, 1H), 2,16-1,93 (m, 3H), 1,77-1,52 (m, 2H), 0,78-0,68 (m, 4H).
Ejemplo 150 ácido 1-Propionil-piperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)-amida.
Etapa. ácido 1-(2,2,2-Trifluoroacetil)-piperidina-4-carboxílico (4-bromofenil)-metil-amida.
A 1-(2,2,2-Trifluoroacetil)-piperidina-4-carbonil cloruro (0,400 g, 1,64 mmol) y DIPEA (0,858 mL, 4,92 mmol) en DCM (6 mL) se añadió (4-bromofenil)-metilamina (0,413 mL, 3,29 mmol). Después de agitar 4 h a temperatura ambiente la mezcla se concentró, se disolvió en EtOAc y se lavó con en Na2 CO3 , agua y salmuera luego se secó sobre MgSO4. El producto se purificó por gel de sílice cromatografía (15% EtOAc/hexanos) para dar un aceite viscoso. Análisis: LCMS m/z = 394 (M 1).
Etapa 2. ácido piperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)amida.
Acetato de paladio (0,00571 g, 0,0254 mmol) y trifenilfosfina (0,0267 g, 0,102 mmol) en dioxano se agitaron 15 min bajo una atmósfera de nitrógeno. ácido 1-(2,2,2-trifluoro-acetil)-piperidina-4-carboxílico (4-bromo-fenil)-metil-amida (0,200 g, 0,509 mmol), ácido quinolina-7-borónico (0,0968 g, 0,560 mmol), DMF (2 mL) y 1 M de carbonato de sodio (2,03 mL, 2,03 mmol) se añadieron, se purgó bajo una atmósfera de nitrógeno y se calentó a 80 °C por 17 h. La mezcla se concentró, se disolvió en EtOAc se lavó con en Na2CO3, agua y salmuera, luego se secó sobre MgSO4. El producto se purificó por ISCO (gel de sílice, 0-25% MeOH/1%iPrNH2,DCM) para dar el compuesto como un aceite. Análisis: LCMS m/z = 346 (M 1).
Etapa 3. ácido 1-propionil-piperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)-amida.
A ácido piperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)amida (0,070 g, 0,20 mmol) y DIPEA (0,14 mL, 0,81 mmol) en THF (3 mL) se añadió cloruro de propanoilo (0,035 mL, 0,40 mmol). Después de agitar 4 h a temperatura ambiente, la mezcla se concentró, se diluyó con EtOAc y se lavó con en Na2CO3, agua y salmuera luego se secó (MgSO4). El producto se purificó por ISCO de gel de sílice (0-5% MOH/DCM). La sal de HCl se preparó añadiendo 2 M HCl-éter a una solución de DCM de base y se recristalizó a partir de DCM-éter dio un sólido amarillo claro (60 mg, 73%). Análisis: LCMS m/z = 402 (M 1); 1H NMR (DMSO-d6, Sal de HCl) 6: 9,20 (d, 1H, J=4Hz), 8,91 (d, 1H, J=8Hz), 8,523 (s, 1H), 8,34 (d, 1H, J=8Hz), 8,23 (d, 1H, J=8Hz), 7,99 (d, 2H, J=8Hz), 8,88-8,92 (m, 1H), 7,57 (d, 2H, J=8Hz), 4,31 (d, 1H, J=12Hz), 3,78 (d, 1H, J=12Hz), 3,37 (q, 1H, J=7,8Hz), 3,22 (s, 3H), 2,8 (b, 1H), 2,23-2,32 (m, 2H), 1,53-1,65 (m, 3H),
1,42 (m, 1H), 1,09 (t, 2H, J=7,3Hz), 0,95 (t, 3H, J=7,3Hz).
Ejemplo 151. ácido 1-propionil-piperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida.
Este ejemplo se sintetizó usando el procedimiento para el ejemplo 150. A ácido piperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida (0,048 g, 0,14 mmol) y DIp Ea (0,097 mL, 0,55 mmol) en THF (2 mL) se añadió cloruro de propanoilo (0,024 mL, 0,28 mmol). Después de 4h de agitación a temperatura ambiente, la mezcla se concentró, se diluyó con EtOAc y se lavó con en Na2CO3, agua y salmuera luego se secó (MgSO4). El producto se purificó por ISCO (gel de sílice) 0-5% MeOH/DCM. La sal de HCl se obtuvo a partir de 2N HCl éter y se recristalizó a partir de DCM-éter para dar un sólido blanco (33 mg, 59%). Análisis: LCMS m/z = 402 (M 1); 1H NMR (DMSO) 6: 9,82 s, 1H), 8,67 (m, 2H), 8,57 (d, 1H, J = 8 Hz), 8,37-8,42 (m, 2H), 8,06 d, 2H, J = 8 Hz), 7,59 (d, 2H, J = 8 Hz), 4,32 (d, 1H, J = 12 Hz), 3,78 (d, 2H, J = 12 Hz), 3,23 (s, 3H), 2,77 (b, 1H), 2,23-2,32 (m, 3H), 1,53-1,65 (m, 3H), 1,37-1,45 (m, 1H), 0,95 (t, 3H, J=7 Hz).
Ejemplo 152 -y Ejemplo 153 (como una mezcla)
Una mezcla de 3-[4-(piperidin-4-iloxi)-fenil]-quinolina; 2HCl (100 mg, 0,27 mmol), hidrato de ácido glioxálico (25,6 mg, 0,28 mmol), N,N,N',N'-tetrametil-O-(7-azabenzo-triazol-1-il)uronio hexafluorofosfato (HATU), 121 mg, 0,32 mmol), y DIPEA (462 pL, 2,65 mmol) en THF (7 mL) se agitó a temperatura ambiente por 1 h. A la reacción se añadió 2-bromoetanol (150 mL, 2,10 mmol) seguido por K2 CO3 (73,3 mg, 0,53 mmol). Después de agitación a 60 °C por 24 h, a la reacción se añadió 8 eq. de K2 CO3 adicional y se continuó agitando por 3 h adicionales. Después de enfriar hasta la temperatura ambiente, se diluyó con DCM (50 mL), se lavó con H2 O, se secó (Na2SO4), y se concentró. Las mezclas de dos productos se separaron por HPLC preparativa y las fracciones de cada producto se combinaron, se neutralizaron con NaHCO3 (25 mL) sat., se extrajeron con DCM (3 x 25 mL), y las capas orgánicas combinadas se secaron (Na2SO4), y se concentraron. Ambos productos se disolvieron en DCM (~5 mL) y se mezclaron con 1,2 eq. de 2 M HCl en Et2 O y se concentraron. Ambos residuos se disolvieron en una pequeña cantidad de DCM y se concentraron - se repitió este procedimiento varias veces, se secaron para dar para dar el Ejemplo 152 (43 mg, 37%) y Ejemplo 153 (35 mg, 35%).
Ejemplo 152. Oxo-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-acetaldehído, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 405 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,49 - 9,55 (1 H, m), 9,13 - 9,19 (1 H, m), 8,22 - 8,33 (2 H, m), 7,90 - 8,03 (3 H, m), 7,82 - 7,89 (1 H, m), 7,19 - 7,26 (2 H, m), 5,68 - 5,72 (1 H, m), 4,75 - 4,84 (1 H, m), 3,88 - 4,02 (4 H, m), 3,77 - 3,88 (2 H, m), 3,41 - 3,52 (1 H, m), 3,27 - 3,38 (1 H, m), 1,91 - 2,08 (2 H, m), 1,51 - 1,74 (2 H, m).
Ejemplo 153. 4-(4-Quinolin-3-il-fenoxi)-piperidina-1-carbaldehído, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 333 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,50 - 9,57 (1 H, m), 9,15 - 9,23 (1 H, m), 8,23 - 8,35 (2 H, m), 7,91 - 8,06 (4 H, m), 7,82 - 7,90 (1 H, m), 7,19 - 7,28 (2 H, m), 4,76 - 4,85 (1 H, m), 3,72 - 3,83 (1H, m), 3,58-3,69 (1H, m), 3,21-3,40 (2H, m), 1,90-2,08 (2H, m), 1,50-1,71 (2H, m).
E je m p lo 154. ( (2 R ,3 S ) /(2 S ,3 R ) -3 -M e t i l- te t ra h id ro fu ra n -2 - i l) - [4 - (4 -q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] -m e ta n o n a , H C l.
Etapa 1. ácido (2R,3S)/(2S,3R)-3-Metil-tetrahidrofuran-2-carboxílico.
Una botella Parr cargada con ácido 3-metil-2-furóico (0,50 g, 4,0 mmol) y 5% Rh/C (5:95, Rodio:negro de carbón) (50 mg, 0,02 mmol) en metanol (25 mL) se hidrogenó a 50 psi por 79 h. La reacción se filtró a través de una almohadilla de Celite, se eluyó con MeOH, y el filtrado se concentró para dar el producto crudo de aceite marrón claro como una mezcla racémica. Este material se usó para la siguiente etapa sin purificación adicional. Análisis: 1H NMR (400 MHz, DMSO-d6) 6: 12,18 - 12,80 (1H, m), 4,24 (1 H, d, J=7,5 Hz), 3,92-4,00 (1H, m), 3,68-3,76 (1H, m), 2,42-2,49 (1H, m), 1,99-2,09 (1H, m), 1,51-1,63 (1H, m), 0,93 (3H, d, J=7,0 Hz).
Etapa 2. Un vial cargado con 3-[4-(piperidin-4-iloxi)-fenil]-quinolina; 2HCl (110 mg, 0,29 mmol), ácido (2R,3S)/(2S,3R)-3-metil-tetrahidrofuran-2-carboxílico (47 mg, 0,36 mmol), N,N,N',N'-tetrametil-O-(7-azabenzotriazol-1-il)uronio hexafluorofosfato (HATU,122 mg, 0,32 mmol), y DIPEA (305 pL, 1,75 mmol) en THF (10 mL) se agitó a temperatura ambiente 16 h. La reacción se concentró y el residuo se purificó por HPLC preparativa y las fracciones del producto se combinaron, se neutralizaron con NaHCO3 (25 mL) sat., se extrajeron con d Cm (3 x 25 mL), y las capas orgánicas combinadas se secaron (Na2SO4), y se concentraron. El producto se disolvió en DCM (~5 mL) y se mezcló con 1,2 eq. de 2 M HCl en Et2 O y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se secó para dar un sólido amarillo 93 mg (71%). Análisis: LCMS m/z = 417 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,50 - 9,56 (1 H, m), 9,15 - 9,21 (1 H, m), 8,23 - 8,34 (2 H, m), 7,91 - 8,03 (3 H, m), 7,82 - 7,90 (1 H, m), 7,18 - 7,27 (2 H, m), 4,72 - 4,85 (2 H, m), 3,92 - 4,01 (2 H, m), 3,79 - 3,91 (1 H, m), 3,66 -3,77 (1 H, m), 3,18 - 3,52 (2 H, m), 2,52 - 2,61 (1 H, m), 1,91 - 2,10 (3 H, m), 1,49 - 1,73 (3 H, m), 0,84 - 0,94 (3 H, m).
Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 154.
Ejemplo 155. ((2R,3S,5R)/(2S,3R,5S)-3,5-Dimetil-tetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 431 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,50 - 9,54 (1 H, m), 9,14 - 9,18 (1 H, m), 8,22 - 8,32 (2 H, m), 7,91 - 8,02 (3 H, m), 7,82 - 7,89 (1 H, m), 7,19 - 7,26 (2 H, m), 4,71 - 4,84 (2 H, m), 3,89 - 4,04 (1 H, m), 3,79 - 3,89 (1 H, m), 3,70 - 3,79 (1 H, m), 3,30 - 3,53 (1 H, m), 3,17 - 3,27 (1 H, m), 2,53 - 2,61 (1 H, m), 2,08 - 2,19 (1 H, m), 1,91 - 2,08 (2 H, m), 1,49 - 1,70 (2 H, m), 1,22 - 1,27 (4 H, m), 0,86 - 0,93 (3 H, m).
Ejemplo 156. ((2R,3S,5R)/(2S,3R,5S)-3,5-Dimetil-tetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
((2R,4R,5R)/(2S,4S,5S)-4,5-Dimetil-tetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-met-anona, HCL. El producto se aisló como un sólido amarillo. Análisis: Lc Ms m/z = 431 (M+1); 1H NMr (400 MHz, DMSO-d6) 6: 9,48 -9,51 (1 H, m), 9,10 - 9,14 (1 H, m), 8,21 - 8,28 (2 H, m), 7,90 - 8,00 (3 H, m), 7,81 - 7,87 (1 H, m), 7,19 -7,25(2 H, m), 4,74 - 4,82 (1 H, m), 4,53 - 4,59 (1 H, m), 3,98 - 4,05 (1 H, m), 3,79 - 3,91 (2 H, m), 3,38 - 3,51 (1 H, m), 3,25- 3,37 (1
H, m), 2,21 - 2,29 (1 H, m), 2,09 - 2,18 (1 H, m), 1,86 - 2,05 (3 H, m), 1,51 - 1,69 (2 H, m), 0,98-1,02 (3H, m), 0,87-0,90 (3H, m).
Ejemplo 157. ácido 1-propionilpiperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida.
Etapa 1. terc-butil éster del ácido 4-[(4-Bromo-2-fluorobenzoil)-metilamino]-piperidina-1-carboxílico.
A terc-butil éster del ácido 4-Metilamino-piperidina-1-carboxílico (0,40 g, 1,87 mmol) y DIPEA (1,30 mL, 7,47 mmol) en DCM (5 mL) se añadió 4-bromo-2-fluoro-benzoil cloruro (0,488 g, 2,05 mmol). Después de 2 h de agitación a temperatura ambiente la mezcla se concentró, se disolvió en EtOAc y se lavó con en Na2CO3, agua y salmuera. El producto se purificó por gel de sílice cromatografía (20% EtOAc/hexanos) para dar un aceite (0,6 g, 77%). Análisis: LCMS m/z = 416 (M 1).
Etapa 2. 2-Fluoro-4-isoquinolin-6-il-N-metil-N-piperidin-4-il-benzamida.
Acetato de paladio (0,007568 g, 0,03371 mmol) y trifenilfosfina (0,03537 g, 0,1348 mmol) en dioxano se agitaron 15 min bajo una atmósfera de nitrógeno. terc-butil éster del ácido 4-[(4-bromo-2-fluoro-benzoil)-metil-amino]-piperidina-1-carboxílico (0,3500 g, 0,8428 mmol), ácido isoquinolina-6-borónico (0,2187 g, 1,264 mmol), DMF (6 mL) y 1 M de carbonato de sodio (2,56 mL) se añadió y se calentó a 80 °C por 17 h. La mezcla se concentró, se disolvió en EtOAc, se lavó con en Na2CO3, agua y salmuera luego se secó (MgSO4). El producto se purificó por ISCO (gel de sílice, 12 g, 0-5% MeOH/DCM) para dar un sólido blanco. Este material se disolvió en 4 M HCl en 1,4-dioxano (6 mL, 20 mmol) y se calentó a 65 °C por 4 h. El material se concentró, se particionó entre EOAc y 1N Na2CO3, se lavó con agua y salmuera luego se secó sobre MgSO4 para dar un aceite. La amina se purificó por ISCO (4g de gel de sílice, 0-10% MeOH con 1% IPA/DCM) para dar un aceite (0,25 g, 81%). Análisis: Lc Ms m/z = 364 (M 1).
Etapa 3. ácido 1-propionilpiperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida.
A ácido piperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida (0,048 g, 0,14 mmol) y DIPEA (0,097 mL, 0,55 mmol) en THF (2 mL) se añadió cloruro de propanoilo (0,024 mL, 0,28 mmol). Después de 4 h de agitación a temperatura ambiente, la mezcla se concentró, se diluyó con EtOAc y se lavó con en Na2CO3, agua y salmuera luego se secó (MgSO4). El producto se purificó por ISCO (gel de sílice) 0-5% MeOH/DCM. La sal de HCl se preparó a partir de 2N HCl éter y se recristalizó a partir de DCM-éter para dar un sólido blanco (33 mg, 59%). Análisis: LCMS m/z = 402 (M 1); 1H NMR (DMSO; Sal de HCl) 6: 9,82 (s, 1H), 8,67 (m, 2H), 8,57 (d, 1H, J = 8 Hz), 8,37-8,42 (m, 2H), 8,06 d, 2H, J = 8 Hz), 7,59 (d, 2H, J = 8 Hz), 4,32 (d, 1H, J = 12 Hz), 3,78 (d, 2H, J = 12 Hz), 3,23 (s, 3H), 2,77 (b, 1H), 2,23 2,32 (m, 3H), 1,53-1,65 (m, 3H), 1,37-1,45 (m, 1H), 0,95 (t, 3H, J = 7 Hz).
Ejemplo 158. 2-Fluoro-4-isoquinolin-6-il-N-metil-N-(1-propionil-piperidin-4-il)-benzamida.
Este ejemplo se sintetizó usando el procedimiento para el ejemplo 157. Análisis: LCMS m/z = 420 (M 1); 1H NMR (DMSO; Sal de HCl) 6: 9,84 (s, 1H), 8,70 (m, 2H), 8,58 (d, 2H, J = 8,5 Hz), 8,38-8,42 (m, 2H), 7,96 (t, 1H, J = 10 Hz), 7,88 (m, 1H), 7,95-7,69 (m, 1H), (rotomeros 2:1) 4,58/4,44 (m, 2H), 3,98/3,86 (bd, 1H), 3,54/3,12 (1:1, m, 1H), 2,91/2,75 (1:2, s, 3H), 2,80/2,62 (1:1, m, 1H), 2,77-2,83 (m, 3H), 1,61-1,80 (m, 4H), 0,93-1,02 (m, 3H).
E je m p lo 159. 1 - {4 -[4 -(3 -T r if lu o ro m e t i l-1 ,2 ,4 - t r ia z o lo [4 ,3 -a ]p ir id in -6 - i l) - fe n o x i] -p ip e r id in -1 - i l} -p ro p a n -1 -o n a , H C l
Etapa 1. terc-butil éster del ácido 4-[4-(3-Trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidina-1-carboxílico. Un frasco cargado con ácido 4-(4-yodo-fenoxi)-piperidina-1-carboxílico terc-butil (368 mg, 0,91 mmol), 6-(4,4,5,5-tetrametil-1,3, 2-dioxaborolan-2-il)-3-trifluorometil-1,2,4-triazolo[4,3-a]piridina (0,30 g, 0,96 mmol), acetato de paladio (20,5 mg, 0,91 mmol), trifenilfosfina (47,9 mg, 0,18 mmol), 1,0 M de Na2CO3 en agua (5 mL, 5 mmol), 1,4-dioxano (5 mL), y DMF (5 mL) se enjuagó con N2 por 15 min. La reacción se agitó a 90 °C por 16 h luego se enfrió hasta la temperatura ambiente y se concentró. El residuo se particionó en EtOAc (80 mL) y solución NaHCO3 sat. (30 mL), la capa orgánica se separó y la capa de agua se extrajo con EtOAc (50 mL). Las capas orgánicas combinadas se lavaron con H2 O, salmuera, se secaron (Na2SO4), y se concentraron. El residuo se sometió a cromatografía en gel de sílice (10-70% EtOAc/Hexanos) para dar un sólido blancuzco (404 mg, 96%). Análisis: 1H NMR (400 MHz, DMSO-d6) 6: 8,59 - 8,61 (1 H, m), 8,09 - 8,14 (1 H, m), 7,95 - 8,00 (1 H, m), 7,71 - 7,76 (2 H, m), 7,11-7,16 (2H, m), 4,63-4,72 (1H, m), 3,63-3,72 (2H, m), 3,16-3,28 (2H, m), 1,90-1,98 (2H, m), 1,50-1,61 (2H, m), 1,41 (9H, s).
Etapa 2. 6-[4-(Piperidin-4-iloxi)-fenil]-3-trifluorometil-1,2,4-triazolo[4,3-a]piridina, 2HCl.
A una solución de terc-butil éster del ácido 4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]piperidina-1-carboxílico (396 mg, 0,86 mmol) en DCM (15 mL) se añadió 4,0 M de cloruro de hidrógeno en 1,4-dioxano (2,14 mL, 8,56mmol) y se agitó a temperatura ambiente por 18 h. El precipitado blanco resultante se recogió por filtración, se lavó con DCM, se secó para dar un sólido blanco 370 mg (99%). Análisis: LCMS m/z = 363 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,15 (1 H, br. s.), 8,59 - 8,63 (1 H, m), 8,10 - 8,16 (1 H, m), 7,96 - 8,02 (1 H, m), 7,74 - 7,79 (2 H, m), 7,14 - 7,20 (2 H, m), 4,73 - 4,82 (1 H, m), 3,18 - 3,30 (2 H, m), 3,03 - 3,15 (2 H, m), 2,10 - 2,21 (2 H, m), 1,83 - 1,95 (2 H, m).
Etapa 3. A una solución de 6-[4-(piperidin-4-iloxi)-fenil]-3-trifluorometil-1,2,4-triazolo[4,3-a]piridina; 2HCl (85 mg, 0,20 mmol), DIPEA (170 pL, 0,98 mmol) en THF (6 mL) se añadió cloruro de propanoilo (19 pL, 0,22 mmol). Después de 25 min, la reacción se concentró y el residuo se sometió a cromatografía en gel de sílice (0-10% MeOH/DCM) y el producto aislado se disolvió en dCm (~5 mL) y se mezcló con 1,2 eq. de 2 M HCl en Et2 O y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se secó para dar para dar un sólido marrón claro 63 mg (71%). Análisis: LCMS m/z = 419 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,58 - 8,63 (1 H, m), 8,09 - 8,15 (1 H, m), 7,96 - 8,01 (1 H, m), 7,71-7,78 (2H, m), 7,12-7,18 (2H, m), 4,68-4,78 (1H, m), 3,82-3,93 (1H, m), 3,66-3,76 (1H, m), 3,22-3,41 (2H, m), 2,35 (2 H, q, J=7,5Hz), 1,87-2,04 (2H, m), 1,47-1,69 (2H, m), 1,00 (3H, t, J=7,4Hz).
Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 159.
Ejemplo 160. Ciclopropil-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
El producto se aisló como un sólido blancuzco. Análisis: LCMS m/z = 431 (M+1); 1H NMR (400 MHz, DMSO- d6) 6: 8,59 - 8,63 (1 H, m), 8,10 - 8,15 (1 H, m), 7,96 - 8,01 (1 H, m), 7,72 - 7,78 (2 H, m), 7,13 - 7,18 (2 H, m), 4,71 - 4,79 (1 H, m), 3,83 - 4,04 (2 H, m), 3,50 - 3,63 (1 H, m), 3,24 - 3,35 (1 H, m), 1,88 - 2,09 (3 H, m), 1,48 - 1,71 (2 H, m), 0,67 -0,75 (4 H, m).
Ejemplo 161. (R)-Tetrahidrofuran-2-il-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
A una solución de 6-[4-(piperidin-4-iloxi)-fenil]-3-trifluorometil-1,2,4-triazolo[4, 3-a]piridina; 2HCl (85 mg, 0,20 mmol), HATU (81,7 mg. 0,22 mmol), DIPEA (170 mL, 0,98 mmol) en THF (6 mL) se añadió ácido (R)-tetrahidrofuran-2-carboxílico (20 pL, 0,21 mmol) y se agitó a temperatura ambiente por 1 h. La reacción se concentró y el residuo se purificó por cromatografía en gel de sílice (0-10% MeOH/DCM) para dar un sólido blanco 71 mg (79%). Análisis: LCMS m/z = 461 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,59 - 8,62 (1 H, m), 8,10 - 8,15 (1 H, m), 7,96 - 8,01 (1 H, m), 7,72 - 7,77 (2H, m), 7,12 - 7,18 (2 H, m), 4,66 - 4,78 (2 H, m), 3,70 - 3,87 (4 H, m), 2,68 - 2,70 (2 H, m), 1,92 - 2,10 (4 H, m), 1,79 -1,88 (2 H, m), 1,49 - 1,69 (2 H, m).
Ejemplo 162. 3-[4-(1-Metanosulfonil-piperidin-4-iloxi)-fenil]-quinolina.
Etapa 1. ácido metanosulfónico (R)-1-(tetrahidrofuran-2-il)metil éster.
A una solución de (R)-1-(tetrahidrofuran-2-il)-metanol (0,50 g, 4,9 mmol), y DIPEA (2,56 mL, 14,7 mmol) en cloruro de metileno (20 mL) a 0 °C se añadió metanosulfonil-cloruro (398 pL, 5,14 mmol). Después de 1 h a 0 °C, la reacción se agitó a temperatura ambiente durante toda la noche (16 h) luego se apagó con H2 O (20 mL), se extrajo con DCM (3 x 30 mL). Las capas orgánicas combinadas se lavaron con H2 O, se secaron (Na2SO4) y se concentraron para dar 551 mg (62%) de producto crudo. Este material se usó para la siguiente etapa sin purificación adicional.
Etapa 2. Un vial cargado con 3-[4-(piperidin-4-iloxi)-fenil]-quinolina; 2HCl (85 mg, 0,22 mmol), ácido metanosulfónico (R)-1-(tetrahidrofuran-2-il)metil éster (61 mg, 0,34 mmol), carbonato de potasio (160 mg, 1,1 mmol), y acetonitrilo (6 mL) se agitó a 90°C por 1,5 h. Después de enfriar hasta la temperatura ambiente, se diluyó con DCM (50 mL), se lavó con H2 O, se secó (Na2SO4), y se concentró. El residuo se sometió a cromatografía en gel de sílice (0-10% MeOH/DCM) para dar un sólido blanco 76 mg (88%). Análisis: LCMS m/z = 373 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,22 - 9,25 (1 H, m), 8,57 - 8,59 (1 H, m), 8,01 - 8,06 (2 H, m), 7,82 - 7,87 (2 H, m), 7,72 - 7,78 (1 H, m), 7,61 - 7,67 (1 H, m), 7,15 - 7,20 (2 H, m), 4,64 - 4,72 (1 H, m), 3,34 - 3,43 (2 H, m), 3,14 - 3,20 (2 H, m), 2,92 (3 H, s), 2,01 - 2,10 (2 H, m), 1,74 - 1,85 (2 H, m).
Ejemplo 163. (4,4-Difluorotetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona, HCl.
Etapa 1. ácido 4-oxo-tetrahidrofuran-2-carboxílico.
A una suspensión de hidruro de sodio, 60% disp. en aceite mineral (830 mg, 20,7 mmol) en THF (35 mL) se añadió una solución de glicolato de etilo (2,0 mL, 20,7 mmol) en THF (5 mL x 2) en forma de gotas a temperatura ambiente (baño de agua). Después de que terminó la evolución de H2 (~5 min), a la reacción se añadió ácido (Z)-2-butenedióico, dietil-éster (2,75 mL, 17,0 mmol). La reacción se agitó a 65 °C por 1 h y luego a temperatura ambiente por 5 días. El disolvente se retiró y al residuo se añadió cuidadosamente agua helada (50 mL) y en solución de HCl (50 mL), se extrajo con EtOAc (2 x 50 mL), las capas orgánicas combinadas se concentraron. Este residuo se calentó a reflujo (100 °C) con 10% H2 OS4 agua solución por 5 h y se enfrió hasta la temperatura ambiente. La reacción se extrajo con
EtOAc (3 x 50 mL) y las capas orgánicas combinadas se lavaron con salmuera, se secaron (Na2SÜ4), y se concentraron. Este material se usó para la siguiente etapa sin purificación adicional.
Etapa 2. ácido 4-oxo-Tetrahidrofuran-2-carboxílico 4-nitro-benzil éster.
A una mezcla de ácido 4-oxo-tetrahidrofuran-2-carboxílico (2,21 g, 17,0 mmol), DIPEA (2,95 mL, 16,9 mmol), 4-dimetilaminopiridina (156 mg, 1,27 mmol), carbonato de potasio (3,52 g, 25,5 mmol) en THF (35 mL) se añadió una solución de 4-nitrobenzil cloroformato (2,75 g, 12,7 mmol) en THF (5 mL) a temperatura ambiente (baño de agua). Después de 5 min, el disolvente se retiró y el residuo se añadió H2 O (30 mL), se extrajo con EtOAc (2 x 50 mL). Las capas orgánicas combinadas se lavaron con salmuera, se secaron (Na2SO4), y se concentraron. El residuo se sometió a cromatografía en gel de sílice (0-50% EtOAc/Hexanos) para dar un sólido blanco (934 mg, 28%, 3 etapas). Análisis: 1H NMR (400 MHz, CDCls) 6: 8,22 - 8,28 (2 H, m), 7,50 -7,57(2 H, m), 5,29 - 5,33 (2 H, m), 4,96 - 5,03 (1 H, m), 4,15 - 4,23 (1 H, m), 4,00 - 4,07 (1 H, m), 2,81 - 2,91 (1 H, m), 2,60 - 2,69 (1 H, m).
Etapa 3. ácido 4,4-Difluorotetrahidrofuran-2-carboxílico 4-nitrobenzil éster.
Una botella de teflón cargada con ácido 4-oxo-tetrahidrofuran-2-carboxílico 4-nitro-benzil éster (538 mg, 2,03 mmol) en DCM (10 mL) se añadió bis(2-metoxietil)aminoazufre trifluoruro (1,12 mL, 6,08 mmol) y se agitó a temperatura ambiente por 18 h. A la reacción se añadió cuidadosamente solución de NH4Cl sat. (15 mL) enfriando con baño de agua, se extrajo con DCM (3 x 10 mL). Las capas orgánicas combinadas se secaron (Na2SO4) y se concentraron. El residuo se sometió a cromatografía en gel de sílice (0-30% EtOAc/Hexanos) para dar un aceite incoloro (496 mg, 85%). Análisis: 1H NMR (400 MHz, CDCla) 6: 8,22 - 8,27 (2 H, m), 7,51 - 7,56 (2 H, m), 5,31 (2 H, s), 4,75 - 4,81 (1 H, m), 4,00 - 4,24 (2 H, m), 2,70 - 2,84 (1 H, m), 2,54-2,68 (1 H, m).
Etapa 4. ácido 4,4-Difluorotetrahidrofuran-2-carboxílico.
A una solución de ácido 4,4-difluorotetrahidrofuran-2-carboxílico 4-nitro-benzil éster (270 mg, 0,94 mmol) en THF (6 mL) se añadió 1,0 M de tetra-n-butilamonio fluoruro en THF (2,35 mL, 2,35 mmol) y se agitó por 30 min. A la reacción se añadió H2 O (10 mL) y EtOAc (10 mL) luego se extrajo con solución 5% NaHCO3 (3 x 15 mL). Las capas de agua combinadas se acidificaron hasta f~1 con HCl, se extrajeron con EtOAc (3 x 20 mL). Las capas orgánicas combinadas se lavaron con salmuera, se secaron (Na2SO4), y se concentraron para dar un aceite marrón 140 mg. Este material se usó para la siguiente etapa sin purificación adicional.
Etapa 5.
Una mezcla de 3-[4-(piperidin-4-iloxi)-fenil]-quinolina; 2HCl (106 mg, 0,28 mmol), ácido 4,4-difluorotetrahidrofuran-2-carboxílico (51 mg, 0,34 mmol), Ha Tu (107 mg, 0,28 mmol), DIPEA (245 pL, 1,40 mmol) en THF (8 mL) se agitó a temperatura ambiente por 1 h y se concentró. El residuo se purificó por HPLC preparativa y las fracciones del producto se combinaron y se concentraron. El residuo se añadió EtOAc (25 mL), se lavó con solución de NaHCO3 sat. (10 mL), salmuera, se secó (Na2SO4), y se concentró. El producto se disolvió en DCM (~5 mL) y se mezcló con 1,2 eq. de 2 M HCl en Et2 O y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se secó para dar un sólido amarillo 117 mg (88%). Análisis: LCMS m/z = 439 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,50 - 9,55 (1 H, m), 9,14 - 9,19 (1 H, m), 8,23 - 8,32 (2 H, m), 7,96-8,02 (1 H, m), 7,91-7,96 (2 H, m), 7,83-7,89 (1 H, m), 7,19-7,25 (2H, m), 5,08-5,16 (1H, m), 4,75-4,84 (1H, m), 3,88-4,09 (3H, m), 3,75-3,85 (1H, m), 3,27-3,53 (2H, m), 2,71-2,88 (1H, m), 2,54-2,71 (1H, m), 1,99 (2H, s), 1,54-1,70 (2H, m).
Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 163.
Ejemplo 164. (4,4-Difluorotetrahidrofuran-2-il)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
El producto se aisló como un sólido marrón. Análisis: LCMS m/z = 453 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,10 -9,15 (1 H, m), 8,76 - 8,87 (1 H, m), 8,03 - 8,11 (1 H, m), 7,79 - 7,89 (1H, m), 7,64-7,71 (1H, m), 7,37-7,45 (2H, m), 7,11-7,19 (2H, m), 5,08-5,17 (1H, m), 4,69-4,79 (1H, m), 3,99-4,05 (2H, m), 3,73-3,90 (2H, m), 3,25-3,53 (2H, m), 2,75 2,89 (1H, m), 2,72 (3H, s), 2,54-2,70 (1H, m), 1,99 (2H, s), 1,55-1,73 (2H, m).
E je m p lo 165. (4 ,4 -D if lu o ro te t ra h id ro fu ra n -2 - i l) - {4 - [4 - (1 -m e t i l is o q u in o lin -6 - i l ) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a , H C l.
El producto se aisló como un sólido blancuzco. Análisis: LCMS m/z = 453 (M+1); 1H NMR (400 MHz, DMSO- d6) 8: 8,55 - 8,63 (2 H, m), 8,45 - 8,49 (1 H, m), 8,32 - 8,37 (1 H, m), 8,26 - 8,30 (1 H, m), 7,92 - 7,98 (2 H, m), 7,19 -7,25(2 H, m), 5,09 - 5,16 (1 H, m), 4,76 - 4,85 (1 H, m), 3,97 - 4,07 (2 H, m), 3,73-3,96 (2H, m), 3,41-3,50 (2H, m), 3,21 (3H, s), 2,71-2,88 (1H, m), 2,55-2,70 (1H, m), 1,94-2,05 (2H, m), 1,52-1,75 (2H, m).
Ejemplo 166. 5-[4-(4-Quinolin-3-il-fenoxi)-piperidina-1-carbonil]dihidrofuran-3-ona.
Una mezcla de 3-[4-(piperidin-4-iloxi)-fenil]- quinolina; 2HCl (105 mg, 0,278 mmol), ácido 4-oxo-tetrahidrofuran-2-carboxílico (38 mg, 0,29 mmol), HATU (116 mg, 0,31 mmol), DIPEA (242 pL, 1,39 mmol) en THF (8 mL) se agitó a temperatura ambiente por 1 h y se concentró. El residuo se purificó por HPLC preparativa y las fracciones del producto se combinaron y se concentraron. El residuo se añadió EtOAc (25 mL), se lavó con solución de NaHCO3 sat. (10 mL), salmuera, se secó (Na2SO4), se concentró para dar un sólido blanco 17 mg (15%). Análisis: LCMS m/z = 417 (M+1); 1H NMR (400 MHz, DMSO-d6) 8: 8,57- 8,60 (1 H, m), 8,01 - 8,06 (2 H, m), 7,82 - 7,86 (2 H, m), 7,72 - 7,78 (1 H, m), 7,61 - 7,66 (1 H, m), 7,16 - 7,20 (2H, m), 5,33 - 5,39 (1 H, m), 4,72 - 4,81 (1 H, m), 3,98 (2 H, s), 3,77 - 3,94 (2 H, m), 3,38 - 3,58 (2 H, m), 3,26 - 3,31 (1H, m), 2,66 - 2,72 (2 H, m), 1,91 - 2,12 (2 H, m), 1,51 - 1,79 (2 H, m).
Ejemplo 167. 1-{4-[4-(8-Etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Etapa 1. 7-Bromo-8-etoxiquinolina.
Un frasco cargado con 7-bromoquinolin-8-ol (1,0 g, 4,46 mmol), yodoetano (375 pL, 4,69 mmol), y K2 CO3 (1,23 g, 8,93 mmol) en dimetil sulfóxido (25 mL) se agitó a temperatura ambiente por 24 h. La reacción se diluyó con DCM, se lavó con H2 O (2 x 30 mL), salmuera, se secó (Na2SO4), y se concentró. El residuo se sometió a cromatografía en gel de sílice (0-50% EtOAc/Hexanos) para dar 1,03 g (92%) como un aceite amarillento.
Etapa 2. t-butil éster del ácido 4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico.
Un frasco cargado con terc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (1,62 g, 4,01 mmol), 7-bromo-8-etoxiquinolina (1,01 g, 4,01 mmol), acetato de paladio (91 mg, 0,40 mmol), trifenilfosfina (0,21 g, 0,80 mmol), 1,0 M de Na2CO3 en agua (20 mL, 20 mmol), 1,4-dioxano (20 mL), y DMF (20 mL) se enjuagó con N2 por 15 min. Después de agitación a 85 °C por 17 h, la reacción se enfrió hasta la temperatura ambiente, y se añadió EtOAc (100 mL), se lavó con solución de NaHCO3 sat. (35 mL), la capa de agua se extrajo nuevamente con EtOAc (50 mL). Las capas orgánicas combinadas se lavaron con H2 O (35 mL), salmuera, se secaron (Na2SO4), y se concentraron. El residuo se sometió a cromatografía en gel de sílice (0-70% EtOAc/Hexanos) para dar 1,21 g (67%) como una goma amarillenta. Análisis: 1H NMR (400 MHz, DMSO-d6) 8: 8,91 - 8,95 (1 H, m), 8,35 - 8,40 (1 H, m), 7,73 - 7,78 (1 H, m), 7,56-7,62 (3 H, m), 7,51-7,56 (1 H, m), 7,07-7,13 (2 H, m), 4,59-4,69 (1 H, m), 4,14-4,24 (2 H, m), 3,66-3,76 (2 H, m), 3,13-3,28 (2 H, m), 1,91-2,02 (2H, m), 1,50-1,63 (2H, m), 1,42 (9H, s), 1,14-1,21 (3H, m).
Etapa 3. 8-Etoxi-7-[4-(piperidin-4-iloxi)-fenil]-quinolina, 2HCl.
A una solución de terc-butil éster del ácido 4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidina-1-carboxílico (1,20 g, 2,68 mmol) en DCM (30 mL) se añadió 4,0 M de HCl en 1,4-dioxano (6,69 mL, 26,8 mmol) lentamente. La reacción se agitó a temperatura ambiente por 2 h y luego se concentró. El residuo sólido se lavó con disolvente mezclado (DCM -EtOAc ~ 1:1) y se secó para dar 976 mg (87%) como un sólido amarillo.
Etapa 4. A una solución de 8-etoxi-7-[4-(piperidin-4-iloxi)-fenil]-quinolina; 2HCl (150 mg, 0,36 mmol) y DIPEA (310 pL, 1,78 mmol) en THF (10 mL) se añadió cloruro de propanoilo (34 pL, 0,39 mmol) y se agitó por 25 min. El disolvente se retiró y el residuo se purificó por HPLC preparativa. Las fracciones del producto se combinaron y se neutralizaron con solución de NaHCO3 sat. (25 mL), se extrajo con DCM (3 x 25 mL), se secó (Na2SO4), y se concentró. El producto se disolvió en DCM (~5 mL) y se mezcló con 1,2 eq. de 2 M HCl en Et2 O y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se secó para dar 97 mg (62%) de sólido amarillo. Análisis: LCMS m/z = 405 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,13 - 9,20 (1 H, m), 8,94 - 9,05 (1 H, m), 8,04 - 8,11 (1 H, m), 7,86 - 8,01 (2 H, m), 7,67 - 7,75 (2 H, m), 7,14 - 7,22 (2 H, m), 4,68 - 4,78 (1 H, m), 3,93 (3 H, q, J=6,8 Hz), 3,67 - 3,79 (1 H, m), 3,20 - 3,43 (2 H, m), 2,36 (2 H, q, J=7,4 Hz), 1,90 - 2,09 (2 H, m), 1,48 - 1,71 (2 H, m), 1,21 (3 H, t, J=7,0 Hz), 1,00 (3 H, t, J=7,4 Hz).
Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 167.
Ejemplo 168. Ciclopropil-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 417 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,14 - 9,20 (1 H, m), 8,97 - 9,06 (1 H, m), 8,05 - 8,12 (1 H, m), 7,86 - 8,02 (2 H, m), 7,68 - 7,75 (2 H, m), 7,16 - 7,22 (2 H, m), 4,71 - 4,81 (1 H, m), 3,87 - 3,97 (3 H, m), 3,50 - 3,62 (1 H, m), 3,22 - 3,35 (1 H, m), 1,99 (4 H, s), 1,49 - 1,73 (2 H, m), 1,22 (3 H, t, J=7,0 Hz), 0,62 - 0,85 (4 H, m).
Ejemplo 169. 1-{4-[4-(8-Isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 419 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,16 - 9,21 (1 H, m), 9,01-9,11 (1 H, m), 8,06-8,14 (1 H, m), 7,96-8,04 (1 H, m), 7,89-7,95 (1 H, m), 7,68-7,75 (2 H, m), 7,15 7,22 (2 H, m), 4,68-4,78 (1 H, m), 4,14-4,27 (1 H, m), 3,90-3,97 (1 H, m), 3,71-3,77 (1 H, m), 3,21-3,41 (2 H, m), 2,36 (2 H, q, J=7,3 Hz), 1,91-2,07 (2 H, m), 1,48-1,70 (2 H, m), 1,11 (6 H, d, J=6,0 Hz), 1,00 (3 H, t, J=7,4 Hz).
Ejemplo 170. Ciclopropil-{4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 431 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,16 - 9,22 (1 H, m), 9,03 - 9,12 (1 H, m), 8,07 - 8,14 (1 H, m), 7,97 - 8,05 (1 H, m), 7,90 - 7,96 (1 H, m), 7,69 - 7,76 (2 H, m), 7,16 - 7,23 (2 H, m), 4,71 - 4,81 (1 H, m), 4,15 - 4,27 (1 H, m), 4,00 - 4,05 (1 H, m), 3,90 - 3,97 (1 H, m), 3,53-3,60 (1 H, m), 3,23-3,32 (1 H, m), 1,92-2,11 (3 H, m), 1,50-1,71 (2 H, m), 1,12 (6 H, d, J = 6,0 Hz), 0,67-0,78 (4 H, m).
E je m p lo 171. 1 -(4 - {4 -[8 -(2 -M o r fo l in -4 - i l -e to x i) -q u in o lin -7 - i l ] - fe n o x i} -p ip e r id in -1 - i l) -p ro p a n -1 -o n a , 2 H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 490 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,06 - 9,17 (1 H, m), 8,70 - 8,87 (1 H, m), 7,96 - 8,06 (1 H, m), 7,72 - 7,91 (2 H, m), 7,61 - 7,71 (2 H, m), 7,11 - 7,20 (2 H, m), 4,69 - 4,76 (1 H, m), 4,24 - 4,37 (2 H, m), 3,87 - 3,99 (5 H, m), 3,69 - 3,77 (1 H, m), 3,51-3,56 (2 H, m), 3,22-3,43 (4 H, m), 2,36 (2 H, q, J=7,5 Hz), 1,89-2,08 (2 H, m), 1,48-1,72 (2 H, m), 1,15-1,32 (2 H, m), 1,01 (3 H, t, J=7,4 Hz).
Ejemplo 172. Ciclopropil-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxil}-piperidin-1-il)-metanona, 2HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 502 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 - 9,14 (1 H, m), 8,68 - 8,84 (1 H, m), 7,96 - 8,04 (1 H, m), 7,74 - 7,88 (2 H, m), 7,67 (2 H, d, J=8,8 Hz), 7,17 (2H, d, J=8,8 Hz), 4,72-4,78 (1 H, m), 4,26-4,36 (2 H, m), 3,89 - 4,05 (6 H, m), 3,49 - 3,64 (4 H, m), 3,22 - 3,48 (4 H, m), 1,91 2,14 (3 H, m), 1,49 - 1,76 (2 H, m), 0,68 - 0,79 (4 H, m).
Ejemplo 173. 1-(4-{4-[8-(2-Pirrolidin-1-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 474 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,16 - 9,25 (1 H, m), 8,95 - 9,10 (1 H, m), 8,08 - 8,18 (1 H, m), 7,95 - 8,05 (1 H, m), 7,86 - 7,94 (1 H, m), 7,71 (2 H, d, J = 8,5 Hz), 7,20 (2 H, d, J = 8,8 Hz), 4,70 - 4,79 (1 H, m), 4,08 - 4,19 (2 H, m), 3,86 - 3,97 (1 H, m), 3,53 - 3,79 (5 H, m), 3,23 - 3,43 (2 H, m), 3,00 - 3,16 (2 H, m), 2,36 (2 H, q, J = 7,3 Hz), 1,90 - 2,09 (6 H, m), 1,48 - 1,72 (2 H, m), 1,01 (3 H, t, J = 7,4 Hz).
Ejemplo 174. Ciclopropil-(4-{4-[8-(2-pirrolidin-1-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 486 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 - 9,17 (1 H, m), 8,72 - 8,92 (1 H, m), 7,98 - 8,09 (1 H, m), 7,77 - 7,94 (2 H, m), 7,69 (2 H, d, J=8,5 Hz), 7,18 (2H, d, J=8,5 Hz), 4,71 - 4,80 (1 H, m), 4,16 - 4,26 (2 H, m), 3,87 - 4,08 (2 H, m), 3,49 - 3,72 (5 H, m), 3,23 - 3,37 (1 H, m), 3,00 - 3,20 (2 H, m), 1,92 - 2,10 (7 H, m), 1,49 - 1,75 (2 H, m), 0,66 - 0,79 (4 H, m).
E je m p lo 175. 1 -(4 - {4 -[8 -(3 -P ir ro l id in -1 - i l- p ro p o x i) -q u in o lin -7 - i l ] - fe n o x i} -p ip e r id in -1 - i l) -p ro p a n -1 -o n a , H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 488 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,07 - 9,13 (1 H, m), 8,71 - 8,82 (1 H, m), 7,95 - 8,02 (1 H, m), 7,74 - 7,85 (2 H, m), 7,67 (2 H, d, J=7,9 Hz), 7,18 (2H, d, J=8,8 Hz), 4,68 - 4,77 (1 H, m), 3,89 - 3,99 (3 H, m), 3,69 - 3,79 (1 H, m), 3,58 - 3,69 (2 H, m), 3,32 - 3,42 (1 H, m), 3,20 - 3,31 (3 H, m), 2,93 - 3,06 (2 H, m), 2,36 (2 H, q, J=7,4 Hz), 2,00 - 2,12 (5 H, m), 1,86 - 1,98 (3 H, m), 1,49 -1,70 (2 H, m), 1,01 (3 H, t, J=7,4 Hz).
Ejemplo 176. Ciclopropil-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 500 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 - 9,15 (1 H, m), 8,72 - 8,83 (1 H, m), 7,96 - 8,03 (1 H, m), 7,75 - 7,88 (2 H, m), 7,68 (2 H, d, J=8,8 Hz), 7,19 (2 H, d, J=8,8 Hz), 4,71 - 4,80 (1 H, m), 4,01 - 4,07 (1H, m), 3,88-3,99 (3H, m), 3,52-3,68 (3H, m), 3,19-3,33 (3H, m), 2,93-3,07 (2H, m), 2,00-2,13 (6H, m), 1,87-1,98 (3H, m), 1,51-1,74 (2H, m), 0,67-0,79 (4H, m).
Ejemplo 177. 1-[4-[4-[8-[2-(4-Metilpiperazin-1-il)etoxi]-7-quinolil]fenoxi]-1-piperidil]propan-1-ona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 503 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,10 (1 H, d, J=3,3 Hz), 8,60 - 8,78 (1 H, m), 7,97 (1 H, d, J=8,5 Hz), 7,71 - 7,83 (2 H, m), 7,67 (2 H, d, J = 8,5 Hz), 7,16 (2 H, d, J = 8,8 Hz), 4,73 (1 H, dt, J = 7,8, 4,0 Hz), 4,31 (2 H, br. s.), 3,87 - 4,05 (3 H, m), 3,67 - 3,80 (3 H, m), 3,43 - 3,67 (6 H, m), 3,22 - 3,42 (2 H, m), 2,87 (3 H, s), 2,36 (2 H, q, J = 7,3 Hz), 1,93 - 2,04 (2 H, m), 1,49 - 1,71 (2 H, m), 1,01 (3 H, t, J = 7,4 Hz).
Ejemplo 178. 1-[4-[4-[8-(2-Metoxietoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 435 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,13 - 9,19 (1 H, m), 8,93 - 9,02 (1 H, m), 8,03 - 8,08 (1 H, m), 7,91 - 7,98 (1 H, m), 7,85 - 7,90 (1 H, m), 7,69 (2 H, d, J=7,9 Hz), 7,17 (2 H, d, J=9,0 Hz), 4,73 (1 H, dt, J=7,8, 4,1 Hz), 4,02 - 4,08 (2 H, m), 3,87 - 3,97 (1 H, m), 3,69 - 3,78 (1 H, m), 3,54 - 3,59 (2 H, m), 3,21 - 3,41 (2 H, m), 3,05 (3 H, s), 2,36 (2 H, q, J=7,5 Hz), 1,91 - 2,07 (2 H, m), 1,48 - 1,70 (2 H, m), 1,00 (3 H, t, J=7,4 Hz).
E je m p lo 179. 1 -[4 -[4 -[8 -(3 -M e to x ip ro p o x i) -7 -q u in o li l ] fe n o x i] -1 -p ip e r id i l ]p ro p a n -1 -o n a , H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 449 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,15 (1 H, d, J=3,8 Hz), 8,93 (1 H, br. s.), 8,04 (1 H, d, J=8,5 Hz), 7,89 - 7,96 (1 H, m), 7,85 (1 H, d, J=8,8 Hz), 7,66 (2 H, d, J=8,8 Hz), 7,17 (2 H, d, J=8,8 Hz), 4,69 - 4,78 (1 H, m), 3,87 - 3,98 (3 H, m), 3,69 - 3,78 (1 H, m), 3,28 - 3,42 (1 H, m), 3,25 (3 H, t, J=6,4 Hz), 3,10 (3 H, s), 2,36 (2 H, q, J=7,5 Hz), 1,92 - 2,06 (2 H, m), 1,88 (2 H, quin, J = 6,5 Hz), 1,49 -1,70 (2 H, m), 1,00 (3 H, t, J = 7,4 Hz).
Ejemplo 180. {4-[4-(8-Isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, HCl
Una mezcla de 8-isopropoxi-7-[4-(piperidin-4-iloxi)-fenil]-quinolina; 2HCl (151 mg, 0,35 mmol), ácido (R)-tetrahidrofuran-2-carboxílico (35 pL, 0,36 mmol), HATU (145 mg, 0,38 mmol), y DIPEA (300 pL, 1,73 mmol) en THF (10 mL) se agitó a temperatura ambiente por 1 h. El disolvente se retiró y el residuo se purificó por HPLC preparativa. Las fracciones del producto se combinaron y se concentraron para dar aceite amarillento. Este aceite se diluyó en EtOAc (25 mL), se lavó con solución de NaHCO3 sat. (10 mL), salmuera, se secó (Na2SO4), y se concentró. El producto se disolvió en DCM (~5 mL) y se mezcló con 1,2 eq. de 2 M HCl en Et2 O y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se secó para dar 129 mg (75%) de sólido amarillo. Análisis: LCMS m/z = 461 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,15 - 9,20 (1 H, m), 8,99 - 9,09 (1 H, m), 8,05 - 8,12 (1 H, m), 7,95 - 8,03 (1 H, m), 7,88 - 7,95 (1 H, m), 7,69 - 7,75 (2 H, m), 7,15 - 7,22 (2 H, m), 4,67 - 4,80 (2 H, m), 4,17 - 4,27 (1 H, m), 3,72 - 3,87 (5 H, m), 3,24 - 3,48 (2 H, m), 2,00 - 2,09 (3 H, m), 1,77 - 1,89 (2 H, m), 1,48 - 1,71 (2 H, m), 1,11 (6 H, d, J=6,0 Hz).
Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 180.
Ejemplo 181. {4-[4-(8-Etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, HCl.
El producto se aisló como un sólido marrón. Análisis: LCMS m/z = 447 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,11 -9,19 (1 H, m), 8,91 - 9,04 (1 H, m), 8,03 - 8,11 (1 H, m), 7,85 - 7,99 (2 H, m), 7,67-7,75 (2H, m), 7,13-7,22 (2H, m), 4,65-4,82 (2H, m), 4,03 (1H, q, J=7,1 Hz), 3,92-3,97 (2H, m), 3,82-3,89 (1H, m), 3,73-3,81 (2H, m), 3,18-3,52 (2H, m), 2,00-2,08 (2H, m), 1,84 (2 H, d, J=7,3 Hz), 1,48-1,73 (2H, m), 1,12-1,28 (5H, m).
Ejemplo 182. (4-{4-[8-(2-Morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona, 2HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 532 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,09 - 9,16 (1 H, m), 8,72 - 8,86 (1 H, m), 7,98 - 8,06 (1 H, m), 7,74 - 7,89 (2 H, m), 7,67 (2 H, d, J=8,8 Hz), 7,17 (2 H, d, J=8,5 Hz), 4,67 - 4,78 (3 H, m), 4,25 - 4,35 (2 H, m), 3,91 - 3,98 (4 H, m), 3,71 - 3,89 (4 H, m), 3,51 - 3,55 (2 H, m), 3,22 - 3,50 (5 H, m), 1,93 - 2,13 (4 H, m), 1,75 - 1,92 (2 H, m), 1,50 - 1,73 (2 H, m).
Ejemplo 183. (4-{4-[8-(2-Pirrolidin-1 -il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-(R)-tetrahidrofuran-2-il-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 516 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 10,67 - 10,91 (1 H, m), 9,08 - 9,17 (1 H, m), 8,72 - 8,93 (1 H, m), 7,98 - 8,09 (1 H, m), 7,77 - 7,92 (2 H, m), 7,68 (2 H, d, J=8,5 Hz), 7,18 (2 H, d, J=8,5 Hz), 4,67 - 4,78 (2 H, m), 4,15 - 4,24 (2 H, m), 3,81 - 3,96 (2 H, m), 3,73 - 3,81 (2H, m), 3,59 -3,72 (2 H, m), 3,49 - 3,57 (2 H, m), 3,22 - 3,47 (2 H, m), 3,01 - 3,20 (2 H, m), 1,96 - 2,11 (8 H, m), 1,78 -1,90 (2 H, m), 1,49 - 1,73 (2 H, m).
Ejemplo 184. (4-{4-[8-(3-Pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 530 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,07 - 9,14 (1 H, m), 8,72 - 8,83 (1 H, m), 7,95 - 8,02 (1 H, m), 7,75 - 7,86 (2 H, m), 7,67 (2 H, d, J=8,8 Hz), 7,18 (2H, d, J=8,5 Hz), 4,67 - 4,77 (2 H, m), 3,93 - 3,98 (2 H, m), 3,83 - 3,90 (1 H, m), 3,73 - 3,80 (2 H, m), 3,59 - 3,67 (2 H, m), 3,33 - 3,50 (1 H, m), 3,21 - 3,27 (2 H, m), 2,94 - 3,06 (2 H, m), 1,97 - 2,10 (8 H, m), 1,89 - 1,96 (2 H, m), 1,78 - 1,89 (2 H, m), 1,51 - 1,71 (2 H, m).
Ejemplo 185. [4-[4-[8-[2-(4-Metilpiperazin-1-il)etoxi]-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 545 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,09 (1 H, d, J=3,5 Hz), 8,58 - 8,71 (1 H, m), 7,92 - 7,99 (1 H, m), 7,70 - 7,80 (2 H, m), 7,67 (2 H, d, J=8,5 Hz), 7,16 (2 H, d, J=8,5 Hz), 4,67 - 4,79 (2 H, m), 4,32 (2 H, br. s.), 3,84 - 4,01 (3 H, m), 3,69 - 3,82 (4 H, m), 3,20 - 3,66 (9 H, m), 2,86(3 H, s), 1,94 - 2,11 (4 H, m), 1,78 - 1,91 (2 H, m), 1,53 - 1,72 (2 H, m).
E je m p lo 186. [4 -[4 -[8 -(2 -M e to x ie to x i) -7 -q u in o li l ] fe n o x i] -1 -p ip e r id i l ] -[ (2 R ) - te t ra h id ro fu ra n -2 - i l ]m e ta n o n a , H C l.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 477 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,13 - 9,18 (1 H, m), 8,92 - 9,00 (1 H, m), 8,05 (1 H, d, J=8,8 Hz), 7,90 - 7,97 (1 H, m), 7,87 (1 H, d, J=8,5 Hz), 7,70 (2 H, d, J=8,8 Hz), 7,17 (2H, d, J=8,5 Hz), 4,67-4,80 (2H, m), 4,03-4,09 (2H, m), 3,72-3,89 (5H, m), 3,53-3,58 (2H, m), 3,27 3,40 (1H, m), 3,05 (3H, s), 1,95-2,09 (4H, m), 1,79-1,91 (2H, m), 1,50-1,72 (2H, m).
Ejemplo 187. [4-[4-[8-(3-Metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona, HCl.
El producto se aisló como un sólido amarillo. Análisis: LCMS m/z = 491 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,16 (1 H, d, J=4,8 Hz), 8,98 (1 H, d, J=7,8 Hz), 8,06 (1 H, d, J=8,8 Hz), 7,95 (1 H, dd, J=8,0, 5,0 Hz), 7,87 (1 H, d, J=8,5 Hz), 7,66 (2 H, d, J=8,8 Hz), 7,18 (2 H, d, J=8,8 Hz), 4,67 - 4,80 (2 H, m), 3,93 (2 H, t, J=6,5 Hz), 3,80 - 3,89 (2 H, m), 3,71 - 3,80 (2 H, m), 3,28 - 3,50 (2 H, m), 3,25 (2 H, t, J=6,3 Hz), 3,10 (3 H, s), 1,94 - 2,10 (4 H, m), 1,79 - 1,94 (4 H, m), 1,51 - 1,71 (2 H, m).
Ejemplo 188. 1-{4-[4-(8-Hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Etapa 1. 7-Bromo-8-(terc-butil-dimetil-silaniloxi)-quinolina.
Una mezcla de 7-bromoquinolin-8-ol (5,00 g, 22,3 mmol), tertbutildimetilsilil cloruro (3,70 g, 24,5 mmol), DIPEA (9,72 mL, 55,8 mmol), y DCM (100 mL) se agitó a temperatura ambiente por 3 días. La reacción se particionó en DCM (100) y H2 O (50 mL), la capa orgánica se separó luego se lavó con salmuera, se secó (Na2SO4), y se concentró. El residuo se sometió a cromatografía en gel de sílice (DCM) para dar 7,37 g de sólido blanco.
Etapa 2. terc-butil 4-[4-(8-hidroxi-7-quinolil)fenoxi]piperidina-1-carboxilato.
Un frasco cargado con terc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (3,0 g, 7,44 mmol), 7-bromo-8-(terc-butildimetil-silaniloxi)-quinolina (2,77 g, 8,18 mmol), acetato de paladio (170 mg, 0,75 mmol), trifenilfosfina (0,39 g, 1,49 mmol), 1,0 M de carbonato de sodio en agua (40 mL, 4,88 mmol), 1,4-dioxano (40 mL), y DMF (40 mL) se enjuagó con N2 por 25 min. La reacción se agitó a 90 °C por 18 h y se enfrió hasta la temperatura ambiente. La mezcla de reacción se particionó entre EtOAc (150 mL), se lavó con solución de NaHCO3 sat. (100 mL), la capa orgánica se separó y la capa de agua se extrajo con EtOAc (100 mL). Las capas orgánicas combinadas se lavaron con H2 O, salmuera, se secaron (Na2SO4), y se concentraron. El residuo se agitó en DCM (35 mL) a 0 °C y se añadió 1,0 M de tetra-n-butilamonio fluoruro en THF (4,88 mL, 4,88 mmol). Después de 1 h a temperatura ambiente, la reacción se lavó con H2 O (20 mL), salmuera, se secó (Na2SO4) y se concentró. El residuo se sometió a cromatografía en gel de sílice (0-70% EtOAc/Hexanos) para dar (1,03 g, 33%).
Etapa 3. 7-[4-(Piperidin-4-iloxi)-fenil]-quinolin-8-ol, HCl.
A una solución de terc-butil 4-[4-(8-hidroxi-7-quinolil)fenoxi]piperidina-1-carboxilato (638 mg, 1,52 mmol) en DCM (20 mL) se añadió 4,0 M de HCl en 1,4-dioxano (1,90 mL, 7,59 mmol). Después de 22 h, el precipitado resultante se
recogió por filtración, se lavó con DCM y se secó para dar 418 mg (77%) de sólido marrón claro.
Etapa 4. Una mezcla de 7-[4-(piperidin-4-iloxi)-fenil]-quinolin-8-ol; HCl (110 mg, 0,31 mmol), ácido propanoico (27 pL, 0,36 mmol), HATU (117 mg, 0,31 mmol), DIPEA (244 pL, 1,40 mmol), y THF (8 mL) se agitó a temperatura ambiente por 1 h. La mezcla de reacción se concentró y el residuo se purificó por HPLC preparativa. Las fracciones del producto se combinaron y se neutralizaron con solución de NaHCÜ3 sat. (25 mL), se extrajo con DCM (3 x 25 mL), se secó (Na2SÜ4), y se concentró. El producto se disolvió en DCM (~5 mL) y se mezcló con 1,2 eq. de 2 M HCl en Et2 Ü y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se secó para dar 82 mg (64%) de sólido blancuzco. Análisis: LCMS m/z = 377 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,76 - 10,69 (1 H, m), 8,98 - 9,03 (1 H, m), 8,70 - 8,78 (1 H, m), 7,77 - 7,84 (1 H, m), 7,65 - 7,77 (4 H, m), 7,10 - 7,17 (2 H, m), 4,68 - 4,73 (1 H, m), 3,84 - 3,95 (1 H, m), 3,67 - 3,78 (1 H, m), 3,21 - 3,43 (2 H, m), 2,35 (2 H, q, J=7,4 Hz), 1,89 - 2,06 (2 H, m), 1,49 - 1,72 (2 H, m), 1,00 (3 H, t, J=7,4 Hz).
Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 188.
Ejemplo 189. Ciclopropil-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
El producto se aisló como un sólido blancuzco. Análisis: LCMS m/z = 389 (M+1); 1H NMR (400 MHz, DMSO- d6) ó: 9,74 - 10,73 (1 H, m), 9,01 - 9,06 (1 H, m), 8,77 - 8,84 (1 H, m), 7,81 - 7,88 (1 H, m), 7,66 - 7,79 (4 H, m), 7,12 - 7,18 (2 H, m), 4,69 - 4,78 (1 H, m), 3,85 - 4,07 (2 H, m), 3,51 - 3,64 (1 H, m), 3,24 - 3,37 (1 H, m), 1,90 - 2,11 (3 H, m), 1,49 - 1,74 (2 H, m), 0,67 - 0,79 (4 H, m).
Ejemplo 190. {4-[4-(8-Hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, HCl.
El producto se aisló como un aceite naranja. Análisis: LCMS m/z = 419 (M+1); 1H NMR (400 MHz, DMSO- d6) ó: 9,63 10,98 (1H, m), 9,01-9,06 (1H, m), 8,78-8,84 (1H, m), 7,81-7,89 (1H, m), 7,65-7,79 (4H, m), 7,11-7,18 (2H, m), 4,69 4,73 (1H, m), 3,71-3,96 (4H, m), 3,22-3,51 (2H, m), 1,90-2,12 (5H, m), 1,76-1,90 (2H, m), 1,49-1,72 (2H, m).
Ejemplo 191. 1-[4-(2-Cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Etapa 1. terc-butil éster del ácido 4-(4-Bromo-2-cloro-fenoxi)-piperidina-1-carboxílico.
A una solución agitada 0-5 °C de trifenilfosfina (3,1 g, 11,7 mmol) y 40% p/p DEAD en tolueno (5,12 mL, 13,0 mmol) en THF (25 mL) se añadió una mezcla de 4-bromo-2-cloro-fenol (1,5 g, 7,2 mmol) y terc-butil éster del ácido 4-hidroxipiperidina-1-carboxílico (1,89 g, 9,39 mmol) en THF (5 mL) bajo argón. El baño de enfriamiento se retiró y la reacción se agitó a temperatura ambiente por 20 h, se concentró, luego se agitó con éter y se filtró. El filtrado se concentró al vacío y el producto se purificó por columna de gel de sílice cromatografía (0-20% EtOAC en hexanos) para dar 2,30 g (81%). Análisis: LCMS = 291 (M-100 - BOC).
Etapa 2. terc-butil éster del ácido 4-(2-Cloro-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico.
Un frasco cargado de 50 mL R. B. con 1,4-dioxano (2,5 mL), trifenilfosfina (0,119 g, 0,454 mmol), y acetato de paladio (0,026 g, 0,12 mmol) se agitó a temperatura ambiente por 15 min., se añadieron terc-butil éster del ácido 4-(4-bromo-2-cloro-fenoxi)-piperidina-1-carboxílico (0,89 g, 2,3 mmol), ácido 3-quinolinaborónico (0,59 g, 3,4 mmol), DMF (3,00 mL) y 1M carbonato de sodio (5 mL) acuoso y se enjuagó con argón cinco veces. La mezcla de reacción se calentó a 80 °C por 7 h y se concentró. El residuo se suspendió en una mezcla de 1M Na2CO3 y EtOAc y luego se filtró a través de una almohadilla de Celite/gel de sílice. El filtrado se separó y la capa acuosa se extrajo dos veces con EtOAc. Los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para dar un producto crudo. El producto se purificó por gel de sílice cromatografía usando 0-5% MeOH en DCM para dar 0,90 g (90%). Análisis: LCMS m/z 439 (M H).
Etapa 3. 3-[3-Cloro-4-(piperidin-4-iloxi)-fenil]-quinolina.
A una solución agitada de terc-butil éster del ácido 4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico (0,90 g, 2,0 mmol) en DCM (15,00 mL) se añadió 4M HCl en dioxano (2 mL, 23,1 mmol) a temperatura ambiente. La mezcla de reacción se agitó a temperatura ambiente por 17 h y se evaporó. El producto crudo se trató dos veces con EtOAc y se evaporó, se cristalizó a partir de una mezcla de DCM, MeOH, y éter para producir 3-[3-cloro-4-(piperidin-4-iloxi)-fenil]-quinolina, 0,67 g (96%) como un sólido amarillo. Análisis: mp: 274-276 °C (DCM, éter, y MeOH); 1H NMR (DMSO-d6) 6: 9,54 (d, 1H, J=2 Hz), 9,2-9,35 (brs, 2H), 9,19 (s, 1H), 8,30 (d, 1H, J=8 Hz), 8,23 (d, 1H, J = 8 Hz), 8,15 (d, 1H, J=2 Hz), 7,93-8,03 (m, 2H), 7,85 (t, 1H, J=7 Hz), 7,50 (d, 1H, J=9 Hz), 4,88-4,99 (m, 1H), 3,05-3,30 (m, 4H), 2,12-2,27 (m, 2H), 1,89-2,03 (m, 2H). Etapa 4. 1-[4-(2-Cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
A una solución agitada de 3-[3-cloro-4-(piperidin-4-iloxi)-fenil]-quinolina (0,125 g, 0,369 mmol) 2HCl y DIPEA (0,450 mL, 2,58 mmol) en DCM (3,00 mL) se añadió cloruro de propanoilo (0,0641 mL, 0,738 mmol) a temperatura ambiente. La mezcla de reacción se agitó por 2 h y se evaporó. El producto crudo se purificó por Gilson. El producto se agitó con 4M HCl en dioxano (1 mL) por 15 min y se recristalizó a partir de una mezcla de DCM, MeOH, y éter y se secó a 60 °C por 16 h para dar un sólido amarillo (0,1 g, 68%). Análisis: mp: 183-185 °C; LCMS m/z 395 (M 1); 1H NMR (DMSO-d6) 6: 9,46(d, 1H, J = 2 Hz), 9,04 (s, 1H), 8,14-8,23 (m, 2H), 8,10 (d, 1H, J = 2 Hz), 7,88-7,98 (m, 2H), 7,79 (t, 1H, J = 7 Hz), 7,47(d, 1H, 9 Hz), 4,84-4,93 (m, 1H), 3,63-3,77 (m, 2H), 3,38-3,53 (m, 2H), 2,37 (q, 2H, J = 7 Hz), 1,85-2,04 (m, 2H), 1,57-1,80 (m, 2H), 1,00 (t, 3H, J = 7 Hz).
Los siguientes ejemplos se sintetizaron usando el método del ejemplo 191.
Ejemplo 192. 1-[4-(2-Cloro-4-quinolin-3-il-fenoxi)-piperidin-1-y1]-2-metil-propan-1-ona.
Análisis: LCMS m/z 409 (M 1); 1H NMR (DMSO-d6) 6: 9,56 (d, 1H, J = 2 Hz), 9,23 (s, 1H), 8,31 (d, 1H, J = 8Hz), 825 (d, 1H, J = 8 Hz), 8,14 (d, 1H, J = 2 Hz), 7,96-8,07 (m, 1H), 7,93-7,96 (m, 1H), 7,86 (t, 1H, J = 8 Hz), 7,49 (d, 1H, J = 9 Hz), 4,85-4,96 (m, 1H), 3,68-3,80 (m, 2H), 3,40-3,58 (m, 2H), 2,83-2,99 (m, 1H), 1,82-2,05 (m, 2H), 1,52-1,78 (m, 2H), 1,01 (d, 6H, J = 7 Hz).
Ejemplo 193. [4-(2-Cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-ciclopropil-metanona.
Análisis: LCMS m/z 407 (M 1); 1H NMR (DMSO-d6) 6: 9,58 (s, 1H), 9,20 (s, 1H), 8,29 (d, 1H, J = 8 Hz), 8,24 (d, 1H, J = 8 Hz), 8,15 (s, 1H), 7,90-8,09 (m, 2H), 7,85 (t, 1H, J = 8 Hz), 7,50 (d, 1H, J = 8 Hz), 4,87-4,96 (m, 1H), 3,34-4,06 (m, 4H), 1,81-2,07 (m, 3H), 1,53-1,81 (m, 2H), 0,65-0,82 (m, 4H).
E je m p lo 194. 1 -[4 -(2 -C lo ro -4 -q u in o lin -7 - i l - fe n o x i) -p ip e r id in -1 - i l ] - p ro p a n -1 -o n a .
Análisis: LCMS m/z 395 (M 1); 1H NMR (DMSO-d6) 6: 9,19 (d, 1H, J = 3 Hz), 8,90 (d, 1H, J = 8Hz), 8,44 (s, 1H), 8,31 (d, 1H, J = 8 Hz), 8,21 (d, 1H, J = 1H), 8,00 (d, 1H, J = 2 Hz), 7,79-7,93 (m, 2H), 7,47 (d, 1H, J = 9 Hz), 4,82-4,92 (m, 1H), 3,62-3,78 (m, 2H), 3,37-3,51 (m, 2H), 2,36, (q, 2H, J = 7 Hz), 1,85-2,41 (m, 2H), 1,55-1,80 (m, 2H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 195. 1-[4-(2-Cloro-4-quinolin-7-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z 409 (M 1); 1H NMR (DMSO-d6) 6: 9,15-9,24 (m, 1H), 8,85-8,97 (m,1H), 8,40-8,49 (m, 1H), 8,27 8,37 (m, 1H), 8,16-8,25 (m, 1H), 7,99 (d, 1H, J= 2 Hz), 7,70-7,83 (m, 2H), 7,47 (d, 1H, J = 8 Hz), 4,83-4,92 (m, 1H), 3,34-3,83 (m, 4H), 2,87-2,98 (m, 1H), 1,83-2,08 (m, 2H), 1,56-1,80 (m, 2H), 1,01 (d, 6H, J = 7 Hz).
Ejemplo 196. 1-[4-(2-Metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (DMSO-d6) 6: 9,51(d, 1H, J = 2 Hz), 9,11 (s, 1H), 7,95 (t, 1H, J = 8Hz), 7,82 (t, 1H, J = 8 Hz), 7,57 (d, 1H, J = 2 Hz), 7,50 (d, 1H, J = 8 Hz), 7,26 (d, 1H, J = 8 Hz), 4,60-4,69 (m, 1H), 3,81 4,00 (m, 4H), 3,63-3,79 (m, 1H), 3,21-3,42 (m, 2H), 2,34 (q, 2H, J = 7 Hz), 1,82 (m, 2H, 1,45-1,69 (m, 2H) 1,00 (t, 3H, J = 7 Hz).
Ejemplo 197. 1-[4-(2-Metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z = 405 (M 1); 1H NMR (DMSO-d6) 6: 9,46 (d,1H, J = 2 Hz), 9,01 (s, 1H), 8,18 (d, 1H, J = 8 Hz), 7,91 (t, 1H, J = 7 Hz), 7,79 (t, 1H, J = 7 Hz), 7,56 (d, 1H, J = 2 Hz), 7,47 (d, 1H, J = 8 Hz), 7,26 (d, 1H, J = 8 Hz), 4,61 4,68 (m, 1H), 3,75-3,97 (m, 5H), 3,20-3,48 (m, 2H), 2,84-2,96 (m, 1H), 1,82-2,05 (m, 2H), 1,45-1,68 (m, 2H), 1,01 (d, 6H, J = 7 Hz).
E je m p lo 198. C ic lo p ro p il-[4 -(2 -m e to x i-4 -q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] -m e ta n o n a .
Análisis: LCMS m/z = 403 (M 1); 1H NMR (DMSO-d6) 6: 9,55 (d, 1H, J = 2 Hz), 9,15 (s, 1H), 8,20-8,32 (m, 2H), 7,98 (t, 1H, J = 8 Hz), 7,85 (t, 1H, J = 8 Hz), 7,60 (d, 1H, J = 2 Hz), 7,52 (d, 1H, J = 8 Hz), 7,29 (d, 1H, J = 8 Hz), 4,64-4,75 (m, 1H), 3,80-4,10 (m, 5H), 3,48-3,63 (m, 1H), 3,21-3,39 (m, 1H), 1,84-2,15 (m, 3H), 1,43-1,78 (m, 2H), 0,67-0,82 (4H).
Ejemplo 199. 1-[4-(2-Metoxi-4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 391 (M+1); 1H NMR (DMSO-d6) 6: 9,15 (d, 1H, J = 5 Hz), 8,90 (d, 1H, J = 8 Hz), 8,43 (s, 1H), 8,29 (d, 1H, J = 9 Hz), 8,22 (d, 1H, J = 9 Hz), 7,82-7,91 (m, 1H), 7,47 (d, 1H, J = 2 Hz), 7,42 (d, 1H, J = 8 Hz), 7,25 (d, 1H, J = 8 Hz), 4,60-4,70 (m, 1H), 3,84-3,95 (m, 5H), 3,64-3,84 (m, 2H), 3,20-3,30 (m, 2H), 2,35 (q, 2H, J = 7 Hz), 1,83 2,04 (m, 2H), 1,45-1,71 (m, 2H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 200. 1-[4-(3-Fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z 379 (M 1); 1H NMR (DMSO-d6) 6: 9,24 (s, 1H), 8,85 (s, 1H), 8,20 (d, 1H, J = 9 Hz), 7,94 (t, 1H, J = 7 Hz), 7,79 (t, 1H, J = 7 Hz), 7,71 (t, 1H, J = 9 Hz), 7,16 (dd, 1H, J = 2 Hz, J = 13 Hz), 7,06 (dd, 1H, J = 2 Hz, J = 9 Hz), 4,73-4,82 (m, 1H), 3,84-3,97 (m, 2H), 3,65-3,79 (m, 2H), 3,18-3,42 (m, 2H), 2,35 (q, 2H, J = 7 Hz), 1,89-2,07 (m, 2H), 1,46-1,70 (m, 2H), 1,00 (t, 3H, 7Hz).
Ejemplo 201.1-[4-(3-Fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metilpropan-1-ona.
Análisis: LCMS m/z = 393 (M+1). 1H NMR (DMSO-d6) 6: 9,23 (s, 1H), 8,81 (s, 1H), 8,18 (d, 2H, J = 8 Hz), 7,94 (t, 1H, J = 7 Hz), 7,78 (t, 1H, J = 8 Hz), 7,73 (t, 1H, J = 9 Hz), 7,16 (dd, 1H, J= 2 Hz, J = 9 Hz), 7,06 (dd, 1H, J = 2 Hz, J = 8 Hz), 4,74-4,83 (m, 1H), 3,86-3,97 (m, 1H), 3,74-3,85 (m, 1H), 3,35-3,47 (m, 1H), 3,19-3,31 (m, 1H), 2,84-2,97 (m, 1H), 1,89-2,09 (m, 2H, 1,47-1,70 (m, 2H), 1,01 (d, 6H, J = 7 Hz).
E je m p lo 202. C ic lo p ro p il-[4 -(3 - f lu o ro -4 -q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] -m e ta n o n a .
Análisis: LCMs m/z = 391 (M+1); 1H NMR (DMSO-d6) 6: 9,23 (s, 1H), 8,81 (s, 1H), 8,13-8,23 (m, 2H), 7,93 (t, 1H, J = 8 Hz), 7,67-7,82 (m, 2H), 7,17 (dd, 1H, J = 2 Hz), J = 13 Hz), 7,07 (dd, 1H, J = 2 Hz), J = 9 Hz), 4,73-4,87 (m, 1H), 3,82-4,10 (m, 2H), 3,47-3,65 (m, 1H), 3,19-3,36 (m, 1H), 1,87-2,14 (m, 3H), 1,45-1,75 (m, 2H), 0,64-0,79 (m, 4H). Ejemplo 203. 1-[4-(3-Cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 395 (M+1); 1H NMR (DMSO-d6) 6: 9,16 (s, 1H), 8,75 (s, 1H), 8,15-8,25 (m,2H), 7,96 (t, 1H, J = 7 Hz), 7,79 (t, 1H, J = 7 Hz), 7,58 (d, 1H, J = 8 Hz), 7,34 (d, 1H, J = 2 Hz), 7,19 (dd, 1H, J = 2 Hz, J = 9 Hz), 4,74-4,84 (m, 1H), 3,83-3,96 (m, 2H), 3,21-3,42 (m, 2H), 2,35 (q, 2H, J = 7 Hz), 1,88-2,07 (m, 2H), 1,46-1,70 (m, 2H, 1,00 (t, 3H, J = 7 Hz).
Ejemplo 204. 1-[4-(3-Cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z = 409 (M+1); 1H NMR (DMSO-d6) 6: 9,16 (d, 1H, J = 2 Hz), 8,76 (s, 1H), 8,20 (t, 1H, J = 8 Hz), 7,96 (t, 1H, J = 8 Hz), 7,80 (t, 1H, J = 8 Hz), 7,59 (d, 1H, J= 8 Hz), 7,35 (d, 1H, J= 2 Hz), 7,19 (dd, 1H, J = 2 Hz, J = 9 Hz), 4,75-4,85 (m, 1H), 3,74-3,97 (m, 2H), 3,35-3,48 (m, 1H), 3,20-3,33 (m, 1H), 2,84-2,97 (m, 1H), 1,88-2,09 (m, 2H), 1,46-1,70 (m, 2H), 1,00 (d, 6H, J = 7 Hz).
Ejemplo 205. [4-(3-Cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-ciclopropil-metanona.
Análisis: LCMS m/z 407 (M+1); 1H NMR (DMSO-d6) 6: 9,12 (s, 1H), 8,70 (s, 1H), 8,17 (t, 2H, J = 7 Hz), 7,93 (t, 1H, J = 7 Hz), 7,77 (t, 1H, J = 7 Hz), 7,58 (d, 1H, J = 8 Hz), 7,34 (s, 1H), 7,19 (d, 1H, J = 7 Hz), 4,75-4,88 (m, 1H), algunos picos se unieron con pico de agua, 3,19-3,37 (m, 1H), 1,87-2,13 (m, 3H), 1,44-1,75 (m, 2H), 0,63-0,80 (m, 4H).
E je m p lo 206. 2 -M e t il-1 -[4 -(3 -m e t i l- 4 -q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] - p ro p a n -1 -o n a .
Análisis: LCMS m/z = 389 (M+1); 1H NMR (DMSO-d6) 6: 9,17 (d, 1H, J = 2 Hz), 8,80 (s, 1H), 8,17-8,30 (m, 2H), 7,99 (t, 1H, J = 8 Hz), 7,83 (t, 1H, J = 7 Hz), 7,37 (d, 1H, J = 8 Hz), 6,97-7,09 (m, 2H), 4,67-4,78 (m, 1H), 3,72-3,96 (m, 2H), 3,21-3,48 (m, 2H), 2,83-2,98 (m,1H), 2,32 (s, 3H), 1,87-2,08 (m,2H), 1,44-1,71 (m,2H), 1,01 (d,6H, J = 7Hz).
Ejemplo 207. 1-[4-(3-Metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 375 (M+1); 1H NMR (DMSO-d6) 6: 9,14 (d, 1H, J = 2 Hz), 8,74 (s, 1H), 8,20 (t, 2Hz, J = 8 Hz), 7,96 (t, 1H, J = 7 Hz), 7,81 (t, 1H, J=7 Hz), 7,36 (d, 1H, J=9Hz), 6,96-7,08 (m, 2H), 4,65-4,75 (m, 1H), 3,82-3,94 (m, 2H), 3,65-3,77 (m, 2H), 3,21-3,42 (m, 2H), 2,35 (q, 2H, J = 7 Hz), 2,31 (s, 3H), 1,87-2,05 (m, 2H), 1,46-1,70 (m, 2H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 208. éster metílico del ácido 4-(3-Metil-4-quinolin-3-il-fenoxi)-piperidina-1 -carboxílico.
Análisis: LCMS m/z = 377 (M+1); 1H NMR (DMSO-d6) 6: 9,15 (d, 1H, J = 2H), 8,79 (s, 1H), 8,22 (t, 2H, J = 8 Hz), 7,98 (t, 1H, J = 8 Hz), 7,83 (t, 2H, J = 8 Hz), 7,36 (d, 1H, J = 8 Hz), 6,96-7,07 (m, 2H), 4,62-4,73 (m, 1H), 3,65-3,79 (m, 2H), 3,22-3,36 (m, 2H), 2,31 (s, 3H), 1,90-2,10 (m, 2H), 1,52-1,66 (m, 2H).
Ejemplo 209. 1-[4-(3-Metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 391 (M+1); 1H NMR (DMSO-d6) 6: 9,22 (d, 1H, J = 2 Hz), 8,79 (s, 1H), 8,18 (d, 2H, J = 8 Hz), 7,93 (t, 1H, J = 8Hz), 7,78 (t, 1H, J=8Hz), 7,50 (d, 1H, J=8Hz), 6,75-6,85 (m, 2H), 4,70-4,82 (m, 1H), 3,80-3,96 (m, 2H), 3,84 (s, 3H), 3,22-3,44 (m, 2H), 2,35 (d, 2H, J=8Hz), 1,87-2,08 (m, 2H), 1,46-1,73 (m, 2H), 1,00 (t, 3H, J=7Hz).
Ejemplo 210. 1-[4-(3-Metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z = 405 (M+1); 1H NMR (DMSO-d6) 6: 9,23 (d, 1H, J = 2 Hz), 8,81 (s, 1H), 8,13-8,23 (m, 2H), 7,93 (t, 1H, J = 8 Hz), 7,78 (t, 1H, J = 8 Hz), 7,50 (d, 1H, J = 8 Hz), 6,77-6,85 (m 2H), 4,73-4,84 (m, 1H), 3,73-3,95 (m, 2H), 3,84 (s, 3H), 3,23-3,49 (m, 2H), 2,85-2,97 (m, 1H), 1,88-2,09 (m, 2H), 1,46-1,71 (m, 2H), 1,01 (d, 6H, J = 6 Hz).
Ejemplo 211. Ciclopropil-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 403 (M+1); 1H NMR (DMSO-d6) 6: 9,19 (d, 1H, J = 2 Hz), 8,73 (s, 1H), 8,15 (d, 2H, J = 8 Hz), 7,90 (t, 1H, J = 8 Hz), 7,76 (t, 1H, J = 8 Hz), 7,49 (d, 1H, J = 8 Hz), 6,77-6,86 (m, 2H), 4,73-4,84 (m, 1H), 3,80-4,07 (m, 2H), 3,84 (s, 3H), 3,49-3,66 (m, 1H), 3,23-3,39 (m, 1H), 1,87-2,13 (m, 3H), 1,46-1,76 (m, 2H), 0,63-0,79 (m, 4H).
Ejemplo 212. 1-[4-(2-Metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 375 (M+1); 1H NMR (DMDSO-d6) 6: 9,47 (s, 1H, J = 2 Hz), 9,06 (s, 1H), 8,22 (d, 2H, J = 8 Hz), 7,94 (t, 1H, J = 7 Hz), 7,86-7,73 (m, 3H), 7,24 (d, 1H, J = 8 Hz), 4,83-4,73 (m, 1H), 3,80-3,59 (m, 2H), 3,50-3,37 (m, 2H), 2,36 (q, 2H, J = 7 Hz), 2,29 (s, 3H), 2,04-1,84 (m, 2H), 1,76-1,54 (m, 2H), 1,01 (t, 3H, J = 7 Hz).
Ejemplo 213. 2-Metil-1-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 389 (M+1); 1H NMR (DMSO-d6) 6: 9,37 (d, 1H, J = 2 Hz), 8,86 (s, 1H), 8,13 (t, 2H, J = 7 Hz), 7,86 (t, 1H, 7 Hz), 7,68-7,81 (m, 3H), 7,22 (d, 1H, J = 8 Hz), 4,72-4,83 (m, 1H), 2,84-2,97 (m, 1H), 2,29 (s, 3H), 1,84 2,06 (m, 2H), 1,51-1,77 (m, 2H), 1,01 (d, 6H, J = 7 Hz).
Ejemplo 214. Ciclopropil-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 386 (M+1); 1H NMR (DMSO-d6) 6: 9,43 (d, 1H, J=2 Hz), 8,98 (s, 1H), 8,18 (d, 2H, J=9 Hz), 7,91 (t, 1H, J=7 Hz), 7,71-7,84 (m, 3H), 7,23 (d, 1H, J=8 Hz), 4,74-4,85 (m, 1H), algunos picos se unieron con H2 O, 2,29 (s, 3H), 1,82-2,10 (m, 3H), 1,52-1,81 (m, 2H).
E je m p lo 215. 1 -[4 -(2 ,5 -D if lu o ro -4 -q u in o lin -3 - i l- fe n o x i) -p ip e r id in -1 - i l ] - p ro p a n -1 -o n a .
Análisis: LCMS m/z = 397 (M+1); 1H NMR (DMSO-d6) 6: 9,17 (s, 1H), 8,72 (s, 1H), 8,12 (d, 2H, J = 9 Hz), 7,84-7,91 (m, 1H), 7,69-7,81 (m, 2H), 7,47-7,56 (m, 1H), 4,75-4,85 (m, 1H), 3,66-3,77 (m, 2H), 3,20-3,41 (m, 2H), 2,35 (q, 2H, J = 7 Hz), 1,90-2,09 (m, 2H), 1,49-1,74 (m, 2H), 1,00 (t, 3H, J = 7 Hz).
Ejemplo 216. 1-[4-(2,5-Difluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z = 411 (M+1); 1H NMR (DMSO-d6) 6: 9,20 (d, 1H, J = 2 Hz), 8,77 (s, 1H), 8,14 (d, 2H, J = 9 Hz), 7,90 (t, 1H, J = 7 Hz), 7,72-7,82 (m, 2H), 7,48-7,57 (m, 1H), 4,76-4,86 (m, 1H), 3,77-4,00 (m, 2H), 3,41 (t, 1H, J = 10 Hz), 3,25 (t, 1H, J = 9 Hz), 2,83-2,98 (m, 1H), 1,91-2,12 (m, 2H), 1,49-1,74 (m, 2H), 1,01 (d, 6H, J = 7 Hz).
Ejemplo 217. Ciclopropil-[4-(2,5-difluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 409 (M+1); 1H NMR (DMSO-d6) 6: 9,15 (t, 1H, 2H), 8,69 (s, 1H), 8,10 (d, 2H, J = 9 Hz), 7,86 (t, 1H, J = 7 Hz), 7,68-7,80 (m, 2H), 7,47-7,57 (m, 1H), 4,77-4,87 (m, 1H), 3,84 -4,09 (m, 2H), 3,20-3,36 (m, 1H), 1,90 2,15 (m, 3H), 1,49-1,77 (m, 2H), 0,65-0,79 (m, 4H).
Ejemplo 218. 3-Oxo-3-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propionitrilo.
Un frasco de 25 mL R. B. se cargó con ácido cianoacético (0,04 g, 0,47 mmol), 3-[4-(piperidin-4-iloxi)-fenil]-quinolina (0,11 g, 0,36 mmol), acetonitrilo (2 mL), DIPEA (0,504 mL, 2,89 mmol), y HAt U (0,302 g, 0,795 mmol). La mezcla de reacción se agitó a temperatura ambiente y se monitoreó por métodos HPLC y LCMS. Después del completamiento, la mezcla de reacción se evaporó al vacío para obtener un producto crudo. El producto crudo se purificó por Gilson y luego se liofilizó para producir 3-Oxo-3-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propionitrilo, 0,102 g (60%). Análisis: LCMS m/z = 372 (M 1); 1H NMR (DMSO-d6) 6: 9,34 (d, 1H, J = 2 Hz), 8,80 (s, 1H), 8,10 (t, 2H, J = 9 Hz), 7,80-7,92 (m, 3H), 7,71 (t, 1H, J= 8 Hz), 7,19 (d, 2H, J = 8 Hz), 4,70-4,80 (m, 1H), 4,08 (s, 2H), 3,78-3,89 (m, 1H), 3,54-3,65 (m, 1H), 3,27-3,40 (m, 2H), 1,90-2,08 (m, 2H), 1,65-1,77 (m, 1H), 1,53-1,65 (m, 1H).
E je m p lo 219. 1 - {4 -[2 -F lu o ro -4 -(8 -m e to x i-q u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 409 (M 1); 1H NMR (DMSO-d6) 6: 9,04 - 9,11 (m, 1 H) 8,72 (d, J=8,28 Hz, 1 H) 7,95 (d, J=8,53 Hz, 1 H) 7,75 - 7,83 (m, 2 H) 7,60 (dd, J=12,55, 2,01 Hz, 1 H) 7,38 - 7,53 (m, 2 H) 4,74 (dt, J=7,84, 3,98 Hz, 1 H) 3,86 - 3,97 (m, 1 H) 3,85 (s, 3 H) 3,66 - 3,78 (m, 1 H) 3,22 - 3,42 (m, 2 H) 2,36 (q, J=7,45 Hz, 2 H) 1,91 - 2,09 (m, 2 H) 1,51 - 1,75 (m, 2 H) 1,01 (t, J=7,40 Hz, 3 H).
Ejemplo 220. Ciclopropil-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 421 (M+1); 1H NMR (DMSO-d6) 6: 9,05 (dd, J=4,52, 1,51 Hz, 1 H) 8,67 (d, J=8,03 Hz, 1 H) 7,92 (d, J=8,53 Hz, 1 H) 7,71 - 7,80 (m, 2 H) 7,59 (dd, J=12,80, 2,01 Hz, 1 H) 7,38-7,52 (m, 2H) 4,76 (dt, J=7,72, 4,05Hz, 1H) 3,81-4,09 (m, 5H) 3,57 (br. s., 1H) 3,30 (br. s., 1H) 1,90-2,14 (m, 3H) 1,49-1,79 (m, 2H) 0,63-0,82 (m, 4H).
Ejemplo 221. {4-[2-Fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Un frasco 50 mL R.B cargado con 7-[3-fluoro-4-(piperidin-4-iloxi)-fenil]-8-metoxiquinolina (0,237 g, 0,673 mmol), ácido (R)-tetrahidrofuran-2-carboxílico (0,091 g, 0,79 mmol), HATU (0,30 g, 0,79 mmol), Et3N (0,55 mL, 3,9 mmol) y Dc M (3 mL) se agitó a temperatura ambiente 1,5 h. La mezcla de reacción se concentró, y se particionó entre EtOAc y NaHCO3 saturado acuoso. La capa acuosa se extrajo dos veces con EtOAc y los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se concentraron para dar un producto crudo que se purificó por Gilson para producir {4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, 85 mg (28%). Análisis: LCMS m/z = 451 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,06 (dd, J=4,52, 1,51 Hz, 1 H) 8,68 (d, J=8,03 Hz, 1 H) 7,93 (d, J=8,53 Hz, 1 H) 7,72 - 7,80 (m, 2 H) 7,59 (dd, J=12,55, 2,01 Hz, 1 H) 7,38 - 7,52 (m, 2 H) 5,76 (s, 2 H) 4,65 - 4,81 (m, 4 H) 3,70 - 3,96 (m, 8H) 3,20 - 3,52 (m, 2H) 1,92-2,13 (m, 4H) 1,77-1,91 (m, 2H) 1,51-1,75 (m, 2H).
Ejemplo 222. {4-[4-(8-Cloroquinolin-7-il)-2-fluorofenoxi]-piperidin-1-il}-ciclopropil-metanona.
Análisis: LCMS m/z = 425 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 (dd, J=4,14, 1,63 Hz, 1 H) 8,51 (dd, J=8,28, 1,76 Hz, 1 H) 8,05 (d, J=8,53 Hz, 1 H) 7,63 - 7,73 (m, 2 H) 7,49 (dd, J=12,30, 2,26 Hz, 1 H) 7,39 - 7,46 (m, 1H) 7,31 -7,38 (m, 1 H) 4,76 (tt, J=7,81, 3,73 Hz, 1 H) 3,83 - 4,10 (m, 2 H) 3,57 (br. s., 1 H) 3,29 (br. s., 1 H) 1,90 - 2,15 (m, 3 H) 1,50 - 1,80 (m, 2 H) 0,65 - 0,81 (m, 4 H).
E je m p lo 223. {4 -[4 -(8 -C lo ro q u in o lin -7 - i l) -2 - f lu o ro fe n o x i] -p ip e r id in -1 - i l} -(R ) - te t ra h id ro fu ra n -2 - i l-m e ta n o n a .
Análisis: LCMS m/z = 455 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,07 (dd, J=4,27, 1,76 Hz, 1 H) 8,51 (dd, J=8,28, 1,76 Hz, 1 H) 8,05 (d, J=8,53 Hz, 1 H) 7,62 - 7,73 (m, 2 H) 7,49 (dd, J=12,17, 2,13 Hz, 1 H) 7,38 - 7,45 (m, 1 H) 7,31 -7,37 (m, 1 H) 4,66 - 4,81 (m, 2 H) 3,69 - 3,97 (m, 4 H) 3,20 - 3,52 (m, 2 H) 1,92 - 2,14 (m, 4 H) 1,77 - 1,91 (m, 2 H) 1,50-1,77 (m, 2 H).
Ejemplo 224. 1-{4-[4-(8-Cloroquinolin-7-il)-2-fluorofenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 413 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,03 - 9,11 (m, 1 H) 8,51 (dd, J=8,28, 1,76 Hz, 1 H) 8,05 (d, J=8,53 Hz, 1 H) 7,62 - 7,72 (m, 2 H) 7,48 (dd, J=12,17, 2,13 Hz, 1 H) 7,41 (d, J=8,78 Hz, 1 H) 7,35 (d, J=1,25 Hz, 1 H) 4,74 (dt, J=7,91,4,08 Hz, 2 H) 3,84 - 3,97 (m, 1 H) 3,66 - 3,79 (m, 1 H) 3,21 - 3,43 (m, 2 H) 2,36 (q, J=7,53Hz, 2H) 1,98 (d, J=18,57Hz, 2H) 1,51-1,75 (m, 2H) 1,01 (t, J=7,40Hz, 3H).
Ejemplo 225. 1-{4-[2-Fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 393 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,04 (dd, J=4,52, 1,76 Hz, 1 H) 8,55 (dd, J=8,16, 1,38 Hz, 1 H) 7,95 (d, J=8,28 Hz, 1 H) 7,68 (dd, J=8,28, 4,52Hz, 1H) 7,57 (d, J=8,53Hz, 1H) 7,33-7,44 (m, 2H) 7,22 (dt, J=8,47, 1,04 Hz, 1H) 4,72 (dt, J=7,78, 4,14 Hz, 1H) 3,84-3,96 (m, 1H) 3,67-3,78 (m, 1H) 3,21-3,43 (m, 2H) 2,69 (s, 3H) 2,30-2,42 (m, 2H) 1,90-2,08 (m, 2H) 1,51-1,75 (m, 2H) 1,01 (t, J=7,40 Hz, 3H).
Ejemplo 226. {4-[2-Fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-®-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 435 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,03 (dd, J=4,27, 1,76 Hz, 1 H) 8,53 (d, J=8,28 Hz, 1 H) 7,94 (d, J=8,28 Hz, 1 H) 7,67 (dd, J=8,28, 4,27 Hz, 1 H) 7,56 (d, J=8,53 Hz, 1 H) 7,33 - 7,44 (m, 2 H) 7,22 (dd, J=8,41, 1,13 Hz, 1 H) 4,66 - 4,78 (m, 2 H) 3,70 - 3,98 (m, 4 H) 3,20 - 3,53 (m, 2 H) 2,69 (s, 3 H) 1,92 - 2,14 (m, 4 H) 1,77 - 1,91 (m, 2 H) 1,51 - 1,76 (m, 2 H).
E je m p lo 227. C ic lo p ro p il- {4 -[2 - f lu o ro -4 -(8 -m e t i lq u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 405 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,04 (dd, J=4,27, 1,76 Hz, 1 H) 8,54 (dd, J=8,28, 1,51 Hz, 1 H) 7,95 (d, J=8,28 Hz, 1 H) 7,67 (dd, J=8,28, 4,52 Hz, 1 H) 7,57 (d, J=8,53 Hz, 1 H) 7,33 - 7,45 (m, 2 H) 7,23 (dt, J=8,41, 1,07 Hz, 1 H) 4,74 (dt, J=7,84, 3,98 Hz, 1 H) 3,82 - 4,09 (m, 2 H) 3,57 (br. s., 1 H) 3,29 (br. s., 1 H) 2,70 (s, 3 H) 1,88 - 2,14 (m, 3 H) 1,50 - 1,78 (m, 2 H) 0,62 - 0,81 (m, 4 H).
Ejemplo 228. 1-{4-[2-Fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 393 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,04 (dd, J=4,27, 1,76 Hz, 1 H) 8,54 (dd, J=8,28, 1,51 Hz, 1 H) 7,95 (d, J=8,28 Hz, 1 H) 7,67 (dd, J=8,28, 4,52 Hz, 1 H) 7,57 (d, J=8,53 Hz, 1 H) 7,33 - 7,45 (m, 2 H) 7,23 (dt, J=8,41, 1,07 Hz, 1 H) 4,74 (dt, J=7,84, 3,98 Hz, 1 H) 3,82 - 4,09 (m, 2 H) 3,57 (br. s., 1 H) 3,29 (br. s., 1 H) 2,70 (s, 3 H) 1,88 - 2,14 (m, 3 H) 1,50 - 1,78 (m, 2 H) 0,62 - 0,81 (m, 4 H).
Ejemplo 229. Ciclopropil-{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 405 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,95 (s, 1 H) 8,34 (d, J=7,78 Hz, 1 H) 8,14 (d, J=7,78 Hz, 1 H) 7,90 - 7,98 (m, 1 H) 7,78 - 7,86 (m, 1 H) 7,42 - 7,52 (m, 2 H) 7,30 (dd, J=8,41, 1,13 Hz, 1 H) 4,73 -4,82 (m, 1 H) 3,83 - 4,09 (m, 2 H) 3,58 (br. s., 1 H) 3,30 (br. s., 1 H) 2,73 (s, 3 H) 1,90 - 2,15 (m, 3 H) 1,50 - 1,79 (m, 2 H) 0,65 - 0,80 (m, 4 H).
Ejemplo 230. {4-[2-Fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 435 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,92 (s, 1 H) 8,32 (d, J=8,03 Hz, 1 H) 8,12 (d, J=8,28 Hz, 1 H) 7,91 (t, J=7,65 Hz, 1 H) 7,75 - 7,85 (m, 1 H) 7,39 - 7,52 (m, 2 H) 7,29 (d, J=8,28 Hz, 1H) 4,66-4,82 (m, 3H) 3,68-3,97 (m, 6H) 3,20-3,53 (m, 3H) 2,72 (s, 3H) 1,92-2,12 (m, 4H) 1,77-1,92 (m, 2H) 1,52-1,77 (m, 2H).
E je m p lo 231. 1 - {4 -[4 -(4 -A m in o q u in o lin -3 - i l) - fe n o x i] -p ip e r id in -1 - i l} -p ro p a n -1 -o n a
Etapa 1. t-butil éster del ácido 4-[4-(4-Aminoquinolin-3-il)-fenoxi]-piperidina-1-carboxílico.
Un frasco de 50 mL R. B. cargado con 1,4-dioxano (5,00 mL), trifenilfosfina (0,0941 g, 0,359 mmol) y acetato de paladio (0,0201 g, 0,0896 mmol) se agitó a temperatura ambiente por 15 min bajo una atmósfera de argón. Se añadieron tercbutil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,796 g, 1,97 mmol), 3-bromo-quinolin-4-ilamina (0,4 g, 2 mmol), DMF (5,00 mL) y 1M carbonato de sodio acuoso (7 mL) y se enjuagó con argón cinco veces. La mezcla de reacción se calentó a 80 °C por 7 h y se concentró. El residuo crudo se suspendió en una mezcla de 1M Na2CO3 acuoso y EtOAc y luego se filtró a través de una almohadilla de Celite/gel de sílice, se lavó con EtOAc. El filtrado se separó y la capa acuosa se extrajo dos veces con EtOAc. Los compuestos orgánicos combinados se lavaron con salmuera, se secaron (Na2SO4), se filtraron, y se evaporaron para dar un producto que se usó para la siguiente reacción sin purificación adicional. Análisis: LCMS m/z = 420 (M 1).
Etapa 2. terc-butil éster del ácido 4-{4-[4-(2,2,2-Trifluoroacetilamino)-quinolin-3-il]-fenoxi}-piperidina-1-carboxílico.
A una solución agitada enfriada con hielo (0 °C) de terc-butil éster del ácido 4-[4-(4-amino-quinolin-3-il)-fenoxi]-piperidina-1-carboxílico (1,2 g, 2,9 mmol) y trietilamina (1,2 mL, 8,6 mmol) en DCM (10 mL) se añadió anhídrido trifluoroacético (0,52 mL, 3,7 mmol). La mezcla de reacción se agitó a temperatura ambiente por 1,5 h y luego se evaporó. El residuo se particionó entre el NaHCO3 saturado acuoso y EtOAc y la capa acuosa se extrajo dos veces con EtOAc. Los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para producir un producto crudo. El producto se cristalizó a partir de una mezcla de DCM, MeOH, éter y hexano para producir terc-butil éster del ácido 4-{4-[4-(2,2,2-trifluoroacetilamino)-quinolin-3-il]-fenoxi}-piperidina-1-carboxílico, (0,7 g, 76%). Análisis: LCMS m/z = 516 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,95 (s, 1 H) 8,15 - 8,23 (m, 1 H) 7,93 - 8,07 (m, 1 H) 7,75 - 7,83 (m, 2 H) 7,63 - 7,71 (m, 1 H) 7,33 (d, J=8,78 Hz, 2 H) 7,04 (d, J=8,78 Hz, 2 H) 4,51 - 4,59 (m, 1 H) 3,66 - 3,77 (m, 2 H) 3,31 - 3,42 (m, 2 H) 1,89 - 2,02 (m, 2 H) 1,73 - 1,85 (m, 2 H) 1,57 (br. s., 2 H) 1,47 (s, 9 H).
Etapa 3,1-{4-[4-(4-Aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
A una solución de terc-butil éster del ácido 4-{4-[4-(2,2,2-Trifluoroacetilamino)-quinolin-3-il]-fenoxi}-piperidina-1-carboxílico (0,34 g, 0,66 mmol) en DCM (5 mL) se añadió ácido trifluoroacético (1,5 mL, 19 mmol) en forma de gotas a temperatura ambiente. Después del completamiento, la reacción se evaporó y se concentró dos veces con EtOAc. A una solución del producto anterior y DIPEA (0,80 mL, 4,6 mmol) en d Cm (5 mL, 80 mmol) se añadió cloruro de propanoilo (0,07 mL, 0,8 mmol) a temperatura ambiente. Después de 2 h la reacción se concentró y se usó en la siguiente etapa sin purificación adicional.
Etapa 4. 1-{4-[4-(4-Aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona
Una solución del material anterior y K2 CO3 (1,5 g, 11 mmol) en metanol (8 mL) y agua (2 mL) se calentó a 65 °C por 2 días. Después del completamiento, la mezcla de reacción se concentró y se particionó entre EtOAc y agua. La capa acuosa se extrajo dos veces EtOAc y los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para dar un producto crudo. El producto se purificó por Gilson y luego se liofilizó para producir 1-{4-[4-(4-aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, 0,268 g (83%). Análisis: LCMS m/z = 376 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 13,99 (br. s., 1 H) 9,00 (br. s., 1 H) 8,62 (d, J=8,28 Hz, 1 H) 8,46 (br. s., 1 H) 7,83 - 8,03 (m, 3 H) 7,71 (ddd, J=8,34, 6,84, 1,38 Hz, 1 H) 7,40-7,49 (m, 2H) 7,19 (d, J=8,78 Hz, 2H) 4,72 (dt, J=7,72, 4,05 Hz, 1H) 3,85-3,96 (m, 1H) 3,73 (d, J=14,31 Hz, 1H) 3,22-3,43 (m, 2H) 2,36 (q, J=7,53 Hz, 2H) 1,89-2,08 (m, 2H) 1,47-1,72 (m, 2H) 1,01 (t, J=7,40 Hz, 3H).
Ejemplo 232. 1-{4-[4-(4-Dimetilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. 3-Bromoquinolin-4-il)-dimetilamina.
Un recipiente de reacción a presión de 50 mL cargado con 3-bromo-4-cloroquinolina (0,545 g, 2,25 mmol), dimetilamina (9 mL, 200 mmol, 2M solución en THF), K2 CO3 (1,5 g, 11 mmol), y acetonitrilo (5 mL, 100 mmol) se calentó a 135 °C y se monitoreó por HPLC y LCMS. Después de 24 h, la mezcla de reacción se concentró y luego se particionó entre EtOAc y NaHCO3 saturado acuoso. La capa acuosa se extrajo dos veces EtOAc y los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para dar un producto crudo. El producto se purificó por Gilson y luego se liofilizó para producir (3-bromoquinolin-4-il)-dimetilamina, 0,4 g (70%). Análisis: LCMS m/z = 251 (M+1); 1H NMR (400 MHz, CDCla) 6: 8,80 (s, 1 H) 8,12 (dd, J=8,53, 0,75 Hz, 1 H) 8,00 - 8,06 (m, 1 H) 7,63 - 7,71 (m, 1 H) 7,49 - 7,57 (m, 1 H) 3,14 (s, 7 H).
Etapa 2. 1-{4-[4-(4-Dimetilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Este ejemplo se sintetizó usando 3-bromoquinolin-4-il)-dimetilamina usando los métodos descritos para el ejemplo 231. Análisis: LCMS m/z = 404 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,66 (s, 1 H) 8,42 (d, J=8,28 Hz, 1 H) 7,95 -8,07 (m, 2 H) 7,76 (dd, J=8,53, 1,51 Hz, 1 H) 7,33 - 7,41 (m, 2 H) 7,12 - 7,19 (m, 2 H) 4,72 (dt, J=7,84, 3,98 Hz, 1 H) 3,85 - 3,96 (m, 3 H) 3,71 (br. s., 2 H) 3,20 - 3,41 (m, 2 H) 3,04 (s, 6 H) 2,35 (q, J=7,53 Hz, 2 H) 1,89 - 2,07 (m, 2 H) 1,55 (br. s., 2 H) 1,00 (t, J=7,40 Hz, 3 H).
Los siguientes ejemplos se prepararon usando los métodos descritos para los ejemplos 231 y 232.
Ejemplo 233. {4-[4-(4-Dimetilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 446 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,66 (s, 1 H) 8,42 (d, J=8,53 Hz, 1 H) 7,94 - 8,07 (m, 2 H) 7,76 (ddd, J=8,66, 6,90, 1,51 Hz, 1 H) 7,37 (d, J=8,78 Hz, 2 H) 7,16 (d, J=8,53 Hz, 2 H) 4,65 - 4,78 (m, 3 H) 3,70 - 3,98 (m, 4 H) 3,19 - 3,52 (m, 2 H) 3,04 (s, 6 H) 1,75 - 2,13 (m, 6 H) 1,46 - 1,72 (m, 2 H).
Ejemplo 234. {4-[4-(4-Aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Análisis: LCMS m/z = 418 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 13,98 (br. s., 1 H) 8,92 - 9,08 (m, 1 H) 8,62 (d, J=8,53 Hz, 1 H) 8,46 (br. s., 1 H) 7,94 (td, J=8,28, 7,03 Hz, 3 H) 7,71 (ddd, J=8,34, 6,84, 1,38 Hz, 1 H) 7,45 (d, J=8,53 Hz, 2 H) 7,19 (d, J=8,53 Hz, 2 H) 4,71 (d, J=7,78 Hz, 2 H) 3,69 - 3,98 (m, 6 H) 3,21 - 3,53 (m, 3 H) 1,90 - 2,13 (m, 4 H) 1,77 - 1,90 (m, 2 H) 1,47 - 1,74 (m, 2 H).
Ejemplo 235. 1-{4-[4-(4-Metilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Un frasco seco de 50 mL R. B. bajo una atmósfera de argón se cargó con 1 -{4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona (0,15 g, 0,38 mmol), metilamina (0,253 mL, 5,70 mmol), acetato de paladio (9,9 mg, 0,044 mmol), bis(2-difenil-fosfinofenil)éter (0,047 g, 0,088 mmol), tert-butóxido de sodio (0,0730 g, 0,760 mmol), y 1,4-dioxano (2 mL). La mezcla de reacción se purgó con argón y se agitó a 85 °C durante toda la noche. La mezcla de reacción se enfrió hasta la temperatura ambiente y el disolvente se evaporó al vacío. El residuo se disolvió en EtOAc y se lavó con salmuera, se secó, se filtró, y se concentró. El producto crudo se purificó por Gilson y luego se liofilizó para producir
1-{4-[4-(4-Metilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.TFA, 130 mg (68%). Análisis: LCMS m/z = 390 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 13,98 (br. s., 1 H) 8,80 (br. s., 1 H) 8,52 (d, J=8,53 Hz, 1 H) 8,45 (s, 1 H) 7,89 - 8,00 (m, 2 H) 7,74 (ddd, J=8,41, 6,53, 1,63 Hz, 1 H) 7,37 - 7,45 (m, 2 H) 7,11 (d, J=8,78 Hz, 2 H) 4,71 (dt, J=7,84, 3,98 Hz, 1 H) 3,85 - 3,96 (m, 2 H) 3,66 - 3,78 (m, 1 H) 3,30 - 3,41 (m, 1 H) 3,20 - 3,30 (m, 1 H) 2,65 (br. s., 3 H) 2,35 (q, J=7,28 Hz, 2 H) 1,99 (br. s., 2 H) 1,46 - 1,70 (m, 2 H) 1,00 (t, J=7,40 Hz, 3 H).
Ejemplo 236. {4-[4-(4-Metilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
A un frasco seco de 50 mL R. B. bajo una atmósfera de argón se añadió {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona (0,16 g, 0,38 mmol), metilamina (0,253 mL, 5,70 mmol), acetato de paladio (9,9 mg, 0,044 mmol), bis(2-difenilfosfinofenil)éter (0,047 g, 0,088 mmol), t-butóxido de sodio (0,0730 g, 0,760 mmol) y 1,4-dioxano (2 mL). La mezcla de reacción se purgó con argón y se agitó a 85°C durante toda la noche, se enfrió hasta la temperatura ambiente y se concentró. El producto crudo se disolvió en EtOAc, se lavó con salmuera y se secó para obtener un producto crudo. El producto se purificó por Gilson y luego se liofilizó para producir {4-[4-(4-metilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.TFA, 47 mg (24%). Análisis: LCMS m/z = 432 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 13,92 (br. s., 1 H) 8,79 (br. s., 1 H) 8,52 (d, J=8,53 Hz, 1 H) 8,45 (br. s., 1 H) 7,88 - 8,00 (m, 2 H) 7,71 - 7,78 (m, 1 H) 7,41 (d, J=8,53 Hz, 2 H) 7,11 (d, J=8,78 Hz, 2 H) 4,65 - 4,77 (m, 2 H) 3,70 -3,81 (m, 6 H) 3,19 - 3,51 (m, 4 H) 2,58 - 2,73 (m, 3 H) 1,90 - 2,12 (m, 5 H) 1,77 - 1,89 (m, 2 H) 1,46 - 1,72 (m, 2 H).
Los siguientes compuestos se sintetizaron usando el procedimiento descrito en Ejemplos 235 y 236.
Ejemplo 237. 1-{4-[4-(4-Morfolin-4-il-quinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 446 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,77 (s, 1 H) 8,30 (d, J=8,03 Hz, 1 H) 8,05 - 8,13 (m, 1 H) 7,99 (t, J=7,28 Hz, 1 H) 7,80 (t, J=7,78 Hz, 1 H) 7,39 (d, J=8,53 Hz, 2 H) 7,18 (d, J=8,78 Hz, 2 H) 4,68 - 4,78 (m, 1 H) 3,86 - 3,98 (m, 2 H) 3,67 - 3,79 (m, 6 H) 3,14 - 3,41 (m, 7 H) 2,36 (q, J=7,36 Hz, 2 H) 1,90 - 2,08 (m, 2 H) 1,47 - 1,71 (m, 2 H) 1,00 (t, J=7,40 Hz, 3 H).
Ejemplo 238. {4-[4-(4-Morfolin-4-il-quinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 488 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,76 (s, 1 H) 8,30 (d, J=8,28 Hz, 1 H) 8,09 (d, J=7,78 Hz, 1 H) 7,99 (t, J=7,65 Hz, 1 H) 7,77 - 7,83 (m, 1 H) 7,40 (d, J=8,53 Hz, 2 H) 7,18 (d, J=8,53 Hz, 2 H) 4,66 -4,80 (m, 2 H) 3,70 - 3,97 (m, 12 H) 3,17 - 3,24 (m, 6 H) 1,91 - 2,12 (m, 5 H) 1,77 - 1,91 (m, 2H) 1,47-1,72 (m, 2H).
E je m p lo 239. 1 -(4 - {4 -[4 -(4 -M e t ilp ip e ra z in -1 - i l) -q u in o lin -3 - i l ] - fe n o x i} -p ip e r id in -1 - i l ) -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 459 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 10,03 (br. s., 1 H) 8,77 (s, 1 H) 8,23 (d, J=8,28 Hz, 1 H) 8,11 (d, J=8,03 Hz, 1 H) 7,93 (t, J=7,28 Hz, 1 H) 7,74 - 7,83 (m, 1 H) 7,36 (d, J=8,53 Hz, 2 H) 7,16 (d, J=8,53 Hz, 2 H) 4,63 - 4,77 (m, 1 H) 3,84 (br. s., 28 H) 3,20 - 3,49 (m, 10 H) 2,95 - 3,12 (m, 2 H) 2,85 (s, 3 H) 2,36 (q, J=7,28 Hz, 2 H) 1,90 - 2,08 (m, 2 H) 1,48 - 1,72 (m, 2 H) 1,01 (t, J=7,40 Hz, 3 H).
Ejemplo 240. (4-{4-[4-(4-Metilpiperazin-1-il)-quinolin-3-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 501 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,59 (br. s., 1 H) 8,73 (s, 1 H) 8,21 (d, J=8,28 Hz, 1 H) 8,09 (d, J=8,53 Hz, 1 H) 7,88 (t, J=7,53 Hz, 1 H) 7,75 (t, J=7,28 Hz, 1 H) 7,36 (d, J=8,78 Hz, 2 H) 7,17 (d, J=8,53 Hz, 2 H) 4,64 - 4,78 (m, 2 H) 3,69 - 3,91 (m, 22 H) 3,26 - 3,51 (m, 11 H) 2,90 - 3,04 (m, 3 H) 2,84 (br. s., 3 H) 1,91 -2,13 (m, 5 H) 1,85 (s, 3 H) 1,48 - 1,73 (m, 3 H).
Ejemplo 241. 3-[4-(4-Quinolin-3-il-fenoxi)-piperidina-1-carbonil]-oxazolidin-2-ona.
A una solución agitada de oxazolidin-2-ona (0,2 g, 2 mmol) en tolueno (5 mL) se añadió hidruro de sodio (0,11 g, 4,6 mmol) bajo argón y luego se calentó a 60 °C por 15 h. Trifosgeno (0,34 g, 1,1 mmol) se añadió a la mezcla de reacción a - 20 °C y se calentó lentamente hasta la temperatura ambiente. Se añadieron trietilamina (1 mL, 7 mmol) y 3-[4-(piperidin-4-iloxi)-fenil]-quinolina (0,15 g, 0,49 mmol) a 0 °C, luego se calentó hasta la temperatura ambiente y la reacción se monitoreó por HPLC y LCMS. Después de 2 h, la mezcla de reacción se apagó con NaHCO3 saturado acuoso, se extrajo dos veces con EtOAc y los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para dar un producto crudo. El producto se purificó por Gilson y luego se liofilizó para producir 3-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-oxazolidin-2-ona.TFA, 0,103 g (39%). Análisis: LCMS m/z = 418 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,34 (d, J=2,26 Hz, 1 H) 8,75 - 8,85 (m, 1 H) 8,10 (t, J=8,91 Hz, 2 H) 7,79 - 7,92 (m, 3 H) 7,66 - 7,76 (m, 1 H) 7,20 (d, J=8,78 Hz, 2 H) 4,73 - 4,83 (m, 1 H) 4,39 (t, J=7,65 Hz, 2 H) 3,85 (t, J=7,78 Hz, 2 H) 3,66 - 3,78 (m, 2 H) 3,32 - 3,45 (m, 2 H) 1,97 - 2,09 (m, 2 H) 1,63 - 1,78 (m, 2 H).
Ejemplo 242. 1 -[4-(4-Quinolin-3-il-fenoxi)-piperidin-1 -il]-butano-1,3-diona.
Un frasco de 50 mL R. B. se cargó con 3-[4-(piperidin-4-iloxi)-fenil]-quinolina (0,175 g, 0,575 mmol), acetonitrilo (3 mL), 3-ácido oxobutanoico etil éster (0,523 mL, 4,11 mmol), y carbonato de potasio (0,284 g, 2,05 mmol) y luego se calentó a 97 °C bajo una atmósfera de argón por 8 h. La mezcla de reacción se evaporó al vacío, y se particionó entre agua y EtOAc. La capa acuosa se acidificó con ácido cítrico hasta f 5 luego se extrajo dos veces con EtOAc y los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para dar un producto crudo. El producto se purificó por Gilson y luego se liofilizó para producir 1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-butano-1,3-diona, TFA, 0,180 g (62%). Análisis: LCMS m/z = 389 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,37 (d, J=2,26 Hz, 1 H) 8,80 - 8,89 (m, 1 H) 8,12 (dd, J=11,80, 8,28 Hz, 2 H) 7,82 - 7,93 (m, 3 H) 7,70 - 7,78 (m, 1 H) 7,15 - 7,25 (m, 2 H) 4,70 - 4,82 (m, 1 H) 3,81 - 3,94 (m, 1 H) 3,69 (s, 2 H) 3,55 - 3,65 (m, 1 H) 3,25 - 3,38 (m, 2 H) 2,17 (s, 3 H) 1,88 - 2,05 (m, 3 H) 1,50 - 1,72 (m, 2 H).
Ejemplo 243. 1-[4-(4-Quinolin-3-il-fenoxi)-piperidina-1-carbonil]-pirrolidin-2-ona.
A una solución agitada fría (0 °C) de 2-pirrolidinona (0,2 g, 2 mmol) y trietilamina (2 mL, 20 mmol) en 1,2-dicloroetano (5 mL) se añadió trifosgeno (0,3 g, 1 mmol) y se agitó a temperatura ambiente por 1,5 h. Se añadieron 3-[4-(piperidin-4-iloxi)-fenil]-quinolina (0,12 g, 0,39 mmol) y K2 CO3 a la mezcla de reacción a 0 °C y luego se agitó a temperatura ambiente por 4 h. La mezcla de reacción se evaporó y se particionó entre NaHCO3 saturado acuoso y EtOAc. La capa acuosa se extrajo dos veces con EtOAc y los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para dar un producto crudo. El producto se purificó por Gilson y luego se liofilizó para producir 1-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-pirrolidin-2-ona.TFA, 0,125 g (61%). Análisis: LCMS m/z = 416 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,34 (d, J=2,26 Hz, 1 H) 8,80 (s, 1 H) 8,10 (t, J=8,91 Hz, 2 H) 7,80 - 7,93 (m, 3 H) 7,68 - 7,76 (m, 1 H) 7,20 (d, J=8,78 Hz, 2 H) 4,71 - 4,82 (m, 1 H) 3,61 (t, J=7,03 Hz, 4 H) 3,54 - 3,80 (m, 4 H) 3,26 - 3,42 (m, 2 H) 2,40 (t, J=7,91 Hz, 2 H) 1,92 - 2,09 (m, 4 H) 1,60 - 1,78 (m, 2 H).
Ejemplo 244. 4'-[1-(®-Tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-bifenil-4-carbonitrilo
Etapa 1. terc-butil éster del ácido 4-(4'-Cianobifenil-4-iloxi)-piperidina-1-carboxílico.
Un frasco de 50 mL R. B. cargado con 1,4-dioxano (4,00 mL), trifenilfosfina (0,0607 g, 0,231 mmol), y acetato de paladio (0,0130 g, 0,0578 mmol) se agitó a temperatura ambiente por 15 min bajo una atmósfera de argón. Se añadieron t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,6 g, 1 mmol), 4-bromobenzonitrilo (0,210 g, 1,16 mmol), DMF(4,00 mL), y 1M Na2CO3 (4 mL) acuoso y se enjuagó con argón cinco veces. La mezcla de reacción se calentó a 80 °C por 7 h y se concentró. El residuo se suspendió en una mezcla de 1M Na2CO3 acuoso y EtOAc y luego se filtró a través de una almohadilla de Celite/gel de sílice. El filtrado se separó en dos capas y la capa acuosa se extrajo dos veces con EtOAc. Los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se evaporaron para dar un producto crudo que se purificó por columna de gel de sílice cromatografía (columna de 80 g ISCO, usando 0 a 40% EtOAc en hexano) para dar 0,5 g (90%). Análisis: LCMS m/z = 379 (M+1); 1H NMR (400 MHz, CLOROFORM-d) ó: 7,60-7,74 (m, 4H), 7,53 (d, J = 8,8 Hz, 2H), 6,98-7,04 (m, 2H), 4,50-4,58 (m, 1H), 3,65-3,77 (m, 2H), 3,32-3,42 (m, 2H), 1,89-2,01 (m, 2H), 1,73-1,84 (m, 2H), 1,44 1,51 (m, 11H).
Etapa 2. 4'-(Piperidin-4-iloxi)-bifenil-4-carbonitrilo.
A terc-butil éster del ácido una solución de 4-(4'-cian-bifenil-4-iloxi)-piperidina-1 -carboxílico (0,5 g, 1 mmol) en DCM (7 mL) se añadió TFA (0,51 mL, 6,6 mmol) a temperatura ambiente. La mezcla de reacción se agitó 3 h y luego se concentró. Este material se usó directamente en la siguiente etapa. Análisis: LCMS m/z = 279 (M+1).
Etapa 3. 4'-[1-((R)-Tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-bifenil-4-carbonitrilo.
A una solución agitada fría (5 °C) de ácido (R)-tetrahidrofuran-2-carboxílico (0,250 g, 2,16 mmol) y trietilamina (2,00
mL, 14,4 mmol) en DCM (5 mL) se añadió HATU (0,765 g, 2,01 mmol). Después de 15 min 4'-(piperidin-4-iloxi)-bifenil-4-carbonitrilo (0,4 g, 1 mmol) se añadió y se agitó adicionalmente a temperatura ambiente por 2 h. La mezcla de reacción se concentró y luego se particionó entre EtOAc y NaHCO3 saturado acuoso. La capa acuosa se extrajo dos veces con EtOAc y los compuestos orgánicos combinados se lavaron con salmuera, se secaron, se filtraron, y se concentraron. El producto se purificó por Gilson y luego se liofilizó para producir 4'-[1-((R)-tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-bifenil-4-carbonitrilo, 0,313 g (en total 58%). Análisis: Lc MS m/z = 377 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 7,81 - 7,91 (m, 2 H) 7,71 (d, J=8,78 Hz, 1 H) 7,12 (d, J=8,53 Hz, 1 H) 4,65 - 4,77 (m, 1 H) 3,76 (d, J=6,78 Hz, 2 H) 3,18-3,51 (m, 2H) 1,74-2,11 (m, 3H) 1,44-1,70 (m, 1H).
Los siguientes compuestos se sintetizaron usando los procedimientos de Ejemplos 1-7.
Ejemplo 245. 1-[4-(4-Benzofuran-2-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 350 (M 1); 1H NMR (400 MHz, CDCla) 6 : 7,76 - 7,83 (m, 2 H), 7,47 - 7,58 (m, 2 H), 7,18 - 7,26 (m, 2 H), 6,96 - 7,02 (m, 2 H), 6,90 (s, 1 H), 4,61 (tt, J=6,59, 3,33 Hz, 1 H), 3,76 - 3,86 (m, 1 H), 3,61 - 3,75 (m, 2 H), 3,38 - 3,49 (m, 1 H), 2,38 (q, J=7,36 Hz, 2 H), 1,77 - 2,02 (m, 4 H), 1,17 (t, J=7,40 Hz, 3 H).
Ejemplo 246. 1-{4-[4-(1H-Indol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 349 (M 1); 1H NMR (400 MHz, CD3 OD): 6:7,81 (d, J=7,78 Hz, 1 H), 7,58 (d, J=8,28 Hz, 2 H), 7,34 - 7,43 (m, 2 H), 7,11 - 7,18 (m, 1 H), 7,02 - 7,09 (m, 3 H), 4,65 (tt, J=6,93, 3,48 Hz, 1 H), 3,75 - 3,92 (m, 2 H), 3,46 - 3,63 (m, 2 H), 2,42 - 2,51 (m, 2 H), 1,96 - 2,09 (m, 2 H), 1,73 - 1,89 (m, 2 H), 1,13 - 1,18 (m, 3 H).
Ejemplo 247. 1-[4-(4-Benzo[b]tiofen-5-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 366 (M 1); 1H NMR (400 MHz, CDCla) 6:7,97 (d, J=1,51 Hz, 1 H), 7,91 (d, J=8,53 Hz, 1 H), 7,51 - 7,62 (m, 3 H), 7,45 - 7,50 (m, 1 H), 7,37 (d, J=5,52 Hz, 1 H), 6,97 - 7,07 (m, 2 H), 4,60 (tt, J=6,65, 3,26 Hz, 1 H), 3,79 - 3,87 (m, 1 H), 3,63 - 3,77 (m, 2 H), 3,39 - 3,49 (m, 1 H), 2,34 - 2,45 (m, 2 H), 1,80 - 2,03 (m, 4 H), 1,17 (t, J=7,53 Hz, 3 H).
Ejemplo 248. 1-{4-[4-(1H-Indazol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 350 (M 1); 1H NMR (400 MHz, CDCI3 ) 6:10,07 (br. s., 1 H), 8,01 (d, J=8,28 Hz, 1 H), 7,91(d, J=8,78 Hz, 1 H), 7,39 - 7,57 (m, 2 H), 7,19 - 7,34 (m, 4 H), 7,06 (d, J=8,78 Hz, 2 H), 4,63 (tt, J=6,59, 3,45 Hz, 1 H), 3,58 - 3,94 (m, 3 H), 3,32 - 3,55 (m, 1 H), 2,39 (q, J=7,53 Hz, 2 H), 1,74 - 2,12 (m, 4H), 1,18 (t, J=7,53Hz, 3H).
Ejemplo 249. 1-{4-[4-(1-Metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona, sal de TFA.
Análisis: LCMS m/z = 364 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,01 (d, J=0,75 Hz, 1 H), 7,74 - 7,81 (m, 1 H), 7,61 (d, J=8,78 Hz, 2 H), 7,50 (s, 1 H), 7,38 (dd, J=8,53, 1,25 Hz, 1 H), 6,99 - 7,06 (m, 2 H), 4,60 - 4,69 (m, 1 H), 4,12(s, 3 H), 3,67 - 3,83 (m, 3H), 3,43-3,57 (m, 1H), 2,42-2,47 (m, 2H), 1,87-2,04 (m, 4H), 1,19 (t, J=7,53Hz, 3H).
Ejemplo 250. 1-[4-(4-Tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-propan-1-ona, sal de TFA.
Análisis: LCMS m/z = 367 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,85 (d, J=1,76 Hz, 1 H), 8,31 (d, J=2,01 Hz, 1 H), 7,63 (d, J=5,77 Hz, 1 H), 7,55 - 7,60 (m, 2 H), 7,36 (d, J=6,02 Hz, 1 H), 7,01 - 7,10 (m, 2 H), 4,63 - 4,69 (m, 1 H), 3,76(br. S., 3 H), 3,50 (br. S., 1 H), 2,43 (q, J=7,36 Hz, 2 H), 1,82 - 2,05 (m, 4 H), 1,19 (t, J=7,53 Hz, 3 H).
Ejemplo 251. 1-{4-[4-(2-Metil-2H-indazol-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 364 (M 1); 1H NMR (400 MHz, CDCb) 6: 7,97 (s, 1 H), 7,89 (d, J=1,25 Hz, 1 H), 7,74 (dd, J=8,78, 1,00 Hz, 1 H), 7,56 - 7,66 (m, 2 H), 7,45 (dd, J=8,78, 1,51 Hz, 1 H), 6,98 - 7,05 (m, 2 H), 4,60 - 4,71 (m, 1H), 4,33 (s, 3 H), 3,69 - 3,89 (m, 3 H), 3,46 - 3,59 (m, 1 H), 2,46 (q, J=7,53 Hz, 2 H), 1,86 - 1,98 (m, 4 H), 1,20 (t, J=7,53 Hz, 3 H).
Ejemplo 252. 1-[4-(4-[1,8]Naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona, sal de TFA.
Análisis: LCMS m/z = 362 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,57 (d, J=2,26 Hz, 1 H), 9,32 (dd, J=4,52, 1,51 Hz, 1 H), 8,48 - 8,59 (m, 2 H), 7,78 (dd, J=8,28, 4,52 Hz, 1H), 7,66-7,73 (m, 2H), 7,07-7,16 (m, 2H), 4,62 - 4,76 (m, 1H), 3,77 (br. s., 3H), 3,43-3,62 (m, 1H), 2,44 (q, J=7,53 Hz, 2H), 1,84-2,09 (m, 4H), 1,19 (t, J=7,53Hz, 3H).
E je m p lo 253. 1 - {4 -[4 -(2 -M e t i lq u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -p ro p a n -1 -o n a , s a l d e T F A .
Análisis: LCMS m/z = 375 (M 1); 1H NMR (400 MHz, CDCls) 6: 8,74 (d, J=1,00 Hz, 1 H), 8,57 (d, J=8,53 Hz, 1 H), 8,03 (d, J=1,00 Hz, 2 H), 7,73 - 7,81 (m, 2 H), 7,54 (d, J=8,53 Hz, 1 H), 7,06 - 7,14 (m, 2 H), 4,65 (tt, J=6,62, 3,42 Hz, 1 H), 3,67 - 3,90 (m, 3 H), 3,42 - 3,53 (m, 1 H), 3,07 (s, 3 H), 2,40 (d, J=7,53 Hz, 2 H), 1,84 - 2,07 (m, 4 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 254. (R)-Tetrahidrofuran-2-il-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona, sal de TFA.
Análisis: LCMS m/z = 409 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,85 (d, J=2,01 Hz, 1 H), 8,32 (d, J=2,01 Hz, 1 H), 7,63 (d, J=5,77 Hz, 1 H), 7,58 (d, J=8,53 Hz, 2 H), 7,37 (d, J=6,02 Hz, 1 H), 7,02-7,10 (m, 2 H), 4,61-4,72 (m, 2 H), 3,47-4,05 (m, 6 H), 1,80-2,16 (m, 8 H).
Ejemplo 255. Ciclopropil-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona, sal de TFA.
Análisis: LCMS m/z = 379 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,82 (d, J = 2,26 Hz, 1 H), 8,27 (d, J = 2,26 Hz, 1 H), 7,55 - 7,64 (m, 3 H), 7,34 (d, J = 5,77 Hz, 1 H), 7,04 - 7,11 (m, 2 H), 4,65 (tt, J = 6,56, 3,36 Hz, 1 H), 3,75 - 4,03 (m, 2 H), 3,70 (ddd, J = 13,49, 6,84, 4,02 Hz, 2 H), 1,84 - 2,09 (m, 4 H), 1,79 (tt, J = 8,00, 4,67 Hz, 1 H), 0,98 - 1,05 (m, 2 H), 0,79 (dd, J = 8,03, 3,01 Hz, 2 H).
Ejemplo 256. 1-[4-(4-Imidazo[1,2-a]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona, sal de TFA.
Análisis: LCMS m/z = 350 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,34 - 8,45 (m, 2 H), 7,89 - 8,01 (m, 2 H), 7,75 (d, J=1,76 Hz, 1 H), 7,51 (d, J=8,78 Hz, 2 H), 7,07 (d, J=8,78 Hz, 2 H), 4,65 (tt, J=6,46, 3,33 Hz, 1 H), 3,74 (br. s., 4 H), 3,48 - 3,57 (m, 1 H), 2,38 - 2,49 (m, 2 H), 1,82 - 2,07 (m, 4 H), 1,18 (t, J=7,40 Hz, 3 H).
E je m p lo 257. {4 -[4 -(4 -C lo ro q u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -® - te t ra h id ro - fu ra n -2 - i l-m e ta n o n a , sa l d e T F A .
Análisis: LCMS m/z = 437 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,04 (d, J=5,52 Hz, 1 H), 8,56 (s, 1 H), 8,40 (d, J=9,03 Hz, 1 H), 8,06 - 8,16 (m, 1H), 7,72-7,82 (m, 3H), 7,09 (d, J=8,78 Hz, 2H), 4,63-4,73 (m, 2H), 3,51-4,02 (m, 6H), 1,91 2,13 (m, 8H).
Ejemplo 258. {4-[4-(4-Cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona, sal de TFA.
Análisis: LCMS m/z = 407 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,05 (d, J=5,52 Hz, 1 H), 8,57 (d, J=1,51 Hz, 1 H), 8,40 (d, J=8,78 Hz, 1 H), 8,10 (dd, J=9,03, 1,76 Hz, 1 H), 7,72 - 7,81 (m, 3 H), 7,06 - 7,15 (m, 2 H), 4,62 - 4,75 (m, 1 H), 3,76 - 4,02 (m, 2 H), 3,67 - 3,76 (m, 2 H), 1,87 - 2,13 (m, 4 H), 1,75 - 1,85 (m, 1 H), 1,02 (dd, J=4,52, 2,76 Hz, 2 H), 0,80 (dd, J=8,03, 3,01 Hz, 2 H).
Ejemplo 259. 1-{4-[4-(4-Cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, sal de TFA.
Análisis: LCMS m/z = 395 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,03 (d, J=5,52 Hz, 1 H), 8,55 (d, J=1,51 Hz, 1 H), 8,39 (d, J=8,78 Hz, 1 H), 8,08 (dd, J=8,78, 1,76 Hz, 1 H), 7,67 - 7,80 (m, 3 H), 7,09 (d, J=8,78 Hz, 2 H), 4,61 - 4,73 (m, 1 H), 3,54 - 3,92 (m, 4 H), 2,41 (d, J=7,53 Hz, 2 H), 1,83 - 2,06 (m, 4 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 260. {4-[4-(8-Cloro-quinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, sal de TFA.
A n á lis is : L C M S m /z = 437 (M 1); 1H N M R (400 M H z , C D C b ) 6: 9 ,33 (d, J = 4 ,52 H z, 1 H ), 8 ,51 - 8 ,58 (m , 1 H ), 7 ,93 (d, J = 8 ,53 H z, 1 H ), 7 ,70 - 7 ,79 (m , 2 H ), 7 ,52 (d, J = 8 ,53 H z, 2 H ), 7 ,05 (d, J = 8 ,78 H z, 2 H ), 4 ,65 - 4 ,73 (m , 2 H ), 3 ,53 - 4 ,03 (m , 6 H ), 1 ,89 - 2 ,31 (m , 8 H).
E je m p lo 261. 1 - {4 -[4 -(8 -C lo ro q u in o lin -7 - i l) - fe n o x i]-p ip e r id in -1 - i l } -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 395 (M 1); 1H NMR (400 MHz, CDCla) 6: 9,10 (dd, J=4,14, 1,63 Hz, 1 H), 8,22 (dd, J=8,28, 1,51 Hz, 1 H), 7,79 (d, J=8,53 Hz, 1 H), 7,47 - 7,59 (m, 4 H), 7,00 - 7,08 (m, 2 H), 4,59 - 4,69 (m, 1 H), 3,80 -3,91(m, 1 H), 3,64 - 3,78 (m, 2H), 3,40-3,51 (m, 1H), 2,33-2,45 (m, 2H), 1,82-2,06 (m, 4H), 1,18 (t, J=7,53Hz, 3H).
Ejemplo 262. {4-[4-(7-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Etapa 1. t-butil éster del ácido 4-[4-(7-Metoxiquinolin-3-il)-fenoxi]-piperidina-1-carboxílico
Este compuesto se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-7-metoxiquinolina (443 mg, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,46 g, 85%). Análisis: LCMS m/z = 435 (M+1).
Etapa 2. 7-Metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina
Este compuesto se preparó a partir de terc-butil éster del ácido 4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidina-1-carboxílico (0,46 g, 1,05 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,24 g, 68%). Análisis: LCMS m/z = 335 (M+1).
Etapa 3. {4-[4-(7-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona
Este compuesto se preparó a partir de 7-metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (90 mg, 0,3 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (52 uL, 0,54 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,02 g, 20%). Análisis: LCMS m/z = 433 (M+1). 1H NMR (DMSO-d6) 6: 9,14 (d, 1H, J = 2,4 Hz), 8,49 (d, 1H, J = 2,3 Hz), 7,94 (d, 1H, J = 9,0 Hz), 7,79 (m, 2H), 7,41 (d, 1H, J = 2,4 Hz), 7,29 (m, 1H), 7,15 (m, 2H), 4,72 (m, 2H), 3,93 (s, 3H), 3,77 (br m, 4H), 3,36 (m, 1H), 3,29 (m, 1H), 2,06 (br m, 4H), 1,84 (m, 2H), 1,60 (m, 2H).
Ejemplo 263. (R)-Tetrahidrofuran-2-il-[4-(4-tieno[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-metanona, sal de TFA.
Análisis: LCMS m/z = 409 (M 1); 1H NMR (400 MHz, CDCla) 6; 9,10 (d, J=1,76 Hz, 1 H), 8,71 (d, J=1,25 Hz, 1 H), 8,05 (d, J=5,77 Hz, 1 H), 7,94 (d, J=5,52 Hz, 1 H), 7,62 (d, J=8,53 Hz, 2 H), 7,06 - 7,14 (m, 2 H), 4,66 (dd, J=7,40, 5,65 Hz, 2 H), 3,64 - 4,01 (m, 6 H), 2,24 - 2,38 (m, 1 H), 1,86 - 2,16 (m, 7 H).
E je m p lo 264. 1 -[4 -(4 -T ie n o [3 ,2 -b ]p ir id in -6 - i l- fe n o x i) -p ip e r id in -1 - i l ] -p ro p a n -1 -o n a , s a l d e T F A .
Análisis: LCMS m/z = 367 (M 1); 1H NMR (400 MHz, CDCls) 6: 9,11 (d, J=1,76 Hz, 1 H), 8,73 (s, 1 H), 8,06 (s, 1 H), 7,92 - 8,00 (m, 1 H), 7,62 (d, J=8,78 Hz, 2 H), 7,08 (d, J=8,78 Hz, 2 H), 4,59 - 4,73 (m, 1 H), 3,75 - 3,84 (m, 2 H), 3,49 - 3,59 (m, 2 H), 2,38 - 2,50 (m, 2 H), 1,86 - 2,06 (m, 4 H), 1,19 (t, J=7,40 Hz, 3 H).
Ejemplo 265. {4-[4-(3-Cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, sal de TFA.
Análisis: LCMS m/z = 437 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,93 (d, J=2,26 Hz, 1 H), 8,34 (d, J=0,75 Hz, 1 H), 8,27 (d, J=1,76 Hz, 1 H), 7,83 - 7,93 (m, 2 H), 7,70 (d, J=8,78 Hz, 2 H), 7,06 (d, J=8,78 Hz, 2 H), 4,66 (dd, J=7,40, 5,65 Hz, 2 H), 3,46 - 4,01 (m, 6 H), 2,28 - 2,34 (m, 1 H), 1,87 - 2,15 (m, 7 H).
Ejemplo 266. 1-{4-[4-(3-Cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, sal de TFA.
Análisis: LCMS m/z = 395 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,94 (d, J=2,26 Hz, 1 H), 8,35 (s, 1 H), 8,29 (d, J=2,26 Hz, 1 H), 7,82 - 7,94 (m, 2 H), 7,70 (d, J=8,78 Hz, 2 H), 7,06 (d, J=8,78 Hz, 2 H), 4,61 - 4,72 (m, 1 H), 3,64 - 3,88 (m, 3 H), 3,41 - 3,56 (m, 1 H), 2,39 - 2,48 (m, 2 H), 1,85 - 2,03 (m, 4 H), 1,18 - 1,23 (m, 3 H).
Ejemplo 267. [4-(4-Benzotiazol-5-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona, sal de TFA.
Análisis: LCMS m/z = 409 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,15 (s, 1 H), 8,33 (d, J=1,25 Hz, 1 H), 8,01 (d, J=8,28 Hz, 1 H), 7,67 - 7,74 (m, 1H), 7,62 (d, J=8,53Hz, 2H), 7,04 (d, J=8,78 Hz, 2H), 4,62-4,73 (m, 2H), 3,62-4,06 (m, 6H), 1,87-2,31 (m, 8H).
Ejemplo 268. [4-(4-Benzotiazol-5-il-fenoxi)-piperidin-1-il]-ciclopropilmetanona, sal de TFA.
Análisis: LCMS m/z = 379 (M 1); 1H NMR (400 MHz, CDCI3 ) 6: 9,19 (s, 1 H), 8,32 - 8,37 (m, 1 H), 7,97 - 8,07 (m, 1 H), 7,68 - 7,75 (m, 1 H), 7,63 (d, J=8,78 Hz, 2 H), 7,05 (d, J=8,78 Hz, 2 H), 4,61 - 4,71 (m, 1 H), 3,73 - 3,81 (m, 4 H), 1,88 - 2,10 (m, 4 H), 1,78 - 1,86 (m, 1 H), 1,02 - 1,08 (m, 2 H), 0,79 - 0,88 (m, 2 H).
Ejemplo 269. 1-[4-(4-Benzotiazol-5-il-fenoxi)-piperidin-1-il]-propan-1-ona; sal de TFA
Análisis: LCMS m/z = 367 (M 1); 1H NMR (400 MHz, CDCla) 6: 9,15 - 9,21 (m, 1 H), 8,33 (d, J=1,25 Hz, 1 H), 8,01 (d, J=8,28 Hz, 1 H), 7,71 (dd, J=8,28, 1,51 Hz, 1 H), 7,59 - 7,66 (m, 2 H), 7,00 - 7,10 (m, 2 H), 4,65 (br. s., 1 H), 3,71 -3,88 (m, 3 H), 3,48 - 3,61 (m, 1 H), 2,46 (d, J=7,53 Hz, 2 H), 1,95 (br. s., 4 H), 1,20 (t, J=7,53 Hz, 3 H).
Ejemplo 270. Ciclopropil-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-metanona. sal de TFA.
Análisis: LCMS m/z = 376 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,05 (1 H, s), 7,79 (1 H, d, J=8,5 Hz), 7,57 - 7,64 (2 H, m), 7,51 (1 H, s), 7,37 - 7,43 (1 H, m), 7,04 (2 H, d, J=8,8 Hz), 4,63 - 4,71 (1 H, m), 3,78 (4 H, br. s.), 1,87 - 2,07 (4 H, m), 1,76 - 1,85 (1 H, m), 0,99 - 1,10 (2 H, m), 0,75 - 0,87 (2 H, m).
Ejemplo 271. Ciclobutil-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-metanona, sal de TFA.
Análisis: LCMS m/z = 390 (M 1); 1H NMR (400 MHz, CD3ÜD): 6: 8,37 (1 H, d, J=1,0 Hz), 8,17 (1 H, dd, J=8,5, 0,8 Hz), 8,02 - 8,11 (3 H, m), 7,81 (1 H, dd, J=8,5, 1,5 Hz), 7,39 - 7,52 (2 H, m), 5,08 (1 H, dt, J=7,0, 3,5 Hz), 4,24 (1 H, td, J=8,7, 4,0 Hz), 4,03 - 4,15 (1 H, m), 3,80 - 4,00 (3 H, m), 2,54 - 2,77 (4 H, m), 2,05 - 2,50 (6 H, m).
Ejemplo 272. {4-[4-(8-Metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, sal de TFA.
Análisis: LCMS m/z = 433 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,49 (dd, J=5,27, 1,51 Hz, 1 H), 8,66 - 8,78 (m, 1 H), 7,85 (s, 3 H), 7,72 (d, J=8,78 Hz, 2 H), 7,07 (d, J = 9,04 Hz, 2 H), 4,62 - 4,73 (m, 2 H), 3,54 - 4,03 (m, 9 H), 2,26 - 2,37 (m, 1 H), 1,89 - 2,00 (m, 7H).
E je m p lo 273. 1 - {4 -[4 -(8 -M e to x iq u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -p ro p a n -1 -o n a , sa l d e T F A .
Análisis: LCMS m/z = 433 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,42 - 9,52 (m, 1 H), 8,79 (dd, J=8,41, 1,13 Hz, 1 H), 7,85 - 7,93 (m, 3 H), 7,67 - 7,76 (m, 2 H), 7,04 - 7,12 (m, 2 H), 4,64 - 4,73 (m, 1 H), 3,73 - 3,86 (m, 3 H), 3,70 (s, 3 H), 3,45 - 3,59 (m, 1 H), 2,37 - 2,50 (m, 2 H), 1,82 - 2,08 (m, 4 H), 1,19 (t, J=7,53 Hz, 3 H).
Ejemplo 274. Ciclopropil-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
Análisis: LCMS m/z = 403 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,40 (d, J=4,52 Hz, 1 H), 8,84 (d, J=7,78 Hz, 1 H), 7,87 - 7,98 (m, 3 H), 7,72 - 7,80 (m, 2 H), 7,09 (d, J=8,78 Hz, 2 H), 4,62 - 4,76 (m, 1 H), 3,87 (s, 5 H), 3,66 - 3,76 (m, 2 H), 1,99 - 2,13 (m, 2 H), 1,91 (br. s., 2 H), 1,74 - 1,84 (m, 1 H), 0,96 - 1,04 (m, 2 H), 0,74 - 0,83 (m, 2 H).
Ejemplo 275. {4-[4-(6-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Análisis: LCMS m/z = 417 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,87 (dd, J=4,27, 1,76 Hz, 1 H), 8,09 (s, 1 H), 7,95 (s, 1 H), 7,68 (s, 1 H), 7,33 - 7,40 (m, 3 H), 7,01 (d, J=8,78 Hz, 2 H), 4,66 (dd, J=7,15, 5,65 Hz, 2 H), 3,49 - 4,01 (m, 6 H), 2,44 (s, 3 H), 2,28 - 2,37 (m, 1 H), 1,85 - 2,11 (m, 7 H).
Ejemplo 276. 1-{4-[4-(6-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 375 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,87 (dd, J=4,27, 1,76 Hz, 1 H), 8,07 - 8,14 (m, 1 H), 7,95 (s, 1 H), 7,68 (s, 1 H), 7,35 (d, J=8,78 Hz, 3 H), 7,00 (d, J=8,78 Hz, 2 H), 4,59 - 4,67 (m, 1 H), 3,81 - 3,90 (m, 1 H), 3,62 - 3,79 (m, 2 H), 3,41 - 3,51 (m, 1 H), 2,44 (s, 3 H), 2,36 - 2,43 (m, 2 H), 1,94 - 2,04 (m, 2 H), 1,83 - 1,93 (m, 2 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 277. 7-[4-(1-Propionil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo.
Análisis: LCMS m/z = 386 (M 1); 1H NMR (400 MHz, CDCI3 ) 6: 9,04 (d, J=2,26 Hz, 1 H), 8,53 (d, J=1,25 Hz, 1 H), 8,32 (d, J=1,00 Hz, 1 H), 7,93 (d, J=1,00 Hz, 2 H), 7,72 (d, J=8,78 Hz, 2 H), 7,07 (d, J=8,78 Hz, 2 H), 4,59 - 4,71 (m, 1 H), 3,79 - 3,88 (m, 1 H), 3,65 - 3,77 (m, 2 H), 3,39 - 3,51 (m, 1 H), 2,39 (d, J=7,53 Hz, 2 H), 1,96 - 2,03 (m, 2 H), 1,82 - 1,94 (m, 2 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 278. 7-{4-[1-((R)-Tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-fenil}-quinolina-3-carbonitrilo.
Análisis: LCMS m/z = 428 (M 1); 1H NMR (400 MHz, CDCla) 6: 9,04 (d, J=2,01 Hz, 1 H), 8,53 (dd, J=2,26, 0,75 Hz, 1 H), 8,32 (d, J=1,00 Hz, 1 H), 7,94 (d, J=1,26 Hz, 2 H), 7,72 (d, J=8,78 Hz, 2 H), 7,07 (d, J=8,78 Hz, 2 H), 4,65 (dd, J=7,28, 5,52 Hz, 2 H), 3,54 - 4,02 (m, 6 H), 2,29 - 2,40 (m, 1 H), 1,87 - 2,13 (m, 7 H).
Ejemplo 279. 7-[4-(1-Ciclopropanocarbonil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo.
Análisis: LCMS m/z = 398 (M 1); 1H NMR (400 MHz, CDCla) 6: 9,04 (d, J=2,01 Hz, 1 H), 8,53 (dd, J=2,26, 0,75 Hz, 1 H), 8,33 (d, J=0,75 Hz, 1 H), 7,94 (d, J=1,00 Hz, 2 H), 7,72 (d, J=8,78 Hz, 2 H), 7,08 (d, J=9,03 Hz, 2 H), 4,61 - 4,72 (m, 1 H), 3,77 - 4,05 (m, 2 H), 3,65 - 3,76 (m, 2 H), 2,01 (s, 4 H), 1,79 (s, 1 H), 0,97 - 1,05 (m, 2 H), 0,78 (dd, J=8,03, 3,01 Hz, 2 H).
Ejemplo 280. 1-{4-[4-(3-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 375 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,78 (d, J=2,01 Hz, 1 H), 8,23 (s, 1 H), 7,90 - 7,98 (m, 1 H), 7,73 - 7,83 (m, 2 H), 7,69 (d, J=8,78 Hz, 2 H), 7,04 (d, J=8,78 Hz, 2 H), 4,62 (tt, J=6,56, 3,36 Hz, 1 H), 3,83 (br. s., 1 H), 3,63 - 3,77 (m, 2 H), 3,45 (dd, J=6,90, 4,39 Hz, 1 H), 2,53 (s, 3 H), 2,39 (d, J=7,03 Hz, 2 H), 1,93 - 2,04 (m, 2 H), 1,81 - 1,92 (m, 2 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 281. {4-[4-(3-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
A n á lis is : L C M S m /z = 417 (M 1); 1H N M R (400 M H z , C D C b ) 6: 8 ,78 (d , J = 2 ,01 H z, 1 H ), 8 ,21 - 8 ,25 (m , 1 H ), 7 ,90 -7 ,96 (m , 1 H ), 7 ,73 - 7 ,83 (m , 2 H ), 7 ,67 - 7 ,71 (m , 2 H ), 7 ,04 (d , J = 9 ,04 H z, 2 H ), 4 ,72 - 4 ,79 (m , 1 H ), 3 ,37 - 3 ,68 (m , 4 H ), 3 ,13 (s, 2 H ), 3 ,07 (s, 5 H ), 2 ,53 (s, 3 H ), 2 ,15 - 2 ,27 (m , 2 H ), 2 ,03 (b r. s., 2 H ).
E je m p lo 282. C ic lo p ro p il- {4 -[4 -(3 -m e t i lq u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 387 (M 1); 1H NMR (400 MHz, CDCls) 6: 8,78 (d, J=2,26 Hz, 1 H), 8,24 (s, 1 H), 7,91 - 7,96 (m, 1 H), 7,74 - 7,83 (m, 2 H), 7,69 (d, J=8,78 Hz, 2 H), 7,05 (d, J=8,78 Hz, 2 H), 4,61-4,69 (m, 1 H), 3,79-4,01 (m, 2 H), 3,63-3,73 (m, 2 H), 2,53 (s, 3 H), 1,84-2,12 (m, 4 H), 1,79 (s, 1 H), 1,00 (dd, J=4,39, 2,89 Hz, 2 H), 0,77 (dd, J=7,91, 3,14 Hz, 2 H).
Ejemplo 283. {4-[4-(8-Metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 406 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,19 (d, J=0,75 Hz, 1 H), 7,76 (s, 1 H), 7,66 (d, J=1,51 Hz, 1 H), 7,49 (d, J=8,53 Hz, 2 H), 7,43 (br. s., 1 H), 6,99 - 7,07 (m, 2 H), 4,65 (dd, J=7,15, 5,65 Hz, 2 H), 3,50 - 4,01 (m, 6 H), 2,81 (s, 3 H), 2,27 - 2,39 (m, 1 H), 1,90 - 2,11 (m, 7 H).
Ejemplo 284. 1-{4-[4-(8-Metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 364 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,13 (dd, J=1,51, 0,75 Hz, 1 H), 7,62 (dd, J=10,79, 1,00 Hz, 2 H), 7,48 (d, J=8,78 Hz, 2 H), 7,17 - 7,24 (m, 1 H), 7,01 (d, J=8,78 Hz, 2 H), 4,55 - 4,65 (m, 1 H), 3,60 - 3,88 (m, 3 H), 3,39 - 3,51 (m, 1H), 2,67 (s, 3H), 2,39 (d, J=7,53 Hz, 2H), 1,75-2,04 (m, 4H), 1,16-1,22 (m, 3H).
Ejemplo 285. {4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
A n á lis is : L C M S m /z = 406 (M 1); 1H N M R (400 M H z , C D C la) 6: 7 ,73 (d, J = 1 ,25 H z, 1 H ), 7 ,52 - 7 ,61 (m , 2 H ), 7 ,28 (s, 2 H ), 7 ,18 (d , J = 9 ,03 H z, 1 H ), 7 ,00 (d , J = 8 ,78 H z, 2 H ), 4 ,55 - 4 ,71 (m , 2 H ), 3 ,49 - 4 ,00 (m , 6 H ), 2 ,55 (s, 3 H ), 2 ,26 - 2 ,40 (m , 1 H ), 2 ,01 (s, 7 H ).
E je m p lo 286. 1 - {4 -[4 -(5 -M e t il im id a z o [1 ,2 -a ]p ir id in -6 - i l) - fe n o x i] -p ip e r id in -1 - i l} -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 364 (M 1); 1H NMR (400 MHz, CDCls) 6: 7,73 (d, J=1,26 Hz, 1 H), 7,51 - 7,60 (m, 2 H), 7,28 (s, 2 H), 7,18 (d, J=9,29 Hz, 1 H), 7,00 (d, J=8,78 Hz, 2 H), 4,56 - 4,66 (m, 1 H), 3,64 - 3,90 (m, 3 H), 3,41 - 3,49 (m, 1 H), 2,55 (s, 3 H), 2,35 - 2,44 (m, 2 H), 1,82 - 2,05 (m, 4 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 287. Ciclopropil-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 376 (M 1); 1H NMR (400 MHz, CDCla) 6: 7,73 (d, J=1,00 Hz, 1 H), 7,58 (d, J=9,04 Hz, 1 H), 7,53 (s, 1 H), 7,26 - 7,29 (m, 3 H), 7,18 (d, J=9,03 Hz, 1 H), 6,98 - 7,05 (m, 2 H), 4,58 - 4,67 (m, 1 H), 3,79 - 4,03 (m, 2 H), 3,64-3,73 (m, 2 H), 2,55 (s, 3 H), 2,01 (s, 4 H), 1,75-1,83 (m, 1 H), 1,01 (dd, J=4,39, 2,89 Hz, 2 H), 0,78 (dd, J=7,91, 3,14 Hz, 2 H).
Ejemplo 288. Ciclopropil-{4-[4-(8-metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 376 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,13 (d, J=0,75 Hz, 1 H), 7,62 (dd, J=10,041,25 Hz, 2 H), 7,45 - 7,52 (m, 2 H), 7,20 (d, J=1,25 Hz, 1 H), 6,99 - 7,06 (m, 2 H), 4,58 - 4,67 (m, 1 H), 3,75-4,00 (m 2H), 3,61 3,74 (m, 2H), 2,67 (s, 3H), 2,01 (s, 4H), 1,78 (s, 1H), 0,97-1,06 (m, 2H), 0,78 (dd, J=8,03, 3,01Hz, 2H).
Ejemplo 289. {4-[4-(2,3-Dimetilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran 2-il-metanona.
Análisis: LCMS m/z = 420 (M 1); 1H NMR (400 MHz, CDCb) 6: 7,88 (s, 1 H), 7,55 (dd, J=9,29, 0,75 Hz, 1 H), 7,50 (d, J=8,53 Hz, 2 H), 7,33 (dd, J=9,29, 1,76 Hz, 1 H), 6,98 - 7,04 (m, 2 H), 4,55 - 4,69 (m, 2 H), 3,95 (s, 6 H), 2,44 (d, J=3,51 Hz, 6 H), 2,28 - 2,38 (m, 1 H), 1,86 - 2,11 (m, 7 H).
Ejemplo 290. 1-{4-[4-(2,3-Dimetilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 378 (M 1); 1H NMR (400 MHz, CDCI3 ) 6: 7,88 (s, 1 H), 7,55 (d, J=9,29 Hz, 1 H), 7,48 - 7,52 (m, 2 H), 7,33 (dd, J=9,29, 1,76 Hz, 1 H), 6,98 - 7,05 (m, 2 H), 4,55 - 4,66 (m, 1 H), 3,65 - 3,88 (m, 3 H), 3,42 - 3,50 (m, 1 H), 2,34 - 2,48 (m, 8 H), 1,96 (d, J=4,02 Hz, 4 H), 1,17 (t, J=7,40 Hz, 3 H).
Ejemplo 291. Ciclopropil-{4-[4-(2,3-dimetilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 390 (M 1); 1H NMR (400 MHz, CDCla) 6: 7,88 (s, 1 H), 7,48 - 7,58 (m, 3 H), 7,33 (dd, J=9,03, 1,76 Hz, 1 H), 7,03 (d, J=8,78 Hz, 2 H), 4,58 - 4,67 (m, 1 H), 3,77 - 4,02 (m, 2 H), 3,62 - 3,73 (m, 2 H), 2,44 (d, J=3,51 Hz, 6 H), 1,75 - 2,11 (m, 5 H), 0,97 - 1,05 (m, 2 H), 0,74 - 0,81 (m, 2 H).
Ejemplo 292. {4-[4-(7-Metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 406 (M 1); 1H NMR (400 MHz, CDCla) 6: 7,95 (s, 1 H), 7,59 (d, J=1,26 Hz, 1 H), 7,43 - 7,53 (m, 2 H), 7,24 (s, 2 H), 6,98 (d, J=8,78 Hz, 2 H), 4,57 - 4,70 (m, 2 H), 3,54 - 4,00 (m, 6 H), 2,30 - 2,38 (m, 1 H), 2,26 (s, 3H), 1,87-2,12 (m, 7H).
Ejemplo 293. 1-{4-[4-(7-Metilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 364 (M 1); 1H NMR (400 MHz, CDCls) 6: 7,94 (s, 1 H), 7,59 (d, J=1,25 Hz, 1 H), 7,46 - 7,52 (m, 2 H), 7,24 (s, 2 H), 6,98 (d, J=8,53 Hz, 2 H), 4,53 - 4,65 (m, 1 H), 3,63 - 3,89 (m, 3 H), 3,40 - 3,50 (m, 1 H), 2,38 (s, 2 H), 2,26 (d, J=0,75 Hz, 3 H), 1,79 - 2,04 (m, 4 H), 1,18 (t, J=7,40 Hz, 3 H).
Ejemplo 294. {4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
A ná lis is : LC M S m /z = 426 (M 1); 1H N M R (400 M Hz, C D C ls) 6: 7 ,86 (d, J = 0 ,75 Hz, 1 H), 7 ,74 (d, J = 1 ,25 Hz, 1 H), 7 ,64 (d, J = 9 ,03 Hz, 1 H), 7,41 (d, J = 8 ,53 Hz, 2 H), 7 ,24 (s, 1 H), 7,01 (d, J= 8 ,78 Hz, 2 H), 4 ,59 - 4 ,70 (m, 2 H), 3 ,55 -4 ,00 (m, 6 H), 2 ,29 - 2 ,40 (m, 1 H), 1,85 - 2 ,14 (m, 7 H).
E je m p lo 295. {4 -[4 -(5 -C lo ro im id a z o [1 ,2 -a ]p ir id in -6 - i l) - fe n o x i] -p ip e r id in -1 - i l} -(R ) - te t ra h id ro fu ra n -2 - i l -m e ta n o n a .
Análisis: LCMS m/z = 426 (M 1); 1H NMR (400 MHz, CDCb) 6: 7,86 (d, J = 0,75 Hz, 1 H), 7,74 (d, J = 1,25 Hz, 1 H), 7,64 (d, J = 9,03 Hz, 1 H), 7,41 (d, J = 8,53 Hz, 2 H), 7,24 (s, 1 H), 7,01 (d, J = 8,78 Hz, 2 H), 4,59 - 4,70 (m, 2 H), 3,55 - 4,00 (m, 6 H), 2,29 - 2,40 (m, 1 H), 1,85 - 2,14 (m, 7 H).
Ejemplo 296. 1-{4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 384 (M 1); 1H NMR (400 MHz, CDCb) 6: 7,85 - 7,88 (m, 1 H), 7,74 (d, J=1,26 Hz, 1 H), 7,64 (dd, J=9,03, 0,75 Hz, 1 H), 7,41 (d, J=8,78 Hz, 2 H), 7,24 (s, 1 H), 6,98 - 7,04 (m, 2 H), 4,57 - 4,65 (m, 1 H), 3,71 (d, J=3,51 Hz, 3 H), 3,41 - 3,51 (m, 1 H), 2,38 (s, 2 H), 1,82 - 2,05 (m, 4 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 297. {4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona.
Análisis: LCMS m/z = 396 (M 1); 1H NMR (400 MHz, CDCb) 6: 7,86 (d, J=1,76 Hz, 1 H), 7,74 (d, J=1,51 Hz, 1 H), 7,64 (dd, J=9,29, 0,75 Hz, 1 H), 7,39 - 7,44 (m, 2 H), 7,24 (s, 1 H), 6,99 - 7,06 (m, 2 H), 4,61 - 4,67 (m, 1 H), 3,78 -4,01 (m, 2 H), 3,66 - 3,73 (m, 2 H), 1,79 (s, 5 H), 1,00 (dd, J=4,52, 3,01Hz, 2H), 0,78 (dd, J=8,03, 3,01Hz, 2H).
Ejemplo 298. [4-(4-Imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-(R)-tetrahidro-furan-2-il-metanona.
Análisis: LCMS m/z = 392 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,17 (s, 1 H), 8,05 (d, J=1,25 Hz, 1 H), 7,42 - 7,53 (m, 4 H), 6,93 - 7,05 (m, 3 H), 4,58 - 4,70 (m, 2 H), 3,54 - 4,02 (m, 6 H), 2,28 - 2,39 (m, 1 H), 2,01 (s, 7 H).
Ejemplo 299. 1-[4-(4-Imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS m/z = 350 (M 1); 1H NMR (400 MHz, CDCI3 ) 6: 8,14 (s, 1 H), 8,04 (q, J=1,17 Hz, 1 H), 7,42 - 7,53 (m, 4 H), 6,95 - 7,04 (m, 3 H), 4,55-4,64 (m, 1 H), 3,64-3,87 (m, 3 H), 3,39-3,48 (m, 1 H), 2,39 (d, J=7,28 Hz, 2 H), 1,80-2,04 (m, 4 H), 1,17 (t, J=7,40 Hz, 3 H).
Ejemplo 300. Ciclopropil-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 362 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,15 (s, 1 H), 8,05 (d, J=1,25 Hz, 1 H), 7,42 - 7,53 (m, 4 H), 7,02 (d, J=8,78 Hz, 3 H), 4,57 - 4,67 (m, 1 H), 3,77 - 4,01 (m, 2 H), 3,63 - 3,72 (m, 2 H), 1,74 - 2,09 (m, 5 H), 0,97-1,04 (m, 2 H), 0,75-0,82 (m, 2 H).
Ejemplo 301. ácido 1-[4-(4-Imidazo[1,5-a]piridin-6-il-fenoxi)-piperidina-1-carbonil]-ciclopropanocarboxílico amida.
Análisis: LCMS m/z = 405 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,15 (s, 1 H), 8,04 (d, J=1,25 Hz, 1 H), 7,41 - 7,52 (m, 4 H), 6,94 - 7,05 (m, 3 H), 5,89 - 6,04 (m, 1 H), 5,33 - 5,47 (m, 1 H), 4,60 - 4,67 (m, 1 H), 3,67 - 3,90 (m, 4 H), 1,88 - 2,02 (m, 4 H), 1,47 -1,53 (m, 2 H), 1,23-1,29 (m, 2 H).
Ejemplo 302. (1-Hidroxiciclopropil)-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 378 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,15 (s, 1 H), 8,05 (d, J=1,25 Hz, 1 H), 7,42 - 7,54 (m, 4 H), 6,94 - 7,06 (m, 3 H), 4,59 - 4,66 (m, 1 H), 3,87 - 4,01 (m, 2 H), 3,74 (br. s., 2 H), 3,01 - 3,10 (m, 1 H), 1,96 -2,07 (m, 2 H), 1,83 - 1,94 (m, 2 H), 1,12 - 1,18 (m, 2 H), 0,96 - 1,03 (m, 2 H).
Ejemplo 303. (1-Hidroxiciclopropil)-{4-[4-(8-metoxi-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 419 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,98 (dd, J=4,27, 1,76 Hz, 1 H), 8,16 (dd, J=8,28, 1,76 Hz, 1 H), 7,54 - 7,71 (m, 4 H), 7,41 (dd, J=8,16, 4,14 Hz, 1 H), 7,02 - 7,08 (m, 2 H), 4,58 - 4,72 (m, 1 H), 3,92 -4,06 (m, 2 H), 3,87 (s, 3 H), 3,71 - 3,82 (m, 2 H), 3,12-3,37 (m, 1 H), 2,01-2,08 (m, 2 H), 1,88-1,98 (m, 2 H), 1,15 (d, J=2,76 Hz, 2 H), 0,99 (d, J=2,51 Hz, 2 H).
E je m p lo 304. (1 -H id ro x im e t ilc ic lo p ro p il) - {4 -[4 -(5 -m e t i l- im id a z o [1 ,2 -a ]p ir id in -6 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 406 (M 1); 1H NMR (400 MHz, CDCb) 6: 7,74 (d, J=1,25 Hz, 1 H), 7,53 - 7,60 (m, 2H), 7,26 -7,29 (m, 2 H), 7,18 (d, J=9,03 Hz, 1 H), 7,00 (d, J=8,78 Hz, 2 H), 4,59 - 4,66 (m, 1 H), 3,84 - 3,95 (m, 2 H), 3,68 (s, 4 H), 2,55 (s, 3 H), 1,85 - 2,05 (m, 4 H), 1,78 - 1,84 (m, 1 H), 0,99 - 1,05 (m, 2 H), 0,80 - 0,85 (m, 2 H).
Ejemplo 305. (1-Aminociclopropil)-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 391 (M 1); 1H NMR (400 MHz, CDCb) 6: 7,74 (d, J=1,25 Hz, 1 H), 7,53 - 7,61 (m, 2 H), 7,28 (d, J=8,78 Hz, 2 H), 7,18 (d, J=9,29 Hz, 1 H), 7,01 (d, J=8,78 Hz, 2 H), 4,58 - 4,69 (m, 1 H), 3,85 - 3,97 (m, 2 H), 3,68 - 3,78 (m, 2 H), 2,55 (s, 3 H), 1,76 - 2,08 (m, 6 H), 1,04 (d, J=2,26 Hz, 2 H), 0,83 (d, J=2,26 Hz, 2 H).
Ejemplo 306. (1-Hidroxiciclopropil)-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 379 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,81 (d, J=0,75 Hz, 1 H), 8,12 - 8,20 (m, 1 H), 7,88 -7,94 (m, 1 H), 7,61 (d, J=8,78 Hz, 2 H), 7,13 - 7,17 (m, 1 H), 7,05 (d, J=8,78 Hz, 2 H), 4,59 - 4,71 (m, 1 H), 3,87 - 4,02 (m, 2 H), 3,68 - 3,82 (m, 2 H), 2,90 - 2,98 (m, 1 H), 1,97 - 2,09 (m, 2 H), 1,84 - 1,94 (m, 2 H), 1,12-1,19 (m, 2 H), 0,97 1,04 (m, 2 H).
Ejemplo 307. (R)-Tetrahidrofuran-2-il-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 393 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,80 (d, J=0,75 Hz, 1 H), 8,15 (dd, J=7,28, 1,00 Hz, 1 H), 7,88 - 7,93 (m, 1 H), 7,61 (d, J=8,53 Hz, 2 H), 7,13 (dd, J=7,28, 1,76 Hz, 1 H), 7,04 (d, J=8,78 Hz, 2 H), 4,59 -4,71 (m, 2 H), 3,51 - 4,01 (m, 6 H), 2,28 - 2,39 (m, 1 H), 1,87 - 2,11 (m, 7 H).
Ejemplo 308. Ciclopropil-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS m/z = 363 (M 1); 1H NMR (400 MHz, CDCI3 ) 6: 8,81 (s, 1 H), 8,15 (dd, J=7,03, 1,00 Hz, 1 H), 7,86 -7,95 (m, 1 H), 7,61 (d, J=8,78 Hz, 2 H), 7,14 (dd, J=7,15, 1,63 Hz, 1 H), 7,03 - 7,10 (m, 2 H), 4,60 - 4,70 (m, 1 H), 3,77 - 4,02 (m, 2 H), 3,68 (ddd, J=13,36, 6,96, 4,02 Hz, 2 H), 2,01 (s, 4 H), 1,79 (t, J=4,64 Hz, 1 H), 1,00 (dd, J=4,52, 3,01 Hz, 2 H), 0,78 (dd, J=7,78, 3,01 Hz, 2 H).
Ejemplo 309. (1-Hidroxiciclopropil)-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 392 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,81 (s, 1 H), 8,15 (dd, J=7,03, 1,00 Hz, 1 H), 7,86 -7,95 (m, 1 H), 7,61 (d, J=8,78 Hz, 2 H), 7,14 (dd, J=7,15, 1,63 Hz, 1 H), 7,03 - 7,10 (m, 2 H), 4,60 - 4,70 (m, 1 H), 3,77 - 4,02 (m, 2 H), 3,68 (ddd, J=13,36, 6,96, 4,02 Hz, 2 H), 2,01 (s, 4 H), 1,79 (t, J=4,64 Hz, 1 H), 1,00 (dd, J=4,52, 3,01 Hz, 2 H), 0,78 (dd, J=7,78, 3,01 Hz, 2 H).
Ejemplo 310.2-Hidroxi-2-metil-1-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1- ona.
Análisis: LCMS m/z = 394 (M 1); 1H NMR (400 MHz, CDCla) 6: 7,74 (d, J=1,25 Hz, 1 H), 7,56 - 7,61 (m, 1 H), 7,54 (s, 1 H), 7,29 (s, 2 H), 7,17 - 7,22 (m, 1 H), 7,00 (d, J=8,78 Hz, 2 H), 4,62 - 4,71 (m, 1 H), 4,49 (s, 1 H), 3,81 - 3,94 (m, 2 H), 3,73 (s, 2 H), 2,55 (s, 3 H), 1,88 - 2,06 (m, 4 H), 1,53 (s, 6 H).
Ejemplo 311. {4-[4-(5-Metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 407 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,39 (s, 1 H), 7,67 (s, 1 H), 7,49 (d, J=9,03 Hz, 1 H), 7,30 (d, J=8,53 Hz, 2 H), 7,02 (d, J=8,78 Hz, 2 H), 4,57-4,72 (m, 2H), 3,53-4,04 (m, 6H), 2,78 (s, 3H), 2,28-2,40 (m, 1H), 1,88-2,13 (m, 7H).
Ejemplo 312. (1-Hidroxiciclopropil)-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 393 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,39 (s, 1 H), 7,66 - 7,73 (m, 1 H), 7,47 - 7,54 (m, 1 H), 7,28 - 7,34 (m, 2 H), 7,30 (d, J=8,78 Hz, 2 H), 7,03 (d, J=8,78 Hz, 2 H), 4,61 - 4,69 (m, 1 H), 3,90-4,03 (m, 2H), 3,69-3,81 (m, 2H), 2,78 (s, 4H), 1,99-2,09 (m, 2H), 1,87-1,97 (m, 2H), 1,14-1,19 (m, 2H), 1,00 (d, J=2,76Hz, 2H).
E je m p lo 313. 1 - {4 -[4 -(5 -M e t il-[1 ,2 ,4 ] t r ia z o lo [1 ,5 -a ]p ir id in -6 - i l) - fe n o x i] -p ip e r id in -1 - i l } -p ro p a n -1 -o n a .
Análisis: LCMS m/z = 365 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,39 (s, 1 H), 7,69 (d, J=9,04 Hz, 1 H), 7,49 (d, J=9,03 Hz, 1 H), 7,30 (d, J=8,78 Hz, 2 H), 7,02 (d, J=8,78 Hz, 2 H), 4,56 - 4,67 (m, 1 H), 3,63 - 3,91 (m, 3 H), 3,38 - 3,51 (m, 1 H), 2,78 (s, 3 H), 2,34 - 2,47 (m, 2 H), 1,83 - 2,06 (m, 4 H), 1,18 (s, 3 H).
Ejemplo 314. Ciclopropil-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 377 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,39 (s, 1 H), 7,63 - 7,73 (m, 1 H), 7,50 (d, J=9,29 Hz, 1 H), 7,30 (d, J=8,78 Hz, 2 H), 7,03 (d, J=8,78 Hz, 2 H), 4,58 - 4,69 (m, 1 H), 3,77 - 4,02 (m, 2 H), 3,63 - 3,74 (m, 2 H), 2,78 (s, 3 H), 1,72 - 2,12 (m, 6 H), 0,95 - 1,05 (m, 2 H), 0,75 - 0,81 (m, 2 H).
Ejemplo 315. {4-[4-(8-Metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(1-trifluoro-metilciclopropil)-metanona.
Análisis: LCMS m/z = 455 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,99 (dd, J=4,27, 1,76 Hz, 1 H), 8,16 (dd, J=8,28, 1,76 Hz, 1 H), 7,70 (d, J=8,53 Hz, 1 H), 7,46 (d, J=8,28 Hz, 1 H), 7,42 (dd, J=8,28, 4,27 Hz, 1 H), 7,32 - 7,38 (m, 2 H), 6,98 - 7,05 (m, 2 H), 4,66 (t, J=3,51 Hz, 1 H), 3,81 (br. s., 4 H), 2,77 (s, 3 H), 1,91 - 2,08 (m, 4 H), 1,31 - 1,42 (m, 2 H), 1,19 (s, 2 H).
Ejemplo 316. (1-Aminociclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 402 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,94 - 9,08 (m, 1 H), 8,13 - 8,21 (m, 1 H), 7..66 - 7,74 (m, 1 H), 7,45 - 7,50 (m, 1 H), 7,38-7,45 (m, 1 H), 7,32-7,38 (m, 2 H), 7,00-7,07 (m, 2 H), 4,60-4,72 (m, 1 H), 3,86-3,98 (m, 2 H), 3,73 (dd, J=6,90, 4,14 Hz, 2 H), 2,77 (s, 3 H), 1,98-2,08 (m, 2 H), 1,78-1,98 (m, 4 H), 1,01-1,08 (m, 2 H), 0,79 0,88 (m, 2 H).
Ejemplo 317. {4-[4-(1-Metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; compuesto con ácido trifluoroacético.
Análisis: LCMS m/z = 406 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,04 (1 H, d, J=1,0 Hz), 7,78 (1 H, dd, J=8,5, 0,8 Hz), 7,61 (2 H, d, J=8,5 Hz), 7,50 (1 H, s), 7,40 (1 H, dd, J=8,4, 1,4 Hz), 6,96 - 7,07 (2 H, m), 4,66 - 4,72 (1 H, m), 4,09 -4,19 (3 H, m), 3,40 - 4,05 (6 H, m), 1,80 - 2,34 (8 H, m).
Ejemplo 318. [4-(4-Imidazo[1,2-a]piridin-6-il-fenoxi)-piperidin-1-il]-(R)-tetrahidro-furan-2-il-metanona; compuesto con ácido trifluoroacético.
Análisis: LCMS m/z = 392 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,26 (1 H, s), 7,58 - 7,72 (3 H, m), 7,48 (2 H, d, J=8,5 Hz), 7,39 (1 H, dd, J=9,3, 1,8 Hz), 7,02 (2 H, d, J=8,5 Hz), 4,57 - 4,72 (2 H, m), 3,43 - 4,03 (6 H, m), 2,31 (1 H, br. s.), 1,80-2,14 (7H, m).
Ejemplo 319. 1-{4-[4-(8-Metilquinolin-7-il)-fenoxi]-piperidina-1-carbonil}-ciclopropano-carbonitrilo.
Análisis: LCMS m/z = 412 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,99 (dd, J=4,27, 1,76 Hz, 1 H), 8,16 (dd, J=8,28, 1,76 Hz, 1 H), 7,70 (d, J=8,28 Hz, 1 H), 7,47 (d, J=8,53 Hz, 1 H), 7,33 - 7,44 (m, 3 H), 6,99 - 7,09 (m, 2 H), 4,68 - 4,77 (m, 1 H), 3,65 - 4,10 (m, 4 H), 2,77 (s, 3 H), 1,94 - 2,19 (m, 4 H), 1,65 (br. s., 4 H).
Ejemplo 320. (1-Metilciclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 401 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,99 (dd, J=4,14, 1,88 Hz, 1 H), 8,11 - 8,20 (m, 1 H), 7,69 (s, 1 H), 7,47 (d, J=8,53 Hz, 1 H), 7,39 - 7,45 (m, 1 H), 7,35 (d, J=8,53 Hz, 2 H), 7,02 (d, J=8,78 Hz, 2 H), 4,57 -4,68 (m, 1 H), 3,85-4,00 (m, 2 H), 3,61-3,76 (m, 2 H), 2,77 (s, 3 H), 1,84-2,05 (m, 4 H), 1,34 (s, 3 H), 0,96 (d, J=1,76 Hz, 2 H), 0,60 (d, J=1,76 Hz, 2 H).
E je m p lo 321. ( (S ) -2 ,2 -D im e t ilc ic lo p ro p il) - {4 -[4 -(8 -m e t i l- q u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 415 (M 1); 1H NMR (400 MHz, CDCls) 6: 8,99 (dd, J=4,02, 1,76 Hz, 1 H), 8,16 (dd, J=8,16, 1,63 Hz, 1 H), 7,70 (d, J=8,53 Hz, 1 H), 7,48 (s, 1 H), 7,42 (dd, J=8,03, 4,27 Hz, 1 H), 7,35 (d, J=8,53 Hz, 2 H), 7,03 (d, J=8,53 Hz, 2 H), 4,63 (br. s., 1 H), 3,56 - 4,02 (m, 4 H), 2,77 (s, 3 H), 1,82 - 2,14 (m, 4 H), 1,18 - 1,28 (m, 5 H), 1,08 (br. s., 3 H), 0,68 - 0,77 (m, 1 H).
Ejemplo 322. (2,2-Dimetilciclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 415 (M 1); 1H NMR (400 MHz, CDCls) 6: 8,99 (dd, J=3,89, 1,38 Hz, 1 H), 8,16 (dd, J=8,16, 1,38 Hz, 1 H), 7,70 (d, J=8,53 Hz, 1 H), 7,39 - 7,51 (m, 2 H), 7,35 (d, J=8,28 Hz, 2 H), 7,03 (d, J=8,53 Hz, 2 H), 4,63 (br. s., 1 H), 3,59 - 4,02 (m, 4 H), 2,77 (s, 3 H), 1,84 - 2,12 (m, 4 H), 1,14 - 1,26 (m, 5 H), 1,07 (d, J=1,76 Hz, 3 H), 0,73 (dd, J=7,78, 4,52 Hz, 1 H).
Ejemplo 323. [4-[4-[8-(4-Metilpiperazin-1-il)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona
Método A
Etapa 1 terc-butil 4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]fenoxi]piperidina-1-carboxilato.
A un frasco secado en un horno bajo una atmósfera de argón se añadió terc-butil 4-[4-(8-cloro-7-quinolil)fenoxi]piperidina-1-carboxilato (0,200 g, 0,456 mmol), 1-metilpiperazina (0,06 mL, 0,5 mmol), acetato de paladio (6,1 mg, 0,027 mmol), bifenil-2-il-di-terc-butil-fosfano (16,3 mg, 0,0547 mmol), tert-butóxido de sodio (0,0701 g, 0,729 mmol), seguido por tolueno (5 mL). La mezcla de reacción se purgó bajo a atmósfera de nitrógeno y se agitó a 99 °C durante toda la noche. La reacción continuó ~50% de material de partida sin reaccionar. Se añadieron tertbutóxido de sodio (0,0701 g, 0,729 mmol), bifenil-2-il-di-terc-butil-fosfano (16,3 mg, 0,0547 mmol), acetato de paladio (6,1 mg, 0,027 mmol), 1-metilpiperazina (0,06 mL, 0,5 mmol) adicionales. La mezcla de reacción se agitó por unas 4 h adicionales. El disolvente se evaporó bajo presión reducida. Los sólidos se diluyeron con salmuera (50 mL), se extrajeron con EtOAc (3 x 50 mL), se secaron (Na2 SO4 ) y el disolvente se evaporó bajo presión reducida. El producto crudo se purificó por HPLC (fase inversa, 5-55% ACN/H2 O). Las fracciones acuosas combinadas se diluyeron con Na2CO3 sat. (25 mL) se extrajeron con DCM (3 x 30 mL) para dar terc-butil 4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]fenoxi]piperidina-1-carboxilato (base libre) como una espuma blancuzca (50 mg, 20%); Análisis: LCMS m/z = 503 (M 1); 1H NMR (400 MHz, CDCla) 6: 7,85 - 7,92 (m, 2 H), 7,60 - 7,70 (m, 3 H), 7,43 - 7,49 (m, 1 H), 6,93 - 7,05 (m, 3 H), 4,47 - 4,59 (m, 1 H), 3,66 - 3,84 (m, 6 H), 3,31 - 3,43 (m, 2 H), 2,52 - 2,60 (m, 4 H), 2,37 (s, 3 H), 1,92 - 2,00 (m, 2 H), 1,74 - 1,86 (m, 2 H), 1,48 (s, 9 H).
Etapa 2. 8-(4-Metilpiperazin-1-il)-7-[4-(4-piperidiloxi)fenil]quinolina hidrocloruro.
A una solución agitada de terc-butil 4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]_fenoxi]piperidina-1-carboxilato (50 mg, 0,1 mmol) en DCM (1 mL) se añadió 4,0 M de HCl en 1,4-dioxano (0,25 mL, 0,99 mmol) en forma de gotas. La reacción
se agitó a 35 °C 4 h y se concentró bajo presión reducida. Los contenidos crudos se disolvieron nuevamente en DCM (2 x 30 mL) y se concentró bajo presión reducida. El producto crudo se trituró con Et2 O (2 x 50 mL) para dar 8-(4-metilpiperazin-1 -il)-7-[4-(4-piperidiloxi)fenil]-quinolina HCl como un sólido amarillo (43 mg, 90%); Análisis: LCMS m/z = 403 (M 1). Este material se usó en la siguiente etapa sin purificación adicional.
Etapa 3. [4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona.
Una solución de ácido (R)-tetrahidrofuran-2-carboxílico (0,01 mL, 0,1 mmol), HATU (40 mg, 0,1 mmol) y DIPEA (0,07 mL, 0,4 mmol) en acetonitrilo (0,4 mL) se agitó a temperatura ambiente por 10 min. 8-(4-Metilpiperazin-1-il)-7-[4-(4-piperidiloxi)fenil]-quinolina dihidrocloruro (43 mg, 0,098 mmol) se añadió y la mezcla se agitó a temperatura ambiente por 1 h. La reacción se apagó por la adición de MeOH (1 mL) y el disolvente se evaporó al vacío. El producto crudo se purificó por HPLC (fase inversa, 5-50% ACN/H2 O). Las fracciones acuosas combinadas se diluyeron con Na2CO3 sat. (25 mL) se extrajeron con DCM (3 x 30 mL) para dar el producto deseado (base libre) como una espuma blancuzca. El compuesto se liofilizó para dar [4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona como un sólido blancuzco (20 mg, 39%); Análisis:LCMS m/z = 501 (M 1); 1H Nm R (400 MHz, CDCb) ó: 7,83-7,95 (m, 2 H), 7,65 (dd, J=14,31, 8,28 Hz, 3 H), 7,46 (dd, J=8,16, 1,38 Hz, 1 H), 6,93-7,05 (m, 3 H), 4,56-4,69 (m, 2 H), 3,53-4,01 (m, 10 H), 2,57 (t, J=4,64 Hz, 4 H), 2,37 (s, 3 H), 2,27-2,34 (m, 1 H), 1,84-2,12 (m, 7 H).
Ejemplo 324. [4-[4-(8-Amino-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona
Método B
Etapa 1. terc-butil 4-[4-(8-amino-7-quinolil)fenoxi]piperidina-1-carboxilato.
terc-butil 4-[4-(8-cloro-7-quinolil)fenoxi]piperidina-1-carboxilato (0,300 g, 0,683 mmol), acetato de paladio (15 mg, 0,068 mmol), (±)-BINAP (85 mg, 0,14 mmol), carbonato de dicesio (668 mg, 2,05 mmol) y benzofenona imina (0,14 mL, 0,82 mmol) en tolueno (6 mL) se desgasificó bajo una atmósfera de argón, luego se calentó a 100 °C por 4 h. El disolvente luego se evaporó bajo presión reducida. Los sólidos se diluyeron con salmuera (50 mL), se extrajeron con EtOAc (3 x 50 mL), se secaron (Na2SO4) y se concentraron bajo presión reducida. El aceite resultante se purificó en HPLC (fase inversa, 20-70 % ACN/H2 O). Las fracciones acuosas combinadas se diluyeron con Na2CO3 sat. (50 mL) se extrajeron con DCM (3 x 60 mL) para dar el producto deseado (base libre) como un aceite marrón. El producto crudo se purificó por gel de sílice cromatografía (0-50% EtOAc/hexanos) para dar terc-butil 4-[4-(8-amino-7-quinolil)fenoxi]-piperidina-1-carboxilato como un aceite amarillento (50 mg; 20%); Análisis: LCMS m/z = 420 (M 1); 1H NMR (400 MHz, CDCb) ó: 8,78 (dd, J=4,14, 1,63 Hz, 1 H), 8,08 (dd, J=8,28, 1,51 Hz, 1 H), 7,46 - 7,56 (m, 2 H), 7,31 - 7,42 (m, 2 H), 7,19 (d, J=8,28 Hz, 1 H), 7,00 - 7,09 (m, 2 H), 5,04 - 5,29 (m, 2 H), 4,53 (s, 1 H), 3,67 - 3,83 (m, 2 H), 3,37 (ddd, J=13,43, 7,78, 3,89 Hz, 2 H), 1,96 (br. s., 2 H), 1,82 (d, J=3,76 Hz, 2 H), 1,49 (s, 9 H).
Etapa 2. 7-[4-(4-Piperidiloxi)fenil]quinolin-8-amina HCl.
A una solución agitada de terc-butil 4-[4-(8-amino-7-quinolil)fenoxi]piperidina-1-carboxilato (50 mg, 0,1 mmol) en DCM (2 mL) se añadió 4,0 M de HCl en 1,4-dioxano (0,30 mL, 1,2 mmol) solución en forma de gotas. La reacción se agitó a 35 °C 4 h y luego se concentró bajo presión reducida. Los contenidos crudos se disolvieron nuevamente en DCM (2x30 mL) y se concentró bajo presión reducida para dar el producto deseado como una espuma amarilla. El producto crudo se trituró con Et2 O (2x10 mL) para dar 7-[4-(4-piperidiloxi)fenil]quinolin-8-amina HCl como un sólido amarillo (35 mg; 80%); Análisis: LCMS m/z = 320 (M 1). Este material se usó sin purificación adicional.
Etapa 3. [4-[4-(8-Amino-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona.
Una solución de ácido (R)-tetrahidrofuran-2-carboxílico (0,01 mL, 0.a mmol), HATU (39 mg, 0,10 mmol) y DIPEA (0,069 mL, 0,39 mmol) en acetonitrilo (0,4 mL) se agitó a temperatura ambiente por 10 min. 7-[4-(4-piperidiloxi)fenil]quinolin-8-amina HCl (35 mg, 0,098 mmol) se añadió y la mezcla se agitó a temperatura ambiente por 1 hora. La reacción se apagó por la adición de MeOH (1 mL). El disolvente se evaporó al vacío. El producto crudo se purificó por HPLC (fase inversa, 13-55% ACN/H2 O). Las fracciones acuosas combinadas se diluyeron con Na2CO3 sat. (25 mL) se extrajeron con DCM (3 x 30 mL) para dar el producto deseado (base libre) como una espuma amarilla. El producto se trituró con Et2 O (5 mL) y hexanos (5 mL) para dar [4-[4-(8-amino-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidro-furan-2-il]metanona como un sólido amarillo claro (8 mg; 20%); Análisis: Lc Ms m/z = 418 (M 1); 1H Nm R (400 MHz, CDCb) Ó: 8,80 (br. s., 1 H), 8,16 (d, J=7,28 Hz, 1 H), 7,51 (d, J=8,28 Hz, 2 H), 7,34 - 7,46 (m, 2 H), 7,22 (d, J=8,28 Hz, 1 H), 7,05 (d,
J=8,53 Hz, 2 H), 4,68 - 6,04 (m, 2 H), 4,65 (d, J=6,02 Hz, 2 H), 3,55 - 4,02 (m, 6 H), 2,26 - 2,40 (m, 1 H), 1,87 - 2,14 (m, 7 H).
Los siguientes compuestos se sintetizaron usando los procedimientos de Ejemplos 323 o 324.
Ejemplo 325. {4-[4-(8-Metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 432 (M 1); 1H NMR (400 MHz, CDCls) 6: 8,77 (dd, J=4,14, 1,63 Hz, 1 H), 8,09 (dd, J=8,16, 1,63 Hz, 1 H), 7,51 (d, J=8,53 Hz, 2 H), 7,33 - 7,42 (m, 2 H), 7,21 (d, J=8,53 Hz, 1 H), 6,94 - 7,02 (m, 2 H), 6,31-6,42 (m, 1H), 4,66 (dd, J=7,15, 5,65Hz, 2H), 3,56-4,01 (m, 6H), 2,58 (s, 3H), 2,25-2,38 (m, 1H), 1,93 (br. s., 7H).
Ejemplo 326. 1-{4-[4-(8-Metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 390 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,77 (dd, J=4,27, 1,76 Hz, 1 H), 8,09 (dd, J=8,28, 1,76 Hz, 1 H), 7,47 - 7,56 (m, 2 H), 7,33 - 7,44 (m, 2 H), 7,21 (d, J=8,28 Hz, 1 H), 6,98 (d, J=8,78 Hz, 2 H), 6,31 - 6,45 (m, 1 H), 4,60 (dt, J=6,53, 3,26 Hz, 1 H), 3,80 - 3,90 (m, 1 H), 3,63 - 3,79 (m, 2 H), 3,39 - 3,51 (m, 1 H), 2,58 (s, 3 H), 2,36 - 2,45 (m, 2 H), 1,80 - 2,05 (m, 4 H), 1,18 (t, J=7,53 Hz, 3 H).
Ejemplo 327. (4-{4-[8-(2-Metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 476 (M 1); 1H NMR (400 MHz, CD3ÜD): 6: 8,82 (dd, J=4,27, 1,76 Hz, 1 H), 8,23 (dd, J=8,28, 1,76 Hz, 1 H), 7,55 (d, J=8,53 Hz, 2 H), 7,46 - 7,51 (m, 1 H), 7,38 (s, 2 H), 7,10 (d, J=8,53 Hz, 2 H), 4,70 - 4,83 (m, 2 H), 3,90 (s, 4 H), 3,61 - 3,74 (m, 1 H), 3,49 - 3,60 (m, 1 H), 3,35 - 3,39 (m, 4 H), 3,26 (s, 3 H), 2,98 (t, J=5,40 Hz, 2 H), 2,19 - 2,32 (m, 1 H), 1,78 - 2,15 (m, 7 H).
Ejemplo 328. 1-(4-{4-[8-(2-Metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona.
Análisis: LCMS m/z = 434 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,80 (dd, J=4,02, 1,51 Hz, 1 H), 8,08 (dd, J=8,28, 1,51 Hz, 1 H), 7,53 (d, J=8,53 Hz, 2 H), 7,30 - 7,42 (m, 2 H), 7,20 - 7,25 (m, 1 H), 6,98 (d, J=8,53 Hz, 2 H), 6,57 (br. s., 1 H), 4,60 (br. s., 1 H), 3,80 - 3,94 (m, 1 H), 3,61 - 3,80 (m, 2 H), 3,41 - 3,53 (m, 1 H), 3,37 (t, J=5,52 Hz, 2 H), 3,27 (s, 3 H), 2,99 (t, J=5,40 Hz, 2 H), 2,39 (q, J=7,45 Hz, 2 H), 1,81 - 2,05 (m, 4 H), 1,18 (t, J=7,53 Hz, 3 H).
E je m p lo 329. (4 - {4 -[8 -(2 -D im e t i la m in o e t i la m in o ) -q u in o lin -7 - i l ] - fe n o x i} -p ip e r id in -1 - i l) -(R ) te t ra h id ro fu ra n -2 - i l-m e ta n o n a .
Análisis: LCMS m/z = 489 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,79 (dd, J=4,02, 1,76 Hz, 1 H), 8,08 (dd J=8,28, 1,76 Hz, 1 H), 7,52 (d, J=8,28 Hz, 2 H), 7,31 - 7,44 (m, 2 H), 7,23 (d, J=8,53 Hz, 1 H), 6,96 - 7,03 (m, 2 H), 6,25 - 6,73 (m, 1 H), 4,66 (dd, J=7,40, 5,65 Hz, 2 H), 3,52 - 4,02 (m, 6 H), 2,90 (t, J=6,53 Hz, 2 H), 2,38 (t, J=6,40 Hz, 2 H), 2,28 - 2,34 (m, 1 H), 2,15 (s, 6 H), 1,86 - 2,10 (m, 7 H).
Ejemplo 330. 7-[4-(1-Propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carbonitrilo.
Un frasco de fondo redondo secado en un horno se añadió 1-[4-[4-(8-cloro-7-quinolil)-fenoxi]-1-piperidil]propan-1-ona (120 mg, 0,30 mmol), cianuro de zinc (54 mg, 0,46 mmol), zinc activado pulverizado (4 mg, 0,06 mmol), [1,1' bis(difenilfosfino)ferroceno]-dicloropaladio(II), complejo (DPPF-Pd) con DCM (1:1) (12 mg, 0,015 mmol) y DMF (1 mL) bajo una atmósfera de nitrógeno. La mezcla de reacción se calentó a 90 °C y se agitó durante toda la noche bajo una atmósfera de nitrógeno. La mezcla de reacción se enfrió temperatura ambiente y filtró a través de Celite, se lavó con EtOAc (2 x 20 mL) y se concentró bajo presión reducida. El producto crudo se purificó por HPLC (fase inversa, 23-65% ACN/H2 O). Las fracciones acuosas combinadas se diluyeron con Na2CO3 sat. (25 mL), se extrajeron con DCM (3 x 30 mL) para dar el producto deseado (base libre) como un aceite amarillo. La muestra se liofilizó durante toda la noche para dar 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carbonitrilo como un sólido blancuzco (4,1 mg; 3,3%); Análisis: LCMS m/z = 386 (M 1); 1H NMR (400 MHz, CDCb) 6: 9,14 (dd, J=4,27, 1,76 Hz, 1 H), 8,22 - 8,29 (m, 1 H), 8,06 (d, J=8,53 Hz, 1 H), 7,70 (dd, J=8,78, 1,00 Hz, 3 H), 7,52 - 7,57 (m, 1 H), 7,06 - 7,12 (m, 2 H), 4,61 - 4,70 (m, 1 H), 3,78 - 3,90 (m, 1 H), 3,65 - 3,77 (m, 2 H), 3,40 - 3,51 (m, 1 H), 2,40 (d, J=7,78 Hz, 2 H), 1,95 - 2,05 (m, 2 H), 1,81 - 1,92 (m, 2 H), 1,17 - 1,21 (m, 3 H).
Ejemplo 331. [4-[4-[8-(Dimetilamino)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona
Etapa 1. ácido trifluorometanosulfónico 7-bromoquinolin-8-il éster.
A una solución de 7-bromoquinolin-8-ol (5 g, 20 mmol) en DCM (120 mL) a 0 °C se añadió piridina (9,02 mL, 112 mmol) y anhídrido trifluorometanosulfónico (tríflico) (5,63 mL, 33,5 mmol). Después de agitar por 30 min a 0 °C, la reacción se apagó con ac. sat. solución de NaHCO3 ac. sat. (25 mL). La capa orgánica se separó y la capa de agua se extrajo con DCM (2 x 30 mL). Las capas orgánicas combinadas se lavaron con agua (50 mL), salmuera (50 mL), se secaron (Na2SO4), y se concentraron para dar ácido trifluorometanosulfónico 7-bromoquinolin-8-il éster como un sólido grisáceo (7 g; 79%); LCMS m/z = 357 (M 1). Este material se usó para la siguiente etapa sin purificación adicional.
Etapa 2. terc-butil éster del ácido 4-[4-(8-Trifluorometanosulfoniloxi-quinolin-7-il)-fenoxi]-piperidina-1-carboxílico. Un frasco cargado con terc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (5 g, 10 mmol), ácido trifluorometanosulfónico 7-bromo-quinolin-8-il éster (4,86 g, 13,6 mmol), acetato de paladio (280 mg, 1,2 mmol), trifenilfosfina (0,65 g, 2,5 mmol), 1,4-dioxano (60 mL) y 1,0 M de Na2CO3 en H2 O (62,0 mL, 62,0 mmol) se enjuagó con nitrógeno por 5 min. La reacción se calentó a 85 °C por 1,5 h. Después de enfriar hasta la temperatura ambiente, la reacción se diluyó con EtOAc (200 mL), se lavó con una solución de NaHCO3 ac.
sat. (100 mL). La capa de agua se extrajo nuevamente con EtOAc (2 x 50 mL). Las capas orgánicas combinadas se lavaron con salmuera (50 mL), se secaron (Na2SO4), y se concentraron. El producto crudo se purificó por cromatografía de gel de sílice (0-50% EtOAc/hexanos) para dar terc-butil éster del ácido 4-[4-(8-trifluorometanosulfoniloxi-quinolin-7-il)-fenoxi]-piperidina-1-carboxílico como un sólido blanco (5 g; 60%); Análisis: LCMS m/z = 553 (M 1); 1H Nm R (400 MHz, CDCl3) 6: 9,06 - 9,10 (m, 1 H), 8,20 - 8,28 (m, 1 H), 7,87 (d, J=8,53 Hz, 1 H), 7,62 (d, J=8,53 Hz, 1 H), 7,50 - 7,56 (m, 3 H), 7,05 (d, J=9,03 Hz, 2 H), 4,48 - 4,63 (m, 1 H), 3,69 - 3,80 (m, 2 H), 3,29 - 3,44 (m, 2 H), 1,92 - 2,03 (m, 2 H), 1,75 - 1,85 (m, 2 H), 1,48 (s, 9 H).
Etapa 3. terc-butil 4-[4-[8-(dimetilamino)-7-quinolil]fenoxi]piperidina-1-carboxilato.
A un frasco secado en un horno bajo una atmósfera de argón se añadió terc-butil éster del ácido 4-[4-(8-trifluorometanosulfoniloxi-quinolin-7-il)-fenoxi]-piperidina-1-carboxílico (1 g, 2 mmol), dimetilamina (2M solución en THF, 10,3 mL, 22,8 mmol), acetato de paladio (51 mg, 0,23 mmol), (±)-BINAP (142 mg, 0,228 mmol), carbonato de cesio (1,039 g, 3,189 mmol), seguido por THF (10 mL). La mezcla de reacción se purgó bajo una atmósfera de argón y se agitó a 65 °C por 20h en un tubo sellado. El disolvente se evaporó bajo presión reducida. Los sólidos se diluyeron con salmuera (250 mL), se extrajeron con EtOAc (3x50 mL), se secaron (Na2SO4) y el disolvente se evaporó bajo presión reducida. El producto crudo se purificó por en cromatografía de gel de sílice (0-30% EtOAc/hexanos). Las fracciones acuosas combinadas se evaporaron bajo presión reducida para producir el producto deseado como un sólido amarillo (420 mg; 40%). Análisis: LCMS m/z = 448 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,94 (dd, J=4,14, 1,88 Hz, 1 H), 8,11 (dd, J=8,28, 1,76 Hz, 1 H), 7,46 - 7,52 (m, 1 H), 7,32 - 7,42 (m, 4 H), 6,99 (d, J=8,78 Hz, 2 H), 4,50 -4,58 (m, 1 H), 3,70 - 3,81 (m, 2 H), 3,32 - 3,42 (m, 2 H), 2,89 (s, 6 H), 1,94 - 2,01 (m, 2 H), 1,81 (dd, J=13,18, 3,89 Hz, 2 H), 1,48 (s, 9 H).
Etapa 4. N,N-Dimetil-7-[4-(4-piperidiloxi)fenil]quinolin-8-amina hidrocloruro.
A una solución agitada de terc-butil 4-[4-[8-(dimetilamino)-7-quinolil]fenoxi]piperidina-1-carboxilato (420 mg, 0,94 mmol) en DCM (10 mL) se añadió 4,0 M de HCl en 1,4-dioxano (2,35 mL, 9,38 mmol) en forma de gotas. La reacción se agitó a 35 °C (4 h) y se concentró bajo presión reducida. Los contenidos crudos se disolvieron nuevamente en DCM (2x30 mL) y se concentró bajo presión reducida. El producto crudo se trituró con Et2 O (2x25 mL) para dar el N,N-dimetil-7-[4-(4-piperidiloxi)fenil]quinolin-8-amina HCl deseado como un sólido amarillo (360 mg; 95%); LCMS m/z = 348 (M 1). Se usó sin purificación adicional.
Etapa 5. [4-[4-[8-(Dimetilamino)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona.
[0874] A solución de ácido (R)-tetrahidrofuran-2-carboxílico (0,04 mL, 0,4 mmol), HATU (156 mg, 0,410 mmol) y DIPEA (0,27 mL, 1,6 mmol) en acetonitrilo (2 mL) se agitó a temperatura ambiente por 10 min. Se añadió [A] N,N-dimetil-7-[4-(4-piperidiloxi)fenil]quinolin-8-amina HCl (150 mg, 0,39 mmol) y la mezcla se agitó a temperatura ambiente por 1 hora. La reacción se apagó por la adición de MeOH (1 mL). El disolvente se evaporó al vacío. El producto crudo se purificó por HPLC (fase inversa, 10-55% ACN/H2 O). Las fracciones acuosas combinadas se diluyeron con Na2CO3 sat. (25 mL) se extrajeron con DCM (3x30 mL) para dar el producto deseado (base libre) como un sólido amarillo (120 mg; 66%). Análisis: LCMS m/z = 446 (M 1); 1H NMR (400 MHz, CDCla) 6: 8,95 (dd, J=4,14, 1,88 Hz, 1 H), 8,09 - 8,16 (m, 1 H), 7,46 - 7,56 (m, 1 H), 7,32 - 7,42 (m, 4 H), 6,93 - 7,06 (m, 2 H), 4,55 - 4,73 (m, 2 H), 3,53 - 4,04 (m, 6 H), 2,90 (s, 6 H), 2,26 - 2,41 (m, 1 H), 1,89 - 2,14 (m, 7 H). Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 331:
Ejemplo 332. 1-{4-[4-(8-Dimetilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 404 (M 1); 1H NMR (400 MHz, CDCls) 6: 8,95 (dd, J=4,02, 1,76 Hz, 1 H), 8,09 - 8,16 (m, 1 H), 7,47 - 7,54 (m, 1 H), 7,32 - 7,43 (m, 4 H), 7,00 (d, J=8,53 Hz, 2 H), 4,53 - 4,66 (m, 1 H), 3,61-3,92 (m, 3H), 3,40-3,50 (m, 1H), 2,90 (s, 6H), 2,36-2,46 (m, 2H), 1,94-2,05 (m, 2H), 1,84-1,92 (m, 2H), 1,18 (t, J=7,53Hz, 3H).
E je m p lo 333. C ic lo p ro p il- {4 -[4 -(8 -d im e t i la m in o -q u in o lin -7 - i l) - fe n o x i] -p ip e r id in -1 - i l} -m e ta n o n a .
Análisis: LCMS m/z = 416 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,95 (dd, J=4,27, 1,76 Hz, 1 H), 8,08 - 8,18 (m, 1 H), 7,47 - 7,56 (m, 1 H), 7,33 - 7,44 (m, 4 H), 7,01 (d, J=8,78 Hz, 2 H), 4,57 - 4,68 (m, 1 H), 3,82 - 4,02 (m, 2 H), 3,64 -3,73 (m, 2 H), 2,90 (s, 6 H), 2,01 (s, 5 H), 1,01 (br. s., 2 H), 0,78 (dd, J=8,03, 3,01 Hz, 2 H).
Ejemplo 334. (4-{4-[8-(2-Pirrolidin-1-il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona.
Análisis: LCMS m/z = 515 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,78 (dd, J=4,02, 1,76 Hz, 1 H), 8,05 - 8,12 (m, 1 H), 7,53 (d, J=8,53 Hz, 2 H), 7,34 (d, J=8,53 Hz, 2 H), 7,23 (s, 1 H), 6,98 (d, J=8,78Hz, 2H), 6,36-6,76 (m, 1H), 4,58-4,70 (m, 2H), 3,48-4,04 (m, 6H), 2,94 (s, 2H), 2,54 (s, 2H), 2,24-2,40 (m, 5H), 1,84-2,13 (m, 7H), 1,70 (s, 4H).
Ejemplo 335. 1-(4-{4-[8-(2-Pirrolidin-1-il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona.
Análisis: LCMS m/z = 473 (M 1); 1H NMR (400 MHz, CDCb) 6: 8,78 (dd, J=4,27, 1,76 Hz, 1 H), 8,08 (dd, J=8,28, 1,76 Hz, 1 H), 7,50 - 7,57 (m, 2 H), 7,30 - 7,40 (m, 2 H), 7,22 (d, J=8,53 Hz, 1 H), 6,92 - 7,02 (m, 2 H), 6,32 - 6,75 (m, 1 H), 4,52 - 4,67 (m, 1 H), 3,63 - 3,90 (m, 3 H), 3,39 - 3,51 (m, 1 H), 2,94 (s, 2 H), 2,54 (t, J=6,78 Hz, 2 H), 2,33 - 2,45 (m, 6 H), 1,82 - 2,02 (m, 4 H), 1,68 - 1,76 (m, 4 H), 1,18 (t, J=7,40 Hz, 3 H)
Ejemplo 336. 7-[4-[[1-[(2R)-Tetrahidrofuran-2-carbonil]-4 piperidil]oxi]fenil]quinolina-8-carboxamida
Etapa 1. terc-butil 4-[4-(8-ciano-7-quinolil)fenoxi]pipendina-1-carboxilato.
Un frasco de fondo redondo secado en un horno se cargó con terc-butil éster del ácido 4-[4-(8-trifluorometanosulfoniloxi-quinolin-7-il)-fenoxi]-piperidina-1 -carboxílico (1 g, 2 mmol), cianuro de zinc (319 mg, 2,71 mmol), zinc activado pulverizado (24 mg, 0,36 mmol), DPPF-Pd(II), complejo con DCM (1:1) (74 mg, 0,090 mmol), y DMF (6 mL) bajo una atmósfera de nitrógeno. La mezcla de reacción se llevó a un manto calentado previamente a 90 °C y se agitó durante toda la noche a esta temperatura bajo una atmósfera de nitrógeno. La mezcla de reacción se enfrió hasta la temperatura ambiente y filtró a través de Celite, se lavó con EtOAc (2x20 mL) y se concentró bajo presión reducida. El producto crudo se purificó por cromatografía de gel de sílice (0-60% EtOAc/hexanos). Las fracciones combinadas se evaporaron bajo presión reducida para dar tertbutil 4-[4-(8-ciano-7-quinolil)fenoxi]piperidina-1-carboxilato como un
sólido blanco (750 mg, 90%). Análisis: LCMS m/z = 430 (M 1); 1H NMR (400 MHz, CDCI3 ) ó: 9,10 - 9,22 (m, 1 H), 8,21 - 8,30 (m, 1 H), 8,05 (s, 1 H), 7,69 (dd, J=8,66, 1,13 Hz, 3 H), 7,50-7,59 (m, 1H), 7,07 (d, J=8,78Hz, 2H), 4,52 4,67 (m, 1H), 3,65-3,83 (m, 2H), 3,32-3,49 (m, 2H), 1,94-2,03 (m, 2H), 1,78-1,88 (m, 2H), 1,48 (s, 9H).
Etapa 2. ácido 7-[4-(4-Piperidiloxi)fenil]quinolina-8-carboxamida; 2,2,2-trifluoroacético.
A una solución agitada de terc-butil 4-[4-(8-ciano-7-quinolil)fenoxi]piperidina-1-carboxilato (250 mg, 0,58 mmol) en etanol (4 mL) se añadió 0,5 M de hidróxido de sodio en H2 O (12,8 mL, 6,40 mmol), seguido por 30% peróxido de hidrógeno ac. (0,6 mL, 6 mmol). La reacción se agitó a 50 °C (24 h), pero solamente se observó 8-10% de producto deseado. La mezcla de reacción se enfrió hasta la temperatura ambiente y se neutralizó con 10 % H2 SO4 ac. y se concentró bajo presión reducida. La mezcla de reacción cruda se disolvió nuevamente en 1-metoxi-2-propanol (10 mL). Se añadió hidróxido de sodio sólido (0,256 g, 6,40 mmol), seguido por H2 O (1 mL) y 30% peróxido de hidrógeno ac. (0,6 ml, 6 mmol). La reacción se agitó a 98 °C (24 h) y esta vez se observó ~40% de producto deseado. Hidróxido de sodio adicional (0,256, 6,40 mmol) y se añadió 30% peróxido de hidrógeno ac. (0,6 ml, 6 mmol). Después de calentar adicionalmente a 98 °C (12 h), se observó -60% de producto deseado. Se añadió hidróxido de sodio adicional (0,256, 6,4026 mmol) y 30% peróxido de hidrógeno ac. (0,6 ml, 6 mmol) y la mezcla de reacción se calentó a 98 °C por 4h adicionales. La mezcla de reacción se enfrió hasta la temperatura ambiente, se neutralizó con H2 SO4 conc. ac. y se evaporó bajo presión reducida. Los contenidos del frasco se disolvieron en DMSO, los sólidos se filtraron y la solución resultante se purificó por HPLC (fase inversa, 5-52% ACN/H2 O). Las fracciones combinadas se liofilizaron para producir el producto deseado ácido 7-[4-(4-piperidiloxi)fenil]quinolina-8-carboxamida; 2,2,2-trifluoroacético como un sólido amarillo (60 mg, 20%). Análisis: lCm S m/z = 348 (M 1 ). Etapa 3. 7-[4-[[1-[(2R)-Tetrahidrofuran-2-carbonil]-4-piperidil]oxi]fenil]quinolina-8-carboxamida.
Una solución de ácido (R)-tetrahidrofuran-2-carboxílico (0,006 mL, 0,07 mmol), HATU (26 mg, 0,068 mmol) y DIPEA (0,045 mL, 0,26 mmol) en acetonitrilo (0,2 mL, 5 mmol) se agitó a temperatura ambiente por 10 min. 7-[4-(4-piperidiloxi)fenil]quinolina-8-carboxamida; TFA (30 mg, 0,06 mmol) se añadió y la mezcla se agitó a temperatura ambiente por 1 hora. La reacción se apagó por la adición de MeOH (1 mL). El disolvente se evaporó al vacío. El producto crudo se purificó por HPLC (fase inversa, 5-52% ACN/H2 O). Las fracciones acuosas combinadas se diluyeron con Na2CO3 sat. (25 mL), se extrajeron con DCM (3x30 mL) para dar el producto deseado (base libre) como un sólido blanco. El producto se liofilizó para dar 7-[4-[[1-[(2R)-tetrahidrofuran-2-carbonil]-4 piperidil]oxi]fenil]quinolina-8-carboxamida como un sólido blanco (25 mg, 80%). Análisis: LCMS m/z = 446 (M 1); 1H NMR (400 MHz, CDCb) ó: 9,03 (dd, J=4,27, 1,76 Hz, 1 H), 8,16 - 8,25 (m, 1 H), 7,88 - 7,96 (m, 1 H), 7,61 (s, 3 H), 7,43 - 7,49 (m, 1 H), 7,00 (d, J=8,78 Hz, 2 H), 5,75 - 5,92 (m, 2 H), 4,56 - 4,72 (m, 2 H), 3,51 - 4,01 (m, 6 H), 2,27 - 2,40 (m, 1 H), 1,85 - 2,13 (m, 7 H).
El siguiente compuesto se sintetizó usando el procedimiento para el ejemplo 336:
Ejemplo 337. ácido 7-[4-(1-Propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carboxílico amida.
Análisis: LCMS m/z = 404 (M 1); 1H NMR (400 MHz, CDCb) ó: 9,03 (dd, J=4,27, 1,76 Hz, 1 H), 8,17 - 8,26 (m, 1 H), 7,90 (d, J=8,53 Hz, 1 H), 7,60 (dd, J=8,66, 2,38 Hz, 3 H), 7,41 - 7,50 (m, 1 H), 7,00 (d, J=8,78 Hz, 2 H), 5,79-5,94 (m, 2 H), 4,55-4,67 (m, 1 H), 3,63-3,92 (m, 3 H), 3,40-3,54 (m, 1 H), 2,34-2,47 (m, 2 H), 1,83-2,03 (m, 4 H), 1,18 (t, J = 7,40 Hz, 3 H).
Ejemplo 338. 1-(3-(4-(Quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona.
Etapa 1. terc-butil 3-(4-bromofenoxi)azetidina-1-carboxilato.
A terc-butil 3-((metilsulfonil)oxi)azetidina-1-carboxilato (7 g, 0,027 mol) y Cs2CO3 (10,9g, 0,033mol) en DMF (200 mL) se añadió 4-bromofenol (4,82g,0,027mol). La reacción se calentó hasta 80 °C por 18 h, y luego se enfrió hasta la
temperatura ambiente. Se añadió agua helada a la mezcla de reacción cuando se obtuvo un sólido blanco terc-butil 3-(4-bromofenoxi)azetidina-1-carboxilato que se filtró, se lavó con agua y se secó (6,5 g, 71%). Análisis: 1H NMR (400 MHz, DMSO-d6) ó: 7,50-7,41 (m, 2H), 6,85-6,76 (m, 2H), 5,0-4,96 (m, 1H), 4,32-4,23 (m, 2H), 3,77 (m, 2H), 1,38 (s, 9H); LCMS (ESI): 328 (M 1).
Etapa 2. terc-butil 3-(4-(quinolin-3-il)fenoxi)azetidina-1-carboxilato.
Una solución de terc-butil 3-(4-bromofenoxi)azetidina-1-carboxilato (1,5 g, 4,57 mmol), ácido quinolin-3-borónico (948 mg, 5,5 mmol) y Na2CO3 (1,2 g, 11,42 mmol) en 1,4-dioxano (60 mL) y agua (15 mL) se desgasificó por argón por 15 min. Tetraquis-(trifenilfosfina) paladio(0) (264 mg, 0,23 mmol) se añadió luego bajo atmósfera de argón y la mezcla de reacción se calentó a 100 °C por 15 h. La mezcla de reacción se enfrió hasta la temperatura ambiente y filtró a través de almohadilla de Celite, se lavó con ETOAc. Filtrado se lavó con agua y salmuera, se secó sobre Na2SO4, se filtró y se concentró. El producto crudo se purificó por cromatografía de columna (50% EtOAc-Hexano) para dar terc-butil 3-(4-(quinolin-3-il)fenoxi)azetidina-1-carboxilato (950 mg, 55%). Análisis: LCMS (ESI): 377 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,22 (d, J = 2,3 Hz, 1H), 8,58 (d, J = 2,5 Hz, 1H), 8,03 (d, J = 8,3 Hz, 2H), 7,84 (d, J = 8,2 Hz, 2H), 7,81 7,70 (m, 1H), 7,63 (t, J = 7,5 Hz, 1H), 7,02 (d, J = 8,2 Hz, 2H), 5,08 (m, 1H), 4,35 (t, J = 7,9 Hz, 2H), 3,84 (dd, J = 10,1, 4,0 Hz, 2H), 1,40 (s, 9H). Etapa 3. 3-(4-(Azetidin-3-iloxi)fenil)quinolina hidrocloruro.
A una solución de t-butil 3-(4-(quinolin-3-il)fenoxi)azetidina-1-carboxilato (950 mg) en DCM (20 mL) se añadió 4M HCl en 1,4-dioxano (6 mL) a 0 °C. La mezcla de reacción se agitó a temperatura ambiente por 2 h. Después del completamiento de la reacción, se concentró bajo presión reducida para dar 3-(4-(azetidin-3-iloxi)fenil)quinolina HCl (800 mg, 98%) que se usó en la siguiente etapa sin purificación adicional. Análisis: LCMS (ESI): 277 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,24-9,19 (m, 1H), 8,57 (s, 1H), 8,03 (d, J = 8,3 Hz, 2H), 7,78 (dd, J = 33,2, 8,2 Hz, 3H), 7,63 (t, J = 7,6 Hz, 1H), 6,99 (t, J = 10,9 Hz, 2H), 5,76 (s, 1H), 5,11 - 5,06 (m, 1H), 3,87-3,78 (m, 2H), 3,55 (t, J = 7,0 Hz, 1H), 1,23 (s, 1H).
Etapa 4. 1-(3-(4-(Quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona.
A una solución agitada de 3-(4-(azetidin-3-iloxi)fenil)quinolina HCl (1 eq.) y Et3N (3 eq.) en DCM se añadió en forma de gotas cloruro ácido (1,1 eq.) a 0 °C y la mezcla de reacción luego se agitó a temperatura ambiente por 2 hora. Después del completamiento de la reacción, la mezcla de reacción se diluyó con DCM y se lavó con agua. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró bajo presión reducida. La purificación por cromatografía de columna usando gel de sílice y 5-6% MeOH/DCM como eluyente dio 1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona. Análisis: mp 172 °C; LCMS (ESI): 333 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,23 (d, J = 2,4 Hz, 1H), 8,59 (d, J = 2,4 Hz, 1H), 8,04 (d, J = 8,5 Hz, 2H), 7,90-7,82 (m, 2H), 7,78-7,75 (m, 1H), 7,68-7,59 (m, 1H), 7,08-6,99 (m, 2H), 5,16 - 5,13 (m, 1H), 4,64-4,55 (m, 1H), 4,34 (dd, J = 10,5, 6,5 Hz, 1H), 4,12 (dd, J = 9,6, 3,8 Hz, 1H), 3,81 (dd, J = 10,4, 3,8 Hz, 1H), 2,19-2,04 (m, 2H), 0,98 (q, J = 7,5 Hz, 3H).
Los siguientes ejemplos se prepararon usando el procedimiento del Ejemplo 338, usando el cloruro ácido requerido en la Etapa 4.
Ejemplo 339. 2-Metil-1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona.
Análisis: mp 162 °C; LCMS (ESI): 347 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 9,23 (d, J = 2,4 Hz, 1H), 8,59 (d, J = 2,4 Hz, 1H), 8,04 (d, J = 8,3 Hz, 2H), 7,91-7,81 (m, 2H), 7,80-7,71 (m, 1H), 7,64 (t, J=7,6 Hz, 1H), 7,04 (d, J = 8,5 Hz, 2H), 5,14 (m, 1H), 4,66 (dd, J=9,3, 6,4 Hz, 1H), 4,39-4,29 (m, 1H), 4,16 (dd, J = 9,4, 3,8 Hz, 1H), 3,81 (m, 1H), 0,99 (t, J=6,5 Hz, 7H).
Ejemplo 340. Ciclopropil(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)metanona.
Análisis: mp 187 °C; LCMS (ESI): 345 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,23 (d, J = 2,4 Hz, 1H), 8,59 (d, J = 2,4 Hz, 1H), 8,04 (d, J = 8,5 Hz, 2H), 7,90-7,82 (m, 2H), 7,80-7,71 (m, 1H), 7,64 (t, J = 7,5 Hz, 1H), 7,05 (d, J = 8,6 Hz, 2H), 5,19-5,17 (m, 1H), 4,75 (t, J = 8,1 Hz, 1H), 4,36 (dd, J = 10,5, 6,5 Hz, 1H), 4,24 (dd, J = 9,7, 3,7 Hz, 1H), 3,83 (dd, J = 10,9, 3,9 Hz, 1H), 1,20-1,04 (m, 1H), 0,88-0,63 (m, 4H).
Ejemplo 341. 3-Metil-1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)butan-1-ona.
Análisis: mp 201 °C; LCMS (ESI): 361 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,23 (d, J = 2,4 Hz, 1H), 8,58 (d, J = 2,4 Hz, 1H), 8,03 (d, J = 8,4 Hz, 2H), 7,85 (d, J = 8,5 Hz, 2H), 7,80-7,59 (m, 2H), 7,04 (d, J = 8,3 Hz, 2H), 5,15-5,12 (m, 1H), 4,60 (dd, J = 9,6, 6,4 Hz, 1H), 4,34 (dd, J = 10,6, 6,5 Hz, 1H), 4,11 (dd, J = 9,7, 3,8 Hz, 1H), 3,81 (dd, J = 10,8, 3,9 Hz, 1H), 2,49 (s, 1H), 1,98 (d, J = 2,9 Hz, 2H), 0,96-0,79 (m, 6H).
Ejemplo 342. (S)-1-(3-(4-(Quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona, HCl
Etapa 1. (R)-1-(3-Hidroxipirrolidin-1-il)propan-1-ona.
A una solución de (R)-3-hidroxipirrolidina (1,5 g, 0,017 mol) en DCM (20 mL) se añadió trietilamina (6,6 mL 0,051 mol) a 0 °C. La mezcla de reacción se agitó a 0 °C por 10 minutos, cuando cloruro de propionilo (1,59 g, 0,017 mol) se añadió en forma de gotas, y la mezcla se agitó a temperatura ambiente por 15 h. Después del completamiento de la reacción se monitoreó por TLC, la mezcla de reacción se particionó entre DCM y agua. La capa orgánica se lavó con salmuera, se secó sobre sulfato de sodio anhidro, se filtró y se concentró bajo presión reducida para obtener el producto crudo que se purificó por cromatografía de columna usando gel de sílice para dar (R)-1-(3-hidroxipirrolidin-1-il)propan-1-ona (2,3g, 92%) como un aceite incoloro. Análisis: 1H NMR (400 MHz, CDCb) 6: 4,55-4,50 (m, 1H), 3,69 3,37 (m, 4H), 2,74-2,64 (m, 2H), 2,36-2,16 (m, 2H), 1,14 (t, J = 7,5 Hz, 3H).
Etapa 2. (S)-1-(3-(4-Bromofenoxi)pirrolidin-1-il)propan-1-ona.
(R)-1-(3-Hidroxipirrolidin-1-il)propan-1-ona (2,3 g, 0,015 mol), se llevó a DCM (30 mL) a lo que se añadió ADDP (4,8 g, 0,019 mol) a temperatura ambiente seguido por adición de trifenilfosfina (5,01 g, 0,019 mol). 4-bromofenol (4,23 g, 0,019 mol) se añadió luego y la mezcla de reacción se agitó a temperatura ambiente por 15 h. La mezcla de reacción se diluyó con DCM y se lavó con en HCl solución, solución de NaCO3 sat. sucesivamente. Capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró. El producto crudo se purificó por cromatografía de columna (neutral alúmina, 2% MeoH en DCM), para dar (S)-1-(3-(4-bromo-fenoxi)pirrolidin-1-il)propan-1-ona (1,9 g, 40%) como un aceite amarillo claro. Análisis: LCMS (ESI): 298 (M+1); 1H NMR (400 MHz, CDCb) 6: 7,53-7,33 (m, 2H), 6,80-6,70 (m, 2H), 4,86 (m, 1H), 3,86-3,52 (m, 4H), 2,39-2,00 (m, 4H), 1,16 (q, J = 7,3 Hz, 3H).
Etapa 3. (S)-1-(3-(4-(Quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona hidrocloruro.
A solución de (S)-1-(3-(4-bromofenoxi)pirrolidin-1-il)propan-1-ona (300 mg, 1,0 mmol) en 1,4 dioxano:agua (9ml:3ml) se añadió Na2CO3 (320 mg, 3 mmol), ácido quinolin-7-borónico (209 mg, 1,2 mmol) y se desgasificó con argón por 20min. A esto siguió la adición de tetraquis Pd (12 mg, 0,01 mmol) y la mezcla de reacción se calentó a 120 °C por 15 h. La mezcla de reacción se enfrió hasta la temperatura ambiente y se filtró almohadilla de Celite, el filtrado se diluyó etil-acetato y se lavó con agua. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El producto crudo se purificó por cromatografía de columna usando gel de sílice (2-3% MeOH/DCM) para dar base libre que se trató con 4M HCl en dioxano para dar (S)-1-(3-(4-(quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona HCl (110 mg, 32%) como un sólido pegajoso amarillo pálido. Análisis: LCMS (ESI): 347 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,22 (d, J = 5,0 Hz, 1H), 9,01 (d, J = 8,2 Hz, 1H), 8,46 (t, J = 2,5 Hz, 1H), 8,35 (d, J = 8,7 Hz, 1H), 8,23 (dd, J = 8,7, 1,8 Hz, 1H), 7,98-7,82 (m, 3H), 7,23-7,13 (m, 2H), 5,13 (m, 1H), 3,75-3,30 (m, 4H), 2,33-2,07 (m, 4H), 1,23 (d, J = 3,6 Hz, 3H).
E je m p lo 343. (S ) -1 -(3 -(4 -(Q u in o lin -3 - i l ) fe n o x i)p ir ro l id in -1 - i l)p ro p a n -1 -o n a , H C l.
Este ejemplo se sintetizó usando el método del ejemplo 341, usando ácido quinolin-3-borónico en Etapa 3.
Análisis: mp 60 °C; LCMS (ESI): 347 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,67-9,61 (m, 1H), 9,45-9,39 (m, 1H), 8,44 (d, J = 8,5 Hz, 1H), 8,38-8,31 (m, 1H), 8,1-808 (m, 1H), 8,04-7,90 (m, 3H), 7,25-7,15 (m, 2H), 5,16 (m, 1H), 3,69 3,49 (m, 3H), 3,43-3,30 (m, 1H), 2,35-2,02 (m, 4H), 1,13-0,93 (m, 3H).
Los siguientes ejemplos se prepararon por analogía con Ejemplos 342 y 343, usando (S)-3-hidroxipirrolidina en Etapa 1.
Ejemplo 344 (R)-1-(3-(4-(Quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona, HCl.
Análisis: mp 53 °C; LCMS (ESI): 347 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,99 (s, 1H), 8,83 (d, J = 7,4 Hz, 1H), 8,15 (s, 2H), 7,87-7,75 (m, 3H), 7,26 (s, 1H), 7,02 (d, J = 8,2 Hz, 2H), 5,06 (s, 1H), 3,81-3,60 (m, 4H), 2,40-2,31 (m, 3H), 2,23 (s, 1H), 1,28-1,15 (m, 3H).
Ejemplo 345. (R)-1-(3-(4-(quinolin-3-il)fenoxi)pirrolidin-1-il)propan-1-ona, HCl.
Análisis: mp 51 °C; LCMS (ESI): 347 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,26-9,20 (m, 1H), 8,62-8,54 (m, 1H), 8,03 (d, J = 8,4 Hz, 2H), 7,93-7,68 (m, 3H), 7,63 (t, J = 7,6 Hz, 1H), 7,20-7,09 (m, 2H), 5,12 (t, J = 3,3 Hz, 1H), 3,69 3,49 (m, 2H), 3,23 (d, J = 4,7 Hz, 2H), 2,33-2,03 (m, 4H), 0,99 (m, 3H).
Ejemplo 346. 1-(4-(4-(5-Metilquinolin-7-il)fenoxi)piperidin-1-il)propan-1-ona, HCl
Etapa 1. 5-Bromo-7-metilquinolina y 7-Bromo-5-metilquinolina.
A una mezcla de 3-bromo-5-metilanilina (2,0 g), glicerol (2,8 eq.) y sodio-3-nitrobencenosulfonato (1,8 eq.) en H2 O (16 ml), sulfúrico ácido conc. (16 ml) se añadió a 0 °C en forma de gotas. La mezcla de reacción se calentó a 140 °C por 4 días. La mezcla de reacción se enfrió hasta la temperatura ambiente y se vertió en hielo, luego se ajustó cuidadosamente para basificar f (f ~ 8) con 20% solución de NaOH ac. La mezcla luego se extrajo con acetato etilo (3X100 mL). Las capas orgánicas combinadas se secaron sobre Na2SO4 y la concentración dio el producto crudo que se purificó por HPLC preparativa para dar 5-bromo-7-metilquinolina (240 mg) y 7-bromo-5-metilquinolina (210 mg).
E ta p a 2. te rc -b u t il 4 -(4 -(5 -m e t i lq u in o lin -7 - i l) fe n o x i)p ip e r id in a -1 -c a rb o x i la to .
A una solución desgasificada de terc-butil éster del ácido 4-[4-(4,4,5,5-tetrametil-[1,3,2]dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (1 eq.), 5-Bromo-7-metilquinolina (1 eq.) y carbonato de sodio (2,6 eq.) en dioxano/agua (3:1), se añadió tetraquis-(trifenil-fosfino)paladio (13 mg, 0,012 mmol) y la mezcla de reacción se calentó a 100 °C por 15h cuando TLC confirmó el completamiento de la reacción. La reacción se filtró a través de un lecho de Celite y el filtrado se diluyó con acetato etilo y se lavó con agua. Las fases orgánicas combinadas se concentraron para obtener el producto crudo se purificó por cromatografía de columna usando gel de sílice y 30-40% EtOAc/hexano como eluyente para dar terc-butil 4-(4-(5-metilquinolin-7-il)fenoxi)piperidina-1-carboxilato (64%). Análisis: LCMS (ESI): 419 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,86 (d, J = 4,2 Hz, 1H), 8,15 (d, J = 8,6 Hz, 1H), 7,81 (s, 1H), 7,47-7,34 (m, 4H), 7,13 (d, J = 8,4 Hz, 2H), 4,64 (m, 1H), 3,75-3,61 (m, 2H), 3,21 (m, 2H), 2,55 (s, 3H), 1,97 (m, 2H), 1,64-1,50 (m, 2H), 1,41 (s, 9H).
Etapa 3. 5-Metil-7-(4-(piperidin-4-iloxi)fenil)quinolina.
A una solución de terc-butil 4-(4-(5-metilquinolin-7-il)fenoxi)piperidina-1-carboxilato (1 eq.) en DCM (20 mL) se añadió TFA (0,4 mL) a 0 °C, y la mezcla de reacción luego se agitó por 2 h a temperatura ambiente. Los volátiles se eliminaron a presión reducida. El residuo se trituró con éter para dar 5-metil-7-(4-(piperidin-4-iloxi)fenil)quinolina. Análisis: LCMS (ESI): 319 (M+1)
Etapa 4. 1-(4-(4-(5-Metilquinolin-7-il)fenoxi)piperidin-1-il)propan-1-ona, HCl.
A una solución de 5-metil-7-(4-(piperidin-4-iloxi)fenil)quinolina (1 eq.) en DCM (20 mL) se añadió a 0 °C, Et3N (3 eq.) y cloruro de propanoilo (1 eq.) y la mezcla de reacción se agitó por 3 h a temperatura ambiente. Después del completamiento de la reacción, la mezcla de reacción se diluyó con DCM y se lavó con agua. La capa orgánica se lavó con salmuera, se secó sobre Na2 SO4 , se filtró y se concentró. El producto crudo se purificó por cromatografía de columna usando gel de sílice y 2-3% MeOH/DCM como eluyente. La base libre purificada se convirtió a la sal de hidrocloruro mediante tratamiento con 4M HCl en dioxano, seguido por trituración en etil-acetato:hexano, filtración y secado al vacío para dar 1-(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)propan-1-ona HCl. Análisis: LCMS (ESI): 375 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,91 (d, J = 4,2 Hz, 1H), 8,45 (d, J = 8,4 Hz, 1H), 8,08 (s, 1H), 7,84-7,75 (m, 3H), 7,53 (m, 1H), 7,14 (d, J = 8,4 Hz, 2H), 4,71 (m, 1H), 3,95-3,84 (m, 1H), 3,77-3,66 (m, 1H), 3,37 (m, 1H), 3,26 (m, 1H), 2,73 (s, 3H), 2,35 (q, J = 7,4 Hz, 2H), 2,05-1,88 (m, 2H), 1,62 (m, 1H), 1,56 (m, 1H), 1,00 (t, J=7,4Hz, 3H).
Los siguientes ejemplos se prepararon por analogía con el Ejemplo 346, usando el bromuro de heteroarilo requerido en la Etapa b y cloruro ácido en Etapa d o con ácido (R)-tetrahidrofuran-2-carboxílico en presencia de EDCI y HOBT por Etapa 4.
Ejemplo 347. Ciclopropil(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)metanona, HCl.
Análisis: LCMS (ESI): 387 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,19 (d, J = 5,0 Hz, 1H), 9,03 (d, J = 8,4 Hz, 1H), 8,30 (s, 1H), 8,08 (s, 1H), 7,95-7,80 (m, 3H), 7,20 (d, J = 8,8 Hz, 2H), 4,77 (m, 1H), 3,99 (m, 1H), 3,89 (m, 1H), 3,59 (m, 1H), 3,34 (m, 1H), 2,82 (s, 3H), 2,03 (m, 3H), 1,66 (m, 1H), 1,54 (m, 1H), 0,72 (m, 4H).
Ejemplo 348. 1-(4-(4-(7-metilquinolin-5-il)fenoxi)piperidin-1-il)propan-1-ona HCl.
Análisis: LCMS (ESI): 375 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,23 (d, J = 5,2 Hz, 1H), 8,85 (d, J = 8,6 Hz, 1H), 8,14 (s, 1H), 7,94 (m, 1H), 7,74 (s, 1H), 7,46 (d, J = 8,4 Hz, 2H), 7,20 (d, J = 8,4 Hz, 2H), 4,75 (m, 1H), 3,91 (m, 1H),
3,78-3,65 (m, 1H), 3,44-3,21 (m, 2H), 2,67 (s, 3H), 2,36 (q, J = 7,4 Hz, 2H), 2,04-1,93 (m, 2H), 1,61 (m, 1H), 1,56 (m, 1H), 1,00 (t, J = 7,4 Hz, 3H).
Ejemplo 349. Cidopropil-{4-[4-(7-metil-quinolm-5-il)-fenoxi]-piperidm-1-il}-metanona, HCl
Análisis: LCMS (ESI): 387 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,19 (d, J = 5,0 Hz, 1H), 8,76 (d, J = 8,5 Hz, 1H), 8,08 (s, 1H), 7,87 (m, 1H), 7,69 (s, 1H), 7,48 (d, J = 8,4 Hz, 2H), 7,21 (d, J = 8,4 Hz, 2H), 4,77 (m, 1H), 4,01 (m, 1H), 3,91 (m, 1H), 3,60 (m, 1H), 3,31 (m, 1H), 2,66 (s, 3H), 2,09-1,94 (m, 3H), 1,68 (m, 1H), 1,57 (m, 1H), 0,79-0,66 (m, 4H).
Ejemplo 350. 1-(4-(4-(6-Metilquinolin-5-il)fenoxi)piperidin-1-il)propan-1-ona HCl.
Análisis: LCMS (ESI): 375 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,82 (d, J = 4,3 Hz, 1H), 7,95 (d, J = 8,6 Hz, 1H), 7,72 (m, 2H), 7,41 (m, 1H), 7,17 (d, J = 8,4 Hz, 2H), 7,14 (d, J = 8,4 Hz, 2H), 4,71 (m, 1H), 3,95 (m, 1H), 3,75 (m, 1H), 3,37 (m, 1H), 3,24 (m, 1H), 2,36 (q, J = 7,4 Hz, 2H), 2,24 (s, 3H), 2,02 (m, 2H), 1,66 (m, 1H), 1,55 (m, 1H), 0,99 (q, J = 7,4 Hz, 3H).
Ejemplo 351. Ciclopropil(4-(4-(6-metilquinolin-5-il)fenoxi)piperidin-1-il)metanona, HCl.
Análisis: LCMS (ESI): 387 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,14 (d, J = 4,9 Hz, 1H), 8,26 (m, 2H), 8,03 (d, J = 8,8 Hz, 1H), 7,82 (m, 1H), 7,25 (d, J = 8,4 Hz, 2H), 7,20 (d, J = 8,4 Hz, 2H), 4,75 (m, 1H), 4,03 (m, 1H), 3,95 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,32 (s, 3H), 2,08-1,96 (m, 3H), 1,69 (s, 1H), 1,58 (s, 1H), 0,73 (m, 4H).
Ejemplo 352. (R)-(4-(4-(5-Metilquinolin-7-il)fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona.
Análisis: LCMS (ESI): 417 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,91 (d, J = 4,2 Hz, 1H), 8,45 (m, 1H), 8,05 (s, 1H), 7,80 (m, 3H), 7,53 (m, 1H), 7,14 (d, J = 8,6 Hz, 2H), 4,77-4,65 (m, 2H), 3,78 (m, 4H), 3,51 (m, 1H), 3,30 (m, 1H), 2,73 (s, 3H), 2,13-1,75 (m, 6H), 1,65-1,49 (m, 2H).
E je m p lo 353. (R )-(4 -(4 -(7 -M e t i lq u in o l in -5 - i l) fe n o x i)p ip e r id in -1 - i l) ( te t ra h id ro fu ra n -2 - i l)m e ta n o n a .
Análisis: LCMS (ESI): 417 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,86 (d, J = 4,2 Hz, 1H), 8,15 (m, 1H), 7,82 (s, 1H), 7,48-7,35 (m, 4H), 7,15 (d, J=8,4 Hz, 2H), 4,77-4,65 (m, 2H), 3,96-3,69 (m, 4H), 3,51 (m, 1H), 3,21 (m, 1H), 2,56 (s, 3H), 2,13-1,74 (m, 6H), 1,73-1,51 (m, 2H).
Ejemplo 354. (R)-(4-(4-(6-Metilquinolin-5-il)fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona.
Análisis: LCMS (ESI): 417 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,82 (d, J=4,1 Hz, 1H), 7,96 (d, J=8,6 Hz, 1H), 7,76 7,68 (m, 2H), 7,41 (m, 1H), 7,18 (m, 4H), 4,71 (m, 2H), 4,01-3,70 (m, 4H), 3,50 (m, 1H), 3,21 (m, 1H), 2,25 (s, 3H), 2,12-2,01 (m, 4H), 1,95-1,76 (m, 2H), 1,72-1,52 (m, 2H).
Ejemplo 355. (±)-(7S,8aS)-7-(4-(8-Metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona
Etapa 1. 7-(4-Fluorofenil)-8-metilquinolina.
Una solución de 7-bromo-8-metilquinolina (1,0 g, 4,52 mmol), ácido 4-fluorofenil-borónico (0,74 g, 5,36 mmol) y Na2CO3 (1,62 g, 15,3 mmol) en 1,4-dioxano (20 mL) y agua (4 mL) se desgasificó con argón por 30 min tetraquis(trifenilfosfina)paladio(0) (0,26 g, 0,22 mmol) se añadió y mezcla de reacción se calentó a 100 °C por 15 h. La mezcla de reacción se enfrió hasta la temperatura ambiente y filtró a través de almohadilla de Celite, se lavó con etilacetato. Filtrado se lavó con agua y salmuera, se secó sobre Na2SO4, se filtró y se concentró. La purificación se llevó a cabo por cromatografía de columna para dar 7-(4-fluorofenil)-8-metilquinolina (0,99 g, 92%). Análisis: LCMS (ESI): 238 (M+1); 1H NMR (400 MHz, CDCls) 6: 9,00 (dd, J=4,2, 1,9 Hz, 1H), 8,17 (dd, J=8,2, 1,9 Hz, 1H), 7,71 (d, J=8,4 Hz, 1H), 7,41-7,39 (m, 4H), 7,22-7,11 (m, 2H), 2,74 (s, 3H).
Etapa 2. (±)-(7S,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona.
A una solución de (±)-(7S,8aS)-7-hidroxihexahidroindolizin-3(2H)-ona (0,25g, 1,61mmol) (preparada de acuerdo con Schoemaker, H. E. et al, Tetrahedron, 1978, 34, 163-172) en n Mp , enfriado a 0 °C, se añadió NaH (60% en aceite, 0,077 g, 1,93 mmol) y se agitó a 0 °C por 30 min. A esta solución 7-(4-fluorofenil)-8-metilquinolina (0,4 g, 1,69 mmol) en NMP se añadió en forma de gotas seguido por calentamiento a 100 °C por 12 h. La mezcla de reacción se apagó con agua y se extrajo con etil-acetato. La capa orgánica se lavó nuevamente con agua, salmuera, se secó sobre Na2SO4 y se concentró. El residuo se purificó por cromatografía de columna (sílice, 3-5% metanol en DCM para dar (±)-(7S,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona (0,11 g, 18%). -LCMS (ESI): 373 (M+1); 1H NMR (400 MHz, CDCLs) 6: 9,02-8,96 (m, 1H), 8,16 (dd, J = 8,3, 1,9 Hz, 1H), 7,70 (d, J = 8,4 Hz, 1H), 7,54-7,31 (m, 4H), 7,01 (dd, J = 8,6, 2,5 Hz, 2H), 4,45-4,41 (m, 1H), 4,29-4,27 (m, 1H), 3,69-3,57 (m, 1H), 2,87-2,72 (m, 4H), 2,45 (s, 3H), 2,3-2,28 (m, 2H), 1,78-1,56 (m, 2H), 1,45-1,42 (m, 1H).
Ejemplo 356. (±)-(7R,8aS)-7-(4-(8-Metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona
Etapa 1. 4-(8-Metilquinolin-7-il)-fenol.
Una solución de 7-bromo-8-metilquinolina (1,0 g, 4,52 mmol), ácido 4-hidroxifenilborónico (0,76 g, 5,41 mmol) y Na2CO3 (1,62 g, 15,3 mmol) en 1,4-dioxano (20 mL) y agua (4 mL) se desgasificó con argón por 30 min tetraquis(trifenilfosfina)-paladio(0) (0,26g, 0,22 mmol) se añadió y mezcla de reacción se calentó a 100 °C por 15 h. La mezcla de reacción se enfrió hasta la temperatura ambiente y filtró a través de almohadilla de Celite, se lavó con etil-acetato. Filtrado se lavó con agua y salmuera, se secó sobre Na2SO4, se filtró y se concentró. La purificación se llevó a cabo por cromatografía de columna para dar 4-(8-metilquinolin-7-il)-fenol (1,0 g, 93%). Análisis: LCMS (ESI): 236 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,57 (s, 1H), 8,96 (dd, J = 4,2, 1,8 Hz, 1H), 8,35 (dd, J = 8,2, 1,8 Hz, 1H), 7,83 (d, J = 8,4 Hz, 1H), 7,53 (dd, J = 8,2, 4,2 Hz, 1H), 7,45 (d, J = 8,4 Hz, 1H), 7,30-7,20 (m, 2H), 6,93-6,84 (m, 2H), 2,67 (s, 3H).
Etapa 2. (±)-(7R,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona
A una solución de (±)-(7S,8aS)-7-hidroxihexahidroindolizin-3(2H)-ona (0,4 g, 2,58 mmol) y 4-(8-metilquinolin-7-il)-fenol (0,63 g, 2,70 mmol) en THF, enfriada a 0 °C, se añadió trifenilfosfina (0,87 g, 3,35 mmol) y se agitó a 0 °C por 20 min. A esta solución se añadió di-terc-butil azodicarboxilato (0,77 g, 3,35 mmol) seguido por agitación a temperatura ambiente por 12h. La mezcla de reacción se concentró bajo presión reducida. El residuo se purificó por cromatografía de columna (sílice, 1-2% metanol en DCM) para dar (±)-(7R,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona (0,12 g, 13%). Análisis: LCMS (ESI): 373 (M+1); 1H NMR (400 MHz, CDCla) 6: 9,00 (dd, J = 4,1, 1,8Hz, 1H), 8,16 (d, J=8,1Hz, 1H), 7,70 (d, J=8,4Hz, 1H), 7,50-7,27 (m, 4H), 7,02 (dd, J=8,7, 3,0Hz, 2H), 4,83 (d, J=3,4Hz, 1H), 4,11-3,91 (m, 2H), 3,18-3,16 (m, 1H), 2,78 (s, 3H), 2,49-2,17 (m,4H), 2,14 (d, J = 14,3 Hz,1H), 1,76-1,56 (m,2H), 1,47 1,45 (m,1H).
Ejemplo 357. 2,2,2-Trifluoro-1-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-etanona
Etapa 1. t-butil éster del ácido 4-[4-(8-Metilquinolin-7-il)-fenoxi]-piperidina-1 -carboxílico.
terc-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (1,01 g, 2,51 mmol), 7-bromo-8-metilquinolina (0,556 g, 2,50 mmol), tetraquis(trifenilfosfina)paladio(0) (0,123 g, 0,106 mmol) y K2 CO3 (0,556 g, 4,02 mmol) se combinaron en agua (6,0 mL): 1,4-dioxano (24,0 mL). La mezcla se desgasificó brevemente al vacío luego se agitó a 80 °C bajo una atmósfera de nitrógeno durante toda la noche. La mezcla se enfrió, se particionó entre EtOAc (100 mL) y agua (20 mL) y las capas se separaron. La capa acuosa se extrajo con EtOAc (50 mL) y los compuestos orgánicos combinados se lavaron con salmuera (50 mL), se secaron sobre sodio sulfate y se filtraron a través de 2 mL gel de sílice. El filtrado se concentró al vacío para dar t-butil éster del ácido 4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidina-1-carboxílico.
Etapa 2. 8-Metil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina dihidrocloruro.
terc-butil éster del ácido 4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidina-1-carboxílico crudo se disolvió en metanol (10,0 mL, 247 mmol) y se añadió 4,0 M de HCl en 1,4-dioxano (3,00 mL, 12,0 mmol). Después de agitar durante toda la noche, la mezcla se diluyó con etil-acetato:hexanos (1:1, 60 mL) y los sólidos resultantes se recogieron por filtración, se lavaron con etil-acetato:hexanos (1:1, 10 mL) luego se secaron al vacío para dar 8-metil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina dihidrocloruro (0,830 g; 84,7%). Análisis: 1H NMR (400 MHz, DMSO-d6) 6: 8,94 - 9,34 (3 H, m), 8,62 -8,94 (1 H, m), 8,06 (1 H, d, J=8,5 Hz), 7,73 - 7,87 (1 H, m), 7,66 (1 H, d, J=8,3 Hz), 7,43 (2 H, d, J=8,8 Hz), 7,17 (2 H, d, J=8,8 Hz), 4,60 - 5,00 (1 H, m), 3,18-3,34 (2 H, m), 2,99-3,15 (2 H, m), 2,72 (3 H, s), 2,10-2,23 (2 H, m), 1,74-1,98 (2 H, m). Etapa 3. 2,2,2-Trifluoro-1-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-etanona.
Anhídrido trifluoroacético (67,7 uL, 0,479 mmol) se añadió a 8-metil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina 2HCl (0,125 g, 0,319 mmol) y DIPEA (0,250 mL, 1,44 mmol) en DMF (3,00 mL). Después de 2 h, la mezcla se concentró al vacío. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (24 g, 0-5% metanol:DCM) para dar 2,2,2-trifluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-etanona (92 mg, 69%) después de reconcentración a partir de éter. Análisis: LCMS (ESI): 415 (M+1); 1H Nm R (400 Mhz, DMSO-d6) ó: 8,97 (1 H, dd, J=4,3, 1,8 Hz), 8,37 (1 H, dd, J=8,3, 1,8 Hz), 7,86 (1 H, d, J=8,3 Hz), 7,55 (1H, dd, J=8,2, 4,1Hz), 7,48 (1H, d, J=8,5Hz), 7,39 (2H, d, J=7,6Hz), 7,13 (2H, d, J=7,4Hz), 4,68-4,84 (1H, m), 3,72-3,93 (2H, m), 3,47-3,66 (2H, m), 2,68 (3H, s), 1,99-2,15 (2H, m), 1,68-1,82 (2H, m); 19F NMR (377 MHz, DMSO-d6) ó -68,07 (3F, s).
Ejemplo 358. 2,2-Difluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Ácido 2,2-difluoropropiónico (0,0527 g, 0,479 mmol) en DMF (1,00 mL, 12,9 mmol) se añadió a 8-metil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina 2HCl (0,125 g, 0,319 mmol) y DIPEA (0,250 mL, 1,44 mmol) en DMF (3,0 mL), luego se trató con HATU (0,146 g, 0,37 mmol). Después de 2 h, la mezcla se concentró al vacío. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (24 g, 0-5% metanol:DCM) para dar 2,2-difluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona HCl (83 mg, 58%) después del tratamiento de las fracciones del producto se redisolvió en metanol con 2M HCl en éter, reconcentrando a partir de éter. Análisis: LCMS (ESI): 411 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,10 (1 H, dd, J=4,5, 1,5 Hz), 8,74 (1 H, br. s.), 8,03 (1 H, d, J=8,5 Hz), 7,79 (1 H, dd, J=7,4, 4,6 Hz), 7,64 (1 H, d, J=8,5 Hz), 7,41 (2 H, d, J=8,8 Hz), 7,15 (2 H, d, J=8,8 Hz), 4,74 - 4,84 (1 H, m), 3,89 (2 H, br. s.), 3,51 - 3,67 (1 H, m), 3,46 (1 H, t, J=9,3 Hz), 2,71 (3 H, s), 2,04 (2 H, br. s.), 1,83 (3 H, t, J=20,1 Hz), 1,61 - 1,76 (2 H, m); 19F NMR (377 MHz, DMSO-d6) ó -91,22 (d, J=27,2 Hz).
Ejemplo 359.2-Fluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Se preparó en analogía con el Ejemplo 358. Análisis: LCMS (ESI): 393 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,04 (1 H, dd, J=4,4, 1,4 Hz), 8,59 (1 H, d, J=6,5 Hz), 7,96 (1 H, d, J=8,3 Hz), 7,65 - 7,78 (1 H, m), 7,58 (1 H, d, J=8,5 Hz), 7,31 - 7,45 (2 H, m), 7,14 (2 H, d, J=8,8 Hz), 5,56 (1 H, dq, J=47,7, 6,5 Hz), 4,74 (1 H, d, J=3,3 Hz), 3,91 (2 H, m), 3,24-3,49 (2H, m), 2,69 (3H, s), 2,02 (2H, m), 1,64 (2H, m), 1,42 (3H, dd, J=24,9, 6,5Hz).
Ejemplo 360. {exo-3-[4-(8-Metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-(R)-tetrahidrofuran-2-il-metanona, HCl.
Etapa 1. terc-butil éster del ácido exo-3-[4-(8-Metil-quinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]octane-8-carboxílico.
exo-3-Hidroxi-8-aza-biciclo[3,2. ácido 1]octano-8-carboxílico terc-butil éster (379 mg, 1,67 mmol) y NaH, 60% de dispersión en aceite mineral (101 mg, 2,52 mmol) se combinaron en N-metilpirrolidinona (NMP) (4,00 mL). Después de 20 min, una solución de 7-(4-fluorofenil)-8-metil-quinolina (294 mg, 1,24 mmol) en NMP (1,5 mL) se añadió y la mezcla se calentó a 100 °C por 48h, a cuyo punto la conversión ha alcanzado ca. 50% como se determinó por LCMS. La mezcla se enfrió, diluyó con acetato etilo (75 mL) y hexanos (25 mL) luego se lavó con agua (3x10 mL) y salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró al vacío. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (40 g, 0-40% etil-acetato: hexano) para dar tercbutil éster del ácido exo-3-[4-(8-Metil-quinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]octano-8-carboxílico (0,192 g, 34,8%). Análisis: 1H NMR (400 MHz, metanol-d4) ó: 8,89 (dd, J=4,3, 2,0 Hz, 1 H) 8,32 (dd, J=8,3, 1,8 Hz, 1 H) 7,79 (d, J=8,5 Hz, 1 H) 7,51 (dd, J=8,3, 4,3 Hz, 1 H) 7,47 (d, J=8,3 Hz, 1 H) 7,32 (d, J=8,8 Hz, 2 H) 7,07 (d, J=8,8 Hz, 2 H) 4,86 - 4,95
(m, 1 H) 4,25 - 4,32 (m, 2 H) 2,68 (s, 3 H) 2,17 - 2,26 (m, 2 H) 2,01 - 2,08 (m, 2 H) 1,83 - 1,93 (m, 2 H) 1,66 - 1,79 (m, 2 H) 1,51 (s, 9 H).
Etapa 2. 7-{4-[exo-(8-Aza-biciclo[3,2,1]oct-3-il)oxi]-fenil}-8-metil-quinolina, 2HCL.
terc-butil éster del ácido exo-3-[4-(8-Metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]octano-8-carboxílico (0,192 g, 0,432 mmol) y 4,0 M de HCl en 1,4-dioxano (0,450 mL, 1,80 mmol) se combinaron en metanol (7,0 mL) y se agitaron a temperatura ambiente. Después de 22 h, la mezcla se concentró al vacío para dar 7-{4-[exo-(8-aza-biciclo[3,2,1]oct-3-il)oxi]-fenil}-8-metil-quinolina 2HCl (0,180 g, 99,8%).
Etapa 3. {exo-3-[4-(8-Metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-(R)-tetrahidrofuran-2-il-metanona, HCl.
7-{4-[exo-(8-Aza-biciclo[3,2,1]oct-3-il)oxi]-fenil}-8-metilquinolina 2HCl (90,0 mg, 0,216 mmol), ácido (R)-tetrahidrofuran-2-carboxílico (28,8 mg, 0,248 mmol) y D iPEA (0,225 mL, 1,29 mmol) se combinaron en DCM (3,0 mL) y se añadió HATU (102 mg, 0,270 mmol). Después de 2 h, la mezcla se diluyó con EtOAc (20 mL), se lavó con NaHCO3 sat. (5 mL) y salmuera (5 mL), se secó sobre Na2SO4, se filtró y se concentró al vacío. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (12 g, 10-70% etil-acetato: hexano) para dar la base libre purificada después de la concentración de fracciones del producto. La base libre se disolvió en metanol y se trató con 4M HCl en dioxano luego se concentró para dar {exo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-azabiciclo[3,2,1 ]oct-8-il}-(R)-tetrahidrofuran-2-il-metanona HCl (95 mg, 92%). Análisis: LCMS (ESI): 443 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,04 (d, J=3,0Hz, 1H) 8,50-8,68 (m, 1H) 7,96 (d, J=8,3Hz, 1H) 7,64-7,76 (m, 1H) 7,57 (d, J=8,5Hz, 1H) 7,37 (d, J=8,8Hz, 2H) 7,13 (d, J=8,5Hz,2H) 4,87-4,99 (m,1H) 4,46-4,63 (m,3H) 3,72-3,92 (m, 2H) 2,69 (s, 3H) 2,14-2,31 (m, 2H) 1,79-2,10 (m, 8H) 1,66-1,79 (m, 1H) 1,53-1,63 (m, 1H).
Ejemplo 361. 1-{exo-3-[4-(8-Metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-propan-1-ona HCl.
7-{4-[exo-(8-Aza-biciclo[3,2,1]oct-3-il)oxi]-fenil}-8-metilquinolina 2HCl (90,0 mg, 0,216 mmol), y DIPEA (0,225 mL, 1,29 mmol) se combinaron en DCM (3,0 mL) y se añadió cloruro de propanoilo (22,9 mg, 0,248 mmol). Después de 2 h, la mezcla se diluyó con acetato etilo (20 mL), se lavó con NaHCO3 sat. (5 mL) y salmuera (5 mL), se secó sobre Na2SO4, se filtró y se concentró al vacío. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (12 g, 10-60% etil-acetato:hexano) para dar la base libre purificada después de la concentración de fracciones del producto. La base libre se disolvió en metanol y se trató con 4M HCl en dioxano luego se concentró para dar 1-{exo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-propan-lona HCl (74 mg, 78%). Análisis: LCMS (ESI): 401 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,10 (d, J=3,3 Hz, 1 H) 8,68 - 8,84 (m, 1 H) 8,04 (d, J=8,5 Hz, 1 H) 7,75 - 7,86 (m, 1 H) 7,64 (d, J=8,3 Hz, 1 H) 7,38 (d, J=8,8 Hz, 2 H) 7,14 (d, J=8,8 Hz, 2 H) 4,93 - 4,98 (m, 1 H) 4,53 - 4,58 (m, 1H) 4,31-4,37 (m, 1H) 2,70 (s, 3H) 2,13-2,44 (m, 4H) 1,79-2,03 (m, 4H) 1,50-1,62 (m, 2H) 1,02 (t, J=7,4 Hz, 3H).
Ejemplo 362. {2-Metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, HCl.
Se preparó como una mezcla de cuatro diastereómeros, análogo al Ejemplo 360, usando terc-butil éster del ácido 4-hidroxi-2-metil-piperidina-1-carboxílico en Etapa 1. Análisis: LCMS (ESl): 443 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 - 9,16 (m, 1 H) 8,75 - 8,89 (m, 1 H) 8,02 - 8,15 (m, 1 H) 7,80 - 7,93 (m, 1 H) 7,64 - 7,73 (m, 1 H) 7,37 - 7,47 (m, 2 H) 7,07 - 7,19 (m, 2 H) 4,84 - 4,92 (m, 1 H) 4,57 - 4,76 (m, 2 H) 3,71 - 3,84 (m, 2 H) 2,66 - 2,76 (m, 9 H) 1,76 - 2,19 (m, 6 H) 1,13 - 1,47 (m, 3 H).
Ejemplo 363. 1-{2-Metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Se preparó como una mezcla de diastereómeros 1:1, análogo al Ejemplo 361, usando terc-butil éster del ácido 4-hidroxi-2-metil-piperidina-1-carboxílico y cloruro de propanoilo.
Análisis: LCMS (ESI): 389 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,01 - 9,12 (m, 1 H) 8,58 - 8,78 (m, 1 H) 7,94 - 8,08 (m, 1 H) 7,68 - 7,84 (m, 1 H) 7,56 - 7,67 (m, 1 H) 7,34 - 7,47 (m, 2 H) 7,06 - 7,18 (m, 2 H) 4,78 - 4,94 (m, 1 H) 4,30 -4,52 (m, 1 H) 3,64 - 3,73 (m, 1 H) 3,28 - 3,52 (m, 1 H) 2,67 - 2,73 (m, 3 H) 2,29 - 2,39 (m, 1 H) 1,87 - 2,22 (m, 2 H) 1,16 - 1,36 (m, 3 H) 0,95 - 1,07 (m, 3 H).
Ejemplo 364. 1-{2-Metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Se preparó como una mezcla de diastereómeros 1:9, enriquecida en el diastereómero más polar, análogo al Ejemplo 361, usando terc-butil éster del ácido 4-hidroxi-2-metil-piperidina-1-carboxílico y cloruro de propanoilo. Análisis: LCMS (ESI): 389 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,01 - 9,12 (m, 1 H) 8,58 - 8,78 (m, 1 H) 7,94 - 8,08 (m, 1 H) 7,68 -7,84 (m, 1 H) 7,56 - 7,67 (m, 1 H) 7,34 - 7,47 (m, 2 H) 7,06 - 7,18 (m, 2 H) 4,78 - 4,94 (m, 1 H) 4,30 - 4,52 (m, 1 H) 3,64 - 3,73 (m, 1 H) 3,28 - 3,52 (m, 1 H) 2,67 - 2,73 (m, 3 H) 2,29 - 2,39 (m, 1 H) 1,87 - 2,22 (m, 2 H) 1,16 - 1,36 (m, 3 H) 0,95 - 1,07 (m, 3 H).
Ejemplo 365. Ciclopropil-{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona HCl.
Se preparó como una mezcla racémica de diastereómeros, de manera análoga al Ejemplo 361, usando terc-butil éster del ácido 4-hidroxi-2-metil-piperidina-1-carboxílico y cloruro de ciclopropilcarbonilo. Análisis: LCMS (ESI): 401 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,00 - 9,10 (m, 1 H) 8,55 - 8,70 (m, 1 H) 7,92 - 8,05 (m, 1 H) 7,66 - 7,78 (m, 1 H) 7,56 - 7,67 (m, 1 H) 7,35 - 7,46 (m, 2 H) 7,06 - 7,19 (m, 2 H) 4,84 - 4,91 (m, 1 H) 4,57 - 4,69 (m, 1 H) 4,13 - 4,22 (m, 1 H) 3,63 - 3,75 (m, 1 H) 2,70 (s, 3 H) 1,68 - 2,27 (m, 5 H) 1,20 - 1,41 (m, 3 H) 0,64 - 0,82 (m, 4 H).
Ejemplo 366. {cis-3-Fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona HCl.
Etapa 1. t-butil éster del ácido cis-3-Fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidina-1-carboxílico.
Di-t-butil azodicarboxilato (0,405 g, 1,76 mmol) se añadió a una solución a -10 °C de 4-(8-metil-quinolin-7-il)-fenol (0,267 g, 1,13 mmol), t-butil éster del ácido trans-3-Fluoro-4-hidroxi-piperidina-1-carboxílico (0,387 g, 1,76 mmol), y
trifenilfosfina (0,461 g, 1,76 mmol) en THF (12,0 mL). La mezcla se dejó calentar lentamente en el baño de enfriamiento luego se agitó durante toda la noche bajo una atmósfera de nitrógeno. La mezcla se calentó a 60 °C por 24 h, resultando en una conversión significativa al producto. La mezcla se enfrió y se concentró al vacío en gel de sílice (5 g) y se purificó en gel de sílice (80 g, 5-35% etil-acetato:hexano) para dar terc-butil éster del ácido cis-3-fluoro-4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidina-1-carboxílico (0,409 g, 82,6%). Análisis: LCMS (ESI): 437 (M+1); 1H NMR (400 MHz, metanol-d4) ó 8,90 (dd, J=4,3, 1,8 Hz, 1 H) 8,32 (dd, J=8,2, 1,9 Hz, 1 H) 7,79 (d, J=8,5 Hz, 1 H) 7,52 (dd, J=8,3, 4,3 Hz, 1 H) 7,48 (d, J=8,3 Hz, 1 H) 7,35 (d, J=8,8 Hz, 2 H) 7,13 (d, J=8,5 Hz, 2 H) 4,59 - 4,75 (m, 1 H) 4,15 - 4,25 (m, 1 H) 3,92 - 4,03 (m, 1 H) 3,56 - 3,83 (m, 1 H) 3,34 - 3,44 (m, 1 H) 3,17 - 3,25 (m, 1 H) 2,69 (s, 3 H) 1,84 - 1,98 (m, 2 H) 1,45 (s, 9 H);
Etapa 2. 7-[4-(cis-3-Fluoropiperidin-4-iloxi)-fenil]-8-metilquinolina 2HCl.
t-butil éster del ácido cis-3-Fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidina-1-carboxílico (0,495 g, 1,13 mmol) y 4,0 M de HCl en 1,4-dioxano (3,0 mL, 12 mmol) se combinaron en metanol (10,0 mL) y se maduró a temperatura ambiente por 3 h. La mezcla se concentró al vacío para dar 7-[4-(cis-3-fluoro-piperidin-4-iloxi)-fenil]-8-metil-quinolina 2HCl (0,449 g, 96,7%). Análisis: 1H NMR (400 MHz, metanol-d4) ó 9,21 (d, J=8,3 Hz, 1 H) 9,17 (dd, J=5,5, 1,5 Hz, 1 H) 8,23 (d, J=8,5 Hz, 1 H) 8,11 (dd, J=8,2, 5,6 Hz, 1 H) 7,88 (d, J=8,5 Hz, 1 H) 7,47 (d, J=8,8 Hz, 2 H) 7,25 (d, J=8,8 Hz, 2 H) 5,15 - 5,35 (m, 1 H) 4,87 - 4,98 (m, 1 H) 3,69 - 3,86 (m, 1 H) 3,39 - 3,57 (m, 3 H) 2,78 (s, 3 H) 2,23 - 2,35 (m, 2 H); 19F NMR (377 MHz, metanol-d4) 8-192,91 (s, 1 F).
Etapa 3. {cis-3-Fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona HCl.
Ácido (R)-tetrahidrofuran-2-carboxílico (47,4 mg, 0,408 mmol) HATU (168 mg, 0,443 mmol) se combinaron en DCM (1,6 mL, 24,8 mmol) y se agitó por 30 min. se añadió luego una solución de 7-[4-(cis-3-fluoro-piperidin-4-iloxi)-fenil]-8-metil-quinolina 2HCl (148 mg, 0,362 mmol) y DIPEA (0,309 mL, 1,77 mmol) en DCM (4,8 mL). Después de agitar por 2h, la mezcla se diluyó con acetato etilo (15 mL) y NaHCO3 sat. ac. (7 mL). Las capas se separaron, la capa acuosa se extrajo con EtOAc (5 mL) y los compuestos orgánicos combinados se secaron sobre sulfato de sodio, se filtraron y se concentraron. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (24 g, 10-80% EtOAc:hexano) para dar {cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona HCl (0,131 g, 76,9%) como una mezcla de diastereómeros 1:1, R-THF con 3R,4S piperidina y R-THF con 3S,4R piperidina después del tratamiento de las fracciones del producto con 4,0 M de HCl en 1,4-dioxano (0,355 mL, 1,42 mmol) y reconcentración a partir de metanol. Análisis: Lc Ms (ESI): 435 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,06 - 9,17 (m, 1 H) 8,70 - 8,96 (m, 1 H) 7,99 - 8,11 (m, 1 H) 7,76 - 7,88 (m, 1 H) 7,61 - 7,70 (m, 1 H) 7,40 - 7,49 (m, 2 H) 7,14 - 7,27 (m, 2 H) 4,91 - 5,14 (m, 1 H) 4,79 - 4,90 (m, 1 H) 4,62 - 4,76 (m, 1 H) 3,93 -4,55 (m, 2 H) 3,59 - 3,84 (m, 3 H) 2,71 (s, 3 H) 1,93 - 2,11 (m, 3 H) 1,72 - 1,85 (m, 2H) 1,21 - 1,33 (m, 4H); 19F NMR (377 MHz, DMSO-d6) ó -69,2 (s, IF) y -71,1 (s, IF).
Los siguientes ejemplos se prepararon en analogía con cloruro de propanoilo o cloruro de ciclopropilcarbonilo en la Etapa c como se requirió y el derivado de N-Boc-piperidin-4-ol requerido.
Ejemplo 367. 1-{cis-3-Fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Análisis: LCMS (ESI): 393 (M+1); 1H NMR (400 MHz, DMSO-d6) ó: 9,02 - 9,10 (m, 1 H) 8,59 - 8,69 (m, 1 H) 7,95 - 8,03 (m, 1 H) 7,70 - 7,77 (m, 1 H) 7,55 - 7,64 (m, 1 H) 7,37 - 7,45 (m, 2 H) 7,13 - 7,22 (m, 2 H) 4,90 - 5,13 (m, 1 H) 4,77 -4,88 (m, 1 H) 4,47 - 4,54 (m, 1 H) 4,29 - 4,37 (m, 1 H) 4,09 - 4,19 (m, 1 H) 3,66 - 3,91 (m, 1 H) 3,42 - 3,57 (m, 1 H) 3,12 - 3,34 (m, 1 H) 2,28 - 2,43 (m, 2 H) 1,89 - 1,97 (m, 1 H) 0,95 - 1,06 (m, 3 H).
Ejemplo 368. Ciclopropil-{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
Análisis: LCMS (ESI): 405 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,00 - 9,10 (m, 1 H) 8,58 - 8,67 (m, 1 H) 7,98 (d, J=8,3 Hz, 1 H) 7,68 - 7,76 (m, 1 H) 7,59 (d, J=8,5 Hz, 1 H) 7,42 (d, J=8,8 Hz, 2 H) 7,19 (d, J=8,8 Hz, 2 H) 4,93 - 5,15 (m, 1 H) 4,78 - 4,90 (m, 1 H) 4,44 - 4,55 (m, 1 H) 4,21 - 4,35 (m, 1 H) 3,37 - 3,52 (m, 1 H) 2,70 (s, 3 H) 1,93 - 2,07 (m, 2 H) 1,66 - 1,81 (m, 1 H) 0,67 - 0,80 (m, 5 H).
Ejemplo 369. 1-{endo-3-[4-(8-Metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-propan-1-ona, HCl.
Análisis: A partir de terc-butil éster del ácido exo-3-Hidroxi-8-aza-biciclo[3,2,1]octano-8-carboxílico. LCMS (ESI): 401 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,09 (dd, J=4,5, 1,3 Hz, 1 H) 8,63 - 8,79 (m, 1 H) 8,02 (d, J=8,5 Hz, 1 H) 7,72 - 7,82 (m, 1 H) 7,64 (d, J=8,3 Hz, 1 H) 7,42 (d, J=8,8 Hz, 2 H) 7,04 (d, J=8,8 Hz, 2 H) 4,76 - 4,84 (m, 1 H) 4,47 - 4,53 (m, 1 H) 4,25 - 4,31 (m, 1H) 2,71 (s, 3H) 1,77 - 2,43 (m, 10H) 1,02 (t, J=7,4 Hz, 3H).
Ejemplo 370. Ciclopropil-{endo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo-[3,2,1]oct-8-il}-metanona, HCl.
Análisis: LCMS (ESI): 413 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,03 - 9,13 (m, 1 H) 8,61 - 8,78 (m, 1 H) 8,01 (d, J=8,5 Hz, 1 H) 7,71 - 7,82 (m, 1 H) 7,63 (d, J=8,5 Hz, 1 H) 7,42 (d, J=8,8 Hz, 2 H) 7,05 (d, J=8,8 Hz, 2 H) 4,79 - 4,85 (m, 1 H) 4,57 - 4,64 (m, 1 H) 4,44 - 4,49 (m, 1 H) 2,71 (s, 3 H) 2,02 - 2,30 (m, 6 H) 1,92 (d, J=7,8 Hz, 3 H) 1,49 - 1,57 (m, 1 H) 1,36 - 1,43 (m, 2 H) 0,70 - 0,80 (m, 2 H).
Ejemplo 371. {endo-3-[4-(8-Metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-(R)-tetrahidrofuran-2-il-met-anona, HCl.
Análisis: LCMS (ESI): 443 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,06 (d, J=2,8 Hz, 1 H) 8,65 (br. s., 1 H) 7,99 (d, J=8,8 Hz, 1 H) 7,70 - 7,80 (m, 1 H) 7,61 (d, J=8,3 Hz, 1 H) 7,41 (d, J=8,5 Hz, 2 H) 6,96 - 7,11 (m, 2 H) 4,77 - 4,85 (m, 1 H) 4,55 - 4,61 (m, 1 H) 4,48 - 4,52 (m, 1 H) 4,41 - 4,45 (m, 1 H) 3,72 - 3,84 (m, 2 H) 2,70 (s, 3 H) 2,09 - 2,25 (m, 3 H) 1,92 - 2,06 (m, 6 H) 1,74 - 1,90 (m, 3 H).
Ejemplo 372. {(trans)-3-Fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, HCl.
Análisis: a partir de t-butil éster del ácido cis-3-Fluoro-4-hidroxipiperidina-1-carboxílico como una mezcla de diastereómeros 1:1. LCMS (ESI): 435 (M+1); 1H NMR (400 MHz, DMSO-d6, 95 °C) 6: 8,92 - 9,01 (m, 1 H) 8,38 - 8,48 (m, 1 H) 7,86 (d, J=8,3 Hz, 1 H) 7,57 (dd, J=8,3, 4,3 Hz, 1 H) 7,48 (d, J=8,5 Hz, 1 H) 7,32 - 7,40 (m, 2 H) 7,12 - 7,20
(m, 2 H) 4,57 - 4,78 (m, 3 H) 3,99 - 4,17 (m, 1 H) 3,73 - 3,85 (m, 4 H) 3,37 - 3,50 (m, 1 H) 2,68 (s, 3 H) 1,97 - 2,17 (m, 3 H) 1,81 - 1,92 (m, 2 H) 1,64 - 1,76 (m, 1 H).
Ejemplo 373. 1-{trans-3-Fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Análisis: LCMS (ESI): 393 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,96 (dd, J=4,3, 1,8 Hz, 1 H) 8,37 (dd, J=8,3, 1,8 Hz, 1 H) 7,84 (d, J=8,3 Hz, 1 H) 7,54 (dd, J=8,3, 4,3 Hz, 1 H) 7,46 (d, J=8,5 Hz, 1 H) 7,36 (d, J=8,8 Hz, 2 H) 7,15 (d, J=8,8 Hz, 2 H) 4,58 - 4,79 (m, 2 H) 3,96 - 4,09 (m, 1 H) 3,64-3,74 (m, 2H) 3,54-3,62 (m, 1H) 3,40-3,49 (m, 1H) 2,67 (s, 3H) 2,32-2,41 (m, 2H) 2,08-2,16 (m, 1H) 1,64-1,77 (m, 1H) 1,04 (t, J=7,4Hz, 3H).
Ejemplo 374. Ciclopropil-{trans-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
Análisis: LCMS (ESI): 405 (M+1); 1H NMR (400 MHz, DMSO-d6, 95 °C) 6: 8,99 (dd, J=4,5, 1,8 Hz, 1 H) 8,44 (dd, J=8,3, 1,8 Hz, 1 H) 7,87 (d, J=8,5 Hz, 1 H) 7,59 (dd, J=8,2, 4,4 Hz, 1 H) 7,50 (d, J=8,3 Hz, 1 H) 7,37 (d, J=8,8 Hz, 2 H) 7,17 (d, J=8,8 Hz, 2 H) 4,70 - 4,79 (m, 2 H) 4,61 - 4,66 (m, 1 H) 4,06 - 4,21 (m, 1 H) 3,77 - 3,90 (m, 1 H) 3,63 - 3,77 (m, 1 H) 3,51 - 3,60 (m, 1 H) 2,69 (s, 3 H) 2,08-2,19 (m, 1 H) 1,92-2,03 (m, 1 H) 1,67-1,79 (m, 1 H) 0,67-0,81 (m, 7 H).
Ejemplo 375. 1-{3-Metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona, sal de TFA.
A partir de terc-butil éster del ácido 4-Hidroxi-3-metil-piperidina-1-carboxílico como una mezcla de diastereómeros. Análisis: LCMS (ESI): 389 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,99 - 9,06 (m, 1 H) 8,46 - 8,58 (m, 1 H) 7,88 - 7,98 (m, 1 H) 7,60 - 7,70 (m, 1 H) 7,51 - 7,60 (m, 1 H) 7,34 - 7,44 (m, 2 H) 7,08 - 7,20 (m, 2 H) 4,15 - 4,70 (m, 1 H) 2,91 -3,90 (m, 4 H) 2,69 (s, 3 H) 2,31-2,42 (m, 2H) 1,60-2,16 (m, 3H) 0,95-1,04 (m, 6H).
Ejemplo 376. Ciclopropil-{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona, sal de TFA.
Análisis: LCMS (ESI): 401 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,98 - 9,07 (1 H, m), 8,52 (1 H, d, J=7,8 Hz), 7,93 (1 H, d, J=8,3 Hz), 7,65 (1 H, dd, J=8,2, 4,4 Hz), 7,55 (1 H, d, J=8,5 Hz), 7,36 - 7,43 (2 H, m), 7,10 - 7,18 (2 H, m), 4,62
- 4,74 (1 H, m), 4,04 - 4,36 (1 H, m), 3,74 - 3,90 (1 H, m), 3,48 - 3,71 (1 H, m), 2,96 - 3,48 (1 H, m), 2,69 (3 H, s), 1,62 - 2,26 (4 H, m), 0,91 - 1,11 (3 H, m), 0,67 - 0,82 (4 H, m).
Ejemplo 377. {3-Metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, sal de TFA.
Análisis: LCMS (ESI): 431 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 8,96 - 9,08 (1 H, m), 8,47 - 8,60 (1 H, m), 7,86 -7,98 (1 H, m), 7,61 - 7,71 (1 H, m), 7,52 - 7,59 (1 H, m), 7,35 - 7,43 (2 H, m), 7,09 - 7,18 (2 H, m), 4,59 - 4,84 (2 H, m), 3,86 - 4,42 (1 H, m), 2,90 - 3,84 (5 H, m), 2,69 (3 H, s), 1,61 - 2,22 (7 H, m), 0,86 - 1,11 (3 H, m).
Ejemplo 378. 1-{4-[4-(6-Fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(6-Fenilpiridin-3-il)-fenoxi]-piperidina-1 -carboxílico.
A un frasco Schlenck se añadió t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol), 5-bromo-2-fenilpiridina (0,44 g, 1,86 mmol), tetraquis(trifenilfosfina)paladio(0) (0,14 g, 0,12 mmol), en carbonato de sodio (3,72 mL, 3,72 mmol), seguido por 1,4-dioxano (10 mL) y se desgasificó bajo una atmósfera de argón por 5 min y se calentó a 100 °C durante toda la noche. La reacción se enfrió, se filtró a través de una almohadilla de Celite, se lavó con en carbonato de sodio, agua, salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10-30% EtOAc/hexanos) y se concentró y se aisló (0,48 g, 90%). Análisis: LCMS m/z = 431 (M+1).
Etapa 2. 2-Fenil-5-[4-(piperidin-4-iloxi)-fenil]-piridina.
A una solución de t-butil éster del ácido 4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidina-1-carboxílico (0,48 g, 1,11 mmol) en DCM (10 mL) se añadió TFA (2 mL) en forma de gotas y se agitó a temperatura ambiente por 1 h y se concentró. La reacción se particionó entre DCM/1N Na2CO3, se lavó con agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se aisló como un sólido beige (0,37 g, 100%). LCMS m/z = 331 (M+1).
Etapa 3. A 2-fenil-5-[4-(piperidin-4-iloxi)-fenil]-piridina (94 mg, 0,28 mmol) en DCM (5 mL) se añadió TEA (1 mL, 7 mmol), seguido por cloruro de propanoilo (40 uL, 0,5 mmol) en forma de gotas y la reacción se agitó a temperatura ambiente por 1 h. La reacción se diluyó con DCM, se lavó con en Na2CO3, agua, y salmuera, se secó sobre Na2SO4, y se concentró. El producto se purificó usando la Gilson (0,1%TFA en agua/0,1%TFA en gradiente de acetonitrilo) y se colocó en el liofilizador durante toda la noche. 1-{4-[4-(6-Fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona TFA sal se aisló (0,07 g, 49%). Análisis: LCMS m/z = 387 (M+1). 1H NMR (DMSO-d6) 6: 8,97 (m, 1H), 8,14 (m, 3H), 8,05 (d, 1H, J = 8,3 Hz), 7,75 (d, 2H, J = 8,7 Hz), 7,53 (m, 2H), 7,45 (m, 1H), 7,14 (d, 2H, J = 8,8 Hz), 4,70 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,26 (m, 2H), 2,33 (m, 2H), 1,97 (m, 2H), 1,54 (m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 379. 2-Metil-1-{4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
A 2-fenil-5-[4-(piperidin-4-iloxi)-fenil]-piridina (94 mg, 0,28 mmol) en DCM (5 mL) se añadió trietilamina (1 mL, 7 mmol), seguido por cloruro de isobutirilo (50 uL, 0,5 mmol) en forma de gotas y la reacción se agitó a temperatura ambiente por 1 h y se concentró. La reacción se particionó entre DCM/1N carbonato de sodio, se lavó con agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (8%metanol/DCM) y se concentró. 2-Metil-1-{4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona se aisló como un sólido (0,07g, 57%). Análisis: LCMS m/z = 401 (M+1). 1H NMR (DMSO-d6) ó: 8,96 (m, 1H), 8,14 (m, 3H), 8,03 (d, 1H, J = 8,2 Hz), 7,72 (m, 2H), 7,51 (m, 2H), 7,44 (m, 1H), 7,14 (d, 2H, J = 8,8 Hz), 4,71 (m, 1H), 3,88 (m, 1H), 3,77 (m, 1H), 3,40 (m, 1H), 3,26 (m, 1H), 2,90 (m, 1H), 1,99 (m, 2H), 1,53 (m, 2H), 1,01 (d, 6H, J = 6,7 Hz).
Los siguientes ejemplos se sintetizaron usando el procedimiento para los ejemplos 378 y 379.
Ejemplo 380. Ciclopropil-{4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 399 (M+1). 1H NMR (DMSO-d6) ó: 8,96 (m, 1H), 8,14 (m, 3H), 8,03 (d, 1H, J = 8,2 Hz), 7,72 (m, 2H), 7,51 (m, 2H), 7,44 (m, 1H), 7,14 (d, 2H, J = 8,8 Hz), 4,72 (m, 1H), 4,07 (m, 1H), 3,98 (m, 1H), 3,55 (m, 1H), 3,29 (m, 1H), 2,00 (m, 3H), 1,54-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 381. Ciclobutil-{4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Análisis: LCMS m/z = 413 (M+1). 1H NMR (DMSO-d6) ó: 8,96 (m, 1H), 8,14 (m, 3H), 8,03 (d, 1H, J = 8,2 Hz), 7,72 (m, 2H), 7,51 (m, 2H), 7,44 (m, 1H), 7,14 (d, 2H, J = 8,8 Hz), 4,69 (m, 1H), 3,85 (m, 1H), 3,56 (m, 1H), 3,36 (m, 1H), 3,25 (m, 2H), 2,09 (m, 4H), 1,92 (m, 3H), 1,74 (m, 1H), 1,55 (m, 2H).
Ejemplo 382. 1-{4-[4-(5-Fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. terc-butil éster del ácido 4-[4-(5-Fenil-piridin-3-il)-fenoxi]-piperidina-1 -carboxílico
El compuesto se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-5-fenilpiridina (0,44 g, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,51 g, 96%). Análisis: LCMS m/z = 431 (M+1).
Etapa 2. 3-Fenil-5-[4-(piperidin-4-iloxi)-fenil]-piridina
El compuesto se preparó a partir de terc-butil éster del ácido 4-[4-(5-fenil-piridin-3-il)-fenoxi]-piperidina-1 -carboxílico (0,48 mg, 1,11 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,37 g, 100%). Análisis: LCMS m/z = 331 (M+1).
E tapa 3. 1 -{4 -[4 -(5 -F e n ilp ir id in -3 - il)- fe n o x i]-p ip e r id in -1 - il}-p ro p a n -1 -o n a
El compuesto se preparó a partir de 3-fenil-5-[4-(piperidin-4-iloxi)-fenil]-piridina (95 mg, 0,29 mmol) y cloruro de propanoilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 378 para dar un sólido (0,06 g, 54%). Análisis: LCMS m/z = 387 (M+1). 1H NMR (DMSO-d6) 6: 8,82 (m, 2H), 8,25 (m, 1H), 7,83 (m, 2H), 7,77 (m, 2H), 7,53 (m, 2H), 7,45 (m, 1H), 7,12 (m, 2H), 4,71 (m, 1H), 3,86 (m, 1H), 3,70 (m, 1H), 3,27 (m, 2H), 2,33 (m, 2H), 1,97 (m, 2H), 1,61 (m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 383. 2-Metil-1-{4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS m/z = 401 (M+1). 1H NMR (DMSO-d6) 6: 8,82 (m, 2H), 8,25 (m, 1H), 7,83 (m, 2H), 7,77 (m, 2H), 7,53 (m, 2H), 7,45 (m, 1H), 7,12 (m, 2H), 4,72 (m, 1H), 3,87 (m, 1H), 3,76 (m, 1H), 3,41 (m, 1H), 3,29 (m, 1H), 2,90 (m, 1H), 1,99 (m, 2H), 1,54 (m, 2H), 1,01 (d, 6H, J = 6,6 Hz).
Ejemplo 384. Ciclopropil-{4-[4-(5-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona, sal de TFA.
Análisis: LCMS m/z = 399 (M+1). 1H NMR (DMSO-d6) 6: 8,94 (m, 2H), 8,52 (m, 1H), 7,90 (m, 4H), 7,56 (m, 2H), 7,49 (m, 1H), 7,18 (m, 2H), 4,76 (m, 1H), 3,99 (m, 1H), 3,89 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (m, 3H), 1,55 (br m, 2H), 0,71 (m, 4H).
Ejemplo 385. Ciclobutil-{4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-metanona, sal de TFA.
Este ejemplo se sintetizó a partir de 3-fenil-5-[4-(piperidin-4-iloxi)-fenil]-piridina (95 mg, 0,29 mmol) y cloruro de ciclobutanocarbonilo (60 uL, 0,5 mmol) para dar un sólido (0,08 g, 50%). Análisis: LCMS m/z = 413 (M+1). 1H NMR (DMSO-d6) 6: 8,94 (m, 2H), 8,52 (m, 1H), 7,90 (m, 4H), 7,56 (m, 2H), 7,49 (m, 1H), 7,18 (m, 2H), 4,72 (m, 1H), 3,84 (m, 1H), 3,56 (m, 1H), 3,36 (m, 1H), 3,26 (m, 2H), 2,09 (br m, 4H), 1,93 (m, 3H), 1,74 (m, 1H), 1,56 (m, 2H).
Ejemplo 386. 1-{4-[4-(6-Morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(6-Morfolin-4-il-piridin-3-il)-fenoxi]-piperidina-1-carboxílico
El compuesto se preparó a partir de terc-butil éster del ácido 4-(4-yodofenoxi)-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 4-[5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-piridin-2-il]-morfolina (0,54 g, 1,86 mmol) como se describió previamente. El producto se aisló como un sólido (0,44 g, 81%). Análisis: LCMS m/z = 440 (M+1).
E tapa 2. 4 -{5 -[4 -(P ip e rid in -4 - ilo x i)- fe n il]-p ir id in -2 -il}-m o rfo lin a
El compuesto se preparó a partir de t-butil éster del ácido 4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidina-1-carboxílico (0,44 mg, 1,01 mmol) y TFA (2 mL). El producto se aisló como un sólido (0,34 g, 100%). Análisis: LCMS m/z = 340 (M+1).
Etapa 3. 1-{4-[4-(6-Morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona
El compuesto se preparó a partir de 4-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-morfolina (95 mg, 0,28 mmol) y cloruro de propanoilo (40 uL, 0,5 mmol). El producto se aisló como un sólido (0,04 g, 36%). Análisis: LC/MS 396 (M+H). 1H NMR (DMSO-d6) 6: 8,41 (d, 1H, J = 2,3 Hz), 7,81 (m, 1H), 7,54 (m, 2H), 7,03 (m, 2H), 6,90 (d, 1H, J = 8,8 Hz), 4,63 (m, 1H), 3,84 (m, 1H), 3,71 (m, 5H), 3,46 (m, 4H), 3,33 (m, 1H), 3,24 (m, 1H), 2,32 (m, 2H), 1,94 (m, 2H), 1,51 (m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 387. Ciclopropil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 4-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-morfolina (95 mg, 0,28 mmol) y cloruro de ciclopropanocarbonilo (40 mL, 0,5 mmol). El producto se aisló como un sólido (0,07 g, 61%). Análisis: LCMs m/z = 408 (M+1). 1H NMR (DMSO-d6) 6: 8,41 (d, 1H, J = 2,3 Hz), 7,81 (m, 1H), 7,54 (m, 2H), 7,03 (m, 2H), 6,90 (d, 1H, J = 8,8 Hz), 4,66 (m, 1H), 3,96 (m, 1H), 3,87 (m, 1H), 3,71 (m, 4H), 3,53 (m, 1H), 3,46 (m, 4H), 3,29 (m, 1H), 1,99 (m, 2H), 1,97 (m, 1H), 1,63 (m, 1H), 1,52 (m, 1H), 0,71 (m, 4H).
Ejemplo 388. Ciclobutil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Se sintetizó a partir de 4-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-morfolina (95 mg, 0,28 mmol) y cloruro de ciclobutanocarbonilo (50 uL, 0,5 mmol). El producto se aisló como un sólido (0,06 g, 51%). Análisis: LCMs m/z = 422 (M+1). 1H NMR (DMSO-d6) 6: 8,41 (d, 1H, J = 2,3 Hz), 7,81 (m, 1H), 7,54 (m, 2H), 7,03 (m, 2H), 6,90 (d, 1H, J = 8,8 Hz), 4,62 (m, 1H), 3,86 (m, 1H), 3,71 (m, 4H), 3,58 (m, 1H), 3,46 (m, 4H), 3,33 (m, 1H), 3,23 (m, 2H), 2,06-2,19 (br m, 4H), 1,90 (m, 3H), 1,74 (m, 1H), 1,49 (m, 2H).
Ejemplo 389. 1-{4-[4-(6-Fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(6-Fenoxi-piridin-3-il)-fenoxi]-piperidina-1-carboxílico
El compuesto se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 5-bromo-2-fenoxi-piridina (0,47 g, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,44 g, 80%). Análisis: LCMS m/z = 447 (M+1).
Etapa 2. 2-Fenoxi-5-[4-(piperidin-4-iloxi)-fenil]-piridina
El compuesto se preparó a partir de tertbutil éster del ácido 4-[4-(6-fenoxi-piridin-3-M)-fenoxi]-piperidina-1 -carboxílico (0,44 g, 0,99 mmol) y TFA (2 mL). El producto se aisló como un sólido (0,32 g, 95%). Análisis: Lc MS m/z = 347 (M+1).
Etapa 3. 1-{4-[4-(6-Fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona
El compuesto se preparó a partir de 2-fenoxi-5-[4-(piperidin-4-iloxi)-fenil]-piridina (95 mg, 0,27 mmol) y cloruro de propanoilo (40 uL, 0,5 mmol) para dar un sólido (0,07 g, 60%). Análisis: lCm S m/z = 403 (M+1). 1H NMR (DMSO-d6) ó: 8,40 (d, 1H, J = 2,2 Hz), 8,08 (m, 1H), 7,58 (m, 2H), 7,43 (m, 2H), 7,22 (m, 1H), 7,16 (m, 2H), 7,09 (m, 3H), 4,66 (m, 1H), 3,89 (m, 1H), 3,71 (m, 1H), 3,35 (m, 1H), 3,24 (m, 1H), 2,32 (m, 2H), 1,95 (m, 2H), 1,49-1,62 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 390. Ciclopropil-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 2-fenoxi-5-[4-(piperidin-4-iloxi)-fenil]-piridina (95 mg, 0,27 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,5 mmol) para dar un sólido (0,08 g, 70%). Análisis: LCMS m/z = 415 (M+1). 1H NMR (DMSO-d6) ó: 8,40 (d, 1H, J = 2,2 Hz), 8,08 (m, 1H), 7,58 (m, 2H), 7,43 (m, 2H), 7,22 (m, 1H), 7,16 (m, 2H), 7,09 (m, 3H), 4,70 (m, 1H), 3,97 (m, 1H), 3,87 (m, 1H), 3,54 (m, 1H), 3,26 (m, 1H), 1,91-2,02 (br m, 3H), 1,62 (m, 1H), 1,52 (m, 1H), 0,71 (m, 4H).
Ejemplo 391. Ciclobutil-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 2-fenoxi-5-[4-(piperidin-4-iloxi)-fenil]-piridina (95 mg, 0,27 mmol) y cloruro de ciclobutanocarbonilo (50 uL, 0,5 mmol) para dar un sólido (0,09 g, 72%). Análisis: LCMS m/z = 429 (M+1). 1H NMR (DMSO-d6) ó: 8,40 (d, 1H, J = 2,2 Hz), 8,08 (m, 1H), 7,58 (m, 2H), 7,43 (m, 2H), 7,22 (m, 1H), 7,16 (m, 2H), 7,09 (m, 3H), 4,65 (m, 1H), 3,87 (m, 1H), 3,55 (m, 1H), 3,35 (m, 1H), 3,23 (m, 2H), 2,06-2,19 (br m, 4H), 1,90 (br m, 3H), 1,74 (m, 1H), 1,53 (m, 2H).
Ejemplo 392. 1-{4-[4-(6-Fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, sal de TFA.
Etapa 1. t-butil éster del ácido 4-[4-(6-Fenilaminopiridin-3-il)-fenoxi]-piperidina-1-carboxílico
El compuesto se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y (5-bromo-piridin-2-il)-fenil-amina (0,46 g, 1,86 mmol) para dar un sólido. Análisis: LCMS m/z = 446 (M+1).
Etapa 2. Fenil-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-amina
El compuesto se preparó a partir de terc-butil éster del ácido 4-[4-(6-fenilamino-piridin-3-il)-fenoxi]-piperidina-1-carboxílico y ácido trifluoroacético (2 mL). El producto se aisló como un sólido. Análisis: LCMS m/z = 346 (M+1).
E tapa 3. 1 -{4 -[4 -(6 -F e n ila m in o p ir id in -3 - il) - fe n o x i]-p ip e r id in -1 - il}-p ro p a n -1 -o n a , sa l de T F A
El compuesto se preparó a partir de fenil-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-amina (95 mg, 0,27 mmol) y cloruro de propanoilo (40 uL, 0,5 mmol). El producto se aisló como un sólido (0,03 g, 21%). Análisis: LCMS m/z 402 (M+1).
1H NMR (DMSO-d6) 6: 9,55 (br s, 1H), 8,36 (d, 1H, J = 2,2 Hz), 7,99 (m, 1H), 7,59 (m, 4H), 7,34 (m, 2H), 7,08 (m, 4H), 4,66 (m, 1H), 3,85 (m, 1H), 3,71 (m, 1H), 3,25 (m, 2H), 2,33 (m, 2H), 1,95 (m, 2H), 1,47-1,64 (br m, 2H), 0,99 (t, 3H, J = 7,3 Hz).
Ejemplo 393. Ciclopropil-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-metanona, sal de TFA.
Se preparó a partir de fenil-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-amina (95 mg, 0,27 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,5 mmol) para dar un sólido (0,08 g, 55%). Análisis: LCMS m/z = 414 (M+1). 1H NMR (DMSO-d6) 6: 9,55 (br s, 1H), 8,36 (d, 1H, J = 2,2 Hz), 7,99 (m, 1H), 7,59 (m, 4H), 7,34 (m, 2H), 7,08 (m, 4H), 4,68 (m, 1H), 3,88-3,97 (br m, 2H), 3,54 (m, 1H), 3,27 (m, 1H), 1,91-2,02 (br m, 3H), 1,49-1,79 (br m, 2H), 1,01 (m, 4H). Ejemplo 394. Ciclobutil-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-metanona, sal de TFA.
Este ejemplo se sintetizó a partir de fenil-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-amina (95 mg, 0,27 mmol) y cloruro de ciclobutanocarbonilo (50 uL, 0,5 mmol) para dar un sólido (0,05 g, 34%). LCMS m/z = 428 (M+1). 1H Nm R (DMSO) 6: 9,55 (br s, 1H), 8,36 (d, 1H, J = 2,2 Hz), 7,99 (m, 1H), 7,59 (m, 4H), 7,34 (m, 2H), 7,08 (m, 4H), 4,64 (m, 1H), 3,84 (m, 1H), 3,58 (m, 1H), 3,35 (m, 1H), 3,21 (m, 2H), 2,05-2,19 (br m, 4H), 1,85-1,94 (br m, 3H), 1,74 (m, 1H), 1,53 (m, 2H).
Ejemplo 395. 1-[4-(2'-Fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona.
Etapa 1. A un frasco Schlenck se añadió ácido (3-bromo-2-fluorofenil)borónico (0,5 g, 2,28 mmol), 2-bromopiridina (0,32 mL, 3,43 mmol), tetraquis(trifenilfosfina)paladio(0) (0,26 g, 0,23 mmol), 1N Na2CO3 (6,9 mL, 6,86 mmol), seguido por 1,4-dioxano (10 mL) y se desgasificó bajo una atmósfera de argón por 5 min y se calentó a 100°C por 1 h. La reacción se enfrió, se filtró a través de una almohadilla de Celite, se lavó con en Na2CO3, agua y salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10%acetato de etilo/hexanos) y se concentró para dar 2-(3-bromo-2-fluoro-fenil)-piridina (0,54 g, 94%). Análisis: LCMS m/z = 253 (M+1).
Etapa 2. t-butil éster del ácido 4-(2'-Fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidina-1 -carboxílico se preparó a partir de terc-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 2-(3-bromo-2-fluoro-fenil)-piridina (0,54 g, 2,15 mmol) Análisis: Lc MS m/z = 449 (M+1).
Etapa 3. 2-[2-Fluoro-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina se preparó a partir de terc-butil éster del ácido 4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidina-1 -carboxílico y ácido trifluoroacético (2 mL) para dar un sólido. Análisis: LCMS m/z = 349(M+1).
Etapa 4. 1-[4-(2'-Fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona se preparó a partir de 2-[2-fluoro-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina (73 mg, 0,21 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol). El producto se aisló como un sólido (0,03 g, 35%). Análisis: LCMS m/z = 405 (M+H). 1H NMR (DMSO-d6) ó: 8,73 (m, 1H), 7,93 (m, 1H), 7,81 (m, 2H), 7,54 (m, 3H), 7,38 (m, 2H), 7,11 (d, 2H, J = 8,7 Hz), 4,69 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,34 (m, 1H), 3,25 (m, 1H), 2,35 (m, 2H), 1,97 (m, 2H), 1,54 (br m, 2H), 0,99 (t, 3H, J = 7,3 Hz).
Ejemplo 396. Ciclopropil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona.
A 2-[2-fluoro-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina (73 mg, 0,21 mmol) en DCM (4 mL) se añadió trietilamina (0,7 mL, 5 mmol), seguido por cloruro de ciclopropanocarbonilo (30 uL, 0,4 mmol) en forma de gotas y la reacción se agitó a temperatura ambiente por 1 h y se concentró. La reacción se particionó entre DCM y en Na2CO3, se lavó con agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó usando la Gilson (0,1%TFA en agua/0,1%TFA en gradiente de acetonitrilo), se diluyó en fracciones limpias con DCM, se lavó con en sodio carbonato/salmuera, se secó sobre sulfato de sodio, y se concentró para dar un sólido (0,03 g, 25%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) ó: 8,73 (m, 1H), 7,93 (m, 1H), 7,81 (m, 2H), 7,54 (m, 3H), 7,38 (m, 2H), 7,11 (d, 2H, J = 8,7 Hz), 4,71 (m, 1H), 3,99 (m, 1H), 3,89 (m, 1H), 3,55 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,54-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 397. 1-{4-[4-(5-Fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, TFA.
Etapa 1. t-butil éster del ácido 4-[4-(5-Fenoxipiridin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-(4-yodo-fenoxi)-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y ácido (5-fenoxi-3-piridil)borónico (0,4 g, 1,86 mmol). LCMS m/z = 447 (M+1).
Etapa 2. 3-Fenoxi-5-[4-(piperidin-4-iloxi)-fenil]-piridina se preparó a partir de t-butil éster del ácido 4-[4-(5-fenoxipiridin-3-il)-fenoxi]-piperidina-1-carboxílico y TFA (2 mL). Análisis: LCMS m/z = 347 (M+1).
Etapa 3. 1-{4-[4-(5-Fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; sal de TFA se preparó a partir de 3-fenoxi-5-[4-(p i pe ridin-4-il oxi)-fe n il]-p iridina (90 mg, 0,2 mmol) y cloruro de propanoilo (40 uL, 0,4 mmol) para dar un sólido (0,09 g, 70%). Análisis: LCMS m/z = 403 (M+1). 1H NMR (DMSO-d6) ó: 8,72 (br s, 1H), 8,34 (br s, 1H), 7,77 (m, 1H), 7,69 (m, 2H), 7,46 (m, 2H), 7,23 (m, 1H), 7,11 (m, 4H), 4,69 (m, 1H), 3,85 (m, 1H), 3,71 (m, 1H), 3,36 (m, 2H), 2,32 (m, 2H), 1,95 (m, 2H), 1,48-1,62 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 398. Ciclobutil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona, HCl.
A 2-[2-fluoro-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina (73 mg, 0,21 mmol) en DCM (4 mL) se añadió TEA (0,7 mL, 5 mmol), seguido por cloruro de ciclobutanocarbonilo (40 uL, 0,4 mmol) en forma de gotas y la reacción se agitó a temperatura ambiente por 1 h. La reacción se particionó entre DCM/1N Na2CO3, se lavó con agua/salmuera, se secó sobre Na2SO4, y se concentró. El producto se purificó usando Gilson (0,1%TFA en agua/0,1% TFA en gradiente de acetonitrilo), las fracciones limpias se diluyeron con DCM, se lavaron con en Na2CO3/agua/salmuera, se secaron sobre Na2SO4, y se concentraron. El compuesto se disolvió en DCM, 2M de HCl en éter de dietilo (105 uL, 0,21 mmol) se
añadió y se concentró, luego se secó bajo vacío a 65°C durante toda la noche para dar un sólido (0,03 g, 31%). Análisis: LCMS m/z = 431 (M+1). 1H NMR (DMSO-d6) ó: 8,79 (m, 1H), 8,07 (m, 1H), 7,92 (m, 1H), 7,80 (m, 1H), 7,57 (m, 4H), 7,41 (m, 1H), 7,11 (m, 2H), 4,68 (m, 1H), 3,89 (m, 1H), 3,56 (m, 1H), 3,36 (m, 1H), 3,24 (m, 2H), 2,05-2,22 (br m, 4H), 1,92 (br m, 3H), 1,74 (m, 1H), 1,55 (m, 2H).
Ejemplo 399. Ciclopropil-{4-[4-(5-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
El compuesto se preparó a partir de 3-fenoxi-5-[4-(piperidin-4-iloxi)-fenil]-piridina (90 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol). El producto se aisló como un sólido (0,05g, 40%). Análisis: LCMS m/z = 415 (M+1). 1H NMR (DMSO-d6) ó: 8,73 (m, 1H), 8,34 (d, 1H, J = 2,2 Hz), 7,81 (m, 1H), 7,70 (m, 2H), 7,45 (m, 2H), 7,22 (m, 1H), 7,16 (m, 4H), 4,72 (m, 1H), 3,97 (m, 1H), 3,87 (m, 1H), 3,54 (m, 1H), 3,26 (m, 1H), 1,90-2,02 (br m, 3H), 1,62 (br m, 2H), 0,70 (m, 4H).
Ejemplo 400. Ciclobutil-{4-[4-(5-fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
Este ejemplo se preparó a partir de 3-fenoxi-5-[4-(piperidin-4-iloxi)-fenil]-piridina (90 mg, 0,2 mmol) y cloruro de ciclobutanocarbonilo (50 uL, 0,4 mmol) para dar un sólido (0,04g, 30%). Análisis: Lc MS m/z = 429 (M+1). 1H NMR (DMSO-d6) ó: 8,74 (d, 1H, J = 1,7 Hz), 8,35 (d, 1H, J = 2,5 H), 7,83 (m, 1H), 7,70 (m, 2H), 7,47 (m, 2H), 7,24 (m, 1H), 7,16 (m, 2H), 7,09 (m, 2H), 4,68 (m, 1H), 3,85 (m, 1H), 3,58 (m, 1H), 3,35 (m, 1H), 3,23 (m, 2H), 2,04-2,21 (br m, 4H), 1,92 (br m, 3H), 1,74 (m, 1H), 1,51 (m, 2H).
Ejemplo 401.1-{4-[4-(5-Fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, sal de TFA.
Etapa 1. t-butil éster del ácido 4-[4-(5-Bromopiridin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-(4-yodofenoxi)-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y ácido (5-bromo-3-piridil)borónico (0,38 g, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,14 g, 25%). Análisis: LCMS m/z = 434 (M+1).
Etapa 2. Un frasco Schlenck secado en un horno bajo una atmósfera de argón se cargó con ácido 4-[4-(5-bromopiridin-3-il)-fenoxi]-piperidina-1-carboxílico t-butil éster (0,14 g, 0,31 mmol), anilina (0,04 mL, 0,47 mmol), tris(dibencilidenoacetona)dipaladio(0) (28 mg, 0,02 mmol), 9,9-dimetil-4,5-bis(difenilfosfino)xanteno (36 mg, 0,06 mmol), sodio t-butóxido (90 mg, 0,94 mmol), seguido por 1,4-dioxano (5 mL) y la reacción se desgasificó 3 veces bajo una atmósfera de argón y se calentó a 100 °C por 2 h. La mezcla se enfrió, se filtró a través de una almohadilla de Celite, se lavó con DCM, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10-30% EtOAc/hexanos) y se concentró. t-butil éster del ácido 4-[4-(5-Fenilamino-piridin-3-il)-fenoxi]-piperidina-1-carboxílico se aisló (0,12 g, 88%). Análisis: LCMS m/z = 446 (M+1).
Etapa 3. Fenil-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-3-il}-amina se preparó a partir de t-butil éster del ácido 4-[4-(5-fenilamino-piridin-3-il)-fenoxi]-piperidina-1 -carboxílico (0,12 g, 0,27 mmol) y t Fa (1 mL) de manera análoga al Ejemplo 599b. El producto se aisló como un sólido (0,07 g, 75%). Análisis: LCMS m/z = 346 (M+1).
Etapa 4. El producto se preparó a partir de fenil-{5-[4-(piperidin-4-iloxi)-fenil]-piridin-3-il}-amina (71 mg, 0,20 mmol) y cloruro de propanoilo (21 uL, 0,25 mmol) de manera análoga al Ejemplo 599c. El producto se aisló como un sólido (0,04 g, 33%). Análisis: LCMS m/z = 402 (M+1). 1H NMR (DMSO-d6) ó: 9,00 (s, 1H), 8,45 (d, 1H, J = 1 Hz), 8,32 (d, 1H, J = 2,1 Hz), 7,95 (m, 1H), 7,66 (m, 2H), 7,39 (m, 2H), 7,27 (m, 2H), 7,15 (m, 2H), 7,05 (m, 1H), 4,71 (m, 1H), 3,87 (m, 1H), 3,72 (m, 1H), 3,36 (m, 1H), 3,25 (m, 1H), 2,33 (m, 2H), 1,91-1,97 (br m, 2H), 1,50-1,63 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 402. 1-{4-[4-(2-Fenilpiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona, TFA.
Etapa 1. terc-butil éster del ácido 4-[4-(2-Bromopiridin-4-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de tercbutil éster del ácido 4-(4-yodo-fenoxi)-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y ácido (2-bromo-4-piridil)borónico (0,38 g, 1,86 mmol). El producto se aisló como un sólido (0,19 g, 36%). Análisis: LCm S m/z 434 (M+1).
Etapa 2. terc-butil éster del ácido 4-[4-(2-Fenilpiridin-4-il)-fenoxi]-piperidina-1 -carboxílico se preparó a partir de tercbutil éster del ácido 4-[4-(2-bromopiridin-4-il)-fenoxi]-piperidina-1-carboxílico (0,19 g, 0,44 mmol) y ácido fenilborónico (81 mg, 0,67 mmol). El producto se aisló como un sólido. Análisis: LCMS m/z = 431 (M+1).
Etapa 3. 2-Fenil-4-[4-(piperidin-4-iloxi)-fenil]-piridina se preparó a partir de terc-butil éster del ácido 4-[4-(2-fenilpiridin-4-il)-fenoxi]-piperidina-1-carboxílico y TFA (1 mL). El producto se aisló como un sólido. Análisis: LCMS m/z = 331 (M+1).
Etapa 4. El producto del título se preparó a partir de 2-fenil-4-[4-(piperidin-4-iloxi)-fenil]-piridina (56 mg, 0,17 mmol) y cloruro de propanoilo (29 uL, 0,34 mmol). El producto se aisló como un sólido (0,05 g, 59%). Análisis: LCMS m/z 387 (M+1). 1H NMR (DMSO-d6) ó: 8,74 (d, 1H, J = 5,6 Hz), 8,33 (s, 1H), 8,15 (m, 2H), 7,98 (m, 2H), 7,87 (d, 1H, J = 4,4 Hz), 7,56 (m, 3H), 7,19 (m, 2H), 4,77 (m, 1H), 3,87 (m, 1H), 3,72 (m, 1H), 3,24-3,38 (m, 2H), 2,33 (m, 2H), 1,98 (m, 2H), 1,53-1,65 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 403. Ciclopropil-{4-[4-(2-fenilpiridin-4-il)-fenoxi]-piperidin-1-il}-metanona, sal de TFA.
Este ejemplo se preparó a partir de 2-fenil-4-[4-(piperidin-4-iloxi)-fenil]-piridina (56 mg, 0,17 mmol) y cloruro de ciclopropanocarbonilo (31 uL, 0,34 mmol). El producto se aisló como un sólido (0,35 g, 40%). Análisis: LCMS m/z = 399 (M+1). 1H NMR (DMSO-d6) ó: 8,74 (d, 1H, J = 5,6 Hz), 8,33 (s, 1H), 8,15 (m, 2H), 7,98 (m, 2H), 7,87 (d, 1H, J = 4,4 Hz), 7,56 (m, 3H), 7,19 (m, 2H), 4,79 (m, 1H), 3,89-3,98 (br m, 2H), 3,57 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,50-1,79 (br m, 2H), 0,71 (m, 4H).
Ejemplo 404. 1-{4-[4-(2-Fenilaminopiridin-4-il)-fenoxi]-piperidin-l-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(2-Cloropiridin-4-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-(4-yodofenoxi)-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y ácido 2-cloropiridina-4-borónico (0,29 g, 1,86 mmol). El producto se aisló como un sólido (0,24 g, 49%). Análisis: lCm S m/z 389 (M+1).
Etapa 2. terc-butil éster del ácido 4-[4-(2-Fenilaminopiridin-4-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de terc-butil éster del ácido 4-[4-(2-cloro-piridin-4-il)-fenoxi]-piperidina-1 -carboxílico (0,24 g, 0,61 mmol) y anilina (0,08 mL, 0,91 mmol) de manera análoga al Ejemplo 402, Etapa 2. El producto se aisló como un sólido (0,19 g, 69%). Análisis: LCMS m/z 446 (M+1).
Etapa 3. Fenil-{4-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-amina se preparó a partir de terc-butil éster del ácido 4-[4-(2-fenilaminopiridin-4-il)-fenoxi]-piperidina-1-carboxílico (0,19 g, 0,42 mmol) y ácido trifluoroacético (1 mL). El producto se aisló como un sólido (0,14 g, 100%). Análisis: LCMS m/z 346 (M+1).
Etapa 4. El producto del título se preparó a partir de fenil-{4-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-amina (73 mg, 0,21 mmol) y cloruro de propanoilo (28 uL, 0,32 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,03 g, 35%). Análisis: LCMS m/z = 402 (M+1). 1H NMR (DMSO-d6) ó: 9,04 (s, 1H), 8,17 (d, 1H, J = 5,4 Hz), 7,70 (d, 2H, J = 7,6 Hz), 7,65 (d, 2H, J = 8,8 Hz), 7,26 (m, 2H), 7,13 (d, 2H, J = 8,8 Hz), 7,02 (m, 2H), 6,88 (m, 1H), 4,69 (m, 1H), 3,88 (m, 1H), 3,70 (m, 1H), 3,37 (m, 1H), 3,25 (m, 1H), 2,33 (m, 2H), 1,96 (br m, 2H), 1,50-1,63 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 405. Ciclopropil-{4-[4-(2-fenilaminopiridin-4-il)-fenoxi|-piperidin-1-il}-metanona.
Este ejemplo se preparó a partir de fenil-{4-[4-(piperidin-4-iloxi)-fenil]-piridin-2-il}-amina (73 mg, 0,21 mmol) y cloruro de ciclopropanocarbonilo (29 uL, 0,32 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,04 g, 40%). Análisis: LCMS m/z = 414 (M+1). 1H NMR (DMSO-d6) ó: 9,04 (s, 1H), 8,17 (d, 1H, J = 5,4 Hz), 7,70 (d, 2H, J = 7,6 Hz), 7,65 (d, 2H, J = 8,8 Hz), 7,26 (m, 2H), 7,13 (d, 2H, J = 8,8 Hz), 7,02 (m, 2H), 6,88 (m, 1H), 4,72 (m, 1H), 3,98 (m, 1H), 3,89 (m, 1H), 3,55 (m, 1H), 3,29 (m, 1H), 1,94-2,03 (br m, 3H), 1,54-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 406. 1-[4-(2'-Metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona; sal de TFA.
Etapa 1.2-(3-Bromo-2-metilfenil)-piridina se preparó a partir de ácido 3-bromo-2-metil-fenilborónico (0,5 g, 2,33 mmol) y 2-bromopiridina (0,33 mL, 3,49 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,5 g, 87%). Análisis: LCMS m/z 249 (M+1).
Etapa 2. terc-butil éster del ácido 4-(2'-Metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidina-1 -carboxílico se preparó a partir de terc-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 2-(3-bromo-2-metil-fenil)-piridina (0,46 g, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,5 g, 89%). Análisis: Lc Ms m/z 445 (M+1).
Etapa 3. 2-[2-Metil-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina se preparó a partir de terc-butil éster del ácido 4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidina-1-carboxílico (0,5 g, 1,11 mmol) y t Fa (2 mL) de manera análoga al Ejemplo 378, Etapa 2. El producto se aisló como un sólido (0,3 g, 87%). Análisis: LCMS m/z 345 (M+1).
Etapa 4. El producto del título se preparó a partir de 2-[2-metil-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina (110 mg, 0,32 mmol) y cloruro de propanoilo (50 uL, 0,5 mmol) de manera análoga al Ejemplo 378 Etapa 3. El producto se aisló como un sólido (0,07 g, 40%). Análisis: LCMS m/z = 401 (M+1). 1H NMR (DMSO-d6) ó: 8,78 (d, 1H, J = 4,5 Hz), 8,17 (m, 1H), 7,78 (d, 1H, J = 7,8 Hz), 7,63 (m, 1H), 7,39 (m, 2H), 7,30 (m, 3H), 7,08 (d, 2H, J = 8,6 Hz), 4,66 (m, 1H), 3,90 (m, 1H), 3,71 (m, 1H), 3,33 (m, 1H), 3,24 (m, 1H), 2,33 (m, 2H), 2,12 (s, 3H), 1,96 (m, 2H), 1,51-1,63 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
E je m p lo 407. C ic lo p ro p il-[4 -(2 '-m e til-3 '-p ir id in -2 - il-b ife n il-4 - ilo x i)-p ip e r id in -1 - il]-m e ta n o n a , sal de TFA.
El compuesto del título se preparó a partir de 2-[2-metil-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina (110 mg, 0,32 mmol) y cloruro de ciclopropanocarbonilo (50 pL, 0,5 mmol) de manera análoga al Ejemplo 378 Etapa 3. El producto se aisló como un sólido (0,14 g, 80%). Análisis: LCMS m/z = 413 (M+1). 1H NMR (DMSO-d6) 6: 8,78 (d, 1H, J = 4,5 Hz), 8,17 (m, 1H), 7,78 (d, 1H, J = 7,8 Hz), 7,63 (m, 1H), 7,39 (m, 2H), 7,30 (m, 3H), 7,08 (d, 2H, J = 8,6 Hz), 4,68 (m, 1H), 3,99 (m, 1H), 3,90 (m, 1H), 3,54 (m, 1H), 3,26 (m, 1H), 2,12 (s, 3H), 2,00 (br m, 3H), 1,54-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 408. Ciclobutil-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona, sal de TFA.
El compuesto del título se preparó a partir de 2-[2-metil-4'-(piperidin-4-iloxi)-bifenil-3-il]-piridina (110 mg, 0,32 mmol) y cloruro de ciclobutanocarbonilo (60 uL, 0,5 mmol) de manera análoga al Ejemplo 378 Etapa 3. El producto se aisló como un sólido (0,08 g, 43%). Análisis: LCMS m/z = 427 (M+1). 1H NMR (DMSO-d6) 6: 8,78 (d, 1H, J = 4,5 Hz), 8,17 (m, 1H), 7,78 (d, 1H, J = 7,8 Hz), 7,63 (m, 1H), 7,39 (m, 2H), 7,30 (m, 3H), 7,08 (d, 2H, J = 8,6 Hz), 4,65 (m, 1H), 3,90 (m, 1H), 3,57 (m, 1H), 3,36 (m, 1H), 3,23 (m, 2H), 2,15 (m, 2H), 2,11 (s, 3H), 2,09 (m, 2H), 1,93 (m, 3H), 1,74 (m, 1H), 1,53 (m, 2H).
Ejemplo 409. 1-{4-[4-(2-Fenoxipiridin-4-il)-fenoxi]-piperidin-il}-propan-1-ona.
Etapa 1. terc-butil éster del ácido 4-[4-(2-Fluoropiridin-4-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-(4-yodofenoxi)-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y ácido 2-fluoropiridina-4-borónico (0,26 g, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,2 g, 44%). Análisis: LCMS m/z 373 (M+1).
Etapa 2. 2-Fluoro-4-[4-(piperidin-4-iloxi)-fenil]-piridina se preparó a partir de terc-butil éster del ácido 4-[4-(2-fluoropiridin-4-il)-fenoxi]-piperidina-1-carboxílico (0,2 g, 0,55 mmol) y ácido trifluoroacético (1 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,15 g, 98%). Análisis: LCMS m/z 273 (M+1).
Etapa 3. A fenol (59 mg, 0,63 mmol) en DMF (5 mL) a 0 °C se añadió NaH, 60% disp. en aceite mineral (65 mg, 1,62 mmol). Después de agitar 0,5 h a temperatura ambiente, 1-{4-[4-(2-fluoropiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona (0,17 g, 0,52 mmol) se añadió en forma de gotas en DMF (2 mL) y la reacción se agitó a 100 °C durante toda la noche. La reacción se diluyó con EtOAc, se lavó con agua/salmuera, se secó sobre Na2SO4, y se concentró. El producto se purificó usando Gilson (0,1%TFA en agua/0,1%TFA en gradiente de acetonitrilo). Las fracciones limpias se diluyeron con DCM, se lavaron con en Na2CO3/agua/salmuera, se secaron sobre Na2SO4, se concentraron, y se secaron bajo alto vacío a 50 °C durante toda la noche. 1-{4-[4-(2-fenoxi-piridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona se aisló como un sólido (0,05 g, 21%). Análisis: LCMS m/z = 403 (M+1). 1H NMR (DMSO-d6) 6: 8,15 (d, 1H, J = 5,3 Hz), 7,79 (m, 2H), 7,42 (m, 3H), 7,30 (s, 1H), 7,21 (m, 1H), 7,13 (m, 4H), 4,71 (m, 1H), 3,90 (m, 1H), 3,70 (m, 1H), 3,35 (m, 1H), 3,25 (m, 1H), 2,33 (m, 2H), 1,97 (br m, 2H), 1,50-1,62 (br m, 2H), 0,99 (t, 3H, J = 7,3 Hz).
E je m p lo 410. 1 -{4 -[4 -(4 -M e to x ip ira zo lo [1 ,5 -a ]p ir id in -6 - il) - fe n o x i]-p ip e r id in -1 - il}-p ro p a n -1 -o n a , HCl.
Etapa 1. 6-Bromopirazolo[1,5-a]piridin-4-ol (0,5 g, 2,35 mmol) en DMF (5 mL) bajo una atmósfera de nitrógeno se añadió carbonato de cesio (2,3 g, 7,04 mmol), seguido por yoduro de metilo (0,22 mL, 3,52 mmol) y la reacción se calentó a 80 °C por 1 h. La reacción se enfrió a temperatura ambiente, se diluyó con etil-acetato, se lavó con agua varias veces, se lavó con salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10%acetato de etilo/hexanos) y se concentró. 6-Bromo-4-metoxi-pirazolo[1,5-a]piridina se aisló como un sólido (0,43 g, 80%). Análisis: LCMS m/z = 228 (M+1).
Etapa 2. t-butil éster del ácido 4-[4-(4-Metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 6-bromo-4-metoxi-pirazolo-[1,5-a]piridina (0,42 g, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,4 g, 78%). Análisis: Lc MS m/z 424 (M+1).
Etapa 3. 4-Metoxi-6-[4-(piperidin-4-iloxi)-fenil]-pirazolo[1,5-a]piridina se preparó a partir de terc-butil éster del ácido 4-[4-(4-metoxi-pirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidina-1-carboxílico (0,4 g, 0,97 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,25 g, 79%). Análisis: LCMS m/z 324 (M+1).
Etapa 4. El compuesto del título se preparó a partir de 4-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-pirazolo[1,5-a]piridina (82 mg, 0,25 mmol) y cloruro de propanoilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,07 g, 62%). Análisis: LCMS m/z = 380 (M+1). 1H NMR (DMSO-d6) 6: 8,57 (s, 1H), 7,94 (d, 1H, J = 2.2 Hz), 7,73 (d, 2H, J = 8,7 Hz), 7,51 (br m, 1H), 7,10 (d, 2H, J = 8,8 Hz), 6,89 (s, 1H), 6,62 (m, 1H), 4,69 (m, 1H), 4.03 (s, 3H), 3,85 (m, 1H), 3,68 (m, 1H), 3,35 (br m, 2H), 2,33 (m, 2H), 1,96 (m, 2H), 1,51-1,63 (br m, 2H), 0,99 (t, 3H, J = 7,3 Hz).
Ejemplo 411. Ciclopropil-{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi|-piperidin-1-il}-metanona, HCl.
Este ejemplo se preparó a partir de 4-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-pirazolo[1,5-a]piridina (82 mg, 0,25 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,08 g, 72%). Análisis: LCMS m/z = 392 (M+1). 1H NMR (DMSO-d6) 6: 8,57 (s, 1H), 7,94 (d, 1H, J=2,2 Hz), 7,73 (d, 2H, J=8,7 Hz), 7,10 (d, 2H, J=8,8 Hz), 6,89 (s, 1H), 6,62 (m, 1H), 4,71 (m, 1H), 4,20 (br m, 1H), 4,02 (s, 3H), 3,97 (m, 1H), 3,87 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,54-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 412. Ciclobutil-{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
Este ejemplo se preparó a partir de 4-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-pirazolo[1,5-a]piridina (82 mg, 0,25 mmol) y cloruro de ciclobutanocarbonilo (50 uL, 0,4 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,04 g, 36%). Análisis: LCMS m/z = 406 (M+1). 1H NMR (DMSO-d6) 6: 8,57 (s, 1H), 7,94 (d, 1H, J = 2,2 Hz),
7,73 (d, 2H, J = 8,7 Hz), 7,10 (d, 2H, J = 8,8 Hz), 6,89 (s, 1H), 6,62 (m, 1H), 4,70 (m, 1H), 4,45 (br m, 1H), 4,02 (s, 3H), 3,88 (m, 1H), 3,59 (m, 1H), 3,36 (m, 1H), 3,26 (m, 2H), 2,07-2. 51 (br m, 7H), 1,74 (m, 1H), 1,55 (m, 2H).
Ejemplo 413. 1-{4-[4-(3-Cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(3-Cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 6-bromo-3-doro-isoquinolina (0,3 g, 1,24 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,47 g, 87%). Análisis: LCMS m/z 439 (M+1).
Etapa 2. 3-Cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir de terc-butil éster del ácido 4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,23 g, 0,52 mmol) y ácido trifluoroacético (1 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,15 g, 86%). Análisis: LCMS m/z 339 (M+1).
Etapa 3. El compuesto del título se preparó a partir de 3-cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (75 mg, 0,22 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,03 g, 34%). Análisis: LCMS m/z = 395 (M+1). 1H NMR (DMSO-d6) 6: 9,19 (s, 1H), 8,21 (m, 2H), 8,03 (m, 2H), 7,80 (m, 2H), 7,15 (m, 2H), 4,72 (m, 1H), 3,88 (m, 1H), 3,69 (m, 1H), 3,35 (m, 1H), 3,27 (m, 1H), 2,35 (m, 2H), 1,97 (br m, 2H), 1,52-1,64 (br m, 2H), 1,00 (t, 3H, J=7,3 Hz).
Ejemplo 414. {4-[4-(3-Cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona.
Este ejemplo se preparó a partir de 3-cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (75 mg, 0,22 mmol) y cloruro de ciclopropanocarbonilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,05 g, 56%). Análisis: LCMS m/z = 407 (M+1). 1H NMR (DMSO-d6) 6: 9,19 (s, 1H), 8,21 (m, 2H), 8,03 (m, 2H), 7,80 (m, 2H), 7,15 (m, 2H), 4,75 (m, 1H), 4,02 (m, 1H), 3,89 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,56-1,66 (br m, 2H), 0,71 (m, 4H).
Ejemplo 415. 1-{4-[4-(3-Metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(3-Metoxi-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de tbutil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,57 g, 1,40 mmol) y 6-bromo-3-metoxi-isoquinolina (0,5 g, 2,10 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,51 g, 84%). Análisis: LCMS m/z 435 (M+1).
Etapa 2. 3-Metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir de terc-butil éster del ácido 4-[4-(3-metoxi-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,51 g, 1,2 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,36 g, 91%). Análisis: LCMS m/z 335 (M+1).
Etapa 3. El compuesto del título se preparó a partir de 3-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (89 mg, 0,27 mmol) y cloruro de propanoilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 379. El producto se aisló como un sólido (0,06 g, 58%). Análisis: LCMS m/z = 391 (M+1). 1H NMR (DMSO-d6) 6: 9,04 (s, 1H), 8,04 (m, 2H), 7,95 (m, 3H),
7,20 (s, 1H), 7,14 (m, 2H), 4,71 (m, 1H), 3,95 (s, 3H), 3,87 (m, 1H), 3,69 (m, 1H), 3,35 (m, 1H), 3,26 (m, 1H), 2,35 (m, 2H), 1,98 (br m, 2H), 1,52-1,64 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 416. CidopropN-{4-[4-(3-metoxNsoquinolin-6-il)-fenoxi]-piperidin-1-N}-metanona.
Este ejemplo se sintetizó a partir de 3-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (89 mg, 0,27 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,08 g, 75%). Análisis: LCMS m/z = 403 (M+1). 1H NMR (DMSO-d6) 6: 9,04 (s, 1H), 8,04 (m, 2H), 7,75 (m, 3H), 7,20 (s, 1H), 7,14 (m, 2H), 4,73 (m, 1H), 4,00 (m, 1H), 3,95 (s, 3H), 3,90 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,65 (br m, 2H), 0,74 (m, 4H).
Ejemplo 417. Ciclobutil-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 3-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (89 mg, 0,27 mmol) y cloruro de ciclobutanocarbonilo (50 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,08 g, 68%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 9,04 (s, 1H), 8,04 (m, 2H), 7,95 (m, 3H), 7,20 (s, 1H), 7,14 (m, 2H), 4,69 (m, 1H), 3,95 (s, 3H), 3,85 (m, 1H), 3,56 (m, 1H), 3,36 (m, 1H), 3,25 (m, 2H), 2,17 (br m, 4H), 1,92 (br m, 3H), 1,75 (m, 1H), 1,53 (m, 2H).
Ejemplo 418. {4-[4-(3-Metoxi-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetra-hidrofuran-2-il-metanona.
A 3-etoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,09 g, 0,27 mmol) en DMF (3 mL) se añadió HATU (0,15 g, 0,4 mmol), DIPEa (0,14 mL, 0,8 mmol), seguido por ácido (R)-tetrahidrofuran-2-carboxílico (0,05 mL, 0,53 mmol) y la mezcla se agitó a temperatura ambiente por 1 h. La mezcla se vertió en etil-acetato, se lavó con en sodio carbonato/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó usando Gilson (0,1%TFA en agua/0,1%TFA en gradiente de acetonitrilo), se diluyó en fracciones limpias con DCM, se lavó con en sodio carbonato/salmuera, se secó sobre sulfato de sodio, y se concentró. {4-[4-(3-Metoxi-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona se aisló como un sólido (0,09 g, 74%). Análisis: Lc Ms m/z = 433 (M+1). 1H NMR (DMSO-d6) 6: 9,04 (s, 1H), 8,04 (m, 2H), 7,95 (m, 3H), 7,20 (s, 1H), 7,14 (m, 2H), 4,69 (m, 2H), 3,95 (s, 3H), 3,77 (m, 4H), 3,42 (m, 2H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,63 (m, 2H).
Ejemplo 419. 1-{4-[4-(1-Cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(1-Cloroisoquinolin-6-il)-fenoxil-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 6-bromo-1-cloro-isoquinolina (0,3 g, 1,24 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,2 g, 36%). Análisis: LCMS m/z 439 (M+1).
Etapa 2. 1-Cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir de terc-butil éster del ácido 4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,2 g, 0,45 mmol) y TFA (1 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,14 g, 93%). Análisis: LCm S m/z 339 (M+1).
Etapa 3. El compuesto del título se preparó a partir de 1-cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (70 mg, 0,2 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 379. El producto se aisló como un sólido (0,04 g, 40%). Análisis: LCMS m/z = 395 (M+1). 1H NMR (DMSO-d6) ó: 8,31 (m, 3H), 8,15 (m, 1H), 7,93 (m, 1H), 7,84 (m, 2H), 7,18 (m, 2H), 4,73 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,35 (m, 1H), 3,27 (m, 1H), 2,34 (m, 2H), 1,98 (br m, 2H), 1,52-1,64 (br m, 2H), 1,00 (t, 3H, J = 7,4 Hz).
Ejemplo 420. {4-[4-(1-Cloroisoquinolin-6-il)-fenoxil-piperidin-1-il}-ciclopropil-metanona.
Este ejemplo se sintetizó a partir de 1-cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (70 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,04 g, 50%). Análisis: LCMS m/z = 407 (M+1). 1H NMR (DMSO-d6) ó: 8,31 (m, 3H), 8,15 (m, 1H), 7,93 (m, 1H), 7,84 (m, 2H), 7,18 (m, 2H), 4,75 (m, 1H), 3,99 (m, 1H), 3,89 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,04 (br m, 3H), 1,55-1,65 (br m, 2H), 0,74 (m, 4H).
Ejemplo 421. 1-{4-[4-(3-Dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(3-Cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 6-bromo-3-cloroisoquinolina (0,3 g, 1,24 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,47 g, 87%). Análisis: LCMS m/z 439 (M+1).
Etapa 2. A un frasco secado en un horno bajo una atmósfera de argón se añadió t-butil éster del ácido 4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,2 g, 0,46 mmol), 2M de dimetilamina en THF (0,68 mL, 1,37 mmol), dímero de cloruro de cinnamilpaladio (24 mg, 0,05 mmol), di(1-adamantil)-2-dimetilaminofenilfosfina (38 mg, 0,09 mmol), sodio t-butóxido (0,13 g, 1,37 mmol), seguido por tolueno (40 mL) y la reacción se desgasificó 3 veces bajo una atmósfera de argón y se agitó a 90 °C durante toda la noche. Se enfrió a temperatura ambiente, se diluyó con DCM, se filtró a través de una almohadilla de Celite, se lavó con agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10-20% EtOAc/hexanos) y se concentró. t-butil éster del ácido 4-[4-(3-Dimetilamino-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se aisló como un sólido (0,1 g, 53%). Análisis: LCMS m/z 448 (M+1).
Etapa 3. Dimetil-{6-[4-(piperidin-4-iloxi)-fenil]-isoquinolin-3-il}-amina se preparó a partir de terc-butil éster del ácido 4-[4-(3-dimetil-amino-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,1 g, 0,24 mmol) y TFA (1 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,08 g, 92%). Análisis: LCMS m/z 348 (M+1).
Etapa 4) El compuesto del título se preparó a partir de dimetil-{6-[4-(piperidin-4-iloxi)-fenil]-isoquinolin-3-il}-amina (76 mg, 0,22 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,04 g, 45%). Análisis: LCMS m/z = 404 (M+1). 1H NMR (DMSO-d6) ó: 8,92 (s, 1H), 7,84 (m, 2H), 7,71 (m, 2H), 7,50 (m, 1H), 7,12 (d, 2H, J = 8,8 Hz), 6,79 (s, 1H), 4,69 (m, 1H), 3,90 (m, 1H), 3,69 (m, 1H), 3,37 (m, 1H), 3,29 (m, 1H), 3,11 (s, 6H), 2,35 (m, 2H), 1,98 (br m, 2H), 1,51-1,64 (br m, 2H), 0,99 (t, 3H, J = 7,3 Hz).
E je m p lo 422. 1 -{4 -[4 -(3 -A m in o iso q u in o lin -6 - il) - fe n o x i]-p ip e r id in -1 - il}-p ro p a n -1 -o n a .
Etapa 1. 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,3 g, 0,74 mmol) y TFA (1 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,2 g, 87%). Análisis: LCMS m/z 304 (M+1).
Etapa 2. 1-{4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidin-1-il}-propan-1-ona se preparó a partir del producto de la Etapa 1 (97 mg, 0,32 mmol) y cloruro de propanoilo (50 uL, 0,5 mmol) de manera análoga al Ejemplo 378 Etapa 3. El producto se aisló como un sólido (0,11 g, 97%). Análisis: LCMS m/z = 360 (M+1).
Etapa 3. 1-{4-[4-(3-Aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona se preparó a partir del producto de la Etapa 2 (0,11 g, 0,32 mmol) y 6-bromoisoquinolin-3-ilamina (0,11 g, 0,48 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,05 g, 42%). Análisis: LCMS m/z = 376 (M+1). 1H NMR (DMSO-d6) 6: 8,78 (s, 1H), 7,84 (d, 1H, J = 8,6 Hz), 7,70 (m, 3H), 7,44 (m, 1H), 7,11 (m, 2H), 6,65 (s, 1H), 5,91 (s, 2H), 4,69 (m, 1H), 3,88 (m, 1H), 3,69 (m, 1H), 3,34 (m, 1H), 3,29 (m, 1H), 2,33 (m, 2H), 1,96 (br m, 2H), 1,50-1,64 (br m, 2H), 0,99 (t, 3H, J = 7,3 Hz).
Ejemplo 423. {4-[4-(3-Aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona.
Etapa 1. Ciclopropil-{4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidin-1-il}-metanona se preparó a partir de 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina (97 mg, 0,32 mmol) y cloruro de ciclopropanocarbonilo (50 uL, 0,5 mmol) de manera análoga al Ejemplo 378 Etapa 3. El producto se aisló como un sólido (0,12 g, 100%). Análisis: LCMS m/z = 372 (M+1).
Etapa 2. El compuesto del título se preparó a partir del producto de la Etapa 2 (0,13 g, 0,35 mmol) y 6-bromoisoquinolin-3-ilamina (0,12 g, 0,52 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,07 g, 52%). Análisis: LCMS m/z = 388 (M+1). 1H NMR (DMSO-d6) 6: 8,78 (s, 1H), 7,84 (d, 1H, J = 8,6 Hz), 7,70 (m, 3H), 7,44 (m, 1H), 7,11 (m, 2H), 6,65 (s, 1H), 5,91 (s, 2H), 4,71 (m, 1H), 3,98 (m, 1H), 3,88 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,54-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 424. {4-[4-(4-Metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-met-anona, HCl.
A 4-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-pirazolo[1,5-a]piridina (0,09 g, 0,28 mmol) en DMF (3 mL) se añadió HATU (0,16 g, 0,42 mmol), DIPEA (0,15 mL, 0,84 mmol), seguido por ácido (R)-tetrahidrofuran-2-carboxílico (0,05 mL, 0,56 mmol) y se agitó a temperatura ambiente por 1 h. La solución se vertió en EtOAc, se lavó con en Na2CO3/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó usando Gilson (0,1%TFA en agua/0,1%TFA en gradiente de acetonitrilo), se diluyó en fracciones limpias con DCM, se lavó con en Na2CO3/salmuera, se secó sobre sulfato de sodio, y se concentró. El compuesto disuelto en DCM, 2 M de HCl en éter de dietilo (0,14 mL, 0,28 mmol) se añadió y se concentró. La muestra se secó bajo alto vacío a 40 °C durante toda la noche. {4-[4-(4Metoxipirazolo[1,5-a]piridin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona; HCl se aisló como un sólido (0,03 g, 24%). Análisis: LCMS m/z = 422 (M+1). 1H NMR (DMSO-d6) ó: 8,57 (s, 1H), 7,94 (d, 1H, J = 2,2 Hz), 7,73 (m, 2H), 7,10 (d, 2H, J = 8,7 Hz), 6,89 (s, 1H), 6,62 (m, 1H), 4,68 (m, 2H), 4,02 (s, 3H), 3,78 (m, 4H), 3,37 (m, 1H), 3,25 (m, 1H), 1,80-2,08 (br m, 6H), 1,53-1,65 (br m, 2H).
Ejemplo 425. 1-{4-[4-(1-Metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(1-Cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 6-bromo-1-cloroisoquinolina (0,3 g, 1,24 mmol)) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,14 g, 26%). Análisis: LCMS m/z 439 (M+1).
Etapa 2. A un frasco Schlenck secado en un horno bajo una atmósfera de argón se añadió terc-butil éster del ácido 4-[4-(1-Cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,14 g, 0,32 mmol), ácido metilborónico (96 mg, 1,59 mmol), complejo DPPF-Pd(II) con DCM (1:1) (52 mg, 0,06 mmol), fosfato de potasio (338 mg, 1,59 mmol), seguido por 1,4-dioxano (5 mL) y se desgasificó bajo una atmósfera de argón por 5 min y se calentó a 99 °C durante toda la noche. La reacción se enfrió, se filtró a través de una almohadilla de Celite, se lavó con en sodio carbonato/agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10-50%acetato de etilo/hexanos) y se concentró. t-butil éster del ácido 4-[4-(1-metil-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se aisló como un sólido (0,06 g, 46%). Análisis: LCMS m/z 419 (M+1).
Etapa 3. 1-Metil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir de terc-butil éster del ácido 4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,06 g, 0,14 mmol) y ácido trifluoroacético (1 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,05 g, 100%). Análisis: LCMS m/z 319 (M+1).
Etapa d) El compuesto del título se preparó a partir del producto de la Etapa 3 (60 mg, 0,2 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,03 g). Análisis: LCMS m/z = 375 (M+1). 1H NMR (DMSO-d6) ó: 8,34 (d, 1H, J = 5,7 Hz), 8,23 (m, 1H), 8,17 (m, 1H), 7,98 (m, 1H), 7,81 (m, 2H), 7,70 (m, 1H), 7,13 (m, 2H), 4,71 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,35 (m, 1H), 3,29 (m, 1H), 2,89 (s, 3H), 2,35 (m, 2H), 1,98 (br m, 2H), 1,52 - 1,65 (br m, 2H), 1,00 (t, 3H, J=7,3Hz).
Ejemplo 426. 1-{4-[4-(4-Hidroxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Este ejemplo se sintetizó a partir de 1-{4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidin-1-il}-propan-1-ona (0,1 g, 0,28 mmol) y 6-bromo-pirazolo[1,5-a]piridin-4-ol (89 mg, 0,42 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,03 g, 29%). Análisis: LCMS m/z = 366 (M+1). 1H NMR (DMSO-d6) ó: 10,61 (s, 1H), 8,46 (m, 1H), 7,89 (d, 1H, J = 2,2Hz), 7,60 (m, 2H), 7,08 (m, 2H), 6,72 (m, 1H), 6,63 (m, 1H), 4,66 (m, 1H), 3,89 (m, 1H), 3,72 (m, 1H), 3,35 (m, 1H), 3,25 (m, 1H), 2,33 (m, 2H), 1,95 (br m, 2H), 1,48-1,62 (br m, 2H), 0,99 (t, 3H, J=7,3Hz).
E je m p lo 427. C ic lo b u til- {4 -[4 -(4 -h id ro x i-p ira z o lo [1 ,5 -a ]p ir id in -6 - il) - fe n o x i]-p ip e r id in -1 - il}-m e ta n o n a .
Ciclobutil-{4-[4-(4-hidroxi-pirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona1-{4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidin-1-il}-propan-1-ona (0,1 g, 0,28 mmol) y 6-bromo-pirazo-lo[1,5-a]piridin-4-ol (91 mg, 0,43 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,04 g, 37%). Análisis: LCMS m/z = 392 (M+1). 1H NMR (DMSO-d6) 6: 10,61 (s, 1H), 8,46 (m, 1H), 7,89 (d, 1H, J=2,2 Hz), 7,60 (m, 2H), 7,08 (m, 2H), 6,72 (m, 1H), 6,63 (m, 1H), 4,65 (m, 1H), 3,85 (m, 1H), 3,55 (m, 1H), 3,36 (m, 1H), 3,24 (m, 2H), 2,14 (m, 4H), 1,92 (m, 3H), 1,74 (m, 1H), 1,54 (m, 2H).
Ejemplo 428. {4-[4-(1-Cloroisoquinolin-6-il)-fenoxil-piperidin-1-il}-ciclobutil-metanona.
Este ejemplo se sintetizó a partir de 1-cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (40 mg, 0,1 mmol) y cloruro de ciclobutanocarbonilo (20 uL, 0,2 mmol) de manera análoga al Ejemplo 379. El producto se aisló como un sólido (0,03 g, 50%). Análisis: LCMS m/z = 421 (M+1). 1H NMR (DMSO-d6) 6: 8,31 (m, 3H), 8,15 (m, 1H), 7,93 (m, 1H), 7,84 (m, 2H), 7,18 (m, 2H), 4,72 (m, 1H), 3,85 (m, 1H), 3,56 (m, 1H), 3,36 (m, 1H), 3,29 (m, 2H), 2,17 (m, 2H), 2,09 (m, 2H), 1,93 (m, 3H), 1,74 (m, 1H), 1,56 (m, 2H).
Ejemplo 429. {4-[4-(1-Cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Este ejemplo se sintetizó a partir de 1-cloro-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,04 g, 0,12 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (0,02 mL, 0,24 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,02 g, 39%). Análisis: LCMS m/z = 437 (M+1). 1H NMR (DMSO-d6) 6: 8,31 (m, 3H), 8,15 (m, 1H), 7,93 (m, 1H), 7,84 (m, 2H), 7,18 (m, 2H), 4,75 (m, 1H), 4,69 (m, 1H), 3,77 (m, 4H), 3,34 (m, 1H), 3,29 (m, 1H), 2,01 (m, 4H), 1,84 (m, 2H), 1,52-1,65 (br m, 2H).
Ejemplo 430. 1-{4-[4-(3-Metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. A un frasco Schlenck secado en un horno bajo una atmósfera de argón se añadió t-butil éster del ácido 4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,44 g, 1 mmol), ácido metilborónico (301 mg, 5,02 mmol), amphos (142 mg, 0,2 mmol), carbonato de cesio (1,64 g, 5,02 mmol), seguido por 1,4-dioxano (60 mL) y se desgasificó bajo una atmósfera de argón por 5 min y se calentó a 99 °C durante toda la noche. La reacción se enfrió, se filtró a través de una almohadilla de Celite, se lavó con en carbonato de sodio, agua, salmuera, se secó sobre sulfato de
sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10-30%etil acetato/hexanos) y se concentró. terc-butil éster del ácido 4-[4-(3-metil-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se aisló como un sólido (0,11 g, 27%). Análisis: LCMS m/z = 419 (M+1).
Etapa 2. 3-Metil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir de terc-butil éster del ácido 4-[4-(3-metilisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,11 g, 0,27 mmol) y ácido trifluoroacético (1 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,08 g, 87%). Análisis: LCMS m/z = 319 (M+1).
Etapa 3. El compuesto del título se preparó a partir de 3-metil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (75 mg, 0,24 mmo) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,05 g, 51%). Análisis: LCMS m/z = 375 (M+1). 1H NMR (DMSO-d6) ó: 9,20 (s, 1H), 8,12 (d, 1H, J = 8,6 Hz), 8,07 (s, 1H), 7,90 (m, 1H), 7,78 (m, 2H), 7,66 (s, 1H), 7,15 (d, 2H, J = 8,8 Hz), 4,71 (m, 1H), 3,88 (m, 1H), 3,73 (m, 1H), 3,36 (m, 1H), 3,29 (m, 1H), 2,61 (s, 3H), 2,33 (m, 2H), 1,98 (br m, 2H), 1,52-1,64 (br, m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 431. {4-[4-(1-Metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Este ejemplo se sintetizó a partir de 1-metil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (50 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (30 uL, 0,31 mmol) de manera análoga al Ejemplo 639. El producto se aisló como un sólido. Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) ó: 8,34 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,7 Hz), 8,18 (m, 1 H), 7,98 (m, 1H), 7,81 (d, 2H. J = 8,7 Hz), 7,70 (d, 1 H, J = 5,8 Hz), 7,16 (d, 2H, J = 8,7 Hz), 4,69 (m, 2H), 3,77 (m, 4H), 3,43 (m, 1H), 3,26 (m, 1H), 2,89 (s, 3H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,52-1,66 (br m, 2H).
Ejemplo 432. {4-[4-(1-Metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Etapa 1. t-butil éster del ácido 4-[4-(1-Metoxiisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de tbutil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 6-bromo-1-metoxi-isoquinolina (443 mg, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido. Análisis: LCMS m/z = 435 (M+1).
Etapa 2. 1-Metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 1 y ácido trifluoroacético (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido. Análisis: LCMS m/z = 335 (M+1).
Etapa 3. El compuesto del título se preparó a partir de ácido 1 -metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,09 g, 0,27 mmol) y (R)-tetrahidrofuran-2-carboxílico (0,05 mL, 0,53 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,04 g, 30%). Análisis: LCMS m/z = 433 (M+1). 1H NMR (DMSO-d6) ó: 8,21 (d, 1H, J = 8,7 Hz), 8,13 (s, 1H), 8,02 (d, 1H, J = 5,8 Hz), 7,92 (m, 1H), 7,79 (d, 2H, J = 8,7 Hz), 7,43 (d, 1H, J = 5,7 Hz), 7,15 (d, 2H, J = 8,7 Hz), 4,73 (m, 2H), 4,07 (s, 3H), 3,75 (br m, 4H), 3,42 (m, 1H), 3,25 (m, 1H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,54 1,66 (br m, 2H).
E je m p lo 433. 1 -{4 -[4 -(1 -M e to x iiso q u in o lin -6 - il) - fe n o x i]-p ip e r id in -1 - il}-p ro p a n -1 -o n a .
Este ejemplo se sintetizó a partir de 1-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,09 g, 0,27 mmol) y cloruro de propanoilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 379. El producto se aisló como un sólido (0,06 g, 53%). Análisis: LCMS m/z = 391 (M+1). 1H NMR (DMSO-d6) 6: 8,21 (d, 1H, J = 8,7 Hz), 8,13 (s, 1H), 8,02 (d, 1H, J = 5,8 Hz), 7,92 (m, 1H), 7,79 (d, 2H, J =8,7Hz), 7,43 (d, 1H, J=5,7Hz), 7,15 (d, 2H, J=8,7Hz), 4,71 (m, 1H), 4,07 (s, 3H), 3,88 (m, 1H), 3,72 (m, 1H), 3,35 (m, 1H), 3,26 (m, 1H), 2,33 (m, 2H), 1,98 (br m, 2H), 1,52-1,64 (br m, 2H), 0,99 (t, 3H, J=7,4Hz).
Ejemplo 434. Ciclobutil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 1-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,09 g, 0,27 mmol) y cloruro de ciclobutanocarbonilo (50 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,07 g, 60%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 8,21 (d, 1H, J = 8,7 Hz), 8,13 (s, 1H), 8,02 (d, 1H, J = 5,8 Hz), 7,92 (m, 1H), 7,79 (d, 2H, J = 8,7 Hz), 7,43 (d, 1H, J = 5,7 hZ), 7,15 (d, 2H, J = 8,7 Hz), 4,70 (m, 1H), 4,07 (m, 3H), 3,88 (m, 1H), 3,56 (m, 1H), 3,36 (m, 1H), 3,25 (m, 2H), 2,07-2,20 (br m, 4H), 1,92 (br m, 3H), 1,74 (m, 1H), 1,56 (m, 2H).
Ejemplo 435. Ciclopropil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 1-metoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,09 g, 0,27 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,03 g, 29%). Análisis: LCMS m/z = 403 (M+1). 1H NMR (DMSO-d6) 6: 8,21 (d, 1H, J = 8,7 Hz), 8,13 (s, 1H), 8,02 (d, 1H, J = 5,8 Hz), 7,92 (m, 1H), 7,79 (d, 2H, J = 8,7 Hz), 7,43 (d, 1H, J = 5,7 Hz), 7,15 (d, 2H, J = 8,7 Hz), 4,73 (m, 1H), 4,07 (s, 3H), 3,98 (m, 1H), 3,88 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,55-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 436. {4-[4-(3-Aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Etapa 1. A 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenoxi]piperidina (0,09 g, 0,3 mmol) en DMF (3 mL) se añadió Ha Tu (0,17 g, 0,44 mmol), DIPEA (0,15 mL, 0,88 mmol), seguido por ácido (R)-tetrahidrofuran-2-carboxílico (0,05 mL,
0,59 mmol) y se agitó a temperatura ambiente por 1 h. La solución se vertió en etil-acetato, se lavó con en sodio carbonato/salmuera, se secó sobre sulfato de sodio, y se concentró. [(2R)-tetrahidrofuran-2-il]-[4-[4-(4,4,5,5-tetrametill , 3,2-dioxaborolan-2-il)fenoxi]-1-piperidil]metanona se aisló (0,05 g, 46%). Análisis: LCMS m/z = 402 (M+1).
Etapa 2. A un frasco Schlenck secado en un horno se añadió [(2R)-tetrahidrofuran-2-il]-[4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenoxi]-1-piperidil]metanona (0,11 g, 0,26 mmol), 6-bromoisoquinolin-3-ilamina (0,09 g, 0,39 mmol), tetraquis(trifenilfosfina)paladio(0) (0,03 g, 0,03 mmol), 1N Na2CO3 (0,79 mL, 0,79 mmol), seguido por 1,4-dioxano (2 mL) y se desgasificó bajo una atmósfera de argón por 5 min y se calentó a 99 °C por 2 h. La reacción se enfrió, se filtró a través de una almohadilla de Celite, se lavó con en Na2CO3/agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó usando Gilson (0,1%TFA en agua/0,1% TFA en gradiente de acetonitrilo), se diluyó en fracciones limpias con DCM, se lavó con en Na2CO3/salmuera, se secó sobre sulfato de sodio, y se concentró. {4-[4-(3-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona se aisló como un sólido (0,04 g, 34%). Análisis: LCMS m/z = 403 (M+1). 1H NMR (DMSO-d6) ó: 8,78 (s, 1H), 7,84 (d, 1H, J = 8,6 Hz), 7,70 (m, 3H), 7,44 (m, 2H), 7,11 (m, 2H), 6,65 (s, 1H), 5,91 (s, 2H), 4,68 (m, 2H), 3,76 (m, 4H), 3,41 (m, 1H), 3,29 (m, 1H), 2,01 (br m, 4H), 1,84 (m, 2H) 1,51-1,65 (br m, 2H).
Ejemplo 437. {4-[4-(3-Metilisoquinolin-6-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Este ejemplo se sintetizó a partir de 3-metil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,14 g, 0,43 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (0,08 mL, 0,86 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,06 g, 30%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) ó: 9,20 (s, 1H), 8,12 (d, 1H, J = 8,6 Hz), 8,07 (s, 1H), 7,90 (m, 1H), 7,78 (m, 2H), 7,66 (s, 1H), 7,15 (d, 2H, J = 8,8 Hz), 4,69 (m, 2H), 3,73 - 3,80 (m, 4H), 3,37 (m, 1H), 3,30 (m, 1H), 2,61 (s, 3H), 2,00 (br m, 4H), 1,84 (m, 2H), 1,53 - 1,65 (br m, 2H).
Ejemplo 438. {4-[4-(1 -Etilisoquinolin -6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, HCl.
Etapa 1. t-butil éster del ácido 4-[4-(1-Etilisoquinolin-6-il)-fenoxi]-piperidina-1 -carboxílico se preparó a partir de tercbutil éster del ácido 4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,12 g, 0,26 mmol) y ácido etilborónico (0,1 g, 1,31 mmol) de manera análoga al Ejemplo 425 Etapa 2. El producto se aisló como un sólido. Análisis: LCMS m/z = 433 (M+1).
Etapa 2. 1-Etil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 1 y TFA (0,8 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido. Análisis: LCMS m/z = 333 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 (42 mg, 0,13 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (24 uL, 0,25 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,04 g, 59%). Análisis: LCMS m/z = 431 (M+1). 1H NMR (DMSO-d6) ó: 8,65 (d, 1H, J = 9,0 Hz), 8,54 (s, 1H), 8,48 (d, 1H, J = 6,4 Hz), 8,31 (d, 1H, J = 8,0 Hz), 8,24 (d, 1H, J = 6,0 Hz), 7,94 (d, 2H, J = 8,8 Hz), 7,22 (d, 2H, J = 8,8 Hz), 4,78 (m, 1H), 4,69 (m, 1H), 3,77 (m, 4H), 3,54 (m, 2H), 3,35 (m, 1H), 3,26 (m, 1H), 2,00 (br m, 4H), 1,84 (m, 2H), 1,50-1,66 (br m, 2H), 1,43 (t, 3H, J = 7,5Hz).
E je m p lo 439. 1 -{4 -[4 -(1 -C ic lo p ro p il- iso q u in o lin -6 - il) - fe n o x i]-p ip e r id in -1 - il}-p ro p a n -1 -o n a .
Etapa 1. terc-butil éster del ácido 4-[4-(1-Ciclopropilisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de terc-butil éster del ácido 4-[4-(1-Cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,24 g, 0,55 mmol) y ácido ciclopropilborónico (0,24 g, 2,76 mmol) de manera análoga al Ejemplo 425 Etapa 2. El producto se aisló como un sólido (0,15 g, 61%). Análisis: LCMS m/z = 445 (M+1).
Etapa 2. 1-Ciclopropil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 1 (0,15 g, 0,33 mmol) y t Fa (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,12 g, 100%). Análisis: LCMS m/z = 345 (M+1).
Etapa 3. El compuesto del título se preparó a partir de 1-ciclopropil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (59 mg, 0,17 mmol) y cloruro de propanoilo (20 uL, 0,3 mmol) de manera análoga al Ejemplo 379. El producto se aisló como un sólido (0,03 g, 48%). Análisis: LCMS m/z = 401 (M+1). 1H NMR (DMSO-d6) 6: 8,56 (d, 1H, J = 9,0 Hz), 8,31 (d, 1H, J=5,6 Hz), 8,17 (s, 1H), 7,99 (m, 1H), 7,82 (m, 2H), 7,61 (d, 1H, J=5,6 Hz), 7,16 (m, 2H), 4,71 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,36 (m, 1H), 3,27 (m, 1H), 2,94 (m, 1H), 2,35 (m, 2H), 1,98 (br m, 2H), 1,53-1,65 (br m, 2H), 1,07-1,15 (m, 4H), 1,00 (t, 3H, J = 7,4Hz).
Ejemplo 440. {4-[4-(1-Ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetra-hidrofuran-2-il-metanona.
Este ejemplo se sintetizó a partir de 1-ciclopropil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (59 mg, 0,17 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (33 uL, 0,34 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,05 g, 62%). Análisis: LCMS m/z = 443 (M+1). 1H NMR (DMSO-d6) 6: 8,56 (d, 1H, J = 9,0 Hz), 8,31 (d, 1H, J = 5,6 Hz), 8,17 (s, 1H), 7,99 (m, 1H), 7,82 (m, 2H), 7,61 (d, 1H, J = 5,6 Hz), 7,16 (m, 2H), 4,69 (m, 2H), 3,77 (br m, 4H), 3,36 (m, 1H), 3,29 (m, 1H), 2,94 (m, 1H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,53-1,66 (br m, 2H), 1,07-1,15 (br m, 4H)
Ejemplo 441. 1-{4-[4-(7-Metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(7-Metoxi-6-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de terc-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-7-metoxi-6-metilquinolina (469 mg, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,56 g, 100%). LCMS m/z = 449 (M+1).
Etapa 2. El producto de la Etapa 1 (0,56 g, 1,27 mmol) se disolvió en DCM (6 mL), TFA (2 mL) se añadió en forma de gotas y la reacción se agitó a temperatura ambiente por 1 h y se concentró. El producto se particionó entre DCM/1N carbonato de sodio, se lavó con salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se disolvió
DCM, 2M de cloruro de hidrógeno en éter de dietilo (1,24 mL, 2,48 mmol) se añadió y se concentró. 4-[4-(7-Metoxi-6-metil-quinolin-2-il)-fenoxi]-piperidina 2HCl se aisló como un sólido (419 mg 78%). Análisis: LCMS m/z = 349 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 (90 mg, 0,2 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,05 g, 50%). Análisis: LCMS m/z = 405 (M+1). 1H NMR (DMSO-d6) ó: 9,06 (d, 1H, J = 2,3 Hz), 8,37 (d, 1H, J = 2,3 Hz), 7,75 (m, 3H), 7,36 (s, 1H), 7,14 (d, 2H, J = 8,7 Hz), 4,70 (m, 1H), 3,96 (s, 3H), 3,87 (m, 1H), 3,69 (m, 1H), 3,36 (m, 1H), 3,29 (m, 1H), 2,35 (m, 5H), 1,97 (br m, 2H), 1,52-1,64 (br m, 2H), 0,99 (t, 3H, J = 7,4Hz).
Ejemplo 442. Ciclopropil-{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidina, 2HCl (90 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,06 g, 70%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) ó: 9,06 (d, 1H, J = 2,3 Hz), 8,37 (d, 1H, J = 2,2 Hz), 7,75 (m, 3H), 7,36 (s, 1H), 7,14 (d, 2H, J = 8,7 Hz), 4,72 (m, 1H), 4,14 (m, 1H), 3,96 (s, 3H), 3,90 (m, 1H), 3,36 (m, 1H), 3,29 (m, 1H), 2,35 (s, 3H), 2,00 (br m, 3H), 1,55 - 1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 443. {4-[4-(7-Metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Este ejemplo se sintetizó a partir de 4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidina 2HCl (90 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (41 uL, 0,43 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,06 g, 60%). Análisis: LCMS m/z = 447 (M+1). 1H NMR (DMSO-d6) ó: 9,06 (d, 1H, J=2,3 Hz), 8,37 (d, 1H, J=2,2 Hz), 7,75 (m, 3H), 7,36 (s, 1H), 7,14 (d, 2H, J=8,7 Hz), 4,69 (m, 2H), 3,96 (s, 3H), 3,77 (m, 4H), 3,42 (m, 1H), 3,29 (m, 1H), 2,35 (s, 3H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,52-1,66 (br m, 2H).
Ejemplo 444. 1-{4-[4-(6-Fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. t-butil éster del ácido 4-[4-(6-Fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-6-fluoro-7-metoxiquinolina (476 mg, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,5 g, 88%). Análisis: LCMS m/z = 453 (M+1).
Etapa 2. 6-Fluoro-7-metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina se preparó a partir del producto de la Etapa 1 (0,5 g, 1,1 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,36 g, 93%). Análisis: LCMS m/z = 353 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (90 mg, 0,2 mmol) y cloruro de propanoilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido. Análisis: LCMS m/z = 409 (M+1). 1H NMR (DMSO-d6) ó: 9,13 (d, 1H, J = 2,2 Hz), 8,47 (d, 1H, J = 2,2 Hz), 7,76 (m, 3H), 7,60 (d, 1H,
J = 8,4 Hz), 7,14 (m, 2H), 4,71 (m, 1H), 4,02 (s, 3H), 3,90 (m, 1H), 3,69 (m, 1H), 3,36 (m, 1H), 3,29 (m, 1H), 2,35 (m, 2H), 2,07 (br m, 2H), 1,52-1,64 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
Ejemplo 445. CidopropN-{4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 6-fluoro-7-metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (90 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,06 g, 60%). Análisis: LCMS m/z = 421 (M+1). 1H NMR (DMSO-d6) 6: 9,13 (d, 1H, J = 2,2 Hz), 8,47 (d, 1H, J = 2,2 Hz), 7,76 (m, 3H), 7,60 (d, 1H, J=8,4 Hz), 7,14 (m, 2H), 4,73 (m, 1H), 4,02 (s, 3H), 4,00 (m, 1H), 3,88 (m, 1H), 3,57 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,54 - 1,65 (br m, 2H), 0,71 (m, 4H).
Ejemplo 446. {4-[4-(6-Fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Este ejemplo se sintetizó a partir de 6-fluoro-7-metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (90 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (49 uL, 0,51 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,04 g, 30%). Análisis: LCMS m/z = 451 (M+1). 1H NMR (DMSO-d6) 6: 9,13 (d, 1H, J=2,2 Hz), 8,47 (d, 1H, J=2,2 Hz), 7,76 (m, 3H), 7,60 (d, 1H, J=8,4 Hz), 7,14 (m, 2H), 4,69 (m, 2H), 4,02 (s, 3H), 3,77 (br m, 4H), 3,43 (m, 1H), 3,25 (m, 1H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,51-1,66 (br m, 2H).
Ejemplo 447. 1-{4-[4-(6-Cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Etapa 1. terc-butil éster del ácido 4-[4-(6-Cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de terc-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-6-cloro-7-metoxi-quinolina (338 mg, 1,24 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,5 g, 86%). Análisis: LCMS m/z = 469 (M+1).
Etapa 2. 4-[4-(6-Cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidina 2HCl se preparó a partir del producto de la Etapa 1 anterior (0,5 g, 1,06 mmol) y TFA (2 mL) de manera análoga al Ejemplo 441 Etapa 2. El producto se aisló como un sólido (0,4 g, 85%). Análisis: LCMS m/z = 369 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (90 mg, 0,2 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,05 g, 50%). Análisis: LCMS m/z = 425 (M+1). 1H NMR (DMSO-d6) 6: 9,17 (d, 1H, J = 2,4 Hz), 8,48 (d, 1H, J = 2,3 Hz), 8,17 (s, 1H), 7,76 (m, 2H), 7,57 (s, 1H), 7,16 (m, 2H), 4,71 (m, 1H), 4,03 (s, 3H), 3,88 (m, 1H), 3,73 (m, 1H), 3,35 (m, 1H), 3,29 (m, 1H), 2,33 (m, 2H), 1,98 (br m, 2H), 1,52-1,64 (br m, 2H), 0,99 (t, 3H, J = 7,4 Hz).
E je m p lo 448. {4 -[4 -(6 -C lo ro -7 -m e to x iq u in o lin -3 - il) - fe n o x i]-p ip e r id in -1 - il}-c ic lo -p ro p ilm e ta n o n a .
Este ejemplo se sintetizó a partir de 4-[4-(6-cloro-7-metoxi-quinolin-3-il)-fenoxi]-piperidina 2HCl (90 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,06 g, 60%). Análisis: LCMS m/z = 437 (M+1). 1H NMR (DMSO-d6) 6: 9,17 (d, 1H, J = 2,4 Hz), 8,48 (d, 1H, J=2,3 Hz), 8,17 (s, 1H), 7,76 (m, 2H), 7,57 (s, 1H), 7,16 (m, 2H), 4,73 (m, 1H), 4,03 (s, 3H), 3,89 (m, 2H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,55-1,64 (br m, 2H), 0,71 (m, 4H).
Ejemplo 449. {4-[4-(6-Cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Este ejemplo se sintetizó a partir de 4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidina 2HCl (90 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (41 uL, 0,43 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,05 g, 50%). Análisis: LCMS m/z = 467 (M+1). 1H NMR (DMSO-d6) 6: 9,17 (d, 1H, J = 2,4 Hz), 8,48 (d, 1H, J = 2,3 Hz), 8,17 (s, 1H), 7,76 (m, 2H), 7,57 (s, 1H), 7,16 (m, 2H), 4,73 (m, 2H), 4,03 (s, 3H), 3,87 (m, 4H), 3,36 (m, 1H), 3,29 (m, 1H), 2,01 (m, 4H), 1,84 (m, 2H), 1,52-1,66 (br m, 2H).
Ejemplo 450. {4-[4-(6-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, HCl.
Etapa 1. t-butil éster del ácido 4-[4-(6-Metoxiquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 2-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-6-metoxi-quinolina (295 mg, 1,24 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,52 g, 96%). Análisis: LCMS m/z = 435 (M+1).
Etapa 2. 4-[4-(6-Metoxiquinolin-3-il)-fenoxi]-piperidina 2HCl se preparó a partir del producto de la Etapa 1 anterior (0,52 g, 1,2 mmol) y TFA (2 mL) de manera análoga al Ejemplo 441 Etapa 2. El producto se aisló como un sólido (0,39 g, 80%). Análisis: LCMS m/z = 335 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (90 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (41 uL, 0,43 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,07 g, 60%). Análisis: LCMS m/z = 433 (M 1). 1H NMR (DMSO-d6) 6: 9,26 (d, 1H, J = 1,8 Hz), 8,86 (s, 1H), 8,08 (d, 1H, J = 10,0 Hz), 7,88 (d, 2H, J = 8,8 Hz), 7,55 (m, 2H), 7,21 (d, 2H, J = 8,8 Hz), 4,75 (m, 1H), 4,69 (m, 1H), 3,95 (s, 3H), 3,77 (br m, 4H), 3,23-3,48 (br m, 2H), 1,99 (br m, 4H), 1,84 (m, 2H), 1,52-1,67 (br m, 2H).
Ejemplo 451. {4-[4-(3-Isopropoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetra-hidrofuran-2-il-metanona.
Etapa 1. A 6-bromoisoquinolin-3-ol (0,5 g, 2,23 mmol) en DMF (4 mL) bajo a atmósfera de nitrógeno se añadió carbonato de cesio (2,18 g, 6,69 mmol), seguido por yoduro de isopropilo (0,22 mL, 2,23 mmol) y la reacción se calentó a 80 °C por 2 h. La reacción se enfrió a temperatura ambiente, se diluyó con EtOAc, se lavó con agua varias veces, se lavó con salmuera, se secó sobre Na2SO4, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (5% EtOAc /hexanos) y se concentró. 6-Bromo-3-isopropoxiisoquinolina se aisló como un sólido (0,2 g, 33%). Análisis: LCMS m/z = 267 (M+1).
Etapa 2. t-butil éster del ácido 4-[4-(3-Isopropoxi-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,25 g, 0,61 mmol) y 6-bromo-3-isopropoxi-isoquinolina (195 mg, 0,73 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,25 g, 89%). Análisis: LCMS m/z = 463 (M+1).
Etapa 3. 3-Isopropoxi-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 2 anterior (0,25 g, 0,54 mmol) y t Fa (1 mL) de manera análoga al Ejemplo 378 Etapa 2. El producto se aisló como un sólido (0,19 g, 98%). Análisis: LCMS m/z=363 (M+1).
Etapa 4. {4-[4-(3-Isopropoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona se preparó a partir del producto de la Etapa 3 anterior (90 mg, 0,2 mmol y ácido (R)-tetrahidrofuran-2-carboxílico (27 uL, 0,28 mmol) de manera análoga al Ejemplo 418. Se aisló como un sólido (0,08 g, 60%). Análisis: LCMS m/z = 461 (M+1). 1H NMR (DMSO-d6) 6: 8,99 - 9,06 (m, 1 H), 8,02 - 8,09 (m, 1 H), 7,98 - 8,02 (m, 1 H), 7,68-7,79 (m, 3 H), 7,11-7,17 (m, 3 H), 5,25-5,34 (m, 1 H), 4,64-4,78 (m. 2 H), 3,69-3,86 (m, 4 H), 3,33-3,38 (m, 1 H), 3,20-3,29 (m, 1 H), 1,89-2,13 (m, 4 H), 1,75-1,88 (m, 2 H), 1,44-1,70 (m, 2 H), 1,34 (d, 6 H, J=6,3 Hz)
Ejemplo 452. {4-[4-(1-Morfolin-4-il-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona.
Etapa 1. A un frasco secado en un horno bajo una atmósfera de argón se añadió t-butil éster del ácido 4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,2 g, 0,46 mmol), morfolina (0,08 mL, 0,91 mmol), dímero de cloruro de cinnamilpaladio (24 mg, 0,046 mmol), di(1-adamantil)-2-dimetilaminofenilfosfina (38 mg, 0,09 mmol), sodio tbutóxido (0,13 g, 1,37 mmol), seguido por tolueno (10 mL) y la reacción se desgasificó 3X bajo una atmósfera de argón y se agitó a 99 °C durante toda la noche. La reacción se enfrió a temperatura ambiente, se diluyó con DCM, se filtró a través de una almohadilla de Celite, se lavó con agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10-30-50%acetato de etilo/hexanos) y se concentró. tercbutil éster del ácido 4-[4-(1-Morfolin-4-il-isoquinolin-6-il)-fenoxi]-piperidina-1 -carboxílico se aisló como un sólido (0,1 g, 43%). Análisis: LCMS m/z = 490 (M+1).
Etapa 2. 1-Morfolin-4-il-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 1 anterior (0,1 g, 0,2 mmol) y TFA (1 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,07 g, 88%). Análisis: LCMS m/z = 390 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (67 mg, 0,17 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (18 uL, 0,19 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,06 g, 72%). Análisis: LCMS m/z = 488 (M+1). 1H NMR (DMSO-d6) 6: 8,12 (m, 3H), 7,89 (m, 1H), 7,78 (d, 2H, J = 8,7 Hz), 7,45 (d, 1H, J = 5,8 Hz), 7,15 (d, 2H, J = 8,7 Hz), 4,69 (m, 2H), 3,86 (m, 4H), 3,76 (m, 4H), 3,22-3,45 (br m, 6H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,54-1,65 (br m, 2H).
Ejemplo 453. {4-[4-(1-Dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il metananona, HCl.
Etapa 1. t-butil éster del ácido 4-[4-(1-Dimetilaminoisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(1-Cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,2 g, 0,46 mmol) y 2M dimetilamina en THF (0,46 mL, 0,91 mmol) de manera análoga al Ejemplo 673a. El producto se aisló como un sólido (0,1 g, 52%). Análisis: LCMS m/z = 448 (M+1).
Etapa 2. Dimetil-{6-[4-(piperidin-4-iloxi)-fenil]-isoquinolin-1-il}-amina se preparó a partir del producto de la Etapa 1 anterior (0,1 g, 0,24 mmol) y TFA (1 mL) de manera análoga al Ejemplo 599b. El producto se aisló como un sólido (0,06 g, 67%). LCMS m/z = 348 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (55 mg, 0,16 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (17 uL, 0,17 mmol) de manera análoga al Ejemplo 645. El producto se aisló como un sólido (0,04 g, 52%). Análisis: LCMS m/z = 446 (M+1). 1H NMR (DMSO-d6) 6: 12,84 (br s, 1H), 8,43 (d, 1H, J = 9,0 Hz), 8,28 (s, 1H), 8,02 (m, 1H), 7,87 (d, 2H, J = 8,8 Hz), 7,75 (d, 1H, J = 6,3 Hz), 7,41 (d, 1H, J = 6,6 Hz), 7,19 (d, 2H, J = 8,8 Hz), 4,75 (m, 1H), 4,69 (m, 1H), 3,76 (br m, 4H), 3,44 (s, 3H), 3,41 (s, 3H), 3,33 (m, 1H), 3,25 (m, 1H), 1,99 (br m, 4H), 1,84 (m, 2H), 1,52-1,68 (br m, 2H).
Ejemplo 454. {4-[4-(1-Aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Este ejemplo se sintetizó a partir de [(2R)-tetrahidrofuran-2-il]-[4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenoxi]-1-piperidil]metanona (0,1 g, 0,2 mmol) y 6-bromoisoquinolin-1-ilamina (67 mg, 0,3 mmol) de manera análoga al Ejemplo 436. El producto se aisló como un sólido (0,03 g, 30%). Análisis: LCMS m/z = 418 (M+1). 1H NMR (DMSO-d6) 6: 8,28 (m, 1H), 7,95 (s, 1H), 7,75 (m, 4H), 7,12 (m, 2H), 6,95 (m, 3H), 4,72 (m, 2H), 3,80 (m, 4H), 3,36 (m, 1H), 3,29 (m, 1H), 1,99 (br m, 4H), 1,82 (m, 2H), 1,60 (br m, 2H).
Ejemplo 455. {4-[4-(1-Dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, 2HCL.
Etapa 1. t-butil éster del ácido 4-{4-[1-(4-Metilpiperazin-1 -il)-isoquinolin-6-il]-fenoxi}-piperidina-1 -carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(1-cloro-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,2 g, 0,46 mmol) y 1-metilpiperazina (0,1 mL, 0,91 mmol) de manera análoga al Ejemplo 452. El producto se aisló como un sólido (0,08 g, 36%). Análisis: LCMS m/z = 503 (M+1).
Etapa 2. El producto de la Etapa 1 anterior se disolvió en DCM (4 mL), TFA (1 mL) se añadió en forma de gotas y se agitó a temperatura ambiente por 1 h y se concentró. 1-(4-Metilpiperazin-1-il)-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina di-trifluoroacetato se aisló como el producto crudo. Análisis: LCMS m/z = 403 (M+1).
Etapa 3. El compuesto del título se preparó a partir de 4-{4-[1-(4-met¡lp¡peraz¡n-1-¡l)-¡soqu¡nol¡n-6-¡l]-fenox¡}-p¡per¡d¡na tri-trifluoroacetato (14 mg, 0,19 mmol) y ác¡do (R)-tetrah¡drofuran-2-carboxíl¡co (20 uL, 0,21 mmol) de manera análoga al Ejemplo 424. El producto se a¡sló como un sól¡do (0,04 g, 37%). Anál¡s¡s: LCMS m/z = 501 (M+1). 1H NMR (DMSO-d6) ó: 11,13 (br s, 1H), 8,26 (s, 1H), 8,22 (d, 1H, J = 8,8 Hz), 8,09 (d, 1H, J = 6,0 Hz), 7,98 (m, 1H), 7,83 (d, 2H, J = 8,8 Hz), 7,60 (d, 1H, J = 6,2 Hz), 7,18 (d, 2H, J = 8,8 Hz), 4,69 (m, 2H), 3,25-4,04 (br m, 15 H), 2,87 (s, 3H), 2,02 (m, 4H), 1,84 (m, 2H), 1,52-1,66 (br m, 2H).
Ejemplo 456. {4-[4-(1-Met¡lam¡no¡soqu¡nol¡n-6-¡l)-fenox¡]-p¡per¡d¡n-1-¡l}-(R)-tetra-h¡drofuran-2-¡l-metanona.
Etapa 1. t-but¡l éster del ác¡do 4-[4-(1-Met¡lam¡no¡soqu¡nol¡n-6-¡l)-fenox¡]-p¡per¡d¡na-1-carboxíl¡co se preparó a part¡r de t-but¡l éster del ác¡do 4-[4-(1-Cloro¡soqu¡nol¡n-6-¡l)-fenox¡]-p¡per¡d¡na-1-carboxíl¡co (0,09 g, 0,2 mmol) y 2M met¡lam¡na en THF (0,2 mL, 0,4 mmol) de manera análoga al Ejemplo 452. El producto se a¡sló como un sól¡do (0,07 g, 80%). Anál¡s¡s: LCMS m/z = 434 (M+1).
Etapa 2. Met¡l-{6-[4-(p¡per¡d¡n-4-¡lox¡)-fen¡l]-¡soqu¡nol¡n-1-¡l}-am¡na se preparó a part¡r del producto de la Etapa 1 anter¡or (0,07g, 0,16 mmol) y TFA (0,5 mL) de manera análoga al Ejemplo 379. El producto se a¡sló como un sól¡do (0,05 g, 100%). LCMS m/z = 334 (M+1).
Etapa 3.) El compuesto del título se preparó a part¡r del producto de la Etapa 2 anter¡or (53 mg, 0,16 mmol) y ác¡do (R)-tetrah¡drofuran-2-carboxíl¡co (15 uL, 0,16 mmol) de manera análoga al Ejemplo 418. El producto se a¡sló como un sól¡do (0,02 g, 29%). Anál¡s¡s: LCMS m/z = 432 (M+1). 1H NMR (DMSO-d6) ó: 8,22 (m, 1H), 8,92 (m, 2H), 7,75 (m, 3H), 7,45 (m, 1H), 7,12 (m, 2H), 6,90 (m, 1H), 4,72 (m, 2H), 3,80 (m, 4H), 3,36 (m, 1H), 3,29 (m, 1H), 2,98 (m, 3H), 2,00 (br m, 4H), 1,85 (m, 2H), 1,52-1,64 (br m, 2H).
Ejemplo 457. 1-{4-[4-(4-Met¡l¡soqu¡nol¡n-6-¡l)-fenox¡]-p¡per¡d¡n-1-¡l}-propan-1-ona HCl.
Etapa 1. terc-but¡l éster del ác¡do 4-[4-(4-Met¡l¡soqu¡nol¡n-6-¡l)-fenox¡]-p¡per¡d¡na-1-carboxíl¡co se preparó a part¡r de terc-but¡l éster del ác¡do 4-[4-(4,4,5,5-Tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)-fenox¡]-p¡per¡d¡na-1-carboxíl¡co (0,5 g, 1,24 mmol) y 6-bromo-4-met¡l-¡soqu¡nol¡na (0,33 g, 1,49 mmol) de manera análoga al Ejemplo 378. El producto se a¡sló como un sól¡do (0,55 g, 100%). Anál¡s¡s: LCMS m/z = 419 (M+1).
Etapa 2. 4-[4-(4-Met¡l¡soqu¡nol¡n-6-¡l)-fenox¡]-p¡per¡d¡na, 2HCl se preparó a part¡r del producto de la Etapa 1 anter¡or (0,55 g, 1,32 mmol) y TFA (1 mL) de manera análoga al Ejemplo 662b. El producto se a¡sló como un sól¡do (0,39 g, 76%).
Anál¡s¡s: LCMS m/z = 319 (M+1).
Etapa 3. El compuesto del título se preparó a part¡r del producto de la Etapa dos anter¡or (90 mg, 0,2 mmol) y cloruro de propano¡lo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 619. El producto se a¡sló como un sól¡do (0,04 g, 40%). Anál¡s¡s: LCMS m/z = 375 (M+1). 1H NMR (DMSO-d6) ó: 9,68 (s, 1 H), 8,50 - 8,62 (m, 2 H), 8,42 (s, 1 H), 8,27 - 8,35 (m, 1 H), 7,98 (d, 2 H, J = 8,8 Hz), 7,21 (d, 2 H, J = 8,8 Hz), 4,66 - 5,01 (m, 1 H), 4,01 - 4,32 (br m, 1 H), 3,79 - 3,96 (m, 1 H), 3,60 - 3,76 (m, 1 H), 3,15 - 3,40 (m, 2 H), 2,82 (s, 3 H), 2,35 (d, 2 H, J = 7,5 Hz), 1,82 - 2,13 (m, 2 H), 1,45 -1,77 (m, 2 H), 1,00 (t, 3 H, J = 7,4 Hz).
E je m p lo 458. C ic lo p ro p il-{4 -[4 -(4 -m e tilis o q u in o lin -6 - il) -fe n o x i]-p ip e r id in -1 - il}-m e ta n o n a , HCl.
Este ejemplo se sintetizó a partir de 4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidina, 2HCl (90 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,06 g, 60%). Análisis: LCMS m/z = 387 (M+1). 1H NMR (DMSO-d6) 6: 9,67 (s, 1 H), 8,49-8,60 (m, 2 H), 8,42 (s, 1 H), 8,25-8,35 (m, 1 H), 7,99 (d, 2 H, J=8,8 Hz), 7,22 (d, 2 H, J=8,8 Hz), 4,65-4,99 (m, 1 H), 3,43-4,17 (m, 4H), 3,18-3,38 (m, 1 H), 2,82 (s, 3 H), 1,81-2,23 (m, 3H), 1,41-1,79 (m, 2H), 0,52-0,92 (m, 4H).
Ejemplo 459. {4-[4-(4-Metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, HCl.
Este ejemplo se sintetizó a partir de 4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidina, 2HCl (90 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (0,02 mL, 0,25 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,07 g, 62%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 9,65 (s, 1 H), 8,48 - 8,59 (m, 2 H), 8,40 (s, 1H), 8,32 (m, 1 H), 7,98 (d, 2 H, J = 8,8 Hz), 7,21 (d, 2 H, J = 8,5 Hz), 4,54 - 4,87 (m, 2 H), 3,52 - 3,92 (m, 5 H), 3,20 - 3,50 (m, 2 H), 2,82 (s, 3 H), 1,93 - 2,18 (m, 4 H), 1,73 - 1,90 (m, 2 H), 1,45 - 1,66 (m, 2 H).
Ejemplo 460. 1-{4-[4-(5-Metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Etapa 1. t-butil éster del ácido 4-[4-(5-Cloroquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-5-cloro-quinolina (0,36 g, 1,49 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido. Análisis: LCMS m/z = 439 (M+1).
Etapa 2. t-butil éster del ácido 4-[4-(5-Metil-quinolin-3-il)-fenoxi]-piperidina-1 -carboxílico se preparó a partir del producto de la Etapa 1 anterior (0,58 g, 1,32 mmol) y ácido metilborónico (396 mg, 6,62 mmol) de manera análoga al Ejemplo 430. El producto se aisló como un sólido. Análisis: LCMS m/z = 419 (M+1).
Etapa 3. 4-[4-(5-Metil-quinolin-3-il)-fenoxi]-piperidina 2HCl se preparó a partir del producto de la Etapa 2 anterior y TFA (2 mL) de manera análoga al Ejemplo 441 Etapa 2. El producto se aisló como un sólido. LCMS m/z = 319 (M+1).
Etapa 4. El compuesto del título se preparó a partir del producto de la Etapa 3 anterior (90 mg, 0,2 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,05 g, 50%). Análisis: LCMS m/z = 375 (M+1). 1H NMR (DMSO-d6) 6: 9,39 (s, 1 H), 8,83 - 8,90 (m, 1 H), 8,01 (d, 1 H, J = 8,8 Hz), 7,93 (d, 2 H, J = 8,8 Hz), 7,74 - 7,83 (m, 1 H), 7,55 - 7,64 (m, 1 H), 7,20 (d, 2 H, J = 8,8 Hz), 4,70 - 4,81 (m, 1 H), 4,40 (br m, 1H), 3,82 - 3,97 (m, 1 H), 3,63-3,79 (m, 1H), 3,19-3,47 (m, 2H), 2,80 (s, 3H), 2,28-2,42 (m, 2H), 1,87-2,09 (m, 2H), 1,47-1,72 (m, 2H), 1,00 (t, 3H, J=7,4Hz).
E je m p lo 461. C ic lo p ro p il-{4 -[4 -(5 -m e til-q u in o lin -3 - il) - fe n o x i]-p ip e r id in -1 - il}-m e ta n o n a , HCl.
Este ejemplo se sintetizó a partir de 4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidina, 2HCl (90 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,05 g, 50%). Análisis: LCMS m/z = 387 (M+1). 1H NMR (DMSO-d6) 6: 9,48 (s, 1 H), 8,93 - 9,08 (m, 1 H), 8,04 - 8,13 (m, 1 H), 7,97 (d, 2 H, J = 8,5 Hz), 7,79 - 7,89 (m, 1 H), 7,50 - 7,72 (m, 1 H), 7,23 (d, 2 H, J=8,8Hz), 4,68-4,88 (m, 1H), 3,78 4,09 (m, 2H), 3,53-3,69 (m, 1H), 3,22-3,38 (m, 1H), 2,83 (s, 3H), 1,86 - 2,17 (m, 3H), 1,46-1,77 (m, 2H), 0,73 (d, 4H, J=8,8Hz).
Ejemplo 462. {4-[4-(5-Metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, HCl.
Este ejemplo se sintetizó a partir de 4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidina 2HCl (90 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (0,02 mL, 0,25 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,06 g, 53%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 9,45 (d, 1 H, J =1,8 Hz), 8,96 (s, 1 H), 8,02 - 8,10 (m, 1 H), 7,96 (d, 2 H, J = 8,8 Hz), 7,74 - 7,86 (m, 1 H), 7,58 - 7,70 (m, 1 H), 7,21 (d, 2 H, J = 8,5 Hz), 4,59 - 4,84 (m, 2 H), 3,76 (d, 4H, J=6,8Hz), 3,17-3,57 (m, 2H), 2,82 (s, 3H), 1,91-2,15 (m, 4H), 1,76-1,89 (m, 2H), 1,46-1,71 (m, 2H).
Ejemplo 463. 1-{4-[4-(5-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Etapa 1. t-butil éster del ácido 4-[4-(5-Metoxiquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-5-metoxi-quinolina (0,35 g, 1,49 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido. (0,53 g, 100%). Análisis: LCMS m/z = 435 (M+1).
Etapa 2. 5-Metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina 2HCl se preparó a partir del producto de Etapa 1 anterior (0,53 g, 1,24 mmol) y TFA (2 mL) de manera análoga al Ejemplo 461. El producto se aisló como un sólido (0,48 g, 95%). LCMS m/z = 335 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (90 mg, 0,2 mmol) y cloruro de propanoilo (30 uL, 0,4 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,05 g, 50%). LCMS m/z = 391 (M+1). 1H NMR (DMSO) 6: 9,43 (d, 1H, J = 2,2 Hz), 8,95 (s, 1H), 7,89 (m, 3H), 7,79 (m, 1H), 7,26 (m, 1H), 7,19 (m, 2H), 4,74 (m, 1H), 4,07 (s, 3H), 3,88 (m, 1H), 3,69 (m, 1H), 3,25-3,39 (br m, 2H), 2,34 (m, 2H), 1,98 (m, 2H), 1,53-1,68 (br m, 2H), 1,00 (t, 3H, J = 7,4 Hz).
E je m p lo 464. C ic lo p ro p il-{4 -[4 -(5 -m e to x iq u in o lin -3 - il) - fe n o x i]-p ip e r id in -1 - il}-m e ta n o n a .
Este ejemplo se sintetizó a partir de 5-metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina, 2HCl (90 mg, 0,2 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,4 mmol) de manera análoga al Ejemplo 619. El producto se aisló como un sólido (0,07 g, 70%). Análisis: LCMS m/z = 403 (M+1). 1H NMR (DMSO-d6) 6: 9,44 (d, 1 H, J = 2,3 Hz), 8,97 (s, 1 H), 7,89 (m, 3 H), 7,79 - 7,81 (m, 1 H), 7,24 - 7,29 (m, 1 H), 7,20 (d, 2 H, J = 8,8 Hz), 4,60 - 4,90 (m, 1 H), 4,08 (s, 3 H), 3,96 -4,02 (m, 1 H), 3,81 - 3,92 (m, 1 H), 3,51 - 3,70 (m, 1 H), 3,20 - 3,38 (m, 1 H), 2,01 (m, 3 H), 1,45 - 1,77 (m, 2 H), 0,64 0,77 (m, 4H).
Ejemplo 465. {4-[4-(5-Metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona, HCl.
Este ejemplo se sintetizó a partir de 5-metoxi-3-[4-(piperidin-4-iloxi)-fenil]-quinolina, 2HCl (90 mg, 0,2 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (0,02 mL, 0,24 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,06 g, 58%). Análisis: LCMS m/z = 433 (M+1). 1H NMR (DMSO-d6) 6: 9,44 (d, 1 H, J = 2,3 Hz), 8,96 (s, 1 H), 7,89 (m, 3 H), 7,73 - 7,81 (m, 1 H), 7,23 - 7,32 (m, 1 H), 7,19 (d, 2 H, J = 8,8 Hz), 4,62 - 4,84 (m, 2 H), 4,08 (s, 3 H), 3,76 (m, 4 H), 3,08 - 3,56 (m, 2 H), 2,00 (m, 4 H), 1,74 - 1,92 (m, 2 H), 1,41 - 1,70 (m, 2 H).
Ejemplo 466. Ciclopropil-[4-(4-isoquinolin-6-il-fenoxi)-piperidin-1-il]-metanona.
Etapa 1. t-butil éster del ácido 4-(4-Isoquinolin-6-il-fenoxi)-piperidina-1-carboxílico se preparó a partir de t-butil éster del 4-(4-yodo-fenoxi)-piperidina-1-carboxílico ácido (0,5 g, 1,24 mmol) y ácido 6-isoquinolilborónico (0,26 g, 1,49 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,33 g, 65%). Análisis: LCMS m/z = 405 (M+1).
Etapa 2. 6-[4-(Piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 1 anterior (0,33 g, 0,8 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,24 g, 97%). Análisis: LCMS m/z = 305 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior y cloruro de ciclopropanocarbonilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,06 g, 50%). Análisis: LCMS m/z = 373 (M+1). 1H NMR (DMSO-d6) 6: 9,31 (s, 1 H), 8,50 (d, 1 H, J = 5,8 Hz), 8,19 (m, 2 H), 8,01 (d, 1 H, J = 1,8 Hz), 7,81 (m, 3 H), 7,16 (d, 2 H, J = 8,8 Hz), 4,70 - 4,83 (m, 1 H), 3,83 - 4,07 (m, 2 H), 3,52 3,64 (m, 1H), 3,24-3,31 (m, 1H), 1,90-2,09 (m, 3H), 1,49-1,72 (m, 2H), 0,73 (m, 4H).
E je m p lo 467. [4 -[4 -(6 -Is o q u in o lil) fe n o x i]-1 -p ip e rid il]- [(2 R )-te tra h id ro fu ra n -2 -il]-m e ta n o n a HCl.
Este ejemplo se sintetizó a partir de 6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (0,09 g, 0,30 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (0,03 mL, 0,33 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,08 g, 59%). Análisis: LCMS m/z = 403 (M+1). 1H NMR (DMSO-d6) 6: 9,78 (s, 1 H), 8,61 - 8,68 (m, 1 H), 8,47 - 8,58 (m, 2 H), 8,29 - 8,42 (m, 2 H), 7,93 (d, 2 H, J = 8,8 Hz), 7,09 - 7,27 (m, 2 H), 4,74 - 4,83 (m, 1 H), 4,70 (m, 1 H), 3,77 (s, 4 H), 3,20 - 3,53 (m, 2 H), 1,91 - 2,13 (m, 4 H), 1,76 - 1,91 (m, 2 H), 1,47-1,73 (m, 2 H).
Ejemplo 468. {4-[4-(5-Metilisoquinolin-6-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidro-furan-2-il-metanona, HCl.
Etapa 1. A 6-metoxi-5-metil-isoquinolina (0,14 g, 0,81 mmol) bajo una atmósfera de nitrógeno en DCM (10 mL) a 0 °C se añadió 1M de BBr3 en DCM (2,85 mL, 2,85 mmol) y la reacción se calentó hasta la temperatura ambiente durante toda la noche. La reacción se vertió lentamente en sodio bicarbonato sat. (30 mL) a 0 °C con agitación vigorosa, se extrajo, se lavó con agua/salmuera, se secó sobre sulfato de sodio, y se concentró. 5-Metil-isoquinolin-6-ol se aisló como producto crudo (0,1 g, 83%). Análisis: LCMS m/z = 160 (M+1).
Etapa 2. A una solución de 5-metilisoquinolin-6-ol (0,13 g, 0,8 mmol) en DMF (3 mL) y DIPEA (0,42 mL, 2,39 mmol) se añadió N-fenilbis(trifluorometanosulfonimida) (0,31 g, 0,88 mmol) y se agitó a temperatura ambiente por 30 min. La reacción se diluyó con etil-acetato, se lavó con agua/salmuera, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (10-30% EtOAc/hexanos) y se concentró. ácido trifluorometanosulfónico 5-metilisoquinolin-6-il éster se aisló como un sólido (0,14 g, 59%). Análisis: LCMS m/z = 292 (M+1).
Etapa 3. t-butil éster del ácido 4-[4-(5-Metilisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,16 g, 0,4 mmol) y la producto de la Etapa 2 anterior (0,14 g, 0,47 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,13 g, 75%).
Análisis: LCMS m/z = 419 (M+1).
Etapa 4. 5-Metil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 3 anterior (0,14 g, 0,3 mmol) y TFA (0,5 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,09 g, 89%). Análisis: LCMS m/z = 319 (M+1).
Etapa 5. El compuesto del título se preparó a partir del producto de la Etapa 4 anterior (0,09 g, 0,27 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (0,03 mL, 0,3 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,09 g, 74%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 9,83 (s, 1 H), 8,72 (d, 1 H, J = 6,5 Hz), 8,51 (d, 1 H, J = 6,8 Hz), 8,38 (d, 1 H, J = 8,5 Hz), 7,87 (d, 1 H, J = 8,8 Hz), 7,43 (d, 2 H, J = 8,8 Hz), 7,17 (d, 2 H, J = 8,5 Hz), 4,70 (m, 2 H), 3,68 - 3,97 (m, 4 H), 3,20 - 3,51 (m, 2 H), 2,67 (s, 3 H), 2,02 (br m, 4 H), 1,78 - 1,92 (m, 2 H), 1,49 - 1,73 (m, 2 H).
E je m p lo 469. 1 -[4 -[4 -(1 ,4 -D im e til-6 - iso q u in o lil) fe n o x i]-1 -p ip e rid il]p ro p a n -1 -o n a , HCl.
Etapa 1. t-butil éster del ácido 4-[4-(1-Cloro-4-metil-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 6-bromo-1-cloro-4-metilisoquinolina (0,32 g, 1,24 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,4 g, 70%). Análisis: lCm S m/z = 453 (M+1).
Etapa 2. A un frasco Schlenck bajo una atmósfera de argón se añadió el producto de la Etapa 1 anterior (0,4 g, 0,87 mmol), ácido metilborónico (0,26 g, 4,34 mmol), complejo DPPF-Pd(II) con DCM (1:1) (142 mg, 0,17 mmol), fosfato de potasio (0,92 g, 4,34 mmol), seguido por 1,4-dioxano (10 mL) y se desgasificó bajo una atmósfera de argón por 5 min y se calentó a 99 °C por 2 h. La reacción se enfrió, se filtró a través de una almohadilla de Celite, se lavó con en Na2CO3/agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice usando (20-50% EtOAc/hexanos) y se concentró. T-butil 4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]piperidina-1-carboxilato se disolvió en DCM (7 mL), TFA (2 mL) se añadió en forma de gotas y la reacción se agitó a temperatura ambiente por 1 h y se concentró. La reacción se particionó entre DCM /1N carbonato de sodio, se lavó con salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se disolvió en DCM, 2M de HCl en éter de dietilo (0,43 mL, 0,87 mmol) se añadió y se concentró. 1,4-Dimetil-6-[4-(4-piperidiloxi)fenil]isoquinolina dihidrocloruro se aisló como un sólido (0,22 g, 62%). LCMS m/z = 333 (M+1).
Etapa 3. 1-[4-[4-(1,4-Dimetil-6-isoquinolil)fenoxi]-1-piperidil]propan-1-ona HCl se preparó a partir de 1,4-dimetil-6-[4-(4-piperidiloxi)fenil]isoquinolina 2HCl (72 mg, 0,18 mmol) y cloruro de propanoilo (30 uL, 0,3 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,04 g, 53%). Análisis: LCMS m/z = 389 (M+1). 1H NMR (DMSO-d6) 6: 8,60 (d, 1 H, J = 8,8 Hz), 8,29 - 8,41 (m, 3 H), 7,99 (d, 2 H, J = 8,8 Hz), 7,21 (d, 2 H, J = 8,8 Hz), 4,71 - 4,84 (m, 1 H), 3,83 - 3,96 (m, 1 H), 3,67 - 3,77 (m, 1 H), 3,23 - 3,64 (br m, 3 H), 3,17 (s, 3 H), 2,78 (s, 3 H), 2,35 (m, 2 H), 1,86 - 2,10 (m, 2 H), 1,48 - 1,72 (m, 2 H), 1,00 (t, 3 H, J = 7,4 Hz).
Ejemplo 470. Ciclopropil-[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1-piperidil]metanona, HCl.
Este ejemplo se sintetizó a partir de 1,4-dimetil-6-[4-(4-piperidiloxi)fenil]isoquinolina, 2HCl (72 mg, 0,18 mmol) y cloruro de ciclopropanocarbonilo (30 uL, 0,3 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,04 g, 52%). Análisis: LCMS m/z = 401 (M+1). 1H NMR (DMSO-d6) 6: 8,60 (d, 1 H, J = 9,0 Hz), 8,29 - 8,42 (m, 3 H), 7,99 (d, 2 H, J = 8,8 Hz), 7,22 (d, 2 H, J = 8,8 Hz), 4,80 (m, 1 H), 3,83 - 4,10 (m, 2 H), 3,24 - 3,69 (m, 3 H), 3,17 (s, 3 H), 2,78 (s, 3 H), 1,88 - 2,11 (m, 3 H), 1,47 - 1,76 (m, 2 H), 0,64 - 0,76 (m, 4 H).
Ejemplo 471. [4-[4-(1,4-Dimetil-6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona, HCl.
Este ejemplo se sintetizó a partir de 1,4-dimetil-6-[4-(4-piperidiloxi)fenil]isoquinolina 2HCl (72 mg, 0,18 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (19 uL, 0,2 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un
sólido (0,03 g, 36%). LCMS m/z = 432 (M+1). 1H NMR (DMSO) ó: 8,59 (d, 1 H, J = 8,8 Hz), 8,28 - 8,42 (m, 3 H), 7,99 (d, 2 H, J=8,8 Hz), 7,21 (d, 2 H, J=8,5 Hz), 4,85 (m, 1H), 4,64 (m, 1 H), 3,70-3,95 (m, 4 H), 3,23-3,61 (m, 3 H), 3,15 (s, 3 H), 2,78 (s, 3 H), 1,92-2,15 (m, 4 H), 1,79-1,91 (m, 2 H), 1,50-1,73 (m, 2 H).
Ejemplo 472. 1-[4-[4-(1,5-Dimetil-6-isoquinolil)fenoxi]-1-piperidil]propan-1-ona HCl.
Etapa 1.5-Cloro-6-metoxi-1-metilisoquinolina se preparó a partir de 1,5-dicloro-6-metoxiisoquinolina (0,5 g, 2,19 mmol) y ácido metilborónico (656 mg, 11 mmol) de manera análoga al Ejemplo 425. El producto se aisló como un sólido (0,4 g, 91%). LCMS m/z = 208 (M+1).
Etapa 2. 6-Metoxi-1,5-dimetilisoquinolina se preparó a partir del producto de la Etapa 1 anterior (0,4 g, 1,99 mmol) y ácido metilborónico (597 mg, 9,97 mmol) de manera análoga al Ejemplo 430. El producto se aisló como un sólido (0,37 g, 100%). Análisis: LCMS m/z = 188 (M+1).
Etapa 3. 1,5-Dimetilisoquinolin-6-ol se preparó a partir de 6-metoxi-1,5-dimetilisoquinolina (0,4 g, 2,06 mmol) y 1M de BBr3 en DCM (7,2 mL, 7,2 mmol) de manera análoga al Ejemplo 468. El producto se aisló (0,25 g, 69%). Análisis: LCMS m/z = 174 (M+1).
Etapa 4. ácido trifluorometanosulfónico 1,5-dimetilisoquinolin-6-il éster se preparó a partir de 1,5-dimetilisoquinolin-6-ol (0,25 g, 1,42 mmol) y N-fenilbis(trifluorometanosulfonimida) (0,56 g, 1,56 mmol) de manera análoga al Ejemplo 468. El producto se aisló como un sólido (0,22 g, 50%). Análisis: LCMS m/z = 306 (M+1).
Etapa 5. A un frasco Schlenck se añadió t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,25 g, 0,61 mmol), el producto de la Etapa 4 anterior (0,22 g, 0,71 mmol), tetraquis(trifenilfosfina)paladio(0) (0,07 g, 0,06 mmol), 1M de Na2CO3 (1,82 mL, 1,82 mmol), seguido por 1,4-dioxano (6 mL) y se desgasificó bajo argón por 5 min y se calentó a 99 °C durante toda la noche. La reacción se enfrió, se filtró a través de una almohadilla de Celite, se lavó con en Na2CO3/agua/salmuera, se secó sobre Na2SO4, y se concentró. El producto se purificó mediante cromatografía de gel de sílice (20-50% EtOAc/hexanos) y se concentró. T-butil 4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]piperidina-1-carboxilato se disolvió en DCM (6 mL), TFA (0,8 mL) se añadió en forma de gotas y se agitó a temperatura ambiente por 2 h y se concentró. El compuesto se particionó entre DCM /1N Na2CO3, se lavó con agua/salmuera, se secó sobre Na2SO4, y se concentró. El producto se disolvió en DCM, 2M de HCl en éter de dietilo (0,3 mL, 0,61 mmol) se añadió y se concentró. 1,5-Dimetil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se aisló como un sólido (0,22 g, 90%). Análisis: lCm S m/z = 333 (M+1).
Etapa 6. El compuesto del título se preparó a partir de 1,5-dimetil-6-[4-(4-piperidiloxi)fenil]-isoquinolina 2HCl (74 mg, 0,18 mmol) y cloruro de propanoilo (30 uL, 0,3 mmol) de manera análoga al Ejemplo 619. El producto se aisló como un sólido (0,05 g, 64%). Análisis: LCMS m/z = 389 (M+1). 1H NMR (DMSO-d6) ó: 8,53 (d, 1 H, J = 6,8 Hz), 8,41 (d, 1 H, J = 8,8 Hz), 8,34 (d, 1 H, J = 6,3 Hz), 7,83 (d, 1 H, J = 8,8 Hz), 7,42 (d, 2 H, J = 8,8 Hz), 7,16 (d, 2 H, J = 8,5 Hz), 4,73 (m, 1 H), 3,86 - 3,99 (m, 1 H), 3,73 (m, 1 H), 3,22 - 3,45 (br m, 2 H), 3,19 (s, 3 H), 2,65 (s, 3 H), 2,36 (m, 2 H), I , 97 (m, 2 H), 1,48 - 1,75 (m, 2 H), 1,00 (t, 3 H, J = 7,4 Hz).
Ejemplo 473. Ciclopropil-[4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]metanona HCl.
Este ejemplo se sintetizó a partir de 1,5-dimetil-6-[4-(4-piperidiloxi)fenil]isoquinolina, 2HCl (74 mg, 0,18 mmol) y cloruro de ciclopropanocarbonilo (30 uL, 0,3 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,05 g, 56%). Análisis: LCMS m/z = 401 (M+1). 1H NMR (DMSO-d6) ó: 8,55 (d, 1 H, J = 7,0 Hz), 8,44 (d, 1 H, J = 8,8Hz), 8,38 (d, 1H, J=6,8Hz), 7,86 (d, 1H, J=8,8Hz), 7,40-7,46 (m, 2H), 7,13-7,20 (m, 2H), 4,68-4,83 (m, 1H), 3,814,08 (m, 2H), 3,49-3,65 (m, 2H), 3,23-3,36 (m, 1H), 3,20 (s, 3H), 2,67 (s, 3H), 1,91-2,14 (m, 3H), 1,50-1,76 (m, 2H), 0,66-0,78 (m, 4H).
Ejemplo 474. [4-[4-(1,5-Dimetil-6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona, HCl.
Este ejemplo se sintetizó a partir de 1,5-dimetil-6-[4-(4-piperidiloxi)fenil]isoquinolina, 2HCl (74 mg, 0,18 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (19 uL, 0,2 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,04 g, 47%). Análisis: LCMS m/z = 432 (M+1). 1H NMR (DMSO-d6) 6: 8,54 (d, 1 H, J = 7,0 Hz), 8,44 (d, 1 H, J = 8,8 Hz), 8,39 (d, 1 H, J = 6,8 Hz), 7,86 (d, 1 H, J = 8,8 Hz), 7,42 (d, 2H, J=8,8Hz), 7,17 (d, 2H, J=8,5Hz), 4,70 (m, 2H), 3,52-3,96 (br m, 5H), 3,23-3,51 (br m, 2H), 3,21 (s, 3H), 2,66 (s, 3H), 1,93-2,11 (m, 4H), 1,76-1,91 (m, 2H), 1,49 1,72 (m, 2H).
Ejemplo 475. [4-[4-(8-Ciclopropil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona, HCl.
Etapa 1. t-Butil 4-[4-(8-cloro-7-quinolil)fenoxi]piperidina-1-carboxilato se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,25 g, 0,62 mmol) y 7-bromo-8-cloroquinolina (0,17 g, 0,68 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,23 g, 85%). Análisis: LCMS m/z = 439 (M+1).
Etapa 2. A un frasco Schlenck bajo una atmósfera de argón se añadió el producto de la Etapa 1(0,23 g, 0,53 mmol), ácido ciclopropilborónico (0,23 g, 2,63 mmol), amphos (74,5 mg, 0,11 mmol), carbonato de cesio (0,86 g, 2,63 mmol), seguido por 1,4-dioxano (20 mL)/Agua (0,670 mL) y se desgasificó bajo una atmósfera de argón por 5 min y se calentó a 120°C por 4 h y se enfrió a temperatura ambiente. La reacción se filtró a través de una almohadilla de Celite, se lavó con DCM, se lavó con agua/salmuera, se secó sobre sulfato de sodio, y se concentró. El producto se purificó mediante cromatografía de gel de sílice usando placas de TLC preparativa (30% EtOAc/hexanos) y se concentró. Terc-butil 4-[4-(8-ciclopropil-7-quinolil)fenoxi]piperidina-1 -carboxilato se disolvió en DCM (4 mL), TFA (1 mL) se añadió y se agitó a temperatura ambiente por 2 h y se concentró. El producto se lavó con en Na2CO3/salmuera, se secó sobre sulfato de sodio, y se concentró. 8-Ciclo-propil-7-[4-(piperidin-4-iloxi)-fenil]-quinolina se aisló como un aceite amarillo (0,05 g, 29%). LCMS m/z = 345 (M+1).
Etapa 3. [4-[4-(8-Ciclopropil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]-metanona HCl se preparó a partir del producto de la Etapa 2 anterior (52 mg, 0,15 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (16 uL, 0,17 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,04 g, 55%). Análisis: LCMS m/z = 444 (M+1).
1H NMR (DMSO-d6) 6: 9,23 (s, 1 H), 8,95 - 9,12 (br m, 1 H), 8,15 - 8,26 (m, 1 H), 7,95 - 8,06 (m, 1 H), 7,78 - 7,88 (m, 1 H), 7,57 (d, 2 H, J=8,5Hz), 7,15 (d, 2 H, J=8,5 Hz), 4,71 (m, 2H), 4,30 (br m, 1H), 3,66-3,97 (m, 4H), 3,18-3,54 (m, 2H), 2,39-2,47 (m, 1H), 1,94-2,12 (m, 4H), 1,84 (m, 2H), 1,48-1,73 (m, 2H), 0,88-1,12 (m, 2H), 0,23-0,39 (m, 2H).
Ejemplo 476. {4-[4-(3-Etilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona.
Etapa 1. t-butil éster del ácido 4-[4-(3-Etil-isoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,67 g, 1,53 mmol) y ácido etilborónico (0,57 g, 7,65 mmol) análogo al Ejemplo 430. El producto se aisló como un sólido. Análisis: LCMS m/z = 433 (M+1).
Etapa 2. 3-Etil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 1 anterior y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,09 g, 97%). Análisis: LCMS m/z = 333 (M+1).
Etapa 3. {4-[4-(3-Etilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona se preparó a partir del producto de la Etapa 2 anterior (88 mg, 0,26 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (51 uL, 0,53 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,05 g, 40%). Análisis: LCMS m/z = 431 (M+1).
1H NMR (DMSO-d6) ó: 9,22 (s, 1H), 8,12 (d, 2H, J = 8,8 Hz), 7,91 (m, 1H), 7,79 (d, 2H, J = 8,8 Hz), 7,66 (s, 1H), 7,15 (d, 2H, J = 8,7 Hz), 4,69 (m, 2H), 3,77 (br m, 4H), 3,36 (m, 1H), 3,25 (m, 1H), 2,90 (m, 2H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,52-1,66 (br m, 2H), 1,32 (t, 3H, J=7,6Hz).
Ejemplo 477. Ciclopropil-{4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Etapa 1. t-butil éster del ácido 4-[4-(7-Fluoroquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-7-fluoroquinolina (0,28 g, 1,24 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido. Análisis: LCMS m/z = 423 (M+1).
Etapa 2. 7-Fluoro-3-[4-(piperidin-4-iloxi)-fenil]-quinolina se preparó a partir del producto de la Etapa 1 anterior y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,29 g, 96%). Análisis: LCMS m/z = 323 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (95 mg, 0,29 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,06 g, 52%). Análisis: LCMS m/z = 391 (M+1). 1H NMR (DMSO-d6) ó: 9,25 (s, 1H), 8,64 (s, 1H), 8,12 (m, 1H), 7,81 (m, 2H), 7,76 (m, 1H), 7,58 (m, 1H), 7,18 (m, 2H), 4,74 (m, 1H), 3,98 (m, 1H), 3,89 (m, 1H), 3,56 (m, 1H), 3,29 (m, 1H), 2,00 (br m, 3H), 1,55-1,66 (br m, 2H), 0,74 (m, 4H).
Ejemplo 478. 1-{4-[4-(7-Fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Este ejemplo se sintetizó a partir de 7-fluoro-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (95 mg, 0,29 mmol) y cloruro de propanoilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,02 g, 19%). Análisis: LCMS m/z = 379 (M+1). 1H NMR (DMSO-d6) ó: 9,25 (s, 1H), 8,64 (s, 1H), 8,12 (m, 1H), 7,81 (m, 2H), 7,76 (m, 1H), 7,58 (m, 1H), 7,18 (m, 2H), 4,72 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,35 (m, 1H), 3,27 (m, 1H), 2,35 (m, 2H), 1,98 (br m, 2H), 1,50-1,65 (br m, 2H), 1,00 (t, 3H, J = 7,4 Hz).
E je m p lo 479. {4 -[4 -(7 -F lu o ro q u in o lin -3 - il) - fe n o x i]-p ip e r id in -1 - il}-(R )-te tra h id ro -fu ra n -2 - il-m e ta n o n a .
Este ejemplo se sintetizó a partir de 7-fluoro-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (95 mg, 0,29 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (60 uL, 0,63 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,09 g, 65%). Análisis: LCMS m/z = 421 (M+1). 1H NMR (DMSO-d6) 6: 9,25 (s, 1H), 8,64 (s, 1H), 8,12 (m, 1H), 7,81 (m, 2H), 7,76 (m, 1H), 7,58 (m, 1H), 7,18 (m, 2H), 4,71 (m, 2H), 3,77 (br m, 4H), 3,36 (m, 1H), 3,26 (m, 1H), 2,02 (m, 4H), 1,84 (m, 2H), 1,52-1,66 (m, 2H).
Ejemplo 480. {4-[4-(3-Ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetra-hidrofuran-2-il-metanona.
Etapa 1. t-butil éster del ácido 4-[4-(3-Ciclopropilisoquinolin-6-il)-fenoxi]-piperidina-1 -carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidina-1-carboxílico (0,59 g, 1,35 mmol) y ácido ciclopropilborónico (0,58 g, 6,74 mmol) de manera análoga al Ejemplo 430. El producto se aisló como un sólido (0,08 g, 14%). Análisis: LCMS m/z = 445 (M+1).
Etapa 2. 3-Ciclopropil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina se preparó a partir del producto de la Etapa 1 anterior (0,08 g, 0,19 mmol) y t Fa (4 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,06 g, 95%). Análisis: LCMS m/z = 345 (M+1).
Etapa 3. {4-[4-(3-Ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidro-furan-2-il-metanona se preparó a partir del producto de la Etapa 3 anterior (61 mg, 0,18 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (34 uL, 0,35 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,03 g, 41%). Análisis: LCMS m/z = 443 (M+1).
1H NMR (DMSO-d6) 6: 9,14 (s, 1H), 8,05 (d, 2H, J = 9,4 Hz), 7,86 (m, 1H), 7,76 (m, 2H), 7,70 (s, 1H), 7,15 (d, 2H, J = 8,7 Hz), 4,69 (m, 2H), 3,77 (br m, 4H), 3,36 (m, 1H), 3,29 (m, 1H), 2,22 (m, 1H), 2,01 (m, 4H), 1,80 (m, 2H), 1,54 - 1,65 (br m, 2H), 0,99 (m, 4H).
Ejemplo 481. Ciclopropil-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 1-metil-6-[4-(piperidin-4-iloxi)-fenil]-isoquinolina (63 mg, 0,20 mmol) y cloruro de ciclopropanocarbonilo (30 uL, 0,3 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,05 g, 63%). Análisis: LCMS m/z = 387 (M+1). 1H NMR (DMSO-d6) 6: 8,34 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H J = 8,7 Hz), 8,18 (m, 1H), 7,98 (m, 1H), 7,81 (d, 2H, J = 8,7 Hz), 7,70 (d, 1H, J = 5,8 Hz), 7,16 (d, 2H, J = 8,7 Hz), 4,74 (m, 1H), 3,98 (m, 1H), 3,89 (m, 1H), 3,56 (m, 1H), 3,29 (m,1H), 2,70 (s, 3H), 2,00 (br m, 3H), 1,55-1,65 (br m, 2H), 0,71 (m, 4H).
E je m p lo 482. {4 -[4 -(7 -M e tilq u in o lin -3 - il) - fe n o x i]-p ip e r id in -1 - il} -(R )-te tra h id ro -fu ra n -2 - il-m e ta n o n a , HCl.
Este ejemplo se sintetizó a partir de 7-metil-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (90 mg, 0,3 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (54 uL, 0,57 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,06 g, 50%). LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 9,28 (s, 1H), 8,71 (s,1H), 7,93 (d, 1H, J = 7,9 Hz), 7,86 (m, 2H), 7,67 (d, 1H, J=6,9 Hz), 7,57 (m, 1H), 7,19 (d, 2H, J=8,6 Hz), 5,58 (br m, 1H), 4,74 (m, 2H), 3,77 (m, 4H), 3,35-3,48 (br m, 2H), 2,76 (s, 3H), 2,02 (br m, 4H), 1,84 (m, 2H), 1,52-1,69 (br m, 2H).
Ejemplo 483. 1-{4-[4-(6-Metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Etapa 1. t-butil éster del ácido 4-[4-(6-Metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-6-metil-quinolina (413 mg, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,49 g, 94%). Análisis: LCMS m/z = 419 (M+1).
Etapa 2. 6-Metil-3-[4-(piperidin-4-iloxi)-fenil]-quinolina se preparó a partir del producto de la Etapa 2 anterior (0,49 g, 1,16 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,35 g, 94%). Análisis: LCMS m/z = 319 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (86 mg, 0,27 mmol) y cloruro de propanoilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,06 g, 54%). Análisis: LCMS m/Z = 375 (M+1). 1H NMR (DMSO-d6) 6: 9,38 (s, 1H), 8,94 (s, 1H), 8,13 (d, 1H, J = 8,6Hz), 7,96 (s, 1H), 7,90 (m, 2H), 7,80 (m, 1H), 7,21 (m, 2H), 4,75 (m, 1H), 3,89 (m, 1H), 3,70 (m, 1H), 3,25-3,38 (br m, 2H), 2,56 (s, 3H), 2,34 (m, 2H), 1,99 (br m, 2H), 1,51-1,67 (br m, 2H), 1,00 (t, 3H, J = 7,4 Hz).
Ejemplo 484. Ciclopropil-{4-[4-(6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona, HCl.
Este ejemplo se sintetizó a partir de 6-metil-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (86 mg, 0,27 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 398. El producto se aisló como un sólido (0,06 g, 61%). Análisis: LCMS m/z = 387 (M+1). 1H NMR (DMSO-d6) 6: 9,38 (s, 1H), 8,94 (s, 1H), 8,13 (d, 1H, J = 8,6 Hz), 7,96 (s, 1H), 7,90 (m, 2H), 7,80 (m, 1H), 7,21 (m, 2H), 4,77 (m, 1H), 3,99 (m, 1H), 3,89 (m, 1H), 3,57 (m, 1H), 3,30 (m, 1H), 2,56 (s, 3H), 2,01 (br m, 3H), 1,50-1,66 (br m, 2H), 0,72 (m, 4H).
E je m p lo 485. {4 -[4 -(6 -M e tilq u in o lin -3 - il) - fe n o x i]-p ip e r id in -1 - il} -(R )-te tra h id ro -fu ra n -2 - il-m e ta n o n a , HCl.
Este ejemplo se sintetizó a partir de 6-metil-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (86 mg, 0,27 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (52 uL, 0,54 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,05 g, 41%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 9,38 (s, 1H), 8,94 (s, 1H), 8,13 (d, 1H, J = 8,6 Hz), 7,96 (s, 1H), 7,90 (m, 2H), 7,80 (m, 1H), 7,21 (m, 2H), 4,76 (m, 1H), 4,69 (m, 1H), 3,77 (m, 4H), 3,23-3,48 (br m, 2H), 2,56 (s, 3H), 1,99 (br m, 4H), 1,84 (br m, 2H), 1,54-1,67 (br m, 2H).
Ejemplo 486. 1-{4-[4-(8-Metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona, HCl.
Etapa 1. t-butil éster del ácido 4-[4-(8-Metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico se preparó a partir de t-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (0,5 g, 1,24 mmol) y 3-bromo-8-metil-quinolina (413 mg, 1,86 mmol) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,49 g, 94%). Análisis: LCMS m/z = 419 (M+1).
Etapa 2. 8-Metil-3-[4-(piperidin-4-iloxi)-fenil]-quinolina se preparó a partir del producto de la Etapa 1 anterior (0,49 g, 1,17 mmol) y TFA (2 mL) de manera análoga al Ejemplo 378. El producto se aisló como un sólido (0,36 g, 98%). Análisis: LCMS m/z = 319 (M+1).
Etapa 3. El compuesto del título se preparó a partir del producto de la Etapa 2 anterior (91 mg, 0,28 mmol) y cloruro de propanoilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 424. El producto se aisló como un sólido (0,07 g, 59%). Análisis: LCMS m/z = 375 (M+1). 1H NMR (DMSO-d6) 6: 9,46 (s, 1H), 9,14 (s, 1H), 8,17 (d, 1H, J = 8,4 Hz), 8,05 (s, 1H), 7,92 (d, 2H, J = 8,8 Hz), 7,72 (m, 1H), 7,21 (d, 2H, J = 8,8 Hz), 4,75 (m, 1H), 3,90 (m, 1H), 3,87 (m, 1H), 3,24 3,38 (br m, 2H), 2,61 (s, 3H), 2,34 (m, 2H), 1,92 (br m, 2H), 1,50-1,67 (m, 2H), 1,00 (t, 3H, J = 7,4 Hz).
Ejemplo 487 Ciclopropil-{4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona.
Este ejemplo se sintetizó a partir de 8-metil-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (91 mg, 0,28 mmol) y cloruro de ciclopropanocarbonilo (40 uL, 0,5 mmol) de manera análoga al Ejemplo 396. El producto se aisló como un sólido (0,03 g, 28%). Análisis: LCMS m/z = 387 (M+1). 1H NMR (DMSO-d6) 6: 9,17 (d, 1H, J = 2,4 Hz), 8,51 (d, 1H, J = 2,1 Hz), 7,93 (m, 1H), 7,79 (m, 3H), 7,48 (m, 1H), 7,15 (m, 2H), 4,74 (m, 1H), 3,98 (m, 1H), 3,89 (m, 1H), 3,36 (m, 2H), 2,54 (s, 3H), 2,00 (br m, 3H), 1,55-1,66 (br m, 2H), 0,71 (m, 4H).
E je m p lo 488. {4 -[4 -(8 -M e tilq u in o lin -3 - il) - fe n o x i]-p ip e r id in -1 - il} -(R )-te tra h id ro -fu ra n -2 - il-m e ta n o n a .
Este ejemplo se sintetizó a partir de 8-metil-3-[4-(piperidin-4-iloxi)-fenil]-quinolina (91 mg, 0,28 mmol) y ácido (R)-tetrahidrofuran-2-carboxílico (55 uL, 0,57 mmol) de manera análoga al Ejemplo 418. El producto se aisló como un sólido (0,05 g, 45%). Análisis: LCMS m/z = 417 (M+1). 1H NMR (DMSO-d6) 6: 9,17 (d, 1H, J = 2,4 Hz), 8,51 (d, 1H, J = 2,1 Hz), 7,93 (m, 1H), 7,79 (m, 3H), 7,48 (m, 1H), 7,15 (m, 2H), 4,73 (m, 2H), 3,71-3,87 (br m, 4H), 3,37 (m, 1H), 3,25 (m, 1H), 2,54 (s, 3H), 2,01 (br m, 4H), 1,84 (m, 2H), 1,53-1,66 (br m, 2H).
Ejemplo 489 t-butil éster del ácido 4-(3',4'-Dimetoxibifenil-4-iloxi)-piperidina-1-carboxílico.
Acetato de paladio (0,008 g, 0,04 mmol), trifenilfosfina (0,023 g, 0,088 mmol) y 1,4-dioxano (4,6 mL) se combinaron y se agitaron. t-butil éster del ácido 4-(4-Yodofenoxi)-piperidina-1-carboxílico (0,408 g, 1,01 mmol), ácido 3,4-dimetoxifenilborónico (0,218 g, 1,20 mmol), DMF (6,7 mL), 1 M de solución acuosa de Na2CO3 (1,5 mL, 1,5 mmol) se añadieron y la reacción se purgó con nitrógeno y se calentó a 80 °C por 2 horas. La reacción se concentró y el residuo se disolvió en EtOAc, se lavó con 1M Na2CO3, agua, y salmuera. La fase orgánica se secó sobre MgSO4, se filtró, se concentró y se purificó por normal fase cromatografía eluyendo con EtOAc/hexano para producir 220 mg (53%) de un sólido blancuzco. Análisis: LCMS: m/z = 314 (M+1); 1H NMR (400 MHz, CDCb) 6:: 7,46 (m, 2H), 7,07 (m, 2H), 6,94 (m, 3H), 4,50 (m, 1H), 3,94 (s, 3H), 3,91 (s, 3H), 3,72 (m, 2H), 3,36 (m, 2H), 1,93 (m, 2H), 1,79 (m, 2H), 1,48 (s, 9H).
Ejemplo 490. t-butil éster del ácido 4-(4'-Ciano-bifenil-4-iloxi)-piperidina-1 -carboxílico.
Este ejemplo se preparó usando el procedimiento anterior con ácido 4-cianofenil-borónico para producir el compuesto del título, un sólido blanco (60). Análisis: LCMS: m/z = 379 (M+1); 1H NMR (400 MHz, DMSO-d6) 6:: 7,85 (m, 4H), 7,70 (m, 2H), 7,10 (m, 2H), 4,65 (m, 1H), 3,67 (m, 2H), 3,20 (m, 2H), 1,94 (m, 2H), 1,54 (m, 2H), 1,41 (s, 9H).
Ejemplo 491. 1-[4-(3',4'-Dimetoxi-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona
Etapa 1. t-butil éster del ácido 4-(3',4'-Dimetoxibifenil-4-iloxi)-piperidina-1-carboxílico (0,200 g, 0,484 mmol) y 4 M de HCl en 1,4-dioxano (5,0 mL, 20 mmol) se agitaron a 60 °C por 80 min. La reacción se concentró y el residuo se disolvió en etil-acetato, se lavó con 1M Na2CO3, agua, y salmuera. La fase orgánica se secó con sulfato de magnesio, se filtró, se concentró y se purificó por normal fase cromatografía eluyendo con DCM y luego 60/40/0,4 DCM/metanol/isopropilamina para producir 82 mg (54%) de un sólido blanco. Análisis: LCMS: m/z = 314 (M+1); 1H
NMR (400 MHz,DMSO-d6) 6: 7,53 (m, 2H), 7,12 (m, 2H), 6,99 (m, 3H), 4,41 (m, 1H), 3,83 (s, 3H), 3,77 (s, 3H), 2,94 (m, 2H), 2,57 (m, 2H), 1,91 (m, 2H), 1,45 (m, 2H).
Etapa 2. 4-(3',4'-Dimetoxibifenil-4-iloxi)-piperidina (0,032 g, 0,10 mmol) y DIPEA (0,0534 mL, 0,306 mmol) en THF (2 mL) se añadió cloruro de propanoilo (18 uL, 0,20 mmol) y se agitó a temperatura ambiente por 1 h. La reacción se concentró, se disolvió en EtOAc, y se lavó con 1 M Na2CO3 acuoso, agua, y salmuera. La fase orgánica se secó con MgSO4 , se filtró y se concentró. El residuo se purificó por normal fase cromatografía eluyendo con hexano/etil acetato para producir 21,5 mg (57%) de un sólido amarillo. Análisis: LCMS m/z = 370 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,55 (m, 2H), 7,13 (m, 2H), 7,01 (m, 3H), 4,64 (m, 1H), 3,89 (m, 1H), 3,88 (s, 3H), 3,77 (s, 3H), 3,69 (m, 1H), 3,36 (m, 1H), 3,25 (m, 1H), 2,33 (m, 2H), 1,93 (m, 2H), 1,56 (m, 2H), 0,99 (m, 3H).
Ejemplo 492. 1-[4-(3',4'-Dimetoxibifenil-4-iloxi)-piperidin-1-il]-2-metil-propan-1-ona.
Este ejemplo se sintetizó usando cloruro de isobutirilo para producir un sólido amarillo (70%). Análisis: LCMS m/z = 384 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,55 (m, 2H), 7,13 (m, 2H), 7,01 (m, 3H), 4,65 (m, 1H), 3,86 (m, 1H), 3,83 (s, 3H), 3,77 (s, 3H), 3,76 (m, 1H), 3,39 (m, 1H), 3,26 (m, 1H), 2,90 (m, 1H), 1,97 (m, 2H), 1,54 (m, 2H), 1,00 (d, 6H, J = 6,7 Hz)
Los siguientes ejemplos se sintetizaron usando el procedimiento para los Ejemplos 541 y 543.
Ejemplo 493. 4'-(1-Propionil-piperidin-4-iloxi)-bifenil-4-carbonitrilo.
El producto se aisló como un sólido blanco. Análisis: LCMS m/z = 335 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,86 (m, 4H), 7,70 (m, 2H), 7,11 (m, 2H), 4,71 (m, 1H), 3,87 (m, 1H), 3,68 (m, 1H), 3,25 (m, 2H), 2,34 (m, 2H), 1,91 (m, 2H), 1,55 (m, 2H), 0,99 (m, 3H).
Ejemplo 494. 4'-(1-Isobutirilpiperidin-4-iloxi)-bifenil-4-carbonitrilo.
A ná lis is : LC M S m /z = 349 (M 1); 1H N M R (400 M H z, D M S O -d6) 6: 7 ,86 (m, 4H ), 7 ,70 (m, 2H ), 7,11 (m, 2H ), 4 ,72 (m, 1H), 3 ,83 (m, 2H ), 3 ,33 (m, 2H ), 2 ,90 (m, 1H), 1 ,98 (m, 2H ), 1 ,57 (m, 2H ), 1,00 (d, 6H , J = 6 ,7 Hz).
E je m p lo 495. 4 '-(1 -C ic lo p ro p a n o c a rb o n il-p ip e r id in -4 - ilo x i)-b ife n il-4 -c a rb o n itr ilo .
Análisis: LCMS: m/z = 347 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,86 (m, 4H), 7,71 (m, 2H), 7,12 (m, 2H), 4,73 (m, 1H), 3,94 (m, 2H), 3,54 (m, 1H), 3,27 (m, 1H), 1,96 (m, 3H), 1,58 (m, 2H), 0,71 (m, 4H).
Ejemplo 496. 1-[4-(3-Quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona.
Este ejemplo se sintetizó a partir de t-butil éster del ácido 4-(3-bromofenoxi)-piperidina-1-carboxílico. Análisis: LCMS: m/z = 361 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,25 (d, 1H, J = 2,3 Hz), 8,66 (m, 1H), 8,06 (m, 2H), 7,78 (m, 1H), 7,66 (m, 1H), 7,46 (m, 3H), 7,09 (m, 1H), 4,79 (m, 1H), 3,89 (m, 1H), 3,72 (m, 1H), 3,33 (m, 2H), 2,34 (m, 2H), 1,99 (m, 2H), 1,59 (m, 2H), 1,00 (m, 3H).
Ejemplo 497. Ciclopropil-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona.
Análisis: LCMS: m/z=3732 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,25 (d, 1H, J=2,4 Hz), 8,67 (m, 1H), 8,05 (m, 2H), 7,78 (m, 1H), 7,66 (m, 1H), 7,48 (m, 3H), 7,10 (m, 1H), 4,82 (m, 1H), 3,99 (m, 2H), 3,57 (m, 1H), 3,33 (m, 1H), 2,01 (m, 3H), 1,62 (m, 2H), 0,72 (m, 4H).
Ejemplo 498. 1-{4-[4-(5,6-Dimetoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
Análisis: LCMS: m/z = 371 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,93 (d, 1H, J = 1,6 Hz), 7,60 (d, 2H, J = 8,6 Hz), 7,48 (s, 1H), 7,07 (d, 2H, J = 8,6 Hz), 4,67 (m, 1H), 3,87 (m, 7H), 3,70 (m, 1H), 3,27 (m, 2H), 2,33 (m, 2H), 1,93 (m, 2H), 1,58 (m, 2H), 0,99 (m, 3H).
E je m p lo 499. C ic lo p ro p il-{4 -[4 -(5 ,6 -d im e to x ip ir id in -3 - il) - fe n o x i]-p ip e r id in -1 - il}-m e ta n o n a .
Análisis: LCMS: m/z =383 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,93 (d, 1H, J=2,0 Hz), 7,61 (d, 2H, J=8,8 Hz), 7,47 (d, 1H, J=2,0 Hz), 7,07 (d, 2H, J=8,8 Hz), 4,69 (m, 1H), 3,97 (m, 1H), 3,88 (m, 7H), 3,56 (m, 1H), 3,28 (m, 1H), 1,97 (m, 3H), 1,57 (m, 2H), 0,71 (m, 4H).
Ejemplo 500. 1-[4-(3',4'-Diclorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS: m/z = 378 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,88 (d, 1H, J = 2,0 Hz), 7,66 (m, 4H), 7,08 (d, 2H, J = 8,8 Hz), 4,69 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,25 (m, 2H), 2,33 (m, 2H), 1,96 (m 2H), 1,56 (m, 2H), 0,99 (m, 3H).
Ejemplo 501. Ciclopropil-[4-(3',4'-diclorobifenil-4-iloxi)-piperidin-1-il]-metanona.
Análisis: LCMS: m/z = 390 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,88 (d, 1H, J = 2,0 Hz), 7,66 (m, 4H), 7,09 (d, 2H, J = 8,8 Hz), 4,71 (m, 1H), 3,93 (m, 2H), 3,56 (m, 1H), 3,25 (m, 1H), 1,97 (m, 3H), 1,58 (m, 2H), 0,71 (m, 4H).
Ejemplo 502. 1-{4-[4-(2,3-Dihidro-1,4-benzodioxin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona.
A ná lis is : LC M S : m /z = 368 (M 1); 1H N M R (400 M H z, D M SO -d6) 6: 7 ,49 (d, 2H , J = 8 ,8 Hz), 7 ,03 (m, 4H ), 6 ,89 (d, 1H, J = 8 ,4H z), 4 ,63 (m , 1H), 4 ,26 (s, 4H ), 3 ,87 (m, 1H), 3 ,68 (m, 1H), 3 ,24 (m, 2H ), 2 ,33 (m, 2H ), 1 ,93 (m, 2H ), 1 ,55 (m, 2H ), 0 ,99 (m, 3H).
E je m p lo 503. C ic lo p ro p il-{4 -[4 -(2 ,3 -d ih id ro -1 ,4 -b e n z o d io x in -6 - il) - fe n o x i]-p ip e r id in -1 - il}-m e ta n o n a .
Análisis: LCMS: m/z = 380 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 7,50 (d, 2H, J = 8,8 Hz), 7,04 (m, 4H), 6,89 (m, 1H), 4,65 (m, 1H), 4,26 (s, 4H), 3,93 (m, 2H), 3,54 (m, 1H), 3,26 (m, 1H), 1,96 (m, 3H), 1,57 (m, 2H), 0,71 (m, 4H). Ejemplo 504. 1-[4-(4'-Benziloxi-2'-fluoro-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS: m/z = 434; 1H NMR (400 MHz, DMSO-d6) 6: 7,41 (m, 8H), 6,99 (m, 4H), 5,16 (s, 2H), 4,65 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,30 (m, 2H), 2,33 (m, 2H), 1,94 (m, 2H), 1,56 (m, 2H), 0,99 (m, 3H).
Ejemplo 505. [4-(4'-Benziloxi-2'-fluorobifenil-4-iloxi)-piperidin-1-il]-ciclopropil-metanona.
Análisis: LCMS: m/z = 446; 1H NMR (400 MHz, DMSO-d6) 6: 7,41 (m, 8H), 7,06 (d, 2H, J = 8,8 Hz), 6,96 (m, 2H), 5,16 (s, 2H), 4,68 (m, 1H), 3,93 (m, 2H), 3,54 (m, 1H), 3,27 (m, 1H), 1,97 (m, 3H), 1,58 (m, 2H), 0,71 (m, 4H).
Ejemplo 506. 1-[4-(5'-Benziloxi-3'-fluorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona.
A ná lis is : LC M S : m /z = 434; 1H N M R (400 M Hz, D M S O -d6) 6: 7 ,63 (m, 2H ), 7 ,48 (m, 2H ), 7,41 (m, 2H ), 7 ,34 (m, 1H), 7 ,07 (m, 4H ), 6 ,85 (m, 1H), 5 ,19 (s, 2H ), 4 ,68 (m, 1H), 3 ,87 (m, 1H), 3 ,68 (m, 1H), 3 ,28 (m, 2H ), 2 ,34 (m, 2H ), 1 ,93 (m, 2H ), 1,56 (m, 2H ), 0 ,99 (m, 3H).
E je m p lo 507. [4 -(5 '-B e n z ilo x i-3 '- f lu o ro b ife n il-4 - ilo x i)-p ip e r id in -1 - il]-c ic lo p ro p il-m e ta n o n a .
Análisis: LCMS: m/z = 446; 1H NMR (400 MHz, DMSO-d6) 6: 7,63 (m, 2H), 7,48 (m, 2H), 7,41 (m, 2H), 7,35 (m, 1H), 7,07 (m, 4H), 6,85 (m, 1H), 5,20 (s, 2H), 4,70 (m, 1H), 3,93 (m, 2H), 3,55 (m, 1H), 3,28 (m, 1H), 1,97 (m, 3H), 1,58 (m, 2H), 0,71 (m, 4H).
Ejemplo 508. 1-[4-(4'-Fenoxibifenil-4-iloxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS: m/z = 402; 1H NMR (400 MHz, DMSO-d6) 6: 8,75 (m, 2H), 7,62 (m, 2H), 7,56 (m, 2H), 7,41 (m, 2H), 7,16 (m, 1H), 7,05 (m, 6H), 4,65 (m, 1H), 3,88 (m, 1H), 3,69 (m, 1H), 3,27 (m, 2H), 2,34 (m, 2H), 1,95 (m, 2H), 1,55 (m, 2H), 0,99 (m, 3H).
Ejemplo 509. Ciclopropil-[4-(4'-fenoxibifenil-4-iloxi)-piperidin-1-il]-metanona.
Análisis: LCMS: m/z = 414; 1H NMR (400 MHz, DMSO-d6) 6: 7,60 (m, 4H), 7,41 (m, 2H), 7,16 (m, 1H), 7,06 (m, 6H), 4,68 (m, 1H), 3,94 (m, 2H), 3,55 (m, 1H), 3,27 (m, 1H), 1,97 (m, 3H), 1,58 (m, 2H), 0,71 (m, 4H).
Ejemplo 510. 1-[4-(3'-Fenoxibifenil-4-iloxi)-piperidin-1-il]-propan-1-ona.
Análisis: LCMS: m/z = 402; 1H NMR (400 MHz, DMSO-d6) 6: 7,56 (m, 2H), 7,41 (m, 4H), 7,23 (m, 1H), 7,16 (m, 1H), 7,06 (m, 4H), 6,92 (m, 1H), 4,65 (m, 1H), 3,87 (m, 1H), 3,69 (m, 1H), 3,27 (m, 2H), 2,33 (m, 2H), 1,95 (m, 2H), 1,56 (m, 2H), 0,99 (m, 3H).
E je m p lo 511. C ic lo p ro p il-[4 -(3 '- fe n o x ib ife n il-4 - ilo x i)-p ip e r id in -1 - il]-m e ta n o n a .
Análisis: LCMS: m/z = 414; 1H NMR (400 MHz, DMSO-d6) 6: 7,57 (m, 2H), 7,42 (m, 4H), 7,23 (m, 1H), 7,16 (m, 1H), 7,06 (m, 4H), 6,93 (m, 1H), 4,68 (m, 1H), 3,93 (m, 2H), 3,54 (m, 1H), 3,27 (m, 1H), 1,96 (m, 3H), 1,58 (m, 2H), 0,71 (m, 4H).
Ejemplo 512. 2-Metil-1-[4-(4-quinolin-7-il-bencenosulfonil)-piperidin-1-il]-propan-1-ona.
Etapa 1. 1-[4-(4-Bromobencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona.
4-(4-Bromobencenosulfonil)piperidina HCl (0,300 g, 0,881 mmol) suspended en THF (5 mL) se añadió DIPEA (0,767 mL, 4,40 mmol) a temperatura ambiente. Cloruro de isobutirilo (0,186 mL, 1,76 mmol) se añadió en forma de gotas y la mezcla se agitó 4 h y se concentró. El residuo se particionó entre EtOAc y en Na2CO3, se lavó con agua y salmuera y luego se secó. El producto se trituró con éter para dar un sólido blanco (275 mg, 85%). LCMS m/z = 375 (M 1); 1H NMR (CDCla) 6: 7,70 (s, 4H), 4,76 (m, 1H), 4,09 (m, 1H), 2,98-3,14 (m, 2H), 2,69-2,77 (m, 1H), 2,48 (m, 1H), 2,11 (m, 1H), 1,95 (m, 1H), 1,60-1,72 (m, 2H), 1,10 (d, 6H, J = 7 Hz).
Etapa 2. 2-Metil-1-[4-(4-quinolin-7-il-bencenosulfonil)-piperidin-1-il]-propan-1-ona.
Acetato de paladio (0,00195 g, 0,00868 mmol) y trifenilfosfina (0,00911 g, 0,0347 mmol) en 1,4-dioxano (2 mL, 20 mmol) se agitaron bajo una atmósfera de nitrógeno por 15 min. 1-[4-(4-Bromobencenosulfonil)-piperidin-1-il]-2-metilpropan-1-ona (0,0650 g, 0,174 mmol), ácido quinolina-7-borónico (0,0360 g, 0,208 mmol), DMF (4 mL) y 1 M de carbonato de sodio (0,695 mL) se añadieron y se calentaron a 80 °C por 16 h. La mezcla se concentró, se disolvió en EtOAc y se lavó con en Na2CO3, agua y salmuera luego se secó sobre MgSO4. El producto se purificó en ISCO (95/5 DCM/MeOH). La sal de HCl se sintetizó añadiendo en HCl-éter a una solución EtOAC de la base, y se cristalizó el sólido blanco a partir de éter de acetona. Análisis: LCMS m/z = 423 (M 1); 1H NMR (DMSO) 6: 9,14 (d, 1H, J = 3 Hz), 8,77 (d, 1H, J =8 Hz), 8,50 (s, 1H), 8,30 (d, 1H, J = 8,7 Hz), 8,16-8,20 (m, 3H), 8,02 (d, 2H, J =8,6 Hz), 7,81 (dd, 1H, J = 4, 8 Hz), 4,49 (d, 1H, J = 12 Hz), 4,05 (d, 1H, J = 12 Hz), 3,63-3,69 (m, 1H), 3,03 (t, 1H, J =12Hz), 2,84 (q, 1H, J=7,6 Hz), 1,92 (bm, 2H), 1,47 (m, 1H), 1,35 (m, 1H), 0,96 (d, 6H, J=7 Hz).
Los siguientes ejemplos se sintetizaron usando 1-[4-(4-bromobencenosulfonil)piperidin-1-il]-2-metil-propan-1-ona y el ácido borónico apropiado para el procedimiento anterior.
Ejemplo 513. 1-[4-(4-Isoquinolin-7-il-bencenosulfonil)-piperidin-1-il]-2-metilpropan-1-ona.
Análisis: LCMS m/z = 423 (M 1); 1H NMR (CDCla) 6: 9,36 (s, 1H), 8,60 (d, 1H, J = 6 Hz), 8,27 (s, 1H), 8,00 (d, 2H, J = 8,5Hz), 7,97 (s, 2H), 7,91 (d, 2H, J =8,5 Hz), 7,71 (d, 1H, J =6 Hz), 4,78 (d, 1H, J = 10 Hz), 4,09 (d, 1H, J = 10 Hz),
3,18 (tt, 1H, J = 4, 12 Hz),3,04 (t, 1H, J = 12 Hz), 2,76 (q, 1H, J = 6 Hz), 2,51 (t, 1H, J = 12 Hz), 2,20 (d, 1H, J = 12 Hz), 2,02 (d, 1H, J =12 Hz),1,67-1,73 (m, 3H), 1,10 (d, 6H, J = 8 Hz).
Ejemplo 514. 1-[4-(4-Isoquinolin-6-il-bencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona
Análisis: LCMS m/z = 423 (M 1); 1H NMR (DMSO-d6) 6: 9,22 (s, 1H), 8,60 (d, 1H, J = 6 Hz), 8,12 (d, 1H, J =8,3 Hz), 8,05 (s, 1H), 8,00 (d, 2H, J =8,3 Hz), 7,91 (d, 2H, J =8,3 Hz), 7,86 (dd, 1H, J = 2, 8 Hz), 7,74 (d, 1H, J = 6 Hz), 4,78 (d, 1H, J =12 Hz), 4,10 (d, 1H, J = 12 Hz), 3,19 (tt, 1H, J =4, 12 Hz), 3,04 (t, 1H, J =12 Hz), 2,76 (q, 1H, J = 7Hz), 2,51 (t, 1H, J =12,5 Hz), 2,21 (d, 1H, J = 10,4 Hz), 2,01 (d, 1H, J = 12 Hz), 1,68-1,78 (m, 2H), 1,10 (d, 6H, J = 7 Hz).
Ejemplo 5151-[4-(4-Benzofuran-5-il-bencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona.
Análisis: LCMS m/z = 412 (M 1); 1H NMR (CDCla) 6: 7,92 (d, 2H, J = 8 Hz), 7,83 (d, 1H, J =2 Hz),7,81 (d, 2H, J = 8 Hz), 7,70 (d, 1h, J = 2 Hz), 7,61 (d, 1H, J= 8,6Hz), 7,54 (dd, 1H, J=2, 8Hz), 6,86 (d, 1H, J=2Hz), 4,78 (d, 1H, J=11 Hz), 4,08 (d, 1H, J=11 Hz), 3,16 (tt, 1H, J=4, 12Hz), 3,03 (t, 1H, J=12Hz), 2,76 (q, 1H, J=7Hz), 2,51 (t, 1H, J=12Hz, 2,18 (d, 1H, J=11 Hz), 2,00 (d, 1H, J=12Hz), 1,61-1,73 (m, 2H), 1,10 (d, 6H, J=7Hz).
Ejemplo 516. 1-(4-((4-(quinolin-7-il)fenil)tio)piperidin-1-il)propan-1-ona, HCl.
Etapa 1. 1-(4-((4-Bromofenil)tio)piperidin-1-il)propan-1-ona
A una solución de 4-((4-bromofenil)tio)piperidina (500 mg, 1,83 mmol) en DCM (10 mL) se añadió TEA (0,8 mL, 5,5 mmol) a temperatura ambiente y la mezcla de reacción se enfrió hasta 0 °C cuando se añadió cloruro de propionilo (254 mg, 2,75 mol) en forma de gotas. La reacción luego se agitó a temperatura ambiente por 15 h. Después del completamiento, la reacción se diluyó con DCM y se lavó con agua. La capa orgánica se secó sobre Na2SO4, se concentró y el producto crudo se purificó por cromatografía de columna usando gel de sílice para dar 1-(4-((4-bromofenil)tio)piperidin-1-il)propan-1-ona (600 mg, 90%) como un aceite incoloro. Análisis: 1H NMR (400 MHz, CDaOD) 6: 7,49 (m, 2H), 7,35 (m, 2H), 4,30 (m, 1H), 3,91 (m, 1H), 3,42 (m, 1H), 3,23 (m, 1H), 2,95 (m, 1H), 2,39 (q, J = 7,5 Hz, 2H), 1,99 (m, 2H), 1,48 (m, 2H), 1,10 (t, J = 7,5 Hz, 3H).
Etapa 2. 1-(4-((4-(Quinolin-7-il)fenil)tio)piperidin-1-il)propan-1-ona, HCl.
A una solución del producto de la Etapa 1 (1 equiv) en 1,4 dioxano: agua (3:1) se añadió Na2CO3 (3 equiv) y ácido quinolin-7-borónico (1,2 equiv) y la mezcla de reacción se desgasificó con argón por 20 min. A esto le siguió la adición de tetraquis(trifenilfosfina)-paladio (0,01 equiv) y la mezcla de reacción se calentó a 100 °C por 15 h. La mezcla de reacción se enfrió hasta la temperatura ambiente y filtró a través de celite, el filtrado se concentró, se diluyó con EtOAc y se lavó con agua. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El producto crudo se purificó por cromatografía de columna usando gel de sílice para obtener la base libre que se convirtió a la sal de hidrocloruro
mediante tratamiento con 4M HCl en dioxano para dar 1-(4-((4-(quinolin-7-il)fenil)tio)piperidin-1-il)propan-1-ona hidrocloruro (32%). mp 188 °C; Análisis: LCMS (ESI) 377 (M+1); 1H NMR (400 MHz, DMSO-d6) 6 : 9,29 (d, J = 5,2 Hz, 1H), 9,13 (d, J = 8,3 Hz, 1H), 8,61 (s, 1H), 8,43 (d, J = 8,7 Hz, 1H), 8,29 (d, J = 8,7 Hz, 1H), 8,03 (dd, J = 8,3, 5,2 Hz, 1H), 7,86 (d, J = 8,4 Hz, 2H), 7,61(d, J = 8,4 Hz, 2H), 4,21 (d, J = 13,3 Hz, 1H), 3,81 (d, J = 13,3 Hz, 1H), 3,68 (m, 1H), 3,19 (m, 1H), 2,88 (m, 1H), 2,31 (t, J = 7,4 Hz, 2H), 1,99 (m, 2H), 1,56 -1,29 (m, 2H), 0,97 (t, J = 7,4 Hz, 3H).
Los siguientes ejemplos se prepararon por analogía con el Ejemplo 516, usando ácido heteroarilborónico y cloruro ácido requeridos.
Ejemplo 517. 1-(4-((4-(Isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona, HCl.
Análisis: mp 222 °C; 1H NMR (400 MHz, DMSO-d6) 6 : 9,89 (s, 1H), 8,74 - 8,58 (m, 3H), 8,49 (d, J = 6 , 6 Hz, 1H), 8,40 (d, J = 8,7, 1H), 7,95 (d, J = 8,4 Hz, 2H), 7,64(d, J = 8,4 Hz, 2H), 4,21 (m, 1H), 3,82 (m, 1H), 3,71 (m, 1H), 3,20 (m, 1H), 2,89 (m, 1H), 2,31 (q, J = 7,4 Hz, 2H), 1,99 (m, 2H), 1,47 (m, 1H), 1,38 (m, 1H), 0,97 (t, J = 7,4 Hz, 3H).
Ejemplo 518. 1-(4-((4-(Quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona, HCl.
Análisis: mp 70°C; 1H NMR (400 MHz, CD3 OD) 6 : 9,15 (s, 1H), 8,60 (s, 1H), 8,11 - 8,00 (m, 2H), 7,85 - 7,75 (m, 2H), 7,71 - 7,51 (m, 4H), 4,32 (m, 1H), 3,93 (m, 1H), 3,55 (m, 1H), 3,00 (m, 1H), 2,41 (q, J = 7,5 Hz, 2H), 2,07 (m, 1H), 1,64 - 1,54 (m, 1H), 1,56 - 1,47 (m, 1H), 1,34 - 1,20 (m, 2H), 1,11 (t, J = 7,5 Hz, 3H).
Ejemplo 519. 1-(4-((4-(Isoquinolin-4-il)fenil)tio)piperidin-1-il)propan-1-ona, HCl.
Análisis: mp 8 8 °C; 1H NMR (400 MHz, DMSO-d6) 6 : 9,95 (s, 1H), 8,70 - 8,62 (m, 2H), 8,21 (m, 1H), 8,12 - 8,01 (m, 2H), 7,62 (m, 4H), 4,22 (m, 1H), 3,82 (m, 1H), 3,72 (m, 1H), 3,21 (m, 1H), 2,92 (m, 1H), 2,32 (q, J = 7,4 Hz, 2H), 2,07 - 1,96 (m, 2H), 1,58 - 1,32 (m, 2H), 0,98 (t, J = 7,4 Hz, 3H).
Ejemplo 520. 1-(4-((4-(Isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona, HCl.
Análisis: mp 120 °C; LCMS (ESI): 391 (M+H)+; 1H NMR (400 MHz, DMSO-d6) 6 : 9,23 (d, J = 5,0 Hz, 1H), 9,00 (d, J = 8,3 Hz, 1H), 8,53 (s, 1H), 8,37 (d, J = 8,7 Hz, 1H), 8,23 (d, J = 8,7 Hz, 1H), 7,94 (dd, J = 8,3, 5,0 Hz, 1H), 7,86 (d, J =
8,4 Hz, 2H), 7,60 (d, J = 8,4 Hz, 2H), 4,22 (d, J = 13,5 Hz, 1H), 3,80 (d, J = 13,5 Hz, 1H), 3,68 (m, 1H), 3,23 (m, 1H), 2,87 (m, 2H), 2,00 (m, 2H), 1,47 (m, 1H), 1,36 (m, 1H), 0,98 (d, J = 6,0 Hz, 6H).
Ejemplo 521. 1-(4-((4-(Isoquinolin-6-il)fenil)tio)piperidin-1-il)-2-metilpropan-1-ona HCl.
Análisis: mp 228 °C; LCMS (ESI): 391 (M+H)+; 1H NMR (400 MHz, DMSO-d6) 6: 9,82 (s, 1H), 8,70 - 8,52 (m, 3H), 8,40 (d, J = 6,0 Hz, 1H), 8,34 (d, J = 8,4Hz, 1H), 7,93 (d, J=8,0Hz, 2H), 7,60 (d, J=8,0Hz, 2H), 4,26-4,17 (m, 1H), 3,91 (m, 1H), 3,70 (m, 1H), 3,24 (m, 1H), 2,86 (m, 2H), 2,07-1,93 (m, 2H), 1,51-1,33 (m, 2H), 0,98 (d, J=6,7Hz, 6H).
Ejemplo 522. 2-Metil-1-(4-((4-(quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona, HCl.
Análisis: mp 130 °C; LCMS (ESI): 391 (M+H)+; 1H NMR (400 MHz, DMSO-d6) 6: 9,48 (s, 1H), 9,09 (s, 1H), 8,22 (d, J = 8,6 Hz, 2H), 7,96 (d, J = 8,6 Hz, 2H), 7,82 (t, J = 7,6 Hz, 1H), 7,67 - 7,50 (m, 3H), 4,22 (m, 1H), 3,91 (m, 1H), 3,69 (m, 1H), 3,23 (m, 1H), 2,87 (m, 2H), 2,06 - 1,92 (m, 2H), 1,45 - 1,31 (m, 2H), 0,98 (d, J = 6,5 Hz, 6H).
Ejemplo 523. 1-(4-((4-(Isoquinolin-4-il)fenil)tio)piperidin-1-il)-2-metilpropan-1-ona HCl.
Análisis: mp 120 °C; LCMS (ESI): 391 (M+H)+; 1H NMR (400 MHz, DMSO-d6) 6: 9,80 (s, 1H), 8,64 (s, 1H), 8,55 (d, J = 8,2 Hz, 1H), 8,12 (m, 1H), 8,07 - 7,96 (m, 2H), 7,67 - 7,50 (m, 4H), 4,24 (m, 1H), 3,92 (m, 1H), 3,71 (m, 1H), 3,25 (m, 1H), 2,88 (m, 2H), 2,03 (m, 2H), 1,49 (m, 1H), 1,39 (m, 1H), 0,99 (d, J = 7,0 Hz, 6H).
Ejemplo 524. 1-{4-[Metil-(4-quinolin-3-il-fenil)-amino]-piperidin-l-il}-propan-1-ona, HCl
Etapa 1. terc-butil éster del ácido 4-[(4-Bromofenil)-metil-amino]-piperidina-1-carboxílico.
Una mezcla de t-butil éster del ácido 4-(4-bromofenilamino)-piperidina-1-carboxílico (1,5 g, 4,22 mmol), K2 CO3 (2,91 g, 21,1 mmol), yoduro de metilo (788 pL, 12,6 mmol), y acetonitrilo (30 mL) se calentó a 80 °C por 24 h. Después de enfriar hasta la temperatura ambiente, la mezcla de reacción se concentró. El residuo se diluyó con DCM (100 mL), se lavó con H2 O, salmuera, se secó (Na2SO4), y se concentró. El residuo se purificó por cromatografía en gel de sílice (0-10% MeOH/DCM) proporcionó 1,0 g (64%) de aceite incoloro. Análisis: 1H NMR (400 MHz, DMSO-d6) 6: 7,25 - 7,31
(2H, m), 6,74 - 6,80 (2H, m), 3,97 - 4,10 (2H, m), 3,73 - 3,85 (1H, m), 2,74 - 2,92 (2H, m), 2,66 (3H, s), 1,48-1,63 (4H, m), 1,40 (9H, s).
Etapa 2 t-butil éster del ácido 4-[Metil-(4-quinolin-3-il-fenil)-amino]-piperidina-1 -carboxílico.
Un frasco cargado con t-butil éster del ácido 4-[(4-bromofenil)-metilamino]-piperidina-1-carboxílico (1,0 g, 2,71 mmol), ácido 3-quinolinaborónico (482 mg, 2,79 mmol), acetato de paladio (61 mg, 0,271 mmol), trifenilfosfina (142 mg, 0,542 mmol), 1,0 M de Na2CO3 (13,5 mL, 13,5 mmol), 1,4-dioxano (10 mL), y DMF (10 mL) se enjuagó con nitrógeno por 15 min. La mezcla de reacción se calentó a 85 °C por 4 h y luego a temperatura ambiente por 2 días. La mezcla de reacción se concentró y el residuo se diluyó con EtOAc (100 mL), se lavó con 1M Na2CO3 solución (35 mL), la capa de agua se extrajo nuevamente con EtOAc (50 mL). Las capas orgánicas combinadas se lavaron con H2 O, salmuera, se secaron (Na2SO4), y se concentraron. El residuo se sometió a cromatografía en gel de sílice (0-70% EtOAc/Hexanos) produjo 586 mg (52%) de aceite amarronado claro. Análisis: 1H NMR (400 MHz, DMSO-d6) 6: 9,21 -9,23 (1H, m), 8,48 - 8,50 (1H, m), 7,98 - 8,02 (2H, m), 7,72 - 7,76 (2H, m), 7,67-7,72 (1H, m), 7,57-7,63 (1H, m), 6,96 7,01 (2H, m), 4,01-4,12 (2H, m), 3,90-4,00 (1H, m), 2,82-2,97 (2H, m), 2,78 (3H, s), 1,53-1,70 (4H, m), 1,42 (9H, s) ppm.
Etapa 3. Metilpiperidin-4-il-(4-quinolin-3-il-fenil)-amina.
A una solución de t-butil éster del ácido 4-[metil-(4-quinolin-3-il-fenil)-amino]-piperidina-1-carboxílico (586 mg, 1,40 mmol) en DCM (20 mL) se añadió 4,0 M de HCl en 1,4-dioxano (3,51 mL, 14,0 mmol) en forma de gotas. Después de 18 h, la precipitación de un sólido rojo se recogió por filtración, se lavó con DCM, se secó para dar 630 mg (100%) de la sal de HCl. Análisis: 1H NMR (400 MHz, DMSO-d6) 6: 9,58 - 9,61 (1 H, m), 9,28 - 9,32 (1 H, m), 8,99 - 9,22 (2 H, m), 8,36 - 8,42 (1 H, m), 8,28 - 8,33 (1 H, m), 8,00 - 8,06 (1 H, m), 7,87 - 7,96 (3 H, m), 7,12 - 7,17 (1 H, m), 4,13 - 4,25 (1 H, m), 3,32 - 3,41 (2 H, m), 3,00 - 3,14 (2 H, m), 2,87 (3 H, s), 2,00 - 2,15 (2 H, m), 1,76-1,87 (2 H, m).
Etapa 4. Un vial cargado con metil-piperidin-4-il-(4-quinolin-3-il-fenil)-amina 3HCl (110 mg, 0,26 mmol), DIPEA (449 pL, 2,58 mmol) en DCM (7 mL) se añadió cloruro de propanoilo (25 pL, 0,28 mmol). Después de 30 min, la reacción se apagó con MeOH (3 mL) y se concentró. El residuo se purificó por HPLC preparativa y las fracciones aisladas se combinaron, se neutralizaron con solución sat. de NaHCO3 (25 mL), se extrajeron con DCM (3 x 25 mL). Las capas orgánicas combinadas se secaron (Na2SO4), y se concentraron. El producto se disolvió en DCM (~5 mL) y se mezcló con 1,2 equivalentes de 0,5 M HCl en MeOH y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se recogió y se secó para dar 91 mg (86%) de sólido rojo. Análisis: LCMS m/z 374 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,55 - 9,61 (1 H, m), 9,24 - 9,30 (1 H, m), 8,26 - 8,39 (2 H, m), 7,93 - 8,08 (3 H, m), 7,86 - 7,93 (1 H, m), 7,16 - 7,49 (1 H, m), 4,49 - 4,60 (2 H, m), 3,92 - 4,10 (2 H, m), 3,06 - 3,19 (1 H, m), 2,85 - 3,00 (3 H, m), 2,55 - 2,70 (1 H, m), 2,34 (2 H, q, J=7,5 Hz), 1,47 - 1,85 (4 H, m), 1,00 (3 H, t, J=7,4 Hz).
Los siguientes compuestos se sintetizaron usando el procedimiento para el ejemplo 524.
Ejemplo 525. Ciclopropil-{4-[metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-metanona, HCl.
El producto se aisló como un sólido rojo. Análisis: LCMS m/z 386 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,57 - 9,61 (1 H, m), 9,26 - 9,31 (1 H, m), 8,34 - 8,39 (1 H, m), 8,27 - 8,33 (1 H, m), 7,94 - 8,07 (3 H, m), 7,86 - 7,93 (1 H, m), 6,90 - 7,75 (2 H, m), 4,47 - 4,58 (1 H, m), 4,34 - 4,45 (1 H, m), 4,01 - 4,13 (1 H, m), 3,12 - 3,28 (1 H, m), 2,83 - 3,04 (3 H, m), 2,54 - 2,74 (1 H, m), 1,96 - 2,05 (1 H, m), 1,65 - 1,91 (3 H, m), 1,51 - 1,65 (1 H, m), 0,64 - 0,81 (4 H, m).
E je m p lo 526. 1 -[4 -(4 -Q u in o lin -3 - il- fe n ila m in o )-p ip e rid in -1 - il]-p ro p a n -1 -o n a , HC l
El producto se aisló como un sólido rojo oscuro. Análisis: LCMS m/z 360 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,52 - 9,57 (1 H, m), 9,18 - 9,24 (1 H, m), 8,24 - 8,35 (2 H, m), 7,96 - 8,04 (1 H, m), 7,82 - 7,91 (3 H, m), 6,94 - 7,06 (2 H, m), 4,27 - 4,37 (1 H, m), 3,82 - 3,92 (1 H, m), 3,59 - 3,71 (1 H, m), 3,11 - 3,22 (1 H, m), 2,74 - 2,86 (1 H, m), 2,34 (2 H, q, J=7,3 Hz), 1,89 - 2,04 (2 H, m), 1,25 - 1,47 (2 H, m), 1,00 (3 H, t, J=7,4 Hz).
Ejemplo 527. Ciclopropil-[4-(4-quinolin-3-il-fenilamino)-piperidin-1-il]-metanona, HCl.
El producto se aisló como un sólido rojo oscuro. Análisis: LCMS m/z 372 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,49 - 9,53 (1 H, m), 9,13-9,19 (1 H, m), 8,22-8,32 (2 H, m), 7,94-8,01 (1 H, m), 7,80-7,90 (3 H, m), 6,91-7,02 (2 H, m), 4,19 4,34 (2 H, m), 3,62-3,73 (1 H, m), 3,22-3,37 (1 H, m), 2,77-2,92 (1 H, m), 1,88-2,09 (3 H, m), 1,25-1,51 (2 H, m), 0,68 0,76 (4 H, m).
Ejemplo 528. {4-[Metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona, HCl.
Una mezcla de metilpiperidin-4-il-(4-quinolin-3-il-fenil)-amina; 3HCl (110 mg, 0,26 mmol), (R)-tetrahidro-furan-2-carboxílico ácido (27 mL, 0,28 mmol), HATU (117 mg, 0,31 mmol), DIPEA (449 pL, 2,58 mmol) en DCM (5 mL) se agitó a temperatura ambiente por 1 h. El disolvente se retiró y el residuo se purificó por HPLC preparativa. Las fracciones aisladas se combinaron, se neutralizaron con solución sat. de NaHCO3 (25 mL), se extrajeron con DCM (3 x 25 mL). Las capas orgánicas combinadas se secaron (Na2SO4), y se concentraron. El producto se disolvió en DCM (~5 mL) y se mezcló con 1,2 equivalente de 0,5 M HCl en MeOH y se concentró. El residuo se disolvió en una pequeña cantidad de DCM y se concentró - este procedimiento se repitió varias veces, se secó para dar 108 mg (93%) de sólido rojo. Análisis: LCMS m/z 416 (M+1); 1H NMR (400 MHz, DMSO-d6) 6: 9,55 - 9,61 (1 H, m), 9,23 - 9,29 (1 H, m), 8,25 -8,38 (2 H, m), 7,93 - 8,06 (3 H, m), 7,85 - 7,92 (1 H, m), 6,88 - 7,71 (2 H, m), 4,65 - 4,71 (1 H, m), 4,46 - 4,51 (1 H, m), 4,02 - 4,17 (2 H, m), 3,69 - 3,85 (2 H, m), 3,06 - 3,24 (1 H, m), 2,81 - 3,00 (3 H, m), 2,61 - 2,76 (1 H, m), 1,92 - 2,15 (2 H, m), 1,48 - 1,91 (6 H, m).
Ejemplo 529. N-Etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida
E tapa 1. te rc -b u til 4 -[4 -(2 -m e to x i-8 -m e til-7 -q u in o lil) fe n o x i]p ip e r id in a -1 -c a rb o x ila to .
Acetato de paladio (0,028 g, 0,124 mmol) y trifenilfosfina (0,13 g, 0,50 mmol) en dioxano (10 mL) se agitaron 15 min bajo una atmósfera de nitrógeno. terc-butil éster del ácido 4-[4-(4,4,5,5-Tetrametil-1,3,2-dioxaborolan-2-il)-fenoxi]-piperidina-1-carboxílico (1,00 g, 2,5 mmol), 7-bromo-8-metil-2-metoxiquinolina (0,688 g, 2,73 mmol), DMF (10 mL) y 1 M Na2CO3 (7 mL) se añadieron y se calentaron a 90 °C por 18 h. La mezcla se concentró, se disolvió en EtOAc, se lavó con en Na2 CO3 , agua y salmuera, luego se secó (MgSO4 ). El producto se purificó por ISCO (gel de sílice, columna de 80g; 20-80% EtOAc/hexanos) para dar un sólido blanco (0,8 g, 72%). Análisis: LCMS m/z = 449 (M 1). 1H NMR (CDCl3) S 7,98 (d, J = 8,8 Hz, 1H), 7,59 (d, J = 8,0 Hz, 1H), 7,35-7,31 (m, 2H), 7,28 (d, J = 8,3 Hz, 1H), 7,04-6,95 (m, 2H), 6,90 (d, J = 8,8 Hz, 1H), 4,54 (dquin, J = 7,1, 3,3 Hz, 1H), 4,09 (s, 3H), 3,83-3,67 (m, 2H), 3,45-3,29 (m, 2H), 2,65 (s, 3H), 2,04-1,93 (m, 2H), 1,89-1,75 (m, 2H), 1,48 (s, 9H). Etapa 2. 8-Metil-7-[4-(4-piperidiloxi)fenil]quinolin-2-ol, HCl. terc-butil 4-[4-(2-metoxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato (750 mg. 1,7 mmol) en 4N HCl en dioxano (10 mL) se calentó a 70 °C por 12 h y se concentró. El sólido se trituró con éter, se recogió y se secó para dar 600 mg (97%) de un sólido canela como la sal de HCl. LCMS = 335 m/z(M 1); 1H NMR (DMSO-d6) S 10,84 (br s, 1H), 8,76 (br s, 2H), 7,93 (d, J = 9,5 Hz, 1H), 7,55 (d, J = 8,0 Hz, 1H), 7,29 (d, J = 8,8 Hz, 2H), 7,09 (d, J = 8,8 Hz, 2H), 7,05 (d, J = 8,0 Hz, 1H), 6,52 (d, J = 9,5 Hz, 1H), 4,72 (dt, J = 7,2, 3,8 Hz, 1H), 3,26 (br s, 2H), 3,10 (br d, J = 5,8 Hz, 2H), 2,31 (s, 3H), 2,24-2,08 (m, 2H), 1,96-1,78 (m, 2H).
Etapa 3. N-Etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida
8-Metil-7-[4-(4-piperidiloxi)fenil]quinolin-2-ol HCl (100 mg, 0,27 mmol), isocianatoetano (38 mg, 0,43 mmol), diisopropiletilamina (0,14 mL) en DCM (3mL) se agitó a temperatura ambiente por 4h. La mezcla se concentró, se disolvió en EtOAc y se lavó con 1N Na2 CO3 y salmuera y luego se secó (MgSO4 ). El producto se sometió a cromatografía en Isco (12 g de gel de sílice, 0-5% MeOH/DCM) para dar un sólido blanco. Análisis: LCMS m/z = 406 (M 1); 1H NMR (DMSO-d6 (dimetilsulfóxido deuterado)) 6: 10,82 (s, 1H), 7,92 (d, J = 9,5 Hz, 1H), 7,54 (d, J = 8,0 Hz, 1H), 7,26 (d, J = 8,8 Hz, 2H), 7,10-6,97 (m, 3H), 6,57-6,45 (m, 2H), 4,59 (dt, J = 8,1, 4,4 Hz, 1H), 3,75-3,63 (m, 2H), 3,17-3,01 (m, 4H), 2,31 (s, 3H), 2,02-1,87 (m, 2H), 1,59-1,46 (m, 2H), 1,01 (t, J = 7,2 Hz, 3H)
Los siguientes ejemplos se sintetizaron usando el procedimiento de Ejemplo 73, Método A.
Ejemplo 530. 4-[4-(8-Metil-7-quinolil)fenoxi]-N-(2-pirrolidin-1-iletil)piperidina-1-carboxamida HCl
LCMS m/z = 459 (M 1); 1H NMR (CLOROFORM-d) 6: 8,99 (dd, J = 4,3, 1,8 Hz, 1H), 8,16 (dd, J = 8,3, 1,8 Hz, 1H), 7,69 (d, J = 8,3 Hz, 1H), 7,47 (d, J = 8,3 Hz, 1H), 7,41 (dd, J = 8,2, 4,1 Hz, 1H), 7,33 (d, J = 8,5 Hz, 2H), 7,00 (d, J = 8,8 Hz, 2H), 6,84 (br s, 1H), 4,61-4,52 (m, 1H), 3,89-3,78 (m, 2H), 3,71-3,63 (m, 2H), 3,54-3,42 (m, 3H), 3,28-3,19 (m, 2H), 2,77 (s, 3H), 2,17 (br s, 4H), 2,10-1,96 (m, 3H), 1,93-1,80 (m, 4H)
Ejemplo 531. 4-[4-(8-Metil-7-quinolil)fenoxi]-N-(2-morfolinoetil)piperidina-1-carboxamida HCl
LCMS m/z = 475 (M 1); 1H NMR (400 MHz, DMSO-d6) 6:10,62 (br s, 1H), 9,07 (d, J = 3,0 Hz, 1H), 8,66 (br s, 1H), 8,00 (br d, J = 8,3 Hz, 1H), 7,75 (br s, 1H), 7,61 (d, J = 8,5 Hz, 1H), 7,40 (d, J = 8,8 Hz, 2H), 7,12 (d, J = 8,8 Hz, 2H), 7.03 (br s, 1H), 4,66 (dt, J = 8,0, 4,2 Hz, 1H), 3,97 (br d, J = 10,5 Hz, 4H), 3,79 (br t, J = 11,3 Hz, 4H), 3,50 (br d, J = 12.3 Hz, 2H), 3,44 (br d, J = 7,0 Hz, 2H), 3,24-3,02 (m, 7H), 2,70 (s, 3H), 1,98 (br d, J = 8,5 Hz, 2H), 1,63-1,53 (m, 2H)
Ejemplo 532. (4-Isopropilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona, HCl.
Etapa 1. A 4-Nitrofenil) 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato 8-Metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,8 g, 2,51 mmol) en Dc M (15 mL) se añadió TEA (0,70 mL, 5,03 mmol) y (4-nitrofenil) carbonocloridato (0,66 g, 3,27 mmol) en un baño de hielo. La solución se agitó por 2h a temperatura ambiente y luego se concentró. El residuo se disolvió en EtOAc y se lavó con en Na2CO3, y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (80 g de gel de sílice, 30-60% EtOAc/hexanos). Las fracciones que contienen el producto puro se concentraron para dar un sólido blanco (900 mg, 73%). Este material se usó en la siguiente etapa. Análisis: LCMS m/z = 484 (M 1); 1H NMR (400 MHz, DCCla) 6: 9,00 (dd, J = 4,3, 1,8 Hz, 1H), 8,32-8,24 (m, 2H), 8,20-8,13 (m, 1H), 7,71 (d, J = 8,5 Hz, 1H), 7,47 (d, J = 8,3 Hz, 1H), 7,43 (dd, J = 8,3, 4,3 Hz, 1H), 7,38-7,31 (m, 3H), 7,10-6,99 (m, 2H), 4,68 (tt, J = 6,2, 3,3 Hz, 1H), 3,96-3,63 (m, 4H), 2,78 (s, 3H), 2,14-1,94 (m, 4H)
Etapa 2. (4-Isopropilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona, HCl.
(4-Nitrofenil) 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato (0,04 g, 0,082 mmol), 1-isopropil-piperazina (0,042 g, 0,33 mmol), y 1,4-dioxano (1 mL) se calentó a 125 °C por un total de 4h en el microondas. La mezcla se diluyó en EtOAc, se lavó con 1N Na2CO3 y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (4g, MeOH/DCM 0-10%) para dar un aceite. La sal de HCl se sintetizó añadiendo 2N HCl-éter a una solución de DCM de base para dar un sólido amarillo claro (25 mg, 58%). Análisis: LCMS m/z = 473 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 10,61 (br s, 1H), 9,07 (br d, J = 3,3 Hz, 1H), 8,66 (br s, 1H), 8,00 (br d, J = 8,3 Hz, 1H), 7,75 (br s, 1H), 7,61 (br d, J = 8,5 Hz, 1H), 7,40 (d, J = 8,5 Hz, 2H), 7,13 (d, J = 8,5 Hz, 2H), 4,68 (br s, 1H), 3,66 (br d, J = 13,6 Hz, 2H), 3,59 3,44 (m, 3H), 3,40-3,27 (m, 4H), 3,15 (br t, J = 9,5 Hz, 2H), 3,07-2,95 (m, 2H), 2,70 (s, 3H), 1,99 (br s, 2H), 1,69-1,58 (m, 2H), 1,28 (d, J = 6,5 Hz, 6H).
Ejemplo 533. (4-Metillpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona, HCl.
(4-Nitrofenil) 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato (0,1 g, 0,21 mmol), 1-metilpiperazina (0,1 g, 1,0 mmol), y 1,4-dioxano (2 mL) se calentó a 125 °C por a total de 4 h en el microondas. La mezcla se diluyó en EtOAc, se lavó con 1N Na2CO3 y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (4g, MeOH/DCM 0-10%) para dar un aceite. La sal de HCl se sintetizó añadiendo 2N HCl-éter a una solución de DCM de base, y se concentró para dar una sal amarilla (55 mg, 59%). Análisis: LCMS m/z = 445 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 10,75 (br s, 1H), 9,08 (br d, J = 3,5 Hz, 1H), 8,68 (br s, 1H), 8,01 (br d, J = 8,8 Hz, 1H), 7,77 (br s, 1H), 7,62 (br d, J = 8,3 Hz, 1H), 7,40 (br d, J = 8,5 Hz, 2H), 7,13 (br d, J = 8,8 Hz, 2H), 4,68 (br s, 1H), 3,66 (br d, J = 14,1 Hz, 2H), 3,53 (br d, J = 13,3 Hz, 2H), 3,41-3,33 (m, 2H), 3,26-3,12 (m, 4H), 3,07-2,97 (m, 2H), 2,80-2,76 (m, 3H), 2,71 (s, 3H), 1,99 (br s, 2H), 1,65 (br d, J = 9,0 Hz, 2H).
Ejemplo 534. [4-[4-(8-Metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperidil)metanona, HCl.
(4-Nitrofenil) 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato (0,075 g, 0,16 mmol), 4-(4-piperidil)morfolina (0,13 g, 0,78 mmol) y 1 -metil-2-pirrolidinona (2,058 g, 2 mL, 20,76 mmol) se calentó a 155 °C por 1,5 h en el microondas. La mezcla se diluyó en EtOAc, se lavó con 1N Na2CO3 y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (4g, MeOH/DCM 0-10%) para dar un sólido. Este material se trituró con éter y hexanos luego se recogió para dar un sólido blanco (40 mg. 49%). Análisis: LCMS m/z = 515 (M 1); 1H NMR (CLOROFORM-d) 6: 8,99 (dd, J = 4,3, 1,8 Hz, 1H), 8,16 (dd, J = 8,3, 1,8 Hz, 1H), 7,70 (d, J = 8,3 Hz, 1H), 7,47 (d, J = 8,5 Hz, 1H), 7,41 (dd, J = 8,2, 4,1 Hz, 1H), 7,37-7,31 (m, 2H), 7,01 (d, J = 8,8 Hz, 2H), 4,55 (dt, J = 7,1, 3,6 Hz, 1H), 3,82-3,68 (m, 6H), 3,64-3,50 (m, 2H), 3,28-3,12 (m, 2H), 2,84-2,78 (m, 2H), 2,77 (s, 3H), 2,57 (br s, 3H), 2,42-2,27 (m, 1H), 2,10-1,98 (m, 2H), 1,90 1,81 (m, 4H), 1,55-1,43 (m, 2H)
Ejemplo 535. (4-Etil lpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona tosilato
(4-Nitrofenil) 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato (0,1 g, 0,21 mmol), 1 -etilpiperazina (0,12 g, 1,03 mmol), y 1 -metil-2-pirrolidinona (1 mL) se calentó a 160 °C por 1 h en el microondas. La mezcla se diluyó en EtOAc, se lavó con 1N Na2CO3 y salmuera luego se secó sobre MgSO4. El producto se purificó por ISCO (4g, MeOH/DCM 0-10%) para dar un aceite. La sal de tosilato se sintetizó añadiendo ácido p-toluenosulfónico monohidrato en acetona (2 mL) a una solución de acetona de base y se concentró. El sólido amarillo claro se suspendió en DCM y éter se añadió, el producto se recogió y se secó bajo vacío (75 mg, 68%). Análisis: LCMS m/z = 459 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,32 (br s, 1H), 9,02 (br d, J = 3,0 Hz, 1H), 8,52 (br s, 1H), 7,93 (br d, J = 8,3 Hz, 1H), 7,65 (br s, 1H), 7,54 (br d, J = 7,8 Hz, 1H), 7,47 (d, J = 8,0 Hz, 4H), 7,39 (d, J = 8,5 Hz, 2H), 7,15-7,08 (m, 6H), 4,68 (br s, 1H), 3,68 (br d, J = 13,8 Hz, 2H), 3,54 (br d, J = 14,3 Hz, 2H), 3,45 (br d, J = 11,5 Hz, 2H), 3,21-2,95 (m, 8H), 2,68 (s, 3H), 2,29 (s, 6H), 1,99 (br s, 2H), 1,65 (br d, J = 8,3 Hz, 2H), 1,22 (t, J = 7,3 Hz, 3H)
Ejemplo 536. N-Etil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida
7-Metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina dihidrocloruro (0,08 g, 0,21 mmol) y trietilamina (0,09 mL) en DCM (3 mL) se añadió isocianatoetano (0,03 g, 0,022 mL, 0,42 mmol) en forma de gotas. Después de agitar a temperatura ambiente por 4h la solución se concentró, se disolvió en EtOAc, se lavó con 1N Na2CO3 y salmuera y luego se secó sobre MgSO4. El producto se purificó por ISCO (12 g de gel de sílice, 40-90% EtOAc/hexanos), y se recristalizó a partir de éter para dar un sólido blanco (60 mg, 75%); LCMS m/z = 379 (M 1); 1H NMR (400 MHz, CLOROFORM-d) 6: 8,03 (d, J = 2,3 Hz, 1H), 7,50 (d, J = 9,0Hz, 1H), 7,29 (d, J=8,5Hz, 2H), 7,11 (d, J=9,0Hz, 1H), 6,99 (d, J=8,8Hz, 2H), 6,59 (d, J=2,3Hz, 1H), 4,56 (dt, J=6,8, 3,5Hz, 1H), 4,43 (br s, 1H), 3,75-3,61 (m, 2H), 3,42-3,26 (m, 4H), 2,75 (s, 3H), 2,00 (td, J=8,6, 3,9Hz, 2H), 1,91-1,78 (m, 2H), 1,17 (t, J=7,3Hz, 3H).
Ejemplo 537. N-Isopropoxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida
O-Isopropilhidroxilamina hidrocloruro (0,073 g, 0,66 mmol), DCI (0,107 g, 0,658 mmol) DIEA en dicloroetano (4 mL) se agitó por 2h a temperatura ambiente. 7-Metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina dihidrocloruro (0,125 g,
0,329 mmol) se añadió y se agitó a temperatura ambiente durante toda la noche. La mezcla se concentró, se disolvió en EtOAc, se lavó con salmuera y luego se secó sobre MgSO4. El producto se purificó por ISCO (12 g de gel de sílice, 40-90% EtOAc/hexanos). El producto se cristalizó a partir de éter y hexanos para dar un sólido blanco (70 mg, 52%). LCMS m/z = 409 (M 1); 1H NMR (400 MHz, DCCla) ó: 8,03 (d, J = 2,3 Hz, 1H), 7,55-7,45 (m, 1H), 7,34-7,27 (m, 2H), 7,11 (d, J = 9,0 Hz, 1H), 7,05-6,96 (m, 2H), 6,93 (s, 1H), 6,59 (d, J = 2,3 Hz, 1H), 4,59 (tt, J = 6,5, 3,3 Hz, 1H), 4,06 (spt, J = 6,2 Hz, 1H), 3,75-3,61 (m, 2H), 3,43 (ddd, J = 13,4, 7,0, 3,9 Hz, 2H), 2,75 (s, 3H), 2,07-1,95 (m, 2H), 1,93 1,80 (m, 2H), 1,25 (d, J = 6,0 Hz, 6H).
Ejemplo 538. N-Etoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida
Se sintetizó usando el método del Ejemplo 538 usando O-etilhidroxilamina hidrocloruro. LCMS m/z = 395 (M 1);1H NMR (400 MHz, CLOROFORM-d) ó: 8,03 (d, J = 2,3 Hz, 1H), 7,55-7,45 (m, 1H), 7,30 (d, J = 8,5 Hz, 2H), 7,11 (d, J = 9,0 Hz, 1H), 7,05-6,92 (m, 3H), 6,59 (d, J = 2,3 Hz, 1H), 4,59 (dt, J = 6,5, 3,2 Hz, 1H), 3,93 (q, J = 7,0 Hz, 2H), 3,75 3,62 (m, 2H), 3,47-3,41 (m, 2H), 2,75 (s, 3H), 2,07-1,95 (m, 2H), 1,93-1,82 (m, 2H), 1,27 (t, J = 7,0 Hz, 3H) Ejemplo 539. N-Metoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida
Se sintetizó usando el método del Ejemplo 538 usando O-metilhidroxilamina hidrocloruro. LCMS m/z = 381 (M 1);1H NMR (400 MHz, CCCla) ó: 8,05 (d, J = 2,0 Hz, 1H), 7,51 (d, J = 9,0 Hz, 1H), 7,30 (d, J = 8,5 Hz, 2H), 7,14 (d, J = 9,0 Hz, 1H), 6,99 (d, J = 8,5 Hz, 2H), 6,60 (d, J = 2,3 Hz, 1H), 4,62-4,57 (m, 1H), 3,74 (s, 3H), 3,66 (br dd, J = 8,7, 4,6 Hz, 2H), 3,46-3,40 (m, 2H), 2,77 (s, 3H), 2,02-1,96 (m, 2H), 1,92-1,87 (m, 2H)
Ejemplo 540. N-(Ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida, HCl.
1-Isocianato-2-metilpropano (30,5 mg, 0,302 mmol) se añadió a una solución de 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina dihidrocloruro (80 mg, 0,25 mmol), y N,N-diisopropiletilamina (0,131 mL, 0,751 mmol) en diclorometano (3 mL) a 0 °C. Después de agitar por 1 h, la reacción se concentró y se particionó entre EtOAc y 1 M Na2 CO3. La capa orgánica se lavó con salmuera, y luego se secó sobre MgSO4, se filtró y se concentró al vacío. El producto se purificó en ISCO (columna de 12 g de gel de sílice, 45-90% EtOAc en hexanos) para producir un aceite. La sal de HCl se sintetizó añadiendo 1 mL de 4M HCl-dioxano solución a una solución de metanol de base. La sal se concentró para producir N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida HCl (72 mg, 63%). Análisis: LCMS m/z = 416 (M 1); 1H NMR (400 MHz, DCCla) ó: 9,46 (1 H, br d, J=4,0 Hz), 8,86 (1 H, d, J=8,0 Hz), 8,00 (1 H, d, J=8,5 Hz), 7,89 - 7,96 (1 H, m), 7,83 (1 H, d, J=8,5 Hz), 7,33 (2 H, d, J=8,8 Hz), 7,07 (2 H, d, J=8,8 Hz), 4,64 (1 H, dt, J=6,5, 3,0 Hz), 3,71 (2 H, ddd, J=13,0, 8,8, 3,5 Hz), 3,32 - 3,46 (2 H, m), 3,13 (2 H, d, J=7,3 Hz), 3,08 (1 H, s), 3,04 - 3,10 (1 H, m), 2,07 - 2,22 (2 H, m), 1,86 - 2,02 (3H, m), 0,93-1,10 (1H, m), 0,46-0,62 (2H, m), 0,15-0,27 (2H, m), 0,04-0,05 (1H, m).
Los siguientes ejemplos se realizaron usando el procedimiento anterior.
E je m p lo 541. N -Iso b u til-4 -[4 -(8 -m e til-7 -q u in o lil) fe n o x i]p ip e r id in a -1 -ca rb o xa m id a , HCl.
Usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina 2HCl y 1-isocianato-2-metilpropano. Análisis: LCMS m/z = 418 (M 1); 1H NMR (400 MHz, DCCla) 6: 9,46 (1 H, br d, J=4,3 Hz), 8,87 (1 H, d, J=7,3 Hz), 8,00 (1 H, d, J=8,5 Hz), 7,93 (1 H, dd, J=8,3, 5,3 Hz), 7,83 (1 H, d, J=8,5 Hz), 7,30 - 7,38 (2 H, m), 7,02 - 7,13 (2 H, m), 4,68 (1 H, dt, J=6,0, 3,0 Hz), 3,73 (2 H, ddd, J=13,0, 9,3, 3,5 Hz), 3,31 - 3,47 (2 H, m), 3,12 (2 H, d, J=6,8 Hz), 3,07 (3 H, s), 2,15 - 2,29 (2 H, m), 1,98 -2,11 (2 H, m), 1,84 (1 H, dt, J=13,5, 6,7 Hz), 0,96 (6 H, d, J=6,8 Hz).
Ejemplo 542. N-(2-Metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida HCl
Usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina 2HCl y 1-isocianato-2-metoxietano. Análisis: LC-MS m/z = 420 (M 1); 1H NMR (400 MHz, DCCls) 6: 9,46 (1 H, br s), 8,96 (1 H, br d, J=4,3 Hz), 7,91 - 8,18 (2 H, m), 7,83 (1 H, br d, J=8,0 Hz), 7,24-7,40 (2H, m), 7,06 (2H, br d, J=8,3Hz), 4,80-5,28 (1H, m), 4,62 (1H, br s), 3,60-3,87 (2H, m), 3,24-3,59 (11 H, m), 3,06 (3H, s), 1,95-2,22 (2H, m), 1,87 (2H, br d, J=6,5Hz).
Ejemplo 543. N-Isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida
A 0°C, 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona 2 HCl (100 mg, 0,31 mmol) en DCM (3 mL) se trató con N,N-diisopropiletilamina (0,219 mL, 1,26 mmol) y luego trifosgeno (95,1 mg, 0,314 mmol). Después del completamiento del cloruro ácido, la reacción se particionó entre CH2 Cl2 y salmuera, las capas orgánicas se separaron y se secaron sobre MgSO4, luego se concentraron al vacío hasta un aceite marrón. Al aceite en 1,2 dicloroetano, se añadió DIPEA (0,219 mL, 1,26 mmol), y luego O-isopropilhidroxilamina hidrocloruro (72 mg, 0,63 mmol) y se calentó hasta 70 °C por 20 h. La reacción se concentró, se disolvió en EtOAc, se lavó con salmuera, y luego se secó sobre MgSO4. El producto se purificó por Gilson, (10-55% ACN con 0,1% TFA/H2 O con 0,1% TFA). El producto se concentró con tolueno, luego la base se liberó con Na2CO3 para producir N-isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida (39 mg, 30%). LCMS m/z = 420 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,50 (1 H, s), 8,97 (1 H, dd, J=4,3, 1,8 Hz), 8,36 (1 H, dd, J=8,3, 1,8 Hz), 7,85 (1 H, d, J=8,3 Hz), 7,55 (1 H, dd, J=8,2, 4,1 Hz), 7,47 (1 H, d, J=8,5 Hz), 7,37 (2 H, d, J=8,5 Hz), 7,10 (2 H, d, J=8,8 Hz), 4,63 (1 H, dt, J=8,2, 4,3 Hz), 3,88 (1 H, quin, J=6,2 Hz), 3,55 - 3,72 (2 H, m), 3,04 - 3,25 (2 H, m), 2,68 (3 H, s), 1,79 - 2,09 (2 H, m), 1,56 (2 H, ddt, J=12,9, 8,6, 4,3, 4,3 Hz), 1,23 (1 H, s), 1,12 (6 H, d, J=6,3 Hz).
E je m p lo 544. N -Is o b u to x i-4 -[4 -(8 -m e til-7 -q u in o lil) fe n o x i]p ip e r id in a -1 -c a rb o x a m id a
Etapa 1. 8-Metil-7-[4-(4-piperidiloxi)fenil]quinolina (300 mg, 0,9422 mmol) en DCM (10 mL) a 0°C, se trató con DIPEA (2 equiv., 1,884 mmol) y trifosgeno (1 equiv., 0,942 mmol). Después de 2 h, la solución se particionó entre DCM y salmuera, la capa orgánica se secó sobre MgSO4 , se filtró y se concentró para producir 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1 -carbonil cloruro.
Etapa 2. 4-[4-(8-Metil-7-quinolil)fenoxi]piperidina-1 -carbonil cloruro (0,10 g, 0,26 mmol) en DCE (2 mL), se añadió DIPEA (0,22 mL, 1,26 mmol), y o-isobutilhidroxilamina HCl (0,068 g, 0,53 mmol). La reacción se calentó hasta 70 °C. por 5 h, se enfrió hasta la temperatura ambiente se diluyó con EtOAc y se lavó con agua y salmuera luego se secó sobre MgSO4. El producto se purificó por GILSON (columna Gemini-NX-5u, C18110A 150x30 mm 5 micras), (15-60% ACN/H2 O con 0,1% TFA). Las fracciones con producto se concentraron, y la base se liberó con Na2CO3 para producir N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida (39 mg, 34%). Análisis: LCMS m/z = 434 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,65 (1 H, s), 8,97 (1 H, dd, J=4,1, 1,9 Hz), 8,36 (1 H, dd, J=8,3, 1,8 Hz), 7,85 (1 H, d, J=8,3 Hz), 7,55 (1 H, dd, J=8,2, 4,1 Hz), 7,47 (1 H, d, J=8,5 Hz), 7,34 - 7,40 (2 H, m), 7,06 - 7,13 (2 H, m), 4,63 (1 H, dt, J=7,9, 4,1 Hz), 3,55 - 3,71 (2 H, m), 3,49 (2 H, d, J=6,8 Hz), 3,05 - 3,20 (2 H, m), 2,68 (3 H, s), 1,78 - 2,03 (3 H, m), 1,56 (2 H, td, J=8,5, 4,5 Hz), 0,90 (6 H, d, J=6,5 Hz).
Ejemplo 545. N-(2-Dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida HCl
Se preparó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y N,N-dimetiletilenedi-amina. Análisis: LCMS m/z = 433 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,77 (1 H, br s), 8,97 - 9,06 (1 H, m), 8,53 (1 H, br s), 7,94 (1 H, br d, J=9,0 Hz), 7,66 (1 H, br s), 7,55 (1 H, d, J=8,3 Hz), 7,39 (2 H, d, J=8,8 Hz), 7,12 (2 H, d, J=8,8 Hz), 6,86 -6,99 (1 H, m), 4,59-4,75 (1H, m), 3,67-3,81 (2H, m), 3,32-3,45 (2H, m), 3,03-3,27 (4H, m), 2,80 (6H, d, J=5,0Hz), 2,69 (3H, s), 1,97 (2H, br s), 1,48-1,71 (2H, m)
Ejemplo 546. 2-Morfolinoetil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato 2HCl
Se preparó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y 2-morfolinoetanol. Análisis: LCMS m/z = 460 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6:11,70 (1 H, br s), 9,17 (1 H, dd, J=4,8, 1,3 Hz), 8,92 (1 H, br d, J=68 Hz), 8,03 - 8,22 (1 H, m), 7,92 (1 H, br dd, J=7,9, 4,9 Hz), 7,61 - 7,83 (1 H, m), 7,32 - 7,52 (2 H, m), 7,12 - 7,18 (2 H, m), 4,71 (1 H, dt, J=7,8, 4,1 Hz), 4,34 - 4,49 (2 H, m), 3,63 - 4,05 (6 H, m), 3,23 - 3,47 (6 H, m), 3,07 - 3,17 (2 H, m), 2,75 (3 H, s), 2,01 (2 H, dt, J=6,7, 3,0 Hz), 1,52 - 1,75 (2 H, m).
E je m p lo 547. 2 -P irro lid in -1 -ile til 4 -[4 -(8 -m e til-7 -q u in o lil) fe n o x i]p ip e r id in a -1 -c a rb o x ila to , 2H C l.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y N-(2-hidroxietil)pirrolidina. Análisis: LCMS m/z = 460 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 11,28 (1 H, br s), 9,17 (1 H, dd, J=4,9, 1,4 Hz), 8,92 (1 H, br d, J=75 Hz), 8,12 (1 H, d, J=8,5 Hz), 7,91 (1 H, br dd, J=7,8, 5,0 Hz), 7,72 (1 H, d, J=8,5 Hz), 7,34 - 7,51 (2 H, m), 7,15 (2 H, d, J=8,8 Hz), 4,71 (1 H, dt, J=7,7, 4,0 Hz), 4,28 - 4,43 (2 H, m), 3,69 - 3,94 (2 H, m), 3,55 (2 H, br dd, J=10,3, 5,0 Hz), 3,26 - 3,48 (4 H, m), 2,91 - 3,12 (2 H, m), 2,75 (3 H, s), 1,81 - 2,10 (6 H, m), 1,54 - 1,73 (2 H,m).
Ejemplo 548. N-[2-(1H-Imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida, 2HCl.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro e histamina. Análisis: LCMS m/z = 456 (M 1); 1NMR (400 MHz, DMSO-cfe) 6: 14,52 (1 H, br s), 14,28 (1 H, br s), 9,12 (1 H, br d, J=3,3 Hz), 9,03 (1 H, s), 8,79 (1 H, br s), 8,06 (1 H, br d, J=8,5 Hz), 7,84 (1 H, br s), 7,67 (1 H, d, J=8,5 Hz), 7,45 (1 H, s), 7,41 (2 H, d, J=8,8 Hz), 7,13 (2 H, d, J=8,8 Hz), 6,80 (1 H, br s), 4,64 (1 H, dt, J=8,2, 4,2 Hz), 3,61 - 3,77 (2 H, m), 3,35 (2 H, br t, J=6,7 Hz), 3,07 - 3,20 (2 H, m), 2,82 (2 H, t, J=6,8 Hz), 2,73 (3 H, s), 1,93 (2 H, br dd, J=10,7, 5,6 Hz), 1,45 - 1,61 (2 H, m).
Ejemplo 549. 4-[4-(8-Metil-7-quinolil)fenoxi]-N-tetrahidropiran-4-il-piperidina-1-carboxamida, HCl.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y 4-aminotetrahidropiran. Análisis: LCMS m/z = 446 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,03 - 9,17 (1 H, m), 8,76 (1 H, br s), 8,05 (2 H, br d, J=8,3 Hz), 7,81 (1 H, br s), 7,65 (2 H, d, J=8,5 Hz), 7,28 - 7,52 (2 H, m), 7,06 - 7,21 (2 H, m), 6,33 (2 H, br s), 4,63 (1 H, br d, J=4,3 Hz), 3,83 (2 H, br dd, J=11,9, 2,1 Hz), 3,54 - 3,78 (3 H, m), 3,31 (2 H, td, J=11,7, 1,9 Hz), 3,05 - 3,21 (2 H, m), 2,71 (3 H, s), 1,86 - 2,03 (2 H, m), 1,68 (2 H, br dd, J=12,4, 2,4 Hz), 1,34 - 1,60 (4 H, m).
E je m p lo 550. Isobu til 4 -[4 -(8 -m e til-7 -q u in o lil) fe n o x i]p ip e r id in a -1 -c a rb o x ila to , HCl.
Isobutil cloroformato (0,085 mL, 0,64 mmol) se añadió a una solución de 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (100 mg, 0,3141 mmol) y DIPEA (0,11 mL) en 1,2-dicloroetano (5 mL) a 0°C. Después de 0,5 h, la reacción se diluyó con EtOAc y se lavó con agua, H2 O y salmuera; luego se secó sobre MgSO4. El producto se purificó por GILSON (columna Gemini-NX-5u, C18 110A 150x30 mm 5 micras), (5-60% ACN/H2 O con 0,1% TFA) para producir isobutil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato HCl (15 mg, 10%) Análisis: LCMS m/z = 419 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,04 (1 H, dd, J=4,4, 1,6 Hz), 8,58 (1 H, br s), 7,96 (1 H, br d, J=8,3 Hz), 7,62 - 7,75 (1 H, m), 7,57 (1 H, d, J=8,3 Hz), 7,33 - 7,45 (2 H, m), 7,04 - 7,17 (2 H, m), 4,68 (1 H, dt, J=8,0, 4,0 Hz), 3,81 (4 H, d, J=6,5 Hz), 3,29 (2 H, br s), 2,69 (3 H, s), 1,93 - 2,07 (2 H, m), 1,88 (1 H, dt, J=13,4, 6,7 Hz), 1,60 (2 H, dtd, J=12,9, 8,7, 8,7, 4,1 Hz), 0,90 (6 H, d, J=6,8 Hz).
Ejemplo 551. Alil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato, HCl.
Se sintetizó usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona 2 HCl y cloroformato de alilo. Análisis: LC-MS m/z = 403 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,17 (1 H, dd, J=4,8, 1,3 Hz), 8,94 (1 H, br d, J=7,3 Hz), 8,13 (1 H, d, J=8,5 Hz), 8,04 - 8,21 (1 H, m), 7,93 (1 H, br dd, J=7,9, 5,1 Hz), 7,73 (1 H, d, J=85 Hz), 7,42 (2 H, d, J=85 Hz), 7,15 (2 H, d, J=8,5 Hz), 5,80-6,12 (1 H, m), 5,30 (1 H, dq, J=17,3, 1,7 Hz), 5,21 (1 H, dq, J=10,5, 1,5 Hz), 4,70 (1 H, dt, J=7,8, 4,1 Hz), 4,55 (2 H, dt, J=5,3, 1,5 Hz), 3,61 - 3,88 (2 H, m), 3,32 (2 H, br s), 2,75 (3 H, s), 2,00 (2 H, ddd, J=9,5, 6,1, 2,8 Hz), 1,45 - 1,73 (2 H, m).
Ejemplo 552. N-Ciclobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida HCl.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y ciclobutilamina. Análisis: LCMS m/z = 416 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,15 (1 H, dd, J=4,8, 1,5 Hz), 8,88 (1 H, br d, J=7,3 Hz), 8,10 (1 H, br d, J=8,5 Hz), 7,89 (1 H, br dd, J=7,9, 4,9 Hz), 7,71 (1 H, d, J=8,5 Hz), 7,32 - 7,50 (2 H, m), 7,00 - 7,20 (2 H, m), 6,67 (1 H, br s), 4,63 (1 H, dt, J=8,2, 4,3 Hz), 4,11 (1 H, br t, J=8,4 Hz), 3,57 - 3,85 (2 H, m), 2,92 - 3,26 (2 H, m), 2,73 (3 H, s), 2,01 - 2,19 (2 H, m), 1,77 - 1,99 (4 H, m), 1,36 - 1,68 (4 H, m).
E je m p lo 553: C ic lo p ro p ilm e til 4 -[4 -(8 -m e til-7 -q u in o lil) fe n o x i]p ip e rid in a -1 -ca rb o x ila to HCl.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y ciclopropanometanol. Análisis: LCMS m/z = 417 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,11 (1 H, dd, J=4,6, 1,4 Hz), 8,77 (1 H, br s), 8,05 (1 H, br d, J=8,3 Hz), 7,75 - 7,95 (1 H, m), 7,66 (1 H, d, J=8,3 Hz), 7,30 - 7,50 (2 H, m), 7,06 - 7,27 (2 H, m), 4,68 (1 H, tt, J=7,8, 3,8 Hz), 3,86 (2 H, d, J=7,0 Hz), 3,68 - 3,80 (2 H, m), 3,29 (2 H, br s), 2,72 (3 H, s), 1,84 - 2,06 (2 H, m), 1,61 (2 H, dtd, J=12,9, 8,7, 8,7, 4,0 Hz), 1,03 - 1,22 (1 H, m), 0,38 - 0,59 (2 H, m), 0,14 - 0,36 (2 H, m).
Ejemplo 554. ácido 4-[4-(8-Metil-7-quinolil)fenoxi]piperidina-1-carbohidroxámico, HCl.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro, e hidroxilamina HCl. Análisis: LCMS m/z = 378 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,13 (1 H, br d, J=3,8 Hz), 8,84 (1 H, br s), 8,08 (1 H, br d, J=8,3 Hz), 7,86 (1 H, br s), 7,69 (1 H, br d, J=8,3 Hz), 7,37 - 7,44 (2 H, m), 7,09 - 7,18 (2 H, m), 4,66 (1 H, dt, J=8,0, 4,2 Hz), 3,57 - 3,77 (2 H, m), 3,03 - 3,22 (2 H, m), 2,72 (3 H, s), 1,87 - 2,08 (2 H, m), 1,55 (2 H, td, J=8,6, 4,4 Hz).
Ejemplo 555. 2-Metoxietil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato, HCl.
Se sintetizó usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona y 2-metoxietil cloroformato. Análisis: LCMS m/z = 421 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,15 (1 H, dd, J=4,8, 1,3 Hz), 8,89 (1 H, br s), 8,11 (1 H, br d, J=8,5 Hz), 7,81 - 7,95 (1 H, m), 7,71 (1 H, d, J=8,3 Hz), 7,32 - 7,48 (2 H, m), 7,08 - 7,22 (2 H, m), 4,69 (1 H, dt, J=7,8, 4,1 Hz), 4,01 -4,21 (2 H, m), 3,68 - 3,85 (2 H, m), 3,45 - 3,63 (2 H, m), 3,28 (5 H, s), 2,73 (3 H, s), 1,99 (2 H, ddd, J=9,6, 6,0, 3,0 Hz), 1,61 (2 H, dtd, J=12,9, 8,7, 8,7, 3,9 Hz).
Ejemplo 556. Tetrahidropiran-4-il 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato.
Etapa 1. Se añadió piridina (0,317 mL, 3,92 mmol) a una solución de trifosgeno (0,326 g, 1,08 mmol) en THF (10 mL) a 0°C y se agitó por 10 min, luego tetrahidropiran-4-ol (200 mg, 1,958 mmol), se añadió y se agitó 45 min mientras se calentó hasta la temperatura ambiente. La reacción se concentró, se disolvió en EtOAc (20 mL) y se lavó con agua (20 mL) y luego salmuera. La capa de EtOAc se secó sobre MgSO4, se filtró y se concentró para producir tetrahidropiran-4-il carbonocloridato.
Etapa 2. Se sintetizó usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona y tetrahidropiran-4-il carbono-cloridato. Análisis: LCMS m/z = 447 (m 1); 1H NMR (400 MHz, DMSO-cfe) ó: 8,97 (1 h, dd, j=4,1, 1,9 hz), 8,37 (1 h, dd, j=8,2, 1,9 hz), 7,85 (1 h, d, j=8,3 hz), 7,55 (1 h, dd, j=8,2, 4,1 hz), 7,48 (1 h, d, j=8,5 hz), 7,34 - 7,41 (2 h, m), 7,07 - 7,15 (2 h, m), 4,76 (1 h, tt, j=8,3, 4,1 hz), 4,67 (1 h, dt, j=7,8, 4,1 hz), 3,69 - 3,86 (4 h, m), 3,47 (2 h, ddd, j=11,6, 8,7, 3,0 hz), 3,34 (2 h, br s), 2,68 (3 h, s), 1,93 - 2,07 (2 h, m), 1,79 - 1,92 (2 h, m), 1,45 - 1,69 (4 h, m).
Ejemplo 557. Tetrahidropiran-3-il 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato.
Se sintetizó usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona y tetrahidropiran-3-il carbonocloridato mediante el método del Ejemplo 557. Análisis: LCMS m/z = 447 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 8,97 (1 H, dd, J=4,3, 1,8 Hz), 8,37 (1 H, dd, J=8,3, 1,8 Hz), 7,85 (1 H, d, J=8,5 Hz), 7,55 (1 H, dd, J=8,2, 4,1 Hz), 7,48 (1 H, d, J=8,5 Hz), 7,38 (2 H, d, J=8,5 Hz), 7,11 (2 H, d, J=8,8 Hz), 4,61 - 4,75 (1 H, m), 4,56 (1 H, dt, J=6,0, 3,0 Hz), 3,65 - 3,85 (3 Hm), 3,55 (2 H, t, J=5,3 Hz), 3,46 (1 H, dd, J=11,7, 5,6 Hz), 3,33 (2 H, s), 2,68 (3 H, s), 1,85 - 2,06 (3 H, m), 1,42 - 1,81 (5 H, m). Ejemplo 558. [4-[4-(8-Metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)metanona.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y 1,2-oxazinano HCl. Análisis: LCMS m/z = 432 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó: 8,97 (1 H, dd, J=4,3, 1,8 Hz), 8,37 (1 H, dd, J=8,3, 1,8 Hz), 7,85 (1 H, d, J=8,5 Hz), 7,52 - 7,61 (1 H, m), 7,51 - 7,52 (1 H, m), 7,48 (1 H, d, J=8,3 Hz), 7,37 (2 H, d, J=8,8 Hz), 7,11 (2 H, d, J=8,8 Hz), 4,68 (1 H, tt, J=7,9, 3,7 Hz), 3,90 (2 H, t, J=4,9 Hz), 3,65 - 3,78 (2 H, m), 3,21 - 3,30 (4 H, m), 2,68 (3 H, s), 2,01 (2 H, ddd, J=9,5, 5,9, 3,1 Hz), 1,54 - 1,74 (6 H, m).
Ejemplo 559. Tetrahidrofuran-3-il 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato.
Se sintetizó usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona y tetrahidrofuran-3-il carbonocloridato. Análisis LCMS m/z = 433 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó: 8,97 (1 H, dd, J=4,3, 1,8 Hz), 8,36 (1 H, dd, J=8,3, 2,0 Hz), 7,85 (1 H, d, J=8,5 Hz), 7,52 - 7,60 (1 H, m), 7,48 (1 H, d, J=8,5 Hz), 7,37 (2 H, d, J=8,8 Hz), 7,11 (2 H, d, J=8,8 Hz), 5,15
(1 H, td, J=4,3, 2,1 Hz), 4,58 - 4,72 (1 H, m), 3,63 - 3,90 (6 H, m), 3,15 - 3,42 (2 H, m), 2,68 (3 H, s), 2,05 - 2,20 (1 H, m), 1,84 - 2,03 (3 H, m), 1,61 (2 H, ddt, J=12,8, 8,6, 4,4, 4,4 Hz).
Ejemplo 560. N-(Cidobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y cidobutilmetilamina. Análisis: LCMS m/z = 430 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,97 (1 H, dd, J=4,3, 1,8 Hz), 8,37 (1 H, dd, J=8,3, 1,8 Hz), 7,85 (1 H, d, J=8,3 Hz), 7,55 (1 H, dd, J=8,3, 4,3 Hz), 7,48 (1 H, d, J=8,5 Hz), 7,32 - 7,40 (2 H, m), 7,00 - 7,16 (2 H, m), 6,52 (1 H, t, J=5,5 Hz), 4,61 (1 H, dt, J=8,3, 4,2 Hz), 3,64 - 3,83 (2 H, m), 2,93 - 3,20 (4 H, m), 2,68 (3 H, s), 2,40 (1 H, dq, J=15,0, 7,5 Hz), 1,88 - 2,02 (4 H, m), 1,73 - 1,87 (2 H, m), 1,41 - 1,71 (4 H, m).
Ejemplo 561. Ciclobutil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato.
Se sintetizó usando 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona y ciclobutil carbonocloridato. Análisis: LCMS m/z = 417 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,97 (1 H, dd, J=4,1, 1,9 Hz), 8,37 (1 H, dd, J=8,2, 1,9 Hz), 7,85 (1 H, d, J=8,3 Hz), 7,55 (1 H, dd, J=8,2, 4,1 Hz), 7,48 (1 H, d, J=85 Hz), 7,37 (2 H, d, J=88 Hz), 7,10 (2 H, d, J=8,8 Hz), 4,84 (1 H, dd, J=7,9, 7,2 Hz), 4,65 (1 H, dt, J=8,0, 4,2 Hz), 3,73 (2 H, br d, J=12,8 Hz), 3,34 (6 H, br s), 2,63 - 2,77 (3 H, m), 2,16 - 2,33 (2 H, m), 1,88 - 2,05 (4 H, m), 1,46 - 1,80 (4 H, m)
Ejemplo 562. Azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona.
Se sintetizó usando 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil cloruro y hexametileneimina. Análisis: LCMS m/z = 444 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,97 (1H, dd, J=4,1, 1,9Hz), 8,36 (1H, dd, J=8,3, 2,0Hz), 7,85 (1H, d, J=8,3Hz), 7,55 (1H, dd, J=8,2, 4,1Hz), 7,47 (1H, d, J=8,5Hz), 7,37 (2H, d, J=8,8Hz), 7,10 (2H, d, J=8,8Hz), 4,61 (1H, dt, J=8,0, 4,2Hz), 3,20-3,44 (8H, m), 2,97 (2H, ddd, J=12,9, 9,5, 2,9Hz), 2,68 (3H, s), 1,93-2,08 (2H, m), 1,58-1,77 (6H, m), 1,36-1,55 (4H, m).
Ejemplo 563. N-Butil-4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida
E tapa 1. te rc -b u til 4 -[4 -(5 -c lo ro im id a z o [1 ,2 -a ]p ir id in -6 - il) fe n o x i]p ip e r id in a -1 -c a rb o x ila to .
Acetato de paladio (0,046 g, 0,205 mmol), trifenilfosfina (0,202 g, 0,770 mmol) y 1,4-dioxano (10 g, 9 mL, 100 mmol) se combinaron en un frasco y se agitó por 40 min bajo nitrógeno. 6-Bromo-5-cloroimidazo[1,2-a]piridina (1,008 g, 4,35 mmol), terc-butil 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenoxi]piperidina-1-carboxilato (1,514 g, 3,754 mmol), 1 M Na2CO3 en agua (14,9 mL, 10 mmol) y DMF (10 g, 20 mL, 200 mmol) luego se añadieron. La reacción se purgó con argón y se calentó a 80 °C bajo nitrógeno por 4 h. La reacción luego se enfrió hasta la temperatura ambiente, se diluyó con ETOAc y se lavó con en Na2 CO3 , y salmuera, luego se secó sobre sulfato de sodio, se filtró y se concentró. El residuo se purificó por Isco normal fase cromatografía, eluyendo con EtOAc/heptano para dar un sólido blancuzco (519 mg, 70%). LC-MS: m/z = 428 (M 1); 1H NMR (400 MHz, DMSO-cfe) 68,11 (m, 1H), 7,78 (m, 1H), 7,73 (d, 1H, J = 9,2 Hz), 7,48 (m, 2H), 7,38 (d, 1H, J = 9,2 Hz), 7,13 (m, 2H), 4,68 - 4,64 (m, 1H), 3,74 - 3,69 (m, 2H), 3,28 - 3,20 (m, 2H), 2,01 - 1,96 (m, 2H), 1,62 - 1,54 (m, 2H), 1,44 (s, 9H).
Etapa 2. 5-cloro-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina. terc-butil 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato (0,519 g, 1,213 mmol) y HCl acuoso (6 M) (3 mL, 18 mmol) se combinaron en un frasco y se agitó a temperatura ambiente por 2 h. La reacción se concentró; el residuo se disolvió en EtOAc y se lavó con solución de NaHCO3 , agua y salmuera. La fase acuosa se extrajo nuevamente varias veces con EtOAc. La fase orgánica se secó sobre MgSO4, se filtró y se concentró para dar un sólido blancuzco (330 mg, 79%). LC-MS: m/z = 328 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,10 (m, 1H), 7,78 (d, 1H, J = 1,3 Hz), 7,72 (m, 1H), 7,46 (m, 2H), 7,37 (d, 1H, J = 9,2 Hz), 7,09 (m, 2H), 4,52 - 4,46 (m, 1H), 3,01 - 2,96 (m, 2H), 2,65 - 2,59 (m, 2H), 1,99 - 1,95 (m, 2H), 1,55 - 1,46 (m, 2H).
Etapa 3. N-Butil-4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
5-Cloro-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina (0,068 g, 0,2074 mmol), DIPEA (0,081 g, 0,11 mL, 0,61 mmol) y DCM (3 g, 2 mL, 40 mmol) se combinaron en a vial. Butil isocianato (0,030 g, 0,034 mL, 0,30 mmol) se añadió, y la reacción se agitó a temperatura ambiente por 17 h. La reacción se lavó con 1 N solución acuosa de Na2CO3, luego salmuera. La capa orgánica se secó sobre MgSO4, se filtró y se concentró. El residuo se purificó por Isco normal fase cromatografía eluyendo con 0% a 8% metanol en DCM para dar un sólido blanco (62 mg, 70%). mp: 171 - 177 °C; HPLC 5,25 min. rt = 2,359 min.;LC-MS: m/z = 427 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,08 (m, 1H), 7,76 (d, 1H, J = 1,3 Hz), 7,70 (m, 1H), 7,46 (m, 2H), 7,36 (m, 1H), 7,10 (m, 2H), 6,48 (m, 1H), 4,64 - 4,60 (m, 1H), 3,72 - 3,69 (m, 2H), 3,14 - 3,08 (m, 2H), 3,04 - 2,99 (m, 2H), 1,93 (m, 2H), 1,56-1,47 (m, 2H), 1,43-1,36 (m, 2H), 1,34-1,22 (m, 2H), 0,88 (m, 3H).
Ejemplo 564. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-etil-piperidina-1-carboxamida.
El compuesto del título, un sólido blanco, se preparó de manera similar al procedimiento usado para preparar el Ejemplo 564 en 68% de rendimiento. mp: 189 - 193 °C; HPLC 5,25 min. rt = 1,970 min.; LC-MS: m/z = 399 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,08 (s, 1H), 7,76 (d, 1H, J = 1,3 Hz), 7,70 (d, 1H, J = 9,3 Hz), 7,46 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,10 (m, 2H), 6,50 (m, 1H), 4,64 - 4,60 (m, 1H), 3,72 - 3,68 (m, 2H), 3,14 - 3,02 (m, 4H), 1,94 (m, 2H), 1,56 - 1,49 (m, 2H), 1,01 (m, 3H).
Ejemplo 565. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isobutil-piperidina-1-carboxamida.
Este compuesto se preparó de manera similar al procedimiento descrito en el Ejemplo 564 en 67% de rendimiento. mp: 201 °C; LC-MS: m/z = 427 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,08 (s, 1H), 7,76 (d, 1H, J = 1,2 Hz), 7,70 (d, 1H, J = 9,2 Hz), 7,46 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,10 (m, 2H), 6,54 (m, 1H), 4,65 - 4,60 (m, 1H), 3,75 - 3,71
(m, 2H), 3,15 - 3,09 (m, 2H), 2,86 - 2,83 (m, 2H), 1,95 - 1,91 (m, 2H), 1,73 - 1,67 (m, 1H), 1,55 - 1,47 (m, 2H), 0,84 -0,82 (d, 6H, J = 6,7 Hz).
Ejemplo 566. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida
El compuesto del título se preparó de manera similar al procedimiento usado para preparar el Ejemplo 564 para dar un sólido blanco en 56% de rendimiento. mp: 184°C; LC-MS: m/z = 413 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,08 (s, 1H), 7,76 (d, 1H, J = 1,3 Hz), 7,70 (m, 1H), 7,48 - 7,44 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,10 (m, 2H), 6,51 (m, 1H), 4,65 - 4,60 (m, 1H), 3,74 - 3,68 (m, 2H), 3,15 - 3,08 (m, 2H), 3,01 - 2,96 (m, 2H), 1,93 (m, 2H), 1,56 - 1,47 (m, 2H), 1,46 - 1,37 (m, 2H), 0,85 - 0,81 (m, 3H).
Ejemplo 567. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-(2-metoxietil)-piperidina-1-carboxamida
El compuesto del título se preparó de manera similar al procedimiento usado para preparar el Ejemplo 564 en 30% de rendimiento. mp: 135 - 138 °C; LC-MS: m/z = 429 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,09 (s, 1H), 7,76 (d, 1H, J = 1,2 Hz), 7,70 (d, 1H, J = 9,6 Hz), 7,45 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,10 (m, 2H), 6,58 (m, 1H), 4,65 - 4,60 (m, 1H), 3,73 - 3,69 (m, 2H), 3,37 - 3,27 (m, 2H), 3,24 (s, 3H), 3,20 - 3,09 (m, 4H), 1,94 (m, 2H), 1,55 - 1,49 (m, 2H).
Ejemplo 568. 4-[4-(5-Cloroimidazo[l,2-a]piridin-6-il)fenoxi]-N-(ciclopropilmetil)-piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar al procedimiento usado para preparar el Ejemplo 564 en 75% de rendimiento. mp: 183 °C - 185 °C; LC-MS: m/z = 425 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,08 (s, 1H), 7,76 (d, 1H, J = 0,3 Hz), 7,70 (d, 1H, J = 9,1 Hz), 7,46 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,11 (m, 2H), 6,59 (m, 1H), 4,65 - 4,60 (m, 1H), 3,74 - 3,69 (m, 2H), 3,16 - 3,09 (m, 2H), 2,93 - 2,90 (m, 2H), 1,96 - 1,93 (m, 2H), 1,57 - 1,49 (m, 2H), 0,98 -0,88 (m, 1H), 0,39 - 0,35 (m, 2H), 0,16 - 0,13 (m, 2H)
Ejemplo 569. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopropoxi-piperidina-1-carboxamida.
5-Cloro-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina HCl (0,053 g, 0,1455 mmol) y TEA (0,08 mL, 0,574 mmol) en DCM (2 mL) se añadió trifosgeno (0,043 g, 0,144904 mmol) y la reacción se agitó a temperatura ambiente por 2 h. Se
añadieron porciones adicionales de trifosgeno (25 mg) y TEA (20 uL), la reacción se agitó por 30 min adicionales, luego se concentró. El residuo se disolvió en 1,2-dicloroetano (3 mL) y DIPEA (0,11 mL, 0,631 mmol) se añadió seguido por O-isopropilhidroxilamina HCl (0,041 g, 0,36748 mmol). La reacción se calentó a 70 °C por 5 h luego se agitó a temperatura ambiente por 16 h. La reacción se concentró, se diluyó con EtOAc, se lavó con en Na2CO3 acuoso, y luego salmuera. La fase orgánica se secó sobre MgSO4 , se filtró y se concentró. El residuo se purificó por Cromatografía Isco de fase normal (metanol/DCM) luego se purificó adicionalmente por HPLC preparativa y se liofilizó. El material liofilizado se diluyó con EtOAc, se lavó con 1 N Na2CO3 acuoso, luego con salmuera, se secó sobre sulfato de magnesio, se filtró y se concentró para producir un sólido blanco (24 mg, 37%). mp: 175 °C; LC-MS: m/z = 429 (M 1); 1H NMR (400 MHz, MeOD) ó: 8,04 (s, 1H), 7,72 (s, 1H), 7,63 (d, 1H, J = 9,2 Hz), 7,45 - 7,39 (m, 3H), 7,08 (m, 2H), 4,70 - 4,65 (m, 1H), 3,99 - 3,93 (m, 1H), 3,38 - 3,33 (m, 2H), 2,04 - 1,98 (m, 2H), 1,79 - 1,71 (m, 2H), 1,21 (d, 6H, J = 6,2 Hz).
Ejemplo 570. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopropil-piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar con 45% de rendimiento. mp: 220 °C; LC-MS: m/z = 413 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó: 8,09 (s, 1H), 7,76 (d, 1H, J = 1,3 Hz), 7,72 - 7,69 (m, 1H), 7,36 (d, 1H, J = 9,2 Hz), 7,11 (m, 2H), 6,21 (d, 1H, J = 7,6 Hz), 4,63 - 4,59 (m, 1H), 3,79 - 3,69 (m, 3H), 3,13 - 3,07 (m, 2H), 1,95 - 1,92 (m, 2H), 1,56 - 1,47 (m, 2H), 1,06 (d, 6H, J = 6,6 Hz).
Ejemplo 571. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isobutoxi-piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar en 19% de rendimiento. mp: 157 °C; LC-MS: m/z = 443 (M 1); 1H NMR (400 MHz, MeOD) ó: 8,04 (s, 1H), 7,72 (d, 1H, J = 1,3 Hz), 7,63 (d, 1H, J = 9,2 Hz), 7,45 - 7,40 (m, 3H), 7,08 (m, 2H), 4,70 - 4,65 (m, 1H), 3,70 - 3,64 (m, 2H), 3,57 (d, 2H, J = 6,8 Hz), 3,37 - 3,32 (m, 2H), 2,04 - 1,94 (m, 3H), 1,79 - 1,71 (m, 2H), 0,95 (d, 6H, J = 6,7 Hz).
Ejemplo 572. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-isopentil-piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar en 65% de rendimiento. mp: 185 °C; LC-MS: m/z = 441 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó: 8,09 (m, 1H), 7,76 (d, 1H, J = 1,3 Hz), 7,71 (m, 1H), 7,46 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,10 (m, 2H), 6,47 (m, 1H), 4,63 - 4,60 (m, 1H), 3,72 - 3,69 (m, 2H), 3,16 - 3,01 (m, 4H), 1,94 - 1,91 (m, 2H), 1,60 - 1,47 (m, 3H), 1,33 - 1,28 (m, 2H), 0,87 (d, 6H, J = 6,6 Hz).
E je m p lo 573. 4 -[4 -(5 -C lo ro im id a z o [1 ,2 -a ]p ir id in -6 - il) fe n o x i]-N -e to x i-p ip e r id in a -1 -c a rb o x a m id a .
El compuesto del título se preparó de manera similar al procedimiento usado para preparar el Ejemplo 7 en 28% de rendimiento. mp: 210 °C; LC-MS: m/z = 443 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,66 (s, 1H), 8,09 (s, 1H), 7,76 (d, 1H, J = 1,2 Hz), 7,70 (d, 1H, J = 9,2 Hz), 7,46 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,10 (m, 2H), 4,66 - 4,62 (m, 1H), 3,77 - 3,72 (m, 2H), 3,66 - 3,60 (m, 2H), 3,15 - 3,10 (m, 2H), 1,95 (m, 2H), 1,58 - 1,50 (m, 2H), 1,14 - 1,11 (m, 3H).
Ejemplo 574. 4-[4-(8-Metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida.
1,1'-Carbonildiimidazolo (0,082 g, 0,506 mmol), O-propilhidroxilamina HCl (0,05 g, 0,43 mmol) y DIPEA (0,11 mL, 0,63 mmol) en DCM (2,0 mL) y THF (0,5 mL) se agitó a temperatura ambiente por 2h. En un vial separado, 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,097 g, 0,305 mmol), DIp Ea (0,11 mL, 0,63 mmol) y DCM (2,5 mL) se combinaron, se añadieron a la reacción y se agitó a temperatura ambiente por 24 h. La reacción se diluyó con EtOAc y se lavó con solución sat. de NH4Cl, agua, solución sat. de NaHCO3, y luego salmuera. La capa orgánica se secó sobre Na2SO4, se filtró y se concentró. El residuo se trituró con éter, y se secó bajo presión reducida a 40 °C para producir un sólido (65 mg, 51%) mp: 75 °C; LC-MS: m/z = 420 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,65 (s, 1H), 8,97 (m, 1H), 8,36 (m, 1H), 7,85 (d, 1H, J = 8,4 Hz), 7,55 (m, 1H), 7,47 (d, 1H, J = 8,4 Hz), 7,37 (m, 2H), 7,10 (m, 2H), 4,65 - 4,61 (m, 1H), 3,68 - 3,62 (m, 4H), 3,16-3,10 (m, 2H), 2,68 (s, 3H), 1,96 (m, 2H), 1,59-1,50 (m, 4H), 0,92-0,88 (m, 3H).
Ejemplo 575. ácido 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carbohidroxámico.
El compuesto del título se preparó de manera similar al procedimiento anterior usando hidroxilamina HCl en a 10% de rendimiento. mp: 232 °C; LC-MS: m/z = 387 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,08 (s, 1H), 8,09 (s, 1H), 7,99 (s, 1H), 7,76 (d, 1H, J = 1,3 Hz), 7,70 (m, 1H), 7,46 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,11 (m, 2H), 4,66 - 4,61 (m, 1H), 3,69 - 3,64 (m, 2H), 3,16 - 3,09 (m, 2H), 1,96 - 1,92 (m, 2H), 1,57 - 1,50 (m, 2H).
Ejemplo 576. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxi-piperidina-1-carboxamida
El compuesto del título se preparó de manera similar al procedimiento en 82% de rendimiento. LC-MS: m/z = 429 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,64 (s, 1H), 8,09 (s, 1H), 7,76 (d, 1H, J = 1,2 Hz), 7,70 (m, 1H), 7,46 (m, 2H),
7,36 (d, 1H, J = 9,2 Hz), 7,10 (m, 2H), 4,67 - 4,61 (m, 1H), 3,68 - 3,61 (m, 4H), 3,15 - 3,10 (m, 2H), 1,97 - 1,92 (m, 2H), 1,58 - 1,50 (m, 4H).
Ejemplo 577. 4-[4-(5-Cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida
El compuesto del título se preparó de manera similar usando isocianato-(trimetil)silano para dar a 36% de rendimiento. mp: 204 °C; LC-MS: m/z = 371 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,09 (s, 1H), 7,76 (d, 1H, J = 1,3 Hz), 7,70 (m, 1H), 7,46 (m, 2H), 7,36 (d, 1H, J = 9,2 Hz), 7,11 (m, 2H), 5,97 (s, 2H), 4,65 - 4,59 (m, 1H), 3,73 - 3,67 (m, 2H), 3,15 - 3,09 (m, 2H), 1,95 - 1,91 (m, 2H), 1,57 - 1,48 (m, 2H).
Ejemplo 578. N-Etil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar en 60% de rendimiento. mp: 211 °C; LC-MS: m/z = 390 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,33 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,8 Hz), 8,17 (d, 1H, J = 1,7 Hz), 7,97 (m, 1H), 7,79 (m, 2H), 7,69 (d, 1H, J = 5,8 Hz), 7,14 (m, 2H), 6,51 (m, 1H), 4,67 - 4,62 (m, 1H), 3,72 - 3,67 (m, 2H), 3,16 -3,02 (m, 4H), 2,89 (s, 3H), 1,95 - 1,92 (m, 2H), 1,57 - 1,48 (m, 2H), 1,03 - 0,99 (m, 3H).
Ejemplo 579. 4-[4-(1-Metil-6-isoquinolil)fenoxi]-N-propil-piperidina-1-carboxamida
El compuesto del título se preparó de manera similar en 75% de rendimiento. mp: 181 °C; LC-MS: m/z = 404 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,34 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,8 Hz), 8,17 (d, 1H, J = 1,7 Hz), 7,97 (m, 1H), 7,79 (m, 2H), 7,69 (d, 1H, J = 5,8 Hz), 7,14 (m, 2H), 6,52 (m, 1H), 4,67 - 4,62 (m, 1H), 3,73 - 3,68 (m, 2H), 3,16 -3,10 (m, 2H), 3,01 - 2,96 (m, 2H), 2,89 (s, 3H), 1,95 (m, 2H), 1,56 - 1,48 (m, 2H), 1,46 - 1,36 (m, 2H), 0,85 - 0,81 (m, 3H).
Ejemplo 580. N-Isobutil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida
El compuesto del título se preparó de manera similar al procedimiento anterior en 24% de rendimiento. mp: 157 °C; LC-MS: m/z = 418 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó: 8,34 (d, 1H, J = 5,8 Hz), 8,24 (d, 1H, J = 8,8 Hz), 8,17 (d, 1H, J = 1,7 Hz), 7,97 (m, 1H), 7,79 (m, 2H), 7,69 (d, 1H, J = 5,8 Hz), 7,13 (m, 2H), 6,54 (m, 1H), 4,67 - 4,63 (m, 1H), 3,74 - 3,70 (m, 2H), 3,17 - 3,10 (m, 2H), 2,89 (s, 3H), 2,86 - 2,83 (m, 2H), 1,95 - 1,92 (m, 2H), 1,75 - 1,65 (m, 1H), 1,55 - 1,48 (m, 2H), 0,83 (d, 6H, J = 6,7 Hz).
Ejemplo 581. 4-[4-(1-Metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida
El compuesto del título se preparó de manera similar usando isocianato(trimetil)silano en 64% de rendimiento. mp: 232 °C; LC-MS: m/z = 362 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó: 8,34 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,8 Hz), 8,18 (d, 1H, J = 1,7 Hz), 7,97 (m, 1H), 7,80 (m, 2H), 7,70 (d, 1H, J = 5,8 Hz), 7,14 (m, 2H), 5,98 (s, 2H), 4,68 - 4,62 (m, 1H), 3,72 - 3,66 (m, 2H), 3,17 - 3,11 (m, 2H), 2,89 (s, 3H), 1,96 - 1,91 (m, 2H), 1,57 - 1,49 (m, 2H).
Ejemplo 582. N-(Ciclopropilmetil)-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar en 37% de rendimiento. mp: 188 °C; LC-MS: m/z = 416 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó 8,33 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,8 Hz), 8,17 (d, 1H, J = 1,7 Hz), 7,98 (m, 1H), 7,79 (m, 2H), 7,69 (d, 1H, J = 5,8 Hz), 7,14 (m, 2H), 6,60 (m, 1H), 4,67 - 4,62 (m, 1H), 3,73 - 3,68 (m, 2H), 3,17 -3,11 (m, 2H), 2,93 - 2,89 (m, 5H), 1,95 - 1,92 (m, 2H), 1,57 - 1,49 (m, 2H), 0,98 - 0,88 (m, 1H), 0,39 - 0,35 (m, 2H), 0,16 - 0,13 (m, 2H).
Ejemplo 583. N-Isopropoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar en 55% de rendimiento. mp: 189 °C; HPLC 5,25 min. rt = 2,223 min.; LC-MS: m/z = 420 (M 1); 1H NMR (400 MHz, DMSO-cfe) ó: 9,50 (s, 1H), 8,34 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,8 Hz), 8,17 (d, 1H, J = 1,7 Hz), 7,97 (m, 1H), 7,79 (m, 2H), 7,69 (d, 1H, J = 5,8 Hz), 7,13 (m, 2H), 4,69 - 4,64 (m, 1H), 3,90 - 3,84 (m, 1H), 3,67 - 3,61 (m, 2H), 3,17 - 3,11 (m, 2H), 2,89 (s, 3H), 1,97 - 1,92 (m, 2H), 1,59 - 1,50 (m, 2H), 1,12 (d, 6H, J = 6,2 Hz).
E je m p lo 584. 4 -[4 -(1 -M e til-6 - is o q u in o lil) fe n o x i]-N -p ro p o x ip ip e r id in a -1 -c a rb o x a m id a
El compuesto del título se preparó de manera similar en 59% de rendimiento. mp: 165 °C; LC-MS: m/z = 420 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,64 (s, 1H), 8,34 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,8 Hz), 8,17 (d, 1H, J = 1,6 Hz), 7,97 (m, 1H), 7,80 (m, 2H), 7,69 (d, 1H, J = 5,8 Hz), 7,14 (m, 2H), 4,68 - 4,64 (m, 1H), 3,68 - 3,59 (m, 4H), 3,17 -3,11 (m, 2H), 2,89 (s, 3H), 1,99 - 1,93 (m, 2H), 1,59 - 1,50 (m, 4H), 0,92 - 0,88 (m, 3H).
Ejemplo 585. ácido 4-[4-(1-Metil-6-isoquinolil)fenoxi]piperidina-1-carbohidroxámico
El compuesto del título se preparó de manera similar usando hidroxilamina HCl en 7% de rendimiento. mp: 185 °C; LC-MS: m/z = 378 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,09 (br s, 1H), 8,55 (d, 1H, J = 9,0 Hz), 8,50 (s, 1H), 8,46 (d, 1H, J = 6,4 Hz), 8,29 (m, 1H), 8,19 (m, 1H), 7,92 (m, 2H), 7,19 (m, 2H), 4,72 - 4,68 (m, 1H), 3,68 - 3,62 (m, 2H), 3,18 - 3,13 (m, 5H), 1,96 - 1,93 (m, 2H), 1,58 - 1,50 (m, 2H)
Ejemplo 586. N-Etoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida
El compuesto del título se preparó de manera similar en 16% de rendimiento. mp: 208 °C; LC-MS: m/z = 406 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,66 (s, 1H), 8,34 (d, 1H, J = 5,8 Hz), 8,25 (d, 1H, J = 8,8 Hz), 8,17 (d, 1H, J = 1,8 Hz), 7,97 (m, 1H), 7,80 (m, 2H), 7,69 (d, 1H, J = 5,9 Hz), 7,14 (m, 2H), 4,68 - 4,64 (m, 1H), 3,77 - 3,72 (m, 2H), 3,64 -3,60 (m, 2H), 3,17 - 3,11 (m, 2H), 2,89 (s, 3H), 1,96 - 1,92 (m, 2H), 1,59 - 1,50 (m, 2H), 1,14 - 1,11 (m, 3H).
Ejemplo 587. N-Etoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida
El compuesto del título se preparó de manera similar en 59% de rendimiento. mp: 152 °C; LC-MS: m/z = 406 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,66 (s, 1H), 8,73 (s, 1H), 8,19 (d, 1H, J = 8,3 Hz), 8,04 (d, 1H, J = 8,2 Hz), 7,79
7,75 (m, 1H), 7,70 - 7,66 (m, 1H), 7,40 (d, 2H, J = 8,6 Hz), 7,13 (d, 2H, J = 8,6 Hz), 4,67 - 4,63 (m, 1H), 3,78 - 3,73 (m, 2H), 3,66 - 3,63 (m, 2H), 3,17 - 3,11 (m, 2H), 2,63 (s, 3H), 1,99 - 1,95 (m, 2H), 1,60 - 1,52 (m, 2H), 1,15 - 1,11 (m, 3H)
Ejemplo 588. N-Isopropoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida
El compuesto del título se preparó de manera similar en 51% de rendimiento. mp: 80 °C; LC-MS: m/z = 420 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,51 (s, 1H), 8,73 (s, 1H), 8,19 (d, 1H, J = 7,7Hz), 8,04 (d, 1H, J=8,3Hz), 7,79-7,75 (m, 1H), 7,70-7,66 (m, 1H), 7,40 (m, 2H), 7,13 (m, 2H), 4,67-4,63 (m, 1H), 3,92-3,83 (m, 1H), 3,68-3,63 (m, 2H), 3,17 3,11 (m, 2H), 2,63 (s, 3H), 1,99-1,95 (m, 2H), 1,60-1,52 (m, 2H), 1,12 (d, 6H, J=6,2Hz).
Ejemplo 589. 4-[4-(4-Metil-3-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida
El compuesto del título se preparó de manera similar en 61% de rendimiento. mp: 75 °C; LC-MS: m/z = 420 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 9,65 (s, 1H), 8,73 (s, 1H), 8,18 (d, 1H, J = 7,7 Hz), 8,04 (d, 1H, J = 8,0 Hz), 7,79 -7,75 (m, 1H), 7,70 - 7,66 (m, 1H), 7,40 (m, 2H), 7,13 (m, 2H), 4,67 - 4,63 (m, 1H), 3,68 - 3,62 (m, 4H), 3,17 - 3,10 (m, 2H), 2,63 (s, 3H), 1,99 - 1,95 (m, 2H), 1,59 - 1,52 (m, 4H), 0,92 - 0,88 (m, 3H).
Ejemplo 590. N-Isobutil-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar en 54% de rendimiento. mp: 153 °C; HPLC 5,25 min. rt = 2,490 min.; LC-MS: m/z = 418 (M 1); 1H NMR (400 MHz, DMSO-cfe) 6: 8,73 (s, 1H), 8,19 (d, 1H, J = 7,7 Hz), 8,04 (d, 1H, J = 7,6 Hz), 7,79 - 7,75 (m, 1H), 7,70 - 7,66 (m, 1H), 7,40 (m, 2H), 7,13 (m, 2H), 6,56 - 6,53 (m, 1H), 4,66 - 4,62 (m, 1H), 3,76 - 3,72 (m, 2H), 3,16 - 3,10 (m, 2H), 2,87 - 2,84 (m, 2H), 2,63 (s, 3H), 1,95 (m, 2H), 1,74 - 1,67 (m, 1H), 1,57 - 1,49 (m, 2H), 0,83 (d, 6H, J = 6,7 Hz).
Ejemplo 591. 4-[4-(4-Metil-3-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida.
El compuesto del título se preparó de manera similar en 64% de rendimiento. mp: 171 °C; min; LC-MS: m/z = 404 (M 1); 1H NMR (400 MHz, DMSO-cfe) 68,73 (s, 1H), 8,19 (m, 1H), 8,04 (m, 1H), 7,79 - 7,74 (m, 1H), 7,70 - 7,66 (m, 1H),
7,41 - 7,38 (m, 2H), 7,13 (m, 2H), 6,53 (m, 1H), 4,65 - 4,61 (m, 1H), 3,75 - 3,70 (m, 2H), 3,15 - 3,09 (m, 2H), 3,01 -2,96 (m, 2H), 2,63 (s, 3H), 1,99 - 1,94 (m, 2H), 1,57 - 1,49 (m, 2H), 1,46 - 1,37 (m, 2H), 0,85 - 0,82 (m, 3H).
Ejemplo 592. N-Etil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,060 g, 0,158 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0826 mL, 0,0612 g, 0,473 mmol) seguido por isocianatoetano (0,0187 mL, 0,0168 g, 0,237 mmol). La solución se agitó a temperatura ambiente durante toda la noche. se añadió solución sat. acuoso de NaHCO3 (3 mL) a la reacción. El vial se agitó y las capas se separaron. La capa orgánica se retiró mediante una jeringa y se cargó directamente en una columna ISCo de 24 g de gel de sílice (se repitió con 2 x 2 mL de DCM). La cromatografía rápida en ISCO (0 a 100% (33% 20:1:1 EtOH:NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos) produjo el compuesto deseado como un sólido blanco (0,041 g, 69%). Análisis: LCMS m/z = 379 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,31 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,11-7,05 (m, 2H), 6,50 (t, J = 5,3 Hz, 1H), 4,60 (tt, J = 8,1, 3,8 Hz, 1H), 3,76-3,65 (m, 2H), 3,16-3,00 (m, 4H), 2,54 (s, 3H), 1,99-1,88 (m, 2H), 1,58-1,46 (m, 2H), 1,02 (t, J = 7,0 Hz, 3H).
Ejemplo 593. N-Isobutil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0600 g, 0,158 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0826 mL, 0,0612 g, 0,473 mmol) seguido por 1-isocianato-2-metil-propano (0,0235 g, 0,237 mmol). La solución se agitó a temperatura ambiente durante toda la noche. se añadió solución sat. acuoso de NaHCO3 (3 mL) a la reacción. El vial se agitó y las capas se dejaron separar. La capa orgánica se retiró mediante una jeringa y aguja y se cargó directamente en una columna Is Co de 24 g de gel de sílice (se repitió con 2 x 2 mL de Dc M). La cromatografía rápida en ISCO (0 a 100% (33% 20:1:1 EtOH:NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos) produjo el compuesto deseado como un sólido blanco (0,047 g, 73%). Análisis: LCMS m/z = 407 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 7,89 (s, 1H), 7,68 (d, J = 1,0 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,30 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,12-7,05 (m, 2H), 6,54 (t, J = 5,5 Hz, 1H), 4,61 (tt, J = 8,2, 3,9 Hz, 1H), 3,78-3,67 (m, 2H), 3,12 (ddd, J = 13,2, 9,7, 3,0 Hz, 2H), 2,85 (dd, J = 6,8, 5,8 Hz, 2H), 2,54 (s, 3H), 1,99-1,88 (m, 2H), 1,70 (dquin, J = 13,6, 6,8 Hz, 1H), 1,58-1,45 (m, 2H), 0,83 (d, J = 6,8 Hz, 6H).
Ejemplo 594. 4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida.
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0600 g, 0,158 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0826 mL, 0,0612 g, 0,473 mmol) seguido por 1-isocianato-propano (0,0222 mL, 0,0201 g, 0,237 mmol). La solución se agitó a temperatura ambiente durante toda la noche. se añadió solución sat. acuoso de NaHCO3 (3 mL) a la reacción. El vial se agitó y las capas se dejaron separar. La capa orgánica se retiró mediante una jeringa y aguja y se cargó directamente en una columna ISCO de 24 g de gel de sílice (se repitió con 2 x 2 mL de DCM). La cromatografía rápida en ISCO (0 a 100% (33% 20:1:1 EtOH: NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos) produjo el compuesto deseado como un sólido
blanco (0,050 g, 81%). Análisis: LCMS m/z = 393 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,30 (m, 2H), 7,20 (d, J = 9,0 Hz, 1H), 7,11-7,05 (m, 2H), 6,51 (t, J = 5,4 Hz, 1H), 4,65-4,55 (m, 1H), 3,77-3,66 (m, 2H), 3,11 (ddd, J = 13,2, 9,6, 3,0 Hz, 2H), 3,03-2,94 (m, 2H), 2,54 (s, 3H), 1,99 1,88 (m, 2H), 1,58-1,47 (m, 2H), 1,42 (sxt, J=7,3Hz, 2H), 0,83 (t, J=7,4Hz, 3H).
Ejemplo 595. N-(Ciclopropilmetil)-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]piperidina-1-carboxamida
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0600 g, 0,158 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0826 mL, 0,0612 g, 0,473 mmol) seguido por isocianato-metilciclopropano (0,0230 g, 0,237 mmol). La solución se agitó a temperatura ambiente durante toda la noche. se añadió solución sat. acuoso de NaHCO3 (3 mL) a la reacción. El vial se agitó y las capas se dejaron separar. La capa orgánica se retiró mediante una jeringa y aguja y se cargó directamente en una columna Is Co de 24 g de gel de sílice (se repitió con 2 x 2 mL de Dc M). La cromatografía rápida en ISCO (0 a 100% (33% 20:1:1 EtOH: NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos) produjo el compuesto deseado como un sólido blanco (0,053 g, 83%). Análisis: LCMS m/z = 405 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 7,74 (s, 1H), 7,52 (d, J = 1,0 Hz, 1H), 7,38 (d, J = 9,3 Hz, 1H), 7,22-7,16 (m, 2H), 7,05 (d, J = 9,3 Hz, 1H), 6,97-6,90 (m, 2H), 6,45 (t, J = 5,6 Hz, 1H), 4,46 (tt, J = 8,1, 3,8 Hz, 1H), 3,62-3,52 (m, 2H), 2,97 (ddd, J = 13,2, 9,5, 3,1 Hz, 2H), 2,76 (t, J = 6,0 Hz, 2H), 2,39 (s, 3H), 1,84-1,74 (m, J = 9,3 Hz, 1H), 1,84-1,74 (m, 2H), 1,44-1,31 (m, 2H), 0,84-0,73 (m, 1H), 0,25-0,18 (m, 2H), 0,03- 0,04 (m, 2H).
Ejemplo 596. 4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(3-piridil)piperidina-1-carboxamida
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0700 g, 0,184 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0963 mL, 0,0714 g, 0,552 mmol) seguido por 3-isocianato-piridina (0,0442 g, 0,368 mmol). La solución se agitó a temperatura ambiente durante toda la noche. se añadió solución sat. acuoso de NaHCO3 (3 mL) a la reacción. El vial se agitó y las capas se dejaron separar. La capa orgánica se concentró y el residuo se purificó por HPLC preparativa en Gilson (5 a 40% MeCN - 95 a 60% agua (ambos con 0,1% TFA) sobre 15 min.; columna Fenomenex Gemini 5pm NX-C18 100A 150 x 30 mm). Las fracciones se combinaron y se particionaron entre solución sat. acuosa de NaHCO3 y DCM, luego se separaron, se secaron con Na2SO4, y se concentraron para producir el compuesto deseado como la base libre, un sólido blancuzco (0,049 g, 62%). Análisis: LCMS m/z = 428 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 8,76 (s, 1H), 8,65 (d, J = 2,3 Hz, 1H), 8,15 (dd, J = 4,8, 1,5 Hz, 1H), 7,91-7,86 (m, 2H), 7,68 (d, J = 1,0 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,38-7,33 (m, 2H), 7,27 (dd, J = 8,7, 4,4 Hz, 1H), 7,21 (d, J = 9,3 Hz, 1H), 7,14-7,09 (m, 2H), 4,69 (tt, J = 8,0, 4,0 Hz, 1H), 3,93-3,81 (m, 2H), 3,39-3,36 (m, 1H), 2,55 (s, 3H), 2,04 (ddd, J = 9,4, 6,0, 3,1 Hz, 2H), 1,70-1,59 (m, 2H).
Ejemplo 597. N-(2-Metoxietil)-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-piperidina-1-carboxamida.
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0600 g, 0,158 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0826 mL, 0,0612 g, 0,473
mmol) seguido por 1-isocianato-2-metoxi-etano (0,0239 g, 0,237 mmol). La solución se agitó a temperatura ambiente durante toda la noche. se añadió solución sat. acuoso de NaHCO3 (3 mL) a la reacción. El vial se agitó y las capas se dejaron separar. La capa orgánica se retiró mediante una jeringa y aguja y se cargó directamente en una columna Is Co de 24 g de gel de sílice (se repitió con 2 x 2 mL de Dc M). La cromatografía rápida en ISCO (0 a 100% (33% 20:1:1 EtOH:NH4OH:H2O - 67% EtoAc) - 100 a 0% hexanos) produjo el compuesto deseado como un sólido blancuzco (0,062 g, 96%). Análisis: LCMS m/z = 409 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 7,89 (s, 1H), 7,67 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,36-7,31 (m, 2H), 7,20 (d, J = 9,0 Hz, 1H), 7,11-7,06 (m, 2H), 6,58 (t, J = 5,5 Hz, 1H), 4,60 (tt, J = 8,1, 3,9 Hz, 1H), 3,76-3,65 (m, 2H), 3,36-3,33 (m, 2H), 3,24 (s, 3H), 3,22-3,08 (m, 4H), 2,54 (s, 3H), 1,98 1,89 (m, 2H), 1,58-1,46 (m, 2H).
Ejemplo 598. [4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]-1-piperidil]-(4-metilpiperazin-1-il)metanona.
Etapa 1. (4-Nitrofenil) 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato
A una solución de 4-nitrofenil cloroformato (0,233 g, 1,16 mmol) en DCM anhidro (2,0 mL) en un vial de centelleo en un baño de agua fría bajo N2 se añadió una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,400 g, 1,05 mmol) y TEA (0,484 mL, 0,351 g, 3,47 mmol) en DCM anhidro (enjuague 2,0 mL 2 x 1,0 mL). La reacción se agitó por 60 min. La suspensión se particionó entre DCM y agua y se separó. La capa acuosa se extrajo nuevamente con DCM. Las capas orgánicas se combinaron y se lavaron con salmuera, luego se secaron sobre Na2SO4, se filtraron, y se concentraron. La cromatografía de gel de sílice en ISCO (0 a 100% (20% MeOH - 80% EtOAc) - 100 a 0% hexanos; columna de 40 g) produjo el compuesto deseado como una espuma amarillenta (0,330 g, 66%). Análisis: LCMS m/z = 473 (M 1); 1H NMR (400 MHz, DCCla) ó: 8,30-8,24 (m, 2H), 7,75 (d, J = 1,3 Hz, 1H), 7,62 (d, J = 9,3 Hz, 1H), 7,55 (s, 1H), 7,35-7,27 (m, 4H), 7,21 (d, J = 9,0 Hz, 1H), 7,05-7,00 (m, 2H), 4,67 (tt, J = 6,3, 3,3 Hz, 1H), 3,95-3,63 (m, 4H), 2,57 (s, 3H), 2,12-1,94 (m, 5H).
Etapa 2. [4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]-1 -piperidil]-(4-metilpiperazin-1 -il)metanona.
Una mezcla de (4-nitrofenil) 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato (0,060 g, 0,13 mmol), 1-metilpiperazina (0,070 mL, 0,064 g, 0,63 mmol), y K2 CO3 (0,026 g, 0,19 mmol) en DMF anhidro (2,0 mL) en un vial pequeño de microondas bajo Ar se calentó en el microondas a 150 °C por 15 min. La mezcla se particionó entre DCM y solución sat. acuosa de NaHCO3 y se separó. La capa acuosa se extrajo nuevamente con 40 mL de DCM. Las capas orgánicas se combinaron y se lavaron con agua, luego salmuera, luego se secaron sobre Na2SO4, se filtraron, y se concentraron. El residuo se purificó por HPLC preparativa en Gilson (5 a 40% MeCN - 95 a 60% agua (ambos con 0,1% TFA) sobre 15 min.; columna Fenomenex Gemini 5pm NX-C18 100Á 150 x 30 mm). Las fracciones buenas se combinaron y se particionaron entre solución sat. acuosa de NaHCO3 y DCM, luego se separaron, se secaron con Na2SO4, y se concentraron para producir el compuesto deseado as la base libre, un sólido amarillo. Análisis: LCMS m/z = 434 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 7,89 (s, 1H), 7,67 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,31 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,11-7,05 (m, 2H), 4,62 (tt, J = 8,0, 3,8 Hz, 1H), 3,51-3,41 (m, 2H), 3,20 3,11 (m, 4H), 3,06 (ddd, J = 13,0, 9,3, 3,0 Hz, 2H), 2,54 (s, 3H), 2,28 (t, J = 4,8 Hz, 4H), 2,17 (s, 3H), 2,02-1,92 (m, 2H), 1,67-1,55 (m, 2H).
Ejemplo 599. N,N-Dimetil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida
Una mezcla de (4-nitrofenil) 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxi]piperidina-1-carboxilato (0,060 g, 0,13 mmol), O-isopropilhidroxilamina HCl (0,043 g, 0,38 mmol), y K2 CO3 (0,079 g, 0,57 mmol) en DMF anhidro (2,0 mL) en un vial pequeño de microondas bajo Ar se calentó en el microondas a 150 °C por 15 min. LC-MS mostró principalmente material de partida sin reaccionar y ~22% del producto N,N-dimetilurea derivado de descomposición a alta temperatura de DMF. La reacción se calentó uno 45 min. adicionales a 150 °C, y LCMS mostró casi exclusivamente el producto
N,N-dimetilurea. La mezcla se particionó entre DCM y solución sat. acuosa de NaHCO3 y se separó. La capa acuosa se extrajo nuevamente con 40 mL de DCM. Las capas orgánicas se combinaron y se lavaron con agua, luego salmuera, luego se secaron sobre Na2SO4, se filtraron, y se concentraron. La cromatografía de gel de sílice en ISCO (0 a 100% (33% 20:1:1 EtOH:NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos) produjo el compuesto como un sólido canela (0,034 g, 71%). Análisis: LCMS m/z = 379 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 7,89 (s, 1H), 7,68 (d, J = 1,0 Hz, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37-7,31 (m, 2H), 7,21 (d, J = 9,0 Hz, 1H), 7,11-7,06 (m, 2H), 4,62 (tt, J = 8,1, 3,9 Hz, 1H), 3,47-3,39 (m, 2H), 3,02 (ddd, J = 13,1, 9,4, 3,1 Hz, 2H), 2,75 (s, 6H), 2,54 (s, 3H), 2,04-1,93 (m, 2H), 1,68 1,56 (m, 2H).
Ejemplo 600. N-Isopropoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
Etapa 1: A una solución de trifosgeno (0,049 g, 0,17 mmol) en DCM anhidro (2,0 mL) en un vial de centelleo grande a 0 °C bajo N2 se añadió una solución de 5-metil-6-[4-(4-piperidiloxi)-fenil]imidazo[1,2-a]piridina 2HCl (0,060 g, 0,16 mmol) y TEA (0,088 mL, 0,064 g, 0,63 mmol) en Dc M anhidro (enjuagues 1,5 mL 2 x 0,5 mL) en forma de gotas. La solución amarillenta se agitó a 0 °C por aproximadamente 60 min. La reacción se concentró para producir un sólido amarillento.
Etapa 2: En un vial separado, O-isopropilhidroxilamina HCl (0,053 g, 0,47 mmol) se suspendió en 1,2-dicloroetano anhidro (1,5 mL), y se añadió DIPEA (0,12 mL, 0,092 g, 0,71 mmol). La solución resultante se añadió en forma de gotas al vial que contiene el cloruro de carbamoilo, que luego se calentó hasta 70 °C antes de apagar el calor y la reacción se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NaHCO3 y se separó. La capa orgánica se lavó con agua, luego salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (33% 20:1:1 EtOH:NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blancuzco (0,034 g, 53%). Análisis: LCMS m/z = 409 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 9,50 (s, 1H), 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37-7,30 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,11-7,05 (m, 2H), 4,62 (tt, J = 8,0, 3,8 Hz, 1H), 3,87 (spt, J = 6,2 Hz, 1H), 3,70-3,59 (m, 2H), 3,13 (ddd, J = 13,1, 9,5, 3,3 Hz, 2H), 2,54 (s, 3H), 2,00-1,89 (m, 2H), 2,00-1,89 (m, 2H), 1,60-1,48 (m, 2H), 1,12 (d, J = 6,3 Hz, 6H).
Ejemplo 601. N-Isobutoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
Etapa 1: A una solución de trifosgeno (0,049 g, 0,17 mmol) en DCM anhidro (2,0 mL) en un vial de centelleo grande a 0 °C bajo N2 se añadió una solución de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,060 g, 0,16 mmol) y TEA (0,088 mL, 0,064 g, 0,63 mmol) en Dc M anhidro (enjuagues 1,5 mL 2 x 0,5 mL) en forma de gotas. La solución amarillenta se agitó a 0 °C por aproximadamente 60 min. La reacción se concentró para producir un sólido amarillento.
Etapa 2: en un vial separado, O-isobutilhidroxilamina HCl (0,059 g, 0,47 mmol) se suspendió en 1,2-dicloroetano anhidro (1,5 mL), y se añadió DIPEA (0,12 mL, 0,092 g, 0,71 mmol). La solución resultante se añadió en forma de gotas al vial que contiene el cloruro de carbamoilo, que luego se calentó hasta 80 °C por varias horas. La mezcla se particionó entre EtOAc y solución sat. acuosa de NaHCO3 y se separó. La capa orgánica se lavó con agua, luego salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (33% 20:1:1 EtOH: NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blancuzco (0,030 g, 45%). Análisis: LCMS m/z = 423 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 9,64 (s, 1H), 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37-7,30 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,11 7,05 (m, 2H), 4,66-4,57 (m, J = 8,1, 4,1, 4,1 Hz, 1H), 3,68-3,57 (m, 2H), 3,49 (d, J = 6,8 Hz, 2H), 3,18-3,08 (m, 2H), 2,54 (s, 3H), 1,99-1,90 (m, 2H), 1,90-1,80 (m, 1H), 1,60-1,48 (m, 2H), 0,89 (d, J = 6,8 Hz, 6H).
Ejemplo 602. Isobutil 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1 -carboxilato.
A una solución de carbonocloridato de isobutilo (0,031 mL, 0,032 g, 0,24 mmol) en DCM anhidro (1,5 mL) en un vial de centelleo grande a 0 °C bajo N2 se añadió una solución de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,060 g, 0,16 mmol) y DIPEA (0,11 mL, 0,082 g, 0,63 mmol) en DCM anhidro (enjuague 1,0 mL 2 x 0,5 mL) en forma de gotas. La reacción se agitó a 0 °C por 90 min. La reacción se apagó añadiendo 3 mL de solución sat. acuosa de NaHCO3, luego se particionó entre EtOAc y solución sat. acuosa de NaHCO3 adicional y se separó. La capa orgánica se lavó con agua, luego salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 80% (33% 20:1:1 EtOH: NH4OH:H2O - 67% EtOAc) - 100 a 20% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blancuzco (0,047 g, 73%). Análisis: LCMS m/z = 408 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,31 (m, 2H), 7,21 (d, J = 9,3 Hz, 1H), 7,12-7,06 (m, 2H), 4,65 (tt, J = 7,9, 3,7 Hz, 1H), 3,80 (d, J = 6,5 Hz, 2H), 3,78-3,69 (m, 2H), 3,31-3,20 (m, 2H), 2,54 (s, 3H), 2,02-1,93 (m, 2H), 1,88 (dquin, J = 13,3, 6,7 Hz, 1H), 1,59 (dtd, J = 12,8, 8,6, 3,9 Hz, 2H), 0,90 (d, J = 6,8 Hz, 6H).
Ejemplo 603. N-Isopropil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0600 g, 0,158 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0826 mL, 0,0612 g, 0,473 mmol) seguido por 2-isocianato-propano (0,0232 mL, 0,0201 g, 0,237 mmol). La solución se agitó a temperatura ambiente durante toda la noche. se añadió solución sat. acuoso de NaHCO3 (3 mL) a la reacción. El vial se agitó y las capas se dejaron separar. La capa orgánica se retiró mediante una jeringa y aguja y se cargó directamente en una columna ISCO de 24 g de gel de sílice (se repitió con 2 x 2 mL de DCM). La cromatografía rápida en ISCO (0 a 100% (33% 20:1:1 EtOH: NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos) produjo el compuesto deseado como un sólido blanco (0,051 g, 82%). Análisis: LCMS m/z = 393 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37-7,31 (m, 2H), 7,21 (d, J = 9,3 Hz, 1H), 7,12-7,05 (m, 2H), 6,21 (d, J = 7,8 Hz, 1H), 4,65-4,55 (m, 1H), 3,83-3,66 (m, 3H), 3,10 (ddd, J = 13,1, 9,6, 3,1 Hz, 2H), 2,54 (s, 3H), 1,98-1,88 (m, 2H), 1,58-1,45 (m, 2H), 1,06 (d, J = 6,5 Hz, 6H).
Ejemplo 604. 4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(1-metilpirazol-4-il)piperidina-1-carboxamida.
A una suspensión de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0600 g, 0,158 mmol) en DCM anhidro (3,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,0826 mL, 0,0612 g, 0,473 mmol) seguido por 4-isocianato-1-metil-pirazolo (0,0291 g, 0,237 mmol). La solución se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NaHCO3 y se separó. La capa orgánica se lavó con agua, luego salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. El residuo se purificó por HPLC preparativa en Gilson (5 a 50% MeCN - 95 q 50% agua (ambos con 0,1% TFA) por 15 min.; columna Fenomenex Gemini 5mm NX- C18 100A 150 x 30 mm). Las fracciones buenas se combinaron y se particionaron entre solución sat. acuosa de NaHCO3 y DCM, luego se separaron, se secaron con Na2SO4, y se concentraron para producir
el compuesto deseado como la base libre, un sólido blancuzco (0,048 g, 71%). Análisis: LCMS m/z = 431 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 8,55 (s, 1H), 7,90 (s, 1H), 7,68 (s, 1H), 7,67 (s, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,38-7,31 (m, 3H), 7,21 (d, J = 9,3 Hz, 1H), 7,13-7,07 (m, 2H), 4,70-4,61 (m, J = 8,0, 4,2, 4,2 Hz, 1H), 3,85-3,77 (m, 2H), 3,75 (s, 3H), 3,25 (ddd, J = 13,2, 9,6, 3,0 Hz, 2H), 2,55 (s, 3H), 2,04-1,95 (m, 2H), 1,64-1,54 (m, 2H).
Ejemplo 605. terc-butil 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato.
Trifenilfosfina (0,702 g, 2,68 mmol) y paladio(II) acetato (0,150 g, 0,669 mmol) se colocaron en un frasco a presión, luego se disolvió en 1,4-dioxano (27mL). Se burbujeó gas nitrógeno a través de la solución por varios minutos, luego el frasco se tapó y se agitó a temperatura ambiente por 30 min. Mientras se burbujeaba nuevamente con N2 a través de la mezcla, terc-butil 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenoxi]piperidina-1-carboxilato (5,40 g, 13,4 mmol), 6-bromo-5-metil-imidazo[1,2-a]piridina (2,97 g, 14,1 mmol), DMF (38 mL), y 1 M solución acuosa de Na2CO3 (40,2 mmol) se añadieron, y el frasco se tapó y se calentó hasta 80 °C por aproximadamente ocho horas antes de apagar el calor y la reacción se agitó a temperatura ambiente durante toda la noche. La mezcla se concentró, luego se particionó entre EtOAc y solución sat. acuosa de NaHCO3 y se separó. La capa acuosa se extrajo nuevamente con 100 mL de EtOAc. Las capas orgánicas se combinaron y se lavaron con agua (2X), luego salmuera, luego se secaron sobre Na2SO4, se filtraron, y se concentraron. La cromatografía de gel de sílice en ISCO (0 a 100% (20% 20:1:1 EtOH:NH4OH:H2O - 80% EtOAc) - 100 a 0% hexanos; columna de 120 g) produjo el compuesto deseado como un sólido blanco. Análisis: LCMS m/z = 408 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 7,89 (s, 1H), 7,68 (d, J = 1,0 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,31 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,12-7,06 (m, 2H), 4,63 (tt, J = 8,0, 3,7 Hz, 1H), 3,74-3,65 (m, 2H), 3,26-3,14 (m, J = 9,5, 9,5 Hz, 2H), 2,54 (s, 3H), 2,00-1,90 (m, 2H), 1,61-1,50 (m, 2H), 1,41 (s, 9H).
Ejemplo 606. 4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(2,2,2-trifluoroetil)piperidina-1-carboxamida.
A una solución de 1,1'-carbonildiimidazolo (0,0426 g, 0,263 mmol) en a 4:1 mezcla de DCM anhidro (1,60 mL) y THF (0,40 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió 2,2,2-trifluoroetanamina (0,0125 mL, 0,0173 g, 0,175 mmol). La solución se agitó a temperatura ambiente por aproximadamente dos horas antes de añadir una solución de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,0832 g, 0,219 mmol) y DIPEA (0,0916 mL, 0,0679 g, 0,525 mmol) en d Cm anhidro (enjuagues 1,0 mL 2 x 0,5 mL) en forma de gotas. La reacción se agitó a temperatura ambiente por 72 horas. La mezcla se particionó entre EtOAc y solución sat. acuosa de NaHCO3 y se separó. La capa orgánica se lavó con agua, luego salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. El residuo se purificó por HPLC preparativa en Gilson (10 a 50% MeCN - 90 a 50% agua (ambos con 0,1% TFA) por 15 min.; columna Fenomenex Gemini 5mm NX-C18 100Á 150 x 30 mm). Las fracciones se combinaron y se particionaron entre solución sat. acuosa de NaHCO3 y DCM, luego se separaron, se secaron con Na2SO4, y se concentraron para producir el compuesto deseado como la base libre, un sólido blancuzco (0,038 g, 50%). Análisis: LCMS m/z = 433 (M 1); 1H NMR (400 MHz, DMSO-d6) ó 7,90 (s, 1H), 7,68 (s, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37 7,31 (m, 2H), 7,24-7,16 (m, 2H), 7,12-7,06 (m, 2H), 4,69-4,59 (m, J = 8,0, 4,2, 4,2 Hz, 1H), 3,84 (qd, J = 9,8, 6,3 Hz, 2H), 3,78-3,70 (m, 2H), 3,20 (ddd, J = 13,2, 9,6, 3,0 Hz, 2H), 2,54 (s, 3H), 2,01-1,91 (m, 2H), 1,60-1,49 (m, 2H). 19F NMR (377 MHz, DMSO-d6) ó -71,22 (s, IF).
Ejemplo 607. 4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxi-piperidina-1-carboxamida
A una solución de 1,1'-carbonildiimidazolo (0,051 g, 0,31 mmol) en a 4:1 mezcla de DCM anhidro (1,60 mL) y THF (0,40 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió una solución de O-propilhidroxilamina HCl (0,032 g, 0,29 mmol) y DIPEA (0,058 mL, 0,043 g, 0,34 mmol) en la mezcla de disolvente 4:1 (enjuagues 1,0 mL 2 x 0,5 mL) en forma de gotas. La solución se agitó a temperatura ambiente por aproximadamente dos horas antes de añadir una solución de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,085 g, 0,22 mmol) y DIPEA (0,058 mL, 0,043 g, 0,34 mmol) en d Cm anhidro (enjuagues 1,0 mL 2 x 0,5 mL) en forma de gotas. La reacción se agitó a temperatura ambiente por dos horas. La mezcla se particionó entre EtOAc y solución sat. acuosa de NaHCO3 y se separó. La capa orgánica se lavó con agua, luego salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (33% 20:1:1 EtOH: NH4OH:H2O - 67% EtOAc) -100 a 0% hexanos; columna de 24 g) produjo un sólido blancuzco. El compuesto se particionó entre DCM y solución sat. acuosa de NH4Cl y se separó. La capa acuosa se extrajo nuevamente con DCM. Las capas orgánicas se combinaron y se lavaron con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secaron sobre Na2SO4, se filtraron, y se concentraron para producir el compuesto deseado como un sólido blancuzco (0,058 g, 64%). Análisis: LCMS m/z = 409 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,64 (s, 1H), 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37-7,31 (m, 2H), 7,20 (d, J = 9,0 Hz, 1H), 7,12-7,05 (m, 2H), 4,62 (tt, J = 7,9, 3,7 Hz, 1H), 3,69-3,59 (m, 4H), 3,13 (ddd, J = 13,2, 9,5, 3,1 Hz, 2H), 2,54 (s, 3H), 2,00-1,89 (m, 2H), 1,60-1,48 (m, 4H), 0,90 (t, J = 7,5 Hz, 3H).
Ejemplo 608. N-Etoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
A una solución de 1,1'-carbonildiimidazolo (0,051 g, 0,32 mmol) en a 4:1 mezcla de DCM anhidro (2,00 mL) y THF (0,50 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió DIPEA (0,073 mL, 0,054 g, 0,42 mmol) seguido por O-etilhidroxilamina HCl (0,029 g, 0,29 mmol). La mezcla se agitó a temperatura ambiente por aproximadamente dos horas antes de añadir una solución de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,080 g, 0,21 mmol) y DIPEA (0,073 mL, 0,054 g, 0,42 mmol) en DCM anhidro (enjuagues 1,0 mL 2 x 0,5 mL) en forma de gotas. La mezcla resultante se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con 15 mL de agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (33% 20:1:1 EtOH:NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blanco (0,073 g, 88%). Análisis: LCMS m/z = 395 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,66 (s, 1H), 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,31 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,11-7,06 (m, 2H), 4,67-4,57 (m, J = 8,0, 4,3, 4,3 Hz, 1H), 3,74 (q, J = 7,0 Hz, 2H), 3,68-3,58 (m, 2H), 3,13 (ddd, J = 13,2, 9,5, 3,1 Hz, 2H), 2,54 (s, 3H), 2,00-1,89 (m, 2H), 1,60-1,48 (m, 2H), 1,13 (t, J = 7,0 Hz, 3H).
Ejemplo 609. 2-Amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona, 2HCl.
Etapa 1: A una suspensión de ácido 2-(tert-butoxicarbonilamino)acético (0,30 mmol) y HATU (0,11 g, 0,30 mmol) en DCM anhidro (2,0 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió DIPEA (0,18 mL, 0,13
g, 1,0 mmol). La mezcla se agitó por 20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona (0,080 g, 0,25 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3 , y salmuera, se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - 100 a 0% hexanos; columna de 24 g) produjo terc-butil N-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil-2-oxo-etil]carbamato como una espuma blancuzca.
Etapa 2: A una solución de terc-butil N-[2-[4-4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil]carbamato (0,120 gn 0,252 mmol) en EtOAc anhidro (3,0 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió HCl (4 mol/L) en 1,4-dioxoane (3,0 mL, 12 mmol) en forma de gotas. Un precipitado amarillento se formó inmediatamente. La reacción se agitó a temperatura ambiente por aproximadamente dos horas. La reacción se concentró. El residuo se particionó entre EtOAc y solución sat. acuosa de NaH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3 , y salmuera, luego se secó sobre Na2SO4, se filtró y se concentró para producir un aceite amarillento. El material se transfirió a un vial, luego se disolvió en 0,5 mL de DCM antes de añadir 0,250 mL de solución de 4,0 M HCl-dioxano durante la agitación. Un precipitado se formó inmediatamente. La reacción se concentró y se secó bajo vacío para producir el producto deseado como sal de dihidrocloruro, un sólido amarillo (0,090 g, 80%). Análisis: LCM m/z = 376 (M+1); 1H NMR (400 MHz, DMSO-d6) 6:9,06 (dd, J=4,3, 1,5 Hz, 1H), 8,69-8,51 (m, 1H), 8,14 (t, J = 5,0 Hz, 3H), 7,98 (d, J = 8,5 Hz, 1H), 7,72 (dd, J = 7,7, 4,4 Hz, 1H), 7,59 (d, J = 8,3 Hz, 1H), 7,41 (d, J = 8,8 Hz, 2H), 7,14 (d, J = 8,8 Hz, 2H), 4,76 (tt, J = 7,6, 3,6 Hz, 1H), 3,92 (d, J = 5,8 Hz, 3H), 3,42-3,31 (m, 3H), 2,71 (s, 3H), 2,10-1,95 (m, 1H), 1,77-1,66 (m, 1H), 1,66-1,54 (m, J = 12,6, 8,5, 4,1 Hz, 1H).
Ejemplo 610. (2R)-2-Amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona, 2HCl.
Etapa 1: A una suspensión de ácido (2R)-2-(tert-butoxicarbonilamino)propanoico (0,057 g, 0,30 mmol) y HATU (0,11 g, 0,30 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió DIPEA (0,18 mL, 0,13 g, 1,0 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,080 g, 0,25 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3 , y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró para producir a aceite incoloro turbio. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - 100 a 0% hexanos; columna de 24 g) produjo terc-butil N-[(1R)-1-metil-2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil]carbamato como una espuma blanca.
Etapa 2: A una solución de terc-butil N-[(1R)-1-metil-2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil]carbamato en EtOAc anhidro (5,0 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió HCl (4 mol/L) en 1,4-dioxano (5,0 mL, 20 mmol) en forma de gotas. La mezcla se agitó por varias horas antes de que la reacción se concentrara para producir el producto deseado como la sal de dihidrocloruro, un sólido amarillo (0,116 g, 100%). Análisis: LCMS m/z = 390 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 (dd, J = 4,4, 1,1 Hz, 1H), 8,67 (d, J = 6,3 Hz, 1H), 8,18 (d, J = 4,0 Hz, 3H), 8,01 (d, J = 8,5 Hz, 1H), 7,75 (dd, J = 7,8, 4,5 Hz, 1H), 7,61 (d, J = 8,5 Hz, 1H), 7,41 (d, J = 8,0 Hz, 2H), 7,15 (d, J = 8,5 Hz, 2H), 4,84-4,69 (m, 1H), 4,47-4,35 (m, 1H), 4,22-4,09 (m, 1H), 4,06-3,97 (m, J = 12,3 Hz, 1H), 3,52-3,44 (m, 5H), 3,34-3,25 (m, 1H), 2,71 (s, 3H), 2,11-1,92 (m, 3H), 1,77-1,53 (m, 2H), 1,34 (dd, J = 6,8, 2,3 Hz, 3H).
Ejemplo 611. N-Metoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
A una solución de 1,1'-carbonildiimidazolo (0,051 g, 0,32 mmol) en a 4:1 mezcla de DCM anhidro (2,00 mL) y THF (0,50 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió DIPEA (0,073 mL, 0,054 g, 0,42 mmol) seguido por O-metilhidroxilamina HCl (0,025 g, 0,29 mmol). La solución se agitó a temperatura ambiente por
aproximadamente dos horas antes de añadir DIPEA adicional (0,073 mL, 0,054 g, 0,42 mmol) y 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,080 g, 0,21 mmol). La mezcla resultante se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (33% 20:1:1 EtOH: NH4OH:H2O - 67% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el producto deseado como un sólido blanco (0,061 g, 76%). Análisis: LCMS m/z = 381 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,74 (s, 1H), 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,0 Hz, 1H), 7,37-7,30 (m, 2H), 7,20 (d, J = 9,0 Hz, 1H), 7,11-7,05 (m, 2H), 4,62 (tt, J = 8,0, 3,7 Hz, 1H), 3,68-3,57 (m, 2H), 3,54 (s, 3H), 3,18-3,08 (m, 2H), 2,54 (s, 3H), 2,00-1,89 (m, 2H), 1,61-1,49 (m, 2H).
Ejemplo 612. (2S)-2-Amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona 2HCl.
Etapa 1: A una suspensión de ácido (2S)-2-(tert-butoxicarbonilamino)propanoico (0,057 g, 0,30 mmol) y HATU (0,11 g, 0,30 mmol) en DCM anhidro en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,18 mL, 0,13 g, 1,0 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,080 g, 0,25 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc -100 a 0% hexanos; columna de 24 g) produjo terc-butil N-[(1S)-1-metil-2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil]carbamato como una espuma blanca.
Etapa 2: A una solución de terc-butil N-[(1S)-1-metil-2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil]carbamato en EtOAc anhidro (5,0 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió HCl (4 mol/L) en 1,4-dioxano solución (5,0 mL, 20 mmol) en forma de gotas. La mezcla se agitó por varias horas antes de que la reacción se concentrara para producir el producto deseado como la sal de dihidrocloruro, un sólido amarillo (0,113 g, 97%). Análisis: LCMS m/z = 390 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 (dd, J = 4,4, 1,4 Hz, 1H), 8,68 (d, J = 6,8 Hz, 1H), 8,18 (d, J = 4,3 Hz, 3H), 8,01 (d, J = 8,5 Hz, 1H), 7,76 (dd, J = 7,8, 4,3 Hz, 1H), 7,62 (d, J = 8,3 Hz, 1H), 7,42 (d, J = 8,0 Hz, 2H), 7,15 (d, J = 8,8 Hz, 2H), 4,84-4,69 (m, 1H), 4,47-4,36 (m, 1H), 4,14-4,10 (m, 1H), 4,07-3,96 (m, J = 12,8 Hz, 1H), 3,33-3,25 (m, 1H), 2,71 (s, 3H), 2,11-1,93 (m, 4H), 1,77-1,53 (m, 2H), 1,34 (dd, J = 6,9, 2,4 Hz, 3H).
Ejemplo 613. ácido 4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carbo-hidroxámico
Etapa 1: A una solución de trifosgeno (0,064 g, 0,22 mmol) en 1,2-dicloroetano anhidro (2,0 mL) en un vial de centelleo grande a 0 °C bajo N2 se añadió una solución de 5-metil-6-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,075 g, 0,20 mmol) y DiPeA (0,14 mL, 0,10 g, 0,79 mmol) en 1,2-dicloroetano anhidro (enjuagues 1,0 mL 2 x 0,5 mL) en forma de gotas. La solución amarillenta se agitó a 0 °C por aproximadamente 60 min. DIPEA adicional (0,14 mL, 0,10 g, 0,79 mmol) se añadió, seguido inmediatamente por hidroxilamina HCl (0,041 g, 0,59 mmol). La solución resultante se calentó hasta 75 °C. Después de varias horas, LC-MS mostró principalmente material de partida, sin señal obvia del producto deseado. DIPEA adicional (0,210 mL, 0,15 g, 1,19 mmol) e hidroxilamina HCl (0,041 g, 0,59 mmol) se añadieron, y la reacción se calentó hasta 70 °C durante toda la noche. La mezcla se particionó entre DCM y solución sat. acuosa de NaHCO3 y se separó. La capa acuosa se extrajo nuevamente con DCM. Las capas orgánicas se combinaron y se lavaron con agua, luego salmuera, luego se secaron sobre Na2SO4, se filtraron, y se concentraron. El residuo se purificó por HPLC preparativa en Gilson (5 a 40% MeCN - 95 a 60% agua (ambos con 0,1% TFA) por 15 min.; columna Fenomenex Gemini 5mm NX-C18 100A 150 x 30 mm). Las fracciones se combinaron y se particionaron entre solución sat. acuosa de NaHCO3 y DCM, luego se separaron, se secaron con Na2SO4, y se concentraron para producir el compuesto deseado como la base libre, un sólido blanco (0,017 g, 24%). Análisis: LCMS m/z = 367 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 (d, J = 2,0 Hz, 1H), 8,00 (d, J = 2,0 Hz, 1H), 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz,
1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37-7,30 (m, 2H), 7,20 (d, J = 9,3 Hz, 1H), 7,12-7,05 (m, 2H), 4,62 (tt, J = 8,1, 3,8 Hz, 1H), 3,71-3,61 (m, 2H), 3,13 (ddd, J = 13,2, 9,5, 3,1 Hz, 2H), 2,54 (s, 3H), 1,99-1,89 (m, 2H), 1,59-1,47 (m, 2H).
Ejemplo 614. 2-(Dimetilamino)-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-etanona.
A una suspensión de ácido 2-(dimetilamino)acético (0,027 g, 0,26 mmol) y HATU (0,10 g, 0,26 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,15 mL, 0,11 g, 0,88 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,070 g, 0,22 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (40% 20:1:1 EtOH:NH4OH:H2O - 60% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blancuzco (0,088 g, 99%). Análisis: LCMS m/z = 404 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 8,97 (dd, J = 4,3, 1,8 Hz, 1H), 8,37 (dd, J = 8,2, 1,9 Hz, 1H), 7,86 (d, J = 8,5 Hz, 1H), 7,59-7,52 (m, 1H), 7,48 (d, J = 8,3 Hz, 1H), 7,42-7,35 (m, 2H), 7,15-7,08 (m, 2H), 4,77-4,68 (m, 1H), 3,97-3,86 (m, 1H), 3,80-3,69 (m, J = 13,8 Hz, 1H), 3,60 (br. s., 2H), 2,68 (s, 3H), 2,45 (s, 6H), 2,10-1,93 (m, 2H), 1,75-1,64 (m, 1H), 1,64-1,53 (m, 1H).
Ejemplo 615. 4-[4-(5-Metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
A una solución de 1,1'-carbonildiimidazolo (0,048 g, 0,30 mmol) en DMF anhidro (2,0 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió NH4Cl (0,018 g, 0,35 mmol) seguido por DIPEA (0,17 mL, 0,13 g, 0,99 mmol). La solución se agitó a temperatura ambiente por aproximadamente dos horas, y el sólido NH4Cl se disolvió gradualmente. 5-Metil-6-[4-(4-piperidiloxi)-fenil]imidazo[1,2-a]piridina 2HCl (0,075 g, 0,20 mmol) se añadió luego, y la reacción se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (40% 20:1:1 EtOH: NH4OH:H2O - 60% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blanco (0,049 g, 71%). Análisis: LCMS m/z = 351 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 7,89 (s, 1H), 7,68 (d, J = 1,3 Hz, 1H), 7,53 (d, J = 9,3 Hz, 1H), 7,37-7,30 (m, 2H), 7,21 (d, J = 9,3 Hz, 1H), 7,12-7,05 (m, 2H), 5,97 (s, 2H), 4,61 (tt, J = 8,2, 3,9 Hz, 1H), 3,75-3,65 (m, 2H), 3,12 (ddd, J = 13,2, 9,5, 3,1 Hz, 2H), 2,54 (s, 3H), 1,99-1,88 (m, 2H), 1,59 1,46 (m, 2H).
Ejemplo 616. [(2R)-1-Metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona.
A una suspensión de ácido (2R)-1-metilpirrolidina-2-carboxílico HCl (0,037 g, 0,23 mmol) y HATU (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente por ~72 horas. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (50% 20:1:1
EtOH:NH4OH:H2O - 50% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blancuzco (0,077 g, 95%). Análisis: LCMS m/z = 430 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 8,97 (dd, J = 4,3, 1,8 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,86 (d, J = 8,5 Hz, 1H), 7,59-7,52 (m, 1H), 7,48 (d, J = 8,5 Hz, 1H), 7,38 (d, J = 8,8 Hz, 2H), 7,16-7,08 (m, 2H), 4,78-4,67 (m, J = 3,5 Hz, 1H), 4,05-3,75 (m, 2H), 3,66 (br. s., 1H), 3,54-3,43 (m, J = 9,5 Hz, 1H), 3,25-3,16 (m, 1H), 2,68 (s, 3H), 2,44 (s, 3H), 2,26 (br. s., 1H), 2,11-1,93 (m, 2H), 1,92-1,68 (m, 4H), 1,68-1,51 (m, 2H).
Ejemplo 617. [(2S)-1-Metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona.
A una suspensión de ácido (2S)-1-metilpirrolidina-2-carboxílico hidrato (0,033 g, 0,23 mmol) y HATU (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente por ~72 horas. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (50% 20:1:1 EtOH:NH4OH:H2O - 50% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blancuzco (0,077 g, 95%). Análisis: LCMS m/z = 430 (M 1); 1H NMR (400 MHz, DMSO-d6) ó 8,97: (dd, J = 4,0, 1,8 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,86 (d, J = 8,5 Hz, 1H), 7,58-7,52 (m, 1H), 7,48 (d, J = 8,3 Hz, 1H), 7,42 7,35 (m, J = 8,5 Hz, 2H), 7,16-7,08 (m, 2H), 4,78-4,67 (m, 1H), 4,72 (dt, J = 7,0, 3,5 Hz, 1H), 4,07-3,58 (m, 4H), 3,52 3,40 (m, 2H), 3,28-3,16 (m, 2H), 2,68 (s, 3H), 2,60-2,52 (m, 1H), 2,45 (s, 3H), 2,27 (br. s., 1H), 1,99 (s, 2H), 1,93-1,67 (m, 4H), 1,67-1,52 (m, 2H).
Ejemplo 618. S-Isopropil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbotioato.
A una solución de 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) en DCM anhidro (2,0 mL) en un vial de centelleo grande a 0 °C bajo N2 se añadió una solución de DIPEA (0,066 mL, 0,049 g, 0,38 mmol) seguido por S-isopropil clorometanotioato (0,035 mL, 0,039 g, 0,28 mmol) en forma de gotas. La mezcla se agitó a 0 °C por ~90 min. La reacción se apagó añadiendo ~2 mL de solución sat. acuosa de NaHCO3, luego se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc -100 a 0% hexanos; columna de 24 g) produjo el producto deseado como un sólido blancuzco ceroso (0,0706 g, 89%). Análisis: LCMS m/z = 421 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 8,97 (dd, J = 4,0, 1,8 Hz, 1H), 8,37 (dd, J = 8,2, 1,9 Hz, 1H), 7,85 (d, J = 8,5 Hz, 1H), 7,55 (dd, J = 8,2, 4,1 Hz, 1H), 7,48 (d, J = 8,5 Hz, 1H), 7,41-7,34 (m, 2H), 7,15 7,07 (m, 2H), 4,75-4,67 (m, 1H), 3,77 (br. s., 2H), 3,55-3,43 (m, 1H), 3,42-3,36 (m, 2H), 2,68 (s, 3H), 2,05-1,94 (m, 2H), 1,63 (dtd, J = 12,7, 8,5, 4,0 Hz, 2H), 1,29 (d, J = 6,8 Hz, 6H).
Ejemplo 619. 2-Amino-2-metil-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona.
Etapa 1: A una suspensión de ácido 2-(tert-butoxicarbonilamino)-2-metil-propanóico (0,054 g, 0,26 mmol) y HATU (0,10 g, 0,26 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió DIPEA (0,15 mL, 0,11 g, 0,88 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4piperidiloxi)fenil]quinolina (0,070 g, 0,22 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - hexanos; columna de 24 g) produjo terc-butil N-[1,1-dimetiI-2-[4-[4-(8-metiI-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil]carbamato como una espuma blanca.
Etapa 2: A una solución de terc-butil N-[1,1-dimetil-2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil]carbamato en EtOAc anhidro (10 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió Hcí (4 mol/L) en 1,4-dioxano (5 mL, 20 mmol) en forma de gotas. Un precipitado amarillo inmediatamente comenzó a formarse. La mezcla se agitó durante toda la noche. La reacción se concentró para producir un sólido canela. El análisis mostró que ocurrió parte de la hidrólisis de la amida. El residuo se purificó por HPLC preparativa en Gilson (5 a 40% MeCN - 95 a 60% agua (ambos con 0,1% TFA) por 15 min.; columna Fenomenex Gemini 5pm NX-C18 100A 150 x 30 mm). Las fracciones buenas se combinaron y se particionaron entre solución sat. acuosa de NaHCO3 y DCM, luego se separaron, se secaron con Na2SO4, y se concentraron para producir el compuesto deseado como la base libre, un sólido blanco (0,0488 g, 55%). Análisis: LCMS m/z = 404 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 8,97 (dd, J = 4,1, 1,9 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,85 (d, J = 8,3 Hz, 1H), 7,59-7,52 (m, 1H), 7,48 (d, J = 8,5 Hz, 1H), 7,41-7,34 (m, 2H), 7,15-7,06 (m, 2H), 4,69 (tt, J = 7,9, 3,9 Hz, 1H), 4,29 (br. s., 2H), 3,75-3,41 (m, 2H), 2,68 (s, 3H), 2,05-1,88 (m, 3H), 1,67-1,54 (m, 2H), 1,28 (s, 6H).
Ejemplo 620. [4-[4-(8-Metil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-pirrolidin-2-il]metanona.
Etapa 1: A una suspensión de ácido (2R)-1-tert-butoxicarbonilpirrolidina-2-carboxílico (0,049 g, 0,23 mmol) y HATU (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metiI-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente por ~72 horas. La reacción se particionó entre EtOAc y solución sat. acuosa de NH4 CI y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% (10% 20:1:1 EtOH:NH4OH:H2O - 90% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo terc-butil (2R)-2-[4-[4-(8-metiI-7-quinoIiI)fenoxi]piperidina-1-carboniI]pirroIidina-1-carboxiIato como una espuma blanca.
Etapa 2: A una solución de terc-butil (2R)-2-[4-[4-(8-metiI-7-quinoIiI)fenoxi]piperidina-1-carboniI]pirroIidina-1-carboxilato en DCM anhidro (3 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió ácido trifluoroacético (1 mL, 1,508 g, 13,23 mmol). La mezcla se agitó a temperatura ambiente por ~2 horas antes de que la reacción se concentrara. Para generar la base libre, el residuo se disolvió en metanol y se cargó en un tubo Fenomenex Strata-X-C 33u Polymeric Strong Cation 2g/20mL Giga, luego se eluyó usando 2,0 M amoníaco en metanol. El eluente se concentró para producir el compuesto deseado como un sólido blancuzco (0,0691 g, 88%). Análisis: LCMS m/z = 416 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 8,97 (dd, J = 4,0, 1,8 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,86 (d, J = 8,3 Hz, 1H), 7,55 (dd, J = 8,2, 4,1 Hz, 1H), 7,48 (d, J = 8,5 Hz, 1H), 7,42-7,34 (m, 2H), 7,16-7,08 (m, 2H), 4,72 (qt, J = 7,7, 3,8 Hz, 1H), 3,99-3,85 (m, 2H), 3,85-3,71 (m, 1H), 3,02 (dt, J = 10,6, 5,4 Hz, 1H), 2,72-2,63 (m, 4H), 2,11-1,92 (m, 3H), 1,76-1,51 (m, 5H).
Ejemplo 621. [4-[4-(8-MetiI-7-quinoIiI)fenoxi]-1-piperidiI]-[(2S)-pirroIidin-2-iI]-metanona.
Etapa 1: A una suspensión de ácido (2S)-1-tert-butoxicarboniIpirroIidina-2-carboxíIico (0,049 g, 0,23 mmol) y HATU (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metiI-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente por ~72 horas. La reacción se particionó entre EtOAc y solución sat. acuosa de NH4 CI y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de
sílice en ISCO (0 a 100% (10% 20:1:1 EtOH:NH4OH:H2O - 90% EtOAc) - 100 a 0% hexanos; columna de 24 g) produjo terc-butil (2S)-2-[4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil]pirrolidina-1-carboxilato como una espuma blanca.
Etapa 2: A una solución de terc-butil (2S)-2-[4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil]pirrolidina-1-carboxilato en DCM anhidro (3 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió ácido trifluoroacético (1 mL, 1,508 g, 13,23 mmol). La mezcla se agitó a temperatura ambiente por ~2 horas antes de que la reacción se concentrara. Para generar la base libre, el residuo se disolvió en metanol y se cargó en un tubo Fenomenex Strata-X-C 33u Polymeric Strong Cation 2g/20mL Giga, luego se eluyó usando 2,0 M amoníaco en metanol. El eluente se concentró para producir el compuesto deseado como un sólido blancuzco (0,0641 g, 82%). Análisis: LCMS m/z = 416 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 8,97 (dd, J = 4,1, 1,9 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,86 (d, J = 8,5 Hz, 1H), 7,55 (dd, J = 8,3, 4,0 Hz, 1H), 7,48 (d, J = 8,3 Hz, 1H), 7,41-7,35 (m, 2H), 7,16-7,08 (m, J = 8,5 Hz, 2H), 4,78-4,65 (m, J = 7,7, 7,7, 3,6, 3,6 Hz, 1H), 4,00-3,85 (m, 2H), 3,85-3,71 (m, J = 15,4, 15,4 Hz, 1H), 3,01 (dt, J = 10,6, 5,4 Hz, 1H), 2,71-2,61 (m, 4H), 2,10-1,93 (m, 3H), 1,76-1,51 (m, 5H).
Ejemplo 622. [1-(Metilamino)ciclopropil]-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona.
Etapa 1. ácido 1-[tert-butoxicarbonil(metil)amino]ciclopropanocarboxílico. A una solución de ácido 1-(tert-butoxicarbonilamino)ciclopropanocarboxílico (0,250 g, 1,24 mmol) en THF anhidro (6,2 mL) en un RBF pequeño a 0 °C bajo N2 se añadió yodometano (0,155 mL, 0,353 g, 2,48 mmol) seguido por NaH (0,149 g, 3,73 mmol). Gas evolucionó vigorosamente. Después de ~15 min., el baño de hielo se retiró, y la mezcla se agitó a temperatura ambiente durante toda la noche. La suspensión blanca se enfrió hasta 0 °C y se apagó añadiendo agua cuidadosamente en forma de gotas hasta que no evolucionó más gas. La reacción se concentró para retirar el THF, y el residuo se disolvió en ~10 mL de agua. Esta capa acuosa se extrajo con 15 mL de éter; la capa de éter luego se extrajo con 10 mL de solución sat. acuosa de NaHCO3. Las dos capas acuosas se combinaron en un frasco con 10 mL de EtOAc, se enfrió hasta 0 °C, y se acidificó hasta f ~2 por adición en forma de gotas de 10% solución acuosa de KHSO4. La mezcla se transfirió a un embudo de separación con 10 mL de EtOAc adicional, las capas se separaron, y la capa acuosa se extrajeron nuevamente con 2 x 20 mL de EtOAc. Las capas orgánicas se combinaron y se lavaron con 5 mL de agua, luego salmuera, luego se secaron sobre Na2SO4, se filtraron, se concentraron, y se secaron bajo vacío para producir el compuesto deseado como a sólido ceroso blanco (0,264 g, 99%). 1H NMR (400 MHz, DMSO-d6) 612,46 (br. s., 1H), 2,84-2,71 (m, 3H), 1,42-1,32 (m, 10H), 1,18-1,08 (m, 2H).
Etapa 2. A una suspensión de ácido 1-[tert-butoxicarbonil(metil)amino]ciclopropanocarboxílico (0,053 g, 0,24 mmol) y HATu (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo grande a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - 100 a 0% hexanos; columna de 24 g) produjo terc-butil N-metil-N-[1-[4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil]ciclopropil]carbamato como una espuma blanca.
Etapa 3. A una solución de terc-butil N-metil-N-[1-[4-[4-(8-metil-7-quinolil)fenoxi]-piperidina-1-carbonil]ciclopropil]carbamato en DCM anhidro (3,0 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió ácido trifluoroacético (0,5 mL, 0,8 g, 7 mmol). Después de ~ 2 hrs., la reacción se concentró. Para generar la base libre, el residuo se disolvió en metanol y se cargó en un tubo Fenomenex Strata-X-C 33u Polymeric Strong Cation 2g/20mL Giga, luego se eluyó usando 2,0 M amoníaco en metanol. El eluente se concentró para producir el compuesto deseado como un sólido blanco (0,0511 g, 65%). Análisis: LCMS m/z = 416 (M 1); 1H n Mr (400 MHz, DMSO-d6) 6: 8,97 (dd, J = 4,3, 1,8 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,86 (d, J = 8,3 Hz, 1H), 7,55 (dd, J = 8,2, 4,1 Hz, 1H), 7,48 (d, J = 8,3 Hz, 1H), 7,41-7,34 (m, 2H), 7,12 (s, 1H), 7,15-7,09 (m, 2H), 4,71 (tt, J = 7,9, 3,7 Hz, 1H), 4,02 (br. s., 2H), 2,68 (s, 3H), 2,23 (s, 3H), 2,06-1,96 (m, J = 11,3 Hz, 2H), 1,70-1,53 (m, J = 8,5 Hz, 2H), 0,87-0,80 (m, 2H), 0,70 0,63 (m, 2H).
Ejemplo 623. 3-Amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona, 2HCl.
Etapa 1. A una suspensión de ácido 3-(tert-butoxicarbonilamino)propanoico (0,043 g, 0,23 mmol) y HATU (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolona (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - 100 a 0% hexanos; columna de 24 g) produjo terc-butil N-[3-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-3-oxopropil]carbamato como una espuma blanca/clear, aceite incoloro.
Etapa 2. A una solución de terc-butil N-[3-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-3-oxo-propil]carbamato (0,080 g, 0,16 mmol) en DCM anhidro (5 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió 4,0 M HCl en 1,4-Dioxano (5 mL, 20 mmol) en forma de gotas. La mezcla se volvió turbia después de varios minutos, y luego se volvió clara cuando una pequeña cantidad de precipitado quedó pegada en las paredes del frasco. La reacción se agitó a temperatura ambiente por aproximadamente dos horas antes de que la mezcla se concentrara. Para generar la base libre, el residuo se disolvió en metanol y se cargó en un tubo Fenomenex Strata-X-C 33u Polymeric Strong Cation 2g/20mL Giga, luego se eluyó usando 2,0 M amoníaco en metanol. El eluente se concentró. Después de que fallaron varios intentos para concentrar el compuesto a partir de diclorometano/éter, para producir un sólido fácilmente pesable, la sal de HCl se sintetizó disolviendo el compuesto en diclorometano anhidro y tratando con un ligero exceso de 2,0 M HCl-éter. La concentración y el secado bajo vacío produjo el compuesto deseado como la sal de dihidrocloruro, un sólido amarillo (0,0652 g, 75%). Análisis: LCMS m/z = 390 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,00 (dd, J = 4,3, 1,8 Hz, 1H), 8,46 (d, J = 7,8 Hz, 1H), 7,90 (d, J = 8,3 Hz, 1H), 7,80 (br. s., 3H), 7,61 (dd, J = 8,2, 4,1 Hz, 1H), 7,52 (d, J = 8,5 Hz, 1H), 7,42-7,36 (m, 2H), 7,16-7,09 (m, 2H), 4,73 (tt, J = 7,8, 3,7 Hz, 1H), 3,98-3,89 (m, 1H), 3,71 (dt, J = 13,7, 5,1 Hz, 1H), 3,01 (sxt, J = 5,9 Hz, 2H), 2,74 (t, J = 6,3 Hz, 2H), 2,69 (s, 3H), 2,11-1,93 (m, 2H), 1,75-1,54 (m, 2H).
Ejemplo 624. 2-Isopropoxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona, HCl.
A una suspensión de ácido 2-isopropoxiacético (0,027 g, 0,23 mmol) y HATU (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - 100 a 0% hexanos; columna de 24 g) produjo un aceite claro incoloro. La sal de HCl se sintetizó disolviendo el compuesto en diclorometano anhidro y se trató con un ligero exceso de 2,0 M HCl-éter, luego se concentró y se secó bajo vacío para producir el compuesto deseado como un sólido amarillo (0,0627 g, 73%). Análisis: LCMS m/z = 419 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 9,08 (dd, J = 4,5, 1,5 Hz, 1H), 8,69 (d, J = 7,8 Hz, 1H), 8,01 (d, J = 8,3 Hz, 1H), 7,76 (dd, J = 8,0, 4,5 Hz, 1H), 7,62 (d, J = 8,5 Hz, 1H), 7,44-7,36 (m, 2H), 7,18-7,10 (m, 2H), 4,72 (tt, J = 7,8, 3,6 Hz, 1H), 4,11 (d, J = 1,3 Hz, 2H), 3,93-3,84 (m, 2H), 3,78-3,69 (m, J = 12,5 Hz, 3H), 3,40-3,32 (m, 2H), 3,32-3,23 (m, 2H), 2,71 (s, 3H), 2,09-1,92 (m, J = 19,3 Hz, 2H), 1,74-1,62 (m, 1H), 1,62-1,50 (m, 1H), 1,12 (d, J = 6,0 Hz, 6H).
E je m p lo 625. [2 -[4 -[4 -(8 -M e til-7 -q u in o lil) fe n o x i]-1 -p ip e rid il]-2 -o x o -e til] ace ta to .
A una solución de 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y DIPEA (0,13 mL, 0,097 g, 0,75 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N 2 se añadió (2-cloro-2-oxoetil) acetato (0,026 mL, 0,033 g, 0,24 mmol) en forma de gotas. La mezcla se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - 100 a 0% hexanos; columna de 24 g) produjo el compuesto deseado como un sólido blancuzco (0,065 g, 82%). Análisis: LCMS m/z = 419 (M 1); 1H Nm R (400 Mhz , DMSO-d6) 6: 8,97 (dd, J = 4,1, 1,9 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,86 (d, J = 8,5 Hz, 1H), 7,55 (dd, J = 8,2, 4,1 Hz, 1H), 7,48 (d, J = 8,5 Hz, 1H), 7,41-7,35 (m, 2H), 7,15-7,09 (m, J = 8,8 Hz, 2H), 4,81 (s, 2H), 4,72 (tt, J = 7,7, 3,7 Hz, 1H), 3,91-3,79 (m, 1H), 3,70-3,58 (m, J = 14,1 Hz, 1H), 3,31-3,25 (m, 1H), 2,68 (s, 3H), 2,09 (s, 3H), 2,07-1,91 (m, 2H), 1,75-1,63 (m, 1H), 1,63-1,51 (m, 1H).
Ejemplo 626. 2-Hidroxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona.
A una suspensión de [2-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-2-oxo-etil] acetato (0,060 g, 0,14 mmol) en metanol (2 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió 1,0 N solución acuosa de hidróxido de litio (0,22 mL, 0,22 mmol). La mezcla se volvió homogénea, y se agitó a temperatura ambiente por ~2,5 hrs. antes de añadir 1,0 N solución acuosa de HCl (0,220 mL, 0,22 mmol), luego se concentró parcialmente para retirar el metanol. El residuo se particionó entre acetato etilo y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró para producir el compuesto deseado como un sólido blancuzco (0,0509 g, 94%). Análisis: LCMS m/z = 377 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 8,97 (dd, J = 4,3, 1,8 Hz, 1H), 8,37 (dd, J = 8,3, 1,8 Hz, 1H), 7,85 (d, J = 8,3 Hz, 1H), 7,59-7,52 (m, 1H), 7,48 (d, J = 8,3 Hz, 1H), 7,42-7,34 (m, 2H), 7,15-7,08 (m, 2H), 4,71 (tt, J = 7,8, 3,7 Hz, 1H), 4,54 (t, J = 5,5 Hz, 1H), 4,12 (d, J = 5,5 Hz, 2H), 3,97-3,84 (m, 1H), 3,67-3,55 (m, J = 14,3 Hz, 1H), 3,32-3,24 (m, 2H), 2,68 (s, 3H), 2,07-1,93 (m, 2H), 1,73-1,52 (m, 2H).
Ejemplo 627. (1-Aminociclobutil)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-metanona.
Etapa 1: A una suspensión de ácido 1-(tert-butoxicarbonilamino)ciclobutanocarboxílico (0,053 g, 0,24 mmol) y HATU (0,079 g, 0,21 mmol) en DCM anhidro (2,00 mL) en un vial de centelleo a temperatura ambiente bajo N2 se añadió DIPEA (0,13 mL, 0,097 g, 0,75 mmol). La mezcla se agitó por ~20 min. antes de añadir 8-metil-7-[4-(4-piperidiloxi)fenil]quinolina (0,060 g, 0,19 mmol) y se agitó a temperatura ambiente durante toda la noche. La mezcla se particionó entre EtOAc y solución sat. acuosa de NH4Cl y se separó. La capa orgánica se lavó con agua, solución sat. acuosa de NaHCO3, y salmuera, luego se secó sobre Na2SO4, se filtró, y se concentró. La cromatografía de gel de sílice en ISCO (0 a 100% EtOAc - 100 a 0% hexanos; columna de 24 g) produjo terc-butil N-[1-[4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil]ciclobutil]carbamato como una espuma blanca.
Etapa 2: A una solución de terc-butil N-[1-[4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbonil]ciclobutil]carbamato en DCM anhidro (5,0 mL) en un RBF pequeño a temperatura ambiente bajo N2 se añadió 4,0 M HCl en 1,4-dioxano (5,0 mL, 20 mmol) en forma de gotas. La reacción se agitó a temperatura ambiente por aproximadamente dos horas antes de que esta se concentró para producir un sólido amarillo. El residuo se purificó por HPLC preparativa en Gilson (5 a 40% MeCN - 95 a 60% agua (ambos con 0,1% TFA) sobre 15 min.; columna Fenomenex Gemini 5pm NX-C18 100Á 150 x 30 mm). Las fracciones buenas se combinaron y se particionaron entre solución sat. acuosa de NaHCÜ3 y DCM, luego se separaron, se secaron con Na2SÜ4, y se concentraron para producir el compuesto deseado como la base libre, a aceite claro incoloro que cristalizó eventualmente en un sólido blanco. (0,0409 g, 52%). Análisis: LCMS m/z = 416 (M 1); 1H NMR (400 MHz, DMSO-d6) ó 8,97 (dd, J = 4,1, 1,9 Hz, 1H), 8,36 (dd, J = 8,2, 1,9 Hz, 1H), 7,85 (d, J = 8,3 Hz, 1H), 7,55 (dd, J = 8,2, 4,1 Hz, 1H), 7,48 (d, J = 8,5 Hz, 1H), 7,41-7,34 (m, 2H), 7,15-7,07 (m, 2H), 4,74-4,64 (m, J = 7,9, 4,1, 4,1 Hz, 1H), 3,88 (br. s., 2H), 3,26 (br. s., 1H), 2,68 (s, 3H), 2,59-2,52 (m, 2H), 2,21 (br. s., 2H), 1,97 (br. s., 2H), 1,93-1,79 (m, 3H), 1,74-1,44 (m, 3H).
Ejemplo 628. N-Etil-4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxamida, HCl.
Etapa 1. terc-butil 4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxilato HCl acetato de paladio (0,021 g, 0,094 mmol) y trifenilfosfina (0,10 g, 0,38 mmol) se combinaron en un frasco en 1,4-dioxano (6,0 mL). Después de agitar por 30 min, DMF (5,7 g, 6,0 mL, 78 mmol), terc-butil 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenoxi]piperidina-1-carboxilato (0,75 g, 1,9 mmol), 7-bromoimidazo[1,2-a]piridina (0,44 g, 2,2 mmol) y Na2CO3 ac. (0,5 M) (12,0 mL, 6,0 mmol) se añadieron y el frasco se calentó bajo nitrógeno a 90 °C durante toda la noche. La mezcla se diluyó con agua (60 mL) luego se extrajo con EtOAc (3x50 mL). Los extractos orgánicos se combinaron, se lavaron con salmuera (50 mL), se secaron sobre sulfato de sodio se filtraron y se concentraron al vacío. El residuo se disolvió en EtOAc (40 mL) luego se trató con 2M HCl en éter (1,5 mL) con agitación. Los sólidos resultantes se recogieron por filtración, se lavaron con EtOAc (30 mL) y hexano (10 mL), luego se secaron en un embudo Buchner para dar terc-butil 4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1 -carboxilato HCl (0,495 g, 62% de rendimiento) como un sólido beige. LCMS (ESI): 394 (M 1); 1H NMR (400 MHz, DMSO-d6) ó 8,91 (d, J = 7,2 Hz, 1H), 8,30 (d, J = 1,5 Hz, 1H), 8,14 (d, J = 2,0 Hz, 1H), 8,09 (s, 1H), 7,93-7,84 (m, 3H), 7,19 (d, J = 8,8 Hz, 2H), 4,71 (dt, J = 7,8, 4,1 Hz, 1H), 3,73-3,51 (m, 2H), 3,29-3,14 (m, 2H), 1,97-1,88 (m, 2H), 1,61-1,51 (m, 2H), 1,41 (s, 9H).
Etapa 2. 7-[4-(4-Piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl
Acetil cloruro (0,6 g, 0,5 mL, 7 mmol) se añadió a etanol (10,0 mL) y la mezcla se añadió luego a terc-butil 4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxilato HCl (0,495 g, 1,15 mmol). Después de agitar a temperatura ambiente por 1h, la mezcla se calentó a 60 °C por 3 h. La mezcla se enfrió hasta la temperatura ambiente luego se diluyó con éter (10 mL), que resultó en formación de una goma. La mezcla se transfirió a un frasco tarado usando metanol luego se concentró al vacío y se secó al vacío para dar 7-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,415 g, 1,13 mmol, 98,4% de rendimiento) como un sólido amarillo con restos de etanol. LCMS (ESI): 294 (M 1); 1H NMR (400 MHz, DMSO-d6) ó: 9,13 (brs, 2H), 8,97-8,93 (m, 1H), 8,32 (d, J = 2,0 Hz, 1H), 8,17 (d, J = 2,0 Hz, 1H), 8,12-8,09 (m, 1H), 7,95 - 7,86 (m, 3H), 7,22 (d, J= 9,0 Hz, 2H), 4,86-4,75 (m, 1H), 3,31-3,18 (m, 2H), 3,15-3,02 (m, 2H), 2,23-2,10 (m, 2H), 1,96-1,82 (m, 2H).
Etapa 3. N-Etil-4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxamida HCl
Una mezcla de 7-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,095 g, 0,26 mmol) y DIPEA (0,15 g, 0,20 mL, 1,1 mmol) en THF (5,0 mL) con ACN (1,0 mL) se trató a temperatura ambiente con isocianato de etilo (0,045 g, 0,050 mL, 0,63 mmol). Después de agitar durante toda la noche la mezcla se particionó entre NaHCO3(10 mL) sat. ac. y DCM (5 mL). Las capas se separaron, la fase acuosa se extrajo además con DCM (2x10 mL) y los compuestos orgánicos combinados se secaron sobre sulfato de sodio, se filtraron y se concentraron al vacío. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (12 g, 0-7% metanol:DCM). Las fracciones del producto se combinaron, se trataron con 2M HCl en éter (1 mL) luego se concentraron al vacío. El residuo se concentró nuevamente a partir de etanol luego se secó al vacío para dar N-etil-4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxamida HCl (0,069 g, 0,17 mmol, 66% de rendimiento) como una espuma naranja dura. LCMS (ESI): 365 (M 1); 1H NMR (400 MHz, DMSO-d6) ó 14,39 (br s, 1H), 8,93 (d, J = 7,3 Hz, 1H), 8,32 (d, J = 1,8 Hz, 1H), 8,17 (d, J = 1,8 Hz, 1H), 8,10 (s, 1H), 7,92-7,87 (m, 3H), 7,19 (d, J = 8,8 Hz, 2H), 6,63-6,46 (m, 1H), 4,74-4,66 (m, 1H), 3,73-3,68 (m, 2H), 3,17-3,08 (m, 2H), 3,05 (q, J = 7,2 Hz, 2H), 1,98-1,89 (m, 1H), 1,57-1,46 (m, 2H), 1,01 (t, J = 7,2 Hz, 3H).
E je m p lo 629. N -E til-4 -[4 -(8 -m e tilim id a zo [1 ,2 -a ]p ir id in -7 - il) fe n o x i]p ip e r id in a -1 -ca rb o xa m id a , HCl.
Etapa 1. 7-Bromo-8-metil-imidazo[1,2-a]piridina.
Una mezcla de 4-bromo-3-metil-piridin-2-amina (0,45 g, 2,4 mmol) y bromoacetaldehído dietil acetal (0,98 g, 0,75 mL, 5.0 mmol) en etanol (2,4 mL) se trató con 48 % HBr ac. (0,37 g, 0,25 mL, 2,2 mmol) luego la mezcla se calentó a 60 °C en un vial resellable. Después de agitar por siete días, la mezcla se enfrió hasta la temperatura ambiente, se trató con 0,5M Na2CO3 (10 mL) luego se extrajo con DCM (10 mL luego 5 mL). El extracto orgánico se secó sobre Na2SO4, se filtró y se concentró al vacío. El residuo se disolvió en DCM, se aplicó a un cartucho de carga de gel de sílice (5 g) y se purificó en gel de sílice (40 g, 0-5% metanol:DCM) para dar 7-bromo-8-metil-imidazo[1,2-a]piridina (0,436 g, 2,07 mmol, 86% de rendimiento) después de la concentración de las fracciones del producto. LCMS (ESI): 211 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 8,39-8,35 (m, 1H), 7,96 (d, J = 1,3 Hz, 1H), 7,55 (d, J = 1,3 Hz, 1H), 7,05 (d, J = 7,3 Hz, 1H), 2,56 (s, 3H).
Etapa 2. terc-butil 4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxilato
Análogo al Ejemplo 628 Etapa 1, 7-bromo-8-metil-imidazo[1,2-a]piridina y terc-butil 4-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenoxi]piperidina-1-carboxilato se acoplaron para preparar terc-butil 4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1 -carboxilato (0,68 g, 81% de rendimiento). LCMS (ESI): 408 (M 1); 1H NMR (400 Mhz , DMSO-d6) 6: 8,42 (d, J = 7,0 Hz, 1H), 7,93 (d, J = 1,3 Hz, 1H), 7,56 (d, J = 1,0 Hz, 1H), 7,35 (d, J = 8,8 Hz, 2H), 7,08 (d, J = 8,8 Hz, 2H), 6,80 (d, J = 7,0 Hz, 1H), 4,63 (tt, J = 8,0, 3,7 Hz, 1H), 3,75-3,63 (m, 2H), 3,26-3,16 (m, 2H), 2,46 (s, 3H), 1,98-1,89 (m, 2H), 1,62-1,49 (m, 2H), 1,41 (s, 9H).
Etapa 3. 8-Metil-7-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina, 2HCl.
Análogo al Ejemplo 628 Etapa 2, terc-butil 4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxilato que se convirtió a 8-metil-7-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,65 g, 99% de rendimiento). MS (ESI): 308 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 14,71 (br s, 1H), 9,08 (br s, 2H), 8,81 (d, J = 6,8 Hz, 1H), 8,38 (d, J = 2,3 Hz, 1H), 8,25 (d, J = 2,0 Hz, 1H), 7,52-7,40 (m, 3H), 7,19 (d, J = 8,8 Hz, 2H), 4,81-4,74 (m, 1H), 3,31-3,19 (m, 2H), 3,15 3,04 (m, 2H), 2,56 (s, 3H), 2,21-2,10 (m, 2H), 1,95-1,84 (m, 2H).
Etapa 3. 8-Metil-7-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina, 2HCl.
Análogo al Ejemplo 628 Etapa 3 8-metil-7-[4-(4-piperidiloxi)fenil]-imidazo[1,2-a]piridina 2HCl (0,110 g, 0,289 mmol) que se convirtió a N-etil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida HCl (0,091 g, 0,22 mmol, 76% de rendimiento). LCMS (ESI): 379 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 14,52 (br s, 1H), 8,80 (d, J = 6,8 Hz, 1H), 8,38 (d, J = 2,0 Hz, 1H), 8,26 (d, J = 2,0 Hz, 1H), 7,49-7,41 (m, 3H), 7,16 (d, J = 8,5 Hz, 2H), 6,56-6,48 (m, 1H), 4,69-4,62 (m, 1H), 3,76-3,67 (m, 2H), 3,18-3,01 (m, 4H), 2,55 (s, 3H), 1,99-1,89 (m, 2H), 1,58-1,47 (m, 2H), 1.01 (t, J = 7,0 Hz, 3H).
Ejemplo 630. N-Isopropoxi-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida, HCl.
Una mezcla de O-isopropilhidroxilamina HCl (0,058 g, 0,52 mmol), N,N'-carbonildiimidazolo (0,071 g, 0,44 mmol) y DIPEA (0,37 g, 0,50 mL, 2,9 mmol) en DCM (3,0 mL) se agitó por 2 h, luego 8-metil-7-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,076 g, 0,20 mmol) se añadió a la reacción. Después de agitar durante toda la noche, la reacción solución se aplicó a una columna cargada con gel de sílice (25 g) luego se purificó en gel de sílice (12 g, 0-5% metanol:DCM). Las fracciones del producto se concentraron al vacío luego se concentraron nuevamente a partir de HCl etanólico (1 mL, 1M) y etanol para dar N-isopropoxi-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida HCl (0,063 g, 0,14 mmol, 71% de rendimiento) como una espuma blanca después de secado al vacío. LCMS (ESI) = 409 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 14,51 (br s, 1H), 9,52 (s, 1H), 8,79
(d, J = 7 ,0 Hz, 1H), 8 ,36 (d, J = 2 ,3 Hz, 1H), 8 ,23 (d, J = 2 ,0 Hz, 1H), 7 ,47-7 ,41 (m , 3H ), 7 ,16 (d, J = 8 ,8 Hz, 2H ), 4 ,70 4 ,64 (m, 1H), 3 ,87 (qu in , J = 6,1 Hz, 1H), 3 ,71 -3 ,60 (m, 2H ), 3 ,14 (ddd, J = 13,1, 9,5, 3 ,3 Hz, 2H ), 2 ,55 (s, 3H ), 1 ,99 1,91 (m, 2H ), 1 ,59 -1 ,50 (m, 2H ), 1 ,12 (d, J = 6 ,3 Hz, 6H ).
Ejemplo 631. 4-[4-(8-Metilimidazo[1,2-a]piridin-7-il)fenoxi]-N-propil-piperidina-1-carboxamida, HCl.
Análogo al Ejemplo 628 Etapa 3, 8-metil-7-[4-(4-piperidiloxi)fenil]-imidazo[1,2-a]piridina 2HCl (0,076 g, 0,20 mmol) se hizo reaccionar con propil isocianato para dar 4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]-N-propil-piperidina-1-carboxamida HCl (0,063 g, 0,15 mmol, 73% de rendimiento). LCMS (ESI) = 393 (M 1); 1H NMR (400 MHz, DMSO-d6) 6: 14,73 (br s, 1H), 8,82 (d, J = 6,8 Hz, 1H), 8,39 (d, J = 2,0 Hz, 1H), 8,25 (d, J = 2,0 Hz, 1H), 7,49-7,41 (m, 3H), 7,16 (d, J = 8,8 Hz, 2H), 6,56 (br s, 1H), 4,70-4,62 (m, 1H), 3,78-3,67 (m, 2H), 3,18-3,06 (m, 2H), 3,03-2,92 (m, 2H), 2,57 (s, 3H), 2,00-1,88 (m, 2H), 1,57-1,47 (m, 2H), 1,47-1,36 (m, 2H), 0,83 (t, J = 7,4 Hz, 3H).
Ejemplo 632. N-Isobutil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida.
Análogo al Ejemplo 628 Etapa 3, 8-metil-7-[4-(4-piperidiloxi)fenil]imidazo[1,2-a]piridina 2HCl (0,076 g, 0,20 mmol) se hizo reaccionar con isobutil isocianato para dar N-isobutil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida (0,055 g, 0,14 mmol, 68% de rendimiento). LCMS (ESI) = 407 (M 1); 1H NMR (400 MHz, DMSO-d6) 6 8,42 (d, J = 7,0 Hz, 1H), 7,93 (d, J = 1,3 Hz, 1H), 7,56 (d, J = 1,3 Hz, 1H), 7,35 (d, J = 7,8 Hz, 2H), 7,08 (d, J = 7,9 Hz, 2H), 6,80 (d, J = 7,0 Hz, 1H), 6,54 (t, J = 5,5 Hz, 1H), 4,65-4,56 (m, 1H), 3,76-3,68 (m, 2H), 3,16-3,07 (m, 2H), 2,85 (dd, J = 6,9, 5,9 Hz, 2H), 2,46 (s, 3H), 1,97-1,89 (m, 2H), 1,75-1,65 (m, 1H), 1,56-1,46 (m, 2H), 0,83 (d, J = 6,5 Hz, 6H).
Ejemplo 633. N-Isobutil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
Este compuesto puede sintetizarse usando el procedimiento para el ejemplo 537 usando 1 -isocianato-2-metil-propano. Ejemplo 634. 4-[4-(7-Metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
Este compuesto puede sintetizarse usando el procedimiento para el ejemplo 539 con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina2HCl.
E je m p lo 635. ác ido 4 -[4 -(7 -M e tilp ira z o lo [1 ,5 -a ]p ir id in -6 - il) fe n o x i]p ip e r id in a -1 -c a rb o h id ro x á m ic o .
Este compuesto puede sintetizarse usando el procedimiento para el ejemplo 576 comenzando con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina dihidrocloruro.
Ejemplo 636. N,N-Dimetil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
Este compuesto puede sintetizarse usando el procedimiento para el ejemplo 89 comenzando con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y dimetilamina.
Ejemplo 637. [4-[4-(7-Metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]-pirrolidin-1 -il-metanona.
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 94 comenzando con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y pirrolidina.
Ejemplo 638. [(3S)-3-Fluoropirrolidin-1-il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]metanona.
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 94 comenzando con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y S-3-fluoropirrolidina.
Ejemplo 639. [(3R)-3-Fluoropirrolidin-1-il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]metanona.
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 94 comenzando con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y R-3-fluoropirrolidina.
E je m p lo 640. 4 -[4 -(7 -M e tilp ira z o lo [1 ,5 -a ]p ir id in -6 - il) fe n o x i]-N -m e tils u lfa n il-p ip e r id in a -1 -c a rb o x a m id a .
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 94 comenzando con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y metanosulfenamida.
Ejemplo 641. N-Etilsulfanil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida.
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 94 comenzando con 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y etilsulfenamida.
Ejemplo 642. 4-[4-(4-Metil-3-quinolil)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida.
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 94 comenzando con 4-metil-3-[4-(4-piperidiloxi)fenil]quinolona 2HCl y metanosulfenamida.
Ejemplo 643. 4-[4-(4-Metil-3-quinolil)fenoxi]-N-etilsulfanil-piperidina-1-carboxamida.
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 94 comenzando con 4-metil-3-[4-(4-piperidiloxi)fenil]quinolona 2HCl y metanosulfenamida.
Ejemplo 644. 1-[4-[4-(7-Metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona.
Este compuesto puede sintetizarse usando 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y pirrolidin-2-ona.
Ejemplo 645. 1-[4-[4-(4-Metil-3-quinolil)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona.
Este compuesto puede sintetizarse usando 4-metil-3-[4-(4-piperidiloxi)fenil]quinolona 2HCl y pirrolidin-2-ona.
Ejemplo 646. 4-[4-(7-Metilpirazolo[1,5-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 537 usando 7-metil-6-[4-(4-piperidiloxi)fenil]pirazolo[1,5-a]piridina 2HCl y 1-isocianato-3-propano.
Ejemplo 647. N-etil-4-[4-(2-fluoro-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida.
Este compuesto puede sintetizarse usando el procedimiento para el Ejemplo 88 con 7-bromo-2-fluoro-8-metil-quinolina en lugar de 7-bromo -8-metil-quinolina usando el producto intermedio de ejemplo 529 Etapa 2, y reaccionando con oxicloruro fósforo seguido por la reacción con tetrabutilamonio fluoruro.
En la presente memoria se han descrito varias modalidades de la invención. No obstante, como apreciarán los expertos en la técnica, son posibles numerosas modificaciones y variaciones de la presente invención a la luz de las enseñanzas anteriores; sin apartarse del alcance de la invención que se describe en la presente memoria. Por lo tanto, se entiende que, dentro del alcance de las reivindicaciones adjuntas, la invención puede ponerse en práctica de manera diferente a como se describe específicamente en la presente memoria, y se pretende que el alcance de la invención abarque todas estas variaciones.
Claims (25)
- REIVINDICACIONESUn compuesto de acuerdo con la Fórmula I:o una sal farmacéuticamente aceptable del mismo, en donde:A se selecciona de -C(=O)- y -SO2-;R1 se selecciona de -H, -(C1-C10 ) hidrocarbilo, -(C1-C10 ) hidrocarbilo sustituido, heterociclilo de 3 a 7 miembros, heterociclilo sustituido de 3 a 7 miembros, -(C6-C10 ) arilo, -(C6-C10 ) arilo sustituido, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, -NR7R8, -OR7, -Sr 7, -N(OR8)R7, -N(SR8)R7 y -C(=O)-(C1-C6 ) alquilo;a y b se seleccionan independientemente de 0 y 1;cada R2 se selecciona independientemente de -H y -(C1-C4 ) alquilo;cada R3 se selecciona independientemente de -H y -(C1-C4 ) alquiloR4 se selecciona de -H, (C1-C6 ) alquilo, =O, -OH, -O(C1-C6 ) alquilo, halógeno y -CN; en donde uno de los grupos R3 puede opcionalmente conectarse estructuralmente a uno de los grupos R2 para formar un puente alquileno para producir un anillo bicíclico; ouno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R1 para formar un anillo heterociclilo de 5 a 7 miembros fusionado a la cara 1-2 del anillo de piperidina; ouno de los grupos R3 puede opcionalmente conectarse estructuralmente al grupo R4 para formar un anillo carbocíclico o heterocíclico de 5 a 7 miembros fusionado a la cara 2-3 del anillo de piperidina;—....... indica que el enlace designado es un simple enlace carbono-carbono o un doble enlace carbonocarbono;X se selecciona de -O-, -S-, -SO-, -SO2-, -NH- y -NR9-;W1, W2 y W3 se seleccionan independientemente de N, CH y C-R10; siempre que W2 y W 3 no sean N; R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3 ) haloalquilo, -OR7a, -CN-NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a-C(=O)OR7a, heteroarilo de 5 a 6 miembros, heteroarilo sustituido de 5 a 6 miembros, heteroarilo bicíclico de 8 a 10 miembros y heteroarilo bicíclico sustituido de 8 a 10 miembros;n es un número entero seleccionado de 1, 2, 3 y 4;R6 se selecciona de:en donde, cuando R6 es (i), Q1, Q2, Q3, Q4, Q5, Q6 y Q7 se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sean N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 sea C-R12;cuando R6 es (ii), Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a se seleccionan independientemente de N y C-R12, siempre que 1, 2 o 3 de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sean N, y el resto de Q1a, Q2a, Q3a, Q4a, Q5a, Q6a y Q7a sea C-R12;cuando R6 es (iii), Q8 se selecciona de O, S y N-R12n, Q9, Q10 y Q11 se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9, Q10 y Q11 sean N, y el resto de Q9, Q10 y Q11 sea C-R12;cuando R6 es (iv), Q8a se selecciona de O, S y N-R12n, Q9a, Q10a y Q11a se seleccionan independientemente de N y C-R12, siempre que 1 o 2 de Q9a, Q10a y Q11a sean N, y el resto de Q9a, Q10a y Q11a sea C-R12; cuando R6 es (v), Q12, Q13 y Q14 se seleccionan independientemente de N y C-R12; ycuando R6 es (vi), Q12a, Q13a y Q14a se seleccionan independientemente de N y C-R12;cuando R6 es (vii), Q15 se selecciona de N-R12n y C-R12 y Q16 se selecciona de N y C-R12; siempre que Q15 y Q16 no sean C-R12;en donde los átomos del anillo de carbono del anillo que no son cabeza de puente en (i), (ii), (iii), (iv), (v), (vi) y (vii) que no se designan como Q1, Q2, Q3, Q4, Q5, Q6, Q7, Q8, Q9, Q10, Q11, Q12, Q13, Q14, Q15, Q16, Q1a, Q2a, Q3a, Q4a, Q5a, Q6a, Q7a, Q8a, Q9a, Q10a, Q11a Q12a, Q13a o Q14a están sustituidos o no sustituidos;R7 se selecciona de -H, -(C1-C7 ) hidrocarbilo, -(C1-C7 ) hidrocarbilo sustituido, -C(=O)R8, -(C1-C6 ) heteroalquilo, arilo de 5 a 6 miembros, heteroarilo de 5 a 6 miembros y heterociclilo de 5 a 6 miembros; R8 se selecciona de -H, y -(C1-C6 ) alquilo, en donde R7 puede opcionalmente conectarse estructuralmente a R8 para formar un anillo heterociclilo de 5 a 7 miembros;R7a se selecciona de -H, -(C1-C7 ) hidrocarbilo, -(C1-C7 ) hidrocarbilo sustituido, -C(=O)R8, y -(C1-C6 ) heteroalquilo;R8a se selecciona de -H y -(C1-C6 ) alquilo, en donde R7a puede opcionalmente conectarse estructuralmente a R8a para formar un anillo heterociclilo de 5 a 7 miembros;R9 se selecciona de -(C1-C7 ) hidrocarbilo, en donde R9 puede opcionalmente conectarse estructuralmente a R4 para formar un anillo heterociclilo de 5 a 7 miembros;cada R10 se selecciona independientemente de -(C1-C7 ) hidrocarbilo, -(C1-C7 ) hidrocarbilo sustituido, halógeno, -C(=O)(C1-C7)hidrocarbilo, -C(=O)NH2 , -C(=O)NH(C1-C7)hidrocarbilo, -C(=O)N((C1-C7)hidrocarbilo)2, -OH, -O(C1-C7) hidrocarbilo, -O(C1-C7) hidrocarbilo sustituido, -(C3-C6)heterociclilo, -(C3-C6)heterociclilo sustituido, -CN, -NH2 , -NH(C1-C6 )alquilo, -N(C1-C6 alquilo)2 , -NH(CH2 )m-R11, -N(C1-C6 alquilo)(CH2 )m-R11, -O-(CH2 )m-R11 y -(C1-C6 ) heteroalquilo;m es un número entero seleccionado independientemente de 1, 2, 3 y 4; yR11 se selecciona de -O(C1-C6 ) alquilo, -N(C1-C6 alquilo)2 , -(C3-C6 ) heterociclilo y -(C3-C6 ) heterociclilo sustituido; y en donde cada R12 se selecciona independientemente de -H, halógeno, -(C1-C6 ) alquilo, -(C3-C6) cicloalquilo, heterociclilo de 5 a 6 miembros, -OH, -O(C1-C6 ) alquilo, -O(CH2 )r-(heterociclilo de 5 a 6 miembros), -O(CH2 )r-O(C1-C6 ) alquilo, -NH2 , -CN, -NH(C1-C6 ) alquilo, -N(C1-C6 alquilo)2 , -NH(CH2 )r-O(C1-C6) alquilo, -NH(CH2 )r-N(C1-C6 alquilo)2 , -C(=O)NH2 , -C(=O)NH(C1-C6 ) alquilo y -C(=O)N(C1-C6 alquilo)2 ; en donde r es un número entero seleccionado independientemente de 1,2, 3 y 4; ycada R12n se selecciona independientemente de -H, -(C1-C7 ) hidrocarbilo y -(C1-C7 ) hidrocarbilo sustituido.
- 4. El compuesto de acuerdo con la reivindicación 1 o una sal farmacéuticamente aceptable del mismo, en donde W1, W2 y W3 son CH.
- 5. El compuesto de acuerdo con la reivindicación 1 o una sal farmacéuticamente aceptable del mismo, en donde R1 se selecciona de -(C1-C10 ) hidrocarbilo, -SR7, -NR7R8 y -N(OR8)R7.
- 6. El compuesto de acuerdo con la reivindicación 1 o una sal farmacéuticamente aceptable del mismo, en donde X es -O-.
- 7. El compuesto de acuerdo con la reivindicación 1 o una sal farmacéuticamente aceptable del mismo, en donde R4 es -H o halógeno.
- 8. El compuesto de acuerdo con la reivindicación 1 o una sal farmacéuticamente aceptable del mismo, en donde:A es -C(=O)-;R1 se selecciona de -NR7R8 y -N(OR8)R7;a es 1; b es 1;cada R2 es -H; cada R3 es -H;R4 se selecciona de -H, -(C1-C6 ) alquilo, -OH, -O(C1-C6 ) alquilo, halógeno y -CN;--------- es un simple enlace carbono-carbono;X se selecciona de -O- y -S-;W1, W2 y W3 son cada uno CH;R5 se selecciona de -H, -C1-C7 hidrocarbilo, -C3-C6 heterociclilo; halógeno, -(C1-C3 ) haloalquilo, -OR7a, -CN, -NR7aR8a, -O(CH2)nNR7aR8a, -O(CH2)nOR8a, -NR8a(CH2)nNR7aR8a, -NR8a(CH2)nOR8a, -C(=O)NR7aR8a, -C(=O)OR7a, heteroarilo de 5 a 6 miembros y heteroarilo sustituido de 5 a 6 miembros;R6 esyR7 se selecciona de -H, -(C1-C7 ) hidrocarbilo, -(C1-C7 ) hidrocarbilo sustituido, -C(=O)R8 y -(C1-C6 ) heteroalquilo.
- 9. El compuesto de acuerdo con la reivindicación 8 o una sal farmacéuticamente aceptable del mismo, en dondeX es -O-.
- 10. El compuesto de acuerdo con la reivindicación 8 o una sal farmacéuticamente aceptable del mismo, en dondeR5 se selecciona de -H, -(C1-C7 ) hidrocarbilo y halógeno.
- 11. El compuesto de acuerdo con la reivindicación 8 o una sal farmacéuticamente aceptable del mismo, en dondeuno de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es N, y el resto de Q1, Q2, Q3, Q4, Q5, Q6 y Q7 es C-R12.
- 12. El compuesto de acuerdo con la reivindicación 11 o una sal farmacéuticamente aceptable del mismo, en dondeuno de Q2 y Q6 es N; el otro de Q2 y Q6 es C-R12; y Q1, Q3, Q4, Q5 y Q7 son C-R12.
- 13. El compuesto de acuerdo con la reivindicación 8, seleccionado de:isoxazolidin-2-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-isoxazolidin-2-il-metanona;isoxazolidin-2-il-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona;{4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona;isoxazolidin-2-il-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;isoxazolidin-2-il-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;isoxazolidin-2-il-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;isoxazolidin-2-il-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona;ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoxiamida;ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoximetil-amida;ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico etilamida;ácido 4-[4-(8-metoxiqumolm-7-il)-fenoxi]-piperidina-1-carboxílico metilamida;ácido 4-[4-(8-metoxiqumolm-7-il)-fenoxi]-piperidina-1-carboxílico etilamida;ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico hidroxiamida;N-etil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N,N-dimetil-4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxamida;N-metoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-isopropil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-etoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-pirrolidin-1-il-metanona;N-metil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;4-[4-(8-metil-7-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida;4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(1-piperidil)metanona;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-morfolinometanona;N-metoxi-4-[4-(8-metoxi-7-quinolil)fenoxi]piperidina-1-carboxamida;3- [4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-oxazolidin-2-ona;1-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-pirrolidin-2-ona;N-etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;4- [4-(8-metil-7-quinolil)fenoxi]-N-(2-pirrolidin-1 -iletil)piperidina-1 -carboxamida;4-[4-(8-metil-7-quinolil)fenoxi]-N-(2-morfolinoetil)piperidina-1-carboxamida;(4-isopropilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona; (4-metilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperidil)metanona; (4-etilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona;N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-isobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-(2-metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-(2-dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxamida; N-[2-(1H-imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;4-[4-(8-metil-7-quinolil)fenoxi]-N-tetrahidropiran-4-il-piperidina-1-carboxamida; N-ciclobutil-4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxamida;ácido 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbohidroxámico;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)metanona;N-(ciclobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona;4-[4-(8-metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida;N-etil-4-[4-(l-metil-6-isoquinolil)fenoxilpiperidina-1-carboxamida;4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propil-piperidina-1-carboxamida;N-isobutil-4-[4-(1-metil-6-isoquinolil)fenoxilpiperidina-1-carboxamida;4-[4-(-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;N-(ciclopropilmetil)-4-[4-(1-metil-6-isoquinolil)fenoxilpiperidina-1-carboxamida; N-isopropoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propoxipiperidina-1-carboxamida;ácido 4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carbohidroxámico;N-etoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;N-etoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida;N-isobutil-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-etilsulfanil-piperidina-1-carboxamida,1-[4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona;y sales farmacéuticamente aceptables de los mismos.
- 14. Una composición farmacéutica que comprende al menos un compuesto de acuerdo con la reivindicación 1 o una sal farmacéuticamente aceptable del mismo, y al menos un excipiente farmacéuticamente aceptable.
- 15. Un compuesto de acuerdo con la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento de un sujeto que sufre de un trastorno mediado por la sintasa de ácidos grasos.
- 16. Una composición farmacéutica de acuerdo con la reivindicación 14, para su uso en el tratamiento de un sujeto que sufre de un trastorno mediado por la sintasa de ácidos grasos.
- 17. El compuesto, o sal farmacéuticamente aceptable del mismo, para su uso de acuerdo con la reivindicación 15 o la composición farmacéutica para su uso de acuerdo con la reivindicación 16, en donde el trastorno mediado por la sintasa de ácidos grasos es esteatosis hepática no alcohólica (NASH).
- 18. Un compuesto de acuerdo con la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento de un sujeto que sufre de aumento de peso asociado con la terapia farmacológica con un agente antipsicótico.
- 19. El compuesto para su uso de la reivindicación 18, en donde el agente antipsicótico se selecciona de clozapina, risperidona, aripiprazol, olanzapina, quetiapina y ziprasidona y sus combinaciones.
- 20. El compuesto de acuerdo con la reivindicación 1, seleccionado de:1-[4-(4-isoquinolin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona;1- [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;2- metil-1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona;f-butil éster del ácido 4-(2-fluoro-4-quinolin-3-il-fenox)piperidina-1-carboxílico;1-[4-(2-fluoro-4-quinolin-3-il-fenoxi)piperidin-1-il]propan-1-ona;1-[4-(2-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;1- [4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;2- metil-1-[4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(4-1,5-naftiridin-3-il-fenoxi)-piperidin-1-il]-metanona;éster metílico del ácido 4-(2-fluoro-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico; 1-{4-[4-(2-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(2-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona;1-{4-[4-(2-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-fluoroquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxil-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-fluoro-2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(5-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-{4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; ciclopropil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona;1-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il}-propan-1-ona;ciclobutil-[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-metanona;[4-(4-quinolin-2-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona;1-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona;ciclobutil-[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-metanona;[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona;{4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclobutilmetanona;1-{4-[4-(4-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-[4-(4-Furo[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona;Ciclopropil-[4-(4-furo[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-metanona;1-{4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(6,7-dimetoxiquinolin-3-il)-fenoxil-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(6,7-dimetoxiquinolin-3-il)-fenoxi]-pipendin-1-il}-metanona;1-{4-[4-(8-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(8-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona;1-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona;[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(S)-tetrahidrofuran-2-il-metanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1 -{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1 -il}-propano-1,2-diona; isoxazolidin-2-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;[4-(4-isoquinolin-3-il-fenoxi)-piperidin-1-il]-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(8-metil-quinolin-7-il)-fenoxi]-pipendin-1-il}-metanona; {4-[4-(4-cloroquinolin-3-il)-fenoxi]-piperidin-1-il}-isoxazolidin-2-il-metanona;{4-[4-(8-cloroquinolin-7-il)-fenoxil-piperidin-1-il-isoxazolidin-2-il-metanona; isoxazolidin-2-il-{4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-{4-[-piperidin-1-il}-metanona;isoxazolidin-2-il-{4-[4-(7-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; isoxazolidin-2-il-[4-(4-quinoxalin-2-il-fenoxi)-piperidin-1-il]-metanona;ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico metoxiamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxil-piperidina-1-carboxílico metoximetil-amida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico etilamida; ácido 4-[4-(8-metoxiqumolm-7-il)-fenoxi]-piperidina-1-carboxílico metilamida; ácido 4-[4-(8-metoxiqumolm-7-il)-fenoxi]-piperidina-1-carboxílico etilamida; ácido 4-[4-(4-metilquinolin-3-il)-fenoxi]-piperidina-1-carboxílico hidroxiamida; N-etil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N,N-dimetil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;etil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato;N-metoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-isopropil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-etoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;[4-[4-(8-metil-7-quinolil)fenoxi]-1 -piperidil]-pirrolidin-1 -il-metanona;N-metil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;4-[4-(8-metil-7-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida;4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(1-piperidil)metanona;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-morfolino-metanona;ciclopropil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;ciclobutil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;ciclopentil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona;[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(S)-tetrahidrofuran-2-il-metanona;2-metoxi-1-[4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona;[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona;[4-(4-quinolin-3-il-fenoxil)-piperidin-1-il]-(tetrahidrofuran-3-il)-metanona;(R) -2-metoxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;(S) -2-metoxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il-propan-1-ona;2-hidroxi-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona;[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidropiran-2-il)-metanona;1- [4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona;2- metil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;2,2-dimetil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;(2-metiltetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; (2-metil-1,3-dioxolan-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 2-metanosulfonil-1-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-etanona;(1,1-dioxidotetrahidrotiofen-2-il)(4-(4-(quinolin-3-il)fenoxi)piperidin-1-il)-metanona; (3,3-difluorociclobutil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;(R)-5-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-dihidrofuran-2-ona;(3-metilfuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;(3,5-dimetilfuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; oxazol-2-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;isoxazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;isotiazol-3-il-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-(tetrahidrofuran-2-il)-metanona; fenil-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;(2,5-dimetilfenil)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;[3-(1H-imidazol-2-il)-fenil]-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;[3-(1H-bencimidazol-2-il)-fenil]-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; N-metoxi-4-[4-(8-metoxi-7-quinolil)fenoxi]piperidina-1-carboxamida;1- [4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona;2- metil-1-[4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(5-quinolin-3-il-piridin-2-iloxi)-piperidin-1-il]-metanona;1- [4-(5-quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona;2- metil-1-[4-(5-quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(5-quinolin-7-il-piridin-2-iloxi)-piperidin-1-il]-metanona;2-metil-1-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-metanona;1- [4-(6-quinolin-3-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona;2- metil-1-[4-(6-quinolin-3-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(6-quinolin-3-il-piridin-3-iloxi)-piperidin-1-il]-metanona;1-[4-(5-quinolin-3-il-pirimidin-2-iloxi)-piperidin-1-il]-propan-1-ona;1- [4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona;2- metil-1-[4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; ciclopropil-[4-(6-quinolin-7-il-piridin-3-iloxi)-piperidin-1-il]-metanona;1-[4-(6-isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-propan-1-ona; 1-[4-(6-isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-2-metil-propan-1-ona;ciclopropil-[4-(6-isoquinolin-6-il-piridin-3-iloxi)-piperidin-1-il]-metanona;oxo-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-acetaldehído;4- (4-quinolin-3-il-fenoxi)-piperidina-1-carbaldehído;((2R,3S)/(2S,3R)-3-metil-tetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;((2R,3S,5R)/(2S,3R,5S)-3,5-dimetil-tetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; ((2R,3S,5R)/(2S,3R,5S)-3,5-dimetil-tetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona; 3-[4-(1-metanosulfonil-piperidin-4-iloxi)-fenil]-quinolina;(4,4-difluorotetrahidrofuran-2-il)-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;(4,4-difluorotetrahidrofuran-2-il)-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;(4,4-difluorotetrahidrofuran-2-il)-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona;5- [4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]dihidrofuran-3-ona;1-{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-[4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;1-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona;ciclopropil-(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxil}-piperidin-1-il)-metanona;1-(4-{4-[8-(2-pirrolidin-1-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona;ciclopropil-(4-{4-[8-(2-pirrolidin-1-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona;1-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-pipendin-1-il)-propan-1-ona;ciclopropil-(4-{4-[8-(3-pirrolidin-1-il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-metanona;1-[4-[4-[8-[2-(4-metilpiperazin-1-il)etoxil-7-quinolil]fenoxi]-1-piperidil]propan-1-ona;1-[4-[4-[8-(2-metoxietoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona;1-[4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]propan-1-ona;{4-[4-(8-isopropoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(8-etoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;(4-{4-[8-(2-morfolin-4-il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona;(4-{4-[8-(2-pirrolidin-1 -il-etoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-(R)-tetrahidrofu ran-2-il-metanona; (4-{4-[8-(3-pirrolidin-1 -il-propoxi)-quinolin-7-il]-fenoxi}-piperidin-1 -il)-(R)-tetrahidrofu ran-2-il-metanona;[4-[4-[8-[2-(4-metilpiperazin-1-il)etoxil-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il] metanona;[4-[4-[8-(2-metoxietoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;[4-[4-[8-(3-metoxipropoxi)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;1-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(8-hidroxiquinolin-7-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-[4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;[4-(2-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-ciclopropilmetanona;1-[4-(2-cloro-4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(2-cloro-4-quinolin-7-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;1-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;ciclopropil-[4-(2-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;1-[4-(2-metoxi-4-quinolin-7-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(3-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(3-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metilpropan-1-ona;ciclopropil-[4-(3-fluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;1-[4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1- [4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;[4-(3-cloro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-ciclopropilmetanona;2- metil-1-[4-(3-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(3-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;éster metílico del ácido 4-(3-metil-4-quinolin-3-il-fenoxi)-piperidina-1-carboxílico;1-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;ciclopropil-[4-(3-metoxi-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;1- [4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;2- metil-1-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(2-metil-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;1 -[4-(2,5-difluoro-4-quinolin-3-il-fenoxi)-piperidin-1 -il-propan-1 -ona;1-[4-(2,5-difluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;ciclopropil-[4-(2,5-difluoro-4-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;3- oxo-3-[4-(4-quinolin-3-il-fenoxi)-piperidin-1-il]-propionitrilo;1-{4-[2-fluoro-4-(8-metoxi-quinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona; {4-[2-fluoro-4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(8-cloroquinolin-7-il)-2-fluorofenoxi]-piperidin-1-il}-ciclopropilmetanona;{4-[4-(8-cloroquinolin-7-il)-2-fluorofenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(8-cloroquinolin-7-il)-2-fluorofenoxi]-pipendin-1-il}-propan-1-ona;1-{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[2-fluoro-4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;{4-[2-fluoro-4-(4-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(4-aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{4-[4-(4-dimetilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(4-dimetilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(4-aminoquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(4-metilaminoquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(4-metilaminoquinolin-3-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(4-morfolin-4-il-quinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(4-morfolin-4-il-quinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-(4-{4-[4-(4-metilpiperazin-1-il)-quinolin-3-il]-fenoxi}-piperidin-1-il)-propan-1-ona;(4-{4-[4-(4-metilpiperazin-1-il)-quinolin-3-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 3-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-oxazolidin-2-ona;1 -[4-(4-quinolin-3-il-fenoxi)-piperidin-1 -il]-butano-1,3-diona;1-[4-(4-quinolin-3-il-fenoxi)-piperidina-1-carbonil]-pirrolidin-2-ona;1-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{4-[4-(2-metil-2H-indazol-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-[4-(4-[1,8]naftiridin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-{4-[4-(2-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-[4-(4-imidazo[1,2-a]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona;{4-[4-(4-cloroquinolin-7-il)-fenoxil-piperidin-1-il-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona;1-{4-[4-(4-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(8-cloro-quinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(8-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;(R)-tetrahidrofuran-2-il-[4-(4-tieno[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il}-metanona;1-[4-(4-tieno[3,2-b]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona;{4-[4-(3-cloroquinolin-7-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(3-cloroquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;[4-(4-benzotiazol-5-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona;[4-(4-benzotiazol-5-il-fenoxi)-piperidin-1-il]-ciclopropilmetanona;1 -[4-(4-benzotiazol-5-il-fenoxi)-piperidin-1 -il]-propan-1 -ona;ciclopropil-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(8-metoxiquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(6-metilquinolin-7-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(6-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo;7-{4-[1-((R)-tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-fenil}-quinolina-3-carbonitrilo;7-[4-(1-ciclopropanocarbonil-piperidin-4-iloxi)-fenil]-quinolina-3-carbonitrilo;1 -{4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona;{4-[4-(3-metilquinolin-7-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[4-(3-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(2,3-dimetilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran 2-il-metanona; 1-{4-[4-(2,3-dimetilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(2,3-dimetilimidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona;[4-(4-imidazo[1,5-alpiridin-6-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona;1-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-metanona;ácido 1-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidina-1-carbonil]-ciclopropanocarboxílico amida; (1-hidroxiciclopropil)-[4-(4-imidazo[1,5-a]piridin-6-il-fenoxi)-piperidin-1-il]-metanona;(1-hidroxiciclopropil)-{4-[4-(8-metoxi-quinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;(1-hidroxiciclopropil)-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona;(R)-tetrahidrofuran-2-il-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona; ciclopropil-[4-(4-[1,2,4]triazolo[4,3-a]piridin-7-il-fenoxi)-piperidin-1-il]-metanona; {4-[4-(8-metilquinolin-7-il)-fenoxil-piperidin-1-il}-(1-trifluorometilciclopropil)-metanona;(1-aminociclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxil-piperidin-1-il-metanona;{4-[4-(1-metil-1H-indazol-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;[4-(4-imidazo[1,2-a]piridin-6-il-fenoxi)-piperidin-1-il]-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(8-metilquinolin-7-il)-fenoxil-piperidina-1-carbonil}-ciclopropanocarbonitrilo;(1-metilciclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxil-piperidin-1 -il}-metanona;((S)-2,2-dimetilciclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxil-piperidin-1-il}-metanona;(2,2-dimetilciclopropil)-{4-[4-(8-metil-quinolin-7-il)-fenoxil-piperidin-1-il metanona;[4-[4-[8-(4-metilpiperazin-1-il)-7-quinolil]fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;[4-[4-(8-amino-7-quinolil)fenoxil-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;{4-[4-(8-metilaminoquinolin-7-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(8-metilaminoquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;(4-{4-[8-(2-metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-metoxietilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-propan-1-ona;(4-{4-[8-(2-dimetilaminoetilamino)-quinolin-7-il]-fenoxil-piperidin-1-il)-(R)tetrahidrofuran-2-il-metanona; 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carbonitrilo;[4-[4-[8-(dimetilamino)-7-quinolilfenoxil-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;1-{4-[4-(8-dimetilaminoquinolin-7-il)-fenoxil-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(8-dimetilamino-quinolin-7-il)-fenoxil-piperidin-1-il}-metanona;(4-{4-[8-(2-pirrolidin-1-il-etilamino)-quinolin-7-il]-fenoxi}-piperidin-1-il)-(R)-tetrahidrofuran-2-il-metanona; 1-(4-{4-[8-(2-pirrolidin-1-il-etilamino)-quinolin-7-il]-fenoxil-piperidin-1-il)-propan-1-ona;7-[4-[[1-[(2R)-tetrahidrofuran-2-carbonil]-4piperidil]oxi]fenil]quinolina-8-carboxamida;ácido 7-[4-(1-propionil-piperidin-4-iloxi)-fenil]-quinolina-8-carboxílico amida;1- (3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona;2- metil-1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)propan-1-ona;ciclopropil(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)metanona;3- metil-1-(3-(4-(quinolin-3-il)fenoxi)azetidin-1-il)butan-1-ona;(S)-1-(3-(4-(quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona;(S)-1-(3-(4-(quinolin-3-il)fenoxi)pirrolidin-1-il)propan-1-ona;(R)-1-(3-(4-(quinolin-7-il)fenoxi)pirrolidin-1-il)propan-1-ona;(R)-1-(3-(4-(quinolin-3-il)fenoxi)pirrolidin-1-il)propan-1-ona;1-(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)propan-1-ona;ciclopropil(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)metanona;1-(4-(4-(7-metilquinolin-5-il)fenoxi)piperidin-1-il)propan-1-ona;ciclopropil-{4-[4-(7-metil-quinolin-5-il)-fenoxi]-piperidin-1-il}-metanona;1- (4-(4-(6-metilquinolin-5-il)fenoxi)piperidin-1-il)propan-1-ona;ciclopropil(4-(4-(6-metilquinolin-5-il)fenoxi)piperidin-1-il)metanona;(R)-(4-(4-(5-metilquinolin-7-il)fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona;(R)-(4-(4-(7-metilquinolin-5-il)fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona;(R)-(4-(4-(6-metilquinolin-5-il)fenoxi)piperidin-1-il)(tetrahidrofuran-2-il)metanona;(±)-(7S,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona;(±)-(7R,8aS)-7-(4-(8-metilquinolin-7-il)fenoxi)hexahidroindolizin-3(2H)-ona;2.2.2- trifluoro-1-{4-[4-(8-metil-quinolin-7-il)-fenoxil-piperidin-1-il}-etanona;2.2- difluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxil-piperidin-1-il}-propan-1-ona;2- fluoro-1-{4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{exo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{exo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-propan-1-ona;{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{2-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il(R)-tetrahidrofuran-2-il-metanona;1-{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{cis-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;1-{endo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-propan-1-ona;ciclopropil-{endo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-metanona;{endo-3-[4-(8-metilquinolin-7-il)-fenoxi]-8-aza-biciclo[3,2,1]oct-8-il}-(R)-tetrahidrofuran-2-il-metanona; {(trans)-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{trans-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{trans-3-fluoro-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;1-{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-metanona;{3-metil-4-[4-(8-metilquinolin-7-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(3-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropil-metanona;1-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(3-metoxiisoquinoln-6-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(3-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(3-metoxi-isoquinolin-6-il)-fenoxi]-piperidin-1-il} -(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona;1-{4-[4-(3-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{4-[4-(3-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(3-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona;1-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-ciclobutil-metanona;{4-[4-(1-cloroisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(3-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(1-metilisoquinolin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclobutil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona;ciclopropil-{4-[4-(1-metoxiisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(3-aminoisoquinolin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(3-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(1-etilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(1-ciclopropil-isoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(1-ciclopropilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(7-metoxi-6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxil-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(6-fluoro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxil-piperidin-1-il}-propan-1-ona;{4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-ciclopropilmetanona;{4-[4-(6-cloro-7-metoxiquinolin-3-il)-fenoxi]-pipendin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(6-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(3-isopropoxiisoquinolin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-morfolin-4-il-isoquinolin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahyrofuran-2-il metanona; {4-[4-(1-aminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-dimetilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(1-metilaminoisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(4-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(5-metilquinolin-3-il)-fenoxil-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(5-metil-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(5-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(5-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(5-metoxiquinolin-3-il)-fenoxil-piperidin-1-il}-metanona;{4-[4-(5-metoxiquinolin-3-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-[4-(4-isoquinolin-6-il-fenoxi)-piperidin-1-il]-metanona;[4-[4-(6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;{4-[4-(5-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1 -[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1 -piperidil]propan-1 -ona;ciclopropil-[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1-piperidil]metanona;[4-[4-(1,4-dimetil-6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;1-[4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]propan-1-ona;ciclopropil-[4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]metanona;[4-[4-(1,5-dimetil-6-isoquinolil)fenoxi]-1-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;[4-[4-(8-ciclopropil-7-quinolil)fenoxi]-1l-piperidil]-[(2R)-tetrahidrofuran-2-il]metanona;{4-[4-(3-etilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(7-fluoroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;{4-[4-(7-fluoroquinolin-3-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;{4-[4-(3-ciclopropilisoquinolin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; ciclopropil-{4-[4-(1-metilisoquinolin-6-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(7-metilquinolin-3-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona;1-{4-[4-(6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(6-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona; {4-[4-(6-metilquinolin-3-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1- {4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;cidopropil-{4-[4-(8-metilquinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(8-metilquinolin-3-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 2- metil-1-[4-(4-quinolin-7-il-bencenosulfonil)-piperidin-1-il]-propan-1-ona;1-[4-(4-isoquinolin-7-il-bencenosulfonil)-piperidin-1-il]-2-metilpropan-1-ona;1-[4-(4-isoquinolin-6-il-bencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona;1-(4-((4-(quinolin-7-il)fenil)tio)piperidin-1-il)propan-1-ona;1-(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona;1-(4-((4-(quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona;1-(4-((4-(isoquinolin-4-il)fenil)tio)piperidin-1-il)propan-1-ona;1-(4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)propan-1-ona;1- (4-((4-(isoquinolin-6-il)fenil)tio)piperidin-1-il)-2-metilpropan-1-ona;2- metil-1-(4-((4-(quinolin-3-il)fenil)tio)piperidin-1-il)propan-1-ona;1-(4-((4-(isoquinolin-4-il)fenil)tio)piperidin-1-il)-2-metilpropan-1-ona;1-14-[metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-metanona;1- [4-(4-quinolin-3-il-fenilamino)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(4-quinolin-3-il-fenilamino)-piperidin-1-il]-metanona;14-[metil-(4-quinolin-3-il-fenil)-amino]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; N-etil-4-[4-(2-hidroxi-8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;4-[4-(8-metil-7-quinolil)fenoxil-N-(2-pirrolidin-1 -iletil)piperidina-1 -carboxamida;4-[4-(8-metil-7-quinolil)fenoxil-N-(2-morfolinoetil)piperidina-1-carboxamida;(4-isopropilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona;(4-metilpiperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(4-morfolino-1-piperidil)metanona;(4-etil piperazin-1-il)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona;N-etil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxilpiperidina-1-carboxamida;N-(ciclopropilmetil)-4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxamida;N-isobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-(2-metoxietil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-isobutoxi-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida;N-(2-dimetilaminoetil)-4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxamida;2- morfolinoetil 4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxilato;2-pirrolidin-1-iletil4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato;N-[2-(1H-imidazol-4-il)etil]-4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxamida; 4-[4-(8-metil-7-quinolil)fenoxil-N-tetrahidropiran-4-il-piperidina-1-carboxamida; isobutil 4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxilato;alil 4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carboxilato;N-ciclobutil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ciclopropilmetil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato;ácido 4-[4-(8-metil-7-quinolil)fenoxilpiperidina-1-carbohidroxámico;2-metoxietil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; tetrahidropiran-4-il 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato; tetrahidropiran-3-il 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-(oxazinan-2-il)metanona; tetrahidrofuran-3-il 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato;N-(ciclobutilmetil)-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida; ciclobutil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxilato;azepan-1-il-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]metanona;4-[4-(8-metil-7-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida;N-etil-4-[4-(1-metil-6-isoquinolil)fenoxilpiperidina-1-carboxamida;4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propil-piperidina-1-carboxamida;N-isobutil-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;N-(ciclopropilmetil)-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;4-[4-(1-metil-6-isoquinolil)fenoxi]-N-propoxipiperidina-1-carboxamida;ácido 4-[4-1-metil-6-isoquinolil)fenoxilpiperidina-1-carbohidroxámico;N-etoxi-4-[4-(1-metil-6-isoquinolil)fenoxi]piperidina-1-carboxamida;N-etoxi-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(4-metil-3-quinolil)fenoxilpiperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-propoxi-piperidina-1-carboxamida;N-isobutil-4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-propil-piperidina-1-carboxamida; 2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]etanona;(2R)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]propan-1-ona;(2S)-2-amino-1-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]propan-1-ona;ácido 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxilpiperidina-1-carbohidroxámico;2-(dimetilamino)-1-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]etanona;[(2R)-1 -metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1 -piperidil]-metanona;[(2S)-1 -metilpirrolidin-2-il]-[4-[4-(8-metil-7-quinolil)fenoxi]-1 -piperidil]-metanona;S-isopropil 4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carbotioato;2- amino-2-metil-1-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]propan-1-ona;[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]-[(2R)-pirrolidin-2-il]metanona;[4-[4-(8-metil-7-quinolil)fenoxi]-1 -piperidil]-[(2S)-pirrolidin-2-il]metanona;[1-(metilamino)ciclopropil]-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]-metanona;3- amino-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]propan-1-ona;2-isopropoxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona;[2-[4-[4-(8-metil-7-quinolil)fenoxil-1-piperidil]-2-oxo-etil]acetato;2-hidroxi-1-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]etanona;(1-aminociclobutil)-[4-[4-(8-metil-7-quinolil)fenoxi]-1-piperidil]metanona;N-etil-4-(4-imidazo[1,2-a]piridin-7-ilfenoxi)piperidina-1-carboxamida;4- [4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxil-N-metilsulfanil-piperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-metilsulfanil-piperidina-1-carboxamida;4-[4-(4-metil-3-quinolil)fenoxi]-N-etilsulfanil-piperidina-1-carboxamida;1-[4-[4-(4-metil-3-quinolil)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona;N-etil-4-[4-(2-fluoro-8-metil-7-quinolil)fenoxilpiperidina-1-carboxamida;{4-[4-(8-metilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1 -{4-[4-(8-metilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1 -il-propan-1 -ona;{4-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-14-[4-(5-metilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona;ciclopropil-{4-[4-(8-metilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-metanona;{4-[4-(7-metilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(7-metilimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-propan-1-ona;{4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; {4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1- {4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-propan-1-ona;{4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-ciclopropilmetanona;(1-hidroximetilciclopropil)-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; (1-aminociclopropil)-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il} metanona;(1-hidroxiciclopropil)-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxil-piperidin-1-il}-metanona;2- hidroxi-2-metil-1-{4-[4-(5-metil-imidazo[1,2-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona; {4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; (1-hidroxiciclopropil)-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1 -il}-metanona; 1-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il]-propan-1-ona; ciclopropil-{4-[4-(5-metil-[1,2,4]triazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il metanona;1-{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il]-propan-1-ona;ciclopropil-1{-4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona; ciclobutil-{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-metanona;{4-[4-(4-metoxipirazolo[1,5-a]piridin-6-il)-fenox]-piperidin-1-il}-(R)-tetrahidrofuran-2-il-metanona; 1-{4-[4-(4-Hidroxipirazolo[1,5-a]piridin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclobutil-{4-[4-(4-hidroxi-pirazolo[1,5-a]piridin-6-il)-fenoxil-piperidin-1-il metanona;N-etil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-etoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-metoxioxi-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxilpiperidina-1-carboxamida;N-butil-4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-etil-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-isobutil-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-propil-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-(2-metoxietil)piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-(ciclopropilmetil)piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-isopropoxi-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-isopropil-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-isobutoxi-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-isopentil-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxil-N-etoxi-piperidina-1-carboxamida;ácido 4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxilpiperidina-1-carbohidroxámico;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxi-piperidina-1-carboxamida;4-[4-(5-cloroimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-etil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-isobutil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida;N-(ciclopropilmetil)-4-[4-(5-metilimidazo[1,2-alpiridin-6-il)fenoxilpiperidina-1-carboxamida;4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxil-N-(3-piridil)piperidina-1-carboxamida;N-(2-metoxietil)-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxilpiperidina-1-carboxamida;[4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-1-piperidil]-(4-metilpiperazin-1-il)metanona;N,N-dimetil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-isobutoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;isobutil 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato;N-isopropil-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(1-metilpirazol-4-il)piperidina-1-carboxamida; terc-butil 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxilato;4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-(2,2,2-trifluoroetil)piperidina-1-carboxamida; 4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]-N-propoxi-piperidina-1-carboxamida;N-etoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-metoxi-4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;4-[4-(5-metilimidazo[1,2-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;N-etil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida;N-isopropoxi-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida;4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]-N-propil-piperidina-1-carboxamida;N-isobutil-4-[4-(8-metilimidazo[1,2-a]piridin-7-il)fenoxi]piperidina-1-carboxamida;N-isobutil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;ácido 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carbohidroxámico;N,N-dimetil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil]-pirrolidin-1 -il-metanona;[(3S)-3-fluoropirrolidin-1 -il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1-piperidil] metanona;[(3R)-3-fluoropirrolidin-1 -il]-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-1 -piperidil]metanona; 4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxil-N-metilsulfanil-piperidina-1-carboxamida;N-etilsulfanil-4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carboxamida;1-[4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]piperidina-1-carbonil]pirrolidin-2-ona;4-[4-(7-metilpirazolo[1,5-a]piridin-6-il)fenoxi]-N-propil-piperidina-1-carboxamida;y sales farmacéuticamente aceptables de los mismos.
- 21. Un compuesto seleccionado del grupo que consiste en:1 -[4-(4-benzo[b]tiofen-5-il-fenoxi)-piperidin-1 -il]-propan-1 -ona;1-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(3-quinolin-3-il-fenoxi)-piperidin-1-il]-metanona;1-[4-(4-benzofuran-5-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-[4-(4-benzofuran-5-il-fenoxi)-piperidin-1-il]-2-metil-propan-1-ona;1- [4-(4-naftalen-2-il-fenoxi)-piperidin-1-il]-propan-1-ona;2- metil-1 -[4-(4-naftalen-2-il-fenoxi)-piperidin-1 -il]-propan-1 -ona;ciclopropil-{4-[4-(5,6,7,8-tetrahidro-quinolin-3-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxil-piperidin-1-il}-metanona;1- {4-[4-(5,6,7,8-tetrahidroquinolin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1 -{4-[4-(1 H-pirrolo[2,3-b]piridin-5-il)-fenoxi]-piperidin-1 -il}-propan-1 -ona;ciclopropil-{4-[4-(1H-pirrolo[2,3-b]piridin-5-il)-fenoxil-piperidin-1-il}-metanona;ácido 1 -propionil-piperidina-4-carboxílico metil-(4-quinolin-7-il-fenil)-amida;ácido 1 -propionil-piperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida;ácido 1 -propionilpiperidina-4-carboxílico (4-isoquinolin-6-il-fenil)-metilamida;2- fluoro-4-isoquinolin-6-il-N-metil-N-(1-propionil-piperidin-4-il)-benzamida;1-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxil-piperidin-1-il}-propan-1-ona; ciclopropil-{4-[4-(3-trifluorometil-1,2,4-triazolo[4,3-a]piridin-6-il)-fenoxi]-piperidin-1 -il}-metanona; (R)-tetrahidrofuran-2-il-14-[4-(3-trifluorometil-1,2,4-triazolo[4,3-alpiridin-6-il)-fenoxi]-piperidin-1-il}-metanona;4'-[1-((R)-tetrahidrofuran-2-carbonil)-piperidin-4-iloxi]-bifenil-4-carbonitrilo;1-[4-(4-benzofuran-2-il-fenoxi)-piperidin-1-il]-propan-1-ona;1-{4-[4-(1H-indol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{4-[4-(1H-indazol-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1 -[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1 -il]-propan-1 -ona;(R)-tetrahidrofuran-2-il-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona; ciclopropil-[4-(4-tieno[2,3-b]piridin-5-il-fenoxi)-piperidin-1-il]-metanona;1- {4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;2- metil-1-{4-[4-(6-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(6-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;1- {4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;2- metil-1-{4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(5-fenil-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(5-fenilpiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(6-morfolin-4-il-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(6-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(6-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;1-{4-[4-(5-fenoxipiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclobutil-[4-(2'-fluoro-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;ciclopropil-{4-[4-(5-fenoxi-piridin-3-il)-fenoxi]-piperidin-1-il}-metanona;ciclobutil-{4-[4-(5-fenoxipiridin-3-il)-fenoxil-piperidin-1-il}-metanona;1-{4-[4-(5-fenilaminopiridin-3-il)-fenoxi]-piperidin-1-il}-propan-1-ona;1-{4-[4-(2-fenilpiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(2-fenilpiridin-4-il)-fenoxi]-piperidin-1-il}-metanona;1-{4-[4-(2-fenilaminopiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(2-fenilaminopiridin-4-il)-fenoxi]-piperidin-1-il}-metanona;1-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;ciclobutil-[4-(2'-metil-3'-piridin-2-il-bifenil-4-iloxi)-piperidin-1-il]-metanona;1-{4-[4-(2-fenoxipiridin-4-il)-fenoxi]-piperidin-1-il}-propan-1-ona;t-butil éster del ácido 4-(3',4'-dimetoxibifenil-4-iloxi)-piperidina-1-carboxílico;t-butil éster del ácido 4-(4'-ciano-bifenil-4-iloxi)-piperidina-1 -carboxílico;1-[4-(3',4'-dimetoxi-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;1-[4-(3',4'-dimetoxibifenil-4-iloxi)-piperidin-1-il]-2-metil-propan-1-ona;4'-(1-propionil-piperidin-4-iloxi)-bifenil-4-carbonitrilo;4'-(1-isobutirilpiperidin-4-iloxi)-bifenil-4-carbonitrilo;4'-(1-ciclopropanocarbonil-piperidin-4-iloxi)-bifenil-4-carbonitrilo;1-{4-[4-(5,6-dimetoxipiridin-3-il)-fenoxil-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(5,6-dimetoxipiridin-3-il)-fenoxi]-piperidin-1-il}-metanona;1-[4-(3',4'-diclorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(3',4'-diclorobifenil-4-iloxi)-piperidin-1-il]-metanona;1-{4-[4-(2,3-dihidro-1,4-benzodioxin-6-il)-fenoxi]-piperidin-1-il}-propan-1-ona;ciclopropil-{4-[4-(2,3-dihidro-1,4-benzodioxin-6-il)-fenoxi]-piperidin-1-il}-metanona;1-[4-(4'-benziloxi-2'-fluoro-bifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;[4-(4'-benziloxi-2'-fluorobifenil-4-iloxi)-piperidin-1-il]-ciclopropil-metanona;1-[4-(5'-benziloxi-3'-fluorobifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;[4-(5'-benziloxi-3'-fluorobifenil-4-iloxi)-piperidin-1-il]-ciclopropil-metanona;1-[4-(4'-fenoxibifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(4'-fenoxibifenil-4-iloxi)-piperidin-1-il]-metanona;1-[4-(3'-fenoxibifenil-4-iloxi)-piperidin-1-il]-propan-1-ona;ciclopropil-[4-(3'-fenoxibifenil-4-iloxi)-piperidin-1-il]-metanona;1-[4-(4-benzofuran-5-il-bencenosulfonil)-piperidin-1-il]-2-metil-propan-1-ona;y sales farmacéuticamente aceptables de los mismos.
- 22. Un compuesto de acuerdo con la reivindicación 13, en donde dicho compuesto es N-etil-4-[4-(8-metil-7-quinolil)fenoxi]piperidina-1-carboxamida o una sal farmacéuticamente aceptable del mismo.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562181384P | 2015-06-18 | 2015-06-18 | |
| PCT/US2016/038058 WO2016205633A1 (en) | 2015-06-18 | 2016-06-17 | 1, 4-substituted piperidine derivatives |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2821049T3 true ES2821049T3 (es) | 2021-04-23 |
Family
ID=56373111
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16736649T Active ES2821049T3 (es) | 2015-06-18 | 2016-06-17 | Derivados de piperidina 1,4 sustituidos |
Country Status (16)
| Country | Link |
|---|---|
| US (6) | US9902696B2 (es) |
| EP (1) | EP3310441B1 (es) |
| JP (2) | JP6999424B2 (es) |
| KR (1) | KR20180026459A (es) |
| CN (1) | CN107847765B (es) |
| AU (1) | AU2016280255A1 (es) |
| BR (1) | BR112017027339A2 (es) |
| CL (1) | CL2017003245A1 (es) |
| CO (1) | CO2018000344A2 (es) |
| EA (1) | EA201890086A1 (es) |
| ES (1) | ES2821049T3 (es) |
| IL (1) | IL256324B (es) |
| MX (1) | MX386166B (es) |
| PE (1) | PE20180572A1 (es) |
| PH (1) | PH12017502331A1 (es) |
| WO (1) | WO2016205633A1 (es) |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PH12015502097B1 (en) | 2013-03-13 | 2023-02-03 | Forma Therapeutics Inc | Novel compounds and compositions for inhibition of fasn |
| EA201890086A1 (ru) * | 2015-06-18 | 2018-06-29 | Сефалон, Инк. | 1,4-замещенные производные пиперидина |
| WO2016205590A1 (en) | 2015-06-18 | 2016-12-22 | Cephalon, Inc. | Substituted 4-benzyl and 4-benzoyl piperidine derivatives |
| EP3684761A1 (en) | 2017-09-18 | 2020-07-29 | Basf Se | Substituted trifluoromethyloxadiazoles for combating phytopathogenic fungi |
| TWI767148B (zh) | 2018-10-10 | 2022-06-11 | 美商弗瑪治療公司 | 抑制脂肪酸合成酶(fasn) |
| WO2020077071A1 (en) * | 2018-10-10 | 2020-04-16 | Forma Therapeutics, Inc. | Inhibiting fatty acid synthase (fasn) |
| US10793554B2 (en) | 2018-10-29 | 2020-10-06 | Forma Therapeutics, Inc. | Solid forms of 4-(2-fluoro-4-(1-methyl-1H-benzo[d]imidazol-5-yl)benzoyl)piperazin-1-yl)(1-hydroxycyclopropyl)methanone |
| EP4087836B1 (en) * | 2020-01-08 | 2025-10-08 | Cantero Therapeutics, Inc. | Processes for preparing triazole glycolate oxidase inhibitors |
| WO2021257863A1 (en) | 2020-06-19 | 2021-12-23 | Incyte Corporation | Pyrrolotriazine compounds as jak2 v617f inhibitors |
| WO2021257857A1 (en) | 2020-06-19 | 2021-12-23 | Incyte Corporation | Naphthyridinone compounds as jak2 v617f inhibitors |
| US11767323B2 (en) | 2020-07-02 | 2023-09-26 | Incyte Corporation | Tricyclic pyridone compounds as JAK2 V617F inhibitors |
| US11780840B2 (en) | 2020-07-02 | 2023-10-10 | Incyte Corporation | Tricyclic urea compounds as JAK2 V617F inhibitors |
| WO2022046989A1 (en) | 2020-08-27 | 2022-03-03 | Incyte Corporation | Tricyclic urea compounds as jak2 v617f inhibitors |
| AU2021338497A1 (en) * | 2020-09-03 | 2023-02-09 | F. Hoffmann-La Roche Ag | Heterocyclic compounds |
| WO2022140231A1 (en) | 2020-12-21 | 2022-06-30 | Incyte Corporation | Deazaguaine compounds as jak2 v617f inhibitors |
| US11958861B2 (en) | 2021-02-25 | 2024-04-16 | Incyte Corporation | Spirocyclic lactams as JAK2 V617F inhibitors |
| EP4053113A1 (de) | 2021-03-03 | 2022-09-07 | Bayer AG | Verbessertes verfahren zur herstellung von alky-4-oxo-tetrahydrofuran-2,3-dicarboxylate |
| EP4053112A1 (de) | 2021-03-03 | 2022-09-07 | Bayer AG | Verfahren zur herstellung von substituiertem 4-oxo-tetrahydrofuran |
| MX2024002173A (es) | 2021-08-18 | 2024-03-26 | Chemocentryx Inc | Compuestos de arilsulfonilo como inhibidores de ccr6. |
| MX2024002139A (es) | 2021-08-18 | 2024-03-06 | Chemocentryx Inc | Arilsulfonil(hidroxi)piperidinas como inhibidores de ccr6. |
| CA3237199A1 (en) | 2021-11-02 | 2023-05-11 | Flare Therapeutics Inc. | Pparg inverse agonists and uses thereof |
| EP4444421A2 (en) * | 2021-12-10 | 2024-10-16 | Prothena Biosciences Limited | Heterocyclic compounds as dyrk1a inhibitors |
| TW202337453A (zh) | 2022-03-17 | 2023-10-01 | 美商英塞特公司 | 作為jak2 v617f抑制劑之三環脲化合物 |
| JP2025510384A (ja) | 2022-03-28 | 2025-04-14 | バイエル アクチェンゲゼルシャフト | シス-4-アミノテトラヒドロフラン-2-カルボン酸エステルの調製方法 |
| CN120590286A (zh) * | 2025-04-16 | 2025-09-05 | 广东回旋医药科技股份有限公司 | F-18标记的5-ht转运体示踪剂及其制备方法和应用 |
Family Cites Families (78)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5486525A (en) | 1993-12-16 | 1996-01-23 | Abbott Laboratories | Platelet activating factor antagonists: imidazopyridine indoles |
| CN1344256A (zh) * | 1998-12-18 | 2002-04-10 | Axys药物公司 | (杂)芳基双环杂芳基衍生物,其制备方法和用作蛋白酶抑制剂的用途 |
| WO2002014261A2 (en) | 2000-08-10 | 2002-02-21 | Eli Lilly And Company | 4-substituted d-glutamic acid derivatives for use as antibiotic |
| WO2003053975A1 (en) | 2001-12-13 | 2003-07-03 | Daiichi Suntory Pharma Co., Ltd. | Pyrazolopyrimidinone derivatives having pde7-inhibitory activity |
| WO2004026883A1 (ja) | 2002-09-17 | 2004-04-01 | Chisso Corporation | ケイ素化合物 |
| WO2005014543A1 (ja) | 2003-08-06 | 2005-02-17 | Japan Tobacco Inc. | 縮合環化合物及びそのhcvポリメラーゼ阻害剤としての利用 |
| JP2007507547A (ja) | 2003-10-06 | 2007-03-29 | グラクソ グループ リミテッド | キナーゼ阻害剤としての1,7−二置換アザベンゾイミダゾールの調製 |
| WO2005049622A1 (ja) | 2003-11-19 | 2005-06-02 | Japan Tobacco Inc. | 5-5員縮合複素環化合物及びそのhcvポリメラーゼ阻害剤としての用途 |
| BRPI0507629A (pt) | 2004-02-13 | 2007-07-03 | Banyu Pharma Co Ltd | composto, antagonista do receptor e agonista inverso do receptor da histamina h3, agente profilático ou terapêutico para uma doença metabólica, uma doença circulatória ou uma doença do sistema nervoso, ou um seu sal farmaceuticamente aceitável |
| EP1719761A4 (en) | 2004-02-23 | 2007-10-10 | Dainippon Sumitomo Pharma Co | NEW HETEROCYCLIC CONNECTION |
| CA2572218C (en) * | 2004-06-30 | 2013-06-11 | Janssen Pharmaceutica, N.V. | Aryl-substituted benzimidazole and imidazopyridine ethers as anti-cancer agents |
| AU2006331882A1 (en) | 2005-12-21 | 2007-07-05 | Schering Corporation | Phenoxypiperidines and analogs thereof useful as histamine H3 antagonists |
| WO2007089634A2 (en) | 2006-01-30 | 2007-08-09 | Merck & Co., Inc. | Inhibitors of fatty acid synthase (fas) |
| CA2652385A1 (en) | 2006-06-08 | 2007-12-21 | Eli Lilly And Company | Novel mch receptor antagonists |
| US7625746B2 (en) | 2006-07-24 | 2009-12-01 | Nanosphere, Inc. | Method of denaturing and fragmenting DNA or RNA using ultrasound |
| DK2069312T3 (da) | 2006-07-25 | 2013-02-04 | Cephalon Inc | Pyridazinonderivater |
| TW200831092A (en) | 2006-12-21 | 2008-08-01 | Astrazeneca Ab | Therapeutic agents |
| US8895745B2 (en) | 2006-12-22 | 2014-11-25 | Astex Therapeutics Limited | Bicyclic heterocyclic compounds as FGFR inhibitors |
| AR065194A1 (es) | 2007-02-05 | 2009-05-20 | Xenon Pharmaceuticals Inc | Compuestos de piridopirimidinona de utilidad en el tratamiento de enfermedades o condiciones patologicas mediadas por los canales de sodio |
| WO2008138834A1 (en) * | 2007-05-09 | 2008-11-20 | Novartis Ag | Substituted imidazopyridazines as pi3k lipid kinase inhibitors |
| AR067326A1 (es) | 2007-05-11 | 2009-10-07 | Novartis Ag | Imidazopiridinas y pirrolo -pirimidinas sustituidas como inhibidores de cinasa de lipido |
| JP2011521978A (ja) | 2008-06-02 | 2011-07-28 | ファスジェン, インコーポレイテッド | 新規化合物、それを含む医薬組成物、およびこれらの使用方法 |
| US20110136790A1 (en) | 2008-07-23 | 2011-06-09 | De Lera Ruiz Manuel | Tricyclic Heterocyclic Derivatives and Methods of Use |
| WO2010048149A2 (en) * | 2008-10-20 | 2010-04-29 | Kalypsys, Inc. | Heterocyclic modulators of gpr119 for treatment of disease |
| WO2010106436A2 (en) | 2009-03-18 | 2010-09-23 | Resverlogix Corp. | Novel anti-inflammatory agents |
| PT2434891T (pt) | 2009-05-27 | 2020-10-23 | Ptc Therapeutics Inc | Métodos para tratamento de cancro e afeções não neoplásicas |
| US8614238B2 (en) | 2009-10-19 | 2013-12-24 | Boehringer Ingelheim International Gmbh | Cyclopentanecarboxamide derivatives, medicaments containing such compounds and their use |
| US20120208827A1 (en) | 2009-10-27 | 2012-08-16 | Glaxosmithkline Llc | Benzimidazoles as fatty acid synthase inhibitors |
| JP2013032290A (ja) | 2009-11-20 | 2013-02-14 | Dainippon Sumitomo Pharma Co Ltd | 新規縮合ピリミジン誘導体 |
| JP2013512245A (ja) | 2009-11-24 | 2013-04-11 | グラクソスミスクライン・リミテッド・ライアビリティ・カンパニー | 脂肪酸合成酵素阻害剤としてのアザベンズイミダゾール |
| KR101819199B1 (ko) | 2010-02-16 | 2018-01-16 | 아라곤 파마슈티컬스, 인코포레이티드 | 안드로겐 수용체 조절제 및 이의 용도 |
| WO2011103516A2 (en) * | 2010-02-18 | 2011-08-25 | The Trustees Of Princeton University | Inhibitors of long and very long chain fatty acid metabolism as broad spectrum anti-virals |
| MX2012009720A (es) | 2010-02-22 | 2012-10-09 | Glaxosmithkline Llc | Triazolonas como inhibidores de acido graso sintasa. |
| CA2798330A1 (en) | 2010-05-05 | 2011-11-10 | Infinity Pharmaceuticals, Inc. | Tetrazolones as inhibitors of fatty acid synthase |
| WO2011138427A2 (en) | 2010-05-07 | 2011-11-10 | Boehringer Ingelheim International Gmbh | Pyridazinones as gpr119 agonists |
| JP2013166700A (ja) | 2010-06-02 | 2013-08-29 | Dainippon Sumitomo Pharma Co Ltd | 新規4,5−縮環ピリミジン誘導体 |
| WO2012036233A1 (ja) | 2010-09-17 | 2012-03-22 | 塩野義製薬株式会社 | メラニン凝集ホルモン受容体アンタゴニスト活性を有する縮合へテロ環誘導体 |
| EP2637660A4 (en) | 2010-11-08 | 2014-04-09 | Glaxosmithkline Ip No 2 Ltd | GRAS SYNTHASE ACID INHIBITORS |
| AU2011333472A1 (en) * | 2010-11-26 | 2013-06-06 | Lupin Limited | Bicyclic GPR119 modulators |
| US20130303551A1 (en) | 2011-01-10 | 2013-11-14 | Nicholas D. Adams | Pyrimidinone derivatives as fatty acid synthase inhibitors |
| ES2883274T3 (es) | 2011-03-08 | 2021-12-07 | Sagimet Biosciences Inc | Moduladores heterocíclicos de la síntesis de lípidos |
| AR086042A1 (es) * | 2011-04-28 | 2013-11-13 | Galapagos Nv | Compuesto util para el tratamiento de enfermedades degenerativas e inflamatorias y composicion farmaceutica |
| WO2012167423A1 (en) * | 2011-06-08 | 2012-12-13 | Hutchison Medipharma Limited | Substituted pyridopyrazines as novel syk inhibitors |
| WO2012175520A1 (en) | 2011-06-20 | 2012-12-27 | Novartis Ag | Hydroxy substituted isoquinolinone derivatives |
| US9309250B2 (en) | 2011-06-22 | 2016-04-12 | Vertex Pharmaceuticals Incorporated | Substituted pyrrolo[2,3-b]pyrazines as ATR kinase inhibitors |
| JP5964426B2 (ja) | 2011-08-19 | 2016-08-03 | グラクソスミスクライン、インテレクチュアル、プロパティー、ナンバー2、リミテッドGlaxosmithkline Intellectual Property No.2 Limited | 脂肪酸シンターゼ阻害剤 |
| WO2013028445A1 (en) | 2011-08-19 | 2013-02-28 | Glaxosmithkline Llc | Fatty acid synthase inhibitors |
| WO2013052716A1 (en) | 2011-10-07 | 2013-04-11 | Glaxosmithkline Llc | Fatty acid synthase inhibitors |
| WO2013053051A1 (en) | 2011-10-12 | 2013-04-18 | University Health Network | Indazole compounds as kinase inhibitors and method of treating cancer with same |
| GB201205669D0 (en) | 2012-03-30 | 2012-05-16 | Agency Science Tech & Res | Bicyclic heterocyclic derivatives as mnk2 and mnk2 modulators and uses thereof |
| US8889730B2 (en) | 2012-04-10 | 2014-11-18 | Pfizer Inc. | Indole and indazole compounds that activate AMPK |
| US20130281399A1 (en) | 2012-04-19 | 2013-10-24 | Rvx Therapeutics Inc. | Treatment of diseases by epigenetic regulation |
| IN2012CH01573A (es) | 2012-04-20 | 2015-07-10 | Advinus Therapeutics Ltd | |
| KR101415174B1 (ko) | 2012-04-26 | 2014-07-04 | (주) 메디프론디비티 | 신규한 벤조옥사졸계 유도체 또는 이의 약학적으로 허용가능한 염, 이의 제조방법 및 이를 포함하는 rage 수용체 관련 질환의 예방 또는 치료용 약학적 조성물 |
| TWI585088B (zh) | 2012-06-04 | 2017-06-01 | 第一三共股份有限公司 | 作爲激酶抑制劑之咪唑并[1,2-b]嗒衍生物 |
| WO2014004863A2 (en) | 2012-06-27 | 2014-01-03 | Alzheimer's Institute Of America, Inc. | Compounds, compositions, and therapeutic uses thereof |
| AU2013286894B2 (en) | 2012-07-03 | 2017-12-07 | Sagimet Biosciences Inc. | Heterocyclic modulators of lipid synthesis |
| US9353107B2 (en) * | 2012-07-03 | 2016-05-31 | Aurigene Discovery Technologies Limited | 3-(pyrazolyl)-1H-pyrrolo[2,3-b]pyridine derivatives as kinase inhibitors |
| CN104718004A (zh) * | 2012-08-22 | 2015-06-17 | 默沙东公司 | 新的氮杂苯并咪唑六氢呋喃并[3,2-b]呋喃衍生物 |
| US20150099730A1 (en) | 2012-09-07 | 2015-04-09 | Janssen Pharmaceutica, Nv | Imidazolin-5-one derivative useful as fasn inhibitors for the treatment of cancer |
| AR092211A1 (es) | 2012-09-24 | 2015-04-08 | Merck Patent Ges Mit Beschränkter Haftung | Derivados de hidropirrolopirrol |
| WO2014053568A1 (en) * | 2012-10-02 | 2014-04-10 | Sanofi | Indolyldihydroimidazopyrimidinone derivatives, preparation thereof and therapeutic use thereof |
| SG11201503628YA (en) | 2012-11-16 | 2015-06-29 | Merck Patent Gmbh | 3-aminocyclopentane carboxamide derivatives |
| PH12015502097B1 (en) | 2013-03-13 | 2023-02-03 | Forma Therapeutics Inc | Novel compounds and compositions for inhibition of fasn |
| JP6542192B2 (ja) * | 2013-03-14 | 2019-07-10 | ザ ブリガム アンド ウィメンズ ホスピタル インコーポレイテッドThe Brigham and Women’s Hospital, Inc. | Bmp阻害剤およびその使用方法 |
| UY35400A (es) | 2013-03-15 | 2014-10-31 | Novartis Ag | Compuestos y composiciones para el tratamiento de enfermedades parasitarias |
| CA2907657A1 (en) | 2013-03-21 | 2014-09-25 | Merck Patent Gmbh | Piperazine derivatives as fasn inhibitors |
| KR101524208B1 (ko) | 2013-04-26 | 2015-05-29 | 한국화학연구원 | 벤조옥사졸 유도체, 이의 제조방법 및 이를 포함하는 의약 조성물 |
| US9172428B2 (en) | 2013-06-28 | 2015-10-27 | Intel Corporation | Determining the spectral energy content of a data bus |
| ES2633969T3 (es) | 2013-07-29 | 2017-09-26 | Merck Patent Gmbh | Derivados de ciclopentano 1,3-disustituidos |
| DE102013215035B3 (de) | 2013-07-31 | 2014-11-06 | Siemens Aktiengesellschaft | Soft-Redundanzprotokoll |
| JP6611358B2 (ja) * | 2013-12-03 | 2019-11-27 | ヤンセン ファーマシューティカ エヌ.ベー. | 癌治療のためのfasn阻害剤として有用なベンズアミド誘導体 |
| US10513521B2 (en) | 2014-07-15 | 2019-12-24 | The Brigham And Women's Hospital, Inc. | Compositions and methods for inhibiting BMP |
| WO2016041201A1 (zh) | 2014-09-19 | 2016-03-24 | 上海创诺医药集团有限公司 | 噻吩并嘧啶类衍生物、其制备方法及其在医药上的应用 |
| TW201629033A (zh) | 2014-10-08 | 2016-08-16 | 健生藥品公司 | 作為治療第二型糖尿病之gpr40促效劑的經取代苯并噻吩基衍生物 |
| WO2016205590A1 (en) | 2015-06-18 | 2016-12-22 | Cephalon, Inc. | Substituted 4-benzyl and 4-benzoyl piperidine derivatives |
| EA201890086A1 (ru) * | 2015-06-18 | 2018-06-29 | Сефалон, Инк. | 1,4-замещенные производные пиперидина |
| JP6986872B2 (ja) | 2017-06-23 | 2021-12-22 | 昭和電工株式会社 | ウェハ支持台、化学気相成長装置、及び、SiCエピタキシャルウェハの製造方法 |
-
2016
- 2016-06-17 EA EA201890086A patent/EA201890086A1/ru unknown
- 2016-06-17 US US15/185,710 patent/US9902696B2/en active Active
- 2016-06-17 KR KR1020187001524A patent/KR20180026459A/ko not_active Withdrawn
- 2016-06-17 JP JP2017565816A patent/JP6999424B2/ja active Active
- 2016-06-17 ES ES16736649T patent/ES2821049T3/es active Active
- 2016-06-17 WO PCT/US2016/038058 patent/WO2016205633A1/en not_active Ceased
- 2016-06-17 PE PE2017002764A patent/PE20180572A1/es not_active Application Discontinuation
- 2016-06-17 EP EP16736649.1A patent/EP3310441B1/en active Active
- 2016-06-17 AU AU2016280255A patent/AU2016280255A1/en not_active Abandoned
- 2016-06-17 CN CN201680042132.8A patent/CN107847765B/zh active Active
- 2016-06-17 MX MX2017016669A patent/MX386166B/es unknown
- 2016-06-17 BR BR112017027339-0A patent/BR112017027339A2/pt not_active Application Discontinuation
-
2017
- 2017-12-14 IL IL256324A patent/IL256324B/en active IP Right Grant
- 2017-12-15 PH PH12017502331A patent/PH12017502331A1/en unknown
- 2017-12-18 CL CL2017003245A patent/CL2017003245A1/es unknown
-
2018
- 2018-01-15 CO CONC2018/0000344A patent/CO2018000344A2/es unknown
- 2018-02-23 US US15/903,150 patent/US10221135B2/en active Active
-
2019
- 2019-01-25 US US16/257,591 patent/US10851057B2/en active Active - Reinstated
-
2020
- 2020-11-05 US US17/090,375 patent/US11702388B2/en active Active
-
2021
- 2021-12-22 JP JP2021208163A patent/JP7307144B2/ja active Active
-
2023
- 2023-06-02 US US18/327,986 patent/US12098130B2/en active Active
-
2024
- 2024-09-23 US US18/893,279 patent/US20250257035A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US12098130B2 (en) | 1,4-substituted piperidine derivatives | |
| ES2773303T3 (es) | Compuestos de quinolina sustituidos selectivamente | |
| ES2824495T3 (es) | Moduladores alostéricos positivos del receptor muscarínico M1 | |
| ES2849951T3 (es) | Derivados de piperidina 4-bencil y 4-benzoil sustituidos | |
| US10239873B2 (en) | 7-azaindole or 4,7-diazaindole derivatives as IKKϵ epsilon and TBK1 inhibitor and pharmaceutical composition comprising same | |
| ES2997111T3 (en) | Pyridazinyl amino derivatives as alk5 inhibitors | |
| TW202237597A (zh) | 新型egfr降解劑 | |
| JP7162591B2 (ja) | スピロピペリジン誘導体 | |
| ES2861382T3 (es) | Derivados de pirazolopirimidina como inhibidores de cinasas CaM | |
| CA3014554C (en) | 1,4-substituted piperidine derivative for treating a disorder mediated by fatty acid synthase | |
| TW202604506A (zh) | 四氫吡唑并吡啶衍生物 | |
| HK1253048B (zh) | 1,4-取代的哌啶衍生物 | |
| HK1252793B (en) | 1, 4-substituted piperidine derivatives | |
| KR20250076403A (ko) | 이미다졸로-피리딘 유도체 및 이의 용도 | |
| OA21105A (en) | New macrocyclic LRRK2 kinase inhibitors. | |
| HK1252794B (en) | Substituted 4-benzyl and 4-benzoyl piperidine derivatives |