ES2833459T3 - Compuestos que inhiben la ARN polimerasa, composiciones que incluyen dichos compuestos y su uso - Google Patents
Compuestos que inhiben la ARN polimerasa, composiciones que incluyen dichos compuestos y su uso Download PDFInfo
- Publication number
- ES2833459T3 ES2833459T3 ES15765295T ES15765295T ES2833459T3 ES 2833459 T3 ES2833459 T3 ES 2833459T3 ES 15765295 T ES15765295 T ES 15765295T ES 15765295 T ES15765295 T ES 15765295T ES 2833459 T3 ES2833459 T3 ES 2833459T3
- Authority
- ES
- Spain
- Prior art keywords
- compound
- mmol
- compounds
- pyrido
- benzo
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 155
- 239000000203 mixture Substances 0.000 title description 29
- 102000004163 DNA-directed RNA polymerases Human genes 0.000 title description 2
- 108090000626 DNA-directed RNA polymerases Proteins 0.000 title description 2
- 210000004027 cell Anatomy 0.000 claims description 35
- 239000008194 pharmaceutical composition Substances 0.000 claims description 29
- 206010028980 Neoplasm Diseases 0.000 claims description 28
- 201000011510 cancer Diseases 0.000 claims description 21
- 239000003937 drug carrier Substances 0.000 claims description 17
- 239000013543 active substance Substances 0.000 claims description 16
- 230000000694 effects Effects 0.000 claims description 14
- 239000003814 drug Substances 0.000 claims description 11
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 10
- 101000909256 Caldicellulosiruptor bescii (strain ATCC BAA-1888 / DSM 6725 / Z-1320) DNA polymerase I Proteins 0.000 claims description 9
- 101000902592 Pyrococcus furiosus (strain ATCC 43587 / DSM 3638 / JCM 8422 / Vc1) DNA polymerase Proteins 0.000 claims description 9
- 201000010099 disease Diseases 0.000 claims description 9
- 210000004962 mammalian cell Anatomy 0.000 claims description 7
- 238000011282 treatment Methods 0.000 claims description 6
- 230000003463 hyperproliferative effect Effects 0.000 claims description 4
- 238000000034 method Methods 0.000 description 46
- 239000007787 solid Substances 0.000 description 44
- -1 small molecule compounds Chemical class 0.000 description 37
- 150000003839 salts Chemical class 0.000 description 24
- 238000005481 NMR spectroscopy Methods 0.000 description 22
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- 125000000217 alkyl group Chemical group 0.000 description 18
- 238000005160 1H NMR spectroscopy Methods 0.000 description 17
- 102100031593 DNA-directed RNA polymerase I subunit RPA1 Human genes 0.000 description 15
- 101710081420 DNA-directed RNA polymerase I subunit RPA1 Proteins 0.000 description 15
- 108020004414 DNA Proteins 0.000 description 12
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 12
- 239000002246 antineoplastic agent Substances 0.000 description 12
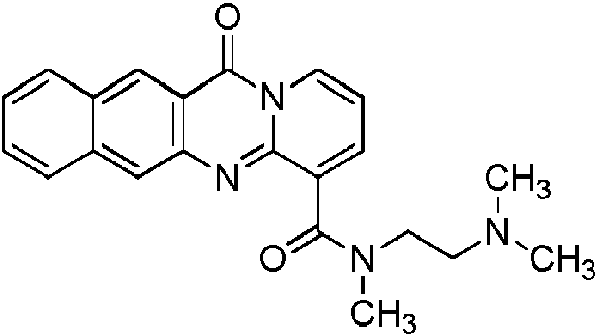
- BXYDVWIAGDJBEC-UHFFFAOYSA-N n-[2-(dimethylamino)ethyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCCN(C)C)=O)C3=CC2=C1 BXYDVWIAGDJBEC-UHFFFAOYSA-N 0.000 description 12
- 238000009472 formulation Methods 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 10
- 229940034982 antineoplastic agent Drugs 0.000 description 10
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 9
- 125000003118 aryl group Chemical group 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 8
- 239000000969 carrier Substances 0.000 description 8
- 229960001866 silicon dioxide Drugs 0.000 description 8
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 7
- 241000124008 Mammalia Species 0.000 description 7
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 7
- 125000003282 alkyl amino group Chemical group 0.000 description 7
- 230000000118 anti-neoplastic effect Effects 0.000 description 7
- 238000004587 chromatography analysis Methods 0.000 description 7
- 229910052757 nitrogen Inorganic materials 0.000 description 7
- 239000000741 silica gel Substances 0.000 description 7
- 229910002027 silica gel Inorganic materials 0.000 description 7
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- 102100025064 Cellular tumor antigen p53 Human genes 0.000 description 6
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 6
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 6
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 6
- 239000002202 Polyethylene glycol Substances 0.000 description 6
- 108020001027 Ribosomal DNA Proteins 0.000 description 6
- 239000002253 acid Substances 0.000 description 6
- 125000004423 acyloxy group Chemical group 0.000 description 6
- 125000003545 alkoxy group Chemical group 0.000 description 6
- 125000000304 alkynyl group Chemical group 0.000 description 6
- 125000004104 aryloxy group Chemical group 0.000 description 6
- 229910052799 carbon Inorganic materials 0.000 description 6
- 239000012043 crude product Substances 0.000 description 6
- 125000004093 cyano group Chemical group *C#N 0.000 description 6
- 125000000753 cycloalkyl group Chemical group 0.000 description 6
- 239000003599 detergent Substances 0.000 description 6
- 125000004663 dialkyl amino group Chemical group 0.000 description 6
- 125000000623 heterocyclic group Chemical group 0.000 description 6
- 230000037361 pathway Effects 0.000 description 6
- 229920001223 polyethylene glycol Polymers 0.000 description 6
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 6
- 239000012453 solvate Substances 0.000 description 6
- 239000002904 solvent Substances 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- 125000003441 thioacyl group Chemical group 0.000 description 6
- 238000013518 transcription Methods 0.000 description 6
- 230000035897 transcription Effects 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 125000006528 (C2-C6) alkyl group Chemical group 0.000 description 5
- IBRSSZOHCGUTHI-UHFFFAOYSA-N 2-chloropyridine-3-carboxylic acid Chemical compound OC(=O)C1=CC=CN=C1Cl IBRSSZOHCGUTHI-UHFFFAOYSA-N 0.000 description 5
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 5
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 5
- 101000721661 Homo sapiens Cellular tumor antigen p53 Proteins 0.000 description 5
- 125000003342 alkenyl group Chemical group 0.000 description 5
- 230000000340 anti-metabolite Effects 0.000 description 5
- 229940100197 antimetabolite Drugs 0.000 description 5
- 239000002256 antimetabolite Substances 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- 238000013270 controlled release Methods 0.000 description 5
- 239000008121 dextrose Substances 0.000 description 5
- 235000014113 dietary fatty acids Nutrition 0.000 description 5
- 239000003085 diluting agent Substances 0.000 description 5
- 239000000194 fatty acid Substances 0.000 description 5
- 229930195729 fatty acid Natural products 0.000 description 5
- 239000003112 inhibitor Substances 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 235000019198 oils Nutrition 0.000 description 5
- 229940002612 prodrug Drugs 0.000 description 5
- 239000000651 prodrug Substances 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- 125000001424 substituent group Chemical group 0.000 description 5
- 229910052717 sulfur Inorganic materials 0.000 description 5
- 238000003786 synthesis reaction Methods 0.000 description 5
- OSKFWHVKBOWROV-UHFFFAOYSA-N 12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxylic acid Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)O)=O)C3=CC2=C1 OSKFWHVKBOWROV-UHFFFAOYSA-N 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 4
- SGWXJCJVFFTSJY-LBPRGKRZSA-N N[C@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C Chemical compound N[C@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C SGWXJCJVFFTSJY-LBPRGKRZSA-N 0.000 description 4
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 4
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 4
- 125000004414 alkyl thio group Chemical group 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 4
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 4
- 238000010191 image analysis Methods 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000009830 intercalation Methods 0.000 description 4
- 230000002687 intercalation Effects 0.000 description 4
- 238000001990 intravenous administration Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 4
- 239000004094 surface-active agent Substances 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 125000004001 thioalkyl group Chemical group 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 3
- ILCIRAGSNQDBPD-UHFFFAOYSA-N 11-oxopyrido[2,1-b]quinazoline-6-carboxylic acid Chemical compound C1=CC=C2C(=O)N3C=CC=C(C(=O)O)C3=NC2=C1 ILCIRAGSNQDBPD-UHFFFAOYSA-N 0.000 description 3
- XFXOLBNQYFRSLQ-UHFFFAOYSA-N 3-amino-2-naphthoic acid Chemical compound C1=CC=C2C=C(C(O)=O)C(N)=CC2=C1 XFXOLBNQYFRSLQ-UHFFFAOYSA-N 0.000 description 3
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 3
- 229920002261 Corn starch Polymers 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 239000001856 Ethyl cellulose Substances 0.000 description 3
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 3
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 229920002907 Guar gum Polymers 0.000 description 3
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 3
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 3
- SGWXJCJVFFTSJY-GFCCVEGCSA-N N[C@@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C Chemical compound N[C@@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C SGWXJCJVFFTSJY-GFCCVEGCSA-N 0.000 description 3
- ZIIGGQCDJSQPDH-UHFFFAOYSA-N O=C1N2C(=NC=3C=C4C(=CC1=3)C=CC=C4)C(=CC=C2)C(=O)NCCC1=CC=NC=C1 Chemical compound O=C1N2C(=NC=3C=C4C(=CC1=3)C=CC=C4)C(=CC=C2)C(=O)NCCC1=CC=NC=C1 ZIIGGQCDJSQPDH-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 102000017143 RNA Polymerase I Human genes 0.000 description 3
- 108010013845 RNA Polymerase I Proteins 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 229920002125 Sokalan® Polymers 0.000 description 3
- 235000021355 Stearic acid Nutrition 0.000 description 3
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 125000002252 acyl group Chemical group 0.000 description 3
- 125000005035 acylthio group Chemical group 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 150000001299 aldehydes Chemical class 0.000 description 3
- 229910052783 alkali metal Inorganic materials 0.000 description 3
- 239000002168 alkylating agent Substances 0.000 description 3
- 229940100198 alkylating agent Drugs 0.000 description 3
- 125000003368 amide group Chemical group 0.000 description 3
- 150000001408 amides Chemical class 0.000 description 3
- 239000003242 anti bacterial agent Substances 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 125000001691 aryl alkyl amino group Chemical group 0.000 description 3
- HONIICLYMWZJFZ-UHFFFAOYSA-N azetidine Chemical compound C1CNC1 HONIICLYMWZJFZ-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 3
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 3
- 125000001951 carbamoylamino group Chemical group C(N)(=O)N* 0.000 description 3
- 229960001631 carbomer Drugs 0.000 description 3
- 125000004181 carboxyalkyl group Chemical group 0.000 description 3
- 230000015556 catabolic process Effects 0.000 description 3
- 239000008120 corn starch Substances 0.000 description 3
- 229940099112 cornstarch Drugs 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 3
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 3
- 238000006731 degradation reaction Methods 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 235000019325 ethyl cellulose Nutrition 0.000 description 3
- 229920001249 ethyl cellulose Polymers 0.000 description 3
- 150000004665 fatty acids Chemical class 0.000 description 3
- 125000002795 guanidino group Chemical group C(N)(=N)N* 0.000 description 3
- 239000000665 guar gum Substances 0.000 description 3
- 235000010417 guar gum Nutrition 0.000 description 3
- 229960002154 guar gum Drugs 0.000 description 3
- 125000001475 halogen functional group Chemical group 0.000 description 3
- 125000001072 heteroaryl group Chemical group 0.000 description 3
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 3
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 3
- 125000002883 imidazolyl group Chemical group 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 3
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 3
- 125000001041 indolyl group Chemical group 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 3
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 3
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 3
- 125000001715 oxadiazolyl group Chemical group 0.000 description 3
- 125000002971 oxazolyl group Chemical group 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 125000005499 phosphonyl group Chemical group 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 235000013772 propylene glycol Nutrition 0.000 description 3
- 125000004076 pyridyl group Chemical group 0.000 description 3
- 229940083542 sodium Drugs 0.000 description 3
- 229910052708 sodium Inorganic materials 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 125000005420 sulfonamido group Chemical group S(=O)(=O)(N*)* 0.000 description 3
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- 125000000335 thiazolyl group Chemical group 0.000 description 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 3
- 125000004954 trialkylamino group Chemical group 0.000 description 3
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 description 2
- AEIAMRMQKCPGJR-HWYNEVGZSA-N (2r)-propane-1,2-diamine;dihydrochloride Chemical compound Cl.Cl.C[C@@H](N)CN AEIAMRMQKCPGJR-HWYNEVGZSA-N 0.000 description 2
- JNYAEWCLZODPBN-JGWLITMVSA-N (2r,3r,4s)-2-[(1r)-1,2-dihydroxyethyl]oxolane-3,4-diol Chemical class OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O JNYAEWCLZODPBN-JGWLITMVSA-N 0.000 description 2
- WZZBNLYBHUDSHF-DHLKQENFSA-N 1-[(3s,4s)-4-[8-(2-chloro-4-pyrimidin-2-yloxyphenyl)-7-fluoro-2-methylimidazo[4,5-c]quinolin-1-yl]-3-fluoropiperidin-1-yl]-2-hydroxyethanone Chemical compound CC1=NC2=CN=C3C=C(F)C(C=4C(=CC(OC=5N=CC=CN=5)=CC=4)Cl)=CC3=C2N1[C@H]1CCN(C(=O)CO)C[C@@H]1F WZZBNLYBHUDSHF-DHLKQENFSA-N 0.000 description 2
- TXTDKLMFBBYADC-UHFFFAOYSA-N 12-oxo-n-(2-piperidin-1-ylethyl)-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NCCN1CCCCC1 TXTDKLMFBBYADC-UHFFFAOYSA-N 0.000 description 2
- ULZAEDZUQQVQJD-UHFFFAOYSA-N 12-oxo-n-(2-pyridin-2-ylethyl)-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NCCC1=CC=CC=N1 ULZAEDZUQQVQJD-UHFFFAOYSA-N 0.000 description 2
- JWSYTXYIBVSVJR-UHFFFAOYSA-N 12-oxo-n-(2-pyridin-3-ylethyl)-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NCCC1=CC=CN=C1 JWSYTXYIBVSVJR-UHFFFAOYSA-N 0.000 description 2
- QTAFSEJFKCZGEE-UHFFFAOYSA-N 12-oxo-n-(2-pyrrolidin-1-ylethyl)-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NCCN1CCCC1 QTAFSEJFKCZGEE-UHFFFAOYSA-N 0.000 description 2
- HLWKVUFQFSYKFH-UHFFFAOYSA-N 12-oxo-n-[2-(2-oxoimidazolidin-1-yl)ethyl]-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NCCN1CCNC1=O HLWKVUFQFSYKFH-UHFFFAOYSA-N 0.000 description 2
- XDOFQFKRPWOURC-UHFFFAOYSA-N 16-methylheptadecanoic acid Chemical compound CC(C)CCCCCCCCCCCCCCC(O)=O XDOFQFKRPWOURC-UHFFFAOYSA-N 0.000 description 2
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 2
- JFGHZYXCOQFYFA-UHFFFAOYSA-N 4-(4-propan-2-ylpiperazine-1-carbonyl)-12h-benzo[g]pyrido[2,1-b]quinazoline-12-one Chemical compound C1CN(C(C)C)CCN1C(=O)C1=CC=CN2C(=O)C3=CC4=CC=CC=C4C=C3N=C12 JFGHZYXCOQFYFA-UHFFFAOYSA-N 0.000 description 2
- OAJTVMLBAZMIAU-UHFFFAOYSA-N 4-[3-(diethylamino)pyrrolidine-1-carbonyl]-12h-benzo[g]pyrido[2,1-b]quinazoline-12-one Chemical compound C1C(N(CC)CC)CCN1C(=O)C1=CC=CN2C(=O)C3=CC4=CC=CC=C4C=C3N=C12 OAJTVMLBAZMIAU-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- OJRUSAPKCPIVBY-KQYNXXCUSA-N C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N Chemical compound C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N OJRUSAPKCPIVBY-KQYNXXCUSA-N 0.000 description 2
- 0 CCCCCN(C)CCCCC*(C)C Chemical compound CCCCCN(C)CCCCC*(C)C 0.000 description 2
- OIAUQUHKSXDAER-UHFFFAOYSA-N CN(C(CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)(C)C)C Chemical compound CN(C(CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)(C)C)C OIAUQUHKSXDAER-UHFFFAOYSA-N 0.000 description 2
- DIHLEIRADLVBRW-AWEZNQCLSA-N CN([C@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C)C Chemical compound CN([C@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C)C DIHLEIRADLVBRW-AWEZNQCLSA-N 0.000 description 2
- YKECAZAIXGFHQE-UHFFFAOYSA-N CN1CC(C1)NC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3 Chemical compound CN1CC(C1)NC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3 YKECAZAIXGFHQE-UHFFFAOYSA-N 0.000 description 2
- XGPBJCHFROADCK-UHFFFAOYSA-N CX-5461 Chemical compound C1CN(C)CCCN1C1=CC=C2C(=O)C(C(=O)NCC=3N=CC(C)=NC=3)=C3SC4=CC=CC=C4N3C2=N1 XGPBJCHFROADCK-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- DLGOEMSEDOSKAD-UHFFFAOYSA-N Carmustine Chemical compound ClCCNC(=O)N(N=O)CCCl DLGOEMSEDOSKAD-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 229940126639 Compound 33 Drugs 0.000 description 2
- 229920000858 Cyclodextrin Polymers 0.000 description 2
- 230000005778 DNA damage Effects 0.000 description 2
- 231100000277 DNA damage Toxicity 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 2
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 2
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 208000008839 Kidney Neoplasms Diseases 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 2
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 2
- YOBNXMPTJQNFNU-UHFFFAOYSA-N NC(CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)(C)C Chemical compound NC(CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)(C)C YOBNXMPTJQNFNU-UHFFFAOYSA-N 0.000 description 2
- SGWXJCJVFFTSJY-UHFFFAOYSA-N NC(CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C Chemical compound NC(CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C SGWXJCJVFFTSJY-UHFFFAOYSA-N 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 2
- 206010038389 Renal cancer Diseases 0.000 description 2
- 208000006265 Renal cell carcinoma Diseases 0.000 description 2
- PNUZDKCDAWUEGK-CYZMBNFOSA-N Sitafloxacin Chemical compound C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 PNUZDKCDAWUEGK-CYZMBNFOSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 2
- 229940122803 Vinca alkaloid Drugs 0.000 description 2
- 229960000583 acetic acid Drugs 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 239000002295 alkylating antineoplastic agent Substances 0.000 description 2
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 2
- 150000001412 amines Chemical group 0.000 description 2
- 229940045799 anthracyclines and related substance Drugs 0.000 description 2
- RWZYAGGXGHYGMB-UHFFFAOYSA-N anthranilic acid Chemical compound NC1=CC=CC=C1C(O)=O RWZYAGGXGHYGMB-UHFFFAOYSA-N 0.000 description 2
- 230000001093 anti-cancer Effects 0.000 description 2
- 229940088710 antibiotic agent Drugs 0.000 description 2
- 239000003101 antineoplastic hormone agonist and antagonist Substances 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 235000006708 antioxidants Nutrition 0.000 description 2
- 125000003710 aryl alkyl group Chemical group 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 229940125904 compound 1 Drugs 0.000 description 2
- 229940125758 compound 15 Drugs 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 229940097362 cyclodextrins Drugs 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 125000004985 dialkyl amino alkyl group Chemical group 0.000 description 2
- FLKPEMZONWLCSK-UHFFFAOYSA-N diethyl phthalate Chemical compound CCOC(=O)C1=CC=CC=C1C(=O)OCC FLKPEMZONWLCSK-UHFFFAOYSA-N 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 238000001317 epifluorescence microscopy Methods 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 2
- 229940093471 ethyl oleate Drugs 0.000 description 2
- 229960002949 fluorouracil Drugs 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229940014259 gelatin Drugs 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 2
- 150000004820 halides Chemical class 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 125000001183 hydrocarbyl group Chemical group 0.000 description 2
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 2
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 2
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 2
- 229940071676 hydroxypropylcellulose Drugs 0.000 description 2
- 239000007972 injectable composition Substances 0.000 description 2
- 238000001361 intraarterial administration Methods 0.000 description 2
- 201000010982 kidney cancer Diseases 0.000 description 2
- 239000012669 liquid formulation Substances 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 239000011976 maleic acid Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 239000002207 metabolite Substances 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- NUKUDYATSNPVIG-UHFFFAOYSA-N n-(1-methylpiperidin-4-yl)-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1CN(C)CCC1NC(=O)C1=CC=CN2C(=O)C3=CC4=CC=CC=C4C=C3N=C12 NUKUDYATSNPVIG-UHFFFAOYSA-N 0.000 description 2
- ZTTNRKBKTLNNOF-UHFFFAOYSA-N n-(2-imidazol-1-ylethyl)-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NCCN1C=CN=C1 ZTTNRKBKTLNNOF-UHFFFAOYSA-N 0.000 description 2
- HVPNYGPYDGPRDO-UHFFFAOYSA-N n-(2-methylsulfonylethyl)-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCCS(=O)(=O)C)=O)C3=CC2=C1 HVPNYGPYDGPRDO-UHFFFAOYSA-N 0.000 description 2
- KXSCXXIFXNDHCZ-UHFFFAOYSA-N n-(2-morpholin-4-ylethyl)-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NCCN1CCOCC1 KXSCXXIFXNDHCZ-UHFFFAOYSA-N 0.000 description 2
- FCWDGRZECVKNPO-UHFFFAOYSA-N n-[2-(1-methylpyrrolidin-2-yl)ethyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound CN1CCCC1CCNC(=O)C1=CC=CN2C(=O)C3=CC4=CC=CC=C4C=C3N=C12 FCWDGRZECVKNPO-UHFFFAOYSA-N 0.000 description 2
- MEAJDCQREQYNNH-UHFFFAOYSA-N n-[2-(1h-indol-3-yl)ethyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(NCCC=4C5=CC=CC=C5NC=4)=O)=O)C3=CC2=C1 MEAJDCQREQYNNH-UHFFFAOYSA-N 0.000 description 2
- QUYXHGPHIJMFOU-UHFFFAOYSA-N n-[2-(4-methylpiperazin-1-yl)ethyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1CN(C)CCN1CCNC(=O)C1=CC=CN2C(=O)C3=CC4=CC=CC=C4C=C3N=C12 QUYXHGPHIJMFOU-UHFFFAOYSA-N 0.000 description 2
- HQLRYFKVXYDKRV-UHFFFAOYSA-N n-[2-(diethylamino)ethyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCCN(CC)CC)=O)C3=CC2=C1 HQLRYFKVXYDKRV-UHFFFAOYSA-N 0.000 description 2
- XCQOLHONWRNHIG-UHFFFAOYSA-N n-[2-(dimethylamino)ethyl]-n-ethyl-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)N(CCN(C)C)CC)=O)C3=CC2=C1 XCQOLHONWRNHIG-UHFFFAOYSA-N 0.000 description 2
- HHHOSJFOQVRKIN-UHFFFAOYSA-N n-[2-(dimethylamino)ethyl]-n-methyl-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)N(C)CCN(C)C)=O)C3=CC2=C1 HHHOSJFOQVRKIN-UHFFFAOYSA-N 0.000 description 2
- DIHLEIRADLVBRW-UHFFFAOYSA-N n-[2-(dimethylamino)propyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCC(C)N(C)C)=O)C3=CC2=C1 DIHLEIRADLVBRW-UHFFFAOYSA-N 0.000 description 2
- UTMWPORTWADFBY-UHFFFAOYSA-N n-[2-[di(propan-2-yl)amino]ethyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCCN(C(C)C)C(C)C)=O)C3=CC2=C1 UTMWPORTWADFBY-UHFFFAOYSA-N 0.000 description 2
- XVGSCMMLGFRPFR-UHFFFAOYSA-N n-[3-(dimethylamino)propyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCCCN(C)C)=O)C3=CC2=C1 XVGSCMMLGFRPFR-UHFFFAOYSA-N 0.000 description 2
- PTDYOSCIUCOUFB-UHFFFAOYSA-N n-[4-(dimethylamino)butyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCCCCN(C)C)=O)C3=CC2=C1 PTDYOSCIUCOUFB-UHFFFAOYSA-N 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 150000007523 nucleic acids Chemical class 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 2
- 239000004006 olive oil Substances 0.000 description 2
- 235000008390 olive oil Nutrition 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 239000011148 porous material Substances 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 150000003230 pyrimidines Chemical class 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 125000004434 sulfur atom Chemical group 0.000 description 2
- LMBFAGIMSUYTBN-MPZNNTNKSA-N teixobactin Chemical compound C([C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H](CCC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H]1C(N[C@@H](C)C(=O)N[C@@H](C[C@@H]2NC(=N)NC2)C(=O)N[C@H](C(=O)O[C@H]1C)[C@@H](C)CC)=O)NC)C1=CC=CC=C1 LMBFAGIMSUYTBN-MPZNNTNKSA-N 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- PYOKUURKVVELLB-UHFFFAOYSA-N trimethyl orthoformate Chemical compound COC(OC)OC PYOKUURKVVELLB-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- APJYDQYYACXCRM-UHFFFAOYSA-N tryptamine Chemical compound C1=CC=C2C(CCN)=CNC2=C1 APJYDQYYACXCRM-UHFFFAOYSA-N 0.000 description 2
- 238000000825 ultraviolet detection Methods 0.000 description 2
- UAOUIVVJBYDFKD-XKCDOFEDSA-N (1R,9R,10S,11R,12R,15S,18S,21R)-10,11,21-trihydroxy-8,8-dimethyl-14-methylidene-4-(prop-2-enylamino)-20-oxa-5-thia-3-azahexacyclo[9.7.2.112,15.01,9.02,6.012,18]henicosa-2(6),3-dien-13-one Chemical compound C([C@@H]1[C@@H](O)[C@@]23C(C1=C)=O)C[C@H]2[C@]12C(N=C(NCC=C)S4)=C4CC(C)(C)[C@H]1[C@H](O)[C@]3(O)OC2 UAOUIVVJBYDFKD-XKCDOFEDSA-N 0.000 description 1
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 1
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 1
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 1
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 1
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 1
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 1
- AVAWMINJNRAQFS-LURJTMIESA-N (3s)-n,n-dimethylpyrrolidin-3-amine Chemical compound CN(C)[C@H]1CCNC1 AVAWMINJNRAQFS-LURJTMIESA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 1
- OPCJOXGBLDJWRM-UHFFFAOYSA-N 1,2-diamino-2-methylpropane Chemical compound CC(C)(N)CN OPCJOXGBLDJWRM-UHFFFAOYSA-N 0.000 description 1
- PODSUMUEKRUDEI-UHFFFAOYSA-N 1-(2-aminoethyl)imidazolidin-2-one Chemical compound NCCN1CCNC1=O PODSUMUEKRUDEI-UHFFFAOYSA-N 0.000 description 1
- KQZLRWGGWXJPOS-NLFPWZOASA-N 1-[(1R)-1-(2,4-dichlorophenyl)ethyl]-6-[(4S,5R)-4-[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylcyclohexen-1-yl]pyrazolo[3,4-b]pyrazine-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)Cl)[C@@H](C)N1N=C(C=2C1=NC(=CN=2)C1=CC[C@@H]([C@@H](C1)C)N1[C@@H](CCC1)CO)C#N KQZLRWGGWXJPOS-NLFPWZOASA-N 0.000 description 1
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 1
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 1
- 125000006021 1-methyl-2-propenyl group Chemical group 0.000 description 1
- VVNBEYKDTSEYRZ-UHFFFAOYSA-N 1-methylazetidin-3-amine;dihydrochloride Chemical compound Cl.Cl.CN1CC(N)C1 VVNBEYKDTSEYRZ-UHFFFAOYSA-N 0.000 description 1
- ALOCUZOKRULSAA-UHFFFAOYSA-N 1-methylpiperidin-4-amine Chemical compound CN1CCC(N)CC1 ALOCUZOKRULSAA-UHFFFAOYSA-N 0.000 description 1
- RRQHLOZQFPWDCA-UHFFFAOYSA-N 1-n,1-n-dimethylpropane-1,2-diamine Chemical compound CC(N)CN(C)C RRQHLOZQFPWDCA-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- WHKWMTXTYKVFLK-UHFFFAOYSA-N 1-propan-2-ylpiperazine Chemical compound CC(C)N1CCNCC1 WHKWMTXTYKVFLK-UHFFFAOYSA-N 0.000 description 1
- 125000000579 2,2-diphenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])(C1=C([H])C([H])=C([H])C([H])=C1[H])C([H])([H])* 0.000 description 1
- PNHGJPJOMCXSKN-UHFFFAOYSA-N 2-(1-methylpyrrolidin-2-yl)ethanamine Chemical compound CN1CCCC1CCN PNHGJPJOMCXSKN-UHFFFAOYSA-N 0.000 description 1
- GOWUDHPKGOIDIX-UHFFFAOYSA-N 2-(4-methyl-1-piperazinyl)ethanamine Chemical compound CN1CCN(CCN)CC1 GOWUDHPKGOIDIX-UHFFFAOYSA-N 0.000 description 1
- UJFSPWWMVCSPFD-UHFFFAOYSA-N 2-(dimethylamino)ethyl 12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxylate Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)OCCN(C)C)=O)C3=CC2=C1 UJFSPWWMVCSPFD-UHFFFAOYSA-N 0.000 description 1
- MIJDSYMOBYNHOT-UHFFFAOYSA-N 2-(ethylamino)ethanol Chemical compound CCNCCO MIJDSYMOBYNHOT-UHFFFAOYSA-N 0.000 description 1
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 1
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 1
- NPRYCHLHHVWLQZ-TURQNECASA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynylpurin-8-one Chemical compound NC1=NC=C2N(C(N(C2=N1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C NPRYCHLHHVWLQZ-TURQNECASA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- YCIRHAGYEUJTFH-UHFFFAOYSA-N 2-imidazol-1-ylethanamine Chemical compound NCCN1C=CN=C1 YCIRHAGYEUJTFH-UHFFFAOYSA-N 0.000 description 1
- 125000004200 2-methoxyethyl group Chemical group [H]C([H])([H])OC([H])([H])C([H])([H])* 0.000 description 1
- 125000006020 2-methyl-1-propenyl group Chemical group 0.000 description 1
- 125000006022 2-methyl-2-propenyl group Chemical group 0.000 description 1
- SDNXQWUJWNTDCC-UHFFFAOYSA-N 2-methylsulfonylethanamine Chemical compound CS(=O)(=O)CCN SDNXQWUJWNTDCC-UHFFFAOYSA-N 0.000 description 1
- WNLWBCIUNCAMPH-UHFFFAOYSA-N 2-n,2-n-dimethylpropane-1,2-diamine Chemical compound NCC(C)N(C)C WNLWBCIUNCAMPH-UHFFFAOYSA-N 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- CJNRGSHEMCMUOE-UHFFFAOYSA-N 2-piperidin-1-ylethanamine Chemical compound NCCN1CCCCC1 CJNRGSHEMCMUOE-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- NAHHNSMHYCLMON-UHFFFAOYSA-N 2-pyridin-3-ylethanamine Chemical compound NCCC1=CC=CN=C1 NAHHNSMHYCLMON-UHFFFAOYSA-N 0.000 description 1
- IDLHTECVNDEOIY-UHFFFAOYSA-N 2-pyridin-4-ylethanamine Chemical compound NCCC1=CC=NC=C1 IDLHTECVNDEOIY-UHFFFAOYSA-N 0.000 description 1
- XPQIPUZPSLAZDV-UHFFFAOYSA-N 2-pyridylethylamine Chemical compound NCCC1=CC=CC=N1 XPQIPUZPSLAZDV-UHFFFAOYSA-N 0.000 description 1
- WRXNJTBODVGDRY-UHFFFAOYSA-N 2-pyrrolidin-1-ylethanamine Chemical compound NCCN1CCCC1 WRXNJTBODVGDRY-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000000474 3-butynyl group Chemical group [H]C#CC([H])([H])C([H])([H])* 0.000 description 1
- 125000006201 3-phenylpropyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 1
- WGQBIIIENKBDDJ-KRWDZBQOSA-N 4-[(3s)-3-(dimethylamino)pyrrolidine-1-carbonyl]-12h-benzo[g]pyrido[2,1-b]quinazoline-12-one Chemical compound C1[C@@H](N(C)C)CCN1C(=O)C1=CC=CN2C(=O)C3=CC4=CC=CC=C4C=C3N=C12 WGQBIIIENKBDDJ-KRWDZBQOSA-N 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 1
- 208000003200 Adenoma Diseases 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 208000007860 Anus Neoplasms Diseases 0.000 description 1
- 108010039627 Aprotinin Proteins 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 201000001320 Atherosclerosis Diseases 0.000 description 1
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 108010006654 Bleomycin Proteins 0.000 description 1
- 206010005949 Bone cancer Diseases 0.000 description 1
- 208000018084 Bone neoplasm Diseases 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 239000004255 Butylated hydroxyanisole Substances 0.000 description 1
- SBGLOBYJZXAPMU-UHFFFAOYSA-N C1=CC=C2C3=NC(C(=O)N)=NC=C3C=CC2=N1 Chemical class C1=CC=C2C3=NC(C(=O)N)=NC=C3C=CC2=N1 SBGLOBYJZXAPMU-UHFFFAOYSA-N 0.000 description 1
- KTVQLMYDLMSVTH-UHFFFAOYSA-N C1=CC=C2C=C(N=C3C(C(=O)N)=CC=CN3C3)C3=CC2=C1 Chemical compound C1=CC=C2C=C(N=C3C(C(=O)N)=CC=CN3C3)C3=CC2=C1 KTVQLMYDLMSVTH-UHFFFAOYSA-N 0.000 description 1
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 1
- DIHLEIRADLVBRW-CQSZACIVSA-N CN([C@@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C)C Chemical compound CN([C@@H](CNC(=O)C1=CC=CN2C1=NC=1C=C3C(=CC=1C2=O)C=CC=C3)C)C DIHLEIRADLVBRW-CQSZACIVSA-N 0.000 description 1
- 101100411918 Camellia sinensis pRB gene Proteins 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 206010007279 Carcinoid tumour of the gastrointestinal tract Diseases 0.000 description 1
- 208000009458 Carcinoma in Situ Diseases 0.000 description 1
- 241001466804 Carnivora Species 0.000 description 1
- 101710150820 Cellular tumor antigen p53 Proteins 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- RJHPRCPIGISVRB-UHFFFAOYSA-N Cl.CC(CN(C)C)NC(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O Chemical compound Cl.CC(CN(C)C)NC(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O RJHPRCPIGISVRB-UHFFFAOYSA-N 0.000 description 1
- KGBZQLDPMVRBEE-UHFFFAOYSA-N Cl.CN(C)CCCN(C)C(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O Chemical compound Cl.CN(C)CCCN(C)C(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O KGBZQLDPMVRBEE-UHFFFAOYSA-N 0.000 description 1
- UTKOQPPUPHDMCM-LMOVPXPDSA-N Cl.CN(C)[C@H]1CCN(C1)C(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O Chemical compound Cl.CN(C)[C@H]1CCN(C1)C(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O UTKOQPPUPHDMCM-LMOVPXPDSA-N 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 229940126657 Compound 17 Drugs 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 229920002785 Croscarmellose sodium Polymers 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 102100031594 DNA-directed RNA polymerase I subunit RPA12 Human genes 0.000 description 1
- 102100027700 DNA-directed RNA polymerase I subunit RPA2 Human genes 0.000 description 1
- 101710081418 DNA-directed RNA polymerase I subunit RPA2 Proteins 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- 241000282324 Felis Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 208000022072 Gallbladder Neoplasms Diseases 0.000 description 1
- 201000003741 Gastrointestinal carcinoma Diseases 0.000 description 1
- BLCLNMBMMGCOAS-URPVMXJPSA-N Goserelin Chemical compound C([C@@H](C(=O)N[C@H](COC(C)(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NNC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 BLCLNMBMMGCOAS-URPVMXJPSA-N 0.000 description 1
- 108010069236 Goserelin Proteins 0.000 description 1
- 101710088172 HTH-type transcriptional regulator RipA Proteins 0.000 description 1
- 208000005794 Hairy Leukoplakia Diseases 0.000 description 1
- 208000017604 Hodgkin disease Diseases 0.000 description 1
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 1
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 1
- 241001272567 Hominoidea Species 0.000 description 1
- 101000729452 Homo sapiens DNA-directed RNA polymerase I subunit RPA12 Proteins 0.000 description 1
- 206010021042 Hypopharyngeal cancer Diseases 0.000 description 1
- 206010056305 Hypopharyngeal neoplasm Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 102000000588 Interleukin-2 Human genes 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 206010023825 Laryngeal cancer Diseases 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 206010024291 Leukaemias acute myeloid Diseases 0.000 description 1
- GDBQQVLCIARPGH-UHFFFAOYSA-N Leupeptin Natural products CC(C)CC(NC(C)=O)C(=O)NC(CC(C)C)C(=O)NC(C=O)CCCN=C(N)N GDBQQVLCIARPGH-UHFFFAOYSA-N 0.000 description 1
- 108010000817 Leuprolide Proteins 0.000 description 1
- 206010024612 Lipoma Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 229930192392 Mitomycin Natural products 0.000 description 1
- 229920000881 Modified starch Polymers 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 1
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 1
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 1
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- 206010028729 Nasal cavity cancer Diseases 0.000 description 1
- 208000001894 Nasopharyngeal Neoplasms Diseases 0.000 description 1
- 206010061306 Nasopharyngeal cancer Diseases 0.000 description 1
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 1
- 208000010505 Nose Neoplasms Diseases 0.000 description 1
- 102000007999 Nuclear Proteins Human genes 0.000 description 1
- 108010089610 Nuclear Proteins Proteins 0.000 description 1
- RFDWUELJPPJPDL-UHFFFAOYSA-N OC(=O)C(F)(F)F.CN(C1CCN(C)C1)C(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O Chemical compound OC(=O)C(F)(F)F.CN(C1CCN(C)C1)C(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O RFDWUELJPPJPDL-UHFFFAOYSA-N 0.000 description 1
- AAXNSYFMNTYFAK-UHFFFAOYSA-N OC(=O)C(F)(F)F.COCCN(C)CCNC(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O Chemical compound OC(=O)C(F)(F)F.COCCN(C)CCNC(=O)c1cccn2c1nc1cc3ccccc3cc1c2=O AAXNSYFMNTYFAK-UHFFFAOYSA-N 0.000 description 1
- WRILIIFKXVPXCM-UHFFFAOYSA-N OC(=O)C(F)(F)F.O=C(NC1CNC1)c1cccn2c1nc1cc3ccccc3cc1c2=O Chemical compound OC(=O)C(F)(F)F.O=C(NC1CNC1)c1cccn2c1nc1cc3ccccc3cc1c2=O WRILIIFKXVPXCM-UHFFFAOYSA-N 0.000 description 1
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 102000043276 Oncogene Human genes 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 239000012270 PD-1 inhibitor Substances 0.000 description 1
- 239000012668 PD-1-inhibitor Substances 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 102000014160 PTEN Phosphohydrolase Human genes 0.000 description 1
- 108010011536 PTEN Phosphohydrolase Proteins 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 208000009565 Pharyngeal Neoplasms Diseases 0.000 description 1
- 206010034811 Pharyngeal cancer Diseases 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 229920002319 Poly(methyl acrylate) Polymers 0.000 description 1
- 229920000954 Polyglycolide Polymers 0.000 description 1
- 229920000037 Polyproline Polymers 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 102000004245 Proteasome Endopeptidase Complex Human genes 0.000 description 1
- 108090000708 Proteasome Endopeptidase Complex Proteins 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 208000015634 Rectal Neoplasms Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 208000032383 Soft tissue cancer Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 241001493546 Suina Species 0.000 description 1
- ULUAUXLGCMPNKK-UHFFFAOYSA-N Sulfobutanedioic acid Chemical class OC(=O)CC(C(O)=O)S(O)(=O)=O ULUAUXLGCMPNKK-UHFFFAOYSA-N 0.000 description 1
- 235000019486 Sunflower oil Nutrition 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- 239000012317 TBTU Substances 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- 206010057644 Testis cancer Diseases 0.000 description 1
- 208000024770 Thyroid neoplasm Diseases 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical class OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- DOOTYTYQINUNNV-UHFFFAOYSA-N Triethyl citrate Chemical compound CCOC(=O)CC(O)(C(=O)OCC)CC(=O)OCC DOOTYTYQINUNNV-UHFFFAOYSA-N 0.000 description 1
- 101710102803 Tumor suppressor ARF Proteins 0.000 description 1
- 208000023915 Ureteral Neoplasms Diseases 0.000 description 1
- 206010046392 Ureteric cancer Diseases 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 206010053648 Vascular occlusion Diseases 0.000 description 1
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 206010047741 Vulval cancer Diseases 0.000 description 1
- 208000004354 Vulvar Neoplasms Diseases 0.000 description 1
- LJOOWESTVASNOG-UFJKPHDISA-N [(1s,3r,4ar,7s,8s,8as)-3-hydroxy-8-[2-[(4r)-4-hydroxy-6-oxooxan-2-yl]ethyl]-7-methyl-1,2,3,4,4a,7,8,8a-octahydronaphthalen-1-yl] (2s)-2-methylbutanoate Chemical compound C([C@H]1[C@@H](C)C=C[C@H]2C[C@@H](O)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)CC1C[C@@H](O)CC(=O)O1 LJOOWESTVASNOG-UFJKPHDISA-N 0.000 description 1
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 1
- SMNRFWMNPDABKZ-WVALLCKVSA-N [[(2R,3S,4R,5S)-5-(2,6-dioxo-3H-pyridin-3-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [[[(2R,3S,4S,5R,6R)-4-fluoro-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl] hydrogen phosphate Chemical compound OC[C@H]1O[C@H](OP(O)(=O)OP(O)(=O)OP(O)(=O)OP(O)(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)C2C=CC(=O)NC2=O)[C@H](O)[C@@H](F)[C@@H]1O SMNRFWMNPDABKZ-WVALLCKVSA-N 0.000 description 1
- CLZISMQKJZCZDN-UHFFFAOYSA-N [benzotriazol-1-yloxy(dimethylamino)methylidene]-dimethylazanium Chemical compound C1=CC=C2N(OC(N(C)C)=[N+](C)C)N=NC2=C1 CLZISMQKJZCZDN-UHFFFAOYSA-N 0.000 description 1
- 235000011054 acetic acid Nutrition 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 125000005108 alkenylthio group Chemical group 0.000 description 1
- 125000005109 alkynylthio group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 206010065867 alveolar rhabdomyosarcoma Diseases 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000003098 androgen Substances 0.000 description 1
- 238000011394 anticancer treatment Methods 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 229960004405 aprotinin Drugs 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 239000008135 aqueous vehicle Substances 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 1
- KVVMXWRFYAGASO-UHFFFAOYSA-N azetidine-1-carboxylic acid Chemical compound OC(=O)N1CCC1 KVVMXWRFYAGASO-UHFFFAOYSA-N 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- 239000003613 bile acid Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 229960001561 bleomycin Drugs 0.000 description 1
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- 229940043253 butylated hydroxyanisole Drugs 0.000 description 1
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- BPKIGYQJPYCAOW-FFJTTWKXSA-I calcium;potassium;disodium;(2s)-2-hydroxypropanoate;dichloride;dihydroxide;hydrate Chemical compound O.[OH-].[OH-].[Na+].[Na+].[Cl-].[Cl-].[K+].[Ca+2].C[C@H](O)C([O-])=O BPKIGYQJPYCAOW-FFJTTWKXSA-I 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 229960004562 carboplatin Drugs 0.000 description 1
- 150000003857 carboxamides Chemical class 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229960005243 carmustine Drugs 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 238000003570 cell viability assay Methods 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 230000004637 cellular stress Effects 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 201000007455 central nervous system cancer Diseases 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940125797 compound 12 Drugs 0.000 description 1
- 229940126543 compound 14 Drugs 0.000 description 1
- 229940126142 compound 16 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940125810 compound 20 Drugs 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 229940126208 compound 22 Drugs 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 229940125961 compound 24 Drugs 0.000 description 1
- 229940125846 compound 25 Drugs 0.000 description 1
- 229940125851 compound 27 Drugs 0.000 description 1
- 229940127204 compound 29 Drugs 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 229940125877 compound 31 Drugs 0.000 description 1
- 229940125878 compound 36 Drugs 0.000 description 1
- 229940125807 compound 37 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 229960001681 croscarmellose sodium Drugs 0.000 description 1
- 229960000913 crospovidone Drugs 0.000 description 1
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 239000002254 cytotoxic agent Substances 0.000 description 1
- 231100000599 cytotoxic agent Toxicity 0.000 description 1
- 229960000640 dactinomycin Drugs 0.000 description 1
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 1
- 229960000975 daunorubicin Drugs 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 230000001687 destabilization Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 150000004683 dihydrates Chemical class 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- IUNMPGNGSSIWFP-UHFFFAOYSA-N dimethylaminopropylamine Chemical compound CN(C)CCCN IUNMPGNGSSIWFP-UHFFFAOYSA-N 0.000 description 1
- 125000005982 diphenylmethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 229960003668 docetaxel Drugs 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 230000008482 dysregulation Effects 0.000 description 1
- 210000000959 ear middle Anatomy 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 238000000132 electrospray ionisation Methods 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 201000004101 esophageal cancer Diseases 0.000 description 1
- HQPMKSGTIOYHJT-UHFFFAOYSA-N ethane-1,2-diol;propane-1,2-diol Chemical compound OCCO.CC(O)CO HQPMKSGTIOYHJT-UHFFFAOYSA-N 0.000 description 1
- 235000019439 ethyl acetate Nutrition 0.000 description 1
- 229960004667 ethyl cellulose Drugs 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000013265 extended release Methods 0.000 description 1
- 230000007185 extracellular pathway Effects 0.000 description 1
- 208000024519 eye neoplasm Diseases 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 206010016629 fibroma Diseases 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 235000019688 fish Nutrition 0.000 description 1
- 238000003818 flash chromatography Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 210000000232 gallbladder Anatomy 0.000 description 1
- 201000007487 gallbladder carcinoma Diseases 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 229960002913 goserelin Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 1
- 229920000591 gum Polymers 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 201000011066 hemangioma Diseases 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 239000000017 hydrogel Substances 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 206010020718 hyperplasia Diseases 0.000 description 1
- 201000006866 hypopharynx cancer Diseases 0.000 description 1
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 238000010166 immunofluorescence Methods 0.000 description 1
- 238000003125 immunofluorescent labeling Methods 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 238000012744 immunostaining Methods 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 201000004933 in situ carcinoma Diseases 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 208000037903 inflammatory enteropathy Diseases 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- ZPNFWUPYTFPOJU-LPYSRVMUSA-N iniprol Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC=4C=CC=CC=4)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC=4C=CC=CC=4)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC2=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]2N(CCC2)C(=O)[C@@H](N)CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2[C@@H](CCC2)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N2[C@@H](CCC2)C(=O)N3)C(=O)NCC(=O)NCC(=O)N[C@@H](C)C(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H](C(=O)N1)C(C)C)[C@@H](C)O)[C@@H](C)CC)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZPNFWUPYTFPOJU-LPYSRVMUSA-N 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 201000002313 intestinal cancer Diseases 0.000 description 1
- 230000031146 intracellular signal transduction Effects 0.000 description 1
- 210000003228 intrahepatic bile duct Anatomy 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 206010023841 laryngeal neoplasm Diseases 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 201000010260 leiomyoma Diseases 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- GDBQQVLCIARPGH-ULQDDVLXSA-N leupeptin Chemical compound CC(C)C[C@H](NC(C)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C=O)CCCN=C(N)N GDBQQVLCIARPGH-ULQDDVLXSA-N 0.000 description 1
- 108010052968 leupeptin Proteins 0.000 description 1
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 1
- 229960004338 leuprorelin Drugs 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 201000007270 liver cancer Diseases 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 230000000527 lymphocytic effect Effects 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 150000002680 magnesium Chemical class 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 208000006178 malignant mesothelioma Diseases 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 208000026037 malignant tumor of neck Diseases 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 210000000713 mesentery Anatomy 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- OKKJLVBELUTLKV-VMNATFBRSA-N methanol-d1 Chemical compound [2H]OC OKKJLVBELUTLKV-VMNATFBRSA-N 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000000693 micelle Substances 0.000 description 1
- 239000004530 micro-emulsion Substances 0.000 description 1
- 201000003956 middle ear cancer Diseases 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 150000004682 monohydrates Chemical class 0.000 description 1
- CURJNMSGPBXOGK-UHFFFAOYSA-N n',n'-di(propan-2-yl)ethane-1,2-diamine Chemical compound CC(C)N(C(C)C)CCN CURJNMSGPBXOGK-UHFFFAOYSA-N 0.000 description 1
- GCOWZPRIMFGIDQ-UHFFFAOYSA-N n',n'-dimethylbutane-1,4-diamine Chemical compound CN(C)CCCCN GCOWZPRIMFGIDQ-UHFFFAOYSA-N 0.000 description 1
- XHOADYKJSBCVBJ-UHFFFAOYSA-N n,n-diethylpyrrolidin-3-amine Chemical compound CCN(CC)C1CCNC1 XHOADYKJSBCVBJ-UHFFFAOYSA-N 0.000 description 1
- BNXCVFYAJFUJGK-UHFFFAOYSA-N n-(azetidin-3-yl)-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)NC1CNC1 BNXCVFYAJFUJGK-UHFFFAOYSA-N 0.000 description 1
- NAZSUSPAXCYQQA-UHFFFAOYSA-N n-[1-(dimethylamino)propan-2-yl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NC(CN(C)C)C)=O)C3=CC2=C1 NAZSUSPAXCYQQA-UHFFFAOYSA-N 0.000 description 1
- UIZOCZLARAMGLG-UHFFFAOYSA-N n-[2-[2-methoxyethyl(methyl)amino]ethyl]-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)NCCN(C)CCOC)=O)C3=CC2=C1 UIZOCZLARAMGLG-UHFFFAOYSA-N 0.000 description 1
- SJJQXAOOKJWUAB-UHFFFAOYSA-N n-[3-(dimethylamino)propyl]-n-methyl-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C1=CC=C2C=C(C(N3C=CC=C(C3=N3)C(=O)N(C)CCCN(C)C)=O)C3=CC2=C1 SJJQXAOOKJWUAB-UHFFFAOYSA-N 0.000 description 1
- RWIVICVCHVMHMU-UHFFFAOYSA-N n-aminoethylmorpholine Chemical compound NCCN1CCOCC1 RWIVICVCHVMHMU-UHFFFAOYSA-N 0.000 description 1
- JCTNIPHUVLTFRA-UHFFFAOYSA-N n-methyl-n-(1-methylpyrrolidin-3-yl)-12-oxo-12h-benzo[g]pyrido[2,1-b]quinazoline-4-carboxamide Chemical compound C=1C=CN(C(C2=CC3=CC=CC=C3C=C2N=2)=O)C=2C=1C(=O)N(C)C1CCN(C)C1 JCTNIPHUVLTFRA-UHFFFAOYSA-N 0.000 description 1
- 210000003928 nasal cavity Anatomy 0.000 description 1
- 201000007425 nasal cavity carcinoma Diseases 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 239000000346 nonvolatile oil Substances 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 201000008106 ocular cancer Diseases 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 210000002747 omentum Anatomy 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 201000005443 oral cavity cancer Diseases 0.000 description 1
- 206010030979 oral hairy leukoplakia Diseases 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000002895 organic esters Chemical class 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 201000008968 osteosarcoma Diseases 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 108091075611 p53 family Proteins 0.000 description 1
- 102000041788 p53 family Human genes 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 229940121655 pd-1 inhibitor Drugs 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 229960002621 pembrolizumab Drugs 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 210000000578 peripheral nerve Anatomy 0.000 description 1
- 210000004303 peritoneum Anatomy 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 125000000286 phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 210000004224 pleura Anatomy 0.000 description 1
- 201000003437 pleural cancer Diseases 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 229920001993 poloxamer 188 Polymers 0.000 description 1
- 229920001987 poloxamine Polymers 0.000 description 1
- 229920000747 poly(lactic acid) Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 239000008389 polyethoxylated castor oil Substances 0.000 description 1
- 239000004633 polyglycolic acid Substances 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 108010026466 polyproline Proteins 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 description 1
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 229940116317 potato starch Drugs 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 229940069328 povidone Drugs 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000001855 preneoplastic effect Effects 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- AOHJOMMDDJHIJH-UHFFFAOYSA-N propylenediamine Chemical compound CC(N)CN AOHJOMMDDJHIJH-UHFFFAOYSA-N 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 230000005588 protonation Effects 0.000 description 1
- 150000003212 purines Chemical class 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- 238000010814 radioimmunoprecipitation assay Methods 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 229940044601 receptor agonist Drugs 0.000 description 1
- 239000000018 receptor agonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 206010038038 rectal cancer Diseases 0.000 description 1
- 201000001275 rectum cancer Diseases 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000000754 repressing effect Effects 0.000 description 1
- 230000028617 response to DNA damage stimulus Effects 0.000 description 1
- 208000037803 restenosis Diseases 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 230000028710 ribosome assembly Effects 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- 235000017550 sodium carbonate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- JUJBNYBVVQSIOU-UHFFFAOYSA-M sodium;4-[2-(4-iodophenyl)-3-(4-nitrophenyl)tetrazol-2-ium-5-yl]benzene-1,3-disulfonate Chemical compound [Na+].C1=CC([N+](=O)[O-])=CC=C1N1[N+](C=2C=CC(I)=CC=2)=NC(C=2C(=CC(=CC=2)S([O-])(=O)=O)S([O-])(=O)=O)=N1 JUJBNYBVVQSIOU-UHFFFAOYSA-M 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 230000003381 solubilizing effect Effects 0.000 description 1
- 239000001593 sorbitan monooleate Substances 0.000 description 1
- 235000011069 sorbitan monooleate Nutrition 0.000 description 1
- 229940035049 sorbitan monooleate Drugs 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 229940071117 starch glycolate Drugs 0.000 description 1
- 201000000498 stomach carcinoma Diseases 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000002600 sunflower oil Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 229960001603 tamoxifen Drugs 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- DKPFODGZWDEEBT-QFIAKTPHSA-N taxane Chemical class C([C@]1(C)CCC[C@@H](C)[C@H]1C1)C[C@H]2[C@H](C)CC[C@@H]1C2(C)C DKPFODGZWDEEBT-QFIAKTPHSA-N 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- WPGLRFGDZJSQGI-UHFFFAOYSA-N tert-butyl 3-aminoazetidine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CC(N)C1 WPGLRFGDZJSQGI-UHFFFAOYSA-N 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 201000002510 thyroid cancer Diseases 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 229960001727 tretinoin Drugs 0.000 description 1
- 239000001069 triethyl citrate Substances 0.000 description 1
- VMYFZRTXGLUXMZ-UHFFFAOYSA-N triethyl citrate Natural products CCOC(=O)C(O)(C(=O)OCC)C(=O)OCC VMYFZRTXGLUXMZ-UHFFFAOYSA-N 0.000 description 1
- 235000013769 triethyl citrate Nutrition 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 150000004684 trihydrates Chemical class 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 201000011294 ureter cancer Diseases 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 208000021331 vascular occlusion disease Diseases 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 231100000747 viability assay Toxicity 0.000 description 1
- 238000003026 viability measurement method Methods 0.000 description 1
- 229960003048 vinblastine Drugs 0.000 description 1
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 201000005102 vulva cancer Diseases 0.000 description 1
- 229920003169 water-soluble polymer Polymers 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Un compuesto seleccionado del grupo que consiste en: **(Ver fórmula)**
Description
DESCRIPCIÓN
Compuestos que inhiben la ARN polimerasa, composiciones que incluyen dichos compuestos y su uso
Antecedentes de la invención
El ADN ribosómico (ADNr) es la región genómica más transcrita del genoma humano y se encuentra en un compartimento subcelular especializado, el nucleolo. La transcripción del ARNr está mediada por la ARN polimerasa I (Pol I) que transcribe las numerosas copias del gen del ADNr como un precursor de ARNr 47S largo. El precursor 47S del ARNr se procesa a través de varios pasos para obtener los ARNr maduros 18S, 5.8S y 28S necesarios para el ensamblaje de los ribosomas. La transcripción de la Pol I se inicia mediante la fijación de un complejo de preiniciación con numerosas subunidades al promotor del ADNr, que recluta estocásticamente el holocomplejo de Pol I. El holocomplejo de Pol I está compuesto por 14 subunidades en los eucariotas, de las cuales las subunidades RPA194, RPA135 y RPA12 forman el centro activo desde el punto de vista catalítico. La desestabilización de la hélice del ADNr, o la pérdida del armazón proteico, detendrá con eficacia la transcripción. La tasa de transcripción del ARNr está estrechamente controlada por vías de señalización externas que provocan el ensamblaje y la fijación del complejo de preiniciación. La desregulación de la síntesis del ARNr es muy frecuente en los cánceres humanos. Esto se debe a la activación de vías de señalización extracelulares e intracelulares y a oncogenes tales como Myc. Por el contrario, la pérdida de función de los supresores tumorales p53, pRB, ARF y PTEN conduce a la activación de la transcripción de Pol I. Por tanto, los inhibidores de la transcripción de Pol I pueden proporcionar estrategias novedosas para los tratamientos contra el cáncer.
A pesar del impacto clave que tiene la Pol I a la hora de definir las características de las células cancerosas, su explotación terapéutica ha sido mínima. Los presentes inventores han presentado recientemente el descubrimiento de una molécula pequeña contra el cáncer, la 12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida, N-[2 (dimetilamino)etil]-12-oxo (BMH-21) con un modo nítido de inhibición de la Pol I en comparación con el CX-5461 (solicitud de patente de los EE. UU. n.° 12/665,473, registrada el 1 de marzo de 2010 (figura 1)). Estos estudios demostraron que la BMH-21 se intercala en el ADNr rico en GC, inhibe la Pol I y provoca la degradación de RPA194 mediada por el proteasoma. La BMH-21 también mostró una actividad anticancerígena amplia y potente en las líneas celulares de cáncer NCI60 y redujo la carga tumoral en los ensayos de xenoinjerto en los ratones. Estos estudios han proporcionado una confirmación en los estudios preliminares de que la acción selectiva sobre la Pol I es una estrategia viable para el control del cáncer. Peltonen et al., en Cáncer Cell, 2014, 25, 77-90, describen la actividad y los mecanismos de acción de la BMH-21 para atacar selectivamente el cáncer. Colis et al., en J. Med. Chem., 2014, 57 (11), 4950-61, que es un estado de la técnica solo en la medida en que la reivindicación de prioridad de 20 de marzo de 2014 no sea válida, describen el diseño, la síntesis y las relaciones entre la estructura y la actividad de las piridoquinazolincarboxamidas como inhibidores de la ARN polimerasa I sobre la base del descubrimiento del prototipo molecular BMH- 21.
En el documento US 2010/179155 A1, y WO 2008/155468 A1 y WO 2008/155441 A1 se describen métodos para identificar compuestos de tipo molécula pequeña que son activadores de la vía de la proteína p53 supresora de tumores, y métodos para destruir las células tumorales y tratar los cánceres u otras afecciones que requieren la activación de las vías de los miembros de la familia de p53 y las vías de respuesta al daño del ADN con las moléculas pequeñas. El documento US 5,908,840 A se describe un compuesto de tipo molécula pequeña y su uso como agente antineoplásico. En el documento US 2009/163545 A1 se describe un compuesto que altera la longevidad para administrarlo a un organismo eucariota.
Compendio de la invención
La presente invención da a conocer un compuesto según la reivindicación 1. También se da a conocer una composición farmacéutica que comprende un compuesto según la reivindicación 1 y un vehículo farmacéuticamente aceptable, y una composición farmacéutica que comprende un compuesto según la reivindicación 1 y un vehículo farmacéuticamente aceptable para ser usados como medicamento, por ejemplo, para ser usados en el tratamiento de una enfermedad hiperproliferativa en un sujeto.
Se describe en la presente memoria, pero no se reivindica, un compuesto de fórmula I:
donde X es NR2 ;
en donde L es R3 o una cicloamina opcionalmente sustituida
en donde R1 es un grupo de hidrocarburo C1-C6 de cadena lineal o ramificada (por ejemplo, un grupo alquilo, un grupo alquenilo, un grupo alquinilo, un grupo alquilol, un grupo hidroxialquilo, un grupo alcoxi, un grupo alcoxialquilo, grupos cíclicos, sustituidos o sin sustitución, tales como ciclopentilo, ciclohexilo, piramido, fenilo o bencilo, cicloalquilo, heterociclilo, indol, en el que cada uno de los restos alquilo, arilo o heterociclilo puede estar sin sustituir o sustituido con uno o más sustituyentes seleccionados del grupo que consiste en halo, hidroxi, carboxi, fosforilo, fosfonilo, fosfonoalquilo(C1-C6), carboxialquilo(C1-C6), dicarboxialquilo(C1-C6), dicarboxihaloalquilo(C1-C6), sulfonilo, ciano, nitro, alcoxi, alquiltio, acilo, aciloxi, tioacilo, aciltío, ariloxi, amino, alquilamino, dialquilamino, trialquilamino, arilalquilamino, guanidino, aldehído, ureido y aminocarbonilo, un alquilamino de cadena lineal o ramificada, dialquilanino, o alquilo o dialquilaminoalquilo, o tioalquilo, tioalquenilo, tioalquinilo, ariloxi, aciloxi, tioacilo, amido, sulfonamido, etc.), o similares; cuando X es NR2, R2 es H o un grupo alquilo (C1-C6) de cadena lineal;
cuando L es R3 , R3 es un grupo alquilo (C2-C6) de cadena lineal o ramificada;
cuando L es
m = 1-8 y cada Y se selecciona independientemente de (CH2)nY1p , en donde n = 1-8, p = 0-4 y la suma de n y p es al menos 2, y cada Y1 se selecciona independientemente de NR4 , O, S o P, en donde R4 es tal y como se define anteriormente en la presente memoria para R3, y X + O; o una sal, solvato, estereoisómero o profármaco del mismo farmacéuticamente aceptable.
En la presente memoria se describe, pero no se reivindica, un estereoisómero quiralmente puro del compuesto de fórmula I, en el que L es R3 y R3 es un grupo alquilo C2-C6 de cadena lineal o ramificada que tiene al menos un carbono quiral. Se describen en la presente memoria, pero no se reivindican, los compuestos de fórmula II,
en donde R1 = H y R2 = alquilo(C1-C6), sustituido con uno o más alquilo(C1-C4), OH, NH2, NR3R4 , ciano, SO2R3, arilo sustituido o sin sustituir, heteroarilo sustituido o sin sustituir (que incluye, entre otros, imidazolilo, imidazolidinonilo, piridilo, indolilo, oxazolilo, tiazolilo, oxadiazolilo), cicloalquilo sustituido o sin sustituir, o heterociclos que contienen nitrógeno sustituidos o sin sustituir, entre ellos pero sin limitarse a ellos, azetidina, pirrolidina, piperidina, piperazina, azapina, morfolino; en donde R3 y R4 , se seleccionan independientemente del grupo que incluye H, alquilo(C1-C6) y alcoxil(C1-C4)alquilo, que tiene al menos un carbono quiral, cuando R2 está sustituido con al menos un grupo NR3R4. En la presente memoria se describe, pero no se reivindica, una composición farmacéutica que comprende un compuesto de fórmula I y/o fórmula II, y un vehículo farmacéuticamente aceptable.
En la presente memoria se describe, pero no se reivindica, un método para activar las vías por delante de p53 en una célula de mamífero que comprende poner en contacto una célula o población de células con un compuesto de fórmula I y/o fórmula II.
Se describe en la presente memoria, pero no se reivindica, un método para modular la actividad de la ARN Pol I en
una célula de mamífero que comprende poner en contacto una célula o población de células con un compuesto de fórmula I y/o fórmula II.
Se describe en la presente memoria, pero no se reivindica, un método para tratar el cáncer en un sujeto que comprende administrar al sujeto una composición farmacéutica que comprende un compuesto de fórmula I y/o fórmula II.
Se describe en la presente memoria, pero no se reivindica, un método para tratar el cáncer en un sujeto que comprende administrar al sujeto una composición farmacéutica que comprende un compuesto de fórmula I y/o fórmula II, y al menos otro agente biológicamente activo.
Breve descripción de los dibujos
En la figura 1 se representa CX-5461, el inhibidor de la ARN Pol I, la molécula original BMH-21 y su análogo inactivo BMH-21a.
En la figura 2 se muestra el efecto de los compuestos sobre la expresión y localización de RPA194 y NCL. Tinción por inmunofluorescencia de las células U2OS tratadas con los compuestos indicados (0,5 pM) durante 3 horas. En las células se tiñeron (A) RPA194 (rojo) y (B) NCL (verde) y se contratiñó el ADN (azul). Barras de escala: 10 pm.
En la figura 3 se representa el análisis de imagen cuantitativo de la expresión y localización de RPA194 y NCL mediante derivados. Las células U2OS se trataron con los compuestos a 0, 0,1,0,5, 1 y 5 pM, y se incubaron durante 3 horas. Las células se fijaron y se les tiñó (A) RPA194 y (B) NCL, y se contratiñó el ADN, y se obtuvieron imágenes por epifluorescencia. El análisis de imagen cuantitativo para la degradación de RPA194 (A) y la pérdida de la intensidad nucleolar de NCL se realizó sobre la base de dos réplicas biológicas y se muestra las veces que cambia con respecto al control. Las barras de error son el EEM.
En la figura 4 se muestran los análisis de expresión de proteínas para RPA194 y NCL. Las células U2OS se trataron con los compuestos a 0, 0,1, 1 y 10 pM, y se incubaron durante 3 h. Las proteínas se extrajeron con el tampón de lisis RIPA y se realizó la transferencia de tipo Western para RPA194, NCL y GAPDH como control.
En la figura 5 se representan los ensayos de viabilidad celular. Las células U2OS se trataron con los compuestos a 0, 0,5 y 5 pM, y se incubaron durante 48 horas. La viabilidad celular se determinó con el ensayo WST-1. N = 2 repeticiones biológicas, las barras de error son el EEM.
Descripción detallada de la invención
De acuerdo con la presente invención, se prepararon y evaluaron una serie de variantes de la BMH-21 como posibles agentes anticancerígenos nuevos que actúan mediante la represión de la actividad de la Pol I. La actividad de la BMH-21 se debe a su capacidad para intercalarse en las secuencias de ADNr ricas en GC, lo que la hace muy diferente de otras antraciclinas de 4 anillos, que provocan daños en el ADN. Sus modalidades de intercalación también se diferencian bastante de las antraciclinas que se intercalan en dirección perpendicular a la hélice del ADN, mientras que la BMH-21 se intercala de forma casi paralela. Si bien los modelados anteriores han sugerido algunos determinantes moleculares para esta actividad, la alta sensibilidad a la cadena colgante de la BMH-21, como se ejemplifica en los compuestos identificados en la presente memoria, sugiere que puede haber otros componentes del complejo entre la BMH-21 y el ADN que conducen a su actividad biológica. En concreto, todos los derivados casi equipotentes retuvieron la protonación predicha de la amina terminal y tenían un pKa básico cercano al de 8,6 de la molécula original. Estos hallazgos indicaron que la carga total de las moléculas de la invención era crítica, además del mantenimiento de la longitud y la carga básica cerca del extremo del brazo de la carboxamida. Sin quererse ver limitados por ninguna teoría o mecanismo de acción en concreto, estos hallazgos sugieren que la BMH-21 se intercala con el ADN ácido a través de interacciones electrostáticas. También plantea la posibilidad de que los derivados con restos con mucha más carga puedan cambiar la naturaleza de la intercalación o que aquellos con tamaños moleculares más grandes alteren la cavidad de intercalación en el ADN. Esto implica además que tales moléculas pueden perturbar otros procesos metabólicos del ADN.
En la presente memoria se describe, pero no se reivindica, un compuesto de fórmula I:
en donde X es NR2 ;
en donde L es R3 o una cicloamina opcionalmente sustituida
en donde R1 es un grupo de hidrocarburo (C1-C6) de cadena lineal o ramificada (por ejemplo, un grupo alquilo, un grupo alquenilo, un grupo alquinilo, un grupo alquilol, un grupo hidroxialquilo, un grupo alcoxi, un grupo alcoxialquilo, grupos cíclicos, sustituidos o son sustituir, tales como ciclopentilo, ciclohexilo, piramido, fenilo o bencilo, cicloalquilo, heterociclilo, indol, en el que cada uno de los restos alquilo, arilo o heterociclilo puede estar sin sustituir o sustituido con uno o más sustituyentes seleccionados del grupo que consiste en halo, hidroxi, carboxi, fosforilo, fosfonilo, fosfonoalquilo(C1-C6), carboxialquilo(C1-C6), dicarboxialquilo(C1-C6), dicarboxihaloalquilo(C1-C6), sulfonilo, ciano, nitro, alcoxi, alquiltio, acilo, aciloxi, tioacilo, aciltío, ariloxi, amino, alquilamino, dialquilamino, trialquilamino, arilalquilamino, guanidino, aldehído, ureido y aminocarbonilo, un alquilamino de cadena lineal o ramificada, dialquilamino, o alquilo o dialquilaminoalquilo, o tioalquilo, tioalquenilo, tioalquinilo, ariloxi, aciloxi, tioacilo, amido, sulfonamido, etc.), o similares; cuando X es NR2, R2 es H o un grupo alquilo (C1 -C6) de cadena lineal;
cuando L es R3 , R3 es un grupo alquilo (C2-C6) de cadena lineal o ramificada;
cuando L es
m = 1-8 y cada Y se selecciona independientemente de (CH2)nY1p en donde n = 1-8, p = 0-4 y la suma de n y p es al menos 2, y cada Y1 se selecciona independientemente de NR4 , O, S o P, en donde R4 es tal y como se define más arriba en la presente memoria para R3 , y X + O; o una sal, solvato, estereoisómero o profármaco farmacéuticamente aceptable del mismo.
También se describe en la presente memoria, pero no se reivindica, un estereoisómero quiralmente puro del compuesto de fórmula I, en el que L es R3 y R3 es un grupo alquilo (C2-C6) de cadena lineal o ramificada que tiene al menos un carbono quiral.
También se describen en la presente memoria, pero no se reivindican, los compuestos de fórmula II,
en donde R1 = H y R2 = alquilo (C1-C6), sustituido con uno o más alquilo(C1-C4), OH, NH2, NR3R4 , ciano, SO2R3, arilo sustituido o sin sustituir, heteroarilo sustituido o sin sustituir (que incluye, entre otros, imidazolilo, imidazolidinonilo, piridilo, indolilo, oxazolilo, tiazolilo, oxadiazolilo), cicloalquilo sustituido o sin sustituir, o heterociclos que contienen nitrógeno sustituidos o sin sustituir, entre ellos, pero sin limitarse a ellos, azetidina. pirrolidina, piperidina, piperazina, azapina, morfolino; en donde R3 y R4 , se seleccionan independientemente del grupo que incluye H, alquilo(C1-C6) y alcoxilalquilo(C1-C4), que tiene al menos un carbono quiral, cuando R2 está sustituido con al menos un grupo NR3R4. También se describe en la presente memoria, pero no se reivindica, un estereoisómero quiralmente puro del compuesto de fórmula II cuando R2 está sustituido con al menos un grupo NR3R4.
Tal y como se usa en la presente memoria, los ejemplos del término "alquilo" incluyen preferiblemente un alquilo (C1-6) (por ejemplo, metilo, etilo, propilo, isopropilo, butilo, isobutilo, sec-butilo, te/t-butilo, pentilo, hexilo, etc.) y similares.
Tal y como se usa en la presente memoria, los ejemplos del término "alquenilo" incluyen preferiblemente alquenilo (C2-6) (por ejemplo, vinilo, alilo, isopropenilo, 1-butenilo, 2-butenilo, 3-butenilo, 2-metil-2-propenilo, 1 -metil-2-propenilo, 2-metil-1-propenilo, etc.) y similares.
Tal y como se usa en la presente memoria, los ejemplos del término "alquinilo" incluyen preferiblemente alquinilo (C2-6) (por ejemplo, etinilo, propargilo, 1 -butinilo, 2-butinilo, 3-butinilo, 1-hexinilo, etc.) y similares.
Los ejemplos del término "arilo" incluyen preferiblemente un arilo(C6-14) (por ejemplo, un grupo fenilo, 1 -naftilo, 2-naftilo, 2-bifenililo, 3-bifenililo, 4-bifenililo, 2-antracenilo, etc.) y similares.
Los ejemplos del término "arilalquilo" incluyen preferiblemente un arilalquilo (C6-14) (por ejemplo, bencilo, feniletilo, difenilmetilo, 1 -naftilmetilo, 2-naftilmetilo, 2,2-difeniletilo, 3-fenilpropilo, 4-fenilbutilo, 5-fenilpentilo, etc.) y similares.
El término "hidroxialquilo" abarca los grupos alquilo lineales o ramificados que tienen de uno a aproximadamente diez átomos de carbono, alguno de los cuales puede estar sustituido con uno o más grupos hidroxilo.
El término "alquilamino" incluye monoalquilamino. El término "monoalquilamino" significa un amino que está sustituido con un alquilo, tal y como se define en la presente memoria. Los ejemplos de sustituyentes monoalquilamino incluyen, pero no se limitan a ellos, metilamino, etilamino, isopropilamino, f-butilamino y similares. El término "dialquilamino" significa un amino, que está sustituido con dos alquilos tal y como se define en la presente memoria, en donde dichos alquilos pueden ser iguales o diferentes. Los ejemplos de sustituyentes dialquilamino incluyen dimetilamino, dietilamino, etilisopropilamino, diisopropilamino, dibutilamino y similares.
Los términos de grupo "alquiltío", "alqueniltío" y "alquiniltío" significan un grupo que consiste en un átomo de azufre enlazado a un grupo alquilo, alquenilo o alquinilo, que está enlazado a través del átomo de azufre a la entidad a la que está enlazado el grupo.
Quedan incluidas dentro de los compuestos descritos en la presente memoria las formas tautoméricas de los compuestos descritos, las formas isoméricas que incluyen diastereoisómeros, y las sales farmacéuticamente aceptables de los mismos.
Ciertos compuestos descritos en la presente memoria poseen átomos de carbono asimétricos (centros ópticos o quirales) o dobles enlaces; los enantiómeros, racematos, diastereómeros, tautómeros, isómeros geométricos, formas estereoisoméricas, que pueden definirse en términos de estereoquímica absoluta como (R)- o (S)-, y los isómeros individuales, están englobados dentro del alcance de la descripción. Los compuestos de la presente invención no incluyen los que se sabe en la técnica que son demasiado inestables para ser sintetizados y/o aislados. La descripción pretende incluir compuestos en las formas racémicas y ópticamente puras, en concreto unidos al sustituyente R3 del compuesto de fórmula I. Los isómeros (R)- y (S)- ópticamente activos se pueden preparar con el uso de sintones quirales o reactantes quirales tal y como se describe en la presente memoria, o se pueden resolver mediante las técnicas convencionales. Cuando los compuestos descritos en la presente memoria contienen enlaces olefínicos u otros centros de asimetría geométrica, y a menos que se especifique lo contrario, se pretende que los compuestos incluyan los isómeros geométricos E y Z
El término "sales farmacéuticamente aceptables" abarca las sales utilizadas habitualmente para formar sales de metales alcalinos y para formar sales por adición de ácidos libres o bases libres. Los ejemplos de ácidos que se pueden emplear para formar las sales por adición de ácido farmacéuticamente aceptables incluyen ácidos inorgánicos, tales como ácido clorhídrico, ácido sulfúrico y ácido fosfórico, y ácidos orgánicos, tales como ácido maleico, ácido succínico y ácido cítrico. Otras sales farmacéuticamente aceptables incluyen las sales con metales alcalinos o metales alcalinotérreos, tales como sodio, potasio, calcio y magnesio, o con bases orgánicas, tal como diciclohexilamina. Las sales farmacéuticamente aceptables idóneas de los compuestos de la presente invención incluyen, por ejemplo, sales por adición de ácido que pueden, por ejemplo, formarse por la mezcla de una solución del compuesto de acuerdo con la invención con una solución de un ácido farmacéuticamente aceptable, tal como ácido clorhídrico, ácido sulfúrico, ácido metanosulfónico, ácido fumárico, ácido maleico, ácido succínico, ácido acético, ácido benzoico, ácido oxálico, ácido cítrico, ácido tartárico, ácido carbónico o ácido fosfórico. Todas estas sales se pueden preparar por los medios convencionales al hacer reaccionar, por ejemplo, el ácido o la base apropiados con los compuestos correspondientes de la presente invención.
Las sales formadas a partir de grupos carboxilo libres también se pueden derivar de bases inorgánicas, tales como, por ejemplo, hidróxidos de sodio, potasio, amonio, calcio o férrico, y bases orgánicas tales como isopropilamina, trimetilamina, 2-etilaminoetanol, histidina, procaína y similares.
Para su uso en medicamentos, las sales de los compuestos de la presente invención deben ser sales farmacéuticamente aceptables. Sin embargo, pueden resultar útiles otras sales para la preparación de los compuestos según la invención o de sus sales farmacéuticamente aceptables.
Además, las realizaciones de la invención incluyen hidratos de los compuestos de la presente invención. El término "hidrato" incluye, pero no se limita a ellos, hemihidrato, monohidrato, dihidrato, trihidrato y similares. Los hidratos de los compuestos de la presente invención se pueden preparar al poner en contacto los compuestos con agua en las
condiciones idóneas para producir el hidrato de elección.
La presente invención da a conocer un compuesto seleccionado del grupo que consiste en:
Se describen en la presente memoria, pero no se reivindican, las composiciones farmacéuticas que comprenden los compuestos de fórmula I, o sus sales, solvatos o estereoisómeros, y un vehículo farmacéuticamente aceptable.
En la presente memoria se describe un procedimiento para preparar productos farmacéuticos que comprenden los compuestos. El término "producto farmacéutico" significa una composición idónea para uso farmacéutico (composición farmacéutica), según se define en la presente memoria. Las composiciones farmacéuticas formuladas para aplicaciones concretas que comprenden los compuestos de la presente invención también forman parte de esta invención y deben considerarse una realización de la misma.
En la presente memoria se describe, pero no reivindicada, una composición farmacéutica que comprende el compuesto de fórmula I:
en donde L es R3 o una cicloamina opcionalmente sustituida
en donde R1 es un grupo hidrocarburo (C1-C6) de cadena lineal o ramificada (por ejemplo, un grupo alquilo, un grupo alquenilo, un grupo alquinilo, un grupo alquilol, un grupo hidroxialquilo, un grupo alcoxi, un grupo alcoxialquilo, grupos cíclicos, sustituidos o sin sustituir, tales como ciclopentilo, ciclohexilo, piramido, fenilo o bencilo, cicloalquilo, heterociclilo, indol, en el que cada uno de los restos alquilo, arilo o heterociclilo puede estar sin sustituir o sustituido con uno o más sustituyentes seleccionados del grupo que consiste en halo, hidroxi, carboxi, fosforilo, fosfonilo, fosfonoalquilo(C1-C6), carboxialquilo(C1-C6), dicarboxialquilo(C1-C6), dicarboxihaloalquilo(C1-C6), sulfonilo, ciano, nitro,
alcoxi, alquiltío, acilo, aciloxi, tioacilo, aciltío, ariloxi, amino, alquilamino, dialquilamino, trialquilamino, arilalquilamino, guanidino, aldehido, ureido y aminocarbonilo, un alquilamino de cadena lineal o ramificada , dialquilamino, o alquilo o dialquilaminoalquilo, o tioalquilo, tioalquenilo, tioalquinilo, ariloxi, aciloxi, tioacilo, amido, sulfonamido, etc.), o similares; cuando X es NR2, R2 es H o un grupo alquilo (C1-C6) de cadena lineal;
cuando L es R3, R3 es un grupo alquilo (C2-C6) de cadena lineal o ramificada;
cuando L es
m = 1-8 y cada Y se selecciona independientemente de (CH2)nY1p en donde n = 1-8, p = 0-4 y la suma de n y p es al menos 2, y cada Y1 se selecciona independientemente de NR4 , O, S o P, en donde R4 es tal y como se define anteriormente en la presente memoria para R3, y X + O;
o una sal, solvato, estereoisómero o un profármaco farmacéuticamente aceptable del mismo, y un vehículo farmacéuticamente aceptable, en una cantidad eficaz, para ser usado como medicamento, preferiblemente para ser usado en la inhibición de la ARN Pol I en una célula, o población de células, de mamífero, o para ser usado en el tratamiento del cáncer en un sujeto.
También se describe en la presente memoria, pero no se reivindica, una composición farmacéutica que comprende un estereoisómero quiralmente puro del compuesto de fórmula I, en el que L es R3 y R3 es un grupo alquilo (C2-C6) de cadena lineal o ramificada que tiene al menos un carbono quiral, y un vehículo farmacéuticamente aceptable. La composición farmacéutica puede comprender además al menos un agente biológicamente activo adicional.
También se describe en la presente memoria, pero no se reivindica, una composición farmacéutica que comprende compuestos de fórmula II,
en donde R1 = H y R2 = alquilo (C1-C6), sustituido con uno o más alquilo(C1-C4), OH, NH2, NR3R4 , ciano, SO2R3, arilo sustituido o sin sustituir, heteroarilo sustituido o sin sustituir (que incluye, entre otros, imidazolilo, imidazolidinonilo, piridilo, indolilo, oxazolilo, tiazolilo, oxadiazolilo), cicloalquilo sustituido o sin sustituir, o heterociclos que contienen nitrógeno sustituidos o sin sustituir, que incluyen, pero sin limitarse a ellos, azetidina, pirrolidina, piperidina, piperazina, azapina, morfolino; en donde R3 y R4 se seleccionan independientemente del grupo que incluye H, alquilo(C1-C6) y alcoxil(C1-C4)alquilo, que tiene al menos un carbono quiral, cuando R2 está sustituido con al menos un grupo NR3R4 . También se describe en la presente memoria, pero no se reivindica, una composición farmacéutica que comprende un estereoisómero quiralmente puro del compuesto de fórmula II cuando R2 está sustituido con al menos un grupo NR3R4 , y un vehículo farmacéuticamente aceptable. La composición farmacéutica puede comprender además al menos un agente biológicamente activo adicional.
La presente invención da a conocer una composición farmacéutica que comprende al menos uno de los compuestos seleccionados del grupo que consiste en:
compuesto 1 (LI-361);
- );
y un vehículo farmacéuticamente aceptable, en una cantidad eficaz, para ser usado como medicamento, preferiblemente para ser usado para la inhibición de la ARN Pol I en una célula, o población de células, de mamífero, o para ser usado en el tratamiento del cáncer en un sujeto.
Se describe en la presente memoria, pero no se reivindica, un compuesto seleccionado del grupo que consiste en lo siguiente, y una composición farmacéutica que comprende al menos uno de los siguientes compuestos y un vehículo farmacéuticamente aceptable, en una cantidad eficaz, para ser usado como medicamento, preferiblemente para ser usado para inhibir la ARN Pol I en una célula, o población de células, de mamífero, o para ser usado para el tratamiento del cáncer en un sujeto:
- 5);
Con respecto a las composiciones farmacéuticas descritas en la presente memoria, el vehículo farmacéuticamente aceptable puede ser cualquiera de los usados convencionalmente, y está limitado únicamente por cuestiones físicoquímicas, tales como la solubilidad y la falta de reactividad con el compuesto o compuestos activos, y por la vía de administración. Los vehículos farmacéuticamente aceptables descritos en la presente memoria, por ejemplo, vehículos, adyuvantes, excipientes y diluyentes, los conocen de sobra los expertos en la técnica y están fácilmente disponibles para el público. Los ejemplos de vehículos farmacéuticamente aceptables incluyen los vehículos solubles, tales como tampones conocidos que pueden ser fisiológicamente aceptables (por ejemplo, tampón fosfato), así como composiciones sólidas, tales como vehículos en estado sólido o perlas de látex. Se prefiere que el vehículo farmacéuticamente aceptable sea uno que sea químicamente inerte para el agente o agentes activos, y uno que tenga pocos o ningún efecto secundario perjudicial ni toxicidad en las condiciones de uso.
Los vehículos o diluyentes usados en la presente memoria pueden ser vehículos sólidos o diluyentes para formulaciones sólidas, vehículos líquidos o diluyentes para formulaciones líquidas, o mezclas de los mismos.
Los vehículos o diluyentes sólidos incluyen, pero no se limitan a ellos, gomas, almidones (por ejemplo, almidón de maíz, almidón pregelatinizado), azúcares (por ejemplo, lactosa, manitol, sacarosa, dextrosa), materiales celulósicos (por ejemplo, celulosa microcristalina), acrilatos (por ejemplo, polimetilacrilato), carbonato de calcio, óxido de magnesio, talco, o mezclas de los mismos.
Para las formulaciones líquidas, los vehículos farmacéuticamente aceptables pueden ser, por ejemplo, soluciones acuosas o no acuosas, suspensiones, emulsiones o aceites. Ejemplos de solventes no acuosos son propilenglicol, polietilenglicol y ésteres orgánicos inyectables, tales como oleato de etilo. Los vehículos acuosos incluyen, por ejemplo, agua, soluciones alcohólicas/acuosas, ciclodextrinas, emulsiones o suspensiones, que incluyen medios salinos y tamponados.
Ejemplos de aceites son los de origen petrolífero, animal, vegetal o sintético, por ejemplo, aceite de cacahuete, aceite de soja, aceite mineral, aceite de oliva, aceite de girasol, aceite de hígado de pescado, aceite de sésamo, aceite de semilla de algodón, aceite de maíz, aceite de oliva, vaselina y minerales. Los ácidos grasos idóneos para ser usados en las formulaciones parenterales incluyen, por ejemplo, ácido oleico, ácido esteárico y ácido isoesteárico. El oleato de etilo y el miristato de isopropilo son ejemplos de ésteres de ácidos grasos idóneos.
Los vehículos parenterales (para inyección subcutánea, intravenosa, intraarterial o intramuscular) incluyen, por ejemplo, la solución de cloruro de sodio, dextrosa de Ringer, dextrosa y cloruro de sodio, lactada de Ringer y aceites no volátiles. Las formulaciones idóneas para la administración parenteral incluyen, por ejemplo, soluciones inyectables estériles isotónicas acuosas y no acuosas, que pueden contener antioxidantes, tampones, bacteriostáticos y solutos que hacen que la formulación sea isotónica con la sangre del receptor deseado, y suspensiones estériles no acuosas y acuosas que pueden incluir agentes de suspensión, solubilizantes, espesantes, estabilizadores y conservantes.
Los vehículos intravenosos incluyen, por ejemplo, reponedores de fluidos y nutrientes, reponedores de electrolitos tales como los basados en la dextrosa de Ringer y similares. Los ejemplos son líquidos estériles, tales como agua y aceites, con o sin la adición de un tensioactivo y otros adyuvantes farmacéuticamente aceptables. En general, el agua, la solución salina, la dextrosa acuosa y las soluciones de azúcares afines, y los glicoles, tales como propilenglicoles o polietilenglicol, son los vehículos líquidos preferidos, particularmente para las soluciones inyectables.
Además, en una realización, los compuestos de la presente invención pueden comprender además, por ejemplo, aglutinantes (por ejemplo, goma arábiga, almidón de maíz, gelatina, carbómero, etilcelulosa, goma guar, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, povidona), disgregantes (por ejemplo, almidón de maíz, almidón de patata, ácido algínico, dióxido de silicio, croscarmelosa sódica, crospovidona, goma guar, glicolato de almidón y de
sodio), tampones (por ejemplo, Tris-HCl, acetato, fosfato) de distintos pH y fuerzas iónicas, aditivos tales como albúmina o gelatina para impedir que se absorban a las superficies, detergentes (p. ej., Tween 20, Tween 80, Pluronic F68, sales de ácidos biliares), inhibidores de proteasas, tensioactivos (p. ej., laurilsulfato de sodio), potenciadores de la permeabilidad, solubilizantes (p. ej., cremofor, glicerol, polietilenglicerol, cloruro de benzalconio, benzoato de bencilo, ciclodextrinas, ésteres de sorbitano, ácidos esteáricos), antioxidantes (por ejemplo, ácido ascórbico, metabisulfito de sodio, hidroxianisol butilado), estabilizantes (por ejemplo, hidroxipropilcelulosa, hidroxipropilmetilcelulosa), agentes que aumentan la viscosidad (por ejemplo, carbómero, dióxido de silicio coloidal, etilcelulosa, goma guar), edulcorantes (por ejemplo, aspartamo, ácido cítrico), conservantes (por ejemplo, timerosal, alcohol bencílico, parabenos), lubricantes (por ejemplo, ácido esteárico, estearato de magnesio, polietilenglicol, laurilsulfato de sodio), auxiliares de flujo (por ejemplo, dióxido de silicio coloidal), plastificantes (por ejemplo, ftalato de dietilo, citrato de trietilo), emulsionantes (por ejemplo, carbómero, hidroxipropilcelulosa, laurilsulfato de sodio), revestimientos poliméricos (por ejemplo, poloxámeros o poloxaminas), agentes de revestimiento y formadores de películas (por ejemplo, etilcelulosa, acrilatos, polimetacrilatos) y/o adyuvantes.
La elección del vehículo vendrá determinada, en parte, por el compuesto en concreto, así como por el método concreto usado para administrar el compuesto. Por consiguiente, existe una variedad de formulaciones idóneas de la composición farmacéutica de la invención. Las siguientes formulaciones para la administración parenteral, subcutánea, intravenosa, intramuscular, intraarterial, intratecal e interperitoneal son de ejemplo y no limitan en modo alguno. Puede usarse más de una vía para administrar los compuestos y, en ciertos casos, una vía en concreto puede proporcionar una respuesta más inmediata y más eficaz que otra vía.
Los jabones idónenos para ser usados en las formulaciones parenterales incluyen, por ejemplo, sales grasas de metales alcalinos, amonio y trietanolamina, y los detergentes idóneos incluyen, por ejemplo, (a) detergentes catiónicos, tales como, por ejemplo, haluros de dimetildialquilamonio y haluros de alquilpiridinio, (b) detergentes aniónicos tales como, por ejemplo, sulfonatos de alquilo, arilo y olefina, sulfatos de monoglicéridos de alquilo, olefina, éter, y sulfosuccinatos, (c) detergentes no iónicos, tales como, por ejemplo, óxidos de aminas grasas, alcanolamidas de ácidos grasos y copolímeros de polioxietilenpolipropileno, (d) detergentes anfóteros, tales como, por ejemplo, alquilp-aminopropionatos y sales de amonio cuaternario de 2-alquilimidazolina, y (e) mezclas de los mismos.
Las formulaciones parenterales contendrán típicamente de aproximadamente el 0,5% a aproximadamente el 25% en peso de los compuestos en solución. Se pueden usar conservantes y tampones. Con el fin de disminuir al mínimo o eliminar la irritación en el lugar de la inyección, dichas composiciones pueden contener uno o más tensioactivos no iónicos, por ejemplo, que tengan un equilibrio entre hidrófilo e lipófilo (HLB) de aproximadamente 12 a aproximadamente 17. La cantidad de tensioactivo en tales formulaciones variará típicamente de aproximadamente el 5% a aproximadamente el 15% en peso. Los tensioactivos idóneos incluyen, por ejemplo, ésteres de ácidos grasos con sorbitano y polietilenglicol, tales como monooleato de sorbitano y los aductos de óxido de etileno de alta masa molecular con una base hidrófoba, formados por la condensación de óxido de propileno con propilenglicol.
Las formulaciones parenterales se pueden presentar en envases sellados de dosis unitaria o multidosis, tales como ampollas y viales, y se pueden almacenar en un estado liofilizado que requiere solo la adición del excipiente líquido estéril, por ejemplo, agua, para inyecciones, inmediatamente antes de su uso. Pueden prepararse soluciones y suspensiones para inyección extemporánea a partir de polvos, gránulos y comprimidos estériles.
Las formulaciones inyectables están de acuerdo con la invención. Los requisitos de vehículos farmacéuticos eficaces para las composiciones inyectables son de sobra conocidos por los expertos en la técnica (véanse, por ejemplo, Pharmaceutics and Pharmacy Practice, J. B. Lippincott Company, Filadelfia, PA, Banker y Chalmers, eds., páginas 238-250 (1982), y ASHP Handbook on Injectable Drugs, Trissel, 15.a ed., páginas 622-630 (2009)).
La cantidad o la dosis de los compuestos, sales, solvatos o estereoisómeros de cualquiera de los compuestos de la fórmula I, tal y como se establece más arriba, que se administra debe ser suficiente para producir, por ejemplo, una respuesta terapéutica o profiláctica en el sujeto durante un marco de tiempo razonable. La dosis estará determinada por la eficacia del compuesto concreto y la dolencia de un humano, así como la masa corporal de un humano a tratar.
Los expertos en la materia entenderán que los compuestos de la presente invención son inhibidores de la ARN polimerasa I a través de uno o más mecanismos de acción. Sin verse limitados por ninguna teoría en particular, los compuestos de la presente invención pueden inhibir la ARN Pol I por intercalación en los ácidos nucleicos en las regiones ricas en G-C, lo que bloquea la actividad de la polimerasa.
Un experto en la materia sabe que la p53 es una molécula altamente sensible al estrés celular y al daño del ADN, y que está implicada en diversas enfermedades como cáncer, isquemia, trastornos neuronales, inflamación, y también durante procesos fisiológicos como en el metabolismo celular normal, el desarrollo y el envejecimiento. Por tanto, los compuestos de la presente invención son útiles para prevenir o tratar las enfermedades en las que intervienen las vías de la p53.
Por tanto, de acuerdo con una realización, la presente invención da a conocer los compuestos o las composiciones farmacéuticas de la invención en una cantidad eficaz para ser usada en la activación de de las vías anteriores a la p53 en una célula de mamífero que comprende poner en contacto una célula o población de células con el compuesto.
De acuerdo con una realización, la presente invención da a conocer los compuestos o las composiciones
farmacéuticas de la invención en una cantidad eficaz para su uso en la modulación de la actividad de la ARN Pol I en una célula de mamífero que comprende poner en contacto una célula o población de células con el compuesto.
De acuerdo con una realización, la presente invención da a conocer los compuestos o las composiciones farmacéuticas de la invención en una cantidad eficaz para ser usados en el tratamiento del cáncer o de una enfermedad hiperproliferativa en un sujeto, que comprende administrar al sujeto una composición farmacéutica que comprende el compuesto. En una realización alternativa, el uso incluye al menos un agente biológicamente activo adicional.
La dosis de los compuestos, sales, solvatos o estereoisómeros de cualquiera de los compuestos de la fórmula I, tal y como se establece más arriba, también estará determinada por la existencia, naturaleza y extensión de cualquier efecto secundario adverso que pueda acompañar a la administración de un compuesto en concreto. Típicamente, el médico tratante decidirá la dosis del compuesto con la que tratar a cada uno de los pacientes, teniendo en cuenta una serie de factores, tal como la edad, el peso corporal, la salud general, la dieta, el sexo, el compuesto que se administrará, la vía de administración y la intensidad de la afección que se está tratando. A modo de ejemplo, y sin pretender limitar la invención, la dosis del compuesto puede ser de aproximadamente 0,001 a aproximadamente 1000 mg/kg de masa corporal del sujeto a tratar por día, de aproximadamente 0,01 a aproximadamente 100 mg/kg de masa corporal por día, o de aproximadamente 1 mg a aproximadamente 100 mg/kg de masa corporal por día. En algunas realizaciones, la dosificación del compuesto puede estar en el margen de aproximadamente 0,1 pM a aproximadamente 100 pM, preferiblemente de aproximadamente 1 pM a aproximadamente 50 pM.
Como alternativa, los compuestos de la presente invención se pueden modificar para que sean una forma de liberación prolongada, de modo que la forma en que se libera el compuesto en el cuerpo al que se administra está controlada con respecto al tiempo y la ubicación dentro del cuerpo (véase, por ejemplo, la patente de los EE. UU. n.° 4,450,150). Las formas de liberación prolongada de los compuestos pueden ser, por ejemplo, una composición implantable que comprende el compuesto y un material poroso o no poroso, tal como un polímero, en donde el compuesto está encapsulado por este material, o se difunde por todo él, y/o por la degradación del material no poroso. A continuación, el medicamento de liberación prolongada se implanta en la ubicación deseada dentro del cuerpo y los compuestos se liberan desde el implante a una velocidad predeterminada.
En una realización, los compuestos de la presente invención dados a conocer en la presente memoria pueden ser composiciones de liberación controlada, es decir, composiciones en las que uno o más compuestos se liberan durante un período de tiempo después de la administración. Las composiciones de liberación controlada o prolongada incluyen formulaciones en depósitos lipófilos (por ejemplo, ácidos grasos, ceras, aceites). En otra realización, la composición es una composición de liberación inmediata, es decir, una composición en la que todo el compuesto, o sustancialmente todo él, se libera inmediatamente después de la administración.
En otra realización más, los compuestos de la presente invención se pueden administrar en un sistema de liberación controlada. Por ejemplo, el agente puede administrarse mediante la infusión intravenosa, una bomba osmótica implantable, un parche transdérmico u otros modos de administración. En una realización, se puede utilizar una bomba. En una realización, se pueden usar materiales poliméricos. En otra realización más, se puede colocar un sistema de liberación controlada cerca de la diana terapéutica, es decir, el cerebro, lo que requiere así solo una fracción de la dosis sistémica (véase, por ejemplo, Design of Controlled Release Drug Delivery Systems , Xiaoling Li y Bhaskara R. Jasti eds. (McGraw-Hill, 2006)).
Los compuestos incluidos en las composiciones farmacéuticas de la presente invención también pueden incluir la incorporación de los ingredientes activos en o sobre preparaciones en partículas de compuestos poliméricos, tales como ácido poliláctico, ácido poliglicólico, hidrogeles, etc., o sobre liposomas, microemulsiones, micelas, vesículas unilaminares o multilaminares, eritrocitos fantasma o esferoplastos. Tales composiciones influirán en el estado físico, solubilidad, estabilidad, velocidad de liberación in vivo y tasa de eliminación in vivo.
De acuerdo con la presente invención, los compuestos de la presente invención pueden modificarse mediante, por ejemplo, la unión covalente de polímeros hidrosolubles, tales como polietilenglicol, copolímeros de polietilenglicol y polipropilenglicol, carboximetilcelulosa, dextrano, alcohol polivinílico, polivinilpirrolidona o poliprolina. Se sabe que los compuestos modificados exhiben semividas en sangre sustancialmente más prolongadas después de la inyección intravenosa que los correspondientes compuestos sin modificación. Tales modificaciones también pueden incrementar la solubilidad de los compuestos en solución acuosa, eliminar la agregación, mejorar la estabilidad física y química del compuesto, y reducir en gran medida la inmunogenia y la reactividad del compuesto. Como resultado, la actividad biológica deseada in vivo se puede lograr mediante la administración de tales aductos entre el polímero y el compuesto con menos frecuencia, o en dosis más bajas que con el compuesto sin modificación.
Un agente activo y un agente biológicamente activo se usan indistintamente en la presente memoria para hacer referencia a un compuesto químico o biológico que induce un efecto farmacológico y/o fisiológico deseado, en el que el efecto puede ser profiláctico o terapéutico. Los términos también abarcan los derivados farmacológicamente activos farmacéuticamente aceptables de los agentes activos mencionados específicamente en la presente memoria, que incluyen, pero no se limitan a ellos, sales, ésteres, amidas, profármacos, metabolitos activos, análogos y similares. Cuando se usan los términos "agente activo", "agente farmacológicamente activo" y "fármaco", entonces, debe entenderse que la invención incluye el propio agente activo, así como sales, ésteres, amidas, profármacos,
metabolitos, análogos, etc., farmacológicamente activos y farmacéuticamente aceptables. El agente activo puede ser una entidad biológica, tal como un virus o una célula, ya sea de origen natural o artificial, tal como transformado.
Otros ejemplos de agentes biológicamente activos incluyen, sin limitación, enzimas, antagonistas o agonistas de receptores, hormonas, factores de crecimiento, médula ósea autógena, antibióticos, agentes antimicrobianos, moléculas de ARN y ADN y ácidos nucleicos, y anticuerpos. Los ejemplos específicos de agentes biológicamente activos útiles de las categorías anteriores incluyen: antineoplásicos, tales como inhibidores de andrógenos, antimetabolitos, agentes citotóxicos e inmunomoduladores.
Los agentes biológicamente activos también incluyen agentes contra el cáncer, tales como agentes alquilantes, agentes alquilantes de tipo clormetina, agentes alquilantes de tipo nitrosourea, antimetabolitos, antimetabolitos análogos de la purina, antimetabolitos análogos de la pirimidina, antineoplásicos hormonales, antineoplásicos naturales, antineoplásicos naturales antibióticos y antineoplásicos naturales de tipo alcaloides de vinca.
Otros ejemplos de antineoplásicos alquilantes incluyen carboplatino y cisplatino; agentes antineoplásicos alquilantes de tipo nitrosourea, tales como carmustina (BCNU); agentes antineoplásicos antimetabolitos, tales como metotrexato; agentes antineoplásicos análogos de la pirimidina, tales como fluorouracilo (5-FU) y gemcitabina; antineoplásicos hormonales, tales como goserelina, leuprorelina y tamoxifeno; antineoplásicos naturales, tales como aldesleucina, interleucina-2, docetaxel, etopósido, interferón; paclitaxel, otros derivados del taxano, y tretinoína (ATRA); antineoplásicos naturales de naturaleza antibiótica, tales como bleomicina, dactinomicina, daunorubicina, doxorubicina y mitomicina; antineoplásicos naturales de tipo alcaloides de vinca, tales como vinblastina y vincristina, e inhibidores de PD1, tal como lambrolizumab.
Tal como se usa en la presente memoria, el término "sujeto" se refiere a cualquier mamífero, incluidos, entre otros, los mamíferos del orden Rodentia, tales como ratones y hámsteres, y los mamíferos del orden Logomorpha, tal como conejos. Se prefiere que los mamíferos sean del orden Carnívora, que incluye los felinos (gatos) y los cánidos (perros). Se prefiere más que los mamíferos sean del orden Artiodactyla, que incluye los bovinos (vacas) y los porcinos (cerdos) o del orden Perssodactyla, que incluye los equinos (caballos). Lo más preferido es que los mamíferos sean del orden Primates, Ceboides o Simoides (monos) o del orden Antropoides (humanos y simios). Un mamífero especialmente preferido es el ser humano.
Tal y como se usa en la presente memoria, el término "modular" significa que los compuestos de fórmula I, descritos en la presente memoria, incrementan o disminuyen la actividad de la ARN Pol I.
Tal y como se usa en la presente memoria, el término "enfermedad hiperproliferativa" incluye el cáncer y otras enfermedades, tales como las neoplasias y las hiperplasias. Las enfermedades proliferativas celulares incluyen, por ejemplo, artritis reumatoide, enteropatía inflamatoria, osteoartritis, leiomiomas, adenomas, lipomas, hemangiomas, fibromas, oclusión vascular, reestenosis, arterosclerosis, una lesión preneoplásica, carcinoma in situ, leucoplaquia pilosa oral o psoriasis. De acuerdo con una o más realizaciones, el término cáncer puede incluir cualquiera de cáncer linfocítico agudo, leucemia mieloide aguda, rabdomiosarcoma alveolar, cáncer de hueso, cáncer de cerebro, cáncer del sistema nervioso central, tumores de la lámina nerviosa periférica, cáncer de mama, cáncer de ano, canal anal o anorrectal, cáncer de ojo, cáncer del conducto biliar intrahepático, cáncer de articulaciones, cáncer de cuello, de la vesícula biliar o de la pleura, cáncer de nariz, de la cavidad nasal o del oído medio, cáncer de cavidad oral, cáncer de vulva, leucemia linfocítica crónica, cáncer mieloide crónico, cáncer de colon, cáncer de esófago, cáncer de cuello uterino, tumor carcinoide gastrointestinal. Linfoma de Hodgkin, cáncer de hipofaringe, cáncer de riñón, cáncer de laringe, cáncer de hígado, cáncer de pulmón, mesotelioma maligno, melanoma, mieloma múltiple, cáncer de nasofaringe, linfoma no de Hodgkin, cáncer de ovario, cáncer de páncreas, cáncer de peritoneo, de epiplón y mesenterio, cáncer de faringe, cáncer de próstata, cáncer de recto, cáncer de riñón (p. ej., carcinoma de células renales (CCR)), cáncer de intestino delgado, cáncer de partes blandas, cáncer de estómago, cáncer de testículo, cáncer de tiroides, cáncer de uréter y cáncer de vejiga urinaria.
Ejemplos
Células y ensayo de viabilidad. Las células se mantuvieron a 37 °C en una atmósfera humidificada que contenía el 5 % de CO2. Se cultivaron las células de osteosarcoma U2OS en DMEM complementado con suero bovino fetal al 15 %. Las células se sembraron en placas de 96 pocillos a una densidad de 10000 células/pocillo por triplicado y se incubaron durante 48 horas con los compuestos. La viabilidad se determinó con el reactivo de proliferación celular WST-1 (Roche Diagnostics).
Inmunofluorescencia, microscopía de epifluorescencia y análisis de imágenes. Las células U2OS cultivadas en cubreobjetos se fijaron en paraformaldehído al 3,5 %, se permeabilizaron con NP-40 al 0,5 % y se bloquearon con SAB al 3 %, tal y como se describe en Peltonen et al. (Mol. Cancer Ther. 2014). En las células se tiñeron RPA194 (C-1, Santa Cruz Biotechnology) y NCL (4E2, Abcam). Los anticuerpos antirratón o anticonejo conjugados con Alexa 488 y Alexa 594 eran de Invitrogen. El ADN se contratiñó con DAPI (Invitrogen). Las imágenes se capturaron con un microscopio de fluorescencia Axioplan2 (Zeiss) equipado con una cámara CCD AxioCam HRc y el programa informático AxioVision 4.5 con un objetivo EC Plan-Neofluar 20x/0,75 (Zeiss). Las imágenes se cuantificaron con el programa informático de análisis de imágenes FrIDA, tal y como se describe en Peltonen et al. (2014). La saturación
de tono y el margen de brillo se definieron por separado para RPA194 y NCL. Todos los valores se normalizaron por el contenido de ADN. Se registraron dos o cuatro campos de cada tratamiento y la cuantificación se basó en un promedio de 200 células.
Inmunotransferencia. La lisis de las células se realizó en el tampón con NP-40 al 0,5 % (Tris-HCl a 25 mM, pH 8,0, NaCl a 120 mM, NP-40 al 0,5 %, NaF a 4 mM, Na3VÜ4 a 100 pM, 100 KlU/ml de aprotinina, 10 pg/ml de leupeptina). Las proteínas se separaron en gel de poliacrilamida con SDS y se transfirieron como en (Peltonen et al. 2010). Se utilizaron los siguientes anticuerpos: n Cl (4E2, Abcam), RPA194 (C-1, Santa Cruz Biotechnology), GAPDH (Europa Bioproducts). Los anticuerpos secundarios conjugados con HRP eran de DAKO.
Determinación de la CI50 de RPA194 y NCL. Las células U2OS cultivadas en cubreobjetos se trataron con los compuestos a 0,1,0,5, 1, 5 y 10 pM, o se trataron con vehículo (DMSO) durante 3 h, y se fijaron y tiñeron como más arriba. Todos los compuestos, excepto cuando se indica, se comprobaron en experimentos biológicos independientes por duplicado. La inmunotinción de NCL y RPA194 se realizó por separado y a las células se contratiñó el ADN. Se capturaron de dos a cuatro campos de cada tratamiento con la microscopía de epifluorescencia como más arriba, y contenían una media de 200 células/análisis. Las imágenes se cuantificaron con el programa informático de análisis de imágenes FrIDA, tal y como se describe en la referencia 14. La saturación del tono y el margen de brillo se definieron por separado para RPA194 y NCL, y todos los valores se normalizaron por el contenido de ADN. Se determinó las veces que cambiaba con respecto al control. Se determinó la CI50 con GraphPad Prism para Windows (versión 6.01) usando un ajuste de tres parámetros.
Síntesis. Métodos generales. Todos los reactivos y solventes disponibles en el mercado se usaron sin purificación adicional a menos que se indique lo contrario. La cromatografía ultrarrápida automatizada se realizó en un ISCO CombiFlash Rf o un Biotage Isolera con cartuchos Biotage Flash con detección de picos a 254 nm. La purificación en fase inversa se logró con un manipulador de líquidos Gilson 215 equipado con una columna Phenomenex C18 (D. I. de 150 x 20 mm, S-5 pm). La recolección de picos se desencadenó mediante la detección UV a 214 o 254 nm. Los espectros de la RMN de 1H se registraron en un instrumento Bruker 400 que funcionaba a 400 MHz con tetrametilsilano o el solvente protonado residual usado como referencia. La CL/EM analítica se realizó con un Agilent 1260 equipado con un muestreador automático (columna Agilent Poroshell 120 C18 (D. I. de 50 x 4,6 mm, 3,5 pm); TFA al 0,1 % en gradiente de agua/acetonitrilo; detección UV a 215 y 254 nm) e ionización por electropulverización.
El esquema general de la síntesis es:
Ácido 12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxílico (3a). Una mezcla de ácido 3-amino-2-naftoico (2) (2,00 g, 10,68 mmol), ácido 2-cloronicotínico (1) (1,68 g, 10,68 mmol) y ácido clorhídrico (0,9 ml, 29,13 mmol) en etanol (70 ml) se agitó a 80 °C durante 66 h (por comodidad). Después de enfriarla, se filtró la suspensión de color naranja rojizo, se lavó con etanol y se secó al aire para dar el ácido 12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxílico (1,56 g, 5,37 mmol, rendimiento del 50,3 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, DMSO-ds): 5 ppm 9,16 (s, 1 H), 9,03 (dd, J = 7,20, 1,64 Hz, 1 H), 8,63 (dd, J = 6,95, 1,64 Hz, 1 H), 8,49 (s, 1 H), 8,34 (d, J = 8,34 Hz, 1 H), 8,19 (d, J = 8,08 Hz, 1 H), 7,76 (t, J = 7,07 Hz, 1 H), 7,64 (t, J = 6,95 Hz, 1 H), 7,18 (t, J = 7,07 Hz, 1 H). EM [M 1] = 291.
Ácido 11-oxopirido[2,1-b]quinazolín-6-carboxílico (3b). Se agitó una mezcla de ácido 2-aminobenzoico (250 mg, 1,82 mmol), ácido 2-cloronicotínico (287,2 mg, 1,82 mmol) y ácido clorhídrico (0,3 ml, 9,85 mmol) en etanol (20 ml) a 80 °C durante 48 h (por comodidad). Después de enfriarla, se filtró la suspensión de color naranja rojizo, se lavó con etanol y se secó al aire para dar el ácido 11-oxopirido[2,1-b]quinazolín-6-carboxílico (107 mg, 0,45 mmol, rendimiento del 24,5 %) como un sólido amarillo pálido. r Mn de 1H (400 MHz, CDCh): 5 ppm 9,50 (dd, J = 7,07, 1,52 Hz, 3 H), 9,18 (dd, J = 7,45, 1,64 Hz, 3 H), 8,56 (dd, J = 8,21, 1,39 Hz, 3 H), 8,17 (ddd, J = 8,46, 7,20, 1,52 Hz, 3 H), 8,03 (s, 2 H), 8,01 (s, 1 H), 7,80 (ddd, J = 8,15, 7,26, 1,01 Hz, 4 H), 7,72 (t, J = 7,20 Hz, 3 H). EM [M 1] = 241.
Método A: Síntesis de análogos de amida (4). W-[2-(dimetilamino)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida. A una solución de ácido 12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxílico (50 mg, 0,17 mmol) y TBTU (82,9 mg, 0,26 mmol) en DMF (1 ml) se le añadió DiPeA (90 pl, 0,52 mmol). Después de agitar el contenido a temperatura ambiente durante 15 minutos, se le añadió W,W-dimetiletilendiamina (28,4 pl, 0,26 mmol) y se continuó agitando durante 16 horas (por comodidad). Se añadió la mezcla de reacción a 100 ml de agua fría con agitación. Se recogió el sólido por filtración y se secó al vacío para dar la W-[2-(dimetilamino)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (36 mg, 0,10 mmol, rendimiento del 58,0 %) como un sólido amarillo. RMN de 1H (400 MHz, DMSO-ds): 5 ppm 11,50 (s ancho, 1 H), 9,10 (s, 1 H), 8,91 (d, J = 5,81 Hz, 1 H), 8,55 (d, J = 5,56 Hz, 1 H), 8,28 - 8,34 (m, 2 H), 8,12 (d, J = 8,34 Hz, 1 H), 7,73 (t, J = 7,45 Hz, 1 H), 7,61 (t, J = 7,33 Hz, 1 H), 7,05 (t, J = 7,07 Hz, 1
H), 3,56 (d, J = 5,05 Hz, 2 H), 2,59 (t, J = 5,94 Hz, 2 H), 2,40 (s, 6 H). RMN de 1H (400 MHz, CDCI3): 5 ppm 11,70 (s ancho, 1 H), 9,10 (s, 1 H), 8,94 (dd, J = 7,33, 1,77 Hz, 1 H), 8,73 (dd, J = 6,82, 1,77 Hz, 1 H), 8,29 (s, 1 H), 8,12 (d, J = 8,59 Hz, 1 H), 8,00 (d, J = 8,34 Hz, 1 H), 7,66 (t, J = 7,58 Hz, 1 H), 7,52 - 7,60 (m, 1 H), 6,89 (t, J = 7,07 Hz, 1 H), 3,66 - 3,77 (m, 2 H), 2,71 (t, J = 6,06 Hz, 2 H), 2,49 (s, 6 H). EM [M 1] = 361.
Ejemplo 1
N-[2-(dimetilamino)etil]-N-metil-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 1). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N,N,N'-trimetiIetiIendiamina (21,3 gl, 0,17 mmol) de acuerdo con el método A para dar el trifluoroacetato de N-[2-(dimetilamino)etil]-N-metil-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (18,8 mg, 0,050 mmol, rendimiento del 29,1 %) como un sólido naranja. RMN de 1H (400 MHz, CDCla): 5 ppm 9,14 (s, 1 H), 8,93 (d, J = 7,33 Hz, 1 H), 8,28 (s, 1 H), 8,14 (d, J = 8,34 Hz, 1 H), 8,04 (d, J = 8,84 Hz, 1 H), 7,93 (d, J = 6,82 Hz, 1 H), 7,67 - 7,74 (m, 1 H), 7,58 - 7,64 (m, 1 H), 6,97 (t, J = 7,07 Hz, 1 H), 4,12 (t, J = 5,94 Hz, 2 H), 3,57 (t, J = 6,19 Hz, 2 H), 3,12 (s, 6 H), 3,10 (s, 3 H). EM [M 1] = 375.
Ejemplo 2
N-[2-(dimetilamino)etil]-N-etil-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 2). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N,N-dimetil-W-etiletilendiamina (27,1 gl, 0,17 mmol) de acuerdo con el método A para dar el trifluoroacetato de N-[2-(dimetilamino)etil]-N-etil-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (36,1 mg, 0,093 mmol, rendimiento del 54 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCla): 5 ppm 9,13 (s, 1 H), 8,87 (d, J = 7,33 Hz, 1 H), 8,21 (s, 1 H), 8,13 (d, J = 8,34 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,65 - 7,71 (m, 1 H), 7,56 - 7,62 (m, 2 H), 6,84 (t, J = 7,07 Hz, 1 H), 4,06 (m, 2 H), 3,62 (t, J = 6,69 Hz, 2 H), 3,39 (q, J = 7,24 Hz, 2 H), 3,12 (s, 6 H), 1,20 (t, J = 7,07 Hz, 3 H). EM [M 1] = 389.
Ejemplo 3
N-(2-imidazol-1-iletil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 3). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 2-imidazol-1-iletanamina (16,6 gl, 0,17 mmol) de acuerdo con el método A para dar la N-(2-imidazol-1-iletil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (28,5 mg, 0,074 mmol, 43 % de rendimiento) como un sólido amarillo anaranjado. RMn de 1H (400 MHz, CDCh): 5 ppm 11,57 (s ancho, 1 H), 9,08 (s, 1 H), 8,98 (dd, J = 7,07, 1,77 Hz, 1 H), 8,73 (dd, J = 7,07, 1,77 Hz, 1 H), 8,10 (t, J = 8,34 Hz, 3 H), 7,94 (s, 1 H), 7,66 - 7,72 (m, 3 H), 7,55 - 7,60 (m, 2 H), 7,22 (s, 1 H), 7,16 (s, 1 H), 6,91 (t, J = 7,07 Hz, 2 H), 4,32 - 4,37 (m, 2 H), 4,01 - 4,07 (m, 2 H). EM [M 1] = 384.
Ejemplo 4
12-oxo-N-[2-(2-piridil)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 4). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 2-(2-aminoetil)piridina (20,6 gl, 0,17 mmol) de acuerdo con el método A para dar la 12-oxo-N-[2-(2-piridil)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (40,7 mg, 0,103 mmol, rendimiento del 60 %) como un sólido naranja. RMN de 1H (400 MHz, DMSO-d6): 5 ppm 11,39 (s ancho, 1 H), 9,12 (s, 1 H), 8,96 (dd, J = 7,33, 1,77 Hz, 1 H), 8,75 (dd, J = 7,07, 1,77 Hz, 1 H), 8,26 (s, 1 H), 8,13 (d, J = 8,59 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,64 - 7,72 (m, 1 H), 7,53 - 7,61 (m, 1 H), 6,91 (t, J = 7,07 Hz, 1 H), 3,64 - 3,74 (m, 2 H), 2,50 -2.58 (m, 2 H). EM [M 1] = 395.
Ejemplo 5
12-oxo-N-[2-(3-piridil)etil]-12H-benzo[g]pirido[2,1-b]quinazolina-4-carboxamida (compuesto 5). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 3-(2-aminoetil)piridina (20,5 gl, 0,17 mmol) de acuerdo con el método A para dar la 12-oxo-N-[2-(3-piridil)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (55 mg, 0,14 mmol, rendimiento del 81 %) como un sólido naranja. RMN de 1H (400 MHz, DMSO-d6): 5 ppm 11,39 (s ancho, 1 H), 9,12 (s, 1 H), 8,96 (dd, J = 7,33, 1,77 Hz, 1 H), 8,75 (dd, J = 7,07, 1,77 Hz, 1 H), 8,26 (s, 1 H), 8,13 (d, J = 8,59 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,64 - 7,72 (m, 1 H), 7,53 - 7,61 (m, 1 H), 6,91 (t, J = 7,07 Hz, 1 H), 3,64 - 3,74 (m, 2 H), 2,50 -2.58 (m, 2 H). EM [M 1] = 395.
Ejemplo 6
12-oxo-N-[2-(2-oxoimidazolidín-1 -il)etil]- 12H-benzo[g]pirido[2,1 -b]quinazolín-4-carboxamida (compuesto 6). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 1-(2-aminoetil)imidazolidín-2-ona (19,6 gl, 0,17 mmol) de acuerdo con el método A para dar la 12-oxo-N-[2-(2-oxoimidazolidín-1-il)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (6,5 mg, 0,016 mmol, rendimiento del 9,4 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCta): 5 ppm 11,54 (s ancho, 1 H), 9,12 (s, 1 H), 8,98 (dd, J = 7,20, 1,64 Hz, 1 H), 8,74 (d, J = 7,07 Hz, 1 H), 8,43 (s, 1 H), 8,12 (dd, J = 12,63, 8,08 Hz, 2 H), 7,66 - 7,71 (m, 1 H), 7,57 (dd, J = 15,79, 8,72 Hz, 2 H), 7,02 (s, 1 H), 6,91 (t , J = 7,33 Hz, 1 H), 3,80 - 3,88 (m, 2 H), 3,61 - 3,69 (m, 4 H), 3,47 (m, 2 H). EM [M 1] = 402.
Ejemplo 7
N-[2-(1H-indol-3-il)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 7). Este compuesto se
sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la triptamina (27,6 mg, 0,17 mmol) de acuerdo con el método A para
dar la N-[2-(1H-indol-3-il)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (22,9 mg, 0,053 mmol, rendimiento del 30,7 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCh): 5 ppm 11,43 - 11,50 (m,
1 H), 9,04 (s, 1 H), 8,91 - 8,95 (m, 1 H), 8,77 (dd, J = 6,82, 1,77 Hz, 1 H), 8,06 (s, 2 H), 7,83 (d, J = 7,33 Hz, 1 H), 7,74
(d, J = 8,08 Hz, 1 H), 7,60 - 7,67 (m, 1 H), 7,54 (s, 1 H), 7,47 (s, 1 H), 7,34 (s, 2 H), 7,19 - 7,26 (m, 3 H), 7,16 (d, J =
2,02 Hz, 2 H), 6,90 (t, J = 7,20 Hz, 1 H), 4,08 (d, J = 6,06 Hz, 2 H), 3,27 (m, 2 H). EM [M 1] = 433.
Ejemplo 8
N-(2-metilsulfoniletil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 8). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 2-metilsulfoniletanamina (21,2 mg, 0,17 mmol) de acuerdo con el método A para dar la N-(2-metilsulfoniletil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (2,1 mg, 0,0053 mmol, rendimiento del 3,1 %) en forma de un sólido de color amarillo anaranjado. RMN de 1H (400 MHz, CDCla): 5 ppm 11,93 (s ancho, 1 H), 9,12 (s, 1 H), 9,00 (dd, J = 7,45, 1,64 Hz, 1 H), 8,73 (dd, J = 6,95, 1,64 Hz, 1 H),
8,49 (s, 1 H), 8,12 (t, J = 8,84 Hz, 2 H), 7,67 - 7,72 (m, 1 H), 7,56 - 7,62 (m, 1 H), 6,92 (t, J = 7,07 Hz, 1 H), 4,16 - 4,22
(m, 2 H), 3,49 - 3,54 (m, 2 H), 3,07 (s, 3 H). EM [M 1] = 396.
Ejemplo 9
N-[3-(dimetilamino)propil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 9). Este compuesto
se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N,N-dimetil-1,3-propanodiamina (21,7 pl, 0,17 mmol) de acuerdo
con el método A para dar la N-[3-(dimetilamino)propil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida
(18,1 mg, 0,048 mmol, rendimiento del 28,1 %) como un sólido naranja. r MN de 1H (400 MHz, DMSO-ds): 5 ppm
11,39 (s ancho, 1 H), 9,12 (s, 1 H), 8,96 (dd, J = 7,33, 1,77 Hz, 1 H), 8,75 (dd, J = 7,07, 1,77 Hz, 1 H), 8,26 (s, 1 H), 8.13 (d, J = 8,59 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,64 - 7,72 (m, 1 H), 7,53 - 7,61 (m, 1 H), 6,91 (t , J = 7,07 Hz, 1
H), 3,64 - 3,74 (m, 2 H), 2,50 - 2,58 (m, 2 H), 2,33 (s, 6 H), 1,98 (quin, J = 7,14 Hz, 2 H). EM [M 1] = 375.
Ejemplo 10
N-[4-(dimetilamino)butil]- 12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 10). Este compuesto
se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N',N'-dimetilbutano-1,4-diamina (24,5 pl, 0,17 mmol) de acuerdo
con el método A para dar la N-[4-(dimetilamino)butil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (22,1
mg, 0,057 mmol, 33 % de rendimiento) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCl3): 5 ppm
11,35 - 11,41 (m, 1 H), 9,13 (s, 1 H), 8,98 (dd, J = 7,20, 1,64 Hz, 1 H), 8,76 (dd, J = 6,95, 1,64 Hz, 1 H), 8,26 (s, 1 H), 8.14 (d, J = 8,59 Hz, 1 H), 8,06 (d, J = 8,59 Hz, 1 H), 7,66 - 7,72 (m, 1 H), 7,54 - 7,63 (m, 1 H), 6,92 (t, J = 7,07 Hz, H), 3,62 - 3,73 (m, 2 H), 2,46 - 2,52 (m, 2 H), 2,32 (s, 6 H), 1,59 - 1,91 (m, 4 H). EM [M 1] = 389.
Ejemplo 11
N-[2-(1-metilpirrolidín-2-il)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 11). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 2-(2-aminoetil)-1 -metilpirrolidina (22 mg, 25 pl, 0,17
mmol) de acuerdo con el método A para dar la N-[2-(1-metilpirrolidín-2-il)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (18 mg, 0,045 mmol, rendimiento del 26 %) como un sólido amarillo anaranjado. RMN
de 1H (400 MHz, CDCla): 5 ppm 11,59 (s ancho, 1 H), 9,10 (s, 1 H), 8,98 (dd, J = 7,33, 1,77 Hz, 1 H), 8,70 (dd, J =
6,82, 1,77 Hz, 1 H), 8,28 (s, 1 H), 8,11 (t, J = 7,71 Hz, 2 H), 7,70 (dd, J = 8,59, 7,33 Hz, 1 H), 7,56 - 7,62 (m, 1 H), 6,92
(t, J = 7,20 Hz, 1 H), 3,66 - 3,88 (m, 1 H), 3,26 (m, 2 H), 3,16 (m, 1 H), 2,94 (s ancho, 3 H), 2,86 - 2,92 (m, 1 H), 2,83
(d, J = 4,04 Hz, 1 H), 2,46 - 2,60 (m, 2 H), 2,20 - 2,36 (m, 2 H), 2,05 - 2,20 (m, 2 H). EM [M 1] = 401.
Ejemplo 12
N-[3-(dimetilamino)propil]-N-metil-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 12). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N,N,W-trimetil-1,3-propandiamina (25,3 pl, 0,17 mmol) de acuerdo con el método A para dar el hidrocloruro de N-[3-(dimetilamino)propil]-N-metil-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (27,7 mg, 0,071 mmol, rendimiento del 41,4 %) como un sólido amarillo. RMN de 1H (400 MHz, DMSO-d6): 5 ppm 9,12 (s, 1 H), 8,77 (d, J = 7,33 Hz, 1 H), 8,32 (d, J = 6,32 Hz, 2 H),
8,10 - 8,21 (m, 1 H), 7,54 - 7,75 (m, 3 H), 6,90 - 7,01 (m, 1 H), 3,41 (m, 2 H), 3,10 (m, 3 H), 2,87 - 2,93 (m, 8 H), 2,13
(m, 2 H). EM [M 1] = 389.
Ejemplo 13
N-(1-metil-4-piperidil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 13). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 4-amino-1-metilpiperidina (21,6 pl, 0,17 mmol) de acuerdo con el método A para dar la N-(1-metil-4-piperidil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (32,4 mg,
0,084 mmol, rendimiento del 48,7 %) como un sólido naranja. RMN de 1H (400 MHz, CDCh): 5 ppm 11,55 (d, J = 8,34
Hz, 2 H), 9,12 (s, 1 H), 8,97 (dd, J = 7,33, 1,77 Hz, 1 H), 8,75 (dd, J = 6,82, 1,77 Hz, 1 H), 8,22 (s, 1 H), 8,13 (d, J =
8,84 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,68 - 7,72 (m, 1 H), 7,56 - 7,61 (m, 1 H), 6,92 (t, J = 7,07 Hz, 1 H), 4,19 (s ancho, 1 H), 2,96 (s ancho, 2 H), 2,43 (s, 3 H), 2,33 (s ancho, 2 H), 2,21 (d, J = 9,60 Hz, 2 H), 1,85 - 1,95 (m, 2 H). EM
[M 1] = 387.
Ejemplo 14
N-(azetidín-3-il)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 14). Se trató una solución del compuesto 15 (76 mg, 0,17 mmol) en cloroformo (1 ml) con el ácido trifluoroacético (1,5 ml, 19,6 mmol) a temperatura ambiente durante 24 h (por comodidad). Los solventes se eliminaron al vacío para dar el trifluoroacetato de N-(azetidín-3-il)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (76,1 mg, 0,17 mmol, 99 % de rendimiento) como un sólido amarillo. RMN de 1H (400 MHz, CDCh): 5 ppm 9,14 - 9,20 (m, 1 H), 9,10 (d, J = 5,81 Hz, 1 H), 8,67 - 8,74 (m, 1 H), 8,46 (s, 1 H), 8,20 - 8,27 (m, 1 H), 8,12 (s, 1 H), 7,92 (s, 1 H), 7,75 (d, J = 7,83 Hz, 1 H), 7,65 (d, J = 6,82 Hz, 1 H), 7,11 (t, J = 7,20 Hz, 1 H), 4,67 (dd, J = 7,07, 4,55 Hz, 1 H), 4,53 (d, J = 7,33 Hz, 2 H), 2,83 (s ancho, 3 H). EM [M 1] = 345.
Ejemplo 15
3- [(12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carbonil)amino]azetidina-1-carboxilato de tert-butilo (compuesto 15). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 1-Boc-3-(amino)azetidina (29,7 mg, 0,17 mmol) de acuerdo con el método A para dar el 3-[(12-oxo-12H-benzo[g]pirido[2,1-b]quinazolm-4-carbonil)amino]azetidina-1-carboxilato de terf-butilo (76 mg, 0,17 mmol, rendimiento del 99 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCla): 5 ppm 11,98 (s ancho, 1 H), 9,15 (s, 1 H), 9,00 (dd, J = 7,33, 1,77 Hz, 1 H), 8,73 (dd, J = 7,07, 1,77 Hz, 1 H), 8,25 (s, 1 H), 8,13 (dd, J = 17,56, 7,71 Hz, 2 H), 7,70 - 7,76 (m, 1 H), 7,58 - 7,64 (m, 1 H), 6,91 - 6,95 (m, 1 H), 4,90 (d, J = 6,32 Hz, 1 H), 4,46 - 4,53 (m, 2 H), 4,11 (s ancho, 2 H), 1,52 (s, 9 H). EM [M 1] = 445.
Ejemplo 16
4- (4-isopropilpiperazín-1-carbonil)-12H-benzo[g]pirido[2,1-b]quinazolín-12-ona (compuesto 16). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 1 -isopropilpiperazina (26,4 pl, 0,17 mmol) de acuerdo con el método A para dar la 4-(4-isopropilpiperazín-1-carbonil)-12H-benzo[g]pirido[2,1-b]quinazolín-12-ona (40,9 mg, 0,102 mmol, rendimiento del 59,4 %) como un sólido amarillo anaranjado. Rm N de 1H (400 MHz, CDCl3): 5 ppm 9,11 - 9,14 (m, 1 H), 8,79 - 8,82 (m, 1 H), 8,30 (s, 1 H), 8,10 - 8,15 (m, 1 H), 7,99 - 8,03 (m, 1 H), 7,62 - 7,68 (m, 1 H), 7,53 - 7,59 (m, 1 H), 7,45 (dd, J = 6,57, 1,52 Hz, 1 H), 6,73 - 6,79 (m, 1 H), 4,10 (m, 2 H), 3,87 (m, 2 H), 3,48 (m, 1 H), 3,36 (m, 1 H), 2.74 - 2,92 (m, 1 H), 2,68 (m, 1 H), 2,40 (m, 1 H), 1,10 (d, J = 6,57 Hz, 6 H). EM [M 1] = 401.
Ejemplo 17
N-metil-N-( 1 -metilpirrolidín-3-il)-12-oxo- 12H-benzo[g]pirido[2,1 -b]quinazolín-4-carboxamida (compuesto 17). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N,W-dimetil-3-aminopirrolidina (19,7 mg, 0,17 mmol) de acuerdo con el método A para dar el trifluoroacetato de N-metil-N-(1-metilpirrolidín-3-il)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (6 mg, 0,016 mmol, rendimiento del 9,0 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, MeOD): 5 ppm 9,11 (s, 1 H), 8,83 - 8,92 (m, 1 H), 8,24 - 8,33 (m, 1 H), 8,19 (d, J = 8,08 Hz, 1 H), 8,07 (d, J = 8,34 Hz, 1 H), 7,92 (s, 1 H), 7,55 - 7,74 (m, 3 H), 6,95 (q, J = 7,33 Hz, 1 H), 4,60 (d, J = 9,35 Hz, 1 H), 4,25 (d, J = 11,87 Hz, 1 H), 4,02 - 4,14 (m, 1 H), 3,47 - 3,62 (m, 1 H), 3,17 - 3,28 (m, 4 H), 3,07 (m, 3 H), 2,67 - 2,85 (m, 2 H). EM [M 1] = 387.
Ejemplo 18
4-[(3S)-3-(dimetilamino)pirrolidín-1-carbonil]-12H-benzo[g]pirido[2,1-b]quinazolín-12-ona (compuesto 18). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la (3S)-(-)-3-(dimetilamino)pirrolidina (19,7 mg, 0,17 mmol) de acuerdo con el método A para dar el hidrocloruro de 4-[(3S)-3-(dimetilamino)pirrolidín-1-carbonil]-12H-benzo[g]pirido[2,1-b]quinazolín-12-ona (34,1 mg, 0,088 mmol, rendimiento del 51,2 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCl3): 5 ppm 1,96 (s ancho, 2 H), 9,12 (s, 1 H), 8,82 (td, J = 6,63, 1,64 Hz, 1 H), 8,31 - 8,35 (m, 1 H), 8,12 (d, J = 8,59 Hz, 1 H), 8,03 (d, J = 8,08 Hz, 1 H), 7,62 - 7,68 (m, 1 H), 7,53 - 7,58 (m, 1 H), 6.74 - 6,80 (m, 1 H), 3,47 (m, 2 H), 2,91 (m, 2 H), 2,43 - 2,49 (m, 1 H), 2,39 (s, 3 H), 2,24 - 2,33 (m, 1 H), 2,20 (s, 3 H), 2.11 (m, 1 H). EM [M 1] = 387.
Ejemplo 19
4-[3-(dietilamino)pirrolidín-1-carbonil]-12H-benzo[g]pirido[2,1-b]quinazolín-12-ona (compuesto 19). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 3-(dietilamino)pirrolidina (24,5 mg, 0,17 mmol) de acuerdo con el método A para dar la 4-[3-(dietilamino)pirrolidín-1 -carbonil]-12H-benzo[g]pirido[2,1-b]quinazolín-12-ona (54,7 mg, 0,13 mmol, rendimiento del 76,6 %) como un sólido de color amarillo anaranjado. RMN de 1H (400 MHz, CDCl3): 5 ppm 9.12 (s, 1 H), 8,82 (dd, J = 7,58, 1,52 Hz, 1 H), 8,28 - 8,37 (m, 2 H), 8,12 (d, J = 8,59 Hz, 1 H), 7,65 - 7,74 (m, 2 H), 7,57 - 7,63 (m, 1 H), 6,97 - 7,02 (m, 1 H), 4,10 (m, 1 H), 3,97 (m, 1 H), 3,81 - 3,93 (m, 1 H), 3,63 (m 1 H), 3,38 (d, J = 7,33 Hz, 1 H), 3,14 (m, 1 H), 2,87 (m, 1 H), 2,33 (s ancho, 1 H), 2,26 (s ancho, 1 H), 1,33 - 1,38 (m, 1 H), 1,26 - 1,33 (m, 1 H), 1,14 (t, J = 7,07 Hz, 3 H), 1,01 (t, J = 7,07 Hz, 3 H). EM [M 1] = 415.
Ejemplo 20
N-[2-(dietilamino)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 20). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N',W-dietiletano-1,2-diamina (24,3 pl, 0,17 mmol) de acuerdo con el método A para dar la N-[2-(dietilamino)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (18,2 mg,
0,047 mmol, rendimiento del 27 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCI3): 5 ppm 11,56 -11,65 (m, 1 H), 9,12 (s, 1 H), 8,94 - 8,99 (m, 1 H), 8,75 (d, J = 7,07 Hz, 1 H), 8,41 (s, 1 H), 8,14 (d, J = 8,08 Hz, 1 H), 8,01 (d, J = 7,83 Hz, 1 H), 7,68 (t, J = 7,58 Hz, 1 H), 7,51 - 7,62 (m, 1 H), 6,91 (t, J = 7,07 Hz, 1 H), 3,77 (s ancho, 2 H), 2,83 (m, 6 H), 1,21 (t, J = 7,20 Hz, 6 H). EM [M 1] = 389.
Ejemplo 21
N-[2-(diisopropilamino)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 21). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N,N-diisopropiletilendiamina (29,9 gl, 0,17 mmol) de acuerdo con el método A para dar la N-[2-(diisopropilamino)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (33 mg, 0,079 mmol, 46 % de rendimiento) como un sólido naranja. RMN de 1H (400 MHz, DMSO-cfe): 5 ppm 11,07 (s ancho, 1 H), 9,11 (s, 1 H), 8,92 (d, J = 7,33 Hz, 1 H), 8,58 (d, J = 6,32 Hz, 1 H), 8,42 (s, 1 H), 8,31 (d, J = 7,83 Hz, 1 H), 8,09 (d, J = 7,83 Hz, 1 H), 7,73 (t, J = 7,07 Hz, 1 H), 7,57 - 7,66 (m, 1 H), 7,05 (t, J = 7,33 Hz, 1 H), 3,50 (d, J = 5,56 Hz, 2 H), 3,13 - 3,23 (m, 2 H), 2,66 - 2,75 (m, 2 H), 1,07 (d, J = 6,57 Hz, 12 H). RMN de 1H (400 MHz, CDCla): 5 ppm 11,33 (s ancho, 1 H), 9,12 (s, 1 H), 8,96 (d, J = 6,06 Hz, 1 H), 8,76 (d, J = 6,57 Hz, 1 H), 8,36 (s, 1 H), 8,13 (d, J = 8,08 Hz, 1 H), 8,01 (d, J = 9,09 Hz, 1 H), 7,63 - 7,72 (m, 1 H), 7,52 - 7,61 (m, 1 H), 6,90 (t, J = 7,07 Hz, 1 H), 3,66 (d, J = 5,56 Hz, 2 H), 3,22 (d, J = 6,57 Hz, 2 H), 2,81 (s ancho, 2 H), 1,14 (d, J = 6,32 Hz, 12 H). EM [M 1] = 417.
Ejemplo 22
12-oxo-N-(2-pirrolidín-1-iletil)-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 22). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 2-pirrolidín-1-iletanamina (21,8 gl, 0,17 mmol) de acuerdo con el método A para dar la 12-oxo-N-(2-pirrolidín-1-iletil)-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (32,4 mg, 0,084 mmol, 48,7 % de rendimiento) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCl3): 5 ppm 11,65 (s ancho, 1 H), 9,11 (s, 1 H), 8,96 (dd, J = 7,20, 1,64 Hz, 1 H), 8,71 - 8,77 (m, 1 H), 8,37 (s, 1 H), 8,13 (d, J = 8,34 Hz, 1 H), 8,02 (d, J = 7,83 Hz, 1 H), 7,64 - 7,72 (m, 1 H), 7,54 - 7,63 (m, 1 H), 6,87 - 6,94 (m, 1 H), 3,79 - 3,88 (m, 2 H), 2,96 - 3,03 (m, 2 H), 2,89 (m, 2 H), 2,78 (m, 2 H), 2,00 (m, 4 H). EM [M 1] = 387.
Ejemplo 23
12-oxo-N-[2-(1-piperidil)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 23). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 1-(2-aminoetil)piperidina (24,6 gl, 0,17 mmol) de acuerdo con el método A para dar la 12-oxo-N-[2-(1-piperidil)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (25 mg, 0,062 mmol, rendimiento del 36,2 %) como un sólido naranja. RMN de 1H (400 MHz, CDCl3): 5 ppm 11,48 (s ancho, 1 H), 9.12 (s, 1 H), 8,96 (dd, J = 7,33, 1,77 Hz, 1 H), 8,74 (dd, J = 6,95, 1,64 Hz, 1 H), 8,44 (s, 1 H), 8,13 (d, J = 8,34 Hz, 1 H), 8,00 (d, J = 8,34 Hz, 1 H), 7,68 (dd, J = 8,08, 7,07 Hz, 1 H), 7,53 - 7,61 (m, 1 H), 6,90 (t, J = 7,07 Hz, 1 H), 3,75 (q, J = 5,81 Hz, 2 H), 2,73 (t, J = 6,19 Hz, 2 H), 2,61 (s ancho, 4 H), 1,78 (dt, J = 11,24, 5,75 Hz, 4 H), 1,54 - 1,59 (m, 2 H). EM [M 1] = 401.
Ejemplo 24
N-(2-morfolinoetil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 24). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N-(2-aminoetil)morfolina (22,6 gl, 0,17 mmol) de acuerdo con el método A para dar la N-(2-morfolinoetil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (28,7 mg, 0,071 mmol, rendimiento del 41,4 %) como un sólido naranja. RMN de 1H (400 MHz, DMSO-d6): 5 ppm 11,50 (s ancho, 1 H), 9.12 (s, 1 H), 8,96 (dd, J = 7,33, 1,77 Hz, 1 H), 8,75 (dd, J = 6,82, 1,77 Hz, 1 H), 8,38 (s, 1 H), 8,13 (d, J = 8,59 Hz, 1 H), 8,00 (d, J = 8,34 Hz, 1 H), 7,64 - 7,73 (m, 1 H), 7,54 - 7,62 (m, 1 H), 6,90 (t, J = 7,07 Hz, 1 H), 3,88 - 3,97 (m, 4 H), 3,77 (q, J = 5,89 Hz, 2 H), 2,78 (t, J = 6,19 Hz, 2 H), 2,68 (s ancho, 4 H). EM [M 1] = 403.
Ejemplo 25
N-[2-(4-metilpiperazín-1-il)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 25). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 2-(4-metilpiperazín-1-il)etanamina (27,6 gl, 0,17 mmol) de acuerdo con el método A para dar la N-[2-(4-metilpiperazín-1-il)etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (11,7 mg, 0,028 mmol, rendimiento del 16,3 %) en forma de un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCla): 5 ppm 11,46 (s ancho, 1 H), 9,14 (s, 1 H), 8,98 (dd, J = 7,33, 1,77 Hz, 1 H), 8,76 (dd, J = 6,82, 1,77 Hz, 1 H), 8,43 (s, 1 H), 8,16 (d, J = 8,59 Hz, 1 H), 8,08 (d, J = 8,34 Hz, 1 H), 7,65 - 7,73 (m, 1 H), 7,60 (dd, J = 6,82, 1,26 Hz, 1 H), 6,92 (t, J = 7,07 Hz, 1 H), 3,74 - 3,83 (m, 2 H), 2,60 - 2,88 (m, 10 H), 2,38 (s, 3 H). EM [M 1] = 416.
Ejemplo 26
N-[2-[2-metoxietil(metil)amino]etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 26). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la W-(2-metoxietil)-W-metiletano-1,2-diamina (27,3 mg, 0,21 mmol) de acuerdo con el método A para dar el trifluoroacetato de N-[2-[2-metoxietil(metil)amino]etil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (15 mg, 0,037 mmol, rendimiento del 21,5 %) como una goma de naranja. RMN de 1H (400 MHz, CDCh): 5 ppm 11,79 (s ancho, 1 H), 9,10 (s, 2 H), 9,00 (dd, J = 7,33, 1,52 Hz, 1 H), 8,68 - 8,73 (m, 1 H), 8,43 (s, 1 H), 8,10 (dd, J = 13,64, 8,34 Hz, 3 H), 7,70 (t, J = 7,58 Hz, 2 H), 7,56 - 7,62 (m, 2 H), 6,94 (t, J = 7,20 Hz, 1 H), 4,07 (s ancho, 2 H), 3,80 (t, J = 4,55 Hz, 2 H), 3,68 (s ancho, 1 H), 3,55 (s ancho, 2 H), 3,36
- 3,41 (m, 4 H), 3,07 (s, 3 H). RMN de 19F (376 MHz, CDCI3): 5 ppm -170,87 (s ancho, 3 F). EM [M 1] = 405.
Ejemplo 27
N-[2-(dimetilamino)-1 -metiletil]- 12-oxo- 12H-benzo[g]pirido[2,1 -b]quinazolín-4-carboxamida (compuesto 27). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la N1,N1-dimetiIpropano-1,2-diamina (22,2 gl, 0,17 mmol) de acuerdo con el método A para dar el hidrocloruro de N-[2-(dimetilamino)-1 -metiletil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (38,7 mg, 0,103 mmol, rendimiento del 60 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCla): 5 ppm 9,12 (s, 1 H), 8,82 (td, J = 6,63, 1,64 Hz, 1 H), 8,31 - 8,35 (m, 1 H), 8,12 (d, J = 8,59 Hz, 1 H), 8,03 (d, J = 8,08 Hz, 1 H), 7,62 - 7,68 (m, 1 H), 7,53 - 7,58 (m, 1 H), 6,74 - 6,80 (m, 1 H), 3,47 (s ancho, 1 H), 2,91 (s ancho, 1 H), 2,43 - 2,49 (m, 1 H), 2,39 (s, 3 H), 2,20 (s, 3 H), 1,96 (s ancho, 3 H). EM [M 1] = 375.
Ejemplo 28
N-[2-(dimetilamino)propil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 28). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y de la 2-(dimetilamino)propán-1-amina (21,1 mg, 0,21 mmol) de acuerdo con el método A para dar la N-[2-(dimetilamino)propil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (52 mg, 0,139 mmol, 80,6 % de rendimiento) como un sólido amarillo. RMN de 1H (400 MHz, CDCl3): 5 ppm 11,70 (s ancho, 1 H), 9,09 (s, 1 H), 8,94 (dd, J = 7,33, 1,77 Hz, 1 H), 8,73 (dd, J = 6,82, 1,77 Hz, 1 H), 8,27 (s, 1 H), 8,12 (d, J = 8,59 Hz, 1 H), 7,99 (d, J = 8,59 Hz, 1 H), 7,66 (dd, J = 7,96, 6,95 Hz, 1 H), 7,53 - 7,58 (m, 1 H), 6,89 (t, J = 7,07 Hz, 1 H), 3,77 (dt, J = 14,02, 5,62 Hz, 1 H), 3,40 - 3,48 (m, 1 H), 2,95 - 3,05 (m, 1 H), 2,51 (s, 6 H), 1,15 (d, J = 6,32 Hz, 3 H). EM [M 1] = 375.
Ejemplo 29
N-(1-metilazetidín-3-il)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 29). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y del dihidrocloruro de 1-metilazetidín-3-amina (28,4 gl, 0,26 mmol) de acuerdo con el método A para dar el producto bruto, que se purificó mediante cromatografía de fase normal automatizada (MeOH del 0 al 20 %/DCM, cartucho de gel de sílice de 4 g) para dar la N-(1-metilazetidín-3-il)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (32,8 mg, 0,092 mmol, rendimiento del 53,1 %) como un cristal rojo anaranjado. RMN de 1H (400 MHz, DMSO-ds ): 5 ppm 11,45 (d, J = 6,57 Hz, 1 H), 9,11 (s, 1 H), 8,93 (dd, J = 7,33, 1.77 Hz, 1 H), 8,50 (dd, J = 6,82, 1,77 Hz, 1 H), 8,42 (s, 1 H), 8,31 (d, J = 8,59 Hz, 1 H), 8,20 (d, J = 8,59 Hz, 1 H), 7,71 - 7,76 (m, 1 H), 7,59 - 7,64 (m, 1 H), 7,05 (t, J = 7,07 Hz, 1 H), 4,54 - 4,63 (m, 1 H), 3,84 (t, J = 7,83 Hz, 2 H), 3,35 - 3,38 (m, 2 H), 2,47 (s, 3 H). EM [M 1] = 359.
Ejemplo 30
N-(2-amino-2-metilpropil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 30). Este compuesto se sintetizó a partir de 3a (100 mg, 0,34 mmol) y de la 2-metilpropano-1,2-diamina (106 gl, 1,03 mmol) de acuerdo con el método A para dar la N-(2-amino-2-metilpropil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (110 mg, 0,31 mmol, rendimiento del 88,6 %) como un sólido naranja. RMN de 1H (400 MHz, DMSO-d6): 5 ppm 11,38 (t, J = 5,31 Hz, 1 H), 9,12 (s, 1 H), 8,92 (dd, J = 7,33, 1,77 Hz, 1 H), 8,54 (dd, J = 6,95, 1,64 Hz, 1 H), 8,38 (s, 1 H), 8,31 (d, J = 8,34 Hz, 1 H), 8,13 (d, J = 8,59 Hz, 1 H), 7,73 (dd, J = 8,34, 6,82 Hz, 1 H), 7,58 - 7,63 (m, 1 H), 7,06 (t, J = 7,07 Hz, 1 H), 3,34 - 3,40 (m, 2 H), 2,69 (s, 2 H), 1,21 (s, 6 H). MS [M 1] = 361.
Ejemplo 31
Método B: Bismetilación de amina primaria. N-[2-(dimetilamino)-2-metilpropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 31). A una solución del compuesto 30 (77 mg, 0,21 mmol) en MeCN (1,5 ml) y ortoformiato de trimetilo (0,50 ml) se le añadió formaldehído (128 gl, 2,14 mmol), cianoborohidruro de sodio (85 mg, 2,14 mmol) y una gota de ácido acético glacial. El contenido se agitó a temperatura ambiente durante 4 h, luego se trató con NaOH a 1 M, se recogió en EtOAc, se lavó con Na2CO3 al 10 % (3x), salmuera, se secó sobre MgSO4, se filtró y se eliminó el solvente al vacío para dar un residuo naranja. Este material se purificó mediante cromatografía de fase normal automatizada (MeOH del 0 al 20 %/DCM, cartucho de gel de sílice de 4 g) para dar la N-[2-(dimetilamino)-2-metilpropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (45 mg, 0,12 mmol, 54 % de rendimiento) como un sólido naranja. RMN de 1H (400 MHz, CDCl3): 5 ppm 11,87 (s ancho, 1 H), 9,11 (s, 1 H), 8,95 (dd, J = 7,33, 1.77 Hz, 1 H), 8,73 (dd, J = 7,07, 1,77 Hz, 1 H), 8,29 (s, 1 H), 8,13 (d, J = 8,34 Hz, 1 H), 8,00 (d, J = 8,34 Hz, 1 H), 7,67 (ddd, J = 8,27, 6,88, 1,26 Hz, 1 H), 7,56 (ddd, J = 8,21,6,82, 1,14 Hz, 1 H), 6,90 (t, J = 7,07 Hz, 1 H), 3,63 (d, J = 4,80 Hz, 2 H), 2,56 (s, 6 H), 1,28 (s, 6 H). EM [M 1] = 389.
Ejemplo 32
N-(2-aminopropil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 32). Este compuesto se sintetizó a partir de 3a (100 mg, 0,17 mmol) y del 1,2-diaminopropano (88 gl, 1,03 mmol) de acuerdo con el método A para dar un producto bruto, que se purificó mediante cromatografía de fase normal automatizada (MeOH del 0 al 20 %/DCM, cartucho de gel de sílice de 4 g) para dar la N-(2-aminopropil)-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (23,9 mg, 0,069 mmol, 20 % de rendimiento) como un sólido naranja. RMN de 1H (400 MHz, DMSO-ds ): 5 ppm 11,27 (s ancho, 1 H), 9,11 (s, 1 H), 8,92 (dd, J = 7,20, 1,64 Hz, 1 H), 8,52 (dd, J = 6,82, 1,77 Hz, 1 H), 8,43
(s, 1 H), 8,31 (d, J = 8,59 Hz, 1 H), 8,14 (d, J = 8,59 Hz, 1 H), 7,73 (t, J = 7,71 Hz, 1 H), 7,58 - 7,63 (m, 1 H), 7,06 (t, J = 7,07 Hz, 1 H), 3,42 - 3,51 (m, 1 H), 3,35 - 3,39 (m, 1 H), 3,20 (dd, J = 12,51, 5,94 Hz, 1 H), 1,19 (d, J = 6,57 Hz, 3 H). EM [M 1] = 347.
Ejemplo 33
N-[(2R)-2-aminopropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 33). Este compuesto se sintetizó a partir de 3a (100 mg, 0,17 mmol) y del dihidrocloruro de (2R)-propán-1,2-diamina (152 mg, 1,03 mmol) de acuerdo con el método A para dar el producto bruto, que se purificó mediante una cromatografía de fase normal automática (MeOH del 0 al 30 %/DCM, cartucho de gel de sílice de 4 g) para dar la N-[(2R)-2-aminopropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (42,2 mg, 0,122 mmol, 35 % de rendimiento) como un sólido amarillo anaranjado. Rm N de 1H (400 MHz, CDCto): 5 ppm 11,57 (s ancho, 1 H), 9,12 (s, 1 H), 8,97 (dd, J = 7,20, 1,64 Hz, 1 H), 8,75 (dd, J = 6,82, 1,52 Hz, 1 H), 8,28 (s, 1 H), 8,12 (d, J = 8,08 Hz, 1 H), 8,03 (d, J = 8,59 Hz, 1 H), 7,67 (dd, J = 8,21, 6,95 Hz, 1 H), 7,54 - 7,60 (m, 1 H), 6,91 (t, J = 7,07 Hz, 1 H), 3,71 (dt, J = 13,14, 5,31 Hz, 1 H), 3,33 - 3,48 (m, 2 H) 1,31 (d, J = 6,32 Hz, 3 H). EM [M 1] = 347.
Ejemplo 34
N-[(2R)-2-(dimetilamino)propil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 34). Este compuesto se sintetizó a partir del compuesto 33 (35 mg, 0,10 mmol) de acuerdo con el método B para dar el producto bruto, que se purificó por cromatografía automatizada de fase normal (MeOH del 0 al 20 %/DCM, cartucho de gel de sílice de 4 g) para dar la N-[(2R)-2-aminopropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (22,3 mg, 0,060 mmol, 59 % de rendimiento) como un sólido amarillo anaranjado. Rm N de 1H (400 MHz, CDCh): 5 ppm 11,73 (s ancho, 1 H), 9,11 (s, 1 H), 8,95 (dd, J = 7,33, 1,77 Hz, 1 H), 8,73 (dd, J = 7,07, 1,77 Hz, 1 H), 8,29 (s, 1 H), 8,12 (d, J = 8,34 Hz, 1 H), 8,01 (d, J = 8,08 Hz, 1 H), 7,67 (ddd, J = 8,34, 6,82, 1,26 Hz, 1 H), 7,56 (ddd, J = 8,27, 6,88, 1,26 Hz, 1 H), 6,89 (t, J = 7,07 Hz, 1 H), 3,74 - 3,81 (m, 1 H), 3,47 (ddd, J = 14,08, 8,78, 3,41 Hz, 1 H), 3,00 - 3,08 (m, 1 H), 2,53 (s, 6 H), 1,17 (d, J = 6,57 Hz, 3 H). EM [M 1] = 375.
Ejemplo 35
N-[(2S)-2-aminopropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 35). Este compuesto se sintetizó a partir de 3a (100 mg, 0,17 mmol) y el dihidrocloruro de (2R)-propano-1,2-diamina (152 mg, 1,03 mmol) de acuerdo con el método A para dar un producto bruto, que se purificó mediante cromatografía automática de fase normal (MeOH del 0 al 30 %/DCM, cartucho de gel de sílice de 4 g) para dar la N-[(2S)-2-aminopropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (33,1 mg, 0,096 mmol, rendimiento del 28 %) como un sólido de color amarillo anaranjado. RMN de 1H (400 MHz, CDCl3): 5 ppm 11,57 (s ancho, 1 H), 9,12 (s, 1 H), 8,97 (dd, J = 7,33, 1,77 Hz, 1 H), 8,75 (dd, J = 6,82, 1,77 Hz, 1 H), 8,28 (s, 1 H), 8,13 (d, J = 8,08 Hz, 1 H), 8,03 (d, J = 8,34 Hz, 1 H), 7,67 (ddd, J = 8,27, 6,88, 1,26 Hz, 1 H), 7,54 - 7,59 (m, 1 H), 6,91 (t, J = 7,20 Hz, 1 H), 3,71 (ddd, J = 13,07, 5,87, 4,55 Hz, 1 H), 3,33 - 3,51 (m, 2 H), 1,31 (d, J = 6,32 Hz, 3 H). EM [M 1] = 347.
Ejemplo 36
N-[(2S)-2-(dimetilamino)propil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 36). Este compuesto se sintetizó a partir del compuesto 35 (26,5 mg, 0,080 mmol) de acuerdo con el método B para dar el producto bruto, que se purificó por cromatografía de fase normal automatizada (MeOH del 0 al 20 %/DCM, cartucho de gel de sílice de 4 g) para dar la N-[(2S)-2-aminopropil]-12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (19 mg, 0,051 mmol, rendimiento del 66 %) como un sólido amarillo anaranjado. RMN de 1H (400 MHz, CDCh): 5 ppm 11,71 (s ancho, 1 H), 9,11 (s, 1 H), 8,94 (dd, J = 7,33, 1,77 Hz, 1 H), 8,73 (dd, J = 7,07, 1,77 Hz, 1 H), 8,28 (s, 1 H), 8,12 (d, J = 8,08 Hz, 1 H), 8,00 (d, J = 8,08 Hz, 1 H), 7,67 (ddd, J = 8,27, 6,88, 1,26 Hz, 1 H), 7,56 (ddd, J = 8,21,6,82, 1,14 Hz, 1 H), 6,89 (t, J = 7,07 Hz, 1 H), 3,77 (ddd, J = 14,02, 6,06, 5,18 Hz, 1 H), 3,45 (ddd, J = 13,96, 8,91,3,41 Hz, 1 H), 2,97 - 3,06 (m, 1 H), 2,52 (s, 6 H), 1,16 (d, J = 6,57 Hz, 3 H). EM [M 1] = 375.
Ejemplo 37
12-oxo-N-[2-(4-piridil)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (compuesto 37). Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y la 4-(2-aminoetil)piridina (20,8 pl, 0,17 mmol) de acuerdo con el método A para dar la 12-oxo-N-[2-(4-piridil)etil]-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxamida (43,5 mg, 0,11 mmol, rendimiento del 64 %) como un sólido naranja. RMN de 1H (400 MHz, CDCh): 5 ppm 11,42 (s ancho, 1 H), 9,09 (s, 1 H), 8,97 (dd, J = 7,33, 1,77 Hz, 1 H), 8,76 (dd, J = 7,07, 1,77 Hz, 1 H), 8,62 - 8,67 (m, 2 H), 8,09 (dd, J = 17,81, 8,46 Hz, 2 H), 7,66 - 7,74 (m, 1 H), 7,54 - 7,62 (m, 1 H), 7,48 (s, 1 H), 7,37 (d, J = 6,06 Hz, 2 H), 6,92 (t, J = 7,07 Hz, 1 H), 3,97 - 4,08 (m, 2 H), 3,05 - 3,15 (m, 2 H). EM [M 1] = 395.
Ejemplo 38
12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxilato de 2-(dimetilamino)etilo. Este compuesto se sintetizó a partir de 3a (50 mg, 0,17 mmol) y del 2-dimetilaminoetanol (41,6 pl, 0,41 mmol) de acuerdo con el método A para dar el 12-oxo-12H-benzo[g]pirido[2,1-b]quinazolín-4-carboxilato de 2-(dimetilamino)etilo (47 mg, 0,13 mmol, rendimiento del 47,2 %) como un sólido naranja. RMN de 1H (400 MHz, CDCh): 5 ppm 9,10 (s, 1 H), 8,87 (dd, J = 7,45, 1,64 Hz, 1 H),
8,36 (s, 1 H), 8,11 (d, J = 8,34 Hz, 1 H), 8,02 (d, J = 8,34 Hz, 1 H), 7,78 (dd, J = 6,69, 1,64 Hz, 1 H), 7,64 (ddd, J = 8,27, 6,76, 1,14 Hz, 1 H), 7,52 - 7,57 (m, 1 H), 6,72 (dd, J = 7,33, 6,57 Hz, 1 H), 4,58 (t, J = 5,81 Hz, 2 H), 2,80 (t, J = 5,68 Hz, 2 H), 2,38 (s, 6 H). EM [M 1] = 362.
Como indican los datos en la presente memoria, se encontró que una amplia variedad de compuestos de fórmula I eran eficaces a baja concentración. El valor de la CI50 para los compuestos de ejemplo de fórmula I (véase más arriba para el nombre y la estructura de los compuestos) se da a conocer en la tabla 1 que viene a continuación.
TABLA 1: Compuestos y su eficacia
El uso de los términos "un" y "una", "la" y "el", y referencias similares en el contexto de la descripción de la invención (sobre todo en el contexto de las reivindicaciones que vienen a continuación) debe interpretarse que cubre tanto el singular como el plural, a menos que se indique lo contrario en la presente memoria o se contradiga con claridad con el contexto. Los términos "que comprende", "que tiene", "que incluye" y "que contiene" se deben interpretar como términos abiertos (es decir, que significan "que incluye, pero no se limita a") a menos que se indique lo contrario. La mención explícita de márgenes de valores en la presente memoria está destinada simplemente a servir de método abreviado para referirse por separado a cada valor independiente que se encuentre dentro del margen, a menos que se indique lo contrario en la presente memoria, y cada uno de los valores se incorpora en la especificación como si se hiciera mención explicita a cada uno de ellos en la presente memoria. Todos los métodos descritos en la presente memoria se pueden realizar en cualquier orden adecuado, a menos que se indique lo contrario en la presente memoria o que el contexto lo contradiga con claridad. El uso de todos y cada uno de los ejemplos, o lenguaje ejemplar (por ejemplo, "tal como") que se da a conocer en la presente memoria, está destinado simplemente a iluminar mejor la invención y no supone una limitación en el alcance de la invención a menos que se reivindique lo contrario. Ningún lenguaje en la especificación debe interpretarse en el sentido de que indica algún elemento no reivindicado como esencial para la puesta en práctica de la invención.
Las realizaciones preferidas de esta invención se describen en la presente memoria, incluido el mejor modo conocido por los inventores para llevar a cabo la invención. Las variaciones de esas realizaciones preferidas pueden resultar evidentes para los expertos en la técnica tras la lectura de la descripción anterior. Los inventores esperan que los expertos en la técnica empleen tales variaciones según sea apropiado, y los inventores pretenden que la invención se lleve a la práctica de una manera diferente a la descrita específicamente en la presente memoria. Además, la invención abarca cualquier combinación de los elementos descritos más arriba en todas las posibles variaciones de los mismos, a menos que se indique lo contrario en la presente memoria o que el contexto lo contradiga con claridad.
Claims (7)
2. Una composición farmacéutica que comprende un compuesto de acuerdo con la reivindicación 1 y un vehículo farmacéuticamente aceptable.
3. Una composición farmacéutica que comprende un compuesto de acuerdo con la reivindicación 1, y un vehículo farmacéuticamente aceptable, para ser usada en el tratamiento de una enfermedad hipe rprolife rativa en un sujeto.
4. La composición farmacéutica para ser usada según la reivindicación 3, en la que la enfermedad hiperproliferativa es cáncer.
5. La composición farmacéutica para ser usada de acuerdo con la reivindicación 4, que además comprende al menos otro agente biológicamente activo.
6. La composición farmacéutica para ser usada de acuerdo con la reivindicación 3 o 4, en la que la composición farmacéutica modula la actividad de la ARN Pol I en una célula, o población de células, de mamífero.
7. Una composición farmacéutica que comprende un compuesto de acuerdo con la reivindicación 1, y un vehículo farmacéuticamente aceptable, para ser usada como medicamento.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201461968079P | 2014-03-20 | 2014-03-20 | |
| US201462062197P | 2014-10-10 | 2014-10-10 | |
| PCT/US2015/021699 WO2015143293A1 (en) | 2014-03-20 | 2015-03-20 | Compounds which inhibit rna polymerase, compositions including such compounds, and their use |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2833459T3 true ES2833459T3 (es) | 2021-06-15 |
Family
ID=54145373
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15765295T Active ES2833459T3 (es) | 2014-03-20 | 2015-03-20 | Compuestos que inhiben la ARN polimerasa, composiciones que incluyen dichos compuestos y su uso |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US11001581B2 (es) |
| EP (2) | EP3778600A1 (es) |
| CA (1) | CA2943022C (es) |
| ES (1) | ES2833459T3 (es) |
| WO (1) | WO2015143293A1 (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3037928A1 (en) | 2016-09-23 | 2018-03-29 | The Johns Hopkins University | Combinatory treatment strategies of cancer based on rna polymerase i inhibition |
| CA3066009A1 (en) * | 2017-06-01 | 2018-12-06 | Oncostellae, S.L. | Pyridoquinazoline derivatives useful as protein kinase inhibitors |
| ES2692433A1 (es) * | 2017-06-01 | 2018-12-03 | Oncostellae, S.L. | Derivados de ácidos carboxílicos como inhibidores de proteinas quinasa |
| CA3073877A1 (en) | 2017-08-24 | 2019-02-28 | The Johns Hopkins University | Materials and methods for assessing cancer risk and treating cancer |
| ES2968796T3 (es) * | 2019-05-31 | 2024-05-14 | Ideaya Biosciences Inc | Derivados de tiadiazolilo como inhibidores de la ADN polimerasa theta |
| EP4214208A4 (en) * | 2020-09-15 | 2024-10-16 | The Johns Hopkins University | Compounds which inhibit rna polymerase |
| US20230265091A1 (en) * | 2020-09-15 | 2023-08-24 | The Johns Hopkins University | Compounds which inhibit rna polymerase |
| WO2022060799A1 (en) * | 2020-09-15 | 2022-03-24 | The Johns Hopkins University | Compounds which inhibit rna polymerase and their use |
| CN113717922B (zh) * | 2021-09-13 | 2022-10-25 | 上海欧易生物医学科技有限公司 | 一种适用于拟南芥叶片组织原生质体分离的含转录抑制剂的试剂盒及其应用 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US896688A (en) * | 1905-08-16 | 1908-08-18 | Josiah Cratty | Safety-razor. |
| US4450150A (en) | 1973-05-17 | 1984-05-22 | Arthur D. Little, Inc. | Biodegradable, implantable drug delivery depots, and method for preparing and using the same |
| US5908840A (en) | 1996-11-26 | 1999-06-01 | American Cyanamid Company | Hetero-biaryl-pyridoquinazolinone derivatives as anti-cancer agents |
| WO2008155441A1 (en) | 2007-06-20 | 2008-12-24 | Marikki Laiho | Activators and therapeutic applications thereof |
| JP2011507910A (ja) | 2007-12-21 | 2011-03-10 | ユニバーシティー オブ ロチェスター | 真核生物の寿命を変更するための方法 |
| CA3037928A1 (en) * | 2016-09-23 | 2018-03-29 | The Johns Hopkins University | Combinatory treatment strategies of cancer based on rna polymerase i inhibition |
| WO2022060799A1 (en) * | 2020-09-15 | 2022-03-24 | The Johns Hopkins University | Compounds which inhibit rna polymerase and their use |
-
2015
- 2015-03-20 ES ES15765295T patent/ES2833459T3/es active Active
- 2015-03-20 EP EP20196005.1A patent/EP3778600A1/en not_active Withdrawn
- 2015-03-20 WO PCT/US2015/021699 patent/WO2015143293A1/en not_active Ceased
- 2015-03-20 CA CA2943022A patent/CA2943022C/en active Active
- 2015-03-20 US US15/126,588 patent/US11001581B2/en active Active
- 2015-03-20 EP EP15765295.9A patent/EP3119781B1/en active Active
-
2021
- 2021-03-08 US US17/195,149 patent/US20210261542A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CA2943022A1 (en) | 2015-09-24 |
| US20170081322A1 (en) | 2017-03-23 |
| EP3119781A1 (en) | 2017-01-25 |
| EP3119781A4 (en) | 2017-08-16 |
| US11001581B2 (en) | 2021-05-11 |
| US20210261542A1 (en) | 2021-08-26 |
| CA2943022C (en) | 2024-01-16 |
| EP3778600A1 (en) | 2021-02-17 |
| EP3119781B1 (en) | 2020-09-16 |
| WO2015143293A1 (en) | 2015-09-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2833459T3 (es) | Compuestos que inhiben la ARN polimerasa, composiciones que incluyen dichos compuestos y su uso | |
| JP7447002B2 (ja) | SHP2のオクタヒドロシクロペンタ[c]ピロールのアロステリック阻害剤 | |
| ES3036496T3 (en) | Fused tricyclic ring derivatives as src homology-2 phosphatase inhibitors | |
| US10774065B2 (en) | 1-pyridazin-/triazin-3-yl-piper(-azine)/idine/pyrolidine derivatives and compositions thereof for inhibiting the activity of SHP2 | |
| ES2699354T3 (es) | Derivados de 1-(triazin-3-il/piridazin-3-il)-piper(-azin)idina y composiciones de las mismas para inhibir la actividad de SHP2 | |
| JP5886411B2 (ja) | 新規のピリミジン誘導体 | |
| EA031573B1 (ru) | N-азаспироциклоалканзамещенные n-гетероарильные соединения и композиции для ингибирования активности shp2 | |
| US20140309192A1 (en) | Modulators of the g protein-coupled mas receptor and the treatment of disorders related thereto | |
| CN107660202B (zh) | 水溶性前药 | |
| JP2009513703A5 (es) | ||
| JP2015533782A (ja) | スルファモイル−アリールアミド及びb型肝炎の治療のための薬剤としてのその使用 | |
| CA3083228A1 (en) | Small molecule degraders that recruit dcaft15 | |
| ES3002745T3 (en) | Multifunctional inhibitors of mek/pi3k and mtor/mek/pi3k biological pathways and therapeutic methods using the same | |
| WO2019012172A1 (es) | Nuevos derivados heteroaryl amida como inhibidores selectivos de histona deacetilasa 1 y 2 (hdac1/2) | |
| ES2374449T3 (es) | Compuestos de imidazol sustituidos como inhibidores de ksp. | |
| JP2010512355A (ja) | 癌の処置のためのジフェニルオキシ−インドール−2−オン化合物のプロドラッグ | |
| CA2891900A1 (en) | Derivatives of indole for the treatment of cancer, viral infections and lung diseases | |
| KR20130118731A (ko) | 항증식성 질환 치료에 사용하기 위한 pi3k 억제제로서 피페라지노트리아진 | |
| CN106459011B (zh) | 作为抗肿瘤化合物的σ-2受体配体药物缀合物、其合成方法及其用途 | |
| JP2010535204A5 (es) | ||
| CN1839129A (zh) | 新的n-取代吲哚基-3-乙醛酰胺,其作为药物的用途及其制备方法 | |
| EA040967B1 (ru) | 1,2,4-оксадиазольные и тиадиазольные соединения в качестве иммуномодуляторов |