ES2851499T3 - Proceso para fabricar una forma cristalina de gefitinib - Google Patents
Proceso para fabricar una forma cristalina de gefitinib Download PDFInfo
- Publication number
- ES2851499T3 ES2851499T3 ES16820268T ES16820268T ES2851499T3 ES 2851499 T3 ES2851499 T3 ES 2851499T3 ES 16820268 T ES16820268 T ES 16820268T ES 16820268 T ES16820268 T ES 16820268T ES 2851499 T3 ES2851499 T3 ES 2851499T3
- Authority
- ES
- Spain
- Prior art keywords
- gefitinib
- vol
- water
- theta
- degrees
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 title claims abstract description 60
- 239000005411 L01XE02 - Gefitinib Substances 0.000 title claims abstract description 46
- 229960002584 gefitinib Drugs 0.000 title claims abstract description 46
- 238000000034 method Methods 0.000 title claims abstract description 31
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims abstract description 28
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 claims abstract description 17
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 16
- 238000004519 manufacturing process Methods 0.000 claims abstract description 7
- 239000011877 solvent mixture Substances 0.000 claims abstract description 7
- 239000000843 powder Substances 0.000 claims abstract description 6
- 230000005855 radiation Effects 0.000 claims abstract description 3
- 238000000634 powder X-ray diffraction Methods 0.000 claims abstract 2
- 239000000203 mixture Substances 0.000 claims description 13
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 description 15
- 238000003756 stirring Methods 0.000 description 7
- 239000002904 solvent Substances 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 4
- 239000013078 crystal Substances 0.000 description 3
- 102000001301 EGF receptor Human genes 0.000 description 2
- 108060006698 EGF receptor Proteins 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- 230000001394 metastastic effect Effects 0.000 description 2
- 206010061289 metastatic neoplasm Diseases 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 229940002501 gefitinib 250 mg Drugs 0.000 description 1
- 229940084651 iressa Drugs 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 150000004682 monohydrates Chemical class 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 150000004684 trihydrates Chemical class 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
- C07D239/72—Quinazolines; Hydrogenated quinazolines
- C07D239/86—Quinazolines; Hydrogenated quinazolines with hetero atoms directly attached in position 4
- C07D239/94—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Un proceso para fabricar la Forma 1 cristalina de gefitinib de fórmula (1), **(Ver fórmula)** caracterizada por un patrón de difracción de polvo XRPD que comprende los máximos en aproximadamente 7,14, 11,26, 14,25, 15,86, 24,33 y 26,40 grados 2 theta (± 0,2 grados 2 theta), cuando se mide con radiación CuKα1 (λ = 1,54060 Å), comprendiendo el proceso las etapas: 1. Disolver gefitinib en una mezcla de disolventes que comprende agua y un alcohol seleccionado de etanol y butanol, en donde la relación entre agua y alcohol está entre 1:16 y 1:25 (vol:vol); 2. Aislar la forma 1 de gefitinib.
Description
DESCRIPCIÓN
Proceso para fabricar una forma cristalina de gefitinib
Antecedentes de la invención
La presente invención se refiere a un proceso mejorado para fabricar la Forma 1 cristalina de gefitinib.
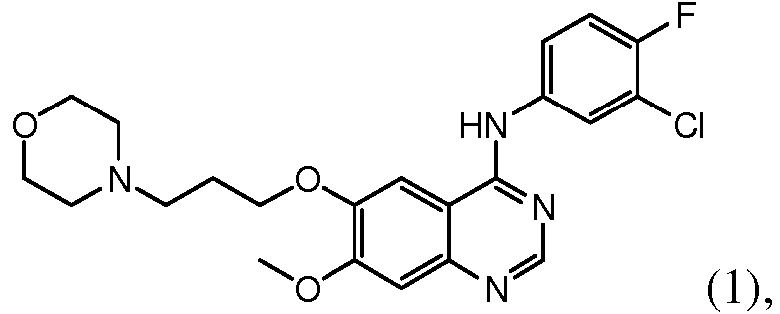
Gefitinib, químicamente 4-(3-cloro-4-fluorofenilamino)-7-metoxi-6-[3-(4-morfolinil)propoxi]quinazolina) de fórmula (1),
es un compuesto farmacéuticamente activo que actúa como un inhibidor selectivo de la tirosina quinasa del receptor del factor de crecimiento epidérmico (EGFR). Gefitinib se usa como un medicamento para el tratamiento de, por ejemplo, cáncer de pulmón no microcítico (NSCLC) localmente avanzado o metastásico, y está disponible, por ejemplo, bajo la marca Iressa®, como comprimidos de gefitinib de 250 mg para administración oral.
Gefitinib se desveló genéricamente en el documento EP566226. Específicamente, gefitinib y sus sales se desvelaron en el documento EP 823900, mientras que diferentes formas polimórficas de la base de gefitinib se desvelaron en el documento EP1480650 (Forma 1, anhidrato y Forma 5, trihidrato) y en el documento WO2006/090413 (Forma 6, monohidrato).
Entre las formas en estado sólido de gefitinib, la Forma 1 cristalina del documento EP1480650 es particularmente preferida en la industria farmacéutica ya que es suficientemente estable y no higroscópica con una buena capacidad de procesamiento y compatibilidad con excipientes farmacéuticos para fabricar formas de dosificación en estado sólido.
Los procesos para la preparación de gefitinib Forma 1 se han desvelado en varios documentos de la técnica anterior, por ejemplo, en el documento CN103102316 o en el documento CN101973944. El inconveniente de los procesos es el uso de grandes volúmenes de disolventes debido a la baja solubilidad del gefitinib.
Breve descripción de la invención
La presente invención se refiere a un proceso sencillo para fabricar la Forma 1 cristalina de gefitinib, como se define en lo sucesivo en el presente documento, que es eficaz en un entorno de producción fiable a escala industrial sin la necesidad de usar grandes volúmenes de disolventes para disolver gefitinib.
El primer objetivo de esta invención es un proceso para la preparación de la Forma 1 cristalina de gefitinib de fórmula (1) caracterizada por un patrón de difracción de polvo XRPD que comprende, entre otros, máximos en aproximadamente 7,14, 11,26, 14,25, 15,86, 24,33 y 26,40 grados 2 theta (± 0,2 grados 2 theta),
comprendiendo el proceso las etapas:
1. Disolver gefitinib en una mezcla de disolventes que comprende agua y un alcohol seleccionado de etanol y butanol, en donde la relación entre agua y alcohol está entre 1:16 y 1:25 (vol:vol);
2. Aislar la Forma 1 de gefitinib.
Breve descripción de los dibujos
La Figura 1 representa el difractograma de rayos X en polvo (XRPD) de la Forma 1 de gefitinib obtenida mediante el proceso del Ejemplo 2.
Descripción detallada de la invención
La presente invención se refiere a un proceso para fabricar la Forma 1 cristalina de gefitinib. A lo largo de la divulgación y las reivindicaciones, la "Forma 1" de gefitinib es una forma cristalina caracterizada por un patrón de difracción de polvo XRPD que comprende, entre otros, máximos en aproximadamente 7,14, 11,26, 14,25, 15,86, 24,33 y 26,40 grados 2 theta (± 0,2 grados 2 theta) obtenidos cuando se mide con radiación CuKa1 (A = 1,54060 A). El patrón XRPD de la Forma 1 de gefitinib que puede obtenerse mediante el proceso de la presente invención corresponde sustancialmente a aquel desvelado para la Forma 1 de gefitinib en el documento EP1480650. "Corresponde sustancialmente" pretende abarcar variaciones/diferencias en el patrón que un experto en la materia entendería que no representa una diferencia en la estructura cristalina, sino más bien diferencias en la técnica y la preparación de muestras.
La Forma 1 de gefitinib producida mediante el proceso de la presente invención tiene una excelente uniformidad de lote a lote en el tamaño y la forma de los cristales formados. De acuerdo con un aspecto particular de la invención, los cristales de la Forma 1 de gefitinib producidos mediante el proceso de la presente invención preferentemente están sustancialmente libres de otras formas cristalinas de gefitinib. En este sentido, "sustancialmente libre" significa que menos del 10% y más preferentemente menos del 5% de otras formas cristalinas están presentes en el producto precipitado y/o aislado que comprende la Forma 1 de gefitinib.
El material de partida para el proceso de la invención, gefitinib, está disponible en el mercado o puede producirse de acuerdo con procedimientos conocidos, por ejemplo, de acuerdo con lo desvelado en el documento WO96/33980. El objetivo es un proceso para la preparación de la Forma 1 cristalina de gefitinib de fórmula (1) caracterizada por un patrón de difracción de polvo XRpD que comprende, entre otros, máximos en aproximadamente 7,14, 11,26, 14,25, 15,86, 24,33 y 26,40 grados 2 theta (± 0,2 grados 2 theta),
comprendiendo el proceso las etapas:
1. Disolver gefitinib en una mezcla de disolventes que comprende agua y un alcohol seleccionado de etanol y butanol, en donde la relación entre agua y alcohol está entre 1:16 y 1:25 (vol:vol);
2. Aislamiento de la Forma 1 de gefitinib.
En la primera etapa del proceso de la presente invención, el compuesto de fórmula (1) se combina, normalmente en agitación, con una mezcla de disolventes que comprende agua y un alcohol seleccionado de alcohol alifático C1-C6, preferentemente etanol o butanol. El butanol puede ser 1-butanol o 2-butanol o una mezcla de los mismos. La relación entre el agua y un alcohol está entre 1:16 y 1:25 (vol:vol), preferentemente entre 1:18 y 1:20 (vol:vol), la relación más preferida es 1:20 (vol:vol). Las mezclas de disolventes con mayor contenido de agua muestran la presencia de diferentes polimorfos del polimorfo 1 (por ejemplo, formas hidratadas de gefitinib) en el gefitinib aislado. La mezcla de disolventes y gefitinib puede calentarse, por ejemplo a la temperatura de reflujo de la mezcla, para disolver gefitinib en la mezcla de disolventes. Después de la disolución del gefitinib en la mezcla, la mezcla puede enfriarse a una temperatura entre 50 - 75 °C, preferentemente a 75 °C. La mezcla después se siembra preferentemente con partículas de la Forma 1 de gefitinib. La mezcla puede enfriarse además a una temperatura entre -10 °C y la temperatura ambiente (20-25 °C), preferentemente a temperatura ambiente. La mezcla se agita a esta temperatura durante 5 - 20 horas, preferentemente durante 10 - 16 horas en donde la Forma 1 cristalina de gefitinib precipita de la mezcla.
La mezcla de disolventes que comprende agua y un alcohol seleccionado de etanol o butanol y su relación son esenciales para la invención presentada. La Forma 1 de gefitinib puede precipitarse de la mezcla por cualquier técnica, por ejemplo, cristalización, evaporación de los disolventes, etc.
El producto precipitado puede aislarse de la mezcla por técnicas convencionales, por ejemplo, filtración o centrifugación, y puede lavarse y secarse.
Usando el proceso descrito, la cantidad de disolvente o disolventes usados para la cristalización de la Forma 1 de gefitinib puede reducirse sorprendentemente en comparación con los procesos de la técnica anterior.
La Forma 1 de gefitinib preparada mediante el proceso de la presente invención puede formularse y usarse en composiciones farmacéuticas. Por ejemplo, una composición farmacéutica adecuada puede comprender la Forma 1 de gefitinib y al menos un excipiente farmacéuticamente aceptable.
La Forma 1 de gefitinib preparada mediante el proceso de la presente invención es adecuada para el tratamiento de un amplio intervalo de afecciones que incluyen, por ejemplo, cáncer de pulmón no microcítico (NSCLC) localmente avanzado o metastásico. La invención se describirá adicionalmente con referencia a los siguientes ejemplos.
Ejemplos
Ejemplo 1
Se calentó una suspensión de gefitinib (10 g, 22,29 mmol) en 2-butanol (85,3 ml) y agua (4,7 ml) a 94 °C (reflujo) con agitación para obtener una solución transparente. La solución se enfrió a 75 °C con agitación. Se sembró con la Forma 1 de gefitinib y la suspensión resultante se agitó a 75 °C durante 1 hora. Después se enfrió a 23 °C durante 2 horas, se agitó durante 12 horas adicionales, se filtró, se lavó con 2-butanol (10 ml) y se secó para proporcionar la Forma 1 de Gefitinib con un rendimiento del 87 %.
Ejemplo 2
Se calentó una suspensión de gefitinib (10 g, 22,29 mmol) en 2-butanol (88 ml) y agua (4,4 ml) a 94 °C (reflujo) con agitación para obtener una solución transparente. La solución se enfrió a 75 °C con agitación. Se sembró con la Forma 1 de gefitinib y la suspensión resultante se agitó a 75 °C durante 1 hora. Después se enfrió a 23 °C durante 2 horas, se agitó durante 12 horas adicionales, se filtró, se lavó con 2-butanol (10 ml) y se secó para proporcionar la Forma 1 de Gefitinib con un rendimiento del 85 %.
Ejemplo 3
Se calentó una suspensión de gefitinib (10 g, 22,29 mmol) en etanol (88 ml) y agua (4,4 ml) a reflujo con agitación para obtener una solución transparente. La solución se enfrió a 75 °C con agitación. Se sembró con la Forma 1 de gefitinib y la suspensión resultante se agitó a 75 °C durante 1 hora. Después se enfrió a 23 °C durante 2 horas, se agitó durante 13 horas adicionales, se filtró, se lavó con etanol (10 ml) y se secó para proporcionar la Forma 1 de Gefitinib con un rendimiento del 86 %.
A continuación, se obtuvo un XRPD (Presentado en la figura 1) que corresponde a la Forma 1 de gefitinib usando las siguientes condiciones de medición:
Difractómetro Bruker-AXS D8 Vario con geometría 0/2© (modo de reflexión), equipado con un detector Vantec PSD
Claims (4)
1. Un proceso para fabricar la Forma 1 cristalina de gefitinib de fórmula (1),
caracterizada por un patrón de difracción de polvo XRPD que comprende los máximos en aproximadamente 7,14, 11,26, 14,25, 15,86, 24,33 y 26,40 grados 2 theta (± 0,2 grados 2 theta), cuando se mide con radiación CuKa1 (A = 1,54060 A), comprendiendo el proceso las etapas:
1. Disolver gefitinib en una mezcla de disolventes que comprende agua y un alcohol seleccionado de etanol y butanol, en donde la relación entre agua y alcohol está entre 1:16 y 1:25 (vol:vol);
2. Aislar la forma 1 de gefitinib.
2. El proceso de acuerdo con la reivindicación 1, en donde la relación entre agua y el alcohol está entre 1:18 y 1:20 (vol:vol).
3. El proceso de acuerdo con las reivindicaciones 1 o 2 en donde la relación es 1:20 (vol:vol).
4. El proceso de acuerdo con cualquiera de las reivindicaciones 1 a 3, en donde la concentración de gefitinib en la mezcla está entre 0,08 g/ml y 0,15 g/ml.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15203106 | 2015-12-30 | ||
| PCT/EP2016/082322 WO2017114735A1 (en) | 2015-12-30 | 2016-12-22 | Process for making crystalline form a of gefitinib |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2851499T3 true ES2851499T3 (es) | 2021-09-07 |
Family
ID=55027578
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16820268T Active ES2851499T3 (es) | 2015-12-30 | 2016-12-22 | Proceso para fabricar una forma cristalina de gefitinib |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US10259805B2 (es) |
| EP (1) | EP3397618B1 (es) |
| JP (1) | JP6871255B2 (es) |
| ES (1) | ES2851499T3 (es) |
| WO (1) | WO2017114735A1 (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110101668B (zh) * | 2019-05-29 | 2021-09-07 | 华东理工大学 | 一种吉非替尼复合微粒的制备方法 |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU661533B2 (en) | 1992-01-20 | 1995-07-27 | Astrazeneca Ab | Quinazoline derivatives |
| GB9508538D0 (en) | 1995-04-27 | 1995-06-14 | Zeneca Ltd | Quinazoline derivatives |
| ES2342660T3 (es) | 2002-02-26 | 2010-07-12 | Astrazeneca Ab | Nuevas formas cristalinas del compuesto anticancerigeno zd1839. |
| WO2006090413A1 (en) | 2005-02-23 | 2006-08-31 | Natco Pharma Limited | Novel crystalline form of gefitinib and a process for its preparation |
| JP5411847B2 (ja) * | 2007-04-25 | 2014-02-12 | Msd株式会社 | Weelキナーゼインヒビターとしてのジヒドロピラゾロピリミジノン誘導体の多形 |
| CN101973944B (zh) * | 2010-10-14 | 2012-07-04 | 江苏先声药物研究有限公司 | 一种Gefitinib Form 1 晶型的制备方法 |
| CN103030599B (zh) * | 2011-10-09 | 2014-12-10 | 齐鲁制药有限公司 | 吉非替尼中间体及其制备方法 |
| CN103319422B (zh) * | 2012-03-21 | 2016-05-04 | 石药集团中奇制药技术(石家庄)有限公司 | 一种吉非替尼晶型及其制备方法 |
| CN103896862B (zh) * | 2012-12-25 | 2017-05-10 | 江苏天士力帝益药业有限公司 | 一种吉非替尼Form 1晶型的制备方法 |
| CN103896863B (zh) * | 2012-12-26 | 2017-06-13 | 亚宝药业集团股份有限公司 | 抗癌化合物zd1839的晶型及其制备方法 |
| CN103910690A (zh) * | 2013-01-06 | 2014-07-09 | 上海科胜药物研发有限公司 | 一种吉非替尼新晶型及其制备方法 |
| CN103102316A (zh) * | 2013-01-17 | 2013-05-15 | 李彦 | ZD1839Form 1晶型的制备方法 |
| CN103360326B (zh) * | 2013-04-19 | 2016-03-30 | 南京优科生物医药研究有限公司 | 吉非替尼晶型i的精制方法 |
| KR20150001936A (ko) * | 2013-06-28 | 2015-01-07 | 제일약품주식회사 | 게피티닙의 신규한 결정형 및 이의 제조방법 |
| WO2015170345A1 (en) * | 2014-05-09 | 2015-11-12 | Council Of Scientific & Industrial Research | Pharmaceutical cocrystals of gefitinib |
| RU2577518C2 (ru) * | 2014-06-02 | 2016-03-20 | Олег Ростиславович Михайлов | КРИСТАЛЛИЧЕСКАЯ БЕЗВОДНАЯ γ-МОДИФИКАЦИЯ 4-(3'-ХЛОР-4'-ФТОРАНИЛИНО)-7-МЕТОКСИ-6-(3-МОРФОЛИНОПРОПОКСИ)ХИНАЗОЛИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ |
| CN104277005A (zh) * | 2014-09-19 | 2015-01-14 | 成都新恒创药业有限公司 | 一种吉非替尼Form 1晶型的制备方法 |
| CN104693127B (zh) * | 2015-02-14 | 2016-06-15 | 齐鲁制药有限公司 | 吉非替尼乙二醇溶剂合物及其制备方法和用途 |
| CN106588943B (zh) * | 2015-10-19 | 2018-10-16 | 广东东阳光药业有限公司 | 一种egfr抑制剂的盐、晶型及其用途 |
| JP6921818B2 (ja) * | 2015-11-14 | 2021-08-18 | サンシャイン・レイク・ファーマ・カンパニー・リミテッドSunshine Lake Pharma Co.,Ltd. | 置換キノリン化合物の結晶形およびその医薬組成物 |
| CN105294715B (zh) * | 2015-11-18 | 2017-12-22 | 乳源瑶族自治县大众药品贸易有限公司 | 一种氨基喹唑啉类衍生物的富马酸盐及其晶型 |
| CN106083739B (zh) * | 2016-05-31 | 2019-05-14 | 华南理工大学 | 吉非替尼新晶型及其基于超临界反溶剂技术的制备方法 |
-
2016
- 2016-12-22 EP EP16820268.7A patent/EP3397618B1/en active Active
- 2016-12-22 JP JP2018534677A patent/JP6871255B2/ja active Active
- 2016-12-22 US US16/067,330 patent/US10259805B2/en active Active
- 2016-12-22 ES ES16820268T patent/ES2851499T3/es active Active
- 2016-12-22 WO PCT/EP2016/082322 patent/WO2017114735A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| JP2019505509A (ja) | 2019-02-28 |
| EP3397618A1 (en) | 2018-11-07 |
| WO2017114735A1 (en) | 2017-07-06 |
| EP3397618B1 (en) | 2020-11-18 |
| US20190010147A1 (en) | 2019-01-10 |
| US10259805B2 (en) | 2019-04-16 |
| JP6871255B2 (ja) | 2021-05-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102522895B1 (ko) | Jak 키나아제 억제제 바이설페이트의 결정형 및 이의 제조방법 | |
| KR102078077B1 (ko) | 타이로신 키나제 억제제 다이말리에이트의 결정형 아이 및 그의 제조 방법 | |
| US20180155291A1 (en) | New crystal form of lenvatinib methanesulfonate salt and preparation method thereof | |
| WO2011095059A1 (zh) | 达沙替尼多晶型物及其制备方法和药物组合物 | |
| AU2015330554B2 (en) | Crystal form of bisulfate of JAK inhibitor and preparation method therefor | |
| CN104379582A (zh) | 包含达沙替尼和所选择的共晶体形成剂的多组分晶体 | |
| ES2745157T3 (es) | Un método para la preparación, aislamiento y purificación de formas farmacéuticamente aplicables de AHU-377 | |
| CN106661015A (zh) | 达沙替尼盐 | |
| CA3173755A1 (en) | Integrin inhibitor and uses thereof | |
| ES2879294T3 (es) | Formas polimórficas de Belinostat y procesos para la preparación de las mismas | |
| JP2015508090A (ja) | 固体形態のダビガトランエテキシレートメシレート及びその調製方法 | |
| US10870654B2 (en) | Pharmaceutically acceptable salts and polymorphic forms of hydrocodone benzoic acid enol ester and processes for making same | |
| ES2814499T3 (es) | Formas en estado sólido de sales de Nilotinib | |
| CN105408329A (zh) | 呈晶体形式的达沙替尼的盐 | |
| ES2874577T3 (es) | Formas cristalinas de bilastina y procedimientos para su preparación | |
| ES2733813T3 (es) | Proceso para preparar una forma cristalina de lenalidomida | |
| ES2851499T3 (es) | Proceso para fabricar una forma cristalina de gefitinib | |
| TW202404604A (zh) | [(1S)-1-[(2S,4R,5R)-5-(5-胺基-2-酮基-噻唑并[4,5-d]嘧啶-3-基)-4-羥基-四氫呋喃-2-基]丙基]乙酸酯之新穎固態形式 | |
| EP3271351A1 (en) | Novel polymorphic form x of nilotinib dihydrochloride hydrate | |
| CN106928218A (zh) | 吗啉衍生物的盐及其晶型、其制备方法及药物组合物、用途 | |
| CN101353343A (zh) | 高纯度盐酸诺拉曲塞二水合物的制备方法 | |
| TWI707851B (zh) | 哌嗪化合物的新穎結晶 | |
| EP3941472A1 (en) | <smallcaps/>? ? ?n? ? ? ? ?crystalline and amorphous forms of-(5-((4-ethylpiperazin-1-yl)methyl)pyridine-2-yl)-5-fluoro-4-(3-isopropyl-2-methyl-2 <ns1:i>h</ns1:i>?-indazol-5-yl)pyrimidin-2-amine and its salts, and preparation methods and therapeutic uses thereof | |
| WO2019057165A1 (zh) | 盐酸伊达比星一水合物的晶型 | |
| HU231012B1 (hu) | Lapatinib sók |