ES2938417T3 - Derivado de poliestireno sulfonado para su uso en el tratamiento y/o profilaxis de la gripe felina - Google Patents
Derivado de poliestireno sulfonado para su uso en el tratamiento y/o profilaxis de la gripe felina Download PDFInfo
- Publication number
- ES2938417T3 ES2938417T3 ES19845729T ES19845729T ES2938417T3 ES 2938417 T3 ES2938417 T3 ES 2938417T3 ES 19845729 T ES19845729 T ES 19845729T ES 19845729 T ES19845729 T ES 19845729T ES 2938417 T3 ES2938417 T3 ES 2938417T3
- Authority
- ES
- Spain
- Prior art keywords
- kda
- polymer
- feline
- virus
- infection
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/74—Synthetic polymeric materials
- A61K31/795—Polymers containing sulfur
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
- A61P31/22—Antivirals for DNA viruses for herpes viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Virology (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Communicable Diseases (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Oncology (AREA)
- Molecular Biology (AREA)
- Epidemiology (AREA)
- Biotechnology (AREA)
- Engineering & Computer Science (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Polymers & Plastics (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
La presente invención se refiere a un derivado de poliestireno sulfonado de fórmula I para uso en el tratamiento y/o profilaxis de la gripe felina, especialmente la infección causada por calicivirus felino o herpesvirus felino, solo o en terapia combinada. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Derivado de poliestireno sulfonado para su uso en el tratamiento y/o profilaxis de la gripe felina
La presente invención se refiere a un derivado de poliestireno sulfonado, en particular sulfonato de poliestireno de sodio, para su uso en el tratamiento y/o profilaxis de la gripe felina, en particular, la infección causada por el calicivirus felino o el herpesvirus felino, solo o en combinación con otros fármacos.
La enfermedad de las vías respiratorias superiores (EVRS) en gatos, llamada "gripe felina", es una enfermedad común cuyos síntomas incluyen tos, estornudos, rinorrea, enrojecimiento de los ojos, fiebre o la aparición de secreción purulenta de la nariz y los ojos [1, 2]. La enfermedad es considerada como una de las principales causas de muerte en los refugios de animales y en las guarderías [3]. Los principales factores etiológicos virales de esta enfermedad son el herpesvirus felino tipo 1 (FHV-1, FeHv-1) y el calicivirus felino (FCV) [1, 3-5].
El herpesvirus felino tipo 1 (FHV-1, FeHv-1) es un miembro de la familia Herpesviridae, que abarca los virus de ADN envueltos. Los herpesvirus son patógenos que infectan a los seres humanos y a muchas especies animales: mamíferos, reptiles, aves, anfibios y peces [6]. Uno de los patógenos más comunes que se encuentran en los seres humanos es el virus del herpes simple tipo 1 (VHS-1) responsable de las úlceras que se presentan principalmente en la cara, aunque también son posibles infecciones en otras regiones del cuerpo. Las infecciones causadas por los herpesvirus pueden provocar el desarrollo de enfermedades más graves o la muerte [6, 7]. El herpesvirus felino está relacionado con el HSV-1 y se propaga en todo el mundo en la población felina. Se estima que hasta el 90 % de la población felina es seropositiva para este patógeno, mientras que en el 80 % el virus está presente en estado latente [8, 9]. Las infecciones por FHV-1 se asocian principalmente con la inflamación de las vías respiratorias superiores, infecciones de las mucosas e infecciones oculares (úlceras corneales, conjuntivitis aguda y queratitis), que puede llevar a la ceguera [10-13]. Y lo que es más, las coinfecciones bacterianas son especialmente peligrosas para los gatitos y las personas inmunodeprimidas, ya que pueden ser mortales.
El herpesvirus felino se replica principalmente en el tejido epitelial y conduce a una inflamación aguda [13]. Después de la infección de las células epiteliales, el virus es transportado dentro de las neuronas sensoriales por vía retrógrada, es decir, hacia el cuerpo celular, y luego entra en un estado de latencia. El virus latente se presenta en forma episomal, sin embargo, puede reactivarse y la enfermedad puede reaparecer en caso de debilitamiento del sistema inmunitario del hospedador [8, 14, 15].
Para tratar infecciones herpesvirales en seres humanos se utilizan actualmente análogos de nucleósidos. Aciclovir, penciclovir, idoxuridina, cidovir y vidarabina pertenecen a este grupo. Estas moléculas inhiben la replicación viral al bloquear el centro activo de la ADN polimerasa viral. Los análogos de nucleósidos se administran a la célula en forma inactiva y la activación se produce como resultado de la fosforilación realizada por la timidina cinasa (TK) del herpesvirus. En la siguiente etapa, hay otras dos fosforilaciones de la molécula, llevadas a cabo por las GMP cinasas del hospedador [16, 17]. El compuesto trifosforilado puede ser utilizado por la ADN polimerasa viral como sustrato durante la reacción de extensión de la cadena de polinucleótidos, y una vez que el derivado se incorpora al ADN, la elongación se detiene. Los análogos de nucleósidos tienen una afinidad mucho mayor por la polimerasa viral que por la polimerasa del hospedador [18]. Sorprendentemente, a pesar de los síntomas similares de la enfermedad y la similitud filogenética de los virus, el perfil de eficacia de los fármacos individuales varía en humanos y gatos. Algunos medicamentos que son seguros y eficaces en humanos son tóxicos para el gato [19-21]. Por ejemplo, el aciclovir (ACV) es un inhibidor muy eficaz de la replicación del virus HSV-1 en humanos, pero en gatos no mostró una actividad igualmente alta y su biodisponibilidad fue baja [22]. El valaciclovir (VCV) es un compuesto transformado por esterasas hepáticas en ACV, que también se usa con mucha frecuencia en humanos para tratar infecciones herpesvirales [23]. A pesar de la alta actividad antiviral deL VCV In vitro, los gatos que tomaron el medicamento no mejoraron los síntomas de la enfermedad y, además, hubo muchos efectos adversos, como la mielosupresión o la necrosis hepática y renal que conduce a la muerte del animal [24]. Sin embargo, otro derivado del aciclovir, penciclovir (PCV), parece ser una solución eficaz y segura [20, 25, 26]. Además, famciclovir, un precursor del PCV, ha sido probado en el tratamiento y la profilaxis de la infección por FHV en gatos y ha demostrado ser seguro [27, 28]. Famciclovir se convierte en PCV por las aldehído oxidasas hepáticas [29, 30], se transporta al interior de la célula y, como el ACV, es a continuación fosforilado por la TK viral. A continuación, se realizan otras dos fosforilaciones por enzimas celulares y se inhibe la extensión de la cadena polinucleotídica del material genético del virus [31]. Sin embargo, la concentración de PCV en gatos fue mucho más baja de lo esperado, lo que probablemente esté asociado con una actividad mucho menor de las aldehído oxidasas hepáticas en gatos que en otros mamíferos, de modo que el precursor, es decir, famciclovir, no se convierte a la forma activa, es decir, PCV [26, 27, 32]. La solicitud internacional WO2013/007703 A1 sugiere el uso de oligonucleótidos que contienen CpG para la prevención de infecciones virales en gatos.
El FCV es un miembro de la familia Caliciviridae, que incluye virus sin envoltura que contienen material genético en forma de ARN monocatenario con polaridad positiva. Debido a la relación filogenética, los calicivirus se han dividido hasta ahora en cinco tipos: Lagovirus, Nebovirus, Norovirus, Sapovirus y Vesivirus [45], aunque en febrero de 2019 el Comité Internacional de Taxonomía de Virus (ICTV) formuló una nueva clasificación en la que, debido a la gran diversidad genética de los miembros de la familia Caliciviridae, se clasificaron seis nuevos géneros (además de los cinco anteriores): Bavovirus, Minovirus, Nacovirus, Nebovirus, Recovirus y Valovirus. Los virus de esta familia pueden
infectar tanto a humanos como a animales. Uno de los representantes más conocidos de esta familia son los norovirus y los sapovirus, que causan gastroenteritis no bacteriana en mamíferos. Los lagovirus causan fiebre hemorrágica letal en conejos. En gatos, el FCV a menudo causa inflamación de las vías respiratorias superiores, siendo especialmente peligroso para los individuos con un sistema inmunitario debilitado [46-48]. El FCV es un patógeno que se encuentra en la población felina de todo el mundo [45, 49]. Suele causar conjuntivitis leve e inflamación de las vías respiratorias superiores, sin embargo, los síntomas también incluyen ulceración y estomatitis crónica, salivación, y rara vez cojera asociada con sinovitis aguda [50-52]. El material genético del FCV es ARN monocatenario, y la alta variabilidad del genoma significa que el virus puede adaptarse muy rápidamente a las condiciones ambientales cambiantes [53]. Aunque existe una vacuna relativamente eficaz contra el FCV y las infecciones no suelen poner en peligro la vida del animal, las infecciones bacterianas secundarias representan una gran amenaza para los gatos [54]. En los últimos años, también se ha demostrado que las cepas de FCV pertenecientes a los llamados VS-FCv (FCV sistémico virulento) aparecen en la población de gatos, y que son la causa de una epidemia con una tasa de mortalidad de hasta el 60 % asociada a un fallo multiorgánico; de acuerdo con la bibliografía, una cepa causó síntomas de fiebre hemorrágica [48, 55-58]. El tratamiento de una infección causada por el FCV se basa únicamente en la terapia con antibióticos, cuyo objetivo es prevenir infecciones bacterianas secundarias. Actualmente, en medicina veterinaria no se utiliza ningún agente terapéutico que actúe directamente sobre el FCV. Vale la pena mencionar que se ha demostrado una actividad antiviral in vitro muy alta para compuestos como el cloruro de litio [59] y la mefloquina [60]. La solicitud de patente internacional WO2006/029507 A1 divulga un efecto de la asparaginasa sobre el FCV en cultivo celular. Desafortunadamente, no se han realizado estudios sobre la eficacia de estos compuestos en gatos in vivo [59, 60]. Asimismo, la ribavirina, que también inhibe la infección por FCV in vitro, es demasiado tóxica después de la administración oral para ser utilizado en gatos [61].
Los ejemplos anteriores indican que los agentes actualmente disponibles para el tratamiento y/o profilaxis del síndrome respiratorio en gatos que puede ser causado por virus, tal como FHV o FCV, no son lo suficientemente eficaces y/o son demasiado tóxicos. Por lo tanto, existe la necesidad de encontrar un agente terapéutico eficaz que reduzca de manera eficaz la infección y la transmisión de ambos virus, siendo seguro para los gatos.
Se conocen derivados de poliestireno sulfonado. Sus propiedades antimicrobianas, en particular antivirales, también son conocidas, así como a su uso en medicina, p. ej., para el tratamiento de la hipercalemia. Un derivado de poliestireno sulfonado representativo conocido es sulfonato de poliestireno de sodio (poli(estireno sulfonato de sodio, PSSNa)). Es conocido por su actividad antibacteriana y antiviral. Se ha demostrado que inhibe la replicación de muchos patógenos, que incluyen: VIH, VPH, HSV-1, HSV-2, Gardnerella vaginalis, Chlamydia trachomatis y Neisseria gonorrhoeae [33-37]. Hasta ahora, sin embargo, no se ha demostrado la posibilidad de su uso en el caso de infección causada por el virus FCV o FHV-1. En el caso del HSV, se ha demostrado que el polímero PSSNa inhibe la replicación al evitar que los viriones se unan a la superficie celular, lo que dificulta la transmisión del virus de una célula infectada a una célula sana [35]. Considerando que el mecanismo de acción propuesto implica la actividad antiviral en las primeras etapas de la infección, se ha sugerido que PSSNa es un imitador del heparán sulfato (HS), es decir, es capaz de "imitar" el HS presente en la superficie de las células infectadas, el cual sirve como molécula de adherencia para el HSV. Además, se ha demostrado que otros imitadores del heparán sulfato, como los fucosanoides, sulfatos de dextrano y sulfatos de manano, bloquean la unión de los virus HSV-1 y HSV-2 a los agentes adhesivos [38-41]. Asimismo, los A-carragenanos tipo IV, que también se consideran imitadores del HS, son capaces de unirse al virus FHV-1, lo que lleva a bloquear su interacción con el factor de adherencia (HS). A pesar del hecho de que los resultados obtenidos con el uso de A-carragenanos tipo IV in vitro eran prometedores, no se observó mejoría en el estado de salud tras la administración del preparado que contiene este compuesto en gatos [42].
Existe la necesidad de obtener nuevos inhibidores de la replicación del herpesvirus felino y del calicivirus, en particular FHV-1 y FCV, especialmente agentes con un mecanismo de acción diferente al actualmente disponible para el tratamiento y/o prevención de la infección causada por el herpesvirus felino y el calicivirus felino, que también fuese adecuado para la terapia combinada para este tipo de infección.
El objeto de la invención descrita en la presente solicitud de patente es, por tanto, obtener una nueva sustancia activa eficaz para su uso en el tratamiento y/o profilaxis de la gripe felina, en particular, la infección causada por el calicivirus felino o el herpesvirus, en particular el FHV-1, para obtener un nuevo agente eficaz para su uso en el tratamiento y/o profilaxis de la gripe felina, especialmente la infección causada por calicivirus felino o herpesvirus, que se pueda utilizar en terapia combinada con terapias ya disponibles para este tipo de infección, así como demostrar la posibilidad de utilizar dicho preparado para el tratamiento de este tipo de infecciones.
Estos objetivos se lograron con las soluciones presentadas en las reivindicaciones de patente adjuntas. Sorprendentemente, se ha observado que estos objetivos se pueden lograr utilizando un derivado de poliestireno sulfonado.
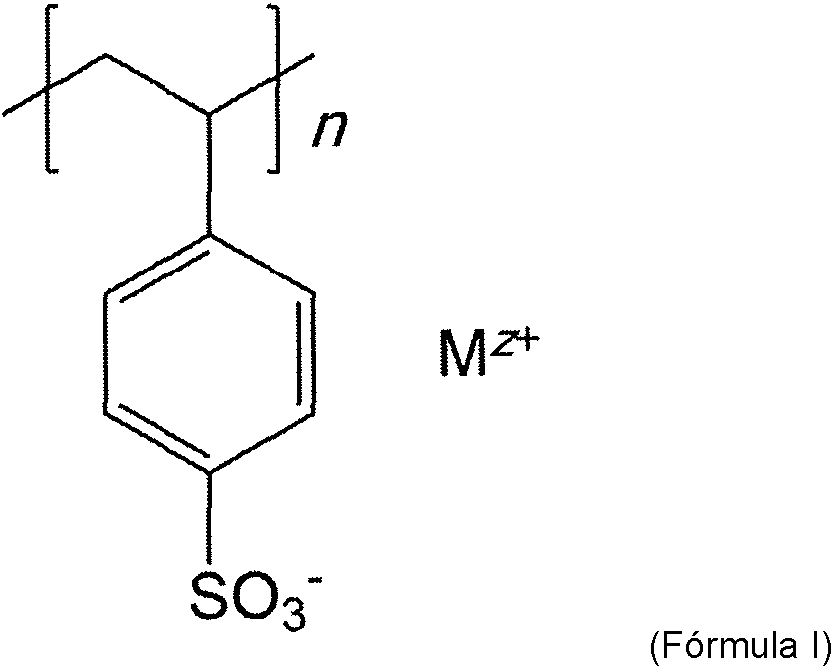
La presente invención se refiere a un derivado de poliestireno sulfonado de fórmula I:
para su uso en el tratamiento y/o profilaxis de la gripe felina, especialmente la infección causada por calicivirus felino 0 herpesvirus felino.
Preferentemente, el derivado de poliestireno sulfonado a utilizar de acuerdo con la invención está en forma de sal, más preferentemente, el derivado de poliestireno sulfonado está en forma de sal de sodio, que es la sal de sodio del sulfonato de poliestireno (PSSNa).
Preferentemente, el derivado de poliestireno sulfonado a utilizar de acuerdo con la invención tiene un peso molecular de al menos 1,5 kDa, más preferentemente al menos 8 kDa.
Incluso más preferentemente, el derivado de poliestireno sulfonado a utilizar de acuerdo con la invención tiene un peso molecular en el intervalo de 8 kDa a 1200 kDa, e incluso más preferentemente tiene un peso molecular seleccionado del grupo que consiste en 8 kDa, 19,3 kDa, 35 kDa, 46 kDa, 93,5 kDa, 200 kDa, 400 kDa, 780 kDa y 1200 kDa, lo más preferentemente tiene un peso molecular de 93,5 kDa o 780 kDa.
Preferentemente, la infección causada por el herpesvirus felino o el calicivirus felino es la gripe felina.
Preferentemente, la infección causada por el herpesvirus felino es una infección causada por el herpesvirus felino tipo 1 (FHV-1).
Preferentemente, de acuerdo con la invención, el derivado de poliestireno sulfonado es para su uso en terapia combinada, que incluye preferentemente el uso simultáneo de otro agente para el tratamiento de la gripe felina, especialmente la infección causada por calicivirus felino o herpesvirus felino.
Por uso simultáneo se entiende en el presente documento administrar un compuesto de la invención simultáneamente con otro agente, preferentemente para el tratamiento de la gripe felina, especialmente la infección causada por calicivirus felino o herpesvirus felino, en una formulación o en formulaciones separadas.
Más preferentemente, dicho otro agente para el tratamiento de la infección por FHV-1 es un análogo de nucleósido, más preferentemente aciclovir (ACV) y/o penciclovir (PCV).
El derivado de poliestireno sulfonado de acuerdo con la invención se presenta preferentemente en forma de sal, en particular una sal de sodio. Un derivado de poliestireno sulfonado representativo es el sulfonato de poliestireno de sodio (PSSNa). Un ejemplo de otra sal de sulfonato de poliestireno puede ser la sal de calcio o la sal de potasio.
Los derivados de poliestireno sulfonado, como el sulfonato de poliestireno de sodio (PSSNa), se pueden preparar por cualquier método conocido para un experto en la materia. Estos compuestos pueden incluirse después en la composición farmacéutica junto con excipientes, diluyentes y/o sustratos farmacéuticamente aceptables adecuados. Las composiciones de este tipo se pueden preparar en forma de formulaciones adecuadas para su administración por cualquier vía de administración, tales como, por ejemplo, la vía tópica, la vía nasal, o la vía oral. Las composiciones de este tipo pueden, por ejemplo, estar en forma de una formulación tópica, por ejemplo, una pomada o una formulación oral, por ejemplo una solución o suspensión.
Los compuestos a utilizar de acuerdo con la invención permiten la profilaxis y/o el tratamiento de la gripe felina, especialmente la infección causada por el calicivirus felino o el herpesvirus felino y reducir el riesgo de infecciones secundarias. Los compuestos para su uso de acuerdo con la invención permiten además el alivio del curso de la gripe felina, especialmente la infección causada por calicivirus felino o herpesvirus felino. Los compuestos para su uso de acuerdo con la invención son extremadamente eficaces porque conducen a una inhibición casi completa de la
replicación in vitro de los virus que causan la gripe felina y además tienen una toxicidad muy baja o indetectable. Asimismo, los compuestos para su uso de acuerdo con la invención son adecuados para su uso en terapia combinada de la gripe felina, especialmente la infección causada por calicivirus felino o herpesvirus felino, en especial el FHV-1, junto con al menos un agente adicional utilizado para tratar este tipo de infecciones, especialmente con un mecanismo de acción diferente al del derivado de poliestireno sulfonado, especialmente la sal de sodio de sulfonato de poliestireno. Ejemplos de tales otros agentes utilizados para tratar este tipo de infección son los análogos de nucleósidos. Los compuestos para usar de acuerdo con la invención son particularmente adecuados para usar junto con penciclovir (PCV). Este uso combinado de un derivado sulfonado de poliestireno y un análogo de nucleósido permite un efecto sinérgico que es extremadamente importante. in vivo, permitiendo un aumento en la eficacia de la terapia de la gripe felina causada por el FHV-1, especialmente la infección causada por el herpesvirus felino, rebajando las dosis de los agentes terapéuticos utilizados y reduciendo la posible toxicidad y efectos secundarios. También permite tratar la gripe felina, especialmente la infección provocada por calicivirus felino o la infección provocada por herpesvirus felino resistente a los agentes terapéuticos disponibles en la actualidad utilizados para este fin.
La investigación ha demostrado que un derivado de poliestireno sulfonado, preferentemente PSSNa, no actúa sobre la célula infectada, sino que se une a un herpesvirus, como preferentemente el FHV-1, y así bloquea la propagación de este virus, limitando la infección que provoca. Gracias a esto, tal derivado es extremadamente eficaz. Además, tiene muy baja toxicidad y no provoca efectos adversos.
La investigación también mostró que el derivado sulfonado del poliestireno, preferentemente PSSNa, tiene un mecanismo diferente de actividad antiviral que los agentes actualmente comercializados. Gracias a esto, se puede usar eficazmente en terapia combinada con otros fármacos antivirales utilizados en caso de infección causada por el herpesvirus felino, preferentemente con análogos de nucleósidos, especialmente aciclovir y/o penciclovir, para lograr un efecto sinérgico. Esto permite aumentar la eficacia de la terapia para la infección causada por el herpesvirus felino, reducir las dosis de los agentes utilizados y reducir la toxicidad manteniendo una eficacia terapéutica o profiláctica adecuada, así como para el tratamiento eficaz de la infección causada por mutantes de herpesvirus felinos resistentes a las terapias actualmente disponibles.
A pesar del hecho de que el factor de adherencia para el FCV es el ácido siálico [62], y no el HS, cuyo imitador es el polímero en estudio, los inventores han demostrado que las sales de sodio de sulfonato de poliestireno de alto peso molecular inhiben eficazmente la infección inducida por el FCV in vitro causada tanto por la cepa de laboratorio F9 como por seis cepas clínicas K1, K2, K3, K5, K8 y K10. La inhibición se observa principalmente en las últimas etapas de la infección, pero la actividad antiviral también se observa en las primeras etapas de la infección.
La investigación también mostró que cuanto mayor sea el peso molecular del sulfonato de poliestireno de sodio utilizado, mayor es su actividad contra el FCV. Por ejemplo, un polímero con un peso molecular de 8 kDa tiene una actividad antiviral similar a los polímeros de sulfonato de poliestireno con un peso molecular más bajo. En cambio, los polímeros de sulfonato de poliestireno con un peso molecular superior a 35 kDa presentan una actividad antiviral significativamente mayor. La diferencia en la actividad se debe, al menos en parte, al hecho de que el PSSNa con un peso molecular más alto inhibe el proceso de infección del FCV también en las primeras etapas de la infección, al inhibir la adherencia del virus a la superficie celular.
La presente invención se ilustrará ahora por medio de realizaciones y figuras que no están, sin embargo, destinadas a limitar el alcance de la protección de la invención de cualquier manera como se define en las reivindicaciones de la patente.
Breve descripción de las figuras
La FIG. 1 muestra los resultados de un estudio sobre el efecto de polímeros de diferentes pesos moleculares en la supervivencia de células renales felinas de Crandell-Rees (CrFK). Los resultados se presentaron para dos concentraciones seleccionadas, las cuáles fueron la concentración más alta probada y la concentración a la que se demostró una actividad antiviral elevada, respectivamente: 500 pg/ml (Fig. 1 A) y 20 pg/ml (Fig. 1 B). Los valores se normalizaron al 100 % de supervivencia de células de control no tratadas.
La FIG. 2 muestra la relación entre el peso molecular de un polímero y su actividad contra el virus FHV-1. Usando la PCR en tiempo real, se determinó el número de copias de ADN viral en 1 ml de medio (Fig. 2 A), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 2 B). La prueba de replicación se realizó utilizando polímeros de diferentes pesos moleculares a una concentración de 20 pg/ml. Para determinar la aparición de diferencias estadísticamente significativas entre los grupos comparados y el control no tratado, se realizó un análisis de la varianza ANOVA unidireccional respaldado por la prueba post-hoc de Tukey. Los valores que fueron significativamente diferentes desde el punto de vista estadístico del control viral se marcaron con ***, p < 0,001; **, p < 0,01; *, p < 0,05, mientras que los valores que no eran estadísticamente diferentes se marcaron como "ns". Los resultados se expresan como media ± ETM.
La Fig. 3 muestra la relación entre la concentración de polímero y su actividad contra el virus FHV-1. Usando la PCR en tiempo real, se determinó el número de copias de ADN viral en 1 ml de medio (Fig. 3 A, Fig. 3 B), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 3 C, Fig. 3 D). La prueba de replicación se realizó utilizando diferentes concentraciones de un polímero con un peso molecular de 93,5 kDa
(Fig. 3 A, Fig. 3 C) y un polímero con un peso molecular de 780 kDa (Fig. 3 B, Fig. 3 D ). Los valores se han normalizado al control viral.
La Fig. 4 muestra los resultados de los estudios sobre el mecanismo de acción de los polímeros PSSNa. Se realizaron cuatro pruebas funcionales para identificar la etapa en la que se inhibe la replicación del virus FHV-1 por el polímero PSSNa. Usando la PCR en tiempo real, se determinó el número de copias de ADN viral en 1 ml de medio (Fig. 4 A), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 4 B). La prueba I se llevó a cabo usando diferentes concentraciones de un polímero con un peso molecular de 93,5 kDa (Fig. 4 C) y un polímero con un peso molecular de 780 kDa (Fig. 4 D). Para determinar la aparición de diferencias estadísticamente significativas entre los grupos comparados y el control de polímero sin tratar, se realizó un análisis de la varianza ANOVA unidireccional respaldado por la prueba post-hoc de Tukey. Los valores que fueron significativamente diferentes desde el punto de vista estadístico del control viral se marcaron con *** p < 0,001; **, p < 0,01; *, p < 0,05, mientras que los valores que no eran estadísticamente diferentes se marcaron como "ns". Los resultados se expresan como media ± ETM.
La Fig. 5 muestra la visualización de la inhibición de la infección por el virus FHV-1 de células CrFK por polímeros PSSNa. Los canales individuales y una combinación de 3 canales se muestran por separado. El canal azul presenta núcleos celulares, el canal rojo es F-actina, mientras que el canal verde son viriones del FHV-1. La figura muestra visualizaciones de células de control (en blanco), control viral, células tratadas con PSSNa de 93,5 kDa y células tratadas con PSSNa de 780 kDa. La barra de escala marca 10 pm.
La Fig. 6 muestra el análisis cuantitativo de las imágenes obtenidas en un microscopio confocal después de realizar la prueba II (Fig. 6A) y la prueba III (Fig. 6B) realizadas en ImageJ FiJi. La cantidad de virus por célula se presenta como recuentos por célula (% de la media obtenida para el control viral). Los resultados se expresan como media ± ETM; los datos procedían del análisis de 10 células diferentes; las imágenes eran de tres experimentos independientes. Para determinar la ocurrencia de diferencias estadísticamente significativas entre los grupos comparados, se realizó un análisis de la varianza ANOVA unidireccional, respaldado por la prueba post-hoc de Tukey. Los valores que fueron significativamente diferentes desde el punto de vista estadístico del control viral se marcaron con ****, p < 0,0001, mientras que los valores que no eran estadísticamente diferentes se marcaron como "ns". Los resultados se expresan como media ± ETM.
La Fig. 7 muestra la relación entre la concentración de polímero y su actividad frente a la cepa clínica FHV-1 K7. Se determinó un cambio logarítmico en el número de ADN viral por 1 ml de medio de cultivo (Fig. 7A) mediante PCR en tiempo real, mientras que los ensayos de placa permitieron determinar el cambio logarítmico en el número de viriones infecciosos (UFP/ml) (Fig. 7B). La prueba se llevó a cabo utilizando polímeros PSSNa con dos pesos moleculares diferentes (93,5 kDa y 780 kDa) a tres concentraciones diferentes (20, 200 y 500 pg/ml). Los valores se normalizaron al control viral, es decir, células infectadas no incubadas con el polímero. Los resultados se expresan como media ± ETM.
La Fig. 8 muestra el análisis de la capacidad de los polímeros PSSNa para unirse al virus FHV-1, que se presentó como el número de recuentos (viriones) por plano confocal. Se registraron recuentos de 12 planos para cada muestra. Debido al hecho de que los datos proporcionados no cumplieron con los requisitos para usar la prueba paramétrica, se realizó la prueba no paramétrica de Kruskal-Wallis respaldada por la prueba post-hoc de Dunn. Los valores que fueron significativamente diferentes desde el punto de vista estadístico del control viral se marcaron con ****, p < 0,0001; ***, p < 0,001; **, p < 0,01; mientras que los valores que no eran estadísticamente diferentes se marcaron como "ns". Los resultados se presentaron como mediana ± intervalo intercuartílico.
La Fig. 9 muestra la relación entre el peso molecular de un polímero y su actividad anti-FCV. Utilizando reacciones de RT-qPCR en tiempo real, se determinó el número de copias de ARN viral en 1 ml de medio (Fig. 9 A), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 9 B). La prueba se realizó utilizando polímeros de diferentes pesos moleculares a una concentración de 200 pg/ml. Para determinar la aparición de diferencias estadísticamente significativas entre los grupos comparados y el control de polímero sin tratar, se realizó un análisis de la varianza ANOVA unidireccional respaldado por la prueba post-hoc de Tukey. Los valores que fueron significativamente diferentes desde el punto de vista estadístico entre sí del control viral se marcaron con ****, p< 0,0001; p< 0,01; *, p < 0,05, mientras que los valores que no eran estadísticamente diferentes se marcaron como "ns". Los resultados se expresan como media ± ETM.
La Fig. 10 muestra la relación entre la concentración de polímero y su actividad contra el FCV. Utilizando reacciones de RT-qPCR en tiempo real, se determinó el número de copias de ARN viral en 1 ml de medio (Fig. 10 A, Fig. 10 B), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 10 C, Fig. 10 D). La prueba se realizó utilizando diferentes concentraciones de un polímero con un peso molecular de 93,5 kDa (Fig. 10 A, Fig. 10 C) y un polímero con un peso molecular de 780 kDa (Fig. 10 B, Fig. 10 D). Los valores se han normalizado al control viral.
La Fig. 11 muestra los resultados de los estudios sobre el mecanismo de acción de los polímeros PSSNa. Para identificar la etapa en la que el polímero PSSNa inhibe la infección por el FCV, se realizaron 4 pruebas funcionales, descritas a continuación, usando un polímero con una concentración de 200 pg/ml. Utilizando reacciones de RT-qPCR en tiempo real, se determinó el número de copias de ARN viral en 1 ml de medio (Fig. 11 A), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 11 B). La prueba III se llevó a cabo usando diferentes concentraciones del polímero con un peso molecular de 93,5 kDa (Fig. 11 C) y un polímero con un peso molecular de 780 kDa (Fig. 11 D). Para determinar la aparición de diferencias estadísticamente significativas entre los grupos comparados y el control de polímero sin tratar, se realizó un análisis de la varianza ANOVA unidireccional respaldado por la prueba post-hoc de Tukey. Los valores que fueron significativamente diferentes desde el punto de vista estadístico del control viral se marcaron con ***, p < 0,001; **, p < 0,01, mientras
que los valores que no eran estadísticamente diferentes se marcaron como "ns". Los resultados se expresan como media ± ETM.
La Fig. 12 muestra una visualización de la inhibición de la infección por el FCV de células CrFK por polímeros PSSNa a una concentración de 1000 pg/ml. Los canales individuales y una combinación de 3 canales se muestran por separado. El canal azul presenta núcleos celulares, el canal rojo es F-actina, mientras que el canal verde son viriones del FCV. La figura muestra visualizaciones de células de control, control viral, células tratadas con PSSNa con un peso molecular de 93,5 kDa y células tratadas con PSSNa con un peso molecular de 780 kDa. La barra de escala marca 10 pm.
La Fig. 13 muestra el análisis cuantitativo de las imágenes obtenidas en un microscopio confocal después de realizar la prueba II (A) y la prueba III (B) realizadas en ImageJ FiJi. La cantidad de virus por célula se presenta como recuentos por célula (% de la media obtenida para el control viral). Los resultados se expresan como media ± ETM; los datos procedían del análisis de 10 células diferentes; las imágenes eran de tres experimentos independientes. Para determinar la ocurrencia de diferencias estadísticamente significativas entre los grupos comparados, se realizó un análisis de la varianza ANOVA unidireccional respaldado por la prueba post-hoc de Tukey. Los valores que fueron significativamente diferentes desde el punto de vista estadístico del control viral se marcaron con ****, p < 0,0001, mientras que los valores que no eran estadísticamente diferentes se marcaron como "ns".
La Fig. 14 muestra la relación entre la concentración de polímero y su actividad contra las cepas clínicas de FCV. Utilizando reacciones de RT-qPCR en tiempo real, se determinó el número de ARN viral por 1 ml de medio de cultivo, mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos. La prueba se llevó a cabo utilizando polímeros con dos pesos moleculares diferentes (93,5 kDa y 780 kDa) a tres concentraciones diferentes (200, 500 y 1000 pg/ml). Los valores se normalizaron al control viral, es decir, células infectadas no incubadas con el polímero. Los resultados se expresan como media ± ETM.
La Fig. 15 muestra un análisis de la capacidad de los polímeros PSSNa para unirse al virus, presentado como el número de recuentos (viriones) por plano confocal. Se realizaron recuentos de 12 planos para cada muestra. Debido al hecho de que los datos proporcionados no cumplieron con los requisitos para usar la prueba paramétrica, se realizó la prueba no paramétrica de Kruskal-Wallis respaldada por la prueba post-hoc de Dunn. Los valores que fueron significativamente diferentes desde el punto de vista estadístico del control viral se marcaron con ****, p < 0,0001, **, p < 0,01, mientras que los valores que no eran estadísticamente diferentes se marcaron como "ns". Los resultados se presentaron como mediana ± intervalo intercuartílico.
La FIG. 16 muestra el análisis in vitro de la actividad antiviral del hidrogel PSSNa-PEG. La citotoxicidad de PEG400 a concentraciones de 100, 50, 40, 30, 25, 20, 15 y 10 mg/ml se determinó mediante la prueba XTT (A). Los resultados se normalizaron a las células de control (sin tratar con polímero), que fue del 100%. El ensayo de replicación viral se realizó utilizando células CrFK en presencia de PEG400 (30 mg/ml) y PSSNa1000kDa (200 pg/ml) para FHV-1 (B, C) y FCV (D, E). La inhibición de la infección viral se determinó mediante PCR en tiempo real y se presentó como un cambio logarítmico en el número de copias de ADN (para FHV-1) o ARN (para FCV) por mililitro (B, D) o mediante un ensayo de placa y se presentó como el cambio logarítmico en el número de UFP/ml (C, E). Los resultados se normalizaron al control viral, es decir, células infectadas no tratadas con polímero y presentadas como media ± ETM de tres experimentos independientes.
Ejemplos
Todas las pruebas y procedimientos experimentales que se describen a continuación se llevaron a cabo utilizando kits de prueba, reactivos y aparatos comercializados, siguiendo las recomendaciones de los fabricantes de los kits, reactivos y aparatos utilizados, a menos que se indique expresamente otra cosa. Los parámetros de prueba indicados anteriormente se midieron usando métodos convencionales, comúnmente conocidos utilizados en el campo al que pertenece la presente invención.
Ejemplo 1
El efecto del sulfonato de poliestireno de sodio (PSSNa) de diferente peso molecular en la supervivencia de las células CrFK
La citotoxicidad de los polímeros se determinó utilizando el kit de ensayo de viabilidad XTT (Biological Industries, Israel), que cuantifica la capacidad de las células metabólicamente activas para transformar un sustrato en su derivado coloreado. Para realizar el experimento se utilizó la línea celular permisiva CrFK (corteza renal de gato de Crandell-Rees, Felis catus, células renales felinas Crandell-Rees, ATCC® CCL-94™). Las condiciones de prueba fueron estándar. Las células se cultivaron durante 48 h en medio DMEM (medio de Eagle modificado por Dulbecco) suplementado con FBS al 3 % (suero bovino fetal inactivado por calor), penicilina, estreptomicina, polímeros de gentamicina y PSSNa con diferentes pesos moleculares. La Fig. 1 muestra los resultados para dos concentraciones de polímero seleccionadas: 500 pg/ml (Fig. 1 A, concentración más alta probada) y 20 pg/ml (Fig. 1 B, concentración a la que se demostró una alta actividad antiviral). Brevemente, después de cultivar células CrFK en una placa de 96 pocillos durante 24 horas, se retiró el medio antiguo y se añadieron a cada pocillo de la placa 100 pl de medio fresco que contenía la concentración de polímero seleccionada. La muestra de control no contenía polímero en el medio. A continuación, se eliminó el medio polimérico y se añadieron a cada pocillo 100 pl de medio nuevo con 20 pl de 2,3-bis-(2-metoxi-4-nitro-5-sulfenil)-(2H)-tetrazolina carboxianilida (XTT) activada. Después de 2 h de incubación, el
sobrenadante se transfirió a una placa transparente de 96 pocilios y se midió la absorbancia a 480 nm de manera convencional usando un espectrofotómetro. Los valores de los resultados obtenidos se normalizaron a la absorbancia medida para las células de control (sin polímeros), a los que se les asignó un valor de supervivencia del 100 %. Se probaron once polímeros PSSNa con diferentes pesos moleculares (1.5; 5,4; 8; 19,3; 35; 46; 93,5; 200; 400; 780 y 1200 kDa).
Los resultados obtenidos indican la falta de citotoxicidad significativa de los polímeros en el intervalo de peso molecular probado y en el intervalo de concentración probado, es decir, de 20 pg/ml a 500 pg/ml.
Ejemplo 2
El efecto del sulfonato de poliestireno de sodio (PSSNa) en la replicación del herpesvirus felino tipo 1 (FHV-1)
Para determinar la actividad del sulfonato de poliestireno de sodio (PSSNa) frente al herpesvirus felino tipo 1 (cepa C-27, ATCC: VR-636), se realizó una prueba del efecto de este polímero sobre la replicación viral. En este experimento, el polímero estuvo presente en cada etapa de la replicación viral, antes, durante y después de la infección. Brevemente, se sembraron células CrFK completamente confluentes 24 h antes del experimento en una placa de 96 pocillos. A continuación, se descartó el medio y se añadieron 20 pl de medio nuevo que contenía polímero. Las placas se incubaron durante 30 min a 37 °C, a continuación se descartó el medio con el polímero y se añadieron 50 pl de solución de polímero en DMEM al 3 % o DMEM al 3 % sin polímero (muestra control) con blanco o virus FHV-1 (cepa C-27) con un título TCID50 (50 % de la dosis infectiva del cultivo tisular) = 400/ml. Las placas se incubaron durante 2 horas a 37 °C, a continuación, las células se lavaron dos veces con 1 x PBS para eliminar las partículas virales no unidas. Por último, se añadieron 100 pl de solución de polímero en DMEM al 3 % a cada pocillo y las células se incubaron durante 48 horas. Después de este tiempo, el sobrenadante se recogió para cuantificar la infección usando (a) PCR cuantitativa (qPCR) y (b) ensayo de placa de la siguiente manera:
(a) qPCR
El aislamiento del ADN viral se llevó a cabo 48 horas después de la infección utilizando la prueba de aislamiento Viral DNA/RNA Isolation Kit (A&A Biotechnology, Polonia) de acuerdo con el protocolo proporcionado por el fabricante. El ADN así aislado fue el molde para realizar la PCR cuantitativa en tiempo real (qPCR). Se utilizaron cebadores conocidos en la técnica para amplificar un fragmento conservado de la secuencia del gen de la glicoproteína B y una sonda complementaria a este fragmento [43]. Las secuencias de cebadores y sondas utilizadas se muestran en la Tabla 1.
Tabl 1. n i l r l n iliz r l P R n i m real
Brevemente, la reacción de qPCR se llevó a cabo del siguiente modo. Se amplificaron 2,5 pl de ADN viral aislado en una reacción de 10 pl que contenía 1 x mezcla Kapa Probe Fast qPCR MasterMix (Sigma-Aldrich, Polonia), 100 nM de sonda específica marcada con 6-carboxifluoresceína (FAM) y 6-carboxitetrametilrodamina (TAMRA) (5'-FAM - TAT ATG TGT CCA CCA CCT TCA GGA TCT ACT GTC GT - TAMRA - 3'), y 450 nM de cada iniciador (5' - AGA GGC TAA CGG ACC ATC GA - 3' y 5' - GCC CGT GGT GGC TCT AAA C - 3'). La sonda específica y los cebadores mencionados anteriormente amplificaron un fragmento de secuencia de 81 pb del gen de la glicoproteína B (gB) del FHV-1 para medir el número de copias de ADN viral en la muestra [43]. La reacción se realizó en un termociclador (CFX96 Touch™ Real-197 Time PCR Detection System, Bio-Rad) en las siguientes condiciones: 3 min a 95 °C, a continuación 39 ciclos de 15 segundos a 95 °C y 30 segundos a 58 °C.
Se prepararon patrones apropiados para evaluar el número de copias de ADN viral en la muestra. El fragmento de la secuencia gB se amplificó utilizando los cebadores descritos anteriormente. El ADN así obtenido se clonó en el plásmido pTZ57R/T (Thermo Scientific, Polonia) utilizando el InsTAclone PCR Cloning Kit (Thermo Scientific, Polonia). La transformación de E. coli cepa TOP10 (Life Technologies, Polonia) y la propagación del vector plásmido se realizaron de la manera convencional. A continuación, el plásmido se purificó utilizando el GeneJET Plasmid Miniprep Kit (Thermo Scientific, Polonia) y se sometió a linealización mediante digestión con la enzima de restricción Kpnl. La concentración de ADN linealizado se evaluó mediante medidas espectrofotométricas y se calculó el número de copias de ADN en 1 ml de medio. Se usaron ocho diluciones consecutivas en serie de 10 veces como molde para la PCR en tiempo real. La capacidad de los polímeros para inhibir la replicación del virus FHV-1 se determinó como una disminución en el número de copias de ADN viral en 1 ml de medio.
b) Ensayos de placa
El análisis cuantitativo de los viriones del FHV-1 infecciosos se realizó en células CrFK que se sembraron en placas de 24 pocillos. El 80-90 % de las células confluentes se infectaron 24 horas después de la siembra mediante la adición
de diluciones en serie de 10 veces de sobrenadantes nuevos, después de lo cual las células se incubaron durante 1 hora a 37 °C en una atmósfera que contenía un 5 % de CO2. A continuación, las células se lavaron una vez con 1 x PBS para eliminar las partículas virales no unidas y se aplicó 0,5 ml de medio DMEM suplementado con suero bovino fetal inactivado por calor al 10 % (FBS, Life Technologies, Polonia), penicilina (100 U/ml), estreptomicina (100 pg/ml) y metilcelulosa al 1 % (Sigma-Aldrich, Polonia). El tiempo que tardan en formarse las placas por el virus FHV-1 es de unas 72 horas. Después de este tiempo, las células se fijaron y tiñeron con solución de cristal violeta al 0,1 % disuelta en metanol al 50 % (v/v): agua. Se contaron las placas y los valores obtenidos se representaron gráficamente como UFP (unidad formadora de placas) por ml de medio.
De esta manera, se investigó la relación entre el peso molecular del polímero y su actividad contra el virus FHV-1. El número de copias de ADN viral en 1 ml de medio se determinó mediante PCR cuantitativa en tiempo real, mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos. Tal como se muestra en la Fig. 2, la prueba de replicación se realizó utilizando polímeros con diferentes pesos moleculares y una concentración de 20 pg/ml. Los resultados de los valores obtenidos se normalizaron y se presentaron como un cambio logarítmico en relación con el control viral.
Las investigaciones realizadas han demostrado que los polímeros probados tienen actividad antiviral e inhiben la replicación del virus FHV-1. No hubo correlación entre la actividad antiviral y el peso molecular del polímero. Sin embargo, se observó que los polímeros con un peso molecular superior a 8 kDa mostraron la mejor actividad antiviral. Los polímeros con un peso molecular inferior a 8 kDa mostraron una actividad antiviral más débil.
Ejemplo 3
Relación entre la actividad antiviral del sulfonato de poliestireno de sodio (PSSNa) y su concentración en el medio
Para determinar la CI50 (50 % de concentración inhibidora, 50 % de inhibición de la replicación viral) del sulfonato de poliestireno sódico (PSSNa), se probó el efecto de diferentes concentraciones de este polímero sobre la replicación viral. Esta prueba se llevó a cabo de forma análoga a la del Ejemplo 2. Se investigó la relación entre la concentración de polímero y su actividad contra el virus FHV-1.
Brevemente, el número de copias de ADN viral en 1 ml de medio se determinó mediante PCR en tiempo real (Fig. 3 A, Fig. 3 B), mientras que las pruebas de placa permitieron determinar el número de viriones infecciosos (Fig. 3 C, Fig. 3 D). La prueba de replicación se realizó utilizando diferentes concentraciones del polímero con un peso molecular de 93,5 kDa (Fig. 3 A, Fig. 3 C) y un peso molecular de 780 kDa (Fig. 3 B, Fig. 3 D). Los valores se han normalizado al control viral.
Los valores de la CI50 calculada se muestran en la Tabla 2 siguiente.
Tabla 2. V l r I r lím r rmin r P R n i m r l n placa
Se ha demostrado que los polímeros probados inhiben la replicación del virus FHV-1, en particular a bajas concentraciones no tóxicas.
Ejemplo 4
Determinación del mecanismo de la acción antiviral de los polímeros PSSNa
El mecanismo de acción de los polímeros PSSNa se estudió de la siguiente manera. Para identificar la etapa en la que el polímero PSSNa inhibe la replicación del virus FHV-1, se realizaron las 4 pruebas funcionales descritas a continuación.
Prueba I (prueba de inactivación)
La suspensión concentrada de virus se incubó con el polímero durante 1 hora a 22 °C con agitación, y luego las muestras se diluyeron para reducir la concentración de polímero por debajo del intervalo de concentraciones en las que era activo, y el título viral se evaluó utilizando un ensayo de placa.
Esta prueba permite determinar si la inhibición se produce a través de la interacción entre el polímero y el virus, lo que previene la infección de las células. En otras palabras, puede determinar si el compuesto de prueba tiene un efecto directo sobre el virus.
Prueba II (prueba de protección celular)
Las células sembradas 24 horas antes del experimento se incubaron en presencia o ausencia de polímero durante 1 hora a 37 °C. A continuación, las placas se lavaron dos veces con 1 x PBS para eliminar las partículas de polímero no unidas, después de lo cual se añadió medio fresco con muestra simulada o el virus (400 TCID50/ml a cada pocillo en igual volumen y se incubó durante 2 horas a 37 °C. A continuación, las placas se lavaron dos veces con 1 x PBS para eliminar las partículas virales no unidas, se aplicó medio fresco a las células y se incubaron durante 48 horas a 37 °C. Finalmente, se recogieron los sobrenadantes y se cuantificó la replicación del virus mediante ensayo de placa y qPCR.
Esta prueba determina si el polímero, p. ej., mediante la unión a las superficies celulares es capaz de "protegerlas" de la infección al evitar la interacción con el receptor de entrada.
Prueba III (prueba de adherencia)
Esta prueba se llevó a cabo a 4 °C a la que se inhibe el transporte intracelular. Brevemente, las células CrFK confluentes se enfriaron a 4 °C durante 20 min. A continuación, se aplicó a las células medio fresco frío con o sin virus (400 TCID50/ml) y con o sin polímero. Las placas se incubaron durante 1 hora a 4 °C. El transporte intracelular a esta temperatura se detuvo, pero era posible la adsorción de los virus a los receptores celulares. Después de la incubación, las células se lavaron dos veces con 1 x PBS enfriado con hielo para eliminar las partículas virales no unidas y el polímero no unido, se añadió medio fresco y las células se incubaron durante 48 horas a 37 °C. Después de 48 h, se recogió el sobrenadante y se cuantificó el virus mediante qPCR y ensayo de placa.
Esta prueba permite determinar si la inhibición se produce por la competencia del polímero con el virus por el agente de adherencia y/o si el polímero, interactuando con el agente de adherencia, previene su interacción con el virus.
Prueba IV (prueba de las etapas tardías: replicación, ensamblaje y liberación)
En esta prueba, la infección se llevó a cabo primero incubando las células con el virus, a continuación, después de la incubación, los viriones no unidos se lavaron con solución de PBS y se aplicó el polímero. Brevemente, se aplicó medio fresco que contiene una muestra simulada no infecciosa o una muestra de virus (400 TCID50/ml) en igual volumen a células CrFK confluentes, a continuación las placas se incubaron durante 2 horas a 37 °C. Después de la incubación, los pocillos se lavaron dos veces con 1 x PBS para eliminar las partículas virales no unidas, a continuación se añadió a cada pocillo medio fresco que contenía la concentración de polímero seleccionada. Las placas se incubaron durante 48 h a 37 °C. Después de 48 h se recogieron los sobrenadantes, a continuación se añadió PBS por separado a los pocillos y las células se sometieron a dos ciclos de congelación y descongelación para obtener lisados celulares, la replicación del virus se cuantificó mediante ensayo de placa y qPCR.
Esta prueba muestra si la inhibición de la replicación del virus se produce en las últimas etapas de la infección, p. ej., replicación, ensamblaje, liberación. Mientras que una determinación separada del título viral en sobrenadantes y lisados celulares permite determinar si la inhibición ocurre en la etapa de replicación viral o en la etapa de liberación de viriones infecciosos.
En las pruebas descritas anteriormente, el número de copias de ADN viral en 1 ml de medio se determinó mediante PCR en tiempo real (Fig. 4 A), mientras que los ensayos de placa permitieron determinar el número de viriones (Fig. 4 B). La prueba I se llevó a cabo utilizando diferentes concentraciones de PSSNa de 93,5 kDa (Fig. 4 C) y PSSNa de 780 kDa (Fig. 4 D).
La investigación realizada mostró que el polímero interactúa directamente con el virus, lo que evita que el virus entre en la célula CrFK. También se ha demostrado que cuanto mayor es la concentración de polímero, mayor es su eficacia en la unión del FHV-1. Una inhibición muy fuerte de la infección también es visible en la etapa de adherencia, pero vale la pena señalar que durante esta prueba el polímero y el virus están al mismo tiempo en el medio de cultivo, lo que permite que el polímero se una al virus e inhiba su capacidad de internalización. La actividad antiviral también es visible en las últimas etapas de la infección, que está relacionada con la interacción de los viriones de la progenie con el polímero presente en el medio, la posibilidad de un segundo mecanismo de acción independiente fue excluido por experimentos adicionales.
Ejemplo 5
Visualización de la inhibición de la replicación del herpesvirus felino tipo 1 por dos polímeros PSSNa seleccionados por microscopía confocal
Para preparar cortes, las células CrFK se sembraron en placas de manera convencional en portaobjetos de microscopio 24 horas antes del experimento. A continuación, las células se enfriaron y se incubaron durante una hora a 4 °C de manera convencional en presencia de virus o virus y polímero. Después de un tiempo de incubación determinado, las partículas virales no unidas fueron eliminadas, las preparaciones se fijaron y tiñeron de manera convencional. Para la tinción por inmunofluorescencia, se usaron anticuerpos primarios anti-FHV-1 de ratón y anticuerpos secundarios anti-ratón de cabra conjugados con el colorante fluorescente Alexa Fluor 488 para visualizar
viriones, faloidina conjugada con Alexa Fluor 647 para teñir los filamentos de F-actina y 4',6'-diamidina-2-fenilindol (DAPI) para teñir el a Dn nuclear. Se presentaron proyecciones máximas.
La Fig. 5 muestra la visualización de la inhibición de la infección por el virus FHV-1 de células CrFK por polímeros PSSNa. La señal de cada uno de los colores se presenta por separado (canales azul, rojo y verde) y la combinación de las señales de los tres tintes (canales combinados). Los núcleos celulares se muestran en azul, F-actina en rojo y viriones del FHV-1 en verde. La figura muestra visualizaciones de células de control (muestra simulada), control viral, células tratadas con PSSNa de 93,5 kDa y células tratadas con PSSNa de 780 kDa. La barra de escala corresponde a 10 |jm.
Las visualizaciones microscópicas muestran una reducción significativa del número de viriones del FHV-1 en células CrFK en presencia de los polímeros PSSNa probados. El estudio confirma la eficacia del derivado de poliestireno sulfonado contra la infección provocada por el herpesvirus felino.
Ejemplo 6
Evaluación del efecto sinérgico de derivados de poliestireno sulfonado y análogos de nucleósidos
El efecto sinérgico de un derivado de poliestireno sulfonado representativo, PSSNa, y análogos de nucleósidos de ejemplo con un mecanismo diferente de actividad antiviral, es decir, aciclovir (ACV) y penciclovir (PCV), han sido estudiados según se conoce [44], con algunas modificaciones. El experimento se llevó a cabo en dos sistemas. Un sistema usó una concentración constante de PSSNa (compuesto II) y diferentes concentraciones del análogo de nucleósido de prueba correspondiente (compuesto I), mientras que el otro sistema usó una concentración constante del análogo de nucleósido de prueba correspondiente (compuesto II) y diferentes concentraciones de PSSNa (compuesto I). Brevemente, la prueba XTT se realizó primero como se describió anteriormente para excluir la toxicidad asociada con el fármaco, a continuación se realizó la prueba de replicación del virus como se describió anteriormente para determinar el valor de CI50 para FHV-1 cepa C-27 a 400 TCIDso/ml para ACV y PCV (usando qPCR). A continuación, se prepararon dos tipos de diluciones en serie para evaluar el efecto sinérgico de ACV/PCV y un polímero PSSNa con un peso molecular de 780 kDa (PSSNa780): (1) seis diluciones en serie de 2 veces del compuesto I a partir de una concentración igual a CI50 del compuesto I mezclado con el compuesto II a una concentración igual a CI 50 del compuesto II; (2) seis diluciones en serie de 2 veces del compuesto II a partir de una concentración igual a la CI 50 del compuesto II se mezclaron con el compuesto I a una concentración igual a la CI50 del compuesto I. Las concentraciones máximas de ambos compuestos fueron por lo tanto iguales a la mitad de su CI50. Como se ha descrito anteriormente, el ensayo de replicación del virus se llevó a cabo en células CrFK completamente confluentes. Después de 48 horas, se recogieron los sobrenadantes y se evaluó el número de viriones usando una reacción de qPCR cuantitativa de manera convencional.
El efecto sinérgico se evaluó calculando el índice de combinación (IC) de acuerdo con la fórmula:
IC = ÍL ^ l
D1 D2
(1)
en donde:
d1 es la concentración del compuesto I en presencia de una CI50 /2 del compuesto II que provoca una reducción del 50 % en el número de viriones;
d2 es la concentración del compuesto II en presencia de una CI50 /2 del compuesto I que provoca una reducción del 50 % en el número de viriones;
D1 es la CI50 del compuesto I;
D2 es la CI50 del compuesto II.
El IC indica el efecto sinérgico de los fármacos: IC > 1 significa un efecto antagonista, IC de aproximadamente 1 significa un efecto aditivo, y CI < 1 significa un efecto sinérgico.
La investigación realizada mostró que dos análogos de nucleósidos, que tienen mecanismos de acción diferentes al mecanismo de acción de PSSNa, es decir, aciclovir (ACV) y penciclovir (PCV), muestran un efecto sinérgico con la sal de sodio del sulfonato de poliestireno (PSSNa). Los valores de CI calculados para estos compuestos fueron 0,92 para PSSNa780/ACV y 0,46 para PSSNa780/PCV. Este efecto sinérgico es particularmente relevante en contextos clínicos in vivo.
Ejemplo 7
Análisis cuantitativo de la inhibición de las etapas iniciales de la infección celular después de la incubación con o sin polímero PSSNa con un peso molecular de 93,5 kDa y 780 kDa.
Las imágenes microscópicas representativas que se muestran en el Ejemplo 5 se cuantificaron en ImageJ FiJi y se
contó el número de viriones del FHV-1 C-27 por célula, tanto partículas internalizadas como adheridas a la célula. El análisis porcentual de los recuentos de virus por célula se muestra en la Fig. 6. Se demostró que después de la prueba de protección celular (prueba II), el número de viriones del FHV no disminuyó en presencia de polímero, lo cual concuerda con los resultados obtenidos previamente. También se confirmó que después de realizar la prueba de adherencia (prueba III) se observaba una disminución estadísticamente significativa en la cantidad de virus por célula en comparación con el control viral tanto después de usar el polímero con un peso molecular de 93,5 kDa como de 780 kDa. Los resultados para cada uno de los sistemas se presentan como recuentos medios de 10 células CrFK. Mediante análisis cuantitativo de imágenes microscópicas, se ha demostrado que los polímeros inhiben la infección en las etapas iniciales de la infección. El análisis porcentual obtenido de los recuentos de virus por célula concuerda con las observaciones microscópicas.
Ejemplo 8
El efecto del sulfonato de poliestireno de sodio (PSSNa) sobre la infectividad de la cepa clínica FHV-1 K7
La cepa veterinaria se obtuvo gracias a la amabilidad de los veterinarios del Refugio de Animales sin Hogar en Cracovia, quienes tomaron frotis de gatos que mostraban síntomas de infección de las vías respiratorias superiores. Se tomaron frotis de la garganta y la cavidad nasal utilizando bastoncillos de algodón especiales para el transporte de muestras clínicas virales. Para eliminar posibles infecciones bacterianas y fúngicas, las muestras se filtraron con filtros estériles, desechables con un diámetro de poro de 0,2 pm, que no debería ser una barrera para los viriones del FHV. El medio de transporte filtrado se transfirió a una placa de 12 pocillos con células CrFK confluentes. Las placas se incubaron hasta 96 horas, controlando los pocillos dos veces al día. Si el efecto citopático (ECP) era visible, el sobrenadante se recogía y se sometía a ensayos de placa (procedimiento descrito en el Ejemplo 10b). Después de 48 h, se seleccionaron placas individuales bien visibles y se perforó el agar en este sitio con una punta de pipeta estéril. A continuación, se transfirió la punta y se puso en contacto con el medio en una nueva placa de 12 pocillos que contenía células CrFK totalmente confluentes. Si se producía un efecto citopático, el sobrenadante se transfería y dividía en alícuotas en tubos de congelación nuevos y se conservaba a -80 °C. La afiliación de especies de cada cepa se confirmó mediante secuenciación de fragmentos de secuencia para la TK timidina cinasa. El origen de la cepa clínica FHV-1 K7 se caracteriza en la Tabla 3.
Tabla 3. Ori en de la ce a clínica de FHV.
Para determinar la actividad antiviral del sulfonato de poliestireno de sodio (PSSNa) frente a la cepa clínica aislada FHV-1 K7, se probó el efecto de diferentes concentraciones de este polímero con dos pesos moleculares seleccionados (93,5 kDa y 780 kDa) sobre la infección viral. La prueba de replicación viral se llevó a cabo de manera análoga al Ejemplo 2. Brevemente, se determinó un cambio logarítmico en el número de copias de ADN viral por ml del material infeccioso aislado mediante PCR cuantitativa en tiempo real (Fig. 7A), mientras que los ensayos de placa permitieron determinar el cambio logarítmico en el número infeccioso de viriones (Fig. 7B). Los valores se normalizaron al control viral, es decir, células infectadas no incubadas con el polímero.
Las pruebas confirmaron que los polímeros probados tienen actividad antiviral también contra la cepa clínica del FHV en concentraciones bajas no tóxicas. El polímero inhibió por completo la replicación viral, tanto el número de copias de ADN viral como el número de viriones infecciosos estaban por debajo del umbral de detección.
Ejemplo 9
Prueba de interacción: análisis de la capacidad de unión del virus FHV-1 a superficies recubiertas con polímero PSSNa, análisis de la interacción directa virus-polímero.
La prueba de interacción permite determinar si existe una interacción directa entre el inhibidor y el virus. Se colocaron cubreobjetos estériles dentro de una placa de 12 pocillos. Para compensar la carga negativa de los cubreobjetos, se incubaron con FBS al 3 % o colágeno bovino (Purecol) en PBS durante 2 h a 37 °C, los portaobjetos incubados en PBS fueron el control. A continuación, los portaobjetos se lavaron dos veces con PBS y se incubaron con solución de PBS o se añadió polímero a una concentración de 20 pg/ml en una cantidad de 1 ml por pocillo. Las muestras se incubaron durante 2 horas a 37 °C. Esta etapa consiste en cubrir los portaobjetos con un polímero cargado negativamente. A continuación, las partículas de polímero no unidas se lavaron con solución de PBS. La siguiente etapa fue la incubación de portaobjetos con una suspensión viral de TCID50 igual a 63.000.000/ml o control durante 2 horas a 37 °C. Se asumió que si existe una interacción directa entre el polímero y el virus, los viriones se unirán a la superficie cubierta con el polímero. Las partículas no unidas se eliminaron por lavado con solución de PBS y el material
se preparó para obtener imágenes de microscopía confocal. Se realizó tinción inmunofluorescente, se visualizaron las preparaciones y luego se contó el número de partículas virales por plano confocal en ImageJ FiJi. El análisis cuantitativo se muestra en la Fig. 8.
Ejemplo 10
Efecto del sulfonato de poliestireno de sodio (PSSNa) en la infección por FCV
Para determinar la actividad antiviral del sulfonato de poliestireno de sodio (PSSNa) frente al FCV (cepa F-9, ATCC® VR-782™), se realizó una prueba del efecto de los compuestos sobre la infección viral. En este experimento, el polímero estuvo presente en cada etapa de la infección viral. En el experimento, se usaron células CrFK completamente confluentes después de 24 horas desde la siembra en una placa de 96 pocillos. Se eliminó el medio y se añadieron 20 pl de medio fresco que contenía polímero. Las placas se incubaron durante 30 min a 37 °C, a continuación se eliminó el medio con el polímero y se añadieron 50 pl de solución de polímero en DMEM al 3 % o DMEM al 3 % sin polímero (muestra de control), sin virus (muestra de control) o con FCV título 400 TCIDso/ml. Las placas se incubaron durante 1,5 horas a 37 °C, a continuación las células se lavaron dos veces con solución de PBS para eliminar las partículas virales no unidas. Por último, se añadieron 100 pl de solución de polímero en DMEM al 3 % a cada pocillo y las células se incubaron durante 18 horas. Después de este tiempo, se recogió el sobrenadante para evaluar el número de virus usando (a) RT-PCR cuantitativa (RT-qPCR) y (b) ensayos de placa, como se indica a continuación:
a) RT - qPCR
El aislamiento del ARN viral se llevó a cabo de manera convencional utilizando un kit de aislamiento de ARN comercializado (Viral DNA/RNA Isolation Kit, A&A Biotechnology, Polonia) de acuerdo con el protocolo proporcionado por el fabricante. El ARN aislado se transcribió de forma inversa (RT) utilizando un kit comercializado (High Capacity cDNA Reverse Transcription Kit, Life Technologies, Polonia). El cADN así obtenido fue el molde para realizar la PCR cuantitativa en tiempo real (qPCR). Se utilizaron cebadores conocidos en la técnica para amplificar un fragmento conservativo de la secuencia del genoma del FCV y una sonda complementaria a este fragmento [63]. Las secuencias de los cebadores y la sonda utilizados se muestran en la Tabla 4.
Tabla 4. n i l r l n iliz r l P R n i iv n i mpo real
Brevemente, la reacción de qPCR se llevó a cabo del siguiente modo. Se amplificaron 2,5 pl de ADN viral aislado en una reacción de 10 pl que contenía 1 * mezcla Kapa Probe Fast qPCR MasterMix (Sigma-Aldrich, Polonia), 100 nM de una sonda específica marcada con 6-carboxifluoresceína (FAM) y 6-carboxitetrametilrodamina (TAMRA) (5' - FAM - CTT AAA TAY TAT GAT TGG GAY CCC CA - TAMRA - 3'), y 450 nM de cada iniciador (5' - CAA CCT GCG CTA ACG - 3' y 5' - TCC CAY ACA GTT CCA AAT T - 3'). La sonda y los cebadores específicos antes mencionados se usaron para amplificar un fragmento de secuencia de 151 pb derivado del genoma del FCV para medir el número de copias de ARN viral en la muestra [63]. La reacción se llevó a cabo en un termociclador (CFX96 Touch™ Real-197 Time PCR Detection System, Bio-Rad) en las siguientes condiciones: 3 min a 95 °C, a continuación 39 ciclos de 15 segundos a 95 °C y 30 segundos a 51 °C.
Se prepararon patrones apropiados para evaluar el número inicial de moléculas de ARN viral en la muestra. El fragmento de secuencia transcrito de ADNc se amplificó utilizando los cebadores descritos anteriormente. El ADN así obtenido se clonó en el plásmido pTZ57R/T (Thermo Scientific, Polonia) utilizando el InsTAclone PCR Cloning Kit (Thermo Scientific, Polonia). La transformación de E. coli cepa TOP10 (Life Technologies, Polonia) y la propagación del vector plásmido se realizaron de la manera convencional. A continuación, el plásmido se purificó utilizando el GeneJET Plasmid Miniprep Kit (Thermo Scientific, Polonia) y se sometió a linealización mediante digestión con la enzima de restricción Kpnl. La concentración de ADN linealizado se evaluó mediante medidas espectrofotométricas y se calculó el número de copias por mililitro. Se usaron ocho diluciones en serie de 10 veces como molde para la PCR en tiempo real. La capacidad de los polímeros para inhibir la replicación del FCV se determinó como una reducción en el número de copias de ARN viral en función del logaritmo por mililitro de medio.
b) Ensayos de placa
El análisis cuantitativo de los viriones infecciosos del FCV se llevó a cabo mediante ensayos de placa utilizando agarosa de bajo punto de fusión. Se prepararon diluciones en serie de 10 veces de los sobrenadantes recogidos, a continuación se aplicó a las células y se incubó durante 1 hora. A continuación, se retiró el medio y se aplicó a las células agarosa líquida al 0,6 % mezclada con el medio de cultivo DMEM. Las placas se incubaron a temperatura
ambiente durante aproximadamente 20 minutos y a continuación las placas se transfirieron a la incubadora. El tiempo necesario para que se formaran las placas fue de unas 24 horas. Después de este tiempo, las células se fijaron durante un mínimo de 12 h (el tiempo necesario para penetrar en la agarosa) con una solución de formaldehído al 4 % y a continuación se tiñeron con una solución de violeta cristal al 0,1 % disuelta en metanol:agua al 50 % (v/v). Las placas se contaron y representaron gráficamente como el número de UFP (unidad formadora de placa) por ml.
La investigación realizada ha demostrado que los polímeros probados presentan actividad antiviral e inhiben la replicación del FCV. Se ha demostrado una relación positiva entre la actividad antiviral y el peso molecular del polímero. Los resultados se resumen en la Fig. 9.
Ejemplo 11
La relación entre la actividad antiviral del sulfonato de poliestireno de sodio (PSSNa) y su concentración en el medio Para determinar la CI50 de la sal sódica de poliestireno sulfonato (PSSNa), se probó el efecto de varias concentraciones de este polímero sobre la infección viral. Esta prueba se llevó a cabo de forma análoga a la del Ejemplo 10. Se investigó la relación entre la concentración de polímero y su actividad contra el FCV. Brevemente, el número de copias de ARN viral por ml se determinó mediante RT-qPCR (Fig. 10 A, Fig. 10 B), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 10 C, Fig. 10 D). La prueba se llevó a cabo utilizando polímeros con un peso molecular de 93,5 kDa (Fig. 10 A, Fig. 10 C) y 780 kDa (Fig. 10 B, Fig. 10 D) en varias concentraciones. Los valores se han normalizado al control viral.
Los valores de la CI50 calculada se muestran en la Tabla 5 siguiente.
Tabla 5. V l r I rmin r lím r m i n RT- P R n i m r l n o de placa
La investigación realizada ha demostrado que los polímeros probados tienen actividad antiviral e inhiben la replicación del FCV en bajas concentraciones no tóxicas.
Ejemplo 12
Determinación del mecanismo de acción antiviral de los polímeros PSSNa
Para determinar el mecanismo de acción del polímero PSSNa e identificar la etapa en la que el PSSNa inhibe la infección celular inducida por FCV, se realizaron las 4 pruebas funcionales que se describen a continuación a una concentración de polímero de 200 pg/ml.
Prueba I (prueba de inactivación)
La suspensión concentrada de virus se incubó con el polímero durante 1 hora a 22 °C con agitación, y a continuación las muestras se diluyeron para reducir la concentración de polímero por debajo del intervalo de concentraciones en las que es activo. Los títulos de virus se evaluaron usando un ensayo de placa.
La prueba I permite determinar si la inhibición se produce a través de la interacción entre el polímero y el virus, en otras palabras, permite determinar si el compuesto de prueba tiene un efecto directo sobre el virus.
Prueba II (prueba de protección celular)
Se incubaron células CrFK totalmente confluentes en presencia o ausencia del polímero durante 1 hora a 37 °C. Las placas se lavaron a continuación dos veces con 1 x p Bs para eliminar las partículas de polímero no unidas, después de lo cual se añadió medio fresco sin virus (muestra de control) o con virus (400 TCID50/ml) a cada pocillo en igual volumen y se incubó durante 1,5 horas a 37 °C. Las placas se lavaron a continuación dos veces con 1 x PBS para eliminar las partículas virales no unidas. Se aplicó medio fresco a las células y se incubaron durante 18 horas a 37 °C. Finalmente, se recogió el sobrenadante del cultivo para evaluar la eficiencia de la replicación mediante la cuantificación del número de partículas virales infecciosas y el número de copias de ARN viral mediante ensayos de placa y reacciones de RT-qPCR, respectivamente.
Esta prueba determina si el polímero, p. ej., mediante la unión a las superficies celulares es capaz de "protegerlas" de la infección al evitar la interacción con el receptor de entrada.
Prueba III (prueba de adherencia)
Esta prueba se llevó a cabo a 4 °C a la que se inhibe el transporte intracelular. Brevemente, las células CrFK completamente confluentes se enfriaron a 4 °C durante 20 min. Después, se aplicó medio fresco sin virus (muestra de control) o con virus (400 TCID50/ml) con o sin polímero a las células. Las placas se incubaron durante 1 hora a 4 °C. El transporte intracelular a esta temperatura se detuvo, aunque era posible la adsorción de virus a los receptores celulares. Después de la incubación, las células se lavaron dos veces con 1 x PBS enfriado con hielo para eliminar las partículas virales no unidas y el polímero no unido, se añadió medio fresco y las células se incubaron durante 18 horas a 37 °C. Después de 18 h, se recogió el sobrenadante y se cuantificó el número de partículas virales mediante RT-qPCR y ensayos de placa.
Esta prueba permite determinar si la inhibición se produce por la competencia del polímero con el virus por el agente de adherencia y/o si el polímero, interactuando con el agente de adherencia, previene su interacción con el virus.
Prueba IV (etapas tardías: replicación, ensamblaje y liberación)
En esta prueba, la infección se llevó a cabo primero incubando las células con el virus, y sólo después de la infección se aplicó el polímero. Se aplicó medio fresco que contenía una muestra no infecciosa o una muestra de virus (400 TCID50/ml) a células CrFK confluentes, a continuación las placas se incubaron durante 1,5 h a 37 °C. Después de la incubación, los pocillos se lavaron dos veces con PBS para eliminar las partículas virales no unidas, a continuación se añadió a cada pocillo medio fresco que contenía la concentración de polímero seleccionada. Las placas se incubaron durante 18 horas a 37 °C. Después de 18 h se recogieron los sobrenadantes, a continuación se añadió PBS por separado a los pocillos y las células se sometieron a dos ciclos de congelación y descongelación para obtener lisados celulares, a continuación se evaluó la replicación del virus y se cuantificó usando ensayos de placa y RT-qPCR.
Esta prueba permite determinar si la inhibición de la propagación del virus se produce en etapas tardías de la infección, p. ej., replicación, ensamblaje o liberación.
Después de realizar cada una de las pruebas funcionales, las células se incubaron durante 18 horas a 37 °C. Después de este tiempo, se recogió el sobrenadante (y el lisado celular en el caso de la prueba IV) y se realizaron ensayos de placa y RT-qPCR en tiempo real para identificar la etapa en la que se inhibe la infección. La excepción fue la prueba I, para la cual, por razones técnicas, sólo se podían realizar ensayos de placa.
En las pruebas descritas anteriormente, el número de copias de ARN viral en 1 ml de medio se determinó mediante RT-qPCR en tiempo real (Fig. 11A), mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos en la muestra (Fig. 11B). Los ensayos se realizaron utilizando diferentes concentraciones de polímeros con un peso molecular de 93,5 kDa (Fig. 11 C) y 780 kDa (Fig. 11 D).
Como resultado de la investigación, se determinó que los polímeros PSSNa presentan actividad antiviral en las etapas tardías de la infección (prueba IV), probablemente en la etapa de replicación viral. La eficacia antiviral de los polímeros con un peso molecular de 93,5 kDa y 780 kDa en las etapas tardías de la infección fue similar, mientras que el polímero con mayor peso molecular en la prueba general (Fig. 11) es más eficaz, lo que indica un posible mecanismo adicional de su acción. Esta observación concuerda con los resultados de la prueba III, que indican que un polímero de mayor peso molecular inhibe la infección viral también en las primeras etapas de la infección, en la etapa de adherencia del virus a la superficie celular, mientras que el polímero de menor peso molecular no tenía la capacidad de inhibir el virus en esta etapa (Fig. 11 C, Fig. 11 D).
Ejemplo 13
Visualización de la inhibición de las etapas iniciales de la infección celular inducida por el FCV por el polímero PSSNa con masa molecular de 93,5 kDa y 780 kDa por microscopía confocal
Para hacer preparaciones para obtener imágenes usando un microscopio confocal, las células CrFK se sembraron en portaobjetos de microscopio 24 horas antes del experimento. A continuación, las células se enfriaron y se incubaron durante una hora a 4 °C en presencia de virus o virus y polímero, de manera convencional. Después de un tiempo de incubación determinado, las partículas virales no unidas fueron eliminadas, las preparaciones fijadas y teñidas de manera convencional. Para la tinción por inmunofluorescencia, se usaron anticuerpos primarios dirigidos contra la proteína de la cápside del FCV (número de catálogo: sc-80785, Santa Cruz CA, EE. UU.), seguido de anticuerpos secundarios conjugados con Alexa Fluor 488 (Invitrogen, Polonia) para visualizar viriones, faloidina conjugada con Alexa Fluor 647 (Invitrogen, Polonia) para teñir F-actina y DAPI (Sigma-Aldrich, Polonia) para teñir ADN nuclear. Se presentaron proyecciones máximas.
La Fig. 12 muestra una visualización de la inhibición de la infección de células CrFK inducida por el FCV por polímeros PSSNa. La señal de cada color (canales azul, rojo y verde) y la combinación de señales de los tres tintes (canales combinados) se presentan por separado. Los núcleos celulares (ADN nuclear) se muestran en azul, la actina F se muestra en rojo y los viriones del FCV se muestran en verde. La figura muestra visualizaciones de células de control no infectadas, control viral, 1000 pg/ml de células tratadas con PSSNa93,5 y 1000 pg/ml de células tratadas con PSSNa780. La barra de escala corresponde a 10 pm.
Las visualizaciones microscópicas muestran una disminución significativa en el número de viriones del FCV presentes en las células CrFK en presencia del polímero PSSNa con un alto peso molecular de 780 kDa, mientras que la disminución en el número de viriones del FCV después de usar un polímero con un peso molecular de 93,5 kDa no es apreciable. El estudio confirma la eficacia del derivado de poliestireno sulfonado, en particular el de alto peso molecular, en la inhibición de la infección inducida por FCV también en las etapas iniciales de la infección.
Ejemplo 14
Análisis cuantitativo de la inhibición de las etapas iniciales de la infección celular después de la incubación con o sin polímero PSSNa con un peso molecular de 93,5 kDa y 780 kDa
Las imágenes microscópicas representativas del Ejemplo 13 se cuantificaron en ImageJ FiJi y se contó el número de viriones del FCV F9 por célula, tanto partículas internalizadas como adheridas a la superficie celular. Se demostró que después de la prueba de protección celular (prueba II) el número de viriones del FCV F9 no disminuyó en presencia de polímero, lo cual concuerda con los resultados obtenidos previamente. También se comprobó que después de realizar la prueba de adherencia (prueba III) se observó una reducción estadísticamente significativa en el número de virus por célula en comparación con el control viral, pero solo en el caso de un polímero con un peso molecular más alto. Los resultados para cada uno de los sistemas se presentan como recuentos medios de 10 células CrFK. El análisis cuantitativo de las imágenes microscópicas mostró que un polímero con un peso molecular de 780 kDa también inhibía la infección en las etapas iniciales de la infección. Para un polímero con un peso molecular de 93,5 kDa, no hubo diferencia estadísticamente significativa entre las células de control y las incubadas con el inhibidor. El análisis porcentual obtenido de los recuentos de virus por célula concuerda con las observaciones microscópicas.
Ejemplo 15
El efecto del sulfonato de poliestireno de sodio (PSSNa) sobre la infectividad de las cepas clínicas del FCV
Las cepas veterinarias se obtuvieron gracias a la amabilidad de los veterinarios de la clínica veterinaria 'Ambuvet' y del Refugio de Animales sin Hogar en Cracovia, quienes tomaron frotis de gatos que mostraban síntomas de infección de las vías respiratorias superiores. Se tomaron frotis de la garganta y la cavidad nasal utilizando bastoncillos de algodón especiales para el transporte de muestras clínicas virales. Para eliminar posibles infecciones bacterianas y fúngicas, las muestras se filtraron con filtros estériles, desechables con un diámetro de poro de 0,2 pm, que no debería ser una barrera para los calicivirus con un diámetro de unos 35 nm. El medio de transporte filtrado se transfirió a una placa de 12 pocillos con células CrFK confluentes. Las placas se incubaron hasta 96 horas, controlando los pocillos dos veces al día. Si el efecto citopático (ECP) era visible, se tomaba el sobrenadante para ensayos de placa (procedimiento descrito en el Ejemplo 10b). Después de 24 horas, se seleccionaron placas individuales bien visibles y se perforó el agar en este sitio con una punta de pipeta estéril. A continuación, se transfirió la punta y se puso en contacto con el medio en una nueva placa de 12 pocillos que contenía células CrFK totalmente confluentes. Si se producía un efecto citopático, el sobrenadante se transfería y se dividía en alícuotas en tubos de congelación nuevos y se conservaba a -80 °C. La afiliación de especies de cada cepa se confirmó mediante secuenciación de fragmentos de secuencia para la proteína principal de la cápside VP1. El origen de seis cepas veterinarias (FCV K1, K2, K3, K5, K8 y K10) se caracterizan en la Tabla 6.
Tabla 6. Ori en de las ce as clínicas del FCV.
continuación
Para determinar la actividad antiviral del sulfonato de poliestireno de sodio (PSSNa) frente a cepas clínicas aisladas del FCV, se probó el efecto de diferentes concentraciones de este polímero con dos pesos moleculares seleccionados (93,5 kDa y 780 kDa) sobre la infección viral. El ensayo de replicación viral se llevó a cabo de manera análoga al Ejemplo 9. Brevemente, las copias de ARN viral por ml se determinaron mediante transcripción inversa y PCR cuantitativa en tiempo real, mientras que los ensayos de placa permitieron determinar el número de viriones infecciosos (Fig. 14). Los valores se normalizaron al control viral, es decir, células infectadas no incubadas con el polímero.
La investigación realizada confirmó que los polímeros probados tienen actividad antiviral contra todas las cepas clínicas aisladas del FCV en concentraciones bajas no tóxicas. La replicación de cada una de las cepas clínicas se redujo al menos 20 veces (cepa FCV K1), mientras que en el caso de dos cepas (FCV K5 y K10) la infección se inhibió por completo. Se demostró una relación positiva entre la actividad antiviral y el peso molecular, idéntica a la de la cepa de laboratorio FCV F9, cuyos resultados se muestran en el Ejemplo 10.
Ejemplo 16
Prueba de interacción: análisis de la capacidad de unión del virus FCV a superficies recubiertas con polímero PSSNa, análisis de la interacción directa virus-polímero.
La prueba de interacción permite determinar si existe una interacción directa entre el inhibidor y el virus. Se colocaron cubreobjetos estériles dentro de una placa de 12 pocillos. Para compensar la carga negativa de los cubreobjetos, se incubaron con FBS al 3 % o colágeno bovino (Purecol) en PBS durante 2 h a 37 °C, los portaobjetos incubados en PBS fueron el control. A continuación, los portaobjetos se lavaron dos veces con PBS y se añadió una solución o polímero de PBS a una concentración de 20 pg/ml en una cantidad de 1 ml por pocillo. Las muestras se incubaron durante 2 horas a 37 °C. Esta etapa consiste en cubrir los portaobjetos con un polímero cargado negativamente. A continuación, las partículas de polímero no unidas se lavaron con solución de PBS. La siguiente etapa fue la incubación de portaobjetos con una suspensión viral de TCID50 igual a 13.000.000/ml o control durante 2 horas a 37 °C. Se asumió que si existe una interacción directa entre el polímero y el virus, los viriones se unirán a la superficie cubierta con el polímero. Las partículas no unidas se eliminaron por lavado con solución de PBS y el material se preparó para obtener imágenes de microscopía confocal. Se realizó tinción inmunofluorescente, se visualizaron las preparaciones y luego se contó el número de partículas virales por plano confocal en ImageJ FiJi.
Para portaobjetos recubiertos con PSSNa 780 kDa, el número de viriones fue mucho mayor que para los portaobjetos no recubiertos con polímero o recubiertos con PSSNa 93,5 kDa. Vale la pena señalar que para portaobjetos recubiertos con FBS y recubiertos con PSSNa93,5, también se observó un aumento estadísticamente significativo en el número de viriones por plano confocal, sin embargo, era mucho más pequeño que en el caso del PSSNa780. Los resultados anteriores indican que el PSSNa 780 kDa interactúa directamente con la partícula viral, pero se desconoce la influencia de esta interacción en la infectividad del FCV.
Ejemplo 17
Determinación de la actividad antiviral in vitro del hidrogel de PEG-PSSNa
El objetivo del estudio fue determinar la formulación en la que se puede aplicar PSSNa a la piel del animal y luego determinar el efecto de la formulación sobre el proceso de infección y la toxicidad transdérmica de la formulación.
La primera etapa determinó la mayor concentración no tóxica de polietilenglicol con un peso molecular de 400 Da (PEG, Sigma-Aldrich, Polonia, Pm = 400) (PEG400)), que se puede utilizar para experimentos in vitro utilizando la línea celular CrFK. Con este fin, se prepararon 8 soluciones de polímero PEG con concentraciones: 100, 50, 40, 30, 25, 20, 15 y 10 mg/ml. Las células se incubaron con el polímero a una concentración específica durante 48 h, seguido de un ensayo XTT análogo a los ejemplos anteriores. Se ha demostrado que las concentraciones superiores a 30 mg/ml son tóxicas para las células CrFK y no se pueden utilizar en otros experimentos. Por lo tanto, en estudios posteriores se decidió utilizar la concentración no tóxica más alta de PEG400 de 30 mg/ml. Los resultados de citotoxicidad normalizados al control (células no tratadas con polímero) se muestran en la Fig. 16 A.
Para preparar el hidrogel de PSSNa-PEG, el PSSNa de 1000 kDa (PSSNa1000kDa) se disolvió en agua y luego se añadió gota a gota a la solución de PEG400 diluida en medio de cultivo DMEM. La concentración final de PSSNa1000kDa en la solución fue de 200 pg/ml, mientras que la concentración de PEG400 fue de 30 mg/ml.
Para comprobar que el hidrogel por sí solo no afecta a la actividad antiviral del principio activo PSSNa, se realizó una prueba de replicación viral. Brevemente, las células CrFK se infectaron en presencia de un hidrogel antes, durante y después de la infección. Los experimentos se llevaron a cabo de forma análoga a la descrita en los ejemplos anteriores. Las células se incubaron durante 18 h (infección por FCV) o 48 h (infección por FHV-1). Después de este tiempo, se recogió el sobrenadante, seguido de PCR en tiempo real y los títulos de virus se verificaron mediante ensayos de placa. Los resultados obtenidos se muestran en la Figura l6 para el virus FHV-1 (B, C) y para el virus FCV (D, E).
Se ha demostrado que la composición del hidrogel no es tóxica y no afecta a la actividad antiviral del sulfonato de poliestireno de sodio.
Ejemplo 18
Determinación de la toxicidad dérmica del sulfonato de poliestireno de sodio en un modelo de ratón
El objetivo del experimento fue determinar la dosis dérmica máxima no tóxica de sulfonato de poliestireno de sodio en un modelo de ratón. El material de prueba fueron ratones hembra de 6 semanas de edad de la cepa BALB/c obtenidos del Centro de Medicina Experimental de la Universidad Médica de Bialystok. El consentimiento para el experimento N.° 281/2018 se obtuvo de la 2.a Comisión de Ética Local para Experimentos con Animales en Cracovia en el Instituto de Farmacología de la Academia de Ciencias de Polonia. Los animales fueron puestos en cuarentena durante 5 días. Después de la cuarentena, se realizó un examen médico general y veterinario.
Durante la cuarentena y el experimento, los animales permanecieron en habitaciones con parámetros controlados: temperatura 22 °C ± 2 °C, humedad 55 % ± 5 % e iluminación: artificial, fotoperíodo: 12 horas de luz/12 horas de oscuridad. Se utilizó alimentación de mantenimiento de Altromin. Solo los individuos sanos seleccionados al azar fueron calificados para el experimento. Los animales se dividieron en grupos, en cada experimento el grupo contenía 5 individuos: grupo de control - solución salina, grupo experimental - PSSNa 50 mg/ml, grupo experimental - PSSNa 75 mg/ml, grupo experimental - PSSNa 100 mg/ml.
El material de prueba se aplicó directamente a la piel dorsal afeitada en un volumen de 100 pl/ratón, una vez al día durante 7 días. Se realizaron observaciones clínicas detalladas diariamente desde el día de la administración del compuesto. La medición del peso corporal del animal se llevó a cabo antes de la administración del material de prueba y diariamente durante la observación. Al final del experimento, los animales se sometieron a eutanasia. Se realizaron necropsias y se recogió sangre para análisis bioquímico.
El hidrogel de PSSNa-PEG se preparó mezclando PEG con un peso molecular de 400 Da con agua (en una proporción de 9:1, volumen/volumen). El PSSNa se disolvió en agua y a continuación se añadió gota a gota a la solución de PEG. El análisis de toxicidad dérmica se realizó utilizando un hidrogel con una concentración de PSSNa de 50, 75 y 100 mg/ml. Después de 5 días de cuarentena, se afeitó a los ratones en el lado lateral del lomo y luego se aplicaron 100 pl de hidrogel o solución salina a la piel afeitada. El experimento duró 7 días, el hidrogel se aplicó diariamente. Los ratones se pesaron y controlaron todos los días (las medidas de peso diarias se muestran en las Tablas 7a-b). Después de 7 días, los ratones restantes fueron sacrificados por dislocación cervical. La piel en el sitio de la inyección de hidrogel se controló de cerca para detectar enrojecimiento, ulceración u otras lesiones de la piel cada día de acuerdo con la siguiente escala de salud:
0 - buena salud, sin síntomas evidentes
1 - apatía, piel levantada
2 - silueta encorvada, ligera pérdida de peso
3 - anorexia, aumento del esfuerzo respiratorio y mayor pérdida de peso
4 - agonía
5 - muerte
Los resultados de salud se muestran en las Tablas 8a-b.
Después de la eutanasia animal, se recogió sangre, hígado, riñón y bazo para su posterior análisis. El análisis bioquímico incluyó GLU (mg/dl), BUN (mg/dl), ALP (Ul/l), TP (g/dl), GPT (Ul/l) y CRE (mg/dl). Los resultados de los análisis bioquímicos se presentan en las Tablas 9a-b.
En estudios con animales, el sulfonato de poliestireno después de la administración directa sobre la piel a dosis de 50, 75 y 100 mg/ml no provocó síntomas clínicos. No se observaron síntomas clínicos durante las pruebas bioquímicas y la medición del peso en animales. Después de las necropsias, no se encontraron cambios macroscópicos en los órganos.
El sulfonato de poliestireno sódico administrado durante 7 días sobre la piel en forma de hidrogel con polímero PEG a dosis de 50, 75 y 100 mg/ml no es tóxico para los animales y puede utilizarse en el futuro para probar la actividad antiviral en animales.
T l 7 : M ii n l r r l l r n r n l x rim n i i m r 218)
T l 7 : M ii n l r r l l r n r n l x rim n n r 21 )
Tabla 8a: Observaciones clínicas durante el ex erimento diciembre de 2018)
I
Tabla 8b: Observaciones clínicas durante el experimento enero de 2019)
Tabla 9a: Resultados del análisis bio uímico tras la eutanasia del animal diciembre de 2018
continuación
Tabla 9b: Resultados del análisis bioquímico tras la eutanasia del animal enero de 2019
Bibliografía
1. Helps, C.R. et al., Factors associated with upper respiratory tract disease caused by feline herpesvirus, feline calicivirus, Chlamydophila felis and Bordetella bronchiseptica in cats: experience from 218 European catteries. Vet Rec, 2005. 156(21): pp. 669-73.
2. Binns, S.H. et al., A study of feline upper respiratory tract disease with reference to prevalence and risk factors for infection with feline calicivirus and feline herpesvirus. J Feline Med Surg, 2000. 2(3): pp. 123-33.
3. Bannasch, M.J. and J.E. Foley, Epidemiologic evaluation of multiple respiratory pathogens in cats in animal shelters. J Feline Med Surg, 2005. 7(2): pp. 109-19.
4. Fernandez, M. et al., Prevalence of feline herpesvirus-1, feline calicivirus, Chlamydophila felis and Mycoplasma felis DNA and associated risk factors in cats in Spain with upper respiratory tract disease, conjunctivitis and/or gingivostomatitis. J Feline Med Surg, 2017. 19(4): pp. 461-469.
5. Cohn, L.A., Feline respiratory disease complex. Vet Clin North Am Small Anim Pract, 2011. 41(6): pp. 1273-89.
6. Fields BN, K.D., Howley PM, Fields virology. 6th ed., ed. W.K. Health/Lippincott and W. Wilkins. 2013.
7. Xu, F. et al., Seroprevalence and coinfection with herpes simplex virus type 1 and type 2 in the United States, 1988-1994. J Infect Dis, 2002. 185(8): pp. 1019-24.
8. Gaskell, R.M. and R.C. Povey, Experimental induction of feline viral rhinotracheitis virus re-excretion in FVR-recovered cats. Vet Rec, 1977. 100(7): pp. 128-33.
9. Maggs, D.J. et al., Evaluation of serologic and viral detection methods for diagnosing feline herpesvirus-1 infection in cats with acute respiratory tract or chronic ocular disease. J Am Vet Med Assoc, 1999. 214(4): pp. 502 7.
10. Gould, D., Feline herpesvirus-1: ocular manifestations, diagnosis and treatment options. J Feline Med Surg, 2011. 13(5): pp. 333-46.
11. Hartley, C., Aetiology of corneal ulcers assume FHV-1 unless proven otherwise. J Feline Med Surg, 2010. 12(1): pp. 24-35.
12. Bistner, S.I. et al., Ocular manifestations of feline herpesvirus infection. J Am Vet Med Assoc, 1971. 159(10): pp. 1223-37.
13. Stiles, J., Feline herpesvirus. Clin Tech Small Anim Pract, 2003. 18(3): pp. 178-85.
14. Gaskell, R.M. and R.C. Povey, Re-excretion of feline viral rhinotracheitis virus following corticosteroid treatment. Vet Rec, 1973. 93(7): pp. 204-5.
15. Nasisse, M.P. et al., Isolation of feline herpesvirus 1 from the trigeminal ganglia of acutely and chronically infected cats. J Vet Intern Med, 1992. 6(2): pp. 102-3.
16. Miller, W.H. and R.L. Miller, Phosphorylation of acyclovir diphosphate by cellular enzymes. Biochem Pharmacol, 1982. 31(23): pp. 3879-84.
17. Miller, W.H. and R.L. Miller, Phosphorylation of acyclovir (acycloguanosine) monophosphate by GMP kinase. J Biol Chem, 1980. 255(15): pp. 7204-7.
18. Elion, G.B., The biochemipy and mechanism of action of acyclovir. J Antimicrob Chemother, 1983. 12 Suppl B: pp. 9-17.
19. Maggs, D.J., Update on pathogenesis, diagnosis, and treatment of feline herpesvirus type 1. Clin Tech Small Anim Pract, 2005. 20(2): pp. 94-101.
20. Maggs, D.J. and H.E. Clarke, In vitro efficacy of ganciclovir, cidofovir, penciclovir, foscarnet, idoxuridine, and acyclovir against feline herpesvirus type-1. Am J Vet Res, 2004. 65(4): pp. 399-403.
21. Nasisse, M.P. et al., In vitro susceptibility of feline herpesvirus-1 to vidarabine, idoxuridina, trifluridine, acyclovir, or bromovinyldeoxyuridine. Am J Vet Res, 1989. 50(1): pp. 158-60.
22. Collins, P., The spectrum of antiviral activities of acyclovir in vitro and in vivo. J Antimicrob Chemother, 1983.
12 Suppl B: pp. 19-27.
23. Soul-Lawton, J. et al., Absolute bioavailability and metabolic disposition of valaciclovir, the L-valyl ester of acyclovir, following oral administration to humans. Antimicrob Agents Chemother, 1995. 39(12): pp. 2759-64. 24. Nasisse, M.P. et al., Effects of valacyclovir in cats infected with feline herpesvirus 1. Am J Vet Res, 1997. 58(10): pp. 1141-4.
25. Hussein, I.T., R.V. Menashy, and H.J. Field, Penciclovir is a potent inhibitor of feline herpesvirus-1 with susceptibility determined at the level of virus-encoded thymidine kinase. Antiviral Res, 2008. 78(3): pp. 268-74. 26. Groth, A.D. et al., In vitro cytotoxicity and antiviral efficacy against feline herpesvirus type 1 of famciclovir and its metabolites. Vet Ophthalmol, 2014. 17(4): pp. 268-74.
27. Thomasy, S.M. et al., Evaluation of orally administered famciclovir in cats experimentally infected with feline herpesvirus type-1. Am J Vet Res, 2011. 72(1): pp. 85-95.
28. Malik, R. et al., Treatment of feline herpesvirus-1 associated disease in cats with famciclovir and related drugs. J Feline Med Surg, 2009. 11(1): pp. 40-8.
29. Filer, C.W. et al., Metabolic and pharmacokinetic studies following oral administration of 14C-famciclovir to healthy subjects. Xenobiotica, 1994. 24(4): pp. 357-68.
30. Pue, M.A. et al., Linear pharmacokinetics of penciclovir following administration of single oral doses of famciclovir 125, 250, 500 and 750 mg to healthy volunteers. J Antimicrob Chemother, 1994. 33(1): pp. 119-27. 31. Hussein, I.T. et al., Substrate specificity and molecular modelling of the feline herpesvirus-1 thymidine kinase. Arch Virol, 2008. 153(3): pp. 495-505.
32. Dalvie, D. et al., Interspecies variation in the metabolism of zoniporide by aldehyde oxidase. Xenobiotica, 2013.
43(5): pp. 399-408.
33. Anderson, R.A. et al., Evaluation of poly(styrene-4-sulfonate) as a preventive agent for conception and sexually transmitted diseases. J Androl, 2000. 21(6): pp. 862-75.
34. Christensen, N.D. et al., Papillomavirus microbicidal activities of high-molecular-weight cellulose sulfate, dextran sulfate, and polystyrene sulfonate. Antimicrob Agents Chemother, 2001. 45(12): pp. 3427-32.
35. Herold, B.C. et al., Poly(sodium 4-styrene sulfonate): an effective candidate topical antimicrobial for the prevention of sexually transmitted diseases. J Infect Dis, 2000. 181(2): pp. 770-3.
36. Simoes, J.A. et al., Two novel vaginal microbicides (polystyrene sulfonate and cellulose sulfate) inhibit Gardnerella vaginalis and anaerobes commonly associated with bacterial vaginosis. Antimicrob Agents Chemother, 2002. 46(8): pp. 2692-5.
37. Zaneveld, L.J. et al., Efficacy and safety of a new vaginal contraceptive antimicrobial formulation containing high molecular weight poly(sodium 4-styrenesulfonate). Biol Reprod, 2002. 66(4): pp. 886-94.
38. Ito, M. et al., In vitro activity of mannan sulfate, a novel sulfated polysaccharide, against human immunodeficiency virus type 1 and other enveloped viruses. Eur J Clin Microbiol Infect Dis, 1989. 8(2): pp. 171-3.
39. Baba, M. et al., Sulfated polysaccharides are potent and selective inhibitors of various enveloped viruses, including herpes simplex virus, cytomegalovirus, vesicular stomatitis virus, and human immunodeficiency virus. Antimicrob Agents Chemother, 1988. 32(11): pp. 1742-5.
40. Mohan, P. et al., Sulfonic acid polymers as a new class of human immunodeficiency virus inhibitors. Antiviral Res, 1992. 18(2): pp. 139-50.
41. Zacharopoulos, V.R. and D.M. Phillips, Vaginal formulations of carrageenan protect mice from herpes simplex virus infection. Clin Diagn Lab Immunol, 1997. 4(4): pp. 465-8.
42. Stiles, J. et al., Effects of lambda-carrageenan on in vitro replication of feline herpesvirus and on experimentally induced herpetic conjunctivitis in cats. Invest Ophthalmol Vis Sci, 2008. 49(4): pp. 1496-501.
43. Vogtlin, A. et al., Quantification of feline herpesvirus 1 DNA in ocular fluid samples of clinically diseased cats by real-time TaqMan PCR. J Clin Microbiol, 2002. 40(2): pp. 519-23.
44. Benzekri, R. et al., Anti HSV-2 activity of Peganum harmala (L.) and isolation of the active compound. Microb Pathog, 2018. 114: pp. 291-298.
45. Fields BN, K.D., Howley PM, Fields virology. 6th ed., ed. W.K. Health/Lippincott and W. Wilkins. 2013.
46. Ohlinger, V.F., B. Haas, and H.J. Thiel, Rabbit hemorrhagic disease (r Hd ): characterization of the causative calicivirus. Vet Res, 1993. 24(2): pp. 103-16.
47. Bank-Wolf, B.R., M. Konig, and H.J. Thiel, Zoonotic aspects of infections with noroviruses and sapoviruses. Vet Microbiol, 2010. 140(3-4): pp. 204-12.
48. Hurley, K.E. et al., An outbreak of virulent systemic feline calicivirus disease. J Am Vet Med Assoc, 2004. 224(2): pp. 241-9.
49. Radford, A.D. et al., Feline calicivirus infection. ABCD guidelines on prevention and management. J Feline Med Surg, 2009. 11(7): pp. 556-64.
50. Dawson, S. et al., Acute arthritis of cats associated with feline calicivirus infection. Res Vet Sci, 1994. 56(2): pp.
133-43.
51. Reubel, G.H., D.E. Hoffmann, and N.C. Pedersen, Acute and chronic faucitis of domestic cats. A feline calicivirus-induced disease. Vet Clin North Am Small Anim Pract, 1992. 22(6): pp. 1347-60.
52. TerWee, J. et al., Comparison of the primary signs induced experimental exposure to either a pneumotrophic or a 'limping' strain of feline calicivirus. Vet Microbiol, 1997. 56(1-2): pp. 33-45.
53. Arias, A. et al., Norovirus Polymerase Fidelity Contributes to Viral Transmission In Vivo. mSphere, 2016. 1(5).
54. Hurley, K.F. and J.E. Sykes, Update on feline calicivirus: new trends. Vet Clin North Am Small Anim Pract, 2003.
33(4): pp. 759-72.
55. Coyne, K.P. et al., Lethal outbreak of disease associated with feline calicivirus infection in cats. Vet Rec, 2006.
158(16): pp. 544-50.
56. Pedersen, N.C. et al., An isolated epizootic of hemorrhagic-like fever in cats caused a novel and highly virulent strain of feline calicivirus. Vet Microbiol, 2000. 73(4): pp. 281-300.
57. Reynolds, B.S. et al., A nosocomial outbreak of feline calicivirus associated virulent systemic disease in France. J Feline Med Surg, 2009. 11(8): pp. 633-44.
58. Schulz, B.S. et al., Two outbreaks ofvirulent systemicfeline calicivirus infection in cats in Germany. Berl Munch Tierarztl Wochenschr, 2011. 124(5-6): pp. 186-93.
59. Wu, H. et al., Antiviral effect of lithium chloride on feline calicivirus in vitro. Arch Virol, 2015. 160(12): pp. 2935 43.
60. McDonagh, P. et al., Antiviral effect of mefloquine on feline calicivirus in vitro. Vet Microbiol, 2015. 176(3-4): pp.
370-7.
61. Povey, R.C., Effect of orally administered ribavirin on experimental feline calicivirus infection in cats. Am J Vet Res, 1978. 39(8): pp. 1337-41.
62. Stuart, A.D. and T.D. Brown, Alpha2,6-linked sialic acid acts as a receptor for Feline calicivirus. J Gen Virol, 2007. 88(Pt 1): pp. 177-86.
63. Chander Y, T.A., Sajja S, Ramakrishnan MA, Faaberg KS, Goyal SM, A TaqMan RT-PCR Assay for the Detection of Feline calicivirus. International Journal of Virology, 2007. 3(3): pp. 100-106.
Claims (12)
2. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 1, caracterizado por que está en forma de sal.
3. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 2, caracterizado por que está en forma de sal de sodio.
4. Un derivado de poliestireno sulfonado para su uso de acuerdo con una de las reivindicaciones 1 a 3, caracterizado por que tiene un peso molecular de al menos 1,5 kDa, preferentemente al menos 8 kDa.
5. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 4, caracterizado por que tiene un peso molecular en el intervalo de 8 kDa a 1200 kDa.
6. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 5, caracterizado por que tiene el peso molecular seleccionado del grupo que consiste en 8 kDa, 19,3 kDa, 35 kDa, 46 kDa, 93,5 kDa, 200 kDa, 400 kDa, 780 kDa y 1200 KDa.
7. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 6, caracterizado por que tiene el peso molecular de 93,5 kDa o 780 kDa.
8. Un derivado de poliestireno sulfonado para su uso de acuerdo con cualquiera de las reivindicaciones 1 a 7, caracterizado por que el herpesvirus felino es el herpesvirus felino tipo 1 (FHV-1).
9. Un derivado de poliestireno sulfonado para su uso de acuerdo con cualquiera de las reivindicaciones 1 a 8, caracterizado por que está diseñado para su uso en terapia combinada.
10. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 9, caracterizado por que la terapia combinada implica el uso simultáneo de otro agente para el tratamiento de la gripe felina, especialmente la infección causada por calicivirus felino o herpesvirus felino.
11. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 10, caracterizado por que el otro agente es un análogo de nucleósido.
12. Un derivado de poliestireno sulfonado para su uso de acuerdo con la reivindicación 11, caracterizado por que el análogo de nucleósido es aciclovir (ACV) y/o penciclovir (PCV).
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PL428024A PL239391B1 (pl) | 2018-12-03 | 2018-12-03 | Sulfonowana pochodna polistyrenu do zastosowania w leczeniu i/lub profilaktyce infekcji wywołanej przez kociego herpeswirusa |
| PL428583A PL239515B1 (pl) | 2019-01-15 | 2019-01-15 | Sulfonowana pochodna polistyrenu do zastosowania w leczeniu i/lub profilaktyce infekcji wywołanej przez kociego kaliciwirusa |
| PCT/PL2019/050071 WO2020117080A1 (en) | 2018-12-03 | 2019-12-03 | A sulfonated polystyrene derivative for use in the treatment and/or prophylaxis of cat flu |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2938417T3 true ES2938417T3 (es) | 2023-04-10 |
Family
ID=70974321
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19845729T Active ES2938417T3 (es) | 2018-12-03 | 2019-12-03 | Derivado de poliestireno sulfonado para su uso en el tratamiento y/o profilaxis de la gripe felina |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US11857566B2 (es) |
| EP (1) | EP3890754B1 (es) |
| JP (1) | JP2022509615A (es) |
| KR (2) | KR20260023101A (es) |
| BR (1) | BR112021010775A2 (es) |
| CA (1) | CA3121899A1 (es) |
| ES (1) | ES2938417T3 (es) |
| WO (1) | WO2020117080A1 (es) |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6210653B1 (en) * | 1995-03-30 | 2001-04-03 | Arturo G. Bellettini | Method for the treatment of HIV infected cells |
| JP3098401B2 (ja) * | 1995-07-12 | 2000-10-16 | 株式会社エルティーティー研究所 | 経鼻投与用製剤 |
| US6239182B1 (en) * | 1995-10-13 | 2001-05-29 | Rush-Presbyterian-St. Lukes Medical Center | Method for preventing sexually transmitted diseases |
| US20040142910A1 (en) * | 2002-10-21 | 2004-07-22 | Aegis Biosciences Llc | Sulfonated styrene copolymers for medical uses |
| CA2574719A1 (en) * | 2004-09-13 | 2006-03-23 | Her Majesty The Queen In Right Of Canada, As Represented By The Minister Of Health Canada | Inhibition of feline calicivirus replication by asparaginase |
| US8454937B2 (en) * | 2006-09-12 | 2013-06-04 | Temple University—Of The Commonwealth System of High Education | Method and composition for the site-selective delivery using viruses encapsulated in microbubbles |
| US20090105195A1 (en) * | 2007-10-17 | 2009-04-23 | O'brien Chris | Composition comprising microbicidal active ingredients |
| JP2011020993A (ja) * | 2009-06-16 | 2011-02-03 | Sekisui Chem Co Ltd | Rnaウイルス感染阻止成形用組成物及びrnaウイルス感染阻止成形品 |
| WO2013007703A1 (en) * | 2011-07-08 | 2013-01-17 | Universität Zürich | CLASS A CpG OLIGONUCLEOTIDES FOR PREVENTION OF VIRAL INFECTION IN CATS |
-
2019
- 2019-12-03 EP EP19845729.3A patent/EP3890754B1/en active Active
- 2019-12-03 WO PCT/PL2019/050071 patent/WO2020117080A1/en not_active Ceased
- 2019-12-03 KR KR1020267004051A patent/KR20260023101A/ko active Pending
- 2019-12-03 BR BR112021010775-4A patent/BR112021010775A2/pt unknown
- 2019-12-03 JP JP2021527090A patent/JP2022509615A/ja active Pending
- 2019-12-03 ES ES19845729T patent/ES2938417T3/es active Active
- 2019-12-03 CA CA3121899A patent/CA3121899A1/en active Pending
- 2019-12-03 US US17/298,777 patent/US11857566B2/en active Active
- 2019-12-03 KR KR1020217018759A patent/KR102926435B1/ko active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US11857566B2 (en) | 2024-01-02 |
| WO2020117080A1 (en) | 2020-06-11 |
| BR112021010775A2 (pt) | 2021-08-31 |
| US20220175824A1 (en) | 2022-06-09 |
| EP3890754A1 (en) | 2021-10-13 |
| KR20260023101A (ko) | 2026-02-20 |
| EP3890754B1 (en) | 2022-11-30 |
| KR102926435B1 (ko) | 2026-02-20 |
| KR20210099598A (ko) | 2021-08-12 |
| JP2022509615A (ja) | 2022-01-21 |
| CA3121899A1 (en) | 2020-06-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2910136T3 (es) | Métodos de tratamiento de la gripe | |
| CN101264083A (zh) | 用于预防和治疗粘膜炎及体重减轻的组合物和方法 | |
| ES2877808T3 (es) | Producto combinado para tratar o mejorar una infección por virus respiratorio sincicial | |
| EA035439B1 (ru) | Амидное соединение и его применение в качестве средства для лечения и профилактики заболеваний, вызываемых рнк- и/или днк-содержащими вирусами, и сопутствующих заболеваний | |
| Synowiec et al. | Cat flu: Broad spectrum polymeric antivirals | |
| JP2015193672A (ja) | Hsv−2の伝播を防ぐための局所用抗ウイルス処方物 | |
| Thieulent et al. | Identification of antiviral compounds against equid herpesvirus-1 using real-time cell assay screening: Efficacy of decitabine and valganciclovir alone or in combination | |
| RU2573977C2 (ru) | 4,6-ди(3,12-диаза-6,9-диазониадиспиро[5.2.5.2]гексадекан-1-ил)-2-метил-5-нитропиримидин тетрахлорид дигидрохлорид гексагидрат для лечения герпетической инфекции, фармацевтическая композиция для местного применения | |
| JP2023533041A (ja) | ウイルスに対するタウロリジンの使用 | |
| ES2938417T3 (es) | Derivado de poliestireno sulfonado para su uso en el tratamiento y/o profilaxis de la gripe felina | |
| Smee et al. | Treatment of lethal cowpox virus respiratory infections in mice with 2-amino-7-[(1, 3-dihydroxy-2-propoxy) methyl] purine and its orally active diacetate ester prodrug | |
| Ekblad et al. | Anti-herpes simplex virus activities of two novel disulphated cyclitols | |
| Himaki et al. | Efficacy of ASP2151, a helicase–primase inhibitor, against thymidine kinase-deficient herpes simplex virus type 2 infection in vitro and in vivo | |
| CN116392482A (zh) | Bms-265246在制备抗疱疹病毒药物中的应用和药物组合物 | |
| Mundinger et al. | Herpes simplex virus: Drug resistance and new treatment options using natural products | |
| US20230097553A1 (en) | Anti-rna virus drug and application thereof | |
| Smith et al. | Experimental Ocular Herpetic Infections in Rabbits: Treatment With 9-([2-Hydroxy-1-(hydroxymethyl) ethoxy] methyl) guanine | |
| PL239391B1 (pl) | Sulfonowana pochodna polistyrenu do zastosowania w leczeniu i/lub profilaktyce infekcji wywołanej przez kociego herpeswirusa | |
| US20250177392A1 (en) | Broad spectrum inhibitors of cytomegalovirus | |
| CN119113089B (zh) | 生物活性蛋白在制备治疗疱疹病毒感染药物中的应用及治疗疱疹病毒感染的药物组合物 | |
| CN113197912B (zh) | 异戊酰螺旋霉素类化合物及其组合物在制备抗病毒药物中的应用 | |
| Li et al. | Pralatrexate effectively inhibits the replication of monkeypox virus in vitro and in vivo | |
| Long et al. | 5-Bromo-2′-deoxyuridine inhibits African swine fever virus (ASFV) replication via interfering viral DNA replication and suppressing the formation of viral factories | |
| Johnson et al. | Synergistic inhibition of anatid herpesvirus replication by acyclovir and phosphonocompounds | |
| Verini et al. | Antiviral activity of a pyrazino-pyrazine derivative. |