ES2939889T3 - Formulación microgranular novedosa - Google Patents
Formulación microgranular novedosa Download PDFInfo
- Publication number
- ES2939889T3 ES2939889T3 ES13869051T ES13869051T ES2939889T3 ES 2939889 T3 ES2939889 T3 ES 2939889T3 ES 13869051 T ES13869051 T ES 13869051T ES 13869051 T ES13869051 T ES 13869051T ES 2939889 T3 ES2939889 T3 ES 2939889T3
- Authority
- ES
- Spain
- Prior art keywords
- preparation
- sugar
- examples
- mouth
- microgranules
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5015—Organic compounds, e.g. fats, sugars
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/138—Aryloxyalkylamines, e.g. propranolol, tamoxifen, phenoxybenzamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/4045—Indole-alkylamines; Amides thereof, e.g. serotonin, melatonin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4178—1,3-Diazoles not condensed 1,3-diazoles and containing further heterocyclic rings, e.g. pilocarpine, nitrofurantoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/167—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction with an outer layer or coating comprising drug; with chemically bound drugs or non-active substances on their surface
- A61K9/1676—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction with an outer layer or coating comprising drug; with chemically bound drugs or non-active substances on their surface having a drug-free core with discrete complete coating layer containing drug
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Inorganic Chemistry (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Medicinal Preparation (AREA)
Abstract
Se proporciona una formulación microgranular para administración oral caracterizada porque un núcleo inactivo recubierto con una capa de fármaco se mezcla con azúcar o alcohol de azúcar. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Formulación microgranular novedosa
Campo Técnico
[0001] La presente invención se refiere una preparación de microgránulos que se puede tomar sin agua y se disuelve rápidamente cuando se administra por vía oral. Más específicamente, se refiere a la preparación que minimiza la cantidad de residuo que permanece en un recipiente de envase o papel para envolver tras la administración, y puede regular con precisión la cantidad de un fármaco distribuido en el papel para envolver de una dosificación unitaria en un procedimiento de preparación, la preparación es la preparación de microgránulos preparada mediante el recubrimiento del fármaco en el núcleo inerte y su mezclado posterior con azúcar o alcohol de azúcar. La preparación de microgránulos de la presente invención se caracteriza por no tener ninguna sensación de irritación y sensación residual en la boca, cuando se administra por vía oral, y además, puede disgregarse y disolverse rápidamente en la boca, junto con una reducción de la cantidad de residuo en el papel para envolver y la regulación exacta del contenido de la preparación distribuido en el papel para envolver.
Antecedentes de la Técnica
[0002] Un comprimido o una cápsula es la forma de administración más preferida entre las preparaciones farmacéuticas para su administración por vía oral, pero si un paciente tiene dificultad para tragar o necesita consumirlo sin agua, se puede considerar la preparación que se disgrega y/o se disuelve rápidamente en la boca.
[0003] En este caso, en general, se puede considerar un comprimido que se disgrega rápidamente en la boca (comprimido bucodispersable, ODT (comprimido de disgregación oral)) o preparaciones de película que se disuelven rápidamente en la boca (preparación en tiras en la boca, ODF (película de disgregación oral)). Sin embargo, en el caso de ODT, normalmente se necesitan como mínimo 30 segundos para la disgregación y la disolución completa en la boca. De manera particular, debido a que se tiene una fuerte sensación de irritación en la boca hasta que se complete la disgregación, aunque se puede tomar sin agua, no aumenta significativamente la comodidad de tomar un fármaco para el paciente.
[0004] En el caso de ODF, es la preparación que se produce mediante la carga de un ingrediente eficaz a una tira con un tipo de película y que se utiliza como un enjuague bucal, etc., pero básicamente existe una limitación de la cantidad del ingrediente eficaz cargado en la preparación, y también debido a que la macromolécula que forma la película es cohesiva, existe un desagrado debido a la sensación de irritación y sensación residual en la boca y así se causa la molestia al paciente. Mientras tanto, en lo que se refiere a la preparación granular que se administra por vía oral, existe un ejemplo de que un extracto medicinal de hierbas que se convierte en el agente granulado, pero no es la preparación que se disuelve rápidamente en la boca después de la administración, se debe administrar con agua, y, también, la sensación de irritación en la boca es muy alta, por lo que se ha considerado como una preparación independiente de una mayor facilidad de toma de fármaco para los pacientes. También, se ha considerado que las preparaciones granulares existentes son adecuadas para ser mezcladas con una bebida o tomarse con alimentos y se ha considerado menos como un medio alternativo independiente para la administración oral que se puede reemplazar por un comprimido o una cápsula. Además, en el campo técnico al que pertenece la presente solicitud, es habitual que el gránulo sea considerado como un intermediario necesario para la formación de comprimido o el relleno de cápsula, y es de conocimiento común que la facilidad de toma del gránulo disminuya considerablemente cuando se convierte en la preparación de la administración final. Por consiguiente, es difícil encontrar un ejemplo para aumentar la facilidad de toma del fármaco convirtiendo el gránulo en una preparación de administración independiente.
[0005] En particular, para la facilidad de toma del fármaco se puede intentar producir el gránulo o el excipiente para los ingredientes eficaces a un tamaño menor que el gránulo convencional, por ejemplo, polvo, pero en este caso, se afronta el problema causado por una preparación, tal como el polvo, el problema es que es difícil administrar la cantidad exacta del polvo cuando el paciente lo toma.
[0006] En otras palabras, en el caso de un comprimido o una cápsula que es una preparación de administración oral ordinaria, una preparación de dosis unitaria se separa fácilmente de un recipiente de envasado, pero en el caso de polvo, se quedaría una gran masa en el recipiente de envasado. Por lo tanto, en el caso de prescripción solamente del medicamento que necesita un tratamiento profesional y el efecto terapéutico puede diferenciarse considerablemente según la dosis de administración, no el caso de compuestos farmacéuticos generales, tales como una vitamina, etc., cuando se fabrica como polvo, existen problemas de que un paciente no tome todos los medicamentos incluidos en el papel de envolver y algunos de los medicamentos permanecen en el papel de envolver. Además, en el proceso de fabricación, debido a que existe una limitación de fluidez en la preparación, había muchos casos en los que la cantidad del medicamento a insertar era diferente en cada papel de envolver, y, por consiguiente, el problema era que los contenidos de los ingredientes eficaces variaban sustancialmente en cada forma de dosis unitaria.
[0007] El documento US 2011/0244050 A1 está dirigida a una composición de sildenafilo de liberación pulsada y el
procedimiento de preparación de dicha composición.
Divulgación
Problema Técnico
[0008] Por tanto, el objeto de la presente invención es resolver los problemas mencionados anteriormente, es decir, proporcionar medios para minimizar la cantidad de la preparación permanente en el papel de envolver y, también, mejorar la fluidez de la preparación para cada forma de dosis unitaria para que contenga el contenido exacto de los ingredientes eficaces. También, además, el problema a solucionar en la presente invención es proporcionar nuevas preparaciones en las que la velocidad de disolución en la boca sea rápida y eliminar la sensación de irritación y la sensación residual en la boca.
Solución Técnica
[0009] Para resolver los problemas mencionados anteriormente, de acuerdo con la presente invención, se proporciona un medio técnico tal como se indica a continuación:
Se proporciona una composición de preparación de microgránulos para la administración oral de acuerdo con la reivindicación 1.
[0010] En la preparación anterior, se proporciona la preparación de microgránulos, la preparación se caracteriza por que el núcleo inerte es preferiblemente azúcar o alcohol de azúcar.
[0011] En la preparación anterior, se proporciona la preparación de microgránulos, la preparación se caracteriza por que se selecciona preferiblemente azúcar o alcohol de azúcar entre el grupo que consiste en xilitol, manitol, isomalt, sorbitol, maltitol, el azúcar blanco refinado, lactosa, inositol, eritritol, fructosa cristalina, trehalosa, ribitol, arabitol, galactitol, lactitol y maltotritol.
Efectos Beneficiosos
[0012] De acuerdo con la presente invención, se puede proporcionar una preparación de microgránulos para la administración oral que se disuelve rápidamente en la boca cuando se administra por vía oral, la preparación tiene efectos, donde el efecto de enmascarar la amargura de un fármaco con un gusto amargo es excelente y no existe ninguna sensación de irritación y sensación residual en la boca después de la administración, a diferencia del polvo o gránulos generales existentes.
Descripción de las Figuras
[0013]
La Figura 1 muestra un resultado de evaluación de sensación de irritación.
La Figura 2 muestra un resultado de evaluación de sensación residual en la boca.
La Figura 3 muestra un resultado de evaluación de velocidad de disolución en la boca.
La Figura 4 muestra un resultado de evaluación de cantidades del residuo en un recipiente de envasado.
La Figura 5 muestra un resultado de evaluación de uniformidad de los contenidos.
Las Figuras 6 a 8 muestran una evaluación de análisis general de los ejemplos y el ejemplo de comparación.
Modo óptimo de la Invención
[0014] El término “preparación de microgránulos” se utiliza como los significados a los que se hace referencia habitualmente, pero no se limitan a un polvo, un microgránulo y un grano definido por la Farmacopea Coreana y significa una preparación granular fabricada de las partículas finas o generales pequeñas.
[0015] De manera particular, la preparación de microgránulos de la presente invención se constituye mediante la mezcla de un núcleo inerte recubierto con una capa de fármaco que incluye el ingrediente eficaz y azúcar o alcohol de azúcar.
[0016] El término «fármaco», tal como se utiliza en la presente invención, significa un ingrediente eficaz que se puede incluir en la preparación de la presente invención y es farmacológicamente activo. La presente invención es la que se caracteriza por la preparación en sí y posee una premisa básica de que se puede incluir un ingrediente eficaz
en la preparación de la presente invención, y, de este modo, el ingrediente eficaz no está limitado.
[0017] Como ingrediente eficaz que se incluye en la presente invención se enumeran Sildenafilo, Tadalafilo, Udenafilo, Donepezilo, Glimepida, Dexibuprofeno, Pranlukast, Desmopresina, Acetaminofeno, Pitavastatina, Rebamipida, Azitromicina, HCl de Pseudoefedrina, HCl de Ranitidina, HCl de Levocetirizina y se puede incluir también la sal farmacéuticamente aceptable de los mismos.
[0018] El término «azúcar o alcohol de azúcar», tal como se utiliza en la presente invención, significa el material que puede disolverse rápidamente cuando se administra por vía oral y se utiliza como materia prima de la perla inerte y durante el mezclado posterior. Como ejemplo específico, pueden mencionarse el azúcar o alcohol de azúcar farmacéuticamente aceptable, tal como xilitol, sacarosa, manitol, isomalt, sorbitol, maltitol, el azúcar blanco refinado, lactosa, inositol, eritritol, fructosa cristalina, trehalosa, ribitol, arabitol, dulcitol, lactitol y maltotritol, etc. y las mezclas de los mismos, pero no están limitados a los mismos.
[0019] En la presente invención «núcleo inactivo» significa un material que no es farmacéuticamente activo y puede recubrir una capa de fármaco. Se puede utilizar una perla globular que tiene un tamaño de aproximadamente 50 ~ 400 um. Como ejemplo específico, se puede utilizar, pero no está limitado al mismo, azúcar o alcohol de azúcar mencionado anteriormente, tal como perla de sacarosa.
[0020] La sensación de irritación, tal como se utiliza en la presente memoria, hace referencia a la sensación que causa un desagrado a un paciente que ha tomado un medicamento debido a que el paciente percibe el medicamento como una sustancia extraña después de su administración y comprende, por ejemplo, una sensación espinosa, tal como arena, o una sensación de irritación de la mucosa de la boca o la lengua y también una sensación pegajosa, tal como una sustancia mocosa.
[0021] Una sensación residual en la boca, tal como se utiliza en la presente memoria, significa que aunque haya pasado una cantidad sustancial de tiempo después de la administración de la preparación, por ejemplo, a pesar de que hayan pasado 20 segundos después de la administración oral, y, a continuación, la preparación que comprende los ingredientes eficaces ya se haya disuelto y haya sido absorbida por el cuerpo, la sensación de que una preparación o una parte de la misma permanece en la boca o la sensación asociada a un residuo de la toma de la medicación, tal como un gusto o una sensación de que la preparación aún no ha sido eliminada de la boca. se mantiene dentro de la boca, y significa la sensación que causa un desagrado según el paciente, aunque no corresponde a la sensación de irritación. Cuando está presente dicha sensación residual en la boca, puede provocar un deseo de tomar más agua o bebida, y en este caso, dado que no se ejerce la particularidad de la preparación caracterizada por tomarse sin agua, se debe considerar mejorar la cualidad de la preparación conjuntamente con la sensación de irritación.
[0022] De aquí en adelante, la presente invención se explicará de manera específica.
[0023] Cuando los ingredientes eficaces se preparan en forma de polvo o gránulos y, a continuación, se administran, están presentes varias limitaciones, tales como una dosificación, una presencia de sensación residual en la boca o una sensación de irritación en la boca, un enmascarado de amargura, etc., pero no se puede ignorar el problema de que la preparación se queda en el papel de envolver.
[0024] Es decir, en el caso de un comprimido o una cápsula, se separa fácilmente del papel de envolver, y cuando se separa, raramente se produce una pérdida de contenido. Pero en el caso de polvo o gránulos, dado que la cantidad sustancial del medicamento permanece en el papel de envolver, la dosis de administración del ingrediente eficaz finalmente varía y, de este modo, no puede ignorarse la posibilidad de afectar al efecto del tratamiento debido a la variación. De manera particular, para prevenir este problema, se conoce en la técnica anterior el procedimiento que junta un ingrediente eficaz y un excipiente y, a continuación, se transforman en el gránulo, no simplemente mezclándolos. Sin embargo, aunque se transforman en el gránulo, dado que el gránulo puede pulverizarse mediante un impacto suave, cuando se almacena, no se puede resolver el problema básico de que el ingrediente eficaz se queda en el papel de envolver durante la administración debido a la aparición de partículas finas durante su almacenamiento.
[0025] La presente invención se desarrolla en base a los fundamentos de este problema, y en una preparación de medicamento en la que el polvo o el gránulo se coloca en el papel de envolver y, a continuación, se suministra, como resultado de formas estudiadas cuidadosamente para que el medicamento completo se descargue sin quedarse en el papel de envolver, cuando un paciente lo toma, se descubrió que cuando la capa del medicamento recubre el núcleo inerte, a diferencia del polvo o el gránulo existente que se forma simplemente mezclando el ingrediente eficaz y el excipiente o ensamblando el ingrediente eficaz para obtener el gránulo, dado que rara vez se producen partículas finas, la resistencia al impacto es excelente y la fluidez es mejor, queda poca cantidad restante del medicamento en el papel de envolver, cuando el paciente lo recibe.
[0026] De manera particular, dado que la preparación de microgránulos novedosa de la presente invención posee una excelente resistencia al impacto y también tiene una gran fluidez, se puede distribuir la cantidad exacta en cada unidad de envasado durante el proceso de fabricación, y, de este modo, tiene un efecto ventajoso en la constitución del
medicamento cuya dosis de administración es relativamente pequeña tal como en forma de polvo.
[0027] La preparación de microgránulos de la presente invención se fabrica recubriendo la capa de fármaco que comprende el ingrediente eficaz sobre un núcleo inerte, por ejemplo, perla de sacarosa, y mezclándolo a continuación con azúcar o alcohol de azúcar.
[0028] Más específicamente, el ingrediente eficaz se disuelve o se dispersa en la solución de recubrimiento que consiste en la base de recubrimiento y el disolvente. El producto resultante se consigue haciendo fluir el núcleo inerte que consiste en azúcar o alcohol de azúcar, es decir, la perla global en una máquina de recubrimiento de lecho fluido y recubriéndolo de manera simultánea con la solución de recubrimiento que comprende el ingrediente eficaz fabricado previamente mediante un pulverizador de recubrimiento. Adicionalmente, se obtiene una mezcla final mezclando el producto resultante con azúcar o alcohol de azúcar.
[0029] La preparación de microgránulos obtenida mediante dicho procedimiento tiene un efecto de que se minimiza la cantidad restante en el papel de envolver y también la velocidad de disgregación en la boca es alta, y no hay sensación residual y sensación de irritación en la boca.
[0030] La sensación de irritación en la boca hace referencia a la sensación que causa el desagrado a la persona que toma el medicamento debido a que la persona lo percibe como un material extraño en la boca, cuando se administra, según la investigación de los presentes inventores, dicha sensación de irritación se basaba en que estaba estrechamente relacionada con la disgregación microscópica y el patrón de disolución de la preparación administrada en la boca. Es decir, para reducir la sensación de irritación, se descubrió que la integración y la disolución en la boca deberían empezar de manera simultánea cuando se administra la preparación, y también las velocidades de disgregación y disolución en la boca deberían ser muy constantes.
[0031] Para conseguirlo, la presente invención utiliza azúcar o alcohol de azúcar como un núcleo inerte, y tomando tal constitución, cuando se administra la preparación, la integración y la disolución empiezan de manera instantánea en la boca, la disgregación y disolución rápidas y continuas tienen lugar dentro de un periodo microscópico que oscila entre varios segundos hasta docenas de segundos, y finalmente se obtiene una nueva preparación sin ninguna sensación de irritación.
[0032] Además, según la investigación de los inventores de la presente solicitud, se ha observado que el uso de un núcleo inerte afecta a la sensación residual en la boca y se identifica que no existe ninguna sensación en la boca debido a la administración de la preparación al desplazarse de manera instantánea al tracto gastrointestinal conjuntamente con la saliva sin permanecer en la boca el núcleo inerte que se incluye en la preparación conjuntamente con el ingrediente eficaz y azúcar o alcohol de azúcar para su mezclado posterior.
[0033] De manera particular, la preparación de microgránulos de la presente invención posee rasgos característicos que pueden disgregarse y disolverse rápidamente en la boca, y tal efecto se considera también como un efecto que se obtiene utilizando azúcar o alcohol de azúcar como un núcleo inerte. Es decir, en el caso de otra preparación que se toma sin agua como la de presente invención, por ejemplo, ODF u ODT que se pueden utilizar comercialmente, la preparación permanece en la boca como mínimo docenas de segundos después de la administración, pero la preparación de la presente invención se disgrega completamente y se disuelve en varios segundos (sustancialmente al mismo tiempo que la administración) y, a continuación, se desplaza al tracto gastrointestinal, y es lo que la diferencia de la «preparación que se administra sin agua» existente.
Realización para Poner en Práctica la Invención
[0034] De aquí en adelante, la presente invención se explicará a través de los ejemplos de trabajo. Sin embargo, se debe destacar que los siguientes ejemplos no limitan el alcance de los derechos de la presente invención.
Ejemplo 1 a 6
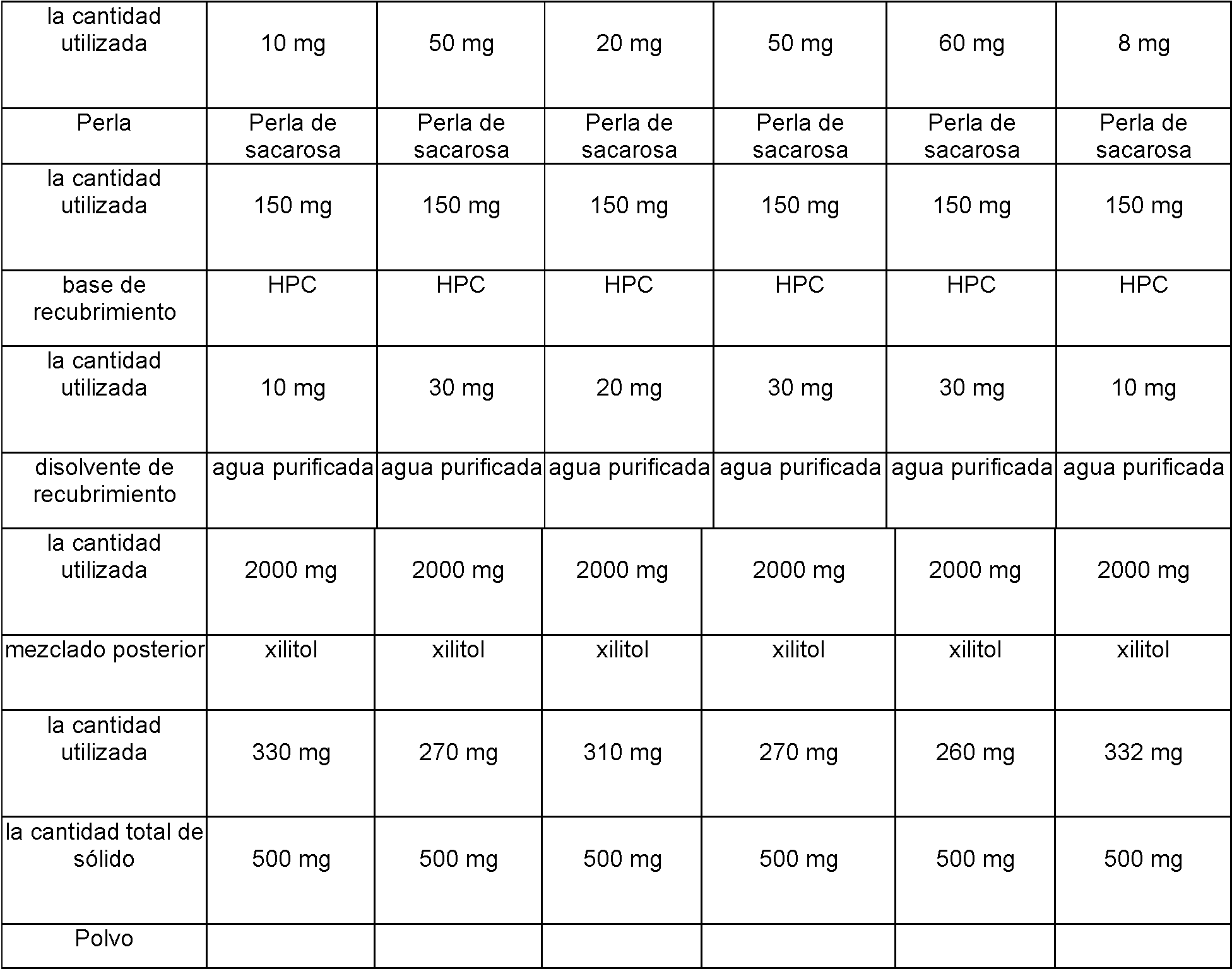
[0035] De acuerdo con la Tabla 1 a continuación, se disuelven o se dispersan varios ingredientes eficaces en la solución de recubrimiento que consiste en la base de recubrimiento y la solución. El producto resultante se obtiene recubriendo una perla globular (diámetro de partícula: 50 ~ 400 pm) que consiste en azúcar o alcohol de azúcar con la solución de recubrimiento preparada anteriormente que comprende un ingrediente eficaz en forma de pulverizador de recubrimiento, con la perla globular fluyendo en una máquina de recubrimiento con fluidos (la temperatura de viento: 50°C). Adicionalmente, la mezcla final se obtiene mezclando el producto resultante con azúcar o alcohol de azúcar.
T l 1
Ejemplos de comparación 1 a 6
[0036] Los gránulos húmedos que corresponden a los Ejemplos 1 a 6 se prepararon utilizando un Mezclador de Alta Velocidad. De manera específica, se mezclaron intensamente un ingrediente eficaz y sacarosa (malla 200) y se introdujeron en HSM, tal como se describe en la Tabla 2, y, a continuación, se introdujo un agente aglutinante disuelto en un líquido aglutinante con agitación. El producto resultante obtenido mediante asociación a alta velocidad durante 3 minutos se tamizó mediante un oscilador de malla 20 y, a continuación, se secó en un secador de aire caliente a 60 grados centígrados. El producto resultante obtenido se tamizó de nuevo mediante un oscilador de malla 20 y se añadió xilitol al mismo mediante mezclado posterior, se mezclaron durante 5 minutos y, a continuación, se obtuvo el producto resultante final.
[Tabla 2]
Ejemplos de comparación 7 a 12
[0037] Los gránulos húmedos que corresponden a los Ejemplos 1 a 6 se prepararon utilizando un Extrusor de Alta Presión.
[0038] De manera específica, un ingrediente eficaz y sacarosa (malla 200) se mezclaron intensamente y se introdujeron en HSM, tal como se describe en la Tabla 3, y, a continuación, se introdujo un agente aglutinante disuelto en un líquido aglutinante con agitación. El producto resultante obtenido mediante la asociación a alta velocidad durante 3 minutos se extrajo mediante un extrusor de bóveda única que tenía un tamaño de filtro de la bóveda de 1 mm y, a continuación, se secó en un secador de aire caliente a 60 grados centígrados. El producto resultante obtenido se tamizó de nuevo mediante un oscilador de malla 30 y se le añadió xilitol al mismo mediante mezclado posterior, se mezclaron durante 5 minutos y, a continuación, se obtuvo el producto resultante final.
Tabla 3
Ejemplos de comparación 13 a 18
[0039] Los gránulos húmedos que corresponden a los Ejemplos 1 a 6 se prepararon utilizando un Granulador de Lecho Fluidizado (FBG, Fluid Bed Granulator). De manera específica, el ingrediente eficaz y la sacarosa (malla 200) se mezclaron en flujo en el FBG. El producto resultante se obtuvo mediante la disolución de la base de recubrimiento en la solución de recubrimiento y, a continuación, ensamblando la solución de recubrimiento mediante pulverización, haciendo fluir la mezcla que comprende el ingrediente eficaz en FBG (la temperatura del viento: 50 °C). Adicionalmente, azúcar o alcohol de azúcar se mezcló con el producto resultante y, a continuación, se obtuvo la mezcla final.
T l 41
Ejemplo experimental 1. Experimento de la sensación de irritación en la boca
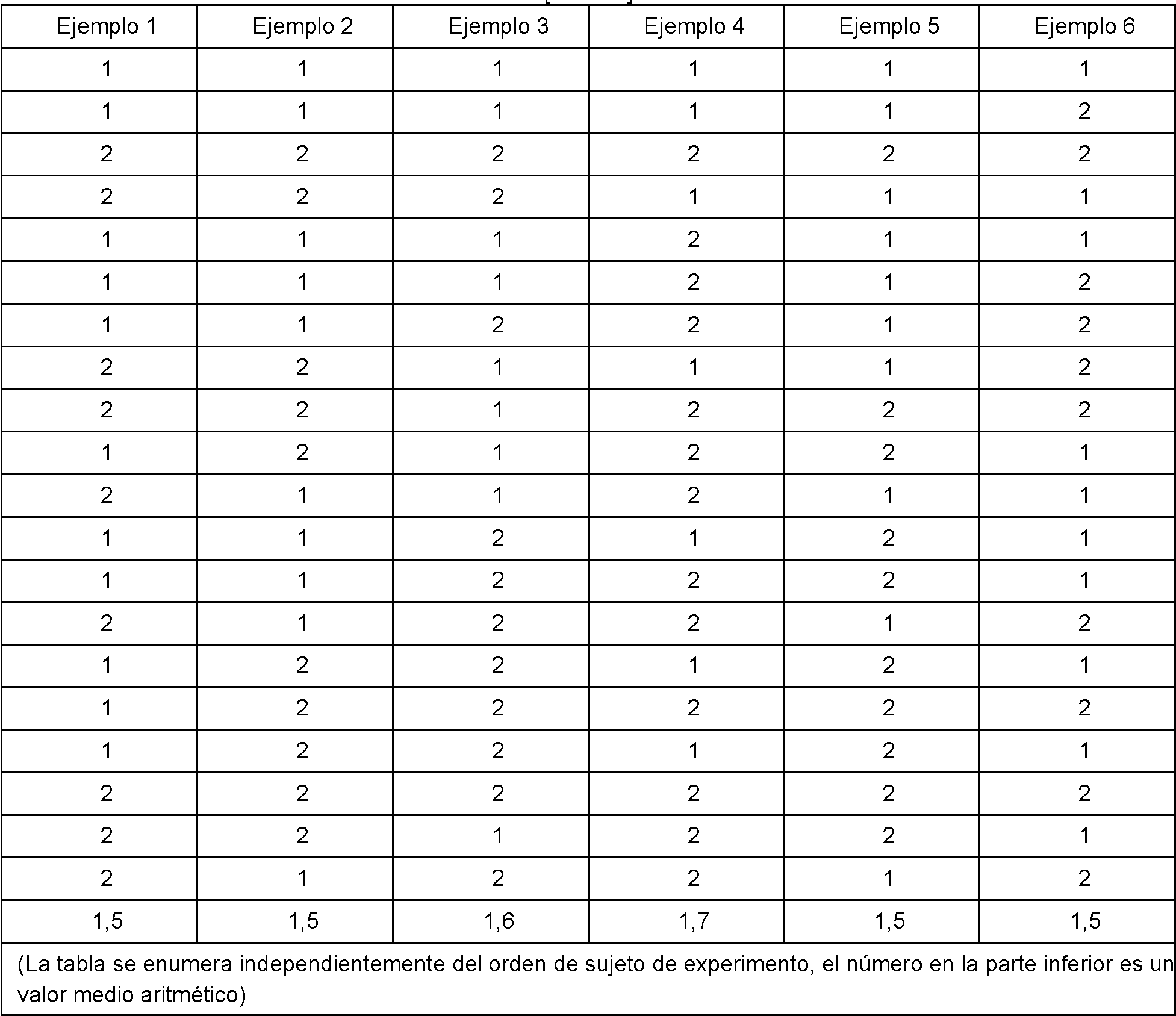
[0040] Se realizaron pruebas sensoriales a veinte (20) adultos sanos para determinar la sensación de irritación en la boca con respecto a las composiciones farmacéuticas preparadas en los ejemplos anteriores 1 a 6 y los ejemplos de comparación 1 a 18, disolviendo la composición farmacéutica preparada en la boca. En este caso, se siguió una prueba a ciegas para los sujetos de prueba en todas las pruebas. Los resultados se estimaron de acuerdo con los criterios de evaluación siguientes y, a continuación, se muestran los resultados de pruebas.
[0041] Puntuación 1: No hay sensación de irritación.
[0042] Puntuación 2: Presencia de sensación de irritación, pero hay poca sensación.
[0043] Puntuación 3: Poca sensación de irritación.
[0044] Puntuación 4: Presencia de sensación de irritación y repulsión.
[0045] Puntuación 5: Sensación de irritación muy grave.
[0046] Las siguientes tablas 5 a 8 muestran los resultados medidos por cada sujeto.
T l 1
T l 1
T l 7
T l 1
[0047] Basándose en las Tablas 5 a 8 anteriores, después de determinar la significancia a través de las pruebas t de los Ejemplos y de los Ejemplos de comparación para el mismo componente principal, se obtuvieron las siguientes Tablas 9 a 11.
T l
[0048] Tal como se puede observar a partir de la Tabla 9, se verificó que todos los Ejemplos 1-6 diferían con una significancia estadística en el límite de confianza del 95 % con respecto a los Ejemplos de comparación 1~6.
T l 11
[0049] Tal como se puede observar a partir de la Tabla 10, se verificó que todos los Ejemplos 1-6 diferían con una significancia estadística en el límite de confianza del 95 % con respecto a los Ejemplos de comparación 1~6
T l 111
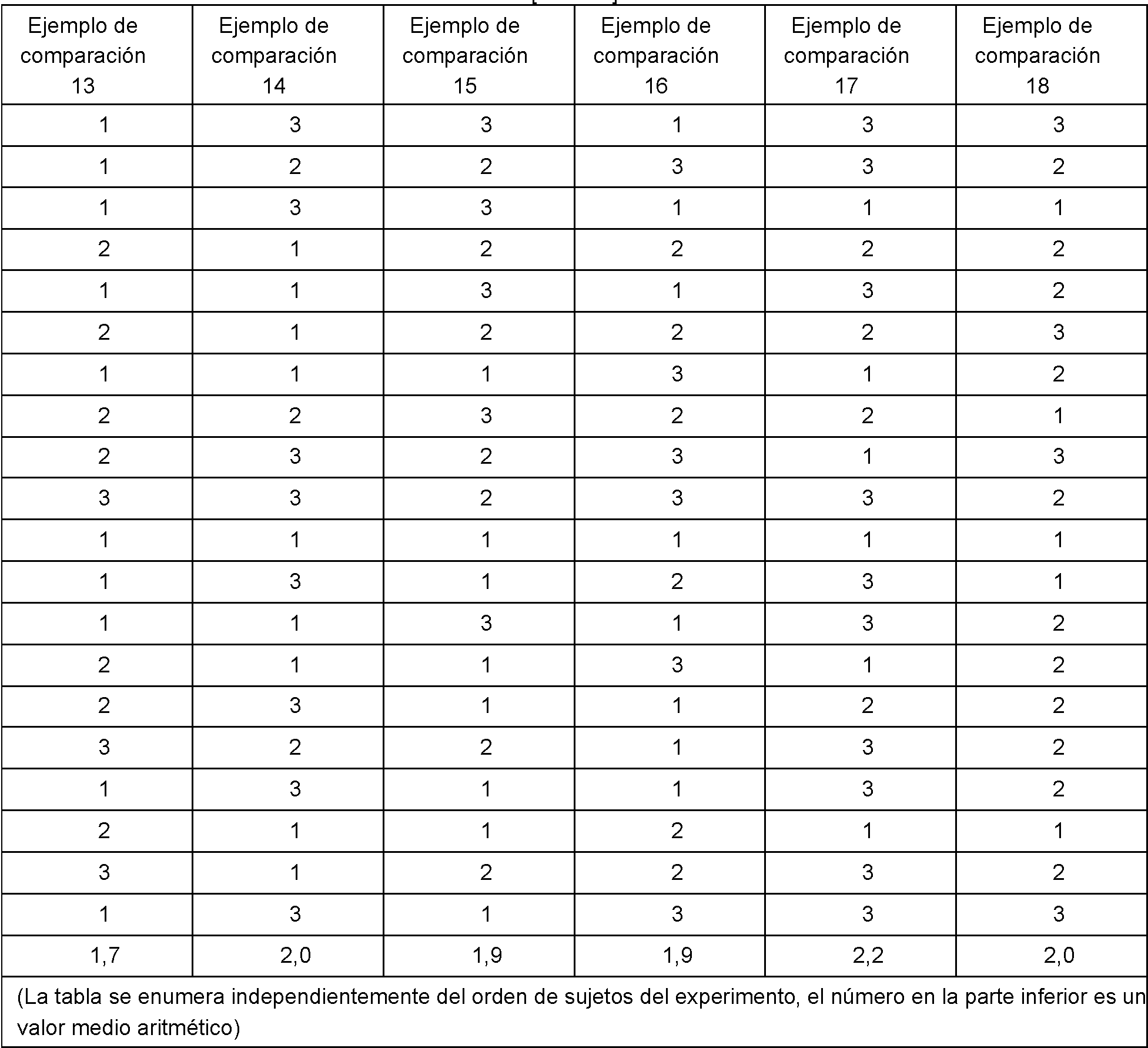
[0050] El ejemplo 1 y el Ejemplo de comparación 13, el Ejemplo 2 y el Ejemplo de comparación 14, el Ejemplo 3 y el Ejemplo de comparación 15 y el Ejemplo 4 y el Ejemplo de comparación 16 no muestran ninguna diferencia significativa estadísticamente en el límite de confianza del 95 %, pero el Ejemplo 5 y el Ejemplo de comparación 17 y el Ejemplo 6 y el Ejemplo de comparación 18 muestran una diferencia significativa estadísticamente en el límite de confianza de 95 %.
Ejemplo experimental 2: Experimento de sensación residual en la boca
[0051] Se realizaron pruebas sensoriales a veinte (20) adultos sanos para determinar la sensación residual en la boca con respecto a las composiciones farmacéuticas preparadas en los ejemplos anteriores 1 a 6 y los ejemplos de comparación 1 a 18, disolviéndolas en la boca. En este caso, se siguió una prueba a ciegas para los sujetos de prueba en todas las pruebas. Los resultados se estimaron de acuerdo con los criterios de evaluación siguientes y, a continuación, se representaron los resultados de las pruebas.
[0052] Las siguientes Tablas 12 a 15 repersentan el resultado puntuado por cada sujeto.
T l 121
T l 11
[Tabla 14]
T l 1
[0053] Basándose en las Tablas 12 a 15 anteriores, después de determinar la significancia a través de las pruebas t de los Ejemplos y los Ejemplos de comparación para el mismo componente principal, se obtuvieron las siguientes Tablas 16 a 18.
T l 11
[0054] Tal como se puede observar a partir de la Tabla 16, se verificó que todos los Ejemplos 1-6 diferían con una significancia estadística en el límite de confianza del 95 % con respecto a los Ejemplos de comparación 1~6.
T l 17
[0055] Se verificó que todos los Ejemplos 1-6 diferían con una significancia estadística en el límite de confianza del 95 % con respecto a los Ejemplos de comparación 1~6.
T l 11
[0056] El ejemplo 1 y el Ejemplo de comparación 13, el Ejemplo 4 y el Ejemplo de comparación 16 y el Ejemplo 6 y el Ejemplo de comparación 18 no mostraron ninguna significancia estadística en el límite de confianza del 95 %, pero el Ejemplo 2 y el Ejemplo de comparación 14, el Ejemplo 3 y el Ejemplo de comparación 15 y el Ejemplo 5 y el Ejemplo de comparación 17 mostraron que la diferencia tenía una significancia estadística en el límite de confianza de 95 %. Ejemplo experimental 3: Experimento de la velocidad de disolución en la boca
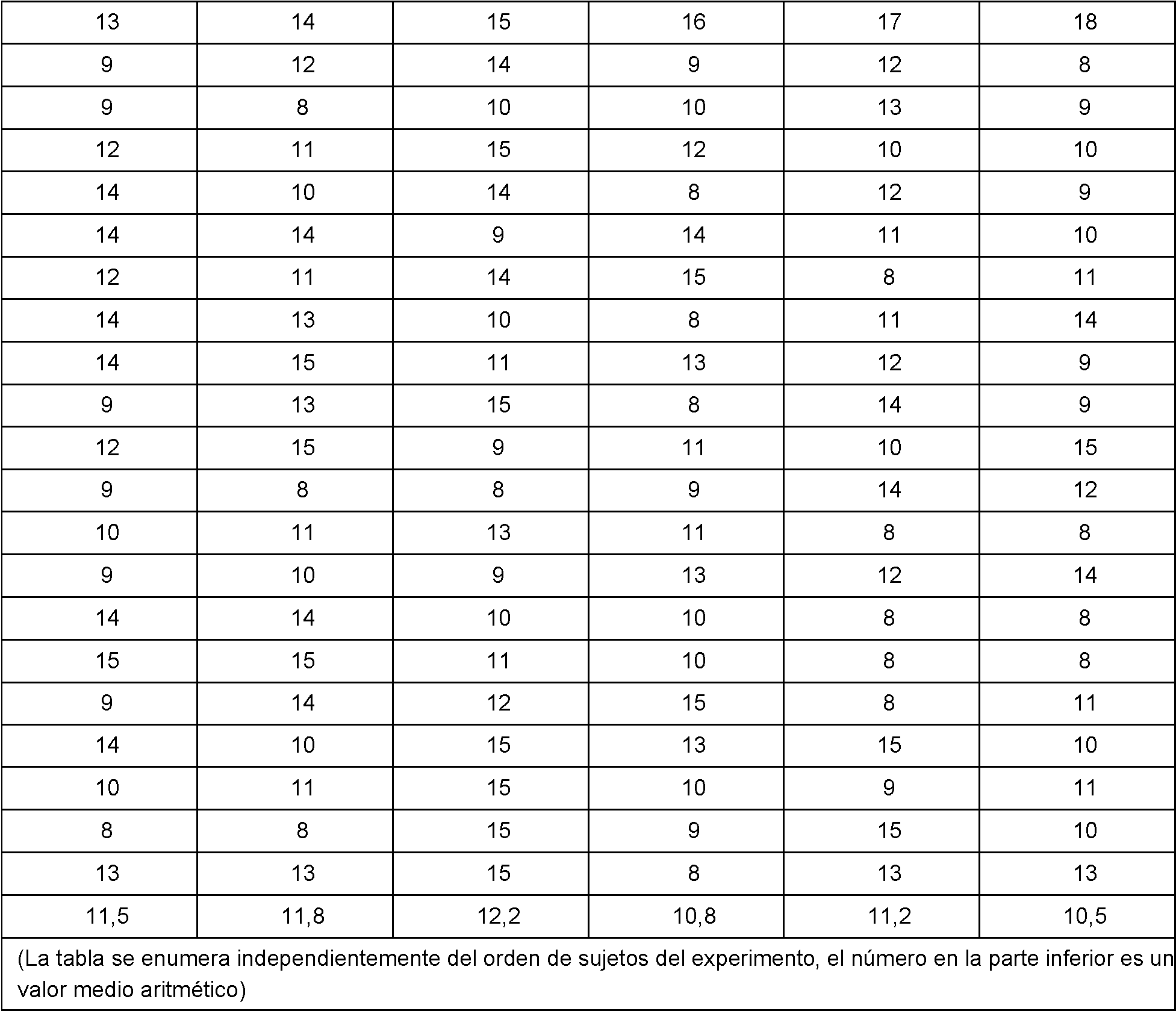
[0057] Se determinó la velocidad de disolución en la boca en veinte (20) adultos sanos con respecto a las composiciones farmacéuticas preparadas en los ejemplos 1 a 6 y los ejemplos de comparación 1 a 18 anteriores
disolviéndolas en la boca (unidad de determinación: segundo). En este caso, se siguió una prueba a ciegas para los sujetos de prueba en todas las pruebas.
[0058] Los resultados de las pruebas puntuadas por cada sujeto se mostraron en las Tablas 19 a 22 a continuación.
T l 11
T l 21
T l 211
T l 221
[0059] Basándose en las tablas 19 a 22 tal como se mencionan anteriormente, cuando se determinó la significancia para el mismo componente a través de la prueba t para los ejemplos y los ejemplos de comparación, se obtuvieron las Tablas 23 a 25 a continuación.
T l 21
[0060] Se verificó que todos los Ejemplos 1-6 diferían con una significancia estadística en el límite de confianza del 95 % con respecto a los Ejemplos de comparación 1~6.
T l 24
[0061] Tal como se puede observar a partir de la Tabla 24, se verificó que todos los Ejemplos 1-6 diferían con una
significancia estadística en el límite de confianza del 95 % con respecto a los Ejemplos de comparación 7~12.
T l 21
[0062] Tal como se puede observar a partir de la Tabla 25, se verificó que todos los Ejemplos 1-6 diferían con una significancia estadística en el límite de confianza del 95 % con respecto a los Ejemplos de comparación 13~18. Ejemplo experimental 4: Evaluación de la cantidad que permanece en el papel de envolver
[0063] Las composiciones farmacéuticas preparadas en los Ejemplos 1 a 6 y en los Ejemplos de comparación 1 a 18 se envasaron cada una en 100 líneas utilizando una máquina de envasado en sobres en 6 filas que tenían un tamaño de 5 cm x 7 cm. Entre estas, se tomaron 10 muestras de la tercera fila situada justo en la parte central y el fármaco en el papel de envolver se extrajo al mismo tiempo. Después de medir el peso del papel de envolver con polvos finos, todo el contenido restante en el papel de envolver se extrajo y, a continuación, se determinó de nuevo el peso del papel de envolver sin los polvos finos y se representó como la media de todo el contenido. (unidad: %)
[0064] Las Tablas 26 a 29 a continuación muestran el resultado de la prueba para cada muestra.
T l 2
T l 271
T l 21
T l 21
[0065] Basándose en las Tablas 26 a 29 anteriores, cuando se determinó la significancia del mismo componente principal a través de la prueba t para los ejemplos y los ejemplos de comparación, se obtuvieron las Tablas 30 a 32 a continuación.
[Tabla 30]
[0066] Tal como se puede observar en la Tabla 30, se verificó que todos los Ejemplos 1~6 diferían con una significancia estadística en el 95 % de límite de confianza con respecto a los Ejemplos de comparación 1~6.
T l 1
[0067] Tal como se puede observar en la Tabla 31, se verificó que todos los Ejemplos 1~6 diferían con una significancia estadística en el 95 % de límite de confianza con respecto a los Ejemplos de comparación 7~12.
T l 2
[0068] Tal como se puede observar en la Tabla 32, se verificó que todos los Ejemplos 1~6 diferían con una significancia estadística en el 95 % de límite de confianza con respecto a los Ejemplos de comparación 13~18. Ejemplo experimental 5. Estimación de la uniformidad de los contenidos
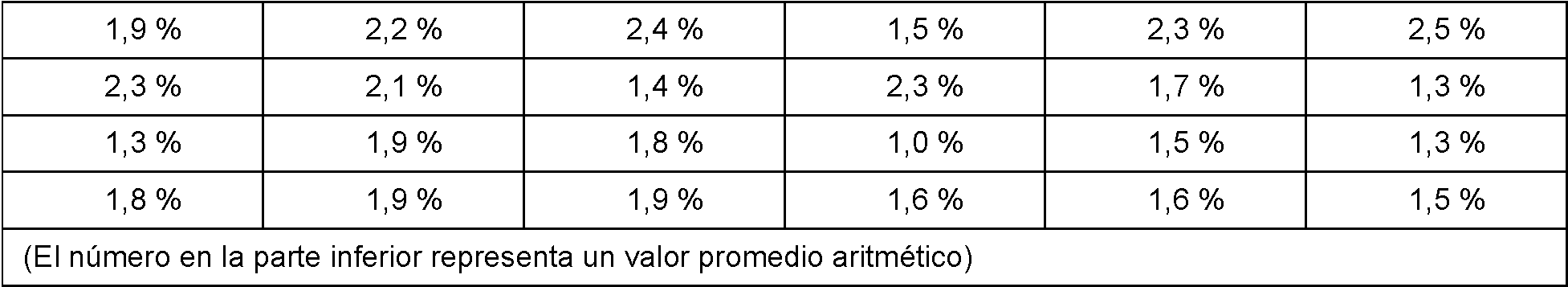
[0069] Las composiciones farmacéuticas preparadas en los Ejemplos 1 a 6 y los Ejemplos de comparación 1 a 18 se envasaron cada una en 100 líneas utilizando una máquina de envasado en sobres de 6 filas que tenían el tamaño de 5 cm x 7 cm. Entre estas, se tomaron al azar 10 muestras y se midieron las cantidades de los contenidos de acuerdo con el procedimiento de la prueba para la uniformidad de los contenidos en la prueba de uniformidad de la preparación del procedimiento de prueba general de la farmacopea. Se calcularon las desviaciones estándar de los contenidos de las muestras y se calculó el valor de determinación de la uniformidad de los contenidos multiplicando por un coeficiente de decisión (k) 2,4 cuando las muestras eran 10. Las Tablas 33 a 35 a continuación muestran el resultado de cada muestra.
T l
T l 41
T l 1
T l 1
[0070] Tal como se puede observar en las Tablas 33 a 36, los Ejemplos 1~6 muestran el valor de determinación inferior a 5 y poseen muy buena uniformidad de contenido, pero los Ejemplos de comparación 1 a 17 muestran valores altos entre 7,4 y 15,5 y poseen una uniformidad de contenido que no es buena.
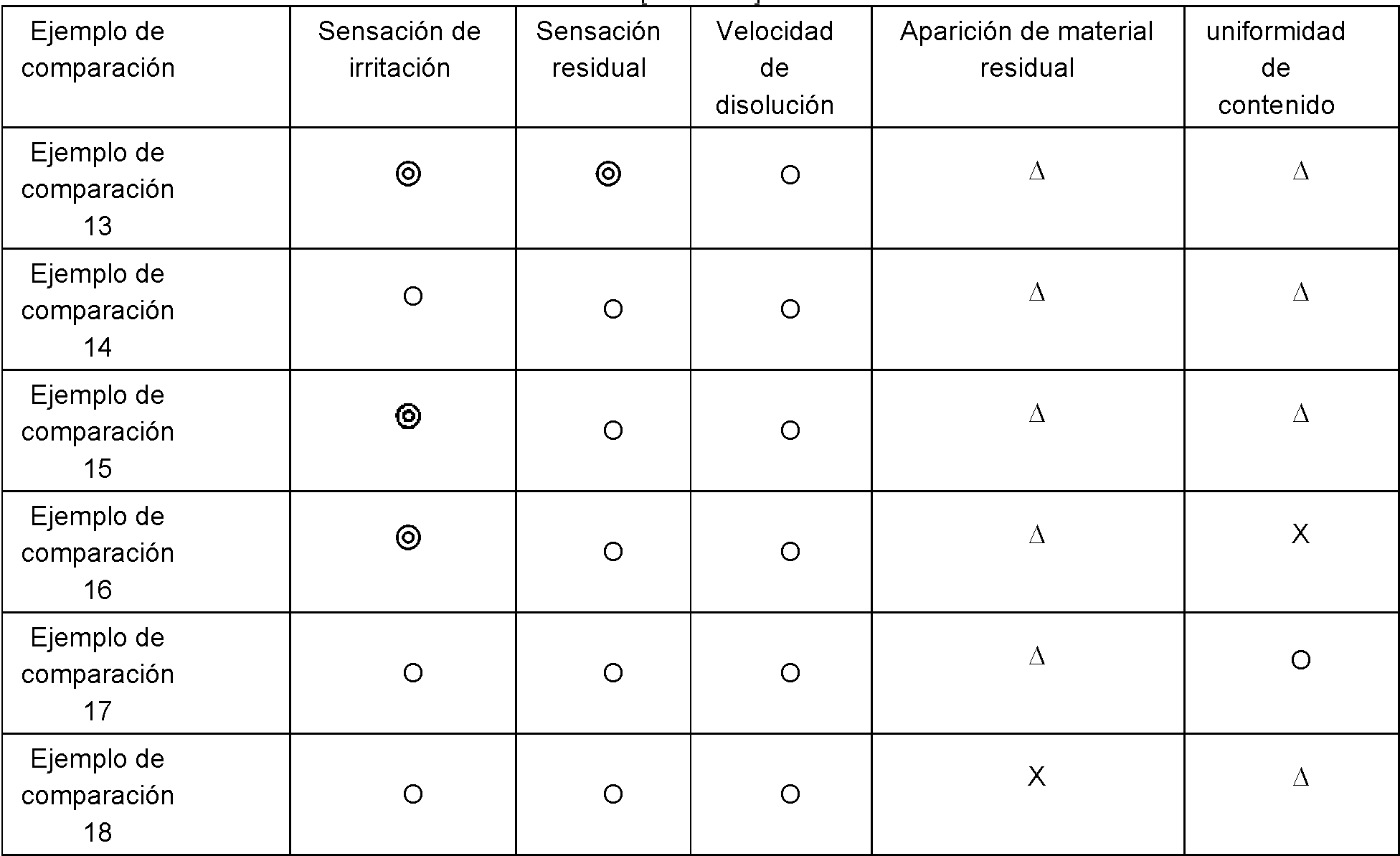
[0071] Para evaluar de manera general los resultados de los ejemplos mencionados anteriormente, las Tablas 38 a 41 a continuación representan la evaluación general de acuerdo con los criterios de estimación representados en la Tabla 37 a continuación.
T l 7
T l 1
T l 1
T l 41
T l 411
Disponibilidad Industrial
[0072] Una preparación de microgránulos de la presente invención minimiza las cantidades de la preparación que permanecen en el papel de envolver y al mismo tiempo asegura la uniformidad del contenido de la preparación incluida en cada unidad del papel de envolver.
[0073] Además, se da a conocer la preparación de microgránulos que muestra una rápida velocidad de disolución en la boca y no tiene ninguna sensación residual y sensación de irritación en la boca. De manera particular, dado que la preparación de la presente invención puede lograr el efecto de la presente invención independientemente de los tipos de los ingredientes eficaces, se puede aplicar a diferentes ingredientes eficaces. Además, dado que el proceso de fabricación para ello es relativamente simple, se puede lograr un procedimiento con alta eficacia a bajo coste.
Claims (4)
1. Composición de preparación de microgránulos para administración oral, que consiste en
(i) un microgránulo que consiste en un núcleo inerte y una capa de fármaco, en el que el núcleo inerte está recubierto con la capa de fármaco, y en el que la capa de fármaco consiste en un ingrediente eficaz y una base de recubrimiento; y
(ii) azúcar o alcohol de azúcar, que está mezclado con el microgránulo,
en la que el ingrediente eficaz se selecciona del grupo que consiste en Sildenafilo, Tadalafilo, Udenafilo, Donepezilo, Glimepida, Dexibuprofeno, Pranlukast, Desmopresina, Acetaminofeno, Pitavastatina, Rebamipida, Azitromicina, HCl de Pseudoefedrina, HCl de Ranitidina y HCl de Levocetirizina.
2. Composición de preparación de microgránulos de acuerdo con la reivindicación 1, en la que el núcleo inerte es azúcar o alcohol de azúcar.
3. Composición de preparación de microgránulos de acuerdo con la reivindicación 1 o 2,
en la que el azúcar o alcohol de azúcar se selecciona del grupo que consiste en xilitol, manitol, isomalt, sorbitol, maltitol, la sacarosa blanca refinada, lactosa, inositol, eritritol, fructosa cristalina, trehalosa, ribitol, arabitol, galactitol, lactitol y maltotritol.
4. Composición de preparación de microgránulos de acuerdo con cualquiera de las reivindicaciones 1 a 3, en la que dicha preparación de microgránulos se disuelve rápidamente cuando se administra por vía oral sin agua.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120158709A KR101340733B1 (ko) | 2012-12-31 | 2012-12-31 | 신규한 마이크로그래뉼 제형 |
| PCT/KR2013/012346 WO2014104840A1 (ko) | 2012-12-31 | 2013-12-27 | 신규한 마이크로그래뉼 제형 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2939889T3 true ES2939889T3 (es) | 2023-04-27 |
Family
ID=49988132
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13869051T Active ES2939889T3 (es) | 2012-12-31 | 2013-12-27 | Formulación microgranular novedosa |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20150328167A1 (es) |
| EP (1) | EP2939661B1 (es) |
| JP (1) | JP6537185B2 (es) |
| KR (1) | KR101340733B1 (es) |
| CN (1) | CN104936580A (es) |
| ES (1) | ES2939889T3 (es) |
| PL (1) | PL2939661T3 (es) |
| WO (1) | WO2014104840A1 (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112336690B (zh) * | 2020-12-10 | 2022-10-11 | 浙江海翔药业股份有限公司 | 一种盐酸克林霉素棕榈酸酯颗粒及其制备方法 |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5229135A (en) * | 1991-11-22 | 1993-07-20 | Prographarm Laboratories | Sustained release diltiazem formulation |
| FR2692146B1 (fr) * | 1992-06-16 | 1995-06-02 | Ethypharm Sa | Compositions stables de microgranules d'omeprazole gastro-protégés et leur procédé d'obtention. |
| US20010056177A1 (en) * | 1997-12-20 | 2001-12-27 | Becker Nathaniel T. | Matrix granule |
| CN1116877C (zh) * | 1999-10-28 | 2003-08-06 | 东北制药厂 | 可经口腔粘膜吸收的卡前列甲酯制剂及其制备方法 |
| WO2003074029A1 (en) * | 2002-03-07 | 2003-09-12 | Vectura Limited | Fast melt multiparticulate formulations for oral delivery |
| AU2003249478A1 (en) * | 2002-07-19 | 2004-02-09 | Ranbaxy Laboratories Limited | Taste masked sumatriptan tablets and processes for their preparation |
| AR040157A1 (es) * | 2003-06-06 | 2005-03-16 | Rodriguez Julio Cesar | Una formulacion en microgranulos para administracion oral en suspension acuosa |
| US20070275853A1 (en) * | 2004-04-08 | 2007-11-29 | Kyowa Hakko Kogyo Co., Ltd. | Solid Products with Improved Stability and Method for Producing the Same |
| CN101583620B (zh) * | 2005-11-28 | 2016-08-17 | 马里纳斯医药公司 | 加奈索酮组合物及其制备和使用方法 |
| WO2007126136A2 (en) * | 2006-04-27 | 2007-11-08 | Takeda Pharmaceutical Company Limited | Mask- tasting solid preparation of pioglitazone |
| MX2009001294A (es) * | 2006-08-04 | 2009-05-21 | Ethypharm Sa | Granulo y tableta que se desintegra por vía oral que comprende oxicodona. |
| KR101109633B1 (ko) * | 2007-08-03 | 2012-01-31 | 제이더블유중외제약 주식회사 | 활성성분의 코팅막이 보호되는 구강내붕해제형을 제조하기위한 조성물 |
| CA2708152A1 (en) * | 2007-12-10 | 2009-06-18 | Eurand, Inc | Orally disintegrating tablets comprising diphenhydramine |
| CA2742680C (en) * | 2008-11-07 | 2013-12-31 | Samyang Corporation | Pharmaceutical compositions for release control of methylphenidate |
| US20110244050A1 (en) * | 2008-12-12 | 2011-10-06 | Siegfried Rhein S.A. De C.V. | Pulsed-release sildenafil composition and method for preparing said composition |
| MX2012007448A (es) * | 2009-12-22 | 2012-09-12 | Abbott Healthcare Private Ltd | Composicion farmaceutica de liberacion controlada. |
| WO2011158334A1 (ja) * | 2010-06-15 | 2011-12-22 | 株式会社ナリス化粧品 | ゼデロン又はゼデロン類縁物質を有効成分として含む美白用の食品及び経口投与剤 |
| JP4803686B2 (ja) | 2010-08-31 | 2011-10-26 | 協和発酵キリン株式会社 | 苦味を呈する薬物を含有する顆粒および口腔内崩壊錠 |
| CA2819663C (en) | 2010-12-02 | 2019-12-24 | Adare Pharmaceuticals, Inc. | Rapidly dispersing granules, orally disintegrating tablets and methods |
-
2012
- 2012-12-31 KR KR1020120158709A patent/KR101340733B1/ko active Active
-
2013
- 2013-12-27 WO PCT/KR2013/012346 patent/WO2014104840A1/ko not_active Ceased
- 2013-12-27 US US14/758,457 patent/US20150328167A1/en not_active Abandoned
- 2013-12-27 JP JP2015550328A patent/JP6537185B2/ja active Active
- 2013-12-27 EP EP13869051.6A patent/EP2939661B1/en active Active
- 2013-12-27 ES ES13869051T patent/ES2939889T3/es active Active
- 2013-12-27 PL PL13869051.6T patent/PL2939661T3/pl unknown
- 2013-12-27 CN CN201380069048.1A patent/CN104936580A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP6537185B2 (ja) | 2019-07-03 |
| PL2939661T3 (pl) | 2023-03-20 |
| WO2014104840A1 (ko) | 2014-07-03 |
| EP2939661A1 (en) | 2015-11-04 |
| KR101340733B1 (ko) | 2013-12-12 |
| EP2939661B1 (en) | 2022-11-23 |
| CN104936580A (zh) | 2015-09-23 |
| JP2016504354A (ja) | 2016-02-12 |
| US20150328167A1 (en) | 2015-11-19 |
| EP2939661A4 (en) | 2016-08-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5674666B2 (ja) | 崩壊性粒子組成物及び口腔内速崩壊錠 | |
| EP2397161B1 (en) | Disintegrating particle composition and rapidly disintegrating compression-molded material comprising same | |
| ES2701443T3 (es) | Formulación aglutinante de fosfato para ingestión simple | |
| CN110290781A (zh) | 胃肠特定部位控制释放的剂型 | |
| CN101574521A (zh) | 掩盖了不快的味道的口服组合物 | |
| JP2012072166A (ja) | 粘膜分配用組成物と方法 | |
| JP5956475B2 (ja) | 苦味マスク顆粒含有口腔内崩壊錠 | |
| CN102946857A (zh) | 制备意图口服给药的包含一种或多种活性成分的药物组合物的方法以及包含其的组合物 | |
| Sah et al. | Sublingual tablets: an overview | |
| KR20080026754A (ko) | 생물학적 활성성분을 함유하는 방출 제어형 입자, 및 이의제조방법 | |
| CN101985044A (zh) | 一种掩味的药物涂层组合物 | |
| Yee et al. | Recent advances in orally disintegrating tablet: properties, formulation and production | |
| ES2939889T3 (es) | Formulación microgranular novedosa | |
| JP5275815B2 (ja) | リスペリドンを含有する口腔内崩壊錠剤および苦味抑制製剤 | |
| ES2325599T3 (es) | Sistema de enmascaramiento del sabor para farmacos no plastificantes. | |
| Kumar et al. | Mouth dissolving tablets: A modern approach to delivery of drug | |
| WO2001070172A2 (es) | Forma farmaceutica solida de administracion oral dispersable en agua que comprende rifampicina, isoniazida y piridoxina hidrocloruro, procedimiento para su obtencion y forma de presentacion de dicha forma farmaceutica | |
| CN102000344A (zh) | 一种掩味的药物涂层组合物 | |
| KR20090029255A (ko) | 생물학적 활성성분을 함유하는 방출 제어형 입자, 및 이의 제조방법 | |
| JPWO2005011637A1 (ja) | 用時分散型製剤 | |
| Gupta et al. | An overview of novel techniques employed in mouth dissolving drug delivery system | |
| US20180318226A1 (en) | Drug Delivery with Orally Dissolving Capsules | |
| CN106267220B (zh) | 愈创甘油醚氢溴酸右美沙芬无水吞服掩味制剂 | |
| Khailkhura et al. | Orally disintegrating tablet: A review | |
| HK40128271A (zh) | 胃肠特定部位控制释放的剂型 |