ES2951267T3 - Un comprimido farmacéutico sólido - Google Patents
Un comprimido farmacéutico sólido Download PDFInfo
- Publication number
- ES2951267T3 ES2951267T3 ES19714544T ES19714544T ES2951267T3 ES 2951267 T3 ES2951267 T3 ES 2951267T3 ES 19714544 T ES19714544 T ES 19714544T ES 19714544 T ES19714544 T ES 19714544T ES 2951267 T3 ES2951267 T3 ES 2951267T3
- Authority
- ES
- Spain
- Prior art keywords
- tablet
- calcium carbonate
- weight
- layer
- release
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/06—Aluminium, calcium or magnesium; Compounds thereof, e.g. clay
- A61K33/10—Carbonates; Bicarbonates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
- A61K9/0058—Chewing gums
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2031—Organic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyethylene oxide, poloxamers
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Inorganic Chemistry (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Zoology (AREA)
- Pain & Pain Management (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
La invención se refiere a un comprimido farmacéutico sólido para administración oral, comprendiendo el comprimido carbonato de calcio en una cantidad superior al 30% en peso del comprimido y componentes orgánicos insolubles en agua en una cantidad superior al 20% en peso del comprimido. en el que el comprimido está diseñado para ser masticado hasta obtener un residuo coherente que contiene los componentes orgánicos insolubles en agua, y en el que el comprimido está adaptado para liberar más del 80% del carbonato de calcio dentro de los 5 minutos de la masticación. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Un comprimido farmacéutico sólido
Campo de la invención
La invención se refiere a un comprimido farmacéutico sólido para la administración oral según las reivindicaciones.
Antecedentes de la invención
Los comprimidos que contienen carbonato de calcio son bien conocidos. Tales comprimidos son diseñados y usados, por ejemplo, para beneficio gastrointestinal. Un desafío con tales comprimidos conocidos es que tales comprimidos son típicamente más adecuados para tragar; como tales, los comprimidos incluyen cantidades significativas de carbonato de calcio. Se espera que estas cantidades significativas de carbonato de calcio condujesen a malestar oral en términos de textura o sensación en la boca si los comprimidos se administrasen como comprimidos masticables.
La solicitud de patente internacional WO 03/059082 describe gomas de mascar con relleno central que comprenden un compuesto que contiene calcio suspendido en el relleno central.
Resumen de la invención
La invención se refiere a un comprimido farmacéutico sólido para administración oral, comprendiendo el comprimido carbonato de calcio en una cantidad de más del 30 % en peso del comprimido y componentes orgánicos insolubles en agua en una cantidad de más del 20 % en peso del comprimido, en donde el comprimido está diseñado para masticarse en un residuo coherente que contiene los componentes orgánicos insolubles en agua,
en donde el comprimido se proporciona como un comprimido multicapa que comprende una primera capa y una segunda capa, en donde el comprimido comprende elastómero y resinas, en donde el elastómero y las resinas están contenidos en la primera capa, y en donde la segunda capa comprende al menos 70 % en peso de dicho carbonato de calcio, en donde el comprimido está compuesto por una mezcla prensada de partículas y/o gránulos, y en donde el comprimido está adaptado para liberar más del 80 % del carbonato de calcio en 5 minutos de masticación.
Según una realización de la invención, se ha proporcionado un comprimido farmacéutico sólido que permite una liberación ventajosa de carbonato de calcio en la cavidad oral de un usuario. La liberación, obtenida mediante el uso de componentes orgánicos insolubles en agua, que pueden enmascararse en un residuo coherente que contiene los componentes orgánicos insolubles en agua, es significativo y el comprimido de la invención proporciona una solución en la que un usuario puede evitar tragarse el comprimido al tiempo que aún se obtiene una cantidad significativa de carbonato de calcio. Al mismo tiempo, también es posible obtener la liberación deseada sin inferir una sensación de textura negativa por un usuario, que generalmente se esperaría cuando se liberasen tales cantidades altas de carbonato de calcio en la boca de un usuario por medio de un producto masticable.
Así, la textura obtenida dista, inesperadamente, de la sensación calcárea que un usuario puede tener al masticar un comprimido que contiene grandes cantidades de carbonato cálcico o al introducir carbonato cálcico en polvo en la cavidad oral.
En otras palabras, el comprimido de la invención es un vehículo de suministro atractivo para carbonato de calcio dirigido específicamente a los desafíos con la administración y liberación de carbonato de calcio de un comprimido.
Por lo tanto, el presente comprimido de la invención puede considerarse un nuevo vehículo de administración para carbonato de calcio, que es particularmente ventajoso cuando se usa carbonato de calcio como un ingrediente farmacéutico activo, es decir, un ingrediente destinado a un efecto farmacéutico específico.
Una ventaja adicional, que puede obtenerse según las disposiciones de la invención, es una reducción del riesgo de sobredosis. Un usuario que mastique el comprimido de la invención puede prolongar típicamente la masticación del comprimido debido a la presencia del residuo coherente, por lo tanto, al menos prolongando el tiempo hasta que se aplique un nuevo comprimido. Esto es importante, ya que una sobredosis sostenida de carbonato de calcio a lo largo del tiempo puede conducir a hipercalcemia. Los síntomas de la hipercalcemia pueden incluir anorexia, sed, náuseas, vómitos, estreñimiento, dolor abdominal, debilidad muscular, fatiga, trastornos mentales, polidipsia, poliuria, dolor óseo, nefrocalcinosis, nefrolitiasis y, en casos graves, arritmias cardíacas. La hipercalcemia extrema puede resultar en coma y muerte. Los niveles de calcio persistentemente altos pueden conducir a daño renal irreversible y calcificación de los tejidos blandos.
El carbonato de calcio aplicado puede ser ventajosamente un DC -grado disponible comercialmente (DC: Compresible directo) de carbonato de calcio.
En una realización de la invención, el comprimido comprende carbonato de calcio en una cantidad del 30 al 60 % en peso del comprimido.
Según una realización ventajosa, el comprimido puede comprender cantidades significativas de carbonato de calcio. El comprimido de la invención puede comprender, por lo tanto, carbonato de calcio en una cantidad del 30 al 60 % en peso del comprimido.
En una realización de la invención, el comprimido comprende carbonato de calcio en una cantidad del 35 al 55 % en peso del comprimido.
En una realización de la invención, el comprimido comprende carbonato de calcio en una cantidad del 40 al 50 % en peso del comprimido.
Según una realización ventajosa, el comprimido puede comprender cantidades significativas de carbonato de calcio. El comprimido de la invención puede comprender ventajosamente aproximadamente un 45 % en peso del comprimido, facilitando así la liberación de una cantidad eficaz de ingrediente farmacéuticamente activo, es decir, el carbonato de calcio, sin comprometer la capacidad o el deseo del usuario para invocar la liberación.
En una realización de la invención, el comprimido está adaptado para liberar más del 85 % del carbonato de calcio en 5 minutos de masticación del comprimido.
Por lo tanto, el comprimido puede diseñarse para liberar una cantidad significativa del carbonato de calcio, por ejemplo, 85 % del carbonato contenido dentro del producto del comprimido dentro de un período de tiempo muy corto. La liberación rápida, aunque aún retardada puede considerarse una clave para obtener el efecto farmacéutico deseado, como una sensación de textura inferior durante la masticación, típicamente datos de la máscara para la masticación continua y, por lo tanto, reducir el efecto farmacéutico deseado que debe obtenerse a través de carbonato de calcio liberado.
La liberación referida de carbonato de calcio puede determinarse de dos maneras diferentes dentro del alcance de la invención, liberación In Vivo o liberación In Vitro.
Liberación In Vivo: se instruyeron 6 evaluadores para masticar cada muestra con 60 masticaciones por minuto durante un tiempo de masticación total de 3 a 10 minutos.
Los evaluadores fueron instruidos para no comer o beber nada a no ser agua durante los últimos 30 minutos antes de la prueba. Antes del inicio de la prueba, los evaluadores enjuagaron sus bocas con agua.
Para cada muestra probada, los evaluadores masticaron un comprimido durante 3 minutos, otro comprimido durante 5 minutos y otro comprimido durante 10 minutos para producir residuos de comprimidos para cada instante de tiempo. Esto se repitió una vez para obtener réplicas para cada evaluador en cada instante de tiempo en la prueba
Liberación In Vitro: La liberación del carbonato de calcio en este ejemplo se determinó in vitro. Las mediciones se llevaron a cabo según el procedimiento expuesto en la Ph. Eur. 6a ed. 2.9.25, en un tampón fosfato con pH = 7,4, una velocidad de masticación de 60 masticaciones por minuto, y con la temperatura del medio ajustada a 37 0C. El procedimiento de masticación se interrumpe cada minuto para reemplazar el tampón fosfato, evitando así la saturación del tampón y simulando la deglución en el procedimiento de masticación in vivo.
Para cada muestra, un comprimido se masticó en intervalos de tiempo especificados 3, 5 y 10 minutos para producir residuos de comprimidos para cada instante de tiempo. Esto se repitió 6 veces para obtener 6 réplicas para cada instante de tiempo en la prueba.
El contenido de carbonato de calcio de los residuos después de la masticación, in vitro o in vivo, puede determinarse mediante espectroscopía de absorción atómica estándar (AAS). Para el análisis, se disolvió un comprimido residual en una mezcla de ácido clorhídrico (HCl) y tolueno. Después de la dilución y filtración adecuadas, la fase ácida se pasó a través del dispositivo de AAS analizando Ca (a una longitud de onda de 442,7 nm).
La liberación se calculó luego comparando el contenido de Ca del residuo después de la masticación con el contenido de Ca del comprimido no masticado.
Alternativamente, se pueden usar técnicas de titulación estándar para determinar el contenido de carbonato de calcio antes y después de la masticación.
En una realización de la invención, el comprimido está adaptado para liberar más del 90 % del carbonato de calcio en 5 minutos de masticación del comprimido.
En una realización de la invención, el comprimido está adaptado para liberar más del 60 % del carbonato de calcio en 3 minutos de masticación del comprimido.
Según la invención, el comprimido está compuesto por una mezcla prensada de partículas y/o gránulos.
Según una realización ventajosa de la invención, el comprimido puede formarse mediante una mezcla prensada de partículas y/o gránulos. Esto es particularmente relevante cuando las partículas y los gránulos son de diferente naturaleza en términos de contenido y, p.ej., tamaño, ya que ambos pueden presionarse juntos con el fin de formar un comprimido mecánicamente estable y, lo que es más importante, usarse como expositores interactivos de carbonato de calcio.
Un gránulo en el presente contexto se entiende como un aglomerado de polvo/partículas. Un gránulo es, por lo tanto, una estructura producida por granulación. Este procedimiento de granulación por sí mismo es bien conocido en la técnica.
En una realización de la invención, el carbonato de calcio y los componentes orgánicos insolubles en agua están contenidos en diferentes partículas y/o gránulos antes de la formación de los comprimidos.
El efecto antes mencionado de los expositores interactivos en relación con el carbonato de calcio puede obtenerse ventajosamente cuando el carbonato de calcio del comprimido está contenido en partículas distintas de las partículas que comprenden los componentes orgánicos insolubles en agua. Durante la masticación, tal configuración de una matriz de comprimido expositor puede provocar que el carbonato de calcio se libere inmediatamente, pero también que parte del carbonato de calcio liberado inmediatamente se mastique mecánicamente en el residuo coherente y luego nuevamente, al menos parcialmente, se libere del residuo coherente.
En una realización de la invención, más del 80 % del carbonato de calcio está contenido en partículas y/o gránulos diferentes de las partículas y/o gránulos que comprenden los componentes orgánicos insolubles en agua antes de la formación de los comprimidos.
Por lo tanto, el carbonato de calcio puede estar contenido en diferentes tipos de partículas y/o gránulos, obteniendo así un tipo híbrido de liberación, manteniendo al mismo tiempo una liberación muy rápida global y una liberación relativamente completa del carbonato de calcio. Una liberación relativamente completa del carbonato de calcio en el presente contexto se refiere a que solo una fracción minoritaria del carbonato de calcio originalmente contenido todavía está contenida en el residuo coherente en el momento dado después del inicio de la masticación.
En una realización de la invención, el comprimido comprende componentes orgánicos insolubles en agua en una cantidad del 20 al 50 % en peso del comprimido.
Los componentes orgánicos insolubles en agua pueden constituir una cantidad significativa del comprimido, manteniendo al mismo tiempo la liberación rápida deseada de carbonato de calcio y manteniendo al mismo tiempo una sensación agradable en la boca.
En una realización de la invención, el comprimido comprende elastómero en una cantidad de al menos 2 % en peso del comprimido, tal como al menos 4 % en peso del comprimido.
En una realización de la invención, el comprimido comprende elastómero en una cantidad inferior al 35 % en peso del comprimido, tal como menos de aproximadamente el 25 % en peso del comprimido, tal como menos del 20 %, el 15 % o el 10 % en peso del comprimido.
En una realización de la invención, el comprimido comprende elastómero en una cantidad de 1-15 % en peso del comprimido.
En una realización de la invención, el comprimido comprende resina en una cantidad del 0,1 al 50 % en peso del comprimido, tal como del 2 al 40 % en peso del comprimido.
En una realización de la invención, el comprimido comprende resinas naturales en una cantidad del 0,1 al 30 %, tal como del 1 al 25 %, tal como del 3 al 25 % o del 5 al 25 %, en peso del comprimido.
En una realización de la invención, el comprimido está libre de resinas naturales.
En una realización de la invención, el comprimido comprende resinas sintéticas en una cantidad del 0,1 al 30 %, tal como del 1 al 25 %, tal como del 3 al 25 % o del 5 al 25 %, en peso del comprimido.
En una realización de la invención, el comprimido se proporciona como un comprimido de dos capas o un comprimido de tres capas.
En una realización de la invención, el comprimido se proporciona como un comprimido de dos capas.
Una ventaja de la realización anterior puede ser que se pueda obtener una liberación más rápida de carbonato de calcio, al tiempo que es posible la separación de los ingredientes, por ejemplo, manteniendo componentes orgánicos insolubles en agua y el carbonato de calcio en capas separadas.
En una realización de la invención, la segunda capa comprende al menos el 80 % en peso de dicho carbonato de calcio.
En una realización de la invención, el comprimido comprende una primera capa y una segunda capa, en donde el elastómero y las resinas están contenidos en la primera capa, y en donde la segunda capa comprende 70 a 100 % en peso de dicho carbonato de calcio, tal como 80-100 % en peso de dicho carbonato de calcio.
En una realización de la invención, el comprimido comprende un comprimido de dos capas que comprende una primera capa y una segunda capa, en donde el elastómero y las resinas están contenidos en la primera capa, y en donde la segunda capa comprende al menos el 70 % en peso de dicho carbonato de calcio, tal como al menos el 80 % en peso de dicho carbonato de calcio.
En una realización de la invención, el comprimido tiene una dureza de al menos 70 N.
Según una realización de la invención, el comprimido tiene una dureza de 70-130 N, tal como 75-120, tal como 80 115 N.
Según una realización de la invención, el comprimido tiene una dureza de 70-115 N.
Según una realización de la invención, el comprimido está adaptado para liberar más de 80 y hasta 100 por ciento en peso del carbonato de calcio en 5 minutos de masticación.
Según una realización de la invención, el comprimido está adaptado para liberar entre 80 y 98 por ciento en peso del carbonato de calcio en 5 minutos de masticación, tal como entre 80 y 95 por ciento en peso.
En una realización de la invención, el carbonato de calcio tiene un tamaño de partícula promedio de al menos 75 micrómetros, tal como al menos 150 micrómetros.
Según una realización de la invención, el carbonato de calcio tiene un tamaño de partícula promedio de entre 75 y 400 micrómetros, tal como entre 150 y 300 micrómetros.
En una realización de la invención, menos del 5 % del carbonato de calcio tiene un tamaño de partícula por debajo de 74 micrómetros, tal como menos del 5 % del carbonato de calcio que tiene un tamaño de partícula por debajo de 53 micrómetros.
En una realización de la invención, entre 0 y 5 % del carbonato de calcio tiene un tamaño de partícula por debajo de 74 micrómetros, tal como entre 0 y 5 % del carbonato de calcio que tiene un tamaño de partícula por debajo de 53 micrómetros.
En una realización de la invención, el comprimido tiene una friabilidad inferior al 1,0 %, tal como inferior al 0,7 %, en donde la friabilidad se mide según la Farmacopea Europea 9.1, procedimiento de ensayo 2.9.7.
Por ejemplo, un equipo de ensayo de friabilidad farmacéutica PTF 10E de Pharma Test puede usarse cuando se mide la friabilidad.
En una realización de la invención, el comprimido tiene una friabilidad del 0-1,0 %, tal como del 0- 0,7 %, en donde la friabilidad se mide según la Farmacopea Europea 9.1, procedimiento de ensayo 2.9.7.
En una realización de la invención, el comprimido tiene una friabilidad de 0,01 -1,0 %, tal como 0,01 -0,7 %, en donde la friabilidad se mide según la Farmacopea Europea 9.1, procedimiento de ensayo 2.9.7.
La invención se refiere además a un comprimido farmacéutico sólido para administración oral, el comprimido comprende carbonato de calcio en una cantidad de más del 15 % en peso del comprimido y componentes orgánicos insolubles en agua en una cantidad de más del 25 % en peso del comprimido, en donde el comprimido está diseñado para masticarse en un residuo coherente que contiene los componentes orgánicos insolubles en agua,
en donde el comprimido se proporciona como un comprimido multicapa que comprende una primera capa y una segunda capa,
en donde el comprimido comprende elastómero y resinas, en donde el elastómero y las resinas están contenidos en la primera capa, en donde la segunda capa comprende al menos 70 % en peso de dicho carbonato de calcio, en donde el comprimido está compuesto por una mezcla prensada de partículas y/o gránulos, y
en donde el comprimido está adaptado para liberar más del 80 % del carbonato de calcio en 5 minutos de masticación. Según la invención, el comprimido farmacéutico sólido suministra carbonato de calcio. El carbonato de calcio puede liberarse del comprimido con poco o ningún malestar oral y el carbonato de calcio puede tener, por lo tanto, una mayor probabilidad de éxito en términos del resultado o el tratamiento previsto, simplemente debido al hecho de que un usuario del comprimido estará motivado para masticar el comprimido. El efecto farmacéutico deseado, por supuesto, se reduciría si un usuario tendería a abstenerse de usar el comprimido o se abstenga de masticar el comprimido debido a, por ejemplo, el malestar o el mal sabor.
En una realización de la invención, la masticación del comprimido proporciona un beneficio de limpieza de los dientes. Por lo tanto, el comprimido puede proporcionar un beneficio de limpieza de los dientes no solo por causa del carbonato de calcio liberado, sino también debido a la fricción entre los dientes y el residuo coherente durante la masticación. En una realización de la invención, la masticación del comprimido no proporciona una sensación de sabor a tiza. El comprimido de la invención, que es un excelente expositor oral de carbonato de calcio, puede usarse ventajosamente como un sistema de administración “ bidireccional” , que libera carbonato de calcio del comprimido, y al mismo tiempo libera carbonato de calcio para su incorporación en el residuo coherente durante la masticación, proporcionando así un “tampón de liberación” físico, que puede considerarse como un facilitador para la textura ventajosa en uso del producto.
Fue una sorpresa para el inventor de la presente invención que fuera posible obtener una liberación de carbonato de calcio según la invención sin proporcionar una sensación de sabor a tiza durante la masticación. Se esperaría que una liberación relativamente alta de carbonato de calcio según la invención diese como resultado una sensación calcárea más pronunciada durante la masticación. Esto es muy sorprendente en vista del pensamiento convencional. De hecho, la alta liberación de carbonato de calcio según la invención es muy sorprendente dado el contenido de componentes orgánicos insolubles en agua en la formulación según la invención.
La fuerza de presión aplicada durante la formación de comprimidos de partículas/gránulos en un comprimido puede influir en la sensación calcárea y la sensación calcárea no deseada puede reducirse cuando se aplica una fuerza de compresión mayor o igual que 25 kN.
En una realización de la invención, menos del 15 % de carbonato de calcio está presente en el residuo coherente que contiene los componentes orgánicos insolubles en agua después de 5 minutos de masticación.
En una realización de la invención, entre 0,1 y 15 % de carbonato de calcio está presente en el residuo coherente que contiene los componentes orgánicos insolubles en agua después de 5 minutos de masticación, tal como entre 1 y 15 %.
En una realización de la invención, menos del 15 % de carbonato de calcio se mastica en el residuo coherente que contiene los componentes orgánicos insolubles en agua después de 5 minutos de masticación.
En una realización de la invención, entre 0,1 y 15 % de carbonato de calcio se mastica en el residuo coherente que contiene los componentes orgánicos insolubles en agua después de 5 minutos de masticación, tal como entre 1 y 15 %.
El comprimido de la invención, que es un excelente expositor oral de carbonato de calcio, puede usarse ventajosamente como un sistema de suministro bidireccional, que libera carbonato de calcio del comprimido, y al mismo tiempo libera carbonato de calcio para su incorporación en el residuo coherente durante la masticación, proporcionando así un “tampón de liberación” físico, que puede considerarse como un facilitador para la textura ventajosa en uso del producto.
En una realización de la invención, la liberación de carbonato de calcio proporciona un beneficio oral y/o gastrointestinal.
Descripción detallada
En algunas realizaciones de la invención, el comprimido comprende carbonato de calcio y componentes orgánicos insolubles en agua. En algunas realizaciones de la invención, el comprimido comprende un ingrediente farmacéutico
activo, tal como carbonato de calcio, y componentes orgánicos insolubles en agua. Los componentes orgánicos insolubles en agua según diversas realizaciones se describen a continuación.
Los componentes orgánicos insolubles en agua en el presente contexto generalmente se refieren a resinas de elastómero, naturales o sintéticas u otros componentes insolubles en agua, tales como suavizante insoluble en agua.
El término “orgánico” se usa en su significado habitual dentro de la química, particularmente como el sujeto de compuestos y materia dentro de la química orgánica en oposición a la química inorgánica.
Como se usa en esta invención, la frase “comprimido” se refiere a un comprimido fabricado por compresión en una máquina de formación de comprimidos presionando el material de comprimido para formar el comprimido. Por ejemplo, el material del comprimido puede exponerse a un medio de golpeo en una máquina de formación de comprimidos, presionando, p.ej., gránulos y/o polvo en una masa unida de material prensado.
La formación de comprimidos se puede realizar a una cierta presión, por ejemplo, generalmente definida como fuerza de compresión. Se conocen en la técnica diferentes tipos de máquinas de fabricación de comprimidos, tales como un dispositivo de prensa rotativa disponible con Fette.
Como se utiliza en la presente memoria, “%” o “ porcentaje” se refiere al peso/porcentaje en peso a menos que se indique lo contrario.
Como se usa en esta invención, la frase “gránulos” se refiere a entidades hechas, por ejemplo, por granulación, y típicamente pueden contener una pluralidad de partículas adheridas entre sí.
Por la frase “textura” se entiende una medida cualitativa de las propiedades viscoelásticas del comprimido y de la sensación en la boca en general experimentada por el usuario durante el procedimiento de masticación. Por lo tanto, el término “textura” abarca cantidades medibles tales como dureza y elasticidad, así como parámetros más subjetivos relacionados con la sensación de masticación experimentada por un usuario.
“Carbonato de calcio” en el presente contexto se refiere principalmente al carbonato de calcio compresible directo (DC), aunque se pueden aplicar cantidades menores de carbonato de calcio compresible no directo (no DC) dentro del alcance de la invención. Típicamente, tal ‘no DC’, si se aplica, se usa como relleno, a menudo mezclado dentro de los compuestos orgánicos insolubles en agua. Dicho carbonato de calcio ‘no DC’ a menudo se libera poco durante la masticación. Por lo tanto, cuando se hace referencia a la liberación de carbonato de calcio, esto se refiere típicamente a cualquier cantidad de carbonato de calcio DC en lugar de carbonato de calcio ‘no DC’ aplicado como relleno, si lo hay.
Por lo tanto, el carbonato de calcio se puede aplicar como partículas, pero en las presentes realizaciones, el carbonato de calcio se puede aplicar típicamente como un granulado. Por lo tanto, el carbonato de calcio se puede granular de forma típica con almidón, almidón pregelatinizado, maltodextrina, poli-vinilpirrolidona (PVP), goma arábiga/acacia u otro aglutinante adecuado para hacer que el carbonato de calcio sea directamente compresible.
Cuando se hace referencia a la liberación de carbonato de calcio en esta invención, se entiende la liberación in vivo a menos que se especifique lo contrario, donde la liberación in vivo se evalúa de la siguiente manera: al menos 5 evaluadores entrenados se instruyen para masticar cada muestra con 60 masticaciones por minuto durante un tiempo de masticación total de 3 a 10 minutos. Los evaluadores fueron instruidos para no comer o beber nada a no ser agua durante los últimos 30 minutos antes de la prueba. Antes del inicio de la prueba, los evaluadores enjuagaron sus bocas con agua. Para cada muestra probada, los evaluadores masticaron un comprimido durante 3 minutos, otro comprimido durante 5 minutos y otro comprimido durante 10 minutos para producir residuos de comprimidos para cada instante de tiempo. Esto se repitió una vez para obtener réplicas para cada evaluador en cada instante de tiempo en la prueba. El contenido de carbonato de calcio de los residuos después de la masticación se determinó por espectroscopía de absorción atómica estándar (AAS). La liberación se calculó luego comparando el contenido de Ca del residuo después de la masticación con el contenido de Ca del comprimido no masticado.
El carbonato de calcio preferido es, por lo tanto, grados de DC, incluyendo, por ejemplo, CS90 y CM90 de SPI Pharma. Otros grados de DC disponibles comercialmente de carbonato de calcio se pueden aplicar dentro del alcance de la invención, tal como Scoralite LL250 DC 97PVP de Scora S.A.S, carbonato de calcio Dc 90S de Lohmann o DiCOM L100 de Speciality Minerals. También pueden usarse otras marcas de carbonato de calcio de grado DC.
Para obtener un comprimido adaptado para liberar más del 80 % del carbonato de calcio en 5 minutos de masticación, se puede ajustar un intervalo de parámetros.
Ejemplos típicos de diseños estratificados incluyen diseños de dos capas y tres capas. Dependiendo de si el comprimido se fabrica como, por ejemplo, un comprimido de dos o tres capas, una serie de consideraciones son importantes, lo que se explicará con más detalle a continuación. Primero, cuando se usan dos o más capas, el carbonato de calcio y los componentes orgánicos insolubles en agua pueden agruparse juntos en una o más capas o
pueden separarse parcial o totalmente en capas separadas. Al diseñar el comprimido para que tenga el carbonato de calcio en una capa libre de los componentes orgánicos insolubles en agua, la liberación es típicamente más rápida, es decir, se puede obtener una liberación más alta después de 5 minutos. Además, esto está influenciado por la dureza del comprimido o cualquier capa individual.
Además, la velocidad de liberación también puede depender de la dureza obtenida del comprimido. Nuevamente, la dureza del comprimido puede depender de varios parámetros, donde los parámetros importantes incluyen la fuerza de compresión usada cuando se comprime y el grado de compresibilidad de los ingredientes. Se ha observado que la dureza puede influir en la liberación de diferentes maneras dependiendo del diseño del comprimido. Para comprimidos de una capa (de una sola capa), se observó que una dureza aumentada conduce a una liberación más lenta, es decir, una disminución de la liberación después de cinco minutos de masticación. Sin embargo, para comprimidos multicapa, donde el carbonato de calcio se incluyó en una capa libre de componentes orgánicos insolubles en agua, se observó que una mayor dureza conduce a una liberación aumentada después de cinco minutos de masticación, es decir, una liberación más rápida.
Otro parámetro que influyen en la velocidad de liberación es la friabilidad. Típicamente, la friabilidad disminuye al aumentar la fuerza de compresión (y, por lo tanto, aumentar la dureza) y, por lo tanto, una mayor friabilidad puede dar como resultado una liberación más rápida para los comprimidos de una capa. Para comprimidos multicapa, tales como comprimidos de dos capas, se observó una mayor dureza de la capa que contiene carbonato de calcio correspondiente a una menor friabilidad para dar como resultado una liberación más rápida de carbonato de calcio. En cualquier caso, generalmente se considera deseable tener una friabilidad relativamente baja.
Además, el uso de diferentes alcoholes de azúcar puede influir en la velocidad de liberación de carbonato de calcio. Para comprimidos multicapa, son especialmente los alcoholes de azúcar incluidos en la o las capas que contienen el carbonato de calcio que influyen en la velocidad de liberación. Por ejemplo, el sorbitol es típicamente más compresible que, por ejemplo, la isomaltosa y, por lo tanto, la sustitución de isomaltosa con el sorbitol daría como resultado un comprimido más duro (o capa de comprimido más dura). Como se explica, dependiendo del diseño del comprimido, la aplicación de sorbitol en la formulación disminuye la velocidad de liberación para comprimidos de una sola capa, al tiempo que aumenta la velocidad de liberación para comprimidos de múltiples capas cuando se usa en una capa que contiene carbonato de calcio. Un aspecto adicional a considerar es que diferentes alcoholes de azúcar tienen diferente solubilidad en agua y, por lo tanto, en la saliva. La utilización de alcoholes de azúcar de disolución más rápida facilita la liberación de carbonato de calcio. Por ejemplo, el manitol es un ejemplo de un alcohol de azúcar con baja solubilidad en agua en comparación con otros alcoholes de azúcar. Otro aspecto adicional a considerar es que los diferentes alcoholes de azúcar inducen diferentes niveles de secreción de saliva. Por ejemplo, se considera generalmente que xilitol y eritritol proporcionan una excelente generación de saliva.
Incluyendo uno o más aglutinantes en el comprimido también se puede afectar a la velocidad de liberación. Por ejemplo, el carbonato de calcio puede ser granulado típicamente, opcionalmente, con uno o más de almidón, almidón pregelatinizado, maltodextrina, poli-vinilpirrolidona (PVP), goma arábiga/acacia u otro aglutinante adecuado para hacer que sea compresible directo. Por lo tanto, variar el tipo y la cantidad de aglutinante también afecta a la compresibilidad del carbonato de calcio, lo que puede afectar de nuevo a la dureza del comprimido o la capa que contiene carbonato de calcio.
La variación de la composición de componentes orgánicos insolubles en agua también afecta a la velocidad de liberación del carbonato de calcio. Por ejemplo, las cantidades y el tipo de elastómero y/o resina pueden alterarse para afectar la velocidad de liberación del carbonato de calcio.
Un parámetro adicional que afecta a la liberación de carbonato de calcio es la cantidad de resinas y elastómeros incluidos. Disminuir la cantidad de resinas y elastómeros, por ejemplo, disminuyendo el contenido de componentes orgánicos insolubles en agua, aumenta la liberación de carbonato de calcio. Por otro lado, la disminución de la cantidad de elastómero y demasiada resina puede dar como resultado un mal rendimiento del comprimido con respecto a la coherencia y también puede dar como resultado una textura y sensación en la boca inaceptables, tales como una sensación calcárea mayor.
Además, el tamaño de partícula del carbonato de calcio aplicado también puede afectar a la velocidad de liberación. Generalmente, usando un tamaño de partícula más pequeño de carbonato de calcio se aumenta la liberación de carbonato de calcio, debido a una mayor relación de superficie a volumen en las partículas. Por otro lado, el carbonato de calcio de grado ‘no DC’ tiene un tamaño de partícula más pequeño que el carbonato de calcio de grado DC, y el tamaño de partícula demasiado pequeño del carbonato de calcio puede reducir la compresibilidad y las propiedades de flujo del carbonato de calcio y, por lo tanto, hacer que el comprimido sea susceptible de romperse y difícil de procesar en un dispositivo de formación de comprimidos.
Además, en algunas realizaciones se pueden incluir otros ingredientes opcionales que influyen en la liberación de carbonato de calcio. Estos incluyen disgregantes que aumentan la desintegración del comprimido tras la masticación y, por lo tanto, aumenta el contacto entre la saliva oral y las partículas de comprimidos desintegrados, particularmente el carbonato de calcio para aumentar la liberación de carbonato de calcio.
En realizaciones preferidas, los componentes orgánicos insolubles en agua comprenden elastómeros y resinas, por ejemplo, en una cantidad de al menos 50 % en peso de los componentes orgánicos insolubles en agua, tales como al menos 70 % en peso de los componentes orgánicos insolubles en agua. En tales realizaciones, los componentes orgánicos insolubles en agua también se pueden denominar base de goma.
En realizaciones de la invención, los componentes orgánicos insolubles en agua comprenden elastómeros y resinas en cantidades de al menos el 6 % en peso del comprimido, tal como al menos el 15 % en peso del comprimido, o como el 6-50 % en peso del comprimido, tal como el 15-45 % en peso del comprimido.
Como se ha mencionado anteriormente, los componentes orgánicos insolubles en agua comprenden resinas en realizaciones de la invención. Las resinas pueden ser resinas naturales o resinas sintéticas, o una combinación de resinas naturales y resinas sintéticas.
En algunas realizaciones de la presente invención, los componentes orgánicos insolubles en agua comprenden, por ejemplo,
- elastómero en el intervalo de 1-15 % en peso del comprimido,
- resina natural y/o sintética en el intervalo de 5-35 % en peso del comprimido, y
- otros componentes orgánicos insolubles en agua en el intervalo del 5-30 % en peso del comprimido.
Es evidente que la cantidad total global de estos componentes orgánicos insolubles en agua anteriores debe ajustarse mutuamente para corresponderse con los requisitos con respecto al contenido de comprimidos de carbonato de calcio, edulcorante, sabor, etc.
En algunas realizaciones de la presente invención, el comprimido comprende resinas naturales en una cantidad del 0,1 al 30 %, tal como 1 al 25 %, tal como del 3 al 25 % o del 5 al 25 %, en peso del comprimido.
En algunas realizaciones de la presente invención, el comprimido comprende resinas naturales en una cantidad de al menos 10 % en peso del comprimido.
En algunas realizaciones de la presente invención, el comprimido comprende resinas naturales en una cantidad de 10 a 30 % en peso del comprimido.
En algunas realizaciones de la presente invención, el comprimido está libre de resinas naturales.
En realizaciones de la presente invención, el comprimido comprende resinas sintéticas en una cantidad del 0,1 al 30 %, tal como del 1 al 25 %, tal como del 3 al 25 % o del 5 al 25 %, en peso del comprimido.
Como se mencionó anteriormente, los componentes orgánicos insolubles en agua comprenden elastómero en realizaciones de la invención.
En realizaciones de la presente invención, el comprimido comprende elastómero en una cantidad de al menos 2 % en peso del comprimido, tal como al menos 4 % en peso del comprimido.
En realizaciones de la presente invención, el comprimido comprende elastómero en una cantidad inferior al 35 % en peso del comprimido, tal como menos de aproximadamente el 25 % en peso del comprimido, tal como menos del 20 %, el 15 % o el 10 % en peso del comprimido.
En realizaciones de la presente invención, el comprimido comprende elastómero en una cantidad de 2-35 % en peso del comprimido, tal como 4-25 % en peso del comprimido, tal como 4-20 % en peso del comprimido.
En una realización de la invención, los otros componentes orgánicos insolubles en agua comprenden o consisten en suavizantes, tales como cera, grasas y/o emulsionantes.
En realizaciones de la presente invención, el comprimido comprende uno o más agentes saborizantes, preferiblemente en forma de polvo, seleccionados del grupo que consiste en aceites esenciales, esencias, extractos, polvos, ácidos, coco, café, chocolate, vainilla, toronja, naranja, lima, mentol, regaliz, aroma de caramelo, aroma de miel, maní, nuez, marañón, avellana, almendras, piña, fresa, frambuesa, manzana, pera, melocotón, albaricoque, mora, cereza, piña, esencia de ciruela, aceite de clavo, aceite de laurel, anís, tomillo, aceite de hoja de cedro, nuez moscada, canela, menta, gaulteria, menta verde, eucalipto, menta o cualquier combinación de los mismos.
En realizaciones de la presente invención, el comprimido comprende uno o más humectantes, tales como propilenglicol o glicerol.
En realizaciones de la presente invención, el comprimido está provisto de un recubrimiento.
En realizaciones de la presente invención, el comprimido tiene un peso en el intervalo de 0,1 a 10 gramos, tal como en el intervalo de 0,5 a 4 gramos o tal como en el intervalo de 1,5 a 2,5 gramos.
Según una realización de la invención, el comprimido puede comprender relleno. En realizaciones de la presente invención, el comprimido comprende un relleno adicional en una cantidad de 0,1 a 40 % en peso del comprimido.
Los elastómeros proporcionan la naturaleza gomosa, cohesiva al comprimido, que varía dependiendo de la estructura química del ingrediente y cómo puede combinarse con otros ingredientes. Los elastómeros adecuados para su uso en el comprimido de la presente invención pueden incluir tipos naturales o sintéticos.
Los plastificantes de elastómero varían la firmeza de los componentes orgánicos insolubles en agua. Su especificidad en la interacción intermolecular de elastómero (plastificación) junto con sus puntos de reblandecimiento variables provoca diversos grados de firmeza de comprimidos terminados y compatibilidad con otros ingredientes. Esto puede ser importante cuando se quiere proporcionar una exposición más elastomérica de la cadena a las cadenas de alcanos de las ceras. Los plastificantes de elastómero pueden ser típicamente resinas, tales como resinas sintéticas y/o resinas naturales.
Los elastómeros empleados en el comprimido pueden variar dependiendo de diversos factores tales como la textura deseada del residuo coherente (es decir, el comprimido después de la masticación) y los otros componentes usados en la formulación para hacer el comprimido. El elastómero puede ser cualquier polímero insoluble en agua conocido en la técnica. Los ejemplos ilustrativos de polímeros adecuados en el comprimido incluyen elastómeros naturales y sintéticos. Por ejemplo, aquellos polímeros que son adecuados en el comprimido incluyen sustancias naturales (de origen vegetal) tales como goma de endivia, caucho natural, goma corona, nispero, rosidinha, jelutong, perillo, niger gutta, tunu, balata, gutapercha, lechi capsi, sorva, gutta kay y similares, y mezclas de los mismos. Ejemplos de elastómeros sintéticos incluyen copolímeros de estireno-butadieno (SBR), poliisobutileno, copolímeros de isobutilenoisopreno (es decir, caucho de butilo), polietileno y similares, y mezclas de los mismos.
Las resinas naturales se pueden usar según la invención y pueden ser ésteres de colofonia naturales, incluyendo como ejemplos ésteres de glicerol de colofonias parcialmente hidrogenadas, ésteres de glicerol de colofonias polimerizadas, ésteres de glicerol de colofonias parcialmente dimerizadas, ésteres de glicerol de colofonias de tally oil, ésteres de pentaeritritol de colofonias parcialmente hidrogenadas, ésteres metílicos de colofonias, ésteres metílicos de colofonias parcialmente hidrogenadas, ésteres de colofonias de pentaeritritol, resinas sintéticas tales como resinas terpénicas derivadas de alfa-pineno, beta-pineno y/o d-limoneno y resinas terpénicas naturales.
En una realización de la invención, la resina comprende resinas terpénicas, p.ej., derivados de alfa-pineno, betapineno y/o d-limoneno, resinas terpénicas naturales, ésteres de glicerol de colofonias de goma, colofonias de tall oil, colofonias de madera u otros derivados de los mismos tales como ésteres de glicerol de colofonias parcialmente hidrogenadas, ésteres de glicerol de colofonias polimerizadas, ésteres de glicerol de colofonias parcialmente dimerizadas, ésteres de pentaeritritol de colofonias parcialmente hidrogenadas, ésteres de metilo de colofonias, ésteres de metilo de colofonias parcialmente hidrogenadas o ésteres de colofonias de pentaeritritol y combinaciones de los mismos.
En una realización de la invención, una resina sintética puede incluir acetato de polivinilo (PVAc) y/o copolímeros de acetato de vinilo-laurato de vinilo (VA-VL).
En una realización de la invención, elo comprimido puede comprender uno o más componentes seleccionados del grupo que consiste en edulcorantes a granel, sabores, aglutinantes secos, auxiliares para la formación de comprimidos, agentes antiaglomerantes, emulsionantes, antioxidantes, potenciadores, potenciadores de la absorción, edulcorantes de alta intensidad., suavizantes, colorantes o cualquier combinación de los mismos.
En una realización de la invención, el comprimido comprende edulcorantes, tales como edulcorantes a granel, edulcorantes de azúcar, edulcorantes sustitutos de azúcar, edulcorantes artificiales, edulcorantes de alta intensidad o cualquier combinación de los mismos.
Los edulcorantes a granel adecuados incluyen componentes edulcorantes tanto de azúcar como sin azúcar. Los edulcorantes a granel constituyen típicamente de aproximadamente 5 a aproximadamente 95 % en peso del comprimido, más típicamente de aproximadamente 20 a aproximadamente 80 % en peso, tal como 30 a 70 % o 30 a 60 % en peso del comprimido.
Los edulcorantes de azúcar útiles son componentes que contienen sacáridos comúnmente conocidos en la técnica del comprimido, incluyendo sacarosa, dextrosa, maltosa, lactosa, dextrinas, trehalosa, D-tagatosa, azúcar invertido seco, fructosa, lebulosa, galactosa, sólidos de jarabe de maíz y similares, solos o en combinación.
Como ejemplo, el sorbitol se puede usar como edulcorante sin azúcar. Otros edulcorantes que no tienen azúcar útiles incluyen otros alcoholes de azúcar tales como manitol, xilitol, maltitol, isomalt, eritritol, lactitol y similares, solos o en combinación.
Los agentes edulcorantes artificiales de alta intensidad también se pueden usar solos o en combinación con los edulcorantes anteriores. Por ejemplo, edulcorantes de alta intensidad incluyen sucralosa, aspartamo, sales de acesulfamo, alitamo, sacarina y sus sales, ácido ciclámico y sus sales, glicirricina, dihidrocalconas, taumatina, monelina, esteviósido (edulcorante de intensidad natural) y similares, solos o en combinación. Para proporcionar dulzor y percepción de sabor más duraderos, puede ser deseable encapsular o controlar de otro modo la liberación de al menos una porción de los edulcorantes artificiales. Las técnicas tales como granulación en húmedo, granulación en cera, secado por pulverización, enfriamiento por pulverización, recubrimiento de lecho fluido, conservación, encapsulación en células de levadura y extrusión de fibras pueden usarse para lograr las características de liberación deseadas. También se puede proporcionar encapsulación de agentes edulcorantes.
El nivel de uso del edulcorante artificial variará considerablemente y dependerá de factores tales como la potencia del edulcorante, la velocidad de liberación, el dulzor deseado del producto, el nivel y el tipo de sabor usado y consideraciones de coste. Por lo tanto, el nivel activo de edulcorante artificial puede variar de aproximadamente 0,001 a aproximadamente 8 % en peso (preferiblemente de aproximadamente 0,02 a aproximadamente 8 % en peso). Cuando se incluyen portadores utilizados para la encapsulación, el nivel de uso del edulcorante encapsulado será proporcionalmente más alto. Se pueden usar combinaciones de edulcorantes de azúcar y/o sin azúcar en formulación del comprimido.
Un comprimido según la invención puede, si se desea, incluir uno o más rellenos/texturizantes que incluyen, por ejemplo, magnesio, sulfato de sodio, piedra caliza molida, compuestos de silicato tales como silicato de magnesio y aluminio, caolín y arcilla, óxido de aluminio, óxido de silicio, talco, óxido de titanio, fosfatos de mono-, di- y tri-calcio, carbonato de calcio y magnesio, polímeros de celulosa, tales como madera o celulosa microcristalina (MCC), y combinaciones de los mismos.
Dentro del alcance de la presente invención se pueden aplicar varios materiales de comprimidos bien conocidos en la técnica. Tales componentes son ceras, grasas, suavizantes, rellenos, sabores, antioxidantes, emulsionantes, agentes colorantes, agentes aglutinantes y acidulantes
Los gránulos o algunos de los gránulos pueden, por ejemplo, consistir o comprender en gran medida o consistir en componentes orgánicos insolubles en agua y dichos gránulos pueden fabricarse mediante extrusión y granulación en agua.
El tamaño de tales gránulos de componentes orgánicos insolubles en agua puede controlarse según la presente invención por varios factores tales como tamaños de abertura, la composición, la temperatura y la caída de presión, si se usa una placa de matriz en la extrusora. Debido a una interacción entre la composición presurizada, la temperatura y la fricción en las aberturas del dispositivo de matriz, el diámetro promedio de los gránulos producidos es normalmente mayor que los diámetros de las aberturas en el dispositivo de matriz. La relación entre los diámetros de las aberturas en el dispositivo de matriz y los diámetros promedio de los gránulos producidos a partir de una composición específica puede determinarse por el experto en base a los experimentos rutinarios.
Según la invención, también es posible producir gránulos con diferentes diámetros promedio haciendo gránulos con un diámetro, y mezclar posteriormente los gránulos con diferentes diámetros promedio en proporciones deseadas.
Aunque las aberturas de una matriz de un dispositivo extrusor pueden tener secciones transversales de cualquier forma deseada, por ejemplo, circular, ovalada, cuadrada, etc., en algunas realizaciones se prefiere que el dispositivo de matriz comprenda aberturas con sección transversal y diámetros sustancialmente circulares en el intervalo de 0,1 a 1,3 mm. Un primer conjunto de aberturas puede, por ejemplo, tener un primer diámetro en el intervalo de 0,07 a 0,7 mm, tal como en el intervalo de 0,15 a 0,6 mm, y adecuadamente en el intervalo de 0,2 a 0,5 mm. Un segundo conjunto de aberturas puede tener un segundo diámetro mayor que dicho primer diámetro. El segundo diámetro está convenientemente en el intervalo de 0,4 a 1,3 mm, tal como en el intervalo de 0,7 a 1,2 mm.
En algunas realizaciones, el sistema de granulación comprende además un dispositivo de secado. Se puede añadir edulcorante en polvo o talco a los gránulos en una etapa de secado final. El dispositivo de secado puede ser un secador centrífugo convencional u otro secador adecuado, por ejemplo, un secador de lecho fluido. El dispositivo de secado puede incluir, por ejemplo, un mezclador. En una realización, el edulcorante en polvo puede ser sorbitol, que se mezcla con los gránulos secos o parcialmente secos. Cantidades menores de humedad residual sobre la superficie de los gránulos, p. ej., 2 % en peso, basado en el peso total de los gránulos, pueden contribuir a la adherencia del polvo de sorbitol a la superficie de los gránulos. Es posible usar un agente antiaglomerante convencional como, por ejemplo, talco, pero el polvo de sorbitol puede funcionar como un agente antiaglomerante, y al mismo tiempo sirve como edulcorante. Aunque se encuentra que el sorbitol es más adecuado, otros edulcorantes a granel basados en polioles también pueden ser adecuados, p. ej., manitol, xilitol, maltitol, isomalt, eritritol y lactitol.
En una realización, el sistema de granulación de comprimidos según la invención comprende además uno o más tamices adaptados para eliminar gránulos con un diámetro promedio tal como por encima de 1,3 mm. La eliminación de gránulos más grandes mejora un procedimiento posterior de formación de comprimidos.
Según una realización de la invención, al menos la extrusora y/o el dispositivo de matriz comprenden medios para controlar la temperatura de la composición. Los medios para controlar la temperatura pueden ser dispositivos de enfriamiento o calentamiento, y pueden servir para facilitar el flujo de la composición a través de la extrusora y el dispositivo de matriz. En una realización, la extrusora comprende medios de suministro para suministrar edulcorante y/o sabor a la composición de comprimido en la extrusora.
Durante la extrusión de la composición, la presión diferencial entre la composición en la extrusora y la composición en la cámara llena de líquido, es decir, sobre el dispositivo de matriz, es adecuadamente superior a 10 bar, tal como superior a 18 bar, tal como en el intervalo de 25 a 90 bar. La temperatura de la composición en la extrusora puede estar, por ejemplo, en el intervalo de 40 a 125 0C, adecuadamente en el intervalo de 50 a 115 0C. La temperatura del dispositivo de matriz puede estar, por ejemplo, en el intervalo de 60 a 250 0C, adecuadamente en el intervalo de 80 a 180 0C. La temperatura del líquido en la cámara llena de líquido está convenientemente en el intervalo de 8 a 40 0C. Lo óptimo para las presiones y temperaturas en el procedimiento según la invención puede, sin embargo, ser determinado por la persona experta como materia de rutina. Los valores óptimos para composiciones específicas varían, por supuesto, dependiendo de la composición.
El enfriamiento rápido en la cámara llena de aire o llena de agua puede actuar para preservar posibles ingredientes frágiles en la composición, de modo que sus cualidades se mantienen mejor intactas y se transportan a los gránulos incluidos en el producto final. Esta calidad mejorada de la composición en los gránulos que comprenden los componentes orgánicos insolubles en agua mejora la composición general del comprimido.
Las fracciones de gránulos de diferentes pesos promedio pueden producirse con dos configuraciones diferentes, produciendo cada una un lote de gránulos de un peso promedio particular, seguido de una mezcla de las fracciones. También es posible diseñar un medio de matriz con aberturas de matriz de al menos dos tamaños diferentes para obtener simultáneamente gránulos con diferente diámetro promedio. Por lo tanto, es posible obtener gránulos que tengan diferentes pesos. Se pueden obtener más de dos pesos promedio diferentes, dependiendo del diseño de los medios de matriz en uso. Por ejemplo, es posible obtener gránulos con tres, cuatro o más pesos promedio diferentes.
Los gránulos pueden cortarse en una cámara muy grande llena de líquido, en la que los gránulos también se enfrían. En algunas realizaciones, el enfriamiento se combina con la transferencia de los gránulos lejos de la cámara. Esto se puede hacer, por ejemplo, enfriando los gránulos cortados en agua durante la transferencia desde la cámara llena de líquido hasta un dispositivo de deshidratación. El tiempo de transferencia desde el corte a deshidratar puede ser inferior a 6 s. La ventaja de esto es que los ingredientes solubles en agua en la composición no se lavan innecesariamente de los gránulos. Opcionalmente, el tiempo total de contacto entre gránulos y agua de enfriamiento puede limitarse adicionalmente a menos de 4 s.
El comprimido de la invención puede formarse mediante partículas prensadas y/gránulos. Cuando estos son comprimidos, se establecen enlaces entre las partículas o gránulos, lo que confiere una cierta resistencia mecánica al comprimido. De las partículas/gránulos, el comprimido comprende carbonato de calcio en una cantidad de más del 30 % en peso del comprimido.
Cuando se aplica presión a las partículas/gránulos, se reduce el volumen a granel y disminuye la cantidad de aire. Durante este procedimiento se consume energía. A medida que las partículas/gránulos entran más cerca entre sí durante el procedimiento de reducción de volumen, pueden establecerse enlaces entre las partículas o gránulos. La formación de enlaces se asocia con una reducción en la energía del sistema a medida que se libera energía.
La reducción de volumen tiene lugar por diversos mecanismos y pueden establecerse diferentes tipos de enlaces entre las partículas o gránulos dependiendo de la presión aplicada y las propiedades de las partículas o gránulos.
Ejemplos de componentes orgánicos insolubles en agua aplicables para comprimidos de la presente invención se describen en el documento PCT/DK02/00461 y PCT/DK02/00462.
La composición de componentes orgánicos insolubles en agua, que se mezclan con los ingredientes de los comprimidos como se definen a continuación, pueden variar sustancialmente dependiendo del producto particular que se va a preparar y de las características enmascarantes y otras características deseadas del producto final. Sin embargo, los intervalos típicos (% en peso) de los componentes orgánicos insolubles en agua anteriores son:
- elastómero en el intervalo de 1-15 % en peso del comprimido,
- resina natural y/o sintética en el intervalo del 5-35 % en peso del comprimido, y
- otros componentes orgánicos insolubles en agua en el intervalo del 5-30 % en peso del comprimido.
Es evidente que la cantidad total global de estos componentes orgánicos insolubles en agua anteriores debe ajustarse mutuamente para corresponderse con los requisitos con respecto al contenido de comprimidos de carbonato de calcio, edulcorante, sabor, etc.
Los gránulos de componentes orgánicos insolubles en agua pueden fabricarse según procedimientos convencionales o, por ejemplo, los descritos en el documento PCT/DK02/00461 y PCT/DK02/00462.
Los siguientes ejemplos ilustran diferentes variaciones de la presente invención. Los ejemplos están destinados a indicar el concepto inventivo; Por tanto, los ejemplos mencionados no deben entenderse como exhaustivos para la presente invención.
Ejemplos
Ejemplos 1-7
Siete muestras diferentes, que fueron numeradas 101-107, de complejos de compuestos orgánicos insolubles en agua se proporcionan en los Ejemplos 1-7. Las composiciones se dan en la Tabla 1 y las muestras se prepararon mediante el siguiente procedimiento:
Los elastómeros y aproximadamente 1/3 de la resina se mezclan a 120 °C junto con el relleno en un mezclador precalentado que tiene brazos con forma de Z colocados horizontalmente para mezclar. Los rellenos son talco o carbonato de calcio 'no DC'. La acción mecánica del mezclador provoca el cizallamiento y la molienda, lo que resulta en el ablandamiento de los elastómeros.
Cuando los elastómeros se ablandan, se añade lentamente más resina al elastómero, resina y relleno hasta que la mezcla se vuelve homogénea. La resina restante se añade a continuación al mezclador y se mezcla durante 10 20 minutos. Los suavizantes, es decir, emulsionante, cera y grasa vegetal, se añaden y mezclan a continuación durante 20-40 minutos hasta que toda la mezcla se vuelve homogénea.
Después de un tiempo de mezclado total de aproximadamente 45-60 minutos, la mezcla es sometida a peletización en una unidad de granulación en agua (UWP) que da como resultado gránulos coherentes con un diámetro promedio de aproximadamente 1 mm. Sabor, si corresponde, puede añadirse a la composición justo antes de la granulación.
El poliisobutileno aplicado puede ser, p. ej., Opanol B12, acetato de polivinilo (PVAc), p. ej., los copolímeros de VA-VL de Vinnapas B 1,5 sp, (copolímeros de acetato de vinilo-laurato de vinilo) pueden, por ejemplo, ser Vinnapas B 500/20 VL, resina natural puede, por ejemplo, ser Staybelite 5E o Piccolyte C85, el suavizante puede, por ejemplo, ser grasa vegetal hidrogenada tal como aceite de girasol hidrogenado. El relleno de carbonato de calcio usado es un material 'no DC' estándar con un tamaño de partícula promedio inferior a 20 micrómetros. El edulcorante a granel puede ser, p. ej., sorbitol, sabor, p. ej., cristales de mentol. Se enfatiza que los componentes mencionados específicamente son, por supuesto, una descripción destinada a ayudar a un experto en la producción de la presente invención.
En el caso del Ejemplo 7 (muestra n.° 107), la mezcla homogénea no se somete a granulación, sino que simplemente se descarga en una cubeta y se deja enfriar a temperatura ambiente.
Después, la mezcla se añade a otro mezclador que tiene brazos en forma de Z colocados horizontalmente para mezclar que funciona a una temperatura de aproximadamente 40 0C. Se añade edulcorante a granel y se mezcla hasta obtener una masa homogénea.
La masa se descarga y se enfría mediante nitrógeno líquido antes de introducirse en un dispositivo de molienda, en el que la masa se muele para obtener material particulado que está listo para la formación de comprimidos.
Tabla 1 - Los números se proporcionan en porcentaje en peso del comprimido. El contenido total de resina es el contenido combinado de resina natural y resina sintética.
Ejemplo 8-14
Preparación de comprimidos
Los comprimidos, con números de muestra dados 1001 - 1007, usando los compuestos proporcionados en los Ejemplos 1-7, respectivamente, se prepararon de la siguiente forma:
Los compuestos de los Ejemplos 1-7 están presentes en forma de partículas/gránulos.
Los compuestos particulados de los Ejemplos 1-7, compuestos de comprimidos adicionales y el carbonato de calciocalcio (con un ensayo de aproximadamente 100 % ) se pesan en las cantidades adecuadas según las composiciones de la tabla 2A.
Las cantidades pesadas se añaden a continuación a un mezclador Turbula en un recipiente de acero inoxidable y se mezclan a 50 rpm durante 4 minutos y luego se añaden estearato de magnesio y mezclando un minuto adicional.
Las mezclas se comprimen entonces por medio de un Piccola RIA DC-SC- 041-2. También se puede aplicar una Fette 3090i.
Los comprimidos resultantes según los Ejemplos 8-14 se obtienen entonces mediante formación de comprimidos con una fuerza de presión adecuada a aproximadamente 28-30 kN como fuerza de compresión principal. El peso del comprimido es de 1,8 g para todas las muestras.
El edulcorante a granel aplicado puede, por ejemplo, ser isomalt, un edulcorante de alta intensidad puede, por ejemplo, ser de sucralosa, el sabor puede, por ejemplo, menta en forma de polvo. También aquí, se enfatiza que los componentes mencionados específicamente son, por supuesto, una descripción destinada a ayudar a un experto en la producción de la presente invención.
Tabla 2A - El número se proporciona en porcentaje en peso del comprimido
Ejemplo 15 - Liberación in vitro de carbonato de calcio de comprimidos
La liberación del carbonato de calcio en este ejemplo se determinó in vitro. Las mediciones se llevaron a cabo según el procedimiento expuesto en la Ph. Eur. 6a ed. 2.9.25, en un tampón fosfato con pH = 7,4, una velocidad de masticación de 60 masticaciones por minuto, y con la temperatura del medio ajustada a 37 0C. El procedimiento de masticación se interrumpe cada minuto para reemplazar el tampón fosfato, evitando así la saturación del tampón y simulando la deglución en el procedimiento de masticación in vivo. Para cada muestra, un comprimido se masticó en intervalos de tiempo especificados 3, 5 y 10 minutos para producir residuos de comprimidos para cada instante de tiempo. Esto se repitió 6 veces para obtener 6 réplicas para cada instante de tiempo en la prueba.
El contenido de carbonato de calcio de los residuos después de la masticación se determinó por espectroscopia de absorción atómica estándar (AAS). Para el análisis, se disolvió un comprimido residual en una mezcla de ácido clorhídrico (HCl) y tolueno. Después de la dilución y filtración adecuadas, la fase ácida se pasó a través del dispositivo de AAS analizando Ca (a una longitud de onda de 442,7 nm).
La liberación se calculó luego comparando el contenido de Ca del residuo después de la masticación con el contenido de Ca del comprimido no masticado.
Alternativamente, se pueden usar técnicas de titulación estándar para determinar el contenido de carbonato de calcio antes y después de la masticación.
Los resultados (promedios de resultados replicados) se muestran en la tabla 2B.
Tabla 2B - Liberación de carbonato de calcio después de 5 minutos de masticación
Ejemplo 16 - Evaluación de la capacidad de limpieza de dientes de las muestras 1001 (Ej. 8) y 1002 (Ej. 9) Se utilizó un panel de prueba de 8 personas entrenadas para evaluación sensorial. Las personas entrenadas fueron instruidas para no comer o beber nada que no fuese agua durante los últimos 30 minutos antes de la prueba. El panel de prueba se instruyó para masticar las muestras a una velocidad de 60 masticaciones por minuto para un tiempo de masticación total de 10 minutos.
Además de la evaluación de los atributos sensoriales estándar, tales como la suavidad y la intensidad del gusto, se instruyó a las personas capacitadas para evaluar la capacidad de limpieza de los dientes de las muestras al responder a la pregunta: “ ¿Queda algún residuo de comprimido en los dientes?” (sí/no) en distintos instantes de tiempo durante el procedimiento de masticación.
Los resultados de esta evaluación se proporcionan en las tablas 3 y 4 a continuación.
Tabla 3 - Evaluación de la capacidad para la limpieza de los dientes
Tabla 4 - Evaluación de la capacidad para la limpieza de los dientes
Ejemplo 17 - Evaluación de la sensación calcárea, es decir, residuo de carbonato de calcio de las muestras 1001 (Ej.
8) y 1002 (Ej. 9)
Se utilizó un panel de prueba de 8 personas entrenadas para evaluación sensorial. Las personas entrenadas fueron instruidas para no comer o beber nada que no fuese agua durante los últimos 30 minutos antes de la prueba. El panel de prueba se instruyó para masticar las muestras a una velocidad de 60 masticaciones por minuto para un tiempo de masticación total de 5 minutos.
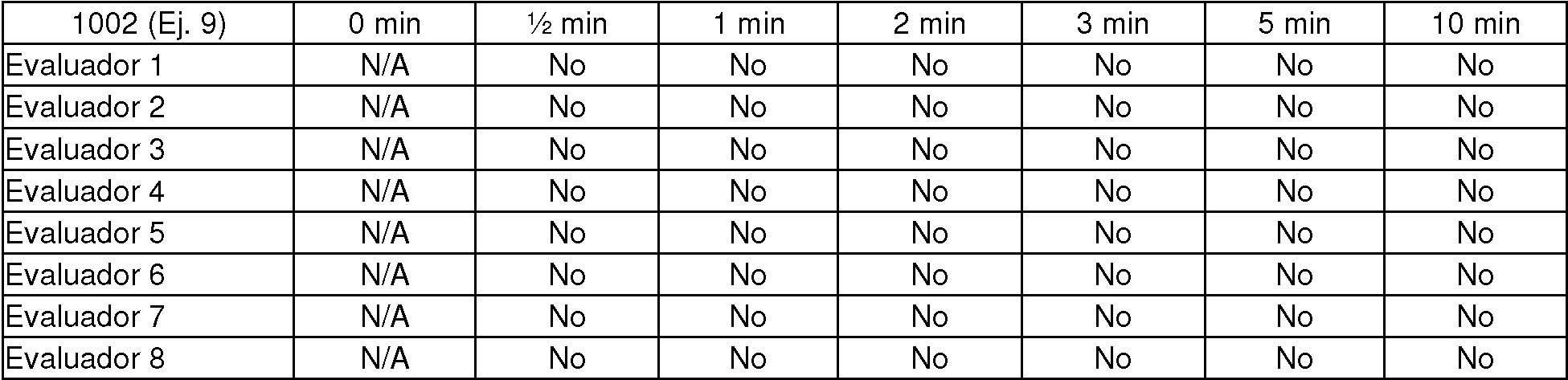
Además de la evaluación de los atributos sensoriales estándar, tales como la suavidad y la intensidad del gusto, las personas entrenadas fueron instruidas en esta prueba para evaluar la sensación calcárea, es decir, la sensación de residuos de carbonato de calcio en la cavidad oral, al responder a la pregunta: “ ¿Hay algún residuo de carbonato de calcio que se quede en la boca, es decir, hay alguna sensación calcárea presente;?” (sí/no) en distintos instantes de tiempo durante el procedimiento de masticación.
Los resultados de esta evaluación se proporcionan en las tablas 5 y 6 a continuación.
Tabla 5 - Evaluación de la sensación calcárea
Tabla 6 - Evaluación de la sensación calcárea
Ejemplo 18-21
Se proporcionan cuatro muestras diferentes, que recibieron números 108-111, de complejos de compuestos orgánicos insolubles en agua en los Ejemplos 18-21. Las composiciones se dan en la Tabla 7 y las muestras se prepararon mediante el siguiente procedimiento:
Los elastómeros y aproximadamente 1/3 de la resina se mezclan a 120 0C junto con el relleno en un mezclador precalentado que tiene brazos con forma de Z colocados horizontalmente para mezclar. Los rellenos son talco. La acción mecánica del mezclador provoca el cizallamiento y la molienda, lo que resulta en el ablandamiento de los elastómeros.
Cuando los elastómeros se ablandan, se añade lentamente más resina al elastómero, resina y relleno hasta que la mezcla se vuelve homogénea. La resina restante se añade a continuación al mezclador y se mezcla durante 10 20 minutos. Los suavizantes, es decir, emulsionante, cera y grasa vegetal, se añaden y mezclan a continuación durante 20-40 minutos hasta que toda la mezcla se vuelve homogénea.
Después de un tiempo de mezclado total de aproximadamente 45-60 minutos, la mezcla es sometida a granulación en una unidad estándar de granulación debajo del agua (UWP ) lo que da como resultado gránulos coherentes con un diámetro promedio de aproximadamente 1 mm. Se puede añadir sabor a la composición justo antes de la granulación.
El poliisobutileno aplicado puede ser, p. ej., Opanol B12, acetato de polivinilo (PVAc), p. ej., los copolímeros de VA-VL de Vinnapas B 1,5 sp, (copolímeros de acetato de vinilo-laurato de vinilo) pueden, por ejemplo, ser Vinnapas B 500/20 VL, resina natural puede, por ejemplo, ser Staybelite 5E o Piccolyte C85, el suavizante puede, por ejemplo, ser grasa vegetal hidrogenada tal como aceite de girasol hidrogenado. El sabor puede ser, p. ej., cristales de mentol.
Se enfatiza que los componentes mencionados específicamente son, por supuesto, una descripción destinada a ayudar a un experto en la producción de la presente invención.
Tabla 7 - Los números se proporcionan en porcentaje en peso del comprimido. El contenido total de resina es el contenido combinado de resina natural y resina sintética.
Ejemplo 22-24
Preparación de comprimidos de una capa
Los comprimidos de una capa, dadas las muestras de los números 1008 - 1110, usando los compuestos proporcionados en los Ejemplos 18-21, respectivamente, se prepararon de la siguiente forma:
Los compuestos de los Ejemplos 18-21 están presentes en forma de partículas/gránulos.
Los compuestos particulados de los Ejemplos 18-21, compuestos de comprimidos adicionales y el carbonato de calcio-DC (con un ensayo de aproximadamente 100 % ) se pesan en las 5 cantidades adecuadas según las composiciones de la tabla 8A.
Para obtener una mezcla de los ingredientes de comprimido a usar, las cantidades pesadas se añaden a continuación a un mezclador Turbula en un recipiente de acero inoxidable y se mezclan a 50 rpm durante 4 minutos y luego se añaden estearato de magnesio y mezclando un minuto adicional.
Las mezclas se comprimen entonces por medio de un Piccola RIA DC-SC- 041-2. También se puede aplicar una Fette 3090i.
Los comprimidos de una capa resultantes según los Ejemplos 22-24 se obtienen entonces mediante formación de comprimidos con una fuerza de presión adecuada a aproximadamente 28-30kN como fuerza de compresión principal. El peso del comprimido de una capa es de 1,8 g para todas las muestras.
Tabla 8A - El número se proporciona en porcentaje en peso del comprimido
Los Ejemplos 22-24 caen fuera del alcance de las reivindicaciones.
Ejemplo 25-28
Preparación de comprimidos de dos capas
Comprimidos de dos capas, con números de muestra dados 1111 - 1114, usando los compuestos proporcionados en los Ejemplos 18-21, respectivamente, se prepararon de la siguiente manera:
Los compuestos de los Ejemplos 18-21 están presentes en forma de partículas/gránulos.
Primero, los ingredientes para la capa 1 se pesan en las cantidades adecuadas según las composiciones de la tabla 8B. A continuación, los ingredientes para la capa 2 se pesan en las cantidades adecuadas también según las composiciones de la tabla 8B.
Cada una de las dos composiciones se mezcla mediante un mezclador Turbula en un recipiente de acero inoxidable y se mezcla a 50 rpm durante 4 minutos y luego añadiendo estearato de magnesio y mezclando un minuto adicional.
Las mezclas se comprimen entonces por medio de un Piccola RIA DC-SC- 041-2. También se puede aplicar una Fette 3090i.
Para cada comprimido de dos capas 1111-1114, los ingredientes de la capa 1 se presionan inicialmente a una primera presión relativamente baja. Los ingredientes para la capa 2 se alimentan a continuación al molde y después se comprime un comprimido final de dos capas a una fuerza de presión más alta adecuada de aproximadamente 28 30 kN como fuerza de compresión principal, produciendo así comprimidos finales de dos capas 1111-1114. El peso del comprimido de dos capas es de 1,8 g para todas las muestras.
El edulcorante a granel aplicado usado en los ejemplos 22-28 puede, por ejemplo, ser isomalt, un edulcorante de alta intensidad puede, por ejemplo, ser sucralosa, el sabor puede ser, por ejemplo, menta en forma de polvo. También aquí, se enfatiza que los componentes mencionados específicamente son, por supuesto, una descripción destinada a ayudar a un experto en la producción de la presente invención. El carbonato de calcio-DC aplicado tiene un ensayo de aproximadamente 100 %.
Tabla 8B - El número se proporciona en porcentaje en peso del comprimido
Ejemplo 31-37
Los comprimidos del ejemplo 31-37 se fabricaron mediante un procedimiento correspondiente al del ejemplo 22 (comprimido de una capa), pero con los materiales especificados en la tabla 9 obteniendo comprimidos con un peso de 1,8 gramos.
Como se muestra en el ejemplo 31-37, se muestran comprimidos de una capa con diversas cantidades y tipos de edulcorante a granel. Para comparación, el ejemplo 37 se fabrica con el mismo contenido que el ejemplo 32, pero como una goma de mascar extruida convencional sin recubrimiento, es decir, una composición obtenida mediante mezclado intensivo en un mezclador Sigma-Blade seguido de extrusión, laminación y marcación.
El edulcorante de alta intensidad aplicado usado en los ejemplos 31 -37 es sucralosa, y el sabor es menta en forma de polvo. También aquí, se enfatiza que los componentes mencionados específicamente son, por supuesto, una
descripción destinada a ayudar a un experto en la producción de la presente invención. El carbonato de calcio-DC aplicado tiene un ensayo de aproximadamente 100 %.
Tabla 9 - El número se proporciona en porcentaje en peso del comprimido
Los Ejemplos 31-37 se encuentran fuera del alcance de las reivindicaciones.
Ejemplo 41-48
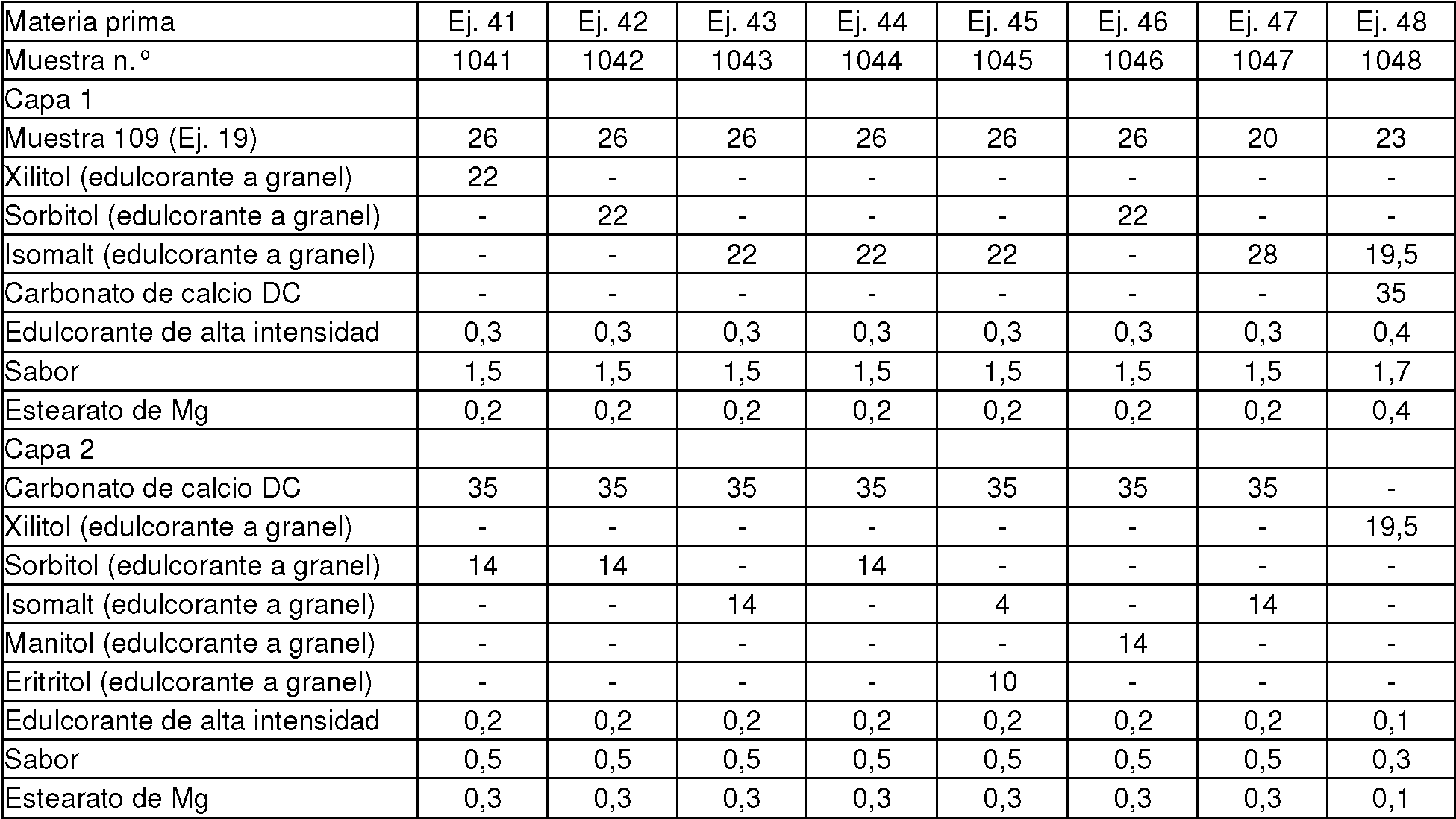
Los comprimidos de ejemplo 41-48 se prepararon mediante un procedimiento correspondiente al del ejemplo 25 (comprimido de dos capas), pero con los materiales especificados en la tabla 10 obteniendo comprimidos con un peso de 1,8 gramos.
Como se muestra en el ejemplo, se muestra de 41-48 comprimidos de dos capas con diversas cantidades y tipos de edulcorante a granel. El Ejemplo 48 muestra el uso de carbonato de calcio junto con los componentes orgánicos insolubles en agua en la misma capa de un comprimido de dos capas.
El edulcorante de alta intensidad aplicado usado en los ejemplos 41 -48 es sucralosa, y el sabor es menta en forma de polvo. También aquí, se enfatiza que los componentes mencionados específicamente son, por supuesto, una descripción destinada a ayudar a un experto en la producción de la presente invención. El carbonato de calcio-DC aplicado tiene un ensayo de aproximadamente 100 %.
Tabla 10 - El número se proporciona en porcentaje en peso del comprimido
Ejemplo 51-57
Los comprimidos de ejemplo 51-57 se fabricaron mediante un procedimiento correspondiente al del ejemplo 25 (comprimido de dos capas), pero con los materiales especificados en la tabla 11 obteniendo comprimidos con un peso de 1,8 gramos.
Como se muestra en los ejemplos 51 -57, se pueden usar varias cantidades y tipos de aglutinante con el carbonato de calcio aplicado. Se observa que la ligera variación del carbonato de calcio de grado DC usado se debe a las variaciones en cantidades de aglutinante aplicado. Por lo tanto, la cantidad de carbonato de calcio es comparable para todas las muestras en estos ejemplos.
El edulcorante a granel aplicado usado en los ejemplos 51-57 es isomalt, el edulcorante de alta intensidad es sucralosa, y el sabor es menta en forma de polvo. También aquí, se enfatiza que los componentes mencionados específicamente son, por supuesto, una descripción destinada a ayudar a un experto en la producción de la presente invención.
Tabla 11 - El número se da en porcentaje en peso del comprimido
Ejemplo 61-64
Los comprimidos del ejemplo 61-64 se fabricaron mediante un procedimiento correspondiente al del ejemplo 25 (comprimido de dos capas), pero con los materiales especificados en la tabla 12 obteniendo comprimidos con un peso de 1,8 gramos.
Como se muestra en el ejemplo 61 -64, se usaron varias cantidades y tipos de ingredientes farmacéuticos activos. Los Ejemplos 61-63 muestran paracetamol (acetaminofén) y el Ejemplo 64 usa ibuprofeno. Además, se usaron varias cantidades y tipos de edulcorante a granel en los ejemplos 61 -64. El edulcorante de alta intensidad es sucralosa, y el sabor es menta en forma de polvo.
El paracetamol y el ibuprofeno usados fueron de grado DC estándar que contienen aproximadamente 10 % de aglutinante.
Tabla 12 - El número se proporciona en porcentaje en peso del comprimido
Ej. 61-64 no cae dentro del alcance de las reivindicaciones.
Ej. 71 - Liberación In vivo de carbonato de calcio
Liberación In Vivo: Se instruyeron 6 evaluadores para masticar cada muestra con 60 masticaciones por minuto durante un tiempo de masticación total de 3 a 10 minutos.
Los evaluadores fueron instruidos para no comer o beber nada a no ser agua durante los últimos 30 minutos antes de la prueba. Antes del inicio de la prueba, los evaluadores enjuagaron sus bocas con agua.
Para cada muestra probada, los evaluadores masticaron un comprimido durante 3 minutos, otro comprimido durante 5 minutos y otro comprimido durante 10 minutos para producir residuos de comprimidos para cada instante de tiempo. Esto se repitió una vez para obtener réplicas para cada evaluador en cada instante de tiempo en la prueba
El contenido de carbonato de calcio de los residuos después de la masticación se determinó por espectroscopía de absorción atómica estándar (AAS). La liberación se calculó luego comparando el contenido de Ca del residuo después de la masticación con el contenido de Ca del comprimido no masticado.
Alternativamente, se pueden usar técnicas de titulación estándar para determinar el contenido de carbonato de calcio antes y después de la masticación.
Los resultados (promedios de resultados replicados de los evaluadores individuales) se muestran en la tabla 13. Tabla 13 - Liberación de carbonato de calcio después de 5 minutos de masticación
Como puede verse en la tabla 13, algunos comprimidos ilustrativos tienen una liberación muy alta, incluyendo ej. 25 27 y 44. Otros ejemplos de comprimidos muestran una liberación inferior, pero aún por encima del 80 % después de 5 minutos de masticación. Por ejemplo, la diferencia entre ej. 44-46 se cree que surge del uso de diferentes edulcorantes a granel, por ejemplo, que el ej. 46 usa manitol con una solubilidad en agua más baja. Además, el uso de sorbitol en un comprimido de una capa dio una liberación ligeramente más lenta, como puede verse del ej. 32, cuando se compara con el Ej. 23 usando isomaltosa como edulcorante a granel. Por otro lado, el sorbitol en la segunda capa (ej. 44) parece contribuir a una mayor velocidad de liberación. Además, la tabla 13 muestra que los comprimidos de dos capas tienden a tener una velocidad de liberación más alta en comparación con los comprimidos de una capa. Además, parece que un contenido más bajo de elastómero y resina contribuye a una mayor velocidad de liberación de ej. 36 en comparación con ej. 32. Como también se puede ver, el ejemplo 24 (comparativo) libera menos del 80 % del carbonato de calcio en 5 minutos de masticación.
El Ejemplo 37, una goma extruida comparativa, libera significativamente menos, con solo 35 % liberado después de 5 minutos de masticación.
Ej. 72 - Evaluación de la sensación calcárea, es decir, residuo de carbonato de calcio de las muestras 1044 (Ej. 44) y comprimidos sin goma masticables “Tums Chewy Bites” (comparativo), intensidad: 750 mg de carbonato de calcio
Se utilizó un panel de prueba de 8 personas entrenadas para evaluación sensorial. Las personas entrenadas fueron instruidas para no comer o beber nada que no fuese agua durante los últimos 30 minutos antes de la prueba. El panel de prueba se instruyó para masticar las muestras a una velocidad de 60 masticaciones por minuto para un tiempo de masticación total de 5 minutos.
Además de la evaluación de los atributos sensoriales estándar, tales como la suavidad y la intensidad del gusto, las personas entrenadas fueron instruidas en esta prueba para evaluar la sensación calcárea, es decir, la sensación de residuos de carbonato de calcio en la cavidad oral, al responder a la pregunta: “ ¿Hay algún residuo de carbonato de calcio que se quede en la boca, es decir, hay alguna sensación calcárea presente;?” (sí/no) en distintos instantes de tiempo durante el procedimiento de masticación.
Los resultados de esta evaluación se proporcionan en las tablas 14 y 15 a continuación.
Tabla 14 - Evaluación de la sensación calcárea
Tabla 15 - Evaluación de la sensación calcárea
Como puede verse en la tabla 14-15, el comprimido de la invención (comprimido 1044 del ej.44) no produjo sensación calcárea en la boca de ninguno de los evaluadores en ninguno de los tiempos de medición, lo que es una mejora considerable con respecto a Tums Chewy Bites, que se evalúa como inductor de sensación calcárea, especialmente
después de 1 y 2 minutos después de la administración, y para algunos evaluadores incluso después de 3 minutos después de la administración.
Ej. 81 - Liberación de paracetamol
Liberación In Vivo: se instruyeron 6 evaluadores para masticar cada muestra con 60 masticaciones por minuto para un tiempo de masticación total de 5 y 10 minutos.
Los evaluadores fueron instruidos para no comer o beber nada a no ser agua durante los últimos 30 minutos antes de la prueba. Antes del inicio de la prueba, los evaluadores enjuagaron sus bocas con agua.
Para cada muestra analizada, los evaluadores masticaron un comprimido durante 5 minutos y otro comprimido durante 10 minutos para producir residuos de comprimidos para cada instante de tiempo. Esto se repitió una vez para obtener réplicas para cada evaluador en cada instante de tiempo en la prueba.
El contenido de Paracetamol de los residuos después de la masticación se determinó mediante técnicas de HPLC estándar. La liberación se calculó luego comparando el contenido de paracetamol del residuo después de la masticación con el contenido de paracetamol del comprimido no masticado.
Los resultados (promedios de resultados replicados de los evaluadores individuales) se muestran en la tabla 16. Tabla 16 - Liberación de paracetamol después de 5 minutos de masticación
Ej. 62 no está dentro del alcance de las reivindicaciones.
Claims (16)
1. Un comprimido farmacéutico sólido para la administración oral, el comprimido comprende carbonato de calcio en una cantidad de más del 30 % en peso del comprimido y componentes insolubles en agua orgánica en una cantidad de más del 20 % en peso del comprimido, en donde el comprimido está diseñado para masticarse en un residuo coherente que contiene los componentes orgánicos insolubles en agua,
en donde el comprimido se proporciona como un comprimido multicapa que comprende una primera capa y una segunda capa,
en donde el comprimido comprende elastómero y resinas, en donde el elastómero y las resinas están contenidos en la primera capa, y en donde la segunda capa comprende al menos 70 % en peso de dicho carbonato de calcio,
en donde el comprimido está compuesto por una mezcla prensada de partículas y/o gránulos, y en donde el comprimido está adaptado para liberar más del 80 % del carbonato de calcio en 5 minutos de masticación.
2. El comprimido según la reivindicación 1, en donde el comprimido comprende carbonato de calcio en una cantidad del 30 al 60 % en peso del comprimido, tal como en una cantidad del 35 al 55 % en peso del comprimido, tal como en una cantidad del 40 al 50 % en peso del comprimido.
3. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido está adaptado para liberar más del 85 % del carbonato de calcio en 5 minutos de masticación del comprimido, tal como más del 90 % del carbonato de calcio en 5 minutos de masticación del comprimido.
4. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido está adaptado para liberar más del 60 % del carbonato de calcio en 3 minutos de masticación del comprimido.
5. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el carbonato de calcio y los componentes orgánicos insolubles en agua están contenidos en diferentes partículas y/o gránulos antes de la formación de los comprimidos.
6. Comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido comprende elastómero en una cantidad de al menos 2 % en peso del comprimido, tal como al menos 4 % en peso del comprimido.
7. Comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido comprende elastómero en una cantidad de 1 - 15 % en peso del comprimido.
8. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido comprende resina en una cantidad del 0,1 al 50 % en peso del comprimido, tal como del 2 al 40 % en peso del comprimido.
9. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido comprende resinas naturales en una cantidad del 0,1 al 30 %, tal como del 1 al 25 %, tal como del 3 al 25 % o del 5 al 25 %, en peso del comprimido.
10. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido comprende resinas sintéticas en una cantidad del 0,1 al 30 %, tal como del 1 al 25 %, tal como del 3 al 25 % o del 5 al 25 %, en peso del comprimido.
11. El comprimido según cualquiera de las reivindicaciones 1-18, en donde el comprimido se proporciona como un comprimido de dos capas o un comprimido de tres capas.
12. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido comprende una primera capa y una segunda capa, en donde el elastómero y las resinas están contenidos en la primera capa, y en donde la segunda capa comprende al menos el 80 % en peso de dicho carbonato de calcio.
13. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido tiene una dureza de al menos 70 N.
14. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el carbonato de calcio tiene un tamaño de partícula promedio de al menos 75 micrómetros, tal como al menos 150 micrómetros.
15. El comprimido según cualquiera de las reivindicaciones anteriores, en donde el comprimido tiene una friabilidad inferior al 1,0 %, tal como inferior al 0,7 %, en donde la friabilidad se mide según la Farmacopea Europea 9.1, procedimiento de ensayo 2.9.7.
16. Un comprimido farmacéutico sólido para la administración oral, el comprimido comprende carbonato de calcio en una cantidad de más del 15 % en peso del comprimido y componentes orgánicos insolubles en agua en una cantidad de más del 25 % en peso del comprimido, en donde el comprimido está diseñado para masticarse en un residuo coherente que contiene los componentes orgánicos insolubles en agua,
en donde el comprimido se proporciona como un comprimido multicapa que comprende una primera capa y una segunda capa,
en donde el comprimido comprende elastómero y resinas, en donde el elastómero y las resinas están contenidos en la primera capa, en donde la segunda capa comprende al menos 70 % en peso de dicho carbonato de calcio,
en donde el comprimido está compuesto por una mezcla prensada de partículas y/o gránulos, y en donde el comprimido está adaptado para liberar más del 80 % del carbonato de calcio en 5 minutos de masticación.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15/933,942 US10980831B2 (en) | 2018-03-23 | 2018-03-23 | Solid pharmaceutical tablet |
| PCT/DK2019/050100 WO2019179589A1 (en) | 2018-03-23 | 2019-03-21 | A solid pharmaceutical tablet |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2951267T3 true ES2951267T3 (es) | 2023-10-19 |
Family
ID=65995450
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19714544T Active ES2951267T3 (es) | 2018-03-23 | 2019-03-21 | Un comprimido farmacéutico sólido |
Country Status (10)
| Country | Link |
|---|---|
| US (3) | US10980831B2 (es) |
| EP (2) | EP3831368A1 (es) |
| JP (1) | JP7303211B2 (es) |
| CN (1) | CN111902135A (es) |
| AU (2) | AU2019239514B2 (es) |
| BR (1) | BR112020018025A2 (es) |
| CA (1) | CA3094737A1 (es) |
| ES (1) | ES2951267T3 (es) |
| PL (1) | PL3768248T3 (es) |
| WO (1) | WO2019179589A1 (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2025230986A1 (en) * | 2024-04-29 | 2025-11-06 | Anju Majeed | Aqueous dispersion of molecules-process, formulation and method thereof |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4327076A (en) * | 1980-11-17 | 1982-04-27 | Life Savers, Inc. | Compressed chewable antacid tablet and method for forming same |
| US4753805A (en) | 1984-01-31 | 1988-06-28 | Warner-Lambert Company | Tabletted chewing gum composition and method of preparation |
| ZA87994B (en) | 1986-02-27 | 1987-09-30 | Warner Lambert Co | Antacid chewing gum |
| JPH0695888B2 (ja) | 1989-10-18 | 1994-11-30 | 株式会社サンギ | カルシウム補給用チューインガム |
| US5637313A (en) | 1994-12-16 | 1997-06-10 | Watson Laboratories, Inc. | Chewable dosage forms |
| RU2226060C2 (ru) | 1999-04-15 | 2004-03-27 | Вм.Ригли Дж.Компани | Не содержащая сахара жевательная резинка для реминерализации зубной эмали (варианты) и способ реминерализации зубов |
| US7244455B2 (en) | 2002-01-16 | 2007-07-17 | Warner-Lambert Company | Center-filled chewing gum containing a deliverable form of calcium |
| EP1495680A1 (en) | 2003-07-08 | 2005-01-12 | Gum Base Co. S.p.A. | Gum base for chewing gum |
| CA2578595C (en) * | 2004-06-29 | 2013-02-19 | Fertin Pharma A/S | Tobacco alkaloid releasing chewing gum |
| ATE418328T1 (de) | 2004-07-06 | 2009-01-15 | Gumlink As | Komprimierte kaugummitablette |
| US8765178B2 (en) | 2006-07-19 | 2014-07-01 | Watson Laboratories, Inc. | Controlled release formulations and associated methods |
| AU2008220845B2 (en) | 2007-02-26 | 2013-10-03 | Revolymer Limited | Medicated chewing gum |
| WO2015070875A1 (en) | 2013-11-15 | 2015-05-21 | Fertin Pharma A/S | Chewing gum suitable for diabetics |
| JP6682450B2 (ja) | 2014-04-08 | 2020-04-15 | フェルティン ファルマ アー/エス | 医療用チューインガム |
| GB2542192A (en) * | 2015-09-11 | 2017-03-15 | Revolymer (Uk) Ltd | Chewable medicament |
| WO2017059858A1 (en) | 2015-10-07 | 2017-04-13 | Fertin Pharma A/S | Chewing gum comprising nicotine |
| ITUA20163230A1 (it) | 2016-05-06 | 2017-11-06 | Perfetti Van Melle Spa | Gomma da masticare con stevia |
| US10933017B2 (en) | 2019-03-01 | 2021-03-02 | Nordiccan A/S | Tableted cannabinoid chewing gum with polyvinyl acetate elastomer plasticizers |
-
2018
- 2018-03-23 US US15/933,942 patent/US10980831B2/en active Active
-
2019
- 2019-03-21 US US17/040,444 patent/US11730757B2/en active Active
- 2019-03-21 JP JP2020550793A patent/JP7303211B2/ja active Active
- 2019-03-21 BR BR112020018025-4A patent/BR112020018025A2/pt unknown
- 2019-03-21 PL PL19714544.4T patent/PL3768248T3/pl unknown
- 2019-03-21 CA CA3094737A patent/CA3094737A1/en active Pending
- 2019-03-21 WO PCT/DK2019/050100 patent/WO2019179589A1/en not_active Ceased
- 2019-03-21 CN CN201980021188.9A patent/CN111902135A/zh active Pending
- 2019-03-21 AU AU2019239514A patent/AU2019239514B2/en active Active
- 2019-03-21 EP EP20216277.2A patent/EP3831368A1/en active Pending
- 2019-03-21 EP EP19714544.4A patent/EP3768248B1/en active Active
- 2019-03-21 ES ES19714544T patent/ES2951267T3/es active Active
-
2021
- 2021-03-19 US US17/206,226 patent/US11723918B2/en active Active
-
2024
- 2024-05-01 AU AU2024202892A patent/AU2024202892B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3768248B1 (en) | 2023-06-14 |
| US20210205355A1 (en) | 2021-07-08 |
| EP3768248C0 (en) | 2023-06-14 |
| US11730757B2 (en) | 2023-08-22 |
| JP2021518412A (ja) | 2021-08-02 |
| US20210023128A1 (en) | 2021-01-28 |
| JP7303211B2 (ja) | 2023-07-04 |
| EP3831368A1 (en) | 2021-06-09 |
| EP3768248A1 (en) | 2021-01-27 |
| WO2019179589A1 (en) | 2019-09-26 |
| US11723918B2 (en) | 2023-08-15 |
| AU2019239514B2 (en) | 2024-02-01 |
| US20190290684A1 (en) | 2019-09-26 |
| CN111902135A (zh) | 2020-11-06 |
| BR112020018025A2 (pt) | 2020-12-22 |
| CA3094737A1 (en) | 2019-09-26 |
| US10980831B2 (en) | 2021-04-20 |
| AU2019239514A1 (en) | 2020-10-29 |
| AU2024202892A1 (en) | 2024-05-23 |
| AU2024202892B2 (en) | 2025-01-16 |
| PL3768248T3 (pl) | 2023-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN106456560B (zh) | 医用口香糖 | |
| ES2870142T3 (es) | Vehículo de administración oral | |
| RU2770035C1 (ru) | Таблетированная жевательная резинка, подходящая для активных фармацевтических ингредиентов | |
| US6949264B1 (en) | Nutraceuticals or nutritional supplements and method of making | |
| CN1324978C (zh) | 含钙的夹心口香糖 | |
| US6627234B1 (en) | Method of producing active agent coated chewing gum products | |
| ES2843581T3 (es) | Goma de mascar médica que comprende cannabinoide | |
| US6541048B2 (en) | Coated chewing gum products containing an acid blocker and process of preparing | |
| US6569472B1 (en) | Coated chewing gum products containing antacid and method of making | |
| CN112153964B (zh) | 包含非直接可压糖醇颗粒的适用于活性药物成分的经口片剂 | |
| WO2000035298A1 (en) | Chewing gum containing medicament active agents | |
| US6645535B2 (en) | Method of making coated chewing gum products containing various antacids | |
| US6579545B2 (en) | Coated chewing gum products containing an antigas agent | |
| AU2024202892B2 (en) | A solid pharmaceutical tablet | |
| CA2355779C (en) | Improved release of medicament active agents from a chewing gum coating | |
| WO2017042592A1 (en) | Chewable medicament | |
| JP2024538788A (ja) | 向上された食感を有するデキストロース錠剤 | |
| BR112019008138B1 (pt) | Comprimido de fornecimento oral que compreende agente aglutinante e eritritol separados |