ES2954325T3 - Compuestos orgánicos volátiles como biomarcadores de cáncer - Google Patents
Compuestos orgánicos volátiles como biomarcadores de cáncer Download PDFInfo
- Publication number
- ES2954325T3 ES2954325T3 ES18773823T ES18773823T ES2954325T3 ES 2954325 T3 ES2954325 T3 ES 2954325T3 ES 18773823 T ES18773823 T ES 18773823T ES 18773823 T ES18773823 T ES 18773823T ES 2954325 T3 ES2954325 T3 ES 2954325T3
- Authority
- ES
- Spain
- Prior art keywords
- concentration
- compound
- subject
- aldehyde
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/497—Physical analysis of biological material of gaseous biological material, e.g. breath
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/5758—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumours, cancers or neoplasias, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides or metabolites
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57525—Immunoassay; Biospecific binding assay; Materials therefor for cancer of the liver or pancreas
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/497—Physical analysis of biological material of gaseous biological material, e.g. breath
- G01N33/4975—Physical analysis of biological material of gaseous biological material, e.g. breath other than oxygen, carbon dioxide or alcohol, e.g. organic vapours
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/88—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86
- G01N2030/8809—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample
- G01N2030/8813—Integrated analysis systems specially adapted therefor, not covered by a single one of the groups G01N30/04 - G01N30/86 analysis specially adapted for the sample biological materials
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/52—Predicting or monitoring the response to treatment, e.g. for selection of therapy based on assay results in personalised medicine; Prognosis
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Physics & Mathematics (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- General Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Cell Biology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Gastroenterology & Hepatology (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
La invención se refiere a biomarcadores y a nuevos marcadores biológicos para diagnosticar diversas afecciones, como el cáncer. En particular, la invención se refiere al uso de estos compuestos como marcadores de diagnóstico y pronóstico en ensayos para detectar cáncer, tal como cáncer de páncreas y/o cáncer colorrectal, y métodos de detección correspondientes. La invención también se refiere a métodos para determinar la eficacia del tratamiento de estas enfermedades con un agente terapéutico y a aparatos para llevar a cabo los ensayos y métodos. Los ensayos son cualitativos y/o cuantitativos y se pueden adaptar a ensayos clínicos y de detección a gran escala. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Compuestos orgánicos volátiles como biomarcadores de cáncer
La presente invención se refiere a biomarcadores y, en particular, aunque no exclusivamente, a novedosos marcadores biológicos para diagnosticar diversas afecciones, tales como el cáncer. En particular, la invención se refiere al uso de estos compuestos como marcadores de diagnóstico y pronóstico en ensayos para detectar cáncer, tales como el cáncer de páncreas, y los correspondientes métodos de detección. La invención también se refiere a métodos para determinar la eficacia del tratamiento de estas enfermedades con un agente terapéutico y al uso de un aparato para llevar a cabo los ensayos y métodos. Los ensayos son cualitativos y/o cuantitativos, y son adaptables a ensayos clínicos y de detección a gran escala.
Se estima que el cáncer de páncreas causa más de 40,000 muertes al año en los EE. UU. y se estima que es el cuarto factor que más contribuye a las muertes por cáncer en general en 2017 [1]. Solo el 15-20% de los pacientes tienen una enfermedad potencialmente curable en el momento del diagnóstico [2,3]. Las remisiones para la investigación de la sospecha de cáncer de páncreas desde la atención primaria dependen del reconocimiento de los síntomas. Grandes estudios de bases de datos de atención primaria y encuestas de pacientes indican que los pacientes con cáncer de páncreas visitan a su médico de cabecera con frecuencia en los meses y años previos al diagnóstico [4]. Sin embargo, casi la mitad de los pacientes todavía son diagnosticados como resultado de una visita de emergencia al hospital en el Reino Unido [5]. Las pautas de referencia actuales del Instituto Nacional para la Excelencia en Salud y Atención (NICE) para evaluar el cáncer de páncreas incluyen a personas de 60 años o más con pérdida de peso y otros síntomas [6] . Los primeros síntomas son intermitentes y se superponen con otras condiciones benignas comunes. La dificultad en el reconocimiento de los síntomas se ve agravada por la falta de métodos de diagnóstico objetivos y efectivos que puedan emplearse en la práctica general. La gran mayoría de los estudios de biomarcadores se han dirigido a grupos de alto riesgo, tales como la pancreatitis hereditaria, el cáncer de páncreas familiar y las neoplasias mucinosas papilares intraductales. La traducción de biomarcadores al uso clínico hasta la fecha ha fallado por una variedad de razones, incluida la falta de incluir controles apropiados tales como la pancreatitis crónica y la falta de consideración de factores de confusión tales como la obstrucción biliar y la diabetes [7,8].
Cuando el cáncer colorrectal (CRCa) se diagnostica en su etapa más temprana, más de 9 de cada 10 personas con CRCa sobrevivirán a la enfermedad durante cinco años o más, en comparación con menos de 1 de cada 10 cuando se diagnostica en la última etapa de la enfermedad [1]. Se ha demostrado que la utilización de los síntomas intestinales como base diagnóstica primaria para el CRCa tiene un valor predictivo positivo muy bajo [2]. El riesgo de CRCa en pacientes sintomáticos puede evaluarse mediante diferentes investigaciones. La sigmoidoscopia flexible es la investigación estándar de oro, pero la gran escala de su aplicación tiene implicaciones de recursos y su rentabilidad depende de los valores predictivos de diferentes síntomas. La prueba de sangre oculta en heces con guayaco tiene una buena sensibilidad del 87-98 % en la detección de CRCa, pero una especificidad muy variable y, a menudo, insatisfactoria (13-79 %), lo que requiere la repetición de la prueba en múltiples muestras de heces. Hasta la fecha, la prueba de sangre oculta en heces no se recomienda ni está disponible para su uso como prueba intermedia [3-6]. La prueba inmunoquímica fecal requiere una sola muestra de heces. Cuatro sistemas están totalmente automatizados y proporcionan una medida cuantitativa de la hemoglobina, lo que permite la selección de un umbral de positividad para adaptarse a circunstancias específicas. Como resultado, los datos de investigación disponibles sobre sensibilidad y especificidad para CRCa se basan en un pequeño número de cánceres. Los datos sugieren que, según el umbral de positividad seleccionado, la sensibilidad para CRCa varía entre el 35 % y el 86 %, con una especificidad entre el 85 % y el 95 % [5,6]. Sin embargo, no hay datos sobre la sensibilidad de la prueba cuantitativa más nueva para los cánceres en etapa temprana. La prueba multidiana de ADN en heces, comparada con la prueba inmunoquímica fecal en un gran estudio multicéntrico, mostró una mejor especificidad (92 contra 73%), pero una menor sensibilidad (90 contra 96%) [7] .
Navantheen et al., "Volatile organic compounds in bile can diagnose malignant biliary strictures in the setting of pancreatic cancer: a preliminary observation", Gastrointestinal Endoscopy, vol. 80, no. 6, 11 de junio de 2014, páginas 1038-1045, describe un método para identificar VOC potenciales en la bilis de pacientes con estenosis biliares malignas de cáncer de páncreas. Bradley et al., "Pancreatic adenocarcinoma is associated with a unique spectrum of serum volatile organic compounds that distinguishes it from chronic pancreatitis and healthy controls", Cancer, vol.
148, no. 4, 1 de abril de 2015, página S391, divulga un método de identificación de VOC que discrimina a los pacientes con adenocarcinoma ductal pancreático de aquellos con pancreatitis crónica y controles sanos. Navaneethan et al., "Volatile Organic Compounds in Urine for Noninvasive Diagnosis of Malignant Biliary Strictures: A Pilot Study", Digestive Diseases and Sciences, vol. 60, no. 7, 24 de febrero de 2015, páginas 2150-2157, enseña un método de espectrometría de masas de tubo de flujo de iones seleccionados para analizar la concentración de VOCs en muestras de orina para diagnosticar estenosis biliares malignas. El documento WO 2017/137741 divulga un método para diagnosticar el cáncer, en el que se determinan los niveles de VOC en una muestra de orina obtenida del sujeto. Zenhausern et al., Zenhausern et al., "Solid phase micro-extraction (SPME) of volatile molecules in body fluids as a diagnostic measure for pancreatic cancer", Cancer Research, 1 de abril de 2008, analizan la metodología que utiliza microextracción en fase sólida (SPME) en combinación con cromatografía de gases y espectrometría de masas (GC/MS) para identificar compuestos orgánicos volátiles de pronóstico y diagnóstico relacionados con el cáncer de páncreas. Además, Cambridge Network "Vésae Owlstone Medical's ReCIVA Breath Sampler at London's Science
Museum", 21 de agosto de 2017, divulga un muestreador de aliento ReCIVA, que analiza biomarcadores del aliento para diagnosticar enfermedades.
Un enfoque alternativo para las pruebas basadas en heces es la prueba del aliento exhalado con el potencial de un alto cumplimiento debido a la naturaleza de la prueba y la posibilidad de probar más de una enfermedad con diferentes firmas discriminatorias de VOC [8,9]. Los investigadores que utilizan espectrometría de masas por cromatografía de gases (GC-MS) han sugerido la existencia de un perfil de compuestos orgánicos volátiles (VOC) en el aliento específico para CRCa [10]. GC-MS es una buena técnica para la identificación de VOC, sin embargo, es de naturaleza semicuantitativa y, por lo tanto, tiene una capacidad limitada para reproducir los resultados de la investigación por parte de diferentes grupos de investigación. Además, hay un tiempo analítico sustancial para cada muestra, lo que naturalmente no se presta a un análisis de alto rendimiento. La espectrometría de masas de tubo de flujo iónico seleccionado (SIFT-MS) tiene la ventaja de ser cuantitativa y permite el análisis en tiempo real [11,12].
Solo ha habido un estudio previo que evalúe el perfil respiratorio de los pacientes después de la resección quirúrgica curativa del cáncer colorrectal [13]. Ese estudio utilizó GC-MS y sugirió que después de la eliminación del CRCa hubo un cambio en el perfil de v Oc del aliento exhalado, lo que destaca además una posible asociación entre el metabolismo del tumor y la producción de VOC. Los autores también plantearon la hipótesis de que estos resultados pueden proporcionar una justificación para el uso del análisis del aliento en el seguimiento de los pacientes después de la cirugía y el control de la supervivencia libre de enfermedad [13]. Sin embargo, ese estudio no examinó pacientes con evidencia de recidiva de CRCa. Ninguno de los estudios anteriores ha validado externamente los hallazgos del descubrimiento inicial.
Lo que se requiere es un marcador no invasivo fiable para identificar a los pacientes que padecen cáncer, tales como el cáncer de páncreas y/o el cáncer colorrectal. Un método de diagnóstico para identificar a los pacientes con cáncer de páncreas y/o cáncer colorrectal sería de gran beneficio para los pacientes y aumentaría la posibilidad de un tratamiento temprano y un mejor pronóstico.
Los inventores ahora han determinado varios biomarcadores o los llamados compuestos característicos como indicativos de cáncer de páncreas y/o cáncer colorrectal.
Los inventores centraron su atención en primer lugar en el diagnóstico del cáncer de páncreas. Como se describe en el Ejemplo 1, los pacientes fueron reclutados en dos cohortes separadas, un estudio de desarrollo inicial y una segunda cohorte de validación. El grupo de cáncer incluyó pacientes con cáncer localizado y metastásico, mientras que el grupo de control incluyó pacientes con enfermedad pancreática benigna o páncreas normal. La prueba de control de comparación fue la imagen radiológica con tomografía computarizada abdominal, ecografía o ecoendoscopia confirmada con examen histopatológico, según correspondiera. El aliento de la cohorte de desarrollo se recolectó con bolsas de aluminio y de la cohorte de validación utilizando el sistema ReCIVA descrito en el Ejemplo y como se muestra en la Figura 1. El análisis se realizó usando espectrometría de masas por cromatografía de gases. Se reclutaron 68 pacientes para la cohorte de desarrollo (25 con cáncer, 43 sin cáncer) y 64 para la cohorte de validación (32 con cáncer, 32 sin cáncer). De los 66 compuestos orgánicos volátiles (VOC) característicos identificados, 13 fueron significativamente diferentes entre los grupos en el análisis univariable dentro de la cohorte de desarrollo. El análisis de las características operativas del receptor usando volátiles significativos y la cohorte de validación produjo un área bajo la curva de 0,767 (sensibilidad 81,3 %, especificidad 71,9 %) que diferencia cáncer vs. No canceroso y 0,828 (sensibilidad 77,8 %, especificidad 75 %) que diferencia adenocarcinoma y No canceroso.
La invención es tal como se define en las reivindicaciones.
En un primer aspecto de la invención, se proporciona un método para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico de la condición del sujeto, comprendiendo el método analizar la concentración de un compuesto característico en una muestra corporal de un sujeto de prueba y comparar esta concentración con una referencia para la concentración del compuesto característico en un individuo que no sufre de cáncer de páncreas, donde un aumento en la concentración del compuesto característico seleccionado de un aldehído C1 o c3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto.
En un segundo aspecto de la invención, se proporciona un método para determinar la eficacia de tratar a un sujeto que padece cáncer de páncreas con un agente terapéutico o una dieta especializada, comprendiendo el método analizar la concentración de un compuesto característico en una muestra corporal de un sujeto de prueba y comparando esta concentración con una referencia para la concentración del compuesto característico en un individuo que no sufre de cáncer de páncreas, donde una disminución en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es eficaz, o donde un aumento en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es ineficaz.
En un tercer aspecto de la invención, se proporciona el uso de un aparato para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico de la condición del sujeto, comprendiendo el aparato:
(i) medios para determinar la concentración de un compuesto característico en una muestra de un sujeto de prueba; y
(ii) una referencia para la concentración del compuesto característico en una muestra de una persona que no padece cáncer de páncreas,
en el que el aparato se utiliza para identificar: un aumento en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto.
En un cuarto aspecto de la invención, se proporciona el uso de un aparato para determinar la eficacia del tratamiento de un sujeto que padece cáncer de páncreas con un agente terapéutico o una dieta especializada, comprendiendo el aparato:
(a) medios para determinar la concentración de un compuesto característico en una muestra de un sujeto de prueba; y
(b) una referencia para la concentración del compuesto característico en una muestra de un individuo que no padece cáncer de páncreas,
en el que el aparato se utiliza para identificar:
(i) una disminución en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es eficaz; o
(ii) un aumento en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es ineficaz.
En un quinto aspecto de la invención, se proporciona el uso de un compuesto característico seleccionado del grupo que consiste en un aldehído C1 o C3 como biomarcador para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico del estado del sujeto.
Por lo tanto, en un ejemplo, se proporciona un método para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico de la condición del sujeto, comprendiendo el método analizar la concentración de un compuesto característico en una muestra corporal de un sujeto de prueba y comparar esta concentración con una referencia para la concentración del compuesto característico en un individuo que no sufre de cáncer de páncreas, donde (i) un aumento en la concentración del compuesto característico seleccionado de un aldehído C1-C3, alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, o (ii) una disminución en la concentración del compuesto característico seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto.
En un ejemplo, se proporciona un método para determinar la eficacia de tratar a un sujeto que padece cáncer de páncreas con un agente terapéutico o una dieta especializada, comprendiendo el método analizar la concentración de un compuesto característico en una muestra corporal de un sujeto de prueba y comparar esta concentración con una referencia para la concentración del compuesto característico en un individuo que no padece cáncer de páncreas, en donde (i) una disminución en la concentración del compuesto característico seleccionado de un aldehído C1-C3 , alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, o (ii ) un aumento en la concentración del compuesto característico seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es eficaz, o donde (i) un aumento en la concentración de el compuesto característico seleccionado de un aldehído C1-C3 , alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, o (ii ) una disminución en la concentración del compuesto característico seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, en la muestra corporal del sujeto
de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es ineficaz.
En un ejemplo, se proporciona un aparato para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico de la condición del sujeto, comprendiendo el aparato:
(i) medios para determinar la concentración de un compuesto característico en una muestra de un sujeto de prueba; y
(ii) una referencia para la concentración del compuesto característico en una muestra de una persona que no padece cáncer de páncreas,
en el que el aparato se utiliza para identificar: (i) un aumento en la concentración del compuesto característico seleccionado de un aldehído C1-C3 , alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -Oh , o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, o (ii) una disminución en la concentración del compuesto característico seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el sujeto sufre de cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto .
En un ejemplo, se proporciona un aparato para determinar la eficacia del tratamiento de un sujeto que padece cáncer de páncreas con un agente terapéutico o una dieta especializada, comprendiendo el aparato:
(a) medios para determinar la concentración de un compuesto característico en una muestra de un sujeto de prueba; y
(b) una referencia para la concentración del compuesto característico en una muestra de un individuo que no padece cáncer de páncreas,
en el que el aparato se utiliza para identificar:
(i) una disminución en la concentración del compuesto característico seleccionado de un aldehído C1-C3, alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, o un aumento en la concentración del compuesto característico seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es eficaz; o
(ii) un aumento en la concentración del compuesto característico seleccionado de un aldehído C1-C3, alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, o una disminución en la concentración del compuesto característico seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es ineficaz.
Los métodos de la divulgación pueden comprender administrar o haber administrado, al sujeto, un agente terapéutico o someter al sujeto a una dieta especializada, en donde el agente terapéutico o la dieta especializada previene, reduce o retrasa la progresión del cáncer de páncreas.
De acuerdo con otro ejemplo, se proporciona un método para tratar a un individuo que padece cáncer de páncreas, comprendiendo dicho método las etapas de:
(i) determinar la concentración de un compuesto característico en una muestra de la concentración de un sujeto de prueba, donde (i) un aumento en la concentración del compuesto característico seleccionado de un aldehído C1-C3, alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, o (ii) una disminución en la concentración del compuesto característico seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o tiene un pronóstico negativo; y
(ii) administrar o haber administrado, al sujeto de prueba, un agente terapéutico o someter al sujeto de prueba a una dieta especializada, en donde el agente terapéutico o la dieta especializada previene, reduce o retrasa la progresión del cáncer de páncreas.
En otro ejemplo, se proporciona el uso de un compuesto característico seleccionado del grupo que consiste en un aldehido C1-C3, alcohol C1-C3 , alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH; alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, o un análogo o derivado del mismo, tales como biomarcador para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico del estado del sujeto.
Como se describe en el Ejemplo 1, los inventores han demostrado que un aumento en la concentración de formaldehído, metanol, alcohol isopropílico o acetoína, o una disminución en la concentración de pentano, n-hexano,
1-butanol, ácido propanoico, octanal, nonanal, decanal, undecanal, tetradecano, es indicativo de cáncer de páncreas.
Los métodos, aparatos y usos descritos en este documento también pueden comprender el análisis de la concentración de un análogo o un derivado de los compuestos característicos descritos en este documento. Los ejemplos de análogos o derivados adecuados de grupos químicos que pueden analizarse incluyen alcoholes, cetonas, compuestos aromáticos, ácidos orgánicos y gases (tales como CO, CO2 , NO NO2 , H2S, SO2, CH4).
En un ejemplo en el que el compuesto característico es un aldehído C1-C3, preferiblemente el compuesto es un aldehído C1, C2 o C3, más preferiblemente un aldehído C1, es decir, formaldehído.
En un ejemplo en el que el compuesto característico es un alcohol C1-C3 , preferiblemente el compuesto es un alcohol
C1, C2 o C3 , más preferiblemente un alcohol C1 (es decir, metanol) o un alcohol C3 (es decir, alcohol isopropílico).
En un ejemplo en el que el compuesto característico es un alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, preferiblemente el compuesto es un C1, C2 , C3, C4 , C5, C6 C7 , C8, Cg o C10 donde un primer átomo de carbono está sustituido con el grupo
=O y un segundo átomo de carbono está sustituido con un grupo -OH. Preferiblemente, el átomo de carbono sustituido con el grupo =O no es un átomo de carbono terminal. Más preferiblemente, el compuesto es un alcano C3-C6, y lo más preferiblemente el compuesto es un alcano C4 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, es decir, acetoína.
En un ejemplo en el que el compuesto característico es un alcano C1-C20, preferiblemente el compuesto es un alcano
C1, C2 , C3 , C4 , C5 , C6 C7 , C8, Cg, C10, C11, C12, C13, C14, C15, C16 C17, C18, C19 o C20, más preferibl C15. Se prefiere que el compuesto sea un alcohol C5-C14. Por ejemplo, preferiblemente el compuesto es un alcohol C5 , es decir, pentano. Preferiblemente, el compuesto es un alcohol Ce, es decir, hexano. Preferiblemente, el compuesto es un alcohol C14, es decir, tetradecano.
En un ejemplo en el que el compuesto característico es un alcohol C4-C10, , preferiblemente el compuesto es un alcohol
C4 , C5 , C6 C7, C8, Cg, C10. Preferiblemente, el compuesto es un alcohol C4-C7, más preferiblemente un alcohol C4 , es decir, butanol.
En un ejemplo en el compuesto de la firma es un ácido carboxílico, preferiblemente el compuesto es un C1-C6 C1, C2,
C3 , C4 , C5, Ce ácido carboxílico. Preferiblemente, el compuesto es un ácido carboxílico C2-C4, más preferiblemente un ácido carboxílico C3, es decir, ácido propanoico.
En un ejemplo en el compuesto de la firma es un aldehído C4-C20, preferiblemente el compuesto es un aldehído C4,
C5 , C6 C7 , C8, Cg, C10, C11, C12, C13, C14, C15, C16 C17, C18, C1g o c20. Preferiblemente, el compuesto es un aldehído C5-C15, más preferiblemente un aldehído C7-C13. Preferiblemente, el compuesto es un aldehído C8, es decir, octanal.
Preferiblemente, el compuesto es un aldehído Cg, es decir nonanal. Preferiblemente, el compuesto es un aldehído C10, es decir, detanal. Preferiblemente, el compuesto es un aldehído C11, es decir, undecanal.
Así, en un ejemplo, se proporciona un método para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico de la condición del sujeto, comprendiendo el método analizar la concentración de un compuesto característico en una muestra corporal de un sujeto de prueba y comparando esta concentración con una referencia para la concentración del compuesto característico en un individuo que no padece cáncer de páncreas, donde (i) un aumento en la concentración del compuesto característico seleccionado de formaldehído, metanol, isopropilo alcohol y acetoína, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, o (ii) una disminución en la concentración del compuesto característico seleccionado de pentano, hexano, butanol, ácido propanoico, octanal, nonanal, decanal, undecanal, tetradecano, o un análogo o derivado del mismo, en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto.
Se apreciará que los ejemplos también implican la detección de los mismos compuestos característicos que en el párrafo anterior.
A continuación, los inventores centraron su atención en el diagnóstico del cáncer colorrectal. Como se describe en el Ejemplo 2, las muestras de aliento exhalado se recogieron usando bolsas de Nalophan de doble capa de 2 litros y se analizaron usando espectrometría de masas de tubo de flujo de iones seleccionados. La prueba estándar de oro para la comparación fue la endoscopia para la inspección luminal y la TC para confirmar la recidiva del cáncer. Se realizaron tres estudios: (i) estudio de perfil: 150 pacientes; 50 CRCa y 100 controles; (ii) validación de diagnóstico: 7g pacientes;
25 CRCa y 54 controles; y (iii) validación clínica con recidiva tumoral: 40 pacientes; 19 postoperatorios (sin recidiva) y 21 recidivas de CRCa. En el análisis multivariado, un solo VOC, propanal, se elevó significativamente en la cohorte de cáncer en comparación con los pacientes de control. Con un umbral de 28 ppbv, se obtuvo una sensibilidad del 96 % y una especificidad del 76 % para el diagnóstico de CRCa. El propanal se elevó de manera similar con CRCa y usando un umbral de 28 ppbv, esto dio una sensibilidad del 83,3 % y una especificidad del 84,7 %. Después de la cirugía, el propanal se redujo a los niveles esperados en los pacientes de control y, con la recidiva, los niveles aumentaron significativamente. Con un umbral de 28 ppbv, la sensibilidad para la identificación de la recidiva de CRCa fue del 71,4 % y la especificidad del 90,9 %.
Como se describe en el Ejemplo 2, los inventores han demostrado que un aumento de propanal es indicativo de cáncer colorrectal. Los métodos, aparatos y usos descritos en este documento también pueden comprender el análisis de la concentración de un análogo o un derivado de los compuestos característicos descritos en este documento. Ejemplos de análogos o derivados adecuados de grupos químicos que pueden analizarse incluyen alcoholes, cetonas, compuestos aromáticos, ácidos orgánicos y gases (tales como CO, CO2 , NO NO2 , H2S, SO2, CH4).
Una característica importante de cualquier biomarcador útil utilizado en el diagnóstico y pronóstico de enfermedades es que exhibe una alta sensibilidad y especificidad para una enfermedad determinada. Como se explica en los ejemplos, los inventores han demostrado sorprendentemente que una serie de compuestos característicos que se encuentran en el aliento exhalado de los sujetos de prueba sirven como biomarcadores sólidos para enfermedades, tales como el cáncer de páncreas y el cáncer colorrectal, y por lo tanto pueden usarse para la detección de estas enfermedades y pronóstico de enfermedades. Además, los inventores han demostrado que el uso de dichos compuestos distintivos como biomarcadores de enfermedades emplea un ensayo que es simple, reproducible, no invasivo y económico, y con molestias mínimas para el paciente.
Ventajosamente, los métodos y aparatos de la invención proporcionan un medio no invasivo para diagnosticar varios tipos de cáncer. Los métodos de acuerdo con esta descripción son útiles para permitir que un médico tome decisiones con respecto al mejor curso de tratamiento para un sujeto que actualmente sufre o puede sufrir cáncer de páncreas o cáncer colorrectal, respectivamente. Se prefiere que los métodos de esta descripción sean útiles para permitir que un médico decida cómo tratar a un sujeto que actualmente padece cáncer. Además, los métodos de esta divulgación son útiles para monitorizar la eficacia de un tratamiento putativo para el cáncer relevante. Por ejemplo, si el cáncer es cáncer de páncreas, entonces el tratamiento puede comprender la administración de quimioterapia, quimiorradioterapia con o sin cirugía. Por ejemplo, si el cáncer es cáncer colorrectal, entonces el tratamiento puede comprender la administración de quimioterapia, quimiorradioterapia con o sin cirugía o resección endoscópica.
Por tanto, el aparato según esta divulgación es útil para proporcionar un pronóstico del estado del sujeto, de modo que el médico pueda llevar a cabo el tratamiento según esta divulgación. El aparato de esta descripción se puede usar para monitorizar la eficacia de un tratamiento putativo para el cáncer. Por lo tanto, los métodos y aparatos son muy útiles para guiar un régimen de tratamiento para el médico y para controlar la eficacia de tal régimen de tratamiento. El médico puede usar el aparato de la invención junto con las pruebas de diagnóstico existentes para mejorar la precisión del diagnóstico.
El sujeto puede ser cualquier animal de interés veterinario, por ejemplo, un gato, un perro, un caballo, etc. Sin embargo, se prefiere que el sujeto sea un mamífero, tal como un humano, ya sea macho o hembra.
Preferiblemente, se toma una muestra del sujeto y luego se mide la concentración del compuesto característico en la muestra corporal.
Los compuestos característicos, que se detectan, se conocen como compuestos orgánicos volátiles (VOCs), que conducen a un perfil de fermentación, y pueden detectarse en la muestra corporal mediante una variedad de técnicas. En una realización, estos compuestos pueden detectarse dentro de una muestra líquida o semisólida en la que se disuelven. Sin embargo, en una realización preferida, los compuestos se detectan a partir de gases o vapores. Por ejemplo, dado que los compuestos distintivos son VOC, pueden emanar de la muestra o formar parte de ella y, por lo tanto, pueden detectarse en forma gaseosa o de vapor.
El aparato de esta divulgación puede comprender medios de extracción de muestras para obtener la muestra del sujeto de prueba. Los medios de extracción de muestras pueden comprender una aguja o jeringa o similar. El aparato puede comprender un recipiente de recolección de muestras para recibir la muestra extraída, que puede ser líquida, gaseosa o semisólida.
Preferiblemente, la muestra es cualquier muestra corporal en la que está presente o secretado el compuesto característico. Por ejemplo, la muestra puede comprender orina, heces, cabello, sudor, saliva, sangre o lágrimas. Los inventores creen que los VOC son productos de descomposición de otros compuestos que se encuentran en la sangre. En una realización, las muestras de sangre pueden analizarse inmediatamente para determinar los niveles del compuesto característico. Alternativamente, la sangre se puede almacenar a bajas temperaturas, por ejemplo, en un frigorífico o incluso congelada antes de que se determine la concentración del compuesto característico. La medición del compuesto característico en la muestra corporal se puede realizar en sangre entera o sangre procesada.
En otra realización, la muestra puede ser una muestra de orina. Se prefiere que la concentración del compuesto característico en la muestra corporal se mida in vitro de una muestra de orina tomada del sujeto. El compuesto puede detectarse a partir de gases o vapores que emanan de la muestra de orina. Se apreciará que se prefiere la detección del compuesto en la fase gaseosa emitida por la orina.
También se apreciará que las muestras corporales "frescas" pueden analizarse inmediatamente después de haberlas tomado de un sujeto. Alternativamente, las muestras pueden congelarse y almacenarse. La muestra puede entonces descongelarse y analizarse en una fecha posterior.
Sin embargo, lo más preferiblemente, la muestra corporal puede ser una muestra de aliento del sujeto de prueba. La muestra puede ser recogida por el sujeto realizando una exhalación por la boca, preferiblemente después de una inhalación nasal. Preferiblemente, la muestra comprende el aire alveolar del sujeto. Preferiblemente, el aire alveolar es recolectado sobre el aire del espacio muerto capturando el aliento al final de la espiración. A continuación, los VOC de las bolsas de aliento se preconcentraron preferentemente en tubos de desorción térmica transfiriendo el aliento a través de los tubos.
La diferencia en la concentración del compuesto característico en los métodos o el aparato de esta divulgación puede ser un aumento o una disminución en comparación con la referencia. Como se describe en los ejemplos, los inventores controlaron la concentración de los compuestos característicos en numerosos pacientes que padecían cáncer de páncreas o colorrectal, y los compararon con la concentración de estos mismos compuestos en individuos que no padecían la enfermedad (es decir, referencia o controles). Demostraron que hubo un aumento o disminución estadísticamente significativa en la concentración de estos compuestos en los pacientes que padecían la enfermedad.
Se apreciará que la concentración del compuesto característico en pacientes que padecen una enfermedad depende en gran medida de una serie de factores, por ejemplo, hasta qué punto ha progresado la enfermedad y la edad y el género del sujeto. También se apreciará que la concentración de referencia del compuesto característico en individuos que no padecen la enfermedad puede fluctuar hasta cierto punto, pero que en promedio durante un período de tiempo dado, la concentración tiende a ser sustancialmente constante. Además, debe apreciarse que la concentración del compuesto característico en un grupo de individuos que padecen una enfermedad puede ser diferente a la concentración de ese compuesto en otro grupo de individuos que no padecen la enfermedad. Sin embargo, es posible determinar la concentración promedio del compuesto característico en individuos que no padecen cáncer, y esto se denomina concentración de referencia o "normal" del compuesto característico. La concentración normal corresponde a los valores de referencia discutidos anteriormente.
En una realización, los métodos de la invención preferiblemente comprenden determinar la proporción de sustancias químicas dentro de la respiración (es decir, usar otros componentes dentro de ella como referencia) y luego comparar estos marcadores con la enfermedad para mostrar si están elevados o reducidos.
El compuesto característico es preferiblemente un compuesto orgánico volátil (VOC), que conduce a un perfil de fermentación, y puede detectarse en o a partir de la muestra corporal mediante una variedad de técnicas. Por lo tanto, estos compuestos pueden detectarse utilizando un analizador de gases. Ejemplos de detectores adecuados para detectar el compuesto característico incluyen preferiblemente un sensor electroquímico, un sensor de óxido de metal semiconductor, un sensor de microbalanza de cristal de cuarzo, un sensor de colorante óptico, un sensor de fluorescencia, un sensor de polímero conductor, un sensor de polímero compuesto o espectrometría óptica.
Los inventores han demostrado que los compuestos característicos se pueden detectar de forma fiable mediante cromatografía de gases, espectrometría de masas, GCMS o TOF. Se podrían usar sensores dedicados para la etapa de detección.
Los valores de referencia pueden obtenerse analizando un número estadísticamente significativo de muestras de control (es decir, muestras de sujetos que no padecen la enfermedad). En consecuencia, la referencia (ii) según el aparato de esta divulgación puede ser una muestra de control (para ensayo).
El aparato preferiblemente comprende un control positivo (lo más preferiblemente proporcionado en un recipiente), que corresponde a los compuestos característicos. El aparato comprende preferiblemente un control negativo (preferiblemente proporcionado en un recipiente). En una realización preferida, el aparato puede comprender la referencia, un control positivo y un control negativo. El aparato también puede comprender controles adicionales, según sea necesario, tales como controles de "adición" para proporcionar una referencia para la concentración y controles positivos adicionales para cada uno de los compuestos característicos, o un análogo o derivado del mismo.
En consecuencia, los inventores se han dado cuenta de que la diferencia en las concentraciones del compuesto característico entre la referencia normal (es decir, el control) y los niveles aumentados/disminuidos puede usarse como un marcador fisiológico, que sugiere la presencia de una enfermedad en el sujeto de prueba. Se apreciará que si un sujeto tiene una concentración aumentada/disminuida de uno o más compuestos característicos que es considerablemente mayor/menor que la concentración "normal" de ese compuesto en el valor de control de referencia, entonces tendría un mayor riesgo de tener la enfermedad, o una condición más avanzada, que si la concentración de ese compuesto fuera solo marginalmente más alta/más baja que la concentración 'normal'.
Los inventores han notado que la concentración de compuestos característicos a los que se hace referencia aquí en los individuos de prueba fue estadísticamente mayor que la concentración de referencia (tal como se calculó utilizando el método descrito en el Ejemplo). Esto puede denominarse en el presente documento como la concentración "aumentada" del compuesto característico.
El técnico experto apreciará cómo medir las concentraciones del compuesto característico en un número estadísticamente significativo de individuos de control, y la concentración del compuesto en el sujeto de prueba, y luego usará estas cifras respectivas para determinar si el sujeto de prueba tiene un aumento/disminución estadísticamente significativos de la concentración del compuesto, y por tanto inferir si ese sujeto padece la enfermedad que se ha cribado.
En el método y el aparato de esta divulgación, la diferencia en la concentración del compuesto característico en la muestra corporal en comparación con la concentración correspondiente en la referencia es indicativa de la eficacia del tratamiento de la enfermedad del sujeto con el agente terapéutico y la resección quirúrgica. La diferencia puede ser un aumento o una disminución en la concentración del compuesto característico en la muestra corporal en comparación con el valor de referencia. En los ejemplos en los que la concentración del compuesto en la muestra corporal es menor que la concentración correspondiente en la referencia, esto indicaría que el agente terapéutico o la dieta especializada está tratando con éxito el trastorno en el sujeto de prueba. Por el contrario, cuando la concentración del compuesto característico en la muestra corporal es mayor que la concentración correspondiente en la referencia, esto indicaría que el agente terapéutico o la dieta del especialista no están tratando con éxito el trastorno.
Todas las características descritas en este documento (incluidas las reivindicaciones, el resumen y los dibujos adjuntos), y/o todas las etapas de cualquier método o proceso así divulgado, pueden combinarse con cualquiera de los aspectos anteriores en cualquier combinación, excepto combinaciones en las que al menos algunas de tales características y/o etapas son mutuamente excluyentes.
Para una mejor comprensión de la invención, y para mostrar cómo se pueden llevar a cabo las realizaciones de la misma, ahora se hará referencia, a modo de ejemplo, a las figuras adjuntas, en las que:
la Figura 1 muestra un aparato y un método utilizado para concentrar VOC de bolsas de aliento de acero en tubos de desorción térmica;
la Figura 2 muestra gráficos ROC de sensibilidad frente a 1-especificidad producidos para A) Cáncer vs. no cancerosos y B) Todos los adenocarcinomas vs. no cancerosos utilizando datos de la cohorte de desarrollo (Bolsas). Las siguientes tablas resumen los datos del análisis ROC, incluido el área bajo la curva (AUC);
la Figura 3 muestra gráficos ROC de sensibilidad frente a 1-especificidad producidos para A) Cáncer vs. no cancerosos y B) Todos los adenocarcinomas vs. no cancerosos utilizando datos de la cohorte de validación (ReCIVA). Las siguientes tablas resumen los datos del análisis ROC, incluido el área bajo la curva (AUC);
la Figura 4 muestra los resultados del Estudio (i) - validación de diagnóstico de perfiles; Análisis ROC para propanal como marcador diagnóstico de cáncer colorrectal en comparación con pacientes de control negativo (AUC = 0,90 ± 0,03, CI del 95 % 0,83-0,96);
la Figura 5 muestra los resultados del Estudio (ii) - validación de diagnóstico independiente; Análisis ROC del estudio de validación independiente de propanal para el diagnóstico de cáncer colorrectal (AUC = 0,79 ± 0,06, CI del 95 %: 0,66-0,91);
la Figura 6 muestra los resultados del Estudio (iii) - validación clínica con recidiva del tumor; regulación positiva de propanal asociada con la presencia de recidiva de CRCa después de la resección quirúrgica primaria de CRCa (AUC = 0,81 ± 0,07, CI del 95%: 0,68-0,94); y
la Figura 7 muestra los cambios observados en la concentración promedio de propanal en los tres estudios y cuatro estados de enfermedad estudiados.
Ejemplos
Los inventores investigaron el uso de VOC para detectar una variedad de tipos de cáncer diferentes, incluido el cáncer de páncreas y colorrectal.
Ejemplo 1: cáncer de páncreas
El cáncer de páncreas tiene un pronóstico muy malo ya que la mayoría de los pacientes son diagnosticados en una etapa avanzada cuando los tratamientos curativos no son posibles. Los compuestos orgánicos volátiles del aliento han mostrado potencial como novedosos biomarcadores para detectar otros tipos de cáncer. Este estudio identificó y validó un perfil único de compuestos orgánicos volátiles en el aliento asociado con la presencia de cáncer de páncreas, lo que sugiere el potencial del análisis del aliento para su inclusión en la ruta de diagnóstico del cáncer de páncreas.
El objetivo principal de este estudio fue perfilar los cambios observados en los VOC del aliento exhalado utilizando espectrometría de masas con cromatografía de gases por desorción térmica (TD-GC-MS) para pacientes con cáncer de páncreas primario, enfermedad de control positivo y páncreas normal. El objetivo secundario fue desarrollar modelos de diagnóstico para la identificación de neoplasias pancreáticas y específicamente adenocarcinoma, con una mayor validación en una segunda cohorte de pacientes recolectada de forma independiente. El tercer objetivo fue cuantificar las diferencias en compuestos orgánicos volátiles en el aliento exhalado de pacientes con cáncer de páncreas en comparación con cohortes sin cáncer y generar modelos de diagnóstico de cáncer.
Materiales y métodos
Se realizaron dos estudios. En el primer estudio de creación de perfiles, se recolectó y analizó el aliento exhalado para identificar los VOC que diferían en la concentración entre los pacientes con cáncer y los de control. Esos compuestos se usaron para desarrollar el modelo de diagnóstico para el cáncer de páncreas. Luego, este modelo se validó utilizando una segunda cohorte de pacientes recolectada de forma independiente.
Población de estudio
Todos los pacientes inscritos fueron reclutados del fideicomiso Imperial College NHS desde marzo de 2016 hasta diciembre de 2016. Se concedió la aprobación ética regional para (REC ref: 14/LO/1136). Los detalles del estudio se explicaron a todos los pacientes elegibles y se obtuvo un consentimiento informado y por escrito antes de la inscripción. Se recopiló información demográfica y clínica.
Tanto en los estudios de perfilado como de validación, los pacientes con cáncer de páncreas se compararon con grupos de control que incluyen enfermedades pancreáticas benignas. Para el grupo de cáncer de páncreas, se tomaron muestras de pacientes con cáncer de páncreas localizado antes de la operación en salas quirúrgicas o de la unidad de endoscopia antes de someterse a una ecografía endoscópica. Los pacientes con enfermedad pancreática metastásica fueron reclutados de clínicas de oncología. Para el grupo de control, se reclutaron pacientes con diagnóstico de otras afecciones pancreáticas, entre ellas; neoplasia mucinosa papilar intraductal (IPMN), quistes, pseudoquistes y pancreatitis crónica. Los pacientes programados para una ecografía abdominal superior (US) electiva con un páncreas de apariencia normal en las imágenes fueron reclutados para este grupo.
Prueba de referencia
Todos los casos fueron confirmados con una prueba de referencia estándar. El cáncer de páncreas se confirmó mediante tomografía computarizada (TC) abdominal o ultrasonido endoscópico e histológicamente mediante biopsia por aspiración con aguja fina. La TC o la ecografía abdominal examinaron el páncreas de los pacientes del grupo de control.
Recolección de aire exhalado
La recolección de aire exhalado se realizó usando una metodología previamente validada [11] que fue informada por las investigaciones de los inventores sobre la influencia de las maniobras de respiración y el ambiente hospitalario en las mediciones de VOC [17,18]. Todos los pacientes estuvieron en ayunas durante un mínimo de 4 horas antes de la muestra de aliento para minimizar el riesgo de contaminación oral o la ingesta dietética actuando como un factor de confusión. También se analizó el aire atmosférico de las salas de recolección de muestras y el laboratorio para investigar los efectos de los VOC de fondo en las muestras de aliento recolectadas. El método de muestreo de aliento se cambió de bolsas de aluminio inertes (Bedfont Scientific Ltd., Maidstone, Reino Unido) en el estudio de perfilado inicial al sistema de muestreo de aliento ReCIVA (Owlstone Medical Inc., Cambridge, Reino Unido) en el estudio de validación.
Haciendo referencia a la Figura 1, se muestra un aparato ReCIVA utilizado para el muestreo del aliento de acuerdo con la invención. El aparato ReCIVA es un sistema reproducible que permite recoger directamente el aliento en los tubos de desorción térmica, que es el sistema que se utilizará en futuros estudios multicéntricos.
El aliento se recolectó utilizando bolsas de aluminio inerte de 500 ml que se lavaron con aire sintético antes del muestreo. Se pidió a los pacientes que realizaran una inhalación nasal profunda seguida de una exhalación completa por la boca. El aire alveolar se recolectó preferentemente sobre el aire del espacio muerto al capturar el aliento al final de la espiración. Los VOC de las bolsas de aliento se preconcentraron (véase la Figura 1) en tubos de desorción térmica transfiriendo 250 ml de aliento a 50 ml/s a través de los tubos con tubos de 10 mm de diámetro y bombas de aire manuales (210-1002MTX, SKC ltd., Dorset , REINO UNIDO).
Para el sistema ReCIVA, el muestreo de aliento sigue siendo completamente no invasivo e implica colocar una máscara facial desechable alrededor de la nariz y la boca del paciente e instruirlo para que realice una respiración corriente normal. El sistema Capser (Owlstone Medical Inc., Cambridge, Reino Unido) ventila un suministro constante de aire a la máscara del paciente, lo que garantiza que el paciente solo inspire aire limpio. El aparato ReCIVA utiliza un monitor de CO2 interno y sensores de presión para capturar preferentemente el aliento alveolar y transferirlo directamente a los tubos de desorción térmica. De manera similar a la recolección de bolsas, se transfirió un total de 250 ml de aliento alveolar a los tubos de desorción térmica.
Análisis espectrométrico de masas
Todas las muestras de aire se analizaron dentro de las 48 horas posteriores a la recolección. Los datos de los estudios de degradación han demostrado que los volátiles permanecen estables dentro de las bolsas de aliento durante 48 horas [19]. TD-GC-MS es un método analítico utilizado para la identificación y cuantificación de compuestos volátiles y semivolátiles. Los VOC que ingresan al dispositivo viajan a través de la columna de cromatografía (GC 7890B, Agilent Technologies, Cheadale, Reino Unido), se separan según su afinidad con la fase estacionaria y abandonan la columna en un tiempo de retención específico. Luego, los VOC ingresan a un espectrómetro de masas (5977A MSD, Agilent Technologies, Reino Unido), donde se ionizan, aceleran, desvían y detectan con base en sus relaciones masa/carga (m/z). La combinación de cromatografía de gases y espectrometría de masas permite una mejor identificación de compuestos que el uso de cualquiera de los componentes individualmente.
Se usaron tubos de desorción térmica para concentrar los volátiles antes del análisis GC-MS fijándolos al sorbente Tenax que recubre el interior del tubo. Todos los tubos Tenax TA (Markes International, Reino Unido) se acondicionaron (TC-20, Markes International, Reino Unido) a 300°C durante 1 hora y 10 minutos. Los tubos se cargaron en carruseles, se comprobaron si había fugas en los tubos y luego se secaron durante 3 minutos para eliminar el exceso de humedad y asegurar que los VOC no se oxidaran al calentarse. A continuación, los tubos se sometieron a desorción (TD-100, Markes International, Reino Unido) a 280 °C en una trampa fría a 10 °C durante 10 minutos (flujo de nitrógeno 50 ml/min). Luego, la trampa fría se calentó rápidamente a 290 °C y se transfirieron los VOC a la columna de cromatografía. En un intento por minimizar los VOC de fondo fijados en los tubos, el tiempo desde el acondicionamiento de los tubos hasta la preconcentración nunca excedió una hora.
Metodología GC-MS
La temperatura inicial del horno se mantuvo a 40 °C durante 4 min, luego aumentó de 5 °C/min a 100 °C con una retención de 1 minuto, aumentó de 5 °C/min a 110 °C con una retención de 1 minuto, aumentó 5 °C/min a 200 °C, y finalmente aumentó 10 °C/min a 240 °C con una retención de 4 minutos. El tiempo total de análisis de GC fue de 47 minutos. El espectrómetro de masas se hizo funcionar con el modo de ionización por impacto de electrones, barriendo iones de masa 20-250 m/z a 5,9 barridos/seg. La temperatura del cuadrupolo y de la fuente de los espectrómetros de masas fue de 230°C y 150°C respectivamente. Se usó un retraso de solvente de 3 minutos al comienzo de la ejecución para minimizar la interferencia del agua.
Extracción de datos
Los cromatogramas y los datos de espectros de masas se extrajeron en un software de análisis cualitativo (Agilent Masshunter Qualitative Analysis, Reino Unido). La identidad química de cada pico, con tiempos de retención entre 3 47 minutos, se confirmó luego con la base de datos del NIST El tiempo de retención y el ion m/z característico de los VOC identificados se utilizaron para cuantificar su abundancia (Agilent Masshunter Quantitative Analysis, Reino Unido) en todos los cromatogramas. En la cuantificación se utilizó un rango de tiempo de retención de ±0,1 minutos, lo que garantiza que solo se cuantificaron los iones característicos de un rango de 0,2 minutos.
Análisis estadístico
Todos los análisis estadísticos se realizaron utilizando IBM SPSS 24 (IBM corp., Armonk, NY). Los valores de p inferiores a 0,05 se consideraron significativos y todas las pruebas estadísticas fueron bilaterales. El estado de la enfermedad del cáncer y los factores de confusión se consideraron variables independientes y la abundancia de VOC se consideró la variable dependiente. Se realizó una prueba estadística de Shapiro-Wilk.
Las diferencias significativas en la abundancia de volátiles entre los grupos con cáncer y sin cáncer en la cohorte de desarrollo se evaluaron mediante pruebas estadísticas univariadas de Mann-Whitney U (ya que los datos no tenían una distribución normal). Los VOC que se encontraron significativos en el análisis univariante se incluyeron en el análisis de regresión logística para formar la base de un modelo de diagnóstico para uso en la cohorte de validación. Los gráficos de Características Operativas del Receptor (ROC) se produjeron representando la tasa de verdaderos positivos (sensibilidad) frente a la tasa de falsos positivos (1-especificidad). Se produjeron dos gráficos ROC para comparaciones de cáncer frente a No canceroso y adenocarcinoma frente a No canceroso. El área bajo la curva (AUC) se utilizó para evaluar el poder de predicción del modelo y su capacidad para distinguir entre cáncer y No canceroso. Los valores de sensibilidad y especificidad se extrajeron de las coordenadas de los gráficos ROC. El grupo con cáncer incluyó todos los subgrupos de cáncer de páncreas, mientras que el grupo sin cáncer incluyó tanto grupos de control positivo como de páncreas normal. El grupo de adenocarcinoma consistía en subgrupos de adenocarcinoma tanto localizado como metastásico.
También se realizó un análisis estadístico para identificar diferencias significativas entre los grupos en edad, etnia, sexo, enfermedad por reflujo gastroesofágico (GERD), pancreatitis, enfermedad hepática, hepatitis, diabetes mellitus, tabaquismo e ingesta de alcohol. Se empleó Kruskal-Wallis para los datos de edad continuos, mientras que todos los demás datos de posibles factores de confusión nominales se evaluaron mediante la prueba exacta de Chicuadrado/Fisher/relación de verosimilitud dependiendo de los números de recuento esperados y el número de variables probadas. Todos los factores de confusión se probaron posteriormente frente a la abundancia de VOC con regresión lineal.
Resultados
Pacientes
Un total de 68 pacientes (véase Tabla 1) fueron reclutados para la cohorte de desarrollo del modelo. Los pacientes fueron asignados a grupos con cáncer (n=25) y sin cáncer (n=43), incluidos adenocarcinoma localizado (n=7), tumor neuroendocrino (NET) localizado (n=4), adenocarcinoma metastásico (n=10), NET metastásico (n=4), control positivo (n=20) y páncreas normal (n=23).
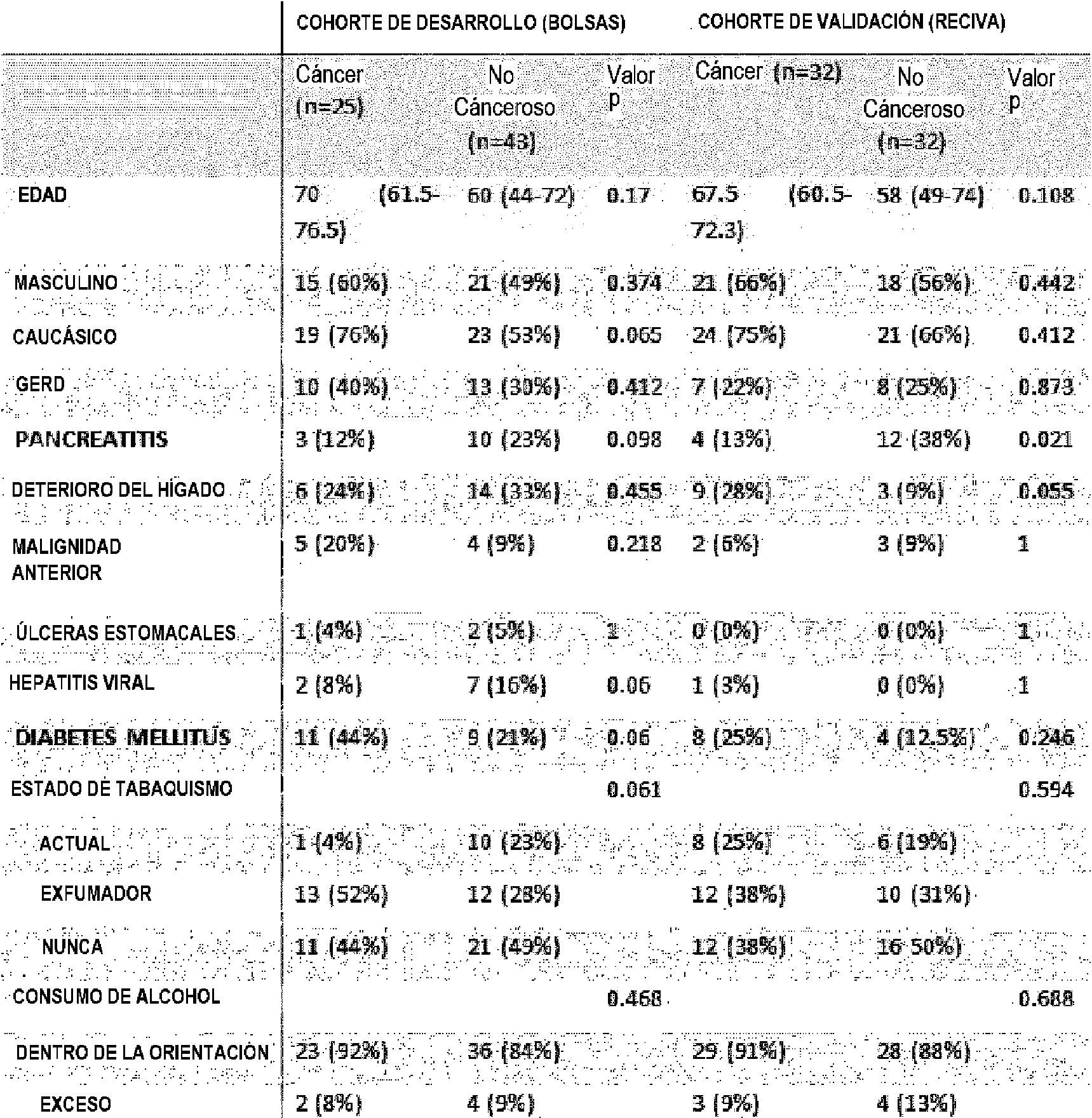
Tabla 1 - Características demográficas y de los pacientes de ambas cohortes. Se muestran datos de mediana y rango intercuartil para la edad. Todos los demás datos se presentan como valores de n y porcentajes entre paréntesis. Krustal Sallis se utilizó para la edad. Para todos los demás factores se utilizaron pruebas de Chi-cuadrado/prueba exacta de Fisher/relaciones de verosimilitud.
Otros 64 pacientes fueron reclutados para la cohorte de validación. Los pacientes se dividieron nuevamente en grupos con cáncer (n = 32) y sin cáncer (n = 32), e incluyeron adenocarcinoma local (n = 14), NET local (2), adenocarcinoma metastásico (14), n Et metastásico (3), control positivo (24) y páncreas normal (8). No hubo diferencias significativas en la demografía de los pacientes ni en las comorbilidades entre los grupos de cáncer y de control (véase la Tabla 1). Análisis de VOC
El análisis cualitativo de los cromatogramas produjo 66 VOC que fueron identificables en la base de datos del NIST. Veintidós de estos VOC se excluyeron de un análisis posterior porque se encontró que se encontraban en altas concentraciones en el aire de fondo o se consideró poco probable que se produjeran endógenamente. La identidad de los 44 VOC restantes, así como sus tiempos de retención y la relación m/z característica, se utilizaron posteriormente para cuantificar la abundancia de VOC.
Las pruebas de Shapiro-Wilk revelaron que los datos de abundancia de todos los VOC no se distribuyeron normalmente. Las pruebas U de Mann Whitney univariadas revelaron 9 VOC (Tabla 2) con abundancias significativamente alteradas en el cáncer dentro de la cohorte de desarrollo (formaldehído, metanol, pentano, alcohol isopropílico, n-hexano, acetoína, octanal, undecanal, tetradecano).
Tabla 2 - Tabla de 11 VOC significativos. Las flechas indican la dirección del cambio para la cohorte de cáncer. Las flechas se omiten para los VOC no significativos. Valores de P producidos a partir de las pruebas U de Mann Whitney para cáncer frente a No canceroso y adenocarcinoma frente a No canceroso
Un análisis adicional también reveló 11 VOC (Tabla 2) con abundancias significativamente alteradas en una comparación de adenocarcinoma versus no cancerosa (formaldehído, metanol, pentano, alcohol isopropílico, nhexano, 1-butanol, acetoína, ácido propanoico, octanal, nonanal, decanal).
De estos VOC significativos, se encontró que la abundancia de 4 aumentó en el cáncer (formaldehído, metanol, alcohol isopropílico, acetoína), y se encontró que los 9 restantes se redujeron en el aliento del cáncer (pentano, n-hexano, 1-butanol, ácido propanoico, octanal, nonanal, decanal, undecanal, tetradecano) (Tabla 2). Se encontró que esta dirección de cambio era la misma para todos los VOC significativos en los datos de las cohortes de desarrollo y validación.
El análisis de regresión lineal (Tabla 3) reveló que el estado de la enfermedad del cáncer de páncreas era el predictor más fuerte para todas las abundancias significativas de VOC. No se encontró que los factores de confusión fueran predictores independientes de la abundancia de ninguno de los VOC significativos.
Análisis de la Característica del Operador del Receptor (ROC)
Se construyeron gráficos ROC (véanse las Figuras 2 y 3) para ambas cohortes utilizando solo los VOC que se encontraron significativamente alterados en el aliento de los pacientes con cáncer en la cohorte de desarrollo.
Para el estudio de desarrollo del modelo, los gráficos ROC produjeron un AUC de 0,892 (CI del 95 %, 0,806-0,978) para distinguir entre cáncer y No canceroso, sensibilidad del 84 % y especificidad del 88,4 %. El AUC producido a partir del ROC de adenocarcinoma frente a no canceroso fue de 0,943 (CI del 95 %, 0,886-0,999) con una sensibilidad del 88,2 % y una especificidad del 90,7 %. Para el estudio de validación del modelo, el AUC para distinguir entre cáncer y No canceroso fue de 0,768 (CI del 95 %, 0,65-0,885), lo que produce una sensibilidad del 78,8 % y una especificidad del 75,0 %. El AUC para distinguir entre adenocarcinoma y no canceroso fue de 0,851 (CI del 95 %, 0,753-0,948) con una sensibilidad del 85,2 % y una especificidad del 70,0 %.
Discusión
La cuantificación espectrométrica de masas por cromatografía de gases de VOC en el aire exhalado ha identificado un total de 13 compuestos que se alteraron significativamente con la presencia de cáncer de páncreas. Los VOC significativos procedían de tres grupos químicos principales, a saber, aldehídos, ácidos grasos y alcoholes. Todos los modelos ROC mostraron una buena discriminación con AUC superiores a 0,7. La discriminación también fue más fuerte en los modelos que distinguen el adenocarcinoma del No canceroso. Estos resultados sientan las bases para un estudio multicéntrico más grande que podría establecer aún más el potencial de las pruebas de VOC en el aliento como herramienta de diagnóstico para el cáncer de páncreas.
El grupo químico con el mayor número de VOC del aliento significativamente desregulados en el cáncer de páncreas fue el grupo aldehído. Actualmente, el antígeno carbohidrato 19-9 (CA19-9) es el marcador tumoral más utilizado para el cáncer de páncreas. Sin embargo, a menudo es inespecífico y está elevado en una serie de afecciones tanto benignas como malignas, incluyendo pancreatitis, cirrosis, colangitis aguda y cáncer colorrectal [3]. Tampoco se expresa en el 5-10% de la población caucásica debido a un genotipo Lewis a-/b [24]. En general, solo el 65 % de los pacientes con cáncer de páncreas resecable quirúrgicamente tendrán una CA elevada-^ [3]. Teniendo en cuenta la fase de descubrimiento y validación temprana de este estudio, no es recomendable hacer comparaciones firmes entre las pruebas de VOC del aliento y CA19-9.
La fuerza del estudio radica en su novedad y diseño. El estudio proporciona el potencial para una prueba de aliento no invasiva para diagnosticar el cáncer de páncreas, una enfermedad de necesidad insatisfecha que se presenta en una etapa tardía con poca supervivencia a largo plazo. Las ventajas del diseño del estudio incluyen la inclusión de un grupo de control positivo, una prueba de referencia para cada paciente y una cohorte independiente de pacientes para validar biomarcadores volátiles empleando un método de recolección de aliento diferente. El método adoptado en el estudio de validación se presta a investigaciones clínicas multicéntricas, ya que ReCIVA proporciona un método de recolección de aliento reproducible, mientras que los tubos de desorción térmica ofrecen un sistema de transporte sólido que mantiene estables los compuestos volátiles durante aproximadamente 4 semanas.
El rendimiento de la prueba debe examinarse en el cáncer de páncreas temprano como objetivo final de la prueba del aliento que podría cambiar el patrón del estadio del cáncer en la presentación e influir en la supervivencia de la enfermedad. El estudio actual incluyó pacientes con enfermedad metastásica y localmente avanzada, ya que este grupo representa la mayoría de los pacientes con cáncer de páncreas en la práctica clínica y no debe pasarse por alto en el modelo de diagnóstico.
El muestreo de VOC del aliento es una prueba completamente no invasiva con una aceptabilidad muy alta por parte de pacientes y médicos, como se observa en el estudio actual y en otros realizados por nuestro equipo [11,17,18,19]. Los inventores contemplan el uso de pruebas de aliento exhalado como una investigación de clasificación para establecer el riesgo de cáncer de páncreas en pacientes que presentan síntomas no específicos para guiar la derivación a imágenes de TC. Otro lugar de prueba es la detección de grupos de alto riesgo, tales como la pancreatitis hereditaria, el cáncer de páncreas familiar, la diabetes de aparición reciente y las neoplasias mucinosas papilares intraductales. La ubicación final de la prueba del aliento en la vía de atención al paciente dependerá de la sensibilidad y la especificidad de la prueba en grandes ensayos clínicos multicéntricos y de su rendimiento en el estadio temprano del cáncer de páncreas y en los grupos de alto riesgo.
Conclusiones
Los volátiles del aliento tienen el claro potencial de distinguir el cáncer de páncreas de los pacientes sin cáncer.
Referencias
1. Siegel LR, Miller DK, Jemal A. Cancer Statistics 2017. CA Cancer J Clin 2017; 67: 7-30.
2. Li D, Xie K, Wolff R, et al. Pancreatic cancer. Lancet 2004; 363: 1049-57.
3. Goggins M. Molecular markers of early pancreatic cáncer. J Clin Oncol 2005; 23: 4524 - 31.
4. Stapley S, Peters TJ, Neal RD, et al. The risk of pancreatic cancer in symptomatic patients in primary care: a large case-control study using electronic records. Br J Cancer 2012; 106: 1940 -4.
5. PCUK. Study for survival. Secondary study for survival 2011. http://www.pancreaticcancer.org.uk/media/100292/report.final
6. http://www.nice.org.uk/guidance/ng12/chapter/1-Recommendations-organised-by-site-of-cancer#uppergastrointestinal-tract-cancers
7. Jenkinson C, Earl K, Ghaneh P, et al. Biomarkers for early diagnosis of pancreatic cancer. Expert Rev Gastroenterol Hepatol 2015; 9: 305-15.
8. Lennon AM, Wolfgang CL, Canto MI, et al. The early detection of pancreatic cancer: what will it take to diagnose and treat curable pancreatic neoplasia? Cancer Res 2014; 74: 3381-9.
9. Phillips M, Cataneo RN, Ditkoff BA, et al. Prediction of breast cancer using volatile biomarkers in the breath. Breast Cancer Res Treat 2006; 99: 19-21.
10. Kumar S, Huang J, Abbassi-Ghadi N, et al. Selected ion flow tube mass spectrometry analysis of exhaled breath for volatile organic compound profiling of esophago-gastric cancer. Anal Chem 2013; 85: 6121-8.
11. Kumar S, Huang J, Abbassi-Ghadi N, et al. Mass spectrometric analysis of exhaled breath for the identification of volatile organic compound biomarkers in esophageal and gastric adenocarcinoma. Ann Surg 2015; 262: 981-90. 12. Markar SR, Wiggins T, Kumar S, et al. Exhaled breath analysis for the diagnosis and assessment of endoluminal gastrointestinal diseases. J Clin Gastroenterol 2015; 49: 1-8.
13. Altomare DF, Di Lena M, Porcelli F, et al. Exhaled volatile organic compounds identify patients with colorectal cancer. Br J Surg 2013; 100: 144-50.
14. Phillips M, Gleeson K, Hughes JM, et al. Volatile organic compounds in breath as markers of lung cancer: a crosssectional study. Lancet 1999; 353: 1930-3.
15. Markar SR, Lagergren J, Hanna GB. Research protocol for a diagnostic study of non-invasive exhaled breath analysis for the prediction of oesophago-gastric cancer. BMJ Open 2016; 6: 0009139.
16. Markar SR, Chin ST, Romano A, et al. Breath volatile organic compound profiling of colorectal cancer using selected ion flow-tube mass spectrometry. Under review with Gastroenterology.
17. Boshier PR, Priest OH, Hanna GB, et al. Influence of respiratory variables on the on-line detection of exhaled trace gases by PTR-MS]. Thorax 2011; 66: 919-20.
18. Boshier PR, Cushnir JR, Priest OH, et al. Variation in the levels of volatile trace gases within three hospital environments: implications for clinical breath testing. J Breath Res 2010; 4: 031001.
19. Markar SR. Non-invasive volatile organic compound analysis from Exhaled Breath for the prediction of oesophagogastric cancer. PhD thesis, Imperial College London 2017.
20. Poli D, Goldoni M, Corradi M, et al. Determination of aldehydes in exhaled breath of patients with lung cancer by means of on-fiber-derivatisation SPME-GC/MS. J Chromatogr B Anal Technol Biomed Life Sci 2010; 878: 2643-51.
21. Mochalski P, Sponring A, King J, et al. Release and uptake of volatile organic compounds by human hepatocellular carcinoma cells (HepG2) in vitro. Cancer Cell Int 2013; 13: 72.
22. Ma I, Allan AL. The role of human aldehyde dehydrogenase in normal and cancer stem cells. Stem Cell Rev Reports. 2011; 7: 292-306.
23. Deng S, Yang X, Lassus H, et al. Distinct expression levels and patterns of stem cell marker, aldehyde dehydrogenase isoform 1 (ALDH1), in human epithelial cancers. PLos One 2010; 5: 010277.
24. Rosen AVon, Linder S, Harmenberg U, et al. Serum CA 19-9 and CA 50 in relation to lewis blood cell status in patients with malignant and benign pancreatic disease. Pancreas 1993; 8: 160-5.
Ejemplo 2 - Cáncer colorrectal
El siguiente ejemplo no forma parte de la invención y se presenta únicamente con fines ilustrativos.
Cuando el cáncer colorrectal (CRCa) se diagnostica en su etapa más temprana, más de 9 de cada 10 personas con CRCa sobrevivirán a la enfermedad durante cinco años o más, en comparación con menos de 1 de cada 10 cuando se diagnostica en la última etapa de la enfermedad [1]. Sin embargo, se ha demostrado que la utilización de los síntomas intestinales como base diagnóstica primaria para el CRCa tiene un valor predictivo positivo muy bajo [2]. Este estudio identificó y validó un perfil único de compuestos orgánicos volátiles en el aliento asociado con la presencia de cáncer colorrectal, lo que sugiere el potencial del análisis del aliento para su inclusión en la ruta de diagnóstico del cáncer colorrectal.
Los objetivos de este estudio fueron: (i) identificar cambios en la concentración de VOC en el aliento exhalado de pacientes con CRCa en comparación con aquellos con otras enfermedades colorrectales o tracto gastrointestinal inferior normal (control) de un estudio de cohorte prospectivo; (ii) validar estos hallazgos en otra cohorte prospectiva de pacientes con síntomas o enfermedad colorrectal; y (iii) identificar los cambios en los VOC del aire exhalado observados con la presencia de recidiva después de la resección quirúrgica de CRCa.
Materiales y métodos
Tamaño de la muestra:
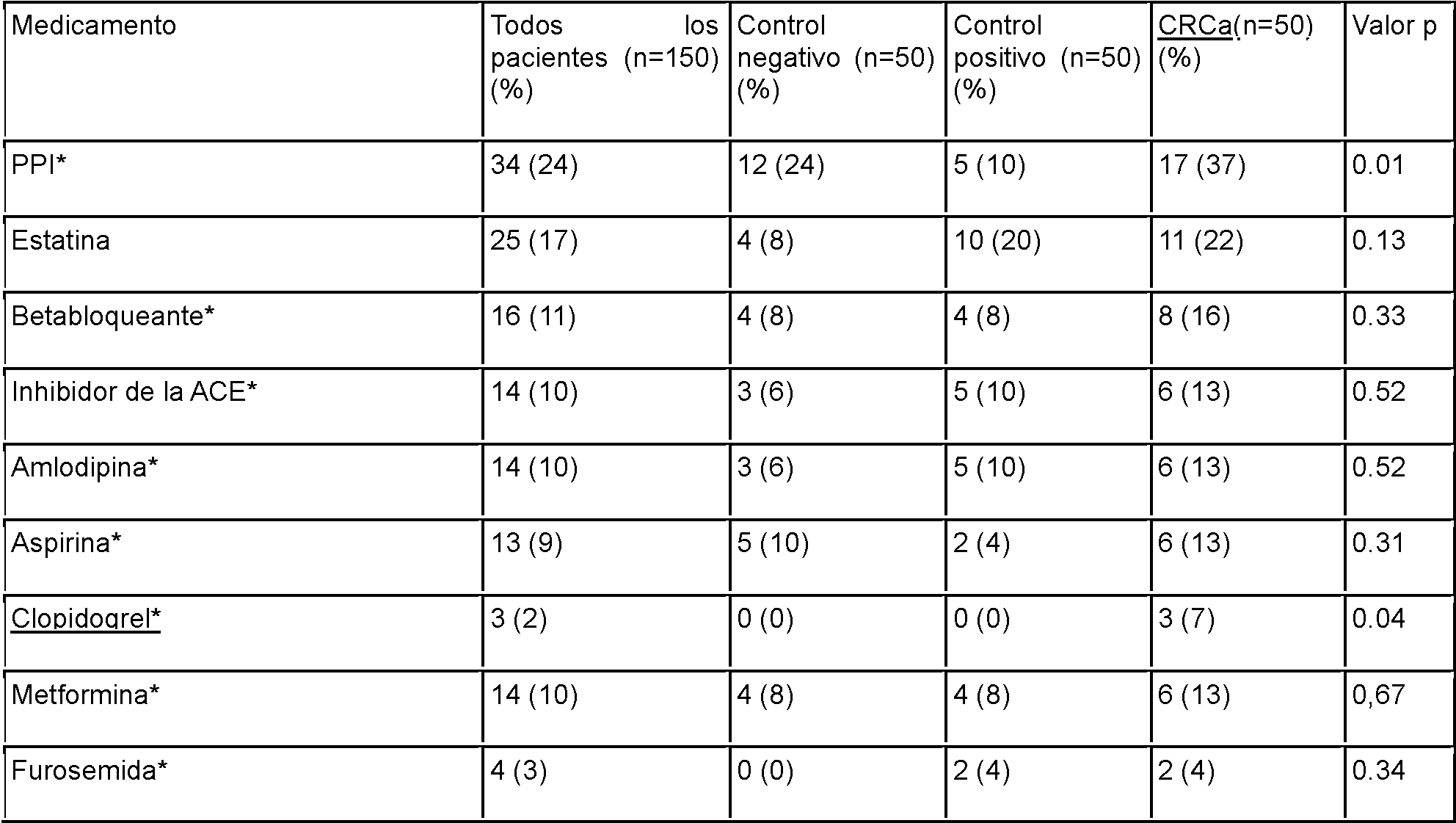
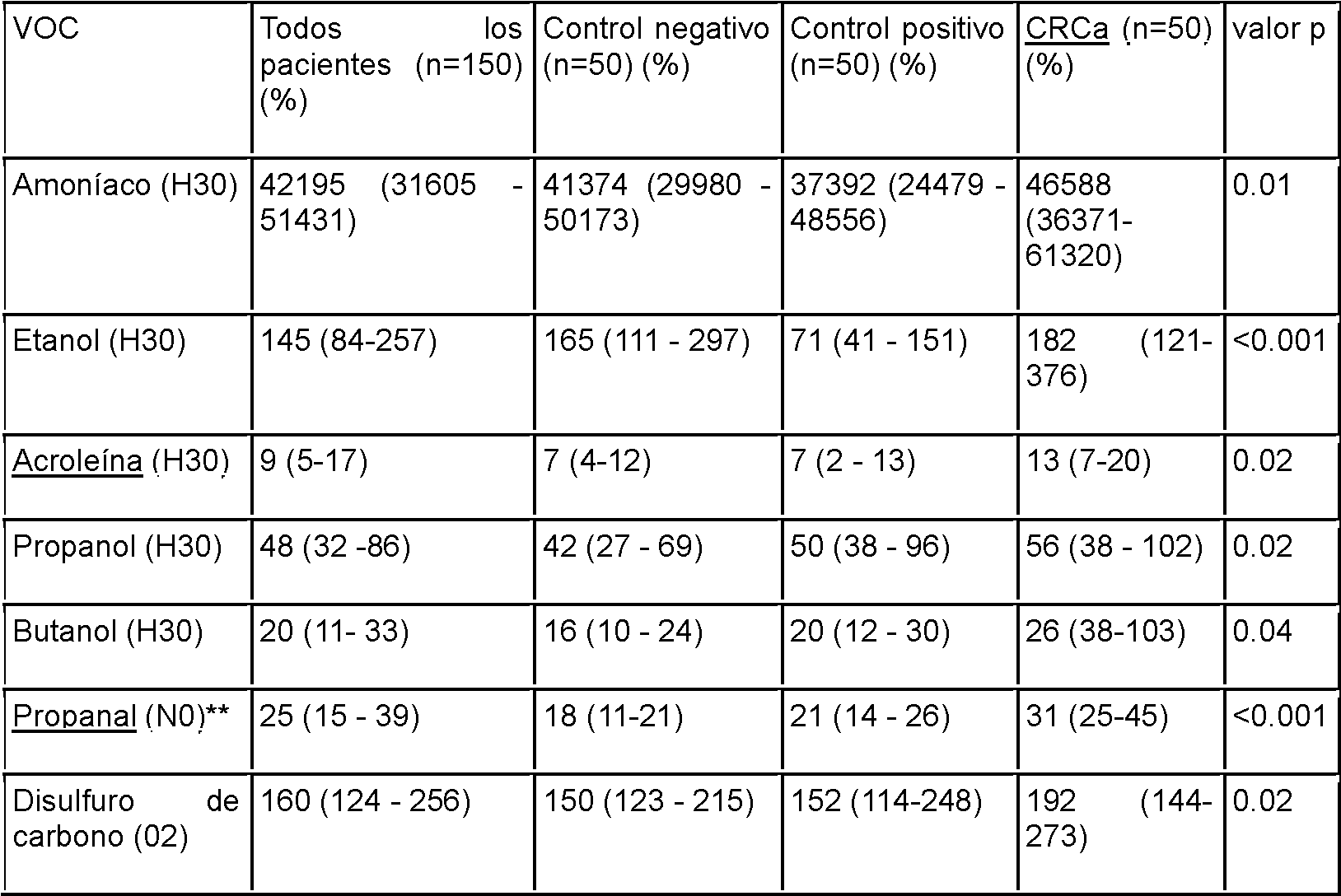
Estudio (i): investigación diagnóstica de perfiles en 150 pacientes (50 con cáncer colorrectal; 50 controles positivos que incluyen enfermedad inflamatoria intestinal, pólipos y enfermedad diverticular y 50 controles negativos con una endoscopia del tracto gastrointestinal inferior (LGI) normal).
Estudio (ii) - Validación diagnóstica independiente en 79 pacientes; 25 con CRCa y 54 pacientes de control, que era una mezcla de pacientes de control positivo y negativo.
Estudio (iii) - Validación clínica con recidiva tumoral en 40 pacientes; 19 pacientes postoperatorios sin evidencia de recidiva y 21 pacientes con recidiva hepática o peritoneal documentada. Todos los pacientes tenían al menos 6 meses después de la cirugía colorrectal inicial.
Sitio; St Mary's Hospital.
Aprobación ética; NHS Health Research Authority (NRES Committee London - Camden and Islington) aprobación obtenida el 16el Julio 2014 (Referencia REC 14/LO/1136). Número de registro de ensayos: UKCRN18063
Criterios de inclusión: Pacientes que asisten al St Mary's Hospital para una endoscopia gastrointestinal inferior o una cirugía por cáncer colorrectal o investigación de síntomas de LGI (estudios (i) y (ii)). Los pacientes que acudieron a la clínica oncológica para el seguimiento fueron reclutados para el estudio (iii).
Criterio de exclusión: Pacientes con una infección activa documentada o enfermedades hepáticas.
Metodología de muestreo de aliento: A todos los pacientes se les pidió que firmaran un formulario de consentimiento para ser incluidos en este estudio. Los inventores siguieron el protocolo de muestreo utilizado en estudios clínicos previos [9] que se basó en sus investigaciones sobre la influencia de las maniobras de respiración y el entorno hospitalario en la medición de VOC [14,15]. Los pacientes estuvieron en ayunas durante un mínimo de cuatro horas antes de la recolección de la muestra de aliento. Los pacientes descansaron en la misma área durante al menos 20 minutos antes de la muestra de aliento y todas las muestras de aliento se recuperaron antes de la endoscopia o la cirugía. Se pidió a los pacientes que realizaran una sola inhalación nasal profunda seguida de una exhalación completa a través de la boca en bolsas de Nalophan (Kalle UK Ltd., Witham, Reino Unido) de doble grosor (2 * 25 pm) mediante una jeringa Luer lok de 1 ml (Terumo Europe, Lovaina). Bélgica).
Análisis de muestra: Para cada medición de VOC, se retiró el émbolo de la jeringa de 1 ml Luer lok y la bolsa de Nalophan se conectó directamente mediante el cilindro de la jeringa al brazo de entrada de muestra del instrumento SIFT-MS. Para el modo de monitorización de múltiples iones, se analizaron los VOC selectivos del aliento durante un total de 6os y se promediaron las concentraciones medidas durante este tiempo para cada VOC. Como se trataba de un estudio de un solo centro, cada muestra de aliento se analizó en el plazo de una hora desde que se tomó la muestra del paciente y, por lo tanto, se utilizaron bolsas de aliento de Nalophan como en investigaciones anteriores realizadas por nuestro grupo [9]. Los estudios metodológicos demostraron la estabilidad de trazas de VOC hasta dos horas desde el momento de la toma de muestras del paciente [16].
Espectrometría de masas de tubo de flujo de iones seleccionados (SIFT-MS): SIFT-MS permite la cuantificación de VOC en línea y en tiempo real [11,12]. El principio de SIFT-MS se basa en el análisis espectrométrico de masas directo mediante ionización química de los VOC en muestras de aire o vapor. Iones precursores seleccionados (H3O+, NO+ y O2+) se inyectan en el gas portador helio e ionizan los VOC dentro de las muestras de aliento, con la generación de iones de producto característicos, que son detectados por el espectrómetro de masas de cuadrupolo corriente abajo. Al medir la tasa de conteo tanto de los iones precursores como de los iones característicos del producto en el sistema de detección corriente abajo, se logra una cuantificación en tiempo real, dándose cuenta de la concentración absoluta
de trazas y compuestos volátiles en partes por billón por volumen o partes por -millones por volumen. SIFT-MS se ha utilizado en el estudio de VOC en el aliento y la orina de pacientes con afecciones que incluyen fibrosis quística y cáncer de vejiga [17,18]. La técnica SIFT-MS permite la detección y cuantificación en tiempo real de VOC en muestras biológicas, tales como el aliento exhalado, sin preparación de la muestra [19]. Los inventores han confirmado previamente la reproducibilidad de las mediciones de VOC utilizando SIFT-MS [20].
Datos clinicos: El médico o becario de investigación que dio su consentimiento completó un formulario médico detallado utilizando la información proporcionada por el paciente, así como las investigaciones clínicas. Estos datos incluyeron datos demográficos de los pacientes, características del tumor, comorbilidades, medicamentos y medidas del estilo de vida. La endoscopia diagnóstica y/o los hallazgos operatorios se registraron para cada paciente.
Criterio estándar para la comparación: Los hallazgos de la endoscopia confirmados con el examen histológico se usaron como el estándar de oro para la clasificación de los pacientes en las cohortes CRCa o de control. Para los pacientes posoperatorios, se utilizó la última tomografía computarizada realizada como parte del seguimiento de rutina para identificar a aquellos pacientes con recidiva posoperatoria.
Análisis estadístico: Los datos de salida de SIFT-MS proporcionan la concentración medida de VOC del aliento exhalado. Estas concentraciones luego se compararon utilizando estadísticas univariadas, prueba de Kruskal-Wallis, entre los grupos de estudio. Los VOC que fueron significativos en las estadísticas univariadas se llevaron luego a un modelo de regresión logística multivariable con la variable dependiente como la presencia de CRCa. Para construir las curvas de características operativas del receptor (ROC), se utilizó el estado del cáncer como variable dependiente y la suma de las concentraciones de VOC significativos del modelo de regresión logística multivariable se utilizaron como variables independientes. Se utilizó un valor de p de <0,05 para asignar la significación estadística. Todos los análisis estadísticos se realizaron con el software estadístico SPSS (versión 22).
Validación de plataforma cruzada con GC-MS: Para confirmar la identificación de los VOC obtenidos en el aliento exhalado usando SIFT-MS, los inventores realizaron una validación de plataforma cruzada con GC-MS como técnica de separación estándar. El aliento exhalado se recogió usando la misma metodología de 20 pacientes. El contenido de v Oc de cada bolsa de aliento de Nalophan se transfirió usando una bomba de bolsillo para muestreo de aire de la serie SKC 210-1002 (PA, EE. Llantrisant, Reino Unido) antes del análisis GC-MS. Se utilizó un GC Agilent 7890B con MSD 5977A (Agilent Technologies, Cheshire, Reino Unido), acoplado a una unidad de desorción térmica (TDU) Markes TD-100. Se utilizó un programa de desorción térmica de dos etapas a un caudal de helio constante de 50 ml/min. En la etapa de desorción primaria, la muestra del tubo TD se purgó en seco durante 3 min antes de calentar a 280 °C durante 10 min. Durante la etapa de desorción secundaria, los VOC de la trampa fría (U-T12ME-2S) se desorbieron rápidamente de 10 °C a 290 °C a una tasa de calentamiento de 99 °C/min y se mantuvieron durante 4 min para transferir completamente los VOC al GC. La ruta de flujo desde la TDU hasta el GC se calentó constantemente a 140 °C.
La separación de VOC se realizó en una columna capilar ZB-624 (60 m * 0,25 mm DI * 1,40 pm dFi Phenomenex Inc, Torrance, EE. UU.) programado a 1,0 ml/min de portador de helio. El perfil de temperatura del horno se fijó a 40 °C inicialmente durante 4 min, rampa a 100 °C (5 °C/min con 1 min de retención), rampa a cero °C (5 °C/min con 1 min de retención), rampa a 200 °C (5 °C/min con 1 min de retención), rampa final a 240 °C a 10 °C/min con 4 min de retención. La línea de transferencia de MS se mantuvo a 240 °C mientras que la fuente de EI se fijó en 70 eV y 230 °C. El analizador de MS se configuró para adquirir en el rango de 20-250 m/z con una adquisición de datos aproximada a 6 barridos/seg. Los datos de GC-MS se procesaron con el software MassHunter versión B.07 SP1 (Agilent Technologies), mientras que los datos de MS del componente VOC separado se comparan con la biblioteca espectral de masas NIST (National Institute of Standards and Technology, versión 2.0) para su identificación.
Resultados
Estudio (i) - perfilado de investigación diagnóstica
150 pacientes (50 pacientes con cáncer colorrectal, 50 pacientes con otras afecciones del tracto gastrointestinal inferior (controles positivos) y 50 pacientes con un tracto gastrointestinal inferior normal (controles negativos)). De los pacientes de control positivo, 15 (30 %) tenían enfermedad inflamatoria intestinal, 21 (42 %) tenían pólipos en el tracto gastrointestinal inferior y 14 (28 %) tenían enfermedad diverticular. Todos los pacientes con enfermedad diverticular y enfermedad inflamatoria intestinal no tenían diverticulitis o colitis activa en el momento de la muestra de aliento.
El análisis comparativo de las comorbilidades médicas de los pacientes no reveló diferencias significativas entre los grupos, con la excepción de un aumento en la proporción de pacientes de 70 años o más en el grupo CRCa (véase Tabla 1a).
Tabla 1a: Comparación de las comorbilidades médicas de los pacientes
*7 pacientes con datos faltantes
También hubo una mayor proporción de pacientes que recibieron preparación intestinal en los grupos de control (Tabla 1a). El análisis comparativo de los síntomas de presentación que estimularon la derivación para una endoscopia gastrointestinal inferior no mostró diferencias significativas entre los grupos, con la excepción de una mayor proporción de pacientes con anemia en el grupo CRCa (véase la Tabla 1b).
Tabla 1b: Comparación de los síntomas de presentación
*7 pacientes con datos faltantes
El análisis comparativo de la utilización de medicación entre los grupos mostró un aumento en el uso del inhibidor de la bomba de protones y clopidogrel dentro del grupo CRCa (véase Tabla 1c).
Tabla 1c: Comparación de la utilización de medicamentos
*7 pacientes con datos faltantes
De los 50 pacientes con CRCa, el 52 % eran tumores de recto, el 66 % tumores moderadamente diferenciados, el 48 % T3 y el 52 % sin tumores, y el 34 % de los pacientes recibieron terapia neoadyuvante en el preoperatorio (véase Tabla 2).
Tabla 2: Características tumorales de los pacientes con cáncer colorrectal incluidas
Se encontró que siete compuestos eran significativamente diferentes entre los grupos de cáncer y de control, de los cuales solo el propanal (NO+) se asoció significativamente con el cáncer colorrectal en el análisis multivariante (véase Tabla 3).
Tabla 3: Análisis SIFT-MS de la respiración exhalada de pacientes colorrectales
** solo VOC significativo en análisis multivariado
Investigaciones anteriores han demostrado una cuantificación fiable del aldehido propanal mediante SIFT-MS debido a que se produce una reacción de transferencia de hidruro específica entre el aldehído saturado y el reactivo de NO+ [18]. Paralelamente al análisis SIFT-MS, el análisis de plataforma cruzada por GC-MS revela que el pico de propanal se observó claramente en el cromatograma de gases en el tiempo de retención (RT) de 8,92 min entre las muestras de aliento con cáncer. La columna capilar ZB-624 seleccionada ha proporcionado una eficiencia de resolución suficiente para separar el propanal del pico abundante de acetona (RT de 9,11 min), aunque ambos poseen el ion de fragmento común de 58 m/z. Los inventores han mostrado una gran similitud de los detalles espectrales de masas desconvolucionados del pico de propanal (iones característicos de 29 m/z, 39 m/z y 58 m/z) con la coincidencia de la biblioteca NIST
La Tabla 4 muestra un rango de VOC que se probaron como biomarcadores y, de nuevo, se demostró que el propanal está significativamente asociado con el cáncer colorrectal en un análisis multivariado.
Tabla 4: Análisis SIFT-MS de la respiración exhalada de pacientes colorrectales
*VOC significativamente asociado con el cáncer colorrectal en el análisis multivariante.
El propanal (NO+) se desempeñó bien como biomarcador de una sola respiración para el cáncer colorrectal en comparación con controles negativos (área bajo la curva ROC = 0,90 ± 0,03 (véase Figura 1a)) y controles positivos (área bajo la curva ROC = 0,83 ± 0,04 (véase Figura 1b)). Al distinguir CRCa de los controles negativos, el propanal como un biomarcador de aliento único basado en un umbral de 28 ppbv, tuvo una sensibilidad del 96 % y una
especificidad del 76 %. El propanal en un umbral de 28 ppbv también pudo distinguir el CRCa de los pacientes de control positivo con una sensibilidad del 90 % y una especificidad del 66 %.
Para garantizar que la concentración elevada de propanal observada en el CRCa no fuera el resultado de un factor de confusión que difería entre los grupos, se realizó un análisis de regresión lineal multivariable y se demostró que la presencia de CRCa era el único factor significativamente asociado con niveles elevados de propanal.
Estudio (ii) - validación de diagnóstico independiente
En total se estudiaron 79 pacientes, 25 con CRCa y 54 pacientes control. De los 54 pacientes de control, 31 (57,4 %) tenían un tracto gastrointestinal inferior normal en la endoscopia, 12 (22 %) tenían pólipos, 7 (13 %) tenían enfermedad diverticular y 4 (7 %) tenían enfermedad inflamatoria intestinal. El análisis comparativo de las comorbilidades médicas de los pacientes, el uso de medicamentos y los síntomas de presentación no reveló diferencias significativas entre los grupos, con la excepción de un aumento en la proporción de pacientes de 70 años o más y una mayor presentación con anemia en el grupo de cáncer colorrectal.
El propanal se elevó significativamente en el grupo de CRCa en comparación con el grupo de control (mediana de 30 frente a 19 ppbv; P <0,01). El propanal (NO+) se desempeñó bien como biomarcador de respiración única para CRCa en comparación con pacientes de control con un área bajo la curva ROC de 0,79 ± 0,06 (Figura 2). Nuevamente, al usar un umbral de 28 ppbv, esto le dio al propanal una sensibilidad del 83,3 % y una especificidad del 84,7 % para el diagnóstico de CRCa.
Estudio (iii) - validación clínica con recidiva tumoral
En total se estudiaron 40 pacientes, 19 pacientes postoperatorios sin evidencia de recidiva y 21 pacientes con recidiva documentada. De los pacientes con recidiva, 5 pacientes tuvieron recidiva hepática aislada y 16 pacientes tuvieron recidiva peritoneal sola o recidiva hepática y peritoneal simultáneamente. El análisis comparativo de las comorbilidades médicas de los pacientes y el uso de medicamentos no reveló diferencias significativas entre los grupos.
La concentración de propanal fue significativamente elevada en pacientes con recidiva de CRCa en comparación con el grupo sin recidiva (mediana de 38 vs. 19 ppbv; P <0,01). Se empleó propanal (NO+) como biomarcador de aliento único para identificar pacientes postoperatorios con recidiva de CRCa con un área bajo la curva ROC de 0,81 ± 0,07 (Figura 3). Usando un umbral de 28 ppbv, esto le dio al propanal una sensibilidad del 71,4 % y una especificidad del 90,9 % en la identificación de pacientes con recidiva después de la cirugía. La Figura 4 muestra los cambios en la concentración de propanal en los cuatro estados de enfermedad.
En los tres estudios, todos los pacientes invitados a participar en el estudio aceptaron la invitación y participaron en el estudio, lo que da una tasa de aceptabilidad del 100 %.
Discusión
Los resultados de este estudio sugieren que el propanal tiene el potencial de ser un biomarcador de aliento único para el diagnóstico de CRCa. Propanal pareció distinguir con una buena precisión diagnóstica a los pacientes con CRCa de los pacientes con otras enfermedades colorrectales y sujetos con un tracto gastrointestinal inferior endoscópicamente normal. Esos hallazgos han sido validados en un estudio de diagnóstico independiente y en pacientes con recidiva del cáncer colorrectal. La elevación de la concentración de propanal no estuvo influenciada por factores del paciente, como se muestra en el análisis multivariado. El propanal no era un componente del modelo de aliento VOC previamente generado y validado para el cáncer esófago-gástrico [9], lo que sugiere que los cánceres del tracto gastrointestinal superior e inferior tienen perfiles de aliento distintos que no se superponen que pueden permitir un análisis específico del cáncer en la práctica clínica futura.
Un estudio previo realizado por Altomare et al utilizando GC-MS identificó 15 VOC del aire exhalado que diferían significativamente entre los pacientes con CRCa y los de control [10]. De estos nonanal y decanal fueron los únicos aldehídos detectados. Altomare et al intentaron validar sus hallazgos en una cohorte prospectiva de pacientes, sin embargo, el modelo inicial que se desarrolló en 78 pacientes se validó solo en 25 pacientes. La metodología empleada por Altomare et al utilizó un análisis de aldehídos sin subdividir en GC-MS, lo que permite la medición de aldehídos de cadena larga, tales como nonanal y decanal, pero no de aldehídos más cortos, tales como propanal, que se pierden porque son más volátiles. Este puede ser un factor importante en la diferencia en los resultados observados entre nuestra investigación y el estudio de Altomare [10]. Además, un estudio reciente de Amal et al, que utilizó GC-MS de manera similar, no identificó aldehídos en el aliento exhalado que difirieran entre los grupos CRCa y de control [21]. Las diferentes técnicas de espectrometría de masas pueden explicar las diferencias entre los estudios. Una combinación de aldehídos de cadena corta y larga como base para el modelo de diagnóstico en CRCa necesita más investigación.
Propanal (CH3CH2CHO) es un aldehído saturado de 3 carbonos y es un isómero estructural de la acetona. La validación de plataforma cruzada mediante cromatografía de gases y espectrometría de masas confirmó la identidad de propanal. La explicación más plausible de la elevación de la concentración de propanal es el trastorno del metabolismo de los aldehídos en el cáncer colorrectal [22]. Específicamente, se ha demostrado que la expresión de
aldehido deshidrogenasa-1 está desregulada en el cáncer colorrectal y afecta de manera independiente la supervivencia a largo plazo, junto con la respuesta a la quimioterapia neoadyuvante [23,24]. Otro factor que contribuye a la elevación del propanal son los cambios en la microbiota intestinal y la compleja interacción entre el microbioma y la respuesta inmunitaria adaptativa en el desarrollo del cáncer [25,26].
Como investigación inicial hacia el desarrollo de una prueba de aliento para el cáncer colorrectal, las ventajas de estos estudios incluyen: (i) el descubrimiento de un único biomarcador volátil, (ii) el establecimiento de un umbral de prueba para el diagnóstico utilizando una técnica de espectrometría de masas cuantitativa que no requiere preparación de muestras; (iii) la realización de una validación independiente en dos cohortes prospectivas de pacientes con CRCa y con recidiva tumoral después de la resección y (iv) todos los pacientes tenían endoscopia digestiva baja como criterio estándar de comparación. Utilizando un umbral de 28 ppbv, fue posible distinguir el cáncer de los grupos de control con una precisión de diagnóstico que oscilaba entre el 79 % y el 90 %, y es comparable con las pruebas inmunoquímicas y de sangre oculta en heces que se utilizan actualmente en la práctica clínica [3-6]. Los estudios previos sobre el aliento se han basado en gran medida en la combinación de cambios en varios VOC para generar un modelo de predicción de riesgos [9,10,21]. Solo unos pocos estudios han demostrado la asociación de un solo biomarcador VOC con un estado de enfermedad; cianuro de hidrógeno en la infección por pseudomonas aeruginosa y pentano en la enfermedad inflamatoria intestinal [27,28]. Por otro lado, las investigaciones de los inventores tienen las limitaciones de un estudio de un solo centro tanto en aspectos clínicos como analíticos. Actualmente se está planificando un estudio multicéntrico más grande que tiene la potencia para proporcionar una respuesta definitiva sobre la precisión de la prueba. La realización de la prueba de aliento requiere investigaciones en etapas tempranas de CRCa. Aunque los inventores han demostrado la repetibilidad de las mediciones experimentales durante un período de tiempo corto [20], se debe examinar cuidadosamente la reproducibilidad de los resultados utilizando instrumentos de espectrometría de masas en diferentes laboratorios o con los mismos instrumentos en un laboratorio central durante un período de tiempo prolongado. antes de la aceptación clínica de cualquier prueba de aliento propuesta. Además, el mecanismo de producción de propanal y la desregulación de aldehído sigue siendo un área importante para el trabajo futuro que puede mejorar la comprensión de los factores de confusión y mejorar las medidas de control en la administración de la prueba.
El descubrimiento descrito en este documento y los experimentos de validación se realizaron en pacientes colorrectales sintomáticos con cáncer colorrectal, enfermedad benigna o colon endoscópicamente normal. Al planificar un estudio definitivo de precisión diagnóstica, es importante estudiar la ubicación propuesta de una prueba de aliento exhalado para el cáncer colorrectal. Los inventores contemplan el uso de dicha prueba como una investigación de clasificación para indicar a los pacientes que se sometan a una endoscopia. Si la prueba tiene una sensibilidad y especificidad aceptables y la aceptabilidad del paciente, puede resultar rentable y mejorar la vía de diagnóstico en pacientes con síntomas colorrectales; un impacto que requiere varios estudios para investigar, pero una visión importante para delinear en una etapa temprana.
Conclusiones
Este estudio sugiere la asociación de un biomarcador de aliento único (propanal) con la presencia primaria y recidiva de CRCa. Se requieren estudios adicionales de validación multicéntricos para validar estos hallazgos.
Referencias
1. Torre LA, Bray F, Siegel RL, et al. Global cancer statistics, 2012. CA Cancer J Clin 2015; 65: 87-108.
2. Ewing M, Naredi P, Zhang C, et al. Identification of patients with non-metastatic colorectal cancer in primary care: a case-control study. Br J Gen Pract 2016; 66: e88o-e886.
3. Lieberman DA, Weiss D; Veterans Affairs Cooperative Study Group 380. One-time screening for colorectal cancer with combined fecal occult-blood testing and examination of the distal colon. N Engl J Med 2001; 345: 555-560.
4. Imperiale TF, Ranshoff DF, Itzkowitz SH, et al. Fecal DNA versus fecal occult blood for colorectal-cancer screening in an average-risk population. N Engl J Med 2004; 351: 2704-2714.
5. Allison JE, Tekawa IS, Ransom LJ, et al. A comparison of fecal occult-blood tests for colorectal-cancer screening. N Engl J Med 1996; 334: 155-159.
6. Allison JE, Sakoda LC, Levin TR, et al. Screening for colorectal neoplasms with new fecal occult blood tests: update on performance characteristics. J Natl Cancer Inst. 2007; 99: 1462-1470.
7. Imperiale TF, Ransohoff DF, Itzkowitz SH, et al. Multitarget stool DNA testing for colorectal-cancer screening. N Engl J Med 2014; 370: 1287-1297.
8. Nakhleh MK, Amal H, Jeries R, et al. Diagnosis and classification of 17 diseases from 1404 subjects via pattern analysis of exhaled molecules. ACS Nano 2017; 11: 112-125.
9. Kumar S, Huang J, Abbassi-Ghadi N, et al. Mass spectrometric analysis of exhaled breath for the identification of volatile organic compound biomarkers in esophageal and gastric adenocarcinoma. Ann Surg 2015; 262; 981-990. 10. Altomare DF, Di Lena M, Porcelli F, et al. Exhaled volatile organic compounds identify patients with colorectal cancer. Br J Surg 2013; 100: 144-150
11. Spanel P, Smith D. Selected ion flow tube mass spectrometry for on-line trace gas analysis in biology and medicine. Eur J Mass Spectrom 2007; 13: 77-82
12. Spanel P, Smith D, Progress in SIFT-MS: breath analysis and other applications. Mass Spectrom Rev 2011; 30: 236-267
13. Altomare DF, Di Lena M, Porcelli F, et al. Effects of curative colorectal cancer surgery on exhaled volatile organic compounds and potential implications in clinical follow-up. Ann Surg 2015; 262: 862-866.
14. Boshier PR, Cushnir JR, Priest OH, et al. Variation in the levels of volatile trace gases within three hospital environments: implications for clinical breath testing. J Breath Res 2010; 4: 031001.
15. Boshier PR, Priest OH, Hanna GB, et al. Influence of respiratory variables on the on-line detection of exhaled trace gases by PTR-MS. Thorax 2011; 66: 919-920.
16. Markar SR. Non-invasive volatile organic compound analysis from Exhaled Breath for the prediction of oesophagogastric cancer. PhD thesis, Imperial College London 2017.
17. Spanel P, Smith D, Holland TA, et al. Analysis of formaldehyde in the headspace of urine from bladder and prostate cancer patients using selected ion flow tube mass spectrometry. Rapid Commun Mass Spectrom. 1999; 13: 1354-1359 18. Smith D, Sovova K, Dryahina K, et al. Breath concentration of acetic acid vapour is elevated in patients with cystic fibrosis. J Breath Res 2016; 10: 021002.
19. Boshier PR, Cushnir JR, Mistry V, et al. On-line, real time monitoring of exhaled trace gases by SIFT-MS in the perioperative setting: a feasibility study. Analyst 2011; 136: 3233-3237.
20. Boshier PR, Marczin N, Hanna GB. Repeatability of the measurement of exhaled volatile metabolites using selected ion flow tube mass spectrometry. J Am Soc Mass Spectrom 2010; 21: 1070-1074.
21. Amal H, Leja M, Funka K, et al. Breath testing as potential colorectal cancer screening tool. Int J Cancer 2016; 138: 229-236.
22. Brown DG, Rao S, Weir TL, et al. Metabolomics and metabolic pathway networks from human colorectal cancers, adjacent mucosa, and stool. Cancer Metab 2016; 4: 11.
23. Li H, Jiang Y, Pei F, et al. Aldehyde dehydrogenase 1 and nodal as significant prognostic markers in colorectal cancer. Pathol Oncol 2016; 22: 121-7.
24. Deng Y, Zhou J, Fang L, et al. ALDH1 is an independent prognostic factor for patients with stages II-NI rectal cancer after receiving radiochemotherapy. Br J Cancer 2014; 110: 430-4.
25. Vogtmass E, Hua X, Zeller G, et al. Colorectal cancer and human gut microbiome: reproducibility with wholegenome shotgun sequencing. PLos One 2016; 11: 00155362.
26. Lasry A, Zinger A, Ben-Neriah Y. Inflammatory networks underlying colorectal cancer. Nat Immunol 2016; 17: 230 40.
27. Dryahina K, Spanel P, Pospisilova V, et al. Quantification of pentane in exhaled breath, a potential biomarker of bowel disease, using selected ion flow tube mass spectrometry. Rapid Commun Mass Spectrom. 2013; 27: 198 -192 28. Smith D, Spanel P, Gilchrist FJ. Hydrogen cyanide, a volatile biomarker of pseudomonas aeruginosa infection. J Breath Res 2013; 7: 044001.
Claims (15)
1. Un método para diagnosticar a un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico de la condición del sujeto, comprendiendo el método analizar la concentración de un compuesto característico en una muestra corporal de un sujeto de prueba y comparar esta concentración con una referencia para la concentración del compuesto característico en un individuo que no padece cáncer de páncreas, en el que un aumento en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto.
2. Un método para determinar la eficacia de tratar a un sujeto que padece cáncer de páncreas con un agente terapéutico o una dieta especializada, comprendiendo el método analizar la concentración de un compuesto característico en una muestra corporal de un sujeto de prueba y comparar esta concentración con una referencia para la concentración del compuesto característico en un individuo que no padece cáncer de páncreas, en el que una disminución en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es eficaz, o en el que un aumento en la concentración del compuesto característico seleccionado de un aldehído C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es ineficaz.
3. Un método de acuerdo con la reivindicación 1, en el que (i) un aumento en la concentración de un compuesto característico adicional seleccionado de un alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono del alcano C2-C10 se sustituye con un grupo =O y un segundo átomo de carbono se sustituye con un grupo -OH, en la muestra corporal del sujeto de prueba, o (ii) una disminución en la concentración de un compuesto característico adicional seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto.
4. Un método de acuerdo con la reivindicación 2, en el que (i) una disminución en la concentración de un compuesto característico adicional seleccionado de un alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono del alcano C2-C10 se sustituye con un grupo =O y un segundo átomo de carbono se sustituye con un grupo -OH, en la muestra corporal del sujeto de prueba, en comparación con la referencia, o (ii) un aumento en la concentración de un compuesto característico adicional seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es eficaz, o en el que (i) un aumento en la concentración de un compuesto característico adicional seleccionado de un alcohol C1-C3 y alcano C2-C10 en el que un primer átomo de carbono del alcano C2-C10 se sustituye con un grupo =O y un segundo átomo de carbono se sustituye con un grupo -OH, en la muestra corporal del sujeto de prueba, en comparación con la referencia, o (ii) una disminución en la concentración de un compuesto característico adicional seleccionado de un alcano C1-C20, alcohol C4-C10, ácido carboxílico C1-C6 y aldehído C4-C20, en la muestra corporal del sujeto de prueba, en comparación con la referencia, sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es ineficaz.
5. Un método de acuerdo con cualquiera de las reivindicaciones 1 o 2, en el que el compuesto característico es un aldehído C1.
6. Un método de acuerdo con cualquiera de las reivindicaciones 3 o 4, en el que cuando el compuesto característico adicional es un alcohol C1-C3 , el compuesto es un alcohol C1 o un alcohol C3.
7. Un método de acuerdo con cualquiera de las reivindicaciones 3 o 4, en el que cuando el compuesto característico adicional es un alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, el átomo de carbono sustituido con el grupo =O no es un átomo de carbono terminal, o en el que cuando el compuesto distintivo adicional es un alcano C2-C10 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH, el compuesto es un alcano C3-C6 o un alcano C4 en el que un primer átomo de carbono está sustituido con el grupo =O y un segundo átomo de carbono está sustituido con un grupo -OH.
8. Un método de acuerdo con cualquiera de las reivindicaciones 3 o 4, en el que cuando el compuesto característico es un alcano C1-C20, el compuesto es un alcano C3-C15 o un alcohol C5-C14, o en el que cuando el compuesto característico adicional es un alcano C1-C20, el compuesto es un alcohol C5, alcohol C6 o un alcohol C14.
9. Un método de acuerdo con cualquiera de las reivindicaciones 3 o 4, en el que cuando el compuesto característico adicional es un alcohol C4-C10, , el compuesto es un alcohol C4-C7 o un alcohol C4, o en el que cuando el compuesto característico adicional es un ácido carboxílico C1-C6, el compuesto es un ácido carboxílico C2-C4 o un ácido carboxílico C3.
10. Un método de acuerdo con cualquiera de las reivindicaciones 3 o 4, en el que cuando el compuesto característico adicional es un aldehído C4-C20, el compuesto es un aldehído C5-C15 o aldehído C7-C13, o en el que cuando el
compuesto característico adicional es un aldehido C4-C20, el compuesto es un aldehido C8, o un aldehido C9, o un aldehido C10, o un aldehido C11.
11 Uso de un aparato para diagnosticar a un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico del estado del sujeto, comprendiendo el aparato:
(i) medios para determinar la concentración de un compuesto característico en una muestra de un sujeto de prueba; y
(ii) una referencia para la concentración del compuesto característico en una muestra de un individuo que no padece cáncer de páncreas,
en el que el aparato se utiliza para identificar: un aumento en la concentración del compuesto característico seleccionado de un aldehido C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el sujeto padece cáncer de páncreas, o tiene una predisposición al mismo, o proporciona un pronóstico negativo de la condición del sujeto.
12. Uso de un aparato para determinar la eficacia del tratamiento de un sujeto que padece cáncer de páncreas con un agente terapéutico o una dieta especializada, comprendiendo el aparato:
(a) medios para determinar la concentración de un compuesto característico en una muestra de un sujeto de prueba; y
(b) una referencia para la concentración del compuesto característico en una muestra de un individuo que no padece cáncer de páncreas,
en el que el aparato se utiliza para identificar:
(i) una disminución en la concentración del compuesto característico seleccionado de un aldehido C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es eficaz; o
(ii) un aumento en la concentración del compuesto característico seleccionado de un aldehido C1 o C3 en la muestra corporal del sujeto de prueba, en comparación con la referencia, lo que sugiere que el régimen de tratamiento con el agente terapéutico o la dieta especializada es ineficaz.
13. Uso de un aparato de acuerdo con la reivindicación 11 o la reivindicación 12, en el que se determina la concentración de un compuesto característico adicional, en el que el compuesto característico adicional es como se define en una cualquiera de las reivindicaciones 6-10.
14. Uso in vitro de un compuesto característico seleccionado del grupo que consiste en un aldehido C1 o C3 como biomarcador para diagnosticar un sujeto que padece cáncer de páncreas, o una predisposición al mismo, o para proporcionar un pronóstico del estado del sujeto.
15. Uso de acuerdo con la reivindicación 14, en el que se utiliza un compuesto distintivo adicional, en el que el compuesto distintivo adicional es como se define en una cualquiera de las reivindicaciones 6-10.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1714797.6A GB2566681B (en) | 2017-09-14 | 2017-09-14 | Biomarker |
| PCT/GB2018/052574 WO2019053414A1 (en) | 2017-09-14 | 2018-09-11 | VOLATILE ORGANIC COMPOUNDS AS BIOMARKERS OF CANCER |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2954325T3 true ES2954325T3 (es) | 2023-11-21 |
Family
ID=60159315
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18773823T Active ES2954325T3 (es) | 2017-09-14 | 2018-09-11 | Compuestos orgánicos volátiles como biomarcadores de cáncer |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20200378973A1 (es) |
| EP (2) | EP3682243B1 (es) |
| JP (2) | JP7451397B2 (es) |
| KR (2) | KR20250031228A (es) |
| CN (1) | CN111602055B (es) |
| AU (2) | AU2018332171B2 (es) |
| CA (1) | CA3075595A1 (es) |
| ES (1) | ES2954325T3 (es) |
| GB (1) | GB2566681B (es) |
| WO (1) | WO2019053414A1 (es) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3860457A1 (en) * | 2018-10-06 | 2021-08-11 | The Cleveland Clinic Foundation | Method for diagnosing clostridioides difficile infection |
| CN110045035B (zh) * | 2019-04-30 | 2021-05-11 | 上海交通大学 | 唾液中的胃癌voc标志物及其在制备胃癌诊断试剂中的应用 |
| GB2584300A (en) * | 2019-05-29 | 2020-12-02 | Imperial College Innovations Ltd | Detection of biomarkers |
| GB2591133A (en) * | 2020-01-17 | 2021-07-21 | Imp College Innovations Ltd | Cancer |
| ES2881149B2 (es) * | 2020-05-26 | 2022-11-25 | Univ Alicante | Aparatos y métodos para el diagnóstico de cáncer colorrectal |
| US20240081675A1 (en) * | 2020-10-30 | 2024-03-14 | The Children's Hospital Of Philadelphia | Breath biomarkers of sars-cov-2 in children and methods of use thereof for the diagnosis and treatment of covid-19 |
| US20240044832A1 (en) * | 2020-12-21 | 2024-02-08 | Technion Research And Development Foundation Ltd. | Methods for diagnosing cancer based on volatile organic compounds in blood and urine samples |
| US20240159755A1 (en) * | 2021-03-01 | 2024-05-16 | The Johns Hopkins University | Detection of stage i lung cancer biomarkers |
| GB202103951D0 (en) * | 2021-03-22 | 2021-05-05 | Imperial College Innovations Ltd | Biomarkers |
| KR102827804B1 (ko) * | 2021-04-15 | 2025-06-30 | 고려대학교 산학협력단 | 마스크를 이용한 호흡 생검 방법 및 이를 이용한 호흡 생검 장치 |
| EP4086622A1 (en) * | 2021-05-04 | 2022-11-09 | Koninklijke Philips N.V. | Using chromatogram features to identify biological changes in volatile organic compound patterns |
| CA3221298A1 (en) * | 2021-06-03 | 2022-12-08 | Ricardo Daniel DE SIMONE | A device for detecting health disorders from biological samples and a detection process |
| WO2023010143A2 (en) * | 2021-07-30 | 2023-02-02 | The Board Of Trustees Of The Leland Stanford Junior University | Genetically-encoded volatile synthetic biomarkers for breath-based cancer detection |
| WO2024162662A1 (ko) * | 2023-01-31 | 2024-08-08 | 고려대학교 산학협력단 | 호기 내 휘발성 유기화합물 기반 대장암 진단 |
| EP4666941A1 (en) | 2023-02-16 | 2025-12-24 | Gustavo Senna Chelles | Exhaled air sample collector for pre-diagnosis of pathologies, and method for using same |
| ES3005483A1 (es) * | 2023-09-12 | 2025-03-14 | Fund Rioja Salud | Compuestos orgánicos volátiles como marcadores para el diagnóstico y pronóstico del cáncer de páncreas |
| CN117250354B (zh) * | 2023-09-25 | 2024-05-10 | 西安交通大学医学院第一附属医院 | 十一种代谢标志物的检测试剂在制备乳腺癌诊断和预后产品中的应用 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2253093A1 (en) * | 1998-11-06 | 2000-05-06 | Jiri J. Krepinsky | Screening test for early detection of colorectal cancer |
| JP2007292746A (ja) * | 2006-03-31 | 2007-11-08 | Shizuoka Prefecture | 胃癌の判定方法 |
| US20150065366A1 (en) * | 2011-11-11 | 2015-03-05 | Metabolon, Inc. | Biomarkers for Bladder Cancer and Methods Using the Same |
| US9528979B2 (en) * | 2011-11-15 | 2016-12-27 | Technion Research And Development Foundation Ltd. | Breath analysis of pulmonary nodules |
| WO2014063743A1 (en) * | 2012-10-25 | 2014-05-01 | Association Pour La Recherche Thérapeutique Anti-Cancéreuse | Methylglyoxal as a marker of cancer |
| US10393745B2 (en) * | 2013-07-11 | 2019-08-27 | The USA, as represented by the Secretary, Department of Heath and Human Services | Method for the diagnosis and prognosis of cancer |
| US11016082B2 (en) | 2015-07-31 | 2021-05-25 | University Of Louisville Research Foundation, Inc. | Noninvasive detection of cancer originating in tissue outside of the lung using exhaled breath |
| EP3557250A1 (en) * | 2015-09-29 | 2019-10-23 | Nissha Co., Ltd. | Cancer development risk assessment device, program, and method for testing cancer development risk |
| GB201602394D0 (en) * | 2016-02-10 | 2016-03-23 | Mdb Medical Services Ltd | Method |
| MX2018010053A (es) * | 2016-02-18 | 2019-05-06 | Pulse Health Llc | Metodos, sistemas y composiciones para la deteccion de aldehidos. |
-
2017
- 2017-09-14 GB GB1714797.6A patent/GB2566681B/en active Active
-
2018
- 2018-09-11 KR KR1020257006501A patent/KR20250031228A/ko active Pending
- 2018-09-11 JP JP2020515240A patent/JP7451397B2/ja active Active
- 2018-09-11 AU AU2018332171A patent/AU2018332171B2/en active Active
- 2018-09-11 WO PCT/GB2018/052574 patent/WO2019053414A1/en not_active Ceased
- 2018-09-11 CA CA3075595A patent/CA3075595A1/en active Pending
- 2018-09-11 US US16/646,339 patent/US20200378973A1/en active Pending
- 2018-09-11 EP EP18773823.2A patent/EP3682243B1/en active Active
- 2018-09-11 CN CN201880073420.9A patent/CN111602055B/zh active Active
- 2018-09-11 EP EP23189987.3A patent/EP4293358A3/en active Pending
- 2018-09-11 ES ES18773823T patent/ES2954325T3/es active Active
- 2018-09-11 KR KR1020207010710A patent/KR102775827B1/ko active Active
-
2024
- 2024-03-06 JP JP2024033617A patent/JP7820429B2/ja active Active
-
2025
- 2025-06-13 AU AU2025204444A patent/AU2025204444A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20200378973A1 (en) | 2020-12-03 |
| JP2024079698A (ja) | 2024-06-11 |
| WO2019053414A1 (en) | 2019-03-21 |
| KR20200088293A (ko) | 2020-07-22 |
| KR20250031228A (ko) | 2025-03-06 |
| EP3682243B1 (en) | 2023-08-09 |
| AU2018332171B2 (en) | 2025-03-20 |
| CA3075595A1 (en) | 2019-03-21 |
| EP4293358A3 (en) | 2024-01-24 |
| GB201714797D0 (en) | 2017-11-01 |
| AU2025204444A1 (en) | 2025-07-03 |
| EP4293358A2 (en) | 2023-12-20 |
| GB2566681B (en) | 2021-07-28 |
| KR102775827B1 (ko) | 2025-03-04 |
| GB2566681A (en) | 2019-03-27 |
| JP2020533602A (ja) | 2020-11-19 |
| JP7820429B2 (ja) | 2026-02-25 |
| EP3682243A1 (en) | 2020-07-22 |
| EP3682243C0 (en) | 2023-08-09 |
| JP7451397B2 (ja) | 2024-03-18 |
| CN111602055B (zh) | 2024-04-12 |
| AU2018332171A1 (en) | 2020-04-23 |
| CN111602055A (zh) | 2020-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2954325T3 (es) | Compuestos orgánicos volátiles como biomarcadores de cáncer | |
| Markar et al. | Breath volatile organic compound profiling of colorectal cancer using selected ion flow-tube mass spectrometry | |
| Xiang et al. | Volatile organic compounds in human exhaled breath to diagnose gastrointestinal cancer: a meta-analysis | |
| ES2961916T3 (es) | Isopropanol como biomarcador del cáncer colorrectal | |
| Wu et al. | GC/MS-based metabolomic approach to validate the role of urinary sarcosine and target biomarkers for human prostate cancer by microwave-assisted derivatization | |
| US20240369563A1 (en) | Biomarker combination for assessing risk of adenoma and colorectal cancer, and use thereof | |
| JP5676275B2 (ja) | 酸化ストレス検出用マーカー、肝臓疾患マーカー及び医薬品の検定方法 | |
| ES2698374T3 (es) | Medios y procedimientos de diagnóstico de cáncer pancreático en un sujeto basándose en un panel de metabolitos | |
| Zhang et al. | Breath volatile organic compound analysis: An emerging method for gastric cancer detection | |
| BR112017004773B1 (pt) | Biomarcadores para avaliação do câncer de mama | |
| Kałużna-Czaplińska et al. | Current applications of chromatographic methods for diagnosis and identification of potential biomarkers in cancer | |
| Xiang et al. | Volatolomics analysis of exhaled breath and gastric-endoluminal gas for distinguishing early upper gastrointestinal cancer from benign | |
| JP2018169376A (ja) | 大腸がん検査方法 | |
| Ma et al. | Application of electronic nose technology in the diagnosis of gastrointestinal diseases: a review | |
| Zhao et al. | Advancements and challenges in salivary metabolomics for early detection and monitoring of systemic diseases | |
| CN110824037A (zh) | Mit和/或dit作为甲状腺癌标志物的应用及试剂盒 | |
| CN118011003A (zh) | 一种用于诊断胃癌的生物标志物组合物及其应用 | |
| AU2022245358A1 (en) | Volatile biomarkers for colorectal cancer | |
| Sha et al. | Volatile organic compounds in urine reveals distinct diagnostic signatures for gastric cancer | |
| Abbassi-Ghadi et al. | Mass Spectrometric Analysis of Exhaled Breath for the Identification of Volatile Organic Compound Biomarkers in Esophageal and Gastric Adenocarcinoma | |
| Fusegawa et al. | Noninvasive Breathomics for Developing Carbonyl Biomarkers in Esophageal Cancer | |
| Dezi et al. | Exhaled Volatile Organic Compounds in the Diagnosis of Colorectal Cancer | |
| Liu et al. | A Novel Exhaled Gas Detection Model for Diagnosis and Prognosis Prediction of Colorectal Cancer | |
| WO2025056826A1 (es) | Compuestos orgánicos volátiles como marcadores para el diagnóstico y pronóstico del cáncer de páncreas | |
| Kalinowska et al. | Instrumental techniques used in the analysis of exhaled air |