ES2955227A2 - Proceso para preparar ácido B-[(7alfa,17beta)-17-hidroxi-7-[9-[(4,4,5,5,5-pentafluoropentil)sulfinil]nonil]estra-1,3,5(10)-trien-3-il]-borónico - Google Patents
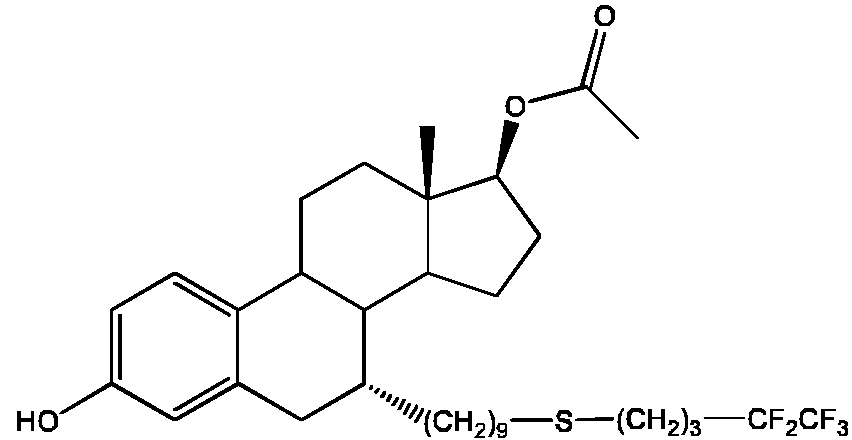
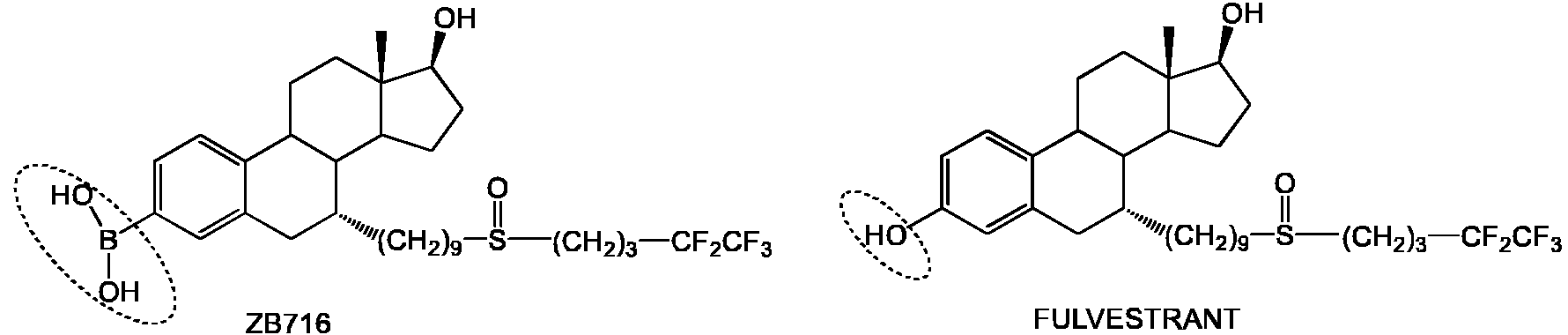
Proceso para preparar ácido B-[(7alfa,17beta)-17-hidroxi-7-[9-[(4,4,5,5,5-pentafluoropentil)sulfinil]nonil]estra-1,3,5(10)-trien-3-il]-borónico Download PDFInfo
- Publication number
- ES2955227A2 ES2955227A2 ES202390146A ES202390146A ES2955227A2 ES 2955227 A2 ES2955227 A2 ES 2955227A2 ES 202390146 A ES202390146 A ES 202390146A ES 202390146 A ES202390146 A ES 202390146A ES 2955227 A2 ES2955227 A2 ES 2955227A2
- Authority
- ES
- Spain
- Prior art keywords
- pentafluoropentyl
- estra
- sulfinyl
- nonyl
- trien
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J31/00—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring
- C07J31/006—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring not covered by C07J31/003
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J31/00—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J51/00—Normal steroids with unmodified cyclopenta(a)hydrophenanthrene skeleton not provided for in groups C07J1/00 - C07J43/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J75/00—Processes for the preparation of steroids in general
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Steroid Compounds (AREA)
Abstract
Description
Claims (6)
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IT102021000008066A IT202100008066A1 (it) | 2021-03-31 | 2021-03-31 | PROCESSO PER LA PREPARAZIONE DI ACIDO B-[(7α,17β)-17-IDROSSI-7-[9-[(4,4,5,5,5-PENTAFLUOROPENTIL)SULFINIL]NONIL]ESTRA-1,3,5(10)-TRIEN-3-IL]-BORONICO E INTERMEDI DEL PROCESSO |
| PCT/EP2022/058213 WO2022207607A1 (en) | 2021-03-31 | 2022-03-29 | PROCESS FOR PREPARING B-[(7α,17β)-17-HYDROXY-7-[9-[(4,4,5,5,5-PENTAFLUOROPENTYL)SULFINYL]NONYL]ESTRA-1,3,5(10)-TRIEN-3-YL]-BORONIC ACID |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| ES2955227A2 true ES2955227A2 (es) | 2023-11-29 |
| ES2955227R1 ES2955227R1 (es) | 2024-10-18 |
| ES2955227B2 ES2955227B2 (es) | 2025-04-10 |
Family
ID=76921074
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES202390146A Active ES2955227B2 (es) | 2021-03-31 | 2022-03-29 | Proceso para preparar ácido B-[(7alfa,17beta)-17-hidroxi-7-[9-[(4,4,5,5,5-pentafluoropentil)sulfinil]nonil]estra-1,3,5(10)-trien-3-il]-borónico |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20240174711A1 (es) |
| CN (1) | CN117295754A (es) |
| CH (1) | CH719827B1 (es) |
| ES (1) | ES2955227B2 (es) |
| FR (2) | FR3121443A1 (es) |
| IT (1) | IT202100008066A1 (es) |
| WO (2) | WO2022208157A1 (es) |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK72693D0 (da) * | 1993-06-18 | 1993-06-18 | Lundbeck & Co As H | Compounds |
| ITMI20071479A1 (it) | 2007-07-23 | 2009-01-24 | Ind Chimica Srl | Processo per la preparazione di 7alfa-[9-(4,4,5,5,5-pentafluortiopentil)nonil]estra-1,3,5(10)-trien-3,17beta-diolo |
| EP3164405A4 (en) | 2014-07-02 | 2018-05-23 | Xavier University Of Louisiana | Boron-based prodrug strategy for increased bioavailability and lower-dosage requirements for drug molecules containing at least one phenol (or aromatic hydroxyl) group |
| WO2017192991A1 (en) | 2016-05-06 | 2017-11-09 | Xavier University Of Louisiana | Selective estrogen receptor down-regulators (serds) |
| IT201900004041A1 (it) * | 2019-03-20 | 2020-09-20 | Farmabios Spa | Procedimento per la preparazione di un derivato del fulvestrant |
-
2021
- 2021-03-31 IT IT102021000008066A patent/IT202100008066A1/it unknown
- 2021-10-29 WO PCT/IB2021/060013 patent/WO2022208157A1/en not_active Ceased
- 2021-10-29 FR FR2111509A patent/FR3121443A1/fr not_active Ceased
-
2022
- 2022-03-29 CN CN202280024289.3A patent/CN117295754A/zh active Pending
- 2022-03-29 ES ES202390146A patent/ES2955227B2/es active Active
- 2022-03-29 CH CH001074/2023A patent/CH719827B1/it unknown
- 2022-03-29 WO PCT/EP2022/058213 patent/WO2022207607A1/en not_active Ceased
- 2022-03-29 US US18/281,943 patent/US20240174711A1/en active Pending
- 2022-03-30 FR FR2202890A patent/FR3121441B1/fr active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CH719827B1 (it) | 2025-08-29 |
| US20240174711A1 (en) | 2024-05-30 |
| FR3121441B1 (fr) | 2025-03-21 |
| WO2022207607A1 (en) | 2022-10-06 |
| WO2022208157A1 (en) | 2022-10-06 |
| IT202100008066A1 (it) | 2022-10-01 |
| CN117295754A (zh) | 2023-12-26 |
| FR3121443A1 (fr) | 2022-10-07 |
| FR3121441A1 (fr) | 2022-10-07 |
| ES2955227B2 (es) | 2025-04-10 |
| ES2955227R1 (es) | 2024-10-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Zhong et al. | Synthesis and biological evaluation of novel oleanolic acid analogues as potential α-glucosidase inhibitors | |
| ES2915058B2 (es) | Proceso para preparar (15alfa,16alfa,17beta)-estra-1,3,5(10)-trieno-3,15,16,17-tetrol (Estetrol) e intermedios de dicho proceso | |
| CA2877122A1 (en) | Preparation, uses and solid forms of obeticholic acid | |
| CN104447739A (zh) | 一种氘代Palbociclib衍生物、制备方法及应用 | |
| BG107289A (bg) | 3 - азот - 6,7 - дикислородни стероиди и тяхното използване | |
| ES2970336T3 (es) | Intermedios para la síntesis de derivados de ácidos biliares, en particular del ácido obeticólico | |
| JP2001510200A (ja) | ステロイドスルファターゼ阻害剤並びにその製造及び使用方法 | |
| Hou et al. | The synthesis and cytotoxicity of fructose-1-SNAP, a novel fructose conjugated S-nitroso nitric oxide donor | |
| ES2955227B2 (es) | Proceso para preparar ácido B-[(7alfa,17beta)-17-hidroxi-7-[9-[(4,4,5,5,5-pentafluoropentil)sulfinil]nonil]estra-1,3,5(10)-trien-3-il]-borónico | |
| Baimuratov et al. | Reactions of tetracyclic γ-sultones with N-nucleophiles. Novel synthesis of 3, 4-disubstituted homoadamantanes | |
| ES2957913B2 (es) | Proceso para la preparación de ácido B-[(7alfa,17beta)-17-hidroxi-7-[9-[(4,4,5,5,5-pentafluoropentil)sulfinil]nonil]estra-1,3,5(10)-trien-3-il]-borónico e intermedios de dicho proceso | |
| Levina et al. | In vivo study on biotransformation of pentacyclic analogs of progesterone: Identification of their metabolites by HPLC-MS method | |
| EP2890705B1 (en) | Process for the preparation of abiraterone or abiraterone acetate | |
| ES2976011B2 (es) | Proceso para preparar acido b-[(7alfa,17beta)-17-hidroxi-7-[9-[(4,4,5,5,5-pentafluoropentil)sulfinil]nonil]estra-1,3,5(10)-trien-3-il]-boronico e intermedios del proceso | |
| WO2020018997A1 (en) | 3,4-thiazolo steroids and methods of making and using the same | |
| Virtanen et al. | 1H-, 13C-, and 15N-NMR and ESI-TOF+ MS studies of a supramolecular complex of silver (I) and a cholaphane | |
| ES2693259T3 (es) | Síntesis de ent-progesterona e intermedios de la misma | |
| Jovanović-Šanta et al. | Evaluation of biological activity of new hemiesters of 17-hydroxy-16, 17-secoestra-1, 3, 5 (10)-triene-16-nitrile | |
| CN102234288B (zh) | 唑他莫司的制备方法 | |
| JP2003342291A (ja) | エストラジオール抱合体 | |
| CN117777047B (zh) | N-取代氮杂螺癸单烯酮类化合物及其制备方法和应用 | |
| JPS5927360B2 (ja) | ステロイド化合物およびその製造方法 | |
| Heyl et al. | Synthesis of lyxoflavin | |
| JP3769668B2 (ja) | 重水素又はトリチウム標識されたステロイド化合物 | |
| Ötvös et al. | Synthesis of high specific activity [15, 16‐3H2] buprenorphine |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| BA2A | Patent application published |
Ref document number: 2955227 Country of ref document: ES Kind code of ref document: A2 Effective date: 20231129 |
|
| EC2A | Search report published |
Ref document number: 2955227 Country of ref document: ES Kind code of ref document: R1 Effective date: 20241011 |
|
| FG2A | Definitive protection |
Ref document number: 2955227 Country of ref document: ES Kind code of ref document: B2 Effective date: 20250410 |