JP2004202086A - エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法 - Google Patents
エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法 Download PDFInfo
- Publication number
- JP2004202086A JP2004202086A JP2002377275A JP2002377275A JP2004202086A JP 2004202086 A JP2004202086 A JP 2004202086A JP 2002377275 A JP2002377275 A JP 2002377275A JP 2002377275 A JP2002377275 A JP 2002377275A JP 2004202086 A JP2004202086 A JP 2004202086A
- Authority
- JP
- Japan
- Prior art keywords
- electroporation
- drug
- electrode
- drug administration
- administration
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 238000004520 electroporation Methods 0.000 title claims abstract description 137
- 239000003814 drug Substances 0.000 title claims abstract description 108
- 229940079593 drug Drugs 0.000 title claims abstract description 90
- 238000000034 method Methods 0.000 title claims abstract description 20
- 230000005684 electric field Effects 0.000 claims abstract description 17
- 239000003792 electrolyte Substances 0.000 claims abstract description 13
- 230000005611 electricity Effects 0.000 claims abstract description 8
- 238000001647 drug administration Methods 0.000 claims description 115
- 238000009434 installation Methods 0.000 claims description 17
- 239000000126 substance Substances 0.000 claims description 15
- 239000000463 material Substances 0.000 claims description 13
- 239000000853 adhesive Substances 0.000 claims description 12
- 230000001070 adhesive effect Effects 0.000 claims description 12
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 claims description 10
- 229910052697 platinum Inorganic materials 0.000 claims description 5
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 claims description 4
- 229910021607 Silver chloride Inorganic materials 0.000 claims description 4
- 239000004020 conductor Substances 0.000 claims description 4
- 229910052709 silver Inorganic materials 0.000 claims description 4
- 239000004332 silver Substances 0.000 claims description 4
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 claims description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 3
- 239000000956 alloy Substances 0.000 claims description 3
- 229910045601 alloy Inorganic materials 0.000 claims description 3
- 229910052799 carbon Inorganic materials 0.000 claims description 3
- ORTQZVOHEJQUHG-UHFFFAOYSA-L copper(II) chloride Chemical compound Cl[Cu]Cl ORTQZVOHEJQUHG-UHFFFAOYSA-L 0.000 claims description 3
- 239000003795 chemical substances by application Substances 0.000 claims 1
- 206010067484 Adverse reaction Diseases 0.000 abstract 2
- 230000006838 adverse reaction Effects 0.000 abstract 2
- 210000003491 skin Anatomy 0.000 description 19
- 238000010521 absorption reaction Methods 0.000 description 12
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 12
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 8
- 239000008103 glucose Substances 0.000 description 8
- 210000004369 blood Anatomy 0.000 description 7
- 239000008280 blood Substances 0.000 description 7
- 206010040880 Skin irritation Diseases 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 229960000905 indomethacin Drugs 0.000 description 6
- 210000004400 mucous membrane Anatomy 0.000 description 6
- 230000036470 plasma concentration Effects 0.000 description 6
- -1 polyoxymethylene Polymers 0.000 description 6
- 231100000475 skin irritation Toxicity 0.000 description 6
- 230000036556 skin irritation Effects 0.000 description 6
- 230000007423 decrease Effects 0.000 description 5
- 230000009931 harmful effect Effects 0.000 description 5
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical class N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 5
- 230000007383 nerve stimulation Effects 0.000 description 5
- 241000283973 Oryctolagus cuniculus Species 0.000 description 4
- 210000001367 artery Anatomy 0.000 description 4
- 210000000883 ear external Anatomy 0.000 description 4
- 229960004393 lidocaine hydrochloride Drugs 0.000 description 4
- YECIFGHRMFEPJK-UHFFFAOYSA-N lidocaine hydrochloride monohydrate Chemical compound O.[Cl-].CC[NH+](CC)CC(=O)NC1=C(C)C=CC=C1C YECIFGHRMFEPJK-UHFFFAOYSA-N 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- BQJCRHHNABKAKU-KBQPJGBKSA-N morphine Chemical compound O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O BQJCRHHNABKAKU-KBQPJGBKSA-N 0.000 description 4
- 229960005195 morphine hydrochloride Drugs 0.000 description 4
- XELXKCKNPPSFNN-BJWPBXOKSA-N morphine hydrochloride trihydrate Chemical compound O.O.O.Cl.O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O XELXKCKNPPSFNN-BJWPBXOKSA-N 0.000 description 4
- 210000003462 vein Anatomy 0.000 description 4
- 239000011148 porous material Substances 0.000 description 3
- RPTUSVTUFVMDQK-UHFFFAOYSA-N Hidralazin Chemical compound C1=CC=C2C(NN)=NN=CC2=C1 RPTUSVTUFVMDQK-UHFFFAOYSA-N 0.000 description 2
- 102000004877 Insulin Human genes 0.000 description 2
- 108090001061 Insulin Proteins 0.000 description 2
- 241000047703 Nonion Species 0.000 description 2
- 239000011358 absorbing material Substances 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- OROGSEYTTFOCAN-DNJOTXNNSA-N codeine Chemical compound C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC OROGSEYTTFOCAN-DNJOTXNNSA-N 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 229960003529 diazepam Drugs 0.000 description 2
- AAOVKJBEBIDNHE-UHFFFAOYSA-N diazepam Chemical compound N=1CC(=O)N(C)C2=CC=C(Cl)C=C2C=1C1=CC=CC=C1 AAOVKJBEBIDNHE-UHFFFAOYSA-N 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- 229940125396 insulin Drugs 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 229960005181 morphine Drugs 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 230000002123 temporal effect Effects 0.000 description 2
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 2
- DNXIKVLOVZVMQF-UHFFFAOYSA-N (3beta,16beta,17alpha,18beta,20alpha)-17-hydroxy-11-methoxy-18-[(3,4,5-trimethoxybenzoyl)oxy]-yohimban-16-carboxylic acid, methyl ester Natural products C1C2CN3CCC(C4=CC=C(OC)C=C4N4)=C4C3CC2C(C(=O)OC)C(O)C1OC(=O)C1=CC(OC)=C(OC)C(OC)=C1 DNXIKVLOVZVMQF-UHFFFAOYSA-N 0.000 description 1
- DIWRORZWFLOCLC-HNNXBMFYSA-N (3s)-7-chloro-5-(2-chlorophenyl)-3-hydroxy-1,3-dihydro-1,4-benzodiazepin-2-one Chemical compound N([C@H](C(NC1=CC=C(Cl)C=C11)=O)O)=C1C1=CC=CC=C1Cl DIWRORZWFLOCLC-HNNXBMFYSA-N 0.000 description 1
- UCTWMZQNUQWSLP-VIFPVBQESA-N (R)-adrenaline Chemical compound CNC[C@H](O)C1=CC=C(O)C(O)=C1 UCTWMZQNUQWSLP-VIFPVBQESA-N 0.000 description 1
- 229930182837 (R)-adrenaline Natural products 0.000 description 1
- METKIMKYRPQLGS-GFCCVEGCSA-N (R)-atenolol Chemical compound CC(C)NC[C@@H](O)COC1=CC=C(CC(N)=O)C=C1 METKIMKYRPQLGS-GFCCVEGCSA-N 0.000 description 1
- PJJGZPJJTHBVMX-UHFFFAOYSA-N 5,7-Dihydroxyisoflavone Chemical compound C=1C(O)=CC(O)=C(C2=O)C=1OC=C2C1=CC=CC=C1 PJJGZPJJTHBVMX-UHFFFAOYSA-N 0.000 description 1
- GJSURZIOUXUGAL-UHFFFAOYSA-N Clonidine Chemical compound ClC1=CC=CC(Cl)=C1NC1=NCCN1 GJSURZIOUXUGAL-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 102400000739 Corticotropin Human genes 0.000 description 1
- 101800000414 Corticotropin Proteins 0.000 description 1
- 241000208011 Digitalis Species 0.000 description 1
- WDJUZGPOPHTGOT-OAXVISGBSA-N Digitoxin Natural products O([C@H]1[C@@H](C)O[C@@H](O[C@@H]2C[C@@H]3[C@@](C)([C@@H]4[C@H]([C@]5(O)[C@@](C)([C@H](C6=CC(=O)OC6)CC5)CC4)CC3)CC2)C[C@H]1O)[C@H]1O[C@@H](C)[C@H](O[C@H]2O[C@@H](C)[C@@H](O)[C@@H](O)C2)[C@@H](O)C1 WDJUZGPOPHTGOT-OAXVISGBSA-N 0.000 description 1
- LTMHDMANZUZIPE-AMTYYWEZSA-N Digoxin Natural products O([C@H]1[C@H](C)O[C@H](O[C@@H]2C[C@@H]3[C@@](C)([C@@H]4[C@H]([C@]5(O)[C@](C)([C@H](O)C4)[C@H](C4=CC(=O)OC4)CC5)CC3)CC2)C[C@@H]1O)[C@H]1O[C@H](C)[C@@H](O[C@H]2O[C@@H](C)[C@H](O)[C@@H](O)C2)[C@@H](O)C1 LTMHDMANZUZIPE-AMTYYWEZSA-N 0.000 description 1
- 101710158332 Diuretic hormone Proteins 0.000 description 1
- 101710204261 Diuretic hormone class 2 Proteins 0.000 description 1
- 102000009025 Endorphins Human genes 0.000 description 1
- 108010049140 Endorphins Proteins 0.000 description 1
- 108050009340 Endothelin Proteins 0.000 description 1
- 102000002045 Endothelin Human genes 0.000 description 1
- 108010092674 Enkephalins Proteins 0.000 description 1
- 206010015150 Erythema Diseases 0.000 description 1
- 102000003951 Erythropoietin Human genes 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- VMZUTJCNQWMAGF-UHFFFAOYSA-N Etizolam Chemical compound S1C(CC)=CC2=C1N1C(C)=NN=C1CN=C2C1=CC=CC=C1Cl VMZUTJCNQWMAGF-UHFFFAOYSA-N 0.000 description 1
- WMFSSTNVXWNLKI-UHFFFAOYSA-N Flutazolam Chemical compound O1CCN2CC(=O)N(CCO)C3=CC=C(Cl)C=C3C21C1=CC=CC=C1F WMFSSTNVXWNLKI-UHFFFAOYSA-N 0.000 description 1
- 102400000921 Gastrin Human genes 0.000 description 1
- 108010052343 Gastrins Proteins 0.000 description 1
- 102400000321 Glucagon Human genes 0.000 description 1
- 108060003199 Glucagon Proteins 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- URLZCHNOLZSCCA-VABKMULXSA-N Leu-enkephalin Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(O)=O)NC(=O)CNC(=O)CNC(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=CC=C1 URLZCHNOLZSCCA-VABKMULXSA-N 0.000 description 1
- NNJVILVZKWQKPM-UHFFFAOYSA-N Lidocaine Chemical compound CCN(CC)CC(=O)NC1=C(C)C=CC=C1C NNJVILVZKWQKPM-UHFFFAOYSA-N 0.000 description 1
- 239000000232 Lipid Bilayer Substances 0.000 description 1
- 102000009151 Luteinizing Hormone Human genes 0.000 description 1
- 108010073521 Luteinizing Hormone Proteins 0.000 description 1
- XADCESSVHJOZHK-UHFFFAOYSA-N Meperidine Chemical compound C=1C=CC=CC=1C1(C(=O)OCC)CCN(C)CC1 XADCESSVHJOZHK-UHFFFAOYSA-N 0.000 description 1
- 206010052904 Musculoskeletal stiffness Diseases 0.000 description 1
- CMWTZPSULFXXJA-UHFFFAOYSA-N Naproxen Natural products C1=C(C(C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-UHFFFAOYSA-N 0.000 description 1
- 102400001103 Neurotensin Human genes 0.000 description 1
- 101800001814 Neurotensin Proteins 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- LCAHPIFLPICNRW-SVYNMNNPSA-N Oxymetebanol Chemical compound C1[C@H](O)CC[C@@]2(O)[C@H]3CC4=CC=C(OC)C(OC)=C4[C@]21CCN3C LCAHPIFLPICNRW-SVYNMNNPSA-N 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 108090000445 Parathyroid hormone Proteins 0.000 description 1
- 102000003982 Parathyroid hormone Human genes 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000004820 Pressure-sensitive adhesive Substances 0.000 description 1
- 102000003946 Prolactin Human genes 0.000 description 1
- 108010057464 Prolactin Proteins 0.000 description 1
- LCQMZZCPPSWADO-UHFFFAOYSA-N Reserpilin Natural products COC(=O)C1COCC2CN3CCc4c([nH]c5cc(OC)c(OC)cc45)C3CC12 LCQMZZCPPSWADO-UHFFFAOYSA-N 0.000 description 1
- QEVHRUUCFGRFIF-SFWBKIHZSA-N Reserpine Natural products O=C(OC)[C@@H]1[C@H](OC)[C@H](OC(=O)c2cc(OC)c(OC)c(OC)c2)C[C@H]2[C@@H]1C[C@H]1N(C2)CCc2c3c([nH]c12)cc(OC)cc3 QEVHRUUCFGRFIF-SFWBKIHZSA-N 0.000 description 1
- 108010086019 Secretin Proteins 0.000 description 1
- 102100037505 Secretin Human genes 0.000 description 1
- 102000005157 Somatostatin Human genes 0.000 description 1
- 108010056088 Somatostatin Proteins 0.000 description 1
- 102000011923 Thyrotropin Human genes 0.000 description 1
- 108010061174 Thyrotropin Proteins 0.000 description 1
- 102000004338 Transferrin Human genes 0.000 description 1
- 108090000901 Transferrin Proteins 0.000 description 1
- 229960004892 acemetacin Drugs 0.000 description 1
- FSQKKOOTNAMONP-UHFFFAOYSA-N acemetacin Chemical compound CC1=C(CC(=O)OCC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 FSQKKOOTNAMONP-UHFFFAOYSA-N 0.000 description 1
- 239000003470 adrenal cortex hormone Substances 0.000 description 1
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 description 1
- 229960002213 alprenolol Drugs 0.000 description 1
- PAZJSJFMUHDSTF-UHFFFAOYSA-N alprenolol Chemical compound CC(C)NCC(O)COC1=CC=CC=C1CC=C PAZJSJFMUHDSTF-UHFFFAOYSA-N 0.000 description 1
- 229960003556 aminophylline Drugs 0.000 description 1
- FQPFAHBPWDRTLU-UHFFFAOYSA-N aminophylline Chemical compound NCCN.O=C1N(C)C(=O)N(C)C2=C1NC=N2.O=C1N(C)C(=O)N(C)C2=C1NC=N2 FQPFAHBPWDRTLU-UHFFFAOYSA-N 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 239000002220 antihypertensive agent Substances 0.000 description 1
- 229940127088 antihypertensive drug Drugs 0.000 description 1
- 239000000164 antipsychotic agent Substances 0.000 description 1
- 229940005529 antipsychotics Drugs 0.000 description 1
- 239000002249 anxiolytic agent Substances 0.000 description 1
- 230000000949 anxiolytic effect Effects 0.000 description 1
- 229940005530 anxiolytics Drugs 0.000 description 1
- 229960002274 atenolol Drugs 0.000 description 1
- 230000001746 atrial effect Effects 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 229940124630 bronchodilator Drugs 0.000 description 1
- 239000000168 bronchodilator agent Substances 0.000 description 1
- 229960001736 buprenorphine Drugs 0.000 description 1
- RMRJXGBAOAMLHD-IHFGGWKQSA-N buprenorphine Chemical compound C([C@]12[C@H]3OC=4C(O)=CC=C(C2=4)C[C@@H]2[C@]11CC[C@]3([C@H](C1)[C@](C)(O)C(C)(C)C)OC)CN2CC1CC1 RMRJXGBAOAMLHD-IHFGGWKQSA-N 0.000 description 1
- IFKLAQQSCNILHL-QHAWAJNXSA-N butorphanol Chemical compound N1([C@@H]2CC3=CC=C(C=C3[C@@]3([C@]2(CCCC3)O)CC1)O)CC1CCC1 IFKLAQQSCNILHL-QHAWAJNXSA-N 0.000 description 1
- 229960001113 butorphanol Drugs 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- AOXOCDRNSPFDPE-UKEONUMOSA-N chembl413654 Chemical compound C([C@H](C(=O)NCC(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC=CC=1)C(N)=O)NC(=O)[C@@H](C)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)CNC(=O)[C@@H](N)CCC(O)=O)C1=CC=C(O)C=C1 AOXOCDRNSPFDPE-UKEONUMOSA-N 0.000 description 1
- 229960001076 chlorpromazine Drugs 0.000 description 1
- ZPEIMTDSQAKGNT-UHFFFAOYSA-N chlorpromazine Chemical compound C1=C(Cl)C=C2N(CCCN(C)C)C3=CC=CC=C3SC2=C1 ZPEIMTDSQAKGNT-UHFFFAOYSA-N 0.000 description 1
- 229960002896 clonidine Drugs 0.000 description 1
- 229960004126 codeine Drugs 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- IDLFZVILOHSSID-OVLDLUHVSA-N corticotropin Chemical compound C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)NC(=O)[C@@H](N)CO)C1=CC=C(O)C=C1 IDLFZVILOHSSID-OVLDLUHVSA-N 0.000 description 1
- 229960000258 corticotropin Drugs 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 229960001193 diclofenac sodium Drugs 0.000 description 1
- 229960000648 digitoxin Drugs 0.000 description 1
- WDJUZGPOPHTGOT-XUDUSOBPSA-N digitoxin Chemical compound C1[C@H](O)[C@H](O)[C@@H](C)O[C@H]1O[C@@H]1[C@@H](C)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3C[C@@H]4[C@]([C@@H]5[C@H]([C@]6(CC[C@@H]([C@@]6(C)CC5)C=5COC(=O)C=5)O)CC4)(C)CC3)C[C@@H]2O)C)C[C@@H]1O WDJUZGPOPHTGOT-XUDUSOBPSA-N 0.000 description 1
- 229960005156 digoxin Drugs 0.000 description 1
- LTMHDMANZUZIPE-PUGKRICDSA-N digoxin Chemical compound C1[C@H](O)[C@H](O)[C@@H](C)O[C@H]1O[C@@H]1[C@@H](C)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3C[C@@H]4[C@]([C@@H]5[C@H]([C@]6(CC[C@@H]([C@@]6(C)[C@H](O)C5)C=5COC(=O)C=5)O)CC4)(C)CC3)C[C@@H]2O)C)C[C@@H]1O LTMHDMANZUZIPE-PUGKRICDSA-N 0.000 description 1
- LTMHDMANZUZIPE-UHFFFAOYSA-N digoxine Natural products C1C(O)C(O)C(C)OC1OC1C(C)OC(OC2C(OC(OC3CC4C(C5C(C6(CCC(C6(C)C(O)C5)C=5COC(=O)C=5)O)CC4)(C)CC3)CC2O)C)CC1O LTMHDMANZUZIPE-UHFFFAOYSA-N 0.000 description 1
- 229950005448 drotebanol Drugs 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000010292 electrical insulation Methods 0.000 description 1
- ZUBDGKVDJUIMQQ-UBFCDGJISA-N endothelin-1 Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(O)=O)NC(=O)[C@H]1NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@@H](CC=2C=CC(O)=CC=2)NC(=O)[C@H](C(C)C)NC(=O)[C@H]2CSSC[C@@H](C(N[C@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N2)=O)NC(=O)[C@@H](CO)NC(=O)[C@H](N)CSSC1)C1=CNC=N1 ZUBDGKVDJUIMQQ-UBFCDGJISA-N 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 229960005139 epinephrine Drugs 0.000 description 1
- 231100000321 erythema Toxicity 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- 229960004404 etizolam Drugs 0.000 description 1
- ZPAKPRAICRBAOD-UHFFFAOYSA-N fenbufen Chemical compound C1=CC(C(=O)CCC(=O)O)=CC=C1C1=CC=CC=C1 ZPAKPRAICRBAOD-UHFFFAOYSA-N 0.000 description 1
- 229960001395 fenbufen Drugs 0.000 description 1
- 229960002428 fentanyl Drugs 0.000 description 1
- PJMPHNIQZUBGLI-UHFFFAOYSA-N fentanyl Chemical compound C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 PJMPHNIQZUBGLI-UHFFFAOYSA-N 0.000 description 1
- 229960004930 fludiazepam Drugs 0.000 description 1
- ROYOYTLGDLIGBX-UHFFFAOYSA-N fludiazepam Chemical compound N=1CC(=O)N(C)C2=CC=C(Cl)C=C2C=1C1=CC=CC=C1F ROYOYTLGDLIGBX-UHFFFAOYSA-N 0.000 description 1
- 229960002390 flurbiprofen Drugs 0.000 description 1
- SYTBZMRGLBWNTM-UHFFFAOYSA-N flurbiprofen Chemical compound FC1=CC(C(C(O)=O)C)=CC=C1C1=CC=CC=C1 SYTBZMRGLBWNTM-UHFFFAOYSA-N 0.000 description 1
- 229950009354 flutazolam Drugs 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 1
- 229960004666 glucagon Drugs 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 229960003878 haloperidol Drugs 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229960002474 hydralazine Drugs 0.000 description 1
- OROGSEYTTFOCAN-UHFFFAOYSA-N hydrocodone Natural products C1C(N(CCC234)C)C2C=CC(O)C3OC2=C4C1=CC=C2OC OROGSEYTTFOCAN-UHFFFAOYSA-N 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- MPGBPFMOOXKQRX-UHFFFAOYSA-N indenolol Chemical compound CC(C)NCC(O)COC1=CC=CC2=C1C=CC2 MPGBPFMOOXKQRX-UHFFFAOYSA-N 0.000 description 1
- 229950008838 indenolol Drugs 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- DKYWVDODHFEZIM-UHFFFAOYSA-N ketoprofen Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 DKYWVDODHFEZIM-UHFFFAOYSA-N 0.000 description 1
- 229960000991 ketoprofen Drugs 0.000 description 1
- 238000002386 leaching Methods 0.000 description 1
- WABPQHHGFIMREM-UHFFFAOYSA-N lead(0) Chemical compound [Pb] WABPQHHGFIMREM-UHFFFAOYSA-N 0.000 description 1
- 229960004194 lidocaine Drugs 0.000 description 1
- 229960004391 lorazepam Drugs 0.000 description 1
- 229940040129 luteinizing hormone Drugs 0.000 description 1
- 229960003464 mefenamic acid Drugs 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229950000412 mexazolam Drugs 0.000 description 1
- ANUCDXCTICZJRH-UHFFFAOYSA-N mexazolam Chemical compound C=1C=C(Cl)C=C2C=1NC(=O)CN1C(C)COC21C1=CC=CC=C1Cl ANUCDXCTICZJRH-UHFFFAOYSA-N 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 229960002009 naproxen Drugs 0.000 description 1
- CMWTZPSULFXXJA-VIFPVBQESA-N naproxen Chemical compound C1=C([C@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-VIFPVBQESA-N 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- PCJGZPGTCUMMOT-ISULXFBGSA-N neurotensin Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 PCJGZPGTCUMMOT-ISULXFBGSA-N 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 229960001454 nitrazepam Drugs 0.000 description 1
- KJONHKAYOJNZEC-UHFFFAOYSA-N nitrazepam Chemical compound C12=CC([N+](=O)[O-])=CC=C2NC(=O)CN=C1C1=CC=CC=C1 KJONHKAYOJNZEC-UHFFFAOYSA-N 0.000 description 1
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 1
- 229960004535 oxazepam Drugs 0.000 description 1
- ADIMAYPTOBDMTL-UHFFFAOYSA-N oxazepam Chemical compound C12=CC(Cl)=CC=C2NC(=O)C(O)N=C1C1=CC=CC=C1 ADIMAYPTOBDMTL-UHFFFAOYSA-N 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- VOKSWYLNZZRQPF-GDIGMMSISA-N pentazocine Chemical compound C1C2=CC=C(O)C=C2[C@@]2(C)[C@@H](C)[C@@H]1N(CC=C(C)C)CC2 VOKSWYLNZZRQPF-GDIGMMSISA-N 0.000 description 1
- 229960005301 pentazocine Drugs 0.000 description 1
- 229960000482 pethidine Drugs 0.000 description 1
- 229960002508 pindolol Drugs 0.000 description 1
- PHUTUTUABXHXLW-UHFFFAOYSA-N pindolol Chemical compound CC(C)NCC(O)COC1=CC=CC2=NC=C[C]12 PHUTUTUABXHXLW-UHFFFAOYSA-N 0.000 description 1
- 229960002702 piroxicam Drugs 0.000 description 1
- QYSPLQLAKJAUJT-UHFFFAOYSA-N piroxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 QYSPLQLAKJAUJT-UHFFFAOYSA-N 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920006324 polyoxymethylene Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 1
- IENZQIKPVFGBNW-UHFFFAOYSA-N prazosin Chemical compound N=1C(N)=C2C=C(OC)C(OC)=CC2=NC=1N(CC1)CCN1C(=O)C1=CC=CO1 IENZQIKPVFGBNW-UHFFFAOYSA-N 0.000 description 1
- 229960001289 prazosin Drugs 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 229940097325 prolactin Drugs 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- BJOIZNZVOZKDIG-MDEJGZGSSA-N reserpine Chemical compound O([C@H]1[C@@H]([C@H]([C@H]2C[C@@H]3C4=C([C]5C=CC(OC)=CC5=N4)CCN3C[C@H]2C1)C(=O)OC)OC)C(=O)C1=CC(OC)=C(OC)C(OC)=C1 BJOIZNZVOZKDIG-MDEJGZGSSA-N 0.000 description 1
- 229960003147 reserpine Drugs 0.000 description 1
- MDMGHDFNKNZPAU-UHFFFAOYSA-N roserpine Natural products C1C2CN3CCC(C4=CC=C(OC)C=C4N4)=C4C3CC2C(OC(C)=O)C(OC)C1OC(=O)C1=CC(OC)=C(OC)C(OC)=C1 MDMGHDFNKNZPAU-UHFFFAOYSA-N 0.000 description 1
- 229960002052 salbutamol Drugs 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229960002101 secretin Drugs 0.000 description 1
- OWMZNFCDEHGFEP-NFBCVYDUSA-N secretin human Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(N)=O)[C@@H](C)O)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)C1=CC=CC=C1 OWMZNFCDEHGFEP-NFBCVYDUSA-N 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- JGMJQSFLQWGYMQ-UHFFFAOYSA-M sodium;2,6-dichloro-n-phenylaniline;acetate Chemical compound [Na+].CC([O-])=O.ClC1=CC=CC(Cl)=C1NC1=CC=CC=C1 JGMJQSFLQWGYMQ-UHFFFAOYSA-M 0.000 description 1
- NHXLMOGPVYXJNR-ATOGVRKGSA-N somatostatin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CSSC[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N1)[C@@H](C)O)NC(=O)CNC(=O)[C@H](C)N)C(O)=O)=O)[C@H](O)C)C1=CC=CC=C1 NHXLMOGPVYXJNR-ATOGVRKGSA-N 0.000 description 1
- 229960000553 somatostatin Drugs 0.000 description 1
- 210000000434 stratum corneum Anatomy 0.000 description 1
- 230000001839 systemic circulation Effects 0.000 description 1
- 229960000278 theophylline Drugs 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 239000012581 transferrin Substances 0.000 description 1
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
Images
Landscapes
- Electrotherapy Devices (AREA)
Abstract
【課題】従来に比べて、生体への有害作用が低減され、かつ薬物の供給及び送達の効率が良く、かつ取り扱いが容易である、エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法を提供する。
【解決手段】電極支持体113に形成した複数の凹部114に電極112を設け、かつ上記凹部は薬物及び電解質を含む薬剤131を収納するように構成した。よって、上記電極が直接に投与対象物135に接触しないことから、従来に比べて、生体への有害作用が低減することができる。又、薬剤を介して電極からの通電が可能となるので、微小電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行うことができる。
【選択図】図1
【解決手段】電極支持体113に形成した複数の凹部114に電極112を設け、かつ上記凹部は薬物及び電解質を含む薬剤131を収納するように構成した。よって、上記電極が直接に投与対象物135に接触しないことから、従来に比べて、生体への有害作用が低減することができる。又、薬剤を介して電極からの通電が可能となるので、微小電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行うことができる。
【選択図】図1
Description
【0001】
【発明の属する技術分野】
本発明は、皮膚又は粘膜に対し高電圧パルス通電を行うことにより発生する電場を利用して、経皮又は経粘膜的薬物投与を行うための、エレクトロポレーション用薬物投与部、該薬物投与部を備えたエレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法に関する。
【0002】
【従来の技術】
皮膚は、皮膚最外層に存在する角質層に保護されているため外界に対するバリアー機能として作用している。そのため、一般に薬物、特に水溶性薬物の皮膚からの吸収が困難であることが知られている。そのような皮膚を通して薬物吸収を促進する方法として、経皮吸収促進剤、薬物のプロドラッグ化、イオントフォレシスや、超音波等が利用されている。さらには、細胞や組織中にDNAやRNAを入れる遺伝子導入技術であるエレクトロポレーションも利用されている。中でも、エレクトロポレーションは、高電圧パルスを短時間に印加することで脂質二重層膜に小孔を生じさせ新しい透過経路を形成する。エレクトロポレーションは、今までの経皮吸収促進法と異なり、薬物の透過経路を新たに形成するため、幅広い薬物の経皮又は経粘膜的薬物投与法としての可能性がある。
【0003】
本明細書においてエレクトロポレーションを利用した経皮又は経粘膜的薬物投与とは、皮膚又は粘膜上に、薬物溶液やゲル等に製剤化したものを塗布するなどして薬物を供給し、その部位に高電圧のパルスをごく短時間通電することにより、皮膚又は粘膜に小孔を形成し、この小孔を介して薬物を皮膚又は粘膜へ、又は全身循環血中へ移行させことである。
【0004】
エレクトロポレーションに用いられ、上記高電圧パルス印加用の電極の形状は、ほとんど棒状、針状、板状、輪状等であり、これらの電極は、電極を設けた電極設置部材に突設されている。又、陰極と陽極とは区別されて設置されている(例えば、特許文献1〜特許文献4参照。)。
上述の特許文献に開示される電極は、エレクトロポレーションによる薬物透過を効率よく行えるものの、陽極と陰極との間隔が大きいため、通電時に電場が生体の深部まで届き、神経を刺激して痛みや筋肉硬直を生じる可能性が高い。又、電極の極性が固定されており、かつ電極も固定して生体に設置されるため、電極の適用部位は不変である。よって、該適用部位の紅斑や浮腫といった皮膚刺激が生じやすいという欠点がある。
【0005】
このような有害作用を防ぐ目的で、櫛状の陰極と陽極とを狭い間隔で交互に入り組ませた平面状の電極が提案されている(例えば、特許文献5〜特許文献7参照。)。
エレクトロポレーションにより形成される小孔は、主に電極の直下に形成される。又、薬剤が皮膚に接触する面積が大きい方が、薬物が皮膚に吸収される量が多くなる。しかしながら、上記平面状の電極は、皮膚に接置する面積が大きく、薬剤を適用すると電極直下に薬剤が進入できず、薬剤と皮膚との接触面積が減少するだけでなく、形成された小孔を効率よく活用できない。よって結果的に薬物の透過面積が減少しエレクトロポレーションの効率が低下すると考えられる。
【0006】
【特許文献1】
特開平11−290058号公報
【特許文献2】
特開平10−234366号公報
【特許文献3】
特表平11−503349号公報
【特許文献4】
特表平11−506630号公報
【特許文献5】
米国特許第5318514号明細書
【特許文献6】
特表2002−520101号公報
【特許文献7】
特表2002−536133号公報
【0007】
【発明が解決しようとする課題】
上述の各種電極を備えた従来の装置は、いずれも取り扱いが煩雑で、患者自らあるいは介護者が使用することは難しく、臨床的使用には実用的でないと考えられる。さらに、上記従来の装置を用いたエレクトロポレーションにおける薬物供給方法は、溶液あるいはゲル等の製剤を塗布するか、多孔性物質よりなる電極支持部から溶液を浸出させる等にて行われるが、いずれの方法も、目的の薬物透過量に対して非常に過剰な投与量が必要であり、損失が大きいという問題もある。
本発明は、このような問題点を解決するためになされたもので、エレクトロポレーションを利用した経皮又は経粘膜的薬物投与において、従来に比べて、生体への有害作用が低減され、かつ薬物の供給及び送達の効率が良く、かつ取り扱いが容易である、エレクトロポレーション用薬物投与部、該薬物投与部を備えたエレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法を提供することを目的とする。
【0008】
【課題を解決するための手段】
上記目的を達成するため、本発明は以下のように構成する。
即ち、本発明の第1態様のエレクトロポレーション用薬物投与部は、エレクトロポレーションを利用して経皮又は経粘膜的薬物投与を行う電場を発生させる複数の電極と、
それぞれの上記電極を電極設置部に設けた電極支持体であって、上記電極設置部に対向して位置し薬物投与される投与対象物に直接又は間接に接触する接触面を有し、それぞれの上記電極に対応して形成される凹部であって上記接触面から各上記電極へ到達しかつ上記電極への通電による上記投与対象物への薬物投与のための導電性物質を収納する複数の凹部を形成した電極支持体と、
を備えたことを特徴とする。
【0009】
又、上記凹部は、上記接触面における形状が直径5mm以下の円形で深さ5mm以下の円筒状で、隣接する該凹部を10mm以下の間隔にて配置した構成を採ることもできる。
【0010】
又、上記電極は、白金、銀、塩化銀、炭素、塩化銅、又はこれらの合金からなる導電性材料にて構成することもできる。
【0011】
又、上記電極支持体は可塑性、柔軟性,及び可撓性の少なくとも一つ、並びに耐水性を有する材料にて構成することもできる。
【0012】
又、上記接触面に設けられ、上記電極支持体を上記投与対象物に接着させる粘着剤をさらに有する構成を採ることもできる。
【0013】
又、上記電極支持体に形成された上記凹部は、上記導電性物質及び上記薬物を含む薬剤で上記電極への通電により上記投与対象物への通電及び薬物投与を行う薬剤を収納する構成を採ることもできる。
【0014】
又、本発明の第2態様のエレクトロポレーション用薬物投与システムは、第1態様のエレクトロポレーション用薬物投与部と、
上記エレクトロポレーション用薬物投与部に備わるそれぞれの電極に接続され、各電極に対して、極性を変化させながらパルス状に電圧を印加する通電装置と、を備えたことを特徴とする。
【0015】
上記第2態様において、上記通電装置は、それぞれの上記電極における極性をランダムに変化させる制御部と、該制御部と接続されかつ上記パルス状の電圧印加を行う電圧発生部とを有する構成を採ることもできる。
【0016】
上記第2態様において、上記電圧発生部は、1〜1000Vの電圧を、10マイクロ秒〜1000ミリ秒の通電時間で、0.1〜数十回/秒の回数にて、数ミリ〜1000ミリ秒の間隔で、上記パルス状の電圧印加を各電極に対して行う構成を採ることもできる。
【0017】
上記第2態様において、上記エレクトロポレーション用薬物投与部に備わるそれぞれの凹部は、上記通電装置による上記電極への通電前に、投与対象物へ投与される薬物及び電解質を含む薬剤で上記電極への通電により上記投与対象物への通電及び薬物投与を行う薬剤を予め充填している構成を採ることもできる。
【0018】
又、本発明の第3態様のエレクトロポレーション用薬物投与方法は、エレクトロポレーションを利用して経皮又は経粘膜的薬物投与を行うエレクトロポレーション用薬物投与方法において、
電極支持体に形成された複数の凹部におけるそれぞれの底部に上記薬物投与を行う電場を発生させる電極を設け、投与対象物へ投与される薬物及び電解質を含む薬剤を上記凹部に充填したエレクトロポレーション用薬物投与部を上記投与対象物へ貼着し、
それぞれの上記電極における極性を変化させながら、パルス状の電圧を上記電極に印加して上記電場を発生させ、上記経皮又は経粘膜的薬物投与を行う、
ことを特徴とする。
【0019】
上記第3態様において、上記電極への電圧印加は、1〜1000Vの電圧を、10マイクロ秒〜1000ミリ秒の通電時間で、0.1〜数十回/秒の回数にて、数ミリ〜1000ミリ秒の間隔で行うようにすることもできる。
【0020】
【発明の実施の形態】
本発明の実施形態である、エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法について、図を参照しながら以下に詳しく説明する。尚、各図において、同じ構成部分については同じ符号を付している。
【0021】
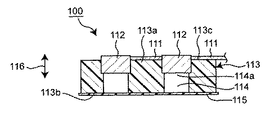
図1及び図2には、本実施形態のエレクトロポレーション用薬物投与部100の一例を示している。エレクトロポレーション用薬物投与部100は、エレクトロポレーションを利用して、薬物の投与対象物に相当する生体例えば人体に対して、経皮又は経粘膜的薬物投与を行う電場を上記人体に発生させる複数の電極112と、電極112を電極設置部113aに設けた電極支持体113とを有し、薬物投与のために上記投与対象物に貼着される部分である。
【0022】
上記電極支持体113は、図2に示すように例えば円形の平面形状にてなる例えば板状の部材であり、一方面側に上記電極設置部113aを、該電極設置部113aに対向する他方面側には上記投与対象物に直接又は間接に接触する接触面113bを有する。勿論、電極支持体113の形状は、このような板状に限定されるものではなく、又、サイズも限定されるものではなく、当該電極支持体113を貼付する投与対象物の場所に応じて任意の形状、例えば円形、楕円、方形等、及びサイズを選択することができる。
【0023】
電極支持体113を形成する材料としては、非イオン伝導性及び電気絶縁性を有する材料であり、さらに、上記接触面113bを投与対象物に接触、好ましくは密着させる必要があることから、可塑性、柔軟性、可撓性、及び形状保持性の少なくとも一つを有し、さらに耐水性を備えた材料にて作製されるのが望ましい。例えば、アクリル、ポリ塩化ビニル、ポリアクリル、ポリアミド、ポリスルホン、ポリスチレン、ポリエステル、ポリオキシメチレン、ポリカーボネート、ポリエステル、及びこれらの素材の共重合体を、電極支持体113の素材として使用できる。勿論、これらの素材に限定されるものではなく、上記性質を有する材料が使用可能である。
又、電極支持体113が上記可塑性、柔軟性、可撓性、及び形状保持性の少なくとも一つを有する材料にて成形されることで、投与対象物の貼着部になじみ易く貼着を容易とすることができる。又、耐水性を有することで、薬剤等により劣化することもない。
【0024】
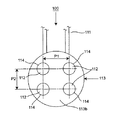
又、電極設置部113aには、本例では、方形の4つの頂点をそれぞれ中心として、円形の電極112を4つ設けている。本例の場合、各電極112は、図示するように、電極支持体113の電極設置面113cに電極112の一部を露出させた形態にて、電極支持体113に埋設されているが、電極112の設置形態はこれに限定されず上記電極設置面113cに例えば印刷等にて形成することもできる。又、各電極112の配列構造について、隣接する電極同士の間隔P1、P2は、略10mm以下又は10mm以下の一定間隔であり、好ましくは下限を3mm、さらに好ましくは1mmとし、上限を5mmとし、さらに好ましくは3mmとする間隔である。尚、このような条件を満たす限り、図示するような格子状の配列に限定するものではない。
電極112を構成する材料としては、銀、塩化銀、白金、炭素、銅、塩化銅、又はこれらの一つを含む合金といった、導電性材料である。好ましくは銀、塩化銀、白金のいずれか、さらに好ましくは白金である。
又、電極設置面113cには、各電極112に接続され各電極112への通電を行う複数の配線111が、例えば印刷等にて形成されている。
【0025】
さらに、電極支持体113には、該電極支持体113の厚み方向116に沿ってそれぞれの電極112に対応して形成され、上記接触面113bから各電極112へ到達する複数の凹部114が形成されている。該凹部114は、上記接触面113bから各電極112へ到達する円筒形状の溝であり、本例では上述のように4つの電極112を設けていることから、凹部114も4つ形成されている。このように各凹部114は、接触面113bに開口し底部114aには電極112が存在するという形態をなす。本例では、接触面113bにおける凹部114は、直径ほぼ5mm以下又は5mm以下、好ましくは3mm、さらに好ましくは1mmの円形であり、上記厚み方向116に沿った接触面113bから電極112までの深さは、ほぼ5mm以下又は5mm以下、好ましくは3mm、さらに好ましくは1mmである。尚、上記深さをほぼ5mmとしたのは、使用上の利便性及び薬剤コストを考慮したものである。尚、凹部114の形状は、本例では電極112に対応して円筒形状であるが、勿論円筒形状に限定されるものではない。
【0026】
このように形成される凹部114は、本実施形態では主に薬物及び電解質を含む薬剤を使用する場合を想定していることから、上記投与対象物へ投与される薬物及び電解質を含む薬剤で電極112への通電により投与対象物への通電を行うと伴に薬物投与を行う薬剤を収納する部分である。尚、上記薬剤は、薬物の投与直前に凹部114へ充填されればよく、当該エレクトロポレーション用薬物投与部100に含まれる必要はない。
【0027】
尚、上記薬剤において上記電解質は必須の構成要素ではない。薬剤に電解質を含まない場合、電極112と投与対象物との導通を取るため、上記凹部は、上記電解質の役割を行う導電性物質を収納する部分となる。又、このように導電性物質を凹部114内に収納したときには、薬剤は、凹部114に収納することなく、皮膚又は粘膜に塗布することになる。尚、上記導電性物質としては、金属以外の物質であり、例えば粘性を有することで凹部114から容易に排出しない物質であり、例えば溶液、ゲル、軟膏、若しくはクリーム状等の物質である。
【0028】
又、上記接触面113bには、当該エレクトロポレーション用薬物投与部100を投与対象物に貼着するときに、貼着を容易にするための接着剤又は粘着剤115を設けることもできる。尚、接着剤又は粘着剤115は、投与対象物への薬物の透過に影響しない材料が使用可能である。
【0029】
上記薬物としては、例えば、中枢性鎮痛薬のモルヒネ、フェンタニル、コデイン、オキシメテバノール、ペチジン、ブプレノルフィン、エプタゾシン、ブトルファノール、ペンタゾシンなどや、非ステロイド系抗炎症薬のサリチル酸、メフェナム酸、ジクロフェナックナトリウム、フェンブフェン、インドメタシン、アセメタシン、イブプロフェン、ケトプロフェン、フルルビプロフェン、ナプロキセン、ピロキシカムなどや、抗不安薬のエチゾラム、クロチアゼパム、フルタゾラム、ロラゼパム、ブロマエパム、オキサゼパム、フルジアゼパム、メキサゾラム、ジアゼパム、メダゼパム、オキサゾラム、フルトプラゼパプ、プラゼパムなどや、抗精神病薬のハロペリドール、クロルプロマジン、ジアゼパム、ニトラゼパムなどや、抗狭心症薬のジゴキシン、ジギタリス、ジギトキシンなどや、抗高血圧薬のクロニジン、レセルピン、プラゾシン、ヒドララジン、ピンドロール、アルプレノロール、インデノロール、アテノロールなどや、気管支拡張薬のエピネフリン、サルブタモール、ツロブテモール、テオフィリン、アミノフィリンなどや、ペプチド類のインスリン、ソマトスタチン、グルカゴン、ガストリン、セクリチン、エンドルフィン、エンケファリン、エンドセリン、コレストキニン、ニューロテンシン、インターフェロン、エリスロポエチン、トランスフェリン、コルチコトロピン、ウロガストロン、プロラクチン、顆粒球刺激因子(G−CSF)、ヒト心房性利尿ペプチド(h−ANP)、副腎皮質ホルモン、黄体形成ホルモン、甲状腺刺激ホルモン、副甲状腺刺激ホルモン、ワクチン類、DNA類などがあるが使用される。尚、薬物は、これらに限らず、経皮吸収あるいは経粘膜吸収できる薬物であれば使用可能である。
【0030】
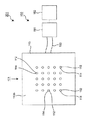
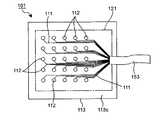
次に、上述したような構造を有するエレクトロポレーション用薬物投与部を備えた、本発明の実施形態におけるエレクトロポレーション用薬物投与システムについて、図3から図5を参照して説明する。尚、該エレクトロポレーション用薬物投与システム201では、上述のエレクトロポレーション用薬物投与部100に比べて電極112の数を増したエレクトロポレーション用薬物投与部101を使用している。又、図4及び図5では、図3に示すエレクトロポレーション用薬物投与部101のみを図示しており、図5はエレクトロポレーション用薬物投与部101の電極設置面113cを見た平面図である。一方、図3に示すエレクトロポレーション用薬物投与部101は、接触面113bを見たときの平面図として図示している。
【0031】
上記エレクトロポレーション用薬物投与システム201は、エレクトロポレーション用薬物投与部101と、エレクトロポレーション用薬物投与部101に備わるそれぞれの電極112に接続され、各電極112に対して、極性を変化させながらパルス状に電圧を印加する通電装置150とを備える。又、エレクトロポレーション用薬物投与部101と通電装置150とはリード線153にて電気的に接続される。又、エレクトロポレーション用薬物投与部101、及び通電装置150を一体化し、柔軟性及び可撓性を有する1枚の板状にて形成することも可能である。
【0032】
エレクトロポレーション用薬物投与部101の基本的構造は、上述したエレクトロポレーション用薬物投与部100と変わるところはなく、上述のように電極112の数が多い点、及び電極支持体113の電極設置面113cに形成されている電極112及び配線111を保護するため、電極設置面113cに保護カバー127を設けた点のみが両者で相違する。よって、ここでの、エレクトロポレーション用薬物投与部101の詳しい構造説明は省略する。
尚、上記保護カバー127は、非イオン伝導性かつ電気絶縁性で可塑性、柔軟性、可撓性、及び自由に形成可能な素材からなり、例えばプラスチック等が採用可能である。
【0033】
上記通電装置150は、エレクトロポレーション用薬物投与部101に備わるそれぞれの電極112における極性を変化させる制御部151と、該制御部151に接続され、上記パルス状の電圧印加を行う電圧発生部152とを有し、単極性パルス及び両極性パルスの少なくとも一方を発生することが可能である。尚、通電装置150の回路構成において、制御部151と電圧発生部152との接続順は、図示するものに限定されず、例えば逆転した形態とすることもできる。
上記制御部151は、電源としての電圧発生部152の電流出力を経時的に制御するマイクロプロセッサを有する。制御部151にて、各電極112における極性を変化、例えばランダムに変化させることで、投与対象物におけるエレクトロポレーションによる局所的な炎症を抑えることができる。本実施形態では、電圧発生部152から各電極112へ電圧を印加する各パルス毎に、各電極112の極性を変化させているが、極性変化の周期はパルス毎に限定されず、例えば数パルス毎等、適宜設定することができる。又、上記「ランダム」とは、各電極112の配置位置、及び極性の変化の周期等を考慮せずに任意に各電極112の極性を設定することを意味するが、電極112の配置位置を考慮しないとき、極端な場合には、一方の領域の電極群は全て正極となり、他方の領域の電極群は全て負極となるような場合も発生する。よって、このような状態の発生を防止するため、隣接する電極112間では異なる極性にするよう、予め制御部151を設定しておいてもよい。
【0034】
上記電圧発生部152には、薄型又は小型の電池を備え、さらに、集積回路やトランジスタ等で構成されたパルス発生回路、及び該パルス発生回路にて発生した出力数Vから十数Vのパルスを最大数百Vに増幅するためのパルス増幅回路が設けられている。又、電圧発生部152には、複数本からなる電極対を任意あるいはランダムに選び出して、選択した電極対にパルスを通電するためのマイクロコンピュータあるいはデジタルスイッチ回路も付設されている。該電圧発生部152によるパルス状の電圧印加は、以下の条件で行われる。即ち、パルス電圧について、下限を1V、好ましくは10V、さらに好ましくは30V、上限を1000V、好ましくは500V、さらに好ましくは200Vとし、パルス通電時間について、下限を10マイクロ秒間、好ましくは100マイクロ秒間、さらに好ましくは10ミリ秒間、上限を1000ミリ秒間、好ましくは500ミリ秒間、さらに好ましくは300ミリ秒間とし、パルス発生回数について、下限を0.1回/秒、好ましくは1回/秒、上限を数十回/秒、好ましくは10回/秒とし、パルス間隔時間について、下限を数ミリ秒間、好ましくは10ミリ秒間、さらに好ましくは100ミリ秒間、上限を数分間、好ましくは100秒間、さらに好ましくは1000ミリ秒間とし、パルス形状について、矩形、指数関数型減衰形、その他の波形を自由に設定できるものとし、好ましくは矩形波を選択する。尚、上述の電圧印加条件では、上限値及び下限値を適宜選択して条件を設定することができる。
【0035】
以上のように構成されるエレクトロポレーション用薬物投与システム201における動作について、即ち、該システム201を用いたエレクトロポレーション用薬物投与方法について以下に説明する。
投与対象物への薬物投与を開始するに当たり、まず、エレクトロポレーション用薬物投与部101の各凹部114に、薬物及び電解質を含み、溶液、ゲル、軟膏、若しくはクリーム状、等にてなる薬剤131を充填する。該充填動作により、薬剤131と電極112とは接触し、通電装置150による電極112への電力供給により薬剤131を介して投与対象物へのエレクトロポレーションが可能となる。尚、上記薬剤131の形態は、上述のゲル等に限定されるものではなく、例えば、凹部114に吸水性材料を詰めておき、該吸水性材料に薬剤131を含ませてもよく、要するに、凹部114内から薬剤131が排出しないような工夫、例えば粘性を調整する等を施した形態を採ることができる。尚、たとえ粘性の小さい薬剤131であっても、凹部114の開口面積を小さくする等により凹部114の容積を小さくすることで、毛細管現象や表面張力により薬剤131を凹部114内に留めることも可能である。
【0036】
尚、本実施形態では上述のように、凹部114に予め薬剤131を充填したが、毛細管現象等により凹部114内へ浸透可能な薬剤131等の場合、該薬剤131を投与対象物へ塗布し、塗布した薬剤131上へエレクトロポレーション用薬物投与部101を貼付してもよい。
【0037】
さらに、薬剤131ではなく金属以外の導電性物質を凹部114に充填したときには、上記導電性物質にて電極112と投与対象物135との導通を図ることができることから、薬剤131又は薬物のみを凹部114に充填する操作は不要となり、薬剤131又は薬物のみは、投与対象物135に塗布することになる。
【0038】
又、投与対象物の対側にある、電極支持体113の電極設置面113cより細いチューブ等を凹部114へ設けて、該チューブ等を通して薬剤131を凹部114へ持続的に補充するようにしてもよい。
【0039】
このように薬剤131を設けたエレクトロポレーション用薬物投与部101の接触面113bに、上記接着剤又は粘着剤115を設けることもできる。勿論、接着剤又は粘着剤115を通して投与対象物への導電性は確保される。
以上の準備を終えたエレクトロポレーション用薬物投与部101は、接触面113bを直接に、又は接着剤又は粘着剤115を介して間接に、投与対象物135、例えば人間の、例えば皮膚に貼着される。該貼着後、通電装置150のスイッチを入れることで、それぞれの電極112には、上述した電圧印加条件にて、パルス状にて電圧が印加され、かつ該パルス状の電圧印加毎に、各電極112における極性が変化される。該通電動作により、凹部114の薬剤131に含まれる薬物が、エレクトロポレーションを利用して、経皮投与される。尚、投与終了後、通電装置150のスイッチを切り、エレクトロポレーション用薬物投与部101を投与対象物135から取り外す。尚、繰り返し薬物を投与するときには、一定時間、投与対象物135にエレクトロポレーション用薬物投与部101を貼着することもできる。
【0040】
エレクトロポレーションによる皮膚刺激を回避するためには、可能な限り高電圧を用いないことや、同じ部位を何度も刺激しないことである。又、神経刺激に対しては、陰極と陽極の間隔を狭くすることや、通電時間を短くすることといった対策を講じることが有効な手段となる。上述した、エレクトロポレーション用薬物投与部100、エレクトロポレーション用薬物投与部101、及びエレクトロポレーション用薬物投与システム201によれば、エレクトロポレーション用薬物投与部100及びエレクトロポレーション用薬物投与部101における接触面113bには複数の凹部114を設け、各凹部114の底部114aに電極112を設け、かつ各凹部114に、薬物及び電解質を含む薬剤131を充填した。したがって、電極112が直接に皮膚等に接触しないことから、皮膚刺激を軽減でき、かつ神経刺激を防ぐことができる。又、薬剤131を介して凹部114の電極112からの通電が可能となることから、又、電場強度は導体端部の半径に反比例することから、凹部114を微小にすることで同じ適用電圧であっても凹部114は微小な電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行える。さらに、本実施形態では、上記凹部114の形状を、直径が5mm以下、奥行きが5mm以下の大きさとしたことで、皮膚刺激の軽減、神経刺激の防止、及び電場強度を高めて高いエレクトロポレーション効率を達成することができる。
【0041】
又、凹部114を多数配列することにより、各凹部114と接触する皮膚の部位面積が大きくなるため、通電強度つまり通電時間及び通電回数を下げることができる。よって、皮膚刺激を軽減できるばかりでなく、より多くの薬物を皮膚及び粘膜に投与することが可能となる。
又、各凹部114の配置間隔を10mm以下としたこと、及び薬剤131を介して電極112と投与対象物との導電を取ることにより、投与対象物135の浅い部分に限定して電場が作用し、神経刺激を防ぐことができる。
さらに、これら多数の電極112の極性を変化、例えばランダムに変化させながら通電することにより、極性の偏りが少なくなり、同じ部位への刺激が減少し、さらに有害作用を軽減することが可能となる。この通電方法は、制御部151に備わるマイクロプロセッサで制御され、電源も極薄あるいは小型の電池を使用しており、又、エレクトロポレーション用薬物投与部100、エレクトロポレーション用薬物投与部101自体、小型、軽量であるため、装置の取り扱いは簡単である。尚、一例として、薬物投与部100又は101におけるサイズは、30mm×30mm、重量は10g以下である。
又、投与対象物135に対する薬物の投与量は、凹部114に充填させる薬剤131の量程度の少量に抑えることができることから、従来のように目的の薬物透過量に対して非常に過剰な投与量を必要とするということもない。又、薬剤131の供給方法は、エレクトロポレーション用薬物投与システム201を使用する前に、皮膚に塗布するか、予め凹部114に充填しておくことができ、容易に行える。
【0042】
以下には、図1及び図2に示すエレクトロポレーション用薬物投与部100及び通電装置150とを用いて行った薬物投与試験について説明する。使用したエレクトロポレーション用薬物投与部100において、電極支持体113は、円形で、アクリルにてなり、方形状の4つの頂点部に形成された4つの凹部114の底部114aのそれぞれに電極112が形成されている。又、凹部114は直径5mmの円形で、接触面113bから電極112までの距離は5mmである。
【0043】
試験例1:
インスリン溶液(14.28mg/mL)を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
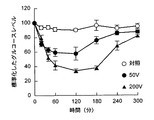
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から印加電圧を50V又は200Vとし、パルス発生回数を1Hzとし、通電時間を200msecとして、矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、グルコース量を測定した。該グルコース量は、エレクトロポレーション適用前のグルコース量で標準化した。その結果を、図6に示す。
エレクトロポレーション適用の場合と未処置の場合とにおけるグルコースレベルを比較すると明らかにエレクトロポレーション処置した方がグルコースレベルの減少が増強した。
【0044】
試験例2:
上述の試験例1に対して、隣接する電極同士の間隔P1、P2を3mmとし、上記通電装置150からの印加電圧を30Vとして試験を行った。その他の条件は、試験例1の場合に同一である。
結果を、図7に示す。電極間距離5mmに比べ3mmの方がグルコースレベルの減少が増強した。
【0045】
試験例3:
5%の塩酸モルヒネ溶液を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から50V、1Hz、200msecの矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、血漿中のモルヒネ量を測定した。その結果を、図8に示す。
エレクトロポレーション適用の場合と未処置の場合とにおける塩酸モルヒネの血中濃度を比較すると、明らかにエレクトロポレーション処置した方が塩酸モルヒネの血漿中濃度が高くなった。
【0046】
試験例4:
5%のインドメタシン溶液を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から50V、1Hz、200msecの矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、血漿中のインドメタシン量を測定した。その結果を、図9に示す。
エレクトロポレーション適用の場合と未処置の場合とにおけるインドメタシンの血中濃度を比較すると、明らかにエレクトロポレーション処置した方がインドメタシンの血漿中濃度が高くなった。
【0047】
試験例5:
5%の塩酸リドカイン溶液を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から50V、1Hz、200msecの矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、血漿中のリドカイン量を測定した。その結果を、図10に示す。
エレクトロポレーション適用の場合と未処置の場合とにおける塩酸リドカインの血中濃度を比較すると、明らかにエレクトロポレーション処置した方が塩酸リドカインの血漿中濃度が高くなった。
【0048】
上述した各試験例の結果から明らかとなるように、電極112間の距離P1、P2を狭くすることで、更なる薬物の経皮、経粘膜吸収を促進することができる。又、薬物の経皮及び経粘膜的吸収は、一般に薬物の吸収面積を大きく、又は吸収部位を多くすることで、吸収量を向上させることができる。
【0049】
【発明の効果】
以上詳述したように本発明の第1態様のエレクトロポレーション用薬物投与部、第2態様のエレクトロポレーション用薬物投与システム、及び第3態様のエレクトロポレーション用薬物投与方法によれば、電極支持体に形成した複数の凹部におけるそれぞれの底部に電極を設け、かつ上記凹部は導電性物質を収納するように構成した。よって、上記電極が直接に投与対象物に接触しないことから、皮膚刺激を軽減でき、かつ投与対象物の浅い部分に限定して電場が作用することから神経刺激を防ぐことができる。よって、従来に比べて、生体への有害作用を低減することができる。又、薬剤を介して凹部の電極からの通電が可能となることから、微小な電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行うことができる。
【0050】
上記凹部を直径5mm以下の円形、深さ5mm以下とし、これらの凹部を10mm以下の間隔で配置することで、上記電極は、さらに、微小電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行うことができる。
【0051】
さらに又、通電装置を設け、電極における極性を変化させ、かつパルス状の電圧を上記電極へ印加するようにしたことから、極性の偏りが少なくなり、投与対象物において同じ部位への刺激が減少し、上記有害作用をさらに軽減することができる。
【0052】
又、薬物の使用量は、凹部に充填される程度の少量でよく、従来のように目的の薬物透過量に対して非常に過剰な薬剤量を必要とするということもなく、効率がよい。又、薬物の供給は、装置の適用前に投与対象物に塗布するか、凹部への充填にて保持させることもでき容易である。又、エレクトロポレーション用薬物投与部及び通電装置が小型、軽量であることや、制御部を用いた通電制御により、装置の取り扱いが簡単である。
【図面の簡単な説明】
【図1】本発明の実施形態におけるエレクトロポレーション用薬物投与部の一例の断面図である。
【図2】図1に示すエレクトロポレーション用薬物投与部の平面図である。
【図3】本発明の実施形態におけるエレクトロポレーション用薬物投与システムの構成を示す図である。
【図4】図3に示すエレクトロポレーション用薬物投与システムに備わるエレクトロポレーション用薬物投与部の断面図である。
【図5】図3に示すエレクトロポレーション用薬物投与システムに備わるエレクトロポレーション用薬物投与部の平面図である。
【図6】図1に示すエレクトロポレーション用薬物投与部を用いたインスリンの経皮吸収におけるエレクトロポレーション後のグルコースレベルの時間変化を示すグラフである。
【図7】図6の場合と試験条件を変更した場合におけるグルコースレベルの変化を示すグラフである。
【図8】図1に示すエレクトロポレーション用薬物投与部を用いた塩酸モルヒネの経皮吸収におけるエレクトロポレーション後の血漿中濃度の時間変化を示すグラフである。
【図9】図1に示すエレクトロポレーション用薬物投与部を用いたインドメタシンの経皮吸収におけるエレクトロポレーション後の血漿中濃度の時間変化を示すグラフである。
【図10】図1に示すエレクトロポレーション用薬物投与部を用いた塩酸リドカインの経皮吸収におけるエレクトロポレーション後の血漿中濃度の時間変化を示すグラフである。
【符号の説明】
100、101…エレクトロポレーション用薬物投与部、
112…電極、113…電極支持体、113a…電極設置部、
113b…接触面、114…凹部、115…粘着剤、131…薬剤、
135…投与対象物、150…通電装置、151…制御部、
152…電圧発生部、201…エレクトロポレーション用薬物投与システム。
【発明の属する技術分野】
本発明は、皮膚又は粘膜に対し高電圧パルス通電を行うことにより発生する電場を利用して、経皮又は経粘膜的薬物投与を行うための、エレクトロポレーション用薬物投与部、該薬物投与部を備えたエレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法に関する。
【0002】
【従来の技術】
皮膚は、皮膚最外層に存在する角質層に保護されているため外界に対するバリアー機能として作用している。そのため、一般に薬物、特に水溶性薬物の皮膚からの吸収が困難であることが知られている。そのような皮膚を通して薬物吸収を促進する方法として、経皮吸収促進剤、薬物のプロドラッグ化、イオントフォレシスや、超音波等が利用されている。さらには、細胞や組織中にDNAやRNAを入れる遺伝子導入技術であるエレクトロポレーションも利用されている。中でも、エレクトロポレーションは、高電圧パルスを短時間に印加することで脂質二重層膜に小孔を生じさせ新しい透過経路を形成する。エレクトロポレーションは、今までの経皮吸収促進法と異なり、薬物の透過経路を新たに形成するため、幅広い薬物の経皮又は経粘膜的薬物投与法としての可能性がある。
【0003】
本明細書においてエレクトロポレーションを利用した経皮又は経粘膜的薬物投与とは、皮膚又は粘膜上に、薬物溶液やゲル等に製剤化したものを塗布するなどして薬物を供給し、その部位に高電圧のパルスをごく短時間通電することにより、皮膚又は粘膜に小孔を形成し、この小孔を介して薬物を皮膚又は粘膜へ、又は全身循環血中へ移行させことである。
【0004】
エレクトロポレーションに用いられ、上記高電圧パルス印加用の電極の形状は、ほとんど棒状、針状、板状、輪状等であり、これらの電極は、電極を設けた電極設置部材に突設されている。又、陰極と陽極とは区別されて設置されている(例えば、特許文献1〜特許文献4参照。)。
上述の特許文献に開示される電極は、エレクトロポレーションによる薬物透過を効率よく行えるものの、陽極と陰極との間隔が大きいため、通電時に電場が生体の深部まで届き、神経を刺激して痛みや筋肉硬直を生じる可能性が高い。又、電極の極性が固定されており、かつ電極も固定して生体に設置されるため、電極の適用部位は不変である。よって、該適用部位の紅斑や浮腫といった皮膚刺激が生じやすいという欠点がある。
【0005】
このような有害作用を防ぐ目的で、櫛状の陰極と陽極とを狭い間隔で交互に入り組ませた平面状の電極が提案されている(例えば、特許文献5〜特許文献7参照。)。
エレクトロポレーションにより形成される小孔は、主に電極の直下に形成される。又、薬剤が皮膚に接触する面積が大きい方が、薬物が皮膚に吸収される量が多くなる。しかしながら、上記平面状の電極は、皮膚に接置する面積が大きく、薬剤を適用すると電極直下に薬剤が進入できず、薬剤と皮膚との接触面積が減少するだけでなく、形成された小孔を効率よく活用できない。よって結果的に薬物の透過面積が減少しエレクトロポレーションの効率が低下すると考えられる。
【0006】
【特許文献1】
特開平11−290058号公報
【特許文献2】
特開平10−234366号公報
【特許文献3】
特表平11−503349号公報
【特許文献4】
特表平11−506630号公報
【特許文献5】
米国特許第5318514号明細書
【特許文献6】
特表2002−520101号公報
【特許文献7】
特表2002−536133号公報
【0007】
【発明が解決しようとする課題】
上述の各種電極を備えた従来の装置は、いずれも取り扱いが煩雑で、患者自らあるいは介護者が使用することは難しく、臨床的使用には実用的でないと考えられる。さらに、上記従来の装置を用いたエレクトロポレーションにおける薬物供給方法は、溶液あるいはゲル等の製剤を塗布するか、多孔性物質よりなる電極支持部から溶液を浸出させる等にて行われるが、いずれの方法も、目的の薬物透過量に対して非常に過剰な投与量が必要であり、損失が大きいという問題もある。
本発明は、このような問題点を解決するためになされたもので、エレクトロポレーションを利用した経皮又は経粘膜的薬物投与において、従来に比べて、生体への有害作用が低減され、かつ薬物の供給及び送達の効率が良く、かつ取り扱いが容易である、エレクトロポレーション用薬物投与部、該薬物投与部を備えたエレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法を提供することを目的とする。
【0008】
【課題を解決するための手段】
上記目的を達成するため、本発明は以下のように構成する。
即ち、本発明の第1態様のエレクトロポレーション用薬物投与部は、エレクトロポレーションを利用して経皮又は経粘膜的薬物投与を行う電場を発生させる複数の電極と、
それぞれの上記電極を電極設置部に設けた電極支持体であって、上記電極設置部に対向して位置し薬物投与される投与対象物に直接又は間接に接触する接触面を有し、それぞれの上記電極に対応して形成される凹部であって上記接触面から各上記電極へ到達しかつ上記電極への通電による上記投与対象物への薬物投与のための導電性物質を収納する複数の凹部を形成した電極支持体と、
を備えたことを特徴とする。
【0009】
又、上記凹部は、上記接触面における形状が直径5mm以下の円形で深さ5mm以下の円筒状で、隣接する該凹部を10mm以下の間隔にて配置した構成を採ることもできる。
【0010】
又、上記電極は、白金、銀、塩化銀、炭素、塩化銅、又はこれらの合金からなる導電性材料にて構成することもできる。
【0011】
又、上記電極支持体は可塑性、柔軟性,及び可撓性の少なくとも一つ、並びに耐水性を有する材料にて構成することもできる。
【0012】
又、上記接触面に設けられ、上記電極支持体を上記投与対象物に接着させる粘着剤をさらに有する構成を採ることもできる。
【0013】
又、上記電極支持体に形成された上記凹部は、上記導電性物質及び上記薬物を含む薬剤で上記電極への通電により上記投与対象物への通電及び薬物投与を行う薬剤を収納する構成を採ることもできる。
【0014】
又、本発明の第2態様のエレクトロポレーション用薬物投与システムは、第1態様のエレクトロポレーション用薬物投与部と、
上記エレクトロポレーション用薬物投与部に備わるそれぞれの電極に接続され、各電極に対して、極性を変化させながらパルス状に電圧を印加する通電装置と、を備えたことを特徴とする。
【0015】
上記第2態様において、上記通電装置は、それぞれの上記電極における極性をランダムに変化させる制御部と、該制御部と接続されかつ上記パルス状の電圧印加を行う電圧発生部とを有する構成を採ることもできる。
【0016】
上記第2態様において、上記電圧発生部は、1〜1000Vの電圧を、10マイクロ秒〜1000ミリ秒の通電時間で、0.1〜数十回/秒の回数にて、数ミリ〜1000ミリ秒の間隔で、上記パルス状の電圧印加を各電極に対して行う構成を採ることもできる。
【0017】
上記第2態様において、上記エレクトロポレーション用薬物投与部に備わるそれぞれの凹部は、上記通電装置による上記電極への通電前に、投与対象物へ投与される薬物及び電解質を含む薬剤で上記電極への通電により上記投与対象物への通電及び薬物投与を行う薬剤を予め充填している構成を採ることもできる。
【0018】
又、本発明の第3態様のエレクトロポレーション用薬物投与方法は、エレクトロポレーションを利用して経皮又は経粘膜的薬物投与を行うエレクトロポレーション用薬物投与方法において、
電極支持体に形成された複数の凹部におけるそれぞれの底部に上記薬物投与を行う電場を発生させる電極を設け、投与対象物へ投与される薬物及び電解質を含む薬剤を上記凹部に充填したエレクトロポレーション用薬物投与部を上記投与対象物へ貼着し、
それぞれの上記電極における極性を変化させながら、パルス状の電圧を上記電極に印加して上記電場を発生させ、上記経皮又は経粘膜的薬物投与を行う、
ことを特徴とする。
【0019】
上記第3態様において、上記電極への電圧印加は、1〜1000Vの電圧を、10マイクロ秒〜1000ミリ秒の通電時間で、0.1〜数十回/秒の回数にて、数ミリ〜1000ミリ秒の間隔で行うようにすることもできる。
【0020】
【発明の実施の形態】
本発明の実施形態である、エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法について、図を参照しながら以下に詳しく説明する。尚、各図において、同じ構成部分については同じ符号を付している。
【0021】
図1及び図2には、本実施形態のエレクトロポレーション用薬物投与部100の一例を示している。エレクトロポレーション用薬物投与部100は、エレクトロポレーションを利用して、薬物の投与対象物に相当する生体例えば人体に対して、経皮又は経粘膜的薬物投与を行う電場を上記人体に発生させる複数の電極112と、電極112を電極設置部113aに設けた電極支持体113とを有し、薬物投与のために上記投与対象物に貼着される部分である。
【0022】
上記電極支持体113は、図2に示すように例えば円形の平面形状にてなる例えば板状の部材であり、一方面側に上記電極設置部113aを、該電極設置部113aに対向する他方面側には上記投与対象物に直接又は間接に接触する接触面113bを有する。勿論、電極支持体113の形状は、このような板状に限定されるものではなく、又、サイズも限定されるものではなく、当該電極支持体113を貼付する投与対象物の場所に応じて任意の形状、例えば円形、楕円、方形等、及びサイズを選択することができる。
【0023】
電極支持体113を形成する材料としては、非イオン伝導性及び電気絶縁性を有する材料であり、さらに、上記接触面113bを投与対象物に接触、好ましくは密着させる必要があることから、可塑性、柔軟性、可撓性、及び形状保持性の少なくとも一つを有し、さらに耐水性を備えた材料にて作製されるのが望ましい。例えば、アクリル、ポリ塩化ビニル、ポリアクリル、ポリアミド、ポリスルホン、ポリスチレン、ポリエステル、ポリオキシメチレン、ポリカーボネート、ポリエステル、及びこれらの素材の共重合体を、電極支持体113の素材として使用できる。勿論、これらの素材に限定されるものではなく、上記性質を有する材料が使用可能である。
又、電極支持体113が上記可塑性、柔軟性、可撓性、及び形状保持性の少なくとも一つを有する材料にて成形されることで、投与対象物の貼着部になじみ易く貼着を容易とすることができる。又、耐水性を有することで、薬剤等により劣化することもない。
【0024】
又、電極設置部113aには、本例では、方形の4つの頂点をそれぞれ中心として、円形の電極112を4つ設けている。本例の場合、各電極112は、図示するように、電極支持体113の電極設置面113cに電極112の一部を露出させた形態にて、電極支持体113に埋設されているが、電極112の設置形態はこれに限定されず上記電極設置面113cに例えば印刷等にて形成することもできる。又、各電極112の配列構造について、隣接する電極同士の間隔P1、P2は、略10mm以下又は10mm以下の一定間隔であり、好ましくは下限を3mm、さらに好ましくは1mmとし、上限を5mmとし、さらに好ましくは3mmとする間隔である。尚、このような条件を満たす限り、図示するような格子状の配列に限定するものではない。
電極112を構成する材料としては、銀、塩化銀、白金、炭素、銅、塩化銅、又はこれらの一つを含む合金といった、導電性材料である。好ましくは銀、塩化銀、白金のいずれか、さらに好ましくは白金である。
又、電極設置面113cには、各電極112に接続され各電極112への通電を行う複数の配線111が、例えば印刷等にて形成されている。
【0025】
さらに、電極支持体113には、該電極支持体113の厚み方向116に沿ってそれぞれの電極112に対応して形成され、上記接触面113bから各電極112へ到達する複数の凹部114が形成されている。該凹部114は、上記接触面113bから各電極112へ到達する円筒形状の溝であり、本例では上述のように4つの電極112を設けていることから、凹部114も4つ形成されている。このように各凹部114は、接触面113bに開口し底部114aには電極112が存在するという形態をなす。本例では、接触面113bにおける凹部114は、直径ほぼ5mm以下又は5mm以下、好ましくは3mm、さらに好ましくは1mmの円形であり、上記厚み方向116に沿った接触面113bから電極112までの深さは、ほぼ5mm以下又は5mm以下、好ましくは3mm、さらに好ましくは1mmである。尚、上記深さをほぼ5mmとしたのは、使用上の利便性及び薬剤コストを考慮したものである。尚、凹部114の形状は、本例では電極112に対応して円筒形状であるが、勿論円筒形状に限定されるものではない。
【0026】
このように形成される凹部114は、本実施形態では主に薬物及び電解質を含む薬剤を使用する場合を想定していることから、上記投与対象物へ投与される薬物及び電解質を含む薬剤で電極112への通電により投与対象物への通電を行うと伴に薬物投与を行う薬剤を収納する部分である。尚、上記薬剤は、薬物の投与直前に凹部114へ充填されればよく、当該エレクトロポレーション用薬物投与部100に含まれる必要はない。
【0027】
尚、上記薬剤において上記電解質は必須の構成要素ではない。薬剤に電解質を含まない場合、電極112と投与対象物との導通を取るため、上記凹部は、上記電解質の役割を行う導電性物質を収納する部分となる。又、このように導電性物質を凹部114内に収納したときには、薬剤は、凹部114に収納することなく、皮膚又は粘膜に塗布することになる。尚、上記導電性物質としては、金属以外の物質であり、例えば粘性を有することで凹部114から容易に排出しない物質であり、例えば溶液、ゲル、軟膏、若しくはクリーム状等の物質である。
【0028】
又、上記接触面113bには、当該エレクトロポレーション用薬物投与部100を投与対象物に貼着するときに、貼着を容易にするための接着剤又は粘着剤115を設けることもできる。尚、接着剤又は粘着剤115は、投与対象物への薬物の透過に影響しない材料が使用可能である。
【0029】
上記薬物としては、例えば、中枢性鎮痛薬のモルヒネ、フェンタニル、コデイン、オキシメテバノール、ペチジン、ブプレノルフィン、エプタゾシン、ブトルファノール、ペンタゾシンなどや、非ステロイド系抗炎症薬のサリチル酸、メフェナム酸、ジクロフェナックナトリウム、フェンブフェン、インドメタシン、アセメタシン、イブプロフェン、ケトプロフェン、フルルビプロフェン、ナプロキセン、ピロキシカムなどや、抗不安薬のエチゾラム、クロチアゼパム、フルタゾラム、ロラゼパム、ブロマエパム、オキサゼパム、フルジアゼパム、メキサゾラム、ジアゼパム、メダゼパム、オキサゾラム、フルトプラゼパプ、プラゼパムなどや、抗精神病薬のハロペリドール、クロルプロマジン、ジアゼパム、ニトラゼパムなどや、抗狭心症薬のジゴキシン、ジギタリス、ジギトキシンなどや、抗高血圧薬のクロニジン、レセルピン、プラゾシン、ヒドララジン、ピンドロール、アルプレノロール、インデノロール、アテノロールなどや、気管支拡張薬のエピネフリン、サルブタモール、ツロブテモール、テオフィリン、アミノフィリンなどや、ペプチド類のインスリン、ソマトスタチン、グルカゴン、ガストリン、セクリチン、エンドルフィン、エンケファリン、エンドセリン、コレストキニン、ニューロテンシン、インターフェロン、エリスロポエチン、トランスフェリン、コルチコトロピン、ウロガストロン、プロラクチン、顆粒球刺激因子(G−CSF)、ヒト心房性利尿ペプチド(h−ANP)、副腎皮質ホルモン、黄体形成ホルモン、甲状腺刺激ホルモン、副甲状腺刺激ホルモン、ワクチン類、DNA類などがあるが使用される。尚、薬物は、これらに限らず、経皮吸収あるいは経粘膜吸収できる薬物であれば使用可能である。
【0030】
次に、上述したような構造を有するエレクトロポレーション用薬物投与部を備えた、本発明の実施形態におけるエレクトロポレーション用薬物投与システムについて、図3から図5を参照して説明する。尚、該エレクトロポレーション用薬物投与システム201では、上述のエレクトロポレーション用薬物投与部100に比べて電極112の数を増したエレクトロポレーション用薬物投与部101を使用している。又、図4及び図5では、図3に示すエレクトロポレーション用薬物投与部101のみを図示しており、図5はエレクトロポレーション用薬物投与部101の電極設置面113cを見た平面図である。一方、図3に示すエレクトロポレーション用薬物投与部101は、接触面113bを見たときの平面図として図示している。
【0031】
上記エレクトロポレーション用薬物投与システム201は、エレクトロポレーション用薬物投与部101と、エレクトロポレーション用薬物投与部101に備わるそれぞれの電極112に接続され、各電極112に対して、極性を変化させながらパルス状に電圧を印加する通電装置150とを備える。又、エレクトロポレーション用薬物投与部101と通電装置150とはリード線153にて電気的に接続される。又、エレクトロポレーション用薬物投与部101、及び通電装置150を一体化し、柔軟性及び可撓性を有する1枚の板状にて形成することも可能である。
【0032】
エレクトロポレーション用薬物投与部101の基本的構造は、上述したエレクトロポレーション用薬物投与部100と変わるところはなく、上述のように電極112の数が多い点、及び電極支持体113の電極設置面113cに形成されている電極112及び配線111を保護するため、電極設置面113cに保護カバー127を設けた点のみが両者で相違する。よって、ここでの、エレクトロポレーション用薬物投与部101の詳しい構造説明は省略する。
尚、上記保護カバー127は、非イオン伝導性かつ電気絶縁性で可塑性、柔軟性、可撓性、及び自由に形成可能な素材からなり、例えばプラスチック等が採用可能である。
【0033】
上記通電装置150は、エレクトロポレーション用薬物投与部101に備わるそれぞれの電極112における極性を変化させる制御部151と、該制御部151に接続され、上記パルス状の電圧印加を行う電圧発生部152とを有し、単極性パルス及び両極性パルスの少なくとも一方を発生することが可能である。尚、通電装置150の回路構成において、制御部151と電圧発生部152との接続順は、図示するものに限定されず、例えば逆転した形態とすることもできる。
上記制御部151は、電源としての電圧発生部152の電流出力を経時的に制御するマイクロプロセッサを有する。制御部151にて、各電極112における極性を変化、例えばランダムに変化させることで、投与対象物におけるエレクトロポレーションによる局所的な炎症を抑えることができる。本実施形態では、電圧発生部152から各電極112へ電圧を印加する各パルス毎に、各電極112の極性を変化させているが、極性変化の周期はパルス毎に限定されず、例えば数パルス毎等、適宜設定することができる。又、上記「ランダム」とは、各電極112の配置位置、及び極性の変化の周期等を考慮せずに任意に各電極112の極性を設定することを意味するが、電極112の配置位置を考慮しないとき、極端な場合には、一方の領域の電極群は全て正極となり、他方の領域の電極群は全て負極となるような場合も発生する。よって、このような状態の発生を防止するため、隣接する電極112間では異なる極性にするよう、予め制御部151を設定しておいてもよい。
【0034】
上記電圧発生部152には、薄型又は小型の電池を備え、さらに、集積回路やトランジスタ等で構成されたパルス発生回路、及び該パルス発生回路にて発生した出力数Vから十数Vのパルスを最大数百Vに増幅するためのパルス増幅回路が設けられている。又、電圧発生部152には、複数本からなる電極対を任意あるいはランダムに選び出して、選択した電極対にパルスを通電するためのマイクロコンピュータあるいはデジタルスイッチ回路も付設されている。該電圧発生部152によるパルス状の電圧印加は、以下の条件で行われる。即ち、パルス電圧について、下限を1V、好ましくは10V、さらに好ましくは30V、上限を1000V、好ましくは500V、さらに好ましくは200Vとし、パルス通電時間について、下限を10マイクロ秒間、好ましくは100マイクロ秒間、さらに好ましくは10ミリ秒間、上限を1000ミリ秒間、好ましくは500ミリ秒間、さらに好ましくは300ミリ秒間とし、パルス発生回数について、下限を0.1回/秒、好ましくは1回/秒、上限を数十回/秒、好ましくは10回/秒とし、パルス間隔時間について、下限を数ミリ秒間、好ましくは10ミリ秒間、さらに好ましくは100ミリ秒間、上限を数分間、好ましくは100秒間、さらに好ましくは1000ミリ秒間とし、パルス形状について、矩形、指数関数型減衰形、その他の波形を自由に設定できるものとし、好ましくは矩形波を選択する。尚、上述の電圧印加条件では、上限値及び下限値を適宜選択して条件を設定することができる。
【0035】
以上のように構成されるエレクトロポレーション用薬物投与システム201における動作について、即ち、該システム201を用いたエレクトロポレーション用薬物投与方法について以下に説明する。
投与対象物への薬物投与を開始するに当たり、まず、エレクトロポレーション用薬物投与部101の各凹部114に、薬物及び電解質を含み、溶液、ゲル、軟膏、若しくはクリーム状、等にてなる薬剤131を充填する。該充填動作により、薬剤131と電極112とは接触し、通電装置150による電極112への電力供給により薬剤131を介して投与対象物へのエレクトロポレーションが可能となる。尚、上記薬剤131の形態は、上述のゲル等に限定されるものではなく、例えば、凹部114に吸水性材料を詰めておき、該吸水性材料に薬剤131を含ませてもよく、要するに、凹部114内から薬剤131が排出しないような工夫、例えば粘性を調整する等を施した形態を採ることができる。尚、たとえ粘性の小さい薬剤131であっても、凹部114の開口面積を小さくする等により凹部114の容積を小さくすることで、毛細管現象や表面張力により薬剤131を凹部114内に留めることも可能である。
【0036】
尚、本実施形態では上述のように、凹部114に予め薬剤131を充填したが、毛細管現象等により凹部114内へ浸透可能な薬剤131等の場合、該薬剤131を投与対象物へ塗布し、塗布した薬剤131上へエレクトロポレーション用薬物投与部101を貼付してもよい。
【0037】
さらに、薬剤131ではなく金属以外の導電性物質を凹部114に充填したときには、上記導電性物質にて電極112と投与対象物135との導通を図ることができることから、薬剤131又は薬物のみを凹部114に充填する操作は不要となり、薬剤131又は薬物のみは、投与対象物135に塗布することになる。
【0038】
又、投与対象物の対側にある、電極支持体113の電極設置面113cより細いチューブ等を凹部114へ設けて、該チューブ等を通して薬剤131を凹部114へ持続的に補充するようにしてもよい。
【0039】
このように薬剤131を設けたエレクトロポレーション用薬物投与部101の接触面113bに、上記接着剤又は粘着剤115を設けることもできる。勿論、接着剤又は粘着剤115を通して投与対象物への導電性は確保される。
以上の準備を終えたエレクトロポレーション用薬物投与部101は、接触面113bを直接に、又は接着剤又は粘着剤115を介して間接に、投与対象物135、例えば人間の、例えば皮膚に貼着される。該貼着後、通電装置150のスイッチを入れることで、それぞれの電極112には、上述した電圧印加条件にて、パルス状にて電圧が印加され、かつ該パルス状の電圧印加毎に、各電極112における極性が変化される。該通電動作により、凹部114の薬剤131に含まれる薬物が、エレクトロポレーションを利用して、経皮投与される。尚、投与終了後、通電装置150のスイッチを切り、エレクトロポレーション用薬物投与部101を投与対象物135から取り外す。尚、繰り返し薬物を投与するときには、一定時間、投与対象物135にエレクトロポレーション用薬物投与部101を貼着することもできる。
【0040】
エレクトロポレーションによる皮膚刺激を回避するためには、可能な限り高電圧を用いないことや、同じ部位を何度も刺激しないことである。又、神経刺激に対しては、陰極と陽極の間隔を狭くすることや、通電時間を短くすることといった対策を講じることが有効な手段となる。上述した、エレクトロポレーション用薬物投与部100、エレクトロポレーション用薬物投与部101、及びエレクトロポレーション用薬物投与システム201によれば、エレクトロポレーション用薬物投与部100及びエレクトロポレーション用薬物投与部101における接触面113bには複数の凹部114を設け、各凹部114の底部114aに電極112を設け、かつ各凹部114に、薬物及び電解質を含む薬剤131を充填した。したがって、電極112が直接に皮膚等に接触しないことから、皮膚刺激を軽減でき、かつ神経刺激を防ぐことができる。又、薬剤131を介して凹部114の電極112からの通電が可能となることから、又、電場強度は導体端部の半径に反比例することから、凹部114を微小にすることで同じ適用電圧であっても凹部114は微小な電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行える。さらに、本実施形態では、上記凹部114の形状を、直径が5mm以下、奥行きが5mm以下の大きさとしたことで、皮膚刺激の軽減、神経刺激の防止、及び電場強度を高めて高いエレクトロポレーション効率を達成することができる。
【0041】
又、凹部114を多数配列することにより、各凹部114と接触する皮膚の部位面積が大きくなるため、通電強度つまり通電時間及び通電回数を下げることができる。よって、皮膚刺激を軽減できるばかりでなく、より多くの薬物を皮膚及び粘膜に投与することが可能となる。
又、各凹部114の配置間隔を10mm以下としたこと、及び薬剤131を介して電極112と投与対象物との導電を取ることにより、投与対象物135の浅い部分に限定して電場が作用し、神経刺激を防ぐことができる。
さらに、これら多数の電極112の極性を変化、例えばランダムに変化させながら通電することにより、極性の偏りが少なくなり、同じ部位への刺激が減少し、さらに有害作用を軽減することが可能となる。この通電方法は、制御部151に備わるマイクロプロセッサで制御され、電源も極薄あるいは小型の電池を使用しており、又、エレクトロポレーション用薬物投与部100、エレクトロポレーション用薬物投与部101自体、小型、軽量であるため、装置の取り扱いは簡単である。尚、一例として、薬物投与部100又は101におけるサイズは、30mm×30mm、重量は10g以下である。
又、投与対象物135に対する薬物の投与量は、凹部114に充填させる薬剤131の量程度の少量に抑えることができることから、従来のように目的の薬物透過量に対して非常に過剰な投与量を必要とするということもない。又、薬剤131の供給方法は、エレクトロポレーション用薬物投与システム201を使用する前に、皮膚に塗布するか、予め凹部114に充填しておくことができ、容易に行える。
【0042】
以下には、図1及び図2に示すエレクトロポレーション用薬物投与部100及び通電装置150とを用いて行った薬物投与試験について説明する。使用したエレクトロポレーション用薬物投与部100において、電極支持体113は、円形で、アクリルにてなり、方形状の4つの頂点部に形成された4つの凹部114の底部114aのそれぞれに電極112が形成されている。又、凹部114は直径5mmの円形で、接触面113bから電極112までの距離は5mmである。
【0043】
試験例1:
インスリン溶液(14.28mg/mL)を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から印加電圧を50V又は200Vとし、パルス発生回数を1Hzとし、通電時間を200msecとして、矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、グルコース量を測定した。該グルコース量は、エレクトロポレーション適用前のグルコース量で標準化した。その結果を、図6に示す。
エレクトロポレーション適用の場合と未処置の場合とにおけるグルコースレベルを比較すると明らかにエレクトロポレーション処置した方がグルコースレベルの減少が増強した。
【0044】
試験例2:
上述の試験例1に対して、隣接する電極同士の間隔P1、P2を3mmとし、上記通電装置150からの印加電圧を30Vとして試験を行った。その他の条件は、試験例1の場合に同一である。
結果を、図7に示す。電極間距離5mmに比べ3mmの方がグルコースレベルの減少が増強した。
【0045】
試験例3:
5%の塩酸モルヒネ溶液を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から50V、1Hz、200msecの矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、血漿中のモルヒネ量を測定した。その結果を、図8に示す。
エレクトロポレーション適用の場合と未処置の場合とにおける塩酸モルヒネの血中濃度を比較すると、明らかにエレクトロポレーション処置した方が塩酸モルヒネの血漿中濃度が高くなった。
【0046】
試験例4:
5%のインドメタシン溶液を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から50V、1Hz、200msecの矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、血漿中のインドメタシン量を測定した。その結果を、図9に示す。
エレクトロポレーション適用の場合と未処置の場合とにおけるインドメタシンの血中濃度を比較すると、明らかにエレクトロポレーション処置した方がインドメタシンの血漿中濃度が高くなった。
【0047】
試験例5:
5%の塩酸リドカイン溶液を含んだ薬剤131を各凹部114に充填した。ここでは、隣接する電極同士の間隔P1、P2は、5mmである。
このようなエレクトロポレーション用薬物投与部100を、2kgの白色ウサギの耳の外耳側を除毛後、動脈上に接触させた。そして、上記通電装置150から50V、1Hz、200msecの矩形パルスの印加を1分間隔で10分間行い、さらに、この操作を20分ごとに3回繰り返した。各測定時間毎に、エレクトロポレーション用薬物投与部100を貼付した耳とは反対側の耳の静脈から採血を行い、血漿中のリドカイン量を測定した。その結果を、図10に示す。
エレクトロポレーション適用の場合と未処置の場合とにおける塩酸リドカインの血中濃度を比較すると、明らかにエレクトロポレーション処置した方が塩酸リドカインの血漿中濃度が高くなった。
【0048】
上述した各試験例の結果から明らかとなるように、電極112間の距離P1、P2を狭くすることで、更なる薬物の経皮、経粘膜吸収を促進することができる。又、薬物の経皮及び経粘膜的吸収は、一般に薬物の吸収面積を大きく、又は吸収部位を多くすることで、吸収量を向上させることができる。
【0049】
【発明の効果】
以上詳述したように本発明の第1態様のエレクトロポレーション用薬物投与部、第2態様のエレクトロポレーション用薬物投与システム、及び第3態様のエレクトロポレーション用薬物投与方法によれば、電極支持体に形成した複数の凹部におけるそれぞれの底部に電極を設け、かつ上記凹部は導電性物質を収納するように構成した。よって、上記電極が直接に投与対象物に接触しないことから、皮膚刺激を軽減でき、かつ投与対象物の浅い部分に限定して電場が作用することから神経刺激を防ぐことができる。よって、従来に比べて、生体への有害作用を低減することができる。又、薬剤を介して凹部の電極からの通電が可能となることから、微小な電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行うことができる。
【0050】
上記凹部を直径5mm以下の円形、深さ5mm以下とし、これらの凹部を10mm以下の間隔で配置することで、上記電極は、さらに、微小電極として働き、電場強度を高めることができエレクトロポレーションを効率よく行うことができる。
【0051】
さらに又、通電装置を設け、電極における極性を変化させ、かつパルス状の電圧を上記電極へ印加するようにしたことから、極性の偏りが少なくなり、投与対象物において同じ部位への刺激が減少し、上記有害作用をさらに軽減することができる。
【0052】
又、薬物の使用量は、凹部に充填される程度の少量でよく、従来のように目的の薬物透過量に対して非常に過剰な薬剤量を必要とするということもなく、効率がよい。又、薬物の供給は、装置の適用前に投与対象物に塗布するか、凹部への充填にて保持させることもでき容易である。又、エレクトロポレーション用薬物投与部及び通電装置が小型、軽量であることや、制御部を用いた通電制御により、装置の取り扱いが簡単である。
【図面の簡単な説明】
【図1】本発明の実施形態におけるエレクトロポレーション用薬物投与部の一例の断面図である。
【図2】図1に示すエレクトロポレーション用薬物投与部の平面図である。
【図3】本発明の実施形態におけるエレクトロポレーション用薬物投与システムの構成を示す図である。
【図4】図3に示すエレクトロポレーション用薬物投与システムに備わるエレクトロポレーション用薬物投与部の断面図である。
【図5】図3に示すエレクトロポレーション用薬物投与システムに備わるエレクトロポレーション用薬物投与部の平面図である。
【図6】図1に示すエレクトロポレーション用薬物投与部を用いたインスリンの経皮吸収におけるエレクトロポレーション後のグルコースレベルの時間変化を示すグラフである。
【図7】図6の場合と試験条件を変更した場合におけるグルコースレベルの変化を示すグラフである。
【図8】図1に示すエレクトロポレーション用薬物投与部を用いた塩酸モルヒネの経皮吸収におけるエレクトロポレーション後の血漿中濃度の時間変化を示すグラフである。
【図9】図1に示すエレクトロポレーション用薬物投与部を用いたインドメタシンの経皮吸収におけるエレクトロポレーション後の血漿中濃度の時間変化を示すグラフである。
【図10】図1に示すエレクトロポレーション用薬物投与部を用いた塩酸リドカインの経皮吸収におけるエレクトロポレーション後の血漿中濃度の時間変化を示すグラフである。
【符号の説明】
100、101…エレクトロポレーション用薬物投与部、
112…電極、113…電極支持体、113a…電極設置部、
113b…接触面、114…凹部、115…粘着剤、131…薬剤、
135…投与対象物、150…通電装置、151…制御部、
152…電圧発生部、201…エレクトロポレーション用薬物投与システム。
Claims (12)
- エレクトロポレーションを利用して経皮又は経粘膜的薬物投与を行う電場を発生させる複数の電極(112)と、
それぞれの上記電極を電極設置部(113a)に設けた電極支持体であって、上記電極設置部に対向して位置し薬物投与される投与対象物(135)に直接又は間接に接触する接触面(113b)を有し、それぞれの上記電極に対応して形成される凹部であって上記接触面から各上記電極へ到達しかつ上記電極への通電による上記投与対象物への薬物投与のための導電性物質を収納する複数の凹部(114)を形成した電極支持体(113)と、
を備えたことを特徴とするエレクトロポレーション用薬物投与部。 - 上記凹部は、上記接触面における形状が直径5mm以下の円形で深さ5mm以下の円筒状で、隣接する該凹部を10mm以下の間隔にて配置した、請求項1記載のエレクトロポレーション用薬物投与部。
- 上記電極は、白金、銀、塩化銀、炭素、塩化銅、又はこれらの合金からなる導電性材料にてなる、請求項1又は2記載のエレクトロポレーション用薬物投与部。
- 上記電極支持体は可塑性、柔軟性,及び可撓性の少なくとも一つ、並びに耐水性を有する材料にてなる、請求項1から3のいずれかに記載のエレクトロポレーション用薬物投与部。
- 上記接触面に設けられ、上記電極支持体を上記投与対象物に接着させる粘着剤(115)をさらに有する、請求項1から4のいずれかに記載のエレクトロポレーション用薬物投与部。
- 上記電極支持体に形成された上記凹部は、上記導電性物質及び上記薬物を含む薬剤で上記電極への通電により上記投与対象物への通電及び薬物投与を行う薬剤(131)を収納する、請求項1から5のいずれかに記載のエレクトロポレーション用薬物投与部。
- 請求項1から6のいずれかに記載のエレクトロポレーション用薬物投与部(100、101)と、
上記エレクトロポレーション用薬物投与部に備わるそれぞれの電極(112)に接続され、各電極に対して、極性を変化させながらパルス状に電圧を印加する通電装置(150)と、
を備えたことを特徴とするエレクトロポレーション用薬物投与システム。 - 上記通電装置は、それぞれの上記電極における極性をランダムに変化させる制御部(151)と、該制御部と接続されかつ上記パルス状の電圧印加を行う電圧発生部(152)とを有し、単極性パルス及び両極性パルスの少なくとも一方を発生する、請求項7記載のエレクトロポレーション用薬物投与システム。
- 上記電圧発生部は、1〜1000Vの電圧を、10マイクロ秒〜1000ミリ秒の通電時間で、0.1〜数十回/秒の回数にて、数ミリ〜1000ミリ秒の間隔で、上記パルス状の電圧印加を各電極に対して行う、請求項8記載のエレクトロポレーション用薬物投与システム。
- 上記エレクトロポレーション用薬物投与部に備わるそれぞれの凹部(114)は、上記通電装置による上記電極への通電前に、投与対象物(135)へ投与される薬物及び電解質を含む薬剤で上記電極への通電により上記投与対象物への通電及び薬物投与を行う薬剤(131)を予め充填している、請求項7から9のいずれかに記載のエレクトロポレーション用薬物投与システム。
- エレクトロポレーションを利用して経皮又は経粘膜的薬物投与を行うエレクトロポレーション用薬物投与方法において、
電極支持体(113)に形成された複数の凹部(114)におけるそれぞれの底部(114a)に上記薬物投与を行う電場を発生させる電極(112)を設け、投与対象物(135)へ投与される薬物及び電解質を含む薬剤(131)を上記凹部に充填したエレクトロポレーション用薬物投与部(100、101)を上記投与対象物へ貼着し、
それぞれの上記電極における極性を変化させながら、パルス状の電圧を上記電極に印加して上記電場を発生させ、上記経皮又は経粘膜的薬物投与を行う、
ことを特徴とするエレクトロポレーション用薬物投与方法。 - 上記電極への電圧印加は、1〜1000Vの電圧を、10マイクロ秒〜1000ミリ秒の通電時間で、0.1〜数十回/秒の回数にて、数ミリ〜1000ミリ秒の間隔で行う、請求項11記載のエレクトロポレーション用薬物投与方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002377275A JP2004202086A (ja) | 2002-12-26 | 2002-12-26 | エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002377275A JP2004202086A (ja) | 2002-12-26 | 2002-12-26 | エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2004202086A true JP2004202086A (ja) | 2004-07-22 |
Family
ID=32814490
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002377275A Pending JP2004202086A (ja) | 2002-12-26 | 2002-12-26 | エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2004202086A (ja) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007051243A1 (en) * | 2005-11-04 | 2007-05-10 | Acrux Dds Pty Ltd | Method and system for transdermal drug delivery |
| WO2007056027A1 (en) * | 2005-11-02 | 2007-05-18 | May-Ruben Technologies, Inc. | High impedance system for generating electric fields and method of use |
| JP2010510821A (ja) * | 2006-11-24 | 2010-04-08 | コーニンクレッカ フィリップス エレクトロニクス エヌ ヴィ | イオン導入デバイス |
| EP2399984A1 (de) * | 2010-06-22 | 2011-12-28 | Lonza Cologne GmbH | Verfahren und Elektrodenanordnung zur Behandlung von adhärenten Zellen |
| JP2017113579A (ja) * | 2005-06-17 | 2017-06-29 | 日東電工株式会社 | 浸透物デリバリーシステムおよびその使用方法 |
| WO2019220697A1 (ja) * | 2018-05-17 | 2019-11-21 | パナソニックIpマネジメント株式会社 | 生体貼付け用選択透過膜、経皮吸収キットおよび美容方法 |
| CN115282478A (zh) * | 2022-08-08 | 2022-11-04 | 北京载愈生物科技有限公司 | 一种递送系统及递送方法 |
| JP2023021507A (ja) * | 2021-08-02 | 2023-02-14 | Nok株式会社 | 経皮薬液導入装置 |
-
2002
- 2002-12-26 JP JP2002377275A patent/JP2004202086A/ja active Pending
Cited By (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017113579A (ja) * | 2005-06-17 | 2017-06-29 | 日東電工株式会社 | 浸透物デリバリーシステムおよびその使用方法 |
| US8221596B2 (en) | 2005-11-02 | 2012-07-17 | May-Ruben Technologies, Inc. | High impedance system for generating electric fields |
| WO2007056027A1 (en) * | 2005-11-02 | 2007-05-18 | May-Ruben Technologies, Inc. | High impedance system for generating electric fields and method of use |
| JP2009515168A (ja) * | 2005-11-02 | 2009-04-09 | メイ−ルーベン テクノロジーズ,インク. | 電場を発生させる高インピーダンスシステムおよび使用方法 |
| US8226811B2 (en) | 2005-11-02 | 2012-07-24 | May-Ruben Technologies, Inc. | High impedance system for generating electric fields and method of use |
| GB2446341A (en) * | 2005-11-04 | 2008-08-06 | Acrux Dds Pty Ltd | Method and system for transdermal drug delivery |
| WO2007051243A1 (en) * | 2005-11-04 | 2007-05-10 | Acrux Dds Pty Ltd | Method and system for transdermal drug delivery |
| JP2010510821A (ja) * | 2006-11-24 | 2010-04-08 | コーニンクレッカ フィリップス エレクトロニクス エヌ ヴィ | イオン導入デバイス |
| EP2399984A1 (de) * | 2010-06-22 | 2011-12-28 | Lonza Cologne GmbH | Verfahren und Elektrodenanordnung zur Behandlung von adhärenten Zellen |
| US12415998B2 (en) | 2010-06-22 | 2025-09-16 | Lonza Cologne Gmbh | Method and device for uniformly treating adherent cells |
| WO2011161092A1 (de) * | 2010-06-22 | 2011-12-29 | Lonza Cologne Gmbh | Verfahren und elektrodenanordnung zur behandlung von adhärenten zellen |
| US9624486B2 (en) | 2010-06-22 | 2017-04-18 | Lonza Cologne Gmbh | Method and electrode assembly for treating adherent cells |
| EP2399985A1 (de) * | 2010-06-22 | 2011-12-28 | Lonza Cologne GmbH | Verfahren und Vorrichtung zur gleichmässigen Behandlung von adhärenten Zellen |
| US9701954B2 (en) | 2010-06-22 | 2017-07-11 | Lonza Cologne Gmbh | Method and device for uniformly treating adherent cells |
| KR101853514B1 (ko) | 2010-06-22 | 2018-04-30 | 론차 콜로그네 게엠베하 | 부착 세포를 처리하기 위한 방법 및 전극 조립체 |
| WO2011161106A1 (de) * | 2010-06-22 | 2011-12-29 | Lonza Cologne Gmbh | Verfahren und vorrichtung zur gleichmässigen behandlung von adhärenten zellen |
| US11021698B2 (en) | 2010-06-22 | 2021-06-01 | Lonza Cologne Gmbh | Method and device for uniformly treating adherent cells |
| WO2019220697A1 (ja) * | 2018-05-17 | 2019-11-21 | パナソニックIpマネジメント株式会社 | 生体貼付け用選択透過膜、経皮吸収キットおよび美容方法 |
| JP7170285B2 (ja) | 2018-05-17 | 2022-11-14 | パナソニックIpマネジメント株式会社 | 生体貼付け用選択透過膜、経皮吸収キットおよび美容方法 |
| JPWO2019220697A1 (ja) * | 2018-05-17 | 2021-06-17 | パナソニックIpマネジメント株式会社 | 生体貼付け用選択透過膜、経皮吸収キットおよび美容方法 |
| JP2023021507A (ja) * | 2021-08-02 | 2023-02-14 | Nok株式会社 | 経皮薬液導入装置 |
| CN115282478A (zh) * | 2022-08-08 | 2022-11-04 | 北京载愈生物科技有限公司 | 一种递送系统及递送方法 |
| CN115282478B (zh) * | 2022-08-08 | 2026-04-03 | 北京载愈生物科技有限公司 | 一种递送系统及递送方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4262410B2 (ja) | 低い初期抵抗を有する電気伝達電極アセンブリ | |
| JP6577934B2 (ja) | 治療および医薬目的のための活性剤を経皮送達するためのイオン導入システム | |
| US6591133B1 (en) | Apparatus and methods for fluid delivery using electroactive needles and implantable electrochemical delivery devices | |
| CN100379473C (zh) | 包括抗菌相容储液组合物的跨皮肤的电迁移输送装置 | |
| Banga et al. | Iontophoresis and electroporation: comparisons and contrasts | |
| US5298017A (en) | Layered electrotransport drug delivery system | |
| KR100194851B1 (ko) | 이온삼투요법용 장치 | |
| CN1104264C (zh) | 电输送剂输送方法及装置 | |
| JPH04312471A (ja) | イオントフォレーゼに際しての電極再生のためのデバイスおよび方法 | |
| JP2001521798A (ja) | 治療薬剤の生体内送出しのための装置および方法 | |
| JPH06509254A (ja) | 経皮投与デバイス | |
| JPH06506616A (ja) | イオン電気導入薬剤投与中の刺激を軽減させるためのデバイス | |
| JPH05506165A (ja) | イオン導入用送出装置 | |
| JP2809510B2 (ja) | イオントフォレーゼ用システム | |
| KR19990022341A (ko) | 펜타닐과 서펜타닐을 경피성 일렉트로트랜스포트 투여하기위한 장치 | |
| JPH04224770A (ja) | イオントフォレーシス用装置 | |
| JP2004202086A (ja) | エレクトロポレーション用薬物投与部、エレクトロポレーション用薬物投与システム、及びエレクトロポレーション用薬物投与方法 | |
| EP1355697A1 (en) | Apparatus and methods for fluid delivery using electroactive needles and implantable electrochemical delivery devices | |
| WO1990004434A1 (fr) | Interface pour endermose electrique | |
| JP2889024B2 (ja) | イオントフォレシス用装置 | |
| JP2009523712A (ja) | 電気的輸送適用における薬剤リザーバーとしての乾燥マトリックス | |
| JP2845501B2 (ja) | イオントフォレーシス用インタフェース | |
| JP2001190694A (ja) | 生体用の電極構造体 | |
| JPH1176428A (ja) | イオントフォレシス用装置 | |
| JP3566346B2 (ja) | 経皮投薬素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20051206 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080325 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20080729 |