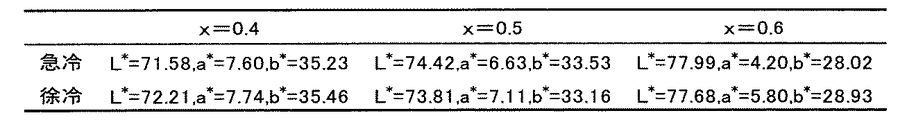JP2005225711A - 酸化鉄系黄色顔料及びその製造方法 - Google Patents
酸化鉄系黄色顔料及びその製造方法 Download PDFInfo
- Publication number
- JP2005225711A JP2005225711A JP2004035656A JP2004035656A JP2005225711A JP 2005225711 A JP2005225711 A JP 2005225711A JP 2004035656 A JP2004035656 A JP 2004035656A JP 2004035656 A JP2004035656 A JP 2004035656A JP 2005225711 A JP2005225711 A JP 2005225711A
- Authority
- JP
- Japan
- Prior art keywords
- pigment
- iron oxide
- yellow
- yellow pigment
- iron
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Compounds Of Iron (AREA)
- Pigments, Carbon Blacks, Or Wood Stains (AREA)
Abstract
【解決手段】 本発明にかかる酸化鉄系黄色顔料は、Zn(Fe(1-x)Alx)2O4(ただし0<x<1)なる構造をもつAl置換Znフェライトを、500℃〜1400℃において焼成することにより製造することができる。特に上記xが0.075以上0.8以下の場合において、その色調が鮮明な黄色系を呈する。
【選択図】 図1
Description
Zn、Fe、Alからなる酸化鉄系顔料であって、
式Zn(Fe(1-x)Alx)2O4(ただし式中0<x<1)で表されるAl置換Znフェライトを含み、かつ黄色を呈する酸化鉄系黄色顔料の製造する際に、
錯体重合法または湿式共沈法または固相反応法を用いることを特徴としている。
本黄色顔料の製造方法は特に限定されるものではないが、例えば自体公知の錯体重合法または湿式共沈法または固相反応法が好適に用いることが可能である。
「錯体重合法」は、簡単にはクエン酸による金属イオンの錯体化(キレート化)とエチレングリコールによる3次元ネットワークを経て金属イオンを均一に分散させる方法である。図2を用いてさらに説明すれば、複数種の金属イオン(Fe3+、Al3+)とクエン酸を水に溶解し、安定なキレート錯体を形成させ、これにエチレングリコールを加えて加熱重合エステル化させ、オリゴマーを経て最終的に3次元ネットワーク構造を有する高分子ゲル、すなわち錯体重合を形成する方法である。当該方法によれば、金属イオンを均一に分散させることができ固溶域の拡大が期待できる。また原料コストも安価である。
「湿式共沈法」は、各原料の混合水溶液を、水酸化ナトリウム(NaOH)等を沈殿剤として加えて共沈させ、生成した沈殿をろ過、焼成、粉砕して顔料試料を製造する方法である。図4に湿式共沈法を用いて顔料試料を製造する一例を示す。まず硝酸鉄(Fe(NO3)3・9H2O)と硝酸アルミニウム(Al(NO3)3・9H2O)と硝酸亜鉛(Zn(NO3)2・6H2O)とを秤量して混合し、原料水溶液を調製する。この時目標とするAl置換比率(上記式中x)に対応する比率で、硝酸アルミニウムと硝酸鉄を混合する。例えば、上記式中xが0.4を目標とするときには、アルミニウム(Al)と鉄(Fe)のモル比が0.4:0.6となるように混合する。またこのときの各金属塩水溶液の濃度は、金属塩の溶解度によっても異なるが最大1M程度が好ましい範囲である。次に上記原料水溶液に2MのNaOHをpH7.5または8.0になるまで滴下し、水酸化亜鉛・水酸化鉄・水酸化アルミニウムの混合物を共沈させる(合成・反応)。次にろ過等によって生成した水酸化亜鉛・水酸化鉄・水酸化アルミニウムの混合物と溶媒とを分離する(固液分離)。次にろ別した水酸化亜鉛・水酸化鉄・水酸化アルミニウムの混合物を水洗し、NaNO3を完全に除去する。次に水酸化亜鉛・水酸化鉄・水酸化アルミニウムの混合物を乾燥後、500℃〜1400℃で2時間焼成を行なってAl置換Znフェライトを得る。焼成して得られたAl置換Znフェライトを冷却後、粉砕を行なって最終的に顔料サンプルを製造する。
「固相反応法」は原料である金属化合物を固体のまま混合し、高温で焼成し、冷却後粉砕を行なうことによって顔料試料を製造する方法である。
(2−1.Al置換比率(上記式中x)の確認と固溶体生成の確認)
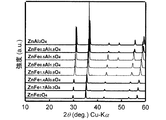
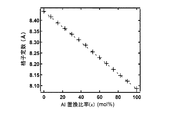
上記製造方法によって製造された種々の顔料試料については、X線回析によってAl置換比率(上記式中x)を確認している。その結果の一例を図5に示す。図5は、1,000℃で2時間焼成して得られた各Al置換比率の顔料試料についてX線回析を行なった結果を示している。図5の結果によれば上記式中のFeがAlに置換されている様子が確認できる。上記確認を600℃〜1400℃の焼成条件で製造した顔料試料について行なっているが、全ての条件においてAl置換Znフェライトの生成が確認できた。なお上記X線回析は、リガク社製RINT−2000を用いて粉末X線回析法を行なった。
上記製造方法によって製造した種々の顔料試料について、色彩・色調の評価を行なっている。評価方法は特に限定されるものではないが、本発明者等は,L*a*b*表示系により行なっている。それ以外の評価方法としては、xyz表色系・マンセル表色系・L*c*h*表色系・ハンター表色系等が利用可能である。
(方法)金属原料として可溶性金属塩であるZn(NO3)2・6H2O(99.0%)、Fe(NO3)3・9H2O(99.0%)、Al(NO3)3・9H2O(99.0%)を用いた。上記各金属塩を適当な組成比となるように混合した後、各金属イオンの合計に対してモル比で50倍量の水を添加し水溶液を製造した。次に各金属塩の合計に対してモル比で5倍量のクエン酸を添加してキレート錯体化を行ない、同じくモル比で15倍量のエチレングリコールを加えてゲル化し、180℃で12時間重合を行なった後、大気中にて450℃・24時間熱分解を行ったものを前駆体とした。次にこの前駆体を種々の温度で焼成・冷却・粉砕を行なって顔料試料とした。なお焼成時間は2時間とした。
(方法)金属原料としてZn(NO3)2・6H2O(99.0%)、Fe(NO3)3・9H2O(99.0%)、Al(NO3)3・9H2O(99.0%)を用いた。上記各試薬を式Zn(Fe(1-x)Alx)2O4中x=0.4〜0.6を持つ0.1M水溶液に調整した。それぞれの水溶液にNaOH(0.1M)滴下し、pH7.0,7.5,8.0の条件にて共沈を行なった。固液分離を行なった後水洗し、NaNO3を完全に除去した。乾燥させた試料をプレス成形し、各種温度にて2時間焼成を行なった。急冷(加熱炉から試料を取り出し室温まで冷やす)、または徐冷(10℃/分の割合で冷却)により冷却を行なった後、粉砕して顔料試料とした。評価方法は、実施例1の方法に準じて行なった。
Claims (10)
- Zn、Fe、Alからなる酸化鉄系顔料であって、
式Zn(Fe(1-x)Alx)2O4(ただし式中0<x<1)で表されるAl置換Znフェライトを含み、かつ黄色を呈することを特徴とする酸化鉄系黄色顔料。 - 上記式中のxが0.075以上0.8以下であることを特徴とする請求項1に記載の酸化鉄系黄色顔料。
- 上記式中xが0.4以上0.8以下であることを特徴とする請求項2に記載の酸化鉄系黄色顔料。
- 上記式中xが0.15以上0.6以下であることを特徴とする請求項2に記載の酸化鉄系黄色顔料。
- 1200℃以下において黄色を呈することを特徴とする請求項1ないし4のいずれか1項に記載の酸化鉄系黄色顔料
- Zn、Fe、Alからなる酸化鉄系顔料であって、
式Zn(Fe(1-x)Alx)2O4(ただし式中0<x<1)で表されるAl置換Znフェライトを含み、かつ黄色を呈する酸化鉄系黄色顔料の製造する際に、
錯体重合法または湿式共沈法または固相反応法を用いることを特徴とする酸化鉄系黄色顔料の製造方法。 - 上記式中xが0.075以上0.8以下である場合において、
焼成温度が500℃を超え1400℃未満であることを特徴とする請求項6に記載の酸化鉄系黄色顔料の製造方法。 - 上記式中xが0.4以上0.8以下である場合において、
焼成温度が500℃を超え900℃未満であることを特徴とする請求項7に記載の酸化鉄系黄色顔料の製造方法。 - 上記式中xが0.15以上0.6以下である場合において、
焼成温度が800℃以上1400℃未満であることを特徴とする請求項7に記載の酸化鉄系黄色顔料の製造方法。 - 湿式共沈法を用いる場合において、
pH7.5以上の条件下で共沈を行なうことを特徴とする請求項6ないし9のいずれか1項に記載の酸化鉄系黄色顔料の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004035656A JP2005225711A (ja) | 2004-02-12 | 2004-02-12 | 酸化鉄系黄色顔料及びその製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004035656A JP2005225711A (ja) | 2004-02-12 | 2004-02-12 | 酸化鉄系黄色顔料及びその製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005225711A true JP2005225711A (ja) | 2005-08-25 |
Family
ID=35000719
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004035656A Pending JP2005225711A (ja) | 2004-02-12 | 2004-02-12 | 酸化鉄系黄色顔料及びその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005225711A (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007088215A (ja) * | 2005-09-22 | 2007-04-05 | Doshisha | 磁性体材料及びその製造方法 |
| JP2007238392A (ja) * | 2006-03-09 | 2007-09-20 | Admetech:Kk | 生体加熱材料として用いられるMgFe2O4の製造方法及びこの製造方法により得られたMgFe2O4 |
| JP2008156494A (ja) * | 2006-12-25 | 2008-07-10 | Sanyo Chem Ind Ltd | スラッシュ成形用樹脂粉末組成物 |
| JP2014225655A (ja) * | 2013-04-25 | 2014-12-04 | 中部電力株式会社 | 熱電変換材料 |
-
2004
- 2004-02-12 JP JP2004035656A patent/JP2005225711A/ja active Pending
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007088215A (ja) * | 2005-09-22 | 2007-04-05 | Doshisha | 磁性体材料及びその製造方法 |
| JP2007238392A (ja) * | 2006-03-09 | 2007-09-20 | Admetech:Kk | 生体加熱材料として用いられるMgFe2O4の製造方法及びこの製造方法により得られたMgFe2O4 |
| JP2008156494A (ja) * | 2006-12-25 | 2008-07-10 | Sanyo Chem Ind Ltd | スラッシュ成形用樹脂粉末組成物 |
| JP2014225655A (ja) * | 2013-04-25 | 2014-12-04 | 中部電力株式会社 | 熱電変換材料 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5723894B2 (ja) | 日射反射率改良のための顔料添加剤 | |
| EP2890640B1 (en) | Blue inorganic colourants/pigments and process for preparation thereof | |
| CA2072667A1 (en) | Temperature-resistant black pigment, a process for its production and its use | |
| US8303706B2 (en) | Yellow inorganic pigment from samarium and molybdenum compounds and a process for preparing the same | |
| Elakkiya et al. | Vanadium substituted AlPO4 as environmentally benevolent cool yellow pigment | |
| JP2001164042A (ja) | Mg−Al系ハイドロタルサイト型粒子粉末、塩素含有樹脂安定剤及びMg−Al系ハイドロタルサイト型粒子粉末の製造法 | |
| JP2005225711A (ja) | 酸化鉄系黄色顔料及びその製造方法 | |
| JP2000264639A (ja) | ストロンチウム鉄酸化物粒子粉末及びその製造方法 | |
| JP2741499B2 (ja) | 耐熱性無機顔料粉末及びその製造方法 | |
| KR101630554B1 (ko) | 복합 산화물 블랙 안료 및 그 제조 방법 | |
| JP6935505B2 (ja) | Alを含有する酸化鉄顔料 | |
| CN105189360A (zh) | 同时取代的烧绿石和相关结构的颜料 | |
| JP5102926B2 (ja) | チタン−鉄系複合酸化物顔料の製造方法 | |
| JP5224031B2 (ja) | Mg−Al系ハイドロタルサイト型粒子粉末、塩素含有樹脂安定剤 | |
| JP2002053722A (ja) | 塩素含有樹脂組成物 | |
| JP2723176B2 (ja) | LiFeO2粉末の製造方法及びその粉末からなる耐熱性黄色系顔料 | |
| Trif et al. | Preparation and characterization of hexagonal W-type barium ferrite nanoparticles | |
| JP2001040288A (ja) | 黄色塗料及び黄色ゴム・樹脂組成物 | |
| JP3828401B2 (ja) | コバルト系黒色顔料及びその製造方法 | |
| KR20130140837A (ko) | 내열성 흑색 분체 및 그의 제조 방법, 상기 내열성 흑색 분체를 이용한 도료 및 수지 조성물 | |
| Calbo et al. | Synthesis of nickel-iron spinel by non-conventional methods | |
| CA1201255A (en) | Dark brown pigments of pseudobrookite structure | |
| KR101616003B1 (ko) | 에멀젼 공정에 의한 Zn1-xCoxAl2O4 무기안료 나노분말의 제조방법 | |
| JPH10226521A (ja) | 酸化ニッケル粒子およびその製造方法 | |
| Chen et al. | Preparation and Chromaticity Control of CoTiO3/NiTiO3 Co-Coated TiO2 Composite Pigments. Materials 2022, 15, 1456 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20051209 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20051209 |
|
| A977 | Report on retrieval |
Effective date: 20080328 Free format text: JAPANESE INTERMEDIATE CODE: A971007 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20081111 |
|
| A02 | Decision of refusal |
Effective date: 20090324 Free format text: JAPANESE INTERMEDIATE CODE: A02 |