JP2006527770A - Cb1モジュレーターとしての2−置換5,6−ジアリール−ピラジン誘導体 - Google Patents
Cb1モジュレーターとしての2−置換5,6−ジアリール−ピラジン誘導体 Download PDFInfo
- Publication number
- JP2006527770A JP2006527770A JP2006517043A JP2006517043A JP2006527770A JP 2006527770 A JP2006527770 A JP 2006527770A JP 2006517043 A JP2006517043 A JP 2006517043A JP 2006517043 A JP2006517043 A JP 2006517043A JP 2006527770 A JP2006527770 A JP 2006527770A
- Authority
- JP
- Japan
- Prior art keywords
- group
- formula
- chlorophenyl
- bis
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- DXKPUMBQEYEEQA-UHFFFAOYSA-N OC(c1nc(-c(cc2)ccc2Cl)c(-c(cc2)ccc2Cl)nc1)=O Chemical compound OC(c1nc(-c(cc2)ccc2Cl)c(-c(cc2)ccc2Cl)nc1)=O DXKPUMBQEYEEQA-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/10—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D241/14—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D241/24—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/14—Prodigestives, e.g. acids, enzymes, appetite stimulants, antidyspeptics, tonics, antiflatulents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
- A61P25/10—Antiepileptics; Anticonvulsants for petit-mal
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
- A61P25/12—Antiepileptics; Anticonvulsants for grand-mal
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/32—Alcohol-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/34—Tobacco-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/36—Opioid-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/10—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D241/12—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Public Health (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Addiction (AREA)
- Psychiatry (AREA)
- Diabetes (AREA)
- Pain & Pain Management (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Psychology (AREA)
- Endocrinology (AREA)
- Communicable Diseases (AREA)
- Cardiology (AREA)
- Immunology (AREA)
- Heart & Thoracic Surgery (AREA)
- Hospice & Palliative Care (AREA)
- Emergency Medicine (AREA)
- Oncology (AREA)
- Child & Adolescent Psychology (AREA)
- Pulmonology (AREA)
- Nutrition Science (AREA)
- Urology & Nephrology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
本発明は、5,6−ジアリール−ピラジン−2−カルボキサミド及び2−エステル誘導体と、そのような化合物を製造する方法、肥満、精神医学系及び神経系の障害の治療におけるその使用、その療法的使用の方法、並びにそれらを含有する医薬組成物に関する。本化合物は、カンナビノイド受容体1(CB1)モジュレーターである。
Description
発明の分野
本発明は、式Iのあるピラジン化合物、そのような化合物を製造する方法、肥満、精神医学系及び神経系の障害の治療におけるそれらの使用、その治療使用の方法、及びそれらを含有する医薬組成物に関する。
本発明は、式Iのあるピラジン化合物、そのような化合物を製造する方法、肥満、精神医学系及び神経系の障害の治療におけるそれらの使用、その治療使用の方法、及びそれらを含有する医薬組成物に関する。
背景技術
あるCB1モジュレーター(modulator;アンタゴニスト又はインバースアゴニストとして知られる)は、肥満、精神医学系及び神経系の障害の治療に有用であることが知られている(WO01/70700及びEP656354)。しかしながら、改善された物理化学特性、及び/又はDMPK特性、及び/又は薬物動態特性を有するCB1モジュレーターへのニーズがある。
あるCB1モジュレーター(modulator;アンタゴニスト又はインバースアゴニストとして知られる)は、肥満、精神医学系及び神経系の障害の治療に有用であることが知られている(WO01/70700及びEP656354)。しかしながら、改善された物理化学特性、及び/又はDMPK特性、及び/又は薬物動態特性を有するCB1モジュレーターへのニーズがある。
ピラジンカルボキサミドは、抗血栓特性を保有することが報告されている(WO92/02513)。この文書において開示される化合物は、本発明の化合物の特許請求項からは無関係である。5,6−ジフェニル−2−ピラジンカルボン酸は、CH458 361に開示されている。
同時出願中の特許出願PCT/GB02/05742は、一般式(I):
[式中、R1とR2は、独立して:
C1−6アルキル基;
(アミノ)C1−4アルキル基(式中、アミノは、1若しくはそれより多くのC1−3アルキル基により置換されていてもよい);
置換されていてもよい非芳香族C3−15炭素環式基;
(C3−12シクロアルキル)C1−3アルキル基;
基:−(CH2)r(フェニル)s(式中、rは、0、1、2、3又は4であり、sは、rが0であるとき1であり、他の場合、sは1又は2であり、フェニル基は、Zにより表される、1、2、又は3の基により独立して置換されていてもよい);
ナフチル;
アントラセニル;
1つの窒素と場合により以下のもの、即ち、酸素、イオウ、又は追加の窒素の1つとを含有する飽和の5〜8員複素環式基(ここで、複素環式基は、1若しくはそれより多くのC1−3アルキル基、ヒドロキシ、又はベンジルにより置換されていてもよい);
1−アダマンチルメチル;
基:−(CH2)tHet(式中、tは、0、1、2、3又は4であり、アルキレン鎖は、1若しくはそれより多くのC1−3アルキル基により置換されていてもよく、Hetは、C1−5アルキル基、C1−5アルコキシ基、又はハロより選択される1、2、又は3の基により置換されていてもよい芳香族複素環を表す)を表す;
又は、R1はHを表し、R2は、上記に定義される通りである;
又は、R1とR2は、それらが付く窒素原子と一緒に、1つの窒素と場合により以下野物、即ち、酸素、イオウ、又は追加の窒素の1つを含有する飽和の5〜8員複素環式基(ここで、複素環式基は、1若しくはそれより多くのC1−3アルキル基、ヒドロキシ、又はベンジルにより置換されていてもよい)を表す;
Xは、CO又はSO2であり;
Yは、非存在であるか、又はC1−3アルキル基により置換されていてもよいNHを表し;
R3とR4は、独立して、フェニル、チエニル、又はピリジルを表し、それらの各々は、Zにより表される1、2、又は3の基により置換されていてもよく;
Zは、C1−3アルキル基、C1−3アルコキシ基、ヒドロキシ、ハロ、トリフルオロメチル、トリフルオロメチルチオ、トリフルオロメトキシ、トリフルオロメチルスルホニル、ニトロ、アミノ、モノ若しくはジC1−3アルキルアミノ、モノ若しくはジC1−3アルキルアミド、C1−3アルキルスルホニル、C1−3アルコキシカルボニル、カルボキシ、シアノ、カルバモイル、モノ若しくはジC1−3アルキルカルバモイル、スルファモイル、及びアセチルを表し;そして
R5は、H、C1−3アルキル基、C1−3アルコキシメチル基、トリフルオロメチル、ヒドロキシルC1−3アルキル基、C1−3アルコキシカルボニル、カルボキシ、シアノ、カルバモイル、モノ若しくはジC1−3アルキルカルバモイル、アセチル、又は式:−CONHNRaRb(ここで、RaとRbは、それぞれR1とR2についてすでに定義された通りである)のヒドラジノカルボニルである;
但し、R1とR2が、それらが付く窒素原子と一緒に4−メチルピペラジン−1−イルを表すか、又はR1がHを表して、R2がメチル又は1−ベンジルピペリジン−4−イルを表し;XがCOであり;Yが非存在であり、そしてR5がHであるとき;そのときR3とR4がともに4−メトキシフェニルを表すことはない]の化合物とその医薬的に許容される塩、プロドラッグ、溶媒和物、及び結晶形と、肥満、精神医学系及び神経系の障害の治療におけるそれらの使用を開示する。
C1−6アルキル基;
(アミノ)C1−4アルキル基(式中、アミノは、1若しくはそれより多くのC1−3アルキル基により置換されていてもよい);
置換されていてもよい非芳香族C3−15炭素環式基;
(C3−12シクロアルキル)C1−3アルキル基;
基:−(CH2)r(フェニル)s(式中、rは、0、1、2、3又は4であり、sは、rが0であるとき1であり、他の場合、sは1又は2であり、フェニル基は、Zにより表される、1、2、又は3の基により独立して置換されていてもよい);
ナフチル;
アントラセニル;
1つの窒素と場合により以下のもの、即ち、酸素、イオウ、又は追加の窒素の1つとを含有する飽和の5〜8員複素環式基(ここで、複素環式基は、1若しくはそれより多くのC1−3アルキル基、ヒドロキシ、又はベンジルにより置換されていてもよい);
1−アダマンチルメチル;
基:−(CH2)tHet(式中、tは、0、1、2、3又は4であり、アルキレン鎖は、1若しくはそれより多くのC1−3アルキル基により置換されていてもよく、Hetは、C1−5アルキル基、C1−5アルコキシ基、又はハロより選択される1、2、又は3の基により置換されていてもよい芳香族複素環を表す)を表す;
又は、R1はHを表し、R2は、上記に定義される通りである;
又は、R1とR2は、それらが付く窒素原子と一緒に、1つの窒素と場合により以下野物、即ち、酸素、イオウ、又は追加の窒素の1つを含有する飽和の5〜8員複素環式基(ここで、複素環式基は、1若しくはそれより多くのC1−3アルキル基、ヒドロキシ、又はベンジルにより置換されていてもよい)を表す;
Xは、CO又はSO2であり;
Yは、非存在であるか、又はC1−3アルキル基により置換されていてもよいNHを表し;
R3とR4は、独立して、フェニル、チエニル、又はピリジルを表し、それらの各々は、Zにより表される1、2、又は3の基により置換されていてもよく;
Zは、C1−3アルキル基、C1−3アルコキシ基、ヒドロキシ、ハロ、トリフルオロメチル、トリフルオロメチルチオ、トリフルオロメトキシ、トリフルオロメチルスルホニル、ニトロ、アミノ、モノ若しくはジC1−3アルキルアミノ、モノ若しくはジC1−3アルキルアミド、C1−3アルキルスルホニル、C1−3アルコキシカルボニル、カルボキシ、シアノ、カルバモイル、モノ若しくはジC1−3アルキルカルバモイル、スルファモイル、及びアセチルを表し;そして
R5は、H、C1−3アルキル基、C1−3アルコキシメチル基、トリフルオロメチル、ヒドロキシルC1−3アルキル基、C1−3アルコキシカルボニル、カルボキシ、シアノ、カルバモイル、モノ若しくはジC1−3アルキルカルバモイル、アセチル、又は式:−CONHNRaRb(ここで、RaとRbは、それぞれR1とR2についてすでに定義された通りである)のヒドラジノカルボニルである;
但し、R1とR2が、それらが付く窒素原子と一緒に4−メチルピペラジン−1−イルを表すか、又はR1がHを表して、R2がメチル又は1−ベンジルピペリジン−4−イルを表し;XがCOであり;Yが非存在であり、そしてR5がHであるとき;そのときR3とR4がともに4−メトキシフェニルを表すことはない]の化合物とその医薬的に許容される塩、プロドラッグ、溶媒和物、及び結晶形と、肥満、精神医学系及び神経系の障害の治療におけるそれらの使用を開示する。
発明の説明
本発明は、式(I):
本発明は、式(I):
[式中、R1とR2は、独立して、フェニル、チエニル、又はピリジルを表し、それらの各々は、Zにより表される1つ若しくはそれより多くの基により独立して置換されていてもよく;
Zは、C1−8アルキル基、C1−6アルコキシ基、ヒドロキシ、ハロ、トリフルオロメチル、トリフルオロメチルチオ、トリフルオロメトキシ、トリフルオロメチルスルホニル、ニトロ、モノ若しくはジC1−3アルキルアミド、C1−3アルキルスルホニル、C1−3アルキルスルホニルオキシ、C1−3アルコキシカルボニル、カルボキシ、シアノ、カルバモイル、モノ若しくはジC1−3アルキルカルバモイル、スルファモイル、アセチル、ハロ、アルキル、トリフルオロメチル又はトリフルオロメトキシにより置換されていてもよい芳香族複素環式基、及び、窒素、酸素、又はイオウより選択される1つ若しくはそれより多くのヘテロ原子を含有する飽和又は一部不飽和の5〜8員複素環式基を表し、ここで該複素環式基は、1つ若しくはそれより多くのC1−3アルキル基、ヒドロキシ、フルオロ、ベンジル、又はアミノ基:−NRxRy(式中、RxとRyは、独立してH又はC1−4アルキルを表す)により置換されていてもよく;
R3は、式:(CH2)nCOOR7:
{式中、nは、0、1、2、3又は4であり、R7は、C4−12アルキル基、C3−12シクロアルキル基、又は(C3−12シクロアルキル)C1−3アルキル基を表し、それらの各々は、以下のもの、即ちC1−6アルキル基;フルオロ、アミノ、又はヒドロキシのうち1つ若しくはそれより多くにより置換されていてもよいか、又は
R7は、基:−(CH2)aフェニル(式中、aは、0、1、2、3又は4であり、フェニル基は、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により置換されていてもよい)を表すか、又は
R7は、以下のもの、即ち、酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、飽和又は一部不飽和の5〜8員複素環式基を表し、ここで該複素環式基は、1つ若しくはそれより多くのC1−3アルキル基、C1−3アシル基、ヒドロキシ、アミノ、又はベンジルにより置換されていてもよい}の基を表す;又は
R3は、式:−(CH2)o−O−(CH2)p−R8{式中、oは、1、2、3又は4の整数を表し、pは、0、1、2、3又は4の整数を表し、そしてR8は、以下のもの、即ち、C1−6アルキル基;フルオロ、ヒドロキシ、又はアミノ基:NRxRy(式中、RxとRyは、独立してH又はC1−4アルキルを表す)のうち1つ若しくはそれより多くの基により置換されるC1−12アルキル基を表すか;
又は、R8は、1つ若しくはそれより多くのZ基によりに独立して置換されていてもよいフェニルを表すか、又はR8は、以下のもの、即ち、酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、芳香族複素環式基又は飽和又は一部不飽和の5〜8員複素環式基(ここで、これらの環のそれぞれは、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により置換されていてもよい)を表す}の基を表す;又は、
R3は、式:−(CH2)qR9{式中、qは、2、3又は4であり、R9は、C3−12シクロアルキル基、フェニル、以下:酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、芳香族複素環式基又は飽和又は一部不飽和の5〜8員複素環式基(ここで、これらの環のそれぞれは、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により随意に置換される)を表す}の基を表す;又は、
R3は、式:−(CH2)m−O−(CO)−R10{式中、mは、0、1、2、3又は4の整数を表し、式中R10は、1つ若しくはそれより多くのフルオロ、ヒドロキシ、又はアミノにより随意に置換されるC1−12アルキル基を表すか、又はR10は、式:−(CH2)qR9(式中、qとR9は、上記に記載される通りである)の基を表す}の基を表す;又は、
R3は、以下の式:
Zは、C1−8アルキル基、C1−6アルコキシ基、ヒドロキシ、ハロ、トリフルオロメチル、トリフルオロメチルチオ、トリフルオロメトキシ、トリフルオロメチルスルホニル、ニトロ、モノ若しくはジC1−3アルキルアミド、C1−3アルキルスルホニル、C1−3アルキルスルホニルオキシ、C1−3アルコキシカルボニル、カルボキシ、シアノ、カルバモイル、モノ若しくはジC1−3アルキルカルバモイル、スルファモイル、アセチル、ハロ、アルキル、トリフルオロメチル又はトリフルオロメトキシにより置換されていてもよい芳香族複素環式基、及び、窒素、酸素、又はイオウより選択される1つ若しくはそれより多くのヘテロ原子を含有する飽和又は一部不飽和の5〜8員複素環式基を表し、ここで該複素環式基は、1つ若しくはそれより多くのC1−3アルキル基、ヒドロキシ、フルオロ、ベンジル、又はアミノ基:−NRxRy(式中、RxとRyは、独立してH又はC1−4アルキルを表す)により置換されていてもよく;
R3は、式:(CH2)nCOOR7:
{式中、nは、0、1、2、3又は4であり、R7は、C4−12アルキル基、C3−12シクロアルキル基、又は(C3−12シクロアルキル)C1−3アルキル基を表し、それらの各々は、以下のもの、即ちC1−6アルキル基;フルオロ、アミノ、又はヒドロキシのうち1つ若しくはそれより多くにより置換されていてもよいか、又は
R7は、基:−(CH2)aフェニル(式中、aは、0、1、2、3又は4であり、フェニル基は、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により置換されていてもよい)を表すか、又は
R7は、以下のもの、即ち、酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、飽和又は一部不飽和の5〜8員複素環式基を表し、ここで該複素環式基は、1つ若しくはそれより多くのC1−3アルキル基、C1−3アシル基、ヒドロキシ、アミノ、又はベンジルにより置換されていてもよい}の基を表す;又は
R3は、式:−(CH2)o−O−(CH2)p−R8{式中、oは、1、2、3又は4の整数を表し、pは、0、1、2、3又は4の整数を表し、そしてR8は、以下のもの、即ち、C1−6アルキル基;フルオロ、ヒドロキシ、又はアミノ基:NRxRy(式中、RxとRyは、独立してH又はC1−4アルキルを表す)のうち1つ若しくはそれより多くの基により置換されるC1−12アルキル基を表すか;
又は、R8は、1つ若しくはそれより多くのZ基によりに独立して置換されていてもよいフェニルを表すか、又はR8は、以下のもの、即ち、酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、芳香族複素環式基又は飽和又は一部不飽和の5〜8員複素環式基(ここで、これらの環のそれぞれは、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により置換されていてもよい)を表す}の基を表す;又は、
R3は、式:−(CH2)qR9{式中、qは、2、3又は4であり、R9は、C3−12シクロアルキル基、フェニル、以下:酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、芳香族複素環式基又は飽和又は一部不飽和の5〜8員複素環式基(ここで、これらの環のそれぞれは、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により随意に置換される)を表す}の基を表す;又は、
R3は、式:−(CH2)m−O−(CO)−R10{式中、mは、0、1、2、3又は4の整数を表し、式中R10は、1つ若しくはそれより多くのフルオロ、ヒドロキシ、又はアミノにより随意に置換されるC1−12アルキル基を表すか、又はR10は、式:−(CH2)qR9(式中、qとR9は、上記に記載される通りである)の基を表す}の基を表す;又は、
R3は、以下の式:
{式中、R11は、ヒドロキシ、フルオロ、カルボキシ、C1−6アルコキシカルボニル基、又はアミノ基:−NRxRy(式中、RxとRyは、独立して、H又はC1−4アルキルを表す)を表し;
dは、1、2又は3であり、そして
R12は、H又はC1−3アルキル基を表す}の基を有する;又は
R3は、式:CONH−Rz(式中、Rzは、C1−6アルカノイル基により置換されるピペリジニル環である)の基を表すか、又はR3は、基:−COG(式中、Gは、窒素を介してカルボニルへ連結するジヒドロインドール又はジヒドロイソインドールである)の基を表す]の化合物とその医薬的に許容される塩に関する。
dは、1、2又は3であり、そして
R12は、H又はC1−3アルキル基を表す}の基を有する;又は
R3は、式:CONH−Rz(式中、Rzは、C1−6アルカノイル基により置換されるピペリジニル環である)の基を表すか、又はR3は、基:−COG(式中、Gは、窒素を介してカルボニルへ連結するジヒドロインドール又はジヒドロイソインドールである)の基を表す]の化合物とその医薬的に許容される塩に関する。
置換基Zが1より多くの基において存在する場合、これらの置換基は独立して選択されて、同じでも異なってもよいと理解されたい。
本発明の式の別の態様において、R3は、以下の式:
本発明の式の別の態様において、R3は、以下の式:
[式中、R11は、ヒドロキシ、フルオロ、カルボキシ、C1−6アルコキシカルボニル基、又はアミノ基:−NRxRy(式中、RxとRyは、独立して、H又はC1−4アルキルを表す)を表し;
dは、1、2、又は3であり;
R12は、H又はC1−3アルキル基を表す]を有し、その医薬的に許容される塩(が含まれる)。
dは、1、2、又は3であり;
R12は、H又はC1−3アルキル基を表す]を有し、その医薬的に許容される塩(が含まれる)。
用語「芳香族複素環式基」は、酸素、窒素、及びイオウより選択される最大5個までの環ヘテロ原子のある、芳香族の5、6、又は7員の単環式環、又は9若しくは10員の二環式環を意味する。好適な芳香族複素環式基には、例えば、フリル、ピロリル、チエニル、オキサゾリル、イソオキサゾリル、イミダゾリル、ピラゾリル、チアゾリル、イソチアゾリル、オキサジアゾリル、チアジアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピリダジニル、ピリミジニル、ピラジニル、1,3,5−トリアゼニル、ベンゾフラニル、インドリル、ベンゾチエニル、ベンゾオキサゾリル、ベンゾイミダゾリル、ベンゾチアゾリル、インダゾリル、ベンゾフラザニル、キノリル、イソキノリル、キナゾリニル、キノキサリニル、シンノリニル、又はナフチリジニル、好ましくは、フリル、ピロリル、チエニル、オキサゾリル、イソオキサゾリル、イミダゾリル、ピラゾリル、オキサゾリル、チアゾリル、イソチアゾリル、オキサジアゾリル、チアジアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピリダジニル、ピリミジニル、ピラジニル、又は1,3,5−トリアゼニル、そしてより好ましくは、ピロリル、チエニル、イミダゾリル、オキサゾリル、又はピリジルが含まれる。
窒素、酸素、又はイオウより選択される1若しくはそれより多くのヘテロ原子を含有する、好適な飽和又は一部不飽和の5〜8員複素環式基には、例えば、オキシラニル、オキセタニル、テトラヒドロフラニル、テトラヒドロピラニル、2,3−ジヒドロ−1,3−チアゾリル、1,3−チアゾリジニル、ピロリニル、ピロリジニル、モルホリニル、テトラヒドロ−1,4−チアジニル、1−オキソテトラヒドロチエニル、1,1−ジオキソテトラヒドロ−1,4−チアジニル、ピペリジニル、ホモピペリジニル、ピペラジニル、ホモピペラジニル、ジヒドロピリジニル、テトラヒドロピリジニル、ジヒドロピリミジニル、又はテトラヒドロピリミジニル、好ましくは、テトラヒドロフラニル、テトラヒドロピラニル、ピロリジニル、モルホリニル、ピペリジニル、又はピペラジニル、より好ましくは、テトラヒドロフラン−3−イル、テトラヒドロピラン−4−イル、ピロリジン−3−イル、モルホリノ、ピペリジノ、ピペリジン−4−イル、又はピペラジン−1−イルが含まれる。
式Iの化合物中のR1、R2、及びR3のさらなる意義が以下に続く。そのような意義は、上記又は下記の定義、特許請求項、又は態様のいずれでも適宜使用してよいと理解されたい。
特にR1とR2は、それぞれ独立して1若しくはそれより多くのクロロにより置換されていてもよいフェニルを表す。
特にR3は、C4−12アルコキシカルボニルを表す。
特にR3は、C4−12アルコキシカルボニルを表す。
特にR3は、ベンジルオキシメチル基を表し、該ベンジルオキシメチル基のベンジル基のフェニル環においてZにより置換されていてもよい。
特にR3は、基:C(O)O−Het(式中、Hetは、ピペリジノ、モルホリノ、又はピロリジノである)を表す。
特にR3は、基:C(O)O−Het(式中、Hetは、ピペリジノ、モルホリノ、又はピロリジノである)を表す。
式Iの化合物の第一の群では、R1とR2がそれぞれ4−クロロフェニルを表す。
式Iの化合物の第二の群では、dが1であり、R11がヒドロキシ、アミノ、又はC1−6アルコキシカルボニル基である。
式Iの化合物の第二の群では、dが1であり、R11がヒドロキシ、アミノ、又はC1−6アルコキシカルボニル基である。
式Iの化合物の第三の群では、dが2であり、R11がFであり、そして両方のフルオロがシクロヘキシル環の同じ炭素に付いている。
式Iの化合物の第四の群では、R12がHである。
式Iの化合物の第四の群では、R12がHである。
第五の群では、芳香族複素環式基が、フリル、ピロリル、チエニル、オキサゾリル、イソオキサゾリル、イミダゾリル、ピラゾリル、オキサゾリルチアゾリル、イソチアゾリル、オキサジアゾリル、チアジアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピリダジニル、ピリミジニル、ピラジニル、又は1,3,5−トリアゼニルである。
第六の群では、芳香族複素環式基が、ピロリル、チエニル、イミダゾリル、オキサゾリル、又はピリジルである。
第七の群では、飽和又は一部不飽和の5〜8員複素環式基が、テトラヒドロフラニル、テトラヒドロピラニル、ピロリジニル、モルホリニル、ピペリジニル、又はピペラジニルである。
第七の群では、飽和又は一部不飽和の5〜8員複素環式基が、テトラヒドロフラニル、テトラヒドロピラニル、ピロリジニル、モルホリニル、ピペリジニル、又はピペラジニルである。
第八の群では、飽和又は一部不飽和の5〜8員複素環式基が、テトラヒドロフラン−3−イル、テトラヒドロピラン−4−イル、ピロリジン−3−イル、モルホリノ、ピペリジノ、ピペリジン−4−イル、又はピペラジン−1−イルである。
「医薬的に許容される塩」には、そのような塩が可能である場合、医薬的に許容される酸付加塩と塩基付加塩の両方が含まれる。式Iの化合物の好適な医薬的に許容される塩は、例えば、十分に塩基性である式Iの化合物の酸付加塩、例えば、塩酸、臭化水素酸、硫酸、トリフルオロ酢酸、クエン酸、又はマレイン酸のような無機酸又は有機酸との酸付加塩であるか;又は、例えば、十分に酸性である式Iの化合物の塩、例えば、ナトリウム、カルシウム、又はマグネシウム塩のようなアルカリ又はアルカリ土類金属塩、又はアンモニウム塩、又はメチルアミン、ジメチルアミン、トリエチルアミン、ピペリジン、モルホリン、又はトリス−(2−ヒドロキシ−エチル)アミンのような有機塩基との塩である。
本明細書と付帯の特許請求の範囲を通して、所与の化学式又は名称には、すべての立体及び光学異性体とそのラセミ体、並びに個々のエナンチオマーの様々な比率の混合物(そのような異性体及びエナンチオマーが存在する場合)、並びに、その医薬的に許容される塩と、例えば水和物のような溶媒和物が含まれる。異性体は、慣用の技術、例えば、クロマトグラフィー又は分別結晶を使用して分離することができる。エナンチオマーは、例えば、分別結晶、分割、又はHPLCによって、ラセミ体の分離により単離することができる。ジアステレオマーは、例えば、分別結晶、HPLC、又はフラッシュクロマトグラフィーによって、異性体混合物の分離により単離することができる。あるいは、立体異性体は、ラセミ化もエピマー化も起さない条件下でのキラルな出発材料からのキラル合成によるか、又はキラル試薬を用いた誘導化によって作製してよい。すべての立体異性体が本発明の範囲内に含まれる。すべての互変異性体が、可能である場合、本発明の範囲内に含まれる。
以下の定義は、本明細書と付帯の特許請求項を通して適用される。
他に言明又は明示しなければ、用語「アルキル」は、直鎖又は分岐鎖のアルキル基を意味する。前記アルキルの例には、メチル、エチル、n−プロピル、イソプロピル、n−ブチル、イソブチル、sec−ブチル、及びt−ブチルが含まれる。好ましいアルキル基は、メチル、エチル、プロピル、イソプロピル、及び三級ブチルである。
他に言明又は明示しなければ、用語「アルキル」は、直鎖又は分岐鎖のアルキル基を意味する。前記アルキルの例には、メチル、エチル、n−プロピル、イソプロピル、n−ブチル、イソブチル、sec−ブチル、及びt−ブチルが含まれる。好ましいアルキル基は、メチル、エチル、プロピル、イソプロピル、及び三級ブチルである。
他に言明又は明示しなければ、用語「アルコキシ」は、基:O−アルキルを意味し、ここでアルキルは、上記に定義される通りである。
他に言明又は明示しなければ、用語「ハロゲン」は、フッ素、塩素、臭素、又はヨウ素を意味する。
他に言明又は明示しなければ、用語「ハロゲン」は、フッ素、塩素、臭素、又はヨウ素を意味する。
本発明の具体的な化合物は、以下の化合物、即ち、
5,6−ビス(4−クロロフェニル)−N−(cis−2−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(trans−2−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(4−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(4,4−ジフルオロシクロヘキシル)ピラジン−2−カルボキサミド、
N−(1−アセチルピペリジン−3−イル)−5,6−ビス(4−クロロフェニル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸tert−ブチル、
5,6−ビス(4−クロロフェニル)−ピラジン−2−イル−(1,3−ジヒドロ−イソインドール−2−イル)−メタノン、
2,3−ビス(4−クロロフェニル)−5−{[(4−フルオロベンジル)オキシ]メチル}ピラジン、
2,3−ビス(4−クロロフェニル)−5−[(ピペリジン−1−イルオキシ)カルボニル]ピラジンの1若しくはそれより多くと、その医薬的に許容される塩である。
5,6−ビス(4−クロロフェニル)−N−(cis−2−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(trans−2−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(4−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(4,4−ジフルオロシクロヘキシル)ピラジン−2−カルボキサミド、
N−(1−アセチルピペリジン−3−イル)−5,6−ビス(4−クロロフェニル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸tert−ブチル、
5,6−ビス(4−クロロフェニル)−ピラジン−2−イル−(1,3−ジヒドロ−イソインドール−2−イル)−メタノン、
2,3−ビス(4−クロロフェニル)−5−{[(4−フルオロベンジル)オキシ]メチル}ピラジン、
2,3−ビス(4−クロロフェニル)−5−[(ピペリジン−1−イルオキシ)カルボニル]ピラジンの1若しくはそれより多くと、その医薬的に許容される塩である。
製造の方法
本発明の化合物は、「実施例」において概説されるように、そして類似の方法によって製造することができる。しかしながら、本発明は、これらの方法に限定されず、本化合物は、先行技術において構造的に関連した化合物について記載されるように製造してもよい。
本発明の化合物は、「実施例」において概説されるように、そして類似の方法によって製造することができる。しかしながら、本発明は、これらの方法に限定されず、本化合物は、先行技術において構造的に関連した化合物について記載されるように製造してもよい。
当業者は、本発明の化合物を代わりの、場合によってはより簡便なやり方で得るために、上記に言及される個別の方法工程を異なる順序で実施しても、及び/又は個別の反応を全体経路の異なる段階で実施してもよい(即ち、上記の特別な反応に関連した中間体と異なる中間体に対して化学変換を実施してよい)ことを理解されよう。
医薬品
通常、本発明の化合物は、有効成分又は医薬的に許容される付加塩を医薬的に許容される剤形において含む医薬品(pharmaceutical preparation)の形態で、経口、非経口、静脈内、筋肉内、皮下、又は他の注射可能なやり方で、頬内、直腸、膣、経皮、及び/又は経鼻の経路、及び/又は吸入により投与する。治療すべき障害及び患者と投与の経路に依存して、本組成物は、変動する用量で投与してよい。
通常、本発明の化合物は、有効成分又は医薬的に許容される付加塩を医薬的に許容される剤形において含む医薬品(pharmaceutical preparation)の形態で、経口、非経口、静脈内、筋肉内、皮下、又は他の注射可能なやり方で、頬内、直腸、膣、経皮、及び/又は経鼻の経路、及び/又は吸入により投与する。治療すべき障害及び患者と投与の経路に依存して、本組成物は、変動する用量で投与してよい。
本発明の化合物のヒトの治療的処置において好適な1日用量は、約0.001〜10mg/kg(体重)、好ましくは0.01〜1mg/kg(体重)である。
0.5mg〜500mgの範囲、例えば1mg、3mg、5mg、10mg、25mg、50mg、100mg、及び250mgの活性化合物の用量を提供するには、経口製剤、特に、当業者に知られた方法によって製剤化することができる錠剤又はカプセル剤が好ましい。
0.5mg〜500mgの範囲、例えば1mg、3mg、5mg、10mg、25mg、50mg、100mg、及び250mgの活性化合物の用量を提供するには、経口製剤、特に、当業者に知られた方法によって製剤化することができる錠剤又はカプセル剤が好ましい。
本発明のさらなる側面によれば、本発明の化合物のいずれか、又はその医薬的に許容される誘導体が医薬的に許容されるアジュバント、希釈剤及び/又は担体との混合において含まれる医薬製剤も提供される。
薬理学的特性
式(I)の化合物は、肥満、精神異常症、精神分裂病、双極性障害、不安症、不安うつ病、うつ病、認知障害、記憶障害、強迫性障害、無食欲症、過食症、ADHDのような注意異常症、てんかん、及び関連状態のような精神医学上の障害、並びに痴呆症、神経系障害(例、多発性硬化症)、レイノー症候群、パーキンソン病、ハンチントン舞踏病、及びアルツハイマー病のような神経系障害の治療に有用である。本化合物は、免疫、心臓血管系、生殖系、及び内分泌系の障害、敗血症ショック、呼吸系及び胃腸系に関連した疾患(例、下痢)の治療にも潜在的に有用である。本化合物は、長期乱用、嗜癖、及び/又は再発の適応症の治療、例えば、薬物(ニコチン、エタノール、コカイン、オピエート、等)依存症を治療すること、及び/又は薬物(ニコチン、エタノール、コカイン、オピエート、等)禁断症状を治療することの薬剤としても潜在的に有用である。本化合物は、禁煙に通常付随する、体重の増加を消失させる可能性もある。
式(I)の化合物は、肥満、精神異常症、精神分裂病、双極性障害、不安症、不安うつ病、うつ病、認知障害、記憶障害、強迫性障害、無食欲症、過食症、ADHDのような注意異常症、てんかん、及び関連状態のような精神医学上の障害、並びに痴呆症、神経系障害(例、多発性硬化症)、レイノー症候群、パーキンソン病、ハンチントン舞踏病、及びアルツハイマー病のような神経系障害の治療に有用である。本化合物は、免疫、心臓血管系、生殖系、及び内分泌系の障害、敗血症ショック、呼吸系及び胃腸系に関連した疾患(例、下痢)の治療にも潜在的に有用である。本化合物は、長期乱用、嗜癖、及び/又は再発の適応症の治療、例えば、薬物(ニコチン、エタノール、コカイン、オピエート、等)依存症を治療すること、及び/又は薬物(ニコチン、エタノール、コカイン、オピエート、等)禁断症状を治療することの薬剤としても潜在的に有用である。本化合物は、禁煙に通常付随する、体重の増加を消失させる可能性もある。
別の側面において、本発明は、医薬品として使用するための、上記に定義される通りの式Iの化合物を提供する。
さらなる側面において、本発明は、肥満、精神異常症、精神分裂病、双極性障害、不安症、不安うつ病、うつ病、認知障害、記憶障害、強迫性障害、無食欲症、過食症、ADHDのような注意異常症、てんかん、及び関連状態のような精神医学障害、痴呆症、神経系障害(例、多発性硬化症)、パーキンソン病、ハンチントン舞踏病、及びアルツハイマー病のような神経系障害、免疫、心臓血管系、生殖系、及び内分泌系の障害、敗血症ショック、呼吸系及び胃腸系に関連した疾患(例、下痢)、及び、長期乱用、嗜癖、及び/又は再発の適応症(例えば、薬物(ニコチン、エタノール、コカイン、オピエート、等)依存症を治療すること、及び/又は薬物(ニコチン、エタノール、コカイン、オピエート、等)禁断症状を治療すること)の治療又は予防用の医薬品の製造における、式Iの化合物の使用を提供する。
さらなる側面において、本発明は、肥満、精神異常症、精神分裂病、双極性障害、不安症、不安うつ病、うつ病、認知障害、記憶障害、強迫性障害、無食欲症、過食症、ADHDのような注意異常症、てんかん、及び関連状態のような精神医学障害、痴呆症、神経系障害(例、多発性硬化症)、パーキンソン病、ハンチントン舞踏病、及びアルツハイマー病のような神経系障害、免疫、心臓血管系、生殖系、及び内分泌系の障害、敗血症ショック、呼吸系及び胃腸系に関連した疾患(例、下痢)、及び、長期乱用、嗜癖、及び/又は再発の適応症(例えば、薬物(ニコチン、エタノール、コカイン、オピエート、等)依存症を治療すること、及び/又は薬物(ニコチン、エタノール、コカイン、オピエート、等)禁断症状を治療すること)の治療又は予防用の医薬品の製造における、式Iの化合物の使用を提供する。
なおさらなる側面において、本発明は、肥満、精神異常症、精神分裂病、双極性障害、不安症、不安うつ病、うつ病、認知障害、記憶障害、強迫性障害、無食欲症、過食症、ADHDのような注意異常症、てんかん、及び関連状態のような精神医学障害、痴呆症、神経系障害(例、多発性硬化症)、パーキンソン病、ハンチントン舞踏病、及びアルツハイマー病のような神経系障害、免疫、心臓血管系、生殖系、及び内分泌系の障害、敗血症ショック、呼吸系及び胃腸系に関連した疾患(例、下痢)、及び、長期乱用、嗜癖、及び/又は再発の適応症(例えば、薬物(ニコチン、エタノール、コカイン、オピエート、等)依存症を治療すること、及び/又は薬物(ニコチン、エタノール、コカイン、オピエート、等)禁断症状を治療すること)を治療する方法を提供し、該方法は、式Iの化合物の薬理学的有効量をその必要な患者へ投与することを含む。
本発明の化合物は、例えば、食欲及び体重の抑制、減量の維持、及びリバウンドの予防によって、肥満の治療に特に適している。
組合せ療法
本発明の化合物は、高血圧症、高脂血症、脂質異常症、糖尿病、及びアテローム性動脈硬化症のような、肥満の進展及び進行に関連した障害の治療に有用である別の治療薬剤と組み合わせてよい。例えば、本発明の化合物は、熱産生、脂肪分解、脂肪吸収、満腹、又は腸管運動に影響を及ぼす化合物と組み合わせて使用してよい。本発明の化合物は、LDL:HDLの比を減少させる別の薬剤、又はLDL−コレステロールの循環レベルの減少を引き起こす別の治療薬剤と組み合わせてよい。糖尿病の患者では、微小血管症に関連した合併症を治療するために使用する治療薬剤と本発明の化合物を組み合わせてもよい。
組合せ療法
本発明の化合物は、高血圧症、高脂血症、脂質異常症、糖尿病、及びアテローム性動脈硬化症のような、肥満の進展及び進行に関連した障害の治療に有用である別の治療薬剤と組み合わせてよい。例えば、本発明の化合物は、熱産生、脂肪分解、脂肪吸収、満腹、又は腸管運動に影響を及ぼす化合物と組み合わせて使用してよい。本発明の化合物は、LDL:HDLの比を減少させる別の薬剤、又はLDL−コレステロールの循環レベルの減少を引き起こす別の治療薬剤と組み合わせてよい。糖尿病の患者では、微小血管症に関連した合併症を治療するために使用する治療薬剤と本発明の化合物を組み合わせてもよい。
本発明の化合物は、肥満とその関連合併症、代謝症候群、及び2型糖尿病の治療用の他の療法とともに使用してよく、これらには、ビグアニド薬、インスリン(合成インスリン類似体)、及び経口の抗高脂血症剤(これらは、食事グルコース調節剤とα−グルコシダーゼ阻害剤へ分類される)が含まれる。
本発明の別の側面において、式Iの化合物、又はその医薬的に許容される塩は、PPTR調節剤とともに投与してよい。PPAR調節剤には、限定されないが、PPARα及び/又はγ−アゴニスト又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグが含まれる。好適なPPARα及び/又はγ−アゴニスト、その医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグは、当該技術分野でよく知られている。
さらに、本発明の組合せは、スルホニル尿素と一緒に使用してよい。本発明には、コレステロール降下剤と組み合わせた本発明の化合物も含まれる。本出願において言及されるコレステロール降下剤には、限定されないが、HMG−CoAレダクターゼ(3−ヒドロキシ−3−メチルグルタリル補酵素Aレダクターゼ)の阻害剤が含まれる。好適には、HMG−CoAレダクターゼ阻害剤は、スタチンである。
本出願において、用語「コレステロール降下剤」には、エステル、プロドラッグ、及び代謝産物のような、HMG−CoAレダクターゼ阻害剤の化学修飾物も、活性であれ不活性であれ、含まれる。
本発明には、回腸胆汁酸輸送系の阻害剤(IBAT阻害剤)と組み合わせた本発明の化合物も含まれる。本発明には、胆汁酸結合樹脂と組み合わせた本発明の化合物も含まれる。
本発明には、胆汁酸封鎖剤、例えば、コレスチポール又はコレスチラミン又はコレスタゲルと組み合わせた本発明の化合物も含まれる。
本発明の追加のさらなる側面によれば、式Iの化合物、又はその医薬的に許容される塩の有効量を、場合により医薬的に許容される希釈剤又は担体と一緒に、以下より選択される1若しくはそれより多くの薬剤:
CETP(コレステリルエステル転移タンパク質)阻害剤;
コレステロール吸収アンタゴニスト;
MTP(ミクロソーム転移タンパク質)阻害剤;
ニコチン酸誘導体(徐放性製品及び組合せ製品が含まれる);
フィトステロール化合物;
プロブコール;
抗凝固薬;
ω−3脂肪酸;
別の抗肥満化合物;
降圧化合物(例えば、アンギオテンシン変換酵素(ACE)阻害剤、アンギオテンシンII受容体アンタゴニスト、アドレナリン作用ブロッカー、α−アドレナリン作用ブロッカー、β−アドレナリン作用ブロッカー、混合型α/β−アドレナリン作用ブロッカー、アドレナリン作用刺激薬、カルシウムチャネルブロッカー、AT−1ブロッカー、塩排泄利尿薬、利尿薬、又は血管拡張薬);
メラニン濃縮ホルモン(MCH)アンタゴニスト;
PDK阻害剤;又は
核受容体のモジュレーター、例えばLXR、FXR、RXR、及びRORα;
SSRI;
セロトニンアンタゴニスト;
又はこれらの医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグとの同時、連続、又は分離した投与で、場合により医薬的に許容される希釈剤又は担体と一緒に、そのような治療的処置の必要なヒトのような温血動物へ投与することを含む、組合せ治療が提供される。
本発明の追加のさらなる側面によれば、式Iの化合物、又はその医薬的に許容される塩の有効量を、場合により医薬的に許容される希釈剤又は担体と一緒に、以下より選択される1若しくはそれより多くの薬剤:
CETP(コレステリルエステル転移タンパク質)阻害剤;
コレステロール吸収アンタゴニスト;
MTP(ミクロソーム転移タンパク質)阻害剤;
ニコチン酸誘導体(徐放性製品及び組合せ製品が含まれる);
フィトステロール化合物;
プロブコール;
抗凝固薬;
ω−3脂肪酸;
別の抗肥満化合物;
降圧化合物(例えば、アンギオテンシン変換酵素(ACE)阻害剤、アンギオテンシンII受容体アンタゴニスト、アドレナリン作用ブロッカー、α−アドレナリン作用ブロッカー、β−アドレナリン作用ブロッカー、混合型α/β−アドレナリン作用ブロッカー、アドレナリン作用刺激薬、カルシウムチャネルブロッカー、AT−1ブロッカー、塩排泄利尿薬、利尿薬、又は血管拡張薬);
メラニン濃縮ホルモン(MCH)アンタゴニスト;
PDK阻害剤;又は
核受容体のモジュレーター、例えばLXR、FXR、RXR、及びRORα;
SSRI;
セロトニンアンタゴニスト;
又はこれらの医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグとの同時、連続、又は分離した投与で、場合により医薬的に許容される希釈剤又は担体と一緒に、そのような治療的処置の必要なヒトのような温血動物へ投与することを含む、組合せ治療が提供される。
故に、本発明の追加の特徴において、肥満とその関連合併症をその治療の必要なヒトのような温血動物において治療する方法が提供され、該方法は、この組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、その医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグの有効量との同時、連続、又は分離した投与において式Iの化合物、又はその医薬的に許容される塩の有効量を前記動物へ投与することを含む。
故に、本発明の追加の特徴において、高脂血症状態をその治療の必要なヒトのような温血動物において治療する方法が提供され、該方法は、この組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグの有効量との同時、連続、又は分離した投与において式Iの化合物、又はその医薬的に許容される塩の有効量を前記動物へ投与することを含む。
本発明のさらなる側面によれば、式Iの化合物、又はその医薬的に許容される塩とこの組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグを医薬的に許容される希釈剤又は担体とともに含む医薬組成物が提供される。
本発明のさらなる側面によれば、式Iの化合物、又はその医薬的に許容される塩とこの組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグを含むキットが提供される。
本発明のさらなる側面によれば:
a)式Iの化合物、又はその医薬的に許容される塩を第一の単位剤形において;
b)この組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグを第二の単位剤形において;そして
c)前記第一及び第二の剤形を含有するためのコンテナ手段を含むキットが提供される。
a)式Iの化合物、又はその医薬的に許容される塩を第一の単位剤形において;
b)この組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグを第二の単位剤形において;そして
c)前記第一及び第二の剤形を含有するためのコンテナ手段を含むキットが提供される。
本発明のさらなる側面によれば:
a)式Iの化合物、又はその医薬的に許容される塩を医薬的に許容される希釈剤又は担体と一緒に第一の単位剤形において;
b)この組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグを第二の単位剤形において;そして
c)前記第一及び第二の剤形を含有するためのコンテナ手段を含むキットが提供される。
a)式Iの化合物、又はその医薬的に許容される塩を医薬的に許容される希釈剤又は担体と一緒に第一の単位剤形において;
b)この組合せ療法の節に記載の他の化合物のクラスの1つからの化合物、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグを第二の単位剤形において;そして
c)前記第一及び第二の剤形を含有するためのコンテナ手段を含むキットが提供される。
本発明の別の特徴によれば、式Iの化合物又はその医薬的に許容される塩と、この組合せ療法の節に記載の他の化合物の1つ又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグの、肥満とその関連合併症のヒトのような温血動物における治療に使用の医薬品の製造における使用が提供される。
本発明の別の特徴によれば、式Iの化合物又はその医薬的に許容される塩と、この組合せ療法の節に記載の他の化合物の1つ又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグの、高脂血症状態のヒトのような温血動物における治療に使用の医薬品の製造における使用が提供される。
本発明のさらなる側面によれば、医薬的に許容される希釈剤又は担体と随意に一緒の式Iの化合物又はその医薬的に許容される塩の有効量を、医薬的に許容される希釈剤又は担体と随意に一緒のこの組合せ療法の節に記載の他の化合物の1つ、又はその医薬的に許容される塩、溶媒和物、そのような塩の溶媒和物、又はこれらのプロドラッグの有効量の同時、連続、又は分離した投与とともに、そのような治療的処置の必要なヒトのような温血動物へ投与することを含む、組合せ治療が提供される。
さらに、本発明の化合物は、肥満に関連した障害又は状態(II型糖尿病、代謝症候群、脂質異常症、耐糖能低下、高血圧症、冠動脈性心疾患、非アルコール性脂肪便(steatorheic)肝炎、骨関節炎、及びある種の癌のような)と精神医学系及び神経系の状態の治療に有用である治療薬剤と組み合わせてもよい。
実験の部
略語:
DCM−ジクロロメタン
DMF−ジメチルホルムアミド
DMAP−4−ジメチルアミノピリジン
EDC−1−(3−ジメチルアミノプロピル)−3−エチルカルボジイミド
TEA−トリエチルアミン
TFA−トリフルオロ酢酸
DMSO−ジメチルスルホキシド
DEA−ジエチルアミン
PCC−クロロクロム酸ピリジニウム
PyBOP−ベンゾトリアゾール−1−イル−オキシトリ−ピロリジノホスホニウムヘキサフルオロリン酸塩
HBTU−O−ベンゾトリアゾール−1−イル−N,N,N’,N’−テトラメチルウロニウムヘキサフルオロリン酸塩
DAST−三フッ化(ジエチルアミノ)イオウ
DIEA−N,N−ジイソプロピルエチルアミン
THF−テトラヒドロフラン
FA−ギ酸
t 三重項
s 一重項
d 二重項
q 四重項
qvint 五重項
m 多重項
br ブロード
bs ブロード一重項
dm 多重項の二重項
bt ブロード三重項
dd 二重項の二重項
一般的な実験手順
質量スペクトルは、いずれも空気支援エレクトロスプレーインターフェイス装着式(LC−MS)Micromass ZQ単一四重極又はMicromass LCZ単一四重極のいずれかの質量分析計で記録した。1H NMR測定は、300及び500MHzの1H振動数でそれぞれ作動する、Varian Mercury 300又はVarian Inova 500のいずれかで実施した。化学シフトは、CDCl3を内部標準としてppmで示す。他に述べなければ、NMRの溶媒としてCDCl3を使用する。質量起動式フラクションコレクター付き半分取用HPLC、19x100mm C8カラム装着式のShimadzu QP 8000単一四重極質量分析計で精製を実施した。使用する移動相は、他に何も述べなければ、アセトニトリルと緩衝液(0.1M NH4Ac:アセトニトリル 95:5)であった。
略語:
DCM−ジクロロメタン
DMF−ジメチルホルムアミド
DMAP−4−ジメチルアミノピリジン
EDC−1−(3−ジメチルアミノプロピル)−3−エチルカルボジイミド
TEA−トリエチルアミン
TFA−トリフルオロ酢酸
DMSO−ジメチルスルホキシド
DEA−ジエチルアミン
PCC−クロロクロム酸ピリジニウム
PyBOP−ベンゾトリアゾール−1−イル−オキシトリ−ピロリジノホスホニウムヘキサフルオロリン酸塩
HBTU−O−ベンゾトリアゾール−1−イル−N,N,N’,N’−テトラメチルウロニウムヘキサフルオロリン酸塩
DAST−三フッ化(ジエチルアミノ)イオウ
DIEA−N,N−ジイソプロピルエチルアミン
THF−テトラヒドロフラン
FA−ギ酸
t 三重項
s 一重項
d 二重項
q 四重項
qvint 五重項
m 多重項
br ブロード
bs ブロード一重項
dm 多重項の二重項
bt ブロード三重項
dd 二重項の二重項
一般的な実験手順
質量スペクトルは、いずれも空気支援エレクトロスプレーインターフェイス装着式(LC−MS)Micromass ZQ単一四重極又はMicromass LCZ単一四重極のいずれかの質量分析計で記録した。1H NMR測定は、300及び500MHzの1H振動数でそれぞれ作動する、Varian Mercury 300又はVarian Inova 500のいずれかで実施した。化学シフトは、CDCl3を内部標準としてppmで示す。他に述べなければ、NMRの溶媒としてCDCl3を使用する。質量起動式フラクションコレクター付き半分取用HPLC、19x100mm C8カラム装着式のShimadzu QP 8000単一四重極質量分析計で精製を実施した。使用する移動相は、他に何も述べなければ、アセトニトリルと緩衝液(0.1M NH4Ac:アセトニトリル 95:5)であった。
異性体の単離には、Kromasil CN E9344(250x20mm内径)カラムを使用した。移動相(1ml/分)としてヘプタン:酢酸エチル:DEA 95:5:0.1を使用した。UV検出器(330nm)を使用して、分画採取を導いた。
精製は、他に何も述べなければ、充填済カラム(Si 12+M又はSi 25+M)を使用するBiotage Horizon HPFC Systemで実施した。UV検出器(254nm)を使用して、分画採取を導いた。
出発材料及び中間体の製法
工程A:1,2−ビス(4−クロロフェニル)−2−ヒドロキシエタノン
工程A:1,2−ビス(4−クロロフェニル)−2−ヒドロキシエタノン
4−クロロベンズアルデヒド(140.6g,1モル)のエタノール(130ml)懸濁液へシアン化ナトリウム(10.6g,0.216モル)の水(105ml)溶液を加えた。この混合物を還流で2.5時間加熱してから、塩化メチレンで抽出した。有機相を酸性亜硫酸ナトリウム溶液で洗浄して、溶媒を蒸発させた。ジエチルエーテル/ヘプタンからの結晶化により化合物を単離した。48g,34%。
1H NMR (400 MHz) δ 7.82 (d, 2H), 7.38 (d, 2H), 7.30 (d, 2H), 7.24 (d, 2H), 5.87 (s, 1H), 4.47 (s, 1H).
MS m/z 279, 281 (M-H)-。
MS m/z 279, 281 (M-H)-。
工程B:1,2−ビス(4−クロロフェニル)エタン−1,2−ジオン
1,2−ビス(4−クロロフェニル)−2−ヒドロキシエタノン(90g,0.320モル)と硝酸(170ml)を100℃で加熱すると、4時間後に酸化窒素の発生が止んだ。この反応混合物を冷やして、水(250ml)を注意深く加えた。この粗生成物を濾過し、水で数回洗浄し、減圧で乾燥させて、表題化合物(40.4g,45%)を黄色い固形物として得た。
1H NMR (500 MHz) δ 7.94 (d, 4H), 7.53 (d, 4H).
工程C:5,6−ビス−(4−クロロフェニル)ピラジン−2−カルボン酸
工程C:5,6−ビス−(4−クロロフェニル)ピラジン−2−カルボン酸
2,3−ジアミノプロピオン酸の一塩酸塩(2.5g,17.78ミリモル)と1,2−ビス(4−クロロフェニル)エタン−1,2−ジオン(4.965g,17.78ミリモル)を水酸化ナトリウム(3.0g,75ミリモル)のメタノール(100ml)溶液に溶かして、アルゴン下に2時間還流させた。空気を泡立てて通して、反応を室温で20時間続けた。メタノールを蒸発させて、生成物を水に再び溶かした。この混合物がpH2に達するまで、塩酸(2M水溶液)を加えた。この溶液をジエチルエーテルで抽出し、MgSO4で乾燥させた。メタノールからの再結晶により、表題化合物(1.57g,26%)を得た。
1H NMR (399.964 MHz) δ 9.41 (s, 1H), 7.48-7.32 (m, 8H).
MS m/z 343, 345, 347 (M-H)-。
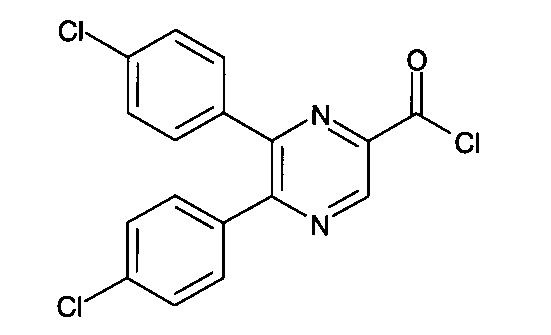
工程D:5,6−ビス(4−クロロフェニル)ピラジン−2−カルボニルクロリド
MS m/z 343, 345, 347 (M-H)-。
工程D:5,6−ビス(4−クロロフェニル)ピラジン−2−カルボニルクロリド
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸、中間体C(485mg,1.41ミリモル)のDCM(5ml)懸濁液へ塩化オキサリル(1ml,7.88ミリモル)のDCM(10ml)及びDMF(0.2ml)溶液を室温で加えた。溶媒と未反応の塩化オキサリルを蒸発させた。この粗生成物をさらに精製せずに使用した。
工程E:[5,6−ビス(4−クロロフェニル)ピラジン−2−イル]メタノール
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸、中間体C(900mg,2.61ミリモル)のTHF(25ml)懸濁液へクロロギ酸エチル(340mg,3.13ミリモル)とDIEA(505mg,3.91ミリモル)を加えた。この混合物を室温で5時間撹拌した。メタノール(2ml)を加えてから、NaBH4(600mg,15.86ミリモル)を0℃で少量ずつ加えた。撹拌を0℃でさらに1時間続けた。ジエチルエーテル(15ml)を加えて、生成物をジエチルエーテルで抽出した。エーテル相をMgSO4で乾燥させた。フラッシュクロマトグラフィー(SiO2,トルエン:酢酸エチル)による精製によって、表題化合物(230mg,44%)を得た。
1H NMR (400 MHz) δ 8.61 (s, 1H), 7.27-7.22 (m, 4H), 7.36-7.30 (m, 4H), 4.81 (s, 2H), 4.60-4.10 (br, 1H).
13C NMR (100 MHz) δ 153.28, 150.23, 150.15, 140. 45, 136.64, 136.62, 135.46, 135.33, 131.23, 129.27, 128. 94, 63.16.
MS m/z 331, 333, 335 (M+H)+。
13C NMR (100 MHz) δ 153.28, 150.23, 150.15, 140. 45, 136.64, 136.62, 135.46, 135.33, 131.23, 129.27, 128. 94, 63.16.
MS m/z 331, 333, 335 (M+H)+。
実施例1
5,6−ビス(4−クロロフェニル)−N−(cis−2−ヒドロキシシクロヘキシル)ピラジン−2−カルボキサミド
5,6−ビス(4−クロロフェニル)−N−(cis−2−ヒドロキシシクロヘキシル)ピラジン−2−カルボキサミド
cis−2−シクロヘキサノール塩酸塩(107mg,0.71ミリモル),5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸(200mg,0.579ミリモル)、及びTEA(0.5ml)を5ml DCMに溶かして、0℃へ冷やした。PyBOP(0.539mg,1.04ミリモル)の1ml DCM溶液を滴下した。温度を0℃に15分間保った。反応を室温で3時間続けた。この混合物を水で洗浄して、MgSO4で乾燥させた。これをフラッシュクロマトグラフィー(SiO2,100%トルエン〜100%酢酸エチルの勾配)により精製して、表題化合物(216mg,84%)を得た。
1H NMR (399.964 MHz) δ 9.32 (s, 1H), 8.16 (d, 1H), 7.46-7.27 (m, 8H), 4.22-4.10 (m, 1H), 4.09-4.02 (br, 1H), 2.24-2.13 (br, 1H), 1.87-1.54 (m, 6H), 1.54-1.37 (m, 2H).
13C NMR (100.58 MHz) δ 162.80, 153.86, 149.46, 142.14, 141.94, 136.27, 136.03, 135.83, 131.30, 131.18, 129.10, 129.05, 69.26, 51.29, 32.11, 27.35, 23.96, 20.04.
MS m/z 442, 444, 446 (M+H)+。
13C NMR (100.58 MHz) δ 162.80, 153.86, 149.46, 142.14, 141.94, 136.27, 136.03, 135.83, 131.30, 131.18, 129.10, 129.05, 69.26, 51.29, 32.11, 27.35, 23.96, 20.04.
MS m/z 442, 444, 446 (M+H)+。
実施例2
5,6−ビス(4−クロロフェニル)−N−(trans−2−ヒドロキシシクロヘキシル)ピラジン−2−カルボキサミド
5,6−ビス(4−クロロフェニル)−N−(trans−2−ヒドロキシシクロヘキシル)ピラジン−2−カルボキサミド
trans−2−シクロヘキサノール塩酸塩(107mg,0.71ミリモル)と5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸(200mg,0.579ミリモル)を実施例1に記載のように反応させて、表題化合物(179mg,70%)を得た。
1H NMR (399.964 MHz) δ 9.34 (s, 1H), 7.79 (d, 1H), 7.44-7.26 (m, 8H), 3.95-3.80 (m, 1H), 3.55-3.43 (m, 1H), 3.34-2.79 (br, 1H), 2.20-2.00 (m, 2H), 1.87-1.66 (m, 2H), 1.50-1.18 (m, 4H).
13C NMR (100.58 MHz, CDCL3) δ 164.23, 154.11, 149.56, 142.14, 141.79, 136.24, 136.11, 135.89, 131.32, 131.18, 129.05, 129.14, 75.13, 56.11, 34.77, 31.76, 24.81, 24.32.
MS m/z 442, 444, 446 (M+H)+。
13C NMR (100.58 MHz, CDCL3) δ 164.23, 154.11, 149.56, 142.14, 141.79, 136.24, 136.11, 135.89, 131.32, 131.18, 129.05, 129.14, 75.13, 56.11, 34.77, 31.76, 24.81, 24.32.
MS m/z 442, 444, 446 (M+H)+。
実施例3
5,6−ビス(4−クロロフェニル)−N−(trans−4−ヒドロキシシクロヘキシル)ピラジン−2−カルボキサミド
5,6−ビス(4−クロロフェニル)−N−(trans−4−ヒドロキシシクロヘキシル)ピラジン−2−カルボキサミド
trans−4−シクロヘキサノール塩酸塩(107mg,0.71ミリモル)と5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸(200mg,0.579ミリモル)を実施例1に記載のように反応させて、表題化合物(231mg,90%)を得た。
1H NMR (399.964 MHz) δ 9.37 (s, 1H), 7.61 (d, 1H), 7.44-7.27 (m, 8H), 4.07-3.93 (m, 1H), 3.73-3.60 (m, 1H), 2.17-1.99 (m, 4H), 1.76-1.62 (br, 1H), 1.56-1.32 (m, 4H).
13C NMR (100.58 MHz) δ 162.41, 153.94, 149.48, 142.11, 142.11, 136.32, 136.18, 136.06, 135.87, 131.31, 131.16, 129.14, 129.06, 69.94, 48.01, 34.18, 30.98.
MS m/z 442, 444, 446 (M+H)+。
13C NMR (100.58 MHz) δ 162.41, 153.94, 149.48, 142.11, 142.11, 136.32, 136.18, 136.06, 135.87, 131.31, 131.16, 129.14, 129.06, 69.94, 48.01, 34.18, 30.98.
MS m/z 442, 444, 446 (M+H)+。
実施例4
5,6−ビス(4−クロロフェニル)−N−(4,4−ジフルオロシクロヘキシル)ピラジン−2−カルボキサミド
5,6−ビス(4−クロロフェニル)−N−(4,4−ジフルオロシクロヘキシル)ピラジン−2−カルボキサミド
工程A (4,4−ジフルオロシクロヘキシル)アミン
N−4−Boc−シクロヘキサノン(600mg,2.81ミリモル)のDCM(3ml)溶液へ0℃でDAST(455mg,2.81ミリモル)を滴下した。70分後、温度を室温へ高めて、3時間後、5分間還流させた。溶媒を真空で除去して、生成物をフラッシュカラム(シリカゲル、100%トルエン〜100% EtOAc)で精製した。このBoc保護化材料のメタノール(5ml)懸濁液を塩化チオニル(2ml,27.57ミリモル)のメタノール(20ml)溶液で滴下処理した。この反応を室温で30分間続けた。溶媒を真空で蒸発させた。粗製材料をピリジン(5ml)に再び取り、クロロギ酸ベンジル(532mg,3.12ミリモル)の1ml DCM溶液で処理した。この混合物を58時間撹拌した。これをHCl(水溶液)とK2CO3(水溶液)で洗浄した。このZ保護化化合物をフラッシュクロマトグラフィー(SiO2,トルエン)により精製した。212mg(28%)。パラジウム担持活性炭(40mg,10重量% Pd)入りのTHF(10ml)においてH2気体下に4時間撹拌することによって、Z基を外した。これをCelite 521に通して濾過して、真空で蒸発させて、粗製材料を得た。
工程B 5,6−ビス(4−クロロフェニル)−N−(4,4−ジフルオロシクロヘキシル)ピラジン−2−カルボキサミド
(4,4−ジフルオロシクロヘキシル)アミンと5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸(200mg,0.579ミリモル)を実施例1に記載のように反応させた。DCMの代わりにTHF(60ml)を使用した。生成物を分取用HPLC(kromasil C8カラム、酢酸アンモニウム(0.1M水溶液):アセトニトリル)で精製して、表題化合物(116mg,43%)を白い粉末として得た。
(4,4−ジフルオロシクロヘキシル)アミンと5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸(200mg,0.579ミリモル)を実施例1に記載のように反応させた。DCMの代わりにTHF(60ml)を使用した。生成物を分取用HPLC(kromasil C8カラム、酢酸アンモニウム(0.1M水溶液):アセトニトリル)で精製して、表題化合物(116mg,43%)を白い粉末として得た。
1H NMR (399.964 MHz) δ 9.35 (s, 1H), 7.69 (d, 1H), 7.43-7.28 (m, 8H), 4.20-4.08 (m, 1H), 2.21-2.06 (m, 4H), 2.03-1.83 (m, 2H), 1.78-1.64 (m, 2H).
13C NMR (100.58 MHz) δ 162.55, 154.13, 149.57, 142.03, 141.80, 136.19, 136.12, 135.94, 131.30, 131.13, 129.17, 129.06, 122.53 (t), 46.61, 32.47 (t), 28.90, 28.81.
MS m/z 462, 464, 466 (M+H)+。
13C NMR (100.58 MHz) δ 162.55, 154.13, 149.57, 142.03, 141.80, 136.19, 136.12, 135.94, 131.30, 131.13, 129.17, 129.06, 122.53 (t), 46.61, 32.47 (t), 28.90, 28.81.
MS m/z 462, 464, 466 (M+H)+。
実施例5
工程A:3−({[5,6−ビス(4−クロロフェニル)ピラジン−2−イル]カルボニル}アミノ)ピペリジン−1−カルボン酸tert−ブチル
工程A:3−({[5,6−ビス(4−クロロフェニル)ピラジン−2−イル]カルボニル}アミノ)ピペリジン−1−カルボン酸tert−ブチル
DCM(1ml)に溶かしたPyBOP(508mg,0.976ミリモル)をDCM(5ml)及びTEA(0.5ml)に溶かした3−アミノピペリジン−1−カルボン酸tert−ブチル(151mg,0.754ミリモル)及び5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸(200mg,0.579ミリモル)へ0℃で加えた。この反応を0℃で15分間、その後室温で3時間続けた。この溶液を水で抽出して、MgSO4で乾燥させた。最後に、生成物をフラッシュクロマトグラフィー(SiO2,トルエン:酢酸エチル 9:1)により精製して、副題化合物(263mg,86%)を得た。
1H NMR (400 MHz, CDCl3) δ 9.34 (s, 1H), 8.12-7.72 (br, 1H), 7.42-7.24 (m, 8H), 4.20-4.09 (m, 1H), 3.74-3.32 (m, 4H), 1.98-1.48 (m, 4H), 1.34 (s, 9H).
13C NMR (100 MHz, CDCl3) δ 162.59, 155.20, 153.94, 149.54, 141.93, 136.21, 135.99, 135.76, 131.29, 131.16, 129.20, 129.09, 128.99, 80.06, 48.39, 45.72, 43.84, 29.95, 28.48, 22.73.
+MS m/z 527, 529, 531 (M+H)+。
工程B:5,6−ビス(4−クロロフェニル)−N−ピペリジン−3−イルピラジン−2−カルボキサミド塩酸塩
13C NMR (100 MHz, CDCl3) δ 162.59, 155.20, 153.94, 149.54, 141.93, 136.21, 135.99, 135.76, 131.29, 131.16, 129.20, 129.09, 128.99, 80.06, 48.39, 45.72, 43.84, 29.95, 28.48, 22.73.
+MS m/z 527, 529, 531 (M+H)+。
工程B:5,6−ビス(4−クロロフェニル)−N−ピペリジン−3−イルピラジン−2−カルボキサミド塩酸塩
メタノール(10ml)に溶かした塩化チオニル(1ml,13.79ミリモル)2mlメタノールに溶かした3−({[5,6−ビス(4−クロロフェニル)ピラジン−2−イル]カルボニル}アミノ)ピペリジン−1−カルボン酸tert−ブチル(263mg,0.498ミリモル)へ滴下した。この反応を室温で1時間続け、その後で溶媒を蒸発させて、生成物を凍結乾燥させた。副題化合物(230mg,99%)を白い粉末として得た。
1H NMR (400 MHz, CDCl3)δ 10.00-9.68 (br, 2H), 9.28 (s, 1H), 8.22 (d, 1H), 7.54-7.28 (m, 8H), 4.64-4.50 (m, 1H), 3.60-3.48 (m, 1H), 3.34-3.21 (m, 2H), 3.21-3.11 (m, 1H), 2.07-1.98 (m, 3H), 1.98-1.86 (m, 1H).
13C NMR (100 MHz, CDCl3)δ 163.33, 154.19, 149.74, 141.87, 141.43, 136.13, 136.09, 135.99, 135.81, 131.55, 131.28, 129.02, 47.17, 44.11, 43.81, 28.40, 20.44.
HRMS [C22H21N4OCl2]+の計算値:427.109.実測値:427.110.
工程C:N−(1−アセチルピペリジン−3−イル)−5,6−ビス(4−クロロフェニル)ピラジン−2−カルボキサミド
13C NMR (100 MHz, CDCl3)δ 163.33, 154.19, 149.74, 141.87, 141.43, 136.13, 136.09, 135.99, 135.81, 131.55, 131.28, 129.02, 47.17, 44.11, 43.81, 28.40, 20.44.
HRMS [C22H21N4OCl2]+の計算値:427.109.実測値:427.110.
工程C:N−(1−アセチルピペリジン−3−イル)−5,6−ビス(4−クロロフェニル)ピラジン−2−カルボキサミド
2ml DCMに溶かした塩化アセチル(100mg,1.27ミリモル)を3.5mlピリジンに溶かした5,6−ビス(4−クロロフェニル)−N−ピペリジン−3−イルピラジン−2−カルボキサミド塩酸塩(67.0mg,0.145ミリモル)へ加え、室温で2.5時間反応させた。水とジエチルエーテルを加え、相を分離させて、有機相をHCl(水溶液)、K2CO3(水溶液)で抽出し、MgSO4で乾燥させて、副題化合物(67.0mg,99%)をやや黄色の粉末として得た。
1H NMR (400 MHz, CDCl3, T=25℃, 回転異性体)δ 9.36 及び 9.32 (s, 1H); 8.02 及び 7.78 (d, 1H), 7.50-7.20 (m, 8H), 4.24-4.06 (m, 1H), 3.89 及び 3.76 (d, 2H), 3.52-3.40 及び3.35-3.24 (m, 2H), 2.14 及び2.11 (s, 3H), 2.12-2.02 及び2.02-1.88 (m, 2H), 1.82-1.70 及び1.70-1.58 (m, 2H).
13C NMR (100 MHz, CDCl3, T=25℃, 回転異性体)δ 170.05, 169.68, 162.95, 162.61, 154, 36, 153.89, 149.71, 149.32, 141.88, 141.73, 141.60, 141.48, 136.28, 136.20, 136.03, 135.88, 131.30, 131.10, 129.22, 129.09, 129.05, 51.04, 47.20, 46.48, 46.33, 46.01, 41.98, 30.21, 29.85, 23.40, 23.01, 21.76, 21.71.
HRMS [C24H22N4O2Cl2+H]+の計算値:469.120.実測値:469.119.
実施例6
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸tert−ブチル
13C NMR (100 MHz, CDCl3, T=25℃, 回転異性体)δ 170.05, 169.68, 162.95, 162.61, 154, 36, 153.89, 149.71, 149.32, 141.88, 141.73, 141.60, 141.48, 136.28, 136.20, 136.03, 135.88, 131.30, 131.10, 129.22, 129.09, 129.05, 51.04, 47.20, 46.48, 46.33, 46.01, 41.98, 30.21, 29.85, 23.40, 23.01, 21.76, 21.71.
HRMS [C24H22N4O2Cl2+H]+の計算値:469.120.実測値:469.119.
実施例6
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸tert−ブチル
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸(152mg,0.44ミリモル)をトルエン(5ml)中で77℃まで加熱した。ジtert−ブトキシメチル)ジメチルアミン(358mg,1.76ミリモル)を加え、この混合物を一晩(20時間)還流させた。水とジエチルエーテルを加えた。相を分離させて、有機相をNaHCO3(水溶液)と水で抽出した。最後に、生成物をフラッシュクロマトグラフィー(SiO2,トルエン)により精製して、やや黄色い粉末(92mg,52%)を得た。
1H NMR (400 MHz, CDCl3)δ 9.16 (s, 1H), 7.48-7.28 (m, 8H), 1.66 (s, 9H).
13C NMR (100 MHz, CDCl3)δ 162.96, 153.53, 151.09, 143.17, 142.06, 136.29, 136.23, 136.08, 135.76, 131.41, 131.28, 129.07, 129.01, 83.45, 28.33.
HRMS [C21H18N2O2Cl2+H]+の計算値:401.082.実測値:401.080.
実施例7
5,6−ビス(4−クロロフェニル)−ピラジン−2−イル]−(1,3−ジヒドロ−イソインドール−2−イル)−メタノン
13C NMR (100 MHz, CDCl3)δ 162.96, 153.53, 151.09, 143.17, 142.06, 136.29, 136.23, 136.08, 135.76, 131.41, 131.28, 129.07, 129.01, 83.45, 28.33.
HRMS [C21H18N2O2Cl2+H]+の計算値:401.082.実測値:401.080.
実施例7
5,6−ビス(4−クロロフェニル)−ピラジン−2−イル]−(1,3−ジヒドロ−イソインドール−2−イル)−メタノン
5,6−ビス(4−クロロフェニル)−ピラジン−2−カルボン酸(100mg,0.29ミリモル)、トリエチルアミン(0.81ml,20当量)、及びイソインドリン(48mg,1.4当量)をジクロロメタン(8ml)に懸濁させて、氷浴において0℃へ冷やした。ジクロロメタン(2ml)に溶かしたベンゾトリアゾール−1−イル−オキシトリ−ピロリジノホスホニウムヘキサフルオロリン酸塩(256mg,1.7当量)を滴下し、生じる懸濁液を0℃で15分間、次いで室温で3時間撹拌した。
この反応混合物をジクロロメタン(60ml)で希釈して、水(4x20ml)と塩水(20ml)で洗浄した。有機層を乾燥(MgSO4)させ、濾過して、減圧で濃縮した。残渣をフラッシュクロマトグラフィー(酢酸エチル−ヘプタン)により精製し、溶媒の除去の後で、生成物を淡黄色の固形物として得た。
1H-NMR (CDCl3): 5.12 (s, 2H), 5.33 (s, 2 H), 7.28-7.53 (m, 12H), 9.26 (s, 1H).
MS: m/z 446 (M+H)。
実施例8
2,3−ビス(4−クロロフェニル)−5−{[(4−フルオロベンジル)オキシ]メチル}ピラジン
MS: m/z 446 (M+H)。
実施例8
2,3−ビス(4−クロロフェニル)−5−{[(4−フルオロベンジル)オキシ]メチル}ピラジン
[5,6−ビス(4−クロロフェニル)ピラジン−2−イル]メタノール、中間体E(230mg,0.69ミリモル)をDCM(3ml)に溶かして、水(2ml)と混合した。NaOH(0.53mg,13.25ミリモル)と硫酸水素テトラブチルアンモニウム(18mg,0.05ミリモル)を室温で加えた。臭化4−フルオロベンジル(145mg,0.77ミリモル)を加えて、この混合物を室温で4時間撹拌した。ジエチルエーテル(10ml)を加え、生成物を水で抽出して、乾燥(MgSO4)させて、生成物(285mg,93%)を得た。
1H NMR (399.964 MHz)δ 8.78 (s, 1H), 7.41-7.35 (m, 6H), 7.31-7.27 (m, 4H), 7.09-7.01 (m, 2H), 4.79 (s, 2H), 4.69 (s, 2H)。
実施例9
2,3−ビス(4−クロロフェニル)−5−[(ピペリジン−1−イルオキシ)カルボニル]ピラジン
実施例9
2,3−ビス(4−クロロフェニル)−5−[(ピペリジン−1−イルオキシ)カルボニル]ピラジン
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボニルクロリド、中間体D(84mg,0.23ミリモル)のDCM(1ml)溶液へヒドロキシピペリジン(93mg,0.91ミリモル)のピリジン(5ml)溶液を室温でゆっくり加えた。室温で40分後、溶媒を真空で除去して、残渣をジエチルエーテルに再び溶かした。1M HCl(水溶液)とK2CO3(水溶液)で抽出して、乾燥(MgSO4)させた。溶媒を真空で除去して、副題化合物(58mg,59%)を得た。
1H NMR (399.964 MHz)δ 9.19 (s, 1H), 7.47-7.26 (m, 8H), 3.71-3.50 (m, 2H), 3.16-2.74 (m, 2H), 1.98-1.77 (m, 4H), 1.77-1.57 (m, 1H), 1.40-1.23 (m, 1H).
13C NMR (100.58 MHz)δ 162.59, 154.17, 151.20, 143.18, 140.79, 136.22, 136.17, 136.09, 135.89, 131.42, 131.29, 129.08, 129.04, 57.87, 25.30, 23.27.
MS m/z 428, 430, 432 (M+H)+.
薬理学的活性
本発明の化合物は、CB1遺伝子の受容体産物に対して活性がある。本発明の化合物の中枢カンナビノイド受容体へのアフィニティーは、Devane et al., Molecular Pharmacology, 1988, 34, 605 に記載の方法か、又はWO01/70700又はEP656354に記載の方法で実証可能である。あるいは、このアッセイは、以下のように実施してよい。
13C NMR (100.58 MHz)δ 162.59, 154.17, 151.20, 143.18, 140.79, 136.22, 136.17, 136.09, 135.89, 131.42, 131.29, 129.08, 129.04, 57.87, 25.30, 23.27.
MS m/z 428, 430, 432 (M+H)+.
薬理学的活性
本発明の化合物は、CB1遺伝子の受容体産物に対して活性がある。本発明の化合物の中枢カンナビノイド受容体へのアフィニティーは、Devane et al., Molecular Pharmacology, 1988, 34, 605 に記載の方法か、又はWO01/70700又はEP656354に記載の方法で実証可能である。あるいは、このアッセイは、以下のように実施してよい。
CB1遺伝子で安定的にトランスフェクトした細胞より調製した10μgの膜を200μlの100mM NaCl,5mM MgCl2,1mM EDTA,50mM HEPES(pH7.4),1mM DTT,0.1% BSA,及び100μM GDPに懸濁させた。これへEC80濃度のアゴニスト(CP55940)と、必要とされる濃度の試験化合物と0.1μCi[35S]−GTPγSを加えた。反応を30℃で45分間進行させた。次いで、細胞採取器を使用して、試料をGF/Bフィルター上へ移し、洗浄緩衝液(50mM Tris(pH7.4),5mM MgCl2,50mM NaCl)で洗浄した。次いで、フィルターをシンチラントでカバーして、フィルターの保持した[35S]−GTPγSの量を計数した。
活性は、全リガンドの非存在下(最小活性)又はEC80濃度のCP55940の存在下(最大活性)で測定する。これらの活性をそれぞれ0%と100%の活性として設定する。新規リガンドの様々な濃度で、最大活性の百分率として活性を計算して、プロットする。等式:y=A+((B−A)/1+((C/x)UD))を使用してデータを適合させて、使用する条件下でGTPγS結合の最大半値阻害をもたらすのに必要とされる濃度としてIC50値を決定する。
本発明の化合物は、CB1受容体で活性である(IC50<1マイクロモル濃度)。最も好ましい化合物は、200ナノモル濃度未満のIC50を有する。
式Iの化合物を、よりよい in vivo 効果をもたらす、その優れた in vitro 効力及び/又はより高いアフィニティーのために選択する。この化合物はまた、in vivo 安全性を改善すると期待される、よりよい選択性プロフィールを有する。
式Iの化合物を、よりよい in vivo 効果をもたらす、その優れた in vitro 効力及び/又はより高いアフィニティーのために選択する。この化合物はまた、in vivo 安全性を改善すると期待される、よりよい選択性プロフィールを有する。
さらに、本発明の化合物は、改善されたDMPK(薬物代謝及び薬物動態)特性、例えば改善されたin vitro 代謝安定性又はバイオアベイラビリティを有する可能性がある。本化合物はまた、改善された溶解性及び/又は有望な毒性学的プロフィールを有する。
Claims (20)
- 式(I):
Zは、C1−8アルキル基、C1−6アルコキシ基、ヒドロキシ、ハロ、トリフルオロメチル、トリフルオロメチルチオ、トリフルオロメトキシ、トリフルオロメチルスルホニル、ニトロ、モノ若しくはジC1−3アルキルアミド、C1−3アルキルスルホニル、C1−3アルキルスルホニルオキシ、C1−3アルコキシカルボニル、カルボキシ、シアノ、カルバモイル、モノ若しくはジC1−3アルキルカルバモイル、スルファモイル、アセチル、ハロ、アルキル、トリフルオロメチル又はトリフルオロメトキシにより置換されていてもよい芳香族複素環式基、及び、窒素、酸素、又はイオウより選択される1つ若しくはそれより多くのヘテロ原子を含有する飽和又は一部不飽和の5〜8員複素環式基を表し、ここで該複素環式基は、1つ若しくはそれより多くのC1−3アルキル基、ヒドロキシ、フルオロ、ベンジル、又はアミノ基:−NRxRy(式中、RxとRyは、独立してH又はC1−4アルキルを表す)により置換されていてもよく;
R3は、式:(CH2)nCOOR7:
{式中、nは、0、1、2、3又は4であり、R7は、C4−12アルキル基、C3−12シクロアルキル基、又は(C3−12シクロアルキル)C1−3アルキル基を表し、それらの各々は、以下のもの、即ち、C1−6アルキル基;フルオロ、アミノ、又はヒドロキシの1つ若しくはそれより多くにより置換されていてもよいか、又は
R7は、基:−(CH2)aフェニル(式中、aは、0、1、2、3又は4であり、フェニル基は、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により置換されていてもよい)を表すか、又は
R7は、以下のもの、即ち、酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、飽和又は一部不飽和の5〜8員複素環式基を表し、ここで該複素環式基は、1つ若しくはそれより多くのC1−3アルキル基、C1−3アシル基、ヒドロキシ、アミノ、又はベンジルにより置換されていてもよい}の基を表すか;又は
R3は、式:−(CH2)o−O−(CH2)p−R8{式中、oは、1、2、3又は4の整数を表し、pは、0、1、2、3又は4の整数を表し、そしてR8は、以下のもの、即ち、C1−6アルキル基;フルオロ、ヒドロキシ、又はアミノ基:−NRxRy(式中、RxとRyは、独立してH又はC1−4アルキルを表す)のうち1つ若しくはそれより多くにより置換されていてもよいC1−12アルキル基を表すか;
又は、R8は、1つ若しくはそれより多くのZ基により独立して置換されていてもよいフェニルを表すか、又はR8は、以下のもの、即ち、酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、芳香族複素環式基又は飽和若しくは一部不飽和の5〜8員複素環式基(ここで、これらの環のそれぞれは、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により置換されていてもよい)を表す}の基を表す;又は、
R3は、式:−(CH2)qR9{式中、qは、2、3又は4であり、R9は、C3−12シクロアルキル基、フェニル、以下のもの、即ち、酸素、イオウ又は窒素のうち1つ若しくはそれより多くを含有する、芳香族複素環式基又は飽和若しくは一部不飽和の5〜8員複素環式基(ここで、これらの環のそれぞれは、Zにより表される、同じでも異なってもよい1つ若しくはそれより多くの基により置換されていてもよい)を表す}の基を表す;又は、
R3は、式:−(CH2)m−O−(CO)−R10{式中、mは、0、1、2、3又は4の整数を表し、式中R10は、1つ若しくはそれより多くのフルオロ、ヒドロキシ、又はアミノにより置換されていてもよいC1−12アルキル基を表すか、又はR10は、式:−(CH2)qR9(式中、qとR9は、上記に記載される通りである)の基を表す}の基を表す;又は、
R3は、以下の式:
dは、1、2又は3であり、そして
R12は、H又はC1−3アルキル基を表す}の基を有する;又は
R3は、式:CONH−Rz(式中、Rzは、C1−6アルカノイル基により置換されるピペリジニル環である)の基を表すか、又はR3は、基:−COG(式中、Gは、窒素を介してカルボニルへ連結するジヒドロインドール又はジヒドロイソインドールである)の基を表す]の化合物とその医薬的に許容される塩。 - R1とR2が、それぞれ独立して1つ若しくはそれより多くのクロロにより置換されていてもよいフェニルを表す、請求項1〜2のいずれかに記載の化合物。
- R3がC4−12アルコキシカルボニルを表す、請求項1〜3のいずれかに記載の化合物。
- R3がベンジルオキシメチル基を表し、該ベンジルオキシメチル基はベンジル基のフェニル環においてZにより置換されていてもよい、請求項1〜4のいずれかに記載の化合物。
- R3が基:C(O)O−Het(式中、Hetは、ピペリジノ、モルホリノ、又はピロリジノである)を表す、請求項1〜5のいずれかに記載の化合物。
- R1とR2がそれぞれ4−クロロフェニルを表す、請求項1〜6のいずれかに記載の化合物。
- dが1であり、R11がヒドロキシ、アミノ、又はC1−6アルコキシカルボニル基である、請求項1〜7のいずれかに記載の化合物。
- dが2であり、R11がFであり、そして両方のフルオロがシクロヘキシル環の同じ炭素に付いている、請求項1〜8のいずれかに記載の化合物。
- R12がHである、請求項1〜9のいずれかに記載の化合物。
- 芳香族複素環式基が、フリル、ピロリル、チエニル、オキサゾリル、イソオキサゾリル、イミダゾリル、ピラゾリル、オキサゾリル、チアゾリル、イソチアゾリル、オキサジアゾリル、チアジアゾリル、トリアゾリル、テトラゾリル、ピリジル、ピリダジニル、ピリミジニル、ピラジニル、又は1,3,5−トリアゼニルである、請求項1〜10のいずれかに記載の化合物。
- 芳香族複素環式基が、ピロリル、チエニル、イミダゾリル、オキサゾリル、又はピリジルである、請求項1〜11のいずれかに記載の化合物。
- 飽和又は一部不飽和の5〜8員複素環式基が、テトラヒドロフラニル、テトラヒドロピラニル、ピロリジニル、モルホリニル、ピペリジニル、又はピペラジニルである、請求項1〜12のいずれかに記載の化合物。
- 飽和又は一部不飽和の5〜8員複素環式基が、テトラヒドロフラン−3−イル、テトラヒドロピラン−4−イル、ピロリジン−3−イル、モルホリノ、ピペリジノ、ピペリジン−4−イル、又はピペラジン−1−イルである、請求項1〜13のいずれかに記載の化合物。
- 以下の化合物、即ち、
5,6−ビス(4−クロロフェニル)−N−(cis−2−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(trans−2−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(4−ヒドロキシピペリジン−1−イル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)−N−(4,4−ジフルオロシクロヘキシル)ピラジン−2−カルボキサミド、
N−(1−アセチルピペリジン−3−イル)−5,6−ビス(4−クロロフェニル)ピラジン−2−カルボキサミド、
5,6−ビス(4−クロロフェニル)ピラジン−2−カルボン酸tert−ブチル、
5,6−ビス(4−クロロフェニル)−ピラジン−2−イル−(1,3−ジヒドロ−イソインドール−2−イル)−メタノン、
2,3−ビス(4−クロロフェニル)−5−{[(4−フルオロベンジル)オキシ]メチル}ピラジン、
2,3−ビス(4−クロロフェニル)−5−[(ピペリジン−1−イルオキシ)カルボニル]ピラジンの1つ若しくはそれより多くから選択される化合物とその医薬的に許容される塩。 - 医薬品として使用するための、請求項1〜15のいずれかに記載の式Iの化合物。
- 請求項1〜15のいずれかに記載の式Iの化合物と医薬的に許容されるアジュバント、希釈剤、又は担体を含む医薬製剤。
- 肥満、精神異常症、精神分裂病及び双極性障害、不安症、不安うつ病、うつ病、認知障害、記憶障害、強迫性障害、無食欲症、過食症、注意異常症、てんかん及び関連状態のような精神医学上の障害、並びに痴呆、神経系障害、パーキンソン病、ハンチントン舞踏病及びアルツハイマー病のような神経系障害、免疫、心臓血管系、生殖系、及び内分泌系の障害、敗血症ショック、呼吸系及び胃腸系に関連した疾患、及び、長期乱用、嗜癖、及び/又は再発の適応症の治療又は予防用の医薬品の製造における、請求項1〜15のいずれかに記載の式Iの化合物の使用。
- 肥満、精神医学上の障害、精神異常症、精神分裂病及び双極性障害、不安症、不安うつ病、うつ病、認知障害、記憶障害、強迫性障害、無食欲症、過食症、注意異常症、てんかん及び関連状態、神経系障害、神経系障害、パーキンソン病、ハンチントン舞踏病及びアルツハイマー病、免疫、心臓血管系、生殖系、及び内分泌系の障害、敗血症ショック、呼吸系及び胃腸系に関連した疾患、及び、長期乱用、嗜癖、及び/又は再発の適応症を治療する方法であって、請求項1〜15のいずれかに記載の式Iの化合物の薬理学的有効量を治療の必要な患者へ投与することを含む、前記方法。
- 肥満の治療に使用の、請求項1〜15のいずれかに記載の化合物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB0314059A GB0314059D0 (en) | 2003-06-18 | 2003-06-18 | Therapeutic agents |
| GB0314061A GB0314061D0 (en) | 2003-06-18 | 2003-06-18 | Therapeutic agents |
| PCT/SE2004/000969 WO2004111033A1 (en) | 2003-06-18 | 2004-06-16 | 2-substitued 5, 6-diaryl-pyrazine derivatives as cb1 modulator. |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2006527770A true JP2006527770A (ja) | 2006-12-07 |
Family
ID=33554154
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006517043A Withdrawn JP2006527770A (ja) | 2003-06-18 | 2004-06-16 | Cb1モジュレーターとしての2−置換5,6−ジアリール−ピラジン誘導体 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20060135523A1 (ja) |
| EP (1) | EP1641779A1 (ja) |
| JP (1) | JP2006527770A (ja) |
| AR (1) | AR044829A1 (ja) |
| AU (1) | AU2004247615B2 (ja) |
| CA (1) | CA2527033A1 (ja) |
| TW (1) | TW200504034A (ja) |
| UY (1) | UY28374A1 (ja) |
| WO (1) | WO2004111033A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011157391A (ja) * | 2008-06-19 | 2011-08-18 | Takeda Chem Ind Ltd | 複素環化合物およびその用途 |
Families Citing this family (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1546115A4 (en) | 2002-09-27 | 2010-08-04 | Merck Sharp & Dohme | Substituted pyrimidines |
| GB0230088D0 (en) * | 2002-12-24 | 2003-01-29 | Astrazeneca Ab | Therapeutic agents |
| GB0230087D0 (en) * | 2002-12-24 | 2003-01-29 | Astrazeneca Ab | Therapeutic agents |
| GB0302672D0 (en) * | 2003-02-06 | 2003-03-12 | Astrazeneca Ab | Pharmaceutical formulations |
| GB0314057D0 (en) * | 2003-06-18 | 2003-07-23 | Astrazeneca Ab | Therapeutic agents |
| MX2007012213A (es) | 2005-04-06 | 2007-12-10 | Hoffmann La Roche | Derivados de piridin-3-carboxamida como agonistas inversos de canabinoides. |
| CA2606288A1 (en) * | 2005-04-18 | 2006-10-26 | Neurogen Corporation | Subtituted heteroaryl cb1 antagonists |
| US7629346B2 (en) * | 2006-06-19 | 2009-12-08 | Hoffmann-La Roche Inc. | Pyrazinecarboxamide derivatives as CB1 antagonists |
| JP2010500300A (ja) | 2006-08-08 | 2010-01-07 | サノフィ−アベンティス | アリールアミノアリール−アルキル−置換イミダゾリジン−2,4−ジオン、それらの製造法、それらの化合物を含有する薬剤、およびそれらの使用 |
| US7781593B2 (en) | 2006-09-14 | 2010-08-24 | Hoffmann-La Roche Inc. | 5-phenyl-nicotinamide derivatives |
| CA2664621A1 (en) | 2006-10-04 | 2008-04-10 | F. Hoffmann-La Roche Ag | Pyrazine-2-carboxamide derivatives |
| EP2450350A1 (en) | 2006-10-04 | 2012-05-09 | F. Hoffmann-La Roche AG | 3-Pyridinecarboxamide and 2-pyrazinecarboxamide derivatives as HDL-cholesterol raising agents |
| EP2025674A1 (de) | 2007-08-15 | 2009-02-18 | sanofi-aventis | Substituierte Tetrahydronaphthaline, Verfahren zu ihrer Herstellung und ihre Verwendung als Arzneimittel |
| WO2010003624A2 (en) | 2008-07-09 | 2010-01-14 | Sanofi-Aventis | Heterocyclic compounds, processes for their preparation, medicaments comprising these compounds, and the use thereof |
| MX2011004258A (es) | 2008-10-22 | 2011-06-01 | Merck Sharp & Dohme | Derivados de bencimidazol ciclicos novedosos utiles como agentes anti-diabeticos. |
| JP5557845B2 (ja) | 2008-10-31 | 2014-07-23 | メルク・シャープ・アンド・ドーム・コーポレーション | 糖尿病用剤として有用な新規環状ベンゾイミダゾール誘導体 |
| CA2786314A1 (en) | 2010-02-25 | 2011-09-01 | Merck Sharp & Dohme Corp. | Novel cyclic benzimidazole derivatives useful anti-diabetic agents |
| JP5782438B2 (ja) | 2010-06-16 | 2015-09-24 | 武田薬品工業株式会社 | アミド化合物の結晶 |
| US8410107B2 (en) | 2010-10-15 | 2013-04-02 | Hoffmann-La Roche Inc. | N-pyridin-3-yl or N-pyrazin-2-yl carboxamides |
| US8669254B2 (en) | 2010-12-15 | 2014-03-11 | Hoffman-La Roche Inc. | Pyridine, pyridazine, pyrimidine or pyrazine carboxamides as HDL-cholesterol raising agents |
| EP2677869B1 (en) | 2011-02-25 | 2017-11-08 | Merck Sharp & Dohme Corp. | Novel cyclic azabenzimidazole derivatives useful as anti-diabetic agents |
| EP2683702B1 (de) | 2011-03-08 | 2014-12-24 | Sanofi | Neue substituierte phenyl-oxathiazinderivate, verfahren zu deren herstellung, diese verbindungen enthaltende arzneimittel und deren verwendung |
| WO2012120052A1 (de) | 2011-03-08 | 2012-09-13 | Sanofi | Mit carbozyklen oder heterozyklen substituierte oxathiazinderivate, verfahren zu deren herstellung, diese verbindungen enthaltende arzneimittel und deren verwendung |
| WO2012120056A1 (de) | 2011-03-08 | 2012-09-13 | Sanofi | Tetrasubstituierte oxathiazinderivate, verfahren zu deren herstellung, ihre verwendung als medikament sowie sie enthaltendes arzneimittel und deren verwendung |
| WO2012120053A1 (de) | 2011-03-08 | 2012-09-13 | Sanofi | Verzweigte oxathiazinderivate, verfahren zu deren herstellung, ihre verwendung als medikament sowie sie enthaltendes arzneimittel und deren verwendung |
| EP2683705B1 (de) | 2011-03-08 | 2015-04-22 | Sanofi | Di- und trisubstituierte oxathiazinderivate, verfahren zu deren herstellung, ihre verwendung als medikament sowie sie enthaltendes arzneimittel und deren verwendung |
| EP2683699B1 (de) | 2011-03-08 | 2015-06-24 | Sanofi | Di- und trisubstituierte oxathiazinderivate, verfahren zu deren herstellung, ihre verwendung als medikament sowie sie enthaltendes arzneimittel und deren verwendung |
| EP2683703B1 (de) | 2011-03-08 | 2015-05-27 | Sanofi | Neue substituierte phenyl-oxathiazinderivate, verfahren zu deren herstellung, diese verbindungen enthaltende arzneimittel und deren verwendung |
| CA2880901A1 (en) | 2012-08-02 | 2014-02-06 | Merck Sharp & Dohme Corp. | Antidiabetic tricyclic compounds |
| MX2015010935A (es) | 2013-02-22 | 2015-10-29 | Merck Sharp & Dohme | Compuestos biciclicos antidiabeticos. |
| EP2970119B1 (en) | 2013-03-14 | 2021-11-03 | Merck Sharp & Dohme Corp. | Novel indole derivatives useful as anti-diabetic agents |
| WO2015051496A1 (en) | 2013-10-08 | 2015-04-16 | Merck Sharp & Dohme Corp. | Antidiabetic tricyclic compounds |
| MX381180B (es) * | 2014-11-18 | 2025-03-12 | Merck Sharp & Dohme | Compuestos aminopirazina con propiedades antagonistas a2a. |
| WO2018106518A1 (en) | 2016-12-06 | 2018-06-14 | Merck Sharp & Dohme Corp. | Antidiabetic heterocyclic compounds |
Family Cites Families (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4348385A (en) * | 1980-11-17 | 1982-09-07 | Mobay Chemical Corporation | Flowable pesticides |
| US4610868A (en) * | 1984-03-20 | 1986-09-09 | The Liposome Company, Inc. | Lipid matrix carriers for use in drug delivery systems |
| US4826689A (en) * | 1984-05-21 | 1989-05-02 | University Of Rochester | Method for making uniformly sized particles from water-insoluble organic compounds |
| FR2608988B1 (fr) * | 1986-12-31 | 1991-01-11 | Centre Nat Rech Scient | Procede de preparation de systemes colloidaux dispersibles d'une substance, sous forme de nanoparticules |
| US5145648A (en) * | 1988-06-28 | 1992-09-08 | Matsushita Electric Industrial Co., Ltd. | Exhaust smoke purifier apparatus |
| FR2651680B1 (fr) * | 1989-09-14 | 1991-12-27 | Medgenix Group Sa | Nouveau procede de preparation de microparticules lipidiques. |
| JP3282731B2 (ja) * | 1990-06-15 | 2002-05-20 | メルク エンド カムパニー インコーポレーテッド | 結晶の構造および大きさを改良する結晶化方法 |
| JPH06501926A (ja) * | 1990-08-06 | 1994-03-03 | 藤沢薬品工業株式会社 | 複素環式化合物 |
| US5145684A (en) * | 1991-01-25 | 1992-09-08 | Sterling Drug Inc. | Surface modified drug nanoparticles |
| US5932245A (en) * | 1991-12-05 | 1999-08-03 | Alfatec Pharma Gmbh | Gelatin or collagen hydrolysate containing drug formulation that provides for immediate release of nanoparticle drug compounds |
| FR2713225B1 (fr) * | 1993-12-02 | 1996-03-01 | Sanofi Sa | N-pipéridino-3-pyrazolecarboxamide substitué. |
| FR2692575B1 (fr) * | 1992-06-23 | 1995-06-30 | Sanofi Elf | Nouveaux derives du pyrazole, procede pour leur preparation et compositions pharmaceutiques les contenant. |
| US5468604A (en) * | 1992-11-18 | 1995-11-21 | Eastman Kodak Company | Photographic dispersion |
| GB9319129D0 (en) * | 1993-09-15 | 1993-11-03 | Dowelanco Ltd | Storage and dilution of stable aqueous dispersions |
| SE9303281D0 (sv) * | 1993-10-07 | 1993-10-07 | Astra Ab | New formulation |
| SE9403846D0 (sv) * | 1994-11-09 | 1994-11-09 | Univ Ohio State Res Found | Small particle formation |
| DE4440337A1 (de) * | 1994-11-11 | 1996-05-15 | Dds Drug Delivery Services Ges | Pharmazeutische Nanosuspensionen zur Arzneistoffapplikation als Systeme mit erhöhter Sättigungslöslichkeit und Lösungsgeschwindigkeit |
| US5665331A (en) * | 1995-01-10 | 1997-09-09 | Nanosystems L.L.C. | Co-microprecipitation of nanoparticulate pharmaceutical agents with crystal growth modifiers |
| US6048550A (en) * | 1996-10-03 | 2000-04-11 | Chan; Daniel C. F. | Hydrophilic microparticles and methods to prepare same |
| US6127520A (en) * | 1997-04-15 | 2000-10-03 | Regents Of The University Of Michigan | Compositions and methods for the inhibition of neurotransmitter uptake of synaptic vesicles |
| FR2766368B1 (fr) * | 1997-07-24 | 2000-03-31 | Univ Claude Bernard Lyon | Procede de preparation de nanocapsules de type vesiculaire, utilisables notamment comme vecteurs colloidaux de principes actifs pharmaceutiques ou autres |
| US6375986B1 (en) * | 2000-09-21 | 2002-04-23 | Elan Pharma International Ltd. | Solid dose nanoparticulate compositions comprising a synergistic combination of a polymeric surface stabilizer and dioctyl sodium sulfosuccinate |
| FR2789079B3 (fr) * | 1999-02-01 | 2001-03-02 | Sanofi Synthelabo | Derive d'acide pyrazolecarboxylique, sa preparation, les compositions pharmaceutiques en contenant |
| US6383471B1 (en) * | 1999-04-06 | 2002-05-07 | Lipocine, Inc. | Compositions and methods for improved delivery of ionizable hydrophobic therapeutic agents |
| RU2245878C2 (ru) * | 2000-03-23 | 2005-02-10 | Солвей Фармасьютикалс Б.В. | Производные 4,5-дигидро-1н-пиразола, обладающие cb1-антагонистической активностью |
| ATE365537T1 (de) * | 2001-08-06 | 2007-07-15 | Astrazeneca Ab | Wässrige dispersion stabiler nanopartikel eines wasserunlöslichen wirkstoffs und ein hilfsstoff wie mittelkettige triglyceride (mct) |
| US20060003012A9 (en) * | 2001-09-26 | 2006-01-05 | Sean Brynjelsen | Preparation of submicron solid particle suspensions by sonication of multiphase systems |
| SE0104330D0 (sv) * | 2001-12-19 | 2001-12-19 | Astrazeneca Ab | Therapeutic agents |
| SE0104332D0 (sv) * | 2001-12-19 | 2001-12-19 | Astrazeneca Ab | Therapeutic agents |
| GB0216700D0 (en) * | 2002-07-18 | 2002-08-28 | Astrazeneca Ab | Process |
| GB0302671D0 (en) * | 2003-02-06 | 2003-03-12 | Astrazeneca Ab | Pharmaceutical formulations |
| GB0302672D0 (en) * | 2003-02-06 | 2003-03-12 | Astrazeneca Ab | Pharmaceutical formulations |
| GB0302673D0 (en) * | 2003-02-06 | 2003-03-12 | Astrazeneca Ab | Pharmaceutical formulations |
| GB0314057D0 (en) * | 2003-06-18 | 2003-07-23 | Astrazeneca Ab | Therapeutic agents |
-
2004
- 2004-06-16 JP JP2006517043A patent/JP2006527770A/ja not_active Withdrawn
- 2004-06-16 WO PCT/SE2004/000969 patent/WO2004111033A1/en not_active Ceased
- 2004-06-16 AU AU2004247615A patent/AU2004247615B2/en not_active Ceased
- 2004-06-16 EP EP04749011A patent/EP1641779A1/en not_active Withdrawn
- 2004-06-16 CA CA002527033A patent/CA2527033A1/en not_active Abandoned
- 2004-06-16 US US10/561,060 patent/US20060135523A1/en not_active Abandoned
- 2004-06-18 UY UY28374A patent/UY28374A1/es not_active Application Discontinuation
- 2004-06-18 TW TW093117713A patent/TW200504034A/zh unknown
- 2004-06-18 AR ARP040102139A patent/AR044829A1/es unknown
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011157391A (ja) * | 2008-06-19 | 2011-08-18 | Takeda Chem Ind Ltd | 複素環化合物およびその用途 |
| JP2014094950A (ja) * | 2008-06-19 | 2014-05-22 | Takeda Chem Ind Ltd | 複素環化合物およびその用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20060135523A1 (en) | 2006-06-22 |
| AU2004247615A1 (en) | 2004-12-23 |
| WO2004111033A1 (en) | 2004-12-23 |
| AU2004247615B2 (en) | 2008-02-21 |
| EP1641779A1 (en) | 2006-04-05 |
| UY28374A1 (es) | 2005-01-31 |
| TW200504034A (en) | 2005-02-01 |
| CA2527033A1 (en) | 2004-12-23 |
| AR044829A1 (es) | 2005-10-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2006527770A (ja) | Cb1モジュレーターとしての2−置換5,6−ジアリール−ピラジン誘導体 | |
| JP2005517655A (ja) | Cb1アンタゴニストとしての5,6−ジアリール−ピラジン−2−アミド誘導体 | |
| US20060122229A1 (en) | 4,5-diarylthiazole derivatives as cb-1 ligands | |
| JP2006513201A (ja) | 1,5−ジアリール−ピロール−3−カルボキサミド誘導体およびそのカンナビノイド受容体モジュレーターとしての使用 | |
| WO2003051850A1 (en) | Pyrazine compounds and pharmaceutical compositions containing them | |
| JP2006527771A (ja) | Cb1モジュレーターとしての3−置換5,6−ジアリールピラジン−2−カルボキサミドおよび−2−スルホンアミド誘導体 | |
| JP2006527769A (ja) | Cb1モジュレーターとしての2,3位置換5,6−ジアリール−ピラジン誘導体 | |
| WO2004111038A1 (en) | 5,6-bis (4-chlorophenyl)-n-piperidin1-yl-3-(piperidin-1-yl-carbonyl)pyrazine-2-carboxamide | |
| JP4177435B2 (ja) | 治療薬 | |
| US20080300232A1 (en) | N-Piperidine Derivatives as Ccr3 Modulators | |
| JP2007512298A (ja) | 治療薬 | |
| US20070185119A1 (en) | Therapeutic agents II | |
| HK1096670B (en) | Pyrrolo-pyrazine derivatives useful as cb1-modulators | |
| HK1066810A1 (en) | Piperazinylpyrazines compounds as antagonists of serotonin 5-ht2 receptor |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070111 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20090818 |