JP2009123473A - 非水電解質電池 - Google Patents
非水電解質電池 Download PDFInfo
- Publication number
- JP2009123473A JP2009123473A JP2007295302A JP2007295302A JP2009123473A JP 2009123473 A JP2009123473 A JP 2009123473A JP 2007295302 A JP2007295302 A JP 2007295302A JP 2007295302 A JP2007295302 A JP 2007295302A JP 2009123473 A JP2009123473 A JP 2009123473A
- Authority
- JP
- Japan
- Prior art keywords
- negative electrode
- ppm
- positive electrode
- active material
- electrode active
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
【課題】オリビン構造を有する正極材料を用いた場合でも、十分なサイクル特性を得ることができる非水電解質電池を提供する。
【解決手段】負極活物質層22Bは、リチウムをドープおよび脱ドープ可能な負極活物質を含んでいる。負極活物質は、満充電状態にて7LiのNMR(Nuclear magnetic resonance)を測定した場合に塩化リチウム基準の化学シフト値が0ppmから100ppmの範囲に複数のピークに起因するスペクトルを有し、ピーク分離した際にピーク位置が少なくとも1ppm、31ppm、44ppmおよび58ppmに存在する炭素材料を含むものである。
【選択図】図2
【解決手段】負極活物質層22Bは、リチウムをドープおよび脱ドープ可能な負極活物質を含んでいる。負極活物質は、満充電状態にて7LiのNMR(Nuclear magnetic resonance)を測定した場合に塩化リチウム基準の化学シフト値が0ppmから100ppmの範囲に複数のピークに起因するスペクトルを有し、ピーク分離した際にピーク位置が少なくとも1ppm、31ppm、44ppmおよび58ppmに存在する炭素材料を含むものである。
【選択図】図2
Description
この発明は、非水電解質電池に関する。さらに詳しくは、正極にオリビン構造のリチウムリン酸化合物を含む非水電解質電池に関する。
近年、カメラー体型VTR(Video Tape Recorder)、携帯電話、ラップトップコンピュータなどのポータブル電子機器が多く登場し、その小型軽量化が図られている。そしてこれらの電子機器のポータブル電源として、電池、特に二次電池について、エネルギー密度を向上させるための研究開発が活発に進められている。
非水電解液を用いた電池、中でも、リチウムイオン二次電池は、従来の水溶液系電解液二次電池である鉛電池、ニッケルカドミウム電池と比較して大きなエネルギー密度が得られるため、期待度が大きくなっており、市場も著しく成長している。
とりわけ近年、リチウムイオン二次電池の軽量、高エネルギー密度という特徴が電気自動車やハイブリッド電気自動車用途に適することから、同電池の大型化、高出力化を目指した検討が盛んとなっている。
リチウムイオン二次電池に代表される非水系二次電池では、正極活物質としてLiCoO2、LiNiO2、LiMn2O4などの酸化物正極が用いられることが一般的である。これは高容量、高電圧が得られ、かつ高充填性に優れるため、携帯機器の小型・軽量化に有利であるためである。
しかし、これらの正極は、充電状態で加熱すると200℃〜300℃において酸素放出を開始する。酸素放出が始まると、電解液として可燃性の有機電解液を用いるため、電池が熱暴走する危険性がある。よって、酸化物正極を用いた場合には、特に大型電池での安全性確保が容易ではない。
これに対して、A.K.Padhi等が報告しているオリビン構造を有する正極材料では、350℃を超えても酸素放出が起こらず、安全性に非常に優れることが示されている。(非特許文献1参照)
J.Electrochem.Soc.,Vol.144,p.1188
このオリビン構造を有する正極材料では、充放電がLiFePO4、FePO4の二層共存状態で進行するため、電位平坦性が非常に高い。このため、通常のリチウムイオン電池の充電方式である、定電流・定電圧充電を行うと、ほとんど定電流充電状態で充電が行われるという特徴がある。したがって、オリビン構造を有する正極材料を用いた電池では、LiCoO2、LiNiO2、LiMn2O4などの従来の正極材料に比べ、同じ充電レートで充電した場合、充電時間の短縮が可能である。
しかしながら、オリビン構造を有する正極材料を用いた電池では、高い電流値での充電が比較的長く続くため、負極内でのLiイオンの移動が追従せず、負極と電解液との界面でのLiイオン濃度が高まり、負極上へLi金属が析出しやすくなってしまう。この結果、従来の負極炭素材料を用いた場合に、オリビン構造を有する正極材料を用いた電池では、十分なサイクル特性が得られなかった。
したがって、この発明の目的は、オリビン構造を有する正極材料を用いた場合でも、十分なサイクル特性を得ることができる非水電解質電池を提供することにある。
上述した課題を解決するために、
この発明は、オリビン構造を有するリチウムリン酸化合物を含む正極と、リチウムをドープおよび脱ドープ可能な負極活物質を含む負極と、非水電解質と、を備え、負極活物質は、満充電状態にて7LiのNMRを測定した場合に塩化リチウム基準の化学シフト値が0ppmから100ppmの範囲に複数のピークに起因するスペクトルを有し、且つピーク分離した際にピーク位置が少なくとも1ppm、31ppm、44ppmおよび58ppmに存在する炭素材料を含むこと
を特徴とする非水電解質電池である。
この発明は、オリビン構造を有するリチウムリン酸化合物を含む正極と、リチウムをドープおよび脱ドープ可能な負極活物質を含む負極と、非水電解質と、を備え、負極活物質は、満充電状態にて7LiのNMRを測定した場合に塩化リチウム基準の化学シフト値が0ppmから100ppmの範囲に複数のピークに起因するスペクトルを有し、且つピーク分離した際にピーク位置が少なくとも1ppm、31ppm、44ppmおよび58ppmに存在する炭素材料を含むこと
を特徴とする非水電解質電池である。
この発明では、負極材料は、満充電状態にて7LiのNMRを測定した場合に塩化リチウム基準の化学シフト値が0ppmから100ppmの範囲に複数のピークに起因するスペクトルを有し、且つピーク分離した際にピーク位置が少なくとも1ppm、31ppm、44ppmおよび58ppmに存在する炭素材料を含むようにしたので、オリビン構造を有するリチウムリン酸化合物を用いた場合でも、十分なサイクル特性を得ることができる。
この発明によれば、オリビン構造を有する正極材料を用いた場合でも、十分なサイクル特性を得ることができる。
以下、この発明の実施の形態について図面を参照して説明する。図1は、この発明の一実施形態による非水電解液電池の断面構造を示す。この電池は、例えば非水電解液二次電池であり、例えばリチウムイオン二次電池である。
図1に示すように、この二次電池は、いわゆる円筒型といわれるものであり、ほぼ中空円柱状の電池缶11の内部に、帯状の正極21と帯状の負極22とがセパレータ23を介して巻回された巻回電極体20を有している。電池缶11は、例えばニッケル(Ni)のめっきがされた鉄(Fe)により構成されており、一端部が閉鎖され他端部が開放されている。電池缶11の内部には、巻回電極体20を挟むように巻回周面に対して垂直に一対の絶縁板12,13がそれぞれ配置されている。
電池缶11の開放端部には、電池蓋14と、この電池蓋14の内側に設けられた安全弁機構15および熱感抵抗素子(Positive Temperature Coefficient;PTC素子)16とが、ガスケット17を介してかしめられることにより取り付けられており、電池缶11の内部は密閉されている。電池蓋14は、例えば、電池缶11と同様の材料により構成されている。
安全弁機構15は、熱感抵抗素子16を介して電池蓋14と電気的に接続されており、内部短絡あるいは外部からの加熱などにより電池の内圧が一定以上となった場合にディスク板15Aが反転して電池蓋14と巻回電極体20との電気的接続を切断するようになっている。熱感抵抗素子16は、温度が上昇すると抵抗値の増大により電流を制限し、大電流による異常な発熱を防止するものである。ガスケット17は、例えば、絶縁材料により構成されており、表面にはアスファルトが塗布されている。
巻回電極体20は、例えば、センターピン24を中心に巻回されている。巻回電極体20の正極21にはアルミニウム(Al)などよりなる正極リード25が接続されており、負極22にはニッケル(Ni)などよりなる負極リード26が接続されている。正極リード25は安全弁機構15に溶接されることにより電池蓋14と電気的に接続されており、負極リード26は電池缶11に溶接され電気的に接続されている。
図2は図1に示した巻回電極体20の一部を拡大して表すものである。正極21は、例えば、対向する一対の面を有する正極集電体21Aと、正極集電体21Aの両面に設けられた正極活物質層21Bとを有している。なお、正極集電体21Aの片面のみに正極活物質層21Bが存在する領域を有するようにしてもよい。正極集電体21Aは、例えば、アルミニウム(Al)箔などの金属箔により構成されている。
正極活物質層21Bは、例えば、正極活物質を含んでおり、必要に応じてカーボンブラックやグラファイトなどの導電剤と、ポリフッ化ビニリデンなどの結着剤とを含んでいてもよい。正極活物質としては、例えば、オリビン構造を有するリチウムリン酸化合物を用いる。
オリビン構造を有するリチウムリン酸化合物としては、例えば、化Iで表される化合物を挙げることができる。
(化I)
LiFe1-yMyPO4
(式中、Mはマンガン(Mn)、コバルト(Co)、ニッケル(Ni)、マグネシウム(Mg)、亜鉛(Zn)、クロム(Cr)、チタン(Ti)、バナジウム(V)よりなる群から選ばれる少なくとも1種である。yは0≦y≦0.8である。)
(化I)
LiFe1-yMyPO4
(式中、Mはマンガン(Mn)、コバルト(Co)、ニッケル(Ni)、マグネシウム(Mg)、亜鉛(Zn)、クロム(Cr)、チタン(Ti)、バナジウム(V)よりなる群から選ばれる少なくとも1種である。yは0≦y≦0.8である。)
負極22は、例えば、対向する一対の面を有する負極集電体22Aと、負極集電体22Aの両面に設けられた負極活物質層22Bとを有している。なお、負極集電体22Aの片面のみに負極活物質層22Bが存在する領域を有するようにしてもよい。負極集電体22Aは、例えば銅(Cu)箔などの金属箔により構成されている。
負極活物質層22Bは、リチウムをドープおよび脱ドープ可能な負極活物質を含んでおり、必要に応じてポリフッ化ビニリデンなどの結着剤を含んでいてもよい。
負極活物質は、満充電状態にて7LiのNMR(Nuclear magnetic resonance)を測定した場合に塩化リチウム基準の化学シフト値が0ppmから100ppmの範囲に複数のピークに起因するスペクトルを有し、ピーク分離した際にピーク位置が少なくとも1ppm、31ppm、44ppmおよび58ppmに存在する炭素材料を含むものである。
この炭素材料は、例えば、コールタールピッチなどの有機材料を高温熱処理し、粉砕・分級することにより得られる。高温熱処理は、例えば、アルゴンガスなどの不活性ガス雰囲気において、1800℃〜2400℃の範囲で、適宜の時間で保持することにより行われる。
負極活物質は、上記炭素材料と物性の異なる他の炭素材料を含むものであってもよい。その際の上記炭素材料の含有量は、サイクル特性を改善する効果と直流抵抗を低減する効果を勘案すると、負極活物質層22Bに対して、7wt%〜50wt%の範囲内が好ましい。物性の異なる他の炭素材料は、例えば、コールタールピッチなどの有機材料を不活性ガス雰囲気下、1800℃未満または2400℃より高い温度で熱処理し、粉砕・分級して得ることが可能である。
セパレータ23としては、例えば、ポリエチレン多孔質フィルム、ポリプロピレン多孔質フィルム、合成樹脂製不織布などを用いることができる。セパレータ23には、液状の電解質である電解液が含浸されている。
電解液は、液状の溶媒、例えば有機溶媒などの非水溶媒と、この非水溶媒に溶解された電解質塩とを含むものである。
非水溶媒は、例えば、エチレンカーボネートおよびプロピレンカーボネートなどの環状炭酸エステルのうちの少なくとも1種を含んでいることが好ましい。サイクル特性を向上させることができるからである。特に、エチレンカーボネートと、プロピレンカーボネートとを混合して含むようにすれば、よりサイクル特性を向上させることができるので好ましい。
非水溶媒は、また、ジエチルカーボネート、ジメチルカーボネート、エチルメチルカーボネートあるいはメチルプロピルカーボネートなどの鎖状炭酸エステルのうちの少なくとも1種を含んでいることが好ましい。サイクル特性をより向上させることができるからである。
非水溶媒は、さらに、2,4−ジフルオロアニソールおよびビニレンカーボネートのうちの少なくとも一方を含んでいることが好ましい。2,4−ジフルオロアニソールは放電容量を改善することができ、ビニレンカーボネートはサイクル特性をより向上させることができるからである。特に、これらを混合して含んでいれば、放電容量およびサイクル特性を共に向上させることができるのでより好ましい。
非水溶媒は、さらに、ブチレンカーボネート、γ−ブチロラクトン、γ−バレロラクトン、これら化合物の水素基の一部または全部をフッ素基で置換したもの、1,2−ジメトキシエタン、テトラヒドロフラン、2−メチルテトラヒドロフラン、1,3−ジオキソラン、4−メチル−1,3−ジオキソラン、酢酸メチル、プロピオン酸メチル、アセトニトリル、グルタロニトリル、アジポニトリル、メトキシアセトニトリル、3−メトキシプロピロニトリル、N,N−ジメチルフォルムアミド、N−メチルピロリジノン、N−メチルオキサゾリジノン、N,N−ジメチルイミダゾリジノン、ニトロメタン、ニトロエタン、スルホラン、ジメチルスルフォキシドあるいはリン酸トリメチルなどのいずれか1種または2種以上を含んでいてもよい。
組み合わせる電極によっては、上記非水溶媒群に含まれる物質の水素原子の一部または全部をフッ素原子で置換したものを用いることにより、電極反応の可逆性が向上する場合がある。したがって、これらの物質を適宜用いることも可能である。
電解質塩としては、リチウム塩を用いることができる。リチウム塩としては、例えば、LiPF6、LiBF4、LiAsF6、LiSbF6、LiClO4、LiB(C6H5)4、LiCH3SO3、LiCF3SO3、LiN(SO2CF3)2、LiC(SO2CF3)3、LiAlCl4、LiSiF6、LiCl、LiBF2(ox)〔リチウムジフルオロオキサレートボレート〕、LiBOB(リチウムビスオキサレートボレート)、LiBrなどが適当であり、これらのうちのいずれか1種をまたは2種以上を混合して、用いる。なかでも、LiPF6は、高いイオン伝導性を得ることができるとともに、サイクル特性を向上させることができるので好ましい。
この二次電池は、例えば以下に説明するようにして、製造することができる。まず、例えば、正極活物質と、導電剤と、結着剤とを混合して正極合剤を調製し、この正極合剤をN−メチルピロリドンなどの溶剤に分散させて正極合剤スラリーとする。続いて、この正極合剤スラリーを正極集電体21Aに塗布し溶剤を乾燥させたのち、ロールプレス機などにより圧縮成型して正極活物質層21Bを形成し、正極21を作製する。
また、例えば、負極活物質と、結着剤とを混合して負極合剤を調製し、この負極合剤をN−メチルピロリドンなどの溶剤に分散させて負極合剤スラリーとする。続いて、この負極合剤スラリーを負極集電体22Aに塗布し溶剤を乾燥させたのち、ロールプレス機などにより圧縮成型して負極活物質層22Bを形成し、負極22を作製する。
次いで、正極集電体21に正極リード25を溶接などにより取り付けるとともに、負極集電体22に負極リード26を溶接などにより取り付ける。そののち、正極21と負極22とをセパレータ23を介して巻回し、正極リード25の先端部を安全弁機構15に溶接すると共に、負極リード26の先端部を電池缶11に溶接して、巻回した正極21および負極22を一対の絶縁板12,13で挟み電池缶11の内部に収納する。
正極21および負極22を電池缶11の内部に収納したのち、上述した電解液を電池缶11の内部に注入し、セパレータ23に含浸させる。そののち、電池缶11の開口端部に電池蓋14、安全弁機構15および熱感抵抗素子16を、ガスケット17を介してかしめることにより固定する。以上により、図1に示した二次電池を製造できる。
この二次電池では、充電を行うと、例えば、正極21からリチウムイオンが離脱し、電解液を介して負極22に吸蔵される。放電を行うと、例えば、負極22からリチウムイオンが離脱し、電解液を介して正極21に吸蔵される。
この発明の具体的な実施例について詳細に説明する。ただし、この発明はこれらの実施例に限定されるものではない。
<実施例1>
[炭素材料(I)の作製]
コールタールピッチを不活性ガス雰囲気下で1900℃にて加熱処理し、炭素材料(I)を得た。
コールタールピッチを不活性ガス雰囲気下で1900℃にて加熱処理し、炭素材料(I)を得た。
[円筒セルの作製]
炭素材料(I)92質量部とポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。この負極合剤塗料を、厚さ15μmの銅箔の両面に塗布し、乾燥後、プレスして帯状の負極電極を作製した。
炭素材料(I)92質量部とポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。この負極合剤塗料を、厚さ15μmの銅箔の両面に塗布し、乾燥後、プレスして帯状の負極電極を作製した。
LiCO3と、FeSO4・7H2Oと、NH4H2PO4とを所定量混合し、さらに前記混合粉とカーボンブラックとを97:3の重量比となるように混合した後、ボールミルにて乾式混合を10時間行った。この混合粉を窒素雰囲気下にて550℃焼成を行い、カーボンを被覆したLiFePO4で表されたオリビン構造を有するリチウムリン酸化合物を得た。
このリチウムリン酸化合物85質量部と、ポリフッ化ビニリデン10質量部と、人造黒鉛5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、正極合剤塗料を得た。この正極合剤塗料を厚さ15μmのアルミニウム箔の両面に塗布し、乾燥後、プレスして帯状の正極電極を作製した。
正極電極と負極電極との間に厚さ25μmのポリプロピレン製微孔フィルムをはさんで巻回し、エチレンカーボネートとジメチルカーボネートとを等容量で混合した混合溶媒にLiPF61mol/lを溶解させた非水電解液とともに直径18mm、高さ65mmの金属ケースに入れ、容量が1Ahの18650サイズの実施例1の円筒セルを作製した。
<実施例2>
[炭素材料(II)の作製]
コールタールピッチを不活性ガス雰囲気下で2800℃にて加熱処理し、炭素材料(II)を得た。
[炭素材料(II)の作製]
コールタールピッチを不活性ガス雰囲気下で2800℃にて加熱処理し、炭素材料(II)を得た。
[円筒セルの作製]
炭素材料(I)7質量部と、炭素材料(II)85質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例2の円筒セルを作製した。
炭素材料(I)7質量部と、炭素材料(II)85質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例2の円筒セルを作製した。
<実施例3>
[円筒セルの作製]
炭素材料(I)42質量部と、炭素材料(II)50質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例3の円筒セルを作製した。
[円筒セルの作製]
炭素材料(I)42質量部と、炭素材料(II)50質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例3の円筒セルを作製した。
<実施例4>
[円筒セルの作製]
炭素材料(I)52質量部と、炭素材料(II)40質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た点以外は、実施例1と同様にして、実施例4の円筒セルを作製した。
[円筒セルの作製]
炭素材料(I)52質量部と、炭素材料(II)40質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た点以外は、実施例1と同様にして、実施例4の円筒セルを作製した。
<実施例5>
[円筒セルの作製]
炭素材料(I)5質量部と、炭素材料(II)87質量部と、ポリフッ化ビニリデン5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例5の円筒セルを作製した。
[円筒セルの作製]
炭素材料(I)5質量部と、炭素材料(II)87質量部と、ポリフッ化ビニリデン5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例5の円筒セルを作製した。
<実施例6>
[円筒セルの作製]
Li2Co3と、MnCO3と、FeSO4・7H2Oと、NH4H2PO4とを所定量混合し、さらに前記混合粉とカーボンブラックとを97:3の重量比となるように混合した後、ボールミルにて乾式混合を10時間行った。この混合粉を窒素雰囲気下にて550℃焼成を行い、LiMn0.7Fe0.3PO4で表されるMnFeオリビン正極活物質材料を得た。このMnFeオリビン正極活物質材料85質量部と、ポリフッ化ビニリデン10質量部と、人造黒鉛5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、正極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例6の円筒セルを作製した。
[円筒セルの作製]
Li2Co3と、MnCO3と、FeSO4・7H2Oと、NH4H2PO4とを所定量混合し、さらに前記混合粉とカーボンブラックとを97:3の重量比となるように混合した後、ボールミルにて乾式混合を10時間行った。この混合粉を窒素雰囲気下にて550℃焼成を行い、LiMn0.7Fe0.3PO4で表されるMnFeオリビン正極活物質材料を得た。このMnFeオリビン正極活物質材料85質量部と、ポリフッ化ビニリデン10質量部と、人造黒鉛5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、正極合剤塗料を得た。以上の点以外は、実施例1と同様にして、実施例6の円筒セルを作製した。
<比較例1>
[円筒セルの作製]
炭素材料(II)92質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、比較例1の円筒セルを作製した。
<比較例2>
[円筒セルの作製]
コバルト酸リチウム85質量部と、ポリフッ化ビニリデン10質量部と、人造黒鉛5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、正極合剤塗料を得た。以上の点以外は、比較例1と同様にして、比較例2の円筒セルを作製した。
[円筒セルの作製]
炭素材料(II)92質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例1と同様にして、比較例1の円筒セルを作製した。
<比較例2>
[円筒セルの作製]
コバルト酸リチウム85質量部と、ポリフッ化ビニリデン10質量部と、人造黒鉛5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、正極合剤塗料を得た。以上の点以外は、比較例1と同様にして、比較例2の円筒セルを作製した。
<比較例3>
コバルト酸リチウム85質量部と、ポリフッ化ビニリデン10質量部と、人造黒鉛5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、正極合剤塗料を得た。以上の点以外は、実施例1と同様にして、比較例3の円筒セルを作製した。
コバルト酸リチウム85質量部と、ポリフッ化ビニリデン10質量部と、人造黒鉛5質量部と、分量外のN−メチル−2−ピロリドンとを混練し、正極合剤塗料を得た。以上の点以外は、実施例1と同様にして、比較例3の円筒セルを作製した。
<比較例4>
[円筒セルの作製]
炭素材料(II)92質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例6と同様にして、比較例4の円筒セルを作製した。
[円筒セルの作製]
炭素材料(II)92質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、負極合剤塗料を得た。以上の点以外は、実施例6と同様にして、比較例4の円筒セルを作製した。
(評価)
実施例1〜実施例6および比較例1〜比較例4について、以下に説明する(I)〜(IV)の評価を行った。
実施例1〜実施例6および比較例1〜比較例4について、以下に説明する(I)〜(IV)の評価を行った。
(I)満充電状態での7Li−NMR測定
炭素材料(I)92質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、実施例1と同様の負極合剤塗料を得た。この負極合剤塗料を、厚さ15μmの銅箔の片面にのみ塗布した後、乾燥してプレスし、15mmφに打ち抜くことによりコインセル用の電極を作製した。なお、粉体塗布量は、5mg/cm2〜10mg/cm2(片面)であることが望ましいので、粉体塗布量をこの範囲内になるように調整した。
炭素材料(I)92質量部と、ポリフッ化ビニリデン8質量部と、分量外のN−メチル−2−ピロリドンとを混練し、実施例1と同様の負極合剤塗料を得た。この負極合剤塗料を、厚さ15μmの銅箔の片面にのみ塗布した後、乾燥してプレスし、15mmφに打ち抜くことによりコインセル用の電極を作製した。なお、粉体塗布量は、5mg/cm2〜10mg/cm2(片面)であることが望ましいので、粉体塗布量をこの範囲内になるように調整した。
作製したコインセル用と対極としてのLi金属との間に、厚さ25μmのポリプロピレン製微多孔フィルムをはさみ、電解液は実施例1と同じ組成のものを用いて、コインセルを作製した。このコインセルを、定電流定電圧充電(0.1C−0V−15h)、放電(0.1C 2V)にて1サイクル充放電した後、再度同じ充電条件にて充電した。
この状態でコインセルを解体し、負極電極を取り出し、DMC(ジメチルカーボネート)にて洗浄した後、銅箔から負極粉末を削り落とした後、以下の条件にて7Li−NMR測定を行った。また、比較例1についても、比較例1と同様の負極合剤塗料を用いてコインセルを作製し、同様に7Li−NMR測定を行った。
装置:ブルカー社製 核磁気共鳴装置 AVANCE400 (2.5mm MASプローブを装着)
温度:室温
測定核:7Li
試料回転速度 :30kHz(マジックアングルスピニング法)
基準物質:1M LiCl aq
装置:ブルカー社製 核磁気共鳴装置 AVANCE400 (2.5mm MASプローブを装着)
温度:室温
測定核:7Li
試料回転速度 :30kHz(マジックアングルスピニング法)
基準物質:1M LiCl aq
7Li−NMR測定によって得られた、炭素材料(I)および炭素材料(II)の7Li−NMRスペクトルを図3に示す。
図3において、実線で示されるのが炭素材料(I)の7Li−NMR測定の測定結果であり、上向き矢印はピーク分離した際のピーク位置を示す。点線で示されるのが炭素材料(II)の7Li−NMR測定結果であり、下向き矢印はピーク位置を示す。
図3に示すように、炭素材料(I)の7Li−NMRスペクトルでは、0〜100ppmに4個のピークが確認され、そのピーク位置はそれぞれ1ppm、31ppm、44ppm、58ppmであった。炭素材料(II)の7Li−NMRスペクトルでは、0〜100ppmに2個のピークが確認され、そのピーク位置はそれぞれ5ppm、44ppmであった。
(II)サイクル特性評価
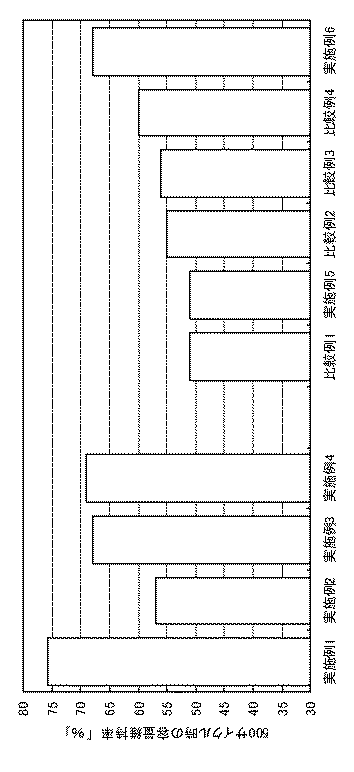
実施例1〜実施例6および比較例1〜比較例4の円筒セルについて、それぞれ定電流定電圧充電(1A 3.6V 0.1Acut)と、定電流放電(7A 2.0V)とを繰り返す、サイクル試験を行い、1サイクル時の放電容量に対する500サイクル時の放電容量の容量維持率を求め、実施例および比較例それぞれの容量維持率を棒グラフにまとめた。図4に、実施例1〜実施例6および比較例1〜比較例4のサイクル容量維持率をまとめたグラフを示す。
実施例1〜実施例6および比較例1〜比較例4の円筒セルについて、それぞれ定電流定電圧充電(1A 3.6V 0.1Acut)と、定電流放電(7A 2.0V)とを繰り返す、サイクル試験を行い、1サイクル時の放電容量に対する500サイクル時の放電容量の容量維持率を求め、実施例および比較例それぞれの容量維持率を棒グラフにまとめた。図4に、実施例1〜実施例6および比較例1〜比較例4のサイクル容量維持率をまとめたグラフを示す。
図4に示すように、実施例1〜実施例5では、正極にオリビン構造を有するLiFePO4を用いた場合において、負極に炭素材料(I)を含むので、比較例1より優れたサイクル特性が得られた。
また、正極活物質がLiCoO2である比較例2と比較例3との比較によると、サイクル特性に差異が認められなかった。これはLiFePO4に比べて充電時に定電流領域が短いため、負極違いによるサイクル特性への影響が小さかったものと考えられる。同様に実施例6と比較例4との比較からわかるように、正極活物質として、LiMn0.7Fe0.3PO4を用いた場合にサイクル特性の改善効果があるが、正極活物質として、LiFePO4ほどの改善効果は得られないことがわかった。
(III)負極電極容量比較
実施例1〜実施例5、比較例1で得た負極合剤塗料を用いて、評価(I)と同様にコインセルを作製し、定電流定電圧充電(0.1C−0V−15h)、放電(0.1C 2V)にて1サイクル充放電を行い、0.1C放電容量を測定し、負極活物質重量あたりの放電容量を求めた。
実施例1〜実施例5、比較例1で得た負極合剤塗料を用いて、評価(I)と同様にコインセルを作製し、定電流定電圧充電(0.1C−0V−15h)、放電(0.1C 2V)にて1サイクル充放電を行い、0.1C放電容量を測定し、負極活物質重量あたりの放電容量を求めた。
(IV)直流抵抗測定
実施例1〜実施例5および比較例1の円筒セルについて、満充電状態の状態から10A放電を行い、1秒後の電圧V1と放電直前の電圧V0を用いて直流抵抗を(式1)により算出した。
直流抵抗=(V0−V1)/10・・・(式1)
実施例1〜実施例5および比較例1の円筒セルについて、満充電状態の状態から10A放電を行い、1秒後の電圧V1と放電直前の電圧V0を用いて直流抵抗を(式1)により算出した。
直流抵抗=(V0−V1)/10・・・(式1)
(III)〜(IV)の測定結果を表1に示す。なお、(IV)については、比較例1の直流抵抗値を100%とした場合の比較値をまとめたものである。
表1に示すように、炭素材料(II)は、黒鉛構造が発達したため、高容量を得られるが、炭素材料(I)は、黒鉛構造が比較的未発達であるため、容量が低いことがわかった。
また、実施例2〜実施例3および比較例1によると、炭素材料(I)は、炭素材料(II)に比べ、直流抵抗を下げる効果が大きいことがわかった。しかしながら、炭素材料(I)の混合量が多すぎると、負極での容量が低くなり、負極の塗布量を増加させる必要が生じるため、実施例1のように電池の直流抵抗が大きすぎるという弊害が生じてしまう。
以上、サイクル特性の改善効果と直流抵抗低減の効果から勘案して、負極活物質層に含まれる炭素材料(I)の含有量しては、7wt%以上50wt%以下の範囲内であることが望ましいことがわかった。
この発明は、上述したこの発明の実施形態に限定されるものでは無く、この発明の要旨を逸脱しない範囲内で様々な変形や応用が可能である。例えば、上述した実施形態では、円筒型電池を例に挙げて説明したが、この発明はこれに限定されるものではなく、例えば角型電池、コイン型電池、ボタン型電池などといった外装材に金属製容器などを用いた電池、薄型電池といった外装材にラミネートフィルムなどを用いた電池など、様々な形状や大きさにすることも可能である。
また、例えば、電解液に代えて、他の電解質、例えば高分子化合物に電解液を保持させたゲル状の電解質を用いてもよい。電解液(すなわち液状の溶媒、電解質塩および添加剤)については上述のとおりであり、高分子化合物としては、例えば、ポリアクリロニトリル、ポリフッ化ビニリデン、ポリフッ化ビニリデンとポリヘキサフルオロプロピレンとの共重合体、ポリテトラフルオロエチレン、ポリヘキサフルオロプロピレン、ポリエチレンオキサイド、ポリプロピレンオキサイド、ポリフォスファゼン、ポリシロキサン、ポリ酢酸ビニル、ポリビニルアルコール、ポリメタクリル酸メチル、ポリアクリル酸、ポリメタクリル酸、スチレン−ブタジエンゴム、ニトリル−ブタジエンゴム、ポリスチレン、ポリカーボネートが挙げられる。特に電気化学的な安定性を考慮すると、ポリアクリロニトリル、ポリフッ化ビニリデン、ポリヘキサフルオロプロピレン、ポリエチレンオキサイドなどが好ましい。
また、他の電解質としては、イオン伝導性高分子を利用した高分子固体電解質、またはイオン伝導性無機材料を利用した無機固体電解質なども挙げられ、これらを単独あるいは他の電解質と組み合わせて用いてもよい。高分子固体電解質に用いることができる高分子化合物としては、ポリエーテル、ポリエステル、ポリフォスファゼン、あるいはポリシロキサンなどが挙げられる。無機固体電解質としては、イオン伝導性セラミックス、イオン伝導性結晶、あるいはイオン伝導性ガラスなどが挙げられる
11・・・電池缶
12,13・・・絶縁板
14・・・電池蓋
15・・・安全弁機構
16・・・熱抵抗素子
17・・・ガスケット
20・・・巻回電極体
21・・・正極
21A・・・正極集電体
21B・・・正極活物質層
22・・・負極
22A・・・負極集電体
22B・・・負極活物質層
23・・・セパレータ
24・・・センターピン
25・・・正極リード
26・・・負極リード
12,13・・・絶縁板
14・・・電池蓋
15・・・安全弁機構
16・・・熱抵抗素子
17・・・ガスケット
20・・・巻回電極体
21・・・正極
21A・・・正極集電体
21B・・・正極活物質層
22・・・負極
22A・・・負極集電体
22B・・・負極活物質層
23・・・セパレータ
24・・・センターピン
25・・・正極リード
26・・・負極リード
Claims (3)
- オリビン構造を有するリチウムリン酸化合物を含む正極と、リチウムをドープおよび脱ドープ可能な負極活物質を含む負極と、非水電解質と、を備え、
上記負極活物質は、満充電状態にて7LiのNMRを測定した場合に塩化リチウム基準の化学シフト値が0ppmから100ppmの範囲に複数のピークに起因するスペクトルを有し、且つピーク分離した際にピーク位置が少なくとも1ppm、31ppm、44ppmおよび58ppmに存在する炭素材料を含むこと
を特徴とする非水電解質電池。 - 負極活物質層に含まれる上記炭素材料の含有量が、7wt%〜50wt%の範囲内であること
を特徴とする請求項1記載の非水電解質電池。 - 上記オリビン構造を有するリチウムリン酸化合物は、LiFePO4で表される化合物であること
を特徴とする請求項1記載の非水電解質電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007295302A JP2009123473A (ja) | 2007-11-14 | 2007-11-14 | 非水電解質電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007295302A JP2009123473A (ja) | 2007-11-14 | 2007-11-14 | 非水電解質電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2009123473A true JP2009123473A (ja) | 2009-06-04 |
Family
ID=40815419
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007295302A Pending JP2009123473A (ja) | 2007-11-14 | 2007-11-14 | 非水電解質電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2009123473A (ja) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05121066A (ja) * | 1991-10-29 | 1993-05-18 | Asahi Chem Ind Co Ltd | 非水電池負極 |
| WO1998024134A1 (fr) * | 1996-11-26 | 1998-06-04 | Kao Corporation | Materiau d'electrode negative pour pile secondaire non aqueuse |
| JPH11167920A (ja) * | 1997-12-05 | 1999-06-22 | Kansai Coke & Chem Co Ltd | 非水系二次電池用負極材の製造法 |
| JP2005108681A (ja) * | 2003-09-30 | 2005-04-21 | Mitsubishi Chemicals Corp | リチウム二次電池用正極材料、リチウム二次電池用正極及びリチウム二次電池 |
| JP2006310265A (ja) * | 2005-03-31 | 2006-11-09 | Mitsubishi Chemicals Corp | 非水電解液二次電池用負極材料およびそれを用いた非水電解液二次電池 |
| JP2007294323A (ja) * | 2006-04-26 | 2007-11-08 | Gs Yuasa Corporation:Kk | 非水電解質電池の製造方法 |
-
2007
- 2007-11-14 JP JP2007295302A patent/JP2009123473A/ja active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05121066A (ja) * | 1991-10-29 | 1993-05-18 | Asahi Chem Ind Co Ltd | 非水電池負極 |
| WO1998024134A1 (fr) * | 1996-11-26 | 1998-06-04 | Kao Corporation | Materiau d'electrode negative pour pile secondaire non aqueuse |
| JPH11167920A (ja) * | 1997-12-05 | 1999-06-22 | Kansai Coke & Chem Co Ltd | 非水系二次電池用負極材の製造法 |
| JP2005108681A (ja) * | 2003-09-30 | 2005-04-21 | Mitsubishi Chemicals Corp | リチウム二次電池用正極材料、リチウム二次電池用正極及びリチウム二次電池 |
| JP2006310265A (ja) * | 2005-03-31 | 2006-11-09 | Mitsubishi Chemicals Corp | 非水電解液二次電池用負極材料およびそれを用いた非水電解液二次電池 |
| JP2007294323A (ja) * | 2006-04-26 | 2007-11-08 | Gs Yuasa Corporation:Kk | 非水電解質電池の製造方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6884546B1 (en) | Secondary battery | |
| CN100438147C (zh) | 锂二次电池的正极及采用它的锂二次电池 | |
| JP5910627B2 (ja) | 二次電池 | |
| JP3797197B2 (ja) | 非水電解質二次電池 | |
| JP5262175B2 (ja) | 負極および二次電池 | |
| CN109216758B (zh) | 非水电解质电池以及非水电解质电池的制造方法 | |
| JP5070753B2 (ja) | 電池 | |
| CN102792509B (zh) | 锂离子二次电池 | |
| CN103493276A (zh) | 锂二次电池 | |
| JP4968225B2 (ja) | 非水電解質電池 | |
| JP5412843B2 (ja) | 電池 | |
| JP5141582B2 (ja) | 非水電解質二次電池 | |
| US20140227562A1 (en) | Lithium secondary-battery pack, electronic device using same, charging system, and charging method | |
| JP2009123474A (ja) | 非水電解質電池 | |
| CN101924244A (zh) | 电池 | |
| JP4715848B2 (ja) | 電池 | |
| JP2009134970A (ja) | 非水電解質電池 | |
| JP4424895B2 (ja) | リチウム二次電池 | |
| JP4560854B2 (ja) | 非水電解質二次電池 | |
| CN100466364C (zh) | 一种安全锂离子电池 | |
| US8372541B2 (en) | Non-aqueous electrolyte secondary battery | |
| JP2010135115A (ja) | 非水電解質二次電池 | |
| JP4938923B2 (ja) | 二次電池 | |
| JP2015018602A (ja) | 非水電解液二次電池 | |
| JP2007157538A (ja) | 電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100812 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20120822 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120828 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130312 |