JP2012503473A - 耐熱性耐圧性生物の材料への取り込み - Google Patents
耐熱性耐圧性生物の材料への取り込み Download PDFInfo
- Publication number
- JP2012503473A JP2012503473A JP2011527359A JP2011527359A JP2012503473A JP 2012503473 A JP2012503473 A JP 2012503473A JP 2011527359 A JP2011527359 A JP 2011527359A JP 2011527359 A JP2011527359 A JP 2011527359A JP 2012503473 A JP2012503473 A JP 2012503473A
- Authority
- JP
- Japan
- Prior art keywords
- viable
- bar
- microorganisms
- polymer
- pressure
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
- C12N1/205—Bacterial isolates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B29—WORKING OF PLASTICS; WORKING OF SUBSTANCES IN A PLASTIC STATE IN GENERAL
- B29C—SHAPING OR JOINING OF PLASTICS; SHAPING OF MATERIAL IN A PLASTIC STATE, NOT OTHERWISE PROVIDED FOR; AFTER-TREATMENT OF THE SHAPED PRODUCTS, e.g. REPAIRING
- B29C43/00—Compression moulding, i.e. applying external pressure to flow the moulding material; Apparatus therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N11/00—Carrier-bound or immobilised enzymes; Carrier-bound or immobilised microbial cells; Preparation thereof
- C12N11/02—Enzymes or microbial cells immobilised on or in an organic carrier
- C12N11/08—Enzymes or microbial cells immobilised on or in an organic carrier the carrier being a synthetic polymer
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N11/00—Carrier-bound or immobilised enzymes; Carrier-bound or immobilised microbial cells; Preparation thereof
- C12N11/02—Enzymes or microbial cells immobilised on or in an organic carrier
- C12N11/08—Enzymes or microbial cells immobilised on or in an organic carrier the carrier being a synthetic polymer
- C12N11/089—Enzymes or microbial cells immobilised on or in an organic carrier the carrier being a synthetic polymer obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- C12N11/093—Polyurethanes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N11/00—Carrier-bound or immobilised enzymes; Carrier-bound or immobilised microbial cells; Preparation thereof
- C12N11/02—Enzymes or microbial cells immobilised on or in an organic carrier
- C12N11/08—Enzymes or microbial cells immobilised on or in an organic carrier the carrier being a synthetic polymer
- C12N11/089—Enzymes or microbial cells immobilised on or in an organic carrier the carrier being a synthetic polymer obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- C12N11/096—Polyesters; Polyamides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12R—INDEXING SCHEME ASSOCIATED WITH SUBCLASSES C12C - C12Q, RELATING TO MICROORGANISMS
- C12R2001/00—Microorganisms ; Processes using microorganisms
- C12R2001/01—Bacteria or Actinomycetales ; using bacteria or Actinomycetales
- C12R2001/07—Bacillus
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S435/00—Chemistry: molecular biology and microbiology
- Y10S435/8215—Microorganisms
- Y10S435/822—Microorganisms using bacteria or actinomycetales
- Y10S435/832—Bacillus
- Y10S435/839—Bacillus subtilis
Landscapes
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Medicinal Chemistry (AREA)
- Mechanical Engineering (AREA)
- Fodder In General (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Environmental & Geological Engineering (AREA)
- Immobilizing And Processing Of Enzymes And Microorganisms (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
【選択図】なし
Description
しかしながら、これらの有益な特性が材料に取り入れられるように微生物を材料中に取り込むことは容易ではない。実際、ポリマー、樹脂等だけではなく、食品、動物用飼料、医薬品、薬物にまで至る多くの材料が、高温、高圧の条件下で調製される。例えば、永久非生分解性ポリマーの加工温度は、常圧条件であったとしても100℃よりずっと高く、生体材料を取り込ませるには温度が高すぎる。生きている活性微生物をこのレベルの温度でその生物に致命的な影響を与えることなく着床させるのは不可能である。
そのため、導入する生物が通常は正常な周囲温度で有用な活動を行うとしても、材料製造中に生きているかまたは生存能力のある生物を取り込むことができないならば、利点は得られない。これはポリマーやプラスチックだけではなく、人間や動物が消費する材料(例えば、食物、薬物)にも言える。
材料を加工する温度が(可能性は否めないものの)必ずしもこれほど高いわけではないが、材料は、高温プロセス、例えば、食品の押出成形、調理時の押出成形、その他の押出成形プロセス(例えば、特許文献1)、ペレット化、圧力調理、成型、熱成形等を経ることが多い。これらの高圧プロセスもまた、高温(また恐らくは乾燥)と組み合わされることが多く、典型的な微生物の生存能に悪影響を及ぼす。例えば、Biourgeらは、バチルス株(CIP5832)をドッグフードに含めようとしたが、押出成形/発泡/乾燥プロセスによって芽胞の99%より多くが失われてしまうことから、バチルス株CIP5832を押出成形/発泡/乾燥プロセスの前にドッグフードに含めるべきではないと結論付けている(非特許文献1)。
マトリックス成分と微生物とを分けて維持することから、これらの応用例では必然的にプロセス工程の数が多くなり、より複雑でコストの高い方法となる。更に、これらのプロセスは、微生物を材料から分離し得る場合にしか適用できず(例えば、微生物が材料の外側にくる)、活性が材料の外側ではなく内側で起きるべき場合は使用することができない。単細胞または多細胞生物の疎水性ポリマーへの取り込みが特許文献5で提案されていて、これは100℃より高い温度ではあるが依然として標準的な圧力条件下の場合のものである。しかしながら、これは(単細胞または多細胞)生物を使用した実施例が含まれていないことから、そのような生物が記載の疎水性ポリマーの調製に使用されても依然として生存可能か否かは不明であり、生物の生存は考えにくい。これらの条件下では細胞中の水が沸騰し始めるからである。
しかし驚くべきことに、材料加工温度でも生き延びる特殊な細菌(特にはその芽胞)を、生存能を大きく失うことなく使用可能なことが発見された。更に、この細菌は材料加工温度でも様々な材料に取り込むことが可能であり、細菌は材料に取り込まれてもその特性を維持可能である。最も注目すべきことは、この特殊な細菌が、微生物を使用した作業で通常想定される温度よりはるかに高い温度にも耐えることである。しかしながら、そのような高温は、材料加工の分野(例えば、ポリマー加工、食品加工)では一般的であり、典型的には100〜350℃の範囲、より具体的には120〜300℃の範囲、より一層具体的には130〜300℃の範囲、最も具体的には150〜300℃の範囲である。特定の実施形態において、温度範囲の上限は(例えば生存能を上昇させるために)220℃、210℃、200℃、より一層具体的には150〜200℃に限定される。更に、材料加工中に印加される圧力下でも生存能を大きく失うことなく生き延びる特殊な細菌(特にはその芽胞)を使用可能である。ここでもまた、その細菌を、材料加工圧力下で様々な材料に取り込むことが可能であり、細菌は材料に取り込まれてもその特性を維持可能である。
重量%=(M2−M1)×100/M1
全ての測定は好ましくは2度行われて、平均をとるべきである。特定の実施形態において、吸収値は少なくとも0.01、具体的には少なくとも0.02、より具体的には少なくとも0.1、最も具体的には少なくとも0.2であるべきである。
更に特定の実施形態において、極性及び吸水値は組み合わされ、例えば、ポリマーは、望ましい特性に応じて少なくとも17(MPa)1/2の極性値及び少なくとも0.01の吸水値を有する。高い吸水値は、ポリマーが時間の経過に伴ってより多くの水を吸収することを意味し、高い極性値は、ポリマー鎖と極性溶媒(すなわち、水)との間の相互作用がより大きいことを示す。ポリマーの極性は、所定の溶媒における溶解度に依存し、この溶解度は、化学構造、鎖分岐の量及び結晶化度に左右される。極めて特定の実施形態において、ポリマーは酸素透過性である。
これにより、生存能力のある生物が含まれた材料を製造するための方法が提供され、この方法は、天然または合成ポリマー、樹脂、食品、動物用飼料及び薬物から選択されるマトリックスと、温度100〜350℃及び/または圧力1.5〜400バールで生存可能な、微生物の生きているまたは生存能力のある芽胞とを、温度100〜350℃及び/または圧力1.5〜400バールで混合することを含む。特定の実施形態において、微生物は、マトリックス/加工材料全体に均等に(均質に)分散させられる。
別の実施形態においては、微生物が二酸化炭素を消費するまたは内容物中で脱着を行って浸透バリアとして機能する二酸化炭素を産生する場合、二酸化炭素バリアが得られる。これらの用途では、脱水状態/乾燥状態の生物に再度水分補給が可能である必要がある。このため、このような用途で使用されるポリマーは、水飽和が可能であるべきであり、すなわちポリマーは、中の芽胞がその含水量を増大させて代謝的に活性な生物に戻れるように十分な含水が可能でなくてはならない。これは極性ポリマーの使用によって達成し得る。特定の実施形態において、マトリックス成分として使用されるポリマーは極性ポリマーである。或いはまたはそれに加えて、十分に高い吸水値を有するポリマーが使用される。特定の実施形態において、ポリマーのH2O吸収値は少なくとも0.01、少なくとも0.02、少なくとも0.1または少なくとも0.2である。極めて特定の実施形態において、ポリマーは、十分に高い吸水値を有する極性ポリマーである。
本方法の利用の別の例が、人間または動物が消費する材料(例えば、食品、動物用飼料(ペットフード)、薬物、医薬品等)の調製における利用である。典型的には、このような材料に取り込まれる微生物は、摂取されることによって生物の健康に与えるその有益な特性を目的として使用され、すなわちプロバイオティクスである。プロバイオティクス細菌または酵母培養物は、身体の天然の腸管内菌叢(微生物の生態系)の再構築の支援を目的としたものである。これらは抗生物質の投与後または消化管関連カンジダ症の治療の一環として推奨されることがある。プロバイオティクスによってアレルギー、過度のアルコール摂取、ストレス、有毒物質への暴露及びその他の疾患に対抗するための免疫系が強化されると言われている。これらの場合、人間の身体での効果が高い細菌は、有害な細菌が人間の健康に害を与えるほど増殖する事象の発生回数を低下させ得る。プロバイオティクスは、例えば乳糖不耐症への対処、大腸がんの予防、コレステロールの低下、血圧の低下、免疫機能の改善、感染症の防止、ヘリコバクター・ピロリ感染症の治療、抗生物質関連下痢の軽減、炎症の軽減、ミネラル吸収の改善、ストレス下での有害な細菌の増殖の防止並びに過敏性腸症候群及び潰瘍性大腸炎の症状の改善において有益であることが判明している。特定の実施形態において、(マトリックス)材料は人間または動物による消費用であり、微生物またはその芽胞はプロバイオティクスである。
このため、押出成形工程、ペレット化工程、圧力調理工程、熱成型工程、圧縮成形工程、射出成形工程、熱成形工程、含浸工程、真空成形工程、発泡工程またはホットメルト工程を、マトリックス材料と微生物またはその芽胞との混合中またはその後に行う方法が提供される。更に特定の実施形態において、押出成形工程、ペレット化工程、圧力調理工程、熱成型工程、圧縮成形工程、射出成形工程、熱成形工程、含浸工程、真空成形工程、発泡工程またはホットメルト工程は、温度100〜350℃で行われる。別の特定の実施形態において、押出成形工程、ペレット化工程、圧力調理工程、熱成型工程、圧縮成形工程、射出成形工程、熱成形工程、含浸工程、真空成形工程、発泡工程またはホットメルト工程は、圧力1.5〜400バールで行われる。更に別の実施形態において、押出成形工程、ペレット化工程、圧力調理工程、熱成型工程、圧縮成形工程、射出成形工程、熱成形工程、含浸工程、真空成形工程、発泡工程またはホットメルト工程は、温度100〜350℃及び圧力1.5〜400バールで行われる(材料を高圧にさらした後に高温にさらす、またはその反対が可能であり、またこの加工工程中に両方が起こることは、温度と圧力とが同時に上昇することを必然的に示唆するものではないが、それも1つの可能性である)。
・微生物の培養
4種類のコロニー(ID9698 t1、ID9698 t2、ID9698 t3、ID9698 t4)を原料から単離することができ、個々のコロニーを純化し、分析した。原料は、アンティアトラス山脈の乾燥地帯であるモロッコのビウグラ(Biougra)から入手した。ここでは太陽光にさらされた乾燥した有機培養基上で夏の極めて高い温度にも耐える芽胞を発見する可能性があった。脂肪酸分析を行い、4種類の培養物全てが「バチルス及び関連種」の群に割り振られた。続いて、部分16S rDNA配列解析を行ったところ、4種類の培養物全てが、Bacillus subtilis複合体に属すると同定された。
部分gyrA配列解析及び系統学的研究:Bacillus subtilis複合体内での種の識別のためのgyrA配列の利用可能性はChun及びBaeによって報告されていて(非特許文献7)、また既に実証に成功している。gyrA遺伝子は、RAPD分析の一環で抽出されたDNAからPCRによって増幅された。PCRで増幅されたgyrAは、NucleoFast(登録商標)96 PCR Clean−up Kit(Macherey−Nagel、デューレン、ドイツ)を使用して精製された。シーケンシング反応は、BigDye(登録商標)Terminator Cycle Sequencing Kit(Applied Biosystems、フォスターシティ、カリフォルニア州、米国)を使用して行われ、BigDye(登録商標)XTerminatorT Purification Kit(Applied Biosystems、フォスターシティ、カリフォルニア州、米国)を使用して精製された。シーケンシングは、ABI Prism(登録商標)3130XL Genetic Analyzer(Applied Biosystems、フォスターシティ、カリフォルニア州、米国)を使用して行われた。プライマーは、配列を部分的に重複させて選択され、信頼性の高いデータが集められた。配列アセンブリングは、プログラムであるAutoAssembler(商標)(Applied Biosystems、フォスターシティ、カリフォルニア州、米国)を使用して行われた。類似性マトリックスは、ソフトウェアパッケージであるBioNumerics(Applied Maths、ベルギー)を使用して、ギャップペナルティ0%で不明な塩基の排除後に相同性を計算することによって作成され、類似性マトリックスは、オープンギャップペナルティ100%、ユニットギャップペナルティ0%のペアワイズアラインメントに基づく。
1.ID9698 t1の系統学的位置は、明らかにBacillus subtilis複合体にある。
2.幾つかのBacillus amyloliquefaciens株に見られた高いgyrA配列類似性(95.9〜99.7%)は、ID9698 t1がこの種に属することを実証している。
・材料及び方法
以下の微生物を試験した。
1.株ID9698(Bacillus amyloliquefaciensと同定)
2.LMG8197:Bacillus subtilis subsp.Spizizenii;gyrA配列がSEQ ID NO:1に対して70%より大きい配列同一性を示す細菌
3.Enterol(登録商標):生酵母(プロバイオティクス)(Saccharomyces boulardii)の入った市販の薬物
4.Probactiol(登録商標):乳酸菌生菌(プロバイオティクス)(Lactobacillus acidophilus NCFMとBifidobacterium lactis Bl−07との1/1混合物)の入った市販の薬物
なお、結果でも同じ番号を使用した。
既知の量の異なる微生物の粉末を直径8mmのガラス試験管(VWR、製品番号212−0011)に移し、適切なプラスチックキャップで閉じた。最大で試験管の1/4まで粉末を入れた。試験管の3/4を、100℃±0.1及び110℃±0.1のフライ油並びに240℃±5及び280℃±5の金属浴(バチルスの場合のみ)に沈めた。浴の温度を、データロガー付き熱電対で観察した。全ての処理において、温度を、砂を1/4充填した試験管でも観察した。これらの測定から、サンプルを所望の温度にまで温めるには1分かかると思われた。この温度を更に1分間にわたって維持した(2分間の処理)。酵母のサンプルだけは240℃で1分しか浸漬しなかったが、これは物理的に2分は実行不可能だからであった(サンプルの過剰な発泡)。また、バチルス株のサンプルは280℃で1分間だけ処理された。
図1の結果から、100℃及び110℃での乳酸菌は既に±3.50logの低下を見せたように思われた。これらの温度でのバチルス株の場合の低下は±1〜1.5log単位であり、酵母株の場合、(コロニー形成能は初期に既に低かったものの)低下は観察されなかった。240℃で、酵母と乳酸菌の両方が依然として若干の増殖を見せる。しかしながら、これはわずかなものであった。両方のサンプルにおいて、cfuの数は絶対数で>108cfuから10cfuに低下した。このわずかな割合の生き残りは、試験管のキャップについた微生物で間違いない。サンプルのこの部分は浴に沈めていないことから、同程度には加熱されなかった。若干異なる装置を使用した第2の実験において、Bacillus amyloliquefaciens株ID9698の乾熱耐性を、酵母及び乳酸菌の乾熱耐性と比較した。
以下の微生物を試験した。
1.株ID9698(Bacillus amyloliquefaciensと同定)
2.酵母:パン酵母Bruggeman Instant(Algist Bruggeman、ヘント)(Saccharomyces cerevisiae)
3.Probactiol(登録商標):乳酸菌生菌(プロバイオティクス)(Lactobacillus acidophilus NCFMとBifidobacterium lactis Bl−07との1/1混合物)の入った市販の薬物
乾熱処理を、熱重量分析機(TGA)で行った。処理温度は100〜240℃の範囲で10℃間隔で変化させた。10.89log芽胞/gのB.amyloliquefaciens、10.17log cfu/gの酵母または9.09log cfu/gの乳酸菌をそれぞれ含有する既知の量(約15mg)を乾燥粉末を処理温度にまで予備加熱されたTGAに入れ、2分間にわたって熱処理した。この粉末を滅菌マイクロピペットに移し、1mlの滅菌生理食塩水(PPS)に再懸濁させた。その後、適切な希釈物をB.amyloliquefaciensについては強化栄養寒天培地、乳酸菌についてはMRS寒天培地、酵母についてはYGC寒天培地上で培養した。全てのプレートを3日間にわたって30℃でインキュベートしてからコロニー数を数えた。
試験した微生物の熱安定性における大きな違いを示した。処理温度130℃では、乳酸菌の場合、5logより大きい減少が起きた(表1)。同じ温度で、B.amyloliquefaciens及び酵母では減少はほとんど観察されなかった。酵母の場合、処理温度150℃で大幅な減少が起き(3.61log)、B.amyloliquefaciensでは180℃まで減少がほとんど見られなかった(<1log)。
なお、表1は、乾燥粉末の15mgサンプルにおける減少(log cfu)を示し、「>」は、検出限界を表す。
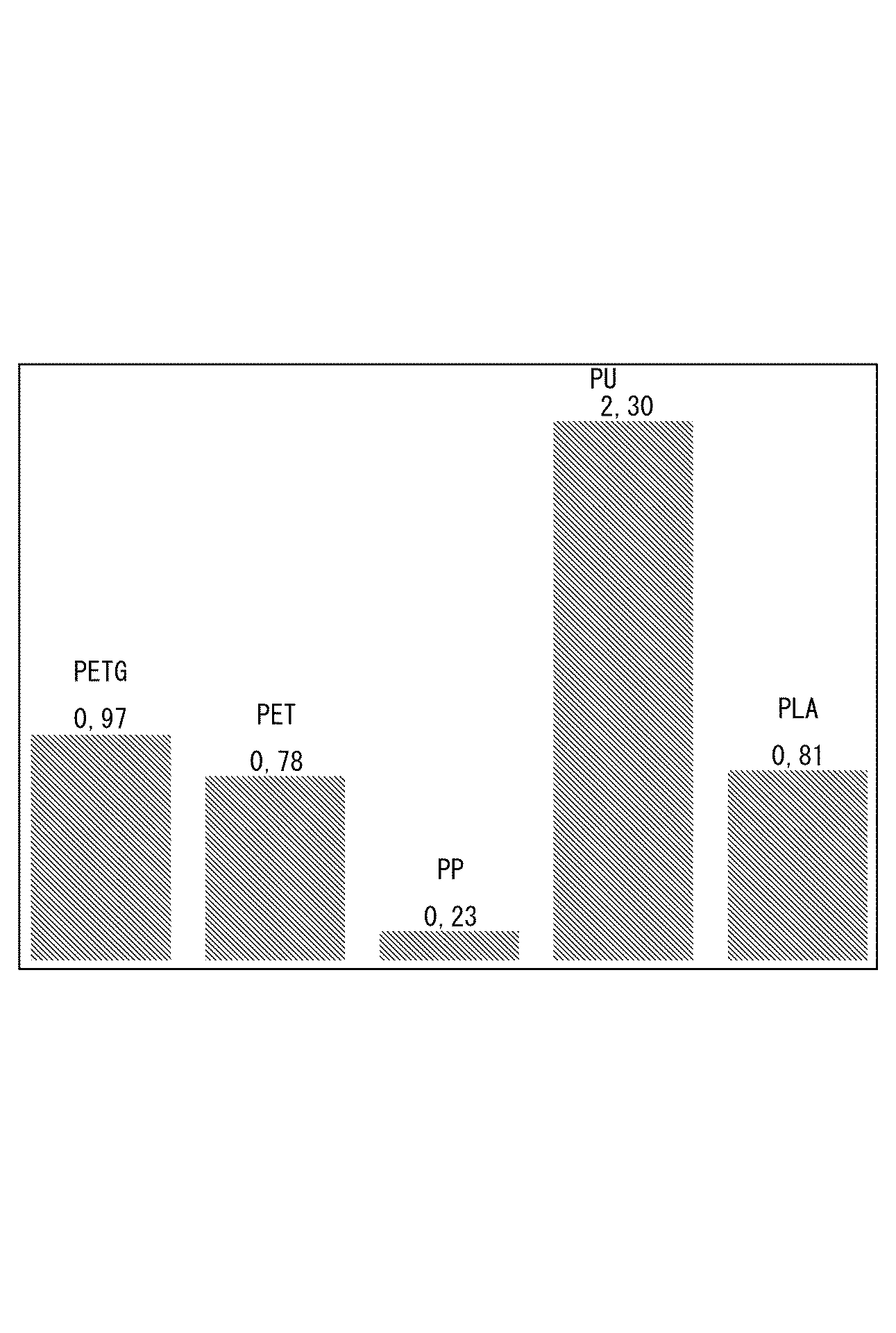
全ての試験ポリマーについて、時間の経過に伴う吸水量の増加が観察された(図2、図3)。図3において、PUは極めて高い吸水量を示し、これは残り3つのポリマーと対照的である。これらの測定において、PUは3日後に停滞状態に達する。PETg及びBioPETg(すなわち、Bacillus amyloliquefaciens芽胞とPETgとの混合物)の場合、高い吸収値も観察される。図3において、これら2種類のポリマー間でのわずかな差をはっきりと観察することができる。BioPETgの停滞状態は、1〜3日目に得られた。4日目からは、上昇を観察することができる。時間の経過に伴うPETの吸水量の少なさは予測可能であった。図4は、湿度100%に3日間にわたってさらされた後の液体含有量(%)を示す。表2は、幾つかのポリマーについての極性値及び吸水値を示す。
・導入
乾燥した芽胞材料を、高温及び高圧下でポリエステル中に取り込んだ。取り込みプロセス後の芽胞の生存率を、このポリエステルから芽胞を抽出することによって測定した。生きている芽胞の数を平板培養技法によって数えた。
乾燥芽胞粉末は、適切な発酵プロセス及び下流処理によって製造された。乾燥芽胞をポリエステルに取り込んだ。ポリエステルの典型的な例として、PETGを使用した。取り込みは、4%w/w濃度のポリマープレスで行われた。芽胞を含有していないポリマーのプレート(素材片)は、210℃、圧力10kNで5分間にわたってプレスされた。乾燥芽胞粉末を、素材片である2枚のポリマープレート間に正しい濃度でプレスすることによって、芽胞を取り込んだ1枚の新しいサンプルを得た。加工は210℃、29バールで5分間にわたって行わされた。
実験によって、100%のクロロホルムでの10分間の処理によって芽胞の数が最大で1.7log減少することが判明した(図5)。抽出された芽胞は速やかに水相に移動し、クロロホルムとの接触時間は最小限に抑えられる。このため、抽出プロセスは芽胞の生き残りに最小限の影響しか与えないと予想することができる。表3の結果から、選択された芽胞がポリマーマトリックス中への高温及び高圧取り込み後も生き残り、取り込み後にこれらの生物を更に利用できることが見て取れる。なお、表3は、ポリエステル中への取り込み後の芽胞の減少を示す。
・導入
乾燥した芽胞材料を異なるポリマー材料に取り込んだ。ポリマーは、幅広い極性で選択された(表2)。ポリウレタン(PU)の極性>ポリ乳酸(PLA)。ポリマーの極性は、ポリマー吸湿性に大きな影響を与える。ポリマーの極性が高ければ高いほど、吸水量は多くなる。これは、幾つかのポリマーについての吸水データによって実証される(表2)。
乾燥した芽胞粉末は、適切な発酵プロセス及び下流処理によって製造された。乾燥芽胞を、2種類のポリマー(PU、PLA)に4%w/w濃度で取り込んだ。ポリマーマトリックスへの取り込みは、ポリマープレスによって行われた。芽胞を含有していないポリマーのプレート(素材片)は、PUについては130℃、PLAについては170℃の圧力10kNで5分間にわたってプレスされた。乾燥した芽胞粉末を、素材片である2枚のポリマープレート間で正しい濃度でプレスすることによって、芽胞をポリマーマトリックス内で溶融混合し、1枚の新しい混合サンプルを得た。加工は5分間にわたってPUについては130℃、PLAについては170℃の10kNで行われた。ヘッドスペース内の酸素の濃度を、窒素でのフラッシングによって±5%に設定した。9mlの滅菌脱塩水の添加によって、芽胞の発芽に必要な高い湿度を達成した。酸素消費微生物の水中での増殖を防止するために、10mg/lのアンピリシン、様々な抗生物質を添加した。酸素吸収測定は、1.2gのプレス加工されたサンプルを21mlのヘッドスペースを有する閉鎖容器に入れることによって行われた。
平均酸素吸収率(oxygen absorption rate:OAR)(mlO2/日)を2回繰り返した測定について計算した。PU及びPLAに取り込まれた芽胞の酸素吸収率のデータを表4に示す。
Claims (17)
- ベルギー微生物保存機関(BCCM)にID9698で寄託されているBacillus amyloliquefaciens株であるか、
または、gyrA配列が、BCCMにID9698で寄託されているBacillus amyloliquefaciens株の部分gyrA配列(SEQ ID NO:1)と少なくとも70%同一である
ことを特徴とするバチルス株。 - 生存能力のある生物が含まれた材料を製造する方法であって、
天然または合成ポリマーから選択されるマトリックスと、
温度100〜220℃及び/または圧力1.5〜50バールで生存可能であり、微生物の生きているまたは生存能力のある芽胞とを、
温度100〜220℃及び/または圧力1.5〜50バールで混合するステップを有する
ことを特徴とする製造方法。 - 微生物またはその芽胞が、温度100〜220℃及び圧力1.5〜50バールで生存可能である
請求項2に記載の方法。 - 微生物またはその芽胞が、BCCMにID9698で寄託されているBacillus amyloliquefaciens株、または、gyrA配列が、BCCMにID9698で寄託されているBacillus amyloliquefaciens株の部分gyrA配列(SEQ ID NO:1)と少なくとも70%同一であるバチルス株である
請求項2または3に記載の方法。 - ポリマーが、アクリレート、メタクリレート、アクリルアミド、メタクリルアミド、アルコール、アミン、無水物、エポキシド、スチレン、官能化ビニル、官能化アリル、プロペン、ブタジエン、エチレン、イソシアネート、ラクタム、ラクトン、糖類、グルコース、エステルから成る群から選択される少なくとも1種のモノマーを含む
請求項2ないし4のいずれかに記載の方法。 - ポリマーが、極性ポリマーである
請求項2ないし5のいずれかに記載の方法。 - ポリマーが、少なくとも20(MPa)1/2の極性を有する
請求項6に記載の方法。 - ポリマーが、少なくとも0.2の吸水値を有する
請求項2ないし7のいずれかに記載の方法。 - 押出成形工程、ペレット化工程、圧力調理工程、熱成型工程、圧縮成形工程、射出成形工程、熱成形工程、含浸工程、真空成形工程、発泡工程またはホットメルト工程を、混合するステップの最中か、混合するステップの後に行う
請求項2ないし8のいずれかに記載の方法。 - 押出成形工程、ペレット化工程、圧力調理工程、熱成型工程、圧縮成形工程、射出成形工程、熱成形工程、含浸工程、真空成形工程、発泡工程またはホットメルト工程を、温度100〜220℃及び/または圧力1.5〜50バールで行う
請求項9に記載の方法。 - 乾燥条件下で高温となる
請求項2ないし10のいずれかに記載の方法。 - 生存能力のある生物が含まれた材料であって、
請求項2ないし11に記載の方法によって得られる
ことを特徴とする材料。 - 生物が、好気性微生物である
請求項12に記載の材料。 - 生物が、BCCMにID9698で寄託されているBacillus amyloliquefaciens株、または、gyrA配列が、BCCMにID9698で寄託されているBacillus amyloliquefaciens株の部分gyrA配列(SEQ ID NO:1)と少なくとも70%同一であるバチルス株である
請求項12または13に記載の材料。 - 生存能力のある生物が含まれた材料の使用であって、
請求項13ないし14に記載の材料を酸素バリアとして使う
ことを特徴とする使用。 - 微生物の生きているまたは生存能力のある芽胞の使用であって、
生存能力のある微生物が含まれた材料を製造するために、温度100〜220℃及び/または圧力1.5〜50バールで生存可能である微生物の生きているまたは生存能力のある芽胞を使う
ことを特徴とする使用。 - 芽胞が、BCCMにID9698で寄託されているBacillus amyloliquefaciens株、または、gyrA配列が、BCCMにID9698で寄託されているBacillus amyloliquefaciens株の部分gyrA配列(SEQ ID NO:1)と少なくとも70%同一であるバチルス株に由来するものである
請求項16に記載の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US19415808P | 2008-09-24 | 2008-09-24 | |
| US61/194,158 | 2008-09-24 | ||
| EP09168652.7 | 2009-08-26 | ||
| EP09168652 | 2009-08-26 | ||
| PCT/EP2009/062389 WO2010034776A1 (en) | 2008-09-24 | 2009-09-24 | Incorporation of thermo-resistant and/or pressure-resistant organisms in materials |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2012503473A true JP2012503473A (ja) | 2012-02-09 |
Family
ID=41254669
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011527359A Pending JP2012503473A (ja) | 2008-09-24 | 2009-09-24 | 耐熱性耐圧性生物の材料への取り込み |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US11028454B2 (ja) |
| EP (2) | EP3508342A1 (ja) |
| JP (1) | JP2012503473A (ja) |
| KR (2) | KR101764592B1 (ja) |
| CN (1) | CN102369105A (ja) |
| AU (2) | AU2009295886A1 (ja) |
| BR (1) | BRPI0913683A2 (ja) |
| CA (1) | CA2738602A1 (ja) |
| EA (1) | EA201100533A1 (ja) |
| MX (1) | MX348019B (ja) |
| WO (1) | WO2010034776A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018083946A (ja) * | 2016-11-24 | 2018-05-31 | 喬福材料科技股▲ふん▼有限公司Chiao Fu Material Technology Co.,Ltd. | 生分解性フィルム材料、及びその製造方法 |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012145803A2 (en) * | 2011-04-29 | 2012-11-01 | Resilux N.V. | Method for producing a polymer product from multidimensional aggregated components as barrier or carriers of living microbial cells and biological barriers in plastic and textile |
| EP2518138A1 (en) * | 2011-04-29 | 2012-10-31 | Resilux | Method for producing a polymer product from polar lipids from archaea as carriers of living microbial cells and biological barriers in plastic and textile |
| BE1019981A5 (nl) * | 2011-05-18 | 2013-03-05 | Resilux | Holle voorwerpen, i.h.b. kunststofvoorvormen, res.-behouders, met een barrierelaag en spuitgietwerkwijze, resp. inrichting voor het vervaardigen ervan. |
| US9476835B2 (en) | 2012-04-13 | 2016-10-25 | Empire Technology Development Llc | Bioluminescent packaging |
| US20140183090A1 (en) * | 2012-07-05 | 2014-07-03 | Empire Technology Development Llc | Bioactive packaging |
| AU2015292271B2 (en) * | 2014-07-25 | 2020-09-10 | The University Of Queensland | Bacillus amyloliquefaciens probiotic compositions, methods of production, and methods of use |
| CN107474426B (zh) * | 2017-08-07 | 2020-11-06 | 佛山粤泓益生物科技有限公司 | 聚氯乙烯微生态农业塑料母料及由其制成的育秧盘 |
| CN107474356B (zh) * | 2017-08-07 | 2020-10-09 | 佛山粤泓益生物科技有限公司 | 聚乙烯微生态农业塑料母料及由其制成的育秧盘 |
| CN117431192B (zh) * | 2023-12-20 | 2024-04-23 | 航天神舟生物科技集团有限公司 | 一株解淀粉芽孢杆菌及其在行星保护领域中的应用 |
| WO2025186462A1 (en) | 2024-03-07 | 2025-09-12 | Fair-Fusion B.V. | Incorporation of viable micro-organisms in a plastic product |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH03503963A (ja) * | 1988-02-17 | 1991-09-05 | ディフシャム アーベー | 生物学的滅菌制御のためのゲル体および方法 |
| JP2001300477A (ja) * | 2000-04-21 | 2001-10-30 | Shinada Kikai Seisakusho:Kk | 微生物製剤を利用して有機性廃棄物を高速安定分解する廃棄物処理方法 |
| JP2003507428A (ja) * | 1999-08-26 | 2003-02-25 | ガネデン バイオテック, インコーポレイテッド | 共生バクテリア、芽胞および細胞外産物を含む、改良された局所用組成物、ならびにそれらの使用 |
| WO2006024115A1 (en) * | 2004-09-03 | 2006-03-09 | Resilux | Process for manufacturing hydrophobic polymers |
| WO2007064741A2 (en) * | 2005-11-29 | 2007-06-07 | Kemin Industries, Inc. | The use of bacillus pb6 for the prophylaxis or treatment of gastrointestinal and immuno-related diseases |
| JP2007300931A (ja) * | 2001-02-21 | 2007-11-22 | Hitachi Plant Technologies Ltd | 加熱担体及びその製造方法、並びに加熱担体を用いた環境浄化方法 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SE8702840D0 (sv) | 1987-07-10 | 1987-07-10 | Plm Ab | Barrierforsterkning |
| US6423345B2 (en) * | 1998-04-30 | 2002-07-23 | Acusphere, Inc. | Matrices formed of polymer and hydrophobic compounds for use in drug delivery |
| US6248321B1 (en) * | 1999-01-14 | 2001-06-19 | Her Majesty The Queen In Right Of Canada, As Represented By The Minister Of Natural Resources, Canadian Forestry Service | Encapsulation of microparticles in teardrop shaped polymer capsules of cellular size |
| GB0005839D0 (en) * | 2000-03-10 | 2000-05-03 | Provita Eurotech Ltd | Storage and delivery of micro-organisms |
| FR2806417B1 (fr) * | 2000-03-16 | 2003-12-26 | Lallemand Sa | Particules enrobees contenant des microorganismes vivants, procede de production et application desdites particules dans les compositions pharmaceutiques, dietetiques ou alimentaires |
| JP2002274521A (ja) * | 2001-03-16 | 2002-09-25 | Yoshino Kogyosho Co Ltd | 環境に優しいプラスチック容器 |
| GB0205867D0 (en) * | 2002-03-13 | 2002-04-24 | Univ Nottingham | Polymer composite loaded with functioning matter |
| US20040109853A1 (en) * | 2002-09-09 | 2004-06-10 | Reactive Surfaces, Ltd. | Biological active coating components, coatings, and coated surfaces |
| KR100427600B1 (ko) * | 2003-03-07 | 2004-04-28 | (주)한국바이오케미칼 | 바실러스 아밀로리쿼파시엔스 및 이를 포함하는 사료 첨가제 |
| US20050238721A1 (en) | 2004-04-07 | 2005-10-27 | Acquarulo Lawrence A Jr | One step compounding extrusion of drug filled polymers |
| US20060228448A1 (en) | 2005-04-11 | 2006-10-12 | The Iams Company | Pet food compositions comprising two components |
| US8592343B2 (en) * | 2005-09-09 | 2013-11-26 | Embrapa And Universidade Federal Rural Do Rio De Janeiro | Polymeric compositions containing rhizobium and/or plant growth-promoting rhizobacteria inoculant, use thereof and seeds treated with the compositions |
| WO2007060539A2 (en) | 2005-11-28 | 2007-05-31 | Jorrocks Pty Ltd. | Methods for preparation of animal feeds |
-
2009
- 2009-09-24 EA EA201100533A patent/EA201100533A1/ru unknown
- 2009-09-24 EP EP18200290.7A patent/EP3508342A1/en not_active Withdrawn
- 2009-09-24 KR KR1020177002961A patent/KR101764592B1/ko not_active Expired - Fee Related
- 2009-09-24 JP JP2011527359A patent/JP2012503473A/ja active Pending
- 2009-09-24 US US13/120,908 patent/US11028454B2/en active Active
- 2009-09-24 CN CN2009801373603A patent/CN102369105A/zh active Pending
- 2009-09-24 AU AU2009295886A patent/AU2009295886A1/en not_active Abandoned
- 2009-09-24 CA CA2738602A patent/CA2738602A1/en not_active Abandoned
- 2009-09-24 WO PCT/EP2009/062389 patent/WO2010034776A1/en not_active Ceased
- 2009-09-24 EP EP20090783376 patent/EP2352641A1/en not_active Withdrawn
- 2009-09-24 MX MX2011003048A patent/MX348019B/es active IP Right Grant
- 2009-09-24 BR BRPI0913683A patent/BRPI0913683A2/pt not_active Application Discontinuation
- 2009-09-24 KR KR1020117009450A patent/KR20110098996A/ko not_active Ceased
-
2016
- 2016-01-17 AU AU2016200258A patent/AU2016200258B2/en not_active Ceased
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH03503963A (ja) * | 1988-02-17 | 1991-09-05 | ディフシャム アーベー | 生物学的滅菌制御のためのゲル体および方法 |
| JP2003507428A (ja) * | 1999-08-26 | 2003-02-25 | ガネデン バイオテック, インコーポレイテッド | 共生バクテリア、芽胞および細胞外産物を含む、改良された局所用組成物、ならびにそれらの使用 |
| JP2001300477A (ja) * | 2000-04-21 | 2001-10-30 | Shinada Kikai Seisakusho:Kk | 微生物製剤を利用して有機性廃棄物を高速安定分解する廃棄物処理方法 |
| JP2007300931A (ja) * | 2001-02-21 | 2007-11-22 | Hitachi Plant Technologies Ltd | 加熱担体及びその製造方法、並びに加熱担体を用いた環境浄化方法 |
| WO2006024115A1 (en) * | 2004-09-03 | 2006-03-09 | Resilux | Process for manufacturing hydrophobic polymers |
| WO2007064741A2 (en) * | 2005-11-29 | 2007-06-07 | Kemin Industries, Inc. | The use of bacillus pb6 for the prophylaxis or treatment of gastrointestinal and immuno-related diseases |
Non-Patent Citations (5)
| Title |
|---|
| JPN5011012941; AGTHE O: 'INVESTIGATIONS ON THE SURVIVAL OF SPORES OF BACILLUS STEAROTHERMOPHILUS 以下備考' ARCHIVES OF MEAT, FISH ANDDAIRY SCIENCE V47 N2, 19960529, P40-42 * |
| JPN6013061279; Database DDBJ/EMBL/GenBank [online], Accession No. EF176773: '<http://www.ncbi.nlm.nih.gov/nuccore/129921060?sat=4&satkey=19724584>03-DEC-2007 updated, [retrieved' Definition: Bacillus amyloliquefaciens strain LSC04 GyrA gene, partial cds * |
| JPN6013061280; Appl. Environ. Microbiol., 2006, 72(5), pp.3476-3481 * |
| JPN6013061282; J. Biomed. Mater. Res., 1997, 38(2), pp.115-119 * |
| JPN6013061284; Innov. Food Sci. Emerg. Technol. 2001, 2(4), pp.261-272 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018083946A (ja) * | 2016-11-24 | 2018-05-31 | 喬福材料科技股▲ふん▼有限公司Chiao Fu Material Technology Co.,Ltd. | 生分解性フィルム材料、及びその製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2010034776A1 (en) | 2010-04-01 |
| AU2009295886A1 (en) | 2010-04-01 |
| EP3508342A1 (en) | 2019-07-10 |
| KR101764592B1 (ko) | 2017-08-23 |
| MX348019B (es) | 2017-05-23 |
| AU2016200258B2 (en) | 2017-08-31 |
| KR20110098996A (ko) | 2011-09-05 |
| US20110217758A1 (en) | 2011-09-08 |
| BRPI0913683A2 (pt) | 2015-11-24 |
| CA2738602A1 (en) | 2010-04-01 |
| MX2011003048A (es) | 2011-05-19 |
| EA201100533A1 (ru) | 2011-10-31 |
| KR20170017001A (ko) | 2017-02-14 |
| US11028454B2 (en) | 2021-06-08 |
| CN102369105A (zh) | 2012-03-07 |
| EP2352641A1 (en) | 2011-08-10 |
| AU2016200258A1 (en) | 2016-02-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2012503473A (ja) | 耐熱性耐圧性生物の材料への取り込み | |
| Tan et al. | Prospects of kefiran as a food-derived biopolymer for agri-food and biomedical applications | |
| Kosin et al. | Microbial and processing criteria for production of probiotics: a review | |
| Rubel et al. | In vitro prebiotic activity of inulin-rich carbohydrates extracted from Jerusalem artichoke (Helianthus tuberosus L.) tubers at different storage times by Lactobacillus paracasei | |
| Purutoğlu et al. | Diversity and functional characteristics of lactic acid bacteria from traditional kefir grains | |
| Naeem et al. | Isolation characterization and identification of lactic acid bacteria from fruit juices and their efficacy against antibiotics | |
| Lei et al. | Degradation of zearalenone in swine feed and feed ingredients by Bacillus subtilis ANSB01G | |
| Zheng et al. | Antimicrobial activity and safety evaluation of Enterococcus faecium KQ 2.6 isolated from peacock feces | |
| TW200904340A (en) | Processing of natural polysaccharides by selected non-pathogenic microorganisms and methods of making and using the same | |
| CA3136385A1 (en) | Methods and systems for stabilization and preservation of microbes | |
| US20220132834A1 (en) | Methods, apparatuses, and systems for improving microbial preservation yield through rescue and serial passage of preserved cells | |
| KR20170068694A (ko) | 생균제 기능을 지니는 신규 천연 소독제 | |
| Zwielehner et al. | DGGE and real‐time PCR analysis of lactic acid bacteria in bacterial communities of the phyllosphere of lettuce | |
| Lahmamsi et al. | Lactic acid bacteria as an eco-friendly approach in plant production: Current state and prospects | |
| Villarreal-Morales et al. | Metagenomics of traditional beverages | |
| Esawy et al. | Bacillus spp. Isolated from Honey | |
| EP2166083B1 (en) | Novel Lactobacillus paracasei subsp. paracasei SG96, a bacteriostatic composition containing the same and use thereof | |
| Prayoonthien et al. | In vitro fermentation of copra meal hydrolysate by chicken microbiota | |
| Chen et al. | Isolation and characterization of lactic acid bacteria from pobuzihi (fermented cummingcordia), a traditional fermented food in Taiwan | |
| KR20180134128A (ko) | 항산화 활성 및 면역 활성을 가지는 꽃송이버섯 발효물 및 그 제조방법 | |
| Euanorasetr et al. | Isolation and characterization of aerobic actinomycetes with probiotic properties in Nile tilapia | |
| Zhang et al. | Ultrasonic and enzymatic pretreatments of Monascus fermentation byproduct for a sustainable production of Bacillus subtilis | |
| Yoo et al. | Production of an antimicrobial compound by Bacillus subtilis LS 1–2 using a citrus-processing byproduct | |
| Abdel-Aziz et al. | Role of nutrient in microbial developments and microbial metabolic diversity | |
| Muthuramamoorthy et al. | Rubber Seed Shell as Low-cost Medium to Produce Lactic Acid Using Lactobacillus plantarum LB2 and Fabrication of a Polylactic Acid-Chitosan Composite for Fish Fillet Packing. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120330 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20120502 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130226 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20130228 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131217 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140314 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140324 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140414 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140421 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140909 |