JP4219085B2 - 分析エレメントによる核酸の種特異的検出 - Google Patents
分析エレメントによる核酸の種特異的検出 Download PDFInfo
- Publication number
- JP4219085B2 JP4219085B2 JP2000358273A JP2000358273A JP4219085B2 JP 4219085 B2 JP4219085 B2 JP 4219085B2 JP 2000358273 A JP2000358273 A JP 2000358273A JP 2000358273 A JP2000358273 A JP 2000358273A JP 4219085 B2 JP4219085 B2 JP 4219085B2
- Authority
- JP
- Japan
- Prior art keywords
- nucleic acid
- detection
- analytical element
- zone
- sample
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 108020004707 nucleic acids Proteins 0.000 title claims abstract description 93
- 102000039446 nucleic acids Human genes 0.000 title claims abstract description 93
- 150000007523 nucleic acids Chemical class 0.000 title claims abstract description 93
- 238000011895 specific detection Methods 0.000 title description 2
- 238000001514 detection method Methods 0.000 claims abstract description 80
- 239000000523 sample Substances 0.000 claims abstract description 79
- 239000003153 chemical reaction reagent Substances 0.000 claims abstract description 33
- 238000009396 hybridization Methods 0.000 claims abstract description 27
- 239000007788 liquid Substances 0.000 claims abstract description 19
- 238000000034 method Methods 0.000 claims description 54
- 238000012360 testing method Methods 0.000 claims description 26
- 230000003321 amplification Effects 0.000 claims description 16
- 238000003199 nucleic acid amplification method Methods 0.000 claims description 16
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 claims description 15
- 238000012546 transfer Methods 0.000 claims description 13
- 239000000126 substance Substances 0.000 claims description 12
- 238000004458 analytical method Methods 0.000 claims description 11
- 239000000872 buffer Substances 0.000 claims description 10
- 239000003550 marker Substances 0.000 claims description 10
- 230000003196 chaotropic effect Effects 0.000 claims description 8
- 239000000463 material Substances 0.000 claims description 8
- 230000008569 process Effects 0.000 claims description 8
- 239000002585 base Substances 0.000 claims description 7
- ZJYYHGLJYGJLLN-UHFFFAOYSA-N guanidinium thiocyanate Chemical compound SC#N.NC(N)=N ZJYYHGLJYGJLLN-UHFFFAOYSA-N 0.000 claims description 6
- 239000003463 adsorbent Substances 0.000 claims description 5
- 238000004925 denaturation Methods 0.000 claims description 5
- 230000036425 denaturation Effects 0.000 claims description 5
- 238000002372 labelling Methods 0.000 claims description 4
- 230000000295 complement effect Effects 0.000 claims description 3
- 244000005700 microbiome Species 0.000 claims description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 claims description 2
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical class NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 claims description 2
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 claims description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 claims description 2
- 229910001854 alkali hydroxide Inorganic materials 0.000 claims description 2
- 150000008044 alkali metal hydroxides Chemical group 0.000 claims description 2
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical group I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 claims description 2
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 claims description 2
- 230000003472 neutralizing effect Effects 0.000 claims description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-M perchlorate Inorganic materials [O-]Cl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-M 0.000 claims description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 claims description 2
- 229940066528 trichloroacetate Drugs 0.000 claims description 2
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 claims description 2
- 108020004414 DNA Proteins 0.000 claims 2
- 102000053602 DNA Human genes 0.000 claims 2
- 239000003795 chemical substances by application Substances 0.000 abstract 1
- 108091034117 Oligonucleotide Proteins 0.000 description 12
- 238000006243 chemical reaction Methods 0.000 description 8
- 238000004587 chromatography analysis Methods 0.000 description 8
- 230000035945 sensitivity Effects 0.000 description 8
- 238000001179 sorption measurement Methods 0.000 description 8
- 239000000243 solution Substances 0.000 description 7
- 239000012491 analyte Substances 0.000 description 6
- 239000012528 membrane Substances 0.000 description 6
- 239000013612 plasmid Substances 0.000 description 6
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 239000012876 carrier material Substances 0.000 description 4
- 229920002678 cellulose Polymers 0.000 description 4
- 239000001913 cellulose Substances 0.000 description 4
- 238000013375 chromatographic separation Methods 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 239000000020 Nitrocellulose Substances 0.000 description 3
- 239000011149 active material Substances 0.000 description 3
- 230000000274 adsorptive effect Effects 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 239000000835 fiber Substances 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 230000001900 immune effect Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 229920001220 nitrocellulos Polymers 0.000 description 3
- 125000003729 nucleotide group Chemical group 0.000 description 3
- 102100027518 1,25-dihydroxyvitamin D(3) 24-hydroxylase, mitochondrial Human genes 0.000 description 2
- 101000849787 Brucella melitensis biotype 1 (strain 16M / ATCC 23456 / NCTC 10094) Ribosome-recycling factor Proteins 0.000 description 2
- 101000861278 Homo sapiens 1,25-dihydroxyvitamin D(3) 24-hydroxylase, mitochondrial Proteins 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 102000006943 Uracil-DNA Glycosidase Human genes 0.000 description 2
- 108010072685 Uracil-DNA Glycosidase Proteins 0.000 description 2
- 229960002685 biotin Drugs 0.000 description 2
- 235000020958 biotin Nutrition 0.000 description 2
- 239000011616 biotin Substances 0.000 description 2
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- 238000005470 impregnation Methods 0.000 description 2
- 201000001371 inclusion conjunctivitis Diseases 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 239000002773 nucleotide Substances 0.000 description 2
- 229920002647 polyamide Polymers 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- 206010044325 trachoma Diseases 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 229920003043 Cellulose fiber Polymers 0.000 description 1
- 241000606161 Chlamydia Species 0.000 description 1
- 241000606153 Chlamydia trachomatis Species 0.000 description 1
- 229920001634 Copolyester Polymers 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 101000880187 Homo sapiens Craniofacial development protein 1 Proteins 0.000 description 1
- 101000875401 Homo sapiens Sterol 26-hydroxylase, mitochondrial Proteins 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 108020005187 Oligonucleotide Probes Proteins 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 108091093037 Peptide nucleic acid Proteins 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 229920000297 Rayon Polymers 0.000 description 1
- 102100036325 Sterol 26-hydroxylase, mitochondrial Human genes 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- 108010006785 Taq Polymerase Proteins 0.000 description 1
- 241001122767 Theaceae Species 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000012670 alkaline solution Substances 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 238000007846 asymmetric PCR Methods 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 229940038705 chlamydia trachomatis Drugs 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 238000004374 forensic analysis Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- ZRALSGWEFCBTJO-UHFFFAOYSA-O guanidinium Chemical compound NC(N)=[NH2+] ZRALSGWEFCBTJO-UHFFFAOYSA-O 0.000 description 1
- 229940094991 herring sperm dna Drugs 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000003100 immobilizing effect Effects 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 244000000010 microbial pathogen Species 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 229940124276 oligodeoxyribonucleotide Drugs 0.000 description 1
- 239000002751 oligonucleotide probe Substances 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 229920006149 polyester-amide block copolymer Polymers 0.000 description 1
- 229920005594 polymer fiber Polymers 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 108020004418 ribosomal RNA Proteins 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- 239000002759 woven fabric Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/14—Heterocyclic carbon compound [i.e., O, S, N, Se, Te, as only ring hetero atom]
- Y10T436/142222—Hetero-O [e.g., ascorbic acid, etc.]
- Y10T436/143333—Saccharide [e.g., DNA, etc.]
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Analytical Chemistry (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Saccharide Compounds (AREA)
Description
【発明の属する技術分野】
本発明は、試料適用ゾーンと検出ゾーンを含み、試料適用ゾーンから検出ゾーンへの液体移送が可能な分析エレメントにて核酸を検出する方法に関する。この方法は、試料を前記分析エレメントの試料適用ゾーンに適用し、試料に含まれる核酸を検出ゾーンにて検出プローブとのハイブリダイゼーションにより定性的に、また好ましくはマーカー基により定量的に検出し得るものである。さらに、核酸を検出するための新規分析エレメントおよび試薬キットも提供する。
【0002】
【従来の技術】
現在、診断用途において、PCRで得られた増幅産物などの核酸は、検出すべき核酸と検出プローブ(通常、オリゴヌクレオチドである)との特異的ハイブリダイゼーションならびに検出すべき核酸または/および検出プローブに存在し得るマーカー基を利用した非放射性検出反応により検出されている。この検出反応には様々な異なる方法を用いることができる。例えば、検出すべき核酸は、マイクロタイタープレート(Amplicor Detection Kit, Roche Diagnostics, 欧州特許出願公開EP-A-0 420 260号)などの固相に固定した検出プローブと直接ハイブリダイズさせることができる。さらに、検出すべき核酸を、標識した検出プローブと予めハイブリダイズさせることができ、かかるプロセスで形成された複合体を、マイクロタイタープレート(PCR-Detection Kit, Roche Diagnostics)などの固相上に捕獲することができる。
【0003】
診断手順での検査ストリップの使用は長きにわたり知られている。例えば、検査ストリップを用いたアナライトの検出は、主に免疫学的試験法に関する欧州特許EP-B-0 186 799号、欧州特許EP-B-0 262 328号および欧州特許出願公開EP-A-0 926 498号に記載されている。
【0004】
Jouら(Human Mutation 5(1995), 86-93)は、クロマトグラフ検査ストリップでの核酸検出方法を記載しており、この方法では、検出すべき核酸にハプテン基を導入して検出すべき核酸の抗ハプテン抗体による検査ストリップ上への免疫学的固定化を可能にしている。検査ストリップ上の固定化検出プローブに特異的ハイブリダイゼーションさせることによる検出すべき核酸の捕獲は、例えば、米国特許第5,310,650号、欧州特許EP-B-0 612 354号、Reinhartzら(Gene 136(1993), 221-226)およびRuleら(Clin. Chem. 42(1996), 1206-1209)に記載されている。
【0005】
【発明が解決しようとする課題】
しかしながら、検査ストリップ上での核酸検出を記載する上記の方法にはいくつかの欠点がある。例えば、核酸をサンドイッチ複合体により固定化する場合、感度が低下する。例えば検査容量を増大させることによる感度の増大は、検出すべき核酸へのマーカー基の組込みが限定されることにより制限される。
【0006】
また、前記方法を用いて核酸を直接検出するのは不可能である。標的核酸とハイブリダイゼーションプローブとの複合体を、まず、前工程で形成させる。この目的のために、標的核酸を変性させ(熱処理またはアルカリ溶液の添加により変性する)、必要に応じて中和し、プローブを加え、ハイブリダイゼーション条件に設定する。検査担体上での実際の検出は、この前処理後にのみ行うことができる。この処理は、試薬を適量に分けて添加することと装置(例えば加熱装置)を使用することを含むので、検査ストリップに基づく方法の本質的な利点、例えば装置に対する要求事項が少ないこと、取り扱いが簡単なこと、作業工程が少ないこと、訓練していない人がこの方法を行うことが可能であることなどを利用することができない。さらに、これらの追加の工程により汚染のリスクが生じるので、増幅核酸を検出する場合に偽陽性の結果がもたらされる可能性がある。
【0007】
また、検出すべき核酸と分析エレメント上のハイブリダイゼーションプローブとの直接ハイブリダイゼーションを可能にする方法の場合、従来技術では検出すべき核酸の前処理を必要としない感度のよい検査手順は知られていない。つまりこれらの従来技術の手順では核酸は直接検出できないか、増幅プロセス後に直接検出されない。これらの手順では、標的核酸(これは通常2本鎖の形態で存在する)は、ハイブリダイゼーションのために1本鎖コンホメーションに変換される。これについての方法がいくつか記載されている。例えば、よく知られたハイブリダイゼーション法によれば、核酸を分析エレメントに適用する前に、例えば熱処理またはアルカリ試薬の添加により完全に変性させている。また標的核酸の一方の鎖を特異的消化することが可能な酵素的方法も知られている(Ruleら, Clinical Chemistry 42, 1206-1209頁(1996))。
【0008】
前処理は、標的核酸がすでに完全に1本鎖として存在する場合のみ省略することができる。しかし、このことは通常すでに困難である。なぜならば、リボソーム標的核酸を検出する場合、これらの1本鎖核酸の天然二次構造の大部分の領域が2本鎖形態(例えばrRNA)にあるからである。机上の代案は、一方の核酸鎖のみの特異的合成を可能にする増幅方法である。例えば、非対称PCRである。しかしながら、この方法は、線状(linear)増幅のために通常のPCR法よりも極めて効率が悪く、感度がかなり制限され、低濃度でしか存在しないアナライトの検出には不十分である。したがって、従来技術において知られた、分析エレメント上で検出すべき核酸の直接ハイブリダイゼーションを可能にする方法も、間接検出法で見られるのと同じ欠点をもつ。
【0009】
【課題を解決するための手段】
本発明の主な利点は、上述した検出すべき核酸の前処理を省略でき、核酸を分析エレメントに直接または増幅プロセス後に直接適用できるということである。分析エレメントには試薬が含浸されているのが好ましく、この試薬が分析エレメント上での標的核酸の完全または部分的変性を可能にし、2本鎖コンホメーションで適用される核酸のハイブリダイゼーションも可能にする。本発明は、このことに対する可能性をいくつか提供する。例えば、変性試薬は、好ましくは核酸を完全に変性させるために予め検査担体上に適当な濃度で乾燥形態にて置くことができる。標的核酸は、例えばPCR反応溶液に含有させた液体形態にて分析エレメントに適用することができる。試薬の溶解後、標的核酸は完全に変性する。プローブオリゴヌクレオチドへのハイブリダイゼーションはこれらの条件下では生じ得ないので、この化学物質を適切に変更しなければならず、それと同時にアナライトは、好ましくはクロマトグラフィーにより検査担体を通って移送される。一方、これは、適当なクロマトグラフィーバッファーまたは下流に配置されている試薬により行うことができる。これには、塩基、特にNaOHによる変性および酸による中和が好ましい。あるいは、標的核酸の2本鎖コンホメーションを不安定化させ(部分的に変性させ)、プローブオリゴヌクレオチドへのハイブリダイゼーションを可能にするか促進するように化学物質を調節することができる。クロマトグラフィー中の化学物質の変更は、この変形法には必要ない。この実施形態に好適な試薬は、カオトロピック塩であり、特にチオシアン酸グアニジニウム(GuSCN)が好ましい。
【0010】
プローブオリゴヌクレオチドにハイブリダイズした標的核酸を検出するために、さらにその複合体を標識する必要がある。マーカー基は、事前に実施する任意の増幅プロセス中に酵素的組込みにより増幅標的核酸に組み込んでもよく、または別の適切に標識されたプローブオリゴヌクレオチドとハイブリダイズさせることにより標的核酸に結合させてもよい。
【0011】
驚くべきことに、上記の方法を用いると、分析エレメントに適用される二本鎖形態の標的核酸は、分析エレメント全体への該標的核酸のクロマトグラフ移送の間に利用できる時間が非常に短いにもかかわらず、非常に効率的にプローブオリゴヌクレオチドにハイブリダイズし、高感度で検出できることが分かった。
【0012】
よって、本発明は、試料適用ゾーンと検出ゾーンとを含み、該試料適用ゾーンから該検出ゾーンへの液体移送が可能な分析エレメントにて核酸を検出する方法であって、
検出すべき核酸を含む試料を該試料適用ゾーンに適用する工程、および
該検出ゾーン内で検出プローブとのハイブリダイゼーションにより該核酸を検出する工程
を含んでなり、該検出すべき核酸を該分析エレメント上で変性させることを特徴とする方法を提供する。
【0013】
「変性」は、本明細書で用いる場合、古典的な意味での完全な変性と解釈されるのみならず、核酸の二本鎖がプローブとハイブリダイズし得るのに十分な程度に不安定化されるプロセスにおける部分的変性も意図するものである。したがって、二本鎖を完全に分離させる必要はないが、もちろんそのような実施形態も本発明に含まれる。
【0014】
本発明によれば、検出すべき核酸は、分析エレメント上で変性され、すなわち、核酸は、分析エレメントに変性されていない好ましくは二本鎖の形態で適用され、分析エレメントに適用された後にはじめて変性試薬と接触することになる。変性試薬は、試料中の核酸を変性させるのに十分な量の塩基または/およびカオトロピック物質を含み得る。好ましい塩基には、例えば、アルカリ水酸化物、特にNaOHがある。好ましいカオトロピック物質には、例えば、ヨウ化物、酢酸塩、過塩素酸塩、チオシアン酸塩、トリフルオロ酢酸塩、トリクロロ酢酸塩または/およびグアニジニウム化合物がある。特に好ましいのはチオシアン酸グアニジニウムである。一方、カオトロピック物質の使用は、二本鎖を不安定化させ、検出すべき核酸と検出プローブとの間のハイブリダイゼーションを促進する。さらに重要な機能は、核酸の特異的な融解点を低下させて室温での特異的ハイブリダイゼーションを可能にすることである。
【0015】
このようなカオトロピック物質の作用は、溶液中でのハイブリダイゼーションに関して既に知られているが(国際公開WO-A-87 06621号, ThompsonおよびGillespie, Anal. Biochem. 163(1987), 281-291; Van NessおよびChen, Nucleic Acid Res. 19(1991), 5143-5151)、分析エレメントでのハイブリダイゼーションによる核酸の検出のための本発明の範囲内では初めて利用される。この技術の分析エレメントへの応用は、当業者には自明ではなかった。というのは、従来技術は、1時間程度のオーダーのハイブリダイゼーション時間を推奨しているからである。しかしながら、本発明の分析エレメントを用いた場合、試料適用から検出までの検査は、10分以内に既に完了している。検出プローブとのハイブリダイゼーションは、試料の検出ゾーンへのクロマトグラフ移送中に、プローブと試料が数秒間、場合によっては1分以下接触しただけで既に生じている。
【0016】
本発明の分析エレメントの本質的な特徴は、液体が分析エレメント内で試料適用ゾーンから検出ゾーンに移動し得ることである。液体のそのような流れは、例えば、適切に構築された中空体における引力により達成され得る。引力の1つのタイプである遠心力による液体移送を可能にする装置が、例えば欧州特許EP-B-0 052 769に記載されている。しかしながら、本発明の分析エレメントは、好ましくは、毛管力(capillary force)により液体を移動させ得る吸着材料を含む。本発明の分析エレメントの個々のゾーンの吸着材料は、この場合、同一でも異なってもよい。異なるゾーンが最適に機能するために異なる材料からなる場合が多い。
【0017】
吸着性の毛管力活性のある材料として可能なものは、例えば、米国特許US-A-4,861,711号、米国特許US-A-5,591,645号または欧州特許出願公開EP-A-0 291 194号に記載されているような、基本的に、いわゆる「乾式検査」において液体の取込みに用いられ得るもの全てである。膜、例えばニトロセルロース膜のような多孔質材料がこれに都合がよいことが判明した。しかしながら、フリース、織物またはメリヤス生地のような繊維状吸着マトリックス材料を用いることも可能である。特に好ましいのはフリースである。繊維状マトリックス材料は、ガラス、セルロース、セルロース誘導体、ポリエステル、ポリアミドを含んでもよく、さらにビスコース、セルウール(cell wool)または/およびポリビニルアルコールを含んでもよい。例えば、セルロースに基づく繊維、ポリエステルおよび/またはポリアミドに基づくポリマー繊維ならびに欧州特許EP-B-0 326 135に記載されているようなOH基および/またはエステル基を有する有機結合剤から製造されたフリースが、本発明に用いられ得る。欧州特許出願0 571 941号に記載されたような溶融コポリエステル繊維、セルロース繊維またはセルロース誘導体繊維を含むフリース材料も本発明の分析エレメントに用いることができる。ティーバッグ紙などの紙も簡単に用いることができる。
【0018】
本発明の分析エレメントの取り扱いを改善するために、吸着性の毛管力活性材料または種々の吸着性の毛管力活性材料を、液体不透過性であるがマトリックス材料内の液体の流れに悪影響を及ぼさず、分析エレメント内で生じる反応に関して不活性に挙動する剛性の支持担体材料上に配置することができる。例えば、液体移送を可能にするマトリックス材料が取り付けられたポリエステル箔が好ましい支持担体材料であり得る。
【0019】
本発明の分析エレメントにおける個々のゾーンは、上下に重なるように、隣り合わせになるように、一部が上下に重なるように、または一部が隣り合わせになるように支持担体材料上に配置することができる。本発明の分析エレメントは、試料適用ゾーンおよび検出ゾーンが支持担体材料上に隣り合わせで位置しているのが特に好ましい。この場合、隣り合わせとは、これらのゾーンが互いに直接接触しているか、または本質的に一つの平面内にその他のゾーンで分離された状態で配置されていることを意味する。
【0020】
試料適用ゾーンは、本発明の分析エレメントにおける試料が適用される領域である。検出ゾーンは、本発明の分析エレメントにおける領域であって、分析エレメントに適用される試料中に検査すべきアナライトまたは該アナライトから誘導される物質もしくは該アナライトを呈示する物質が存在するか否かを測定する領域である。この測定は、定性的、半定量的または定量的であり得る。これに関連して、半定量的とは、アナライトから誘導された物質またはアナライトを呈示する物質についての具体的な濃度の値が測定されるのではなく、アナライトの濃度が位置する濃度範囲を測定することを意味する。
【0021】
本発明の第1の実施形態では、試料を適用する前に分析エレメントに変性試薬を含浸させる。変性試薬は、分析エレメント上、好ましくは試料適用ゾーン上に液体または乾燥形態で存在し得る。変性試薬は好ましくは乾燥形態で存在する。さらなる実施形態では、試料を適用した後にはじめて分析エレメントに変性試薬を含浸させる。検出すべき試料に存在する核酸と変性試薬の接触により、核酸の二本鎖の変性が生じ、生じた核酸の一本鎖と検出プローブとのハイブリダイゼーションが可能になる。変性試薬が塩基を含む場合、分析エレメントは、試料適用ゾーンと検出ゾーンの間に中和試薬(例えば、リン酸または硫酸のような液体と接触して酸性反応する塩)を好ましくは乾燥形態で含んでいることが都合がよい。
【0022】
試料中に存在する検出すべき核酸の結合に用いられる検出プローブは、好ましくは、検査条件下でハイブリダイゼーションを可能にするのに十分なほどに検出すべき核酸と相補的である配列を含むオリゴヌクレオチドである。検出プローブは、好ましくはオリゴデオキシリボヌクレオチドであるが、検出プローブとして改変型ヌクレオチド構築ブロックまたはペプチド核酸を含む核酸類似体を用いることも可能である。検出プローブは、好ましくは検出ゾーンに固定された形態で存在する。すなわち、検出プローブは、検査条件下で本質的に検出ゾーンから溶出しない。固定化は、検出プローブを適用し、次いで、例えば昇温、放射線照射等の適当な方法で該プローブを固定することにより行い得る。あるいは、プローブは、検出ゾーンに高アフィニティー相互作用、例えばビオチン/ストレプトアビジンもしくはアビジンまたはハプテン/抗ハプテン抗体、糖/レクチンによって固定されてもよい。適当に改変された、例えばビオニチル化検出プローブの調製は、当業者にはよく知られており、ここで詳細に説明する必要はない。あるいは、検出すべき核酸と検出プローブとの間のハイブリダイゼーションは、検出ゾーンの上流側で生じてもよく、そのハイブリダイゼーション複合体は分析エレメントを移送中に例えば前記のような高アフィニティー相互作用により検出ゾーンに選択的に固定化することができる。
【0023】
核酸は、好ましくはマーカー基によって検出され、基本的に従来技術により知られたマーカー基は全て適している。酵素標識のような視覚的に検出可能なマーカー基が好ましいが、特に、金またはラテックス粒子のような粒状の標識が好ましい。この場合、標識は、検出すべき核酸に直接位置していてもよいが(直接標識)、核酸に、例えば上記のような高アフィニティー相互作用、例えばハプテン/抗ハプテン抗体により間接的に結合していてもよい(間接標識)。検出すべき核酸への間接マーカー基の結合は、ハイブリダイゼーション中、または洗浄工程後に生じ得る。
【0024】
本発明は、検査ストリップ上で核酸を検出する簡単な方法を提供する。検出すべき核酸は、好ましくは増幅産物、例えばPCRで産生された増幅産物である。この場合、増幅産物は、増幅反応を行ったバッファー溶液をクロマトグラフィー溶媒として用いて直接検査ストリップに適用することができる。
【0025】
本発明はさらに、試料適用ゾーンと検出ゾーンとを含み、該試料適用ゾーンから該検出ゾーンへの液体移送が可能な核酸検出用分析エレメントを提供するものであり、該エレメントは核酸の変性試薬で含浸され、変性試薬は好ましくは乾燥形態で存在する。分析エレメントは、クロマトグラフ移送を可能にする吸着材料を含み得るものであり、好ましくは検査ストリップとして構築される。好ましくは、検出すべき核酸に相補的な検出プローブが分析エレメントの検出ゾーンに固定された形態で存在する。
【0026】
最後に、本発明は、本発明の分析エレメント、ならびに核酸を検出するのに必要な追加の試薬、例えば標識試薬、バッファーなどを含む核酸検出用キットに関する。
【0027】
本発明により提供される方法、分析エレメントおよび試薬キットは、特に、核酸増幅産物の検出、例えば試料中の選択された生物または生物の一部(例えば細胞)の存在または量を検出するのに適している。この目的のために、例えば、試料中の生物または細胞由来のリボソームRNAまたはそれをコードするDNA配列の増幅などにより、試料中の核酸の属特異的および種特異的検出を行うことができる。この方法を用いて、臨床試料、食物、水試料等に含まれる微生物、例えば病原性微生物またはウイルスを検出することができる。さらに、この方法を法医学的分析に用いて特定の個体を探知することもできる。クラミジア・トラコーマ(Chlamydia trachomatis)由来の核酸の本発明の方法による検出を、下記の実施例に示す。
【0028】
【実施例】
実施例1 概念
1.分析エレメントの準備
図1に示した分析エレメントの吸着フリース(1)に、含浸バッファー(10mMのKPO4、pH7.5、100mMのNaCl、2または2.5Mのチオシアン酸グアニジニウム(GuSCN)、0.5%Triton-X100、25mMのNaOH、2%RPLAタイプ4(Roche Diagnostics、カタログ番号1726544-106)および3mg/mlニシン精子DNA)を含浸させた。この目的のために、吸着フリースをペトリ皿中で含浸バッファーで完全に湿らせて、循環空気中で45℃にて3時間乾燥した。
【0029】
15mmのニトロセルロース膜を液体移送ゾーン(2)として用いた。検出ゾーン(4)を、該膜に検出オリゴヌクレオチドプローブ(40pmol/検査ストリップ)を適用することにより調製した。このために、オリゴヌクレオチドの溶液(200μM)を検出ラインの形態で自動ディスペンサー(Hamilton Microlab N)を用いて適用し、オリゴヌクレオチドを膜上に80℃で30分間固定化した。一方、ビオチン標識オリゴヌクレオチドを、予めポリストレプトアビジンでコーティングした検出ゾーン(4)に適用した。このために、オリゴヌクレオチド溶液(8pmol/検査ストリップ)をニトロセルロース膜に適用し、10μlの標準クロマトグラフィーバッファーを用いてポリストレプトアビジンで前コーティングした検出ゾーン上でクロマトグラフィーによる分離を行った。
【0030】
クラミジア・トラコーマプラスミドpCTT1(C.トラコーマの塩基1〜7496)由来のpCTT1の354〜374位に相当する配列(5'-GTC TCT CAT CGA GAC AAA GTG-3')(配列番号1)を有するオリゴヌクレオチドを、検出プローブとして用いた(SriprakashおよびMacavoy, Plasmid 18(1987), 205-214)。
【0031】
2. PCR プロトコル
オリゴヌクレオチドCP24(5'-GGGATTCCTGTAACAACAAGTCAGG-3')(配列番号2)(pCTT1の195〜219位)およびCP27(5'-CCTCTTCCCCAGAACAATAAGAACAC-3')(配列番号3)(pCTT1の401〜376位)を任意に5'-ビオチニル化形態または5'-ジゴキシゲニル化形態で増幅用のプライマーとして用いた。
【0032】
反応容量は100μlであった(PCRバッファー(Roche Diagnosticsカタログ番号1600753)中に、4mMのMgCl2、それぞれ0.1mMのdNTP、それぞれ300nMのプライマーCP24およびCP27、2.5UのTaqポリメラーゼ、2UのUNG(ウラシルDNAグリコシラーゼ)ならびに鋳型を加えたもの)。
【0033】
反応シーケンスは下記のとおりであった:
・37℃で10分間、95℃で5分間、60℃で1分間、
・95℃、3秒および60℃、6秒を34サイクル、
・72℃で10分間、
・50℃に保持
PCR反応は、種々の量の鋳型を用いて行った(0〜100000プラスミドコピー/混合物)。
【0034】
3.検出
50μlの増幅液(実施例2)を検査ストリップの吸着フリースに適用し、4分間クロマトグラフィーによる分離を行った。続いて、30μlの標準クロマトグラフィーバッファー(0.15MのNaCl、9.6mMのKH2PO4、40.5mMのK2HPO4、0.25%のTween 20、2%のRPLAタイプ4、0.09%のアジ化ナトリウム)を適用し、4分間クロマトグラフィーによる分離を行った。その後、20μlの抗ジゴキシゲニン抗体金コンジュゲート溶液(2.1pmol)を適用し、4分間クロマトグラフィーによる分離を行った。次いで、50μlの標準クロマトグラフィーバッファーを2回適用し、4分間クロマトグラフィーによる分離を行った。
【0035】
この実験の結果を図2に示す。図2Aは、サンドイッチ様式を用いる免疫学的方法により核酸を検出する欧州特許出願公開EP-A-0 926 489号の検査ストリップを用いた結果を示す。図2Bには、実施例1の検査ストリップを用いた本発明の検出方法の結果を示す。図2Aの検査ストリップを用いた場合は感度が低いが(混合物当たり1000コピー以上のプラスミドの検出のみ)、本発明の方法を用いた場合はかなり低いプラスミドコピー数(50)の検出でも可能であった。一般に、検出シグナルは、ΔRem-%が3以上である場合にポジティブであることがわかる。高感度であることに加えて、本発明の方法は、かなり広いダイナミックレンジも有している。すなわち、検出すべき核酸の濃度範囲が広い場合にもシグナルの有意な変化をもたらす。
【0036】
実施例2
図1の分析エレメントを、吸着フリースの含浸バッファーがNaOHを含んでない以外は実施例1.1にしたがって調製した。0.5M、1.5Mおよび2.5M(飽和限界付近)のグアニジニウム濃度について試験した。
【0037】
50μlのPCR増幅液(100プラスミド/混合物)を、実施例1.2にしたがって調製した各分析エレメントに適用した。検出は、実施例1.3にしたがって行った。
【0038】
結果を図3に示す。チオシアン酸グアニジニウムの添加により有意に検出感度が改善されるということが分かる。
【図面の簡単な説明】
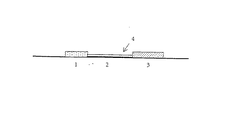
【図1】吸着フリースとして設計された試料適用ゾーン(1)、液体移送ゾーン(2)、該液体移送ゾーン内に位置する検出ゾーン(4)、および吸着フリースとして設計された吸着ゾーン(3)を含んでなる、本発明の検査ストリップの概略構造を示す図である。
【図2】本発明の方法(B)と欧州特許出願公開EP-A-0 926 498号に記載された方法(A)の感度の比較を示す図である。
【図3】分析エレメントの感度とチオシアン酸グアニジニウム(GuSCN)の濃度との関係を示す図である。
Claims (23)
- 試料適用ゾーンと検出ゾーンとを含み、該試料適用ゾーンから該検出ゾーンへの液体移送が可能な分析エレメントにて核酸を検出する方法であって、
検出すべき核酸を含む試料を該試料適用ゾーンに適用する工程、
該検出すべき核酸を該分析エレメント上で変性させる工程、および
該検出ゾーン内で検出プローブとのハイブリダイゼーションにより該核酸を検出する工程を含み、該検出すべき核酸が2本鎖 DNA であることを特徴とする、上記方法。 - 前記核酸の変性が、塩基または/およびカオトロピック物質を含む変性試薬との接触により行われる、請求項1に記載の方法。
- 前記塩基がアルカリ水酸化物から選択され、特にNaOHである、請求項2に記載の方法。
- 前記カオトロピック物質が、ヨウ化物、酢酸塩、過塩素酸塩、チオシアン酸塩、トリフルオロ酢酸塩、トリクロロ酢酸塩または/およびグアニジニウム化合物から選択される、請求項2に記載の方法。
- カオトロピック物質がチオシアン酸グアニジニウムである、請求項4に記載の方法。
- 前記分析エレメントがクロマトグラフ移送を可能にする吸着材料を含む、請求項1〜5のいずれか1項に記載の方法。
- 試料を適用する前に、前記分析エレメントに変性試薬を含浸させる、請求項1〜6のいずれか1項に記載の方法。
- 前記変性試薬が分析エレメント上に乾燥形態で存在する、請求項7に記載の方法。
- 前記試料適用ゾーンに前記変性試薬を予め含浸させる、請求項7または8に記載の方法。
- 試料を適用した後に、前記分析エレメントに変性試薬を含浸させる、請求項1〜6のいずれか1項に記載の方法。
- 前記分析エレメントが、前記試料適用ゾーンと前記検出ゾーンとの間に中和試薬を含む、請求項1〜10のいずれか1項に記載の方法。
- 前記検出すべき核酸が増幅産物である、請求項1〜11のいずれか1項に記載の方法。
- 前記検出プローブが前記検出ゾーン内に固定された形態で存在する、請求項1〜12のいずれか1項に記載の方法。
- 前記核酸がマーカー基により検出される、請求項1〜13のいずれか1項に記載の方法。
- 間接マーカー基が用いられる、請求項14に記載の方法。
- 試料適用ゾーンと検出ゾーンとを含み、該試料適用ゾーンから該検出ゾーンへの液体移送が可能な核酸検出用分析エレメントであって、核酸の変性試薬が含浸されており、検出すべき核酸が2本鎖 DNA である、上記分析エレメント。
- 前記変性試薬が乾燥形態で存在する、請求項16に記載の分析エレメント。
- クロマトグラフ移送を可能にする吸着材料を含む、請求項16または17に記載の分析エレメント。
- 検査ストリップとして設計されている、請求項16〜18のいずれか1項に記載の分析エレメント。
- 前記検出ゾーン内に検出すべき核酸に相補的な検出プローブを固定化形態で含む、請求項16〜19のいずれか1項に記載の分析エレメント。
- (a) 請求項16〜20のいずれか1項に記載の分析エレメント、および
(b) 標識試薬およびバッファーからなる群から選択される少なくとも1種の試薬
を含む、核酸検出用キット。 - 核酸増幅産物を検出するための請求項16〜20のいずれか1項に記載の分析エレメントまたは請求項21に記載のキットの使用。
- 試料中の選択された微生物または微生物の一部の存在もしくは量を検出するための請求項22に記載の使用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19956820A DE19956820A1 (de) | 1999-11-25 | 1999-11-25 | Spezies-spezifischer Nachweis von Nukleinsäuren mittels eines Analyseelementes |
| DE19956820.0 | 1999-11-25 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2001190291A JP2001190291A (ja) | 2001-07-17 |
| JP4219085B2 true JP4219085B2 (ja) | 2009-02-04 |
Family
ID=7930340
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000358273A Expired - Lifetime JP4219085B2 (ja) | 1999-11-25 | 2000-11-24 | 分析エレメントによる核酸の種特異的検出 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US6485915B1 (ja) |
| EP (1) | EP1103622B1 (ja) |
| JP (1) | JP4219085B2 (ja) |
| AT (1) | ATE291098T1 (ja) |
| DE (2) | DE19956820A1 (ja) |
| ES (1) | ES2237377T3 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7807802B2 (en) | 2002-11-12 | 2010-10-05 | Abbott Lab | Polynucleotides for the amplification and detection of Chlamydia trachomatis and Neisseria gonorrhoeae |
| DE602004032125D1 (de) * | 2003-05-07 | 2011-05-19 | Coris Bioconcept Sprl | Einstufige oligochromatographische vorrichtung und verfahren zu ihrer verwendung |
| JP5165383B2 (ja) * | 2004-12-23 | 2013-03-21 | アイ−スタツト・コーポレイシヨン | 分子診断システム及び方法 |
| EP1893770B1 (de) * | 2005-05-30 | 2012-03-14 | Qiagen GmbH | Vorrichtung und verfahren zur normalisierung von nukleinsäure-konzentrationen |
| US8703445B2 (en) | 2005-12-29 | 2014-04-22 | Abbott Point Of Care Inc. | Molecular diagnostics amplification system and methods |
| WO2009039239A2 (en) * | 2007-09-18 | 2009-03-26 | Idexx Laboratories, Inc. | Lateral flow assay using centrifugal force |
| DE102008047790A1 (de) * | 2008-09-17 | 2010-04-15 | Qiagen Gmbh | Verfahren zur Normierung des Gehalts von Biomolekülen in einer Probe |
| EP3253788A4 (en) * | 2015-02-06 | 2018-08-08 | Cell IDX, Inc. | Antigen-coupled immunoreagents |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4652517A (en) * | 1984-06-11 | 1987-03-24 | Diagnostic Research Limited Partnership | Methods for the in vitro detection and identification of unknown pathogens or genetic entities |
| US4740468A (en) * | 1985-02-14 | 1988-04-26 | Syntex (U.S.A.) Inc. | Concentrating immunochemical test device and method |
| CA1301606C (en) | 1986-05-02 | 1992-05-26 | David H. Gillespie | Chaotropic method for evaluating nucleic acids in a biological sample |
| US4960691A (en) * | 1986-09-29 | 1990-10-02 | Abbott Laboratories | Chromatographic test strip for determining ligands or receptors |
| US5310650A (en) * | 1986-09-29 | 1994-05-10 | Abbott Laboratoires | Method and device for improved reaction kinetics in nucleic acid hybridizations |
| IL102486A (en) * | 1991-10-04 | 1997-11-20 | Orgenics Ltd | Method and apparatus for detection of nucleic acid sequences with a nucleic acid probe |
| US6037127A (en) * | 1994-03-31 | 2000-03-14 | E. I. Du Pont De Nemours And Company | Method for detection of non-denatured nucleic acid fragments |
| WO1995027081A1 (en) * | 1994-03-31 | 1995-10-12 | E.I. Du Pont De Nemours And Company | A method for detection of nucleic acid fragments |
| DE19816550A1 (de) | 1997-12-24 | 1999-06-24 | Roche Diagnostics Gmbh | Universell verwendbarer Aufbau eines Analysenelements und dessen Einsatz zur Analytbestimmung |
-
1999
- 1999-11-25 DE DE19956820A patent/DE19956820A1/de not_active Withdrawn
-
2000
- 2000-11-17 US US09/716,013 patent/US6485915B1/en not_active Expired - Lifetime
- 2000-11-24 JP JP2000358273A patent/JP4219085B2/ja not_active Expired - Lifetime
- 2000-11-24 EP EP00125818A patent/EP1103622B1/de not_active Expired - Lifetime
- 2000-11-24 ES ES00125818T patent/ES2237377T3/es not_active Expired - Lifetime
- 2000-11-24 AT AT00125818T patent/ATE291098T1/de active
- 2000-11-24 DE DE50009774T patent/DE50009774D1/de not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| US6485915B1 (en) | 2002-11-26 |
| DE50009774D1 (de) | 2005-04-21 |
| ATE291098T1 (de) | 2005-04-15 |
| EP1103622A2 (de) | 2001-05-30 |
| ES2237377T3 (es) | 2005-08-01 |
| JP2001190291A (ja) | 2001-07-17 |
| DE19956820A1 (de) | 2001-05-31 |
| EP1103622A3 (de) | 2003-08-13 |
| EP1103622B1 (de) | 2005-03-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US5972692A (en) | Gene detection method | |
| EP0478319B1 (en) | Gene detection method | |
| JP2573443B2 (ja) | 遺伝子検出法 | |
| EP0235726B1 (en) | Rapid detection of nucleic acid sequences in a sample by labeling the sample | |
| AU2009231582B2 (en) | Amplicon rescue multiplex polymerase chain reaction for amplificaton of multiple targets | |
| EP3018215B1 (en) | Gene expression assays conducted by elemental analysis | |
| EP3348640B1 (en) | Amplified nucleic acid detection method and detection device | |
| EP2843058B1 (en) | Method for amplifying nucleic acid and method for detecting amplified nucleic acid | |
| US5580971A (en) | Fungal detection system based on rRNA probes | |
| WO2004092342A2 (en) | Lateral flow system for nucleic acid detection | |
| JPH08501689A (ja) | 改良型の鎖置換アッセイおよびそれに有用な複合体 | |
| KR20150139582A (ko) | 나노파티클-지원 신호 증폭을 이용한 rna 마이크로칩 검출 | |
| EP0892856A1 (en) | A method for the amplification and detection of a nucleic acid fragment of interest | |
| JP4219085B2 (ja) | 分析エレメントによる核酸の種特異的検出 | |
| US20010039012A1 (en) | Methods for diagnostic screening | |
| JPH0998799A (ja) | 核酸の定量的検出法 | |
| EP0425217A2 (en) | A hybridization assay for campylobacter rRNA | |
| WO1988006189A1 (en) | Test system, test device and method for detecting pathogenic organisms and antibiotic resistance genes in body fluids | |
| EP0622464A2 (en) | Nucleic acid assay procedure | |
| WO2000011215A2 (en) | Method for diagnostic screening | |
| EP3967772A1 (en) | Tools & methods usefool for detection of lactose intolerance and uses thereof | |
| JP2000342282A (ja) | サルモネラ属の増幅および検出 | |
| EP0311388B1 (en) | A rapid method for identifying a specific nucleic acid sequence | |
| JPH03123500A (ja) | 核酸の分別方法 | |
| US20050239078A1 (en) | Sequence tag microarray and method for detection of multiple proteins through DNA methods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20040330 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20040713 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20040901 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20040924 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20080124 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20080129 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080922 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081111 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111121 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 4219085 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121121 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131121 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |