JP5113828B2 - 動的腫瘍の放射線治療装置および動的腫瘍の放射線治療プログラム - Google Patents
動的腫瘍の放射線治療装置および動的腫瘍の放射線治療プログラム Download PDFInfo
- Publication number
- JP5113828B2 JP5113828B2 JP2009500232A JP2009500232A JP5113828B2 JP 5113828 B2 JP5113828 B2 JP 5113828B2 JP 2009500232 A JP2009500232 A JP 2009500232A JP 2009500232 A JP2009500232 A JP 2009500232A JP 5113828 B2 JP5113828 B2 JP 5113828B2
- Authority
- JP
- Japan
- Prior art keywords
- tumor
- annihilation
- rays
- count rate
- ray
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/10—X-ray therapy; Gamma-ray therapy; Particle-irradiation therapy
- A61N5/1048—Monitoring, verifying, controlling systems and methods
- A61N5/1049—Monitoring, verifying, controlling systems and methods for verifying the position of the patient with respect to the radiation beam
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B90/00—Instruments, implements or accessories specially adapted for surgery or diagnosis and not covered by any of the groups A61B1/00 - A61B50/00, e.g. for luxation treatment or for protecting wound edges
- A61B90/39—Markers, e.g. radio-opaque or breast lesions markers
- A61B2090/392—Radioactive markers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/10—X-ray therapy; Gamma-ray therapy; Particle-irradiation therapy
- A61N5/1048—Monitoring, verifying, controlling systems and methods
- A61N5/1049—Monitoring, verifying, controlling systems and methods for verifying the position of the patient with respect to the radiation beam
- A61N2005/1052—Monitoring, verifying, controlling systems and methods for verifying the position of the patient with respect to the radiation beam using positron emission tomography [PET] single photon emission computer tomography [SPECT] imaging
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/10—X-ray therapy; Gamma-ray therapy; Particle-irradiation therapy
- A61N5/1048—Monitoring, verifying, controlling systems and methods
- A61N5/1064—Monitoring, verifying, controlling systems and methods for adjusting radiation treatment in response to monitoring
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Pathology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Radiology & Medical Imaging (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Radiation-Therapy Devices (AREA)
- Nuclear Medicine (AREA)
Description
1.放射線治療に際し、患者の体への負担を低減することができる。
2.腫瘍50の位置を直接的に検出することができるため検出精度が向上し、腫瘍50の動きを精度よく追認することができるため、腫瘍50への放射線照射が正確になる。
3.腫瘍以外の細胞へ無駄な放射線照射することを極力低減することができるため患者の被爆量を低減することができ、副作用の影響も抑制できる等の効果を奏する。
10 放射線照射手段
20 γ線検出手段
30 記憶手段
40 演算処理手段
50 腫瘍
60 水ファントム
21 γ線検出器
22 γ線検出器
23 コリメータ
31 プログラム記憶部
32 変位閾値記憶部
33 境界閾値記憶部
41 計数率算出部
42 時間測定部
43 閾値比較部
44 腫瘍位置判別部
45 照射制御部
46 時間差位置特定部
51 測定領域
52 腫瘍境界部分
53 腫瘍の動的変位における静止位置の境界部分
61 線源
62 アクリル容器
63 アクチュエータ
64 人体ファントム
65 肺ファントム
Claims (9)
- 体内に投与されることで腫瘍に蓄積する放射性薬剤から放出される消滅γ線を検出するγ線検出手段と、
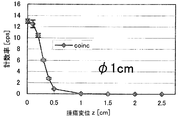
消滅γ線の計数率と線源の変位との関係に基づいて定められた前記計数率の閾値を記憶する変位閾値記憶手段と、
前記γ線検出手段により検出された消滅γ線の検出信号に基づいて計数率を算出するγ線計数率算出手段と、
前記γ線計数率算出手段から取得した消滅γ線の計数率と前記変位閾値記憶手段から取得した計数率の閾値とを比較する閾値比較手段と、
前記閾値比較手段による比較結果に基づいて腫瘍が放射線照射スポット外へ変位したか否かを判別する腫瘍位置判別手段と、
前記腫瘍位置判別手段により腫瘍が放射線照射スポット外へ変位したと判断されたとき、放射線照射手段による放射線照射を停止制御する、または停止指示信号を出力する照射制御手段と
を有することを特徴とする動的腫瘍の放射線治療装置。 - 請求項1において、前記γ線検出手段は、一対のγ線検出器を腫瘍を間にして対向配置して消滅γ線を検出するとともに、前記γ線計数率算出手段は、消滅γ線を同時計数して計数率を算出することを特徴とする動的腫瘍の放射線治療装置。
- 体内に投与されることで腫瘍に蓄積する放射性薬剤から放出される消滅γ線を、腫瘍境界部分または腫瘍が変位する静止境界部分に複数の測定領域を設定して検出するγ線検出手段と、
消滅γ線の計数率と線源の変位との関係に基づいて定められた前記計数率の閾値を記憶する境界閾値記憶手段と、
前記γ線検出手段により検出された消滅γ線の検出信号に基づいて計数率を算出するγ線計数率算出手段と、
前記γ線計数率算出手段から取得した消滅γ線の計数率と前記境界閾値記憶手段から取得した計数率の閾値とを比較する閾値比較手段と、
前記閾値比較手段による比較結果に基づいて腫瘍が放射線照射スポット外へ変位したか否かを判別する腫瘍位置判別手段と、
前記腫瘍位置判別手段により腫瘍が放射能照射スポット外へ変位したと判断されたとき、放射線照射手段による放射線照射を停止制御する、または停止指示信号を出力する照射制御手段と
を有することを特徴とする動的腫瘍の放射線治療装置。 - 請求項3において、前記γ線検出手段は、各測定領域に一対のγ線検出器を対向配置し、前記γ線計数率算出手段がそれら一対のγ線検出器により検知される消滅γ線を同時計数することにより消滅γ線の計数率を算出することを特徴とする動的腫瘍の放射線治療装置。
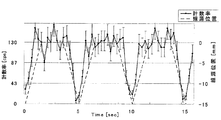
- 請求項1または請求項3において、閾値比較手段は、経過時間に伴って減少する消滅γ線の計数率に応じてその時間での閾値を取得することを特徴とする動的腫瘍の放射線治療装置。
- 請求項2または請求項4において、前記γ線検出手段は、対向配置した前記一対のγ線検出器に対してさらに他の一対のγ線検出器を交叉方向に対向配置し、前記γ線計数率算出手段が消滅γ線を同時計数することにより計数率を算出することを特徴とする動的腫瘍の放射線治療装置。
- 請求項2または請求項4において、一対のγ線検出器に到達する消滅γ線の到達時間差を求め、この到達時間差から一対のγ線検出器間における奥行き方向の線源位置を特定する時間差位置特定手段を備えていることを特徴とする動的腫瘍の放射線治療装置。
- 体内に投与されることで腫瘍に蓄積する放射性薬剤から放出される消滅γ線を検出するγ線検出手段と、
消滅γ線の計数率と線源の変位との関係に基づいて定められた前記計数率の閾値を記憶する変位閾値記憶手段と、
前記γ線検出手段により検出された消滅γ線の検出信号に基づいて計数率を算出するγ線計数率算出手段と、
前記γ線計数率算出手段から取得した消滅γ線の計数率と前記変位閾値記憶手段から取得した計数率の閾値とを比較する閾値比較手段と、
前記閾値比較手段による比較結果に基づいて腫瘍が放射線照射スポット外へ変位したか否かを判別する腫瘍位置判別手段と、
前記腫瘍位置判別手段により腫瘍が放射線照射スポット外へ変位したと判断されたとき、放射線照射手段による放射線照射を停止制御する、または停止指示信号を出力する照射制御手段
としてコンピュータを機能させることを特徴とする動的腫瘍の放射線治療プログラム。 - 体内に投与されることで腫瘍に蓄積する放射性薬剤から放出される消滅γ線を、腫瘍境界部分または腫瘍が変位する静止境界部分に複数の測定領域を設定して検出するγ線検出手段と、
測定領域における消滅γ線の計数率と線源の変位との関係に基づいて定められた計数率の閾値を記憶する境界閾値記憶手段と、
前記γ線検出手段により検出された消滅γ線の検出信号に基づいて計数率を算出するγ線計数率算出手段と、
前記γ線計数率算出手段から取得した消滅γ線の計数率と前記境界閾値記憶手段から取得した計数率の閾値とを比較する閾値比較手段と、
前記閾値比較手段による比較結果に基づいて腫瘍が放射線照射スポット外へ変位したか否かを判別する腫瘍位置判別手段と、
前記腫瘍位置判別手段により腫瘍が放射線照射スポット外へ変位したと判断されたとき、放射線照射手段による放射線照射を停止制御する、または停止指示信号を出力する照射制御手段
としてコンピュータを機能させることを特徴とする動的腫瘍の放射線治療プログラム。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009500232A JP5113828B2 (ja) | 2007-02-21 | 2008-02-21 | 動的腫瘍の放射線治療装置および動的腫瘍の放射線治療プログラム |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007041373 | 2007-02-21 | ||
| JP2007041373 | 2007-02-21 | ||
| JP2009500232A JP5113828B2 (ja) | 2007-02-21 | 2008-02-21 | 動的腫瘍の放射線治療装置および動的腫瘍の放射線治療プログラム |
| PCT/JP2008/052944 WO2008102843A1 (ja) | 2007-02-21 | 2008-02-21 | 動的腫瘍の放射線治療装置および動的腫瘍の放射線治療プログラム |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2008102843A1 JPWO2008102843A1 (ja) | 2010-05-27 |
| JP5113828B2 true JP5113828B2 (ja) | 2013-01-09 |
Family
ID=39710115
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009500232A Expired - Fee Related JP5113828B2 (ja) | 2007-02-21 | 2008-02-21 | 動的腫瘍の放射線治療装置および動的腫瘍の放射線治療プログラム |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8428218B2 (ja) |
| EP (1) | EP2127697B1 (ja) |
| JP (1) | JP5113828B2 (ja) |
| WO (1) | WO2008102843A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024010261A1 (ko) * | 2022-07-06 | 2024-01-11 | 고려대학교 산학협력단 | 양전자 및 감마선 이중 검출기 및 이를 이용한 악성 종양 진단정보 제공방법 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9155909B2 (en) | 2009-03-24 | 2015-10-13 | National University Corporation Hokkaido University | Radiation therapy apparatus |
| US11446520B2 (en) * | 2017-03-14 | 2022-09-20 | National Univ. Corporation Hokkaido Univ. | Radiation therapy apparatus configured to track a tracking object moving in an irradiation object |
| CN108761387B (zh) * | 2018-06-01 | 2022-03-08 | 西安邮电大学 | 一种固定辐射源的双站时差频差联合定位方法 |
| US20220347491A1 (en) * | 2021-05-03 | 2022-11-03 | Washington University | Systems and methods of adaptive radiotherapy with conventional linear particle accelerator (linac) radiotherapy devices |
| CN117991320B (zh) * | 2024-01-10 | 2024-11-08 | 北京方鸿智能科技有限公司 | 放射源的定位方法、装置、设备及存储介质 |
| CN118217551B (zh) * | 2024-05-22 | 2024-08-23 | 四川省肿瘤医院 | 基于图像引导的放射治疗定位系统 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6427569A (en) * | 1987-07-23 | 1989-01-30 | Mitsubishi Electric Corp | Cancer treatment apparatus employing charge corpuscular beam |
| JPH0299075A (ja) * | 1988-10-07 | 1990-04-11 | Olympus Optical Co Ltd | 温熱治療装置 |
| JP2004533273A (ja) * | 2000-11-29 | 2004-11-04 | セノルクッス・インコーポレーテッド | 歩哨リンパ節の位置決めおよび生検 |
| JP2005514969A (ja) * | 2001-06-08 | 2005-05-26 | カリプソー メディカル テクノロジーズ インコーポレイテッド | 誘導放射線療法システム |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS60187660A (ja) | 1984-02-24 | 1985-09-25 | Honda Motor Co Ltd | 部分硬化鋳鉄部材 |
| JPH1034423A (ja) | 1996-07-18 | 1998-02-10 | Dijet Ind Co Ltd | フライス装置 |
| US8788020B2 (en) | 1998-10-23 | 2014-07-22 | Varian Medical Systems, Inc. | Method and system for radiation application |
| US7297958B2 (en) * | 2001-12-03 | 2007-11-20 | Hitachi, Ltd. | Radiological imaging apparatus |
| US7221733B1 (en) * | 2002-01-02 | 2007-05-22 | Varian Medical Systems Technologies, Inc. | Method and apparatus for irradiating a target |
| US20070055090A1 (en) | 2004-08-12 | 2007-03-08 | Navotek Medical Ltd. | Medical Treatment System and Method |
-
2008
- 2008-02-21 JP JP2009500232A patent/JP5113828B2/ja not_active Expired - Fee Related
- 2008-02-21 US US12/449,682 patent/US8428218B2/en not_active Expired - Fee Related
- 2008-02-21 EP EP08711733A patent/EP2127697B1/en not_active Not-in-force
- 2008-02-21 WO PCT/JP2008/052944 patent/WO2008102843A1/ja not_active Ceased
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6427569A (en) * | 1987-07-23 | 1989-01-30 | Mitsubishi Electric Corp | Cancer treatment apparatus employing charge corpuscular beam |
| JPH0299075A (ja) * | 1988-10-07 | 1990-04-11 | Olympus Optical Co Ltd | 温熱治療装置 |
| JP2004533273A (ja) * | 2000-11-29 | 2004-11-04 | セノルクッス・インコーポレーテッド | 歩哨リンパ節の位置決めおよび生検 |
| JP2005514969A (ja) * | 2001-06-08 | 2005-05-26 | カリプソー メディカル テクノロジーズ インコーポレイテッド | 誘導放射線療法システム |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024010261A1 (ko) * | 2022-07-06 | 2024-01-11 | 고려대학교 산학협력단 | 양전자 및 감마선 이중 검출기 및 이를 이용한 악성 종양 진단정보 제공방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2127697B1 (en) | 2012-08-15 |
| WO2008102843A1 (ja) | 2008-08-28 |
| JPWO2008102843A1 (ja) | 2010-05-27 |
| EP2127697A4 (en) | 2010-07-28 |
| EP2127697A1 (en) | 2009-12-02 |
| US20100142677A1 (en) | 2010-06-10 |
| US8428218B2 (en) | 2013-04-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5113828B2 (ja) | 動的腫瘍の放射線治療装置および動的腫瘍の放射線治療プログラム | |
| US9155909B2 (en) | Radiation therapy apparatus | |
| Parodi et al. | Experimental study on the feasibility of in-beam PET for accurate monitoring of proton therapy | |
| Shakirin et al. | Implementation and workflow for PET monitoring of therapeutic ion irradiation: a comparison of in-beam, in-room, and off-line techniques | |
| US5813985A (en) | Apparatus and methods for providing attenuation guidance and tumor targeting for external beam radiation therapy administration | |
| JP6046756B2 (ja) | 放射誘導の放射線治療の方法および装置 | |
| CN103890611B (zh) | 数据驱动的对事件接受/拒绝逻辑的优化 | |
| JPWO2010109586A1 (ja) | 遮蔽型放射線治療・画像化複合装置 | |
| US12285633B2 (en) | Device and a method for monitoring a treatment of a body part of a patient with particles | |
| JP5916434B2 (ja) | 治療計画装置及び治療計画方法並びにそのプログラム | |
| EP3405814A1 (en) | System and method for the determination of a dose in radiotherapy | |
| Duan et al. | Real‐time monitoring and verification of in vivo high dose rate brachytherapy using a pinhole camera | |
| JP5818718B2 (ja) | 放射線治療装置制御装置、放射線治療装置制御方法及び放射線治療装置のコンピュータに実行されるプログラム | |
| KR101835123B1 (ko) | 방사선 치료 평가 시스템 | |
| JP2015188589A (ja) | 生体機能観測装置および放射線治療システム | |
| Fiedler et al. | Online irradiation control by means of PET | |
| US20140107392A1 (en) | Method of Dose Comparison for In Vivo Dosimetry | |
| JP2011130929A (ja) | 放射線治療部位監視装置、放射線治療装置、及びその制御方法 | |
| US20210170201A1 (en) | Systems and methods for tissue tracking with radiation therapy beams | |
| US20110309242A1 (en) | Radiation-activated Fiducial Markers for Organ Tracking | |
| Craft et al. | EP-1435: Evaluation of single material and multimaterial patient-specific, 3D-printed radiotherapy phantoms | |
| US20220008696A1 (en) | System for determining location inside body | |
| US20220008697A1 (en) | Balloon inflation composition and system for in vivo location confirmation | |
| GB2593359A (en) | Balloon inflation composition and system for in vivo location confirmation | |
| Smeenk et al. | The influence of an endorectal balloon on intrafraction prostate motion |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20110224 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120919 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121012 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151019 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |