JP5773473B2 - Nk活性増強剤およびその利用 - Google Patents
Nk活性増強剤およびその利用 Download PDFInfo
- Publication number
- JP5773473B2 JP5773473B2 JP2009200935A JP2009200935A JP5773473B2 JP 5773473 B2 JP5773473 B2 JP 5773473B2 JP 2009200935 A JP2009200935 A JP 2009200935A JP 2009200935 A JP2009200935 A JP 2009200935A JP 5773473 B2 JP5773473 B2 JP 5773473B2
- Authority
- JP
- Japan
- Prior art keywords
- activity
- cells
- lymphocytes
- blood
- nanobubble water
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 230000000694 effects Effects 0.000 title claims description 115
- 239000003623 enhancer Substances 0.000 title claims description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 130
- 229910001868 water Inorganic materials 0.000 claims description 129
- 239000002101 nanobubble Substances 0.000 claims description 122
- 210000004698 lymphocyte Anatomy 0.000 claims description 65
- 210000005087 mononuclear cell Anatomy 0.000 claims description 53
- 239000008280 blood Substances 0.000 claims description 47
- 210000004369 blood Anatomy 0.000 claims description 45
- 201000011510 cancer Diseases 0.000 claims description 44
- 238000000034 method Methods 0.000 claims description 43
- 206010028980 Neoplasm Diseases 0.000 claims description 41
- 238000002360 preparation method Methods 0.000 claims description 35
- 238000012258 culturing Methods 0.000 claims description 27
- 238000002296 dynamic light scattering Methods 0.000 claims description 20
- 230000007969 cellular immunity Effects 0.000 claims description 15
- 210000000822 natural killer cell Anatomy 0.000 claims description 11
- 239000010836 blood and blood product Substances 0.000 claims description 9
- 229940125691 blood product Drugs 0.000 claims description 9
- 208000036142 Viral infection Diseases 0.000 claims description 8
- 230000009385 viral infection Effects 0.000 claims description 8
- 239000004480 active ingredient Substances 0.000 claims description 7
- 238000004519 manufacturing process Methods 0.000 claims description 5
- 230000005779 cell damage Effects 0.000 claims 10
- 208000037887 cell injury Diseases 0.000 claims 10
- 230000003013 cytotoxicity Effects 0.000 claims 2
- 231100000135 cytotoxicity Toxicity 0.000 claims 2
- 210000004027 cell Anatomy 0.000 description 81
- 238000012360 testing method Methods 0.000 description 44
- 239000000126 substance Substances 0.000 description 41
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 36
- 239000001301 oxygen Substances 0.000 description 36
- 229910052760 oxygen Inorganic materials 0.000 description 36
- 239000001257 hydrogen Substances 0.000 description 26
- 229910052739 hydrogen Inorganic materials 0.000 description 26
- 239000002245 particle Substances 0.000 description 26
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 25
- 239000002609 medium Substances 0.000 description 25
- 239000000243 solution Substances 0.000 description 22
- 108010002350 Interleukin-2 Proteins 0.000 description 21
- 238000009169 immunotherapy Methods 0.000 description 20
- 239000012980 RPMI-1640 medium Substances 0.000 description 15
- 239000002158 endotoxin Substances 0.000 description 13
- 238000005259 measurement Methods 0.000 description 12
- 239000000523 sample Substances 0.000 description 12
- 230000001413 cellular effect Effects 0.000 description 11
- 210000005259 peripheral blood Anatomy 0.000 description 11
- 239000011886 peripheral blood Substances 0.000 description 11
- 230000002708 enhancing effect Effects 0.000 description 10
- 238000001802 infusion Methods 0.000 description 10
- 239000003795 chemical substances by application Substances 0.000 description 9
- 241000282412 Homo Species 0.000 description 7
- 238000005119 centrifugation Methods 0.000 description 7
- 238000001914 filtration Methods 0.000 description 7
- GNPVGFCGXDBREM-UHFFFAOYSA-N germanium atom Chemical compound [Ge] GNPVGFCGXDBREM-UHFFFAOYSA-N 0.000 description 7
- 230000005484 gravity Effects 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 239000000047 product Substances 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 208000035473 Communicable disease Diseases 0.000 description 6
- 230000001472 cytotoxic effect Effects 0.000 description 6
- 230000002265 prevention Effects 0.000 description 6
- 238000000926 separation method Methods 0.000 description 6
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 6
- 241000894006 Bacteria Species 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 238000009826 distribution Methods 0.000 description 5
- 239000002504 physiological saline solution Substances 0.000 description 5
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- 239000002246 antineoplastic agent Substances 0.000 description 4
- 210000001185 bone marrow Anatomy 0.000 description 4
- 238000004113 cell culture Methods 0.000 description 4
- 239000012091 fetal bovine serum Substances 0.000 description 4
- 239000012530 fluid Substances 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- UZOVYGYOLBIAJR-UHFFFAOYSA-N 4-isocyanato-4'-methyldiphenylmethane Chemical compound C1=CC(C)=CC=C1CC1=CC=C(N=C=O)C=C1 UZOVYGYOLBIAJR-UHFFFAOYSA-N 0.000 description 3
- 208000023275 Autoimmune disease Diseases 0.000 description 3
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 3
- 108091006905 Human Serum Albumin Proteins 0.000 description 3
- 102000008100 Human Serum Albumin Human genes 0.000 description 3
- 206010061598 Immunodeficiency Diseases 0.000 description 3
- 208000029462 Immunodeficiency disease Diseases 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 229940034982 antineoplastic agent Drugs 0.000 description 3
- 210000000601 blood cell Anatomy 0.000 description 3
- 230000023555 blood coagulation Effects 0.000 description 3
- 239000003130 blood coagulation factor inhibitor Substances 0.000 description 3
- 238000005868 electrolysis reaction Methods 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 230000007813 immunodeficiency Effects 0.000 description 3
- 230000006698 induction Effects 0.000 description 3
- 238000000691 measurement method Methods 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- 229960005322 streptomycin Drugs 0.000 description 3
- 238000010998 test method Methods 0.000 description 3
- -1 that is Substances 0.000 description 3
- 208000030507 AIDS Diseases 0.000 description 2
- 208000035143 Bacterial infection Diseases 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 2
- 241000725303 Human immunodeficiency virus Species 0.000 description 2
- 241000239218 Limulus Species 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 208000026935 allergic disease Diseases 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 208000022362 bacterial infectious disease Diseases 0.000 description 2
- 239000012503 blood component Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 230000001112 coagulating effect Effects 0.000 description 2
- 238000010293 colony formation assay Methods 0.000 description 2
- 238000004737 colorimetric analysis Methods 0.000 description 2
- 239000000306 component Substances 0.000 description 2
- 230000007123 defense Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 239000012470 diluted sample Substances 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 210000004700 fetal blood Anatomy 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 229910052732 germanium Inorganic materials 0.000 description 2
- 229960002897 heparin Drugs 0.000 description 2
- 229920000669 heparin Polymers 0.000 description 2
- 230000036039 immunity Effects 0.000 description 2
- 230000003053 immunization Effects 0.000 description 2
- 238000002649 immunization Methods 0.000 description 2
- 239000000367 immunologic factor Substances 0.000 description 2
- 239000002955 immunomodulating agent Substances 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 239000003978 infusion fluid Substances 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 208000032839 leukemia Diseases 0.000 description 2
- 210000003810 lymphokine-activated killer cell Anatomy 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- 239000003761 preservation solution Substances 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000011550 stock solution Substances 0.000 description 2
- KZDCMKVLEYCGQX-UDPGNSCCSA-N 2-(diethylamino)ethyl 4-aminobenzoate;(2s,5r,6r)-3,3-dimethyl-7-oxo-6-[(2-phenylacetyl)amino]-4-thia-1-azabicyclo[3.2.0]heptane-2-carboxylic acid;hydrate Chemical compound O.CCN(CC)CCOC(=O)C1=CC=C(N)C=C1.N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 KZDCMKVLEYCGQX-UDPGNSCCSA-N 0.000 description 1
- 208000029483 Acquired immunodeficiency Diseases 0.000 description 1
- 208000035285 Allergic Seasonal Rhinitis Diseases 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- 208000003174 Brain Neoplasms Diseases 0.000 description 1
- 241000218645 Cedrus Species 0.000 description 1
- 208000007190 Chlamydia Infections Diseases 0.000 description 1
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 206010010099 Combined immunodeficiency Diseases 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- 235000005956 Cosmos caudatus Nutrition 0.000 description 1
- 241000701022 Cytomegalovirus Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 206010015108 Epstein-Barr virus infection Diseases 0.000 description 1
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 1
- 229910052693 Europium Inorganic materials 0.000 description 1
- 206010017533 Fungal infection Diseases 0.000 description 1
- 208000022072 Gallbladder Neoplasms Diseases 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 208000001204 Hashimoto Disease Diseases 0.000 description 1
- 208000030836 Hashimoto thyroiditis Diseases 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010021450 Immunodeficiency congenital Diseases 0.000 description 1
- 102000006992 Interferon-alpha Human genes 0.000 description 1
- 108010047761 Interferon-alpha Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- RJQXTJLFIWVMTO-TYNCELHUSA-N Methicillin Chemical compound COC1=CC=CC(OC)=C1C(=O)N[C@@H]1C(=O)N2[C@@H](C(O)=O)C(C)(C)S[C@@H]21 RJQXTJLFIWVMTO-TYNCELHUSA-N 0.000 description 1
- 206010028470 Mycoplasma infections Diseases 0.000 description 1
- 208000031888 Mycoses Diseases 0.000 description 1
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 1
- 230000006051 NK cell activation Effects 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 208000031845 Pernicious anaemia Diseases 0.000 description 1
- 102000009097 Phosphorylases Human genes 0.000 description 1
- 108010073135 Phosphorylases Proteins 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 206010037075 Protozoal infections Diseases 0.000 description 1
- 241000589517 Pseudomonas aeruginosa Species 0.000 description 1
- 235000001630 Pyrus pyrifolia var culta Nutrition 0.000 description 1
- 240000002609 Pyrus pyrifolia var. culta Species 0.000 description 1
- 208000015634 Rectal Neoplasms Diseases 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- 206010048908 Seasonal allergy Diseases 0.000 description 1
- 206010054979 Secondary immunodeficiency Diseases 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 241000700584 Simplexvirus Species 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- 241000191967 Staphylococcus aureus Species 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- 206010057644 Testis cancer Diseases 0.000 description 1
- 208000024780 Urticaria Diseases 0.000 description 1
- 208000002495 Uterine Neoplasms Diseases 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 201000009628 adenosine deaminase deficiency Diseases 0.000 description 1
- 239000003570 air Substances 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 230000009876 antimalignant effect Effects 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 238000005311 autocorrelation function Methods 0.000 description 1
- 208000036556 autosomal recessive T cell-negative B cell-negative NK cell-negative due to adenosine deaminase deficiency severe combined immunodeficiency Diseases 0.000 description 1
- 230000008512 biological response Effects 0.000 description 1
- 238000001815 biotherapy Methods 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- UBAZGMLMVVQSCD-UHFFFAOYSA-N carbon dioxide;molecular oxygen Chemical compound O=O.O=C=O UBAZGMLMVVQSCD-UHFFFAOYSA-N 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 208000028512 chlamydia infectious disease Diseases 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000002301 combined effect Effects 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 230000000214 effect on organisms Effects 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- OGPBJKLSAFTDLK-UHFFFAOYSA-N europium atom Chemical compound [Eu] OGPBJKLSAFTDLK-UHFFFAOYSA-N 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000012997 ficoll-paque Substances 0.000 description 1
- 201000010175 gallbladder cancer Diseases 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- JEGUKCSWCFPDGT-UHFFFAOYSA-N h2o hydrate Chemical compound O.O JEGUKCSWCFPDGT-UHFFFAOYSA-N 0.000 description 1
- 239000012510 hollow fiber Substances 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 229940125721 immunosuppressive agent Drugs 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 206010022000 influenza Diseases 0.000 description 1
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 1
- 229910001410 inorganic ion Inorganic materials 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 229940047124 interferons Drugs 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 229960003085 meticillin Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 239000002213 purine nucleotide Substances 0.000 description 1
- 150000003212 purines Chemical class 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 206010038038 rectal cancer Diseases 0.000 description 1
- 201000001275 rectum cancer Diseases 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 208000002491 severe combined immunodeficiency Diseases 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- YEENEYXBHNNNGV-XEHWZWQGSA-M sodium;3-acetamido-5-[acetyl(methyl)amino]-2,4,6-triiodobenzoate;(2r,3r,4s,5s,6r)-2-[(2r,3s,4s,5r)-3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound [Na+].CC(=O)N(C)C1=C(I)C(NC(C)=O)=C(I)C(C([O-])=O)=C1I.O[C@H]1[C@H](O)[C@@H](CO)O[C@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 YEENEYXBHNNNGV-XEHWZWQGSA-M 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 238000004879 turbidimetry Methods 0.000 description 1
- 229910021642 ultra pure water Inorganic materials 0.000 description 1
- 239000012498 ultrapure water Substances 0.000 description 1
- 210000003954 umbilical cord Anatomy 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 206010046766 uterine cancer Diseases 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
Images
Landscapes
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
(I)NK活性増強剤
(I-1)動的光散乱法で求められる個数平均径が300nm以下の気泡を含むナノバブル水を有効成分とする、NK活性増強剤。
(II-1)生体から分取したリンパ球を(I-1)に記載するNK活性増強剤の存在下で培養して調製される、NK活性増強リンパ球。
(II-2)生体から分取したリンパ球を、(I-1)に記載するNK活性増強剤の存在下で培養する工程を有する、NK活性増強リンパ球の調製方法。
(II-3)生体から分取したリンパ球を含む単核球を、(I-1)に記載するNK活性増強剤の存在下で培養して調製される、NK活性増強単核球。
(II-4)生体から分取したリンパ球を含む単核球を、(I-1)に記載するNK活性増強剤の存在下で培養する工程を有する、NK活性増強単核球の調製方法。
(II-5)(II-1)に記載するNK活性増強リンパ球またはNK活性増強単核球を含有する細胞免疫製剤。
(II-6)生体から分取したリンパ球またはリンパ球を含む単核球を、(I-1)に記載するNK活性増強剤の存在下で培養する工程を有する、(II-5)に記載する細胞免疫製剤の調製方法。
(II-7)(II-1)に記載するNK活性増強リンパ球、(II-3)に記載するNK活性増強単核球、または(II-5)に記載する細胞免疫製剤を含有する輸液製剤。
(III-1)生体から分取した少なくともリンパ球を含む血液を、(I-1)に記載するNK活性増強剤の存在下で培養して調製される、NK活性増強血液製剤。
(III-2)生体から分取した少なくともリンパ球を含む血液を、(I-1)に記載するNK活性増強剤の存在下で培養する工程を有する、NK活性増強血液製剤の調製方法。
本発明のNK活性増強剤は、動的光散乱法で求められる個数平均径が300nm以下の微細気泡を含むナノバブル水を有効成分とすることを特徴とする。
個数 :n1、n2、・・・、ni、・・・、nk
粒子径:d1、d2、・・・、di、・・・、dk
体積 :v1、v2、・・・、vi、・・・、vk。
本発明が対象とするNK活性増強リンパ球および単核球は、それぞれ生体から分取したリンパ球および単核球を、前述するNK活性増強剤の存在下で培養することにより調製することができる。
前述するNK活性増強リンパ球またはNK活性増強単核球を、例えばヒトアルブミンを含む輸液用生理食塩液中に懸濁した形態で製剤化することにより、悪性腫瘍(ガン)あるいは各種感染症を予防または治療するための細胞免疫製剤として用いることができる。
本発明のNK活性増強血液製剤は、生体から分取した少なくともリンパ球を含む血液を、前述するNK活性増強剤の存在下で培養することで調製することができる。ここで血液は、末梢血、臍帯血、または骨髄液であってもよい。取得の容易性から好ましくは末梢血である。また、少なくともリンパ球を含むものであればよく、必ずしも全血である必要はなく、例えば末梢血から得られるPBMCであってもよい。なお、PBMCは、生体から採取した血液から(II)で説明する比重遠心分離法を用いて調製することができる。
(1)NK活性の測定方法
まず被験者の末梢血からNK細胞を含むPBMCを分取し、これに被験物質を添加して、RPMI-1640培地を用いて、5%CO2、37℃の条件で20時間培養する。
被験物質として、下記の方法で調製した(a)酸素ナノバブル水、(b)有機ゲルマニウム粉末、および(c)ハナビラタケを使用した。これらの被験物質のうち、(b)と(c)は、NK細胞活性作用があると報告されている物質である(特開平10-330207号公報、特開2004-292415号公報参照)。
酸素ナノバブル水として、(株)NAGA MRE販売の500ml入り酸素ナノバブル水(製品名:ナーガの雫)(賞味期限2008年9月20日)(原水)を使用した。原水を0.22μmフィルターで濾過滅菌し試験に使用した。具体的には、原水と培地とを混合し培養時に原水が6倍希釈されたもの(原水を16.7%含有)を試験濃度「1倍」とし、原水と培地とを混合し培養時に原水が60倍希釈されたもの(原水を1.67%含有)を試験濃度「1/10倍」とした。なお、当該酸素ナノバブル水中に含まれる酸素ナノバブルの粒径を動的光散乱法(検出法:ヘテロダイン法)に基づいて測定したところ(動的光散乱式粒子径・粒度分析計ナノトラックUPA-UT151型、日機装(株)製)、下記に説明する方法で算出される体積平均径(MV)が0.3734μm(標準偏差:SD=0.0784μm)、個数平均径(MN)が0.2995μm(標準偏差:SD=0.1002μm)と、動的光散乱法による個数平均径が300nm未満のナノバブルであることが確認された。
一つの粉体の集団を仮定する。この中に粒子径の小さな順から、d1、d2、・・・、di、・・・、dkの粒子径(μm)を有する粒子がそれぞれn1、n2、・・・、ni、・・・、nk個あるとする。また粒子1個当たりの体積(μm3)をv1、v2、・・・、vi、・・・、vkとする。すなわち、個数と粒子径と体積は下記の関係にある。
個数 :n1、n2、・・・、ni、・・・、nk
粒子径:d1、d2、・・・、di、・・・、dk
体積 :v1、v2、・・・、vi、・・・、vk。
有機ゲルマニウム粉末として、(株)浅井ゲルマニウム研究所製のものを使用した。 これをRPMI-1640 培地に懸濁し、室温で1時間撹拌し溶解した。これを0.22μmフィルターで濾過滅菌した後、RPMI-1640 培地で培養時の最終濃度が0.022mg/mlとなるように希釈し、試験に使用した。
ハナビラタケとして、(株)ミネターから購入した乾燥粉末製品(ハナビラタケ100:商品名)を使用した。これをRPMI-1640 培地に懸濁し、室温で1時間撹拌し溶解した。これを0.22μmフィルターで濾過滅菌した後、RPMI-1640 培地で培養時の最終濃度が0.022mg/mlとなるように希釈し、試験に使用した。
上記(1)に記載する方法に従って、上記各種の被験物質で処理したPBMCのNK活性を測定した。具体的には、まず、被験者(60代男性)1名の末梢血(全血採血後、30時間以内に使用)から比重遠心分離法を用いてPBMC層を分離した後、一定濃度(培養時濃度:2×106cells/ml)のPBMC溶液を調製した。
酸素ナノバブル水に代えて水素ナノバブル水を用いて実験例1と同様にしてPBMCを処理して、NK活性を測定した。
水素ナノバブル水として、電気分解から得られた、エヌディーアクア株式会社製の水素ナノバブル水(商標名:「真・水素水」、賞味期限2008年12月12日、ロット番号2008.12.12)(原水)を用いた。原水を0.22μmフィルターで濾過滅菌し試験に使用した。具体的には、原水と培地とを混合し培養時に原水が6倍希釈されたもの(原水を16.7%含有)を試験濃度「1倍」とし、原水と培地とを混合し培養時に原水が60倍希釈されたもの(原水を1.67%含有)を試験濃度「1/10倍」とした。ちなみに電気分解によって得られたアルカリイオン水中の水素気泡は3〜200nmであり、水素ナノバブル水には200nm以下の径のバブルが存在することが知られている(“電解アルカリ性水の科学”、ウォーター研究会会報、No.8、p.5(2001))。そこで、当該水素ナノバブル水中に含まれる水素ナノバブルの粒径を、実験例1に記載する方法に従って動的光散乱法に基づいて測定したところ(動的光散乱式粒子径・粒度分析計ナノトラックUPA-UT151型、日機装(株)製)、実験例1で説明する方法で算出される体積平均径(MV)は0.0027μm(標準偏差SD=0.0004μm)、個数平均径(MN)が0.0024μm(標準偏差SD=0.0005μm)と、動的光散乱法による個数平均径が300nm未満(3nm未満)のナノバブルであることが確認された。
実験例1(1)に記載する方法に従って、上記被験物質(水素ナノバブル水)で処理したPBMCのNK活性を測定した。具体的には、まず、被験者2名(50代男性:被験者1、60代男性:被験者2)の末梢血(全血採血後、30時間以内に使用)から比重遠心分離法を用いてPBMC層を分離した後、一定濃度(培養時濃度:2×106cells/ml)のPBMC溶液を調製した。
酸素ナノバブル水に代えて大気ナノバブル水を用いて実験例1と同じ方法でPBMCを処理してNK活性を測定した。
大気ナノバブル水として、ジャパンエコール株式会社製の大気ナノバブル水(ロット番号08121602)(原水)を用いた。大気中には窒素が約78%、酸素が約20.9%および二酸化炭素が約0.03%含まれている。なお、大気ナノバブル水の作成にあたり、空気(山梨県忍野村)を「インライン型クリーンフィルター、FCS500シリーズ」(ポリプロピレン+ウレタン製中空糸膜、濾過精度0.01μm、除去効率99.99%のフィルター)(CKD社製)に通して調製した大気を使用した。
実験例1(1)に記載する方法に従って、上記被験物質(大気ナノバブル水)で処理したPBMCのNK活性を測定した。具体的には、まず、(健常な男女7名:平均年齢47.3±13.7歳)の末梢血(全血採血後、30時間以内に使用)から比重遠心分離法を用いてPBMC層を分離した後、大気ナノバブル水を65%含む培地を使用して、一定濃度(培養時濃度:2×106cells/ml)のPBMC溶液を調製した。
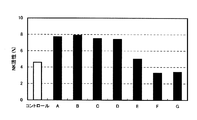
(1)酸素ナノバブル水および大気ナノバブル水によるNK活性の増強
被験物質として下記のナノバブル水を使用して、実験例1の記載に従ってPBMCを処理して、NK活性(%)を測定した。
A:酸素ナノバブル水(ナーガの雫:(株)NAGA MRE製)、体積平均径(MV):0.3734μm(標準偏差SD=0.0784μm)、個数平均径(MN):0.2995μm(標準偏差SD=0.1002μm)
B:大気ナノバブル水(Lot.08121602、ジャパンエコール(株)製)、体積平均径(MV):0.0019μm(標準偏差SD=0.0003μm)、個数平均径(MN):0.0018μm(標準偏差SD=0.0003μm)
C:酸素ナノバブル水(美粒水:ジャパンエコール(株)製)、体積平均径(MV):0.0015μm(標準偏差SD=0.0002μm)、個数平均径(MN):0.0014μm(標準偏差SD=0.0002μm)。
被験物質としてIL−2単独(0〜50ng/ml)、およびIL−2(0〜50ng/ml)と上記ナノバブル水A〜Cとを組み合わせて使用し、実験例1の記載に従ってPBMCを処理して、NK活性を測定した。
Claims (3)
- 動的光散乱法で求められる個数平均径が300nm以下の気泡を含むナノバブル水を有効成分とする、NK細胞のがん細胞傷害及びウイルス感染細胞傷害に関わる活性増強剤。
- 生体から分取したリンパ球または単核球を、請求項1に記載するNK細胞のがん細胞傷害及びウイルス感染細胞傷害に関わる活性増強剤の存在下で培養する工程を有する、NK細胞のがん細胞傷害及びウイルス感染細胞傷害に関わる活性増強リンパ球又はNK細胞のがん細胞傷害及びウイルス感染細胞傷害に関わる活性増強単核球を含有する細胞免疫製剤の製造方法。
- 生体から分取した少なくともリンパ球を含む血液を、請求項1に記載するNK細胞のがん細胞傷害及びウイルス感染細胞傷害に関わる活性増強剤の存在下で培養する工程を有する、NK細胞のがん細胞傷害及びウイルス感染細胞傷害に関わる活性増強血液製剤の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009200935A JP5773473B2 (ja) | 2008-09-01 | 2009-08-31 | Nk活性増強剤およびその利用 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008223076 | 2008-09-01 | ||
| JP2008223076 | 2008-09-01 | ||
| JP2009200935A JP5773473B2 (ja) | 2008-09-01 | 2009-08-31 | Nk活性増強剤およびその利用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010075180A JP2010075180A (ja) | 2010-04-08 |
| JP5773473B2 true JP5773473B2 (ja) | 2015-09-02 |
Family
ID=42206412
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009200935A Expired - Fee Related JP5773473B2 (ja) | 2008-09-01 | 2009-08-31 | Nk活性増強剤およびその利用 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5773473B2 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5319607B2 (ja) * | 2010-05-31 | 2013-10-16 | 丸井 智敬 | 微小気泡を含有する液体の組成物、および、微小気泡を含有する組成物の製造方法 |
| US9908089B2 (en) | 2012-12-04 | 2018-03-06 | Chung-Ang University Industry-Academy Cooperation Foundation | Device for producing microbubble water by using ultrasonic vibrator, cell culture medium containing microbubble water, cell culturing method using same, high efficiency mixed fuel using microbubbles, and method for manufacturing same |
| KR101588246B1 (ko) * | 2012-12-04 | 2016-01-26 | 중앙대학교 산학협력단 | 미세버블수를 함유한 세포 배양 배지 및 이를 이용한 세포 배양 방법 |
| HK1223975A1 (zh) * | 2013-12-27 | 2017-08-11 | 水活力株式会社 | 含纳米气泡的组合物及其用途 |
| JP5934735B2 (ja) * | 2014-03-28 | 2016-06-15 | 株式会社オプトクリエーション | ナノバブル・フコイダン水素水 |
| WO2016037073A2 (en) | 2014-09-05 | 2016-03-10 | Tennant Company | Systems and methods for supplying treatment liquids having nanobubbles |
| JP6555880B2 (ja) * | 2014-12-11 | 2019-08-07 | 株式会社メニコン | 微細気泡含有滅菌液の製造方法、該製造方法により得られる微細気泡含有滅菌液、および微細気泡含有滅菌液 |
| JP6351044B2 (ja) * | 2015-09-11 | 2018-07-04 | 株式会社熊本アイディーエム | 輸液生成装置 |
| KR102162400B1 (ko) | 2016-05-13 | 2020-10-06 | 시그마 테크놀로지 유겐가이샤 | 생체 투여 가능한 수용액 및 그 제조 방법 |
| JP2023066654A (ja) * | 2021-10-29 | 2023-05-16 | キヤノン株式会社 | ウルトラファインバブル含有液の製造方法、およびウルトラファインバブルの製造装置 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001029191A1 (fr) * | 1999-10-21 | 2001-04-26 | Keisuke Teshigawara | Methode de culture in vitro de lymphocytes et compositions de therapie genique |
| JP3904374B2 (ja) * | 2000-02-29 | 2007-04-11 | 独立行政法人科学技術振興機構 | キラー活性を増強したリンパ球 |
| JP2002255849A (ja) * | 2001-02-28 | 2002-09-11 | Morinaga Milk Ind Co Ltd | 細胞免疫療法補助剤 |
| JP4080440B2 (ja) * | 2004-03-05 | 2008-04-23 | 独立行政法人産業技術総合研究所 | 酸素ナノバブル水およびその製造方法 |
| JP2006213688A (ja) * | 2005-02-07 | 2006-08-17 | Toshio Oshiro | Nk活性増強剤 |
| JP4275680B2 (ja) * | 2006-04-28 | 2009-06-10 | 裕 照沼 | リンパ球の活性・増殖に係る培養方法 |
| JP4611328B2 (ja) * | 2007-02-28 | 2011-01-12 | シャープ株式会社 | インスリン量を増加させるとともに血糖値を低下させる装置 |
-
2009
- 2009-08-31 JP JP2009200935A patent/JP5773473B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2010075180A (ja) | 2010-04-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5773473B2 (ja) | Nk活性増強剤およびその利用 | |
| US11883429B2 (en) | Therapeutic pooled blood apoptotic cell preparations and uses thereof | |
| Wu et al. | Granulocytic myeloid-derived suppressor cell exosomal prostaglandin E2 ameliorates collagen-induced arthritis by enhancing IL-10+ B cells | |
| Parida et al. | Cellular therapy in tuberculosis | |
| JP2007535486A (ja) | 高分子量のヒアルロン酸を用いた内因性又は埋め込まれた又は移植された幹細胞の機能回復を促進するための方法 | |
| KR20200030084A (ko) | 씨디39 기질 줄기세포 단리 방법 및 용도 | |
| Ehx et al. | Comprehensive analysis of the immunomodulatory effects of rapamycin on human T cells in graft-versus-host disease prophylaxis | |
| Liu et al. | Glutaminolysis is required in maintaining immune regulatory functions in B cells | |
| CN109803681B (zh) | 用于治疗免疫病症的免疫抑制组合物 | |
| WO2011036722A1 (ja) | Nk活性増強剤およびその利用 | |
| JP2009514530A (ja) | 生体外で制御性t細胞を生成するためのアポトーシス細胞の利用 | |
| Song et al. | The role of regulatory B cells (Bregs) in the Tregs-amplifying effect of Sirolimus | |
| JP2023540827A (ja) | 高純度及び高効率の自然殺害細胞の製造方法及びその用途 | |
| TW201110972A (en) | Methods for treating allergic disease | |
| CN101229362B (zh) | 血清胸腺因子在制备抗肿瘤药物、肿瘤物理及化学治疗药物的保护药物方面的用途 | |
| Banyer et al. | Combinations of IFN-γand IL-4 induce distinct profiles of dendritic cell-associated immunoregulatory properties | |
| Tao et al. | Nicotine Protects Dendritic Cells from Apoptosis and Support DCs-dependent CD4+ T-cell Priming in vitro. | |
| Yavuz et al. | Gold-based nano-adjuvants | |
| JP7601394B2 (ja) | Htlv-i特異的ctl活性化剤 | |
| Simonetta et al. | Moving Towards Allogeneic Cellular Therapies: Opportunities and Challenges | |
| Wu et al. | Prostaglandin E2 Ameliorates Collagen-Induced Arthritis by Enhancing IL-10+ B Cells | |
| Aktanova et al. | ASSESSING EFFECTS OF CUCURBITURILS ON MONOCYTES AND NK-CELLS IN HEALTHY VOLUNTEERS | |
| Surana | The Role of BET Proteins on M1/M2 Macrophage Polarization | |
| KR20260041732A (ko) | 혈액 유래 물질 및 면역세포를 포함하는 암 또는 면역질환의 예방 또는 치료용 약학조성물 | |
| WO2018043660A1 (ja) | ナチュラルキラーt(nkt)細胞を刺激する樹状細胞の製造方法、およびnkt細胞を刺激する樹状細胞とnkt細胞とを含む細胞組成物の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120823 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140304 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140425 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141021 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141220 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20141220 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20141225 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20141222 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150212 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150605 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150626 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5773473 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |