JP7242536B2 - 免疫細胞および薬物ホーミング、移動ならびに腫瘍細胞毒性についての高スループット3dアッセイ - Google Patents
免疫細胞および薬物ホーミング、移動ならびに腫瘍細胞毒性についての高スループット3dアッセイ Download PDFInfo
- Publication number
- JP7242536B2 JP7242536B2 JP2019542516A JP2019542516A JP7242536B2 JP 7242536 B2 JP7242536 B2 JP 7242536B2 JP 2019542516 A JP2019542516 A JP 2019542516A JP 2019542516 A JP2019542516 A JP 2019542516A JP 7242536 B2 JP7242536 B2 JP 7242536B2
- Authority
- JP
- Japan
- Prior art keywords
- cells
- tumor
- assay method
- chamber
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5011—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing antineoplastic activity
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0693—Tumour cells; Cancer cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5014—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing toxicity
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/502—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing non-proliferative effects
- G01N33/5029—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing non-proliferative effects on cell motility
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5082—Supracellular entities, e.g. tissue, organisms
- G01N33/5088—Supracellular entities, e.g. tissue, organisms of vertebrates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/02—Compounds of the arachidonic acid pathway, e.g. prostaglandins, leukotrienes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/21—Chemokines, e.g. MIP-1, MIP-2, RANTES, MCP, PF-4
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/28—Vascular endothelial cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2503/00—Use of cells in diagnostics
- C12N2503/02—Drug screening
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2513/00—3D culture
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/10—Screening for compounds of potential therapeutic value involving cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Cell Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- General Health & Medical Sciences (AREA)
- Toxicology (AREA)
- Biochemistry (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Food Science & Technology (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Organic Chemistry (AREA)
- Oncology (AREA)
- General Engineering & Computer Science (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
本明細書で使用する場合、文脈でそうでないことが明示されていない限り、単数形「a」、「an」、および「the」は複数の指示対象を包含する。したがって、例えば「~の構造の底面」に対する言及は、文脈でそうでないことが明示されていない限り、2つ以上のそのような「構造の底面」を有する例を包含する。
ート、6ウェルプレート、12ウェルプレート、24ウェルプレート、96ウェルプレート、1536ウェルプレート、または任意の他のマルチウェルプレート形態であり得る。
あり得る。スフェロイドの最大サイズは、一般に、拡散の検討事項によって制約を受ける(例えば、スフェロイド及びスフェロイド容器の概説については、Achilli,T-M,et.al.Expert Opin.Biol.Ther.(2012)12(10)を参照のこと)。
になる」を使用して記載することができるものを包含する別の実施形態を暗示すると理解されるべきである。
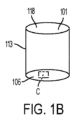
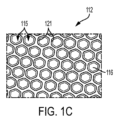
て、上部開口部は、250μmから1mm、またはそれらの測定値内の任意の範囲の上部開口部(幅w)の直径を画定する。いくつかの実施形態において、上部開口部から最下点までの距離(深さ「d」)は200μmから900μm、または400から600μmである。マイクロキャビティのアレイは、様々な形状,例えば、放物型、双曲型、山型、および断面形状、またはそれらの組み合わせを有していてもよい。実施形態において、マイクロキャビティは、それらの下に、それらが実験台またはテーブルなどの表面と直接接触することから保護する保護層130を有していてもよい。いくつかの実施形態において、ウェルの底部119と保護層との間に空間110が設けられていてもよい。実施形態において、空間110は外部環境と連通していてもよいし、または閉じられていてもよい。
ブロモクレゾールパープル)、選択剤(例えば、化学薬品、抗菌薬)などを含む)を含む。
オキセノン;オリゴヌクレオチド;オナプリストン;オンダンセトロン;オンダンセトロン;オラシン(oracin);口腔サイトカインインデューサー;オルマプラチン;オサテロン;オキサリプラチン;オキサウノマイシン;パクリタキセル;パクリタキセルアナログ;パクリタキセル誘導体;パラウアミン;パルミトイルリゾキシン;パミドロン酸;パナキシトリオール;パノミフェン;パラバクチン;パゼリプチン(pazelliptine);ペガスパルカーゼ;ペルデシン;ペントサンポリスルフェートナトリウム;ペントスタチン;ペントロゾール;パーフルブロン;ペルフォスファミド;ペリリルアルコール;フェナジノマイシン;フェニルアセテート;ホスファターゼ阻害剤;ピシバニール;塩酸ピロカルピン;ピラルビシン;ピリトレキシム;プラセチンA;プラセチンB;プラスミノーゲンアクチベータ阻害剤;白金錯体;白金化合物;白金-トリアミン複合体;ポルフィマーナトリウム;ポルフィロマイシン;プレドニゾン;プロピルビス-アクリドン;プロスタグランジンJ2;プロテアソーム阻害剤;タンパク質A系免疫モジュレータ;タンパク質キナーゼC阻害剤;タンパク質キナーゼC阻害剤、微細藻類;タンパク質チロシンホスファターゼ阻害剤;プリンヌクレオシドホスホリラーゼ阻害剤;プルプリン;ピラゾロアクリジン;ピリドキシル化ヘモグロビンポリオキシエチレンコンジュゲート;rafアンタゴニスト;ラルチトレキセド;ラモセトロン;rasファルネシルタンパク質トランスフェラーゼ阻害剤;ras阻害剤;ras-GAP阻害剤;脱メチル化レテリプチン;レニウムRe186エチドロネート;リゾキシン;リボザイム;RIIレチナミド;ログレチミド;ロヒツキン(rohitukine);ロムルチド;ロキニメックス;ルビギノンB1;ルボキシル;サフィンゴール;サイントピン;SarCNU;サルコフィトール(sarcophytol)A;サルグラモスチム;Sdi1模倣物;セムスチン;老化由来(senescence derived)阻害剤1;センスオリゴヌクレオチド;シグナル変換阻害剤;シグナル変換モジュレータ;単鎖抗原結合タンパク質;シゾフィラン;ソブゾキサン;ボロカプチン酸ナトリウム(sodium borocaptate);フェニル酢酸ナトリウム;ソルベロール;ソマトメジン結合タンパク質;ソネルミン;スパルフォス酸;スピカマイシンD;スピロムスチン;スプレノペンチン;スポンジスタチン1;スクワラミン;幹細胞阻害剤;幹細胞分裂阻害剤;スチピアミド;ストロメリシン阻害剤;スルフィノシン;超活性血管作動性腸ペプチドアンタゴニスト;スラジスタ;スラミン;スワインソニン;合成グリコサミングリカン;タリムスチン;タモキシフェンメチオジド;タウロムスチン;タザロテン;テコガランナトリウム;テガフール;テルラピリリウム;テロメラーゼ阻害剤;テモポルフィン;テモゾロマイド;テニポシド;テトラクロロデカオキシド;テトラゾミン(tetrazomine);タリブラスチン(thaliblastine);チオコラリン;トロンボポエチン;トロンボポエチン模倣物;チマルファシン;チモポエチン受容体アゴニスト;チモトリナン;甲状腺刺激ホルモン;エチルエチオプルプリンスズ;チラパザミン;チタノセンジクロリド;トプセチン;トレミフェン;分化全能性幹細胞因子;翻訳阻害剤;トレチノイン;トリアセチルウリジン;トリシリビン;トリメトレキサート;トリプトレリン;トロピセトロン;ツロステリド;チロシンキナーゼ阻害剤;チルホスチン(tyrphostins);UBC阻害剤;ウベニメクス;尿生殖洞由来の成長阻害因子;ウロキナーゼ受容体アンタゴニスト;バプレオチド;バリオリン(variolin)B;ベクターシステム、赤血球遺伝子療法;ベラレソール(velaresol);べラミン(veramine);ベルディンス(verdins);ベルテポルフィン;ビノレルビン;ビンキサルチン;ビタキシン(vitaxin);ボロゾール;ザノテロン;ゼニプラチン;ジラスコルブ;およびジノスタチンスチマラマーが挙げられる。
細胞培養
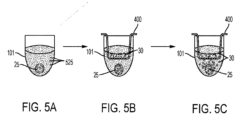
A549/GFP細胞(Cell Biolabs,Inc.カタログ番号AKR-209)は、10%ウシ胎仔血清(FBS)(Corningカタログ番号35-010-CV)を追加したIscoveの修飾DMEM(IMDM)(Corningカタログ番号10-016-CM)中にウェルあたり2,000個の細胞で96ウェルスフェロイドマイクロプレート(Corningカタログ番号4515)に播種した。翌日、培地を、30ng/mLのヒトSDF-1α(SDF-1α)/CXCL12(Shenandoah Biotechnology Inc(商標)カタログ番号100-20)またはビヒクル対照を含む200μLのIMDM10%FBSと置換した。NK92-MI細胞を80μM細胞Tracker(商標)Blue CMHC Dye(Molecular Probes(商標)カタログ番号C2110)で1時間染色し、同時に血清を含まないIMDM中2μg/mLのプロスタグランジンE2(PGE2)(Tocrisカタログ番号2296)またはビヒクル対照で1時間処理した。HTS Transwell-96Well Permeable Supportを96ウェルスフェロイドプレートに入れた(概略図を図1Aおよび図4Cに示す)。NK-92MI細胞を次に無血清IMDM中に再懸濁させ、インサートのアピカルチャンバーに50,000細胞/インサートで播種した。24時間後、インサートを取り出し、スフェロイドマイクロプレートをフローサイトメトリーのために処理した。簡単に言うと、培地を除去し、150μLのTrypLE(商標)Select Enzyme(10X)(Gibco(商標)カタログ番号A1217701)で置換し、スフェロイドを最小のピペッティングで単細胞に分解することができるようになるまで37℃でインキュベートした。細胞を次にMiltenyi Biotec MacsQuant(登録商標)を利用してフローサイトメトリーにより分析した。
A549/GFP細胞のNK-92MI移動および殺腫瘍活性は、図4および図5で示すように、Corning 96ウェルスフェロイドマイクロプレートとともに市販のCorning HTS 96Transwellインサートを利用して評価した。悪性腫瘍構造中のある特定の免疫細胞の存在は、患者生存率の増加と相関することが示されている。免疫細胞毒性を研究するためにより一般的に用いられる2Dインビトロモデルとは異なり、腫瘍スフェロイドへの免疫細胞浸透を観察するために3Dモデルを使用することができる。図6は、図5で示す実施形態にしたがって、3D中に培養されるA549/GFP腫瘍細胞へのNK細胞の移動を示すグラフである。データは2つの独立した研究の平均で示し、ボンフェローニポストテストを伴う一元配置分散分析でN=24。***=p<0.0001そして**=p<0.001。図6は、免疫細胞移動は、どのようにしてSDF-1αなどのケモカインの添加によって増強することができ、またPGE2などの阻害剤の添加によって抑制できるかを示す。NK移動は、化学誘引物質SDF-1αがスフェロイドマイクロプレート中に腫瘍スフェロイドとともに存在する場合、有意に増大した。図7は、図4A、図4B、および図5で示す実施形態にしたがって3Dに培養されたA549/GFP腫瘍細胞のNK誘発性細胞毒性を示すグラフである。反対に、免疫回避の形態としてがん細胞によって多くの場合分泌される免疫細胞機能の公知阻害剤であるPGE2にNK細胞が曝露された場合、移動が有意に減少した。殺腫瘍活性は、移動データとよく相関し、PGE2を含まないSDF-1αに曝露されたNK細胞で観察されたA549/GFP腫瘍細胞の生存率は最低である(図7)。
血液脳関門モデル
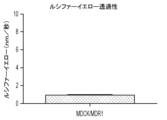
MDCKII/MDR1細胞をPiet Borst博士(Netherlands Cancer Institute、オランダ国アムステルダム)から入手し、10%ウシ胎仔血清(FBS)(Corningカタログ番号35-010-CV)を追加した100μLのDulbecco’s Modification of Eagle’s Medium(DMEM)(Corningカタログ番号10-013-CM)中で1cm2あたり100,000個の細胞でHTS96-ウェルTranswell(Corningカタログ番号3391または3977)中に播種した。アッセイの24時間前に培地を交換してそれらを5日間培養した。単層完全性をルシファーイエロー透過性(図10A)(シグマカタログ番号L0144)およびローダミン123輸送(図10B)(シグマカタログ番号R8004)により評価した。製造業者のプロトコル(データは不掲載)どおりに密着結合タンパク質ZO1(Thermo Fisherカタログ番号339188)およびオクルディン(Thermo Fisherカタログ番号331588)の存在を確認するために、MDCKII/MDR1単層の免疫染色を実施した。
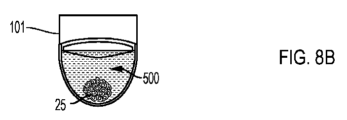
LN229細胞(ATCC(登録商標)カタログ番号CRL-2611(商標))を、10%FBSを含むDMEM中でルーチン的に培養した。細胞をAccutase(登録商標)細胞分離溶液(Corningカタログ番号25-058-CI)で収集し、96ウェルスフェロイドマイクロプレートにウェルあたり1,000細胞でアッセイ前24時間播種した(図8B)。
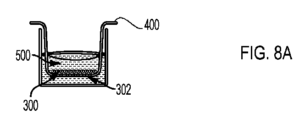
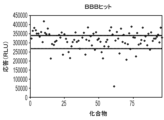
図8Aから8Gに示すように、血液脳関門/神経膠腫球モデル試験を、血液脳関門をシミュレートするように構成された多孔質膜の使用を含むモデルにおいて治療薬の移動能および細胞毒性を検出するための本開示の方法の一実施形態で実施した。まず、図8Aに示すように、BBBをシミュレートするために使用するMDCKII/MDR1細胞を細胞培養インサート304の多孔質膜302上に播種した。LN229腫瘍細胞をCorning96ウェルスフェロイドプレート中で成長させた(図8Bに示すとおり)。スフェロイドに発生したLN229腫瘍細胞(図8Bに示すとおり)および細胞培養インサートの多孔質膜上のBBBをシミュレートするMDCKII/MDR1内皮細胞のコンフルエントな単層(図8Aに示すとおり)が形成されたら、細胞培養インサートをウェルに入れた。図8Cを参照して、薬物、シスプラチンまたはピペロングミンなどの薬物をインサートのキャビティに2時間添加した。薬物インキュベーション後、細胞培養インサートを取り出し、単層完全性について試験した(データは不掲載)。スフェロイドをさらに2日間培養し(図8Dおよび図8Eに示すとおり)、次いで、例えばCellTiter-Glo(登録商標)3Dなどの染色によって、腫瘍細胞溶解について分析した(図8Fに示すとおり。処理後のスフェロイド生理機能(図8Gに示すとおり)も試験した。図9は、化合物シスプラチンおよびピペロングミンとともに直接培養した48時間後のLN229スフェロイドの用量依存性細胞毒性を示すグラフである。濃度あたりN=12ウェルで2回の独立した研究を行う。図11は血液脳関門サロゲートの有無でのシスプラチンまたはピペロングミンのLN229 細胞毒性を示すグラフである。BBBの有無でのTranswellによる2時間の薬物曝露後48時間のLN229スフェロイドの生存百分率を示す。薬物なしの対照を100%生存率に標準化することによって生存率を評価した。データは3つの独立した研究の平均として示し、ボンフェローニポストテストを伴う一元配置分散分析でN=30。***=p<0.0001。図12Aおよび図12Bは、BBB有(図12B)およびBBB無(図12A)で見られるヒットを示すTocrisライブラリからの代表的なスクリーンを示すグラフである。上の点線は平均緩衝液対照であり、下の点線は緩衝液応答より低い3シグマを表す。図13Aおよび13Bは、BBBの有無で見られるヒットのコンピレーションを示す図12Aおよび図12Bのスクリーンの概要のグラフである。ヒットは、それらが3つの独立したスクリーンのうち少なくとも2つにおいて、緩衝液応答よりも低い3シグマであるか否かを考慮した。横縞のハッチングを施したボックス(緩衝液単独以外に)はBBBなしでのみ見られるヒットである。斜めのハッチングを施したボックスは、BBBの存在下および非存在下で見られるヒットであった。したがって、本明細書中で提示するデータは、CorningスフェロイドマイクロプレートとHTS Transwell96-ウェル透過性支持体との組み合わせを含み得る本開示の方法によって、結果として得られる神経膠腫球(または他の3D腫瘍スフェロイド)細胞毒性も調査しながら、BBBを通過することができる化合物と通過できない化合物とを区別することができる新規3Dモデルが可能になることを示す。
治療薬の移動能および細胞毒性を検出するためのアッセイ法であって:
a)腫瘍細胞を3Dスフェロイドコンフォメーションに成長させるような構造のチャンバーを含む細胞培養製品中で腫瘍細胞を培養してスフェロイドを形成し、
b)多孔質膜を含むインサートを前記細胞培養製品に入れ、治療薬を当該インサート中に導入し、
c)前記インサートから前記細胞培養製品チャンバーへの前記治療薬の移動能を検出し、そして
d)腫瘍細胞応答を検出すること
を含む、アッセイ法。
前記チャンバーが:
側壁、
上部開口部、および
少なくとも1つの陥凹面を含む液体不透過性底部であって、当該底部の少なくとも一部が当該少なくとも1つの陥凹面中または上に低接着性または非接着性材料を含む、液体不透過性底部
を含む、実施形態1に記載のアッセイ法。
少なくとも1つの陥凹面を含む前記液体不透過性底部がガス透過性である、実施形態1または2に記載のアッセイ法。
前記側壁が不透明である、実施形態2に記載のアッセイ法。
前記底部の少なくとも一部が透明である、実施形態2から4のいずれか1つに記載のアッセイ法。
前記細胞培養製品が、1から約2000の前記チャンバーを含み、各チャンバーは互いに物理的に離間されている、実施形態2から5のいずれか1つに記載のアッセイ法。
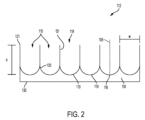
前記少なくとも1つの陥凹面が同じチャンバー内で複数の陥凹面を含む、実施形態2から6のいずれか1つに記載のアッセイ法。
前記少なくとも1つの陥凹面が半球状面、前記側壁から前記底面へと30から約60度のテーパーを有する円錐面、またはそれらの組み合わせを含む、実施形態2から7のいずれか1つに記載のアッセイ法。
前記側壁面が、垂直円筒、前記チャンバー頂部から底面へと直径が減少する垂直円錐の一部、前記少なくとも1つの陥凹底面に対して、円錐遷移部を有する垂直な方形シャフト、またはそれらの組み合わせを含む、実施形態2に記載のアッセイ法。
前記製品が吸引のためにピペットチップを受容するためのチャンバー付属物をさらに含み、当該チャンバー付属物は前記チャンバーに隣接し、前記チャンバーと流体連通した表面を含み、当該チャンバー付属物は前記底面より上方に離間した第二底部を有し、当該第二底部はピペットから分配された流体を当該底面からそれさせる、実施形態2に記載のアッセイ法。
前記インサートがインサートプレートを含む、実施形態1から10のいずれか1つに記載のアッセイ法。
前記多孔質膜の少なくとも一部が血液脳関門をシミュレートするように構成される、実施形態1から11のいずれか1つに記載のアッセイ法。
前記多孔質膜の少なくとも一部が微小血管内皮細胞の本質的にコンフルエントな単層を含む、実施形態12に記載のアッセイ法。
前記治療薬の移動能および腫瘍細胞応答の両方がフローサイトメトリーによって検出される、実施形態1から13のいずれか1つに記載のアッセイ法。
腫瘍細胞応答の検出が、前記治療薬の前記腫瘍細胞スフェロイドへの浸透を検出することを含む、実施形態1から14のいずれか1つに記載のアッセイ法。
腫瘍細胞応答の検出が、腫瘍細胞溶解を測定することを含む、実施形態1から15のいずれか一項に記載のアッセイ法。
前記治療薬が薬物または細胞治療薬を含む、実施形態1から16のいずれか1つに記載のアッセイ法。
前記治療薬が白血球またはリンパ球を含む、実施形態17に記載のアッセイ法。
前記治療薬が薬物である、実施形態10から18のいずれか一項に記載のアッセイ法。
11 スフェロイドプレート
25 3D腫瘍細胞スフェロイド
30、310 治療薬
101 ウェル
105 中心軸
106 底面
110 空間
112 マイクロキャビティ
113 側壁
115 マイクロウェル
116 底面、最下点
118、418 上部開口部
119、419 底部
120 遷移ゾーン
121、421 側壁
130 フレーム、保護層
300、306、525 細胞
302 多孔質膜
304、400 インサート
312、キャビティ、インサートチェンバー
315 アッセイチャンバー
401 インサートプレート
420 キャビティ
500 培地
w 幅
d 深さ
Claims (16)
- 治療薬の移動能および細胞毒性を検出するためのアッセイ法であって:
a)腫瘍細胞を3Dスフェロイドコンフォメーションに成長させるような構造のチャンバーを含む細胞培養製品中で腫瘍細胞を培養してスフェロイドを形成し、
b)少なくとも一部が微小血管内皮細胞の本質的にコンフルエントな単層を含み、血液脳関門をシミュレートするように構成された多孔質膜を含むインサートを前記細胞培養製品に入れ、治療薬を該インサート中に導入し、
c)前記インサートから前記細胞培養製品チャンバーへの前記治療薬の移動能を検出し、そして
d)腫瘍細胞応答を検出すること
を含む、アッセイ法。 - 前記チャンバーが、
側壁、
上部開口部、および
少なくとも1つの陥凹面を含む液体不透過性底部を含み、
前記少なくとも1つの陥凹面および/または側壁上に低接着性または非接着性コーティングを有する、請求項1に記載のアッセイ法。 - 少なくとも1つの陥凹面を含む前記液体不透過性底部がガス透過性である、請求項2に記載のアッセイ法。
- 前記側壁が不透明である、請求項2に記載のアッセイ法。
- 前記底部の少なくとも一部が透明である、請求項2から4のいずれか一項に記載のアッセイ法。
- 前記細胞培養製品が、1から2000の前記チャンバーを含み、各チャンバーは互いに物理的に離間されている、請求項2から5のいずれか一項に記載のアッセイ法。
- 前記少なくとも1つの陥凹面が前記同じチャンバー内で複数の陥凹面を含む、請求項2から6のいずれか一項に記載のアッセイ法。
- 前記少なくとも1つの陥凹面が、半球状面と、前記側壁から前記底面へと30から60度のテーパーを有する円錐面、またはそれらの組み合わせを含む、請求項2から7のいずれか一項に記載のアッセイ法。
- 前記側壁面の形状が、垂直円筒であるか、前記チャンバーの頂部から底面へと直径が減少する垂直円錐の一部であるか、前記チャンバーの方形の頂部から陥凹底面への円錐形遷移部を有する垂直方形シャフトであるか、またはそれらの組み合わせである、請求項2に記載のアッセイ法。
- 前記b)の後に一定期間インキュベーション後、前記インサートを前記細胞培養製品から取り出し、単層完全性を検出することをさらに含む、請求項1から9のいずれか一項に記載のアッセイ法。
- 前記治療薬の移動能および腫瘍細胞応答の両方がフローサイトメトリーによって検出される、請求項1から10のいずれか一項に記載のアッセイ法。
- 腫瘍細胞応答の検出が、前記治療薬の前記腫瘍細胞スフェロイドへの浸透を検出することを含む、請求項1から11のいずれか一項に記載のアッセイ法。
- 腫瘍細胞応答の検出が、腫瘍細胞溶解を測定することを含む、請求項1から12のいずれか一項に記載のアッセイ法。
- 前記治療薬が薬物または細胞治療薬を含む、請求項1から13のいずれか一項に記載のアッセイ法。
- 前記治療薬が白血球またはリンパ球を含む、請求項14に記載のアッセイ法。
- 前記治療薬が薬物である、請求項1から14のいずれか一項に記載のアッセイ法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762455881P | 2017-02-07 | 2017-02-07 | |
| US62/455,881 | 2017-02-07 | ||
| PCT/US2018/017081 WO2018148208A1 (en) | 2017-02-07 | 2018-02-06 | A high throughput 3d assay for immune cell and drug homing, migration and tumor cytotoxicity |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020510414A JP2020510414A (ja) | 2020-04-09 |
| JPWO2018148208A5 JPWO2018148208A5 (ja) | 2022-05-27 |
| JP7242536B2 true JP7242536B2 (ja) | 2023-03-20 |
Family
ID=61244768
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019542516A Active JP7242536B2 (ja) | 2017-02-07 | 2018-02-06 | 免疫細胞および薬物ホーミング、移動ならびに腫瘍細胞毒性についての高スループット3dアッセイ |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US10859565B2 (ja) |
| EP (1) | EP3580333B1 (ja) |
| JP (1) | JP7242536B2 (ja) |
| CN (1) | CN110312791A (ja) |
| CA (1) | CA3052970A1 (ja) |
| PL (1) | PL3580333T3 (ja) |
| SG (1) | SG11201907277XA (ja) |
| WO (1) | WO2018148208A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022177250A2 (ko) * | 2021-02-16 | 2022-08-25 | 연세대학교 산학협력단 | 고순도의 암 오가노이드, 및 이의 제조방법 |
| US20240269678A1 (en) * | 2021-06-07 | 2024-08-15 | Plexium, Inc. | Transfer dispensers for assay devices with bead size exclusion |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016520307A (ja) | 2013-04-30 | 2016-07-14 | コーニング インコーポレイテッド | スフェロイド細胞培養ウェル製品およびその方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20090094814A (ko) * | 2006-10-10 | 2009-09-08 | 스퀴코어 | 암의 치료 및 진단을 위한 조성물 및 방법 |
| WO2009126524A2 (en) * | 2008-04-08 | 2009-10-15 | Massachusetts Institute Of Technology | Three-dimensional microfluidic platforms and methods of use thereof |
| US8163537B2 (en) * | 2009-01-27 | 2012-04-24 | Corning Incorporated | Nested permeable support device and method for using the nested permeable support device |
| JP6832042B2 (ja) * | 2014-10-29 | 2021-02-24 | コーニング インコーポレイテッド | スフェロイド捕捉用挿入体 |
-
2018
- 2018-02-06 PL PL18706096T patent/PL3580333T3/pl unknown
- 2018-02-06 EP EP18706096.7A patent/EP3580333B1/en active Active
- 2018-02-06 CA CA3052970A patent/CA3052970A1/en not_active Abandoned
- 2018-02-06 CN CN201880010756.0A patent/CN110312791A/zh active Pending
- 2018-02-06 US US15/889,766 patent/US10859565B2/en active Active
- 2018-02-06 JP JP2019542516A patent/JP7242536B2/ja active Active
- 2018-02-06 SG SG11201907277XA patent/SG11201907277XA/en unknown
- 2018-02-06 WO PCT/US2018/017081 patent/WO2018148208A1/en not_active Ceased
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016520307A (ja) | 2013-04-30 | 2016-07-14 | コーニング インコーポレイテッド | スフェロイド細胞培養ウェル製品およびその方法 |
Non-Patent Citations (3)
| Title |
|---|
| Frontiers in Bioengineering and Biotechnology ,Volume 4, Article 12,pp.1-14 |
| MOLECULAR ONCOLOGY 9(2015)44-57 |
| PNAS, Vol. 113, No. 3, pp.710-715 |
Also Published As
| Publication number | Publication date |
|---|---|
| US10859565B2 (en) | 2020-12-08 |
| PL3580333T3 (pl) | 2021-08-02 |
| SG11201907277XA (en) | 2019-09-27 |
| WO2018148208A1 (en) | 2018-08-16 |
| CN110312791A (zh) | 2019-10-08 |
| JP2020510414A (ja) | 2020-04-09 |
| CA3052970A1 (en) | 2018-08-16 |
| US20180224428A1 (en) | 2018-08-09 |
| EP3580333B1 (en) | 2021-04-21 |
| EP3580333A1 (en) | 2019-12-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2138571B1 (en) | Process for the preparation of multicellular spheroids | |
| EP2526978B1 (en) | Device and method of generating in vitro blood vessels | |
| US11555180B2 (en) | Methods and apparatuses for patient-derived micro-organospheres | |
| Rodrigues et al. | Osteosarcoma tumor microenvironment: the key for the successful development of biologically relevant 3D in vitro models | |
| JP5881031B2 (ja) | 薬剤感受性試験用バイオチップ | |
| US20260077355A1 (en) | Vascular flow-based microfluidic platform | |
| Lim et al. | Formation of size-controllable tumour spheroids using a microfluidic pillar array (μFPA) device | |
| Silberman et al. | Modeled vascular microenvironments: immune-endothelial cell interactions in vitro | |
| JP7242536B2 (ja) | 免疫細胞および薬物ホーミング、移動ならびに腫瘍細胞毒性についての高スループット3dアッセイ | |
| Liu et al. | A tumor-on-a-chip for in vitro study of CAR-T cell immunotherapy in solid tumors | |
| US20150377863A1 (en) | Method for Testing the Response of Cells to Exposure with Therapeutics | |
| Adriani et al. | Studying TCR T cell anti-tumor activity in a microfluidic intrahepatic tumor model | |
| Wei et al. | A microfluidic platform culturing two cell lines paralleled under in-vivo like fluidic microenvironment for testing the tumor targeting of nanoparticles | |
| JP2022010049A (ja) | 薬剤耐性を有する細胞を作製する方法、及び抗ガン剤をスクリーニングするための方法 | |
| EP4444863A1 (en) | Method of production of organoids and uses thereof | |
| JPWO2018148208A5 (ja) | ||
| US20250320462A1 (en) | Methods and apparatuses for testing hepatocyte toxicity using microorganospheres | |
| US20260055431A1 (en) | Methods of delivering components to microorganospheres | |
| 風間 et al. | Studies on Cell Dome as a cell culture and | |
| Dey | Reconstituting the 3D Breast Cancer Microenvironment for Chemo and Immunotherapy | |
| Rodrigues | Tumor-on-a-chip for osteosarcoma drug screening: development of the tumor microenvironment compartment | |
| Ali | Engineering a Segregated Co-Culture Microdevice Platform for Studying Tumor Mediated Pro-Angiogenic Endothelial Dysregulations | |
| Carter et al. | A Superhydrophobic 3D Cell Culture System Reveals the Mechanobiological Role of Cancer‐Associated Fibroblasts in Prostate Cancer Metastasis | |
| Geyer | Development of Novel Microfluidic-Based Pancreaticcancer-On-A-Chip Models | |
| WO2025117593A1 (en) | Bioprinted 3d culture scaffolds |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210208 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20211020 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211027 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220127 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20220328 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220803 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20221104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221130 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230208 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230308 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7242536 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |