JP7601376B2 - Crp結合核酸分子、crp検出用センサ、crp検出試薬、crpの検出方法、およびcrp結合領域 - Google Patents
Crp結合核酸分子、crp検出用センサ、crp検出試薬、crpの検出方法、およびcrp結合領域 Download PDFInfo
- Publication number
- JP7601376B2 JP7601376B2 JP2021001681A JP2021001681A JP7601376B2 JP 7601376 B2 JP7601376 B2 JP 7601376B2 JP 2021001681 A JP2021001681 A JP 2021001681A JP 2021001681 A JP2021001681 A JP 2021001681A JP 7601376 B2 JP7601376 B2 JP 7601376B2
- Authority
- JP
- Japan
- Prior art keywords
- crp
- nucleic acid
- acid molecule
- binding
- seq
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 102000039446 nucleic acids Human genes 0.000 title claims description 142
- 108020004707 nucleic acids Proteins 0.000 title claims description 142
- 150000007523 nucleic acids Chemical class 0.000 title claims description 142
- 230000027455 binding Effects 0.000 title claims description 104
- 238000001514 detection method Methods 0.000 title claims description 48
- 239000003153 chemical reaction reagent Substances 0.000 title claims description 15
- 108010074051 C-Reactive Protein Proteins 0.000 claims description 123
- 102100032752 C-reactive protein Human genes 0.000 claims description 123
- 108091033319 polynucleotide Proteins 0.000 claims description 53
- 102000040430 polynucleotide Human genes 0.000 claims description 53
- 239000002157 polynucleotide Substances 0.000 claims description 53
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical class CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 claims description 23
- 238000000034 method Methods 0.000 claims description 21
- 229940113082 thymine Drugs 0.000 claims description 10
- 108091023037 Aptamer Proteins 0.000 description 52
- 125000003729 nucleotide group Chemical group 0.000 description 19
- 239000000126 substance Substances 0.000 description 13
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 12
- 238000002372 labelling Methods 0.000 description 11
- 108020004414 DNA Proteins 0.000 description 10
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical class O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 7
- 239000000178 monomer Substances 0.000 description 7
- 239000002773 nucleotide Substances 0.000 description 7
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 7
- 238000003786 synthesis reaction Methods 0.000 description 7
- 230000015572 biosynthetic process Effects 0.000 description 6
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 6
- 125000002652 ribonucleotide group Chemical group 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- 238000013461 design Methods 0.000 description 5
- 239000000975 dye Substances 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 4
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 4
- 239000007853 buffer solution Substances 0.000 description 4
- 239000000470 constituent Substances 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 3
- 101710163270 Nuclease Proteins 0.000 description 3
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 3
- 238000000605 extraction Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 125000000714 pyrimidinyl group Chemical group 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 108091093037 Peptide nucleic acid Proteins 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 238000007385 chemical modification Methods 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 238000006911 enzymatic reaction Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 2
- 230000003100 immobilizing effect Effects 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000002504 physiological saline solution Substances 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- 238000004451 qualitative analysis Methods 0.000 description 2
- 238000004445 quantitative analysis Methods 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 235000011178 triphosphate Nutrition 0.000 description 2
- 239000001226 triphosphate Substances 0.000 description 2
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- 241001316595 Acris Species 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- OHOQEZWSNFNUSY-UHFFFAOYSA-N Cy3-bifunctional dye zwitterion Chemical compound O=C1CCC(=O)N1OC(=O)CCCCCN1C2=CC=C(S(O)(=O)=O)C=C2C(C)(C)C1=CC=CC(C(C1=CC(=CC=C11)S([O-])(=O)=O)(C)C)=[N+]1CCCCCC(=O)ON1C(=O)CCC1=O OHOQEZWSNFNUSY-UHFFFAOYSA-N 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 108091008102 DNA aptamers Proteins 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000942118 Homo sapiens C-reactive protein Proteins 0.000 description 1
- 101000922020 Homo sapiens Cysteine and glycine-rich protein 1 Proteins 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 125000003275 alpha amino acid group Chemical group 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 102000051143 human CRP Human genes 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- -1 isotopes Substances 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 108700043045 nanoluc Proteins 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 238000001668 nucleic acid synthesis Methods 0.000 description 1
- 210000002381 plasma Anatomy 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 239000001044 red dye Substances 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000001022 rhodamine dye Substances 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- ABZLKHKQJHEPAX-UHFFFAOYSA-N tetramethylrhodamine Chemical compound C=12C=CC(N(C)C)=CC2=[O+]C2=CC(N(C)C)=CC=C2C=1C1=CC=CC=C1C([O-])=O ABZLKHKQJHEPAX-UHFFFAOYSA-N 0.000 description 1
- MPLHNVLQVRSVEE-UHFFFAOYSA-N texas red Chemical compound [O-]S(=O)(=O)C1=CC(S(Cl)(=O)=O)=CC=C1C(C1=CC=2CCCN3CCCC(C=23)=C1O1)=C2C1=C(CCC1)C3=[N+]1CCCC3=C2 MPLHNVLQVRSVEE-UHFFFAOYSA-N 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 108700012359 toxins Proteins 0.000 description 1
- 229910021642 ultra pure water Inorganic materials 0.000 description 1
- 239000012498 ultrapure water Substances 0.000 description 1
- 229940035893 uracil Drugs 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Landscapes
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Description
配列番号3:CCCGGTTACAGATGATCAGGGG
配列番号4:CCGGTTACAGATGATCAGGGGCATTCGA
配列番号5:AGCCCGGTTACAGATGATCAGGGGCATTCGACAGGCT
配列番号6:GTGATAAAAGCCCGGTTACAGATGATCAGGGG
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号8:CGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号9:GTGATAAAAGCCCGGTTACAGATGATCAG
配列番号10:GTGATAAAAGCCCGGTTACAGATGATCAGG
配列番号11:GTGATAAAAGCCCGGTTACAGATGATCAGGG
(a)配列番号2の塩基配列からなるポリヌクレオチド
(b)前記(a)の塩基配列において、1個の塩基が欠失、置換、挿入および/または付加された塩基配列からなり、CRPに結合するポリヌクレオチド
配列番号2:CGGTTACAGATGATCA
前記核酸分子が、前記本発明のCRP結合核酸分子であり、
前記検出工程において、前記試料中のCRPと前記核酸分子とを結合させて、前記結合により、前記試料中のCRPを検出することを特徴とする。
(a)配列番号2の塩基配列からなるポリヌクレオチド
(b)前記(a)の塩基配列において、1個の塩基が欠失、置換、挿入および/または付加された塩基配列からなり、CRPに結合するポリヌクレオチド
配列番号2:CGGTTACAGATGATCA
(1-1)第1のCRP結合核酸分子
本発明の第1のCRP(C反応タンパク質)結合核酸分子は、下記配列番号3~11のいずれかの塩基配列のポリヌクレオチドからなることを特徴とする。
配列番号3:CCCGGTTACAGATGATCAGGGG
配列番号4:CCGGTTACAGATGATCAGGGGCATTCGA
配列番号5:AGCCCGGTTACAGATGATCAGGGGCATTCGACAGGCT
配列番号6:GTGATAAAAGCCCGGTTACAGATGATCAGGGG
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号8:CGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号9:GTGATAAAAGCCCGGTTACAGATGATCAG
配列番号10:GTGATAAAAGCCCGGTTACAGATGATCAGG
配列番号11:GTGATAAAAGCCCGGTTACAGATGATCAGGG
配列番号3:CCCGGTTACAGATGATCAGGGG
配列番号4:CCGGTTACAGATGATCAGGGGCATTCGA
配列番号5:AGCCCGGTTACAGATGATCAGGGGCATTCGACAGGCT
配列番号6:GTGATAAAAGCCCGGTTACAGATGATCAGGGG
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号8:CGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号9:GTGATAAAAGCCCGGTTACAGATGATCAG
配列番号10:GTGATAAAAGCCCGGTTACAGATGATCAGG
配列番号11:GTGATAAAAGCCCGGTTACAGATGATCAGGG
配列番号2:CGGTTACAGATGATCA
配列番号6:GTGATAAAAGCCCGGTTACAGATGATCAGGGG
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号8:CGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号9:GTGATAAAAGCCCGGTTACAGATGATCAG
配列番号10:GTGATAAAAGCCCGGTTACAGATGATCAGG
配列番号11:GTGATAAAAGCCCGGTTACAGATGATCAGGG
本発明の第2のCRP結合核酸分子は、下記(a)または(b)のいずれかのポリヌクレオチドを含むことを特徴とする。
(a)配列番号2の塩基配列からなるポリヌクレオチド
(b)前記(a)の塩基配列において、1個の塩基が欠失、置換、挿入および/または付加された塩基配列からなり、CRPに結合するポリヌクレオチド
配列番号2:CGGTTACAGATGATCA
配列番号2:CGGTTACAGATGATCA
本発明のCRP結合領域は、下記(a)または(b)のいずれかのポリヌクレオチドからなることを特徴とする。
(a)配列番号2~11の塩基配列からなるポリヌクレオチド
(b)前記(a)の塩基配列において、1個の塩基が欠失、置換、挿入および/または付加された塩基配列からなり、CRPに結合するポリヌクレオチド
配列番号2:CGGTTACAGATGATCA
配列番号3:CCCGGTTACAGATGATCAGGGG
配列番号4:CCGGTTACAGATGATCAGGGGCATTCGA
配列番号5:AGCCCGGTTACAGATGATCAGGGGCATTCGACAGGCT
配列番号6:GTGATAAAAGCCCGGTTACAGATGATCAGGGG
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号8:CGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号9:GTGATAAAAGCCCGGTTACAGATGATCAG
配列番号10:GTGATAAAAGCCCGGTTACAGATGATCAGG
配列番号11:GTGATAAAAGCCCGGTTACAGATGATCAGGG
本発明の検出用センサは、前述のように、CRPの検出用センサであって、前記本発明の核酸分子を含むことを特徴とする。本発明の検出用センサは、前記本発明の核酸分子を含んでいればよく、その他の構成は、特に制限されない。本発明の検出用センサを使用すれば、例えば、前記核酸分子と前記CRPとを結合させることで、前述のように、前記CRPを検出できる。
本発明の検出試薬は、前記本発明のCRP結合核酸分子を含むことを特徴とする。本発明の検出試薬は、前記本発明の核酸分子を含んでいればよく、その他の構成は何ら制限されない。本発明の検出試薬を使用すれば、前述のように、例えば、前記CRPの検出等を行うことができる。
本発明の検出方法は、前述のように、試料と核酸分子とを接触させ、前記試料中のCRPを検出する工程を含み、前記核酸分子が、前記本発明のCRP結合核酸分子であり、前記検出工程において、前記試料中のCRPと前記核酸分子とを結合させて、前記結合により、前記試料中のCRPを検出することを特徴とする。本発明の検出方法は、前記本発明の核酸分子を使用することが特徴であって、その他の工程および条件等は、特に制限されない。また、本発明の検出方法は、前記本発明の核酸分子として、前記本発明のCRP検出用センサを使用してもよい。
候補アプタマーとして、CRPに対する結合性を有するアプタマーを用い、前記候補アプタマーの構造の推定、小型化アプタマー配列の設計、前記小型化アプタマーの構造の推定、スコア算出、及び、前記スコアが予め定めた値以上である小型化アプタマー配列の抽出を行った。
候補アプタマーとして、CRPに対する結合性を有するアプタマーを用いた(配列番号1)。前記配列番号1のポリヌクレオチドを以下に示す。
GGTTACGCCGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGCATTCGACAGGCTGGACATATC
配列番号1において、推定結合領域(配列番号2)に、下線を付している。前記推定結合領域は、FSBC(fast string-based clustering)により、文献(Kato S, Ono T, Minagawa H, Horii K, Shiratori I, Waga I, et al. FSBC: fast string-based clustering for HT-SELEX data. BMC Bioinformatics. 2020 Jun 24;21(1):263.)に記載の手法に従って推定を行った。前記推定結合領域は、モチーフ配列ともいうことができる。
CGGTTACAGATGATCA
参考文献1:Lorenz R, Bernhart SH, Hoener Zu Siederdissen C, Tafer H, Flamm C, Stadler PF, et al. ViennaRNA Package 2.0. Algorithms Mol Biol. 2011 Nov 24;6:26.
参考文献2:D.H. Mathews, M.D. Disney, D. Matthew, J.L. Childs, S.J. Schroeder, J. Susan, M. Zuker, D.H. Turner (2004), "Incorporating chemical modification constraints into a dynamic programming algorithm for prediction of RNA secondary structure", Proc. Natl. Acad. Sci. USA: 101, pp 7287-7292
参考文献3:D.H Turner, D.H. Mathews (2009), "NNDB: The nearest neighbor parameter database for predicting stability of nucleic acid secondary structure", Nucleic Acids Research: 38, pp 280-282
前記式(1)において、各記号等の意味は、以下の通りである。
M:状態
Ei:状態iの時のエネルギー
k:ボルツマン定数
T:絶対温度
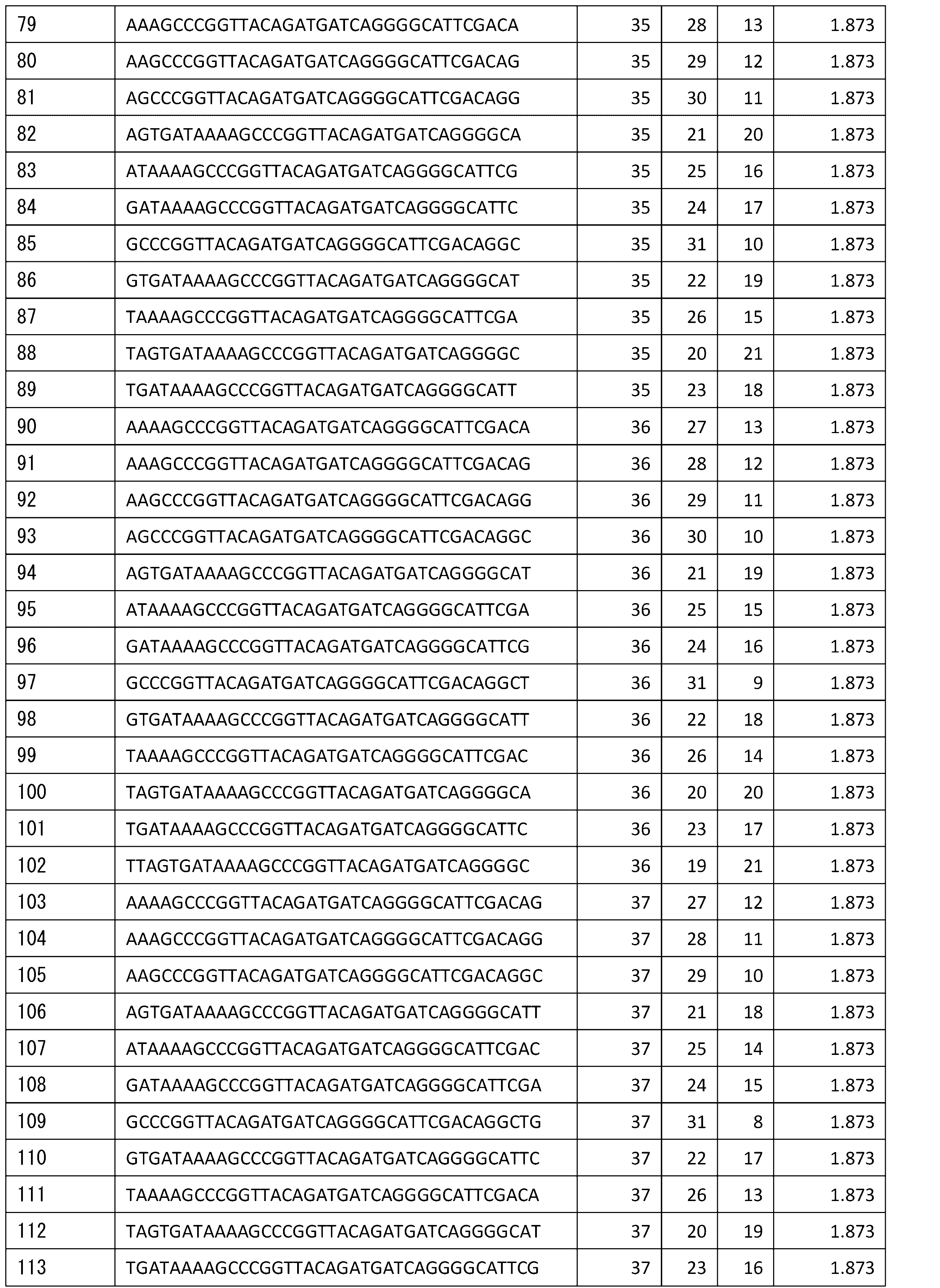
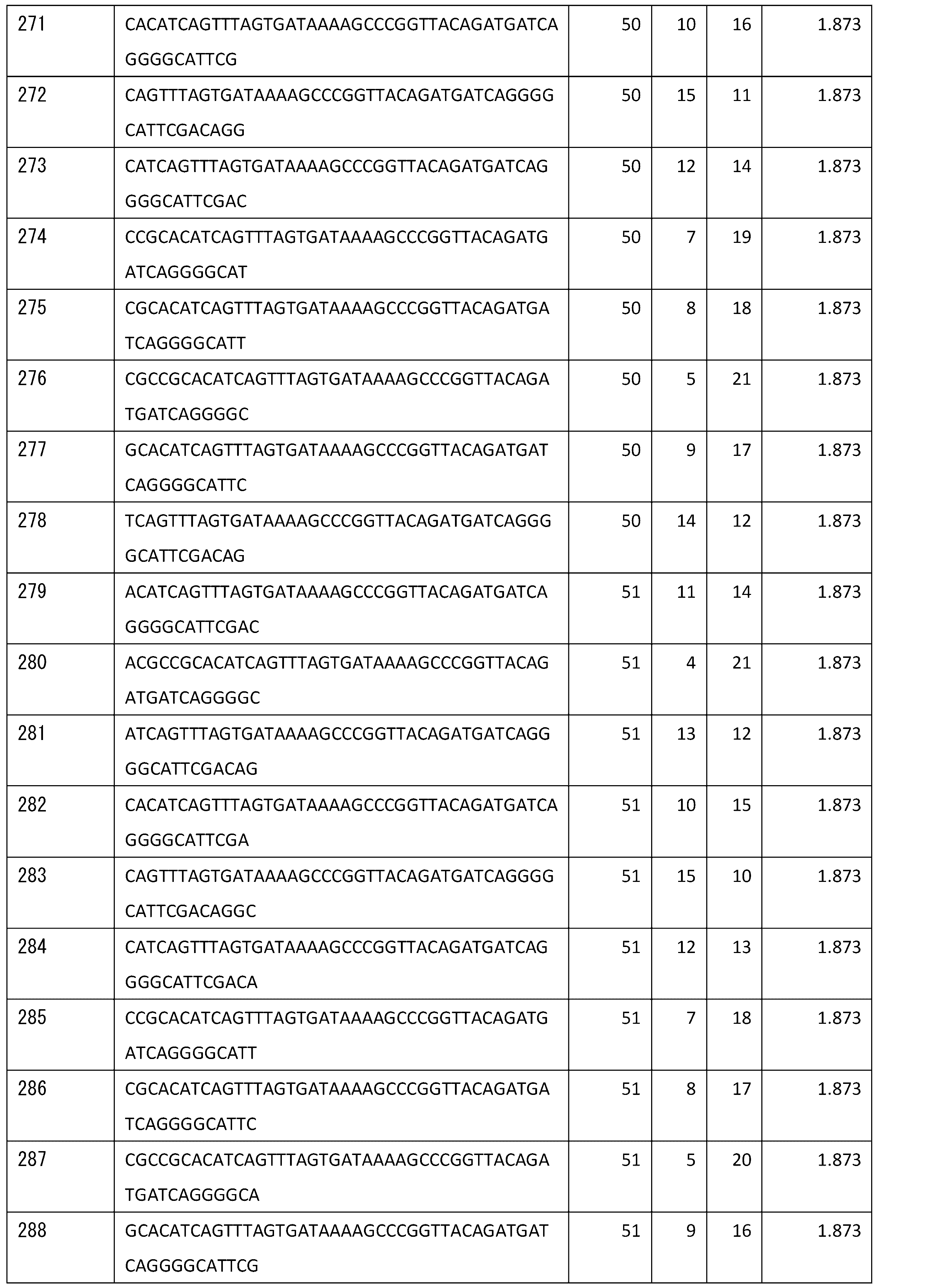
つぎに、推定結合領域がとり得る各々の二次構造に対して,小型化配列を設計した。以下の説明において、前記候補アプタマーの5’末端からm塩基、3’末端からn塩基削除した小型化配列を、S(m,n)と示す。本明細書及び図面において、「S(m,n)」、並びに、m及びnの値の組合せの記載により、これらに対応する配列が一意に定まり、開示される。
前記小型化配列(S(m,n))のそれぞれについて、前述と同様にして、モチーフ構造1~5の存在確率を算出した。
前記算出した、前記小型化配列(S(m,n))におけるモチーフ構造1~5の前記存在確率を、前記候補アプタマーにおけるモチーフ構造1~5の前記存在確率でそれぞれ除算することにより、これらの比(存在確率の相対値)を求めた。前記比を、モチーフ構造1~5ごとのスコアである、スコア1とした。
さらに、前記小型化配列(S(m,n))の中から、前記スコアが所定値以上である小型化アプタマー配列を抽出した。
S(m,n):5’末端からm塩基,3’末端からn塩基削除した小型化配列
S : アプタマー全長配列
Pr(u, S(m,n)) : 小型化配列S(m,n)の時の,推定結合領域がuの時の存在確率
Pr(u, S) : 全長配列Sの時の,推定結合領域がuの時の存在確率
u : 全長配列Sにおいて,推定結合領域がとりうる構造
R(u, S(m,n),S) : 二次構造uの小型化配列S(m,n)での存在確率と全長配列Sでの存在確率の相対値
一次ノルム|・|は文字列の長さを示す。
Ωs : 推定結合領域が全長配列においてとり得る二次構造の集合
実施例1で抽出した小型化アプタマーについて、CRPに対する結合評価を行った。
小型化配列として、下記表5に示すポリヌクレオチド(小型化配列1~6)を合成した。小型化配列1~6の合成において、下記表5の下線で示すチミンを含むヌクレオチド残基を、前記式(1)に示すヌクレオチド残基(KS9)とした。小型化配列1は、実施例1で抽出した小型化配列(S(32,22);配列番号3)に基づき、酵素法による合成を行うため、最も3’側のチミンから左に15塩基をプライマー領域とした配列(S(22,22);配列番号6)とした。小型化配列2は、小型化配列1よりも1塩基長い配列(S(22,21);配列番号7)であり、小型化配列3は、小型化配列1よりも15塩基長い配列(S(8,21);配列番号8)である。また、小型化配列4~6は、それぞれ、小型化配列1よりも1~3塩基短い配列である。
小型化配列1~6について、SPRによる結合性の解析を行った。
Claims (8)
- 下記配列番号7または8の塩基配列のポリヌクレオチドからなることを特徴とする、CRP(C反応タンパク質)結合核酸分子。
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号8:CGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGC - 下記配列番号7の塩基配列のポリヌクレオチドを含むことを特徴とする、CRP結合核酸分子。
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC - 前記結合核酸分子が、塩基が修飾基で修飾された修飾塩基を含む、請求項1または2記載のCRP結合核酸分子。
- 前記修飾塩基が、チミン塩基が修飾基で修飾された修飾チミン塩基である、請求項3記載のCRP結合核酸分子。
- 請求項1から4のいずれか一項に記載のCRP結合核酸分子を含むことを特徴とする、CRP検出用センサ。
- 請求項1から4のいずれか一項に記載のCRP結合核酸分子を含むことを特徴とする、CRP検出試薬。
- 試料と核酸分子とを接触させ、前記試料中のCRPを検出する工程を含み、
前記核酸分子が、請求項1から4のいずれか一項に記載のCRP結合核酸分子であり、
前記検出工程において、前記試料中のCRPと前記核酸分子とを結合させて、前記結合により、前記試料中のCRPを検出することを特徴とする、CRPの検出方法。 - 下記配列番号7または8の塩基配列のポリヌクレオチドからなることを特徴とする、CRP結合領域。
配列番号7:GTGATAAAAGCCCGGTTACAGATGATCAGGGGC
配列番号8:CGCACATCAGTTTAGTGATAAAAGCCCGGTTACAGATGATCAGGGGC
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021001681A JP7601376B2 (ja) | 2021-01-07 | 2021-01-07 | Crp結合核酸分子、crp検出用センサ、crp検出試薬、crpの検出方法、およびcrp結合領域 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021001681A JP7601376B2 (ja) | 2021-01-07 | 2021-01-07 | Crp結合核酸分子、crp検出用センサ、crp検出試薬、crpの検出方法、およびcrp結合領域 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022106581A JP2022106581A (ja) | 2022-07-20 |
| JP7601376B2 true JP7601376B2 (ja) | 2024-12-17 |
Family
ID=82457121
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021001681A Active JP7601376B2 (ja) | 2021-01-07 | 2021-01-07 | Crp結合核酸分子、crp検出用センサ、crp検出試薬、crpの検出方法、およびcrp結合領域 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7601376B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN119530235A (zh) * | 2024-12-05 | 2025-02-28 | 浙江工业大学 | 识别c反应蛋白的核酸适体及其应用和含有其的产品 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010158238A (ja) | 2008-12-09 | 2010-07-22 | Tokyo Univ Of Agriculture & Technology | C反応性タンパク質結合性アプタマー及びその用途 |
| WO2018052063A1 (ja) | 2016-09-15 | 2018-03-22 | Necソリューションイノベータ株式会社 | ヌクレオシド誘導体またはその塩、ポリヌクレオチドの合成試薬、ポリヌクレオチドの製造方法、ポリヌクレオチド、および結合核酸分子の製造方法 |
-
2021
- 2021-01-07 JP JP2021001681A patent/JP7601376B2/ja active Active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010158238A (ja) | 2008-12-09 | 2010-07-22 | Tokyo Univ Of Agriculture & Technology | C反応性タンパク質結合性アプタマー及びその用途 |
| WO2018052063A1 (ja) | 2016-09-15 | 2018-03-22 | Necソリューションイノベータ株式会社 | ヌクレオシド誘導体またはその塩、ポリヌクレオチドの合成試薬、ポリヌクレオチドの製造方法、ポリヌクレオチド、および結合核酸分子の製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022106581A (ja) | 2022-07-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9404919B2 (en) | Multiplexed analyses of test samples | |
| ES2604764T3 (es) | Análisis de muestras de ensayo | |
| US7855054B2 (en) | Multiplexed analyses of test samples | |
| US6515120B1 (en) | Method for sequencing and characterizing polymeric biomolecules using aptamers and a method for producing aptamers | |
| US8785132B2 (en) | Aptamer sandwich assays | |
| JP5596903B2 (ja) | インスリン結合性アプタマー | |
| JP2015529076A (ja) | 鎖置換交換反応を使用する非核酸分析物の検出 | |
| CN1419606A (zh) | 将分子识别转导成不同信号的信号适体 | |
| JP2012198225A (ja) | 標的分子の検出法 | |
| US20220243196A1 (en) | Screening method of aptamer and immunoassay using the aptamer | |
| US20200340042A1 (en) | In vitro selection for nucleic acid aptamers | |
| CN107760686B (zh) | Dkk-1蛋白的核酸适配体及其应用 | |
| US10760084B2 (en) | α-amylase-binding nucleic acid molecule and use thereof | |
| US20140303015A1 (en) | Molecular Constructs for Differentiating a Target Molecule from an Off-Target Molecule | |
| JP7601376B2 (ja) | Crp結合核酸分子、crp検出用センサ、crp検出試薬、crpの検出方法、およびcrp結合領域 | |
| US20040197779A1 (en) | Methods for analyzing mixtures of proteins | |
| CN117487813B (zh) | 特异性识别阿奇霉素的单链dna适配体序列及其应用 | |
| JP5783590B2 (ja) | チログロブリン結合性アプタマー及びアプタマー多量体の作製方法 | |
| JP7405400B2 (ja) | 核酸分子およびその用途 | |
| JP7609468B2 (ja) | SARS-CoV-2スパイク糖タンパク質結合核酸分子、SARS-CoV-2検出用センサ、SARS-CoV-2検出試薬、SARS-CoV-2の検出方法、およびSARS-CoV-2ウイルスの不活性化剤 | |
| US20260022495A1 (en) | Aptamer discovery and selection techniques | |
| KR20210004884A (ko) | 중증열성혈소판감소증후군 바이러스에 특이적으로 결합하는 dna 압타머 및 압타머를 이용한 면역 분석 방법 | |
| JP6963221B2 (ja) | 核酸分子およびその用途 | |
| KR102691401B1 (ko) | 매 라운드 dna 풀의 ngs 분석 및 프라이머 영역 가림 방식을 통한 앱타머 스크리닝 방법 | |
| JP2019149979A (ja) | 分泌型免疫グロブリンA(sIgA)結合核酸分子、sIgA検出用センサ、sIgA検出試薬、およびsIgAの分析方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20220630 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231214 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240925 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241001 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241016 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241105 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241128 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7601376 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |