KR20140077658A - Chewable tablet comprising a phosphodiesterase-5 inhibitor - Google Patents
Chewable tablet comprising a phosphodiesterase-5 inhibitor Download PDFInfo
- Publication number
- KR20140077658A KR20140077658A KR1020120146705A KR20120146705A KR20140077658A KR 20140077658 A KR20140077658 A KR 20140077658A KR 1020120146705 A KR1020120146705 A KR 1020120146705A KR 20120146705 A KR20120146705 A KR 20120146705A KR 20140077658 A KR20140077658 A KR 20140077658A
- Authority
- KR
- South Korea
- Prior art keywords
- disintegrant
- subject
- inhibitor
- disintegration
- crospovidone
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
- A61K9/0058—Chewing gums
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2027—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Zoology (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
본 발명은 포스포다이에스터라제-5 (phosphodiesterase-5, PDE-5) 억제제, 및 팽창계수가 4 내지 8 L/kg인 붕해제를 포함하는 츄정에 관한 것으로, 본 발명의 츄정은 물 없이 복용가능하고 구강 내 잔류감이 남지 않아 환자의 복약순응도 및 복약만족도를 높일 수 있으며 구강 내 용해성이 우수하여 약효를 신속히 발현시킬 수 있으므로 남성의 발기부전 치료제제로서 유용하다.The present invention relates to a quinquer comprising a phosphodiesterase-5 (PDE-5) inhibitor and a disintegrant having an expansion coefficient of from 4 to 8 L / kg, And it is useful as a therapeutic agent for erectile dysfunction in men because it is possible to increase the patient's compliance with medication and satisfaction of medication,
Description
본 발명은 포스포다이에스터라제-5 (Phosphodiesterase-5, PDE-5) 억제제 또는 이의 약학적으로 허용 가능한 염; 및 팽창계수를 조절한 붕해제를 포함하는 츄정에 관한 것이다.
The present invention relates to a phosphodiesterase-5 (PDE-5) inhibitor or a pharmaceutically acceptable salt thereof; And a disintegration in which the expansion coefficient is adjusted.
발기부전이란 여러 가지 원인에 의해 남성의 음경 해면체로의 혈류의 공급이 원활하지 않거나 혈류가 공급이 되더라도 해면체에서 차단이 되지 않고 정맥으로 유출됨으로 인해 해면체 내압이 상승하지 않아 발기가 일정시간이 유지되지 않은 상태이며, 이 때 남녀 모두가 만족스러울 정도의 성생활을 하지 못하는 경우가 전체 성생활 중 25% 이상일 경우를 말한다. 발기부전은 모든 연령층에서 일어날 수 있는 흔한 질병이며, 특히 55세 이상의 연령에서 대체적으로 많이 발생한다. 일반적으로 성인 남성의 5∼10% 정도가 발기부전이 있는 것으로 알려져 있다.Erectile dysfunction is caused by a variety of causes, such as malnutrition of male blood flow to the corpus cavernosum or blood supply to the corpuscle is not blocked by the blood flow to the venous outflow due to the corpuscular pressure is not rising because the erection is maintained for a certain time And it is said that the case where the sex life is not satisfactory enough for both sexes is more than 25% of the total sex life. Erectile dysfunction is a common disease that can occur in all age groups, especially in older people aged 55 years or older. In general, about 5% to 10% of men are known to have impotence.
일반적으로 발기부전 치료제로 알려져 있는 PDE-5 억제제로는 사이클릭 구아노신 3',5'-모노포스페이트 포스포다이에스터라제 5형(cGMP PDE-5)의 선택적 억제제로서 바데나필(Vardenafil, 1-[[3-(1,4-다이하이드로-5-메틸-4-옥소-7-프로필이미다조[5,1-f][1,2,4]트리아진-2-일)-4-에톡시페닐]설포닐]-4-에틸, C23H32N6O4S), 실데나필(Sildenafil, 1-[[3-(6,7-다이하이드로-1-메틸-7-옥소-3-프로필-1H-피라졸로[4,3-d] 피리미딘-5-일)-4-에톡시페닐] 설포닐]-4-메틸피페라진, C22H30N6O4S), 타달라필(Tadalafil, (6R,12aR)-6-(1,3-벤조다이옥솔-5-일)-2,3,6,7,12,12a-헥사하이드로-2-메틸-피라지노[1',2':1,6]피리도[3,4-b]인돌-1,4-다이온, C22H19N3O4), 유데나필(Udenafil, C25H36N6O4S) 등의 약물이 개발되어 있다. 바데나필은 대한민국 특허 제0430355호에, 실데나필은 대한민국 특허 제0262926호에, 타달라필은 대한민국 특허 제0357411호에, 유데나필은 대한민국 특허 제0353014호에 발기부전 치료제로 사용됨이 개시되어 있다.PDE-5 inhibitors, commonly known as erectile dysfunction agents, include Vardenafil, 1- [5-aminopyrimidin-5-yl] Propyl imidazo [5,1-f] [1,2,4] triazin-2-yl) -4-ethoxy-4- ethoxyphenyl] sulfonyl] -4-ethyl, C 23 H 32 N 6 O 4 S), sildenafil (sildenafil, 1 - [[3- (6,7- dihydro-1-methyl-7-oxo-3 profile -1H- pyrazolo [4,3-d] pyrimidin-5-yl) -4-ethoxyphenyl] sulfonyl] -4-methylpiperazine, C 22 H 30 N 6 O 4 S), the other changes Methyl-pyrazino [1 ', 5 ' , 2 ': 1,6] pyrido [3,4-b] indole-1,4-dione, C 22 H 19 N 3 O 4), Udenafil (Udenafil, C 25 H 36 N 6 O 4 S) have been developed. It is disclosed that vardenafil is used in Korean Patent No. 0430355, sildenafil is used in Korean Patent No. 0262926, tadalafil is used in Korean Patent No. 0357411, and Udenapil is used in Korean Patent No. 0353014 as an erectile dysfunction agent.
이들 PDE-5 억제제는 대부분 경구용 정제 형태로 사용되고 있으며, 바데나필은 레비트라라는 상품명으로 바이엘사에서 시판되고 있고 실데나필은 비아그라라는 상품명으로 화이자사에서 시판되고 있으며 타달라필은 시알리스라는 상품명으로 릴리사에서 시판되고 있다. 또한 유데나필은 동아제약사에서 자이데나라는 상품명으로 판매되고 있다. 이들 약물들은 약효발현시간이 약 60분에서 90분이 소요되기 때문에 성관계시 약효발현시간을 염두해 미리 약물을 복용해야 하는 단점이 있다. 또한 일반 정제로 복용 시 물과 함께 복용해야 하는 점으로 인해 야기되는 불편함이 있다. 따라서 물 없이 복용 가능하고 구강 내에서 신속한 흡수가 가능한 PDE-5 억제제 제제의 개발이 절실히 요구되고 있다.These PDE-5 inhibitors are mostly used in the form of oral tablets, and vardenafil is marketed by Bayer under the name Levitra, sildenafil is marketed under the name Viagra by Pfizer, and tadalafil is marketed by Lilly And is commercially available. Yudenapil is also sold under the brand name Zydena in Dong-A Pharm. Because these drugs take about 60 to 90 minutes to express the drug, they have to take drugs in advance in consideration of the efficacy of the drug during sexual intercourse. In addition, there are inconveniences caused by the fact that they should be taken with water when they are used in general tablets. Therefore, there is a desperate need for the development of a PDE-5 inhibitor formulation that can be taken without water and capable of rapid absorption in the oral cavity.
또한 남성의 발기부전 치료제로 쓰이는 PDE-5 억제제류는 환자의 삶의 질을 높여주는 약물, 이른바 해피드럭으로 불리는 약으로서 약물의 효능은 물론이고 복약편의성 및 복약만족감 등의 요소들도 제제 개발 시 중요하게 고려되어야 한다. 기존의 구강붕해정이나 츄정 등은 구강 내 붕해는 빠르나, 복용 후 구강 내에 모래가 남는 느낌의 이물감을 완전히 해결하기는 어려웠다.In addition, the PDE-5 inhibitor used as a treatment for erectile dysfunction in men is a drug called "Happy Drug" which improves the quality of life of the patient. It also includes factors such as drug efficacy, convenience of medication and satisfaction with medication. It should be considered important. Conventional oral disintegration and quinqueride disintegration in the oral cavity is fast, but it is difficult to completely solve the impression of feeling that the sand remains in the oral cavity after taking it.
이에, 본 발명자들은 PDE-5 억제제 제제의 복약순응도를 향상시키고 복약만족감을 높이며, 물 없이 복용가능하고 복용 후에도 구강 내 잔류감이 남지 않으며 신속하게 붕해되어 약효의 발현이 빠른 츄정을 개발하고자 연구를 수행하였다.
Accordingly, the present inventors have conducted research to develop a PDE-5 inhibitor formulation that improves compliance with medicines, increases medication satisfaction, can be taken without water, and has a quick disintegration after oral administration, Respectively.
[특허문헌 1] 대한민국 특허 제0430355호[Patent Document 1] Korean Patent No. 0430355
[특허문헌 2] 대한민국 특허 제0262926호[Patent Document 2] Korean Patent No. 0262926
[특허문헌 3] 대한민국 특허 제0357411호[Patent Document 3] Korean Patent No. 0357411
[특허문헌 4] 대한민국 특허 제0353014호
[Patent Document 4] Korean Patent No. 0353014
따라서, 본 발명의 목적은 구강 내 잔류감이 없고 구강 내에서 신속하게 붕해되어 간편하게 복용할 수 있는, PDE-5 억제제 함유 츄정을 제공하는 것이다.
Accordingly, an object of the present invention is to provide a PDE-5 inhibitor-containing toothpaste which can be easily disintegrated in the oral cavity without remaining in the mouth.
상기 목적을 달성하기 위하여, 본 발명은 PDE-5 억제제 또는 이의 약학적으로 허용 가능한 염; 및 팽창계수가 4 내지 8 L/kg인 붕해제를 포함하는 츄정을 제공한다.In order to achieve the above object, the present invention provides a pharmaceutical composition comprising a PDE-5 inhibitor or a pharmaceutically acceptable salt thereof; And a disintegration with an expansion coefficient of 4 to 8 L / kg.
또한, 본 발명은 상기 츄정에 당류, 당알콜류 또는 이들의 혼합물을 더 포함하는 츄정을 제공한다.
Further, the present invention provides a quartz crystal further comprising saccharides, sugar alcohols or a mixture thereof in the quartz crystal.
본 발명에 따른 PDE-5 억제제를 함유하는 츄정은 물 없이 복용가능하고 구강 내 잔류감이 남지 않아 환자의 복약순응도 및 복약만족도를 높일 수 있으며, 구강 내 용해성이 우수하여 약효를 신속히 발현시킬 수 있으므로 남성의 발기부전 치료제제로서 유용하다.
The chew containing the PDE-5 inhibitor according to the present invention can be taken without water and does not leave a residue in the oral cavity, thereby improving the patient's compliance with medication compliance and medicinal satisfaction, and having excellent oral solubility, It is useful as a remedy for male erectile dysfunction.
본 발명의 츄정은 유효성분으로 PDE-5 억제제 또는 이의 약학적으로 허용가능한 염을 팽창계수를 조절한 붕해제와 함께 포함함으로써 구강 내에서 신속하게 붕해되면서도 구강 내 잔류감을 남기지 않아 복약만족도가 높고 약효의 발현이 빠른 장점이 있다.The chewing tablet of the present invention contains PDE-5 inhibitor or a pharmaceutically acceptable salt thereof as an active ingredient together with a disintegrant with controlled expansion coefficient, thereby rapidly disintegrating in the oral cavity, The expression of the gene is rapidly promoted.
본 발명의 츄정의 유효성분으로는 PDE-5 억제제인 바데나필, 실데나필, 타달라필, 유데나필 또는 이들의 약학적으로 허용가능한 염을 사용할 수 있으며, 바람직하게는 실데나필 유리 염기를 사용할 수 있다.The active ingredient of the present invention may be PDE-5 inhibitors vardenafil, sildenafil, tadalafil, idenapil or pharmaceutically acceptable salts thereof, preferably sildenafil free base.
PDE-5 억제제 또는 이의 약학적으로 허용가능한 염은 정제당 5 내지 100 ㎎의 양으로 함유될 수 있고, 제제의 총 중량을 기준으로 0.1 내지 80 중량%, 바람직하게는 1 내지 70 중량%로 함유되는 것이 좋다.The PDE-5 inhibitor or pharmaceutically acceptable salt thereof may be contained in an amount of 5 to 100 mg per tablet and may be contained in an amount of 0.1 to 80% by weight, preferably 1 to 70% by weight, based on the total weight of the preparation It is good.
상기 붕해제는 본 발명에 따른 츄정을 빠르게 붕해시키기 위한 중요한 성분으로서, 제제의 총 중량을 기준으로 1.5 내지 15 중량%로 함유되는 것이 좋다. 만일 상기 붕해제의 함량이 15 중량%를 초과하면 타정성이 저하되어 제제의 형태를 유지할 수 없는 문제가 있으며, 1.5 중량% 미만이면 붕해제로서의 역할을 충분히 하지 못하여 정제의 붕해가 느려질 수 있다.The disintegrant is an important component for the rapid disintegration of the quench according to the present invention, and it is preferably contained in an amount of 1.5 to 15% by weight based on the total weight of the preparation. If the content of the disintegrant exceeds 15% by weight, the tabletability may deteriorate and the form of the preparation may not be maintained. If the content of the disintegrant is less than 1.5% by weight, the disintegration of the tablets may be delayed.
붕해제가 정제를 붕해시키는 원리에는 크게 세 가지가 있다: 첫 번째, 정제가 타액과 같은 액체에 노출되게 될 때 붕해제가 급격히 팽창하면서 정제를 붕해시키는 것으로, 이러한 유형의 부형제로는 크로스카르복시메틸셀룰로오스나트륨, 전분글리콜산나트륨, 전호화전분 등을 예시할 수 있다; 두 번째, 정제가 타액과 같은 액체에 노출되게 될 때 붕해제의 모세관 작용으로 수분을 정제 안으로 유입시킴으로써 정제를 붕해시키는 것으로, 이러한 유형의 부형제로는 옥수수전분, 알긴산나트륨 등을 예시할 수 있다; 세 번째, 정제가 타액과 같은 액체에 노출되게 될 때 붕해제가 압축 이전의 형태로 급격히 돌아감으로써 정제를 붕해시키는 것으로, 이러한 유형의 부형제로는 크로스포비돈, 전분그레인(starch grain) 등을 예시할 수 있다(John C. Carter, The role of disintegrants in solid oral dosage manufacturing, Carter Pharmaceutical Consulting, Inc). Disintegration disintegrates tablets in three major ways: first, when the tablet is exposed to a liquid such as saliva, the disintegrant expands rapidly to disintegrate the tablet, and this type of excipient may be croscarmellose Cellulose sodium, starch glycolic acid sodium, pregelatinized starch, and the like; Secondly, when the tablet is exposed to a liquid such as saliva, the tablet is disintegrated by introducing moisture into the tablet by the capillary action of the disintegrant. Examples of this type of excipient include corn starch, sodium alginate and the like; Third, when the tablet is exposed to a liquid such as saliva, the disintegrant disintegrates by rapidly returning to its pre-compression form. Examples of this type of excipient include crospovidone, starch grain, etc. (John C. Carter, The role of disintegrants in solid oral dosage manufacturing, Carter Pharmaceutical Consulting, Inc.).
상기 붕해제들은 보통 수불용성이기 때문에 츄정을 입안에서 씹어 복용할 때 붕해제는 녹지 않고 남아 입안 잔류감의 주된 원인이 된다. 따라서 붕해제의 입경 및 팽창계수는 츄정의 입안 잔류감을 결정하는데 대단히 중요한 요소이다. 붕해제의 입경이 클수록 입안 잔류감이 커지며, 붕해제의 팽창계수가 클수록 복용시 입경이 팽창되는 정도가 크므로 입안 잔류감이 커진다. 하지만 팽창계수가 너무 작을 경우 붕해제 본연의 기능을 못하게 되므로 오히려 큰 입자가 입안에 남아 입안 잔류감이 커지게 된다. 적절한 범위의 입경과 팽창계수를 가진 붕해제를 사용할 때 훌륭한 붕해력과 동시에 작은 입안 잔류감을 가지는 츄정을 제조할 수 있다.Since the disintegrants are usually water-insoluble, when disintegrating by mouth, the disintegrant does not melt and remains the main cause of residual perspiration in the mouth. Therefore, the particle diameter and the expansion coefficient of the disintegrant are very important factors for determining the restitution of the mouth. The greater the particle size of the disintegrant, the larger the feeling of mouth retention. The larger the expansion coefficient of the disintegrant, the greater the degree of swelling of the particle upon administration. However, if the expansion coefficient is too small, the disintegrating function will not be achieved, and large particles will remain in the mouth, resulting in a large residual in the mouth. When using a disintegrant having an appropriate range of particle size and expansion coefficient, it is possible to manufacture a quartz having a good disintegration force and a small mouthwash.
본 발명에 사용가능한 붕해제는 팽창계수가 2 내지 12 L/kg일 수 있으며, 4 내지 8 L/kg인 것이 좋다. 또한, 붕해제의 입경은 상기 팽창계수를 고려하여 다양하게 정해질 수 있으며, 예를 들어, 5 내지 250 ㎛의 범위 내에서 선택될 수 있다. The disintegrant which can be used in the present invention may have an expansion coefficient of from 2 to 12 L / kg and preferably from 4 to 8 L / kg. Further, the particle size of the disintegrant can be variously determined in consideration of the expansion coefficient, and can be selected within a range of, for example, 5 to 250 탆.
본 발명의 하나의 실시양태에 따라, 예시적으로 다음과 같이 상기 범위 내의 팽창계수를 갖는 붕해제들이 사용될 수 있다: 크로스포비돈 (Polyplasdone XL-10) 5.4 L/kg, 크로스포비돈 (Polypladone XL) 5.8 L/kg, 크로스포비돈 (Kollidon CL) 4.3 L/kg, 크로스포비돈 (Kollidon CL-M) 7.2 L/kg, 크로스카르복시메틸셀룰로오스나트륨 (Ac-Di-Sol) 13.5 L/kg, 옥수수전분 (StarCap 1500) 1.8 L/kg.According to one embodiment of the present invention, disintegrants having a coefficient of expansion within the above range can be used, illustratively, as follows: Polyplasdone XL-10 5.4 L / kg, Polypladone XL 5.8 (Kollidon CL) 4.3 L / kg, Crospovidone (Kollidon CL-M) 7.2 L / kg, Ac-Di-Sol 13.5 L / kg, StarCap 1500 ) 1.8 L / kg.
본 발명에 사용가능한 붕해제는 상기 붕해제에 한정되는 것은 아니며, 적절한 입경 및 팽창계수를 갖는 붕해제는 어느 것이나 사용될 수 있다. The disintegrant usable in the present invention is not limited to the disintegrant, and any disintegrant having an appropriate particle diameter and expansion coefficient may be used.
본 발명의 츄정은 당류, 당알콜류 또는 이들의 혼합물을 더 포함할 수 있다. 상기 당류, 당알콜류 또는 이들의 혼합물은 츄정의 구강 내에서의 단맛, 용해성 및 촉감 등에 영향을 주는 중요한 성분으로, 이러한 효과를 나타내기 위해서는 단맛과 수용해성이 좋아야 한다. 사용가능한 당류로는 유당, 글루코오스, 수크로오스, 과당, 레불로오스, 말토덱스트린, 파라티노오스 등이 있고, 당알콜류로는 만니톨, 솔비톨, 자일리톨, 에리스리톨 등이 있다. 특히, 상기 당류 또는 당알콜류는 분무건조 등에 의해 다공화된 것을 사용하는 것이 구강 내에서의 용해성을 증가시킬 수 있으므로 바람직하다. 본 발명의 하나의 실시양태에 따라 분무건조 만니톨(Mannitol SD200)을 사용할 수 있다. 상기 당류, 당알콜류 또는 이들의 혼합물은 제제의 총 중량을 기준으로 10 내지 98 중량%, 바람직하게는 20 내지 95 중량%로 함유되는 것이 좋다. 상기 당류, 당알콜류 또는 이들의 혼합물의 함량이 10 중량% 미만이면, 츄정의 단맛과 구강 내 촉감이 좋지 못한 문제가 있다.
The chewing gum of the present invention may further comprise saccharides, sugar alcohols or a mixture thereof. These saccharides, sugar alcohols, or their mixtures are important ingredients that affect the sweetness, solubility, and tactile properties in the oral cavity of Cheongju. In order to exhibit such effects, sweetness and water solubility should be good. Usable saccharides include lactose, glucose, sucrose, fructose, levulose, maltodextrin and parathinose, and sugar alcohols include mannitol, sorbitol, xylitol, and erythritol. Particularly, it is preferable to use the above-mentioned saccharides or sugar alcohols which have been multiply repelled by spray drying or the like because they can increase the solubility in the oral cavity. Spray-dried mannitol (Mannitol SD200) may be used according to one embodiment of the present invention. The saccharides, sugar alcohols or their mixture may be contained in an amount of 10 to 98% by weight, preferably 20 to 95% by weight, based on the total weight of the preparation. If the content of the above-mentioned saccharides, sugar alcohols, or a mixture thereof is less than 10% by weight, there is a problem that the sweetness of the sweet taste and the feeling in the oral cavity are poor.
상기 성분들 외에도 본 발명의 조성물은 약제학적으로 허용 가능한 첨가제로서 예를 들어 착향제, 착색제, 감미제 및 활택제로 이루어진 군으로부터 선택되는 어느 하나 이상을 추가로 포함할 수 있다.In addition to the above components, the composition of the present invention may further comprise at least one selected from the group consisting of pharmaceutically acceptable additives such as flavorings, colorants, sweeteners and glidants.
상기 착향제는 츄정 복용 시에 향을 나타내는 첨가제로서 구강 내 느낌 및 맛을 개선시키는 기능이 있으며, 구체적인 예로는 페퍼민트 향, 스피아민트 향, 각종 과일 향 등을 들 수 있다.The flavoring agent is a flavor-enhancing additive which has the function of improving the sensation and taste in the oral cavity. Specific examples thereof include peppermint flavor, spearmint flavor, various fruit flavor and the like.
상기 착색제는 츄정의 색감을 향상시키기 위한 첨가제로서 녹색 3호, 적색 2호, 적색 3호, 청색 1호, 청색 2호, 황색 4호, 황색 5호, 캐러멜, 산화티타늄, 산화제이철, 기타 천연 색소 등이 사용될 수 있다.The coloring agent is selected from the group consisting of green 3, red 2, red 3, blue 1, blue 2, yellow 4, yellow 5, caramel, titanium oxide, Coloring matter, etc. may be used.
상기 감미제는 츄정 복용 시에 구강 내에서 단맛을 내며, 촉감을 부드럽게 하여 복약 순응도를 향상시킬 수 있는 기능이 있으며, 구체적인 예로는 스테비오사이드, 자일리톨, 수크랄로오스, 아스파탐, 아세설팜칼륨, 수크로오스, 에리스리톨 및 이들의 혼합물을 들 수 있다.The sweetener has a function of improving the adherence and compliance of medicines by softening the tastes in the oral cavity when taking a quercetin. Specific examples thereof include stevioside, xylitol, sucralose, aspartame, acesulfame potassium, sucrose , Erythritol, and mixtures thereof.
상기 활택제의 구체적인 예로는 스테아린산, 스테아린산칼슘 또는 스테아린산마그네슘과 같은 스테아린산금속염류, 탈크, 콜로이드 실리카, 자당지방산에스테르, 수소 첨가된 식물성 오일, 고융점의 왁스, 글리세릴 지방산 에스테르류, 글리세롤디베헤네이트 및 이들의 혼합물을 들 수 있다.
Specific examples of the lubricant include stearic acid metal salts such as stearic acid, calcium stearate or magnesium stearate, talc, colloidal silica, sucrose fatty acid ester, hydrogenated vegetable oil, high melting point wax, glyceryl fatty acid esters, glycerol dibehenate And mixtures thereof.
본 발명의 츄정은 신속한 구강 내 붕해를 위하여 경도를 조절하는 것이 바람직한데, 2 kp 내지 17 kp 범위의 평균 경도를 나타내는 것이 바람직하다. 예를 들어, 본 발명에 따른 츄정은 평균 경도가 2 내지 15 kp 범위일 수 있으며, 보다 바람직하게는 8 내지 15 kp의 경도를 가질 수 있다. 경도가 2 kp 미만인 경우에는 츄정이 쉽게 깨지게 되어 포장 및 유통의 어려움이 있고, 경도가 17 kp를 초과하는 경우에는 츄정이 구강 내에서 신속하게 붕해되지 못하여 복약 순응도 향상을 기대할 수 없는 단점이 있다.
It is preferred that the chew of the present invention should have a controlled hardness for rapid intraoral disintegration, preferably an average hardness in the range of 2 kp to 17 kp. For example, the chewing gum according to the present invention may have an average hardness in the range of 2 to 15 kp, and more preferably 8 to 15 kp. When the hardness is less than 2 kp, the chewing easily breaks and it is difficult to pack and distribute. When the hardness exceeds 17 kp, the chewing gum can not be disintegrated quickly in the oral cavity, so that the improvement in compliance can not be expected.
이하, 본 발명을 하기 실시예에 의거하여 상세하게 설명하고자 한다. 단, 하기 실시예는 본 발명을 예시하기 위한 것일 뿐 본 발명의 범위가 이에 한정되는 것은 아니다.
Hereinafter, the present invention will be described in detail based on the following examples. However, the following examples are intended to illustrate the present invention, but the scope of the present invention is not limited thereto.
참고예: 붕해제의 팽창계수 측정Reference example: Determination of expansion coefficient of disintegrant
크로스포비돈 (Polyplasdone XL-10, ISP사, 미국), 크로스포비돈 (Polypladone XL, ISP사, 미국), 크로스포비돈 (Kollidon CL, BASF사, 독일), 크로스포비돈 (Kollidon CL-M, BASF사, 독일), 크로스카르복시메틸셀룰로오스나트륨 (Ac-Di-Sol, DFE, 독일), 및 옥수수전분 (StarCap 1500, ROQUETTE, 프랑스)을 각각 10g씩 100mL의 부피플라스크에 담고 물을 채워 넣은 후, 24시간 동안 교반한 후 팽창되는 정도를 측정하였다(Anisul Q. et al., A comparative study of current superdisintegrants, Pharmaceutical technology 2006). 붕해제의 팽창계수는 다음과 같았다: 크로스포비돈 (Polyplasdone XL-10) 5.4L/kg, 크로스포비돈 (Polypladone XL) 5.8L/kg, 크로스포비돈 (Kollidon CL) 4.3L/kg, 크로스포비돈 (Kollidon CL-M) 7.2L/kg, 크로스카르복시메틸셀룰로오스나트륨 (Ac-Di-Sol) 13.5L/kg, 옥수수전분 (StarCap 1500) 1.8L/kg.
(Kollidon CL, BASF, Germany), crospovidone (Kollidon CL-M, BASF, Germany), crospovidone (Polyplasone XL- ), Croscarmellose sodium cellulose (Ac-Di-Sol, DFE, Germany), and corn starch (StarCap 1500, ROQUETTE, France) were placed in a 100 mL volumetric flask in an amount of 10 g each, (Anisul Q. et al., A comparative study of current superdisintegrants, Pharmaceutical technology 2006). The expansion coefficient of the disintegrant was as follows: 5.4 L / kg of Polyplasdone XL-10, 5.8 L / kg of Polypladone XL, 4.3 L / kg of Crospovidone, Kollidon CL -M) 7.2 L / kg, 13.5 L / kg of croscarmokylmethylcellulose sodium (Ac-Di-Sol), 1.8 L / kg of corn starch (StarCap 1500).
실시예 1 및 비교예 1, 2: 붕해제의 종류를 달리한 츄정의 제조EXAMPLE 1 and COMPARATIVE EXAMPLES 1 and 2: Preparation of a specimen having different types of disintegrant
하기 표 1과 같은 조성으로 실데나필 유리염기(동우신테크, 한국), 분무건조 만니톨(ROQUETTE, 프랑스), 크로스포비돈(입경 30 내지 50 ㎛, Polyplasdone XL-10, ISP사, 미국), 효소처리 스테비아(대평, 한국), 박하향 분말(삼정, 한국), 청색2호 알루미늄레이크(보락, 한국) 및 스테아르산마그네슘(NOF, 일본)을 사용하여 실데나필을 유효성분으로 하는 츄정을 제조하였다. 구체적으로, 표 1에 기재된 각 조성물을 혼합한 후 정제기(MRC-45, 세종파마텍, 한국)를 사용하여 약 5 kN의 힘이 가해지도록 타정하여 경도가 약 15 kp인 츄정을 제조하였다.(ROQUETTE, France), crospovidone (particle diameter 30-50 μm, Polyplasdone XL-10, ISP Company, USA), enzyme-treated Stevia (Korea), Blue No.2 Aluminum Lake (Borac, Korea), and Magnesium Stearate (NOF, Japan) were used to prepare quinqueradiene containing sildenafil as an active ingredient. Specifically, each of the compositions shown in Table 1 was mixed, and a quartz having a hardness of about 15 kp was prepared by using a refiner (MRC-45, Sejong Pharmatech, Korea) and tumbling to apply a force of about 5 kN.
또한, 비교예 1 및 2로서, 크로스포비돈 대신 크로스카르복시메틸셀룰로오스나트륨(입경 45 내지 74 ㎛, DFE, 독일) 또는 옥수수전분(입경 74 내지 125 ㎛, ROQUETTE, 프랑스)을 사용하여 동일한 공정으로 츄정을 제조하였다.As Comparative Examples 1 and 2, using croscarmokylmethylcellulose sodium (particle diameter: 45 to 74 mu m, DFE, Germany) or corn starch (particle diameter: 74 to 125 mu m, ROQUETTE, France) instead of crospovidone, .
실시예 1 내지 4: 크로스포비돈의 입경을 달리한 츄정의 제조EXAMPLES 1 to 4: Preparation of chewing gum with different diameters of crospovidone
하기 표 2와 같은 조성으로 실시예 1과 동일한 방법으로 제조하되, 시판되는 크로스포비돈 중에 입경을 달리하여 폴리플라스돈(Polyplasdone) XL(입경 100 내지 130 ㎛, ISP사, 미국), 콜리돈(Kollidon) CL(입경 50 내지 250 ㎛, BASF사, 독일) 및 콜리돈(Kollidon) CL-M(입경 5 내지 15 ㎛, BASF사, 독일)을 사용하여 츄정을 제조하였다.Polyplasdone XL (particle diameter 100 to 130 탆, ISP Company, USA) and cololidone (manufactured by Kollidon Corporation) were prepared in the same manner as in Example 1, ) CL (particle diameter 50 to 250 탆, BASF, Germany) and Kollidon CL-M (particle diameter 5 to 15 탆, BASF, Germany).
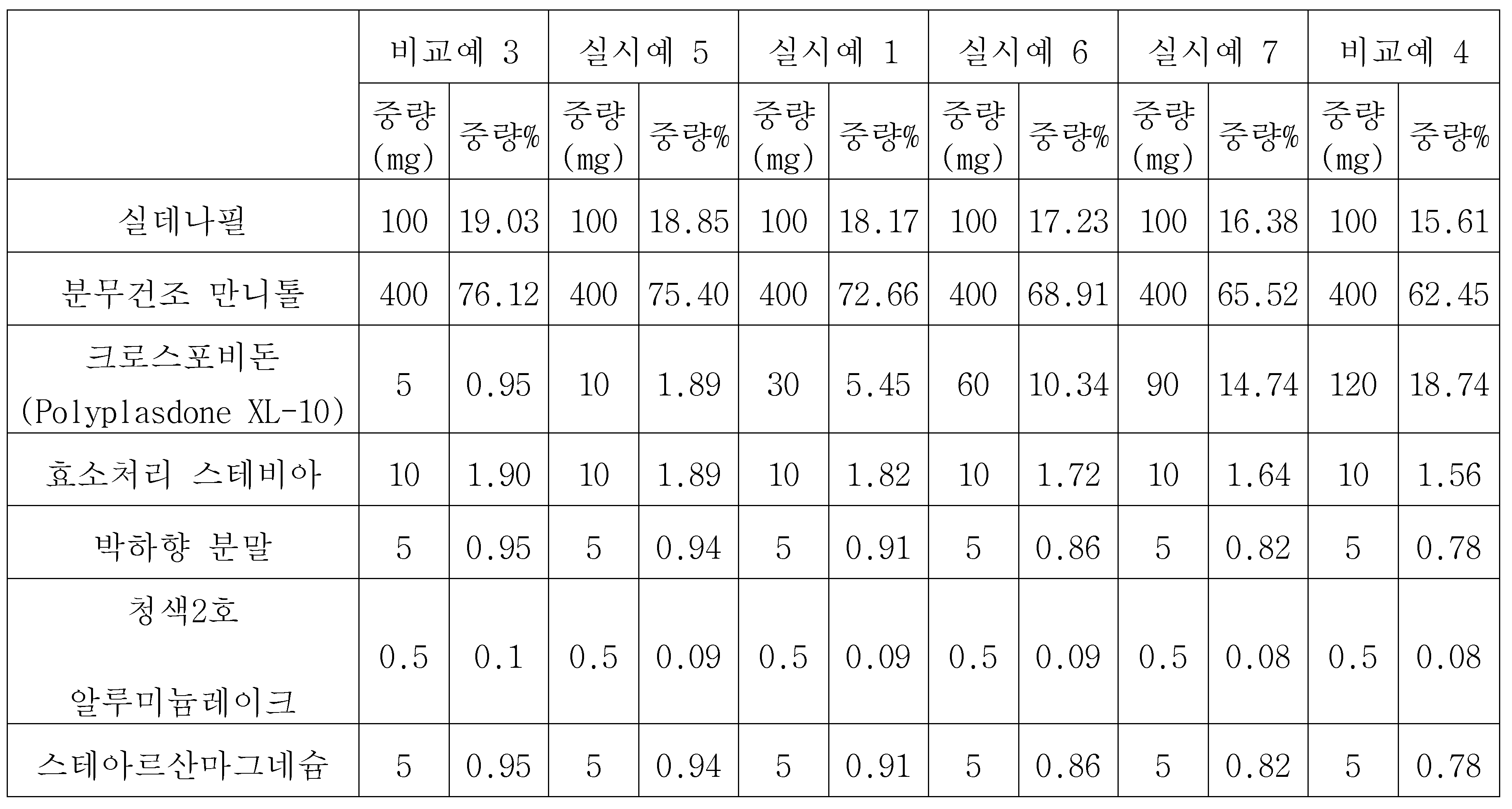
실시예 1, 5 내지 7 및 비교예 3, 4: 크로스포비돈의 양을 달리한 츄정의 제조Examples 1, 5 to 7 and Comparative Examples 3 and 4: Preparation of chewing gum with varying amounts of crospovidone
하기 표 3과 같은 조성으로 실시예 1과 동일한 방법으로 제조하되, 크로스포비돈의 양을 달리하여 츄정을 제조하였다.Were prepared in the same manner as in Example 1 except that the amount of crospovidone was changed.
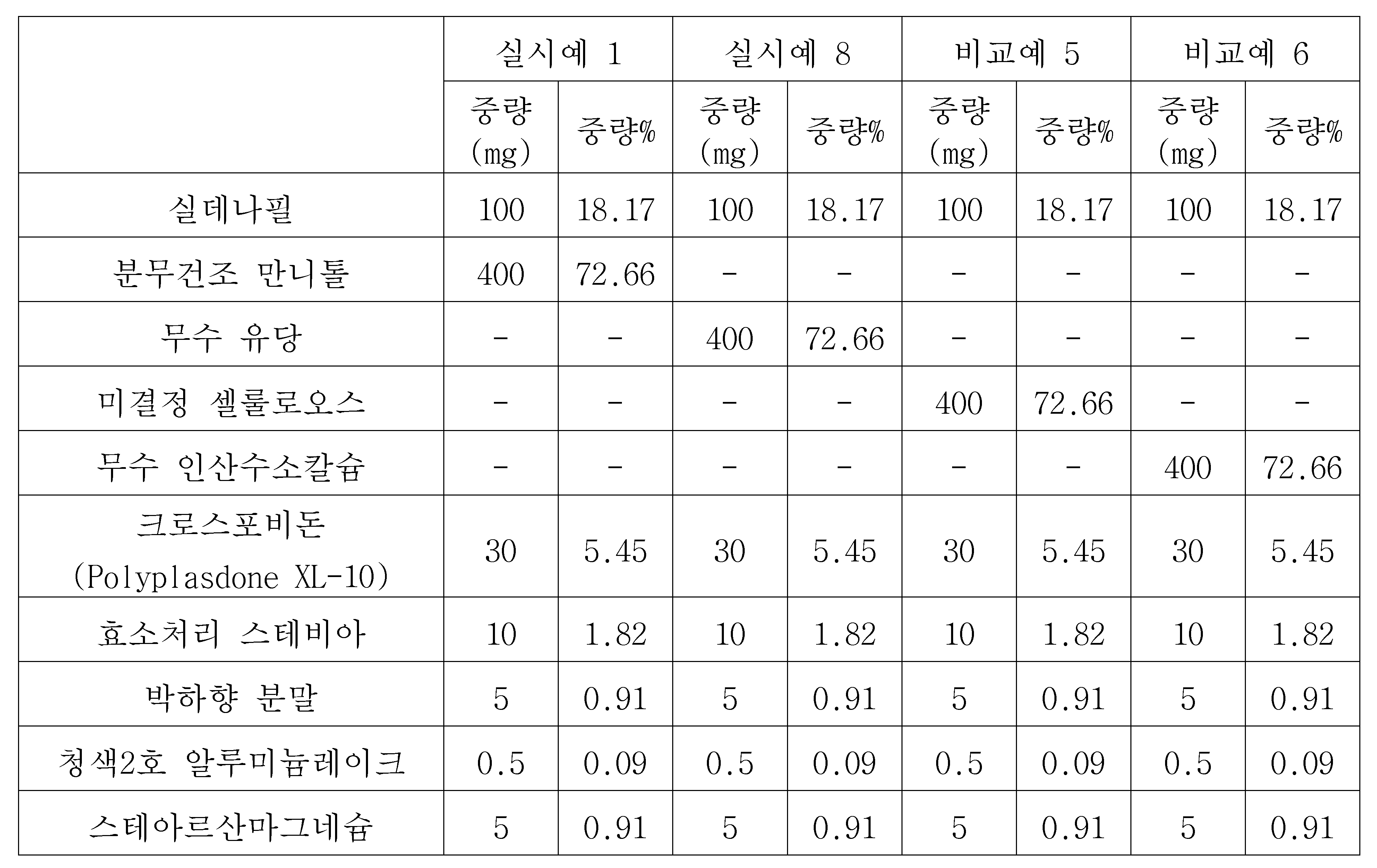
실시예 1, 8 및 비교예 5, 6: 부형제의 종류를 달리 한 츄정의 제조Examples 1 and 8 and Comparative Examples 5 and 6: Manufacture of different types of excipients
하기 표 4와 같은 조성으로 실시예 1과 동일한 방법으로 제조하되, 분무건조 만니톨 대신에 무수 유당(DFE, 독일), 미결정 셀룰로오스(MINGTAI, 대만) 또는 무수 인산수소칼슘(INNOPHOS, 미국)을 사용하여 츄정을 제조하였다.(DFE, Germany), microcrystalline cellulose (MINGTAI, Taiwan) or anhydrous calcium hydrogen phosphate (INNOPHOS, USA) instead of spray-dried mannitol was prepared in the same manner as in Example 1, Quenched.
시험예Test Example : : 츄정의Definition 구강 내 Oral 잔류감Residual feeling 시험 및 Testing and 붕해시험Disintegration test
(1) 구강 내 잔류감 시험(1) Oral residual test
실시예 1 내지 8 및 비교예 1 내지 6에서 얻어진 실데나필을 함유한 츄정에 대해 복용시 구강 내 잔류감을 측정하고 수치화하여 그 결과를 하기 표 5, 7, 9 및 11에 나타내었다. The intraoral retention was measured and quantified by taking the sildenafil containing tinctures obtained in Examples 1 to 8 and Comparative Examples 1 to 6, and the results are shown in Tables 5, 7, 9 and 11.
시험은 건강한 20대의 남성 자원자 10명을 대상으로 진행하였으며 시험 개체간의 오차를 최소화하기 위해 다음과 같이 투약법을 정하여 시험하였다: 1) 입 마름을 방지하기 위해 투약 전 20 mL의 물로 구강 내를 적신다; 2) 투약 후 정제를 씹을 때 어금니에 약물이 끼지 않도록 최대한 앞니에 가까운 치아를 사용하도록 하며 20초 이내에 모두 씹도록 한다; 3) 약물을 혀와 입천장에 마찰시키면서 구강 내 잔류감을 평가한다. 결과는 0 내지 5의 숫자로 수치화하였다(1: 잔류감이 15초 이내에 사라진다, 2: 잔류감이 30초 이내에 사라진다, 3: 잔류감이 45초 이내에 사라진다, 4: 잔류감이 60초 이내에 사라진다, 5: 잔류감이 60초 이상 지속되며 삼키기 힘들다).
The study was conducted on 10 healthy volunteers in 20 male volunteers. In order to minimize the error between the test subjects, the following dosing regimens were tested: 1) To prevent dry mouth, wet the mouth with 20 mL of water before dosing ; 2) When chewing tablets after medication, use the teeth near the front teeth as much as possible so that the molars do not get any drugs, and chew them all within 20 seconds; 3) Evaluate the residue in the mouth while rubbing the drug against the tongue and palate. The results are digitized from 0 to 5 (1: the residue disappears within 15 seconds, 2: the residue disappears within 30 seconds, 3: the residue disappears within 45 seconds, 4: the residue disappears within 60 seconds , 5: persistence persists for more than 60 seconds and is difficult to swallow).
(2) 츄정의 붕해시험(2) Deflection test
실시예 1 내지 8 및 비교예 1 내지 6에서 얻어진 실데나필을 함유한 츄정에 대해 붕해시간을 측정하여 그 결과를 하기 표 6, 8, 10 및 12에 나타내었다. 붕해시험은 대한약전에 수재된 붕해시험법을 근거로 실시하였으며, 붕해액으로는 정제수를 사용하였고, 붕해기 바닥에서 정제가 완전히 사라지는 시간을 붕해시간으로 하였다.
Disintegration times were measured for the sildenafil containing tinctures obtained in Examples 1 to 8 and Comparative Examples 1 to 6, and the results are shown in Tables 6, 8, 10 and 12. The disintegration test was conducted based on the disintegration test method described in Korean Pharmacopoeia. The disintegration time was defined as the time at which the tablets disappeared completely from the bottom of the disintegration device.
(3) 결과 및 고찰(3) Results and discussion
붕해제의 종류를 달리하여 제조한 실시예 1 및 비교예 1, 2의 츄정의 구강 내 잔류감 시험 및 붕해시험의 결과를 하기 표 5 및 6에 각각 나타내었다. The results of the retention test and the disintegration test in the oral cavity of Example 1 and Comparative Examples 1 and 2 prepared by different kinds of disintegration are shown in Tables 5 and 6, respectively.
상기 표 5에서 볼 수 있듯이, 크로스포비돈을 사용한 실시예 1의 츄정의 구강 내 잔류감은 0.9로 복용만족도가 높으나, 크로스카르복시메틸셀룰로오스나트륨 및 옥수수전분을 사용한 비교예 1 및 2의 츄정의 구강 내 잔류감은 4.3 및 2.9로 잔류감이 매우 커서 복용만족도도 낮았다. 이는, 사용된 크로스포비돈은 입경이 30 내지 50 ㎛ 이고 물에 접촉하여도 크게 팽창되지 않기 때문에 구강 내 잔류감이 작으나, 크로스카르복시메틸셀룰로오스나트륨은 입경이 45 내지 74㎛이나 물에 접촉 시 약 13.5배 팽창하고, 옥수수전분은 입경이 74 내지 125㎛이나 붕해력이 낮아 복용 후 구강 내에서 모래가 남는 느낌의 잔류감이 크기 때문이다. 따라서 본 발명의 츄정에 가장 바람직한 붕해제는 크로스포비돈으로 판단된다.As can be seen from the above Table 5, the residual sensation in the oral cavity of Example 1 using crospovidone was high at 0.9, but the residual in oral cavity of Comparative Examples 1 and 2 using croscarmellose methylcellulose sodium and corn starch The feeling was 4.3 and 2.9, which means that the feeling of staying was very high and satisfaction was low. This is because the crospovidone used has a particle size of 30 to 50 占 퐉 and does not significantly expand even when brought into contact with water, so that the residual in the mouth is small, but the croscarmex sodium cellulose has a particle size of 45 to 74 占 퐉, And the corn starch has a grain size of 74 to 125 탆 but the disintegration force is low, so that there is a feeling of residual feeling of remaining sand in the oral cavity after taking it. Therefore, the most preferred disintegrant for the quinquer of the present invention is judged to be crospovidone.
또한 상기 표 6과 같이, 실시예 1 및 비교예 1의 츄정의 붕해시간은 모두 약 10초 내외로 크로스포비돈, 크로스카르복시메틸셀룰로오스나트륨은 붕해제로서의 기능이 우수하나 비교예 2의 옥수수전분은 붕해력이 낮음을 볼 수 있다.
Also, as shown in Table 6, crospovidone and croscarmic carboxymethylcellulose sodium were excellent in disintegration, while the disintegration times of the chewiness of Example 1 and Comparative Example 1 were all within about 10 seconds, while the corn starch of Comparative Example 2 was superior You can see the damage is low.
한편, 크로스포비돈의 입경을 달리하여 제조한 실시예 1 내지 4의 츄정의 구강 내 잔류감 시험 및 붕해시험의 결과를 하기 표 7 및 8에 각각 나타내었다. On the other hand, the results of the retention test and the disintegration test in the oral cavity of Examples 1 to 4, which were prepared by varying the particle diameters of crospovidone, are shown in Tables 7 and 8, respectively.
상기 표 7에서 볼 수 있듯이, 크로스포비돈을 입경별로 사용한 실시예 1 내지 4의 츄정은 구강 내 잔류감이 모두 2.2 이하로 복용만족도가 높았다.As can be seen from Table 7, the chews of Examples 1 to 4, in which crospovidone was used at different particle diameters, had a satisfactory degree of oral residual remission of 2.2 or less.
또한, 상기 표 8에서 볼 수 있듯이, 팽창계수에 따라 붕해시간이 약간 다르지만 실시예 1 내지 4의 츄정 모두 붕해시간은 빨랐다.As can be seen from Table 8, although the disintegration time was slightly different depending on the expansion coefficient, the disintegration time of all the quenched samples of Examples 1 to 4 was fast.
표 7과 8의 결과를 종합하여 볼 때, 본 발명의 츄정에서 팽창계수가 4 내지 8 L/kg 범위에 포함되는, 입경이 5 내지 250 ㎛ 인 크로스포비돈을 사용할 경우 모두 높은 복용만족도와 빠른 붕해 시간을 보여준다.
Taking all the results of Tables 7 and 8 into consideration, when crospovidone having a particle size of 5 to 250 μm, which has a coefficient of expansion of 4 to 8 L / kg in the quench of the present invention, is used, Show time.
한편, 크로스포비돈의 양을 달리하여 제조한 실시예 1, 5 내지 7 및 비교예 3 및 4의 츄정의 구강 내 잔류감 시험 및 붕해시험의 결과를 하기 표 9 및 10에 각각 나타내었다. On the other hand, the results of the retention test and the disintegration test in the oral cavity of Examples 1, 5 to 7 and Comparative Examples 3 and 4 prepared by varying the amount of crospovidone are shown in Tables 9 and 10, respectively.
상기 표 9에서 볼 수 있듯이, 크로스포비돈을 5 내지 90mg으로 사용한 비교예 3과 실시예 1, 5 내지 7의 츄정은 구강 내 잔류감이 모두 3 이하로 복용만족도가 높았고, 크로스포비돈이 120mg(18.74 중량%)으로 사용된 비교예 4의 츄정은 상대적으로 잔류감이 컸다. 그 이유는 크로스포비돈이 물에 불용성이어서 사용량이 많아질수록 구강 내에 남는 양이 많아지기 때문이다.As can be seen from Table 9, the chewings of Comparative Example 3, which used crospovidone at 5 to 90 mg, and the chewings of Examples 1 and 5 to 7, were highly satisfied with the oral cavity residual feeling of 3 or less and the crospovidone content was 120 mg Weight%) of Comparative Example 4 had a relatively large residual feeling. The reason for this is that crospovidone is insoluble in water, so that the amount of crospovidone remaining in the mouth increases as the amount used increases.
또한, 상기 표 10에서 볼 수 있듯이, 크로스포비돈의 함유량이 높아질수록 붕해시간이 짧아졌다. 가장 소량의 크로스포비돈을 사용한 비교예 3의 츄정은 붕해시간이 36.3초이며, 긴 붕해시간 때문에 구강 내 잔류감 역시 표 9에서 보듯이 크로스포비돈의 사용량에 비해서는 상대적으로 크게 느껴짐을 알 수 있다.Further, as shown in Table 10, the disintegration time was shortened as the content of crospovidone was increased. In Comparative Example 3 using the smallest amount of crospovidone, the disintegration time was 36.3 seconds, and the residual in the mouth due to the long disintegration time was also relatively large compared to the amount of crospovidone as shown in Table 9.
표 9와 10의 결과를 종합하여 볼 때, 본 발명의 츄정에서 크로스포비돈은 제제 총 중량을 기준으로 1.5 내지 15 중량%의 양으로 포함되는 것이 바람직하다.
Based on the results of Tables 9 and 10, it is preferred that the crospovidone in the quench of the present invention is contained in an amount of 1.5 to 15% by weight based on the total weight of the preparation.
한편, 부형제의 종류를 달리하여 제조한 실시예 1, 8 및 비교예 5, 6의 츄정의 구강 내 잔류감 시험 및 붕해시험의 결과를 하기 표 11 및 12에 각각 나타내었다. On the other hand, the results of the retention test and disintegration test in the oral cavity of Examples 1 and 8 and Comparative Examples 5 and 6 prepared by different kinds of excipients are shown in Tables 11 and 12, respectively.
상기 표 11에서 볼 수 있듯이, 분무건조 만니톨 및 무수 유당을 사용한 실시예 1 및 8의 경우 구강 내 잔류감이 0.9 내지 1.5로 복용만족도가 높았으며, 미결정 셀룰로오스 및 무수 인산수소칼슘을 사용한 비교예 5 및 6의 경우 구강 내 잔류감이 3.3 내지 3.6으로 실시예의 츄정보다는 잔류감이 느껴지지만 복용에 불편함은 없는 정도였다. 이렇게 구강 내 잔류감의 차이가 나는 이유는 분무건조 만니톨과 무수 유당은 물에 대한 용해도가 높고, 미결정 셀룰로오스와 무수 인산수소칼슘은 물에 거의 녹지 않기 때문이다. 하지만 비교예 5 및 6에서 사용된 미결정 셀룰로오스와 무수 인산수소칼슘의 입경이 100 내지 200 ㎛로 작기 때문에 잔류감에 의한 불쾌함은 거의 없었다.As can be seen from Table 11, in Examples 1 and 8 using spray-dried mannitol and lactose anhydrous, the satisfaction in the oral cavity remained in 0.9 to 1.5 was high, and in Comparative Example 5 using microcrystalline cellulose and anhydrous calcium hydrogen phosphate And 6, the residual sensation in the oral cavity was 3.3 to 3.6, and the feeling of staying in the chew information of the example was felt, but there was no inconvenience to taking. The reason for this difference in oral cavity residues is that spray-dried mannitol and anhydrous lactose have high solubility in water, and microcrystalline cellulose and anhydrous calcium hydrogen phosphate hardly dissolve in water. However, since the diameters of the microcrystalline cellulose and anhydrous calcium hydrogen phosphate used in Comparative Examples 5 and 6 were as small as 100 to 200 占 퐉, there was almost no discomfort due to the residual feeling.
또한, 상기 표 12에서 보듯이, 부형제의 용해도에 따라 붕해시간 역시 달랐다. 분무건조 만니톨과 무수 유당을 사용한 실시예 1 및 8의 츄정은 붕해시간이 각각 11.8초와 13.7초로 빠르게 붕해되었고, 미결정 셀룰로오스와 무수 인산수소칼슘을 사용한 비교예 5 및 6의 츄정은 붕해시간이 각각 39.5초와 43.5초로 상대적으로 느리게 붕해되었다.Also, as shown in Table 12, the disintegration time was different depending on the solubility of the excipient. The disintegration times of the chews of Examples 1 and 8 using spray-dried mannitol and anhydrous lactose were rapidly disintegrated to 11.8 seconds and 13.7 seconds, respectively. The chewings of Comparative Examples 5 and 6 using microcrystalline cellulose and anhydrous calcium hydrogen phosphate had disintegration times It disintegrated relatively slowly at 39.5 seconds and 43.5 seconds.
상기 표 11 및 12의 결과에서 알 수 있듯이, 본 발명의 츄정에 바람직한 부형제는 분무건조 만니톨과 무수 유당이며, 특히 분무건조 만니톨이 가장 효과가 좋다. 이는 분무건조 만니톨이 분무건조를 통해 얻은 다공성 표면이라는 특성과 만니톨 자체의 높은 용해도 때문에 구강 내에서 신속하게 녹기 때문이다.As can be seen from the results of Tables 11 and 12, the excipients suitable for the quench of the present invention are spray-dried mannitol and anhydrous lactose, and spray-dried mannitol is most effective. This is because the spray-dried mannitol rapidly melts in the oral cavity due to the characteristics of the porous surface obtained through spray drying and the high solubility of mannitol itself.
Claims (11)
상기 PDE-5 억제제가 실데나필 유리 염기인 츄정.The method according to claim 1,
Wherein the PDE-5 inhibitor is a sildenafil free base.
상기 츄정이 당류, 당알콜류 또는 이들의 혼합물을 더 포함하는, 츄정.The method according to claim 1,
Wherein the chewing gum further comprises a saccharide, a sugar alcohol, or a mixture thereof.
상기 당류가 유당, 글루코오스, 수크로오스, 과당, 레불로오스, 말토덱스트린 및 파라티노오스로 이루어진 군으로부터 선택되고, 상기 당알콜류가 만니톨, 솔비톨, 자일리톨 및 에리스리톨로 이루어진 군으로부터 선택되는, 츄정.The method of claim 3,
Wherein the saccharide is selected from the group consisting of lactose, glucose, sucrose, fructose, levorphose, maltodextrin and paratinose, and the sugar alcohols are selected from the group consisting of mannitol, sorbitol, xylitol and erythritol.
상기 당알콜류가 분무건조 만니톨인 츄정.The method of claim 3,
Wherein the sugar alcohols are spray dried mannitol.
상기 당류, 당알콜류 또는 이들의 혼합물이 제제의 총 중량을 기준으로 10 내지 98 중량%의 양으로 포함되는 츄정.The method of claim 3,
Wherein the saccharides, sugar alcohols or mixtures thereof are included in an amount of 10 to 98% by weight based on the total weight of the formulation.
상기 붕해제의 입경이 5 내지 250 ㎛인 츄정.The method according to claim 1,
Wherein the disintegrant has a particle size of 5 to 250 占 퐉.
상기 붕해제가 제제의 총 중량을 기준으로 1.5 내지 15 중량%의 양으로 포함되는 츄정.The method according to claim 1,
Wherein the disintegrant is included in an amount of from 1.5 to 15% by weight based on the total weight of the formulation.
상기 츄정의 평균 경도가 2 내지 17 kp 범위인 것을 특징으로 하는, 츄정.The method according to claim 1,
Characterized in that the average roughness of the tooth is in the range of 2 to 17 kp.
상기 츄정이 실데나필 유리 염기, 분무건조 만니톨 및 팽창계수가 4 내지 8 L/kg인 붕해제를 포함하는 츄정.The method of claim 3,
Wherein the chew comprises sildenafil free base, spray dried mannitol and a disintegrant having an expansion coefficient of from 4 to 8 L / kg.
상기 츄정이 감미제, 착향제, 착색제 및 활택제로 이루어진 군으로부터 선택되는 어느 하나 이상을 추가로 포함하는 츄정.The method according to claim 1,
Wherein the chewing gum further comprises at least one selected from the group consisting of sweeteners, flavors, colorants and glidants.
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120146705A KR101953735B1 (en) | 2012-12-14 | 2012-12-14 | Chewable tablet comprising a phosphodiesterase-5 inhibitor |
| PCT/KR2013/010739 WO2014092358A1 (en) | 2012-12-14 | 2013-11-25 | Chewable tablet comprising a phosphodiesterase-5 inhibitor |
| ARP130104461A AR093707A1 (en) | 2012-12-14 | 2013-12-03 | MASTICABLE TABLET INCLUDED BY A PHOSPHODESTERASE-5 INHIBITOR |
| TW102146092A TW201427721A (en) | 2012-12-14 | 2013-12-13 | Chewable tablet comprising a phosphodiesterase-5 inhibitor |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120146705A KR101953735B1 (en) | 2012-12-14 | 2012-12-14 | Chewable tablet comprising a phosphodiesterase-5 inhibitor |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140077658A true KR20140077658A (en) | 2014-06-24 |
| KR101953735B1 KR101953735B1 (en) | 2019-03-04 |
Family
ID=50934596
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020120146705A Active KR101953735B1 (en) | 2012-12-14 | 2012-12-14 | Chewable tablet comprising a phosphodiesterase-5 inhibitor |
Country Status (4)
| Country | Link |
|---|---|
| KR (1) | KR101953735B1 (en) |
| AR (1) | AR093707A1 (en) |
| TW (1) | TW201427721A (en) |
| WO (1) | WO2014092358A1 (en) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112826802B (en) * | 2021-01-22 | 2021-09-28 | 上海普康药业有限公司 | Sildenafil citrate chewable tablet and preparation method thereof |
| CN115337276B (en) * | 2021-05-14 | 2024-02-09 | 南京科默生物医药有限公司 | Preparation method of sildenafil citrate orally disintegrating tablet |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100262926B1 (en) | 1993-06-09 | 2000-09-01 | 디. 제이. 우드, 무어 제임스 더블유 | Pyrazolopyrimidinones for the treatment of impotence |
| KR100353014B1 (en) | 1998-11-11 | 2002-09-18 | 동아제약 주식회사 | Pyrazolopyrimidinone derivatives for the treatment of impotence |
| KR100357411B1 (en) | 1994-01-21 | 2003-02-05 | 아이코스 코포레이션 | Tetracyclic Derivatives, Manufacturing Methods and Applications |
| KR20030076051A (en) * | 2002-03-22 | 2003-09-26 | 한미약품 주식회사 | Fast dissolving formulation of sildenafil lactate |
| KR100430355B1 (en) | 1997-11-12 | 2004-05-04 | 바이엘 악티엔게젤샤프트 | 2-Phenyl Substituted Imidazotriazinones as Phosphodiesterase Inhibitors |
| JP2008127320A (en) * | 2006-11-20 | 2008-06-05 | Zensei Yakuhin Kogyo Kk | Solid preparation quickly disintegrating in oral cavity |
| WO2009074995A1 (en) * | 2007-12-10 | 2009-06-18 | Ajanta Pharma Limited | Taste masked chewable compositions of sildenafil citrate |
| WO2011030351A2 (en) * | 2009-09-03 | 2011-03-17 | Rubicon Research Private Limited | Taste - masked pharmaceutical compositions |
| JP2012007320A (en) * | 2010-06-23 | 2012-01-12 | Hitachi Constr Mach Co Ltd | Work machine |
| WO2012120522A1 (en) * | 2011-03-04 | 2012-09-13 | Genepharm India Private Limited | A taste masked chewable tablet of sildenafil |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0219516D0 (en) * | 2002-08-21 | 2002-10-02 | Phoqus Ltd | Fast dissolving and taste masked oral dosage form comprising sildenafil |
| EP2338474A1 (en) * | 2009-12-23 | 2011-06-29 | Ratiopharm GmbH | Fusion tablet containing compacted sildenafil base |
-
2012
- 2012-12-14 KR KR1020120146705A patent/KR101953735B1/en active Active
-
2013
- 2013-11-25 WO PCT/KR2013/010739 patent/WO2014092358A1/en not_active Ceased
- 2013-12-03 AR ARP130104461A patent/AR093707A1/en unknown
- 2013-12-13 TW TW102146092A patent/TW201427721A/en unknown
Patent Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100262926B1 (en) | 1993-06-09 | 2000-09-01 | 디. 제이. 우드, 무어 제임스 더블유 | Pyrazolopyrimidinones for the treatment of impotence |
| KR100357411B1 (en) | 1994-01-21 | 2003-02-05 | 아이코스 코포레이션 | Tetracyclic Derivatives, Manufacturing Methods and Applications |
| KR100430355B1 (en) | 1997-11-12 | 2004-05-04 | 바이엘 악티엔게젤샤프트 | 2-Phenyl Substituted Imidazotriazinones as Phosphodiesterase Inhibitors |
| KR100353014B1 (en) | 1998-11-11 | 2002-09-18 | 동아제약 주식회사 | Pyrazolopyrimidinone derivatives for the treatment of impotence |
| KR20030076051A (en) * | 2002-03-22 | 2003-09-26 | 한미약품 주식회사 | Fast dissolving formulation of sildenafil lactate |
| JP2008127320A (en) * | 2006-11-20 | 2008-06-05 | Zensei Yakuhin Kogyo Kk | Solid preparation quickly disintegrating in oral cavity |
| WO2009074995A1 (en) * | 2007-12-10 | 2009-06-18 | Ajanta Pharma Limited | Taste masked chewable compositions of sildenafil citrate |
| WO2011030351A2 (en) * | 2009-09-03 | 2011-03-17 | Rubicon Research Private Limited | Taste - masked pharmaceutical compositions |
| JP2012007320A (en) * | 2010-06-23 | 2012-01-12 | Hitachi Constr Mach Co Ltd | Work machine |
| WO2012120522A1 (en) * | 2011-03-04 | 2012-09-13 | Genepharm India Private Limited | A taste masked chewable tablet of sildenafil |
Non-Patent Citations (1)
| Title |
|---|
| 삭제 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2014092358A1 (en) | 2014-06-19 |
| KR101953735B1 (en) | 2019-03-04 |
| AR093707A1 (en) | 2015-06-17 |
| TW201427721A (en) | 2014-07-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7398374B2 (en) | solid oral nicotine formulation | |
| CN111447921B (en) | Nicotine tablets | |
| ES2393640T3 (en) | Orodisintegrable tablets | |
| EP2698145B1 (en) | Pharmaceutical Formulations comprising dapoxetine and a PDE5 inhibitor | |
| Bhatt | Mouth dissolving tablets challenges, preparation strategies with a special emphasis on Losartan potassium–A review | |
| US20040076665A1 (en) | Modified release oral dosage form | |
| JP2009114113A (en) | Orally disintegrating tablet and method for producing the same | |
| US20070082048A1 (en) | Sleep aid formulations | |
| WO2000020033A1 (en) | Tablets immediately disintegrating in the oral cavity | |
| RS54238B1 (en) | ORAL FILM FORMULATIONS CONTAINING DAPOXETINE AND TADALAFIL | |
| KR102239291B1 (en) | Chewable tablet formulation comprising tadalafil or a pharmaceutically acceptable salt thereof | |
| JP5656258B2 (en) | Orally disintegrating tablets containing galantamine | |
| JP2008285434A (en) | Orally disintegrating tablets | |
| WO2014027981A2 (en) | Effervescent tablet formulations of dapoxetine and a pde5 inhibitor | |
| KR101953735B1 (en) | Chewable tablet comprising a phosphodiesterase-5 inhibitor | |
| JP5848432B2 (en) | Orally disintegrating tablets containing mirtazapine | |
| KR101304343B1 (en) | Fast dissolving oral formulation of pde-5 inhibitors | |
| KR20130021888A (en) | Orally disintegrating tablet comprising sildenafil free base | |
| CN101203246B (en) | Medical composition | |
| JP4944467B2 (en) | Pharmaceutical composition | |
| WO2014027978A1 (en) | Chewing gum formulations comprising dapoxetine and tadalafil | |
| Malik et al. | Recent patents on fast dissolving tablets-A Review | |
| HK40017837A (en) | Orally disintegrated tablet comprising carbamate compound | |
| HK1111619A (en) | Pharmaceutical composition |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| R17-X000 | Change to representative recorded |
St.27 status event code: A-3-3-R10-R17-oth-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 7 |
|
| U11 | Full renewal or maintenance fee paid |
Free format text: ST27 STATUS EVENT CODE: A-4-4-U10-U11-OTH-PR1001 (AS PROVIDED BY THE NATIONAL OFFICE) Year of fee payment: 7 |