KR20170068480A - 다발성 경화증의 치료를 위한 시포니모드 및 라퀴니모드를 포함하는 조합물 - Google Patents
다발성 경화증의 치료를 위한 시포니모드 및 라퀴니모드를 포함하는 조합물 Download PDFInfo
- Publication number
- KR20170068480A KR20170068480A KR1020177009900A KR20177009900A KR20170068480A KR 20170068480 A KR20170068480 A KR 20170068480A KR 1020177009900 A KR1020177009900 A KR 1020177009900A KR 20177009900 A KR20177009900 A KR 20177009900A KR 20170068480 A KR20170068480 A KR 20170068480A
- Authority
- KR
- South Korea
- Prior art keywords
- mode
- combination
- amount
- composition
- multiple sclerosis
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4704—2-Quinolinones, e.g. carbostyril
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/397—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having four-membered rings, e.g. azetidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Immunology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Telephonic Communication Services (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
Abstract
본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물 및 제약 조성물, 및 다발성 경화증, 특히 이차 진행형 다발성 경화증의 치료를 위한 상기 조합물 및/또는 조성물의 용도에 관한 것이다.
Description
본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물 및 제약 조성물, 및 다발성 경화증의 치료를 위한 의약으로서 상기 조합물 및/또는 조성물의 용도에 관한 것이다.
다발성 경화증: 재발형 및 진행형 형태
다발성 경화증 (MS)은 전 세계적으로 1백만 명이 넘는 사람들에게 영향을 미치는 신경계 질환이다. 이는 청년 및 중년 성인에서 신경학적 장애의 가장 흔한 원인이며 대상체 및 그의 가족, 친구 및 헬스 케어를 담당하는 단체에 주요 신체적, 심리적, 사회적 및 재정적 영향을 미친다.
MS가 초기에는 감염에 의해 촉발되고 유전적 소인에 따라 덧붙여질 수 있는 일부 자가면역 과정에 의해 매개되는 것으로 일반적으로 추정된다. 이는 중추 신경계 (CNS)의 미엘린을 손상시키는 만성 염증성 병태이다. MS의 발병기전은 미엘린 항원에 대항해 지시된 순환으로부터의 림프구 (즉, 자가반응성 T 세포)가 CNS 내로 침윤하는 것을 특징으로 한다. MS에서의 염증기에 더하여, 축삭 손실이 질환의 과정에서 초기에 발생하며 시간이 지남에 따라 광범위해져서, 점진적이고 영구적인 신경학적 손상 및, 빈번하게 중증 장애가 후속적으로 발생할 수 있다. 상기 질환과 연관된 증상은 피로, 경직, 운동 실조, 쇠약, 배뇨 및 배변 장애, 성기능 장애, 통증, 진전, 발작 징후, 시각 장애, 심리적 문제 및 인지 기능 장애를 포함한다.
다양한 MS 질환 단계 및/또는 유형이 다발성 경화증 치료법에 기재되어 있다 (Duntiz, Ed. Rudick and Goodkin, London: Taylor & Francis, 1999). 이 중에서, 재발 완화형 다발성 경화증 (RRMS)은 최초 진단시 가장 흔한 형태이다. 진단시에, MS 환자의 80% 내지 90%가 RRMS를 갖는다. 이 형태의 MS는 신경학적 증상의 반복적인 재발, 즉 급성 에피소드(acute episode)와 후속하는 회복 기간 (완화(remissions))을 특징으로 한다. RRMS 환자의 약 80%에서, 이 형태는 질환 발병 약 19년 후에 이차 진행형 다발성 경화증 (SPMS)으로 나중에 진행된다.
SPMS가 발병된 환자의 경우, 질환 질행은 재발 사이에 완화가 없거나 또는 단지 약한 완화와 함께 간헐적으로 재발하거나 또는 재발 없이 진행되며, 재발 (존재할 경우)과 무관하게, 증상적으로 장애의 지속적인 악화를 특징으로 한다. SPMS로의 이동을 나타내는 증상은 쇠약 및 조화운동불능상태의 꾸준한 증가, 뻣뻣하고, 단단한 다리 근육; 배변 및 배뇨 문제; 더 큰 피로, 우울증, 및 사고의 문제를 포함한다. 일반적으로, 염증성 침윤의 수는 감소하는 한편, 신경변성이 SPMS의 더 두드러진 특징이 된다.
그러나, 최근에 뇌에서의 염증은 RRMS 환자에서뿐만 아니라, SPMS 환자에서도 발생한다는 것이 밝혀졌다. 더욱이, SPMS를 가진 환자에서, 뇌척수막의 염증이 발견될 수 있다. 이들 면역 응집체는 T 세포 및 B 세포가 풍부한 구조이다. 이들 구조들 옆의 피질 조직은 상당히 증가된 병리상태를 보인다 (Serafini et al, 2004). 뇌척수막에서 염증의 정도는 신경변성의 양과 상관관계가 있는 것으로 밝혀졌으며; 더욱이 이들 구조는 SPMS 환자에서만 보고되었으며 - 이들은 RRMS 또는 PPMS 환자에서는 관찰되지 않았다 (Magliozzi et al 2007). 사후 동정된 CNS 응집체를 가진 SPMS 환자는 초기 질환 발병, 진행형 MS로의 신속한 전환 및 급속한 이환율을 가졌다 (Howell et al 2011). 따라서, 염증은 적어도 일부 환자에서 조직 변성을 유도하는 것으로 보인다.
비록 RRMS가 예측불가능하긴 하지만, 명확한 엄습에 뒤이은 회복의 패턴은 전형적으로 일관성이 있다. SPMS의 경우, 재발은 덜 뚜렷한 경향이 있으며, 많은 인자에 따라, 재발은 덜 종종 일어나거나 또는 전혀 일어나지 않을 수 있다. 그러나, SPMS 환자에서 재발이 발생하는 경우, 그의 회복은 정상적으로 RRMS 환자에서와 만큼 완전하지는 않다.
RRMS를 치료하기 위한 여러 약물은 공지되어 있지만, SPMS는 일반적으로 치료하기가 더 어렵다.
MS를 위한 시판 단독요법
현재 재발형 MS (RMS)에서 사용하도록 승인된 다수의 질환-완화 의약(disease-modifying medication)이 있다. 이들은 비경구 의약, 인터페론 베타 1-a (예를 들어 아보넥스(Avonex)?, 레비프(Rebif)?, 플레그리디(Plegridy)?), 인터페론 베타 1-b (베타세론(Betaseron)?, 엑스타비아(Extavia)?), 글라티라머 아세테이트 (코팍손(Copaxone)?), 미톡산트론 (노반트론(Novantrone)?), 나탈리주맙 (티사브리(Tysabri)?) 및 알렘투주맙 (렘트라다(Lemtrada)?); 및 경구 의약, 핑골리모드 (길렌야(Gilenya)?), 테리플루노미드 (아우바기오(Aubagio)?) 및 디메틸 푸마레이트 (텍피데라(Tecfidera)?)를 포함한다. 이들 의약의 대부분은 면역조정제로서 작용하는 것으로 여겨진다. 미톡산트론 및 나탈리주맙은 면역억제제로 작용하는 것으로 여겨진다. 그러나, 각각의 작용 메커니즘은 단지 부분적으로 설명되었다.
다른 치료 접근법은 증상적 치료 (질환에 의해 유발된 증상을 개선하기 위해 적용되는 모든 요법을 지칭함) 및 코르티코스테로이드를 사용한 급성 재발의 치료를 포함한다. 스테로이드가 시간이 지남에 따라 MS의 과정에 영향을 미치지 않지만, 이들은 일부 대상체에서 엄습의 지속 기간 및 중증도를 감소시킬 수 있다.
개발 중인 MS의 단독요법의 예
시포니모드
시포니모드는 스핑고신 1-포스페이트 (S1P) 수용체 조정제로 칭해지는 약물의 부류에 속한다. 상기 군의 또 다른 구성원은 RRMS를 치료하기 위해 시판되는 핑골리모드 (길렌야?)이다.
시포니모드는 II상 임상 시험에서 시험되었고 여기서 0.25 mg, 0.5 mg, 1.25 mg, 2 mg 및 10 mg의 용량으로 경구로 제공되는 경우 RRMS (즉, 볼드(BOLD) 시험)를 치료하는 데 용량 의존적 효능을 나타내었다.
S1P 수용체 조정제는 림프절로부터 말초 혈액으로 이동하는 백혈구의 능력을 차단하는 것으로 공지되어 있다. 상기 조정제는 림프절에 있는 림프구를 격리시켜, 다발성 경화증에서 림프구가 자가면역 반응을 위해 중추 신경계로 이동하지 못하도록 할 수 있다.
그러나, 시포니모드는 혈액-뇌-장벽을 가로지르고 또한 CNS에서 세포에 직접적인 유익한 영향을 미칠 수 있다. S1P 수용체 조정제는 SPMS에서 효능의 기초를 형성할 수 있을 것인 손상 후에 신경아교세포 및 전구체 세포의 복구 과정을 자극하는 것으로 보고되었다 (Alejandro Horga et al, Expert Rev Neurother 8(5), 699-714, 2008).
라퀴니모드
라퀴니모드는 RRMS의 치료를 위한 경구 제제로서 제안되어 있다. 이는 두 가지 III상 임상시험에서 시험되었고 여기서 24개월의 기간에 걸쳐 1일 1회 0.6 mg의 용량으로 경구로 제공되는 경우 RRMS (즉, 브라보(BRAVO) 시험 및 알레그로(ALLEGRO) 시험)를 치료하는 데 효능을 나타내었다.
라퀴니모드 및 그의 나트륨 염 형태는, 예를 들어 US6077851에 기재되어 있다. 라퀴니모드의 작용 메커니즘은 완전히 이해되어 있지는 않다.
질환-완화 의약의 조합 요법
주어진 병태, 예컨대 MS를 치료하기 위한 2종의 약물의 투여는 다수의 잠재적인 문제를 야기한다. 2종의 약물 간의 생체내 상호작용은 복잡하다. 임의의 단일 약물의 효과는 그의 흡수, 분배 및 제거와 관련이 있다. 2종의 약물이 체내에 도입되는 경우, 각각의 약물은 다른 하나의 약물의 흡수, 분배 및 제거에 영향을 미치므로, 다른 하나의 약물의 효과를 변경할 수 있다. 예를 들어, 하나의 약물은 다른 하나의 약물을 제거하는 대사 경로에 관여하는 효소의 생성을 억제, 활성화 또는 유도할 수 있다.
WO2013055907에서, 실험 약물 라퀴니모드 및 시판 약물 핑골리모드를 포함하는 조합물이 RRMS에 대한 동물 모델 (즉, 마우스의 C57Bl/6 계통에서의 MOG-유도 실험적 자가면역 뇌척수염 (EAE))에서 시험된다. 이 모델은 RRMS를 치료하는 예방제로서의 의약의 효능을 시험하기 위한 확립된 모델이다. 10 mg/kg의 라퀴니모드와 0.3 mg/kg의 핑골리모드의 조합물은 질환 중증도를 예방하는데 상승작용적 효과를 나타냈다.
그러나, 약물 조합의 다른 예에서, 상승작용의 부족 또는 심지어 길항작용이 나타났고 다른 원치 않는 부작용이 보고되었다.
핑골리모드 및 인터페론의 조합 투여는 양쪽 용법의 임상적 유효성을 방해하는 것으로 나타났다 (Brod et al, Annals of Neurology, 47, 127-131, 2000).
또 다른 실험에서, 인터페론 베타와의 조합 요법에서 프레드니손의 첨가가 그의 상향-조절제 효과를 길항한다는 것으로 보고되었다 (Salama et al, Multiple Sclerosis, 9, 28-31, 2003).
한 예에서, 나탈리주맙과 인터페론 베타 1-a의 조합은 예기치 않은 부작용의 위험을 증가시키는 것으로 관찰되었다 (Rudick et al, New England Journal of Medicine, 354, 911-923, 2006; Kleinschmidt-DeMasters, New England Journal of Medicine, 353, 369-379, 2005; Langer-Gould, New England Journal of Medicine, 353, 369-379, 2005).
따라서, 2종의 약물이 동일한 병태를 치료하기 위해 투여되는 경우, 대상체에서 다른 하나의 치료 활성을 각각이 보완할 것인지, 영향을 미치게 될 것인지, 또는 방해할 것인지 여부는 예측할 수 없다. 2종의 약물 간의 상호작용이 각각의 약물의 의도된 치료 활성에 영향을 미칠 뿐만 아니라, 상호작용이 독성 대사 물질의 수준을 증가시킬 수도 있다. 상호작용은 또한 각각의 약물의 부작용을 증가시키거나 감소시킬 수 있다. 따라서, 질환을 치료하기 위해 2종의 약물을 투여하면, 각각의 약물의 부정적인 면의 프로필에서 어떤 변화가 일어날 것인지 예측할 수 없다. 게다가, 2종의 약물 간의 상호작용의 효과가 언제 나타날지 정확하게 예측하기는 어렵다. 예를 들어, 제2 약물의 초기 투여시에, 2종의 약물이 정상 상태 농도에 도달한 후에 또는 약물 중 하나의 중단시에 약물 간의 대사 상호작용이 분명해질 수 있다.
그러므로, 출원 시점에서의 기술적 수준은 2종의 특정 약물, 특히 시포니모드 및 라퀴니모드의 조합 요법의 효과가 조합 연구의 결과가 이용가능할 때까지는 예측할 수 없다는 것을 의미한다.
자가면역 질환, 예를 들어 SPMS의 치료를 위한 효과적인 의약을 제공할 필요가 있다.
발명의 개요
놀랍게도, 시포니모드와 라퀴니모드의 조합 요법은, 자가면역 질환, 특히 SPMS의 치료, 예방 또는 진행의 지연에서 상당한 이점을 제공한다.
놀랍게도, 시포니모드 및 라퀴니모드를 포함하는 조합물은 손상된 CNS에서 (예를 들어 질환 발병 후에/재발이 발생한 후) MS를 치료하는 데 효과적이며 림프구의 수를 상승작용적으로 감소시키는 것으로 밝혀졌다. 따라서 예를 들어, 시포니모드 및 라퀴니모드를 포함하는 조합물은 (i) 염증적 사건, 예를 들어 SPMS 환자의 CNS에서, 뇌척수막에서의 염증을 감소시키는 것이 가능하고/거나 (ii) SPMS 환자에서 재발의 횟수 및/또는 중증도를 효과적으로 감소시키는 것으로 기대된다.
놀랍게도, 약물-약물 상호작용에 어떤 증거도 없는 것으로 밝혀졌다. 본 발명의 조합 요법의 상승작용적 활성은 증진된 생물학적 반응을 나타낸다.
놀랍게도, 시포니모드 및 라퀴니모드를 포함하는 조합물의 치료의 효과는 시포니모드 또는 라퀴니모드 중 어느 하나를 사용한 단독요법과 비교시 더 신속히 개시되는 것으로 밝혀졌다
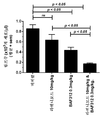
도 1: MOG/CFA/백일해 독소-면역화 C57/Bl6 마우스에서 림프구를 감소시키기 위한 시포니모드 및 라퀴니모드의 사용.
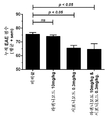
도 2: C57/Bl6 마우스에서 MOG/CFA/백일해 독소-유도 실험적 자가면역 뇌척수염 (EAE)을 치료하기 위한 시포니모드 및 라퀴니모드의 사용. 치료는, 예를 들어, 뒷다리 마비를 특징으로 하는 중증 CNS 손상 후에 시작된다.
도 3: C57/Bl6 마우스에서 실험적 자가면역 뇌척수염 (EAE) 동안에 혈액 및 뇌 조직 중 시포니모드 및 라퀴니모드의 수준. 약물-약물 상호작용의 어떤 증거도 없다.
도 4: C57/Bl6 마우스에서 MOG/CFA/백일해 독소-유도 실험적 자가면역 뇌척수염 (EAE)을 치료하기 위한 시포니모드 및 라퀴니모드의 사용. 진행중인 CNS 손상 동안에 (예를 들어 질환 발병 후에) 치료가 시작되었다.
도 2: C57/Bl6 마우스에서 MOG/CFA/백일해 독소-유도 실험적 자가면역 뇌척수염 (EAE)을 치료하기 위한 시포니모드 및 라퀴니모드의 사용. 치료는, 예를 들어, 뒷다리 마비를 특징으로 하는 중증 CNS 손상 후에 시작된다.
도 3: C57/Bl6 마우스에서 실험적 자가면역 뇌척수염 (EAE) 동안에 혈액 및 뇌 조직 중 시포니모드 및 라퀴니모드의 수준. 약물-약물 상호작용의 어떤 증거도 없다.
도 4: C57/Bl6 마우스에서 MOG/CFA/백일해 독소-유도 실험적 자가면역 뇌척수염 (EAE)을 치료하기 위한 시포니모드 및 라퀴니모드의 사용. 진행중인 CNS 손상 동안에 (예를 들어 질환 발병 후에) 치료가 시작되었다.
발명의 상세한 설명
본 발명은 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연에서 사용하기 위한, 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공한다.
본 발명의 추가 측면은 의약으로서 사용하기 위한, 시포니모드 및 라퀴니모드를 포함하는 조합물에 관한 것이다.
본 발명의 또 다른 추가 측면은 시포니모드 및 라퀴니모드를 포함하는 조합물에 관한 것이다.
본 발명의 또 다른 추가 측면은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 제약 조성물에 관한 것이다.
본 발명의 또 다른 추가 측면은 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 필요로 하는 대상체에게 치료 유효량의, 시포니모드 및 라퀴니모드를 포함하는 조합물을 투여하는 것을 포함하는, 상기 대상체에서 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연 방법에 관한 것이다.
본 발명의 또 다른 추가 측면은
(i) 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 필요로 하는 대상체에서 상기 이차 진행형 다발성 경화증을 진단하고,
(ii) 상기 대상체에게 치료 유효량의, 시포니모드 및 라퀴니모드를 포함하는 조합물을 투여하는 것
을 포함하는, 상기 대상체에서 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연 방법에 관한 것이다.
의심의 여지를 피하기 위해, "배경"이란 표제로 본 명세서에서 위에서 개시된 정보는 본 발명과 관련이 있는 것이며, 본 발명의 개시의 일부로서 읽혀져야 하는 것으로 여기에 명시된다.
본원에 사용된 바와 같이, 그리고 달리 명시되지 않는 한, 다음 용어 각각은 아래에 명시된 정의를 가져야 한다.
본 명세서의 상세한 설명 및 청구범위 전반에 걸쳐, 단어 "포함하다" 및 "함유하다" 및 그의 변형은 "포함하나 그에 제한되지 않음"을 의미하며, 다른 모이어티, 첨가제, 성분, 정수 또는 단계를 배제시키려는 의도는 아니다 (시키지 않는다).
본 명세서의 상세한 설명 및 청구범위 전반에 걸쳐, 단수는 문맥상 달리 요구되지 않는 한 복수를 포함한다. 특히, 부정관사가 사용되는 경우, 명세서 (이 용어는 상세한 설명 및 청구범위 둘 다를 포함한다)는 문맥상 달리 요구되지 않는 한 복수형뿐만 아니라 단수형도 고려하는 것으로 이해되어야 한다.
본 발명의 특정한 측면, 실시양태 또는 실시예와 관련하여 기재된 특징, 정수, 특성, 화합물, 화학적 모이어티 또는 기는 그와 부적합하지 않는 한, 본원에 기재된 임의의 다른 측면, 실시양태 또는 실시예에 적용 가능하다는 것으로 이해되어야 한다. (첨부한 청구범위, 요약서 및 도면을 포함한) 본 명세서에 개시된 모든 특징, 및/또는 그렇게 개시된 임의의 방법 또는 공정의 모든 단계는, 이러한 특징 및/또는 단계 중 적어도 일부는 상호 배타적인 경우를 제외하고는, 임의의 조합으로 조합될 수 있다. 본 발명은 임의의 전술한 실시양태의 세부 사항에 한정되지 않는다. 본 발명은 (임의의 첨부한 청구범위, 요약서 및 도면을 포함한) 본 명세서에 개시된 특징의, 임의의 신규한 것 또는 신규한 조합, 또는 그렇게 개시된 임의의 방법 또는 공정의 단계의, 임의의 신규한 것 또는 임의의 새로운 조합으로 확장된다.
본원에 사용된 바와 같은 "시포니모드"는 화학식 I의 화합물뿐만 아니라 그의 제약상 허용되는 염, 다형체, 용매화물 및/또는 수화물을 포함하는 것으로 이해되어야 한다.
<화학식 I>
본원에 사용된 바와 같은 시포니모드는 IUPAC 명칭 1-{4-[1-((E)-4-시클로헥실-3-트리플루오로메틸-벤질옥시이미노)-에틸]-2-에틸-벤질}-아제티딘-3-카르복실산 (BAF312)을 갖는다. 본 발명의 바람직한 실시양태에서, 시포니모드는 시포니모드 유리 염기 또는 시포니모드 염의 형태로 존재한다. 시포니모드의 제약상 허용되는 염의 예는 무기 산과의 염, 예컨대 히드로클로라이드, 히드로브로마이드 및 술페이트, 유기 산과의 염, 예컨대 아세테이트, 푸마레이트, 헤미푸마레이트, 말레에이트, 벤조에이트, 시트레이트, 말레이트, 메탄술포네이트 및 벤젠술포네이트 염, 또는, 적절한 경우, 금속, 예컨대 나트륨, 칼륨, 칼슘 및 알루미늄과의 염, 아민, 예컨대 트리에틸아민과의 염 및 이염기성 아미노산, 예컨대 리신과의 염을 포함한다. 바람직한 실시양태에서 시포니모드는 시포니모드 헤미푸마레이트이다.
본원에 사용된 바와 같은 "라퀴니모드"는 화학식 II의 화합물뿐만 아니라 그의 제약상 허용되는 염, 다형체, 용매화물 및/또는 수화물을 포함하는 것으로 이해되어야 한다.
<화학식 II>
본원에 사용된 바와 같은 라퀴니모드는 IUPAC 명칭 5-클로로-N-에틸-4-히드록시-1-메틸-2-옥소-N-페닐-1,2-디히드로퀴놀린-3-카르복사미드를 갖는다. 본 발명의 바람직한 실시양태에서, 라퀴니모드는 라퀴니모드 유리 산 또는 라퀴니모드 염의 형태로 존재한다. 라퀴니모드의 제약상 허용되는 염의 예는 금속, 예컨대 나트륨, 칼륨, 칼슘 및 알루미늄과의 염을 포함한다. 한 실시양태에서 라퀴니모드는 라퀴니모드 소듐이다.
본원에 사용된 바와 같이, 밀리그램으로 측정된 바와 같은 시포니모드 또는 라퀴니모드의 "양" 또는 "용량"은 제제의 형태와 상관없이, 제제에 존재하는 시포니모드 유리 염기 또는 라퀴니모드 유리 산의 밀리그램을 지칭한다. "0.6 mg 라퀴니모드의 용량"은 제제의 형태와 상관없이, 제제 중 라퀴니모드 유리 산의 양은 0.6 mg이다. 따라서, 염, 예를 들어 라퀴니모드 소듐의 형태의 경우, 0.6 mg 라퀴니모드 유리 산의 용량을 제공하는 데 필요한 염의 중량은 추가의 염 이온의 존재로 인해 0.6 mg보다 클 것이다 (예를 들어, 0.64 mg). 유사하게, 시포니모드가 염, 예를 들어 시포니모드 헤미푸마레이트의 형태인 경우, 0.5 mg 시포니모드 유리 염기의 용량을 제공하는 데 필요한 염의 중량은 추가의 염 이온의 존재로 인해 0.5 mg보다 클 것이다.
본원에 사용된 바와 같은, "단위 용량", "단위 용량들" 및 "단위 투여 형태 (들)"는 단일 약물 투여 실재물/실재물들을 의미한다.
본원에 사용된 바와 같이, 수치 값 또는 범위의 맥락에서의 "약"은 언급되거나 청구되는 수치 값 또는 범위의 ±10%를 의미한다.
파라미터 범위가 제공되는 경우, 그 범위 내의 모든 정수, 및 그의 10분의 1 단위도 본 발명에 의해 또한 제공되는 것으로 이해된다. 예를 들어, "0.1-2.5 mg/일"은 0.1 mg/일, 0.2 mg/일, 0.3 mg/일 등 내지 2.5 mg/일까지 포함한다.
조합물
:
본 발명은 동시, 개별 또는 순차적 사용을 위한, 시포니모드 및 라퀴니모드를 포함하는 조합물, 예컨대 조합된 제제 또는 제약 조성물에 관한 것이다.
본원에 사용된 바와 같은 용어 "조합된 제제"는, 시포니모드 및 라퀴니모드가 개별 형태로 또는 구별되는 양의 활성 성분과의 상이한 고정된 조합물의 사용에 의해, 독립적으로 투여될 수 있다는 의미에서 특별히 "부분의 키트(kit of parts)"를 정의한다. 조합된 제제로 투여되는 시포니모드의 양에 대한 라퀴니모드의 비는, 예를 들어 치료받는 환자 하위 집단의 필요성 또는 단일 환자의 필요성에 대처하기 위해 다양할 수 있으며, 이러한 필요성은 환자의 연령, 성별, 체중 등에 따라 상이할 수 있다. 부분의 키트의 부분은 부분의 키트의 임의의 부분에 대해, 예를 들어 상이한 시점에서 그리고 동등하거나 상이한 시간 간격으로 동시에 또는 시간별로 시차를 두고 투여될 수 있다.
조합물은 부가 요법(add-on therapy)으로서 추가로 사용될 수 있다. 본원에 사용된 바와 같이, "부가" 또는 "부가 요법"은 요법에서 사용하기 위한 시약의 집합을 의미하며, 치료를 받는 대상체는 제1 치료 요법에 부가하여 1종 이상의 상이한 시약의 제2 치료 요법을 시작하기 전에 1종 이상의 시약의 제1 치료 요법을 시작하여, 요법에 사용되는 모든 시약이 동시에 시작되지는 않도록 한다. 예를 들어, 시포니모드 요법을 이미 받는 환자에게 라퀴니모드 요법을 부가하는 것.
시포니모드 및 라퀴니모드를 포함하는 조합물의 투여는 시포니모드 및 라퀴니모드를 포함하는 조합물에서 사용되는 활성 성분 중 단지 하나를 적용하는 단독요법과 비교하여, 유익한, 예를 들어 상승작용적 치료 효과 또는 다른 놀라운 유익한 효과, 예를 들어 더 거의 없고/거나 약한 부작용을 초래한다.
특히, 유효 용량 미만의(subeffective dose) 시포니모드 및 유효 용량 미만의 라퀴니모드를 포함하는, 시포니모드 및 라퀴니모드를 포함하는 조합물은 어느 한 화합물 단독의 유효 용량과 동일한 효과를 달성할 수 있다.
특히, 라퀴니모드에 반응하지 않는 환자에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은 시포니모드 단독을 사용한 단독요법과 비교하여 더 높은 치료 효과를 달성할 수 있다.
특히, 시포니모드에 반응하지 않는 환자에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은 라퀴니모드 단독을 사용한 단독요법과 비교하여 더 높은 치료 효과를 달성할 수 있다.
추가 이점은 라퀴니모드 또는 시포니모드 중 단지 하나를 적용하는 단독요법과 비교하여 시포니모드 및 라퀴니모드의 더 낮은 용량을 사용할 수 있다는 점이다. 예를 들어, 사용된 투여량은 더 작을뿐만 아니라, 덜 빈번하게 적용될 수도 있다. 또한, 부작용의 발생률이 감소될 수 있고/거나 라퀴니모드 또는 시포니모드를 기반으로 하는 요법에 대한 응답자 비가 더 높을 수 있다. 이 모든 것은 치료받는 환자의 욕구와 요구 사항에 따른다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 시포니모드 및 라퀴니모드는 치료 유효량으로 존재한다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 시포니모드 및 라퀴니모드는 상승작용적 치료 효과를 초래하는 양으로 존재한다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.1 내지 10 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.1 내지 2.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.1 내지 1.2 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.1 내지 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.2 내지 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 1.2 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.6 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.3 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 라퀴니모드의 양은 0.25 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 라퀴니모드는 라퀴니모드 소듐이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 0.1 내지 10 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 0.1 내지 2.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 0.25 내지 1.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 0.5 내지 1.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 2.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 1.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 1.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 조합물 중 시포니모드의 양은 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드를 포함하는 조합물을 제공하며, 여기서 시포니모드는 시포니모드 헤미푸마레이트이다.
시포니모드
및
라퀴니모드를
포함하는 제약 조성물:
본 발명은 또한 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 제약 조성물에 관한 것이다.
"제약상 허용되는 담체"는 과도한 유해한 부작용 (예컨대 독성, 자극, 및 알레르기 반응) 없이 인간 및/또는 동물과 사용하기에 적합하며 합리적인 이익/위험 비에 부합하는 담체 또는 부형제를 지칭한다. 상기 담체는 본 발명의 화합물을 대상체에게 전달하기 위한, 제약상 허용되는 용매, 현탁제 또는 비히클일 수 있다.
치료 유효량의 활성 성분 및 1종 이상의 제약상 허용되는 담체를 포함하는, 본 발명에 따른 제약 조성물은, 온혈 동물 (인간 및 동물)에게, 바람직하게는, 경장 투여, 예컨대 경구 또는 직장 투여; 또는 비경구 투여, 예컨대 근육내, 정맥내, 비강 또는 경피 투여에 적합하다.
경구 투여용 조성물이 바람직하다.
경장 또는 비경구 투여를 위한 조성물은 예를 들어, 단위 투여 형태, 예컨대 정제, 캡슐, 좌제 또는 앰플이다.
개개 용량 중 활성 성분의 단위 함량은, 이러한 양이 복수의 용량 단위의 투여에 의해 도달될 수 있기 때문에, 그 자체로 치료 유효량을 구성할 필요는 없다. 본 발명에 따른 조성물은, 예를 들어, 활성 성분의 치료 유효량의 약 10% 내지 약 100%를 함유할 수 있다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.1 내지 10 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.1 내지 2.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.1 내지 1.2 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.1 내지 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.2 내지 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 1.2 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.6 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.3 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 라퀴니모드의 양은 0.25 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 라퀴니모드는 라퀴니모드 소듐이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 0.1 내지 10 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 0.1 내지 2.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 0.25 내지 1.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 0.5 내지 1.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 2.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 1.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 1.0 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 조성물 중 시포니모드의 양은 0.5 mg이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 조성물을 제공하며, 여기서 시포니모드는 시포니모드 헤미푸마레이트이다.
달리 명시되지 않으면, 본 발명에 따른 제약 조성물은, 예를 들어 종래의 혼합, 과립화, 코팅, 용해 또는 동결 건조 공정에 의해 그 자체로 공지된 방식으로 제조된다. 경구 투여 형태용 조성물을 제조하는 데 있어서, 통상의 제약 매질 중 임의의 것, 예를 들어 물, 글리콜, 오일, 알콜, 담체, 예컨대 전분, 당, 또는 미세결정질 셀룰로스, 희석제, 과립화제, 윤활제, 결합제, 붕해제 등이 사용될 수 있다. 정제 및 캡슐은, 그의 투여가 용이하기 때문에, 가장 유리한 경구 투여 단위 형태를 나타내며, 이 경우에 고체 제약 담체가 분명히 사용된다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 제약 조성물을 제공하며, 여기서 조성물은 정제 또는 캡슐이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 제약 조성물을 제공하며, 여기서 조성물은 정제이다.
한 실시양태에서, 본 발명은 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 제약 조성물을 제공하며, 여기서 조성물은 캡슐이다.
자가면역 질환, 예를 들어
SPMS를
치료하기 위해
시포니모드
및
라퀴니모드를
포함하는
조합물을
사용:
놀랍게도, 시포니모드 및 라퀴니모드를 포함하는 조합물이 치유적 EAE 모델, 즉 EAE를 MOG/CFA/백일해 독소 주입에 의해 유도하고 임상 증상이 분명해진 후에 C57/Bl6 마우스에게 투여하는 것에서, 림프구의 수를 상승작용적으로 감소시키고 질환 부담을 개선하는 데 효과적인 것으로 밝혀졌다.
이 모델은 손상된 CNS (예를 들어 질환 발병 후에/재발이 발생한 후)에게 투여된 MS 치료를 위한 모델이므로, 이 모델은 말기 단계의 RRMS 환자 또는 SPMS 환자와 특별히 관련이 있으며 임상적으로 정상인 환자의 재발 방지를 위한 것은 아니다.
결과적으로, 시포니모드 단독을 사용하는 요법과 비교하여, 시포니모드 및 라퀴니모드를 포함하는 조합물은 염증성 사건, 예를 들어 SPMS 환자의 CNS에서 뇌척수막에서의 염증을 감소시키는 것이 가능할 수 있고/있거나 (ii) SPMS 환자에서 재발의 횟수 및/또는 중증도를 효과적으로 감소시킨다.
시포니모드 및 라퀴니모드를 포함하는 조합물은 자가면역 질환, 예컨대 다발성 경화증 (MS), 예를 들어 재발 완화형 MS (RRMS), 일차 진행형 MS (PPMS), 이차 진행형 MS (SPMS) 및 재발형 SPMS의 치료에서 사용될 수 있다. 본 발명의 시포니모드는 바람직하게는 RRMS 및/또는 SPMS, 가장 바람직하게는 SPMS의 치료에 사용된다.
SPMS"는 "초기 재발 완화형 질환 과정 후에 간헐적 재발, 약한 완화 및 정체기가 있거나 또는 없이 진행되는 것"으로 정의된다 (Lublin, F.D., Reingold, S.C. (1996) Defining the clinical course of multiple sclerosis. Neurology, 46: 907-911). 재발 완화형 질환 과정을 가진 MS의 진단은 2010년 개정 맥도날드(2010 Revised McDonald) 기준에 의해 정의된다. (Polman CH, Reingold S, Banwell B, et al. (2011) Diagnostic criteria for multiple sclerosis: 2010 revisions to the McDonald criteria. Ann Neurol; 68: 292-302). 진행은 지난 6개월에 걸쳐 신경학적 손상의 지속적인 악화를 의미하고 (Rovaris M., Confavreux C., Furlan R. et al. (2006). Secondary progressive multiple sclerosis: current knowledge and future challenges; Lancet Neurology 5: 343-354) 재발로부터의 불완전한 회복으로 설명되지 않는다 (Lublin, F.D., Baier, M., Cutter, G. (2003) Effect of relapses on development on residual deficit in multiple sclerosis. Neurology, 51: 1528-1532).
한 실시양태에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은 재발의 부재 또는 재발과 무관하게 적어도 6개월의 지속 기간의 장애의 점진적인 증가를 특징으로 하는 SPMS 환자의 치료에 사용된다.
한 실시양태에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은 2.0 내지 8.0, 보다 바람직하게는 2.5 내지 7.0, 가장 바람직하게는 3.0 내지 6.5의 EDSS 점수를 가진 장애 상태를 갖는 SPMS 환자의 치료에 사용된다.
"EDSS"는 다발성 경화증에서의 장애를 정량화하는 방법인, 쿠르츠케 확장 장애 상태 척도(Kurtzke Expanded Disability Status Scale)를 나타낸다 (표 1 참조). EDSS는 여덟 가지의 기능 계통(Functional Systems) (FS)에서 장애를 정량화하고 이들 중 각각에서 신경과 전문의가 기능 계통 점수(Functional System Score) (FSS)를 할당할 수 있게 한다. 쿠르츠케는 기능 계통을 다음과 같이 정의한다: 피라미드, 소뇌, 뇌간, 감각, 장 및 방광, 시각, 대뇌, 기타.
기능 계통 (FS)은 임상적으로 관찰된 장애의 수준을 가장 잘 반영하기 위해 0 (낮은 수준의 문제)에서 5 (높은 수준의 문제)의 등급으로 점수가 매겨진다. "기타" 카테고리는 수치로 등급이 매겨지지는 것이 아니라, 운동 손실과 같은 특정 사안과 관련된 장애를 측정한다.
대조적으로, 총 EDSS 점수는 두 가지 인자, 즉 보행 및 FS 점수에 의해 결정된다. 4.0 미만의 EDSS 점수는 FS 점수 단독에 의해 결정된다. 4.0 이상의 EDSS 점수를 가진 사람들은 어느 정도의 보행 장애가 있다. 4.0 내지 9.5의 점수는 보행 능력 및 FS 점수 둘 다에 의해 결정된다.
<표 1> - 쿠르츠케 확장 장애 상태 척도
본원에 사용된 바와 같은 용어 "치료"/"치료하는"은 다음을 포함한다: (1) 상태, 장애 또는 병태를 앓거나 그에 걸리기 쉬울 수 있지만 아직 이러한 상태, 장애 또는 병태의 임상적 또는 준임상적 증상을 경험하지 않거나 나타내지 않는, 동물, 특히 포유동물, 특별히 인간에서 발생하는 상태, 장애 또는 병태의 임상적 증상의 출현을 예방하거나 지연시키는 것; (2) 상태, 장애 또는 병태를 억제하는 것 (예를 들어 질환의 진행, 또는 유지 치료의 경우 그의 재발, 질환의 적어도 하나의 임상적 또는 준임상적 증상을 저지, 감소 또는 지연시키는 것); 및/또는 (3) 병태를 경감시키는 것 (즉, 상태, 장애 또는 병태, 또는 그의 임상적 증상 또는 준임상적 증상 중 적어도 하나의 퇴행을 유발하는 것)을 포함한다. 치료받는 환자에 대한 이익은 통계적으로 유의하거나 환자나 의사에게 적어도 인지할 수 있다. 그러나, 의약을 환자에게 투여하여 질환을 치료하는 경우, 결과가 항상 효과적인 치료가 아닐 수 있음을 이해할 것이다.
한 실시양태에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은 RRMS 또는 SPMS, 바람직하게는 SPMS의 증상을 감소시키는 데 효과적이다. 한 실시양태에서, 증상은 MRI-모니터링된 다발성 경화증 질환 활성, 장애 진행, 뇌 위축, 신경 기능장애(neuronal dysfunction), 신경 손상, 신경 퇴행, 시각 기능의 저하, 운동 장애, 인지 장애, 뇌 부피의 감소, 전반적인 건강 상태의 저화, 기능 상태 및/또는 삶의 질이다.
한 실시양태에서, SPMS를 가진 환자에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은, 예를 들어 EDSS에 의해 평가된 바와 같이, 장애 진행을 지연시킨다.
한 실시양태에서, 치료는 치료되지 않은 환자와 비교하여 EDSS에 의해 측정된 바와 같이 SPMS를 가진 환자에서 3개월의 확인된 장애 진행까지의 시간을 증가시키는 것을 포함한다. EDSS에 의해 측정한 바와 같은 장애 진행은 전형적으로 적어도 1점 (3.0 또는 5.0의 기준치 EDSS 점수를 가진 환자에서) 또는 적어도 0.5 점 (5.5 내지 6.5의 기준치 EDSS 점수를 가진 환자에서)의 기준치로부터의 증가로 정의된다. 진행이 지속되는 지를 확인하기 위해, 이 증가는 3개월 후에 방문에서 존재하여야 한다.
한 실시양태에서, 3개월의 확인된 장애 진행까지의 시간은 적어도 10% 증가된다.
한 실시양태에서, 3개월의 확인된 장애 진행까지의 시간은 적어도 25% 증가된다.
한 실시양태에서, 3개월의 확인된 장애 진행까지의 시간은 적어도 20 내지 75% 증가된다.
한 실시양태에서, 3개월의 확인된 장애 진행까지의 시간은 적어도 10 내지 75% 증가된다.
또 다른 실시양태에서, 3개월의 확인된 장애 진행까지의 시간은 적어도 25 내지 50% 증가된다.
또 다른 실시양태에서, 3개월의 확인된 장애 진행까지의 시간은 적어도 25 내지 40% 증가된다.
한 실시양태에서, SPMS를 가진 환자에서, 본 발명의 시포니모드 및 라퀴니모드를 포함하는 조합물은, 예를 들어 시간 측정 25-피트 보행 시험(timed 25-foot walk test) (T25-FW)에 의해 평가된 바와 같이, 운동 장애의 악화를 지연시킨다.
T25-FW는 시간 측정 25-보행에 기반한 정량적 운동능력(mobility) 및 다리 기능 수행 시험이다. 환자는 명확하게 표시된 25-피트 코스의 한쪽 끝으로 향하며, 가능한 빠르지만 안전하게 25 피트를 보행하도록 지시된다. 시간은 출발 지시의 개시로부터 계산되며, 환자가 25-피트 표시에 도달되었을 때 종료한다. 과제는 환자가 동일 거리를 걸어서 되돌아오게 함으로써 즉시 다시 반복된다. T25-FW는 상지 기능, 보행 및 인지 기능을 평가하는 복합 척도인, 다발성 경화증 기능성 복합(Multiple Sclerosis Functional Composite) (MSFC)의 세 구성요소 중 하나이다 (Fisher JS et al. for the National MS Society Clinical Outcomes Assessment Task Force (1999). The multiple sclerosis functional composite measure: an integrated approach to MS clinical outcome assessment. Mult Scler; 5: 244-250).
한 실시양태에서, 치료는 치료되지 않은 환자와 비교하여 T25-FW에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간을 지연시키는 것을 포함한다.
한 실시양태에서, 치료되지 않은 환자와 비교하여 T25-FW에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간은 적어도 10% 증가된다.
한 실시양태에서, 치료되지 않은 환자와 비교하여 T25-FW에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간은 적어도 25% 증가된다.
한 실시양태에서, 치료되지 않은 환자와 비교하여 T25-FW에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간은 10 내지 80% 증가된다.
한 실시양태에서, 치료되지 않은 환자와 비교하여 T25-FW에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간은 20 내지 80% 증가된다.
또 다른 실시양태에서, 치료되지 않은 환자와 비교하여 T25-FW에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간은 25 내지 70% 증가된다.
또 다른 실시양태에서, 치료되지 않은 환자와 비교하여 T25-FW에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간은 25 내지 50% 증가된다.
한 실시양태에서, SPMS를 가진 환자에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은, T2 병변 부피의 증가, 예를 들어 자기 공명 영상화 (MRI)에 의해 측정된, 치료되지 않은 환자와 비교하여 기준치로부터의 치료 2년 이내의 증가를 감소시킨다. T2 병변은 T2 콘트라스트를 강조하는 MR-영상을 사용하여 검출된다. T2 병변은 새로운 염증 활성을 나타낸다.
한 실시양태에서, 기준치로부터의 치료 2년 이내에 T2 병변 부피의 증가가 치료되지 않은 환자와 비교하여 적어도 10% 감소된다.
한 실시양태에서, 기준치로부터의 치료 2년 이내에 T2 병변 부피의 증가가 치료되지 않은 환자와 비교하여 적어도 25% 감소된다.
한 실시양태에서, 기준치로부터의 치료 2년 이내에 T2 병변 부피의 증가가 치료되지 않은 환자와 비교하여 10 내지 100% 감소된다.
한 실시양태에서, 기준치로부터의 치료 2년 이내에 T2 병변 부피의 증가가 치료되지 않은 환자와 비교하여 20 내지 100% 감소된다.
또 다른 실시양태에서, 기준치로부터의 치료 2년 이내에 T2 병변 부피의 증가가 치료되지 않은 환자와 비교하여 25 내지 90% 감소된다.
또 다른 실시양태에서, 기준치로부터의 치료 2년 이내에 T2 병변 부피의 증가가 치료되지 않은 환자와 비교하여 30 내지 80% 감소된다.
한 실시양태에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은 퍼센트 뇌 부피 변화에 의해 측정된, SPMS를 가진 환자에서 뇌 부피의 감소를 저하시키거나 억제한다.
한 실시양태에서, SPMS를 가진 환자에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은, EQ-5D에 의해 정의된 바와 같이, 전반적인 건강 상태를 증가시키거나 전반적인 건강 상태의 저하를 지연시킨다. EQ-5D는 전반적인 건강 상태를 측정하기 위해 사용되는 표준화된 설문지이다. 그것은 다섯 가지 영역 (운동능력, 자기 관리, 평소의 활동, 통증/불편함, 불안/우울증)을 측정한다.
한 실시양태에서, SPMS를 가진 환자에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은, 다발성 경화증의 신체적 (20개 항목) 및 심리적 (9개 항목) 영향을 측정하는 도구인, 다발성 경화증 영향 척도(Multiple Sclerosis Impact Scale) (MSIS-29)에 의해 측정된 바와 같은 건강-관련 삶의 질을 증가시키거나 그의 감소를 지연시킨다.
한 실시양태에서, SPMS를 가진 환자에서, 시포니모드 및 라퀴니모드를 포함하는 조합물은, 연간 재발률을 감소시킨다. 본원에 사용된 바와 같은 용어 "재발률"은 단위 시간당 확인된 재발의 횟수를 의미한다. 본원에 사용된 바와 같은 용어 "연간 재발률"은 각각의 환자의 확인된 재발의 횟수에 365을 곱하고 환자가 약물을 복용한 일수로 나눈 평균 값을 지칭한다.
본원에 사용된 바와 같은 용어 "대상체"는 바람직하게는 인간, 특별히 MS, 예를 들어 SPMS로 진단된 환자를 지칭한다.
본원에 사용된 바와 같은 용어 "치료 유효량"은 전형적으로 대상체에게 투여시 치료 이익을 제공하기에 충분한, 예를 들어 SPMS를 치료, 예방 또는 진행을 지연시키는 데 충분한, 활성 성분 또는 활성 성분의 조합물의 양 (예를 들어, 양은 증상의 개선을 제공한다)을 지칭한다.
상기 언급된 적응증 (병태 및 장애)의 경우, 활성 성분의 적절한 투여량은, 예를 들어, 사용된 화합물의 고체 형태, 숙주, 투여 형태 및 치료되는 질환의 병태의 성질 및 중증도에 따라 달라질 것이다.
인간에서, 라퀴니모드에 대한 명시된 1일 투여량은, 예를 들어, 1일 4회 (예를 들어 시포니모드 및 라퀴니모드를 포함하는 조합물의 동일한 단위 투여 형태의 하루 4회 투여)까지 분할된 용량으로, 편리하게 투여되는 라퀴니모드의 약 0.1 내지 약 10 mg, 예를 들어 약 0.1 내지 약 2.0 mg 또는 약 0.1 내지 약 1.2 mg 범위이다.
인간에서, 시포니모드에 대한 명시된 1일 투여량은, 예를 들어, 1일 4회 (예를 들어 시포니모드 및 라퀴니모드를 포함하는 조합물의 동일한 단위 투여 형태의 하루 4회 투여)까지 분할된 용량으로, 편리하게 투여되는 시포니모드의 약 0.1 내지 약 10 mg, 예를 들어 약 0.1 내지 약 2.0 mg 또는 약 0.25 내지 약 1.5 mg 범위이다.
통상의 기술자인 의사 또는 임상의는 적절한 투여량 요법을 쉽게 결정하고 처방할 것이다.
라퀴니모드의 단위 투여 형태는 0.1 - 10 mg 라퀴니모드 (경구용)를 함유할 수 있다.
시포니모드의 단위 투여 형태는 0.1 - 10 mg 라퀴니모드 (경구용)를 함유할 수 있다.
상기 언급된 장애, 예를 들어 SPMS의 치료에서 시포니모드 및 라퀴니모드를 포함하는 조합물의 유용성은, 아래 명시된 것들을 포함한 다양한 표준 시험에서 확인할 수 있다.
실시예
실시예
1: 동물 모델로부터의 데이터
실시예
1.1: 마우스에서 뇌척수액 (
CSF
) 중의
시포니모드의
수준
암컷 C57Bl/6 마우스를 8일 동안 매일 3 mg/kg 시포니모드로 경구로 처리하였다. 마지막 투여 후 8시간에, 동물을 희생시키고 혈액, 뇌 및 CSF에서 시포니모드의 수준을 측정하였다.
데이터를 아래의 표 1에 요약하였다. 3-5 마리의 동물의 평균값 및 평균의 표준 오차 (괄호 안에)를 나타냈다
<표 1>
상기 표는 시포니모드 (3 mg/kg 마우스에서)의 임상적으로 관련된 용량이 S1P1 (0.4 nM) 및 S1P5 (1 nM)에 대한 EC50 초과로 CSF에서 노출을 야기한다는 것을 나타낸다.
실시예
1.2:
MOG
/CFA/백일해 독소-처리 C57/
Bl6
마우스에서 림프구를 감소시키기 위한
시포니모드
,
라퀴니모드
및 그의
조합물의
사용
암컷 C57Bl/6 마우스를 CFA 중 200 ㎍의 재조합 MOG1-125로 피하 면역화시킨 후, 100 ng의 백일해 독소를 1회 복강내 주사하였다. 2일 후 100 ng의 백일해 독소의 추가의 복강내 주사를 투여하였다. 최초 임상적 증상 후 3일에, 마우스를 비히클, 0.3 mg/kg 시포니모드, 10 mg/kg 라퀴니모드 또는 0.3 mg/kg 시포니모드 + 10 mg/kg 라퀴니모드에 무작위화하여 29일 동안 상기 용량으로 매일 처리하였다. C57/Bl6 마우스에서의 MOG/CFA/백일해 독소-유도 실험적 자가면역 뇌척수염 모델은 문헌 [Quancard et al (Chem Biol. 19(9):1142-51, 2012)]에 기재되어 있다.
결과를 도 1에 나타냈다. 10 mg/kg 라퀴니모드를 사용한 처리는 림프구를 유의하게 감소시키지 않았다. 0.3 mg/kg 시포니모드를 사용한 처리는 림프구를 감소시켰다. 0.3 mg/kg 시포니모드 + 10 mg/kg 라퀴니모드의 조합물은 림프구 감소에 상승작용적 효과를 나타냈다. 통계적 유의성 p <0.05.
실시예
1.2: C57/
Bl6
마우스에서
MOG
/CFA/백일해 독소-면역 실험적 자가면역 뇌척수염 (
EAE
)을 치료하기 위한
시포니모드
,
라퀴니모드
및 그의
조합물의
사용
암컷 C57Bl/6 마우스를 CFA 중 200 ㎍의 재조합 MOG1-125로 피하 면역화시킨 후, 100 ng의 백일해 독소를 1회 복강내 주사하였다. 2일 후 100 ng의 백일해 독소의 추가의 복강내 주사를 투여하였다. 최초 임상적 증상 후 3일에, 마우스를 비히클, 0.3 mg/kg 시포니모드, 10 mg/kg 라퀴니모드 또는 0.3 mg/kg 시포니모드 + 10 mg/kg 라퀴니모드에 무작위화하여 30일 동안 상기 용량으로 매일 처리하였다. 중증 CNS 신경학적 질환 및 조직 손상이 발생한 후 처리가 개시되었다. 보다 구체적으로는 뒷다리 마비를 특징으로 할 수 있는 중증 CNS 손상이 이미 발생한 후에.
결과를 도 2에 나타냈다. 10 mg/kg 라퀴니모드를 사용한 처리는 질환 부담 (누적 EAE 점수)을 유의하게 개선하지 않았다. 0.3 mg/kg 시포니모드를 사용한 처리는 질환 부담 (누적 EAE 점수)을 감소시켰다. 0.3 mg/kg 시포니모드 + 10 mg/kg 라퀴니모드의 조합물은 비히클-처리 동물과 비교하여 유의하게 개선된 질환 부담 (누적 EAE 점수)을 나타냈다. 통계적 유의성 p <0.05.
실시예
1.3: C57/
Bl6
마우스에서에서
실험적 자가면역 뇌척수염 (
EAE
) 동안에 혈액 및 뇌 조직 중의 시포니모드 및 라퀴니모드의 수준
암컷 C57Bl/6 마우스를 CFA 중 200 ㎍의 재조합 MOG1-125로 피하 면역화시킨 후, 100 ng의 백일해 독소를 1회 복강내 주사하였다. 2일 후 100 ng의 백일해 독소의 추가의 복강내 주사를 투여하였다. 마우스에게 비히클, 0.3 mg/kg 시포니모드, 10 mg/kg 라퀴니모드 또는 0.3 mg/kg 시포니모드 + 10 mg/kg 라퀴니모드를 최대 21일 동안 투여하였다. 면역 세포가 CNS에 진입하여 마비 및 국소화된 조직 손상을 초래한 후에 치료가 개시되었다.
결과를 도 3에 나타냈다. 조합 요법은 시포니모드 또는 라퀴니모드의 혈액 또는 뇌 농도를 유의하게 변경시키지 않았다. 약물-약물 상호작용의 어떤 증거도 없었다. 조합 요법의 효능은 향상된 생물학적 반응을 나타낸다. 통계적 유의성 없음 p > 0.05.
실시예
1.4: C57/
Bl6
마우스에서
MOG
/CFA/백일해 독소-면역 실험적 자가면역 뇌척수염 (
EAE
)을 치료하기 위한
시포니모드
,
라퀴니모드
및 그의
조합물의
사용
암컷 C57Bl/6 마우스를 CFA 중 200 ㎍의 재조합 MOG1-125로 피하 면역화시킨 후, 100 ng의 백일해 독소를 1회 복강내 주사하였다. 2일 후 100 ng의 백일해 독소의 추가의 복강내 주사를 투여하였다. 면역 세포가 CNS에 침윤하여 조직 손상을 개시한 후에, 마우스를 비히클, 0.3 mg/kg 시포니모드, 10 mg/kg 라퀴니모드 또는 0.3 mg/kg 시포니모드 + 10 mg/kg 라퀴니모드에 무작위화하여 21일 동안 상기 용량으로 매일 처리하였다.
결과를 도 4에 나타냈다. 10 mg/kg 라퀴니모드를 사용한 처리는 매일 질환의 중증도를 유의하게 개선하지 않았다. 0.3 mg/kg 시포니모드를 사용한 처리는 일시적으로 신경 마비를 감소시켰지만 (면역 후 18-21일), 동물은 궁극적으로 만성적인 비-완화기(non-remitting phase)로 진입하였다. 0.3 mg/kg 시포니모드 + 10 mg/kg 라퀴니모드의 조합물은 비히클-처리 동물과 비교하여 유의하게 개선된 질환 부담을 나타냈다. 신경 마비로부터의 회복은 라퀴니모드 또는 시포니모드 단독요법보다 유의하게 더 컸다. 통계적 유의성 p < 0.05.
실시예
2: 임상 연구
이차 진행형 다발성 경화증을 가진 환자에서 시포니모드와 라퀴니모드의 조합물의 효능 및 안전성을 평가하는 다기관, 무작위, 이중 맹검, 평행 군, 위약-대조 가변 치료 지속기간 연구
1. 연구 목표
a) 일차 목표
일차 목표는 EDSS에 의해 측정된 바와 같이 SPMS를 가진 환자에서 3개월의 확인된 장애 진행까지의 시간을 지연시키는 데 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 입증하는 것이다.
b) 핵심 이차 목표
제1 핵심 이차 목표는 시간 측정 25-피트 보행 시험 (T25-FW)에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화까지의 시간을 지연시키는 데 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 입증하는 것이다.
제2 핵심 이차 목표는 기준치로부터 연구의 종료까지 T2 병변 부피의 증가를 감소시키는 데 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 입증하는 것이다.
c) 추가의 이차 목표는 다음을
포함한다
· EDSS에 의해 측정된 바와 같이 6개월의 확인된 장애 진행까지의 시간을 지연시키는 데 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 평가하는 것
· 연간 재발률 (ARR)에 의해 평가된 바와 같이 확인된 재발의 빈도를 감소시키는 데 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 평가하는 것, 및 최초 재발까지의 시간 및 재발이 없는 환자의 비율을 평가하는 것
· 환자가 보고한 결과인 다발성 경화증 보행 척도(Multiple Sclerosis Walking Scale) (MSWS-12)에 대해 위약과 비교하여 시포니모드와 라퀴니모드의 조합물의 영향을 평가하는 것
· 통상의 MRI에 의해 측정된 바와 같은, 염증성 질환 활성 및 질환의 부담 (T1 Gd-증진 병변, 신규 또는 확대 T2 병변, 뇌 부피)에 관하여, 위약과 비교하여 시포니모드와 라퀴니모드의 조합물의 효능을 평가하는 것
· 시포니모드와 라퀴니모드의 조합물 대 위약의 안전성 및 내약성을 평가하는 것
d) 탐구적 목표는 다음을
포함한다
· 하기 환자가 보고한 결과에 대해 위약과 비교하여 시포니모드와 라퀴니모드의 조합물의 영향을 평가하는 것:
· 다발성 경화증 영향 척도 (MSIS-29)에 의해 측정된 바와 같은 건강-관련 삶의 질 (QoL)
· EQ-5D에 의해 측정된 바와 같은 건강-관련 삶의 질 (QoL)
· 정의된 인지 검사에 대한 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 탐구하는 것:
· 페이스드 청각 연속 덧셈 검사(Paced Auditory Serial Addition Test) (PASAT)
· 기호 숫자 모달리티 검사(Symbol Digit Modalities Test) (SDMT)
· 개정된 간편 시공간 기억 검사(Brief Visuospatial Memory Test Revised) (BVMTR)
· MRI에 의한 만성 블랙홀(black hole)로의 급성 병변의 진화에서 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 평가하는 것
· MSFC z-점수에 대해 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 평가하는 것
· 다음까지의 시간을 지연시키는 데 위약에 비해서 시포니모드와 라퀴니모드의 조합물의 효능을 평가하는 것 :
· 시간 측정 25-피트 보행 시험 (T25W)에서의 기준치로부터의 적어도 20%의 3개월의 확인된 악화 또는
· EDSS 점수에 의해 측정된 바와 같은 3개월의 확인된 장애 진행
· 손 중 어느 한쪽 (우성 또는 비우성)에서 9-홀 펙 검사(9-hole peg test) (9-HPT)에서 기준선으로부터 적어도 20%의 3개월의 확인된 악화
· 장애 진행 종점과 약물 농도/림프구 수 사이의 관계를 탐구하는 것
· 선택된 안전성 파라미터와 약물 농도/림프구 수 사이의 관계를 탐구하는 것
· 시포니모드 및 라퀴니모드의 약역학을 평가하는 것
2. 모집단
연구 모집단은 이차 진행형 질환 과정을 가진 MS (SPMS)로 진단받은 18세 내지 60세 연령이고 3.0 내지 6.5의 EDSS 점수를 가진 보행가능 환자로 이루어진다.
3. 연구 설계
이는 SPMS를 가진 환자에서 무작위화, 다기관, 이중 맹검, 위약-대조 병행 군 연구이다. 환자는 무작위화되어 시포니모드와 라퀴니모드의 조합물 또는 위약 중 어느 하나를 수령한다.
다음은 본 발명의 추가 실시양태이다:
실시양태 1: 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연에서 사용하기 위한, 시포니모드 및 라퀴니모드를 포함하는 조합물.
실시양태 1.1: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 10 mg인 조합물.
실시양태 1.2: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 1.3: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 1.2 mg인 조합물.
실시양태 1.4: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 0.5 mg인 조합물.
실시양태 1.5: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.2 내지 0.5 mg인 조합물.
실시양태 1.6: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 1.2 mg인 조합물.
실시양태 1.7: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.6 mg인 조합물.
실시양태 1.8: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.5 mg인 조합물.
실시양태 1.9: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.3 mg인 조합물.
실시양태 1.10: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.25 mg인 조합물.
실시양태 1.11: 실시양태 1 내지 1.10 중 어느 한 실시양태에 있어서, 라퀴니모드가 라퀴니모드 소듐인 조합물.
실시양태 1.12: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.1 내지 10 mg인 조합물.
실시양태 1.13: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 1.14: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.25 내지 1.5 mg인 조합물.
실시양태 1.15: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.5 내지 1.0 mg인 조합물.
실시양태 1.16: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 2.0 mg인 조합물.
실시양태 1.17: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 1.5 mg인 조합물.
실시양태 1.18: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 1.0 mg인 조합물.
실시양태 1.19: 실시양태 1 내지 1.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.5 mg인 조합물.
실시양태 1.20: 실시양태 1 내지 1.19 중 어느 한 실시양태에 있어서, 시포니모드가 시포니모드 헤미푸마레이트인 조합물.
실시양태 2: 의약으로서 사용하기 위한, 시포니모드 및 라퀴니모드를 포함하는 조합물.
실시양태 2.1: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 10 mg인 조합물.
실시양태 2.2: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 2.3: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 1.2 mg인 조합물.
실시양태 2.4: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 0.5 mg인 조합물.
실시양태 2.5: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.2 내지 0.5 mg인 조합물.
실시양태 2.6: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 1.2 mg인 조합물.
실시양태 2.7: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.6 mg인 조합물.
실시양태 2.8: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.5 mg인 조합물.
실시양태 2.9: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.3 mg인 조합물.
실시양태 2.10: 실시양태 2에 있어서, 조합물 중 라퀴니모드의 양이 0.25 mg인 조합물.
실시양태 2.11: 실시양태 2 내지 2.10 중 어느 한 실시양태에 있어서, 라퀴니모드가 라퀴니모드 소듐인 조합물.
실시양태 2.12: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.1 내지 10 mg인 조합물.
실시양태 2.13: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 2.14: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.25 내지 1.5 mg인 조합물.
실시양태 2.15: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.5 내지 1.0 mg인 조합물.
실시양태 2.16: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 2.0 mg인 조합물.
실시양태 2.17: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 1.5 mg인 조합물.
실시양태 2.18: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 1.0 mg인 조합물.
실시양태 2.19: 실시양태 2 내지 2.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.5 mg인 조합물.
실시양태 2.20: 실시양태 2 내지 2.19 중 어느 한 실시양태에 있어서, 시포니모드가 시포니모드 헤미푸마레이트인 조합물.
실시양태 3: 시포니모드 및 라퀴니모드를 포함하는 조합물.
실시양태 3.1: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 10 mg인 조합물.
실시양태 3.2: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 3.3: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 1.2 mg인 조합물.
실시양태 3.4: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 0.5 mg인 조합물.
실시양태 3.5: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.2 내지 0.5 mg인 조합물.
실시양태 3.6: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 1.2 mg인 조합물.
실시양태 3.7: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.6 mg인 조합물.
실시양태 3.8: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.5 mg인 조합물.
실시양태 3.9: 실시양태 3에 있어서, 조합물 중 라퀴니모드의 양이 0.3 mg인 조합물.
실시양태 3.10: 실시양태 1에 있어서, 조합물 중 라퀴니모드의 양이 0.25 mg인 조합물.
실시양태 3.11: 실시양태 3 내지 3.10 중 어느 한 실시양태에 있어서, 라퀴니모드가 라퀴니모드 소듐인 조합물.
실시양태 3.12: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.1 내지 10 mg인 조합물.
실시양태 3.13: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 3.14: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.25 내지 1.5 mg인 조합물.
실시양태 3.15: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.5 내지 1.0 mg인 조합물.
실시양태 3.16: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 2.0 mg인 조합물.
실시양태 3.17: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 1.5 mg인 조합물.
실시양태 3.18: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 1.0 mg인 조합물.
실시양태 3.19: 실시양태 3 내지 3.11 중 어느 한 실시양태에 있어서, 조합물 중 시포니모드의 양이 0.5 mg인 조합물.
실시양태 3.20: 실시양태 3 내지 3.19 중 어느 한 실시양태에 있어서, 시포니모드가 시포니모드 헤미푸마레이트인 조합물.
실시양태 4: 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 제약 조성물.
실시양태 4.1: 실시양태 4에 있어서, 조성물이 경구 투여용인 제약 조성물.
실시양태 4.2: 실시양태 4에 있어서, 조성물이 경구 투여용 고체 조성물인 제약 조성물.
실시양태 4.3: 실시양태 4에 있어서, 조성물이 정제 또는 캡슐인 제약 조성물.
실시양태 4.4: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.1 내지 10 mg인 제약 조성물.
실시양태 4.5: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 4.6: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.1 내지 1.2 mg인 조합물.
실시양태 4.7: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.1 내지 0.5 mg인 조합물.
실시양태 4.8: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.2 내지 0.5 mg인 조합물.
실시양태 4.9: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 1.2 mg인 조합물.
실시양태 4.10: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.6 mg인 조합물.
실시양태 4.11: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.5 mg인 조합물.
실시양태 4.12: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.3 mg인 조합물.
실시양태 4.13: 실시양태 4 내지 4.3 중 어느 한 실시양태에 있어서, 조성물 중 라퀴니모드의 양이 0.25 mg인 조합물.
실시양태 4.14: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 라퀴니모드는 라퀴니모드 소듐인 조합물.
실시양태 4.15: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 0.1 내지 10 mg인 조합물.
실시양태 4.16: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 0.1 내지 2.0 mg인 조합물.
실시양태 4.17: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 0.25 내지 1.5 mg인 조합물.
실시양태 4.18: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 0.5 내지 1.0 mg인 조합물.
실시양태 4.19: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 2.0 mg인 조합물.
실시양태 4.20: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 1.5 mg인 조합물.
실시양태 4.21: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 1.0 mg인 조합물.
실시양태 4.22: 실시양태 4 내지 4.13 중 어느 한 실시양태에 있어서, 조성물 중 시포니모드의 양이 0.5 mg인 조합물.
실시양태 4.21: 실시양태 4 내지 4.19 중 어느 한 실시양태에 있어서, 시포니모드가 시포니모드 헤미푸마레이트인 조합물.
실시양태 5:
(a) 라퀴니모드,
(b) 시포니모드,
(c) 이차 진행형 다발성 경화증의 치료에서 그의 동시, 개별 또는 순차적 사용을 위한 사용 설명서, 및
(d) 성분 (a) 및 (b)를 함유하는 적어도 하나의 용기를 포함하는 키트.
실시양태 6: 시포니모드 및 라퀴니모드를 포함하는 조합물 및 이차 진행형 다발성 경화증의 치료에서 그의 동시, 개별 또는 순차적 사용을 위한 서면 사용 설명서를 포함하는 제약 패키지.
실시양태 7: 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 위한 시포니모드 및 라퀴니모드를 포함하는 조합물의 용도.
실시양태 8: 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 위한 의약의 제조를 위한 시포니모드 및 라퀴니모드를 포함하는 조합물의 용도.
실시양태 9: 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 필요로 하는 대상체에게 치료 유효량의, 시포니모드 및 라퀴니모드를 포함하는 조합물을 투여하는 것을 포함하는, 상기 대상체에서 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연 방법.
실시양태 10: (i) 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 필요로 하는 대상체에서 상기 이차 진행형 다발성 경화증을 진단하고,
(ii) 상기 대상체에게 치료 유효량의, 시포니모드 및 라퀴니모드를 포함하는 조합물을 투여하는 것
을 포함하는, 상기 대상체에서 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연 방법.
상기 실시양태는 제공되어 본 발명을 예시하는 것이지, 제한하는 것이 아니다.
Claims (15)
- 시포니모드 및 라퀴니모드를 포함하는, 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연에서 사용하기 위한 조합물.
- 제1항에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 1.2 mg이고 조합물 중 시포니모드의 양이 0.1 내지 2.0 mg인 조합물.
- 제1항에 있어서, 조합물 중 라퀴니모드의 양이 0.2 내지 0.5 mg이고 조합물 중 시포니모드의 양이 0.5 내지 1.5 mg인 조합물.
- 시포니모드 및 라퀴니모드를 포함하는, 의약으로서 사용하기 위한 조합물.
- 제4항에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 1.2 mg이고 조합물 중 시포니모드의 양이 0.1 내지 2.0 mg인 조합물.
- 제4항에 있어서, 조합물 중 라퀴니모드의 양이 0.2 내지 0.5 mg이고 조합물 중 시포니모드의 양이 0.5 내지 1.5 mg인 조성물.
- 시포니모드 및 라퀴니모드를 포함하는 조합물.
- 제7항에 있어서, 조합물 중 라퀴니모드의 양이 0.1 내지 1.2 mg이고 조합물 중 시포니모드의 양이 0.1 내지 2.0 mg인 조합물.
- 제7항에 있어서, 조합물 중 라퀴니모드의 양이 0.2 내지 0.5 mg이고 조합물 중 시포니모드의 양이 0.5 내지 1.5 mg인 조성물.
- 시포니모드 및 라퀴니모드 및 적어도 1종의 제약상 허용되는 담체를 포함하는 제약 조성물.
- 제10항에 있어서, 경구 투여용 고체 조성물인 제약 조성물.
- 제10항 또는 제11항에 있어서, 조성물 중 라퀴니모드의 양이 0.1 내지 1.2 mg이고 조성물 중 시포니모드의 양이 0.1 내지 2.0 mg인 제약 조성물.
- 제10항 또는 제11항에 있어서, 조성물 중 라퀴니모드의 양이 0.2 내지 0.5 mg이고 조성물 중 시포니모드의 양이 0.5 내지 1.5 mg인 제약 조성물.
- 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 필요로 하는 대상체에게 치료 유효량의, 시포니모드 및 라퀴니모드를 포함하는 조합물을 투여하는 것을 포함하는, 상기 대상체에서 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연 방법.
- (i) 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연을 필요로 하는 대상체에서 상기 이차 진행형 다발성 경화증을 진단하고,
(ii) 상기 대상체에게 치료 유효량의, 시포니모드 및 라퀴니모드를 포함하는 조합물을 투여하는 것
을 포함하는, 상기 대상체에서 이차 진행형 다발성 경화증의 치료, 예방 또는 진행의 지연 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462064537P | 2014-10-16 | 2014-10-16 | |
| US62/064,537 | 2014-10-16 | ||
| PCT/IB2015/057870 WO2016059571A1 (en) | 2014-10-16 | 2015-10-14 | Combinations comprising siponimod and laquinimod for the treatment of multiple sclerosis |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170068480A true KR20170068480A (ko) | 2017-06-19 |
Family
ID=54352484
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177009900A Withdrawn KR20170068480A (ko) | 2014-10-16 | 2015-10-14 | 다발성 경화증의 치료를 위한 시포니모드 및 라퀴니모드를 포함하는 조합물 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US10537566B2 (ko) |
| EP (1) | EP3206682B1 (ko) |
| JP (1) | JP6731915B2 (ko) |
| KR (1) | KR20170068480A (ko) |
| CN (2) | CN114699409A (ko) |
| AU (1) | AU2015332037A1 (ko) |
| BR (1) | BR112017007414A2 (ko) |
| CA (1) | CA2964315A1 (ko) |
| ES (1) | ES2710460T3 (ko) |
| MX (1) | MX2017004808A (ko) |
| RU (1) | RU2017116740A (ko) |
| WO (1) | WO2016059571A1 (ko) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11840565B2 (en) | 2016-12-29 | 2023-12-12 | University Of Miami | Methods and compositions for treating virus-associated inflammation |
| JP2020535401A (ja) * | 2017-09-20 | 2020-12-03 | ユニバーシティ オブ マイアミ | 神経障害のバイオマーカーとしてインフラマソームタンパク質を検出するための方法 |
| CA3105129A1 (en) | 2018-07-03 | 2020-01-09 | University Of Miami | Compositions and methods for treating inflammasome related diseases or conditions |
| WO2020234423A1 (en) * | 2019-05-21 | 2020-11-26 | Synthon B.V. | Siponimod maleic acid and fumaric acid salt |
| IL292529A (en) * | 2019-10-31 | 2022-06-01 | Idorsia Pharmaceuticals Ltd | Combination of cxcr7 antagonist with s1p1 receptor modulator |
| WO2021158843A1 (en) * | 2020-02-07 | 2021-08-12 | Argentum Pharmaceuticals Llc | Treatment and dosing regimen for s1p receptor modulator |
| WO2021158841A1 (en) * | 2020-02-07 | 2021-08-12 | Argentum Pharmaceuticals Llc | Treatment and dosing regimen for s1p receptor modulator |
| WO2021158844A1 (en) * | 2020-02-07 | 2021-08-12 | Argentum Pharmaceuticals Llc | Treatment and dosing regimen for s1p receptor modulator |
| WO2021158838A1 (en) | 2020-02-07 | 2021-08-12 | Argentum Pharmaceuticals Llc | Dosage regimen of an s1p receptor modulator |
| WO2021158839A1 (en) * | 2020-02-07 | 2021-08-12 | Argentum Pharmaceuticals Llc | Treatment and dosing regimen for s1p receptor modulator |
| WO2021158847A1 (en) * | 2020-02-07 | 2021-08-12 | Argentum Pharmaceuticals Llc | Treatment and dosing regimen for s1p receptor modulator |
| WO2021158845A1 (en) * | 2020-02-07 | 2021-08-12 | Argentum Pharmaceuticals Llc | Treatment and dosing regimen for s1p receptor modulator |
| CN113527250B (zh) * | 2020-04-16 | 2024-01-05 | 广东东阳光药业股份有限公司 | 辛波莫德中间体及其制备方法 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6077851A (en) | 1998-04-27 | 2000-06-20 | Active Biotech Ab | Quinoline derivatives |
| BR112013014061A2 (pt) * | 2010-12-07 | 2016-09-13 | Teva Pharma | uso de laquinimod para redução da fadiga, melhorando o estado fundicional e melhorando a qualidade de vida nos pacientes com esclerose múltipla |
| CN106344576A (zh) | 2011-10-12 | 2017-01-25 | 泰华制药工业有限公司 | 以拉喹莫德和芬戈莫德的组合治疗多发性硬化症 |
| US20140235670A1 (en) * | 2013-02-15 | 2014-08-21 | Teva Pharmaceutical Industries, Ltd. | Treatment of progressive forms of multiple sclerosis with laquinimod |
| SG11201506493VA (en) * | 2013-04-04 | 2015-10-29 | Novartis Ag | Identifying patient response to s1p receptor modulator administration |
-
2015
- 2015-10-14 RU RU2017116740A patent/RU2017116740A/ru unknown
- 2015-10-14 EP EP15784974.6A patent/EP3206682B1/en not_active Not-in-force
- 2015-10-14 AU AU2015332037A patent/AU2015332037A1/en not_active Abandoned
- 2015-10-14 CN CN202210376999.4A patent/CN114699409A/zh active Pending
- 2015-10-14 US US15/517,280 patent/US10537566B2/en not_active Expired - Fee Related
- 2015-10-14 CN CN201580056374.8A patent/CN107072988A/zh active Pending
- 2015-10-14 JP JP2017520503A patent/JP6731915B2/ja not_active Expired - Fee Related
- 2015-10-14 BR BR112017007414A patent/BR112017007414A2/pt not_active Application Discontinuation
- 2015-10-14 CA CA2964315A patent/CA2964315A1/en not_active Abandoned
- 2015-10-14 ES ES15784974T patent/ES2710460T3/es active Active
- 2015-10-14 KR KR1020177009900A patent/KR20170068480A/ko not_active Withdrawn
- 2015-10-14 MX MX2017004808A patent/MX2017004808A/es unknown
- 2015-10-14 WO PCT/IB2015/057870 patent/WO2016059571A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| CA2964315A1 (en) | 2016-04-21 |
| US10537566B2 (en) | 2020-01-21 |
| AU2015332037A1 (en) | 2017-04-27 |
| ES2710460T3 (es) | 2019-04-25 |
| US20170304289A1 (en) | 2017-10-26 |
| JP2017531021A (ja) | 2017-10-19 |
| RU2017116740A (ru) | 2018-11-16 |
| JP6731915B2 (ja) | 2020-07-29 |
| CN114699409A (zh) | 2022-07-05 |
| EP3206682A1 (en) | 2017-08-23 |
| BR112017007414A2 (pt) | 2017-12-19 |
| CN107072988A (zh) | 2017-08-18 |
| WO2016059571A1 (en) | 2016-04-21 |
| MX2017004808A (es) | 2017-07-26 |
| EP3206682B1 (en) | 2018-09-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20170068480A (ko) | 다발성 경화증의 치료를 위한 시포니모드 및 라퀴니모드를 포함하는 조합물 | |
| CA3073996C (en) | Combination therapy of lasmiditan and a cgrp antagonist for use in the treatment of migraine | |
| US8889627B2 (en) | Treatment of multiple sclerosis with combination of laquinimod and fingolimod | |
| HK1226940A1 (zh) | 用拉喹莫德与醋酸格拉替雷的组合治疗多发性硬化症 | |
| US12318380B2 (en) | Treatment of demyelinating diseases | |
| JP7788154B2 (ja) | 多発性硬化症患者の亜集団の処置のためのマシチニブ | |
| JP2010534628A (ja) | 神経変性障害を治療するためのネラメキサンの新規組合せ | |
| US10576045B2 (en) | Low dosage combinations of fluoxetine and reboxetine for treating obesity | |
| US20240050427A1 (en) | Treatments for obsessive compulsive disorder | |
| US20170007596A1 (en) | Treatment of multiple sclerosis with combination of laquinimod and flupirtine | |
| US20240358693A1 (en) | Methods of treating pain | |
| RU2805061C2 (ru) | Лечение демиелинизирующих заболеваний |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20170412 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination |