본 발명의 요약
만능 줄기 세포를 시험관내에서 무한대로 증식 및 확장시켜 인간 요법을 위한 비공여자 유래 세포의 잠재적으로 무진장한 공급원을 제공할 수 있다. 만능 줄기 세포의 성숙한 RG 세포(균질한, 또는 거의 균질한 성숙한 RG 세포 집단 포함) 및/또는 조기 및/또는 후기 RG 전구체 세포(균질한, 또는 거의 균질한 RG 전구체 세포 집단 포함)로의 분화는 이식 및 망막 질환 치료, 또는 시험관내 용도, 예컨대, 스크리닝 검정법을 위한 비공여자 유래 세포를 충분히 공급할 수 있다. 고도로 정제된 성숙한 RG 세포 집단은 앞서 수득된 바 없으며, 충분한 개수 또는 순도의 RG 전구체 세포 집단 또한 앞서 수득된 적 없다. 본 발명은 적어도 선행 기술의 방법 및 조성물이 가지는 이러한 한계를 극복한다.
본 발명은 그 중에서도 특히 RG 전구체 세포 및/또는 성숙한 RG 세포를 포함하는 조성물 또는 제제 뿐만 아니라, 상기 세포 및 상기 제제를 제조하는 방법을 제공한다. 놀랍게도, 본 발명의 RG 전구체 세포 및 성숙한 RG 세포는 1차 신경절 세포에 비하여 더욱 우수한 통합 및 이동 특성, 및 장기화된 생존 기간을 보이는 것으로 나타났다.
특정 실시양태에서, 본 발명은 복수 개의 RG 전구체 세포, 및 RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, 망막 신경절(RG) 전구체 세포의 실질적으로 순수한 제제를 제공한다. 상기 배지는 글루코스, 인슐린, cAMP 수준을 증가시키는 인자, 예컨대, 포스콜린, 및 신경 영양 인자, 예컨대, 섬모 신경 영양 인자(CNTF) 및 뇌 유래 신경 영양 인자(BDNF)를 포함할 수 있다.
특정 실시양태에서, 본 발명은 50% 이상의 RG 전구체 세포를 함유하는 복수 개의 세포, 및 RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, RG 전구체 세포의 제제를 제공한다.
특정 실시양태에서, 본 발명은 RG 전구체 세포가 아닌 세포, 예컨대, 만능 줄기 세포, 안구 영역 전구체 세포, 광수용기 전구체 세포, 성숙한 광수용기, 및/또는 아마크린 세포는 실질적으로 함유하지 않는, 복수 개의 RG 전구체 세포를 포함하는 RG 전구체 세포의 제제를 제공한다. 일부 실시양태에서, 제제는 RG 전구체 세포가 아닌 세포를 10% 미만으로, 및 더욱더 바람직하게는, 상기 세포를 5%, 2%, 1%, 0.1% 미만으로, 또는 심지어 0.01% 미만으로 포함한다. 일부 실시양태에서, 제제는 RG 세포(즉, 성숙한 RG 세포)를 실질적으로 함유하지 않을 수 있다. 상기 제제 중 임의의 것은 RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 추가로 포함할 수 있다.
일부 실시양태에서, 제제는 성숙한 RG 세포 및 RG 전구체의 혼합물을 포함할 수 있지만, 다른 세포 유형, 예컨대, 만능 줄기 세포, 안구 영역 전구체 세포, 광수용기 전구체 세포, 성숙한 광수용기, 및/또는 아마크린 세포는 포함하지 않을 수 있다.
특정 실시양태에서, 본 발명은 복수 개의 RG 전구체 세포; 및 포유동물 환자 내로의 이식을 위해 RG 전구체 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 포함하는, 포유동물 환자에서의 사용에 적합한 RG 전구체 세포의 약학 제제를 제공한다.
특정 실시양태에서, 본 발명은 109개 이상의 RG 전구체 세포, 및 RG 전구체 세포에 맞고, 해동 후 상기 세포의 생존능을 유시시킬 수 있는 냉동보존 시스템을 포함하는, 극저온 세포 제제를 제공한다.
RG 전구체 세포를 포함하는 제제의 일부 실시양태에서, 제제 중 70% 이상의 세포는 면역세포화학적으로 Math5(+)이고, 더욱더 바람직하게, 제제 중 80%, 90%, 95% 또는 98% 이상의 세포는 면역세포화학적으로 Math5(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Brn3a(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Brn3b(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Isl1(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Brn3a(+) 및 Brn3b(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Brn3a(+), Brn3b(+) 및 Isl1(+)이다.
RG 전구체 세포를 포함하는 일부 제제에서, 제제 중 70% 이상의 세포는 면역세포화학적으로 Math5(+) 및 Brn3a(+)(즉, Math5 및 Brn3a에 대해 양성)이고, 더욱더 바람직하게, 제제 중 80%, 90%, 95% 또는 98% 이상의 세포는 면역세포화학적으로 Math5(+) 및 Brn3a(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Brn3b(+)이다. 일부 실시양태에서, 제제 중 50%, 60%, 70%, 80%, 90%, 95% 또는 98% 이상의 세포는 면역세포화학적으로 Math5(+), Brn3a(+) 및 Brn3b(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Isl1(+)이다. 일부 실시양태에서, 제제 중 50%, 60%, 70%, 80%, 90%, 95% 또는 98% 이상의 세포는 면역세포화학적으로 Math5(+), Brn3a(+), Brn3b(+) 및 Isl(+)이다. 일부 실시양태에서, 30%, 20%, 10%, 5%, 1% 미만의 세포가 Thy1을 발현하거나, 또는 어떤 세포도 Thy1을 발현한다. RG 전구체 세포 또한 Tuj1을 발현할 수 있다.
RG 전구체 세포를 포함하는 일부 제제에서, 제제 중 50%, 60% 또는 70% 이상의 세포는 면역세포화학적으로 Brn3a(+) 및/또는 신경미세섬유(+)이고, 더욱더 바람직하게, 제제 중 80%, 90%, 95% 또는 98% 이상의 세포는 면역세포화학적으로 Brn3a(+) 및/또는 신경미세섬유(+)이다. 일부 실시양태에서, 제제 중 50%, 60% 또는 70% 이상의 세포는 면역세포화학적으로 Brn3a(+) 및 신경미세섬유(+)이고, 더욱더 바람직하게, 제제 중 80%, 90%, 95% 또는 98% 이상의 세포는 면역세포화학적으로 Brn3a(+) 및 신경미세섬유(+)이다. 일부 실시양태에서, 제제 중 세포는 또한 Thy1(+)이다. 일부 실시양태에서, 제제 중 50%, 60% 또는 70% 이상의 세포는 면역세포화학적으로 Brn3a(+), 신경미세섬유(+) 및 Thy1(+)이다. RG 전구체 세는 또한 Tuj1을 발현할 수 있다.
RG 전구체 세포는 증식성 세포이다. 일부 실시양태에서, RG 전구체 세포의 제제 중 70%, 80%, 90%, 95% 또는 98% 이상의 세포는 증식성 세포이다.
특정 실시양태에서, RG 전구체 세포가 HLA-유전자형적으로 동일한 것이고, 바람직하게, 게놈적으로 동일한 것이다.
특정 실시양태에서, RG 전구체 세포의 평균 말단 제한 절편 길이(TRF)는 7 kb, 7.5 kb, 8 kb, 8.5 kb, 9 kb, 9.5 kb, 10 kb, 10.5 kb, 11 kb, 11.5 kb 또는 심지어 12 kb보다 더 길다.
특정 실시양태에서, RG 전구체 세포는 인간 환자에게 투여하는 데 적합한 것이다.
특정 실시양태에서, RG 전구체 세포는 인간외 수의학적 환자에게 투여하는 데 적합한 것이다.
상기 제제의 바람직한 실시양태에서, RG 전구체 세포는 바람직하게, 배아 줄기 세포 및 유도성 만능 줄기 세포로 이루어진 군으로부터 선택되는, 포유동물 만능 줄기 세포, 특히, 인간 만능 줄기 세포로부터 유래된 것이다.
특정 실시양태에서, RG 전구체 세포는 공통 만능 줄기 세포 공급원으로부터 분화된 것이다.
특정 실시양태에서, RG 전구체 세포는 안내압이 높은 녹내장 마우스 또는 래드 모델 시스템의, 또는 시신경(ON) 압박 손상 마우스 모델 시스템의 유리체 또는 망막하 공간 내로 이식될 수 있고, 신경절 세포층으로 이동할 것이며, 모델 시스템 중 임의의 것에서 패턴 ERG(망막전위도검사) 반응 및 시력을 개선시킬 것이다. 특정 실시양태에서, RG 세포 및 RG 전구체 세포는 시신경을 재생시킬 수 있다.
특정 실시양태에서, RG 전구체 세포 및 RG 세포는 하나 이상의 신경보호 인자를 분비하고, 이로써, 신경보호를 효과를 일으킨다. 상기 신경보호는 시신경 손상 또는 녹내장을 앓는 동물 모델을 사용하여 측정될 수 있다.
특정 실시양태에서, RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지는 배양 배지, 냉동보존제, 및 인간 환자에서 주사하기 적합한 생체적합성 주사용 배지로 이루어진 군으로부터 선택된다.
특정 실시양태에서, RG 전구체 세포 제제는 발열원 및 마이코젠 무함유이다
본 발명의 또 다른 측면은, 만능 줄기 세포 유래 RG 세포를 포함하는, 포유동물 환자에서 사용하기에 적합한, RG 세포의 약학 제제로서, 여기서, 제제 중의 세포는 신경미세섬유 및/또는 Brn3a에 대하여 면역세포화학적으로 양성이고, 따라서, 일부 경우에서, 신경미세섬유(+) Brn3a(+)일 수 있는 것인, RG 세포의 약학 제제를 제공한다. RG 세포는 Tuj1(+)일 수 있고, 이는 또한 임의적으로, Thy1(+)일 수 있다. 약학 제제는 포유동물 환자 내로의 이식을 위해 RG 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 추가로 포함할 수 있다.
본 발명의 또 다른 측면은, 만능 줄기 세포 유래 RG 세포, 및 포유동물 환자 내로의 이식을 위해 RG 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 포함하는, 포유동물 환자에서 사용하기에 적합한, RG 세포의 약학 제제로서, 여기서, 제제 중의 세포는 면역세포화학적으로 신경미세섬유(+) Brn3a(+) 및 Tuj1(+), 및 임의적으로, Thy1(+)인 것인, RG 세포의 약학 제제를 제공한다.
본 발명의 또 다른 측면은, 만능 줄기 세포 유래 RG 세포, 및 포유동물 환자 내로의 이식을 위해 RG 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 포함하는, 포유동물 환자에서 사용하기에 적합한, RG 세포의 약학 제제로서, 여기서, 70%, 80%, 90%, 95% 또는 심지어 98% 초과의 세포는 면역세포화학적으로 신경미세섬유(+) 및 Brn3a(+)인 것인, RG 세포의 약학 제제를 제공한다. 일부 경우에서, 제제 중 50%, 60% 또는 70% 초과의 세포는 면역세포화학적으로 Thy1(+)이다. 일부 실시양태에서, 70%, 80%, 90%, 95% 또는 심지어 98% 이상의 세포는 면역세포화학적으로 Tuj1(+)이다.
일부 실시양태에서, RG 세포의 약학 제제 중의 세포는 유사분열상 불활성이고(또는 유사분열 이후의 것이고), 이는 상기 세포 비증식성 세포라는 것을 의미한다. 이는 당업계에 공지되는 증식 검정법, 예컨대, 삼중수소 티미딘 흡수 검정법 등을 사용하여 측정될 수 있다. 일부 실시양태에서, 제제 중 50%, 60%, 70%, 80%, 90%, 95%, 또는 98% 초과의 세포는 유사분열상 불활성이다.
일부 실시양태에서, RG 세포의 약학 제제 중의 세포는 RG 전구체 부류보다 더 많은 개수의 수상 돌기 및/또는 더욱 복잡한 수상 돌기를 포함한다. 일부 실시양태에서, 제제 중 50%, 60%, 70%, 80%, 90%, 95%, 또는 98% 초과의 세포는 (전구체 부류와 비교하였을 때) 더 많은 개수의 수상 돌기 및/또는 더욱 복잡한 수상 돌기를 포함한다. 따라서, 성숙한 RG 세포는 RG 전구체 세포와 비교하였을 때, 증가된 개수의 1차 수상 돌기 및/또는 2차, 3차 및 더 높은 수준에서 증가된 수상 돌기 분기, 및/또는 증가된 수상 돌기 총 길이를 나타낸다. 예를 들어, RG 세포는 RG 전구체 세포보다 세포 1개 기준으로 2-5배 더 많은 수상 돌기를 가질 수 있다(예컨대, RG 세포는 세포 1개당 4-5개의 수상 돌기를 가질 수 있고, RG 전구체 세포는 세포 1개당 1-2개의 수상 돌기를 가질 수 있다).
본 발명의 추가의 또 다른 측면은 망막 색소 상피 세포, 광수용기 전구체 세포, 및/또는 광수용기 세포와 함께 RG 전구체 세포 및/또는 RG 세포; 및 포유동물 환자 내로의 이식을 위해 RG 전구체 세포 및/또는 RG 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 포함하는 약학 제제를 제공한다. 제제는 또한 양극 세포 및/또는 아마크린 세포를 포함할 수 있다. 세포의 제제는 (함께 혼합되거나, 또는 공동으로 전달하고자 하는 개별 용량의 세포를 포함하는 키트 형태의) 세포 현탁액으로서, 3차원 구조로서, 예를 들어,(임의적으로, 생체적합성 매트릭스 또는 고체 지지체 상에 배치된) 시트 또는 단층 또는 다층 세포 이식편으로서 제공될 수 있다. 다층 세포 이식편의 경우, RPE 세포는 단층, 바람직하게, 분극된 단층으로서 제공될 수 있다. 따라서, 일부 실시양태에서, RG 세포 및/또는 RG 전구체 세포는 RPE 세포, 광수용기 세포 또는 광수용기 전구체 세포를 비롯한, 다른 신경망막 감각 세포와 함께 사용된다.
본 발명의 추가의 또 다른 측면은 본원에 기술된 상기 약학 제제, 예컨대, RG 전구체 세포 또는 RG 세포의 제제, 또는 그 둘 모두를 투여하는 단계를 포함하는, 환자에서 망막 신경절 세포의 손실 또는 기능 장애에 의해 유발되는 질환 및 장애를 치료하는 방법을 제공한다. 제제는 국소적으로 예컨대, 환자 안구의 망막하 공간 내로, 환자의 유리체 내로 주사할 수 있거나, 또는 전신으로 전달할 수 있거나, 또는 세포가 존속할 수 있는 다른 체강 내로 전달할 수 있다.
망막 신경절 세포의 손실에 의해 유발되는 질환 또는 장애로는 녹내장, 시신경 손상, 허혈성 시신경병증, 시신경염, 당뇨병성 망막증, 유전성 신경절 변성, 및 유전성 망막 이영양증을 포함한다.
따라서, 피험체에서 망막 신경절 세포의 손실 또는 기능 장애에 의해 유발되는 질환 또는 장애 치료용 의약 제조에서의, 본원에 기술되고/거나, 본원에 기술된 방법을 사용하여 제조된 RG 전구체 세포 집단 중 임의의 것의 용도 또한 제공한다. 피험체에서 망막 신경절 세포의 손실 또는 기능 장애에 의해 유발되는 질환 또는 장애 치료 방법에서 사용하기 위한, 본원에 기술되고/거나, 본원에 기술된 방법을 사용하여 제조된 RG 전구체 세포 집단 중 임의의 것의 용도 또한 제공한다.
유사하게, 피험체에서 망막 신경절 세포의 손실 또는 기능 장애에 의해 유발되는 질환 또는 장애 치료용 의약 제조에서의, 본원에 기술되고/거나, 본원에 기술된 방법을 사용하여 제조된 RG 세포 집단 중 임의의 것의 용도 또한 제공한다. 피험체에서 망막 신경절 세포의 손실 또는 기능 장애에 의해 유발되는 질환 또는 장애 치료 방법에서 사용하기 위한, 본원에 기술되고/거나, 본원에 기술된 방법을 사용하여 제조된 RG 세포 집단 중 임의의 것의 용도 또한 제공한다.
특정 실시양태에서, 본 발명은
(a) 안구 영역 전구체 세포를, 바람직하게, 세포 클러스터로서, 및 바람직하게, 저부착 또는 비부착 조건하에서 상기 세포 클러스터가 RG 전구체 세포를 포함하는 개별 세포 구체를 형성하는 데 충분한 기간 동안 신경절 세포 배지 중에서 배양하는 단계; 및
(b) 배양물 중 세포 대다수가 Brn3a(+) 및/또는 신경미세섬유(+) (및 바람직하게, Brn3a(+) 및 신경미세섬유(+)) 및 Tuj1(+), 및 임의적으로, 또한 Thy1(+)인 것을 특징으로 하는 RG 세포가 될 때까지, 세포 구체를 부착 조건하에 망막 신경절 세포 분화 배지 중에서, 바람직하게, 매트릭스(예컨대, 생체물질 스캐폴드) 상에서 배양하는 단계를 포함하는, RG 세포를 제조하는 방법을 제공한다.
특정 실시양태에서, 본 발명은 안구 영역 전구체 세포를, 바람직하게, 세포 클러스터로서, 및 바람직하게, 저부착 또는 비부착 조건하에서 상기 세포 클러스터가 RG 전구체 세포를 형성하는 데 충분한 기간 동안 신경절 세포 배지 중에서 배양하는 단계를 포함하는 방법을 제공한다. 배양물 중 세포 대다수가 Brn3a(+), 신경미세섬유(+) 및 Tuj1(+), 및 임의적으로, Thy1(+)인 것을 특징으로 하는 RG 세포가 될 때까지, RG 전구체 세포를 임의적으로 부착 조건하에 망막 신경절 세포 분화 배지 중에서, 바람직하게, 매트릭스(예컨대, 생체물질 스캐폴드) 상에서 배양할 수 있다.
일부 실시양태에서, 안구 영역 전구체 세포는 Pax6(+) 및 Rx1(+) 및 Oct4(-) 및 Nanog(-)인 것을 특징으로, 예컨대, 면역세포화학상 특징으로 하고, 더욱더 바람직하게, 이는 또한 Six3(+), Six6(+), Lhx2(+), Tbx3(+), Sox2(+), Otx2(+) 및 네스틴(+)인 것을 특징으로 하고, 예컨대, 이는 면역염색 및/또는 유세포 분석법 또는 세포에서 마커 발현의 특징을 규명하는 데 사용되는 다른 표준 검정법에 의해 측정될 수 있다.
일부 실시양태에서, RG 전구체 세포는 Math5(+), 또는 Math5(+) 및 Brn3a(+), 또는 Math5(+), Brn3a(+) 및 Brn3b(+), 또는 Math5(+), Brn3a(+), Brn3b(+) 및 Isl1(+), 또는 Brn3a(+) 및 신경미세섬유(+), 또는 Brn3a(+), 신경미세섬유(+) 및 Thy1(+)인 것을 특징으로 하고, 이는 예컨대, 면역염색 및/또는 유세포 분석법 또는 세포에서 마커 발현의 특징을 규명하는 데 사용되는 다른 표준 검정법에 의해 측정될 수 있다.
특정 실시양태에서, 부착 조건은, 단지, 예시를 위해, 폴리에스테르, 폴리프로필렌, 폴리알킬렌, 폴리플루오로클로로에틸렌, 폴리비닐 클로라이드, 폴리비닐 플루오라이드 수지, 폴리스티렌, 폴리술폰, 폴리우레탄, 폴리에틸렌 테레프탈레이트, 셀룰로스, 유리 섬유, 세라믹 입자, 생체물질 스캐폴드, 폴리-L-락트산, 덱스트란, 불활성 금속 섬유, 실리카, 나트론 유리, 보로실리케이트 유리, 키토산, 또는 수세미 중 하나 이상의 것을 포함할 수 있는, 부착성 물질을 포함하는, 세포가 부착할 수 있는 표면을 가지는 배양 시스템을 포함한다. 일부 실시양태에서, 부착성 물질은 정전기적으로 하전된 것이다. 특정 실시양태에서, 생체물질 스캐폴드는 세포외 매트릭스, 예컨대, 콜라겐(예컨대, 콜라겐 IV형 또는 I형), 804G-유도된 매트릭스, 피브로넥틴, 비트로넥틴, 콘드로넥틴, 라미닌 또는 마트리겔(Matrigel)™이다. 다른 실시양태에서, 생체물질은 젤라틴, 알기네이트, 폴리글리콜리드, 피브린, 또는 자가 조립 펩티드이다.
특정 실시양태에서, RG 전구체 세포, 및 그 결과로서의 RG 세포는 만능 줄기 세포, 예컨대, 배아 줄기 세포 또는 유도성 만능 줄기 세포로부터 유래된 것이다.
바람직한 실시양태에서, 만능 줄기 세포를 실질적으로 함유하지 않는, 생성된, RG 전구체 세포의 제제를 제공하며, 즉, 제제 중 10% 미만의 세포는 만능 줄기 세포이고, 더욱더 바람직하게, 제제 중 5%, 2%, 1%, 0.1% 미만 또는 심지어 0.01% 미만의 세포는 만능 줄기 세포이다.
바람직한 실시양태에서, 안구 영역 전구체 세포를 실질적으로 함유하지 않는, 생성된, RG 전구체 세포의 제제를 제공하며, 즉, 제제 중 10% 미만, 및 더욱더 바람직하게, 5%, 2%, 1%, 0.1% 미만 또는 심지어 0.01% 미만의 세포는 안구 영역 전구체 세포이다.
바람직한 실시양태에서, 생성된, RG 전구체 세포의 제제의 세포 성분은 다른 세포 유형 대비 50% 이상으로 순수하고(즉, 제제 중 50% 이상의 세포는 RG 전구체 세포이다), 바람직하게, 제제 중 75% 이상, 85% 이상, 95% 이상, 99% 이상 또는 약 100%의 세포는 RG 전구체이다.
특정 실시양태에서, 본 방법은 RG 전구체 세포 또는 RG 세포를 냉동보존하는 추가 단계를 포함한다. 세포는 바람직하게는 냉동된 세포의 해동물(및 해동된 세포 그 자체)에 맞는 냉동보존제 중에서 냉동되고, 임의적으로, 세포를 세척하여 냉동보존제를 제거한 후, RG 전구체 세포 또는 RG 세포는 (예컨대, 배양 효율 기준으로) 25% 이상의 세포 생존능, 및 더욱 바람직하게, 50%, 60%, 70%, 80% 이상 또는 심지어 90% 이상의 세포 생존능을 유지한다.
RG 전구체 세포 또는 RG 세포는 냉동보존될 수 있다. 일부 실시양태에서, RG 전구체 세포는 구체로서 냉동보존된다.
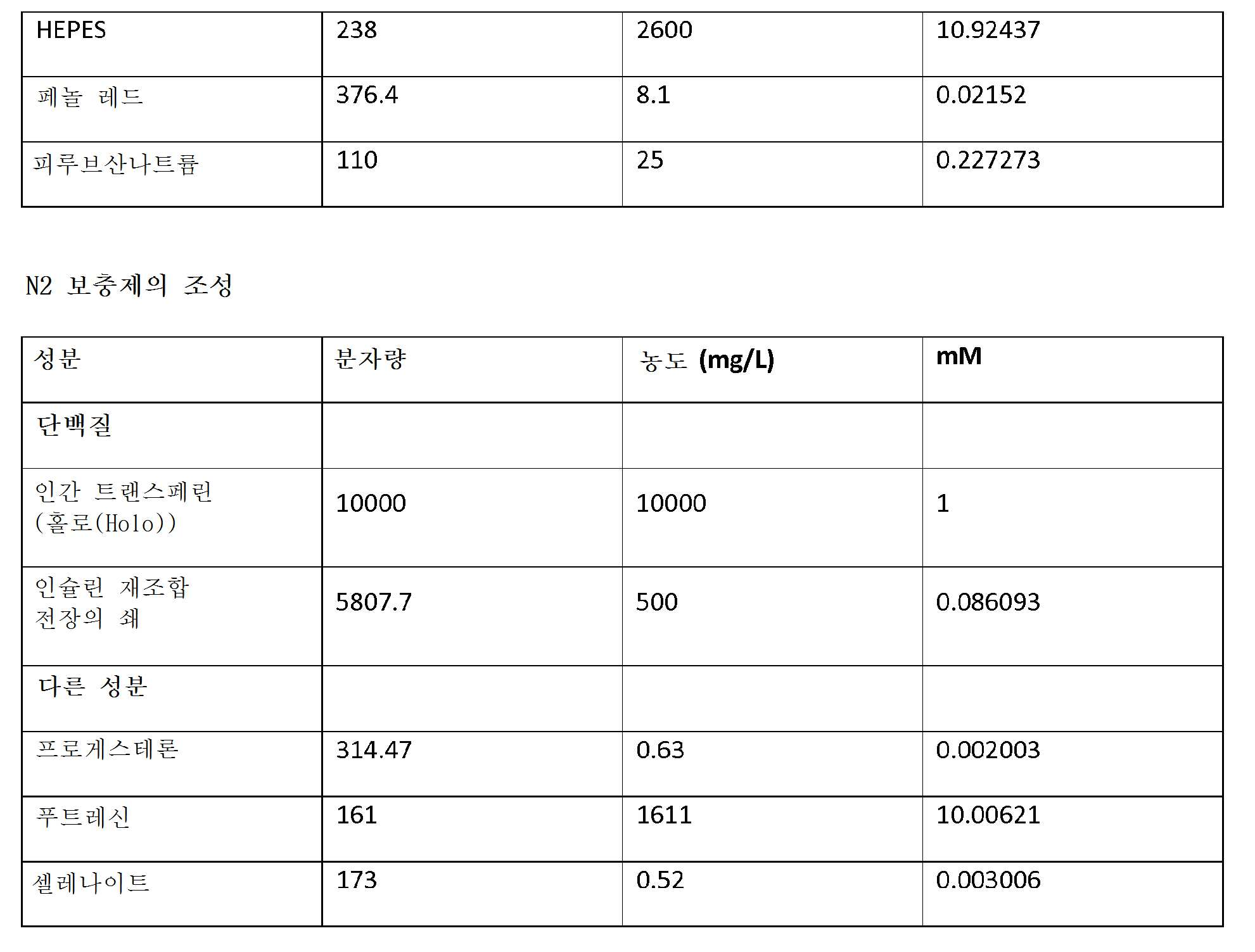
특정 실시양태에서, 신경절 세포 배지는 기본 배지, 예컨대, 뉴로베이살(Neurobasal)™ 배지(라이프 테크놀러지스(Life Technologies))(또는 유사 성분을 포함하는 다른 배지), D-글루코스, 항생제, 예컨대, 페니실린, 및 스트렙토마이신, 글루타맥스™(GlutaMAX), N2 보충제(인비트로겐(Invitrogen)), B27 보충제(이 또한 인비트로겐으로부터 입수), 포스콜린, BDNF 및 CNTF를 포함할 수 있다. B27 보충제는 그 중에서도 특히, SOD, 카탈라제 및 다른 항산화제 (GSH), 및 독특한 지방산, 예컨대, 리놀레산, 리놀렌산, 리포산을 함유한다. N2 보충제는 예를 들어, 하기 칵테일: 트랜스페린(10 g/L), 인슐린(500 mg/L), 프로게스테론(0.63 mg/L), 푸트레신(1611 mg/L) 및 셀레나이트(0.52 mg/L)로 대체될 수 있다.
상기 측면 및 실시양태의 특정 실시양태에서, RG 전구체 세포는 만능 줄기 세포 공급원으로부터, 예컨대, Oct4, 알칼리성 포스파타제, Sox2, SSEA-3, SSEA-4, TRA-1-60, 및 TRA-1-80을 발현하는 만능 줄기 세포(예컨대, 제한하는 것은 아니지만, 배아 줄기(ES: embryonic stem) 세포주 또는 유도성 만능 줄기(iPS) 세포주)로부터, 및 더욱더 바람직하게, 공통 만능 줄기 세포 공급원으로부터 분화된 것이다.
상기 측면 및 실시양태의 특정 실시양태에서, RG 전구체 세포의 평균 말단 제한 절편 길이(TRF)는 7 kb, 7.5 kb, 8 kb, 8.5 kb, 9 kb, 9.5 kb, 10 kb, 10.5 kb, 11 kb, 11.5 kb 또는 심지어 12 kb보다 길다.
상기 측면 및 실시양태의 특정 실시양태에서, 제제는 인간 환자에게 투여하는 데 적합하고, 더욱 바람직하게, 발열원 무함유이고/거나, 인간외 동물 생성물을 함유하지 않는다.
상기 측면 및 실시양태의 특정 실시양태에서, 제제는 인간외 수의학적 포유동물, 예컨대, 제한하는 것은 아니지만, 개, 고양이, 또는 말에게 투여하는 데 적합하다.
한 측면에서, 본 개시내용은 만능 줄기 세포를 (i) 망막 유도(RI) 배지, (ii) 신경 분화(ND) 배지, 및 (iii) 신경절 세포(GC) 배지 중에서 순차적으로 배양하는 단계를 포함하는, RG 전구체 세포를 제조하는 방법을 제공한다.
만능 줄기 세포는 인간 세포일 수 있다. 일부 실시양태에서, 만능 줄기 세포는 인간 ES 세포 또는 인간 iPS 세포일 수 있다. 만능 줄기 세포는 비분화된 상태로 피더세포 무함유 및/또는 제노 프리 조건하에서 임의적으로, 매트릭스 존재하에서 배양될 수 있다. 만능 줄기 세포는 비분화된 상태로 기판, 예컨대, 제한하는 것은 아니지만, 마트리겔™을 포함하는 기판 상에서, 및 임의적으로, mTESR1 배지 중에서 배양될 수 있다.
분화는 만능 줄기 세포를 망막 유도 배지 중에서 배양함으로써 시작된다. 망막 유도 배지는 기본 배지, 예컨대, DMEM/F12, DMEM/고 글루코스, 또는 DMEM/넉 아웃, 또는 DMEM/F12의 성분을 포함하는 배지, 또는 DMEM/고 글루코스의 성분을 포함하는 배지, 또는 DMEM/넉 아웃의 성분을 포함하는 배지를 포함할 수 있다.
망막 유도 배지는 D-글루코스를 포함할 수 있다.
신경 분화 배지는 D-글루코스를 포함할 수 있다. D-글루코스는 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml인 농도로 존재할 수 있다.
망막 유도 배지는 하나 이상의 항생제를 포함할 수 있다. 항생제는 페니실린, 및 스트렙토마이신 중 어느 하나, 또는 그 둘 모두를, 임의적으로, 약 0-100 유니트/ml 또는 약 100 유니트/ml 농도의 페니실린, 및 임의적으로, 약 0-100 ㎍/ml 또는 약 100 ㎍/ml 농도의 스트렙토마이신을 포함할 수 있다.
망막 유도 배지는 하나 이상의 혈청 보충제를 포함할 수 있다. 망막 유도 배지는 N2 보충제를 포함할 수 있다. N2 보충제는 약 0.1 내지 5% (부피/부피, 또는 v/v) 또는 약 0.1 내지 2% (v/v) 또는 약 1% (v/v)인 농도로 존재할 수 있다.
망막 유도 배지는 B-27 보충제를 포함할 수 있다. B-27 보충제는 약 0.05-2.0% (v/v)또는 약 0.2% (v/v)인 농도로 존재할 수 있다.
망막 유도 배지는 비필수 아미노산 또는 최소 필수 배지(MEM) 비필수 아미노산을 포함할 수 있다. 비필수 아미노산 또는 MEM 비필수 아미노산은 스톡으로부터 1X 농도로 존재할 수 있으며, 여기서, 스톡은 전형적으로 100X인 것으로 간주된다. (스톡 농도의 1X인) 글리신의 최종 농도는 약 0.1 mM이고, 따라서, 스톡은 10 mM 글리신이다. 스톡은 전형적으로 L-알라닌, L-아스파라긴, L-아스파르트산, L-글루탐산, L-프롤린, 및 L-세린 또한 포함한다.
망막 유도 배지는 인슐린을 포함할 수 있다. 인슐린은 인간 인슐린일 수 있다. 인슐린은 약 5-50 ㎍/ml 또는 약 20 ㎍/ml인 농도로 존재할 수 있다.
망막 유도 배지는 BMP 신호전달 억제제를 포함할 수 있다. BMP 신호전달 억제제는 노긴(Noggin) 폴리펩티드, 도소모르핀, LDN-193189, 및 그의 임의 조합으로 이루어진 군으로부터 선택될 수 있다.
망막 유도 배지는 노긴 폴리펩티드를 포함할 수 있다. 노긴 폴리펩티드는 약 5-100 ng/ml 또는 약 10-100 ng/ml 또는 약 10-500 ng/ml 또는 약 50 ng/ml인 농도로 존재할 수 있다. 일부 실시양태에서, 노긴 폴리펩티드는 약 10-500 ng/ml로 존재한다.
망막 유도 배지는 전체적으로 또는 부분적으로 매일 새 망막 유도 배지로 대체될 수 있다. 일부 경우에서, 세포는 2 x 104/㎠ 내지 6 x 104/㎠ 범위의 밀도로 성장된다.
망막 유도 배지 중에서 배양하는 것은 약 4-6일, 또는 약 4일, 약 5일, 또는 약 6일 동안 이루어질 수 있다.
신경 분화 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스), 또는 뉴로베이살™ 배지의 성분을 포함하는 기본 배지를 포함할 수 있다.
신경 분화 배지는 D-글루코스를 포함할 수 있다. D-글루코스는 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml인 농도로 존재할 수 있다.
신경 분화 배지는 하나 이상의 항생제를 포함할 수 있다. 항생제는 페니실린, 및 스트렙토마이신 중 어느 하나, 또는 그 둘 모두를, 임의적으로, 약 0-100 유니트/ml 또는 약 100 유니트/ml 농도의 페니실린, 및 임의적으로, 약 0-100 ㎍/ml 또는 약 100 ㎍/ml 농도의 스트렙토마이신을 포함할 수 있다.
신경 분화 배지는 하나 이상의 혈청 보충제를 포함할 수 있다. 신경 분화 배지는 N2 보충제를 포함할 수 있다. N2 보충제는 약 0.1 내지 5% (v/v) 또는 0.1 내지 2% (v/v) 또는 약 1% (v/v)인 농도로 존재할 수 있다.
신경 분화 배지는 B-27 보충제(라이프 테크놀러지스)를 포함할 수 있다. B-27 보충제는 약 0.05 내지 5.0% (v/v), 약 0.5 내지 2.0% (v/v) 또는 약 2% (v/v)인 농도로 존재할 수 있다.
신경 분화 배지는 비필수 아미노산 또는 MEM 비필수 아미노산 또는 글루타민 또는 글루타맥스™를 포함할 수 있다. 비필수 아미노산 또는 MEM 비필수 아미노산은 스톡 농도의 약 1X로 존재할 수 있으며, 여기서, 스톡은 약 200 mM이다 (그리고, 100X로 간주된다). 글루타맥스™는 (200 mM인 100X 스톡 용액을 사용하여) 2 mM 또는 1X 스톡 희석액으로 존재할 수 있다.
신경 분화 배지는 BMP 신호전달 억제제를 포함할 수 있다. BMP 신호전달 억제제는 노긴 폴리펩티드, 도소모르핀, LDN-193189, 및 그의 임의 조합으로 이루어진 군으로부터 선택될 수 있다.
신경 분화 배양 배지는 노긴 폴리펩티드를 포함할 수 있다. 노긴 폴리펩티드는 약 10 내지 1000 ng/ml, 또는 약 10 내지 500 ng/ml, 또는 10 내지 100 ng/ml, 또는 약 50 ng/ml인 농도로 존재할 수 있다.
신경 분화 배지의 존재하에서 배양하는 것은 약 8-12일, 또는 약 9-10일, 또는 약 9일 동안 이루어질 수 있다. 신경 분화 배지는 전체적으로 또는 부분적으로 매일, 또는 매 2일마다, 또는 매 3일마다 교체될 수 있다.
신경절 세포 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스) 또는 뉴로베이살™ 배지의 성분을 포함하는 배지를 포함할 수 있다.
신경절 세포 배지는 D-글루코스를 포함할 수 있다. 신경 분화 배지는 D-글루코스를 포함할 수 있다. D-글루코스는 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml인 농도로 존재할 수 있다.
신경절 세포 배지는 하나 이상의 항생제를 포함할 수 있다. 항생제는 페니실린, 및 스트렙토마이신 중 어느 하나, 또는 그 둘 모두를, 임의적으로, 0-100 유니트/ml 또는 약 100 유니트/ml 농도의 페니실린, 및 임의적으로, 0-100 ㎍/ml 또는 약 100 ㎍/ml의 스트렙토마이신을 포함할 수 있다.
신경절 세포 배지는 하나 이상의 혈청 보충제를 포함할 수 있다. 신경절 세포 배지는 N2 보충제를 포함할 수 있다. N2 보충제는 약 0.1 내지 5% (v/v) 또는 0.1 내지 2% (v/v) 또는 약 1% (v/v)인 농도로 존재할 수 있다.
신경절 세포 배지는 B-27 보충제(포뮬러 번호 080085-SA)(라이프 테크놀러지스)를 포함할 수 있다. B-27 보충제(포뮬러 번호 080085-SA)는 약 0.05 내지 5.0% (v/v), 약 1.5 내지 2.5% (v/v) 또는 약 2% (v/v)인 농도로 존재할 수 있다.
신경절 세포 배지는 글루타맥스™를 포함할 수 있다. 글루타맥스™는 (200 mM인 100X 스톡 용액을 사용하여) 1X 스톡 희석액으로 존재할 수 있다.
신경절 세포 배지는 포스콜린, BDNF 및 CNTF 중 하나, 둘, 또는 그들 모두를 포함할 수 있다. 포스콜린은 1-20 μM 또는 1-10 μM 또는 약 5 μM인 농도로 존재할 수 있다. BDNF는 1-200 ng/ml 또는 5-50 ng/ml 또는 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재할 수 있다. CNTF는 1-200 ng/ml 또는 5-50 ng/ml 또는 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재할 수 있다. BDNF는 인간 BDNF일 수 있다. CTNF는 인간 CTNF일 수 있다.
신경절 세포 배지의 존재하에서 배양하는 것은 약 40-50일, 또는 약 45일 동안 이루어질 수 있다. 신경절 세포 배지는 전체적으로 또는 부분적으로, 매일, 또는 매 2일마다, 또는 매 3일마다, 또는 덜 빈번하게 교체될 수 있다.
본 방법에 의해 제조된 RG 전구체는 배양물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 이상 또는 약 100%의 세포를 포함할 수 있고, 임의적으로, 상기 배양물은 1주, 2주, 또는, 3주, 4주 또는 더 긴 시간을 비롯한, 2주 초과 동안 증식될 수 있다.
RG 전구체 세포는 마커: Math5, Brn3a, Brn3b, Isl1, 신경미세섬유, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), Isl1(+), 신경미세섬유(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 마커: Math5, Brn3a, Brn3b, 및 Isl1 중 하나 이상의 것을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), 및/또는 Isl1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 마커: Brn3a, 신경미세섬유 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체는 Pax6 및/또는 Rx1을 발현하지 않을 수 있고, 따라서, Pax6(-) 및/또는 Rx1(-)인 것을 특징으로 할 수 있다. 특정 RG 전구체 세포는 Math5 및/또는 Brn3b를 발현하지 않을 수 있고, 따라서, Math5(-) 및/또는 Brn3b(-)인 것을 특징으로 할 수 있다.
RG 전구체 세포는 Math5(+), 또는 Math5(+), Brn3a(+), 또는 Math5(+), Brn3a(+), Brn3b(+), 또는 Math5(+), Brn3a(+), Brn3b(+), Isl1(+), 또는 Brn3a(+), 또는 신경미세섬유(+), 또는 Brn3a(+), 신경미세섬유(+), 또는 Brn3a(+), 신경미세섬유(+), Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체는 Pax6 및/또는 Rx1을 발현하지 않을 수 있고, 따라서, Pax6(-) 및/또는 Rx1(-)인 것을 특징으로 할 수 있다. RG 전구체 세포는 Tuj1(+)일 수 있다. RG 전구체 세포는 증식성일 수 있다.
RG 전구체 세포는 냉동보존될 수 있다. RG 전구체 세포는 인간 세포일 수 있다.
본 방법은 망막 신경절 세포(RGC) 분화 배지의 존재하에서의 후속 배양 단계를 추가로 포함할 수 있다. 상기 단계는 중간 냉동보존 단계 없이 이루어질 수 있거나, 또는 RG 전구체 세포의 냉동보존 및 해동 이후에 이루어질 수 있다.
RGC 분화 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스) 또는 뉴로베이살™ 배지의 성분을 포함하는 배지를 포함할 수 있다.
RGC 분화 배지는 D-글루코스를 포함할 수 있다. 신경 분화 배지는 D-글루코스를 포함할 수 있다. D-글루코스는 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml인 농도로 존재할 수 있다.
RGC 분화 배지는 하나 이상의 항생제를 포함할 수 있다. 항생제는 페니실린, 및 스트렙토마이신 중 어느 하나, 또는 그 둘 모두를, 임의적으로, 0-100 유니트/ml 또는 약 100 유니트/ml 농도의 페니실린, 및 임의적으로, 0-100 ㎍/ml 또는 약 100 ㎍/ml의 스트렙토마이신을 포함할 수 있다.
RGC 분화 배지는 하나 이상의 혈청 보충제를 포함할 수 있다. RGC 분화 배지는 B-27 보충제(포뮬러 080085-SA)를 포함할 수 있다. B-27 보충제는 약 0.05 내지 5.0% (v/v), 약 1.5 내지 2.5% (v/v) 또는 약 2% (v/v)인 농도로 존재할 수 있다.
RGC 분화 배지는 글루타맥스™를 포함할 수 있다. 글루타맥스™는 1X 스톡 희석액으로 존재할 수 있다.
RGC 분화 배지는 레티노산을 포함할 수 있다. 레티노산은 약 0.5-20 μM, 약 0.5-10 μM, 약 1-5 μM, 또는 약 2 μM인 농도로 존재할 수 있다.
RGC 분화 배지는 포스콜린, BDNF, CNTF, cAMP, 및 DAPT 모두를 비롯한, 그들 중 하나 이상의 것을 포함할 수 있다. RGC 분화 배지는 BDNF 및 CNTF 중 하나, 또는 그 둘 모두를 포함할 수 있다. RGC 분화 배지는 포스콜린, cAMP, 및 DAPT 또는 다른 노치(Notch) 경로 억제제 또는 노치 억제제 (예컨대, 노치 차단 항체 또는 항체 단편, 노치 음성 조절 영역 항체 또는 항체 단편, 알파-세크레타제 억제제, 감마-세크레타제 억제제, 스테이플드 펩티드, 소분자 차단제 및 siRNA, shRNA 및 miRNA) 모두를 비롯한, 그들 중 하나 이상의 것을 포함할 수 있다. 포스콜린은 1-20 μM 또는 1-10 μM 또는 약 5 μM인 농도로 존재할 수 있다. BDNF는 1-200 ng/ml 또는 5-50 ng/ml 또는 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재할 수 있다. CNTF는 1-200 ng/ml 또는 5-50 ng/ml 또는 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재할 수 있다. BDNF는 인간 BDNF일 수 있다. CTNF는 인간 CTNF일 수 있다. cAMP는 1-500 ng/ml 또는 10-250 ng/ml 또는 5-150 ng/ml 또는 약 100 ng/ml인 농도로 존재할 수 있다. APT는 1-100 μM 또는 1-50 μM 또는 1-20 μM, 또는 약 10 μM인 농도로 존재할 수 있다.
RGC 분화 배지는 인슐린을 포함할 수 있다. 인슐린은 인간 인슐린일 수 있다. 인슐린은 약 5-50 ㎍/ml 또는 약 20 ㎍/ml인 농도로 존재할 수 있다.
RGC 분화 배지의 존재하에서 배양하는 것은 약 1-4주 또는 약 2-4주 또는 약 2-3주 또는 약 2주 동안 이루어질 수 있다. RGC 분화 배지는 전체적으로 또는 부분적으로, 매일, 또는 매 2일마다, 또는 매 3일마다, 또는 덜 빈번하게 교체될 수 있다.
본 방법에 의해 제조된 RG 세포는 배양물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%의 세포를 포함할 수 있고, 임의적으로, 상기 배양물은 1주, 2주, 또는, 3주, 4주 또는 더 긴 시간을 비롯한, 2주 초과 동안 증식될 수 있다.
RG 세포는 마커: Brn3a, 신경미세섬유, Tuj1 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), Tuj1(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 세포는 Brn3a(+), 신경미세섬유(+), 또는 Brn3a(+), 신경미세섬유(+), Thy1(+), 또는 Brn3a(+), 신경미세섬유(+), Thy1(+), 또는 Brn3a(+), 신경미세섬유(+), Tuj1(+), 또는 Brn3a(+), 신경미세섬유(+), Tuj1(+), Thy1(+)인 것을 특징으로 할 수 있다. RG 세포는 유사분열 이후의 것일 수 있고, RG 전구체 세포보다 더 많은 개수, 더 긴 및/또는 더욱 복잡한 수상 돌기를 포함할 수 있다.
RG 세포는 냉동보존될 수 있다. RG 세포는 인간 세포일 수 있다.
또 다른 측면에서, 본 개시내용은 신경절 세포 배지 중에서 안구 영역 전구체 세포를 배양하는 단계를 포함하는, RG 전구체 세포를 제조하는 방법을 제공한다.
안구 영역 전구체 세포는, 그 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%가 안구 영역 전구체 세포인, 세포 집단으로서 제공될 수 있다. 안구 영역 전구체 세포는 Pax6(+) 및 Rx1(+) 및 임의적으로, 또는 Six3(+), Six6(+), Lhx2(+), 및/또는 Tbx3(+)일 수 있다. 안구 영역 전구체 세포는 또한 Sox2(+)일 수 있다. 안구 영역 전구체 세포는 네스틴(Nestin)(+)일 수 있다. 안구 영역 전구체 세포는 또한 Otx2(+)일 수 있다.
안구 영역 전구체는 만능 줄기 세포의 시험관내 분화에 의해 수득될 수 있다. 일부 실시양태에서, 만능 줄기 세포는 ES 세포 또는 iPS 세포일 수 있다. 만능 줄기 세포는 피더세포 무함유 및/또는 제노 프리 조건하에서 배양될 수 있다.
안구 영역 전구체 세포의 배양은 약 5-45일, 또는 약 5-20일, 또는 약 35-45일 동안 이루어질 수 있다. 신경절 세포 배지, 및 신경절 세포 배지에서의 배양 파라미터는 상기 기술된 바와 같을 수 있다.
본 방법에 의해 제조된 RG 전구체 세포는 배양물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 이상 또는 약 100%의 세포를 포함할 수 있고, 임의적으로, (RG 전구체 세포를 상기 비율(%)로 포함하는) 상기 배양물은 1주, 2주, 또는, 3주, 4주 또는 더 긴 시간을 비롯한, 2주 초과 동안 증식될 수 있다.
RG 전구체 세포의 표현형은 상기 기술된 바와 같다. 따라서, 한 예로서, RG 전구체 세포는 마커: Math5, Brn3a, Brn3b, Isl1, 신경미세섬유, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), Isl1(+), 신경미세섬유(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 마커: Math5, Brn3a, Brn3b, 및 Isl1 중 하나 이상의 것을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), 및/또는 Isl1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 마커: Brn3a, 신경미세섬유, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체는 Pax6 또는 Rx1을 발현하지 않을 수 있고, 따라서, Pax6(-) 및/또는 Rx1(-)인 것을 특징으로 할 수 있다. RG 전구체 세포는 증식성일 수 있다. 다른 표현형은 상기 기술된 바와 같다.
RG 전구체 세포는 냉동보존될 수 있다. RG 전구체 세포는 인간 세포일 수 있다.
또 다른 측면에서, 본 개시내용은 안구 영역 전구체 세포를 신경절 세포 배지 및 망막 신경절 세포(RGC) 분화 배지 중에서 순차적으로 배양하는 단계를 포함하는, RG 세포를 제조하는 방법을 제공한다.
안구 영역 전구체 세포는, 그 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%가 안구 영역 전구체 세포인, 세포 집단으로서 제공될 수 있다. 안구 영역 전구체 세포는 Pax6(+) 및 Rx1(+) 및 임의적으로, 또한 Six3(+), Six6(+), Lhx2(+), 및/또는 Tbx3(+)일 수 있다. 안구 영역 전구체 세포는 또한 Sox2(+)일 수 있다. 안구 영역 전구체 세포는 네스틴(+)일 수 있다. 안구 영역 전구체 세포는 또한 Otx2(+)일 수 있다.
안구 영역 전구체는 만능 줄기 세포의 시험관내 분화에 의해 수득될 수 있다. 일부 실시양태에서, 만능 줄기 세포는 ES 세포 또는 iPS 세포일 수 있다. 만능 줄기 세포는 피더세포 무함유 및/또는 제노 프리 조건하에서 배양될 수 있다.
신경절 세포 배지, 및 신경절 세포 배지에서의 배양 파라미터는 상기 기술된 바와 같을 수 있다. RGC 분화 배지, 및 RGC 분화 배지에서의 배양 파라미터는 상기 기술된 바와 같을 수 있다.
본 방법에 의해 제조된 RG 세포는 배양물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%의 세포를 포함할 수 있고, 임의적으로, (RG 세포를 상기 비율(%)로 포함하는) 상기 배양물은 1주, 2주, 또는, 3주, 4주 또는 더 긴 시간을 비롯한, 2주 초과 동안 증식될 수 있다.
RG 세포의 표현형은 상기 기술된 바와 같다. 따라서, 한 예로서, RG 세포는 마커: 마커: Brn3a, 신경미세섬유, Tuj1, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), Tuj1(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 세포는 유사분열 이후의 것일 수 있다. RG 세포는 유사분열 이후의 것일 수 있고, RG 전구체 세포보다 더 복잡한 수상 돌기, 더 긴 수상 돌기, 및/또는 더 많은 수상 돌기를 가질 수 있다. 다른 표현형은 상기 기술되어 있다.
RG 세포는 냉동보존될 수 있다. RG 세포는 인간 세포일 수 있다.
또 다른 측면에서, 본 개시내용은 RG 전구체 세포를 망막 신경절 세포(RGC) 분화 배지 중에서 배양하는 단계를 포함하는, RG 세포를 제조하는 방법을 제공한다.
RG 전구체 세포는, 그 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%가 RG 전구체 세포인, 세포 집단으로서 제공될 수 있다. RG 전구체 세포는 마커: Math5, Brn3a, Brn3b, Isl1, 신경미세섬유, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), Isl1(+), 신경미세섬유(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 마커: Math5, Brn3a, Brn3b, 및 Isl1 중 하나 이상의 것을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), 및/또는 Isl1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 마커: Brn3a, 신경미세섬유, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체는 Pax6 또는 Rx1 발현하지 않을 수 있고, Pax6(-) 및/또는 Rx1(-)인 것을 특징으로 할 수 있다. RG 전구체는 만능 줄기 세포의 시험관내 분화에 의해 수득될 수 있다. 일부 실시양태에서, 만능 줄기 세포는 ES 세포 또는 iPS 세포일 수 있다. 만능 줄기 세포는 피더세포 무함유 및/또는 제노 프리 조건하에서 배양될 수 있다.
RGC 분화 배지 및 RGC 분화 배지에서의 배양 파라미터는 상기 기술된 바와 같을 수 있다.
본 방법에 의해 제조된 RG 세포는 배양물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 이상 또는 약 100%의 세포를 포함할 수 있고, 임의적으로, (RG 세포를 상기 비율(%)로 포함하는) 상기 배양물은 1주, 2주, 또는, 3주, 4주 또는 더 긴 시간을 비롯한, 2주 초과 동안 증식될 수 있다.
RG 세포는 마커: Brn3a, 신경미세섬유, Tuj1, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), Tuj1(+), 및 Thy1(+)인 것을 특징으로 할 수 있다.
RG 세포는 냉동보존될 수 있다. RG 세포는 인간 세포일 수 있다.
또 다른 측면에서, 본 개시내용은 본원에 기술된 바와 같은, 예컨대, 이전 단락에서 기술된 바와 같은 방법을 사용하여 제조된 RG 전구체 세포를 포함하는 조성물을 제공한다.
또 다른 측면에서, 본 개시내용은 임의적으로, 인간 세포인 것인, RG 전구체 세포를 포함하는 조성물을 제공한다.
RG 전구체 세포는 조성물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%의 세포를 포함할 수 있다.
RG 전구체 세포는 마커: Math5, Brn3a, Brn3b, Isl1, 신경미세섬유, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), Isl1(+), 신경미세섬유(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 Math5, Brn3a, Brn3b, 및 Isl1을 발현할 수 있고, 따라서, Math5(+), Brn3a(+), Brn3b(+), 및 Isl1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포는 Brn3a, 신경미세섬유, 및 Thy1을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), 및 Thy1(+)인 것을 특징으로 할 수 있다. RG 전구체 세포에 대한 다른 표현형은 상기 기술된 바와 같다.
RG 전구체 세포는 냉동보존될 수 있다. RG 전구체 세포는 인간 세포일 수 있다.
또 다른 측면에서, 본 개시내용은 치료를 필요로 하는 개체에게 RG 전구체 세포를 포함하는 조성물(예컨대, 본원에 기술된 바와 같은 조성물 또는 본원에 기술된 바와 같은 방법을 사용하여 제조된 조성물)을 투여하는 단계를 포함하는, 치료를 필요로 하는 개체를 치료하는 방법을 제공한다.
조성물은 안구, 유리체, 망막하 공간, 또는 정맥내로 투여될 수 있다. RG 전구체 세포는 인간 세포일 수 있다.
또 다른 측면에서, 본 개시내용은 본원에, 예컨대, 이전 단락에 기술된 바와 같은 방법에 따라 제조된 RG 세포를 포함하는 조성물을 제공한다.
본 방법에 의해 제조된 RG 세포는 조성물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%의 세포를 포함할 수 있고, 임의적으로, (RG 세포를 상기 비율(%)로 포함하는) 상기 조성물은 1주, 2주, 또는, 3주, 4주 또는 더 긴 시간을 비롯한, 2주 초과 동안 증식될 수 있다.
RG 세포는 마커: Brn3a, 신경미세섬유, Tuj1, 및 Thy1 중 하나 이상의 것을 발현할 수 있고, 따라서, Brn3a(+), 신경미세섬유(+), Tuj1(+), 및/또는 Thy1(+)인 것을 특징으로 할 수 있다.
RG 세포는 냉동보존될 수 있다. RG 세포는 인간 세포일 수 있다.
또 다른 측면에서, 본 개시내용은 치료를 필요로 하는 개체에게 RG 세포를 포함하는 조성물, 예컨대, 본원에, 예컨대, 이전 단락에 기술된 바와 같은 조성물 또는 본원에, 예컨대, 이전 단락에 기술된 바와 같은 방법에 의해 제조된 조성물을 투여하는 단계를 포함하는, 치료를 필요로 하는 개체를 치료하는 방법을 제공한다.
조성물은 안구, 유리체, 망막하 공간, 또는 정맥내로 투여될 수 있다.
또 다른 실시양태에서, 본 발명은 마우스 섬유아세포 피더세포 플랫폼상에서 성장시키지 않은 세포로부터 기원된, 인간 기원의 세포, 바람직하게는 비공여자 유래 RG 전구체 세포 또는 RG 세포의 실질적으로 순수한 제제에 관한 것이다. 예를 들어, 제제는 85%-95% 순수한 것일 수 있다. 한 실시양태에서, 본 발명은 마우스 섬유아세포 피더세포 플랫폼으로부터 유래된 세포에 대한 필요성이 생략된 인간 기원의 RG 전구체 세포 또는 RG 세포의 실질적으로 순수한 제제를 제조하는 방법에 관한 것이다. 피더세포 시스템을 본 발명의 방법으로 교체하면, 예컨대, 75% 내지 100% 또는 85% 내지 95%로 더욱 균질한 RG 전구체 세포 또는 RG 세포를 얻을 수 있다. 피더세포 무함유 줄기 세포의 분화는 또한 외인성 유도 인자의 도입 없이도 일어날 수 있으며, 이것이 선행 기술에 비하여 더 나은 실질적으로 개선된 점이다. 그러나, 비록 분화가 필수적인 것은 아니지만, 노긴 폴리펩티드의 임의적 첨가는 줄기 세포의 분화를 가속화시킬 수 있다.
또 다른 실시양태에서, 분화 방법은 피더세포 무함유 및 제노 프리이다. 따라서, 일부 실시양태에서, 인간 세포는 인간외 종으로부터 유래된 임의의 배지 성분 부재하에서 배양된다.
본 발명의 상세한 설명
본 발명은 망막 신경절(RG) 세포 및 RG 전구체 세포를 생성하는 방법을 제공한다. 본 방법은 만능 줄기 세포 및 안구 영역(EF) 전구체를 비롯한, 더 이른 시점의 전구체로부터의 시험관내 분화를 포함한다. 본원에서 제공하는 본 방법은 출발 물질로서 상기 전구체 집단 중 임의의 것(줄기 세포 포함)을 사용할 수 있다.
본 발명은 시험관내에서 1차 안구 영역(EF) 전구체(즉, 피험체로부터 수득된 EF 전구체 세포)로부터 RG 세포 및 RG 전구체 세포를 생성하는 것도 추가로 고려한다.
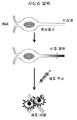
생체내 또는 시험관내에서의 망막 신경 발생은 다수의 발생 단계를 거쳐 이루어지며, 이들은 각각 (예컨대, 마커 발현 프로파일에 의해) 표현형에 의해, 및/또는 기능적으로 정의될 수 있다. 시험관내에서 만능 줄기 세포는 EF 전구체로 분화되고, 이어서, 조기 RG 전구체 세포 및 후기 RG 전구체 세포를 포함할 수 있는 RG 전구체 세포로 분화되고, 최종적으로는 성숙한 RG 세포(본원에서 RG 세포로 지칭됨)로 분화된다. RG 전구체 세포 내에서, 조기 RG 전구체 세포는 후기 RG 전구체 세포로 분화될 수 있다. 후기 RG 전구체 세포는 성숙한 RG 세포로 분화될 수 있다. 조기 RG 전구체 세포는 성숙한 RG 세포로 직접 분화될 수 있다. 본원에서 제공하는 방법은 RG 세포 및 RG 전구체 세포를 효율적으로 생성한다.
만능 줄기 세포에서 RG 전구체 세포 및 RG 세포로의 발생에 관한 전반적인 발생 경로는 도 9에 개략적으로 도시되어 있다. 각 발생 단계에 대한 마커 발현 프로파일 또한 제시되어 있다.
본원에서 사용되는 바, 전구체 세포란, 유사분열은 유지하면서, 더 많은 전구체 세포를 생산할 수 있거나, 또는 최종 세포 계통으로 분화될 수 있는 세포를 의미한다. 전구체 및 전구라는 용어는 상호교환적으로 사용된다. 이들 각 단계의 세포는 본원에서 보다 상세하게 논의될 것이다.
본원에서 제공하는 RG 전구체 및 RG 세포는 다양한 생체내 및 시험관내 방법에서 사용될 수 있다. 예를 들어, RG 전구체 세포는 생체내에서 녹내장, 예컨대, 개방각 녹내장, 녹내장, 정상 안압 녹내장, 선천성 녹내장, 색소 녹내장, 속발성 녹내장, 가박탈성 녹내장, 외상 녹내장, 신생혈관 녹내장, 및 홍채 각막 내피 증후군 뿐만 아니라, 시신경 손상, 임의적으로, 자가면역 질환, 외상, 바이러스 감염, 및 허혈성 재관류 손상, 임의적으로, 뇌졸중과 관련된 허혈성 재관류 손상과 관련된 시신경 손상, 당뇨병성 망막증, 또는 눈으로의 혈액 공급을 손상시키는 다른 병태를 포함하나, 이에 제한되지 않는, 망막 병태를 치료하는 데 사용될 수 있다.
본 발명은 본원에 기술된 방법에 의해 수득된 RG 전구체 세포 및 RG 세포를 추가로 제공한다. RG 전구체 세포 및 RG 세포는 만능 줄기 세포 또는 그의 분화된 자손, 예컨대, 안구 영역 전구체 세포의 시험관내 분화에 의해 수득된다. 안구 영역 전구체 세포 그 자체는 만능 줄기 세포의 시험관내 분화로부터 수득될 수 있거나, 또는 피험체로부터 수득된 1차 안구 영역 전구체일 수 있다.
본 발명은 1차 공급원으로부터 획득한 것이 아니거나, 또는 획득할 수 없는 RG 전구체 세포 집단 및 RG 세포 집단을 제공한다. 상기 집단은 그의 세포 내용물에 있어서 균질성이거나, 또는 거의 균질성일 수 있다. 예를 들어, 상기 집단 중 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95% 이상, 99%, 또는 약 100%의 세포는 RG 전구체 세포일 수 있다. 또 다른 예로서, 상기 집단 중 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95% 이상, 99%, 또는 약 100%의 세포는 RG 세포일 수 있다. 상기 집단 중 상기 세포는 단일 일배체형일 수 있다. 예를 들어, 이는 HLA 매칭될 수 있다. 상기 집단 중 상기 세포는 유전적으로 동일할 수 있다. 본 발명은 HLA 유형의 RG 전구체 세포 은행을 추가로 제공한다. 상기 세포는 다양한 인간 피험체에서 사용될 수 있다.
추가로, 본원에서 제공하는 방법은 다르게는 1차 공급원으로서는 가능한 것이 아닌, 다수의 RG 전구체 세포 및 RG 세포를 생성하는 데 사용될 수 있다. 예를 들어, 본 방법은 출발 만능 세포 100만 개당 108개의 RG 전구체 세포 또는 108개의 RG 세포를 생산할 수 있다.
분화된(
비줄기
) 세포 유형
안구 영역 전구체 세포( EF 전구체 세포). EF 전구체 세포는 최소 Pax6(+) 및 Rx1(+) 세포로 정의된다. 이는 또한 Six3(+), Six6(+), Lhx2(+), 및 Tbx3(+)일 수 있다. 상기 마커들 모두 전사 인자이다. EF 전구체 세포는 또한 네스틴(+) 및/또는 Sox2(+), 및/또는 Otx2(+)일 수 있다. EF 전구체 세포는 Oct4 및 Nanog를 발현하지 않는다(즉, 이는 Oct4(-) 및 Nanog(-)이다). EF 전구체 세포는 만능 줄기 세포의 시험관내 분화를 통해 형성될 수 있다. 상기 분화는 망막 유도(RI) 배지의 존재하에서 발생할 수 있고, 외인성 인자, 예컨대, 노긴 폴리펩티드 또는 노긴 유사 화합물의 존재 또는 부재하에서 발생할 수 있다.
망막 신경절( RG ) 전구체 세포. 본 발명의 분화 방법을 통해 RG 발생은 이전에 가능했던 것보다 한층 더 깊이 분석될 수 있으며, 이로써, 2개의 RG 전구체 단계가 밝혀졌다. EF 전구체 세포로부터 발생하는 제1 단계는 조기 RG 전구체 세포 단계이다. 상기 세포는 Math5, Brn3a, Brn3b, 및 Isl1 중 하나 이상 또는 그들 모두의 발현(즉, Math5(+) 및/또는 Brn3a(+) 및/또는 Brn3b(+) 및/또는 Isl1(+))에 의해 및 Pax6 및 Rx1의 비발현 또는 검출불가능한 발현(즉, Pax6(-) 및 Rx1(-))에 의해 정의된다. 상기 RG 전구체는 Math5(+), 또는 Math5(+), Brn3a(+), 또는 Math5(+), Brn3a(+), Brn3b(+), 또는 Math5(+), Brn3a(+), Brn3b(+), Isl1(+)일 수 있다. 상기 조기 RG 전구체 세포는 후기 RG 전구체 세포로 추가로 분화된다. 상기 세포는 Brn3a, 신경미세섬유, 및 Thy1 중 하나 이상 또는 그들 모두의 발현(즉, Brn3a(+) 및/또는 신경미세섬유(+) 및/또는 Thy1(+))에 의해 및 Math5, Brn3b, 및 Isl1의 비발현 또는 검출불가능한 발현(즉, 즉, Math5(-), Brn3b(-) 및 Isl1(-))에 의해 정의된다. 상기 RG 전구체는 Brn3a(+), 신경미세섬유(+) 및 Thy1(+)일 수 있다. 이어서, 상기 후기 RG 전구체 세포는 RG 세포로 분화된다. 조기 RG 전구체 세포는 또한, 예를 들어, RGC 분화 배지 중에서 배양되었을 때에는 RG 세포로 직접 분화될 수 있다. RG 전구체 세포는 증식성이다.
망막 신경절( RG ) 세포. RG 세포는 최소 신경미세섬유, Tuj1, Thy1 및 Brn3a 중 하나 이상 또는 그들 모두의 발현(즉, 즉, 신경미세섬유(+) 및/또는 Tuj1(+) 및/또는 Thy1(+) 및/또는 Brn3a(+))에 의해 정의된다. RG 세포는 Brn3a(+), 신경미세섬유(+), Tuj1(+) 및 임의적으로, Thy1(+)일 수 있다. RG 세포는 유사분열 이후의 것이다. RG 세포는 RG 전구체 세포보다 더 많은 수상 돌기, 더욱 복잡한 수상 돌기, 및 더욱 긴 수상 돌기를 가질 수 있다.
배양 방법
만능 줄기 세포 유지 배양. 만능 줄기 세포는 피더세포 무함유 시스템, 임의적으로, 매트릭스 상에서 유지될 수 있고, 따라서, 증식될 수 있다. 적합한 매트릭스로는 라미닌, 피브로넥틴, 비트로넥틴, 프로테오글리칸, 엔탁틴, 콜라겐, 콜라겐 I, 콜라겐 IV, 콜라겐 VIII, 헤파란 술페이트, 마트리겔™(엔겔브레쓰-홀름-스웜(EHS: Engelbreth-Holm-Swarm) 마우스 육종 세포로부터의 가용성 제제), 셀스타트(Cellstart)(인간 기저막 추출물), 또는 그의 임의 조합을 포함하거나, 또는 그로 이루어진 것을 포함하나, 이에 제한되지 않는다. 일부 실시양태에서, 매트릭스는 마트리겔™을 포함하거나, 그로 이루어지거나, 또는 본질적으로 그로 이루어진다. 마트리겔™은 상업적 공급원, 예컨대, BD 바이오사이언시스(BD Biosciences)로부터 이용가능하다. 재조합 인간 라미닌을 비롯한 라미닌은 마트리겔™에 대한 대체물로서 사용될 수 있다.
예시적인 방법에서, 만능 줄기 세포를 그의 비분화된 상태로 마트리겔™ 또는 라미닌 상에서 피더세포 무함유 조건하에서 유지시킨다. 전형적으로는 전면생장률이 약 80-90%일 때, 세포를 계대접종하거나, 또는 냉동시킨다. 효소적 수단(예컨대, 디스파제) 또는 비효소적 수단(예컨대, PBS 기반 해리 완충제, 인비트로겐)을 사용하여 계대접종을 수행할 수 있다. 일부 실시양태에서, 만능 줄기 세포를 제노 프리 조건하에서 배양할 수 있고, 일부 경우에서, 혈청 보충제, 예컨대, 제한하는 것은 아니지만, N2 혈청 보충제의 존재하에서 배양하는 것을 포함할 수 있다.
만능 줄기 세포 분화 배양. 예를 들어, 배양체(EB)에서 발생할 수 있는 바, 만능 줄기 세포의 RG 세포 또는 RG 전구체 세포로의 분화가 비신경절 세포 계통으로의 분화를 포함하지 않도록 의도하면서, 만능 줄기 세포를 직접 분화시킬 수 있다. 따라서, 본원에서 제공하는 방법은 EB 형성을 필요로 하지 않고, 바람직하게는 그를 회피한다. 이것이 선행 기술 방법에 대해 개선된 점이다.
RG 전구체 세포 또는 RG 세포는 신경구 형성을 포함하는 현탁 배양에 의해 생성될 수 있거나, 또는 매트릭스, 예컨대, 제한하는 것은 아니지만, 마트리겔™ 또는 라미닌에 부착될 수 있다.
하기는 만능 줄기 세포의 RG 전구체 세포 및 RG 세포로의 분화를 위한 대한 예시적인 프로세스이다.
망막 유도(RI) 배지 및 신경 분화(ND) 배지 중에서 만능 줄기 세포를 배양함으로써 만능 줄기 세포를 먼저 EF 전구체 세포로 분화시킨다.
0일째 전면생장률이 약 15-20%인 만능 줄기 세포에 RI 배지를 첨가한다. RI 배지는 기본 배지, 예컨대, DMEM/F12 또는 DMEM/F12의 성분, D-글루코스, 항생제, 예컨대, 페니실린 및 스트렙토마이신, 하나 이상의 혈청 보충제, 예컨대, N2 보충제 및 B27 보충제, 비필수 아미노산, 인슐린, 및 임의적으로, 외인성 분화 인자, 예컨대, 노긴 폴리펩티드 또는 노긴 유사 인자(하기 기술)를 포함하는 배지를 포함한다.
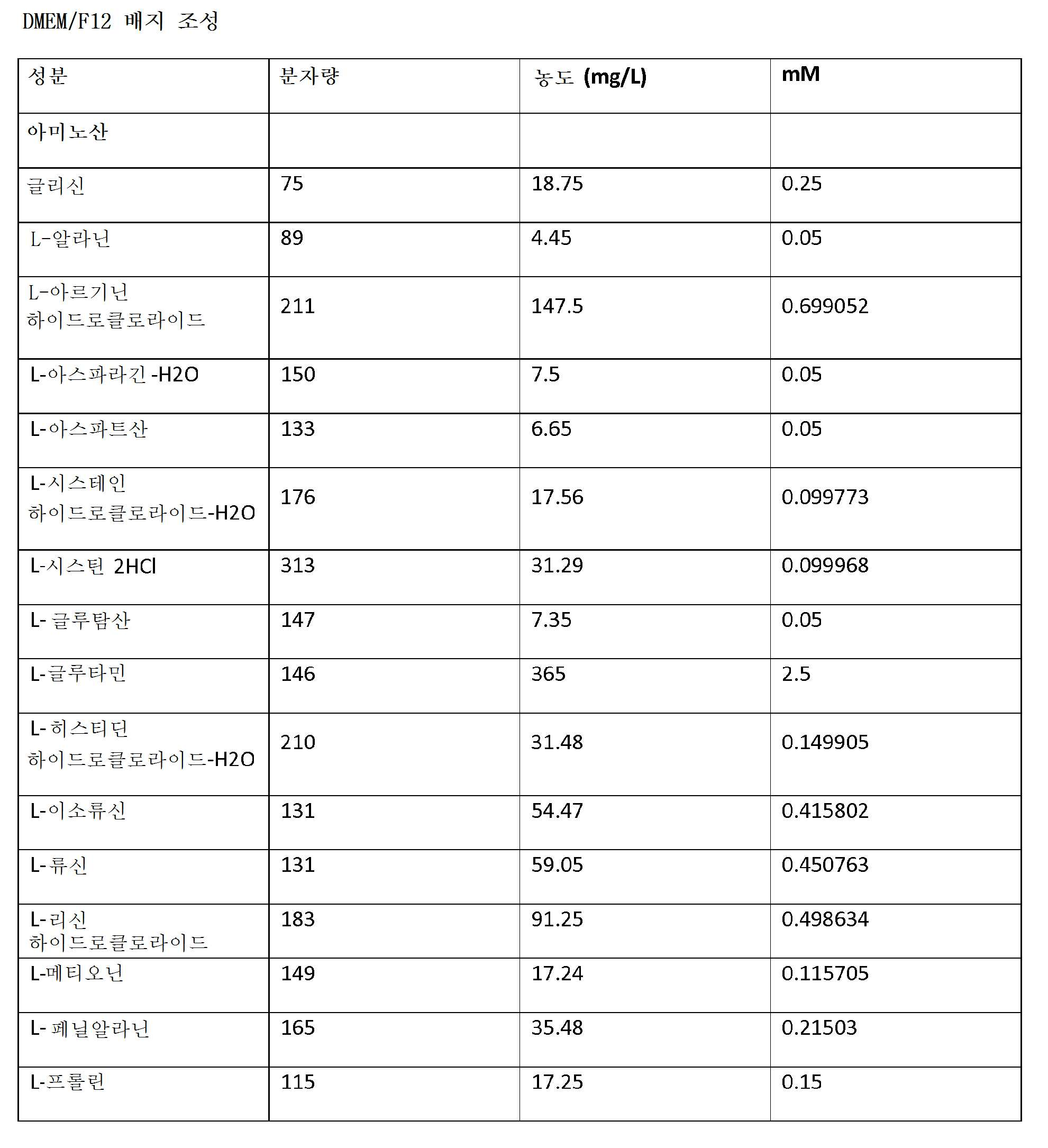
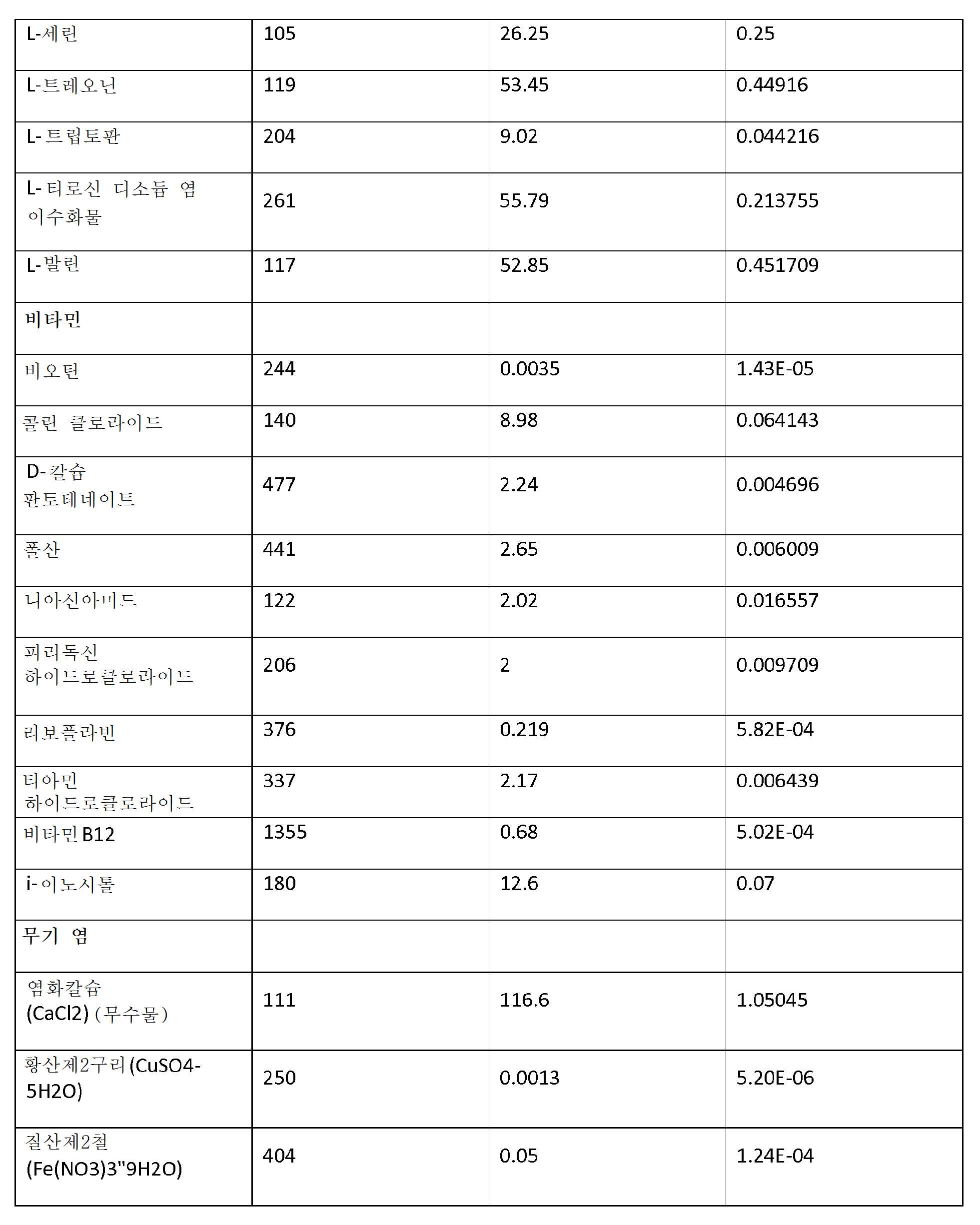
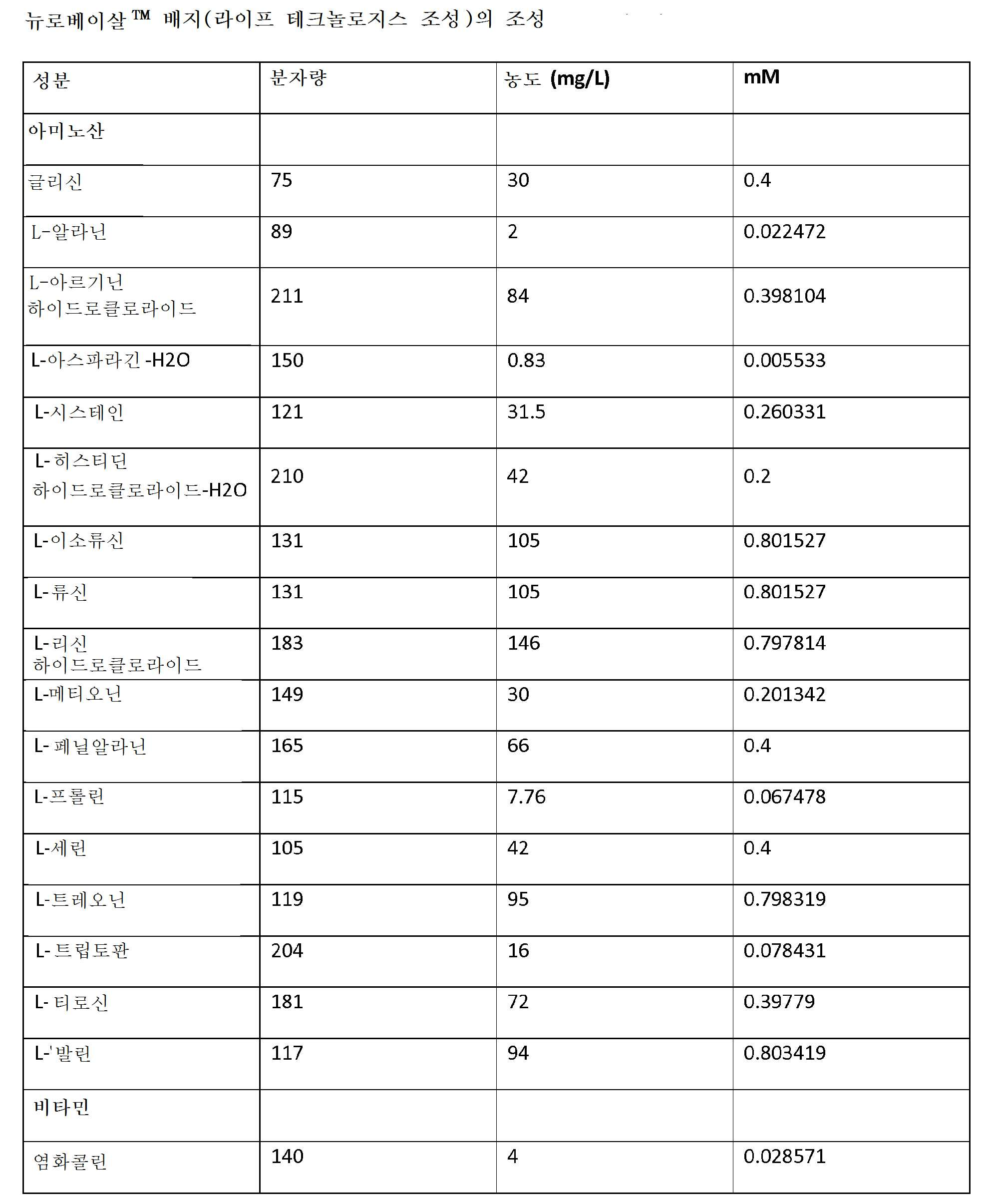
DMEM/F12의 성분, N2 보충제, 및 B27 보충제는 하기 표 1에 제공되어 있다.
RI 배지 중에서의 배양은 약 5일 동안 이루어질 수 있다. 완전한 배지 교체는 1-4일째 수행된다.
약 4일 경과 후(예컨대, 4, 5 또는 6일째 당일 또는 대략 그 시점에), 배지를 신경 분화(ND) 배지로 교체한다. ND 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스), 또는 뉴로베이살™ 배지의 성분, D-글루코스, 항생제, 예컨대, 페니실린 및 스트렙토마이신, 글루타맥스™, 하나 이상의 혈청 보충제, 예컨대, N2 보충제 및 B27 보충제, 비필수 아미노산, 및 임의적으로, 외인성 분화 인자, 예컨대, 노긴 폴리펩티드 또는 노긴 유사 인자(하기 기술)를 포함하는 배지를 포함한다.
뉴로베이살™ 배지(라이프 테크놀러지스) 성분은 하기 표 1에 제공되어 있다.
글루타맥스™는 L-글루타민의 안정화된 형태인, L-알라닐-L-글루타민이다. 이는 배양물 중에서 덜 분해되고, 이로써, 장기간 배양에서 발생할 수 있는 암모니아 증가(ammonia build-up)는 감소된다.
세포를 ND 배지 중에 추가로 약 8일(6-13일째) 동안 배양한다. 배지는 정기적으로 교체한다(예컨대, 대략 매 2일마다). 상기 배양 기간 동안 세포는 콜로니로서 성장하고, 여기서, 가장자리에 있는 세포는 평평하고, 커지게 되는 반면, 더욱 중앙부에 위치하는 세포는 더욱 작아지고, 조밀한 세포 클러스터를 형성하게 된다.
약 10-11일째, 세포는 Pax6을 발현하기 시작한 후, 12일째 Rx1 발현을 시작한다(도 1a). RT-PCR 분석 결과, Oct4 및 Nanog 발현 손실이 나타났다(도 1b). 13일째, 정량화된 유세포 분석법에 따르면, 90% 초과의 세포가 Pax6 및 Rx1을 공동 발현하고(도 2a), 99% 초과의 세포가 네스틴, Otx2 및 Sox2를 발현한다(도 2b). 이러한 결과는 만능 줄기 세포가 EF 전구체 세포로 분화되었다는 것을 나타내는 것이다.
약 14일 경과 후(예컨대, 11, 12, 13, 14, 또는 15일째 당일 또는 대략 그 시점에), 배지를 신경절 세포(GC) 배지로 교체한다. GC 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스) 또는 뉴로베이살™ 배지의 성분, D-글루코스, 하나 이상의 항생제, 예컨대, 페니실린 및 스트렙토마이신, 글루타맥스™, 하나 이상의 혈청 보충제, 예컨대, N2 보충제 및 B27 보충제(포뮬러 080085-SA), 및 포스콜린, BDNF 및 CNTF 모두를 포함하는 것 중 하나 이상의 것을 포함하는 배지를 포함한다. 세포는 약 20일째까지 GC 배지 중에서 계속 배양된다.
약 20일째, 세포 스크레이퍼를 사용하여 성장 표면으로부터 세포를 들어 올리고, GC 배지 중에서 기계적으로 클러스터로 단편화시킨다. 세포 클러스터를 100 mm 초저 부착 배양 디쉬로 옮긴다. 세포 클러스터는 현탁 배양물 중에서 둥근 형태가 되고, 개별 구체를 형성한다. GC 배지를 매 3일마다 교체한다. 약 35일째, 실시간 RT-PCR 결과, Math5, Brn3a, Brn3b 및 Isl1 발현이 강력하게 상향조절된 것으로 나타났다(도 3a). 유세포 분석법 결과, >99% 세포가 전사 인자 Math5 및 Brn3a를 발현한 것으로 나타났다. 약 94% Math5(+) 세포는 Pax6에 대해 음성으로 염색되었다(도 3b). 상기 결과는 조기 RG 전구체 세포가 존재함을 나타낸다.
약 36-60일째 사이에, 신경구를 GC 배지 중에서 배양하고, 여기서, 배지를 약 매 3-4일마다 교체한다.
약 60일째, 실시간 RT-PCR 결과, Brn3a의 발현이 계속되는 것으로 나타났다. Math5 및 Brn3b의 발현 수준은 현저히 하향조절되었다(도 4). 유세포 분석법 결과, 95.3%의 세포가 Brn3a 및 신경미세섬유를 공동 발현한 것으로 나타났다(데이터 나타내지 않음). 이러한 결과는 후기 RG 전구체 세포가 존재함을 나타낸다.
RG 세포를 형성하는 RG 전구체 세포의 분화. 어큐타제(Accutase)® 세포 탈착 용액을 사용하여 RG 전구체 세포를 단일 세포로 해리시킨다. 세포를 약 10-40/㎠의 밀도로 망막 신경절 세포(RGC) 분화 배지 중 폴리-D-리신/라미닌 코팅된 플레이트 상에 플레이팅한다. RCG 분화 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스) 또는 뉴로베이살™ 배지의 성분, D-글루코스, 항생제, 예컨대, 페니실린 및 스트렙토마이신, 글루타맥스™, 하나 이상의 혈청 보충제, 예컨대, B27 보충제(포뮬러 080085-SA), 인슐린, BDNF 및 CNTF 중 하나 또는 그 둘 모두, 및 포스콜린, cAMP 및 DAPT 모두를 포함하는 것 중 하나 이상의 것, 또는 다른 노치 억제제를 포함하는 배지를 포함한다. 뉴로베이살™ 배지의 성분은 하기 표 1에 제공되어 있다. 배지를 약 매 2일마다 교체하였다.
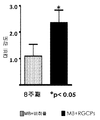
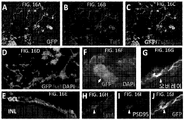
2주 경과 후, 약 72%의 세포가 Thy1에 대하여 양성으로 염색되었다(도 5). 세포는 수상 돌기 및 축삭돌기를 가졌다(도 6a). 면역염색 결과, Brn3a, 신경미세섬유 및 Tuj1의 발현이 나타났다(도 6b). 상기 결과는 RG 세포가 존재함을 나타낸다.
RG 전구체 및 RG 세포 냉동보존. 조기 RG 전구체 세포, 후기 RG 전구체 세포, 및 RG 세포는 신경구로서 동물 무함유 냉동보존 완충제, 예컨대, 크라이오스토르(Cryostor) CS10 중에서 냉동/냉동보존될 수 있다.
세포 배양 배지
본 발명의 실시양태에서, 세포를 다양한 세포 배양 배지 중에서 증식시키거나, 또는 분화시킨다. 상기 배지는 하기에서 더욱 상세하게 기술된다.
망막 유도(RI) 배지. 망막 유도(RI) 배지는 만능 줄기 세포를 EF 전구체 세포로 분화시키는 데 사용된다. 망막 유도(RI) 배지는 기본 배지, 예컨대, DMEM/F12, 또는 DMEM/F12의 성분(하기 표 1에 제시), D-글루코스(임의적으로, 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml), 하나 이상의 항생제, 예컨대, 페니실린(임의적으로, 0-100 유니트/ml 또는 약 100 유니트/ml) 및 스트렙토마이신(임의적으로, 0-100 ㎍/ml 또는 약 100 ㎍/ml), 하나 이상의 혈청 보충제, 예컨대, N2 보충제(임의적으로, 약 0.1 내지 5% (v/v) 또는 약 0.1 내지 2% (v/v) 또는 약 1% (v/v)) 및 B27 보충제(임의적으로, 약 0.05-2.0% (v/v) 또는 약 0.2% (v/v)), MEM 비필수 아미노산 용액(임의적으로, 스톡으로부터 제조된 약 1X 농도, 대략 0.1 mM 글리신), 및 임의적으로, 인슐린(임의적으로, 5-50 ㎍/ml 또는 약 20 ㎍/ml)을 포함하는 배지를 포함한다. RI 배지는 약 5-100 ng/ml 또는 약 10-100 ng/ml 또는 약 10-500 ng/ml 또는 약 50 ng/ml 농도의 노긴 폴리펩티드를 포함할 수 있다. 망막 유도 배지는 임의적으로, 노긴 폴리펩티드, 도소모르핀, LDN-193189, 및 그의 임의 조합으로 이루어진 군으로부터 선택되는 BMP 신호전달 억제제를 포함할 수 있다. RI 배지는 인슐린, 노긴 폴리펩티드, 또는 인슐린 및 노긴 폴리펩티드를 포함할 수 있다.
노긴 폴리펩티드가 존재할 때, (EF 전사 인자 발현 증가로 명시되는 바와 같이) EF 전구체 세포로의 분화 증가가 관찰되기는 하지만, 노긴 폴리펩티드가 반드시 필요한 것은 아니다. 노긴 폴리펩티드는 SB431542를 포함하나, 이에 제한되지 않는, 유사한 활성을 가지는 다른 모이어티로 치환될 수 있다.
노긴 폴리펩티드는 보고에 따르면, 고친화도로 BMP2, BMP4, 및 BMP7에 결합하여 TGFβ 패밀리 활성을 차단하는 것인, 분비된 BMP 억제제이다. SB431542는 보고에 따르면, ACTRIB, TGFβR1, 및 ACTRIC 수용체의 인산화를 차단함으로써 TGFβ/액티빈(Activin)/노달(Nodal)을 억제시키는 소분자이다. SB431542는 내인성 액티빈 및 BMP 신호를 차단함으로써 액티빈- 및 Nanog-매개 만는성 네트워크를 탈안정화시킬 뿐만 아니라, BMP 유도성 영양포, 중배엽, 및 내배엽 세포 운명을 억제시키는 것으로 여겨진다.
예컨대, 개시된 방법 맥락에서 사용되는 바, 상기 언급된 활성 중 하나 이상을 가지는 작용제가 노긴 폴리펩티드 및 SB431542 중 하나, 또는 그 둘 모두의 기능을 대체할 수 있거나, 또는 그를 증강시킬 수 있을 것으로 기대된다. 예를 들어, 노긴 폴리펩티드 및/또는 소분자 SB4312542는 하기의 3가지 표적 영역: 1) 리간드의 수용체에의 결합 방해; 2) 수용체(예컨대, 도소모르핀)의 활성화 차단, 및 3) SMAD 세포내 단백질/전사 인자 억제 중 임의의 것 또는 그들 모두에 영향을 주는 하나 이상의 억제제에 의해 대체되거나, 또는 증강될 수 있다. 잠재적으로 적합한 예시적인 인자로는 천연의 분비된 BMP 억제제 코르딘(Chordin)(BMP4 차단) 및 폴리스타틴(Follistatin)(액티빈 차단) 뿐만 아니라, 그의 유사체 또는 모방체를 포함한다. 노긴 폴리펩티드의 효과를 모방할 수 있는 추가의 예시적인 인자는 BMP2, BMP4, 및/또는 BMP7을 격리시키는 우성 음성 수용체 또는 차단 항체의 사용을 포함한다. 추가로, 수용체 인산화를 차단하는 것과 관련하여, 도소모르핀(또는 화합물 C)은 줄기 세포에 대하여 유사한 영향을 미치는 것으로 보고되었다. 가용성 억제제, 예컨대, SIS3 (6,7-디메톡시-2-((2E)-3-(1-메틸-2-페닐-1H-피롤로[2,3-b]피리딘-3-일-프롭-2-에노일))-1,2,3,4-테트라하이드로이소퀴놀린, Smad의 특이적인 억제제3(Specific Inhibitor of Smad3), SIS3), 억제제 SMAD(예컨대, SMAD6, SMAD7, SMAD10) 중 하나 이상의 것의 과다발현 또는 수용체 SMAD(SMAD1, SMAD2, SMAD3, SMAD5, SMAD8/9) 중 하나에 대한 RNAi를 사용하여 SMAD 단백질을 억제시키는 것 또한 영향을 받을 수 있다. 신경 전구체를 생성하는 데 적합한 것으로 예상되는 인자의 또 다른 조합은 백혈병 억제 인자(LIF), GSK3 억제제(CHIR 99021), 화합물 E(γ 세크레타제 억제제 XXI) 및 신경능선 줄기 세포를 생성하는 데 효과적인 것으로 이미 밝혀져 있는 TGFβ 억제제 SB431542(문헌 [Li et al., Proc Natl Acad Sci U S A. 2011 May 17;108(20):8299-304])의 칵테일을 포함한다. 추가의 예시적인 인자는 SB431542의 유도체, 예컨대, 하나 이상의 첨가된 또는 상이한 치환기, 유사한 작용기 등을 포함하고, 하나 이상의 SMAD 단백질에 대해 유사한 억제 효과를 발휘하는 분자를 포함할 수 있다. 적합한 인자 또는 인자의 조합은 만능 세포를 상기 인자(들)와 접촉시키고, 예를 들어, EF 전구체 세포의 표현형, 예컨대, 특징적인 유전자 발현(본원에 기술된 마커의 발현, EF 전구체 세포 프로모터에 커플링된 리포터 유전자의 발현 등), 본원에 개시된 세포 유형, 예컨대, 망막 신경 전구체 세포, RG 전구체 세포 또는 RG 세포를 형성할 수 있는 능력 채용에 대하여 모니터링함으로써 확인할 수 있다.
바람직하게, 세포를 신경 분화 배지를 사용하여 배양하기 이전에 망막 유도 배지로 처리하거나, 또는 상기 배지 중에서 배양한다.
신경 분화(ND) 배지. 신경 분화(ND) 배지는 만능 줄기 세포를 안구 영역 (EF) 전구체 세포로 분화시키는 데 사용된다. ND 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스), 또는 하기 표 1에 제공되는 뉴로베이살™ 배지의 성분, D-글루코스(임의적으로, 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml), 하나 이상의 항생제, 예컨대, 페니실린(임의적으로, 0-100 유니트/ml 또는 약 100 유니트/ml) 및 스트렙토마이신(임의적으로, 0-100 ㎍/ml 또는 약 100 ㎍/ml), 글루타맥스™(임의적으로, 1X, 대략 2 mM), 하나 이상의 혈청 보충제, 예컨대, N2 보충제(임의적으로, 0.1-5% v/v or 0.1-2% v/v, 1% v/v 포함) 및 B27 보충제(임의적으로, 0.05-2% v/v, 2% v/v 포함), MEM 비필수 아미노산 용액(임의적으로, 스톡 용액으로부터 1X 농도, 또는 대략 0.1 mM 최종 농도), 및 임의적으로, 노긴 폴리펩티드(임의적으로, 10-500 ng/ml, 50 ng/ml 포함)을 포함하는 배지를 포함한다.
신경절 세포( GC ) 배지. 신경절 세포(GC) 배지는 만능 줄기 세포를 망막 신경절(RG) 전구체 세포로 분화시키는 데, 및 더욱 구체적으로, 안구 영역 전구체 세포를 망막 신경절(RG) 전구체 세포로 분화시키는 데 사용된다. GC 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스), 또는 하기 표 1에 제공되는 뉴로베이살™ 배지의 성분, D-글루코스(임의적으로, 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml), 하나 이상의 항생제, 예컨대, 페니실린(임의적으로, 0-100 유니트/ml 또는 약 100 유니트/ml) 및 스트렙토마이신(임의적으로, 0-100 ㎍/ml 또는 약 100 ㎍/ml), 글루타맥스™(임의적으로, 1X, 또는 대략 2 mM), 하나 이상의 혈청 보충제, 예컨대, N2 보충제(임의적으로, 0.1-5% v/v 또는 0.1-2% v/v, 1% v/v 포함) 및 B27 보충제(포뮬러 080085-SA)(임의적으로, 0.5-2% v/v, 2% v/v 포함), 및 포스콜린 중 하나 이상의 것(임의적으로, 1-20 μM, 및 5 μM 포함), BDNF(임의적으로, 1-200 ng/ml, 및 10 ng/ml 포함), 및 CNTF(임의적으로, 1-200 ng/ml, 10 ng/ml 포함)을 포함하는 배지를 포함한다.
망막 신경절 세포( RGC ) 분화 배지. RGC 분화 배지는 만능 줄기 세포를 망막 신경절(RG) 세포로 분화시키는 데, 및 더욱 구체적으로, RG 전구체 세포를 RG 세포로 분화시키는 데 사용된다. RGC 분화 배지는 기본 배지, 예컨대, 뉴로베이살™ 배지(라이프 테크놀러지스), 또는 하기 표 1에 제공되는 뉴로베이살™ 배지의 성분, D-글루코스(임의적으로, 0-10 mg/ml, 2.5-7.5 mg/ml, 3-6 mg/ml, 4-5 mg/ml, 또는 약 4.5 mg/ml), 하나 이상의 항생제, 예컨대, 페니실린(임의적으로, 0-100 유니트/ml 또는 약 100 유니트/ml) 및 스트렙토마이신(임의적으로, 0-100 ㎍/ml 또는 약 100 ㎍/ml), 하나 이상의 혈청 보충제, 예컨대, B-27 보충제(포뮬러 080085-SA)(임의적으로, 약 0.05 내지 5.0% (v/v), 약 1.5 내지 2.5% (v/v) 또는 약 2% (v/v)), 글루타맥스™(임의적으로, 1X, 또는 약 2 mM), 및 포스콜린 모두를 포함하는 하나 이상의 것(임의적으로, 1-20 μM, 및 5 μM 포함), BDNF(임의적으로, 1-200 ng/ml 또는 5-50 ng/ml 또는 5-25 ng/ml 또는 약 10 ng/ml), CNTF(임의적으로, 1-200 ng/ml 또는 5-50 ng/ml 또는 5-25 ng/ml 또는 약 10 ng/ml), cAMP(임의적으로, 1-500 ng/ml 또는 10-250 ng/ml 또는 5-150 ng/ml 또는 약 100 ng/ml), DAPT(임의적으로, 1-100 μM 또는 1-20 μM), 및 임의적으로, 레티노산(임의적으로, 0.5-20 μM 또는 1-5 μM)을 포함하는 배지를 포함한다. BDNF는 인간 BDNF일 수 있다. CTNF는 인간 CTNF일 수 있다. RGC 분화 배지는 BDNF 및 CNTF 중 하나 또는 그 둘 모두를 포함할 수 있다. RGC 분화 배지는 포스콜린, cAMP, 및 DAPT 또는 다른 노치 억제제 모두를 포함하는 하나 이상의 것을 포함할 수 있다. RGC 분화 배지는 인간 인슐린을 비롯한, 인슐린(임의적으로, 약 5-50 ㎍/ml 또는 약 20 ㎍/ml)을 포함할 수 있다.
DMEM/F12, 뉴로베이살™ 배지(라이프 테크놀러지스), N2 혈청 보충제, 및 B27 혈청 보충제 및 B27 혈청 보충제(포뮬러 080085-SA) 성분은 하기 표 1에 제공되어 있다. 본 발명은 상기 특정 배지 및 보충제, 또는 상기 성분을 포함하거나, 그로 이루어지거나, 또는 본질적으로 그로 이루어진 배지 또는 보충제의 용도를 고려한다는 것을 이해하여야 한다.
세포 제제 및 그의 순도
본원에서 사용되는 바, 제제라는 용어, 특히, 세포 제제에 관한 상기 용어는 집단 및 조성물이라는 용어와 함께 상호교환적으로 사용된다. 간략하게 하기 위해, 측면 및 실시양태는 제제라는 용어로 기술될 수 있지만, 상기 기술은 집단 및 조성물에 동일하게 적용된다는 것을 이해하여야 한다. 제제는 다른 비세포 치환체를 포함할 수 있다는 것을 이해하여야 한다.
본 개시내용 전역에 걸쳐 사용되는 바, 세포 제제의 순도 수준은 제제 중 세포의 총 개수 대비 원하는 세포 유형의 하나 이상의 마커(본 출원에서 확인된 상기 마커 또는 당업계에 공지된 다른 것 포함)를 발현하는 제제 중 세포의 비율로서 정량화될 수 있다. 순도는 관심의 대상이 되는 하나 이상의 마커를 발현하는 세포 및/또는 그를 발현하지 않는 세포를 검출하고, 개수를 확인함으로써, 및 임의적으로 세포 총 개수를 확인함으로써 측정될 수 있다. 세포 개수를 확인하는 데 사용될 수 있는 예시적인 방법으로는 제한 없이, 혈광 활성화 세포 분류법(FACS), 면역조직화학법, 계내 하이브리드화, 및 당업계에 공지된 다른 적합한 방법을 포함한다. 전형적으로, 상기 분석은 제제 중 생존불가능한 세포는 배제한다.
본원에서 사용되는 바, 세포 대다수라는 것은 50% 이상인 것을 의미하며, 실시양태에 따라, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95%, 또는 약 100%의 세포인 것을 포함할 수 있다.
본 개시내용은 전구체 세포, 예컨대, 제한하는 것은 아니지만, 만능 줄기 세포를 직접 분화시킬 수 있는 개시된 본 방법의 능력에 기초하여 다양한 세포 집단의 실질적으로 순수한(또는 균질한) 제제를 제공한다. 본원에서 사용되는 바, 직접 분화란, 부분적으로는 전구체 세포에 제공되는 인자 또는 다른 자극제에 기인하여 전구체 세포 집단이 원하는 계통으로 또는 그러한 방향으로 분화됨에 따라, 이로써, 다른 원치않는, 그리고, 이로써, 잠재적으로 오염성을 띠는 계통으로 분화되지 못하게 막는 것을 의도한다. 본원에서 제공하는 방법은 배양체(EB)를 생성하지 않고, 예를 들어, 만능 줄기 세포의 안구 영역 전구체로의 분화를 구동시킨다. 하기 기술되는 바와 같이, EB는 배아 줄기(ES) 세포를 포함하나, 이에 제한되지 않는 만능 줄기 세포의 분화 동안 형성될 수 있고, 전형적으로 중배엽, 외배엽 및 내배엽 계통의 전구체를 비롯한, 세포를 함유하는 3차원 세포 클러스터이다. EB의 3차원적 성질은 본원에 기술된 비EB 기반 방법에서 생성된 것과는 상이한 세포-세포 상호작용 및 상이한 세포-세포 신호전달을 비롯한, 상이한 환경을 생성시킬 수 있다. 추가로, EB 내의 세포는 외인적으로 첨가된 작용제, 예컨대, 주변 배지에 존재하는 분화 인자를 유사한 용량으로 전부 받는 것은 아니며, 이로써, EB의 발생 동안 다양한 분화 이벤트 및 결정이 이루어질 수 있다.
대조적으로, 전구체 세포를 배양하는 본 발명의 배양 방법은 EB 형성을 필요로 하지 않고, 바람직하게는 EB 형성을 회피한다. 대신, 본 방법은 상기 배지 중 인자를 포함하여, 주변 배지와의 균등한 접촉을 세포에 제공하는 조건에서 세포를 배양한다. 세포는 예를 들어, 배양 표면에 부착된 단층 또는 거의 단층으로 성장될 수 있다.
대략적으로 동일한 정도로 그의 주변 배지, 및 따라서, 상기 배지 중의 인자와 접촉할 수 있는 전구체 세포 모두 또는 그들 대다수의 능력을 통해 상기 전구체 세포는 유사한 시점에, 및 유사한 정도로 분화된다. 전구체 세포 집단의 분화 타임라인이 상기와 같이 유사하다는 것은 상기 세포가 동시에 발생된다는 것을 나타낸다. 일부 경우에서 또한 세포는 세포 주기가 동시에 발생되는 것일 수 있다. 상기와 같은 동시 발생성을 통해 그의 세포 구성이 균질성 또는 거의 균질성인 세포 집단이 생성된다. 한 예로서, 본원에 기술된 방법은 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95%, 또는 약 100%의 세포가 관심의 대상이 되는 특정 세포인 것인 세포 집단을 생산할 수 있다. 관심의 대상이 되는 세포는 예를 들어, 세포내 또는 세포외 마커 발현에 의해 표현형에 의해 정의될 수 있다. 관심의 대상이 되는 세포는 안구 영역 전구체 세포, (조기 또는 후기 여부와 상관 없이) RG 전구체 세포, 또는 RG 세포일 수 있다. .
본원에서 사용되는 바, "세포의 실질적으로 순수한 제제"란, 세포가 60% 이상 순수한 세포 제제를 의미한다. 따라서, 제제 중 60% 이상의 세포가 특정 세포 유형의 하나 이상의 마커(본 출원에서 확인된 마커 또는 당업계에 공지된 다른 것 포함)를 발현한다. 세포는 65% 이상 순수 또는 70% 이상 순수한 것일 수 있다. 세포는 75%, 80%, 85% 또는 90% 이상 순수한 것을 비롯하여, 약 70% 초과로 순수한 것일 수 있다.
따라서, 예를 들어, "RG 세포의 실질적으로 순수한 제제"란, 제제 중 60% 이상의 세포가 RG 세포의 하나 이상의 마커(본 출원에서 확인된 마커 또는 당업계에 공지된 다른 것 포함)를 발현하는 세포 제제를 의미한다. 제제 중 70% 이상의 세포가 RG 세포의 하나 이상의 마커를 발현할 수 있고, 이 경우, 제제는 70% 순수한 것이다. 제제 중 85% 이상의 세포가 RG 세포의 하나 이상의 마커를 발현할 수 있고, 이 경우, 제제는 85% 순수한 것이다. 제제 중 95% 이상의 세포가 RG 세포의 하나 이상의 마커를 발현할 수 있고, 이 경우, 제제는 95% 순수한 것이다. 일부 실시양태에서, 제제는 약 85% 내지 95% 순수한 것일 수 있다.
또 다른 예로서, "RG 전구체 세포의 실질적으로 순수한 제제"란, 제제 중 60% 이상의 세포가 RG 전구체 세포의 하나 이상의 마커(본 출원에서 확인된 마커 또는 당업계에 공지된 다른 것 포함)를 발현하는 세포 제제를 의미한다. 제제 중 70% 이상의 세포가 RG 전구체 세포의 하나 이상의 마커를 발현할 수 있고, 이 경우, 제제는 70% 순수한 것이다. 제제 중 85% 이상의 세포가 RG 전구체 세포의 하나 이상의 마커를 발현할 수 있고, 이 경우, 제제는 85% 순수한 것이다. 제제 중 95% 이상의 세포가 RG 전구체 세포의 하나 이상의 마커를 발현할 수 있고, 이 경우, 제제는 95% 순수한 것이다. 일부 실시양태에서, 제제는 약 85% 내지 95% 순수한 것일 수 있다.
본 개시내용의 특정 실시양태에서, RG 전구체 세포 및 RG 세포를 포함하나, 이에 제한되지 않는 세포의 평균 말단 제한 절편 길이(TRF)는 7 kb, 7.5 kb, 8 kb, 8.5 kb, 9 kb, 9.5 kb, 10 kb, 10.5 kb, 11 kb, 11.5 kb 또는 심지어 12 kb보다 더 길다. 평균 말단 제한 절편 길이(TRF)를 측정하는 방법은 당업계에 공지되어 있다. 예를 들어, 문헌 [Kimura et al. Nat. Protocol, 5(9):1596-1607, 2010]을 참조할 수 있다.
발생 단계의 함수로서의 세포
마커
발현
마커, 예컨대, 제한하는 것은 아니지만, Pax6, Rx1, Six3, Six6, Lhx2, Tbx3, Sox2, Chx10, Math5, Brn3(Brn3a 및 Brn3b 포함), Isl1, 신경미세섬유, Tuj1, Thy1, 네스틴, Otx2, Nanog, Oct4의 발현은 단백질 및/또는 mRNA로 평가될 수 있다(문헌 [Fischer AJ, Reh TA, Dev Neurosci. 2001:23(4-5):268-76]; [Baumer et al., Development. 2003 Jul;130(13):2903-15]; [Swaroop et al., Nat Rev Neurosci. 2010 Aug;11(8):563-76]; [Agathocleous and Harris, Annu. Rev. Cell Dev. Biol. 2009. 25:45-69]; [Beby F, Lamonerie T, Exp. Eye Res. 2013; 111, 9-16](상기 문헌들은 각각 그 전문이 본원에서 참조로 포함된다)).
마커는, 예컨대, 문맥상 달리 명시되는 경우를 제외하면, 일반적으로는 인간 마커이다. 세포 마커는, 기술이 당업계의 숙련가에게 널리 공지되어 있는 종래의 면역세포화학법 또는 종래의 PCR 방법을 사용하여 확인될 수 있다.
만능
줄기 세포
본원에서 사용되는 바, "만능 줄기 세포"라는 용어는 (a) 면역결핍(SCID) 마우스에 이식되었을 때, 기형종을 유도할 수 있고; (b) 모든 3종의 배엽층의 세포 유형(예컨대, 외배엽, 중배엽, 및 내배엽 세포 유형)으로 분화될 수 있고; 및 (c) 만능성의 하나 이상의 마커(예컨대, Oct 4, 알칼리성 포스파타제, SSEA-3 표면 항원, SSEA-4 표면 항원, nanog, TRA-1-60, TRA-1-81, SOX2, REX1 등)를 발현하는 세포이다. 특정 실시양태에서, 만능 줄기 세포는 OCT-4, 알칼리성 포스파타제, SSEA-3, SSEA-4, TRA-1-60, 및 TRA-1-81로 이루어진 군으로부터 선택되는 하나 이상의 마커를 발현한다.
만능 줄기 세포는 배아 줄기(ES) 세포, 배아 유래 줄기 세포, 배아 생식(EG) 세포, 배아 암종(EC) 세포, 유도성 만능 줄기(iPS) 세포, 및 자극 유발성의 만능성 획득(STAP) 세포를 포함한다. 예시적인 만능 줄기 세포는 당업계에 공지된 임의의 다양한 방법을 사용하여 생성될 수 있다. 당업계에서 이해되는 바와 같이, 배양체는 그 중에서도 특히 ES 세포 또는 EG 세포로부터 형성될 수 있다. 이 또한 당업계에서 이해되는 바와 같이, ES 세포는 배아 파괴 없이 생성될 수 있다. 예를 들어, ES 세포는 배아가 아닌 단성생식형 난자(난세포)로부터 생성될 수 있고, ES 세포는 의도적으로 생존불가능하도록(예컨대, 이식이 불가능하도록) 조작된 것을 비롯한, 생존불가능한 배아로부터 생성될 수 있고, ES 세포는 생존불가능한 배아를 비롯한, 한 배아의 단일 난할구로부터 생성될 수 있다.
만능 줄기 세포는 수명, 효능, 귀소를 증가시키도록, 및/또는 동종면역 반응을 방해하거나, 감소시키도록, 및/또는 원하는 인자를 만능 줄기 세포의 분화된 자손으로 전달하도록, 및/또는 만능 줄기 세포의 분화된 자손에서 원하는 인자를 발현시키도록 변형(유전적으로 변형 포함)될 수 있다.
만능 줄기 세포는 임의 종으로부터의 것일 수 있다. ES 세포 및 iPS 세포를 비롯한, 각종 만능 줄기 세포 유형은 마우스, 인간 및 다른 종으로부터 생성될 수 있다. 따라서, 본 방법에서 사용되는 만능 줄기 세포는 제한 없이, 인간, 인간외 영장류, 설치류(마우스, 래트), 유제류(소, 양 등), 개(애완견 야생견), 고양이(애완용 고양이 및 야생 고양이, 예컨대, 사자, 호랑이, 치타), 토끼, 햄스터, 염소, 코끼리, 판다(자이언트 판다 포함), 돼지, 라쿤, 말, 얼룩말, 수중 포유동물(돌고래, 고래 등)을 포함하는 임의의 종으로부터 수득될 수 있다. 특정 실시양태에서, 종은 멸종위기 종이다. 특정 실시양태에서, 종은 현재 멸종된 종이다.
배아 줄기( ES ) 세포. 배아 줄기 세포는 그의 공급원 또는 그를 생산하는 데 사용되는 특정 방법과 상관 없이, (i) 모든 3종의 배엽층의 세포 유형으로 분화될 수 있고, (ii) 적어도 Oct 4 및 알칼리성 포스파타제를 발현하고, (iii) 면역결핍(SCID) 동물로 이식되었을 때, 기형종을 생성할 수 있는 세포이다. 상기 용어는 세포주로서 연속적으로 계대접종된 것을 비롯한, 인간 배반포 또는 상실배의 내부 세포괴(ICM: inner cell mass)로부터 유래된 세포; 정자 및 난세포의 인공적인 융합, 정자와의 난세포의 수정, 핵 이식, 예컨대, 체세포 핵 이식(SCNT: somatic cell nuclear transfer), 처녀 생식, 동정 생식에 의해, 또는 염색질의 재프로그래밍화 및 이어서, 재프로그래밍된 염색질의 세포 내로의 도입을 통해 생산된, 접합체, 난할구(예컨대, 분할 단계 또는 상실배 단계 배아의 것), 또는 배반포 단계 포유동물 배아로부터 유래된 세포를 포함한다.
ES 세포라는 용어는 세포가 배아의 파괴를 통해 생성되었다는 것을 의미하는 것으로 추정되지 않고, 그러한 것으로 추정되지 않아야 한다. 대조적으로, 배아, 예컨대, 인간 배아를 파괴하지 않고 ES 세포를 생성하는 데 다양한 방법이 이용가능하며, 사용될 수 있다. 한 예로서, ES 세포는 이식 전 유전자 진단(PGD)을 위한 난할구의 추출과 유사한 방식으로, 배아로부터 유래된 단일 난할구로부터 생성될 수 있다. 상기 세포주의 예로는 NED1, NED2, NED3, NED4, NED5, 및 NED7을 포함한다. 사용될 수 있는 예시적인 인간 배아 줄기 세포주는 MA09 세포이다. MA09 세포의 단리 및 제조는 문헌 [Klimanskaya, et al. (2006) "Human Embryonic Stem Cell lines Derived from Single Blastomeres." Nature 444: 481-485, and Chung et al. (2008) "Human Embryonic Stem Cell Lines Generated without Embryo Destruction, Cell Stem Cell, 2(2):113-117]에 앞서 기술되어 있다. 상기 세포주들은 모두 배아 파괴 없이 생성되었다.
사용될 수 있는 추가의 ES 세포로는 제한 없이, 인간 ES 세포, 예컨대, MA01, MA09, ACT-4, MA142, MA143, MA144, MA145, MA146, MA126(NED1), MA127, (NED2), MA128, (NED3), MA129, (NED4), NED7, No. 3, H1, H7, H9, H14 및 ACT30 ES 세포를 포함한다.
NIH 인간 배아 줄기 세포 등록 센터(NIH Human Embryonic Stem Cell Registry) 또한 참조할 수 있다. 본 개시내용에 따라 사용되는 인간 ES 세포는 당업계에 공지된 GMP 표준에 따라 유래되고, 유지될 수 있다.
본원에서 언급된 바와 같이, ES 세포는 마우스, 인간외 영장류의 다수의 종, 및 인간을 비롯한, 다양한 종으로부터 유래되고, 배아 유래 줄기 세포는 다수의 추가 종으로부터 생성되었다.
유도성 만능 줄기( iPS ) 세포. 유도성 만능 줄기 세포(iPS 세포)는 인자(본원에서 재프로그래밍 인자로 지칭됨)의 조합을 발현함으로써 체세포를 재프로그래밍하여 생성된 세포이다.
iPS 세포는 출발점으로서, 실제로 임의의 발생 단계의 임의의 체세포를 사용하여 생성될 수 있다. 예를 들어, 세포는 배아, 태아, 신생아, 청소년, 또는 성인 공여자로부터 유래될 수 있다. 일부 경우에서, 세포는 신생아, 청소년, 또는 성인 공여자로부터 유래되거나, 또는 양수로부터 수득되고, 따라서, 배아 또는 태아의 파괴가 필요하지 않다. 사용될 수 있는 예시적인 체세포로는 섬유아세포, 예컨대, 피부 샘플 또는 생검에 의해 수득된 피부 섬유아세포, 윤활 조직 유래 활막 세포, 포피 세포, 뺨 세포, 또는 폐 섬유아세포를 포함한다. 특정 실시양태에서, 체세포 섬유아세포가 아니다.
특정 실시양태에서, 1개 이상, 2개 이상, 또는 3개 이상, 또는 4개 이상의 재프로그래밍 인자가 체세포에서 발현되고, 이로써, 체세포는 성공적으로 재프로그래밍된다. 재프로그래밍 인자는, 비록 하기와 같이 제한되는 것은 아니지만, Oct 4(이는 종종 Oct 3/4로도 지칭됨), SOX2, c-Myc, Klf4, Nanog 및 Lin28로부터 선택될 수 있다. 일부 실시양태에서, 재프로그래밍 인자는 Oct 4(이는 종종 Oct 3/4로도 지칭됨), SOX2, c-Myc 및 Klf4의 조합, 또는 Oct 4, SOX2, Nanog 및 Lin28의 조합을 포함한다.
재프로그래밍 인자는 제한 없이, 통합 벡터, 비통합 벡터(예컨대, 에피솜 플라스미드, 예컨대, 문헌 [Yu et al., Science. 2009 May 8;324(5928):797-801]에 기술되어 있는 것), 화학적 수단, 단백질 형질도입, 전기천공, 미세주입, 양이온성 양친매성 물질, 지질 이중층과의 융합, 계면활성제 투과화 등 ) 또는 그의 조합을 비롯한, 다양한 방법들 중 임의의 것을 사용하여 체세포 내로 도입될 수 있다. 추가로, 재프로그래밍 인자의 발현은 체세포와, 재프로그래밍 인자의 발현을 유도하는 1종 이상의 작용제, 예컨대, 소형 유기 분자 작용제를 접촉시킴으로써 유도될 수 있다.
통합 바이러스 벡터를 사용하여 Oct3/4, SOX2, c myc 및 Klf4를 발현시키는 것은 마우스 체세포를 재프로그래밍시키는 데 충분한 것으로 밝혀졌다. 통합 바이러스 벡터를 사용하여 Oct3/4, SOX2, NANOG 및 Lin28을 발현시키는 것은 인간 체세포를 재프로그래밍시키는 데 충분한 것으로 밝혀졌다.
iPS 세포는 세포 은행으로부터 수득될 수 있다. iPS 세포는 특정 환자, 또는 조직이 매칭되는 RG 세포 또는 RG 전구체 세포를 생성하기 위한 목적과 매칭되는 공여자로부터의 물질을 이용하여 특별히 생성될 수 있다. iPS 세포는 의도하는 수혜자에서 실질적으로 면역원성을 띠지 않는 세포로부터 생산될 수 있고, 예컨대, 자가 유래 세포로부터 또는 의도하는 수용자에 조직적합성인 세포로부터 생산될 수 있다.
자극 유발성의 만능성 획득( STAP ) 세포. 자극 유발성의 만능성 획득(STAP) 세포는 준치사 자극, 예컨대, 낮은 pH 노출을 이용하여 체세포를 재프로그래밍함으로써 생산된 만능 줄기 세포이다. 재프로그래밍은 체세포의 유전자 조작 또는 핵 이식을 필요로 하지 않는다. 문헌 [Obokata et al., Nature, 505:676-680, 2014]를 참조할 수 있다.
성인 줄기 세포 . "성인 줄기 세포"란, 성인 조직으로부터 단리된 다능성 세포를 의미하며, 제대혈 줄기 세포 및 지방 줄기 세포를 포함할 수 있고, 인간 기원의 것이다.
본 발명의 방법은 EB 분화 단계를 사용하지 않는다는 점이 중요하다(즉, 분화는 EB 형성 없이 만능 줄기 세포로부터 망막 신경절 세포로의 분화로 이루어진다). 본원에서 논의되는 바와 같이, 상기 분화 과정에 대하여 예상 밖의 이점이 존재한다.
"배양체"는 비부착 조건하에, 예컨대, 저부착성 기판 상에서 또는 "현적"으로 만능 줄기 세포를 배양함으로써 형성될 수 있는, 만능 줄기 세포(예컨대, iPSC 또는 ESC)를 비롯한, 세포 클럼프 또는 클러스터를 의미한다. 상기 배양에서, 만능 세포는 배양체로 명명되는 세포 클럼프 또는 클러스터를 형성할 수 있다. 문헌 [Itskovitz-Eldor et al., Mol Med. 2000 Feb;6(2):88-95](상기 문헌은 그 전문이 본원에서 참조로 포함된다)를 참조할 수 있다. 전형적으로, 배양체는 초기에 만능 세포의 고형 클럼프 또는 클러스터로서 형성되고, 시간이 경과함에 따라 배양체 중 일부는 유체 충전된 체강을 포함하게 되고, 전자는 상기 문헌에서 "단순" EB로 지칭되고, 후자는 "낭성" 배양체로 지칭된다.
적용 및 용도
스크리닝 검정법
본 발명은 안구 영역 전구체 세포의 망막 신경절 계통으로의 분화를 조정하는 각종 작용제를 스크리닝하는 방법을 제공한다. 이는 또한 배양에서 안구 영역 전구체 세포로부터 생성될 수 있는 RG 전구체 세포를 지지하고/거나, 또는 구제하는 치료제를 발현하는 데에도 사용될 수 있다.
본 발명은 RG 전구체 세포의 분화를 조정하는 각종 작용제를 스크리닝하는 방법을 제공한다. 이는 또한 배양에서 RG 전구체 세포로부터 생성되는 성숙한 RG 세포를 지지하고/거나, 또는 구제하는 치료제를 발현하는 데에도 사용될 수 있다.
본 발명의 목적을 위해, "작용제"는 제한하는 것은 아니지만, 생물학적 또는 화학적 화합물, 예컨대, 단순 또는 복합 유기 또는 무기 분자, 펩티드, 단백질(예컨대, 항체), 폴리뉴클레오티드(예컨대, 안티센스, RNA 간섭(RNAi, shRNA, 마이크로RNA)), 또는 리보자임을 포함하는 것으로 의도된다. 예를 들어, 중합체, 예컨대, 폴리펩티드, 및 폴리뉴클레오티드, 및 합성 유기 화합물과 같은, 방대한 양의 수많은 화합물이 다양한 코어 구조에 기초하여 합성될 수 있고, 이들 또한 "작용제"라는 용어에 포함된다. 추가로, 각종 천연 공급원, 예컨대, 식물 또는 동물 추출물 등이 스크리닝용 화합물을 제공할 수 있다. 비록 항상 명확하게 언급되는 것은 아니지만, 작용제는 단독으로 사용되거나, 또는 본 발명의 스크린에 의해 확인된 작용제와 동일하거나, 또는 상이한 생물학적 활성을 가지는 또 다른 작용제와 함께 조합되어 사용된다는 것을 이해하여야 한다.
시험관내에서 스크리닝 방법을 실시하기 위해, 단리된 세포 집단은 본원에 기술된 바와 같이 수득될 수 있다. 작용제가 DNA 또는 RNA 이외의 조성물, 예컨대, 상기 기술된 바와 같은 소분자일 때, 작용제는 세포에 직접 첨가될 수 있거나, 또는 첨가를 위해 배양 배지에 첨가될 수 있다. 당업자에게 자명한 바와 같이, 실험적으로 결정될 수 있는 "유효"량이 첨가되어야 한다. 작용제가 폴리뉴클레오티드일 때, 이는 유전자 총 또는 전기천공의 사용에 의해 직접 첨가될 수 있다. 대안적으로, 유전자 전달 비히클 또는 상기 기술된 다른 방법을 사용하여 세포 내로 삽입될 수 있다. 양성 및 음성 대조군은 약물 또는 다른 작용제의 알려진 활성을 확인하기 위해 검정될 수 있다.
약물 스크리닝
본 발명의 또 다른 측면은 IOP 상승, 글루타메이트 독성, 또는 천연 망막 신경절 세포 및 그의 전구체의 기능 손실 또는 세포 사멸을 유발할 수 있는 다른 환경 또는 유전적 상태의 영향으로부터 신경절을 보호할 수 있는 약물을 확인하는 검정법의 개발 및 용도에 관한 것이다. 보호는 예를 들어, 상기의 각종 영향에 대한 신경절의 감수성을 감소시킴으로써 달성될 수 있다. 다른 실시양태에서, 본 검정법은 천연 망막 신경절 세포 및/또는 그의 전구체의 증식을 촉진시키고/거나, 천연 망막 신경절 전구체의 성숙한 망막 신경절 세포로의 분화/성숙화를 유도할 수 있는 작용제를 확인하는 데 사용될 수 있다. 상기 검정법에서 시험될 수 있는 작용제로는 소분자(예컨대, 분자량이 10,000 원자 질량 단위(amu) 미만인 유기 화합물), 단백질 및 펩티드, 핵산 등을 포함하나, 이에 한정되지 않는다. 시험하고자 작용제는 예를 들어, 박테리아, 효모 또는 다른 유기체(예컨대, 천연 생성물)에 의해 생산될 수 있거나, 화학적으로 생산될 수 있거나(예컨대, 펩티도미메틱스를 비롯한, 소분자), 또는 재조합적으로 생산될 수 있다.
예를 들어, 본 검정법은 배양물 중 망막 신경절 세포(예컨대, 본원에서 제공하는 방법을 사용하여 만능 줄기 세포, 안구 영역 전구체, 또는 RG 전구체 세포의 분화에 의해 유도될 수 있는 것)를 글루타메이트 유도 독성으로부터 보호할 수 있는 화합물의 능력을 평가할 수 있다. 다양한 검정 포맷이 충분할 것이며, 본원에 서 명확하게 기술되지 않았음에도 불구하고, 이러한 것도 본 개시내용에 비추어 당업계의 숙련가는 이해할 수 있을 것이다. 화합물 및 천연 추출물의 라이브러리를 시험하는 다수의 약물 스크리닝 프로그램에서, 주어진 시간 동안 조사되는 화합물 개수를 최대화시키기 위해서는 고처리량 검정법이 바람직할 수 있다. 예를 들어, 아폽토시스 마커의 상대적인 변화를 검출함으로써 시험 작용제의 보호 활성을 검출 및 정량화를 수행할 수 있으며 - 보호성 작용제는 예컨대, 글루타메이트 수준 상승과 같은 신경독성 상태하에서 비처리된 대조군 세포와 비교하였을 때, 아폽토시스 마커의 출현율/그의 발현 수준을 감소시켜야 한다. 작용제의 효능은 다양한 농도의 시험 화합물을 사용하여 수득된 데이터로부터 용량 반응 곡선을 작성함으로써 평가될 수 있다. 비교를 위한 기준선을 제공하기 위해 대조군 검정법 또한 수행될 수 있다. 대조군 검정법에서는 시험 화합물의 부재하에서 아폽토시스 정도를 정량화할 수 있다. 일반적으로, 반응물이 혼합될 수 있는 순서는 달라질 수 있고, 이는 동시에 혼합될 수 있다는 것을 이해할 것이다.
감각신경
망막 구조
RG 전구체 세포, 및 임의적으로, 그로부터 분화된 RG 세포는 망막 색소 상피(RPE) 세포, 광수용기 세포 및 RG 전구체 또는 RG 세포 그 자체를 포함하는 감각신경 망막 구조를 생성하는 데 사용될 수 있다. 예를 들어, 본 발명은 RG 세포 또는 RG 전구체 세포, RPE 세포, 및 광수용기 세포(또는 광수용기 전구체 세포)로 구성된 다층 세포 구조의 생성을 고려한다. 이러한 구조는 약물 스크리닝을 위해, 질환에 대한 모델로서, 또는 약학 제제에서 사용될 수 있다. 후자의 경우, 약학 제제는 "패치"로처 이식될 수 있는 생체적합성 고체 지지체 또는 매트릭스(바람직하게, 생체재흡수성 매트릭스 또는 지지체) 상에 배치될 수 있는, RPE-광수용기-RG 이식편일 수 있다.
RG 세포 또는 RG 전구체 세포는 망막 신경 전구체(예컨대, Chx10(+) 세포)로부터 광수용기와 함께 생성될 수 있고, 상기 세포는 RPE 세포 층(예컨대, 단층)과 함께 이식될 수 있다는 것이 추가로 고려된다.
추가로 예시하기 위해, 세포에 대한 생체적합성 지지체는 망막 전구체 세포에 대한 생체분해성 폴리에스테르 필름 지지체일 수 있다. 생체분해성 폴리에스테르는 망막 전구체 세포의 증식 및 분화를 지지하는 기판 또는 스캐폴드로서 사용하는 데 적합한 임의의 생체분해성 폴리에스테르일 수 있다. 폴리에스테르는 박막, 바람직하게는 미세구조의 막을 형성할 수 있어야 하고, 조직 또는 세포 이식을 위해 사용되는 경우, 생체분해성이어야 한다. 본 발명에서 사용하는 데 적합한 생체분해성 폴리에스테르로는 폴리락트산(PLA), 폴리락티드, 폴리하이드록시알카노에이트, 동종중합체와 공중합체 둘 모두, 예컨대, 폴리하이드록시부티레이트(PHB), 폴리하이드록시부티레이트 코-하이드록시발레레이트(PHBV), 폴리하이드록시부티레이트 코-하이드록시헥사노에이트(PHBHx), 폴리하이드록시부티레이트 코-하이드록시옥토노에이트(PHBO) 및 폴리하이드록시부티레이트 코-하이드록시옥타데카노에이트(PHBOd), 폴리카프로락톤(PCL), 폴리에스테르아미드(PEA), 지방족 코폴리에스테르, 예컨대 폴리부티렌 숙시네이트(PBS) 및 폴리부티렌 숙시네이트/아디페이트(PBSA), 방향족 코폴리에스테르를 포함한다. 고 분자량 및 저 분자량 폴리에스테르 둘 모두, 치환 및 비치환 폴리에스테르, 블록, 분지형 또는 랜덤, 및 폴리에스테르 혼합물 및 블렌드가 사용될 수 있다. 바람직하게, 생체분해성 폴리에스테르는 폴리카프로락톤(PCL)이다.
특정 실시양태에서, 생체적합성 지지체는 폴리(p-크실릴렌) 중합체, 예컨대, 파릴렌 N, 파릴렌 D, 파릴렌-C, 파릴렌 AF-4, 파릴렌 SF, 파릴렌 HT, 파릴렌 VT-4 및 파릴렌 CF, 및 가장 바람직하게, 파릴렌-C이다.
중합체 지지체는 전형적으로 공지된 기술을 사용하여 박막으로 형성될 수 있다. 막 두께는 유리하게는 약 1 ㎛ 내지 약 50 ㎛, 바람직하게는, 약 5 ㎛ 두께이다. 필름 표면은 부드러울 수 있거나, 또는 필름 표면은 부분적으로 또는 완전하게 미세구조일 수 있다. 적합한 표면 구조는 예를 들어, 미세그루브 또는 미세포스트를 포함한다. 필름을 절단 및 성형하여 이식에 적합한 형상을 형성할 수 있다.
RPE, 광수용기 세포 또는 광수용기 전구체 세포, 및 RG 전구체 세포 및/또는 RG 세포는 함께 또는 순차적으로(예컨대, RPE 층이 형성된 후, 광수용기 세포 또는 광수용기 전구체 세포) 필름 상에 직접 플레이팅되어 생체적합성 스캐폴드를 형성할 수 있다. 대안적으로, 중합체 필름은 적합한 코팅 물질, 예컨대, 폴리-D-리신, 폴리-L-리신, 피브로넥틴, 라미닌, 콜라겐 I, 콜라겐 IV, 비트로넥틴 및 마트리겔™로 코팅될 수 있다. 세포는 임의의 바람직한 밀도로 플레이팅될 수 있지만, RPE 세포의 단일 층(RPE 단층)이 바람직하다.
치료학적 용도
한 예시적인 실시양태에서, 세포는 그를 필요로 하는 래트, 예컨대, 안내압이 높은 래트, 또는 다른 질환을 앓는 동물 모델 내로 이식될 수 있고, 시기능에 미친 발생 효과는 시운동 반응 검사, ERG(망막전위도검사), 발광 역치 기록법 및/또는 시중심 혈류량 검정법에 의해 검출될 수 있다 .
본원에서 사용되는 바, 질환의 "징후"란, 광범위하게는 질환의 주관적인 적응증인 증상과 달리, 질환의 객관적인 적응증인, 환자 검사시에 발견될 수 있는, 질환을 나타내는 임의의 이상을 의미한다.
본원에서 사용되는 바, 질환의 "증상"이란, 광범위하게는 환자가 경험하고, 질환을 나타내는, 구조, 기능, 또는 감각에 있어 정상으로부터의 이탈 또는 임의의 병적인 현상을 의미한다.
본원에서 사용되는 바, "요법," 치료학적," "치료하는," "치료하다," 또는 "치료"란, 광범위하게는 질환을 치료하거고/거나, 질환의 발생 또는 그의 임상적 증상을 중지 또는 감소시키고/거나, 질환을 완화시켜 질환 또는 그의 임상적 증상을 퇴행시키는 것을 의미한다. 요법은 예방, 방지, 치료, 치유, 교정, 감소, 완화, 및/또는 질환, 질환의 징후 및/또는 증상의 경감 제공을 포함한다. 요법은 질환 징후 및/또는 증상이 진행되는 환자에서 징후 및/또는 증상의 완화를 포함한다. 요법은 또한 "예방" 및 "방지"를 포함한다. 예방은 환자에서 질환의 치료 이후에 발생되는 질환의 방지 또는 환자에서 질환의 발병률 또는 중증도의 감소를 포함한다. 요법의 목적으로 "감소된"이라는 용어는 광범위하게 징후 및/또는 증상의 임상적으로 유의적인 감소를 의미한다. 요법은 재발 또는 빈발한 징후 및/또는 증상의 치료를 포함한다. 요법은 언제든지 징후 및/또는 증상의 출현의 방지하는 것 뿐만 아니라, 현존 징후 및/또는 증상을 감소시키고/거나, 현존 징후 및/또는 증상을 제거하는 것을 포함하나, 이에 제한되지 않는다. 요법은 만성 질환("유지") 및 급성 질환을 치료하는 것을 포함한다. 예를 들어, 치료는 징후 및/또는 증상의 재발 또는 빈발을 치료 또는 방지하는 것을 포함한다.
일부 실시양태에서, 치료는 안정적이거나, 또는 개선된 암소시 역치 반응, 안정적이거나, 또는 개선된 시운동성 반사(OKR), 안정적이거나, 또는 개선된 시각 유발 전위(VEP), 및/또는 안정적이거나, 또는 개선된 시력(예컨대, ERG로 측정)으로 나타날 수 있다. 안정적이거나, 또는 개선된 수준은 치료 이전의 수준에 대해 상대적인, 또는 치료되지 않은 대조군, 예컨대, 반대쪽 눈에 대해 상대적인 것이다. 일부 경우에서, 상기 기능 또는 반응들 중 하나 이상은 치료되지 않을 경우, 시간이 경과함에 따라 악화될 것이며, 본 발명의 이식된 세포는 그러한 악화를 지연시키거나, 감소시키거나, 또는 제한한다는 것을 이해하여야 한다. 따라서, 일부 경우에서, 기능 똔느 반응은 대조군과 비교하였을 때, 안정적으로 유지됨과 동시에, 다른 경우에서는 개선될 수 있으며, 상기 두 상황 모두 피험체에게 유익한 것으로 간주되고, 이로써, 이는 치료인 것으로 간주된다.
상기 및 다른 실시양태에서, 피험체는 그의 망막 신경절 세포층에 근본적으로 유익한 이득을 경험할 수 있다. 예를 들어, 천연 RG 세포층은 대조군과 비교하였을 때, 생존이 개선될 수 있거나, 또는 세포 손실이 감소될 수 있다. 추가의 다른 실시양태에서, 피험체는 시신경에서 축삭돌기 형성 증가를 경험할 수 있다.
본 발명은 또한 환자에게 본 발명의 RG 전구체 세포, 또는 그로부터 유래된 RG 세포 또는 그의 조합을 포함하는 약학 제제를 투여하는 단계를 포함하는, RG 세포 대체 또는 수복 치료를 필요로 하는 환자에서 RG 세포를 대체 또는 수복시키는 방법을 제공한다. 본원에 기술된 바와 같이, 약학 제제는 시험관내에서 이식가능한 조직으로 형성된 세포의 현탁액 또는 세포일 수 있다. 많은 경우에서, 세포는 안구내 주사(유리체 주사 및 망막 주사 포함)에 의해 투여될 것이다. 따라서, 세포는 이환된 또는 변성된 망막하 공간으로 안구내로 투여될 수 있다. 그러나, RG 전구체 세포 신경보호 효과를 가지고 있는 바, 상기 세포는 국소적으로, 그러나 망막 외부에(예컨대, 유리체)에 또는 데포에 의해 또는 신체의 다른 부분로의 전신 전달에 의해 투여될 수 있다.
본 발명의 약학 제제는 망막 변성 관련 질환을 비롯한, 시각계 악화를 초래하는, 광범위한 질환 및 장애에서 사용될 수 있다. 그러한 질환 및 장애는 노화에 의해 유발될 수 있으며, 따라서, 악화의 실질적인 원인인 것으로 확인될 수 있는 손상 또는 질환은 없는 것으로 보여진다. 당업자는 상기 질환 상태를 진단하고/거나, 상기 손상의 공지된 징후를 검사하는 확립된 방법에 대해 이해할 것이다. 추가로, 문헌은 동물의 시각계 측면에서 연령 관련 쇠퇴 또는 악화에 대한 정보로 충만하다. "망막 변성-관련 질환"이라는 용어는 선천적 또는 생후 망막 변성 또는 이상으로부터 초래되는 임의의 질환을 의미하는 것으로 의도된다. 망막 변성-관련 질환의 예로는 망막 이형성증, 노화 황반 변성, 당뇨병성 망막증, 색소성 망막염, 선천성 망막 이영양증, 레베르 선천성 흑암시, 망막 박리, 녹내장, 시각 신경병증, 및 외상을 포함한다.
추가로 또는 대안적으로, 시계 성분, 예컨대, 감각신경 망막의 악화는 손상, 예를 들어, 시계 그 자체(예컨대, 눈), 머리 또는 뇌, 또는 보다 일반적으로 신체에 대한 외상에 의해 유발될 수 있다. 상기와 같은 특정 손상은 연령 관련 손상, 즉, 노화에 따른 그의 가능성 또는 빈도 증가로 알려져 있다. 상기 손상의 예로는 망막 열공, 황반 천공, 망막 전막, 및 망막 박리를 포함하고, 이들은 각각 임의 연령대의 동물에서 일어날 수 있지만, 다르게는, 건강한 노령 동물을 비롯한, 노령 동물에서 더욱 큰 가능성을 가지고 일어날 수 있거나, 또는 더 높은 빈도로 일어날 수 있다. 다른 경우에서, 시게 성분 악화는 허혈성 및/또는 재관류 손상에 기인하여 발생할 수 있다.
시계 또는 그의 성분의 악화는 또한 질환에 의해 유발될 수 있다. 질환 중에서도 시계에 영향을 미치는 다양한 연령 관련 질환이 포함된다. 이러한 질환은 젊은층보다는 보다 늙은 동물에서 더욱 큰 가능성으로 및/또는 더욱 큰 빈도로 발생한다. 예를 들어, 감각신경 망막층을 비롯한, 시계에 영향을 미치고, 그의 악화를 유발할 수 있는 질환의 예로는 다양한 형태의 망막염, 시신경염, 황반 변성, 증식성 또는 비증식성 당뇨병성 망막증, 당뇨성 황반 부종, 진행성 망막 위축증, 진행성 망막 변성, 급성 망막 변성, 면역 매개 망막병증, 망막 이형성증, 맥락망막염, 망막 허혈, 망막 출혈(전망막, 망막내 및/또는 망막하), 고혈압성 망막병증, 망막 염증, 망막 부종, 망막아세포종, 또는 색소성 망막염을 포함한다.
상기 질환 중 일부는 특정 동물, 예컨대, 반려 동물, 예컨대, 개 및/또는 고양이에 특이적인 경향이 있다. 질환 중 일부는 총칭하여 열거하였으며, 즉, 많은 유형의 망막염, 또는 망막 출혈이 존재할 수 있고; 따라서, 질환 중 일부는 하나의 특정 기병성인자에 의해 유발되지 않지만, 질환의 유형 또는 그 결과를 더욱 잘 기술한다. 시계의 하나 이상의 성분의 쇠퇴 또는 악화를 유발할 수 있는 많은 질환은 동물의 시계에 대해 원발성 및 속발성 또는 그보다 더 먼 이후에 영향을 미치는 효과를 가질 수 있다.
유리하게, 본 발명의 약학 제제는 허혈 재관류 손상, 망막 혈관 질환, (자가면역, 외상, 및/또는 바이러스 기반인지에 상관 없이) 시신경 손상, (유형에 상관 없이) 녹내장, (저산소 및 혈관신생 기반인지에 상관 없이) 당뇨병성 망막증, 유전성 신경절 변성, 및 유전성 시각 신경병증(예컨대, 레베르 유전성 시각 신경병증(LHON: Leber's hereditary optic neuropathy) 또는 레베르 시신경 위축증)을 포함하나, 이에 제한되지 않는, 다수의 병태를 치료 또는 호전시키는 데 사용될 수 있다.
한 측면에서, 세포는 치료 또는 완화를 필요로 하는 환자에서 상기 병태 중 임의의 것의 증상을 치료 또는 완화시킬 수 있다. 세포는 자가 유래이거나, 환자에 동종이계일 수 있다. 추가의 측면에서, 본 발명의 세포는 다른 치료와 함께 조합하여 투여될 수 있다.
본 발명의 RG 전구체 세포는 퇴해성 질환 치료에서 사용될 수 있는 것으로 보여진다. 세포는 세포를 의도하는 안구 부위, 예컨대, 망막의 신경절 세포층에 이식하거나, 또는 그 부위로 이동할 수 있도록 기능이 결핍된 부위를 재구성 또는 재생시킬 수 있도록 허용하는 방식으로 투여된다.
유전적으로 조작된 RG 전구체 세포 또는 RG 세포는 또한 변성 부위로 유전자 생성물을 표적화하는 데 사용될 수 있고, 예를 들어, 분비된 생물학적으로 활성인 단백질, 펩티드 또는 핵산(예컨대, RNA 간섭 분자 또는 압타머) 등을 코딩하는 하나 이상의 유전자로 조작될 수 있다. 이러한 유전자 생성물로는 천연 퇴행 뉴런을 구제하기 위한 생존 촉진 인자, 부위 특이적 뉴런으로 이식된 세포의 생존 및 분화를 촉진하거나 또는 기능적 회복을 허용하는 신경전달물질(들)을 전달하도록 자가분비 방식으로 작용하는 인자를 포함할 수 있다. 예를 들어, 하나 이상의 생물학적으로 활성인 분자(들)로는 항혈관신생 항체 및 분자, 항혈관신생 항체 스캐폴드, 가용성 수용체, 면역 경로 분자를 표적화 및 억제 또는 조정하는 작용제, 성장 인자 억제제, 성장 인자, 신경 영양 인자, 혈관신생 인자, 신경전달물질, 호르몬, 효소, 항염증성 인자, 또는 다른 치료학적 단백질을 포함할 수 있다. 다양한 실시양태에서, 상기 분자로는 C3a 억제제, C3b 억제제, 면역 경로 분자를 표적화 및 억제 또는 조정하는 다른 작용제, 뇌 유래 신경 영양 인자(BDNF), NT-4, 섬모 신경 영양 인자(CNTF), 엑소킨(Axokine), 염기성 섬유아세포 성장 인자(bFGF), 인슐린 유사 성장 인자 I(IGF I), 인슐린 유사 성장 인자 II(IGF II), 산성 섬유아세포 성장 인자(aFGF), 섬유아세포 성장 인자(aFGF) 표피 성장 인자(EGF), 형질전환 성장 인자 알파(TGF-알파), 형질전환 성장 인자 베타(TGF-베타), 신경 성장 인자(NGF), 혈소판 유래 성장 인자(PDGF), 신경교 유래 신경 영양 인자(GDNF), 미드킨(Midkine), 트리오포틴, 액티빈, 티로트로핀 방출 호르몬, 인터루킨, 골 형태형성 단백질, 대식세포 염증성 단백질, 헤파린 술페이트, 앰피레귤린, 레티노산, 종양 괴사 인자 알파, 섬유아세포 성장 인자 수용체, 표피 성장 인자 수용체(EGFR), PEDF, LEDGF, NTN, 뉴블라스틴, 뉴로트로핀, 림포카인, VEGF 억제제, PDGF 억제제, 태반 성장 인자(PIGF) 억제제, Tie2, CD55, C59, VEGF 및 PDGF에 동시에 결합하는 이중특이성 분자, 및 잠재적 표적 조직에 치료학상 유용한 영향을 미칠 것으로 예상되는 다른 작용제를 포함할 수 있지만, 이에 제한되지 않는다. 특정의 바람직한 실시양태에서, 재조합적으로 조작된 RG 전구체 세포 또는 RG 세포는, 망막 변성 모델에서 세포 사멸 과정을 유의적으로 저속화시키는 것으로 밝혀져 있는 인자인, 하나 이상의 재조합 성장 인자 및 뉴로트로핀, 예컨대, FGF2, NGF, 섬모 신경 영양 인자(CNTF), 및 뇌 유래 신경 영양 인자(BDNF)를 발현하도록 조작된다. 한 성장 인자 또는 성장 인자의 조합을 합성하도록 조작된 RG 전구체 및/또는 RG 세포를 사용하는 요법은 신경 보호약물의 지속적인 전달을 보장할 수 있을 뿐만 아니라, 손상된 망막을 재구성할 수도 있다.
특정 실시양태에서, RG 전구체 또는 RG 세포를 조작하는 데 사용되는 유전자 구성체는 신경절 세포 사멸 및/또는 녹내장, 예컨대, 안압(IOP) 상승, 글루타메이트 수준 상승 등을 촉진시키는 병태에 감수성인 전사 및/또는 번역 제어 요소(예컨대, 인핸서 또는 프로모터)를 포함할 수 있다. IOP 상승에 감수성인, 예시적인 프로모터는 매트릭스 Gla 단백질(MGP\) 유전자로부터의 프로모터이다(예를 들어, 문헌 [Gonzalez et al., Investigative Ophthalmology & Visual Science, May 2004, 45(5): 1389](상기 문헌은 그 전문이 본원에서 참조로 포함된다) 참조). 선택적 표적화는 또한, 발현이 특이적으로 TM의 가장 바깥쪽 전방 및 후방 영역으로 지시되는 것인, 키티나제 3 유사 1("Ch3L1": chitinase 3-like 1) 유전자의 5' 프로모터 영역을 사용하여 달성되었다(문헌 [Liton et al., Invest Ophthalmol Vis Sci. 2005, 46:183](상기 문헌은 그 전문이 본원에서 참조로 포함된다)). 추가로, 섬유주대 세포 선택성 프로모터에 대한 추가의 대안적 구조를 제공하는, 섬유주대에 관한 유전자 프로파일링 연구가 다수 공개되어 있다(문헌 [[Gonzalez et al., Invest Ophthalmol Vis Sci. 2000, 41:3678-3693]; [Wirtz et al., Invest Ophthalmol Vis Sci. 2002, 43:3698]; [Tomarev et al., Invest Ophthalmol Vis Sci. 2003, 44:2588-2596]; [Liton et al., Invest Ophthalmol Vis Sci. 2005, 46:183]; [Liton et al., Mol Vis. 2006, 12:774]; [Fan et al., Invest Ophthalmol Vis Sci. 2008, 49:1886]; [Fuchshofer et al., Exp Eye Res. 2009, 88:1020]; [Paylakhi et al., Mol Vis. 2012, 18:241]; 및 [Liu et al., Invest Ophthalmol Vis Sci. 2013, 54:6382](상기 문헌은 각각 그 전문이 본원에서 참조로 포함된다)).
본 발명의 방법에서, 이식되는 세포는 인간 투여를 위해 충분히 멸균성인 조건하에서 제조된 등장성 부형제를 포함하는 임의의 생리적으로 허용되는 부형제 중에서 수혜자에게로 전달된다. 의약 제제의 일반 원리에 대해, 독자는 문헌 [Cell Therapy: Stem Cell Transplantation, Gene Therapy, and Cellular Immunotherapy, by G. Morstyn & W. Sheridan eds, Cambridge University Press, 1996]을 참조한다. 세포 부형제 및 조성물의 임의의 수반 성분에 관한 선택은 투여에 사용되는 장치 및 경로에 따라 적합화될 것이다. 세포는 주사, 카테터 등에 의해 도입될 수 있다. 세포는 액체 질소 온도에서 냉동되고, 장기간 동안 보관될 수 있고, 해동시 사용될 수 있다. 냉동되는 경우, 세포는 10% DMSO, 50% FCS, 40% RPMI 1640 배지 중에서 보관될 수 있다. 바람직한 실시양태에서, 세포는 동물 무함유 냉동보존 완충제, 예컨대, 크라이오스토르 CS10에서 보관될 것이다.
본 발명의 약학 제제는 임의적으로 바람직한 목적을 위해 작성된 설명서와 함께 적합한 용기에 포장된다. 상기 제제는 RG 전구체 또는 RG 세포와의 조합에 적합한 형태로, 망막 분화 및/또는 영양성 인자의 칵테일을 포함할 수 있다. 상기 조성물은 동물에 전달하는 데 적절한 적합한 완충제 및/또는 부형제를 추가로 포함할 수 있다. 상기 조성물은 생착시키고자 하는 세포를 추가로 포함할 수 있다.
약학 제제
RG 전구체 세포 또는 RG 세포는 약학적으로 허용되는 담체와 함께 제제화될 수 있다. 예를 들어, RG 전구체 세포 또는 RG 세포는 단독으로 또는 약학 제제의 성분으로서 투여될 수 있다. 대상 화합물은 의약에서 사용하기 위한 임의의 편리한 방식으로 투여하기 위해 제제화될 수 있다. 투여에 적합한 약학 제제는 항산화제, 완충제, 살균제, 용질 또는 현탁화제 또는 증점화제를 함유할 수 있는, 하나 이상의 약학적으로 허용되는 멸균 등장성 수성 또는 비수성 용액(예컨대, 평형 염 용액(BSS)), 분산액, 현탁액 또는 에멀젼, 또는 사용 직전 멸균 주사액 또는 분산액으로 재구성될 수 있는 멸균 분제와 함께 조합하여, RG 전구체 세포 또는 RG 세포를 포함할 수 있다. 예시적인 약학 제제는 알콘® BSS 플러스®(ALCON® BSS PLUS®)(물 중 각 1 mL 당 염화나트륨 7.14 mg, 염화칼륨 0.38 mg, 염화칼슘 2수화물 0.154 mg, 염화마그네슘 6수화물 0.2 mg, 이염기성 인산나트륨 0.42 mg, 중탄산나트륨 2.1 mg, 덱스트로스 0.92 mg, 글루타티온 디술피드(산화된 글루타티온) 0.184 mg, 염산 및/또는 수산화나트륨(pH를 대략 7.4로 조정하기 위해)를 함유하는 평형 염 용액)와 함께 조합하여 RG 전구체 세포 또는 RG 세포를 포함한다.
투여시, 본 개시내용에서 사용하기 위한 약학 제제는 발열원 무함유, 생리학적으로 허용되는 형태일 수 있다.
RG 전구체 세포 또는 RG 세포를 포함하는 제제는 현탁액, 겔, 콜로이드, 슬러리, 또는 혼합물로 이식될 수 있다. 추가로, 제제는 바람직하게는 망막 또는 맥락막 손상 부위로 전달하기 위해 캡슐화되거나, 또는 유리체액 내로 점성 형태로 주사될 수 있다. 또한, 주사시, 냉동보존된 RG 전구체 세포 또는 RG 세포는 망막하 주사에 의한 투여에 바람직한 오스몰 농도 및 농도를 달성하기 위해 평형 염 용액으로 재현탁될 수 있다. 제제는 투여된 세포의 부착 및/또는 생존을 촉진시킬 수 있는, 질환에 완전하게 소실되지 않은 주변 황반 영역에 투여될 수 있다. 예를 들어, 녹내장 동물 모델인 경우를 비롯한, 일부 경우에서, RG 전구체 및/또는 RG 세포는 유리체내로 투여된다.
RG 전구체 세포 및/또는 RG 세포는 본원에 기술된 바와 같이 냉동(냉동보존)될 수 있다. 해동시, 상기 세포의 생존도는 20% 이상, 30% 이상, 40% 이상, 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95% 이상 또는 약 100%일 수 있다(예컨대, 해동 후 수거된 세포 중 20% 이상, 30% 이상, 40% 이상, 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95% 이상 또는 약 100%의 세포가 생존가능한 것이거나, 또는 처음 냉동된 세포 개수의 20% 이상, 30% 이상, 40% 이상, 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95% 이상 또는 약 100%가 해동 후 생존가능한 상태로 수거된다).
RG 전구체 세포 또는 RG 세포는 안내 주사용으로 적합한 약학적으로 허용되는 안과용 비히클 또는 제제 중에서 제제화되고, 전달될 수 있다. 일부 경우에서, 제제는 세포가 이환된 눈 부위, 예를 들어, 전안방, 후안방, 유리체, 수양액, 유리체액, 각막, 홍채/모양체, 수정체, 맥락막, 망막, 공막, 맥락막상 공간, 결막, 결막하 공간, 공막외 공간, 각막내 공간, 각막외 공간, 초자체 절제, 외과적으로 유도된 무혈관 영역 또는 황반을 투과할 수 있도록 허용하는 충분한 시간 동안 안구 표면과 접촉한 상태로 그대로 유지되도록 디자인된다.
RG 전구체 세포 또는 RG 세포는 세포 시트에 함유될 수 있다. 예를 들어, RG 전구체 세포 또는 RG 세포를 포함하는 세포 시트는 무손상 세포 시트가 박리될 수 있는 기판, 예컨대, 열반응성 중합체, 예컨대, 열반응성 폴리(N-이소프로필아크릴아미드)(PNIPAAm)-이식된 표면 상에서 RG 전구체 세포 또는 RG 세포를 배양함으로써 제조될 수 있고, 그 위에 세포가 부착되고, 배양 온도에서 증식된 후, 이어서, 온도가 변화되었을 때, 표면 특징이 변화되어 배양된 세포 시트가 박리된다(예를 들어, 하한 임계 용액 온도(LCST) 아래로 냉각시킴으로써 이루어짐. 예를 들어, 문헌 [da Silva et al., Trends Biotechnol. 2007 Dec;25(12):577-83]; [Hsiue et al., Transplantation 2006 Feb 15;81(3):473-6]; [Ide, T. et al. (2006); Biomaterials 27, 607-614, Sumide, T. et al. (2005), FASEB J. 20, 392-394]; [Nishida, K. et al. (2004), Transplantation 77, 379-385]; 및 [Nishida, K. et al. (2004), N. Engl. J. Med. 351, 1187-1196](상기 문헌은 각각 그 전문이 본원에서 참조로 포함된다)). 세포 시트는 이식에 적합한 기판, 예컨대, 시트가 숙주 유기체 내로 이식되었을 때, 생체내에서 용해될 수 있는 기판에 부착될 수 있고, 예컨대, 이식에 적합한 기판 상에서 세포를 배양함으로써, 또는 이식에 적합한 기판 상에서 또 다른 기판(예컨대, 열반응성 중합체)으로부터 세포를 박리시킴으로써 제조될 수 있다. 이식에 적합한 예시적인 기판은 젤라틴(문헌 [Hsiue et al., 상기 문헌 동일) 참조)을 포함할 수 있다. 이식에 적합한 대안적인 기판은 피브린계 매트릭스 등을 포함한다. 세포 시트는 망막 변성 질환의 예방용 또는 치료용 의약의 제조에서 사용될 수 있다.
세포 시트는 예를 들어, RG 전구체 세포 또는 RG 세포의 시트를 이식하는 중심와하 막절제술을 비롯한, 수술 또는 다른 침습선 요법과 함께 그를 필요로 하는 눈으로 도입될 수 있다. 따라서, 세포 시트는 중심와하 막절제술과 함께 이식용 의약 제조에서 사용될 수 있다.
본원에 기술된 방법에 따라 투여되는 제제의 부피는 인자, 예컨대, 투여 모드, RG 전구체 세포 또는 RG 세포 개수, 환자 연령 및 체중, 및 치료되는 질환 유형 및 중증도에 의존할 수 있다. 제제를 국소적으로, 예를 들어, 유리체내 주사에 의해 눈으로 투여할 때, 최소 부피로 전달할 수 있도록 제제는 충분히 농축되어야 한다. 예를 들어, 주사에 의해 투여될 때, RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제의 부피는 약 1, 1.5, 2, 2.5, 3, 4, 또는 5 ml, 또는 약 1-2 ml일 수 있다. 예를 들어, 주사에 의해 투여될 때, RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제의 부피는 약 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 100, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 또는 200 ㎕(마이크로리터) 이상일 수 있다. 예를 들어, 본 개시내용의 제제의 부피는 약 10-50, 20-50, 25-50, 또는 1-200 ㎕일 수 있다. 본 개시내용의 제제의 부피는 약 10, 20, 30, 40, 50, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 또는 200 ㎕ 또는 그 초과일 수 있다.
주사를 위한 농도는 본원에 기술된 인자에 의존하여, 효과적이며, 비독성인 임의 수준일 수 있다. 환자 치료용의, RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제는 약 103, 104, 105, 106, 107, 108, 109, 또는 1010개 이상의 RG 전구체 세포 또는 RG 세포/ml를 비롯한, 약 103개 이상의 세포/ml인 용량으로 제제화될 수 있다. 약학 제제는 약 1x103, 2x103, 3x103, 4x103, 5x103, 6x103, 7x103, 8x103, 9x103, 1x104, 2x104, 3x104, 4x104, 5x104, 6x104, 7x104, 8x104, 또는 9x104개 이상의 RG 전구체 세포 또는 RG 세포/㎕를 포함할 수 있다. 제제는 50 ㎕당 100,000개의 RG 전구체 세포 또는 RG 세포, 또는 90 ㎕당 180,000개의 RG 전구체 세포 또는 RG 세포를 비롯한, 2,000개 이상의 RG 전구체 세포 또는 RG 세포/㎕를 포함할 수 있다.
RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제는 약 1,000; 2,000; 3,000; 4,000; 5,000; 6,000; 7,000; 8,000; 또는 9,000개 이상의 RG 전구체 세포 또는 RG 세포를 포함할 수 있다. RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제는 약 1x104, 2x104, 3x104, 4x104, 5x104, 6x104, 7x104, 8x104, 9x104, 1x105, 2x105, 3x105, 4x105, 5x105, 6x105, 7x105, 8x105, 9x105, 1x106, 2x106, 3x106, 4x106, 5x106, 6x106, 7x106, 8x106, 9x106, 1x107, 2x107, 3x107, 4x107, 5x107, 6x107, 7x107, 8x107, 9x107, 1x108, 2x108, 3x108, 4x108, 5x108, 6x108, 7x108, 8x108, 9x108, 1x109, 2x109, 3x109, 4x109, 5x109, 6x109, 7x109, 8x109, 9x109, 1x1010, 2x1010, 3x1010, 4x1010, 5x1010, 6x1010, 7x1010, 8x1010, 또는 9x1010개 이상의 RG 전구체 세포 또는 RG 세포를 포함할 수 있다. RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제는 약 1x102-1x103, 1x102-1x104, 1x104-1x105, 또는 1x103-1x106개 이상의 RG 전구체 세포 또는 RG 세포를 포함할 수 있다. RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제는 약 10,000, 20,000, 25,000, 50,000, 75,000, 100,000, 125,000, 150,000, 175,000, 180,000, 185,000, 190,000, 또는 200,000개 이상의 RG 전구체 세포 또는 RG 세포를 포함할 수 있다. 예를 들어, 전구체 세포 또는 RG 세포로 이루어진 약학 제제는 약 50-200 ㎕ 이상의 부피로 약 20,000-200,000개 이상의 RG 전구체 세포 또는 RG 세포를 포함할 수 있다. 추가로, RG 전구체 세포 또는 RG 세포로 이루어진 약학 제제는 150 ㎕의 부피로 약 50,000개의 RG 전구체 세포 또는 RG 세포, 150 ㎕의 부피로 약 200,000개의 RG 전구체 세포 또는 RG 세포, 또는 약 150 ㎕ 이상의 부피로 약 180,000개 이상의 RG 전구체 세포 또는 RG 세포를 포함할 수 있다.
상기 약학 제제 및 조성물에서, RG 전구체 세포 또는 RG 세포의 개수수 또는 RG 전구체 세포 또는 RG 세포의 농도는 생존가능한 세포를 계수하고, 비생존 생존불가능한 세포는 배제함으로써 결정될 수 있다. 예를 들어, 생존불가능한 RG 전구체 세포 또는 RG 세포는 생염료(예컨대, 트리판 블루) 배제 실패에 의해, 또는 기능성 검정법(예컨대, 배양 기판에 부착할 수 있는 능력 등)를 이용하여 검출될 수 있다. 추가로, RG 전구체 세포 또는 RG 세포의 개수 또는 RG 전구체 세포 또는 RG 세포의 농도는 1하나 이상의 RG 전구체 세포 또는 RG 세포 마커를 발현하는 세포를 계수하고/거나, RG 전구체 세포 또는 RG 세포 이외의 세포 유형을 나타내는 하나 이상의 마커를 발현하는 세포를 배제함으로써 결정될 수 있다.
망막 변성을 치료하는 방법은 면역억제제의 투여를 추가로 포함할 수 있다. 사용될 수 있는 면역억제제로는 항림프구 글로불린(ALG: anti-lymphocyte globulin) 다중클론 항체, 항흉선세포 글로불린(ATG: anti-thymocyte globulin) 다중클론 항체, 아자티오프린, 바실릭시맙(BASILIXIMAB)®(항IL-2Rα 수용체 항체), 사이클로스포린(사이클로스포린 A), 다클리주맙(DACLIZUMAB)®(항IL-2Rα 수용체 항체), 에버롤리무스, 마이코페놀산, 리툭시맙(RITUXIMAB)®(항CD20 항체), 시롤리무스, 및 타클로리무스를 포함하나, 이에 제한되지 않는다. 면역역제제는 약 1, 2, 4, 5, 6, 7, 8, 9, 또는 10 mg/kg 이상으로 투약될 수 있다. 면역억제제가 사용될 때, 이는 전신으로 또는 국소적으로 투여될 수 있고, 이들은 RG 전구체 세포 또는 RG 세포의 투여 이전에, 그와 동시에 또는 그 이후에 투여될 수 있다. 면역억제 요법은 RG 전구체 세포 또는 RG 세포 투여 후 수주, 수개월, 수년 동안, 또는 무한적으로 지속될 수 있다. 예를 들어, 환자는 RG 전구체 세포 또는 RG 세포 투여 후 6주 동안 5 mg/kg 사이클로스포린을 투여받을 수 있다.
망막 변성을 치료하는 방법은 RG 전구체 세포 또는 RG 세포를 단일 용량으로 투여하는 것을 포함할 수 있다. 대안적으로, 본원에 기술된 치료 방법은 RG 전구체 세포 또는 RG 세포를 일부 기간 동안 다회에 걸쳐 투여하는 요법 과정을 포함할 수 있다. 예시적인 치료 과정은 매주, 격주, 매월, 분기별, 반년마다 또는 매년 치료를 포함할 수 있다. 대안적으로, 치료는 단계적으로 진행함으로써, 다회분 용량을 초기에 투여하고(예컨대, 첫주 동안 매일 투약), 이어서, 더 적은 및 덜 빈번한 투약이 요구된다.
안구내 주사를 비롯한, 주사에 의해 투여되는 경우, RG 전구체 세포 또는 RG 세포는 환자 생애 동안 주기적으로 1회 이상 전달될 수 있다. 예를 들어, RG 전구체 세포 또는 RG 세포는 1년에 1회, 6-12개월마다 1회, 3-6개월마다 1회, 1-3개월마다 1회, 또는 1-4주마다 1회 전달될 수 있다. 대안적으로, 특정 병태 또는 장애에 대해서는 더욱 빈번한 투여가 바람직할 수 있다. 임플란트 또는 장치에 의해 투여되는 경우, RG 전구체 세포 또는 RG 세포는 특정 환자 및 치료하려는 장애 및 병태에 대한 필요에 따라, 환자 생애 동안 1회, 또는 1회 이상 주기적으로 투여될 수 있다. 유사하게는, 시간 경과에 따라 변화되는 치료 요법이 고려된다. 예를 들어, 개시 시점에는 더욱 빈번하기 치료가 요구될 수 있다(예컨대, 매일 또는 맺 치료). 시간이 경과함에 따라, 환자의 병태가 호전되면, 치료는 덜 빈번하게 요구되거나, 또는 심지어는 추가 치료가 요구되지 않을 수도 있다.
본원에 기술된 방법은 피험체에서 망막 전위도 반응, 시운동 시력 역치, 또는 발광 역치를 측정하여 치료 또는 예방의 효율을 모니터링하는 단계를 추가로 포함할 수 있다. 본 방법은 또한 눈에서 세포의 이동 또는 통합 또는 생존, 또는 세포의 면역원성을 모니터링함으로써 치료 또는 예방의 효능을 모니터링하는 단계 또한 포함할 수 있다.
RG 전구체 세포 또는 RG 세포는 망막 변성을 치료하기 위한 의약 제조에서 사용될 수 있다. 본 개시내용 또한 실명의 치료에서의, RG 전구체 세포 또는 RG 세포를 포함하는 제제의 용도를 포함한다. 예를 들어, 인간 RG 전구체 세포 또는 RG 세포를 포함하는 제제는 망막 손상 및 실명을 일으키는 다수의 시력 변경 질병, 예컨대, 예컨대, 허혈 재관류 손상, 망막 혈관 질환, (자가면역, 외상, 및/또는 바이러스 기반인지에 상관 없이) 시신경 손상, (유형에 상관 없이) 녹내장, (저산소 및 혈관신생 기반인지에 상관 없이) 당뇨병성 망막증, 및 유전성 시각 신경병증(예컨대, 레베르 유전성 시각 신경병증(LHON) 또는 레베르 시신경 위축증)과 관련된 망막 변성을 치료하는 데 사용될 수 있다. 일부 실시양태에서, 인간 RG 전구체 세포 또는 RG 세포를 포함하는 제제는 단독으로 사용될 수 있거나, 또는 황반 변성(연령 관련 황반 변성, 예컨대, 습식 연령 관련 황반 변성 및 건식 연령 관련 황반 변성), 색소성 망막염, 및 스타르카르트병(황반 안저), 야맹증 및 색맹을 치료하는 다른 치료제(예컨대, 다른 세포 요법, 예컨대, RPE 세포 및/또는 광수용기 세포 집단)와 함께 사용될 수 있다. 본 제제는 약 5,000-500,000개 이상의 RG 전구체 세포 또는 RG 세포(예컨대, 100,000개의 RG 전구체 세포 또는 RG 세포)를 포함할 수 있다.
RG 전구체 세포 및 RG 세포 중 어느 하나, 또는 그 둘 모두가 사용될 수 있다. 인간 세포는 인간 환자에서 뿐만 아니라, 동물 모델 또는 동물 환자에서도 사용될 수 있다. 예를 들어, 인간 세포는 망막 변성을 앓는 마우스, 래트, 고양이, 개, 또는 인간외 영장류 모델에서 시험될 수 있다. 추가로, 인간 세포는 예컨대, 수의학적 의약에서와 같이, 그를 필요로 하는 동물을 치료하는 데 치료학적으로 사용될 수 있다.
본원에서 정의되는 바와 같이, 단수 형태는 예시적인 목적으로 제공되지만, 이는 또한 어구의 복수형에도 적용될 수 있다.
번호로 표기된 본 발명의 다양한 실시양태를 하기에서 언급된다.
1. 복수 개의 RG 전구체 세포, 및
RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, RG 전구체 세포의 실질적으로 순수한 제제로서,
여기서, 상기 제제 중 90% 초과의 세포가 면역세포화학적으로 Math5(+), 및 임의적으로, Math5(+) 및 Brn3a(+)인 것인, RG 전구체 세포의 실질적으로 순수한 제제.
2. 실시양태 1에 있어서, 제제 중 99% 초과의 세포가 면역세포화학적으로 Math5(+), 및 임의적으로, Math5(+) 및 Brn3a(+)인 것인, RG 전구체 세포의 실질적으로 순수한 제제.
3. 실시양태 1 또는 2에 있어서, 제제 중 99% 초과의 세포가 면역세포화학적으로 Pax6(-) 및 Rx1(-)인 것인, RG 전구체 세포의 실질적으로 순수한 제제.
4. 실시양태 1, 2, 또는 3에 있어서, 제제 중 세포가 면역세포화학적으로 Brn3b(+) 및/또는 Isl1(+)인 것인, RG 전구체 세포의 실질적으로 순수한 제제.
5. 복수 개의 RG 전구체 세포, 및
RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, RG 전구체 세포의 실질적으로 순수한 제제로서,
여기서, 상기 제제 중 90% 초과의 세포가 면역세포화학적으로 Brn3a(+) 및 신경미세섬유(+)인 것인, RG 전구체 세포의 실질적으로 순수한 제제.
6. 실시양태 5에 있어서, 제제 중 세포가 Thy1(+)인 것인, RG 전구체 세포의 실질적으로 순수한 제제.
7. 50% 이상의 RG 전구체 세포를 함유하는 복수 개의 세포, 및
RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, RG 전구체 세포의 제제로서,
여기서, RG 전구체 세포는 면역세포화학적으로 Math5(+), Brn3a(+), Brn3b(+), 및 임의적으로, Isl1(+)인 것인, RG 전구체 세포의 제제.
8. 50% 이상의 RG 전구체 세포를 함유하는 복수 개의 세포, 및
RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, RG 전구체 세포의 제제로서,
여기서, RG 전구체 세포는 면역세포화학적으로 Brn3a(+), 신경미세섬유(+), 및 임의적으로, Thy1(+)인 것인, RG 전구체 세포의 제제.
9. 만능 줄기 세포, 성숙한 광수용기, 및/또는 아마크린 세포를 실질적으로 함유하지 않는, 복수 개의 RG 전구체 세포; 및
RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, RG 전구체 세포의 제제로서,
여기서, RG 전구체 세포는 면역세포화학적으로 Math5(+), Brn3a(+), Brn3b(+), 및 임의적으로, Isl1(+)인 것인, RG 전구체 세포의 제제.
10. 만능 줄기 세포, 성숙한 광수용기, 및/또는 아마크린 세포를 실질적으로 함유하지 않는, 복수 개의 RG 전구체 세포; 및
RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, RG 전구체 세포의 제제로서,
여기서, RG 전구체 세포는 면역세포화학적으로 Brn3a(+), 신경미세섬유(+), 및 임의적으로, Thy1(+)인 것인, RG 전구체 세포의 제제.
11. (a) 제제 중 90% 초과의 세포가 면역세포화학적으로 Math5(+), 및 임의적으로, Math5(+) 및 Brn3a(+)인 것인, 복수 개의 RG 전구체 세포; 및
(b) 포유동물 환자 내로의 이식을 위해 RG 전구체 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 포함하는, 포유동물 환자에서의 사용에 적합한 RG 전구체 세포의 약학 제제.
12. 실시양태 11에 있어서, 제제 중 99% 초과의 세포가 면역세포화학적으로 Math5(+), 및 임의적으로, Math5(+) 및 Brn3a(+)인 것인, 약학 제제.
13. 실시양태 11 또는 12에 있어서, 제제 중 99% 초과의 세포가 면역세포화학적으로 Pax6(-) 및 Rx1(-)인 것인, 약학 제제.
14. 실시양태 11, 12, 또는 13에 있어서, 제제 중 세포가 면역세포화학적으로 Brn3b(+) 및/또는 Isl1(+)인 것인, 약학 제제.
15. (a) 제제 중 90% 초과의 세포가 면역세포화학적으로 Brn3a(+) 및 신경미세섬유(+)인 것인, 복수 개의 RG 전구체 세포; 및
(b) 포유동물 환자 내로의 이식을 위해 RG 전구체 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 포함하는, 포유동물 환자에서의 사용에 적합한 RG 전구체 세포의 약학 제제.
16. 실시양태 15에 있어서, 제제 중 세포가 Thy1(+)인 것인, 약학 제제.
17. 109개 이상의 RG 전구체 세포를 포함하는 극저온 세포 제제로서,
(a) 제제 중 90% 초과의 세포가 면역세포화학적으로 Math5(+), 및 임의적으로, Math5(+) 및 Brn3a(+)인 것인, 복수 개의 RG 전구체 세포; 및
(b) 해동시 RG 전구체 세포의 생존능에 맞는 냉동보존 시스템을 포함하는 것인, 극저온 세포 제제.
18. 실시양태 17에 있어서, 제제 중 99% 초과의 세포가 면역세포화학적으로 Math5(+), 및 임의적으로, Math5(+) 및 Brn3a(+)인 것인, 극저온 세포 제제.
19. 실시양태 17 또는 18에 있어서, 제제 중 99% 초과의 세포가 면역세포화학적으로 Pax6(-) 및 Rx1(-)인 것인, 극저온 세포 제제.
20. 실시양태 17, 18 또는 19에 있어서, 제제 중 세포가 면역세포화학적으로 Brn3b(+) 및/또는 Isl1(+)인 것인, 극저온 세포 제제.
21. 109개 이상의 RG 전구체 세포를 포함하는 극저온 세포 제제로서,
(a) 제제 중 90% 초과의 세포가 면역세포화학적으로 Brn3a(+) 및 신경미세섬유(+)인 것인, 복수 개의 RG 전구체 세포, 및
(b) 해동시 RG 전구체 세포의 생존능에 맞는 냉동보존 시스템을 포함하는 것인, 극저온 세포 제제.
22. 실시양태 21에 있어서, 제제 중 세포가 면역세포화학적으로 Thy1(+)인 것인, 극저온 세포 제제.
23. 실시양태 1 내지 22 중 어느 한 실시양태에서, RG 전구체 세포가 만능 줄기 세포로부터 유래된 것인 제제.
24. 실시양태 23에 있어서, 만능 줄기 세포가 인간 배아 줄기 세포 및 유도성 만능 줄기 세포로 이루어진 군으로부터 선택되는 것인 제제.
25. 실시양태 1 내지 24 중 어느 한 실시양태에서, RG 전구체 세포가 인간 세포인 것인 제제.
26. 실시양태 1 내지 25 중 어느 한 실시양태에서, RG 전구체 세포가 HLA-유전자형적으로 동일한 것인 제제.
27. 실시양태 1 내지 26 중 어느 한 실시양태에서, RG 전구체 세포가 게놈적으로 동일한 것인 제제.
28. 실시양태 1 내지 27 중 어느 한 실시양태에서, RG 전구체 세포의 평균 말단 제한 절편 길이(TRF)가 8 kb보다 더 긴 것인 제제.
29. 실시양태 1 내지 28중 어느 한 실시양태에서, RG 전구체 세포가 증가된 세포 생존 및 신경보호 활성을 가지는 것인 제제.
30. 실시양태 11 내지 16 중 어느 한 실시양태에서, 인간 환자에게 투여하기에 적합한 것인 제제.
31. 실시양태 11 내지 16 중 어느 한 실시양태에서, 인간외 수의학적 환자에게 투여하기에 적합한 것인 제제.
32. 실시양태 23 또는 24에 있어서, RG 전구체 세포가 공통 만능 줄기 세포 공급원으로부터 유래되는 것인 제제.
33. 실시양태 1 내지 10 중 어느 한 실시양태에서, RG 전구체 세포의 생존능을 유지시키는 데 적합한 배지가 배양 배지, 냉동보존제, 및 인간 환자에서 주사하기 적합한 생체적합성 주사용 배지로 이루어진 군으로부터 선택되는 것인 제제.
34. 실시양태 1 내지 33 중 어느 한 실시양태에서, RG 전구체 세포가 시신경 압박 모델 마우스의 유리체 공간 내로 이식되었을 때, 마우스에서 외부 유핵 층으로 이동하고, 패턴 ERG 반응을 개선시키고/거나, 시신경 재생을 증진시키는 것인 제제.
35. 실시양태 11 내지 16 중 어느 한 실시양태에서, 제제가 발열원 및 마이코젠 무함유인 것인 제제.
36. 실시양태 1 내지 35 중 어느 한 실시양태에서, RG 전구체 세포가 하나 이상의 신경보호 인자를 분비하는 것인 제제.
37. (a) 60% 초과의 세포가 면역세포화학적으로 Brn3a(+), 신경미세섬유(+), 및 Tuj1(+)인 것인, 만능 줄기 세포 유래 RG 세포; 및
(b) 줄기 세포 유래 RG 세포의 생존능을 유지시키는 데 적합한 배지를 포함하는, 만능 줄기 세포 유래 RG 세포의 실질적으로 순수한 제제.
38. 실시양태 37에 있어서, 제제 중 세포가 Thy1(+)인 것인, 실질적으로 순수한 제제.
39. 실시양태 37 또는 38에 있어서, 약 70% 초과의 세포가 면역세포화학적으로 Brn3a(+), 신경미세섬유(+), 및 Tuj1(+)인 것인, 실질적으로 순수한 제제.
40. (a) 제제 중 60% 초과의 세포가 면역세포화학적으로 Brn3a(+), 신경미세섬유(+), 및 Tuj1(+)인 것인, 만능 줄기 세포 유래 RG 세포; 및
(b) 포유동물 환자 내로의 이식을 위해 RG 세포의 생존능을 유지시키기 위한 약학적으로 허용되는 담체를 포함하는, 포유동물 환자에서의 사용에 적합한 RG 세포의 약학 제제.
41. 실시양태 40에 있어서, 제제 중 세포가 Thy1(+)인 것인, 약학 제제.
42. 실시양태 40에 있어서, 약 70%의 세포가 면역세포화학적으로 Brn3a(+), 신경미세섬유(+), 및 Tuj1(+)인 것인, 약학 제제.
43. 환자에게 실시양태 11 내지 16 중 어느 한 실시양태의 RG 전구체 세포의 약학 제제, 또는 실시양태 40의 RG 세포의 약학 제제, 또는 그 둘 모두를 유효량으로 투여하는 단계를 포함하는, 환자에서 RG 세포 손실에 의해 유발되는 질환 또는 장애를 치료하는 방법.
44. 실시양태 43에 있어서, 세포의 제제를 환자의 망막하 공간 내로 주사하는 것인 방법.
45. 실시양태 43에 있어서, 세포의 제제를 유리체내로 주사하는 것인 방법.
46. 안구 영역 전구체 세포를, 바람직하게, 세포 클러스터로서, 및 바람직하게, 저부착 또는 비부착 조건하에서 상기 세포 클러스터가 Math5(+), Brn3a(+), Brn3b(+), 및 임의적으로, Isl1(+) 또는 Brn3a(+), 신경미세섬유(+) 및 임의적으로, Thy1(+)인 것을 특징으로 하는 RG 전구체 세포를 포함하는 개별 세포 구체를 형성하는 데 충분한 기간 동안 신경절 세포 배지 중에서 배양하는 단계로서, 여기서, 안구 영역 전구체 세포는 면역염색 및/또는 유세포 분석법에 의해 측정된 바, Pax6(+) 및 Rx1(+) 및 Oct4(-) 및 Nanog(-)인 것을 특징으로 하고, 바람직하게, 또한 Six3(+), Six6(+), Lhx2(+), Tbx3(+), Sox2(+), Otx2(+) 및 네스틴(+)인 것을 특징으로 하는 것인 단계를 포함하는, RG 전구체 세포를 제조하는 방법.
47. 실시양태 46에 있어서, 안구 영역 전구체 세포가 만능 줄기 세포가 유래된 것인 방법.
48. 실시양태 47에 있어서, 만능 줄기 세포가 배아 줄기 세포 또는 유도성 만능 줄기 세포, 임의적으로, 인간 배아 줄기 세포 또는 인간 유도성 만능 줄기 세포인 것인 방법.
49. 실시양태 46 또는 47에 있어서, RG 전구체 세포가 만능 줄기 세포를 실질적으로 함유하지 않는 상태로 제공되는 것인 방법.
50. 실시양태 46 내지 49 중 어느 한 실시양태에서, RG 전구체 세포가 다른 세포 유형 대비 50% 이상으로 순수하고, 5% 이상, 85% 이상, 95% 이상, 99% 이상 또는 약 100% 순수한 것인 방법.
51. 실시양태 46 내지 50 중 어느 한 실시양태에서, RG 전구체 세포를 냉동보존하는 단계를 추가로 포함하는 것인 방법.
52. (a) 피더세포 무함유 시스템 중에서 만능 줄기 세포를 배양하여 하나 이상의 안구 영역 전구체 세포를 제조하는 단계;
(b) 상기 하나 이상의 안구 영역 전구체 세포를 배양하여 Math5(+), Brn3a(+), Brn3b(+), 및 임의적으로, Isl1(+) 또는 Brn3a(+), 신경미세섬유(+) 및 임의적으로, Thy1(+)인 RG 전구체 세포를 제조하는 단계를 포함하는, 만능 줄기 세포 유래 RG 전구체 세포의 실질적으로 순수한 배양물을 제조하는 방법.
53. 신경절 세포 배지 중에서 안구 영역(EF) 전구체 세포를 배양하는 단계를 포함하는, RG 전구체 세포를 제조하는 방법.
54. 실시양태 53에 있어서, EF 전구체 세포가 Pax6(+) 및 Rx1(+)인 것인 방법.
55. 실시양태 53 또는 54에 있어서, EF 전구체 세포가 Six3(+), Six6(+), Lhx(+), Tbs(+)인 것인 방법.
56. 실시양태 53 내지 55 중 어느 한 실시양태에 있어서, EF 전구체 세포가 Sox2(+)인 것인 방법.
57. 실시양태 53 내지 56 중 어느 한 실시양태에 있어서, EF 전구체 세포가 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상, 95% 이상, 또는 약 100% EF 전구체 세포인 세포 집단으로서 제공되는 것인 방법.
58. 실시양태 53 내지 57 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 기본 배지, 예컨대, 뉴로베이살™ 배지를 포함하는 것인 방법.
59. 실시양태 53 내지 58 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 BDNF를 포함하는 것인 방법.
60. 실시양태 59에 있어서, BDNF가 인간의 것인 방법.
61. 실시양태 59 또는 60에 있어서, BDNF가 약 1-200 ng/ml, 5-50 ng/ml 또는 약 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재하는 것인 방법.
62. 실시양태 53 내지 61 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 CNTF를 포함하는 것인 방법.
63. 실시양태 62에 있어서, 상기 CNTF가 인간의 것인 방법.
64. 실시양태 63에 있어서, 상기 CNTF가 약 1 - 200 ng/ml, 5-50 ng/ml 또는 약 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재하는 것인 방법.
65. 실시양태 53 내지 64 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 포스콜린을 포함하는 것인 방법.
66. 실시양태 65에 있어서, 상기 포스콜린이 약 1-20 μM 또는 약 1-10 μM 또는 약 5 μM인 농도로 존재하는 것인 방법.
67. 실시양태 53 내지 66 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 약 0-10 mg/ml D-글루코스, 약 2.5-7.5 mg/ml D-글루코스, 약 3-6 mg/ml D-글루코스, 약 4-5 mg/ml D-글루코스, 또는 약 4.5 mg/ml D-글루코스를 포함하는 것인 방법.
68. 실시양태 53 내지 67 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 하나 이상의 항생제를 포함하는 것인 방법.
69. 실시양태 68에 있어서, 하나 이상의 항생제가 임의적으로, 약 0-100 유니트/ml의 페니실린 및 약 0-100 ㎍/ml의 스트렙토마이신인 농도의, 페니실린 및 스트렙토마이신으로 이루어진 군으로부터 선택되는 것인 방법.
70. 실시양태 53 내지 69 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 N2 보충제를 포함하는 것인 방법.
71. 실시양태 70에 있어서, N2 보충제가 약 0.1 내지 5% 또는 약 1%인 농도로 존재하는 것인 방법.
72. 실시양태 53 내지 71 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 B-27 보충제(포뮬러 080085-SA)를 포함하는 것인 방법.
73. 실시양태 72에 있어서, B-27 보충제(포뮬러 080085-SA)가 약 0.05-5.0% 또는 약 1.5-2.5% 또는 약 2.0%인 농도로 존재하는 것인 방법.
74. 실시양태 53 내지 73 중 어느 한 실시양태에 있어서, 신경절 세포 배지가 글루타민 또는 글루타맥스™를 를 포함하는 것인 방법.
75. 실시양태 53 내지 74 중 어느 한 실시양태에 있어서, 안구 영역 전구체 세포가 만능 줄기 세포로부터 유래된 것인 방법.
76. 실시양태 75에 있어서, 만능 줄기 세포가 인간 ES 세포 또는 인간 iPS 세포인 것인 방법.
77. 실시양태 75 또는 76에 있어서, 만능 줄기 세포를 피더세포 무함유 및/또는 제노 프리 조건하에서 배양하는 것인 방법.
78. 실시양태 53 내지 77 중 어느 한 실시양태에 있어서, 배양이 약 5-45일 동안 이루어지는 것인 방법.
79. 실시양태 78에 있어서, 배양이 약 5-20일 동안 이루어지는 것인 방법.
80. 실시양태 78에 있어서, 배양이 약 35-45일 동안 이루어지는 것인 방법.
81. 실시양태 79 또는 80에 있어서, 세포를 냉동보존하는 단계를 추가로 포함하는 것인 방법.
82. 실시양태 53 내지 80 중 어느 한 실시양태에 있어서, 세포를 망막 신경절 세포 분화 배지 중에서 배양함으로써 망막 신경절(RG) 세포를 제조하는 단계를 추가로 포함하는 것인 방법.
83. 실시양태 82에 있어서, 망막 신경절 세포 분화 배지가 뉴로베이살™ 배지를 포함하는 것인 방법.
84. 실시양태 82 또는 83에 있어서, 망막 신경절 세포 분화 배지가 약 0-10 mg/ml D-글루코스, 약 2.5-7.5 mg/ml D-글루코스, 약 3-6 mg/ml D-글루코스, 약 4-5 mg/ml D-글루코스, 또는 약 4.5 mg/ml D-글루코스를 포함하는 것인 방법.
85. 실시양태 82 내지 84 중 어느 한 실시양태에 있어서, 망막 신경절 세포 분화 배지가 하나 이상의 항생제를 포함하는 것인 방법.
86. 실시양태 85에 있어서, 항생제가 임의적으로, 약 0-100 유니트/ml의 페니실린 및 약 0-100 ㎍/ml의 스트렙토마이신인 농도의, 페니실린 및 스트렙토마이신으로 이루어진 군으로부터 선택되는 것인 방법.
87. 실시양태 82 내지 86 중 어느 한 실시양태에 있어서, 망막 신경절 세포 분화 배지가 인슐린, BDNF 및 CNTF 중 하나 이상 또는 그들 모두를 포함하는 것인 방법.
88. 실시양태 87에 있어서, 망막 신경절 세포 분화 배지가 인슐린을 포함하는 것인 방법.
89. 실시양태 88에 있어서, 인슐린이 인간 인슐린인 것인 방법.
90. 실시양태 88 또는 89에 있어서, 인슐린이 약 5-50 ㎍/ml 또는 약 20 ㎍/ml인 농도로 존재하는 것인 방법.
91. 실시양태 87 내지 90 중 어느 한 실시양태에 있어서, 망막 신경절 세포 분화 배지가 BDNF를 포함하는 것인 방법.
92. 실시양태 91에 있어서, BDNF가 인간의 것인 방법.
93. 실시양태 91 또는 92에 있어서, BDNF가 약 1-200 ng/ml, 5-50 ng/ml 또는 약 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재하는 것인 방법.
94. 실시양태 87 내지 93 중 어느 한 실시양태에 있어서, 망막 신경절 세포 분화 배지가 CNTF를 포함하는 것인 방법.
95. 실시양태 94에 있어서, CNTF가 인간의 것인 방법.
96. 실시양태 93 또는 94에 있어서, CNTF가 약 1 - 200 ng/ml, 5-50 ng/ml 또는 약 5-25 ng/ml 또는 약 10 ng/ml인 농도로 존재하는 것인 방법.
97. 실시양태 82 내지 96 중 어느 한 실시양태에 있어서, 망막 신경절 세포 분화 배지가 포스콜린, cAMP 및 DAPT 중 하나 이상 또는 그들 모두를 포함하는 것인 방법.
98. 실시양태 97에 있어서, 망막 신경절 세포 분화 배지가 포스콜린을 포함하는 것인 방법.
99. 실시양태 98에 있어서, 상기 포스콜린이 약 1-20 μM 또는 약 1-10 μM 또는 약 5 μM인 농도로 존재하는 것인 방법.
100. 실시양태 97에 있어서, 망막 신경절 세포 분화 배지가 cAMP를 포함하는 것인 방법.
101. 실시양태 100에 있어서, cAMP가 약 5-200 ng/ml인 농도로 존재하는 것인 방법.
102. 실시양태 97에 있어서, 망막 신경절 세포 분화 배지가 DAPT를 포함하는 것인 방법.
103. 실시양태 102에 있어서, DAPT가 약 1-50 μM인 농도로 존재하는 것인 방법.
104. 실시양태 82 내지 103 중 어느 한 실시양태에 있어서, 망막 신경절 세포 분화 배지가 B-27 보충제(포뮬러 080085-SA)를 포함하는 것인 방법.
105. 실시양태 104에 있어서, B-27 보충제(포뮬러 080085-SA)가 약 0.05-5.0%, 약 0.05-2.5% 또는 약 2%인 농도로 존재하는 것인 방법.
106. 실시양태 82 내지 105 중 어느 한 실시양태에 있어서, 망막 신경절 분화 배지가 글루타민 또는 글루타맥스™를 포함하는 것인 방법.
107. 실시양태 82 내지 106 중 어느 한 실시양태에 있어서, 망막 신경절 분화 배지가 레티노산을 포함하는 것인 방법.
108. 실시양태 107에 있어서, 레티노산이 약 1-50 mM, 약 5-40 mM, 약 10-30 mM, 또는 약 20 mM인 농도로 존재하는 것인 방법.
109. 실시양태 82 내지 106 중 어느 한 실시양태에 있어서, 세포를 망막 신경절 세포 분화 배지 중에서 약 7-60일 또는 약 14-35일 또는 약 24일 동안 배양하는 것인 방법.
110. 실시양태 53 내지 80 중 어느 한 실시양태에 있어서, 망막 신경절 전구체 세포가 배양물 중 50% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 또는 약 100%의 세포를 포함하는 것인 방법.
111. 실시양태 110에 있어서, 망막 신경절 전구체 세포가 마커: Math5, Brn3a, Brn3b 및 Isl1 중 하나 이상 또는 그들 모두를 발현하는 것인 방법.
112. 실시양태 111에 있어서, 90%, 94%, 96%, 98% 또는 99% 이상의 망막 신경절 전구체 세포가 Math5 및 임의적으로, Brn3a를 발현하는 것인 방법.
113. 실시양태 111 또는 112에 있어서, 망막 신경절 전구체 세포가 Pax6(-) 및 Rx1(-)인 것인 방법.
114. 실시양태 113에 있어서, 90%, 92% 또는 94% 이상의 망막 신경절 전구체 세포가 Pax6(-) 및 Rx1(-)인 것인 방법.
115. 실시양태 52 내지 80 중 어느 한 실시양태에 있어서, 망막 신경절 전구체 세포가 Brn3a, 신경미세섬유 및 Thy1 중 하나 이상 또는 그들 모두를 발현하는 것인 방법.
116. 실시양태 115에 있어서, 90%, 92%, 또는 94% 이상의 상기 망막 신경절 전구체 세포가 Brn3a 및 신경미세섬유를 발현하는 것인 방법.
117. 실시양태 115 또는 116에 있어서, 망막 신경절 전구체 세포가 Math5(-) 및/또는 Brn3b(-)인 것인 방법.
118. 실시양태 52 내지 80 중 어느 한 실시양태에 있어서, 망막 신경절 전구체 세포를 망막 신경절 세포로 분화시키는 단계를 추가로 포함하는 것인 방법.
119. 실시양태 52 내지 118 중 어느 한 실시양태의 방법에 따라 제조된 망막 신경절 전구체 세포 또는 망막 신경절 세포를 포함하는 조성물.
120. 망막 신경절 전구체 세포 또는 망막 신경절 세포를 포함하는 조성물.
121. 실시양태 119 또는 120에 있어서, 상기 망막 신경절 전구체 세포가 상기 조성물 중 50% 이상, 70% 이상, 75% 이상, 85% 이상, 95% 이상, 99% 이상 또는 약 100%의 세포를 포함하는 것인 조성물.
122. 실시양태 119 또는 120에 있어서, 상기 망막 신경절 세포가 상기 조성물 중 50% 이상, 60% 이상 또는 70% 이상의 세포를 포함하는 것인 조성물.
123. 실시양태 119 내지 122 중 어느 한 실시양태에 있어서, 망막 신경절 전구체 세포가 마커: Math5, Brn3a, Brn3b 및 Isl1 중 하나 이상 또는 그들 모두를 발현하는 것인 조성물.
124. 실시양태 123에 있어서, 90%, 94%, 96%, 98% 또는 99% 이상의 망막 신경절 전구체가 Math5 및 임의적으로, Brn3a를 발현하는 것인 조성물.
125. 실시양태 123 또는 124에 있어서, 망막 신경절 전구체 세포가 Pax6(-) 및 Rx1(-)인 것인 조성물.
126. 실시양태 125에 있어서, 90%, 92% 또는 94% 이상의 망막 신경절 전구체 세포가 Pax6(-) 및 Rx1(-)인 것인 조성물.
127. 실시양태 119 내지 122 중 어느 한 실시양태에 있어서, 망막 신경절 전구체 세포가 Brn3a, 신경미세섬유 및 Thy1 중 하나 이상 또는 그들 모두를 발현하는 것인 조성물.
128. 실시양태 127에 있어서, 90%, 92%, 또는 95% 이상의 망막 신경절 전구체 세포가 Brn3a 및 신경미세섬유를 발현하는 것인 조성물.
129. 실시양태 127 또는 128에 있어서, 망막 신경절 전구체 세포가 Math5(-) 및 Brn3b(-)인 것인 조성물.
130. 실시양태 119 내지 122 중 어느 한 실시양태에 있어서, 망막 신경절 세포가 Brn3a, 신경미세섬유 및 Tuj1 중 하나 이상 또는 그들 모두를 발현하는 것인 조성물.
131. 실시양태 119 내지 129 중 어느 한 실시양태에 있어서, 망막 신경절 전구체 세포가 냉동보존되는 것인 조성물.
132. 실시양태 131에 있어서, 해동 후, 약 80-90%의 망막 신경절 전구체 세포가 회복되는 것인 조성물.
133. 치료를 필요로 하는 개체에게 실시양태 119 내지 120 중 어느 한 실시양태의 조성물, 또는 해동 후, 실시양태 131 또는 132의 조성물을 투여하는 단계를 포함하는 것인, 치료를 필요로 하는 개체를 치료하는 방법.
134. 실시양태 133에 있어서, 조성물이 눈, 망막하 공간 또는 유리체내로 투여되는 것인 방법.
135. 실시양태 52 내지 80, 및 실시양태 82 내지 117 중 어느 한 실시양태에 있어서, 안구 영역 전구체 세포를 신경절 세포 배지 중에서 배양하는 단계가 (i) 안구 영역 전구체 세포를 단편화하여 세포 클러스터를 수득하는 단계, 및 (ii) 세포 클러스터를 저부착 조건하에서 플레이팅하여 구체를 형성하는 단계를 포함하는 것인 방법.
136. 실시양태 135에 있어서, 단계 (i)이 세포를 저부착 플레이트 상에서 배양하는 것을 포함하는 것인 방법.
137. 실시양태 135 또는 136에 있어서, 단편화가 기계적으로 또는 효소적으로 파괴시킴으로써 수행되는 것인 방법.
138. 실시양태 135 내지 137 중 어느 한 실시양태에 있어서, 세포를 망막 신경절 세포 분화 배지 중에서 배양하는 단계가 세포를 단일 세포로 해리시키고, 구체를 마트리겔™, 라미닌 또는 콜라겐 상에 플레이팅시키는 것을 포함하는 것인 방법.
139. 실시양태 138에 있어서, 해리된 세포를 라미닌 상에 플레이팅시키는 것을 포함하는 것인 방법.
140. 실시양태 138에 있어서, 해리된 세포를 폴리-D-리신/라미닌 코팅된 플레이트 상에 플레이팅시키는 것을 추가로 포함하는 것인 방법.
141. 실시양태 139 또는 140에 있어서, 해리된 세포가 10-40 세포/㎠의 밀도로 플레이팅되는 것인 방법.
하기는 본 발명을 예시하는 실시예이며, 이는 본 발명의 범주를 제한하는 것으로 간주되지 않아야 한다.
실시예
실시예
1. 만능
줄기 세포로부터의
R
G
전구체 세포 및
RG
세포 제조
1. 인간 배아 줄기 세포를 마트리겔™(BD 바이오사이언시스) 상의 mTESR1 배지(스템 셀 테크놀러지(Stem Cell Technology)) 중 피더세포 무함유 조건하에서 배양한다. 전면생장률이 80-90%가 되었을 때, 세포를 계대접종하거나, 냉동시켜야 한다. 줄기 세포의 계대접종은 효소적(예컨대, 디스파제) 또는 비효소적(예컨대, PBS 기반 세포 해리, 인비트로겐) 기술을 사용하여 수행한다.
2. 직접적인 분화 방법은 망막 뉴런/전구체의 생성을 위해 사용된다. 배아체 단계는 없다.
3. 0일째: 15-20%의 전면생장률로 세포 분화가 유도된다. 배지를 망막 유도(RI) 배지: 4.5 mg/ml D-글루코스, 100 유니트/ml의 페니실린, 100 ㎍/ml의 스트렙토마이신, 1% N2 보충제(인비트로겐)(0.1-2%), 0.2% B27 보충제(0.05-2%), 1X MEM 비필수 아미노산 용액, 50 ng/ml 노긴(10-500 ng/ml), 및 20 ㎍/ml 인간 인슐린(5-50 ㎍/ml)으로 보충된, DMEM/F12로 교체한다.
4. 1일째-4일째: 완전한 배지 교체를 매일 수행한다.
5. 5일째: 5일째 세포 배양물의 전면생장률이 80-90%가 된다. 배지를 신경 분화(ND) 배지: 4.5 mg/ml D-글루코스, 100 유니트/ml의 페니실린, 100 ㎍/ml의 스트렙토마이신, 1X 글루타맥스™, 1% N2 보충제(인비트로겐) (0.1-2%), 2% B27 보충제(0.5-2%), 1X MEM 비필수 아미노산 용액, 및 50 ng/ml 노긴(10-500 ㎍/ml)으로 보충된, 뉴로베이살™ 배지(라이프 테크놀러지스)로 교체한다.
6. 6일째-13일째: 세포를 ND 배지 중에 유지시킨다. 매 2일마다 배지를 교체한다. 세포 콜로니는 ND 배지 중에서 계속 성장한다. 가장자리에 있는 세포는 평평하고, 커지게 되는 반면, 중앙부에 위치하는 세포는 더욱 작아지고, 조밀한 세포 클러스터를 형성하게 된다. 10-11일째, 세포는 PAX6을 발현하기 시작하고, 12일째 Rx1 발현을 개시한다(도 1a). RT-PCR 분석 결과, Oct4 및 Nanog 발현 손실이 나타났다(도 1b). 13일째, 정량화된 유세포 분석법에 따르면, 90% 초과의 세포가 Pax6 및 Rx1을 공동 발현한다(도 2a). 99% 초과의 세포가 Otx2, 네스틴 및 Sox2를 발현한다(도 2b). 이러한 결과는 상기 세포가 안구 영역 전구체 세포가 되었다는 것을 나타내는 것이다.
7. 14일째-19일째: 15일째, 배지를 4.5 mg/ml D-글루코스, 100 유니트/ml의 페니실린, 100 ㎍/ml의 스트렙토마이신, 1X 글루타맥스™, 1% N2 보충제(0.1-2%), 2% B27 보충제(포뮬러 번호 080085-SA)(0.5-2%), 5 μM 포스콜린(1-20 μM), 10 ng/ml BDNF(1-200 ng/ml), 및 10 ng/ml CNTF (1-200 ng/ml)로 보충된 신경 기본 배지로 교체한다.
8. 20일째-35일째: 20일째, 성장 표면으로부터 세포를 들어 올리고, GC 배지 중에서 기계적으로 클러스터로 단편화시킨다. 세포 클러스터를 100 mm 초저 부착 배양 디쉬로 옮긴다. 세포 클러스터는 현탁 배양물 중에서 둥근 형태가 되고, 개별 구체를 형성한다. 배지를 매 3일마다 교체한다. 35일째, 실시간 RT-PCR 결과, Math5, Brn3a, Brn3b 및 Isl1 발현이 강력하게 상향조절된 것으로 나타났다(도 3a). 유세포 분석법 결과, >99% 세포가 전사 인자 Math5 및 Brn3a를 발현한 것으로 나타났다. 약 94% Math5 양성 세포는 Pax6에 대해 음성으로 염색되었다(도 3b).
9. 36일째-0일째: 신경구를 GC 배지 중에서 유지시키고, 배지를 약 매 3-4일마다 교체한다. 60일째, 실시간 RT-PCR 결과, Brn3a의 발현이 계속되는 것으로 나타났다. Math5 및 Brn3b의 발현 수준은 현저히 하향조절되었다(도 4). 유세포 분석법 결과, 95.3%의 세포가 Brn3a 및 신경미세섬유를 공동 발현한 것으로 나타났다.
10. RG 전구체 세포의 RG 세포로의 분화:
a. 어큐타제® 세포 해리 완충제를 사용하여 세포를 단일 세포로 해리시킨다. 세포를 RGC 분화 배지: 4.5 mg/ml D-글루코스, 100 유니트/ml의 페니실린, 100 ㎍/ml의 스트렙토마이신, 1X 글루타맥스™, 2% B27 보충제(포뮬러 번호 080085-SA, GC 배지와 동일), 5 μM 포스콜린, 10 ng/ml BDNF, 10 ng/ml CNTF, 100 ng/ml cAMP, 1-50 μM DAPT, 2 μM 레티노산 및 20 ㎍/ml 인간 인슐린으로 보충된 신경 기본 배지 중에서 10-40/㎠의 밀도로 폴리-D-리신/라미닌 코팅된 플레이트 상에 플레이팅한다. 배지 중 절반을 매 2일마다 교체하였다.
b. 2주 경과 후, 약 72%의 세포가 Thy1에 대하여 양성으로 염색되었다(도 5). 세포는 수상 돌기 및 축삭돌기를 가졌다(도 6a). 면역염색 결과, Brn3a, 신경미세섬유 및 Tuj1의 발현이 나타났다(도 6b).
실시예
2. (레이저
광응고술을
사용하여 이루어진) 실험상의 녹내장 모델에서의
RG
전구체 세포
도 7에 개략적으로 나타낸 바와 같이, 실험상의 녹내장 동물 모델을 사용하여 생체내에서의 RG 전구체 세포의 효과를 연구하였다. 상기 모델 시스템에서, 3개월된 브라운 노르웨이(Brown Norway) 수컷 래트에서 섬유주 레이저 광응고술에 의해 만성적인 안압(IOP) 상승을 유도하였다. 다음날, 5 ㎕의 PBS 중에 현탁된 2x105개의 RG(조기) 전구체 세포를 유리체강 내로 주사하였다. 대조군 안구에는 PBS를 주사하였다. 모든 래트는 (처리 2주 전부터 처리 후 5주째까지) 주 2회에 걸쳐 토노랩(TonoLab)에 의해 암기 및 명기 IOP 측정을 받았다. 처리 1주 전부터 처리 후 5주째까지 물 중 사이클로스포린 A를 투여하였다. 처리 후 5주째, Rbpms 면역조직화학법을 사용하여 망막 신경절(RG) 세포의 국소 해부학적 정량화를 수행하였다. 대조군 눈에서의 평균 세포 손실은 27.3% RG 세포인 반면, 세포 처리군에서는 평균 13.5%의, 유의적으로 더 적은 RG 세포 사멸이 이루어졌다(도 8). 이러한 결과는 녹내장 래트 모델에서의 RG 전구체 세포 처리에 의한 RG 세포 사멸 구제를 제안한다.
실시예
3: 인간
RG
전구체 세포 및
RG
세포의 냉동보존
조기 RG 전구체 세포(실시예 1에서 단계 8) 및 후기 RG 전구체 세포(실시예 2에서 단계 9)를 신경구로서 동물 무함유 냉동보존 완충제, 예컨대, 크라이오스토르 CS10, 또는 또 다른 냉동보존 완충제, 예컨대, 90% FBS 및 10% DMSO 중에서 냉동시킬 수 있다. RG 세포 또한 상기 완충제 중에서 냉동보존시킬 수 있다.
실시예
4: 실험상의 녹내장 모델(
마이크로비드
(MB) 주사)에서의
hESC
및/또는 iPSC로부터 유래된 RGCP의 이식
hESC
및
iPSC로부터의
RGCP의
생성
hESC 세포주 GFP-H1(WA01 하에 NIH 등록, 생체내에서 용이한 확인을 위해 GFP 발현), 및 iPSC 세포주 HA1(게놈 통합 없이 mRNA에 의해 생성된 것31)을 앞서 보고된 바와 같이 유지시킨다.31 본원에 기술된 바와 같이 통상적으로, 및 계속해서 수행되는 프로세스에서, 상기 세포를 먼저 EFP로 분화시킨 후, 이어서, 마트리겔 상에 EFP를 리플레이팅하고, 본원에 기술된 바와 같은 조건하에서 배양하여 상이한 발생 단계에서 RGCP를 생성한다. 분화 프로세스 동안, EFP 유전자(Pax6, Rx1, 네스틴 and Sox2)의 발현을 모니터링한다. 생체내 이식 이전에, 후기 단계의 RGCP(신경미세섬유+ Brn3a+ Math5-)를 수집하고, 어큐타제를 사용하여 단일 세포 현탁액으로 해리시킨다.
녹내장 마우스로의
RGCP
이식
성체 C57BL/6J 마우스는 (대조군으로서) PBS를, 또는 고안압증(녹내장)를 유도하기 위해 앞서 기술된 바와 같은 마이크로비드의 전안방 주사를 맞았다.29 생착된 RGCP의 생존이 녹내장 질환 프로세스에 의해 영향을 받지 여부에 관하여 다루기 위해, IOP가 정상인, PBS 주사를 맞은 대조군을 수혜자 마우스 군에 첨가하였다.
PBS 또는 마이크로비드 주사 후 7일이 경과하였을 때, GFP-hESC 또는 HA1-iPSC 유래 RGCP(100,000개의 세포/㎕) 또는 비히클 대조군 용액을 정상 IOP (PBS 주사를 맞은) 및 녹내장(마이크로비드 주사를 맞은) 마우스, 둘 모두에 유리체내로 주사하였다. 질환 증상의 소견을 보이는 환자의 임상 소견에 맞게 잘 조정하기 위해 이식을 위해 상기 시점을 선택하였다. 다른 보고와 일치하여,9 예비 연구에서는 이식된 세포가 면역 특권 부위인 것으로 간주되는 마우스 눈에서 면역 억제인자의 부재하에서 이식 후 최대 8주까지 생존하는 것으로 관찰되었다(도 13, 14, 및 16).
망막에서의 RGC의 전기적 활성을 모니터링하는 pSTR을 4 및 8주째되는 시점에 측정하였으며, 여기서, 첫번째 측정은 기준선 값을 얻기 위해 마이크로비드 주사 전 1-2일째에 수행하였다. 4 및 8주째 pSTR 검사를 사용하여 대조군 및 녹내장 마우스를 분석하였다.
이식된 RGCP의 치료학적 효능을 평가하는 데 사용된 또 다른 검사는 시운동성 반사(OKR)이다. OKR은 눈 및 머리 움직임에 따른 드리프팅 스트라이프 패턴을 추적함으로써 시력 및 대비 감도를 측정한다. 녹내장 마우스는 OKR 검정에서 시력 손상 없이 현저한 시각적 대비 감도 감소를 보인다. 이러한 관찰 결과는 인간 환자에서 관찰되는 것과 일치한다.37 ,38 기준선 OKR은 마이크로비드 주사 전 1-2일째에 기록하였고, 시기능 및 망막 형태 변화를 계속 평가하기 위해 OKR을 PBS 또는 마이크로비드 주사 후 8주째에 평가하였다.
이식된 세포 생존을 유지시키는 데 면역 억제가 필요한지 여부를 시험하기 위해, 면역 억제인자 사이클로스포린-A로 처리한 마우스를 연구한다. 상기 마우스 군은 이식 전 1일째를 시작으로 하여 희생될 때까지 식수 중 사이클로스포린-A로 매일 처리하였다.
이식된 RGCP의 치료학적 효능을 평가하는 데 사용하고자 하는 또 다른 검사는 시각 유발 전위(VEP)이다. VEP는 시각적 자극에 대한 반응으로 피질에 의해 생성되는 총 전기 신호를 측정한다. 녹내장 마우스는 VEP에서 연장된 N1 잠복기 및 감소된 P1-N1 진폭을 보인다. 이러한 관찰 결과는 인간 환자에서 관찰되는 것과 일치한다.37,38 기준선 VEP는 마이크로비드 주사 전 1-2일째에 기록한다.
모든 실험군에서, 시기능 및 망막 형태 변화를 계속 평가하기 위해 VEP 및 SD-OCT를 PBS 또는 마이크로비드 주사 후 4, 8, 및 12주째에 평가한다. PBS 또는 마이크로비드 주사 후 12주째까지 pSTR 및 OKR을 분석한다. PBS 또는 마이크로비드 주사 후 4, 8, 및 12주째에, 마지막 VEP, OKR, pSTR, 및 SD-OCT 평가 후, 마우스를 12주째에 희생시킨다. 망막 및 시신경 절편을 앞서 기술된 바와 같이 제조한다.29 망막 절편을 RGC 특이 마커, 예컨대, Tuj1 또는 Brn3b에 대한 항체로 면역표지하고, 핵 마커 DAPI로 대조염색하여 숙주 RGC 형태학적 성질 및 망막 층 구조를 밝혀낸다. 살아있는 동물에서 SD-OCT에 의해 종양 형성을 모니터링할 뿐만 아니라, 망막 절편에서도 검사한다. 시신경 절편에서 기술된 바와 같이29 축삭돌기 계수를 수행하여 RGCP 이식 후 축삭돌기 변성/보호를 측정한다.
IOP가 상승된 마우스 및 상승되지 않은 마우스(PBS 주사 대 마이크로비드 주사) 상기 후기 시점에 이식된 세포의 생존을 평가하고, 또한 면역 억제를 받은, 또는 그렇지 않은 마우스 군 사이를 비교한다.
추가로, 망막 형태학적 성질을 모니터링하는 데, 잠재적인 종양 형성 뿐만 아니라, 신경절 세포층(GCL) 및 신경 섬유층(NFL) 두께 측정을 포함하는, 임상적으로 적용가능한 비침습성 영상화 기술인 스펙트럼 도메인 광 간섭성 단층촬영기술(SD-OCT)이 사용된다. 다른 연구에서는 녹내장 마우스에서 (GCL 및 NFL을 포함하는) 신경절 세포 복합체(GCC) 층의 얇아지는 것을 정량화하는 데 SD-OCT가 성공적으로 적용되었다고 보고되었고30; 이 관찰 결과는 녹내장 환자에서 관찰되는 것과 일치한다.
통계학적 분석
데이터는 평균 ± 표준 편차로 제시되어 있고, 윈도우스용 그래프패드 프리즘 5.01(GraphPad Prism 5.01 for Windows)(그래프패드 소프트웨어 인크.(GraphPad Software Inc.))을 이용하여 분석된다. 통계학적 분석에 쌍별 ANOVA 및 만-위트니(Mann-Whitney)가 사용된다. 차이는 p < 0.05로 유의적인 것으로 간주되어야 한다.
결과
이전 실시예에서 입증된 바와 같이, 본 개시내용에 따라, 인간 PSC를 강력하게 분화시켜 고도로 균질성인(>95%) RGCP 집단을 생성할 수 있는 신규한 방법이 개발되었다. 또한, 상기 RGCP가 녹내장 마우스 내로 이식되었을 때, 면역조직화학법, pSTR 및 OKR에 의해 측정된 바와 같이, RGC 생존(도 13a) 및 기능(도 14a-d)은 유의적으로 개선된 것이 관찰되었다. 상기 데이터는 이식된 RGCP가 녹내장에서 시력을 보존시킬 수 있다는 것을 시사하는 것이다.
실시예
5:
RGCP
이식 후
RGC
유사 세포의 특징 규명
실시예 5는 (1) 녹내장 마우스 망막 내로의 이식 후, RGCP의 RGC 유사 세포로의 분화율(%)을 조사하고, (2) 면역조직화학법 및 RNA 서열분석(RNA-seq)을 이용하는, 인간 ESC 및 iPSC 유래 RGC 유사 세포의 형태학적 및 분자적 특성을 주사하고, 및 (3) 상기 세포의 유전자 프로파일을 분석한다.
녹내장 마우스로의
RGCP
이식 및
RGC
유사 세포로의
RGCP
분화율(
%
) 정량화
실시예 1 및 4에 기술된 바와 같이 GFP+ hESC 또는 iPSC로부터 RGCP를 생성한다. 성체 C57BL/6J 마우스는 상기 녹내장 모델에서의 고안압증 유도를 위해 전안방에 마이크로비드 주사를 맞는다.29 마이크로비드 주사 후 7일째, 사이클로스포린-A로 매일 처리하거나, 또는 처리하지 않으면서, GFP-hESC 또는 HA1-iPSC 유래 RGCP(100,000개의 세포/㎕)를 녹내장 마우스에 유리체내로 주사한다. 예비 분석에서는 사이클로스포린-A 부재하에서 RGCP 생존 및 분화에 있어서 어떤 이상도 검출되지 않았지만, 세포의 표현형 및 트랜스크립톰 비교는 면역 억제인자가 생착된 RGCP에 미치는 효과에 관한 추가 정보를 제공한다. RGCP 분화를 정량적으로 평가하기 위해, 이식 후 3주째 망막 플랫 마운트를 수집하고, RGC 특이 마커, 예컨대, Brn3b 및 Tuj1에 대해 면역표지한다. 생착된 RGCP는 GFP 발현 또는 인간 특이적 미토콘드리아 항체에 의해 확인된다. 생착된 세포(GFP+) 및 RGC 유사 세포(GFP+/Brn3b+)를 각각 계수하고, RGC 유사 세포(GFP+/Brn3b+)가 된 생착된 RGCP의 비율(%)을 계산한다. 기술된 바와 같이28 ,39, 다른 망막 세포 마커(예컨대, 아마크린 세포, 양극 세포, 광수용기, 및 뮬러(Muller) 세포)에 대한 면역검출 또한 수행하여 생착된 RGCP가 다른 망막 세포 유형으로 발생하였는지 여부를 측정할 수 있다. 시냅스 전 및 시냅스 후 마커, 예컨대, 시냅토태그민, PSD-95, GluR2/3의 면역표지 또한 수행할 수 있고, 시냅스 전 마커(예컨대, 시냅토태그민) 및 시냅스 후 마커(예컨대, PSC95)의 공동 국재화는 기능성 시냅스가 형성되었음을 제안하는 것이다.40 , 41
RGC
분화의
게놈와이드
사인의 확인
생착된 RGCP를 FACS를 사용하여 그의 GFP 발현에 기초하여 (세포 분화를 허용하기 위해) 이식 후 3주째 마우스 망막으로부터 단리시킨다. 전체 RNA를 단리된 GFP+ RGCP로부터, 그뿐만 아니라, 배양된 EFP(Pax6+, Rx1+, 네스틴+ 및 Sox2+ 발현에 의해 확인) 및 RGCP (신경미세섬유+/Brn3a+/Math5-)로부터 추출한다. 4개의 주사맞은 망막으로부터 쉽게 단리시킬 수 있는, ~40,000개의 생착된 세포가 상기 분석에 필요한 양의 RNA를 제공하는 데 충분하다. 간략하면, 일루미나(Illumina) Truseq 키트 v2를 사용하여 RNA-Seq를 위한 라이브러리를 생성하고, 일루미나 HiSeq로 서열분석하였다. 서열을 인간 트랜스크립톰에 대해 정렬하여 정렬된 BAM 파일을 작성하고, 커프링크스(Cufflinks) 알고리즘을 이용하여 공지된 유전자 및 전사체를 정량화한다. 유전자 주해와 함께, 유전자 및 공지 전사체의 차별적인 발현을 측정한다. GSEA 알고리즘을 사용하는 유전자 집단 농축도 분석(Gene Set Enrichment Analysis) 및 인제뉴이티 경로 분석(Ingenuity Pathway Analysis)을 수행한다. 관심의 대상이 되는 후보 전사체를 qPCR에 의해 확인한다. 생착된 RGCP, 및 ESC 및 iPSC 유래 배양물로부터 직접 채취된 EFP 및 RGCP로부터 얻은 데이터를 비교한다. 세포가 EFP에서 RGCP로 분화됨에 따라, 및 또한 이식된 RGCP의 분화에 의해 생체내에서 생산된 RGC 유사 세포에서, RGC 계통 아이덴티티에 상응하는 유전자 발현(예컨대, POU, Islet1, Islet2, Thy1.1)42을 모니터링한다. 예컨대, 광수용기 특이 마커와 같은, 다른 망막 세포 유전자의 발현 또한 RGCP 및 RGC 유사 세포에서 모니터링한다.
통계학적 분석
데이터는 평균 ± 표준 편차로 제시되어 있고, 윈도우스용 그래프패드 프리즘 5.01(그래프패드 소프트웨어 인크.)을 이용하여 분석된다. 통계학적 분석에 쌍별 ANOVA 및 만-위트니가 사용된다. 차이는 p < 0.05로 유의적인 것으로 간주되어야 한다.
실시예
6:
RGCP
이식
실시예 6는 RGCP의 이식이 시력 상실을 역전시키는지 또는 이식된 세포의 성숙한 RGC로의 분화에 의한 기능, 및 뇌로 연결되는 시신경으로의 긴 축삭돌기 연장을 회복시키는지 여부를 조사한다.
시신경 압박 손상된 마우스로의
RGCP
이식
실시예 1 및 4에 기술된 바와 같이 GFP+ hESC 또는 iPSC로부터 RGCP를 생성하였다. GFP+ hESC-RGCP는 그의 GFP 발현에 기인하여 이식 후, hESC-RGCP의 운명을 추적하는 데 더 쉽기 때문에 GFP+ hESC-RGCP를 사용하였다. 성체 C57BL/6J 마우스는 앞서 기술된 바와 같이 시신경 압박 손상되었고, 이로써, 모든 시신경 축삭돌기는 완전히 손상된다.22 손상 후 7일째, GFP+ hESC-RGCP(100,000개의 세포/㎕) 또는 비히클 대조군 용액을 상기 마우스 유리체내에 주사하였다. 손상 후 8일째, 마우스를 희생시켰다.
RGC 생존, 분화, 신경 성장의 정량화를 위해 망막 플랫 마운트 및 종축 시신경 절편을 하기와 같이 제조하였다: (1) RGC 생존 및 분화를 분석하기 위해, 망막 플랫 마운트를 Tuj1로 면역표지하여 내인성(숙주) 및 신생(GFP+) RGC를 확인하였다. 생존 숙주 RGC(오직 Tuj1+만)의 개수 및 새로 생성된 RGC(GFP+/Tuj1+)의 개수를 기록하였고; (GFP+/Tuj1+ 세포를 계수된 GFP+ 세포의 총 개수로 나누어) RGC 마커 Tuj1을 발현하는 이식된 (GFP+) 세포의 비율(%)을 계산하였다. 생착된 RGCP가 추가의 세포 유형을 발생시켰는지 여부를 측정하기 위해 다른 망막 세포 마커에 대한 면역검출 또한 수행하였다; 그리고, (2) 축삭돌기 생존 및 재성장을 평가하기 위해, 종축 시신경 절편을 신경미세섬유 단백질에 대한 1차 항체로 염색하여 내인성 축삭돌기를 나타낸 반면, 신생 축삭돌기는 GFP로 표지하여 확인하였다.
숙주 축삭돌기는 모두 손상 후 4주째까지 압부 부위 너머까지 손상되고, 변성되고, 오직 재생 축삭돌기만이 압박 부위 뒤에서 관찰될 것으로 예상된다. 이를 위해, 종축 신경 절편에서 신생 GFP+ 축삭돌기의 개수 및 그에 의한 이동 거리를 정량화하였다. 신생 축삭돌기가 뇌 중의 중추 표적에 도달하였는지 여부를 측정하기 위해, 마우스 뇌 절편을 수집하고; 시신경의 시삭 및 중추 표적 (외측 슬상핵 및 상구 포함)에서 관찰되는 GFP+ 축삭돌기 개수를 기록한다. 또한, 뇌 절편에서 시냅스 마커, 예컨대, 시냅토피신 및 PSD95에 대한 면역표시를 수행하여 GFP+ 축삭돌기가 시냅스를 발생시키고, 시냅스 전 마커를 발현하였는지 여부를 측정하였다.
다른 마우스는 손상 후 4, 8, 및 12주째에 희생시킨다. 손상 전 1-2일째 및 희생 전에 VEP, pSTR, 및 OKR을 기록하여 RGCP 이식이 가지는 잠재적인 이점을 평가한다. SD-OCT 또한 수행하여 살아있는 마우스에서 망막 형태학적 성질을 모니터링한다.
통계학적 분석
데이터는 평균 ± 표준 편차로 제시되어 있고, 윈도우스용 그래프패드 프리즘 5.01(그래프패드 소프트웨어 인크.)을 이용하여 분석된다. 통계학적 분석에 쌍별 ANOVA 및 만-위트니가 사용된다. 차이는 p < 0.05로 유의적인 것으로 간주되어야 한다.
결과
시신경 손상 후 3주째, GFP+ 세포는 숙주 망막을 재증식시키고, 긴 신경돌기를 연장시켰다. 이식된 세포 중 거의 모두(>95%)가 Tuj1+ RGC로 분화되었다(도 16a-c). 공초점 현미경법 및 광 시트 현미경법, 둘 모두를 이용하였을 때, 시냅스 전 마커 및 시냅스 후 마커의 공동 국재화에 의해 입증되는 바와 같이, 생착된 RGCP가 신경절 세포층으로 통합되었고(도 16d-e), 기능성 시냅스를 발생시킨 것으로 관찰되었다(도 16f-j). 본 데이터는 hESC 유래 RGCP가 시신경이 손상된 마우스 내로의 이식 후 RGC 유사 세포로 분화될 수 있고, 숙주 망막으로 통합될 수 있으며, 기능성 시냅스를 발생시킬 수 있고, 손실된 세포를 대체할 수 있다는 것을 입증한다.
결론
순수하고, 재생가능한, 인간 망막 신경절 세포 전구체(RGCP) 집단을 연구 및 요법에 제공하는 데 있어서 그의 한계를 극복하기 위해, 인간 만능 줄기 세포(PSC)를 망막 뉴런으로 강력하게 분화시키기 위한 정의된 방법이 개발되었다. 본 방법은 고도로 균질성인(>95%) RGCP 집단을 생성하기 위해 다중의 hESC 및 iPSC 세포주(배반포 또는 단일 난할구로부터 hESC 세포주 5개; 에피솜 벡터 또는 mRNA 재프로그래밍에 의해 수득된 6 iPSC 6개)를 사용하여 수행되었다. 본 방법은 상기 모든 세포주에서 망막 분화 프로세스를 동시 발생시킬 수 있고, 이는 일관되게 PSC의 안구 영역 전구체(EFP, 도 2)16 -18, 조기 RGCP(Math5+, 도 3b 및 4)19 -21, 및 후기 RGCP(Math5-/Thy1.1+ 도 3b, 4 및 5)의 단계적인 분화를 유도할 수 있었고, 이는 시험관내 및 생체내에서 성숙한 RGC의 생성을 유도하였다(도 13a, 14a-b, 및 16a-j).
상기 세포의 치료학적 잠재능을 시험하는 예비 연구에서, 녹내장이 유도된 마우스의 유리체 내에 GFP+ hESC-RGCP를 주사하였다. RGCP 이식을 받은 녹내장 마우스에서, RGC의 척도인 양성 암소시 임계 반응(pSTR: positive scotopic threshold response)의 진폭 증가(도 14a-c)과 함께, 이를 동반하여, RGC 생존이 유의적으로 개선된 것이 관찰되었다(도 13a, 하단 패널).
중증 시각 신경병증에서의 RGCP의 치료학적 잠재능을 추가로 확립하기 위해, 시신경 압박 손상 모델에서의 손실된 RGC를 대체할 수 있고, 신생 축삭돌기를 형성할 수 있는 상기 세포의 능력을 분석하였다. 본 결과를 통해 세포 주사 후 3주째, 이식된 세포 모두 Tuj1+ RGC로 분화되었고, 신생 신경돌기의 강력한 이동, 통합, 및 형성을 보인 것으로 나타났다(도 16a-j).
상기의 조합된 결과는 인간 PSC-RGCP가 녹내장 요법에 사용될 수 있고, 이는 또한 다른 형태의 시각 신경병증 치료에 사용될 수 있다는 것을 시사한다.
참고 문헌