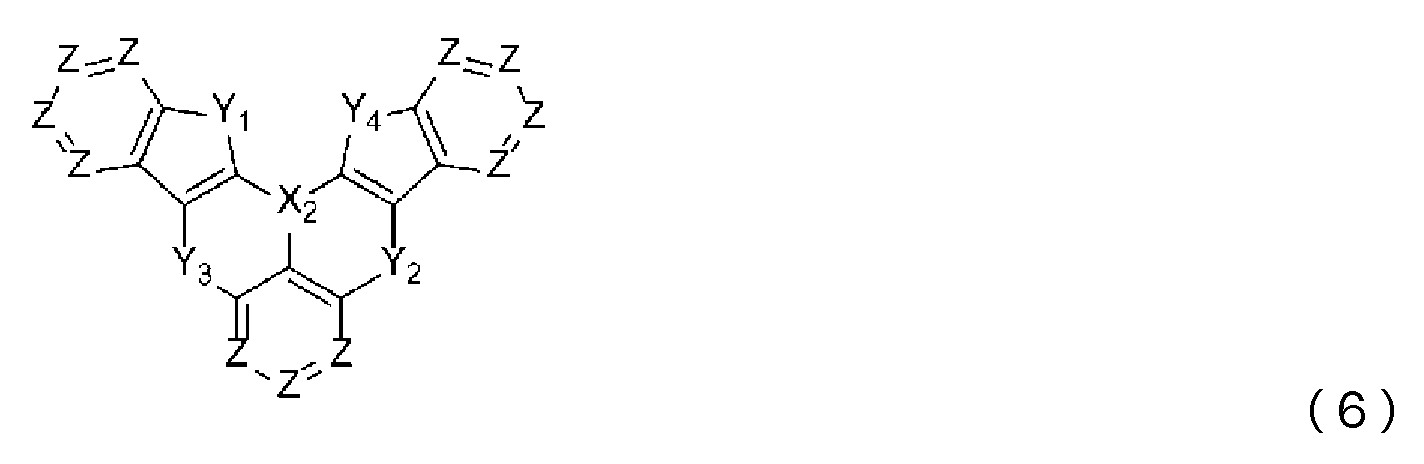KR20230051663A - 유기 일렉트로루미네센스 소자 - Google Patents
유기 일렉트로루미네센스 소자 Download PDFInfo
- Publication number
- KR20230051663A KR20230051663A KR1020237004531A KR20237004531A KR20230051663A KR 20230051663 A KR20230051663 A KR 20230051663A KR 1020237004531 A KR1020237004531 A KR 1020237004531A KR 20237004531 A KR20237004531 A KR 20237004531A KR 20230051663 A KR20230051663 A KR 20230051663A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- unsubstituted
- substituted
- substituent
- organic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/54—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to two or three six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/027—Organoboranes and organoborohydrides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
- H10K50/12—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers comprising dopants
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
- H10K50/156—Hole transporting layers comprising a multilayered structure
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/05—Isotopically modified compounds, e.g. labelled
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1014—Carbocyclic compounds bridged by heteroatoms, e.g. N, P, Si or B
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/658—Organoboranes
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
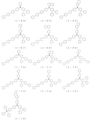
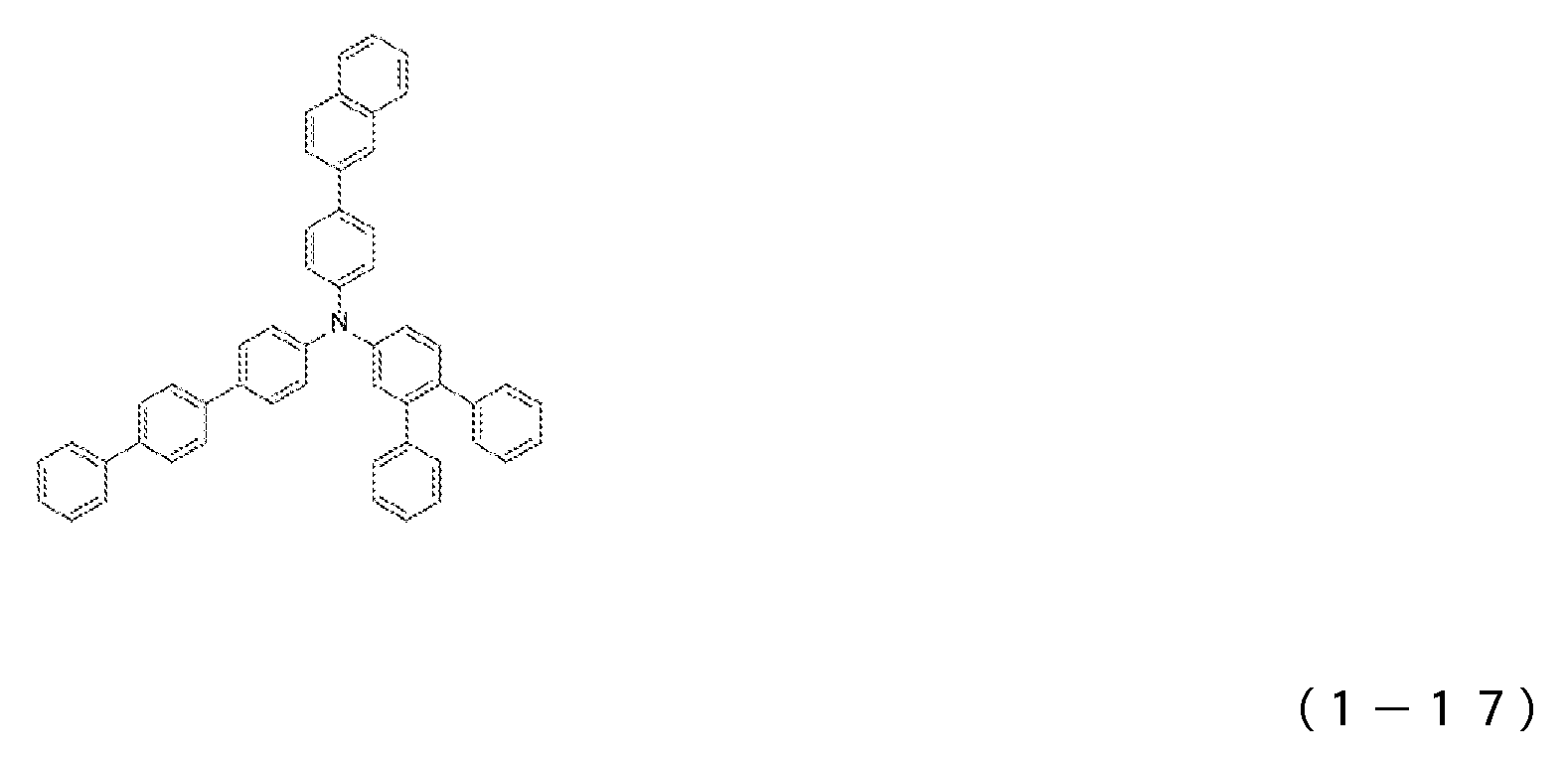
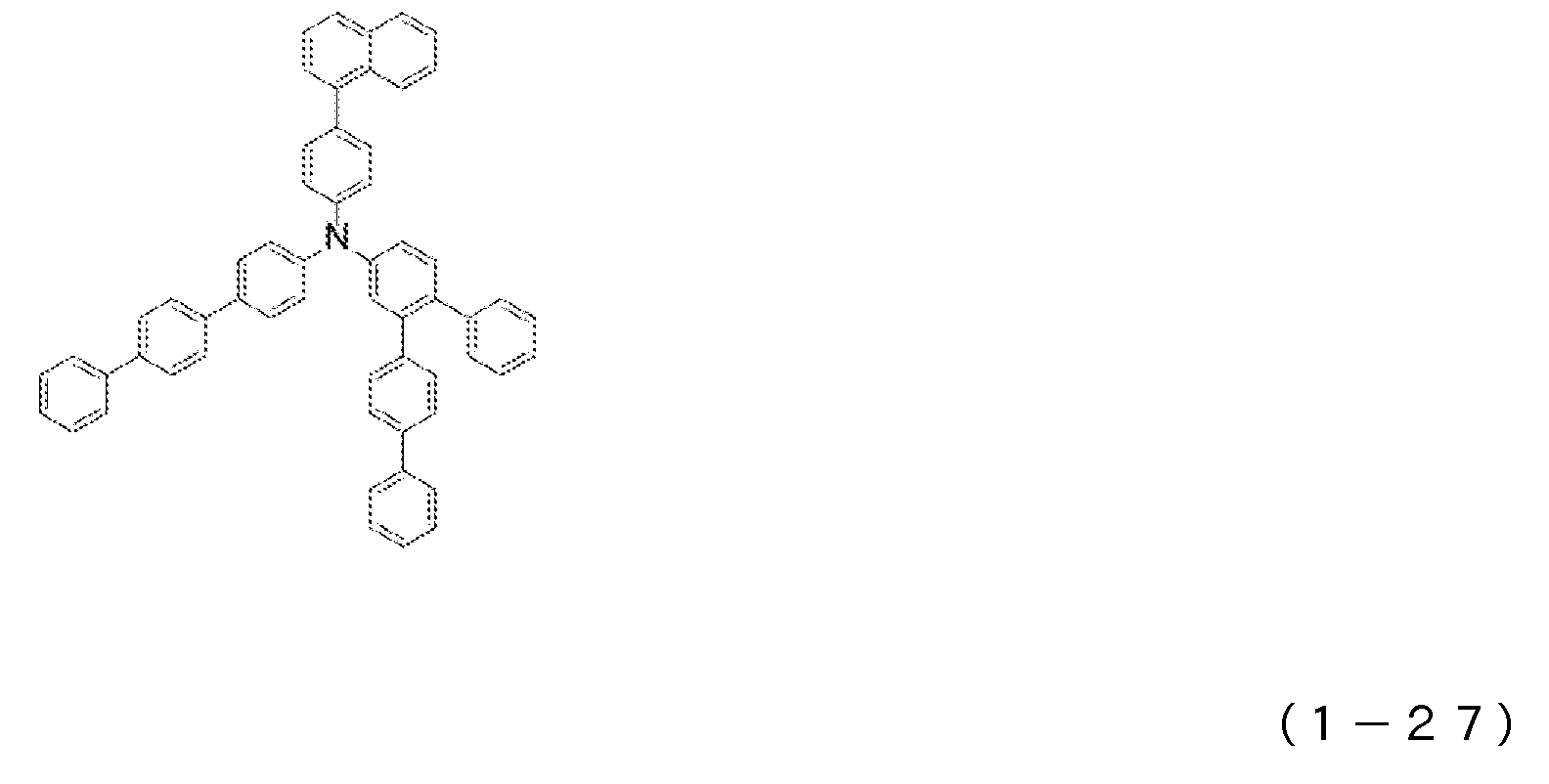
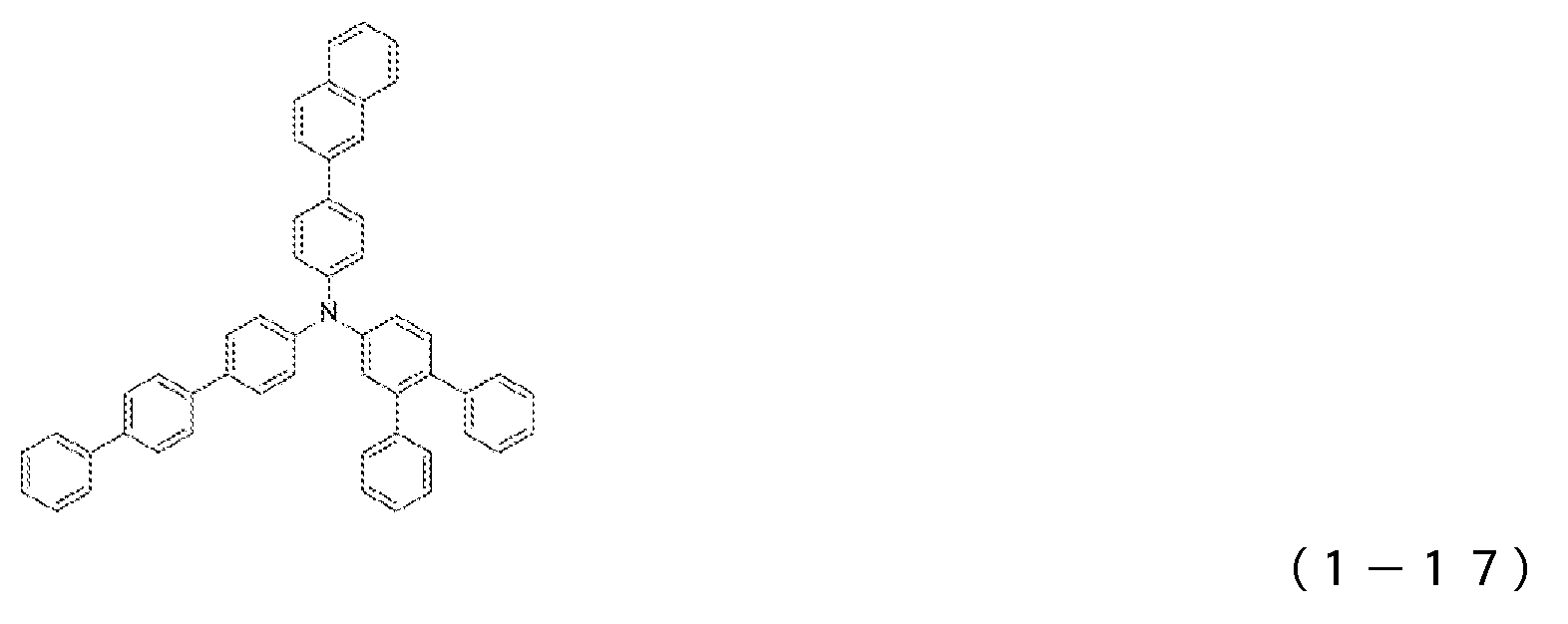
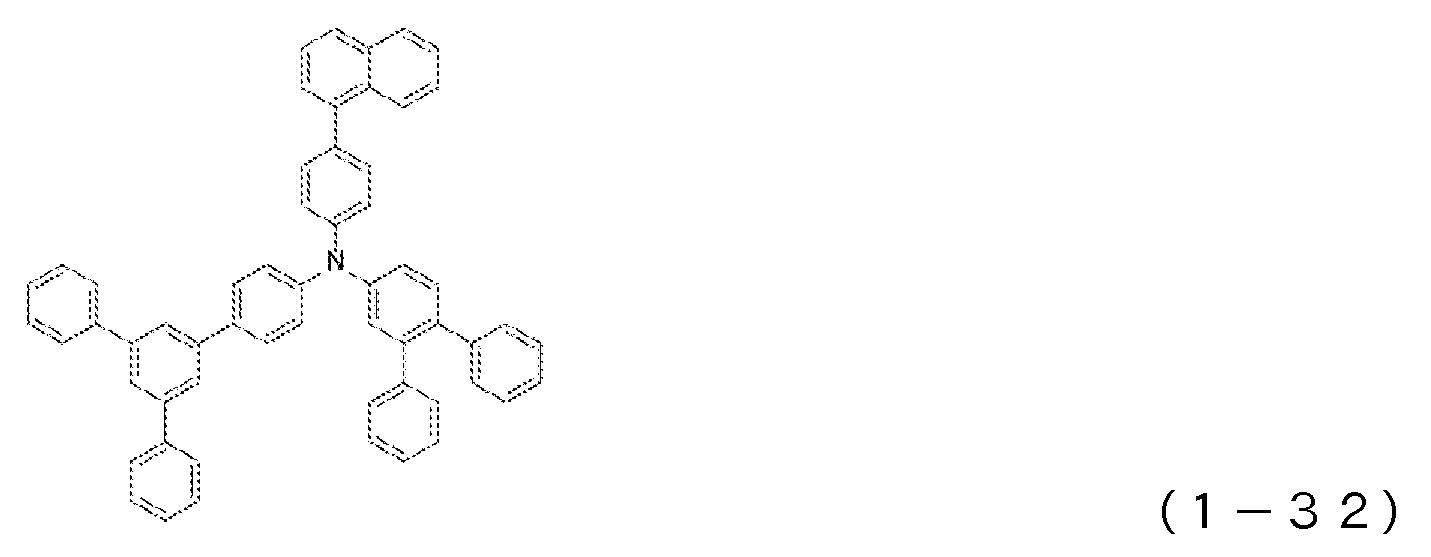
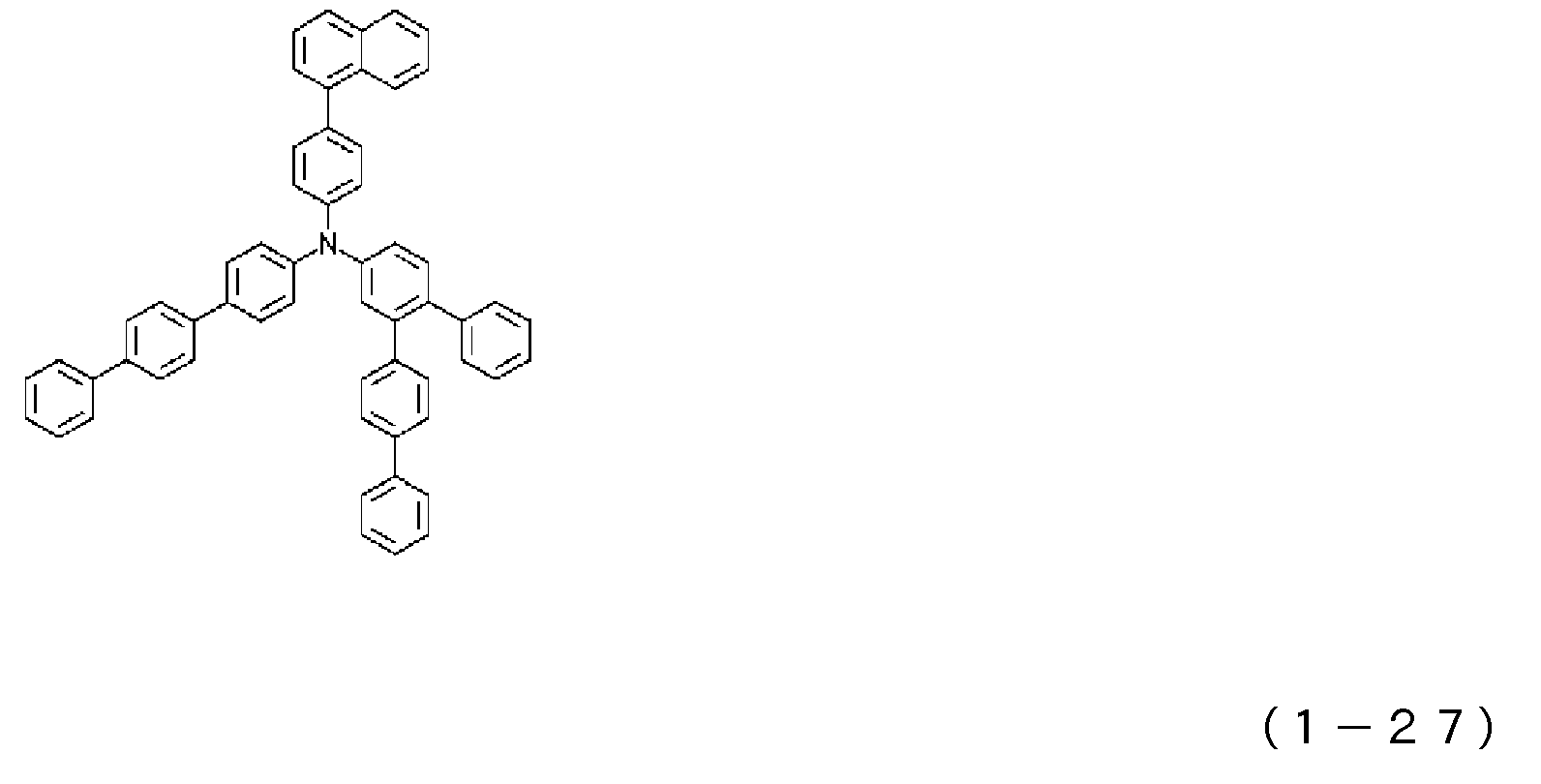
도 2는 일반식 (1)로 표시되는 아릴아민 화합물의 예시로서, 화합물 (1-16) 내지 (1-27)의 구조식을 도시하는 도면이다.
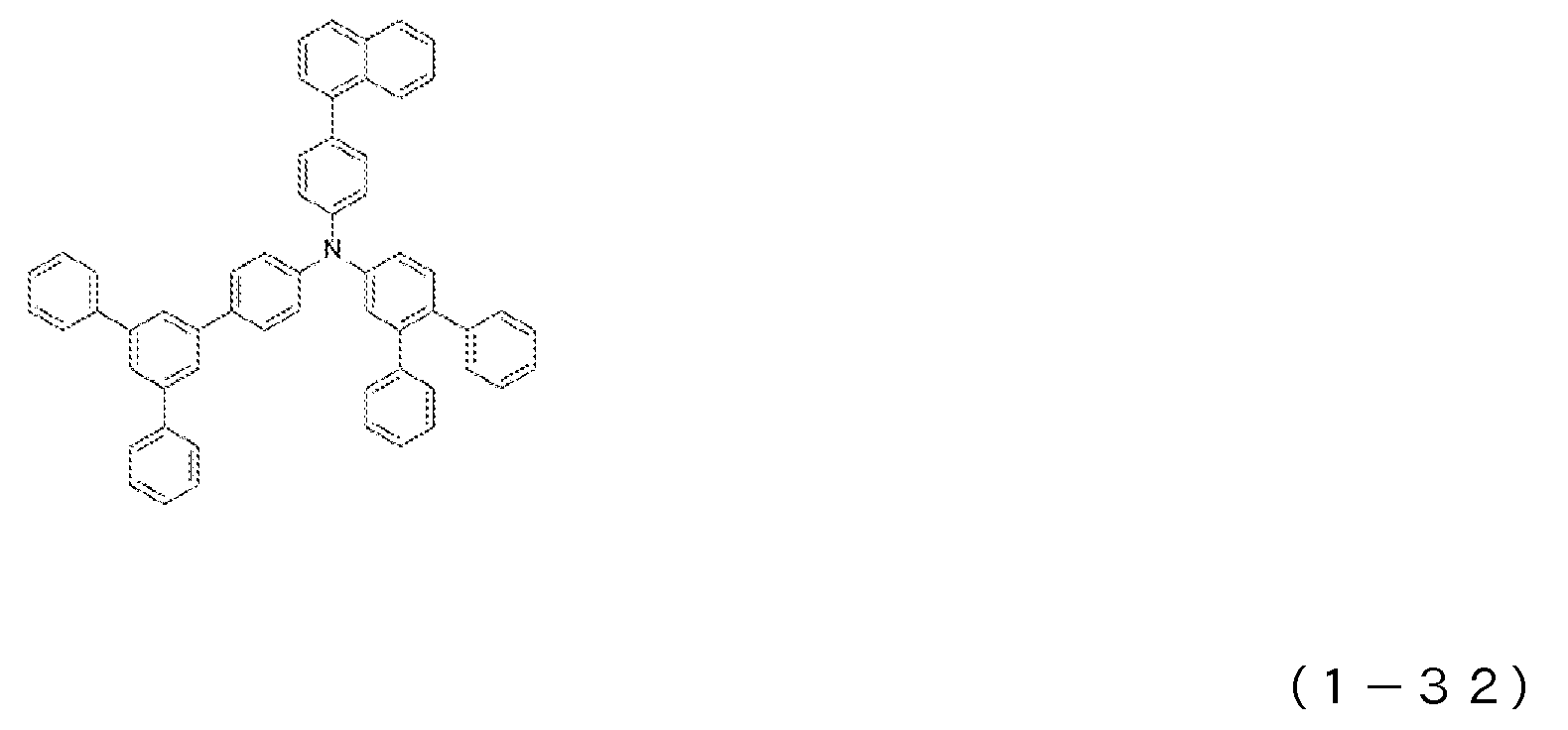
도 3은 일반식 (1)로 표시되는 아릴아민 화합물의 예시로서, 화합물 (1-28) 내지 (1-39)의 구조식을 도시하는 도면이다.
도 4는 일반식 (1)로 표시되는 아릴아민 화합물의 예시로서, 화합물 (1-40) 내지 (1-51)의 구조식을 도시하는 도면이다.
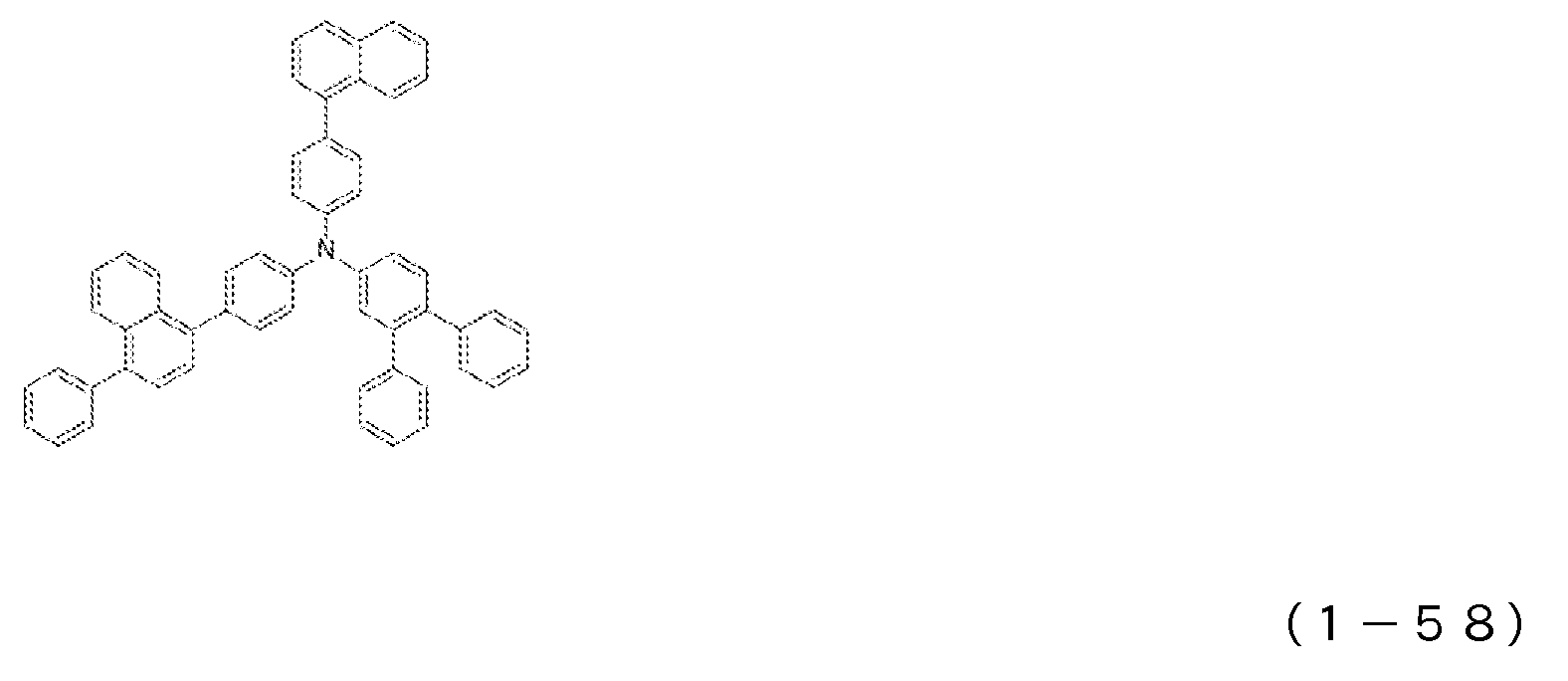
도 5는 일반식 (1)로 표시되는 아릴아민 화합물의 예시로서, 화합물 (1-52) 내지 (1-63)의 구조식을 도시하는 도면이다.
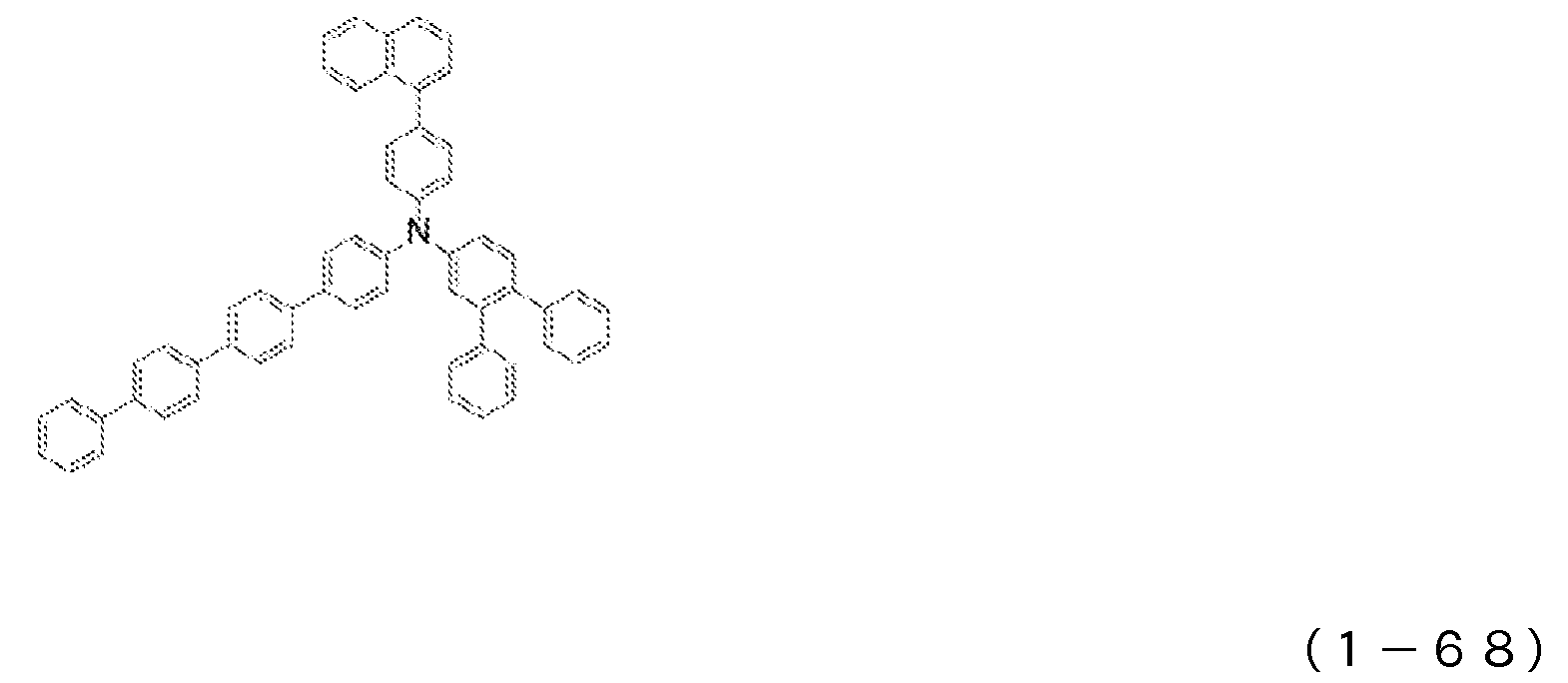
도 6은 일반식 (1)로 표시되는 아릴아민 화합물의 예시로서, 화합물 (1-64) 내지 (1-76)의 구조식을 도시하는 도면이다.
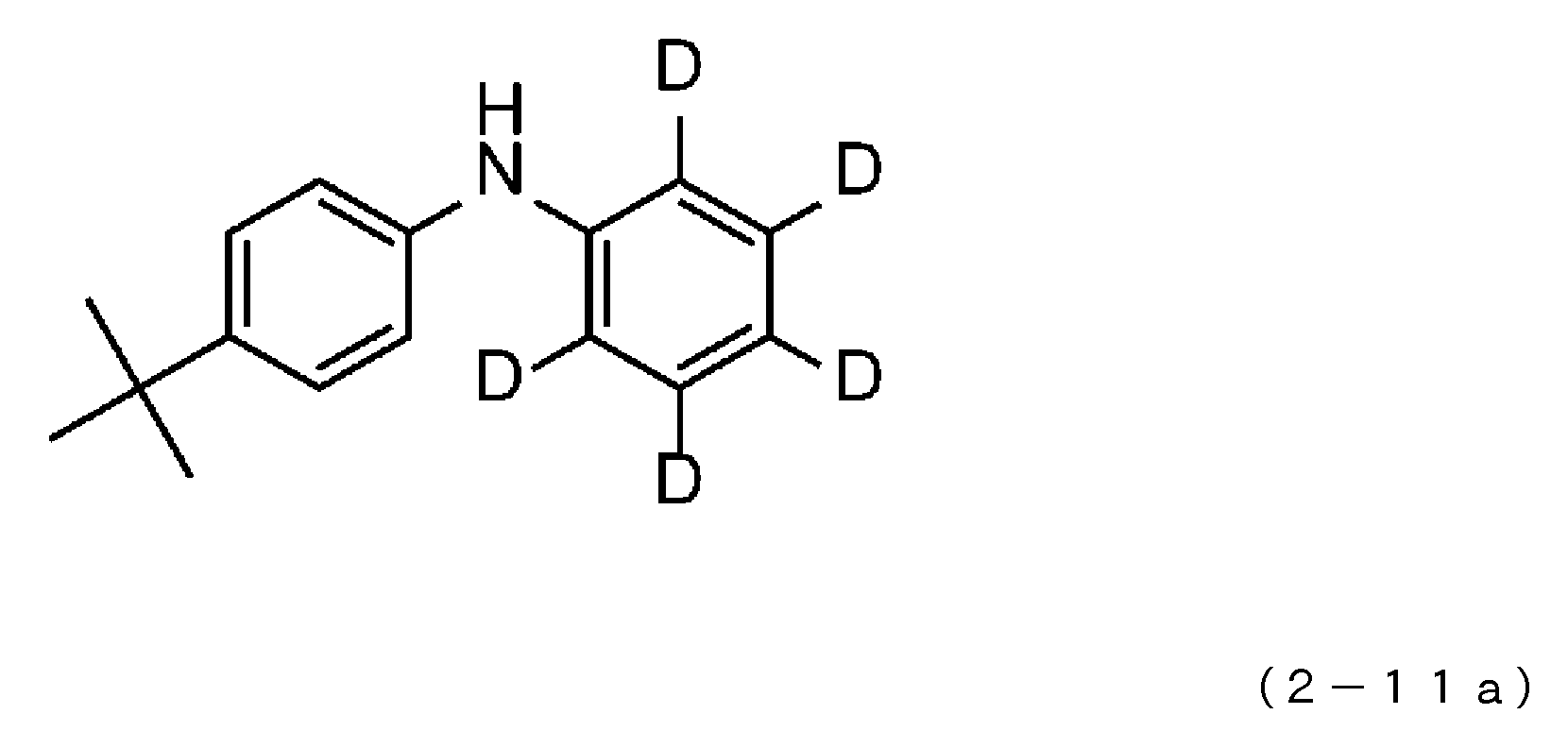
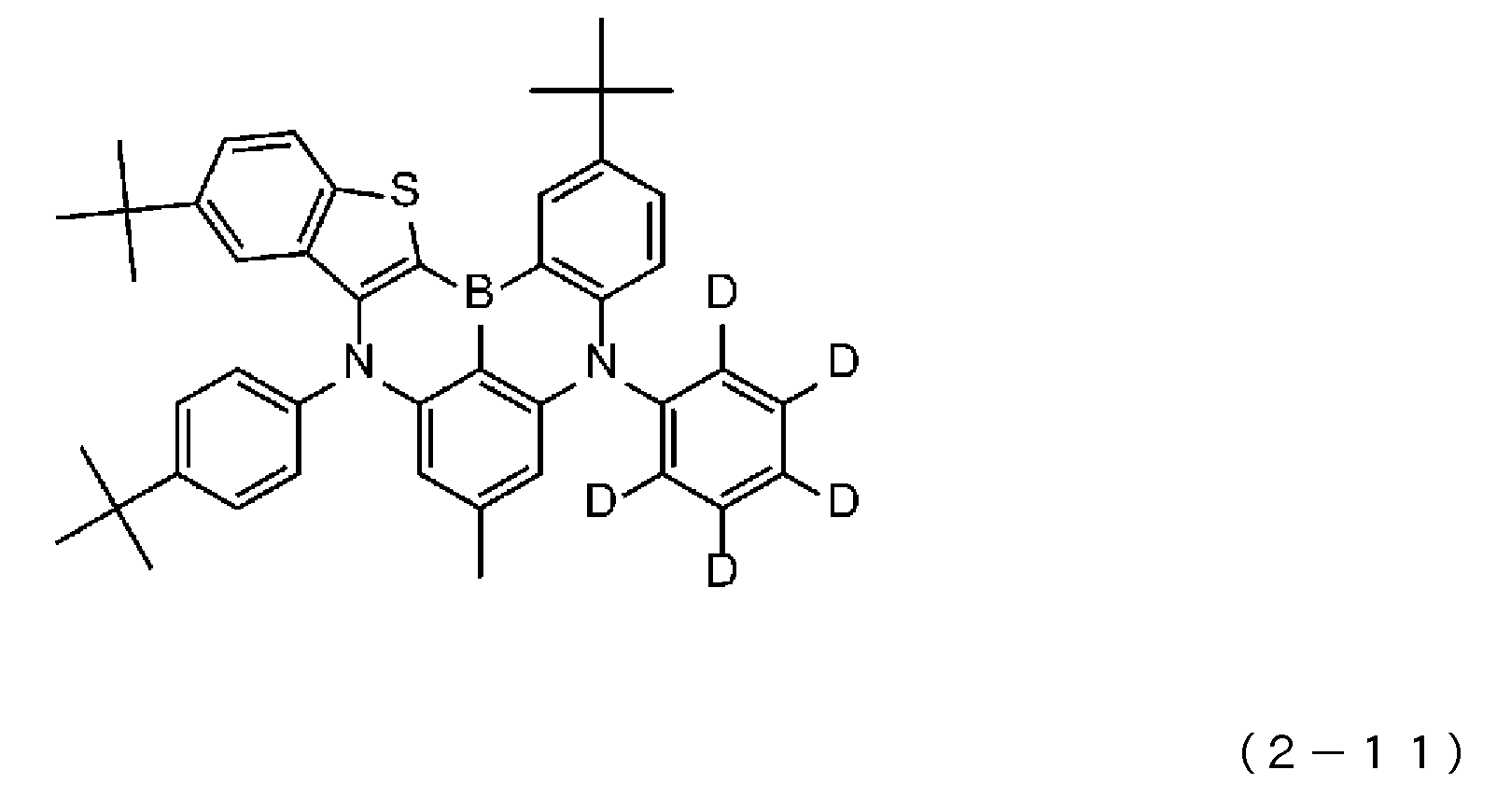
도 7은 일반식 (2)로 표시되는 화합물의 예시로서, 화합물 (2-1) 내지 (2-11)의 구조식을 도시하는 도면이다.
도 8은 일반식 (2)로 표시되는 화합물의 예시로서, 화합물 (2-12) 내지 (2-26)의 구조식을 도시하는 도면이다.
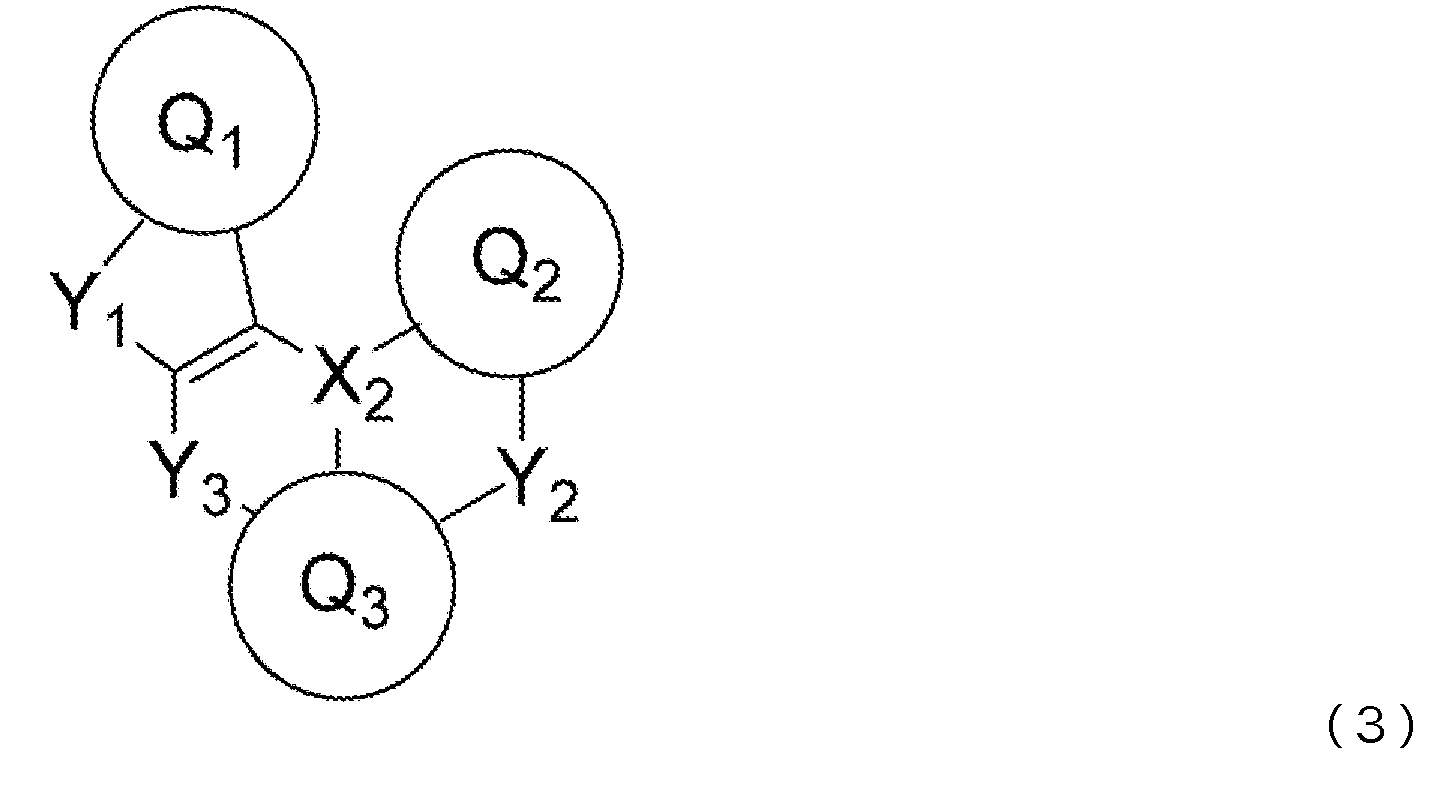
도 9는 일반식 (3)으로 표시되는 화합물의 예시로서, 화합물 (3-1) 내지 (3-12)의 구조식을 도시하는 도면이다.
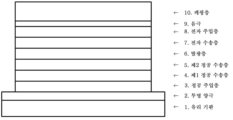
도 10은 본 발명의 실시예와 비교예의 유기 EL 소자 구성을 도시하는 도면이다.
2: 투명 양극
3: 정공 주입층
4: 제1 정공 수송층
5: 제2 정공 수송층
6: 발광층
7: 전자 수송층
8: 전자 주입층
9: 음극
10: 캐핑층
Claims (10)
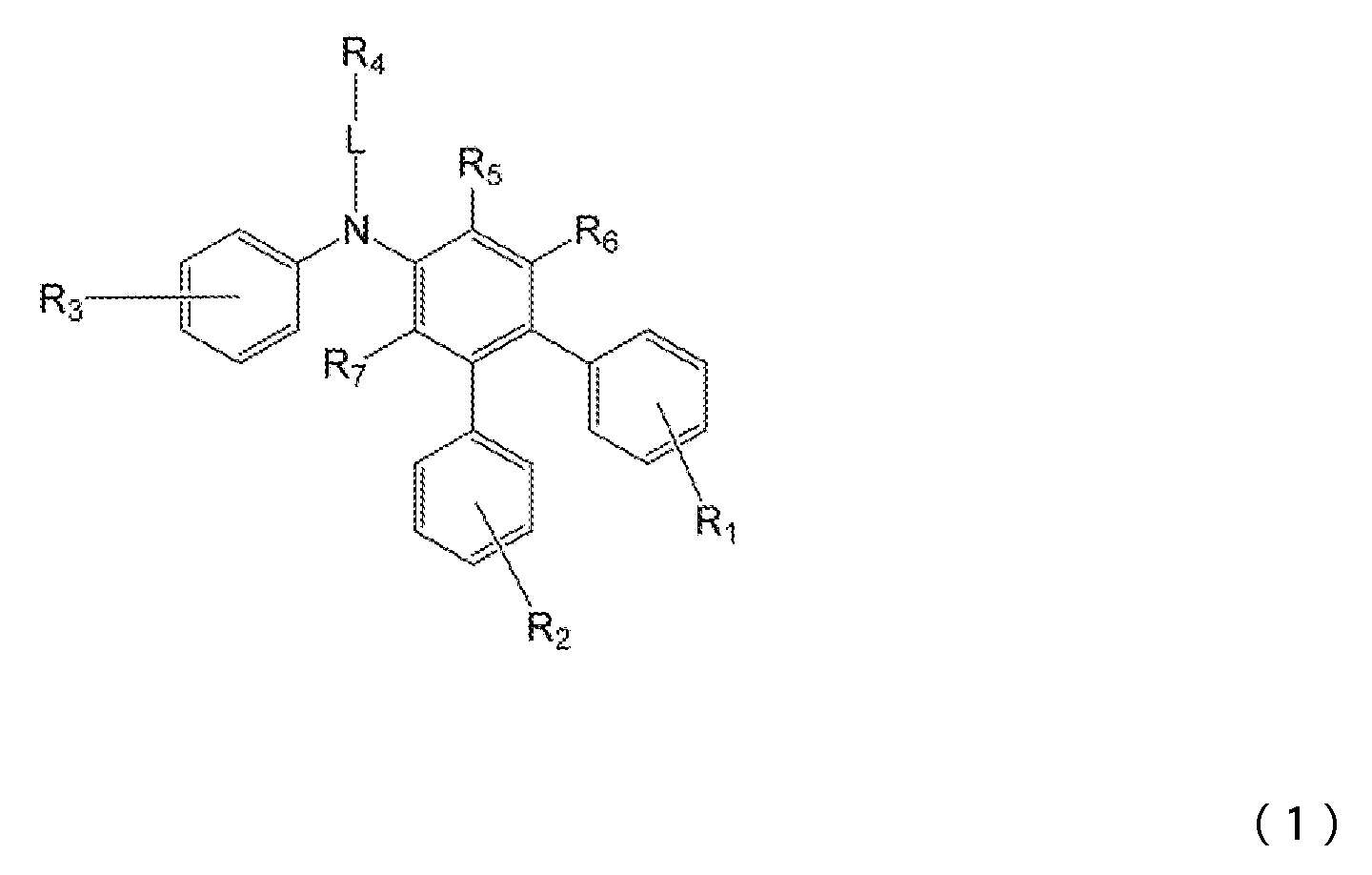
- 적어도 양극, 제1 정공 수송층, 제2 정공 수송층, 청색 발광층, 전자 수송층 및 음극을 이 순으로 갖는 유기 일렉트로루미네센스 소자에 있어서, 상기 제2 정공 수송층이 하기 일반식 (1)로 표시되는 아릴아민 화합물을 함유하는 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
(식 중, R1 내지 R4는 서로 동일해도 되고 달라도 되며, 수소 원자, 중수소 원자, 카르보닐기, 시아노기, 치환기를 갖고 있어도 되는 실릴기, 치환기를 갖고 있어도 되는 포스피노기, 치환기를 갖고 있어도 되는 포스핀옥사이드기, 치환기를 갖고 있어도 되는 탄소 원자수 1 내지 6의 직쇄상 혹은 분지상의 알킬기, 치환 혹은 비치환의 환 형성 탄소 원자수 6 내지 25의 방향족 탄화수소기를 나타낸다. L은 치환 혹은 비치환의 환 형성 탄소 원자수 6 내지 20의 방향족 탄화수소의 2가 기, 또는 단결합을 나타낸다. R5 내지 R7은 수소 원자, 중수소 원자, 치환기를 갖고 있어도 되는 탄소 원자수 1 내지 6의 직쇄상 혹은 분지상의 알킬기, 할로겐 원자, 시아노기를 나타낸다.) - 제1항에 있어서, 상기 일반식 (1)에 있어서, R1, R2는 서로 동일해도 되고 달라도 되며, 수소 원자, 치환기를 갖고 있어도 되는 실릴기 또는 치환 혹은 비치환의 환 형성 탄소 원자수 6 내지 20의 방향족 탄화수소기이고, R3은 치환기를 갖고 있어도 되는 실릴기 또는 치환 혹은 비치환의 환 형성 탄소 원자수 6 내지 25의 방향족 탄화수소기이고, R4는 수소 원자, 치환기를 가져도 되는 실릴기 또는 치환 혹은 비치환의 환 형성 탄소 원자수 6 내지 25의 방향족 탄화수소기인 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
- 제1항 또는 제2항에 있어서, 상기 일반식 (1)에 있어서, R1, R2는 서로 동일해도 되고 달라도 되며, 수소 원자, 비치환의 페닐기, 비치환의 나프틸기, 비치환의 비페닐릴기, 나프틸기로 치환된 페닐기, 비치환의 터페닐릴기 중 어느 것이고, R3은 비치환의 페닐기, 비치환의 비페닐릴기, 나프틸기로 치환된 페닐기, 2개의 페닐기로 치환된 페닐기, 페닐기로 치환된 나프틸기 중 어느 것이고, R4는 비치환의 페닐기, 비치환의 나프틸기, 페닐기로 치환된 나프틸기 중 어느 것인 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 상기 일반식 (1)에 있어서, R1은 비치환의 페닐기, 비치환의 비페닐릴기, 나프틸기로 치환된 페닐기, 비치환의 터페닐릴기 중 어느 것이고, R2는 수소 원자, 비치환의 페닐기, 비치환의 나프틸기, 비치환의 비페닐릴기, 나프틸기로 치환된 페닐기, 비치환의 터페닐릴기 중 어느 것이고, R3은 비치환의 페닐기이고, R4는 비치환의 페닐기, 비치환의 나프틸기, 페닐기로 치환된 나프틸기 중 어느 것인 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
- 제1항 또는 제2항에 있어서, 상기 일반식 (1)에 있어서, R1 내지 R4 중 적어도 하나가 트리페닐실릴기, 또는 트리페닐실릴기로 치환된 페닐기 중 어느 것인 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 상기 일반식 (1)에 있어서, R5 내지 R7의 전부가 수소 원자인 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
- 제1항 내지 제6항 중 어느 한 항에 있어서, 상기 일반식 (1)에 있어서, L이 1,4-페닐렌기인 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
- 제1항 내지 제7항 중 어느 한 항에 있어서, 상기 청색 발광층이, 청색 발광성 도펀트로서, 분자 중에 피렌 골격을 갖는 피렌 유도체를 함유하는 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
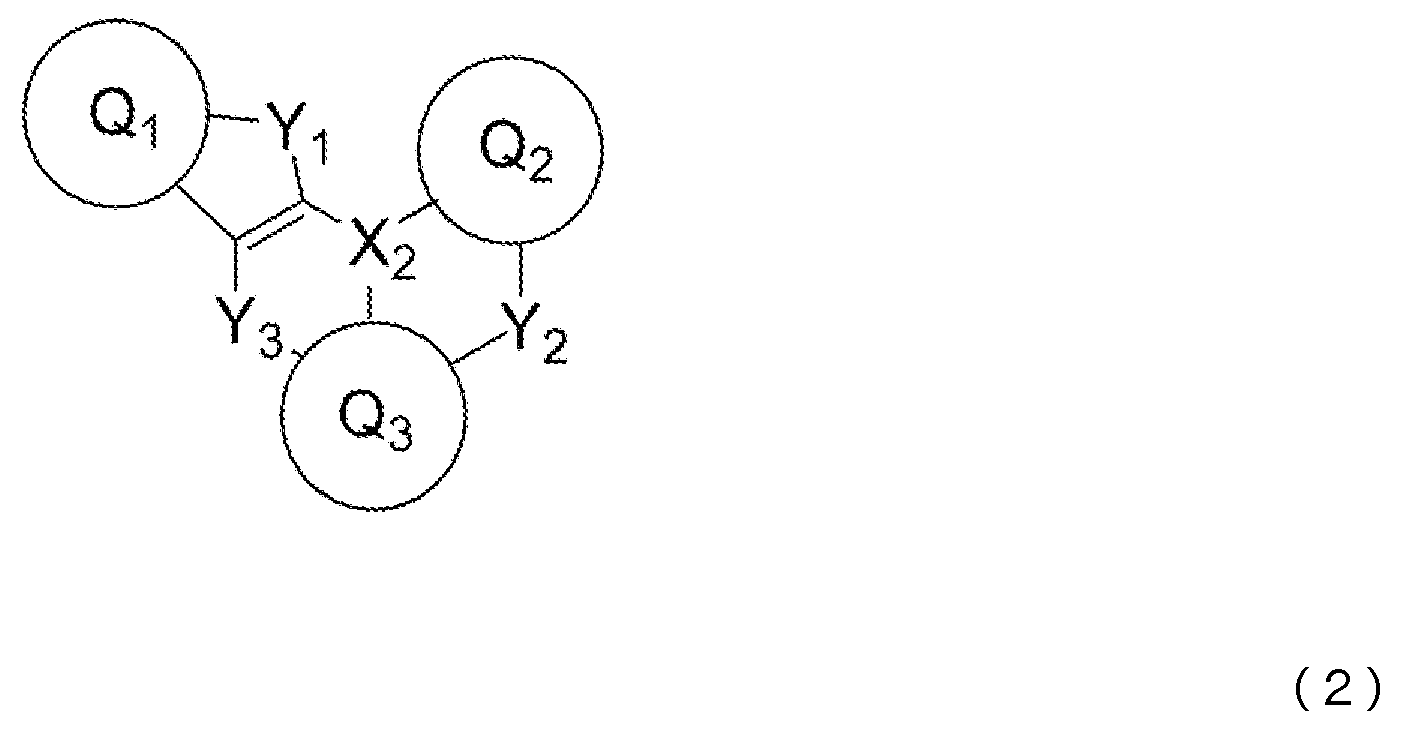
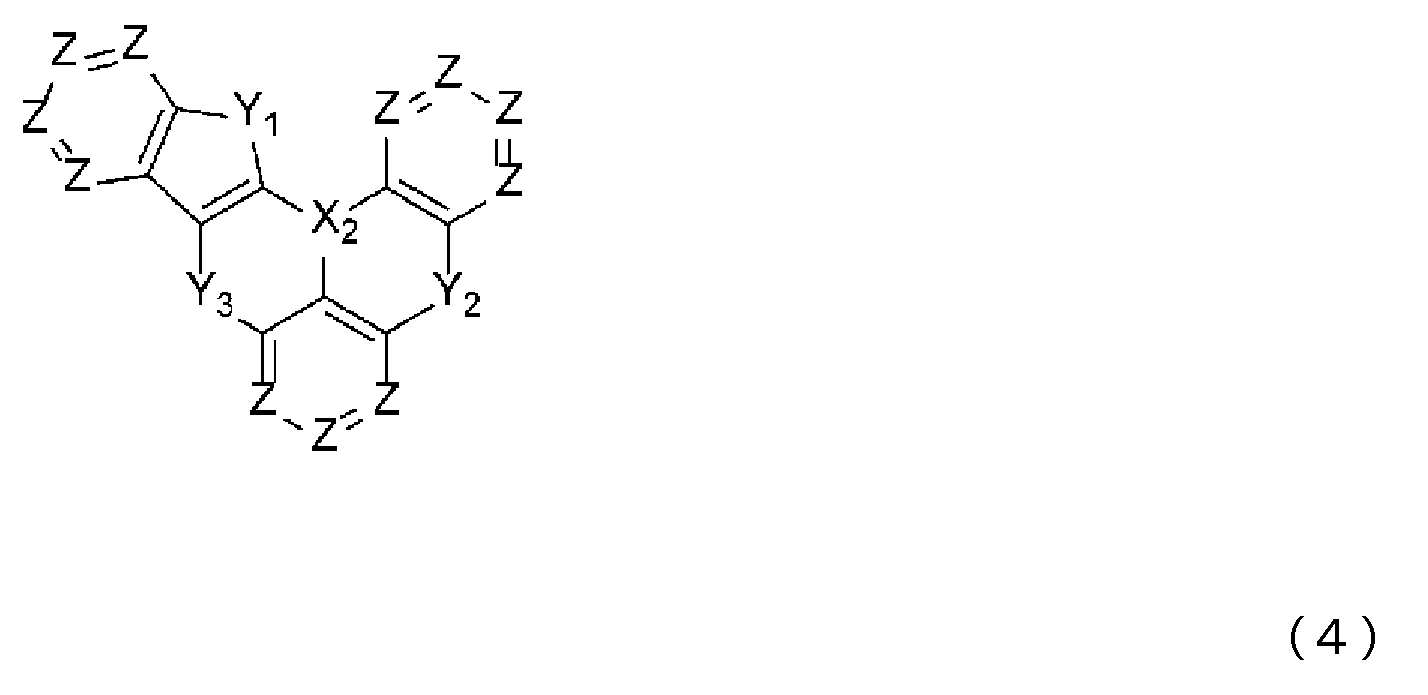
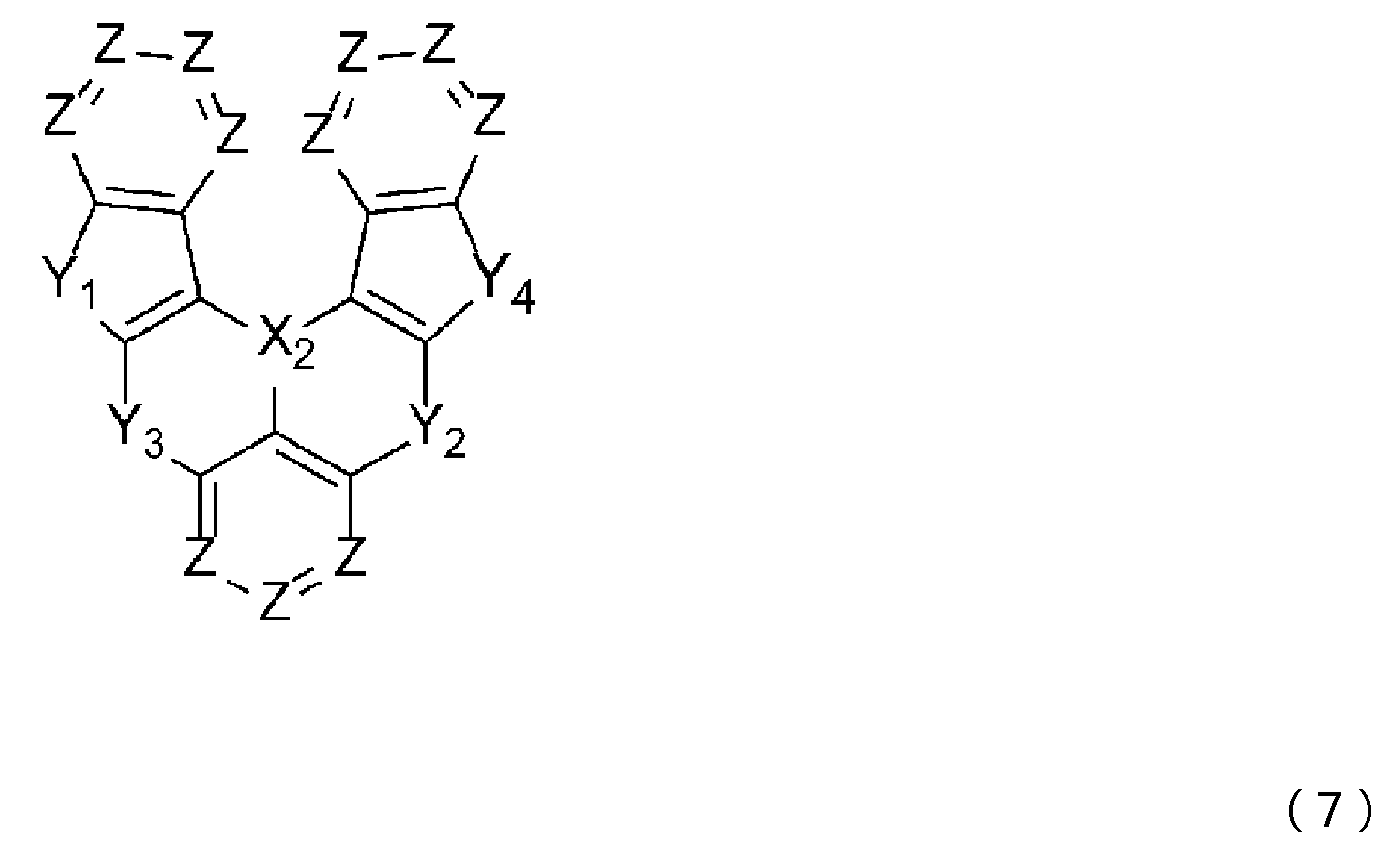
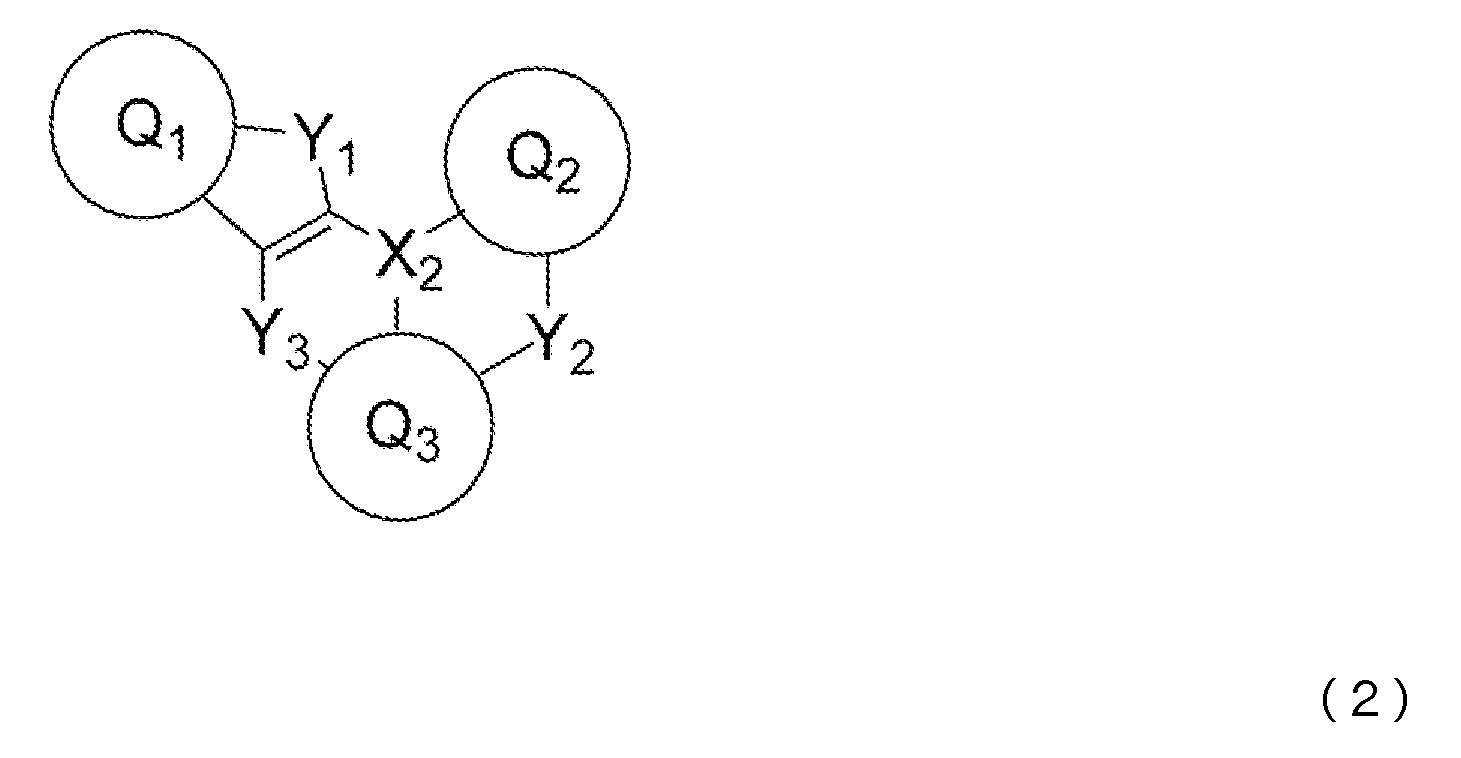
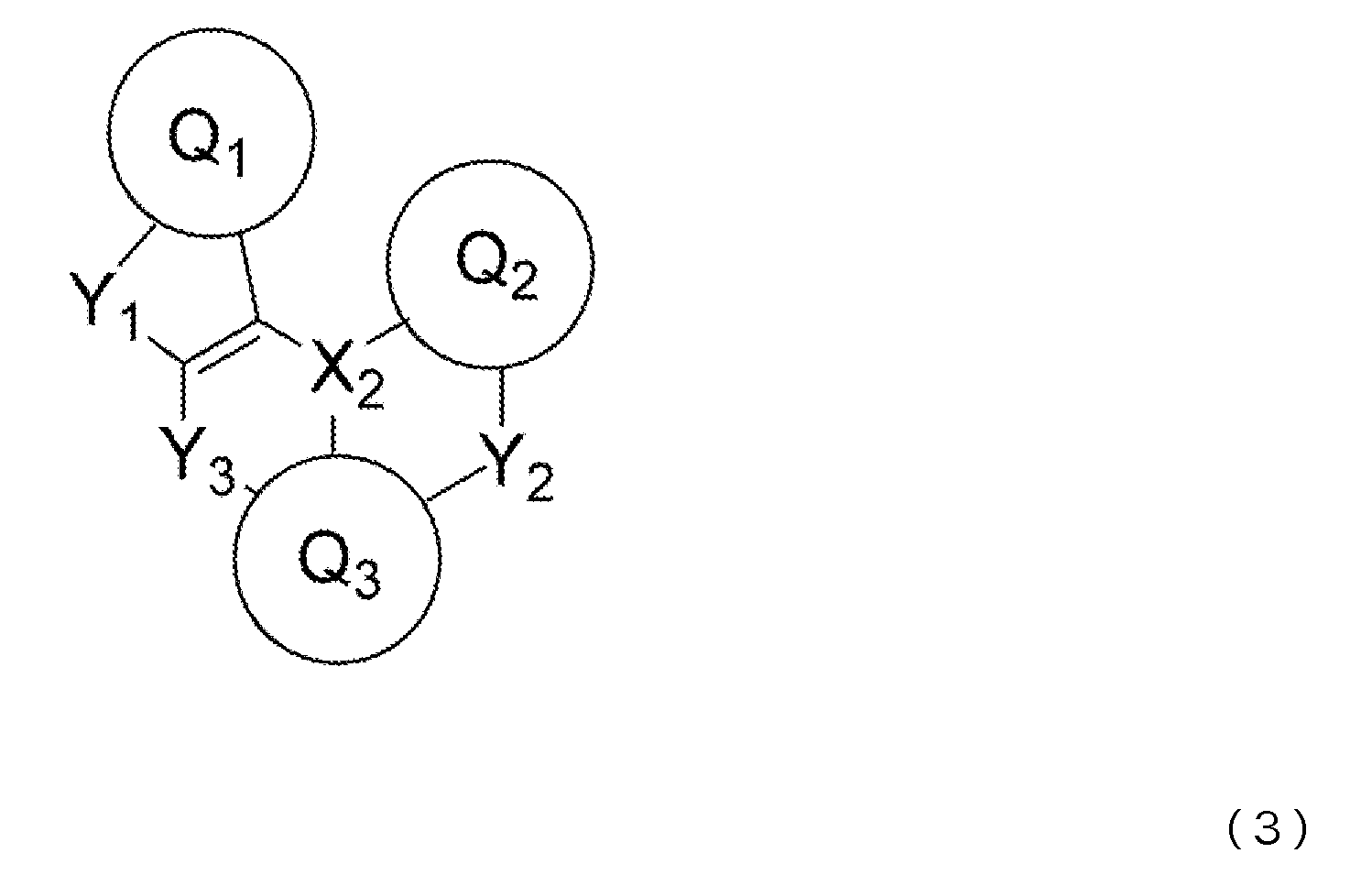
- 제1항 내지 제7항 중 어느 한 항에 있어서, 상기 청색 발광층이, 청색 발광성 도펀트로서, 하기 일반식 (2) 또는 일반식 (3)으로 표시되는 화합물을 함유하는 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
(일반식 (2) 및 일반식 (3) 중, Q1 내지 Q3은 서로 동일해도 되고 달라도 되며, 치환 혹은 비치환의 방향족 탄화수소, 또는 치환 혹은 비치환의 방향족 복소환을 나타낸다. X2는 B, P, P=O 또는 P=S를 나타낸다. Y1 내지 Y3은 서로 동일해도 되고 달라도 되며, N-R8, CR9R10, O, S, Se 또는 SiR11R12 중에서 선택되는 어느 하나이고, 그 R8 내지 R12는 서로 동일해도 되고 달라도 되며, 수소 원자, 중수소 원자, 불소 원자, 염소 원자, 시아노기, 니트로기, 치환기를 갖고 있어도 되는 탄소 원자수 1 내지 6의 직쇄상 혹은 분지상의 알킬기, 치환기를 갖고 있어도 되는 탄소 원자수 5 내지 10의 시클로알킬기, 치환기를 갖고 있어도 되는 탄소 원자수 2 내지 6의 직쇄상 혹은 분지상의 알케닐기, 치환기를 갖고 있어도 되는 탄소 원자수 1 내지 6의 직쇄상 혹은 분지상의 알킬옥시기, 치환기를 갖고 있어도 되는 탄소 원자수 5 내지 10의 시클로알킬옥시기, 치환 혹은 비치환의 방향족 탄화수소기, 치환 혹은 비치환의 방향족 복소환기, 또는 치환 혹은 비치환의 아릴옥시기를 나타낸다. 또한, R9와 R10, R11과 R12는 각각의 기끼리 단결합, 치환 혹은 비치환의 메틸렌기, 산소 원자 또는 황 원자, 1치환 아미노기를 통하여 서로 결합하여 환을 형성해도 된다. 단, Y1 내지 Y3이 N-R8, CR9R10 또는 SiR11R12인 경우, R8 내지 R12는 각각 인접하는 Q1 내지 Q3과, 단결합, 치환 혹은 비치환의 메틸렌기, 산소 원자, 황 원자, 1치환 아미노기 등의 연결기를 통하여 서로 결합하여 환을 형성해도 된다.) - 제1항 내지 제9항 중 어느 한 항에 있어서, 상기 청색 발광층이, 분자 중에 안트라센 골격을 갖는 안트라센 유도체를 함유하는 것을 특징으로 하는 유기 일렉트로루미네센스 소자.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020137612 | 2020-08-17 | ||
| JPJP-P-2020-137612 | 2020-08-17 | ||
| PCT/JP2021/029801 WO2022039106A1 (ja) | 2020-08-17 | 2021-08-13 | 有機エレクトロルミネッセンス素子 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20230051663A true KR20230051663A (ko) | 2023-04-18 |
Family
ID=80322792
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237004531A Ceased KR20230051663A (ko) | 2020-08-17 | 2021-08-13 | 유기 일렉트로루미네센스 소자 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20230345817A1 (ko) |
| EP (1) | EP4198104A4 (ko) |
| JP (1) | JP7771065B2 (ko) |
| KR (1) | KR20230051663A (ko) |
| CN (1) | CN115885022A (ko) |
| WO (1) | WO2022039106A1 (ko) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116217409B (zh) * | 2022-03-24 | 2023-12-22 | 江苏三月科技股份有限公司 | 一种芳香族胺类化合物及其制备的有机电致发光器件 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS4943840B1 (ko) | 1970-12-25 | 1974-11-25 | ||
| JPH0848656A (ja) | 1994-02-08 | 1996-02-20 | Tdk Corp | 有機el素子用化合物および有機el素子 |
| JP3194657B2 (ja) | 1993-11-01 | 2001-07-30 | 松下電器産業株式会社 | 電界発光素子 |
| JP2006151979A (ja) | 2004-11-29 | 2006-06-15 | Samsung Sdi Co Ltd | フェニルカルバゾール系化合物とその製造方法及び有機電界発光素子 |
| WO2008062636A1 (fr) | 2006-11-24 | 2008-05-29 | Idemitsu Kosan Co., Ltd. | Dérivé d'amine aromatique et élément électroluminescent organique utilisant celui-ci |
| WO2014009310A1 (en) | 2012-07-09 | 2014-01-16 | Novaled Ag | Doped organic semiconductive matrix material |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10818844B2 (en) * | 2014-07-09 | 2020-10-27 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent device |
| EP3244462B1 (en) * | 2015-01-06 | 2020-11-11 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent element |
| DE102018125307A1 (de) * | 2018-10-12 | 2020-04-16 | Novaled Gmbh | Organische lichtemittierende Vorrichtung |
| CN112805846B (zh) * | 2018-11-29 | 2024-09-13 | 保土谷化学工业株式会社 | 有机电致发光元件 |
| KR102094830B1 (ko) * | 2018-11-30 | 2020-03-30 | 에스에프씨 주식회사 | 다환 방향족 유도체 화합물 및 이를 이용한 유기발광소자 |
| KR102169567B1 (ko) * | 2018-12-21 | 2020-10-23 | 엘지디스플레이 주식회사 | 유기 발광 소자 |
| CN111029477B (zh) * | 2019-12-10 | 2022-10-18 | 昆山国显光电有限公司 | 一种有机电致发光器件、显示面板及显示装置 |
-
2021
- 2021-08-13 JP JP2022543924A patent/JP7771065B2/ja active Active
- 2021-08-13 US US18/021,251 patent/US20230345817A1/en active Pending
- 2021-08-13 CN CN202180050636.5A patent/CN115885022A/zh active Pending
- 2021-08-13 KR KR1020237004531A patent/KR20230051663A/ko not_active Ceased
- 2021-08-13 WO PCT/JP2021/029801 patent/WO2022039106A1/ja not_active Ceased
- 2021-08-13 EP EP21858253.4A patent/EP4198104A4/en active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS4943840B1 (ko) | 1970-12-25 | 1974-11-25 | ||
| JP3194657B2 (ja) | 1993-11-01 | 2001-07-30 | 松下電器産業株式会社 | 電界発光素子 |
| JPH0848656A (ja) | 1994-02-08 | 1996-02-20 | Tdk Corp | 有機el素子用化合物および有機el素子 |
| JP2006151979A (ja) | 2004-11-29 | 2006-06-15 | Samsung Sdi Co Ltd | フェニルカルバゾール系化合物とその製造方法及び有機電界発光素子 |
| WO2008062636A1 (fr) | 2006-11-24 | 2008-05-29 | Idemitsu Kosan Co., Ltd. | Dérivé d'amine aromatique et élément électroluminescent organique utilisant celui-ci |
| WO2014009310A1 (en) | 2012-07-09 | 2014-01-16 | Novaled Ag | Doped organic semiconductive matrix material |
Non-Patent Citations (4)
| Title |
|---|
| Appl. Phys. Let., 98, 083302(2011) |
| 유기 EL 토론회 제3회 정례회 예고집 13 내지 14페이지(2006) |
| 응용 물리학회 제9회 강습회 예고집 23 내지 31페이지(2001) |
| 응용 물리학회 제9회 강습회 예고집 55 내지 61페이지(2001) |
Also Published As
| Publication number | Publication date |
|---|---|
| JP7771065B2 (ja) | 2025-11-17 |
| TW202219244A (zh) | 2022-05-16 |
| CN115885022A (zh) | 2023-03-31 |
| EP4198104A1 (en) | 2023-06-21 |
| WO2022039106A1 (ja) | 2022-02-24 |
| JPWO2022039106A1 (ko) | 2022-02-24 |
| US20230345817A1 (en) | 2023-10-26 |
| EP4198104A4 (en) | 2024-07-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI646097B (zh) | 具有氮雜茀環結構之螺化合物、發光材料及有機電致發光元件 | |
| CN107709285B (zh) | 芳基胺化合物和有机电致发光器件 | |
| JP7406486B2 (ja) | トリアリールアミン構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| KR20130112850A (ko) | 아크리단환 구조를 가지는 화합물 및 유기 일렉트로 루미네센스 소자 | |
| JP7217320B2 (ja) | 有機エレクトロルミネッセンス素子用材料及び有機エレクトロルミネッセンス素子 | |
| JP7149263B2 (ja) | 有機エレクトロルミネッセンス素子 | |
| CN113396200A (zh) | 有机电致发光元件 | |
| JP7784992B2 (ja) | 有機エレクトロルミネッセンス素子 | |
| EP4398696A1 (en) | Organic electroluminescent element | |
| JP7592020B2 (ja) | 有機エレクトロルミネッセンス素子 | |
| WO2022080490A1 (ja) | アリールアミン化合物、有機エレクトロルミネッセンス素子、および電子機器 | |
| JP7771065B2 (ja) | 有機エレクトロルミネッセンス素子 | |
| KR20240114741A (ko) | 아릴아민 화합물, 유기 일렉트로루미네센스 소자 및 전자 기기 | |
| EP4243105A1 (en) | Organic electroluminescent element | |
| JP2025156207A (ja) | 化合物、有機エレクトロルミネッセンス素子、および電子機器 | |
| CN114867713A (zh) | 芳基胺化合物及有机电致发光元件 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| A201 | Request for examination | ||
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11 | Amendment of application requested |
Free format text: ST27 STATUS EVENT CODE: A-2-2-P10-P11-NAP-X000 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| B15 | Application refused following examination |
Free format text: ST27 STATUS EVENT CODE: N-2-6-B10-B15-EXM-PE0601 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| PE0601 | Decision on rejection of patent |
St.27 status event code: N-2-6-B10-B15-exm-PE0601 |