KR800000038B1 - 벤즈옥사졸의 제조방법 - Google Patents
벤즈옥사졸의 제조방법 Download PDFInfo
- Publication number
- KR800000038B1 KR800000038B1 KR7904055A KR790004055A KR800000038B1 KR 800000038 B1 KR800000038 B1 KR 800000038B1 KR 7904055 A KR7904055 A KR 7904055A KR 790004055 A KR790004055 A KR 790004055A KR 800000038 B1 KR800000038 B1 KR 800000038B1
- Authority
- KR
- South Korea
- Prior art keywords
- alkyl
- hydrogen
- acid
- general formula
- represented
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/52—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings condensed with carbocyclic rings or ring systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
Abstract
Description
Claims (1)
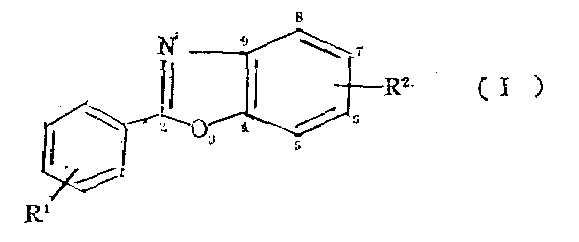
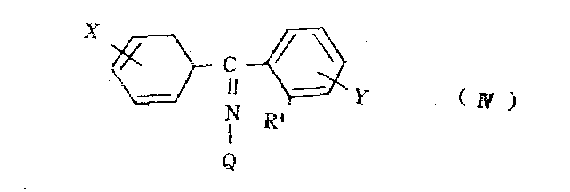
- 하기 일반식(Ⅳ)으로 표시되는 옥심 또는 하이드라존을 산성조건하에서 환화시켜서 제조함을 특징으로 하는 하기 일반식( I )으로 표시되는 5-또는 6-치환 벤즈옥사졸의 제조방법.상기 식에서 R1은 벤젠환의 하나 또는 그 이상의 유용한 위치에 있고 수소, 할로겐 C1-4알킬, C1-4알콕시, R2는 1,2-벤즈이소옥사졸핵의 5-, 6-또는 7-위치에 있는 치환분이고, 수소, C1-4알킬 카르복시 C1-4알킬, 시아노 C1-4알킬,-CH(R3)·COOH, -CH2·COOR3와 -CH(R3)·COOR3(여기서 R3는 C1-4알킬)중의 하나이며, R1이 수소를 나타낼때 R2가 수소가 아닌 것은 제외한다.상기 식에서 Q는 하이드록실기 또는 아미노기이고 R4는 하이드록실기이고 X와 Y기는 각기 R1과 R2를 나타내며, 필요에 따라 X와 Y는 원하는 Rl과 R2기로 변환시킬 수 있다.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR7904055A KR800000038B1 (ko) | 1979-11-20 | 1979-11-20 | 벤즈옥사졸의 제조방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR7904055A KR800000038B1 (ko) | 1979-11-20 | 1979-11-20 | 벤즈옥사졸의 제조방법 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR740003910A Division KR800000029B1 (ko) | 1974-10-23 | 1974-10-23 | 이소옥사졸유도체의 제조방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR800000038B1 true KR800000038B1 (ko) | 1980-01-28 |
Family
ID=19213590
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR7904055A Expired KR800000038B1 (ko) | 1979-11-20 | 1979-11-20 | 벤즈옥사졸의 제조방법 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR800000038B1 (ko) |
-
1979
- 1979-11-20 KR KR7904055A patent/KR800000038B1/ko not_active Expired
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0010029B1 (fr) | Ellipticines substituées en position 1 par une chaîne polyaminée, leur synthèse et médicaments les contenant | |
| EP0506532A1 (fr) | Nouveaux dérivés de l'indole, procédé de préparation et médicaments les contenant | |
| US3951999A (en) | Anti-inflammatory 1,2-benzisoxazole derivatives | |
| FR2598706A1 (fr) | Derives de tetrahydronaphtalene, compositions pharmaceutiques les contenant et procede de preparation | |
| US4025636A (en) | 2-(Optionally substituted)phenyl-5 or 6-substituted benzoxazoles | |
| EP0022118A1 (fr) | Nouveaux dérivés de sulfonyl-aniline, leur procédé de préparation et leur application en thérapeutique | |
| EP0114014A2 (fr) | Dérivés de thiéno (2,3-b) pyrrole, leur procédé de préparation et les compositions pharmaceutiques les renfermant | |
| EP0151072B1 (fr) | Dérivés de l'acide méthylènediphosphonique, procédé d'obtention et compositions pharmaceutiques antirhumatismales les contenant | |
| CH662563A5 (fr) | Derives de coumarine, leurs procedes de preparation et compositions pharmaceutiques les contenant. | |
| EP0109866B1 (fr) | Nouveaux dérivés de la sulfonylurée, leurs procédés de préparation et les compositions pharmaceutiques les renfermant | |
| CA1315283C (fr) | Amines tricycliques derivees du tetrahydro-5,6,7,8 naphto ¬2,3b| dihydro-2,3 furanne, et du tetrahydro-6,7,8,9 5h-benzocyclohepta ¬2,3b| dihydro-2,3 furanne, leurs procedes de preparation et les compositions pharmaceutiques qui les contiennent | |
| FR2553409A1 (fr) | Nouveaux benzenesulfonyl-lactames, leur procede de preparation et leur application comme substance active de compositions pharmaceutiques | |
| US4139538A (en) | Oxazolidinones as therapeutic agents | |
| KR800000038B1 (ko) | 벤즈옥사졸의 제조방법 | |
| LU81676A1 (fr) | Nouveaux derives d'aurones,leur procede de preparation et leur utilisation comme produits pharmaceutiques | |
| FR2492378A1 (fr) | Derives de type 6h-dibenzo(b,d) pyranne 6-substitues utiles notamment comme medicaments antiulcereux, immunomodulateurs et antiviraux et procedes de leur preparation | |
| EP0463944A1 (fr) | Acyl benzoxazolinones, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| WO1990006931A1 (fr) | Composes organometalliques, leurs modes de preparation et compositions pharmaceutiques les contenant | |
| EP0402232A1 (fr) | Dérivés de pyridobenzoindole, leur préparation et les compositions qui les contiennent | |
| US3132176A (en) | Preparation of o, o-dialkanoyl derivatives of d, l-alpha-alkyl-beta-3, 4-dihydroxyphenylalanine by preferential acylation | |
| CH628014A5 (en) | Gamma-aryl-gamma-oxoisovaleric acids having antiphlogistic and antalgic properties | |
| FR2460934A1 (fr) | Derives d'isoquinoleine contenant du soufre, procedes pour leur preparation et compositions pharmaceutiques les contenant | |
| FR2772766A1 (fr) | Nouveaux composes heterocycliques, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| US3594388A (en) | 4-amino-5-(substituted phenyl) furazan | |
| EP0233804B1 (fr) | Monoaryl-5 as triazinones-3 substituées en position 2, leur procédé de préparation et leur application en tant que medicaments |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0107 | Divisional application |
St.27 status event code: A-0-1-A10-A16-div-PA0107 St.27 status event code: A-0-1-A10-A18-div-PA0107 |
|
| PG1605 | Publication of application before grant of patent |
St.27 status event code: A-2-2-Q10-Q13-nap-PG1605 |
|
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
Fee payment year number: 1 St.27 status event code: A-2-2-U10-U11-oth-PR1002 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 4 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 5 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 6 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PR1001 | Payment of annual fee |
Fee payment year number: 7 St.27 status event code: A-4-4-U10-U11-oth-PR1001 |
|
| PC1903 | Unpaid annual fee |
Not in force date: 19870129 Payment event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE St.27 status event code: A-4-4-U10-U13-oth-PC1903 |
|
| PC1903 | Unpaid annual fee |
Ip right cessation event data comment text: Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date: 19870129 St.27 status event code: N-4-6-H10-H13-oth-PC1903 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |