KR800000045B1 - 아데노신 나이트레이트의 제조방법 - Google Patents
아데노신 나이트레이트의 제조방법 Download PDFInfo
- Publication number
- KR800000045B1 KR800000045B1 KR7600379A KR760000379A KR800000045B1 KR 800000045 B1 KR800000045 B1 KR 800000045B1 KR 7600379 A KR7600379 A KR 7600379A KR 760000379 A KR760000379 A KR 760000379A KR 800000045 B1 KR800000045 B1 KR 800000045B1
- Authority
- KR
- South Korea
- Prior art keywords
- amino
- carboxylic acid
- adenosine
- lower alkyl
- nitroadenosine
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
- 238000000034 method Methods 0.000 title claims description 10
- QQVLEBJNJDLCJQ-KQYNXXCUSA-N [(2r,3s,4r,5r)-5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolan-2-yl]methyl nitrate Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO[N+]([O-])=O)[C@@H](O)[C@H]1O QQVLEBJNJDLCJQ-KQYNXXCUSA-N 0.000 title claims description 5
- 150000003839 salts Chemical class 0.000 claims description 14
- 150000001875 compounds Chemical class 0.000 claims description 13
- 125000000217 alkyl group Chemical group 0.000 claims description 12
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 11
- 239000002253 acid Substances 0.000 claims description 10
- 125000002252 acyl group Chemical group 0.000 claims description 7
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 6
- 125000001931 aliphatic group Chemical group 0.000 claims description 5
- 125000003118 aryl group Chemical group 0.000 claims description 5
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 5
- 229910052757 nitrogen Inorganic materials 0.000 claims description 5
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 5
- 125000003545 alkoxy group Chemical group 0.000 claims description 4
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 claims description 3
- 125000006310 cycloalkyl amino group Chemical group 0.000 claims description 3
- 125000000623 heterocyclic group Chemical group 0.000 claims description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 3
- 230000006181 N-acylation Effects 0.000 claims 1
- 230000000802 nitrating effect Effects 0.000 claims 1
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 21
- -1 Adenosine nitrates Chemical class 0.000 description 19
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 19
- 238000000354 decomposition reaction Methods 0.000 description 17
- 238000002844 melting Methods 0.000 description 17
- 230000008018 melting Effects 0.000 description 17
- 239000000203 mixture Substances 0.000 description 15
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 14
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- 239000000243 solution Substances 0.000 description 10
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 8
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 8
- 231100000331 toxic Toxicity 0.000 description 7
- 230000002588 toxic effect Effects 0.000 description 7
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 6
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 6
- 235000015497 potassium bicarbonate Nutrition 0.000 description 6
- 229910000028 potassium bicarbonate Inorganic materials 0.000 description 6
- 239000011736 potassium bicarbonate Substances 0.000 description 6
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 6
- 238000005917 acylation reaction Methods 0.000 description 5
- JLLYLQLDYORLBB-UHFFFAOYSA-N 5-bromo-n-methylthiophene-2-sulfonamide Chemical compound CNS(=O)(=O)C1=CC=C(Br)S1 JLLYLQLDYORLBB-UHFFFAOYSA-N 0.000 description 4
- IBYWUFHJUDTSOC-SOVPELCUSA-N 9-riburonosyladenine Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](C(O)=O)[C@@H](O)[C@H]1O IBYWUFHJUDTSOC-SOVPELCUSA-N 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- 230000010933 acylation Effects 0.000 description 4
- 125000003277 amino group Chemical group 0.000 description 4
- 239000004202 carbamide Substances 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- QKIUAMUSENSFQQ-UHFFFAOYSA-N dimethylazanide Chemical compound C[N-]C QKIUAMUSENSFQQ-UHFFFAOYSA-N 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000001953 recrystallisation Methods 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 239000012043 crude product Substances 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- HIFJUMGIHIZEPX-UHFFFAOYSA-N sulfuric acid;sulfur trioxide Chemical compound O=S(=O)=O.OS(O)(=O)=O HIFJUMGIHIZEPX-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 2
- OIRDTQYFTABQOQ-KQYNXXCUSA-N Adenosine Natural products C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O OIRDTQYFTABQOQ-KQYNXXCUSA-N 0.000 description 2
- 239000002126 C01EB10 - Adenosine Substances 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 229910002651 NO3 Inorganic materials 0.000 description 2
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 241000978776 Senegalia senegal Species 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- 235000010489 acacia gum Nutrition 0.000 description 2
- 229960005305 adenosine Drugs 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000002026 chloroform extract Substances 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 239000000469 ethanolic extract Substances 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 230000014509 gene expression Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 239000012452 mother liquor Substances 0.000 description 2
- WEXRUCMBJFQVBZ-UHFFFAOYSA-N pentobarbital Chemical compound CCCC(C)C1(CC)C(=O)NC(=O)NC1=O WEXRUCMBJFQVBZ-UHFFFAOYSA-N 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- VVIGFSVMHCPTEL-KQYNXXCUSA-N (2R,3R,4S,5R)-2-(6-aminopurin-9-yl)-5-(hydroxymethyl)-2-nitrooxolane-3,4-diol Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@]1([N+]([O-])=O)O[C@H](CO)[C@@H](O)[C@H]1O VVIGFSVMHCPTEL-KQYNXXCUSA-N 0.000 description 1
- BLMHAOGGJQDPLX-LKCKTBJASA-N (2s,3s,4r,5r)-5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolane-2-carboxamide Chemical compound O[C@@H]1[C@H](O)[C@@H](C(=O)N)O[C@H]1N1C2=NC=NC(N)=C2N=C1 BLMHAOGGJQDPLX-LKCKTBJASA-N 0.000 description 1
- YKMOOBLAWBCXFX-UHFFFAOYSA-N 2-(2,4-dinitrophenyl)ethanamine Chemical compound NCCC1=CC=C([N+]([O-])=O)C=C1[N+]([O-])=O YKMOOBLAWBCXFX-UHFFFAOYSA-N 0.000 description 1
- 125000004080 3-carboxypropanoyl group Chemical group O=C([*])C([H])([H])C([H])([H])C(O[H])=O 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 206010002091 Anaesthesia Diseases 0.000 description 1
- 206010002383 Angina Pectoris Diseases 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M Methanesulfonate Chemical compound CS([O-])(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- DFPAKSUCGFBDDF-UHFFFAOYSA-N Nicotinamide Chemical compound NC(=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-UHFFFAOYSA-N 0.000 description 1
- IOVCWXUNBOPUCH-UHFFFAOYSA-M Nitrite anion Chemical compound [O-]N=O IOVCWXUNBOPUCH-UHFFFAOYSA-M 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 229960000583 acetic acid Drugs 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 1
- 150000001266 acyl halides Chemical class 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- KZTZJUQNSSLNAG-UHFFFAOYSA-N aminoethyl nitrate Chemical compound NCCO[N+]([O-])=O KZTZJUQNSSLNAG-UHFFFAOYSA-N 0.000 description 1
- 230000037005 anaesthesia Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 230000004872 arterial blood pressure Effects 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- PASDCCFISLVPSO-UHFFFAOYSA-N benzoyl chloride Chemical compound ClC(=O)C1=CC=CC=C1 PASDCCFISLVPSO-UHFFFAOYSA-N 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 125000000440 benzylamino group Chemical group [H]N(*)C([H])([H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004063 butyryl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- ITMSAWKLJVGBIT-UHFFFAOYSA-N carbocloral Chemical compound CCOC(=O)NC(O)C(Cl)(Cl)Cl ITMSAWKLJVGBIT-UHFFFAOYSA-N 0.000 description 1
- 229950003854 carbocloral Drugs 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000003897 citraconoyl group Chemical group C(\C(\C)=C/C(=O)*)(=O)* 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 210000004351 coronary vessel Anatomy 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- PAFZNILMFXTMIY-UHFFFAOYSA-N cyclohexylamine Chemical compound NC1CCCCC1 PAFZNILMFXTMIY-UHFFFAOYSA-N 0.000 description 1
- 125000006312 cyclopentyl amino group Chemical group [H]N(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 230000009615 deamination Effects 0.000 description 1
- 238000006481 deamination reaction Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- YWEUIGNSBFLMFL-UHFFFAOYSA-N diphosphonate Chemical compound O=P(=O)OP(=O)=O YWEUIGNSBFLMFL-UHFFFAOYSA-N 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 210000001198 duodenum Anatomy 0.000 description 1
- 239000008157 edible vegetable oil Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- CCGKOQOJPYTBIH-UHFFFAOYSA-N ethenone Chemical class C=C=O CCGKOQOJPYTBIH-UHFFFAOYSA-N 0.000 description 1
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 210000001105 femoral artery Anatomy 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 210000005240 left ventricle Anatomy 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 150000002762 monocarboxylic acid derivatives Chemical class 0.000 description 1
- 230000002107 myocardial effect Effects 0.000 description 1
- DILRJUIACXKSQE-UHFFFAOYSA-N n',n'-dimethylethane-1,2-diamine Chemical compound CN(C)CCN DILRJUIACXKSQE-UHFFFAOYSA-N 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 238000006396 nitration reaction Methods 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 150000002828 nitro derivatives Chemical class 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 229940049964 oleate Drugs 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 229960001412 pentobarbital Drugs 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- DLYUQMMRRRQYAE-UHFFFAOYSA-N phosphorus pentoxide Inorganic materials O1P(O2)(=O)OP3(=O)OP1(=O)OP2(=O)O3 DLYUQMMRRRQYAE-UHFFFAOYSA-N 0.000 description 1
- 125000000612 phthaloyl group Chemical group C(C=1C(C(=O)*)=CC=CC1)(=O)* 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- XUWVIABDWDTJRZ-UHFFFAOYSA-N propan-2-ylazanide Chemical compound CC(C)[NH-] XUWVIABDWDTJRZ-UHFFFAOYSA-N 0.000 description 1
- 125000001501 propionyl group Chemical group O=C([*])C([H])([H])C([H])([H])[H] 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000002112 pyrrolidino group Chemical group [*]N1C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 150000003890 succinate salts Chemical class 0.000 description 1
- 238000000967 suction filtration Methods 0.000 description 1
- 229910052717 sulfur Chemical group 0.000 description 1
- 239000011593 sulfur Chemical group 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/16—Purine radicals
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Saccharide Compounds (AREA)
Abstract
내용 없음.
Description
본 발명은 아데노신 나이트레이트와 그의 산 부가염을 제조하는 방법에 관한 것이다.
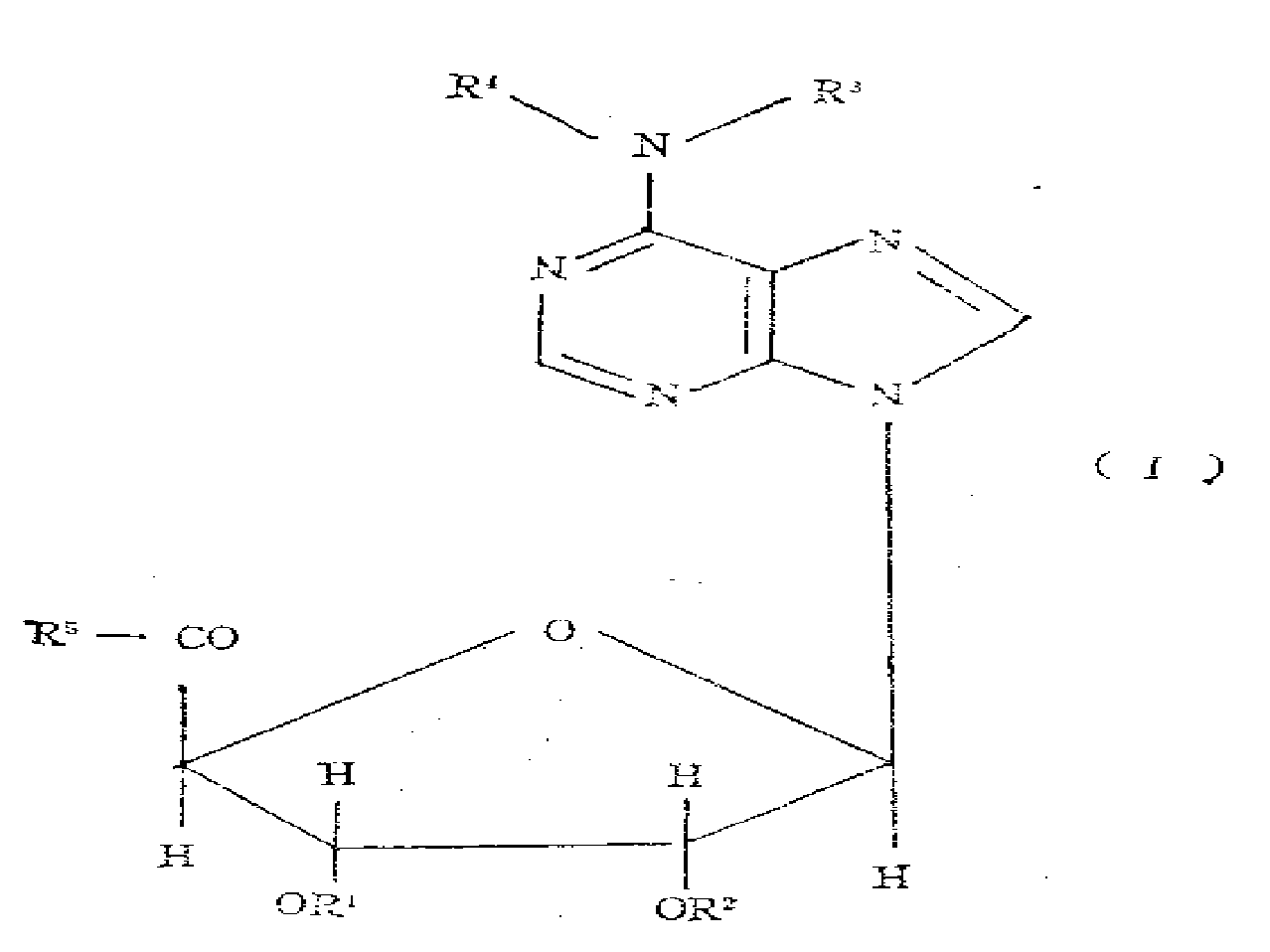
본 발명에 의해 제공되는 아데노신 나이트레이트는 아래의 일반구조식(Ⅰ)을 가지는 화합물 및 그의 생리적으로 무독한 산 부가염들이다.
상기 구조식에서
R1과 R2는 적어도 하나가 니트로그룹을 나타내며 다른 하나는 수소원자나 아실 또는 니트로기를 나타내고,
R3와 R4는 각각 수소원자나 아실그룹을 나타내거나 함께 지방족이나 방항족 디카복실산의 디아실잔기를 나타내며,
R5는 하이드록시, 저급알콕시, 아미노, (저급알킬)아미노, 디-(지급알킬) 아미노, 아릴-(저급알킬) 아미노, 사이클로알킬아미노 그룹이거나 질소윈자에 결합된 질소를 함유하는 복소환을 나타낸다.
일반구조식(I)화합물의 아군에는 일반구조식(I -1), (I -2)와 (I -3)이 있다.
여기서 Rl, R2와 R5는 상술한 바와 같고,
Rll, R2l은 적어도 니트로 그룹을 하나 갖고 있고 나머지는 아실이나 니트로그룹이다.
R31과R41은 각각 아실 잔기를 나타내거나 함께 지방족 또는 방향족 디카복실산의 디아실잔기를 나타낸다. 본 명세서에서 "저급알킬"과 저급 "알콕시"라는 표현은 1 내지 6 탄소원자를 함유하는 직쇄 또는 축쇄그룹(예로서 메틸, 메톡시, 에틸, 에톡시, 프로필, 프로폭시, 이소프로필, 이소프로폭시, 2급부틸, 2급부톡시, 3급부틸, 3급부톡시)을 포함한다. "아실"의 표현은 2 내지 10 탄소원자를 포함하는 지방족 또는 방향족의, 임의로 치환된 모노카복실산(예로서 에톡시카보닐, 아세틸, 프로피오닐, 부티릴, 이소바레릴, 피바로일, 아크릴로일, 프로피오릴, 메타아크릴로일, 크로토노일, 벤조일, 트루오일, 하이드라트로포일, 신나모일)의 잔기를 의미한다· 지방산의 디아실 잔기는 4 내지 10 탄소원자를 함유할 수 있다(예, 석신일, 글루타릴, 아디포일, 마레오일 시트라코노일, 프타로일).
(저급알킬) 아미노 및 디(저급알킬) 아미노 그룹의 예는 메틸아미노, 에틸아미노, 프로필아미노, 부틸아미노, 디메틸아미노, 디에틸아미노 및 디이소프로필 아미노이다. 아릴(저급알킬) 아미노그룹(특히 페닐-(저급알킬)-아미노 그룹이 바람직)의 예는 벤질아미노와 1- 및 2-펜에틸아미노 그룹이다. 사이클로 알킬아미노 그룹은 특별히 탄소원자 7개까지 함유하는 것들(예로서, 사이클로펜틸아미노 및 사이클로헥실아미노)이다. 질소원자에 결합되어 있는 질소 함유하는 복소환은 적어도 하나의 질소원자와 함께 산소나 유황같은 다른 복소원자를 포함할 수 있다. 5-원소 및 6-원소 복소환이 바람직하다. 이와 같은 환의 예는 아지리디노, 아제티디노, 피롤리디노, 피롤로, 이미다졸리디노, 피라졸리노, 티아졸리노, 티아졸리디노, 피페리디노, 몰포리노 및 아제피노 등이다.
구조식( I )의 화합물의 "생리적으로 무독한 산부가염"이란 염산염, 브롬화수소산염, 황산염, 중황산염, 인산염, 아세트산염, 젖산염, 올레산염, 질산염, 메틸설폰산염, 톨릴설폰산염, 구연산염, 말레산염, 호박산염, 주식산염 등과 같은 적당한 유기나 무기산 등의 염을 들수 있다.
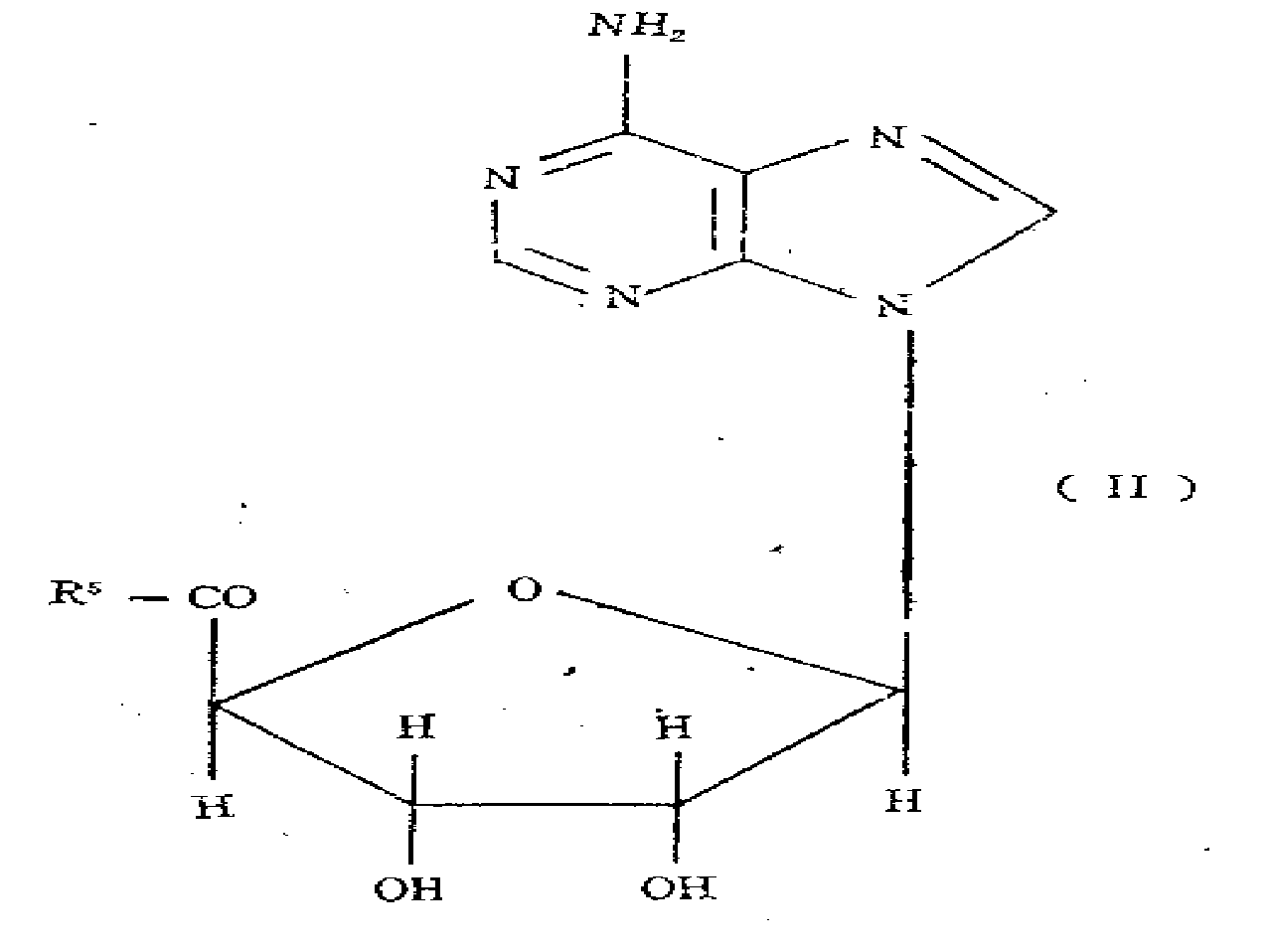
본 발명의 제조방법에 따라서, 앞서말한 아데노신 나이트레이트(즉 구조식(I)의 화합물과 그의 생리적으로 무독한 산부가염)는 다음 일반구조식(Ⅱ)의 화합물을 니트로화하고 임의로 0-및/또는 N-아실화하고 필요시 생성물을 생리적으로 무독한 산부가염으로 전환시켜 제조할 수 있다.
상기 구조식에서 R5는 상술한 바와 같다.
구조식(Ⅱ)의 화합물의 니트로화 및 아실화는 공지의 방법에 의해 수행된다.
고로 니트로화는, 예를들면 질산을 사용해서 수행될 수 있다. 가수분해(반응에서 생긴 물에 의한)나 탈아민화(존재하는 아질산에 의한)는 농황산, 발연황산, 오산화인, 무수초산과 같은 수(水)-결합제 및/또는 요소같은 아질산염 수용체를 가함으로써 쉽게 억제시킬 수 있다.
니트로화는 낮은 온도, 바람직하게는 -30℃에서 25℃ 사이, 그중에서도 특히 -10℃에서 0℃ 사이에서 쉽게 처리된다. 흔히, 문제의 2'-0-니트르, 3'-0-니트로 및 2',3'-디 0-니트로 화합물이 혼합물로 수득되는데, 이것은 기지의 방법(예로서, 크로마토그라피)에 따라 분리되고 순수한 화합물을 얻게된다.
그러나 2',3'-디-0-니트로화합물이 단일 생성물로 분리되도록 조작할 수 있으며, 이것은 앞서 말한 물-결합제를 사용할때 탁월하게 이루어질 수 있다.
니트로 화합물의 아실화는 염화앙세틸, 염화벤조일, 무수아세트산 같은 아실할라이드 또는 산무수물이나 활성화된 에스테르 같은 반응성 산유도체 또는 케텐과 반응시킴으르써 수행될 수 있다. 아실화는 피리딘, 트리에틸아민, 수용성 알카리 존재하에서 수행되어도 좋다. 이 경우 당의 하이드록시기는 바람직하게 에스테르화 되어진다. 선택적인 0-아실화는 비교적 낮은 온도와 짧은 시간이 유리하다.
온도가 높으면 높을수록 그리고 아실화시간이 길면 길수록 6-위치에 존재하는 아미노그룹 또한 처음에 모노아실 유도체로, 다음 디아실유도체로 아실화 한다. 일반적으로 모노-, 디-및/또는 트리아실 유도체의 흔합물이 생성물로 수득되는데, 기지의 방법으로 분리시킬 수 있다.
구조식(I) 화합물의 생리적으로 무독한 산부가염으로의 전환 및 생리적으로 무독하지 않은 부가염으로부터 그러한 염을 형성하는 것은 통상의 방법으로 수행될 수 있다.
구조식(Ⅰ) 화합물과 그의 생리적으로 무독한 산부가염은 실장과 순환계에 상당히 효과가 있으며 따라서 협심증이나 고혈압 치료약물로 사용된다. 투여 한계랑에 따르면 일일 체중 kg당 0.010 내지 30mg이 고려된다. 이러한 용량은 일회 용량으로서 뿐만아니라 여러회로 분할용량으르 투여될 수 있다.
관상 확장작용은 다음 방법에 따라 측정된다.
20 내지 30kg의 몽그랠(잡종의 개)을 시험에 사용한다. 시험동물을 정맥용 펜토바르비탈 약 30mg/kg으르 마취시킨다. 마취는 클로랄로스-우레탄으로 유지시킨다. 인공적으로 실내공기로 호흡하게 한다. 흉부를 열고 심장을 노출시킨 후 전자기 유동메터와 눈금이 새겨진 유동탐침을 흐르는 피의 양을 측정하기 위해서 왼쪽 관상동맥의 라무스-써컴푸랙써스(Ramus circumflexus)의 근처에 놓는다. 동맥압은 압력 변환기(pressure transducer)를 사용해서 대퇴동맥에 있는 카테테트를 거쳐 측정된다. 더우기 눈금이 새겨진 신축성 측정대(calibrated extensible measuring strip)을 심근 수측력의 직접 측정을 위해 좌심실의 표면에꿰매어 놓는다.
혈압의 맥파는 심박도수 측정용 타코그래프(tachograph)상에 기록된다. 화합물을 프로필렌 글리콜에 용해시켜 아라비아검에 현탁시켜 정맥내에나 십이지장 내에 투약한다. 물질의 최대작용은 각 투여량에 따른 출발값의 퍼센트(%)로 계산된다. 관상혈류 측정에서, 작용시간에 특별히 유의한다.
수득된 결과는 다음표에 나타나 있으며 여기서 n은 사용된 동물의 수이다.
[표 1]
본 발명의 아데노신 나이트레이트는 화합물질(배합할 수 있는 담체와 함께)의 직접 방출 혹은 서방출하는 제제형태로서 약물로 사용할 수 있다. 이 담체는 물, 젤라틴, 아라비아검, 유당, 전분, 스테아린산 마그네슘, 탈크, 식용유 폴리알킬렌글리콜 석유젤리 등과 같은, 장내투여, 경피투여, 비경구적 투여에 적당한 유기 혹은 무기불활성 담체다 될 수 있다. 제제는 고형(예:정제, 당의정, 좌약, 캡슐제)이나 반고형(예:연고제)나 액체(예:액제, 현탁제, 유화제)로 만들어질 수 있다. 제제는 무균이어야 하고 또는 보존제, 안정제, 습윤제, 유화제, 향료, 삼투압이나 완충액을 변화시키는 염등과 같은 보조제를 포함할 수 있다. 제제는 기지의 방법에 의해 제조된다.
구조식(Ⅱ)의 출발물질은 알려져 있거나 기지의 방법으로 기지화합물로부터 제조될 수 있다. 다음 실시예는 본 밭명에 의한 제조방법을 예시하였다.
[실시예 1]
6.7g의 요소를 -15℃에서 발연질산(d=1.5) 90㎖에 천천히 가하여 온도가 -10℃를 초과하지 않도록 한다. 이 용액에 연속적으로 -10℃에서 10.8g의 아데노산-5'-카복실산 에틸 에스테르를 가한다. 이 용액을 빙욕에서 3시간 교반하고 225g의 중탄산칼륨과 1000g의 빙수 혼합물 중에 도입하여 침전된 조생성믈(4.4g)을 흡인 여과한다. 클로로포름/메탄올(95:5)로 여액을 추출함으로써 또 다른 4.4g의 조생성물을수득하며 클로로포름/에틸 아세테이트/메탄올(45:45:10)을 용매로 실리카겔상 크로마토그라프하면 다음의 니트로아데노신을 얻게 된다:
융점 135℃ 이상(분해 )의 2',3'-디-0-니트로아데노산-5'-카복실산 에틸에스테르 2.65g(에틸아세테이트/클로로포름에서) ;
융점 170 내지 171℃(분해)의 2-0-니트로아데노신-5'-카복실산에틸 에스테르 0.41g(에틸아세테이트/디에틸에테르) ;
융점 166.5℃ 내지 167。C(분해)의 3'-0-니트로 아데노신-5'-카복실산에틸에스테르 1.3g(에탄올).
[실시예 2]
조심하여 100ml의 발연질산(d=1.50)을 6.7g의 요소로 -20℃에서 처리한다. 10.8g의 이데노신-5'-에틸아미드를 이 용액에 녹이고 온도를 -20℃로 유지시킨디. 이어 혼합물을 -20℃에서 교반한 후 천천히 가온하여 -5。C까지 올리며 총 5시간후 과량의 수용성 중탄산칼륨 용액(230g의 중탄산칼륨을 800ml의 물에 녹인)에 천천히 도입한다. 흡인여과한후 물로 침전을 세척하고 여액은 에틸아세테이트와 5%의 테트라하이드로 푸란의 혼합믈 400ml씩으로 5회 추출한다. 유기층은 포화염화나트륨 용액으르 세척하고 황산마그네슘 상에서 건조시켜 감압하 농축한다. 조생성물의 총수율은 11.5g에 상당한다.
조생정물을 3개의 질산염 에스테르로 분리하기 위해서 에탄올로 수희 재결정시키면 순수한 3'-0-니트로아데노신-5'-에틸아미드를 수득한다. 2',3'-디-0-니트로 아데노신-5'-에틸아미드가 아세토 니트릴로 결정시키므로써 모액으로부터 얻어지고 반면 클로로포름/메탄올/빙초산(90:10:1. V/V)을 용매로 실리카겔상 크로마토그라피를 하면 모액의 완전한 분리가 이루어져 2'-0-니트로아데노신-5'-카복실산에틸아미드를 수득하게 된다.
총수율은:
3.0g(24%)의 3'-0-니트로아데노신-5'-카복실산에틸아미드로 융점 210℃(분해)(에탄올) ;
2.5g(17.8%)의 2',3'-디 0-니트로 아데노신-5'-카복실산에틸 아미드로 융점 164℃(분해)(아세토니트릴);
0.77g(6.2%)의 2'-0-니트로아데노신-5'-카복실산에틸아미드로 융점 208℃(분해)(에탄올).
[실시예 3]
72ml의 발연질산을 4.9g의 요소로 -20℃에서 조심하여 처리한다. 6.9g의 아데노신-5'-카복실산아미드를 이 용액에 천천히 도입하되 혼합물의 온도가 -15℃ 이상 오르지 않도록 주의한다.
혼합물은 최소 5℃까지 빙냉시키면서 5시간 이상 교반한 후 과량의 중탄산 칼륨용액(175g의 중탄산칼륨을 500ml의 물에 용해)에 점적하여 가한다. 여기서 생성물의 일부가 침전된다. 흡인여과하고 물로 세척한후 2',3'-디-0-니트로 아데노신-5'-카복실산아미드와 3'-0-니트로아데노신-5'-카복실산아미드의 혼합물 2.9g을 수득하게 된다.
수용성 용액은 쿨로로포름과 5% 에탄올 150ml씩 3회 추출하고 이어 에틸아세테이트와 5% 테트라하이드로푸란의 150ml씩으로 3회 추출한다. 포화 염화나트륨 용액으르 세척하고 황산마그네슘 상에서 건조한후 클로로포름/에탄올 추출물을 농축하면 거의 순수한 2',3'-디-0-니트로 아데노신-5'-카복실산 아미드 2.0g을 수득하고 에틸 아세테이트/테트라하이드로푸란 추출물로부터 3'-0-니트로아데노신-5'-카복실산 아미드와 2'-올토-니트로 아데노신-5'-카복실산아미드의 혼합물 5.7g을 수득할 수 있다. 클로로포름/에탄올 추출물로 부터 수득된 잔유물의 반복된 재결정은 순수한 융점 172.5℃(분해)의 2',3'-디-0-니트로-아데노신-5'-카복실산아미드 1.17g (12.8%)을 얻는다. 에탄올/이소프로판올로부터 그리고 계속해서 메탄올/물로부터 얻은 에틸 아세테이트/테트라하이드로푸란 추출물로부터 수득된 잔류물의 반복적인 재결정으로부터 3'-0-니트로아데노신-5'-카복실산아미드 2.25g(28.1%)을 얻는다.
[실시예 4]
6.16g의 아데노신-5'-카복실산 디메틸아미드를 -40℃에서 60ml의 발연질산(d=1.50)에 용해시킨다.
-20℃까지 빙냉시킨 30ml의 발연황산과 30ml의 니트로메탄의 혼합물을 온도가 -30℃를 오르지 않는 속도로 30분내에 상기 용액에 점적하여 가한다. 혼합물을 -30℃와 -25℃ 사이의 온도에서 45분간 교반하고 물 1ℓ에 중탄산칼륨 325g을 녹인 용액에 쏟아 넣는다. 클로로포름이나 5% n-프로판올을 함유하는 클로로포름으로 추출환으로써 알콜로 재결정한 후 융점 156.5℃(분해)의 순수한 2',3'-디-0-니트르 아데노신-5'-카복실산 디메틸아미드를 수득한다. 수득량은 5.78g(이론의 72.7%)이다.
같은 방법으로 다음의 2',3'-디-0-니트로아데노신류가 얻어진다.
2',3'-디-0-니트로아데노신-5'-카복실산 이소프로필아미드로 융점 183℃(분해) 수율 77.4%;
2',3'-디-0-니트로아데노신-5'-카복실산사이클로헥실아미드로써 융점 168。(분해) 수율 69.5%;
2',3'-디-0-니트로아데노신-5'-카복실산 2-(디메틸아미노)-에틸-아미드로써 융점 169℃(분해 ), 수율 63%;
2',3'-디-0-니트로아데노신-5'-카복실산 2-(2,4-디니트로 페닐)-에틸-아미드로써 융점 134。C(분해), 수율 30.6%;
2',3'-디-0-니트로아데노신-5'-카복실산 피페리디드로써 융점 160℃(분해), 수율 76.2%;
2',3'-디-0-니트로아데노신-5'-카복실산2-(니트로옥시)-에틸-아미드로써 융점 164℃(분해),수율 58.9%;
2',3'-디-0-니트로아데노신-5'-카복실산 이소프로필 에스테르로써 융점 158℃(분해), 수율 71.6%
[실시예 5]
아데노신-5'-카복실산 디메틸아미드 6.16g을 발연질산 60ml와 반응시키고 실시예 4에 상술한 방법으로 진행시키면(발연황산/니트트 메탄을 가하지 않고) 융점 214℃(분해)의 3'-0-니트로아데노신-5'-카복실산디메틸아미드(이론상의 수율 21%)와 융점 156。C(분해)의 2',3'-디-0-니트로아데노신-5'-카복실산디메틸아미드(이론상 수율 9.3%)의 혼합물을 얻는다. 이상과 같이 실시예를 몇 개 보였으나 본 실시예가 본 발명의 범위를 제함함이 아님을 밝혀두며 다음에 나올 청구범위에 들어 있는 구조식에서 R5가 수소나 저급알콕시나 아미노나 (저급알킬)아미노 또는 디(저급알킬)아미노 그룹인 경우의 아데노신나이트레이트의 제조방법도 본 발명의 범위내임을 밝혀둔다.
Claims (1)
- 다음 일반구조식(Ⅱ)의 화합물을 니트로화 하고 해당한 0-또는 N-아실화해서 다음 일반구조식(I)의 아데노신나이트레이트 및 그의 산 부가염을 제조하는 방법.상기 구조식에서R1과 R2는 적어도 하나가 니트로그룹을 나타내며 다른 하나는 수소원자이거나 아실 또는 니트로기를 나타내고,R3및 R4는 각각 수소원자 또는 아실그룹을 나타내거나, 함께 지방족 또는 방향족 디카복실산의 디아실잔기를 나타내며,R5는 하이드록시, 저급알콕시, 아미노,(저급알킬)아미노, 디-(저급알킬)아미노, 아릴-(저급알킬) 아미노 또는 사이클로알킬아미노 그룹이거나 질소원자에 결합된 질소 원자를 함유하는 복소환을 나타낸다.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR7600379A KR800000045B1 (ko) | 1976-02-16 | 1976-02-16 | 아데노신 나이트레이트의 제조방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR7600379A KR800000045B1 (ko) | 1976-02-16 | 1976-02-16 | 아데노신 나이트레이트의 제조방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR800000045B1 true KR800000045B1 (ko) | 1980-01-28 |
Family
ID=19201979
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR7600379A Expired KR800000045B1 (ko) | 1976-02-16 | 1976-02-16 | 아데노신 나이트레이트의 제조방법 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR800000045B1 (ko) |
-
1976
- 1976-02-16 KR KR7600379A patent/KR800000045B1/ko not_active Expired
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US4443475A (en) | Amides of acyl-carnitines, process for preparing same and pharmaceutical compositions containing such amides | |
| US5063247A (en) | Diphenylurea derivatives | |
| EP0283390B1 (fr) | Dérivés du thiazole actifs sur le système cholinergique, procédé d'obtention et compositions pharmaceutiques en contenant | |
| WO1996009287A1 (en) | Novel heterocyclic derivatives, process for producing the same, and medicinal use thereof | |
| US4479951A (en) | 1.4;3.6-Dianhydrohexitol nitrates substituted by purine bases, processes for their preparation and pharmaceutical compositions | |
| US4104462A (en) | Cardioactive adenosine nitrates | |
| US4340730A (en) | N6 -Substituted adenosines | |
| KR800000045B1 (ko) | 아데노신 나이트레이트의 제조방법 | |
| FR2596051A1 (fr) | Nouveaux derives de la purine, leur preparation et leur utilisation comme medicaments | |
| US3914414A (en) | Method of increasing coronary pO{HD 2 {B in mammals | |
| US4942143A (en) | Imidazothiadiazine derivatives, and their use as medicaments | |
| HU197746B (en) | Process for producing xantin derivatives and pharmaceutical compositions containing them | |
| WO1995018817A1 (fr) | Nouveaux derives de l'adenosine, leurs procedes de preparation, compositions pharmaceutiques les contenant | |
| EP0000452B1 (fr) | Dérivés d'oxadiazole-1,2,4, leur préparation et leur application en thérapeutique. | |
| SE455701B (sv) | Svavelhaltiga isokinolinderivat samt farmaceutiska beredningar innehalllande dem | |
| EP0252422B1 (en) | Pyridazinone derivatives and salts thereof | |
| US4115641A (en) | Ribofuranosyl-imidazole derivatives | |
| IE43210B1 (en) | Nitrates of adenosine-5'-carboxylic acid derivatives, process for their manufacture, and pharmaceutical preparations containing them | |
| US4745118A (en) | Substituted quinazoline-3-oxides providing pharmacological activity | |
| US4508735A (en) | Anti-arrhythmic N-alkanoylaminoalkyl fluorenes | |
| US3971849A (en) | 1,N6 -etheno-5'-adenosine carboxylates for increasing coronary sinus partial pressure of oxygen | |
| US4720501A (en) | 2-(2-thienyl)-imidazo(4,5-c)pyridine derivatives and salts thereof useful in the treatment of myocardial insufficiency | |
| US4182876A (en) | Substituted-phthalazone 7-carboxylic acid and salts and process for preparing same | |
| US4131676A (en) | 2,6-Bis(1-morpholinoalkylideneamino)anthraquinones as anti-amebic agents | |
| US3974164A (en) | Reserpic acid derivatives |