RU2012128351A - Кристаллические формы 3-(2,6-дихлор-3,5-диметоксифенил)-1-{6-[4-(4-этилпиперазин-1-ил)-фениламино]-пиримидин-4-ил}-1-метилмочевины и ее долей - Google Patents
Кристаллические формы 3-(2,6-дихлор-3,5-диметоксифенил)-1-{6-[4-(4-этилпиперазин-1-ил)-фениламино]-пиримидин-4-ил}-1-метилмочевины и ее долей Download PDFInfo
- Publication number
- RU2012128351A RU2012128351A RU2012128351/04A RU2012128351A RU2012128351A RU 2012128351 A RU2012128351 A RU 2012128351A RU 2012128351/04 A RU2012128351/04 A RU 2012128351/04A RU 2012128351 A RU2012128351 A RU 2012128351A RU 2012128351 A RU2012128351 A RU 2012128351A
- Authority
- RU
- Russia
- Prior art keywords
- crystalline form
- powder
- anhydrous crystalline
- ray
- expressed
- Prior art date
Links
- -1 2,6-Dichloro-3,5-dimethoxyphenyl Chemical group 0.000 title 2
- 239000013078 crystal Substances 0.000 title 1
- 210000002700 urine Anatomy 0.000 title 1
- 239000000843 powder Substances 0.000 claims abstract 13
- 150000004682 monohydrates Chemical class 0.000 claims abstract 12
- 150000001875 compounds Chemical class 0.000 claims abstract 10
- 238000000634 powder X-ray diffraction Methods 0.000 claims abstract 9
- 238000000113 differential scanning calorimetry Methods 0.000 claims abstract 8
- 238000001757 thermogravimetry curve Methods 0.000 claims abstract 8
- 239000002253 acid Substances 0.000 claims 9
- 150000003839 salts Chemical class 0.000 claims 9
- 238000000034 method Methods 0.000 claims 6
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 claims 5
- 201000010099 disease Diseases 0.000 claims 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims 5
- 108091000080 Phosphotransferase Proteins 0.000 claims 3
- 239000000203 mixture Substances 0.000 claims 3
- 102000020233 phosphotransferase Human genes 0.000 claims 3
- 239000000725 suspension Substances 0.000 claims 3
- WEVYNIUIFUYDGI-UHFFFAOYSA-N 3-[6-[4-(trifluoromethoxy)anilino]-4-pyrimidinyl]benzamide Chemical compound NC(=O)C1=CC=CC(C=2N=CN=C(NC=3C=CC(OC(F)(F)F)=CC=3)C=2)=C1 WEVYNIUIFUYDGI-UHFFFAOYSA-N 0.000 claims 2
- 101100067974 Arabidopsis thaliana POP2 gene Proteins 0.000 claims 2
- ZEOWTGPWHLSLOG-UHFFFAOYSA-N Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F Chemical compound Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F ZEOWTGPWHLSLOG-UHFFFAOYSA-N 0.000 claims 2
- 101100481408 Danio rerio tie2 gene Proteins 0.000 claims 2
- 102000001301 EGF receptor Human genes 0.000 claims 2
- 102100023593 Fibroblast growth factor receptor 1 Human genes 0.000 claims 2
- 101710182386 Fibroblast growth factor receptor 1 Proteins 0.000 claims 2
- 102100023600 Fibroblast growth factor receptor 2 Human genes 0.000 claims 2
- 101710182389 Fibroblast growth factor receptor 2 Proteins 0.000 claims 2
- 102100027842 Fibroblast growth factor receptor 3 Human genes 0.000 claims 2
- 101710182396 Fibroblast growth factor receptor 3 Proteins 0.000 claims 2
- 102100027844 Fibroblast growth factor receptor 4 Human genes 0.000 claims 2
- 101100118549 Homo sapiens EGFR gene Proteins 0.000 claims 2
- 101000917134 Homo sapiens Fibroblast growth factor receptor 4 Proteins 0.000 claims 2
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 claims 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 claims 2
- 101100481410 Mus musculus Tek gene Proteins 0.000 claims 2
- 206010028980 Neoplasm Diseases 0.000 claims 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims 2
- 238000001069 Raman spectroscopy Methods 0.000 claims 2
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 claims 2
- 101100123851 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) HER1 gene Proteins 0.000 claims 2
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 claims 2
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 claims 2
- 230000000694 effects Effects 0.000 claims 2
- 230000007170 pathology Effects 0.000 claims 2
- 208000024891 symptom Diseases 0.000 claims 2
- 206010004446 Benign prostatic hyperplasia Diseases 0.000 claims 1
- 201000009030 Carcinoma Diseases 0.000 claims 1
- 208000004403 Prostatic Hyperplasia Diseases 0.000 claims 1
- 201000004681 Psoriasis Diseases 0.000 claims 1
- 206010039491 Sarcoma Diseases 0.000 claims 1
- 210000004100 adrenal gland Anatomy 0.000 claims 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims 1
- 210000000481 breast Anatomy 0.000 claims 1
- 210000001072 colon Anatomy 0.000 claims 1
- 150000004683 dihydrates Chemical class 0.000 claims 1
- 239000003085 diluting agent Substances 0.000 claims 1
- 239000003814 drug Substances 0.000 claims 1
- 239000003937 drug carrier Substances 0.000 claims 1
- 208000005017 glioblastoma Diseases 0.000 claims 1
- 230000002401 inhibitory effect Effects 0.000 claims 1
- 210000003734 kidney Anatomy 0.000 claims 1
- 208000032839 leukemia Diseases 0.000 claims 1
- 210000004185 liver Anatomy 0.000 claims 1
- 210000004072 lung Anatomy 0.000 claims 1
- 230000009826 neoplastic cell growth Effects 0.000 claims 1
- 210000001672 ovary Anatomy 0.000 claims 1
- 210000000496 pancreas Anatomy 0.000 claims 1
- 239000000546 pharmaceutical excipient Substances 0.000 claims 1
- 210000002307 prostate Anatomy 0.000 claims 1
- 210000000664 rectum Anatomy 0.000 claims 1
- 210000002784 stomach Anatomy 0.000 claims 1
- 210000001685 thyroid gland Anatomy 0.000 claims 1
- 210000003932 urinary bladder Anatomy 0.000 claims 1
- 210000001215 vagina Anatomy 0.000 claims 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/46—Two or more oxygen, sulphur or nitrogen atoms
- C07D239/48—Two nitrogen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Hematology (AREA)
- Oncology (AREA)
- Endocrinology (AREA)
- Reproductive Health (AREA)
- Dermatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
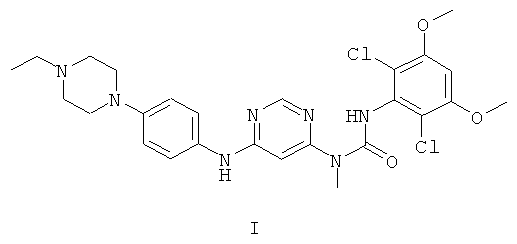
1. Безводная кристаллическая форма соединения формулы Iгде безводная кристаллическая форма обладает порошковой рентгенограммой, содержащей характеристический пик, выраженный в 2θ, расположенный примерно при 12°.2. Безводная кристаллическая форма по п.1, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 10,5°, примерно при 15,2°, примерно при 19,5° и примерно при 21,0°.3. Безводная кристаллическая форма по п.1, обладающая порошковой рентгенограммой, в основном такой, как представленная на фиг.1A.4. Безводная кристаллическая форма по п.1, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, на которой начало эндотермы расположено примерно при 217°C.5. Безводная кристаллическая форма по п.1, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, в основном такой, как представленная на фиг.2A.6. Кристаллическая форма моногидрата соединения формулы Iгде кристаллическая форма моногидрата обладает порошковой рентгенограммой, содержащей характеристический пик, выраженный в 2θ, расположенный примерно при 20,3°.7. Кристаллическая форма моногидрата по п.6, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 21,3° и примерно при 18,8°.8. Кристаллическая форма моногидрата по п.7, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных
Claims (38)
2. Безводная кристаллическая форма по п.1, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 10,5°, примерно при 15,2°, примерно при 19,5° и примерно при 21,0°.
3. Безводная кристаллическая форма по п.1, обладающая порошковой рентгенограммой, в основном такой, как представленная на фиг.1A.
4. Безводная кристаллическая форма по п.1, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, на которой начало эндотермы расположено примерно при 217°C.
5. Безводная кристаллическая форма по п.1, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, в основном такой, как представленная на фиг.2A.
7. Кристаллическая форма моногидрата по п.6, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 21,3° и примерно при 18,8°.
8. Кристаллическая форма моногидрата по п.7, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 4,7°, примерно при 9,4° и примерно при 11,0°.
9. Кристаллическая форма моногидрата по любому из пп.6-8, обладающая порошковой рентгенограммой, в основном такой, как представленная на фиг.1Г.
10. Кристаллическая форма моногидрата по любому из пп.6-8, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, на которой начало эндотермы расположено примерно при 211°C.
11. Кристаллическая форма моногидрата по любому из пп.6-8, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, в основном такой, как представленная на фиг.7.
12. Кристаллическая форма моногидрата по любому из пп.6-8, обладающая характеристическими пиками комбинационного рассеяния, расположенными примерно при 2957, примерно при 2831, примерно при 1618, примерно при 1511, примерно при 1465, примерно при 1361, примерно при 1229, примерно при 1186 и примерно при 994 см-1.
14. Соль монофосфорной кислоты по п.13, которая представляет собой безводную кристаллическую соль монофосфорной кислоты.
15. Безводная кристаллическая соль монофосфорной кислоты по п.14 в форме A, где форма A обладает порошковой рентгенограммой, содержащей характеристический пик, выраженный в 2θ, расположенный примерно при 15°.
16. Безводная кристаллическая соль монофосфорной кислоты в форме A по п.15, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 13,7°, примерно при 16,8°, примерно при 21,3° и примерно при 22,4°.
17. Безводная кристаллическая соль монофосфорной кислоты в форме A по п.16, для которой порошковая рентгенограмма дополнительно содержит один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 9,2°, примерно при 9,6°, примерно при 18,7°, примерно при 20,0°, примерно при 22,9° и примерно при 27,2°.
18. Безводная кристаллическая форма (форма А) соли монофосфорной кислоты соединения формулы I
где безводная кристаллическая форма A обладает порошковой рентгенограммой, содержащей не менее 3 характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 13,7°, примерно при 15°, примерно при 16,8°, примерно при 21,3° и примерно при 22,4°.
19. Безводная кристаллическая форма по любому из пп.15-18, обладающая порошковой рентгенограммой, в основном такой, как представленная на фиг.1Б.
20. Безводная кристаллическая форма по любому из пп.15-18, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, на которой начало эндотермы расположено примерно при 184°C.
21. Безводная кристаллическая форма по любому из пп.15-18, обладающая полученной с помощью дифференциальной сканирующей калориметрии термограммой, в основном такой, как представленная на фиг.2Б.
22. Безводная кристаллическая форма по любому из пп.15-18, обладающая характеристическими пиками комбинационного рассеяния, расположенными примерно при 2950, примерно при 1619, примерно при 1539, примерно при 1297, примерно при 1233, примерно при 1191 и примерно при 998 см-1.
23. Безводная кристаллическая соль монофосфорной кислоты по п.14 в форме B, где форма B обладает порошковой рентгенограммой, содержащей один или большее количество характеристических пиков, выраженных в 2θ,выбранных из числа пиков, расположенных примерно при 9,3°, примерно при 12,5°, примерно при 13,4°, примерно при 15,8° и примерно при 17°.
24. Безводная кристаллическая форма по п.23, обладающая порошковой рентгенограммой, в основном такой, как представленная на фиг.1В.
27. Гидрохлорид по п.26, который представляет собой кристаллический дигидрат.
28. Кристаллический гидрохлорид по п.26 или 27, обладающий порошковой рентгенограммой, содержащей один или большее количество характеристических пиков, выраженных в 2θ, выбранных из числа пиков, расположенных примерно при 10,9°, примерно при 12,1°, примерно при 14,8°, примерно при 20,5°, примерно при 22° и примерно при 25,1°.
29. Кристаллический гидрохлорид по п.26 или 27, обладающий порошковой рентгенограммой, в основном такой, как представленная на фиг.1Д.
30. Гидрохлорид по п.26, который представляет собой аморфную форму.
32. Способ по п.31, дополнительно включающий кристаллизацию безводной кристаллической формы А из суспензии.
33. Способ по п.32, в котором суспензия соединения формулы I содержит изопропанол.
34. Способ по п.31, дополнительно включающий выделение закристаллизовавшейся безводной кристаллической формы А.
35. Композиция, содержащая кристаллическую или аморфную форму по любому из пп.1-30 и фармацевтически приемлемый носитель, инертный наполнитель или разбавитель.
36. Способ лечения, включающий введение терапевтически эффективного количества кристаллической или аморфной формы по любому из пп.1-30 или композиции по п.35 субъекту, страдающему от заболевания, патологии и/или симптомов, когда заболевание можно предупредить, подавить или облегчить его протекание путем ингибирования активности киназы, где киназа выбрана из группы, включающей FGFR1, FGFR2, FGFR3, FGFR4, KDR, HER1, HER2, Bcr-Abl, Tie2 и Ret.
37. Способ по п.36, в котором заболевание выбрано из группы, включающей карциному почек, печени, надпочечников, мочевого пузыря, молочной железы, желудка, яичников, толстой кишки, прямой кишки, предстательной железы, поджелудочной железы, легких, влагалища или щитовидной железы; саркому; глиобластому; лейкоз; опухоли головы или шеи; псориаз; гиперплазию предстательной железы; или неоплазию.
38. Применение кристаллической или аморфной формы по любому из пп.1-30 или композиции по п.35 для приготовления лекарственного средства, предназначенного для лечения у субъекта заболевания, при котором активность киназы FGFR1, FGFR2, FGFR3, FGFR4, KDR, HER1, HER2, Bcr-Abl, Tie2 и/или Ret способствует патологии и/или симптоматике заболевания.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US26715509P | 2009-12-07 | 2009-12-07 | |
| US61/267,155 | 2009-12-07 | ||
| PCT/US2010/059108 WO2011071821A1 (en) | 2009-12-07 | 2010-12-06 | Crystalline forms of 3-(2,6-dichloro-3,5-dimethoxy-phenyl)-1-{6-[4-(4-ethyl-piperazin-1-yl)-phenylamino]-pyrimidin-4-yl}-1-methyl-urea and salts thereof. |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2012128351A true RU2012128351A (ru) | 2014-01-20 |
| RU2572848C2 RU2572848C2 (ru) | 2016-01-20 |
Family
ID=43983750
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2012128351/04A RU2572848C2 (ru) | 2009-12-07 | 2010-12-06 | Кристаллические формы 3-(2,6-дихлор-3,5-диметоксифенил)-1-{ 6-[4-(4-этилпиперазин-1-ил)-фениламино]-пиримидин-4-ил} -1-метилмочевины и ее долей |
Country Status (32)
| Country | Link |
|---|---|
| US (1) | US9067896B2 (ru) |
| EP (1) | EP2509963B1 (ru) |
| JP (2) | JP5714024B2 (ru) |
| KR (1) | KR101787784B1 (ru) |
| CN (5) | CN105061332A (ru) |
| AR (2) | AR079257A1 (ru) |
| AU (1) | AU2010328391B2 (ru) |
| BR (1) | BR112012013784B1 (ru) |
| CA (1) | CA2781431C (ru) |
| CL (1) | CL2012001480A1 (ru) |
| DK (1) | DK2509963T3 (ru) |
| EC (1) | ECSP12012026A (ru) |
| ES (1) | ES2562462T3 (ru) |
| GT (1) | GT201200181A (ru) |
| HR (1) | HRP20160126T1 (ru) |
| HU (1) | HUE026983T2 (ru) |
| IL (1) | IL220012B (ru) |
| JO (1) | JO3061B1 (ru) |
| MA (1) | MA33849B1 (ru) |
| MX (1) | MX2012006562A (ru) |
| MY (1) | MY158333A (ru) |
| NZ (3) | NZ624315A (ru) |
| PE (1) | PE20121499A1 (ru) |
| PH (2) | PH12012501146A1 (ru) |
| PL (1) | PL2509963T3 (ru) |
| RU (1) | RU2572848C2 (ru) |
| SG (1) | SG10201408063SA (ru) |
| SI (1) | SI2509963T1 (ru) |
| TN (1) | TN2012000263A1 (ru) |
| TW (1) | TWI526440B (ru) |
| WO (1) | WO2011071821A1 (ru) |
| ZA (1) | ZA201203612B (ru) |
Families Citing this family (56)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0512324D0 (en) * | 2005-06-16 | 2005-07-27 | Novartis Ag | Organic compounds |
| AR079257A1 (es) * | 2009-12-07 | 2012-01-04 | Novartis Ag | Formas cristalinas de 3-(2,6-dicloro-3-5-dimetoxi-fenil)-1-{6-[4-(4-etil-piperazin-1-il)-fenil-amino]-pirimidin-4-il}-1-metil-urea y sales de las mismas |
| WO2012088266A2 (en) | 2010-12-22 | 2012-06-28 | Incyte Corporation | Substituted imidazopyridazines and benzimidazoles as inhibitors of fgfr3 |
| IN2014DN08969A (ru) | 2012-03-30 | 2015-05-22 | Novartis Ag | |
| HRP20170430T1 (hr) | 2012-06-13 | 2017-06-16 | Incyte Holdings Corporation | Supstituirani triciklični spojevi kao inhibitori fgfr |
| WO2014026125A1 (en) | 2012-08-10 | 2014-02-13 | Incyte Corporation | Pyrazine derivatives as fgfr inhibitors |
| US9266892B2 (en) | 2012-12-19 | 2016-02-23 | Incyte Holdings Corporation | Fused pyrazoles as FGFR inhibitors |
| AR094812A1 (es) | 2013-02-20 | 2015-08-26 | Eisai R&D Man Co Ltd | Derivado de piridina monocíclico como inhibidor del fgfr |
| CA2907243C (en) | 2013-03-15 | 2021-12-28 | Celgene Avilomics Research, Inc. | Substituted dihydropyrimidopyrimidinone compounds and pharmaceutical compositions thereof use fgfr4 inhibitor |
| AR095464A1 (es) | 2013-03-15 | 2015-10-21 | Celgene Avilomics Res Inc | Compuestos de heteroarilo y usos de los mismos |
| WO2014144737A1 (en) | 2013-03-15 | 2014-09-18 | Celgene Avilomics Research, Inc. | Heteroaryl compounds and uses thereof |
| WO2014155268A2 (en) | 2013-03-25 | 2014-10-02 | Novartis Ag | Fgf-r tyrosine kinase activity inhibitors - use in diseases associated with lack of or reduced snf5 activity |
| PL2986610T4 (pl) | 2013-04-19 | 2019-06-28 | Incyte Holdings Corporation | Bicykliczne heterocykle jako inhibitory FGFR |
| EP3019491A4 (en) | 2013-07-09 | 2016-12-21 | Dana Farber Cancer Inst Inc | KINASEHEMMER FOR THE TREATMENT OF DISEASES |
| PE20160679A1 (es) | 2013-10-18 | 2016-08-04 | Eisai Randd Man Co Ltd | Inhibidores de pirimidina del fgfr4 |
| PT3079667T (pt) | 2013-12-13 | 2019-10-10 | Novartis Ag | Formas de dosagem farmacêutica |
| AU2015304465B2 (en) | 2014-08-18 | 2019-05-09 | Eisai R&D Management Co., Ltd. | Salt of monocyclic pyridine derivative and crystal thereof |
| US20170304313A1 (en) | 2014-10-06 | 2017-10-26 | Novartis Ag | Therapeutic Combination For The Treatment Of Cancer |
| US10851105B2 (en) | 2014-10-22 | 2020-12-01 | Incyte Corporation | Bicyclic heterocycles as FGFR4 inhibitors |
| MA41551A (fr) | 2015-02-20 | 2017-12-26 | Incyte Corp | Hétérocycles bicycliques utilisés en tant qu'inhibiteurs de fgfr4 |
| WO2016134294A1 (en) | 2015-02-20 | 2016-08-25 | Incyte Corporation | Bicyclic heterocycles as fgfr4 inhibitors |
| MY197720A (en) | 2015-02-20 | 2023-07-10 | Incyte Corp | Bicyclic heterocycles as fgfr inhibitors |
| ES2887148T3 (es) | 2015-03-25 | 2021-12-21 | Nat Cancer Ct | Agente terapéutico contra el cáncer de vías biliares |
| CN107787226A (zh) * | 2015-03-25 | 2018-03-09 | 诺华股份有限公司 | 药物组合 |
| SG10201810057UA (en) | 2015-04-14 | 2018-12-28 | Eisai R&D Man Co Ltd | Crystalline fgfr4 inhibitor compound and uses thereof |
| CN104803925B (zh) * | 2015-04-16 | 2018-01-12 | 温州医科大学 | 一类以fgfr为靶点的2,4,5‑三取代嘧啶类化合物及其制备方法和用途 |
| WO2016189472A1 (en) | 2015-05-28 | 2016-12-01 | Novartis Ag | Fgfr inhibitor for use in the treatment of the phosphaturic mesenchymal tumor |
| CN108367000A (zh) | 2015-12-17 | 2018-08-03 | 卫材R&D管理有限公司 | 用于乳腺癌的治疗剂 |
| WO2017196854A1 (en) | 2016-05-10 | 2017-11-16 | Eisai R&D Management Co., Ltd. | Drug combinations for reducing cell viability and/or cell proliferation |
| EP3459952B1 (en) * | 2016-05-20 | 2022-01-05 | Zhejiang Hisun Pharmaceutical Co., Ltd. | Pyrimidine derivative, method for preparing same and use thereof in medicine |
| ES2966469T3 (es) * | 2016-08-23 | 2024-04-22 | Eisai R&D Man Co Ltd | Terapias combinadas para el tratamiento del carcinoma hepatocelular |
| AR111960A1 (es) | 2017-05-26 | 2019-09-04 | Incyte Corp | Formas cristalinas de un inhibidor de fgfr y procesos para su preparación |
| CN107176954B (zh) | 2017-06-02 | 2019-01-11 | 无锡双良生物科技有限公司 | 一种egfr抑制剂的药用盐及其晶型、制备方法和应用 |
| CN111315741B (zh) * | 2017-11-01 | 2023-01-24 | 广东众生药业股份有限公司 | 一种作为fgfr4抑制剂化合物的盐型、晶型及其制备方法 |
| MX2020008610A (es) | 2018-03-28 | 2020-09-21 | Eisai R&D Man Co Ltd | Agente terapeutico para carcinoma hepatocelular. |
| JP7568512B2 (ja) | 2018-05-04 | 2024-10-16 | インサイト・コーポレイション | Fgfr阻害剤の塩 |
| BR112020022392A2 (pt) | 2018-05-04 | 2021-02-02 | Incyte Corporation | formas sólidas de um inibidor de fgfr e processos para preparação das mesmas |
| US11628162B2 (en) | 2019-03-08 | 2023-04-18 | Incyte Corporation | Methods of treating cancer with an FGFR inhibitor |
| WO2021007269A1 (en) | 2019-07-09 | 2021-01-14 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| US12122767B2 (en) | 2019-10-01 | 2024-10-22 | Incyte Corporation | Bicyclic heterocycles as FGFR inhibitors |
| KR20220088712A (ko) * | 2019-10-14 | 2022-06-28 | 허치슨 메디파르마 리미티드 | 화합물의 염 및 이의 결정질 형태 |
| JP7675711B2 (ja) | 2019-10-14 | 2025-05-13 | インサイト・コーポレイション | Fgfr阻害剤としての二環式複素環 |
| WO2021076728A1 (en) | 2019-10-16 | 2021-04-22 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| CA3163875A1 (en) | 2019-12-04 | 2021-06-10 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| PE20221504A1 (es) | 2019-12-04 | 2022-09-30 | Incyte Corp | Derivados de un inhibidor de fgfr |
| WO2021146424A1 (en) | 2020-01-15 | 2021-07-22 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| CA3202267A1 (en) * | 2020-12-18 | 2022-06-23 | Riccardo Panicucci | Methods of treating achondroplasia |
| WO2022221170A1 (en) | 2021-04-12 | 2022-10-20 | Incyte Corporation | Combination therapy comprising an fgfr inhibitor and a nectin-4 targeting agent |
| EP4352060A1 (en) | 2021-06-09 | 2024-04-17 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| AR126102A1 (es) | 2021-06-09 | 2023-09-13 | Incyte Corp | Heterociclos tricíclicos como inhibidores de fgfr |
| US11583602B2 (en) | 2021-06-23 | 2023-02-21 | Kimtron, Inc. | System and method for ultra-close proximity irradiation of rotating biomass |
| WO2023174400A1 (zh) * | 2022-03-18 | 2023-09-21 | 上海润石医药科技有限公司 | 一种取代的氨基六元氮杂环类化合物的盐及其晶型、制备方法和应用 |
| CN115785001B (zh) * | 2022-11-23 | 2023-09-15 | 斯坦德药典标准物质研发(湖北)有限公司 | 一种英菲格拉替尼的制备方法 |
| JP2026507903A (ja) | 2023-03-06 | 2026-03-06 | キューイーディー セラピューティクス,インコーポレイテッド | 骨格形成異常の治療方法 |
| WO2025061013A1 (zh) * | 2023-09-18 | 2025-03-27 | 上海润石医药科技有限公司 | 包含杂芳基氧基萘类化合物的药物组合物及其制备方法和应用 |
| WO2025090870A1 (en) | 2023-10-27 | 2025-05-01 | Qed Therapeutics, Inc. | Infigratinib and metabolites thereof for use in methods of treating skeletal disorders |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0512324D0 (en) * | 2005-06-16 | 2005-07-27 | Novartis Ag | Organic compounds |
| CN101242843A (zh) * | 2005-06-10 | 2008-08-13 | 詹森药业有限公司 | 作为激酶调节剂的氨基嘧啶类化合物 |
| EP1957516B1 (en) * | 2005-11-08 | 2016-03-09 | Choongwae Pharma Corporation | Alfa-helix mimetics and method relating to the treatment of cancer stem cells |
| WO2007071752A2 (en) * | 2005-12-21 | 2007-06-28 | Novartis Ag | Pyrimidinyl aryl urea derivatives being fgf inhibitors |
| SG190592A1 (en) * | 2008-04-29 | 2013-06-28 | Novartis Ag | Methods of monitoring the modulation of the kinase activity of fibroblast growth factor receptor and uses of said methods |
| AR079257A1 (es) * | 2009-12-07 | 2012-01-04 | Novartis Ag | Formas cristalinas de 3-(2,6-dicloro-3-5-dimetoxi-fenil)-1-{6-[4-(4-etil-piperazin-1-il)-fenil-amino]-pirimidin-4-il}-1-metil-urea y sales de las mismas |
-
2010
- 2010-12-03 AR ARP100104472A patent/AR079257A1/es not_active Application Discontinuation
- 2010-12-05 JO JOP/2010/0433A patent/JO3061B1/ar active
- 2010-12-06 KR KR1020127017618A patent/KR101787784B1/ko active Active
- 2010-12-06 CN CN201510484635.8A patent/CN105061332A/zh active Pending
- 2010-12-06 NZ NZ624315A patent/NZ624315A/en unknown
- 2010-12-06 SI SI201031119A patent/SI2509963T1/sl unknown
- 2010-12-06 DK DK10788479.3T patent/DK2509963T3/en active
- 2010-12-06 TW TW099142438A patent/TWI526440B/zh active
- 2010-12-06 PE PE2012000772A patent/PE20121499A1/es active IP Right Grant
- 2010-12-06 PH PH1/2012/501146A patent/PH12012501146A1/en unknown
- 2010-12-06 RU RU2012128351/04A patent/RU2572848C2/ru active
- 2010-12-06 JP JP2012543183A patent/JP5714024B2/ja active Active
- 2010-12-06 CN CN201911272657.2A patent/CN111100077A/zh active Pending
- 2010-12-06 CN CN201911278014.9A patent/CN111269186A/zh active Pending
- 2010-12-06 HU HUE10788479A patent/HUE026983T2/en unknown
- 2010-12-06 HR HRP20160126T patent/HRP20160126T1/hr unknown
- 2010-12-06 EP EP10788479.3A patent/EP2509963B1/en active Active
- 2010-12-06 US US13/514,308 patent/US9067896B2/en active Active
- 2010-12-06 NZ NZ700778A patent/NZ700778A/en unknown
- 2010-12-06 CN CN201911273119.5A patent/CN111100078A/zh active Pending
- 2010-12-06 MY MYPI2012002222A patent/MY158333A/en unknown
- 2010-12-06 WO PCT/US2010/059108 patent/WO2011071821A1/en not_active Ceased
- 2010-12-06 PH PH12014502593A patent/PH12014502593A1/en unknown
- 2010-12-06 PL PL10788479T patent/PL2509963T3/pl unknown
- 2010-12-06 MX MX2012006562A patent/MX2012006562A/es active IP Right Grant
- 2010-12-06 ES ES10788479.3T patent/ES2562462T3/es active Active
- 2010-12-06 CN CN2010800550783A patent/CN102639510A/zh active Pending
- 2010-12-06 AU AU2010328391A patent/AU2010328391B2/en active Active
- 2010-12-06 BR BR112012013784-0A patent/BR112012013784B1/pt active IP Right Grant
- 2010-12-06 NZ NZ600070A patent/NZ600070A/en unknown
- 2010-12-06 SG SG10201408063SA patent/SG10201408063SA/en unknown
- 2010-12-06 CA CA2781431A patent/CA2781431C/en active Active
-
2012
- 2012-05-17 ZA ZA2012/03612A patent/ZA201203612B/en unknown
- 2012-05-24 IL IL220012A patent/IL220012B/en active IP Right Grant
- 2012-05-25 TN TNP2012000263A patent/TN2012000263A1/en unknown
- 2012-06-06 CL CL2012001480A patent/CL2012001480A1/es unknown
- 2012-06-07 GT GT201200181A patent/GT201200181A/es unknown
- 2012-06-26 MA MA35005A patent/MA33849B1/fr unknown
- 2012-07-05 EC ECSP12012026 patent/ECSP12012026A/es unknown
-
2015
- 2015-01-20 JP JP2015008550A patent/JP6019142B2/ja active Active
-
2019
- 2019-01-07 AR ARP190100029A patent/AR114946A2/es not_active Application Discontinuation
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2012128351A (ru) | Кристаллические формы 3-(2,6-дихлор-3,5-диметоксифенил)-1-{6-[4-(4-этилпиперазин-1-ил)-фениламино]-пиримидин-4-ил}-1-метилмочевины и ее долей | |
| JP2013512956A5 (ru) | ||
| TWI704151B (zh) | Erk抑制劑 | |
| US20250051330A1 (en) | Heterocyclic compound having anti-tumor activity and use thereof | |
| WO2023213269A1 (en) | Amide-substituted heterocyclic compounds as kras g12d modulators and uses thereof | |
| ES2925212T3 (es) | Compuesto heterocíclico sustituido con alquinilo, método de preparación y uso médico del mismo | |
| US9765056B2 (en) | Indole and pyrrole compounds, a process for their preparation and pharmaceutical compositions containing them | |
| JP2023536948A (ja) | Egfr阻害剤およびその製造方法と応用 | |
| US8268846B2 (en) | Amino heterocyclic linked pyrimidine derivatives | |
| CZ20012638A3 (cs) | Substituované bicyklické deriváty vhodné jako protinádorové prostředky | |
| WO2019177375A1 (ko) | 2, 4, 5-치환된 피리미딘 유도체, 이의 제조방법 및 이를 유효성분으로 포함하는 암의 예방 또는 치료용 약학적 조성물 | |
| EP3640245B1 (en) | Poly(adp-ribose) polymerase inhibitor, preparation method and use | |
| JP2020015670A (ja) | Enpp1阻害剤及びその用途 | |
| EP3705480B1 (en) | Class of amino-substituted nitrogen-containing fused ring compounds, preparation method therefor, and use thereof | |
| CN114436976B (zh) | 一种新型喹唑啉类衍生物及其制备和应用 | |
| CN101189239A (zh) | 蛋白激酶抑制剂 | |
| ES2905985T3 (es) | Compuesto de oxazino-quinazolina y de tipo oxazino-quinazolina, método de preparación y usos de los mismos | |
| CN115073469B (zh) | 吡咯并嘧啶类化合物作为激酶抑制剂的制备及其应用 | |
| JP2009242240A (ja) | 含ホウ素キナゾリン誘導体 | |
| JP4220388B2 (ja) | 異常な細胞増殖を処置するための置換された二環式誘導体の製造方法 | |
| TW201124398A (en) | Quinazoline derivatives | |
| JP2010111702A (ja) | 複素環化合物、その製造法および用途 | |
| CN109422760B (zh) | Fgfr4抑制剂及其应用 | |
| CN117229262A (zh) | 多芳香环egfr抑制剂的制备及其应用 | |
| CN114853752B (zh) | Btk抑制剂吡啶并杂环类化合物的制备及其应用 |