RU2576830C2 - Biologically active derivatives of alloferon-1 - Google Patents
Biologically active derivatives of alloferon-1 Download PDFInfo
- Publication number
- RU2576830C2 RU2576830C2 RU2013141484/15A RU2013141484A RU2576830C2 RU 2576830 C2 RU2576830 C2 RU 2576830C2 RU 2013141484/15 A RU2013141484/15 A RU 2013141484/15A RU 2013141484 A RU2013141484 A RU 2013141484A RU 2576830 C2 RU2576830 C2 RU 2576830C2
- Authority
- RU
- Russia
- Prior art keywords
- gly
- alloferon
- val
- phe
- mice
- Prior art date
Links
- 101710113252 Alloferon-1 Proteins 0.000 title claims abstract description 22
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 22
- 230000000840 anti-viral effect Effects 0.000 claims abstract description 16
- 230000002519 immonomodulatory effect Effects 0.000 claims abstract description 8
- 150000003839 salts Chemical class 0.000 claims abstract description 4
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 3
- 239000000203 mixture Substances 0.000 claims abstract description 3
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 2
- 102000003810 Interleukin-18 Human genes 0.000 abstract description 14
- 108090000171 Interleukin-18 Proteins 0.000 abstract description 14
- 239000003814 drug Substances 0.000 abstract description 11
- 230000006698 induction Effects 0.000 abstract description 10
- 230000000694 effects Effects 0.000 abstract description 7
- 241000700605 Viruses Species 0.000 abstract description 5
- 102000008070 Interferon-gamma Human genes 0.000 abstract description 4
- 108010074328 Interferon-gamma Proteins 0.000 abstract description 4
- 229960003130 interferon gamma Drugs 0.000 abstract description 4
- 239000000126 substance Substances 0.000 abstract description 2
- 239000000654 additive Substances 0.000 abstract 1
- 208000037797 influenza A Diseases 0.000 abstract 1
- 208000037798 influenza B Diseases 0.000 abstract 1
- 230000005764 inhibitory process Effects 0.000 abstract 1
- 230000004936 stimulating effect Effects 0.000 abstract 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 21
- 241000699670 Mus sp. Species 0.000 description 20
- 241001465754 Metazoa Species 0.000 description 15
- 229940079593 drug Drugs 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 238000002474 experimental method Methods 0.000 description 7
- 150000001413 amino acids Chemical class 0.000 description 6
- 238000010171 animal model Methods 0.000 description 6
- 208000015181 infectious disease Diseases 0.000 description 5
- 102000004196 processed proteins & peptides Human genes 0.000 description 5
- 241000713196 Influenza B virus Species 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 230000004071 biological effect Effects 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 238000010254 subcutaneous injection Methods 0.000 description 4
- 239000007929 subcutaneous injection Substances 0.000 description 4
- 238000005303 weighing Methods 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- 241000712431 Influenza A virus Species 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- IWUCXVSUMQZMFG-AFCXAGJDSA-N Ribavirin Chemical compound N1=C(C(=O)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 IWUCXVSUMQZMFG-AFCXAGJDSA-N 0.000 description 3
- 239000003443 antiviral agent Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 229960000329 ribavirin Drugs 0.000 description 3
- HZCAHMRRMINHDJ-DBRKOABJSA-N ribavirin Natural products O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1N=CN=C1 HZCAHMRRMINHDJ-DBRKOABJSA-N 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 230000035622 drinking Effects 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 238000000034 method Methods 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- 206010059193 Acute hepatitis B Diseases 0.000 description 1
- 108010019182 Alloferon Proteins 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 1
- 102000006992 Interferon-alpha Human genes 0.000 description 1
- 108010047761 Interferon-alpha Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- NSTPXGARCQOSAU-VIFPVBQESA-N N-formyl-L-phenylalanine Chemical compound O=CN[C@H](C(=O)O)CC1=CC=CC=C1 NSTPXGARCQOSAU-VIFPVBQESA-N 0.000 description 1
- 208000009608 Papillomavirus Infections Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- PBCJIPOGFJYBJE-UHFFFAOYSA-N acetonitrile;hydrate Chemical compound O.CC#N PBCJIPOGFJYBJE-UHFFFAOYSA-N 0.000 description 1
- 208000037628 acute hepatitis B virus infection Diseases 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000003651 drinking water Substances 0.000 description 1
- 235000020188 drinking water Nutrition 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 102220240796 rs553605556 Human genes 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 208000026425 severe pneumonia Diseases 0.000 description 1
- 238000010532 solid phase synthesis reaction Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 239000005723 virus inoculator Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/10—Peptides having 12 to 20 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Virology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Gastroenterology & Hepatology (AREA)
- Epidemiology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
Description
Изобретение относится к белкам и биологически активным пептидам с иммуномодулирующей и противовирусной активностью.The invention relates to proteins and biologically active peptides with immunomodulating and antiviral activity.
Известна группа противовирусных пептидов, выделенных из насекомых, с общим названием Аллофероны и общей формулой: X1-His-Gly-Х2-His-Gly-Val-Х3 или их фармацевтически приемлемые соли, или эфиры, или амиды, где X1 отсутствует либо содержит не менее 1 аминокислоты, Х2 содержит не менее 1 аминокислоты либо представляет собой пептидную связь; Х3 отсутствует либо содержит не менее 1 аминокислоты, причем указанные аминокислоты выбраны из групп: алифатической, ароматической или гетероциклической (Патент РФ №2172322, МПК С07К 7/06, С07К 7/08, А61К 38/08, А61К 38/10, А61Р 37/02, опубл. 20.08.2001 г.).A known group of antiviral peptides isolated from insects, with the general name Alloferons and the general formula: X 1 -His-Gly-X 2 -His-Gly-Val-X 3 or their pharmaceutically acceptable salts or esters or amides, where X 1 absent or contains at least 1 amino acid, X 2 contains at least 1 amino acid or is a peptide bond; X 3 is absent or contains at least 1 amino acid, and these amino acids are selected from the groups: aliphatic, aromatic or heterocyclic (RF Patent No. 2172322, IPC C07K 7/06, C07K 7/08, A61K 38/08, A61K 38/10, A61P 37/02, published on 08.20.2001).
На основе одного из пептидов этой группы Аллоферона-1, имеющего структуру His-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly, был разработан лекарственный препарат «Аллокин-альфа лиофилизат для приготовления раствора для подкожного введения», который выпускается с 2003 г. в качестве лекарственного средства для лечения хронического рецидивирующего герпеса 1 и 2 типа, острого гепатита В и папилломовирусных инфекций.Based on one of the peptides of this group Alloferon-1, having the structure His-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly, the drug Allokin-alpha lyophilisate for the preparation of solution for subcutaneous administration ”, which has been produced since 2003 as a medicine for the treatment of chronic recurrent herpes of type 1 and 2, acute hepatitis B and papillomavirus infections.
Противовирусная активность Аллоферона-1 обусловлена многими факторами.The antiviral activity of Alloferon-1 is due to many factors.
Так установлено, что он обладает прямым противовирусным действием (1). Однако основным механизмом биологической активности Аллоферона-1 можно считать индукцию цитокинов, в том числе интерферона-альфа (2) и интерлейкина-18 (3).It has been established that it has a direct antiviral effect (1). However, the main mechanism of the biological activity of Alloferon-1 can be considered the induction of cytokines, including interferon-alpha (2) and interleukin-18 (3).
Семейство Аллоферонов, описываемое общей формулой:The Alloferon family described by the general formula:
X1-His-Gly-X2-His-Gly-Val-X3,X1-His-Gly-X2-His-Gly-Val-X3,
включает большое число молекул, построенных на основе природных аминокислот, обладающих широким спектром биологических свойств. Одной из возможностей изменения молекул и, соответственно, их биологической активности является введение в состав пептида химически модифицированных аминокислот. Наиболее простым объектом для модификации является введение в молекулу Аллоферона-1 фенилаланина, содержащего заместители в ароматическом ядре.includes a large number of molecules based on natural amino acids with a wide range of biological properties. One of the possibilities for changing the molecules and, correspondingly, their biological activity is the introduction of chemically modified amino acids into the peptide. The simplest object for modification is the introduction of phenylalanine containing substituents in the aromatic nucleus into the Alloferon-1 molecule.
Технической задачей, на решение которой направлено заявляемое изобретение, является создание новых производных пептида Аллоферона-1, обладающих повышенной биологической активностью, которые могут быть использованы для создания лекарственных препаратов для лечения и профилактики вирусных и микробных инфекций.The technical problem to be solved by the claimed invention is directed is the creation of new derivatives of the Alloferon-1 peptide with enhanced biological activity, which can be used to create drugs for the treatment and prevention of viral and microbial infections.
Поставленная техническая задача решена путем замены в молекуле Аллоферона-1 гистидина в положении 1 на фенилаланин, имеющий в параположении нуклеофильный заместитель, получен пептид:The stated technical problem is solved by replacing the histidine in the Alloferon-1 molecule in position 1 with phenylalanine having a nucleophilic substituent in the para position, the peptide is obtained:
Предложено применение производного Аллоферона-1The use of Alloferon-1 derivative is proposed.
Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly в качестве средства, обладающего высокой иммуномодулирующей и противовирусной активностью.Phe (p-NH2) -Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly as an agent having high immunomodulating and antiviral activity.
Кроме того, предложена иммуномодулирующая и противовирусная композиция, содержащая пептид Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly или его фармацевтически приемлемые соли в сочетании со стандартными вспомогательными веществами.In addition, an immunomodulating and antiviral composition is provided comprising the peptide Phe (p-NH2) -Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly or its pharmaceutically acceptable salts in combination with standard excipients.
Технический результат состоит в том, что полученный пептид обладает высокой иммуномодулирующей и противовирусной активностью, что будет подтверждено примерами.The technical result consists in the fact that the obtained peptide has a high immunomodulating and antiviral activity, which will be confirmed by examples.
Синтез пептида произведен по стандартной Fmoc-процедуре твердофазным способом. Удаление защиты производилось 20%-ным раствором пиперидина в диметилформамиде. Реакцию сочетания проводили с помощью HBTU в присутствии HOBt и NMM в течение 2 часов при комнатной температуре. Финишное отделение пептида проводили с помощью TFA, EDT и воды (95:2,5:2,5) в течение 2 часов при комнатной температуре.The peptide was synthesized using the standard Fmoc procedure by a solid-phase method. Removal of protection was carried out with a 20% solution of piperidine in dimethylformamide. The coupling reaction was performed using HBTU in the presence of HOBt and NMM for 2 hours at room temperature. The final separation of the peptide was carried out using TFA, EDT and water (95: 2.5: 2.5) for 2 hours at room temperature.
Сырой пептид промывали холодным диэтиловым эфиром, растворяли в воде и лиофилизовали. Очистка пептида производилась методом HPLC с использованием колонок TOSOH Bioscience С18 (21,5 мм × 300 мм) (Tosoh, Japan) с UV-детектором 210/240 нм. Процесс проводили в градиенте вода - ацетонитрил содержащий 0,1% TFA при скорости потока 7 мл/мин. Очищенный лиофилизованный пептид имел чистоту более 95%.The crude peptide was washed with cold diethyl ether, dissolved in water and lyophilized. The peptide was purified by HPLC using TOSOH Bioscience C18 columns (21.5 mm × 300 mm) (Tosoh, Japan) with a 210/240 nm UV detector. The process was carried out in a water - acetonitrile gradient containing 0.1% TFA at a flow rate of 7 ml / min. The purified lyophilized peptide had a purity of more than 95%.
Финишная стадия получения пептида - лиофилизация из раствора в 50% уксусной кислоте.The final step in the preparation of the peptide is lyophilization from a solution in 50% acetic acid.
Химическая идентификация пептида была подтверждена методом масс-спектрометрии с использованием масс-спектрометра типа Microflex LT MALDI-TOF (Bruker Daltonics GmbH).Chemical identification of the peptide was confirmed by mass spectrometry using a Microflex LT MALDI-TOF type mass spectrometer (Bruker Daltonics GmbH).
Возможность достижения цели изобретения подтверждается следующими примерами.The ability to achieve the objectives of the invention is confirmed by the following examples.
Пример 1. Изучение влияния Phe(р-NH2)-Аллоферона на индукцию IL-18Example 1. The study of the effect of Phe (p-NH2) -Alloferon on the induction of IL-18
Индукция осуществлялась путем введения подкожно Phe(p-NH2)-Аллоферона и для сравнения Аллоферона-1 однократно в дозе 2 мг на кг веса лабораторных животных. Для эксперимента использовались мыши линии BALB/C, самки, массой 16-22 грамма, возраста 14 недель, полученные из питомника лабораторных животных и прошедшие необходимый карантин. Температура окружающей среды была 22±2°C, относительная влажность 60±5%, содержание аммиака составляло 10 ррм, углекислого газа - не превышало 0,15% к объему воздуха, кратность воздухообмена составляла 10-15 крат/час при скорости движения воздуха - 0,3 м/с. Фильтрование воздуха обеспечивали с помощью фильтров грубой фильтрации. Кормили мышей гранулированным комбикормом, изготовленным в соответствии со стандартами приготовления кормов для лабораторных животных. Корм предварительно стерилизовали в автоклаве с использованием вакуума при 121°C и 1,2 атм. в течение 20 мин. Кормление проводили 1 раз в сутки из расчета 8,0 г на одну мышь, после чистки клеток. Питьевую воду заливали в бутылки-поилки вместимостью 200 мл и стерилизовали при 121°С и 1,2 атм. в течение 45 мин, пробки автоклавировали отдельно. Поилки ежедневно заменяли на новые. Определялся уровень интерлейкина-18 (IL-18) в сыворотке крови методом иммуноферментного анализа, с использованием специфических антител. Количество IL-18 в сыворотке определяли на 1, 2, 3, 4, 5, 6, 8, 12, 16, 24, 32, 40, 48, 56 ч после введения препаратов.Induction was carried out by subcutaneous injection of Phe (p-NH2) -Alloferon and, for comparison, Alloferon-1 once at a dose of 2 mg per kg of weight of laboratory animals. For the experiment, BALB / C mice were used, females weighing 16-22 grams, 14 weeks of age, obtained from the laboratory animal nursery and passed the necessary quarantine. The ambient temperature was 22 ± 2 ° C, relative humidity 60 ± 5%, the ammonia content was 10 ppm, carbon dioxide did not exceed 0.15% of the air volume, the air exchange rate was 10-15 times / hour at an air speed of 0.3 m / s. Air filtration was provided using coarse filters. The mice were fed with granular feed made in accordance with the standards for the preparation of feed for laboratory animals. The food was pre-sterilized in an autoclave using vacuum at 121 ° C and 1.2 atm. within 20 minutes Feeding was carried out 1 time per day at the rate of 8.0 g per mouse, after cleaning the cells. Drinking water was poured into drinking bottles with a capacity of 200 ml and sterilized at 121 ° C and 1.2 atm. for 45 min, plugs were autoclaved separately. Drinking bowls were replaced daily with new ones. The level of interleukin-18 (IL-18) in the blood serum was determined by enzyme-linked immunosorbent assay using specific antibodies. The amount of IL-18 in serum was determined at 1, 2, 3, 4, 5, 6, 8, 12, 16, 24, 32, 40, 48, 56 hours after drug administration.
Параллельно изучалось «фоновое» количество IL-18, присутствующее в сыворотке крови исследуемых животных. Для этой цели использовалось 14 мышей в качестве контрольной группы, которые получали подкожную инъекцию физиологического раствора. В опытной группе использовалось 84 животных. В случае контрольной группы доверительный интервал рассчитывался по измерениям разведения одного и того же образца. В опытной группе доверительный интервал вычислялся относительно трех образцов от трех животных на каждую измеряемую точку.At the same time, the "background" amount of IL-18 present in the blood serum of the studied animals was studied. For this purpose, 14 mice were used as a control group, which received a subcutaneous injection of saline. In the experimental group, 84 animals were used. In the case of the control group, the confidence interval was calculated from the dilution measurements of the same sample. In the experimental group, the confidence interval was calculated relative to three samples from three animals for each measured point.
Через 3-4 часа после введения у пептидов наблюдается небольшой достоверный пик увеличения концентрации IL-18. Через 24 часа наблюдается второй пик значительного увеличения содержания IL-18 в сыворотке крови опытной группы животных, который длится около 20 часов. Наличие первого пика на 3-4 часу возможно обусловлено не специфической индукцией. Значительное повышение IL-18 на 2-3-й день эксперимента свидетельствует о специфической способности препаратов индуцировать изучаемый цитокин.3-4 hours after the administration, the peptides show a small significant peak in the increase in IL-18 concentration. After 24 hours, there is a second peak of a significant increase in the content of IL-18 in the blood serum of the experimental group of animals, which lasts about 20 hours. The presence of the first peak at 3-4 hours is probably due to non-specific induction. A significant increase in IL-18 on the 2-3rd day of the experiment indicates the specific ability of the drugs to induce the studied cytokine.
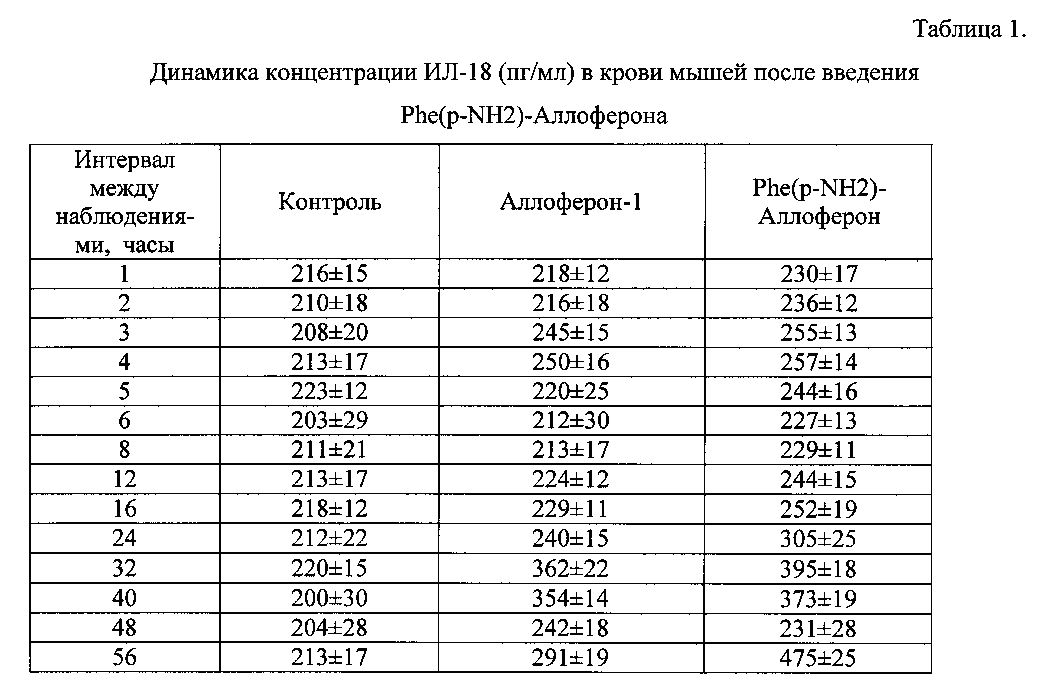
Результаты испытания препарата приведены в таблице 1.The test results of the drug are shown in table 1.
Введение как Phe(p-NH2)-Аллоферона, так и Аллоферона-1, вызвало индукцию ИЛ-18, которая длилась до 3 суток. Максимальная концентрация ИЛ-18 достигается спустя 32 часа после однократного введения пептида. Характер индукции - интенсивность и временной диапазон - для пептидов одинакова. При этом Phe(р-NH2)-Аллоферон показывают более высокий уровень индукции интерлейкина-18, чем Аллоферон-1.The introduction of both Phe (p-NH2) -Alloferon and Alloferon-1 caused the induction of IL-18, which lasted up to 3 days. The maximum concentration of IL-18 is reached 32 hours after a single injection of the peptide. The nature of induction - the intensity and time range - is the same for peptides. Moreover, Phe (p-NH2) -Alloferon show a higher level of induction of interleukin-18 than Alloferon-1.
Максимальный уровень интерлейкина-18 был зафиксирован для Phe(p-NH2)-Аллоферона через 32 часа (395 пг/мл). Фоновый уровень в среднем в группе контрольных животных составил 200 пг/мл.The maximum level of interleukin-18 was recorded for Phe (p-NH2) -Alloferon after 32 hours (395 pg / ml). The average background level in the group of control animals was 200 pg / ml.
Пример 2. Изучение интерфероногенности Phe(p-NH2)-АллоферонаExample 2. The study of interferonogenicity of Phe (p-NH2) -alloferon
Активность определялась путем введения Phe(p-NH2)-Аллоферона и Аллоферона-1 подкожно однократно в дозе 1 мг на кг веса лабораторных животных. Для эксперимента использовались мыши линии BALB/C, самки, массой 16-22 грамма, возраста 18 недель, содержавшиеся в соответствии с протоколом, изложенным выше в примере 1. Определялся уровень интерферона гамма в сыворотке крови методом иммуноферментного анализа, с использованием специфических антител. Количество интерферона в сыворотке определяли на 3, 6, 12, 16, 24, 32, 40 и 48 ч после введения препарата.Activity was determined by introducing Phe (p-NH2) -Alloferon and Alloferon-1 subcutaneously once at a dose of 1 mg per kg of weight of laboratory animals. For the experiment, BALB / C mice were used, females weighing 16-22 grams, 18 weeks of age, contained in accordance with the protocol described above in Example 1. The level of interferon gamma in the blood serum was determined by enzyme-linked immunosorbent assay using specific antibodies. The amount of interferon in the serum was determined at 3, 6, 12, 16, 24, 32, 40 and 48 hours after administration of the drug.
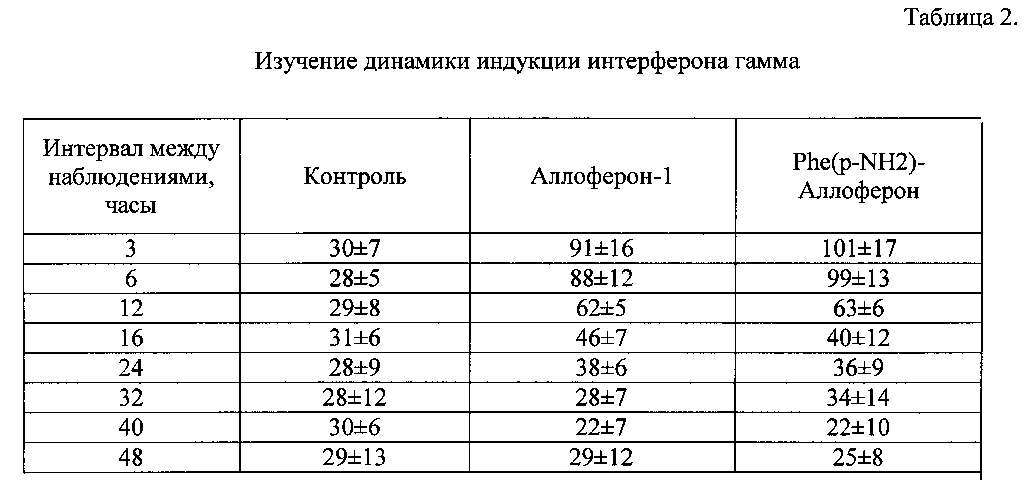
Параллельно изучалось «фоновое» количество интерферона гамма, присутствующее в сыворотке исследуемых животных. Для этой цели использовалось 8 мышей в качестве контрольной группы, которые получали подкожную инъекцию физиологического раствора. Среднее значение по контрольной группе на 5% уровне значимости составило 29±8 пг/мл исследуемой сыворотки. В каждой опытной группе также использовались по 8 мышей, которые получали подкожную инъекцию в дозе 25 мкг с изучаемым Phe(p-NH2)-Аллофероном, а также Аллофероном-1. Результаты испытания препаратов представлены в таблице 2.At the same time, the “background” amount of interferon gamma present in the serum of the studied animals was studied. For this purpose, 8 mice were used as a control group, which received a subcutaneous injection of saline. The average value in the control group at a 5% significance level was 29 ± 8 pg / ml of the studied serum. Each experimental group also used 8 mice that received a subcutaneous injection at a dose of 25 μg with the studied Phe (p-NH2) -Alloferon, as well as Alloferon-1. The test results of the drugs are presented in table 2.
Полученные данные свидетельствуют о том, что Phe(р-NH2)-Аллоферон вызывает индукцию интерферона гамма, превышающую уровень индукции Аллоферона-1.The data obtained indicate that Phe (p-NH2) -Alloferon induces interferon gamma induction that exceeds the level of induction of Alloferon-1.
На основании вышеизложенного можно утверждать, что разработанный пептид обладает всеми заявленными свойствами.Based on the foregoing, it can be argued that the developed peptide has all the claimed properties.
Пример 3. Изучение влияния Phe(p-NH2)-Аллоферона на резистентность мышей к вирусу гриппа АExample 3. The study of the effect of Phe (p-NH2) -Alloferon on the resistance of mice to influenza A virus
Антивирусное действие пептида изучали на модели летальной вирусной инфекции мышей вирусом гриппа А. Суспензию вируса вводили интраназально в дозе, соответствующей 10 LD50. Аллоферон-1 и Phe(p-NH2)-Аллоферон в 0,5 мл 0.9% раствора натрия хлорида вводили внутрибрюшинно за одни сутки до инокуляции вируса, затем через 1, 2, 4, 6 и 8 дней после инокуляции. Препараты испытывали в дозе 25 мкг. В контроле мышам вводили равный объем растворителя. Критерием эффективности служила выживаемость животных через 10 суток после инфицирования вирусом. Для проведения эксперимента были отобраны половозрелые белые мыши, самцы, весом 20,0-22,0 г, полученные из питомника лабораторных животных и прошедшие необходимый карантин. Содержание мышей осуществлялось по протоколу, изложенному выше в примере 1. В эксперименте были использованы 60 мышей.The antiviral effect of the peptide was studied in a model of lethal viral infection of mice with influenza A virus. A suspension of the virus was administered intranasally at a dose corresponding to 10 LD 50 . Alloferon-1 and Phe (p-NH2) -Alloferon in 0.5 ml of 0.9% sodium chloride solution was administered intraperitoneally one day before the virus inoculation, then 1, 2, 4, 6, and 8 days after inoculation. The drugs were tested at a dose of 25 mcg. In control, mice were injected with an equal volume of solvent. The criterion of effectiveness was the survival of animals 10 days after infection with the virus. For the experiment, sexually mature white mice, males weighing 20.0-22.0 g, obtained from the laboratory animal nursery and passed the necessary quarantine, were selected. The mice were maintained according to the protocol described above in Example 1. 60 mice were used in the experiment.
Введение Phe(p-NH2)-Аллоферона и Аллоферона-1 инфицированным животным вызывало дозозависимый протекторный эффект (Таблица 3). Препараты в дозе 25 мкг вызывали значительное увеличение числа выживших в течение срока наблюдения животных. Эффект данной дозы высокодостоверен.Administration of Phe (p-NH2) -Alloferon and Alloferon-1 to infected animals caused a dose-dependent protective effect (Table 3). Drugs at a dose of 25 μg caused a significant increase in the number of survivors during the observation period of animals. The effect of this dose is highly reliable.
Таким образом, результаты примера 3 свидетельствуют о том, что Phe(p-NH2)-Аллоферон в дозе 25 мкг оказывает выраженное антивирусное действие на мышей, инфицированных вирусом гриппа А, превышающее антивирусное действие Аллоферона-1.Thus, the results of example 3 indicate that Phe (p-NH2) -alloferon at a dose of 25 μg has a pronounced antiviral effect on mice infected with influenza A virus, exceeding the antiviral effect of Alloferon-1.
Пример 4. Изучение влияния Phe(р-NH2)-Аллоферона на резистентность мышей к вирусу гриппа ВExample 4. The study of the effect of Phe (p-NH2) -Alloferon on the resistance of mice to influenza B virus
Исследование влияния Phe(р-NH2)-Аллоферона на устойчивость мышей к вирусу гриппа В проводилось на 120 мышах. Для проведения эксперимента были отобраны половозрелые белые мыши, самцы, весом 20,0-22,0 г, полученные из питомника лабораторных животных и прошедшие необходимый карантин. Содержание мышей осуществлялось по протоколу, изложенному выше в примере 1. Мышей инфицировали штаммом LEE 1/40 вируса гриппа В, взятым в инфекционной дозе, соответствующих 30 ЛД50. В качестве позитивного контроля использовали специфический антивирусный препарат Рибавирин.A study of the effect of Phe (p-NH2) -Alloferon on the resistance of mice to influenza B virus was carried out on 120 mice. For the experiment, sexually mature white mice, males weighing 20.0-22.0 g, obtained from the laboratory animal nursery and passed the necessary quarantine, were selected. The mice were maintained according to the protocol described in Example 1 above. The mice were infected with a strain of LEE 1/40 of influenza B virus taken in an infectious dose corresponding to 30 LD 50 . Specific antiviral drug Ribavirin was used as a positive control.
Аллоферон-1 и Phe(р-NH2)-Аллоферон вводили внутрибрюшинно в дозе 25 мкг за 1 сутки до инфицирования вирусом, затем через 1, 2, 4, 6 и 8 суток.Alloferon-1 and Phe (p-NH2) -Alloferon were administered intraperitoneally at a dose of 25 μg 1 day before infection with the virus, then after 1, 2, 4, 6, and 8 days.
Результаты изложены в Таблице 4.The results are summarized in Table 4.
В контроле интраназальное введение вируса вызвало тяжелую пневмонию с высокой летальностью (80%). На этом фоне Рибавирин при высокой инфекционной нагрузке (30 ЛД50) в условиях данного эксперимента оказался малоэффективным. В то же время Phe(р-NH2)-Аллоферон оказал выраженное протекторное действие, превышающее антивирусное действие Аллоферон-1.In control, intranasal administration of the virus caused severe pneumonia with high mortality (80%). Against this background, Ribavirin with a high infectious load (30 LD 50 ) in the conditions of this experiment was ineffective. At the same time, Phe (p-NH2) -Alloferon exerted a pronounced protective effect exceeding the antiviral effect of Alloferon-1.
Таким образом, результаты примера 4 свидетельствуют о том, что Phe(p-NH2)-Аллоферон в дозе 25 мкг оказывает выраженное антивирусное действие на мышей, инфицированных вирусом гриппа В, существенно превышающее защитный эффект Рибавирина, хорошо зарекомендовавшего себя антивирусного средства, а также Аллоферона-1, и может служить основой для создания новых антивирусных препаратов.Thus, the results of example 4 indicate that Phe (p-NH2) -alloferon at a dose of 25 μg has a pronounced antiviral effect on mice infected with influenza B virus, significantly exceeding the protective effect of Ribavirin, a well-established antiviral agent, as well as Alloferon -1, and can serve as the basis for the creation of new antiviral drugs.
Claims (2)
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013141484/15A RU2576830C2 (en) | 2013-09-10 | 2013-09-10 | Biologically active derivatives of alloferon-1 |
| EA201401291A EA035031B1 (en) | 2013-09-10 | 2014-12-19 | Biologically active derivative of alloferon-1 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013141484/15A RU2576830C2 (en) | 2013-09-10 | 2013-09-10 | Biologically active derivatives of alloferon-1 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2013141484A RU2013141484A (en) | 2015-03-20 |
| RU2576830C2 true RU2576830C2 (en) | 2016-03-10 |
Family
ID=53285405
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2013141484/15A RU2576830C2 (en) | 2013-09-10 | 2013-09-10 | Biologically active derivatives of alloferon-1 |
Country Status (2)
| Country | Link |
|---|---|
| EA (1) | EA035031B1 (en) |
| RU (1) | RU2576830C2 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2744206C1 (en) * | 2017-09-12 | 2021-03-03 | Классис Инк. | Gasket to prevent frostbite in relation to the cryolipolysis procedure |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2267496C2 (en) * | 2004-01-15 | 2006-01-10 | Сергей Иванович Черныш | Anti-tumor and antiviral peptides |
| RU2470031C2 (en) * | 2011-02-18 | 2012-12-20 | Общество с ограниченной ответственностью "Аллоферон" | Biologically active peptide complexes |
-
2013
- 2013-09-10 RU RU2013141484/15A patent/RU2576830C2/en active
-
2014
- 2014-12-19 EA EA201401291A patent/EA035031B1/en not_active IP Right Cessation
Non-Patent Citations (2)
| Title |
|---|
| CHERNYSH S., et al., Anti-tumor activity of immunomodulatory peptide alloferon-1 in mouse tumor transplantation model. Int Immunopharmacol. 2012 Jan;12(1):312-4. doi: 10.1016/j.intimp.2011.10.016. Epub 2011 Oct 31. * |
| KUCZER M., et al., New alloferon analogues: synthesis and antiviral properties. Chem Biol Drug Des. 2013 Feb;81(2):302-9. doi: 10.1111/cbdd.12020. Epub 2012 Nov 19. * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2744206C1 (en) * | 2017-09-12 | 2021-03-03 | Классис Инк. | Gasket to prevent frostbite in relation to the cryolipolysis procedure |
| US11759353B2 (en) | 2017-09-12 | 2023-09-19 | Classys Inc. | Frostbite prevention pad for cryolipolysis procedure |
Also Published As
| Publication number | Publication date |
|---|---|
| EA201401291A2 (en) | 2016-01-29 |
| RU2013141484A (en) | 2015-03-20 |
| EA201401291A3 (en) | 2016-02-29 |
| EA035031B1 (en) | 2020-04-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6952379B2 (en) | Nasal pharmaceutical composition for the treatment of acute viral respiratory illness | |
| US20210246177A1 (en) | Cath2 derivatives | |
| CN106232616B (en) | Amphiphilic synthetic antimicrobial peptide, its pharmaceutical composition and its use | |
| US11186619B2 (en) | Antimicrobial peptides based on CMAP27 | |
| KR101267967B1 (en) | Composition and method for preventing and treating immune-related disorder | |
| BG98426A (en) | Peptides of organoprotective activity, method for their preparation and their therapeutical use | |
| EP1006124B1 (en) | Immunomodulatory materials from Calliphora vicina larvae, their preparation and use | |
| CA2133569A1 (en) | Novel lipophilic oligopeptides with immunomodulating activity | |
| RU2576830C2 (en) | Biologically active derivatives of alloferon-1 | |
| EP4448104A1 (en) | Compositions and methods for activating innate immunity | |
| RU2575069C2 (en) | Biologically active peptides | |
| KR102609962B1 (en) | Tripeptide containing histidine derivative and antibacterial composition containing the same | |
| ES2350039T3 (en) | IMMUNOMODULATING COMPOUNDS CONTAINING GAMMA-GLUTAMILO AND BETA-ASPARTILO AND METHODS WITH THEM. | |
| EA031772B1 (en) | Peptides inducing intensified interferon gamma and il-18 formation, and immunomodulatory, antiviral pharmaceutical composition | |
| CN103933554B (en) | A kind of for preventing the interferon white oil compositions of Schweineseuche | |
| CN110563814B (en) | Polypeptide with immunoregulation function and application thereof | |
| CN1602200A (en) | Plant extract active as an immunostimulating agent | |
| JP2007537280A (en) | Treatment or prevention of respiratory viral infections using immunomodulatory compounds | |
| EP2030628A1 (en) | A peptide for preventing or treating liver damage and its derivant and the use | |
| CN103923178B (en) | A kind of purposes of small peptide, its synthetic method and its enhancing domestic animal immunity | |
| CN113813368B (en) | Application of antibacterial peptide in preparation of grass carp reovirus resistant drugs | |
| CN113698460A (en) | Escherichia coli lipid A binding motif PCK and preparation method and application thereof | |
| HK1231775A1 (en) | Antimicrobial peptides based on cmap27 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| HZ9A | Changing address for correspondence with an applicant | ||
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20171016 |