RU2576830C2 - Биологически активные производные аллоферона-1 - Google Patents
Биологически активные производные аллоферона-1 Download PDFInfo
- Publication number
- RU2576830C2 RU2576830C2 RU2013141484/15A RU2013141484A RU2576830C2 RU 2576830 C2 RU2576830 C2 RU 2576830C2 RU 2013141484/15 A RU2013141484/15 A RU 2013141484/15A RU 2013141484 A RU2013141484 A RU 2013141484A RU 2576830 C2 RU2576830 C2 RU 2576830C2
- Authority
- RU
- Russia
- Prior art keywords
- gly
- alloferon
- val
- phe
- mice
- Prior art date
Links
- 101710113252 Alloferon-1 Proteins 0.000 title claims abstract description 22
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 22
- 230000000840 anti-viral effect Effects 0.000 claims abstract description 16
- 230000002519 immonomodulatory effect Effects 0.000 claims abstract description 8
- 150000003839 salts Chemical class 0.000 claims abstract description 4
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 3
- 239000000203 mixture Substances 0.000 claims abstract description 3
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 2
- 102000003810 Interleukin-18 Human genes 0.000 abstract description 14
- 108090000171 Interleukin-18 Proteins 0.000 abstract description 14
- 239000003814 drug Substances 0.000 abstract description 11
- 230000006698 induction Effects 0.000 abstract description 10
- 230000000694 effects Effects 0.000 abstract description 7
- 241000700605 Viruses Species 0.000 abstract description 5
- 102000008070 Interferon-gamma Human genes 0.000 abstract description 4
- 108010074328 Interferon-gamma Proteins 0.000 abstract description 4
- 229960003130 interferon gamma Drugs 0.000 abstract description 4
- 239000000126 substance Substances 0.000 abstract description 2
- 239000000654 additive Substances 0.000 abstract 1
- 208000037797 influenza A Diseases 0.000 abstract 1
- 208000037798 influenza B Diseases 0.000 abstract 1
- 230000005764 inhibitory process Effects 0.000 abstract 1
- 230000004936 stimulating effect Effects 0.000 abstract 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 21
- 241000699670 Mus sp. Species 0.000 description 20
- 241001465754 Metazoa Species 0.000 description 15
- 229940079593 drug Drugs 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 238000002474 experimental method Methods 0.000 description 7
- 150000001413 amino acids Chemical class 0.000 description 6
- 238000010171 animal model Methods 0.000 description 6
- 208000015181 infectious disease Diseases 0.000 description 5
- 102000004196 processed proteins & peptides Human genes 0.000 description 5
- 241000713196 Influenza B virus Species 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 230000004071 biological effect Effects 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 238000010254 subcutaneous injection Methods 0.000 description 4
- 239000007929 subcutaneous injection Substances 0.000 description 4
- 238000005303 weighing Methods 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- 241000712431 Influenza A virus Species 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- IWUCXVSUMQZMFG-AFCXAGJDSA-N Ribavirin Chemical compound N1=C(C(=O)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 IWUCXVSUMQZMFG-AFCXAGJDSA-N 0.000 description 3
- 239000003443 antiviral agent Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 229960000329 ribavirin Drugs 0.000 description 3
- HZCAHMRRMINHDJ-DBRKOABJSA-N ribavirin Natural products O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1N=CN=C1 HZCAHMRRMINHDJ-DBRKOABJSA-N 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 230000035622 drinking Effects 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 238000000034 method Methods 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- 206010059193 Acute hepatitis B Diseases 0.000 description 1
- 108010019182 Alloferon Proteins 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 1
- 102000006992 Interferon-alpha Human genes 0.000 description 1
- 108010047761 Interferon-alpha Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- NSTPXGARCQOSAU-VIFPVBQESA-N N-formyl-L-phenylalanine Chemical compound O=CN[C@H](C(=O)O)CC1=CC=CC=C1 NSTPXGARCQOSAU-VIFPVBQESA-N 0.000 description 1
- 208000009608 Papillomavirus Infections Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- PBCJIPOGFJYBJE-UHFFFAOYSA-N acetonitrile;hydrate Chemical compound O.CC#N PBCJIPOGFJYBJE-UHFFFAOYSA-N 0.000 description 1
- 208000037628 acute hepatitis B virus infection Diseases 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000003651 drinking water Substances 0.000 description 1
- 235000020188 drinking water Nutrition 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 102220240796 rs553605556 Human genes 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 208000026425 severe pneumonia Diseases 0.000 description 1
- 238000010532 solid phase synthesis reaction Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 239000005723 virus inoculator Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/10—Peptides having 12 to 20 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Virology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Gastroenterology & Hepatology (AREA)
- Epidemiology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
Abstract
Группа изобретений относится к медицине и касается применения производного Аллоферона-1 Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly в качестве средства, обладающего высокой иммуномодулирующей и противовирусной активностью. Группа изобретений также касается иммуномодулирующей и противовирусной композиции, содержащей пептид Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly или его фармацевтически приемлемые соли в сочетании со стандартными вспомогательными веществами. Группа изобретений обеспечивает стимулирование индукции интерлейкина-18, интерферона гамма и подавление вирусов гриппа А и В. 2 н.п. ф-лы, 4 пр., 4 табл.
Description
Изобретение относится к белкам и биологически активным пептидам с иммуномодулирующей и противовирусной активностью.
Известна группа противовирусных пептидов, выделенных из насекомых, с общим названием Аллофероны и общей формулой: X1-His-Gly-Х2-His-Gly-Val-Х3 или их фармацевтически приемлемые соли, или эфиры, или амиды, где X1 отсутствует либо содержит не менее 1 аминокислоты, Х2 содержит не менее 1 аминокислоты либо представляет собой пептидную связь; Х3 отсутствует либо содержит не менее 1 аминокислоты, причем указанные аминокислоты выбраны из групп: алифатической, ароматической или гетероциклической (Патент РФ №2172322, МПК С07К 7/06, С07К 7/08, А61К 38/08, А61К 38/10, А61Р 37/02, опубл. 20.08.2001 г.).
На основе одного из пептидов этой группы Аллоферона-1, имеющего структуру His-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly, был разработан лекарственный препарат «Аллокин-альфа лиофилизат для приготовления раствора для подкожного введения», который выпускается с 2003 г. в качестве лекарственного средства для лечения хронического рецидивирующего герпеса 1 и 2 типа, острого гепатита В и папилломовирусных инфекций.
Противовирусная активность Аллоферона-1 обусловлена многими факторами.
Так установлено, что он обладает прямым противовирусным действием (1). Однако основным механизмом биологической активности Аллоферона-1 можно считать индукцию цитокинов, в том числе интерферона-альфа (2) и интерлейкина-18 (3).
Семейство Аллоферонов, описываемое общей формулой:
X1-His-Gly-X2-His-Gly-Val-X3,
включает большое число молекул, построенных на основе природных аминокислот, обладающих широким спектром биологических свойств. Одной из возможностей изменения молекул и, соответственно, их биологической активности является введение в состав пептида химически модифицированных аминокислот. Наиболее простым объектом для модификации является введение в молекулу Аллоферона-1 фенилаланина, содержащего заместители в ароматическом ядре.
Технической задачей, на решение которой направлено заявляемое изобретение, является создание новых производных пептида Аллоферона-1, обладающих повышенной биологической активностью, которые могут быть использованы для создания лекарственных препаратов для лечения и профилактики вирусных и микробных инфекций.
Поставленная техническая задача решена путем замены в молекуле Аллоферона-1 гистидина в положении 1 на фенилаланин, имеющий в параположении нуклеофильный заместитель, получен пептид:
Предложено применение производного Аллоферона-1
Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly в качестве средства, обладающего высокой иммуномодулирующей и противовирусной активностью.
Кроме того, предложена иммуномодулирующая и противовирусная композиция, содержащая пептид Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly или его фармацевтически приемлемые соли в сочетании со стандартными вспомогательными веществами.
Технический результат состоит в том, что полученный пептид обладает высокой иммуномодулирующей и противовирусной активностью, что будет подтверждено примерами.
Синтез пептида произведен по стандартной Fmoc-процедуре твердофазным способом. Удаление защиты производилось 20%-ным раствором пиперидина в диметилформамиде. Реакцию сочетания проводили с помощью HBTU в присутствии HOBt и NMM в течение 2 часов при комнатной температуре. Финишное отделение пептида проводили с помощью TFA, EDT и воды (95:2,5:2,5) в течение 2 часов при комнатной температуре.
Сырой пептид промывали холодным диэтиловым эфиром, растворяли в воде и лиофилизовали. Очистка пептида производилась методом HPLC с использованием колонок TOSOH Bioscience С18 (21,5 мм × 300 мм) (Tosoh, Japan) с UV-детектором 210/240 нм. Процесс проводили в градиенте вода - ацетонитрил содержащий 0,1% TFA при скорости потока 7 мл/мин. Очищенный лиофилизованный пептид имел чистоту более 95%.
Финишная стадия получения пептида - лиофилизация из раствора в 50% уксусной кислоте.
Химическая идентификация пептида была подтверждена методом масс-спектрометрии с использованием масс-спектрометра типа Microflex LT MALDI-TOF (Bruker Daltonics GmbH).
Возможность достижения цели изобретения подтверждается следующими примерами.
Пример 1. Изучение влияния Phe(р-NH2)-Аллоферона на индукцию IL-18
Индукция осуществлялась путем введения подкожно Phe(p-NH2)-Аллоферона и для сравнения Аллоферона-1 однократно в дозе 2 мг на кг веса лабораторных животных. Для эксперимента использовались мыши линии BALB/C, самки, массой 16-22 грамма, возраста 14 недель, полученные из питомника лабораторных животных и прошедшие необходимый карантин. Температура окружающей среды была 22±2°C, относительная влажность 60±5%, содержание аммиака составляло 10 ррм, углекислого газа - не превышало 0,15% к объему воздуха, кратность воздухообмена составляла 10-15 крат/час при скорости движения воздуха - 0,3 м/с. Фильтрование воздуха обеспечивали с помощью фильтров грубой фильтрации. Кормили мышей гранулированным комбикормом, изготовленным в соответствии со стандартами приготовления кормов для лабораторных животных. Корм предварительно стерилизовали в автоклаве с использованием вакуума при 121°C и 1,2 атм. в течение 20 мин. Кормление проводили 1 раз в сутки из расчета 8,0 г на одну мышь, после чистки клеток. Питьевую воду заливали в бутылки-поилки вместимостью 200 мл и стерилизовали при 121°С и 1,2 атм. в течение 45 мин, пробки автоклавировали отдельно. Поилки ежедневно заменяли на новые. Определялся уровень интерлейкина-18 (IL-18) в сыворотке крови методом иммуноферментного анализа, с использованием специфических антител. Количество IL-18 в сыворотке определяли на 1, 2, 3, 4, 5, 6, 8, 12, 16, 24, 32, 40, 48, 56 ч после введения препаратов.
Параллельно изучалось «фоновое» количество IL-18, присутствующее в сыворотке крови исследуемых животных. Для этой цели использовалось 14 мышей в качестве контрольной группы, которые получали подкожную инъекцию физиологического раствора. В опытной группе использовалось 84 животных. В случае контрольной группы доверительный интервал рассчитывался по измерениям разведения одного и того же образца. В опытной группе доверительный интервал вычислялся относительно трех образцов от трех животных на каждую измеряемую точку.
Через 3-4 часа после введения у пептидов наблюдается небольшой достоверный пик увеличения концентрации IL-18. Через 24 часа наблюдается второй пик значительного увеличения содержания IL-18 в сыворотке крови опытной группы животных, который длится около 20 часов. Наличие первого пика на 3-4 часу возможно обусловлено не специфической индукцией. Значительное повышение IL-18 на 2-3-й день эксперимента свидетельствует о специфической способности препаратов индуцировать изучаемый цитокин.
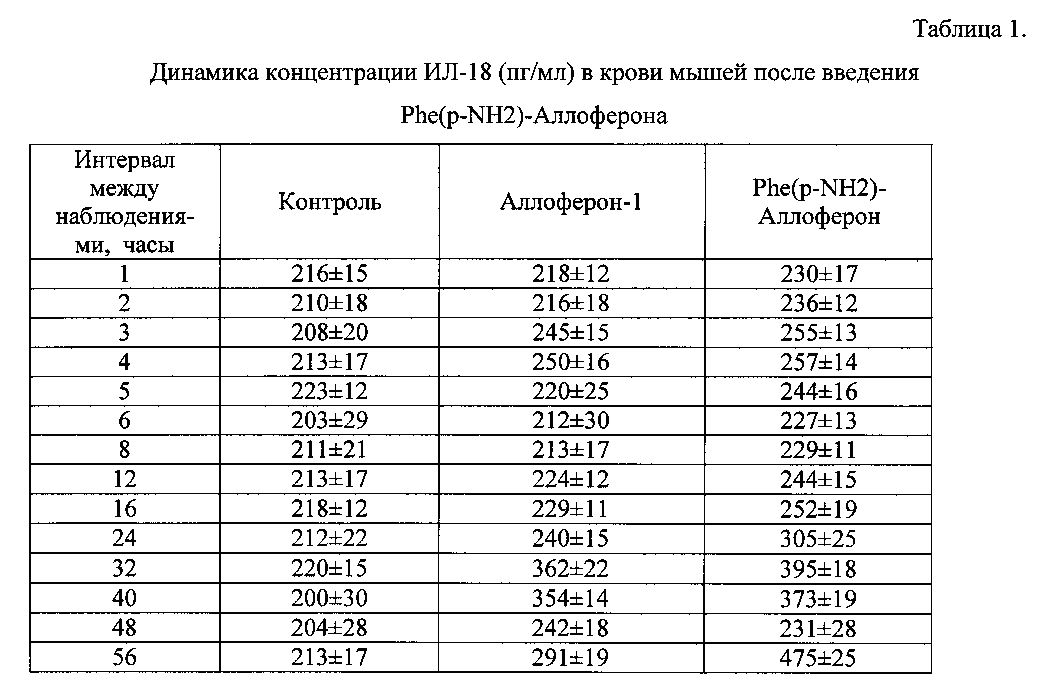
Результаты испытания препарата приведены в таблице 1.
Введение как Phe(p-NH2)-Аллоферона, так и Аллоферона-1, вызвало индукцию ИЛ-18, которая длилась до 3 суток. Максимальная концентрация ИЛ-18 достигается спустя 32 часа после однократного введения пептида. Характер индукции - интенсивность и временной диапазон - для пептидов одинакова. При этом Phe(р-NH2)-Аллоферон показывают более высокий уровень индукции интерлейкина-18, чем Аллоферон-1.
Максимальный уровень интерлейкина-18 был зафиксирован для Phe(p-NH2)-Аллоферона через 32 часа (395 пг/мл). Фоновый уровень в среднем в группе контрольных животных составил 200 пг/мл.
Пример 2. Изучение интерфероногенности Phe(p-NH2)-Аллоферона
Активность определялась путем введения Phe(p-NH2)-Аллоферона и Аллоферона-1 подкожно однократно в дозе 1 мг на кг веса лабораторных животных. Для эксперимента использовались мыши линии BALB/C, самки, массой 16-22 грамма, возраста 18 недель, содержавшиеся в соответствии с протоколом, изложенным выше в примере 1. Определялся уровень интерферона гамма в сыворотке крови методом иммуноферментного анализа, с использованием специфических антител. Количество интерферона в сыворотке определяли на 3, 6, 12, 16, 24, 32, 40 и 48 ч после введения препарата.
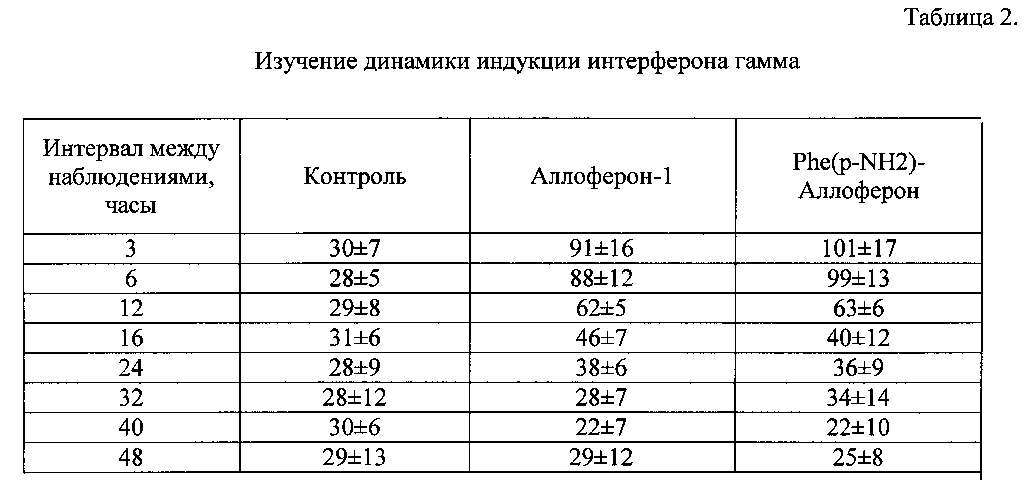
Параллельно изучалось «фоновое» количество интерферона гамма, присутствующее в сыворотке исследуемых животных. Для этой цели использовалось 8 мышей в качестве контрольной группы, которые получали подкожную инъекцию физиологического раствора. Среднее значение по контрольной группе на 5% уровне значимости составило 29±8 пг/мл исследуемой сыворотки. В каждой опытной группе также использовались по 8 мышей, которые получали подкожную инъекцию в дозе 25 мкг с изучаемым Phe(p-NH2)-Аллофероном, а также Аллофероном-1. Результаты испытания препаратов представлены в таблице 2.
Полученные данные свидетельствуют о том, что Phe(р-NH2)-Аллоферон вызывает индукцию интерферона гамма, превышающую уровень индукции Аллоферона-1.
На основании вышеизложенного можно утверждать, что разработанный пептид обладает всеми заявленными свойствами.
Пример 3. Изучение влияния Phe(p-NH2)-Аллоферона на резистентность мышей к вирусу гриппа А
Антивирусное действие пептида изучали на модели летальной вирусной инфекции мышей вирусом гриппа А. Суспензию вируса вводили интраназально в дозе, соответствующей 10 LD50. Аллоферон-1 и Phe(p-NH2)-Аллоферон в 0,5 мл 0.9% раствора натрия хлорида вводили внутрибрюшинно за одни сутки до инокуляции вируса, затем через 1, 2, 4, 6 и 8 дней после инокуляции. Препараты испытывали в дозе 25 мкг. В контроле мышам вводили равный объем растворителя. Критерием эффективности служила выживаемость животных через 10 суток после инфицирования вирусом. Для проведения эксперимента были отобраны половозрелые белые мыши, самцы, весом 20,0-22,0 г, полученные из питомника лабораторных животных и прошедшие необходимый карантин. Содержание мышей осуществлялось по протоколу, изложенному выше в примере 1. В эксперименте были использованы 60 мышей.
Введение Phe(p-NH2)-Аллоферона и Аллоферона-1 инфицированным животным вызывало дозозависимый протекторный эффект (Таблица 3). Препараты в дозе 25 мкг вызывали значительное увеличение числа выживших в течение срока наблюдения животных. Эффект данной дозы высокодостоверен.
Таким образом, результаты примера 3 свидетельствуют о том, что Phe(p-NH2)-Аллоферон в дозе 25 мкг оказывает выраженное антивирусное действие на мышей, инфицированных вирусом гриппа А, превышающее антивирусное действие Аллоферона-1.
Пример 4. Изучение влияния Phe(р-NH2)-Аллоферона на резистентность мышей к вирусу гриппа В
Исследование влияния Phe(р-NH2)-Аллоферона на устойчивость мышей к вирусу гриппа В проводилось на 120 мышах. Для проведения эксперимента были отобраны половозрелые белые мыши, самцы, весом 20,0-22,0 г, полученные из питомника лабораторных животных и прошедшие необходимый карантин. Содержание мышей осуществлялось по протоколу, изложенному выше в примере 1. Мышей инфицировали штаммом LEE 1/40 вируса гриппа В, взятым в инфекционной дозе, соответствующих 30 ЛД50. В качестве позитивного контроля использовали специфический антивирусный препарат Рибавирин.
Аллоферон-1 и Phe(р-NH2)-Аллоферон вводили внутрибрюшинно в дозе 25 мкг за 1 сутки до инфицирования вирусом, затем через 1, 2, 4, 6 и 8 суток.
Результаты изложены в Таблице 4.
В контроле интраназальное введение вируса вызвало тяжелую пневмонию с высокой летальностью (80%). На этом фоне Рибавирин при высокой инфекционной нагрузке (30 ЛД50) в условиях данного эксперимента оказался малоэффективным. В то же время Phe(р-NH2)-Аллоферон оказал выраженное протекторное действие, превышающее антивирусное действие Аллоферон-1.
Таким образом, результаты примера 4 свидетельствуют о том, что Phe(p-NH2)-Аллоферон в дозе 25 мкг оказывает выраженное антивирусное действие на мышей, инфицированных вирусом гриппа В, существенно превышающее защитный эффект Рибавирина, хорошо зарекомендовавшего себя антивирусного средства, а также Аллоферона-1, и может служить основой для создания новых антивирусных препаратов.
Claims (2)
1. Применение производного Аллоферона-1 Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly в качестве средства, обладающего высокой иммуномодулирующей и противовирусной активностью.
2. Иммуномодулирующая и противовирусная композиция, содержащая пептид Phe(p-NH2)-Gly-Val-Ser-Gly-His-Gly-Gln-His-Gly-Val-His-Gly или его фармацевтически приемлемые соли в сочетании со стандартными вспомогательными веществами.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013141484/15A RU2576830C2 (ru) | 2013-09-10 | 2013-09-10 | Биологически активные производные аллоферона-1 |
| EA201401291A EA035031B1 (ru) | 2013-09-10 | 2014-12-19 | Биологически активное производное аллоферона-1 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013141484/15A RU2576830C2 (ru) | 2013-09-10 | 2013-09-10 | Биологически активные производные аллоферона-1 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2013141484A RU2013141484A (ru) | 2015-03-20 |
| RU2576830C2 true RU2576830C2 (ru) | 2016-03-10 |
Family
ID=53285405
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2013141484/15A RU2576830C2 (ru) | 2013-09-10 | 2013-09-10 | Биологически активные производные аллоферона-1 |
Country Status (2)
| Country | Link |
|---|---|
| EA (1) | EA035031B1 (ru) |
| RU (1) | RU2576830C2 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2744206C1 (ru) * | 2017-09-12 | 2021-03-03 | Классис Инк. | Прокладка для предотвращения обморожения применительно к процедуре криолиполиза |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2267496C2 (ru) * | 2004-01-15 | 2006-01-10 | Сергей Иванович Черныш | Противоопухолевые и антивирусные пептиды |
| RU2470031C2 (ru) * | 2011-02-18 | 2012-12-20 | Общество с ограниченной ответственностью "Аллоферон" | Биологически активные пептидные комплексы |
-
2013
- 2013-09-10 RU RU2013141484/15A patent/RU2576830C2/ru active
-
2014
- 2014-12-19 EA EA201401291A patent/EA035031B1/ru not_active IP Right Cessation
Non-Patent Citations (2)
| Title |
|---|
| CHERNYSH S., et al., Anti-tumor activity of immunomodulatory peptide alloferon-1 in mouse tumor transplantation model. Int Immunopharmacol. 2012 Jan;12(1):312-4. doi: 10.1016/j.intimp.2011.10.016. Epub 2011 Oct 31. * |
| KUCZER M., et al., New alloferon analogues: synthesis and antiviral properties. Chem Biol Drug Des. 2013 Feb;81(2):302-9. doi: 10.1111/cbdd.12020. Epub 2012 Nov 19. * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2744206C1 (ru) * | 2017-09-12 | 2021-03-03 | Классис Инк. | Прокладка для предотвращения обморожения применительно к процедуре криолиполиза |
| US11759353B2 (en) | 2017-09-12 | 2023-09-19 | Classys Inc. | Frostbite prevention pad for cryolipolysis procedure |
Also Published As
| Publication number | Publication date |
|---|---|
| EA201401291A2 (ru) | 2016-01-29 |
| RU2013141484A (ru) | 2015-03-20 |
| EA201401291A3 (ru) | 2016-02-29 |
| EA035031B1 (ru) | 2020-04-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6952379B2 (ja) | 急性ウイルス性呼吸器疾患を治療するための経鼻医薬組成物 | |
| US20210246177A1 (en) | Cath2 derivatives | |
| CN106232616B (zh) | 两亲性合成抗菌肽、其药物组合物及其用途 | |
| US11186619B2 (en) | Antimicrobial peptides based on CMAP27 | |
| KR101267967B1 (ko) | 면역 관련 질병을 예방 및 치료하기 위한 조성물 및 방법 | |
| BG98426A (bg) | Пептиди с органо-защитна активност,метод за тяхното получаване и приложението им за лечение | |
| EP1006124B1 (en) | Immunomodulatory materials from Calliphora vicina larvae, their preparation and use | |
| CA2133569A1 (en) | Novel lipophilic oligopeptides with immunomodulating activity | |
| RU2576830C2 (ru) | Биологически активные производные аллоферона-1 | |
| EP4448104A1 (en) | Compositions and methods for activating innate immunity | |
| RU2575069C2 (ru) | Биологически активный пептид и иммуномодулирующая и противовирусная фармацевтическая композиция | |
| KR102609962B1 (ko) | 히스티딘 유도체를 포함하는 트라이펩타이드 및 이를 포함하는 항균 조성물 | |
| ES2350039T3 (es) | Compuestos inmunomoduladores que contienen gamma-glutamilo y beta-aspartilo y métodos con ellos. | |
| EA031772B1 (ru) | Пептиды, индуцирующие повышенное образование интерферона-гамма и il-18, и иммуномодулирующая, противовирусная фармацевтическая композиция | |
| CN103933554B (zh) | 一种用于预防猪口蹄疫的干扰素白油组合物 | |
| CN110563814B (zh) | 具有免疫调节作用的多肽及其应用 | |
| CN1602200A (zh) | 具有免疫刺激剂活性的植物提取物 | |
| JP2007537280A (ja) | 免疫調節性化合物を用いる呼吸器のウイルス感染の治療又は予防 | |
| EP2030628A1 (en) | A peptide for preventing or treating liver damage and its derivant and the use | |
| CN103923178B (zh) | 一种小肽、其合成方法及其增强家畜免疫力的用途 | |
| CN113813368B (zh) | 一种抗菌肽在制备抗草鱼呼肠孤病毒药物中的应用 | |
| CN113698460A (zh) | 一种大肠杆菌lipid A结合基元PCK及其制备方法与应用 | |
| HK1231775A1 (en) | Antimicrobial peptides based on cmap27 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| HZ9A | Changing address for correspondence with an applicant | ||
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20171016 |