明 細 書
一酸化窒素合成阻害剤
技 術 分 野
本発明は医薬と して有用な一酸化窒素合成阻害剤に関 する。
従 来 技 術
一酸化窒素 (n i tcr i e oxide : N O ) は、 血管内皮由 来弛緩因子 ( E D R F ) の本体であり、 脳、 血小板、 マ ク ロフ ァージ、 好中球等ゃ非ァ ドレナリ ン . 非コ リ ン作 動性神経系等の、 血管内皮細胞以外の組織でも、 伝達物 質乃至調節物質と して機能するこ とが明らかにされてき ている。 この一酸化窒素は、 L 一アルギニン (い Arg ) を基質と して、 一酸化窒素合成酵素 (NO synthase ) に より産生されるが、 該一酸化窒素合成酵素には少なく と も 2種類のイ ソ形 (i soiorm ) が存在すると報告されて いる。 その一つは血管内皮や脳に存在する構成型
(cons t i tut ive type ) の酵素であり、 他方はマク ロフ ァージや血管平滑筋に存在している誘導型 (indiu l e type) のそれである。 しかして、 上記誘導型の一酸化窒 素合成酵素は、 イ ンターロイキ ン類 ( I L s ) 、 イ ン夕 一フエロ ン一 y ( I F - r ) 、 腫瘍壊死因子 (T N F ) 等の多様なサイ トカイ ン類及びエン ド トキシン又はそれ
らから誘導される多様なサイ トカイ ン類によ り誘導され る こ とが知られている。
また、 上記一酸化窒素が生体内で過剰に産生 , 放出さ れた場合には、 その木来の血管弛緩作用に加えて、 一酸 化窒素自体の化学的反応性により、 様々な細胞乃至組織 が障害を受ける こ とが報告されている。 殊に、 エン ド 卜 キシンや各種のサイ トカイ ン頹によって誘導される こ と の知られている上記誘導型一酸化窒素合成酵素は、 これ により産生される一酸化窒素により、 エン ド トキシンシ ョ ッ クや出血性等の発症病態に深く 係わっている こ とが 知られており、 その生理的役割よ り はむしろかかる病態 との係わり において、 注目されている ものである。
一方、 上記一酸化窒素の合成を阻害する阻害剤も種々 知られており 、 その内最も汎用されている ものは、 L一 アルギニン (い Arg ) の ω位 (グァニジノ基) にメ チル 基やニ ト ロ基をもつ各種の L— A r g誘導体であり、 之 等は一酸化窒素合成酵素の L一 A r gに対する可逆的或 は不可逆的競合阻害剤である。
上述した従来技術に関しては、 例えば以下の各種文献 が参照される。
( 1 ) 守時英喜、 血管と内皮、 V o l . 2 , N o . 4, p . 3 2 - 4 0 , 1 9 9 2
( 2 ) 赤池孝章、 他、 医学のあゆみ、 V o l 1 6 6 , N o . 3, p . 1 6 1 - 1 6 4, 1 9 9 3 , 7, 1 7 ( 3 ) H i d e k i Mo r i t o k i , , e t a!. , Br. J, Pharmacol. , ( 1991 ), 102, 841 - 846
( 4 ) H i d e k i M o r i t o k i , , e t a 1. , Br. J. Pharmacol. , ( 1992 ) , 107, 361 - 366
発 明 の 開 示
本発明者らは、 従来より、 上記公知の一酸化窒素合成 阻害剤に代わる新しい一酸化窒素合成阻害物質乃至該医 薬品と しての一酸化窒素合成阻害剤を提供することを目 的と して、 鋭意研究を重ねてきたが、 その過程で、 本願 人らが先にイ ンターロイキン— 1 ( I L— 1 ) の阻害活 性を有する物質と して開発した一連のフエナンス レ ン誘 導体及びその塩 (特開平 4 — 2 1 1 0 3 5号公報等参照) が、 上記目的に合致する一酸化窒素合成阻害活性を有す るこ とを見出し、 こ こ に本発明を完成するに至った。
即ち、 本発明は下式 ( 1 ) 〜 ( 1 2 ) で表わされる化 合物からなる群から選ばれたフ エナンス レン誘導体及び それらの塩の少なく とも 1種を有効成分と して含有する こ とを特徴とする一酸化窒素合成阻害剤に係わる。
〔式中ヽ 基— A〜 B—は基 R l 0 0 C C = C C H 3
(R 1 は水素原子又は低級アルキル基) 、 基
^ C = C
0 ^ v 7 I ^ C H 2 O R 2
C H 3
(R 2 は水素原子又は低級アルカノ ィル基) 、 基
R 2 0 ^ " H—?、 C H 2 0 R 2 (R 2 は上記に同じ)
C H 3
又は基一 C H 2 — C
C H 0を示す。 〕
C H 式 ( 2 ) :
( 2 )
〔式中、 R 3 は水素原子又はメ チル基を示す 式 ( 5 ) :
H00C
〔式中、 R
4 は低級アルカノ ィルォキシ基を示す。 R
2 は前記に同じ。 J 一般式 ( 7 ) :
〔式中、 R 3 及び R Q はそれぞれ低級アルコキシ基を示 す。 〕
—般式 ( 8 ) :
〔式中、 R 1πは低級アルキル基を、 R はホルミ ル基^
3Aはヒ ドロキシ基を示すか、 又は R と 3Aとでォキ ソ基を示し、 また R 3Aは後記の R 5Aと互いに結合して二 重結合を形成してもよい。 R 4Aは低級アルキル基を、 R "Aは水素原子、 ヒ ドロキシ低級アルキル基或いは R 3A 又は後記の R 6Aと互いに結合して二重結合を形成し、 6Aは水素原子又は 5Α
R R ΰΛと互いに結合して二重結合を形 成し、 R 7 は水素原子又は低級アルキル基をそれぞれ示
す。 但し、 R 7 がイ ソプロ ピル基の場合、 R 5Aはヒ ドロ キシメ チル基でないものとする。 〕
一般式 ( 9 ) :
〔式中、 R 1A、 R 及び R 7 は前記に同じ。 R 2 aはホル ミ ル基、 ト リ低級アルキルシ リルォキシ基、 ト リ フルォ
0
II
ロメ チルスルホニルォキシ基又は基 P h 2 P C H—
I
O R10
(式中 R 1 Qは低級アルキル基及び P hはフニ二ル基を示 す。 ) を、 R 3 aはヒ ドロキシ基を示すか、 或いは R 2 aと R3 aとでォキソ基又は基 R 0— C H = (式中 R 1Gは前 記に同じ。 ) を示し、 また R 3aは後記の R 5 aと互いに結 合して二重結合を形成してもよい。 R 5aは水素原子、 ヒ ドロキシ低級アルキル基或いは R 3 a又は後記の R 6 aと互 いに結合して二重結合を形成し、 R 6 aは水素原子又は R 5aと互いに結合して二重結合を形成し、 R 8 は水素原 子又は低級アルコキシ基を、 R 9 は低級アルキル基をそ れぞれ示す。 但し、 R 7 がイ ソプロ ピル基の場合、 R 5a
は ヒ ドロキシメ チル基でないもの と し、 R 7 と R 8 が同 時に水素原子である場合は、 R 5 aは R G aと互いに結合し て二重結合を形成しない ものとする。 〕
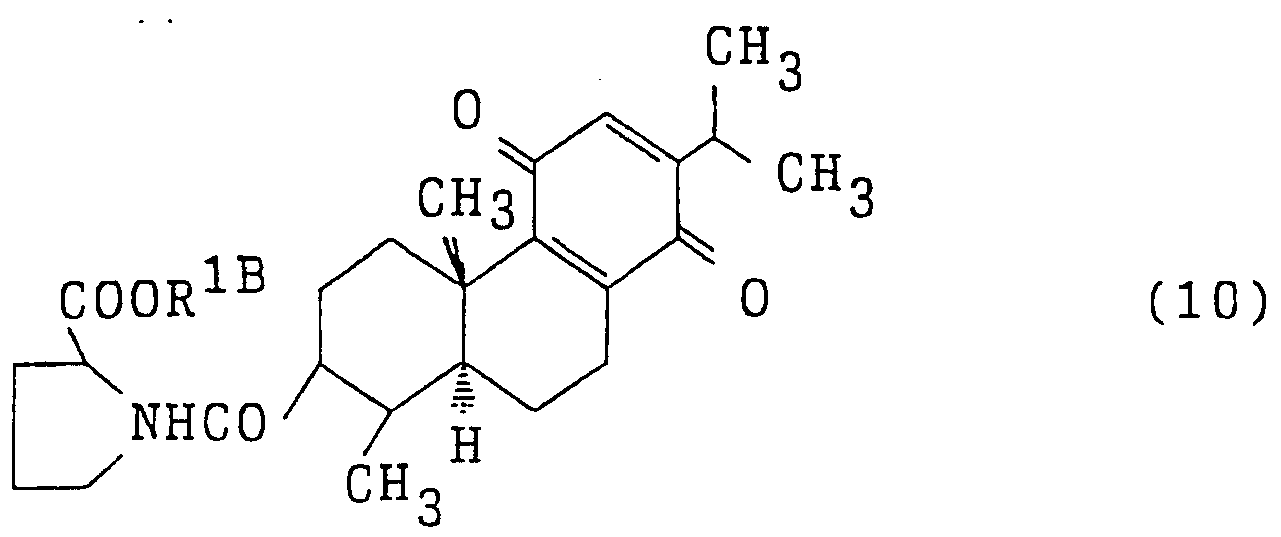
一般式 ( 1 0 ) :
〔式中 R l uは低級アルキル基を示す。 〕
一般式 ( 1 1 ) :
〔式中 R 2Bはヒ ドロキシメ チル基又はカルボキシル基を 示す。 〕
一般式 ( 1 2 ) :
(12)
〔式中 R
3 Bは低級アルコキシカルボニル基又は ヒ ドロキ シメ チル基を、 R
4 B及び R
5 dはそれぞれ低級アルコキシ 基を示す。 〕
本発明有効成分化合物を示す前記一般式 ( 1 ) 〜 ( 1 2 ) における各基は、 それぞれ次の通り である。 即ち、 低級アルキル基と しては、 例えばメ チル、 ェチ ル、 プロ ピル、 イ ソプロ ピル、 ブチル、 t e r t—プチル、 ペンチル、 へキシル基等の炭素数 1 〜 6 の直鎖状も し く は分枝鎖状アルキル基を例示でき る。
低級アルカノ ィル基と しては、 例えばホルミ ル、 ァセ チル、 プロ ピオニル、 プチ リ ル、 イ ソプチ リ ル、 ペン夕 ノ ィル、 へキサノ ィ ル基等の炭素数 1 〜 6 の直鎖状も し く は分枝鎖状アルカノ ィル基を例示でき る。
低級アルカノ ィルォキシ基と しては、 例えばァセチル ォキシ、 プロ ピオニルォキシ、 プチ リ ルォキシ、 イ ソブ チ リ ルォキシ、 ペンタ ノ ィルォキシ、 へキサノ ィルォキ シ基等の炭素数 2 〜 6 の直鎖状も し く は分枝鎖状アル力 ノ ィ ルォキシ基を例示でき る。
低級アルコキシ基と しては、 例えばメ トキシ、 ェ トキ シ、 プロボキシ、 イ ソプロボキン、 ブ トキシ、 t e r t—ブ トキシ、 ペンチルォキシ、 へキシルォキシ基等の炭素数 1 〜 6 の直鎖状も し く は分枝鎖伏アルコキシ基を例示で
さ る o
ヒ ドロキシ低級アルキル基と しては、 例えばヒ ドロキ シメ チル、 1 — ヒ ドロキシェチル、 1 ー ヒ ドロキシプロ ピル、 1 — ヒ ドロキシブチル、 1 — ヒ ドロキシペンチル、 1 — ヒ ドロキシへキシル基等を例示でき る。
ト リ低級アルキルシ リ ルォキシ基と しては、 例えば ト リ メ チルシ リ ルォキシ、 ト リ ェチルシ リ ルォキシ、 ト リ プロ ビルシ リ ルォキシ、 ト リ ブチルシ リ ノレオキシ、 ト リ t e r t—ブチルシ リ ルォキシ、 ト リ ペンチルシ リ ルォキシ、 ト リ へキシルシ リ ルォキシ基等を例示でき る。
低級アルコキシカルボニル基と しては、 例えばメ トキ シカルボニル、 エ トキシカルボニル、 プロポキシカルボ ニル、 イ ソプロポキシカルボニル、 ブ トキシカルボニル、 t e r t—ブ トキシカルボニル、 ペンチルォキシカルボニル、 へキシルォキシカルボ二ル基等を例示でき る。
上記各フ ニナ ンス レ ン誘導体は、 いずれも本発明者ら によ り先に開発されたものである (特開平 4 一
2 1 1 0 3 5号公報、 特願平 3— 2 2 4 2 8 7号、 特願 平 4— 3 4 4 5 9 0号等) 。 之等の一部及びそれらの製 造法は既に公知 (例えば前記特開平 4 _ 2 1 1 0 3 5号 公報参照) となっており、 また他の誘導体は上記公知の 方法に準じてそれぞれ製造する こ とができ る。
例えば上記 ( 8 ) で表わされる化合物は、 下記反応ェ 程式— 1及び一 2に示す方法によ り製造する こ とができ る o
[反応工程式一 1 ]
(2 a) (la)
[式中、 R 1 、 R3 、 R 4 及び R。 は、 一般式 ( 8 ) に おける R 1A、 R 3A、 R4A及び R 6Aに同じ。 R 9 は低級了 ルキル基を示す。 R2'は一般式 ( 8 ) における R2Aと同 じであるか又は水素原子、 カルボキシル基、 低級アルコ キシカルボニル基、 水酸基も し く は低級アルカ ノ ィルォ キシ基を示す。 R 5 は一般式 ( 8 ) における R 5Aと同じ であるか又はホル ミ ル基、 カルボキシル基も し く は低級 アルカノ ィ ルォキシメ チル基を示す。 R 7 aは低級ァルキ ル基を、 R 8 aは低級アルコキシ基を、 R 12は水素原子又 は水酸基をそれぞれ示す。 ]
上記において、 低級アルカ ノ ィ ルォキシ基及び低級ァ ルカ ノ ィ ルォキシメ チル基の低級アル力 ノ ィ ル基と して
は、 例えばホル ミ ル、 ァセチル、 プロ ピオニル、 プチ リ ル、 イ ソプチ リ ル、 ペンタ ノ ィル、 へキサノ ィ ル基等の 炭素数 1〜 6の直鎖状も し く は分鎖状アルカ ノ ィ ル基を 例示でき る。
上記反応工程式一 1に示す化合物 ( 2 a ) の酸化反応 は、 例えばァセ トニ ト リ ル、 ジク ロ ロメ タ ン、 N , N— ジメ チルホルムア ミ ド (D M F) 等の不活性溶媒中で、 セ リ ッ ク ア ンモニゥムニ ト ラー ト
[(NH4 ) 2 Ce (N03 ) β ] (以下 C A Nと略記する) 、 無水ク ロム酸等の酸化剤を用いて実施でき る。 上記酸化 剤の使用量は、 化合物 ( 2 a ) に対して通常 1〜 3倍モ ル量程度とすればよ く 、 反応は一般に 0〜 5 0 °C程度の 温度下に、 約 1 0分〜 3時間程度で完結し、 かく して目 的化合物 ( 1 a ) が得られる。
[反応工程式一 2 ]
[式中、 R 1 、 R 4 及び R 9 は上記に同 じ。 R 5bは ヒ ド
ロキシ低級アルキル基を示す。 ]
上記反応工程式一 2に示す化合物 ( 2 b ) の脱アルキ ル化反応は、 例えばテ トラ ヒ ドロフラ ン ( T H F ) 、 ァ セ トニ ト リ ル、 ジク ロロメ タ ン等の不活性溶媒中で、 ィ匕 合物 ( 2 b ) を、 三臭化硼素、 無水塩化ア ンモニゥム、 臭化水素酸等の脱アルキル化剤を用いて処理することに より実施される。 上記脱アルキル化剤の使用量は、 化合 物 ( 2 b ) に対して通常 1〜 3倍モル量程度とすればよ く、 反応は一般に一 7 8 °C〜 5 0 °C程度の温度下に、 約 3 0分〜 5時間程度を要して行なわれる。
次に上記で得られた化合物 ( 3 b ) を酸化するこ とに より、 目的化合物 ( l b) を得るこ とができる。 該酸化 反応は、 例えばエタノ ール、 ジク ロロメ タ ン等の不活性 溶媒中で、 酸化剤と して例えばジニ 卜 ロスルホ ン酸カ リ ゥム、 ニト ロ ソ ジスルホ ン酸カ リ ウム、 ク ロム酸等を化 合物 ( 3 b ) に対して通常 1〜 3倍モル量程度用い、 更 に必要に応じてリ ン酸水素二力 リ ゥム等の添加剤を加え て、 約 0〜 5 0 °Cの温度条件下に、 5〜 2 0時間程度を 要して実施される。
尚、 上記反応工程式一 1及び一 2において原料と して 用いられる化合物 ( 2 a ) 及び化合物 ( 2 b ) は、 いず れも新規化合物であり、 そのうちのある種のものはク ロ
ズノレ (Tripterygium w i 1 f o r d i i H o o k f i 1 v a r, r e g e 1 i i Maki no)より抽出単離するか又はこれに引続いて適当な 化学処理を施すこ とによ り得られる。 また上記化合物 (2 a ) 及び化合物 (2 b ) に属するそれぞれの化合物 [化合物 (2 c ) 〜化合物 (2 f ) ] は、 以下に該当す る各反応行程式に示す方法に従い製造するこ とができる [反応行程式一 3 ]
[式中、 R 1 、 R4 、 R7 a、 R 8a、 R 9 及び R 1 Qは前記 に同じ。 P hはフ ヱニル基を示す。 R 11は低級アルキル 基を、 Xはハロゲン原子を示し、 破線は二重結合がーつ 存在するこ とを表す。 ]
上記化合物 ( 4 b ) のハロゲン化反応は、 D M F、 ク ロロホルム等の不活性溶媒中で、 N—ブロムコハク酸ィ ミ ド (N B S ) 、 臭素等のハロゲン化剤を化合物 ( 4 b ) に対して 1〜 1. 5倍モル量程度用い、 約 0〜 5 0 °Cの 温度条件に、 1〜 2 0時間程度を要して実施される。
得られる化合物 ( 5 b ) は、 これをアルキル化する こ とによ り化合物 ( 6 b ) に変換される。 該アルキル化反 応は、 無溶媒又はジェチルエーテル、 アセ ト ン等の適当 な不活性溶媒中、 必要に応じて水酸化力 リ ゥム水溶液、 炭酸カ リ ウム等の脱酸剤の存在下に、 ジメ チル硫酸、 ジ ァゾメ タ ン、 ヨ ウ化メ チル等のアルキル化剤を用いて行 なわれ、 反応は約 0〜 3 0 °Cの温度で、 3 0分〜 2時間 程度にて完結する。
続いて、 化合物 ( 6 b ) の化合物 ( 7 b ) への変換反 応は、 D M F、 メ タ ノ ール、 等の不活性溶媒中、 ヨ ウ化 銅 ( I ) の存在下、 ナ ト リ ウムメ トキシ ド、 ナ ト リ ウム ェ トキシ ド等の金属低級アルコキシ ドを用いる こ とによ り行なわれる。 反応条件と しては、 約 5 0〜 1 0 0 °Cの 温度で 3 0分〜 5時間程度が採用される。
次に、 化合物 (7 b ) の還元反応は、 メ タ ノ ール、 ェ 夕 ノ ール、 液体ア ンモニア等の溶媒中、 アルカ リ 金属、 好ま し く は金属ナ ト リ ゥムと約 3 0〜 8 0 °Cの温度で 1 0分〜 1時間処理する こ とによ り実施される。
得られる化合物 ( 8 b ) は、 メ タ ノ ール、 エタ ノ ール 等の不活性溶媒中、 シユ ウ酸、 塩酸等の酸と共に、 加水 分解処理する こ とによ り化合物 ( 9 b ) に変換される。 該反応は約 5 0〜 8 0 °Cの温度で 5〜 2 4時間で完結す
る O
引き続き、 化合物 ( 9 b ) は、 ベンゼン、 ジォキサン, トルエン等の不活性溶媒中、 ピロ リ ジン、 ピぺリ ジン等 のァ ミ ンの存在下、 ヨウィ匕メ チル、 ヨウ化工チル等のハ ロゲン化アルキルと処理する こ とにより、 アルキル化さ れた化合物 ( 1 0 b ) に変換される。 より好ま し く は、 まず化合物 ( 9 b ) を上記不活性溶媒中、 上記のァ ミ ン と共に 2 0〜 5 0 °Cの温度で 3〜 6時間反応させた後、 上記ハロゲン化アルキルを加え、 約 5 0〜 8 0 °Cの温度 で 1 0〜 5 0時間反応させる。
化合物 ( 1 0 b ) は、 ビニルケ ト ン誘導体 ( l i b ) と環化反応を行なう ことにより、 目的化合物 ( 2 c ) へ と導く こ とができる。 該環化反応は、 メ タノ ール、 エタ ノ ール、 T H F等の不活性溶媒中、 水酸化力 リ ゥム水溶 液、 水酸化ナ ト リ ゥム水溶液等の塩基の存在下、 化合物 ( 1 0 ) に対して 1〜 1. 3倍モル量のビニルケ ト ン誘 導体 ( l i b ) を用いて実施される。 反応は、 約一 3 0 〜 3 0 °Cの温度条件で 5〜 1 5時間を要して行なわれる ( 更に化合物 ( 2 c ) は、 これに化合物 ( 1 2 b ) を反 応させる こ とにより、 化合物 ( 2 d ) へと変換される。 該反応は T H F等の不活性溶媒中、 n—プチルリチウム 等のアルキルリ チウム及びジイ ソプロ ピルア ミ ン、 ジェ
チルア ミ ン等のア ミ ンの存在下、 化合物 ( 2 c ) に対し て 1〜 1. 5倍モル量の化合物 ( 1 2 b ) を用いて行な われ、 約— 7 8〜― 6 0 °Cの温度条件で 1〜 3時間で完 る o
上記で得られる化合物 ( 2 d ) は、 DM F、 T H F、 ジェチルエーテル等の不活性溶媒中、 水素化カ リ ウム、 水素化ナ ト リ ウム等のハイ ドライ ド化合物を用いて還元 するこ と によ り、 化合物 ( 2 e ) に変換される。 該還元 反応は、 約— 3 0〜 1 0 °Cの温度条件で 3 0分〜 2時間 を要して行なわれる。
続いて、 化合物 ( 2 e ) を加水分解すれば、 化合物 ( 2 f ) を得ることができる。 該加水分解反応は、 メ タ ノール、 エタノ ール等の不活性溶媒中、 シユウ酸水溶液、 塩酸等の酸を用いて実施される。 尚、 上記溶媒及び酸は 全て脱気したものを用い、 アルゴンや窒素等の不活性ガ ス雰囲気中で反応を行なう必要があり、 反応は、 5 0 °C 〜溶媒の沸点の温度条件で 1〜 6時間にて完了する。
かく して得られる化合物 ( 2 f ) は、 これを通常の酸 化反応に従わせる こ とによ り、 該化合物 ( 2 f ) のアル デヒ ド ( C H 0 ) 基を、 カルボキシル基 ( C 00 H ) に 変換させるこ とができ、 これによつて、 R 2 がカルボキ シル基である対応する化合物 ( 2 a ) を収得できる。
[反応工程式一 4 ]
[式中、 R 1 、 R 4 及び R 7 aは前記に同じ。 R 8bは R 8 a と同じであるか又は低級アルカノィルォキシ基を示す。 R 9 R 9 と同じであるか又は水素原子も し く は低級ァ ルカノ ィル基を示す。 R 2bは 卜 リ低級アルキルシ リ ルォ キシ基を示す。 ]
上記反応工程式一 4に示す方法によれば、 化合物
( 2 c ) より、 化合物 ( 2 f ) 、 化合物 ( 2 g ) 、 化合 物 ( 2 h ) 及び化合物 ( 2 i ) を収得できる。
即ち、 まず化合物 ( 2 c ) を還元すれば化合物 ( 2 g ) が得られる。 該還元反応は、 不活性溶媒中 1 モルの水素
で接触還元するか、 あるいは液体ア ンモニア中、 金属ナ ト リ ウム、 金属 リ チウム等のアルカ リ金属を用いる (バ ーチ還元) こ とによ り実施される。
次に、 化合物 ( 2 h ) への変換反応は、 上記化合物 ( 2 c ) のパーチ還元生成物を、 単離する こ とな く 、 ァ ンモニァを除去して得られる金属エノ ラ ー 卜の状態のま まで、 シ リ ル化反応を行な う こ と によ り実施でき る。 該 シ リ ル化反応は、 T H F、 ジェチルエール等の不活性溶 媒中、 ト リ ェチルァ ミ ン、 ピ リ ジ ン等の脱酸剤の存在下、 塩化 ト リ アルキルシ リ ル等のシ リ ル化剤を用いて、 約— 1 0〜 1 0 °Cの温度で 1 0分〜 1時間程度を要して行な われる。
得られる化合物 ( 2 h ) は、 T H F、 エーテル等の不 活性溶媒中、 メ チルリ チウム、 ブチル リ チウム等のアル キルリ チウムの存在下、 一 1 0。C〜 3 0 °Cの温度にて 3 0分〜 1時間処理した後、 N—フ ヱニル ト リ フルォロ メ タ ンスルホ ンイ ミ ド ( PhNTi2 ) と約一 7 8〜 1 0 °C の温度にて 5〜 1 5時間処理する こ とによ り、 化合物 ( 2 i ) に変換される。
更に化合物 ( 2 i ) は、 スチルら (S t i 11 et a 1. )の方 法 [ J. Am. Chem. Soc. , 108 ( 3 ), 452 ( 1986 )] に基づき、 塩 ィ匕 リ チウム及びテ ト ラキス ( ト リ フ エニルホスフ ィ ン)
パラ ジウム [Pd ( Ph3 P) 4 ] の存在下、 一酸化炭素及び 水素化錫 ト リ ブチル等の鍚ハイ ドライ ドと反応させるこ とにより、 化合物 ( 2 f ) に変換できる。 反応温度及び 時間と しては、 3 0〜 6 0で程度及び 1 5〜 6 0時間程 度がそれぞれ採用される。
[反応工程式一 5 ]
[式中 R 1 、 R 4 、 R 7 a、 R 8 a、 R 9 及び R i Qは前記に 同じ。 ]
上記反応工程式一 5 に示す化合物 ( 2 e ) の酸化反応 は、 シュ ミ ッ ト らの方法 [Angev. Chem., U, 116 ( 1959 ) ] に準じて行なわれる。 即ち、 D M F —水等の含水不活性 溶媒中、 酸素 (空気) の存在下、 塩化パラ ジウム ( 11) と塩化銅 (11) とのコ ンプレ ッ ク スに化合物 ( 2 e ) を 約 5 0〜 1 0 0 °Cの温度で 1 0〜 2 4時間程度作用させ る こ とによ り、 化合物 ( 2 j ) を得る こ とができ る。
[反応工程式一 6 ]
[式中 R 1 、 R 2b、 R" 、 R 5b及び R 9 は前記に同 じ。 ] 化合物 ( 2 b ) は、 公知化合物 ( 1 3 ) よ り反応工程 式一 6に示す方法によ り得る こ とができ る。
即ち、 まず化合物 ( 1 3 ) を還元し、 次にシ リ ル化し て化合物 ( 1 4 ) を得る。 該還元反応及びシ リ ル化反応 は、 反応工程式一 4における化合物 ( 2 c ) の還元反応 及びシ リ ル化反応と同様の方法で行な う こ とができ る。
続いて、 化合物 ( 1 5 ) を T H F、 エーテル等の不活 性溶媒中、 弗化テ ト ラ プチルア ンモニゥム (T B A F ) 等の脱シ リ ル化剤の存在下、 ホルムアルデヒ ドガス等の
アルデヒ ド類を用いて処理するこ とにより、 目的の化合 物 ( 2 b ) を得ることができる。 反応は、 約一 7 8〜 3 0 °Cの温度で 1 0分〜 1時間程度にて完結する。
上記各反応工程式に示す方法により得られるフ ニ ナ ン ス レ ン誘導体は、 慣用の分離手段により単離精製できる。 該手段と しては、 例えば吸着ク ロマ トグラフィ ー、 再結 晶、 溶媒留去、 沈澱、 溶媒抽出等を例示できる。
また、 本発明において有効成分とする前記一般式
( 1 0 ) 〜 ( 1 2 ) で表わされる各化合物は、 前記特開 平 6— 1 9 2 1 5 5号公報記載の方法により製造するこ とができる。
上記各フ ユ ナ ンス レ ン誘導体の製造の詳細は、 後記実 施例 (製造例) に示す通りである。
本発明の一酸化窒素合成阻害剤の有効成分と しては、 上記フ ニナ ンス レ ン誘導体のみならず、 該誘導体の内で 酸性基即ちフ ニノ ール性水酸基及び (又は) カルボキン ル基を有する化合物にあっては、 これと塩基性化合物と の一般的塩形成反応に従い形成される塩をも包含する。 上記塩の製造に利用される塩基性化合物と しては、 具体 的には水酸化ナ ト リ ウム、 水酸化カ リ ウム、 水酸化カル シゥ ム、 炭酸ナ ト リ ウ ム、 炭酸力 リ ウ ム、 炭酸水素ナ ト リ ウム、 水素化ナ 卜 リ ゥム等のアル力 リ金属又はアル力
リ土類金属の水酸化物、 炭酸化物、 水素化物等を例示で き る。 また例えばメ チルァ ミ ン、 ェチルァ ミ ン、 イ ソプ 口 ピルァ ミ ン、 モルホ リ ン、 ピぺラ ジ ン、 ピぺ リ ジ ン、 3 , 4 — ジメ トキシフ エネチルァ ミ ン等の有機ア ミ ン類 も上記塩形成用塩基性化合物と して利用できる。
本発明有効成分化合物は、 また上記各フ ニナンス レ ン 誘導体及びその塩の立体異性体、 光学異性体であっても よい。
本発明において有効成分と して用いる上記フ エナンス レ ン誘導体及びその塩は、 一酸化窒素の生合成を阻害す る作用を奏し得、 従ってこれを有効成分とする本発明の 一酸化窒素合成阻害剤は、 一酸化窒素に起因する各種の 病態、 よ り具体的にはエン ド トキシ ンシ ョ ッ ク、 出血性 シ ョ ッ ク、 各種の虚血性疾患及び血圧降下を伴う各種の 病態等の治療乃至予防に有効に適用できる。 殊に、 本発 明阻害剤は、 前述した誘導型一酸化窒素合成酵素の誘導 を阻害する作用を奏するこ とによって、 該酵素により産 生される一酸化窒素を特異的に阻害するこ とができ、 か かる異常又は過剰に産生 ' 放出される一酸化窒素を抑え 得る点で、 より好ま しい特徴を有する ものである。
上記特徵を有する本発明阻害剤において、 特に好ま し い有効成分化合物は、 キノ ン及びヒ ドロキノ ン構造を有
する ものから選択される。
その一つの具体例と しては、 例えば前記一般式 ( 1 ) で表わされる化合物を例示できる。 他の好ま しい有効成 分化合物の具体例と しては、 前記一般式 ( 4 ) (他だし、 R 3 は水素原子) を例示できる。 更に他の好ま しい具体 例と しては、 前記一般式 ( 1 1 ) で表わされる化合物を 例示でき る。
之等の有効成分化合物中でも、 特に好ま しいものは、 後記表 1 0 に示す化合物 1 〜化合物 6である。
本発明阻害剤は、 慣用される医薬製剤担体を用いて一 般的な医薬製剤組成物の形態に調製され、 ヒ 卜及びその 他の動物に投与できる。 上記医薬製剤担体、 製剤形態
(投与単位形態) 、 その調整、 その投与経路等は、 通常 の医薬製剤のそれらと同様のものとするこ とができる。 即ち、 上記医薬製剤と しては、 本発明有効成分化合物の 有効量を含有する錠剤、 丸剤、 散剤、 液剤、 懸濁剤、 乳 剤、 顆粒剤、 カプセル剤、 坐剤、 注射剤 (液剤、 懸濁剤 等) 等が挙げられる。 上記各種形態の製剤は、 いずれも 常法に従い調整され、 その際用いられる担体も慣用され る各種のものでよい。 例えば錠剤は、 本発明化合物を有 効成分と して、 これをゼラチ ン、 デンプン、 乳糖、 ステ ア リ ン酸マグネシウム、 滑石、 アラ ビアゴム等の賦形剤
と混合して賦形される。 カプセル剤は上記有効成分を、 不活性な製剤充填剤も し く は希釈剤と混合し、 硬質ゼラ チンカプセル、 軟質カプセル等に充填して調整される。 注射剤等の非経口投与剤は、 有効成分と しての本発明化 合物を滅菌した液体担体に溶解乃至懸濁させて製造され、 その際用いられる好ま しい液体担体は水及び生理食塩水 であり、 調整される注射剤等には更に通常の溶解補助剤、 緩衝剤、 無痛化剤等を添加するこ ともできる。 更に、 上 記各種形態の医薬製剤中には、 必要に応じて着色剤、 保 存剤、 香料、 風味剤、 甘味剤等や他の医薬品を含有させ るこ と もできる。
本発明製剤中に有効成分と して含有されるべきフニナ ンス レ ン誘導体及びその塩の量は、 特に限定されず広範 囲から適宜選択できるが、 通常全医薬製剤組成物中に 1 〜 7 0重量%程度、 好ま しく は 1 〜 3 0重量%程度とす るのがよい。 上記で調整される医薬製剤の投与方法は特 に制限されず、 例えば錠剤、 丸剤、 散剤、 顆粒剤、 カブ セル剤等は経口投与され、 また注射剤 (液剤、 懸濁剤等) は単独で又はブ ドウ糖、 ア ミ ノ酸等の通常の補液と混合 して静脈内投与されるか又は必要に応じて単独で筋肉内、 皮内、 皮下も しく は腹腔内投与される。 更に上記医薬製 剤の投与量は、 用法、 患者の年齢、 性別その他の条件、
疾患の程度等により適宜選択されるが、 通常有効成分で ある本発明化合物の量が 1 日当り体重 1 k g当り約 0. l〜 1 0 0 0 m g程度とするのがよ く、 該製剤は 1 日に 1〜 4回に分けて投与することができる。 また投与単位 形態中には有効成分を約 1〜 6 0 O m g程度含有させる のがよい。
発明を実施するための最良の形態 以下、 本発明を更に詳し く説明するため、 本発明にお いて有効成分とするフ ナ ンス レ ン誘導体の製造例を実 施例と して挙げ、 次いで之等誘導体を用いた本発明製剤 の製剤例及び薬理試験例を挙げる。
製剤例 1
後記表 1 0 に示す化合物 1 1 5 0 g 了 ビセル (商標名、 旭化成 (株) 製) 4 0 g コー ンスタ ーチ 3 0 g ステア リ ン酸マグネ シウ ム 2 g ヒ ドロキシプロ ピルメ チゾレセルロ ース 1 0 g ポ リ エチ レ ング リ コ一ル一 6 0 0 0 3 g ヒマ シ油 4 0 g メ タ ノ ール 4 0 g 上記有効成分化合物、 アビセル、 コー ンスターチ及び ステア リ ン酸マグネシウムを混合研磨後、 糖衣 R 1 0 m
mのキネで打錠する。 得られた錠剤を ヒ ドロ キ シプロ ピ ノレメ チノレセノレロ ース、 ポ リ エチ レ ング リ コ 一ノレ一
6 0 0 0、 ヒマ シ油及びメ タ ノ ールから な る フ イ ノレムコ —ティ ング剤で被覆を行ない、 フ ィ ルムコーティ ング錠 を製造する。
製剤例 2
3 , 4 , 4 a , 5, 8, 9 , 1 0, 1 0 a -ォ ク 夕 ヒ ド 口 一 1 , 4 a _ジメ チルー 7 — ( 1 ー メ チルェチル) 一 5 , 8 — ジォキソ 一 2 — フ エナ ンス レ ンカルボン酸
1 5 0. 0 g ク ェン酸 1. 0 g ラ ク ト —ス 3 3. 5 g リ ン酸ニカルシゥム 7 0. 0 g プル口ニ ッ ク F— 6 8 3 0. 0 g ラ ウ リ ル硫酸ナ ト リ ウム 1 5. 0 g ポ リ ビニルピロ リ ドン 1 5. 0 g ポ リ エチ レ ング リ コ ール (カルボワ ッ ク ス 1 5 0 0 )
4. 5 g ポ リ エチ レ ング リ コーノレ (力ソレボワ ッ ク ス 6 0 0 0 )
4 5. 0 g コー ンスタ ーチ 3 0. 0 g 乾燥ラ ウ リ ル硫酸ナ ト リ ウム 3. 0 g
乾燥ステア リ ン酸マグネ シウム 3. 0 g エタ ノ ール 適 量
上記有効成分化合物、 クェン酸、 ラ ク ト 一ス、 リ ン酸 二カルシウム、 プル口ニッ ク F— 6 8及びラ ウ リ ル硫酸 ナ ト リ ウムを混合し、 上記混合物を N 0. 6 0スク リ 一 ンにて篩別し、 ポ リ ビニルピロ リ ドン、 カルボワ ッ ク ス 1 5 0 0及びカルボワ ッ ク ス 6 0 0 0を含むアルコール 性溶液で湿式粒状化する。 必要に応じアルコ ールを添加 し、 粉末をペース ト状塊に し、 コー ンスターチを添加し、 均一な粒子が形成されるまで混合を続ける。 N o . 1 0 スク リ ー ンを通過させ、 ト レイ に入れ、 1 0 0 °Cのォー ブンで 1 2〜 1 4時間乾燥する。 乾燥粒子を N 0. 1 6 スク リ ー ンで篩別し、 乾燥ラ ゥ リ ル硫酸ナ 卜 リ ウム及び 乾燥ステア リ ン酸マグネシウムを加えて混合し、 打錠機 で所望の形状に圧縮成形して芯部を作成する。
上記芯部をワニスで処理し、 タルクを散布して湿気の 吸収を防止させ、 該芯部の周囲に下塗り層を被覆し、 内 服用のために充分な回数のワニス被覆を行ない、 この下 塗り層形成及び平滑被覆を繰返し、 所望色合が得られる まで着色被覆を行ない、 乾燥して被覆錠剤を得る。
実施例 1
5 , 8— ジメ トキシー 1 , 4 a — ジメ チルー 7— ( 1 —
メ チルェチル) 一 4, 4 a , 9, 1 0—テ ト ラ ヒ ドロ ー 2 ( 3 H ) — フ ヱ ナ ンス レノ ンの製造
2 —イ ソプロ ピル一 6—メ トキシー 1 一ナフ ト ール 5 gを DM F l O O m l に溶解し、 氷冷下 N—ブロムコハ ク酸イ ミ ド 4. 0 3 gの D M F ( 5 0 m l ) 溶液を加え、 氷冷下で 3時間攪拌した。 反応混合物に水を加え、 酢酸 ェチルで抽出し、 有機層を飽和食塩水で洗浄した後、 硫 酸マグネシウムで乾燥して濃縮した。 得られた粗生成物 をシ リ 力ゲルカラムク ロマ 卜グラフィ 一 (溶出液…ジェ チルエーテル : n—へキサン : ク ロ 口ホルム = 1 0 : 5 0 : 1 ) にて精製して、 4—ブロム一 2 —イ ソプロ ピ ルー 6—メ トキシ— 1 —ナフ ト一ル 6. l gを得た。 融 点 : 8 1. 5〜 8 3. 5 °Co
^ - NMR ( 5 : p p m) 〔C D C 1 ゥ 〕 :
8. 06 (1 H, d, J = 8. 8) , 1. 58 (1H, s) , 7. 41 (1H, d, J = 2. 4) ,
7. 16 (1H, dd, J = 8.8, 2.4) , 5. 18 (1H, brs), 3. 96 (3H, s) , 3. 20 (1H, sept, J = 6. 8), 1. 33 (3H, d, J = 6, 8)。
次いで、 水酸化力 リ ウム 9 5 6 m gを溶かした水
1. 7 m 1 に、 上記で得られた化合物 1 gを氷冷下で加 え、 次いでジメ チル硫酸 1. 1 m l を加えて氷冷下 4 5 分攪拌した。 反応終了後、 水を加え、 酢酸ェチルで抽出 し、 有機層を飽和食塩水で洗浄した後、 硫酸マグネシゥ
ムで乾燥して濃縮した。 得られた粗生成物をシ リ カゲル カラムク ロマ ト グラ フ ィ 一 (溶出液…ジェチルェ一テル : n—へキサン : ク ロ 口ホルム = 5 : 1 0 0 : 2 ) にて精 製して、 4—ブロム一 2 —イ ソプロ ピル一 1 , 6 — ジメ トキシナフタ レ ン l gを得た。 融点 : 1 0 8〜 1 1 0 °C。
^ - MR ( 5 : p p m) [ C D C 1 3 ] :
7.99 (1H, d, J = 9.0), 1.65 (1H, s), 7.43 (1H, d, 2. 3) ,
7.18 (1H, dd, J = 9.0, 2.3), 3.95 (3H, s), 3.89 (3H, s), 3.50 (1H, sept, J = 7.3), 1.28 (6H, d, J = 7.3)。
次に、 ナ ト リ ウムメ トキシ ド 6 3 1 m gにメ タ ノ ール 3 m l 及び DM F 1. 7 m l を加え、 更にヨ ウ化銅 ( I ) 5 5 9 m gを加えて 9 0 °Cに加熱した。 そこ に、 上記で 得られた化合物 9 0 1 m gの DM F ( 1. 1 7 m l ) 溶 液を滴下し、 2時間加熱還流した。 放冷後、 不溶の固形 物を濾別し、 濾液に水を加え酢酸ェチルで抽出 した。 有 機層を飽和食塩水で洗浄した後、 硫酸マグネ シゥムで乾 燥して濃縮した。 得られた粗生成物をシ リ カゲルカラム ク ロマ ト グラ フ ィ ー (溶出液…ジェチルェ一テル : n— へキサン : ク ロ 口ホルム = 5 : 1 0 0 : 2 ) にて精製し て、 2—イ ソプロ ピル一 1, 4 , 6— ト リ メ トキシナフ タ レン 7 0 0 m gを得た。 融点 : 8 0〜 8 1. 5 °C。
1 H - NMR ί δ : p p m) [ C D C 1 3 ¾
7.93 (1H, d, J = 9.3) , 7.48 (1H, d, J = 2. 5) , 7. 16 (1H, dd, J = 9.3, 2.5), 6.67 (1H, s), 3.99 (3H, s) , 3.92 (3H, s), 3.85 (3H, s), 3.57 (1H, sept, い 7, 3) , 1.29 (3H, d, J = 7.3) 。
上記で得られた化合物 1 6 gをエタノ ール 1 0 O m 1 に溶解し、 5 0〜 6 0 °Cで金属ナ ト リ ウ ム 1 0. 3 gを 4 5分間で加えた。 混合液を 3 0分還流した後、 ェタノ ール 1 7 m 1 を加えて過剰の金属ナ ト リ ゥムを反応させ、 放冷した。 水を加え、 ジェチルェ一テルで抽出し、 有機 層を飽和食塩水で洗浄した後、 硫酸マグネ シ ウ ムで乾燥 して濃縮した。 得られた粗生成物をメ タノ ール 1 7 0 m 1 に溶かし、 シユウ酸 7. 3 gの水溶液 ( 3 0 m l ) を加え、 2 1時間還流した。 放冷後、 水を加え、 ジェチ ルエーテルで抽出し、 有機層を飽和食塩水で洗浄した後、 硫酸マグネシウムで乾燥して濃縮した。 得られた粗生成 物をシリ カゲルカラムク ロマ トグラフィ ー (溶出液…ジ ェチルエーテル : n—へキサ ン : ク ロ ロホノレム = 2 0 : 1 4 0 : 3 ) にて精製して、 5 , 8—ジメ トキシ一 6— イ ソプロ ピル一 3 , 4— ジ ヒ ドロ ー 2 ( 1 H ) 一ナフ タ レノ ン 1 4. 5 g (油状) を得た。
1 H - NMR ( δ : p p m) 〔 C D C 1 3 〕 :
6. 64 (1H, s), 3.81 (3H, s), 3.70 (3H, s), 3.48 (2H, s) , 3. 36 (1H, sept, J = 7.3) , 3.11 (2H, dd, J = 7.3, 6.8) , 2. 55 (2H, dd, J
=7.3, 6. 8), 1.25 (6H, d, J = 7, 3)。
上記で得られた化合物 1 5. 3 gをベ ンゼン 9 l m l に溶解し、 モ レキュ ラ ーシ—ブス 3 Aの 1 2. 6 gと ピ 口 リ ジ ン 5. l gを加え、 室温で 4. 5時間撹拌した。 混合液を減圧で濃縮し、 ジォキサン 1 0 0 m 1 及びヨウ 化メ チル 9 0 gを加えて 4 5時間還流し、 次いで 5 %塩 酸を 4 5 m 1加えて 3時間還流した。 放冷後、 水を加え、 ジェチルエーテルで抽出し、 有機層を飽和食塩水で洗浄 した後、 硫酸マグネシウムで乾燥して濃縮した。 得られ た粗生成物をシ リ カゲルカラムク ロマ トグラフィ ー (溶 出液…ジェチルェ一テル : n—へキサン : ク ロ口ホルム = 2 0 : 1 4 0 : 3 ) にて精製して、 5 , 8—ジメ トキ シ一 6—イ ソプロ ピル一 1 ー メ チノレー 3 , 4— ジ ヒ ドロ 一 2 ( 1 H) 一ナフ タ レノ ン 1 1. 5 gを得た。
1 H - NMR ( 5 : p p m) 〔C D C 1 3 〕 :
6.65 (1H, s), 3.81 (3H, s), 3.75 (1H, q, ] = 7.3) , 3.69 (3H, s) , 3.36 (1H, sept, J = 6.8), 3.28 (III, ddd, J = 16. 0, 6.3, 3.7), 2.91 (1H, ddd, 16.0, 12.3, 4.9) , 2.73 (1H, ddd, J = 16.4, '4.9, 3.7), 2.40 (1H, ddd, J = 16.4, 12.3, 6.3), 1.35 (3 H, d, J = 7.3), 1.27 (3H, d, J = 6.8), 1.23 (3H, d, J = 6.8)。
水酸化カ リ ウ ム 1. 5 1 gの水溶液 ( 4 m 1 ) を 0 °C に冷却し、 メ タノ ールを 4 5 m 1加え、 更に上記で得ら
れた化合物 6. 3 gのメ タ ノ ール ( 9 m l ) 溶液を加え た。 混合液を一 2 0 °Cに冷却し、 ェチルビ二ルケ ト ン 2 gを加え、 一 2 0 DCで 1時間、 次いで室温で 1 5時間撹 拌した。 反応終了後、 希塩酸を注入して酸性と し、 更に 水を加えてク ロ 口ホルムで抽出 した。 ク ロ 口ホルム層を 飽和食塩水で洗浄した後、 硫酸マグネシゥムで乾燥して 濃縮し、 得られた粗生成物をシ リ カゲルカラムク ロマ ト グラ フ ィ 一 (溶出液…ジェチルエーテル : n—へキサン ク ロ 口ホルム = 2 5 : 1 2 5 : 3 ) にて精製して、 目的 化合物 4. 7 gを得た。
得られた化合物の構造及び物性 (融点及び1 H—
NMR) を第 1表に示す。
実施例 2
2— ヒ ドロキシ一 5, 8— ジメ トキシ一 1, 4 a— ジメ チル一 7— ( 1 —メ チルェチル) 一 2— ( 1 —メ トキシ 一 1 —ジフ エニルホスフ ィ ンォキシ ドメ チル) 一 2 , 3 , 4 , 4 a , 9, 1 0—へキサ ヒ ドロ フ エナンス レ ンの製 造
ジイ ソプロ ピルア ミ ン 0. 6 5 m 1 を溶かした T H F ( 1 3. 5 m 1 ) を一 7 8 °Cに冷却し、 n—プチル リ チ ゥムの T H F溶液 ( 1. 6 M) 6. 1 m l を加え、 2 5 分間撹拌した。 これに、 一 7 8 °Cでメ トキシメ チルジフ
ェニルホスフ ィ ンォキシ ド 1. 1 5 gを溶かした T H F 1 3. 5 m 1 を加え、 一 7 8 °Cで 2 5分間撹拌した。 そ こに、 実施例 1で得られた化合物 7 5 0 m gの T H F ( 6 m 1 ) 溶液を加え、 — 7 8 °Cで 2. 5時間撹拌した。 反応終了後、 1 0 %クェン酸水溶液 1 9 m 1 を一 1 0 °C で加え、 酢酸ェチルで抽出した。 有機層を飽和食塩水で 洗浄した後、 硫酸マグネ シウムで乾燥して濃縮した。 得 られた粗生成物をシ リ カゲルカラムク ロマ 卜 グラ フ ィ 一 (溶出液…ク ロ 口ホルム : 酢酸ェチル = 1 0 : 1 ) にて 精製して、 目的化合物 1. 3 gを得た。
得られた化合物の構造及び物性を、 第 1表に併記する。 実施例 3
2— ( 2—メ トキシビニ リ デニル) 一 5 , 8 — ジメ トキ シ一 1 , 4 a— ジメ チルー 7— ( 1 —メ チルェチル) 一 2 , 3, 4, 4 a , 9, 1 0—へキサヒ ドロ フ ヱナンス レ ンの製造
水素化力 リ ウム 9 3 0 m gを懸濁させた D M F
1 9. 6 m 1 を— 1 0 °Cに冷却し、 実施例 2で得られた 化合物 1. 5 3 gの DM F ( 1 9. 6 m l ) 溶液を加え、 0 °Cで 1時間撹拌した。 反応混合物に 1 0 %クェン酸水 溶液 4 0 m 1 を加え、 酢酸ェチルで抽出し、 有機層を飽 和食塩水で洗浄した後、 硫酸マグネシゥムで乾燥して濃
縮した。 得られた粗生成物をシ リ カゲルカ ラ ムク ロマ ト グラフィ 一 (溶出液…ジェチルエーテル : n —へキサン : ク ロ 口ホルム = 5 : 5 0 : 1 ) にて精製して、 目的化合 物 9 2 3 m gを得た。
得られた化合物の構造及び物性を、 第 1表に併記する。 実施例 4及び 5
5 , 8 —ジメ トキシ一 1 , 4 a —ジメ チル一 7 — ( 1 — メ チルェチル) — 3 , 4, 4 a , 9, 1 0 , 1 0 a —へ キサ ヒ ドロ 一 2 — フ エ ナ ンス レ ンアルデヒ ド ( ト ラ ンス 体及びシス体) の製造
実施例 3で得られた化合物 2. 1 gを脱気したメ 夕ノ —ル 4 5 m l に溶かし、 脱気したシユウ酸 6 9 0 m gの 水溶液 ( 7 m 1 ) を加えて、 アルゴン雰囲気中で 4. 5 時間還流した。 放冷後水を加え、 酢酸ェチルで抽出し、 有機層を飽和食塩水で洗浄した後、 硫酸マグネ シウ ムで 乾燥して濃縮した。 得られた粗生成物を、 シ リ カゲル力 ラムク ロマ トグラフィ 一 (溶出液…ジェチルエーテル : n—へキサ ン : ク ロ 口 ホルム = 2 0 : 3 0 0 : 3 ) にて 精製して、 後の画分より リ ングジ ャ ンク シ ョ ンが 卜ラ ン スの目的化合物 3 5 O m gを、 前の画分より リ ングジ ャ ンク シ ヨ ンがシスの目的化合物 1. 4 5 gをそれぞれ得 た。
得られた各化合物の構造及び物性 (融点及び1 H— NMR) を、 第 1表に併記する。
実施例 6
5 , 8 — ジメ ト キ シ一 1 , 4 a — ジメ チル一 7 — ( 1 — メ チルェチル) _ 3, 4 , 4 a , 9 , 1 0 , 1 0 a —へ キサ ヒ ドロ ー 2 ( 1 H) 一 フ エナ ンス レノ ンの製造
液体ア ンモニア 1 5. 6 m l 中に金属リ チウム
2 8. 5 m gを一 7 8 °Cで加え、 5分間撹拌した。 そこ に、 実施例 1で得られた化合物 5 0 0 m gの T H F溶液 ( 1 5. 6 m l ) をゆっ く り滴下した。 — 7 8でで
1. 5時間撹拌後、 ア ンモニアを留去し、 水を加えてジ ェチルエーテルで抽出した。 有機層を飽和食塩水で洗浄 した後、 硫酸マグネ シウムで乾燥して濃縮した。 得られ た粗生成物を、 シ リ カゲルカ ラ ム ク ロ マ ト グラ フ ィ ー (溶出液… ジェチルエーテル : n —へキサ ン : ク ロ ロ ホ ルム = 5 : 5 0 : 1 ) にて精製して、 目的化合物 2 7 0 m gを得た。
得られた化合物の構造及び物性を、 第 1表に併記する。 実施例 7
2 — ヒ ドロキ シ一 5, 8 — ジメ ト キ シ一 1, 4 a — ジメ チル— 7 — ( 1 —メ チルェチル) 一 2 , 3, 4, 4 a , 9 , 1 0 —へキサ ヒ ドロ ー 2 — フ エナ ンス レ ンアルデヒ
ドの製造
塩化パラ ジウム ( I I ) 2 1 1 m g及び塩化銅 ( I I ) 1. 3 gを、 1 0 : 1 D M F—水 9. 9 m l 中に加え、 室温で 1時間撹拌した。 これに、 実施例 3で得られた化 合物 7 5 0 m gの D M F ( 1 3. 5 m l ) 溶液を加え、 7 0 °Cで 2 1時間撹拌した。 反応終了後、 固形物を濾別 し、 濾液に水を加えて酢酸ェチルで抽出した。
有機層を飽和食塩水で洗浄した後、 硫酸マグネ シウム で乾燥して濃縮した。 得られた粗生成物を、 シ リ カゲル カラムク ロマ ト グラ フ ィ ー (溶出液…ジェチルェ一テル : n—へキサン : ク ロ 口ホルム = 5 : 5 0 : 1 ) にて精製 して、 目的化合物 3 0 0 m gを得た。
得られた化合物の構造及び物性を、 第 1表に併記する。 尚、 ク ロマ トグラフィ ーで前の画分より、 副生成物と して 5 , 8 — ジメ トキシー 1 , 4 a — ジメ チル一 7 —
( 1 ーメ チルェチル) 一 3 , 4 , 4 a , 9 —テ ト ラ ヒ ド 口一 2 —フ エナンス レ ンアルデヒ ド 1 5 O m gを得た。 融点 : 1 0 7 °C以上 (分解) 。
1 H - N MR ( 5 : p p m) 〔 C D C 1 。 〕 :
10. 31 (1H, s), 6. 67 (1H, s), 6. 39 (1H, dd, J = o. 1, 3. 1),
3. 84 (3H, s), 3. 71 (3H, s), 3. 68 (1H, dd, J = H. 4, 5. 1), 3. 50 (1H, dd, J = 14. 4, 3. 1), 3. 32 (1H, sept, 6. 8), 3. 05-3. 11
(1H, m) , 2, 47-2.55 (1H, m), 2.35 (3H, s), 2.28 - 2. 36 ( 1 H, m) ,
I.41- 1.51 (1H, m), 1. 31 (3H, s), 1.26 (3H, d, J = 6.8) , 1.23 (3H, d, J = 6.8) o
実施例 8
1 , 4 a —ジメ チル一 1 —ヒ ドロキシメ チルー 8—メ ト キシ一 3 , 4, 4 a , 9, 1 0, 1 0 a—へキサ ヒ ドロ — 2 ( 1 H) — フ ヱナ ンス レノ ンの製造
液体ア ンモニア 3 0 m l 中に金属リ チウム 0. 8 2 g を一 7 8 °Cで加え、 1 5分間撹拌した。 そ こ に、 1 , 4 a —ジメ チルー 8—メ ト キシ一 4 , 4 a , 9 , 1 0 —テ ト ラ ヒ ドロ 一 2 ( 3 H ) 一 フ エナ ンス レノ ン 5 gと t — ブ夕ノ ール 3. 7 m l を溶かした T H F ( 3 5 m l ) を 加え、 — 7 8 °Cで 3 0分間撹拌した。 反応終了後、 イ ソ プレ ン 9 m l を加えて過剰の試薬と反応させ、 窒素気流 下ア ンモニアを留去した。
次に、 残渣に T H F 5 0 m 1 を加えて溶かし、 氷冷下、 塩ィ匕 ト リ メ チルシ リ ル 1 2. 8 gと ト リ エチルァ ミ ン
I I . 8 gを溶かした T H F ( 4 0 m 1 ) を加え、 氷冷 下 3 0分間撹拌した。 反応混合液に飽和重曹水を加え、 ジェチルエーテルで抽出し、 有機層を飽和食塩水で洗浄 した後、 硫酸マグネ シウ ムで乾燥して濃縮した。 得られ た粗生成物を、 シ リ カゲルカ ラム ク ロマ ト グラ フ ィ ー
(溶出液…酢酸ェチル : n—へキサン = 1 : 1 9 ) にて 精製して、 1 , 4 a — ジメ チル一 8 —メ トキシ一 2 — 卜 リ メ チルシ リ ルォキシ一 3, 4, 4 a , 9 , 1 0, 1 0 a —へキサヒ ドロ フ エナンス レ ン 5. 9 5 gを得た。 融 : 7 9 °C 0
1 H - NMR ( δ p p m) ( C D C 1 , :
6. 51-7. 10 (3H, m), 3. 76 (3H, s) , 1. 66 - 2. 87 ( 9 H, m) , 1, 57 (3H, brs), 0. 97 (3H, s), 0, 10 (9H, s)。
上記で得られた化合物 4. 9 gを溶かした T H F
( 8 0 m l ) 中に、 一 7 8 °Cでホルムアルデヒ ドガスを 窒素ガスと共に反応容器内に通気しながら、 テ ト ラ プチ ルア ンモニゥムフルオライ ドの T H F溶液 ( 1. 0 M)
2 2. 3 m 1 を加えた。 混合液を室温にて 1 0分間撹拌 した後、 氷水中に注ぎ込み、 ジェチルェ一テルで抽出 し た。 有機層を飽和食塩水で洗浄した後、 硫酸マグネシゥ ムで乾燥して濃縮した。 得られた粗生成物を、 シ リ カゲ ルカラムク ロマ ト グラ フ ィ ー (溶出液…酢酸ェチル : n —へキサン : = :[ : 4 ) にて精製して、 目的化合物
3. 6 gを得た。
得られた化合物の構造及び物性を、 第 1表に併記する。 実施例 9
1 , 4 a — ジメ チル一 5, 8 — ジメ トキシ一 7 — ( 1 一
メ チルェチル) 一 2 — ト リ メ チルシ リ ルォキシ一 3 , 4 , 4 a , 9, 1 0, 1 0 a —へキサヒ ドロ フ エナ ンス レ ン の製造
液体ア ンモニア 3 0 m l 中に金属リ チウム 1 2 7 m g を— 7 8 °Cで加え、 1 5分間撹拌した。 そ こ に、 実施例 1で得られた化合物 l g と t —ブ夕ノ ール 4 5 0 m gを 溶かした T H F ( 7 m l ) を加え、 — 7 8 °Cで 3 0分間 撹拌した。 反応終了後、 イ ソプレ ン 1. 3 7 m l を加え て過剰の試薬と反応させ、 窒素気流下ア ンモニアを留去 した。
次に、 残渣に T H F 8 m 1 を加えて溶かし、 氷冷下、 塩化 ト リ メ チルシ リ ノレ 1. 9 5 g と ト リ エチルァ ミ ン
2. 4 7 gを溶かした T H F ( 7 m l ) を加え、 氷冷下
3 0分間撹拌した。 反応混合液に飽和重曹水を加え、 ジ ェチルエーテルで抽出し、 有機層を飽和食塩水で洗浄し た後、 硫酸マグネシウムで乾燥して濃縮した。 得られた 粗生成物を、 シ リ カゲルカラ ムク ロマ ト グラ フ ィ ー (溶 出液…ジェチルエーテル : n—へキサン = 1 : 2 0 ) に て精製して、 目的化合物 9 3 0 m gを得た。
得られた化合物の構造及び物性を、 第 1表に併記する。 実施例 1 0
1 , 4 a — ジメ チル一 5 , 8 — ジメ トキシ一 7 — ( 1 一
メ チルェチル) 一 2— ト リ フ ノレオロメ チルスルホニルォ キシ一 3 , 4 , 4 a , 9, 1 0 , 1 0 a —へキサヒ ドロ フ ヱナンス レ ンの製造
実施例 9で得られた化合物 5 0 O m gを T H F 7 m 1 に溶解し、 0 °Cで 1. 4 Mのメ チル リ チウム ジェチルェ —テル溶液 1. 0 7 m 1 を加え、 0 °Cで 1 5分間、 次い で室温にて 3 0分間撹拌した。 反応液を一 7 8 °Cに冷却 し、 N—フ エニル ト リ フルォロメ タ ンスルホ ンイ ミ ド 4 7 5 m gを溶かした T H F ( 7 m l ) を加え、 0〜 5 °Cで 9. 5時間撹拌した。 反応混合液に水を加え、 ジェ チルェ一テルで抽出し、 有機層を飽和食塩水で洗浄した 後、 硫酸マグネシウムで乾燥して濃縮した。 得られた粗 生成物を、 シ リ カゲルカラムク ロマ ト グラ フ ィ ー (溶出 液…ジェチルエーテル : n—へキサン : = 1 : 5 0 ) に て精製して、 目的化合物 3 1 O m gを得た。
得られた化合物の構造及び物性を、 第 1表に併記する。 一方、 テ ト ラキス ( ト リ フ エニルホスフ ィ ン) パラ ジ ゥム 4 0 2 m g及び塩化リ チウム 3 O m gを T H F 8 m 1 中に懸濁させ、 次いで実施例 1 0の化合物 1 6 0 m gを加えて、 アルゴン気流下に室温で 1 5分間攪拌し た。 次に反応液を 5 0 °Cに加熱し、 二酸化炭素を吹き込 みながら 2時間撹拌し、 続いて ト リ プチル錫ハィ ドライ
ド 1 1 8 m gを溶かした T H F 5 m l を 5 0 °Cで 3. 5 時間かけて滴下し、 5 0 DCで 2 1時間攪拌した。 反応混 合液に水を加え、 ジェチルェ一テルで抽出し、 有機層を 飽和食塩水で洗浄した後、 硫酸マグネシウムで乾燥して 濃縮した。 得られた粗生成物を、 シ リ カゲルカラムク ロ マ トグラフィ 一 (溶出液…ジェチルエーテル : n —へキ サン : ク ロ口ホルム = 2 0 : 3 0 0 : 3 ) にて精製して、 実施例 4の化合物と同一化合物の 4 5 m gを得た。
1
R1A:— CH3、 R2a及び R3a: =0、 R4A:ー CH3、
R5a及び R
6A:
ヽ R
7 :— CH (CH
3 )
2、
R8 : -0CH3、 R9 :一 CH3
融 点: 135〜1370C
!H-NMR (6: pm) [CDC ] :
6. 65 (IH, s) , 3. 82 (3H, s) , 3. 65 (3H, s) ,
2. 25-3. 36 (2H, m) , 3. 03 (IH, ddd, J = 13. 3, 5. 1, 2. 5) , 2. 95 (IH, ddd, J = 12. 5, 3. 5,
3. 5) , 2. 67 (IH, ddd, J = 18. 1, 14. 7, 5. 1), 2. 41-2. 53 (2H, m), 2. 20-2. 29 (IH, m) ,
1. 87 (3H, s) , 1. 76-1. 88 (IH, m) , 1. 65 (3H, s) , 1. 24 (3H, d, 1=1. 0) , 1. 22 (3H, d, J =
7. 0)
第 1 表 (続 き) 麵例 2
R1A: -CH3、 R2a: Ph2 、 R3a:—OH、
R4A :—CH3、 R5a及び R6a:ニ嘗给鍵—謎!^)、
R7 : -CH (CH3 ) 2、 R8 : -OCH3ゝ R9 :— CH3
融 点: 95°CRJi (^m
!H-NMR (<5: ppm) [CDC£3 ] :
8. 10-8. 17 (2H, m) , 7. 78-7. 85 (2H, m) , 7. 41-7. 57 (6H, m) , 6. 60 (1H, s) , 5. 41 (IH, s) , 4. 16 (IH, d, J = 9. 1), 3. 68 (3H, s),
3. 28 (IH, s ept, J = 6. 8), 3. 03— 3. 13 (IH, m) , 3. 07 (3H, s) , 2. 73-2. 80 (1H, m) , 2. 35 -2. 45 (IH, m) , 2. 23 (IH, ddd, J =l 3. 1, 3. 4, 3. 4) , 1. 80-2. 13 (3H, m) , 1. 88 (3H, s) , 1. 70-1. 80 (IH, m) , 1. 45 (3H, s), 1. 25 (3H, d, J = 6. 8) , 1. 21 (3H, d, J=6. 8) 難例 3
R1A: - CH3、 R2a及び R3a: =CH-OCH3 、 R4A: -CH:
R5a及び R6a;二^^ ―驟結合)、
R7 :— CH (CH3 ) 2、 R8 : - OCH3ゝ R9 :一 CH3
性 状: 掛伏物
!H-NMR (5: p m) [CDC ] :
6. 61, 6. 60 (IH, s) , 6. 10, 5. 71 (IH, s)
3. 80, 3. 78 (3H, s) 3. 68, 3. 63 (3H, s)
3. 63, 3. 55 (3H, s) 3. 25-3. 36 (1H, m)
3. 06— 3. 17 (IH, m) 2. 78-2. 93 (2H, m)
2. 61-2. 71 (IH, m) 2. 23-2. 48 (2H, m)
2. 08, 1. 80 (3H, s) 1. 91-2. 11 (IH, m)
1. 51, 1. 50 (3H, s) 1. 18-1. 28 (3H, d,
6. 8)
第 1 表 (続 き)
R1A: ^-CH3、 R2a:—CH0、
R3a及び R5a;二 fi^織—職!^)ヽ R4A : 一 CH3、
R6a: α - Hヽ R7 :一 CH (CH3 ) 2、 R8 : -OCH3ヽ
R9 : -CH3
!H-NMR (5: p m) [CDC ] :
10. 21 (IH, s) , 6. 61 (1H, s) , 3. 80 (3H, s) , 3. 70 (3H, s) , 3. 31 (IH, s e t, J = 6. 8) ,
3. 11 (IH, ddd, J = 17. 5, 5. 3, 1. 5) , 3. 03 (1H, ddd, J = 13. 5, 7. 5, 3. 3) , 2. 68 (IH, ddd, J =l 7. 5, 12. 7, 6. 6), 2. 41— 2. 53 (2H, m) , 2. 18— 2. 31 CIH, m) , 2. 23 (3H, d, J =
1. 5) , 1. 25-1. 68 (3H, m) , 1. 23 (3H, d, J = 6. 8) , 1. 22 (3H, d, J = 6. 8), 1. 12 (3H, s) wm 5
R1A: yS-CH3、 R2a:—CHO、
R3a及び R5a:二!!^職一藤結合)ゝ R4A:— CH3、
R6a: /3 - H、 R7 : -CH (CH3 ) 2、 R8 :— OCH3、
R9 : -CH3
融 点: 137〜139。C
!H-NMR {6: p m) [CDC ] :
10. 18 (IH, s) , 6. 60 (IH, s) , 3. 80 (3H, s) , 3. 66 (3 H, s) , 3. 30 (IH, s e t, J = 6. 8) ,
2. 95 (IH, ddd, ]=11. 1, 4. 4, 4. 4), 2. 65 (1
H, ddd, J =l 6. 8, 11. 0, 4. 4) , 2. 26 (3H, s), 2. 01-2. 23 (5H, m), 1. 75-1. 85 (IH, m),
I. 55-1. 65 (1H, m) , 1. 35 (3H, s), 1. 23 (3H, d, J = 6. 8) , 1. 21 (3H, d, J = 6. 8)
第 1 表 (続 き) 辦 |J 6
R1A ;9一 CH3、 R2a及び R3a: =0、 R4A: a-CH3、
R5a - H、 R6a: a— H、 R7 -CH (CH3 ) 2、 R8 -OCH3 R9 -CH3
!H-NMR (6: ppm) [CDC ] :
6. 61 (IH, s) , 3. 80 (3H, s), 3. 67 (3H, s) , 3. 25-3. 35 (2H, m) , 3. 01-3. 09 (IH, m), 2. 38-2. 65 (2H, m) , 1. 87— 1. 95 (IH, m), 1. 55-1. 68 (2H, m) , 1. 43-1. 55 (IH, m) , 1. 42 (3H, s), 1. 23 (3H, d, J=6. 8) , 1. 22 (3H, d, J = 6. 8) , 1. 13 (3H, d, 1 = 1. 3) \ 7
R1A: -CH3、 R2a:— CHO、 R3a : -OH. R4A; -CH3、
R5a及び R6a:二 fi^髓―驟 ヽ :—CH (CH3 ) 2、
R8 : -OCH3、 R9 :— CH3
融 点: 177〜178°C
!H-NMR d: ppm) [CDC 3 ] :
9. 36 (IH, s) , 6. 62 (IH, s), 3. 80 (3H, s) ,
3. 64 (3H, s), 3. 53 (IH, s) , 3. 29 (IH, s ep t,
J=6. 8), 3. 16 (1H, ddd, J =l 6. 6, 4. 4, 2. 5) ,
2. 91 (IH, ddd, J = 13. 2, 3. 4, 3. 4) , 2. 79 (1
H, ddd, J = 12. 7, 4. 4, 2. 5), 2. 43-2. 53 (IH, m) , 2. 05-2. 17 (2H, m) , 1. 57-1. 69 (IH, m),
I. 61 (3H, s), 1. 55 (3H, s) , 1. 45 (IH, ddd, J = 14. 2, 3. 4, 3. 4) , 1. 22 (3H, d, J = 6. 8) , 1. 21 (3H, d, J = 6. 8)
第 1 表 (続 き) 誰例 8
R1A: S— CH3、 R2a及び R3a: =0、 R4A: ;3— CH3、
R5a: a - CH2 OH、 R6a: a_H、 R7 : H、 R8 : H、
R9 :— CH3
融 点: 135°C
XH-NMR (5: ppm) [CDC ] :
7. 15 (IH, dd, J = 8. 0, 8. 0), 6. 90 (IH, d, J = 8. 0), 6. 68 (IH, d, J = 8. 0), 3. 81 (3H, s) , 3. 70 (IH, dd, J =l 1. 2, 6. 6) , 3. 50 (1H, d d, J =l 1. 2, 6. 6) , 1. 60-3. 10 (1 OH, m) , 1. 41 (3H, s), 1. 12 (3H, s) , 難例 9
R1A: β-CUs . R2a: -OS i (CH3 ) 3、
R3A及び R5A: 髓ー驟結合)ゝ R4A:— CH3、 R6a: α一 H、 R7 : -CH (CH3 ) 2、 R8 :— OCH3、 R9 : -CH3
融 点: 124〜125。C
!H-NMR (5: m) [CDC ] :
6. 58 (IH, s) , 3. 78 (3H, s) , 3. 68 (3H, s) , 3. 30 (IH, sept, J = 6. 8) , 3. 10-3. 18 (1H, m) , 2. 97-3. 06 (IH, m) , 2. 66 (IH, ddd, J = 17. 5, 12. 2, 6. 8), 2. 21-2. 40 (2H, m) ,
1. 98-2. 13 (2H, m) , 1. 63 (3H, q- 1 i ke) , 1. 41-1. 53 (2H, m), 1. 22 (6H, d, J = 6. 8) , 1. 16 (3H, s) , 0. 19 (9H, s)
1 表 (続 き) 難例 10
RiA: β-θη3、 R2a: -OS02 CF3、
R
3A及び R
5A:
ヽ R
4A:ー CH
3、 : a-U,
R7 :一 CH (CH3 ) 2、 R8 : -〇CH3、 R9 : -CH3
融 点: 132. 5〜133. 5°C
iH-NMR (5: ppm) [CDC 3 ] :
6. 60 (1H, s), 3. 79 (3H, s) , 3. 68 (3H, s), 3. 25-3. 37 (2H, m) , 3. 03-3. 11 (1H, m) , 2. 68 (1H, ddd, J =l 7. 8, 12. 2, 6. 5) ,
2. 31-2. 65 (3H, m) , 2. 03— 2. 11 (1H, m) .
1. 81 (3H, d, J = 0. 9) , 1. 48-1. 63 (2H, m) , 1. 22 (6H, d, J = 6. 8) , 1. 21 (3H, s)
実施例 1 1
1, 4 a — ジメ チル一 7 — ( 1 —メ チルェチル) 一 5, 8 — ジォキソ ー 3 , 4, 4 a , 5 , 8, 9 , 1 0 , 1 0 a —ォク タ ヒ ドロ一 2 — フ エナンス レンアルデヒ ド (シ ス体) の製造 実施例 5の化合物 3 1 O m gをァセ トニ ト リ ノレ 1 0 m l に溶かし、 これに C A N 1. 2 4 gの水溶液 5 m l を加え、 室温で 3 0分間撹拌した。 反応液を水で希釈し、 ク ロ口ホルムで抽出した。 有機層を飽和食塩水で洗浄し た後、 硫酸マグネシウムで乾燥して濃縮した。 得られた 粗生成物を、 シ リ カゲルカ ラ ムク ロマ ト グラ フ ィ ー (溶 出液…ジェチルエーテル : η —へキサン : ク ロ 口ホルム
= 1 0 : 5 0 : 1 ) にて精製して、 目的化合物 1 5 0 m g 得た。
得られた化合物の構造及び物性を、 第 2表に併記する。 実施例 1 2〜 1 4
実施例 1 1 と同様に して、 実施例 1 2〜 1 4の化合物 を得た。 得られた化合物の構造及び物性を、 第 2表に併
§じす <S 0
実施例 1 5
8 — ヒ ドロキシメ チルー 4 b , 8 — ジメ チルー 5, 6 , 8 , 8 a , 9 , 1 0 —へキサヒ ドロ一 1 , 4 , 7 ( 4 b H) —フ ヱナンス レ ン ト リ オ ンの製造
実施例 8の化合物 1 5 O m gをジク ロロメ タ ン 4 m 1 に溶解し、 氷冷下、 三臭化硼素の n—へキサン溶液
( 1. 0 M) 1. 2 m 1 を加えた。 0 °Cで 1. 5時間撹 拌後、 飽和重曹水を加え、 酢酸ェチルで抽出した。 有機 層を飽和食塩水で洗浄した後、 硫酸マグネシウムで乾燥 して濃縮した。 得られた粗結晶 3 4 m gをエタノ ール 1 0 m 1 に溶解し、 ジニ トロスルホン酸カ リ ウム 8 3 m g と リ ン酸水素二力 リ ゥム 3 4 m gの水溶液 ( 6. 8 m 1 ) を加え、 室温で 1 3時間撹拌した。 反応液を水で 希釈し、 ク ロ口ホルムで抽出して有機層を飽和食塩水で 洗浄した後、 硫酸マグネシウムで乾燥して濃縮した。 得
られた粗生成物を、 シ リ カゲルカラムク ロマ トグラフィ 一 (溶出液…酢酸ェチル : n—へキサン = 1 : 9 ) にて 精製して、 目的化合物 l m gを得た。
得られた化合物の構造及び物性を、 第 2表に記載する c
2
難例 11
R1A: ー CH3、 R2 :— CHO、 R4A:— CH3、
R3及び R5 :ニ ( -m^ ヽ R6 : ー Hゝ
R7 :一 CH (CH3 ) 2
性 状: 油 状
!H-NMR (5: ppm) [CDC ] :
10. 16 (IH, s), 6. 38 (1H, d, J=l. 0) , 3. 00 (1H, s ept d, J=6. 8, 1. 0) , 2. 60 (1H, ddd, J = 10. 0, 5. 0, 5. 0) , 2. 38 (1H, ddd, J = 19. 5, 9. 3, 5. 7) , 2. 22 (3H, s) , 2. 01-2. 27 (2H, m) , 1. 93— 1. 97 (IH, m) , 1. 81— 1. 89 (IH, m) , 1. 55— 1. 67 (2H, m), 1. 31 (3H, s) , 1. 11 (6H, d, J = 6. 8)
例 12
R1A:—CH3、 R2及び R3 : =0、 R4A:—CH3、
R5及び R6 : m^ (^m-m^)ヽ R7 :— CH (CH3 ) 2 融 点: 94〜95°C
!H-NMR (5: pm) [CDC 3 ] :
6. 41 (1H, d, J = l. 5) , 2. 91-3. 08 (3H, m) , 2. 80 (IH, ddd, J = 13. 0, 5. 2, 2. 5), 2. 68 (1
H, ddd, J=17. 3, 14. 8, 5. 2) , 2. 47 (IH, ddd, J = 17. 3, 4. 7, 2. 5), 2. 13-2. 31 (2H, m) ,
I. 84 (3H, d, J = l. 0) , 1. 75— 1. 87 (IH, m) ,
1. 64 (3H, s) , 1. 13 (3H, d, J=6. 8) , 1. 12 (3 H, d, J = 6. 8)
第 2 表 (続 き)
«例13
R1A: ー CH3 、 R2及び R3 : =0、 R4A: a— CH3 ヽ
R5 : ^一 H、 R6 : a—H、 R7 :— CH (CH3 ) 2
融 点: 68〜70°C
!H-NMR (δ: m) [CDC 3 ] :
6. 38 (IH, s), 2. 95-3. 06 (2H, m), 2. 76 (1H, dd, J=20. 3, 4. 6) , 2. 58 (1H, ddd, J =l 5. 1, 13. 2, 6. 8) , 2. 25-2. 48 (3H, m) , 1. 90—
1. 97 (1H, m) , 1. 37— 1. 65 (3H, m) , 1. 45 (3H, s), 1. 12 (3H, d, J = 6. 8) , 1. 11 (3H, d, J = 6. 8) , 1. 10 (3H, d, J = 7. 3) 難例 14
R!A: -CH3 、 R2 : 一 CHO、 R3 : 一 OH、 R4A:— CH3 、
R5及び R6 (^-m^) 、 R7 : -CH (CH3 ) 2 融 点: 128. 5〜130. 5°C
!H-NMR (id: ppm) [CDC 3 ] :
9. 35 (IH, s), 6. 38 (IH, d, J=l. 5) , 3. 62 (1
H, s), 3. 00 (IH, s ep td, J=6. 8, 1. 5) , 2. 88 (IH, ddd, J = 19. 5, 5. 1, 1. 7) , 2. 80 (1H, dd d, J =l 3. 2, 5. 1, 1. 7) , 2. 63 (IH, ddd, J = 12. 7, 3. 6, 3. 6) , 2. 24 (IH, ddd, J = 19. 5, 12. 7, 5. 3) , 1. 98-1. 16 (2H, m), 1. 61—
I. 71 (IH, m) , 1. 58 (3H, s) , 1. 54 (3H, s), 1. 11 (3H, d, J = 6. 8), 1. 10 (3H, d, J = 6. 8)
2 表 (続 き)
難例 15
R1A: ^-CH3ヽ R2及び R3 : =0、 R4A: 一 CH3
: a-CU2 0H、 R6 : 一 H、 R7 : H
!H-NMR (5: ppm) [CDC 3 ] :
6. 72 (1H, d, J =l 0. 0) , 6. 64 (1H, d, J =
10. 0) , 3. 70 (1H, dd, J =l 2. 0, 8. 0) , 3. 35 (1H, dd, J = 12. 0, 8. 0) , 1. 54-2. 93 (10H, m) , 1. 25 (3H, s) , 1. 08 (3H, s)
実施例 1 6 ク ロズル茎 1 0 8 k gを細断し、 メ タ ノ ール 2 0 0 1 を用いて室温下で 7 日間抽出する。 抽出物を減圧下に濃 縮して粗抽出物を得る。 この粗抽出物を水 2 0 1 に懸濁 し、 酢酸ェチル 2 0 1 ずつで 3回抽出し、 酢酸ェチル層 を合わせて減圧下濃縮し、 酢酸ェチル抽出物 1 3 0 0 g を得た。 上記酢酸ェチル抽出物 1 2 0 0 gをシ リ カゲル力ラム ク ロマ ト グラ フ ィ ー (メ ルク シ リ カゲル 6 0 , 7 0 - 2 3 0 メ ッ シュ, 1 5 0 0 g, メ ルク社製) に付し、 2 0 %、 4 0 %、 6 0 %、 8 0 %酢酸ェチル / n —へキサン (νΛΡ 及び酢酸ェチルのそれぞれ 1 0 1 で順次溶出 し、 次いで 1 0 %、 2 0 %、 3 0 %メ タ ノ ールノ酢酸ェチル
(v/v) 及びメ タノ ールのそれぞれ 1 0 1 で順次溶出し、 各々 5 0 0 mlを採取し、 フ ラ ク シ ョ ン ( 1 ) 〜 ( 1 1 ) を得た。
上記フ ラ ク シ ョ ン中、 フ ラ ク シ ョ ン ( 4 ) の溶媒を減 圧下に留去 し、 得られた残渣 5 7 gの内 5 3 gをシ リ カ ゲルク ロマ ト グラ フ ィ ー (メ ノレク シ リ カゲル 6 0, 7 0 — 2 3 0 メ ッ シュ, 1 2 0 0 g ) に付し、 ク ロ 口ホルム 1 0 1、 5 %メ タ ノ ールノク ロ ロ ホルム (v/v%) 1 0 1 で 分画溶出し、 フ ラ ク シ ョ ン ( 4 一 1 ) 〜 ( 4 — 7 ) を得 た。 次に上記フ ラ ク シ ョ ン ( 4 一 4 ) ( 1 9 g ) をシ リ 力ゲルカ ラ ム ク ロ マ ト グラ フ ィ 一 (メ ノレク シ リ カゲル 7 0〜 2 3 0メ ッ シュ、 5 0 0 g) に付し、 7 5 %、 6 6 %、 5 0 %及び 3 3 %の n—へキサン Z酢酸ェチル (νΛ%)並びに酢酸ェチルのそれぞれ 2 1 で順次溶出し、 溶出液各々 1 0 0 m l を採取し、 フ ラ ク シ ョ ン ( 4 — 4 一 1 ) 〜 ( 4 — 4 一 1 1 ) を得た。
更に上記フ ラ ク シ ョ ン ( 4 一 4 一 6 ) 3. 5 gをシ リ 力ゲルカ ラ ム ク ロマ ト グラ フ ィ ー (メ ノレク シ リ カゲル 7 0〜 2 3 0メ ッ シュ、 2 0 0 g ) に付し、 9 5 %ク ロ 口ホルム メ タ ノ ール (v/v%) 2 1 で溶出し、 セフ アデッ ク ス L H - 2 0 ( 5 0 0 mし フ ア ルマ シア社製) を用い て 2回カ ラ ムク ロ マ ト グラ フ ィ ーに付し、 9 0 %メ タ ノ
ール Zク ロ 口ホルムで分画溶出 し、 更にシ リ カゲルカラ ムク ロマ ト グラ フ ィ ー (メ ルク シ リ カゲル 7 0〜 2 3 0 メ ッ シュ、 1 0 0 g ) に付し、 9 9 %ク ロ 口ホルム Zメ 夕 ノ ール (ν/ν ) 1 1 で分画溶出 して精製し、 これをメ タ ノ ールよ り再結晶して、 黄色針伏結晶の 1, 2, 3 , 4
4 a , 5 , 8 , 9 , 1 0, 1 0 a —デカ ヒ ドロ 一 1 , 4 a — ジメ チルー 7 _ ( 1 —メ チルェチル) 一 5 , 8 — ジ ォキソ一 1 一フ エナンス レ ンカルボン酸 0 . 0 5 7 gを 得た。 m p 2 0 7 - 2 0 9 °C 〔 α〕 D = + 8 0 . 5 ( C H C 1 ; c 1 0 )
KBr
I R v c m
m a x _1 : 3 4 0 0 , 1 7 3 0 1 6 9 6 ,
6 5 0, 1 4 7 0, 1 2 7 0 , 2 4 0 9 1 3 ,
8 0 0
U V λ Me 0H ma x nm ( ε ) : 2 6 0 ( 1 5 3 0 0 ) ^ - N M R C C D C l g ) d p m : 1 . 0 1 ( 3 H x 2 , d , J = 6 . 8 H z , H - 1 6 , 1 7 ) , 1 . 2 2 ( 3 H , s , H - 2 0 ) , 1 . 3 1 ( 3 H, s, H - 1 8 ) , 1 . 0 — 1 . 2 ( 2 H , m, H — 1 , H — 3 ) , 1 . 3 0 ( 1 H , m, H — 5 ) , 1 . 5 5 ( 1 H , b r d , J = 1 4 . 2 H z , H - 2 ) 1 . 7 9 ( 1 H , m, H — 6 ) , 1 . 9 6 ( 1 H , m,
H - 2 ) , 2. 1 5 - 2. 2 9 ( 3 H, m, H - 3 , H - 6 , H— 7 ) , 2. 7 0 ( 1 H, b r d, J =
1 6. 1 H z , H - 1 ) , 2. 7 5 ( 1 H , d d, J = 1 9. 5 , 5. 9 H z , H - 7 ) , 2. 9 9 ( 1 H, s e p t, J = 6. 8 H z , H - 1 5 ) . 6. 3 3 ( 1 H, s, H - 1 5 )
E I - M S m/z ( r e 1. int. ) :
3 3 0 〔M〕 + ( 3 5 ) , 3 1 5 (M - C H 3 ) +
( 1 5 ) , 2 8 4 ( 5 5 ) , 2 6 9 ( 1 0 0 ) , 2 2 7 ( 4 4 ) , 2 0 4 ( 3 9 )
H R— M S m/z : 3 3 0. 1 8 6 4 〔M〕 +
(C 20H 26O 4 = 3 3 0. 1 8 3 1 )
実施例 1 7
皮部を除いたク ロズル茎 1 8. 4 k gを細断し、 メ タ ノ ール 2 0 1 を用いて 6 0 °Cで 6時間抽出する。 これを 3回繰り返す。 抽出物を減圧下に濃縮して粗抽出物
( 6 8 0 g ) を得る。 この粗抽出物を水 2 1 に懸濁し、 酢酸ェチル 2 1 で 3回抽出し、 酢酸ェチル層を合わせて 減圧下に濃縮し、 酢酸ェチル抽出物 1 4 0 gを得た。
上記酢酸ェチル抽出物 1 4 0 gをシリ カゲルカラムク 口マ ト グラ フ ィ 一 (メ ルク シ リ カゲノレ 7 0〜 2 3 0メ ッ シュ、 1 k g) に付し、 7 5 %、 6 6 %、 5 0 %及び
3 3 %の n—へキサン Z酢酸ェチル (v/v%)並びに酢酸ェ チルのそれぞれ 3 1 で順次溶出 し、 次いで 9 5 %、 9 0 %及び 8 0 %の酢酸ェチル /メ タ ノ ール並びにメ タ ノ 一 ルのそれぞれ 2 1 で順次溶出 し、 溶出液各々 3 0 0 m 1 を採取し、 フ ラ ク シ ョ ン ( 1 ) 〜 ( 2 0 ) を得た。
上記フラ ク シ ョ ン中、 フ ラ ク シ ョ ン ( 1 0 ) の溶媒を 減圧下に留去し、 得られた残渣 6. 5 gの内 6. 3 7 g をセフ アデッ クス L H— 2 0 ( 5 0 0 m l 、 フ ァ ルマ ン ァ社製) を用いて 1回カ ラ ムク ロマ ト グラ フ ィ ーに付 し、 メ タ ノ ール 2 1 で分画溶出し、 フ ラ ク シ ョ ン ( 1 0 — 1 ) 〜 ( 1 0 — 7 ) を得た。
次に上記フラ ク シ ョ ン ( 1 0 — 3 ) 1. 2 4 gをシ リ 力ゲルカラムク ロマ ト グラ フィ 一 (メ ルク シ リ カゲル 7 0〜 2 3 0メ ッ シュ、 2 0 0 g ) に付し、 9 8 %、
9 5 %ク ロ 口ホルム Zメ タ ノ ール (v/v%)各 1 1 で溶出 し、 同様に 9 8 %ク ロ 口ホルム/メ タ ノ ール (v/v%) 1 1 で溶 出し、 更に高速液体ク ロマ ト グラ フィ ー ( 0 D S ) に付 し 9 0 %メ タ ノ ール 水(v/v ) 5 0 0 m l で溶出し、 更 にシ リ カゲルカラムク ロマ ト グラ フ ィ ー (メ ルク シ リ カ ゲル 7 0〜 2 3 0メ ッ シュ、 1 0 0 g ) に付し、 6 6 % n —へキサンノ酢酸ェチル 5 0 0 m 1 で溶出 して精製 し、 アモルフ ァ ス粉状結晶の 1 , 2 , 3 , 4 , 4 a , 5, 8 ,
9, 1 0 , 1 0 a —デカ ヒ ドロ ー 1 一 (ヒ ドロキシメ チ ル) 一 1, 4 a — ジメ チル一 7 — ( 1 —メ チルェチル) — 5, 8 — ジォキソ一 フ エナンス レ ン 2 4 m gを得た。 I R V KB r max cm"1 : 3 3 7 0 , 1 7 1 0, 1 6 5 0, 1 6 0 0 , 1 2 9 0 , 1 2 6 5 , 1 0 8 0, 9 0 6,
7 5 5
U V λ Me0H max nm ( ε ) : 2 6 0 ( 1 1 8 0 0 )
^ - NMR C C D C l g ) (5 ppm :
1. 0 4 ( 3 H, s, H - 1 8 ) , 1. 0 9 , 2. 0 0 (各 3 H, d, J = 6. 8 H z , H - 1 6 , 1 7 ) ,
1. 2 4 ( 1 H, b r d, J = 1 1. 2 H z , H - 5 ) , 1. 2 8 ( 3 H, s , H - 2 0 ) , 2. 4 4 ( 1 H, m, H— 6 ) , 1. 5 3 ( 1 H, m, H - 2 ) , 1. 6 8 ( 1 H, m, H - 2 ) , 1. 8 0 ( 1 H, r d, J = 1 3. 6 H z , H e q - 3 ) , 1. 9 9 ( 1 H, d d , J = 1 3. 6 , 6. 8 H z , H e q— 6 ) , 2. 2 8 ( 1 H, d d d, J = 2 0. 4 , 1 1. 6 , 7. 2 H z , H a x - 7 ) , 2. 6 9 ( 1 H, d d , J = 2 0. 4 , 5. 2 H z , H e q— 7 ) , 2. 7 5 ( 1 H, b r d, J = 1 3. 2 H z , H e q - 1 ) , 2. 9 8 ( 1 H , s e p t d, J = 7. 2, 1. 0 H z , H - 1 5 ) , 3. 5 6 , 3. 7 8 (各 1 H, A B q , J = 1 1. 2
H z , H— 1 9 ) , 6. 3 2 ( 1 H , d , J = 1. 0 H z , H - 1 2 )
E I - M S m/z ( r e 1. int. ) :
3 1 6 CM) + ( 8 5 ) , 3 0 1 〔M - C H 3 〕 +
( 1 2 ) , 2 9 8 〔M - H 2 0〕 + ( 2 2 ) , 2 8 5 ( 4 2 ) , 2 8 3 〔M - C H 3 - H 2 0〕 + ( 1 0 0 ) ,
2 4 1 ( 4 6 ) , 2 0 3 ( 5 8 ) , 9 1 ( 4 2 ) , 4 3 ( 5 2 )
H R - M S m/z : 3 1 6. 2 0 7 3 〔M〕
+
実施例 1 8
実施例 1 6 と同様の抽出操作により得られた 3 , 4 , 4 a , 5, 8 , 9, 1 0, 1 0 a —才ク タ ヒ ドロー 1 , 4 a — ジメ チルー 7— ( 1 —メ チルェチル) 一 5 , 8— ジォキソ 一 2—フ エナンス レ ンカルボン酸 1 O O m g と プロ リ ンメ チルエステル塩酸塩) 5 5 m gとを溶解した DMF溶液 1. 5 m l に、 氷冷下に ト リェチルァ ミ ン
3 0. 8 m gを加え、 5分間撹拌した。 これに、 氷冷下 D E P C 5 4. 7 m gを溶かした D M F溶液 0. 5 m l を加え、 続いて ト リェチルァ ミ ン 9 2. 4 m gを溶かし た D M F溶液 0. 5 m 1 を加え、 室温にて 3 0分間撹拌 した。 反応混合液に水を加え、 酢酸ェチルにて抽出した c
有機層を飽和食塩水で洗浄後、 無水硫酸マグネシウムで 乾燥し濃縮した。 得られる粗生成物をシ リ カゲルク ロマ トグラフィ 一 (溶出液 ; ク ロマ トグラフィー : 酢酸ェチ ル = 1 0 : 1 ) にて精製して、 3 , 4, 4 a , 5 , 8 , 9, 1 0 , 1 0 a—才クタ ヒ ドロー 1 , 4 a —ジメ チル — 7— ( 1 —メ チルェチル) 一 5 , 8— ジォキソー 2 — フエナンスレンカルボキサミ ドープロ リ ンメ チルエステ ル l O O m g ( 7 4. 7 % ) を得た。
実施例 1 9
室温下、 実施例 1 6で得られた化合物 5 0 m gを
T H F 2 m 1 に溶解し、 その溶液を水 3 m 1 に
N a 2 S 2 04 8 0 0 m gを溶解させた溶液中に加え撹 拌した。 3時間撹拌後反応混合物に水を加え、 ジェチル エーテルで抽出した。 抽出物を飽和食塩水で洗浄し無水 M g S 04 で乾燥した後、 溶媒を留去し、 残渣を得た。 次にその残渣をアセ ト ン 2 m 1 に溶解し、 K n C 03 1 9 0 m 1 と硫酸メ チル 1 7 7 m gをその溶液に加えて. 2時間加熱還流した。 反応混合物を 0 °Cまで冷却し、 1 0 %塩酸を加えて溶液全体を中性と し、 ジェチルエー テルで抽出した。 飽和食塩水で洗浄した後、 無水
M g S 04 で乾燥後溶媒を留去し残渣を得た。
その残渣をシリ 力ゲルカラムク ロマ トグラフィ 一に付
し、 9 5 % n —へキサン Z酢酸ェチル (v/v%) で溶出し、 黄色針伏結晶の 1, 2 , 3, 4 , 4 a , 9, 1 0 , 1 0 a —ォ ク 夕 ヒ ドロ ー 5, 8— ジメ トキ シー 1 , 4 a — ジ メ チルー 7— ( 1 —メ チルェチル) 一 1 —フ エ ナ ンス レ ンカルボン酸メ チルエステル 4 9 m gを得た。
m p 1 3 3 - 1 3 5 °C
〔 〕 D = + 1 6 3. 6 (M e 0 H ; c 0. 2 6 )
I R KB r max cm"1 : 1 7 1 9
1 H - NMR ( 2 0 0 MH z ) ( C D C 1 3 ) δ ppm : 1. 1 2 ( 3 H, s ) , 1. 2 1 ( 3 H x 2 , d,
J = 7. 1 H z ) , 1 2 7 ( 3 H, s ) , 1. 4 0 - 2. 6 6 ( 9 H, m) 2. 9 7 - 3. 4 0 ( 3 H, m ) 3. 6 5 ( 3 H, s ) 3. 6 8 ( 3 H , s ) ,
3. 7 6 ( 3 H, s ) 6. 5 7 ( 1 H, s )
H R -M S m/z : 3 7 4. 2 4 3 7 〔M〕 +
( C 23H 34° 4 = 3 7 4 2 4 5 6 )
実施例 2 0
実施例 1 9で得た化合物 3 8 m gを乾燥させた T H F 0. 5 m l に溶解し、 この溶液を乾燥させた T H F
0. 5 m l に L i A l H 4 3 0 m gを加えて得られる懸 濁液中に 0 °Cで滴下した。 3 0分室温下で撹拌した後、 含水ジェチルエーテルを 0 °Cで注意深く加え反応混合物
をセライ 卜を用いて濾過した。 濾液を M g S 04 で乾燥 し、 溶媒を留去し、 油状の残渣を得た。 次にシ リ カゲル カ ラムク ロマ ト グラ フ ィ ー (n—へキサ ン 一酢酸ェチル、
9 : 1 (v/v¾)) により精製して、 無色油状の 1, 2 , 3, 4, 4 a , 9 , 1 0 , 1 0 a —ォ ク 夕 ヒ ドロ ー (ヒ ドロ キシメ チル) 一 5 , 8— ジメ トキシー 1 , 4 a — ジメ チ ルー 7— ( 1 —メ チルェチル) 一 フ エ ナ ンス レ ン 3 1 m gを得た。
〔な〕 D = + 9 9. 3 (M e 0 H ; c 0. 6 1 )
I R V KB r ma x cm"1 : 3 6 3 1
1 H - NMR ( 2 0 0 MH z ) ( C D C 1 3 ) δ ppm : 1. 0 7 ( 3 H, s ) , 1. 2 1 ( 3 H x 2 , d ,
J = 6. 8 H z ) , 1. 2 8 ( 3 H , s ) , 1. 3 4— 2. 1 1 ( 8 H, m) , 2. 4 9 — 3. 4 0 ( 3 H, m) 3. 5 8 ( 2 H, d , J = 1 0. 7 H z ) , 3. 6 6
( 3 H, s ) , 3. 7 7 ( 3 H, s ) , 3. 8 4 ( 2 H, d, J = 1 0. 7 H z ) , 6. 5 7 ( 1 H, s )
H R - M S i/z : 3 4 6. 2 5 0 5 〔M〕 +
( C 22H 3403 = 3 4 6. 2 5 0 7 )
実施例 2 1
実施例 1 6 と同様の抽出操作により得られた 3, 4 , 4 a , 5 , 8 , 9 , 1 0, 1 0 a —ォクタ ヒ ドロ一 1 ,
4 a — ジメ チルー 7 — ( 1 ーメ チルェチル) 一 5 , 8 - ジォキ ソ ー 2 — フ エ ナ ンス レ ン力ノレボン酸 3 0 O m gを T H F l O m l に溶解し、 1. 6 gの亜ニチオ ン酸ナ ト リ ゥムを溶解した水溶液 1 6 m l を加え、 室温にて 3 0 分間撹拌した。 反応混合液に水を加え、 ジェチルェ—テ ルで抽出 し、 有機層を飽和食塩水で洗浄後、 無水硫酸マ グネシゥムで乾燥し、 濃縮した。 得られた粗精製物を シ リ カゲルカ ラ ムク ロマ ト グラ フ ィ ー (溶出液…ク ロ ロ ホ ルム : メ タ ノ ール = 1 0 0 : 1 ) にて精製 し、 3 , 4 , 4 a , 9 , 1 0, 1 0 a -へキサ ヒ ドロ ー 5 , 8— ジ ヒ ドロキシー 1 , 4 a — ジメ チル一 7— ( 1 ー メ チルェチ ル) 一 2 _フ エナ ンス レ ンカルボン酸 2 9 O m gを得た。 m p 1 2 7 °C以上 (分解)
1 H - NMR ( D M S 0 - d 6 ) δ ppm :
1. 0 6 C 3 H, s ) , 1. 0 7 C 3 H, d, J =
6. 7 H z ) , 1. 1 0 ( 3 H, d , J = 6. 7 H z ) , 1. 2 1 - 1. 5 0 ( 2 H, m) , 1. 9 7 ( 3 H, s ) 2. 0 5 - 2. 5 5 ( 5 H, m) , 2. 8 1 ( 1 H, d d , J = 1 7. 5 , 4. 4 H z ) , 3. 1 0 - 3. 3 3 ( 2 H, m) , 6. 4 2 ( 1 H, s ) ,
7. 1 8 ( 1 H, s ) , 8. 4 7 ( 1 H, s ) ,
1 2. 1 5 ( 1 H, b r s )
薬理試験例 1
摘出血管の弛緩反応の測定試験
( 1 ) 内皮除去大動脈標本の作成
ウ ィ スター系雄性ラ ッ ト ( 8〜 1 0週齢) の胸部大動 脈を摘出後、 速やかに残存血液を除去し、 周囲の脂肪組 織と結合組織を実体顕微鏡下で完全に取り除き、 約 3 m m幅の リ ング状切片を作成した。 血管内腔に適当な大き さの木綿糸を通し、 数回擦過する こ と によって内皮を除 去した。
リ ング状切片の内腔に 2本のステン レスワイヤーを血 管に損傷を与えないように挿入し、 栄養液を満たした容 量 1 0 m 1 の浴 (organ ba th) 中 ( 3 4 °C恒温) に懸垂 した。
ステ ン レスワイヤ一の一方を支持装置に固定し、 他方 をアイ ソメ ト リ ッ ク ト ラ ンスジューサー ( i some t r i c t ransducer, 日本光電社, T B — 6 5 1 T ) に接続した。 標本に予め静止張力 1. 0 gを負荷し、 実験終了までこ の張力を維持した。
標本を測定装置にセッ 卜 して 1 〜 2時間後に内皮依存 性血管弛緩物質であるアセチルコ リ ン (acety l chol i ne ) 1 // Mによる弛緩反応が消失しているこ とをもって内皮 細胞が機能的に損傷している と判定した。 更に、 実験終
了後にも同様の操作を行なって、 時間の経過と共に内皮 細胞の機能が回復していないこ とを確認した。
栄養液と してはク レプス液を用い、 9 5 % 0 9 及び 5 % C 0 0 からなる混合ガスを通気した。 該ク レプス液の p Hは混合ガス通気伏態で約 7. 4であり、 その組成は 次の通りである。
N a C 1 1 1 5 . 3 m M、 K C l 4. 7 m M、
C a C 1 2 2 . 5 m M、 M g S 0 4 1 . 2 m M、
K H o P 04 1 . 2 m M、 N a H C 03 2 5 . 0 m M及びグルコース 1 1 . l m M。
また血管平滑筋における一酸化窒素合成酵素の誘導を 促進させるために、 栄養液には常に リ ポポリ サッ カライ ド ( l ipopol i sacchar i de, L P S ) 1 0 0 n g Zm 1 又 は リ コ ンビナン トイ ンターロイキン l yg ( r I L - 1 ^ ) 0 . 3 n g /m 1 を共存させた。
( 2 ) 血管の弛緩反応の測定
弛緩反応を測定するために、 フ ヱニ レフ リ ン
(pheny l ephr ine ) ( 1 /z M) で予め標本を収縮させて おき、 緊張が一定となったところで薬物を累積的に適用 した。
薬物による反応は標本の張力変化を等尺的にレコーダ 一上に ΐ己録した。
血管の弛緩率 ( ) は、 フ ヱニ レ フ リ ン 1 / Mにより 引き起こされた収縮に対する%と して求めた。
( 3 ) 試験結果
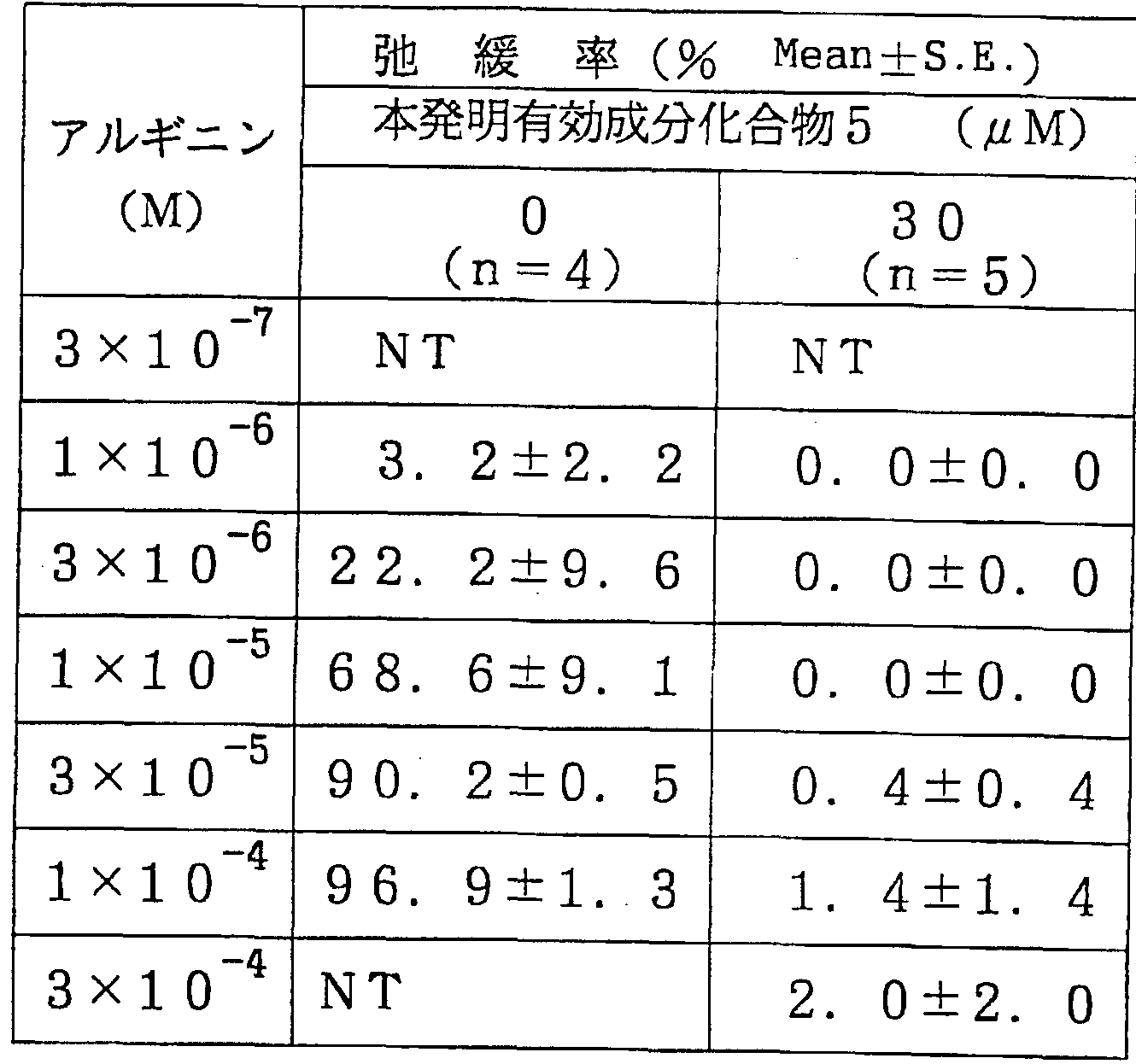
血管摘出直後から、 下記表 1 0に示す本発明有効成分 化合物 1〜 6のそれぞれを適用 (栄養液中に共存) し、 摘出 8〜 1 0時間経過後の血管について得られた観察結 果 (弛緩率 (%) 、 フ ヱニ レフ リ ン 1 / Mによ る収縮を 1 0 0 %とする相対%) を、 各供試化合物毎に表 1 1〜 表 1 6 (—酸化窒素合成酵素誘導促進物質と して L P S 使用の場合) に示す。 また、 一酸化窒素合成酵素誘導促 進物質と して r I L _ l ;5を使用した場合の同結果 (本 発明有効成分化合物 1を使用) を表 1 7に示す。
1 0
1
N T:試験せず
表 1 3
N T:試験せず
表 1 5
T:試験せず
6
N T:試験せず
7
T:試験せず 之等各表より、 本発明有効成分化合物の適用 ( 3 0 ^ M濃度での栄養液中への共存) によれば、 摘出 8〜 1 0時間経過後の血管でもアルギニ ン による弛緩は全く 発現しないこ とが明らかである。
更に、 表 1 8に、 上記試験と同様に して、 ニ ト ロプル シ ド ( II i t r 0 p r U s s i d e ) による弛緩反応に対する本発明 有効成分化合物の影響を求めた結果を示す。
表 1 8
上記表より、 本発明有効成分化合物は、 平滑筋に直接 作用して血管を弛緩させる二 卜 口プルシ ドの弛緩作用に は何等の影響も与えないことが判る。
産業上の利用可能性
本発明の一酸化窒素合成阻害剤は、 エ ン ド トキシ ンシ ョ ッ ク等の一酸化窒素に起因する各種疾患の予防及び治 療に有用である。