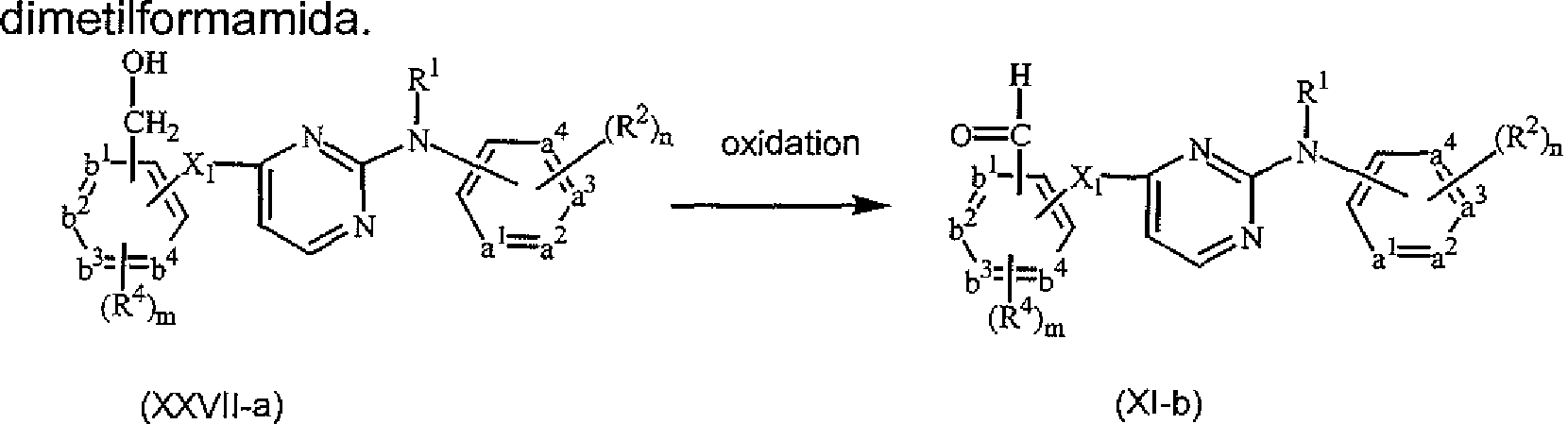
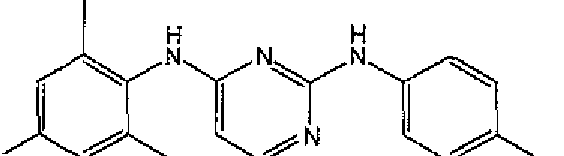
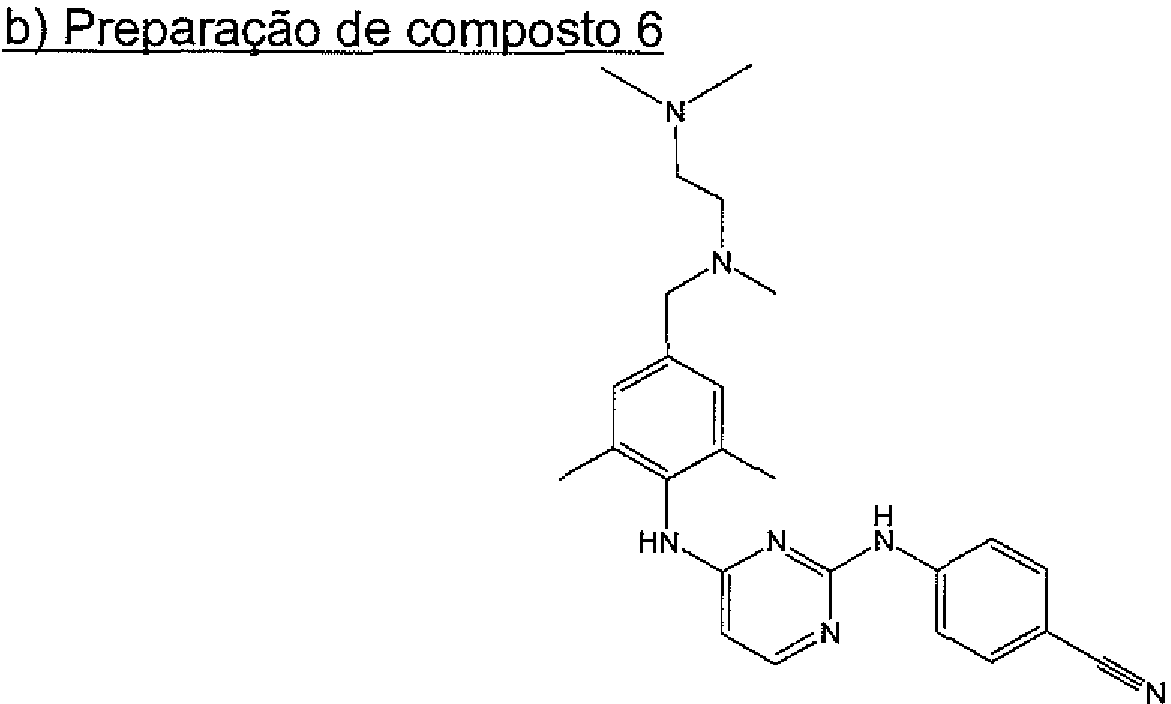
BRPI0316532B1 - Composições farmacêuticas compreendendo uma droga básica ou ácida, um tensoativo, e um ácido ou base solúvel em água fisiologicamente tolerável - Google Patents
Composições farmacêuticas compreendendo uma droga básica ou ácida, um tensoativo, e um ácido ou base solúvel em água fisiologicamente tolerável Download PDFInfo
- Publication number
- BRPI0316532B1 BRPI0316532B1 BRPI0316532-9A BR0316532A BRPI0316532B1 BR PI0316532 B1 BRPI0316532 B1 BR PI0316532B1 BR 0316532 A BR0316532 A BR 0316532A BR PI0316532 B1 BRPI0316532 B1 BR PI0316532B1
- Authority
- BR
- Brazil
- Prior art keywords
- acid
- amino
- formula
- mol
- mixture
- Prior art date
Links
- 239000003814 drug Substances 0.000 title claims abstract description 182
- 239000002253 acid Substances 0.000 title claims abstract description 102
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 24
- 239000007787 solid Substances 0.000 title claims description 27
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 title abstract description 53
- 150000001875 compounds Chemical class 0.000 claims abstract description 288
- 229940079593 drug Drugs 0.000 claims abstract description 156
- 239000000203 mixture Substances 0.000 claims description 379
- -1 2,4,6-trimethylphenyl Chemical group 0.000 claims description 199
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 claims description 84
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 80
- 150000003839 salts Chemical class 0.000 claims description 43
- AOBORMOPSGHCAX-UHFFFAOYSA-N Tocophersolan Chemical compound OCCOC(=O)CCC(=O)OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C AOBORMOPSGHCAX-UHFFFAOYSA-N 0.000 claims description 20
- PYGWGZALEOIKDF-UHFFFAOYSA-N etravirine Chemical compound CC1=CC(C#N)=CC(C)=C1OC1=NC(NC=2C=CC(=CC=2)C#N)=NC(N)=C1Br PYGWGZALEOIKDF-UHFFFAOYSA-N 0.000 claims description 20
- 229920000642 polymer Polymers 0.000 claims description 13
- 239000006185 dispersion Substances 0.000 claims description 12
- 229920001983 poloxamer Polymers 0.000 claims description 10
- 239000007864 aqueous solution Substances 0.000 claims description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims description 9
- 125000000714 pyrimidinyl group Chemical group 0.000 claims description 9
- 239000011734 sodium Substances 0.000 claims description 8
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 claims description 6
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 claims description 6
- 229910052783 alkali metal Inorganic materials 0.000 claims description 6
- 229920001577 copolymer Polymers 0.000 claims description 6
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 claims description 6
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 claims description 6
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 claims description 6
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 claims description 6
- 235000002906 tartaric acid Nutrition 0.000 claims description 6
- 239000011975 tartaric acid Substances 0.000 claims description 6
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 claims description 5
- 229910052708 sodium Inorganic materials 0.000 claims description 5
- 229920002472 Starch Polymers 0.000 claims description 4
- 150000001340 alkali metals Chemical class 0.000 claims description 4
- 239000001768 carboxy methyl cellulose Substances 0.000 claims description 4
- 229920000036 polyvinylpyrrolidone Polymers 0.000 claims description 4
- 239000001267 polyvinylpyrrolidone Substances 0.000 claims description 4
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 claims description 4
- 235000019698 starch Nutrition 0.000 claims description 4
- FXOGXMVMRGLWIG-UHFFFAOYSA-N 4-[[4-[4-(2-cyanoethyl)-2,6-dimethylanilino]pyrimidin-2-yl]amino]benzonitrile Chemical compound CC1=CC(CCC#N)=CC(C)=C1NC1=CC=NC(NC=2C=CC(=CC=2)C#N)=N1 FXOGXMVMRGLWIG-UHFFFAOYSA-N 0.000 claims description 3
- 229920001479 Hydroxyethyl methyl cellulose Polymers 0.000 claims description 3
- 150000003863 ammonium salts Chemical class 0.000 claims description 3
- 229920000609 methyl cellulose Polymers 0.000 claims description 3
- 235000010981 methylcellulose Nutrition 0.000 claims description 3
- 239000001923 methylcellulose Substances 0.000 claims description 3
- 229920000233 poly(alkylene oxides) Polymers 0.000 claims description 3
- 239000005017 polysaccharide Substances 0.000 claims description 3
- 229920003169 water-soluble polymer Polymers 0.000 claims description 3
- VSGUUCVKYPDKPH-UHFFFAOYSA-N 4-[[2-(2-cyanoanilino)pyrimidin-4-yl]amino]-3,5-dimethylbenzonitrile Chemical compound CC1=CC(C#N)=CC(C)=C1NC1=CC=NC(NC=2C(=CC=CC=2)C#N)=N1 VSGUUCVKYPDKPH-UHFFFAOYSA-N 0.000 claims description 2
- 229920001817 Agar Polymers 0.000 claims description 2
- 241000416162 Astragalus gummifer Species 0.000 claims description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 claims description 2
- 229920002101 Chitin Polymers 0.000 claims description 2
- 229920001661 Chitosan Polymers 0.000 claims description 2
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 claims description 2
- 229920000926 Galactomannan Polymers 0.000 claims description 2
- 229920002907 Guar gum Polymers 0.000 claims description 2
- 229920001499 Heparinoid Polymers 0.000 claims description 2
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 claims description 2
- 239000004354 Hydroxyethyl cellulose Substances 0.000 claims description 2
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 claims description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 claims description 2
- 229920002845 Poly(methacrylic acid) Polymers 0.000 claims description 2
- 239000004372 Polyvinyl alcohol Substances 0.000 claims description 2
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 claims description 2
- 229920002125 Sokalan® Polymers 0.000 claims description 2
- 229920001615 Tragacanth Polymers 0.000 claims description 2
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 claims description 2
- 235000010489 acacia gum Nutrition 0.000 claims description 2
- 239000001785 acacia senegal l. willd gum Substances 0.000 claims description 2
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 claims description 2
- 239000008272 agar Substances 0.000 claims description 2
- 235000010419 agar Nutrition 0.000 claims description 2
- 235000010443 alginic acid Nutrition 0.000 claims description 2
- 229920000615 alginic acid Polymers 0.000 claims description 2
- 239000000783 alginic acid Substances 0.000 claims description 2
- 229960001126 alginic acid Drugs 0.000 claims description 2
- 150000004781 alginic acids Chemical class 0.000 claims description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 claims description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 claims description 2
- 229920001525 carrageenan Polymers 0.000 claims description 2
- 235000010418 carrageenan Nutrition 0.000 claims description 2
- 229920002678 cellulose Polymers 0.000 claims description 2
- 235000010417 guar gum Nutrition 0.000 claims description 2
- 239000000665 guar gum Substances 0.000 claims description 2
- 229960002154 guar gum Drugs 0.000 claims description 2
- 229920000669 heparin Polymers 0.000 claims description 2
- 229960002897 heparin Drugs 0.000 claims description 2
- 239000002554 heparinoid Substances 0.000 claims description 2
- 229940025770 heparinoids Drugs 0.000 claims description 2
- 229920013821 hydroxy alkyl cellulose Polymers 0.000 claims description 2
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 claims description 2
- 229920003063 hydroxymethyl cellulose Polymers 0.000 claims description 2
- 229940031574 hydroxymethyl cellulose Drugs 0.000 claims description 2
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 claims description 2
- 239000001863 hydroxypropyl cellulose Substances 0.000 claims description 2
- 239000001814 pectin Substances 0.000 claims description 2
- 229920001277 pectin Polymers 0.000 claims description 2
- 235000010987 pectin Nutrition 0.000 claims description 2
- 229920001987 poloxamine Polymers 0.000 claims description 2
- 229920001451 polypropylene glycol Polymers 0.000 claims description 2
- 229920001282 polysaccharide Polymers 0.000 claims description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 claims description 2
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 claims description 2
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 claims description 2
- 238000013268 sustained release Methods 0.000 claims description 2
- 239000012730 sustained-release form Substances 0.000 claims description 2
- 235000010487 tragacanth Nutrition 0.000 claims description 2
- 239000000196 tragacanth Substances 0.000 claims description 2
- 229940116362 tragacanth Drugs 0.000 claims description 2
- 229920001285 xanthan gum Polymers 0.000 claims description 2
- 235000010493 xanthan gum Nutrition 0.000 claims description 2
- 239000000230 xanthan gum Substances 0.000 claims description 2
- 229940082509 xanthan gum Drugs 0.000 claims description 2
- 229920013820 alkyl cellulose Polymers 0.000 claims 2
- 239000004094 surface-active agent Substances 0.000 abstract description 92
- 239000000543 intermediate Substances 0.000 description 228
- 239000002904 solvent Substances 0.000 description 213
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 114
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 106
- 125000004093 cyano group Chemical group *C#N 0.000 description 83
- 238000002360 preparation method Methods 0.000 description 79
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 76
- 239000000243 solution Substances 0.000 description 75
- RJWLAIMXRBDUMH-ULQDDVLXSA-N N-Acetylleucyl-leucyl-methioninal Chemical compound CSCC[C@@H](C=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(C)=O RJWLAIMXRBDUMH-ULQDDVLXSA-N 0.000 description 70
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 64
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 59
- 238000004440 column chromatography Methods 0.000 description 59
- 239000012044 organic layer Substances 0.000 description 55
- 239000003480 eluent Substances 0.000 description 54
- 239000002585 base Substances 0.000 description 49
- 239000002244 precipitate Substances 0.000 description 47
- 238000000034 method Methods 0.000 description 43
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 39
- 125000000217 alkyl group Chemical group 0.000 description 39
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 36
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 34
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 34
- 238000006243 chemical reaction Methods 0.000 description 33
- 238000004090 dissolution Methods 0.000 description 33
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 32
- 229920006395 saturated elastomer Polymers 0.000 description 31
- 239000000460 chlorine Substances 0.000 description 30
- 239000000741 silica gel Substances 0.000 description 30
- 229910002027 silica gel Inorganic materials 0.000 description 30
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 28
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 28
- 108010037444 diisopropylglutathione ester Proteins 0.000 description 28
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 27
- 125000005843 halogen group Chemical group 0.000 description 27
- 239000002775 capsule Substances 0.000 description 26
- 229920000620 organic polymer Polymers 0.000 description 26
- 235000019439 ethyl acetate Nutrition 0.000 description 25
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 24
- 239000004359 castor oil Substances 0.000 description 24
- 235000019438 castor oil Nutrition 0.000 description 24
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 24
- 229920001223 polyethylene glycol Polymers 0.000 description 24
- 239000000047 product Substances 0.000 description 24
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 23
- 125000001424 substituent group Chemical group 0.000 description 23
- 229910052739 hydrogen Inorganic materials 0.000 description 22
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 21
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 21
- 0 CN(*)c1ncccn1 Chemical compound CN(*)c1ncccn1 0.000 description 20
- 125000003118 aryl group Chemical group 0.000 description 20
- 239000003054 catalyst Substances 0.000 description 20
- 125000002619 bicyclic group Chemical group 0.000 description 19
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 18
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 18
- 239000001257 hydrogen Substances 0.000 description 18
- 229910052763 palladium Inorganic materials 0.000 description 18
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 18
- 229920003091 Methocel™ Polymers 0.000 description 17
- 150000001412 amines Chemical class 0.000 description 17
- 238000000576 coating method Methods 0.000 description 17
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 17
- JNYAEWCLZODPBN-JGWLITMVSA-N (2r,3r,4s)-2-[(1r)-1,2-dihydroxyethyl]oxolane-3,4-diol Chemical compound OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O JNYAEWCLZODPBN-JGWLITMVSA-N 0.000 description 16
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 16
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 15
- 229940049964 oleate Drugs 0.000 description 15
- 239000003826 tablet Substances 0.000 description 15
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 14
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 14
- 239000002202 Polyethylene glycol Substances 0.000 description 14
- 125000004122 cyclic group Chemical group 0.000 description 14
- ZMXDDKWLCZADIW-UHFFFAOYSA-N dimethylformamide Substances CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 14
- 239000012530 fluid Substances 0.000 description 14
- 239000002245 particle Substances 0.000 description 14
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 14
- 230000008569 process Effects 0.000 description 14
- YASYEJJMZJALEJ-UHFFFAOYSA-N Citric acid monohydrate Chemical compound O.OC(=O)CC(O)(C(O)=O)CC(O)=O YASYEJJMZJALEJ-UHFFFAOYSA-N 0.000 description 13
- 229960002303 citric acid monohydrate Drugs 0.000 description 13
- 229910052757 nitrogen Inorganic materials 0.000 description 13
- 239000003921 oil Substances 0.000 description 13
- 239000000843 powder Substances 0.000 description 13
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 12
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 12
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical class C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 12
- 229920002565 Polyethylene Glycol 400 Polymers 0.000 description 12
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 12
- 239000011248 coating agent Substances 0.000 description 12
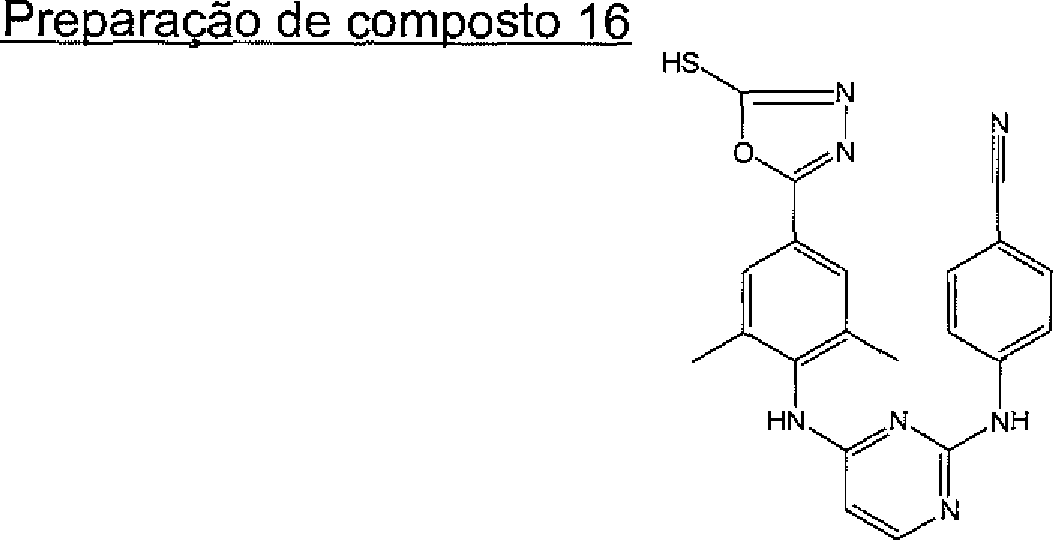
- 239000002361 compost Substances 0.000 description 12
- SNOOUWRIMMFWNE-UHFFFAOYSA-M sodium;6-[(3,4,5-trimethoxybenzoyl)amino]hexanoate Chemical compound [Na+].COC1=CC(C(=O)NCCCCCC([O-])=O)=CC(OC)=C1OC SNOOUWRIMMFWNE-UHFFFAOYSA-M 0.000 description 12
- 229920002690 Polyoxyl 40 HydrogenatedCastorOil Polymers 0.000 description 11
- 125000003545 alkoxy group Chemical group 0.000 description 11
- 125000004432 carbon atom Chemical group C* 0.000 description 11
- 229940125904 compound 1 Drugs 0.000 description 11
- 235000014113 dietary fatty acids Nutrition 0.000 description 11
- 230000000694 effects Effects 0.000 description 11
- 239000000194 fatty acid Substances 0.000 description 11
- 229930195729 fatty acid Natural products 0.000 description 11
- 239000007962 solid dispersion Substances 0.000 description 11
- 239000003795 chemical substances by application Substances 0.000 description 10
- DCSUBABJRXZOMT-IRLDBZIGSA-N cisapride Chemical compound C([C@@H]([C@@H](CC1)NC(=O)C=2C(=CC(N)=C(Cl)C=2)OC)OC)N1CCCOC1=CC=C(F)C=C1 DCSUBABJRXZOMT-IRLDBZIGSA-N 0.000 description 10
- 229960005132 cisapride Drugs 0.000 description 10
- DCSUBABJRXZOMT-UHFFFAOYSA-N cisapride Natural products C1CC(NC(=O)C=2C(=CC(N)=C(Cl)C=2)OC)C(OC)CN1CCCOC1=CC=C(F)C=C1 DCSUBABJRXZOMT-UHFFFAOYSA-N 0.000 description 10
- 239000002552 dosage form Substances 0.000 description 10
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 10
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 10
- 235000019198 oils Nutrition 0.000 description 10
- 239000003981 vehicle Substances 0.000 description 10
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 9
- 241000282472 Canis lupus familiaris Species 0.000 description 9
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 9
- 230000002378 acidificating effect Effects 0.000 description 9
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 9
- 239000003153 chemical reaction reagent Substances 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Natural products C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 9
- 239000011541 reaction mixture Substances 0.000 description 9
- 238000003756 stirring Methods 0.000 description 9
- 125000000165 tricyclic carbocycle group Chemical group 0.000 description 9
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 8
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 8
- 150000007513 acids Chemical class 0.000 description 8
- 238000001914 filtration Methods 0.000 description 8
- 229960004592 isopropanol Drugs 0.000 description 8
- 239000010410 layer Substances 0.000 description 8
- 239000012071 phase Substances 0.000 description 8
- 125000000169 tricyclic heterocycle group Chemical group 0.000 description 8
- 125000001731 2-cyanoethyl group Chemical group [H]C([H])(*)C([H])([H])C#N 0.000 description 7
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 7
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 7
- 238000013459 approach Methods 0.000 description 7
- POULHZVOKOAJMA-UHFFFAOYSA-M dodecanoate Chemical compound CCCCCCCCCCCC([O-])=O POULHZVOKOAJMA-UHFFFAOYSA-M 0.000 description 7
- 238000001035 drying Methods 0.000 description 7
- 150000002148 esters Chemical class 0.000 description 7
- 238000001704 evaporation Methods 0.000 description 7
- 239000000706 filtrate Substances 0.000 description 7
- 238000000338 in vitro Methods 0.000 description 7
- 229940070765 laurate Drugs 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 7
- 235000015320 potassium carbonate Nutrition 0.000 description 7
- 125000006239 protecting group Chemical group 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- 125000004916 (C1-C6) alkylcarbonyl group Chemical group 0.000 description 6
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 6
- 125000004801 4-cyanophenyl group Chemical group [H]C1=C([H])C(C#N)=C([H])C([H])=C1* 0.000 description 6
- 229920000858 Cyclodextrin Polymers 0.000 description 6
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- 239000003810 Jones reagent Substances 0.000 description 6
- 241000124008 Mammalia Species 0.000 description 6
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 6
- 210000004027 cell Anatomy 0.000 description 6
- 238000004587 chromatography analysis Methods 0.000 description 6
- 238000001816 cooling Methods 0.000 description 6
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 6
- 238000001125 extrusion Methods 0.000 description 6
- 239000007903 gelatin capsule Substances 0.000 description 6
- 125000005456 glyceride group Chemical group 0.000 description 6
- 229930195733 hydrocarbon Natural products 0.000 description 6
- 230000001976 improved effect Effects 0.000 description 6
- 238000004811 liquid chromatography Methods 0.000 description 6
- BQJCRHHNABKAKU-KBQPJGBKSA-N morphine Chemical compound O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O BQJCRHHNABKAKU-KBQPJGBKSA-N 0.000 description 6
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 6
- 229940042402 non-nucleoside reverse transcriptase inhibitor Drugs 0.000 description 6
- 239000002726 nonnucleoside reverse transcriptase inhibitor Substances 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 6
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 6
- 150000003254 radicals Chemical class 0.000 description 6
- 239000006104 solid solution Substances 0.000 description 6
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 5
- HQSRVYUCBOCBLY-XOOFNSLWSA-N 2-[(2r)-butan-2-yl]-4-[4-[4-[4-[[(2s,4r)-2-(4-chlorophenyl)-2-[(4-methyl-1,2,4-triazol-3-yl)sulfanylmethyl]-1,3-dioxolan-4-yl]methoxy]phenyl]piperazin-1-yl]phenyl]-1,2,4-triazol-3-one Chemical compound O=C1N([C@H](C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@H]3O[C@@](CSC=4N(C=NN=4)C)(OC3)C=3C=CC(Cl)=CC=3)=CC=2)C=C1 HQSRVYUCBOCBLY-XOOFNSLWSA-N 0.000 description 5
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 5
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 5
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 5
- 239000004215 Carbon black (E152) Substances 0.000 description 5
- 241000725303 Human immunodeficiency virus Species 0.000 description 5
- 125000003342 alkenyl group Chemical group 0.000 description 5
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 5
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 239000003638 chemical reducing agent Substances 0.000 description 5
- 230000008020 evaporation Effects 0.000 description 5
- 125000000524 functional group Chemical group 0.000 description 5
- 239000007789 gas Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 239000002609 medium Substances 0.000 description 5
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- 125000002950 monocyclic group Chemical group 0.000 description 5
- 125000003386 piperidinyl group Chemical group 0.000 description 5
- 229910000027 potassium carbonate Inorganic materials 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- 238000006722 reduction reaction Methods 0.000 description 5
- 239000000523 sample Substances 0.000 description 5
- 239000007858 starting material Substances 0.000 description 5
- 229940114926 stearate Drugs 0.000 description 5
- 235000000346 sugar Nutrition 0.000 description 5
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 5
- 229910052717 sulfur Inorganic materials 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 238000011282 treatment Methods 0.000 description 5
- FFJCNSLCJOQHKM-CLFAGFIQSA-N (z)-1-[(z)-octadec-9-enoxy]octadec-9-ene Chemical compound CCCCCCCC\C=C/CCCCCCCCOCCCCCCCC\C=C/CCCCCCCC FFJCNSLCJOQHKM-CLFAGFIQSA-N 0.000 description 4
- WECGLUPZRHILCT-GSNKCQISSA-N 1-linoleoyl-sn-glycerol Chemical class CCCCC\C=C/C\C=C/CCCCCCCC(=O)OC[C@@H](O)CO WECGLUPZRHILCT-GSNKCQISSA-N 0.000 description 4
- HBXWUCXDUUJDRB-UHFFFAOYSA-N 1-octadecoxyoctadecane Chemical compound CCCCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCCCC HBXWUCXDUUJDRB-UHFFFAOYSA-N 0.000 description 4
- VHVPQPYKVGDNFY-DFMJLFEVSA-N 2-[(2r)-butan-2-yl]-4-[4-[4-[4-[[(2r,4s)-2-(2,4-dichlorophenyl)-2-(1,2,4-triazol-1-ylmethyl)-1,3-dioxolan-4-yl]methoxy]phenyl]piperazin-1-yl]phenyl]-1,2,4-triazol-3-one Chemical compound O=C1N([C@H](C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@@H]3O[C@](CN4N=CN=C4)(OC3)C=3C(=CC(Cl)=CC=3)Cl)=CC=2)C=C1 VHVPQPYKVGDNFY-DFMJLFEVSA-N 0.000 description 4
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 4
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 4
- 244000144725 Amygdalus communis Species 0.000 description 4
- 235000011437 Amygdalus communis Nutrition 0.000 description 4
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 4
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 4
- 238000006546 Horner-Wadsworth-Emmons reaction Methods 0.000 description 4
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 4
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 4
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 4
- 239000004698 Polyethylene Substances 0.000 description 4
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 4
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 239000004809 Teflon Substances 0.000 description 4
- 229920006362 Teflon® Polymers 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 4
- 235000020224 almond Nutrition 0.000 description 4
- 239000011230 binding agent Substances 0.000 description 4
- 210000001124 body fluid Anatomy 0.000 description 4
- 239000010839 body fluid Substances 0.000 description 4
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 239000011575 calcium Substances 0.000 description 4
- 229910052791 calcium Inorganic materials 0.000 description 4
- 229940099898 chlorophyllin Drugs 0.000 description 4
- 235000019805 chlorophyllin Nutrition 0.000 description 4
- 125000000753 cycloalkyl group Chemical group 0.000 description 4
- 238000003745 diagnosis Methods 0.000 description 4
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 235000013305 food Nutrition 0.000 description 4
- 210000004051 gastric juice Anatomy 0.000 description 4
- 229940074046 glyceryl laurate Drugs 0.000 description 4
- 230000002209 hydrophobic effect Effects 0.000 description 4
- 229960004130 itraconazole Drugs 0.000 description 4
- 230000003287 optical effect Effects 0.000 description 4
- 238000007254 oxidation reaction Methods 0.000 description 4
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 description 4
- 235000019371 penicillin G benzathine Nutrition 0.000 description 4
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 4
- 238000011321 prophylaxis Methods 0.000 description 4
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 125000003373 pyrazinyl group Chemical group 0.000 description 4
- 125000002098 pyridazinyl group Chemical group 0.000 description 4
- 125000004076 pyridyl group Chemical group 0.000 description 4
- ARIWANIATODDMH-UHFFFAOYSA-N rac-1-monolauroylglycerol Chemical compound CCCCCCCCCCCC(=O)OCC(O)CO ARIWANIATODDMH-UHFFFAOYSA-N 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000012047 saturated solution Substances 0.000 description 4
- 239000001632 sodium acetate Substances 0.000 description 4
- 235000017281 sodium acetate Nutrition 0.000 description 4
- 229910000104 sodium hydride Inorganic materials 0.000 description 4
- 230000007928 solubilization Effects 0.000 description 4
- 238000005063 solubilization Methods 0.000 description 4
- 210000002784 stomach Anatomy 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 229920001169 thermoplastic Polymers 0.000 description 4
- 239000004416 thermosoftening plastic Substances 0.000 description 4
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 4
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 4
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 4
- 125000004953 trihalomethyl group Chemical group 0.000 description 4
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 4
- 125000004400 (C1-C12) alkyl group Chemical group 0.000 description 3
- FDCJDKXCCYFOCV-UHFFFAOYSA-N 1-hexadecoxyhexadecane Chemical compound CCCCCCCCCCCCCCCCOCCCCCCCCCCCCCCCC FDCJDKXCCYFOCV-UHFFFAOYSA-N 0.000 description 3
- ZVUNTIMPQCQCAQ-UHFFFAOYSA-N 2-dodecanoyloxyethyl dodecanoate Chemical compound CCCCCCCCCCCC(=O)OCCOC(=O)CCCCCCCCCCC ZVUNTIMPQCQCAQ-UHFFFAOYSA-N 0.000 description 3
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 3
- JMTMSDXUXJISAY-UHFFFAOYSA-N 2H-benzotriazol-4-ol Chemical compound OC1=CC=CC2=C1N=NN2 JMTMSDXUXJISAY-UHFFFAOYSA-N 0.000 description 3
- QGLAYJCJLHNIGJ-UHFFFAOYSA-N 4-bromo-2,6-dimethylaniline Chemical compound CC1=CC(Br)=CC(C)=C1N QGLAYJCJLHNIGJ-UHFFFAOYSA-N 0.000 description 3
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 3
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 3
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 3
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical class CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 3
- 101000939500 Homo sapiens UBX domain-containing protein 11 Proteins 0.000 description 3
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 3
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 3
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical class C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- 239000007868 Raney catalyst Substances 0.000 description 3
- 229910000564 Raney nickel Inorganic materials 0.000 description 3
- 229940123237 Taxane Drugs 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 102100029645 UBX domain-containing protein 11 Human genes 0.000 description 3
- 125000001931 aliphatic group Chemical group 0.000 description 3
- 239000003513 alkali Substances 0.000 description 3
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 3
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 3
- 239000012296 anti-solvent Substances 0.000 description 3
- 229940121375 antifungal agent Drugs 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 3
- 229910052794 bromium Inorganic materials 0.000 description 3
- 229910052801 chlorine Inorganic materials 0.000 description 3
- 239000008139 complexing agent Substances 0.000 description 3
- 229940125773 compound 10 Drugs 0.000 description 3
- 229940125782 compound 2 Drugs 0.000 description 3
- 229940097362 cyclodextrins Drugs 0.000 description 3
- GVJHHUAWPYXKBD-UHFFFAOYSA-N d-alpha-tocopherol Natural products OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 3
- DTPCFIHYWYONMD-UHFFFAOYSA-N decaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO DTPCFIHYWYONMD-UHFFFAOYSA-N 0.000 description 3
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical class CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 3
- 150000004665 fatty acids Chemical class 0.000 description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- 238000000227 grinding Methods 0.000 description 3
- 229910052736 halogen Inorganic materials 0.000 description 3
- 150000002367 halogens Chemical class 0.000 description 3
- 125000005842 heteroatom Chemical group 0.000 description 3
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 125000000717 hydrazino group Chemical group [H]N([*])N([H])[H] 0.000 description 3
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 3
- 239000005457 ice water Substances 0.000 description 3
- 125000001041 indolyl group Chemical group 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 238000001746 injection moulding Methods 0.000 description 3
- UEXQBEVWFZKHNB-UHFFFAOYSA-N intermediate 29 Natural products C1=CC(N)=CC=C1NC1=NC=CC=N1 UEXQBEVWFZKHNB-UHFFFAOYSA-N 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 239000011630 iodine Substances 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 239000008108 microcrystalline cellulose Substances 0.000 description 3
- 229940016286 microcrystalline cellulose Drugs 0.000 description 3
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 3
- 125000002911 monocyclic heterocycle group Chemical group 0.000 description 3
- 229960005181 morphine Drugs 0.000 description 3
- 125000002757 morpholinyl group Chemical group 0.000 description 3
- 210000000214 mouth Anatomy 0.000 description 3
- 239000012299 nitrogen atmosphere Substances 0.000 description 3
- 150000007530 organic bases Chemical class 0.000 description 3
- 230000003647 oxidation Effects 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 229910052698 phosphorus Inorganic materials 0.000 description 3
- 239000011574 phosphorus Substances 0.000 description 3
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 3
- 125000004193 piperazinyl group Chemical group 0.000 description 3
- 230000036470 plasma concentration Effects 0.000 description 3
- 239000008389 polyethoxylated castor oil Substances 0.000 description 3
- NNFCIKHAZHQZJG-UHFFFAOYSA-N potassium cyanide Chemical compound [K+].N#[C-] NNFCIKHAZHQZJG-UHFFFAOYSA-N 0.000 description 3
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- 239000002243 precursor Substances 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 125000000168 pyrrolyl group Chemical group 0.000 description 3
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 3
- 238000010956 selective crystallization Methods 0.000 description 3
- 239000012312 sodium hydride Substances 0.000 description 3
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000005809 transesterification reaction Methods 0.000 description 3
- 230000009466 transformation Effects 0.000 description 3
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 3
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 2
- 125000006619 (C1-C6) dialkylamino group Chemical group 0.000 description 2
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 2
- 125000003626 1,2,4-triazol-1-yl group Chemical group [*]N1N=C([H])N=C1[H] 0.000 description 2
- QIZPVNNYFKFJAD-UHFFFAOYSA-N 1-chloro-2-prop-1-ynylbenzene Chemical compound CC#CC1=CC=CC=C1Cl QIZPVNNYFKFJAD-UHFFFAOYSA-N 0.000 description 2
- CMCBDXRRFKYBDG-UHFFFAOYSA-N 1-dodecoxydodecane Chemical compound CCCCCCCCCCCCOCCCCCCCCCCCC CMCBDXRRFKYBDG-UHFFFAOYSA-N 0.000 description 2
- KWVPRPSXBZNOHS-UHFFFAOYSA-N 2,4,6-Trimethylaniline Chemical compound CC1=CC(C)=C(N)C(C)=C1 KWVPRPSXBZNOHS-UHFFFAOYSA-N 0.000 description 2
- UWNADWZGEHDQAB-UHFFFAOYSA-N 2,5-dimethylhexane Chemical group CC(C)CCC(C)C UWNADWZGEHDQAB-UHFFFAOYSA-N 0.000 description 2
- XGLVDUUYFKXKPL-UHFFFAOYSA-N 2-(2-methoxyethoxy)-n,n-bis[2-(2-methoxyethoxy)ethyl]ethanamine Chemical compound COCCOCCN(CCOCCOC)CCOCCOC XGLVDUUYFKXKPL-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- MQFYRUGXOJAUQK-UHFFFAOYSA-N 2-[2-[2-(2-octadecanoyloxyethoxy)ethoxy]ethoxy]ethyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCOCCOCCOCCOC(=O)CCCCCCCCCCCCCCCCC MQFYRUGXOJAUQK-UHFFFAOYSA-N 0.000 description 2
- UHGULLIUJBCTEF-UHFFFAOYSA-N 2-aminobenzothiazole Chemical compound C1=CC=C2SC(N)=NC2=C1 UHGULLIUJBCTEF-UHFFFAOYSA-N 0.000 description 2
- RFVNOJDQRGSOEL-UHFFFAOYSA-N 2-hydroxyethyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCO RFVNOJDQRGSOEL-UHFFFAOYSA-N 0.000 description 2
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 2
- ILAYIAGXTHKHNT-UHFFFAOYSA-N 4-[4-(2,4,6-trimethyl-phenylamino)-pyrimidin-2-ylamino]-benzonitrile Chemical compound CC1=CC(C)=CC(C)=C1NC1=CC=NC(NC=2C=CC(=CC=2)C#N)=N1 ILAYIAGXTHKHNT-UHFFFAOYSA-N 0.000 description 2
- XZIIFPSPUDAGJM-UHFFFAOYSA-N 6-chloro-2-n,2-n-diethylpyrimidine-2,4-diamine Chemical compound CCN(CC)C1=NC(N)=CC(Cl)=N1 XZIIFPSPUDAGJM-UHFFFAOYSA-N 0.000 description 2
- IRBAWVGZNJIROV-SFHVURJKSA-N 9-(2-cyclopropylethynyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC4CC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 IRBAWVGZNJIROV-SFHVURJKSA-N 0.000 description 2
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- 239000004475 Arginine Substances 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- IYHHRZBKXXKDDY-UHFFFAOYSA-N BI-605906 Chemical compound N=1C=2SC(C(N)=O)=C(N)C=2C(C(F)(F)CC)=CC=1N1CCC(S(C)(=O)=O)CC1 IYHHRZBKXXKDDY-UHFFFAOYSA-N 0.000 description 2
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- IELOKBJPULMYRW-NJQVLOCASA-N D-alpha-Tocopheryl Acid Succinate Chemical compound OC(=O)CCC(=O)OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C IELOKBJPULMYRW-NJQVLOCASA-N 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- UGJMXCAKCUNAIE-UHFFFAOYSA-N Gabapentin Chemical compound OC(=O)CC1(CN)CCCCC1 UGJMXCAKCUNAIE-UHFFFAOYSA-N 0.000 description 2
- 102000003886 Glycoproteins Human genes 0.000 description 2
- 108090000288 Glycoproteins Proteins 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- AMIMRNSIRUDHCM-UHFFFAOYSA-N Isopropylaldehyde Chemical compound CC(C)C=O AMIMRNSIRUDHCM-UHFFFAOYSA-N 0.000 description 2
- 239000005639 Lauric acid Substances 0.000 description 2
- 241000270322 Lepidosauria Species 0.000 description 2
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 2
- 239000004472 Lysine Substances 0.000 description 2
- MJVAVZPDRWSRRC-UHFFFAOYSA-N Menadione Chemical compound C1=CC=C2C(=O)C(C)=CC(=O)C2=C1 MJVAVZPDRWSRRC-UHFFFAOYSA-N 0.000 description 2
- 235000006679 Mentha X verticillata Nutrition 0.000 description 2
- 235000002899 Mentha suaveolens Nutrition 0.000 description 2
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical class CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 229930192392 Mitomycin Natural products 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- JRNVZBWKYDBUCA-UHFFFAOYSA-N N-chlorosuccinimide Chemical compound ClN1C(=O)CCC1=O JRNVZBWKYDBUCA-UHFFFAOYSA-N 0.000 description 2
- POFVJRKJJBFPII-UHFFFAOYSA-N N-cyclopentyl-5-[2-[[5-[(4-ethylpiperazin-1-yl)methyl]pyridin-2-yl]amino]-5-fluoropyrimidin-4-yl]-4-methyl-1,3-thiazol-2-amine Chemical compound C1(CCCC1)NC=1SC(=C(N=1)C)C1=NC(=NC=C1F)NC1=NC=C(C=C1)CN1CCN(CC1)CC POFVJRKJJBFPII-UHFFFAOYSA-N 0.000 description 2
- IMONTRJLAWHYGT-ZCPXKWAGSA-N Norethindrone Acetate Chemical compound C1CC2=CC(=O)CC[C@@H]2[C@@H]2[C@@H]1[C@@H]1CC[C@](C#C)(OC(=O)C)[C@@]1(C)CC2 IMONTRJLAWHYGT-ZCPXKWAGSA-N 0.000 description 2
- 239000005642 Oleic acid Substances 0.000 description 2
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 2
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical compound OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 2
- 229920000604 Polyethylene Glycol 200 Polymers 0.000 description 2
- 229920001030 Polyethylene Glycol 4000 Polymers 0.000 description 2
- 229920000388 Polyphosphate Polymers 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- RJKFOVLPORLFTN-LEKSSAKUSA-N Progesterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)C)[C@@]1(C)CC2 RJKFOVLPORLFTN-LEKSSAKUSA-N 0.000 description 2
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- 229930182558 Sterol Natural products 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- QBYJBZPUGVGKQQ-SJJAEHHWSA-N aldrin Chemical compound C1[C@H]2C=C[C@@H]1[C@H]1[C@@](C3(Cl)Cl)(Cl)C(Cl)=C(Cl)[C@@]3(Cl)[C@H]12 QBYJBZPUGVGKQQ-SJJAEHHWSA-N 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 229940100198 alkylating agent Drugs 0.000 description 2
- 239000002168 alkylating agent Substances 0.000 description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 235000011114 ammonium hydroxide Nutrition 0.000 description 2
- 229940035676 analgesics Drugs 0.000 description 2
- 125000000129 anionic group Chemical group 0.000 description 2
- 239000002259 anti human immunodeficiency virus agent Substances 0.000 description 2
- 229940124411 anti-hiv antiviral agent Drugs 0.000 description 2
- 229940088710 antibiotic agent Drugs 0.000 description 2
- 239000003429 antifungal agent Substances 0.000 description 2
- 239000002220 antihypertensive agent Substances 0.000 description 2
- 239000003443 antiviral agent Substances 0.000 description 2
- 229940121357 antivirals Drugs 0.000 description 2
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 2
- OTKPPUXRIADSGD-PPRNARJGSA-N avoparcina Chemical compound O([C@@H]1C2=CC=C(C(=C2)Cl)OC=2C=C3C=C(C=2O[C@H]2C([C@@H](O)[C@H](O)[C@@H](CO)O2)O[C@@H]2O[C@@H](C)[C@H](O)[C@H](N)C2)OC2=CC=C(C=C2)[C@@H](O)[C@H](C(N[C@H](C(=O)N[C@H]3C(=O)N[C@H]2C(=O)N[C@@H]1C(N[C@@H](C1=CC(O)=CC(O)=C1C=1C(O)=CC=C2C=1)C(O)=O)=O)C=1C=CC(O)=CC=1)=O)NC(=O)[C@H](NC)C=1C=CC(O[C@H]2[C@@H]([C@H](O)[C@@H](O)[C@H](C)O2)O)=CC=1)[C@H]1C[C@@H](N)[C@@H](O)[C@H](C)O1 OTKPPUXRIADSGD-PPRNARJGSA-N 0.000 description 2
- 125000000852 azido group Chemical group *N=[N+]=[N-] 0.000 description 2
- BLFLLBZGZJTVJG-UHFFFAOYSA-N benzocaine Chemical compound CCOC(=O)C1=CC=C(N)C=C1 BLFLLBZGZJTVJG-UHFFFAOYSA-N 0.000 description 2
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 2
- 229920001400 block copolymer Polymers 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 125000001246 bromo group Chemical group Br* 0.000 description 2
- 239000004067 bulking agent Substances 0.000 description 2
- HQABUPZFAYXKJW-UHFFFAOYSA-N butan-1-amine Chemical class CCCCN HQABUPZFAYXKJW-UHFFFAOYSA-N 0.000 description 2
- 238000003490 calendering Methods 0.000 description 2
- 125000002837 carbocyclic group Chemical group 0.000 description 2
- 150000001718 carbodiimides Chemical class 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 125000002091 cationic group Chemical group 0.000 description 2
- 239000003093 cationic surfactant Substances 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- 229940125898 compound 5 Drugs 0.000 description 2
- MGNCLNQXLYJVJD-UHFFFAOYSA-N cyanuric chloride Chemical compound ClC1=NC(Cl)=NC(Cl)=N1 MGNCLNQXLYJVJD-UHFFFAOYSA-N 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 230000007812 deficiency Effects 0.000 description 2
- 239000012024 dehydrating agents Substances 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- WHBIGIKBNXZKFE-UHFFFAOYSA-N delavirdine Chemical compound CC(C)NC1=CC=CN=C1N1CCN(C(=O)C=2NC3=CC=C(NS(C)(=O)=O)C=C3C=2)CC1 WHBIGIKBNXZKFE-UHFFFAOYSA-N 0.000 description 2
- 229960004976 desogestrel Drugs 0.000 description 2
- RPLCPCMSCLEKRS-BPIQYHPVSA-N desogestrel Chemical compound C1CC[C@@H]2[C@H]3C(=C)C[C@](CC)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 RPLCPCMSCLEKRS-BPIQYHPVSA-N 0.000 description 2
- JQVDAXLFBXTEQA-UHFFFAOYSA-N dibutylamine Chemical class CCCCNCCCC JQVDAXLFBXTEQA-UHFFFAOYSA-N 0.000 description 2
- 150000005690 diesters Chemical class 0.000 description 2
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 2
- XYYVYLMBEZUESM-UHFFFAOYSA-N dihydrocodeine Natural products C1C(N(CCC234)C)C2C=CC(=O)C3OC2=C4C1=CC=C2OC XYYVYLMBEZUESM-UHFFFAOYSA-N 0.000 description 2
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- ADEBPBSSDYVVLD-UHFFFAOYSA-N donepezil Chemical compound O=C1C=2C=C(OC)C(OC)=CC=2CC1CC(CC1)CCN1CC1=CC=CC=C1 ADEBPBSSDYVVLD-UHFFFAOYSA-N 0.000 description 2
- MVPICKVDHDWCJQ-UHFFFAOYSA-N ethyl 3-pyrrolidin-1-ylpropanoate Chemical compound CCOC(=O)CCN1CCCC1 MVPICKVDHDWCJQ-UHFFFAOYSA-N 0.000 description 2
- 125000004494 ethyl ester group Chemical group 0.000 description 2
- RRAFCDWBNXTKKO-UHFFFAOYSA-N eugenol Chemical compound COC1=CC(CC=C)=CC=C1O RRAFCDWBNXTKKO-UHFFFAOYSA-N 0.000 description 2
- 238000013265 extended release Methods 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 150000002191 fatty alcohols Chemical class 0.000 description 2
- 230000002349 favourable effect Effects 0.000 description 2
- 238000011049 filling Methods 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 239000012458 free base Substances 0.000 description 2
- 125000002541 furyl group Chemical group 0.000 description 2
- ASUTZQLVASHGKV-JDFRZJQESA-N galanthamine Chemical compound O1C(=C23)C(OC)=CC=C2CN(C)CC[C@]23[C@@H]1C[C@@H](O)C=C2 ASUTZQLVASHGKV-JDFRZJQESA-N 0.000 description 2
- 230000002496 gastric effect Effects 0.000 description 2
- 125000001475 halogen functional group Chemical group 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- IIRDTKBZINWQAW-UHFFFAOYSA-N hexaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCO IIRDTKBZINWQAW-UHFFFAOYSA-N 0.000 description 2
- FFUAGWLWBBFQJT-UHFFFAOYSA-N hexamethyldisilazane Chemical compound C[Si](C)(C)N[Si](C)(C)C FFUAGWLWBBFQJT-UHFFFAOYSA-N 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- XGIHQYAWBCFNPY-AZOCGYLKSA-N hydrabamine Chemical compound C([C@@H]12)CC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC[C@@]1(C)CNCCNC[C@@]1(C)[C@@H]2CCC3=CC(C(C)C)=CC=C3[C@@]2(C)CCC1 XGIHQYAWBCFNPY-AZOCGYLKSA-N 0.000 description 2
- OROGSEYTTFOCAN-UHFFFAOYSA-N hydrocodone Natural products C1C(N(CCC234)C)C2C=CC(O)C3OC2=C4C1=CC=C2OC OROGSEYTTFOCAN-UHFFFAOYSA-N 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 2
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 239000002608 ionic liquid Substances 0.000 description 2
- QRXWMOHMRWLFEY-UHFFFAOYSA-N isoniazide Chemical compound NNC(=O)C1=CC=NC=C1 QRXWMOHMRWLFEY-UHFFFAOYSA-N 0.000 description 2
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 2
- 229960001627 lamivudine Drugs 0.000 description 2
- JTEGQNOMFQHVDC-NKWVEPMBSA-N lamivudine Chemical compound O=C1N=C(N)C=CN1[C@H]1O[C@@H](CO)SC1 JTEGQNOMFQHVDC-NKWVEPMBSA-N 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000006193 liquid solution Substances 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- CUONGYYJJVDODC-UHFFFAOYSA-N malononitrile Chemical compound N#CCC#N CUONGYYJJVDODC-UHFFFAOYSA-N 0.000 description 2
- NUJOXMJBOLGQSY-UHFFFAOYSA-N manganese dioxide Chemical compound O=[Mn]=O NUJOXMJBOLGQSY-UHFFFAOYSA-N 0.000 description 2
- 239000000155 melt Substances 0.000 description 2
- 238000007909 melt granulation Methods 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 229960004857 mitomycin Drugs 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- NQDJXKOVJZTUJA-UHFFFAOYSA-N nevirapine Chemical compound C12=NC=CC=C2C(=O)NC=2C(C)=CC=NC=2N1C1CC1 NQDJXKOVJZTUJA-UHFFFAOYSA-N 0.000 description 2
- HYIMSNHJOBLJNT-UHFFFAOYSA-N nifedipine Chemical compound COC(=O)C1=C(C)NC(C)=C(C(=O)OC)C1C1=CC=CC=C1[N+]([O-])=O HYIMSNHJOBLJNT-UHFFFAOYSA-N 0.000 description 2
- 229960001597 nifedipine Drugs 0.000 description 2
- YZUUTMGDONTGTN-UHFFFAOYSA-N nonaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCO YZUUTMGDONTGTN-UHFFFAOYSA-N 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- 229940053934 norethindrone Drugs 0.000 description 2
- 229960001652 norethindrone acetate Drugs 0.000 description 2
- VIKNJXKGJWUCNN-XGXHKTLJSA-N norethisterone Chemical compound O=C1CC[C@@H]2[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 VIKNJXKGJWUCNN-XGXHKTLJSA-N 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- WWZKQHOCKIZLMA-UHFFFAOYSA-N octanoic acid Chemical compound CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 150000001451 organic peroxides Chemical class 0.000 description 2
- 239000007800 oxidant agent Substances 0.000 description 2
- 230000001590 oxidative effect Effects 0.000 description 2
- 125000004043 oxo group Chemical group O=* 0.000 description 2
- 239000003346 palm kernel oil Substances 0.000 description 2
- 239000008188 pellet Substances 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- 150000002978 peroxides Chemical class 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- DLYUQMMRRRQYAE-UHFFFAOYSA-N phosphorus pentoxide Inorganic materials O1P(O2)(=O)OP3(=O)OP1(=O)OP2(=O)O3 DLYUQMMRRRQYAE-UHFFFAOYSA-N 0.000 description 2
- SHUZOJHMOBOZST-UHFFFAOYSA-N phylloquinone Natural products CC(C)CCCCC(C)CCC(C)CCCC(=CCC1=C(C)C(=O)c2ccccc2C1=O)C SHUZOJHMOBOZST-UHFFFAOYSA-N 0.000 description 2
- 229960000502 poloxamer Drugs 0.000 description 2
- 229920002503 polyoxyethylene-polyoxypropylene Polymers 0.000 description 2
- 239000001205 polyphosphate Substances 0.000 description 2
- 235000011176 polyphosphates Nutrition 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 235000011056 potassium acetate Nutrition 0.000 description 2
- XXQBEVHPUKOQEO-UHFFFAOYSA-N potassium superoxide Chemical compound [K+].[K+].[O-][O-] XXQBEVHPUKOQEO-UHFFFAOYSA-N 0.000 description 2
- 238000001092 precipitation with compressed antisolvent Methods 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 2
- 239000011253 protective coating Substances 0.000 description 2
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 2
- LOUPRKONTZGTKE-LHHVKLHASA-N quinidine Chemical compound C([C@H]([C@H](C1)C=C)C2)C[N@@]1[C@H]2[C@@H](O)C1=CC=NC2=CC=C(OC)C=C21 LOUPRKONTZGTKE-LHHVKLHASA-N 0.000 description 2
- 238000001046 rapid expansion of supercritical solution Methods 0.000 description 2
- QEVHRUUCFGRFIF-MDEJGZGSSA-N reserpine Chemical compound O([C@H]1[C@@H]([C@H]([C@H]2C[C@@H]3C4=C(C5=CC=C(OC)C=C5N4)CCN3C[C@H]2C1)C(=O)OC)OC)C(=O)C1=CC(OC)=C(OC)C(OC)=C1 QEVHRUUCFGRFIF-MDEJGZGSSA-N 0.000 description 2
- WBHHMMIMDMUBKC-QJWNTBNXSA-M ricinoleate Chemical compound CCCCCC[C@@H](O)C\C=C/CCCCCCCC([O-])=O WBHHMMIMDMUBKC-QJWNTBNXSA-M 0.000 description 2
- 229940066675 ricinoleate Drugs 0.000 description 2
- 210000003296 saliva Anatomy 0.000 description 2
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- BNRNXUUZRGQAQC-UHFFFAOYSA-N sildenafil Chemical compound CCCC1=NN(C)C(C(N2)=O)=C1N=C2C(C(=CC=1)OCC)=CC=1S(=O)(=O)N1CCN(C)CC1 BNRNXUUZRGQAQC-UHFFFAOYSA-N 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- KSAVQLQVUXSOCR-UHFFFAOYSA-M sodium lauroyl sarcosinate Chemical compound [Na+].CCCCCCCCCCCC(=O)N(C)CC([O-])=O KSAVQLQVUXSOCR-UHFFFAOYSA-M 0.000 description 2
- 229940045902 sodium stearyl fumarate Drugs 0.000 description 2
- 230000003381 solubilizing effect Effects 0.000 description 2
- 229940035044 sorbitan monolaurate Drugs 0.000 description 2
- 238000001694 spray drying Methods 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- 150000003432 sterols Chemical class 0.000 description 2
- 235000003702 sterols Nutrition 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 150000003871 sulfonates Chemical class 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 239000002700 tablet coating Substances 0.000 description 2
- 238000009492 tablet coating Methods 0.000 description 2
- DKPFODGZWDEEBT-QFIAKTPHSA-N taxane Chemical class C([C@]1(C)CCC[C@@H](C)[C@H]1C1)C[C@H]2[C@H](C)CC[C@@H]1C2(C)C DKPFODGZWDEEBT-QFIAKTPHSA-N 0.000 description 2
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 2
- 125000005958 tetrahydrothienyl group Chemical group 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- RUVINXPYWBROJD-ONEGZZNKSA-N trans-anethole Chemical compound COC1=CC=C(\C=C\C)C=C1 RUVINXPYWBROJD-ONEGZZNKSA-N 0.000 description 2
- 238000000844 transformation Methods 0.000 description 2
- 230000001131 transforming effect Effects 0.000 description 2
- TUQOTMZNTHZOKS-UHFFFAOYSA-N tributylphosphine Chemical compound CCCCP(CCCC)CCCC TUQOTMZNTHZOKS-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- COIOYMYWGDAQPM-UHFFFAOYSA-N tris(2-methylphenyl)phosphane Chemical compound CC1=CC=CC=C1P(C=1C(=CC=CC=1)C)C1=CC=CC=C1C COIOYMYWGDAQPM-UHFFFAOYSA-N 0.000 description 2
- 210000001215 vagina Anatomy 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- 239000010457 zeolite Substances 0.000 description 2
- 229960002555 zidovudine Drugs 0.000 description 2
- HBOMLICNUCNMMY-XLPZGREQSA-N zidovudine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](N=[N+]=[N-])C1 HBOMLICNUCNMMY-XLPZGREQSA-N 0.000 description 2
- WWYNJERNGUHSAO-XUDSTZEESA-N (+)-Norgestrel Chemical compound O=C1CC[C@@H]2[C@H]3CC[C@](CC)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 WWYNJERNGUHSAO-XUDSTZEESA-N 0.000 description 1
- DNXHEGUUPJUMQT-UHFFFAOYSA-N (+)-estrone Natural products OC1=CC=C2C3CCC(C)(C(CC4)=O)C4C3CCC2=C1 DNXHEGUUPJUMQT-UHFFFAOYSA-N 0.000 description 1
- XEEQGYMUWCZPDN-DOMZBBRYSA-N (-)-(11S,2'R)-erythro-mefloquine Chemical compound C([C@@H]1[C@@H](O)C=2C3=CC=CC(=C3N=C(C=2)C(F)(F)F)C(F)(F)F)CCCN1 XEEQGYMUWCZPDN-DOMZBBRYSA-N 0.000 description 1
- PROQIPRRNZUXQM-UHFFFAOYSA-N (16alpha,17betaOH)-Estra-1,3,5(10)-triene-3,16,17-triol Natural products OC1=CC=C2C3CCC(C)(C(C(O)C4)O)C4C3CCC2=C1 PROQIPRRNZUXQM-UHFFFAOYSA-N 0.000 description 1
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 1
- UKSZBOKPHAQOMP-SVLSSHOZSA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 UKSZBOKPHAQOMP-SVLSSHOZSA-N 0.000 description 1
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 1
- XMAYWYJOQHXEEK-OZXSUGGESA-N (2R,4S)-ketoconazole Chemical compound C1CN(C(=O)C)CCN1C(C=C1)=CC=C1OC[C@@H]1O[C@@](CN2C=NC=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 XMAYWYJOQHXEEK-OZXSUGGESA-N 0.000 description 1
- XTYSXGHMTNTKFH-BDEHJDMKSA-N (2s)-1-[(2s,4r)-4-benzyl-2-hydroxy-5-[[(1s,2r)-2-hydroxy-2,3-dihydro-1h-inden-1-yl]amino]-5-oxopentyl]-n-tert-butyl-4-(pyridin-3-ylmethyl)piperazine-2-carboxamide;hydrate Chemical compound O.C([C@H](N(CC1)C[C@@H](O)C[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H]2C3=CC=CC=C3C[C@H]2O)C(=O)NC(C)(C)C)N1CC1=CC=CN=C1 XTYSXGHMTNTKFH-BDEHJDMKSA-N 0.000 description 1
- ITOFPJRDSCGOSA-KZLRUDJFSA-N (2s)-2-[[(4r)-4-[(3r,5r,8r,9s,10s,13r,14s,17r)-3-hydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]pentanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H](CC[C@]13C)[C@@H]2[C@@H]3CC[C@@H]1[C@H](C)CCC(=O)N[C@H](C(O)=O)CC1=CNC2=CC=CC=C12 ITOFPJRDSCGOSA-KZLRUDJFSA-N 0.000 description 1
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 1
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 1
- DNXIKVLOVZVMQF-UHFFFAOYSA-N (3beta,16beta,17alpha,18beta,20alpha)-17-hydroxy-11-methoxy-18-[(3,4,5-trimethoxybenzoyl)oxy]-yohimban-16-carboxylic acid, methyl ester Natural products C1C2CN3CCC(C4=CC=C(OC)C=C4N4)=C4C3CC2C(C(=O)OC)C(O)C1OC(=O)C1=CC(OC)=C(OC)C(OC)=C1 DNXIKVLOVZVMQF-UHFFFAOYSA-N 0.000 description 1
- ISHXLNHNDMZNMC-VTKCIJPMSA-N (3e,8r,9s,10r,13s,14s,17r)-13-ethyl-17-ethynyl-3-hydroxyimino-1,2,6,7,8,9,10,11,12,14,15,16-dodecahydrocyclopenta[a]phenanthren-17-ol Chemical compound O/N=C/1CC[C@@H]2[C@H]3CC[C@](CC)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C\1 ISHXLNHNDMZNMC-VTKCIJPMSA-N 0.000 description 1
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 1
- DIWRORZWFLOCLC-HNNXBMFYSA-N (3s)-7-chloro-5-(2-chlorophenyl)-3-hydroxy-1,3-dihydro-1,4-benzodiazepin-2-one Chemical compound N([C@H](C(NC1=CC=C(Cl)C=C11)=O)O)=C1C1=CC=CC=C1Cl DIWRORZWFLOCLC-HNNXBMFYSA-N 0.000 description 1
- RUHCWQAFCGVQJX-RVWHZBQESA-N (3s,8s,9s,10r,13r,14s,17r)-3-hydroxy-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydrocyclopenta[a]phenanthren-1-one Chemical compound C1C=C2C[C@H](O)CC(=O)[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 RUHCWQAFCGVQJX-RVWHZBQESA-N 0.000 description 1
- WRRSFOZOETZUPG-FFHNEAJVSA-N (4r,4ar,7s,7ar,12bs)-9-methoxy-3-methyl-2,4,4a,7,7a,13-hexahydro-1h-4,12-methanobenzofuro[3,2-e]isoquinoline-7-ol;hydrate Chemical compound O.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC WRRSFOZOETZUPG-FFHNEAJVSA-N 0.000 description 1
- QYIXCDOBOSTCEI-QCYZZNICSA-N (5alpha)-cholestan-3beta-ol Chemical compound C([C@@H]1CC2)[C@@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@H](C)CCCC(C)C)[C@@]2(C)CC1 QYIXCDOBOSTCEI-QCYZZNICSA-N 0.000 description 1
- WDLWHQDACQUCJR-ZAMMOSSLSA-N (6r,7r)-7-[[(2r)-2-azaniumyl-2-(4-hydroxyphenyl)acetyl]amino]-8-oxo-3-[(e)-prop-1-enyl]-5-thia-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylate Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)/C=C/C)C(O)=O)=CC=C(O)C=C1 WDLWHQDACQUCJR-ZAMMOSSLSA-N 0.000 description 1
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 1
- 125000006700 (C1-C6) alkylthio group Chemical group 0.000 description 1
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 description 1
- FDKXTQMXEQVLRF-ZHACJKMWSA-N (E)-dacarbazine Chemical compound CN(C)\N=N\c1[nH]cnc1C(N)=O FDKXTQMXEQVLRF-ZHACJKMWSA-N 0.000 description 1
- METKIMKYRPQLGS-GFCCVEGCSA-N (R)-atenolol Chemical compound CC(C)NC[C@@H](O)COC1=CC=C(CC(N)=O)C=C1 METKIMKYRPQLGS-GFCCVEGCSA-N 0.000 description 1
- TVYLLZQTGLZFBW-ZBFHGGJFSA-N (R,R)-tramadol Chemical compound COC1=CC=CC([C@]2(O)[C@H](CCCC2)CN(C)C)=C1 TVYLLZQTGLZFBW-ZBFHGGJFSA-N 0.000 description 1
- BGRJTUBHPOOWDU-NSHDSACASA-N (S)-(-)-sulpiride Chemical compound CCN1CCC[C@H]1CNC(=O)C1=CC(S(N)(=O)=O)=CC=C1OC BGRJTUBHPOOWDU-NSHDSACASA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- KOHIRBRYDXPAMZ-YHBROIRLSA-N (S,R,R,R)-nebivolol Chemical compound C1CC2=CC(F)=CC=C2O[C@H]1[C@H](O)CNC[C@@H](O)[C@H]1OC2=CC=C(F)C=C2CC1 KOHIRBRYDXPAMZ-YHBROIRLSA-N 0.000 description 1
- KYPOHTVBFVELTG-OWOJBTEDSA-N (e)-but-2-enedinitrile Chemical compound N#C\C=C\C#N KYPOHTVBFVELTG-OWOJBTEDSA-N 0.000 description 1
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 1
- TZCPCKNHXULUIY-RGULYWFUSA-N 1,2-distearoyl-sn-glycero-3-phosphoserine Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](COP(O)(=O)OC[C@H](N)C(O)=O)OC(=O)CCCCCCCCCCCCCCCCC TZCPCKNHXULUIY-RGULYWFUSA-N 0.000 description 1
- CUJPFPXNDSIBPG-UHFFFAOYSA-N 1,3-propanediyl Chemical group [CH2]C[CH2] CUJPFPXNDSIBPG-UHFFFAOYSA-N 0.000 description 1
- GGUSQTSTQSHJAH-UHFFFAOYSA-N 1-(4-chlorophenyl)-2-[4-(4-fluorobenzyl)piperidin-1-yl]ethanol Chemical compound C=1C=C(Cl)C=CC=1C(O)CN(CC1)CCC1CC1=CC=C(F)C=C1 GGUSQTSTQSHJAH-UHFFFAOYSA-N 0.000 description 1
- SFOVDSLXFUGAIV-UHFFFAOYSA-N 1-[(4-fluorophenyl)methyl]-n-piperidin-4-ylbenzimidazol-2-amine Chemical compound C1=CC(F)=CC=C1CN1C2=CC=CC=C2N=C1NC1CCNCC1 SFOVDSLXFUGAIV-UHFFFAOYSA-N 0.000 description 1
- MCCACAIVAXEFAL-UHFFFAOYSA-N 1-[2-(2,4-dichlorophenyl)-2-[(2,4-dichlorophenyl)methoxy]ethyl]imidazole;nitric acid Chemical compound O[N+]([O-])=O.ClC1=CC(Cl)=CC=C1COC(C=1C(=CC(Cl)=CC=1)Cl)CN1C=NC=C1 MCCACAIVAXEFAL-UHFFFAOYSA-N 0.000 description 1
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 1
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 1
- PKRRNTJIHGOMRC-UHFFFAOYSA-N 1-benzofuran-2-ylboronic acid Chemical compound C1=CC=C2OC(B(O)O)=CC2=C1 PKRRNTJIHGOMRC-UHFFFAOYSA-N 0.000 description 1
- ZJGSHCNIWOBHOH-UHFFFAOYSA-N 1-cyanoethylphosphonic acid Chemical compound N#CC(C)P(O)(O)=O ZJGSHCNIWOBHOH-UHFFFAOYSA-N 0.000 description 1
- PZNPLUBHRSSFHT-RRHRGVEJSA-N 1-hexadecanoyl-2-octadecanoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[C@@H](COP([O-])(=O)OCC[N+](C)(C)C)COC(=O)CCCCCCCCCCCCCCC PZNPLUBHRSSFHT-RRHRGVEJSA-N 0.000 description 1
- ARXJGSRGQADJSQ-UHFFFAOYSA-N 1-methoxypropan-2-ol Chemical compound COCC(C)O ARXJGSRGQADJSQ-UHFFFAOYSA-N 0.000 description 1
- UUFQTNFCRMXOAE-UHFFFAOYSA-N 1-methylmethylene Chemical compound C[CH] UUFQTNFCRMXOAE-UHFFFAOYSA-N 0.000 description 1
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 1
- RZRNAYUHWVFMIP-KTKRTIGZSA-N 1-oleoylglycerol Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC(O)CO RZRNAYUHWVFMIP-KTKRTIGZSA-N 0.000 description 1
- VSNHCAURESNICA-NJFSPNSNSA-N 1-oxidanylurea Chemical compound N[14C](=O)NO VSNHCAURESNICA-NJFSPNSNSA-N 0.000 description 1
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 description 1
- BFPYWIDHMRZLRN-UHFFFAOYSA-N 17alpha-ethynyl estradiol Natural products OC1=CC=C2C3CCC(C)(C(CC4)(O)C#C)C4C3CCC2=C1 BFPYWIDHMRZLRN-UHFFFAOYSA-N 0.000 description 1
- VOXZDWNPVJITMN-ZBRFXRBCSA-N 17β-estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 VOXZDWNPVJITMN-ZBRFXRBCSA-N 0.000 description 1
- DNCYBUMDUBHIJZ-UHFFFAOYSA-N 1h-pyrimidin-6-one Chemical compound O=C1C=CN=CN1 DNCYBUMDUBHIJZ-UHFFFAOYSA-N 0.000 description 1
- 125000004201 2,4-dichlorophenyl group Chemical group [H]C1=C([H])C(*)=C(Cl)C([H])=C1Cl 0.000 description 1
- 125000004215 2,4-difluorophenyl group Chemical group [H]C1=C([H])C(*)=C(F)C([H])=C1F 0.000 description 1
- GFISDBXSWQMOND-UHFFFAOYSA-N 2,5-dimethoxyoxolane Chemical compound COC1CCC(OC)O1 GFISDBXSWQMOND-UHFFFAOYSA-N 0.000 description 1
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 1
- IUVCFHHAEHNCFT-INIZCTEOSA-N 2-[(1s)-1-[4-amino-3-(3-fluoro-4-propan-2-yloxyphenyl)pyrazolo[3,4-d]pyrimidin-1-yl]ethyl]-6-fluoro-3-(3-fluorophenyl)chromen-4-one Chemical compound C1=C(F)C(OC(C)C)=CC=C1C(C1=C(N)N=CN=C11)=NN1[C@@H](C)C1=C(C=2C=C(F)C=CC=2)C(=O)C2=CC(F)=CC=C2O1 IUVCFHHAEHNCFT-INIZCTEOSA-N 0.000 description 1
- IDTQVQPVUYLMJJ-UHFFFAOYSA-N 2-[2-[2-[2-[2-(2-hydroxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethyl dodecanoate Chemical compound CCCCCCCCCCCC(=O)OCCOCCOCCOCCOCCOCCO IDTQVQPVUYLMJJ-UHFFFAOYSA-N 0.000 description 1
- NLMKTBGFQGKQEV-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-hexadecoxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound CCCCCCCCCCCCCCCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO NLMKTBGFQGKQEV-UHFFFAOYSA-N 0.000 description 1
- OIALAIQRYISUEV-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-hydroxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]e Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO OIALAIQRYISUEV-UHFFFAOYSA-N 0.000 description 1
- ZBIAKUMOEKILTF-UHFFFAOYSA-N 2-[4-[4,4-bis(4-fluorophenyl)butyl]-1-piperazinyl]-N-(2,6-dimethylphenyl)acetamide Chemical compound CC1=CC=CC(C)=C1NC(=O)CN1CCN(CCCC(C=2C=CC(F)=CC=2)C=2C=CC(F)=CC=2)CC1 ZBIAKUMOEKILTF-UHFFFAOYSA-N 0.000 description 1
- VOXBZHOHGGBLCQ-UHFFFAOYSA-N 2-amino-3,7-dihydropurine-6-thione;hydrate Chemical compound O.N1C(N)=NC(=S)C2=C1N=CN2.N1C(N)=NC(=S)C2=C1N=CN2 VOXBZHOHGGBLCQ-UHFFFAOYSA-N 0.000 description 1
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 1
- YSGASDXSLKIKOD-UHFFFAOYSA-N 2-amino-N-(1,2-diphenylpropan-2-yl)acetamide Chemical compound C=1C=CC=CC=1C(C)(NC(=O)CN)CC1=CC=CC=C1 YSGASDXSLKIKOD-UHFFFAOYSA-N 0.000 description 1
- HLCPWBZNUKCSBN-UHFFFAOYSA-N 2-aminobenzonitrile Chemical compound NC1=CC=CC=C1C#N HLCPWBZNUKCSBN-UHFFFAOYSA-N 0.000 description 1
- HUADITLKOCMHSB-AVQIMAJZSA-N 2-butan-2-yl-4-[4-[4-[4-[[(2s,4r)-2-(2,4-difluorophenyl)-2-(1,2,4-triazol-1-ylmethyl)-1,3-dioxolan-4-yl]methoxy]phenyl]piperazin-1-yl]phenyl]-1,2,4-triazol-3-one Chemical compound O=C1N(C(C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@H]3O[C@@](CN4N=CN=C4)(OC3)C=3C(=CC(F)=CC=3)F)=CC=2)C=C1 HUADITLKOCMHSB-AVQIMAJZSA-N 0.000 description 1
- CSDSSGBPEUDDEE-UHFFFAOYSA-N 2-formylpyridine Chemical compound O=CC1=CC=CC=N1 CSDSSGBPEUDDEE-UHFFFAOYSA-N 0.000 description 1
- 125000004200 2-methoxyethyl group Chemical group [H]C([H])([H])OC([H])([H])C([H])([H])* 0.000 description 1
- KIFPIAKBYOIOCS-UHFFFAOYSA-N 2-methyl-2-(trioxidanyl)propane Chemical compound CC(C)(C)OOO KIFPIAKBYOIOCS-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- YFKRLZLGVDDKAL-UHFFFAOYSA-N 3,5-dimethylbenzonitrile Chemical compound CC1=CC(C)=CC(C#N)=C1 YFKRLZLGVDDKAL-UHFFFAOYSA-N 0.000 description 1
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 1
- VGUWZCUCNQXGBU-UHFFFAOYSA-N 3-[(4-methylpiperazin-1-yl)methyl]-5-nitro-1h-indole Chemical compound C1CN(C)CCN1CC1=CNC2=CC=C([N+]([O-])=O)C=C12 VGUWZCUCNQXGBU-UHFFFAOYSA-N 0.000 description 1
- WSGYTJNNHPZFKR-UHFFFAOYSA-N 3-hydroxypropanenitrile Chemical compound OCCC#N WSGYTJNNHPZFKR-UHFFFAOYSA-N 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- PMXMIIMHBWHSKN-UHFFFAOYSA-N 3-{2-[4-(6-fluoro-1,2-benzoxazol-3-yl)piperidin-1-yl]ethyl}-9-hydroxy-2-methyl-6,7,8,9-tetrahydropyrido[1,2-a]pyrimidin-4-one Chemical compound FC1=CC=C2C(C3CCN(CC3)CCC=3C(=O)N4CCCC(O)C4=NC=3C)=NOC2=C1 PMXMIIMHBWHSKN-UHFFFAOYSA-N 0.000 description 1
- AOJJSUZBOXZQNB-VTZDEGQISA-N 4'-epidoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-VTZDEGQISA-N 0.000 description 1
- MXZMACXOMZKYHJ-UHFFFAOYSA-N 4,4-dimethyl-3-oxopentanenitrile Chemical compound CC(C)(C)C(=O)CC#N MXZMACXOMZKYHJ-UHFFFAOYSA-N 0.000 description 1
- OWYLAEYXIQKAOL-UHFFFAOYSA-N 4-(1-pyrrolidinyl)-1-(2,4,6-trimethoxyphenyl)-1-butanone Chemical compound COC1=CC(OC)=CC(OC)=C1C(=O)CCCN1CCCC1 OWYLAEYXIQKAOL-UHFFFAOYSA-N 0.000 description 1
- QXCHAADSAYQDHL-UHFFFAOYSA-N 4-[(4-chloropyrimidin-2-yl)amino]benzonitrile Chemical compound ClC1=CC=NC(NC=2C=CC(=CC=2)C#N)=N1 QXCHAADSAYQDHL-UHFFFAOYSA-N 0.000 description 1
- BBNOJNASJQRRSH-UHFFFAOYSA-N 4-[(6-oxo-1h-pyrimidin-2-yl)amino]benzonitrile Chemical compound N1C(=O)C=CN=C1NC1=CC=C(C#N)C=C1 BBNOJNASJQRRSH-UHFFFAOYSA-N 0.000 description 1
- GNELAKVSOPMFKN-UHFFFAOYSA-N 4-[5-bromo-2-(4-cyanoanilino)pyrimidin-4-yl]oxy-3,5-dimethylbenzonitrile Chemical compound CC1=CC(C#N)=CC(C)=C1OC1=NC(NC=2C=CC(=CC=2)C#N)=NC=C1Br GNELAKVSOPMFKN-UHFFFAOYSA-N 0.000 description 1
- SAVRWVQKFRBTBF-UHFFFAOYSA-N 4-[[2-amino-6-(2,6-dichlorophenoxy)pyrimidin-4-yl]amino]benzonitrile Chemical compound C=1C(OC=2C(=CC=CC=2Cl)Cl)=NC(N)=NC=1NC1=CC=C(C#N)C=C1 SAVRWVQKFRBTBF-UHFFFAOYSA-N 0.000 description 1
- BKXUZQUTEZBQIW-UHFFFAOYSA-N 4-[[4-(2,4,6-trimethylanilino)pyrimidin-2-yl]amino]benzamide Chemical compound CC1=CC(C)=CC(C)=C1NC1=CC=NC(NC=2C=CC(=CC=2)C(N)=O)=N1 BKXUZQUTEZBQIW-UHFFFAOYSA-N 0.000 description 1
- FOAAECKTFHPTHX-UHFFFAOYSA-N 4-[[4-(2,4,6-trimethylphenoxy)pyrimidin-2-yl]amino]benzonitrile Chemical compound CC1=CC(C)=CC(C)=C1OC1=CC=NC(NC=2C=CC(=CC=2)C#N)=N1 FOAAECKTFHPTHX-UHFFFAOYSA-N 0.000 description 1
- UAMROCZGVWMDQT-UHFFFAOYSA-N 4-[[4-(2,6-dibromo-4-propan-2-ylanilino)-5-methylpyrimidin-2-yl]amino]benzonitrile Chemical compound BrC1=CC(C(C)C)=CC(Br)=C1NC1=NC(NC=2C=CC(=CC=2)C#N)=NC=C1C UAMROCZGVWMDQT-UHFFFAOYSA-N 0.000 description 1
- VTRDOEBYNRKPFH-UHFFFAOYSA-N 4-[[4-(2,6-dibromo-4-propylanilino)-5-methylpyrimidin-2-yl]amino]benzonitrile Chemical compound BrC1=CC(CCC)=CC(Br)=C1NC1=NC(NC=2C=CC(=CC=2)C#N)=NC=C1C VTRDOEBYNRKPFH-UHFFFAOYSA-N 0.000 description 1
- RCBOAAIFNPVBKP-UHFFFAOYSA-N 4-[[4-(2,6-dichlorophenyl)sulfanylpyrimidin-2-yl]amino]benzonitrile Chemical compound ClC1=CC=CC(Cl)=C1SC1=CC=NC(NC=2C=CC(=CC=2)C#N)=N1 RCBOAAIFNPVBKP-UHFFFAOYSA-N 0.000 description 1
- ZLDVCBHUWLWCTP-UHFFFAOYSA-N 4-[[4-(2,6-dimethylanilino)pyrimidin-2-yl]amino]benzonitrile Chemical compound CC1=CC=CC(C)=C1NC1=CC=NC(NC=2C=CC(=CC=2)C#N)=N1 ZLDVCBHUWLWCTP-UHFFFAOYSA-N 0.000 description 1
- ULHSEERDVMXBIL-UHFFFAOYSA-N 4-[[4-(n,2,4,6-tetramethylanilino)pyrimidin-2-yl]amino]benzonitrile Chemical compound CC=1C=C(C)C=C(C)C=1N(C)C(N=1)=CC=NC=1NC1=CC=C(C#N)C=C1 ULHSEERDVMXBIL-UHFFFAOYSA-N 0.000 description 1
- BYPMIFBQMHPRFV-UHFFFAOYSA-N 4-[[4-[(2,4-dichlorophenyl)methyl]-6-(4-hydroxybutylamino)pyrimidin-2-yl]amino]benzonitrile Chemical compound N=1C(NC=2C=CC(=CC=2)C#N)=NC(NCCCCO)=CC=1CC1=CC=C(Cl)C=C1Cl BYPMIFBQMHPRFV-UHFFFAOYSA-N 0.000 description 1
- SWUCAIPJSDZLTL-UHFFFAOYSA-N 4-[[4-[(2,6-dichlorophenyl)methyl]-6-(3-hydroxypropylamino)pyrimidin-2-yl]amino]benzonitrile Chemical compound N=1C(NC=2C=CC(=CC=2)C#N)=NC(NCCCO)=CC=1CC1=C(Cl)C=CC=C1Cl SWUCAIPJSDZLTL-UHFFFAOYSA-N 0.000 description 1
- KILCEDZMLBYTRS-UHFFFAOYSA-N 4-[[4-[(2,6-dichlorophenyl)methyl]-6-[(2-hydroxy-2-phenylethyl)amino]pyrimidin-2-yl]amino]benzonitrile Chemical compound C=1C=CC=CC=1C(O)CNC(N=C(NC=1C=CC(=CC=1)C#N)N=1)=CC=1CC1=C(Cl)C=CC=C1Cl KILCEDZMLBYTRS-UHFFFAOYSA-N 0.000 description 1
- QATGXJWJNFUAGP-UHFFFAOYSA-N 4-[[4-[2,6-dichloro-4-(trifluoromethoxy)anilino]pyrimidin-2-yl]amino]benzonitrile Chemical compound ClC1=CC(OC(F)(F)F)=CC(Cl)=C1NC1=CC=NC(NC=2C=CC(=CC=2)C#N)=N1 QATGXJWJNFUAGP-UHFFFAOYSA-N 0.000 description 1
- OJJVULINVLFCDX-UHFFFAOYSA-N 4-[[4-amino-6-[(2,6-dichlorophenyl)methyl]pyrimidin-2-yl]amino]benzonitrile Chemical compound N=1C(NC=2C=CC(=CC=2)C#N)=NC(N)=CC=1CC1=C(Cl)C=CC=C1Cl OJJVULINVLFCDX-UHFFFAOYSA-N 0.000 description 1
- VKQKEROEGYSHIY-UHFFFAOYSA-N 4-[[5-bromo-2-(4-cyanoanilino)pyrimidin-4-yl]amino]-3,5-dimethylbenzonitrile Chemical compound CC1=CC(C#N)=CC(C)=C1NC1=NC(NC=2C=CC(=CC=2)C#N)=NC=C1Br VKQKEROEGYSHIY-UHFFFAOYSA-N 0.000 description 1
- YIYBPEDZAUFQLO-UHFFFAOYSA-N 4-amino-3-chlorobenzoic acid Chemical compound NC1=CC=C(C(O)=O)C=C1Cl YIYBPEDZAUFQLO-UHFFFAOYSA-N 0.000 description 1
- YPELFRMCRYSPKZ-UHFFFAOYSA-N 4-amino-5-chloro-2-ethoxy-N-({4-[(4-fluorophenyl)methyl]morpholin-2-yl}methyl)benzamide Chemical compound CCOC1=CC(N)=C(Cl)C=C1C(=O)NCC1OCCN(CC=2C=CC(F)=CC=2)C1 YPELFRMCRYSPKZ-UHFFFAOYSA-N 0.000 description 1
- BVPWJMCABCPUQY-UHFFFAOYSA-N 4-amino-5-chloro-2-methoxy-N-[1-(phenylmethyl)-4-piperidinyl]benzamide Chemical compound COC1=CC(N)=C(Cl)C=C1C(=O)NC1CCN(CC=2C=CC=CC=2)CC1 BVPWJMCABCPUQY-UHFFFAOYSA-N 0.000 description 1
- VUTBELPREDJDDH-UHFFFAOYSA-N 4-amino-5-hydroxymethyl-2-methylpyrimidine Chemical compound CC1=NC=C(CO)C(N)=N1 VUTBELPREDJDDH-UHFFFAOYSA-N 0.000 description 1
- 125000004800 4-bromophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Br 0.000 description 1
- BJJSUOOEBCCLNY-UHFFFAOYSA-N 4-iodo-2,6-dimethylaniline Chemical compound CC1=CC(I)=CC(C)=C1N BJJSUOOEBCCLNY-UHFFFAOYSA-N 0.000 description 1
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 1
- BUFHUWCYNTVDHM-UHFFFAOYSA-N 4-octadecanoyloxy-4-oxobutanoic acid;propane-1,2-diol Chemical compound CC(O)CO.CCCCCCCCCCCCCCCCCC(=O)OC(=O)CCC(O)=O BUFHUWCYNTVDHM-UHFFFAOYSA-N 0.000 description 1
- WJTFHWXMITZNHS-UHFFFAOYSA-N 5-bromofuran-2-carbaldehyde Chemical compound BrC1=CC=C(C=O)O1 WJTFHWXMITZNHS-UHFFFAOYSA-N 0.000 description 1
- ZNFFMCYSMBXZQU-NSHDSACASA-N 5-chloro-8-methyl-7-(3-methyl-but-2-enyl)-6,7,8,9-tetrahydro-2h-2,7,9a-triaza-benzo[cd]azulene-1-thione Chemical compound C1N(CC=C(C)C)[C@@H](C)CN2C(=S)NC3=CC=C(Cl)C1=C32 ZNFFMCYSMBXZQU-NSHDSACASA-N 0.000 description 1
- SUBDBMMJDZJVOS-UHFFFAOYSA-N 5-methoxy-2-{[(4-methoxy-3,5-dimethylpyridin-2-yl)methyl]sulfinyl}-1H-benzimidazole Chemical compound N=1C2=CC(OC)=CC=C2NC=1S(=O)CC1=NC=C(C)C(OC)=C1C SUBDBMMJDZJVOS-UHFFFAOYSA-N 0.000 description 1
- WYWHKKSPHMUBEB-UHFFFAOYSA-N 6-Mercaptoguanine Natural products N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 1
- SLXKOJJOQWFEFD-UHFFFAOYSA-N 6-aminohexanoic acid Chemical compound NCCCCCC(O)=O SLXKOJJOQWFEFD-UHFFFAOYSA-N 0.000 description 1
- GMMWNTHAIOJBSD-UHFFFAOYSA-N 6-chloro-4-n-(2,3-dimethylphenyl)-2-n,2-n-dimethylpyrimidine-2,4-diamine Chemical compound CN(C)C1=NC(Cl)=CC(NC=2C(=C(C)C=CC=2)C)=N1 GMMWNTHAIOJBSD-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical class O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 1
- BUNGCZLFHHXKBX-UHFFFAOYSA-N 8-methoxypsoralen Natural products C1=CC(=O)OC2=C1C=C1CCOC1=C2OC BUNGCZLFHHXKBX-UHFFFAOYSA-N 0.000 description 1
- GSDSWSVVBLHKDQ-UHFFFAOYSA-N 9-fluoro-3-methyl-10-(4-methylpiperazin-1-yl)-7-oxo-2,3-dihydro-7H-[1,4]oxazino[2,3,4-ij]quinoline-6-carboxylic acid Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)COC3=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-UHFFFAOYSA-N 0.000 description 1
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 102220487426 Actin-related protein 2/3 complex subunit 3_K15M_mutation Human genes 0.000 description 1
- 241000380873 Algon Species 0.000 description 1
- WKEMJKQOLOHJLZ-UHFFFAOYSA-N Almogran Chemical compound C1=C2C(CCN(C)C)=CNC2=CC=C1CS(=O)(=O)N1CCCC1 WKEMJKQOLOHJLZ-UHFFFAOYSA-N 0.000 description 1
- 235000019489 Almond oil Nutrition 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 229930183010 Amphotericin Natural products 0.000 description 1
- QGGFZZLFKABGNL-UHFFFAOYSA-N Amphotericin A Natural products OC1C(N)C(O)C(C)OC1OC1C=CC=CC=CC=CCCC=CC=CC(C)C(O)C(C)C(C)OC(=O)CC(O)CC(O)CCC(O)C(O)CC(O)CC(O)(CC(O)C2C(O)=O)OC2C1 QGGFZZLFKABGNL-UHFFFAOYSA-N 0.000 description 1
- 101710095342 Apolipoprotein B Proteins 0.000 description 1
- 102100040202 Apolipoprotein B-100 Human genes 0.000 description 1
- CEUORZQYGODEFX-UHFFFAOYSA-N Aripirazole Chemical compound ClC1=CC=CC(N2CCN(CCCCOC=3C=C4NC(=O)CCC4=CC=3)CC2)=C1Cl CEUORZQYGODEFX-UHFFFAOYSA-N 0.000 description 1
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 description 1
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 description 1
- 108010081589 Becaplermin Proteins 0.000 description 1
- KUVIULQEHSCUHY-XYWKZLDCSA-N Beclometasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)COC(=O)CC)(OC(=O)CC)[C@@]1(C)C[C@@H]2O KUVIULQEHSCUHY-XYWKZLDCSA-N 0.000 description 1
- 108010006654 Bleomycin Proteins 0.000 description 1
- 208000003508 Botulism Diseases 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- RKLNONIVDFXQRX-UHFFFAOYSA-N Bromperidol Chemical compound C1CC(O)(C=2C=CC(Br)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 RKLNONIVDFXQRX-UHFFFAOYSA-N 0.000 description 1
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- LZZXSPGXTIPUBP-GDNBJRDFSA-N C/C(/C#N)=C/c(cc1C)cc(C)c1NC1=NC(Nc(cc2)ccc2C#N)=NCC1 Chemical compound C/C(/C#N)=C/c(cc1C)cc(C)c1NC1=NC(Nc(cc2)ccc2C#N)=NCC1 LZZXSPGXTIPUBP-GDNBJRDFSA-N 0.000 description 1
- OJRUSAPKCPIVBY-KQYNXXCUSA-N C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N Chemical compound C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N OJRUSAPKCPIVBY-KQYNXXCUSA-N 0.000 description 1
- XBMCSYBBSLIDLV-UHFFFAOYSA-N CC(C)C(c(cc1C)cc(C)c1Nc1ccnc(Nc(cc2)ccc2C#C)n1)=C Chemical compound CC(C)C(c(cc1C)cc(C)c1Nc1ccnc(Nc(cc2)ccc2C#C)n1)=C XBMCSYBBSLIDLV-UHFFFAOYSA-N 0.000 description 1
- PJOUCZJPTOHSOI-BNCCVWRVSA-N CC1(Nc(cc2)ccc2C#N)N=CC=C(N/C(/C(C)=C)=C\C)N1 Chemical compound CC1(Nc(cc2)ccc2C#N)N=CC=C(N/C(/C(C)=C)=C\C)N1 PJOUCZJPTOHSOI-BNCCVWRVSA-N 0.000 description 1
- KZJGHZSEUPRSEA-MDWZMJQESA-N CCCCN(C)C(/C=C/c(cc1C)cc(C)c1Oc1ccnc(Nc(cc2)ccc2NC)n1)=O Chemical compound CCCCN(C)C(/C=C/c(cc1C)cc(C)c1Oc1ccnc(Nc(cc2)ccc2NC)n1)=O KZJGHZSEUPRSEA-MDWZMJQESA-N 0.000 description 1
- UHNRLQRZRNKOKU-UHFFFAOYSA-N CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O Chemical compound CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O UHNRLQRZRNKOKU-UHFFFAOYSA-N 0.000 description 1
- 210000004366 CD4-positive T-lymphocyte Anatomy 0.000 description 1
- QAGYKUNXZHXKMR-UHFFFAOYSA-N CPD000469186 Natural products CC1=C(O)C=CC=C1C(=O)NC(C(O)CN1C(CC2CCCCC2C1)C(=O)NC(C)(C)C)CSC1=CC=CC=C1 QAGYKUNXZHXKMR-UHFFFAOYSA-N 0.000 description 1
- 229940127291 Calcium channel antagonist Drugs 0.000 description 1
- KLWPJMFMVPTNCC-UHFFFAOYSA-N Camptothecin Natural products CCC1(O)C(=O)OCC2=C1C=C3C4Nc5ccccc5C=C4CN3C2=O KLWPJMFMVPTNCC-UHFFFAOYSA-N 0.000 description 1
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 description 1
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 1
- DLGOEMSEDOSKAD-UHFFFAOYSA-N Carmustine Chemical compound ClCCNC(=O)N(N=O)CCCl DLGOEMSEDOSKAD-UHFFFAOYSA-N 0.000 description 1
- 240000000467 Carum carvi Species 0.000 description 1
- 235000005747 Carum carvi Nutrition 0.000 description 1
- ZGMPSYYZUSBNNH-SNAWJCMRSA-N Cc1cc(/C=C/[O]=C)cc(C)c1NI Chemical compound Cc1cc(/C=C/[O]=C)cc(C)c1NI ZGMPSYYZUSBNNH-SNAWJCMRSA-N 0.000 description 1
- CBWFKOPWWJCXIG-UHBFCERESA-N Cc1cc(/C=N\NC(c2ccncc2)=O)cc(C)c1Nc1ccnc(Nc(cc2)ccc2NC)n1 Chemical compound Cc1cc(/C=N\NC(c2ccncc2)=O)cc(C)c1Nc1ccnc(Nc(cc2)ccc2NC)n1 CBWFKOPWWJCXIG-UHBFCERESA-N 0.000 description 1
- KEJCWVGMRLCZQQ-YJBYXUATSA-N Cefuroxime axetil Chemical compound N([C@@H]1C(N2C(=C(COC(N)=O)CS[C@@H]21)C(=O)OC(C)OC(C)=O)=O)C(=O)\C(=N/OC)C1=CC=CO1 KEJCWVGMRLCZQQ-YJBYXUATSA-N 0.000 description 1
- ZKLPARSLTMPFCP-UHFFFAOYSA-N Cetirizine Chemical compound C1CN(CCOCC(=O)O)CCN1C(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-UHFFFAOYSA-N 0.000 description 1
- LZZYPRNAOMGNLH-UHFFFAOYSA-M Cetrimonium bromide Chemical compound [Br-].CCCCCCCCCCCCCCCC[N+](C)(C)C LZZYPRNAOMGNLH-UHFFFAOYSA-M 0.000 description 1
- NPBVQXIMTZKSBA-UHFFFAOYSA-N Chavibetol Natural products COC1=CC=C(CC=C)C=C1O NPBVQXIMTZKSBA-UHFFFAOYSA-N 0.000 description 1
- GHXZTYHSJHQHIJ-UHFFFAOYSA-N Chlorhexidine Chemical compound C=1C=C(Cl)C=CC=1NC(N)=NC(N)=NCCCCCCN=C(N)N=C(N)NC1=CC=C(Cl)C=C1 GHXZTYHSJHQHIJ-UHFFFAOYSA-N 0.000 description 1
- QMBJSIBWORFWQT-DFXBJWIESA-N Chlormadinone acetate Chemical compound C1=C(Cl)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 QMBJSIBWORFWQT-DFXBJWIESA-N 0.000 description 1
- JZUFKLXOESDKRF-UHFFFAOYSA-N Chlorothiazide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC2=C1NCNS2(=O)=O JZUFKLXOESDKRF-UHFFFAOYSA-N 0.000 description 1
- 244000037364 Cinnamomum aromaticum Species 0.000 description 1
- 235000014489 Cinnamomum aromaticum Nutrition 0.000 description 1
- 235000005979 Citrus limon Nutrition 0.000 description 1
- 244000131522 Citrus pyriformis Species 0.000 description 1
- BNAFBXLMOUQHIU-UHFFFAOYSA-N ClC1=CC=C(C=C1)C1(NC=CC(=N1)NC1=C(C=C(C=C1C)C)C)N Chemical compound ClC1=CC=C(C=C1)C1(NC=CC(=N1)NC1=C(C=C(C=C1C)C)C)N BNAFBXLMOUQHIU-UHFFFAOYSA-N 0.000 description 1
- PTOAARAWEBMLNO-KVQBGUIXSA-N Cladribine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)O1 PTOAARAWEBMLNO-KVQBGUIXSA-N 0.000 description 1
- GDLIGKIOYRNHDA-UHFFFAOYSA-N Clomipramine Chemical compound C1CC2=CC=C(Cl)C=C2N(CCCN(C)C)C2=CC=CC=C21 GDLIGKIOYRNHDA-UHFFFAOYSA-N 0.000 description 1
- 244000060011 Cocos nucifera Species 0.000 description 1
- 235000013162 Cocos nucifera Nutrition 0.000 description 1
- 229940126657 Compound 17 Drugs 0.000 description 1
- XZMCDFZZKTWFGF-UHFFFAOYSA-N Cyanamide Chemical compound NC#N XZMCDFZZKTWFGF-UHFFFAOYSA-N 0.000 description 1
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 1
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 1
- 108010036949 Cyclosporine Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- 206010012289 Dementia Diseases 0.000 description 1
- HCYAFALTSJYZDH-UHFFFAOYSA-N Desimpramine Chemical compound C1CC2=CC=CC=C2N(CCCNC)C2=CC=CC=C21 HCYAFALTSJYZDH-UHFFFAOYSA-N 0.000 description 1
- BXZVVICBKDXVGW-NKWVEPMBSA-N Didanosine Chemical compound O1[C@H](CO)CC[C@@H]1N1C(NC=NC2=O)=C2N=C1 BXZVVICBKDXVGW-NKWVEPMBSA-N 0.000 description 1
- WDJUZGPOPHTGOT-OAXVISGBSA-N Digitoxin Natural products O([C@H]1[C@@H](C)O[C@@H](O[C@@H]2C[C@@H]3[C@@](C)([C@@H]4[C@H]([C@]5(O)[C@@](C)([C@H](C6=CC(=O)OC6)CC5)CC4)CC3)CC2)C[C@H]1O)[C@H]1O[C@@H](C)[C@H](O[C@H]2O[C@@H](C)[C@@H](O)[C@@H](O)C2)[C@@H](O)C1 WDJUZGPOPHTGOT-OAXVISGBSA-N 0.000 description 1
- LTMHDMANZUZIPE-AMTYYWEZSA-N Digoxin Natural products O([C@H]1[C@H](C)O[C@H](O[C@@H]2C[C@@H]3[C@@](C)([C@@H]4[C@H]([C@]5(O)[C@](C)([C@H](O)C4)[C@H](C4=CC(=O)OC4)CC5)CC3)CC2)C[C@@H]1O)[C@H]1O[C@H](C)[C@@H](O[C@H]2O[C@@H](C)[C@H](O)[C@@H](O)C2)[C@@H](O)C1 LTMHDMANZUZIPE-AMTYYWEZSA-N 0.000 description 1
- IIUZTXTZRGLYTI-UHFFFAOYSA-N Dihydrogriseofulvin Natural products COC1CC(=O)CC(C)C11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 IIUZTXTZRGLYTI-UHFFFAOYSA-N 0.000 description 1
- 108010049047 Echinocandins Proteins 0.000 description 1
- XPOQHMRABVBWPR-UHFFFAOYSA-N Efavirenz Natural products O1C(=O)NC2=CC=C(Cl)C=C2C1(C(F)(F)F)C#CC1CC1 XPOQHMRABVBWPR-UHFFFAOYSA-N 0.000 description 1
- 240000002943 Elettaria cardamomum Species 0.000 description 1
- 108010061435 Enalapril Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- HTIJFSOGRVMCQR-UHFFFAOYSA-N Epirubicin Natural products COc1cccc2C(=O)c3c(O)c4CC(O)(CC(OC5CC(N)C(=O)C(C)O5)c4c(O)c3C(=O)c12)C(=O)CO HTIJFSOGRVMCQR-UHFFFAOYSA-N 0.000 description 1
- 102000003951 Erythropoietin Human genes 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- DNXHEGUUPJUMQT-CBZIJGRNSA-N Estrone Chemical compound OC1=CC=C2[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CCC2=C1 DNXHEGUUPJUMQT-CBZIJGRNSA-N 0.000 description 1
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 1
- BFPYWIDHMRZLRN-SLHNCBLASA-N Ethinyl estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 BFPYWIDHMRZLRN-SLHNCBLASA-N 0.000 description 1
- 229920003134 Eudragit® polymer Polymers 0.000 description 1
- 239000005770 Eugenol Substances 0.000 description 1
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 1
- PLDUPXSUYLZYBN-UHFFFAOYSA-N Fluphenazine Chemical compound C1CN(CCO)CCN1CCCN1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C21 PLDUPXSUYLZYBN-UHFFFAOYSA-N 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-N Formic acid Chemical compound OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 1
- 206010017533 Fungal infection Diseases 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- JZNWSCPGTDBMEW-UHFFFAOYSA-N Glycerophosphorylethanolamin Natural products NCCOP(O)(=O)OCC(O)CO JZNWSCPGTDBMEW-UHFFFAOYSA-N 0.000 description 1
- ZWZWYGMENQVNFU-UHFFFAOYSA-N Glycerophosphorylserin Natural products OC(=O)C(N)COP(O)(=O)OCC(O)CO ZWZWYGMENQVNFU-UHFFFAOYSA-N 0.000 description 1
- 108010015899 Glycopeptides Proteins 0.000 description 1
- 102000002068 Glycopeptides Human genes 0.000 description 1
- UXWOXTQWVMFRSE-UHFFFAOYSA-N Griseoviridin Natural products O=C1OC(C)CC=C(C(NCC=CC=CC(O)CC(O)C2)=O)SCC1NC(=O)C1=COC2=N1 UXWOXTQWVMFRSE-UHFFFAOYSA-N 0.000 description 1
- 208000031886 HIV Infections Diseases 0.000 description 1
- 208000037357 HIV infectious disease Diseases 0.000 description 1
- 229940122440 HIV protease inhibitor Drugs 0.000 description 1
- 238000004965 Hartree-Fock calculation Methods 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000999322 Homo sapiens Putative insulin-like growth factor 2 antisense gene protein Proteins 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- VSNHCAURESNICA-UHFFFAOYSA-N Hydroxyurea Chemical compound NC(=O)NO VSNHCAURESNICA-UHFFFAOYSA-N 0.000 description 1
- STECJAGHUSJQJN-GAUPFVANSA-N Hyoscine Natural products C1([C@H](CO)C(=O)OC2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 STECJAGHUSJQJN-GAUPFVANSA-N 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- XDXDZDZNSLXDNA-TZNDIEGXSA-N Idarubicin Chemical compound C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(C)=O)C1 XDXDZDZNSLXDNA-TZNDIEGXSA-N 0.000 description 1
- XDXDZDZNSLXDNA-UHFFFAOYSA-N Idarubicin Natural products C1C(N)C(O)C(C)OC1OC1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2CC(O)(C(C)=O)C1 XDXDZDZNSLXDNA-UHFFFAOYSA-N 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102100034343 Integrase Human genes 0.000 description 1
- PWWVAXIEGOYWEE-UHFFFAOYSA-N Isophenergan Chemical compound C1=CC=C2N(CC(C)N(C)C)C3=CC=CC=C3SC2=C1 PWWVAXIEGOYWEE-UHFFFAOYSA-N 0.000 description 1
- KLDXJTOLSGUMSJ-JGWLITMVSA-N Isosorbide Chemical compound O[C@@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 KLDXJTOLSGUMSJ-JGWLITMVSA-N 0.000 description 1
- KJHKTHWMRKYKJE-SUGCFTRWSA-N Kaletra Chemical compound N1([C@@H](C(C)C)C(=O)N[C@H](C[C@H](O)[C@H](CC=2C=CC=CC=2)NC(=O)COC=2C(=CC=CC=2C)C)CC=2C=CC=CC=2)CCCNC1=O KJHKTHWMRKYKJE-SUGCFTRWSA-N 0.000 description 1
- 102100020880 Kit ligand Human genes 0.000 description 1
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 1
- WTDRDQBEARUVNC-UHFFFAOYSA-N L-Dopa Natural products OC(=O)C(N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-UHFFFAOYSA-N 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 239000005517 L01XE01 - Imatinib Substances 0.000 description 1
- MKXZASYAUGDDCJ-SZMVWBNQSA-N LSM-2525 Chemical compound C1CCC[C@H]2[C@@]3([H])N(C)CC[C@]21C1=CC(OC)=CC=C1C3 MKXZASYAUGDDCJ-SZMVWBNQSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- NNJVILVZKWQKPM-UHFFFAOYSA-N Lidocaine Chemical compound CCN(CC)CC(=O)NC1=C(C)C=CC=C1C NNJVILVZKWQKPM-UHFFFAOYSA-N 0.000 description 1
- OJMMVQQUTAEWLP-UHFFFAOYSA-N Lincomycin Natural products CN1CC(CCC)CC1C(=O)NC(C(C)O)C1C(O)C(O)C(O)C(SC)O1 OJMMVQQUTAEWLP-UHFFFAOYSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- GQYIWUVLTXOXAJ-UHFFFAOYSA-N Lomustine Chemical compound ClCCN(N=O)C(=O)NC1CCCCC1 GQYIWUVLTXOXAJ-UHFFFAOYSA-N 0.000 description 1
- YNVGQYHLRCDXFQ-XGXHKTLJSA-N Lynestrenol Chemical compound C1CC[C@@H]2[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 YNVGQYHLRCDXFQ-XGXHKTLJSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229920000877 Melamine resin Polymers 0.000 description 1
- 244000246386 Mentha pulegium Species 0.000 description 1
- 235000016257 Mentha pulegium Nutrition 0.000 description 1
- 235000004357 Mentha x piperita Nutrition 0.000 description 1
- QXKHYNVANLEOEG-UHFFFAOYSA-N Methoxsalen Chemical compound C1=CC(=O)OC2=C1C=C1C=COC1=C2OC QXKHYNVANLEOEG-UHFFFAOYSA-N 0.000 description 1
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 description 1
- HWGBHCRJGXAGEU-UHFFFAOYSA-N Methylthiouracil Chemical compound CC1=CC(=O)NC(=S)N1 HWGBHCRJGXAGEU-UHFFFAOYSA-N 0.000 description 1
- UEQUQVLFIPOEMF-UHFFFAOYSA-N Mianserin Chemical compound C1C2=CC=CC=C2N2CCN(C)CC2C2=CC=CC=C21 UEQUQVLFIPOEMF-UHFFFAOYSA-N 0.000 description 1
- ZFMITUMMTDLWHR-UHFFFAOYSA-N Minoxidil Chemical compound NC1=[N+]([O-])C(N)=CC(N2CCCCC2)=N1 ZFMITUMMTDLWHR-UHFFFAOYSA-N 0.000 description 1
- PCZOHLXUXFIOCF-UHFFFAOYSA-N Monacolin X Natural products C12C(OC(=O)C(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 PCZOHLXUXFIOCF-UHFFFAOYSA-N 0.000 description 1
- 101100136062 Mycobacterium tuberculosis (strain ATCC 25618 / H37Rv) PE10 gene Proteins 0.000 description 1
- 208000031888 Mycoses Diseases 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- STECJAGHUSJQJN-UHFFFAOYSA-N N-Methyl-scopolamin Natural products C1C(C2C3O2)N(C)C3CC1OC(=O)C(CO)C1=CC=CC=C1 STECJAGHUSJQJN-UHFFFAOYSA-N 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- BLXXJMDCKKHMKV-UHFFFAOYSA-N Nabumetone Chemical compound C1=C(CCC(C)=O)C=CC2=CC(OC)=CC=C21 BLXXJMDCKKHMKV-UHFFFAOYSA-N 0.000 description 1
- DDUHZTYCFQRHIY-UHFFFAOYSA-N Negwer: 6874 Natural products COC1=CC(=O)CC(C)C11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 DDUHZTYCFQRHIY-UHFFFAOYSA-N 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- ZBBHBTPTTSWHBA-UHFFFAOYSA-N Nicardipine Chemical compound COC(=O)C1=C(C)NC(C)=C(C(=O)OCCN(C)CC=2C=CC=CC=2)C1C1=CC=CC([N+]([O-])=O)=C1 ZBBHBTPTTSWHBA-UHFFFAOYSA-N 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- IOVCWXUNBOPUCH-UHFFFAOYSA-M Nitrite anion Chemical compound [O-]N=O IOVCWXUNBOPUCH-UHFFFAOYSA-M 0.000 description 1
- SNIOPGDIGTZGOP-UHFFFAOYSA-N Nitroglycerin Chemical compound [O-][N+](=O)OCC(O[N+]([O-])=O)CO[N+]([O-])=O SNIOPGDIGTZGOP-UHFFFAOYSA-N 0.000 description 1
- IGFHQQFPSIBGKE-UHFFFAOYSA-N Nonylphenol Natural products CCCCCCCCCC1=CC=C(O)C=C1 IGFHQQFPSIBGKE-UHFFFAOYSA-N 0.000 description 1
- ICTXHFFSOAJUMG-SLHNCBLASA-N Norethynodrel Chemical compound C1CC(=O)CC2=C1[C@H]1CC[C@](C)([C@](CC3)(O)C#C)[C@@H]3[C@@H]1CC2 ICTXHFFSOAJUMG-SLHNCBLASA-N 0.000 description 1
- 235000019502 Orange oil Nutrition 0.000 description 1
- BRUQQQPBMZOVGD-XFKAJCMBSA-N Oxycodone Chemical compound O=C([C@@H]1O2)CC[C@@]3(O)[C@H]4CC5=CC=C(OC)C2=C5[C@@]13CCN4C BRUQQQPBMZOVGD-XFKAJCMBSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- TZRXHJWUDPFEEY-UHFFFAOYSA-N Pentaerythritol Tetranitrate Chemical compound [O-][N+](=O)OCC(CO[N+]([O-])=O)(CO[N+]([O-])=O)CO[N+]([O-])=O TZRXHJWUDPFEEY-UHFFFAOYSA-N 0.000 description 1
- 239000000026 Pentaerythritol tetranitrate Substances 0.000 description 1
- KFSLWBXXFJQRDL-UHFFFAOYSA-N Peracetic acid Chemical compound CC(=O)OO KFSLWBXXFJQRDL-UHFFFAOYSA-N 0.000 description 1
- 241000264091 Petrus Species 0.000 description 1
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 1
- CXOFVDLJLONNDW-UHFFFAOYSA-N Phenytoin Chemical compound N1C(=O)NC(=O)C1(C=1C=CC=CC=1)C1=CC=CC=C1 CXOFVDLJLONNDW-UHFFFAOYSA-N 0.000 description 1
- PIJVFDBKTWXHHD-UHFFFAOYSA-N Physostigmine Natural products C12=CC(OC(=O)NC)=CC=C2N(C)C2C1(C)CCN2C PIJVFDBKTWXHHD-UHFFFAOYSA-N 0.000 description 1
- 102100040990 Platelet-derived growth factor subunit B Human genes 0.000 description 1
- 229920002511 Poloxamer 237 Polymers 0.000 description 1
- 229920002582 Polyethylene Glycol 600 Polymers 0.000 description 1
- 229920001231 Polysaccharide peptide Polymers 0.000 description 1
- TUZYXOIXSAXUGO-UHFFFAOYSA-N Pravastatin Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(O)C=C21 TUZYXOIXSAXUGO-UHFFFAOYSA-N 0.000 description 1
- 244000028344 Primula vulgaris Species 0.000 description 1
- 235000016311 Primula vulgaris Nutrition 0.000 description 1
- HDSBZMRLPLPFLQ-UHFFFAOYSA-N Propylene glycol alginate Chemical compound OC1C(O)C(OC)OC(C(O)=O)C1OC1C(O)C(O)C(C)C(C(=O)OCC(C)O)O1 HDSBZMRLPLPFLQ-UHFFFAOYSA-N 0.000 description 1
- KNAHARQHSZJURB-UHFFFAOYSA-N Propylthiouracile Chemical compound CCCC1=CC(=O)NC(=S)N1 KNAHARQHSZJURB-UHFFFAOYSA-N 0.000 description 1
- UVMRYBDEERADNV-UHFFFAOYSA-N Pseudoeugenol Natural products COC1=CC(C(C)=C)=CC=C1O UVMRYBDEERADNV-UHFFFAOYSA-N 0.000 description 1
- 102100036485 Putative insulin-like growth factor 2 antisense gene protein Human genes 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- LCQMZZCPPSWADO-UHFFFAOYSA-N Reserpilin Natural products COC(=O)C1COCC2CN3CCc4c([nH]c5cc(OC)c(OC)cc45)C3CC12 LCQMZZCPPSWADO-UHFFFAOYSA-N 0.000 description 1
- QEVHRUUCFGRFIF-SFWBKIHZSA-N Reserpine Natural products O=C(OC)[C@@H]1[C@H](OC)[C@H](OC(=O)c2cc(OC)c(OC)c(OC)c2)C[C@H]2[C@@H]1C[C@H]1N(C2)CCc2c3c([nH]c12)cc(OC)cc3 QEVHRUUCFGRFIF-SFWBKIHZSA-N 0.000 description 1
- 235000004443 Ricinus communis Nutrition 0.000 description 1
- NCDNCNXCDXHOMX-UHFFFAOYSA-N Ritonavir Natural products C=1C=CC=CC=1CC(NC(=O)OCC=1SC=NC=1)C(O)CC(CC=1C=CC=CC=1)NC(=O)C(C(C)C)NC(=O)N(C)CC1=CSC(C(C)C)=N1 NCDNCNXCDXHOMX-UHFFFAOYSA-N 0.000 description 1
- XSVMFMHYUFZWBK-NSHDSACASA-N Rivastigmine Chemical compound CCN(C)C(=O)OC1=CC=CC([C@H](C)N(C)C)=C1 XSVMFMHYUFZWBK-NSHDSACASA-N 0.000 description 1
- 241001620634 Roger Species 0.000 description 1
- QCNVFAQSXRNCES-UHFFFAOYSA-L S(=O)(=O)(O)C(C(=O)OCCCCCCCC)CC(=O)[O-].[Na+].[Na+].C(CCCCCCC)OC(C(CC(=O)[O-])S(=O)(=O)O)=O Chemical compound S(=O)(=O)(O)C(C(=O)OCCCCCCCC)CC(=O)[O-].[Na+].[Na+].C(CCCCCCC)OC(C(CC(=O)[O-])S(=O)(=O)O)=O QCNVFAQSXRNCES-UHFFFAOYSA-L 0.000 description 1
- RYMZZMVNJRMUDD-UHFFFAOYSA-N SJ000286063 Natural products C12C(OC(=O)C(C)(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 RYMZZMVNJRMUDD-UHFFFAOYSA-N 0.000 description 1
- 108010077895 Sarcosine Proteins 0.000 description 1
- LPMRCCNDNGONCD-RITPCOANSA-N Selfotel Chemical compound OC(=O)[C@@H]1C[C@H](CP(O)(O)=O)CCN1 LPMRCCNDNGONCD-RITPCOANSA-N 0.000 description 1
- 229910004298 SiO 2 Inorganic materials 0.000 description 1
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 1
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 1
- BCKXLBQYZLBQEK-KVVVOXFISA-M Sodium oleate Chemical compound [Na+].CCCCCCCC\C=C/CCCCCCCC([O-])=O BCKXLBQYZLBQEK-KVVVOXFISA-M 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- XNKLLVCARDGLGL-JGVFFNPUSA-N Stavudine Chemical compound O=C1NC(=O)C(C)=CN1[C@H]1C=C[C@@H](CO)O1 XNKLLVCARDGLGL-JGVFFNPUSA-N 0.000 description 1
- 239000001833 Succinylated monoglyceride Substances 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- XZAGBDSOKNXTDT-UHFFFAOYSA-N Sucrose monopalmitate Chemical compound CCCCCCCCCCCCCCCC(O)=O.OC1C(O)C(CO)OC1(CO)OC1C(O)C(O)C(O)C(CO)O1 XZAGBDSOKNXTDT-UHFFFAOYSA-N 0.000 description 1
- SEQDDYPDSLOBDC-UHFFFAOYSA-N Temazepam Chemical compound N=1C(O)C(=O)N(C)C2=CC=C(Cl)C=C2C=1C1=CC=CC=C1 SEQDDYPDSLOBDC-UHFFFAOYSA-N 0.000 description 1
- GUGOEEXESWIERI-UHFFFAOYSA-N Terfenadine Chemical compound C1=CC(C(C)(C)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 GUGOEEXESWIERI-UHFFFAOYSA-N 0.000 description 1
- 241001582429 Tetracis Species 0.000 description 1
- FOCVUCIESVLUNU-UHFFFAOYSA-N Thiotepa Chemical compound C1CN1P(N1CC1)(=S)N1CC1 FOCVUCIESVLUNU-UHFFFAOYSA-N 0.000 description 1
- 240000002657 Thymus vulgaris Species 0.000 description 1
- 235000007303 Thymus vulgaris Nutrition 0.000 description 1
- KJADKKWYZYXHBB-XBWDGYHZSA-N Topiramic acid Chemical compound C1O[C@@]2(COS(N)(=O)=O)OC(C)(C)O[C@H]2[C@@H]2OC(C)(C)O[C@@H]21 KJADKKWYZYXHBB-XBWDGYHZSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 1
- 241000219793 Trifolium Species 0.000 description 1
- PHYFQTYBJUILEZ-UHFFFAOYSA-N Trioleoylglycerol Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC(OC(=O)CCCCCCCC=CCCCCCCCC)COC(=O)CCCCCCCC=CCCCCCCCC PHYFQTYBJUILEZ-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 206010057362 Underdose Diseases 0.000 description 1
- 229940122803 Vinca alkaloid Drugs 0.000 description 1
- FPIPGXGPPPQFEQ-BOOMUCAASA-N Vitamin A Natural products OC/C=C(/C)\C=C\C=C(\C)/C=C/C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-BOOMUCAASA-N 0.000 description 1
- 229930003316 Vitamin D Natural products 0.000 description 1
- QYSXJUFSXHHAJI-XFEUOLMDSA-N Vitamin D3 Natural products C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CCCC(C)C)=C/C=C1\C[C@@H](O)CCC1=C QYSXJUFSXHHAJI-XFEUOLMDSA-N 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- 229930003448 Vitamin K Natural products 0.000 description 1
- WREGKURFCTUGRC-POYBYMJQSA-N Zalcitabine Chemical compound O=C1N=C(N)C=CN1[C@@H]1O[C@H](CO)CC1 WREGKURFCTUGRC-POYBYMJQSA-N 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 244000273928 Zingiber officinale Species 0.000 description 1
- 235000006886 Zingiber officinale Nutrition 0.000 description 1
- HOBWAPHTEJGALG-JKCMADFCSA-N [(1r,5s)-8-methyl-8-azoniabicyclo[3.2.1]octan-3-yl] 3-hydroxy-2-phenylpropanoate;sulfate Chemical compound [O-]S([O-])(=O)=O.C([C@H]1CC[C@@H](C2)[NH+]1C)C2OC(=O)C(CO)C1=CC=CC=C1.C([C@H]1CC[C@@H](C2)[NH+]1C)C2OC(=O)C(CO)C1=CC=CC=C1 HOBWAPHTEJGALG-JKCMADFCSA-N 0.000 description 1
- LWZFANDGMFTDAV-BURFUSLBSA-N [(2r)-2-[(2r,3r,4s)-3,4-dihydroxyoxolan-2-yl]-2-hydroxyethyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O LWZFANDGMFTDAV-BURFUSLBSA-N 0.000 description 1
- FOLJTMYCYXSPFQ-CJKAUBRRSA-N [(2r,3s,4s,5r,6r)-6-[(2s,3s,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)-2-(octadecanoyloxymethyl)oxolan-2-yl]oxy-3,4,5-trihydroxyoxan-2-yl]methyl octadecanoate Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](COC(=O)CCCCCCCCCCCCCCCCC)O[C@@H]1O[C@@]1(COC(=O)CCCCCCCCCCCCCCCCC)[C@@H](O)[C@H](O)[C@@H](CO)O1 FOLJTMYCYXSPFQ-CJKAUBRRSA-N 0.000 description 1
- BXNCIERBDJYIQT-PRDVQWLOSA-N [(2r,3s,4s,5r,6s)-6-[2-[3-(1-benzofuran-5-yl)propanoyl]-3-hydroxy-5-methylphenoxy]-3,4,5-trihydroxyoxan-2-yl]methyl methyl carbonate Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](COC(=O)OC)O[C@H]1OC1=CC(C)=CC(O)=C1C(=O)CCC1=CC=C(OC=C2)C2=C1 BXNCIERBDJYIQT-PRDVQWLOSA-N 0.000 description 1
- RKZXQQPEDGMHBJ-LIGJGSPWSA-N [(2s,3r,4r,5r)-2,3,4,5,6-pentakis[[(z)-octadec-9-enoyl]oxy]hexyl] (z)-octadec-9-enoate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@@H](OC(=O)CCCCCCC\C=C/CCCCCCCC)[C@@H](OC(=O)CCCCCCC\C=C/CCCCCCCC)[C@H](OC(=O)CCCCCCC\C=C/CCCCCCCC)[C@@H](OC(=O)CCCCCCC\C=C/CCCCCCCC)COC(=O)CCCCCCC\C=C/CCCCCCCC RKZXQQPEDGMHBJ-LIGJGSPWSA-N 0.000 description 1
- RRGMXBQMCUKRLH-CTNGQTDRSA-N [(3ar,8bs)-3,4,8b-trimethyl-2,3a-dihydro-1h-pyrrolo[2,3-b]indol-7-yl] n-heptylcarbamate Chemical compound C12=CC(OC(=O)NCCCCCCC)=CC=C2N(C)[C@@H]2[C@@]1(C)CCN2C RRGMXBQMCUKRLH-CTNGQTDRSA-N 0.000 description 1
- ATBOMIWRCZXYSZ-XZBBILGWSA-N [1-[2,3-dihydroxypropoxy(hydroxy)phosphoryl]oxy-3-hexadecanoyloxypropan-2-yl] (9e,12e)-octadeca-9,12-dienoate Chemical compound CCCCCCCCCCCCCCCC(=O)OCC(COP(O)(=O)OCC(O)CO)OC(=O)CCCCCCC\C=C\C\C=C\CCCCC ATBOMIWRCZXYSZ-XZBBILGWSA-N 0.000 description 1
- 229960004748 abacavir Drugs 0.000 description 1
- MCGSCOLBFJQGHM-SCZZXKLOSA-N abacavir Chemical compound C=12N=CN([C@H]3C=C[C@@H](CO)C3)C2=NC(N)=NC=1NC1CC1 MCGSCOLBFJQGHM-SCZZXKLOSA-N 0.000 description 1
- BZKPWHYZMXOIDC-UHFFFAOYSA-N acetazolamide Chemical compound CC(=O)NC1=NN=C(S(N)(=O)=O)S1 BZKPWHYZMXOIDC-UHFFFAOYSA-N 0.000 description 1
- 229960000571 acetazolamide Drugs 0.000 description 1
- 229960004150 aciclovir Drugs 0.000 description 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 229960001997 adefovir Drugs 0.000 description 1
- WOZSCQDILHKSGG-UHFFFAOYSA-N adefovir depivoxil Chemical compound N1=CN=C2N(CCOCP(=O)(OCOC(=O)C(C)(C)C)OCOC(=O)C(C)(C)C)C=NC2=C1N WOZSCQDILHKSGG-UHFFFAOYSA-N 0.000 description 1
- 239000012790 adhesive layer Substances 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 238000001056 aerosol solvent extraction system Methods 0.000 description 1
- 239000003741 agents affecting lipid metabolism Substances 0.000 description 1
- 125000005055 alkyl alkoxy group Chemical group 0.000 description 1
- 150000004996 alkyl benzenes Chemical class 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- 150000001351 alkyl iodides Chemical class 0.000 description 1
- 150000008051 alkyl sulfates Chemical class 0.000 description 1
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 description 1
- OFCNXPDARWKPPY-UHFFFAOYSA-N allopurinol Chemical compound OC1=NC=NC2=C1C=NN2 OFCNXPDARWKPPY-UHFFFAOYSA-N 0.000 description 1
- 229960003459 allopurinol Drugs 0.000 description 1
- ZOJBYZNEUISWFT-UHFFFAOYSA-N allyl isothiocyanate Chemical compound C=CCN=C=S ZOJBYZNEUISWFT-UHFFFAOYSA-N 0.000 description 1
- 239000008168 almond oil Substances 0.000 description 1
- 229960002133 almotriptan Drugs 0.000 description 1
- 229950001123 alniditan Drugs 0.000 description 1
- 229940087168 alpha tocopherol Drugs 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- QYIXCDOBOSTCEI-UHFFFAOYSA-N alpha-cholestanol Natural products C1CC2CC(O)CCC2(C)C2C1C1CCC(C(C)CCCC(C)C)C1(C)CC2 QYIXCDOBOSTCEI-UHFFFAOYSA-N 0.000 description 1
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- WUOACPNHFRMFPN-UHFFFAOYSA-N alpha-terpineol Chemical compound CC1=CCC(C(C)(C)O)CC1 WUOACPNHFRMFPN-UHFFFAOYSA-N 0.000 description 1
- 229960004538 alprazolam Drugs 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 229960002684 aminocaproic acid Drugs 0.000 description 1
- 125000006598 aminocarbonylamino group Chemical group 0.000 description 1
- 229960003036 amisulpride Drugs 0.000 description 1
- NTJOBXMMWNYJFB-UHFFFAOYSA-N amisulpride Chemical compound CCN1CCCC1CNC(=O)C1=CC(S(=O)(=O)CC)=C(N)C=C1OC NTJOBXMMWNYJFB-UHFFFAOYSA-N 0.000 description 1
- 229960000836 amitriptyline Drugs 0.000 description 1
- KRMDCWKBEZIMAB-UHFFFAOYSA-N amitriptyline Chemical compound C1CC2=CC=CC=C2C(=CCCN(C)C)C2=CC=CC=C21 KRMDCWKBEZIMAB-UHFFFAOYSA-N 0.000 description 1
- HTIQEAQVCYTUBX-UHFFFAOYSA-N amlodipine Chemical compound CCOC(=O)C1=C(COCCN)NC(C)=C(C(=O)OC)C1C1=CC=CC=C1Cl HTIQEAQVCYTUBX-UHFFFAOYSA-N 0.000 description 1
- 229960000528 amlodipine Drugs 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 229960002519 amoxapine Drugs 0.000 description 1
- QWGDMFLQWFTERH-UHFFFAOYSA-N amoxapine Chemical compound C12=CC(Cl)=CC=C2OC2=CC=CC=C2N=C1N1CCNCC1 QWGDMFLQWFTERH-UHFFFAOYSA-N 0.000 description 1
- LSQZJLSUYDQPKJ-NJBDSQKTSA-N amoxicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=C(O)C=C1 LSQZJLSUYDQPKJ-NJBDSQKTSA-N 0.000 description 1
- 229960003022 amoxicillin Drugs 0.000 description 1
- 229940009444 amphotericin Drugs 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 229960000723 ampicillin Drugs 0.000 description 1
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 1
- 229960001830 amprenavir Drugs 0.000 description 1
- YMARZQAQMVYCKC-OEMFJLHTSA-N amprenavir Chemical compound C([C@@H]([C@H](O)CN(CC(C)C)S(=O)(=O)C=1C=CC(N)=CC=1)NC(=O)O[C@@H]1COCC1)C1=CC=CC=C1 YMARZQAQMVYCKC-OEMFJLHTSA-N 0.000 description 1
- RNLQIBCLLYYYFJ-UHFFFAOYSA-N amrinone Chemical compound N1C(=O)C(N)=CC(C=2C=CN=CC=2)=C1 RNLQIBCLLYYYFJ-UHFFFAOYSA-N 0.000 description 1
- 229960002105 amrinone Drugs 0.000 description 1
- 229960003116 amyl nitrite Drugs 0.000 description 1
- 239000002269 analeptic agent Substances 0.000 description 1
- 230000000202 analgesic effect Effects 0.000 description 1
- 229940011037 anethole Drugs 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 239000010617 anise oil Substances 0.000 description 1
- 230000000954 anitussive effect Effects 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- PYKYMHQGRFAEBM-UHFFFAOYSA-N anthraquinone Chemical class CCC(=O)c1c(O)c2C(=O)C3C(C=CC=C3O)C(=O)c2cc1CC(=O)OC PYKYMHQGRFAEBM-UHFFFAOYSA-N 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 229940005524 anti-dementia drug Drugs 0.000 description 1
- 229940127003 anti-diabetic drug Drugs 0.000 description 1
- 230000036436 anti-hiv Effects 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 229940035678 anti-parkinson drug Drugs 0.000 description 1
- 230000000561 anti-psychotic effect Effects 0.000 description 1
- 230000000798 anti-retroviral effect Effects 0.000 description 1
- 239000003416 antiarrhythmic agent Substances 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 239000001961 anticonvulsive agent Substances 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 239000003472 antidiabetic agent Substances 0.000 description 1
- 229940125714 antidiarrheal agent Drugs 0.000 description 1
- 239000003793 antidiarrheal agent Substances 0.000 description 1
- 229940030225 antihemorrhagics Drugs 0.000 description 1
- 229940125715 antihistaminic agent Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 229940030600 antihypertensive agent Drugs 0.000 description 1
- 229940127088 antihypertensive drug Drugs 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 229940124433 antimigraine drug Drugs 0.000 description 1
- 229940034982 antineoplastic agent Drugs 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 229940045719 antineoplastic alkylating agent nitrosoureas Drugs 0.000 description 1
- 239000002814 antineoplastic antimetabolite Substances 0.000 description 1
- 229940045696 antineoplastic drug podophyllotoxin derivative Drugs 0.000 description 1
- 229940045985 antineoplastic platinum compound Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 239000003904 antiprotozoal agent Substances 0.000 description 1
- 239000000164 antipsychotic agent Substances 0.000 description 1
- 239000003434 antitussive agent Substances 0.000 description 1
- 229940124584 antitussives Drugs 0.000 description 1
- 229960004046 apomorphine Drugs 0.000 description 1
- VMWNQDUVQKEIOC-CYBMUJFWSA-N apomorphine Chemical compound C([C@H]1N(C)CC2)C3=CC=C(O)C(O)=C3C3=C1C2=CC=C3 VMWNQDUVQKEIOC-CYBMUJFWSA-N 0.000 description 1
- 239000010477 apricot oil Substances 0.000 description 1
- BFNCJMURTMZBTE-UHFFFAOYSA-N aptiganel Chemical compound CCC1=CC=CC(N(C)C(N)=NC=2C3=CC=CC=C3C=CC=2)=C1 BFNCJMURTMZBTE-UHFFFAOYSA-N 0.000 description 1
- 229950001180 aptiganel Drugs 0.000 description 1
- 239000011260 aqueous acid Substances 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 229960004372 aripiprazole Drugs 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 150000001502 aryl halides Chemical class 0.000 description 1
- GXDALQBWZGODGZ-UHFFFAOYSA-N astemizole Chemical compound C1=CC(OC)=CC=C1CCN1CCC(NC=2N(C3=CC=CC=C3N=2)CC=2C=CC(F)=CC=2)CC1 GXDALQBWZGODGZ-UHFFFAOYSA-N 0.000 description 1
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 1
- 229960002274 atenolol Drugs 0.000 description 1
- 229960005370 atorvastatin Drugs 0.000 description 1
- 229960002028 atropine sulfate Drugs 0.000 description 1
- HYNPZTKLUNHGPM-KKERQHFVSA-N becaplermin Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](Cc1ccccc1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(=O)O)C(=O)N[C@@H](CC(=O)O)C(=O)N[C@@H](Cc2cnc[nH]2)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(=O)O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(=N)N)C(=O)N3CCC[C@H]3C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)O)NC(=O)[C@@H]4CCCN4C(=O)[C@H](CCCCN)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](C(C)C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](C(C)C)NC(=O)[C@@H]5CCCN5C(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@@H]6CCCN6C(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](CS)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(=O)N)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](CC(=O)N)NC(=O)[C@H](CC(=O)N)NC(=O)[C@H](CS)NC(=O)[C@H](CS)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CS)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](CCC(=O)N)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@@H]7CCCN7C(=O)[C@H](Cc8c[nH]c9c8cccc9)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](Cc1ccccc1)NC(=O)[C@H](CC(=O)N)NC(=O)[C@H](C)NC(=O)[C@H](CC(=O)N)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](CC(=O)O)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H](CO)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H](Cc1ccccc1)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCCNC(=N)N)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CS)NC(=O)[C@H](CCC(=O)O)NC(=O)[C@H](C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CCSC)NC(=O)[C@H](C)NC(=O)[C@@H]1CCCN1C(=O)[C@H](CCC(=O)O)NC(=O)[C@H](C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)N HYNPZTKLUNHGPM-KKERQHFVSA-N 0.000 description 1
- 229960004787 becaplermin Drugs 0.000 description 1
- 229950000210 beclometasone dipropionate Drugs 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229960005274 benzocaine Drugs 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 239000002876 beta blocker Substances 0.000 description 1
- WHGYBXFWUBPSRW-FOUAGVGXSA-N beta-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO WHGYBXFWUBPSRW-FOUAGVGXSA-N 0.000 description 1
- 229960002537 betamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-DVTGEIKXSA-N betamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-DVTGEIKXSA-N 0.000 description 1
- 125000002618 bicyclic heterocycle group Chemical group 0.000 description 1
- 239000003833 bile salt Substances 0.000 description 1
- 229940093761 bile salts Drugs 0.000 description 1
- 229960001561 bleomycin Drugs 0.000 description 1
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 1
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 description 1
- 229960001467 bortezomib Drugs 0.000 description 1
- 229960002802 bromocriptine Drugs 0.000 description 1
- NOJMTMIRQRDZMT-GSPXQYRGSA-N bromocriptine methanesulfonate Chemical compound CS(O)(=O)=O.C1=CC(C=2[C@H](N(C)C[C@@H](C=2)C(=O)N[C@]2(C(=O)N3[C@H](C(N4CCC[C@H]4[C@]3(O)O2)=O)CC(C)C)C(C)C)C2)=C3C2=C(Br)NC3=C1 NOJMTMIRQRDZMT-GSPXQYRGSA-N 0.000 description 1
- 229960004037 bromperidol Drugs 0.000 description 1
- 229960004436 budesonide Drugs 0.000 description 1
- 229960001415 buflomedil Drugs 0.000 description 1
- RMRJXGBAOAMLHD-IHFGGWKQSA-N buprenorphine Chemical compound C([C@]12[C@H]3OC=4C(O)=CC=C(C2=4)C[C@@H]2[C@]11CC[C@]3([C@H](C1)[C@](C)(O)C(C)(C)C)OC)CN2CC1CC1 RMRJXGBAOAMLHD-IHFGGWKQSA-N 0.000 description 1
- 229960001736 buprenorphine Drugs 0.000 description 1
- QWCRAEMEVRGPNT-UHFFFAOYSA-N buspirone Chemical compound C1C(=O)N(CCCCN2CCN(CC2)C=2N=CC=CN=2)C(=O)CC21CCCC2 QWCRAEMEVRGPNT-UHFFFAOYSA-N 0.000 description 1
- 229960002495 buspirone Drugs 0.000 description 1
- 229960002092 busulfan Drugs 0.000 description 1
- RGTXVXDNHPWPHH-UHFFFAOYSA-N butane-1,3-diamine Chemical compound CC(N)CCN RGTXVXDNHPWPHH-UHFFFAOYSA-N 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 229960004301 butriptyline Drugs 0.000 description 1
- ALELTFCQZDXAMQ-UHFFFAOYSA-N butriptyline Chemical compound C1CC2=CC=CC=C2C(CC(C)CN(C)C)C2=CC=CC=C21 ALELTFCQZDXAMQ-UHFFFAOYSA-N 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 239000000480 calcium channel blocker Substances 0.000 description 1
- VSJKWCGYPAHWDS-FQEVSTJZSA-N camptothecin Chemical compound C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-FQEVSTJZSA-N 0.000 description 1
- 229940127093 camptothecin Drugs 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 229960004117 capecitabine Drugs 0.000 description 1
- 229960000830 captopril Drugs 0.000 description 1
- FAKRSMQSSFJEIM-RQJHMYQMSA-N captopril Chemical compound SC[C@@H](C)C(=O)N1CCC[C@H]1C(O)=O FAKRSMQSSFJEIM-RQJHMYQMSA-N 0.000 description 1
- 229960000623 carbamazepine Drugs 0.000 description 1
- FFGPTBGBLSHEPO-UHFFFAOYSA-N carbamazepine Chemical compound C1=CC2=CC=CC=C2N(C(=O)N)C2=CC=CC=C21 FFGPTBGBLSHEPO-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 235000005300 cardamomo Nutrition 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 229960005243 carmustine Drugs 0.000 description 1
- NPAKNKYSJIDKMW-UHFFFAOYSA-N carvedilol Chemical compound COC1=CC=CC=C1OCCNCC(O)COC1=CC=CC2=NC3=CC=C[CH]C3=C12 NPAKNKYSJIDKMW-UHFFFAOYSA-N 0.000 description 1
- 229960004195 carvedilol Drugs 0.000 description 1
- 229960001777 castor oil Drugs 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 229960004841 cefadroxil Drugs 0.000 description 1
- NBFNMSULHIODTC-CYJZLJNKSA-N cefadroxil monohydrate Chemical compound O.C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CC=C(O)C=C1 NBFNMSULHIODTC-CYJZLJNKSA-N 0.000 description 1
- 229960002580 cefprozil Drugs 0.000 description 1
- 229960000590 celecoxib Drugs 0.000 description 1
- RZEKVGVHFLEQIL-UHFFFAOYSA-N celecoxib Chemical compound C1=CC(C)=CC=C1C1=CC(C(F)(F)F)=NN1C1=CC=C(S(N)(=O)=O)C=C1 RZEKVGVHFLEQIL-UHFFFAOYSA-N 0.000 description 1
- 229920003086 cellulose ether Polymers 0.000 description 1
- 229940106164 cephalexin Drugs 0.000 description 1
- AVGYWQBCYZHHPN-CYJZLJNKSA-N cephalexin monohydrate Chemical compound O.C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CC=CC=C1 AVGYWQBCYZHHPN-CYJZLJNKSA-N 0.000 description 1
- 229960001803 cetirizine Drugs 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- KXZJHVJKXJLBKO-UHFFFAOYSA-N chembl1408157 Chemical compound N=1C2=CC=CC=C2C(C(=O)O)=CC=1C1=CC=C(O)C=C1 KXZJHVJKXJLBKO-UHFFFAOYSA-N 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 229940112822 chewing gum Drugs 0.000 description 1
- 235000015218 chewing gum Nutrition 0.000 description 1
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 1
- 229960004630 chlorambucil Drugs 0.000 description 1
- 229960004782 chlordiazepoxide Drugs 0.000 description 1
- ANTSCNMPPGJYLG-UHFFFAOYSA-N chlordiazepoxide Chemical compound O=N=1CC(NC)=NC2=CC=C(Cl)C=C2C=1C1=CC=CC=C1 ANTSCNMPPGJYLG-UHFFFAOYSA-N 0.000 description 1
- 229960003260 chlorhexidine Drugs 0.000 description 1
- 229960001616 chlormadinone acetate Drugs 0.000 description 1
- SXYFAZGVNNYGJQ-UHFFFAOYSA-M chloromethyl(triphenyl)phosphanium;chloride Chemical compound [Cl-].C=1C=CC=CC=1[P+](C=1C=CC=CC=1)(CCl)C1=CC=CC=C1 SXYFAZGVNNYGJQ-UHFFFAOYSA-M 0.000 description 1
- ZPEIMTDSQAKGNT-UHFFFAOYSA-N chlorpromazine Chemical compound C1=C(Cl)C=C2N(CCCN(C)C)C3=CC=CC=C3SC2=C1 ZPEIMTDSQAKGNT-UHFFFAOYSA-N 0.000 description 1
- 229960001076 chlorpromazine Drugs 0.000 description 1
- 229960001265 ciclosporin Drugs 0.000 description 1
- 229960001380 cimetidine Drugs 0.000 description 1
- CCGSUNCLSOWKJO-UHFFFAOYSA-N cimetidine Chemical compound N#CNC(=N/C)\NCCSCC1=NC=N[C]1C CCGSUNCLSOWKJO-UHFFFAOYSA-N 0.000 description 1
- LOUPRKONTZGTKE-UHFFFAOYSA-N cinchonine Natural products C1C(C(C2)C=C)CCN2C1C(O)C1=CC=NC2=CC=C(OC)C=C21 LOUPRKONTZGTKE-UHFFFAOYSA-N 0.000 description 1
- 239000010630 cinnamon oil Substances 0.000 description 1
- DERZBLKQOCDDDZ-JLHYYAGUSA-N cinnarizine Chemical compound C1CN(C(C=2C=CC=CC=2)C=2C=CC=CC=2)CCN1C\C=C\C1=CC=CC=C1 DERZBLKQOCDDDZ-JLHYYAGUSA-N 0.000 description 1
- 229960000876 cinnarizine Drugs 0.000 description 1
- ODQWQRRAPPTVAG-BOPFTXTBSA-N cis-doxepin Chemical compound C1OC2=CC=CC=C2C(=C/CCN(C)C)\C2=CC=CC=C21 ODQWQRRAPPTVAG-BOPFTXTBSA-N 0.000 description 1
- NJMYODHXAKYRHW-DVZOWYKESA-N cis-flupenthixol Chemical compound C1CN(CCO)CCN1CC\C=C\1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C2/1 NJMYODHXAKYRHW-DVZOWYKESA-N 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 229960004106 citric acid Drugs 0.000 description 1
- 229960002436 cladribine Drugs 0.000 description 1
- 229960001791 clebopride Drugs 0.000 description 1
- 229960004606 clomipramine Drugs 0.000 description 1
- DGBIGWXXNGSACT-UHFFFAOYSA-N clonazepam Chemical compound C12=CC([N+](=O)[O-])=CC=C2NC(=O)CN=C1C1=CC=CC=C1Cl DGBIGWXXNGSACT-UHFFFAOYSA-N 0.000 description 1
- 229960003120 clonazepam Drugs 0.000 description 1
- 229960004022 clotrimazole Drugs 0.000 description 1
- VNFPBHJOKIVQEB-UHFFFAOYSA-N clotrimazole Chemical compound ClC1=CC=CC=C1C(N1C=NC=C1)(C=1C=CC=CC=1)C1=CC=CC=C1 VNFPBHJOKIVQEB-UHFFFAOYSA-N 0.000 description 1
- 229960004126 codeine Drugs 0.000 description 1
- OROGSEYTTFOCAN-DNJOTXNNSA-N codeine Natural products C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC OROGSEYTTFOCAN-DNJOTXNNSA-N 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 229940126543 compound 14 Drugs 0.000 description 1
- 229940125758 compound 15 Drugs 0.000 description 1
- 229940126142 compound 16 Drugs 0.000 description 1
- 229940125810 compound 20 Drugs 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 229940126208 compound 22 Drugs 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 229940125961 compound 24 Drugs 0.000 description 1
- 229940125846 compound 25 Drugs 0.000 description 1
- 229940035811 conjugated estrogen Drugs 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 239000010636 coriander oil Substances 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- 229940111134 coxibs Drugs 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- ARPLQAMUUDIHIT-UHFFFAOYSA-M cyanomethyl(triphenyl)phosphanium;chloride Chemical compound [Cl-].C=1C=CC=CC=1[P+](C=1C=CC=CC=1)(CC#N)C1=CC=CC=C1 ARPLQAMUUDIHIT-UHFFFAOYSA-M 0.000 description 1
- 125000004802 cyanophenyl group Chemical group 0.000 description 1
- WZHCOOQXZCIUNC-UHFFFAOYSA-N cyclandelate Chemical compound C1C(C)(C)CC(C)CC1OC(=O)C(O)C1=CC=CC=C1 WZHCOOQXZCIUNC-UHFFFAOYSA-N 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- HCAJEUSONLESMK-UHFFFAOYSA-N cyclohexylsulfamic acid Chemical compound OS(=O)(=O)NC1CCCCC1 HCAJEUSONLESMK-UHFFFAOYSA-N 0.000 description 1
- 239000003255 cyclooxygenase 2 inhibitor Substances 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 229960004397 cyclophosphamide Drugs 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 229960001140 cyproheptadine Drugs 0.000 description 1
- JJCFRYNCJDLXIK-UHFFFAOYSA-N cyproheptadine Chemical compound C1CN(C)CCC1=C1C2=CC=CC=C2C=CC2=CC=CC=C21 JJCFRYNCJDLXIK-UHFFFAOYSA-N 0.000 description 1
- 229960000978 cyproterone acetate Drugs 0.000 description 1
- UWFYSQMTEOIJJG-FDTZYFLXSA-N cyproterone acetate Chemical compound C1=C(Cl)C2=CC(=O)[C@@H]3C[C@@H]3[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 UWFYSQMTEOIJJG-FDTZYFLXSA-N 0.000 description 1
- 230000000120 cytopathologic effect Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 229960003901 dacarbazine Drugs 0.000 description 1
- 229960000640 dactinomycin Drugs 0.000 description 1
- CJBJHOAVZSMMDJ-HEXNFIEUSA-N darunavir Chemical compound C([C@@H]([C@H](O)CN(CC(C)C)S(=O)(=O)C=1C=CC(N)=CC=1)NC(=O)O[C@@H]1[C@@H]2CCO[C@@H]2OC1)C1=CC=CC=C1 CJBJHOAVZSMMDJ-HEXNFIEUSA-N 0.000 description 1
- 229960005107 darunavir Drugs 0.000 description 1
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 1
- 229960000975 daunorubicin Drugs 0.000 description 1
- 230000006837 decompression Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- PLMFYJJFUUUCRZ-UHFFFAOYSA-M decyltrimethylammonium bromide Chemical compound [Br-].CCCCCCCCCC[N+](C)(C)C PLMFYJJFUUUCRZ-UHFFFAOYSA-M 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 229960005319 delavirdine Drugs 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- SQIFACVGCPWBQZ-UHFFFAOYSA-N delta-terpineol Natural products CC(C)(O)C1CCC(=C)CC1 SQIFACVGCPWBQZ-UHFFFAOYSA-N 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- 239000000645 desinfectant Substances 0.000 description 1
- 229960003914 desipramine Drugs 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 229960001985 dextromethorphan Drugs 0.000 description 1
- INUNXTSAACVKJS-OAQYLSRUSA-N dextromoramide Chemical compound C([C@@H](C)C(C(=O)N1CCCC1)(C=1C=CC=CC=1)C=1C=CC=CC=1)N1CCOCC1 INUNXTSAACVKJS-OAQYLSRUSA-N 0.000 description 1
- 229960003701 dextromoramide Drugs 0.000 description 1
- 229960003529 diazepam Drugs 0.000 description 1
- AAOVKJBEBIDNHE-UHFFFAOYSA-N diazepam Chemical compound N=1CC(=O)N(C)C2=CC=C(Cl)C=C2C=1C1=CC=CC=C1 AAOVKJBEBIDNHE-UHFFFAOYSA-N 0.000 description 1
- ZFTFAPZRGNKQPU-UHFFFAOYSA-N dicarbonic acid Chemical compound OC(=O)OC(O)=O ZFTFAPZRGNKQPU-UHFFFAOYSA-N 0.000 description 1
- YFOJTKPOMRZOGM-UHFFFAOYSA-N dichloromethane;triphenylphosphane Chemical compound ClCCl.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 YFOJTKPOMRZOGM-UHFFFAOYSA-N 0.000 description 1
- 229960002656 didanosine Drugs 0.000 description 1
- AZFLJNIPTRTECV-FUMNGEBKSA-N dienogest Chemical compound C1CC(=O)C=C2CC[C@@H]([C@H]3[C@@](C)([C@](CC3)(O)CC#N)CC3)C3=C21 AZFLJNIPTRTECV-FUMNGEBKSA-N 0.000 description 1
- 229960003309 dienogest Drugs 0.000 description 1
- 235000013681 dietary sucrose Nutrition 0.000 description 1
- LXCYSACZTOKNNS-UHFFFAOYSA-N diethoxy(oxo)phosphanium Chemical compound CCO[P+](=O)OCC LXCYSACZTOKNNS-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical class CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- WDJUZGPOPHTGOT-XUDUSOBPSA-N digitoxin Chemical compound C1[C@H](O)[C@H](O)[C@@H](C)O[C@H]1O[C@@H]1[C@@H](C)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3C[C@@H]4[C@]([C@@H]5[C@H]([C@]6(CC[C@@H]([C@@]6(C)CC5)C=5COC(=O)C=5)O)CC4)(C)CC3)C[C@@H]2O)C)C[C@@H]1O WDJUZGPOPHTGOT-XUDUSOBPSA-N 0.000 description 1
- 229960000648 digitoxin Drugs 0.000 description 1
- LTMHDMANZUZIPE-PUGKRICDSA-N digoxin Chemical compound C1[C@H](O)[C@H](O)[C@@H](C)O[C@H]1O[C@@H]1[C@@H](C)O[C@@H](O[C@@H]2[C@H](O[C@@H](O[C@@H]3C[C@@H]4[C@]([C@@H]5[C@H]([C@]6(CC[C@@H]([C@@]6(C)[C@H](O)C5)C=5COC(=O)C=5)O)CC4)(C)CC3)C[C@@H]2O)C)C[C@@H]1O LTMHDMANZUZIPE-PUGKRICDSA-N 0.000 description 1
- 229960005156 digoxin Drugs 0.000 description 1
- LTMHDMANZUZIPE-UHFFFAOYSA-N digoxine Natural products C1C(O)C(O)C(C)OC1OC1C(C)OC(OC2C(OC(OC3CC4C(C5C(C6(CCC(C6(C)C(O)C5)C=5COC(=O)C=5)O)CC4)(C)CC3)CC2O)C)CC1O LTMHDMANZUZIPE-UHFFFAOYSA-N 0.000 description 1
- 150000004683 dihydrates Chemical class 0.000 description 1
- RBOXVHNMENFORY-DNJOTXNNSA-N dihydrocodeine Chemical compound C([C@H]1[C@H](N(CC[C@@]112)C)C3)C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC RBOXVHNMENFORY-DNJOTXNNSA-N 0.000 description 1
- 229960000920 dihydrocodeine Drugs 0.000 description 1
- 229940043279 diisopropylamine Drugs 0.000 description 1
- 239000010621 dill oil Substances 0.000 description 1
- HSUGRBWQSSZJOP-RTWAWAEBSA-N diltiazem Chemical compound C1=CC(OC)=CC=C1[C@H]1[C@@H](OC(C)=O)C(=O)N(CCN(C)C)C2=CC=CC=C2S1 HSUGRBWQSSZJOP-RTWAWAEBSA-N 0.000 description 1
- 229960004166 diltiazem Drugs 0.000 description 1
- 235000019329 dioctyl sodium sulphosuccinate Nutrition 0.000 description 1
- HYPPXZBJBPSRLK-UHFFFAOYSA-N diphenoxylate Chemical compound C1CC(C(=O)OCC)(C=2C=CC=CC=2)CCN1CCC(C#N)(C=1C=CC=CC=1)C1=CC=CC=C1 HYPPXZBJBPSRLK-UHFFFAOYSA-N 0.000 description 1
- 229960004192 diphenoxylate Drugs 0.000 description 1
- WEHWNAOGRSTTBQ-UHFFFAOYSA-N dipropylamine Chemical class CCCNCCC WEHWNAOGRSTTBQ-UHFFFAOYSA-N 0.000 description 1
- IZEKFCXSFNUWAM-UHFFFAOYSA-N dipyridamole Chemical compound C=12N=C(N(CCO)CCO)N=C(N3CCCCC3)C2=NC(N(CCO)CCO)=NC=1N1CCCCC1 IZEKFCXSFNUWAM-UHFFFAOYSA-N 0.000 description 1
- 229960002768 dipyridamole Drugs 0.000 description 1
- YHAIUSTWZPMYGG-UHFFFAOYSA-L disodium;2,2-dioctyl-3-sulfobutanedioate Chemical compound [Na+].[Na+].CCCCCCCCC(C([O-])=O)(C(C([O-])=O)S(O)(=O)=O)CCCCCCCC YHAIUSTWZPMYGG-UHFFFAOYSA-L 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 229940030606 diuretics Drugs 0.000 description 1
- VSJKWCGYPAHWDS-UHFFFAOYSA-N dl-camptothecin Natural products C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)C5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-UHFFFAOYSA-N 0.000 description 1
- TWFQJFPTTMIETC-UHFFFAOYSA-N dodecan-1-amine;hydron;chloride Chemical compound [Cl-].CCCCCCCCCCCC[NH3+] TWFQJFPTTMIETC-UHFFFAOYSA-N 0.000 description 1
- FGXWKSZFVQUSTL-UHFFFAOYSA-N domperidone Chemical compound C12=CC=CC=C2NC(=O)N1CCCN(CC1)CCC1N1C2=CC=C(Cl)C=C2NC1=O FGXWKSZFVQUSTL-UHFFFAOYSA-N 0.000 description 1
- 229960001253 domperidone Drugs 0.000 description 1
- 229960003530 donepezil Drugs 0.000 description 1
- 229960005426 doxepin Drugs 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- JGMOKGBVKVMRFX-HQZYFCCVSA-N dydrogesterone Chemical compound C1=CC2=CC(=O)CC[C@@]2(C)[C@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)C)[C@@]1(C)CC2 JGMOKGBVKVMRFX-HQZYFCCVSA-N 0.000 description 1
- 229960003804 efavirenz Drugs 0.000 description 1
- XPOQHMRABVBWPR-ZDUSSCGKSA-N efavirenz Chemical compound C([C@]1(C2=CC(Cl)=CC=C2NC(=O)O1)C(F)(F)F)#CC1CC1 XPOQHMRABVBWPR-ZDUSSCGKSA-N 0.000 description 1
- 239000008344 egg yolk phospholipid Substances 0.000 description 1
- 229950005455 eliprodil Drugs 0.000 description 1
- GBXSMTUPTTWBMN-XIRDDKMYSA-N enalapril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(O)=O)CC1=CC=CC=C1 GBXSMTUPTTWBMN-XIRDDKMYSA-N 0.000 description 1
- 229960000873 enalapril Drugs 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 229960001904 epirubicin Drugs 0.000 description 1
- 229950010753 eptastigmine Drugs 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- SUBDBMMJDZJVOS-DEOSSOPVSA-N esomeprazole Chemical compound C([S@](=O)C1=NC2=CC=C(C=C2N1)OC)C1=NC=C(C)C(OC)=C1C SUBDBMMJDZJVOS-DEOSSOPVSA-N 0.000 description 1
- 229960004770 esomeprazole Drugs 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- 229960005309 estradiol Drugs 0.000 description 1
- 229930182833 estradiol Natural products 0.000 description 1
- PROQIPRRNZUXQM-ZXXIGWHRSA-N estriol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H]([C@H](O)C4)O)[C@@H]4[C@@H]3CCC2=C1 PROQIPRRNZUXQM-ZXXIGWHRSA-N 0.000 description 1
- 229960001348 estriol Drugs 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 229960003399 estrone Drugs 0.000 description 1
- UVGCAWDXQWPTEK-UHFFFAOYSA-N ethane;hydrate Chemical compound O.CC UVGCAWDXQWPTEK-UHFFFAOYSA-N 0.000 description 1
- 229960002568 ethinylestradiol Drugs 0.000 description 1
- HAPOVYFOVVWLRS-UHFFFAOYSA-N ethosuximide Chemical compound CCC1(C)CC(=O)NC1=O HAPOVYFOVVWLRS-UHFFFAOYSA-N 0.000 description 1
- LRMHFDNWKCSEQU-UHFFFAOYSA-N ethoxyethane;phenol Chemical compound CCOCC.OC1=CC=CC=C1 LRMHFDNWKCSEQU-UHFFFAOYSA-N 0.000 description 1
- SFNALCNOMXIBKG-UHFFFAOYSA-N ethylene glycol monododecyl ether Chemical compound CCCCCCCCCCCCOCCO SFNALCNOMXIBKG-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- 239000010642 eucalyptus oil Substances 0.000 description 1
- 229940044949 eucalyptus oil Drugs 0.000 description 1
- 229960002217 eugenol Drugs 0.000 description 1
- XUFQPHANEAPEMJ-UHFFFAOYSA-N famotidine Chemical compound NC(N)=NC1=NC(CSCCC(N)=NS(N)(=O)=O)=CS1 XUFQPHANEAPEMJ-UHFFFAOYSA-N 0.000 description 1
- 229960001596 famotidine Drugs 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 229960002428 fentanyl Drugs 0.000 description 1
- IVLVTNPOHDFFCJ-UHFFFAOYSA-N fentanyl citrate Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 IVLVTNPOHDFFCJ-UHFFFAOYSA-N 0.000 description 1
- RWTNPBWLLIMQHL-UHFFFAOYSA-N fexofenadine Chemical compound C1=CC(C(C)(C(O)=O)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 RWTNPBWLLIMQHL-UHFFFAOYSA-N 0.000 description 1
- 229960003592 fexofenadine Drugs 0.000 description 1
- RFHAOTPXVQNOHP-UHFFFAOYSA-N fluconazole Chemical compound C1=NC=NN1CC(C=1C(=CC(F)=CC=1)F)(O)CN1C=NC=N1 RFHAOTPXVQNOHP-UHFFFAOYSA-N 0.000 description 1
- 229960004884 fluconazole Drugs 0.000 description 1
- XRECTZIEBJDKEO-UHFFFAOYSA-N flucytosine Chemical compound NC1=NC(=O)NC=C1F XRECTZIEBJDKEO-UHFFFAOYSA-N 0.000 description 1
- 229960004413 flucytosine Drugs 0.000 description 1
- SMANXXCATUTDDT-QPJJXVBHSA-N flunarizine Chemical compound C1=CC(F)=CC=C1C(C=1C=CC(F)=CC=1)N1CCN(C\C=C\C=2C=CC=CC=2)CC1 SMANXXCATUTDDT-QPJJXVBHSA-N 0.000 description 1
- 229960000326 flunarizine Drugs 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- 229960002419 flupentixol Drugs 0.000 description 1
- 229960002690 fluphenazine Drugs 0.000 description 1
- SAADBVWGJQAEFS-UHFFFAOYSA-N flurazepam Chemical compound N=1CC(=O)N(CCN(CC)CC)C2=CC=C(Cl)C=C2C=1C1=CC=CC=C1F SAADBVWGJQAEFS-UHFFFAOYSA-N 0.000 description 1
- 229960003528 flurazepam Drugs 0.000 description 1
- 239000004052 folic acid antagonist Substances 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- ZZUFCTLCJUWOSV-UHFFFAOYSA-N furosemide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(C(O)=O)=C1NCC1=CC=CO1 ZZUFCTLCJUWOSV-UHFFFAOYSA-N 0.000 description 1
- 229960003883 furosemide Drugs 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 229960002870 gabapentin Drugs 0.000 description 1
- 229960003980 galantamine Drugs 0.000 description 1
- ASUTZQLVASHGKV-UHFFFAOYSA-N galanthamine hydrochloride Natural products O1C(=C23)C(OC)=CC=C2CN(C)CCC23C1CC(O)C=C2 ASUTZQLVASHGKV-UHFFFAOYSA-N 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 229960002963 ganciclovir Drugs 0.000 description 1
- 229940125695 gastrointestinal agent Drugs 0.000 description 1
- 239000004083 gastrointestinal agent Substances 0.000 description 1
- 210000003736 gastrointestinal content Anatomy 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- QOIGKGMMAGJZNZ-UHFFFAOYSA-N gepirone Chemical compound O=C1CC(C)(C)CC(=O)N1CCCCN1CCN(C=2N=CC=CN=2)CC1 QOIGKGMMAGJZNZ-UHFFFAOYSA-N 0.000 description 1
- 229960000647 gepirone Drugs 0.000 description 1
- 235000008397 ginger Nutrition 0.000 description 1
- 125000003976 glyceryl group Chemical group [H]C([*])([H])C(O[H])([H])C(O[H])([H])[H] 0.000 description 1
- 229940075529 glyceryl stearate Drugs 0.000 description 1
- 229960003711 glyceryl trinitrate Drugs 0.000 description 1
- 239000003163 gonadal steroid hormone Substances 0.000 description 1
- DDUHZTYCFQRHIY-RBHXEPJQSA-N griseofulvin Chemical compound COC1=CC(=O)C[C@@H](C)[C@@]11C(=O)C(C(OC)=CC(OC)=C2Cl)=C2O1 DDUHZTYCFQRHIY-RBHXEPJQSA-N 0.000 description 1
- 229960002867 griseofulvin Drugs 0.000 description 1
- 159000000011 group IA salts Chemical class 0.000 description 1
- 150000008282 halocarbons Chemical class 0.000 description 1
- 229960003878 haloperidol Drugs 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 239000002874 hemostatic agent Substances 0.000 description 1
- 230000002439 hemostatic effect Effects 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 125000005980 hexynyl group Chemical group 0.000 description 1
- 239000004030 hiv protease inhibitor Substances 0.000 description 1
- 235000001050 hortel pimenta Nutrition 0.000 description 1
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 229960002003 hydrochlorothiazide Drugs 0.000 description 1
- LLPOLZWFYMWNKH-CMKMFDCUSA-N hydrocodone Chemical compound C([C@H]1[C@H](N(CC[C@@]112)C)C3)CC(=O)[C@@H]1OC1=C2C3=CC=C1OC LLPOLZWFYMWNKH-CMKMFDCUSA-N 0.000 description 1
- 229960000240 hydrocodone Drugs 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 125000002349 hydroxyamino group Chemical group [H]ON([H])[*] 0.000 description 1
- 229960001330 hydroxycarbamide Drugs 0.000 description 1
- XSEOYPMPHHCUBN-FGYWBSQSSA-N hydroxylated lecithin Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC(COP([O-])(=O)OCC[N+](C)(C)C)COC(=O)CCCCCCC[C@@H](O)[C@H](O)CCCCCCCC XSEOYPMPHHCUBN-FGYWBSQSSA-N 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 239000003326 hypnotic agent Substances 0.000 description 1
- 230000000147 hypnotic effect Effects 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 229960000908 idarubicin Drugs 0.000 description 1
- KTUFNOKKBVMGRW-UHFFFAOYSA-N imatinib Chemical compound C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 KTUFNOKKBVMGRW-UHFFFAOYSA-N 0.000 description 1
- 229960002411 imatinib Drugs 0.000 description 1
- 125000002962 imidazol-1-yl group Chemical group [*]N1C([H])=NC([H])=C1[H] 0.000 description 1
- 125000003037 imidazol-2-yl group Chemical group [H]N1C([*])=NC([H])=C1[H] 0.000 description 1
- 125000001841 imino group Chemical group [H]N=* 0.000 description 1
- BCGWQEUPMDMJNV-UHFFFAOYSA-N imipramine Chemical compound C1CC2=CC=CC=C2N(CCCN(C)C)C2=CC=CC=C21 BCGWQEUPMDMJNV-UHFFFAOYSA-N 0.000 description 1
- 229960004801 imipramine Drugs 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 229960001936 indinavir Drugs 0.000 description 1
- 229960000905 indomethacin Drugs 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 229960000598 infliximab Drugs 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 239000011872 intimate mixture Substances 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- XJTQJERLRPWUGL-UHFFFAOYSA-N iodomethylbenzene Chemical compound ICC1=CC=CC=C1 XJTQJERLRPWUGL-UHFFFAOYSA-N 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 125000003010 ionic group Chemical group 0.000 description 1
- 239000002563 ionic surfactant Substances 0.000 description 1
- UWKQSNNFCGGAFS-XIFFEERXSA-N irinotecan Chemical compound C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 UWKQSNNFCGGAFS-XIFFEERXSA-N 0.000 description 1
- 229960004768 irinotecan Drugs 0.000 description 1
- 159000000014 iron salts Chemical class 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 229960003350 isoniazid Drugs 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 229960002479 isosorbide Drugs 0.000 description 1
- MOYKHGMNXAOIAT-JGWLITMVSA-N isosorbide dinitrate Chemical compound [O-][N+](=O)O[C@H]1CO[C@@H]2[C@H](O[N+](=O)[O-])CO[C@@H]21 MOYKHGMNXAOIAT-JGWLITMVSA-N 0.000 description 1
- 229960000201 isosorbide dinitrate Drugs 0.000 description 1
- OOYGSFOGFJDDHP-KMCOLRRFSA-N kanamycin A sulfate Chemical compound OS(O)(=O)=O.O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N OOYGSFOGFJDDHP-KMCOLRRFSA-N 0.000 description 1
- 229960002064 kanamycin sulfate Drugs 0.000 description 1
- FPCCSQOGAWCVBH-UHFFFAOYSA-N ketanserin Chemical compound C1=CC(F)=CC=C1C(=O)C1CCN(CCN2C(C3=CC=CC=C3NC2=O)=O)CC1 FPCCSQOGAWCVBH-UHFFFAOYSA-N 0.000 description 1
- 229960005417 ketanserin Drugs 0.000 description 1
- 229960004125 ketoconazole Drugs 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- DKYWVDODHFEZIM-UHFFFAOYSA-N ketoprofen Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 DKYWVDODHFEZIM-UHFFFAOYSA-N 0.000 description 1
- 229960000991 ketoprofen Drugs 0.000 description 1
- JJTUDXZGHPGLLC-UHFFFAOYSA-N lactide Chemical compound CC1OC(=O)C(C)OC1=O JJTUDXZGHPGLLC-UHFFFAOYSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960001848 lamotrigine Drugs 0.000 description 1
- PYZRQGJRPPTADH-UHFFFAOYSA-N lamotrigine Chemical compound NC1=NC(N)=NN=C1C1=CC=CC(Cl)=C1Cl PYZRQGJRPPTADH-UHFFFAOYSA-N 0.000 description 1
- SIXIIKVOZAGHPV-UHFFFAOYSA-N lansoprazole Chemical compound CC1=C(OCC(F)(F)F)C=CN=C1CS(=O)C1=NC2=CC=C[CH]C2=N1 SIXIIKVOZAGHPV-UHFFFAOYSA-N 0.000 description 1
- 229960003174 lansoprazole Drugs 0.000 description 1
- 229940100556 laureth-23 Drugs 0.000 description 1
- 229950005862 lazabemide Drugs 0.000 description 1
- JMPOIZCOJJMTHI-UHFFFAOYSA-N leteprinim Chemical compound C1=CC(C(=O)O)=CC=C1NC(=O)CCN1C(NC=NC2=O)=C2N=C1 JMPOIZCOJJMTHI-UHFFFAOYSA-N 0.000 description 1
- 229950011566 leteprinim Drugs 0.000 description 1
- 229960004002 levetiracetam Drugs 0.000 description 1
- HPHUVLMMVZITSG-ZCFIWIBFSA-N levetiracetam Chemical compound CC[C@H](C(N)=O)N1CCCC1=O HPHUVLMMVZITSG-ZCFIWIBFSA-N 0.000 description 1
- ZCGOMHNNNFPNMX-KYTRFIICSA-N levocabastine Chemical compound C1([C@@]2(C(O)=O)CCN(C[C@H]2C)[C@@H]2CC[C@@](CC2)(C#N)C=2C=CC(F)=CC=2)=CC=CC=C1 ZCGOMHNNNFPNMX-KYTRFIICSA-N 0.000 description 1
- 229960001120 levocabastine Drugs 0.000 description 1
- 229960004502 levodopa Drugs 0.000 description 1
- 229960004400 levonorgestrel Drugs 0.000 description 1
- 229960004194 lidocaine Drugs 0.000 description 1
- 229960001941 lidoflazine Drugs 0.000 description 1
- OJMMVQQUTAEWLP-KIDUDLJLSA-N lincomycin Chemical compound CN1C[C@H](CCC)C[C@H]1C(=O)N[C@H]([C@@H](C)O)[C@@H]1[C@H](O)[C@H](O)[C@@H](O)[C@@H](SC)O1 OJMMVQQUTAEWLP-KIDUDLJLSA-N 0.000 description 1
- 229960005287 lincomycin Drugs 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 description 1
- 229910052808 lithium carbonate Inorganic materials 0.000 description 1
- 229940008015 lithium carbonate Drugs 0.000 description 1
- 229910003002 lithium salt Inorganic materials 0.000 description 1
- 159000000002 lithium salts Chemical class 0.000 description 1
- 239000003589 local anesthetic agent Substances 0.000 description 1
- 229960005015 local anesthetics Drugs 0.000 description 1
- 229960002247 lomustine Drugs 0.000 description 1
- RDOIQAHITMMDAJ-UHFFFAOYSA-N loperamide Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(C(=O)N(C)C)CCN(CC1)CCC1(O)C1=CC=C(Cl)C=C1 RDOIQAHITMMDAJ-UHFFFAOYSA-N 0.000 description 1
- 229960001571 loperamide Drugs 0.000 description 1
- KXVSBTJVTUVNPM-UKPNQBOSSA-N loperamide oxide Chemical compound C1([C@]2(O)CC[N@@+](CC2)([O-])CCC(C(=O)N(C)C)(C=2C=CC=CC=2)C=2C=CC=CC=2)=CC=C(Cl)C=C1 KXVSBTJVTUVNPM-UKPNQBOSSA-N 0.000 description 1
- 229960003954 loperamide oxide Drugs 0.000 description 1
- 229960004525 lopinavir Drugs 0.000 description 1
- 229960003088 loratadine Drugs 0.000 description 1
- JCCNYMKQOSZNPW-UHFFFAOYSA-N loratadine Chemical compound C1CN(C(=O)OCC)CCC1=C1C2=NC=CC=C2CCC2=CC(Cl)=CC=C21 JCCNYMKQOSZNPW-UHFFFAOYSA-N 0.000 description 1
- 229960004391 lorazepam Drugs 0.000 description 1
- PCZOHLXUXFIOCF-BXMDZJJMSA-N lovastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 PCZOHLXUXFIOCF-BXMDZJJMSA-N 0.000 description 1
- 229960004844 lovastatin Drugs 0.000 description 1
- QLJODMDSTUBWDW-UHFFFAOYSA-N lovastatin hydroxy acid Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(C)C=C21 QLJODMDSTUBWDW-UHFFFAOYSA-N 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 229960001910 lynestrenol Drugs 0.000 description 1
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- VXWPONVCMVLXBW-UHFFFAOYSA-M magnesium;carbanide;iodide Chemical compound [CH3-].[Mg+2].[I-] VXWPONVCMVLXBW-UHFFFAOYSA-M 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 235000012054 meals Nutrition 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 229960002985 medroxyprogesterone acetate Drugs 0.000 description 1
- PSGAAPLEWMOORI-PEINSRQWSA-N medroxyprogesterone acetate Chemical compound C([C@@]12C)CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2CC[C@]2(C)[C@@](OC(C)=O)(C(C)=O)CC[C@H]21 PSGAAPLEWMOORI-PEINSRQWSA-N 0.000 description 1
- 229960001962 mefloquine Drugs 0.000 description 1
- 229960001786 megestrol Drugs 0.000 description 1
- JBVNBBXAMBZTMQ-CEGNMAFCSA-N megestrol Chemical compound C1=CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)C)(O)[C@@]1(C)CC2 JBVNBBXAMBZTMQ-CEGNMAFCSA-N 0.000 description 1
- JDSHMPZPIAZGSV-UHFFFAOYSA-N melamine Chemical compound NC1=NC(N)=NC(N)=N1 JDSHMPZPIAZGSV-UHFFFAOYSA-N 0.000 description 1
- BUGYDGFZZOZRHP-UHFFFAOYSA-N memantine Chemical compound C1C(C2)CC3(C)CC1(C)CC2(N)C3 BUGYDGFZZOZRHP-UHFFFAOYSA-N 0.000 description 1
- 229960004640 memantine Drugs 0.000 description 1
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 1
- 229960001428 mercaptopurine Drugs 0.000 description 1
- KBOPZPXVLCULAV-UHFFFAOYSA-N mesalamine Chemical compound NC1=CC=C(O)C(C(O)=O)=C1 KBOPZPXVLCULAV-UHFFFAOYSA-N 0.000 description 1
- 229960004963 mesalazine Drugs 0.000 description 1
- IMSSROKUHAOUJS-MJCUULBUSA-N mestranol Chemical compound C1C[C@]2(C)[C@@](C#C)(O)CC[C@H]2[C@@H]2CCC3=CC(OC)=CC=C3[C@H]21 IMSSROKUHAOUJS-MJCUULBUSA-N 0.000 description 1
- 229960001390 mestranol Drugs 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- XZWYZXLIPXDOLR-UHFFFAOYSA-N metformin Chemical compound CN(C)C(=N)NC(N)=N XZWYZXLIPXDOLR-UHFFFAOYSA-N 0.000 description 1
- 229960003105 metformin Drugs 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 229960004469 methoxsalen Drugs 0.000 description 1
- SQBBOVROCFXYBN-UHFFFAOYSA-N methoxypsoralen Natural products C1=C2OC(=O)C(OC)=CC2=CC2=C1OC=C2 SQBBOVROCFXYBN-UHFFFAOYSA-N 0.000 description 1
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- 229960002545 methylthiouracil Drugs 0.000 description 1
- 229960004503 metoclopramide Drugs 0.000 description 1
- TTWJBBZEZQICBI-UHFFFAOYSA-N metoclopramide Chemical compound CCN(CC)CCNC(=O)C1=CC(Cl)=C(N)C=C1OC TTWJBBZEZQICBI-UHFFFAOYSA-N 0.000 description 1
- IUBSYMUCCVWXPE-UHFFFAOYSA-N metoprolol Chemical compound COCCC1=CC=C(OCC(O)CNC(C)C)C=C1 IUBSYMUCCVWXPE-UHFFFAOYSA-N 0.000 description 1
- 229960002237 metoprolol Drugs 0.000 description 1
- 229960001952 metrifonate Drugs 0.000 description 1
- 229960003955 mianserin Drugs 0.000 description 1
- 229960005040 miconazole nitrate Drugs 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- YMMXHEYLRHNXAB-RMKNXTFCSA-N milameline Chemical compound CO\N=C\C1=CCCN(C)C1 YMMXHEYLRHNXAB-RMKNXTFCSA-N 0.000 description 1
- 229950004373 milameline Drugs 0.000 description 1
- PZRHRDRVRGEVNW-UHFFFAOYSA-N milrinone Chemical compound N1C(=O)C(C#N)=CC(C=2C=CN=CC=2)=C1C PZRHRDRVRGEVNW-UHFFFAOYSA-N 0.000 description 1
- 229960003574 milrinone Drugs 0.000 description 1
- DYKFCLLONBREIL-KVUCHLLUSA-N minocycline Chemical compound C([C@H]1C2)C3=C(N(C)C)C=CC(O)=C3C(=O)C1=C(O)[C@@]1(O)[C@@H]2[C@H](N(C)C)C(O)=C(C(N)=O)C1=O DYKFCLLONBREIL-KVUCHLLUSA-N 0.000 description 1
- 229960004023 minocycline Drugs 0.000 description 1
- 229960003632 minoxidil Drugs 0.000 description 1
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 description 1
- 229960001156 mitoxantrone Drugs 0.000 description 1
- XONPDZSGENTBNJ-UHFFFAOYSA-N molecular hydrogen;sodium Chemical compound [Na].[H][H] XONPDZSGENTBNJ-UHFFFAOYSA-N 0.000 description 1
- XLFWDASMENKTKL-UHFFFAOYSA-N molsidomine Chemical compound O1C(N=C([O-])OCC)=C[N+](N2CCOCC2)=N1 XLFWDASMENKTKL-UHFFFAOYSA-N 0.000 description 1
- 229960004027 molsidomine Drugs 0.000 description 1
- 229960004085 mosapride Drugs 0.000 description 1
- 230000004899 motility Effects 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 239000003149 muscarinic antagonist Substances 0.000 description 1
- 239000008164 mustard oil Substances 0.000 description 1
- 239000001627 myristica fragrans houtt. fruit oil Substances 0.000 description 1
- JZXRLKWWVNUZRB-UHFFFAOYSA-N n-(2-aminoethyl)-5-chloropyridine-2-carboxamide Chemical compound NCCNC(=O)C1=CC=C(Cl)C=N1 JZXRLKWWVNUZRB-UHFFFAOYSA-N 0.000 description 1
- QVSXOXCYXPQXMF-OAHLLOKOSA-N n-[[(2r)-3,4-dihydro-2h-chromen-2-yl]methyl]-n'-(1,4,5,6-tetrahydropyrimidin-2-yl)propane-1,3-diamine Chemical compound C([C@@H]1OC2=CC=CC=C2CC1)NCCCNC1=NCCCN1 QVSXOXCYXPQXMF-OAHLLOKOSA-N 0.000 description 1
- CSDTZUBPSYWZDX-UHFFFAOYSA-N n-pentyl nitrite Chemical compound CCCCCON=O CSDTZUBPSYWZDX-UHFFFAOYSA-N 0.000 description 1
- 229960004270 nabumetone Drugs 0.000 description 1
- 229960001775 nafcillin sodium Drugs 0.000 description 1
- OCXSDHJRMYFTMA-KMFBOIRUSA-M nafcillin sodium monohydrate Chemical compound O.[Na+].C1=CC=CC2=C(C(=O)N[C@@H]3C(N4[C@H](C(C)(C)S[C@@H]43)C([O-])=O)=O)C(OCC)=CC=C21 OCXSDHJRMYFTMA-KMFBOIRUSA-M 0.000 description 1
- MHWLWQUZZRMNGJ-UHFFFAOYSA-N nalidixic acid Chemical compound C1=C(C)N=C2N(CC)C=C(C(O)=O)C(=O)C2=C1 MHWLWQUZZRMNGJ-UHFFFAOYSA-N 0.000 description 1
- 229960000210 nalidixic acid Drugs 0.000 description 1
- UNHGSHHVDNGCFN-UHFFFAOYSA-N naratriptan Chemical compound C=12[CH]C(CCS(=O)(=O)NC)=CC=C2N=CC=1C1CCN(C)CC1 UNHGSHHVDNGCFN-UHFFFAOYSA-N 0.000 description 1
- 229960005254 naratriptan Drugs 0.000 description 1
- 229920005615 natural polymer Polymers 0.000 description 1
- 229960000619 nebivolol Drugs 0.000 description 1
- 229960000884 nelfinavir Drugs 0.000 description 1
- QAGYKUNXZHXKMR-HKWSIXNMSA-N nelfinavir Chemical compound CC1=C(O)C=CC=C1C(=O)N[C@H]([C@H](O)CN1[C@@H](C[C@@H]2CCCC[C@@H]2C1)C(=O)NC(C)(C)C)CSC1=CC=CC=C1 QAGYKUNXZHXKMR-HKWSIXNMSA-N 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 229960002362 neostigmine Drugs 0.000 description 1
- LULNWZDBKTWDGK-UHFFFAOYSA-M neostigmine bromide Chemical compound [Br-].CN(C)C(=O)OC1=CC=CC([N+](C)(C)C)=C1 LULNWZDBKTWDGK-UHFFFAOYSA-M 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229960000689 nevirapine Drugs 0.000 description 1
- 229960001783 nicardipine Drugs 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- SGXXNSQHWDMGGP-IZZDOVSWSA-N nizatidine Chemical compound [O-][N+](=O)\C=C(/NC)NCCSCC1=CSC(CN(C)C)=N1 SGXXNSQHWDMGGP-IZZDOVSWSA-N 0.000 description 1
- 229960004872 nizatidine Drugs 0.000 description 1
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 1
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- SNQQPOLDUKLAAF-UHFFFAOYSA-N nonylphenol Chemical compound CCCCCCCCCC1=CC=CC=C1O SNQQPOLDUKLAAF-UHFFFAOYSA-N 0.000 description 1
- OMLDMGPCWMBPAN-YPMHNXCESA-N norcisapride Chemical compound CO[C@H]1CNCC[C@H]1NC(=O)C1=CC(Cl)=C(N)C=C1OC OMLDMGPCWMBPAN-YPMHNXCESA-N 0.000 description 1
- 229960002667 norelgestromin Drugs 0.000 description 1
- 229960001858 norethynodrel Drugs 0.000 description 1
- 229960001180 norfloxacin Drugs 0.000 description 1
- OGJPXUAPXNRGGI-UHFFFAOYSA-N norfloxacin Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNCC1 OGJPXUAPXNRGGI-UHFFFAOYSA-N 0.000 description 1
- 229960000417 norgestimate Drugs 0.000 description 1
- KIQQMECNKUGGKA-NMYWJIRASA-N norgestimate Chemical compound O/N=C/1CC[C@@H]2[C@H]3CC[C@](CC)([C@](CC4)(OC(C)=O)C#C)[C@@H]4[C@@H]3CCC2=C\1 KIQQMECNKUGGKA-NMYWJIRASA-N 0.000 description 1
- 229960002831 norgestrienone Drugs 0.000 description 1
- GVDMJXQHPUYPHP-FYQPLNBISA-N norgestrienone Chemical compound C1CC(=O)C=C2CC[C@@H]([C@H]3[C@@](C)([C@](CC3)(O)C#C)C=C3)C3=C21 GVDMJXQHPUYPHP-FYQPLNBISA-N 0.000 description 1
- 210000001331 nose Anatomy 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 150000003833 nucleoside derivatives Chemical class 0.000 description 1
- 229960000988 nystatin Drugs 0.000 description 1
- VQOXZBDYSJBXMA-NQTDYLQESA-N nystatin A1 Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/CC/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 VQOXZBDYSJBXMA-NQTDYLQESA-N 0.000 description 1
- GLZWNFNQMJAZGY-UHFFFAOYSA-N octaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCO GLZWNFNQMJAZGY-UHFFFAOYSA-N 0.000 description 1
- 229920002113 octoxynol Polymers 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229960001699 ofloxacin Drugs 0.000 description 1
- 125000001117 oleyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])/C([H])=C([H])\C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 229960000381 omeprazole Drugs 0.000 description 1
- 239000000014 opioid analgesic Substances 0.000 description 1
- 229940005483 opioid analgesics Drugs 0.000 description 1
- 239000006186 oral dosage form Substances 0.000 description 1
- 239000007935 oral tablet Substances 0.000 description 1
- 239000010502 orange oil Substances 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 229940045681 other alkylating agent in atc Drugs 0.000 description 1
- UWYHMGVUTGAWSP-JKIFEVAISA-N oxacillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C1=C(C)ON=C1C1=CC=CC=C1 UWYHMGVUTGAWSP-JKIFEVAISA-N 0.000 description 1
- 229960001019 oxacillin Drugs 0.000 description 1
- BAINIUMDFURPJM-UHFFFAOYSA-N oxatomide Chemical compound O=C1NC2=CC=CC=C2N1CCCN(CC1)CCN1C(C=1C=CC=CC=1)C1=CC=CC=C1 BAINIUMDFURPJM-UHFFFAOYSA-N 0.000 description 1
- 229960002698 oxatomide Drugs 0.000 description 1
- 125000005740 oxycarbonyl group Chemical group [*:1]OC([*:2])=O 0.000 description 1
- 229960002085 oxycodone Drugs 0.000 description 1
- LSQZJLSUYDQPKJ-UHFFFAOYSA-N p-Hydroxyampicillin Natural products O=C1N2C(C(O)=O)C(C)(C)SC2C1NC(=O)C(N)C1=CC=C(O)C=C1 LSQZJLSUYDQPKJ-UHFFFAOYSA-N 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- 125000000913 palmityl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- RUVINXPYWBROJD-UHFFFAOYSA-N para-methoxyphenyl Natural products COC1=CC=C(C=CC)C=C1 RUVINXPYWBROJD-UHFFFAOYSA-N 0.000 description 1
- 229960005489 paracetamol Drugs 0.000 description 1
- 229940127242 parasympathomimetic drug Drugs 0.000 description 1
- 230000001499 parasympathomimetic effect Effects 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 229940072880 peg-10 stearate Drugs 0.000 description 1
- 229940077414 peg-12 stearate Drugs 0.000 description 1
- 238000005453 pelletization Methods 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 229940056360 penicillin g Drugs 0.000 description 1
- 229940059574 pentaerithrityl Drugs 0.000 description 1
- 229960004321 pentaerithrityl tetranitrate Drugs 0.000 description 1
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 125000005981 pentynyl group Chemical group 0.000 description 1
- 150000004965 peroxy acids Chemical class 0.000 description 1
- DDBREPKUVSBGFI-UHFFFAOYSA-N phenobarbital Chemical compound C=1C=CC=CC=1C1(CC)C(=O)NC(=O)NC1=O DDBREPKUVSBGFI-UHFFFAOYSA-N 0.000 description 1
- 229960002695 phenobarbital Drugs 0.000 description 1
- HCTVWSOKIJULET-LQDWTQKMSA-M phenoxymethylpenicillin potassium Chemical compound [K+].N([C@H]1[C@H]2SC([C@@H](N2C1=O)C([O-])=O)(C)C)C(=O)COC1=CC=CC=C1 HCTVWSOKIJULET-LQDWTQKMSA-M 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- 229960002036 phenytoin Drugs 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- WTJKGGKOPKCXLL-RRHRGVEJSA-N phosphatidylcholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCC=CCCCCCCCC WTJKGGKOPKCXLL-RRHRGVEJSA-N 0.000 description 1
- 150000008104 phosphatidylethanolamines Chemical class 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 150000003014 phosphoric acid esters Chemical class 0.000 description 1
- MBWXNTAXLNYFJB-NKFFZRIASA-N phylloquinone Chemical compound C1=CC=C2C(=O)C(C/C=C(C)/CCC[C@H](C)CCC[C@H](C)CCCC(C)C)=C(C)C(=O)C2=C1 MBWXNTAXLNYFJB-NKFFZRIASA-N 0.000 description 1
- 235000019175 phylloquinone Nutrition 0.000 description 1
- 239000011772 phylloquinone Substances 0.000 description 1
- 238000000053 physical method Methods 0.000 description 1
- 239000006069 physical mixture Substances 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- PIJVFDBKTWXHHD-HIFRSBDPSA-N physostigmine Chemical compound C12=CC(OC(=O)NC)=CC=C2N(C)[C@@H]2[C@@]1(C)CCN2C PIJVFDBKTWXHHD-HIFRSBDPSA-N 0.000 description 1
- 229960001697 physostigmine Drugs 0.000 description 1
- 229960001898 phytomenadione Drugs 0.000 description 1
- QYSPLQLAKJAUJT-UHFFFAOYSA-N piroxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=CC=CC=N1 QYSPLQLAKJAUJT-UHFFFAOYSA-N 0.000 description 1
- 229960002702 piroxicam Drugs 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 150000003058 platinum compounds Chemical class 0.000 description 1
- YJGVMLPVUAXIQN-XVVDYKMHSA-N podophyllotoxin Chemical class COC1=C(OC)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@H](O)[C@@H]3[C@@H]2C(OC3)=O)=C1 YJGVMLPVUAXIQN-XVVDYKMHSA-N 0.000 description 1
- 239000003600 podophyllotoxin derivative Substances 0.000 description 1
- 229920001993 poloxamer 188 Polymers 0.000 description 1
- 229940044519 poloxamer 188 Drugs 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920002523 polyethylene Glycol 1000 Polymers 0.000 description 1
- 229940097941 polyglyceryl-10 laurate Drugs 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920005606 polypropylene copolymer Polymers 0.000 description 1
- 108010022457 polysaccharide peptide Proteins 0.000 description 1
- 150000004804 polysaccharides Chemical class 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 1
- 229960002965 pravastatin Drugs 0.000 description 1
- TUZYXOIXSAXUGO-PZAWKZKUSA-N pravastatin Chemical compound C1=C[C@H](C)[C@H](CC[C@@H](O)C[C@@H](O)CC(O)=O)[C@H]2[C@@H](OC(=O)[C@@H](C)CC)C[C@H](O)C=C21 TUZYXOIXSAXUGO-PZAWKZKUSA-N 0.000 description 1
- IENZQIKPVFGBNW-UHFFFAOYSA-N prazosin Chemical compound N=1C(N)=C2C=C(OC)C(OC)=CC2=NC=1N(CC1)CCN1C(=O)C1=CC=CO1 IENZQIKPVFGBNW-UHFFFAOYSA-N 0.000 description 1
- 229960001289 prazosin Drugs 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 229960003912 probucol Drugs 0.000 description 1
- FYPMFJGVHOHGLL-UHFFFAOYSA-N probucol Chemical compound C=1C(C(C)(C)C)=C(O)C(C(C)(C)C)=CC=1SC(C)(C)SC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 FYPMFJGVHOHGLL-UHFFFAOYSA-N 0.000 description 1
- REQCZEXYDRLIBE-UHFFFAOYSA-N procainamide Chemical compound CCN(CC)CCNC(=O)C1=CC=C(N)C=C1 REQCZEXYDRLIBE-UHFFFAOYSA-N 0.000 description 1
- 229960000244 procainamide Drugs 0.000 description 1
- CPTBDICYNRMXFX-UHFFFAOYSA-N procarbazine Chemical compound CNNCC1=CC=C(C(=O)NC(C)C)C=C1 CPTBDICYNRMXFX-UHFFFAOYSA-N 0.000 description 1
- 229960000624 procarbazine Drugs 0.000 description 1
- 229960003387 progesterone Drugs 0.000 description 1
- 239000000186 progesterone Substances 0.000 description 1
- 239000000583 progesterone congener Substances 0.000 description 1
- 229940095055 progestogen systemic hormonal contraceptives Drugs 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 229960003910 promethazine Drugs 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 235000010409 propane-1,2-diol alginate Nutrition 0.000 description 1
- 239000000770 propane-1,2-diol alginate Substances 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- AQHHHDLHHXJYJD-UHFFFAOYSA-N propranolol Chemical compound C1=CC=C2C(OCC(O)CNC(C)C)=CC=CC2=C1 AQHHHDLHHXJYJD-UHFFFAOYSA-N 0.000 description 1
- 229960002662 propylthiouracil Drugs 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- URKOMYMAXPYINW-UHFFFAOYSA-N quetiapine Chemical compound C1CN(CCOCCO)CCN1C1=NC2=CC=CC=C2SC2=CC=CC=C12 URKOMYMAXPYINW-UHFFFAOYSA-N 0.000 description 1
- 229960004431 quetiapine Drugs 0.000 description 1
- ZTHJULTYCAQOIJ-WXXKFALUSA-N quetiapine fumarate Chemical compound [H+].[H+].[O-]C(=O)\C=C\C([O-])=O.C1CN(CCOCCO)CCN1C1=NC2=CC=CC=C2SC2=CC=CC=C12.C1CN(CCOCCO)CCN1C1=NC2=CC=CC=C2SC2=CC=CC=C12 ZTHJULTYCAQOIJ-WXXKFALUSA-N 0.000 description 1
- 229950009172 quingestanol acetate Drugs 0.000 description 1
- FLGJKPPXEKYCBY-AKCFYGDASA-N quingestanol acetate Chemical compound C([C@H]1[C@@H]2CC[C@@]([C@]2(CC[C@@H]1[C@H]1CC2)C)(OC(=O)C)C#C)C=C1C=C2OC1CCCC1 FLGJKPPXEKYCBY-AKCFYGDASA-N 0.000 description 1
- 229960001404 quinidine Drugs 0.000 description 1
- SBYHFKPVCBCYGV-UHFFFAOYSA-N quinuclidine Chemical compound C1CC2CCN1CC2 SBYHFKPVCBCYGV-UHFFFAOYSA-N 0.000 description 1
- GHBFNMLVSPCDGN-UHFFFAOYSA-N rac-1-monooctanoylglycerol Chemical compound CCCCCCCC(=O)OCC(O)CO GHBFNMLVSPCDGN-UHFFFAOYSA-N 0.000 description 1
- HDACQVRGBOVJII-JBDAPHQKSA-N ramipril Chemical compound C([C@@H](C(=O)OCC)N[C@@H](C)C(=O)N1[C@@H](C[C@@H]2CCC[C@@H]21)C(O)=O)CC1=CC=CC=C1 HDACQVRGBOVJII-JBDAPHQKSA-N 0.000 description 1
- 229960003401 ramipril Drugs 0.000 description 1
- RUOKEQAAGRXIBM-GFCCVEGCSA-N rasagiline Chemical compound C1=CC=C2[C@H](NCC#C)CCC2=C1 RUOKEQAAGRXIBM-GFCCVEGCSA-N 0.000 description 1
- 229960000245 rasagiline Drugs 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- CBQGYUDMJHNJBX-RTBURBONSA-N reboxetine Chemical compound CCOC1=CC=CC=C1O[C@H](C=1C=CC=CC=1)[C@@H]1OCCNC1 CBQGYUDMJHNJBX-RTBURBONSA-N 0.000 description 1
- 229960003770 reboxetine Drugs 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 238000006485 reductive methylation reaction Methods 0.000 description 1
- 238000001226 reprecipitation Methods 0.000 description 1
- 229960003147 reserpine Drugs 0.000 description 1
- 239000013557 residual solvent Substances 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- RAPZEAPATHNIPO-UHFFFAOYSA-N risperidone Chemical compound FC1=CC=C2C(C3CCN(CC3)CCC=3C(=O)N4CCCCC4=NC=3C)=NOC2=C1 RAPZEAPATHNIPO-UHFFFAOYSA-N 0.000 description 1
- 229960001534 risperidone Drugs 0.000 description 1
- 229960000311 ritonavir Drugs 0.000 description 1
- NCDNCNXCDXHOMX-XGKFQTDJSA-N ritonavir Chemical compound N([C@@H](C(C)C)C(=O)N[C@H](C[C@H](O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1SC=NC=1)CC=1C=CC=CC=1)C(=O)N(C)CC1=CSC(C(C)C)=N1 NCDNCNXCDXHOMX-XGKFQTDJSA-N 0.000 description 1
- 229960004136 rivastigmine Drugs 0.000 description 1
- 229960000371 rofecoxib Drugs 0.000 description 1
- RZJQGNCSTQAWON-UHFFFAOYSA-N rofecoxib Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C1=C(C=2C=CC=CC=2)C(=O)OC1 RZJQGNCSTQAWON-UHFFFAOYSA-N 0.000 description 1
- MDMGHDFNKNZPAU-UHFFFAOYSA-N roserpine Natural products C1C2CN3CCC(C4=CC=C(OC)C=C4N4)=C4C3CC2C(OC(C)=O)C(OC)C1OC(=O)C1=CC(OC)=C(OC)C(OC)=C1 MDMGHDFNKNZPAU-UHFFFAOYSA-N 0.000 description 1
- 229960000672 rosuvastatin Drugs 0.000 description 1
- BPRHUIZQVSMCRT-VEUZHWNKSA-N rosuvastatin Chemical compound CC(C)C1=NC(N(C)S(C)(=O)=O)=NC(C=2C=CC(F)=CC=2)=C1\C=C\[C@@H](O)C[C@@H](O)CC(O)=O BPRHUIZQVSMCRT-VEUZHWNKSA-N 0.000 description 1
- 235000002020 sage Nutrition 0.000 description 1
- 229950005137 saperconazole Drugs 0.000 description 1
- 229960001852 saquinavir Drugs 0.000 description 1
- QWAXKHKRTORLEM-UGJKXSETSA-N saquinavir Chemical compound C([C@@H]([C@H](O)CN1C[C@H]2CCCC[C@H]2C[C@H]1C(=O)NC(C)(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)C=1N=C2C=CC=CC2=CC=1)C1=CC=CC=C1 QWAXKHKRTORLEM-UGJKXSETSA-N 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 229960002646 scopolamine Drugs 0.000 description 1
- LACQPOBCQQPVIT-SEYKEWMNSA-N scopolamine hydrobromide trihydrate Chemical compound O.O.O.Br.C1([C@@H](CO)C(=O)O[C@H]2C[C@@H]3N([C@H](C2)[C@@H]2[C@H]3O2)C)=CC=CC=C1 LACQPOBCQQPVIT-SEYKEWMNSA-N 0.000 description 1
- 239000000932 sedative agent Substances 0.000 description 1
- 229940125723 sedative agent Drugs 0.000 description 1
- MEZLKOACVSPNER-GFCCVEGCSA-N selegiline Chemical compound C#CCN(C)[C@H](C)CC1=CC=CC=C1 MEZLKOACVSPNER-GFCCVEGCSA-N 0.000 description 1
- 229960003946 selegiline Drugs 0.000 description 1
- 229950009825 selfotel Drugs 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229940035004 seroquel Drugs 0.000 description 1
- FZHAPNGMFPVSLP-UHFFFAOYSA-N silanamine Chemical compound [SiH3]N FZHAPNGMFPVSLP-UHFFFAOYSA-N 0.000 description 1
- 229960003310 sildenafil Drugs 0.000 description 1
- 229960002855 simvastatin Drugs 0.000 description 1
- RYMZZMVNJRMUDD-HGQWONQESA-N simvastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)C(C)(C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 RYMZZMVNJRMUDD-HGQWONQESA-N 0.000 description 1
- 239000012279 sodium borohydride Substances 0.000 description 1
- 229910000033 sodium borohydride Inorganic materials 0.000 description 1
- NRHMKIHPTBHXPF-TUJRSCDTSA-M sodium cholate Chemical compound [Na+].C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC([O-])=O)C)[C@@]2(C)[C@@H](O)C1 NRHMKIHPTBHXPF-TUJRSCDTSA-M 0.000 description 1
- MNWBNISUBARLIT-UHFFFAOYSA-N sodium cyanide Chemical compound [Na+].N#[C-] MNWBNISUBARLIT-UHFFFAOYSA-N 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 1
- OABYVIYXWMZFFJ-ZUHYDKSRSA-M sodium glycocholate Chemical compound [Na+].C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCC([O-])=O)C)[C@@]2(C)[C@@H](O)C1 OABYVIYXWMZFFJ-ZUHYDKSRSA-M 0.000 description 1
- 229940079862 sodium lauryl sarcosinate Drugs 0.000 description 1
- 229940045845 sodium myristate Drugs 0.000 description 1
- RYYKJJJTJZKILX-UHFFFAOYSA-M sodium octadecanoate Chemical compound [Na+].CCCCCCCCCCCCCCCCCC([O-])=O RYYKJJJTJZKILX-UHFFFAOYSA-M 0.000 description 1
- 229940045870 sodium palmitate Drugs 0.000 description 1
- PFUVRDFDKPNGAV-UHFFFAOYSA-N sodium peroxide Chemical compound [Na+].[Na+].[O-][O-] PFUVRDFDKPNGAV-UHFFFAOYSA-N 0.000 description 1
- IJRHDFLHUATAOS-DPMBMXLASA-M sodium ricinoleate Chemical compound [Na+].CCCCCC[C@@H](O)C\C=C/CCCCCCCC([O-])=O IJRHDFLHUATAOS-DPMBMXLASA-M 0.000 description 1
- 229940080350 sodium stearate Drugs 0.000 description 1
- ODFAPIRLUPAQCQ-UHFFFAOYSA-M sodium stearoyl lactylate Chemical compound [Na+].CCCCCCCCCCCCCCCCCC(=O)OC(C)C(=O)OC(C)C([O-])=O ODFAPIRLUPAQCQ-UHFFFAOYSA-M 0.000 description 1
- 229940080352 sodium stearoyl lactylate Drugs 0.000 description 1
- JAJWGJBVLPIOOH-IZYKLYLVSA-M sodium taurocholate Chemical compound [Na+].C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCCS([O-])(=O)=O)C)[C@@]2(C)[C@@H](O)C1 JAJWGJBVLPIOOH-IZYKLYLVSA-M 0.000 description 1
- ADWNFGORSPBALY-UHFFFAOYSA-M sodium;2-[dodecyl(methyl)amino]acetate Chemical compound [Na+].CCCCCCCCCCCCN(C)CC([O-])=O ADWNFGORSPBALY-UHFFFAOYSA-M 0.000 description 1
- JJICLMJFIKGAAU-UHFFFAOYSA-M sodium;2-amino-9-(1,3-dihydroxypropan-2-yloxymethyl)purin-6-olate Chemical compound [Na+].NC1=NC([O-])=C2N=CN(COC(CO)CO)C2=N1 JJICLMJFIKGAAU-UHFFFAOYSA-M 0.000 description 1
- RMLUKZWYIKEASN-UHFFFAOYSA-M sodium;2-amino-9-(2-hydroxyethoxymethyl)purin-6-olate Chemical compound [Na+].O=C1[N-]C(N)=NC2=C1N=CN2COCCO RMLUKZWYIKEASN-UHFFFAOYSA-M 0.000 description 1
- GGXKEBACDBNFAF-UHFFFAOYSA-M sodium;hexadecanoate Chemical compound [Na+].CCCCCCCCCCCCCCCC([O-])=O GGXKEBACDBNFAF-UHFFFAOYSA-M 0.000 description 1
- JUQGWKYSEXPRGL-UHFFFAOYSA-M sodium;tetradecanoate Chemical compound [Na+].CCCCCCCCCCCCCC([O-])=O JUQGWKYSEXPRGL-UHFFFAOYSA-M 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 238000002466 solution-enhanced dispersion by supercritical fluid Methods 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 239000011877 solvent mixture Substances 0.000 description 1
- 229950006451 sorbitan laurate Drugs 0.000 description 1
- 235000011067 sorbitan monolaureate Nutrition 0.000 description 1
- 235000011069 sorbitan monooleate Nutrition 0.000 description 1
- 239000001593 sorbitan monooleate Substances 0.000 description 1
- 229940035049 sorbitan monooleate Drugs 0.000 description 1
- 235000011076 sorbitan monostearate Nutrition 0.000 description 1
- 239000001587 sorbitan monostearate Substances 0.000 description 1
- 229940035048 sorbitan monostearate Drugs 0.000 description 1
- 229950011392 sorbitan stearate Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 229940033331 soy sterol Drugs 0.000 description 1
- 239000008347 soybean phospholipid Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000005563 spheronization Methods 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000012430 stability testing Methods 0.000 description 1
- 229960001203 stavudine Drugs 0.000 description 1
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000000707 stereoselective effect Effects 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 235000019327 succinylated monoglyceride Nutrition 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- 229940035023 sucrose monostearate Drugs 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 229960004940 sulpiride Drugs 0.000 description 1
- KQKPFRSPSRPDEB-UHFFFAOYSA-N sumatriptan Chemical compound CNS(=O)(=O)CC1=CC=C2NC=C(CCN(C)C)C2=C1 KQKPFRSPSRPDEB-UHFFFAOYSA-N 0.000 description 1
- 229960003708 sumatriptan Drugs 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 229920005613 synthetic organic polymer Polymers 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 229960001685 tacrine Drugs 0.000 description 1
- YLJREFDVOIBQDA-UHFFFAOYSA-N tacrine Chemical compound C1=CC=C2C(N)=C(CCCC3)C3=NC2=C1 YLJREFDVOIBQDA-UHFFFAOYSA-N 0.000 description 1
- 229960000835 tadalafil Drugs 0.000 description 1
- IEHKWSGCTWLXFU-IIBYNOLFSA-N tadalafil Chemical compound C1=C2OCOC2=CC([C@@H]2C3=C([C]4C=CC=CC4=N3)C[C@H]3N2C(=O)CN(C3=O)C)=C1 IEHKWSGCTWLXFU-IIBYNOLFSA-N 0.000 description 1
- XVFJONKUSLSKSW-JTQLQIEISA-N talsaclidine Chemical compound C1CC2[C@@H](OCC#C)CN1CC2 XVFJONKUSLSKSW-JTQLQIEISA-N 0.000 description 1
- 229950001645 talsaclidine Drugs 0.000 description 1
- 150000003899 tartaric acid esters Chemical class 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- 229960003188 temazepam Drugs 0.000 description 1
- NRUKOCRGYNPUPR-QBPJDGROSA-N teniposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@@H](OC[C@H]4O3)C=3SC=CC=3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 NRUKOCRGYNPUPR-QBPJDGROSA-N 0.000 description 1
- 229960001278 teniposide Drugs 0.000 description 1
- VCKUSRYTPJJLNI-UHFFFAOYSA-N terazosin Chemical compound N=1C(N)=C2C=C(OC)C(OC)=CC2=NC=1N(CC1)CCN1C(=O)C1CCCO1 VCKUSRYTPJJLNI-UHFFFAOYSA-N 0.000 description 1
- 229960001693 terazosin Drugs 0.000 description 1
- DOMXUEMWDBAQBQ-WEVVVXLNSA-N terbinafine Chemical compound C1=CC=C2C(CN(C\C=C\C#CC(C)(C)C)C)=CC=CC2=C1 DOMXUEMWDBAQBQ-WEVVVXLNSA-N 0.000 description 1
- 229960002722 terbinafine Drugs 0.000 description 1
- 229960000351 terfenadine Drugs 0.000 description 1
- 229940116411 terpineol Drugs 0.000 description 1
- 125000000037 tert-butyldiphenylsilyl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1[Si]([H])([*]C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 150000003510 tertiary aliphatic amines Chemical class 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- ILLKMACMBHTSHP-UHFFFAOYSA-N tetradecaethylene glycol Chemical compound OCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO ILLKMACMBHTSHP-UHFFFAOYSA-N 0.000 description 1
- UWHCKJMYHZGTIT-UHFFFAOYSA-N tetraethylene glycol Chemical compound OCCOCCOCCOCCO UWHCKJMYHZGTIT-UHFFFAOYSA-N 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- 125000004055 thiomethyl group Chemical group [H]SC([H])([H])* 0.000 description 1
- BRNULMACUQOKMR-UHFFFAOYSA-N thiomorpholine Chemical compound C1CSCCN1 BRNULMACUQOKMR-UHFFFAOYSA-N 0.000 description 1
- ZWZVWGITAAIFPS-UHFFFAOYSA-N thiophosgene Chemical compound ClC(Cl)=S ZWZVWGITAAIFPS-UHFFFAOYSA-N 0.000 description 1
- 229960001196 thiotepa Drugs 0.000 description 1
- 239000001585 thymus vulgaris Substances 0.000 description 1
- PBJUNZJWGZTSKL-MRXNPFEDSA-N tiagabine Chemical compound C1=CSC(C(=CCCN2C[C@@H](CCC2)C(O)=O)C2=C(C=CS2)C)=C1C PBJUNZJWGZTSKL-MRXNPFEDSA-N 0.000 description 1
- 229960001918 tiagabine Drugs 0.000 description 1
- 229960003087 tioguanine Drugs 0.000 description 1
- PLHJCIYEEKOWNM-HHHXNRCGSA-N tipifarnib Chemical class CN1C=NC=C1[C@](N)(C=1C=C2C(C=3C=C(Cl)C=CC=3)=CC(=O)N(C)C2=CC=1)C1=CC=C(Cl)C=C1 PLHJCIYEEKOWNM-HHHXNRCGSA-N 0.000 description 1
- 229950011282 tivirapine Drugs 0.000 description 1
- 229960000984 tocofersolan Drugs 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 235000010384 tocopherol Nutrition 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 150000003611 tocopherol derivatives Chemical class 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 229960004394 topiramate Drugs 0.000 description 1
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 description 1
- 229960000303 topotecan Drugs 0.000 description 1
- 239000003440 toxic substance Substances 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 229960004380 tramadol Drugs 0.000 description 1
- TVYLLZQTGLZFBW-GOEBONIOSA-N tramadol Natural products COC1=CC=CC([C@@]2(O)[C@@H](CCCC2)CN(C)C)=C1 TVYLLZQTGLZFBW-GOEBONIOSA-N 0.000 description 1
- LLPOLZWFYMWNKH-UHFFFAOYSA-N trans-dihydrocodeinone Natural products C1C(N(CCC234)C)C2CCC(=O)C3OC2=C4C1=CC=C2OC LLPOLZWFYMWNKH-UHFFFAOYSA-N 0.000 description 1
- 239000003558 transferase inhibitor Substances 0.000 description 1
- 125000004665 trialkylsilyl group Chemical group 0.000 description 1
- 229960005294 triamcinolone Drugs 0.000 description 1
- GFNANZIMVAIWHM-OBYCQNJPSA-N triamcinolone Chemical compound O=C1C=C[C@]2(C)[C@@]3(F)[C@@H](O)C[C@](C)([C@@]([C@H](O)C4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 GFNANZIMVAIWHM-OBYCQNJPSA-N 0.000 description 1
- JOFWLTCLBGQGBO-UHFFFAOYSA-N triazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1Cl JOFWLTCLBGQGBO-UHFFFAOYSA-N 0.000 description 1
- 229960003386 triazolam Drugs 0.000 description 1
- SANWDQJIWZEKOD-UHFFFAOYSA-N tributyl(furan-2-yl)stannane Chemical compound CCCC[Sn](CCCC)(CCCC)C1=CC=CO1 SANWDQJIWZEKOD-UHFFFAOYSA-N 0.000 description 1
- DBGVGMSCBYYSLD-UHFFFAOYSA-N tributylstannane Chemical compound CCCC[SnH](CCCC)CCCC DBGVGMSCBYYSLD-UHFFFAOYSA-N 0.000 description 1
- NFACJZMKEDPNKN-UHFFFAOYSA-N trichlorfon Chemical compound COP(=O)(OC)C(O)C(Cl)(Cl)Cl NFACJZMKEDPNKN-UHFFFAOYSA-N 0.000 description 1
- GPMXUUPHFNMNDH-UHFFFAOYSA-N trifluperidol Chemical compound C1CC(O)(C=2C=C(C=CC=2)C(F)(F)F)CCN1CCCC(=O)C1=CC=C(F)C=C1 GPMXUUPHFNMNDH-UHFFFAOYSA-N 0.000 description 1
- 229960002341 trifluperidol Drugs 0.000 description 1
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 description 1
- 125000004951 trihalomethoxy group Chemical group 0.000 description 1
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 1
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 1
- 229960001930 valpromide Drugs 0.000 description 1
- OMOMUFTZPTXCHP-UHFFFAOYSA-N valpromide Chemical compound CCCC(C(N)=O)CCC OMOMUFTZPTXCHP-UHFFFAOYSA-N 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- PJDFLNIOAUIZSL-UHFFFAOYSA-N vigabatrin Chemical compound C=CC(N)CCC(O)=O PJDFLNIOAUIZSL-UHFFFAOYSA-N 0.000 description 1
- 229960005318 vigabatrin Drugs 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 235000019155 vitamin A Nutrition 0.000 description 1
- 239000011719 vitamin A Substances 0.000 description 1
- 235000019166 vitamin D Nutrition 0.000 description 1
- 239000011710 vitamin D Substances 0.000 description 1
- 150000003710 vitamin D derivatives Chemical class 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 235000019168 vitamin K Nutrition 0.000 description 1
- 239000011712 vitamin K Substances 0.000 description 1
- 150000003721 vitamin K derivatives Chemical class 0.000 description 1
- 235000012711 vitamin K3 Nutrition 0.000 description 1
- 239000011652 vitamin K3 Substances 0.000 description 1
- 229940045997 vitamin a Drugs 0.000 description 1
- 229940046008 vitamin d Drugs 0.000 description 1
- 229940046010 vitamin k Drugs 0.000 description 1
- 229940041603 vitamin k 3 Drugs 0.000 description 1
- 239000000341 volatile oil Substances 0.000 description 1
- BCEHBSKCWLPMDN-MGPLVRAMSA-N voriconazole Chemical compound C1([C@H](C)[C@](O)(CN2N=CN=C2)C=2C(=CC(F)=CC=2)F)=NC=NC=C1F BCEHBSKCWLPMDN-MGPLVRAMSA-N 0.000 description 1
- 229960004740 voriconazole Drugs 0.000 description 1
- 229960005080 warfarin Drugs 0.000 description 1
- PJVWKTKQMONHTI-UHFFFAOYSA-N warfarin Chemical compound OC=1C2=CC=CC=C2OC(=O)C=1C(CC(=O)C)C1=CC=CC=C1 PJVWKTKQMONHTI-UHFFFAOYSA-N 0.000 description 1
- 229960000523 zalcitabine Drugs 0.000 description 1
- MVWVFYHBGMAFLY-UHFFFAOYSA-N ziprasidone Chemical compound C1=CC=C2C(N3CCN(CC3)CCC3=CC=4CC(=O)NC=4C=C3Cl)=NSC2=C1 MVWVFYHBGMAFLY-UHFFFAOYSA-N 0.000 description 1
- 229960000607 ziprasidone Drugs 0.000 description 1
- 239000002888 zwitterionic surfactant Substances 0.000 description 1
- 239000004711 α-olefin Substances 0.000 description 1
- 239000002076 α-tocopherol Substances 0.000 description 1
- 235000004835 α-tocopherol Nutrition 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/44—Oils, fats or waxes according to two or more groups of A61K47/02-A61K47/42; Natural or modified natural oils, fats or waxes, e.g. castor oil, polyethoxylated castor oil, montan wax, lignite, shellac, rosin, beeswax or lanolin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/145—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
- A61K9/1075—Microemulsions or submicron emulsions; Preconcentrates or solids thereof; Micelles, e.g. made of phospholipids or block copolymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/146—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1635—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4866—Organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5084—Mixtures of one or more drugs in different galenical forms, at least one of which being granules, microcapsules or (coated) microparticles according to A61K9/16 or A61K9/50, e.g. for obtaining a specific release pattern or for combining different drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Inorganic Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Virology (AREA)
- Oncology (AREA)
- AIDS & HIV (AREA)
- Tropical Medicine & Parasitology (AREA)
- Communicable Diseases (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
"composições farmacêuticas compreendendo, um composto de droga básico, respectivamente um ácido, um tensoativo e um ácido solúvel em água fisiologicamente tolerável, respectivamente, uma base". a invenção proporciona uma nova composição farmacêutica compreendendo um composto de droga ácido, respectivamente, um básico, um tensoativo e um ácido solúvel em água fisiologicamente tolerável, respectivamente, uma base, caracterizada pelo fato de que a proporção de ácido, respectivamente, base:composto de droga é de pelo menos 1:1 em peso.
Description
(54) Título: COMPOSIÇÕES FARMACÊUTICAS COMPREENDENDO UMA DROGA BÁSICA OU ÁCIDA, UM TENSOATIVO, E UM ÁCIDO OU BASE SOLÚVEL EM ÁGUA FISIOLOGICAMENTE TOLERÁVEL (51) Int.CI.: A61K 9/00 (30) Prioridade Unionista: 29/11/2002 EP PCT/EP02/13558 (73) Titular(es): JANSSEN PHARMACEUTICA N.V.
(72) Inventor(es): ROGER PETRUS GEREBERN VANDECRUYS; JOZEF PEETERS; MARCUS ELI BREWSTER (85) Data do Início da Fase Nacional: 24/05/2005
Relatório Descritivo da Patente de Invenção para COMPOSIÇÕES FARMACÊUTICAS COMPREENDENDO UMA DROGA BÁSICA OU ÁCIDA, UM TENSOATIVO, E UM ÁCIDO OU BASE SOLÚVEL EM ÁGUA FISIOLOGICAMENTE TOLERÁVEL.
A presente invenção refere-se a novas composições farmacêuticas, em particular composições e formas de dosagem que proporcionam captação e liberação aperfeiçoadas da droga quando de administração a cavidades do corpo externamente ocas (por exemplo, o trato gastrointestinal) ou quando de administração tópica, especialmente para compostos de droga solubilizados em ácido.
Muitos composto de drogas, embora possuindo propriedades terapêuticas desejadas, são usados ineficazmente devido à sua baixa solubilidade em água. Assim, por exemplo, onde tais compostos são administrados oralmente, apenas uma pequena fração da droga é captada pelo sangue durante trânsito no trato gastrointestinal. Como um resultado, para se obter captação de droga adequada, pode ser necessário administrar altas doses do composto de droga, para prolongar o período de administração de droga ou fazer administrações frequentes do composto de droga. Na verdade, a baixa solubilidade e, conseqüentemente, baixa biodisponibilidade de uma droga pode fazer com que uma droga alternativa, talvez uma com os efeitos colaterais indesejados ou uma a qual requer administração invasiva (por exemplo, através de injeção ou infusão), tenha de ser usada em lugar a droga baixamente solúvel.
Uma abordagem à baixa solubilidade é derivatizar a molécula de droga para introduzir grupos de solubilização em água, por exemplo, grupos iônicos tais como grupos carboxila ou grupos não-iônicos tais como grupos polihidróxialquila, de modo a produzir um derivado mais solúvel. Essa abordagem, contudo, nem sempre tem sucesso, uma vez que pode não ser possível manter adequadamente alta eficácia terapêutica e, adequadamente, baixa toxicidade ou outros efeitos colaterais. Assim, um exemplo de uma droga baixamente solúvel em água a qual não tenha sido supercultivada por um derivado solubilizado é o agente antifúngico itraconazol. ' ÃÇ
Portanto, tentativas têm sido feitas para intensificar a captação de drogas tal como itraconazol através de aumento da área de superfície do composto de droga exposta à saliva ou fluido gástrico e, conseqüentemente, promover dissolução do composto de droga, através de revestimento fino do composto de droga sobre partículas de veículo essencialmente inerte, por exemplo, glóbulos de açúcar. Isso, contudo, tem a deficiência de que o volume de composição sólida requerido para administração uma determinada quantidade do composto de droga é muito alta, uma vez que o veículo con10 tribur significativamente para o volume global de administração. Uma vez que a administração de cápsulas ou comprimidos de grande volume ou de grandes quantidades de cápsulas ou comprimidos com um volume menor proporciona dificuldades para o paciente, as deficiências dessa abordagem são óbvias.
Ainda outra abordagem tem sido administrar o composto de droga na forma de uma solução do composto de droga e um agente de complexação de droga tal como uma ciclodextrina. Essa abordagem tem limitações também pelo fato de que a formulação está limitada àquelas drogas as quais são capazes de formar complexos com as ciclodextrinas, pelo fato de que o volume de dosagem está limitado pela energia de solubilização do agente de complexação, pelo fato de que formas sólidas prontamente transformadas em unidades não podem ser usadas e pelo fato de que não existe liberação gradual do composto de droga por captação biológica.
O composto de droga também pode ser formulado como uma dispersão sólida em ciclodextrinas junto com um ácido fisiologicamente tolerável solúvel em água e um polímero orgânico fisiologicamente tolerável solúvel em água. Referência, portanto, é feita ao WO 98/55148. Essa abordagem tem limitações pelo fato de que a formulação está limitada àquelas drogas as quais são capazes de formar complexos com as ciclodextrinas e pelo fato de que o volume de dosagem está limitado pela energia de solubilização do agente de complexação.
Outra abordagem é aumentar a liberação da droga da forma de
dosagem e, conseqüentemente, intensificar a biodisponibilidade oral da droga é administrar a droga junto com um tensoativo adequado.
O WO 97/35587 descreve uma formulação líquida compreendendo um inibidor de protease de HIV e um derivado de tocoferol solúvel em água, em particular Vitamina E-TPGS.
O WO 98/08490 descreve uma composição de co-precipitado seco sóiido compreendendo poiietilenoglicol succinato de tocoferol, um ingrediente ativo lipofílico e um adjuvante de dispersão.
O WO 99/26607 descreve dispersões sólidas de uma droga e
Vitamina E TPGS.
O WO 99/45918 descreve composições compreendendo um taxano, um ou mais tensoativos e um ácido. O ácido é incluído na formulação para melhorar a estabilidade do taxano.
O WO 97/02017 descreve dispersões sólidas compreendendo 15 um ingrediente ativo baixamente solúvel em um polímero de poloxâmero hidrofílico. A dispersão pode ainda conter um ácido. O ácido é incluído na dispersão sólida de forma a proporcionar uma disponibilidade gradual do ácido para promover a solubiüzação do ingrediente ativo sobre o grosso da curva da taxa de liberação.
As composições da presente invenção são distinguíveis das composições da técnica anterior peio fato de que elas proporcionam um perfil de dissolução mais rápido do composto de droga e/ou pelo fato de que elas são capazes de proporcionar uma solubilidade maior do composto de droga (criando uma condição super-saturada). isso resulta em uma biodis25 ponibilidade intensificada do composto de droga; uma captação biológica aperfeiçoada do composto de droga (um perfil de tempo aperfeiçoado para um teor de droga no plasma do paciente, isto é, o perfil farmacocinético definido por parâmetros tais como AUC, tmax, Cmax, etc. é aperfeiçoado). A incorporação do composto de droga nas composições da presente invenção tam30 bém é independente da formação de complexo, o que torna as presentes composições adequadas para a formulação de uma ampla faixa de composto de drogas.
ι_
Descobriu-se que as características descritas acima das presentes composições poderíam ser obtidas através de combinação de um composto, de droga ácido, respectivamente, um básico, com um tensoativo e uma quantidade significativa de um ácido solúvel em água, respectivamente, uma base.
Assim, encarada sob um aspecto, a invenção proporciona uma composição farmacêutica compreendendo um composto de droga básico, um tensoativo e um ácido solúvel em água fisiologicamente tolerável caracterizado pelo fato de que a proporção de ácido:composto de droga é pelo menos 1:1 em peso ou compreendendo um composto de droga ácido, um tensoativo e uma base fisiologicamente tolerável solúvel em água caracterizado pelo fato de que a proporção de base.composto de droga é pelo menos 1:1 em peso.
Em outras palavras, a presente invenção proporciona uma composição farmacêutica compreendendo um composto de droga ácido, respectivamente, um básico, um tensoativo e um ácido solúvel em água fisiologicamente tolerável, respectivamente, uma base, caracterizado pelo fato de que a proporção de ácido, respectivamente, base:composto de droga é pelo menos 1:1 em peso.
Vista sob um outro aspecto, a invenção proporciona o uso de um composto de droga ácido, respectivamente, um básico, um tensoativo e um ácido solúvel em água fisiologicamente tolerável, respectivamente, uma base, em uma proporção de ácido, respectivamente, uma base:droga de pelo menos 1:1 em peso para a fabricação de uma composição farmacêutica de acordo com a invenção para uso em um método de profilaxia, terapia ou diagnóstico no corpo de um ser humano ou um animal não-humano (por exemplo, mamífero, réptil ou ave).
Vista sob um outro aspecto, a invenção proporciona um método de profilaxia, terapia ou diagnóstico no corpo de um ser humano ou um animal não-humano (por exemplo, mamífero, réptil ou ave) o qual compreende administração ao referido corpo de uma dose profilátrca, terapêutica ou diagnosticamente eficaz de uma composição farmacêutica, o aperfeiçoamento
compreendendo uso, como a referida composição, da composição de acordo com a presente invenção,
Embora não se deseje estar preso à teoria, acredita-se que o perfil de dissolução vantajoso do composto de droga para as composições da invenção é obtido como um resultado de uma combinação dos efeitos dos componentes da composição quando de exposição à água ou fluidos corporais aquosos.
No caso da composição compreender um composto de droga básico e um ácido solúvel em água fisiologicamente tolerável, a água e o ácido proporcionam, quando de exposição à água ou fluidos corporais aquosos, um microambiente ácido no quai a solubilidade do composto de droga básico é aumentada. A presença do tensoativo causa um aumento adicional na solubilidade do composto de droga, desse modo, produzindo uma solução super-saturada do composto de droga.
No caso da composição compreender um composto de droga ácido e uma base fisiologicamente tolerável solúvel em água, a água e a base proporcionam, quando de administração, um microambiente alcalino no qual a solubilidade do composto de droga ácido é aumentada. O tensoativo, conforme descrito acima, causa a produção de uma solução super-saturada do composto de droga.
A solução super-saturada a qual é criada quando de administração das presentes composições proporciona uma biodisponibilidade aumentada do composto de droga.
Uma vez que as presentes composições proporcionam, em si, 25 um microambiente no qual a solubilidade do composto de droga é aumentada, elas podem ser oralmente administradas a qualquer momento do dia, independentemente do alimento ingerido pelo indivíduo ao qual elas são administradas.
Composições preferidas são aquelas composições compreen30 dendo um composto de droga básico, um tensoativo e um ácido soíúveí em água fisiologicamente tolerável caracterizado pelo fato de que a proporção de ácido:composto de droga é peio menos 1:1 em peso.
Como o tensoativo nas composições da invenção, pode ser usado qualquer um dos tensoativos fisiologicamente toleráveis adequados para uso em uma composição farmacêutica.
É bem conhecido na técnica que um tensoativo é um composto 5 anfifílrco; ele contém porções polares, hidrofílicas, bem como porções nãopolares, hidrofóbicas. Os termos hidrofílica ou hidrofóbica são termos relativos.
A hidrofrlicidade ou hidrofobicidade relativa de um tensoativo pode ser expressa por seu valor de equilíbrio hidrofílico-lipofílico (Valor de
HLB). Tensoativos com um valor de HLB menor são categorizados como sendo tensoativos hidrofóbicos, tensoativos enquanto que tensoativos com um valor de HLB maior são categorizados como sendo tensoativos hidrofílicos. Como uma regra, tensoativos tendo um valor de HLB maior do que cerca de 10 são, geralmente, considerados como sendo tensoativos hidrofíli15 cos; tensoativos tendo um valor de HLB menor do que cerca de 10 são, geralmente, considerados como sendo tensoativos hidrofóbicos.
As presentes composições compreendem, de preferência, um tensoativo hidrofílico.
Será apreciado que o valor de HLB de um tensoativo é apenas uma diretriz geral para indicar a hidrofiiicidade/hidrofobicidade de um tensoativo. O valor de HLB de um tensoativo em particular pode variar, dependendo do método usado para determinar o valor de HLB; dependendo de sua fonte comercial; e está sujeito à variabilidade de lote para lote. Aqueles habilitados na técnica podem identificar prontamente tensoativos hidrofíiicos a25 dequados para uso nas composições farmacêuticas da presente invenção.
O tensoativo da presente invenção pode ser um tensoativo aniônico, um catiônico, um zwitteriônico ou um não-iônico, o último sendo preferido. O tensoativo da presente invenção também pode ser uma mistura de dois ou mais tensoativos.
A escolha do tensoativo pode ser dirigida pelo composto de droga a ser usado em particular na composição da invenção. Assim, o tensoativo com maior capacidade de solubilização para o composto de droga em
particular, com uma capacidade intensificada de proporcionar uma condição super-saturada, pode ser preferido.
Tensoativos adequados para uso nas composições da presente invenção são listados abaixo. Deverá ser enfatizado que a referida lista de tensoativos é apenas ilustrativa, representativa e não exaustiva. Assim, a invenção não está limitada aos tensoativos listados abaixo. Nas presentes composições, também misturas de tensoativos podem ser usadas.
Tensoativos adequados os quais podem ser usados na presente invenção compreendem:
a) monoésteres de ácido graxo de polietileno glicol compreendendo ésteres de ácido láurico, ácido oléico, ácido esteárico, ácido ricinóico e semelhantes com PEG 6, 7, 8, 9, 10, 12, 15, 20, 25, 30, 32, 40, 45, 50, 55, 100, 200, 300, 400, 600 e semelhantes, por exemplo, laurato ou estearato de PEG-6, oleato ou laurato de PEG-7, laurato ou oleato ou estearato de PEG15 8, oleato ou estearato de PEG-9, laurato ou oleato ou estearato de PEG-10, laurato ou oleato ou estearato ou ricinoleato de PEG-12, estearato ou oleato de PEG-15, laurato ou oleato ou estearato de PEG-20, estearato de PEG-25, laurato ou oleato ou estearato de PEG-32, estearato de PEG-30, laurato ou oleato ou estearato de PEG-40, estearato de PEG-45, estearato de PEG-50, estearato de PEG-55, oleato ou estearato de PEG-100, oleato de PEG-200, oleato de PEG-400, oleato de PEG-600; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Cithrol, Algon, Kessco, Lauridac, Mapeg, Cremophor, Emulgante, Nikkol, Myrj, Crodet, Albunol, Lactomul);
b) diésteres de ácido graxo de polietileno glicol compreendendo diésteres de ácido láurico, ácido esteárico, ácido pálmico, ácido oléico e semelhantes com PEG-8, 10, 12, 20, 32, 400 e semelhantes, por exemplo, dilaurato ou diestearato de PEG-8, dipalmitato de PEG-10, dilaurato ou diestearato ou dioleato de PEG-12, dilaurato ou diestearato ou dioleato de PEG20, dilaurato ou diestearato ou dioleato de PEG-32, dioleato ou diestearato de PEG-400; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Mapeg, Polialso, Kessco, Cithrol);
c) misturas de mono- e diéster de ácido graxo de polietileno gli-
col tais como, por exemplo, mono- e dilaurato de PEG 4-150, mono- e dioleato de PEG 4-150, mono- e diestearato de PEG 4-150 e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Kessco);
d) glicerol ésteres de ácido graxo de polietileno glicol tais como, por exemplo, gliceril laurato ou gliceril estearato ou gliceril oleato de PEG-20, gliceril laurato ou gliceril oieato de PEG-30, gliceril laurato de PEG-15, gliceril laurato de PEG-40 e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Tagat, Glycerox L, Capmul);
e) produtos da transesterificação de álcool-óleo compreendendo ésteres de álcoois ou poliálcoois, tais como glicerol, propileno glicol, etileno glicol, polietileno glicol, sorbitol, pentaeritritol e semelhantes com óleos naturais e/ou hidrogenados óleos ou vitaminas solúveis em óleo, tais como óleo de rícino, óleo de rícino hidrogenado, vitamina A, vitamina D, vitamina E, vitamina K, um óleo vegetai ingerívei, por exemplo, óleo de milho, óleo de oliva, óleo de amendoim, óleo de semente de palma, óleo de semente de damasco, óleo de amêndoa e semelhantes, tais como óieo de rícino ou óleo de rícino hidrogenado ou glicerídeos de milho ou glicerídeos de amêndoa de PEG-20, óieo de rícino de PEG-23, óleo de rícino hidrogenado ou trioleato de PEG-25, óleo de rícino de PEG-35, óleo de rícino ou óleo de rícino hidrogenado de PEG-30, óleo de rícino de PEG-38, óieo de rícino ou óleo de rícino hidrogenado ou óleo de semente de palma de PEG-40, óleo de rícino hidrogenado de PEG-45, óleo de rícino ou óleo de rícino hidrogenado de PEG50, óleo de rícino de PEG-56, óleo de rícino ou óleo de rícino hidrogenado ou glicerídeos de milho ou glicerídeos de amêndoa de PEG-60, óleo de rícino hidrogenado de PEG-80, óleo de rícino ou óleo de rícino hidrogenado de PEG-100, óleo de rícino de PEG-200, glicerídeos caprílico/cáprico de PEG8, glicerídeos caprílico/cáprico de PEG-6, glicerídeo de lauroil macrogol-32, glicerídeo de estearoil macrogoí, tocoferil succinato de PEG-1000 (TPGS);
(os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Emalex, Cremophor, Emulgante, Eumulgín, Nikkol, Thomley, Simulsol,
Cerex, Crovol, Labrasol, Softigen, Gelucire, Vitamin E TPGS);
f) ácidos graxos poliglicerizados compreendendo pofígJicerol ésteres de ácido graxos tais como, por exemplo, laurato ou oleato ou estearato de poliglicerila-10, mono- e dioleato de poliglícerila-10, poli-ricinoleato de poliglicerila e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Nikkol Decaglyn, Caprol ou Polimuls);
g) derivados de esterol compreendendo derivados de polietileno glicol de esterol, tais como colesterol éter de PEG-24, colestanol de PEG-30, fito esterol de PEG-25, esterol de soja de PEG-30 e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Solulan® ou Nikkol BPSH);
h) sorbitano ésteres de ácido graxo de polietileno glicol tais como, por exemplo, sorbitano laurato de PEG-10, sorbitano monolaurato ou sorbitano triestearato ou sorbitano monooleato ou sorbitano trioleato ou sorbitano monoisoestearato ou sorbitano monopalmitato ou sorbitano monoestearato de PEG-20, sorbitano monolaurato de PEG-4, sorbitano monooleato de PEG-5, sorbitano monooleato ou sorbitano monolaurato ou sorbitano monoestearato de PEG-6, sorbitano monoestearato de PEG-8, sorbitano tetraoleato de PEG-30, sorbitano oleato ou sorbitano tetraoieato de PEG-40, sorbitano tetraestearato de PEG-60, sorbitano monolaurato de PEG-80, sorbitol hexaoleato de PEG (Atlas G-1086) e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Liposorb, Tween, Dacol MSS, Nikkol, Emalex, Atlas);
i) alquil éteres de polietileno glicol tais como, por exemplo, oleil éter ou cetil éter ou estearil éter de PEG-10, oleil éter ou cetil éter ou estearil éter de PEG-20, lauril éter de PEG-9, lauril éter de PEG-23 (iauret-23), estearil éter de PEG-100 e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Volpo, Brij);
j) ésteres de açúcar tais como, por exemplo, diestearato/monoestearato de sacarose, monoestearato ou monopalmitato ou monolaurato de sacarose e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Sucro ester, Crodesta, Saccharose monolaurato);
k) alquil fenóis de polietileno glicol tais como, por exemplo, nonil fenol de PEG-10-100 (série Triton X), octil fenol éter de PEG-15-100 (série Triton N) e semelhantes;
l) copolímeros em blocos de polioxietileno-polioxipropileno (poloxâmeros) tais como, por exemplo, poloxâmero 108, poloxâmero 188, poloxâmero 237, poloxâmero 288 e semelhantes; (os tensoativos pertencendo a esse grupo são, por exemplo, conhecidos como Synperonic PE, Pluronic, Emkalyx, Lutrol®, Supronic, Monolan, Pluracare, Plurodac);
m) tensoativos iônicos incluindo tensoativos catiônicos, aniônicos e zwitteriônicos, tais como os sais de ácido graxo, por exemplo, oleato de sódio, lauril sulfato de sódio, lauril sarcosinato de sódio, dioctil sulfosuccinato de sódio, miristato de sódio, palmitato de sódio, estearato de sódio, ricinoleato de sódio e semelhantes; tais como sais biliares, por exemplo, colato de sódio, taurocolato de sódio, glicocolato de sódio e semelhantes; tais como fosfolipídios, por exemplo, lecitina de ovo/soja, lecitina hidroxilada, iisofosfatidilcolina, fosfatidilcolina, fosfatidil etanolamina, fosfatidií glicerol, fosfatidil serina e semelhantes; tais como ésteres de ácido fosfórico, por exemplo, oleil éter fosfato de dietanolamônio de polioxietileno-10, os produtos da esterificação de álcoois graxos ou etoxilatos de álcool graxo com ácido ou anidrido fosfórico; tais como carboxilatos, por exemplo, monoglicerídeos succinilados, estearil fumarato de sódio, estearoil hidrogenossuccinato de propileno glicol, ésteres de ácido tartárico mono/diacetilados de mono- e diglicerídeos, ésteres de cítrico ácido de mono- e digiicerídeos, gliceril-lacto ésteres de ácido graxos, ésteres lactílicos de ácidos graxos, estearoil-2lactílato de cálcio/sódio, estearoil lactilato de cálcio/sódio, sais de alginato, alginato de propileno glicol, éter carboxilatos e semelhantes; tais como sulfatos e sulfonatos, por exemplo, alquil sulfatos etoxilados, alquil benzeno sulfatos, alfa-olefin sulfonatos, acil isetionatos, acil tauratos, alquil gliceril éter sulfonatos, octil sulfossuccinato dissódico, undecilenoamido-MEAsulfossuccinato dissódico e semelhantes; tais como tensoativos catiônicos, por exemplo, brometo de hexadecil triamônio, brometo de decil trimetil amônio, brometo de cetil trimetil amônio, cloreto de dodecii amônio, sais de alquil benzildimetilamônío, sais de diisobutií fenoxietoxidi metil benzilamônio, sais de alquilpiridínio, betaínas (lauril betaína), aminas etoxiladas (polioxietileno15 amina de coco) e semelhantes.
Quando na lista acima de tensoativos adequados, diferentes 5 possibilidades são listadas tais como, por exemplo, oleil éter ou cetil éter ou estearil éter de PEG-20, isso significa que oleii éter de PEG-20 e cetil éter de PEG-20 e estearil éter de PEG-20 são considerados. Assim, por exemplo, óieo de rícino ou óleo de rícino hidrogenado ou glicerídeos de milho ou glicerídeos de amêndoa de PEG-20 deve ser lido como óleo de rícino de PEG-20 e óleo de rícino hidrogenado de PEG-20 e glicerídeos de milho de PEG-20 e glicerídeos de amêndoa de PEG-20.
Nas composições da invenção, o tensoativo está presente, de preferência, a 1 a 70% em peso, mais preferivelmente 5 a 55%, ainda mais preferivelmente 10 a 50% em peso (com relação ao peso total de tensoativo, ácido e droga). A quantidade de tensoativo usada, contudo, geralmente, será dependente de uma quantidade de droga e do composto de droga em si. A proporção em peso de tensoativo para droga estará, de preferência, na faixa de 100:1 a 1:5, especialmente 50:1 a 1:2, more especialmente 10:1 a 1:1.
Tensoativos preferidos nas presentes composições pertencem ao grupo dos sorbitano ésteres de ácido graxo de polietileno glicol, ao grupo dos produtos da transesterificação de álcool-óleo ou ao grupos dos copolímeros em blocos de polioxietileno-polioxipropileno. Mais preferivelmente, os tensoativos nas presentes composições pertencem ao grupo dos sorbitano ésteres de ácido graxo de polietileno glicol ou ao grupo dos produtos da transesterificação de álcool-óleo. Tensoativos mais preferidos são os tensoativos conhecidos como Tween, os tensoativos conhecidos como Cremophor e Vitamina E TPGS (α-tocoferil succinato de polietileno glicol, também abreviado como TPGS), especialmente Cremophor RH 40 e Vitamina E TPGS.
Como uma concretização alternativa das composições da pre30 sente invenção, o tensoativo pode ser substituído por uma cera adequada tal como, por exemplo, polietileno glicol e semelhantes.
O ácido usado nas composições da invenção pode ser qualquer
um dos ácidos solúveis em água fisiologicamente toleráveis, em particular qualquer um dos ácidos inorgânicos ou, mais preferivelmente, ácidos orgânicos convencionalmente usados na preparação de sais de ácido de compostos de drogas, por exemplo, ácidos cítrico, fumárico, tartárico, maléico, máli5 co, succínico, oxáiico, malônico, benzóico, mandélico e ascórbico.
Ácido tartárico e mais especialmente ácido cítrico são preferidos, uma vez que os sais que eles formam com os compostos de drogas usualmente têm uma tendência reduzida de se precipitar de soluções aquosas. Em geral, contudo, qualquer ácido o qual não é tão forte para causar degra10 dação do tensoativo e ainda o qual é capaz, quando da adição de água, de gerar um ambiente de baixo pH, de preferência um pH menor do que 4 e idealmente um pH de cerca de 2, pode ser usado. O ácido pode estar na forma líquida (por exemplo, solução) ou sólida; contudo, ácidos os quais são sólidos em condições ambiente em suas formas anídrica ou de hidrato, ge15 ralmente serão preferidos.
A base usada nas composições da invenção pode ser qualquer uma das bases solúveis em água fisiologicamente toleráveis, em particular qualquer uma das bases inorgânicas ou orgânicas convencionalmente usadas na preparação de sais alcalinos de compostos de drogas, por exemplo, as bases de metal alcalino e alcalino-terroso, por exemplo, hidróxido, hidrocarbonato ou carbonato de lítio-, sódio-, potássio-, magnésio- ou cálcio e semelhantes, NH3, benzatina, /V-metil-D-glucamina, hidrabamina, etanolamina, dietanolamina, trietanolamina e semelhantes, amínoácidos tais como, por exemplo, arginina, lisina e semelhantes.
Nas composições da invenção, o ácido está presente em uma proporção de ácído:droga de pelo menos 1:1 em peso, de preferência a proporção em peso de ácido:droga oscila na faixa de 1:1 a 100:1, mais preferivelmente de 1:1 a 50:1, ainda mais preferivelmente de 1:1 a 10:1 e mais preferivelmente de 3:1 a 10:1. A quantidade de ácido usada dependerá do ácido e composto de droga selecionados, mas, em geral, um aumento na proporção relativa de ácido resultará em aceleração da dissolução da droga quando de contato com a água. A quantidade de ácido usada normalmente será pelo menos a quantidade necessária para formar um microambiente ácido quando de contato com a água, em particular um fluido corporal aquoso no qual a solubilidade do composto de droga é aumentada.
O ácido forma uma proporção significativa das presentes com5 posições que se dissolve rapidamente em fluidos corporais. Portanto, a presente invenção também se refere a uma composição farmacêutica compreendendo um composto de droga básico, um tensoativo e um ácido solúvel em água fisioiogicamente tolerável caracterizado pelo fato de que o percentual em peso de ácido oscila na faixa de 30 a 95%, de preferência de 45 a
95%, mais preferivelmente de 50 a 90%, mais preferivelmente de 50 a 65%.
De preferência, o percentual em peso é com relação ao peso do composto de droga básico, do tensoativo e do ácido solúvel em água fisiologicamente tolerável e opcionalmente o polímero.
Alternativamente, a presente invenção também se refere a uma composição farmacêutica compreendendo um composto de droga básico, um tensoativo e um ácido solúvel em água fisiologicamente tolerável caracterizado pelo fato de que a proporção molar de ácidozcomposto de droga é de pelo menos 3:1, de preferência pelo menos 5:1, mais preferivelmente pelo menos 10:1.
A presente invenção também se refere a uma composição farmacêutica compreendendo um composto de droga básico, um tensoativo e um ácido solúvel em água fisiologicamente tolerável caracterizado pelo fato de que o percentual em peso percentual de ácido oscila na faixa de 30 a 95% e caracterizado pelo fato de que a proporção de ácidozcomposto de droga é de pelo menos 1:1 em peso.
Alternativamente, a presente invenção também se refere a uma composição farmacêutica compreendendo um composto de droga básico, um tensoativo e um ácido solúvel em água fisiologicamente tolerável caracterizado pelo fato de que o percentual em peso de ácido oscila na faixa de
30 a 95% e caracterizado pelo fato de que a proporção molar de ácidozcomposto de droga é de pelo menos 3:1.
As quantidades específicas acima para o ácido também são
I
consideradas para a base naquelas composições da presente invenção as quais compreendem um composto de droga ácido, um tensoativo e uma base.
Embora os benefícios das composições da invenção sejam mais 5 pronunciados onde o composto de droga é não mais do que parcamente solúvel, um perfil de dissolução de droga obtenível usando-se a combinação de droga, tensoativo e ácido (ou base) é tal que perfis de captação de droga particularmente aperfeiçoados podem ser obtidos mesmo onde o composto de droga é mais solúvel.
Consequentemente, o composto de droga usado nas composi~ ções da invenção pode ser qualquer material orgânico ou inorgânico. O composto de droga pode exercer um efeito fisiológico local, bem como um efeito sistêmico, quer após penetração na mucosa ou - no caso de administração oral - após transporte para o trato gastrointestinal com saliva.
De preferência, o composto de droga é não mais do que praticamente solúvel, isto é, o qual é praticamente solúvel, ligeiramente solúvel, muito ligeiramente solúvel ou praticamente insolúvel em água pura a 21 °C (isto é, requerendo de 30, de 100, de 1000 ou de 10000 partes de água para colocar 1 parte em peso composto de droga em solução). Em particular, a droga é um composto de droga básico. O termo composto de droga básico define um composto de droga com um valor de pKa acima de 7 ou um composto de droga o qual pode ser solubilizado em um ácido/meio ácido. O termo composto de droga ácido define um composto de droga com um valor de pKa em torno de 7 ou um composto de droga o qual pode ser solubilizado em uma base/meio básico (alcalino).
Exemplos de compostos baixamente solúveis em água que podem ser usados nas composições da invenção incluem: nifedipina;
itraconazol (descrita no EP-A-6711);
saperconazol (veja US-A-4916134);
(-)-[2S-[2a,4a (S*)]]-4-[4-[4-[4-[[2-(4-clorofenil)]-2-[[(4-metil-4H1,2,4-triazol-3-il)tio]metil]-1,3-dioxo[an-4-il]metóxi]fenil]-1-piperazinil]fenil]-2,4-
dihidro-2-(1-metilpropil)-3H-1,2(4-triazol-3-ona (Composto 40 WO96/13499);
cisaprida (descrita no EP-A-76530);
(B)~N-[4-[2-etil-1-(1 H-1,2,4-triazol-1 -il)butil]fenil]-25 benzotiazolamina (descrita no WO-97/49704);
6,11 -d ihidro-11 -[1 -[2-[4-(2-quinolinilmetóxi)fenil]etil]-4piperidinilideno]-5H-imidazo[2,1 -b][3]benzazepina-3-carboxilato de metila (descrita no WO-97/34897);
4-[[4-amino-6-[(2,6-diclorofenil)metil]-1,3,5-triazin-210 il]amino]benzonitriia (descrito no EP-0.834.507);
(B-cis)-1 -[4-[4-[4-[[4-(2 t4-difluorofenil)-4-(1 H-1,2,4-triazol-1i (metil)-1,3-d ioxolan-2-il]metóxi]fen il]-1 -piperazinil]fenil]-3-(1 -metiletil)-2imidazolidinona;
(2S-cis)-1-[4-[4-[4-[[4~(2,4-difluorofenil)-4-(1 H-1,2,4-triazoM 15 ilmetil)-1,3-dioxolan-2-il]metóxi]fenil]-1 -p iperazin iljfen ií]-3-( 1 -metiletií)-2imidazolidinona;
3-[2-[3;4dihidrobenzofuro[3,2-c]piridin-2(1H)-il]etil]-2-metil-4Hpirido[1,2-a]pirimidin-4-ona;
/V-[2-[4-(4-clorofenil)-1-piperazinil]etil]-2-benzotiazolamÍna;
(B1 )-/V-[4-[2-(dimetilamino)-1 -(1 H-imidazol-1 -i l)propii]fen il]-2benzotiazolamina (descrita no WO-97/49704);
(B)-6-[amino(4-clorofenil)(1-metil-1H-imidazol-5-il)metil]-4-(3clorofenil)-1 -metil-2(1 H)-quinolinona', (B)-/V-[4-[2-etil-1 -(1 H-1,2,4-triazol-1 -il )butil]fenil]-225 benzotiazolamina;
monocloridrato de S-te-fdimetilaminoJA-metil-S-piridinil]^^dimetií-/V,/V-dipropilprrazolo[2,3-a]pirimidin-7-amina;
(S)-[1 -[2-[3-[(2,3-dihidro-1H-inden-2-il)óxr]-4-metóxifenil]propil]1 H-imidazol-2-il]cianamida;
(S)-hidroxibutanodioato (1:1) de (+)-(B-trans)-4-[1-[3,5bis(trifluorometil)benzoil]-2-(fenilmetil)-4-piperidinil]-/V-(2t6-dimetilfenil)-1 prperazinaacetamida;
(-)-[2S-[2ct,4a (S*)]]-4-[4-[4-[4-[[2-(4-clorofenil]-2-[[(4-metil-4/71,2,4-triazol~3-i l)tio] met i l]-1,3-dioxolan-4-il]metóxi]fenil]-1 -piperazinil]fenil]-2,4dihidro-2-(1-metilpropil)-3/7-1,2,4-triazol-3-ona;
(+)-(trans)-4-[1-[3,5-bis(trifluorometil)benzoil]-2-(fenilmetil)-45 piperidinil]-/V-(2,6-dimetilfenil)-1-piperazina acetamida;
os compostos descritos no WO 99/50256, WO 00/27828, WO 01/85699, WO 01/85700, WO 01/64674 e EP 0.834.507; os referidos documentos incorporados aqui por referência;
compostos da fórmula (I) (referência, portanto, é feita ao 10 PCT/EP02/08953):
um /V-óxido, um sal de adição farmaceuticamente aceitável, uma amina quaternária ou uma forma estereoquimicamente isomérica dos mesmos, em que:
| -a1=a2-a3=a4- representa um radical bivalente da fórmula: | |
| -CH=CH-CH=CH- -N=CH-CH=CH- -N=CH-N=CH- | (a-1); (a-2); (a-3); |
| -N=CH-CH=N- | (a-4); |
| -N=N-CH=CH- | (a-5); |
| -b1=b2-b3=b4- representa um radical bivalente da fórmula: | |
| -CH=CH-CH=CH- | (b-1); |
| -N=CH-CH=CH- | (b-2); |
| -N=CH-N=CH- | (b-3); |
| -N=CH-CH=N- | (b-4); |
| -N=N-CH=CH- | (b-5); |
n é 0, 1, 2, 3 ou 4; e, no caso de -a1=a2-a3=a4- ser (a-1), então, n pode ser também 5;
m é 1, 2, 3 e, no caso de -b1=b2-b3=b4- ser (b-1), então, m pode ser também 4;
R1 é hidrogênio; arila; formila; Ci-6alquilcarbonila; Ci-galquiia; Ci-6alquilóxicarbonila; Ci-6alquila substituída por formila, Ci-6alquilcarbonila, Ci-6alquiloxicarbonila, Ci-6aiquiicarbonilóxi; Ci_6alquÍlóxiCi-6alquilcarbonila substituída por Ci-6alquilóxicarbonila;
cada R2 é, independentemente, hidróxi, halo, Ci-6alquila opcionalmente substituída por ciano ou -C(=O)R6, C3-7Cicloaiquila, C^alquenila opcionalmente substituída por um ou mais átomos de halogênio ou ciano, C2-6alquinila opcionalmente substituída por um ou mais átomos de halogênio ou ciano, Ci-6alquilóxicarbonila, carboxiia, ciano, nitro, amino, mono- ou di(Ci_6alquil)amÍno, polihalometíla, polihalometiitio, -S(=O)PR6, -NH-S(=O)PR6, -C(=O)R6, -NHC(=O)H, -C(=O)NHNH2, -NHC(=O)R6,-C(=NH)R6 ou um radicai da fórmula:
em que cada Ai é, independentemente, N, CH ou CR6; e A2 é NH, O, S ou NR6;
Xi é -NR5-, -NH-NH-, -N=N-, -O-, -C(=O)-, C^alcanodiíla,
-CHOH-, -S-, -S(=O)P-, -X2-C-i.4aicanodiil- ou -Ci-4alcanodiil-X2-;
X2 é -NR5-, -NH-NH-, -N=N-, -O-, -C(=O)-, -CHOH-, -S-, -S(=O)P-; R3 é NHR13; NR13R14; -C(=O)-NHR13; -C(=O)-NR13R14; -C(=O)R15; -CH=N-NH-C(=O)-R16; Ci-ealquila substituída por um ou mais substitu20 intes, cada um independentemente selecionado de ciano, NR9R10, -C(=O)NR9R10, -C(=O)-Ci-6alquiia ou R7; Cvealquila substituída por um ou mais substituintes, cada um independentemente selecionado de ciano, NR9R16, C(=O)-NR9R10, -C(=O)-C-i-6alquila ou R7 e em que 2 átomos de hidrogênio ligado ao mesmo átomo de carbono são substituídos por C-Malcanodiila; Ci_ 6aiquila substituída por hidróxi e um segundo substituinte selecionado de ciano, NR9R10, -C(=O)-NR9R10, -C(=O)-Ci-6alquila ou R7; Ci-ealquilóxiC^ 6alquila opcionalmente substituída por um ou mais substituintes, cada um independentemente selecionado de ciano, NR9R10, -C(=O)-NR9R10, -C(=O)Ci-6alquila ou R7; C2-6alquenila substituída por um ou mais substituintes, ca30 da um independentemente selecionado de halo, ciano, NR9R10, -C(=O)18
NR9R10, ~C(=0)-Ci_6alquila ou R7; C2-6alquinila substituída por um ou mais substituintes, cada um independentemente selecionado de halo, ciano, NR9R10, -C(=O)-NR9R10, -C^OJ-Cd-ealquila ou R7; -C(=N-O-R8)-Ci-4alquila; R7 ou -X3-R7;
X3 é -NR5-, -NH-NH-, -N=N-, -O-, -C(=O)-, -S-, -S(=O)P-, -X2-Ci-4 aicanodiii-, -Ci^alcanodiil-X2a-, -Ct.4a[canodiil-X2b-Ci-4alcanodiil, -C(=N-OR8)C-Malcanodiil-;
com X2a sendo -NH-NH-, -N=N-, -O-, -C(=O)-, -S-, -S(=O)P-; e com X2b sendo -NH-NH-, -N=N-, -C(=O)-, -S-, -S(=O)P-;
R4 é halo, hidróxi, C^aiquiia, C3.7cicloalquila, C1.6alquilóxi, ciano, nitro, polihaloC-i-6alquila, polihaloC-|.6alquilóxi, aminocarbonila, Cd_ 6alquiloxicarbonila, C1_6alquilcarbonila, formila, amino, mono- ou di(Ci4aÍquil)amino ou R7;
R5 é hidrogênio; ariia; formila; Ci-galquilcarbonila; C^alquila;
6alquiloxicarbonila; C^galquila substituída por formila, Ci-ealquilcarbonila, Ci-galquiloxicarbonila ou C<i-6alquilcarbonilóxi; Ci-.6alquilóxiOi6alquiicarbonila substituída por C-|-6alquiloxicarbonila;
R6 é C^alquila, amino, mono- ou difC^aiquiQamino ou polihaloC^alquila;
R7 é um carbociclo monocíclico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático a heterociclo monocíclico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático, em que cada um dos referidos sistemas de anel carbocíclico ou heterocíclico pode opcionalmente ser substituído por um, dois, três, quatro ou cinco substituintes, cada um in25 dependentemente selecionado de haio, hidróxi, mercapto, C-|-6alquila, hidróxiCi-6alquila, aminoCi-fjalquila, mono- ou di(C-t-6alquil)aminoC-j6aiquila, formila, Ci-galquilcarbonila, C3.7cicloalquila, Ci-6alquilóxi, C-]6alqutlóxicarbonila, C1 _6alquiltio, ciano, nitro, polihaloCi_6alquila, polihaloCi6alquilóxi, aminocarbonila, -CH(=N-O-R8), R7a, -X3-R7a ou R7a-Ci-4alquila;
R7a é um carbociclo monocíclico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático ou um heterociclo monocíclico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático, em que cada um
dos referidos sistemas de anel carbocíciico ou heterocíclico pode opcionalmente ser substituído por um, dois, três, quatro ou cinco substituintes, cada um independentemente selecionado de halo, hidróxi, mercapto, C-|-6alquila, hidróxíCi-6alquila, aminoCi-6alquila, mono ou di(C-i-6a[quil)aminoC-i5 6aiquila, formila, Cl-6alquilcarbonila, C3.7cic[oalquila, C-]-6a[quilóxi, Cigalquílóxicarbonila, Ci-6alquiltio, ciano, nitro, polihaloCi„6alquila, polihaloCi.
6alquilóxi, aminocarbonila, -CH(=N-O-R8);
R8 é hidrogênio, C^alquila, arila ou arilC^alquila;
R9 e R10 são, cada um independentemente, hidrogênio; hidróxi;
C-i-ealquila; Ci-6alquiióxi; C-i-6alquilcarbonila; Ci.6alquiloxicarbonila; amino; mono- ou di(Ci-6alquil)amino; mono- ou di(Cv6alquil)amínocarboníla; CH(=NR11) ou R7, em que cada um dos grupos Ci^alquila antes mencionados pode opcionalmente e cada um individualmente ser substituído por um ou dois substituintes, cada um independentemente selecionado de hidróxi,
Ci.6alquilóxi, hidróxiC-i.6alquilóxi, carboxila, Ci.6alquilóxicarbonila, ciano, amino, imino, mono- ou di(C-]-4alquil)amino, polihalometila, polihalometilóxi, polihalometiltio, -S(=O)PR6, -NH-S(=O)PR6, -C(=O)R6, -NHC(=O)H, C(=O)NHNH2, -NHC(=O)R6,-C(=NH)R6, R7; ou
R9 e R10 podem ser tomados juntos a fim de formar um radical bivalente ou trivalente da fórmula:
| -ch2-ch2-ch2-ch2- | (d-1) |
| -ch2-ch2-ch2-ch2-ch2- | (d-2) |
| -ch2-ch2-o-ch2-ch2- | (d-3) |
| -ch2-ch2-s-ch2-ch2- | (d-4) |
| -ch2-ch2-nr12-ch2-ch2- | (d-5) |
| -ch2-ch=ch-ch2- | (d-6) |
| =CH-CH=CH-CH=CH- | (d-7) |
| R11 é ciano; Ci.4alquila opcionalmente substituída por Ci-4alquiló- |
xi, ciano, amino, mono- ou di(C<i-4alquil)amino ou aminocarbonila; C-i^alquil30 carbonila; Ci^alqurlóxrcarbonila; aminocarbonila; mono- ou di(C-!^alquil)aminocarbonila;
R12 é hidrogênio ou C^alquila;
s
R13 e R14 são, cada um independentemente, C^ealquifa opcionalmente substituída por cíano ou aminocarbonila, C2-6alquenila opcionalmente substituída por ciano ou aminocarbonila, C2.6alquinila opcionaímente substituída por cíano ou aminocarbonila;
R15 é Ci-6alquila substituída por ciano ou aminocarbonila;
R16 é C-i-galquila opcionalmente substituída por ciano ou aminocarbonila, ou R7;
p é 1 ou 2;
aríia é fenila ou fenila substituída por um, dois, três, quatro ou cinco substituintes, cada um independentemente selecionado de halo, hidróxi, mercapto, Ci-6alquila, hidróxiC-i-6alquila, aminoCi-ealquila, mono ou di(C-|-6alquii)aminoCi-6alquila, Cv6alquilcarbonila, C3.7cicloalquila, Ci6alquilóxi, C-i-gaiquilóxicarbonila, C-]-galquiltio, ciano, nitro, polihaloCi. ealquila, polihaloCi_6alquiíóxi, aminocarbonila, R7 ou -X3-R7;
compostos conforme descrito no W099/50250 incorporado aqui como referência, isto é, compostos da fórmula (l-A):
um /V-óxido, um sal de adição farmaceuticamente aceitável ou uma forma estereoquimicamente isomérica dos mesmos, em que:
AéCH, CR4 ou N; n é 0, 1, 2, 3 ou 4;
Q é hidrogênio ou -NR1R2;
R1 e R^ são, cada um, independentemente selecionados de hidrogênio, hidróxi, C-i-i2alquila, Ci-i2alquilóxi, Cj-i2alquücarbonila, C-μ 12alquiioxicarbonila, arila, amino, mono- ou di(Ci--|2alquil)amino, mono- ou di(Ci-i2alqui[)aminocarbonila, em que cada um dos grupos Ci.12alquila antes mencionados pode opcionalmente e cada um individualmente ser substituído por um ou dois substituintes, cada um independentemente selecionado de hidróxi, Ci-6alquilóxi, hidróxiC-i-ealquilóxi, carboxila, C-i-ealquiloxicarbonila,
ciano, amino, imino, aminocarbonila, aminocarbonilamino, mono- ou di(Ci6alquil)amino, arila e Het; ou
R1 e R2 tomados juntos podem formar pirrolidiniia, piperidinila, morfolinila, azido ou mono- ou di(Ci-i2alquil)arninoC-i-4alquilideno;
R2 é hidrogênio, arila, Ci-6alquilcarbonila, Ci-6alquila, C-j6alquiloxicarbonila, Ci-6alquila substituída por Oj-6a[quilóxicarboniia; e cada R4 é, independentemente, hidróxi, halo, Ci-6aiquila, Ci6alquilóxi, ciano, aminocarbonila, nitro, amino, trihalometila, trihalometiióxi ou Ci-6alquila substituída por ciano ou aminocarbonila;
R5 é hidrogênio ou Ci-4alquila;
L é C-|.ioalquila, C3.10alquenila, C3,-joalquinila, C3.7cicloalquila ou Ci-ioalquila substituída por um ou dois substituintes independentemente selecionados de C3.7cicloalquila, indanila, indolila e fenila, em que a referida fenila, indanila e indolila pode ser substituída por um, dois, três, quatro ou, onde possível, cinco substituintes, cada um independentemente selecionado de halo, hidróxi, Ci-galquila, C-ι-galquilóxi, ciano, aminocarbonila, Ci6alquiloxicarbonila, formila, nitro, amino, trihalometila, trihalometiióxi e Cv êalquilcarbonila; ou
L é -X1-R6 ou -X2-Alk-R7 em que:
R6 e R7 são, cada um independentemente, fenila ou fenila substituída por um, dois, três, quatro ou cinco substituintes, cada um independentemente selecionado de halo, hidróxi, Ci-6alquila, Ci-ealquilóxi, Ci6alquilcarbonila, Ci-6alquiloxicarbonila, formila, ciano, aminocarbonila, nitro, amino, trihalometiióxi e trihalometila; e
X1 e X2 são, cada um independentemente, -NR3-, -NH-NH-, N=N-, -O-, -S-, -S(=O)- ou -S(=O)2-;
Alk é Ci-4alcanodiíla;
arila é fenila ou fenila substituída por um, dois, três, quatro ou cinco substituintes, cada um independentemente selecionado de halo, Ci~ 6alquila, C-|-6alquiJóxi, ciano, nitro e trrfluorometila;
Het é um radical heterocíclico alifático ou aromático; o referido radical heterocíclico alifático é selecionado de pirrolidiniia, piperidinila, ho30
mopiperidinila, piperazinila, morfoJinila, tetrahidrofuranila e tetrahidrotienila em que cada um dos referidos radicais heterocíclicos alifáticos pode opcionalmente ser substituído por um grupo oxo; e o referido radical heterocíclico aromático é selecionado de pirrolila, furanila, tienila, piridila, pirimidinila, pirazinila e piridazinila, em que cada um dos referidos radicais heterocíclicos aromáticos pode opcionalmente ser substituído por hidróxi;
compostos descritos no WO 00/27825, incorporado aqui como referência, isto é, compostos da fórmula (l-B):
(i-B) os A/-óxidos, os sais de adição farmaceuticamente aceitáveis, as aminas quaternárias e a forma estereoquimicamente isomérica dos mesmos, em que:
-a1=a2-a3=a4- representa um radical bivalente da fórmula: -CH=CH-CH=CH- (a-1);
-N=CH-CH=CH~N=CH-N=CH-N=CH-CH=N~
-N=N-CH=CH20 (a-2);
(a-3);
(a-4);
(a-5);
n é 0, 1,2, 3 ou 4; e, no caso de -a1=a2-a3=a4- ser (a-1), então, n pode também ser 5;
R1 é hidrogênio; arila; formila; C-i-ealquiicarbonila; C-i-galquila; Ci-galquiloxicarbonila; C-]-6alquíla substituída por formila, Ci6alquilcarbonila, C-j-ealquiloxicarbonila, Ci-6alquilcarbonilóxi; Ci6alquilóxiCi-6aIquilcarbonila substituída ou Cvealquiloxicarbonila;
cada R2 é, independentemente, hidróxi, halo, Ci-6alquila opcionalmente substituída ou ciano ou -C(=O)R6, Cs.ycicloalquila, C2-6alquenila opcionalmente substituída por um ou mais átomos de halogênio ou ciano, C2-ealquini[a opcionalmente substituída por um ou mais átomos de halogênio ou ciano, Ci-6alquilóxi, Ci-galquiloxicarbonila, carboxila, ciano, nitro, amino,
NHC(=O)R6,-C(=NH)R6 ou um radical da fórmula:
b-az (c) em que cada A é, independentemente, N, CH ou CR6;
B é NH, O, S ou NR6; p é 1 ou 2; e
R6 é metila, amino, mono- ou dimetilamino ou polihalometila;
L é Ci-iOalqui!a, C2-ioalquenila, C2-ioalquinila, C3-7cicloalquila, pe10 Io que cada um dos referidos grupos alifáticos pode ser substituído por um ou dois substituintes independentemente selecionados de:
* C3.7cicloalquila, * indolila ou isoindolila, cada uma opcionalmente substituída por um, dois, três ou quatro substituintes, cada um independentemente selecio15 nado de halo, C-í-gjaíquiia, hidróxi, Cj-6alquilóxi, ciano, aminocarbonila, nitro, amino, polihalometila, polihalometilóxi e C-i-galquilcarbonila, * fenila, piridinila, pirimidinila, pirazinila ou piridazinila, em que cada um dos referidos anéis aromáticos pode opcionalmente ser substituído por um, dois, três, quatro ou cinco substituintes, cada um independentemen20 te selecionado dos substituintes definidos em R2; ou
L é -X-R3 em que:
R3 é fenila, piridinila, pirimidinila, pirazinila ou piridazinila, em que cada um dos referidos anéis aromáticos pode opcionalmente ser substituído por um, dois, três, quatro ou cinco substituintes, cada um independentemen25 te selecionado dos substituintes definidos em R2; e
X é -NR1-, -NH-NH-, -N=N-, -O-, -C(=O)-, -CHOH-, -S-, -S(=O)ou -S(=O)2-;
Q representa hidrogênio, Ci-6alquila, halo, polihaloCi-6alquila ou NR4R5; e r4 e r5 são, cada um independentemente, selecionados de hi24 drogênio, hidróxi, C-|-i2aíquiia, Ci--J2alquilóxi, Ci_123Íquilcarbonila, Cf- A 12afqui[oxicarbonila, arila, amino, mono- ou di(C-i-i2alquiI)amino, mono- ou di(Ci-i2alquil)aminocarbonila, em que cada dos grupos C-M2alquila antes mencionados pode opcionalmente, e cada um individualmente, ser substituí5 do por um ou dois substituintes, cada um independentemente selecionado de hidróxi, C-i-ealquilóxi, hidróxiCi-6alquiióxi, carboxila, C^ealquiloxicarbonila, ciano, amino, imino, mono- ou di(Ci-6alquil)amino, políhalometila, polihalometilóxi, polihalometiitio, -S(=O)PR6, -NH-S(=O)PR6, -C(=O)R6, -NHC(=O)H, C(=O)NHNH2, -NHC(=O)Re,-C(=NH)R6, arila e Het; ou
R4 e R5, tomados juntos, podem formar pirrolidinila, piperidinila, morfolinila, azido ou mono- ou difCi-^aÍQuihaminoC^alquilideno;
Y representa hidróxi, halo, C3.7cicloalquila, C2-6alquenila opcionalmente substituída por um ou mais átomos de halogênio, C2-ealquinila opcionalmente substituída por um ou mais átomos de halogênio, Ci-6alquila substituída por ciano ou -C(=O)R6, Ci-6alquilóxi, Ci-6aiquiloxicarbonila, carboxila, ciano, nitro, amino, mono- ou di(C-i-ealquil)amino, polihalometiia, polihalometilóxi, polihalometiitio, -S(=O)PR6, -NH-S(=O)PR6, -C(=O)R6, NHC(=O)H, -C(=O)NHNH2, -NHC(=O)R6,-C(=NH)R6 ou arila;
arila é fenila ou fenii substituída por um, dois, três, quatro ou cin20 co substituintes, cada um independentemente selecionado de halo, Ci_ 6alquila, C3„7cicloalquila, C-]-6alquilóxi, ciano, nitro, polihaloCi-ealquila e polihaloC-i_6alquilóxi;
Het é um radical heterocíclico aiifático ou aromático; o referido radical heterocíclico aiifático é selecionado de pirrolidinila, piperidinila, ho25 mopiperidinila, piperazinila, morfolinila, tetrahidrofuranila e tetrahidrotienila, em que cada um dos referidos radicais heterocíclicos alifáticos pode ser opcionalmente substituído por um grupo oxo; e o referido radical heterocíclico aromático é selecionado de pirrolila, furanila, tieniia, piridinila, pirimidinila, pirazinila e píridazinila, em que cada um dos referidos radicais heterocíclicos aromáticos pode ser opcionalmente substituído por hidróxi.
Compostos da fórmula (I) em particular são compostos 1,25, 84,
133, 152, 179, 233, 239, 247, 248 (veja Tabelas 3, 4 e 5), seus /V-óxidos,
sais de adição farmaceuticamente aceitáveis, aminas quaternárias e formas estereoquimicamente isoméricas dos mesmos.
Mais preferivelmente, o composto da fórmula (I) é: 4-[[4-[[4-(2-cianoetenil)-2,6-d i metílfen i l]a mi no]-2pirimidinil]amino]benzonitrila; um /V-óxido, um sal de adição, uma amina quaternária ou uma forma estereoquimicamente isomérica do mesmo.
Compostos da fórmula (l-A) em particular são: 4-[[4-amino-6-[(2,6-diclorofenil)metil]-2~ pirimidinil]amíno]benzonitrila;
6-[(2,6-diclorofeni[)metil]-W2-(4-fluorofenil)-2,4-pirimidinadiamina;
4-[[4-[(2,4-diclorofenil)metil]-6-[(4-hidroxibutil)amino]-2pirímidinil]amino]benzonitrila;
4-[[4-[(2,6-diclorofenil)metil]-6-[(3-hidroxipropil)amino]-2pirimidinil]amino]benzonitrila;
A/-[2-[(4-cianofenil)amino]-6-[(2,6-diclorofenil)meti[]-4pirimidinil]acetamida;
/V-[2-[(4-cianofenil)amino]-6-[(2,6-diclorofenii)metil]-4pirimidiniljbutanamida;
4-[[2-amino-6-(2,6-diclorofenóxi)-4-pirimidinil]amino]benzonitrila;
4-[[4-[(2,6-diclorofenil)metil]-6-[(2-hÍdróxi-2-feniletil)amino]-2pirimidinil]amino]benzonitrila;
4-[[4-[(2,6-d iclorofen i I )meti l]-6-[[3-(2-oxo-1 pirro[idinil)propil]amino]-2-pirimidinil]amino]benzonitrila;
4-[[4-[(2,6-diclorofenil)metil]-6-[[2-(2-hidróxietóxi)efíl]amino]-2pirimidinil]amino]benzonitrila;
4-[[4-[(2,6-diclorofenil)metil]~6-[(2,3-dihidróxipropil)amino]-2pirimidinil]amino]benzonitrila,·
4-[[4-[(2,6-diclorofenil)metil]-6-(hidróxiamino)-2pirimidini!]amino]benzonitrila;
4-[[4-[(2-cianoetil)amino]-6-[(2,6-diclorofenil)metil]-2pirimidiní[]amino]benzonitrila',
4-[[4-[(2,6-diclorofenil)metil]-6-[[2-(1-pirrolidinil)etil]amrno]-230 pirimidiniljaminojbenzonitri (a; ? S /
4-[[4-amino-6-[(2,6-diclorofenil)metil]-5-metil-2pirimidíniljaminojbenzonitrila;
AZ2-(4-bromofenil)-6-[(2,6-diclorofenil)metil]-5~metil~2,45 pirimidinadiamina;
4-[[4-[(2,4,6-trimetilfenil)amino]-2-pirimidinil]aminojbenzonitriIa;
4-[[2-[(2,4,6-trimetiifenil)amino]-4-pirimidinil]aminoJbenzonitrila;
4-[[4-[(2,6-dimetilfenil)amino]-2-pirimidinil]amino]benzonitrila;
4-[[4-(2,4,6-trimetilfenóxi)-2-pirimidinil]amino]benzonitrila;
4-[[4-[(2,6-diclorofenil)tio]-2-pirimidinil]amino]benzonitrila;
4-[[4-[[2,6-dibromo-4-(1-metiieti[)fenil]amino]-2pirimidiniljaminojbenzonitrila;
4-[[4-[[2,6~dicloro-4-(trifluorometil)feníl]amino]-2pirimidiniljaminojbenzonitrila;
4-[[4-[(2í4-dicIoro-6-metilfenil)amino]-2pirimidiniljaminojbenzonitrila;
4-[[2-[(cianofenil)amino]-4-pirímídinil]amino]“3,5dimetilbenzonitrila;
4'[[4-[(2,4-dibromo-6-fluorofenÍl)amino]-220 pirimidiniljaminojbenzonitrila;
4-[[4-3Γη)ηο-6-[(2,6-άίοΙθΓθίθηίΙ)ιτιβΓιΙ]-5-ΓηβίίΙ-2pirimidiniljaminojbenzenoacetonitrila;
4-[[4-[metiI(2,4,6-trimetilfenil)amino]-2pirimidinil]amino]benzonitrila;
4-[[4-[(2,4J6-tricIorofenil)amino]-2-pirimidiniI]amino]benzonitrila;
4-[[4-[(214J6-trimetilfenil)tio]-2-pirimidinil]aminojbenzonitrila;
4-[[4-[(2,4!6-trimetilfenil)amino-2-pirimidinilJamino]benzonitrila;
4-[[4-amino-6-[(2,4,6-trimetilfenil)amino]-2pirimidiniljaminojbenzonitrila;
4-[[2-amino-6-[(2,4,6-trimetilfenil)arnino]-4pirimidiniljaminojbenzonitrila;
4-[[4-(2-bromo~4-cloro-6-metilfenóxi)-227 ptrimidtnil]amino]benzonitrila;
4-[[4-[(4-cforo-2,6-dimetilfenii)amino]-2pirimid!ni[]amino]benzonitrila;
3,5-d iclo ro-4-[[2-[(4-cia nofeni I )a mi no]-45 pirimidinil]amíno]benzonitriia;
4-[[4-[[2,6-dicloro-4-(trifluorometóxi)fenil]amino]-2pirimidinil]amino]benzonitrila;
4-[[4-[(2,4-dibromo-3(6-diclorofenil)amino]-2pirimidiniljaminojbenzonitrila;
4-[[4-[(2,6-dibromo-4-propilfenil]amino]-2pirimidinil]amino]benzonitrila;
4-[[4-[(2,4,6-trimetilfenil)amino]-2-pirimidinii]amino]benzamida;
4-[[4-[(4-(1,1“dimetiletil)-2,6-dimetilfeni[)amino]-2pirimidinil]amino]benzonitrila;
4-[[2-[(4-cianofenil)amino]-4-pirimidinil]óxi]-3,5-dimetilbenzonitri[a
4-[[4-[(4-cioro-2,6-d i meti Ifen ii)am ino]-5-meti I-2pirimidinil]amino]benzonitrila;
4-[[2-[(4-cianofenil)amino]-5-metil-4-pirimidinil]amino-3,5d i meti ibenzo n itri Ia;
4-E[4-[[4-(1l1-dimetiietil)-2,6-dimetilfenil]amino]-5-metil-2ptrimidinil]amino]benzonitrila;
4- [[4- [(4-bro mo-2,6-d i meti Ifen i I )a m i no]-5-metil-2pirimidinil]amino]benzonitrila;
4-[[5-metil-4-[(2,4,6-trimetilfenil)tio]-225 pirimidinii]amino]benzonitrila;
4-[[4-[(2,6-dibromo-4-propilfenil)amino]-5-metil-2pirimidinil]amino]benzonitrila;
4-[[4-[(2,4,6-trimetilfenil)amino]-2-pirimidinil]amino]benzamidaI
Λ/3-óxido;
A/2-(4-clorofenil)-N4-(2,4,6-trimetilfenil)-2,4-pirimidinadiamina;
4-[[4-[[2,6-dibromo-4-(1 -metileti[)fenil]amino]-5-metil-2pirimidinil]amino]benzonitrila;
4-[[2-[(4-cianofeniI)amino]-5-metil-4-pirimidtnil]amino]-3,5dimetiibenzonitrila;
4-[[4-[(feniimetil)amino]-2-pirimidinil]amino]benzonitrila; um /V-óxido, a sal de adição farmaceuticamente aceitável ou uma 5 forma estereoquimicamente isomérica do mesmo.
Mais preferivelmente, compostos da fórmula (1-A) são: 4-[[2-[(cianofenil)amino]-4-pirimidinil]amino]-3,5dimetilbenzonitrila; ou
4-[[4-[(2,4,6-trímetilfenil)amino]-2-pirimidinil]amino]benzonitrila;
um /V-óxido, um sal de adição farmaceuticamente aceitável ou uma forma estereoquimicamente isomérica dos mesmos.
Compostos da fórmula (l-B) em particular são: 4-[[4-amino-5-cloro-6-[(2,4,6-trimetilfenÍI)amÍno]-2pirimidinil]amino]benzonitrí]a;
4-[[5-cloro-4-[(2!4,6-trimetilfenil)amino]-2pirimidinil]amino]benzonitrila;
4-[[5-bromo-4-(4-ciano-2,6-dimetilfenóxi)-2pirimidinil]amino]benzonitrila;
4-[[4-amino-5-cloro-6-[(4-ciano-2,6-dimeti]fenil)amino]-220 pirimidinil]amino]benzonitrila;
4-[[5-bromo-6-[(4-ciano-2,6-dimetilfenil)amino]-2pirimidinil]amino]benzonitrila;
4-[[4-amino-5-c]oro-6-(4-ciano-2,6-dimetilfenilóxi)-2pirimidinil3amino]benzonitrila; ou
4-[[4-ami ηο-5-b romo-6-(4-ciano-2,6-d i metiifen i lóxi )-2pirimídinil]amino]benzonitrila;
um /V-óxido, um sai de adição, uma amina quaternária ou uma forma estereoquimicamente isomérica dos mesmos.
Mais preferivelmente, o composto da fórmula (l-B) é 4-[[430 amino-5-bromo-6-(4-ciano-2,6-dimetilfenilóxi)-2-pirimidinil]amino]benzonitrila;
um /V-óxido, um sai de adição, uma amina quaternária ou uma forma estereoquimicamente isomérica do mesmo.
Outros compostos de drogas adequados nas composições da presente invenção são:
- drogas analgésicas e anti-inflamatória (NSAIDs, fentanila, indometacína, ibuprofeno, cetoprofeno, nabumetona, paracetamol, piroxicam, tramadol, inibidores de COX-2 tais como celecoxib e rofecoxib);
- drogas antiarrítmicas (procainamida, quinídina, verapamii);
- agentes antrbacterianos e antiprotozoários (amoxiciiina, ampicilina, benzatina, penicilina, benzilpenicilina, cefacior, cefadroxil, cefprozil, cefuroxim axetil, cefalexina, cloranfenicol, cloroquina, ciprofioxacina, claritromi10 cina, ácido clavulânico, clindamicina, doxixiciina, eritromicina, flucioxacilina sódica, halofantrina, isoniazida, sulfato de canamicina, lincomicina, mefloquina, minociclina, nafcilina sódica, ácido nalidíxico, neomicina, norfloxacina, i
ofloxacina, oxacilina, fenoximetil-penicilina de potássio, pirimetaminasulfadoxima, estreptomicina);
- anticoagulantes (warfarina);
- antidepressivos (amitriptilina, amoxapina, butriptilina, clomipramina, desipramína, dotiepina, doxepina, fiuoxetina, reboxetina, aminaptina, selegilina, gepirona, imipramina, carbonato de lítio, mianserina, milnaciprana, nortriptilina, paroxetina, sertralina; 3-[2-[3,4-dihidrobenzofuro[3,2-c]piridin20 2(1 /7)-il]etiJ]-2-meti[-4H-pirido[1,2-a]pirimidin-4-ona);
- drogas antidiabéticas (glibenciamida, metformina, RWJ-394718, RWJ-394720, RWJ-666589, RWJ-37082);
- drogas antiepilépticas (carbamazepina, clonazepam, etosuximida, gabapentina, lamotrigina, levetiracetam, fenobarbitona, fenitoína, prími25 dona, tiagabina, topiramato, valpromida, vigabatrina);
- agentes antifúngicos (anfotericina, clotrimazola, econazoia, fluconazol, flucitosina, griseofulvina, itraconazol, cetoconazol, nitrato de miconazol, nistatina, terbinafina, voriconazol, equinocandinas);
- anti-histaminas (astemizola, cinarizina, ciproheptadina, decar30 boetoxiloratadina, fexofenadina, flunarizina, levocabastina, loratadina, norastemizol, oxatomida, prometazina, terfenadina, cetirizina);
- drogas anti-hipertensivas (captopril, enalapril, cetanserina, list
nopril, minoxidil, prazosina, ramipril, reserpina, terazosina); Ό·· v
- agentes antimuscarínicos (sulfato de atropina, hioscina);
- agentes antineoplásicos e antimetabólitos (compostos de platina, tais como cisplatina, carbopiatina; taxanos, tais como paclitaxel, doceta5 xel; tecanos, tais como camptotecina, irinotecano, topotecano; vinca alcalóides, tais como vinbiastina, vindecina, vincristina, vinoreibina; derivados de nucleosídeo e antagonistas de ácido fólico, tais como 5-fluorouracila, capecitabina, gemcitabina, mercaptopurina, tioguanina, cladribina, metotrexato; agentes de alquilação, tais como as mostardas de nitrogênio, por exemplo, ciclofosfamida, clorambucil, clormetina, ifosfamida, melphalan ou as nitrosouréias, por exempio, carmustina, lomustina ou outros agentes de alquilação, por exemplo, busulphan, dacarbazina, procarbazina, tiotepa; antibióticos, tais como daunorrubicina, doxorrubicina, idarrubicina, epírubícina, bleomicina, dactinomicina, mitomicina; anticorpo HER 2, tal como trastuzumab;
derivados de podofilotoxina, tais como etoposídeo, teniposídeo; inibidores de farnesii transferase, por exemplo, zarnestra; derivados de antraquinona, tais como mitoxantrona); imatinib; bortezomib;
- drogas antienxaqueca (alniditano, naratriptano, sumatriptano, almotriptano);
- drogas anti-Parkinsonismo (mesilato de bromocriptina, levodopa, seiegilina, rasagilina);
- agentes antipsicóticos, hipnóticos e sedativos (alprazolam, amisulprida, buspirona, clordiazepóxido, clorpromazina, ciozapina, diazepam, flupentixol, flufenazina, flurazepam, 9-hidróxi-risperidona, lorazepam, maza25 pertina, olanzapina, oxazepam, pimozida, pipamperona, piracetam, promazina, risperidona, selfotel, seroquel, sertindola, sulpirida, temazepam, tiotixeno, triazolam, trifluperidol, ziprasidona, zoipidem, bromperidol, fluperidoi, haloperidol, quetiapina, aripiprazol);
- agentes antiderrame (lubeiuzola, óxido de lubeluzoia, riiuzola, aptiganel, eliprodil, remacemida);
- antitussígenos (dextrometorfano, laevodropropizina);
- antivirais (aciclovir, ganciclovir, iovirida, tivirapina, zidovudina,
lamivudina, zidovudina + lamivudina, didanosina, zalcitabina, estavudina, abacavir, lopinavir, amprenavir, nevirapina, efavirenz, delavirdina, indinavir, nelfinavir, ritonavir, saquinavir, adefovir, hidroxiuréia, darunavir);
- agentes de bloqueio do beta-adrenoceptor (atenolol, carvedilol, 5 metoprolol, nebívolol, propanolol);
- agentes rnotrópícos cardíacos (amrinona, digitoxina, digoxina, milrinona);
- corticosteróides (dipropionato de beclometasona, betametasona, budesonida, dexametasona, hidrocortisona, metilprednisolona, predniso10 lona, prednisona, triamcinolona);
' - disinfetantes (clorexidina);
- diuréticos (acetazolamida, frusemida, hidroclorotiazida, isosor* bida);
- enzimas;
- óleos essenciais (anetol, óleo de anis, alcaravia, cardamomo, óleo de cássia, cineola, óleo de canela, óleo de trevo, óleo de coentro, óleo de menta desmentolado, óleo de endro, óleo de eucalipto, eugenol, gengibre, óleo de limão, óleo de mostarda, óleo de nérole, óleo de noz-moscada, óleo de laranja, hortelã-pimenta, sálvia, hortelã, terpineol, tomilho);
- agentes gastrointestinais (cimetidina, cisaprida, cleboprida, difenoxilato, domperidona, famotidina, lansoprazol, loperamida, óxido de loperamida, mesalazina, metoclopramida, mosaprída, nizatidina, norcisaprida, olsalazina, omeprazol, pantoprazol, perprazol, prucaloprida, rabeprazola, ranitidina, ridogrel, sulfa-safazina, esomeprazol);
- hemostáticos (ácido aminocapróico);
- agentes de regulação de lipídios (atorvastatina, lovastatina, pravastatina, probucol, simvastatina, rosuvastatina);
- anestésicos locais (benzocaína, lignocaína);
- analgésicos opióides (buprenorfina, codeína, dextromoramida, dihidrocodeína, hidrocodona, oxicodona, morfina);
- drogas parassimpatomiméticas e antidemência (leteprinim, eptastigmina, galantamina, metrifonato, milamelina, neostigmina, fisostigmina, tacrina, donepezil, rivastigmina, sabcomelina, talsaclidina, xanomelina, memantina, lazabemida);
- peptídeos e proteínas (anticorpos, becaplermina, ciciosporina, eritropoietina, imunoglobulínas, insulina, fatores do desenvolvimento, toxina de botulismo, infliximab);
- hormônios sexuais (estrogênios: estrogênios conjugados, etinilestradiol, mestranol, estradiol, estriol, estrona; progestogênios; acetato de clormadinona, acetato de ciproterona, norgestimato de 17-deacetila, desogestrel, dienogest, didrogesterona, diacetato de etinodiol, gestodeno, 3-ceto desogestrel, levonorgestreí, linestrenol, acetato de medróxi-progesterona, megestrol, noretindrona, acetato de noretindrona, noretisterona, acetato de noretisterona, noretinodrel, norgestimato, norgestrel, norgestrienona, progesterona, acetato de quingestanol);
- agentes estimulantes (sildenafil, tadalafil, apomorfina, vardenafii);
- vasodilatores (amlodipina, buflomedil, nitrito de amila, diltiazem, dipiridamol, trinitrato de glicerila, dinitrato de isosorbeto, lidoflazina, molsidomina, nicardipina, nifedipina, oxipentifilina, tetranitrato de pentaeritritol);
seus W-óxidos, seus sais de adição ácidos ou base farmaceuticamente aceitáveis ou suas formas estereoquimicamente isoméricas.
Outros exemplos incluem os seguintes:
8-Metoxipsoraleno Alopurinol alfa-tocoferol Sais de ferro fitomenadiona propiltiouracila
Sais de lítio Sais de magnésio menadiona metiltiouracila
Compostos de droga adequados para uso nas composições da invenção incluem drogas de todos os tipos convencionalmente administradas topicamente (por exemplo, em um emplasto em gel) ou a um duto corporal externamente oco, por exemplo, oral, nasal, aural, retal ou vaginalmente. Tais drogas incluem, em particular, antifúngicos, bloqueadores do canal de cálcio, antibacterianos, anti-hipertensivos, antivírais, analgésicos, inibidores da síntese de apolipoproteína B e drogas as quais modificam o trânsito dos
<3 conteúdos gastrointestinais (por exemplo, agentes antidiarréia ou promotores de motilidade).
A invenção é particularmente aplicáveis a agentes anti-HIV, em particular inibidores da transcriptase reversa de não-nucleosídeo, mais em particular inibidores de transcriptase reversa de não-nucleosídeo derivados de pirimidina.
As composições da invenção podem, convenientemente, conter o composto de droga a 0,001 a 50% em peso, de preferência 0,1 a 35%, mais preferivelmente 0,5 a 30%, especialmente 8 a 25% e ainda mais especialmente 10 a 15% em peso (com relação ao peso total de ácido (base), tensoativo e composto de droga). A quantidade de droga, naturalmente, dependerá do perfil de dissolução desejado, da solubilidade intrínseca do composto de droga e da dosagem de droga requerida onde a droga tem de ser distribuída em unidades de dosagem (por exemplo, cápsulas, comprimidos revestidos, etc.).
Em compostos da fórmula (I), (l-A) ou (I-B), C^alquila, como um grupo ou parte de um grupo, define radicais hidrocarboneto de cadeia reta ou ramificada saturada tendo de 1 a 4 átomos de carbono, tais como metila, etila, propila, 1-metiletila, butila; Ci-6alquila, como um grupo ou parte de um grupo, define radicais hidrocarboneto de cadeia reta ou ramificada saturada tendo de 1 a 6 átomos de carbono, tais como o grupo definido para C-i. 4alquila e pentila, hexila, 2-metilbutila e semelhantes; C2-6alquila, como um grupo ou parte de um grupo, define radicais hidrocarboneto de cadeia reta ou ramificada saturada tendo de 2 a 6 átomos de carbono, tais como etila, propila, 1-metiletila, butila, pentila, hexila, 2-metilbutila e semelhantes; C% 4alcanodíila define radicais hidrocarboneto bivalentes de cadeia reta ou ramificada saturada tendo de 1 a 4 átomos de carbono, tais como metileno, 1,2etanodiila ou 1,2-etilideno, 1,3-propanodiíla ou 1,3-propilideno, 1,4butanodiíia ou 1,4-butilideno e semelhantes; C3.7cicloalquila é genérica a ciciopropila, ciciobutila, ciclopentila, crclohexila e cicloheptila; C2-6alquenila define radicais hidrocarboneto de cadeia reta e ramificada tendo de 2 a 6 átomos de carbono contendo uma ligação dupla, tais como etanila, propeni34
Ia, butenila, pentenila, hexenila e semelhantes; C2-6alquinila define radicais hidrocarboneto de cadeia reta e ramificada tendo de 2 a 6 átomos de carbono contendo uma ligação tripla, tais como etinila, propiniia, butinila, pentinila, hexrnila e semelhantes; um carbociclo monocíciico, bicíclico ou tricíclico sa5 turado representa um sistema de anel consistindo em 1, 2 ou 3 anéis, o referido sistema de anei sendo composto apenas de átomos de carbono e o referido o referido sistema de anel contendo apenas ligações simples; um carbociclo monocíciico, bicíclico ou tricíclico parcialmente saturado representa um sistema de anel consistindo em 1, 2 ou 3 anéis, o referido sistema de anel sendo composto apenas de átomos de carbono e compreendendo pelo ' menos uma ligação dupla, contanto que o sistema de anel não seja um sistema de anel aromático; um carbociclo monocíciico, bicíclico ou tricíclico a$ romátíco representa um sistema de anel aromático consistindo em 1,2 ou 3 anéis, o referido sistema de anel sendo composto apenas de átomos de car15 bono; o termo aromático é bem conhecido por aqueles habilitados na técnica e designa sistemas ciclicamente conjugados de 4n + 2 elétrons, isto é, com 6, 10, 14 etc. π-elétrons (regra de Hückel); um heterociclo monocíciico, bicíclico ou tricíclico saturado representa um sistema de anel consistindo em 1, 2 ou 3 anéis e compreendendo pelo menos um heteroátomo selecionado de
O, N ou S, o referido sistema de anel contendo apenas ligações simples; um heterociclo monocíciico, bicíclico ou tricíclico parcialmente saturado representa um sistema de anel consistindo em 1,2 ou 3 anéis e compreendendo pelo menos um heteroátomo selecionado de O, N ou S e pelo menos uma ligação dupla, contanto que o sistema de anel não seja um sistema de anel aromático; um heterociclo monocíciico, bicíclico ou tricíclico aromático representa um sistema de anel aromático consistindo em 1, 2 ou 3 anéis e compreendendo pelo menos um heteroátomo selecionado de O, N ou S.
Para uso terapêutico, sais do compostos de droga são aqueles em que o contra-íon é farmaceuticamente aceitável. Contudo, sais de ácidos e bases os quais são não-farmaceuticamente aceitáveis podem também encontrar uso, por exemplo, na preparação ou purificação de um composto farmaceuticamente aceitável. Todos os sais, quer farmaceuticamente aceitá-
veis ou não, são incluídos no âmbito da presente invenção.
Entende-se que os sais de adição farmaceuticamente aceitáveis mencionados aqui acima compreendem as formas de sal de adição terapeuticamente ativas não-tóxicas as quais os compostos de droga são capazes de formar. As últimas podem ser, convenientemente, obtidas através de tratamento de uma forma de base com ácidos apropriados, tais como ácidos inorgânicos, por exemplo, ácidos hidrohálicos, por exemplo, clorídrico, hidrobrômíco e semelhantes; ácido sulfúrico; ácido nítrico; ácido fosfórico e semelhantes; ou ácidos orgânicos, por exemplo, ácidos acético, propanóico, hidroxiacético, 210 hidroxipropanóico, 2-oxopropanóico, oxáiico, malônico, succínico, maleico, fumárico, málico, tartárico, 2-hidróxi-1,2,3-propanotricarboxílico, metano-sulfônico, etano-sulfônico, benzeno-sulfônico, 4-metilbenzeno-sulfônico, ciclohexanosulfâmico, 2-hidróxibenzóico, 4-amino-2-hidroxibenzóico e semelhantes. Inversamente, a forma de sai pode ser convertida através de tratamento com um ái15 cali dentro da forma de base livre.
Os compostos de droga contendo prótons ácidos podem ser convertidos em suas formas de sal de adição de metal ou amina terapeuticamente ativas não-tóxicas através de tratamento com bases orgânicas e inorgânicas apropriadas. Formas de sai de base apropriadas compreendem, por exemplo, os sais de amônio, os sais de metal alcalino e alcalino-terroso, por exemplo, os sais de lítio, sódio, potássio, magnésio, cálcio e semelhantes, sais com bases orgânicas, por exemplo, aminas alifáticas e aromáticas primárias, secundárias e terciárias, tais como metilamina, etilamina, propilamina, isopropilamina, os quatro isômeros de butilamina, dimetilamina, dieti25 lamina, dietanolamina, dipropilamina, diisopropilamina, di-n-butilamina, pirrolidina, piperidina, morfolina, trimetilamina, trietilamina, tripropilamina, quinuclidina, piridrna, quinolina e isoquinolrna, de benzatina, /V-metii-D-glucamina,
2-amino-2-(hidroximetii)-1,3-propanodioi, os sais de hidrabamina e sais com aminoácidos tais como, por exemplo, arginina, lisina e semelhantes. Inver30 samente, a forma de sal pode ser convertida através de tratamento com ácido na forma de ácido livre.
O termo sal de adição também compreende as formas de adição de hidrato e soivente as quais os compostos de droga são capazes de formar. Exemplos de tais formas são, por exemplo, hidratos, alcoolatos e semelhantes.
O termo amina quaternária, conforme usado aqui antes, define 5 os sais de amônio quaternário os quais os compostos de droga são capazes de formar através de reação entre um nitrogênio básico de um composto de droga e um agente de quaternização apropriado, tais como, por exemplo, um haleto de alquila, haleto de arila ou haleto de arilalquila opcionalmente substituído, por exemplo, iodeto de metila ou iodeto de benzila. Outros reagentes com bons grupos de condução podem também ser usados, tais como trifluorometano-sulfonatos de alquila, metano-sulfonatos de alquila e p-toluenosulfonatos de alquila. Uma amina quaternária tem um nitrogênio positivamente carregado. Contra-íons farmaceuticameníe aceitáveis incluem cloro, bromo, iodo, trifluoroacetato e acetato. O contra-íon de escolha pode ser introduzido usando-se resinas de troca de íons.
Entende-se que formas de /V-óxido compreendem os compostos de droga em que um ou vários átomos de nitrogênio terciários são oxidados ao assim denominado /V-óxido.
Será apreciado que alguns dos compostos de droga e seus /V20 óxidos, sais de adição, aminas quaternárias e formas estereoquimicamente isoméricas podem conter um ou mais centros de quiralidade e existir como formas estereoquimicamente isoméricas.
O termo formas estereoquimicamente isoméricas, conforme usado aqui antes, define todas as formas estereoisoméricas possíveis as quais os compostos de droga, e seus /V-óxidos, sais de adição, aminas quaternárias ou derivados fisiologicamente funcionais podem possuir. A menos que de outro modo mencionado ou indicado, a designação química dos compostos denota a mistura de todas as formas estereoquimicamente isoméricas possíveis, as referidas misturas contendo todos os diastereômeros e enantiômeros da estrutura molecular básica, bem como cada uma das formas isoméricas individuais e seus /V-óxidos, sais, soivatos ou amina quaternárias substancialmente livres, isto é, associada a menos de 10%, de prefe-
rência menos de 5%, em particular menos de 2% e ainda mais preferivelmente menos de 1 % dos outros isômeros. Assim, quando um composto da fórmula (I) é, por exemplo, especificado como (E), isso significa que o composto é substancialmente isento do isômero (Z).
Em particular, centros estereogênicos podem ter a configuração R- ou S-; substituintes em radicais saturados (parcialmente) bivalentes cíclicos podem ter a configuração cis- ou trans-. Compostos abrangendo ligações duplas podem ter uma estereoquímica E (entgegen) ou Z (zusammen) na referida ligação dupla. Os termos cis, trans, R, S, E e Z são bem conhecidos por aqueles habilitados na técnica, obviamente, se pretende que formas estereoquimicamente isoméricas dos compostos de droga sejam abrangidas dentro do escopo da presente invenção.
Alguns dos compostos de droga podem também existir em sua forma tauromérica. Se pretende que tais formas, embora não explicitamente indicadas na fórmula acima, sejam incluídas dentro do escopo da presente invenção.
Os compostos da fórmula (I) podem ser preparados através de reação de um intermediário da fórmula (II) em que Wi é um grupo de saída adequado tais como, por exemplo, halo, triflato, tosilato, metil-sulfonila e semelhantes, com um intermediário da fórmula (III). Essa reação pode ser realizada em temperatura elevada.
(ii)
Alternativamente, a reação acima pode ser realizada na presença de um solvente adequado. Solventes adequados, são por exemplo, acetonitriia, um álcool, tais como, por exemplo, etanol, 2-propanol, 2-propanolHCI; Λ/,/V-dimetilformamida; /V,/V-dimetiiacetamida,1-metil-2-pirrolidinona; 1,4dioxano, propilenoglicol monometiléter. De preferência o solvente é 2propano!, HCI a 6 N em 2-propanol ou acetonitrila, especialmente acetonitrila. Opcionalmente, hidreto de sódio pode ser presente.
Nesse e nos preparações a seguir, os produtos de reação po25
dem ser isolados do meio de reação e, se necessário, ainda purificados de acordo com metodologias geralmente, conhecidas na técnica tais como, por exemplo, extração, cristalização, destilação, trituração e cromatografia.
Compostos da fórmula (I) em que R3 é R7 representando um sistema de anel monocíclico, bicíclico ou tricíclico aromático, o referido R3 sendo representado por R7 e os referidos compostos sendo representados pela fórmula (l-a), podem ser preparados através de reação de um intermediário da fórmula (IV) em que W2 representa um grupo de saída adequado, tais como, por exemplo, halo, hidróxi, triflato, tosilato, tiometila, metií-sulfonila, trifluorometil-sulfonila e semelhantes, com um intermediário da fórmula (V) em que Ra representa um boronato ou um tri(C-|.4alquila)estanano, tal como tributilestanano, na presença de um catalisador adequado, tais como, por exemplo, tetracis(trifenilfosfina) paládio, um sal adequado, tais como, por exempio, carbonato dissódico, carbonato de dipotássio e Cs2CC>3 e um solvente adequado, tais como, por exemplo, dioxano, dimetil éter, tolueno ou uma mistura de álcool/água, por exemplo, MeOH/H2O. Ra pode também representar halo, tal como, por exemplo, bromo, caso no qual a reação é realizada na presença de 4,4,4'J4',5,5,5',5'-octametil-2,2,-bi-1,3,2-dioxaboroiano.
.....P (V) q=&4 (R4k ,4 (l-a)
Compostos da fórmula (I) em que R3 é R7 representando um sistema de aneí monocíclico, bicíclico ou tricíclico saturado, o referido R3 sendo representado por R7' e os referidos compostos sendo representados peia fórmula (l-b), podem ser preparados através de reação de um intermediário da fórmula (IV) com um intermediário da fórmula (VI).
(VI) ,Ε-TyX:
t|=b
\k= 2 (l-b) .,4 (R‘)n <R')m
Compostos da fórmula (I) em que R3 representa C-i_6alquila subs-
tituída por ciano, o referido R3 sendo representado por C-i.ealquila-CN e os referidos compostos sendo representados pela fórmula (l-c), podem ser preparados através de reação de um intermediário da fórmula (VII) em que W3 representa um grupo de saída adequado, tal como, por exemplo, halo, por exemplo, cloro, com um sal de cianeto adequado, tal como, por exemplo, cianeto de sódio ou cianeto de potássio, na presença de um solvente adequado, tal como, por exemplo, Λ/,/V-dimetilformamjda ou sulfóxido de dimetila.
Compostos da fórmula (I) em que R3 representa Ci_6alquila subs10 tituída por R7; NR9R10 ou C^alquilóxi opcionalmente substituído por CN, R7 ou NR9R10, o referido R3 sendo representado por Ci_6alquila-Q em que Q representa R7; NR9R10 ou Ci-6alquilóxi opcionalmente substituído porCN, R7 ou NR9R10, e os referidos compostos sendo representados pela fórmula (l-d), podem ser preparados através de reação de um intermediário da fórmula (VII) com um intermediário da fórmula (VIII), opcionalmente na presença de um sal adequado, tais como, por exemplo, carbonato de dípotássio, cianeto de potássio, iodeto de potássio, e um solvente adequado, tal como, por e-
Compostos da fórmula (!) em que R3 representa -C(~N-O-R8)-C1_ 4alquila, os referidos compostos sendo representados pela fórmula (l-e), podem ser preparados através de reação de um intermediário da fórmula (IX) com um intermediário da fórmula (X) na presença de um solvente adequado, tal como um álcool, por exemplo, etanol.
Compostos da fórmula (I) em que R3 representa CRc=CRc-CN em que Rc representa hidrogênio ou C^alquila e Rc representa hidrogênio, Ci-4alquíia ou R7, contanto que CRc=CRc esteja limitado a C2-6alquenila, os referidos compostos sendo representados pela fórmula (l-f), podem ser pre5 parados através de reação de um intermediário da fórmula (XI) com um reagente de Wittig ou Horner-Emmons da fórmula (XII), em que Rb- representa, por exemplo, (Fenil)3P+- Cl' ou (CH3CH2-O)2P(=O)-, o qual pode ser considerado um precursor adequado de um ilídeo de fósforo, na presença de um sal adequado, tal como, por exemplo, terc-butóxido de potássio, e um solvente adequado, tal como, por exemplo, tetrahidrofurano.
(XI) (XII) (l-f)
Compostos das fórmulas (l-f-1) e (l-f-2) conforme representado abaixo podem ser preparados através de reação de um intermediário da fórmula (XXXIX) ou um sal de adição apropriado do mesmo, em que W5 representa um grupo de saída adequado, com acrilonitrila ou acrilamida na presença de um catalisador de paládio adequado, uma base adequada base e um solvente adequado.
(ΧΧΧΙΧ) (i-f-1)
Grupos de saída adequados na reação acima são, por exemplo, halo, triflato, tosilato, mesiiato e semelhantes. De preferência, W5 é haio, mais particularmente iodo ou bromo.
O catalisador de paládio (Pd) pode ser um catalisador de Pd ho5 mogêneo, tais como, por exemplo, Pd(OAc)2, PdCI2, Pd(PPh3)4, Pd(PPh3)2CI2, bis(dibenziiideno acetona) paládio, metalaciclo de tiometilfeniígíutaramida de paládio e semelhantes, ou um catalisador de Pd heterogêneo, tais como, por exemplo, paládio sobre carvão, paládio sobre óxidos de metal, paládio sobre zeólitos.
De preferência, o catalisador de paládio é um catalisador de Pd heterogêneo, mais preferivelmente paládio sobre carvão (Pd/C). Pd/C é um catalisador recuperável, é estável e econômico. Ele pode ser facilmente separado (filtração) da mistura de reação, portanto, reduzindo o risco de vestígios de Pd no produto final. O uso de Pd/C também evita a necessidade de ligantes tais como, por exemplo, ligantes de fosfina, os quais são caros, tóxicos e contaminantes dos produtos sintetizados.
Bases adequadas na reação acima são, por exemplo, acetato de sódio, acetato de potássio, /V,/V-dietiletanamina, hidrogencarbonato de sódio, hidróxido de sódio e semelhantes.
Solventes adequados na reação acima são, por exemplo, acetonitrila, /V,A/-dimetilacetamida, um líquido iônico, por exemplo, [bmimjPFe, A/,/V-dimetilforrnamida, água, tetrahidrofurano, sulfóxido de dimetila, 1-metil2-pirrolidinona e semelhantes.
Compostos da fórmula (I) em que R3 representa CRc=CRc -CN com Rc sendo conforme definido aqui acima e Rc representando NR9R10, C(=O)-NR9R10, -C(=O)-C-i-6alquila ou R7, os referidos compostos sendo representados pela fórmula (l-g), podem ser preparados através de reação de um intermediário da fórmula (Xl-a) com um intermediário da fórmula (XIII) na
presença de um solvente adequado, tais como, por exemplo, um álcool e um alcoolato, por exemplo, metanol e etanolato de sódio.
c10
Compostos da fórmula (I) em que R3 representa CH=C(CN)-CH2CN, os referidos compostos sendo representados pela fórmula (l-h), podem ser preparados através de reação de um intermediário da fórmula (Xl-b) com 2-butenodinitrila na presença de tributilfosfina e um solvente adequado, tal
Compostos da fórmula (I) em que R3 representa CH=C(CN)2, os referidos compostos sendo representados pela fórmula (l-h1), podem ser preparados através de reação de um intermediário da fórmula (Xl-b) com propanodinitrila na presença de uma base adequada, tal como, por exemplo, piperidina, e um solvente adequado, tal como, por exemplo, um álcool, por exemplo, etanol e semelhantes.
NC^ ZCN
CN
CH b'-k X, ^N.
ü T (R4)m
(l-h')
Ç53 \‘=?
Compostos da fórmula (I) em que R3 representa -CHOH-CH2CN, os referidos compostos sendo representados pela fórmula (l-i), podem ser preparados através de reação de um intermediário da fórmula (Xl-b) com
CH3-CN na presença de um agente de abstração de prótons adequado, tal como, por exemplo, butil lítio, na presença de um substrato adequado para o agente de abstração de prótons, por exemplo, /V-(1-metiIetil)-2-propanamina, e na presença de um solvente adequado, tal como, por exemplo, tetrahidro5 furano.
(l-i)
Compostos da fórmula (I) em que R3 representa CRc=CRc-halo em que Rc representa hidrogênio ou Ci-4alquila e Rc representa hidrogênio, C^alquila ou R7, contanto que CRc=CRc esteja limitado a C2-6alquenila, os referidos compostos sendo representados pela fórmula (I-j), podem ser pre10 parados através de reação de um intermediário da fórmula (XI) com um reagente de Wittig ou de Horner-Emmons da fórmula (ΧΙΓ), em que Rb- representa, por exemplo, (Fenil)3P+- Cl' ou (CH3CH2-O)2p(=O)-, o qual pode ser considerado como um precursor adequado de um ilídeo de fósforo, na presença de nBuLi, e um solvente adequado, tal como, por exemplo, tetrahidro-
(H)
Compostos da fórmula (I) em que R3 representa CRc=CRc-halo com Rc sendo conforme definido aqui acima e Rc representando CN,
NR9R10, -C(=O)-NR9R10, -C(=O)-Ci,6alquila ou R7, os referidos compostos sendo representados pela fórmula (l-k), podem ser preparados através de reação de um intermediário da fórmula (Xl-a) com um intermediário da fórmula (Xlll-a) na presença de um reagente de Horner-Emmons tais como, por exemplo, (CH3CH2-O)2P(=O)-CI, nBuLi, 1,1,1-trimetil-/V-(trimetFl-sifil)silanamina, e um solvente adequado, tal como, por exemplo, tetrahidrofurano.
Compostos da fórmula (I) em que R3 representa CH=C(Br)2, os referidos compostos sendo representados pela fórmula (l-l), podem ser preparados através de reação de um intermediário da fórmula (XVIII) com CBr4, na presença de um sal de catalisador adequado, tal como, por exemplo, (CuCl)2, e na presença de uma base adequada, tal como, por exemplo, NH3, e um solvente adequado, tal como, por exemplo, sulfóxido de dimetila.
Br
CBr4
C—Br
II
CH
V >-|=b4 \<=*2
Λ (l-l)
Compostos da fórmula (l-m) podem ser preparados através de reação de um intermediário da fórmula (XIV) com CI2C=S na presença de um solvente adequado, tal como, por exemplo, dioxano.
(l-m) (xiv)
Compostos da fórmula (l-n) podem ser preparados através de reação de um intermediário da fórmula (XV) com um intermediário da fórmula (XVI) na presença de um solvente adequado, tal como, por exemplo, um álcool ou um alcooiato, por exemplo, etanol ou metanolato de sódio.
Compostos da fórmula (I) em que R3 representa C2-eaiquenila substituída por C(=O)NR9R10 e opcionalmente ainda substituída por ciano, os referidos compostos sendo representados pela fórmula (i-o) em que C2ealquenila’ representa C2-6alquenila opcionalmente substituída por ciano, pode ser preparados através de reação de um intermediário da fórmula (XXIX) com um intermediário da fórmula (XXX) na presença de hidroxibenzotriazol e etiídimetilaminopropil carbodiimida e um solvente adequado, tal como, por exemplo, cloreto de metileno ou tetrahidrofurano, e opcionalmente na presença de uma base adequada, tais como, por exemplo, Λ/,/V-dietiietanamina, NH4OH e semelhantes.
NHR9R10-►
(xxix) (>c<X) (l-O)
Compostos da fórmula (I) em que R3 representa -C(=O)NR13R14 ou -C(=O)NHR13, os referidos compostos sendo representados pela fórmula (l-p-1) e (l-p-2) podem ser preparados através de reação de um intermediário da fórmula (XXXI) com um intermediário da fórmula (XXXII-1) ou (XXXII2) na presença de hidroxibenzotriazol e etiídimetilaminopropil carbodiimida e um solvente adequado, tal como, por exemplo, cloreto de metileno ou tetrahidrofurano, e opcionalmente na presença de uma base adequada, tais como, por exemplo, Λ/,ΛΑ-dietiletanamina.
(l-p-1)
2) (i-p-2) (I) em que R3 representa CH=N-NHC(=O)-R16, os referidos compostos sendo representados pela fórmula (l-q), podem ser preparados através de reação de um intermediário da fórmula (Xl-b) com um intermediário da fórmula (XXXIII) na presença de um solvente adequado, tal como, por exemplo, cloreto de metileno e um álcool, por exemplo, metanol, etanol e semelhantes.
(X|-b) (XXXIII)
Compostos da fórmula (I) em que R3 representa N(CH3)2, os referidos compostos sendo representados pela fórmula (l-r), podem ser preparados através de metilação redutiva de um intermediário da fórmula (XXXIV) com formaldeído na presença de um catalisador adequado, tal como, por exemplo, um ácido adequado, isto é, ácido acético e semelhantes, paládio sobre carvão, Níquel Raney, e na presença de um agente redutivo adequado, tal como, por exemplo, cia no boro hidreto de sódio ou H2, e um solvente adequado, tal como, por exemplo, acetonitrila.
(XXXIV)
(Ι-Γ)
Compostos da fórmula (I) em que R3 representa pirrolila, os referidos compostos sendo representados pela fórmula (l-s), podem ser preparados através de reação de um intermediário da fórmula (XXXIV) com 2,5dimetóxitetrahidrofurano na presença de um ácido adequado, tal como, por exemplo, ácido acético.
Compostos da fórmula (I) em que R3 representa CH=CH-R7, os referidos compostos sendo representados pela fórmula (l-t), podem ser preparados através de reação de um intermediário da fórmula (XXXV) (Ph indica fenila) com um intermediário da fórmula (XXXVI) na presença de nBuLi e um solvente adequado, tal como, por exemplo, tetrahidrofurano.
R7—CHO (XXXVi)
(l-t)
Os compostos da fórmula (I) pode ainda ser preparados através de conversão de compostos da fórmula (I) em cada um dos outros de acordo com reações de transformação de grupo conhecidas na técnica.
Os compostos da fórmula (I) podem ser convertidos às formas de A/-óxido correspondentes seguindo-se procedimentos conhecidos na técnica para a conversão de um nitrogênio trivalente em sua forma de /V-óxido.
A referida reação de /V-oxidação pode, geralmente, ser realizada através de
....: ' /' /</ reação do material de iniciação da fórmula (I) com um peróxido orgânico οΐι., ;vc, . ; inorgânico apropriado. Peróxidos inorgânicos apropriados compreendem, por exemplo, peróxido de hidrogênio, peróxidos de metal alcalino ou alcalino terroso, por exemplo, peróxido de sódio, peróxido de potássio; peróxidos orgânicos apropriados podem compreender peróxi ácidos tais como, por exemplo, ácido benzenocarboperoxóico ou ácido benzenocarboperoxóico halo substituído, por exemplo, ácido 3-ciorobenzenocarboperoxóico, ácidos peroxoalcanóicos, por exemplo, ácido peroxoacético, alquilhidroperóxidos, por exemplo, hidro-peróxido de terc-butila. Solventes adequados são, por exemplo, água, álcoois inferiores, por exemplo, etanol e semelhantes, hidrocarbonetos, por exemplo, tolueno, cetonas, por exemplo, 2-butanona, hidrocarbonetos halogenados, por exemplo, diclorometano, e misturas de tais solventes.
Por exemplo, um composto da fórmula (I) em que R3 compreen15 de ciano, pode ser convertido em um composto da fórmula (I) em que R3 compreende aminocarbonila, através de reação com HCOOH, na presença de um ácido adequado, tal como ácido clorídrico. Um composto da fórmula (I) em que R3 compreende ciano, pode também ser ainda convertido em um composto da fórmula (I) em que R3 compreende tetrazoliia, através de rea20 ção com azida de sódio na presença de cloreto de amônio e N, N dimetilacetamida.
Compostos da fórmula (I) em que R3 compreendem aminocarbonila, podem ser convertidos em um composto da fórmula (I) em que R3 compreende ciano, na presença de um agente de desidratação adequado. A de25 sidratação pode ser realizada de acordo com metodologias bem conhecidas por aqueles habilitados na técnica, tais como aquelas divulgadas em Comprehensive Organic Transformations. A guide to functional group preparations por Richard C. Larock, John Wiley & Sons, Inc., 1999, páginas 19831985, o qual é incorporado aqui como referência. Diferentes reagentes ade30 quados são enumerados na referida referência, tais como, por exemplo,
SOCI2, HOSO2NH2, CISO2NCO, MeO2CNSO2 NEt3, PhSO2CI, TsCi, P2O5, (Ph3PO3SCF3)O3SCF3, éster de polifosfato, (EtO)2POP(OEt)2l (EtO)3PI2, 249 cloro-1,3,2-dioxafosfolano, 2,2,2-tricloro-2,2-dihidro-1,3,2-dioxafosfolano,
POCI3, PPh3, P(NCI2)3, P(NEt2)3,COCI2, NaCI.AICI3) CICOCOCI, CICO2Me, CI3CCOCI, (CF3CO)2O, CI3CN=CCI2j 2,4,6-tricloro-1 ,3,5-triazina, NaCI.AICI3, HN(SiMe2)3, N(SiMe2)4, LiAIH4 e semelhantes. Todos os reagentes listados na referida publicação são incorporados aqui como referência.
Compostos da fórmula (I) em que R3 compreende C2-6alquenila podem ser convertidos em um composto da fórmula (I) em que R3 compreende Ci-6alquila através de redução na presença de um agente de redução adequado, tal como, por exemplo, H2, na presença de um catalisador ade10 quado, tal como, por exemplo, paládio sobre carvão, e na presença de um solvente adequado, tal como, por exemplo, um álcool, por exemplo, metanol.
Compostos da fórmula (I) em que R3 representa CH(OH)-R16, podem ser convertidos em um composto da fórmula (I) em que R3 representa C(=O)-R16 através de reação com reagente de Jones na presença de um solvente adequado, tal como, por exemplo, 2-propanona.
Compostos da fórmula (I) em que R3 representa C(=O)-CH2-R16a, em que R16a representa ciano ou aminocarbonila, podem ser convertidos em um composto da fórmula (I) em que R3 representa C(CI)=CH-R16a através de reação com POCI3.
Compostos da fórmula (I) em que R3 representa um carbociclo monocíciico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático, um heterociclo monocíciico, bicíclico ou tricíclico saturado, parcial mente saturado ou aromático substituído por formila podem ser convertidos em compostos da fórmula (I) em que R3 representa um carbociclo monocíciico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático, um heterociclo monocíciico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático substituído por CH(=N-O-R8) através de reação com NH2OR8 na presença de uma base adequada, tal como, por exemplo, hidróxido de sódio e um solvente adequado, tal como, por exemplo, um álcool, por exemplo, etanol e semelhantes. Compostos da fórmula (I) em que R3 representa um carbociclo monocíciico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático, um heterociclo monocíciico, bicíclico ou tricíclico saturado, ''5
c7 ?ls10 parcialmente saturado ou aromático substituído por CH(=N-O-R8) podem-^er convertidos em um composto da fórmula (I) em que R3 representa um carbociclo monocíclico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático, um heterociclo monocíclico, bicíclico ou tricíclico saturado, parcialmente saturado ou aromático substituído por CN através de reação com uma carbodirmida na presença de um solvente adequado, tal como, por exemplo, tetrahidrofurano.
Compostos da fórmula (!) em que R4 representa nitro, podem ser convertidos em um composto da fórmula (I) em que R4 é amino, na presença de um agente de redução adequado, tais como, por exemplo, H2, na presença de um catalisador adequado tal como, por exemplo, Níquel de Raney, e na presença de um solvente adequado, tal como, por exemplo, um álcool, por exemplo, metanol.
Compostos da fórmula (I) em que R1 é hidrogênio, podem ser convertidos a um composto da fórmula (I) em que R1 é Ci.6alquila, através de reação com um agente de alquilação adequado tal como, por exemplo, iodo-C-i-ealquila, na presença de uma base adequada, tal como, por exemplo, hidreto de sódio, e um solvente adequado, tal como, por exemplo, tetrahidrofurano.
Alguns dos compostos da fórmula (I) e alguns dos intermediários na presente invenção podem conter um átomo de carbono assimétrico. Formas estereoquimicamente isoméricas puras dos referidos compostos e dos referidos intermediários podem ser obtidas através da aplicação de procedimentos conhecidos na técnica. Por exemplo, diastereoisômeros podem ser separados através de métodos físicos tais como cristalização seletiva ou técnicas cromatográficas, por exemplo, distribuição contracorrente, cromatografia de líquido e métodos semelhantes. Enantiômeros podem ser obtidos a partir de misturas racêmicas primeiro através de conversão das referidas misturas racêmicas com agentes de decomposição adequados, tais como, por exemplo, ácidos quirais, a misturas de sais ou compostos diastereoméricos; então, separação física das referidas misturas de sais ou compostos diastereoméricos através, por exemplo, de cristalização seletiva ou técnicas cromatográficas, por exemplo, cromatografia de líquido e métodos seme- ‘ lhantes; e finaimente conversão dos referidos sais diastereoméricos ou com-?í postos nos enantiômeros correspondentes. Formas estereoquimicamente isoméricas puras podem também ser obtidas a partir das formas estereoquimicamente isoméricas puras dos intermediários e materiais de iniciação apropriados, contanto que as reações intervenientes ocorram estereoespecificamente.
Uma maneira alternativa de separação das formas enantioméricas dos compostos da fórmula (I) e intermediários envolve cromatografia de líquido, em particular cromatografia de líquido usando-se uma fase quíral estacionária.
Alguns dos intermediários e materiais de iniciação são compostos conhecidos e podem estar comercialmente disponíveis ou podem ser preparados de acordo com procedimentos conhecidos na técnica ou alguns dos compostos da fórmula (I) ou dos intermediários descritos podem ser preparados de acordo com os procedimentos descritos no WO 99/50250 e WO 00/27825.
Intermediários da fórmula (II) podem ser preparados através de reação de um intermediário da fórmula (XVII) com um agente de introdução de grupo de saída da fórmula (XIX) em que Wi representa o grupo de saída e R representa a restante do agente de introdução de grupo de saída tal co-
(ii)
Intermediários da fórmula (III) em que Xi representa NH, os referidos intermediários sendo representados pela fórmula (ΙΙΙ-a), podem ser preparados a partir de um intermediário da fórmula (XX) na presença de ZnCí2 e na presença de um solvente adequado, tal como, por exemplo, um álcool, por exemplo, etanol.
*
Intermediários da fórmula (III'-a), conforme representado abaixo, podem ser preparados a partir de um intermediário da fórmula (XX) em que R3 representa C2-ealquenila substituída por CN, o referido intermediário sendo representado pela fórmula (XX-a), na presença de ZnCI2 e na presença de uma Ci.4alquila-OH adequada, tal como, por exemplo, etanol.
o
C—O—Cj-^alkyl
C->-Aalkeny1
(XX-3) (Iir-a)
Intermediários das fórmulas (lll-b-1) e (lll-b-2), conforme representado abaixo, podem ser preparados através de reação de um intermediário da fórmula (XLI) ou um sal de adição de ácido apropriado do mesmo, em que W6 representa um grupo de saída adequado, com acrilonitrila ou acrila10 mida na presença de um catalisador adequado de paládio, uma base adequada e um solvente adequado.
(XLI) (lll-b-2)
Grupos de condução adequados na reação acima são, por exempio, halo, triflato, tosilato, mesilato e semelhantes. De preferência, W6 é halo, mais preferivelmente iodo ou bromo.
O catalisador de paládio (Pd) pode ser um catalisador de paládio 5 homogêneo tais como, por exemplo, Pd(OAc)2, PdCI2, Pd(PPh3)4, Pd(PPh3)2CI2, bis(dibenzilideno acetona)paládio, metalaciclo de tiometilfenilglutaramida de paládio e semelhantes, ou um catalisador de Pd heterogêneo tais como, por exemplo, paládio sobre carvão, paládio óxidos de metal, paládio sobre zeólitos.
De preferência, o catalisador de paládio é um catalisador de Pd heterogêneo, mais preferivelmente paládio sobre carvão (Pd/C). Pd/C é um catalisador recuperável, é estável e relativamente barato. Ele pode ser facilmente separado (filtração) da mistura de reação, desse modo, reduzindo o risco de vestígios de Pd no produto final. O uso of Pd/C também evita a ne15 cessidade de ligantes tais como, por exemplo, ligantes de fosfina, os quais são caros, tóxicos e contaminantes dos produtos sintetizados.
Bases adequadas na reação acima são, por exemplo, acetato de sódio, acetato de potássio, Λ/,/V-dietiletanamina, hidrogenocarbonato de sódio, hidróxido de sódio e semelhantes.
Solventes adequados na reação acima são, por exemplo, acetonitrila, Λ/,/V-dimetilacetamida, um líquido iônico, por exemplo, [bmimjPFe, Λ/,/V-dimetilformamida, água, tetrahidrofurano, sulfóxido de dimetila, 1-metil2-pirrolidinona e semelhantes.
Intermediários da fórmula (lll-b-2) podem ser convertidos a um intermediário da fórmula (lll-b-1) na presença de um agente de desidratação adequado. A desidratação pode ser realizada de acordo com metodologias bem conhecidas por aqueles habilitados na técnica, tais como aquelas divulgadas em Comprehensive Organic Transformations. A guide to functional group preparations por Richard C. Larock, John Wiley & Sons, Inc., 1999, páginas 1983-1985, o qual é incorporado aqui como referência. Diferentes reagentes adequados são enumerados na referida referência, tais como, por exemplo, SOCI2, HOSO2NH2, CISO2NCO, MeO2CNSO2 NEt3, PhSO2CI, Ts-
Cl, P2O5, (Ph3PO3SCF3)O3SCF3, éster de polifosfato, (EtO)2POP(OEt)2, (EtO)3PI2, 2-cloro-1,3,2-dioxafosfolano, 2,2,2-tricloro-2,2-dihidro-1,3,2dioxafosfolano, POCI3, PPh3, P(NCI2)3, P(NEt2)3,COCI2, NaCI.AICfe, CICOCOCI, CICO2Me, CI3CCOCI, (CF3CO)2O, CI3CN=CCI2, 2,4,6-tricloro-1,3,5triazina, NaCI.AICI3, HN(SiMe2)3, N($iMe2)4, LiAIH4 e semelhantes. Todos os reagentes listados na referida publicação são incorporados aqui como referência.
Intermediários da fórmula (XX) em que R3 representa CRc=CRcCN com Rc e Rc' conforme descrito aqui acima, os referidos intermediários sendo representados pela fórmula (XX-b), podem ser preparados a partir de um intermediário da fórmula (XXI) através da reação descrita acima para o preparação de um composto da fórmula (l-f).
(XXI)
R°—ÇHRC CN (XII)
CN
CRc
CR
CT b3=|=b4 (R4U (XX-b)
Intermediários da fórmula (XXI) podem ser preparados através de oxidação de um intermediário da fórmula (XXII) na presença de um agente de oxidação adequado, tal como, por exemplo, KMnO4, na presença de um solvente adequado, tais como, por exemplo, cloreto de metileno e tris[2(2-metoxietóxi)etil]amina.
Re Rc'
I I
HO—CH O=C b’-k N=^ .2 Λ\ Nκ '>
b3=|=b4 (R4)m oxidação iLV=\ \2 4 yb3;|=b4 1
Λ (XXil) (XXI)
Intermediários da fórmula (XXI) em que Rc' é H, os referidos intermediários sendo representados pela fórmula (XXI-a), também podem ser preparados através de reação de um intermediário da fórmula (XXIII) em que
W4 representa um grupo de saída adequado, tal como halo, por exemplo,
um solvente adequado, tal como, por exemplo, tetrahidrofurano.
o=c w4 ,, x> b3=j=b4 (R4)m (XXIII) (RX (XXI-a)
Intermediários da fórmula (XXII) em que Rc representa Ci„ «alquila, os referidos intermediários sendo representados pela fórmula (XXIIa), podem ser preparados através de reação de um intermediário da fórmula (XXIII) com um intermediário da fórmula (XXIV) na presença de nBuLi e na presença de um solvente adequado, tal como, por exemplo, tetrahidrofurano.
w4 s'-lv=
K 5 b3=|=b4 (XXIII)
CI-4alfc/l—C(=O)H (XXIV)
OH I
H—C—C^alkyí b ” 1 Λ
O p b3;|=b4 | (rX (XXI l-a)
Legenda:
Alkyl - Alquila
Intermediários da fórmula (Xi) podem ser preparados através de reação de um intermediário da fórmula (XXV) com um intermediário da fórmula (II), opcionalmente na presença de uma base adequada, tal como, por exemplo, 1-metil-pirrolidin-2-ona, ou um ácido adequado, tal como, por e-
Intermediários da fórmula (XV) podem ser preparados através de reação de um intermediário da fórmula (XXVI) com um intermediário da fórmula (II) na presença de uma base adequada, tais como, por exemplo, 1metil-pirrolidin-2-ona e hidreto de sódio e um solvente adequado, tal como,
Intermediários da fórmula (VII) podem ser preparados através de reação de um intermediário da fórmula (XXVII) com um agente de introdução de grupo de saída da fórmula (XIX1), tal como, por exemplo, SOCb, na presença de um solvente adequado, tal como, por exemplo, cloreto de metileno.
intermediários da fórmula (XXVII) em que Ci-ealquila representa CH2, os referidos intermediários sendo representados pela fórmula (XXVIIa), podem ser preparados através de redução de um intermediário da fórmula (XV) ou da fórmula (XXXI) com um agente de redução adequado, tal como, por exemplo, LiAII-h, na presença de um solvente adequado, tal como, por exemplo, tetrahidrofurano.
Legenda:
alkyl — alquila reduction - redução
Intermediários da fórmula (XXVII-a) podem ser convertidos a um
intermediário da fórmula (XXXI) através de reação com reagente de Jones na presença de um solvente adequado, tal como, por exemplo, acetona.
(XXVII-a) (XXXl)
Legenda:
Jones reagent - reagente Jones
Intermediários da fórmula (Xl-b) podem ser preparados através de oxidação de um intermediário da fórmula (XXVII-a) na presença de um agente de oxidação adequado, tal como, por exemplo, MnO2, e um solvente adequado, tais como, por exemplo, cloreto de metileno, N,N~
Legenda:
Oxidation - oxidação intermediários da fórmula (XIV) podem ser preparados através de reação de um intermediário da fórmula (XV) com H2N-NH2 na presença de um solvente adequado, tal como, por exemplo, um álcool, por exemplo, etanol e semelhantes.
(xv) (XIV)
Legenda:
alkyl - alquila
Intermediários das fórmulas (IX) e (Xi-a) podem ser reduzidos a um intermediário das fórmulas (XXVII’-a) e (XXVIl'-b) na presença de um
agente de redução adequado, tais como, por exemplo, NaBH4, LiAIH4 ou BuLi e um solvente adequado, tais como, por exemplo, tetrahidrofurano ou
(Xl-a) (xxvir-b)
Legenda:
alkyl - alquila reduction - redução
Um intermediário da fórmula (Xl-b) pode ser convertido a um intermediário da fórmula (XXVIΓ-a) através de reação com iodeto de C-i. 4alquila na presença de Mg e um solvente adequado, tal como, por exemplo, dietiléter e tetrahidrofurano.
(Xl-b) (XXVII’-a>
Legenda:
alkyl - alquila alkyliodide - alquiliodeto
Intermediários da fórmula (XVIII) podem ser preparados através de reação de um intermediário da fórmula (Xl-b) com H2N-NH2 na presença de um solvente adequado, tal como, por exemplo, um álcool, por exemplo, etanol e semelhantes.
Intermediários da fórmula (XXIX) ou (XXXI) podem ser preparados através de hidrólise de um intermediário da fórmula (XXXVII) em que C2. 6alquenila' representa C2.6alquenila opcionalmente substituída por ciano, ou de um intermediário da fórmula (XV) na presença de uma solução ácida aquosa adequada, tal como, por exemplo, ácido clorídrico a 2N e semelhantes, e na presença de um solvente adequado, tal como, por exemplo, um álcool, por exemplo, isopropanol e semelhantes.
—C|-6aliyl
(XXIX)
(XV)
(XXXI)
Legenda: alkyl - alquila acid - ácido
Intermediários da fórmula (XXXVII) em que C2-6alqueníla é CH=CH os referidos intermediários sendo representados pela fórmula (XXXVII-a), podem ser preparados através de reação de um intermediário da fórmula (Xl-b) com um reagente de Wittig ou de Horner-Emmons da fórmula (XII), em que Rb representa, por exemplo, (Fenil)3P+~ Cl· ou (CH3CH2O)2P(=O)-, os quais podem ser considerados como um precursor adequado de um ilídeo de fósforo, na presença de um solvente adequado, tal como, por exemplo, tetrahidrofurano.
(XXXVII-a)
Legenda:
alkyl - alquila
Intermediários da fórmula (XXXVII) em que C2.6alquenila' é -CH=C(CN)-, os referidos intermediários sendo representados pela fórmula (XXXVI l-b), podem ser preparados através de reação de um intermediário da fórmula (Xl-b) com NC-CH2-C(=O)O-Ci-6alquila, na presença de uma base adequada, tal como, por exemplo, piperidina, e um solvente adequado, tal como, por exemplo, um álcool, por exemplo, etanol.
p—Ci-ealkyl c=o
(Xl-b) ch2 _>
ç-°
O—cr6alkyl
C—CN II
CH ã y lí b3=|=b4 σόπ,
(XXXVII-b) f „4 \I=-2
Legenda:
alkyl - alquila
Intermediários da fórmula (XXXIV) podem ser preparados através de redução de um intermediário da fórmula (XXXVIII) na presença H2 e um catalisador adequado, tal como, por exemplo, paládio sobre carvão ou Níquel de Raney, e na presença de um solvente adequado, tal como, por
Legenda:
reduction - redução
Intermediários da fórmula (XXXV) podem ser preparados através de reação de um intermediário da fórmula (Vll-a) na presença detrifenilfosfina e um solvente adequado tal como, por exemplo, acetonitrila.
R
I /
1— 2 a—a
Intermediários da fórmula (XXXIX) podem ser preparados através de reação de um intermediário da fórmula (XL) com um intermediário da fórmula (ll-a) em que W5 e Wi são conforme aqui antes definido.
(XXXIX)
O compostos da fórmula (I) conforme preparado nos processos aqui acima descritos podem ser sintetizados como uma mistura de formas estereoisoméricas, em particular na forma de misturas racêmicas de enantiômeros os quais podem ser separados uns dos outros seguindo-se procedimentos de decomposição conhecidos na técnica. Os compostos racêmicos da fórmula (I) podem ser convertidos às formas de sal diastereoméricas correspondentes através de reação com um ácido quirai adequado. As referidas formas de sal diastereoméricas são, subsequentemente, separadas, por exemplo, através de cristalização seletiva ou fracional e os enantiômeros são liberados das mesmas por um álcali. Uma maneira alternativa de separação das formas enantioméricas dos compostos da fórmula (I) envolve cromatografia de líquido usando-se uma fase estacionária quirai. As referidas formas estereoquimicamente isoméricas puras podem também ser derivadas das formas estereoquimicamente isoméricas puras correspondentes dos materiais de iniciação apropriados, contanto que a reação ocorra estereoespecificamente. De preferência, se um estereoisômero específico é desejado, o referido composto será sintetizado através de métodos estereoespecíficos
/Λ$ de preparação. Esses métodos empregarão, vantajosamente, materiais de iniciação enantiomericamente puros.
Será apreciado por aqueles habilitados na técnica que, nos processos descritos acima, pode ser necessário que os grupos funcionais de compostos intermediários sejam bloqueados por grupos de proteção.
Grupos funcionais os quais são desejáveis proteger incluem hidróxi, amino e carboxílico ácido. Grupos de proteção adequados para hidróxi incluem grupos trialquil-silila (por exemplo, ferc-butildimetil-silila, tercbutildifenil-silila ou trimetil-silila), benzila e tetrahidropiranila. Grupos de proteção adequados para amino incluem ferc-butiloxicarbonila ou benzilóxicarbonila. Grupos de proteção adequados para ácido carboxílico incluem C-i_ ealquil ou benzil ésteres.
A proteção e desproteção de grupos funcionais podem ocorrer antes ou após uma etapa de reação.
O uso de grupos de proteção é totalmente descrito em 'Protective Groups in Organic Chemistry', editado por J W F McOmie, Pienum Press (1973) e 'Protective Groups in Organic Synthesis’ 2a edição, T W Greene & P G M Wutz, Wiley interscience (1991).
Os compostos da fórmula (I) ou qualquer subgrupo dos mesmos mostram propriedades anti-retrovirais (propriedades de inibição da transcriptase reversa), em particular contra o Vírus da Imunodeficiência Humana (HIV), o qual é o agente etiológico da Síndrome da Deficiência Imune Adquirida (AIDS) em seres humanos.
Os compostos da fórmula (I) ou qualquer subgrupo dos mesmos também mostram atividade contra gêneros de HIV resistentes à (multi)drogas, em particular gêneros de HIV-1 resistentes a (multi)drogas, mais em particular os presentes compostos mostram atividade contra gêneros de HIV, especialmente gêneros de HIV-1, que tenham adquirido resistência a um ou mais inibidores da transcriptase reversa de não-nucleosídeo conhecidos na técnica. Inibidores da transcriptase reversa de não-nucleosídeo conhecidos na técnica são aqueles outros inibidores da transcriptase reversa de não-nucleosídeo que não os presentes compostos e, em particular, inibi30 dores da transcriptase reversa de não-nucleosídeo comerciais. Os presentes compostos também têm pouca ou nenhuma afinidade de iigação à glicoproteína ácida a-1 humana; a giicoproteína ácida a-1 humana não afeta ou afeta apenas fracamente a atividade anti HIV dos presentes compostos.
Aqueles habilitados na técnica de tratamento de infecção pelo
HIV poderão determinar a quantidade diária eficaz a partir dos resultados dos testes apresentados aqui. Em geral, é considerado que uma quantidade diária eficaz seria de 0,01 mg/kg a 50 mg/kg de peso corporal, mais preferivelmente de 0,1 mg/kg a 10 mg/kg de peso corporal. Pode ser apropriado administrar a dose requerida como duas, três, quarto ou mais subdoses em intervalos apropriados no decorrer do dia. As referidas subdoses podem ser formuladas como formas de dosagem unitária, por exemplo, contendo 1 a 1000 mg e em particular 5 a 200 mg de ingrediente ativo por forma de dosagem unitária.
A dosagem e freqüência exatas de administração dependem do composto da fórmula (I) usado em particular, da condição que está sendo tratada em particular, da gravidade da condição que está sendo tratada, da idade, peso e condição física geral do paciente em particular, bem como outra medicação que o indivíduo possa estar tomando, conforme é bem conhe20 cido por aqueles habilitados na técnica. Além disso, é evidente que a referida quantidade diária eficaz pode ser diminuída ou aumentada dependendo da resposta o indivíduo tratado e/ou dependendo da avaliação do médico que prescreve os compostos da presente invenção. As faixas de quantidade diária eficazes mencionadas aqui acima são, portanto, apenas diretrizes e não se pretende que limitem o escopo ou uso da invenção a qualquer ponto.
Os seguintes exemplos se destinam a ilustrar os compostos da fórmula (I).
Aqui depois, DMF é definido como Λ/,/V-dimetilformamida, DlPE é definido como diisopropil éter, THF é definido como tetrahidrofurano,
DMA é definido como Λ/,/V-dimetilacetamida, DMSO é definido como sulfóxido de dimetila, DME é definido como dimetil éter, EtOAc é definido como acetato de etila, EDCI é definido como /V-(etilcarbonimidoil)-/V,/V-
d i metil-1,3-propanodiamina.
A. Preparação dos compostos intermediários
Exemplo A1
a) Preparação do intermediário 1 \ * N-/ /
nBuLi (0,012 mol) foi adicionado gota a gota a -70°C a uma mistura de W-(4-bromo-2,6-dimetilfenil)-/V,/V-dimetilmetanimidamida (0,0078 moI) em THF (20 ml) sob fluxo de N2. A mistura foi agitada a -30°C durante 30 minutos, então, esfriada para -70°C. Uma mistura de DMF (0,078 mol) em THF (30 ml) for adicionada gota a gota. A mistura foi agitada a -70°C durante 2 horas, então, mantida a 0°C, entornada em H2O e extraída com acetato de etila. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. Rendimento: 1,8 g de intermediário 1.
b) Preparação de intermediário 2
Uma mistura de fosfonato(cianometil) de dietila (0,0037 mol) em THF (10 ml) foi esfriada para 5°C sob fluxo de N2. Terc-butóxido de potássio (0,0037 mol) foi adicionado aos poucos, A mistura foi agitada a 5°C durante 30 minutos, então, agitada em temperatura ambiente durante 30 minutos. Uma mistura de intermediário 1 (0,0024 mol) em THF (10 ml) foi adicionada. A mistura foi agitada em temperatura ambiente durante 1 hora, então, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. Rendimento: 0,82 g (100%) de intermediário 2.
c) Preparação de intermediário 3 e intermediário 22
NH,
Intermediate 3
intermediate 22
ÃA-, ; ......x'
Legenda:
íntermediate - Intermediário '1 s
Uma mistura de intermediário 2 (0,059 mol) e ZnCb (0,299 mol) em etanol (150 ml) foi agitada e submetida a refluxo durante 24 horas, então, entornada em solução de K2CO3 (10 % em água) e extraída com CH2C[2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (9 g) foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,8 g (6%) de intermediário 22. O filtrado foi concentrado e recristalizado a partir de DIPE a fim de se obter 6 g de intermediário
3.
Aiternativamente, o intermediário 3 foi também preparado como segue:
A uma solução de 159 g de 4-iodo-2,6~dimetil-benzenamina foram adicionados 63,8 g de acetato de sódio. A mistura de reação foi mantida sob atmosfera de nitrogênio. 7 g de paládio sobre carvão umedecido (Pd/C 10 %) e 64,4 ml de acrilonitrila foram adicionados. A mistura de reação foi aquecida a 130°C e agitada durante a noite. Após resfriamento à temperatura ambiente, 0,5 l de tolueno e 0,5 I de A/,W-dimetilacetamida foram adicionados. A mistura de reação foi filtrada sobre Dicalite e 0 filtrado foi lavado com 0,5 I de tolueno. Água (6 I) foi adicionada à mistura, a qual foi agitada durante 30 minutos. As camadas foram separadas. A uma camada aquosa, l de tolueno foi adicionado e a mistura foi agitada durante 30 minutos. As camadas foram separadas novamente. As camadas orgânicas separadas foram esfriadas e o solvente foi evaporado, proporcionando 123 g de inter25 mediário 3.
O intermediário 3 foi convertido em seu sal de ácido clorídrico como segue:
A uma mistura de 123 g de intermediário 3 em 630 ml de etanol foi adicionado 1,25 l de diisopropil éter. A mistura de reação foi mantida sob uma atmosfera de nitrogênio. A mistura foi aquecida a 60°C e agitada durante 30 minutos. 120 ml de uma solução de ácido clorídrico a 6 N em 2propanol foram adicionados e a mistura foi agitada durante 30 minutos. Após resfriada para a temperatura ambiente, a mistura de reação foi filtrada e o resíduo foi lavado com 100 ml de 2-propanol. O resíduo resultante foi seco sob pressão reduzida a 50°C. Rendimento: 103 g (77 %) do sal de ácido clorídrico (1:1) de intermediário 3,
O intermediário 3 (E) foi preparado como segue:
x) Preparação de intermediário 3a (E)
Intermediate 3a (E)
Legenda:
Intermediate - Intermediário
Em 10 ml de acetonitrila seca, foram dissolvidos 2,00 g (10,0 moies) de 4-bromo-2,6-dimetilanilina, 1,07 g (1,5 eq) de acrilamida, 224 mg (0,1 eq) de Pd(OAc)2, 609 mg (0,2 eq) de tris(2-metiifenil)fosflna e 1,52 g de Λ/,ΛΖ-dietiletanamina. A mistura foi purgada com N2 durante 20 minutos e agitada durante a noite a 70 °C. A mistura foi diluída com 150 ml de cloreto de metileno, lavada com solução saturada aquosa de NaHCCb, seca (NaCI,
Na2SO4 sat.) e filtrada. O solvente foi evaporado e o resíduo foi agitado em diisopropil éter seguido por filtração. Rendimento: 1,51 g (79,5 %) de intermediário 3a (E).
y) Preparação de intermediário 3 (E)
Intermediate 3 (E)
Legenda:
Intermediate - Intermediário
POCI3 (3 mi) foi esfriado para 0°C e 500 mg (2,63 mmoles) de intermediário 3a (E) foram adicionados. Após 30 minutos, o banho de resfri-
amento foi removido e a mistura foi agitada durante a noite a 20 °C. A mistura foi adicionada gota a gota a 150 ml de diisopropil éter, enquanto agitada vigorosamente, O precipitado foi filtrado e lavado com diisopropil éter. O resíduo foi adicionado a 100 ml de acetato de etila/100 ml de solução saturada aquosa de NaHCO3 e agitado. A camada de acetato de etila foi separada, seca (NaCl, Na2SO4 sat.) e filtrada. O solvente for evaporado. Rendimento: 380 mg (84 %) de intermediário 3 (E).
d) Preparação de intermediário 4
Uma mistura de 4-bromo-2,6-dimetilbenzenamina (0,024 mol) em H2SO4 (30 ml) foi agitada a -5°C. KNO3 (0,024 mol) foi adicionado lentamente. A mistura foi agitada a -5°C durante 30 minutos, entornada em H2O e extraída com acetato de etila. A camada orgânica foi lavada com H2O, separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,058 g, 95%) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: ciclohexano/acetato de etila; 70/30; 15-40pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 4,1 g de intermediário 4. Exemplo A1A
1-cloro-pirrolidina-2,5-diona (0,032 mol) foi adicionada a 60°C a uma mistura de etif éster de ácido 4~amino-3-metil-benzóico [CAS 40800-655] (0,029 mol) em CH3CN (50 ml). A mistura foi agitada e submetida a refluxo lentamente. K2CO3 a 10% foi adicionado. A mistura foi extraída com CH2CI2. A camada orgânica foi evaporada. O resíduo (6,6 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: ciclohexano/EtOAc a 85/15; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 5,2 g de intermediário 28 (84%).
Exemplo A2
Uma mistura de 4-[(1,4-dihidro-4-oxo-2-pirimidinil)amino]benzonitrila (0,12 mol) em POCI3 (90 ml) foi agitada e submetida a refluxo sob argônio durante 20 minutos. A mistura de reação foi lentamente entornada sobre 750 ml de gelo/água e o sólido foi separado através de filtração. O sólido foi suspenso em 500 mi água e o pH da suspensão foi ajustado para neutro através de adição de solução de NaOH a 20%. O sólido foi novamente separado através de filtração, suspenso em 200 ml de 2-propanona e 1000 ml de CH2CI2 foram adicionados. A mistura foi aquecida até todo sólido ser dissolvido. Após esfriada para a temperatura ambiente, a camada aquosa foi separada e a camada orgânica foi seca. Durante remoção do agente de secagem através de filtração, um sólido branco é formado no filtrado. Resfriamento adicional do filtrado no congelador, seguido por filtração, proporcionou 21,38 g (77,2%).de [4-[(4-cloro-2-pirimidinil)amino]benzonitrila (intermediário 5).
Exemplo A3
a) Preparação de intermediário 6
nBuLi (0,024 mol) foi adicionado gota a gota a -70°C a uma mistura de A/-(4-bromo-2,6-dimetilfenil)-A/,/V-dimetilmetanimidamida (0,0157 moI) em THF (50 moles) sob fluxo de Ν2· A mistura foi agitada a -30°C durante 30 minutos, então, esfriada para -70°C. Uma solução de 2-metilpropanal (0,055 mol) em THF (50 ml) foi adicionada. A mistura foi agitada a -70°C durante 2 horas, então, mantida a 0°C, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (6,7 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH/NH4OH a 95/5/0,5; 15-40 pm). Duas frações foram coletadas e o solvente foi evaporado. Fração 1: rendimento: 1,5 g de intermediário 6 (38%).
b) Preparação de intermediário 7
Tris[2-(2-metóxietóxi)etil]amina (0,0193 mol) foi adicionada a temperatura ambiente a uma solução de intermediário 6 (0,0048 mol) em CH2CI2 (20 ml). KMnO4 (0,0193 mol) foi adicionado aos poucos. A mistura foi agitada em temperatura ambiente durante a noite, então, filtrada sobre ceiite e lavada com CH2CI2. A camada orgânica foi lavada com K2CO3 10%, separada, seca (MgSO4), filtrada e o solvente foi evaporado. Rendimento: 1,2 g (100%) de intermediário 7.
c) Preparação de intermediário 8
Uma mistura de intermediário 7 (0,0043 mol) e ZnCI2 (0,017 mol) em etanol (20 ml) foi agitada e submetida a refluxo durante a noite, entornada em H2O e extraída com CH2CI2/CH3OH. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. Rendimento: 0,94 g (82%) de intermediário 8.
d-1) Preparação de intermediário 9
O
Uma mistura de intermediário 8 (0,0049 mol) e intermediário 5 (0,0025 mol) for agitada a 150°C durante 2 horas e captada em K2CO3 /CH2CI2/CH3OH a 10 %. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (1,3 g) foi cristalizado através de DIPE. O precipitado foi filtrado e seco. A camada mãe foi purificada através de cromatografia em coluna sobre sílica-gel (eluente: CH2O2/CH3OH a 98,5/1,5; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,21 g de intermediário 9.
d-2) Preparação de intermediário 29
Uma mistura de intermediário 28 (0,023 mol) e intermediário 5 (preparado de acordo com A2) (0,025 mol) em HCI a 3N (10 ml) foi agitada a 105°C, então, mantida em temperatura ambiente e filtrada. O precipitado foi lavado com DIPE e seco. Rendimento: 8,4 g de intermediário 29 (96%) d-3) Preparação de intermediário 30 ci
o
Uma mistura de etil éster de ácido 4-amino-3-cloro benzóico [CAS 82765-44-4] (0,02 mol) e intermediário 5 (preparada de acordo com A2) (0,0243 mol) em 1-metil-pirrolidin-2-ona (40 ml) foi agitada a 180°C du10 rante 2 horas, então, entornada em H2O e extraída três vezes com EtOac (80 ml). A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (10 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2 a 100%; 15-30 pm). Duas frações foram coletadas e o solvente foi evaporado. Rendimento: 1,7 g de F1 e 1 g de F2. F2 foi captado em dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,95 g de intermediário 30 (12%). e-1) Preparação de intermediário 17
NaBH4 (0,0001 mol) foi adicionado aos poucos a 5°C a uma mistura de intermediário 9 (0,0001 mol) em etanol (7 ml) sob fluxo de N2. A mis20 tura foi agitada a 5°C durante 1 hora, entornada sobre gelo e extraída com
CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,1 g) foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,044 g de intermediário 17.
e-2) Preparação de intermediário 32
N
OH
BuLi a 1,6 M (0,009 mol) foi adicionado a -78°C a uma mistura de o
N (intermediário 31) (preparado de acordo com A4a) (0,0029 mol) em THF (25 ml) sob fluxo de N2- A mistura foi agitada a -78°C durante 10 minutos, então, mantida em temperatura ambiente e agitada durante 3 horas. H2O foi adicionado. A mistura foi extraída com CH2Cl2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente for evaporado. O resíduo (1,28 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH/NH4OH a 98/2/0,1; 15-40 pm). Três frações foram coletadas e o solvente foi evaporado. Rendimento: 0,189 g de fração 1, 0,14 g de fração 2 e 0,5 g de fração 3 (48%). A fração 3 foi purificada através de cromatografia em coluna sobre cromasila (eluente: CH2CI2/EtOAc a 80/20; 10 pm). Duas frações (F1, F2) foram coletadas e o solvente foi evaporado. Rendimento: 0,25 g de F1 (24%) e 0,1 g de F2. F1 foi cristalizado a partir de dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,21 g de intermediário 32 (20%). e-3) Preparação de intermediário 34
OH
Uma solução de iodeto de metilmagnésio (solução em dietrléter a
I Η H
1,0 M) (0,6 ml) foi adicionada a uma solução de o in20 termediário 33 (preparado de acordo com A5.a) (0,0006 mol) em THF (3 ml).
A mistura foi agitada durante 2 horas. H2O foi adicionada. A mistura foi filtrada sobre celite. H2O for adicionada. A mistura for extraída com EtOAc. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,05 g) foi purificado através de cromatografia em coluna so-
bre sílica-gel (eluente: CH2CI2/CH3OH a 96/4; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,015 g de intermediário 34 (7,2%).
Exemplo A4
a) Preparação de intermediário 10
. mol) em 1,4-dioxano (2,5 ml) foi agitado em temperatura ambiente sob fluxo de N2. Hidreto de sódio (0,0033 mol) foi adicionado. A mistura foi agitada ' durante 2 minutos. O Intermediário 5 (0,0028 mol) foi adicionada. A mistura 10 foi agitada durante 10 minutos. 1-metil-2-pirrolidinona (2,5 mi) foi adicionado.
A mistura foi agitada a 150°C durante 12 horas, entornada em H2O e extraída com CH2CI2/CH3OH. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (1,7 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH a 92/8; 1515 40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,7 g de intermediário 10 (70%). b-1) Preparação de intermediário 11
Uma solução de intermediário 10 (0,0005 mol) em THF (5 ml) foi adicionada gota a gota a 0°C a uma suspensão de LiAIH4 (0,001 mol) em
THF (5 ml) sob fluxo de N2. A mistura foi agitada a 0°C durante 1 hora e entornada em H2O (0,5 ml). CH2CI2 foi adicionado. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo for purificado através de cromatografia em coluna sobre cromasila (eluente: CH2CI2
100 a CH2CI2/CH3OH a 99/1; 5 pm). As frações puras foram coletadas e o
'Λ
c./ solvente foi evaporado. Ο resíduo (0,1 g) foi cristalizado a partir de dietil éter/ί'^ν,^ '' =ΪΧ
O precipitado foi filtrado e seco. Rendimento: 0,043 g de intermediário 11 (24%).
b-2) Preparação de intermediário 37
LiAIH4 (0,0196 mol, 0,75 g) foi adicionado aos poucos a 5°C a uma mistura de intermediário 29 (preparada de acordo com A3d-2) (0,0098 mol) em THF (100 ml) sob fluxo de N2. A mistura foi agitada em temperatura ambiente durante a noite, entornada em EtOAc, então, em H2O e filtrada sobre celite. A camada orgânica foi separada, seca (MgSO4), filtrada e o sol10 vente foi evaporado. Rendimento: 3,4 g. Essa fração foi purificada através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH/NH4OH a 97/3/0,1; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 1 g (27%). Essa fração foi cristalizada a partir de DlPE/CH3CN. O precipitado foi filtrado e seco. Rendimento: 0,03 g de interme15 diário 37.
c) Preparação de intermediário
Uma mistura de intermediário 11 (0,0043 mol) em CH2CI2 (50 ml) foi agitada a 0°C. SOCI2 (0,0206 mol) foi adicionado gota a gota. A mistura foi entornada em água gelada/K2CO3. A mistura foi agitada em temperatura ambiente durante 5 minutos. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. Rendimento: 1,5 g de intermediário 12 (98%).
d) Preparação de intermediário 55
Reagente de Jones (0,0084 mol) foi adicionado a uma mistura de intermediário 19 (veja Tabela 1) (preparado de acordo com A4b-1) (0,0028 mol) em acetona (50 ml). A mistura foi agitada em temperatura ambiente durante 2 horas então, entornada em H2O e basifrcada com NaHCO3. O precipitado foi filtrado e seco. Rendimento: 1,39 g. O resíduo (0,1 g) foi purificado através de cromatografia em coluna sobre sílica-ge! (eluente: CH2CI2/CH3OH/NH4OH a 85/15/1 então, CH3OH a 100%). A fração pura foi cristalizada a partir de isopropanol/DIPE. Rendimento: 0,071 g de intermediário 55.
Exemplo A5
a) Preparação de intermediário 13
Uma mistura de intermediário 19 (veja Tabela 1) (preparada de acordo com A4.b-1) (0,0037 mol) e MnO2 (0,0185 mol) em CH2CI2 (100 ml) foi agitada em temperatura ambiente durante a noite, então, filtrada sobre celite. O filtrado foi evaporado. Rendimento: 1,3 g de intermediário 13.
Uma mistura de intermediário 13 (preparada de acordo com
A5.a) (0,0029 mol) e H2N-NH2, H2O (0,0058 mol) em EtOH (10 ml) foi agitada em temperatura ambiente durante a noite. O solvente foi evaporado até secagem. Rendimento: 0,53 g de intermediário 21. Exemplo A6
Preparação de intermediário 14
Hidrazina (0,0077 mol) foi adicionada a uma mistura de
(preparada de acordo com A3.d-1) (0,0005 mol) em EtOH (10 ml). A mistura foi agitada e submetida a refluxo durante a noite. Hidrazina _ (0,028 mol) foi adicionada. A mistura foi agitada e submetida a refluxo durante a noite. Rendimento: 0,28 g de intermediário 14.
Exemplo A7
a) Preparação de intermediário 23
Uma mistura de intermediário 35 (preparada de acordo com A3.d-1) (0,0056 mol) em HCI a 3N (60 mi) e /PrOH (15 ml) foi agitada e submetida a refluxo durante a noite. O precipitado foi filtrado, lavado com H2O, captado em Dl PE e seca. Rendimento: 2,3 g de intermediário 23
Uma mistura de intermediário 10 (preparada de acordo com
A4.a) (0,0012 mol) em HCI a 3N (26 ml) e /PrOH (4 ml) foi agitada e subme-
tida a refluxo durante 12 horas. O solvente foi evaporado até secagem. O resíduo foi captado em (CH3)2CO. O solvente foi evaporado. O resíduo foi captado em dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,4 g (78,5%). Essa fração foi agitada a 60°C durante 20 minutos. Rendimento: 0,19 g. Essa fração foi cristalizada a partir de H2O/2-propanona. O precipitado foi filtrado e seco. Rendimento: 0,12 g de intermediário 56 (26%).
Exemplo A8
a) Preparação de intermediário 24
Uma mistura de intermediário 31 (preparada de acordo com A4.a) (0,0005 mol) e etil éster de ácido (trifenilfosforanilideno)acético [CAS 1099-45-2] (0,0006 mol em THF (5 ml) foi agitada a 80°C durante 48 horas, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,4 g) foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,08 g (33%). Essa fração foi cristalizada a partir de DIPE/CH3CN. O precipitado foi filtrado e seco. Rendimento: intermediário 24 (33%).
b) Preparação de intermediário 25
durante 30 minutos. Intermediário 31 (preparado de acordo com A4.a) (0,0005 mol) foi adicionado. A mistura foi agitada em temperatura ambiente durante 1 hora, entornada em H2O e extraída com CH2CI2- O precipitado foi filtrado e seco. O resíduo (0,2 g) foi cristalizado a partir de CH3CN/DIPE. O precipitado foi filtrado e seco. Rendimento: 0,048 g de intermediário 25 (19%) (mp. 222°C). Exemplo A9
Preparação de intermediário 26
•N
Uma mistura de (preparada de acordo com A3.d-1) (0,0011 mol) e Pd/C (0,2 g) em metanol (30 ml) foi hidrogenada em temperatura ambiente durante 2 horas sob uma pressão bar, então, filtrada sobre celite. A Celite foi lavada com CH3OH. O filtrado foi evaporado , até secagem. O resíduo (0,3 g) foi cristalizado a partir de 2propanona/CH3OH/dietii éter. O precipitado foi filtrado e seco. Rendimento:
0,07 g de fração 1. A fração 1 foi purificada através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 99,5/0,5; 5 pm). Três frações (F1, F2, F3) foram coletadas e o solvente foi evaporado. Rendimento: 0,0516 g de F1, 0,1 g de F2 e 0,15 g de F3. F1 foi captada em dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,028 g de intermediário 26 (8%) (mp. 272°C).
Exemplo A10
Preparação de intermediário 27
Uma mistura de (preparada de acordo com A4.c) (0,0005 mol) e trifenilfosfina (0,0005 mol) em CH3CN (10 ml) foi agitada e submetida a refluxo durante um fim de semana. O solvente foi evaporado até secagem, O resíduo foi captado em dietil éter. O precipitado foi
filtrado e seco. Rendimento: 0,34 g de intermediário 27 (94%). Exemplo A11
Preparação de intermediário 58
Uma mistura de 4-bromo-2,6-dimetilbenzenamina (0,013 mol) e intermediário 5 (0,013 mol) foi agitada a 150°C durante 1 hora. A mistura foi entornada em solução aquosa de K2CO3 a 10% e extraída com CH2CÍ2/ MeOH (95/5). A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo foi cristalizado a partir de diisopropil éter. O precipitado foi filtrado e seco. Rendimento: 2,3 g (45%). A camada mãe foi purificada através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH-NH4OH a 98,5/1,5; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,90 g (17%). O rendimento global de intermediário 5 foi: 3,2 g (62%).
O intermediário 59 foi preparado analogamente.
intermediate 59
Legenda:
Intermediate - Intermediário
As Tabelas 1 e 2 listam os intermediários os quais intervém na preparação de compostos da fórmula (I).
Tabela 1
| Interm. N° | Ex. N° | Xi | R3 | R4a | R4b | Dados físicos |
| 11 | A4b-1 | 0 | -CHs-OH | CH3 | ch3 | |
| 12 | A4c | O | -CH2-CI | ch3 | ch3 | |
| 16 | A3e | NH | -CH(OH)-CH3 | ch3 | ch3 | |
| 17 | A3e | NH | -CH(OH)- CH(CH3)2 | ch3 | ch3 | |
| 18 | A3e | NH | -CH(OH)-CH2- ch3 | ch3 | ch3 | |
| 19 | A4b-1 | NH | -CH2-OH | ch3 | ch3 | |
| 15 | A4c | NH | -CH2-CI | CHs | ch3 | |
| 24 | A8q | 0 | -CH=CH-C(=O)- O-C2H5 | ch3 | ch3 | pf. 180°C; (E) |
| 25 | A8b | 0 | NSz<>-C2H5 | ch3 | ch3 | pf. 222°C; (A) |
| 35 | A3d~1 | NH | -CH=CH-C(=O)- O-C2H5 | ch3 | ch3 | pf. 200°C; (E) |
| 23 | A7a | NH | -CH=CH-COOH | ch3 | ch3 | |
| 34 | A3e-3 | NH | -CH(OH)-CH3 | ch3 | H | pf. 182°C |
| 36 | A4b-1 | NH | -CH2-OH | ch3 | H | pf. 210°C |
| 37 | A4b-2 | NH | -CH2-OH | Cl | CH3 | |
| 38 | A4b-1 | NH | -ch2-oh | Cl | H | pf. 226°C |
| 39 | A3e-1 | O | -CH(OH)-CH3 | ch3 | H | pf. 160°C |
| 40 | A4b-1 | S | -ch2-oh | ch3 | ch3 | pf. 173°C |
| 41 | A4b-1 | NH | -ch2-oh | Br | Η | pf. 234°C |
| 32 | A3e-2 | 0 | -CH(OH)-CH3 | ch3 | ch3 | pf. 193°C |
| 42 | A4b-1 | NH | -CH2-OH | Br | ch3 | pf. 250°C |
| 43 | A4b-1 | NH | -CH2-0H | OH | Η | pf. 124°C |
| 44 | A4b-1 | NH | -CH2-OH | Η | H | pf. 215°C |
| Interm. N° | Ex. N° | X1 | R3 | R4a | R4b | Dados físicos |
| 45 | A4b-1 | NH | -CH2-OH | O~CH3 | Η | |
| 46 | A4b-1 | NH | -ch2-oh | cf3 | Η | pf. 194°C |
| 47 | A4c | NH | -ch2-ci | Cl | ch3 | |
| 48 | A4c | NH | -CH2-CI | Cl | Η | |
| 49 | A3e-1 | O | -CH2-OH | ch3 | Η | |
| 50 | A4c | O | -ch2-ci | ch3 | Η | |
| 51 | A4b-1 | NH | -ch2-oh | C(CH3)3 | Η | |
| 52 | A4c | NH | -CHs-CI | ch3 | Η | |
| 53 | A4b-1 | NH | -ch2-oh | 2-furaniía | ch3 | |
| 54 | A4c | NH | -CH2-CI | Br | ch3 | |
| 57 | A7b | O | -CH=CH-COOH | ch3 | ch3 |
Tabela 2
| Interm. N° j | Ex. N° | X1 | R3 | Dados físicos |
| 20 ___L | A3e | NH | -CHOH-CH3 |
B. Preparação dos compostos finais
Exemplo B1
Preparação de composto 1
Uma mistura de intermediário 3 (0,034 mol) e intermediário 5 (0,0174 mol) foi agitada a 150°C durante 1 hora e captada em K2CO3/CH2CI2/ CH3OH a 10 %. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (10 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/acetato de etila a 80/20; 15-40 pm). A Fração 1 foi cristalizada a partir de /PrOH. O precipitado foi filtrado e seco. Rendimento: 1,3 g de 4-[[4-[[4-(2-cianoetenil)-2,610 dimetilfenii]amino]-2-pirimidinil]amino]benzonitriia (E) (composto 1) (20%). Exempio B1A
O Composto 1 foi também preparado como segue:
Uma mistura de 93,9 g (0,45 mol) do sal de ácido clorídrico de intermediário 3 (preparada de acordo com Exemplo A1c) e 109 g (0,4725 mol) de intermediário 5 em 1,8 I de acetonitrila foi preparada sob atmosfera de nitrogênio. A mistura foi agitada e submetida a refluxo durante 69 horas, então, deixada esfriar a 55 °C. A mistura foi filtrada e o resíduo foi lavado com 200 ml de acetonitrila, seguido por secagem sob pressão reduzida a
50°C durante a noite. 144,6 g (0,3666 mol) do sólido obtido foram mantidos
- em 1 I de soiução aquosa de K2CO3 a 10%. A mistura foi agitada em temperatura ambiente, seguido por filtração. O resíduo obtido foi lavado duas vezes com água, seguido por secagem a 50°C sob pressão reduzida. O resíduo foi mantido em 6,55 I de isopropanol e a mistura foi submetida a refluxo, então, agitada durante a noite e filtrada em temperatura ambiente. O resíduo foi seco a 50°C sob pressão reduzida. Rendimento: 113,2 g (68,6 %) de 4[[4-[[4-(2-cianoetenil)-2,6-dimetilfenil]amino]-2-pÍrimidinil]amino]benzoni-trila (E) (composto 1).
Exemplo B1B
Alternativamente, 0 composto 1 foi também preparado como segue:
a) Uma mistura de intermediário 58 (0,00021 mol), preparada de acordo com Exemplo A11, acrilonitriia (CH2=CH-CN) (0,00213 mol), Pd(OAc)2 (0,000043 mol), /V,/V-dietiletanamina (0,000043 mol) e tris(225 metilfenil)fosfina (0,00021 mol) em CH3CN (7 ml) foi agitada em um vaso vedado a 150°C durante a noite. K2O foi adicionada. A mistura foi extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e 0 solvente foi evaporado. O resíduo (0,15 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/acetato de etila a 80/20;
15-40 μίτη). A Fração 1 foi coletada e o solvente foi evaporado, proporcionando 0,045g de 4-[[4-[[4-(2-cianoetenil)-2,6-dimetilfenil]amino]-2pirimidinil]amino]benzonitrila (E/Z = 80/20). O sólido foi cristalizado a partir
de dietiléter. Rendimento: 0,035g de 4-[[4-[[4-(2-cianoeteni 1)-2,6dimetiifenil]amino]-2-pirimidinil]amino]benzonitrila (E) (composto 1) (55%).
b) 4,41 g (10 mmoles) de intermediário 59 e 15 ml de Λ/,ΛΖdimetilacetamida foram mantidos em um frasco de 100 ml sob nitrogênio. A essa mistura foram adicionados 0,98 g de acetato de sódio (12 mmoles), 107 mg (0,1 mmol Pd) de Pd/C a 10% (úmido) e 1 ml (15 mmoles) de acrilonitrila. A mistura foi aquecida a 140°C e a evolução da reação foi acompanhada por meio de cromatografia líquida. A reação proporcionou 4-[[4-[[4-(2cianoetenil)-2,6-dimetilfenil]amino]-2-pirimidinii]amino]benzonitrila, (E/Z = 80/20) o qual pode ser convertido a 4-[[4-[[4-(2-cianoetenil)-2,6~ dimetilfenil]amino]-2-pirimidinil]amino]benzonitrila (E) conforme descrito acima no Exemplo B1Ba).
Exemplo B2
a) Preparação de composto 2
(preparado de acordo com A3.d-1) (0,0002 mol), ácido 2-benzofuranilborônico (0,0005 mol), Pd(PPh3)4 (0,00002 mol) e Na2CO3 (0,0007 mol) em DME (3 ml) foi agitada e submetida a refluxo em um tubo vedado durante 3 horas. H2O foi adicionada. A mistura foi extraída com acetato de etiia. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,126 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH a 98/2; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,011 g de composto 2 (10%). b) Preparação de composto 3 ,o.
Uma mistura de er ~ ~ v (preparada de acordo com A3.d-1) (0,0002 mol), tributil-2-furanilestanano (0,0005 mol) e Pd(PPh3)4 (0,00001 mol) em dioxano (5 ml) foi agitada a 80°C. O solvente foi evaporado. O resíduo foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2Cl2/CH3OH a 98/2; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,025 g) foi cristalizado a partir de DiPE. O precipitado foi filtrado e seco. Rendimento: 0,021 g de composto 3 (22%).
c) Preparação de composto 104
Pd(PPh3)4 (0,29 g) e K2CO3 (2,8 g, 0,02 mol) em tolueno (100 ml) e etanol/água (5 a 10 ml) foi agitada e submetida a refluxo durante um fim de semana. 5-Bromo-furan-2-carbaldeído (0,0055 mol) e K2CO3 (1,4 g, 0,01 mol) foram adicionados, A mistura foi agitada e submetida a refluxo durante a noite. A mistura (2,25 g) foi purificada através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH a 100/0 a 99/1; 15-40 mm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,135 g de composto 104 (6%).
Exemplo B3
Preparação de composto 4
N
Uma mistura de intermediário 15 (veja Tabela 1) (preparada de acordo com A4.c) (0,0005 mol) e NaCN (0,0011 mol) em DMF (5 ml) foi agitada a 80°C durante a noite, entornada em H2O e extraída com acetato de etila. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,15 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 99/1; 10 pm). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,024 g) foi purificado através de cromatografia em coluna sobre Hipersil (eluente: acetonitrila/H2O a 52/48; 8 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,02 g de composto 4 (10%).
„ Exemplo B4
a) Preparação de composto 5
Uma mistura de % (preparada de acordo com A3.d) (0,0006 mol) e tiomorfolina (0,5 g) foi agitada a 120°C durante 48 15 horas, captada em CH2CI2 e o solvente foi evaporado. O resíduo (0,44 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente:
CH2CI2/CH3OH a 99/1; 10 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,06 g (20%). Essa fração foi cristalizada a partir de dietil éter/2-propanona. O precipitado foi filtrado e seco. Rendimen20 to: 0,035 g de composto 5.
Uma mistura de intermediário 15 (veja Tabela 1) (preparada de acordo com A4.c) (0,000137 mol), A/./V./V-trimetil-l^-etanodiamina (2 equív, 0,000275 mol) e K2CO3 (2 equiv, 0,000275 mol) em CH3CN (q.s.) foi agitada a 80 °C durante 12 horas. H2O foi adicionada. A mistura foi extraída com CH2CI2. O solvente extraído foi evaporado. O resíduo foi purificado através de cromatografia. As frações produzidas foram coletadas e o solvente foi evaporado. Rendimento: 0,006 g de composto 6 (10,16%).
Uma mistura de intermediário 15 (veja Tabela 1) (preparada de acordo com A4.c) (0,0005 mol) em 3-hidróxi-propanonitrila (2 ml) foi agitada durante a noite, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo for purificado através de cromatografia em coluna sobre sílica-gel (eluen15 te: CH2CI2/CH3OH/NH4OH a 99/1/0,1; 15-40 pm). Duas frações (F1, F2) foram coletadas e o solvente foi evaporado. Rendimento: 0,034 g de F1 e 0,514 g de F2. F2 foi lavada com HCI a 3N e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco.
Λ7
Rendimento: 0,039 g de composto 7 (18%)
d) Preparação de composto 105
Uma mistura de intermediário 50 (preparada de acordo com A4c) (0,001 mol), KCN (0,0011 mol) e Kl (0,00005 mol) em EtOH (15 ml) foi agita5 da e submetida a refluxo durante 4 horas. O solvente foi evaporado até secagem. O resíduo foi captado em CH2Cl2/H2O. A mistura foi extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,31 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: ciclohexano/EtOAc a 70/30; 10 pm). Três frações foram coletadas e o solvente foi evaporado. Rendimento: 0,044 g de fração 1, 0,11 g de fração 2 e 0,055 g de fração 3. A Fração 3 foi cristalizada a partir de Dl PE. O precipitado foi filtrado e seco. Rendimento: 0,046 g de composto 105 (12%) (mp. 140°C).
Exemplo B5
a) Preparação de composto 8
Uma mistura de intermediário 9 (0,0001 mol) e hidroxilamina (0,0002 mol) em EtOH (7 ml) foi agitada em temperatura ambiente durante 3 horas, entornada em K2CO3 a 10% e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resí20 duo (0,1 g) foi cristalizado a partir de DIPE/CH3CN. O precipitado foi filtrado e seco. Rendimento: 0,026 g de composto 8.
b) Preparação de composto 9
:N
Uma mistura de intermediário 9 (0,0002 mol) e Ometiihidroxiiamina (0,0003 mol) em EtOH (10 ml) foi agitada em temperatura ambiente durante a noite, entornada em H2O e extraída com CH2CI2. A ca5 mada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,13 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: ciclohexano/iPrOH/NH4OH; 5 pm). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,06 g) foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,036 g de composto 9 (34%).
Exemplo B6
a) Preparação de composto 1 e 10
Composto 1=(E); composto 10=(Z)
Uma mistura de cloreto de (cianometil)trifenilfosfônio (0,0022 mol) e terc-butóxido de potássio (0,0022 mol) em THF (7 ml) foi agitada a
5°C durante 30 minutos sob fluxo de N2, então, agitada a 5°C durante 30 minutos. Uma mistura de intermediário 13 (0,0015 mol) em THF (7 ml) foi adicionada. A mistura foi agitada durante 8 horas no escuro, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (1,4 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: tolueno/iPrOH/NH4OH a 96/4/0,1; 15-40 pm). Duas frações (F1, F2) foram coletadas e o solvente foi evaporado. Rendimento: 0,165 g de F1 (E/Z=32/68) (30%) e 0,225 g de F2 (E/Z = 90/10) (41%). F2 foi cristalizada a partir de CH3CN/dietil éter. Rendimento: 0,036 g de composto 1 (7%). F1 foi purificada através de cromatogra25 fia em coluna sobre Cromasila (eluente: tolueno/iPrOH a 98/2; 5 pm). As fra-
ções puras foram coletadas e o solvente foi evaporado. Rendimento: 0,029 g de composto 10 (5%).
b) Preparação de composto 11 (Z) e composto 103 (E)
Terc-butóxido de potássio (0,0196 mol) foi adicionado aos pou5 cos a 5°C a uma mistura de dietil éster de ácido (l-cianoetii)-fosfônico (0,0196 mol) em THF (25 ml) sob fluxo de N2. A mistura foi agitada a 5°C durante 30 minutos, então, em temperatura ambiente durante 30 minutos. Uma solução de intermediário 13 (0,0130 mol) em THF (25 ml) foi adicionada. A mistura foi agitada em temperatura ambiente durante a noite, entorna10 da em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (5,8 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eiuente: tolueno//PrOH/NH4OH a 92/8/0,5; 15-40 pm). Quatro frações (F1, F2, F3, F4) foram coletadas e o solvente foi evaporado. Rendimento: 0,21 g de F1 (mistu15 ra Z/E = 90/10), 0,836 g de F2 (mistura Z/E = 57/43), 0,9 g de F3 e 0,87 g de F4. F3 foi cristalizada a partir de DIPE//PrOH a fim de se obter 0,7 g de composto 11 (14%). F4 foi cristalizado a partir de DIPE/ZPrOH a fim de se obter 0,67 g de composto 103 (13%).
Legenda:
Compound - Composto
Terc-butóxido de potássio (0,0008 mol) foi adicionado aos pou-
·$>
ς>
Λ1
Ζ Πϊ.
Rub:.
cos a 5°C a uma mistura de dietil éster de ácido (cianometil)fosfônico (0,0005 mol) em THF (20 ml) sob fluxo de N2. A mistura foi agitada em temambiente durante 30 minutos. Uma solução de peratura
O
(preparada de acordo com A3.d-1) (0,0005 mol) em THF (4 ml) foi adicionada gota a gota. A mistura foi agitada em temperatura ambiente durante 4 horas, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. Rendimento: 0,3 g. Essa fração foi purificada através de cromatografia em coluna sobre Cromasila (eiuente: CH2Ci2/CH3OH a 99/1; 5 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,21 g. Essa fração foi purificada através de cromatografia em coluna sobre Cromasila (eluente: ciclohexano/acetato de etila 50/50; 10pm). Duas frações (F1, F2) foram coletadas e o solvente foi evaporado. Rendimento: 0,04 g de F1 e 0,047 g de F2. F1 foi seca a 70°C durante 2 horas. Rendimento: 0,038 g de composto 13 (18%). F2 foi seca a 70°C durante 2 horas. Rendimento: 0,041
Terc-butóxido de potássio (0,0013 mol) foi adicionado a 5°C a uma mistura de dietil éster de ácido (cianometil)fosfônico (0,0013 mol) em
THF (10 ml) sob fluxo de N2. A mistura foi agitada a 5°C durante 30 minutos.
Uma mistura de (preparada de acordo com A3.d-1) (0,0009 mol) em THF (10 ml) foi adicionada. A mistura foi agitada em tempe-
ratura ambiente durante 4 horas, entornada em H2O e extraída com acetato de etila. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,17 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2 a 100% a CH2CI2/CH3OH a 99/1; 5 pm). Duas frações (F1, F2) foram coletadas e o solvente foi evaporado. Rendimento: 0,054 g de F1 e 0,05 g de F2. F1 foi cristalizada a partir de DIPE/CH3CN. O precipitado foi filtrado e seco. Rendimento: 0,046 g de composto 14 (12%).
e) Preparação de composto 15
4-Fluorobenzenoacetonitrila (1,2 equiv, 0,000175 mi) foi adicionado a uma mistura de intermediário 13 (0,000146 mol) em CH3OH (1 ml). NaOCH3/CH3OH (1,2 equiv, 0,000175 mol) foi adicionado em temperatura ambiente. A mistura foi agitada a 60 °C durante 2 horas, então, entornada em gelo-água e extraída com CH2Cl2. O solvente foi evaporado. O resíduo foi purificado através de cromatografia. As frações resultantes foram coletadas e o solvente foi evaporado. Rendimento: 0,009 g de composto 15 (13,42%).
f) Preparação de composto 106
Uma mistura de intermediário 13 (preparada de acordo com
A5.a) (0,0005 mol) e piperídina (0,0005 mol) em etanol (5 ml) foi agitada em temperatura ambiente durante 30 minutos. 4,4-dimetil-3-oxo-pentanonitrila (0,0011 mol) foi adicionado. A mistura foi agitada em temperatura ambiente durante a noite, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resí5 duo (0,3 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CÍ2/CH3OH a 99/1; 10 pm). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,2 g) foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,141 g de composto 106 (54%) (mp. 193°C).
Exemplo B7
Uma mistura de intermediário 14 (0,00005 mol) e dicloreto carbonotióico (0,001 mol) em dioxano (10 ml) foi agitada em temperatura ambiente. H2O foi adicionada. A mistura foi extraída com CH2CI2- Essa fração foi purificada através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH/NH4OH a 90/10/0,1; 15-40 pm). As frações puras foram coletadas e 0 solvente foi evaporado. Rendimento: 0,027 g de composto 16 (95,6%).
Exemplo B8
A mistura de NaOCH3 (0,001 mol) e 2-(dimetilamino)-/\/-hidróxi92
biente durante 30 minutos. (preparado de acordo com
A3.d-1) (0,0005 mol) foi adicionado. A mistura foi agitada e submetida a refluxo durante a noite. H2O foi adicionada. A mistura foi extraída com CH2CÍ2.
O resíduo foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH/NH4OH a 95/5/0.1; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,07 g de composto 17(31%).
Exemplo B9
nBuLi (0,0038 mol) foi adicionado gota a gota a -70°C a uma mistura de /Pr2NH (0,0038 mol) em THF (5 ml) sob fluxo de N2. A mistura foi mantida a ~20°C, agitada durante 30 minutos e esfriada novamente a -70°C. Uma solução de CH3CN (0,0038 mole) em THF (6 ml) foi adicionada gota a gota. A mistura foi mantida a -20°C, agitada durante 1 hora, esfriada novamente a -70°C. Uma mistura de intermediário 13 (0,0009 mol) em THF (1 ml) foi adicionada. A mistura foi agitada durante 2 horas, entornada sobre gelo a -30°C e extraída com acetato de etila. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,433 g) foi purifrca20 do através de cromatografia em coluna sobre sílica-gel (eluente:
CH2CI2/CH3OH a 98/2; 35-70 pm). Duas frações foram coletadas e o solvente foi evaporado. Rendimento: 0,056 g de F1 e 0,23 g de F2 (78%). F1 foi
cristalizada a partir de DIPE/CH3CN. 0 precipitado foi filtrado e seco. Rendimento: 0,036 g de composto 18.
Exemplo B9A
a) Preparação de composto 107
nBuLr[1,6] (0,0026 mol) foi adicionado gota a gota a -70°C a uma mistura de intermediário 13 (preparado de acordo com A5.a) (0,0008 mol) em THF (10 ml) sob fluxo de N2. A mistura foi agitada a -70°C durante 30 minutos. Uma solução de cloreto de (clorometil)trífeniifosfônio (0,0026 mol) em THF (5 ml) foi adicionada gota a gota. A mistura foi agitada em tempera10 tura ambiente durante a noite, entornada em H2O e extraída com EtOAc. A camada orgânica foi separada, seca (MgSC>4), filtrada e o solvente foi evaporado. O resíduo (0,7 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 99/1; 10 pm). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,155 g) foi purifica15 do através de cromatografia em coluna sobre C18 (eluente: CH3CN/NH4Ac a 0,5%, 60/40). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,051 g) foi cristalizado a partir de Dl PE. O precipitado foi filtrado e secO. Rendimento: 0,029 g de composto 107 (9%). (mp. 250°C)
b) Preparação de compostos 108 e 109
Cl (Z) compound 108 (E) compound 109
Legenda:
Compound - Composto nBul_i[1,6] (0,00261 mol) foi adicionado gota a gota a -70°C a uma mistura de cloreto de (clorometil)trifenilfosfônio (0,00261 mol) em THF (10 ml) sob fluxo de N2. A mistura foi agitada durante 30 minutos. Uma solução de intermediário 31 (preparado de acordo com A4.a) (0,00087 mol) em
THF (5 ml) foi adicionada gota a gota. A mistura foi agitada em temperatura ambiente durante a noite, então, entornada em H2O e extraída com EtOAc. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (1,1 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2Cl2/CH3OH/NH4OH A 98/2/0,1; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,3 g) _ foi purificado através de cromatografia em coluna sobre hipersil C18 (eiuente: CH3OH/NH4AC a 0,5%, 70/30). Duas frações (F1, F2) foram coletadas e o ' solvente foi evaporado. Rendimento: 0,097 g de F1 e 0,085 g de F2. F1 foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. Rendimento:
0,045 g de composto 108 (14%) (mp. 165°C). F2 foi cristalizado a partir de
DIPE. O precipitado foi filtrado e seco. Rendimento: 0,049 g de composto 109(15%)(mp. 200°C).
c) Preparação de composto 110
nBuLi[1,6] (1,1 ml, 0,0017 mol) foi adicionado gota a gota a
-70°C a uma mistura de 1,1,1,3,3,3-hexametildi-silazano (HN(TMS)2) (0,0017 mol) em THF (6 ml). A mistura foi agitada a -70°C durante 30 minutos. Cianofluorometila (0,0017 mol) foi adicionada. A mistura foi agitada durante 30 minutos. Dietil éster de ácido fosforoclorídrico (0,0017 mol) foi adicionado. A mistura foi agitada a -70°C durante 15 minutos. nBuLi[1,6] (1,1 ml, 0,0017 mol) foi adicionado gota a gota. A mistura foi agitada durante 30 minutos.
Uma solução de intermediário 31 (preparado de acordo com A4.a) (0,0008 mol) em THF (4 mi) foi adicionada. A mistura foi agitada em temperatura
ambiente durante a noite, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,5 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/EtOAc a 95/5; 15-40 pm). Quatro frações (F1, F2,
F3, F4) foram coletadas e o solvente foi evaporado. Rendimento: 0,026 g de composto 110 (8%) (mp. 254°C).
d) Preparação de composto 111
Br
Uma solução aquosa de (CuCI)2 (0,00015 mol) em NH3 (500μΙ) foi adicionada a uma mistura de intermediário 21 (preparado de acordo com
A5.b) (0,0014 mol) em DMSO (1 ml). Uma solução de CBr4 (0,0044 mol) em
DMSO (1,5 ml) foi adicionada a 0°C. A mistura foi agitada em temperatura ambiente durante a noite, entornada sobre gelo e filtrada. A camadã orgânica foi lavada com CH2CI2, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (2,73 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH a 100/0 a 99/1; 15-40 pm). Duas frações foram coletadas e o solvente foi evaporado. Rendimento: 0,007 g de fração 1 e 0,11 g de fração 2. A Fração 2 foi cristalizada a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,075 g de composto 111 (mp. 223°C).
Uma mistura de intermediário 23 (0,0005 mol), hidróxibenzotriazola (0,0007 moi) e EDCI (0,0007 mol) em CH2CI2 (10 ml) e THF (2 ml) foi agitada. Uma solução de NH(CH3)2.HCI (0,0006 mol) e Et3N (0,0005 mol) foi adicionada. A mistura foi agitada em temperatura ambiente durante 12 horas. H2O foi adicionada. A mistura foi extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 100/0 a 90/10; 5 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,124 g (58%). Essa fração foi purificada através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 99/1; 5 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,045 g de composto 112 (21%) (mp.>264°C).
b) Preparação de composto 113
Uma mistura de intermediário 57 (preparado de acordo com A7.b) (0,0002 mol), 1-hidróxibenzotriazola (0,0003 mol) e EDCI (0,0003 mol) em CH2Cl2 (10 ml) foi agitada. /V-metil-1-butanamina [CAS 110-68-9] (0,0002 mol) foi adicionada. A mistura foi agitada em temperatura ambiente durante 12 horas. H2O foi adicionada. A mistura foi extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. Rendimento: 0,149 g. Essa fração foi purificada através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 100/0 a 90/10; 5 pm). As frações puras foram coletadas e 0 solvente foi evaporado. Rendimento: 0,065 g. Essa fração foi captada em DIPE. O precipitado foi filtrado e seco.
Rendimento: 0,035 g de composto 113 (30%) (mp. 212°C).
c) Preparação de composto 114
Uma mistura de intermediário 23 (preparado de acordo com
A7.a) (0,0005 mol), 1-hidróxibenzotriazola (0,0007 mol) e EDCI (0,0007 mol) em CH2CI2 (10 ml) e THF (2 ml) foi agitada. 3-(metilamino)propanorirtrila
- 5 (0,0006 mol) foi adicionada. A mistura foi agitada em temperatura ambiente durante 12 horas. H2O foi adicionada. A mistura foi extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 100/0 a 90/10; 5 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,068 g. Essa fração foi cristalizada a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,032 g de composto 114 (14%) (mp. 168°C).
d) Preparação de composto 115
Uma mistura de (0,000195 mol) e metilamina
(2 equiv, 0,000390 mol) em THF (5 ml) e Et3N (0,054 ml) foi agitada em temperatura ambiente. EDCI (2 equiv, 0,000390 mol) e 1-hidróxi-benzotriazola (2 equiv, 0,000390 mol) foram adicionados. A mistura de reação foi agitada em temperatura ambiente durante 12 horas e captada em H2O. A camada orgâ5 nica foi separada, seca, filtrada e o solvente evaporado. O produto foi isolado e purificado através de cromatografia em coluna. Rendimento: 0,026 g de composto 115 (17,92%).
Exemplo B9C
Preparação de composto 116
Uma mistura de intermediário 13 (preparado de acordo com
A5.a) (0,000291 mol) e hidrazida de ácido isonicotínico (2,5 equiv., 0,000728 mol) em etanol (1 ml) e CH2CI2 (2 ml) foi agitada e submetida a refluxo durante 12 horas. O solvente foi evaporado até secagem. O resíduo foi purificado através de cromatografia. Rendimento: 0,033 g de composto 116 (24,50%).
Exemplo B9D
a) Preparação de composto 117
Cianoborohidreto de sódio (0,0024 mol) foi adicionado em temperatura ambiente a uma solução de intermediário 26 (preparado de acordo com A9) (0,0008 mol) em formaldeído (0,5 ml) e CH3CN (20 ml) sob fluxo de
N2. Ácido acético (0,5 mi) foi adicionado. A mistura foi agitada em temperatura ambiente durante 2 horas, entornada em H2O/K2CO3 a 10% e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,3 g) foi purificado através de cromato5 grafia em coluna sobre Hipersoi (eluente: CH2Ci2/CH3OH a 97/3; 5 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,08 g (28%). Essa fração foi cristalizada a partir de 2-propanona/dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,012 g de composto 117 (5%) (mp. 132°C).
b) Preparação de composto 118
A9) (0,0015 mol) e tetrahidro-2,5-dimetóxifurano (0,0077 mol) em ácido acético (10 ml) foi agitada e submetida a refluxo durante 1 hora, então, entornada em gelo-água e K2CO3 e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (1 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: ciclohexano/EtOAc a 95/5; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,23 g. Essa fração foi cristalizada a partir de DIPE/dietil éter. O precipitado foi filtrado seco. Rendimento: 0,075 g.
Essa fração foi cristalizada novamente a partir de DIPE/dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,027 g de composto 118 (5%).
100
Exemplo B9E
a) Preparação de composto 119
Tributilfosfina (0,0015 mol) foi adicionada a uma mistura de but2-enodinitriia (0,0015 mol) em THF (8 ml). A mistura foi agitada e submetida
a refluxo durante 2 horas.
A5.a) (0,0005 mol) foi adicionado. A mistura foi agitada e submetida a refluxo durante a noite. H2O foi adicionada. A mistura foi extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,618 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2 a 100%; 10 pm). Duas frações foram coletadas e o solvente foi evaporado. Rendimento : 0,03 g de composto 119 (13%).
b) Preparação de composto 120
Intermediário 13 (preparado de acordo com A5.a) (0,002 mol) foi adicionado a uma mistura de propanodinitrila (0,004 mol) e piperidina (0,004 moles) em etanol (10 ml). A mistura foi agitada em temperatura ambiente durante 5 minutos. O solvente foi evaporado. O resíduo foi captado em
101
CH2CI2 e purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH a 98/2; 15-40 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,6 g de composto 120.
Exemplo B9F
Preparação de composto 122
nBuLi [1,6 M] (0,0016 mol) foi adicionado gota a gota a -78°C a uma mistura de intermediário 27 (preparado de acordo com A10) (0,0004 mol) em THF (10 ml) sob fluxo de N2. A mistura foi agitada a -78°C durante 1 hora, então, mantida a temperatura ambiente, agitada durante 30 minutos e esfriada a -78°C. Uma solução de 2-piridinacarboxaldeído (0,0004 mol) em THF (10 ml) foi adicionada. A mistura foi agitada em temperatura ambiente durante 2 horas, entornada sobre gelo e extraída com EtOAc. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,32 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH/NH4OH 98/2/0,1; 10pm). Duas frações foram coletadas e o solvente foi evaporado. Rendimento; 0,021 g de composto 122 (10,4%) (mp. 120°C).
Exemplo B10
Preparação de composto 20
NaBH4 (0,0015 mol) foi adicionado aos poucos a 5°C a uma mistura de composto 19 (veja tabela 3) (preparado de acordo com B1) (0,0014 mol) em CH3OH (15 ml) sob fluxo de N2. A mistura foi agitada a 5°C durante hora, entornada em H2O e extraída com CH2CI2. A camada orgânica foi
102
separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,15 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eiuente: CH2CI2/CH3OH a 99/1; 10 pm). As frações puras foram coletadas e 0 solvente foi evaporado. O resíduo (0,068 g, 12%) foi cristalizado a partir de DIPE.
O precipitado foi filtrado e seco. Rendimento: 0,032 g de composto 20. Exemplo B11
Preparação de composto 21
Uma mistura de composto 2 (veja tabela 3) (0,0002 mol), ácido
3-tienilborônico (0,0005 mol), Pd(PPh3)4 (0,00002 mol) e Na2CO3 (0,0007 mol) em DME (3 ml) foi agitada e submetida a refluxo em um tubo vedado durante 3 horas. H2O foi adicionada. A mistura foi extraída com acetato de etila. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo foi purificado através de cromatografia em coluna sobre sílica-gel (eiuente: CH2C[2/CH3OH 98/2; 15-40pm). As frações puras fo15 ram coletadas e o solvente foi evaporado. Rendimento: 0,04 g de composto 21 (40%).
Exemplo B12
Preparação de composto 23
Uma mistura de composto 22 (veja tabela 3) (preparado de acor20 do com B4.a) (0,0002 mol) e Níquel de Raney (0,1 g) em CH3OH (10 ml) foi agitada em temperatura ambiente durante 15 minutos sob uma pressão de
H2 de 2 bar, então, filtrada sobre celite. A Celite foi lavada com CH3OH. O filtrado foi evaporado. Rendimento: 0,48 g. Essa fração foi purificada através de cromatografia em coluna sobre Cromasila (eiuente: CH2CI2/CH3OH a
103
99/1; 15-40 pm). Duas frações (F1, F2) foram coletadas e o solvente foi evaporado. Rendimento: 0,13 g de F1 e 0,13 g de F2. F2 foi cristalizada a partir de dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,09 g de composto 23 (20%).
Exemplo B13
Preparação de composto 24
Uma mistura de composto 1 (0,0004 mol) e Pd/C (0,07 g) em CH3OH (10 ml) foi hidrogenada a temperatura ambiente durante 5 horas sob uma pressão de H2 de 3 bar, então, filtrada sobre celite, lavada com CH2CI2 e o solvente foi evaporado até secagem. O resíduo foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. O resíduo (0,7 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 100/0 a 99/1; 5 pm). As frações puras foram coletadas e o solvente foi evaporado. O resíduo (0,06 g) foi cristalizado a partir de DIPE. O precipitado foi filtrado e seco. Rendimento: 0,04 g de composto 24 (27%).
Exemplo B14
Preparação de composto 26
NaH a 60% (0,0004 mol) foi adicionado em temperatura ambiente a uma mistura de composto 25 (veja Tabela 4) (preparado de acordo com
B6.c) (0,0004 mol) em THF (30 ml). A mistura foi agitada em temperatura ambiente durante 1 hora. Uma solução de ICH3 (0,0004 mol) em THF (30 ml) foi adicionada. A mistura for agitada a 60°C durante 2 horas, então, esfriada, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,12 g) for puri25 ficado através de cromatografia em coluna sobre Cromasila (eluente:
104
CH2CI2/CH3OH a 99/1; 10 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,049 g de composto 26 (32%).
Exemplo B15
a) Preparação de composto 123
Reagente de Jones (0,0056 mol) foi adicionado a 5°C a uma mistura de composto 18 (preparado de acordo com B9) (0,0029 mol) em 2propanona (20 ml) sob fluxo de N2. A mistura foi agitada a 5°C durante 2 horas, então, entornada em H2O, basificada com NaHCO3 e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente 10 foi evaporado. O resíduo (1,5 g) foi purificado através de cromatografia em coluna sobre sílica-gel (eluente: CH2CI2/CH3OH/NH4OH a 98/2/0,1; 15-40 pm). Duas frações (F1, F2) foram coletadas e o solvente foi evaporado. Rendimento: 0,122 g de F1 (11%) e 0,19 g de F2 (17%). F2 foi cristalizado a partir de DIPE, O precipitado foi filtrado e seco. Rendimento: 0,034 g de 15 composto 123 (mp. 150°C).
b) Preparação de composto 124
Uma mistura de composto 123 (0,0005 mol) em POCI3 (1,5 ml) foi agitada a 80°C durante 24 horas, entornada em gelo e K2CO3 a 10% e extraída com CH2CI2/CH3OH. A camada orgânica foi separada, seca (Mg20 SO4), filtrada e 0 solvente foi evaporado. O resíduo (0,14 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente:
CH2CI2/CH3OH a 99/1; 10 pm). As frações puras foram coletadas e o solvente foi evaporado. Rendimento: 0,026 g de composto 124.
105
Exemplo Β16
a) Preparação de composto 125
NaOH a 5N (2 ml) foi adicionado gota a gota a 50°C a uma mistura de composto 104 (veja Tabela 3) (preparado de acordo com B2.c) 5 (0,0003 mol) e NH2OH, HCI (0,0004 mol) em etanol (10 ml). A mistura foi agitada a 50°C durante 2 horas. Dois terços da mistura foram evaporados, A mistura foi entornada em K2O e extraída com CH2CI2. A camada orgânica foi lavada com K2CO3 10%, seca (MgSO4), filtrada e o solvente foi evaporado.
Rendimento: 0,21 g de composto 125.
1,T-carboníladiimidazola (0,0012 mol) foi adicionada a uma mistura de composto 125 (0,0003 mol) em THF (20 ml). A mistura foi agitada e submetida a refluxo durante a noite, entornada em H2O e extraída com CH2CI2. A camada orgânica foi separada, seca (MgSO4), filtrada e o solvente foi evaporado. O resíduo (0,17 g) foi purificado através de cromatografia em coluna sobre Cromasila (eluente: CH2CI2/CH3OH a 98/2; 10 pm). Duas frações foram coletadas e o solvente foi evaporado. Rendimento: 0,035 g de fração 1 e 0,05 g de fração 2. Ambas as frações foram misturadas e cristali-
10.6 zadas a partir de dietil éter. O precipitado foi filtrado e seco. Rendimento: 0,05 g de composto 126 (38%) (mp. >260°C).
Exemplo B17
Preparação de composto 253
a) 2,53 ml de acetonitrila, 0,056 g (0,253 mmoi) de Pd(OAc)2 e
0,154 g (0,506 mmol) de tris(2-metilfenil)fosfina foram mantidos em um frasco de 100 ml sob nitrogênio e a mistura foi agitada durante 10 minutos. À mistura foram adicionados 1 g (2,53 mmoles) de intermediário 58, 0,51 ml (3,8 mmoles) de Λ/,/V-dietiletanamina e 0,36 g (5,06 mmoles) de acrilamida.
A mistura for aquecida a refluxo (80°C) durante 5 dias proporcionando 28% de composto 253.
b) Em um frasco de 100 ml sob N2 foram introduzidos 0,8g (4,33 mmoles; 1 eq.) de intermediário 3a (E), 1g (4,33 mmoles; 1 eq.) de intermediário 5 e 16 ml de 2-propanol. A essa mistura, 0,72 ml de HCI a 6N em 215 propanol foram adicionados. A mistura foi agitada sob refluxo durante 72 horas e então, esfriada, proporcionando o sal de ácido clorídrico de composto 253, isto é, composto 254.
O Composto 254 pode ser convertido na base livre de acordo com metodologias conhecidas na técnica (veja também Exemplo B1A).
O Composto 253 pode ser convertido ao composto 1 de acordo com o método descrito acima no Exemplo A1c)y).
As Tabelas 3, 4 e 5 a seguir listam compostos da fórmula (I) conforme preparados de acordo com um dos exemplos acima (Ex. N°).
107
Tabela 3
| Comp. N° | Ex. N° | R3 | R4 | Dados físicos p.f.°C/(MH+)* |
| 2 | B2a | 2-benzofuranila | H | p.f. > 240 |
| 21 | B11 | 3-tienila | H | p.f. 220 |
| 3 | B2b | 2-furanila | H | p.f. 228 |
| 28 | B2a | 2-tienila | H | p.f. 235 |
| 29 | B2a | fenila | H | p.f. 230 |
| 1 | B1/B6a | -CH=CH-CN | H | p.f. 245, (E) |
| 30 | B2a | 2,4-diclorofenila | H | (460) |
| 31 | B2a | 2-benzo[b]tienila | H | (448) |
| 32 | B2a | 1-naftalenila | H | (442) |
| 33 | B2a | 3-clorofeniía | H | (426) |
| 34 | B2a | 3-aceti [fenila | H | (434) |
| 35 | B2a | 3-metilfenila | H | (406) |
| 36 | B2a | 2-naftalenila | H | (442) |
| 37 | B2a | 4-clorofenila | H | (426) |
| 38 | B2a | 4-metoxifenila | H | (422) |
| 39 | B2a | 4-metiltiofenila | H | (438) |
| 40 | B2a | /—ch2oh | H | |
| 19 | B1 | H | p.f.220 | |
| 8 | B5a | -C(=N-OH)-CH(CH3)2 | H | p.f. 156 |
| 20 | B10 | OH | H | p.f. 205 |
| 27 | B1 | vo | H | p.f. 193 |
| 41 | B10 | TV OH - | H | p.f. 200 |
108
109
110
| Comp. N° | Ex. N° | R3 | R4 | Dados físicos p.f.°C/(MH+)* |
| 69 | B4b | H | (399) | |
| 70 | B4b | S \=/ | H | (396) |
| 71 | B4b | -CH2-N(CH2-CH2-O- ch3)2 | H | (461) |
| 72 | B4b | H | (485) | |
| 73 | B4b | ÇH3 A_0Q.ch3 | H | (456) |
| 74 | B4b | H | (492) | |
| 75 | B4b | -CH2-N(CH3)-CH2- ch2-cn | H | (412) |
| 76 | B4b | _/CHí ch3 | H | (443) |
| 77 | B4b | H | (397) | |
| 78 | B4b | H | (417) | |
| 79 | B4b | H | (464) | |
| 80 | B4b | -ch2-nh-ch2-ch2- N(CH2-CH3)2 | H | p.f., 105 |
| 81 | B1 | Aii | H | p.f. 240 |
| 82 | B10 | OH | H | p.f. 170 |
| 24 | B13 | -ch2-ch2-cn | H | p.f. 208 |
| 83 | B8 | ÃyN^jO | H | p.f.>250°C |
111
| Comp. Νθ | Ex. N° | R3 | R4 | Dados físicos ' p.f.°C/(MH+)* |
| 14 | B6d | ’Ά | H | p.f.158 |
| 84 | B6c | -C(CH3)=CH-CN | H | p.f.224°C (E) |
| 18 | B9 | -CH(OH)-CH2-CN | H | p.f.252°C |
| 85 | B4b | Br | H | (474) |
| 86 | B4b | i=n | H | (473) |
| 87 | B4b | ^.OH | H | (426) |
| 88 | B4b | H | (424) | |
| 89 | B4b | % N N | H | (446) |
| 90 | B4b | H | (397) | |
| 91 | B4b | H,C^CH3 | H | (438) |
| 92 | B4b | CH3 | H | (438) |
| 93 | B4b | ÇHj | H | (410) |
| 94 | B4b | H | (410) | |
| 95 | B4b | V-Jyci h3c | H | (478) |
113
131
-CH=N-NH-C(=O)CH2-CN
H
Dados físicos p.f.°C/(MH+)* (425)
132
B9C
B9C
(468)
115
B9Bd
-C(=O)-NH-CH3 (373)
134
B9Bd
-C(=O)-N(CH3)2 (387)
135
B9Bd
-C(=O)-N(CH3)-CH2ch3 (401)
136
B9Bd
-C(=O)-N(CH2-CH3)2 (415)
137
B9Bd
-C(=O)-NH-CH2-CH3 (387)
138
B9Bd
-C(=O)-NH-CH2-CN (398)
139
B9Bd
140
B9Bd
-C(=O)-N(CH3)-CH2CN
-C(=O)-NH-CH2-CHCH (412) (397)
141
B9Bd
-C(=O)-NH~CH2ch=ch2 (399)
142
B9Bd
-C(=O)-NH-CH(CH3)2 (401)
143
B1
-N[CH2-CH(CH3)2]2
p.f. 238°C
144
B13
-CH2-CH(CN)2
p.f. 160°C
106
B6f
-CH=C(CN)-C(=O)C(CH3)3 (E), p.f. 193°C
145
B9F
(E), p.f. 229°C
H
114
| Comp. N° | Ex. N° | R3 | R4 | Dados físicos p.f.°C/(MH+)* |
| 152 | B6b | -CH=C(CH3)-CN | H | (E), p.f. 201°C |
| 153 | B13 | -CH2-CH(CH3)-CN | H | p.f. 187°C |
| 124 | B15b | -C(Ci)=CH-CN | H | |
| 154 | B9Ba | -CH=CH-C(=O)- N(CH3)-CH2-CN | H | (E) |
| 112 | B9Ba | -CH=CH-C(=O)- N(CH3)2 | H | (E), p.f>264°C |
| 155 | B9Bc | o | H | (E), p.f. 156°C |
| 156 | B9Bc | 0 | H | (E), p.f. 168°C |
| 157 | B9Bc | 0 | H | (E), p.f.>265°C |
| 158 | B9Bc | -CH=CH-C(=O)- N(CH3)-CH2-CH3 | H | (E), p.f.>260°C |
| 114 | B9Bc | -CH=CH-C(=O)- N(CH3)-(CH2)2-CN | H | (E), p.f. 168°C |
| 159 | B9Bc | -CH=CH-C(=O)- N(CH2-CH3)2 | H | (E), p.f. 249°C |
| 160 | B6b | -C(CH3)=C(CH3)-CN | H | (E) |
| 107 | B9Aa | -CH=CH-CI | H | (Z), p.f. 250°C |
| 161 | B9Aa | -CH=CH-Br | H | (Z), p.f. 248°C |
| 111 | B9Ad | -CH=C(Br)2 | H | p.f. 223°C |
| 122 | B9F | H | (E), p.f. 120°C | |
| 162 | B9F | H | (E), p.f. >260° C | |
| 163 | B9F | H | p.f. 128°C |
115
| Comp. N° | Ex. N° | R3 | R4 | Dados físicos p.f.°C/(MH+)* |
| 164 | B9FF | H | p.f. 104°C | |
| 125 | B16a | VJ | H | |
| 104 | B2c | H | ||
| 165 | B9F | H | p.f. 112°C | |
| 166 | B9F | Λ_ Γ3 í) | H | p.f. 194°C |
| 167 | B9F | H | p.f. 191°C | |
| 126 | B16b | H | p.f. >260°C | |
| 168 | B4c | -ch2-o-ch2-ch3 | H | p.f. 201 °C |
| 117 | B9Da | H | -N(CH3)2 | p.f. 132°C |
| 120 | B9Eb | -CH=C(CN)2 | H | |
| 253 | B17a/b | -CH=CH-C(=O)NH2 | H | (E) |
| 254 | B17b | -CH=CH-C(=O)NH2 | H | (E) HCl |
* (MH+) define a massa do composto protonado; ela foi determinada com um espectrômetro MicroMass equipado com uma sonda de eietropulverização com um analisador quadripolar.
Tabela 4:
| Comp. N° | Ex. N° | R3 | R1 | Dados físicos p.f.°C/(MH+)* |
| 25 | B6c | “CH=CH-CN | H | p.f. 256°C |
| 99 | B3 | -CH2-CN | H | p.f. 184°C |
| 100 | B4b | -CH2-N(CH2-CH3)2 | H | p.f.172 °C |
116
| Comp. Ν° | Ex. Ν° | R3 | R1 | Dados físicos p.f.°C / (MH+)* |
| 102 | Β13 | -CH2-CH2-CN | H | p.f. 224°C |
| 101 | B4b | -CH2-N(CH3)-CH2-CH2~CN | H | p.f.196°C |
| 26 | Β14 | -CH=CH-CN | ch3 | p.f. 195°C |
| 169 | B9Bd | -C(=O)-N(CH2-CH3)2 | H | p.f. 172°C |
| 170 | B4b | -CH2-N(CH3)-CH2-CN | H | |
| 171 | B4b | H | (398) | |
| 172 | B2a | hü | H | p.f. 158°C |
| 173 | B4b | -CH2-N(CH3)-CH2-CH2-N(CH3)2 | H | p.f. 196°C |
| 174 | B4b | -CH2-N(CH3)-CH=N-CN | H | p.f. 254°C |
| 175 | B14 | 2-furanila | ch3 | p.f. 178°C |
| 118 | B9Db | rd | H | 164°C |
| 176 | B14 | rd | ch3 | p.f. 188°C |
| 177 | B9Aa | -CH=CH-Br | H | (Z), p.f. 169°C |
| 110 | B9Ac | -CH=C(F)-CN | H | (E), p.f. 254°C |
| 178 | B6b | -CH=C(CH3)-CN | H | (2) |
| 179 | B6b | -CH=C(CH3)-CN | H | (E) |
| 180 | B9Bb | FHj /=\ 0 | H | (E) |
| 181 | B9Bc | -CH=CH-C(=O)-NH-ciclopropila | H | (E)(426) |
| 182 | B9Bc | -CH=CH-C(=O)-NH-CH2-CH2- N(CH3)2 | H | (E) (427) |
| 183 | B9Bc | -CH=CH-C(=O)-NH-CH2-CH2- ch2-o-ch3 | H | (E)(458) |
| 184 | B9Bc | -CH=CH-C(=O)-NH-CH2- CH(CH3)2 | H | (E)(442) |
| 185 | B9Bc | -CH=CH-C(=O)-NH-CH2-CH2-CN | H | (E)439) |
117
| Comp. N° | Ex. N° | R3 | R1 | Dados físicos p.f.°C/(MH+)* |
| 186 | B9Bc | r H | H | (E)(468) |
| 187 | B9Bc | -CH=CH-C(=O)-NH-CH2-CH2-CH2- N(CH3)2 | H | (E)(471) |
| 188 | B9Bc | -CH=CH-C(=O)-NH-(CH2)3-O-CH2- ch3 | H | (E)(472) |
| 189 | B9Bc | -CH=CH-C(=O)-NH-CH2-CH3 | H | (E)(414) |
| 190 | B9Bc | -CH=CH-C(=O)-NH-CH2-CH2-O- ch3 | H | (E)(444) |
| 191 | B9Bc | -CH=CH-C(=O)-NH-CH(CH3)2 | H | (E)(428) |
| 192 | B4b | ch3 | H | (E)(491) |
| 193 | B4b | H | (E)(444) | |
| 194 | B4b | -CH=CH-CH2-N(CH3)-CH2-CH2- CN | H | (E)(439) |
| 195 | H | (E)(483) | ||
| 196 | B4b | -CH=CH-CH2-N(CH2-CH2-O-CH3)2 | H | (E)(488) |
| 197 | B4b | H | (E)(476) | |
| 198 | B4b | -CH=CH-CH2-N(CH3)-CH2~CH2- ch3 | H | (E)(428) |
| 199 | B4b | -CH=CH-CH2-N(CH3)-CH2-CH2- N(CH2-CH3)2 | H | (E)(485) |
| 200 | B4b | -CH=CH-CH2-N(CH2-CH3)-CH3 | H | (E)(414) |
| 201 | B4b | -CH=CH-CH2-N(CH2-CH2-CH3)2 | H | (E)(456) |
| 202 | B4b | -CH=CH-CH2-N(CH3)-CH2-CH2- ch2-ch3 | H | (E)(442) |
| 203 | B4b | /—\ | H | (E)(438) |
118
| Comp. N° | Ex. N° | R3 | R1 | Dados físicos p.f.°C / (MH+)* |
| 204 | B4b | x ''•'Ά/° | H | (E)(442) |
| 205 | B4b | A /—\ ^n~ch3 | H | (E)(455) |
| 206 | B4b | -CH=CH-CH2-N(benzil)-CH2-CH2- N(CH3)2 | H | (E)(533) |
| 207 | B4b | -CH=CH-CH2-N(CH3)2 | H | (E)(457) |
| 208 | B4b | -CH=CH-CH2-N(isopropil)2 | H | (E)(456) |
| 121 | B9Bb | -CH=CH-C(=O)-NH2 | H | (E) |
| 209 | B9Bb | o | H | (E), p.f. 116°C |
| 210 | B9Bb | H | (E), p.f. 254°C | |
| 211 | B9Bb | -CH=CH-C(=O)-N(CH3)-CH2-CH2- OH | H | (E), p.f. 222°C |
| 212 | B9Ba | -CH=CH-C(=O)-N(CH3)-CH2-CN | H | (E), p.f. 198°C |
| 213 | B6c | -C(CH3)=CH-CN | H | (E) |
| 214 | B9Bc | -CH=CH-C(=O)-N(CH3)-CH2-CH2- CN | H | (E), p.f. 204°C |
| 215 | B9Bc | -CH=CH-C(=O)-N(CH3)-CH2-CH3 | H | (E), p.f. 211 °C |
| 216 | B9Bc | 0 | H | (E), p.f. 246°C |
| 217 | B9Bc | -CH=CH-C(=O)-N(CH2-CH3)2 | H | (E), p.f. 226°C |
| 218 | B9Bc | o | H | (E), p.f. 196°C |
| 219 | B9Ba | -CH=CH-C(=O)-N(CH3)2 | H | (E), p.f. 225°C |
| 220 | B9E | -CH=C(CN)-CH2-CN | H | (Z), p.f. 195°C |
| 109 | B9Ab | -CH=CH-CI | H | (E), p.f. 200°C |
| 108 | B9Ab | -CH=CH-CI | H | (Z), p.f. 165°C |
| 221 | B9Ba | -CH=CH-C(=O)-NH-CH3 | H | (E), p.f. 260°C |
119
| Comp. N° | Ex. N° | R3 | R1 | Dados físicos p.f.°C / (MH+)* |
| 222 | B9Bb | -CH=CH-C(=O)-N(CH2-CH2-O- ch3)2 | H | (E), p.f. 158°C |
| 223 | B9Bb | r 0 | H | (E), p.f. 208°C |
| 224 | B9Bb | 0 | H | (E), p.f. 208°C |
| 113 | B9Bb | -CH=CH-C(=O)-N(CH3)-CH2-CH2- ch2-ch3 | H | (E), p.f. 212°C |
| 225 | B4b | -CH2-N(CH2-CH2-CN)2 | H | p.f. 154°C |
| 226 | B2a | 2-furanila | H | p.f. 162°C |
* (MH+) define a massa do composto protonado; ela foi determinada com um espectrômetro MicroMass equipado com um sonda de eletropulverização com um analisador quadripolar.
Tabela 5:
R4a
| Comp. N° | Ex. N° | R3 | R49 | R4b | X1 | Dados físicos p.f.°C |
| 227 | B13 | -CH2-CH2-CN | ch3 | H | -NH | p.f. 186°C |
| 228 | B4b | -CH2-N(CH3)-CH2-CN | ch3 | H | -NH | p.f. 138°C |
| 229 | B6b | -CH=C(CH3)-CN | ch3 | H | -NH | p.f. 190°C |
| 230 | B6c | -CH=CH-CN | ch3 | H | -0- | (E), p.f. 254°C |
| 231 | B6b | -CH=C(CH3)-CN | ch3 | H | -O- | p.f. 150°C |
| 232 | B6c | -C(CH3)=CH-CN | ch3 | H | -O- | (E), p.f. 234°C |
| 105 | B4d | -ch2-o-ch2-ch3 | ch3 | H | -O- | p.f. 140°C |
| 233 | B6b | -CH=C(CH3)-CN | ch3 | Cl | -NH | p.f. 214°C |
| 234 | B13 | -ch2-ch2-cn | CHs | H | -0- | p.f. 199°C |
120
| Comp. N° | Ex. N° | R3 | R4a | R4b | X1 | Dados físicos p.f.°C |
| 235 | B13 | -CH(CH3)-CH2-CN | ch3 | H | -O- | p.f. 195°C |
| 236 | B13 | -CH2-CH(CH3)-CN | ch3 | H | -O- | p.f. 161°C |
| 237 | B6c | -CH=CH-CN | ch3 | H | -NH | (E), p-f. >264°C |
| 238 . ..... | B3 | -ch2-cn | ch3 | Cl | -NH | p.f. 184°C |
| 239 | B6c | -CH=CH-CN | ch3 | 2- furanila | -NH | (E) p.f.175°C |
| 119 | B9E | -CH=C(CN)-CH2-CN | ch3 | 2- furanila | -NH | |
| 240 | B9F | ch3 | Cl | -NH | p.f. 248°C Z/E=50/50 | |
| 241 | B4b | -CH2-N(CH3)-CH2- ch2-cn | ch3 | Br | -NH | p.f. 148°C |
| 242 | B1 | -CH=CH-CN | H | isopro- pila | -NH | (E) 30%(Z) 70% |
| 243 | B4b | -CH2-N(CH3)-CH2- ch2-cn | ch3 | Cl | -NH | p.f. 85°C |
| 244 | B6c | -CH=CH-CN | H | Br | -NH | (E), p.f. 270°C |
| 245 | B6c | -CH=CH-CN | H | -och3 | -NH | (E), P-f258°C |
| 246 | B6b | -C(CH3)=C(CH3)-CN | ch3 | H | -0- | (E), p.f. 214°C |
| 247 | B6b | -CH=C(CH3)-CN | ch3 | Br | -NH | p.f. 212°C |
| 248 | B6c | -CH=CH-CN | ch3 | Br | -NH | (E), p.f. 250°C |
| 249 | B6b | -CH=C(CH3)-CN | H | -och3 | -NH | p.f. 166°C |
| 250 | B6b | -CH=C(CH3)-CN | H | Br | -NH | p.f. 186°C |
| 251 | B13 | -CH2-CH2-CN | H | -och3 | -NH | p.f. 228°C |
| 252 | B4c | -CH2-O-CH2-CH2-CN | H | Cl | -NH | p.f. 168°C |
121
Λ?
| Comp. N° | Ex. N° | R3 | R4a | R4b | X1 | Dados físicos p.f.°C |
| 133 | B6c | -CH=CH-CN | CH3 | Cl | -NH | (E), p.f. 258°C |
C. Exemplo farmacológico
A atividade farmacológica dos presentes compostos foi examinada usando-se o seguinte teste.
Um procedimento de ensaio rápido, sensível e automático foi usado durante a evolução in vitro de agentes anti-HIV. Uma linhagem de células T4 HIV-1 transformada, MT-4, a qual foi anteriormente mostrado (Koyanagi e colaboradores, Int. J. Câncer, 36, 445-451, 1985) ser altamente susceptível a e permissiva de infecção pelo HIV, serviu como a linhagem de célula alvo. Inibidores do efeito citopático HlV-induzido foram usados como o ponto final. A viabilidade de células HIV- e placebo-infectadas foi avaliada espectrofotometricamente via uma redução in situ com brometo de 3-(4,5dimetiltiazoi-2-il)-2,5-difeniltetrazólio (MTT). A concentração citotóxica (CC50 em M) a 50% foi definida como a concentração de composto que reduz a absorção da amostra de controle placebo-infectada em 50%. O percentual de proteção obtido através do composto em células HlV-infectadas foi calculado através da seguinte fórmula:
(OPT)H1V ~(ODC)h,v (ODC)mock — (ODC)H|V experso em % pelo que (ODy)H|V é a densidade óptica medida, a qual proporciona a concentração do composto de teste em células HlV-infectadas; (ODq)H)V é a densidade óptica medida para as células HlV-infectadas de controle não tratadas; (ODc)mock é a densidade óptica medida para as células placeboinfectadas de controle não tratadas; todos os valores de densidades ópticas foram determinados a 540 nm. A dose que obtém 50% de proteção de acordo com a fórmula acima foi definida como a concentração de inibidores a
50% (IC50 em Μ). A proporção de CC50 para IC50 foí definida como o índice de seletividade (SI).
A Tabela 6 lista os valores de PIC50 (-logICso), PCC50 (~
122
logCCso) θ pSI (pCCgQ-pICso) para os compostos da fórmula (I). Por exem-<>.... pio, um composto o qual uma IC50 vale de 10'9M, isto é, pIC5Q=9, e uma CC50 vale de 10’5 Ísto PCCso= 5 , tem um Sl de 10'5 M/10'9M = 10.000, isto é, um pSI de 5-9 = -4.
Tabela 6
| Co. N° | PÍC50 (M) | PCC50 (M) | pSI |
| 21 | 8,4 | 4,9 | -3,5 |
| 3 | 8,4 | 5,5 | -2,9 |
| 1 | 9,4 | 5,0 | -4,4 |
| 34 | 8,0 | 4,8 | -3,2 |
| 19 | 8,4 | 4,8 | -3,6 |
| 45 | 8,7 | 5,0 | -3,8 |
| 49 | 8,0 | 4,8 | -3,2 |
| 70 | 8,1 | 4,8 | -3,3 |
| 75 | 9,0 | 5,0 | -4,0 |
| 73 | 8,4 | 4,9 | -3,5 |
| 79 | 8,0 | 5,3 | -2,7 |
| 84 | 9,0 | 4,5 | -4,5 |
| 18 | 8,8 | 4,9 | -4,0 |
| 25 | 9 | 4 | -5 |
| 24 | 9,1 | 5,7 | -3,4 |
| 81 | 9,1 | 5,6 | -3,5 |
| 11 | 9,2 | 5,7 | -3,5 |
| 10 | 9,2 | 6,3 | -2,9 |
| 174 | 8,8 | 5,3 | -3,5 |
| 227 | 9,5 | <4,0 | <-5,5 |
| 144 | 8,6 | 6,4 | -2,2 |
| 229 | 8,8 | <4,0 | <-4,8 |
| 118 | 8,4 | 4,1 | <-4,1 |
| 177 | 8,3 | <4,0 | <-4,3 |
123
| Co. N° | PIC50 (M) | pCC50 (M) | pSI |
| 106 | 77 | 5,2 | -2,5 |
| 145 | 87 | 5,3 | -3,4 |
| 147 | 9,4 | 57 | -37 |
| 148 | 8,8 | 4,9 | -3,9 |
| 230 | 9,2 | <4,0 | <-5,2 |
| 231 | 9,2 | <4,0 | <-5,2 |
| 232 | 8,4 | <4,0 | <-4,4 |
| 105 | 7,2 | <4,0 | <-3,2 |
| 110 | 8,6 | 4,3 | -4,3 |
| 233 | 9,3 | 5,7 | -3,6 |
| 234 | 8,7 | <4,0 | <-4,7 |
| 235 | 9,3 | <4,0 | <-5,3 |
| 236 | 8,8 | <4,0 | <-4,8 |
| 149 | 9,1 | 5,3 | -3,8 |
| 150 | 8,8 | 4,8 | -4,0 |
| 237 | 8,9 | <4,0 | <-4,9 |
| 151 | 9,1 | 5,5 | -3,6 |
| 152 | 9,1 | 4,8 | -4,3 |
| 178 | 8,8 | 5,7 | -3,1 |
| 179 | 8,9 | <4,0 | <-4,9 |
| 153 | 9,2 | 6,3 | -2,9 |
| 124 | 8,5 | 4,7 | -3,8 |
| 238 | 9,5 | 5,6 | -3,9 |
| 112 | 9,1 | 4,9 | -4,2 |
| 244 | 9,2 | 4 | -5,2 |
| 209 | 8,6 | 4,9 | -37 |
| 210 | 8,3 | 4,8 | -3,5 |
| 155 | 8,8 | 6,3 | -2,5 |
| 156 | 7,7 | 5,1 | -2,6 |
124
| Co. N° | pIC50 (M) | pCCgo (M) | pSI |
| 158 | 8 | 5,5 | -2,5 |
| 212 | 9,1 | 5 | -4,1 |
| 114 | 8,6 | 5,1 | -3,5 |
| 213 | 9 | 4,8 | -4,2 |
| 214 | 8,6 | 5,1 | -3,5 |
| 215 | 9,1 | 5,5 | -3,6 |
| 216 | 8,2 | 5 | -3,6 |
| 219 | 9,1 | 5 | -4,1 |
| 245 | 8,8 | 4 | -4,8 |
| 146 | 8,4 | 5,4 | -3 |
| 247 | 9,2 | 6,2 | -3 |
| 248 | 9,3 | 5,7 | -3,5 |
| 249 | 8,5 | 4 | -4,5 |
| 42 | 9 | 6,3 | -2,7 |
| 251 | 8,9 | 5 | -3,9 |
| 133 | 9,2 | 4 | -5,2 |
| 9 | 8,8 | 4,8 | -4 |
| 239 | 8,9 | 5 | -3,9 |
| 241 | 9,4 | 5,3 | -4,1 |
| 126 | 8,4 | 4,9 | -3,5 |
As composições da presente invenção podem compreender um outro polímero orgânico.
A solução supersaturada do composto de droga criada através dos componentes da composição acima quando de exposição à água, con5 forme indicado acima, pode ser estabilizada através dos efeitos de intensificação de viscosidade de um polímero orgânico. A presença do polímero orgânico impedirá precipitação do composto de droga à medida que o microambiente se torna mais diluído, conforme mais água entra.
O polímero orgânico usado nas composições da invenção pode ser qualquer um dos polímeros orgânicos sintéticos, semi-síntéticos ou não
125 sintéticos, solúveis em água, fisiologicamente toleráveis.
Assim, por exemplo, o polímero pode ser um polímero natural, tal como um polissacarídeo ou polipeptídeo, ou um derivado dos mesmos ou um polímero sintético, tais como um óxido de polialquileno (por exemplo,
PEG), poliacrilato, polivinilprrrolidona, etc. Polímeros misturados, por exemplo, copolímeros em blocos e glicopeptídeos, podem, naturalmente, ser usados.
Uma vez que acredita-se que o efeito do polímero orgânico se origina de uma intensificação na viscosidade, o que serve para estabilizar soluções supersaturadas do composto de droga contra dissolução da composição da invenção, o polímero convencional tem um peso molecular na faixa de 500D a 2 MD e, convencionalmente, tem uma viscosidade aparente de 1 a 100 mPa.s quando em uma solução aquosa a 2% a 20°C. Por exemplo, o polímero solúvel em água pode ser selecionado do grupo compreen15 dendo:
- alquiiceluloses, tal como metilcelulose,
- hidroxialquilceluloses, tais como hidroximetilcelulose, hidroxietilcelulose, hidroxipropilcelulose e hidroxibutilcelulose,
- hidroxialquil alquiiceluloses, tais como hidróxietil metilcelulose e hidroxipropil metilcelulose,
- carboxialquilceluloses, tal como carboximetilcelulose,
- sais de metal alcalino de carboxialquilceluloses, tal como carboximetilcelulose de sódio,
- carboxialquilalqutlceluloses, tal como carboximetiletilcelulose,
- ésteres de carboxialquilcelulose,
- amidos,
- pectinas, tal como carboximetilamilopectina de sódio,
- derivados de quitina, tal como quitosan,
- heparina e heparinóides,
- polissacarídeos, tais como ácido algínico, sais de metal alcalino e de amônio dos mesmos, carrageninas, galactomananas, tragacanto, ágarágar, goma arábica, goma de guar e goma de xantana,
126
- ácidos poliacrílicos e os sais dos mesmos,
- ácidos polimetacrílicos e os sais dos mesmos, copolímeros de metacrílato,
- álcool polivinílico,
- polivinilpirrolidona, copolímeros de polivinilpirrolidona com acetato de viniIa,
- óxidos de polialquileno, tais como óxido de polietileno e óxido de polipropileno e copolímeros de óxido etileno e óxido propileno, por exemplo, poioxâmeros e poloxaminas.
Polímeros não-enumerados os quais são farmaceuticamente aceitáveis e têm propriedades físico-química apropriadas, conforme definido aqui antes, são igualmente adequados para a preparação das composições de acordo com a presente invenção.
De preferência o polímero orgânico é um éter de celulose, por exemplo, metil celulose, hidroxietilmetilcelulose ou hidroxipropilmetilcelulose (HPMC), por exemplo, um Methocel® (disponível da Colorcon, Inglaterra), tais como Methocel® A, Methocel® E, Methocel® F, Methocel® K, Methocel® J ou Methocel® HB ou um Metolose®, tais como Metolose® SM, Metolose® SH ou Metolose® SE. Especialmente, de preferência, o polímero orgânico é uma hidroxipropilmetilcelulose, por exemplo, Methocel® E de 5 cps a Methocel® K15M de 15000 cps.
Mesmo quantidades muito pequenas do polímero orgânico servem para se obter um efeito benéfico nas composições da invenção. Assim, nas composições da invenção, o polímero orgânico pode, convencionaimen25 te, estar presente a 0,05 a 35% em peso, de preferência 0,1 a 20%, mais preferivelmente 0,5 a 15%, e ainda mais preferivelmente 2 a 11% em peso (com relação ao peso total de composto de droga, ácido ou base, tensoativo e polímero orgânico). O teor e grau de viscosidade do polímero orgânico afetam o perfil de dissolução do composto de droga nas composições da inven30 ção, com um teor aumentado de polímero orgânico e/ou grau de viscosidade aumentado (por exemplo, 15000 mPa.s em lugar de 5 mPa.s (valores de mPa.s sendo em uma solução aquosa a 2% a 20°)) tendem a desacelerar a
127 dissolução do composto de droga). Conseqüentemente, a seleção da identidade e quantidade do polímero orgânico, geralmente, dependerá do perfil de dissolução que é desejado. Por exemplo, uma composição que proporciona liberação sustentada da droga, compreenderá um polímero solúvel em água tendo uma viscosidade aparente de mais de 1.000 mPa.s, quando dissolvida em solução aquosa a 2% a 20°C.
Assim, as composições de acordo com a invenção podem ser projetadas de uma forma a proporcionar um perfil de dissolução de droga favorável em particular. Por exemplo, a dissolução pode ser suficientemente rápida para assegurar disponibilidade substancialmente completa do composto de droga para captação biológica (por exemplo, a partir da boca, nariz, estômago ou vagina), ainda assim suficientemente lenta para proporcionar um perfil de captação no plasma mais prolongado, por exemplo, evitando-se re-precipitação de droga antes que a composição atinja o estômago.
Como uma concretização preferida, a invenção proporciona uma composição farmacêutica compreendendo um composto de droga básico, um tensoativo, um ácido fisiologicamente tolerável e opcionalmente um polímero orgânico, caracterizado pelo fato de que a 5, 15 e 45 minutos após a adição de uma quantidade da referida composição contendo 100 mg do refe20 rido composto de droga a 600 mL de ácido clorídrico a 0,1 N a 37°C, de 7 a 25% (de preferência 10 a 20, especialmente 12 a 18), 45 a 70% (de preferência 50 a 65, especialmente 54 a 63) e pelo menos 96% (de preferência pelo menos 97, especialmente pelo menos 98), respectivamente, do referido composto de droga estão em solução no referido ácido clorídrico. Esses quadros se referem aos estudos de dissolução in vitro dissolução conduzidos de acordo com a monografia USP 23, <711> Dissolution, páginas 17911793.
Por exemplo, na determinação do perfil de dissolução apresentado acima, a composição é colocada sem um revestimento ou com um re30 vestimenta rapidamente solúvel (por exemplo, uma cápsula com envoltório de gelatina) em HCI a 0,1 N (ou um outro meio apropriado) e a mistura é agitada usando o método USP com uma pá, aparelho 2, a uma velocidade de
128 ou 100 rpm.
As composições da invenção podem, se desejado, ser aquosas, mas, em gerai, de preferência, serão substancialmente isentas de água, por exemplo, contendo até 3% em peso, de preferência menos de 1 % em peso água, e ainda mais preferivelmente menos de 0,5% água, mas podem ser misturadas com água imediatamente antes de administração ou podem ser revestidas e dispersas em um meio aquoso, pelo que o revestimento é rompido apenas após administração. Tais composições aquosas são consideradas como caindo dentro do escopo da invenção. Dependendo da seleção de componentes, as composições da invenção podem ser líquida, sólida ou semi-sóiida - por exemplo, semelhante a gel. De preferência, as composições não são outras de fluxo livre em temperatura ambiente (por exemplo, 21 °C), que não partículas de fluxo livre. Assim, as composições, em temperatura ambiente, são, de preferência, sólidas ou semi-sólidas ou mais preferivelmente, fluidos altamente viscosos.
Nas composições da invenção, o composto de droga, tensoativo, ácido respectivamente base e opcionalmente o polímero orgânico são íntimamente administrados.
Assim, onde a composição é em partículas, o ácido (base), composto de droga, tensoativo e opcionalmente o polímero orgânico são misturados juntos dentro das partículas (por exemplo, a nível molecular; isto pode ser obtido através de remoção do solvente de uma solução desses componentes, resultando na formação de uma dispersão sólida ou semi-sólida). Misturas de granulados onde partículas individuais não contêm todos os três ou opcionalmente quatro componentes ou têm núcleos de um ou mais componentes revestidos com outros componentes não são preferidas. Essa mistura íntima é importante, uma vez que os efeitos dos componentes são complementares, a nível microscópico, durante dissolução das composições da invenção, conforme explicado aqui acima.
De preferência, todos componentes são dispersos de modo a formar um sistema que é química e fisicamente uniforme ou total mente homogêneo, ou consiste em uma fase conforme definido em termodinâmica; tal
129 dispersão será denominada uma fase termoplástica ou sistema aqui depois. Os componentes do sistema termoplástico estão prontamente biodisponíveis aos organismos os quais eles são administrados. Essa vantagem pode, provavelmente, ser explicada pela facilidade com a qual o referido sistema termoplástico pode formar soluções líquidas quando contatadas com um corpo líquido, tal como suco gástrico. A facilidade de dissolução pode ser atribuída, pelo menos em parte, ao fato de que a energia requerida para dissolução dos componentes de um sistema termoplástico ser menor do que aquela requerida para a dissolução de componentes de uma fase sólida cristalina ou microcristalina.
O termo uma dispersão sólida, usado aqui antes ou aqui depois, define um sistema em um estado sólido (em oposição a um estado líquido ou gasoso) compreendendo os componentes das presentes composições, em que um componente se dispersa mais ou menos uniformemente nos outros componentes (os componentes podem incluir agentes de formulação adicionais farmaceuticamente aceitáveis, geralmente conhecidos na técnica, tais como plastificantes, conservantes e semelhantes). Quando a referida dispersão dos componentes é tal que o sistema é química e fisicamente uniforme ou totaimente homogêneo ou consiste em uma fase conforme definido em termodinâmica, tal dispersão sólida será denominada uma solução sólida. Soluções sólidas são sistemas físicos preferidos, porque os componentes nas mesmas estão, usuaimente, prontamente biodisponíveis aos organismos os quais elas são administrados. Essa vantagem pode, provavelmente, ser explicada pela facilidade com a qual as referidas soluções sólidas podem formar soluções líquidas quando contatadas com um meio líquido, tal como os sucos gastrointestinais. A facilidade de dissolução pode ser atribuída, pelo menos em parte, ao fato de que a energia requerida dissolução dos componentes de uma solução sólida ser menor do que aquela requerida para a dissolução de componentes de uma fase sólida cristalina ou microcristalina.
O termo uma dispersão sólida também compreende dispersões as quais são menos homogêneas do que soluções sólidas. Tais dispersões
130 não são totalmente química e fisicamente uniformes ou compreendem mais de uma fase. Por exemplo, o termo uma dispersão sólida também se refere a um sistema tendo domínios ou pequenas regiões em que compostos de droga amorfos, microcristalinos ou cristalinos e/ou tensoativos amorfos, mi5 crocristalinos ou cristalinos e/ou ácidos amorfos, microcristalinos ou cristalinos ou opcionalmente polímeros amorfos, microcristalinos ou cristalinos, são dispersos mais ou menos uniformemente em outra fase compreendendo uma solução sólida compreendendo um composto de droga, um tensoativo, um ácido (base) e opcionalmente um polímero. Os referidos domínios são regiões dentro de uma dispersão sólida distintivamente marcados por alguma característica física, de pequeno tamanho e uniforme e aleatoriamente distribuídas no decorrer de uma dispersão sólida.
As composições da invenção podem ser preparadas fazendo-se uma mistura íntima do composto de droga, tensoativo, ácido (base) e opcio15 nalmente o polímero orgânico. Isso pode ser realizado mais eficazmente através de dissolução desses componentes em um solvente líquido para os mesmos e, subseqüentemente, remoção do solvente. Assim, encarada sob um outro aspecto, a invenção proporciona um processo para a preparação de uma composição farmacêutica, o referido processo compreendendo: dis20 solução de um composto de droga, um tensoativo, um ácido solúvel em água fisiologicamente tolerável (base) e opcionalmente um polímero orgânico solúvel em água fisiologicamente tolerável em um solvente: remoção do solvente de uma solução resultante; opcionalmente transformação do produto resultante em formatos desejados; e opcionalmente revestimento do produto resultante com um material de revestimento fisiologicamente tolerável.
Alternativamente, quando os componentes da composição são termoestáveis, então, a mistura íntima dos referidos componentes também pode ser preparada através de co-fusão dos mesmos. Portanto, a presente invenção também proporciona um processo para o preparação da presente composição farmacêutica, o referido processo compreendendo co-fusão de um composto de droga, um tensoativo, um ácido solúvel em água fisiologicamente tolerável (base) e opcionalmente um polímero orgânico solúvel em
131 água fisiologicamente tolerável; e opcionalmente transformação do produto resultante em formatos desejados; e opcionalmente revestimento do produto resultante com um material de revestimento fisiologicamente tolerável.
Em particular, os processos descritos acima podem ser realiza5 dos usando-se uma das seguintes tecnologias:
a) secagem-pulverização:
Os componentes das presentes composições podem ser dissolvidos em um solvente adequado e, assim, a solução obtida pode ser pulverizada-seca a fim de se obter um pó. O pó pode ser ainda processado, por exemplo, em comprimidos ou enchida em cápsulas.
b) Secagem-congelamento;
Os componentes das presentes composições podem ser dissolvidos em um solvente adequado e, assim, a solução obtida pode então, ser congelada-seca de forma a se obter um pó o qual pode ainda ser processa15 do, por exemplo, em comprimidos ou enchida em cápsulas. Alternativamente, a solução também pode ser congelada-seca diretamente em um modelo adequado, o referido modelo adequado compreendendo a embalagem de blister final.
c) Tecnologia de fluido super crítico (SCF):
Os componentes das presentes composições podem ser dissolvidos em um fluido compressível, em particular um fluido supercrítico (isto é, qualquer substância acima de sua temperatura crítica e pressão crítica, o referido fluido supercrítico possuindo propriedades semelhantes ao gás e ao líquido) (nesse caso, o SCF é considerado como um solvente; referência, portanto, é feita a RESS (Expansão Rápida de Soluções Supercríticas) ou PGSS (partículas de Soluções Saturadas de Gás), seguido pela remoção de SCF (por exemplo, por meio de descompressão) e, assim, obtendo-se um pó o qual pode ainda ser processado, por exemplo, em comprimidos ou enchido em cápsulas. A tecnologia do fluido super crítico também pode ser aplicada quando o SCF é considerado como um anti-solvente (referência, portanto, é feita ao GAS (Gás Anti Solvente), SEDS (Dispersão Intensificada em Solução por fluidos supercríticos), ASES (Sistema de Extração de Solvente em
132
Aerossol), SAS (Anti-solvente supercrítico) ou PCA (Precipitação com Antisolvente Comprimido). Nesse caso, os componentes da composição são dissolvidos em um solvente apropriado e o SCF é usado para intensificar a evaporação do solvente, assim, obtendo-se um pó, o qual pode ainda ser processado conforme descrito acima.
d) Revestimento com veículo:
Os componentes das presentes composições podem ser dissolvidos em um solvente adequado e a solução resultante pode ser revestida, pulverizada, granulada sobre um veículo adequado, seguido por evaporação do solvente. Veículos apropriados que podem ser usados dependem da tecnologia usada, por exemplo, celulose microcristalina pode ser usada quando peletização é pretendida e, então, o equipamento apropriado, por exemplo, um equipamento com leito fluido ou SiO2 fumegada, pode ser usado para a formação de granulados e isso pode ser obtido, por exemplo, em um granulador de elevado cisalhamento ou o veículo pode ser um núcleo inerte, por exemplo, um glóbulo de açúcar, sobre o qual a solução dos componentes da presente composição pode ser pulverizada. Evaporação do solvente pode ser obtida, por exemplo, através de secagem em temperaturas elevadas e/ou sob vácuo ou através de aplicação de microondas.
e) Co-fusão:
Quando os componentes da composição são termoestáveis, eles podem ser misturados fisicamente, fundidos e misturados novamente. A mistura fundida pode, então, ser diretamente formatada nos formatos desejados (calandragem; moldagem por injeção) por exemplo, o fundido pode ser diretamente enchido ou injetado na embalagem de blíster final ou pode ser enchido ou injetado em moldes desejados ou pode ser diretamente enchido ou injetado em uma cápsula, seguido por resfriamento. A mistura fundida pode também ser, primeiro, deixada esfriar e, então, ainda processada, por exemplo, através de trituração a um pó e compressão em comprimidos ou enchimento em cápsulas. A co-fusão dos componentes da presente composição pode ser realizada simplesmente através de aquecimento da mistura física ou através de fusão-extrusão. No último caso, os componentes são fisica30
133 mente misturados e alimentados a um extrusor em estágio quente no qual^ ^s -T' mistura é aquecida, fundida e composta, seguido por formatação do extrudado fundido resultante, conforme descrito acima, por exemplo, através de moldagem por injeção ou o extrudado fundido pode esfriar, seguido por tritu5 ração em um pó o qual pode ainda ser processado em um comprimido ou o qual pode ser enchido em uma cápsula.
Alternativamente, o fundido também pode ser granulado (granulação de fundido; granulador com elevado cisalhamento), pulverizado ou revestido sobre um veículo adequado (referência, portanto, é feita ao item d).
No caso de granuiação de fundido, a fusão pode ser realizada em um extrusor-fusão onde o veículo é adicionado durante o processo extrusão e o extrudado resultante pode ser formatado conforme descrito acima. No caso do veículo ser um excipiente adequado o qual permite esferonização, o extrudado obtido pode ser esferonizado, por exemplo, usando-se um marumari15 zer.
f) Extrusão
Os componentes da composição podem ser misturados e alimentados a um extrusor, por exemplo, via o alimentador de pó seco, e o solvente opcionalmente contendo o tensoativo pode ser adicionado ao extrusor, por exemplo, via um orifício de entrada. O solvente é evaporado enquanto a mistura ainda está no extrusor. Após extrusão, o extrudado é formatado (calandragem).
Alternativamente, uma solução contendo os componentes da invenção pode ser alimentada ao extrusor, o solvente é evaporado enquanto o produto ainda está no extrusor e, finalmente, o extrudado é formatado.
Alternativamente, uma solução dos componentes da composição pode ser granulada sobre um veículo adequado, por exemplo, celulose microcristalina, e o pó umedecido é extrudado. O extrudado resultante é, então, esferonizado, por exemplo, usando-se um marumarizer, após o que, os péletes resultantes são secos a fim de remover o solvente. Os péletes podem ser enchidos díretamente em cápsulas ou eles podem ser ainda processados em comprimidos.
134
De preferência, as presentes composições são preparadas através de extrusão, conforme descrito sob ponto f) acima, aqueles habilitados na técnica são capazes de reconhecer as etapas e parâmetros de processo apropriadas para realizar extrusão da composição compreendendo um sol5 vente, em que o solvente é evaporado no extrusor. Referência, é feita, portanto, por exemplo, WO98/10752.
O solvente usado nos processos descritos acima é, de preferência, um material fisiologicamente tolerável, um solvente orgânico, adequadamente tal como um C-i-e alcanol (por exemplo, etanol), acetona, N,N10 dimetilformamida, um éter linear ou cíclico (por exemplo, dietil éter, dimetil éter, ou tetrahrdrofurano), ciclohexano, sulfóxido de dimetila, etc. ou uma mistura de solvente que também pode compreender água. Para um ácido o qual tem um elevado ponto de fusão, solventes ou misturas de solventes as quais têm elevados pontos de fusão podem, convencíonalmente, ser usados;
geralmente, contudo, o ponto de ebulição do solvente ou sistema de solvente será não mais do que cerca de 100°C. Tais solventes podem ser usados eficazmente na produção das composições da invenção e o nível de solvente residual será mínimo. O solvente pode, convenientemente, ser removido através de evaporação, por exemplo, sob pressão reduzida, e como isso pode deixar alguns resíduos de solvente (por exemplo, até 3% em peso), é particularmente desejável usar um solvente tal como etanol (ou uma mistura de etanoi-água) o qual é um excipiente farmaceuticamente permitido.
Conforme descrito acima, fluidos super críticos também podem ser usados. SCF adequados são, por exemplo, CO2, N2O, N2, aicanos de cadeia curta, tais como, por exempio, metano, etano e semelhantes.
Se o composto de droga é insolúvel ou pobremente solúvel no solvente de escolha, o processo da invenção pode envolver dispersão de micropartículas (por exemplo, nanopartículas tendo uma faixa de partícula de 1 a 100 nm) do composto de droga no solvente ao invés de dissolução total do composto de droga. Se isso é feito, é desejável que as partículas do composto de droga sejam tão pequenas quanto possível. Nanopartículas insolúveis de compostos podem ser preparadas, por exemplo, através de
135 várias técnicas de precipitação ou através de trituração com glóbulos inorgânicos fisiologicamente toleráveis, por exemplo, de zircônia (EP-0,499,299).
A remoção do solvente pode ser essencialmente completa ou pode ser incompleta, no primeiro caso produzindo um sólido ou um sólido ou semi-sólido semelhante a gel e, no último caso, produzindo um fluido viscoso o qual pode, por exemplo, ser enchido em cápsulas.
Em geral, remoção essencialmente completa do solvente será preferida uma vez que o produto resultante pode, então, ser prontamente formatado. Conforme já indicado acima, a formatação pode ser realizada através de secagem-pulverização da solução (proporcionar o produto em forma em partículas), através de evaporação do solvente da solução disposto em moldes, através de moldagem (por exemplo, moldagem por injeção), através de extrusão e semelhantes. Conforme já indicado, o produto pode ser formado quando quente e deixado solidificar quando de resfriamento. O produto formatado pode, da mesma forma, ser produzido na forma de filme ou folha através de evaporação ou entomando-se uma massa aquecida sobre uma chapa e evaporando-se o solvente.
Em uma concretização preferida, o produto é formatado através de enchimento em (por exemplo, entornando-se ou através de extrusão ou injeção) envoltórios de cápsulas, por exemplo, de gelatina.
Um processo alternativo para preparar as composições da invenção é preparar a dispersão do composto de droga, tensoativo e ácido (base) conforme descrito acima e, assim, misturar o produto fisicamente obtido com o polímero orgânico.
Ainda outro processo alternativo para preparação das presentes composições é preparar a dispersão do composto de droga, do ácido (base) e opcionalmente do polímero orgânico através de dissolução dos mesmos no solvente, seguido por remoção do solvente, e subsequentemente, assim, mistura do produto obtido com o tensoativo, opcionalmente em temperatura elevada.
Será reconhecido que para os processos descritos acima, aqueles habilitados na técnica são capazes de reconhecer os parâmetros mais
136 favoráveis e o equipamento mais apropriado. Também é bem conhecido por aqueles habilitados na técnica que o tamanho de partícula, distribuição de tamanho de partícula, cristal in idade e morfologia dos pós obtidos de acordo com os processos descritos acima podem ser adaptadas para requisitos es5 pecíficos através de ajuste apropriado dos parâmetros de processo, tais como, por exemplo, a temperatura, tamanho de bocal e formato, adição de gás no caso de processos de pulverização.
As composições da presente invenção podem ser formuladas em uma forma de dosagem adequada.
Assim, a presente invenção também proporciona formas de dosagem farmacêuticas compreendendo uma quantidade terapeuticamente eficaz da composição, conforme descrito aqui antes.
Por exemplo, se uma droga tem de ser distribuída em uma cápsula padrão (por exemplo, com uma capacidade 900 mg para um sistema termopiástico vítreo, conforme descrito na presente invenção, e a dose desejada de droga é de 100 mg/cápsula), então, as quantidades e componentes naturais da outra composição podem ser selecionados a fim de se obter o perfil de dissolução desejado de droga - em geral, apenas uma pequena quantidade de polímero orgânico, por exemplo, 20 a 50 mg, pode ser neces20 sário, e o equilíbrio pode ser feito a partir do ácido (base) e tensoativo com uma proporção de ácido para tensoativo sendo ajustada de acordo com o perfil requerido de dissolução, por exemplo, com 200 a 400 mg de tensoativo e 450 a 650 mg de ácido (base).
Além do composto de droga, do polímero orgânico, do ácido (ba25 se) e do tensoativo, as composições da invenção podem conter outros excipientes farmaceuticamente convencionais, por exemplo, flavorizantes, agentes de coloração, antioxidantes, agentes de composição de volume, glidantes, lubrificantes, gorduras, ceras, agentes de revestimento, dispersantes, fluidos de suspensão (por exemplo, onde a composição revestida com um revestimento resistente ao suco gástrico e dispersa como partículas em um fluido de suspensão, tais como água ou um xarope), etc. De preferência, tais componentes, quando em mistura íntima com o composto de droga, forma... · >«£. ΓΓΟϊ·*
137
rão apenas uma proporção menor da composição, por exemplo, 0,01 a 10% em peso (com relação ao peso total de ácido (base), tensoativo, composto de droga e opcionalmente o polímero orgânico). Contudo, onde a composição da invenção é encapsulada ou disposta em um veículo (por exemplo, uma matriz fluida ou um sólido ou semi-sólido), os outros componentes que não estão em mistura íntima com o composto de droga (por exemplo, revestimento ou materiais de encapsulação, meios de dispersão, etc.) podem, naturalmente, formar uma proporção menor ou maior, por exemplo, 5 a 95% em peso, da composição global.
O produto pode ser higroscópico e, assim, pode ser viscoso se tocada pela mão, devido à sua absorção de umidade da pele. Consequentemente, é particularmente preferido que o produto seja proporcionado com um revestimento protetor para impedir captação de umidade durante manipulação. Tais revestimentos podem, por exemplo, tomar a forma de envoító15 rios para cápsulas (conforme descrito acima), revestimentos para comprimido, revestimentos em filme ou trama protetora e envoltórios removíveis à prova de umidade. Revestimentos para comprimido podem ser aplicados de modo convencional e podem ser tal de modo a ser dissolvido na boca ou estômago (por exemplo, revestimentos de açúcar ou açúcar/cera de abe20 lhas) ou, alternativamente, pode, ser polímeros resistentes ao suco gástrico (tais como os revestimentos resistentes ao suco gástrico Eudragit® produzidos pela Rohm GmbH), onde se deseja que a captação de droga ocorra nos intestinos. Filmes ou tramas protetoras podem, por exemplo, ser usados, onde o produto tem de ser aplicado topicamente, por exemplo, ou captação através da pele ou um dedo dos pés ou indicador. Nesse evento, um acolchoado da composição estará, geralmente, disposta entre uma camada protetora adesiva superior e uma camada removível inferior. Um exemplo de uma forma de aplicação tópica para aplicação ao nariz e tecido conjuntivo, por exemplo, para o tratamento de infecção fúngica, é mostrado na US-A30 5181914.
As presentes composições podem também compreender lubrificantes adequados tais como, por exemplo, estearil fumarato de sódio, para
ΓΛ·..
138
evitar aderência.
Onde o produto é produzido na forma em partículas, por exemplo, através de secagem-pulverização, as partículas podem ser carregadas em dispositivos de administração herméticos à água (por exemplo, dispositi5 vos de pulverização ou dispositivos de dosagem de pó, tais como inaladores) para administração oral, nasal ou tópica das partículas. Altemativamente, partículas podem ser carregadas em cápsulas ou misturadas com agentes de composição de volume, tais como lactose, amido, celulose microcristalina e misturas dos mesmos, e prensadas a fim de formar comprimidos.
Em outro evento, as partículas podem, adicionalmente, ser proporcionadas com um ou mais revestimentos, por exemplo, para proporcionar uma forma de administração com liberação retardada ou prolongada.
Geralmente, contudo, será preferido formatar o produto em doses individuais e fornecer os mesmos com um revestimento protetor, por exemplo, produzir uma cápsula, comprimido revestido ou uma unidade de dosagem única coberta com um filme.
As composições de acordo com a invenção podem ser em qualquer forma conveniente para administração tópica ou administração a uma cavidade corporal externamente oca (por exemplo, nariz, pulmões, boca, orelha, estômago, reto ou vagina). Formas de administração típicas incluem emplastros, comprimidos, comprimidos bucais, comprimidos, tampões para orelha, tampões para o nariz, comprimidos revestidos, cápsulas, supositórios, goma de mascar, géis, pós, grânulos, xaropes e dispersões, embora emplastos e pós e mais especialmente cápsulas e comprimidos revestidos sejam preferidas. A dosagem da droga dependerá do composto de droga bem como da condição que está sendo tratada e da espécie e tamanho do indivíduo que está sendo tratado.
Ainda, a presente invenção compreende uma composição farmacêutica ou uma forma de dosagem farmacêutica, conforme descrito aqui antes, para uso em um método de profilaxia, terapia ou diagnóstico do corpo de um ser humano ou um animal não-humano.
A presente invenção também se refere a uma composição far-
139 macêutica para uso na fabricação de uma forma de dosagem farmacêutica para administração orai a um mamífero que precisa de tratamento, caracterizada pelo fato de que a referida forma de dosagem pode ser administrada a qualquer momento do dia, independentemente do alimento ingerido pelo re5 ferido mamífero.
Ou, em outras palavras, a presente invenção também se refere o uso de uma composição farmacêutica, conforme descrito aqui antes, para a fabricação de uma forma de dosagem farmacêutica para administração oral a um mamífero que precisa de tratamento, caracterizado pelo fato de que a referida forma de dosagem pode ser administrada a qualquer momento do dia, independentemente do alimento ingerido pelo referido mamífero.
A presente invenção também se refere a um método de profilaxia, terapia ou diagnóstico do corpo de um ser humano ou um animal nãohumano o qual compreende administração, ao referido corpo, de uma dose terapeuticamente ou díagnosticamente eficaz de uma composição farmacêutica de acordo com a presente invenção.
A presente invenção também se refere a uma embalagem farmacêutica adequada para venda comercial compreendendo um recipiente, uma forma de dosagem oral conforme reivindicado em qualquer uma das reivindicações 16 a 18 e, associada à referida embalagem, uma bula por escrito não limitativa sobre como a forma de dosagem pode ser administrada com ou sem alimento.
A invenção agora será ainda descrita com referência aos seguintes Exemplos não-limitativos.
Exemplo 1
As seguintes composições de acordo com a presente invenção foram preparadas:
Composição 1
Cisaprida 114 mg
Ácido tartárico 35,6 mg
Lutrol® F68 457 mg
140
Composição 2
Cisaprida 114 mg
Ácido tartárico 10 g
Lutrol® F68 457 mg
Preparação de composição 1
114 mg de cisaprida e 457 Lutrol™ F68 foram dissolvidos em
1,14 g de acetona. 35,6 mg de ácido tartárico foram dissolvidos em 1,90 ml de EtOH e essa solução foi adicionada à solução de acetona. A mistura resultante foi evaporada sob vácuo (rotavapor) em uma temperatura de 85°C.
O resíduo foi triturado e ainda seco sob vácuo a 80°C, seguido portrituração.
Preparação de composição 2
A Composição 2 foi preparada analogamente à composição 1, exceto que 10 g de ácido tartárico foram dissolvidos em 53,3 ml de EtOH.
O perfil de dissolução das composições 1 e 2 in vitro foi determinado colocando-se essa quantidade de composição 1 ou 2 contendo 5,7 mg de cisaprida em 10 ml de USP mantida em um pH de 6,8 (USP mantida em um pH de 6,8 foi preparada colocando-se 6,805 g de KH2PO4, 109,5 ml de uma solução de NaOH a 0,2 N e 700 ml de água destilada em um béquer de
1 litro. Após dissolução completa enquanto se agita, a mistura resultante foi mantida em um volume de 1 litro com água destilada em um recipiente apropriado) a 37°C e medindo-se o percentual de cisaprida dissolvida como uma função de tempo (a agitação foi efetivada através de um agitador magnético e a concentração de cisaprida dissolvida foi medida através de absorção de
UV).
Os resultados são apresentados na Tabela 7.
Tabela 7
Percentual de cisaprida em solução Tempo Composição 1 Composição 2
0 0
1,68 98,15
1,51 98,33
141
Continuação
Percentual de cisaprida em solução Tempo Composição 1 Composição 2
1,47 98,15
120 1,45 98,24
A Composição 2 mostra, claramente, uma dissolução muito mais rápida in vitro, comparado a composição 1. Assim, a incorporação de uma quantidade significativa de ácido na composição resulta em uma solubilidade intensificada e, consequentemente, o composto de droga se torna muito mais prontamente biodisponívei.
Exemplo 2
Cápsulas de gelatina foram preparadas contendo a seguinte composição:
Composição 3
R103757* 100 mg
Monohidrato de ácido cítrico 500 mg Cremophor RH 40 250 mg
Methocel™ E 5 50 mg * R103757 corresponde a (-)-[2S-[2a,4a(S*)]]-4-[4-[4-[4-[[2-(4-clorofenil]-2[[(4-metil-4/7-1,2,4-triazol-3-il)tio]metii]-1,3-dioxolan-4-il]metóxi]fenil]-1 piperazinil]fenil]-2,4-dihidro-2-(1-metilpropil)-3H-1,2,4-triazol-3-ona
A composição acima foi preparada através de dissolução de 500 mg de R103757, 2,5 g de monohidrato de ácido cítrico, 250 mg de Methocel® E5 e 1,250 mg de Cremophor RH 40 em 2,5 ml de EtOH. Após dissolução completa, a solução foi entornada sobre uma chapa de teflon a qual foi, então, colocada em um forno de secagem durante 2 horas a 80°C sob vácuo. O resíduo resultante foi raspado e a quantidade correspondente a 100 mg de R103757 foi enchida em cápsulas de gelatina (tamanho No 0).
O perfil de dissolução da composição 3 in vitro foi determinado colocando-se uma cápsula contendo composição 3 em 600 mL de HCI a 0,1
N agitado a 37°C e observando-se (absorção UV) o percentual de composto de droga dissolvido nos tempos 0, 5, 15, 30, 45 e 60 minutos (agitação foi
142 efetivada usando o método USP com pá, aparelho 2, 100 rpm). Os resultados são apresentados na Tabela 8.
Tabela 8
Composição 3
Percentual de R103757 em solução
| impo | Amostra 1 | Amostra 2 |
| 0 | 0 | 0 |
| 5 | 14,94 | 14,34 |
| 15 | 62,70 | 59,10 |
| 30 | 94,32 | 93,12 |
| 45 | 101,64 | 102,06 |
| 60 | 102,84 | 103,14 |
Exemplo 3
Cápsulas de gelatina foram preparadas contendo a seguinte composição:
Compos/cão 4
R112625* 100 mg
Monohidrato de ácido cítrico 325 mg
Laureth 23 325 mg
Methocel™ E 5 25 mg * R112625 corresponde a (+)-(trans)-4-[1-[3,5-bis(trifluorometil)benzoil]-2(fenilmetil)-4-piperidinil]-N-(2,6-dimetiifenil)-1-piperazina acetamida
A composição acima foi preparada através de dissolução de 1 g de R112625, 3,25 g de monohidrato de ácido cítrico e 250 mg de Methocel® E5 em 6 ml de EtOH a 70°C. Adicionar 3,25 g de Lauret 23 à referida solução enquanto ainda se agita. Após dissolução completa, a solução foi entornada sobre uma chapa de teflon a qual foi, então, colocada em um forno de secagem durante 2 horas a 80°C sob vácuo. O resíduo resultante foi raspado e a quantidade correspondente a 100 mg de R112625 foi enchida em cápsulas de gelatina (tamanho No 0).
O perfil de dissolução da composição 4 in vitro foi determinado de acordo com o procedimento descrito para a Composição 3.
143
Os resultados são apresentados na Tabela 9. ‘'AvaS
Tabela 9
Composição 4
Percentual de R112625 em solução
| 5 | Tempo | Amostra 1 |
| 0 | 0 | |
| 5 | 10,98 | |
| 15 | 51,87 | |
| 30 | 80,82 | |
| 10 | 45 | 97,08 |
| 60 | 101,91 |
Exemplo 4
Teste de Estabilidade
Cápsulas de gelatina foram preparadas contendo a seguinte 15 composição:
Composição 5
R112625 100 mg
Monohidrato de ácido cítrico 325 mg
Cremophor RH40 325 mg
Methocei® E 5 25 mg
A composição foi preparada analogamente de acordo com o procedimento descrito no Exemplo 3.
Cápsulas contendo composição 5 foram armazenadas durante 1 mês em temperatura ambiente. Medições da dissolução foram feitas de a25 cordo com o método descrito acima para a Composição 3.
Os resultados são apresentados na Tabela 10.
144
Tabela 10
Composição 5
Percentual de R112625 na solução
| Tempo | Testagem ao tempo 0 | Testagem após 1 mês |
| em temperatura | ambiente | |
| 0 | 0 | 0 |
| 5 | 9,26 | 9,75 |
| 15 | 43,74 | 44,16 |
| 30 | 78,13 | 80,22 |
| 45 | 92,64 | 99,09 |
| 60 | 101,64 | 102,39 |
Os resultados acima sustentam a estabilidade das composições da invenção.
Exemplo 5
Formulações com liberação imediatas-liberacão ampliada
As seguintes composições de acordo com a presente invenção foram preparadas:
Composição 6
R165335* 50 mg
Monohidrato de ácido cítrico 500 mg
Cremophor RH 40 250 mg
Composição 7
R165335* 50 mg
Monohidrato de ácido cítrico 500 mg
Cremophor RH 40 250 mg
Poliox® WSR 303 30 mg
Composição 8
R165335* 50 mg
Monohidrato de ácido cítrico 500 mg
Cremophor RH 40 250 mg
Poliox™ WSR 303 50 mg *R165335 corresponde a 4-[[6-amino-5-bromo-2~[(4-cianofenil)amino]-4-
145 pirimidinil]óxi]-3,5-dimetilbenzonitrila,
A Composição 6 foi preparada através de dissolução de 5000 mg de R165335 em 150 ml de acetona a 60°C, seguido pela adição de 50 g de monohidrato de ácido cítrico enquanto se agitava, até dissolução completa.
Conseqüentemente, 25 g de Cremophor RH 40 foram adicionados â solução. Após dissolução completa, a solução foi entornada sobre chapas de teflon, os quais foram, então, colocados em um forno de secagem durante 2 horas a 80°C sob vácuo. O resíduo resultante foi raspado. As Composições 7 e 8 foram preparadas começando a partir de composição 6, através de mistura da quantidade apropriada de Poliox® WSR 303 com a quantidade correspondente de composição 6.
O perfil de dissolução das composições 6, 7 e 8 in vitro foi determinado através colocando-se essa quantidade das composições 6, 7 ou 8 que contêm 50 mg de R165335 em uma cesta em 900 mL de HCl a 0,01 N agitado contendo 2,5% de lauril sulfato de sódio a 37°C e observando-se (absorção UV) o percentual de composto de droga dissolvido nos tempos 0, 5, 15, 30, 45, 60 até 360 minutos (a agitação foi efetivada usando o método USP com cesta, aparelho 1,100 rpm).
Os resultados são apresentados na Tabela 11.
Tabela 11
Composição 5
Percentual de R165335 na solução
| Tempo 0 | Composição 6 0 | Composição 7 0 | Composição 8 0 | |
| 25 | 5 | 22,86 | 8,42 | 4,12 |
| 15 | 65,88 | 20,03 | 7,45 | |
| 30 | 95,82 | 35,96 | 12,17 | |
| 45 | 100,18 | 47,89 | 16,67 | |
| 60 | 100,70 | 58,24 | 24,07 | |
| 30 | 75 | 69,65 | 29,52 | |
| 90 | 78,24 | 35,25 | ||
| 105 | 84,73 | 40,61 |
146
Continuação
Composição 5
Percentual de R165335 na solução
| Tempo | Composição 6 | Composição 7 | Composição 8 |
| 120 | 90,35 | 47,00 | |
| 150 | 101,01 | 56,28 | |
| 180 | 101,90 | 65,30 | |
| 240 | 79,29 | ||
| 300 | 93,45 | ||
| 360 | 100,70 |
Dos resultados listados na Tabela 11, pode ser concluído que a taxa de dissolução das composições da invenção pode ser ampliada através de adição de um polímero orgânico às composições.
A Composição 6 foi também submetida a um teste de estabilida15 de. A composição foi armazenada durante 8 meses em temperatura ambiente e, então, o percentual de R165335 na composição foi determinado através de Cromatografia de Líquido de alto desempenho. Após o período de armazenamento de 8 meses, a composição continha 98,5% de R165335, sustentando a estabilidade do composto de droga na composição.
Exemplo 6
Estudo in vivo
As seguintes composições foram preparadas
| Composição 9 | ||
| R165335 | 125 mg | |
| 25 | Monohidrato de ácido cítrico | 492 mg |
| Cremophor RH 40 | 242 mg | |
| Methocel® E5 | 42 mg | |
| Composição 10 | ||
| R278474* | 50 mg | |
| 30 | Monohidrato de ácido cítrico | 500 mg |
| VitE TPGS | 250 mg | |
| Methocel® E5 | 25 mg |
147
R278474* corresponde a 4-[[4-[[4-(2-cianoetenil)-2,6-dimetilfenil]amino]-2- ? pirimidinil]amino]benzonitrila.
A Composição 9 foi preparada através de dissolução de 500 mg de R165335 em 5 ml de tetrahidrofurano na temperatura de ebulição (solu5 ção A). 1966,6 mg de monohidrato de ácido cítrico, 966 mg de Cremophor RH 40 e 166,66 mg de Methocel® E5 foram dissolvidos em 4 ml de EtOH a 80°C (solução B). A Solução A foi adicionada à solução B enquanto se agitava. Assim, a solução obtida foi entornada sobre uma chapa de teflon a qual foi, então, colocada em um forno de secagem durante 2 horas a 80°C sob vácuo. O resíduo resultante foi raspado e enchido em cápsulas de gelatina (tamanho n° 0) para uso no estudo in vivo.
A Composição 10 foi preparada através de dissolução de 300 mg de R278474, 3 g de monohidrato de ácido cítrico e 150 mg de Methocel® E5 em 5 ml de EtOH a 70°C. A solução foi evaporada a 85°C sob vácuo durante
1 hora. 3 g do resíduo assim obtido foram misturado com 1,304 g de VitE
TPGS a 80°C.
R165335 foi oralmente administrado a cães Beagle machos como uma cápsula contendo composição 9 e como uma solução em PEG-400 (10 mg de R165335/ml de PEG 400) a uma dose de 10 mg/kg. Cada formu20 lação foi testada em 2 cães. Os níveis de R165335 no plasma foram medidos (HPLC) durante 32 horas após administração oral. Os resultados são apresentados na Tabela 12.
R278474 foi oralmente administrado cães Beagle machos como uma cápsula contendo composição 10 e como uma solução em PEG-400 (40 mg de R278474/ml de PEG 400) a uma dose de 5 mg/kg. Cada formulação foi testada em 2 cães. Níveis de R278474 no plasma foram medidos (LC-MS) durante 72 horas após administração oral. Os resultados são apresentados na Tabela 13. A Tabela 14 reporta os valores médios para Cmax, Tmax θ AUC0-72h para o estudo com solução de PEG-400 e o estudo da com30 posição 10.
148
Tabela 12
| Níveis de R165335 no Plasma (ng/ml) | ||||
| Formulação | Dia | Tempo | Cão 1 | Cão 2 |
| Solução de PEG-400 | 0 | 0 h | NQ | NQ |
| 0,5 h | 160 | 93,9 | ||
| 1 h | 251 | 183 | ||
| 2h | 420 | 301 | ||
| 4h | 498 | 351 | ||
| 8 h | 283 | 384 | ||
| 1 | 24 h | 105 | 167 | |
| 32 h | 92,2 | 120 | ||
| Cápsula com composi- | 0 | Oh | NQ | NQ |
| ção 9 | 0,5 h | 53,3 | NQ | |
| 1 h | 898 | 97,2 | ||
| 2 h | 2930 | 1011 | ||
| 4 h | 1868 | 548 | ||
| 8 h | 873 | 243 | ||
| 1 | 24 h | 301 | 113 | |
| 32 h | 227 | 82,5 |
NQ = Não quantificáveis
149
Tabela 13
| Níveis de R278474 no Plasma (ng/ml) | ||||
| Formulação | Dia | Tempo | Cão 1 | Cão 2 |
| Solução de PEG-400 | 0 | Oh | 0 | 0 |
| 0,5 h | 1,8 | 203 | ||
| 1 h | 8,4 | 404 | ||
| 2 h | 35,8 | 520 | ||
| 4h | 115 | 460 | ||
| 6 h | 162 | 367 | ||
| 8 h | 148 | 365 | ||
| 1 | 24 h | 74,0 | 187 | |
| 32 h | 38,4 | 147 | ||
| 2 | 48 h | 31,9 | 94.6 | |
| 3 | 72 h | 19,3 | 70.1 | |
| Cápsulas com compo- | 0 | Oh | 0 | 0 |
| sição 10 | 0,5 h | NQ | 80.2 | |
| 1 h | 13 | 694 | ||
| 2h | 260 | 1178 | ||
| 4h | 899 | 1040 | ||
| 6h | 1056 | 1052 | ||
| 8h | 1111 | 850 | ||
| 1 | 24 h | 427 | 497 | |
| 32 h | 316 | 490 | ||
| 2 | 48 h | 236 | 232 | |
| 3 | 72 h | 181 | 226 |
NQ = Não quantificável
150
Tabela 14
---
| Valores médios | Solução de PEG-400 | Composição 10 |
| Cmax (ng/ml) | 341 | 1144,50 |
| Tmax (h) | 4 | 5 |
| AUCq-72 h (ng.h/ml) | 8359 | 31008 |
Os resultados acima demonstram claramente o desempenho superior da composição 10 comparado a solução de PEG 400. A Composição 10 tem, claramente, um perfil farmacocinético aperfeiçoado, comparado à solução de PEG 400.
Exemplo 7
Efeito do tensoativo sobre solubilidade e sobre a estabilidade da condição supersaturada.
Soluções aquosas a 2,5% (peso/v) de hidroxipropil-β10 ciclodextrina (HPpCD) [1], 2,5% (peso/v) de Vit E TPGS [2], 2,5% (peso/v) de Cremophor RH 40 [3], 2,5% (peso/v) de lauril sulfato de sódio [4] ou 2,5% (peso/v) de PEG 4000 [5] em HCI a 0,01 N a 37°C foram preparadas.
A 10 ml dessas soluções, com agitação, uma solução concentrada de R278474 ou R165335 em A/./V-dimetilformamida (100 mg/ml) foi adi15 cionada gota a gota até que precipitação do composto de droga fosse observada. Após 5, 30, 60 e 120 minutos, a concentração do R278474 ou R165335 dissolvido expressa em mg% (isto é, o número de mg dissolvido em 100 ml) foi determinada. Os resultados são apresentados na Tabela 15.
Tabela 15
| Tempo (minutos) | 0,01 N HCI | [1] | [2] | [3] | [4] | [5] | |
| Concentração | mg% | mg% | mg% | mg% | mg% | mg% | |
| R278474 | 5 | 18,02 | 27,68 | 91,75 | 23,60 | ||
| 30 | 16,30 | 24,80 | 83,50 | 21,60 | |||
| 60 | 15,90 | 24,40 | 76,25 | 20,60 | |||
| 120 | 15,95 | 24,10 | 75,25 | 20,10 | |||
| R165335 | 5 | NM* | 0,04 | 54,20 | 35,09 | 0,02 | |
| 30 | NM | 0,12 | 24,88 | 37,85 | 0,04 | ||
| 60 | NM | 0,17 | 20,06 | 38,80 | 0,07 | ||
| 120 | NM | 0,07 | 18,44 | 38,35 | 0,04 |
151
* NM significa não mensurável
Os resultados apresentados na Tabela 15 demonstram claramente o maior efeito de solubilização (criando uma condição de supersaturação) do tensoativo comparado àquele de uma ciclodextrina, tal como
HPpCD ou um co-solvente, tal como PEG 4000. Os resultados também indicam que os tensoativos são capazes de manter a condição supersaturada por algum tempo.
Claims (14)
- REIVINDICAÇÕES1. Composição farmacêutica sólida ou semi-sólida, caracterizada pelo fato de que compreende um composto de droga básico, Vitamina E TPGS e um ácido solúvel em água fisiologicamente tolerável selecionado5 dentre ácido cítrico ou ácido tartárico, em que a proporção de ácido:composto de droga varia de 1:1 a 100:1 em peso, e em que o composto de droga básico é selecionado dentre 4-[[4-[[4-(2-cianoetenil)-2,6dimetilfenil]amino]-2-pirimidinil]amino]benzonitrila; 4-[[2-[(cianofenil)amino]-4pirimidinil]amino]-3,5-dimetilbenzonitrila; 4-[[4-[(2,4,6-trimetilfenil)amino]-210 pirimidinil]amino]benzonitrila; 4-[[4-amino-5-bromo-6-(4-ciano-2,6dimetilfenilóxi)-2-pirimidinil]amino]benzonitrila; ou um sal farmaceuticamente aceitável ou uma forma estereoquimicamente isomérica do mesmo.
- 2. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que o estado físico da referida composição é uma dispersão15 sólida.
- 3. Composição de acordo com a reivindicação 1 ou 2, caracterizada pelo fato de que o ácido é ácido cítrico.
- 4. Composição de acordo com qualquer uma das reivindicações 1 a 3, caracterizada pelo fato de que ainda compreende um polímero20 orgânico.
- 5. Composição de acordo com a reivindicação 4, caracterizada pelo fato de que o polímero é selecionado de:- alquilceluloses, tal como metilcelulose,- hidroxialquilceluloses, tais como hidroximetilcelulose,25 hidroxietilcelulose, hidroxipropilcelulose e hidroxibutilcelulose,- hidroxialquil alquilceluloses, tais como hidroxietil metilcelulose e hidroxipropil metilcelulose,- carboxialquilceluloses, tal como carboximetilcelulose,- sais de metal alcalino de carboxialquilceluloses, tal como30 carboximetilcelulose de sódio,- carboxialquilalquilceluloses, tal como carboximetiletilcelulose,- ésteres de carboxialquilcelulose,Petição 870180043693, de 24/05/2018, pág. 11/17- amidos,- pectinas, tal como sódio carbóximetilamilopectina,- derivados de quitina, tal como quitosana,- heparina e heparinóides,5 - polissacarídeos, tais como ácido algínico, sais de metal alcalino e de amônio dos mesmos, carrageninas, galactomananas, tragacanto, ágarágar, goma arábica, goma de guar e goma de xantano,- ácidos poliacrílicos e os sais dos mesmos,- ácidos polimetacrílicos e os sais dos mesmos,10 - copolímeros de metacrilato,- álcool polivinílico,- polivinilpirrolidona, copolímeros de polivinilpirrolidona com acetato de vinila,- óxidos de polialquileno, tais como óxido de polietileno e óxido 15 de polipropileno, e- copolímeros de óxido de etileno e óxido de propileno, por exemplo, poloxâmeros e poloxaminas.
- 6. Composição de acordo com a reivindicação 4 ou 5, caracterizada pelo fato de que o polímero tem uma viscosidade aparente de20 1 - 100 mPa.s quando dissolvido em uma solução aquosa a 2% a 20°C.
- 7. Composição de acordo com qualquer uma das reivindicações 4 a 6, caracterizada pelo fato de que o polímero é hidróxipropilmetilcelulose.
- 8. Composição de acordo com a reivindicação 4 ou 5, caracterizada pelo fato de que proporciona liberação sustentada da droga25 em que compreende um polímero solúvel em água tendo uma viscosidade aparente de mais de 1.000 mPa.s quando dissolvido em uma solução aquosa a 2% a 20°C.
- 9. Composição de acordo com a reivindicação 1 ou 2, caracterizada pelo fato de que a Vitamina E TPGS está presente em uma30 concentração de 1 a 70% em peso relativo ao peso total de Vitamina E TPGS, ácido e droga.
- 10. Composição de acordo com a reivindicação 9, caracterizadaPetição 870180043693, de 24/05/2018, pág. 12/17 pelo fato de que a Vitamina E TPGS está presente em uma concentração de 5 a 55% em peso relativo ao peso total de Vitamina E TPGS, ácido e droga.
- 11. Composição de acordo com a reivindicação 10, caracterizada pelo fato de que a Vitamina E TPGS está presente em uma concentração de 10 a 50% em peso relativo do peso total de Vitamina E TPGS, ácido e droga.
- 12. Composição de acordo com a reivindicação 1 ou 2, caracterizada pelo fato de que a proporção em peso de Vitamina E TPGS para a droga está na faixa de 100:1 a 1:5.
- 13. Composição de acordo com a reivindicação 12, caracterizada pelo fato de que a proporção em peso de Vitamina E TPGS para a droga está na faixa de 50:1 a 1:2.
- 14. Composição de acordo com a reivindicação 13, caracterizada pelo fato de que a proporção em peso de Vitamina E TPGS para a droga está na faixa de 10:1 a 1:1.Petição 870180043693, de 24/05/2018, pág. 13/17
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/EP2002/013558 WO2004050068A1 (en) | 2002-11-29 | 2002-11-29 | Pharmaceutical compositions comprising a basic respectively acidic drug compound, a surfactant and a physiologically tolerable water-soluble acid respectively base |
| EPPCT/EP02/13558 | 2002-11-29 | ||
| PCT/EP2003/050890 WO2004050058A2 (en) | 2002-11-29 | 2003-11-25 | Pharmaceutical compositions comprising a basic respectively acidic drug compound, a surfactant and a physiologically tolerable water-soluble acid respectively base |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BR0316532A BR0316532A (pt) | 2005-10-04 |
| BRPI0316532B1 true BRPI0316532B1 (pt) | 2018-07-31 |
| BRPI0316532B8 BRPI0316532B8 (pt) | 2021-05-25 |
Family
ID=32405665
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0316532A BRPI0316532B8 (pt) | 2002-11-29 | 2003-11-25 | composições farmacêuticas compreendendo uma droga básica ou ácida, um tensoativo, e um ácido ou base solúvel em água fisiologicamente tolerável |
Country Status (24)
| Country | Link |
|---|---|
| US (1) | US9192577B2 (pt) |
| EP (1) | EP1567134B1 (pt) |
| JP (1) | JP4951205B2 (pt) |
| KR (1) | KR101107328B1 (pt) |
| CN (2) | CN1720027A (pt) |
| AP (1) | AP2100A (pt) |
| AR (1) | AR042246A1 (pt) |
| AU (2) | AU2002350719A1 (pt) |
| BR (1) | BRPI0316532B8 (pt) |
| CA (1) | CA2505742C (pt) |
| EA (1) | EA010971B1 (pt) |
| ES (1) | ES2763155T3 (pt) |
| HR (1) | HRP20050458B1 (pt) |
| IS (1) | IS7796A (pt) |
| MX (1) | MXPA05005709A (pt) |
| MY (1) | MY148680A (pt) |
| NO (1) | NO20053143D0 (pt) |
| NZ (1) | NZ540846A (pt) |
| PL (1) | PL377057A1 (pt) |
| RS (1) | RS53148B (pt) |
| TW (1) | TWI340034B (pt) |
| UA (1) | UA92448C2 (pt) |
| WO (2) | WO2004050068A1 (pt) |
| ZA (1) | ZA200504312B (pt) |
Families Citing this family (67)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL130602A0 (en) | 1999-06-22 | 2000-06-01 | Dexcel Ltd | Stable benzimidazole formulation |
| US7364752B1 (en) | 1999-11-12 | 2008-04-29 | Abbott Laboratories | Solid dispersion pharamaceutical formulations |
| CA2359945C (en) | 1999-11-12 | 2011-04-26 | Abbott Laboratories | Inhibitors of crystallization in a solid dispersion |
| MY169670A (en) | 2003-09-03 | 2019-05-08 | Tibotec Pharm Ltd | Combinations of a pyrimidine containing nnrti with rt inhibitors |
| US7638522B2 (en) | 2001-08-13 | 2009-12-29 | Janssen Pharmaceutica N.V. | Salt of 4-[[4-[[4-(2-cyanoethenyl)-2,6-dimethylphenyl]amino]-2-pyrimidinyl]amino] benzonitrile |
| US8101629B2 (en) | 2001-08-13 | 2012-01-24 | Janssen Pharmaceutica N.V. | Salt of 4-[[4-[[4-(2-cyanoethenyl)-2,6-dimethylphenyl]amino]-2-pyrimidinyl]amino]benzonitrile |
| JO3429B1 (ar) | 2001-08-13 | 2019-10-20 | Janssen Pharmaceutica Nv | مشتقات برميدينات مثبطة فيروس الايدز |
| TWI329105B (en) | 2002-02-01 | 2010-08-21 | Rigel Pharmaceuticals Inc | 2,4-pyrimidinediamine compounds and their uses |
| ES2445208T3 (es) | 2002-07-29 | 2014-02-28 | Rigel Pharmaceuticals, Inc. | Compuestos de 2,4-pirimidindiamina para uso en métodos para tratar o prevenir enfermedades autoinmunitarias |
| KR101140785B1 (ko) | 2002-08-09 | 2012-05-03 | 얀센 파마슈티카 엔.브이. | 4-〔〔4-〔〔4-(2-시아노에테닐)-2,6-디메틸페닐〕아미노〕-2-피리미디닐〕아미노〕벤조니트릴의 제조방법 |
| BRPI0407329A (pt) * | 2003-02-07 | 2006-01-10 | Janssen Pharmaceutica Nv | Derivados de pirimidina para a prevenção de infecção de hiv |
| ES2325440T3 (es) | 2003-02-20 | 2009-09-04 | Smithkline Beecham Corporation | Compuestos de pirimidina. |
| BRPI0413018B8 (pt) | 2003-07-30 | 2021-05-25 | Rigel Pharmaceuticals Inc | composto, e, uso de um composto |
| US8377952B2 (en) | 2003-08-28 | 2013-02-19 | Abbott Laboratories | Solid pharmaceutical dosage formulation |
| US8025899B2 (en) | 2003-08-28 | 2011-09-27 | Abbott Laboratories | Solid pharmaceutical dosage form |
| ATE550074T1 (de) * | 2004-09-02 | 2012-04-15 | Janssen Pharmaceutica Nv | Fumarat aus 4-((4-((4-(2-cyanoethenyl)-2,6- dimethylphenyl amino -2-pyrimidinyl amino benzonitril |
| ATE508748T1 (de) * | 2004-09-02 | 2011-05-15 | Janssen Pharmaceutica Nv | Salz von 4-ää4-ää4-(2-cyanoethenyl)-2,6- dimethylphenylüaminoü-2- pyrimidinylüaminoübenzonitril. |
| EP1814878B1 (en) | 2004-11-24 | 2012-01-04 | Rigel Pharmaceuticals, Inc. | Spiro-2, 4-pyrimidinediamine compounds and their uses |
| US20090208579A1 (en) * | 2004-12-27 | 2009-08-20 | Eisai R & D Management Co., Ltd. | Matrix Type Sustained-Release Preparation Containing Basic Drug or Salt Thereof, and Method for Manufacturing the Same |
| DE602006010979D1 (de) | 2005-01-19 | 2010-01-21 | Rigel Pharmaceuticals Inc | Prodrugs aus 2,4-pyrimidindiamin-verbindungen und ihre verwendungen |
| SG160357A1 (en) * | 2005-03-03 | 2010-04-29 | Revance Therapeutics Inc | Compositions and methods for topical application and transdermal delivery of botulinum toxins |
| US8178135B2 (en) | 2006-03-07 | 2012-05-15 | Keio University | Aqueous solution of conophylline and/or conophyllidine |
| NZ572702A (en) * | 2006-06-06 | 2011-09-30 | Tibotec Pharm Ltd | Process for preparing spray dried formulations of etravirine in microcrystalline cellulose |
| WO2008027557A2 (en) * | 2006-08-31 | 2008-03-06 | Spherics, Inc. | Topiramate compositions and methods of enhancing its bioavailability |
| ES2555066T3 (es) | 2006-11-17 | 2015-12-28 | Supernus Pharmaceuticals, Inc. | Formulaciones de liberación sostenida de topiramato |
| ES2645719T3 (es) * | 2006-12-04 | 2017-12-07 | Supernus Pharmaceuticals, Inc. | Formulaciones de topiramato de liberación inmediata mejoradas |
| UA97813C2 (uk) * | 2006-12-05 | 2012-03-26 | Янссен Фармацевтика Н.В. | Фумаратна сіль (альфа s, бета r)-6-бром-альфа-[2-(диметиламіно)етил]-2-метоксі-альфа-1-нафталеніл-бета-феніл-3-хінолінетанолу |
| CL2008000746A1 (es) * | 2007-03-14 | 2008-09-22 | Tibotec Pharm Ltd | Composicion farmaceutica en solucion que comprende tmc278 y un polimero soluble en agua; proceso de preparacion de dicha composicion; y uso de un polvo que comprende tmc278 para tratar sida. |
| CN101687044B (zh) * | 2007-05-25 | 2014-10-29 | 不列颠哥伦比亚大学 | 用于口服给药的治疗剂的制剂和相关方法 |
| US20090005395A1 (en) * | 2007-06-26 | 2009-01-01 | Solvay Pharmaceuticals, B.V. | Sildenafil n-oxide as prodrug |
| GB0716591D0 (en) * | 2007-08-24 | 2007-10-03 | Vereniging Het Nl Kanker I | Composition |
| JP5222550B2 (ja) * | 2007-12-27 | 2013-06-26 | 財團法人工業技術研究院 | 徐放性組成物およびその製造方法 |
| ES2552723T3 (es) | 2008-05-06 | 2015-12-01 | Dexcel Pharma Technologies Ltd. | Formulación de bencimidazol estable |
| TWI546290B (zh) | 2008-06-27 | 2016-08-21 | 賽基艾維洛米斯研究股份有限公司 | 雜芳基化合物及其用途 |
| US8338439B2 (en) | 2008-06-27 | 2012-12-25 | Celgene Avilomics Research, Inc. | 2,4-disubstituted pyrimidines useful as kinase inhibitors |
| US11351168B1 (en) | 2008-06-27 | 2022-06-07 | Celgene Car Llc | 2,4-disubstituted pyrimidines useful as kinase inhibitors |
| EP2306980A2 (en) * | 2008-06-30 | 2011-04-13 | Tibotec Pharmaceuticals | Powders for reconstitution |
| CA3014688A1 (en) | 2008-12-19 | 2010-07-15 | Supernus Pharmaceuticals, Inc. | Use of molindone for the treatment of aggression, irritability, or impulsivity |
| US8173342B2 (en) * | 2009-06-29 | 2012-05-08 | Xerox Corporation | Core shell photoconductors |
| WO2011050457A1 (en) | 2009-10-26 | 2011-05-05 | The University Of British Columbia | Stabilized formulation for oral administration of therapeutic agents and related methods |
| WO2011123497A1 (en) | 2010-03-31 | 2011-10-06 | Supernus Pharmaceuticals Inc. | Stabilized formulations of cns compounds |
| JP2013526601A (ja) * | 2010-05-24 | 2013-06-24 | ルピン・リミテッド | プラミペキソールの徐放性製剤 |
| CN105566229A (zh) | 2010-08-10 | 2016-05-11 | 西建阿维拉米斯研究公司 | Btk抑制剂的苯磺酸盐及其用途和制备方法 |
| TWI564008B (zh) * | 2010-09-30 | 2017-01-01 | 鹽野義製藥股份有限公司 | 難溶性藥物之溶解性改善製劑 |
| MX382354B (es) | 2010-11-01 | 2025-03-13 | Celgene Car Llc | Compuestos heterocíclicos y usos de los mismos. |
| EP2635285B1 (en) | 2010-11-01 | 2017-05-03 | Celgene Avilomics Research, Inc. | Heteroaryl compounds and uses thereof |
| CN102552161B (zh) * | 2010-12-28 | 2016-06-22 | 上海中西制药有限公司 | 一种药物固体制剂的制备方法及所得药物固体制剂 |
| US9655849B2 (en) | 2011-03-18 | 2017-05-23 | Particle Dynamics International, Llc | Solid particulate compositions comprising coenzyme Q10 |
| PL2696848T3 (pl) * | 2011-04-15 | 2020-12-28 | Janssen Pharmaceutica N.V. | Liofilizowane nanozawiesiny leków |
| CN106139155A (zh) * | 2011-05-30 | 2016-11-23 | 钟术光 | 缓释释药的药物载体 |
| WO2013038425A1 (en) * | 2011-09-16 | 2013-03-21 | Hetero Research Foundation | Rilpivirine hydrochloride |
| WO2013066903A1 (en) * | 2011-10-31 | 2013-05-10 | Mallinckrodt Llc | Combinational liposome compositions for cancer therapy |
| ES2695099T3 (es) * | 2011-11-23 | 2019-01-02 | Array Biopharma Inc | Formulaciones farmacéuticas |
| KR20130117128A (ko) * | 2012-04-17 | 2013-10-25 | 한국유나이티드제약 주식회사 | 레보드로프로피진 함유 서방정 및 이의 제조방법 |
| WO2013179105A1 (en) * | 2012-06-01 | 2013-12-05 | Laurus Labs Private Limited | Improved process for preparation of rilpivirine and pharmaceutically acceptable salts thereof |
| JP5827178B2 (ja) * | 2012-06-05 | 2015-12-02 | 北越紀州製紙株式会社 | セルロース多孔質体及びその製造方法 |
| US9126950B2 (en) | 2012-12-21 | 2015-09-08 | Celgene Avilomics Research, Inc. | Heteroaryl compounds and uses thereof |
| WO2014202797A1 (en) * | 2013-07-05 | 2014-12-24 | Synthon B.V. | Pharmaceutical composition comprising a solid dispersion of tadalafil |
| US9492471B2 (en) | 2013-08-27 | 2016-11-15 | Celgene Avilomics Research, Inc. | Methods of treating a disease or disorder associated with Bruton'S Tyrosine Kinase |
| KR101428018B1 (ko) * | 2013-10-18 | 2014-08-12 | 주식회사 한독 | 아리피프라졸 함유 구강 붕해 정제 및 이의 제조 방법 |
| KR20150056443A (ko) * | 2013-11-15 | 2015-05-26 | 한미약품 주식회사 | 타다라필 및 암로디핀을 포함하는 복합제제 |
| CN104173600B (zh) * | 2014-07-22 | 2018-03-02 | 河南亚卫动物药业有限公司 | 四味穿心莲散固体分散体及其制备方法 |
| ES3063790T3 (en) | 2015-06-09 | 2026-04-20 | Lonza Sales Ag | Formulations to achieve rapid dissolution of drug from spray-dried dispersions in capsules |
| KR102170146B1 (ko) * | 2019-03-05 | 2020-10-26 | 서울대학교산학협력단 | Pca 공정을 이용한 배양액의 결정화 장치 및 방법 |
| CN111004215B (zh) * | 2019-12-22 | 2022-08-09 | 华北理工大学 | 2,4-取代嘧啶类衍生物及其制备方法和在制备抗肿瘤药物中的应用 |
| CN111538113A (zh) * | 2020-05-08 | 2020-08-14 | 水利部南京水利水文自动化研究所 | 一种减少降水测量仪器承水口水附着量的方法 |
| CN112010810B (zh) * | 2020-09-09 | 2024-01-30 | 瑞阳制药股份有限公司 | 一锅法制备高纯度利匹韦林中间体的方法 |
Family Cites Families (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3237575A1 (de) * | 1982-10-09 | 1984-04-12 | Dr. Karl Thomae Gmbh, 7950 Biberach | Neue orale mopidamolformen |
| DE3320582A1 (de) | 1983-06-08 | 1984-12-13 | Dr. Karl Thomae Gmbh, 7950 Biberach | Gliquidonhaltige zubereitungsformen und verfahren zu ihrer herstellung |
| JPH05255066A (ja) | 1991-04-25 | 1993-10-05 | Takeda Chem Ind Ltd | 製剤用組成物、製剤およびそれらの製造方法 |
| EP0642784B1 (de) | 1993-09-07 | 1999-05-19 | Gerhard Dr. Gergely | Brausemischung mit Alkalisalzen oder Lysinaten saurer, unlöslicher oder schwer löslicher Wirkstoffe |
| IL110752A (en) * | 1993-09-13 | 2000-07-26 | Abbott Lab | Liquid semi-solid or solid pharmaceutical composition for an HIV protease inhibitor |
| IL111991A (en) * | 1994-01-28 | 2000-07-26 | Abbott Lab | Liquid pharmaceutical composition of HIV protease inhibitors in organic solvent |
| DE670160T1 (de) * | 1994-03-01 | 1996-03-14 | Gergely, Gerhard, Dr., Wien | Ein Brausesystem und einen Arzneiwirkstoff enthaltendes granuläres Produkt bzw. Tablette sowie Verfahren zu deren Herstellung. |
| EP0708646A1 (en) | 1994-05-06 | 1996-05-01 | Alcon Laboratories, Inc. | Use of vitamin e tocopheryl derivatives in ophthalmic compositions |
| US5558876A (en) | 1995-03-29 | 1996-09-24 | Alcon Laboratories, Inc. | Topical ophthalmic acidic drug formulations |
| IE80467B1 (en) * | 1995-07-03 | 1998-07-29 | Elan Corp Plc | Controlled release formulations for poorly soluble drugs |
| JPH09202728A (ja) | 1995-12-11 | 1997-08-05 | Hisamitsu Pharmaceut Co Inc | 固形製剤 |
| MY126358A (en) * | 1996-03-22 | 2006-09-29 | Glaxo Group Ltd | Compositions comprising vx478 and a water soluble tocopherol derivative such as vitamin e-tpgs |
| JP2001523221A (ja) | 1996-09-01 | 2001-11-20 | ファーモス コーポレイション | 親油性物質の促進された生物学的利用能のための固形共沈物 |
| NO311614B1 (no) * | 1996-10-01 | 2001-12-17 | Janssen Pharmaceutica Nv | Substituerte diamino-1,3,5-triazinderivater |
| US5891845A (en) | 1997-11-21 | 1999-04-06 | Fuisz Technologies Ltd. | Drug delivery systems utilizing liquid crystal structures |
| IL131217A0 (en) | 1998-03-10 | 2001-01-28 | Napro Biotherapeutics Inc | Novel methods and compositions for delivery of taxanes |
| CZ299380B6 (cs) * | 1998-03-27 | 2008-07-09 | Janssen Pharmaceutica N. V. | Pyrimidinová sloucenina, použití této slouceniny pro prípravu léciva, farmaceutický prostredek tutoslouceninu obsahující, zpusob prípravy tohoto prostredku a uvedené slouceniny a kombinace a produktuvedenou slouceninu obsahující |
| US6383471B1 (en) | 1999-04-06 | 2002-05-07 | Lipocine, Inc. | Compositions and methods for improved delivery of ionizable hydrophobic therapeutic agents |
| DE19945982A1 (de) * | 1999-09-24 | 2001-03-29 | Knoll Ag | Geschwindigkeitsbestimmte Partikel |
| CA2384188C (en) * | 1999-09-24 | 2008-06-17 | Janssen Pharmaceutica N.V. | Antiviral compositions |
| US6136846A (en) * | 1999-10-25 | 2000-10-24 | Supergen, Inc. | Formulation for paclitaxel |
| GEP20053427B (en) | 1999-12-23 | 2005-01-25 | Pfizer Prod Inc | Pharmaceutical Compositions Providing Enhanced Drug Concentrations |
| US20020015731A1 (en) | 1999-12-23 | 2002-02-07 | Appel Leah E. | Hydrogel-Driven Drug Dosage Form |
| US20010049366A1 (en) * | 2000-02-09 | 2001-12-06 | Alcon Universal Ltd. | Topical solution formulations containing an antibiotic and a corticosteroid |
| US6416793B1 (en) | 2000-07-11 | 2002-07-09 | Bioresponse, L.L.C. | Formulations and use of controlled-release indole alkaloids |
| JP2004536026A (ja) * | 2000-11-28 | 2004-12-02 | トランスフォーム ファーマシューティカルズ,インコーポレーティッド. | パクリタキセル、その誘導体、および薬剤として許容される塩を含む医薬品製剤 |
| KR100435141B1 (ko) * | 2000-12-28 | 2004-06-09 | 한미약품 주식회사 | 난용성 항진균제의 경구투여용 조성물 및 그의 제조 방법 |
| US6673373B2 (en) | 2001-02-01 | 2004-01-06 | Carlsbad Technology Inc. | Antifungal formulation and the methods for manufacturing and using the same |
| US6828301B2 (en) * | 2002-02-07 | 2004-12-07 | Boehringer Ingelheim International Gmbh | Pharmaceutical compositions for hepatitis C viral protease inhibitors |
| GB0403165D0 (en) * | 2004-02-12 | 2004-03-17 | Ct | Novel uses for proton pump inhibitors |
-
2002
- 2002-11-29 AU AU2002350719A patent/AU2002350719A1/en not_active Abandoned
- 2002-11-29 WO PCT/EP2002/013558 patent/WO2004050068A1/en not_active Ceased
-
2003
- 2003-11-20 TW TW092132474A patent/TWI340034B/zh not_active IP Right Cessation
- 2003-11-25 EP EP03789453.2A patent/EP1567134B1/en not_active Expired - Lifetime
- 2003-11-25 BR BRPI0316532A patent/BRPI0316532B8/pt not_active IP Right Cessation
- 2003-11-25 CN CNA2003801046197A patent/CN1720027A/zh active Pending
- 2003-11-25 CN CN201010531271.1A patent/CN102000335B/zh not_active Expired - Fee Related
- 2003-11-25 NZ NZ540846A patent/NZ540846A/en not_active IP Right Cessation
- 2003-11-25 HR HRP20050458AA patent/HRP20050458B1/hr not_active IP Right Cessation
- 2003-11-25 PL PL377057A patent/PL377057A1/pl not_active Application Discontinuation
- 2003-11-25 WO PCT/EP2003/050890 patent/WO2004050058A2/en not_active Ceased
- 2003-11-25 CA CA2505742A patent/CA2505742C/en not_active Expired - Fee Related
- 2003-11-25 ES ES03789453T patent/ES2763155T3/es not_active Expired - Lifetime
- 2003-11-25 UA UAA200505210A patent/UA92448C2/uk unknown
- 2003-11-25 RS YU20050407A patent/RS53148B/sr unknown
- 2003-11-25 AU AU2003294038A patent/AU2003294038B2/en not_active Ceased
- 2003-11-25 JP JP2004556332A patent/JP4951205B2/ja not_active Expired - Fee Related
- 2003-11-25 US US10/536,542 patent/US9192577B2/en active Active
- 2003-11-25 AP AP2005003318A patent/AP2100A/en active
- 2003-11-25 EA EA200500891A patent/EA010971B1/ru not_active IP Right Cessation
- 2003-11-25 KR KR1020057007339A patent/KR101107328B1/ko not_active Expired - Fee Related
- 2003-11-25 MX MXPA05005709A patent/MXPA05005709A/es unknown
- 2003-11-27 MY MYPI20034547A patent/MY148680A/en unknown
- 2003-11-28 AR ARP030104403A patent/AR042246A1/es not_active Application Discontinuation
-
2005
- 2005-04-11 IS IS7796A patent/IS7796A/is unknown
- 2005-05-26 ZA ZA200504312A patent/ZA200504312B/en unknown
- 2005-06-27 NO NO20053143A patent/NO20053143D0/no not_active Application Discontinuation
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0316532B1 (pt) | Composições farmacêuticas compreendendo uma droga básica ou ácida, um tensoativo, e um ácido ou base solúvel em água fisiologicamente tolerável | |
| US9028876B2 (en) | Rate-controlled particles | |
| RU2489149C2 (ru) | Стабилизированные аморфные формы иматиниба мезилата | |
| JP2002511073A (ja) | シクロデキストリンを含有する医薬組成物 | |
| RU2001128071A (ru) | Фармацевтическая композиция | |
| JP5288791B2 (ja) | 難水溶性物質含有微細化組成物 | |
| JP2001521899A (ja) | 脂質低下剤組成物 | |
| JPS63303926A (ja) | 製薬学的組成物、温血動物の処置法及び該組成物の製造法 | |
| EP3250188B1 (en) | Pharmaceutical composition comprising aprepitant and method for the preparation thereof | |
| WO2022253945A1 (en) | Pharmaceutical dosage forms comprising 3-(5-methyl-1,3-thiazol-2-yl)-5-[(3r)-tetrahydrofuran-3-yloxy]-n-{(1r)-1-[2-(trifluoromethyl)pyrimidin-5-yl]ethyl}-benzamide | |
| RU2193031C2 (ru) | Форма гидрохлорида 1-[2-(2-нафтил)этил]-4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридина в виде микрочастиц, фармацевтическая композиция на ее основе | |
| HK1153657B (en) | Pharmaceutical compositions comprising a basic or acidic drug compound, a surfactant and a physiologically tolerable water-soluble acid or base | |
| JP2012092079A (ja) | 育毛剤 | |
| AU2012201613B2 (en) | Stabilized amorphous forms of Imatinib mesylate |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] | ||
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 25/11/2003 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 18A ANUIDADE. |
|
| B24J | Lapse because of non-payment of annual fees (definitively: art 78 iv lpi, resolution 113/2013 art. 12) |
Free format text: EM VIRTUDE DA EXTINCAO PUBLICADA NA RPI 2646 DE 21-09-2021 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDA A EXTINCAO DA PATENTE E SEUS CERTIFICADOS, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |