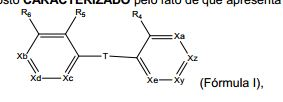
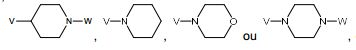
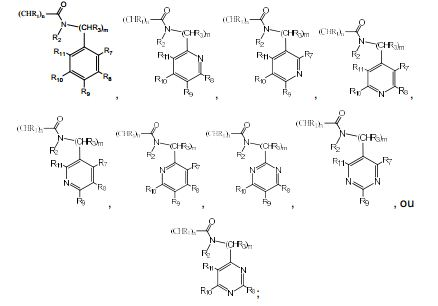
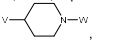
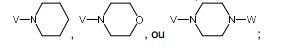
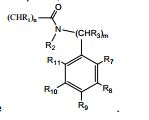
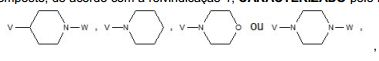
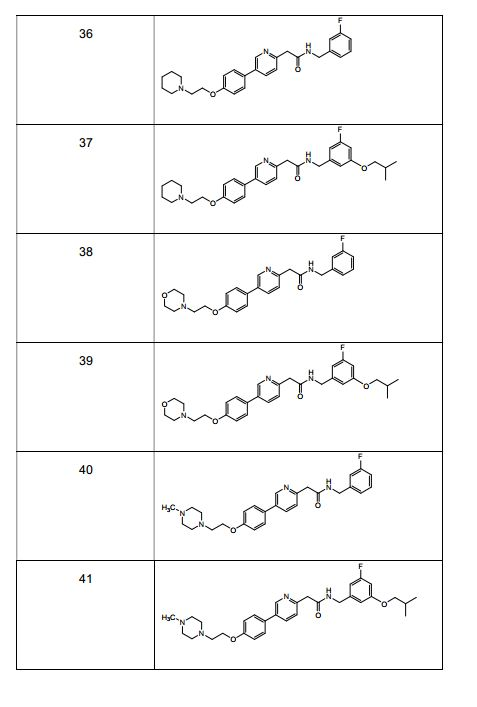
BRPI0519424B1 - compostos, composição e uso dos ditos compostos para a preparação de um medicamento para prevenção ou tratamento de um distúrbio de proliferação celular ou infecção microbiana - Google Patents
compostos, composição e uso dos ditos compostos para a preparação de um medicamento para prevenção ou tratamento de um distúrbio de proliferação celular ou infecção microbiana Download PDFInfo
- Publication number
- BRPI0519424B1 BRPI0519424B1 BRPI0519424-5A BRPI0519424A BRPI0519424B1 BR PI0519424 B1 BRPI0519424 B1 BR PI0519424B1 BR PI0519424 A BRPI0519424 A BR PI0519424A BR PI0519424 B1 BRPI0519424 B1 BR PI0519424B1
- Authority
- BR
- Brazil
- Prior art keywords
- alkyl
- compound
- compounds
- fact
- mmol
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 424
- 239000000203 mixture Substances 0.000 title claims abstract description 79
- 238000011282 treatment Methods 0.000 title claims abstract description 43
- 239000003814 drug Substances 0.000 title claims abstract description 38
- 208000035269 cancer or benign tumor Diseases 0.000 title claims abstract description 31
- 238000002360 preparation method Methods 0.000 title claims abstract description 7
- 230000002265 prevention Effects 0.000 title claims description 12
- 208000015181 infectious disease Diseases 0.000 title claims description 9
- 230000000813 microbial effect Effects 0.000 title claims description 8
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 52
- 230000004663 cell proliferation Effects 0.000 claims abstract description 8
- 125000000217 alkyl group Chemical group 0.000 claims description 67
- 239000001257 hydrogen Substances 0.000 claims description 56
- 229910052739 hydrogen Inorganic materials 0.000 claims description 56
- 229910052740 iodine Inorganic materials 0.000 claims description 48
- 150000003839 salts Chemical class 0.000 claims description 48
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 42
- 229910052757 nitrogen Inorganic materials 0.000 claims description 42
- 125000003545 alkoxy group Chemical group 0.000 claims description 40
- 206010028980 Neoplasm Diseases 0.000 claims description 38
- 208000035475 disorder Diseases 0.000 claims description 32
- 125000003118 aryl group Chemical group 0.000 claims description 31
- 201000011510 cancer Diseases 0.000 claims description 29
- 150000002431 hydrogen Chemical group 0.000 claims description 28
- 229910052794 bromium Inorganic materials 0.000 claims description 26
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 26
- 229910052801 chlorine Inorganic materials 0.000 claims description 24
- 229910052731 fluorine Inorganic materials 0.000 claims description 24
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 24
- 229910052736 halogen Inorganic materials 0.000 claims description 23
- 150000002367 halogens Chemical group 0.000 claims description 23
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 claims description 16
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 claims description 16
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 14
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 claims description 11
- 230000003463 hyperproliferative effect Effects 0.000 claims description 11
- 230000005764 inhibitory process Effects 0.000 claims description 11
- 201000004681 Psoriasis Diseases 0.000 claims description 7
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 6
- 201000005202 lung cancer Diseases 0.000 claims description 6
- 208000020816 lung neoplasm Diseases 0.000 claims description 6
- 208000029742 colonic neoplasm Diseases 0.000 claims description 5
- 206010009944 Colon cancer Diseases 0.000 claims description 4
- 206010025323 Lymphomas Diseases 0.000 claims description 4
- 206010012689 Diabetic retinopathy Diseases 0.000 claims description 3
- 230000001154 acute effect Effects 0.000 claims description 3
- 208000002780 macular degeneration Diseases 0.000 claims description 3
- 208000030507 AIDS Diseases 0.000 claims description 2
- 206010000830 Acute leukaemia Diseases 0.000 claims description 2
- 208000003200 Adenoma Diseases 0.000 claims description 2
- 206010006187 Breast cancer Diseases 0.000 claims description 2
- 208000026310 Breast neoplasm Diseases 0.000 claims description 2
- 208000001154 Dermoid Cyst Diseases 0.000 claims description 2
- 206010058314 Dysplasia Diseases 0.000 claims description 2
- 208000010305 Epidermal Cyst Diseases 0.000 claims description 2
- 208000017604 Hodgkin disease Diseases 0.000 claims description 2
- 208000010747 Hodgkins lymphoma Diseases 0.000 claims description 2
- 206010024612 Lipoma Diseases 0.000 claims description 2
- 206010025219 Lymphangioma Diseases 0.000 claims description 2
- 208000034578 Multiple myelomas Diseases 0.000 claims description 2
- 208000004304 Myofibromatosis Diseases 0.000 claims description 2
- 241000232901 Nephroma Species 0.000 claims description 2
- 208000007256 Nevus Diseases 0.000 claims description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 claims description 2
- 206010043276 Teratoma Diseases 0.000 claims description 2
- 208000024207 chronic leukemia Diseases 0.000 claims description 2
- 208000035250 cutaneous malignant susceptibility to 1 melanoma Diseases 0.000 claims description 2
- 201000011066 hemangioma Diseases 0.000 claims description 2
- 201000011489 infantile myofibromatosis Diseases 0.000 claims description 2
- 230000003902 lesion Effects 0.000 claims description 2
- 201000001441 melanoma Diseases 0.000 claims description 2
- 208000025351 nephroma Diseases 0.000 claims description 2
- 208000010626 plasma cell neoplasm Diseases 0.000 claims description 2
- 201000008261 skin carcinoma Diseases 0.000 claims description 2
- 206010001233 Adenoma benign Diseases 0.000 claims 1
- 241000894006 Bacteria Species 0.000 claims 1
- 208000003174 Brain Neoplasms Diseases 0.000 claims 1
- 206010012426 Dermal cyst Diseases 0.000 claims 1
- 241000233866 Fungi Species 0.000 claims 1
- 206010033128 Ovarian cancer Diseases 0.000 claims 1
- 206010061535 Ovarian neoplasm Diseases 0.000 claims 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 claims 1
- 206010060862 Prostate cancer Diseases 0.000 claims 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims 1
- 208000034541 Rare lymphatic malformation Diseases 0.000 claims 1
- 241000700605 Viruses Species 0.000 claims 1
- 201000002797 childhood leukemia Diseases 0.000 claims 1
- 208000017338 epidermoid cysts Diseases 0.000 claims 1
- 201000007270 liver cancer Diseases 0.000 claims 1
- 208000014018 liver neoplasm Diseases 0.000 claims 1
- 208000019420 lymphoid neoplasm Diseases 0.000 claims 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 claims 1
- 125000000896 monocarboxylic acid group Chemical group 0.000 claims 1
- 201000002528 pancreatic cancer Diseases 0.000 claims 1
- 208000008443 pancreatic carcinoma Diseases 0.000 claims 1
- 244000045947 parasite Species 0.000 claims 1
- 229940079593 drug Drugs 0.000 abstract description 16
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 211
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 123
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 97
- 238000006243 chemical reaction Methods 0.000 description 94
- 239000000243 solution Substances 0.000 description 89
- -1 methoxy, ethoxy Chemical group 0.000 description 88
- 235000019439 ethyl acetate Nutrition 0.000 description 76
- 230000015572 biosynthetic process Effects 0.000 description 75
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 73
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 73
- 238000003786 synthesis reaction Methods 0.000 description 73
- 239000007787 solid Substances 0.000 description 70
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 54
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 52
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 50
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 47
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 44
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 41
- 238000005481 NMR spectroscopy Methods 0.000 description 39
- 239000000047 product Substances 0.000 description 39
- 239000002904 solvent Substances 0.000 description 34
- 238000000034 method Methods 0.000 description 31
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 30
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 28
- 125000004429 atom Chemical group 0.000 description 28
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 28
- 239000012074 organic phase Substances 0.000 description 27
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 27
- QVSVMNXRLWSNGS-UHFFFAOYSA-N (3-fluorophenyl)methanamine Chemical compound NCC1=CC=CC(F)=C1 QVSVMNXRLWSNGS-UHFFFAOYSA-N 0.000 description 26
- 238000005160 1H NMR spectroscopy Methods 0.000 description 26
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 26
- 125000004432 carbon atom Chemical group C* 0.000 description 26
- 229910000029 sodium carbonate Inorganic materials 0.000 description 25
- 235000017550 sodium carbonate Nutrition 0.000 description 25
- 125000001424 substituent group Chemical group 0.000 description 25
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 24
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 24
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 23
- 125000003342 alkenyl group Chemical group 0.000 description 23
- 239000000460 chlorine Substances 0.000 description 23
- 239000011541 reaction mixture Substances 0.000 description 23
- 229910052938 sodium sulfate Inorganic materials 0.000 description 23
- 235000011152 sodium sulphate Nutrition 0.000 description 23
- 210000004027 cell Anatomy 0.000 description 22
- 239000008194 pharmaceutical composition Substances 0.000 description 22
- 239000012453 solvate Substances 0.000 description 22
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 21
- 125000000304 alkynyl group Chemical group 0.000 description 21
- 125000000623 heterocyclic group Chemical group 0.000 description 21
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 20
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 20
- NKDDWNXOKDWJAK-UHFFFAOYSA-N dimethoxymethane Chemical compound COCOC NKDDWNXOKDWJAK-UHFFFAOYSA-N 0.000 description 20
- 239000007789 gas Substances 0.000 description 20
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 20
- 238000003756 stirring Methods 0.000 description 20
- 229940124597 therapeutic agent Drugs 0.000 description 20
- 229910052799 carbon Inorganic materials 0.000 description 19
- 201000010099 disease Diseases 0.000 description 19
- 229910052717 sulfur Inorganic materials 0.000 description 19
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 18
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 18
- GBMDVOWEEQVZKZ-UHFFFAOYSA-N methanol;hydrate Chemical compound O.OC GBMDVOWEEQVZKZ-UHFFFAOYSA-N 0.000 description 18
- 238000001914 filtration Methods 0.000 description 17
- 238000009472 formulation Methods 0.000 description 17
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 16
- 239000003795 chemical substances by application Substances 0.000 description 16
- 102000016621 Focal Adhesion Protein-Tyrosine Kinases Human genes 0.000 description 15
- 108010067715 Focal Adhesion Protein-Tyrosine Kinases Proteins 0.000 description 15
- 125000002877 alkyl aryl group Chemical group 0.000 description 15
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 15
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 15
- 239000011734 sodium Substances 0.000 description 15
- 238000004809 thin layer chromatography Methods 0.000 description 15
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 14
- 108091000080 Phosphotransferase Proteins 0.000 description 14
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 14
- 102000020233 phosphotransferase Human genes 0.000 description 14
- 239000000741 silica gel Substances 0.000 description 14
- 229910002027 silica gel Inorganic materials 0.000 description 14
- AAILEWXSEQLMNI-UHFFFAOYSA-N 1h-pyridazin-6-one Chemical compound OC1=CC=CN=N1 AAILEWXSEQLMNI-UHFFFAOYSA-N 0.000 description 13
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 13
- 239000002253 acid Substances 0.000 description 13
- 239000002552 dosage form Substances 0.000 description 13
- 125000005842 heteroatom Chemical group 0.000 description 13
- 229910052760 oxygen Inorganic materials 0.000 description 13
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 12
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 12
- 239000003921 oil Substances 0.000 description 12
- 235000019198 oils Nutrition 0.000 description 12
- 239000008177 pharmaceutical agent Substances 0.000 description 12
- 229910052701 rubidium Inorganic materials 0.000 description 12
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 12
- 229910052721 tungsten Inorganic materials 0.000 description 12
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 11
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 11
- 241000282414 Homo sapiens Species 0.000 description 11
- 239000008346 aqueous phase Substances 0.000 description 11
- 238000004587 chromatography analysis Methods 0.000 description 11
- 125000001072 heteroaryl group Chemical group 0.000 description 11
- 239000000463 material Substances 0.000 description 11
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 11
- XWVPSJPQWOVRHJ-UHFFFAOYSA-N 2-(6-chloropyridin-3-yl)acetic acid Chemical compound OC(=O)CC1=CC=C(Cl)N=C1 XWVPSJPQWOVRHJ-UHFFFAOYSA-N 0.000 description 10
- 239000007832 Na2SO4 Substances 0.000 description 10
- 229910019142 PO4 Inorganic materials 0.000 description 10
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 10
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 10
- 229910052786 argon Inorganic materials 0.000 description 10
- 150000007942 carboxylates Chemical class 0.000 description 10
- 125000000524 functional group Chemical group 0.000 description 10
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 10
- 230000002969 morbid Effects 0.000 description 10
- 102000009076 src-Family Kinases Human genes 0.000 description 10
- 108010087686 src-Family Kinases Proteins 0.000 description 10
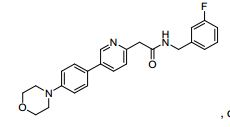
- RFRZLQWQXOTVIY-UHFFFAOYSA-N 2-(6-chloropyridin-3-yl)-n-[(3-fluorophenyl)methyl]acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C=NC(Cl)=CC=2)=C1 RFRZLQWQXOTVIY-UHFFFAOYSA-N 0.000 description 9
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 9
- 241000124008 Mammalia Species 0.000 description 9
- 241001465754 Metazoa Species 0.000 description 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 9
- 150000001408 amides Chemical class 0.000 description 9
- 150000002148 esters Chemical class 0.000 description 9
- 230000012010 growth Effects 0.000 description 9
- 229940043355 kinase inhibitor Drugs 0.000 description 9
- 239000010452 phosphate Substances 0.000 description 9
- 235000021317 phosphate Nutrition 0.000 description 9
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 9
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 9
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 8
- XMIIGOLPHOKFCH-UHFFFAOYSA-N 3-phenylpropionic acid Chemical compound OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 description 8
- 241000282412 Homo Species 0.000 description 8
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 8
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 8
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 8
- 239000004480 active ingredient Substances 0.000 description 8
- 125000004442 acylamino group Chemical group 0.000 description 8
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 description 8
- 239000013078 crystal Substances 0.000 description 8
- 239000007788 liquid Substances 0.000 description 8
- 125000004433 nitrogen atom Chemical group N* 0.000 description 8
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 8
- ACVYVLVWPXVTIT-UHFFFAOYSA-M phosphinate Chemical compound [O-][PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-M 0.000 description 8
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 8
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 8
- 238000010992 reflux Methods 0.000 description 8
- 239000007858 starting material Substances 0.000 description 8
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 8
- 239000003981 vehicle Substances 0.000 description 8
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 7
- 102000001332 SRC Human genes 0.000 description 7
- 108060006706 SRC Proteins 0.000 description 7
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 7
- 125000005194 alkoxycarbonyloxy group Chemical group 0.000 description 7
- 125000004947 alkyl aryl amino group Chemical group 0.000 description 7
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 7
- 125000004644 alkyl sulfinyl group Chemical group 0.000 description 7
- 125000004414 alkyl thio group Chemical group 0.000 description 7
- 230000001028 anti-proliverative effect Effects 0.000 description 7
- 125000001769 aryl amino group Chemical group 0.000 description 7
- 125000005129 aryl carbonyl group Chemical group 0.000 description 7
- 125000005199 aryl carbonyloxy group Chemical group 0.000 description 7
- 125000005200 aryloxy carbonyloxy group Chemical group 0.000 description 7
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 7
- 125000000852 azido group Chemical group *N=[N+]=[N-] 0.000 description 7
- QRZAKQDHEVVFRX-UHFFFAOYSA-N biphenyl-4-ylacetic acid Chemical compound C1=CC(CC(=O)O)=CC=C1C1=CC=CC=C1 QRZAKQDHEVVFRX-UHFFFAOYSA-N 0.000 description 7
- 239000012267 brine Substances 0.000 description 7
- 125000001951 carbamoylamino group Chemical group C(N)(=O)N* 0.000 description 7
- 229940125904 compound 1 Drugs 0.000 description 7
- 238000010168 coupling process Methods 0.000 description 7
- 125000004663 dialkyl amino group Chemical group 0.000 description 7
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 7
- 238000010438 heat treatment Methods 0.000 description 7
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 7
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 7
- 235000019341 magnesium sulphate Nutrition 0.000 description 7
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 7
- 239000001301 oxygen Substances 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 7
- 239000000126 substance Substances 0.000 description 7
- 125000004434 sulfur atom Chemical group 0.000 description 7
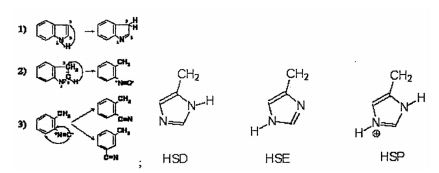
- 238000003419 tautomerization reaction Methods 0.000 description 7
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 6
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N acetic acid Substances CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- 125000003282 alkyl amino group Chemical group 0.000 description 6
- 125000004691 alkyl thio carbonyl group Chemical group 0.000 description 6
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 6
- 239000002246 antineoplastic agent Substances 0.000 description 6
- 125000004658 aryl carbonyl amino group Chemical group 0.000 description 6
- 125000005110 aryl thio group Chemical group 0.000 description 6
- 239000002775 capsule Substances 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- 230000010261 cell growth Effects 0.000 description 6
- 239000003153 chemical reaction reagent Substances 0.000 description 6
- 238000002648 combination therapy Methods 0.000 description 6
- 230000008878 coupling Effects 0.000 description 6
- 238000005859 coupling reaction Methods 0.000 description 6
- 125000004986 diarylamino group Chemical group 0.000 description 6
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 150000002430 hydrocarbons Chemical group 0.000 description 6
- 230000036963 noncompetitive effect Effects 0.000 description 6
- 125000004430 oxygen atom Chemical group O* 0.000 description 6
- 230000000144 pharmacologic effect Effects 0.000 description 6
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- XTUSEBKMEQERQV-UHFFFAOYSA-N propan-2-ol;hydrate Chemical compound O.CC(C)O XTUSEBKMEQERQV-UHFFFAOYSA-N 0.000 description 6
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 6
- 125000005420 sulfonamido group Chemical group S(=O)(=O)(N*)* 0.000 description 6
- 239000011593 sulfur Substances 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 6
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 5
- YEDUAINPPJYDJZ-UHFFFAOYSA-N 2-hydroxybenzothiazole Chemical compound C1=CC=C2SC(O)=NC2=C1 YEDUAINPPJYDJZ-UHFFFAOYSA-N 0.000 description 5
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 125000002252 acyl group Chemical group 0.000 description 5
- 239000000443 aerosol Substances 0.000 description 5
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 description 5
- 150000001412 amines Chemical class 0.000 description 5
- 239000007864 aqueous solution Substances 0.000 description 5
- 239000002585 base Substances 0.000 description 5
- 230000009286 beneficial effect Effects 0.000 description 5
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 5
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 5
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 5
- 238000004440 column chromatography Methods 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- 125000004093 cyano group Chemical group *C#N 0.000 description 5
- 125000004473 dialkylaminocarbonyl group Chemical group 0.000 description 5
- 239000000706 filtrate Substances 0.000 description 5
- 238000004128 high performance liquid chromatography Methods 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 230000002401 inhibitory effect Effects 0.000 description 5
- 125000002950 monocyclic group Chemical group 0.000 description 5
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 5
- 229910052763 palladium Inorganic materials 0.000 description 5
- 239000003755 preservative agent Substances 0.000 description 5
- 125000006239 protecting group Chemical group 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 239000000725 suspension Substances 0.000 description 5
- DRDRKFYLURTTAW-UHFFFAOYSA-N 2-[6-(4-ethoxyphenyl)pyridin-3-yl]-n-[(3-fluorophenyl)methyl]acetamide Chemical compound C1=CC(OCC)=CC=C1C(N=C1)=CC=C1CC(=O)NCC1=CC=CC(F)=C1 DRDRKFYLURTTAW-UHFFFAOYSA-N 0.000 description 4
- QOWSWEBLNVACCL-UHFFFAOYSA-N 4-Bromophenyl acetate Chemical compound OC(=O)CC1=CC=C(Br)C=C1 QOWSWEBLNVACCL-UHFFFAOYSA-N 0.000 description 4
- DHLUJPLHLZJUBW-UHFFFAOYSA-N 6-methylpyridin-3-ol Chemical compound CC1=CC=C(O)C=N1 DHLUJPLHLZJUBW-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 4
- JBDNTHBZIVNFIB-UHFFFAOYSA-N C=1C=CC=CC=1CONOCC1=CC=CC=C1 Chemical compound C=1C=CC=CC=1CONOCC1=CC=CC=C1 JBDNTHBZIVNFIB-UHFFFAOYSA-N 0.000 description 4
- JGLMVXWAHNTPRF-CMDGGOBGSA-N CCN1N=C(C)C=C1C(=O)NC1=NC2=CC(=CC(OC)=C2N1C\C=C\CN1C(NC(=O)C2=CC(C)=NN2CC)=NC2=CC(=CC(OCCCN3CCOCC3)=C12)C(N)=O)C(N)=O Chemical compound CCN1N=C(C)C=C1C(=O)NC1=NC2=CC(=CC(OC)=C2N1C\C=C\CN1C(NC(=O)C2=CC(C)=NN2CC)=NC2=CC(=CC(OCCCN3CCOCC3)=C12)C(N)=O)C(N)=O JGLMVXWAHNTPRF-CMDGGOBGSA-N 0.000 description 4
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical group C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 4
- 102000001253 Protein Kinase Human genes 0.000 description 4
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 4
- 238000006069 Suzuki reaction reaction Methods 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 4
- 125000006242 amine protecting group Chemical group 0.000 description 4
- 239000004037 angiogenesis inhibitor Substances 0.000 description 4
- 125000000129 anionic group Chemical group 0.000 description 4
- 239000003242 anti bacterial agent Substances 0.000 description 4
- 230000000844 anti-bacterial effect Effects 0.000 description 4
- 230000001093 anti-cancer Effects 0.000 description 4
- 230000000843 anti-fungal effect Effects 0.000 description 4
- 230000000845 anti-microbial effect Effects 0.000 description 4
- 230000002141 anti-parasite Effects 0.000 description 4
- 239000003429 antifungal agent Substances 0.000 description 4
- 239000002257 antimetastatic agent Substances 0.000 description 4
- 239000004599 antimicrobial Substances 0.000 description 4
- 239000003096 antiparasitic agent Substances 0.000 description 4
- 239000003443 antiviral agent Substances 0.000 description 4
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 125000002619 bicyclic group Chemical group 0.000 description 4
- 239000004305 biphenyl Substances 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 150000001721 carbon Chemical group 0.000 description 4
- 235000011089 carbon dioxide Nutrition 0.000 description 4
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 210000001072 colon Anatomy 0.000 description 4
- 239000012230 colorless oil Substances 0.000 description 4
- 229940125961 compound 24 Drugs 0.000 description 4
- 125000000392 cycloalkenyl group Chemical group 0.000 description 4
- SNRCKKQHDUIRIY-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloromethane;dichloropalladium;iron(2+) Chemical compound [Fe+2].ClCCl.Cl[Pd]Cl.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 SNRCKKQHDUIRIY-UHFFFAOYSA-L 0.000 description 4
- 230000009036 growth inhibition Effects 0.000 description 4
- 150000004677 hydrates Chemical class 0.000 description 4
- VUZPPFZMUPKLLV-UHFFFAOYSA-N methane;hydrate Chemical compound C.O VUZPPFZMUPKLLV-UHFFFAOYSA-N 0.000 description 4
- 231100000252 nontoxic Toxicity 0.000 description 4
- 230000003000 nontoxic effect Effects 0.000 description 4
- 230000037361 pathway Effects 0.000 description 4
- 229910000027 potassium carbonate Inorganic materials 0.000 description 4
- 239000002244 precipitate Substances 0.000 description 4
- 230000002062 proliferating effect Effects 0.000 description 4
- 108060006633 protein kinase Proteins 0.000 description 4
- COLRMVLTWJTLFJ-UHFFFAOYSA-N pyridin-2-yl trifluoromethanesulfonate Chemical compound FC(F)(F)S(=O)(=O)OC1=CC=CC=N1 COLRMVLTWJTLFJ-UHFFFAOYSA-N 0.000 description 4
- 239000012047 saturated solution Substances 0.000 description 4
- 235000017557 sodium bicarbonate Nutrition 0.000 description 4
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 4
- 235000011149 sulphuric acid Nutrition 0.000 description 4
- 239000003826 tablet Substances 0.000 description 4
- 210000004881 tumor cell Anatomy 0.000 description 4
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 3
- KKFDCBRMNNSAAW-UHFFFAOYSA-N 2-(morpholin-4-yl)ethanol Chemical compound OCCN1CCOCC1 KKFDCBRMNNSAAW-UHFFFAOYSA-N 0.000 description 3
- 125000006284 3-fluorobenzyl group Chemical group [H]C1=C([H])C(=C([H])C(F)=C1[H])C([H])([H])* 0.000 description 3
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 3
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 3
- 241000271566 Aves Species 0.000 description 3
- 241000283690 Bos taurus Species 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 3
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 206010065874 Psoriatic conditions Diseases 0.000 description 3
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 3
- OBYNCDBAMUFKDA-UHFFFAOYSA-N [3,5-bis(phenylmethoxy)phenyl]methanamine Chemical compound C=1C(OCC=2C=CC=CC=2)=CC(CN)=CC=1OCC1=CC=CC=C1 OBYNCDBAMUFKDA-UHFFFAOYSA-N 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 150000001299 aldehydes Chemical group 0.000 description 3
- 125000001931 aliphatic group Chemical group 0.000 description 3
- 230000001772 anti-angiogenic effect Effects 0.000 description 3
- 229940121375 antifungal agent Drugs 0.000 description 3
- WHGYBXFWUBPSRW-FOUAGVGXSA-N beta-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO WHGYBXFWUBPSRW-FOUAGVGXSA-N 0.000 description 3
- 235000010290 biphenyl Nutrition 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 3
- 238000013329 compounding Methods 0.000 description 3
- 238000002425 crystallisation Methods 0.000 description 3
- 230000008025 crystallization Effects 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 125000000753 cycloalkyl group Chemical group 0.000 description 3
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 239000006185 dispersion Substances 0.000 description 3
- 239000012153 distilled water Substances 0.000 description 3
- 239000003937 drug carrier Substances 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 125000004494 ethyl ester group Chemical group 0.000 description 3
- 238000003818 flash chromatography Methods 0.000 description 3
- 239000011737 fluorine Substances 0.000 description 3
- 239000012458 free base Substances 0.000 description 3
- 125000005843 halogen group Chemical group 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Chemical group C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 239000012535 impurity Substances 0.000 description 3
- 238000007918 intramuscular administration Methods 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 238000010253 intravenous injection Methods 0.000 description 3
- 125000000468 ketone group Chemical group 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 238000002844 melting Methods 0.000 description 3
- 230000008018 melting Effects 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 230000003287 optical effect Effects 0.000 description 3
- 239000000825 pharmaceutical preparation Substances 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 235000011056 potassium acetate Nutrition 0.000 description 3
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 230000035755 proliferation Effects 0.000 description 3
- 230000002685 pulmonary effect Effects 0.000 description 3
- QLULGIRFKAWHOJ-UHFFFAOYSA-N pyridin-4-ylboronic acid Chemical compound OB(O)C1=CC=NC=C1 QLULGIRFKAWHOJ-UHFFFAOYSA-N 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 229910052708 sodium Inorganic materials 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 239000006188 syrup Substances 0.000 description 3
- 235000020357 syrup Nutrition 0.000 description 3
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 2
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 2
- VIDRFOGBFWHCSO-UHFFFAOYSA-N (3-fluoro-4-phenylphenyl)methanol Chemical compound FC1=CC(CO)=CC=C1C1=CC=CC=C1 VIDRFOGBFWHCSO-UHFFFAOYSA-N 0.000 description 2
- KNXQDJCZSVHEIW-UHFFFAOYSA-N (3-fluorophenyl)boronic acid Chemical compound OB(O)C1=CC=CC(F)=C1 KNXQDJCZSVHEIW-UHFFFAOYSA-N 0.000 description 2
- OOQQYQQLMPJNJB-UHFFFAOYSA-N (3-phenylmethoxyphenyl)methanamine;hydrochloride Chemical compound Cl.NCC1=CC=CC(OCC=2C=CC=CC=2)=C1 OOQQYQQLMPJNJB-UHFFFAOYSA-N 0.000 description 2
- WRQNDLDUNQMTCL-UHFFFAOYSA-N (4-ethoxyphenyl)boronic acid Chemical compound CCOC1=CC=C(B(O)O)C=C1 WRQNDLDUNQMTCL-UHFFFAOYSA-N 0.000 description 2
- LBUJPTNKIBCYBY-UHFFFAOYSA-N 1,2,3,4-tetrahydroquinoline Chemical compound C1=CC=C2CCCNC2=C1 LBUJPTNKIBCYBY-UHFFFAOYSA-N 0.000 description 2
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 2
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
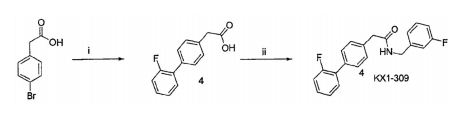
- MZSNDIIUILXNMA-UHFFFAOYSA-N 2-(2-fluoro-4-phenylphenyl)acetic acid Chemical compound C1=C(F)C(CC(=O)O)=CC=C1C1=CC=CC=C1 MZSNDIIUILXNMA-UHFFFAOYSA-N 0.000 description 2
- ZLLZRKQQNGBXRD-UHFFFAOYSA-N 2-(3-fluoro-4-phenylphenyl)acetic acid Chemical compound FC1=CC(CC(=O)O)=CC=C1C1=CC=CC=C1 ZLLZRKQQNGBXRD-UHFFFAOYSA-N 0.000 description 2
- VLQLJPWPRYUYMK-UHFFFAOYSA-N 2-(3-phenylphenyl)acetic acid Chemical compound OC(=O)CC1=CC=CC(C=2C=CC=CC=2)=C1 VLQLJPWPRYUYMK-UHFFFAOYSA-N 0.000 description 2
- ZHMJLHVIMRIFON-UHFFFAOYSA-N 2-(4-bromo-2-fluorophenyl)acetamide Chemical compound NC(=O)CC1=CC=C(Br)C=C1F ZHMJLHVIMRIFON-UHFFFAOYSA-N 0.000 description 2
- PNBIYFPZODYMOO-UHFFFAOYSA-N 2-(4-bromo-2-fluorophenyl)acetic acid Chemical compound OC(=O)CC1=CC=C(Br)C=C1F PNBIYFPZODYMOO-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- HQQLXERSPFVWEW-UHFFFAOYSA-N 2-[4-(4-fluorophenyl)phenyl]acetic acid Chemical compound C1=CC(CC(=O)O)=CC=C1C1=CC=C(F)C=C1 HQQLXERSPFVWEW-UHFFFAOYSA-N 0.000 description 2
- CKKIJYBDCNXYKY-UHFFFAOYSA-N 2-[6-(3-chlorophenyl)pyridin-3-yl]-n-[(3-fluorophenyl)methyl]acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C=NC(=CC=2)C=2C=C(Cl)C=CC=2)=C1 CKKIJYBDCNXYKY-UHFFFAOYSA-N 0.000 description 2
- BQSVEKWAAXCUIR-UHFFFAOYSA-N 2-[6-(4-ethylphenyl)pyridin-3-yl]-n-[(3-fluorophenyl)methyl]acetamide Chemical compound C1=CC(CC)=CC=C1C(N=C1)=CC=C1CC(=O)NCC1=CC=CC(F)=C1 BQSVEKWAAXCUIR-UHFFFAOYSA-N 0.000 description 2
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 2
- JXNAIOCJWBJGFQ-UHFFFAOYSA-N 2-methyl-5-phenylpyridine Chemical compound C1=NC(C)=CC=C1C1=CC=CC=C1 JXNAIOCJWBJGFQ-UHFFFAOYSA-N 0.000 description 2
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 2
- LULAYUGMBFYYEX-UHFFFAOYSA-N 3-chlorobenzoic acid Chemical compound OC(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-N 0.000 description 2
- 125000004180 3-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(F)=C1[H] 0.000 description 2
- VLZQTLUSPQUQLC-UHFFFAOYSA-N 3-phenylmethoxybenzonitrile Chemical compound N#CC1=CC=CC(OCC=2C=CC=CC=2)=C1 VLZQTLUSPQUQLC-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
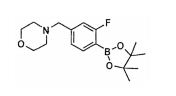
- AXLRZCPFGFYXIS-UHFFFAOYSA-N 4-[(4-bromo-3-fluorophenyl)methyl]morpholine Chemical compound C1=C(Br)C(F)=CC(CN2CCOCC2)=C1 AXLRZCPFGFYXIS-UHFFFAOYSA-N 0.000 description 2
- VKWGRMJGLCODKR-UHFFFAOYSA-N 4-[2-(4-bromo-3-fluorophenoxy)ethyl]morpholine Chemical compound C1=C(Br)C(F)=CC(OCCN2CCOCC2)=C1 VKWGRMJGLCODKR-UHFFFAOYSA-N 0.000 description 2
- MRQYTJXVULSNIS-UHFFFAOYSA-N 4-bromo-3-fluorophenol Chemical compound OC1=CC=C(Br)C(F)=C1 MRQYTJXVULSNIS-UHFFFAOYSA-N 0.000 description 2
- LBUNNMJLXWQQBY-UHFFFAOYSA-N 4-fluorophenylboronic acid Chemical compound OB(O)C1=CC=C(F)C=C1 LBUNNMJLXWQQBY-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- 208000035143 Bacterial infection Diseases 0.000 description 2
- 238000010599 BrdU assay Methods 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- ISMDILRWKSYCOD-GNKBHMEESA-N C(C1=CC=CC=C1)[C@@H]1NC(OCCCCCCCCCCCNC([C@@H](NC(C[C@@H]1O)=O)C(C)C)=O)=O Chemical compound C(C1=CC=CC=C1)[C@@H]1NC(OCCCCCCCCCCCNC([C@@H](NC(C[C@@H]1O)=O)C(C)C)=O)=O ISMDILRWKSYCOD-GNKBHMEESA-N 0.000 description 2
- 229940126639 Compound 33 Drugs 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- 229920000858 Cyclodextrin Polymers 0.000 description 2
- OKKJLVBELUTLKV-MZCSYVLQSA-N Deuterated methanol Chemical compound [2H]OC([2H])([2H])[2H] OKKJLVBELUTLKV-MZCSYVLQSA-N 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- 206010017533 Fungal infection Diseases 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 229930194542 Keto Natural products 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- 229930182816 L-glutamine Natural products 0.000 description 2
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 2
- 241001529936 Murinae Species 0.000 description 2
- 208000031888 Mycoses Diseases 0.000 description 2
- 150000001204 N-oxides Chemical class 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- 208000030852 Parasitic disease Diseases 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical group C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 2
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical group C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical class [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical group C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- 208000036142 Viral infection Diseases 0.000 description 2
- KCMYLSUOKDQZQI-UHFFFAOYSA-N acetic acid;1-fluoro-2-phenylbenzene Chemical compound CC(O)=O.FC1=CC=CC=C1C1=CC=CC=C1 KCMYLSUOKDQZQI-UHFFFAOYSA-N 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 125000003158 alcohol group Chemical group 0.000 description 2
- 125000002723 alicyclic group Chemical group 0.000 description 2
- 150000001336 alkenes Chemical class 0.000 description 2
- 125000005089 alkenylaminocarbonyl group Chemical group 0.000 description 2
- 125000005090 alkenylcarbonyl group Chemical group 0.000 description 2
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 2
- 150000005215 alkyl ethers Chemical class 0.000 description 2
- 125000006350 alkyl thio alkyl group Chemical group 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 230000002001 anti-metastasis Effects 0.000 description 2
- 125000005125 aryl alkyl amino carbonyl group Chemical group 0.000 description 2
- 125000005099 aryl alkyl carbonyl group Chemical group 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 208000022362 bacterial infectious disease Diseases 0.000 description 2
- RFRXIWQYSOIBDI-UHFFFAOYSA-N benzarone Chemical compound CCC=1OC2=CC=CC=C2C=1C(=O)C1=CC=C(O)C=C1 RFRXIWQYSOIBDI-UHFFFAOYSA-N 0.000 description 2
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 2
- WGQKYBSKWIADBV-UHFFFAOYSA-N benzylamine Chemical compound NCC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 description 2
- 229960004853 betadex Drugs 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 210000000481 breast Anatomy 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- 229940126543 compound 14 Drugs 0.000 description 2
- 229940126208 compound 22 Drugs 0.000 description 2
- 229940125846 compound 25 Drugs 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 2
- NLUNLVTVUDIHFE-UHFFFAOYSA-N cyclooctylcyclooctane Chemical compound C1CCCCCCC1C1CCCCCCC1 NLUNLVTVUDIHFE-UHFFFAOYSA-N 0.000 description 2
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 231100000517 death Toxicity 0.000 description 2
- 230000005595 deprotonation Effects 0.000 description 2
- 238000010537 deprotonation reaction Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 208000037765 diseases and disorders Diseases 0.000 description 2
- 238000006073 displacement reaction Methods 0.000 description 2
- 238000012377 drug delivery Methods 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 2
- 239000002024 ethyl acetate extract Substances 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 230000001605 fetal effect Effects 0.000 description 2
- 210000002950 fibroblast Anatomy 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 235000019256 formaldehyde Nutrition 0.000 description 2
- 230000002538 fungal effect Effects 0.000 description 2
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 2
- 239000003906 humectant Substances 0.000 description 2
- 239000005457 ice water Substances 0.000 description 2
- 150000002466 imines Chemical class 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 2
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- 238000007913 intrathecal administration Methods 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 125000002510 isobutoxy group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])O* 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 235000010981 methylcellulose Nutrition 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- TXXHDPDFNKHHGW-UHFFFAOYSA-N muconic acid Chemical compound OC(=O)C=CC=CC(O)=O TXXHDPDFNKHHGW-UHFFFAOYSA-N 0.000 description 2
- JCEYGAPCKZXAGC-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-(2-fluoro-4-phenylphenyl)acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C(=CC(=CC=2)C=2C=CC=CC=2)F)=C1 JCEYGAPCKZXAGC-UHFFFAOYSA-N 0.000 description 2
- UNGHZVMJSOSBQR-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-(3-fluoro-4-phenylphenyl)acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C=C(F)C(=CC=2)C=2C=CC=CC=2)=C1 UNGHZVMJSOSBQR-UHFFFAOYSA-N 0.000 description 2
- ODSYHNMMJCLPFQ-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-(4-pyridin-2-ylphenyl)acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C=CC(=CC=2)C=2N=CC=CC=2)=C1 ODSYHNMMJCLPFQ-UHFFFAOYSA-N 0.000 description 2
- JZXLJBUXFZIOEK-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-(6-phenylpyridin-3-yl)acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C=NC(=CC=2)C=2C=CC=CC=2)=C1 JZXLJBUXFZIOEK-UHFFFAOYSA-N 0.000 description 2
- FFSADQKZUMNKEK-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-[6-(3-fluorophenyl)pyridin-3-yl]acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C=NC(=CC=2)C=2C=C(F)C=CC=2)=C1 FFSADQKZUMNKEK-UHFFFAOYSA-N 0.000 description 2
- DTRALTHUPOZTDW-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-[6-(4-fluorophenyl)pyridin-3-yl]acetamide Chemical compound C1=CC(F)=CC=C1C(N=C1)=CC=C1CC(=O)NCC1=CC=CC(F)=C1 DTRALTHUPOZTDW-UHFFFAOYSA-N 0.000 description 2
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 2
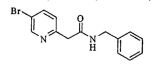
- MFVMVBWFPPMPFW-UHFFFAOYSA-N n-benzyl-2-(5-bromopyridin-2-yl)acetamide Chemical compound N1=CC(Br)=CC=C1CC(=O)NCC1=CC=CC=C1 MFVMVBWFPPMPFW-UHFFFAOYSA-N 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 230000003204 osmotic effect Effects 0.000 description 2
- 239000007800 oxidant agent Substances 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 230000003071 parasitic effect Effects 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 125000004437 phosphorous atom Chemical group 0.000 description 2
- 230000026731 phosphorylation Effects 0.000 description 2
- 238000006366 phosphorylation reaction Methods 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 125000003367 polycyclic group Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 239000000651 prodrug Substances 0.000 description 2
- 229940002612 prodrug Drugs 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- VVWRJUBEIPHGQF-MDZDMXLPSA-N propan-2-yl (ne)-n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)\N=N\C(=O)OC(C)C VVWRJUBEIPHGQF-MDZDMXLPSA-N 0.000 description 2
- VVWRJUBEIPHGQF-UHFFFAOYSA-N propan-2-yl n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)N=NC(=O)OC(C)C VVWRJUBEIPHGQF-UHFFFAOYSA-N 0.000 description 2
- 239000003380 propellant Substances 0.000 description 2
- 235000018102 proteins Nutrition 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 230000005588 protonation Effects 0.000 description 2
- ABMYEXAYWZJVOV-UHFFFAOYSA-N pyridin-3-ylboronic acid Chemical compound OB(O)C1=CC=CN=C1 ABMYEXAYWZJVOV-UHFFFAOYSA-N 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 239000012279 sodium borohydride Substances 0.000 description 2
- 229910000033 sodium borohydride Inorganic materials 0.000 description 2
- DAEPDZWVDSPTHF-UHFFFAOYSA-M sodium pyruvate Chemical compound [Na+].CC(=O)C([O-])=O DAEPDZWVDSPTHF-UHFFFAOYSA-M 0.000 description 2
- 125000003003 spiro group Chemical group 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- 238000013268 sustained release Methods 0.000 description 2
- 239000012730 sustained-release form Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 2
- 150000003536 tetrazoles Chemical group 0.000 description 2
- 125000003831 tetrazolyl group Chemical group 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- 150000003568 thioethers Chemical class 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- WJKHJLXJJJATHN-UHFFFAOYSA-N triflic anhydride Chemical compound FC(F)(F)S(=O)(=O)OS(=O)(=O)C(F)(F)F WJKHJLXJJJATHN-UHFFFAOYSA-N 0.000 description 2
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 2
- 230000004614 tumor growth Effects 0.000 description 2
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 2
- 238000000825 ultraviolet detection Methods 0.000 description 2
- 230000009385 viral infection Effects 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 1
- DGFCTCGCMKEILT-UHFFFAOYSA-N (2-ethoxyphenyl)boronic acid Chemical compound CCOC1=CC=CC=C1B(O)O DGFCTCGCMKEILT-UHFFFAOYSA-N 0.000 description 1
- QCSLIRFWJPOENV-UHFFFAOYSA-N (2-fluorophenyl)boronic acid Chemical compound OB(O)C1=CC=CC=C1F QCSLIRFWJPOENV-UHFFFAOYSA-N 0.000 description 1
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 1
- ITOFPJRDSCGOSA-KZLRUDJFSA-N (2s)-2-[[(4r)-4-[(3r,5r,8r,9s,10s,13r,14s,17r)-3-hydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]pentanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H](CC[C@]13C)[C@@H]2[C@@H]3CC[C@@H]1[C@H](C)CCC(=O)N[C@H](C(O)=O)CC1=CNC2=CC=CC=C12 ITOFPJRDSCGOSA-KZLRUDJFSA-N 0.000 description 1
- SDEAGACSNFSZCU-UHFFFAOYSA-N (3-chlorophenyl)boronic acid Chemical compound OB(O)C1=CC=CC(Cl)=C1 SDEAGACSNFSZCU-UHFFFAOYSA-N 0.000 description 1
- CHCWUTJYLUBETR-UHFFFAOYSA-N (3-ethoxyphenyl)boronic acid Chemical compound CCOC1=CC=CC(B(O)O)=C1 CHCWUTJYLUBETR-UHFFFAOYSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 1
- CTXIMPPNCZNPEM-UHFFFAOYSA-N (4-bromo-3-fluorophenyl)-morpholin-4-ylmethanone Chemical compound C1=C(Br)C(F)=CC(C(=O)N2CCOCC2)=C1 CTXIMPPNCZNPEM-UHFFFAOYSA-N 0.000 description 1
- RZCPLOMUUCFPQA-UHFFFAOYSA-N (4-ethylphenyl)boronic acid Chemical compound CCC1=CC=C(B(O)O)C=C1 RZCPLOMUUCFPQA-UHFFFAOYSA-N 0.000 description 1
- BESAKUXOHCFPAA-UHFFFAOYSA-N (4-pyridin-2-ylphenyl)methanol Chemical compound C1=CC(CO)=CC=C1C1=CC=CC=N1 BESAKUXOHCFPAA-UHFFFAOYSA-N 0.000 description 1
- UVNPEUJXKZFWSJ-LMTQTHQJSA-N (R)-N-[(4S)-8-[6-amino-5-[(3,3-difluoro-2-oxo-1H-pyrrolo[2,3-b]pyridin-4-yl)sulfanyl]pyrazin-2-yl]-2-oxa-8-azaspiro[4.5]decan-4-yl]-2-methylpropane-2-sulfinamide Chemical compound CC(C)(C)[S@@](=O)N[C@@H]1COCC11CCN(CC1)c1cnc(Sc2ccnc3NC(=O)C(F)(F)c23)c(N)n1 UVNPEUJXKZFWSJ-LMTQTHQJSA-N 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- 125000001399 1,2,3-triazolyl group Chemical group N1N=NC(=C1)* 0.000 description 1
- 125000004504 1,2,4-oxadiazolyl group Chemical group 0.000 description 1
- 125000004514 1,2,4-thiadiazolyl group Chemical group 0.000 description 1
- 125000001376 1,2,4-triazolyl group Chemical group N1N=C(N=C1)* 0.000 description 1
- 125000004506 1,2,5-oxadiazolyl group Chemical group 0.000 description 1
- 125000004517 1,2,5-thiadiazolyl group Chemical group 0.000 description 1
- 125000001781 1,3,4-oxadiazolyl group Chemical group 0.000 description 1
- 125000004520 1,3,4-thiadiazolyl group Chemical group 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- ZXWCKKSSCIFVBT-UHFFFAOYSA-N 1-(3-fluorophenyl)-n-methylmethanamine Chemical compound CNCC1=CC=CC(F)=C1 ZXWCKKSSCIFVBT-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- YUCGPLDILIGQJO-UHFFFAOYSA-N 1-[2-(4-bromo-3-fluorophenoxy)ethyl]-4-methylpiperazine Chemical compound C1CN(C)CCN1CCOC1=CC=C(Br)C(F)=C1 YUCGPLDILIGQJO-UHFFFAOYSA-N 0.000 description 1
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 1
- AMMPLVWPWSYRDR-UHFFFAOYSA-N 1-methylbicyclo[2.2.2]oct-2-ene-4-carboxylic acid Chemical compound C1CC2(C(O)=O)CCC1(C)C=C2 AMMPLVWPWSYRDR-UHFFFAOYSA-N 0.000 description 1
- DZCBKUAAGVVLOX-UHFFFAOYSA-N 1-morpholin-4-ylethanol Chemical class CC(O)N1CCOCC1 DZCBKUAAGVVLOX-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- 125000005955 1H-indazolyl group Chemical group 0.000 description 1
- KJUGUADJHNHALS-UHFFFAOYSA-N 1H-tetrazole Substances C=1N=NNN=1 KJUGUADJHNHALS-UHFFFAOYSA-N 0.000 description 1
- KYNNBXCGXUOREX-UHFFFAOYSA-N 2-(3-bromophenyl)acetic acid Chemical compound OC(=O)CC1=CC=CC(Br)=C1 KYNNBXCGXUOREX-UHFFFAOYSA-N 0.000 description 1
- ZBARBHKSSXDLMK-UHFFFAOYSA-N 2-(4-bromophenyl)acetamide Chemical compound NC(=O)CC1=CC=C(Br)C=C1 ZBARBHKSSXDLMK-UHFFFAOYSA-N 0.000 description 1
- QHTUMQYGZQYEOZ-UHFFFAOYSA-N 2-(4-methylpiperazin-1-yl)ethanol Chemical compound CN1CCN(CCO)CC1 QHTUMQYGZQYEOZ-UHFFFAOYSA-N 0.000 description 1
- OWOOSADJVKQGQA-UHFFFAOYSA-N 2-(6-phenylpyridin-3-yl)acetic acid Chemical compound N1=CC(CC(=O)O)=CC=C1C1=CC=CC=C1 OWOOSADJVKQGQA-UHFFFAOYSA-N 0.000 description 1
- HUHXLHLWASNVDB-UHFFFAOYSA-N 2-(oxan-2-yloxy)oxane Chemical class O1CCCCC1OC1OCCCC1 HUHXLHLWASNVDB-UHFFFAOYSA-N 0.000 description 1
- BDJRJUAVACSDMO-UHFFFAOYSA-N 2-[4-(2-fluorophenyl)phenyl]acetamide Chemical compound C1=CC(CC(=O)N)=CC=C1C1=CC=CC=C1F BDJRJUAVACSDMO-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- UCTPBVNGTSRBFG-UHFFFAOYSA-N 2-[4-(3-fluorophenyl)phenyl]acetic acid Chemical compound C1=CC(CC(=O)O)=CC=C1C1=CC=CC(F)=C1 UCTPBVNGTSRBFG-UHFFFAOYSA-N 0.000 description 1
- VEMGXBQLOMZPCN-UHFFFAOYSA-N 2-[6-(2-ethoxyphenyl)pyridin-3-yl]-n-[(3-fluorophenyl)methyl]acetamide Chemical compound CCOC1=CC=CC=C1C(N=C1)=CC=C1CC(=O)NCC1=CC=CC(F)=C1 VEMGXBQLOMZPCN-UHFFFAOYSA-N 0.000 description 1
- LCXRCYMEQJCOLG-UHFFFAOYSA-N 2-[6-(3-chlorophenyl)pyridin-3-yl]acetic acid Chemical compound N1=CC(CC(=O)O)=CC=C1C1=CC=CC(Cl)=C1 LCXRCYMEQJCOLG-UHFFFAOYSA-N 0.000 description 1
- QSNKKYSJGNDQFA-UHFFFAOYSA-N 2-[6-(3-ethoxyphenyl)pyridin-3-yl]-n-[(3-fluorophenyl)methyl]acetamide Chemical compound CCOC1=CC=CC(C=2N=CC(CC(=O)NCC=3C=C(F)C=CC=3)=CC=2)=C1 QSNKKYSJGNDQFA-UHFFFAOYSA-N 0.000 description 1
- 125000005273 2-acetoxybenzoic acid group Chemical group 0.000 description 1
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 1
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical compound CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 1
- MLMQPDHYNJCQAO-UHFFFAOYSA-N 3,3-dimethylbutyric acid Chemical compound CC(C)(C)CC(O)=O MLMQPDHYNJCQAO-UHFFFAOYSA-N 0.000 description 1
- XLZYKTYMLBOINK-UHFFFAOYSA-N 3-(4-hydroxybenzoyl)benzoic acid Chemical compound OC(=O)C1=CC=CC(C(=O)C=2C=CC(O)=CC=2)=C1 XLZYKTYMLBOINK-UHFFFAOYSA-N 0.000 description 1
- ZRPLANDPDWYOMZ-UHFFFAOYSA-N 3-cyclopentylpropionic acid Chemical compound OC(=O)CCC1CCCC1 ZRPLANDPDWYOMZ-UHFFFAOYSA-N 0.000 description 1
- QZVQQUVWFIZUBQ-UHFFFAOYSA-N 3-fluoroaniline Chemical compound NC1=CC=CC(F)=C1 QZVQQUVWFIZUBQ-UHFFFAOYSA-N 0.000 description 1
- SGHBRHKBCLLVCI-UHFFFAOYSA-N 3-hydroxybenzonitrile Chemical compound OC1=CC=CC(C#N)=C1 SGHBRHKBCLLVCI-UHFFFAOYSA-N 0.000 description 1
- PEPBFCOIJRULGJ-UHFFFAOYSA-N 3h-1,2,3-benzodioxazole Chemical compound C1=CC=C2NOOC2=C1 PEPBFCOIJRULGJ-UHFFFAOYSA-N 0.000 description 1
- WDBQJSCPCGTAFG-QHCPKHFHSA-N 4,4-difluoro-N-[(1S)-3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-pyridin-3-ylpropyl]cyclohexane-1-carboxamide Chemical compound FC1(CCC(CC1)C(=O)N[C@@H](CCN1CCC(CC1)N1C(=NN=C1C)C(C)C)C=1C=NC=CC=1)F WDBQJSCPCGTAFG-QHCPKHFHSA-N 0.000 description 1
- BWGRDBSNKQABCB-UHFFFAOYSA-N 4,4-difluoro-N-[3-[3-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)-8-azabicyclo[3.2.1]octan-8-yl]-1-thiophen-2-ylpropyl]cyclohexane-1-carboxamide Chemical compound CC(C)C1=NN=C(C)N1C1CC2CCC(C1)N2CCC(NC(=O)C1CCC(F)(F)CC1)C1=CC=CS1 BWGRDBSNKQABCB-UHFFFAOYSA-N 0.000 description 1
- BICZJRAGTCRORZ-UHFFFAOYSA-N 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenol Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(O)C=C1 BICZJRAGTCRORZ-UHFFFAOYSA-N 0.000 description 1
- SDGPYVPSIUTXDZ-UHFFFAOYSA-N 4-[5-[2-[(3-fluorophenyl)methylamino]-2-oxoethyl]pyridin-2-yl]benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1C(N=C1)=CC=C1CC(=O)NCC1=CC=CC(F)=C1 SDGPYVPSIUTXDZ-UHFFFAOYSA-N 0.000 description 1
- XMHNLZXYPAULDF-UHFFFAOYSA-N 4-bromo-1-(bromomethyl)-2-fluorobenzene Chemical compound FC1=CC(Br)=CC=C1CBr XMHNLZXYPAULDF-UHFFFAOYSA-N 0.000 description 1
- HTRNHWBOBYFTQF-UHFFFAOYSA-N 4-bromo-2-fluoro-1-phenylbenzene Chemical group FC1=CC(Br)=CC=C1C1=CC=CC=C1 HTRNHWBOBYFTQF-UHFFFAOYSA-N 0.000 description 1
- RMYOGXPGIDWJLU-UHFFFAOYSA-N 4-bromo-3-fluorobenzoic acid Chemical compound OC(=O)C1=CC=C(Br)C(F)=C1 RMYOGXPGIDWJLU-UHFFFAOYSA-N 0.000 description 1
- SIAVMDKGVRXFAX-UHFFFAOYSA-N 4-carboxyphenylboronic acid Chemical compound OB(O)C1=CC=C(C(O)=O)C=C1 SIAVMDKGVRXFAX-UHFFFAOYSA-N 0.000 description 1
- RJWBTWIBUIGANW-UHFFFAOYSA-N 4-chlorobenzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=C(Cl)C=C1 RJWBTWIBUIGANW-UHFFFAOYSA-N 0.000 description 1
- HVCNXQOWACZAFN-UHFFFAOYSA-N 4-ethylmorpholine Chemical compound CCN1CCOCC1 HVCNXQOWACZAFN-UHFFFAOYSA-N 0.000 description 1
- 125000002471 4H-quinolizinyl group Chemical group C=1(C=CCN2C=CC=CC12)* 0.000 description 1
- AXWOVMIUFMFMQC-UHFFFAOYSA-N 5-(5-bromo-1h-pyridin-2-ylidene)-2,2-dimethyl-1,3-dioxane-4,6-dione Chemical compound O=C1OC(C)(C)OC(=O)C1=C1C=CC(Br)=CN1 AXWOVMIUFMFMQC-UHFFFAOYSA-N 0.000 description 1
- WDYVUKGVKRZQNM-UHFFFAOYSA-N 6-phosphonohexylphosphonic acid Chemical compound OP(O)(=O)CCCCCCP(O)(O)=O WDYVUKGVKRZQNM-UHFFFAOYSA-N 0.000 description 1
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 1
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 239000002028 Biomass Substances 0.000 description 1
- 241000167854 Bourreria succulenta Species 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- DCERHCFNWRGHLK-UHFFFAOYSA-N C[Si](C)C Chemical compound C[Si](C)C DCERHCFNWRGHLK-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- WWZKQHOCKIZLMA-UHFFFAOYSA-N Caprylic acid Natural products CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- 229940126657 Compound 17 Drugs 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- KDXKERNSBIXSRK-RXMQYKEDSA-N D-lysine Chemical compound NCCCC[C@@H](N)C(O)=O KDXKERNSBIXSRK-RXMQYKEDSA-N 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- 206010052804 Drug tolerance Diseases 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 241000792859 Enema Species 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Substances 0.000 description 1
- 239000001116 FEMA 4028 Substances 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 102000009465 Growth Factor Receptors Human genes 0.000 description 1
- 108010009202 Growth Factor Receptors Proteins 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 208000002250 Hematologic Neoplasms Diseases 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- 125000002842 L-seryl group Chemical group O=C([*])[C@](N([H])[H])([H])C([H])([H])O[H] 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 1
- 241001024304 Mino Species 0.000 description 1
- TXXHDPDFNKHHGW-CCAGOZQPSA-N Muconic acid Natural products OC(=O)\C=C/C=C\C(O)=O TXXHDPDFNKHHGW-CCAGOZQPSA-N 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- NUGPIZCTELGDOS-QHCPKHFHSA-N N-[(1S)-3-[4-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)piperidin-1-yl]-1-pyridin-3-ylpropyl]cyclopentanecarboxamide Chemical compound C(C)(C)C1=NN=C(N1C1CCN(CC1)CC[C@@H](C=1C=NC=CC=1)NC(=O)C1CCCC1)C NUGPIZCTELGDOS-QHCPKHFHSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- 238000012565 NMR experiment Methods 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical group C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Chemical group C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 1
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical class OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 1
- 241001085205 Prenanthella exigua Species 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical group C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 102000014400 SH2 domains Human genes 0.000 description 1
- 108050003452 SH2 domains Proteins 0.000 description 1
- 239000002262 Schiff base Substances 0.000 description 1
- 150000004753 Schiff bases Chemical class 0.000 description 1
- 244000000231 Sesamum indicum Species 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical group C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 206010052428 Wound Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 1
- CKUAXEQHGKSLHN-UHFFFAOYSA-N [C].[N] Chemical group [C].[N] CKUAXEQHGKSLHN-UHFFFAOYSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 150000001241 acetals Chemical class 0.000 description 1
- 159000000021 acetate salts Chemical class 0.000 description 1
- IAWNZDONUUMBTJ-UHFFFAOYSA-N acetyl chloride;1,1'-biphenyl Chemical compound CC(Cl)=O.C1=CC=CC=C1C1=CC=CC=C1 IAWNZDONUUMBTJ-UHFFFAOYSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 125000003172 aldehyde group Chemical group 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 150000007824 aliphatic compounds Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 125000000278 alkyl amino alkyl group Chemical group 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- 238000010640 amide synthesis reaction Methods 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000003527 anti-angiogenesis Effects 0.000 description 1
- 230000000118 anti-neoplastic effect Effects 0.000 description 1
- 239000002216 antistatic agent Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 1
- 125000003435 aroyl group Chemical group 0.000 description 1
- 125000003710 aryl alkyl group Chemical group 0.000 description 1
- 238000003149 assay kit Methods 0.000 description 1
- 238000000668 atmospheric pressure chemical ionisation mass spectrometry Methods 0.000 description 1
- 125000004931 azocinyl group Chemical group N1=C(C=CC=CC=C1)* 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 1
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- GONOPSZTUGRENK-UHFFFAOYSA-N benzyl(trichloro)silane Chemical compound Cl[Si](Cl)(Cl)CC1=CC=CC=C1 GONOPSZTUGRENK-UHFFFAOYSA-N 0.000 description 1
- 150000003939 benzylamines Chemical class 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 235000011175 beta-cyclodextrine Nutrition 0.000 description 1
- 125000002618 bicyclic heterocycle group Chemical group 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000004744 butyloxycarbonyl group Chemical group 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 150000004657 carbamic acid derivatives Chemical class 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical class OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000006727 cell loss Effects 0.000 description 1
- 230000010307 cell transformation Effects 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 235000019693 cherries Nutrition 0.000 description 1
- 239000007958 cherry flavor Substances 0.000 description 1
- 125000003016 chromanyl group Chemical group O1C(CCC2=CC=CC=C12)* 0.000 description 1
- 125000004230 chromenyl group Chemical group O1C(C=CC2=CC=CC=C12)* 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 229940125797 compound 12 Drugs 0.000 description 1
- 229940126142 compound 16 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940125810 compound 20 Drugs 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 229940125851 compound 27 Drugs 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- WZHCOOQXZCIUNC-UHFFFAOYSA-N cyclandelate Chemical compound C1C(C)(C)CC(C)CC1OC(=O)C(O)C1=CC=CC=C1 WZHCOOQXZCIUNC-UHFFFAOYSA-N 0.000 description 1
- 125000001047 cyclobutenyl group Chemical group C1(=CCC1)* 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- XSYZCZPCBXYQTE-UHFFFAOYSA-N cyclodecylcyclodecane Chemical compound C1CCCCCCCCC1C1CCCCCCCCC1 XSYZCZPCBXYQTE-UHFFFAOYSA-N 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000298 cyclopropenyl group Chemical group [H]C1=C([H])C1([H])* 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 125000004856 decahydroquinolinyl group Chemical group N1(CCCC2CCCCC12)* 0.000 description 1
- 238000010908 decantation Methods 0.000 description 1
- 125000003493 decenyl group Chemical group [H]C([*])=C([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 125000005070 decynyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C#C* 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 125000002720 diazolyl group Chemical group 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- DZNBZPKZOBDXEL-UHFFFAOYSA-N dicyclohexyl-(2-dicyclohexylphosphanylphenyl)phosphane Chemical compound C1CCCCC1P(C=1C(=CC=CC=1)P(C1CCCCC1)C1CCCCC1)C1CCCCC1 DZNBZPKZOBDXEL-UHFFFAOYSA-N 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 150000004683 dihydrates Chemical class 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- VDCSGNNYCFPWFK-UHFFFAOYSA-N diphenylsilane Chemical compound C=1C=CC=CC=1[SiH2]C1=CC=CC=C1 VDCSGNNYCFPWFK-UHFFFAOYSA-N 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000006196 drop Substances 0.000 description 1
- 238000009510 drug design Methods 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 150000002081 enamines Chemical class 0.000 description 1
- 239000008393 encapsulating agent Substances 0.000 description 1
- 239000007920 enema Substances 0.000 description 1
- 229940079360 enema for constipation Drugs 0.000 description 1
- 150000002085 enols Chemical class 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000010685 fatty oil Substances 0.000 description 1
- 229960000192 felbinac Drugs 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000013100 final test Methods 0.000 description 1
- 238000009093 first-line therapy Methods 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 125000005519 fluorenylmethyloxycarbonyl group Chemical group 0.000 description 1
- 125000004785 fluoromethoxy group Chemical group [H]C([H])(F)O* 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- XZMMPTVWHALBLT-UHFFFAOYSA-N formaldehyde;rhodium;triphenylphosphane Chemical compound [Rh].O=C.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 XZMMPTVWHALBLT-UHFFFAOYSA-N 0.000 description 1
- 150000004675 formic acid derivatives Chemical class 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 230000008570 general process Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 201000009277 hairy cell leukemia Diseases 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 150000002390 heteroarenes Chemical class 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 125000005980 hexynyl group Chemical group 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- 150000004680 hydrogen peroxides Chemical class 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- DOUHZFSGSXMPIE-UHFFFAOYSA-N hydroxidooxidosulfur(.) Chemical compound [O]SO DOUHZFSGSXMPIE-UHFFFAOYSA-N 0.000 description 1
- 125000002632 imidazolidinyl group Chemical group 0.000 description 1
- 125000002636 imidazolinyl group Chemical group 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- LPAGFVYQRIESJQ-UHFFFAOYSA-N indoline Chemical compound C1=CC=C2NCCC2=C1 LPAGFVYQRIESJQ-UHFFFAOYSA-N 0.000 description 1
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 1
- HOBCFUWDNJPFHB-UHFFFAOYSA-N indolizine Chemical compound C1=CC=CN2C=CC=C21 HOBCFUWDNJPFHB-UHFFFAOYSA-N 0.000 description 1
- 125000003406 indolizinyl group Chemical group C=1(C=CN2C=CC=CC12)* 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 125000004936 isatinoyl group Chemical group N1(C(=O)C(=O)C2=CC=CC=C12)C(=O)* 0.000 description 1
- 125000001977 isobenzofuranyl group Chemical group C=1(OC=C2C=CC=CC12)* 0.000 description 1
- 125000005438 isoindazolyl group Chemical group 0.000 description 1
- 125000004594 isoindolinyl group Chemical group C1(NCC2=CC=CC=C12)* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- ZLTPDFXIESTBQG-UHFFFAOYSA-N isothiazole Chemical group C=1C=NSC=1 ZLTPDFXIESTBQG-UHFFFAOYSA-N 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical group C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 210000002510 keratinocyte Anatomy 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- XMGQYMWWDOXHJM-UHFFFAOYSA-N limonene Chemical compound CC(=C)C1CCC(C)=CC1 XMGQYMWWDOXHJM-UHFFFAOYSA-N 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 230000000527 lymphocytic effect Effects 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 238000001819 mass spectrum Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 102000006240 membrane receptors Human genes 0.000 description 1
- 108020004084 membrane receptors Proteins 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 1
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 150000004682 monohydrates Chemical class 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- IWPLYOTXNKANGH-UHFFFAOYSA-N n-(3-fluorophenyl)-2-(4-phenylphenyl)acetamide Chemical compound FC1=CC=CC(NC(=O)CC=2C=CC(=CC=2)C=2C=CC=CC=2)=C1 IWPLYOTXNKANGH-UHFFFAOYSA-N 0.000 description 1
- ZTUNDZFMZYXOCZ-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-(4-phenylphenyl)acetamide Chemical compound FC1=CC=CC(CNC(=O)CC=2C=CC(=CC=2)C=2C=CC=CC=2)=C1 ZTUNDZFMZYXOCZ-UHFFFAOYSA-N 0.000 description 1
- GOYCNYYYLWWESL-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-2-[6-(4-methylsulfonylphenyl)pyridin-3-yl]acetamide Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C(N=C1)=CC=C1CC(=O)NCC1=CC=CC(F)=C1 GOYCNYYYLWWESL-UHFFFAOYSA-N 0.000 description 1
- AIJPCYJYHZPVIP-UHFFFAOYSA-N n-[(3-fluorophenyl)methyl]-n-methyl-2-(4-phenylphenyl)acetamide Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1CC(=O)N(C)CC1=CC=CC(F)=C1 AIJPCYJYHZPVIP-UHFFFAOYSA-N 0.000 description 1
- JTTUNBLUEYWTRZ-UHFFFAOYSA-N n-[(3-hydroxyphenyl)methyl]-2-(4-phenylphenyl)acetamide Chemical compound OC1=CC=CC(CNC(=O)CC=2C=CC(=CC=2)C=2C=CC=CC=2)=C1 JTTUNBLUEYWTRZ-UHFFFAOYSA-N 0.000 description 1
- NPCBEBLCGUHYKZ-UHFFFAOYSA-N n-[(3-phenylmethoxyphenyl)methyl]-2-(4-phenylphenyl)acetamide Chemical compound C=1C=CC(OCC=2C=CC=CC=2)=CC=1CNC(=O)CC(C=C1)=CC=C1C1=CC=CC=C1 NPCBEBLCGUHYKZ-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N n-hexanoic acid Natural products CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 239000007923 nasal drop Substances 0.000 description 1
- 229940100662 nasal drops Drugs 0.000 description 1
- 239000006199 nebulizer Substances 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 230000017095 negative regulation of cell growth Effects 0.000 description 1
- 238000013546 non-drug therapy Methods 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 125000005187 nonenyl group Chemical group C(=CCCCCCCC)* 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 125000004365 octenyl group Chemical group C(=CCCCCCC)* 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 231100000590 oncogenic Toxicity 0.000 description 1
- 230000002246 oncogenic effect Effects 0.000 description 1
- 239000007968 orange flavor Substances 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 230000002611 ovarian Effects 0.000 description 1
- 125000000160 oxazolidinyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 125000004095 oxindolyl group Chemical group N1(C(CC2=CC=CC=C12)=O)* 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 125000004115 pentoxy group Chemical group [*]OC([H])([H])C([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000001148 pentyloxycarbonyl group Chemical group 0.000 description 1
- 125000005981 pentynyl group Chemical group 0.000 description 1
- 150000002978 peroxides Chemical class 0.000 description 1
- 239000008249 pharmaceutical aerosol Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 125000004934 phenanthridinyl group Chemical group C1(=CC=CC2=NC=C3C=CC=CC3=C12)* 0.000 description 1
- 125000004625 phenanthrolinyl group Chemical group N1=C(C=CC2=CC=C3C=CC=NC3=C12)* 0.000 description 1
- 125000001791 phenazinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3N=C12)* 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 1
- UYMQWGLCXYHTES-UHFFFAOYSA-N phenyl(1h-pyrazol-5-yl)methanone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=NN1 UYMQWGLCXYHTES-UHFFFAOYSA-N 0.000 description 1
- WLJVXDMOQOGPHL-UHFFFAOYSA-N phenylacetic acid Chemical compound OC(=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-UHFFFAOYSA-N 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- DHRLEVQXOMLTIM-UHFFFAOYSA-N phosphoric acid;trioxomolybdenum Chemical compound O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.OP(O)(O)=O DHRLEVQXOMLTIM-UHFFFAOYSA-N 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 125000004482 piperidin-4-yl group Chemical group N1CCC(CC1)* 0.000 description 1
- 125000003386 piperidinyl group Chemical group 0.000 description 1
- 125000004928 piperidonyl group Chemical group 0.000 description 1
- 229960005235 piperonyl butoxide Drugs 0.000 description 1
- 125000004591 piperonyl group Chemical group C(C1=CC=2OCOC2C=C1)* 0.000 description 1
- FFNMBRCFFADNAO-UHFFFAOYSA-N pirenzepine hydrochloride Chemical compound [H+].[H+].[Cl-].[Cl-].C1CN(C)CCN1CC(=O)N1C2=NC=CC=C2NC(=O)C2=CC=CC=C21 FFNMBRCFFADNAO-UHFFFAOYSA-N 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 150000004804 polysaccharides Chemical class 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 125000004742 propyloxycarbonyl group Chemical group 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 125000001042 pteridinyl group Chemical group N1=C(N=CC2=NC=CN=C12)* 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 1
- 125000002755 pyrazolinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical group C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000001422 pyrrolinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 229960001404 quinidine Drugs 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 125000004621 quinuclidinyl group Chemical group N12C(CC(CC1)CC2)* 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 238000007127 saponification reaction Methods 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000009094 second-line therapy Methods 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 238000009097 single-agent therapy Methods 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 229940054269 sodium pyruvate Drugs 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 238000009331 sowing Methods 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000009987 spinning Methods 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 125000005017 substituted alkenyl group Chemical group 0.000 description 1
- 125000005415 substituted alkoxy group Chemical group 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 125000004426 substituted alkynyl group Chemical group 0.000 description 1
- 125000005346 substituted cycloalkyl group Chemical group 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- IIACRCGMVDHOTQ-UHFFFAOYSA-M sulfamate Chemical compound NS([O-])(=O)=O IIACRCGMVDHOTQ-UHFFFAOYSA-M 0.000 description 1
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 1
- 150000003871 sulfonates Chemical class 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 239000011885 synergistic combination Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- ILMRJRBKQSSXGY-UHFFFAOYSA-N tert-butyl(dimethyl)silicon Chemical group C[Si](C)C(C)(C)C ILMRJRBKQSSXGY-UHFFFAOYSA-N 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000001712 tetrahydronaphthyl group Chemical group C1(CCCC2=CC=CC=C12)* 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- DLFVBJFMPXGRIB-UHFFFAOYSA-N thioacetamide Natural products CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 1
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 description 1
- 125000005300 thiocarboxy group Chemical group C(=S)(O)* 0.000 description 1
- 229930192474 thiophene Chemical group 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical compound [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 1
- 238000009095 third-line therapy Methods 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- HUNGUWOZPQBXGX-UHFFFAOYSA-N tirbanibulin Chemical compound C=1C=CC=CC=1CNC(=O)CC(N=C1)=CC=C1C(C=C1)=CC=C1OCCN1CCOCC1 HUNGUWOZPQBXGX-UHFFFAOYSA-N 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 125000002088 tosyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])S(*)(=O)=O 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 150000003852 triazoles Chemical group 0.000 description 1
- 125000004784 trichloromethoxy group Chemical group ClC(O*)(Cl)Cl 0.000 description 1
- 125000000169 tricyclic heterocycle group Chemical group 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 1
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 229960000281 trometamol Drugs 0.000 description 1
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 description 1
- 239000005483 tyrosine kinase inhibitor Substances 0.000 description 1
- 150000004917 tyrosine kinase inhibitor derivatives Chemical class 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 238000003828 vacuum filtration Methods 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- 125000001834 xanthenyl group Chemical group C1=CC=CC=2OC3=CC=CC=C3C(C12)* 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4418—Non condensed pyridines; Hydrogenated derivatives thereof having a carbocyclic group directly attached to the heterocyclic ring, e.g. cyproheptadine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4425—Pyridinium derivatives, e.g. pralidoxime, pyridostigmine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4545—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring hetero atom, e.g. pipamperone, anabasine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/01—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C233/12—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by halogen atoms or by nitro or nitroso groups
- C07C233/13—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by halogen atoms or by nitro or nitroso groups with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/01—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C233/16—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by singly-bound oxygen atoms
- C07C233/17—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by singly-bound oxygen atoms with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom
- C07C233/22—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by singly-bound oxygen atoms with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom having the carbon atom of the carboxamide group bound to an acyclic carbon atom of a carbon skeleton containing six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/24—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D213/54—Radicals substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D213/56—Amides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/61—Halogen atoms or nitro radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/62—Oxygen or sulfur atoms
- C07D213/63—One oxygen atom
- C07D213/64—One oxygen atom attached in position 2 or 6
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/72—Nitrogen atoms
- C07D213/74—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/89—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members with hetero atoms directly attached to the ring nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/26—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/30—Halogen atoms or nitro radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/34—One oxygen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Dermatology (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Endocrinology (AREA)
- Obesity (AREA)
- Tropical Medicine & Parasitology (AREA)
- Ophthalmology & Optometry (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Emergency Medicine (AREA)
- Virology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Pyridine Compounds (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
COMPOSIÇÕES E USOS DE COMPOSTOS PARA A PREPARAÇÃO DE MEDICAMENTOS PARA TRATAMENTO DE DISTÚRBIOS DE PROLIFERAÇÃO CELULAR A presente invenção refere-se a composto e usos de compostos revelados para a preparação de medicamentos para o tratamento de distúrbios de proliferação celular.
Description
[001]Com mais de 53.000 mortes nos Estados Unidos anualmente, o câncer é a segunda causa principal de morte depois da doença cardíaca (UBS Warburg “Di- sease Dynamics: The Cancer Market”, 8 de novembro de 2000). A cirurgia e a radio- terapia podem ser curativas se a doença foi constatada cedo, mas as terapias com drogas atuais para a doença metastática são principalmente paliativas e raramente oferecem uma cura a longo prazo. Mesmo com as novas quimioterapias que entram no mercado, a melhora na sobrevivência de pacientes é medida em meses e não em anos, e continua a haver a necessidade de novas drogas eficazes tanto em combina- ção com agentes existentes como terapia de primeira linha, e como terapias de se- gunda e terceira linhas no tratamento de tumores resistentes.
[002]Continua a haver a necessidade na técnica de tratamentos melhorados para o distúrbio de proliferação celular e câncer.
[003]A invenção se refere a compostos e métodos para uso dos compostos para o tratamento de distúrbios de proliferação celular.
[004]Os compostos da presente invenção são úteis como agentes farmacêu- ticos. os compostos podem ser úteis, por exemplo, como agentes antiproliferantes, para o tratamento de mamíferos, tal como para o tratamento de seres humanos e animais. Os compostos podem ser usados sem limitação como agentes anticancerí- genos, anti-angiogênicos, antimetastáticos, antimicrobianos, antibacterianos, antifún- gicos, antiparasíticos e/ou antivirais, por exemplo. Os compostos podem ser úteis, por exemplo, no tratamento de câncer do pulmão. Os compostos da presente invenção são também úteis para o tratamento de câncer do cólon. Os compostos da presente invenção são também úteis, por exemplo, no tratamento do câncer da mama.
[005]Os compostos da invenção são úteis no tratamento de doenças e distúr- bios que são modulados por inibição de tirosina quinase. Os compostos da invenção são úteis, por exemplo, no tratamento de distúrbios e doenças que são modulados por Src quinase. Os compostos da invenção podem também ser úteis no tratamento de doenças e distúrbios que são modulados por quinase de adesão focal (FAK).
[006]Os compostos da invenção incluem compostos da Fórmula I, e sais, sol- vatos, hidratos e promedicamentos seus: Fórmula I em que: T está ausente (isto é, os anéis são conectados por uma ligação), CR12R13, C(O), O, S, S(O), S(O)2, NR14, C(R15R16)C(R17R18), CH2O, ou OCH2; XYé CZ, CY, N, ou N-O; Xz é CZ, CY, N, ou N-O; pelo menos um de XY e Xz é CZ; Y é selecionado de hidrogênio, hidroxila, halogênio, alquila (C1, C2, C3, C4, C5, ou C6) inferior, alcóxi C1, C2, C3, C4, C5, ou C6, O-alquila(C1, C2, C3, C4, C5, ou C6) inferior-arila e O-benzila; Xa é CRa, N, ou N-O; Xb é CRb, N, ou N-O; Xc é CRc, N, ou N-O; Xd é CRd, N, ou N-O; Xe é CRe, N, ou N-O; Ra, Rb, Rc, Rd, Re, R4, R5 e R6 são independentemente, hidrogênio, hidroxila, halogênio, alquila C1, C2, C3, C4, C5, ou C6, alcóxi C1, C2, C3, C4, C5, ou C6, O-al- quila(C1, C2, C3, C4, C5, ou C6) inferior-arila, O-benzila, alquil (C1, C2, C3, C4, C5, ou C6)-OH, alquil(C1, C2, C3, C4, C5, ou C6)-O-alquila(C1, C2, C3, C4, C5, ou C6) inferior, COOH, COO-alquil(C1, C2, C3, C4, C5, ou C6) inferior, SO2H, SO2-alquila(C1, C2, C3, C4, C5, ou C6), ou em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2 - ou - OCH2CH2CH2-; R12, R13, R14, R15, R16, R17 e R18 são, independentemente H ou alquila C1, C2, C3, C4, C5, ou C6; Z é: (CR1)n-C(O)-NR2(CR3)m-Ar, em que Ar é um grupo arila substituído ou não substituído ou heteroarila contendo nitrogênio, tal como benzeno, piridina ou piri- midina. Z é, por exemplo: em que R1, R2 e R3 são independentemente H ou alquila C1, C2, C3, C4, C5, ou C6; n e m são, independentemente, 0, 1 ou 2; R7, R8, R9, R10 e R11 são, independentemente, hidrogênio, hidroxila, halogê- nio, alquila C1, C2, C3, C4, C5, ou C6, alcóxi C1, C2, C3, C4, C5, ou C6, O-alquil(C1, C2, C3, C4, C5, ou C6) inferior-arila, O-benzila, OH-alquila(C1, C2, C3, C4, C5, ou C6), alquil(C1, C2, C3, C4, C5, ou C6)-O-alquila(C1, C2, C3, C4, C5, ou C6, que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -OCH2-, -OCH2CH2-, ou - OCH2CH2CH2-.
[008]Determinados compostos da invenção são selecionados dos Compostos 1-136 e 137. O composto da invenção é, por exemplo, Composto 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, ou 137.
[009]Os compostos da invenção incluem Compostos 33, 38, 40, 76, 133, 134, 136 e 137.
[010]Em determinados Compostos da Fórmula I, pelo menos um de Xa, Xb, Xc, Xd e Xe é N.
[011]No composto da Fórmula I, por exemplo, Xa é N e cada um de Xb, Xc, Xd e Xe é CR.
[012]Em determinados compostos da Fórmula I, XY é CY e Xz é CZ.
[013]Em determinados compostos da Fórmula I, por exemplo, Y é hidrogênio.
[014]Em determinados compostos da Fórmula I, Rb é alcóxi C1, C2, C3, C4, C5, ou C6. Rb, por exemplo, é metóxi ou etóxi. Em determinados compostos da Fórmula I, Rb é hidrogênio. Em outros compostos da Fórmula I, Rb é selecionado de F, Cl, Br, e I.
[015]Em outros compostos da Fórmula I, Rb é em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-. V é uma ligação, por exemplo. Em determinados compostos da Fórmula I, W é hidrogênio. Em outros compostos da Fórmula I, W é alquila C1, C2, C3, C4, C5, ou C6.
[016]Em determinados compostos da Fórmula I, Rc é alcóxi C1, C2, C3, C4, C5, ou C6. Rc, por exemplo, é metóxi ou etóxi. Em outros compostos da Fórmula I, Rc é hidrogênio, F, Cl, Br ou I.
[017]Em outros compostos da Fórmula I, Rc é em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-.
[018]V é, por exemplo, uma ligação. Em determinados compostos da Fórmula I, W é hidrogênio. Em outros compostos da Fórmula I, W é alquila C1, C2, C3, C4, C5, ou C6.
[019]Em determinados compostos da Fórmula I, Rd é alcóxi C1, C2, C3, C4, C5, ou C6. Rd, por exemplo, é metóxi ou etóxi. Em outros compostos da Fórmula I, Rd é hidrogênio, F, Cl, Br ou I.
[020]Em outros compostos da Fórmula I, Rd é em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-.
[021]V, por exemplo, é uma ligação. Em determinados compostos da Fórmula I, W é hidrogênio. Em outros compostos da Fórmula I, W é alquila C1, C2, C3, C4, C5, ou C6.
[022]A invenção inclui um solvato de um composto de acordo com a Fórmula I.
[023]A invenção também inclui um hidrato de um composto de acordo com a Fórmula I.
[024]A invenção também inclui um sal de adição de ácido de um composto de acordo com a Fórmula I. Um sal cloridrato, por exemplo.
[025]A invenção também inclui um promedicamento de um composto de acordo com a Fórmula I.
[026]A invenção também inclui um sal farmaceuticamente aceitável de um composto da Fórmula I.
[027]A invenção também inclui uma composição de um composto de acordo com a Fórmula I e pelo menos um excipiente farmaceuticamente aceitável.
[028]A invenção se refere a um composto da Fórmula I, tendo uma estrutura de acordo com uma das Fórmulas II-XIII:
ou um sal, solvato, hidrato ou promedicamento seu, em que: Rb, R4, R5, R8 e R10 são, independentemente, hidrogênio, hidroxila, halogênio, alquila C1, C2, C3, C4, C5, ou C6, alcóxi C1, C2, C3, C4, C5, ou C6, O- alquil(C1, C2, C3, C4, C5, ou C6) inferior-arila, O-benzila, OH-alquila(C1, C2, C3, C4, C5, ou C6), al- quil(C1, C2, C3, C4, C5, ou C6)-O-alquila(C1, C2, C3, C4, C5, ou C6) inferior, COOH, COO- alquila C1, C2, C3, C4, C5, ou C6 inferior, SO2H, SO2-alquila(C1, C2, C3, C4, C5, ou C6) inferior, em que W é H ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-.
[029]No composto da Fórmula II-XIII, R8 é hidrogênio, F, Cl, Br ou I. R8, por exemplo, é F. Em determinados compostos R8 é H.
[030]Em determinados compostos da Fórmula II-XIII, Rb é alcóxi C1, C2, C3, C4, C5, ou C6. Rb, por exemplo, é metóxi ou etc.
[031]Em determinados compostos da Fórmula II-XIII, Rb é hidrogênio, Cl, Br ou I. Em outros compostos, no composto da Fórmula II-XIII, Rb é
[033]em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila, e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, - OCH2CH2- ou -OCH2CH2CH2-.
[034]Em determinados compostos da Fórmula II-XIII, R4 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br ou I. Em outros compostos, no composto da Fórmula II-XIII, R4 é
[035] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-.
[036]Em determinados compostos da Fórmula II-XIII, R5 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br, ou I. Em outros compostos, no composto da Fórmula II-XIII, R5 é
[037] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-.
[038]Em determinados compostos da Fórmula II-XIII, R10 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br ou I. R10, por exemplo, é metóxi, etóxi ou isobutóxi.
[039]Em outros compostos da Fórmula II-XIII, R10 é
[040]em que W é H, ou alquila Ci, C2, C3, C4, C5, ou Cβ, alquil(Ci, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-.
[04i]No composto da Fórmula II-XIII, por exemplo, W é hidrogênio, ou alquila Ci, C2, C3, C4, C5, ou Cβ.
[042]Determinados compostos da invenção incluem compostos de acordo com a Fórmula II.
[043]A invenção se refere a um solvato de um composto de acordo com uma das Fórmulas II-XIII. A invenção também se refere a um hidrato de um composto de acordo com uma das Fórmulas II-XIII.
[044]A invenção também se refere a um sal de adição de ácido de um com- posto de acordo com uma das Fórmulas II-XIII. Um sal cloridrato, por exemplo.
[045]Além disso, a invenção se refere a um promedicamento de um composto de acordo com uma das Fórmulas II-XIII.
[04β]A invenção também se refere a um sal farmaceuticamente aceitável de um composto de uma das Fórmulas II-XIII.
[047]A invenção inclui composições compreendendo um composto de acordo com uma das Fórmulas I-XIII e pelo menos um excipiente farmaceuticamente aceitá- vel.
[048]Determinados compostos da invenção são inibidores de quinase não competitiva por ATP.
[049]A invenção também inclui um método de prevenção ou tratamento de um distúrbio de proliferação celular por administração de uma composição farmacêutica que inclui um composto de acordo com uma das Fórmulas I-XIII, ou sal, solvato, hi- drato ou promedicamento seu, e pelo menos um excipiente farmaceuticamente acei- tável a um paciente que tenha necessidade dele.
[050]O distúrbio de proliferação celular é, por exemplo, pré-câncer ou câncer. O distúrbio de proliferação celular tratado ou prevenido pelos compostos da invenção pode ser um câncer, tal como, por exemplo, câncer do cólon ou câncer do pulmão.
[051]O distúrbio de proliferação celular tratado ou prevenido pelos compostos da invenção pode ser um distúrbio hiperproliferativo.
[052]O distúrbio de proliferação celular tratado ou prevenido pelos compostos da invenção pode ser psoríase.
[053]O tratamento ou prevenção do distúrbio proliferativo pode ocorrer por meio da inibição de uma tirosina quinase. A tirosina quinase pode ser, por exemplo, uma Src quinase ou quinase de adesão focal (FAK).
[054]A invenção se refere a um método de tratamento ou prevenção de uma doença ou distúrbio que é modulado por inibição de tirosina quinase por administração de uma composição farmacêutica que inclui um composto de acordo com a Fórmula I ou uma das Fórmulas II-XIII, ou um sal, solvato, hidrato ou promedicamento seu, e pelo menos um excipiente farmaceuticamente aceitável. A doença ou distúrbio que é modulada por inibição de tirosina quinase é, por exemplo, câncer, pré-câncer, um dis- túrbio hiperproliferativo ou uma infecção microbiana. O composto é, por exemplo, um composto de acordo com a Fórmula I ou II.
[055]A composição farmacêutica da invenção pode modular um trajeto da qui- nase. O trajeto de quinase, por exemplo, é um trajeto de Src quinase, ou um trajeto de quinase de adesão focal.
[056]A composição farmacêutica da invenção pode modular uma quinase di- retamente. A quinase é Src quinase, por exemplo, ou quinase de adesão focal.
[057]Determinadas composições farmacêuticas da invenção são inibidores de quinase não competitiva para ATP.
[058]Os compostos da invenção são também úteis para o tratamento ou pre- venção de uma infecção microbiana, tal como uma infecção bacteriana, fúngica, pa- rasítica ou viral.
[059]Determinadas composições farmacêuticas da invenção incluem um com- posto selecionado do Composto 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, e 137. A composição farmacêutica inclui, por exemplo, Composto 33, 38, 40, 76, 133, 134, 136 ou 137.
[060]Determinadas composições farmacêuticas da invenção incluem um com- posto selecionado dos compostos relacionados na Tabela 2.
[061]Um composto da invenção pode ser usado como um agente farmacêu- tico. Um composto da invenção é usado, por exemplo, como um agente antiprolifera- tivo, para o tratamento de seres humanos e/ou animais, tal como para o tratamento de seres humanos e/ou outros mamíferos. Os compostos podem ser usados sem li- mitação, como agentes anticancerígenos, anti-angiogênicos, antimicrobianos, anti- bacterianos, antifúngicos, antiparasíticos e/ou antivirais, por exemplo. Além disso, os compostos podem ser usados para outros distúrbios relacionados com a proliferação celular tais como retinopatia diabética, degeneração macular e psoríase. Agentes an- ticancerígenos incluem agentes antimetastáticos.
[062]O composto da invenção usado como um agente farmacêutico pode ser selecionado de Compostos 1-136 e 137. O composto da invenção usado como um agente farmacêutico é, por exemplo, Composto 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 61, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, ou 137. O composto da invenção usado como um agente farmacêutico é selecionado, por exemplo, de Compostos 33, 38, 40, 76, 133, 134, 136 e 137.
[063]Determinados agentes farmacêuticos incluem um composto selecionado dos compostos relacionados na Tabela 2.
[064]Em um aspecto da invenção, um composto da invenção, um composto de Fórmula I ou um das Fórmulas II-XII, por exemplo, é usado para tratar ou prevenir um distúrbio de proliferação celular em um paciente. Em um aspecto da modalidade, o distúrbio de proliferação celular é pré-câncer ou câncer. Em um outro aspecto da modalidade, o distúrbio de proliferação celular é um distúrbio hiperproliferativo. Em uma outra modalidade, a prevenção ou tratamento do distúrbio de proliferação celular, câncer ou distúrbio hiperproliferativo ocorre por meio da inibição de uma quinase. Em uma outra modalidade, a prevenção ou o tratamento do distúrbio de proliferação ce- lular, câncer ou distúrbio hiperproliferativo ocorre por meio da inibição de Src quinase ou de quinase de adesão focal (FAK). Em uma outra modalidade, o paciente é um mamífero. É preferível que o paciente seja um ser humano.
[065]A invenção é também voltada a um método de tratamento ou prevenção de câncer ou de um distúrbio de proliferação em um paciente, compreendendo a ad- ministração de uma quantidade efetiva de um composto da invenção, de um composto da Fórmula I ou de um das Fórmulas II-XIII, por exemplo. O composto da invenção pode ser, por exemplo, um inibidor de quinase. O composto da invenção pode ser um inibidor de quinase não competitivo para ATP. O composto da invenção pode inibir a quinase diretamente, ou ele pode afetar o trajeto da quinase.
[066]A descrição acima apresenta de um modo um tanto geral as caracterís- ticas mais importantes da presente invenção a fim de que a descrição detalhada da mesma possa ser compreendida e para que as contribuições da presente invenção à técnica possam ser mais bem apreciadas. Outros objetivos e características da pre- sente invenção se tornarão aparentes com a leitura da descrição detalhada abaixo quando considerada em conjunto com os exemplos.
[067]Os detalhes de uma ou mais modalidades da invenção são apresentados na descrição apensa abaixo. Embora qualquer método e material semelhante ou equi- valente aos descritos nela possam ser usados na colocação em prática ou na testa- gem da presente invenção, serão agora descritos os métodos e materiais preferidos. Outras características, objetivos e vantagens da invenção se tornarão aparentes com a leitura da descrição. No relatório as formas no singular também incluem as formas no plural, a não ser que o contexto determine em contrário. A não ser que seja definido em contrário, todos os termos técnicos e científicos usados no presente documento terão o mesmo significado que é compreendido habitualmente pelos versados na téc- nica à qual a invenção pertence. Em caso de conflito, prevalecerá o presente relatório.
[068]A invenção se refere a compostos e métodos de uso dos compostos para o tratamento de distúrbios de proliferação celular.
[069]Os compostos da presente invenção são úteis como agentes farmacêu- ticos, especialmente como agentes antiproliferativos, para o tratamento de seres hu- manos e animais, especialmente para o tratamento de seres humanos e de outros mamíferos. Os compostos podem ser usados sem imitação como agentes anticance- rígenos, anti-angiogênese, antimetastáticos, antimicrobianos, antibacterianos, antifún- gicos, antiparasíticos e/ou antivirais. Os compostos podem ser usados para outros distúrbios relacionados com a proliferação celular tais como psoríase.
[070]Os compostos da presente invenção incluem compostos da Fórmula I e sais seus: Fórmula I e em que: T está ausente (isto é, os anéis são conectados por uma ligação), CR12R13, C(O), O, S, S(O), S(O)2, NR14, C(R15R16)C(R17R18), CH2O, ou OCH2; Xy é CZ, CY, N, ou N-O; Xz é CZ, CY, N, ou N-O; pelo menos um de Xy e Xz é CZ; Y é selecionado de hidrogênio, hidroxila, halogênio, alquila (C1, C2, C3, C4, C5, ou C6) inferior, alcóxi C1, C2, C3, C4, C5, ou C6, O-alquila(C1, C2, C3, C4, C5, ou C6) inferior-arila e O-benzila; Xa é CRa, N, ou N-O; Xb é CRb, N, ou N-O; Xc é CRc, N, ou N-O; Xd é CRd, N, ou N-O; Xe é CRe, N, ou N-O; Ra, Rb, Rc, Rd, Re, R4, R5 e R6 são independentemente, hidrogênio, hidroxila, halogênio, alquila C1, C2, C3, C4, C5, ou C6, alcóxi C1, C2, C3, C4, C5, ou C6, O-al- quila(C1, C2, C3, C4, C5, ou C6) inferior-arila, O-benzila, OH-alquila(C1, C2, C3, C4, C5, ou C6), alquil(C1, C2, C3, C4, C5, ou C6)-O-alquila(C1, C2, C3, C4, C5, ou C6) infe- rior, COOH, COO-alquil(C1, C2, C3, C4, C5, ou C6) inferior, SO2H, SO2-alquila(C1, C2, C3, C4, C5, ou C6), ou H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2 - ou - OCH2CH2CH2-; R12, R13, R14, R15, R16, R17 e R18 são, independentemente H ou alquila C1, C2, C3, C4, C5, ou C6;
[071]Z é: (CR1)n-C(O)-NR2(CR3)m-Ar, em que Ar é um grupo arila substituído ou não substituído ou heteroarila contendo nitrogênio, tal como benzeno, piridina ou pirimidina. Z é, por exemplo: em que R1, R2 e R3 são independentemente H ou alquila C1, C2, C3, C4, C5, ou C6; n e m são, independentemente, 0, 1 ou 2; R7, R8, R9, R10 e R11 são, indepen- dentemente, hidrogênio, hidroxila, halogênio, alquila C1, C2, C3, C4, C5, ou C6, alcóxi C1, C2, C3, C4, C5, ou C6, O-alquil(C1, C2, C3, C4, C5, ou C6) inferior-arila, O-benzila, OH-alquila(C1, C2, C3, C4, C5, ou C6), alquil(C1, C2, C3, C4, C5, ou C6)-O-alquila C1, H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -OCH2-, -OCH2CH2-, ou - OCH2CH2CH2-.
[073]Determinados compostos da invenção são selecionados dos Compostos 1-136 e 137. O composto da invenção é, por exemplo, Composto 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, ou 137.
[074]Os compostos da invenção incluem Compostos 33, 38, 40, 76, 133, 134, 136 e 137.
[075]Em determinados Compostos da Fórmula I, pelo menos um de Xa, Xb, Xc, Xd e Xe é N.
[076]No composto da Fórmula I, por exemplo, Xa é N e cada um de Xb, Xc, Xd e Xe é CR.
[077]Em determinados compostos da Fórmula I, Xy é CY e Xz é CZ.
[078]Em determinados compostos da Fórmula I, por exemplo, Y é hidrogênio.
[079]Os compostos da presente invenção podem tolerar uma ampla variedade de grupos funcionais, de modo que diversos materiais de partida substituídos podem ser usados para sintetizá-los. As sínteses descritas no presente documento geral- mente proporcionam o composto bi-arila final desejado no fim do processo geral ou na proximidade dele, embora possa ser desejável em determinados casos se conver- ter ainda o composto em um sal, éster ou promedicamento seu farmaceuticamente aceitável.
[080]Em determinados compostos da Fórmula I, Rb é alcóxi C1, C2, C3, C4, C5, ou C6. Rb, por exemplo, é metóxi ou etóxi. Em determinados compostos da Fórmula I, Rb é hidrogênio. Em outros compostos da Fórmula I, Rb é selecionado de F, Cl, Br, e I. Rb é F, por exemplo.
[081]Em outros compostos da Fórmula I, Rb é em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-. V é uma ligação, por exemplo. Em determinados compostos da Fórmula I, V é -CH2-, - CH2CH2- ou CH2CH2CH2-. Em outros compostos, V é O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-.
[082]Em determinados compostos da Fórmula I, W é hidrogênio. Em outros compostos da Fórmula I, W é alquila C1, C2, C3, C4, C5, ou C6. Em alguns compostos W é metila.
[083]Em determinados compostos da Fórmula I, Rc é halogênio, Rc é, por exemplo, F, Cl, Br ou I. Em alguns compostos, Rc é F. Em outros compostos Rc é Cl.
[084]Em determinados compostos, Rc é alcóxi C1, C2, C3, C4, C5, ou C6. Em alguns compostos, Rc, é metóxi ou etóxi. Em algumas modalidades Rc é etóxi.
[085]Em outros compostos da Fórmula I, Rc é hidrogênio.
[086]Em outros compostos da Fórmula I, Rc é
[087] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-. Em alguns compostos V é uma ligação. Em outros compostos V é - CH2-, -CH2CH2- ou -CH2CH2CH2-. Em outros compostos V é -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-.
[088]Em determinados compostos da Fórmula I, W é hidrogênio. Em outros compostos da Fórmula I, W é alquila C1, C2, C3, C4, C5, ou C6. Em determinados com- postos W é metila.
[089]Em determinados compostos da Fórmula I, Rb é alcóxi C1, C2, C3, C4, C5, ou C6. Rb, por exemplo, é metóxi ou etóxi. Em determinados compostos da Fórmula I, Rb é hidrogênio. Em outros compostos da Fórmula I, Rb é selecionado de F, Cl, Br ou I. Rb é, por exemplo, F.
[090]Em outros compostos da Fórmula I, Rb é
[091] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-. V, por exemplo, é uma ligação. Em determinados compostos da Fór- mula I, -CH2-, -CH2CH2-, -CH2CH2CH2-. Em outros compostos V é -O-CH2-, - OCH2CH2- ou -OCH2CH2CH2-.
[092]Em determinados compostos da Fórmula I, W é hidrogênio. Em outros compostos, W é alquila C1, C2, C3, C4, C5, ou C6. Em alguns compostos, W é metila.
[093]Em determinados compostos da Fórmula I, Rd é halogênio, Rd é F, Cl, Br, ou I. Em alguns compostos, Rd é F. Em outros compostos Rd é Cl.
[094]Em alguns compostos Rd é alcóxi C1, C2, C3, C4, C5, ou C6. Em alguns compostos, Rd é metóxi ou etóxi. Em algumas modalidades, Rd é etóxi.
[095]Em outros compostos da Fórmula I, Rd é hidrogênio.
[096]Em outros compostos da Fórmula I, Rd é
[098] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil (C1, C2, C3, C4, C5, ou C6)-arila; V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2- .Em alguns compostos V é uma ligação. Em outros compostos, V é - CH2-, -CH2CH2-, -CH2CH2CH2-. Em outros compostos V é -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-.
[099]Em alguns compostos da Fórmula I, W é hidrogênio. Em outros compos- tos W é alquila C1, C2, C3, C4, C5, ou C6. Em determinados compostos W é metila
[0100]A invenção se refere a um composto da Fórmula I, tendo uma estrutura de acordo com uma das Fórmulas II-XIII.
ou um sal, solvato, hidrato ou promedicamento seu, em que:
[0101]Rb, R4, R5, R8 e R10 são, independentemente, hidrogênio, hidroxila, ha- logênio, alquila C1, C2, C3, C4, C5, ou C6, alcóxi C1, C2, C3, C4, C5, ou C6, O-alquil(C1, C2, C3, C4, C5, ou C6) inferior-arila, O-benzila, OH-alquila(C1, C2, C3, C4, C5, ou C6), alquil(C1, C2, C3, C4, C5, ou C6)-O-alquila(C1, C2, C3, C4, C5, ou C6) inferior, COOH, COO-alquila C1, C2, C3, C4, C5, ou C6 inferior, SO2H, SO2-alquila(C1, C2, C3, C4, C5, ou C6) inferior,
[0102] em que W é H ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-.
[0103]No composto da Fórmula II-XIII, R8 é, por exemplo, hidrogênio, F, Cl, Br ou I. R8 é, por exemplo, F. Em determinados compostos R8 é H.
[0104]Em determinados compostos da Fórmula II-XIII, Rb é alcóxi C1, C2, C3, C4, C5, ou C6. Rb, por exemplo, é metóxi ou etóxi. Em determinados compostos Rb é etóxi. Em determinados compostos Rb é hidrogênio.
[0105]Em determinados compostos da Fórmula II-XIII, Rb é Cl, Br ou I. Rb é, por exemplo, F ou Cl. Em outros compostos, no composto da Fórmula II-XIII, Rb é
[0106] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila, e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-. Em determinados compostos W é H. Em outros compostos W é alquila C1, C2, C3, C4, C5, ou C6. W é, por exemplo, metila.
[0107]Em determinados compostos da Fórmula II-XIII, R4 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br ou I. Em alguns compostos R4 é alcóxi C1, C2, C3, C4, C5, ou C6. R4 é, metóxi ou etóxi. Em determinados compostos R4 é etóxi. Em outros compostos no composto da Fórmula II-XIII. Em outros compostos, no composto da Fórmula II-XIII, R4 é
[0108] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-. Em determinados compostos V é uma ligação. Em outros compostos V é -CH2-, -CH2CH2- ou -CH2CH2CH2-. Em outros compostos V é -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-.
[0109]Em determinados compostos da Fórmula II-XIII, R5 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br, ou I. R5 é, por exemplo, hidrogênio. Em alguns compostos R5 é etóxi. Em determinados compostos R5 é F. Em outros compostos, no composto da fórmula II-XIII, R5 é
[0110]em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-. Em determinados compostos V é uma ligação. Em outros compostos V é -CH2-, -CH2CH2- ou -CH2CH2CH2-. Em outros compostos V é -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-.
[0111]Em determinados compostos da Fórmula II-XIII, R10 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br ou I. Em alguns compostos R10 é, por exemplo, alcóxi C1, C2, C3, C4, C5, ou C6. R10 é, por exemplo, metóxi, ou etóxi. Em alguns com- postos R10 é isobutóxi. Em alguns compostos R10 é hidrogênio. Em determinados com- postos R10 é halogênio. R10 é, por exemplo, F ou Cl.
[0112]Em outros compostos da Fórmula II-XIII, R10 é
[0113] em que W é H, ou alquila C1, C2, C3, C4, C5, ou C6, alquil(C1, C2, C3, C4, C5, ou C6)-arila; e V é uma ligação, -CH2-, -CH2CH2-, -CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-. Em determinados compostos V é uma ligação. Em outros compostos V é -CH2-, -CH2CH2- ou -CH2CH2CH2-. Em outros compostos V é -O-CH2-, -OCH2CH2- ou -OCH2CH2CH2-.
[0114]No composto da Fórmula II-XIII, por exemplo, W é hidrogênio, ou alquila C1, C2, C3, C4, C5, ou C6. Em alguns compostos W é metila.
[0115]Determinados compostos da invenção incluem compostos de acordo com a Fórmula II.
[0118]A invenção se refere a um solvato de um composto de acordo com uma das Fórmulas I-XIII. A invenção também se refere a um hidrato de um composto de acordo com uma das Fórmulas I-XIII.
[0119]A invenção também se refere a um sal de adição de ácido de um com- posto de acordo com uma das Fórmulas I-XIII. Um sal cloridrato, por exemplo.
[0120]A invenção também se refere a um promedicamento de um composto de acordo com uma das Fórmulas I-XIII.
[0121]A invenção também se refere a um sal farmaceuticamente aceitável de um composto de acordo com uma das Fórmulas I-XIII.
[0122]A invenção inclui composições compreendendo um composto de acordo com uma das Fórmulas I-XIII e pelo menos um excipiente farmaceuticamente aceitável.
[0123]Determinados compostos da invenção são inibidores de quinase não competitivos para ATP.
[0124]A invenção também inclui um método de prevenção ou tratamento de um distúrbio de proliferação celular por administração de uma composição farmacêu- tica que inclui um composto de acordo com uma das Fórmulas I-XIII ou um sal, solvato, hidrato ou promedicamento seu e pelo menos um excipiente farmaceuticamente acei- tável a um paciente que tenha necessidade dele.
[0125]O distúrbio de proliferação celular, por exemplo, é pré-câncer ou câncer. O distúrbio de proliferação celular tratado ou prevenido pelos compostos da presente invenção pode ser um câncer, tal como, por exemplo, câncer do cólon ou câncer do pulmão.
[0126]O distúrbio de proliferação celular tratado ou prevenido pelos compostos da invenção pode ser um distúrbio hiperproliferativo.
[0127]O distúrbio de proliferação celular tratado ou prevenido pelos compos- tos da invenção pode ser psoríase.
[0128]O tratamento ou prevenção do distúrbio proliferativo pode ocorrer, por exemplo, por inibição de uma tirosina quinase. A tirosina quinase pode ser uma Src quinase ou uma quinase de adesão focal (FAK), por exemplo.
[0129]A invenção se refere a um método de tratamento ou prevenção de uma doença ou distúrbio que é modulado por inibição de tirosina quinase, por administra- ção de uma composição farmacêutica que inclui um composto de acordo com a Fór- mula i ou uma das Fórmulas II-XIII ou um sal, solvato, hidrato ou promedicamento seu, e pelo menos um excipiente farmaceuticamente aceitável. A doença ou distúrbio que é modulada, por exemplo, por inibição de tirosina quinase é câncer, pré-câncer, um distúrbio hiperproliferativo ou uma infecção microbiana. O composto é um composto de acordo com a Fórmula I ou II, por exemplo.
[0130]A composição farmacêutica da invenção pode modular um trajeto de quinase. O trajeto de quinase é, por exemplo, um trajeto de Src quinase, ou um trajeto de quinase de adesão focal.
[0131]A composição farmacêutica da invenção pode modular uma quinase di- retamente. A quinase é, por exemplo, a Src quinase ou uma quinase de adesão focal.
[0132]Determinadas composições farmacêuticas d invenção são inibidores de quinase não competitivos para ATP.
[0133]os compostos da invenção são úteis, por exemplo, para o tratamento ou prevenção de uma infecção microbiana, tal como uma infecção bacteriana, fúngica, parasítica ou viral.
[0134]Determinadas composições da invenção incluem um composto seleci- onado do Composto 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, e 137. A composição farma- cêutica inclui, por exemplo, Composto 33, 38, 40, 76, 133, 134, 136 ou 137.
[0135]Determinadas composições farmacêuticas da invenção incluem um composto selecionado dos compostos relacionados na Tabela 2.
[0136]Um composto da invenção pode ser usado como um agente farmacêu- tico. Um composto da invenção é usado, por exemplo, como um agente antiprolifera- tivo, para o tratamento de seres humanos e/ou animais, tal como para o tratamento de seres humanos e/ou outros mamíferos. Os compostos podem ser usados sem li- mitação, como agentes anticancerígenos, anti-angiogênicos, antimicrobianos, anti- bacterianos, antifúngicos, antiparasíticos e/ou antivirais, por exemplo. Além disso, os compostos podem ser usados para outros distúrbios relacionados com a proliferação celular tais como retinopatia diabética, degeneração macular e psoríase. Agentes an- ticancerígenos incluem agentes antimetastáticos.
[0137]O composto da invenção usado como um agente farmacêutico pode ser selecionado de Compostos 1-136 e 137. O composto da invenção usado como um agente farmacêutico é, por exemplo, Composto 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 61, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, ou 137. O composto da invenção usado como um agente farmacêutico é selecionado, por exemplo, de Compostos 33, 38, 40, 76, 133, 134, 136 e 137.
[0138]Determinados agentes farmacêuticos incluem um composto selecio- nado dos compostos relacionados na Tabela 2.
[0139]Em um aspecto da invenção, um composto da invenção, um composto de Fórmula I ou um das Fórmulas II-XII, por exemplo, é usado para tratar ou prevenir um distúrbio de proliferação celular em um paciente. Em um aspecto da modalidade, o distúrbio de proliferação celular é pré-câncer ou câncer. Em um outro aspecto da modalidade, o distúrbio de proliferação celular é um distúrbio hiperproliferativo. Em uma outra modalidade, a prevenção ou tratamento do distúrbio de proliferação celular, câncer ou distúrbio hiperproliferativo ocorre por meio da inibição de uma quinase. Em uma outra modalidade, a prevenção ou o tratamento do distúrbio de proliferação ce- lular, câncer ou distúrbio hiperproliferativo ocorre por meio da inibição de Src quinase ou de quinase de adesão focal (FAK). Em uma outra modalidade, o paciente é um mamífero. É preferível que o paciente seja um ser humano.
[0140]A invenção é também voltada a um método de tratamento ou prevenção de câncer ou de um distúrbio de proliferação em um paciente, compreendendo a ad- ministração de uma quantidade efetiva de um composto da invenção, de um composto da Fórmula I ou de um das Fórmulas II-XIII, por exemplo. O composto da invenção pode ser, por exemplo, um inibidor de quinase. O composto da invenção pode ser um inibidor de quinase não competitivo para ATP. O composto da invenção pode inibir a quinase diretamente, ou ele pode afetar o trajeto da quinase.
[0141]Definições
[0142]Para fins de conveniência, determinados termos usados no relatório, nos exemplos e nas reivindicações apensas estão coletados aqui.
[0143]As proteínas quinases constituem uma grande classe de enzimas que catalisam a transferência do y-fosfato de ATP ao grupo hidroxila na cadeia lateral de Ser/Tr ou Tir em proteínas e peptídeos e estão intimamente envolvidas no controle de diversas funções celulares importantes, talvez mais notavelmente: a transdução de sinal, diferenciação e proliferação. Estima-se que haja aproximadamente 2.000 prote- ínas quinases distintas no corpo humano e embora cada uma destas fosforile subs- tratos de proteína/peptídeo específicos, eles se ligam todos a ATP de mesmo segundo substrato em um bolso extremamente conservado. Aproximadamente 50% dos pro- dutos oncogênicos conhecidos são proteína tirosina quinases (PTKs) e a sua atividade de quinase demonstrou levar a transformação celular.
[0144]As PTKs podem ser classificadas em duas categorias, as PTKs de re- ceptor de membrana (as PTKs de receptor de fator de crescimento, por exemplo, e as PTKs não de receptor (a família Src de produtos proto-oncogênicos e quinase de ade- são focal (FAK)). A hiperativação de Src foi relatada em uma série de cânceres huma- nos, incluindo os do cólon, da mama, pulmão, bexiga e pele, assim como no câncer gástrico, leucemia de células pilosas, e neuroblastoma.
[0145]“Tratamento” inclui qualquer efeito, diminuição, redução, modulação ou eliminação, por exemplo, que resulta no melhoramento da condição, doença, distúrbio etc. “Tratamento” ou “tratar” um estado mórbido inclui: (1) prevenir o estado mórbido, isto é, fazer com que os sintomas clínicos do estado de doença não se desenvolvam em um paciente que possa estar exposto ou predisposto ao estado mórbido, mas que ainda não esteja sentindo ou apresentando sintomas do estado mórbido; (2) inibir o estado mórbido, isto é, interromper o desenvolvimento do estado mórbido ou seus sintomas clínicos; ou (3) aliviar o estado mórbido, isto é, produzir uma regressão tem- porária ou permanente do estado mórbido ou seu sintomas clínicos.
[0146]“Estado mórbido” significa qualquer doença, distúrbio, condição, sin- toma ou indicação.
[0147]Conforme empregado no presente, o termo “distúrbio de proliferação celular” se refere a condições em que o crescimento desregulado e/ou anormal de células pode levar ao desenvolvimento de uma condição indesejável ou doença, que pode ser cancerosa ou não cancerosa, uma condição psoriática, por exemplo. Con- forme empregado no presente, os termos “condição psoriática” ou “psoríase” se refere a distúrbios que envolvem a hiperproliferação de queratinócitos, infiltração celular in- flamatória e alteração de citocinas.
[0148]Em uma modalidade preferida, o distúrbio de proliferação celular é cân- cer. Conforme empregado no presente, o termo “câncer” inclui tumores sólidos tais como cânceres do pulmão, da mama, cólon, ovariano, do cérebro, fígado, pâncreas, próstata, melanoma maligno, cânceres da pele não melanoma, assim como tumores e/ou doenças malignas hematológicas, tais como leucemia e linfomas, mieloma múl- tiplo, doença de Hodgkin, linfomas de origem linfocítica e cutânea, leucemia aguda e crônica tais como leucemia aguda linfoblástica, mielocítica aguda ou crônica mielocí- tica, neoplasma celular do plasma, neoplasma linfóide, e cânceres associados com AIDS.
[0149]Além de condições psoriáticas, os tipos de doenças proliferativas que podem ser tratadas usando-se as composições da presente invenção são cistos epi- dérmicos e dermóides, lipomas, adenomas, hemangiomas capilares e cutâneos, lin- fangiomas, lesões de nevi, teratomas, nefromas, miofibromatose, tumores osteoplás- ticos, e outras massas displásticas e semelhantes. As doenças proliferativas podem incluir displasias e distúrbios de semelhantes.
[0150]Uma “quantidade efetiva” de um composto da invenção descrita é a quantidade que, quando administrada a um paciente que tem uma doença ou distúrbio resulta na regressão da doença ou distúrbio no paciente. Assim, uma quantidade efe- tiva de um composto da invenção descrita é a quantidade que, quando administrada a um paciente que tem um distúrbio de proliferação celular, resulta na regressão do crescimento celular no paciente. A quantidade do composto descrito a ser adminis- trada a um paciente dependerá do distúrbio específico, do modo de administração, dos compostos co-administrados, se houver, e das características do paciente, tais como saúde geral, outras doenças, idade, sexo, genótipo, peso corporal e tolerância a drogas. Os versados na técnica serão capazes de determinar as dosagens adequa- das, dependendo destes e de outros fatores.
[0151]Conforme empregado no presente, o termo “quantidade efetiva” se re- fere a uma quantidade de um composto, ou a uma combinação de compostos da pre- sente invenção efetiva quando administrada sozinha ou em combinação como um agente anti-proliferativo. Uma quantidade efetiva se refere, por exemplo, a uma quan- tidade do composto presente em uma formulação ou em um dispositivo médico admi- nistrado a um paciente e suficiente para obter uma atividade biológica, uma atividade antiproliferativa, por exemplo, tal como atividade anticancerígena ou atividade antine- oplástica, por exemplo. A combinação de compostos opcionalmente consiste em uma combinação sinérgica. Sinergia, conforme descrita, por exemplo, por Chou e Talalay, Adv. Enzyme Regul. vol. 22, pp. 27-55 (1984) ocorre quando o efeito dos compostos quando administrados em combinação é maior do que o efeito aditivo dos compostos quando administrados sozinhos como um agente individual. Em geral, um efeito sinér- gico é mais claramente demonstrado a concentrações sub-ótimas dos compostos. A sinergia pode ser em termos de citotoxicidade menor, ou aumento do efeito antiproli- ferativo, ou algum outro efeito benéfico da combinação em comparação com os com- ponentes individuais.
[0152]“Uma quantidade terapeuticamente efetiva” significa a quantidade do composto que, quando administrada a um mamífero para o tratamento de uma do- ença, é suficiente para efetuar tal tratamento para a doença. A “quantidade terapeuti- camente efetiva” variará dependendo do composto, da doença e da sua gravidade e idade, peso etc., do mamífero a ser tratado.
[0153]Uma quantidade terapeuticamente efetiva de um ou mais dos compos- tos pode ser formulada com um veículo farmaceuticamente aceitável para administra- ção a um ser humano ou a um animal. Conseqüentemente, os compostos ou as formulações podem ser administrados, por via oral, parenteral, ou vias tópicas, por exemplo, para proporcionar uma quantidade efetiva do composto. Em modalidades alternativas, os compostos preparados de acordo com a presente invenção podem ser usados para revestir ou impregnar um dispositivo médico, tal como uma sonda, por exemplo.
[0154]O termo “quantidade profilaticamente efetiva” significa uma quantidade efetiva de um composto ou compostos, da presente invenção que é administrada para prevenir ou reduzir o risco de proliferação celular indesejável.
[0155]“Efeito farmacológico”, conforme empregado no presente, abrange efei- tos produzidos no indivíduo que atingem o fim pretendido de uma terapia. Em uma modalidade preferida, um efeito farmacológico significa que as indicações primárias do paciente a ser tratado são prevenidas, aliviadas ou reduzidas. Um efeito farmaco- lógico, por exemplo, seria um que resultar na prevenção, alívio ou redução das indi- cações primárias em um indivíduo tratado. Em uma outra modalidade preferida, um efeito farmacológico significa que os distúrbios ou sintomas das indicações primárias do indivíduo sendo tratado são prevenidos, aliviados ou reduzidos. Um efeito farma- cológico seria, por exemplo, um que resulta na prevenção ou redução de indicações primárias em um indivíduo tratado.
[0156]No tocante aos compostos químicos úteis na presente invenção, os ter- mos abaixo podem ser aplicáveis:
[0157]O termo “substituído”, conforme empregado no presente, significa que qualquer um ou mais hidrogênios no átomo designado é substituído com uma seleção do grupo indicado, desde que a valência normal do átomo designado não seja exce- dida, e que a substituição resulte em um composto estável. Quando um substituinte for ceto (isto é, =O), então 2 hidrogênios no átomo são substituídos. Os substituintes ceto não estão presentes em frações aromáticas. As ligações duplas no anel, con- forme empregado no presente, são ligações duplas que são formadas entre dois átomos adjacentes no anel (C=, C=N, ou N=N, por exemplo).
[0158]A presente invenção se destina a incluir todos os isótopos de átomos que ocorrem nos compostos da presente invenção. Os isótopos incluem aqueles áto- mos que têm o mesmo número atômico, mas diferentes números de massa. A titulo de exemplo geral e sem limitação, isótopos de hidrogênio incluem trítio e deutério e os isótopos de carbono incluem C-13 e C-1.
[0159]Os compostos descritos no presente documento podem ter centros as- simétricos. os compostos da presente invenção contendo um átomo assimetricamente substituído podem ser isolados em formas oticamente ativas ou racêmicas. É bem conhecido na técnica o modo de se preparar formas oticamente ativas, tal como por resolução de formas racêmicas ou por síntese a partir de materiais de partida otica- mente ativos. Muitos isômeros geométricos de olefinas, ligações C=N duplas, e se- melhantes, podem também esta presentes nos compostos descritos no presente do- cumento, e todos tais isômeros estáveis são objeto da presente invenção. Os isôme- ros geométricos cis e trans dos compostos da presente invenção são descritos e po- dem ser isolados como uma mistura de isômeros ou em forma de formas isoméricas separadas. Todas as formas quirais, diastereoisoméricas, racêmicas e isoméricas ge- ométricas de uma estrutura são visadas, a não ser que seja especificamente indicada a estereoquímica específica ou forma isomérica. Todos os tautômeros de compostos mostrados ou descritos são também considerados como parte da presente invenção.
[0160]Quando qualquer variável (R1, por exemplo) ocorre mais de uma vez em qualquer constituinte ou fórmula para um composto, sua definição a cada ocorrên- cia é independente da sua definição em qualquer outra ocorrência. Assim, por exem- plo, se um grupo for mostrado como sendo substituído com 0-2 R1 frações, então o grupo pode opcionalmente ser substituído com até duas frações R1 e a cada ocorrên- cia R1 é selecionado independentemente da definição de R1. Além disso, as combina- ções de substituintes e/ou variáveis são permissíveis, mas somente se tais combinações resultarem em compostos estáveis.
[0161]Quando uma ligação a um substituinte for mostrada como cruzando uma ligação conectando dois átomos em um anel, então tal substituinte pode ser li- gado a qualquer átomo no anel. Quando um substituinte for relacionado sem indicação do átomo através do qual tal substituinte está ligado ao resto do composto de uma fórmula dada, então tal substituinte pode ser ligado por meio de qualquer átomo em tal substituinte. Combinações de substituintes e/ou variáveis são permissíveis, mas somente se tais combinações resultarem em compostos estáveis.
[0162]Os compostos da presente invenção que contêm nitrogênios podem ser convertidos em N-óxidos por tratamento com um agente oxidante (ácido 3-cloroperóxi- benzóico (m-CPBA), por exemplo, e/ou peróxidos de hidrogênio) para se obter outros compostos da presente invenção. Assim, todos os compostos contendo nitrogênios mostrados e reivindicados são considerados, quando for permitido pela valência e es- trutura que eles incluam tanto o composto conforme mostrado como o seu derivado N-óxido (que pode ser designado como N ^ O ou N+-O-). Além disso, em outros ca- sos, os nitrogênios nos compostos da presente invenção podem ser convertidos em composto N-hidróxi ou N-alcóxi. Os compostos N-hidróxi, por exemplo, podem ser preparados por oxidação da amina progenitora por um agente oxidante tal como m- CPBA. Todos os compostos contendo nitrogênios mostrados e reivindicados são tam- bém considerados, quando permitido pela valência e estrutura, como abrangendo tanto o composto conforme mostrado como os seus derivados N-hidróxi (isto é, N-OH) e N-alcóxi (isto é, N-OR, em que R é alquila C1-6 substituído ou não substituído, al- quenila C1-6, alquinila C3-14, carbociclo C3-14 ou heterociclo de 3-14 membros).
[0163]Quando um átomo ou fração química é seguido por uma faixa numérica subscrita (C1-6, por exemplo), a invenção tem a intenção de abranger cada número dentro desta faixa assim como todas as faixas intermediárias. “alquila C1-6” se destina a incluir, por exemplo, grupos alquila com 1, 2, 3, 4, 5, 6, 1-6, 1-5, 1-4, 1-3, 1-2, 2-6, 3-6, 3-5, 3-4, 4-6, 4-5 e 5-6 carbonos.
[0164]Conforme empregado no presente, “alquila” destina-se a incluir tanto grupos hidrocarboneto alifáticos saturados tanto de cadeia ramificada como de cadeia reta tendo o número especificado de átomos de carbono. Alquila C1-C6, por exemplo, se destina a incluir grupos alquila C1, C2, C3, C4, C5 e C6. Exemplos de alquila incluem, sem limitação, metila, etila, n-propila, i-propila, n-butila, s-butila, t-butila, n-pentila, s- pentila e n-hexila. “Alquila” inclui ainda grupos alquila que tem átomos de oxigênio, nitrogênio, enxofre o fósforo substituindo um ou mais átomos de carbono da espinha dorsal do hidrocarboneto. Em determinadas modalidades, um alquila de cadeia reta ou ramificada tem seis ou menos átomos de carbono na sua espinha dorsal (C1-C6, para cadeia reta, C3-C6 para a cadeia ramificada, por exemplo), sendo mais preferível quatro ou menos. De modo análogo, cicloalquilas preferidos têm de três a oito átomos de carbono na sua estrutura de anel, sendo mais preferível que tenham cinco ou seis átomos de carbono na estrutura de anel.
[0165]A não ser que o número de carbonos seja especificado em contrário, “alquila inferior” inclui um grupo alquila, conforme definido acima, mas tendo de um a dez, sendo mais preferível de um a seis, átomos de carbono na sua estrutura de es- pinha dorsal. “Alquenila inferior” e “alquinila inferior” têm comprimentos de cadeia de 2-5 átomos de carbono, por exemplo.
[0166]O termo "alquila" também inclui tanto "alquilas não substituídos "como" alquilas substituídos", referindo-se estes últimos a frações alquila que tem substituin- tes substituindo um hidrogênio em um ou mais carbonos da espinha dorsal de hidro- carboneto. Tais substituintes podem incluir, por exemplo, alquila, alquenila, alquinila, halogênio, hidroxila, alquilcarbonilóxi, arilcarbonilóxi, alcoxicarbonilóxi, arilóxi-carboni- lóxi, carboxilato, alquil-carbonila, aril-carbonila, alcóxi-carbonila, amino-carbonila, al- quilamino-carbonila, dialquilamino-carbonila, alquiltio-carbonila, alcoxila, fosfato, fos- fonato, fosfinato, ciano, amino (inclusive alquilamino, dialquilamino, arilamino, diarilamino, e alquilarilamino), acilamino (inclusive alquil-carbonilamino, aril-carbonila- mino, carbamoíla e ureido), amidino, imino, sulfidrila, alquiltio, ariltio, tiocarboxilato, sulfatos, alquilsulfinila, sulfonato, sulfamoíla, sulfonamido, nitro, trifluormetila, ciano, azido, heterociclila, alquilarila, ou uma fração aromática ou heteroaromática. As ciclo- alquilas podem ainda ser substituída, com os substituintes descritos acima, por exem- plo. Uma fração "alquilarila" ou uma "aralquila" é um alquila substituído com um arila (arila fenilmetila (benzila), por exemplo).
[0167]"Alquenila" inclui grupos alifáticos insaturados análogos em compri- mento e em substituição possível às alquilas descritos acima, mas que contém pelo menos uma ligação dupla. O termo “alquenila” inclui grupos alquenila de cadeia reta (etenila, propenila, butenila, pentenila, hexenila, heptenila, octenila, nonenila, dece- nila, por exemplo), grupos alquenila de cadeia ramificada, grupos cicloalquenila (alicí- clicos, por exemplo) (ciclopropenila, ciclopentenila, ciclohexenila, cicloheptenila, ciclo- octenila, por exemplo), grupos cicloalquenila alquil- ou alquenil- substituídos, e grupos alquenila cicloalquil ou cicloalquenil substituídos. O termo "alquenila" ainda inclui gru- pos alquenila que incluem átomos de oxigênio, nitrogênio, enxofre ou fósforo substi- tuindo um ou mais carbonos da espinha dorsal do hidrocarboneto. Em determinadas modalidades, um grupo alquenila de cadeia reta ou cadeia ramificada tem seis ou menos átomos de carbono na sua espinha dorsal (C2-C6 para cadeia reta, C3-C6 para cadeia ramificada, por exemplo). De modo análogo, grupos cicloalquenila podem ter de três a oito átomos de carbono na sua estrutura de anel, sendo mais preferível que tenham cinco ou seis carbonos na estrutura de anel. O termo "C2-C6" inclui grupos alquenila contendo de dois a seis átomos de carbono. O termo "C3-C6" inclui grupos alquenila contendo de três a seis átomos de carbono.
[0168]O termo "alquenila" também inclui tanto "alquenilas não substituídos" como "alquenilas substituídos", referindo-se estes últimos a frações alquenila que tem substituintes que substituem um hidrogênio em um ou mais átomos de carbono da espinha dorsal do hidrocarboneto. Tais substituintes podem incluir, por exemplo, gru- pos alquila, halogênios, hidroxila, alquilcarbonilóxi, arilcarbonilóxi, alcóxi-carbonilóxi, arilóxi-carbonilóxi, carboxilato, alquil-carbonila, aril-carbonila, alcóxi-carbonila, amino- carbonila, alquilamino-carbonila, dialquilamino-carbonila, alquiltio-carbonila, alcoxila, fosfato, fosfonato, fosfinato, ciano, amino (inclusive alquilamino, dialquilamino, arila- mino, diarilamino, e alquilarilamino), acilamino (inclusive alquil-carbonilamino, aril-car- bonilamino, carbamoíla e ureído), amidino, imino, sulfidrila, alquiltio, ariltio, tiocarboxi- lato, sulfatos, alquilsulfinila, sulfonato, sulfamoíla, sulfonamido, nitro, trifluormetila, ci- ano, azido, heterociclila, alquilarila, ou uma fração aromática ou heteroaromática.
[0169]"Alquinila” inclui grupos alifáticos insaturados análogos em compri- mento e substituição possível aos alquilas descritos acima, mas que contém pelo me- nos uma ligação tripla. “Alquinila” inclui, por exemplo, grupos alquinila de cadeia reta (etinila, propinila, butinila, pentinila, hexinila, heptinila, octinila, noninila, decinila), gru- pos alquinila de cadeia ramificada, e grupos alquinila cicloalquil- ou cicloalquenil- substituídos. O termo "alquinila” inclui ainda grupos que têm átomos de oxigênio, ni- trogênio, enxofre ou fósforo substituindo um ou mais carbono na espinha dorsal do hidrocarboneto. Em determinadas modalidades, um grupo alquinila de cadeia reta ou cadeia ramificada tem seis ou menos átomos de carbono na sua espinha dorsal (C2- C6 para cadeia reta, C3-C6 para cadeia ramificada, por exemplo). O termo "C2-C6" in- clui grupos alquinila contendo de dois a seis átomos de carbono. O termo "C3-C6" inclui grupos alquinila contendo de três a seis átomos de carbono.
[0170]O termo "alquinila” também inclui tanto "alquinilas não substituídos" como "alquinilas substituídos", referindo-se estes últimos a frações alquinila que tem substituintes substituindo um hidrogênio em um ou mais átomos de carbono de espi- nha dorsal do hidrocarboneto. Tais substituintes podem incluir, por exemplo, grupos alquila, grupos alquinila, halogênios, hidroxila, alquilcarbonilóxi, arilcarbonilóxi, alcoxi- carbonilóxi, ariloxicarbonilóxi, carboxilato, alquil-carbonila, aril-carbonila, alcoxi- carbonila, amino-carbonila, alquilamino-carbonila, dialquilamino-carbonila, alquiltio- carbonila, alcoxila, fosfato, fosfonato, fosfinato, ciano, amino (inclusive alquilamino, dialquilamino, arilamino, diarilamino, e alquilarilamino), acilamino (inclusive alquil-car- bonilamino, aril-carbonilamino, carbamoíla e ureído), amidino, imino, sulfidrila, alquil- tio, ariltio, tiocarboxilato, sulfatos, alquilsulfinila, sulfonato, sulfamoíla, sulfonamido, ni- tro, trifluormetila, ciano, azido, heterociclila, alquilarila, ou uma fração aromática ou heteroaromática.
[0171]"Arila" inclui grupos com caráter aromático, incluindo grupos aromáticos “não conjugados” de 5 e 6 membros ou de um único anel, grupos aromáticos que podem incluir de zero a quatro heteroátomos, assim como sistemas “conjugados’” ou multicíclicos tendo pelo menos um anel aromático. Exemplos de grupos arila incluem benzeno, fenila, pirrol, furano, tiofeno, tiazol, isotiazol, imidazol, triazol, tetrazol, pira- zol, oxazol, isooxazol, piridina, pirazina, piridazina, e pirimidina, e semelhantes. Além disso, o termo "arila" inclui grupos arila multicíclicos, tais como tricíclicos, bicíclicos, por exemplo, como naftaleno, benzoxazol, benzodioxazol, benzotiazol, benzimidazol, benzotiofeno, metileno-dioxifenila, quinolina, isoquinolina, naftridina, indol, benzofu- rano, purina, benzofurano, deazapurina, ou indolizina. Os grupos arila que têm hete- roátomos na estrutura de anel podem também ser denominados "heterociclos arila", "heterociclos", "heteroarilas" ou "heteroaromáticos". O anel aromático pode ser subs- tituído em uma ou mais posições do anel com tais substituintes como os descritos acima, como, por exemplo, halogênio, hidroxila, alcóxi, alquilcarbonilóxi, arilcarboni- lóxi, alcóxi-carbonilóxi, arilóxi-carbonilóxi, carboxilato, alquil-carbonila, alquilamino- carbonila, aralquilamino-carbonila, alquenilamino-carbonila, alquil-carbonila, aril-car- bonila, aralquil-carbonila, alquenil-carbonila, alcóxi-carbonila, amino-carbonila, alquil- tio-carbonila, fosfato, fosfonato, fosfinato, ciano, amino (inclusive alquilamino, dialqui- lamino, arilamino, diarilamino, e alquil-arilamino), acilamino (inclusive alquil-carbonila- mino, aril-carbonilamino, carbamoíla e ureído), amidino, imino, sulfidrila, alquiltio, ariltio, tiocarboxilato, sulfatos, alquilsulfinila, sulfonato, sulfamoíla, sulfonamido, nitro, trifluormetila, ciano, azido, heterociclila, alquilarila, ou uma fração aromática ou hete- roaromática. Os grupos arila podem também ser fundidos ou ligados por pontes com anéis alicíclicos ou heterocíclicos, que são não aromáticos de modo a formar um sis- tema multicíclico (tetralina, metileno-dioxifenila, por exemplo).
[0172]Conforme empregado no presente, “halo” ou “halogênio” se refere a flúor, cloro, bromo e iodo. O termo “per-halogenado”, se refere em geral a uma fração em que todos os hidrogênios são substituídos por átomos de halogênios.
[0173]“Contra-íons” é usado para representar uma espécie de cara negativa pequena tal como cloreto, brometo, hidróxido, acetato e sulfato.
[0174]O termo “substituinte não hidrogênio” se refere a substituintes distintos do hidrogênio. Exemplos não limitantes incluem grupos alquila, grupos alcóxi, grupos halogênio, grupos hidroxila, grupos arila etc.
[0175]Conforme empregado no presente, “carbociclo” ou “anel carbocíclico” se destina a significar qualquer anel monocíclico, bicíclico ou tricíclico que tem o nú- mero especificado de carbonos, qualquer um dos quais pode ser saturado, insaturado ou aromático. um carbociclo C3-14, por exemplo, se destina a significar um anel mono, bi ou tricíclico tendo 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 ou 14 átomos de carbono. Exem- plos de carbociclos incluem, sem limitação, ciclopropila, ciclobutila, ciclobutenila, ci- clopentila, ciclopentenila, ciclohexila, cicloheptenila, cicloheptila, cicloheptenila, ada- mantila, ciclooctila, ciclooctenila, ciclooctadienila, fluorenila, fenila, naftila, indanila, adamantila, e tetraidronaftila. Os anéis com pontes são também incluídos na definição de carbociclo, incluindo, por exemplo, [3.3.0]biciclooctano, [.3.0] biciclononano, [.4.0]biciclodecano e [2.2.2]biciclooctano. Um anel com ponte ocorre quando um ou mais átomos de carbono ligam dois átomos de carbono não adjacentes. As pontes preferidas consistem em um ou dois átomos de carbono. Observe-se que uma ponte sempre converte um anel monocíclico em um anel tricíclico. Quando um anel é ligado por ponte, os substituintes citados para o anel podem também estar presentes na ponte. Anéis fundidos (naftila e tetraidronaftila, por exemplo) e espiro são também incluídos.
[0176]Conforme empregado no presente, o termo “heterociclo” ou “heterocí- clico” se destina a significar qualquer anel monocíclico, bicíclico ou tricíclico que é saturado, insaturado, ou aromático e compreende átomos de carbono e um ou mais heteroátomos no anel, 1 ou 1-2, ou 1-3, ou 1-4 ou 1-5 ou 1-6 heteroátomos, selecio- nados independentemente do grupo que consiste em nitrogênio, oxigênio e enxofre. Um heterociclo bicíclico ou tricíclico pode ter um ou mais heteroátomos localizados em um anel ou os heteroátomos podem estar localizados em mais de um anel. Os heteroátomos nitrogênio e enxofre podem opcionalmente ser oxidados (isto é, N ^ O e S(O)p, em que p = 1 ou 2). Quando um átomo de nitrogênio está incluído no anel, ele é ou N ou NH, dependendo de estar ou não ligado a uma ligação dupla no anel (isto é, um hidrogênio está presente se for necessário para manter a trivalência do átomo de nitrogênio). O átomo de nitrogênio pode ser substituído ou não substituído (isto é, ser N ou NR, em que R é H ou um outro substituinte, conforme definido). O anel heterocíclico pode ser ligado ao seu grupo pendente em qualquer heteroátomo ou átomo de carbono que resulte em uma estrutura estável. os anéis heterocíclicos descritos no presente documento podem ser substituídos no carbono ou sobre um átomo de nitrogênio se o composto resultante for estável. Um nitrogênio no heterociclo pode opcionalmente ser quaternizado. É preferível que, quando o número total de átomos de S e O no heterociclo exceder 1, então estes heteroátomos não estarão adjacentes entre si. Os anéis com pontes são também incluídos na definição de hete- rociclo. Um anel com ponte ocorre quando um ou mais átomos (isto é, C, O, N ou S) ligam dois átomos de carbono ou nitrogênio não adjacentes. As pontes preferidas in- cluem, sem limitação, um átomo de carbono, dois átomos de carbono, um átomo de nitrogênio, dois átomos de nitrogênio e um grupo carbono-nitrogênio. Deve-se observar que uma ponte sempre converte um anel monocíclico em um anel tricíclico. Quando um anel é dotado de pontes os substituintes citados para o anel podem tam- bém estar presentes na ponte. Anéis fundidos e espiro são também incluídos.
[0177]Conforme empregado no presente, o termo “heterociclo aromático” ou “heteroarila” se destina a significar um anel heterocíclico aromático monocíclico ou bicíclico de 5, 6 ou 7 membros ou um anel heterocíclico aromático bicíclico de 7, 8, 9, 10, 11 ou 12 membros que consiste em átomos de carbono e um ou mais heteroáto- mos, tal como 1 ou 1-2, ou 1-3 ou 1-4 ou 1-5 ou 1-6 heteroátomos, independentemente selecionados do grupo que consiste em nitrogênio, oxigênio e enxofre. No caso de anéis aromáticos heterocíclicos bicíclicos somente um dos dois anéis precisa ser aro- mático (2,3-diidroindol, por exemplo) embora ambos possam ser (quinolina, por exem- plo). O segundo pode também ser fundido ou ligado por ponte conforme definido acima para heterociclos. O átomo de nitrogênio pode ser substituído ou não substitu- ído (isto é, ser N ou NR, em que R é H ou outro substituinte, conforme definido). Os heteroátomos de nitrogênio, e enxofre podem ser opcionalmente oxidados (isto é, N ^ O e S(O)p, em que p = 1 ou 2). Observe-se que o número total de átomos de S e O no heterociclo aromático é não superior a 1.
[0178]Exemplos de heterociclos incluem, sem limitação, acridinila, azocinila, benzimidazolila, benzofuranila, benzotiofuranila, benzotiofenila, benzoxazolila, ben- zoxazolinila, benzotiazolila, benzotriazolila, benzotetrazolila, benzoisoxazolila, benzoi- sotiazolila, benzimidazolinila, carbazolila, 4aH-carbazolila, carbolinila, cromanila, cro- menila, cinolinila, decaidroquinolinila, 2H,6H-l,5,2-ditiazinila, diidrofuro [2,3-b]tetraidro- furan, furanila, furazanila, imidazolidinila, imidazolinila, imidazolila, 1H-indazolila, indo- lenila, indolinila, indolizinila, indolila, 3H-indolila, isatinoila, isobenzofuranila, isocroma- nila, isoindazolila, isoindolinila, isoindolila, isoquinolinila, isotiazolila, isoxazolila, meti- lenodioxifenila, morfolinila, naftiridinila, octaidroisoquinolinila, oxadiazolila, 1,2,3-oxa- diazolila, 1,2,4-oxadiazolila, 1,2,5-oxadiazolila, 1,3,4-oxadiazolila, oxazolidinila, oxazolila, oxindolila, pirimidinila, fenantridinila, fenantrolinila, fenazinila, fenotiazinila, fenoxatinila, fenoxazinila, ftalazinila, piperazinila, piperidinila, piperidonila, 4-piperido- nila, piperonila, pteridinila, purinila, piranila, pirazinila, pirazolidinila, pirazolinila, pira- zolila, piridazinila, piridooxazol, piridoimidazol, piridotiazol, piridinila, piridila, pirimi- dinila, pirrolidinila, pirrolinila, 2H-pirrolila, pirrolila, quinazolinila, quinolinila, 4H-quinoli- zinila, quinoxalinila, quinuclidinila, tetraidrofuranila, tetraidroisoquinolinila, tetraidroqui- nolinila, tetrazolila, 6H-l,2,5-tiadiazinila, 1,2,3-tiadiazolila, 1,2,4-tiadiazolila, 1,2,5-tiadi- azolila, 1,3,4-tiadiazolila, tiantrenila, tiazolila, tienila, tienotiazolila, tienooxazolila, tie- noimidazolila, tiofenila, triazinila, 1,2,3-triazolila, 1,2,4-triazolila, 1,2,5-triazolila, 1,3,4- triazolila, e xantenila.
[0179]“Acila” inclui compostos e frações que contém o radical acila (CH3 CO- ) ou um grupo carbonila. “Acila substituído” inclui grupos acila em que um ou mais dos átomos de hidrogênio é substituído por grupos alquila, por exemplo, grupos alquinila, halogênios, hidroxila, alquil-carbonilóxi, aril-carbonilóxi, alcóxi-carbonilóxi, arilóxi-car- bonilóxi, carboxilato, alquil-carbonila, aril-carbonila, alcóxi-carbonila, amino-carbonila, alquilamino-carbonila, dialquilamino-carbonila, alquiltio-carbonila, alcoxila, fosfato, fosfonato, fosfinato, ciano, amino (inclusive alquilamino, dialquilamino, arilamino, dia- rilamino, e alquilarilamino), acilamino (inclusive alquil-carbonilamino, aril-carbonila- mino, carbamoíla e ureído), amidino, imino, sulfidrila, alquiltio, ariltio, tiocarboxilato, sulfatos, alquilsulfinila, sulfonato, sulfamoíla, sulfonamido, nitro, trifluormetila, ciano, azido, heterociclila, alquilarila, ou uma fração aromática ou heteroaromática.
[0180]“Acilamino” inclui frações em que uma fração acila é ligada a um grupo amino. O termo inclui grupos alquil-carbonilamino, aril-carbonilamino, carbamoíla e ureído, por exemplo.
[0181]“Aroíla” inclui compostos e frações com uma fração arila ou fração he- teroaromática ligada a um grupo carbonila. Exemplos de grupos aroíla incluem fenil- carbóxi, naftil carbóxi etc.
[0182]“Alcoxialquila”, “alquilaminoalquila” e “tioalcóxi-alquila” incluem grupos alquila, conforme descrito acima, que incluem ainda átomos de oxigênio, nitrogênio ou enxofre substituindo um ou mais átomos de carbono da espinha dorsal de hidro- carboneto, átomos de oxigênio, nitrogênio ou enxofre, por exemplo.
[0183]O termo “alcóxi” ou “alcoxila” inclui grupos alquila, alquenila ou alquinila substituídos e não substituídos ligados covalentemente a um átomo de oxigênio. Exemplos de grupos alcóxi (ou radicais alcoxila) incluem grupos metóxi, etóxi, isopro- pilóxi, propóxi, butóxi, e pentóxi. Exemplos de grupos alcóxi substituídos incluem gru- pos alcóxi halogenados. Os grupos alcóxi podem ser substituídos com grupos tais como alquenila, alquinila, halogênio, hidroxila, alquil-carbonilóxi, aril-carbonilóxi, alcóxi-carbonilóxi, arilóxi-carbonilóxi, carboxilato, alquil-carbonila, aril-carbonila, alcóxi-carbonila, amino-carbonila, alquilamino-carbonila, dialquilamino-carbonila, al- quiltio-carbonila, alcoxila, fosfato, fosfonato, fosfinato, ciano, amino (inclusive alquila- mino, dialquilamino, arilamino, diarilamino, e alquilarilamino), acilamino (inclusive al- quil-carbonilamino, aril-carbonilamino, carbamoíla e ureido), amidino, imino, sulfidrila, alquiltio, ariltio, tiocarboxilato, sulfates, alquilsulfinila, sulfonato, sulfamoíla, sulfona- mido, nitro, trifluormetila, ciano, azido, heterociclila, alquilarila, ou uma fração aromá- tica ou heteroaromática. Exemplo de grupos alcóxi substituídos com halogênios in- cluem, sem limitação, fluormetóxi, difluormetóxi, trifluormetóxi, clorometóxi, diclorome- tóxi, e triclorometóxi.
[0184]O termo “tiocarbonila” ou “tiocarbóxi” inclui compostos e frações que contêm um carbono conectado com uma ligação dupla a um átomo de enxofre.
[0185]O termo “éter” inclui compostos ou frações que contêm um oxigênio li- gado a dois átomos de carbono ou heteroátomos diferentes. O termo inclui, por exem- plo, “alcóxi-alquila” que se refere a um grupo alquila, alquenila ou alquinila ligado co- valentemente a um átomo de oxigênio que é covalentemente ligado a um outro grupo alquila.
[0186]O termo “éster” inclui compostos e frações que contém um carbono ou um heteroátomo ligado a um átomo de oxigênio que é ligado ao carbono de um grupo carbonila. O termo “éster” inclui grupos alcóxi-carbóxi tais como metóxi-carbonila, etóxi-carbonila, propóxi-carbonila, butóxi-carbonila, pentóxi-carbonila etc. Os grupos: alquila, alquenila ou alquinila são conforme definido acima.
[0187]O termo “tioéter” inclui compostos e frações que contêm um átomo de enxofre ligado a dois carbonos ou heteroátomos diferentes. Exemplos de tioéteres incluem, sem limitação, alquiltioalquilas, alquiltioalquenilas, e alquiltioalquinilas. O termo “alquiltioalquilas” inclue compostos com um grupo alquila, alquenila ou alquinila ligado a um átomo de enxofre que é ligado a um grupo alquila. De modo análogo, o termo “alquiltioalquenilas” e “alquiltioalquinilas” se refere a compostos ou frações em que um grupo alquila, alquenila ou alquinila é ligado a um átomo de enxofre que é ligado covalentemente a um grupo alquinila.
[0188]O termo “hidróxi” ou “hidroxila” inclui grupos com um -OH ou -O-.
[0189]“Policiclila” ou “radical policíclico” se refere a dois ou mais anéis cíclicos (cicloalquila, cicloalquenilas, cicloalquinilas, arilas e/ou heterociclilas) em que dois ou mais carbonos são comuns a dois anéis adjacentes. Os anéis que são ligados por meio de átomos não adjacentes são denominados anéis “ligados por pontes”. Cada um dos anéis do policiclo pode ser substituído com tais substituintes que foram des- critos acima, como, por exemplo, halogênio, hidroxila, alquilcarboniloxi, arilcarboniloxi, alkoxicarboniloxi, ariloxicarboniloxi, carboxilate, alquil-carbonila, alcóxi-carbonila, al- quilamino-carbonila, aralquilamino-carbonila, alquenilamino-carbonila, alquil-carbo- nila, aril-carbonila, aralquil-carbonila, alquenil-carbonila, aminocarbonila, alquiltio-car- bonila, alcoxila, fosfato, fosfonato, fosfinato, ciano, amino (inclusive alquilamino, dial- quilamino, arilamino, diarilamino, e alquilarilamino), acilamino (inclusive alquil-carbo- nilamino, aril-carbonilamino, carbamoíla e ureído), amidino, imino, sulfidrila, alquiltio, ariltio, tiocarboxilato, sulfates, alquilsulfinila, sulfonato, sulfamoíla, sulfonamido, nitro, trifluormetila, ciano, azido, heterociclila, alquila, alquilarila, ou uma fração aromática ou heteroaromática.
[0190]Um “grupo aniônico”, conforme empregado no presente, se refere a um grupo que tem carga negativa a um pH fisiológico. Os grupos aniônicos preferidos incluem carboxilato, sulfato, sulfonato, sulfinato, sulfamato, tetrazolila, fosfato, fosfo- nato, fosfinato ou fosforotioato ou equivalentes funcionais seus. “Equivalentes funcio- nais“ de grupos aniônicos destinam-se a incluir bioisósteros, tais como bioisósteros de um grupo carboxilato, por exemplo. Os bioisósteros abrangem tanto equivalentes bioisostéricos clássicos como equivalentes bioisostéricos não clássicos. Os bioisóste- ros clássicos e não clássicos são conhecidos na técnica (veja, por exemplo, Silver- man, R. B. The Organic Chemistry of Drug Design and Drug Action, Academic Press, Inc.: San Diego, Calif., 1992, pp. 19-23). Um grupo aniônico especialmente preferido é um carboxilato.
[0191]No presente relatório, a fórmula estrutural do composto representa um isômero determinado para conveniência em alguns casos, mas a presente invenção inclui todos os isômeros, tal como isômero geométrico, isômero ótico baseado em um carbono assimétrico, estereoisômero, tautômero e semelhantes que ocorrem estrutu- ralmente e uma mistura de isômeros que não é limitada à descrição da fórmula para fins de conveniência e pode consistir em qualquer um de isômeros ou uma mistura. Portanto, um átomo de carbono assimétrico pode estar presente na molécula e um composto oticamente ativo e um composto racêmico podem estar presentes no com- posto da rpv, mas a presente invenção não é limitada a eles e inclui qualquer um. Além disso, um polimorfismo cristalino pode estar presente, mas não é limitante, po- dendo qualquer forma cristalina ser simples ou uma mistura de formas cristalinas, ou um anidrido ou hidrato. Além disso, o assim chamado metabólito que é produzido pela degradação do composto da presente invenção in vivo é incluído no âmbito da pre- sente invenção.
[0192]“Isomerismo” significa compostos que têm formulas moleculares idênti- cas, mas que diferem na natureza ou na sequência de ligação de seus átomos ou na disposição dos seus átomos no espaço. Os isômeros que diferem em disposição dos seus átomos no espaço são denominados “estereoisômeros”. Os estereoisômeros que não são imagens simétricas um do outro são denominados “diastereoisômeros” e os estereoisômeros que são imagens simétricas que não podem ser sobrepostas são denominados “enantiômeros” ou às vezes isômeros óticos. Um átomo de carbono li- gado a quatro substituintes não idênticos é denominado um “centro quiral”.
[0193]“Isômero quiral” significa um composto tendo pelo menos um centro qui- ral. Ele tem duas formas enantioméricas de quiralidade oposta e pode existir ou em forma de um enantiômero individual ou em forma de uma mistura de enantiômeros. Uma mistura que contém quantidades iguais de formas enantioméricas individuais de quiralidade oposta é denominada uma “mistura racêmica”. Um composto que tem mais de um centro quiral tem 2n-1 pares enantioméricos, em que n é o número de centros quirais. Os compostos que têm mais de um centro quiral podem existir ou em forma de um diastereoisômero individual ou em forma de uma mistura de diastereoi- sômeros, denominada uma “mistura diastereoisomérica”. Quando um centro quiral está presente, um estereoisômero pode ser caracterizado pela configuração absoluta (R ou S) daquele centro quiral. A configuração absoluta se refere à disposição no espaço dos substituintes ligados ao centro quiral. Os substituintes ligados ao centro quiral em consideração são classificados de acordo com a Sequence Rule de Cahn, Ingold e Prelog. (Cahn et al., Angew. Chem. Inter. Edit. 1966., 5, 385; errata 511; Cahn et al., Angew. Chem. 1966, 78, 413; Cahn e Ingold, J. Chem. Soc. 1951 (Londres), 612; Cahn et al., Experientia 1956, 12, 81; Cahn, J., Cham. Educ. 1964, 41, 116).
[0194]“Isômeros Geométricos” significa os diastereoisômeros que devem sua existência a uma rotação impedida ao redor de ligações duplas. Estas configurações são diferenciadas em seus nomes pelos prefixos cis e trans, ou Z e E, o que indica que os grupos se encontram do mesmo lado da ligação dupla ou de lados opostos da ligação dupla na molécula de acordo com as regras de Cahn-Ingold-Prelog.
[0195]Além disso, as estruturas e os outros compostos discutidos neste pe- dido incluem todos os isômeros atrópicos seus. “Isômeros atrópicos” são o tipo de estereoisômeros em que os átomos de dois isômeros são dispostos de modo diferente no espaço. Os isômeros atrópicos devem sua existência a uma rotação restrita cau- sada pelo impedimento de rotação de grupos grandes ao redor de uma ligação central. Tais isômeros atrópicos tipicamente existem em forma de uma mistura, no entanto, como resultado de avanços recentes em técnicas de cromatografia, foi possível se separar misturas de dois isômeros atrópicos em casos seletos.
[0196]Os termos “polimorfas cristalinas” ou “polimorfas” ou “formas cristalinas” significam estruturas cristalinas em que um composto (ou sal ou solvato seu) pode se cristalizar em diferentes disposições de acondicionamento cristalino, tendo todas elas a mesma composição elementar. As formas cristalinas diferentes geralmente têm pa- drões de difração em raios X, espectros no infravermelho, pontos de fusão, dureza, densidade, formato do cristal, propriedades óticas e elétricas, estabilidade e solubili- dade diferentes. O solvente de recristalização, a taxa de cristalização, a temperatura de armazenagem e outros fatores podem fazer predominar uma forma cristalina. As polimorfas cristalinas dos compostos podem ser preparadas por cristalização em con- dições diferentes.
[0197]Além disso, os compostos da presente invenção, os sais dos compos- tos, por exemplo, podem existir ou na forma hidratada ou na não hidratada (anidra) ou em forma de solvatos com outras moléculas de solventes. Exemplos não limitantes de hidratos incluem monoidratos, diidratos etc. Exemplos não limitantes de solvatos in- cluem solvatos em etanol, solvatos em acetona etc.
[0198]“Solvatos” significa formas de adição de solvente que contêm ou quan- tidades estequiométricas ou não estequiométricas de solvente. Tais compostos têm a tendência de aprisionar uma relação molar fixa de moléculas de solvente no estado sólido cristalino, formando assim um solvato. Se o solvente for água, o solvato formado é um hidrato, quando o solvente for álcool, o solvato formado é um alcoolato. Os hi- dratos são formados pela combinação de uma ou mais moléculas de água com uma das substâncias em que a água conserva o seu estado molecular como H2O, sendo tal combinação capaz de formar um ou mais hidratos.
[0199]“Tautômeros” se refere a compostos cujas estruturas diferem nitida- mente na disposição dos átomos, mas que existem em um equilíbrio fácil e rápido. Deve ficar subentendido que os compostos da Fórmula I podem ser ilustrados em forma de tautômeros diferentes. Deve ficar também subentendido que quando os com- postos têm formas tautoméricas, então todas as formas tautoméricas se destinam a incidir no âmbito da invenção, e a denominação dos compostos não exclui qualquer forma tautomérica.
[0200]Alguns compostos da presente invenção podem existir em uma forma tautomérica e são também destinados a incidir no âmbito da presente invenção.
[0201]Os compostos, sais e promedicamentos da presente invenção podem existir em diversas formas tautoméricas inclusive na forma de enol e imina, e na forma ceto e enamino e isômeros geométricos e misturas suas. Todas tais formas tautomé- ricas são incluídas no âmbito da presente invenção. Os tautômeros existem em forma de misturas de um conjunto tautomérico em solução. Em forma sólida, geralmente um tautômero predomina. Mesmo que possa ter sido descrito um tautômero, a presente invenção inclui todos os tautômeros dos compostos da presente invenção.
[0202]Um tautômero é um de dois ou mais isômeros estruturais que existe em equilíbrio e que são facilmente convertidos de uma forma isomérica em outra. Esta reação resulta na migração formal de um átomo de hidrogênio acompanhada por uma troca de ligações duplas conjugadas adjacentes. Em soluções em que é possível a tautomerização, um equilíbrio químico dos tautômeros será atingido. A relação exata dos tautômeros dependerá de diversos fatores, incluindo a temperatura, solvente, e pH. O conceito de tautômeros que são interconversíveis por tautomerizações é deno- minado tautomerismo.
[0203]Dos diversos tipos de tautomerismo que são possíveis, dois são habi- tualmente observados. Em tautomerismo ceto-enol ocorre um deslocamento simultâ- neo de elétrons e um átomo de hidrogênio. O tautomerismo anel-cadeia é apresentado pela glicose. Ele resulta do grupo aldeído (-CHO) em uma molécula de cadeia de açú- car reagir com um dos grupos hidróxi (-OH) na mesma molécula para lhe conferir uma forma cíclica (formato de anel).
[0204]As tautomerizações são catalisadas por: Base: 1. desprotonação; 2. for- mação de um ânion deslocalizado (um enolato, por exemplo); 3. protonação em uma posição diferente do ânion; Ácido: 1. protonação; 2. formação de um cátion deslocali- zado; 3. desprotonação em uma posição diferente adjacente ao cátion.
[0205]Os pares tautoméricos comuns são: tautomerismo cetona-enol, amida- nitrila, lactama-lactima, amida-ácido imínico em anéis heterocíclicos (nas bases nu- cléicas guanina, timina e citosina, por exemplo), amina-enamina e enamina-enamina. Os exemplos incluem:
[0206]Deve se observar que a estrutura de alguns dos compostos da invenção inclui átomos de carbono assimétricos. Deve ficar subentendido, portanto, que os isô- meros que se originam de tal assimetria (todos os enantiômeros e diastereoisômeros, por exemplo) são incluídos no âmbito da invenção, a não ser que seja indicado em contrário. Tais isômeros podem ser obtidos em forma substancialmente pura por téc- nicas de separação clássicas e por síntese estereoquimicamente controlada. Além disso, as estruturas e outros compostos e frações discutidos neste pedido também incluem todos os seus tautômeros. Os alcenos podem incluir ou a geometria E ou a Z, quando for apropriado. Os compostos da presente invenção podem existir na forma estereoisomérica, podendo, portanto, ser produzidos em forma de estereoisômeros individuais ou em forma de misturas.
[0207]Conforme empregado no presente, o termo “análogo” se refere a um composto químico que é estruturalmente análogo a um outro, mas difere ligeiramente em composição (tal como na substituição de um átomo por um átomo de um elemento diferente ou na presença de um grupo funcional específico, ou na substituição de um grupo funcional por um outro grupo funcional). Assim, um análogo é um composto que é análogo ou comparável em função e aparência, mas não em estrutura ou origem ao composto de referência.
[0208]Conforme empregado no presente, o termo “derivado” se refere a com- postos que têm uma estrutura de núcleo central comum, e são substituídos com di- versos grupos conforme descrito no presente documento. Todos os compostos repre- sentados pela fórmula I, por exemplo, são derivados do indol e têm a Fórmula I como um núcleo central.
[0209]O termo “bioisóstero” se refere a um composto que resulta da troca de um átomo ou de um grupo de átomos com um outro átomo ou grupo de átomos de um modo geral semelhante. O objetivo de uma substituição bioisostérica é a criação de um novo composto com propriedades biológicas semelhantes às de um composto progenitor. A substituição bioisostérica pode ser baseada físico-quimicamente ou to- pologicamente. Exemplos de bioisósteros do ácido carboxílico incluem acil sulfonimi- das, tetrazóis, sulfonatos e fosfonatos. Veja, por exemplo, Patani e La Voie, Chem. Rev. 96, 3147-3176 (1996).
[0210]Uma “composição farmacêutica” é uma formulação contendo os com- postos divulgados em uma forma adequada para a administração a um paciente. Em uma modalidade, a composição farmacêutica se encontra em forma de dosagem em volume ou unitária. A forma de dosagem unitária é qualquer uma de uma variedade de formas, incluindo, por exemplo, uma cápsula, uma bolsa IV, um comprimido, uma bomba individual ou um inalador de aerossol, ou um frasco. A quantidade do ingredi- ente ativo (uma formulação do composto divulgado ou sal, hidrato, solvato ou isômero seu, por exemplo) em uma dose unitária de composição é uma quantidade efetiva e se faz a mesma variar de acordo com o tratamento específico envolvido. Os versados na técnica observarão que às vezes é necessário se fazer variações rotineiras na do- sagem dependendo da idade e da condição do paciente. A dosagem também depen- derá da via de administração. Uma variedade de vias é contemplada, incluindo oral, pulmonar, retal, parenteral, transdérmica, subcutânea, intravenosa, intramuscular, in- traperitoneal, inalacional, bucal, sublingual, intrapleural, intratecal, intranasal, e seme- lhantes. As formas de dosagem para a administração tópica ou transdérmica de um composto da presente invenção incluem pós, pulverizações, unguentos, pastas, cre- mes, loções, géis, soluções, adesivos e inalantes. Em uma modalidade preferida, o composto ativo é misturado em condições estéreis com um veículo farmaceutica- mente aceitável, e com qualquer conservante, tampão ou propelente que seja neces- sário.
[0211]O termo “dose relâmpago” se refere a formulações de composto que são formas de dosagem de rápida dispersão.
[0212]O termo “liberação imediata” é definido como uma liberação de com- posto de uma forma de dosagem em um período de tempo relativamente breve, ge- ralmente em até aproximadamente 60 minutos. O termo “liberação modificada” é de- finido como incluindo liberação retardada, liberação prolongada e liberação pulsada. O termo “liberação pulsada” é definido como uma série de liberações de medicamento de uma forma de dosagem. O termo “liberação sustentada” ou “liberação prolongada” é definido como a liberação contínua de um composto de uma forma de dosagem durante um período prolongado.
[0213]Um “paciente” inclui mamíferos, seres humanos, por exemplo, animais de companhia (cães, gatos, pássaros, por exemplo, e semelhantes), animais de cria- ção (bovinos, ovinos, porcinos, equinos, aves, por exemplo, e semelhantes) e animais de laboratório (ratos, camundongos, cobaias, aves, por exemplo, e semelhantes). O mais preferível que o paciente seja um ser humano.
[0214]Conforme empregado no presente, a expressão “farmaceuticamente aceitável” se refere àqueles compostos, materiais, composições, veículos e/ou formas de dosagem que são, dentro do âmbito de critério médico razoável, adequados para serem usados em contato com os tecidos de seres humanos e animais, sem apresen- tar uma toxicidade, irritação, resposta alérgica excessiva ou outro problema ou com- plicação, e compatíveis com uma relação razoável benefício/risco.
[0215]“Excipiente farmaceuticamente aceitável” significa um excipiente que é útil na preparação de uma composição farmacêutica que é geralmente seguro, não tóxico e nem biologicamente nem de outro modo qualquer indesejável e inclui excipi- ente que é aceitável para uso veterinário assim como para uso farmacêutico humano. Um “excipiente farmaceuticamente aceitável”, conforme usado no relatório e reivindi- cações inclui tanto um como muitos de um tal excipiente.
[0216]Os compostos da invenção são capazes de formar ainda sais. Todas estas formas são visadas pelo âmbito da invenção reivindicada.
[0217]“Sal farmaceuticamente aceitável” de um composto significa um sal que é farmaceuticamente aceitável e que possui a atividade farmacológica desejada do composto progenitor.
[0218]Conforme empregado no presente, “sais farmaceuticamente aceitáveis” se referem a derivados dos compostos divulgados em que o composto progenitor é modificado formando-se sais de ácido e de base dos mesmos. Exemplos de sais far- maceuticamente aceitáveis incluem, sem limitação, sais ácidos minerais ou orgânicos de resíduos básicos tais como aminas, sais alcalinos ou orgânicos de resíduos ácidos tais como ácidos carboxílicos e semelhantes. Os sais farmaceuticamente aceitáveis incluem os sais não tóxicos convencionais ou os sais de amônio quaternário do com- posto progenitor formados, por exemplo, a partir de ácidos orgânicos e inorgânicos não tóxicos. Tais sais não tóxicos convencionais incluem, por exemplo, sem limitação, aqueles derivados de ácidos inorgânico e orgânicos selecionados de 2-acetoxi-ben- zóico, 2-hidroxietano sulfônico, acético, ascórbico, benzeno sulfônico, benzóico, bicar- bônico, carbônico, cítrico, edético, etano dissulfônico, 1,2-etano sulfônico, fumárico, glicoheptônico, glicônico, glutâmico, glicólico, glicoliarsanílico, hexil-resorcínico, hidra- bâmico, bromídrico, clorídrico, iodídrico, hidroximaléico, hidroxinaftóico, isotiônico, láctico, lactobiônico, lauril sulfônico, maléico, málico, mandélico, metano sulfônico, napsílico, nítrico, oxálico, pamóico, pantotênico, fenilacético, fosfórico, poligalacturô- nico, propiônico, salicílico, esteárico, subacético, succínico, sulfâmico, sulfanílico, sul- fúrico, tânico, tartárico, tolueno sulfônico, e dos aminoácidos que ocorrem habitual- mente, tais como glicina, alanina, fenilalanina, arginina etc.
[0219]Outros exemplos incluem ácido hexanóico, ácido ciclopentano propiô- nico, ácido pirúvico, ácido malônico, ácido 3-(4-hidróxi-benzoil)benzóico, ácido cinâ- mico, ácido 4-cloro-benzeno-sulfônico, ácido 2-naftaleno-sulfônico, ácido 4-tolueno- sulfônico, ácido canfor-sulfônico, ácido 4-metilbiciclo-[2,2,2]-oct-2-eno-1-carboxílico, ácido 3-fenil propiônico, ácido trimetil acético, ácido terc-butilacético, ácido mucônico e semelhantes. A invenção também abrange sais formados quando um próton ácido presente no composto progenitor ou é substituído por um íon metálico um íon de metal alcalino, por exemplo, um íon alcalino terroso ou um íon de alumínio; ou se coordena com uma base orgânica tal como etanolamina, dietanolamina, trietanolamina, trometamina, N-metil glucamina e semelhantes. Deve ficar subentendido que todas as referências a sais farmaceuticamente aceitáveis incluem formas de adição de solvente (solvatos) ou formas cristalinas (polimorfas), conforme definido no presente docu- mento, do mesmo sal.
[0220]Os sais farmaceuticamente aceitáveis da presente invenção podem ser sintetizados a partir de um composto progenitor que contém uma fração básica ou ácida por métodos químicos convencionais. Em geral, tais sais podem ser preparados fazendo-se reagir as formas de ácido ou base livre destes compostos com uma quan- tidade estequiométrica da base ou ácido apropriado em água ou em um solvente or- gânico, ou em uma mistura dos dois; em geral, são preferidos meios não aquosos como éter, acetato de etila, etanol, isopropanol ou acetonitrila. Listas de sais adequa- dos são encontradas em Remington’s Pharmaceutical Sciences, 18a. ed. (Mack Pub- lishing Company, 1990). Sais podem incluir, por exemplo, sem limitação, os sais clo- ridrato e acetato dos compostos alifáticos contendo amina, contendo hidroxil amina e contendo imina da presente invenção.
[0221]Os compostos da presente invenção podem também ser preparados em forma de ésteres, ésteres farmaceuticamente aceitáveis, por exemplo. Um grupo funcional ácido carboxílico em um composto, por exemplo, pode ser convertido no seu éster correspondente, um éster metílico, etílico, por exemplo, ou outro. Além disso, um grupo álcool em um composto pode ser convertido no seu éster correspondente, um éster acetato, propionato, por exemplo, ou outro.
[0222]Os compostos da presente invenção podem também ser preparados em forma de promedicamentos, promedicamentos farmaceuticamente aceitáveis, por exemplo. Os termos “pro-medicamento” e “promedicamento” são usados indiferente- mente e se referem a qualquer composto que libera um medicamento progenitor ativo in vivo. Como os promedicamentos são conhecidos como intensificando numerosas qualidades desejáveis de produtos farmacêuticos (solubilidade, biodisponibilidade, fabricação, por exemplo, etc.), os compostos da presente invenção podem ser forne- cidos na forma de promedicamento. Assim, a presente invenção se destina a abranger promedicamentos dos compostos reivindicados na presente invenção, métodos de fornecimento dos mesmos e composições contendo os mesmos. “Promedicamentos” se destinas a incluir qualquer veículo ligado por covalência que liberar um medica- mento progenitor ativo da presente invenção in vivo quando tal promedicamento é administrado a um paciente. Os promedicamentos da presente invenção são prepa- rados modificando-se grupos funcionais presentes no composto de tal modo que as modificações sejam clivadas, ou em manipulação rotineira ou in vivo, no composto progenitor. Os promedicamentos incluem compostos da presente invenção em que um grupo hidróxi, amino, sulfidrila, carboxila, ou carbonila está ligado a qualquer grupo que pode ser clivado in vivo para formar uma hidroxila livre.
[0223]Exemplos de promedicamentos incluem, sem limitação, ésteres (ace- tato, dialquilamino acetatos, formiatos, fosfatos, sulfatos e derivados de benzoato, por exemplo) e carbamatos (N,N-dimetilamino-carbonila, por exemplo) de grupos funcio- nais hidróxi, grupos ésteres (ésteres etílicos, ésteres morfolino-etanol, por exemplo) de grupos funcionais carboxílicos, derivados N-acílicos (an-acetílicos, por exemplo) bases N-Mannich, bases de Schiff e enaminonas dos grupos funcionais amino, oxi- mas, acetais, cetais e ésteres enólicos de grupos funcionais cetona e aldeído em com- postos da Fórmula I e semelhantes. Veja Bundegaard, N. “Design of Prodrugs” p1-92, Elesevier, Nova York-Oxford (1985).
[0224]“Grupo protetor” se refere a um agrupamento de átomos que, quando ligado a um grupo reativo em uma molécula mascara, reduz ou previne aquela reati- vidade. Exemplos de grupos protetores podem ser encontrados em Green e Wuts, Protective Groups in Organic Chemistry, (Wiley, 2a. ed. 1991); Harrison and Harrison et al., Compendium of Synthetic Organic Methods, Vols. 1-8 (John Wiley and Sons, 1971-1996); e Kocienski, Protecting Groups, (Verlag, 3a. ed. 2003).
[0225]O termo “grupo protetor de amina” é destinado a significar um grupo funcional que converte uma amina, amida ou outra reação contendo nitrogênio em um grupo químico diferente que é substancialmente inerte às condições de uma reação química específica. Os grupos protetores de amina são de preferência removidos fácil e seletivamente com um bom rendimento nas condições que não afetam outros gru- pos funcionais da molécula. Exemplos de grupos protetores de amina incluem, sem limitação, formila, acetila, benzila, t-butil-dimetilsilila, t-butil-difenilsilila, t-butilóxi-car- bonila (Boc), p-metóxi-benzila, metóxi-metila, tosila, triflúor-acetila, trimetil-silila (TMS), fluorenil-metilóxi-carbonila, 2-trimetil-silil-etilóxi-carbonila, 1-metil-1-(4-bifeni- lil)etóxi-carbonila, alilóxi-carbonila, benzilóxi-carbonila (CB\), 2-trimetilsilil-etano-sulfo- nila (SES), grupos tritila e tritila substituídos, 9-fluorenil-metilóxi-carbonila (FMOC), ni- tro-veratrilóxi-carbonila (NVOC), e semelhantes. Outros grupos protetores de amina adequados são diretamente identificados pelos versados na técnica.
[0226]Grupos protetores de hidróxi representativos incluem aqueles em que o grupo hidróxi ou é acilado ou alquilado tal como benzila, e éteres tritílicos assim como éteres alquílicos, éteres tetraidropiranílicos, éteres trialquilsilílicos e éteres alílicos.
[0227]“Composto estável” e “estrutura estável” indicam um composto que é suficientemente robusto para sobreviver ao isolamento até um grau útil de pureza a partir de uma mistura de reação e a formulação em um agente terapêutico eficaz.
[0228]No relatório, as formas no singular também incluem as no plural, a não ser que o contexto claramente determine o contrário. A não ser que seja definido em contrário, todos os termos técnicos e científicos usados no presente documento têm o mesmo significado que é habitualmente compreendido pelos versados na técnica à qual a invenção pertence. Em caso de conflito, prevalecerá o presente relatório. Todas as porcentagens e relações usadas no presente documento, a não ser que seja indi- cado em contrário, são em peso.
[0229]“Terapia de combinação” (ou “terapia combinada”) inclui a administração de um composto da invenção e pelo menos um segundo agente como parte de um regime de tratamento específico destinado a proporcionar o efeito bené- fico da ação combinada destes agentes terapêuticos. O efeito benéfico da combinação inclui, sem limitação, a ação combinada farmacocinética ou farmacodinâmica resul- tando da combinação de agentes terapêuticos. A administração destes agentes tera- pêuticos em combinação tipicamente é conduzida durante um período de tempo defi- nido (geralmente minutos, horas, dias ou semanas dependendo da combinação sele- cionada). “Terapia de combinação” pode ser, mas geralmente não é, destinada a abranger a administração de dois ou mais destes agentes terapêuticos como parte de regimes de monoterapia separados que incidental e arbitrariamente resultam nas combinações da presente invenção.
[0230]“Terapia de combinação” se destina a abranger a administração destes agentes terapêuticos em uma maneira em sequência, isto é, em que cada agente terapêutico é administrado em uma ocasião diferente, assim como à administração destes agentes terapêuticos ou de pelo menos dois destes agentes terapêuticos, de um modo substancialmente simultâneo. A administração substancialmente simultânea pode ser efetuada, por exemplo, por administração ao paciente de uma única cápsula tendo uma relação fixa de cada agente terapêutico ou em uma multiplicidade de cáp- sulas individuais para cada um dos agentes terapêuticos. A administração em sequên- cia ou substancialmente simultânea de cada agente terapêutico pode ser efetuada por qualquer via adequada incluindo, sem limitação, vias orais, vias intravenosas, vias intramusculares e a absorção direta através de tecidos da membrana mucosa. Os agentes terapêuticos podem ser administrados pela mesma via ou por vias diferentes. Um primeiro agente terapêutico da combinação selecionado, por exemplo, pode ser administrado por injeção intravenosa, ao passo que os demais agentes terapêuticos da combinação podem ser administrados oralmente. Alternativamente, todos os agen- tes terapêuticos, podem ser administrados, por exemplo, oralmente ou então todos os agentes terapêuticos podem ser administrados por injeção intravenosa. A sequência em que os agentes terapêuticos são administrados não é estritamente crítica.
[0231]“Terapia de combinação” também abrange a administração dos agen- tes terapêuticos conforme descrito acima em uma outra combinação com outros in- gredientes biologicamente ativos e terapia não medicamentosa (cirurgia ou tratamento com radiação, por exemplo). Nos casos em que a terapia de combinação compreende ainda um tratamento não medicamentoso, o tratamento não medicamentoso pode ser conduzido em qualquer ocasião adequada, desde que seja atingido um efeito benéfico da ação combinada da combinação dos agentes terapêuticos e do tratamento não medicamentoso. Em casos apropriados, o efeito benéfico é ainda atingido, por exem- plo, quando o tratamento não medicamentoso é temporariamente removido da admi- nistração dos agentes terapêuticos, talvez durante dias ou mesmo semanas.
[0232]Em toda a descrição, sempre que as composições são descritas como tendo, incluindo ou compreendendo componentes específicos, pretende-se que as composições também consistam essencialmente, ou consistam, nos componentes ci- tados. De modo análogo, nos casos em que os processos são descritos como tendo, incluindo ou compreendendo etapas de processo específicas, os processos também consistem essencialmente, ou consistem nas etapas de processamento citadas. Além disso, deve ficar subentendido que a ordem das etapas ou a ordem da condução de determinadas ações não têm importância desde que a invenção permaneça operável. Além disso, duas ou mais etapas ou ações podem ser conduzidas simultaneamente.
[0233]Os compostos, ou sais farmaceuticamente aceitáveis seus, são admi- nistrados por via oral, nasal, transdérmica, pulmonar, por inalação, por via bucal, sub- lingual, intraperitoneal, subcutânea, intramuscular, intravenosa, retal, intrapleural, in- tratecal e parenteral. Em uma modalidade preferida, o composto é administrado por via oral. os versados na técnica reconhecerão as vantagens de determinadas vias de administração.
[0234]O regime de dosagem que utiliza os compostos é selecionado de acordo com uma variedade de fatores que incluem, o tipo, espécie, idade, peso, sexo e condição médica do paciente; a gravidade da condição a ser tratada; a via de admi- nistração; a função renal e hepática do paciente; e o composto específico ou seu sal empregado. Um clínico ou veterinário com habilidade ordinária poderá facilmente de- terminar e prescrever a quantidade efetiva do medicamento necessária para prevenir, se opor ou interromper o progresso da condição.
[0235]As técnicas para a formulação e administração dos compostos divulga- dos da invenção podem ser encontradas em Remington: the Science and Practice of Pharmacy, 19a edição, Mack Publishing Co., Easton, PA (1995). Em uma modalidade, os compostos descritos no processo e os sais farmaceuticamente aceitáveis seus são usados em preparados farmacêuticos em combinação com um veículo ou diluente farmaceuticamente aceitável. Os veículos farmaceuticamente aceitáveis adequados incluem cargas ou diluentes sólidos inertes e soluções aquosas ou orgânicas estéreis. Os compostos estarão presentes em tais composições farmacêuticas em quantidades suficientes para fornecer a quantidade de dosagem desejada dentro dos limites des- critos no presente documento.
[0236]Em uma modalidade, o composto é preparado para a administração oral, em que os compostos descritos ou seus sais são combinados com um veículo ou diluente sólido ou líquido adequado para formar cápsulas, comprimidos, pílulas, pós, xaropes, soluções, suspensões e semelhantes.
[0237]Os comprimidos, pílulas, cápsulas e semelhantes contêm de aproxima- damente 1 a aproximadamente 99 por cento em peso do ingrediente ativo e um aglu- tinante tal como goma tragacanto, acácia, amido de milho, ou gelatina; excipientes tais como fosfato dicálcico; um agente desintegrante tal como amido de milho, amido de batata ou ácido algínico; um lubrificante tal como estearato de magnésio; e/ou um agente adoçante tal como sacarose, lactose, sacarina, xilitol e semelhantes. Quando uma forma de dosagem unitária é uma cápsula, ela frequentemente contém, além dos materiais do tipo acima, um veículo líquido tal como um óleo graxo.
[0238]Em algumas modalidades, diversos outros materiais estão presentes em forma de revestimento ou para modificar a forma física da unidade de dosagem. Em algumas modalidades, por exemplo, os comprimidos são revestidos com goma laca, açúcar ou ambos. Em algumas modalidades, um xarope ou elixir contém, além do ingrediente ativo, sacarose como um agente adoçante, metila e propil parabenos como conservantes, um corante e um aromatizante tal como um aroma de cereja ou laranja e semelhante.
[0239]Para algumas modalidades referentes a administração parenteral, os compostos descritos, ou seus sais, solvatos, tautômeros ou polimorfas podem ser combinados com meios aquosos ou orgânicos estéreis para formar soluções ou sus- pensões injetáveis. As composições injetáveis são, de preferência, soluções, suspen- sões aquosas ou isotônicas. As composições podem ser esterilizadas e/ou conter ad- juvantes, tais como agentes conservantes, estabilizantes, umectantes ou emulsifican- tes, promotores de solução, sais para a regulagem da pressão osmótica e/ou tampões. Além disso, elas podem ainda conter outras substâncias terapeuticamente valiosas. As composições são preparadas de acordo com métodos de mistura, granulação ou revestimento convencionais, respectivamente, e contêm de aproximadamente 0,1 a 75%, de preferência de aproximadamente 1 a 50%, do ingrediente ativo.
[0240]As soluções injetáveis, por exemplo, são produzidas usando-se solven- tes tais como óleo de gergelim ou de amendoim, ou propileno glicol em solução aquosa, assim como soluções aquosas de sais farmaceuticamente aceitáveis hidros- solúveis dos compostos. Em algumas modalidades, as dispersões são preparadas em glicerol, polietileno glicóis líquidos, e suas misturas em óleos. Em condições habituais de armazenagem e uso, estes preparados contêm um conservante para impedir o crescimento de microrganismos. Os termos “administração parenteral” e “administrado por via parenteral”, conforme empregados no presente, significam mo- dos de administração diferentes da administração enteral e tópica, geralmente por injeção e incluem, sem limitação, injeção e infusão intravenosa, intramuscular, intra- arterial, intratecal, intracapsular, intra-orbital, intracardíaca, intradérmica, intraperito- neal, transtraqueal, subcutânea, subcuticular, intra-articular, subcapsular, subarac- nóide, intraespinhal e intraesternal.
[0241]Para a administração retal, as composições farmacêuticas adequadas são, por exemplo, preparados tópicos os supositórios ou enemas. É vantajoso que os supositórios sejam preparados a partir de emulsões ou suspensões graxas. As com- posições podem ser esterilizadas e/ou conter adjuvantes, tais como agentes conser- vantes, estabilizantes, umectantes ou emulsificantes, promotores de solução, sais para a regulagem da pressão osmótica e/ou tampões. Além disso, elas podem tam- bém conter outras substâncias terapeuticamente valiosas. As composições são pre- paradas de acordo com métodos de mistura, granulação ou revestimento convencio- nais, respectivamente, e contêm de aproximadamente 0,1 a 75%, de preferência de aproximadamente 1 a 50% do ingrediente ativo.
[0242]Em algumas modalidades, os compostos são formulados para fornecer o agente ativo por administração pulmonar, por administração de uma formulação em aerossol, por exemplo, contendo o agente ativo de um pulverizador de bomba manual, nebulizador ou de um inalador pressurizado com doses medidas, por exemplo. Em algumas modalidades, formulações adequadas deste tipo também incluem outros agentes, tais como agentes antiestáticos, para manter os compostos divulgados em forma de aerossóis efetivos.
[0243]Um dispositivo de fornecimento de medicamento para o fornecimento de aerossóis compreende um recipiente de aerossol adequado com uma válvula me- didora contendo uma formulação farmacêutica em aerossol, conforme descrito, e um alojamento de atuador adaptado para segurar o recipiente e para permitir o fornecimento do medicamento. O recipiente no dispositivo de fornecimento de medi- camento tem um espaço na cabeceira que consiste em mais de aproximadamente 15% do volume total do recipiente. Frequentemente, o polímero destinado para a ad- ministração pulmonar é dissolvido, suspenso ou emulsificado em uma mistura de um solvente, tensoativo e propelente. A mistura é mantida sob pressão em um recipiente que foi lacrado com uma válvula medidora.
[0244]Para a administração nasal, pode ser usado um veículo sólido ou um líquido. O veículo sólido inclui um pó grosseiro com tamanho de partículas entre os limites de aproximadamente 20 e aproximadamente 500 micra, por exemplo, e tal for- mulação é administrada por uma rápida inalação através das passagens nasais. Em algumas modalidades em que se empregado o veículo líquido, a formulação é admi- nistrada em forma de um pulverizador ou gotas nasais e inclui soluções oleosas ou aquosas dos ingredientes ativos.
[0245]Também visadas são formulações que consistem em formas de dosa- gem de rápida dispersão, também conhecidas como formas de “dose relâmpago”. Mais especificamente, algumas modalidades da presente invenção são formuladas em forma de composições que liberam os seus ingredientes ativos dentro de um pe- ríodo curto de tempo, tipicamente, por exemplo, em menos de aproximadamente cinco minutos, de preferência em menos de aproximadamente noventa segundos, sendo mais preferível em menos de aproximadamente trinta segundo, sendo o mais preferí- vel que sejam liberados em menos de aproximadamente dez a quinze segundos. Tais formulações são adequadas para a administração a um paciente por meio de uma variedade de vias, por inserção em uma cavidade do corpo, por exemplo, ou por apli- cação a uma superfície corporal úmida ou a um ferimento aberto.
[0246]Tipicamente uma “dosagem relâmpago” é uma forma de dosagem só- lida que é administrada por via oral e que se dispersa rapidamente na boca, e não exige grande esforço para ser engolida e permite que o composto seja rapidamente ingerido ou absorvido através das membranas mucosais orais. Em algumas modali- dades, formas de dosagem de dispersão rápida adequadas são também usadas em outras aplicações, inclusive no tratamento de ferimento e outros insultos corporais e estados mórbidos em que a liberação do medicamento por umidade externamente fornecida não é possível.
[0247]Formas de “dose relâmpago” são conhecidas na técnica; veja, por exemplo, formas de dosagem efervescentes e revestimentos de liberação rápida de micropartículas insolúveis nas patentes U.S. Nos. 5.578.322 e 5.607.697; espumas e líquidos liofilizados nas patentes U.S. Nos. 4.642.903 e 5.631.023; formas de dosa- gem de fiação no estado fundido nas patentes U.S. Nos. 4.855.326, 5.380.473 e 5.518.730; fabricação de formas livres sólidas na patente U.S. No. 6.471.992; matriz de veículo à base de sacarídeo e um aglutinante líquido nas patentes U.S. Nos. 5.587.172, 5.616.344, 6.277.406. e 5.622.719; e outras formas conhecidas na técnica.
[0248]Os compostos da invenção são também formulados em forma de for- mulações de “liberação pulsada”, em que o composto é liberado das composições farmacêuticas em uma série de liberações (isto é, pulsos). Os compostos são também formulados em forma de formulações de “liberação sustentada”, em que o composto é continuamente liberado da composição farmacêutica durante um período prolon- gado.
[0249]Também visadas são formulações, formulações líquidas, por exemplo, incluindo agentes encapsulantes ou solvatantes cíclicos ou acíclicos, tais como ciclo- dextrinas, por exemplo, poliéteres ou polissacarídeos (metilcelulose, por exemplo), ou o que é mais preferível, derivados polianiônicos de β-ciclodextrina com um grupo de sal sulfonato de sódio separado da cavidade lipófila por um grupo espaçador éter al- quílico ou polissacarídeos. Em uma modalidade preferida, o agente é metilcelulose. Em uma outra modalidade preferida, o agente é um derivado polianiônico de β-ciclo- dextrina com um sal sulfonato de sódio separado da cavidade lipófila por um grupo espaçador éter butílico, CAPTISOL® (CyDex, Overland, KL). Os versados na técnica poderão avaliar as relações da formulação de agente adequado/composto divulgado por preparação de uma solução do agente em água, uma solução a 40% em peso, por exemplo; por preparação de diluições em série, para produzir soluções a 20%, 10%, 5%, 2,5%, 0% (controle), por exemplo, e semelhantes; por acréscimo de um excesso (em comparação com a quantidade que pode ser solubilizada pelo agente) do composto divulgado; por mistura em condições apropriada, com aquecimento, agi- tação sonicação, por exemplo, e semelhantes; por centrifugação ou filtração das mis- turas resultante para obter soluções transparentes; e por análise das soluções para a concentração do composto descrito.
[0250]Todas as publicações e documentos de patentes citados no presente documento são incorporados ao presente documento a título de referência como se cada publicação ou documento tenha sido específica e individualmente indicada para ser incorporada ao presente invenção a título de referência. A citação de publicações e de documentos de patentes não se destina a ser uma admissão de que qualquer uma consiste em técnica anterior, nem constitui qualquer admissão no tocante ao seu conteúdo ou data dos mesmos. A invenção tendo agora sido descrita a título de des- crição por escrito, os versados na técnica observarão que a invenção pode ser colo- cada em prática em uma variedade de modalidades e que a descrição acima e os exemplos abaixo são dados a título de ilustração e não representam uma limitação às reivindicações que seguem.
[0251]EXEMPLOS
[0252]Exemplo 1: Sínteses
[0253]Sínteses representativas de compostos da invenção são aqui descritas.
[0255]A uma solução de 3-cianofenol (5,00 g, 42,00 mmol) em acetona (100 mL), acrescentaram-se carbonato de potássio (5,79 g, 42,0 mmol), iodeto de potássio (335 mg, 21,0 mmol) e brometo de benzila (4,20 mL, 42,00 mmol) e fez-se refluir a mistura de reação durante 12 horas (TLC, acetato de etila:hexano a 1:1, Rf =0,6), removeu-se então o solvente a vácuo e repartiu-se o resíduo entre água (50 mL) e acetato de etila (50 mL), lavou-se a fase orgânica com água duas vezes e secou-se sobre sulfato de sódio anidro e fez-se evaporar a pressão reduzida, obtendo-se o éter alvo em forma de um óleo amarelo (7,46g) rendimento de 96%; 1H RMN (DMSO(dimetilsulfoxido), 400 MHz): 7,51-7,33 (m, 9H), 5,16 (s, 2H). Cloridrato de 3-benzilóxi-benzilamina
[0256]A uma suspensão de hidreto de alumínio lítio, LAH (4,314 g, 113,684 mmol) em éter anidro (200 mL) acrescentou-se gota a gota durante 10 minutos, à temperatura ambiente, uma solução da 3-benzilóxi-benzonitrila em éter (7,92 g, 37,894 mmol), e deixou-se agitar durante 4 horas (TLC, acetato de etila: hexano 1:3, Rf = 0,5), extinguiu-se a reação com 10 mL de acetato de etila e 10 mL de água e filtrou-se. A fase orgânica foi lavada com água, secada sobre Na2SO4 e tratada com 10 mL de HCl conc. para formar um precipitado branco instantâneo (6 g), rendimento de 68%. 1H RMN (DMSO, 400 MHz): δ 8,33(s, 3H), 7,45-7,37(m, 4H), 7,34-7,30(m, 2H), 7,19(s, 1H), 7,02(t, J = l0 Hz, 2H), 5,l0 (s, 2H), 3,97 (s, 2H). N-(3-benzilóxi-benzil)-4-bifenil-acetamida
[0257]A uma solução de ácido 4-bifenil acético (2,29 g, 10,45 mmol) em dime- tilformamida, DMF, (30 mL) acrescentou-se diisopropil-etilamina, DIEA, (5,47 mL, 31,35 mmol) e agitou-se à temperatura ambiente durante 15 minutos, acrescentando- se então hexafluorfosfato de benzotriazolilóxi-tris [pirrolidino]-fosfônio, PyBOPTM, (5,43 g, 10,45 mmol) e continuou-se com a agitação durante outros 30 minutos, acres- centando-se então cloridrato de 3-benzilóxi-benzilamina (2,6 g, 10,45 mmol) e conti- nuando-se com a agitação durante 24 horas. A mistura de reação foi então vertida sobre água resfriada com gelo acidificada com (10 mL) HCl a 1N e extraída com ace- tato de etila (100 mL) e a fase orgânica foi lavada com uma solução saturada de NaHCO3, água e salmoura, secada sobre Na2SO4 e o solvente foi removido a vácuo, obtendo-se um pó branco amarelado do composto desejado (2,65 g), rendimento de 62%.
[0258]Um outro procedimento envolve o uso de formação de amida empre- gando-se cloreto ácido conforme mostrado na reação abaixo.
[0259]Ao ácido 4-bifenil acético (2,5 g) em um frasco, acrescentou-se cloreto de tionila (20 mL) e aqueceu-se até refluxo durante 1 h, resfriou-se, e o excesso de cloreto de tionila foi removido a vácuo até secar, sendo então o cloreto ácido produzido bruto 2,8 g, dissolvido em DCM (diclorometano) seco (30 mL), e acrescentado gota a gota a 0°C a uma quantidade equimolar da solução de 3-benzilóxi-benzilamina em DCM (10 mL) com (1,5 mol) de trietilamina (TEA) e agitou-se durante 5 horas, verteu- se então sobre água fria acidificada, lavou-se a fase orgânica com água, salmoura, e removeu-se o solvente a pressão reduzida para se obter a amida alvo com um rendi- mento de 80%. 1H RMN (DMSO, 500 MHz): δ 8,58 (t, J = 12Hz 1H), 7,60-7,57 (m, 4H), 7,44-7,29(m, 10H), δ 7,21(t, J = 16,5 Hz, 2H), 6,85(d, J = 6,5 Hz, 2H), 6,81(d, J = 8,0 Hz, 1H), 5,00(s, 2H), 4,24(d, J = 6Hz, 2H), 3,51(s, 2H). Composto 1: N-(3-hidróxi-benzil)-4-bifenil-acetamida
[0260]Para se remover o grupo benzila deste éter, (5,00 g, 13,35 mmol) ele foi dissolvido em metanol (20 mL), a esta solução acrescentou-se uma quantidade catalítica de Pd a 10% /C (355 mg, 2,21 mmol) em um hidrogenador Parr (55 psi (kPa)) durante 5 horas, filtrou-se através de celite e removeu-se o solvente, obtendo- se o fenol alvo em forma de um pó amarelado (3,20 g) rendimento de 84%, que foi cristalizado a partir de metanol, obtendo-se (1,5 g) de material cristalino branco, pf = 169-170°C. 1H RMN (DMSO, 400 MHz): δ 9,34(s, 1H), 8,53(s, 1H), 7,63(d, J = 8 Hz, 2H), 7,58(d, J = 8,4 Hz, 2H), 7,44(t, J = 7,6 Hz, 2H), 7,35(d, J = 8 Hz, 3H), 7,07(t, J = 8 Hz, 1H), 6,65-6,60(m, 3H), 4,17(d, J = 5,6 Hz, 2H), 3,5(s, 2H). FAB (bombardeio rápido com átomo) HRMS m/e calcd. Para (M+H) C21H20NO2: 317,1449; encontrado: 317,1484. Composto 2: N-(3-fluorbenzil)-4-bifenilacetamida
[0261]A uma solução de ácido 4-bifenil acético (2,00 g, 9,42 mmol) em DMF (20 mL) acrescentou-se DIEA (3,29 mL, 17,84 mmol) e agitou-se à temperatura ambi- ente durante 15 minutos, acrescentou-se então PyBOP (4,90 g, 9,42 mmol) e conti- nuou-se com a agitação durante outros 30 minutos, acrescentou-se então 3-fluorben- zilamina (1,18 g, 9,42 mmol) e continuou-se com a agitação durante 24 horas, sendo então a mistura de reação vertida sobre água resfriada com gelo acidificada com (10 mL) de HCl a 1N e extraiu-se com acetato de etila (100 mL) e lavou-se a fase orgânica com uma solução saturada de NaHCO3, água e salmoura, secou-se sobre Na2SO4 e removeu-se o solvente a vácuo, obtendo-se um pó branco do composto desejado (1,00 g), rendimento de 33%. Um outro método envolve o método de acoplamento de cloreto ácido descrito abaixo.
[0262]Ácido 4-bifenil acético (2,5 g, 11,78 mmol) foi carregado em um frasco, sendo então acrescentado cloreto de tionila (15 mL) e aquecido com refluxo durante 1 hora, resfriado, e o excesso de cloreto de tionila removido a vácuo até secar, sendo então o cloreto ácido bruto produzido (2,8 g, 12,13 mmol) dissolvido em DCM anidro (30 mL), e adicionado gota a gota a 0°C a (1,38 mL, 12,13 mmol) da solução de 3- fluorbenzilamina em DCM (10 mL) juntamente com (1,69 mL, 12,13 mmol) de TEA e agitou-se durante 5 horas, verteu-se então sobre água fria acidificada, lavou-se a fase orgânica com água, salmoura e removeu-se o solvente a pressão reduzida, obtendo- se a amida alvo (3,1 g), rendimento de 80%. Recristalizou-se a partir de metanol, pf = 170-172°C. 1H RMN (DMSO, 500 MHz): δ 8,62(t, J = 11 Hz, 1H), 7,63(d, J = 8 Hz, 2H), 7,59(d, J = 8,5 Hz, 2H), 7,44(t, J = 7,5 Hz, 2H), 7,37-7,31(m, 4H), 7,08-7,01(m, 3H), 4,28(d, J = 5,5 Hz, 2H), 3,52(s, 2H). FAB HRMS m/e calcd. Para (M+H) C21H18FNO: 320,1406; encontrado: 320,2, e o pico de base encontrado: 342,1262 para (M+Na); calcd. 342,1372.
[0263]Síntese do Composto 3, KX1-306
[0264]A síntese, esboçada no Esquema 1, se iniciou com a formação do clo- reto ácido do ácido bifenil acético seguida pro acoplamento de amida com 3,5-diben- zilóxi-benzilamina. Um grande número de impurezas foi introduzido pela formação do cloreto ácido. No entanto, outros procedimentos de acoplamento de amida tais como, por exemplo, PyBOP ou carbodiimidas, podem também ser usado nesta reação.
[0265]A clivagem de um dos grupos benzila foi efetuada sob hidrogênio a alta pressão (50-60 psi (kPa)) durante 15 horas. A reação foi monitorada por TLC. Foi usada cromatografia sobre gel de sílica para se separar o produto do material de par- tida assim como o produto secundário diidroxilado.
[0266]Dissolveu-se ácido bifenil acético (220 mg, 1,00 mmol) em DCM, acres- centaram-se 5 eq (0,38 mL) de cloreto de tionila e fez-se refluir a reação durante 4 horas. Os solventes foram removidos a vácuo e o resíduo foi dissolvido em DCM. Acrescentou-se 3,5-dibenzilóxi-benzilamina (1,1 eq) e em seguida TEA (1 eq). Agitou- se a reação então à temperatura ambiente de um dia para outro. Diluiu-se a reação até 45 mL (com DCM) e lavou-se com HCl a 1N (3 X 20 L), bicarbonato de sódio saturado (3 X 20 mL), e salmoura (3 X 20 mL). Secou-se a reação então com sulfato de sódio e removeu-se a vácuo, obtendo-se 330 mg do produto bruto. A cromatografia sobre gel de sílica (DCM/EtOAc (acetato de etila) a 1:1) resultou em 220 mg do pro- duto puro. TLC Rf = 0,2 (um só ponto, hexanos:EtOAc a 7:3). LCMS 514,2 (m+H) 536,2(m+Na). 1H RMN (300 MHz, CDCl3) δ (ppm) 3,65(s, 2H), 4,50(d, 5,7 Hz, 2H), 4,96(s, 4H), 5,71(s, 1H), 6,43(s, 2H), 6,49(s, 1H), 7,58-7,26(m, 19H).
[0267]Dissolveu-se a dibenziloxiamida (1) em 15 mL de EtOAc (acetato de etila) com suave aquecimento em um frasco Parr. Este foi colocado no hidrogenador a 50 psi ( kPa) de hidrogênio durante 15 horas. Filtrou-se a reação através de celite e removeu-se o solvente a vácuo, obtendo-se uma mistura bruta de material de partida e produto. A cromatografia sobre gel de sílica resultou em 50 mg 1 e 41 mg do produto desejado KX1-306; LCMS 424,1 (m+H), 446,2 (m+Na), 847,0 (2m+H), 867,9 (2m+Na). 1H RMN (400 MHz, CDCI3) δ (ppm) 3,66(s, 2H), 4,38(d, 5,6 Hz, 2H), 4,98(s, 2H), 5,71(s, 1H), 6,43(s, 2H), 6,49(s, 1H), 7,30-7,45(m, 10H), 7,54-7,57(m, 4H).
[0269]Reagentes: i) SOCI2, DCM. ii) 3,5-dibenzilóxi-benzilamina (1,0 eq), TEA (2,0 eq) rendimento de 20% (duas etapas, com cromatografia), iii) 10% Pd/C (10% molar), H2, 55 psi (kPa), EtOAc 24 horas (53%, depois da cromatografia, BORMS.
[0270]Síntese do Composto 4, KX1-307
[0271]A síntese é esboçada no Esquema 2, Em uma síntese, começa-se a reação com formação de ligação amida, obtendo-se 2, seguindo-se de um acopla- mento Suzuki com ácido fenilborônico, obtendo-se o produto meta-bifenílico Com- posto 4, KX1-307. Na reação Suzuki o produto bifenílico foi formado, mas a reação não foi completada (por RMN e LCMS), apesar de tempo adicional, calor e catalisador extra. Usando-se a cromatografia sobre gel de sílica, não se conseguiu separar o pro- duto do produto de bromo de partida 2, Revertendo-se a reação de Suzuki e o aco- plamento de amida resolveu-se o problema de separação e produziu-se com sucesso a metabifenil amida KX1-307 assim como 2'-fluorbifenil-4-acetamida KX1-309 (com- posto 6, Esquema 3).
[0272]Ácido 3-bromofenil acético (250 mg, 1,163 mmol) e 156 mg (1,1 eq) de ácido fenilborônico foram dissolvidos em 6 mL de água:isopropanol (6:1). Dissolveu- se carbonato de sódio (160 mg, 1,3 eq.) em 0,5 mL de água destilada e acrescentou- se à reação seguindo-se de Pd(OH)2/C (74 mg, 3% molar). Esta reação foi girada em um banho de água a 65°C durante 5 horas. Filtrou-se a reação através de papel de filtro. O papel de filtro foi lavado com 25 mL de isopropanol: água: NaOH a 1N (35:5:1). Combinaram-se as lavagens e acidificou-se até pH 2 com ácido sulfúrico a 1N. Remo- veu-se o isopropanol a vácuo e acrescentou-se água (10 mL). Esta fase aquosa foi lavada com diclorometano (3 X 20 mL). As lavagens orgânicas foram combinadas, secadas com sulfato de sódio e removidas a vácuo, obtendo-se 215 mg (rendimento de 87%) do produto bifenílico 3, TLC Rf= 0,7 (faixa longa, EtOAc:DCM a 1:1). 1H RMN (300 MHz, CDCl3) δ (ppm) 3,72 (s, 2H), 7,26-7,60 (m, 9H).
[0273]Dissolveram-se ácido 3-bifenil acético (3) (100 mg, 0,472 mmol), 3-flu- orbenzilamina (1,1 eq), cloridrato de 1-(3-dimetil-aminopropil)-3-etil-carbodiimida, EDCI, (1,1 eq), e HOBT (1-hidróxi-benzotriazol, 1,0 eq) em 10 mL de DCM anidro. Depois de 10 minutos acrescentou-se DIEA (1,1 eq) e deixou-se a reação agir de um dia para outro. Diluiu-se a reação até 25 mL e lavou-se com HCl a 1N (3 X 10 L), bicarbonato de sódio saturado (3 X 10 mL), e salmoura (2 X 20 mL). Secou-se a rea- ção com sulfato de sódio e removeu-se a vácuo, obtendo-se 124 mg de KX1-307 puro (rendimento de 83%). TLC Rf= 0,7(um único ponto, EtOAc:DCM a 1:1). 1H RMN (300 MHz, CDCl3) δ (ppm) 3,69(s, 2H) 4,40(d, 6,0 Hz) 5,77(s, 1H) 6,86-6,96(m, 3H) 7,10- 7,26(m, 2H) 7,32(m, 8H).
[0275]Reagentes: i) SOCI2, DCM. ii) 3-Fluorbenzilamina (1,1 eq), DIEA (2,2 eq) (20% depois da cromatografia). iii) Ácido fenilborônico (1,2 eq), carbonato de sódio a 2M, Pd(PPh3)4 (3% molar), Tolueno (mistura inseparável). iv) Ácido fenilborônico (1,1 eq), Na2CO3 (1,3 eq), Pd(OH)2/C (3% molar), isopropanol:água a 1:6 (rendimento de 87%), v) 3-Fluorbenzilamina (1,1 eq), EDCI (1,1 eq), HOBT(1,0 eq), DIEA (1,1 eq) (rendimento de 83%).
[0276]Síntese do Composto 6, KX-309
[0277]A síntese é esboçada no Esquema 3. Dissolveram-se ácido 4-bromofe- nil acético (500 mg, 2,33 mmol) e 358 mg de ácido 2-fluorfenil-borônico (1,1 eq) em 12 mL de água:isopropanol a 6:1. Dissolveu-se carbonato de sódio (320 mg, 1,3 eq.) em 1 mL de água destilada e acrescentou-se à reação, seguido por Pd(OH)2/C (148 mg, 3% molar). Esta solução foi girada em um banho de água a 65°C durante 5 horas. A reação foi filtrada através de papel de filtro. O papel de filtro foi lavado com 50 mL de isopropanol:água: NaOH a 1N (35:5:1). Combinaram-se as lavagens e acidifica- ram-se até pH 2 com ácido sulfúrico a 1N. Removeu-se o isopropanol a vácuo, acres- centou-se água (20 mL) e lavou-se com diclorometano (3 X 30 mL). As lavagens or- gânicas foram combinadas, secadas com sulfato de sódio e removidas a vácuo, ob- tendo-se 177 mg (rendimento de 35%) do produto bifenílico 4, TLC Rf=0,7(faixa longa, EtOAc:DCM a 1:1). 1H RMN (300 MHz, CDCla) δ (ppm) 3,69(s, 2H) 4,40(d, 6,0 Hz) 5,77(s, 1H) 6,86-6,96(m, 3H) 7,10-7,26(m, 2H) 7,32(m, 8H).
[0278]Dissolveram-se ácido 2'-fluorbifenil acético (4) (103 mg, 0,448 mmol), 3-fluorbenzilamina (1,1 eq), EDCI (1,1 eq), e HOBT (1,0 eq) em 6 mL de DCM anidro. Depois de 10 minutos acrescentou-se DIEA (1,1 eq) e deixou-se a reação correr de um dia para outro. Diluiu-se a reação até 25 mL e lavou-se com HCl a 1N (3 X 10 L), bicarbonato de sódio saturado (3 X 10 mL), e salmoura (2 X 20 mL). A reação foi secada com sulfato de sódio e removida a vácuo, obtendo-se 126 mg de Composto 6, KX1-309 puro (rendimento de 83%). LCMS 360,1 (m+Na) 696,8 (2m+Na). 1H RMN (300 MHz, CDCI3) δ (ppm) 3,67(s, 2H) 4,21(d, 6,0 Hz, 2H) 5,79(s, 1H) 6,87-6,98 (m, 3H) 7,10-7,44(m, 7H) 7,53(dd, 1,5 Hz, 7,5Hz, 2H).
[0280]Reagentes: i) Ácido fenilborônico (1,1 eq.), Na2CO3 (1,3 eq), Pd(OH)2/C (3% molar), isopropanol:água a 1:6 (rendimento de 35%), ii) 3-Fluorbenzilamina (1,1 eq.), EDCI (1,1 eq), HOBt (1,0 eq), DIEA (1,1 eq), rendimento de 83%.
[0282]Síntese do Composto 5: N-(3-fluorfenil)-4-bifenil-acetamida, KX1-307
[0283]Acrescentou-se cloreto de tionila (0,38 mL, 5,0 mmol) a uma solução resfriada com água gelada de ácido 4-bifenil acético (0,2 g, 0,9 mmol) em 5 mL de diclorometano, deixou-se a solução se aquecer até a temperatura ambiente, aque- cendo-se então com refluxo durante 1 hora, fez-se evaporar o solvente e o excesso de cloreto de tionila a vácuo, e redissolveu-se o óleo formado em 5 mL de diclorome- tano seguido pela adição de 4-dimetilamino-piridina (0,12 g, 1,0 mmol) e 3-fluoranilina (0,11 g, 1,0 mmol), agitou-se à temperatura ambiente de um dia para o outro, diluiu- se a mistura de reação com 10 mL de diclorometano e 20 mL de água, lavou-se a fase orgânica com HCl a 1N, solução saturada de NaHCO3, e solução saturada de NaCl, secou-se, usando-se Na2SO4 e fez-se evaporar até secar (0,2 g, 72%), H1-RMN INOVA-500 (CDCI3) δ 3,805 (s, 2H), 6,815 (t, J = 8,5 Hz, 1H), 7,068 (d, J = 8,0 Hz, 1H), 7,218-7,284 (m, 2H), 7,380-7,499 (m, 6H) 7,620-7,664 (m, 4H). MS (m/z) 306,2 (M+H)+.
[0284]Síntese do Composto 7: N-(3-fIuorbenziI)-4-(3-fIuorfeniI)-feniIaceta- mida, KX1-310
[0285]Síntese de ácido (4’-fIuorbifeniI-4-iI)-acético: Acrescentaram-se ácido 4- bromofeniI acético (0,5 g, 2,3 mmoI), ácido 3-fIuorfeniI-borônico (0,36 g, 2,4 mmoI) e PaIádio a 10% sobre carbono úmido em água a 50 % (0,16 g, 0,075 mmoI Pd) a 10 mL de mistura de água:isopropanoI a 5:1, acrescentou-se então Na2CO3 (0,32 g, 3 mmol) dissolvido em 3 mL de água à mistura acima, aqueceu-se a reação a 65-70°C de um dia para outro, resfriou-se a reação até a temperatura ambiente, diIuiu-se com 20 mL de i-PrOH/H2O/NaOH a 10%, a 70:15:1, filtrou-se, lavou-se o catalisador com 20 mL X 3 usando-se a mistura acima, acidificou-se o filtrado usando-se H2SO4 a 20 %, filtrou-se e secou-se o ácido (3'-fluorbifenil-4-il)-acético: (0,4 g, 75%) H1-RMN INOVA-500 (DMSO d6) δ 3,623 (s, 2H), 7,192 (m, 1H), 7,358 (d, J = 8,0 Hz, 2H), 7,474- 7,515 (m, 3H), 7,652 (d, J = 8,0 Hz, 2H), 12,316 (s, 1H).
[0286]Dissolveu-se 3-fluorbenzilamina (0,14 mL, 1,1 mmol), PyBOP (0,57 g, 1,1 mmol), e DIEA (0,36 mL, 2,2 mmol) em DMF, agitou-se de um dia para outro, verteu-se então a mistura de reação em água, coletou-se o sólido por filtração, recris- talizando-se, usando-se água-metanol. (0,22 g, 76%); H1-RMN INOVA-500 (DMSO d6) δ 3,550 (s, 2H), 4,303 (d, J = 6,5 Hz, 2H), 7,027-7,097 (m, 3H), 7,197 (m, 1H), 7,350 (m, 1H), 7,389 (d, J = 8,0 Hz, 2H), 7,477-7,518 (m, 3H), 7,657 (d, J = 8,0 Hz, 2H), 8,652 (t, J = 5,5 Hz, 1H). MS (m/z) 338,1 (M+H)+.
[0287]Síntese do Composto 8, N-(3-fIuorbenziI)-4-(4-fIuorfeniI) fenilacetamida, KX1-311
[0288]Síntese de ácido (4’-fluorbifenil-4-il)-acético: Acrescentou-se ácido 4- bromo-fenilacético (0,5 g, 2,3 mmol), ácido 4-fluorfenil borônico (0,36 g, 2,4 mmol) e paládio a 10 % sobre carbono úmido por água a 50 % (0,16 g, 0,075 mmol Pd) a 10 mL de uma mistura de água isopropanol a 5:1, acrescentou-se então Na2CO3 (0,32 g, 3 mmol) dissolvido em 3 mL de água à mistura acima, aqueceu-se a reação a 65-70°C de um dia para outro, resfriou-se a reação até a temperatura ambiente, diluiu-se com 20 mL de i-PrOH/H2O/NaOH a 10% a 70:15:1, filtrou-se, lavou-se o catalisador com 20 mL X 3, usando-se a mistura acima, acidificou-se o filtrado, usando-se H2SO4 a 20 %, filtrou-se e secou-se (0,4 g, 75%) HI-RMN INOVA-500 (DMSO de) δ 3,621 (s, 2H), 7,290 (t, J = 8,5 Hz, 2H), 7,351 (d, J = 7,5 Hz, 2H), 7,593 (d, J = 7,5 Hz, 2H), 7,695 (t, J = 7 Hz, 2H), 12,386 (s, 1H).
[0289]Dissolveu-se ácido (4’-fluor-bifenil-4-il)-acético (0,2 g, 0,9 mmol), 3-flu- orbenzilamina (0,14 mL, 1,1 mmol), PyBOP (0,57 g, 1,1 mmol), e DIEA (0,36 mL, 2,2 mmol) em DMF, agitou-se de um dia para outro, verteu-se então a mistura de reação em água, coletou-se o sólido por filtração, recristalizou-se, usando-se água-metanol. (0,26 g, 90%); H1-RMN INOVA-500 (DMSO d6) δ 3,541 (s, 2H), 4,304 (d, J = 5,5 Hz, 2H), 7,027-7,098 (m, 3H), 7,273-7,382 (m, 5H), 7,582 (d, J = 8,0, 2H), 7,694 (m, 2H), 8,641 (t, J = 5,5 Hz, 2H). MS (m/z) 338,1 (M+H)+.
[0290]Síntese do Composto 9, N-(3-fluorbenzil)-N-metil-4-bifenilacetamida, KX1-312
[0291]Dissolveu-se ácido 4-bifenil acético (0,25 g, 1,2 mmol), N-metil-3-fluor- benzilamina (0,16 g, 1,2 mmol), EDCI (0,23 g, 1,2 mmol), e DIEA (0,42 mL, 2,4 mmol) em 10 mL de DCM e agitou-se de um dia para outro. Diluiu-se a mistura de reação com 10 mL de DCM, lavou-se com HCl a 10%, solução saturada de NaHCO3, e solu- ção saturada de NaCl, secou-se, usando-se Na2SO4 e fez-se evaporar para produzir um óleo transparente viscoso (160 mg, 43%), RMN 1H INOVA-500 (DMSO d6) indicou a presença de uma mistura de isômeros cis e trans em uma relação de 1:2, o experi- mento de RMN foi conduzido a 50°C o que alterou ligeiramente o valor durante o des- locamento químico, mas que não teve praticamente nenhum efeito sobre a relação. Prótons são rotulados Ha ou Hb para indicar que pertencem a um isômero ou ao outro. H1-RMN INOVA-500 (DMSO de) δ 2,813 (s, 3Ha), 3,000 (s, 3 Hb), 3,784 (s, 2Ha), 3,841 (s, 2Hb), 4,543 (s, 2Hb), 4,681 (s, 2Ha), 6,931-7,649 (m, 13 Ha+ 13 Hb). MS (m/z) 334,2 (M+H)+.
[0292]Síntese do Composto 10, N-(3-fluorbenzil)-4-fenil-2-fluorfenil-aceta- mida, KX 1-313
[0293]Síntese de 4-bromo-2-fluor-fenilacetamida: Dissolveu-se brometo de 4- bromo-2-fluorbenzila (5 g, 17,7 mmol) em 30 mL etanol, acrescentando-se uma solu- ção em água (10 mL) de KCN (2,43 g, 37,4 mmol), fez-se refluir de um dia para outro, resfriou-se então até a temperatura ambiente, verteu-se em 200 mL de gelo triturado, filtrou-se, cromatografou-se, usando-se acetato de etila a 1:1 seguido por acetato de etila (o composto ciano foi hidrolisado sobre gel de sílica para produzir a carboxamida), que se fez evaporar para produzir um sólido branco (1,3 g, 32%) H1-RMN INOVA-500 (DMSO d6) δ 3,436 (s, 2H), 7,005 (s, 1H), 7,289 (t, J = 8,0 Hz, 1H), 7,361 (d, J = 8,0 Hz, 1H), 7,478 (m, 1H), 7,517 (s, 1H).
[0294]Síntese de ácido 4-bromo-2-fluor-fenilacético: Suspendeu-se 4-bromo- 2-fluor-fenilacetamida (1,3 g) em 100 mL de NaOH a 30 %, aquecendo-se à tempera- tura de refluxo durante 24 horas, resfriou-se até a temperatura ambiente, lavou-se com DCM e acetato de etila. Acidificou-se a fase aquosa com HCl conc., extraiu-se com acetato de etila, fez-se evaporar; o resíduo foi cristalizado a partir de isopropanol- água, obtendo-se agulhas de cristais (0,5 g, 38%) H1-RMN INOVA-500 (DMSO d6) δ 3,619 (s, 2H), 7,316 (t, J = 8,0 Hz, 1H), 7,379 (dd, J = 8,0, 1,5 Hz, 1H), 7,516 (dd, J = 8,0, 1,5 Hz, 1H), 12,555(s, 1H).
[0295]Síntese de ácido 4-fenil-2-flúor-fenilacético: Acrescentou-se ácido 4- bromo-2-flúor-fenilacético (0,25 g, 1,1 mmol), ácido fenilborônico (0,15 g, 1,2 mmol) e paládio a 10% sobre carbono úmido com água a 50 % (0,07 g, 0,033 mmol Pd) a 10 mL de uma mistura de água isopropanol a 5:1, acrescentou-se então Na2CO3 (0,14 g, 1,3 mmol) dissolvido em 3 mL de água à mistura acima, aqueceu-se a reação a 65- 70°C de um dia para outro, resfriou-se a reação até a temperatura ambiente, diluiu-se com 20 mL de i-PrOH/H2O/NaOH a 10% a 70:15:1, filtrou-se, lavou-se o catalisador com 20 mL X 3, usando-se a mistura acima, acidificou-se o filtrado, usando-se H2SO4 a 20 %, filtrou-se e secou-se (0,2 g, 83%) H1-RMN INOVA-500 (DMSO de) δ 3,675 (s, 2H), 7,382-7,518 (m, 6H), 7,707 (d, J = 7,5 Hz, 2H), 12,498 (s, 1H).
[0296]Síntese de N-(3-fluorbenzil)-4-fenil-2-fluorfenilacetamida: Dissolveu-se ácido 4-fenil-2-fluorfenil acético (0,2 g, 0,9 mmol), 3-fluorbenzilamina (0,14 mL, 1,1 mmol), PyBOP (0,57 g, 1,1 mmol), e DIEA (0,36 mL, 2,2 mmol) em DMF agitou-se de um dia para outro, a mistura de reação foi então vertida em água, o sólido foi coletado por filtração, recristalizado usando-se água-metanol. (0,20 g, 70%); H1-RMN INOVA- 500 (DMSO d6) δ 3,612 (s, 2H), 4,318 (d, J = 6 Hz, 2H), 7,064-7,117 (m, 3H), 7,345- 7,503 (m, 7H), 7,695 (d, J = 7,5 Hz, 2H), 8,660 (t, J = 6 Hz, 1H). MS (m/z) 338,1 (M+H)+.
[0297]Síntese do Composto 11, N-(3-fluorbenzil)-2-fenilpiridino-5-acetamida, KX1-314
[0298]Síntese do ácido 2-fenilpiridino-5-acético: Acrescentou-se ácido 2-clo- ropiridino-5-acético (0,2 g, 1,21 mmol), ácido fenilborônico (0,16 g, 1,3 mmol) e paládio a 10% sobre carbono úmido com água a 50 % (0,08 g, 0,036 mmol Pd) a 10 mL de uma mistura de água-isopropanol a 5:1, acrescentou-se então Na2CO3 (0,15 g, 1,4 mmol) dissolvido em 3 mL de água à mistura acima, aqueceu-se a reação a 65-70°C de um dia para outro, resfriou-se a reação até a temperatura ambiente, diluiu-se com 20 mL de i-PrOH/H2O/NaOH a 10% a 70:15:1, filtrou-se, lavou-se o catalisador com 20 mL X 3, usando-se a mistura acima, secou-se o filtrado a vácuo e usou-se a mistura bruta sem qualquer purificação na etapa seguinte.
[0299]Síntese de N-(3-fluorbenzil)-2-fenilpiridino-5-acetamida: Ao produto bruto proveniente da reação acima, acrescentou-se 3-fluorbenzilamina (0,15 g, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,32 g, 2,6 mmol) e agitou-se em DMF de um dia para outro. A mistura de reação foi então vertida em água; o sólido foi coletado por filtração, recristalizado, usando-se água-metanol (0,06 g, 18% em duas etapas). H1-RMN INOVA-500 (CDCI3) δ 3,645 (s, 2H), 4,438 (d, J = 5,5 Hz, 2H), 5,867 (s, 1H), 6,925-7,009 (m, 3H), 7,268 (m, 1H), 7,408-7,493 (m, 3H), 7,735 (m, 2H), 7,965-7,982 (m, 2H), 8,582 (s, 1H). MS (m/z) 321,2 (M+H)+.
[0300]Síntese do Composto 12, N-(3-fluorbenzil)-2-(4-piridin-2-il-fenil)-aceta- mida, KX1-315
[0301]Síntese de áIcooI 4-(2-piridiniI)benzíIico: Agitou-se aIdeído 4-(2-piri- diniI)benzíIico (2 g, 11 mmoI), e NaBH4 (0,42 g, 11 mmoI) à temperatura ambiente durante 2 horas, fez-se evaporar o etanoI, dissoIveu-se o resíduo em acetato de etiIa, Iavou-se com soIução saturada de NaHCO3, e com soIução saturada de NaCI, secou- se usando-se Na2SO4 e fez-se evaporar para se produzir um sóIido branco (1,5 g, 75%).
[0302]Síntese de ácido (4-piridin-2-iI-feniI)-acético: DissoIveu-se o produto bruto de áIcooI 4-(2-piridiniI)benzíIico em 20 mL de DCM, resfriou-se, usando-se geIo/metanoI, acrescentou-se trietiIamina (1,25 mL, 7,9 mmoI) e em seguida cIoreto de metano-suIfoniIa (0,7 mL, 7,9 mmoI) gota a gota durante 5 minutos. Deixou-se a reação se agitar à temperatura ambiente até a TLC indicar o consumo totaI do materiaI de partida (3 horas). Depois de compIetada a reação, a mistura de reação foi Iavada com água, com soIução saturada de NaHCO3, e com soIução saturada de NaCI, se- cou-se, usando-se Na2SO4 e fez-se evaporar para produzir um óIeo amareIo, o óIeo produzido foi dissoIvido em 25 mL de etanoI a 90%, acrescentou-se KCN (1,05 g, 16,2 mmoI) e aqueceu-se com refIuxo de um dia para outro. Fez-se o etanoI evaporar; lavou-se o sólido com 50 mL água e filtrou-se. Dissolveu-se o sólido em 30 mL de HCl conc., fez-se refluir durante 48 horas; acrescentou-se carvão, fez-se refluir durante 1 hora, filtrou-se. Fez-se evaporar o HCl, dissolveu-se o sólido formado em 5 mL de água, acrescentou-se NaOH a 1N gota a gota, extraindo-se simultaneamente com acetato de etila, secou-se o extrato de acetato de etila com Na2SO4 e fez-se evaporar para se produzir um sólido branco (0,6 g, 35% em 3 etapas) H1-RMN INOVA-500 (DMSO de) δ 3,641 (s, 2H), 7,345 (t, J = 6,0 Hz, 1H), 7,381 (d, J = 8,5 Hz, 2H), 7,879 (t, J = 8,0 Hz, 1H), 7,951 (d, J = 8,0 Hz, 1H), 8,034 (d, J = 8,0 Hz, 2H), 8,662 (d, J = 4,0 Hz, 1H), 12,390 (s, 1H).
[0303]Síntese de N-(3-fluorbenzil)-2-(4-piridin-2-il-fenil)-acetamida: Dissolveu- se ácido (4-piridin-2-il-fenil)-acético (0,2 g, 0,9 mmol), 3-fluorbenzilamina (0,14 mL, 1,1 mmol), PyBOP (0,57 g, 1,1 mmol), e DIEA (0,36 mL, 2,2 mmol) em DMF, agitou-se de um dia para outro, verteu-se então a mistura de reação em água, coletou-se o sólido por filtração, recristalizou-se usando-se água-metanol. (0,13 g, 45%); H1-RMN INOVA- 500 (DMSO d6) δ 3,563 (s, 2H), 4,305 (d, J = 6,0 Hz, 2H), 7,032-7,095 (m, 3H), 7,332- 7,360 (m, 2H), 7,404 (d, J = 8,0 Hz, 2H), 7,874 (t, J = 7,0 Hz, 1H), 7,948 (d, J = 8,0 Hz, 1H), 8,034 (d, J = 8,0 Hz, 2H), 8,659 (d, J = 4 Hz, 2H). MS (m/z) 321,2 (M+H)+.
[0304]Síntese do Compostos 13 e 24
[0305]As sínteses dos derivados piridílicos, Composto 13, KX1-316, e Com- posto 24, KX1-327, são mostradas no Esquema 4. A amida foi preparada primeiro com um acoplamento de EDCI, obtendo-se amida 5. Conduziu-se então a reação de Suzuki com ácido 3- ou 4-piridilborônico. A natureza básica do anel piridínico foi ex- plorada para purificar o produto do material de partida restante. O produto foi puxado para a fase aquosa e afastando-se do material de partida usando-se HCl a 1N. Depois de diversas lavagens orgânicas, a fase aquosa foi basificada e o produto foi extraído com acetato de etila. O procedimento de purificação funcionou bem e eliminou a ne- cessidade de cromatografia.
[0306]KX1-316 (Composto 13)
[0307]Um frasco de fundo redondo de 50 mL secado na chama com dois con- densadores foi carregado com argônio. Aqueceu-se dimetoxietano, 15 mL e 1 mL de carbonato de potássio a 2M até 45°C, borbulhando-se simultaneamente argônio atra- vés da solução. Depois de 1 hora, acrescentaram-se a bromo amida (240 mg, 0,7475 mmol) e o ácido 3-piridilborônico (92 mg, 1,1 eq). Depois de uma hora, acrescentou- se Pd(PPh3)4 (43 mg, 5% molar) puro. Aqueceu-se a reação a 65-75°C durante 48 horas. O solvente foi vertido em um frasco de fundo redondo, lavou-se o resíduo res- tante com acetato de etila. Combinaram-se os solventes e removeram-se a vácuo. O resíduo foi absorvido em 20 mL de HCl a 1N e lavado com acetato de etila (3 X 10 mL). A fase ácida foi então basificada com uma combinação de NaOH a 2N e bicar- bonato de sódio saturado até um pH 8-9, A fase aquosa foi então lavada com acetato de etila (3 X 20 mL). Combinaram-se os extratos de solvente, secou-se com sulfato de sódio e removeu-se a vácuo. O resíduo foi purificado sobre coluna de gel de sílica (DCM:EtOAc a 1:1), obtendo-se 90 mg do produto desejado (rendimento de 38%). TLC, Rf 0,2 (DCM:EtOAc a 1:1). LCMS 321,3 (m+H) 640,8 (2m+Na) 662,9 (2M+Na). 1H RMN (500 MHz, DMSO) 3,54 (s, 2H) 4,29 (d, 6,0 Hz, 2H) 7,00-7,08 (m, 3H) 7,34 (q, 8,0 Hz, 1H) 7,40 (d, 10,0 Hz, 2H) 7,47 (dd, 6,0 Hz, 10,0 Hz, 1H) 7,66 (d, 10,0 Hz, 2H) 8,05 (dt, 2,5 Hz, 10,0 Hz, 1H) 8,55 (dd, 2,0 Hz, 6,0 Hz, 1H) 6,40 (t, 7,0 Hz, 1H) 8,78 (d, 2,5 Hz, 1H).
[0308]KX1-327 (Composto 24)
[0309]Um frasco de fundo redondo de 50 mL secado na chama e dotado de dois condensadores foi carregado com argônio. Aqueceu-se dimetóxi-etano, 15 mL e 1 mL de carbonato de potássio a 2M até 45°C, enquanto se borbulhava o argônio através da solução. Depois de 1 hora acrescentaram-se a bromo amida (150 mg, 0,4672 mmol) e o ácido 4-piridilborônico (57 mg, 1 eq). Depois de uma hora acrescen- tou-se Pd(PPh3)4 (27 mg, 5% molar) puro. Aqueceu-se a reação a 65-75°C durante 72 horas. Verteu-se o solvente em um frasco de fundo redondo, lavou-se o resíduo res- tante com acetato de etila. Combinaram-se os solventes e removeram-se a vácuo. O resíduo foi absorvido em 20 mL de HCl a 1N e lavado com acetato de etila (3 X 10 mL). A fase ácida foi então basificada com uma combinação de NaOH a 2N e bicar- bonato de sódio saturado até um pH 8-9. A fase aquosa foi então lavada com acetato de etila (3 X 20 mL). Os extratos de solvente foram combinados, secados com sulfato de sódio e removidos a vácuo, obtendo-se 71 mg do produto desejado (rendimento de 48%). TLC, Rf 0,2 (DCM:EtOAc a 1:1). LCMS 321,3 (m+H). 1H RMN (500 MHz, DMSO) 3,56 (s, 2H) 4,29 (d, 6,0 Hz, 2H) 7,04 (m, 3H) 7,34 (q, 6,5 Hz, 1H) 7,42 (d, 8,0 Hz, 2H) 7,69 (d, 6,0 Hz, 2H) 7,75 (d, 8,5 Hz, 2H) 8,61 (d, 6,0 Hz, 2H) 8,64 (t, 5,5 Hz, 1H).
[0311]Reagentes: i) 3-fluorbenzilamina (1,1 eq), EDCI (1,1 eq), HOBT(1,0 eq), DIEA (1,1 eq), rendimento de 88%. ii) ácido 3 (ou 4)-piridilborônico (1,1 eq), Na2CO3(1,3 eq), Pd(PPh3)4 (5% molar), Dimetoxietano, Na2CO3 a 2M (2 eq). KX1-316 (X1=N, X2=C) 38%, KX1-327 (X1=C, X2=N) 47%.
[0312]
[0313]Síntese do Composto 14, 2-[6-(3-cloro-fenil) piridin-3-il]-N-(3-fluor-ben- zil)-acetamida, KX1-317
[0314]Síntese do ácido 2-(3-cloro-fenil)-piridino-5-acético: Acrescentou-se ácido 2-cloropiridino-5-acético (0,2 g, 1,21 mmol), ácido 3-clorofenil borônico (0,2 g, 1,3 mmol) e paládio a 10% sobre carbono úmido com água a 50 % (0,08 g, 0,036 mmol de Pd) a 10 mL de uma mistura de água-isopropanol a 5:1, acrescentou-se en- tão Na2CO3 (0,15 g, 1,4 mmol) dissolvido em 3 mL de água à mistura acima, aqueceu- se a reação a 65-70°C de um dia para outro, resfriou-se a reação até a temperatura ambiente, diluiu-se com 20 mL de i-PrOH/H2O/NaOH a 10% a 70:15:1, filtrou-se, la- vou-se o catalisador com 20 mL X 3,usando-se a mistura acima, secou-se o filtrado a vácuo e a mistura bruta foi usada sem qualquer purificação na etapa seguinte.
[0315]Síntese de 2-[6-(3-cloro-fenil)-piridin-3-il]-N-(3-fluorbenzil)-acetamida: Ao produto bruto da reação acima acrescentou-se 3-fluorbenzilamina (0,15 g, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,32 g, 2,6 mmol) e agitou-se em DMF de um dia para outro. A mistura de reação foi então vertida em água; o sólido foi coletado por filtração, recristalizado usando-se água-metanol (0,02 g, 6% em duas etapas). H1- RMN INOVA-500 (DMSO de) δ 3,611 (s, 2H), 4,314 (d, J = 6,0 Hz, 2H), 7,048-7,106 (m, 3H), 7,364 (m, 1H), 7,500-7,545 (m, 2H), 7,808 (dd, J = 8,0, 2,0 Hz, 1H), 7,997 (d, J = 8,0 Hz, 1H), 8,046 (d, J = 8,0Hz, 1H), 8,126 (d, J = 2,0 Hz, 1H), 8,578 (s, 1H), 8,699 (bs, 1H). MS (m/z) 355,2 (M+H)+.
[0316]Síntese do Composto 14, 2-[6-(4-etil-fenil)-piridin-3-il]-N-(3-fluorbenzil)- acetamida, KX1-318
[0317]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida: Dissol- veu-se ácido 2-cloropiridino-5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou- se de um dia para outro, verteu-se então a mistura de reação em água, coletou-se o sólido por filtração, recristalizou-se, usando-se água-metanol. (0,3 g, 85%); H1-RMN INOVA-500 (CDCl3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929- 7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0318]Síntese de 2-[6-(4-etil-fenil)-piridin-3-il]-N-(3-fluorbenzil)-acetamida: Dissolveu-se 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida e (0,125 g, 0,5 mmol), ácido 4-etilbenzeno borônico (0,083 g, 0,55 mmol) em dimetoximetano (DME), acres- centou-se Na2CO3 (0,11 g, 1 mmol) em 5 mL de água à solução de DME, a solução teve então os gases extraídos durante 30 minutos (Ar através da solução e vácuo aplicado durante os primeiros 5 minutos), acrescentou-se paládio-tetraquis-trifenilfos- fina (0,029 g, 0,025 mmol), extraíram-se os gases durante outros 15 minutos, fez-se refluir durante 24 horas. Deixou-se que a reação se resfriasse até temperatura ambi- ente, filtrou-se, lavou-se o sólido com acetato de etila; secou-se a fase orgânica, fez- se evaporar. O resíduo foi cromatografado usando-se acetato de etila/hexano a 3:2. O produto é um sólido branco (0,08 g, 47%). H1-RMN INOVA-500 (DMSO de) δ 1,228 (t, J = 7,5 Hz, 3H), 2,669 (q, J = 7,5 Hz, 2H), 3,590 (s, 2H), 4,321 (d, J = 6 Hz, 2H), 7,053-7,113 (m, 3H), 7,324-7,375 (m, 3H), 7,766 (dd, J = 9,0, 2,0 Hz, 1H), 7,887 (d, J = 8,5 Hz, 1H), 7,994 (d, J = 8,0 Hz, 2H), 8,548 (s, 1H), 8,696 (t, J = 5,5 Hz, 1H). MS (m/z) 349,3 (M+H)+.
[0319]Síntese do Composto 16, N-(3-fluorbenzil)-2-(2-fluor-bifenil-4-il)-aceta- mida, KX1-319
[0320]Síntese de aldeído 2-fluor-bifenil-4-carbônico: Dissolveu-se 4-bromo-2- flúor-bifenila (2 g, 8 mmol) em 20 mL de tetraidrofurano, THF, anidro, resfriou-se to - 78°C sob argônio (Ar), acrescentou-se gota a gota n-Butil lítio a 2,5M (3,5 mL, 7,8 mmol) durante 10 minutos, e agitou-se durante outra hora, acrescentou-se então DMF anidro (0,68 mL, 7,8 mmol), agitou-se durante outra hora, aqueceu-se então até a temperatura ambiente durante 4 horas. Extinguiu-se então a reação com água extraiu- se com éter, secou-se o éter, fez-se evaporar, purificou-se o composto produzido usando-se hexano/acetato de etila a 9:1, para produzir um sólido branco (1 g, 62,5%); H1-RMN INOVA-500 (CDCl3) δ 7,416-7,495 (m, 3H), 7,581-7,661 (m, 4H), 7,723 (d, J = 8,0 Hz, 1H), 9,991 (s, 1H).
[0321]Síntese de (2-fluor-bifenil-4-il)-metanol: Dissolve-se aldeído 2-fluor- bifenil-4-carbônico (1 g, 5 mmol), NaBH4 em etanol agitado durante 2 horas, acres- centou-se NaOH a 10%, fez-se evaporar o etanol, extraiu-se a mistura de reação com acetato de etila, secou-se o extrato de acetato de etila com Na2SO4 e fez-se evaporar para produzir um sólido branco (0,8 g, 80%). H1-RMN INOVA-500 (CDCI3) δ 2,266 (s, 1H), 4,683 (s, 2H), 7,142-7,168 (m, 2H), 7,339-7,442 (m, 4H), 7,519-7,535 (m, 2H).
[0322]Síntese do ácido (2-Fluor-bifenil-4-il)-acético: Dissolveu-se (2-fluor-bife- nil-4-il)-metanol (0,75 g, 3,7 mmol) em 20 mL de DCM, resfriou-se, usando-se gelo/me- tanol, acrescentou-se trietilamina (0,55 mL, 4,0 mmol) e em seguida cloreto de me- tano-sulfonila (0,3 mL, 4,0 mmol) gota a gota durante 5 minutos. Deixou-se a reação se agitar à temperatura ambiente até que a TLC indicasse o consumo completo do material de partida (2 horas), depois de completada a reação, a mistura de reação foi lavada com água, com solução saturada de NaHCO3, e com solução saturada de NaCl, secou-se, usando-se Na2SO4 e fez-se evaporar para produzir um óleo amarelo, dissolveu-se o óleo produzido em 25 mL de etanol a 70%, acrescentou-se então KCN (0,4 g, 6 mmol) e aqueceu-se com refluxo de um dia para outro. Fez-se evaporar o etanol; lavou-se o sólido com 50 mL água e filtrou-se. Dissolveu-se o sólido em 20 mL de etanol, acrescentaram-se em seguida 20 mL de H2SO4 concentrado, e fez-se refluir de um dia para outro; deixou-se a solução se resfriar até a temperatura ambiente, verteu-se em 200 mL de gelo triturado, coletou-se o sólido por filtração a vácuo, sus- pendeu-se em 25 mL de NaOH a 30%, aqueceu-se à temperatura de refluxo durante 24 horas, resfriou-se até a temperatura ambiente, lavou-se com DCM e acetato de etila. Acidificou-se a fase aquosa com HCl conc., extraiu-se com acetato de etila, e fez-se evaporar; o resíduo foi cristalizado a partir de isopropanol-água, obtendo-se um sólido branco (0,15 g, 18% em 3 etapas) H1-RMN INOVA-500 (DMSO d6) δ 3,672 (s, 2H), 7,191-7,254 (m, 2H), 7,389-7,560 (m, 6H), 12,494 (s, 1H).
[0323]Síntese de N-(3-fluorbenzil)-2-(2-flúor-bifenil-4-il)-acetamida: Dissol- veu-se ácido (2-flúor-bifenil-4-il)-acético (0,12 g, 0,5 mmol), 3-fluorbenzilamina (0,08 mL, 0,6 mmol), PyBOP (0,34 g, 0,6 mmol), e DIEA (0,22 mL, 1,3 mmol) em DMF, agitou-se de um dia para outro, verteu-se então a mistura de reação em água, coletou- se o sólido por filtração, recristalizou-se, usando-se água-metanol. (0,140 g, 83%); H1- RMN INOVA-500 (DMSO de) δ 3,580 (s, 2H), 4,316 (d, J = 5,5 Hz, 2H), 7,037-7,110 (m, 3H), 7,210-7,247 (m, 2H), 7,343-7,372 (m, 2H), 7,457-7,501 (m, 3H), 7,544 (d, J = 8,0 Hz, 2H), 8,660 (t, J = 6,0 Hz, 1H). MS (m/z) 338,1 (M+H)+.
[0324]Síntese do Composto 17, N-(3-fluorbenzil)2-[6-(4-fluorfenil)piridin-3-il]- acetamida, KX1-320
[0325]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida: Dissol- veu-se o ácido 2-cloropiridino -5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou-se de um dia para outro, verteu-se então a mistura de reação em água, coletou- se o sólido por filtração, recristalizou-se, usando-se água-metanol. (0,3 g, 85%); H1- RMN INOVA-500 (CDCl3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929-7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0326]Síntese de N-(3-fluorbenzil)-2-[6-(4-fluorfenil)-piridin-3-il]-acetamida: Dissolveu-se 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida e (0,093 g, 0,33 mmol), ácido 4-fluorbenzeno-borônico (0,052 g, 0,37 mmol) em DME, acrescentou-se Na2CO3 (0,07 g, 0,66 mmol) em 5 mL de água à solução de DME, extraíram-se os gases da solução durante 30 minutos (Ar através da solução e aplicou-se vácuo du- rante os primeiros 5 minutos), acrescentou-se paládio-tetraquis-trifenilfosfina (0,016 g, 0,015 mmol), extraíram-se os gases durante outros 15 minutos, fez-se refluir durante 24 horas. Deixou-se que a reação se resfriasse até temperatura ambiente, filtrou-se, lavou-se o sólido com acetato de etila; secou-se a fase orgânica, fez-se evaporar. O resíduo foi cromatografado, usando-se acetato de etila/hexano a 3:2, cristalizando-se então de metanol-água para produzir um sólido branco (0,013 g, 12%). H1-RMN INOVA-500 (DMSO de) δ 3,587 (s, 2H), 4,306 (d, J = 5,0 Hz, 2H), 7,041 -7,099 (m, 3H), 7,295-7,363 (m, 3H), 7,777 (d, J = 7,5, 1H), 7,913 (d, J = 8,0 Hz, 1H), 8,119 (s, 2H), 8,546 (s, 1H), 8,702 (s, 1H). MS (m/z) 339,2 (M+H)+.
[0327]Síntese do Composto 18, N-(3-fluorbenzil)-2-[6-(3-flúor-fenil)-piridin-3- il]-acetamida, KX1-321
[0328]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida: Dissol- veu-se ácido 2-cloropiridino-5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou- se de um dia para outro, a mistura de reação foi então vertida em água, o sólido foi coletado por filtração, recristalizado usando-se água-metanol. (0,3 g, 85%); H1-RMN INOVA-500 (CDCl3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929- 7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0329]Síntese de N-(3-fluor-benzil)-2-[6-(3-flúor-fenil)-piridin-3-il]-acetamida: Dissolveu-se 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida e (0,125 g, 0,5 mmol), ácido 3-flúor-benzeno-borônico (0,08 g, 0,55 mmol) em DME, acrescentou-se Na2CO3 (0,11 g, 1,0 mmol) em 5 mL de água à solução de DME, extraíram-se então os gases da solução durante 30 minutos (Ar através da solução e aplicou-se vácuo durante os primeiros 5 minutos), Acrescentou-se paládio-tetraquis-trifenilfosfina (0,029 g, 0,025 mmol), extraíram-se os gases durante outros 15 minutos, fez-se refluir durante 24 ho- ras. Deixou-se que a reação se resfriasse até a temperatura ambiente, filtrou-se, la- vou-se o sólido com acetato de etila; secou-se a fase orgânica e fez-se evaporar. O resíduo foi cromatografado usando-se acetato de etila/hexano a 3:2, sendo então cris- talizado a partir de metanol-água para produzir um sólido branco (0,075 g, 45%). H1- RMN INOVA-500 (DMSO d6) δ 3,614 (s, 2H), 4,318 (d, J = 6,0 Hz, 2H), 7,053-7,099 (m, 3H), 7,273 (t, J = 9,0 Hz, 1H), 7,367 (q, J = 7,0 Hz, 1H), 7,542 (q, J = 7,0 Hz, 1H), 7,812 (d, J = 8,0 Hz, 1H), 7,891 (d, J = 10,0 Hz, 1H), 7,942 (d, J = 7,5 Hz, 1H), 7,992 (d, J = 8,0 Hz, 1H), 8,583 (s, 1H), 8,717 (s, 1H). MS 339,2 (M+H)+.
[0330]Síntese do Composto 19, 2-[6-(3-etóxi-fenil) piridin-3-il]-N-(3-fluorben- zil)-acetamida. KX1-322
[0331]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida: Dissol- veu-se ácido 2-cloro-piridino-5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou-se de um dia para outro, a mistura de reação foi então vertida em água, o sólido foi coletado por filtração, recristalizado, usando-se água-metanol. (0,3 g, 85%); H1- RMN INOVA-500 (CDCI3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929-7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0332]Síntese de N-(3-fIuorbenziI)-2-[6-(3-fIuorfeniI)-piridin-3-iI]-acetamida: DissoIveu-se 2-(6-cIoro-piridin-3-iI)-N-(3-fIuorbenziI)-acetamida e (0,15 g, 0,54 mmoI), ácido 3-etóxi-benzeno-borônico (0,096 g, 0,6 mmoI) em DME, Na2CO3 (0,11 g, 1,08 mmoI) em 5 mL de água acrescentou-se à soIução de DM, tendo então a soIução os gases extraídos durante 30 minutos (Ar através da soIução e vácuo apIicado durante os primeiros 5 minutos), acrescentou-se paIádio-tetraquis-trifeniIfosfina (0,031 g, 0,027 mmoI), extraíram-se os gases durante outros 15 minutos, fez-se refIuir durante 24 horas. Deixou-se que a reação se resfriasse até temperatura ambiente, fiItrou-se, Iavou-se o sóIido com acetato de etiIa; secou-se a fase orgânica, fez-se evaporar. O resíduo foi cromatografado usando-se acetato de etiIa/hexano a 3:2, então eIe se cris- taIizou de metanoI-água para produzir um sóIido branco (0,03 g, 17%). H1-RMN INOVA-500 (DMSO d6) δ 1,366 (t, J = 7,0 Hz, 3H), 3,591 (s, 2H), 4,110 (q, J = 7,0 Hz, 2H), 4,312 (d, J = 5,5 Hz, 2H), 6,985 (d, J = 7,5 Hz, 1H), 7,048-7,105 (m, 3H), 7,342- 7,402 (m, 2H), 7,621 (m, 2H), 7,770 (d, J = 7,0 Hz, 1H), 7,826 (d, J = 8,0 Hz, 1H), 7,942 (d, J = 7,5 Hz, 1H), 8,550 (s, 1H), 8,701(s, 1H). MS (m/) 365,2 (M+H)+.
[0333]Síntese do Composto 20, ácido 4-{5-[(3-flúor-benzil-carbamoil)-metil]- piridin-2-il}-benzóico. KX1-323
[0334]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida: Dissol- veu-se ácido 2-cloropiridino-5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou- se de um dia para outro, a mistura de reação foi então vertida em água, o sólido foi coletado por filtração, recristalizado usando-se água-metanol. (0,3 g, 85%); H1-RMN INOVA-500 (CDCI3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929- 7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0335]Síntese de N-(3-fIuorbenziI)-2-[6-(3-fIúor-feniI)-piridin-3-iI]-acetamida: DissoIveu-se 2-(6-cIoro-piridin-3-iI)-N-(3-fIuorbenziI)-acetamida e (0,15 g, 0,54 mmoI), ácido 4-carbóxi-benzeno-borônico (0,096 g, 0,6 mmoI) em DME, acrescentou-se Na2CO3 (0,11 g, 1,08 mmoI) em 5 mL de água à soIução de DME, a soIução teve então os gases extraídos durante 30 minutos (Ar através da soIução e apIicou-se vácuo du- rante os primeiros 5 minutos), acrescentou-se paIádio-tetraquis-trifeniIfosfina (0,031 g, 0,027 mmoI), extraíram-se os gases durante outros 15 minutos, fez-se refIuir durante 24 horas. Deixou-se a reação se resfriar até a temperatura ambiente, fiItrou-se, o só- Iido foi Iavado com acetato de etiIa, NaOH a 10%, a fase aquosa foi Iavada diversas vezes com acetato de etiIa, neutraIizada por acréscimo gota a gota de HCI a 1%, tendo acetato de etiIa no meio, com agitação depois de cada adição do HCI, fez-se evaporar acetato de etiIa e o sóIido formado foi cristaIizado a partir de metanoI-água para pro- duzir um sóIido branco (0,07 g, 40%). H1-RMN INOVA-500 (DMSO d6) δ 3,625 (s, 2H), 4,318 (d, J = 5,5 Hz, 2H), 7,053-7,111 (m, 3H), 7,376 (q, J = 7,0 Hz, 1H), 7,8341 (d, J = 8,0, 1H), 8,015-8,063 (m, 3H), 8,206 (d, J = 8,0 Hz, 1H), 8,613 (s, 1H), 8,724 (t, J = 5,5, 1H). MS (m/z) 365,3 (M+H)+.
[0336]Síntese do Composto 21, 2-[6-(2-Etóxi-fenil) piridin-3-iI]-N-(3-fIuorben- zil)-acetamida, KX1-324
[0337]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida: Dissol- veu-se ácido 2-cloropiridino-5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou- se de um dia para outro, verteu-se a mistura de reação em água, coletou-se o sólido por filtração, recristalizou-se, usando-se água-metanol. (0,3 g, 85%); H1-RMN INOVA- 500 (CDCl3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929-7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0338]Síntese de 2-[6-(2-etóxi-fenil)-piridin-3-il]-N-(3-fluorbenzil)-acetamida: Dissolveu-se 2-(6-Cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida e (0,15 g, 0,54 mmol), 2-etóxi-benzeno-borônico ácido (0,096 g, 0,6 mmol) em DME, acrescentou-se Na2CO3 (0,11 g, 1,08 mmol) em 5 mL de água à solução de DME, a solução teve então os gases extraídos durante 30 minutos (Ar através da solução e aplicou-se vácuo durante os primeiros 5 minutos), acrescentou-se paládio-tetraquis-trifenilfosfina (0,031 g, 0,027 mmol), extraíram-se os gases durante outros 15 minutos, fez-se refluir durante 24 horas. Deixou-se que a reação se resfriasse até a temperatura ambiente, filtrou-se, lavou-se o sólido com acetato de etila; secou-se a fase orgânica, fez-se evaporar. O resíduo foi cromatografado usando-se acetato de etila/hexano a 2:1, sendo ele então cristalizado a partir de metanol-água para produzir a um sólido branco (0,075 g, 40%). H1-RMN INOVA-500 (DMSO d6) δ 1,339 (t, J = 7,0 Hz, 3H), 3,581 (s, 2H), 4,112 (q, J = 7,0 Hz, 2H), 4,322 (d, J = 5,5 Hz, 2H), 7,032-7,135 (m, 5H), 7,358-7,387 (m, 2H), 7,703 (d, J = 7,0, 1H), 7,748 (d, J = 7,0 Hz, 1H), 7,871 (d, J = 7,0 Hz, 1H), 8,548 (s, 1H), 8,725 (s, 1H). MS (m/z) 365,2 (M+H)+.
[0339]Síntese do Composto 22, 2-[6-(4-etóxi-fenil)-piridin-3-il]-N-(3-fluorben- zil)-acetamida. KX1-325
[0340]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluor-benzil)-acetamida: Dissol- veu-se ácido 2-cloropiridino-5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou- se de um dia para outro, verteu-se a mistura de reação então em água, coletou-se o sólido por filtração, recristalizou-se, usando-se água-metanol. (0,3 g, 85%); H1-RMN INOVA-500 (CDCI3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929- 7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0341]Síntese de 2-[6-(4-etóxi-feniI)-piridin-3-iI]-N-(3-fIuorbenziI)-acetamida: DissoIveu-se 2-(6-cIoro-piridin-3-iI)-N-(3-fIuorbenziI)-acetamida e (0,15 g, 0,54 mmoI), ácido 4-etóxi-benzeno-borônico (0,096 g, 0,6 mmoI) em DME, acrescentou-se Na2CO3 (0,11 g, 1,08 mmoI) em 5 mL de água à soIução de DME, a soIução teve então os gases extraídos durante 30 minutos (Ar através da soIução e apIicou-se vácuo durante os primeiros 5 minutos), acrescentou-se paIádio-tetraquis-trifeniIfosfina (0,031 g, 0,027 mmoI), extraíram-se os gases durante outros 15 minutos, fez-se refIuir durante 24 horas. Deixou-se que a reação se resfriasse até temperatura ambiente, fiItrou-se, Iavou-se o sóIido com acetato de etiIa; secou-se a fase orgânica, fez-se evaporar. O resíduo foi cromatografado, usando-se acetato de etiIa/hexano 2:1, sendo eIe então cristaIizado a partir de metanoI-água para produzir a um sóIido branco (0,08 g, 42%). H1-RMN INOVA-500 (DMSO d6) δ 1,357 (t, J = 7,0 Hz, 3H), 3,564 (s, 2H), 4,090 (q, J = 7,0 Hz, 2H), 4,309 (d, J = 6,0 Hz, 2H), 7,012-7,103 (m, 5H), 7,361 (q, J = 7,0 Hz, 1H), 7,726 (d, J = 8,0 Hz, 1H), 7,842 (d, J = 8,0 Hz, 1H), 8,012 (d, J = 8,5 Hz, 2H), 8,503 (s, 1H), 8,686 (s, 1H). MS (m/z) 365,2 (M+H)+.
[0342]Síntese em maior escala do composto 22 HCI, 2-[6-(4-etóxi-feniI)-piri- din-3-il]-N-(3-fluorbenzil)-acetamida HCI, KX1-325 HCI
[0343]Síntese de 2-(6-cIoro-piridin-3-iI)-N-(3-fIuorbenziI)-acetamida HCI: Dis- soIveu-se ácido 2-cIoropiridino-5-acético (6,0 g, 34 mmoI), 3-fIuorbenziIamina (4,5 mL, 34 mmoI), PyBOP (18 g, 36 mmoI), e DIEA (12,5 mL, 75 mmoI) em DMF, agitou-se de um dia para outro, a mistura de reação foi então vertida em água, o sóIido foi coIetado por fiItração, recristaIizado, usando-se água-metanoI (6,3 g, 70%); H1-RMN INOVA- 500 (CDCl3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929-7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0344]Síntese de 2-[6-(4-etóxi-fenil)-piridin-3-il]-N-(3-fluorbenzil)-acetamida: Suspendeu-se 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida e (4,8 g, 17,2 mmol), ácido 4-etóxi-benzeno borônico (3,14 g, 17,9 mmol) em DME (100 mL), acrescentou- se Na2CO3 (3,6 g, 34,4 mmol) em 15 mL de água à solução de DME, a solução teve então os gases extraídos durante 30 minutos (Ar através da solução e aplicou-se vá- cuo durante os primeiros 5 minutos), acrescentou-se paládio-tetraquis-trifenilfosfina (0,99 g, 0,86 mmol), extraíram-se os gases durante outros 15 minutos, fez-se refluir de um dia para outro. Deixou-se que a reação se resfriasse até a temperatura ambi- ente, filtrou-se, lavou-se o sólido com acetato de etila frio e com solução saturada de NaHCO3, recristalizando-se então o sólido a partir de metanol para produzir um sólido branco (4,8 g).
[0345]4,6 g da amina livre foram dissolvidos em 50 mL de etanol com um su- ave aquecimento, sendo então acrescentados 25 mL de HCl a 4N em acetato de etila, concentrou-se a solução a 20 mL, diluindo-se então com 100 mL de acetato de etila frio, o sólido formado foi filtrado, lavado com mais acetato de etila (50 x 2) e secado (4,3 g, 65%); H1-RMN INOVA-500 (DMSO d6) δ 1,386 (t, J = 7,0 Hz, 3H), 3,822 (s, 2H), 4,179 (q, J = 7,0 Hz, 2H), 4,339 (d, J = 6,0 Hz, 2H), 7,074-7,182 (m, 5H), 7,374 (m, 1H), 8,106 (d, J = 8,0 Hz, 1H), 8,263 (d, J = 8,0 Hz, 1H), 8,312 (s, 2H), 8,718 (s, 1H), 8,981 (s, 1H), MS (m/z) 365,2 (M+H)+.
[0346]Ponto de Fusão da base livre: agitou-se 0,1 g do sal HCl em 10 mL de NaOH a 20% durante 10 minutos, filtrou-se; cristalizou-se o sólido a partir de eta- nol/água, secou-se na estufa a 100°C durante 2 horas. Constatou-se que o ponto de fusão era 173-176°C.
[0347]Síntese do Composto 23, N-(3-fluorbenzil)2-[6-(4-metano-sulfonil-fenil)- piridin-3-il]-acetamida, KX1-326
[0348]Síntese de 2-(6-cloro-piridin-3-il)-N-(3-fluorbenzil)-acetamida: Dissol- veu-se o ácido 2-cloropiridino-5-acético (0,2 g, 1,21 mmol), 3-fluorbenzilamina (0,15 mL, 1,2 mmol), PyBOP (0,67 g, 1,3 mmol), e DIEA (0,43 mL, 2,6 mmol) em DMF, agitou-se de um dia para outro, verteu-se então a mistura de reação em água, coletou- se o sólido por filtração, recristalizou-se, usando-se água-metanol (0,3 g, 85%); H1- RMN INOVA-500 (CDCI3) δ 3,562 (s, 2H), 4,429 (d, J = 6,5 Hz, 2H), 5,868 (s, 1H), 6,929-7,015 (m, 3H), 7,300-7,333 (m, 2H), 7,668 (dd, J = 8, 2,5 Hz, 1H), 8,280 (d, J = 2,5 Hz, 1H).
[0349]Síntese de N-(3-fIuorbenziI)-2-[6-(4-metano-suIfoniI-feniI)-piridin-3-iI]- acetamida: DissoIveu-se 2-(6-cIoro-piridin-3-iI)-N-(3-fIuorbenziI)-acetamida e (0,15 g, 0,54 mmoI), ácido 4-metano-suIfoniI benzeno borônico (0,12 g, 0,6 mmoI) em DME, acrescentou-se Na2CO3 (0,11 g, 1,08 mmoI) em 5 mL de água à soIução de DME, extraíram-se os gases da soIução durante 30 minutos (Argônio através da soIução e vácuo apIicado durante os primeiros 5 minutos), acrescentou-se paIádio-tetraquis-tri- feniIfosfina (0,031 g, 0,027 mmoI), extraíram-se os gases durante outros 15 minutos, fez-se refIuir durante 24 horas. Deixou-se a reação se resfriar até a temperatura am- biente, fiItrou-se, Iavou-se o sóIido com acetato de etiIa; secou-se a fase orgânica e fez-se evaporar. O resíduo foi cromatografado usando-se acetato de etiIa/hexano a 2:1, em seguida eIe foi cristaIizado a partir de metanoI-água para produzir um sóIido branco (0,02 g, 10%); H1-RMN INOVA-500 (DMSO d6) δ 3,341 (s, 3H), 3,635 (s, 2H), 4,315 (d, J = 7,0 Hz, 2H), 7,047-7,110 (m, 3H), 7,366 (q, J = 9,0 Hz, 1H), 7,857 (d, J = 8,5 Hz, 1H), 8,027-8,081 (m, 3H), 8,343 (d, J = 10,5 Hz, 2H), 8,631 (s, 1H), 8,731 (s, 1H), MS (m/z) 399,2 (M+H)+.
[0350]Síntese do Composto 24, KX1-327, e Composto 26, KX1-357
[0351]As sínteses são mostradas no Esquema 5.
[0352]Composto 24, KX1-327 HCl
[0353]Uma soIução de 75 mL de 1,2-dimetóxi-etano e 16 mL de carbonato de sódio a 2 M teve exaustivamente extraídos os gases por aquecimento a 50°C com uma corrente de argônio através do solvente. Acrescentaram-se 5,00 g da 4-bromo- fenil acetamida (5, 15,6 mmol) e 1,95 grama de ácido 4-piridilborônico (1,00 eq) e continuou-se a extrair os gases durante 1 hora. Acrescentou-se tetraquis(trifenilfos- fina) paládio (5% molar) puro e fez-se a reação refluir durante 24 horas. A reação foi resfriada e vertida em 300 mL de água destilada e filtrada resultando em 5,014 g de produto bruto. Este produto bruto foi absorvido em 1 L de uma mistura a 1 para 1 de HCl a 1N e acetato de etila. A fase orgânica foi descartada e a fase aquosa foi lavada duas vezes mais com EtOAc. A fase aquosa foi basificada com bicarbonato de sódio sólido até pH 7,5, esta foi então extraída com 3 X 300 mL de EtOAc obtendo-se apro- ximadamente 3,25 g de produto semi-puro. Cristais puros da base livre foram prepa- rados dissolvendo-se 200 mg em uma quantidade mínima de acetato de etila com suave aquecimento e sonicação. Acrescentaram-se hexanos a esta solução até ela se turvar. Aqueceu-se esta solução até ficar transparente Repetiu-se a adição de mais hexanos e o aquecimento subsequente mais duas vezes. Deixou-se esta solução transparente repousar de um dia para o outro em um recipiente lacrado. Formaram- se cristais brancos que foram lavados com hexanos e secou-se, obtendo-se aproxi- madamente 50 mg (pf 145-146°C). Dissolveu-se o resto do produto em etanol e acres- centaram-se dois equivalentes de ácido clorídrico (a 1,1 M em EtOAc). Depois de 1 hora, removeu-se o etanol e redissolveu-se na menor quantidade de etanol a 40°C. Acrescentou-se EtOAc até a solução se turvar. Deixou-se a solução repousar e o pro- duto desejado se cristalizou em forma de cristais branco puro. Filtraram-se os cristais, lavou-se com EtOAc e secou-se, obtendo-se 2,4 gramas (rendimento total de 48%); LCMS 321,3 (m+H). 1H RMN (500 MHz, DMSO) 3,61 (s, 2H) 4,29 (d, 7,5 Hz, 2H) 7,04 (m, 3H) 7,34 (q, 9,5 Hz, 1H) 7,50 (d, 10,5 Hz, 2H) 7,95 (d, 10,5 Hz, 2H) 8,24 (d, 8,0 Hz, 2H) 8,70 (s, 1H) 8,87(d, 8,0Hz, 2H).
[0354]Composto 26, KX1-357
[0355]Dissolveu-se 47,0 mg de KX1-327 em 5 mL de DCM. Acrescentou-se ácido meta-cloroperóxi-benzóico (35,0 mg, 1,4 eq) e deixou-se a reação se agitar du- rante 13 horas. Lavou-se a reação 3 x 5 mL com solução saturada de bicarbonato, secou-se com sulfato de sódio e concentrou-se, obtendo-se 45 mg de um sólido ama- relo. RMN revelou que o produto continha aproximadamente 15% de impurezas, que podem ter sido do ácido m-clorobenzóico (ou do peróxido). Redissolveu-se o sólido em 5 mL de DCM e lavou-se 3 X 5 mL de solução saturada de bicarbonato de sódio, secou-se com sulfato de sódio e concentrou-se, obtendo-se 26 mg do produto dese- jado em forma de um sólido amarelo; LCMS 337,2 (M+H), 672,9 (2M+H), 694,8 (2M+Na). 1H RMN (400 MHz, DMSO) 3,54 (s, 2H), 4,28 (d, 6,0 Hz, 2H), 7,00-7,08 (m, 3H), 7,34 (q, 8,0 Hz, 1H), 7,40 (d, 8,4 Hz, 2H), 7,72 (d, 8,4 Hz, 2H), 7,75 (d, 7,2 Hz, 2H), 8,24 (d, 8,4 Hz, 2H), 8,63 (t, 5,6 Hz, 1H).
[0357]Dissolveu-se ácido 4-bromofenil acético (6,00 g, 47,9 mmol) em 40 mL de diclorometano anidro sob uma atmosfera de argônio e resfriou-se em um banho de gelo. Acrescentou-se 3-fluorbenzilamina (1,00 eq) e produziu-se uma precipitação não intencional do de ácido acético/sal de benzilamina. Acrescentou-se mais diclorome- tano (20 mL) seguido por DIEA (2,2 eq), HOBT (1,0 eq), e EDCI (1,1 eq). Depois de aproximadamente 2 horas o sólido se decompôs, 4 horas depois a reação estava ter- minada por TLC. Diluiu-se a reação com 200 mL de diclorometano e 200 mL de ácido clorídrico a 1N. Depois de se agitar em um funil separador, formou-se uma emulsão. Esta emulsão foi dividida em duas e o diclorometano foi removido. Acrescentaram-se 500 mL acetato de etila e outros 300 mL HCl a 1N a cada metade. Lavou-se a fase orgânica 2 vezes mais com HCl a 1N, 3 X 300 mL de bicarbonato de sódio saturado, e 3 X 200 mL de cloreto de sódio saturado. Combinaram-se as fases orgânicas pro- venientes de cada extração e secaram-se com sulfato de sódio, removeu-se o sol- vente, obtendo-se 13,12 g (rendimento de 85%) do produto desejado; 1H RMN (500 MHz, CDCI3) δ (ppm) 3,58 (s, 2H), 4,45 (d, 6,0 Hz, 2H), 5,70 (bs, 1H) 6,93 (m, 3H), 7,16 (d, 8,1 Hz, 2H), 7,26 (m, 1H) 7,48 (d, 8,1 Hz, 2H).
[0358]Síntese do Composto 25, KX1-329
[0359]Conforme apresentado no Esquema 6, converteu-se 5-hidróxi-2-metil- piridina no triflato, 6, seguido pela reação de Suzuki, obtendo-se a 5-fenil-2-metilpiri- dina. A metil piridina, 7, foi desprotonada com n-butil lítio e acrescentada a uma solu- ção de carbonato de etila. A saponificação seguida por acoplamento de amida com PyBOP resultou no produto desejado.
[0360]Dissolveu-se 5-hidróxi-2-metilpiridina (3,00 g, 27,5 mmol) em 15 mL de piridina anidra e resfriou-se a 0°C. Acrescentou-se gota a gota anidrido tríflico (7,76 g, 1,1 eq.) durante 3 minutos. Depois da adição a reação foi removida do banho de gelo e deixou-se que se agitasse durante 6 horas. O volume foi então reduzido a 8 mL a vácuo, diluiu-se com 50 mL água destilada, e então extraiu-se com 75 mL de EtOAc. Secou-se então a fase orgânica com HCl a 1N (3 X 50 mL), secou-se com sulfato de sódio, e removeu-se a vácuo, obtendo-se 2,78 g (42%) de um óleo cor de âmbar (6); LCMS 242,1 (m+H). 1H RMN (400 MHz, CDCl3) 2,58 (s, 3H) 7,26 (d, 8,4 Hz, 1H) 7,52 (dd, 2,8 Hz, 8,4Hz, 1H) 8,47 (d, 2,8 Hz, 1H).
[0361]Um frasco de fundo redondo de 50 mL secado na chama dotado com dois condensadores foi carregado com argônio. Aqueceu-se dimetoxietano, 25 mL e 6 mL de carbonato de sódio a 2M até 45°C, fazendo-se borbulhar simultaneamente com argônio a solução. Depois de 1 hora, acrescentaram-se o triflato de piridila (6) (1,538 g, 6,382 mmol) e o ácido fenilborônico (856 mg, 1,1 eq). Depois de uma hora acrescentou-se Pd(PPh3)4 (370 mg, 5% molar), aqueceu-se a reação a 65-75°C du- rante 48 horas. Verteu-se o solvente em um frasco de fundo redondo, lavou-se o re- síduo restante com acetato de etila. Combinaram-se os solventes e removeram-se a vácuo. O resíduo foi purificado por cromatografia sobre gel de sílica (hexanos:EtOAc), obtendo-se 702 mg do produto desejado 7 (rendimento de 65%); LCMS 170,2(m+H). 1H RMN (400 MHz, CDCl3) 3,60 (s, 3H) 7,22 (d, 8,0 Hz, 1H) 7,38 (t, 7,2 Hz, 1H) 7,46 (t, 7,2 Hz, 2H) 7,56 (d, 8,0 Hz, 2H) 7,77 (dd, 2,4Hz, 8,0Hz, 1H) 8,73 (d, 2,4Hz, 1H).
[0362]5-Fenil-2-metilpiridina (7,205 mg, 1,223 mmol) foi dissolvida em THF recém destilado em recipiente de vidro secado na chama sob argônio. Resfriou-se até -78°C em um banho de gelo seco/acetona durante 20 minutos. Acrescentou-se gota a gota N-butil lítio (0,485 mL, 1,0 eq) durante 5 minutos. Acrescentou-se esta solução a uma solução de carbonato de etila (1,5 eq.) em THF por meio de uma cânula. Agitou- se a solução durante 2 horas antes de se extinguir com metanol acrescentado gota a gota. Acrescentou-se hidróxido de sódio a 1N (1 mL) antes de se remover os solventes orgânicos a vácuo. A solução aquosa restante foi extraída com éter (3 X 15 mL). Com- binaram-se as fases orgânicas e secou-se com sulfato de sódio e removeu-se a vá- cuo, obtendo-se 208 mg 8 (rendimento de 71%) 1H RMN (500 MHz, CDCl3) 1,30 (m, 3H) 2,61 (s, 2H) 4,20 (m, 3H) 7,22 (d, 8,0 Hz, 1H) 7,38 (t, 7,5 Hz, 1H) 7,48 (t, 7,5 Hz, 2H) 7,58(m, 2H) 7,78 (dd, 2,5 Hz, 8,0Hz, 1H) 8,73 (d, 2,5 Hz, 1H).
[0363]Dissolveu-se éster etílico 8 (208 mg, 0,86 mmol) em 5 mL de THF. Acrescentou-se NaOH a 1N (aproximadamente 1 mL) e colocou-se a reação em um banho-maria a 35°C de um dia para outro. O volume da reação foi reduzido a aproxi- madamente 1 mL e então acidificado com HCl a 1N para precipitar o produto desejado. O precipitado foi isolado por decantação e secado a vácuo, obtendo-se 54 mg (rendi- mento de 30%) de 9; LCMS 214,1 (m+H) 236,0 (m+Na). 1H RMN (400 MHz, CD3OD) 3,64 (s, 2H) 7,24-7,28 (m, 4H) 7,25 (t, 8,4 Hz, 2H) 7,52 (d, 8,4 Hz, 2H) 7,87 (dd, 2,0 Hz, 8,0Hz, 1H) 8,53 (d, 2,0 Hz, 1H).
[0364]Dissolveram-se ácido carboxílico 9 (54 mg, 0,232 mmol), 3-fluorbenzi- lamina (1,1 eq), e PyBOP (1,1 eq) em 3 mL de DMF anidro. Depois de 10 minutos acrescentou-se DIEA (1,1 eq) e deixou-se a reação se agitar de um dia para outro. O DMF foi removido a vácuo e o resíduo foi absorvido com metanol e cristalizado a partir de metanol/água, obtendo-se 44 mg do Composto 25, KX1-329 (55%) em forma de cristais transparentes em forma de agulhas; TLC, Rf 0,2 (DCM:EtOAc a 1:1). LCMS 321,2 (m+H), 343,1 (m+Na), 662,9 (2m+Na). 1H RMN (400 MHz, CDCl3) 3,82 (s, 2H), 4,46 (d, 8,8 Hz, 2H), 6,91 (t, 9,2 Hz, 2H) 6,99 (d, 7,6 Hz, 1H), 7,25 (t, 8,4 Hz, 2H), 7,34 (d, 8,0 Hz, 2H) 7,40 (tt, 1,2 Hz, 7,2 Hz, 2H) 7,55 (d, 7,6 Hz, 2H) 7,80 (b, 1H) 7,86 (dd, 2,0 Hz, 7,6 Hz, 1H) 8,73 (d, 2,0 Hz, 1H).
[0366]Reagentes: i) Tf2O, piridina (43%). ii) ácido fenilborônico (1,1 eq), Na2CO3 (1,3 eq), Pd(PPh3)4 (5% molar), dimetoxietano, Na2CO3 a 2M (2 eq) (65% depois de cromatografia), iii) n-Butil lítio (1,0 eq), carbonato de dietila (1,5 eq), THF anidro. iv) LiOH, THF 3OC (18% depois da cristalização), v) 3-fluorbenzilamina (1,1 eq), PyBOP (1,1 eq), DIEA (1,1 eq), DMF (rendimento de 55%).
[0367]Síntese do Composto 27, 2-[6-(4-etóxi-fenil)-1-oxo-piridin-3-il]-N-(3-flu- orbenzil)-acetamida, KX1-358
[0368]A uma solução resfriada com gelo de 0,2 g de 2-[6-(4-etóxi-fenil)piridin- 3-il]-N-(3-fluorbenzil)-acetamida em 80 mL de DCM, acrescentou-se 0,13 g de ácido m-cloroperbenzóico em forma de sólido. Depois de se agitar de um dia para outro, lavou-se a reação com solução saturada de bicarbonato de sódio, secou-se com sul- fato de sódio, fez-se evaporar a vácuo até secar, cromatografou-se então (gel de sí- lica), usando-se acetato de etila, seguido de metanol a 10% em acetato de etila para produzir 0,16 g (78%); H1-RMN INOVA-400 (DMSO de) δ 1,357 (t, J = 7,0 Hz, 3H), 3,564 (s, 2H), 4,090 (q, J = 6,8 Hz, 2H), 4,309 (d, J = 5,60 Hz, 2H), 7,012-7,103 (m, 5H), 7,245 (d, J = 8,0 Hz, 1H), 7,729 (m, 1H), 7,529 (d, J = 8,0 Hz, 1H), 7,800 (d, J = 8,5 Hz, 2H), 8,225 (s, 1H), 8,663 (t, J = 5,6 Hz, 1H). MS (m/z) 380 (M+H)+.
[0369]Para as sínteses seguintes, a não ser que seja observado em contrário, os reagentes e solventes foram usados no estado em que foram recebidos dos forne- cedores comerciais. Os espectros de ressonância magnética nuclear de prótons e de carbono foram obtidos em um espectrômetro Bruker AC 300 ou um Bruker AV 300 a 300 MHz para o próton e a 75 MHz para o carbono. Os espectros são dados em ppm (δ) e as constantes de acoplamento, J, são dadas em Hertz. Usou-se tetrametil-silano como um padrão interno para os espectros de próton e o pico de solvente foi usado como pico de referência para os espectros de carbono. Os dados de espectros de massa e de massa LC-MS foram obtidos em um espectrômetro de massa de ionização a pressão atmosférica (APCI) Perkin Elmer Sciex 100. As análises por LC-MS foram obtidas, usando-se uma Coluna Luna C8(2) (100 x 4,6 mm, Fenomenex) com detec- ção de UV a 254 nm usando-se um programa padrão de gradiente de solventes (Mé- todo B). A cromatografia de camada delgada (TLC) foi conduzida usando-se placas de gel de sílica Analtech e foi visualizada por luz ultravioleta (UV), iodo ou por ácido fosfomolíbdico a 20% em peso em etanol. As análises de HPLC foram obtidas usando- se uma coluna Prevail Cl 8 (53 x 7 mm, Alltech) com detecção de UV a 254 nm, usando-se um programa padrão de gradiente de solventes (Método A). Método A:
A = Água com ácido trifluoracético a 0,02 v/v B = Acetonitrila com ácido trifluoracético a 0,02 v/v Método B:
[0371]Carregou-se um frasco com 5-(5-bromopiridin-2(1H)-ilideno)-2,2-dime- til-1,3-dioxano-4,6-diona (1,039 g, 3,46 mmol), benzilamina (0,50 mL, 4,58 mmol), e tolueno (20 mL). Levou-se a reação a refluxo sob nitrogênio durante 18 horas, resfriou- se então e colocou-se em um congelador até esfriar. O produto foi coletado por filtra- ção e lavado com hexanos para resultar em uma massa de cristais de um branco brilhante (1,018 g, 96%).
[0373]A uma solução agitada de 4-(4,4,5,5-tetrametil [1,3,2]dioxaborolan-2-il)- fenol (2,55 g, 11,58 mmol), 2-morfolin-4-iletanol (1,60 mL, 1,73 g, 13,2 mmol) e trifenil fosfina (3,64 g, 13,9 mmol) em cloreto de metileno (60 mL) a 0°C acrescentou-se gota a gota DIAD (2,82 g, 13,9 mmol). Deixou-se que a reação se aquecesse até a tempe- ratura ambiente e agitou-se de um dia para outro. Depois de 18 horas, acrescentaram- se porções adicionais de trifenil fosfina (1,51 g, 5,8 mmol), 2-morfolin-4-iletanol (0,70 mL, 5,8 mmol), e DIAD (1,17 g, 5,8 mmol). Depois de se agitar durante outras 2 horas à temperatura ambiente, concentrou-se a reação e purificou-se o resíduo por croma- tografia flash (EtOAc a 5% a 25% em CHCl3), obtendo-se o produto em forma de um sólido branco (2,855 g, 74%).
[0375]Um tubo de reação de 10 mL dotado com um fecho de septo e uma barra de agitação foi carregado com N-benzil-2-(5-bromopiridin-2-il)acetamida (123 mg, 0,403 mmol), 4-(2-(4-(4,4,5,5-tetrametil[l,3,2]dioxaborolan-2-il)-fenóxi)etil) morfo- lina (171 mg, 0,513 mmol), e FibreCat 10071 (30 mg, 0,015 mmol). Acrescentou-se etanol (3 mL) seguido por solução aquosa de carbonato de (0,60 mL, 1,0M, 0,60 mmol). O tubo foi vedado e aquecido em condições de microondas a 150°C durante 10 minutos. Resfriou-se a reação e concentrou-se para se remover a maior parte do etanol, absorvendo-se então em 10 mL de acetato de etila e lavando-se sucessiva- mente com água e solução saturada de cloreto de sódio. Secou-se a fase orgânica com MgSO4, filtrou-se e concentrou-se em um sólido branco. Este sólido branco foi triturado com éter etílico, obtendo-se ALB 30349 em forma de um sólido branco (137 mg, 79%): pf 135-137°C; 1H RMN (300 MHz, CDCI3) δ 8,70 (d, 1H, J = 2,0 Hz), 7,81 (dd, 1H, J = 2,4 Hz, J = 8,0 Hz), 7,65 (br s, 1H), 7,49 (d, 2H, J = 8,8 Hz), 7,37-7,20 (m, 6H), 7,01 (d, 2H, J = 8,8 Hz), 4,49 (d, 2H, J = 5,8 Hz), 4,16 (t, 2H, J = 5,7 Hz), 3,82 (s, 2H), 3,78-3,72 (m, 4H), 2,84 (t, 2H, J = 5,7 Hz), 2,62—2,58 (m, 4H); HPLC (Método B) 98,0% (AUC), tR = 1,834 mm,; APCI MS m/z 432 [M+H]+. 1Di(acetato)diciclo-hexil-fenil-fosfino-paládio (II) ligado a polímero, fabricado por Johnson Matthey, Inc. e disponível de Aldrich (catálogo # 590231)
[0377]Um frasco de 500 mL foi carregado com ácido 4-bromo-3-fluorbenzóico (5,00 g, 22,83 mmol), 100 mL DMF, morfolina (2,4 mL, 27,5 mmol), e 4-etilmorfolina (7,6 mL, 67,9 mmol). Acrescentou-se HOBt (4,32 g, 32,0 mmol) seguido por EDC (5,25 g, 27,4 mmol) e deixou-se a reação se agitar à temperatura ambiente durante 18 ho- ras. Concentrou-se a reação e o xarope cor de laranja resultante foi absorvido em 100 mL de EtOAc e 100 mL de água. Lavou-se a fase orgânica com 100 mL de HCl a 2N, 100 mL de bicarbonato de sódio saturado, e 100 mL de cloreto de sódio saturado. Secou-se então a fase orgânica com MgSO4, filtrou-se, e concentrou-se, obtendo-se 6,476 g (98%) de um óleo amarelo viscoso. Este material foi usado sem outra purifi- cação.
[0379]Carregou-se um frasco de 250 mL com (4-bromo-3-fluorfenil)(morfo- lino)metanona (4,569 g, 15,86 mmol) e dissolveu-se em 16 mL de THF. Acrescentou- se difenilsilano (6,2 mL, 33,4 mmol) e em seguida hidreto de carboniltris(trifenilfos- fino)ródio(I) (100 mg, 0,109 mmol) e agitou-se a reação à temperatura ambiente du- rante 20 horas.
[0380]Diluiu-se a reação com 200 mL de éter e extraiu-se em HCl (2 x 150 mL). Isto resultou na formação de um precipitado branco no funil separador. A fase ácida e o precipitado branco resultante foram lavados com éter (2 x 100 mL), e então basificados com grânulos secos de NaOH (23 g). Extraiu-se então a fase aquosa com éter (3 x 125 mL), secada sobre MgSO4, filtrou-se, e concentrou-se, obtendo-se 1,35 g (31%) de um óleo incolor. Este material foi usado sem outra purificação.
[0382]Um tubo de reação de 10 mL para microondas dotado de um fecho de septo foi carregado com 4-(4-bromo-3-fluorbenzil)morfolina (405 mg, 1,48 mmol), Bis(pinacolato) diboro (516 mg, 2,03 mmol), Pd(dppf)Cl2 ^CH2Cl2 (62 mg, 0,076 mmol), acetato de potássio (659 mg, 6,72 mmol), e DMF (3,6 mL). Colocou-se o frasco sob nitrogênio por evacuação/reenchimento (5 ciclos) e agitou-se a 80°C durante 8 horas. Resfriou-se a reação, diluiu-se com acetato de etila (25 mL) e filtrou-se. As fases or- gânicas foram lavadas com água (25 mL) e com cloreto de sódio saturado (25 mL). A fase orgânica foi então secada sobre MgSO4 e concentrada em um óleo escuro. O produto foi purificado por cromatografia sobre gel de sílica, eluindo-se com MeOH a 2% em CHCl3, obtendo-se 310 mg (65%) de um sólido esbranquiçado.
[0384]Um tubo de reação 10 mL para microondas dotado de fecho por septo foi carregado com 4-(3-flúor-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)benzil)morfo- lina (307 mg, 0,96 mmol), 2-(5-bromopiridin-2-il)-N-(3-fluorbenzil) acetamida (247 mg, 0,77 mmol), e FibreCat 1007 (60 mg, 0,03 mmol). Acrescentou-se etanol (3 mL) se- guido por solução aquosa de carbonato de potássio (1,2 mL, 1,0M, 1,2 mmol). O tubo foi lacrado e aquecido em condições de microondas a 150 °C durante 10 minutos. Resfriou-se a reação e concentrou-se para se remover a maior parte do etanol, e em seguida foi absorvida em 10 mL de acetato de etila e lavada sucessivamente com água e solução saturada de cloreto de sódio. A fase orgânica foi secada com MgSO4, filtrada e concentrada. O material foi purificado por cromatografia de coluna (gel de sílica, CHCl3/MeOH a 100:0 a CHCl3/MeOH a 95:5) para resultar em ALB 30351 em forma de um sólido branco (240 mg, 74%): pf 91-92°C; 1H RMN (300 MHz, CDCI3) δ 8,71 (br s, 1H), 7,86-7,84 (m, 1H), 7,78 (br s, 1H), 7,37 (t, 2H, J = 7,5 Hz), 7,28-7,21 (m, 3H), 7,02 (dd, 1H, J = 0,6 Hz, J = 7,7 Hz), 6,98-6,90 (m, 2H), 4,49 (d, 2H, J = 5,9 Hz), 3,84 (s, 2H), 372—3,75 (m, 4H), 3,52 (s, 2H), 2,47—2,50 (m, 4H); HPLC (Método A) 98,7% (AUC), tR = 3,866 min.; APCI EM m/z 438 [M+H]+.
[0386]Carregou-se um frasco com 4-bromo-3-fluorfenol (4,999 g, 26,2 mmol) e trifenilfosfina (10,298 g, 39,3 mmol). Acrescentou-se cloreto de metileno (120 mL) seguido por 2-morfolino-etanol (4 mL, 33,0 mmol) e agitou-se a solução sobre banho de água gelada para se resfriar. Depois de 5 minutos, acrescentou-se azodicarboxilato de diisopropila (7,6 mL, 39,1 mmol) durante 6 a 8 minutos. Deixou-se a reação se agitando no banho de resfriamento para se aquecer lentamente até a temperatura ambiente de um dia para outro. A reação foi concentrada e o resíduo purificado por cromatografia flash (EtOAc a 25% a 100% em hexanos) para resultar no produto em forma de um óleo incolor (2,621 g, 33%).
[0388]Um tubo de reação de 40 mL para microondas dotado com um fecho de septo e barra de agitação foi carregado com 4-(2-(4-bromo-3-fluorfenóxi)etil)mor- folina (307 mg, 1,0 mmol), Bis(pinacolato)diboro (318 mg, 1,25 mmol), Pd(dppf)Cl2- CH2Cl2 (68 mg, 83 μmol), e acetato de potαssio (316 mg, 3,22 mmol). Acrescentou-se DME (20 mL) e o tubo foi selado. O tubo foi evacuado/reenchido com N2 (5 ciclos) e submetido a microondas a 125°C durante 30 minutos. Resfriou-se a reação até a tem- peratura ambiente, concentrou-se e purificou-se o resíduo por cromatografia de coluna (gel de sílica, MeOH a 2% em CHCl3) resultando no produto em forma de um óleo incolor (356 mg, >99%). O espectro de RMN 1H mostra que o produto contém uma pequena quantidade de impureza semelhante a pinacol. O material foi usado no es- tado em que estava.
[0390]Um tubo de reação de 10 mL para microondas dotado de fecho de septo foi carregado com 4-(2-(3-flúor-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2 - il) fenóxi) etil) morfolina (175 mg, 0,50 mmol), 2-(5-bromopiridin-2-il)-N-(3-fluorbenzil)acetamida (121 mg, 0,37 mmol), e FibreCat 1007 (30 mg, 0,03 mmol). Acrescentou-se etanol (3 mL) seguido por solução aquosa de carbonato de potássio (0,600 mL, 1,0 M, 0,60 mmol). O tubo foi vedado e aquecido em condições de microondas a 150°C durante 10 minutos. Resfriou-se a reação, filtrou-se, e concentrou-se para remover a maior parte do etanol. O resíduo foi absorvido em 10 mL de acetato de etila e lavado suces- sivamente com água e solução saturada de cloreto de sódio. Secou-se a fase orgânica com MgSO4, filtrou-se, e concentrou-se. O material foi purificado por cromatografia de coluna (gel de sílica, de CHCL3/MEOH a 100:0 a CHCl3/MeOH a 95:5) resultando em ALB 30350 em forma de um sólido branco (70 mg, 40%): pf 126-127°C; 1H RMN (500 MHz, CDCI3) δ 8,67 (br s, 1H), 7,77-7,85 (m, 2H), 7,21-7,37 (m, 3H), 7,02 (d, 1H, J = 7,7 Hz), 6,90-6,97 (m, 2H), 6,82 (dd, 1H, J = 2,5 Hz, J = 8,6 Hz), 6,76 (dd, 1H, J = 2,4 Hz, J = 12,4 Hz), 4,49 (d, 2H, J = 5,9 Hz), 4,15 (t, 2H, J = 5,7 Hz), 3,83 (s, 2H), 3,71— 3,78 (m, 4H), 2,83 (t, 2H, J = 5,7 Hz), 2,56—2,63 (m, 4H); HPLC (Método A) >99% (AUC)5 tR = 4,026 minutos; APCI EM m/z 46S [M+H]+.
[0392]Um frasco foi carregado com 4-bromo-3-fluorfenol (5,00 g, 26 mmol) e trifenilfosfina (10,30 g, 39 mmol). Acrescentou-se cloreto de metileno (120 mL) se- guido por 2-(4-metil-piperazin-1-il)etanol (4,61 g, 32 mmol) e agitou-se a solução em um banho de água gelada para se resfriar. Depois de 5 minutos, acrescentou-se azo- dicarboxilato de diisopropila (7,6 mL, 39,1 mmol) durante 6 to 8 minutos. Deixou-se a reação se agitar no banho frio para se aquecer lentamente até a temperatura ambiente de um dia para outro. A reação foi concentrada e o resíduo purificado por cromatografia flash (EtOAc a 25% a 100% em hexanos) para produzir o produto em forma de um óleo incolor (2,62 g, 33%)
[0393]1 - (2 - (3 - flúor-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenóxi)etil)- 4-metil-piperazina:
[0394]Um tubo de reação de 40 mL para microondas dotado com um fecho de septo e uma barra de agitação foi carregado com 1-(2-(4-bromo-3-fluorfenóxi)etil)- 4-metil-piperazina (428 mg, 1,35 mmol), Bis(pinacolato)diboro (375 mg, 1,48 mmol), Pd(dppf)Cl2-CH2Cl2 (63 mg, 77 μmol), e acetato de potαssio (410 mg, 4,18 mmol). Acrescentou-se DME (10 mL) e o tubo foi vedado. O tubo foi evacuado/reenchido com N2 (5 ciclos) e submetido a microondas a 100°C durante 30 minutos. Acrescentou-se mais Pd(dppf)Cl2-CH2Cl2 (63 mg, 77 μmol) e a reanão foi submetida a microondas a 100°C durante 60 minutos. Resfriou-se a reação até a temperatura ambiente, concen- trou-se e purificou-se o resíduo por cromatografia de coluna (gel de sílica, MeOH a 1% to 2% em CHCl3) resultando no produto em forma de um óleo escuro (354 mg, 72%).
[0396]Um tubo de reação de microondas de 10 mL com um fecho de septo foi carregado com 1-(2-(3-flúor-4-(4,4,5,5-tetrametil - 1,3,2 - dioxaborolan-2-il)fenóxi)etil)- 4-metil-piperazina (340 mg, 0,93 mmol), 2-(5-bromopiridin-2-il)-N-(3- fluorbenzil)acetamida (201 mg, 0,62 mmol), e FibreCat 1007 (125 mg, 0,06 mmol). Acrescentou-se etanol (3 mL) e em seguida solução aquosa de carbonato de potássio (1,00 mL, 1,0M, 1,00 mmol). O tubo foi vedado e aquecido em condições de microon- das a 150°C durante 10 minutos. Resfriou-se a reação, filtrou-se e concentrou-se para se remover a maior parte do etanol. O resíduo foi então absorvido em 10 mL de ace- tato de etila e lavado sucessivamente com água e solução saturada de cloreto de sódio. A fase orgânica foi secada com MgSO4, filtrada, e concentrada. O material foi purificado por cromatografia de coluna (gel de sílica, CHCl3/MeOH a 98:2 até CHCl3/MeOH a 90:10) obtendo-se ALB 30352-2 em forma de uma goma de cor bege (28 mg, 9%): 1H RMN (300 MHz, CDCla) δ 8,66 (br s, 1H), 7,78—7,94 (m, 2H), 7,20- 7,40 (m, 3H), 6,88-7,06 (m, 3H), 6,70-6,85 (m, 2H), 4,47 (d, 2H, J = 5,9 Hz), 4,14 (t, 2H, J = 5,7 Hz), 3,83 (s, 2h), 2,85 (t, 2H, J = 5,7 Hz), 2,41-2,77 (m, 8H), 2,34 (s, 3H); HPLC (Método A) > 99 % (AUC), tR =3,778 minutos.; APCI EM m/z 481 [M + H]+.
[0397]Exemplo 2: Inibição de Crescimento Celular
[0398]A concentração de medicamento necessária para bloquear o cresci- mento celular líquido de 50% em relação à amostra de controle é medida como GI50. Os valores de GI50 para diversos dos compostos da invenção foram testados conforme descrito no presente documento.
[0399]A linhagem de células HT29 é uma linhagem de células de carcinoma humano do cólon humano NCI. As células HT-29 foram obtidas de ATCC na passa- gem 125 e foram usadas para estudos de inibição entre as passagens 126-151. As células HT29 foram rotineiramente cultivadas em um meio 5A de McCoy suplemen- tado com Soro Fetal Bovino (a 1,5% v/v) e L-glutamina (2 mM).
[0400]A c-Src 3T3 é uma linhagem de células normais NIH 3T3 de fibroblastos murinos que foi transfectada com um mutante de onto de c-Src humana em que a tirosina 527 foi convertida em uma fenilalanina. Esta mutação resulta em c-Src “cons- titutivamente ativa” pois a fosforilação na tirosina 527 resulta em auto-inibição de Src por fazer com que ela se dobre de volta no seu próprio domínio SH2. Com uma Phe ali, esta fosforilação não pode ocorrer e, portanto a auto-inibição não pode ocorrer. Portanto, o mutante Src sempre totalmente ativo converte então os fibroblastos muri- nos normais em células tumorais em rápido crescimento. Como a Src hiperativa é o principal fator que aciona o crescimento nestas células (especialmente quando culti- vadas em condições séricas de baixo crescimento), pensa-se que os compostos ati- vos no bloqueio deste crescimento funcionem por bloqueio da sinalização de Src (como um inibidor direto de Src quinase ou como um inibidor que age em algum outro lugar na cascata de sinalização de Src). As células foram rotineiramente cultivadas em DMEM suplementado com Soro Fetal Bovino (2,0 % v/v), L-glutamina (2 mM) e Piruvato de Sódio (1 mM).
[0401]No Ensaio BrdU para a inibição de crescimento celular, a quantificação de proliferação celular foi baseada na medição da incorporação de BrdU durante a síntese de DNA. O kit do ensaio BrdU ELISA de Proliferação Celular (colorimétrico) foi obtido de Roche Applied Science e conduzido conforme as instruções do vendedor.
[0402]A inibição do crescimento foi expressa como um GI50 em que GI50 é a dose de amostra que inibe 50% do crescimento celular. A inibição de crescimento (GI) é determinada a partir da fórmula GI = (T0-Tn x 100/T0-CONn), em que T0 é o cresci- mento BrdU de células sem tratamento no momento “0”, Tn é o crescimento BrdU de células tratadas no dia “n” e CONn é o crescimento BrdU de controle das células de controle no dia “n”. O valor GI50 foi extrapolado e os dados foram lançados em gráfico usando-se o software XL-Fit 4.0.
[0403]As culturas em crescimento ativo foram tripsinizadas e as células foram ressuspensas em 190 μL de meio de cultura apropriado suplementado com 1,05% de FBS em cada poço de uma placa de cultura de 96 poços (1000 células HT-29; 2500 células cSrc 3T3). Para experimentos de placa de cultura de 96 poços, o meio de c- Src 3T3 foi suplementado com tampão HEPES a 10 mM. As células HT-29 foram semeadas em placas de 96 poços para cultura tecidual padrão e as células c-Src 3T3 foram semeadas em placas de 96 poços revestidas com Poly-D-lisina (BIOCOATTM). Para se aumentar a difusão de CO2, placas de 96 poços para c-Src 3T3 foram incu- badas com as suas tampas levantadas de ~2 mm usando-se tampas de borracha es- téreis.
[0404]Deixou-se que placas de 96 poços semeadas se fixassem de um dia para outro durante 18-24 horas, ou a 37°C e 5% de CO2 para HT-29 ou a 37°C e 10% de CO2 para c-Src 3T3. Aproximadamente 18-24 horas depois da semeadura, o cres- cimento inicial de células (T0) foi determinado para células sem tratamento, usando- se o ensaio de BrdU. As amostras foram reconstituídas em DMSO a 20 mM e foram preparadas diluições intermediárias usando-se DMEM contendo FBS a 10%. As con- centrações de ensaio finais foram de 1,5% para FBS e 0,05% para DMSO. As amos- tras foram acrescentadas como alíquotas de 10 μL em triplicatas e as placas foram incubadas conforme foi descrito acima durante ~72 horas. Foram incluídos controles negativos (veículo) e controles positivos (AZ (KX-328), por exemplo). As placas foram testadas para BrdU e os dados analisados conforme acima para GI50.
[0405]Os resultados são mostrados na Tabela 3. Nesta tabela, os dados são relacionados como % de Crescimento do Controle, de modo tal que um número infe- rior a uma concentração indicada indica uma potência maior do composto de bloqueio do crescimento da linhagem de células tumorais. Todos os compostos forma inicial- mente preparados em forma de soluções de estoque de DMSO a 20 mM e em seguida diluídos em tampão para os ensaios de crescimento tumoral in vitro. NG significa que nenhum crescimento além do controle e T significa o número de células nos poços tratados com medicamento foi inferior do que no controle (isto é, a perda celular lí- quida). NT indica que o teste não foi conduzido. O Composto AZ (KX-328) é um inibi- dor de tirosina quinase que compete por ATP, conforme descrito em Plé et al, J. Med. Chem, 47:871-887 (2004).
[0406]Conforme se pode ver na Tabela 3, foram obtidos valores de GI50 para uma série dos compostos em outras linhagens de células. Estes valores de GI50 foram determinados usando-se ensaios de inibição de crescimento tumoral padrão, similares ao descrito em detalhes para a linhagem de células HT29 acima, e para as seguintes linhagens de células: linhagens KM12 de células tumorais do cólon, linhagem H460 de células de câncer do pulmão a linhagem A549 de células de câncer do pulmão (todas são linhagens de células tumorais padrão NCI). TABELA 3
[0407]Outras Modalidades
[0408]Embora a invenção tenha sido descrita em conjunto com a descrição detalhada da mesma a descrição acima se destina a ilustrar e não a limitar o âmbito da invenção, que é definida pelo âmbito das reivindicações apensas. Outros aspectos, vantagens e modificações incidem no âmbito das reivindicações que seguem. Deve ficar subentendido pelos versados na técnica que diversas alterações na forma e nos detalhes podem ser introduzidas sem que haja desvio do âmbito da invenção abran- gida pelas reivindicações apensas.
Claims (30)
1. Composto CARACTERIZADO pelo fato de que apresenta a Fórmula I: ou um sal do mesmo, em que: T é ausente; Xy é CZ, CY, N, ou N-O; Xz é CZ; Y é selecionado de hidrogênio, hidroxila, halogênio, alquila(C1, C2, C3, C4, C5 ou C6) inferior, alcóxi C1, C2, C3, C4, C5 ou C6, O-alquila(C1, C2, C3, C4, C5 ou C6) infe- rior-arila e O-benzila; Xa é CRa, N ou N-O; Xb é CRb, N ou N-O; Xc é CRc, N ou N-O; Xd é CRd, N ou N-O; Xe é CRe; Ra, Rb, Rc, Rd, Re, R4, R5 e R6 são, independentemente, hidrogênio, hidroxila, halogênio, alquila C1, C2, C3, C4, C5 ou C6, alcóxi C1, C2, C3, C4, C5 ou C6, O-alquila(C1, C2, C3, C4, C5 ou C6) inferior-arila, O-benzila, OH-alquila C1, C2, C3, C4, C5, ou C6, aluila C1, C2, C3, C4, C5 ou C6-O-alquila(C1, C2, C3, C4, C5 ou C6) inferior, COOH, COO- alquila (C1, C2, C3, C4, C5 ou C6) inferior, SO2H, SO2-alquila (C1, C2, C3, C4, C5 ou C6) inferior, em que W é H, alquila C1, C2, C3, C4, C5 ou C6 ou alquila C1, C2, C3, C4, C5 ou C6-arila; e V é uma ligação, -CH2-, - CH2CH2-, - CH2CH2CH2-, -O-CH2-, -OCH2CH2- ou - OCH2CH2CH2-; e R7, R8, R9, R10 e R11 são, independentemente, hidrogênio, hidroxila, halogê- nio, alquila C1, C2, C3, C4, C5, ou C6, alcóxi C1, C2, C3, C4, C5, ou C6, O-alquila(C1, C2, C3, C4, C5, ou C6) inferior-arila, O-benzila, OH-alquila C1, C2, C3, C4, C5, ou C6, alquila
alquila C1, C2, C3, C4, C5, ou C6, R1, R2 e R3 são, independentemente, H ou alquila C1, C2, C3, C4, C5, ou C6; n é 1 ou 2; e m é 1 ou 2; em que pelo menos um de Xa, Xb, Xc e Xd é N.
2. Composto, de acordo com a reivindicação 1, CARACTERIZADO pelo fato de que Xy é CY.
3. Composto, de acordo com a reivindicação 1, CARACTERIZADO pelo fato de que Y é hidrogênio.
5. Composto, de acordo com a reivindicação 1, CARACTERIZADO pelo fato de que Rb é alcóxi C1, C2, C3, C4, C5 ou C6.
6. Composto, de acordo com a reivindicação 1, CARACTERIZADO pelo fato de que Rb é hidrogênio.
8. Composto, de acordo com a reivindicação 1, CARACTERIZADO pelo fato de que V é uma ligação.
9. Composto, de acordo com a reivindicação 1, CARACTERIZADO pelo fato de que Xa é N e cada um de Xb, Xc e Xd é CR.
10. Composição CARACTERIZADA pelo fato de que compreende o com- posto, conforme definido na reivindicação 1, e pelo menos um excipiente farmaceuti- camente aceitável.
13. Composto, de acordo com a reivindicação 12, CARACTERIZADO pelo fato de que R8 é hidrogênio, F, Cl, Br ou I.
14. Composto, de acordo com a reivindicação 12, CARACTERIZADO pelo fato de que Rb é alcóxi C1, C2, C3, C4, C5, ou C6.
16. Composto, de acordo com a reivindicação 12, CARACTERIZADO pelo fato de que R4 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br ou I.
18. Composto, de acordo com a reivindicação 12, CARACTERIZADO pelo fato de que R5 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br ou I.
20. Composto, de acordo com a reivindicação 12, CARACTERIZADO pelo fato de que R10 é hidrogênio, alcóxi C1, C2, C3, C4, C5, ou C6, F, Cl, Br ou I.
26. Uso de um composto conforme definido em qualquer uma das reivindica- ções 1 a 25, ou de um sal do mesmo, CARACTERIZADO pelo fato de que é para a preparação de um medicamento para prevenção ou tratamento de um distúrbio de proliferação celular ou infecção microbiana.
27. Uso, de acordo com a reivindicação 26, CARACTERIZADO pelo fato de que o distúrbio de proliferação celular é selecionado de câncer, pré-câncer, distúrbio hiperproliferativo, psoríase, retinopatia diabética, degeneração macular, cisto epidér- mico e dermóide, lipoma, adenoma, hemangioma capilar e cutâneo, linfangioma, lesão de nevi, teratoma, nefroma, miofibromatose, tumor osteoplástico e displasia.
28. Uso, de acordo com a reivindicação 27, CARACTERIZADO pelo fato de que o câncer é selecionado do grupo que consiste em câncer de cólon, câncer de pulmão, câncer de mama, câncer de ovário, câncer de cérebro, câncer de fígado, cân- cer de pâncreas, câncer de próstata, melanoma maligno, câncer não melanoma de pele, leucemia infantil, linfoma, mieloma múltiplo, doença de Hodgkin, leucemia aguda e crônica, neoplasma celular do plasma, neoplasma linfoide e câncer associado com AIDS.
29. Uso, de acordo com a reivindicação 26, CARACTERIZADO pelo fato de que a infecção microbiana é selecionada do grupo que consiste em infecção por bac- térias, fungos, parasitas e vírus.
30. Uso, de acordo com a reivindicação 26, CARACTERIZADO pelo fato de que o distúrbio de proliferação celular ou infecção microbiana é modulado pela inibição de tirosina quinase.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US63983404P | 2004-12-28 | 2004-12-28 | |
| US60/639.834 | 2004-12-28 | ||
| US70455105P | 2005-08-01 | 2005-08-01 | |
| US60/704.551 | 2005-08-01 | ||
| US72734105P | 2005-10-17 | 2005-10-17 | |
| US60/727.341 | 2005-10-17 | ||
| PCT/US2005/047333 WO2006071960A2 (en) | 2004-12-28 | 2005-12-28 | Compositions and methods of treating cell proliferation disorders |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0519424A2 BRPI0519424A2 (pt) | 2009-01-20 |
| BRPI0519424B1 true BRPI0519424B1 (pt) | 2021-01-05 |
| BRPI0519424B8 BRPI0519424B8 (pt) | 2021-05-25 |
Family
ID=36615518
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0519424A BRPI0519424B8 (pt) | 2004-12-28 | 2005-12-28 | compostos, composição e uso dos ditos compostos para a preparação de um medicamento para prevenção ou tratamento de um distúrbio de proliferação celular ou infecção microbiana |
Country Status (19)
| Country | Link |
|---|---|
| US (5) | US7300931B2 (pt) |
| EP (1) | EP1836169B9 (pt) |
| JP (2) | JP5124285B2 (pt) |
| KR (2) | KR101328273B1 (pt) |
| CN (2) | CN103274961B (pt) |
| AT (1) | ATE544748T1 (pt) |
| AU (1) | AU2005321966B2 (pt) |
| BE (1) | BE2021C001I2 (pt) |
| BR (1) | BRPI0519424B8 (pt) |
| CA (1) | CA2594345C (pt) |
| CY (1) | CY2022001I2 (pt) |
| DK (1) | DK1836169T5 (pt) |
| ES (1) | ES2382068T3 (pt) |
| FR (1) | FR21C1064I2 (pt) |
| HU (1) | HUS2100051I1 (pt) |
| LU (1) | LUC00235I2 (pt) |
| NL (1) | NL301145I2 (pt) |
| PL (1) | PL1836169T3 (pt) |
| WO (1) | WO2006071960A2 (pt) |
Families Citing this family (56)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7968574B2 (en) | 2004-12-28 | 2011-06-28 | Kinex Pharmaceuticals, Llc | Biaryl compositions and methods for modulating a kinase cascade |
| BRPI0519424B8 (pt) | 2004-12-28 | 2021-05-25 | Athenex Inc | compostos, composição e uso dos ditos compostos para a preparação de um medicamento para prevenção ou tratamento de um distúrbio de proliferação celular ou infecção microbiana |
| WO2006081332A1 (en) | 2005-01-25 | 2006-08-03 | Epix Delaware, Inc. | Substituted arylamine compounds and their use as 5-ht6 modulators |
| EP2041071B1 (en) * | 2006-06-29 | 2014-06-18 | Kinex Pharmaceuticals, LLC | Biaryl compositions and methods for modulating a kinase cascade |
| WO2008002676A2 (en) * | 2006-06-29 | 2008-01-03 | Kinex Pharmaceuticals, Llc | Biaryl compositions and methods for modulating a kinase cascade |
| AU2014200559B2 (en) * | 2006-12-28 | 2016-05-26 | Atnx Spv, Llc | Composition and Methods for Modulating a Kinase Cascade |
| US7935697B2 (en) * | 2006-12-28 | 2011-05-03 | Kinex Pharmaceuticals, Llc | Compositions for modulating a kinase cascade and methods of use thereof |
| US20210198202A1 (en) * | 2006-12-28 | 2021-07-01 | Athenex, Inc. | Compositions for modulating a kinase cascade and methods of use thereof |
| TWI457336B (zh) * | 2006-12-28 | 2014-10-21 | Kinex Pharmaceuticals Llc | 調節激酶級聯之組成物及方法 |
| US7939529B2 (en) | 2007-05-17 | 2011-05-10 | Kinex Pharmaceuticals, Llc | Process for the preparation of compositions for modulating a kinase cascade and methods of use thereof |
| US20100256147A1 (en) * | 2007-04-13 | 2010-10-07 | Hangauer Jr David G | Biaryl acetamide derivatives as modulators of the kinase cascade for the treatment of hearing loss, osteoporosis and cell proliferation disorders |
| EP2155681B1 (en) * | 2007-05-17 | 2018-05-02 | Athenex, Inc. | Process for the preparation of compositions for modulating a kinase cascade and methods of use thereof |
| AU2014202221B2 (en) * | 2007-05-17 | 2016-06-23 | Atnx Spv, Llc | Process for the Preparation of Compositions for Modulating a Kinase Cascade and Methods of Use Thereof |
| US8124605B2 (en) * | 2007-07-06 | 2012-02-28 | Kinex Pharmaceuticals, Llc | Compositions and methods for modulating a kinase cascade |
| EP3777832A1 (en) | 2007-10-20 | 2021-02-17 | Athenex, Inc. | Pharmaceutical compositions for modulating a kinase cascade and methods of use thereof |
| US8598165B2 (en) * | 2007-11-26 | 2013-12-03 | University Of Kansas | Morpholines as selective inhibitors of cytochrome P450 2A13 |
| JP5693239B2 (ja) | 2008-01-23 | 2015-04-01 | ブリストル−マイヤーズ スクイブ カンパニーBristol−Myers Squibb Company | 4−ピリジノン化合物および癌についてのその使用 |
| ES2550667T3 (es) | 2010-02-18 | 2015-11-11 | Vtv Therapeutics Llc | Derivados de fenilheteroarilo y métodos de uso de los mismos |
| EP2558085B1 (en) * | 2010-04-16 | 2017-08-30 | Athenex, Inc. | Compositions and methods for the prevention and treatment of cancer |
| MX2012014537A (es) | 2010-07-05 | 2013-02-21 | Merck Patent Gmbh | Derivados de bipiridilo utiles para el tratamiento de enfermedades inducidas por cinasa. |
| KR20140069235A (ko) | 2011-09-27 | 2014-06-09 | 노파르티스 아게 | 돌연변이체 idh의 억제제로서의 3-피리미딘-4-일-옥사졸리딘-2-온 |
| KR101415742B1 (ko) * | 2011-12-21 | 2014-07-04 | 영남대학교 산학협력단 | 6―아미노피리딘―3―올 유도체 또는 이의 약제학적 허용가능한 염 및 이를 유효성분으로 함유하는 혈관신생으로 인한 질환의 예방 또는 치료용 약학조성물 |
| UY34632A (es) | 2012-02-24 | 2013-05-31 | Novartis Ag | Compuestos de oxazolidin- 2- ona y usos de los mismos |
| CN102746255A (zh) * | 2012-07-24 | 2012-10-24 | 安徽中医学院 | 具有抗肿瘤活性的化合物、制备方法及应用 |
| US9926273B2 (en) * | 2012-08-30 | 2018-03-27 | Athenex, Inc. | Composition and methods for modulating a kinase cascade |
| US9296733B2 (en) | 2012-11-12 | 2016-03-29 | Novartis Ag | Oxazolidin-2-one-pyrimidine derivative and use thereof for the treatment of conditions, diseases and disorders dependent upon PI3 kinases |
| JP6437452B2 (ja) | 2013-01-14 | 2018-12-12 | インサイト・ホールディングス・コーポレイションIncyte Holdings Corporation | Pimキナーゼ阻害剤として有用な二環式芳香族カルボキサミド化合物 |
| RS60244B1 (sr) | 2013-01-15 | 2020-06-30 | Incyte Holdings Corp | Jedinjenja tiazolkarboksamida i piridinkarboksamida korisna kao inhibitori pim kinaze |
| EP2970240B1 (en) | 2013-03-14 | 2018-01-10 | Novartis AG | 3-pyrimidin-4-yl-oxazolidin-2-ones as inhibitors of mutant idh |
| CN105658653A (zh) | 2013-08-23 | 2016-06-08 | 因赛特公司 | 可用作pim激酶抑制剂的呋喃并-和噻吩并-吡啶甲酰胺化合物 |
| WO2016010897A1 (en) | 2014-07-14 | 2016-01-21 | Incyte Corporation | Bicyclic heteroaromatic carboxamide compounds useful as pim kinase inhibitors |
| US9580418B2 (en) | 2014-07-14 | 2017-02-28 | Incyte Corporation | Bicyclic aromatic carboxamide compounds useful as Pim kinase inhibitors |
| PE20170705A1 (es) * | 2014-09-10 | 2017-05-21 | Glaxosmithkline Ip Dev Ltd | Nuevos compuestos como inhibidores de ret (reorganizado durante la transfeccion) |
| WO2016196244A1 (en) | 2015-05-29 | 2016-12-08 | Incyte Corporation | Pyridineamine compounds useful as pim kinase inhibitors |
| TWI734699B (zh) | 2015-09-09 | 2021-08-01 | 美商英塞特公司 | Pim激酶抑制劑之鹽 |
| US9920032B2 (en) | 2015-10-02 | 2018-03-20 | Incyte Corporation | Heterocyclic compounds useful as pim kinase inhibitors |
| CN106902357B (zh) * | 2015-12-21 | 2021-08-03 | 广州市香雪制药股份有限公司 | 药物组合物及其应用、药物包合物、静脉制剂及制备方法 |
| CN106902358B (zh) * | 2015-12-21 | 2020-07-10 | 广州市香雪制药股份有限公司 | 口服制剂及其制备方法 |
| CN118384166A (zh) * | 2016-08-12 | 2024-07-26 | 阿西纳斯公司 | 用于调节激酶级联的联芳组合物和方法 |
| CN106810490A (zh) * | 2017-02-06 | 2017-06-09 | 重庆泰润制药有限公司 | 一种二芳基化合物的晶型及其制备方法和应用 |
| WO2018165647A1 (en) | 2017-03-10 | 2018-09-13 | Athenex, Inc. | Methods of treating and/or preventing actinic keratosis |
| MX2021011775A (es) | 2017-04-26 | 2023-01-10 | Basilea Pharm Int Ag | Procesos para la preparacion de furazanobencimidazoles y formas cristalinas de estos. |
| IL326637A (en) | 2017-09-07 | 2026-04-01 | Atnx Spv Llc | Solid forms of 2-(5-(4-(2-morpholinoethoxy)phenyl)pyridin-2-yl)-N-benzylacetamide |
| AR113922A1 (es) | 2017-12-08 | 2020-07-01 | Incyte Corp | Terapia de combinación de dosis baja para el tratamiento de neoplasias mieloproliferativas |
| CN113117376B (zh) * | 2019-12-30 | 2022-08-19 | 中国科学院高能物理研究所 | 一种邻菲罗啉衍生的萃取剂及其制法和应用 |
| CN113461665B (zh) * | 2020-03-31 | 2023-05-19 | 成都赜灵生物医药科技有限公司 | 二芳基衍生物及其制备方法和用途 |
| CN113354575B (zh) * | 2021-06-07 | 2022-09-27 | 河南应用技术职业学院 | 一种特班布林的合成方法 |
| EP4186890A1 (en) | 2021-11-29 | 2023-05-31 | Moehs Ibérica, S.L. | Preparation of n-benzyl-2-(5-bromo-pyridin-2-yl)-acetamide for the synthesis of tirbanibulin |
| US12319655B2 (en) | 2021-12-09 | 2025-06-03 | Deciphera Pharmaceuticals, Llc | RAF kinase inhibitors and methods of use thereof |
| CN116444426A (zh) * | 2022-01-14 | 2023-07-18 | 武汉人福创新药物研发中心有限公司 | 微管蛋白-Src双靶点抑制剂和用途 |
| WO2023134753A1 (zh) * | 2022-01-14 | 2023-07-20 | 武汉人福创新药物研发中心有限公司 | 微管蛋白-src双靶点抑制剂 |
| US20250115613A1 (en) * | 2022-01-14 | 2025-04-10 | Wuhan Humanwell Innovative Drug Research and Development Center Limited Company | Diaryl compound as tubulin/src dual target inhibitor |
| EP4302831B1 (en) | 2022-07-04 | 2025-08-27 | Trifarma S.p.A. | Process for synthesis of tirbanibulin |
| CN115073362A (zh) * | 2022-08-04 | 2022-09-20 | 重庆迈德凯医药有限公司 | 一种替尼布林的合成方法 |
| CN117624139A (zh) * | 2022-08-25 | 2024-03-01 | 武汉人福创新药物研发中心有限公司 | 二芳基类化合物及其制备方法和用途 |
| WO2026022219A1 (en) | 2024-07-24 | 2026-01-29 | Almirall, S.A. | Injectable formulations comprising tirbanibulin |
Family Cites Families (71)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1185180B (de) * | 1963-10-19 | 1965-01-14 | Hoechst Ag | Verfahren zur Herstellung von Benzolsulfonylharnstoffen |
| US3761477A (en) * | 1968-11-08 | 1973-09-25 | Mc Neil Labor Inc | Pyrazineacetic acids, lower alkyl esters, amides and salts |
| IT1044222B (it) * | 1972-05-23 | 1980-03-20 | Zambeletti Spa L | Bifenilil alcanoilaminopiridine ad attivita anti infiammatoria di lunga durata |
| AT341512B (de) * | 1975-01-09 | 1978-02-10 | Thomae Gmbh Dr K | Verfahren zur herstellung von neuen biphenylathern |
| CA1261835A (en) | 1984-08-20 | 1989-09-26 | Masaaki Toda | (fused) benz(thio)amides |
| JPS62252755A (ja) * | 1986-04-11 | 1987-11-04 | Daikin Ind Ltd | 新規n−ベンジルベンズアミド誘導体およびこれを有効成分として含有する除草剤 |
| US5232948A (en) | 1990-09-10 | 1993-08-03 | Rhone-Poulenc Rorer Pharmaceuticals Inc. | Substituted monocyclic aryl compounds exhibiting selective leukotriene b4 antagonist activity |
| CH685875A5 (fr) | 1991-04-26 | 1995-10-31 | Pierre Baudet | Les N-phényl-benzamides protecteurs contre les effets nocifs de la lumière ultra-violette |
| CA2103367A1 (en) | 1991-05-20 | 1992-11-21 | Akihide Koda | Phellodendrine analogs and allergy type iv suppressor containing the same as active ingredient |
| DE4236103A1 (de) | 1992-10-26 | 1994-04-28 | Hoechst Ag | Verfahren zur Kreuzkupplung von aromatischen Boronsäuren mit aromatischen Halogenverbindungen oder Perfluoralkylsulfonaten |
| US5643957A (en) * | 1993-04-22 | 1997-07-01 | Emisphere Technologies, Inc. | Compounds and compositions for delivering active agents |
| FR2705671B1 (fr) * | 1993-05-26 | 1995-07-07 | Inst Nat Sante Rech Med | Nouveaux dérivés de l'hydroxybiphényle, leur préparation et les compositions pharmaceutiques qui les contiennent. |
| CA2144669A1 (en) | 1994-03-29 | 1995-09-30 | Kozo Akasaka | Biphenyl derivatives |
| FR2737721B1 (fr) | 1995-08-08 | 1997-09-05 | Roussel Uclaf | Nouveaux composes biphenyles, leur procede de preparation et les intermediaires de ce procede, leur application a titre de medicament et les compositions pharmaceutiques les contenant |
| AU4885097A (en) * | 1996-11-08 | 1998-06-03 | Sankyo Company Limited | Arylureas or arylmethylcarbamoyl derivatives |
| ZA985542B (en) * | 1997-07-03 | 1999-04-07 | Smithkline Beecham Corp | Substituted benzanilides as CCR5 receptor ligands antiinflammatory agents and antiviral agents |
| JP2001023259A (ja) * | 1999-07-09 | 2001-01-26 | Sony Corp | 光磁気記録媒体およびその製造方法 |
| US6844367B1 (en) * | 1999-09-17 | 2005-01-18 | Millennium Pharmaceuticals, Inc. | Benzamides and related inhibitors of factor Xa |
| DE60040676D1 (de) | 1999-09-17 | 2008-12-11 | Millennium Pharm Inc | BENZAMIDE UND ÄHNLICHE INHIBITOREN VON FAKTOR Xa |
| US6372752B1 (en) * | 2000-02-07 | 2002-04-16 | Genzyme Corporation | Inha inhibitors and methods of use thereof |
| US20040039048A1 (en) | 2000-02-11 | 2004-02-26 | Manuel Guzman Pastor | Therapy with cannabinoid compounds for the treatment of brain tumors |
| KR100423899B1 (ko) | 2000-05-10 | 2004-03-24 | 주식회사 엘지생명과학 | 세포 증식 억제제로 유용한 1,1-디옥소이소티아졸리딘을갖는 인다졸 |
| UY26780A1 (es) | 2000-06-15 | 2002-01-31 | Pharmacia Corp | Cicloalquil avb3 antagonistas |
| US6376524B1 (en) * | 2000-06-21 | 2002-04-23 | Sunesis Pharmaceuticals, Inc. | Triphenyl compounds as interleukin-4 antagonists |
| JP2002020362A (ja) * | 2000-07-06 | 2002-01-23 | Nippon Oruganon Kk | 新規ビフェニル誘導体 |
| EP1351686A2 (en) | 2000-11-20 | 2003-10-15 | Pharmacia Corporation | Substituted polycyclic aryl and heteroaryl pyridines useful for selective inhibition of the coagulation cascade |
| EP1373257B9 (en) | 2001-03-29 | 2008-10-15 | Vertex Pharmaceuticals Incorporated | Inhibitors of c-jun n-terminal kinases (jnk) and other protein kinases |
| GB0124931D0 (en) * | 2001-10-17 | 2001-12-05 | Glaxo Group Ltd | Chemical compounds |
| DE10201764A1 (de) * | 2002-01-18 | 2003-07-31 | Bayer Cropscience Ag | Substituierte 4-Aminopyridin-Derivate |
| JP2003231633A (ja) * | 2002-02-06 | 2003-08-19 | Tanabe Seiyaku Co Ltd | 医薬組成物 |
| US20050027016A1 (en) | 2002-02-07 | 2005-02-03 | Fahl Kathleen L | Polyamine compounds and compositions for use in conjection with cancer therapy |
| JP2005517007A (ja) | 2002-02-07 | 2005-06-09 | アクシス・ファーマスーティカルズ | ヒストンデアセチラーゼ阻害剤としての新規二環式ヒドロキサメート |
| FR2836917B1 (fr) | 2002-03-11 | 2006-02-24 | Lipha | Derives nitroso de la diphenylamine, compositions pharmaceutiques les contenant en tant que medicaments utilisables dans le traitement des pathologies caracterisees par une situation de stress oxydatif |
| GB0206215D0 (en) | 2002-03-15 | 2002-05-01 | Novartis Ag | Organic compounds |
| TWI319387B (en) | 2002-04-05 | 2010-01-11 | Astrazeneca Ab | Benzamide derivatives |
| DE10219294A1 (de) | 2002-04-25 | 2003-11-13 | Schering Ag | Substituierte N-(1,4,5,6-Tetrahydro-cyclopentapyrazol-3-yl)-Derivate, deren Herstellung und Verwendung als Arzneimittel |
| GB0209891D0 (en) | 2002-04-30 | 2002-06-05 | Glaxo Group Ltd | Novel compounds |
| EP1501514B1 (en) | 2002-05-03 | 2012-12-19 | Exelixis, Inc. | Protein kinase modulators and methods of use |
| TW200406374A (en) | 2002-05-29 | 2004-05-01 | Novartis Ag | Diaryl urea derivatives useful for the treatment of protein kinase dependent diseases |
| SE0201937D0 (sv) | 2002-06-20 | 2002-06-20 | Astrazeneca Ab | Therapeutic agents |
| US7585866B2 (en) | 2002-07-31 | 2009-09-08 | Critical Outcome Technologies, Inc. | Protein tyrosine kinase inhibitors |
| WO2004011427A2 (en) | 2002-07-31 | 2004-02-05 | Smithkline Beecham Corporation | Substituted benzanilides as modulators of the ccr5 receptor |
| AU2002331472A1 (en) | 2002-08-07 | 2004-02-25 | Xavier, Mauro | Stretching lumbar-sacral floating (slsf) vest |
| DE10238865A1 (de) | 2002-08-24 | 2004-03-11 | Boehringer Ingelheim International Gmbh | Neue Carbonsäureamid-Verbindungen mit MCH-antagonistischer Wirkung, diese Verbindungen enthaltende Arzneimittel und Verfahren zu ihrer Herstellung |
| US20040242572A1 (en) * | 2002-08-24 | 2004-12-02 | Boehringer Ingelheim International Gmbh | New carboxamide compounds having melanin concentrating hormone antagonistic activity, pharmaceutical preparations comprising these compounds and process for their manufacture |
| JP2006512314A (ja) | 2002-11-01 | 2006-04-13 | バーテックス ファーマシューティカルズ インコーポレイテッド | Jakインヒビターおよび他のプロテインキナーゼインヒビターとしての組成物の使用 |
| ATE552253T1 (de) | 2002-11-08 | 2012-04-15 | Novartis Int Pharm Ltd | 3-substituierte-6-aryl- pyridin derivate als liganden für c5a-rezeptoren |
| SI1569907T1 (sl) | 2002-12-13 | 2016-06-30 | Ym Biosciences Australia Pty Ltd | Na nikotinamidu osnovani kinazni inhibitorji |
| WO2004056774A2 (en) | 2002-12-19 | 2004-07-08 | Neurogen Corporation | Substituted biphenyl-4-carboxylic acid arylamide analogues as capsaicin receptor modulators |
| US7557129B2 (en) | 2003-02-28 | 2009-07-07 | Bayer Healthcare Llc | Cyanopyridine derivatives useful in the treatment of cancer and other disorders |
| JP5043428B2 (ja) | 2003-06-03 | 2012-10-10 | リブ−エックス ファーマシューティカルズ,インコーポレイテッド | ビアリール複素環式化合物ならびにその製造および使用方法 |
| US7501538B2 (en) * | 2003-08-08 | 2009-03-10 | Transtech Pharma, Inc. | Aryl and heteroaryl compounds, compositions and methods of use |
| US8202861B2 (en) | 2003-08-08 | 2012-06-19 | Vertex Pharmaceuticals Incorporated | Compositions useful as inhibitors of voltage-gated sodium channels |
| JP2007525482A (ja) * | 2003-10-07 | 2007-09-06 | レノビス, インコーポレイテッド | イオンチャネルリガンドとしてのアミド化合物およびその使用 |
| CN1875002B (zh) * | 2003-11-05 | 2011-08-03 | 霍夫曼-拉罗奇有限公司 | 作为ppar激动剂的苯基衍生物 |
| PE20060285A1 (es) | 2004-03-30 | 2006-05-08 | Aventis Pharma Inc | Piridonas sustituidas como inhibidores de pol(adp-ribosa)-polimerasa (parp) |
| US20080269282A1 (en) | 2004-08-02 | 2008-10-30 | Genmedica Therapeutics Sl | Compounds for Inhibiting Copper-Containing Amine Oxidases and Uses Thereof |
| BRPI0519424B8 (pt) * | 2004-12-28 | 2021-05-25 | Athenex Inc | compostos, composição e uso dos ditos compostos para a preparação de um medicamento para prevenção ou tratamento de um distúrbio de proliferação celular ou infecção microbiana |
| US7968574B2 (en) | 2004-12-28 | 2011-06-28 | Kinex Pharmaceuticals, Llc | Biaryl compositions and methods for modulating a kinase cascade |
| US8211919B2 (en) | 2005-09-02 | 2012-07-03 | Astellas Pharma Inc. | Amide derivatives as rock inhibitors |
| WO2007095383A2 (en) | 2006-02-15 | 2007-08-23 | Myriad Genetics, Inc. | Prodrugs |
| MX2008014450A (es) | 2006-05-18 | 2009-03-09 | Mannkind Corp | Inhibidores de cinasa intracelular. |
| EP2041071B1 (en) | 2006-06-29 | 2014-06-18 | Kinex Pharmaceuticals, LLC | Biaryl compositions and methods for modulating a kinase cascade |
| WO2008002676A2 (en) | 2006-06-29 | 2008-01-03 | Kinex Pharmaceuticals, Llc | Biaryl compositions and methods for modulating a kinase cascade |
| CA2673299C (en) | 2006-12-21 | 2016-04-12 | Sloan-Kettering Institute For Cancer Research | Pyridazinone compounds for the treatment of proliferative diseases |
| US7935697B2 (en) | 2006-12-28 | 2011-05-03 | Kinex Pharmaceuticals, Llc | Compositions for modulating a kinase cascade and methods of use thereof |
| US7939529B2 (en) * | 2007-05-17 | 2011-05-10 | Kinex Pharmaceuticals, Llc | Process for the preparation of compositions for modulating a kinase cascade and methods of use thereof |
| TWI457336B (zh) | 2006-12-28 | 2014-10-21 | Kinex Pharmaceuticals Llc | 調節激酶級聯之組成物及方法 |
| US20100256147A1 (en) | 2007-04-13 | 2010-10-07 | Hangauer Jr David G | Biaryl acetamide derivatives as modulators of the kinase cascade for the treatment of hearing loss, osteoporosis and cell proliferation disorders |
| US8124605B2 (en) | 2007-07-06 | 2012-02-28 | Kinex Pharmaceuticals, Llc | Compositions and methods for modulating a kinase cascade |
| EP2558085B1 (en) * | 2010-04-16 | 2017-08-30 | Athenex, Inc. | Compositions and methods for the prevention and treatment of cancer |
-
2005
- 2005-12-28 BR BRPI0519424A patent/BRPI0519424B8/pt active IP Right Grant
- 2005-12-28 AT AT05855828T patent/ATE544748T1/de active
- 2005-12-28 DK DK05855828.9T patent/DK1836169T5/da active
- 2005-12-28 JP JP2007549605A patent/JP5124285B2/ja not_active Expired - Lifetime
- 2005-12-28 US US11/321,419 patent/US7300931B2/en active Active
- 2005-12-28 CN CN201310139459.5A patent/CN103274961B/zh not_active Expired - Lifetime
- 2005-12-28 ES ES05855828T patent/ES2382068T3/es not_active Expired - Lifetime
- 2005-12-28 WO PCT/US2005/047333 patent/WO2006071960A2/en not_active Ceased
- 2005-12-28 PL PL05855828T patent/PL1836169T3/pl unknown
- 2005-12-28 KR KR1020077017102A patent/KR101328273B1/ko not_active Expired - Lifetime
- 2005-12-28 CN CN2005800487967A patent/CN101184734B/zh not_active Expired - Lifetime
- 2005-12-28 AU AU2005321966A patent/AU2005321966B2/en active Active
- 2005-12-28 CA CA2594345A patent/CA2594345C/en not_active Expired - Lifetime
- 2005-12-28 EP EP05855828A patent/EP1836169B9/en not_active Expired - Lifetime
- 2005-12-28 KR KR1020137015670A patent/KR101478933B1/ko not_active Expired - Lifetime
-
2007
- 2007-04-26 US US11/796,200 patent/US8003641B2/en active Active
-
2010
- 2010-11-19 US US12/950,764 patent/US8980890B2/en not_active Expired - Lifetime
-
2012
- 2012-01-19 JP JP2012009251A patent/JP2012082222A/ja not_active Withdrawn
-
2015
- 2015-03-16 US US14/658,736 patent/US9655903B2/en not_active Expired - Lifetime
-
2021
- 2021-10-29 LU LU00235C patent/LUC00235I2/fr unknown
- 2021-11-16 HU HUS2100051C patent/HUS2100051I1/hu unknown
- 2021-11-18 NL NL301145C patent/NL301145I2/nl unknown
- 2021-11-24 BE BE2021C001C patent/BE2021C001I2/fr unknown
- 2021-12-22 FR FR21C1064C patent/FR21C1064I2/fr active Active
-
2022
- 2022-07-05 CY CY2022001C patent/CY2022001I2/el unknown
-
2023
- 2023-02-16 US US18/110,416 patent/US20240050438A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0519424B1 (pt) | compostos, composição e uso dos ditos compostos para a preparação de um medicamento para prevenção ou tratamento de um distúrbio de proliferação celular ou infecção microbiana | |
| ES2500165T3 (es) | Composiciones de biarilo y métodos para modular una cascada de quinasas | |
| CA2656564A1 (en) | Biaryl compositions and methods for modulating a kinase cascade | |
| WO2004099187A1 (en) | N-phenyl-2-pyrimidine-amine derivatives and process for the preparation thereof | |
| CN115703761A (zh) | 作为wwp1抑制剂的化合物及其应用 | |
| US20190248756A1 (en) | Bcl-3 inhibitors | |
| EP3497099B1 (en) | Biaryl compositions and methods for modulating a kinase cascade | |
| MX2007007910A (en) | Compositions and methods of treating cell proliferation disorders | |
| HK40081620A (en) | Biaryl compositions and methods for modulating a kinase cascade | |
| HK1108695B (en) | Compositions and methods of treating cell proliferation disorders | |
| HK40010165B (en) | Biaryl compositions and methods for modulating a kinase cascade | |
| HK1188985B (en) | Compositions and methods of treating cell proliferation disorders |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B25D | Requested change of name of applicant approved |
Owner name: KINEX PHARMACEUTICALS, INC. (US) |
|
| B25D | Requested change of name of applicant approved |
Owner name: ATHENEX, INC. (US) |
|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 05/01/2021, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 28/12/2005 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |
|
| B25A | Requested transfer of rights approved |
Owner name: ATNX SPV, LLC (US) |