BRPI0605921B1 - Compostos orgânicos, seus métodos de preparo e uso, bem como composições farmacêuticas - Google Patents
Compostos orgânicos, seus métodos de preparo e uso, bem como composições farmacêuticas Download PDFInfo
- Publication number
- BRPI0605921B1 BRPI0605921B1 BRPI0605921-0A BRPI0605921A BRPI0605921B1 BR PI0605921 B1 BRPI0605921 B1 BR PI0605921B1 BR PI0605921 A BRPI0605921 A BR PI0605921A BR PI0605921 B1 BRPI0605921 B1 BR PI0605921B1
- Authority
- BR
- Brazil
- Prior art keywords
- compound
- fact
- pharmaceutically acceptable
- methyl
- biphenyl
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/216—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acids having aromatic rings, e.g. benactizyne, clofibrate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4422—1,4-Dihydropyridines, e.g. nifedipine, nicardipine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
- A61K31/5415—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame ortho- or peri-condensed with carbocyclic ring systems, e.g. phenothiazine, chlorpromazine, piroxicam
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/24—Drugs for disorders of the endocrine system of the sex hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/38—Drugs for disorders of the endocrine system of the suprarenal hormones
- A61P5/42—Drugs for disorders of the endocrine system of the suprarenal hormones for decreasing, blocking or antagonising the activity of mineralocorticosteroids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/12—Antidiuretics, e.g. drugs for diabetes insipidus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/06—Antiarrhythmics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/08—Vasodilators for multiple indications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/14—Vasoprotectives; Antihaemorrhoidals; Drugs for varicose therapy; Capillary stabilisers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/01—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C233/45—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by carboxyl groups
- C07C233/46—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by carboxyl groups with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom
- C07C233/47—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having the nitrogen atom of at least one of the carboxamide groups bound to a carbon atom of a hydrocarbon radical substituted by carboxyl groups with the substituted hydrocarbon radical bound to the nitrogen atom of the carboxamide group by an acyclic carbon atom having the carbon atom of the carboxamide group bound to a hydrogen atom or to a carbon atom of an acyclic saturated carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/46—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with hetero atoms directly attached to the ring nitrogen atom
- C07D207/50—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D257/04—Five-membered rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Emergency Medicine (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Obesity (AREA)
- Urology & Nephrology (AREA)
- Endocrinology (AREA)
- Ophthalmology & Optometry (AREA)
- Hospice & Palliative Care (AREA)
- Vascular Medicine (AREA)
- Child & Adolescent Psychology (AREA)
- Pain & Pain Management (AREA)
- Pulmonology (AREA)
- Dermatology (AREA)
- Psychiatry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
compostos orgânicos. uma combinação específica, pró-fármaco ligado ou um composto de um antagonista de receptor de angiotensina e um nepi são empregados no tratamento de hipertensão.
Description
A presente invenção direciona-se a compostos de ação dupla e combinações de bloqueadores de receptor de angiotensina e inibidores de en-dopeptidase neutra, em particular uma molécula de ação dupla onde o bloque- ador de receptor de angiotensina e o inibidor de endopeptidase neutra são ligados por meio de uma ligação não covalente, ou complexos supramoleculares de bloqueadores de receptor de angiotensina e inibidores de endopeptidase neutra, também descritos como pró-fármacos ligados, tais como sais misturados ou co-cristais, bem como às combinações farmacêuticas contendo uma tal combinação ou composto de ação dupla, métodos de preparar tais compostos de ação dupla e métodos de tratar um indivíduo com uma tal combinação ou composto de ação dupla. Especificamente, a invenção direciona-se a um composto de ação dupla ou complexo supramolecular de dois agentes ativos tendo os mesmos ou diferentes métodos de ação em uma molécula.
A angiotensina II é um hormônio que provoca a contração dos vasos sangüíneos. Isto, sucessivamente, pode resultar em tensão e pressão sanguínea elevada sobre o coração. É conhecido que a angiotensina II interage com receptores específicos sobre a superfície de células alvo. Dois subtipos de receptor para angiotensina II, isto é AT1 e AT2, foram identificados até aqui. Em tempos recentes, grandes esforços foram feitos para identificar substâncias que ligam-se ao receptor AT1. Os bloqueadores de receptor de angiotensina (ARBs, antagonistas de angiotensina II) são então conhecidos prevenir a angiotensina II de ligar-se a seus receptores nas paredes dos vasos sangüíneos, desse modo resultando na pressão sangüínea menor. Por causa da inibição do receptor AT1, tais antagonistas podem ser empregados, portanto, como anti-hipertensivos ou para o tratamento de in-suficiência cardíaca congestiva, entre outras indicações. -)O
Endopeptidase neutra (EC 3.4.24.11; encefalinase; atriopeptida- se; NEP) é uma metaloprotease contendo zinco que cliva uma variedade de substratos de peptídeo no lado de amino de resíduos hidrofóbicos [ver Pharmacol Rev, Vol. 45, p. 87 (T903)]. Os substratos para esta enzima incluem, porém não são limitados a, peptídeo natriurético atrial (ANP, também conhecido como ANF), peptídeo natriurético cerebral (BNP), met- e leu- encéfalina, bradicinina, neurocinina A, endotelina-1 e substrato P. ANP é um potente vasorelaxante e agente natriurético [ver J Hypertens, Vol. 19, p. 1923 (2001)]. A infusão de ANP em indivíduos normais resultou em um realce marcado reproduzível de natriurese e diurese, incluindo aumento na excreção fracionai de sódio, taxa de fluxo urinário e taxa de filtragem glomerular [ver J Clin Pharmacol, Vol. 27, p. 927 (1987)]. Entretanto, ANP possui uma meia vida curta na circulação, e NEP em membranas do córtex do rim mostrou ser a enzima principal responsável pela degradação deste peptídeo [ver Peptides, Vol. 9, p. 173 (1988)]. Desse modo, os inibidores de NEP (ini-bidores de endopeptidase neutra, NEPi) devem aumentar os níveis de plasma de ANP e, portanto, são esperados induzir os efeitos natriuréticos e diuréticos.
Ao mesmo tempo que as substâncias, tais como os bloqueado- res de receptor de angiotensina e os inibidores de endopeptidase neutra podem ser úteis no controle de hipertensão, hipertensão essencial é uma doença poligênica e não é sempre controlada adequadamente por monoterapi- a. Aproximadamente 333 milhões de adultos em países economicamente desenvolvidos e cerca de 65 milhões de Americanos (1 em 3 adultos) possuíam pressão sangüínea elevada em 2000 [ver Lancet, Vol. 365, p. 217 (2005); e Hipertensão, Vol. 44, p. 398 (2004)]. A doença vascular hipertensi- va não controlada e prolongada ultimamente induz a uma variedade de alterações patológicas em órgãos alvo, tais como o rim e coração. A hipertensão sustentada pode induzir também a uma ocorrência elevada de acidente vascular cerebral. Portanto, existe uma forte necessidade de avaliar a eficácia da terapia anti-hipertensiva, um exame de finalidade cardiovasculares adicionais, além daqueles de diminuição de pressão sangüínea, para obter
M também discernimentos dos benefícios do tratamento combinado.
A natureza das doenças vasculares hipertensivas é multifatorial. Sob certas circunstâncias, os fármacos com diferentes mecanismos de ação foram combinadas. Entretanto, apenas considerar qualquer combinação de fármacos tendo diferentes métodos de ação não necessariamente induz a combinações com efeitos vantajosos. Conseqüentemente, existe uma necessidade para terapia de combinação eficaz que não possui efeitos colaterais deletérios.
Em um primeiro aspecto, a presente invenção direciona-se a um composto de ação dupla, tal como um complexo supramolecular, compreendendo: (a) um antagonista de receptor de angiotensina; (b) um inibidor de endopeptidase neutra (NEPi); e opcionalmente (c) um cátion farmaceuticamente aceitável.
A presente invenção também direciona-se a um composto de ação dupla, tal como um complexo supramolecular, obtenível: (i) dissolvendo-se um antagonista de receptor de angiotensina e um inibidor de endopeptidase neutra (NEPi) em um solvente adequado; (ii) dissolvendo-se um composto básico de Cat em um solvente adequado, em que Cat é um cátion; (iii) combinando-se as soluções obteníveis nas etapas (i) e (ii); (iv) precipitação do sólido, e secando-se o mesmo para obter o composto de ação dupla; ou alternativa mente obtendo-se o composto de ação dupla alterando-se os solventes empregados nas etapas (i) e (ii) (iva) evaporando-se a solução resultante à secura; (va) re-dissolvendo-se o sólido em um solvente adequado; (via) precipitação do sólido e secando-se o mesmo para obter o composto de ação dupla.
A presente invenção também direciona-se o pró-fámnacos ligados compreendendo: (a) um antagonista de receptor de angiotensina ou um sal far- maceuticamente aceitável deste; e (b) um NEPi ou um sal farmaceuticamente aceitável deste, em que o antagonista de receptor de angiotensina ou um sal farmaceuticamente aceitável deste e o NEPi ou um sal farmaceuticamente aceitável deste são ligados por uma porção de ligação.
A presente invenção é também direcionada a uma combinação compreendendo: (a) um sal farmaceuticamente aceitável de um antagonista de receptor de angiotensina; e (b) um sal farmaceuticamente aceitável de um inibidor de endopeptidase neutra (NEPi); em que o sal farmaceuticamente aceitável do antagonista de receptor de angiotensina e o NEPi é o mesmo e é selecionado de um sal de Na, K ou NH4.
Em modalidades preferidas, o antagonista de receptor de angiotensina e o NEPi possui grupos acídicos que facilitam a formação do composto de ação dupla, tal como o complexo supramolecular da presente invenção.
Preferivelmente, o antagonista de receptor de angiotensina é selecionado do grupo consistindo em valsartan, losartan, irbesartan, telmi- sartan, eprosartan, candesartan, olmesartan, saprisartan, tasosartan, elisar- tan e combinações destes.
Em modalidades preferidas, o NEPi é selecionado do grupo consistindo em: SQ 28,603; N-[/V-[1(S)-carboxil-3-fenilpropil]-(S)-fenilalanil]-(S)- isoserina; /V-[/V-[((1 S)-carb0xi-2-fenil)etil]-(S)-fenilalanil]-β-alanina; /V-[2(S)- mercaptometil-3-(2-metilfenil)-propionil]metionina; (ácido c/s-4-[[[1 -[2-carbóxi- 3-(2-metoxietóxi)propil]-ciclopentil]carbonil]amino]-cicloexanocarboxílico); tiorfan; retro-tiorfan; fosforamidon; SQ 29072; éster de etila de ácido N-(3- carbóxi-1-oxopropil)-(4S)-p-fenilfenilmetil)-4-amino-2R-metilbutanóico; ácido (S)-c/s-4-[1-[2-(5-indaniloxicarbonil)-3-(2-metoxietóxi)propii]-1- ciclopentanocarboxamido]-1-cicloexanocarboxílico; ácido 3-(1-[6-endo- hidroximetilbiciclo[2,2,1]heptano-2-exo-carbamoil]ciclopentil)-2-(2-metoxie- til)propanóico; éster de metila de W-(1-(3-(A/-t-butoxicarbonil-(S)-prolilamino)- 2(S)-f-butoxi-carbonilpropil)ciclopentanocarbonil)-0-benzil-(S)-serina; ácido 4-[[2-(mercaptometil)-1 -oxo-3-fenilpropil]arriino]benzóico; ácido 3-[1 -(c/s-4- carboxicarbonil-c/s-3-butilcicloexil-r-1-carbamoil)ciclopentil]-2S-(2-metoxieto- ximetíl)propanóico; A/-((2S)-2-(4-bifenilmetil)-4-carbóxi-5-fenoxivaleril)glicina; ácido A/-(1-(N-hidroxicarbamoilmetil)-1-ciclopentanocarbonil)-L-fenilalanina; (S)-(2-bifenil-4-il)-1-(1H-tetrazol-5-il)etilamino) metilfosfônico; (S)-5-(/V-(2- (fosfonometilamino)-3-(4-bifenil)propionil)-2-aminoetil)tetrazol; β-alanina; 3- [1 J'-bifenil]-4-il-/V-[difenoxifosfinil)metil]-L-alanila; /V-(2-carbóxi-4-tienil)-3- mercapto-2-benzilpropanamida; ácido 2-(2-mercaptometil-3-fenilpropio- namido)tiazol-4-ilcarboxilico; (L)-(1-((2,2-dimetil-1,3-dioxolan-4-il)-metoxi)car- bonil)-2-feniletil)-L-fenilalanil)-β-alanina; N-[/V-[(/_)-[1-[(2,2-dimetil-1,3-dioxo- lan-4-il)-metoxi]carbonil]-2-feniletil]-/_-fenilalanil]-(R)-alanina; /V-[/V-[(L)-1-car- bóxi-2-feniletil]-/_-fenilalanil]-(R)-alanina; éster de etila de /V-[2-acetiltiometil- 3-(2-metil-fenil)propionil]-metionina; /V-[2-mercaptometil-3-(2-metilfenil)pro- pionil]-metionina; N-[2(S)-mercaptometil-3-(2-metilfenil)propanoil]-(S)-isose- rina; N-(S)-[3-mercapto-2-(2-metilfenil)propionil]-(S)-2-metoxi-(R)-alanina; A/-[1-[[1(S)-benziloxicarbonil-3-fenilpropil]amino]ciclopentilcarbonil]-(S)- isoserina; A/-[1 -[[1 (S)-carbonil-3-fenilpropil]amino]-ciclopentilcarbonil]-(S)-iso- serina; 1,1‘-[ditiobis-[2(S)-(2-metilbenzil)-1-oxo-3,1-propanodiil]]-b/s-(S)-iso- serina; 1,1 *-[ditiobis-[2(S)-(2-metilbenzil)-1 -oxo-3,1 -propanodiil]]-b/s-(S)-meti- onina; A/-(3-fenil-2-(mercaptometil)-propionil)-(S)-4-(metilmercapto)metionina; ácido A/-[2-acetiltiometil-3-fenil-propionil]-3-aminobenzóico; ácido /V-[2- mercaptometíl-3-fenil-propionil]-3-aminobenzóico; A/-[1-(2-carbóxi-4-fenilbu- til)-ciclopentano-carbonil]-(S)-isoserina; éster de etila de /V-[1-(acetiltio- metil)ciclopentano-carbonÍI]-(S)-metionÍna; 3(S)-[2-(acetiltiometil)-3-fenil-pro- pionii]amimo-ε-caprolactam; éster de etila de W-(2-acetiltiometil-3-(2-metilfe- nil)propionil)-metionina; e combinações destes. Preferivelmente, o composto de ação dupla ou combinação, em particular o complexo supramolecular, é um sal misturado ou um co-cristal. É também preferido que o pró-fármaco ligado seja um sal misturado ou um co-cristal.
Em um segundo aspecto, a presente invenção é direcionada à composição farmacêutica compreendendo (a) o composto de ação dupla ou combinação anteriormente mencionado, tal como o complexo anteriormente mencionado; e (b) pelo menos um aditivo farmacêutica mente aceitável.
A presente invenção também direciona-se às composições farmacêuticas compreendendo um pró-fármaco ligado compreendendo: (a) um antagonista de receptor de angiotensina ou um sal far- maceuticamente aceitável deste; (b) um NEPi ou um sal farmaceuticamente aceitável deste, em que o antagonista de receptor de angiotensina ou um sal farmaceuticamente aceitável deste e o NEPi ou um sal farmaceuticamente aceitável deste são ligados por uma porção de ligação; e (c) pelo menos um aditivo farmaceuticamente aceitável.
Em um terceiro aspecto, a presente invenção direciona-se a um método de preparar um composto de ação dupla, em particular um complexo supramolecular, compreendendo (a) um antagonista de receptor de angiotensina; (b) um inibidor de endopeptidase neutra (NEPi); e opcionalmente (c) um cátion farmaceuticamente aceitável selecionado do grupo consistindo em Na, K e NH4; o referido método compreendendo as etapas de: (i) dissolver um antagonista de receptor de angiotensina e um inibidor de endopeptidase neutra (NEPi) em um solvente adequado; (ii) dissolver um composto básico de Cat em um solvente adequado, em que Cat é um cátion; (iii) combinar as soluções obtidas nas etapas (i) e (ii); (iv) precipitação do sólido, e secagem do mesmo para obter o composto de ação dupla; ou alternativamente obter o composto de ação dupla alterando-se os solventes empregados nas etapas (i) e (ii) (iva) evaporando-se a solução resultante à secura; (va) redissolvendo-se o sólido em um solvente adequado; (via) precipitação do sólido e secagem do mesmo para obter o composto de ação dupla.
A presente invenção é também direcionada a um método de preparar um pró-fármaco ligado compreendendo: (a) um antagonista de receptor de angiotensina ou um sal far-maceuticamente aceitável deste; (b) um NEPi ou um sal farmaceuticamente aceitável deste, em que o antagonista de receptor de angiotensina ou um sal farmaceuticamente aceitável deste e o NEPi ou um sal farmaceuticamente aceitável deste são ligados por uma porção de ligação; e compreendendo adicionar uma porção de ligação e um solvente a uma mis-tura de um antagonista de receptor de angiotensina e um NEPi; e (d) isolar o pró-fármaco ligado.
Em um quarto aspecto, esta invenção é direcionada a um método de tratar ou prevenir uma doença ou condição, tais como hipertensão, insuficiência cardíaca (aguda e crônica), insuficiência cardíaca congestiva, disfunção ventricular esquerda e cardiomiopatia hipertrófica, miopatia cardíaca diabética, arritmias supraventricular e ventricular, fibrilação atrial, flutter atrial, remodelagem vascular prejudicial, infarto do miocárdio e suas sequelas, aterosclerose, angina (instável ou estável), insuficiência renal (diabética e não diabética), insuficiência cardíaca, angina pectoris, diabetes, aldoeste- ronismo secundário, hipertensão pulmonar primária e secundária, condições de insuficiência renal, tais como nefropatia diabética, glomerulonefrite, escle- roderma, esclerose glomerular, proteinúria de doença renal primária, e também hipertensão vascular renal, retinopatia diabética, outros distúrbios vasculares, tais como hemicrania, doença vascular periférica, doença de Raynaud, hiperplasia luminal, disfunção cognitiva (tal como Alzheimer), glaucoma e acidente vascular cerebral compreendendo administrar o composto de ação dupla ou combinação anteriormente mencionado, em particular o complexo supramolecular, ou o pró-fármaco ligado anteriormente mencionado, preferivelmente, o complexo, a um indivíduo em necessidade de tal trata- mento. A Figura 1 mostra uma representação pictorial da célula unitária do complexo supramolecular de hemipentaidrato de [3-((1 S,3/?)-1 -bifenil-4- ilmetil-S-etoxicarboπil-l-butilcarbamoiOpropionato-iS^S’-metil^'- (pentanoil{2"-(tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] de trissódio compreendendo duas unidades assimétricas. O seguinte código de cor é empregado: cinza = átomo de carbono; azul = átomo de nitrogênio; vermelho = átomo de oxigênio; violeta = átomo de sódio
A presente invenção refere-se a um composto de ação dupla ou combinação, em particular um complexo supramolecular, ou pró-fármaco ligado ou em particular um complexo supramolecular de dois agentes ativos com diferentes mecanismos de ação, isto é, um antagonista de receptor de angiotensina e um inibidor de endopeptidase neutra, que podem formar uma entidade molecular única para o tratamento de pacientes com várias doenças cardiovasculares e/ou renais.
Uma modalidade da invenção é direcionada a uma combinação física compreendendo: (a) um sai farmaceuticamente aceitável de um antagonista de receptor de angiotensina; e (b) um sal farmaceuticamente aceitável de um inibidor de endopeptidase neutra (NEPi); em que o sal farmaceuticamente aceitável do antagonista de receptor de angiotensina e do NEPi é o mesmo e é selecionado de um sal de Na, K ou NH4.
Especificamente, é preferido que os dois agentes ativos sejam combinados um ao outro a fim de formar um único composto de ação dupla, em particular um complexo supramolecular. Fazendo-se assim, uma nova entidade molecular ou supramolecular ser formada tendo propriedades distintas diferente da combinação física acima.
Desse modo, a presente invenção é direcionada a um composto de ação dupla, em particular um complexo supramolecular, compreendendo: (a) um antagonista de receptor de angiotensina; (b) um inibidor de endopeptidase neutra (NEPi); e (c) um cátion farmaceuticamente aceitável preferivelmente selecionado do grupo consistindo em Na, K e NH4.
A presente invenção é também direcionada a um composto de ação dupla, em particular um complexo supramolecular, obtenível: (1) dissolvendo-se um antagonista de receptor de angiotensina e um inibidor de endopeptidase neutra (NEPi) em um solvente adequado; (Ü) dissolvendo-se um composto básico de Cat tal como (Cat)OH, (Cat)2CO3, (Cat)HCO3 em um solvente adequado, em que o Cat é um cátion preferivelmente selecionado do grupo consistindo em Na, K e NH4; (iii) combinando-se as soluções obteníveis nas etapas (i) e (ii); (iv) precipitação do sólido, e secagem do mesmo para obter o composto de ação dupla; ou altemativamente obter o composto de ação dupla alterando-se os solventes empregados nas etapas (i) e (ii) (iva) evaporando-se a solução resultante à secura; (va) redissolvendo-se o sólido em um solvente adequado; (via) precipitação do sólido e secagem do mesmo para obter o composto de ação dupla. A presente invenção também direciona-se o pró-fármacos ligadas compreendendo: (a) um antagonista de receptor de angiotensina ou um sal far-maceuticamente aceitável deste; e (b) um NEPi ou um sal farmaceuticamente aceitável deste, em que o antagonista de receptor de angiotensina ou um sal farmaceuticamente aceitável deste e o NEPi ou um sal farmaceuticamente aceitável deste sejam ligados por uma porção de ligação.
Os dois componentes são cada um ligados a uma porção de ligação, desse modo, criando-se um pró-fármaco ligado. Preferivelmente, o pró-fármaco ligado é substancialmente puro; como empregada aqui, "subs- tancialmente pura" refere-se a pelo menos 90%, mais preferivelmente pelo menos 95% e mais preferivelmente pelo menos 98% de pureza.
Como uma modalidade preferida da presente invenção, o pró- fármaco ligado possui uma estrutura tal que ligando-se os dois componentes com a porção de ligação, um complexo supramolecular é formado.
Para o propósito da presente invenção, o termo "composto de ação dupla" é destinado descrever que estes compostos possuem dois métodos diferentes de ação em um composto, um é o bloqueio de receptor de angiotensina resultante da porção molecular de ARB do composto e o outro é a inibição de endopeptidase neutra resultante da porção molecular de NEPi do composto.
Para o propósito da presente invenção, o termo "composto" é destinado descrever uma substância química compreendendo ligações cova- lentes dentro de dois agentes farmaceuticamente ativos, as porções moleculares de NEPi e ARB, e as interações não covalentes entre estes dois agentes farmaceuticamente ativos, as porções moleculares de NEPi e ARB. Tipicamente, a ligação de hidrogênio pode ser observada entre os dois agentes farmaceuticamente ativos, as porções moleculares de NEPi e ARB. As ligações iônicas podem estar presentes entre o cátion e um ou ambos dos dois agentes farmaceuticamente ativos, as porções moleculares de NEPi e ARB. Outros tipos de ligações podem também estar presentes dentro do composto tais como as forças de van der Waals. Para os propósitos ilustrativos, o composto de ação dupla da presente invenção pode ser representado como segue: (ARB)-(LMNEPi) em que L é uma porção de ligação, tal como um cátion ou é uma ligação não cova lente e m é um número inteiro de 1 ou mais. Em outras palavras, a porção de ARB e NEPi pode ser conectada por meio de ligações não covalentes tal como ligação de hidrogênio. Altemativamente ou adicionalmente elas podem ser conectadas por meio de uma porção de ligação tal como um cátion. derado ser um pró-fármaco ligado, pelo qual, a porção de ligação tal como o cátion, liga-se aos dois agentes farmaceuticamente ativos, ARB e NEPi, formam o pró-fármaco destes agentes que são liberados uma vez que o pró- fármaco ligado é ingerido e absorvido.
Em uma modalidade preferida, o composto de ação dupla é um complexo, em particular um complexo supramolecular.
Para o propósito da presente invenção, o termo "complexo supramolecular" é destinado descrever uma interação entre os dois agentes farmaceuticamente ativos, os cátions e qualquer outra entidade presente tal como um solvente, em particular água, por meio de ligação intermolecular não covalente entre eles. Esta interação induz a uma associação da espécie presente no complexo supramolecular distinguindo-se este complexo sobre uma mistura física da espécie.
A ligação intermolecular não covalente pode ser quaisquer interações conhecidas na técnica para formar tais complexos supramoleculares, tal como ligação de hidrogênio, forças van der Waals e empilhamento π-π. As ligações iônicas podem também estar presentes. Preferivelmente, aí existe ligação tônica e adicionalmente ligação de hidrogênio para formar uma rede de interações dentro do complexo. O complexo supramolecular existe preferivelmente no estado sólido, porém, pode também estar presente em meio líquido. Como uma modalidade preferida da invenção, o complexo é cristalino e neste caso é preferivelmente um cristal misturado ou co-cristal.
Tipicamente, o composto de ação dupla, em particular o complexo supramolecular exibe propriedades tal como ponto de fusão, espectro de IR etc. que são diferentes de uma mistura física da espécie.
Preferivelmente, o composto de ação dupla, em particular o complexo supramolecular, possui uma rede de ligações não covalentes, em particular ligações de hidrogênio, entre os dois agentes farmaceuticamente ativos e qualquer solvente, se presente, preferivelmente água. Além disso, é preferido que o composto de ação dupla, em particular o complexo supramolecular, possua uma rede de ligações não covalentes, em particular ligações de hidrogênio e iônicas, entre os dois agentes farmaceuticamente ativos, o cátion e qualquer solvente, se presente, preferivelmente água. O cátion é preferivelmente coordenado a vários ligandos de oxigênio, desse modo, fornecendo uma ligação entre estes ligandos de oxigênio. Os ligandos de oxigênio descendem dos grupos de carboxilato e carbonila presentes nos dois 5 agentes farmaceuticamente ativos e preferivelmente também de qualquer solvente, se presente, preferivelmente água.
O composto de ação dupla compreende uma porção molecular de um antagonista de receptor de angiotensina. Isto significa que uma porção molecular derivada de um antagonista de receptor de angiotensina está participando na construção do composto de ação dupla. O antagonista de receptor de angiotensina é parte do composto e conectado ao inibidor de NEP diretamente ou indiretamente por meio de ligações não covalentes. Devido a conveniência, em todo o pedido, o termo "antagonista de receptor de angiotensina" será empregado quando descrevendo esta parte do composto.
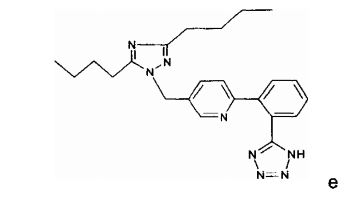
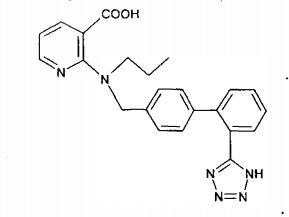
Os antagonistas de receptor de angiotensina (ARBs) adequados para o emprego na presente invenção incluem, sem limitação, valsartan, losartan, irbe- sartan, telmisartan, eprosartan, candesartan, olmesartan saprisartan, taso- sartan, elisartan, o composto com a designação E-1477 da seguinte fórmulao composto com a designação SC-52458 da seguinte fórmula o composto com a designação ZD-8731 da seguinte fórmula
O antagonista de receptor de angiotensina II adequado também inclui, porém não é limitado a, acetato de saralasin, cilexetila de candesar- tan, CGP-63170, EMD-66397, KT3-671, LR-B/081, valsartan, A-81282, Bl- BR-363, BIBS-222, BMS-184698, candesartan, CV-11194, EXP-3174, KW- 3433, L-161177, L-162154, LR-B/057, LY-235656, PD-150304, U-96849, U- 97018, UP-275-22, WAY-126227, WK-1492.2K, YM-31472, potássio de lo- sartan, E-4177, EMD-73495, eprosartan, HN-65021, irbesartan, L-159282, ME-3221, SL-91.0102, Tasosartan, Telmisartan, UP-269-6, YM-358, CGP- 49870, GA-0056, L-159689, L-162234, L-162441, L-163007, PD-123177, A- 81988, BMS-180560, CGP-38560A, CGP-48369, DA-2079, DE-3489, DuP- 167, EXP-063, EXP-6155, EXP-6803, EXP-7711, EXP-9270, FK-739, HR-720, ICI-D6888, ICI-D7155, ICI-D8731, isoteolina, KRI-1177, L-158809, L-158978, L-159874, LR B087, LY-285434, LY-302289, LY-3I5995, RG- 13647, RWJ-38970, RWJ-46458, S-8307, S-8308, saprisartan, saralasin, Sarmesin, WK-1360, X-6803, ZD-6888, ZD-7155, ZD-8731, BIBS39, CI-996, DMP-811, DuP-532, EXP-929, L-163017, LY-301875, XH-148, XR-510, zo- lasartan e PD-123319.
Também incluído dentro do escopo deste aspecto da invenção estão combinações dos ARBs identificados acima.
Os ARBs a serem empregados para preparar a combinação ou complexo de acordo com a presente invenção podem ser adquiridos de fontes comerciais ou podem ser preparados de acordo com métodos conhecidos. Os ARBs podem ser empregados para os propósitos desta invenção em sua forma livre, bem como em qualquer forma de éster ou sal adequada.
As formas de sais preferidas incluem sais de adição de ácido. Os compostos tendo pelo menos um grupo de ácido (por exemplo, COOH ou 5-tetrazolil) podem também formar sais com bases. Os sais adequados com bases são, por exemplo, sais de metal, tais como sais de metal alcalino terroso ou de metal de álcali, por exemplo, sais de sódio, potássio, cálcio ou magnésio, ou sais com amónia ou uma amina orgânica, tal como morfolina, tiomorfolina, piperidina, pirrolidina, uma alquilamina mono-, di- ou tri-inferior, por exemplo, etil-, terc-butil-, dietil-, diisopropil-, trietil-, tributil- ou dimetilpro- pilamina, ou uma alquilamina mono-, di- ou triidróxi inferior, por exemplo, mono-, di- ou tri-etanolamina. Os sais internos correspondentes podem além disso ser formados. Os sais que são inadequados para os empregos farmacêuticos, porém que podem ser empregados, por exemplo, para o isolamento ou purificação de compostos livres I ou seus sais farmaceuticamente aceitáveis, estão também incluídos. Os sais ainda mais preferidos são, por e- xemplo, selecionados do sal de monossódio na forma amorfa; sal de dissó- dio de valsartan na forma cristalina ou amorfa, especialmente na forma de hidrato, deste. Sal de monopotássio de valsartan na forma amorfa; sal de di- potássio de valsartan na forma amorfa ou cristalina, especialmente na forma de hidrato do mesmo.
O sal de cálcio de valsartan na forma cristalina, especialmente na forma de hidrato, primariamente o tetraidrato do mesmo; sal de magnésio de valsartan na forma cristalina, especialmente na forma de hidrato, primariamente o hexaidrato do mesmo; o sal de cálcio/magnésio misturado de valsartan na forma cristalina, especialmente na forma de hidrato; sal de bis- dietilamônio de valsartan na forma cristalina, especialmente na forma de hidrato; sal de b/s-dipropilamônio de valsartan na forma cristalina, especialmente na forma de hidrato; sal de b/s-dibutilamônio de valsartan na forma cristalina, especialmente na forma de hidrato, primariamente o hemiidrato deste; sal de mono-L-arginina de valsartan na forma amorfa; sal de bis-L- arginina de valsartan na forma amorfa; sal de mono-/_-lisina de valsartan na forma amorfa; sal de b/s-L-lisina de valsartan na forma amorfa.
Preferivelmente quando preparando os compostos de ação du-pia, em particular o complexo de acordo com a presente invenção, a forma livre do ARB é empregada.
Em uma modalidade preferida desta invenção, o bloqueador de receptor de angiotensina empregado na combinação ou complexo da pre- sente invenção é Valsartan a estrutura molecular do qual é mostrada abaixo
Valsartan pode ser na forma racêmica ou como um dos sômeros mostrados abaixo((S)-/V-valeril-A/-{[2'-(1 H4etrazol-5-il)-bifeniM-il]-metil}-valina) de Valsartan 10 empregado de acordo com a presente invenção pode ser adquirido de fontes comerciais ou pode ser preparado de acordo com métodos conhecidos. Por 16 exemplo, a preparação de valsartan é descrita na Patente dos Estados Uni-dos n° 5.399.578 e EP 0 443 983, a descrição completa de cada um dos quais é incorporada aqui por referência. Valsartan pode ser empregado para os propósitos desta invenção em sua forma de ácido livre, bem como em qualquer forma de sal adequada. Adicionalmente, os ésteres ou outros deri-vados do grupo carboxílico podem ser aplicados para a síntese de pró- fármacos ligados, bem como sais e derivados do grupo de tetrazol. Com re-ferência a ARBs inclui a referência aos sais farmaceuticamente aceitáveis dos mesmos.
Preferivelmente, o ARB é um ácido diprótico. Desse modo, o bloqueador de receptor de angiotensina possui uma carga de 0, 1 ou 2 de-pendendo do pH da solução.
Na combinação da presente invenção, o ARB está na forma de um sal farmaceuticamente aceitável selecionado de Na, K ou NH4, preferi-velmente Na. Isto inclui igualmente os mono- e dissal destes cátions, preferi-velmente o dissal. Em particular no caso de valsartan isto significa que i- gualmente a porção de ácido carboxílico e a porção de tetrazol formam o sal.
No composto de ação dupla, em particular o complexo supramo- lecular da presente invenção, tipicamente a forma livre do ARB é empregada na preparação e a espécie catiônica presente no complexo é introduzida empregando-se uma base, por exemplo (Cat)OH.
O composto de ação dupla compreende uma porção molecular de um inibidor de endopeptidase neutra. Isto significa que uma porção mole-cular derivada de um inibidor de endopeptidase neutra está participando na preparação do composto de ação dupla. O inibidor de endopeptidase neutra é parte do composto e conectado ao ARB diretamente ou indiretamente por meio de ligações não covalentes. Por causa da conveniência, em todo o pe-dido, o termo "inibidor de endopeptidase neutra" será empregado quando descrevendo esta parte do composto. Os Inibidores de endopeptidase neutra adequados para o emprego na presente invenção incluem aqueles da fórmu- la(l)em que
R2 é alquila de 1-7 carbonos, trifluorometila, fenila, fenila substituída, -(CH2)1 a 4-fenila, ou -(CH2)1 a 4 fenila substituída;
R3 é hidrogênio, alquila de 1-7 carbonos, fenila, fenila substituí-da, -(CH2)1 a 4-fenila ou -(CH2)1 a 4 fenila substituída;
RT é hidroxi, alcóxi de 1-7 carbonos ou NH2; n é um número inteiro de 1-15; e o termo fenila substituída refere-se a um substituinte selecionado de alqui-la inferior de 1-4 carbonos, alcóxi inferior de 1-4 carbonos, alquiltio inferior de 1-4 carbonos, hidroxi, Cl, Brou F.
Os inibidores de endopeptidase neutra preferidos da fórmula (I) incluem os compostos, em que R2 é benzila; Ra é hidrogênio; n é um número inteiro de 1-9; e R1 é hidróxl
Outro inibidor de endopeptidase neutra preferido é o ácido (SS^’R^S-il-P’-ietoxicarbonilH'-fenil-butilJ-ciclopentan-l-carbonilamino}- 2,3,4,5-tetraidro-2-oxo-1H-1-benzazepina-1-acético ou um sal farmaceutica-mente aceitável do mesmo.
Os inibidores de endopeptidase neutra preferidos adequados para o emprego na presente invenção incluem, sem limitação, SQ 28,603; N- [/V-[1 (S)-carboxil-3-fenilpropil]-(S)-fenilalanil]-(S)-isoserina; /V-[A/-[(( 1 S)-carbó- xi-2-fenil)etil]-(S)-fenilalanil]-β-alanina; N-[2(S)-mercaptometil-3-(2-metilfenil)- propionil]metionina; (ácido c/s-4-[[[1 -[2-carbóxi-3-(2-metoxietóxi)propil]-ciclo- pentil]carbonil]amino]-cicloexanocarboxílico); tiorfan; retro-tiorfan; fosforami- don; SQ 29072; éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi- propionilamino)-2-metil-pentanóico; ácido A/-(3-carbóxi-1 -oxopropil)-(4S)-p- fenilfenilmetil)-4-amino-2R-metilbutanóico; ácido (S)-c/s-4-[1 -[2-( 5-ind an i- loxicarbonil)-3-(2-metoxietóxi)propil]-1-ciclopentanocart>oxamido]-1-cicloexa- nocarboxílico; ácido 3-(1-[θ-θndo-hidroximetilbiciclo[2,2,1]heptano-2-exo- carbamoil]ciclopentÍI)-2-(2-metoxietil)propanóico; éster de metila de N-(1-(3- (A/-t-butoxicarbonil-(S)-prolilamino)-2(S)-í-butoxi-carbonilpropilX:iclQpentano- carbonil)-O-benzil-(S)-serina; ácido 4-[[2-(mercaptometil)-1 -oxo-3-fenilpro- pil]amino]benzóico; ácido 3-[1 -(c/s-4-carboxicarbonil-c/s-3-butilcicloexil-r-1- carbamoil)ciclopentil]-2S-(2-metoxietoximetil)propanóico; N-((2S)-2-(4-bife- nilmetil)-4-carbóxi-5-fenoxivaleril)glicina; A/-(1-(W-hidroxicarbamoilmetil)-1- ciclopentanocarbonil)-Z_-fenilalanina; ácido (S)-(2-bifenil-4-il)-1 ~(1 H-tetrazol-5- il)etilamino)metilfosfônico; (S)-5-(/V-(2-(fosfonometilamino)-3-(4-bifenil)propio- nil)-2-aminoetil)tetrazol; β-alanina; 3-[1,1 '-bifenil]-4-il-/V-[difenoxifosfinil)metii]- L-alanil; A/-(2-carbóxi-4-tienil)-3-mercaptO“2-benzilpropanamida; ácido 2-(2- mercaptometil-3-fenilpropionamido)tiazol-4-ilcarboxílico; (L)-(1-((2,2-dimetil- 1,3-dioxolan-4-il)-metoxi)carbonil)-2-feniletil)-Z_-fenilalanil)-β-alanina;
N-[N-[(L)-[1-[(2,2-dimetil-1,3-dioxolan-4-il)-metoxi]carbonil]-2-feniletil]-L-feni- lalanil]-(R)-alanina; A/-[/V-[(Z_)-1 -carbóxi-2-feniletil]-L-fenilalanil]-(R)-alanina; éster de etila de /V-[2-acetiltÍometil-3-(2-metil-fenil)propionil]-metionina; N-[2- mercaptometil-3-(2-metilfenil)propionil]-metionina; /V-[2(S)-mercaptometil-3- (2-metilfenil)propanoil]-(S)-isoserina; N-(S)-[3-mercapto-2-(2-metilfenil)pro- pionil]-(S)-2-metoxi-(R)-alanina; M-[1-[[1(S)-benziloxicarbonil-3-fenilpropÍI]- amÍno]ciclopentilcarbonil]-(S)-isoserina; W-[1 -[[1 (S)-carbonil-3-fenilpropil]- amino]-ciclopentilcarbonil]-(S)-isoserina; 1 ,r-[ditiobis-[2(S)-(2-metilbenzil)-1 - oxo-3,1-propanodiil]]-b/s-(S)-isoserina; 1 ,r-[dítiobis-[2(S)-(2-metilbenzil)-1 - oxo-3,1 -propanodiil]]-b/s-(S)-metionina; A/-(3-feníl-2-(mercaptometil)-propio- nilXSH“(mθtilmercapto)metionina; ácido N-[2-acetiltiometil-3-fenil-propionil]- 3-aminobenzóico; ácido /V-[2-mercaptometil-3-fenil-propionil]-3-aminoben- zóico; A/-[1-(2-carbóxi-4-fenilbutil)-ciclopentano-carbonil]-(S)-isoserina; éster de etila de A/-[1-(acetiltiometil)ciclopentano-carbonil]-(S)-metionina; 3- (S)-[2-(acetiltiometil)-3-fenil-propionil]amimo-ε-caprolactam; éster de etila de A/-(2-acetiltiometil-3-(2-metilfenil)propionil)-metionina; e combinações dos mesmos.
Os inibidores de endopeptidase neutra podem ser adquiridos de fontes comerciais ou podem ser preparados de acordo com métodos conhecidos, tais como aqueles apresentados em qualquer uma Patente dos Estados Unidos n° 4.722.810, Patente dos Estados Unidos n° 5.223.516, Patente dos Estados Unidos n° 4.610.816, Patente dos Estados Unidos n° 4.929.641, Pedido de Patente da África do Sul 84/0670, UK 69578, Patente dos Estados Unidos n° 5.217.996, EP 00342850, GB 02218983, WO 92/14706, EP 00343911, JP 06234754, EP 00361365, WO 90/09374, JP 07157459, WO 94/15908, Patente dos Estados Unidos n° 5.273.990, Patente dos Estados Unidos n° 5.294.632, Patente dos Estados Unidos n° 5.250.522, EP 00636621, WO 93/09101, EP 00590442, WO 93/10773, Patente dos Estados Unidos n° 5.217.996, a descrição de cada um dos quais é incorporada por referência. Os Inibidores de endopeptidase neutra podem ser empregados para os propósitos desta invenção em sua forma livre, bem como em qualquer forma de sal adequada. A referência dos inibidores de endopeptidase neutra inclui a referência aos sais farmaceuticamente aceitáveis dos mesmos.
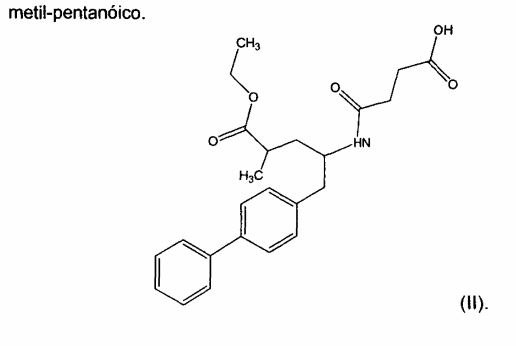
Adicionalmente os ésteres ou outros derivados de qualquer gru-po carboxílico podem ser aplicados para a síntese de pró-fármacos ligados, bem como sais e derivados de qualquer outro grupo acídico. Em uma moda-lidade preferida desta invenção, o NEPi é éster de etila de ácido 5-bifenil4-il- 5-(3-carbóxí-propionilamino)-2-metil-pentanóico da fórmula (II) ou a respecti-va forma hidrolisada de ácido 5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-
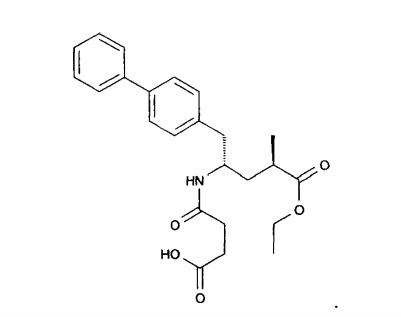
O composto da fórmula (II) pode existir como o isômero (2R,4S), (2R.4S), (2R,4S) ou (2R.4S). Preferido ê o éster de etila de ácido (2R,4S)-5- bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil-pentanóico como mostrado abaixo:
O composto da fórmula (II) é um inibidor específico de NEP e é descrito na Patente dos Estados Unidos n° 5.217.996. Ele pode ser adquirido de fontes comerciais ou pode ser preparado de acordo com métodos co-nhecidos. O composto da fórmula (II) pode ser empregado para os propósitos desta invenção em sua forma livre, bem como em qualquer forma de éster ou sal adequado.
Preferivelmente o NEPi é um ácido monoprótico. Desse modo, o NEPi possui uma carga de 0 ou 1 dependendo do pH da solução.
Na combinação da presente invenção, o NEPi está na forma de um sal farmaceuticamente aceitável selecionado de Na, K ou NH4, preferi-velmente Na.
No composto de ação dupla, em particular o complexo supramo-lecular da presente invenção, tipicamente a forma livre do NEPi é empregada na preparação e a espécie catiônica presente no complexo é introduzida empregando-se uma base, (Cat)OH.
O composto de ação dupla preferivelmente compreende ligações não covalentes entre o ARB e o NEPi. Alternativamente ou além disso, ele opcional mente compreende uma porção de ligação tal como um cátion far-maceuticamente aceitável.
A porção de ligação inclui, porém não é limitada a, compostos geralmente considerados como seguros (GRAS) ou outros compostos far- macologicamente aceitáveis. A porção de ligação pode ser uma molécula neutra ou íon. No caso em que a porção de ligação é um íon, o pró-fármaco ligado é um sal e quando a porção de ligação é uma molécula neutra o pró- fármaco ligado é um co-cristal. Sem ser limitada por qualquer teoria particular, a porção acídica do ARB e NEPi doa um próton à porção de ligação básica tal que todos os três componentes em seguida tornem-se unidos para formarem uma molécula. Quando o pró-fármaco ligado é ingerido pelo indivíduo destinado ser tratado a natureza mais acídica do meio de ingestão motiva o pró-fármaco ligado a separar-se em componentes individuais concomitantes com a ingestão e absorção e portanto ser convertido em agentes ativos para fornecer sua ação biológica benéfica para tratar as doenças pretendidas.
No caso de um sal de pró-fármaco ligado ou do composto de ação dupla, a porção de ligação ou o cátion, respectivamente, é preferivel-mente um cátion mono-, di- ou trivalente positivamente carregado, uma base orgânica ou um aminoácido. Os cátions preferidos (Cat) igual mente para o pró-fármaco ligado em geral e o composto de ação dupla, em particular o complexo são os cátions básicos, ainda mais preferivelmente os cátions me-tálicos. Os cátions metálicos preferidos incluem, porém não são limitados a, Na, K, Ca, Mg, Zn, Fe ou NH4. As bases de amina e os agentes de formação de sal podem também ser empregados, tais como benzatina, hidrabamina, etilenodiamina, n-n-dibenzil-etilenodiamina, L-arginina, hidróxido de colina, N-metil-glucamina, (Meglumina), L-Lisina, dimetilaminoetanol (Deanol), t- butilamina, dietilamina, 2-(dietilamino)-etanol, 4-(2-hidroxietil)-morfolina, Trometanina (TRIS), 4-acetamidofenol, 2-amino-2-metil-1,3-propanodiol, 2- amino-2-metil-propanol, benzilamina, cicloexilamina, dietanolamina, etano- lamina, imidazol, piperazina e trietanolamina.
Mais preferivelmente, o cátion é Na, K ou NFL, tal como Na. Em uma modalidade o Ca é preferido.
No caso de um co-cristal de pró-fármaco ligado, a porção de li- gação também pode ser uma molécula neutra que fornece funcionalidade de ligação de hidrogênio.
Em uma modalidade, os pró-fármacos ligados desta invenção são representadas como apresentado abaixo, em que os esquemas (1) e (2) representam um sal e o esquema (3) representa um co-cristal: NEPi • Xa» ARB esquema (1) NEPi • XaYb* ARB esquema (2) NEPi • Zc« ARB esquema (3), em que Xé Ca, Mg, Zn ou Fe; YéNa, Kou NH4; Z é uma molécula neutra; e a, b e c refletem a estequiometria do pró-fármaco ligado, preferi-velmente, a, b e c são uma valência de 1+, 2+ ou 3+.
Para os pró-fármacos ligados dos esquemas (1) e (2), acima, preferivelmente o NEPi é um ácido monoprótico e o ARB é um ácido dipróti- co. O bloqueador de receptor de angiotensina possui uma carga de 0, 1 ou 2 e o NEPi possui uma carga de 0 ou 1 dependendo do pH da solução, ao mesmo tempo que a molécula total será neutra. As relações de ARB para NEPi serão 1:1, 1:2, 1:3, 3:1, 2:1, 1:1, preferivelmente 1:1, 1:2 ou 1:3, mais preferivelmente 1:1.
Os sais multicomponentes, particularmente com zinco e cálcio foram reportados na literatura, por exemplo, Chem Pharm Bull, Vol. 53, p. 654 (2005). Estes ions requerem uma geometria de coordenação que facilite a cristalização dos sistemas multicomponentes. Os íons de metal possuem geometrias de coordenação reguladas pelas órbitas atômicas para cada es-pécie.
Valsartan compreende dois grupos acídicos: o ácido carboxílico e o tetrazol. Em uma modalidade deste aspecto da presente invenção, a es-trutura molecular dos pró-fármacos ligados de valsartan e um NEPi compre-endem uma ligação entre o ácido carboxílico e a porção de ligação ou uma ligação entre o grupo de tetrazol e a porção de ligação. Em ainda outra mo-dalidade, o pró-fármaco ligado compreende uma porção de ligação trivalente ligada ao grupo de ácido carboxílico de valsartan, o grupo de tetrazol e o grupo de NEPi.
Em uma modalidade deste aspecto da invenção, o valsartan é ligado ao éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi- propionilamino)-2-metil-pentanóico por um íon de sal de cálcio.
Em uma modalidade preferida do presente pedido, o antagonista de receptor de angiotensina e o inibidor de endopeptidase neutra estão pre-sentes em uma relação molar de 1:1, 1:2,1:3, 3:1, 2:1, mais preferivelmente de 1:1 na combinação bem como no complexo supramolecular. Isto é também verdadeiro para o pró-fármaco ligado. Além disso, no complexo, o antagonista de receptor de angiotensina, o inibidor de endopeptidase neutra e o cátion estão presentes em uma relação molar de 1:1:1, 1:1:2, 1:1:3, mais preferivelmente de 1:1:3. Isto aplica-se igualmente ao pró-fármaco ligado.
A combinação ou o composto de ação dupla, em particular o complexo da presente invenção pode conter um solvente. Isto é particular-mente preferido no caso do composto de ação dupla, em particular o com-plexo, onde o solvente pode contribuir com a estrutura intermolecular, por exemplo, as interações supramoleculares. Os solventes preferidos incluem água, metanol, etanol, 2-propanol, acetona, acetato de etila, metil-f-butiléter, acetonitrilo, tolueno, e cloreto de metileno, preferivelmente água. Se um sol-vente está presente, uma ou mais moléculas por molécula do agente ativo podem estar presentes. Neste caso, isto é se uma quantidade estequiomé- trica do solvente está presente, preferivelmente 1, 2, 3, 4 ou 5, mais preferi-velmente 3, moléculas de solvente, tal como água, pode estar presente por molécula de agente ativo. Altemativamente, o solvente pode estar presente em quantidades não estequiométricas. Isto significa preferivelmente qualquer fração estequiométrica do solvente, tal como 0,25, 0,5, 0,75, 1,25, 1,5, 1,75, 2,25, 2,5, 2,75, 3,25, 3,5, 3,75, 4,25, 4,5 e 4,75, preferivelmente 2,5, moléculas de solvente, tal como água, podem estar presentes por molécula de agente ativo. Se o composto de ação dupla, em particular o complexo está na forma cristalina, o solvente pode ser parte da embalagem molecular e ser aprisionado na treliça de cristal.
Desse modo, em uma modalidade preferida da presente inven-ção, o composto de ação dupla, em particular o complexo supramolecular é descrito pela fórmula de soma; [ARB(NEPi)]Nai-3 • xH2O, em que X é 0, 1,2 ou 3, tal como 3, preferivelmente [ARB(NEPi)]Na3 • xH2O, em que X é 0, 1,2 ou 3, tal como 3, mais preferivelmente [éster de etila de ácido de valsartan ((2R,4S)-5-bifenil4-il-5-(3- carbóxi-propionilamino)-2-metil-pentanóico]Na3 • x H2O, em que X é 0, 1,2 ou 3, tal como 3.
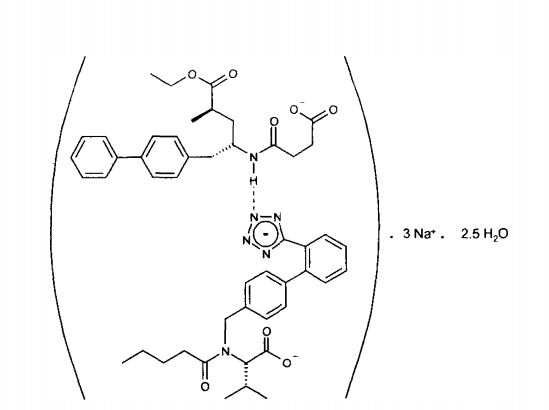
Desse modo, em uma modalidade preferida da presente inven-ção, o composto de ação dupla, em particular o complexo supramolecular é descrito pela fórmula de soma: [ARB(NEPi)]Nai-3 • xH2O, em que X é 0 a 3, tal como 2,5, preferivelmente [ARB(NEPi)]Na3 • xH2O, em que X é 0 a 3, tal como 2,5, mais preferivelmente [(/V-valeril-/V-{[2'-(1H-tetrazol-5-il)-bifenil-4-il]-metil}-valina) éster de etila de ácido (5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil- pentanóico]Na3 • x H2O, em particular [((S)-A/-valeril-/V-{[2’-(1 H-tetrazol-5-il)- bifenil-4-il]-metil}-valina) éster de etila de ácido ((2R,4S)-5-bifenil4-il-5-(3- carbóxi-propionilamino)-2-metil-pentanóico]Na3 • x H2O, em que X é 0 a 3, tal como 2,5. Neste exemplo mais preferido, o complexo é denominado [3-((1 S,3R)-1-bifenil-4-ilmetil-3-etoxicarbonil-1- butilcarbamoil)propionato-(S)-3'-metil-2’-(pentanoil{2"-(tetrazol-5-ilato)bifenil- 4’-ilmetil}amino)butirato] hemipentaidrato de trissódio.
Uma estrutura simplificada de [3-((1S,3R)-1-bifenil-4-ilmetil-3- etoxica rboni 1-1-butilcarba moil )propionato-( meti l-2'-(penta no il{2"- (tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio empregada para formalmente calcular a massa molecular relativa, é mostrada abaixo.
Valsartan compreende dois grupos acídicos: o ácido carboxílico e o tetrazol. Em uma modalidade deste aspecto da presente invenção, a es-trutura molecular do composto de ação dupla, em particular, o complexo, de valsartan e um NEPi compreendem uma interação entre o ácido carboxílico e o cátion, tal como Na, ou o solvente, tal como água, ou uma ligação entre o grupo de tetrazol e o cátion, tal como Na, ou o solvente, tal como água. Em ainda outra modalidade, o composto de ação dupla, em particular, o comple-xo, compreende uma interação entre o grupo de ácido carboxílico de valsar-tan, o grupo de tetrazol ou o grupo de NEPi e o cátion, tal como Na, ou o solvente, tal como água.
A combinação ou o composto de ação dupla, em particular, o complexo, da presente invenção está preferivelmente na forma sólida. No estado sólido ele pode ser na forma cristalina, parcialmente cristalina, amor-fa, ou polimorfa, preferivelmente na forma cristalina.
O composto de ação dupla, em particular, o complexo, da pre-sente invenção é distinto de uma combinação de um ARB e um NEPi obtido por mistura simplesmente física dos dois agentes ativos. Desse modo, ele pode possuir diferentes propriedades que tomam ele particularmente útil para fabricação e aplicações terapêuticas. A diferença do composto de ação dupla, em particular, o complexo, e a combinação pode ser exemplificada pelo composto de ação dupla de (S>/V-valeril-/V-{[2'-(1H-tetrazol-5-il)-bifenil- 44l]-metil}-valina e éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi- propionilamino)-2-metil-pentanóico o qual é caracterizado por picos espec-trais muitos distintos e alterações que não são observadas na mistura física.
Especificamente, um tal composto de ação dupla é preferivel-mente caracterizado por um padrão de difração de pó de raio X tomado com um difractômetro de pó Scintag XDS2000 empregando-se radiação de Cu- Ka (lamda=1,54056 A) com um detector de silício resfriado por Peltier em temperatura ambiente (25 °C). A faixa de varredura foi de 1,5 °C a 40 °C em 2 teta com uma taxa de varredura de 3 graus/minuto. As reflecções mais im-portantes no diagrama de difração de raio X compreende os seguintes inter-valos de plano de intertreliça:
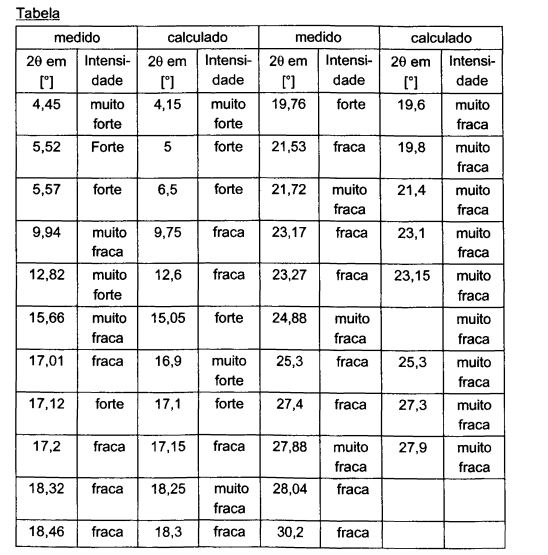
A caracterização preferida de [3-((1S,3R)-1-bifenil-4-ilmeti1-3- etoxicarbonil-1-butilcarbamoil)propionato-(S)-3'-metil-2’-(pentanoil{2"- (tetrazol-5-ilato)bifenil-4’-ilmetil}amino)butirato] hemipentaidrato de trissódio é obtida dos intervalos de plano de intertreliça d dos diagramas de difração de raio X verificados, pelos quais, no seguinte, os valores médios 20 em [°] são indicados (limite de erro de ±0,2) 4,5, 5,5, 5,6, 9,9, 12,8, 15,7, 17,0, 17,1, 17,2, 18,3, 18,5, 19,8, 21,5, 21,7, 23,2, 23,3, 24,9, 25,3, 27,4, 27,9, 28,0, 30,2.
Ou com limite de erro de ±0,1: 4,45, 5,52, 5,57, 9,94, 12,82, 15,66, 17,01, 17,12, 17,2, 18,32, 18,46, 19,76, 21,53, 21,72, 23,17, 23,27, 24,88, 25,3, 27,4, 27,88, 28,04, 30,2.
As reflexões mais intensivas no padrão de difração de raio X mostram os seguintes intervalos de plano de intertreliça: 20 em [°]: .4,5, 5,6, 12,8, 17,0, 17,2, 19,8, 21,5, 27,4, em particular 4,45, 5,57, 17,01, 17,2, 19,76,21,27,4.
Um método preferido de verificar os valores médios acima indi-cados dos intervalos de plano de intertreliça e as intensidades avaliados por experimentação de difração de raio X, para uma substância fornecida, con* siste em calcular estes intervalos e suas intensidades a partir da determina-ção da estrutura de cristal única compreensiva. Esta determinação de estru-tura produz constantes celulares e posições de átomo, que permitem o dia-grama de difração de raio X correspondente ao sólido ser calculado por meio de métodos de cálculo auxiliados por computador. O programa empregado é Powder Pattern dentro do software de aplicação Materials Studio (Accelrys).
Uma comparação destes dados, isto é as intensidades e os intervalos de plano de intertreliça das linhas mais importantes de [3-((1 S,3R)-1 -bifenil-4- ilmetil-3-etoxicarbonil-1-butilcarbamoil)propionato-(S)-3’-metil-2'- (pentanoil{2"-(tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio, obtidos de medidas e de cálculo dos dados de cristal único, é 10 ilustrada na tabela abaixo.
A invenção refere-se a [3-((1 S,3R)-1 -bifenil-4-ilmetil-3- etoxica^bonil-1-butilcarbamoil)propionato-(S)-3'-metil-2’-(pentanoil{2,’- (tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio, um sólido cristalino que é cristalizado pelos dados e parâmetros obtidos da análise de raio X de cristal único e padrões de pó de raio X. Uma discussão a fundo da teoria e métodos de difração de raio X de cristal único e a definição dos dados de cristal avaliados e dos parâmetros podem ser encontrados em Stout & Jensen, X-Ray Structure Determination; A Practical Guide, Mac Millian Co., Nova York, N.Y. (1968) capítulo 3. Dados de Cristal Dados de medida de raio X de cristal único difractômetroNotas:
Dois dados avaliados sobre os dois cristais únicos adequados foram coleta-dos em duas diferentes temperaturas para assegurar que nenhuma mudan-ça de fase ocorra durante o resfriamento.
Nenhum dos átomos de hidrogênio na água ou os átomos de nitrogênio de amina foram observados nos mapas Fourier, assim eles não foram incluídos no refinamento.
Em três dimensões, a célula unitária é definida por três compri-mentos de arestas a, b, e c, e três ângulos interaxiais α, β, e y. Desta forma, o volume da célula unitária Vc é determinado. Uma descrição diferenciada destes parâmetros de cristal é ilustrada no capítulo de Stout & Jensen (ver acima). Os detalhes para [3-((1 S,3R)-1-bifenil-4-ilmetil-3-etoxicarbonil-1- butilcarbamoil)propionato-(S)-3'-metil-2'-(pentanoil{2,,-(tetrazol-5-ilato)bifenil- 4’-ilmetil}amino)butirato] hemipentaidrato de trissódio a partir das medidas de cristal único, especialmente as coordenadas de átomo, os parâmetros térmi-cos isotrópicos, as coordenadas dos átomos de hidrogênio bem como os parâmetros térmicos isotrópicos correspondentes, mostraram que uma célula unitária monoclínica existe, seu conteúdo celular de doze unidades de fórmula de C^HssNeOgNag • 2,5 H2O ocorre como um resultado de duas u- nidades assimétricas sobre posições duplicadas.
O grupo de espaço acêntrico P2i determinado da estrutura de raio X de cristal único é um grupo de espaço comum para as moléculas e- nantiomorficamente puras. Neste grupo de espaço existem duas posições gerais que significa que para doze unidades de fórmula na célula unitária deve ter 18 íons de sódio e 15 de água na unidade assimétrica.
Uma representação ilustrada da célula unitária do complexo su- pramolecular de [3-((1 S,3R)-1-bifenil-4-ilmetil-3-etoxicarbonil-1- butilcarbamoil)propionato-(S)-3'-metil-2’-(pentanoil{2"-(tetrazol-5-ilato)bifenil- 4'-ilmetil}amino)butirato] hemipentaidrato de trissódio compreendendo duas unidades assimétricas é mostrada na Figura 1.
Com base na solução de estrutura de cristal único, a unidade assimétrica da supramolécula de [3-((1S,3R)-1-bifenil-4-ilmetil-3- etoxicarbonil-1-butilcarbamoil)propionato-(S)-3'-metil-2'-(pentanoil{2"- (tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio compreende seis de cada uma das porções de ARB e NEPi, 18 átomos de sódio, e 15 moléculas de água. O [3-(( 1 S,3R)-1 -bifenil-4-iImetiI-3- etoxicarbonil-1-butilca rbamoil)propionato-(S)-3'-metil-2'-( penta noil{2"- (tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio pode ser considerado um complexo supramolecular de sódio, coordenado por ligandos de oxigênio. Estes oxigénios descendem de doze grupos de carboxilato e dezoito grupos de carbonila das porções acima, e de 13 das 15 moléculas de água. O cristal é uma rede 3-dimensional infinita destes com-plexos de sódio.
Um tal composto pode também ser caracterizado por um espectro de absorção infravermelho obtido empregando-se espectrômetro infra-vermelho de transformação Fourier de reflexão total atenuada (ATR-FTIR) (Nicolet Magna-IR 560) exibindo as seguintes faixas significantes, expressas em números de onda recíproca (cm*1 ): 2956 (w), 1711 (st), 1637 (st), 1597 (st), 1488 (w), 1459 (m), 1401 (st), 1357 (w), 1295 (m), 1266 (m), 1176 (w), 1085 (m), 1010 (w), 1942(w), 907 (w), 862 (w), 763 (st), 742 (m), 698 (m), 533 (st). Característico ao complexo são em particular os seguintes picos 1711 (st), 1637(st), 1597(st)e 1401 (st).
A margem de erro para todas as faixas de absorção de ATR-IR é ± 2 cm'1. As intensidades das faixas de absorção são indicadas como segue: (w) = fraca; (m) = média; e (st) = Intensidade forte.
Um tal composto pode também ser caracterizado por um espectro Raman avaliado pelo espectrômetro Raman dispersivo com 785 nm de fonte de excitação de laser (Kaiser Optical Systems, Inc.) exibindo as se- guintes faixas significantes expressas em números de onda recíproca (cm*1): 3061 (m), 2930 (m, extenso), 1612 (st), 1523 (m), 1461 (w), 1427 (w), 1287 (st), 1195 (w), 1108 (w), 11053 (w), 1041 (w), 1011 (w), 997 (m), 866(w), 850 (w), 822 (w), 808 (w), 735 (w), 715 (w), 669 (w), 643 (w), 631 (w), 618 (w), 602 (w), 557 (w), 522 (w), 453 (w), 410 (w), 328 (w).
A margem de erro para todas as faixas Raman é de ± 2 cm'1. As intensidades das faixas de absorção são indicadas como segue: (w) = fraca; (m) = média; e (st) = Intensidade forte.
Um tal composto pode também ser caracterizado por propriedades de fusão distintas avaliadas por calorimetria de varredura diferencial (DSC). Empregando-se o instrumento Q1000 (TA Instruments), a temperatura de início de fusão e a temperatura máxima de pico para um tal complexo são observadas a 139 °C e 145 °C, respectivamente. A razão de aquecimento é de 10 K/minuto.
A segunda modalidade da presente invenção é direcionada ás composições farmacêuticas compreendendo uma combinação, um pró- fármaco ligado ou um composto de ação dupla, em particular o complexo como descrito aqui e pelo menos um aditivo farmaceuticamente aceitável. Os detalhes com respeito a combinação e ao complexo, incluindo o ARB e o NEPi, são como descritos acima com referência a primeira modalidade da invenção.
As composições farmacêuticas de acordo com a invenção podem ser preparadas de uma maneira conhecida de per si e são aquelas a- dequadas para administração enteral, tal como oral ou retal, e parenteral aos mamíferos (animais de sangue quente), incluindo o homem, compreendendo uma quantidade terapeuticamente eficaz da combinação ou composto de ação dupla, em particular o complexo, sozinho ou em combinação com pelo menos um portador farmaceuticamente aceitável, especialmente adequado para aplicação enteral ou parenteral. As formulações orais típicas incluem comprimidos, cápsulas, xaropes, elixires e suspensões. As formulações inje-táveis típicas incluem as soluções e suspensões.
Os aditivos farmaceuticamente aceitáveis adequados para o emprego na presente invenção incluem, sem limitação e contanto que eles sejam quimicamente inertes a fim de que eles não adversamente afetem a combinação ou o composto de ação dupla, em particular o complexo da presente invenção, diluentes ou cargas, desintegrantes, deslizantes, lubrificantes, aglutinantes, colorantes e combinações dos mesmos. A quantidade de cada aditivo em uma formulação de dosagem sólida pode variar dentro de limites convencionais na técnica. Os portadores farmaceuticamente aceitáveis típicos para o emprego nas formulações descritas acima são exemplificados por: açúcares, tais como lactose, sacarose, manitol e sorbitol; amidos, tais como amido de milho, amido de tapioca e amido de batata; celulose e derivados, tais como carboximetil celulose de sódio, etil celulose e metil celulose; fosfatos de cálcio, tais como fosfato de dicálcio e fosfato de tricálcio; sulfato de sódio; sulfato de cálcio; polivtnilpirrolidona; álcool de polivinila; á- cido esteárico; estearatos de metal alcalino terroso, tal como estearato de magnésio e estearato de cálcio; ácido esteárico; óleos vegetais, tais como óleo de amendoim, óleo de caroço de algodão, óleo de sésamo, azeite e óleo de milho; tensoativos não tônicos, catiônícos e aniônicos; polímeros de etileno glicol; β-ciclodextrina; álcoois graxos; e sólidos de cereal hidrolizado, bem como outras cargas compatíveis não tóxicas, aglutinantes, desintegrantes, tampões, preservativos, antioxidantes, lubrificantes, agentes aromatizan- tes e similares comumente empregados em formulações farmacêuticas.
As preparações farmacêuticas para administração enteral ou parenteral são, por exemplo, em formas de dose unitária, tais como compri-midos revestidos, comprimidos, cápsulas ou supositórios e também ampolas. Estas são preparadas de uma maneira que é conhecida de per si, por exemplo, empregando-se processos de mistura convencional, de granulação, de revestimento, solubilizantes ou liofilização. Desse modo, as composições farmacêuticas para o emprego oral podem ser obtidas combinando-se o pró-fármaco ligado, combinação ou o composto de ação dupla, em particular o complexo com excipientes sólidos, se desejado, granulando-se uma mistura que foi obtida, e, se requerido ou necessário, processando-se a mistura ou granulado em comprimidos ou núcleos de comprimidos revestidos
após ter adicionado as substâncias auxiliares adequadas,
A dosagem dos compostos ativos na combinação ou composto de ação dupla, em particular o complexo pode depender de uma variedade de fatores, tal como o método de administração, espécie homeotérmica, idade e/ou a condição individual. A eficácia ressaltada em modelos de doença animal varia de cerca de 0,1 mg/kg/dia a cerca de 1000 mg/kg/dia fornecido oralmente, e a dose projetada para tratamento humano varia de cerca de 0,1 mg/dia a cerca de 2000 mg/dia. As variações preferidas são de cerca de 40 mg/dia a cerca de 960 mg/dia do pró-fármaco ligado, preferivelmente de cerca de 80 mg/dia a cerca de 640 mg/dia. O componente ARB é administrado em uma dosagem de cerca de 40 mg/dia a cerca de 320 mg/dia e o componente NEPi é administrado em uma dosagem de cerca de 40 mg/dia a cerca de 320 mg/dia. Mais especificamente, as dosagens de ARB/NEPi, respectivamente, incluem 40 mg/40 mg, 80 mg/80 mg, 160 mg/160 mg, 320 mg/320 mg, 40 mg/80 mg, 80 mg/160 mg, 160 mg/320 mg, 320 mg/640 mg, 80 mg/40 mg, 160 mg/80 mg e 320 mg/160 mg, respectivamente. Estas dosagens são "quantidades terapeuticamente eficazes". As dosagens preferidas para o pró-fármaco ligado, combinação ou composto de ação dupla, em particular o complexo da composição farmacêutica de acordo com a presente invenção são dosagens terapeuticamente eficazes.
As composições farmacêuticas podem conter além disso outro agente terapêutico, por exemplo, em cada uma dose terapêutica efetiva como reportado na técnica. Tais agentes terapêuticos incluem: a) agentes antidiabéticos tais como insulina, derivados de insuli-na e miméticos; secretagogos de insulina tais como as sulfoniluréias, por exemplo, Glipizida, gliburida e Amarila; ligandos de receptor de sulfoniluréia insulinotrópica tais como meglitinidas, por exemplo, nateglinida e repaglinida; ligandos de receptor ativado por proliferador de peroxissoma (PPAR); inibi-dores de proteína tirosina fosfatase-1B (PTP-1B) tal como PTP-112; inibidores de GSK3 (glicogênio sintase cinase-3) tais como SB-517955, SB- 4195052, SB-216763, NN-57-05441 e NN-57-05445; ligandos de RXR tais como GW-0791 e AGN-194204; inibidores de cotransportador de glicose dependente de sódio tal como T-1095; inibidores de glicogênio fosforilase A tal como BAY R3401; biguanidas tal como metformina; inibidores de alfa- glucosidase tal como acarbose; GLP-1 (peptídeo-1 tipo glucagon), análogos de GLP-1 tais como miméticos de Exendin-4 e GLP-1; e inibidores de DPPIV (dipeptidil peptidase IV) tal como LAF237; b) agentes hipolipidêmicos tais como inibidores de 3-hidróxi-3- metil-glutaril coenzima A (HMG-CoA) reductase, por exemplo, lovastatina, pitavastatina, sinvastatina, pravastatina, cerivastatina, mevastatina, velosta- tina, fluvastatina, dalvastatina, atorvastatina, rosuvastatina e rivastatina; ini-bidores de sintase de esqualeno; FXR (receptor de farnesoid X) e ligandos de LXR (receptor de fígado X); colestiramina; fibratos; ácido nicotínico e aspirina; c) agentes anti-obesidade tal como orlistat; e d) agentes anti-hipertensivo, por exemplo, diuréticos de alça tais como ácido etacrínico, furosemida e torsemida; inibidores de enzima de con-versão de angiotensina (ACE) tais como benazepril, captopril, enalapril, fosi- nopril, lisinopril, moexipril, perinodopril, quinapril, ramipril e trandolapril; inibi-dores da bomba de membrana Na-K-ATPase tal como digoxina; inibidores de ACE/NEP tais como omapatrilat, sampatrilat e fasidotril; bloqueadores de receptor de ü-adrenérgico tal como acebutolol, atenolol, betaxolol, bisopro- lol, metoprolol, nadolol, propranolol, sotalol e timolol; agentes inotrópicos tais como digoxina, dobutamina e milrinona; bloqueadores do canal de cálcio tais como anlodipina, bepridil, diltiazem, felodipina, nicardipina, nimodipina, nife- dipina, nisoldipina e verapamil; antagonistas de receptor de aldoesterona; e inibidores de sintase de aldoesterona. Os parceiros de combinação mais preferidos são os diuréticos, tais como hidroclorotiazida, e/ou os bloqueadores de canal de cálcio, tal como amlodipina ou um sal do mesmo.
Outros composes anti-diabéticos específicos são descritos por Patel Mona em Expert Opin Investig Drugs, 2003, 12(4), 623-633, nas figu-ras de 1 a 7, os quais são incorporados aqui por referência. Um composto da presente invenção pode ser administrado simultaneamente, antes ou após o outro ingrediente ativo, separadamente pela mesma ou diferente rotina de administração ou junto na mesma formulação farmacêutica.
A estrutura dos agentes terapêuticos identificados pelos números códigos, nomes comerciais ou genéricos pode ser tirada da edição atual do resumo padrão "The Merck Index” ou da base de dados, Patents International (por exemplo, IMS World Publications). O conteúdo correspondente deste é incorporado aqui por referência.
Conseqüentemente, a presente invenção fornece composições farmacêuticas além de uma quantidade terapeuticamente eficaz de outro agente terapêutico, preferivelmente selecionado de antidiabéticos, agentes hipolipidêmicos, agentes antiobesidade ou agentes anti-hipertensivos, mais preferivelmente de agentes antidiabéticos, anti-hipertensivos ou agentes hi-polipidêmicos como descrito acima.
A pessoa versada na técnica pertinente é completamente capaz de selecionar um modelo de teste relevante para provar a eficácia de uma combinação da presente invenção nas indicações terapêuticas anteriormente e posteriormente indicadas.
Estudos representativos são realizados com [3-((1S,3R)-1- bifenil-4-ilmetil-3-etoxicarbonil-1-butilcarbamoil)propionato-(S)-3'-metil-2’- (pentanoil{2,,-(tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio, por exemplo, aplicando-se a seguinte metodologia:
As atividades inibitórias anti-hipertensivas e de endopeptidase neutra 24.11 (NEP) de [3-(( 1 S,3R)-1-bifenil-4-ilmetil-3-etoxicarbonil-1- butilcarbamoil)propionato-(S)-3’-metil-2’-(pentanoil{2’'-(tetrazol-5-ilato)bifenil- 4'-ilmetil}amino)butirato] hemipentaidrato de trissódio são avaliadas em ratos conscientes. O efeito de redução da pressão sangüínea é avaliado em ratos duplamente transgênicos (dTGRs) que superexpressam igualmente a renina humana e seu substrato, angiotensinogênio humano (Bohlender, e outros, High human renin hypertension in transgenic rats. Hypertension; 29(1 Pt 2):428-34, 1997). Conseqüentemente, estes animais exibem uma hipertensão dependente de angiotensina II. O efeito inibitório de NEP de [3-((1 S,3R)- 1-bifenil-4-ilmetil-3-etoxicarbonil-1-butilcarbamoil)propionato-(S)-3'-metil-2'- (pentanoil{2"-(tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio é determinado em ratos Sprague-Dawley conscientes infundidos com peptídeo natriurético atrial exógeno (ANP). A potenciação de níveis de ANP de plasma é empregada como um índice de inibição de NEP in vivo. Em ambos os modelos, o [3-{(1S,3R)-1-bifenil-4-ilmetil-3-etoxicarbonil-1- butilcarbamoil)propionato-(S)-3'-metil-2'-(pentanoil{2"-(tetrazol-5-ilato)bifenil- 4'-ilmetil}amino)butirato] hemipentaidrato de trissódio é administrado oral-mente como um pó em mini cápsulas de gelatina. Os resultados são sumari- zados abaixo. • [3-((1S,3R)-1-bifenil-4-ilmetil-3-etoxicarbonil-1-butilcarbamoil)- propionato-(S)-3,-metil-2’-(pentanoil{2"-(tetrazol-5-ilato)bifenil-4,- ilmetil}amino)butirato] hemipentaidrato de trissódio exibe um efeito anti- hipertensivo duradouro e dependente da dose após a administração oral em dTGRs conscientes, um modelo de rato de hipertensão fulminante. • A administração oral de [3-((1S,3R)-1-bifenil-4-ilmetil'3- etoxicarbonil-1-butilcarbamoil)propionato-(S)-3'-metil-2’-(pentanoil{2"- (tetrazol-5-ilato)bifenil-4'-ilmetil}amino)butirato] hemipentaidrato de trissódio rapidamente e dependentemente de dose inibe NEP com uma longa duração de ação, como refletido por sua potenciação de imunoreatividade de ANP de plasma (ANPir) em ratos Sprague-Dawley conscientes infundidos com ANP exógeno.
Os dTGRs são instrumentados com transmissores de radiotele- metria para avaliação contínua da pressão sangüínea arterial e freqüência do coração. Os animais são aleatoriamente designados ao veículo (cápsula vazia) ou grupos de tratamento (em 2, 6, 20 ou 60 mg/kg, p.o.). O valor de referência 24 horas de pressão arterial moderada (MAP) é de aproximadamente 170-180 mmHg em todos os grupos. O [3-((1 S,3R)-1 -bifenil-4-ilmetil- 3-etoxicarbonil-1-butilcarbamoil)propionato-(S)-3’-metil-2'-(pentanoil{2"- (tetrazol-5-ilato)bifenil-4*-ilmetil}amino)butirato] hemipentaidrato de trissódio dependentemente de dose reduz o MAP. Os valores obtidos dos grupos de tratamento são dependentes de dose, e os resultados das três maiores doses são significantemente diferentes dos controles de veículo.
Inibição de NEP /n vivo & extensão e a duração de [3-(( 1 S,3/?)-1 -bifenil-4-ilmetil-3- etoxicarbonil-1-butilcarbamoil)propionato-(S)-3'-metil-2'-(pentanoil{2"- (tetrazol-5-ilato)bifenil-4'-ilmetjl}amino)butirato] hemipentaidrato de trissódio para inibição de NEP in vivo são avaliadas com metodologias como previamente descrito (Trapani, e outros, CGS 35601 e seu pró-fármaco oralmente ativo CGS 37808 como inibidores triplos da enzima-1 de conversão de endo- telina, endopeptidase neutra 24.11, e enzima de conversão de angiotensina. J Cardiovasc Pharmacol; 44(Suppl 1 ):S211-5, 2004). O rato ANP(1-28) é infundido intravenosamente em uma razão de 450 ng/kg/minuto em ratos Sprague-Dawley machos, cronicamente canulados, conscientes. Após uma hora de infusão, os ratos são aleatoriamente designados a um dos seis gru-pos: controle não tratado, controle de veículo (cápsula vazia), ou uma das quatro doses de fármaco (2, 6, 20, ou 60 mg/kg, p.o.). A infusão de ANP é continuada durante um adicional de oito horas. As amostras de sangue são coletadas para medir o ANPir de plasma por um kit de imunoensaio de enzima comercial em -60 minutos (isto é, antes de iniciar a infusão de ANP), - 30 minutos (após 30 minutos de infusão de ANP), 0 minuto ("valor de referência"; após 60 minutos de infusão de ANP, porém antes da dosagem com o fármaco ou seu veículo), e em 0,25, 0,5,1,2,3,4, 5, 6, 7, e 8 horas após a dosagem.
Antes da infusão de ANP, ANPir é baixo (0,9-1,4 ng/ml) e similar em todos os seis grupos. A infusão de ANP rapidamente (por 30 minutos) eleva o ANPir a -10 ng/ml. Este nível de ANPir é sustentado durante a duração do experimento nos grupos de controle de veículo e não tratado. Em contraste, o [3-((1 S,3R)-1-bífenil-4-ilmetil-3-etoxicarbonil-1- butilcarbamoil)propionato-(S)-3’-metil-2,-(pentanoil{2"-(tetrazol-5-Ílato)bifenil- 4'-ilmetil}amino)butirato] hemipentaidrato de trissódio rapidamente (dentro de 15 minutos) e dependentemente de dose eleva o ANPir. Em resumo, o LCZ696 oralmente administrado rapidamente e dependentemente de dose inibiu o NEP com uma longa duração de ação como refletido pela potenciação de ANPir de plasma.
Os resultados disponíveis indicam um efeito terapêutico inespe-rado de um composto de acordo com a invenção.
Em um terceiro aspecto, a presente invenção direciona-se a um método de preparar um pró-fármaco ligado de um ARB ou um sal farmaceu- ticamente aceitável deste e um NEPi ou um sal farmaceuticamente aceitável deste compreendendo as etapas de: (a) adicionar um agente de formação de sal inorgânico a um sol-vente para formar uma solução de formação de sal de pró-fármaco ligado; (b) adicionar a solução de formação de sal a uma mistura de um ARB e um NEPi tal que o ARB e NEPi forme um pró-fármaco ligado; e (c) isolar o pró-fármaco ligado.
Preferivelmente, os componentes são adicionados em uma quantidade equivalente.
O agente de formação de sal inorgânico inclui, porém não é limi-tado a, hidróxido de cálcio, hidróxido de zinco, metóxido de cálcio, acetato de cálcio, carbonato de hidrogênio de cálcio, formiato de cálcio, hidróxido de magnésio, acetato de magnésio, formiato de magnésio e carbonato de hi-drogênio de magnésio, hidróxido de sódio, metóxido de sódio, acetato de sódio, formiato de sódio. O agente de formação de sal inorgânico libera a porção de ligação no solvente tal que, quando um ARB e um NEPi estão presentes, um pró-fármaco ligado é formado.
Os solventes no escopo da presente invenção incluem, porém não são limitados a, solventes em que o ARB, NEPi e o agente de formação de sal inorgânico preferivelmente exibem uma solubilidade menor do que permite o pró-fármaco ligado cristalizar. Tais solventes podem compreender, porém não são limitados a, água, metanol, etanol, 2-propanol, etilacetato, metil-f-butiléter, acetonitrila, tolueno, e cloreto de metileno e misturas de tais solventes.
O agente de formação de sal inorgânico e o solvente quando combinados devem possuir um pH que promova a formação do pró-fármaco ligado. O pH pode ser entre cerca de 2 e cerca de 6, preferivelmente entre cerca de 3 e cerca de 5, mais preferivelmente entre 3,9 e 4,7.
O pró-fármaco ligado é isolado por cristalização e cromatografia. Tipos específicos de cromatografia incluem, por exemplo, cromatografia de resina específica de ligando, cromatografia de resina de fase reversa e cro-matografia de resina de troca de íon.
Um exemplo específico compreende contatar um sal divalente de um componente com um sal monovalente do outro componente do pró- fármaco ligado. Especificamente o sal misturado de valsartan e um NEPi monobásico são sintetizados contatando-se o sal de cálcio de valsartan com o sal de sódio do componente NEPi. O isolamento do sal misturado desejado é realizado por cristalização seletiva ou cromatografia empregando-se resinas específicas de ligando, resinas de fase reversa ou resinas de troca de íon. Similarmente, este processo pode ser conduzido com um sal monovalente de ambos os componentes, tal como o sal de sódio de ambos os componentes.
Em outra modalidade deste aspecto da invenção, um co-cristal do pró-fármaco ligado é obtido. Em um método de preparar um co-cristal de pró-fármaco ligado o agente de formação de sal inorgânico é substituído com uma molécula neutra que fornece propriedades de ligação de hidrogênio. O solvente pode ser parte da embalagem molecular e ser aprisionado na treliça de cristal.
Em uma modalidade preferida do terceiro aspecto, a presente invenção é direcionada a um método de preparar um composto de ação dupla compreendendo (a) um antagonista de receptor de angiotensina; (b) um inibidor de endopeptidase neutra (NEPi); e opcionalmente (c) um cátion farmaceuticamente aceitável; o referido método compreendendo as etapas de: (i) dissolver um antagonista de receptor de angiotensina e um inibidor de endopeptidase neutra (NEPi) em um solvente adequado; (ii) dissolver um composto básico de Cat em um solvente ade-quado, onde o Cat é um cátion; (iii) combinar as soluções obtidas nas etapas (i) e (ii); (iv) precipitação do sólido, e secagem do mesmo para obter o composto de ação dupla; ou altemativamente obter o composto de ação dupla alterando-se os solventes empregados nas etapas (i) e (ii) (iva) evaporando-se uma solução resultante à secura; (va) redissolvendo-se o sólido em um solvente adequado; (via) precipitação do sólido e secagem do mesmo para obter o composto de ação dupla.
Os detalhes quanto ao complexo, incluindo o ARB, o NEPi e o cátion, são como descritos acima com relação à primeira modalidade da in-venção.
Preferivelmente, na etapa (i) o ARB e o NEPi são adicionados em uma quantidade molar equivalente. Ambos os ARB e o NEPi são preferi-velmente empregados na forma livre. O solvente empregado na etapa (i) pode ser qualquer solvente que permita a dissolução de ambos ARB e o NEPi. Os solventes preferidos incluem aqueles mencionados acima, isto é água, metanol, etanol, 2-propanol, acetona, acetato de etila, acetato de iso- propila, metil-t-butiléter, acetonitrilo, tolueno, DMF, NMF e cloreto de metile- no e misturas de tais solventes, tal como etanol-água, metanol-água, 2- propanol-água, acetonitrilo-água, acetona-água, 2-propanol-tolueno, acetato de etila-heptano, acetato de isopropila-acetona, metil-t-butiléter-heptano, metil-t-butiléter-etanol, etanol-heptano, acetona-acetato de etila, acetona- cicloexano, tolueno-heptano, mais preferivelmente acetona.
Preferivelmente, na etapa (ii) o composto básico de Cat é um composto capaz de formar um sal com as funcionalidades acídicas do ARB e NEPi. Os exemplos incluem aqueles acima mencionados, tais como hidróxido de cálcio, hidróxido de zinco, metóxido de cálcio, etóxido de cálcio, acetato de cálcio, carbonato de hidrogênio de cálcio, formiato de cálcio, hidróxido de magnésio, acetato de magnésio, formiato de magnésio, carbonato de hidrogênio de magnésio, hidróxido de sódio, carbonato de sódio, carbonato de hidrogênio de sódio, metóxido de sódio, etóxido de sódio, acetato de sódio, formiato de sódio, hidróxido de potássio, carbonato de potássio, carbo- nato de hidrogênio de potássio, metóxido de potássio, etóxido de potássio, acetato de potássio, formiato de potássio, hidróxido de amónio, metóxido de amónio, etóxido de amónio, e carbonato de amónio. Percloratos podem também ser empregados. As bases de a mina ou os agentes de formação de sal tais como aqueles mencionados acima podem também ser incluídos, em particular benzatina, L-arginina, colina, diamina de etileno, L-lisina ou pipera- zina. Tipicamente uma base inorgânica é empregada com Cat como especificado aqui. Mais preferivelmente, o composto básico é (Cat)OH, (Cat)2CO3, (Cat)HCO3, ainda mais preferivelmente Cat(OH), tal como NaOH. O composto básico é empregado em uma quantidade de pelo menos 3 equivalentes referente a ARB ou a NEPi, preferivelmente ele é empregado em quantidade estequiométrica para obter o composto de ação dupla, em particular o com-plexo com três cátions. O solvente empregado na etapa (ii) pode ser qualquer solvente ou misturas de solventes que permitem a dissolução de Cat(OH). Os solventes preferidos incluem água, metanol, etanol, 2-propanol, acetona, etilacetato, acetato de isopropila, metil-í-butiléter, acetonítrila, tolu- eno, e cloreto de metileno e misturas de tais solventes, mais preferivelmente água.
Na etapa (iii) as soluções obtidas nas etapas (i) e (ii) são combi-nadas. Isto pode ocorrer adicionando-se a solução obtida na etapa (i) à solu-ção obtida na etapa (ii) ou vice versa, preferivelmente, a solução obtida na etapa (ii) à solução obtida na etapa (i).
De acordo com a primeira alternativa, uma vez combinado e pre-ferivelmente misturado, o composto de ação dupla, em particular o complexo precipita na etapa (iv). Esta mistura e precipitação é tipicamente efetuada agitando-se as soluções durante uma quantidade apropriada de tempo tal como 20 minutos a 6 horas, preferivelmente de 30 minutos a 3 horas, mais preferivelmente 2 horas, em temperatura ambiente. É vantajoso adicionar sementes do composto de ação dupla. Este método facilita a precipitação.
Na etapa (iv) de acordo com a primeira alternativa, um co- solvente é tipicamente adicionado. O co-solvente empregado é um solvente no qual o ARB e o NEPi na forma complexada exibe uma solubilidade menor do que permite o composto precipitar. A destilação, contínua ou em etapas, com a substituição por este co-solvente resulta em uma mistura predominantemente do co-solvente. Os solventes preferidos incluem etanol, 2-propanol, acetona, etilacetato, acetato de isopropila, metil-t-butiléter, acetonitrilo, toluene, e cloreto de metileno e misturas de tais solventes, mais preferivelmente acetato de isopropila. Preferivelmente, uma quantidade mínima de solvente é empregada para facilitar a precipitação. O sólido é coletado, por exemplo, por filtragem, e é secado para obter o composto de ação dupla, em particular o complexo de acordo com a presente invenção. A etapa de secagem pode ser realizada em temperatura ambiente ou temperatura elevada tal como de 30 a 60 °C, preferivelmente de 30 a 40 °C. A pressão reduzida pode ser empregada para facilitar a remoção do solvente, preferivelmente, a secagem é efetuada em pressão ambiente ou pressão reduzida de por exemplo, 1 a 3 mPa (10 a 30 bar), tal como 2 mPa (20 bar).
De acordo com uma segunda alternativa, uma vez combinado e preferivelmente misturado, o composto de ação dupla, em particular o com-plexo, a mistura preferivelmente forma uma solução clara. Esta mistura é tipicamente efetuada agitando-se as soluções durante uma quantidade a- propriada de tempo tal como de 20 minutos a 6 horas, preferivelmente de 30 minutos a 3 horas, mais preferivelmente 1 hora, em temperatura ambiente. Se necessário, a temperatura pode ser elevada a fim de assegurar uma solução clara.
A mistura obtida é em seguida também tratada por permuta de solvente para obter o composto de ação dupla, em particular o complexo.
Na etapa (iva) de acordo com esta segunda alternativa, a solução é preferivelmente evaporada à secura em temperaturas elevadas tal como > temperatura ambiente a 50 °C, mais preferivelmente de 30 a 40 °C.
Preferivelmente, na etapa (va) o solvente ou mistura de solvente empregado é um solvente no qual o ARB e o NEPi na forma complexada exibe uma solubilidade menor que permite o composto de ação dupla, em particular o complexo precipitar. Os solventes preferidos incluem aqueles mencionados acima para a etapa (i), tal como água, etanol, 2-propanol, eti- lacetato de acetona, acetato de isopropila, metil-t-butiléter, acetonitrilo, tolu- eno, e cloreto de metileno e misturas de tais solventes, mais preferivelmente acetato de isopropila. Preferivelmente, uma quantidade mínima de solvente ou mistura de solvente é empregada para facilitar a precipitação.
Na etapa (via) a precipitação pode ocorrer em temperatura am-biente. Ela pode ser efetuada deixando-se a mistura repousar ou agitando- se a mistura, preferivelmente agitando-a. Isto é preferivelmente efetuado por agitação e/ou sonicação. Após a precipitação, o sólido é coletado, por e- xemplo, por filtragem, e é secado para obter o composto de acordo com a presente invenção. A etapa de secagem pode ser realizada em temperatura ambiente ou temperatura elevada tal como de 30 a 60 °C, preferivelmente em temperatura ambiente. A pressão reduzida pode ser empregada para facilitar a remoção do solvente, preferivelmente, a secagem é efetuada em pressão ambiente.
Em um quarto aspecto, esta invenção é direcionada a um método de tratar ou prevenir uma doença ou condição, tal como hipertensão, in-suficiência cardíaca (aguda ou crônica), insuficiência cardíaca congestiva, disfunção ventricular esquerda e cardiomiopatia hipertrófica, miopatia cardíaca diabética, arritmia supraventricular e ventricular, fibrilação atrial, flutter atrial, remodelagem vascular prejudicial, infarto do miocárdio e suas seqüe- las, aterosclerose, angina (instável ou estável), insuficiência renal (diabética e não diabética), insuficiência cardíaca, angina pectoris, diabetes, aldoeste- ronismo secundário, hipertensão pulmonar primária e secundária, condições de insuficiência renal, tais como nefropatia diabética, glomerulonefrite, escle- roderma, esclerose glomerular, proteinúria de doença renal primária, e também hipertensão vascular renal, retinopatia diabética, outros distúrbios vasculares, tal como hemicrania, doença vascular periférica, doença de Raynaud, hiperplasia luminal, disfunção cognitiva (tal como Alzheimer), glaucoma e acidente vascular cerebral compreendendo administrar a combinação anteriormente mencionada, pró-fármaco ligado ou o composto de ação dupla, em particular o complexo a um indivíduo em necessidade de tal tratamento.
A combinação, pró-fármaco ligado ou o composto de ação dupla, em particular o complexo da primeira modalidade pode ser administrado so-zinho ou na forma de uma composição farmacêutica de acordo com a segunda modalidade. A informação com respeito a dosagem, isto é, a quantidade terapeuticamente eficaz, etc., é a mesma independente de como a combinação, pró-fármaco ligado ou o composto de ação dupla, em particular o complexo é administrado.
A combinação, o pró-fármaco ligado ou o composto de ação dupla, em particular o complexo é benéfico sobre uma combinação de ARBs ou inibidores de endopeptidase neutra sozinha ou outras combinações de ARB/NEPi com relação ao emprego como a primeira terapia de linha, facilidade de formulação e facilidade de fabricação.
As modalidades específicas da invenção serão agora demons-tradas por referência aos seguintes exemplos. Deve ser entendido que estes exemplos são descritos somente como forma de ilustrar a invenção e não devem ser entendidos de forma alguma como limitantes do escopo da presente invenção.
O composto de ação dupla de valsartan e o éster de etila de ácido (2R,4S)-5-bifenil-4-il-5-(3-carbóxi-propionilamino)-2-metil-pentanóico é preparado dissolvendo-se 0,42 g de ácido livre de éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil-pentanóico (-95% de pureza) e 0,41 g de ácido livre de valsartan em 40 ml de acetona. Sepa-radamente, 0,111 g de NaOH são dissolvidos em 7 ml de H2O. As duas so-luções são combinadas e agitadas em temperatura ambiente durante 1 hora e uma solução clara foi obtida. A solução é evaporada a 35 °C para produzir um sólido transparente. O resíduo sólido transparente é em seguida carregado com 40 ml de acetona e a mistura resultante é agitada e sonicada até a precipitação ocorrer 5 minutos). O precipitado foi filtrado e o sólido é secado em temperatura ambiente em ar aberto durante 2 dias até uma massa constante do sólido cristalino ser obtido.
A caracterização por vários métodos pode confirmar a presença de ambos valsartan e éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3- carbóxi-propionilamino)-2-metil-pentanóico e a formação de complexo em contraste como uma mistura física simples. Picos espectrais significantes para o complexo são observados, por exemplo, na espectroscopia Raman, XRPD e IR, que não estão presentes para a mistura física. Ver abaixo para detalhes sobre a caracterização.
O composto de ação dupla de valsartan e éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil-pentanótco é preparado dissolvendo-se 22,96 mmoles de ácido livre de éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil-pentanóico (~95% de pureza) e valsartan (10,00 g; 22,96 mmoles) em acetona (300 mL). A suspensão é agitada em temperatura ambiente durante 15 minutos para obter uma solução clara. Uma solução de NaOH (2,76 g; 68,90 mmoles) em água (8 mL) a água é em seguida adicionada a esta solução durante um período de 10 minutos. Os sólidos começam a precipitar em 10 minutos. Altemativamente, a precipitação pode ser induzida por semeadura. A suspensão é agitada a 20 - 25 °C durante 2 horas. Esta suspensão é concentrada a 15 - 30 °C sob pressão reduzida (180 - 250 mbar) a um volume de batelada de *150 mL. Acetato de isopropila (150 mL) é em seguida adicionado à batelada e a suspensão é concentrada novamente a 15-30 °C sob pressão reduzida (180-250 mbar) para um volume de batelada de * *150 mL. Esta operação (além de 150 mL de acetato de isopropila para a batelada e concentração) é repetida mais uma vez. A suspensão é agitada a 20-25 °C durante 1 hora. Os sólidos são coletados por filtragem sob nitrogênio por um funil de Büchner, lavados com acetato de isopropila (20 mL), e secados a 35°C sob pressão reduzida (20 mbar) para fornecer o composto.
A caracterização revelou o mesmo produto como no Exemplo 1.
Um reator é carregado com 2,00 kg (2,323 mmoles) de sal de cálcio AHU377 e 20 L de acetato de isopropila. A suspensão é agitada a 23 ± 3°C, e 4,56 L de 2 N de HCI foi adicionado. A mistura é agitada a 23 ± 3°C durante 15 minutos para obter uma solução de duas fases claras. A camada orgânica é separada e lavada com 3 x 4,00 L de água. A camada orgânica é concentrada a 30-100 mbar e 22 ± 5°C a *3,5 L (3,47 kg) de solução de acetato de isopropila de ácido livre AHU377 como uma solução incolor.
Ao reator acima contendo *3,5 L (3,47 kg) de solução de acetato de isopropila de ácido livre AHU377 é adicionado 1,984 kg (4,556 mmoles) de Valsartan e 40 L de acetona. A mistura de reação é agitada a 23 ± 3 °C para obter uma solução clara que é filtrada em um reator. À mistura de reação é adicionado uma solução de 547,6 g (13,690 mmoles) de NaOH em 1,0 L de água a 23 ± 3 °C (que foi pré-resfriada a 20 ± 5 °C e filtrada em linha) durante um período de 15-30 minutos ao mesmo tempo que mantendo a temperatura interna em 20-28 °C (levemente exotérmica). O frasco é enxa- güado com 190 mL de água e adicionado na mistura de reação. A mistura de reação é agitada a 23 ± 3 °C durante 15 minutos e uma suspensão de 4,0 g de [éster de etila de ácido ((2/?,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)- 2-metÍI-pentanóíco de valsartan]Na3 • 2,5 H2O de sementes em 50 mL de acetato de isopropila é adicionada. A mistura é agitada a 23 ± 3 °C durante 2 horas para obter uma suspensão. A suspensão é aquecida a uma temperatura interna de 40 + 3 °C durante um período de 20 minutos e 20 L de acetato de isopropila é adicionado durante um período de 20 minutos ao mesmo tempo que mantendo a temperatura interna em 40 ± 3oC. A suspensão é agitada nesta temperatura durante um adicional de 30 minutos. A mistura é concentrada em uma temperatura interna de 35 ± 5 °C (Tj 45 ± 5 °C) sob pressão reduzida (200-350 mbar) para *35 L de uma suspensão branca (solvente coletado: *25 L). Em seguida, 30 L de acetato de isopropila é adi- cionado a mistura é concentrada em uma temperatura interna de 35 + 5 °C (Tj 45 ± 5 °C) sob pressão reduzida (100-250 mbar) para -30 L de uma suspensão branca (solvente coletado: -40 L). Novamente 40 L de acetato de isopropila é adicionado e a mistura é concentrada em uma temperatura interna de 35 ± 5 °C (Tj 45 ± 5 °C) sob pressão reduzida (100-200 mbar) para -30 L de uma suspensão branca (solvente coletado: -30 L). A mistura de reação é resfriada a 23 ± 3 °C durante -20 minutos e agitada nesta temperatura durante um adicional de 3 horas. O sólido é coletado por filtragem sob nitrogênio sobre uma almofada de polipropileno em funil de Büchner. O sólido é lavado com 2 X 5 L de acetato de isopropila e secado a 35 °C sob pressão reduzida (20 mbar) até o conteúdo de acetato de isopropila <0,5% fornecer o produto acima como um sólido branco.
A caracterização revelou o mesmo produto como no Exemplo 1.
O cálculo dos intervalos de plano de intertreliça de padrão de pó de raio X tomado com um difractômetro de pó Scintag XDS2000 para as linhas mais importantes para a amostra fornece os seguintes resultados: d em [A]: 21,2(s), 17,0(w), 7,1 (s), 5,2(w), 4,7(w), 4,6(w), 4,2(w), 3,5(w), 3,3(w)
A margem de erro para todos os intervalos de plano de intertreliça é de ± 0,1 A. As intensidades dos picos são indicados como segue: (w) = fraca; (m) = média; e (st) = forte.
Os valores médios 20 em [°] são indicados (limite de erro de ±0,2) 4,5, 5,5, 5,6, 9,9, 12,8, 15,7, 17,0, 17,1, 17,2, 18,3, 18,5, 19,8, 21,5, 21,7, 23,2, 23,3, 24,9, 25,3, 27,4, 27,9, 28,0, 30,2.
A análise elementar fornece os seguintes valores avaliados dos elementos presentes na amostra. As descobertas da análise elementar, dentro dos limites de erro, correspondem à fórmula geral de (CAβHssNβOβNaa)» 2,5H2O Encontrado C: 60,05% H: 6,24% N: 8,80% Calculado* C: 60,18% H: 6,31% N: 8,77%
O espectro de absorção infravermelho para a amostra obtida empregando-se espectrômetro de infravermelho de transformação Fourier de reflexão total atenuada (ATR-FTIR) (Nicolet Magna-IR 560) exibe as seguintes faixas significantes, expressas em números de onda recíproca (cm'1): 2956 (w), 1711 (st), 1637 (st), 1597 (st), 1488 (w), 1459 (m), 1401 (st), 1357 (w), 1295 (m), 1266 (m), 1176 (w), 1085 (m), 1010 (w), 1942(w), 907 (w), 862 (w), 763 (st), 742 (m), 698 (m), 533 (st).
A margem de erro para todas as faixas de absorção de ATR-IR é de ±2 cm'1.
As intensidades das faixas de absorção são indicadas como se-gue: (w) = fraca; (m) = média; e (st) = Intensidade forte.
O espectro Raman da amostra avaliada por espectrômetro Raman dispersivo com 785 nm de fonte de excitação a laser (Kaiser Optical Systems, Inc.) exibe as seguintes faixas significantes expressas em números de onda recíproca (cm'1): 3061 (m), 2930 (m, amplo), 1612 (st), 1523 (m), 1461 (w), 1427 (w), 1287 (st), 1195 (w), 1108 (w), 11053 (w), 1041 (w), 1011 (w), 997 (m), 866(w), 850 (w), 822 (w), 808 (w), 735 (w), 715 (w), 669 (w), 643 (w), 631 (w), 618 (w), 602 (w), 557 (w), 522 (w), 453 (w), 410 (w), 328 (w).
A margem de erro para todas as faixas Raman é de ± 2 cm'1.
As intensidades das faixas de absorção são indicadas como se-gue: (w) = fraca; (m) = média; e (st) = Intensidade forte.
As amostras são investigadas por espectroscopia de 13C RMN de alta resolução CP-MAS (Cross Polarization Magic Angle Spinning) em- pregando-se um espectrômetro de RMN Bruker-BioSpin AVANCE 500 equi-pado com urn 1H de alta potência de 300 Watt, dois amplificadores X de alta potência de 500 Watt, pré-amplificadores de alta potência necessários, um controlador "MAS" e uma sonda Bruker de alta resolução de 4 mm BioSolids.
Cada amostra é acondicionada em um rotor de 4 mm ZrO2. Os parâmetros experimentais críticos são 3 msec de tempo de contato 13C, velocidade giratória 12 KHz no ângulo mágico, um tempo de contato "de rampa", empregando-se um esquema de desacoplagem 1H "SPINAL64", um retardo de reciclo de 10 segundos e 1024 varreduras em 293 graus K. As alterações químicas são referenciadas com respeito a uma Glicina carbonil ex- tema a 176,04 ppm. 13C RMN de alta resolução CP-MAS exibe os seguintes picos significantes (ppm): 179,0, 177,9 177,0, 176,7, 162,0, 141,0, 137,2, 129,6, 129,1, 126,7, 125,3, 64,0, 61,5, 60,4, 50,2, 46,4, 40,6, 38,6, 33,5, 32,4, 29,8, 28,7, 22,3, 20,2, 19,1, 17,8, 16,8, 13,1, 12,1,11,1.
Uma mistura física de sais de Na individuais de Valsartan e éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil- pentanóico revelou uma mistura inerte simples dos dois sais. Entretanto, a amostra do complexo preparada no Exemplo 1 exibiu características espectrais nitidamente diferentes em comparação com uma mistura 1:1 do sais de sódio.
Como avaliado por calorimetria de varredura diferencial (DSC) empregando-se o instrumento Q1000 (TA Instruments), a temperatura de início de fusão e a temperatura máxima de pico para a amostra é observada a 139°C e 145°C, respectivamente.
Como mostrado por DSC e análise termogravimétrica (TGA), em aquecimento, a água de hidratação é liberada em duas etapas: a primeira etapa ocorre abaixo de 100 °C e a segunda etapa acima de 120 °C.
Ambos os instrumentos DSC e TGA são operados em uma taxa de aquecimento de 10 K/minuto.
O pró-fármaco ligado do sal de cálcio de valsartan e o éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil- pentanóico é preparada em temperatura ambiente dissolvendo-se 114 mg do sal de cálcio de valsartan e 86 mg de ácido livre de éster de etila de ácido (2R,4S)-5-bifenil-4-il-5-(3-carbóxi-propionilamino)-2-metil-pentanóico em 2 mL de metanol, seguido por evaporação de metanol. O resíduo de sólido transparente é em seguida carregado com 3 mL de acetonitrilo e equilibrado por 10 minutos. Sonicação, seguida por 20 horas de agitação magnética. Aproximadamente 120 mg de sólidos brancos são coletados por filtragem. A cromatografia líquida (LC) e a análise elementar indicam relação de 1:1 entre éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2- metil-pentanóico e valsartan. A amostra é amorfa por difração de pó de raio X.
O pró-fármaco ligado de sal de cálcio de valsartan e éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil- pentanóico e Tris é preparado em temperatura ambiente dissolvendo-se 57 mg do sal de cálcio de valsartan, 43 mg de ácido livre de éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3-carbóxi-propionilamino)-2-metil-pentanóico, e 12,6 mg de tns(hidroximetil)aminometano (Tris) em 2 mL de metanol, seguido por evaporação de metanol. O resíduo sólido transparente é em seguida carregado com 3 mL de acetonitrila e equilibrado por 10 minutos de sonicação, seguido por 20 horas de agitação magnética. Aproximadamente 83 mg dos sólidos brancos são coletados por filtragem. LC e análise elementar indicam relação de 1:1 entre éster de etila de ácido (2R,4S)-5-bifenil4-il-5-(3- carbóxi-propionilamino)-2-metil-pentanóico e valsartan. A amostra é amorfa por difração de pó de raio X.
Enquanto a invenção foi descrita acima com referência às moda-lidades específicas desta, é evidente que muitas mudanças, modificações e variações podem ser feitas sem divergir do conceito inventivo descrito aqui. Conseqüentemente, é pretendido abranger todas tais alterações, modificações e variações que incluem-se no espírito e amplo escopo das reivindicações anexas. Todos os pedidos de patente, patentes, e outras publicações citadas aqui são incorporadas por referência em sua totalidade.
Claims (18)
1. Composto, caracterizado pelo fato de ser hemipentaidrato de [3-((1S,3R)-1-bifenil-4-ilmetil-3-etoxicarbonil-1-butilcarbamoil)propionato-(S)- 3,-metil-2'-(pentanoil{2"-(tetrazol-5-ilato)bifenil-4,-ilmetil}amino)butirato] de trissódio.
2. Composto, de acordo com a reivindicação 1, caracterizado pelo fato de que está na forma cristalina.
3. Composto, de acordo com a reivindicação 1 ou 2, caracterizado pelo fato de que apresenta uma unidade assimétrica compreendendo seis unidades de fórmula de CAβHssNβOβNaa • 2,5 H2O.
4. Composto, de acordo com qualquer uma das reivindicações 1 a 3, caracterizado por um espectro Infravermelho de Transformada de Fourier de Reflexão Total Atenuada (ATR-FTIR) apresentando as seguintes faixas de absorção expressas em números de onda recíproca (cm1)( ± 2 cnr 1): 1711 (st), 1637 (st), 1597 (st), 1401 (st).
5. Composto, de acordo com a reivindicação 4, caracterizado por um espectro Infravermelho de Transformada de Fourier de Reflexão Total Atenuada (ATR-FTIR) apresentando as seguintes faixas de absorção expressas em números de onda recíproca (cnrr1)( ± 2 cm1): 2956 (w), 1711 (st), 1637 (st), 1597 (st), 1488 (w), 1459 (m), 1401 (st), 1357 (w), 1295 (m), 1266 (m), 1176 (w), 1085 (m), 1010 (w), 942(w), 907 (w), 862 (w), 763 (st), 742 (m), 698 (m), 533 (st).
6. Composto, de acordo com qualquer uma das reivindicações 1 a 5, caracterizado por um padrão de difração de pó de raio X tomado com um difractômetro de pó Scintag XDS2000 compreendendo os seguintes intervalos de plano intertreliça: d em [ Â ] (± 0,1 A): 21,2(s), 17,0(w), 7,1 (s), 5,2(w), 4,7(w), 4,6(w), 4,2(w), 3,5(w), 3,3(w).
7. Composição farmacêutica, caracterizada pelo fato de que compreende: (a) o composto, como definido em qualquer uma das reivindicações 1 a 6; e (b) um aditivo farmaceuticamente aceitável.
8. Composição farmacêutica, de acordo com a reivindicação 7, caracterizada pelo fato de que o aditivo farmaceuticamente aceitável é selecionado do grupo consistindo em diluentes ou cargas, desintegrantes, deslizantes, lubrificantes, aglutinantes, colorantes, e combinações destes.
9. Método para preparar o composto, como definido em qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de que compreende as etapas de: (i) dissolver a (S)-/V-valeril-/V-{[2'-(1 /-/-tetrazol-5-il)-bifenil-4-il]- metilj-valina, ou um sal farmaceuticamente aceitável da mesma, e o éster etílico do ácido (2R,4S)-5-bifenil-4-il-4-(3-carboxi-propionilamino)-2-metil- pentanóico, ou um sal farmaceuticamente aceitável do mesmo, em um solvente adequado; (ii) dissolver um composto básico de Na em um solvente adequado; (iii) combinar as soluções obtidas nas etapas (i) e (ii); (iv) precipitar o sólido, e secar o mesmo para obter o composto; ou, alternativamente, obter o composto alterando-se os solventes empregados nas etapas (i) e (ii) por (iva) evaporar a solução resultante à secura; (va) redissolver o sólido em um solvente adequado; (via) precipitar o sólido e secar o mesmo para obter o composto.
10. Método, de acordo com a reivindicação 9, caracterizado pelo fato de que o solvente adequado nas etapas (i) e/ou (iva) é acetona.
11. Método, de acordo com a reivindicação 9 ou 10, caracterizado pelo fato de que o composto básico de Na é NaOH, Na2CO3, NaHCO3, NaOMe, NaOAc ou NaOCHO.
12. Uso do composto, como definido em qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de ser no preparo de um medicamento para o tratamento ou prevenção de uma condição ou doença selecionada do grupo consistindo em hipertensão, insuficiência cardíaca (aguda e crônica), insuficiência cardíaca congestiva, disfunção ventricular esquerda, cardiomiopatia hipertrófica, fibrilação atrial, flutter atrial, remodelagem vascular prejudicial, infarto do miocárdio e suas sequelas, e hipertensão pulmonar primária e secundária.
13. Uso, de acordo com a reivindicação 12, caracterizado pelo fato de que é no tratamento de hipertensão.
14. Uso, de acordo com a reivindicação 12, caracterizado pelo fato de que é para o tratamento de insuficiência cardíaca (aguda e crônica).
15. Composição farmacêutica, caracterizada pelo fato de que compreende (a) o composto, como definido em qualquer uma das reivindicações 1 a 6; (b) amlodipina ou seu sal; e (c) um aditivo farmaceuticamente aceitável.
16. Composição farmacêutica, de acordo com a reivindicação 15, caracterizada pelo fato de que o sal de amlodipina é besilato de amlodipina.
17. Composição farmacêutica, caracterizada pelo fato de que compreende (a) o composto, como definido em qualquer uma das reivindicações 1 a 6; (b) hidroclorotiazida; e (c) um aditivo farmaceuticamente aceitável.
18. Composição farmacêutica, de acordo com qualquer uma das reivindicações 15 a 17, caracterizada pelo fato de que o aditivo farmaceuticamente aceitável é selecionado do grupo consistindo em diluentes ou cargas, desintegrantes, deslizantes, lubrificantes, aglutinantes, colorantes, e combinações destes.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BR122013025375A BR122013025375B8 (pt) | 2005-11-09 | 2006-11-08 | compostos orgânicos, seus métodos de preparo e uso, bem como composições farmacêuticas |
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US73509305P | 2005-11-09 | 2005-11-09 | |
| US60/735,093 | 2005-11-09 | ||
| US73554105P | 2005-11-10 | 2005-11-10 | |
| US60/735,541 | 2005-11-10 | ||
| US78933206P | 2006-04-04 | 2006-04-04 | |
| US60/789,332 | 2006-04-04 | ||
| US82208606P | 2006-08-11 | 2006-08-11 | |
| US60/822,086 | 2006-08-11 | ||
| PCT/US2006/043710 WO2007056546A1 (en) | 2005-11-09 | 2006-11-08 | Pharmaceutical combinations of an angiotensin receptor antagonist and an nep inhibitor |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0605921A2 BRPI0605921A2 (pt) | 2009-05-26 |
| BRPI0605921B1 true BRPI0605921B1 (pt) | 2020-08-18 |
| BRPI0605921B8 BRPI0605921B8 (pt) | 2021-05-25 |
Family
ID=37908343
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0605921A BRPI0605921B8 (pt) | 2005-11-09 | 2006-11-08 | compostos orgânicos, seus métodos de preparo e uso, bem como composições farmacêuticas |
| BR122013025375A BR122013025375B8 (pt) | 2005-11-09 | 2006-11-08 | compostos orgânicos, seus métodos de preparo e uso, bem como composições farmacêuticas |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR122013025375A BR122013025375B8 (pt) | 2005-11-09 | 2006-11-08 | compostos orgânicos, seus métodos de preparo e uso, bem como composições farmacêuticas |
Country Status (36)
| Country | Link |
|---|---|
| US (12) | US8877938B2 (pt) |
| EP (3) | EP2340828B1 (pt) |
| JP (3) | JP4824754B2 (pt) |
| KR (2) | KR101432821B1 (pt) |
| CN (2) | CN102702119B (pt) |
| AR (1) | AR057882A1 (pt) |
| AU (1) | AU2006311481B2 (pt) |
| BR (2) | BRPI0605921B8 (pt) |
| CA (1) | CA2590511C (pt) |
| CY (4) | CY1115004T1 (pt) |
| DK (2) | DK1948158T3 (pt) |
| EC (1) | ECSP14019136A (pt) |
| ES (2) | ES2823749T3 (pt) |
| FR (2) | FR16C0018I2 (pt) |
| GT (1) | GT200700055A (pt) |
| HR (2) | HRP20140274T1 (pt) |
| HU (3) | HUE050870T2 (pt) |
| IL (2) | IL184027A (pt) |
| JO (1) | JO3492B1 (pt) |
| LT (3) | LT2340828T (pt) |
| LU (1) | LUC00195I2 (pt) |
| MA (1) | MA30128B1 (pt) |
| MX (1) | MX2007008075A (pt) |
| MY (1) | MY145462A (pt) |
| NO (3) | NO337288B1 (pt) |
| NZ (2) | NZ600626A (pt) |
| PE (2) | PE20070803A1 (pt) |
| PH (1) | PH12012501539B1 (pt) |
| PL (2) | PL2340828T3 (pt) |
| PT (2) | PT1948158E (pt) |
| RU (1) | RU2503668C2 (pt) |
| SG (1) | SG10201402055YA (pt) |
| SI (2) | SI1948158T1 (pt) |
| TN (1) | TNSN07264A1 (pt) |
| TW (2) | TWI418348B (pt) |
| WO (1) | WO2007056546A1 (pt) |
Families Citing this family (193)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR057882A1 (es) | 2005-11-09 | 2007-12-26 | Novartis Ag | Compuestos de accion doble de bloqueadores del receptor de angiotensina e inhibidores de endopeptidasa neutra |
| WO2007106708A2 (en) * | 2006-03-10 | 2007-09-20 | Novartis Ag | Combinations of the angiotensin ii antagonist valsartan and the nep inhibitor daglutril |
| TW200838501A (en) * | 2007-02-02 | 2008-10-01 | Theravance Inc | Dual-acting antihypertensive agents |
| TWI448284B (zh) | 2007-04-24 | 2014-08-11 | Theravance Inc | 雙效抗高血壓劑 |
| TWI406850B (zh) | 2007-06-05 | 2013-09-01 | Theravance Inc | 雙效苯并咪唑抗高血壓劑 |
| JP2010538071A (ja) | 2007-09-07 | 2010-12-09 | セラヴァンス, インコーポレーテッド | 二重作用性降圧剤 |
| EP3067043B1 (en) * | 2007-11-06 | 2022-11-30 | Novartis AG | Pharmaceutical compositions based on superstructures of angiotensin receptor antagonist/blocker (arb) and neutral endopeptidase (nep) inhibitor |
| JP2011506459A (ja) * | 2007-12-11 | 2011-03-03 | セラヴァンス, インコーポレーテッド | 抗高血圧剤としての二重作用性ベンゾイミダゾール誘導体およびその使用 |
| PE20091364A1 (es) | 2008-01-17 | 2009-10-13 | Novartis Ag | Proceso para la preparacion de inhibidores de nep |
| EP2297113A1 (en) | 2008-04-29 | 2011-03-23 | Theravance, Inc. | Dual-acting antihypertensive agents |
| WO2010011821A2 (en) * | 2008-07-24 | 2010-01-28 | Theravance, Inc. | Dual-acting antihypertensive agents |
| CN103896796B (zh) * | 2009-05-28 | 2016-04-27 | 诺华股份有限公司 | 作为脑啡肽酶抑制剂的取代的氨基丙酸衍生物 |
| EP2435402B1 (en) | 2009-05-28 | 2016-04-13 | Novartis AG | Substituted aminobutyric derivatives as neprilysin inhibitors |
| EP2451782B1 (en) | 2009-07-07 | 2016-11-09 | Theravance Biopharma R&D IP, LLC | Dual-acting pyrazole antihypertensive agents |
| JP2012533626A (ja) | 2009-07-22 | 2012-12-27 | セラヴァンス, インコーポレーテッド | 二重作用オキサゾール降圧剤 |
| EP2281558A1 (en) * | 2009-08-06 | 2011-02-09 | Laboratorios Del. Dr. Esteve, S.A. | Pharmaceutical compounds of O-Desmethyl-Tramadol and COX-inhibitors |
| JO2967B1 (en) | 2009-11-20 | 2016-03-15 | نوفارتس ايه جي | Acetic acid derivatives of carbamoyl methyl amino are substituted as new NEP inhibitors |
| WO2011090929A1 (en) | 2010-01-19 | 2011-07-28 | Theravance, Inc. | Dual-acting thiophene, pyrrole, thiazole and furan antihypertensive agents |
| WO2012027237A1 (en) * | 2010-08-24 | 2012-03-01 | Novartis Ag | Treatment of hypertension and/or prevention or treatment of heart failure in a mammal receiving anti-coagulant therapy |
| BR112013011715A2 (pt) | 2010-11-10 | 2017-10-31 | Theravance Inc | formas cristalinas de um ácido carboxílico bifenil alcoximidazol-1-il metil |
| US8877815B2 (en) * | 2010-11-16 | 2014-11-04 | Novartis Ag | Substituted carbamoylcycloalkyl acetic acid derivatives as NEP |
| US8673974B2 (en) * | 2010-11-16 | 2014-03-18 | Novartis Ag | Substituted amino bisphenyl pentanoic acid derivatives as NEP inhibitors |
| US8586536B2 (en) | 2010-12-15 | 2013-11-19 | Theravance, Inc. | Neprilysin inhibitors |
| ES2548887T3 (es) | 2010-12-15 | 2015-10-21 | Theravance Biopharma R&D Ip, Llc | Inhibidores de neprilisina |
| JP5959066B2 (ja) | 2011-02-17 | 2016-08-02 | セラヴァンス バイオファーマ アール&ディー アイピー, エルエルシー | ネプリライシン阻害剤としての置換アミノ酪酸誘導体 |
| KR101854874B1 (ko) | 2011-02-17 | 2018-05-04 | 세라밴스 바이오파마 알앤디 아이피, 엘엘씨 | 네프릴리신 억제제로서 치환된 아미노부티릭 유도체 |
| KR102158948B1 (ko) | 2011-05-13 | 2020-09-24 | 이비 아이피 하이브리탭스 비.브이. | 약물 전달 시스템 |
| JP5959075B2 (ja) | 2011-05-31 | 2016-08-02 | セラヴァンス バイオファーマ アール&ディー アイピー, エルエルシー | ネプリライシン阻害剤 |
| ES2653215T3 (es) | 2011-05-31 | 2018-02-06 | Theravance Biopharma R&D Ip, Llc | Inhibidores de neprilisina |
| WO2012166389A1 (en) | 2011-05-31 | 2012-12-06 | Theravance, Inc. | Neprilysin inhibitors |
| TWI560172B (en) | 2011-11-02 | 2016-12-01 | Theravance Biopharma R&D Ip Llc | Neprilysin inhibitors |
| TW201336839A (zh) | 2012-02-15 | 2013-09-16 | Theravance Inc | (2s,4r)-5-聯苯-4-基-2-羥甲基-2-甲基-4-[(1h-[1,2,3]三唑-4-羰基)-胺基]-戊酸5-甲基-2-酮基-[1,3]二氧雜環戊烯-4-基甲酯之結晶型 |
| WO2013148768A1 (en) | 2012-03-28 | 2013-10-03 | Theravance, Inc. | Crystalline forms of (r)-3-[n-(3'-chlorobiphenyl-4-ylmethyl)-n'-(3-hydroxyisoxazole-5-carbonyl)hydrazino]-2-hydroxypropionic acid isopropyl ester |
| EP2649996A1 (en) * | 2012-04-11 | 2013-10-16 | Laboratorios Del. Dr. Esteve, S.A. | Crystalline forms of sartans like telmisartan with beta blockers |
| ES2609810T3 (es) | 2012-05-31 | 2017-04-24 | Theravance Biopharma R&D Ip, Llc | Inhibidores de neprilisina donadores de óxido nítrico |
| CN104470521B (zh) | 2012-06-08 | 2017-04-12 | 施万生物制药研发Ip有限责任公司 | 脑啡肽酶抑制剂 |
| MX356260B (es) | 2012-06-08 | 2018-05-21 | Theravance Biopharma R&D Ip Llc | Inhibidores de la neprilisina. |
| MX366149B (es) | 2012-08-08 | 2019-06-28 | Theravance Biopharma R&D Ip Llc | Inhibidores de neprilisina. |
| ES2879550T3 (es) * | 2012-08-24 | 2021-11-22 | Novartis Ag | Inhibidores de epn para tratar enfermedades caracterizadas por la dilatación o remodelación auriculares. |
| US9102635B2 (en) | 2013-02-14 | 2015-08-11 | Novartis Ag | Substituted bisphenyl butanoic acid derivatives as NEP inhibitors with improved in vivo efficacy |
| CU24330B1 (es) | 2013-02-14 | 2018-03-13 | Novartis Ag | Derivados del ácido 4-((1,1) bifenil-4-il)-3-(3-fosfonopropanamido) butanoico, activos como inhibidores de nep (endopeptidasa neutral) |
| CA2902456A1 (en) | 2013-03-05 | 2014-09-12 | Theravance Biopharma R&D Ip, Llc | Neprilysin inhibitors |
| DK3038654T3 (da) | 2013-08-26 | 2020-02-03 | Novartis Ag | Ny anvendelse |
| WO2015030711A1 (en) | 2013-08-26 | 2015-03-05 | Novartis Ag | New use |
| US9585882B2 (en) | 2014-01-30 | 2017-03-07 | Theravance Biopharma R&D Ip, Llc | Neprilysin inhibitors |
| WO2015116786A1 (en) | 2014-01-30 | 2015-08-06 | Theravance Biopharma R&D Ip, Llc | Neprilysin inhibitors |
| CN106414416B (zh) * | 2014-09-09 | 2020-03-27 | 上海翰森生物医药科技有限公司 | 结晶型ARB-NEPi复合物及其制备方法和应用 |
| CN105461647B (zh) * | 2014-09-28 | 2018-06-29 | 四川海思科制药有限公司 | 缬沙坦沙库比曲三钠盐复合物的固态形式及其制备方法和用途 |
| CN105503760A (zh) * | 2014-10-10 | 2016-04-20 | 上海翰森生物医药科技有限公司 | 结晶型ARB-NEPi双阳离子复合物及其制备方法和应用 |
| WO2016074651A1 (en) | 2014-11-14 | 2016-05-19 | Zentiva, K.S. | A method for the preparation, isolation and purification of pharmaceutically applicable forms of ahu-377 |
| PL3229799T3 (pl) | 2014-12-08 | 2019-05-31 | Crystal Pharmatech Co Ltd | Krystaliczne postacie supramolekularnego kompleksu trisodowego zawierającego walsartan i AHU-377 i ich sposoby |
| CN105693543B (zh) * | 2014-12-15 | 2018-08-10 | 四川海思科制药有限公司 | 沙库比曲类衍生物、其药物组合物、制备方法及用途 |
| WO2016051393A2 (en) * | 2014-12-26 | 2016-04-07 | Crystal Pharmatech Inc. | Crystalline form iv of trisodium supramolecular complex comprising valsartan and ahu-377 and methods thereof |
| CN104473938B (zh) * | 2014-12-30 | 2017-06-09 | 北京瑞都医药科技有限公司 | 一种治疗慢性心衰药物及其制备方法 |
| WO2016116942A1 (en) | 2015-01-20 | 2016-07-28 | Anlon Chemical Research Organization | Novel pharmaceutical compounds comprising ticagrelor with salts of aspirin |
| CN105982891A (zh) * | 2015-01-30 | 2016-10-05 | 王召印 | 阿利沙坦脂和脑啡肽酶抑制剂或其前药的药物组合物 |
| US10562866B2 (en) * | 2015-02-06 | 2020-02-18 | Mylan Laboratories Limited | Amorphous trisodium sacubitril valsartan and a process for the preparation thereof |
| KR102640906B1 (ko) | 2015-02-11 | 2024-02-27 | 세라밴스 바이오파마 알앤디 아이피, 엘엘씨 | 네프릴리신 저해제로서 (2s,4r)-5-(5''-클로로-2''-플루오로비페닐-4-일)-4-(에톡시옥살릴아미노)-2-히드록시메틸-2-메틸펜타노익산 |
| CN105985225A (zh) * | 2015-02-12 | 2016-10-05 | 博瑞生物医药(苏州)股份有限公司 | 一种lcz-696及其中间体的制备方法 |
| CN105884644B (zh) * | 2015-02-15 | 2020-06-09 | 深圳信立泰药业股份有限公司 | 一种中性内肽酶抑制剂盐优势形态及其制备方法 |
| CN107250119B (zh) | 2015-02-19 | 2020-09-22 | 施万生物制药研发Ip有限责任公司 | (2r,4r)-5-(5′-氯-2′-氟联苯-4-基)-2-羟基-4-[(5-甲基恶唑-2-羰基)氨基]戊酸 |
| CN106032361A (zh) * | 2015-03-11 | 2016-10-19 | 齐鲁制药有限公司 | Lcz-696的新晶型及其制备方法 |
| CN110801452B (zh) * | 2015-03-12 | 2023-01-13 | 深圳信立泰药业股份有限公司 | 一种含有阿利沙坦酯水解产物或其水解产物盐的药物组合物及其用途 |
| CA2980224C (en) * | 2015-03-20 | 2019-06-25 | Crystal Pharmatech Co., Ltd. | Crystalline form of ahu377, preparation method and use thereof |
| WO2016151525A1 (en) * | 2015-03-26 | 2016-09-29 | Dr. Reddy’S Laboratories Limited | Crystalline form of lcz-696 |
| EP4212152B1 (en) | 2015-05-11 | 2025-04-30 | Novartis AG | Sacubitril-valsartan dosage regimen for treating chronic systolic heart failure |
| US20180140579A1 (en) | 2015-05-29 | 2018-05-24 | Novartis Ag | Sacubitril and valsartan for treating metabolic disease |
| CN104860894B (zh) * | 2015-06-10 | 2017-05-17 | 北京博全健医药科技有限公司 | 一种抗心衰药lcz696的制备方法 |
| KR102254062B1 (ko) * | 2015-06-12 | 2021-05-20 | 테바 파마슈티컬스 인터내셔널 게엠베하 | 삼나트륨 발사르탄:사쿠비트릴의 고체 형태 |
| WO2016203500A2 (en) | 2015-06-19 | 2016-12-22 | Actavis Group Ptc Ehf. | Preparation of sacubitril or salt thereof and novel intermediates in the preparation of sacubitril |
| SI3317248T1 (sl) * | 2015-07-02 | 2021-01-29 | Novartis Ag | Sakubitril kalcijeve soli |
| CN106316973A (zh) * | 2015-07-07 | 2017-01-11 | 江苏柯菲平医药股份有限公司 | 血管紧张素受体拮抗剂和nep抑制剂药物晶型及其制备 |
| WO2017006254A1 (en) | 2015-07-08 | 2017-01-12 | Novartis Ag | Drug combination comprising an angiotensin ii receptor antagonist, a neutral endopeptidase inhibitor and a mineralcorticoid receptor antagonist |
| CN106176723A (zh) * | 2015-07-11 | 2016-12-07 | 凌莉 | 一种固体药物组合物及其制备方法 |
| CN106176725A (zh) * | 2015-07-11 | 2016-12-07 | 凌莉 | 一种提高稳定性的药物组合物及其制备方法和用途 |
| CN106074421A (zh) * | 2015-07-11 | 2016-11-09 | 凌莉 | 一种提高稳定性的药物组合物 |
| CN106176654A (zh) * | 2015-07-11 | 2016-12-07 | 凌莉 | 含有化合物a的固体药物组合物及其制备方法 |
| WO2017009784A1 (en) * | 2015-07-14 | 2017-01-19 | Cadila Healthcare Limited | Solid state forms of trisodium salt of valsartan/sacubitril complex and sacubitril |
| EP3117823A1 (en) | 2015-07-17 | 2017-01-18 | Quimica Sintetica, S.A. | Amorphous solid dispersion comprising an angiotensin receptor blocker and a neutral endopeptidase inhibitor |
| WO2017012600A1 (en) | 2015-07-20 | 2017-01-26 | Zentiva, K.S. | A pharmaceutical composition containing valsartan and sacubitril and methods for preparation and stabilization thereof |
| WO2017013010A1 (de) | 2015-07-23 | 2017-01-26 | Bayer Pharma Aktiengesellschaft | Stimulatoren und/oder aktivatoren der löslichen guanylatzyklase (sgc) in kombination mit einem inhibitor der neutralen endopeptidase (nep inhibitor) und/oder einem angiotensin aii-antagonisten und ihre verwendung |
| CN106397248A (zh) * | 2015-08-03 | 2017-02-15 | 深圳信立泰药业股份有限公司 | 一种lcz696结晶粉末及其制备方法 |
| CN105168205A (zh) * | 2015-08-18 | 2015-12-23 | 泰力特医药(湖北)有限公司 | 一种血管紧张素ii受体和脑啡肽酶受体双重抑制剂lcz696的制备方法 |
| WO2017033212A1 (en) * | 2015-08-26 | 2017-03-02 | Actavis Group Ptc Ehf. | Preparation of sacubitril and salt thereof and novel compounds used in the process |
| ES2966924T3 (es) | 2015-08-28 | 2024-04-25 | Hetero Labs Ltd | Procedimiento para la preparación de un compuesto inhibidor de neprilisina-receptor de angiotensina de doble acción |
| WO2017037596A1 (en) * | 2015-08-28 | 2017-03-09 | Dr. Reddy's Laboratories Limited | Amorphous solid dispersion of lcz-696 |
| EP3355880A1 (en) | 2015-08-28 | 2018-08-08 | Novartis AG | New use |
| WO2017042700A1 (en) * | 2015-09-07 | 2017-03-16 | Sun Pharmaceutical Industries Limited | Solid forms of valsartan and sacubitril |
| WO2017051326A1 (en) | 2015-09-23 | 2017-03-30 | Novartis Ag | New processes and intermediates useful in synthesis of nep inhibitors |
| CN106580908A (zh) * | 2015-10-16 | 2017-04-26 | 深圳信立泰药业股份有限公司 | 一种用于心血管疾病治疗的口服制剂及其制备方法 |
| CN105669581B (zh) * | 2015-11-09 | 2017-03-22 | 成都苑东生物制药股份有限公司 | 一种血管紧张受体拮抗剂和中性内肽酶抑制剂复合物 |
| WO2017085573A1 (en) | 2015-11-20 | 2017-05-26 | Lupin Limited | Amorphous sacubitril-valsartan complex and process for preparation thereof |
| CN105330609B (zh) * | 2015-12-07 | 2017-12-22 | 南京正大天晴制药有限公司 | 一种制备lcz696的方法 |
| CN106854187B (zh) * | 2015-12-08 | 2020-04-14 | 苏州晶云药物科技股份有限公司 | 一种ahu-377和缬沙坦三钠盐共晶水合物晶型ii的制备方法 |
| CN105348209B (zh) * | 2015-12-09 | 2017-12-26 | 浙江天宇药业股份有限公司 | 一种抗心衰药lcz696的制备方法 |
| EP3386945A1 (en) | 2015-12-11 | 2018-10-17 | Zentiva, K.S. | Solid forms of (2r,4s)-5-(biphenyl-4-yl)-4-[(3-carboxypropionyl)amino]-2- -methylpentanoic acid ethyl ester, its salts and a preparation method |
| CN106905253B (zh) * | 2015-12-23 | 2020-01-03 | 正大天晴药业集团股份有限公司 | 一种超分子复合物的结晶 |
| CN105622535B (zh) * | 2015-12-28 | 2018-08-03 | 重庆两江药物研发中心有限公司 | 一种lcz696的制备方法 |
| RS66618B1 (sr) * | 2016-01-20 | 2025-04-30 | Shenzhen Salubris Pharm Co Ltd | Kompozit metabolita antagonista receptora angiotenzina ii i inhibitora nep i postupak za njegovu pripremu |
| CN105646384A (zh) * | 2016-01-27 | 2016-06-08 | 北京沃邦医药科技有限公司 | 一种脑啡肽酶抑制剂与血管紧张素ⅱ受体拮抗剂共晶化合物的精制方法 |
| ES3036922T3 (en) | 2016-02-03 | 2025-09-25 | Novartis Ag | New use of a combination of sacubitril and valsartan |
| CN107033094A (zh) * | 2016-02-04 | 2017-08-11 | 南京卡文迪许生物工程技术有限公司 | 一种药物共晶的晶型及其制备方法和组合物 |
| WO2017141193A1 (en) * | 2016-02-16 | 2017-08-24 | Sun Pharmaceutical Industries Limited | Process for the preparation of sacubitril or salts thereof |
| US10703731B2 (en) * | 2016-03-07 | 2020-07-07 | Msn Laboratories Private Limited | Process for the preparation of Trisodium (4- {[1S,3R)-1-([1,1′-biphenyl]-4-ylmethyl)-4-ethoxy-3-methyl-4-oxobutyl]amino}-4-oxobutanoate)-(N-petanoyl-N-{[2′-(1H-tetrazol-1-1D-5-yl)[1,1′-biphenyl]-4-yl]methyl}- L-valinate) and its polymorphs thereof |
| SMT202100434T1 (it) | 2016-03-08 | 2021-09-14 | Theravance Biopharma R&D Ip Llc | Acido (2s,4r)-5-(5’-cloro-2-fluoro-[1,1’-bifenil]-4-il)-2-(etossimetil)-4-(3-idrossiisossazol-5-carbossammido)-2-metilpentanoico cristallino e suoi usi |
| WO2017191619A2 (en) * | 2016-05-06 | 2017-11-09 | Sun Pharmaceutical Industries Limited | A process for the preparation of a salt of sacubitril and valsartan |
| WO2017191620A1 (en) * | 2016-05-06 | 2017-11-09 | Sun Pharmaceutical Industries Limited | A crystalline form of a salt of sacubitril and a process of its preparation |
| EP3248592A1 (en) | 2016-05-25 | 2017-11-29 | EB IP Hybritabs B.V. | Process for the preparation of drug delivery systems having a testosterone compound present in an outer layer or part, as well as such drug delivery systems |
| CN109415308B (zh) | 2016-07-05 | 2022-09-06 | 诺华股份有限公司 | 用于早期沙卡布曲中间体的新方法 |
| CN106177960B (zh) * | 2016-08-01 | 2019-01-08 | 珠海赛隆药业股份有限公司(长沙)医药研发中心 | 血管紧张素受体拮抗剂和脑啡肽酶抑制剂的复合物及其用途 |
| US10851059B2 (en) | 2016-08-17 | 2020-12-01 | Novartis Ag | Processes and intermediates for NEP inhibitor synthesis |
| CN109641856B (zh) * | 2016-09-02 | 2022-09-30 | 南京诺瑞特医药科技有限公司 | 缬沙坦二钠盐的晶型 |
| WO2018069833A1 (en) | 2016-10-10 | 2018-04-19 | Laurus Labs Limited | Stable amorphous form of sacubitril valsartan trisodium complex and processes for preparation thereof |
| WO2018069937A1 (en) | 2016-10-13 | 2018-04-19 | Mylan Laboratories Limited | Solid dispersions of trisodium sacubitril valsartan and process for the preparation thereof |
| WO2018078592A1 (en) | 2016-10-28 | 2018-05-03 | Biocon Limited | Amorphous trisodium sacubitril valsartan and process for its preparation |
| CN106518709A (zh) * | 2016-11-07 | 2017-03-22 | 济南益新医药技术有限公司 | 一种无定形沙库比曲缬沙坦钠盐复合物的制备方法 |
| JP7138106B2 (ja) | 2016-12-23 | 2022-09-15 | ノバルティス アーゲー | 初期サクビトリル中間体のための新規な方法 |
| WO2018119178A1 (en) * | 2016-12-23 | 2018-06-28 | StemBios Technologies, Inc. | Use of somatic stem cells for decreasing neprilysin level |
| CN106674206B (zh) * | 2016-12-30 | 2021-01-19 | 顾国明 | 一种治疗心衰的共晶体药物 |
| CN111592500A (zh) * | 2017-01-03 | 2020-08-28 | 上海博志研新药物技术有限公司 | ARB-NEPi复合物、晶型、制备方法及应用 |
| CN106800537B (zh) * | 2017-01-18 | 2019-02-01 | 广东隆赋药业股份有限公司 | 丁苯酞-替米沙坦杂合物及其制备方法和用途 |
| WO2018153895A1 (de) | 2017-02-22 | 2018-08-30 | Bayer Pharma Aktiengesellschaft | Selektive partielle adenosin a1 rezeptor-agonisten in kombination mit einem inhibitor der neutralen endopeptidase und/oder einem angiotensin ii rezeptor-antagonisten |
| WO2018178295A1 (en) | 2017-03-31 | 2018-10-04 | Alfred E. Tiefenbacher (Gmbh & Co. Kg) | Stable hot-melt extrudate containing valsartan and sacubitril |
| WO2018211479A1 (en) * | 2017-05-19 | 2018-11-22 | Lupin Limited | Stabilized compositions of angiotensin ii inhibitors and neutral endopeptidase inhibitors and process for preparation thereof |
| WO2019008485A1 (en) | 2017-07-06 | 2019-01-10 | Mankind Pharma Ltd | FIXED DOSE PHARMACEUTICAL COMPOSITION BASED ON VALSARTAN AND SACUBITRIL |
| MX391562B (es) * | 2017-07-28 | 2025-03-21 | Synthon Bv | Composicion farmaceutica que comprende sacubitril y valsartan |
| US10510575B2 (en) | 2017-09-20 | 2019-12-17 | Applied Materials, Inc. | Substrate support with multiple embedded electrodes |
| US20200276129A1 (en) | 2017-10-13 | 2020-09-03 | Alfred E. Tiefenbacher (Gmbh & Co. Kg) | Tablet containing valsartan and sacubitril |
| CN107935958B (zh) * | 2017-11-30 | 2021-02-09 | 中国药科大学 | 一种缬沙坦葛根素钠盐复合物及其制备方法 |
| UY38072A (es) | 2018-02-07 | 2019-10-01 | Novartis Ag | Compuestos derivados de éster butanoico sustituido con bisfenilo como inhibidores de nep, composiciones y combinaciones de los mismos |
| US10555412B2 (en) | 2018-05-10 | 2020-02-04 | Applied Materials, Inc. | Method of controlling ion energy distribution using a pulse generator with a current-return output stage |
| WO2019239432A1 (en) | 2018-06-14 | 2019-12-19 | Cipla Limited | Trisodium sacubitril valsartan complex and hot-melt extruded pharmaceutical composition comprising thereof |
| GB201810326D0 (en) | 2018-06-22 | 2018-08-08 | Johnson Matthey Plc | Crystalline form of sacubitril, its preparation and use |
| EP3840746A1 (en) | 2018-08-23 | 2021-06-30 | Novartis AG | New pharmaceutical use for the treatment of heart failure |
| WO2020039394A1 (en) | 2018-08-24 | 2020-02-27 | Novartis Ag | New drug combinations |
| CN109265406B (zh) * | 2018-09-03 | 2020-09-22 | 石药集团中奇制药技术(石家庄)有限公司 | 一种沙库巴曲缬沙坦钠新晶型及其制备方法和用途 |
| US11476145B2 (en) | 2018-11-20 | 2022-10-18 | Applied Materials, Inc. | Automatic ESC bias compensation when using pulsed DC bias |
| KR20200073676A (ko) | 2018-12-14 | 2020-06-24 | 엠에프씨 주식회사 | 발사탄 및 사쿠비트릴을 포함하는 고체 분산체 및 이를 포함하는 약학 조성물 및 이의 제조 방법 |
| JP7451540B2 (ja) | 2019-01-22 | 2024-03-18 | アプライド マテリアルズ インコーポレイテッド | パルス状電圧波形を制御するためのフィードバックループ |
| US11508554B2 (en) | 2019-01-24 | 2022-11-22 | Applied Materials, Inc. | High voltage filter assembly |
| CN109912525A (zh) * | 2019-03-13 | 2019-06-21 | 陈文辉 | 一种lcz696新晶型及其制备方法 |
| KR102543230B1 (ko) | 2019-05-24 | 2023-06-14 | 주식회사 파마코스텍 | 발사르탄/사쿠비트릴 3소듐염 수화물의 결정형 및 그 제조방법 |
| WO2020238885A1 (zh) * | 2019-05-30 | 2020-12-03 | 深圳信立泰药业股份有限公司 | 血管紧张素ii受体拮抗剂代谢产物与nep抑制剂的复合物的治疗方法 |
| CN114452287B (zh) * | 2019-05-30 | 2023-05-12 | 深圳信立泰药业股份有限公司 | 血管紧张素ii受体拮抗剂代谢产物与nep抑制剂的复合物的新用途 |
| EP3766484B1 (en) | 2019-07-19 | 2021-08-25 | Zentiva, K.S. | Solid pharmaceutical dosage form comprising valsartan and sacubitril |
| KR102752382B1 (ko) | 2019-09-20 | 2025-01-09 | 심천 사루브리스 퍼머수티칼스 컴퍼니 리미티드 | 안지오텐신 ii 수용체 길항제 대사물질 및 nep 억제제의 복합체의 심부전 치료에서의 용도 |
| WO2021126884A1 (en) | 2019-12-16 | 2021-06-24 | Tenax Therapeutics, Inc. | LEVOSIMENDAN FOR TREATING PULMONARY HYPERTENSION WITH HEART FAILURE WITH PRESERVED EJECTION FRACTION (PH-HF-pEF) |
| WO2021143898A1 (zh) * | 2020-01-19 | 2021-07-22 | 深圳信立泰药业股份有限公司 | Arb代谢产物与nep抑制剂的复合物新晶型及其制备方法 |
| KR102149126B1 (ko) * | 2020-02-05 | 2020-08-28 | 유니셀랩 주식회사 | 새로운 사쿠비트릴 칼슘/발사르탄 공결정 |
| KR20200020746A (ko) | 2020-02-07 | 2020-02-26 | 보령제약 주식회사 | 하이브리드 화합물 및 그 제조방법 |
| KR20210101164A (ko) | 2020-02-07 | 2021-08-18 | 보령제약 주식회사 | 하이브리드 화합물 및 그 제조방법 |
| CN111253330B (zh) * | 2020-02-29 | 2023-01-24 | 广州白云山天心制药股份有限公司 | 沙坦类药物的新晶型及其制备方法和用途 |
| KR20210120560A (ko) | 2020-03-27 | 2021-10-07 | 주식회사 유영제약 | 고함량의 주성분을 포함하는 정제 및 그 제조방법 |
| KR102155474B1 (ko) | 2020-04-28 | 2020-09-11 | 유니셀랩 주식회사 | 사쿠비트릴/발사르탄 공동무정형 |
| JP7064527B2 (ja) * | 2020-05-01 | 2022-05-10 | ノバルティス アーゲー | サクビトリルカルシウム塩 |
| CN116036079B (zh) * | 2020-06-18 | 2026-03-06 | 深圳信立泰药业股份有限公司 | 一种复合物的药物组合物及其制备方法 |
| KR20220012821A (ko) | 2020-07-23 | 2022-02-04 | 주식회사 종근당 | 이중 작용 복합 화합물의 결정형 및 이의 제조방법 |
| KR102215623B1 (ko) * | 2020-07-24 | 2021-02-15 | 유니셀랩 주식회사 | 사쿠비트릴 칼슘염 및 사쿠비트릴 유리염기와 발사르탄을 공동분자로 사용한 새로운 신규 공결정 형태 |
| US11462389B2 (en) | 2020-07-31 | 2022-10-04 | Applied Materials, Inc. | Pulsed-voltage hardware assembly for use in a plasma processing system |
| TWI894333B (zh) * | 2020-08-17 | 2025-08-21 | 大陸商深圳信立泰藥業股份有限公司 | 血管收縮素ii受體拮抗劑代謝產物與nep抑制劑的複合物用於心臟衰竭的應用 |
| KR102858594B1 (ko) | 2020-10-08 | 2025-09-11 | 한미약품 주식회사 | 사쿠비트릴 및 발사르탄 나트륨염을 포함하는 경구용 고형제제 |
| US11798790B2 (en) | 2020-11-16 | 2023-10-24 | Applied Materials, Inc. | Apparatus and methods for controlling ion energy distribution |
| US11901157B2 (en) | 2020-11-16 | 2024-02-13 | Applied Materials, Inc. | Apparatus and methods for controlling ion energy distribution |
| TWI905319B (zh) * | 2020-11-25 | 2025-11-21 | 大陸商深圳信立泰藥業股份有限公司 | Arb代謝產物與nep抑制劑的複合物在製備用於預防和/或治療腎病的藥物中的用途 |
| KR20220091767A (ko) | 2020-12-24 | 2022-07-01 | 주식회사 보령 | 사쿠비트릴 발사르탄 하이브리드 화합물 또는 그 약제학적으로 허용되는 염을 유효성분으로 포함하는 약제학적 조성물 |
| KR102486815B1 (ko) | 2021-01-20 | 2023-01-10 | 주식회사 대웅제약 | Nep 저해제 및 arb를 포함하는 약학 조성물 및 이의 제조 방법 |
| US11495470B1 (en) | 2021-04-16 | 2022-11-08 | Applied Materials, Inc. | Method of enhancing etching selectivity using a pulsed plasma |
| WO2022224274A1 (en) | 2021-04-20 | 2022-10-27 | Mylan Laboratories Limited | Polymorphic forms of sacubitril-telmisartan (1:1) |
| US11948780B2 (en) | 2021-05-12 | 2024-04-02 | Applied Materials, Inc. | Automatic electrostatic chuck bias compensation during plasma processing |
| US11791138B2 (en) | 2021-05-12 | 2023-10-17 | Applied Materials, Inc. | Automatic electrostatic chuck bias compensation during plasma processing |
| US11967483B2 (en) | 2021-06-02 | 2024-04-23 | Applied Materials, Inc. | Plasma excitation with ion energy control |
| US12525441B2 (en) | 2021-06-09 | 2026-01-13 | Applied Materials, Inc. | Plasma chamber and chamber component cleaning methods |
| US12148595B2 (en) | 2021-06-09 | 2024-11-19 | Applied Materials, Inc. | Plasma uniformity control in pulsed DC plasma chamber |
| US12525433B2 (en) | 2021-06-09 | 2026-01-13 | Applied Materials, Inc. | Method and apparatus to reduce feature charging in plasma processing chamber |
| US11810760B2 (en) | 2021-06-16 | 2023-11-07 | Applied Materials, Inc. | Apparatus and method of ion current compensation |
| US11569066B2 (en) | 2021-06-23 | 2023-01-31 | Applied Materials, Inc. | Pulsed voltage source for plasma processing applications |
| US11776788B2 (en) | 2021-06-28 | 2023-10-03 | Applied Materials, Inc. | Pulsed voltage boost for substrate processing |
| KR102756994B1 (ko) | 2021-07-22 | 2025-01-22 | 대봉엘에스 주식회사 | 사쿠비트릴, 발사르탄, 및 니코틴아미드의 공동무정형 |
| KR102399717B1 (ko) | 2021-08-10 | 2022-05-19 | 대봉엘에스 주식회사 | 사쿠비트릴 및 아질사르탄 복합 약제학적 조성물, 및 이의 제조방법 |
| US11476090B1 (en) | 2021-08-24 | 2022-10-18 | Applied Materials, Inc. | Voltage pulse time-domain multiplexing |
| CN120661504A (zh) * | 2021-08-26 | 2025-09-19 | 深圳信立泰药业股份有限公司 | 一种ARNi与钙离子拮抗剂的药物组合物与应用 |
| US12106938B2 (en) | 2021-09-14 | 2024-10-01 | Applied Materials, Inc. | Distortion current mitigation in a radio frequency plasma processing chamber |
| US11694876B2 (en) | 2021-12-08 | 2023-07-04 | Applied Materials, Inc. | Apparatus and method for delivering a plurality of waveform signals during plasma processing |
| EP4456897A4 (en) | 2021-12-31 | 2025-12-10 | Tenax Therapeutics Inc | ORAL FORMULATIONS OF LEVOSIMENDAN FOR THE TREATMENT OF PULMONARY HYPERTENSION WITH HEART FAILURE AND PRESERVED EJECTION FRACTION |
| US11972924B2 (en) | 2022-06-08 | 2024-04-30 | Applied Materials, Inc. | Pulsed voltage source for plasma processing applications |
| US12315732B2 (en) | 2022-06-10 | 2025-05-27 | Applied Materials, Inc. | Method and apparatus for etching a semiconductor substrate in a plasma etch chamber |
| US12586768B2 (en) | 2022-08-10 | 2026-03-24 | Applied Materials, Inc. | Pulsed voltage compensation for plasma processing applications |
| US12272524B2 (en) | 2022-09-19 | 2025-04-08 | Applied Materials, Inc. | Wideband variable impedance load for high volume manufacturing qualification and on-site diagnostics |
| US12111341B2 (en) | 2022-10-05 | 2024-10-08 | Applied Materials, Inc. | In-situ electric field detection method and apparatus |
| WO2024210557A1 (ko) | 2023-04-05 | 2024-10-10 | 한미약품 주식회사 | 개선된 안정성과 용출률이 확보된 사쿠비트릴-발사르탄 및 sglt-2 억제제를 포함하는 복합제제 |
| CN116687921A (zh) * | 2023-06-14 | 2023-09-05 | 宁波大学 | 沙库巴曲缬沙坦类物质在制备神经毒性和认知障碍类药物的应用 |
| KR20250066976A (ko) * | 2023-11-07 | 2025-05-14 | 주식회사 노브메타파마 | 아연염 및 사이클로-히스프로를 유효성분으로 포함하는 당뇨병성 신증의 예방, 개선 또는 치료용 조성물 |
| EP4652990A1 (en) | 2024-05-24 | 2025-11-26 | Genepharm S.A. | A solid composition package of valsartan and sacubitril |
Family Cites Families (94)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2499058A (en) | 1950-02-28 | B-haloxantfflne salts of diarylalkyl | ||
| US1954909A (en) | 1929-11-14 | 1934-04-17 | Adler Oscar | Processes for the producing of molecular compounds of the salts of phenyl-quinolinecarboxylic acids with alkylated pyrazolones and alkylated amino-pyrazolones |
| NL76613C (pt) | 1948-07-01 | |||
| US2534813A (en) | 1950-01-21 | 1950-12-19 | Searle & Co | 8-haloxanthine salts of cyclic-aminoalkyl benzohydryl ethers and the production thereof |
| US3057731A (en) | 1958-03-27 | 1962-10-09 | Skanska Attikfabriken Ab | Preparation of bakery products |
| AU538751B2 (en) | 1979-08-20 | 1984-08-23 | Abbott Laboratories | Complex valproate salts |
| US4610816A (en) | 1980-12-18 | 1986-09-09 | Schering Corporation | Substituted dipeptides as inhibitors of enkephalinases |
| DE3116334A1 (de) * | 1981-04-24 | 1982-11-18 | Gefra B.V.,, s'Gravenzande | "vorrichtung zum befestigen einer seitenfuehrung, einer foerdereinrichtung an einer stuetze" |
| ZA84670B (en) | 1983-01-31 | 1985-09-25 | Merck & Co Inc | Thiorphan analogs as enkephalinase and angiotensin converting enzyme inhibitors |
| US4722810A (en) | 1984-08-16 | 1988-02-02 | E. R. Squibb & Sons, Inc. | Enkephalinase inhibitors |
| US4929641B1 (en) | 1988-05-11 | 1994-08-30 | Schering Corp | Mercapto-acylamino acid antihypertensives |
| US4749688A (en) * | 1986-06-20 | 1988-06-07 | Schering Corporation | Use of neutral metalloendopeptidase inhibitors in the treatment of hypertension |
| US4740499A (en) | 1986-07-28 | 1988-04-26 | Monsanto Company | Method of enhancing the bioactivity of atrial peptides |
| GB8811873D0 (en) | 1988-05-19 | 1988-06-22 | Pfizer Ltd | Therapeutic agents |
| GB2218983A (en) | 1988-05-27 | 1989-11-29 | Pfizer Ltd | Spiro-substituted glutaramides as diuretics |
| GB8812597D0 (en) | 1988-05-27 | 1988-06-29 | Pfizer Ltd | Therapeutic agents |
| EP0361365A1 (en) | 1988-09-30 | 1990-04-04 | E.R. SQUIBB & SONS, INC. | Aminobenzoic and aminocyclohexane-carboylic acid compounds, compositions, and their method of use |
| GB8903740D0 (en) | 1989-02-18 | 1989-04-05 | Pfizer Ltd | Therapeutic agents |
| IL97219A (en) * | 1990-02-19 | 1995-12-08 | Ciba Geigy Ag | Biphenyl substituted aliphatic amino compounds process for their preparation and pharmaceutical compositions containing them |
| FR2658571B1 (pt) | 1990-02-21 | 1992-04-24 | Bendix Europ Services Tech | |
| US5223516A (en) * | 1990-03-22 | 1993-06-29 | E. R. Squibb & Sons, Inc. | 3,3,3-trifluoro-2-mercaptomethyl-N-tetrazolyl substituted propanamides and method of using same |
| HUT59656A (en) | 1990-11-15 | 1992-06-29 | Puetter Medice Chem Pharm | Process for producing s/+/-phenyl-alkanoic acids and alpha-amino-acids containing complexes and pharmaceutical compositions containing them as active components |
| AU1256692A (en) | 1991-02-06 | 1992-09-07 | Schering Corporation | Combination of an angiotensin II antagonist or renin inhibitor with a neutral endopeptidase inhibitor |
| GB9103454D0 (en) | 1991-02-19 | 1991-04-03 | Pfizer Ltd | Therapeutic agents |
| EP0509442A1 (en) | 1991-04-16 | 1992-10-21 | Schering Corporation | Use of neutral endopeptidase inhibitors in the treatment of nephrotoxicity |
| US5294632A (en) * | 1991-05-01 | 1994-03-15 | Ciba-Geigy Corporation | Phosphono/biaryl substituted dipetide derivatives |
| US5225401A (en) | 1991-08-12 | 1993-07-06 | E. R. Squibb & Sons, Inc. | Treatment of congestive heart failure |
| US5273990A (en) | 1992-09-03 | 1993-12-28 | Ciba-Geigy Corporation | Phosphono substituted tetrazole derivatives |
| US5250522A (en) | 1992-10-09 | 1993-10-05 | Ciba-Geigy Corporation | Phosphono/biaryl substituted amino acid derivatives |
| GB9123353D0 (en) | 1991-11-04 | 1991-12-18 | Fujisawa Pharmaceutical Co | New mercapto-amide derivatives,processes for the preparation thereof and pharmaceutical composition comprising the same |
| WO1993010773A1 (en) | 1991-12-06 | 1993-06-10 | Schering-Plough S.P.A. | Use of neutral endopeptidase inhibitors in the treatment of left ventricular hypertrophy |
| US5217996A (en) * | 1992-01-22 | 1993-06-08 | Ciba-Geigy Corporation | Biaryl substituted 4-amino-butyric acid amides |
| US5376293A (en) | 1992-09-14 | 1994-12-27 | State Of South Dakota As Represented By The Department Of Transportation | Deicer |
| DE4233296C1 (de) | 1992-10-02 | 1994-03-31 | Heitland Und Petre Int Gmbh | Behälter für Kosmetikprodukte |
| WO1994015908A1 (fr) | 1993-01-14 | 1994-07-21 | Yoshitomi Pharmaceutical Industries, Ltd. | Derive de propionamide et son utilisation medicinale |
| JPH06234754A (ja) | 1993-02-10 | 1994-08-23 | Dai Ichi Seiyaku Co Ltd | 複素環式カルボン酸誘導体 |
| CN1046119C (zh) | 1993-07-22 | 1999-11-03 | 中国科学院广州电子技术研究所 | 聚磷酸盐复盐及其制造方法 |
| IT1266571B1 (it) | 1993-07-30 | 1997-01-09 | Zambon Spa | Derivati della beta-mercapto-propanammide utili nel trattamento delle malattie cardiovascolari |
| JP2810302B2 (ja) * | 1993-10-01 | 1998-10-15 | ティーディーケイ株式会社 | 小型ポンプ |
| JP3576193B2 (ja) | 1993-12-03 | 2004-10-13 | 第一製薬株式会社 | ビフェニルメチル置換バレリルアミド誘導体 |
| CA2168066A1 (en) | 1995-02-08 | 1996-08-09 | James R. Powell | Treatment of hypertension and congestive heart failure |
| US6558699B2 (en) | 1997-11-17 | 2003-05-06 | Smithkline Beecham Corporation | High drug load immediate and modified release oral dosage formulations and processes for their manufacture |
| CA2332608C (en) | 1998-06-17 | 2010-03-23 | Bristol-Myers Squibb Company | Preventing cerebral infarction through administration of adp-receptor antiplatelet and antihypertensive drugs in combination |
| NZ509260A (en) | 1998-07-10 | 2003-09-26 | Novartis Ag | Pharmaceutical composition containing valsartan and a calcium channel blocker |
| CN1069647C (zh) | 1998-08-31 | 2001-08-15 | 靳广毅 | 一种具有广谱抗菌作用的化合物及其用途 |
| HN2000000050A (es) | 1999-05-27 | 2001-02-02 | Pfizer Prod Inc | Sal mutua de amlodipino y atorvastatina |
| EP1180102B9 (en) | 1999-05-27 | 2005-03-02 | Pfizer Products Inc. | Mutual prodrugs of amlodipine and atorvastatin |
| JP2003533440A (ja) * | 2000-04-03 | 2003-11-11 | ブリストル−マイヤーズ スクイブ カンパニー | 隔離心収縮期高血圧症を処置するバソペプチダーゼ抑制剤 |
| BR0112665A (pt) | 2000-07-19 | 2003-06-24 | Novartis Ag | Sais |
| DE10050246C1 (de) * | 2000-10-11 | 2002-06-20 | Nutrinova Gmbh | Calciumdoppelsalze, Verfahren zu ihrer Herstellung und ihre Verwendung zur Konservierung |
| US6737430B2 (en) * | 2000-11-09 | 2004-05-18 | Pfizer, Inc. | Mutual prodrug of amlodipine and atorvastatin |
| US8168616B1 (en) | 2000-11-17 | 2012-05-01 | Novartis Ag | Combination comprising a renin inhibitor and an angiotensin receptor inhibitor for hypertension |
| WO2002083066A2 (en) | 2001-04-11 | 2002-10-24 | Bristol-Myers Squibb Company | Amino acid complexes of c-aryl glucosides for treatment of diabetes and method |
| US6777443B2 (en) | 2001-05-15 | 2004-08-17 | Novartis Ag | Dipeptide derivatives |
| EP1448190A2 (en) | 2001-10-18 | 2004-08-25 | Novartis AG | Salts formed of an at1-receptor antagonist and a cardiovascular agent |
| DK1467728T3 (da) | 2002-01-17 | 2007-12-27 | Novartis Ag | Farmaceutiske sammensætninger indeholdende valsartan og NEP-inhibitorer |
| US6869970B2 (en) * | 2002-02-04 | 2005-03-22 | Novartis Ag | Crystalline salt forms of valsartan |
| US7446107B2 (en) | 2002-02-15 | 2008-11-04 | Transform Pharmaceuticals, Inc. | Crystalline forms of conazoles and methods of making and using the same |
| WO2004078163A2 (en) | 2003-02-28 | 2004-09-16 | Transform Pharmaceuticals, Inc. | Pharmaceutical co-crystal compositions of drugs such as carbamazepine, celecoxib, olanzapine, itraconazole, topiramate, modafinil, 5-fluorouracil, hydrochlorothiazide, acetaminophen, aspirin, flurbiprofen, phenytoin and ibuprofen |
| CA2477923C (en) | 2002-03-01 | 2021-02-23 | University Of South Florida | Multiple-component solid phases containing at least one active pharmaceutical ingredient |
| AU2003223637A1 (en) | 2002-04-15 | 2003-11-03 | Dr. Reddy's Laboratories Limited | Novel crystalline forms of (s)-n-(1-carboxy-2-methyl-prop-1-yl) -n-pentanoyl-n- (2'-(1h-tetrazol-5-yl-)- biphenyl-4-yl methyl) amine (valsartan) |
| TWI299663B (en) | 2002-05-14 | 2008-08-11 | Novartis Ag | Methods of treatment |
| DK1507558T3 (da) | 2002-05-17 | 2011-12-05 | Novartis Pharma Ag | Farmaceutisk sammensætning omfattende en renininhibitor, en calciumkanalblokker og et diuretikum |
| EG24716A (en) * | 2002-05-17 | 2010-06-07 | Novartis Ag | Combination of organic compounds |
| CN1159313C (zh) | 2002-08-27 | 2004-07-28 | 何广卫 | 地洛他定多元酸碱金属或碱土金属盐复合盐及其药用组合物 |
| GB0230025D0 (en) * | 2002-12-23 | 2003-01-29 | Pfizer Ltd | Novel pharmaceuticals |
| ATE550022T1 (de) | 2003-02-28 | 2012-04-15 | Mcneil Ppc Inc | Pharmazeutische mischkristalle von celecoxib- nicotinamid |
| ES2238022T3 (es) | 2003-03-17 | 2008-11-01 | Teva Pharmaceutical Industries Ltd. | Poliformos de valsartan. |
| US20050165075A1 (en) | 2003-03-31 | 2005-07-28 | Hetero Drugs Limited | Novel amorphous form of valsartan |
| CN1247596C (zh) | 2003-05-15 | 2006-03-29 | 中国药品生物制品检定所 | 一种具有螯合结晶水合物的头孢菌素及其制备方法 |
| US20070054947A1 (en) | 2003-05-16 | 2007-03-08 | Cohn Jay N | Pharmaceutical composition comprising valsartan |
| WO2005049587A1 (en) | 2003-11-21 | 2005-06-02 | Ranbaxy Laboratories Limited | Process for preparation of biphenyl tetrazole |
| CN1246482C (zh) | 2004-05-08 | 2006-03-22 | 山东大学齐鲁医院 | 单个核细胞白细胞相容性抗原a和b特异核糖核酸检测方法 |
| CN1279045C (zh) | 2004-07-30 | 2006-10-11 | 广州白云山制药股份有限公司 | 头孢硫脒复盐及其制造方法 |
| CN100500669C (zh) | 2004-12-10 | 2009-06-17 | 山东大学 | 一种丹酚酸黄连素复盐及其制备方法与应用 |
| MY146830A (en) * | 2005-02-11 | 2012-09-28 | Novartis Ag | Combination of organic compounds |
| JP2006234754A (ja) | 2005-02-28 | 2006-09-07 | Tokyo Keiso Co Ltd | 超音波流量計 |
| AR057882A1 (es) | 2005-11-09 | 2007-12-26 | Novartis Ag | Compuestos de accion doble de bloqueadores del receptor de angiotensina e inhibidores de endopeptidasa neutra |
| CN100391961C (zh) | 2005-11-16 | 2008-06-04 | 天津大学 | 五水头孢唑林钠晶体结构及晶体分子组装制备方法 |
| JP2007157459A (ja) | 2005-12-02 | 2007-06-21 | Sony Corp | 非水電解質電池 |
| CN106414416B (zh) | 2014-09-09 | 2020-03-27 | 上海翰森生物医药科技有限公司 | 结晶型ARB-NEPi复合物及其制备方法和应用 |
| CN105503760A (zh) * | 2014-10-10 | 2016-04-20 | 上海翰森生物医药科技有限公司 | 结晶型ARB-NEPi双阳离子复合物及其制备方法和应用 |
| PL3229799T3 (pl) * | 2014-12-08 | 2019-05-31 | Crystal Pharmatech Co Ltd | Krystaliczne postacie supramolekularnego kompleksu trisodowego zawierającego walsartan i AHU-377 i ich sposoby |
| US10562866B2 (en) | 2015-02-06 | 2020-02-18 | Mylan Laboratories Limited | Amorphous trisodium sacubitril valsartan and a process for the preparation thereof |
| CA2980224C (en) | 2015-03-20 | 2019-06-25 | Crystal Pharmatech Co., Ltd. | Crystalline form of ahu377, preparation method and use thereof |
| KR102254062B1 (ko) | 2015-06-12 | 2021-05-20 | 테바 파마슈티컬스 인터내셔널 게엠베하 | 삼나트륨 발사르탄:사쿠비트릴의 고체 형태 |
| WO2017009784A1 (en) | 2015-07-14 | 2017-01-19 | Cadila Healthcare Limited | Solid state forms of trisodium salt of valsartan/sacubitril complex and sacubitril |
| CN105037289B (zh) | 2015-07-17 | 2017-08-22 | 华东理工大学 | 血管紧张素受体拮抗剂和中性内肽酶抑制剂超分子复合体的新晶型 |
| WO2017042700A1 (en) | 2015-09-07 | 2017-03-16 | Sun Pharmaceutical Industries Limited | Solid forms of valsartan and sacubitril |
| CN106905253B (zh) * | 2015-12-23 | 2020-01-03 | 正大天晴药业集团股份有限公司 | 一种超分子复合物的结晶 |
| US10703731B2 (en) | 2016-03-07 | 2020-07-07 | Msn Laboratories Private Limited | Process for the preparation of Trisodium (4- {[1S,3R)-1-([1,1′-biphenyl]-4-ylmethyl)-4-ethoxy-3-methyl-4-oxobutyl]amino}-4-oxobutanoate)-(N-petanoyl-N-{[2′-(1H-tetrazol-1-1D-5-yl)[1,1′-biphenyl]-4-yl]methyl}- L-valinate) and its polymorphs thereof |
| WO2018069833A1 (en) | 2016-10-10 | 2018-04-19 | Laurus Labs Limited | Stable amorphous form of sacubitril valsartan trisodium complex and processes for preparation thereof |
| CN111592500A (zh) | 2017-01-03 | 2020-08-28 | 上海博志研新药物技术有限公司 | ARB-NEPi复合物、晶型、制备方法及应用 |
| CN109912525A (zh) | 2019-03-13 | 2019-06-21 | 陈文辉 | 一种lcz696新晶型及其制备方法 |
-
2006
- 2006-11-07 AR ARP060104878A patent/AR057882A1/es active IP Right Grant
- 2006-11-08 CN CN201210191052.2A patent/CN102702119B/zh active Active
- 2006-11-08 HU HUE10176094A patent/HUE050870T2/hu unknown
- 2006-11-08 KR KR1020077015021A patent/KR101432821B1/ko active Active
- 2006-11-08 DK DK06827689.8T patent/DK1948158T3/en active
- 2006-11-08 WO PCT/US2006/043710 patent/WO2007056546A1/en not_active Ceased
- 2006-11-08 LT LTEP10176094.0T patent/LT2340828T/lt unknown
- 2006-11-08 SI SI200631748T patent/SI1948158T1/sl unknown
- 2006-11-08 MX MX2007008075A patent/MX2007008075A/es active IP Right Grant
- 2006-11-08 KR KR1020137025742A patent/KR101549318B1/ko active Active
- 2006-11-08 PL PL10176094.0T patent/PL2340828T3/pl unknown
- 2006-11-08 ES ES10176094T patent/ES2823749T3/es active Active
- 2006-11-08 MY MYPI20070955A patent/MY145462A/en unknown
- 2006-11-08 PT PT68276898T patent/PT1948158E/pt unknown
- 2006-11-08 SG SG10201402055YA patent/SG10201402055YA/en unknown
- 2006-11-08 PL PL06827689T patent/PL1948158T3/pl unknown
- 2006-11-08 TW TW095141427A patent/TWI418348B/zh active
- 2006-11-08 CN CN2006800017330A patent/CN101098689B/zh active Active
- 2006-11-08 PT PT101760940T patent/PT2340828T/pt unknown
- 2006-11-08 TW TW102137826A patent/TWI554504B/zh active
- 2006-11-08 DK DK10176094.0T patent/DK2340828T3/da active
- 2006-11-08 BR BRPI0605921A patent/BRPI0605921B8/pt active IP Right Grant
- 2006-11-08 JP JP2008516049A patent/JP4824754B2/ja active Active
- 2006-11-08 PE PE2006001388A patent/PE20070803A1/es active Application Revival
- 2006-11-08 PH PH1/2012/501539A patent/PH12012501539B1/en unknown
- 2006-11-08 EP EP10176094.0A patent/EP2340828B1/en active Active
- 2006-11-08 BR BR122013025375A patent/BR122013025375B8/pt active IP Right Grant
- 2006-11-08 CA CA2590511A patent/CA2590511C/en active Active
- 2006-11-08 NZ NZ600626A patent/NZ600626A/xx unknown
- 2006-11-08 ES ES06827689.8T patent/ES2449765T3/es active Active
- 2006-11-08 RU RU2012107219/04A patent/RU2503668C2/ru active
- 2006-11-08 NZ NZ594006A patent/NZ594006A/en unknown
- 2006-11-08 SI SI200632387T patent/SI2340828T1/sl unknown
- 2006-11-08 PE PE2018002010A patent/PE20190374A1/es unknown
- 2006-11-08 AU AU2006311481A patent/AU2006311481B2/en active Active
- 2006-11-08 EP EP06827689.8A patent/EP1948158B1/en not_active Revoked
- 2006-11-08 JO JOP/2006/0402A patent/JO3492B1/ar active
- 2006-11-08 EP EP20155388.0A patent/EP3685833A1/en not_active Withdrawn
- 2006-11-08 US US11/722,360 patent/US8877938B2/en active Active
- 2006-11-08 HR HRP20140274TT patent/HRP20140274T1/hr unknown
-
2007
- 2007-06-18 IL IL184027A patent/IL184027A/en active IP Right Grant
- 2007-07-02 NO NO20073396A patent/NO337288B1/no active Protection Beyond IP Right Term
- 2007-07-07 GT GT200700055A patent/GT200700055A/es unknown
- 2007-07-11 TN TNP2007000264A patent/TNSN07264A1/en unknown
- 2007-10-02 MA MA30270A patent/MA30128B1/fr unknown
-
2011
- 2011-08-12 JP JP2011177091A patent/JP2011252013A/ja not_active Withdrawn
-
2012
- 2012-05-14 IL IL219782A patent/IL219782A0/en unknown
-
2014
- 2014-03-31 CY CY20141100246T patent/CY1115004T1/el unknown
- 2014-06-23 US US14/311,788 patent/US9388134B2/en active Active
- 2014-09-17 EC ECIEPI201419136A patent/ECSP14019136A/es unknown
-
2015
- 2015-02-23 JP JP2015032678A patent/JP2015098485A/ja active Pending
- 2015-12-03 NO NO20151656A patent/NO340315B1/no unknown
-
2016
- 2016-05-17 LT LTPA2016017C patent/LTC1948158I2/lt unknown
- 2016-05-17 FR FR16C0018C patent/FR16C0018I2/fr active Active
- 2016-05-18 NO NO2016008C patent/NO2016008I2/no unknown
- 2016-05-18 CY CY2016014C patent/CY2016014I1/el unknown
- 2016-05-18 HU HUS1600025C patent/HUS1600025I1/hu unknown
- 2016-06-21 US US15/187,872 patent/US20160324821A1/en not_active Abandoned
-
2018
- 2018-06-12 US US16/006,252 patent/US20180344679A1/en not_active Abandoned
-
2019
- 2019-07-03 US US16/502,821 patent/US20190374498A1/en not_active Abandoned
- 2019-07-03 US US16/502,811 patent/US20190374497A1/en not_active Abandoned
- 2019-09-23 US US16/579,581 patent/US11096918B2/en active Active
- 2019-09-23 US US16/579,591 patent/US20200016110A1/en not_active Abandoned
-
2020
- 2020-10-07 HR HRP20201605TT patent/HRP20201605T1/hr unknown
- 2020-10-13 CY CY20201100963T patent/CY1123531T1/el unknown
-
2021
- 2021-01-11 LU LU00195C patent/LUC00195I2/fr unknown
- 2021-01-11 FR FR21C1000C patent/FR21C1000I2/fr active Active
- 2021-01-13 HU HUS2100003C patent/HUS2100003I1/hu unknown
- 2021-01-14 CY CY2021003C patent/CY2021003I2/el unknown
- 2021-01-14 LT LTPA2021502C patent/LTC2340828I2/lt unknown
- 2021-08-05 US US17/395,305 patent/US20210361610A1/en not_active Abandoned
-
2022
- 2022-05-06 US US17/738,565 patent/US20220257551A1/en not_active Abandoned
- 2022-06-23 US US17/847,588 patent/US11642329B2/en active Active
-
2024
- 2024-12-12 US US18/979,457 patent/US20250339395A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11642329B2 (en) | Amorphous solid form of compounds containing S—N-valeryl-N- {[2′-( 1 H-tetrazole-5-yl)-biphenyl-4-yl]-methyl}-valine and (2R,4S)-5-biphenyl-4-yl-4-(3-carboxy-propionylamino)-2-methyl-pentanoic acid ethyl ester moieties and sodium cations | |
| RU2459809C2 (ru) | Фармацевтические комбинации антагониста рецептора ангиотензина и ингибитора nep | |
| HK40023077A (en) | Compound comprising an arb and a nepi | |
| HK1156550A (en) | Pharmaceutical combinations of an angiotensin receptor antagonist and an nep inhibitor | |
| HK1175465B (en) | Pharmaceutical combinations of an angiotensin receptor antagonist and an nep inhibitor | |
| Exhibit | BEFORE THE CONTROLLER OF PATENTS PATENT OFFICE DELHI |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B06H | Technical and formal requirements: requirement cancelled [chapter 6.8 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] |
Free format text: NOTIFICACAO DE ANUENCIA RELACIONADA COM O ART 229 DA LPI |
|
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 18/08/2020, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 08/11/2006 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |