BRPI0607323B1 - composições, usos de polipeptídeos e de anticorpos, bem como kits para a detecção de anticorpo que se liga especificamente a um polipeptídeo - Google Patents
composições, usos de polipeptídeos e de anticorpos, bem como kits para a detecção de anticorpo que se liga especificamente a um polipeptídeo Download PDFInfo
- Publication number
- BRPI0607323B1 BRPI0607323B1 BRPI0607323-9A BRPI0607323A BRPI0607323B1 BR PI0607323 B1 BRPI0607323 B1 BR PI0607323B1 BR PI0607323 A BRPI0607323 A BR PI0607323A BR PI0607323 B1 BRPI0607323 B1 BR PI0607323B1
- Authority
- BR
- Brazil
- Prior art keywords
- seq
- kda
- dipyridyl
- grown
- medium
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/085—Staphylococcus
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/569—Immunoassay; Biospecific binding assay; Materials therefor for microorganisms, e.g. protozoa, bacteria, viruses
- G01N33/56911—Bacteria
- G01N33/56938—Staphylococcus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/164—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/305—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Micrococcaceae (F)
- C07K14/31—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Micrococcaceae (F) from Staphylococcus (G)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from bacteria
- C07K16/1267—Gram-positive bacteria
- C07K16/1271—Micrococcaceae (F); Staphylococcaceae (F), e.g. Staphylococcus (G)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from bacteria
- C07K16/1267—Gram-positive bacteria
- C07K16/1275—Streptococcus (G)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from bacteria
- C07K16/1267—Gram-positive bacteria
- C07K16/1285—Gram-positive bacteria from Corynebacterium (G)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/12—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from bacteria
- C07K16/1267—Gram-positive bacteria
- C07K16/1289—Mycobacteriaceae (F)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
- A61K2039/575—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2 humoral response
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S530/00—Chemistry: natural resins or derivatives; peptides or proteins; lignins or reaction products thereof
- Y10S530/82—Proteins from microorganisms
- Y10S530/825—Bacteria
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Gastroenterology & Hepatology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Epidemiology (AREA)
- Microbiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Biotechnology (AREA)
- Virology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Mycology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Peptides Or Proteins (AREA)
Abstract
COMPOSIÇÕES E USO DE POLIPEPTÍDEOS E KITS PARA A DETECÇÃO DE ANTICORPO QUE SE LIGA ESPECIFICAMENTE A UM POLIPEPTÍDEO. A presente invenção fornece polipeptideos isolados que podem ser isolados partindo de um Staphylococcus spp. São também fornecidas pela presente invenção composições que incluem um ou mais dos polipeptideos e métodos para a produção e métodos para a utilização dos polipeptideos.
Description
Este pedido de patente reivindica o benefício do Pedido de Patente U.S. Provisório No de Série 60/652.843, depositado em 14 de fevereiro de 2005, que é incorporado aqui como referência.
As bactérias gram-positivas constituem notavelmente um grupo diverso de organismos que causam uma variedade de doenças tanto em seres humanos quanto em animais. Alguns dos agentes patogênicos reconhecidos como importantes na saúde de seres humanos e/ou de animais incluem as bactérias que pertencem às famílias de Corynebacteriaceae, Enterococcacae, Micrococcaceae, Mycobacteriaceae, Nocardiaceae e Peptococcaceae, que incluem tais espécies de bactéria como Actinomyces spp., Bifidobacterium spp., Corynebacteryum spp., Enterococcus spp., Erysipelothrix spp., Eubacterium spp., Kytococcus spp., Lactobacillus spp., Micrococcus spp., Mobiluncus spp., Mycobacteria spp., Peptostreptococcus spp., Propionibacteryum spp. e Staphylococcus spp. Estes agentes patogênicos causam um grande número de manifestações clínicas em muitas espécies animais diferentes. O tratamento para tais infecções foi historicamente antibióticos que atacam as estruturas e as funções comuns de organismos gram-positivos. Entretanto, muitos dos organismos gram-positivos ubíquos desenvolveram resistência a várias classes de antibióticos, tornando o tratamento das infecções difícil. O uso bem espalhado de antibióticos no tratamento de doenças bacterianas tanto em seres humanos quanto nos animais para produção de alimentos é provavelmente o fator de contribuição principal na proliferação de cepas resistentes a antibióticos de muitas espécies de organismos gram-positivos. Portanto, há uma grande necessidade de encontrar tratamentos diferentes que previnem ou eliminam infecções por organismos gram-positivos em animais assim como em seres humanos.
Infecções por estafilococos em animais na agricultura.
Na indústria agrícola, um número de doenças importantes é causado por organismos gram-positivos. Os exemplos de estados de saúde clínicos causados por infecções por bactérias gram-positivas incluem, mastite, septicemia, pneumonia, osteomielite, meningoencefalite, linfangite, dermatite, infecções do trato genital, metrite, doença perinatal, abscessos da pituitária, artrite, bursite, orquite, cistite e pielonefrite, linfadenite caseosa, tuberculose, linfangite ulcerativa, erisipelas, laminite, doença de tyzzer, tétano, botulismo, enterite, edema maligno, "braxy" (ou bradsot), hemoglobinúria bacilar, enterotoxemia. Os Staphylococcusspp., em particular, são capazes de infectar muitas espécies diferentes de animais na agricultura e podem causar enormes perdas econômicas. Por exemplo, é estimado que a indústria de laticínios Norte Americana perca aproximadamente $185 por vaca anualmente por causa da mastite, uma doença frequentemente causada por Staphylococcus aureus.Uma vez que há 9,5 milhões de cabeças de vacas de leite nos EUA, o custo anual da mastite é de aproximadamente $1,8 bilhões. Isto é aproximadamente 10% do valor total das vendas de leite das fazendas e aproximadamente dois terços desta perda é causado pela produção reduzida de leite em vacas infectadas de forma subclínica. Outras perdas são causadas pelo leite anormal descartado e pelo leite retido de vacas tratadas com antibióticos, custos da substituição precoce de vacas afetadas, valor de venda reduzido de vacas eliminadas, custos de fármacos e serviços veterinários e maiores custos de trabalho. Em adição a esta prevalência dentro da indústria de laticínios bovina, a mastite causada por cocos grampositivos é também comum entre cabras e ovelhas. Doenças adicionais de animais causadas por S. aureusincluem botriomicose em cavalos, sinovite purulenta e osteomielite nas aves, coriza em coelhos, abortos em suínos e piemia por carrapatos em cordeiros. Outras espécies de estafilococos são os agentes patogênicos de pele principais de caninos (S. intermedius) e de suínos (S. hycius). Nas espécies de aves, os agentes patogênicos de estafilococos causam endocardite e septicemia.
Os Staphylococcusspp. são também agentes patogênicos humanos que causam uma ampla variedade de infecções. A espécie Staphylococcus aureus,um colonizador comum da mucosa e da pele humana, é um agente patogênico oportunista que pode causar várias infecções em seres humanos. Por exemplo, S. aureus é o agente causador de várias infecções de pele, incluindo impetigo, furunculose, celulite e síndrome da pele escaldada, assim como infecções de feridas pós-cirúrgicas potencialmente fatais. Em adição, a exposição de indivíduos imunocomprometidos ao S. aureus nas instalações hospitalares resultou em infecções de órgãos tais como pneumonia, infecções do trato urinário, osteomielite, artrite, bacteremia e endocardite. S. aureusé também o agente causador de toxinoses, mais notavelmente a síndrome de choque tóxico e infecções alimentares. As infecções alimentares causadas pela enterotoxina B de estafilococos é a causa mais comum de doença de origem alimentar, superando até mesmo a salmonelose, a campilobacteriose e a listeriose. Outras espécies de estafilococos também causam doença em seres humanos; S. epidermidis, S. haemolyticus e S. hominis comumente infectam dispositivos médicos implantados e S. saprophyticus está associado com infecções do trato urinário em mulheres.
Os estafilococos infectam uma variedade de tecidos hospedeiros e evadem o sistema imunológico através da produção de vários tipos de proteínas secretadas, fatores de virulência expressos na superfície e sistemas metabólicos planejados para a sobrevivência em meio dos recursos limitados e as defesas ativas associadas com o ambiente hospedeiro. A colonização é a primeira etapa necessária no estabelecimento da infecção; vários fatores incluindo a cápsula, o ácido lipoteicóico e o ácido teicóico são componentes estruturais comuns que contribuem para a colonização. Em adição, as proteínas de superfície tais como a proteína de ligação à fibronectina e as proteínas de ligação à sialoproteína do osso de estafilococos se ligam especificamente aos componentes de tecidos do hospedeiro. As toxinas são comumente produzidas entre os agentes patogênicos de estafilococos e são altamente danificadoras; várias doenças humanas, incluindo infecções alimentares, sindrome do choque tóxico e estados esfoliativos da pele, são o resultado direto de proteínas de toxinas secretadas extracelulares. Um único isolado pode codificar genes para 20-30 toxinas secretadas diferentes. Alguns dos produtos protéicos secretados são superantígenos que podem se ligar de forma inespecífica à molécula de MHC de classe II de uma célula apresentadora de antígenos e, simultaneamente, ao receptor de células T de uma célula T. A ligação induz a sinalização de células T e leva à liberação de altos níveis de fatores pró-inflamatórios, que, em última análise, induzem danos no hospedeiro por causa da resposta imunológica esmagadora. Uma outra classe de fatores de virulência expressos na superfície desvia as bactérias do sistema imunológico do hospedeiro. Por exemplo, a Proteína A expressa na superfície de S. aureusinibe a opsonização e a fagocitose através da ligação do componente Fc do anticorpo do hospedeiro. Várias proteases, hemolisinas (alfa, beta, gama e delta), nucleases, lipases, hialuronidase e colagenase também auxiliam as bactérias na extração de nutrientes das células circundantes e protegendo as mesmas contra as defesas do hospedeiro.
O CDC estima que a cada ano quase 2 milhões de pessoas nos Estados Unidos da América adquirem uma infecção nosocomial, resultando em 90.000 mortes anualmente. Destas infecções fatais, 70% são causados por bactérias resistentes a antibióticos. O aumento na resistência aos antibióticos entre as espécies microbianas é particularmente pronunciado nos colonizadores da pele e de mucosas tal como S. aureus.Por exemplo, a grande maioria de S. aureusisolada de instalações hospitalares é resistente à penicilina e 50% são também resistentes às penicilinas semi-sintéticas, tais como, meticilina, nafcilina e oxacilina. Destes isolados, os referidos como MRSA (S. aureusresistente à metacilina) foram primeiramente observados nos anos 70 e estão agora firmemente estabelecidos nas instalações hospitalares. Recentemente, há vários casos de infecções por MRSA na comunidade, em que os indivíduos infectados não tiveram exposição prévia a hospitais ou trabalhadores da área da saúde. Esta tendência alarmante é intensificada pelo isolamento de isolados de MRSA que são menos susceptíveis à vancomicina, um glicopeptídeo utilizado para tratar MRSA. Foi mostrado que muito poucas cepas são realmente resistentes à vancomicina de acordo com a definição do CDC de resistência à vancomicina, mas várias cepas de MRSA foram caracterizadas como consistindo em subpopulações com susceptibilidade reduzida à vancomicina ou VISA (S. aureusintermediários à vancomicina). Uma vez que o isolamento de cepas resistentes à vancomicina e intermediárias à vancomicina é um desenvolvimento relativamente novo, há poucos dados em relação a sua prevalência em hospitais e/ou na comunidade. Ocasionalmente, VRSA (S. aureusresistente à vancomicina) com resistência total à vancomicina e que carregam um plasmídeo de resistência provavelmente adquirido de Enterococcus spp. foram também recuperados de seres humanos.
A emergência de vários agentes patogênicos gram-positivos que são resistentes a vários antibióticos impulsionou esforços de pesquisa voltados para o desenvolvimento de vacinas preventivas para proteção contra doença. As vacinas são planejadas para serem administradas a pacientes com a finalidade de ativar uma resposta de memória em longo prazo partindo do sistema imunológico, de forma que se o agente patogênico for encontrado em um momento futuro, o sistema imunológico pode mais rapidamente e eficientemente eliminar o agente patogênico. Até hoje, uma vacina amplamente protetora contra agentes patogênicos gram-positivos associados com um número de doenças humanas graves, particularmente as doenças associadas com infecções por estafilococos, não está disponível. As abordagens de desenvolvimento de vacinas para a prevenção de infecções por estafilococos incluem as que relatam o uso de componentes de superfície microbiana que reconhecem as moléculas de matriz [MSCRAMMS (Nilsson e outros 1998. J Clin Invest 101: 2640-9; Menzies e outros 2002. J Infect Dis 185: 937-43; Fattom e outros 2004. Vaccine 22: 880 7], polissacarídeos de superficie (McKenney e outros 2000; McKenney e outros 1999. Science 284: 1523-7; Maira-Litran e outros 2002. Infect Immun 70: 4433-40; Maira-Litran e outros 2004. Vaccine 22: 872-9; Maira-Litran e outros 2005. Infect Immun 73: 6752-62) e exoproteínas mutadas (Lowell e outros 1996. Infect Immun 64: 4686-93; Stiles e outros 2001. Infect Immun 69: 2031-6; Gampfer e outros 2002. Vaccine 20: 3675-84), na forma de antígenos em composições vacinais de subunidades, assim como uma cepa avirulenta viva (Reinoso e outros 2002. Can J Vet Res 66: 285-8) e várias abordagens de vacinas de DNA (Ohwada e outros 1999. J Antimicrob Chemother 44: 767-74); Brouillette e outros 2002. Vaccine 20: 2348-57; Senna e outros 2003. Vaccine 21: 26616). Embora muitas destas composições tenham mostrado algum grau de proteção, estas atingiram pouca proteção cruzada contra cepas de estafilococos diversas e falharam ainda na ativação de respostas imunológicas substanciais em pacientes imunocomprometidos, uma população em risco importante para infecções nosocomiais.
As doenças de estafilococos mais graves são as mediadas pelas exotoxinas purogênicas superantigênicas mencionadas anteriormente (SPEs) que estimulam de forma inespecífica células T independente da apresentação de antígenos. Tais doenças incluem síndrome de choque tóxico, doença esfoliativa da pele e possivelmente síndrome de Kawasaki. Para estas doenças mediadas por SPE, os agentes imunoterapêuticos que reforçam o sistema imunológico durante uma infecção ativa são frequentemente mais eficientes que as vacinas, que são tipicamente administradas antes da infecção. A natureza esmagadora da resposta imunológica às SPE necessita uma redução rápida na atividade da toxina como o primeiro objetivo na terapia. Até hoje, a neutralização de toxinas na doença mediada por S. aureus foi mais eficientemente realizada através da administração da imunoglobulina humana intravenosa (MG), uma preparação de anticorpo humano concentrada proveniente de vários milhares de doadores humanos (Takei e outros. 1993. J Clin Invest 91: 602-7; Stohl e Elliot. 1996. Clin Immunol Immunopathol 79: 122-33). A distribuição bem espalhada de S. aureusque coloniza aproximadamente 30% de adultos humanos saudáveis, coincide com as altas taxas de exposição para a maior parte da população, assim o nível de anticorpos antitoxina antiestafilococos na IVIG é frequentemente suficiente para neutralizar a toxina tempo suficiente para estabilizar a resposta imunológica até a carga bacteriana ser reduzida com antibióticos (Schlievert, 2001. J Allergy Clin Immunol 108 (Supl. 4): S107-110). As preparações de IVIG partindo de vários fabricantes mostraram neutralizar a toxina em ensaios de proliferação com células mononucleares do sangue periférico humano, inibir a diferenciação de células B controlada por células T humanas induzida pela toxina in vitro (Stohl e Elliot. 1996. Clin Immunol Immunopathol 79: 122-33, Stohl e Elliot. 1995. J Immunol 155: 1838-50; Stohl e outros. 1994. J Immunol 153: 117-27) e reduzir a secreção de IL-4 e de IL-3 nas PBMCs estimuladas com a enterotoxina B de estafilococo (Takei e outros. 1993. J Clin Invest 91: 602-7; Darenberg e outros. 2004. Clin Infect Dis 38: 836-42). A terapia com IVIG, com sua capacidade provada de neutralizar as SPE, é agora uma terapia recomendada para a síndrome de Kawasaki e está ganhando aprovação como um método de tratamento para a síndrome de choque tóxico causada por estafilococos (Schlievert 2001. J Allergy Clin Immunol 108 (Supl. 4): S107-110). O uso de MG como uma lavagem de ferimentos imunoprotetora durante a cirurgia também foi investigado em camundongos (Poelstra e outros. 2000. Tissue Eng 6(4): 401-411). Embora a IVIG padronizada tenha utilidade para limitar o avanço de algumas doenças mediadas pelas SPEs de estafilococos, a segurança, a eficiência e a consistência das preparações de IVIG humanas geradas partindo de milhares de doadores humanos não selecionadas permanecem controversas (Baker e outros. 1992. N Engl J Med 327: 213-9; Miller e outros. 2001. J Allergy Clin Immunol 108: S91-4; Sacher, 2001. J Allergy Clin Immunol 108: S139-46; Darenberg e outros. 2004. Clin Infect Dis 38: 836-42). Além disso, o benefício da IVIG na prevenção de algumas infecções por estafilococos é duvidoso (Baker e outros. 1992. N Engl J Med 327: 213-9; Hill, H. R. 2000. J Pediatr 137: 5957; Darenberg e outros. 2004. Clin Infect Dis 38: 836-42). Para aumentar a eficiência da IVIG no tratamento de infecções por estafilococos em certas populações em risco, uma IgG humana antiestafilococos policlonal com doador selecionado derivada do plasma com altos títulos de anticorpo direcionado para o fator de aglomeração A MSCRAMMS de estafilococos (ClfA) e para a proteína G de ligação ao fibrinogênio (SdrG) foi criada e testada com sucesso em bebês com baixo peso ao nascerem para prevenir septicemia causada por estafilococos (Vernachio e outros. 2003. Antimicrob Agents Chemother 47: 3400-6; Bloom e outros. 2005. Pediatr Infect Dis J 24: 858866; Capparelli e outros. 2005. Antimicrob Agents Chemother 49: 4121-7). Um anticorpo monoclonal humanizado específico para o fator de aglomeração A MSCRAMM de S. aureus,também está sendo desenvolvido. O anticorpo foi selecionado de um conjunto de milhares de anticorpos anti-CIfA murinos em relação a sua capacidade de se ligar ao ClfA de uma maneira que impeça a ligação de S. aureusà fibronectina humana e foi subsequentemente humanizado através da mutação de resíduos direcionados específicos para imitar o anticorpo do subgrupo da linhagem germinativa humana homóloga (Hall e outros. 2003. Infect Immun 71: 6864-70; Domanski e outros. 2005. Infect Immun 73: 5229-32). O anticorpo específico está sendo planejado para uso em associação com antibióticos para o tratamento de infecção por S. aureusgrave que ameaça a vida, embora estudos com animais tenham demonstrado um efeito protetor profilático.
A presente invenção fornece composições que incluem dois ou mais polipeptídeos isolados. Os dois ou mais polipeptídeos isolados podem ter um peso molecular de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa, 33 kDa ou uma combinação dos mesmos. Por exemplo, uma composição pode incluir proteínas isoladas de 88 kDa e 55 kDa. Em alguns aspectos, a composição pode incluir polipeptídeos isolados que possuem pesos moleculares de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa e 33 kDa. O peso molecular é determinado por eletroforese em um gel de dodecil sulfato de sódio poliacrilamida. Os polipeptídeos podem ser isolados de um Staphylococcus aureusquando incubado em meio que inclui um quelante de ferro e não podem ser isolados quando cultivado no meio sem o quelante de ferro. A composição protege um animal, tal como um camundongo ou uma vaca ou um ser humano, contra o desafio com uma cepa de S. aureus,por exemplo, a cepa 19636 da ATCC. A composição pode incluir ainda um veículo farmaceuticamente aceitável e pode incluir ainda um polipeptídeo isolado que possui um peso molecular de 150 kDa, 132 kDa, 120 kDa, 75 kDa, 58 kDa, 50 kDa, 44 kDa, 43 kDa, 41 kDa, 40 kDa ou uma combinação dos mesmos e pode ser isolado de um S. aureusquando cultivado no meio sem o quelante de ferro. Em alguns aspectos, os polipeptídeos da composição podem ser isolados da cepa 19636 da ATCC de S. aureus.
A presente invenção fornece ainda métodos para a utilização das composições. Em um aspecto, o método é para o tratamento da infecção em um indivíduo e inclui a administração de uma quantidade eficiente de uma composição da presente invenção ao indivíduo que possui ou está em risco de ter uma infecção causada por Staphylococcusspp. Em um outro aspecto, o método é para o tratamento de um sintoma em um indivíduo e inclui a administração de uma quantidade eficiente de uma composição da presente invenção a um indivíduo que possui uma infecção causada por Staphylococcus spp. O indivíduo pode ser um mamífero, tal como um ser humano, um cavalo ou uma vaca. O Staphylococcusspp. pode ser S. aureus.
A presente invenção fornece ainda métodos para a utilização de anticorpo, por exemplo, anticorpo policlonal, que se liga especificamente aos polipeptídeos da presente invenção. Em um aspecto, o método é para o tratamento de uma infecção em um indivíduo e inclui a administração de uma quantidade eficiente de uma composição a um indivíduo que possui ou que está em risco de ter uma infecção causada por um Staphylococcusspp., em que a composição inclui um anticorpo que se liga especificamente a dois polipeptídeos isolados da presente invenção. Em um outro aspecto, o método é para o tratamento de um sintoma em um indivíduo e inclui a administração de uma quantidade eficiente de uma composição a um indivíduo que possui uma infecção causada por um Staphylococcusspp., em que a composição inclui um anticorpo que se liga especificamente a dois polipeptídeos isolados da presente invenção. O indivíduo pode ser um mamífero, tal como um ser humano, um cavalo ou uma vaca. O Staphylococcusspp. pode ser S. aureus.
São também fornecidos pela presente invenção métodos para diminuir a colonização em um indivíduo. Em um aspecto, o método inclui a administração de uma quantidade eficiente de uma composição da presente invenção a um indivíduo colonizado por um Staphylococcusspp. Em um outro aspecto, o método inclui a administração de uma quantidade eficiente de uma composição a um indivíduo colonizado por Staphylococcusspp., em que a composição inclui um anticorpo que se liga especificamente a dois polipeptídeos isolados da presente invenção.
A presente invenção fornece um kit para a detecção do anticorpo que se liga especificamente a um polipeptídeo. O kit inclui, em recipientes separados, um polipeptídeo isolado da presente invenção e um reagente que detecta um anticorpo que se liga especificamente ao polipeptídeo.
A presente invenção fornece ainda uma composição que inclui dois polipeptídeos isolados que possuem pesos moleculares selecionados de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa e 33 kDa, em que o peso molecular é determinado por eletroforese em um gel de dodecil sulfato de sódio poliacrilamida. Cada polipeptídeo da composição possui um "fingerprint"de massa de pelo menos 80% de similaridade a um "fingerprint"de massa de um polipeptídeo do mesmo peso molecular polipeptídeo expresso pela cepa 19636 da ATCC de Staphylococcus aureus,em que o polipeptídeo pode ser isolado de um Staphylococcus aureusquando incubado em meios que compreendem um quelante de ferro e não pode ser isolado quando cultivado nos meios sem o quelante de ferro. Por exemplo, o polipeptídeo isolado com um peso molecular de 88 kDa possui um "fingerprint"de massa de pelo menos 80% de similaridade a um "fingerprint"de massa de um polipeptídeo de 88 kDa expresso pela cepa 19636 da ATCC de Staphylococcus aureus e o polipeptídeo isolado com um peso molecular de 55 kDa possui um "fingerprint"de massa de pelo menos 80% de similaridade a um "fingerprint" de massa de um polipeptídeo de 55 kDa expresso pela cepa 19636 da ATCC de Staphylococcus aureus.
Figura 1. O perfil eletroforético das proteínas de Staphylococcus aureus de cepas diferentes derivadas de espécies diferentes cultivadas com e sem ferro (faixas marcadas com Fe++ e DP, respectivamente).
Figura 2. A diferença na mortalidade entre camundongos vacinados e não vacinados após desafio homólogo e heterólogo com Staphylococcus aureus.
Figura 3. Curva de sobrevivência de Kaplan-Meier mostrando a porcentagem de sobrevivência após a vacinação e o desafio homólogo com S. aureusATCC 19636.
Figura 4. Curva de sobrevivência de Kaplan-Meier mostrando a porcentagem de sobrevivência após a vacinação e o desafio heterólogo com S. aureusATCC 19636.
Figura 5. A curva de sobrevivência de Kaplan-Meier mostrando a porcentagem de sobrevivência após a imunização passiva e o desafio homólogo com S. aureusATCC 19636.
Figura 6. A curva de sobrevivência de Kaplan-Meier mostrando a porcentagem de sobrevivência após a imunização passiva e o desafio heterólogo com a cepa 1477 de S. aureus.
A presente invenção fornece polipeptídeos e composições que incluem polipeptídeos. Como utilizado aqui, "polipeptídeo" se refere a um polímero de aminoácidos ligado por ligações peptídicas. Assim, por exemplo, os termos peptídeo, oligopeptídeo, proteína e enzima são incluídos dentro da definição de polipeptídeo. Este termo inclui ainda modificações pós-expressão do polipeptídeo, tais como, glicosilações, acetilações, fosforilações e similares. O termo polipeptídeo não significa um comprimento específico de um polímero de aminoácidos. Um polipeptídeo pode ser isolado diretamente de uma fonte natural ou pode ser preparado com o auxílio de técnicas recombinantes, enzimáticas ou químicas. No caso de um polipeptídeo que ocorre naturalmente, tal polipeptídeo está tipicamente isolado. Um polipeptídeo "isolado" é um que foi removido de seu ambiente natural. Por exemplo, um polipeptídeo isolado é um polipeptídeo que foi removido do citoplasma ou da membrana de uma célula e muitos dos polipeptídeos, ácidos nucléicos e outro material celular de seu ambiente natural não estão mais presentes. Um polipeptídeo "que pode ser isolado" é um polipeptídeo que poderia ser isolado de uma fonte particular. Um polipeptídeo "purificado" é um que está pelo menos 60% livre, preferencialmente pelo menos 75% livre e mais preferencialmente pelo menos 90% livre de outros componentes com os quais estaria naturalmente associado. Os polipeptídeos que são produzidos fora do organismo nos quais ocorrem naturalmente, por exemplo, por meios químicos ou recombinantes, são considerados como sendo isolados e purificados por definição, uma vez que nunca estiveram presentes em um ambiente natural. Como utilizado aqui, um "fragmento de polipeptídeo" se refere a uma parte de um polipeptídeo que resulta da digestão de um polipeptídeo com uma protease. A não ser que seja especificado de outra maneira, "um", "uma", "o", "a", "pelo menos um" e "pelo menos uma" são utilizados de forma intercambiável e significam um(a) ou mais de um(a). O termo "compreende" e variações do mesmo não possuem significado limitante quando este termo aparece na descrição e nas reivindicações.
Um polipeptídeo da presente invenção pode ser caracterizado pelo peso molecular, pelo "fingerprint"de massa ou a combinação dos mesmos. O peso molecular de um polipeptídeo, expresso tipicamente em quilodáltons (kDa), pode ser determinado utilizando métodos de rotina incluindo, por exemplo, filtração em gel, eletroforese em gel incluindo eletroforese em gel de dodecil sulfato de sódio (SDS) poliacrilamida (PAGE), eletroforese por capilaridade, espectrometria de massa e cromatografia líquida incluindo HPLC. Preferencialmente, o peso molecular é determinado através da resolução de um polipeptídeo utilizando um gel de SDS poliacrilamida que possui um gel de empilhamento de aproximadamente 4% e um gel de resolução de aproximadamente 10% sob condições redutoras e desnaturantes. A não ser que seja indicado de outra maneira, o peso molecular se refere ao peso molecular que é determinado por SDS-PAGE. Como utilizado aqui, um '"fingerprint"de massa' se refere a uma população de fragmentos de polipeptídeos obtida partindo de um polipeptídeo após a digestão com uma protease. Tipicamente, os fragmentos de polipeptídeos resultantes de uma digestão são analisados utilizando um método espectrométrico de massa.
Cada fragmento de polipeptídeo é caracterizado por uma massa ou por uma proporção de massa (m) em relação à carga (z), que é referida como uma "proporção de m/z" ou um "valor de m/z".
Os métodos para gerar um "fingerprint"de massa de um polipeptídeo são rotineiros. Um exemplo de tal método é descrito no exemplo 13.
Os polipeptídeos da presente invenção podem ser polipeptídeos regulados por metais. Como utilizado aqui, um "polipeptídeo regulado por metais" é um polipeptídeo que é expresso por um microorganismo em um nível maior quando o microorganismo é crescido em condições de baixo teor de metais comparado com o crescimento do mesmo microorganismo em condições de alto teor de metais. As condições de baixo teor de metais e de alto teor de metais são descritas aqui. Por exemplo, uma classe de polipeptídeo regulado por metais produzida por Staphylococcusspp. não é expressa em níveis detectáveis durante o crescimento do microorganismo nas condições de alto teor de metal, mas é expressa em níveis detectáveis durante o crescimento em condições de baixo teor de metais. Os exemplos de tais polipeptídeos regulados por metais que podem ser isolados de S. aureus após o crescimento em condições de baixo teor de ferro possuem pesos moleculares de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa e 33 kDa. Os exemplos de tais polipeptídeos regulados por metais que podem ser isolados de S. aureusapós o crescimento em condições de baixo teor de zinco ou de baixo teor de cobre possuem pesos moleculares de 115 kDa, 88 kDa, 80 kDa, 71 kDa, 69 kDa, 35 kDa, 30 kDa, 29, kDa e 27 kDa.
A presente invenção inclui ainda polipeptídeos que não são regulados por metais. Tais polipeptídeos são expressos na presença de um íon metálico tal como cloreto férrico e também são expressos quando crescidos em condições de baixo teor de ferro. Os exemplos de tais polipeptídeos que podem ser isolados de S. aureuspossuem pesos moleculares de 150 kDa, 132 KDa, 120 kDa, 75 kDa, 58 kDa, 50 kDa, 44 kDa, 43 kDa, 41 kDa e 40 kDa.
O fato de um polipeptídeo ser um polipeptídeo regulado por metais ou não pode ser determinado por métodos úteis para a comparação da presença de polipeptídeos, incluindo, por exemplo, a filtração em gel, a eletroforese em gel incluindo eletroforese em gel de dodecil sulfato de sódiopoliacrilamida (SDS-PAGE), eletroforese por capilaridade, espectrometria de massa e cromatografia líquida incluindo HPLC. Culturas separadas de um microorganismo são crescidas sob condições de alto teor de metais e sob condições de baixo teor de metais, os polipeptídeos da presente invenção são isolados como descrito aqui e os polipeptídeos presentes em cada cultura são resolvidos e comparados. Tipicamente, é utilizada uma quantidade equivalente de polipeptídeos de cada cultura. Preferencialmente, os polipeptídeos são resolvidos utilizando um gel de SDS poliacrilamida que possui um gel de empilhamento de aproximadamente 4% e um gel de resolução de aproximadamente 10% sob condições redutoras e desnaturantes. Por exemplo, 30 microgramas (μg) do polipeptídeo total de cada cultura podem ser utilizados e carregados nos cavidades de um gel. Após correr o gel e corar os polipeptídeos com Coomasie Brilliant Blue (Azul Brilhante de Coomasie), as duas faixas podem ser comparadas. Quando se determina se um polipeptídeo é ou não expresso em um nível detectável, 30 μg do polipeptídeo total de uma cultura são resolvidos em um gel de SDS-PAGE e corados com Coomasie Brilliant Blue utilizando métodos conhecidos na técnica. Um polipeptídeo que pode ser visualizado a olho nu é considerado como sendo expresso em um nível detectável, enquanto um polipeptídeo que não pode ser visualizado a olho nu é considerado como não sendo expresso em um nível detectável.
Os polipeptídeos da presente invenção podem ter atividade imunogênica. "Atividade imunogênica"se refere à capacidade de um polipeptídeo de ativar uma resposta imunológica em um animal. Uma resposta imunológica a um polipeptídeo é o desenvolvimento em um animal de uma resposta imunológica celular e/ou mediada por anticorpos ao polipeptídeo. Geralmente, uma resposta imunológica inclui, mas não está limitada a um ou mais dos efeitos a seguir: a produção de anticorpos, células B, células T helper, células T supressoras e/ou células T citotóxicas, direcionadas para um epitopo ou epitopos do polipeptídeo. "Epitopo" se refere ao local em um antigeno ao qual células B e/ou células T específicas respondem de forma que o anticorpo é produzido. A atividade imunogênica pode ser protetora. "Atividade imunogênica protetora" se refere à capacidade de um polipeptídeo de ativar uma resposta imunológica em um animal que previne ou inibe a infecção por Staphylococcusspp., por exemplo, S. aureus.O fato de um polipeptídeo ter atividade imunogênica protetora pode ser determinado através de métodos conhecidos na técnica, por exemplo, como descrito nos exemplos 5, 9 ou 12. Por exemplo, um polipeptídeo da presente invenção ou uma combinação de polipeptídeos da presente invenção, protege um roedor tal como um camundongo contra o desafio com um Staphylococcusspp. Um polipeptídeo da presente invenção pode ter atividade soroativa. "Atividade soroativa" se refere à capacidade de um polipeptídeo candidato de reagir com o anticorpo presente no soro convalescente de um animal infectado com um Staphylococcusspp., por exemplo, S. aureus.Em alguns aspectos, o soro convalescente pode ser de um animal infectado com o isolado 19636 da ATCC, cepa SAAV1, cepa 2176 ou cepa 1477. Os polipeptídeos da presente invenção podem ter atividade imunorreguladora. "Atividade imunorreguladora" se refere à capacidade de um polipeptídeo de atuar de uma maneira inespecífica para aumentar uma resposta imunológica a um antígeno particular. Os métodos para a determinação do fato de um polipeptídeo ter atividade imunorreguladora são conhecidos na técnica.
Um polipeptídeo da presente invenção pode ter as características de um polipeptídeo expresso por um microorganismo de referência. As características podem incluir tanto o peso molecular quanto o "fingerprint"de massa. O microorganismo de referência pode ser um gram-positivo, preferencialmente um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, Staphylococcus aureus.Os exemplos preferidos de cepa são detalhados na Tabela 1. Tabela 1. Cepas bacterianas.
Quando o microorganismo de referência for o isolado 19636 da ATCC de S. aureus,um polipeptídeo candidato é considerado como sendo um polipeptídeo da presente invenção se este tiver um peso molecular de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa 35 kDa ou 33 kDa e tiver um "fingerprint"de massa que é similar ao "fingerprint"de massa de um polipeptídeo regulado por metais expresso por um microorganismo de referência e que possui um peso molecular de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa 35 kDa ou 33 kDa, respectivamente. Preferencialmente, tais polipeptídeos são regulados por metais. Por exemplo, um polipeptídeo candidato é um polipeptídeo da presente invenção se este tiver um peso molecular de 88 kDa e tiver um "fingerprint"de massa similar ao "fingerprint"de massa de um polipeptídeo de 88 kDa regulado por metais produzido pelo isolado 19636 da ATCC de S. aureusda cepa de referência.
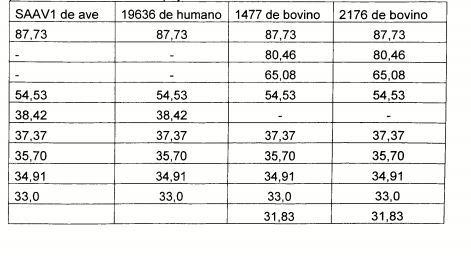
Quando o microorganismo de referência for o isolado SAAV1 de S. aureus,um polipeptídeo candidato é considerado como sendo um polipeptídeo da presente invenção se este tiver um peso molecular (como determinado por SDS-PAGE) de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa ou 33 kDa e tiver um "fingerprint"de massa que é similar ao "fingerprint" de massa de um polipeptídeo expresso por um microorganismo de referência e que possui um peso molecular (como determinado por SDS-PAGE) de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa ou 33 kDa, respectivamente. Preferencialmente, tais polipeptídeos são regulados por metais. Por exemplo, um polipeptídeo candidato é um polipeptídeo da presente invenção se este tiver um peso molecular de 88 kDa e tiver um "fingerprint"de massa similar ao "fingerprint"de massa de um polipeptídeo de 88 kDa regulado por metais produzido pelo isolado SAAV1 de S. aureusda cepa de referência.
Quando o microorganismo de referência for a cepa de 2176 de S. aureus,um polipeptídeo candidato é considerado como sendo um polipeptídeo da presente invenção se este tiver um peso molecular (como determinado por SDS-PAGE) de 88 kDa, 80 kDa, 65 kDa, 55 kDa, 37 kDa, 36 kDa, 35 kDa, 33 kDa ou 32 kDa e tiver um "fingerprint"de massa que é similar ao "fingerprint"de massa de um polipeptídeo expresso por um microorganismo de referência e que possui um peso molecular (como determinado por SDS-PAGE) de 88 kDa, 80 kDa, 65 kDa, 55 kDa, 37 kDa, 36 kDa, 35 kDa, 33 kDa ou 32 kDa, respectivamente. Preferencialmente, tais polipeptídeos são regulados por metais. Por exemplo, um polipeptídeo candidato é um polipeptídeo da presente invenção se este tiver um peso molecular de 88 kDa e tiver um "fingerprint"de massa similar ao "fingerprint"de massa de um polipeptídeo de 88 kDa regulado por metais produzido pelo isolado 2176 de S. aureusda cepa de referência.
Quando o microorganismo de referência for a cepa 1477 de S. aureus,um polipeptídeo candidato é considerado como sendo um polipeptídeo da presente invenção se este tiver um peso molecular (como determinado por SDS-PAGE) de 88 kDa, 80 kDa, 65 kDa, 55 kDa, 37 kDa, 36 kDa, 35 kDa, 33 kDa ou 32 kDa e tiver um "fingerprint"de massa que é similar ao "fingerprint"de massa de um polipeptídeo expresso por um microorganismo de referência e que possui um peso molecular (como determinado por SDSPAGE) de 88 kDa, 80 kDa, 65 kDa, 55 kDa, 37 kDa, 36 kDa, 35 kDa, 33 kDa ou 32 kDa, respectivamente. Preferencialmente, tais polipeptídeos são regulados por metais. Por exemplo, um polipeptídeo candidato é um polipeptídeo da presente invenção se este tiver um peso molecular de 88 kDa e tiver um "fingerprint"de massa similar ao "fingerprint"de massa de um polipeptídeo de 88 kDa regulado por metais produzido pelo isolado 1477 de S. aureusda cepa de referência.
Os polipeptídeos expressos por um microorganismo de referência e referidos anteriormente pelo peso molecular podem ser obtidos através do crescimento do microorganismo de referência sob condições de baixo teor de metais e do isolamento subsequente de um polipeptídeo através dos processos descritos aqui. Um polipeptídeo candidato pode ser isolado de um microorganismo, preferencialmente um microorganismo gram-positivo, mais preferencialmente, um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, Staphylococcus aureus.
Outros microorganismos gram-positivos dos quais os polipeptídeos podem ser isolados incluem Corynebacterium spp., Enterococcusspp.,
Erysipelothrix spp., Kytococcus spp. e Micrococcus spp., Mycobacterium spp. e Erysipelothrix spp. Um polipeptídeo candidato pode também ser produzido utilizando técnicas recombinantes, enzimáticas ou químicas.
Um polipeptídeo candidato pode ser avaliado através da análise espectrométrica de massa para determinar se o polipeptídeo candidato possui um "fingerprint"de massa similar ao de um dos polipeptídeos expressos por um microorganismo de referência e referido anteriormente pelo peso molecular. Tipicamente, o polipeptídeo candidato é isolado, por exemplo, através da resolução do polipeptídeo candidato por eletroforese em gel e do corte da parte do gel contendo o polipeptídeo candidato. Qualquer método de eletroforese em gel que separe os polipeptídeos com base nas características diferentes pode ser utilizado, incluindo a eletroforese em gel de uma dimensão ou bidimensional, assim como a separação cromatográfica líquida baseada, por exemplo, na hidrofobicidade, no pl ou no tamanho. O polipeptídeo candidato é fragmentado, por exemplo, através da digestão com uma protease. Preferencialmente, a protease cliva a ligação peptídica no lado carbóxi-terminal do aminoácido lisina e o aminoácido arginina, exceto quando o aminoácido após a lisina ou a arginina é uma prolina. Um exemplo de tal protease é a tripsina. Os métodos para digestão de um polipeptídeo com tripsina são rotineiros e conhecidos na técnica. Um exemplo de tal método é descrito no exemplo 13.
Os métodos para a análise espectrométrica de massa dos polipeptídeos são rotineiros e conhecidos na técnica e incluem, mas não estão limitados à espectroscopia de massa de tempo de vôo por dessorção/ionização a laser auxiliada por matriz (MALDI-TOF MS). Tipicamente, uma mistura contendo os fragmentos de polipeptídeos obtidos partindo de um polipeptídeo candidato é misturada com uma matriz que funciona para transformar a energia do laser na amostra e produz fragmentos de polipeptídeos ionizados, preferencialmente monoisotópicos. Os exemplos de matrizes que podem ser utilizadas incluem, por exemplo, o ácido sinapínico ou o ácido ciano-4-hidroxicinâmico. Um exemplo de um método para a análise de polipeptídeos por MALDI-TOF MS é descrito no exemplo 13. Os fragmentos de polipeptídeos ionizados são separados de acordo com sua proporção de m/z e detectados por produzirem um espectro de proporção de m/z versus intensidade. O espectro inclui valores de m/z que representam os fragmentos de polipeptídeos derivados do polipeptídeo candidato. Para qualquer polipeptídeo fornecido, a quantidade de cada fragmento de polipeptídeo resultante de uma digestão com tripsina deve ser equimolar. Entretanto, sabe-se que a digestão com tripsina não é sempre 100% eficiente, por exemplo, alguns locais são mais eficientemente clivados. Assim, quando a MALDI-TOF MS é utilizada para determinar os valores de m/z, a intensidade de cada valor m/z tipicamente não é idêntica. De forma geral, um espectro possui um nível de ruído de fundo presente ao longo da maior parte do eixo x (isto é, o eixo que possui os valores das proporções de m/z). Este nível de ruído de fundo varia dependendo das condições de corrida e da máquina utilizada e é facilmente identificado por inspeção visual do espectro. Um valor de m/z é geralmente considerado como representante de um fragmento de polipeptídeo quando a intensidade for pelo menos duas vezes maior, pelo menos 3 vezes maior ou pelo menos 4 vezes maior que o nível de ruído de fundo. O espectro inclui geralmente outros valores de m/z que são artefatos resultantes, por exemplo, da digestão incompleta, da superdigestão, de outros polipeptídeos que podem estar presentes na mistura ou da protease utilizada para digerir o polipeptídeo incluindo valores de m/z resultantes da autólise da protease. Este método de digestão de um polipeptídeo com uma protease é reconhecido na técnica como resultando em um "fingerprint"de massa de maior especificidade que pode ser utilizado para caracterizar acuradamente o polipeptídeo e distinguí-lo de outros polipeptídeos.
Neste aspecto da invenção, quando um polipeptídeo candidato é analisado por espectroscopia de massa, preferencialmente tanto o polipeptídeo candidato quanto o polipeptídeo proveniente do microorganismo de referência são preparados e analisados juntos, diminuindo assim quaisquer artefatos potenciais resultantes das diferenças na manipulação das amostras e das condições de corrida. Preferencialmente, todos os reagentes utilizados para preparar e analisar os dois polipeptídeos são os mesmos. Por exemplo, o polipeptídeo proveniente do microorganismo de referência e o polipeptídeo candidato são isolados sob substancialmente as mesmas condições, fragmentados sob substancialmente as mesmas condições e analisados por MALDI-TOF MS na mesma máquina sob substancialmente as mesmas condições. Um "fingerprint"de massa de um polipeptídeo candidato é considerado como sendo ao "fingerprint"de massa de um polipeptídeo proveniente de um microorganismo de referência quando pelo menos 80%, pelo menos 90%, pelo menos 95% ou substancialmente todos os valores de m/z presentes no espectro do polipeptídeo do microorganismo de referência e acima do nível de ruído de fundo estiverem também presentes no espectro do polipeptídeo candidato.
Em um outro aspecto, um polipeptídeo é considerado como sendo um polipeptídeo da presente invenção se este tiver um peso molecular de um polipeptídeo de referência descrito na Tabela 2, 3, 4 ou 5 e tiver um "fingerprint"de massa que inclui a população de fragmentos de polipeptídeos do polipeptídeo de referência como listado na Tabela 2, 3, 4 ou 5. Por exemplo, um polipeptídeo da presente invenção inclui um polipeptídeo de 88 kDa e um "fingerprint"de massa que inclui fragmentos de polipeptídeos que possuem massas de HVDVR, YSYER, IIGDYRR, IFTDYRK, ELKELGQK, YAQVKPIR, QMQFFGAR, SMQPFGGIR, VSGYA VNFIK, NHATAWQGFK, LWEQVMQLSK, SLGKEPEDQNR, DGISNTFSIVPK, AGVITGLPDAYGR, TSTFLDIYAER, SMQPFGGIRMAK, THNQGVFDAYSR, KAGVITGLPDAYGR, TLLYAINGGKDEK, IEMALHDTEIVR, AGEPFAPGANPMHGR, VALYGVDFLMEEK, KTHNQGVFDAYSR, YGFDLSRPAENFK, TSSIQYENDDIMR, KAGEPFAPGANPMHGR, RVALYGVDFLMEEK, LWEQVMQLSKEER, MLETNKNHATAWQGFK, MHDFNTMSTEMSEDVIR, YGNNDDRVDDIAVDLVER, ETLIDAMEHPEEYPQLTIR, YAQVKPIRNEEGLWDFEIEGDFPK. O "fingerprint"de massa de um polipeptídeo candidato pode ser determinado através de um método espectrométrico de massa, por exemplo, por MALDI-TOF MS. O "fingerprint"de massa de um polipeptídeo candidato terá geralmente fragmentos adicionais de polipeptídeos e, portanto, valores de m/z adicionais sem ser os listados para um polipeptídeo na Tabela 2, 3, 4 ou 5. Preferencialmente, quando o polipeptídeo candidato estiver sendo comparado com um polipeptídeo na Tabela 2, 3, 4 ou 5, o polipeptídeo candidato pode ser isolado de um microorganismo, preferencialmente um microorganismo gram-positivo, mais preferencialmente, um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, Staphylococcus aureus.Outros microorganismos gram-positivos incluem Corynebacterium spp., Enterococcusspp., Erysipelothrix spp., Kytococcusspp., Listeriaspp., Micrococcusspp. e Mycobacteriumspp. e Erysipelothrix spp. Um polipeptídeo candidato pode ser obtido através do crescimento de um microorganismo sob condições de baixo teor de metais e do isolamento subsequente de um polipeptídeo através dos processos descritos aqui.
É bem-conhecido na técnica que modificações de aminoácidos podem ser acidentalmente introduzidas durante a manipulação das amostras, tais como, a oxidação e a formação de derivados de carbamidometila. Ainda, estes tipos de modificações alteram o valor de m/z de um fragmento polipeptídico. Por exemplo, se um fragmento polipeptídico contiver uma metionina que é oxidada, o valor de m/z será aumentado em 16 em relação ao mesmo fragmento que não contém a metionina oxidada. Consequentemente, estes fragmentos polipeptídicos na Tabela 2, 3, 4 ou 5 que possuem a notação "oxidação (M)" possuem um valor de m/z que é maior em 16 em relação ao mesmo fragmento que não contém a metionina oxidada. É entendido que os fragmentos polipeptídicos da Tabela 2, 3 ,4 ou 5 podem ser modificados durante a manipulação das amostras.
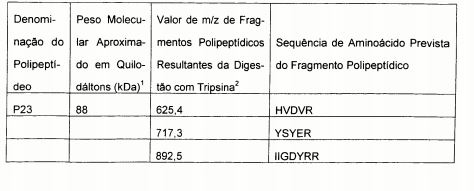
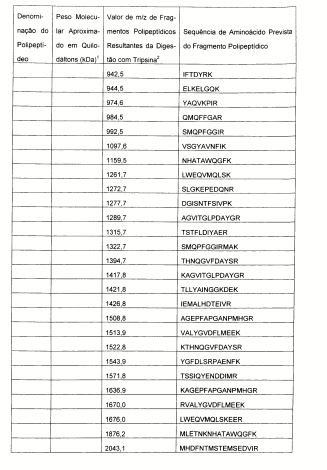
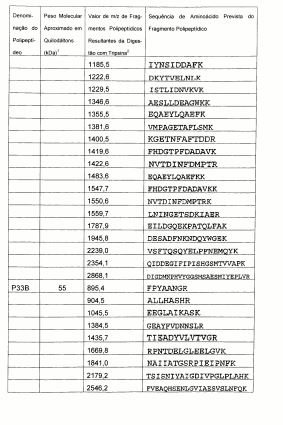
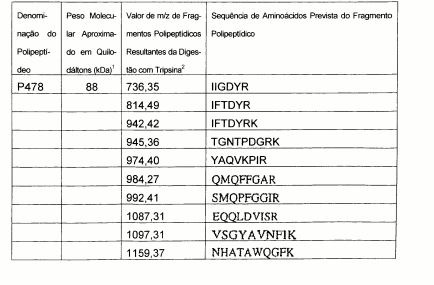
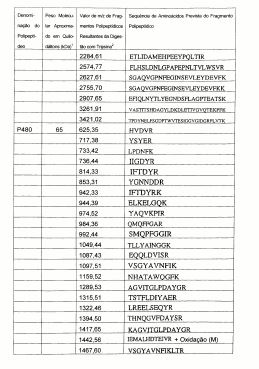
Tabela 2. Características dos polipeptídeos obtidos do isolado 19636 da ATCC de S. aureus.
1. Peso molecular como determinado por SDS-PAGE. 2. O valor de m/z de um fragmento polipeptídico pode ser convertido na massa através da subtração de 1 do valor de m/z. Cada massa inclui uma faixa de mais ou menos 300 partes por milhão (ppm) ou mais ou menos 1 Da.
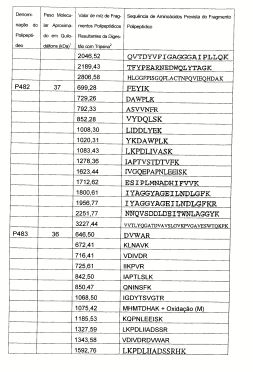
Tabela 3. Características dos polipeptídeos obtidos do isolado SAAV1 de S. aureus.
1. Peso molecular como determinado por SDS-PAGE. 2. O valor de m/z de um fragmento polipeptídico pode ser convertido na massa através da subtração de 1 do valor de m/z. Cada massa inclui uma faixa de mais ou menos 300 partes por milhão (ppm) ou mais ou menos 1 Da.
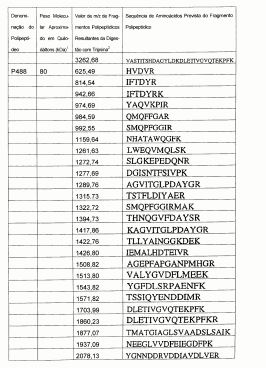
Tabela 4. Características dos polipeptídeos obtidos do isolado 2176 de S. aureus.
1. Peso molecular como determinado por SDS-PAGE. 2. O valor de m/z de um fragmento polipeptídico pode ser convertido na massa através da subtração de 1 do valor de m/z. Cada massa inclui uma faixa de mais ou menos 400 partes por milhão (ppm) ou 1 Dalton.
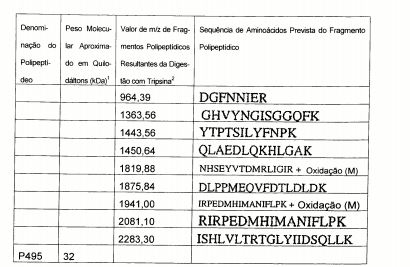
Tabela 5. Características dos polipeptídeos obtidos do isolado 1477 bovino de S. aureus.
1. Peso molecular como determinado por SDS-PAGE.2. O valor de m/z de um fragmento polipeptídico pode ser convertido na massa através da subtração de 1 do valor de m/z. Cada massa inclui uma faixa de mais ou menos 300 partes por milhão (ppm) ou mais ou menos 1 Da.
Ainda em um BLASTP do algoritmo de busca BLAST 2, como descrito por Tatusova e outros, (FEMS Microbiol Lett 1999, 174: 247-250) e disponível na World Wide Web, por exemplo, no site da internet mantido pelo National Center for Biotechnology Information, National Institutes of Health. Preferencialmente, os valores preestabelecidos para todos os parâmetros de busca do BLAST 2 são utilizados, incluindo matriz = BLOSUM62; penalidade de espaço aberto = 11, penalidade de extensão de espaço = 1, espaço x "dropoff'= 50, esperado = 10, tamanho da palavra = 3 e opcionalmente, filtro acionado. Na comparação de duas sequências de aminoácidos utilizando o algoritmo de busca BLAST, a similaridade estrutural é referida como "identidades". Preferencialmente, uma sequência de aminoácidos candidata possui pelo menos 80% de identidade, pelo menos 90% de identidade, pelo menos 95% de identidade, pelo menos 96% de identidade, pelo menos 97% de identidade, pelo menos 98% de identidade ou pelo menos 99% de identidade a uma sequência de aminoácidos de referência. Preferencialmente, o peso molecular da sequência de aminoácidos candidata e da sequência de aminoácidos de referência tem substancialmente o mesmo valor. Preferencialmente, o peso molecular da sequência de aminoácidos candidata e da sequência de aminoácidos de referência é determinado por eletroforese em gel de SDS poliacrilamida. Um polipeptídeo candidato pode ser obtido através do crescimento de um microorganismo sob condições de baixo teor de metais e do isolamento subsequente de um polipeptídeo através dos procedimentos descritos aqui.
Tipicamente, uma sequência de aminoácidos candidata que possui similaridade estrutural a uma sequência de aminoácidos de referência possui atividade imunogênica, atividade imunogênica protetora, atividade soroativa, atividade imunorreguladora ou uma combinação das mesmas.
Tabela 7: S. Aureus Saav1.<<Draw-code>> 1. Peso Molecular Como Determinado Por Sds-page.
Os polipeptideos Um polipeptídeo candidato pode também ser produzido utilizando técnicas recombinantes, enzimáticas ou químicas.
São também fornecidas pela presente invenção preparações de células inteiras de um microorganismo, em que o microorganismo expressa 5 um ou mais dos polipeptídeos da presente invenção. As células presentes em uma preparação de células inteiras são preferencialmente inativadas de forma que as células não podem se replicar, mas a atividade imunogênica dos polipeptídeos da presente invenção expressos pelo microorganismo é mantida. Tipicamente, as células são mortas através da exposição a agentes 10 tal como glutaraldeído, formalina ou formaldeído.
Uma composição da presente invenção pode incluir pelo menos um polipeptídeo descrito aqui ou um número de polipeptídeos que é um número inteiro maior que 1 (por exemplo, pelo menos 2, pelo menos 3, pelo 15 menos 4). Por exemplo, uma composição pode incluir 2, 3, 4, 5 ou mais polipeptídeos regulados por metais isolados que possuem pesos moleculares de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa, 33 kDa ou qualquer subconjunto ou combinação dos mesmos. Uma composição pode incluir polipeptídeos que podem ser isolados de 1 microorganismo ou podem ser isola20 dos de uma combinação de 2 ou mais microorganismos. Por exemplo, uma composição pode incluir polipeptídeos que podem ser isolados de 2 ou mais Staphyloccocus spp. ou de um Staphyloccocus spp. e um microorganismo diferente que não é um membro do gênero Staphyloccocus. A presente invenção fornece ainda composições que incluem uma preparação de células 25 inteiras, em que a célula inteira expressa um ou mais dos polipeptídeos da presente invenção. Por exemplo, a célula inteira pode ser um Staphyloccocus spp. Em alguns aspectos, uma composição pode incluir preparações inteiras de 2, 3, 4, 5 ou 6 cepas.
Opcionalmente, um polipeptídeo da presente invenção pode es30 tar ligado covalentemente ou conjugado a um polipeptídeo veículo para aumentar as propriedades imunológicas do polipeptídeo. Os polipeptídeos veículos úteis são conhecidos na técnica. O acoplamento químico dos polipeptídeos da presente invenção pode ser realizado utilizando métodos conhecidos e rotineiros. Por exemplo, vários reagentes de reticulação homobifunctionais e/ou heterobifunctionais tais como bis (sulfossuccinimidil) suberato, bis (diazobenzidina), adipimidato de dimetila, pimelimidato de dimetila, superimidato de dimetila, suberato de dissuccinimidila, glutaraldeído, mmaleimidobenzoil-N-hidroxissuccinimida, sulfo-m-maleimidobenzoil-Nhidroxissuccinimida, 4-(N-maleimidometil) ciclohexano-1-carboxilato de sulfossuccinimidila, 4-(p-maleimido-fenil) butirato de sulfosuccinimidila e (1-etil3-(dimetil-aminopropil) carbodiimida podem ser utilizados (vide, por exemplo, Harlow e Lane, Antibodies, A Laboratory Manual, de forma geral e Capítulo 5, Cold Spring Harbor Laboratory, Cold Spring Harbor, Nova York, NY (1988)).
As composições da presente invenção incluem ainda opcionalmente um veículo farmaceuticamente aceitável. "Farmaceuticamente aceitável" se refere a um diluente, um veículo, um excipiente, um sal etc, que são compatíveis com os outros ingredientes da composição e não deletérios ao receptor dos mesmos. Tipicamente, a composição inclui um veículo farmaceuticamente aceitável quando a composição for utilizada como descrito aqui. As composições da presente invenção podem ser formuladas em preparações farmacêuticas em uma variedade de formas adaptadas para a rota escolhida de administração, incluindo as rotas adequadas para estimular uma resposta imunológica a um antígeno. Assim, uma composição da presente invenção pode ser administrada através de rotas conhecidas incluindo, por exemplo, oral; parental incluindo intradermal, transcutânea e subcutânea; intramuscular, intravenosa, intraperitoneal etc. e de forma tópica, tai como, intranasal, intrapulmonar, intramamária, intravaginal, intrauterina, intradermal, transcutânea e retal etc. É previsto que uma composição pode ser administrada a uma superfície de mucosa, tal como através da administração na mucosa nasal ou respiratória (por exemplo, spray ou aerossol), para estimular a imunidade da mucosa, tal como a produção de anticorpos IgA secretores, ao longo de todo o corpo do animal.
Uma composição da presente invenção pode ainda ser administrada através de um implante de liberação controlada ou retardada. Os implantes adequados para uso de acordo com a invenção são conhecidos e incluem, por exemplo, os descritos em Emery e Straub (WO 01/37810 (2001)) e Emery e outros, (WO 96/01620 (1996)). Os implantes podem ser produzidos em tamanhos pequenos o suficiente para serem administrados por aerossol ou spray. Os implantes incluem ainda nanoesferas e microesferas.
Uma composição da presente invenção pode ser administrada em uma quantidade suficiente para tratar certos estados de saúde como descrito aqui. A quantidade de polipeptídeos ou de células inteiras presentes em uma composição da presente invenção pode variar. Por exemplo, a dosagemm de polipeptídeos pode estar entre 0,01 microgramas (μg) e 300 mg, tipicamente entre 0,1 mg e 10 mg. Quando a composição for uma preparação de células inteiras, as células podem estar presentes a uma concentração de, por exemplo, 102bactérias/mL, 103 bactérias/mL, 104 bactérias/mL, 105 bactérias/mL, 106 bactérias/mL, 107 bactérias/mL, 108 bactérias/mL ou 109 bactérias/mL. Para uma composição injetável (por exemplo, subcutânea, intramuscular etc.) os polipeptídeos podem estar presentes na composição em uma quantidade tal que o volume total da composição administrada seja de 0,5 mL até 5,0 mL, tipicamente de 1,0-2,0 mL. Quando a composição for uma preparação de células inteiras, as células estão preferencialmente presentes na composição em uma quantidade que o volume total da composição administrada seja de 0,5 mL até 5,0 mL, tipicamente de 1,0-2,0 mL. A quantidade administrada variará dependendo de vários fatores incluindo, mas não limitados aos polipeptídeos específicos escolhidos, ao peso, à condição física e à idade do animal e da rota de administração. Assim, o peso absoluto do polipeptídeo incluído em uma certa forma de dosagemm unitária pode variar amplamente e depende de fatores, tais como, a espécie, a idade, o peso e a condição física do animal, assim como, o método de administração. Tais fatores podem ser determinados por um versado na técnica. Outros exemplos de dosagens adequadas para a invenção são descritos em Emery e outros, (Patente U.S. N2 6.027.736).
As formulações podem ser apresentadas de forma conveniente na forma de dosagem unitária e podem ser preparadas através de métodos bem-conhecidos na técnica da farmácia. Os métodos de preparação de uma composição com um veículo farmaceuticamente aceitável incluem a etapa de colocar o composto ativo (por exemplo, um polipeptídeo ou uma célula inteira da presente invenção) em associação com um veículo que constitui um ou mais ingredientes acessórios. Em geral, as formulações são preparadas colocando uniformente e intimamente o composto ativo em associação com um veículo líquido, um veículo sólido finamente dividido ou ambos e então, se necessário, moldando o produto nas formulações desejadas.
Uma composição que inclui um veículo farmaceuticamente aceitável também pode incluir um adjuvante. Um "adjuvante"se refere a um agente que pode atuar de uma maneira inespecífica para aumentar a resposta imunológica para um antígeno particular, reduzindo potencialmente, assim, a quantidade de antígeno necessária em qualquer certa composição de imunização e/ou a frequência de injeção necessária para gerar uma resposta imunológica adequada para o antígeno de interesse. Os adjuvantes podem incluir, por exemplo, IL-1, IL-2, emulsificantes, dipeptídeo de muramilas, brometo de dimetil dioctadecil amónio (DDA), avridina, hidróxido de alumínio, óleos, saponinas, alfa-tocoferol, polissacarídeos, parafinas emulsificadas (incluindo, por exemplo, as disponíveis sob o nome comercial EMULSIGEN da MVP Laboratories, Ralston, Nebraska), ISA-70, RIBI e outras substâncias conhecidas na técnica. É esperado que os polipeptídeos da presente invenção tenham atividade imunorreguladora e que tais polipeptídeos possam ser utilizados como adjuvantes que atuam diretamente como ativadores de células T e/ou B ou que atuam sobre tipos celulares específicos que aumentam a síntese de várias citocinas ou que ativam as vias de sinalização intracelular. É esperado que tais polipeptídeos aumentem a resposta imunológica para aumentar o índice protetor da composição existente.
Em uma outra modalidade, uma composição da invenção que inclui um veículo farmaceuticamente aceitável pode incluir um modificador da resposta biológica, tal como, por exemplo, IL-2, IL-4 e/ou IL-6, TNF, IFNalfa, IFN-gama e outras citocinas que afetam as células imunológicas. Uma composição de imunização também pode incluir outros componentes conhecidos na técnica tal como um antibiótico, um agente conservante, um antioxidante ou um agente quelante.
A presente invenção fornece ainda métodos para a obtenção dos polipeptídeos descritos aqui. Os polipeptídeos e as células inteiras da presente invenção podem ser isolados de um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, Staphylococcus aureus.Outros microorganismos gram-positivos dos quais os polipeptídeos podem ser isolados incluem Corynebacterum spp., Erysipelothrixspp., Mycobacteriumspp. e Erysipelothrix spp. Os microorganismos úteis para a obtenção dos polipeptídeos da presente invenção e para a produção de preparações de células inteiras estão disponíveis comercialmente em um banco tal como a American Type Culture Collection (ATCC). Em adição, tais microorganismos podem ser facilmente obtidos através de técnicas de rotina e conhecidas na técnica. Os microorganismos podem ser derivados de um animal infectado na forma de um isolado de campo e utilizado para a obteção dos polipeptídeos e/ou das preparações de células inteiras da presente invenção ou armazenados para uso futuro, por exemplo, em um banco congelado a -20°C até -95°C ou -40°C até -50°C, em meios bacteriológicos contendo 20% de glicerol e outros meios similares.
Quando um polipeptídeo da presente invenção tiver que ser obtido partindo de um microorganismo, o microorganismo pode ser incubado sob condições de baixo teor de metais. Como utilizado aqui, a expressão "condições de baixo teor de metais" se refere a um ambiente, tipicamente um meio bacteriológico, que contém quantidades de um metal livre que faz com que um microorganismo expresse os polipeptídeos regulados por metais em um nível detectável. Como utilizado aqui, a expressão "condições de alto teor de metais" se refere a um ambiente que contém quantidades de um metal livre que faz com que um microorganismo não expresse um ou mais dos polipeptídeos regulados por metais descritos aqui em um nível detectável ou diminua a expressão de tal polipeptídeo. Os metais são os presentes na tabela periódica sob os Grupos 1 até 17 (notação IUPAC; também referidos como os Grupos l-A, ll-A, lll-B, IV-B, V-B, Vl-B, VII-B, VIII, l-B, ll-B, lll-A, IV-A, V-A, Vl-A e VIl-A, respectivamente, sob a notação CAS). Preferencialmente, os metais são aqueles nos Grupos 2 até 12, mais preferencialmente, Grupos 3-12. Ainda mais preferencialmente, o metal é ferro, zinco, cobre, magnésio, níquel, cobalto, manganês, molibdênio ou selênio, mais preferencialmente, ferro.
As condições de baixo teor de metais são geralmente o resultado da adição de um composto quelante de metal a um meio bacteriológico, o uso de um meio bacteriológico que contém baixas quantidades de um metal ou a combinação dos mesmos. As condições de alto teor de metais estão geralmente presentes quando um quelante não está presente no meio, um metal é adicionado ao meio ou a combinação dos mesmos. Os exemplos de quelantes de metais incluem compostos naturais e sintéticos. Os exemplos de compostos naturais incluem compostos fenólicos vegetais, tais como, flavenóides. Os exemplos de flavenóides incluem os quelantes de cobre catequina e naringenina e os quelantes de ferro miricetina e quercetina. Os exemplos de quelantes sintéticos de cobre incluem, por exemplo, tetratiomolibdato e os exemplos de quelantes sintéticos de zinco incluem, por exemplo, N,N,N',N'-tetracis (2-piridilmetil)-etileno diamina. Os exemplos de quelantes sintéticos de ferro incluem 2,2-dipiridila (também referido na técnica como α,α'-bipiridila), 8-hidroxiquinolina, ácido etilenodiamina-di-O-hidroxifenilacético (EDDHA), desferrioxamina metanossulfonato (desferol), transferrina, lactoferrina, ovotransferrina, sideróforos biológicos, tais como, os catecolatos e os hidroxamatos e o citrato. Um exemplo de um quelante de cátion divalente geral é a resina Chelex®. Preferencialmente, 2,2’-dipiridila é utilizado para quelar o ferro. Tipicamente, 2,2-dipiridila é adicionado no meio a uma concentração de pelo menos 300 microgramas/mililitro (μg/mL), pelo menos 600 μg/mL ou pelo menos 900 μg/mL. Altos níveis de 2,2'-dipiridila podem ser 1200 μg/mL, 1500 μg/mL ou 1800 μg/mL.
O genoma de S. aureuscodifica três homólogos Fur: Fur, PerR e Zur. Embora as proteínas Zur e PerR pareçam estar primariamente envolvidas na regulação da homeostase do zinco e dos genes de estresse a peróxido, respectivamente, foi demonstrado que a proteína Fur regula vários sistemas de captação de sideróforos de ferro em resposta à limitação de ferro. A proteína Fur também desempenha uma função na resistência ao estresse oxidativo e na virulência. É esperado que um organismo gram-positivo, preferencialmente, um S. aureus,com uma mutação em um gene fur resulte na expressão constitutiva de muitos, se não de todos, os polipeptídeos regulados por metais da presente invenção. A produção de uma mutação fur em um gram-positivo, preferencialmente, um S. aureus,pode ser obtida utilizando métodos de rotina incluindo, por exemplo, mutagênese por transposon, química ou direcionada ao sítio útil para a produção de mutações de nocaute gênico em bactérias gram-positivas.
O meio utilizado para incubar o microorganismo e o volume do meio utilizado para incubar o microorganismo podem variar. Quando um microorganismo estiver sendo avaliado em relação à capacidade de produzir um ou mais dos polipeptídeos descritos aqui, o microorganismo pode ser crescido em um volume adequado, por exemplo, 10 mililitros até 1 litro de meio. Quando um microorganismo estiver sendo crescido para a obtenção de polipeptídeos para uso, por exemplo, na administração a animais, o microorganismo pode ser crescido em um fermentador para permitir o isolamento de quantidades maiores de polipeptídeos. Os métodos para o crescimento de microorganismos em um fermentador são rotineiros e conhecidos na técnica. As condições para o crescimento de um microorganismo incluem preferencialmente um quelante de metal, mais preferencialmente, um quelante de ferro, por exemplo, 2,2'-dipiridila, um pH entre 6,5 e 7,5, preferencialmente entre 6,9 e 7,1 e uma temperatura de 37°C.
Em alguns aspectos da invenção, um microorganismo pode ser coletado após o crescimento. A coleta inclui a concentração do microorganismo em um volume menor e a suspensão em um meio diferente que o meio de cultura. Os métodos para concentrar um microorganismo são rotineiros e conhecidos na técnica e incluem, por exemplo, filtração ou centrifugação. Tipicamente, o microorganismo concentrado é suspenso em um tampão apropriado. Um exemplo de um tampão que pode ser utilizado contém Tris-base (7,3 gramas/litro), em um pH de 8,5. Opcionalmente, o tampão final também minimiza a degradação proteolítica. Isto pode ser realizado possuindo um tampão final em um pH maior que 8,0, preferencialmente, de pelo menos 8,5 e/ou incluindo um ou mais inibidores de proteinase (por exemplo, fluoreto de fenilmetanossulfonila). Opcionalmente e preferencialmente, o microorganismo concentrado é congelado a -20°C ou abaixo disso até ser rompido.
Quando o microorganismo tiver que ser utilizado como uma preparação de células inteiras, as células coletadas podem ser processadas utilizando métodos de rotina e conhecidos para inativar as células. Alternativamente, quando um microorganismo tiver que ser utilizado para preparar os polipeptídeos da presente invenção, o microorganismo pode ser rompido utilizando métodos químicos, físicos ou mecânicos de rotina e conhecidos na técnica, incluindo, por exemplo, fervura, prensa francesa, ultra-som, digestão de peptidoglicana (por exemplo, através da digestão com lisozima) ou homogenização. Um exemplo de um dispositivo adequado útil para a homogenização é um Avestin Homogenizer modelo C500-B, (Avestin Inc, Ottawa Canadá). Como utilizado aqui, "rompimento" se refere à quebra da célula. O rompimento de um microorganismo pode ser medido através de métodos que são rotineiros e conhecidos na técnica, incluindo, por exemplo, alterações na densidade óptica. Tipicamente, um microorganismo é submetido ao rompimento até a transmitância percentual ser aumentada em 20% quando uma diluição de 1:100 é medida. Quando métodos físicos ou mecânicos são utilizados, a temperatura durante o rompimento é mantida tipicamente baixa, preferencialmente a 4°C, para minimizar adicionalmente a degradação proteolítica. Quando os métodos químicos são utilizados, a temperatura pode ser aumentada para otimizar o rompimento celular. Uma combinação de métodos químicos, físicos e mecânicos pode também ser utilizada para solubilizar a parede celular do microorganismo. Como utilizado aqui, o termo "solubilizar" se refere à dissolução de materiais celulares (por exemplo, polipeptídeos, ácidos nucléicos, carboidratos) na fase aquosa do tampão em que o microorganismo foi rompido e à formação de agregados de materiais celulares insolúveis. Sem pretender estar limitado por teoria, acredita-se que as condições para a solubilização resultam na agregação dos polipeptídeos da presente invenção em agregados insolúveis que são grandes o suficiente para permitir o isolamento fácil, por exemplo, através da centrifugação.
Os agregados insolúveis que incluem um ou mais dos polipeptídeos da presente invenção podem ser isolados através de métodos que são rotineiros e conhecidos na técnica. Preferencialmente, os agregados insolúveis são isolados por centrifugação. Tipicamente, a centrifugação dos polipeptídeos, tais como, os polipeptídeos de membrana, pode ser realizada através de forças centrífugas de 100.000 x g. O uso de tais forças centrífugas requer o uso de ultracentrífugas e o aumento da escala para volumes grandes do processo de amostras é frequentemente difícil e não econômico com estes tipos de centrífugas. Os métodos descritos aqui fornecem a produção de agregados insolúveis grandes o suficiente para permitir o uso de centrífugas de fluxo contínuo, por exemplo, T-1 Sharpies (Alfa Laval Separations, Warminster, PA), que podem ser utilizadas com uma vazão de 250 mL/minuto a 0,117 MPa (17 psi) a uma força centrífuga de 46.000 x g até 60.000 x g. Podem ser utilizadas outras centrífugas de grande escala, tais como, as configurações cilindro tubular, de câmara e de disco. Tais centrífugas são utilizadas rotineiramente e conhecidas na técnica e estão disponíveis comercialmente de fabricantes tais como Pennwalt, Westfalia e alpha-Laval.
As proteínas coletadas finais são lavadas e/ou submetidas à diálise contra um tampão apropriado utilizando métodos conhecidos na técnica, por exemplo, diafiltração, precipitação, cromatografia hidrofóbica, cromatografia de troca iônica ou cromatografia de afinidade ou ultrafiltração e lavagem dos polipeptídeos, por exemplo, em álcool, por diafiltração. Após o isolamento, os polipeptídeos são suspensos em tampão e armazenados à baixa temperatura, por exemplo, -20°C ou abaixo.
Em tais aspectos da presente invenção em que uma preparação de células inteiras tem que ser produzida, após o crescimento, um microorganismo pode ser morto com a adição de um agente tal como glutaraldeído, formalins ou formaldeído, a uma concentração suficiente para inativar as células na cultura. Por exemplo, a formalina pode ser adicionada a uma concentração de 0,3% (vol:vol). Após um período de tempo suficiente para inativar as células, as células podem ser coletadas, por exemplo, por diafiltração e/ou centrifugação e lavadas.
Um aspecto da presente invenção é adicionalmente direcionado aos métodos de utilização das composições da presente invenção. Os métodos incluem a administração a um animal de uma quantidade eficiente de uma composição da presente invenção. O animal pode ser, por exemplo, uma ave (incluindo, por exemplo, galinhas ou perus), um bovino (incluindo, por exemplo, gado), um caprino (incluindo, por exemplo, cabras), um ovino (incluindo, por exemplo, ovelha), um suíno (incluindo, por exemplo, porco), um bisão (incluindo, por exemplo, búfalo), um equino (incluindo, por exemplo, cavalos), um animal de companhia (incluindo, por exemplo, cães ou gatos), membros da família Cervidae (incluindo, por exemplo, cervo, alce, alce americano, caribu e rena) ou um ser humano.
Em alguns aspectos, os métodos podem incluir ainda administrações adicionais (por exemplo, uma ou mais administrações de reforço) da composição ao animal para aumentar ou estimular uma resposta imunológica secundária. Um reforço pode ser administrado em um momento após a primeira administração, por exemplo, 1 até 8 semanas, preferencialmente 2 até 4 semanas, após a primeira administração da composição. Os reforços subsequentes podem ser administrados uma, duas, três, quatro ou mais vezes ao ano. Sem pretender estar ligado à teoria, é esperado que em alguns aspectos da presente invenção os reforços anuais não sejam necessários, uma vez que o animal será desafiado no campo através da exposição aos microorganismos expressando os polipeptídeos presentes nas composições que possuem epitopos que são idênticos a ou estruturalmente relacionados aos epitopos presentes nos polipeptídeos da composição administrada ao animal.
Em um aspecto, a invenção está direcionada a métodos de produçâo de anticorpos, por exemplo, através da indução da produção de anticorpo em um animal ou através de técnicas recombinantes. O anticorpo produzido inclui o anticorpo que se liga especificamente a pelo menos um polipeptídeo presente na composição. Neste aspecto da invenção, uma "quantidade eficiente" é uma quantidade eficiente para resultar na produção de anticorpo no animal. Os métodos para a determinação do fato de um animal ter produzido anticorpos que se ligam especificamente aos polipeptídeos presentes em uma composição da presente invenção podem ser determinados como descrito aqui. A presente invenção inclui ainda anticorpos que se ligam especificamente a um polipeptídeo da presente invenção e composições que incluem tais anticorpos. O método pode ser utilizado para produzir o anticorpo que se liga especificamente aos polipeptídeos expressos por um microorganismo sem ser o microorganismo do qual os polipeptídeos da composição foram isolados. Como utilizado aqui, um anticorpo que pode "se ligar especificamente" a um polipeptídeo é um anticorpo que interage com o epitopo do antígeno que induziu a síntese do anticorpo ou que interage com um epitopo relacionado estruturalmente. Pelo menos alguns dos polipeptídeos presentes nas composições da presente invenção incuem tipicamente epitopos que são conservados nos polipeptídeos de espécies diferentes e de gêneros diferentes de microorganismos. Consequentemente, é esperado que o anticorpo produzido utilizando uma composição derivada de um microorganismo se ligue aos polipeptídeos expressos por outros microorganismos e forneça uma proteção de espectro amplo contra organismos gram-positivos. Os exemplos de microorganismos gram-positivos aos quais o anticorpo pode se ligar especificamente são Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, Staphylococcus aureus;membros da família Streptococcaceae, preferencialmente, Streptococcus pyogenes, Streptococcus pneumoniae, Streptococcus agalactiae, Streptococcus uberis, Streptococcus bovis, Streptococcus equi ou Streptococcus dysgalactiae; e Bacillus spp., Clostridium spp., Corynebacterium spp., Enterococcus spp., Erysipelothrix spp., Listeria spp., Micrococcus spp. e Mycobacterium spp., Kytococcus spp. e Erysipelothrix spp.
A presente invenção se direciona ainda ao uso de tal anticorpo para se direcionar a um microorganismo que expressa um polipeptídeo da presente invenção ou um polipeptídeo que possui um epitopo estruturalmente relacionado a um epitopo presente em um polipeptídeo da presente invenção. Um composto pode estar ligado de forma covalente a um anticorpo, em que o composto pode ser, por exemplo, uma toxina. Similarmente, tais compostos podem estar ligados covalentemente a um sideróforo bacteriano para o direcionamento para o microorganismo. O acoplamento ou a conjugação química de um anticorpo da presente invenção ou uma parte do mesmo (tal como um fragmento Fab), pode ser realizada utilizando métodos conhecidos e rotineiros. Em um aspecto, a invenção se direciona ainda ao tratamento de uma infecção em um animal, incluindo um ser humano, causada por um microorganismo gram-positivo, preferencialmente por um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, S. aureus;membros da família Streptococcaceae, preferencialmente, Streptococcus pyogenes, Streptococcus pneumoniae, Streptococcus agalactiae, Streptococcus uberis, Streptococcus bovis, Streptococcus equi ou Streptococcus dysgalactiae; Bacillus spp., Clostridium spp., Corynebacterium spp., Enterococcus spp., Erysipelothrix spp., Kytococcus spp., Listeria spp., Micrococcus spp., Mycobacterium spp. e Erysipelothrix spp. Como utilizado aqui, o termo "infecção"se refere à presença de um microorganismo gram-positivo no corpo de um animal, que pode ou não ser clinicamente evidente. Um animal com uma infecção por um membro do gênero Staphylococcusque não é clinicamente evidente é frequentemente referido como um veículo assintomático. O método inclui a administração de uma quantidade eficiente da composição da presente invenção a um animal que possui uma infecção causada por um microorganismo gram-positivo e a determinação se o número de microorganismos que causam a infecção diminuiu. Os métodos para a determinação do fato de uma infecção ser causada por um microorganismo gram-positivo são rotineiros e conhecidos na técnica, como são os métodos para a determinação se a infecção aumentou.
Em um outro aspecto, a presente invenção está direcionada aos métodos para o tratamento de um ou mais sintomas de certos estados de saúde em um animal que podem ser causados pela infecção por um microorganismo gram-positivo, preferencialmente, por um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, S. aureus',membros da família Streptoococcaceae, preferencialmente, Streptococcus pyogenes, Streptococcus pneumoniae, Streptococcus agalactiae, Streptococcus uteris, Streptococcus bovis, Streptococcus equi ou Streptococcus dysgalactiae; Bacillus spp., Clostridium spp., Corynebacterium spp., Enterococcus spp., Erysipelothrix spp., Kytococcus spp., Listeria spp., Micrococcus spp., Mycobacterium spp. e Erysipelothrix spp. O método inclui a administração de uma quantidade eficiente de uma composição da presente invenção a um animal que tem ou está em risco de ter uma condição ou sintomas de um estado de saúde e a determinação do fato de que pelo menos um sintoma do estado de saúde é alterado, preferencialmente, reduzido. Os exemplos de estados de saúde causados por infecções microbianas incluem, por exemplo, mastite, septicemia, pneumonia, meningoencefalite, linfangite, dermatite, infecções do trato genital, sufocamentos, metrite, doença perinatal, abcessos na pituitária, artrite, bursite, orquite, cistite e pielonefrite, linfadenite caseosa, tuberculose, linfangite ulcerativa, listeriose, erisipelas, laminite, antrax, doença de tyzzer, tétano, botulismo, enterite, edema maligno, "braxy" (ou bradsot), hemoglobinúria bacilar, enterotoxemia, lesões necróticas da pele e infecções nosocomiais. Os exemplos de estados de saúde causados por S. aureusincluem ainda, por exemplo, botriomicose em cavalos, sinovite purilenta e osteomelite em aves, abortos em suínos e piemia por carrapatos em cordeiros. Os exemplos de estados de saúde causados por Streptococcusspp. incluem ainda, por exemplo, inflamação de garganta, febre escarlate, impetigo, endocardite ulcerativa, febre reumática e cervicite glomerulonefrite pós-estreptocóccica em seres humanos, cervicite em equinos e suínos e meningite e abscessos na papada em suínos.
O tratamento dos sintomas associados com estes estados de saúde pode ser profilático ou, alternativamente, pode ser iniciado após o desenvolvimento de um estado de saúde descrito aqui. Como utilizado aqui, o termo "sintoma" se refere a uma evidência objetiva em um indivíduo de um estado de saúde causado pela infecção por um microorganismo. Os sintomas associados com os estados de saúde referidos aqui e as avaliações de tais sintomas são rotineiros e conhecidos na técnica. O tratamento que é 5 profilático, por exemplo, iniciado antes de um indivíduo manifestar os sintomas de um estado de saúde causado por um microorganismo, é referido aqui como tratamento de um indivíduo que está "em risco" de desenvolver o estado de saúde. Tipicamente, um animal "em risco" de desenvolver um estado de saúde é um animal presente em uma área em que animais que têm 10 o estado de saúde foram diagnosticados e/ou provavelmente foram expostos a um microorganismo causador do estado de saúde. Consequentemente, a administração de uma composição pode ser realizada antes, durante ou depois da ocorrência dos estados de saúde descritos aqui. O tratamento iniciado após o desenvolvimento de um estado de saúde pode resultar na diminu15 ição da gravidade dos sintomas de um dos estados de saúde ou na remoção completa dos sintomas. Neste aspecto da invenção, uma "quantidade eficiente" é uma quantidade eficiente para prevenir a manifestação dos sintomas de uma doença, para diminuir a gravidade dos sintomas de uma doença e/ou remover completamente os sintomas. O tratamento bem sucedido de 20 uma infecção por um microorganismo gram-positivo em um animal é descrito no exemplo 5, que demonstra a proteção contra a doença causada por S. aureusem medelos de camundongos através da administração de uma composição da presente invenção. Estes modelos de camundongos constituem um modelo comumente aceito para estudo de doença humana causa25 da por estes microorganismos. O tratamento bem sucedido de uma infecção por microorganismo gram-positivo em um animal é também descrito nos exemplos 10-12, que demonstra a proteção contra a doença causada por S. aureusem vacas através da administração de uma composição da presente invenção.
A presente invenção fornece ainda métodos para diminuir a colonização por microorganismos gram-positivos, por exemplo, bloqueando os sítios de ligação do microorganismo gram-positivo, incluindo tecidos do sistema esquelético (por exemplo, ossos, cartilagem, tendões e ligamentos), sistema muscular, (por exemplo, músculos esqueléticos e lisos), sistema circulatório (por exemplo, coração, vasos sanguíneos, capilares e sangue), sistema nervoso (por exemplo, cérebro, medula espinhal e nervos periféricos), sistema respiratório (por exemplo, narina, traquéia, pulmões, brônquios, bronquicelos, alvéolos), sistema digestivo (por exemplo, boca, glândulas salivares, esôfago, fígado, estômago, intestinos grosso e delgado), sistema excretor (por exemplo, rins, ureteres, bexiga e uretra), sistema endócrino (por exemplo, hipotálamo, pituitária, tiróide, pâncreas e glândulas adrenais), sistema reprodutivo (por exemplo, ovários, oviduto, útero, vagina, glândulas mamárias, testículos e vesículas seminais), sistemas linfático/imunológico (por exemplo, linfa, nodos e vasos linfáticos, células sanguíneas mononucleares ou brancas, tais como, macrófagos, neutrófilos, monócitos, eosinófilos, basófilos, linfócitos e células T e B) e cepas de células específicas (por exemplo, células precursoras, células epiteliais, células-tronco) e similares. Preferencialmente, o microorganismo gram-positivo é um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, S. aureus;um membro da família Streptooccaceae, preferencialmente, Streptococcus pyogenes, Streptococcus pneumoniae, Streptococcus agalactiae, Streptococcus uberis, Streptococcus bovis, Streptococcus equi ou Streptococcus dysgalactiae', Bacillus spp., Clostridium spp., Corynebhacterium spp., Enterococus spp., Erysipelothrix spp., Kytococcus spp., Listeria spp., Micrococcus spp., Mycobacterium spp. e Erysipelothrix spp. O método inclui a administração de uma quantidade eficiente de uma composição da presente invenção a um animal colonizado por ou em risco de ser colonizado por, um microorganismo gram-positivo. Neste aspecto da invenção, uma "quantidade eficiente" é uma quantidade suficiente para diminuir a colonização do animal pelo microorganismo. Os métodos para a avaliação da colonização de um animal por um microorganismo são rotineiros e conhecidos na técnica. Por exemplo, a colonização do trato intestinal de um animal por um microorganismo pode ser determinada através da medida da presença do microorganismo nas fezes do animal. É esperado que a diminuição da colonização de um animal por um microorganismo reduza a transmissão do microorganismo a seres humanos.
Uma composição da invenção pode ser utilizada para fornecer imunização ativa ou passiva contra infecção bacteriana. De forma geral, a composição pode ser administrada a um animal para fornecer imunização ativa. Entretanto, a composição também pode ser utilizada para induzir a produção de produtos imunológicos, tais como, anticorpos, que podem ser coletados do animal produtor e administrados a um outro animal para fornecer imunidade passiva. Componentes imunológicos, tais como, anticorpos, podem ser coletados para preparar composições (preferencialmente contendo anticorpo) partindo do soro, do plasma, do sangue, do colostro etc. para terapias de imunização passiva. As composições de anticorpos incluindo anticorpos monoclonais e/ou antiidiotipos também podem ser preparadas utilizando métodos conhecidos. Os anticorpos quiméricos incluem regiões constantes derivadas de seres humanos das cadeias tanto pesada quanto leve e regiões variáveis derivadas de murinos que são específicas ao antígeno (Morrison e outros, Proc. Natl. Acad. Sei. USA, 1984, 81(21): 6851-5; LoBuglio e outros, Proc. Natl. Acad. Sei. USA, 1989, 86(11): 4220-4; Boulianne e outros, Nature, 1984, 312(5995): 643-6.). Os anticorpos humanizados substituem a região constante e a estrutura murinas (FR) (da região variável) pelos correspondentes humanos (Jones e outros, Nature, 1986, 321(6069): 522-5; Riechmann e outros, Nature, 1988, 332(6162): 323-7; Verhoeyen e outros, Science, 1988, 239(4847): 1534-6; Queen e outros, Proc. Natl. Acad. Sei. USA, 1989, 86(24): 10029-33; Daugherty e outros, Nucleic Acids Res., 1991, 19(9): 2471-6.). Alternativamente, podem ser utilizadas certas cepas de camundongos que foram engenheiradas geneticamente para produzir anticorpos que são quase completamente de origem humana; após a imunização, as células B destes camundongos são coletadas e imortalizadas para a produção de anticorpos monoclonais humanos (Bruggeman e Taussig, Curr. Opin. Biotechnol., 1997, 8(4): 455-8; Lonberg e Huszar, Int. Rev. Immunol., 1995; 13(1): 65-93; Lonberg e outros., Nature, 1994, 368: 856-9; Taylor e outros., Nucleic Acids Res., 1992, 20: 6287-95.). As composições passivas de anticorpos e fragmentos dos mesmos, por exemplo, scFv, Fab, F(ab')2 ou Fv ou outras formas modificadas dos mesmos, podem ser administradas a um receptor na forma de soro, plasma, sangue, colostro e similares. Entretanto, os anticorpos também podem ser isolados do soro, do plasma, do sangue, do colostro e similares, utilizando métodos conhecidos para uso posterior em uma forma concentrada ou reconstituída tal como, por exemplo, soluções para lavagem, molhos impregnados e/ou agentes tópicos e similares. As preparações para imunização passiva podem ser particularmente vantajosas para o tratamento de doença sistêmica aguda ou para a imunização passiva de animais jovens que falharam em receber níveis adequados de imunidade passiva através do colostro materno. Os anticorpos úteis para a imunização passiva podem também ser úteis para a conjugação com vários fármacos ou antibióticos que poderiam ser diretamente direcionados para bactérias que expressam durante uma infecção sistêmica ou localizada um polipeptídeo da presente invenção ou um polipeptídeo que possui um epitopo estruturalmente relacionado a um epitopo presente em um polipeptídeo da presente invenção.
Os modelos de animais, em particular, os modelos de camundongos, estão disponíveis para a avaliação experimental das composições da presente invenção. Estes modelos de camundongos são comumente aceitos para o estudo de doença humana causada por membros do gênero Staphylococcus e S. aureusem particular. Em tais casos em que um membro do gênero Staphylococcuscausa doença em um animal, por exemplo, uma vaca, o hospedeiro natural pode ser utilizado para avaliar experimentalmente as composições da presente invenção.
Um outro aspecto da presente invenção forence métodos para a detecção do anticorpo que se liga especificamente aos polipeptídeos da presente invenção. Estes métodos são úteis, por exemplo, na detecção do fato de um animal ter anticorpo que se liga especificamente aos polipeptídeos da presente invenção e no diagnóstico do fato de um animal poder ter um estado de saúde causado por um microorganismo que expressa os polipeptídeos descritos aqui ou que expressa polipeptídeos que compartilham epitopos com os polipeptídeos descritos aqui. Tais sistemas de diagnóstico podem estar na forma de um kit. Os métodos incluem o contato de um anticorpo com uma preparação que inclui um polipeptídeo da presente invenção para resultar em uma mistura. O anticorpo pode estar presente em uma amostra biológica, por exemplo, sangue, leite ou colostro. O método inclui ainda a incubação da mistura sob condições que permitam que o anticorpo se ligue especificamente ao polipeptídeo para formar um complexo polipeptídeo:anticorpo. Como utilizado aqui, o termo complexo polipeptídeo:anticorpo se refere ao complexo que resulta quando um anticorpo se liga especificamente a um polipeptídeo. A preparação que inclui os polipeptídeos da presente invenção pode incluir ainda reagentes, por exemplo, um tampão, que fornece condições apropriadas para a formação do complexo polipeptídeo:anticorpo. O complexo polipeptídeo:anticorpo é então detectado. A detecção dos anticorpos é conhecida na técnica e pode incluir, por exemplo, imunofluorescência ou peroxidase. Os métodos para a detecção da presença de anticorpos que se ligam especificamente aos polipeptídeos da presente invenção podem ser utilizados em vários formatos que foram utilizados para detectar o anticorpo, incluindo radioimunoensaio e ensaio imunoabsorvente ligado à enzima.
A presente invenção fornece ainda um kit para a detecção do anticorpo que se liga especificamente aos polipeptídeos da presente invenção. O anticorpo detectado pode ser obtido partindo de um animal suspeito de ter uma infecção causada por um microorganismo gram-positivo, mais preferencialmente, um membro da família Micrococcaceae, preferencialmente, Staphylococcusspp., mais preferencialmente, S. aureus; Streptococcus spp., Bacillusspp., Clostridiumspp., Corynebacterium spp., Enterococus spp., Erysipelothrix spp., Kytococcusspp., Listeriaspp., Micrococcusspp., Mycobacteriumspp. e Erysipelothrix spp.
O kit inclui pelo menos um dos polipeptídeos da presente invenção ou um número de polipeptídeos que é um número inteiro maior que 1 (por exemplo, pelo menos 2, pelo menos 3 etc.), em um material de embalagem adequado em uma quantidade suficiente para pelo menos um ensaio.
Opcionalmente, outros reagentes tais como tampões e soluções necessários para a prática da invenção também estão incluídos. Por exemplo, um kit também pode incluir um reagente para permitir a detecção de um anticorpo que se liga especificamente a um polipeptídeo da presente invenção, tal como um anticorpo secundário marcado de forma detectável planejado para se ligar especificamente a um anticorpo obtido de um animal. São também incluídas tipicamente instruções para uso dos polipeptídeos embalados. Como utilizado aqui, a expressão "material embalado" se refere a uma ou mais estruturas físicas utilizadas para armazenar o conteúdo do kit. O material de embalagem é construído através de métodos bem-conhecidos, geralmente para fornecer um ambiente livre de contaminantes esterilizado. O material de embalagem pode ter um rótulo que indica que os polipeptídeos podem ser utilizados para detectar o anticorpo que se liga especificamente aos polipeptídeos da presente invenção. Em adição, o material de embalagem contém instruções que indicam como os materiais dentro do kit são empregados para a detecção do anticorpo. Como utilizado aqui, o termo "embalagem" se refere a um recipiente tal como vidro, plástico, papel, folha de alumínio e similares, capaz de manter dentro de limites fixos os polipeptídeos e outros reagentes, por exemplo, um anticorpo secundário. Assim, por exemplo, uma embalagem pode ser um cavidade de placa em microlitros ao qual quantidades em microgramas de polipeptídeos foram afixadas. Uma embalagem também pode conter um anticorpo secundário. As "instruções para uso" incluem tipicamente uma expressão tangível descrevendo a concentração do reagente ou pelo menos um parâmetro para método de ensaio, tal como as quantidades relativas de reagente e de amostra que devem ser misturadas, os períodos de tempo de manutenção para as misturas de reagente/amostra, a temperatura, as condições de tampão e similares.
A presente invenção é ilustrada pelos exemplos a seguir. Deve ser entendido que os exemplos, os materais, as quantidades e os procedimentos particulares devem ser interpretados amplamente de acordo com o âmbito e o espírito da invenção como apresentado aqui.
As composições derivadas de cepas diferentes de Staphylococcus aureusincluindo novas proteínas expressas sob restrição ao ferro e/ou outros graus de quelação de ions metálicos foram avaliadas em relação à eficiência contra um desafio virulento em camundongos. A eficiência da composição foi avaliada através da coleta de dados sobre os parâmetros a seguir (1) a eficiência de cada composição para fornecer proteção homóloga e heteróloga contra um desafio virulento vivo em camundongos, (2) a eficiência de cada composição para reduzir lesões necróticas da pele e (3) a eficiência das composições derivadas de Staphylococcuscrescido em condições contendo ferro eliminado ou cheio para fornecer proteção.
As cepas de Staphylococcus aureusavaliadas neste estudo eram originadas de três espécies de animais; aves, seres humanos e bovinos. O isolado de aves SAAV1 era um isolado de campo que se originava de um bando de perus doentes possuindo um alto grau de osteomielite e sinovite. Os isolados bovinos (cepa 1477 e cepa 2176) foram obtidos de dois rebanhos de leite comerciais diferentes possuindo uma alta incidência de mastite clínica. O isolado humano foi obtido na ATCC (cepa 19636) e era originado de um paciente que possuía osteomielite clínica.
Os estoques mães para inoculo ("Maste seed Stocks") de cada isolado foram preparados através da inoculação do isolado apropriado em 200 mL de Tryptic Soy Broth (TSB, Difco Laboratories, Detroit, Ml) contendo 300 μM de 2,2-dipiridila (Sigma-Aldrich St. Louis, MO). A cultura foi crescida durante agitação a 200 rpm durante 6 horas a 37°C e coletada por centrifugação a 10.000 x g. O pélete bacteriano foi ressuspenso em 100 mL de caldo TSB contendo 20% de glicerol e distribuído de forma esterilizada em frascos criogênicos de 2 mL (1 mL por frasco) e armazenado a -90°C até o uso.
Cada estoque mãe para inóculo foi expandido em um inoculo de trabalho. Um frasco de cada isolado mãe para inóculo foi inoculado em 200 mL de Tryptic Soy Broth (TSB, Difco Laboratories, Detroit, Ml) contendo 1000 μM de 2,2-dipiridila (Sigma-Aldrich St. Louis, MO). A cultura foi crescida durante agitação a 200 rpm durante 6 horas a 37°C e coletada por centrifugação a 10.000 x g. O pélete bacteriano foi ressuspenso em 100 mL de caldo TSB contendo 20% de glicerol e distribuído de forma esterilizada em frascos criogênicos de 2 mL (1 mL por frasco) e armazenado a -90°C até o uso. O inóculo de trabalho foi utilizado para a produção de composições enriquecidas com proteínas de membrana reguladas pelo ferro, incluindo proteínas de membrana reguladas pelo ferro.
Todas as cepas foram adaptadas para crescerem em meios com ferro altamente eliminado (isto é, meios contendo níveis muito baixos de ferro livre). Isto foi realizado através do subcultivo das bactérias em TSB contendo concentrações crescentes de 2,2-dipiridila (de 300 até 1600 μM).
As proteínas foram preparadas partindo de bactérias como a seguir. As bactérias foram crescidas partindo dos estoques congelados de inóculo de trabalho através do subcultivo em 25 mL de meio com ferro eliminado (contendo 1000 μM de 2,2'-dipiridila) e meio cheio de ferro, então incubadas a 37°C durante agitação a 400 rpm. Após 12 horas de incubação, 5 mL de cada cultura foram transferidos para 500 mL de meios com ferro eliminado ou cheio de ferro pré-incubados a 37°C. As culturas foram incubadas durante 8 horas a 37°C durante agitação a 100 rpm, então as células foram peletizadas por centrifugação a 10.000 x g durante 20 minutos. Os péletes bacterianos foram ressuspensos em 100 mL de solução salina fisiológica esterilizada e centrifugados a 10.000 x g durante 10 minutos. Os péletes foram então ressuspensos em 45 mL de solução salina tamponada com Tris, pH 7,2 (TBS; 25 mM de Tris, 150 de mM NaCI) e as suspensões bacterianas resultantes foram distribuídas na forma de alíquotas de 9 mL em 5 tubos individuais. Um mililitro de TBS contendo 50 unidades de lisoestafina (Sigma, St. Louis, MO) foi adicionado a cada tubo para fornecer um volume final de 5 unidades/mL. Após a incubação a 37°C durante 30 minutos durante agitação a 200 rpm, 1 mL de TBS contendo 0,1 mg de lisozima (Sigma) foi adicionado em cada tubo. As suspensões bacterianas foram então incubadas durante mais 45 minutos durante agitação a 200 rpm. Depois, as suspensões foram centrifugadas a 3050 x g durante 12 minutos a 4°C para peletizar restos celulares grandes. Os sobrenadantes foram coletados por aspiração sem perturbar o pélete. O sobrenadantes foi então centrifugado a 39.000 x g durante 2,5 horas. Os péletes resultantes contendo as proteínas foram ressuspenas em 200 μL de tampão Tris, pH 7,2, sem solução salina. A solução de proteínas para cada isolado foi combinada para um volume final de 1 mL e armazenada a -90°C.
Os extratos enriquecidos com proteínas derivados S. aureusforam fracionados por tamanho em géis de SDS-PAGE utilizando um gel de empilhamento a 4% e um gel de resolução a 10%. As amostras para eletroforese foram preparadas através da combinação de 10 μL de amostra com 30 μL de tampão redutor de amostra de SDS (62,5 mM de Tris-HCI, pH 6,8, 20% de glicerol, 2% de SDS, 5% de β-mercaptoetanol) e fervidas durante 4 minutos. As amostras foram submetidas à eletroforese em corrente constante de 18 mA durante 5 horas a 4°C utilizando um suprimento de força de célula Protein II xi (BioRad Laboratories, Richmond, CA, modelo 1000/500). O peso molecular de cada proteína individual como é observado visualmente no gel de SDS-PAGE foi estimado utilizando um densitômetro GS-800 (BioRad) utilizando um marcador de peso molecular de faixa ampla como um padrão de referência (BioRad).
Os padrões de SDS-PAGE das proteínas de cada isolado quando crescido na presença de 1600 μM de dipiridila mostraram um padrão de expressão de proteínas muito diferente comparado com a mesma cepa quando crescida na presença de 300 μM de dipiridila. Por exemplo, quando crescido em 300 pM de dipiridila, o isolado SAAV1 resultou em proteínas reguladas por metais de 90 kDa, 84 kDa, 72 kDa, 66 kDa, 36 kDa, 32 kDa e 22 kDa, enquanto crescido em 1600 pM de dipiridila resultou em proteínas reguladas por metais de 87,73 kDa, 54,53 kDa, 38,42 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa e 33,0 kDa. Similarmente, quando crescido em 300 pM de dipiridila o isolado 19636 resultou em proteínas de 42 kDa e 36 kDa, enquanto cultivado em 1600 pM de dipiridila resultou em proteínas reguladas por metais de 87,73 kDa, 54,53 kDa, 38,42 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa e 33,0 kDa. Todas as condições incluindo o crescimento em meios cheios de ferro, resultaram na expressão das proteínas a seguir que presumidamente não eram reguladas por metais: 150 kDa, 132 kDa, 120 kDa, 75 kDa, 58 kDa, 50 kDa, 44 kDa, 43 kDa, 41 kDa e 40 kDa.
Além disso, o crescimento de cepas diferentes de S. aureusem 1600 μM de dipiridila resultou em padrões similares de expressão de proteínas. As composições enriquecidas em proteínas de membrana reguladas pelo ferro partindo do isolado de aves (SAAV1) incluíam proteínas com pesos moleculares de 87,73 kDa, 54,53 kDa, 38,42 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa e 33,0 kDa. Os pesos moleculares das proteínas do isolado 19636 da ATCC eram essencialmente idênticos aos do isolado de ave. Ambos os isolados bovinos, quando crescidos com 1600 μM de 2,2-dipiridila, expressavam perfis de bandas similares aos dos isolados de ave e da ATCC para a maior parte das proteínas (87,73 kDa, 54,53 kDa, 37,7 kDa, 35,70 kDa, 34,91 kDa e 33,0 kDa). Entretanto, nenhum dos isolados bovinos produziu a proteína de 38,42 kDa observada nos isolados de ave e da ATCC e os isolados bovinos expressavam três proteínas (80,46 kDa, 65,08 kDa e 31,83 kDa) não observadas com as cepas de ave e da ATCC (ver a figura 1 e a Tabela 10). Todas as condições resultaram na expressão das proteínas a seguir que não eram reguladas por metais: 150 kDa, 132 kDa, 120 kDa, 75 kDa, 58 kDa, 50 kDa, 44 kDa, 43 kDa, 41 kDa e 40 kDa.
Tabela 10. Pesos moleculares de polipeptídeos regulados por metais obtidos partindo de isolados de Staphylococcus aureus.
De forma interessante, não havia diferença nos perfis de proteínas quando examinados por SDS-PAGE entre o sobrenadante clarificado e o pélete bacteriano após o tratamento das bactérias com lisoestafina/lisozima. Tanto o pélete bacteriano extraído quanto o sobrenadante tinham exatamente os mesmos perfis de proteínas quando examinados por SDS-PAGE. Esta mesma observação também foi verificada quando as células bacterianas eram rompidas utilizando um homogeneizador Avestin a 206,84 MPa (30.000 psi). O pélete bacteriano resultante, após a centrifugação à baixa velocidade era idêntico em relação ao seu perfil de proteínas quando comparado com o do sobrenadante clarificado após a centrifugação à alta velocidade a 30.000 x g durante 2,0 horas a 4°C.
As proteínas do isolado humano 19636 da ATCC e do isolado 1477 bovino, crescidos em condições com o ferro eliminado e preparadas como descrito no exemplo 1, foram utilizadas para formular duas composições vacinais. As proteínas do isolado da ATCC tinha pesos moleculares de 87,73 kDa, 54,53 kDa, 38,42 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa e 33,0 kDa, enquanto que o isolado bovino expressava proteínas que possuíam pesos moleculares de 87,73 kDa, 80,46 kDa, 65,08 kDa, 54,53 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa, 33,0 kDa e 31,83 kDa. Cada composição também continha as proteínas a seguir que não eram reguladas por metais: 150 kDa, 132 kDa, 120 kDa, 75 kDa, 58 kDa, 50 kDa, 44 kDa, 43 kDa, 41 kDa e 40 kDa. As vacinas de estoque foram preparadas partindo das duas cepas através da emulsificação de cada suspensão protéica aquosa (500 μg de proteína total/mL) em um adjuvante comercial (EMULSIGEN, MVP Laboratories, Ralston, Nebraska) utilizando um recipiente de homogeneização IKA Ultra Turrax T-50 (IKA, Cincinnati, OH) para fornecer uma dose final de 50 μg de proteína total em um volume injetável de 0,1 mL com uma concentração de adjuvante de 22,5% vol/vol. Como uma vacinação de controle, uma composição protéica foi preparada partindo do isolado 1477 bovino crescido sob condições cheias de ferro (TSB suplementado com 300 μM de cloreto férrico) como descrito no exemplo 1. Uma vacina de placebo foi preparada através da substituição de solução salina fisiológica pela suspensão protéica aquosa no protocolo anterior.
Setenta (N = 70) fêmeas de camundongos CF-1 obtidas de Harlan Breeding Laboratories (Indianápolis, IN) pesando 16-22 gramas foram distribuídas igualmente em 7 grupos (10 camundongos/grupo). Os camundongos foram mantidos em gaiolas para camundongos de policarbonato (Ancore Corporation, Bellmore, NY). Uma única gaiola foi utilizada para cada grupo de tratamento e o alimento e a água foram fornecidos ad libituma todos os camundongos. Todos os camundongos foram vacinados de forma intraperitoneal com 0,1 mL da composição apropriada duas vezes em intervalos de 14 dias como a seguir: Grupo-1: vacinado com Placebo Grupo-2: vacinado com proteínas de 19636 da ATCC expressas sob restrição de ferro. Grupo-3: vacinado com Placebo Grupo-4: vacinado com proteínas de 1477 Bovino expressas sob restrição de ferro. Grupo-5: vacinado com proteínas de 1477 Bovino expressas sob restrição de ferro. Grupo-6: vacinado com proteínas de 19636 da ATCC expressas sob restrição de ferro. Grupo-7: vacinado com 1477 Bovino FeCh, em que "1477 Bovino FeCh" se refere às proteínas obtidas de 1477 Bovino crescido em TSB suplementado com 300 μM de cloreto férrico.
As cepas de Staphylococcus aureus19636 da ATCC e a cepa 1477 descritas anteriormente foram utilizadas como os organismos para desafio. Sucintamente, os isolados de estoques congelados (descritos anteriormente) foram estriados sobre placas de ágar sangue e incubados a 37°C durante 18 horas. Uma colônia isolada de cada isolado foi subcultivada em 50 mL de Tryptic Soy Broth (Difco) contendo 1600 μM de 2,2-dipiridila. As culturas foram incubadas a 37°C durante 6 horas durante rotação a 200 rpm, então centrifugadas a 10.000 x g durante 10 minutos a 4°C para peletizar as bactérias. Os péletes de bactérias foram lavados duas vezes por centrifugação em TBS a 4°C. Os péletes finais foram ressuspensos em TBS até uma densidade óptica de 42% de Transmitância (T) a 562 nm em um volume de aproximadamente 25 mL de TBS e utilizados para o desafio. Logo antes do desafio, 1 mL destas suspensões bacterianas foi diluído em série e plaqueado em ágar para determinar o número de unidades formadoras de colônias (CFU) por dose para camundongo.
Quatorze dias após a segunda vacinação, os camundongos em todos os grupos (1-7) foram desafiados subcutaneamente na parte posterior do pescoço com 0,1 mL do organismo apropriado. Os sete grupos de camundongos foram desafiados como a seguir: Grupo-1 (Vacinado com Placebo): desafiado com 19636 da ATCC Grupo-2 (Vacinado com as proteínas de 19636 da ATCC expressas sob restrição de ferro): desafiado com 19636 da ATCC Grupo-3 (Vacinado com Placebo): desafiado com 1477 Bovino Grupo-4 (Vacinado com as proteínas de 1477 Bovino expressas sob restrição de ferro): desafiado com 1477 Bovino Grupo-5 (Vacinado com as proteínas de 1477 Bovino expressas sob restrição de ferro): desafiado com 19636 da ATCC Grupo-6 (Vacinado com as proteínas de 19636 da ATCC expressas sob restrição de ferro): desafiado com 1477 Bovino Grupo-7 (Vacinado com 1477 Bovino FeCh): desafiado com 1477 Bovino
Como determinado pelo protocolo de enumeração descrito no exemplo 4, a concentração de S. aureus19636 utilizada para desafio era de 1,35 x 108CFU por dose para camundongo e a concentração de S. aureus 1477 utilizada para desafio era de 1,65 x 108 CFU por dose para camundongo. A morbidez, a mortalidade e a patologia grosseira foram registradas diariamente durante 7 dias após o desafio.
Quando são comparados os camundongos desafiados com o isolado 19636 da ATCC, 70% dos camundongos do Grupo 1 vacinados com placebo morreram dentro de um período de 7 dias de desafio (Tabela 11 e figura 2). Isto demonstrava que a cepa 19636 causava uma alta taxa de mortalidade em camundongos no nível de dose administrado. Em contraste aos camundongos no Grupo 1, apenas 10% dos camundongos do Grupo 2 morreram dentro de um período de 7 dias após o desafio. Estes resultados ilustravam que os camundongos desafiados com a cepa 19636 estavam significativamente protegidos pela vacinação com a composição de 19636 (p = 0,020, teste Exato de Fischer). Além disso, uma análise de Kaplan-Meier dos dados de tempo até a morte indicou que a vacina forneceu proteção significativa (p = 0,0042, teste de logrank) contra o desafio homólogo (figura 3). Em adição, apenas 20% dos camundongos no Grupo 5 morreram dentro de um período de 7 dias de desafio, indicando que a composição 1477 bovina oferecia proteção significativa contra o desafio com a cepa 19636 da ATCC (p = 0,015 teste de logrank para mortalidade). Quando os dados foram analisados através de uma curva de sobrevivência de Kaplan-Meier e o teste de logrank (figura 4), a proteção contra a mortalidade foi determinada como sendo significativa (p = 0,015 teste de logrank para mortalidade), indicando que a composição vacinai derivada da cepa 1477 fornecia proteção heteróloga contra o desafio com a cepa 19636.Tabela 11. Mortalidade de Camundongos Vacinados e Não Vacinados Após o Desafio com Staphylococcus aureus(isolado 19636 humano da ATCC e isolado 1477 bovino). * Grupo-1, (Vacinado com Placebo/Desafiado com 19636 da ATCC) * Grupo-2, (Vacinado com as proteínas de 19636 da ATCC expressas sob restrição de ferro/Desafiado com 19636 da ATCC) * Grupo-3, (Vacinado com Placebo/Desafiado com 1477 Bovino) * Grupo-4, (Vacinado com as proteínas de 1477 Bovino expressas sob restrição de ferro/Desafiado com 1477 Bovino) * Grupo-5, (Vacinado com as proteínas de 1477 Bovino expressas sob restrição de ferro/Desafiado com 19636 da ATCC) * Grupo-6, (Vacinado com as proteínas de 19636 da ATCC expressas sob restrição de ferro/Desafiado com 1477 Bovino) * Grupo-7, (Vacinado com 1477 Bovino FeCI3/Desafiado com 1477 Bovino)
Quando são comparados os camundongos desafiados com o isolado 1477 bovino, apenas 20% dos camundongos no grupo vacinado com placebo (Grupo 3) morreram dentro de um período de 7 dias de desafio. Entretanto, o desafio com o isolado 1477 bovino ativou o desenvolvimento de lesões necróticas na pele em 6 (75%) dos camundongos sobreviventes do Grupo 3. Estas lesões foram medidas e o tamanho médio das lesões nos camundongos sobreviventes era de 18,5 mm (Tabela 12). Em contraste, 20% dos camundongos do Grupo 4 morreram dentro de um período de 7 dias de desafio, mas apenas três (38%) dos camundongos sobreviventes desenvolveram lesões (diâmetro médio, 2,7 mm). Os resultados indicam que a composição de 1477 bovino oferecia proteção homóloga significativa contra o desenvolvimento de lesões nos camundongos desafiados com a cepa 1477 bovina (p = 0,009, teste t Student). Em adição, a vacinação com a composição de 19636 da ATCC protegia contra o desafio com a cepa 1477, uma vez que nenhum camundongo morreu no Grupo 6 e apenas três (30%) dos camundongos desenvolveram lesões na pele (diâmetro médio, 3,7 mm). Tomados juntos, a mortalidade reduzida e/ou o desenvolvimento de lesões nos camundongos nos Grupos 5 e 6 demonstram a natureza de proteção cruzada significativa das composições derivadas das cepas 19636 e 1477 (p = 0,012, teste t Student com base no tamanho das lesões). Na demonstração da eficiência da composição quando comparada com as proteínas não reguladas pelo ferro, 20% dos camundongos no Grupo 7 morreram e 4 dos sobreviventes desenvolveram lesões na pele (diâmetro médio, 15,8 mm). Os camundongos do Grupo 7 demonstravam algum grau de proteção através da vacinação com as proteínas do isolado 1477 uma vez que menos camundongos desenvolveram lesões comparados com os do Grupo 3 vacinados com placebo. Entretanto, as lesões na pele observadas nos camundongos no Grupo 7 eram mais frequentes e tinham um diâmetro maior que as lesões nos camundongos do Grupo 4, indicando que, em relação às proteínas isoladas de células crescidas sob condições cheias de ferro, as proteínas isoladas das bactérias crescidas sob restrição de ferro ofereciam proteção superior contra um desafio idêntico. Tabela 12. A Indução de Lesões Necróticas nos Camundongos Sete Dias Após o Desafio com Staphylococcus aureus(Isolado 19636 da ATCC e/ou Isolado 1477 Bovino) * Grupo-1, (Vacinado com Placebo/Desafiado com 19636 da ATCC) * Grupo-2, (Vacinado com as proteínas de 19636 da ATCC expressas sob restrição de ferro/Desafiado com 19636 da ATCC) * Grupo-3, (Vacinado com Placebo/Desafiado com 1477 Bovino) * Grupo-4, (Vacinado com as proteínas de 1477 Bovino expressas sob restrição de ferro/Desafiado com 1477 Bovino) * Grupo-5, (Vacinado com as proteínas de 1477 Bovino expressas sob restrição de ferro/Desafiado com 19636 da ATCC) * Grupo-6, (Vacinado com as proteínas de 19636 da ATCC expressas sob restrição de ferro/Desafiado com 1477 Bovino) * Grupo-7, (Vacinado com 1477 Bovino FeCI3/Desafiado com 1477 Bovino)
A natureza de proteção cruzada das proteínas observada no estudo de desafio com camundongos é sustentada pelos pesos moleculares similares das proteínas das cepas de S. aureusdescritos no Exemplo 1 (Figura 1). Embora houvesse diferenças notáveis no perfil de SDS-PAGE das proteínas dos isolados derivados de bovinos, especificamente a ausência de uma proteína de 38,4 kDa e a presença de 3 proteínas adicionais, as proteínas das cepas tanto 1477 quanto 19636 da ATCC ativavam proteção heteróloga. Estes resultados indicam que proteínas similares entre as cepas 19636 e 1477 são provavelmente responsáveis pela proteção cruzada observada nos Grupos 5 e 6. Em contraste, os perfis de proteínas da cepa 1477 crescida sob condições de ferro eliminado e cheias de ferro são notavelmente diferentes. As proteínas isoladas sob condições de ferro eliminado são mais protetoras quando comparadas com as proteínas isoladas sob condições cheias de ferro, demonstradas pela redução no desenvolvimento de lesões entre os camundongos do Grupo 4 comparados com os camundongos do Grupo 7.
Em mamíferos, foi mostrado que a resposta aos danos de tecidos ou à infecção bacteriana resulta em uma resposta inflamatória aguda. Esta resposta aumenta a permeabilidade de capilares e a infiltração fagocítica resultando nos sinais clínicos reconhecidos como inflamação; inchaço, febre, dor e vermelhidão; se deixada descontrolada, esta pode levar à morte. A ativação de fatores humorais e a liberação de citocinas medeiam os eventos sistêmicos conhecidos coletivamente como a resposta de proteínas de fase aguda que resulta em uma cascata de eventos fisiológicos e bioquímicos. A duração desta resposta está diretamente relacionada com a gravidade dos danos e a magnitude da infecção sistêmica. Foi bem documentado que durante septicemia bacteriana, cirurgia importante, queimaduras e outro trauma corporal, há uma alteração na concentração de um número de íons metálicos no soro tais como, ferro, cobre e zinco. Por exemplo, durante a fase aguda de uma infecção há um decréscimo nos níveis do plasma de ferro e zinco e um aumento no cobre. A alteração destes íons metálicos traços no soro pode afetar diretamente a gravidade e a progressão de qualquer infecção bacteriana.
Neste estudo foi verificada a expressão de proteínas de Staphylococcus aureussob várias condições de restrição de íons metálicos para imitar a expressão de novas proteínas que podem ser expressas durante a invasão sistêmica. As cepas de Staphylococcus aureusavaliadas neste estudo eram originadas de amostras clínicas de três espécies diferentes de animais; aves (cepa SAAV1), humanos (cepa 19636) e bovinos (cepas 1477 e 2176). Sucintamente, as culturas de cada isolado foram preparadas partindo de estoques mães para inoculação em 200 mL de Tryptic Soy Broth (TSB). Cada cultura foi crescida durante agitação a 200 rpm durante 6 horas a 37°C. Dez mL de cada cultura foram transferidos para 500 mL de TSB que sofreu eliminação contendo um dos quatro quelantes de íon metálico; 2,2dipiridila (Dp), 2-piridilmetil-etileno diamina (TPEN), catequina e naringenina (todos obtidos na Sigma, St. Louis, MO). Em adição, cada cultura também foi crescida em meios cheios de cátions contendo cloreto férrico, cloreto de zinco e/ou cloreto de cobre preparados a concentrações de 300 μM. Os quelantes de íons metálicos foram utilizados na concentração a seguir: 2,2-dipiridila (800 μM), catequina e naringenina foram utilizadas a 300 μM e 2-piridilmetiletileno diamina foi utilizada a uma concentração de 100 μM. As culturas foram crescidas com cada quelante durante 8 horas, em cujo ponto de tempo a cultura foi subcultivada uma segunda vez durante 12 horas adicionais. Cada cultura foi subcultivada durante três passagens consecutivas em intervalos de 12 horas. No final da terceira passagem, cada cultura foi coletada por centrifugação a 10.000 x g durante 20 minutos. Cada cultura foi lavada duas vezes por centrifugação a 10.000 x g e ressuspensa em 20 mL de solução salina tamponada com Tris, pH 7,2 a 4°C.
Cada pélete bacteriano foi ressuspensa em 45 mL de solução salina tamponada com Tris, pH 7,2 (25 mM de Tris e 150 mM de NaCI) e as suspensões bacterianas resultantes foram distribuídas na forma de alíquotas de 9 mL em 5 tubos individuais, vinte tubos no total. Um mililitro de TBS contendo 50 unidades de lisoestafina (Sigma, St. Louis, MO) foi adicionado em cada tubo para fornecer uma concentração final de 5 unidades/mL. Após a incubação a 37°C durante 30 minutos durante agitação a 200 rpm, 1 mL de TBS contendo 0,1 mg de lisozima (Sigma) foi adicionado durante 45 minutos adicionais durante agitação a 200 rpm. Depois, as suspensões foram centrifugadas a 3050 x g durante 12 minutos a 4°C para peletizar restos celulares grandes. Os sobrenadantes foram coletados por aspiração sem perturbar o pélete. O sobrenadantes foi então centrifugado a 39.000 x g durante 2,5 horas. Os péletes resultantes, enriquecidas de proteínas de membrana reguladas por metais, foram ressuspensas em 200 μL de tampão Tris, pH 7,2. As soluções de proteínas para cada isolado foram combinadas para um volume total de 1 mL e armazenadas a -90°C.
As proteínas obtidas dos isolados de S. aureusSAAV1, 19636, 1477 e 2176 crescidos sob condições com a eliminação de ferro, zinco e cobre incluíam polipeptídeos regulados por metais.
Os extratos celulares, derivados de cada isolado foram fracionados por tamanho em géis de SDS-PAGE utilizando um gel de empilhamento a 4% e um gel de resolução a 10%. As amostras para eletroforese foram preparadas através da combinação de 10 μL de amostra com 30 pL de tampão redutor de amostra de SDS (62,5 mM de Tris-HCI, pH 6,8, 20% de glicerol, 2% de SDS, 5% de beta-mercaptoetanol) fervidos durante 4 minutos. As amostras foram submetidas à eletroforese a 18 mA de corrente constante durante 5 horas a 4°C utilizando um fornecimento de força Protein II xi cell (BioRad Laboratories, Richmond, CA, modelo 1000/500).
Os padrões de SDS-PAGE das proteínas crescidas sob a presença de quelantes de zinco e/ou cobre exibiram padrões de banda exclusivos em todos os isolados que eram diferentes quando comparados com os mesmos isolados crescidos sob restrição de íons na presença de 2,2'dipiridila. Por exemplo, quando o isolado 19636 foi crescido sob restrição de ferro ou na presença do quelante 2,2'-dipiridila, proteínas exclusivas reguladas pelo ferro foram expressas nas regiões de 87,73 kDa, 54,53 kDa, 38,42 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa e 33,0 kDa. Estas proteínas foram reguladas para menos quando o isolado foi crescido na presença de cloreto férrico. Entretanto, quando o mesmo isolado foi crescido na presença do quelante de zinco e/ou de cobre, um novo subconjunto de proteínas foi expresso em relação às proteínas expressas sob restrição de ferro; os novos peptídeos possuindo pesos moleculares de aproximadamente 115 kDa, 88 kDa, 80 kDa, 71 kDa, 69 kDa, 35 kDa, 30 kDa, 29 kDa e 27 kDa. Em adição, uma proteína de 87,73 kDa foi expressa sob condições de restrição de ferro ou de restrição de cobre, mas não quando as culturas eram restritas de zinco. As proteínas expressas sob restrição de ferro pareciam estar reguladas para menos quando o crescimento estava sob restrição de zinco e/ou restrição de cobre, mas não completamente desligada como observado quando o isolado foi crescido em cloreto férrico.
Parece que há novas proteínas expressas quando o organismo é crescido sob restrição de cobre e/ou restrição de zinco que não são expressas quando o mesmo isolado é crescido sob condições com restrição de ferro. Uma vez que os metais de transição são utilizados por organismos para construir enzimas que catalisam várias reações bioquímicas, os ions metálicos desempenham uma função vital na sobrevivência do microorganismo durante uma infecção sistêmica. É talvez por esta razão que durante a septicemia haja um decréscimo transitório na disponibilidade destes metais de transição, tornando-os indisponíveis para o crescimento do organismo. Estas novas proteínas poderiam muito bem aumentar a eficiência protetora da composição existente crescida sob restrição de ferro porque podem também ser expressas pelas bactérias sob a restrição de ions metálicos sofrida durante a invasão sistêmica.
Um frasco criogênico do inóculo de trabalho (2 mL a 109 CFU/mL) como descrito no exemplo 1 foi utilizado para inocular 500 mL de Tryptic Soy Broth (TSB) sem dextrose (Difco) pré-aquecidos até 37°C contendo 0,125 g/L de 2,2-dipiridila (Sigma), 2,7 gramas de extrato de levedura BiTek (Difco) e glicerol (3% vol/vol). A cultura foi incubada a 37°C durante 12 horas durante agitação a 200 rpm em cujo período de tempo foi utilizada para inocular 2 litros do meio acima e permitida crescer durante 4 horas adicionais a 37°C. Esta cultura foi utilizada para inocular um fermentador de superfície de bancada Virtis de 20 litros, (Virtis, Gardiner, NY) carregado com 13 litros do meio descrito anteriormente. O pH foi mantido constante entre 6,9 e 7,1 por titulação automática com 50% de NaOH e 10% de HCI. A velocidade de agitação foi ajustada em 400 rev/minuto e a cultura foi aerada com 11 litros de ar/minuto a 37°C. A formação de espuma foi controlada automaticamente através da adição de 11 mL de agente desespumante (Mazu DF 204 Chem/Serv, Minneapolis, MN). Foi permitido que a cultura crescesse continuamente nestas condições durante 4 horas em cujo período de tempo foi bombeada de forma esterilizada para um fermentador de 150 litros (W. B. Moore, Easton, PA). O fermentador foi carregado com 120 litros de ("TSB tryptic soy broth")sem dextrose (3.600,0 gramas), extrato de levedura BiTek (600 gramas), glicerol (3.600 mL), 2,2-dipiridila (3,0 gramas) e agente desespumante Mazu DF 204 (60 mL). Os parâmetros da fermentação eram como a seguir: o oxigênio dissolvido (OD) foi mantido a 30% +/10% através do aumento da agitação para 220 rev/minuto purgado com 60 litros de ar/minuto e retropressão de 0,068 MPa (10 libras por polegada quadrada (psi)). O pH foi mantido constante entre 6,9 e 7,1 através da titulação automática com 50% de NaOH e 10% de HCI e a temperatura foi mantida a 37°C. Na hora 4,5 (DO540 8-9) da fermentação, a cultura foi transferida para um fermentador de 1.500 litros New Brunswick Scientific IF-15000 carregado com 1200 litros de ("TSB tryptic soy broth")sem dextrose (36.000 gramas), extrato de levedura BiTek (6.000 gramas), glicerol (36.000 mL), 2,2-dipiridila (30,0 gramas) e agente desespumante Mazu DF 204 (600 mL). Os parâmetros da fermentação eram como a seguir: 0 oxigênio dissolvido (OD) foi mantido em 60% +/10% com oxigênio suplementar através do aumento da agitação para 300 rev/minuto purgado com 300 até 1100 litros de ar/minuto e retropressão de 0,034 MPa (5 libras por polegada quadrada (psi)). À medida que a fermentação progredia o oxigênio suplementar foi adicionado partindo de 0-90 litros/minuto para auxiliar no controle do oxigênio dissolvido. O pH foi mantido constante entre 6,9 e 7,4 através de titulação automática com 50% de NaOH e 10% de HCI e a temperatura foi mantida a 37°C.
Aproximadamente 5 horas após a inoculação do fermentador grande, a cultura foi suplementada com nutrientes adicionais através da alimentação de 70 litros de meio contendo 18.000 gramas de TSB sem dextrose, 3.000 gramas de extrato de levedura, 30,0 gramas de 2,2-dipiridila e 18.000 mL de glicerol. A taxa de alimentação foi ajustada em aproximadamente 28 litros/hora durante agitação crescente. No final da alimentação, foi permitido que a fermentação continuasse durante 4 horas adicionais em cujo ponto a fermentação foi terminada através da diminuição da temperatura do fermentador para 18°C (DO540 35-40 a uma diluição de 1:100).
A fermentação bacteriana foi concentrada e lavada utilizando um Pall Filtron Tangential Flow Maxiset-25 (Pall Filtron Corporation, Northboro, MA) equipado com três filtros de canal aberto Alpha 300-K de 2,78 m2 (30 pés2), N2 de catálogo AS300C5, (Pall Filtron) conectados a uma bomba de alimentação Waukesha Modelo U-60 (Waukesha Cherry-Burrell, Delevan, Wl). O volume da cultura original de 1250 litros foi reduzido para 50 litros (2,5 litros/minuto) utilizando uma pressão de entrada no filtro de 0,206 MPa (30 psi) e uma pressão de retentato de 0,034-0,041 MPa (5-6 psi). O retentato bacteriano foi ajustado de volta para 150 litros utilizando solução salina tamponada com Tris pH 8,5 e então concentrado novamente em 50 litros para auxiliar na remoção de quaisquer proteínas exógenas contaminantes, tais como, exoproteínas incluindo toxinas secretadas e proteases. O pH elevado da solução salina tamponada com Tris ajuda a prevenir muito da degradação proteolítica que pode ocorrer durante 0 armazenamento da suspensão de células inteiras. Os inibidores de protease podem ser utilizados ao invés de ou em adição a um pH elevado. O retentato foi misturado vigorosamente enquanto estava no tanque de 200 litros utilizando uma misturadora controlada magneticamente montada na parte inferior. O retentato foi distribuído de forma esterilizada (3,5 litros) em recipientes Nalgene de 4 litros esterilizados N2 2122 e colocado em um freezer a -20°C para armazenamento como um ponto de quebra na produção ou poderia ser processado adicionalmente. A massa do pélete foi calculada através da centrifugação de amostras de 30 mL da cultura fermentada e do coletado final. Sucintamente, os tubos cônicos Nalgene de 50 mL pré-pesados foram centrifugados a 39.000 x g durante 90 minutos em uma centrífuga Beckman J2-21 utilizando um rotor JA-21 (Beckman Instruments, Paio Alto, CA). No final da corrida, o sobrenadantes foi vertido e os tubos foram pesados novamente. A massa do pélete foi calculada para cada estágio. O processo de fermentação forneceu uma massa de pélete úmida de aproximadamente 60 quilogramas.
Oitenta quilogramas de suspensão de células bacterianas em solução salina tamponada com Tris pH 8,5 foram transferidos assepticamente para um tanque de processo com camisa de 1000 litros com vapor no local (Lee, Modelo 259LU) com uma misturadora montada na parte superior (Eastern, Modelo TME-1/2, EMI Incorporated, Clinton, CT) contendo 900 litros de TBS pH 8,5. A suspensão bacteriana em massa foi resfriada rapidamente até 4°C com mistura contínua durante 18 horas a 200 rpm em cujo período de tempo foi rompida por homogeneização. Sucintamente, o tanque de 1000 litros contendo a suspensão bacteriana foi conectado com um Homogeneizador Avestin modelo C-500-B, (Avestin Inc, Ottawa, Canadá). Um segundo tanque de processo com camisa de 1000 litros (vazio) foi conectado ao homogeneizador de forma que o fluido no tanque de processo pudesse ser passado através do homogeneizador, para dentro do tanque vazio e de volta mais uma vez, permitindo várias passagens de homogeneização enquanto ainda se mantinha um sistema fechado. A temperatura durante a homogeneização foi mantida a 4°C. No início da primeira passagem, o fluido foi circulado a 0,482 MPa (70 psi) através de uma bomba Waukesha modelo 10DO (Waukesha) ao longo do homogeneizador (1892 L (500 galões)/hora), enquanto que a pressão do homogeneizador era ajustada em 206,84 MPa (30.000 psi). Antes da primeira passagem, duas amostras préhomogeneização foram eliminadas do homogeneizador para estabelecer uma linha de base para a determinação do grau de rompimento e para o monitoramento do pH. O grau de rompimento foi monitorado por transmitância (% de T a 540 nm a uma diluição de 1:100) comparada com a da amostra não homogeneizada. O número de passagens através do homogeneizador foi padronizado para fornecer uma transmitância percentual final entre 78-91% de T a uma diluição de 1:100 preferencialmente entre 86-91%. Após a homogeneização, o tanque foi removido do homogeneizador e colocado em uma alça de refrigeração a 4°C e misturado a 240 rpm.
A suspensão bacteriana rompida contendo as proteínas reguladas pelo ferro como ilustrado na figura 1 foi coletada por centrifugação utilizando T-1 Sharpies (Alfa Laval Seperations, Warminster, PA). Sucintamente, o tanque de processo com camisa de 1000 litros contendo o homogenato bacteriano rompido foi alimentado em 12 Sharpies com uma taxa de alimentação de 250 mL/minuto a 0,117 MPa (17 psi) a uma força centrífuga de 60.000 x g. O efluente foi coletado em um segundo tanque de processo com camisa de 1000 litros através de uma alça esterilizada permitindo várias passagens através das centrífugas enquanto se mantinha um sistema fechado. A temperatura durante a centrifugação foi mantida a 4°C. O homogenato foi passado 8 vezes através das centrífugas. Aproximadamente 50% da proteína foram coletados após a segunda passagem, em cujo ponto, o fluido do homogenato foi concentrado em 1/3 de seu volume original, que encurtou o tempo do processo durante as 6 passagens seguintes. O tanque do homogenato foi desconectado assepticamente das centrífugas e conectado a uma estrutura Millipore Pellicon Tangential Flow Filter (Millipore Corporation, Bedford, MA), equipada com um filtro da série Alpha 30K Centrasette de canal com tela de 2,32 m2 (25 pés2) (Pall Filtron) conectado com uma bomba de alimentação Waukesha Modelo U30 para concentração. Após a concentração, a centrifugação foi continuada até o processo estar completado. A proteína foi coletada após cada passagem. A proteína foi coletada, ressuspensa e distribuída em 50 litros de solução salina tamponada com Tris pH 8,5 contendo 0,15% de formulina (Sigma) como conservante.
A suspensão de proteína foi lavada por diafiltração a 4°C para remover quaisquer proteínas exógenas (proteases, toxinas, enzimas citoplasmáticas e metabólicas etc). Sucintamente, os 50 litros de proteína foram transferidos de forma esterilizada para um tanque de processo de 200 litros contendo 150 litros de solução salina tamponada com Tris esterilizada, pH 8,5 equipado com uma misturadora Dayton montada na parte inferior, Modelo 2Z846 (Dayton Electric, Chigago, IL) girando a 125 rev/minuto. O tanque de processo foi conectado de forma esterilizada a uma estrutura Millipore Pellicon Tangential Flow Filter (Millipore Corporation), equipada com um filtro da série Alpha 30K Centrasette de canal com tela de 2,32 m2 (25 pés2) (Pali Filtron) conectado com uma bomba de alimentação Waukesha Modelo U30. A solução de proteína de 200 litros foi concentrada por filtração até um volume alvo de 50 litros em cujo ponto 150 litros de solução salina esterilizada foram adicionados. A suspensão de proteína foi então concentrada até aproximadamente 50 litros. O concentrado de proteína foi armazenado em um tanque de processo com camisa de 50 litros equipado com uma misturadora montada na parte superior e armazenado a 4°C.
É interessante observar que a composição derivada do processo em grande escala utilizando a homogeneização como um meio de rompimento gerou perfis de bandas idênticos quando verificados por SDS-PAGE quando comparados com os do processo em escala menor no exemplo 1. Estes resultados mostram que a lisoestafina poderia ser substituída como o agente de lise bacteriana utilizando o homogeneizador Avestin C500-B. Esta descoberta permite a produção a baixo custo de grandes volumes de proteínas reguladas pelo ferro partindo de staphlylococci.
A imunização passiva com anticorpo purificado isolado de camundongos vacinados com proteínas derivadas de cepas 19636 de S. aureuscrescidas sob condições limitantes de ferro era protetora contra um desafio com S. aureushomólogo e heterólogo. Quinze camundongos CD1 adultos foram vacinados como descrito no exemplo 3 com a composição de proteínas derivada da cepa ATCC19636 de S. aureuscrescida sob condições de eliminação de ferro como descrito nos exemplos 1 e 2. Os camundongos foram vacinados de forma intraperitoneal 3 vezes em intervalos de 7 dias com 50 μg de composição de proteína em cada vacinação. Sete dias após a terceira imunização, os camundongos foram sangrados completamente por perfuração cardíaca. O soro foi agrupado e o anticorpo purificado utilizando a precipitação padronizada com sulfato de amónio. As proteínas exógenas do soro foram removidas logo antes da precipitação dos anticorpos através da adição de 0,5 volume de sulfato de amónio saturado pH 7,2. A solução foi agitada a 100 rpm durante 24 horas a 4°C. A solução foi novamente centrifugada a 3000 x g durante 30 minutos. O sobrenadante foi coletado e precipitado novamente através da adição de sulfato de amónio suficiente para levar a concentração final a 55% de saturação. A solução foi agitada a 100 rpm durante 24 horas a 4°C. O precipitado foi centrifugado a 3000 x g durante 30 minutos. O pélete final de cada amostra foi ressuspensa em 2 mL de PBS pH 7,2. Os anticorpos precipitados foram então submetidos à diálise utilizando uma tubulação de diálise com limite molecular de 50.000 (Pierce, Rockford IL) durante 30 horas contra três trocas de 1 litro de solução salina tamponada com fosfato para remover o sulfato de amónio. As primeiras trocas de 2 litros foram conservadas com azida sódica a 0,02%. O último litro de solução tampão não continha conservante. O produto da diálise foi coletado e centrifugado novamente para remover qualquer resto celular remanescente a 3000 x g durante 30 minutos. A solução de anticorpos foi armazenada a 4°C durante menos que 48 horas antes do uso. Cada amostra foi plaqueada em ágar sangue para verificar a esterilidade antes da infusão.
Para avaliar o efeito protetor do anticorpo infundido produzido contra proteínas de S. aureusexpressas durante a limitação de ferro, dois grupos de 15 camundongos cada receberam infusão intraperitoneal com a preparação do anticorpo purificado (Grupo 1) ou solução salina fisiológica (Grupo 2) em uma infusão de 200 μL. Dois grupos adicionais de 15 camundongos cada receberam infusão subcutânea com a preparação de anticorpo purificado (Grupo 3) ou solução salina fisiológica (Grupo 4). Após 60 minutos, os 2 grupos de 15 camundongos que receberam uma infusão intraperitoneal foram desafiados de forma intraperitoneal com 1,3 x 108 cfU da cepa 19636 de S. aureus.Similarmente, os 2 grupos de 15 camundongos que receberam uma infusão subcutânea foram desafiados de forma subcutânea com 1,3 x 108 cfU da cepa 1477 de S. aureuspara testar em relação à proteção cruzada contra o desafio por uma cepa diferentes de S. aureus.A mortalidade e/ou o tamanho das lesões foi registrado durante 5 dias e os fígados de todos os camundongos foram removidos pós-mortem, homogeneizados e plaqueados para determinar o número de S. aureuspresente como uma medida de infecção sistêmica. As curvas de sobrevivência de Kaplan-Meier (figuras 5 e 6) mostram o efeito protetor fornecido pela infecção de anticorpos de camundongos vacinados com as proteínas de S. aureusexpressas durante a restrição de ferro. Embora a diferença entre os grupos que receberam infusão e os de controle em relação aos grupos desafiados com 19636 da ATCC não fosse significativa (p = 0,076, teste de log-rank), o fígado do camundongo isolado que morreu dentro do grupo que recebeu infusão de anticorpo no Dia 1 foi cultivado em ágar sangue para determinar a ausência e/ou a presença do organismo de desafio (S. aureus).A cultura derivada deste camundongo era negativa em relação a Staphylococcuse não exibia crescimento sobre a placa de ágar sangue ou em meio de cultura. Em contraste, os fígados dos camundongos que morreram dentro do grupo de placebo, eram todos positivos em relação à presença de Staphylococcus,na verdade, foram obtidas culturas puras em cada placa de ágar sangue derivada dos fígados destes camundongos. Embora os dados dos fígados não excluam a possibilidade de que o camundongo que morreu dentro do grupo que recebeu infusão com anticorpo tenha morrido de infecção por S. aureus, a infecção não era sistêmica, como era no grupo de placebo e o camundongo pode ter morrido por outras razões. A observação desta morte do camundongo que recebeu infusão com anticorpo resulta em uma diferença significativa entre os tratamentos com infusão com anticorpo e com placebo (p = 0,015, teste de log-rank). Os dados para o desafio cruzado, em que os camundongos receberam infusão com anticorpo gerados após a vacinação com proteínas derivadas de 19636 da ATCC e desafiados pela cepa 1477 de S. aureus,também exibiram uma tendência protetora. Entre os dias 7 e 14 após o desafio, todos os camundongos nos grupos com infusão e sem infusão começaram a desenvolver lesões necróticas da pele. Entretanto, a verificação superficial dos camundongos revelou claramente um retardo visível na formação de uma lesão que pode ser observada assim como a gravidade da lesão entre os grupos. Os camundongos que receberam infusão desenvolveram lesões mais lentamente quando comparados com os camundongos de controle que não receberam infusão que desenvolveram lesão mais rápida que os camundongos que receberam infusão e em um grau maior de gravidade. Os camundongos que receberam infusão tiveram cicatrização mais rápida que os camundongos que não receberam infusão. Isto era claramente evidente entre 21 e 35 dias após o desafio. A verificação superficial de camundongos 35 dias após o desafio mostrou que os camundongos que não receberam infusão ficavam gravemente desfigurados e revelou um maior grau de formação de cicatrizes. Na verdade, muitos destes camundongos perderam a postura normal, em que tinham uma aparência torcida, em contraste com os camundongos que receberam infusão que não desenvolveram quase o tecido de cicatriz extensivo e/ou desfiguração como ilustrado pela aparência torcida que os camundongos que não receberam infusão desenvolvidas. De forma geral, estes dados sugerem que a infusão intraperitoneal de anticorpos produzidos contra proteínas induzidas pelo ferro de S. aureus pode tanto proteger contra quanto limitar a gravidade da infecção por S. aureus.
Um rebanho de leite comercial possuindo um histórico de contagens de células somáticas altamente crônicas que podem ser atribuídas a Staphylococcus aureusfoi escolhido para a avaliação de uma composição vacinai como descrito no exemplo 1. O critério para o estabelecimento da eficiência da vacina deste estudo experimental era: 1) menor incidência de mastite clínica causada por Staphylococcus aureusentre os vacinados comparados com os controles não vacinados, 2) melhoria (isto é, um decréscimo) na contagem de células somáticas entre os vacinados comparados com os controles e 3) diminuição nas taxas de isolamento positivo de culturas de S. aureusentres vacinados e controles não vacinados. O sangue pode ser tirado no momento da primeira vacinação (dia 0) e novamente em 3 e 6 semanas após a imunização inicial. As reações no local da injeção ou as reações sistêmicas após as vacinações foram monitoradas ao longo de todo o estudo. Em adição, amostras de leite no tanque de massa foram cultivadas e enumeradas quantitativamente para determinar se havia um decréscimo no número de CFU de Staphylococcus aureuscultivado após a vacinação.
Três dos isolados de Staphylococcusderivados de vacas lactantes infectadas de forma crônica dentro do rebanho foram crescidos sob condições de restrição de ferro e condições sem restrição de ferro como descrito no exemplo 1. Os três isolados foram denominados TTX101, TTX102 e TTX103. As amostras extraídas foram examinadas por SDS-PAGE para comparar perfis de bandas entre os isolados. Perfis de bandas idênticos foram observados entre os isolados examinados; as composições produzidas partindo de cada isolado incluíam proteínas possuindo pesos moleculares de 87,73 kDa, 80,46 kDa, 65,08 kDa, 54,53 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa, 33,0 kDa e 31,83 kDa. Estas proteínas possuem os mesmos pesos moleculares que as descritas anteriormente na tabela 10. Em adição, quando foram comparados os isolados, foram observados perfis de bandas idênticos aos das proteínas que foram expressas em todas as condições que não foram reguladas pelo ferro: 150 kDa, 132 kDa, 120 kDa, 75 kDa, 58 kDa, 50 kDa, 44 kDa, 43 kDa, 41 kDa e 40 kDa. Estes resultados eram coerentes com as observações anteriores. Um isolado denominado TTX101 foi escolhido como o isolado para a produção de uma composição que será utilizada neste estudo.
Uma composição foi preparada como descrito no exemplo 1 utilizando o isolado TTX101. A composição incluía proteínas expressas sob condições de eliminação de ferro que possuíam pesos moleculares de 87,73 kDa, 80,46 kDa, 65,08 kDa, 54,53 kDa, 37,37 kDa, 35,70 kDa, 34,91 kDa, 33,0 kDa e 31,83 kDa assim como proteínas não reguladas por metais que possuíam pesos moleculares de 150 kDa, 132 kDa, 120 kDa, 75 kDa, 58 kDa, 50 kDa, 44 kDa, 43 kDa, 41 kDa e 40 kDa. A composição de imunização derivada da cepa TTX101 foi utilizada para preparar a vacina experimental através da emulsificação da suspensão de proteínas extraídas (400 μg de proteínas totais por mililitro) em um adjuvante comercial (EMULSIGEN, MVP Laboratories, Ralston NE) utilizando um recipiente de homogeneização IKA Ultra Turrax T-50 (IKA, Cincinnati, OH) para fornecer uma dose final de 800 μg de proteínas totais em um volume injetável de 2,0 mL com uma concentração de adjuvante de 22,5% vol/vol. A vacina foi administrada de forma subcutânea duas vezes em intervalos de 21 dias.
Dezoito dias antes da primeira vacinação todas as vacas lactantes envolvidas no estudo (N=80) foram testadas em relação a S. aureusatravés de métodos de cultura biológicos aeróbicos padronizados cultivando amostras de leite individuais derivadas de cada vaca lactante. Em adição, as Contagens de Células Somáticas (SCC) foram enumeradas pela Dairy Herd Improvement Association utilizando métodos padronizados. Quatorze das 80 vacas foram diagnosticadas clinicamente com mastite e tiveram cultura positiva para S. aureus.O restante das vacas (N=66) teve teste negativo para S. aureus.As oitenta vacas foram divididas igualmente em dois grupos denominados de grupo-1, vacinado (N=40) e grupo-2, não vacinado (N=40). As quatorze vacas clinicamente diagnosticadas como positivas em relação a Staphylococcusforam distribuídas igualmente entre ambos os grupos de forma que cada grupo de estudo continha 7 vacas com mastite clínica. As SCC médias entre os grupos antes da primeira vacinação eram de 203.219 nos controles não vacinados comparadas com 240.443 nos vacinados (não estatisticamente diferente p = 0,7).
Dezoito dias após a primeira amostragem, todas as vacas no grupo 1 foram vacinadas de forma subcutânea no quarto dianteiro direito superior com 2 mL de vacina como descrito no exemplo 11. Dez dias depois da vacinação, amostras de leite foram tiradas neste período de tempo por DHIA para a enumeração de células somáticas de cada vaca individualmente. As amostras de leite não foram testadas bacteriologicamente neste período de tempo para a determinação da presença de Staphylococcus.A diferença nas SCC entre os grupos neste período de tempo era de 125.241 (vacinados) comparados com 196.297 (controles). Isto era uma diferença de 36% no número de células somáticas entre os vacinados comparados com os controles não vacinados. A diferença nas SCC entre os controles e os vacinados neste período de amostragem não era estatisticamente diferente (p = 0,5). A falta de diferença estatística nas SCC entre os grupos em ambos os períodos de amostragem era por causa da grande variação nas SCC individuais entre as vacas. O local da injeção de cada vaca vacinada também foi examinado neste mesmo período de tempo. Nenhuma das vacas examinadas exibiu qualquer reação adversa ao tecido no local da injeção através de exame físico. Em adição, não havia perda mensurável na produção de leite causada pela vacinação.
Vinte e um dias depois da vacinação, todas as vacas do grupo-1 (vacinadas) receberam sua segunda vacinação ou reforço. Durante o período de tempo entre a primeira e a segunda vacinação, as vacas em ambos os grupos (vacinadas e controles) desenvolveram danos nas tetas causados por uma queda drástica na temperatura ambiental resultando na formação de lesões na extremidade da teta, resultando no desenvolvimento de tetas infectadas e aumentando potencialmente o isolamento de Staphylococcus durante a amostragem, que foi observado no terceiro período de amostragem. Vinte e três dias após a segunda vacinação, amostras de leite foram tiradas por DHIA para a enumeração de Células Somáticas de cada vaca individual. As amostras de leite também foram testadas bacteriologicamente em relação à presença de Staphylococcus aureus.Havia um aumento drástico na taxa de isolamento de S. aureusneste período de tempo nas vacas que tiveram testes negativos no primeiro período de amostragem. Nos controles não vacinados 42,9% destas vacas agora com teste positivo para S. aureus,em contraste com as vacinadas, que exibiam apenas um aumento de 35,5%. Isto era uma diferença de 7,4% entre os vacinados comparados com os controles não vacinados. É difícil dizer que a melhoria na taxa de isolamento de S. aureusno grupo vacinado era causada pelo efeito da vacina isoladamente. Não se pode deixar passar a dificuldade na obtenção de amostras de leite limpas de vacas que tiveram danos nas tetas o que poderia aumentar a contaminação potencial do leite por S. aureusquando a amostra é obtida. Todavia, havia uma diferença significativa nas SCC médias entre as vacinadas comparadas com as de controle. As SCC médias do grupo vacinado era de 222.679 comparadas com 404.278 células somáticas que são medidas no grupo de controle. Isto era uma diferença de 44,9% entre as vacinadas comparadas com as de controle não vacinadas. É interessante especular que a diferença observada nas SCC entre estes grupos também coincide com a diferença na taxa de isolamento de S. aureusentre os grupos. Entretanto, devido a grande variação nas SCC entre animais individuais e o tamanho de amostra pequeno do teste experimental no número de animais, a diferença não era estatisticamente diferente (p = 0,28).
Neste mesmo período de tempo, o local da injeção de cada vaca vacinada foi examinado em relação a qualquer reação adversa ao tecido que pode ter sido causada pela composição vacinai. Nenhuma das vacas examinadas exibia qualquer reação adversa no local da injeção através de exame físico. As composições vacinais pareciam ser altamente compatíveis ao tecido e não causavam perda mensurável na produção de leite após cada vacinação.
O monitoramento das vacas é continuado através da medida das SCC e das amostras de leite em relação à presença ou à ausência de Staphylococcus aureus.Algumas das vacas de cada grupo são vacinadas uma terceira vez 42 dias após a segunda vacinação. Isto parece ser uma diferença que favorece o uso da composição vacinai para diminuir as contagens de células somáticas e para controlar a infecção causada por Staphylococcus aureus.O monitoramento adicional inclui sorologia com base nos títulos de anticorpos para a composição vacinai, alterações na produção de leite nas vacas vacinadas por causa da melhora na saúde e SCC diminuídas de animais vacinados comparados com grupos não vacinados. Em adição, outros experimentos são realizados para investigar o índice de proteção da vacina com base na resposta à dose após o desafio com um S. aureusvirulento.
Uma vez que foi demonstrado que os pesos moleculares das proteínas entre as diferentes cepas de S. aureuseram similares e uma vez que foi observada proteção heteróloga no estudo de desafio com camundongos, procurava-se determinar se as proteínas que compartilhavam pesos moleculares similares na figura 1 era proteínas similares. A técnica escolhida para caracterizar as proteínas foi a espectrometria de massa de dessorção/ionização a laser auxiliada por uma matriz (MALDI-MS). Uma parte da composição foi resolvida utilizando SDS-PAGE como descrito no exemplo 1 e o gel foi corado com azul Brilhante de Coomassie para visualizar as proteínas.
Corte e lavagem. O gel foi lavado durante 10 minutos com água duas vezes. Cada banda de proteína de interesse foi cortada através da incisão o mais próximo possível da banda de proteína para reduzir a quantidade de gel presente na amostra.
Cada pedaço de gel foi cortado em cubos de 1 x 1 mm e colocado em um tubo de 1,5 mL. Os pedaços de gel foram lavados com água durante 15 minutos. Todos os volumes dos solventes utilizados nas etapas de lavagem eram aproximadamente equivalentes a duas vezes o volume do pedaço de gel. O pedaço de gel foi lavado a seguir com água/acetonitrila (1:1) durante 15 minutos. Quando as proteínas foram coradas com prata, a mistura de água/acetonitrila foi removida, os pedaços de gel secos em um SpeedVac (ThermoSavant, Holbrook, NY) e então reduzidos e alquilados como descrito abaixo. Quando os pedaços de gel não eram corados com prata, a mistura de água/acetonitrila era removida e a acetonitrila era adicionada para cobrir até os pedaços de gel ficarem brancos grudentos, em cujo momento a acetonitrila foi removida. Os pedaços de gel foram reidratados em 100 mM de NH4HCO3 e após 5 minutos, urn volume de acetonitrila equivalente a duas vezes 0 volume dos pedaços de gel foi adicionado. Este foi incubado durante 15 minutos, o liquido foi removido e os pedaços de gel secos em um SpeedVac.
Redução & alquilação. Os pedaços secos de gel foram reidratados em 10 mM de DTT e 100 mM de NH4HCO3 e incubados durante 45 minutos a 56°C. Após permitir que os tubos resfriassem até a temperatura ambiente, o líquido foi removido e o mesmo volume de uma mistura de 55 mM de iodoacetamida e 100 mM de NH4HCO3 foi adicionado imediatamente. Este foi incubado durante 30 minutos à temperatura ambiente na escuridão. O líquido foi removido, a acetonitrila foi adicionada para cobrir até os pedaços de gel ficarem brancos grudentos, em cujo momento a acetonitrila foi removida. Os pedaços de gel foram reidratados em 100 mM de NH4HCO3 e após 5 minutos, um volume de acetonitrila equivalente a duas vezes 0 volume dos pedaços de gel foi adicionado. Este foi incubado durante 15 minutos, o líquido foi removido e os pedaços de gel foram secos em um Speed Vac. Se o gel fosse corado com azul de coomassie e ainda ficasse algum coomassie residual, a lavagem com 10 mM de NH4HCO3/acetonitrila era repetida.
Digestão in-gel. Pedaços de gel foram completamente secos em um Speed Vac. Os pedaços foram reidratados em tampão de digestão (50 mM de NH4HCO3, 5 mM de CaCI2, 12,5 nanogramas por microlitro (ng/pL) de tripsina) a 4°C. Foi adicionado tampão suficiente para cobrir os pedaços de gel e mais foi adicionado quando necessário. Os pedaços de gel foram incubados em gelo durante 45 minutos e o sobrenadante foi removido e substituído por 5-2 μL do mesmo tampão sem tripsina. Este foi incubado a 37°C durante a noite em uma incubadora com ar.
Extração dos peptídeos. Um volume suficiente de 25 mM de NH4HCO3 foi adicionado para cobrir os pedaços de gel e incubado durante 15 minutos (tipicamente em um ultra-som em banho). O mesmo volume de acetonitrila foi adicionado e incubado durante 15 minutos (em ultra-som em banho, se possível) e o sobrenadante foi recuperado. A extração foi repetida duas vezes, utilizando ácido fórmico a 5% ao invés de NH4HCO3. Um volume suficiente de ácido fórmico a 5% foi adicionado para cobrir os pedaços de gel e incubado durante 15 minutos (tipicamente em um ultra-som em banho). O mesmo volume de acetonitrila foi adicionado e incubado durante 15 5 minutos (tipicamente em um ultra-som em banho) e o sobrenadante foi recuperado. Os extratos foram agrupados e 10 mM de DTT foram adicionados até uma concentração final de 1 mM de DTT. A amostra foi seca em SpeedVac até um volume final de aproximadamente 5 pL.
Dessalificação dos peptídeos. As amostras foram dessalificadas 10 utilizando ponteiras de pipeta ZIPTIP (C18, Millipore, Billerica, MA) como sugerido pelo fabricante. Sucintamente, uma amostra foi reconstituída em solução de reconstituição (5:95 de acetonitrila:H2O, 0,1% 0,5% de ácido trifluoroacético), centrifugada e 0 pH verificado para observar se este era menor que 3. Uma ZIPTIP foi hidratada através da aspiração de 10 pL da 15 solução 1 (50:50 de acetonitrila:H2O, 0,1% de ácido trifluoroacético) e do descarte das alíquotas aspiradas. Isto foi seguido pela aspiração de 10 pL da solução 2 (0,1% de ácido trifluoroacético em H2O deionizada) e pelo descarte das alíquotas aspiradas. A amostra foi carregada na ponteira através da aspiração de 10 pL da amostra lentamente para dentro da ponteira, expe20 lindo os mesmos no tubo de amostra e repetindo isso 5 a 6 vezes. Dez microlitros da solução 2 foram aspirados para dentro da ponteira, a solução foi descartada expelindo-a e este processo foi repetido 5-7 vezes para lavar. Os peptídeo foram eluídos através da aspiração de 2,5 pL da solução 3 gelada (60:40, acetonitrila:H2O, 0,1% de ácido trifluoroacético), expelindo e então 25 reaspirando a mesma alíquota para dentro e para fora da ponteira 3 vezes.
Após a solução ter sido expelida da ponteira, 0 tubo é tampado e armazenado em gelo.
Mapeamento do peptídeo por espectrometría de massa. Os peptídeos foram suspensos em 10 pL até 30 pL de ácido fórmico a 5% e anali30 sados por MALDI-TOF MS (Bruker Daltonics Inc., Billerica, MA). O espectro de massa dos fragmentos peptídicos foi determinado como sugerido pelo fabricante. Sucintamente, uma amostra contendo os peptídeos resultantes de uma digestão tríptica foi misturada com a matriz de ácido ciano-4hidroxicinâmico, transferida para um alvo e permitida secar. A amostra seca foi colocada no espectrômetro de massa, irradiada e o tempo de vôo de cada íon foi detectado e utilizado para determinar um identificação ("fingerprint") de massa do peptídeo para cada proteína presente na composição. Polipeptídeos conhecidos foram utilizados para padronizar a máquina.
Análise dos dados. As massas observadas experimentalmente para os peptídeos em cada espectro de massa foram comparadas com as massas esperadas de proteínas utilizando o método de busca de Peptide Mass Fingerprint da ferramenta de busca Mascot (Matrix Science Ltd., Londres, Reino Unido e www.matrixscience.com, ver Perkins e outros, Electrophoresis 20, 3551-3567 (1999)). Os parâmetros de busca incluíam: banco de dados, MSDB ou NCBInr; taxonomia, bactérias (eubactérias) ou Firmicutes (bactérias gram-positivas); tipo de busca, "fingerprint" de massa do peptídeo; enzima, tripsina; modificações fixas, carbamidometila (C) ou nenhum; modificações variáveis, oxidação (M), carbamidometila (C), a combinação ou nenhum; valores de massa, monoisotópicos; massa da proteína, irrestrita; tolerância de massa do peptídeo, entre +150 ppm e + 430 ppm ou + 1 Da; estado de carga do peptídeo, Mr; clivagens perdidas máximas, 0 ou 1; número de buscas, 20.
O resultado desta busca foi um "fingerprint"de massa para cada proteína presente na composição como é mostrado nas tabelas 2, 3, 4 e 5.
A descrição completa de todas as patentes, pedidos de patentes e publicações e material disponível eletronicamente (incluindo, por exemplo, submissões de sequências de nucleotídeos, por exemplo, no GenBank e no RefSeq e submissões de sequências de aminoácidos, por exemplo, no SwissProt, PIR, PRF, PDB e traduções das regiões codificadoras anotadas no GenBank e no RefSeq) citada aqui é incorporada como referência. A descrição detalhada e os exemplos anteriores foram fornecidos somente para clareza do entendimento. Não devem ser entendidas quaisquer limitações desnecessárias partindo dos mesmos. A invenção não está limitada aos detalhes exatos mostrados e descritos, uma vez que variações óbvias a um versado na técnica serão incluídas dentro da invenção definida pelas reivindicações.
A não ser que seja indicado de outra maneira, todos os números que expressam quantidades de componentes, pesos moleculares e assim por diante utilizados no relatório descritivo e nas reivindicações, devem ser entendidos como sendo modificados em todos os casos pelo termo "aproximadamente". Consequentemente, a não ser que seja indicado de outra maneira o contrário, os parâmetros numéricos apresentados no relatório descritivo e nas reivindicações são aproximações que podem variar dependendo das propriedades desejadas cuja obtenção é pretendida pela presente invenção. Por último e não como uma tentativa de limitar a doutrina de equivalentes para o âmbito das reivindicações, cada parâmetro numérico deve ser pelo menos interpretado à luz do número de dígitos significativos relatados e através da aplicação de técnicas de arredondamento comuns.
Apesar do fato de que as faixas numéricas e os parâmetros que apresentam o âmbito amplo da invenção são aproximações, os valores numéricos apresentados nos exemplos específicos são relatados de forma mais precisa possível. Todos os valores numéricos, entretanto, contêm inerentemente uma faixa necessariamente resultante do desvio padrão encontrado em suas respectivas medidas de teste.
Todos os títulos são para a conveniência do leitor e não devem ser utilizados para limitar o significado do texto que segue o título, a não ser que seja especificado dessa maneira.
Claims (24)
1. Composição, caracterizada pelo fato de que compreende: ao menos cinco polipeptídeos isolados que possuem pesos moleculares de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa ou 33 kDa, em que o peso molecular é determinado através de eletroforese em um gel de poliacrilamida na presença de dodecil sulfato de sódio; em que o polipeptídeo com um peso molecular de 88 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:19, SEQ ID NO:20, SEQ ID NO:21, SEQ ID NO:22, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:28, SEQ ID NO:29, SEQ ID NO:30, SEQ ID NO:31, SEQ ID NO:32, e SEQ ID NO:33, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 55 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:35, SEQ ID NO:37, SEQ ID NO:39, SEQ ID NO:40, SEQ ID NO:41, SEQ ID NO:42, SEQ ID NO:43, SEQ ID NO:44, SEQ ID NO:45, SEQ ID NO:46, SEQ ID NO:49, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:57, SEQ ID NO:58, e SEQ ID NO:59, e é expresso por um Staphylococcus aureus ATCC em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 38 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:72, SEQ ID NO:75, SEQ ID NO:76, e SEQ ID NO:77, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescidono meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 37 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:80, SEQ ID NO:82, SEQ ID NO:84, SEQ ID NO:85, SEQ ID NO:86, SEQ ID NO:87, SEQ ID NO:89, SEQ ID NO:90, SEQ ID NO:91, SEQ ID NO:94, SEQ ID NO:95, SEQ ID NO:96, SEQ ID NO:97, SEQ ID NO:99, SEQ ID NO:100, e SEQ ID NO:101, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 36 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:103, SEQ ID NO:104, SEQ ID NO:105, SEQ ID NO:106, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, e SEQ ID NO:110, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 35 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114, SEQ ID NO:115, SEQ ID NO:116, SEQ ID NO:117, SEQ ID NO:118, SEQ ID NO:119, SEQ ID NO:120, SEQ ID NO:121, SEQ ID NO:122, SEQ ID NO:123, e SEQ ID NO:124, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e em que o polipeptídeo com um peso molecular de 33 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:126, SEQ ID NO:127, SEQ ID NO:128, SEQ ID NO:129, SEQ ID NO:130, SEQ ID NO:131, SEQ ID NO:132, SEQ ID NO:134, SEQ ID NO:135, SEQ ID NO:136, SEQ ID NO:137, SEQ ID NO:138, SEQ ID NO:140, SEQ ID NO:142, e SEQ ID NO:143, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e um adjuvante.
2. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que compreende ainda um veículo farmaceuticamente aceitável.
3. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os polipeptídeos são isolados da cepa ATCC 19636 de S. aureus.
4. Composição, caracterizada pelo fato de que compreende: polipeptídeos isolados que apresentam pesos moleculares de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa, 33 kDa, em que o peso molecular é determinado através de eletroforese em um gel de poliacrilamida com presença de dodecil sulfato de sódio; em que o polipeptídeo com um peso molecular de 88 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:19, SEQ ID NO:20, SEQ ID NO:21, SEQ ID NO:22, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:28, SEQ ID NO:29, SEQ ID NO:30, SEQ ID NO:31, SEQ ID NO:32, e SEQ ID NO:33, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 55 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:35, SEQ ID NO:37, SEQ ID NO:39, SEQ ID NO:40, SEQ ID NO:41, SEQ ID NO:42, SEQ ID NO:43, SEQ ID NO:44, SEQ ID NO:45, SEQ ID NO:46, SEQ ID NO:49, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:57, SEQ ID NO:58, e SEQ ID NO:59, e é expresso por um Staphylococcus aureus ATCC em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 38 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:72, SEQ ID NO:75, SEQ ID NO:76, e SEQ ID NO:77, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 37 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:80, SEQ ID NO:82, SEQ ID NO:84, SEQ ID NO:85, SEQ ID NO:86, SEQ ID NO:87, SEQ ID NO:89, SEQ ID NO:90, SEQ ID NO:91, SEQ ID NO:94, SEQ ID NO:95, SEQ ID NO:96, SEQ ID NO:97, SEQ ID NO:99, SEQ ID NO:100, e SEQ ID NO:101, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 36 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:103, SEQ ID NO:104, SEQ ID NO:105, SEQ ID NO:106, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, e SEQ ID NO:110, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 35 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114, SEQ ID NO:115, SEQ ID NO:116, SEQ ID NO:117, SEQ ID NO:118, SEQ ID NO:119, SEQ ID NO:120, SEQ ID NO:121, SEQ ID NO:122, SEQ ID NO:123, e SEQ ID NO:124, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e em que o polipeptídeo com um peso molecular de 33 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:126, SEQ ID NO:127, SEQ ID NO:128, SEQ ID NO:129, SEQ ID NO:130,SEQ ID NO:131, SEQ ID NO:132, SEQ ID NO:134, SEQ ID NO:135, SEQ ID NO:136, SEQ ID NO:137, SEQ ID NO:138, SEQ ID NO:140, SEQ ID NO:142, e SEQ ID NO:143, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e um adjuvante.
5. Composição de acordo com a reivindicação 4, caracterizada pelo fato de que os polipeptídeos são isolados da cepa ATCC 19636 de S. aureus.
6. Composição de acordo com a reivindicação 4, caracterizada pelo fato de que compreende um veículo farmaceuticamente aceitável.
7. Uso de pelo menos cinco polipeptídeos apresentando pesos moleculares dentre 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa, ou 33 kDa, em que o peso molecular é determinado por eletroforese em gel de poliacrilamida na presença de dodecil sulfato de sódio; em que o polipeptídeo com um peso molecular de 88 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:19, SEQ ID NO:20, SEQ ID NO:21, SEQ ID NO:22, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:28, SEQ ID NO:29, SEQ ID NO:30, SEQ ID NO:31, SEQ ID NO:32, e SEQ ID NO:33, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 55 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:35, SEQ ID NO:37, SEQ ID NO:39, SEQ ID NO:40, SEQ ID NO:41, SEQ ID NO:42, SEQ ID NO:43, SEQ ID NO:44, SEQ ID NO:45, SEQ ID NO:46, SEQ ID NO:49, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:57, SEQ ID NO:58, e SEQ ID NO:59, e é expresso por umStaphylococcus aureus ATCC em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 38 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:72, SEQ ID NO:75, SEQ ID NO:76, e SEQ ID NO:77, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 37 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:80, SEQ ID NO:82, SEQ ID NO:84, SEQ ID NO:85, SEQ ID NO:86, SEQ ID NO:87, SEQ ID NO:89, SEQ ID NO:90, SEQ ID NO:91, SEQ ID NO:94, SEQ ID NO:95, SEQ ID NO:96, SEQ ID NO:97, SEQ ID NO:99, SEQ ID NO:100, e SEQ ID NO:101, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 36 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:103, SEQ ID NO:104, SEQ ID NO:105, SEQ ID NO:106, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, e SEQ ID NO:110, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 35 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114, SEQ ID NO:115, SEQ ID NO:116, SEQ ID NO:117, SEQ ID NO:118, SEQ ID NO:119, SEQ ID NO:120, SEQ ID NO:121, SEQ ID NO:122, SEQ ID NO:123, e SEQ ID NO:124, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meiosem 2,2’-dipiridil; e em que o polipeptídeo com um peso molecular de 33 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:126, SEQ ID NO:127, SEQ ID NO:128, SEQ ID NO:129, SEQ ID NO:130, SEQ ID NO:131, SEQ ID NO:132, SEQ ID NO:134, SEQ ID NO:135, SEQ ID NO:136, SEQ ID NO:137, SEQ ID NO:138, SEQ ID NO:140, SEQ ID NO:142, e SEQ ID NO:143, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; caracterizado pelo fato de que é para a fabricação de uma composição para o tratamento de uma infecção em um indivíduo que tem ou está em risco de ter uma infecção causada por um Staphylococcus spp., ou diminuição da colonização em um indivíduo colonizado por Staphylococcus spp.
8. Uso de acordo com a reivindicação 7, caracterizado pelo fato de que o indivíduo é um mamífero.
9. Uso de acordo com a reivindicação 8, caracterizado pelo fato de que o mamífero é um humano.
10. Uso de acordo com a reivindicação 7, caracterizado pelo fato de o Staphylococcus spp. é S. aureus.
11. Uso de uma combinação de anticorpos que se ligam especificamente a pelo menos cinco polipeptídeos isolados que possuem pesos moleculares de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa, ou 33 kDa, em que o peso molecular é determinado através de eletroforese em um gel de poliacrilamida na presença de dodecil sulfato de sódio; em que o polipeptídeo com um peso molecular de 88 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:19, SEQ ID NO:20, SEQ ID NO:21, SEQ ID NO:22, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:28, SEQ ID NO:29, SEQ ID NO:30, SEQ ID NO:31, SEQ ID NO:32, e SEQ ID NO:33, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 55 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:35, SEQ ID NO:37, SEQ ID NO:39, SEQ ID NO:40, SEQ ID NO:41, SEQ ID NO:42, SEQ ID NO:43, SEQ ID NO:44, SEQ ID NO:45, SEQ ID NO:46, SEQ ID NO:49, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:57, SEQ ID NO:58, e SEQ ID NO:59, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 38 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:68, SEQ ID NO:33, SEQ ID NO:70, SEQ ID NO:72, SEQ ID NO:75, SEQ ID NO:76, e SEQ ID NO:77, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 37 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:40, SEQ ID NO:82, SEQ ID NO:84, SEQ ID NO:85, SEQ ID NO:86, SEQ ID NO:47, SEQ ID NO:89, SEQ ID NO:90, SEQ ID NO:91, SEQ ID NO:94, SEQ ID NO:95, SEQ ID NO:96, SEQ ID NO:97, SEQ ID NO:99, SEQ ID NO:100, and SEQ ID NO:101, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 36 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:103, SEQ ID NO:104, SEQ ID NO:105, SEQ ID NO:106, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, e SEQ ID NO:110, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 35 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114, SEQ ID NO:115, SEQ ID NO:116, SEQ ID NO:117, SEQ ID NO:118, SEQ ID NO:119, SEQ ID NO:120, SEQ ID NO:121, SEQ ID NO:122, SEQ ID NO:123, e SEQ ID NO:124, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e em que o polipeptídeo com um peso molecular de 33 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:126, SEQ ID NO:127, SEQ ID NO:128, SEQ ID NO:129, SEQ ID NO:130, SEQ ID NO:131, SEQ ID NO:132, SEQ ID NO:134, SEQ ID NO:135, SEQ ID NO:136, SEQ ID NO:137, SEQ ID NO:138, SEQ ID NO:140, SEQ ID NO:142, e SEQ ID NO:143, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; caracterizado pelo fato de que é para a fabricação de uma composição para o tratamento de uma infecção em um indivíduo que tem ou está em risco de ter uma infecção causada por um Staphylococcus spp., ou diminuição da colonização em um indivíduo colonizado por Staphylococcus spp.
12. Uso de acordo com a reivindicação 11, caracterizado pelo fato de que o indivíduo é um mamífero.
13. Uso de acordo com a reivindicação 12, caracterizado pelo fato de que o mamífero é um humano.
14. Uso de acordo com a reivindicação 11, caracterizado pelo fato de que o Staphylococcus spp. é S. aureus.
15. Uso de acordo com a reivindicação 11, caracterizado pelo fato de que o anticorpo é anticorpo policlonal.
16. Kit para a detecção de anticorpo que se liga especificamente a um polipeptídeo, caracterizado pelo fato de que compreende em recipientesseparados: ao menos cinco polipeptídeos isolados que apresentam pesos moleculares dentre 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa, ou 33 kDa, em que o peso molecular é determinado através de eletroforese em um gel de poliacrilamida na presença de dodecil sulfato de sódio; em que o polipeptídeo com um peso molecular de 88 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:19, SEQ ID NO:20, SEQ ID NO:21, SEQ ID NO:22, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:28, SEQ ID NO:29, SEQ ID NO:30, SEQ ID NO:31, SEQ ID NO:32, e SEQ ID NO:33, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 55 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:35, SEQ ID NO:37, SEQ ID NO:39, SEQ ID NO:40, SEQ ID NO:41, SEQ ID NO:42, SEQ ID NO:43, SEQ ID NO:44, SEQ ID NO:45, SEQ ID NO:46, SEQ ID NO:49, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:57, SEQ ID NO:58, e SEQ ID NO:59, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 38 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:68, SEQ ID NO:33, SEQ ID NO:70, SEQ ID NO:72, SEQ ID NO:75, SEQ ID NO:76, e SEQ ID NO:77, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil;em que o polipeptídeo com um peso molecular de 37 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:80, SEQ ID NO:82, SEQ ID NO:84, SEQ ID NO:85, SEQ ID NO:86, SEQ ID NO:87, SEQ ID NO:89, SEQ ID NO:90, SEQ ID NO:91, SEQ ID NO:94, SEQ ID NO:95, SEQ ID NO:96, SEQ ID NO:97, SEQ ID NO:99, SEQ ID NO:100, and SEQ ID NO:101, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 36 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:103, SEQ ID NO:104, SEQ ID NO:105, SEQ ID NO:106, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, e SEQ ID NO:110, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 35 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114, SEQ ID NO:115, SEQ ID NO:116, SEQ ID NO:117, SEQ ID NO:118, SEQ ID NO:119, SEQ ID NO:120, SEQ ID NO:121, SEQ ID NO:122, SEQ ID NO:123, e SEQ ID NO:124, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e em que o polipeptídeo com um peso molecular de 33 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:126, SEQ ID NO:127, SEQ ID NO:128, SEQ ID NO:129, SEQ ID NO:130, SEQ ID NO:131, SEQ ID NO:132, SEQ ID NO:134, SEQ ID NO:135, SEQ ID NO:136, SEQ ID NO:137, SEQ ID NO:138, SEQ ID NO:140, SEQ ID NO:142, e SEQ ID NO:143, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e um reagente que detecta um anticorpo que se ligaespecificamente a um dos polipeptídeos.
17. Composição, caracterizada pelo fato de que compreende: uma combinação de anticorpos isolados que se ligam especificamente a polipeptídeos que possuem pesos moleculares de 88 kDa, 55 kDa, 38 kDa, 37 kDa, 36 kDa, 35 kDa ou 33 kDa, em que o peso molecular é determinado através de eletroforese em um gel de poliacrilamida na presença de dodecil sulfato de sódio; em que o polipeptídeo com um peso molecular de 88 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:19, SEQ ID NO:20, SEQ ID NO:21, SEQ ID NO:22, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:28, SEQ ID NO:29, SEQ ID NO:30, SEQ ID NO:31, SEQ ID NO:32, e SEQ ID NO:33, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 55 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:35, SEQ ID NO:37, SEQ ID NO:39, SEQ ID NO:40, SEQ ID NO:41, SEQ ID NO:42, SEQ ID NO:43, SEQ ID NO:44, SEQ ID NO:45, SEQ ID NO:46, SEQ ID NO:49, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:57, SEQ ID NO:58, e SEQ ID NO:59, e é expresso por um Staphylococcus aureus ATCC em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 38 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:64, SEQ ID NO:65, SEQ ID NO:66, SEQ ID NO:68, SEQ ID NO:69, SEQ ID NO:70, SEQ ID NO:72, SEQ ID NO:75, SEQ ID NO:76, e SEQ ID NO:77, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 37 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:40, SEQ ID NO:82, SEQ ID NO:84, SEQ ID NO:85, SEQ ID NO:86, SEQ ID NO:47, SEQ ID NO:89, SEQ ID NO:90, SEQ ID NO:91, SEQ ID NO:94, SEQ ID NO:95, SEQ ID NO:96, SEQ ID NO:97, SEQ ID NO:99, SEQ ID NO:100, e SEQ ID NO:101, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 36 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:103, SEQ ID NO:104, SEQ ID NO:105, SEQ ID NO:106, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, e SEQ ID NO:110, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; em que o polipeptídeo com um peso molecular de 35 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114, SEQ ID NO:115, SEQ ID NO:116, SEQ ID NO:117, SEQ ID NO:118, SEQ ID NO:119, SEQ ID NO:120, SEQ ID NO:121, SEQ ID NO:122, SEQ ID NO:123, e SEQ ID NO:124, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μM comparado a quando crescido no meio sem 2,2’-dipiridil; e em que o polipeptídeo com um peso molecular de 33 kDa compreende as sequências de aminoácidos apresentadas em SEQ ID NO:126, SEQ ID NO:127, SEQ ID NO:128, SEQ ID NO:129, SEQ ID NO:130, SEQ ID NO:131, SEQ ID NO:132, SEQ ID NO:134, SEQ ID NO:135, SEQ ID NO:136, SEQ ID NO:137, SEQ ID NO:138, SEQ ID NO:140, SEQ ID NO:142, e SEQ ID NO:143, e é expresso por um Staphylococcus aureus em alto nível quando crescido em meio que compreende 2,2’-dipiridil a 1600 μMcomparado a quando crescido no meio sem 2,2’-dipiridil.
18. Composição de acordo com a reivindicação 17, caracterizada pelo fato de que compreende ainda um veículo farmaceuticamente aceitável.
19. Composição de acordo com a reivindicação 17, caracterizada pelo fato de que os anticorpos são anticorpos policlonais.
20. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os polipeptídeos são isolados de um Staphylococcus aureus quando incubados em meios compreendendo 1600 μM de 2,2’-dipiridil e não são isolados quando crescidos nos meios sem 1600 μM de 2,2’-dipiridil.
21. Composição de acordo com a reivindicação 4, caracterizada pelo fato de que os polipeptídeos são isolados de um Staphylococcus aureus quando incubados em meios compreendendo 1600 μM de 2,2’-dipiridil e não são isolados quando crescidos nos meios sem 1600 μM de 2,2’-dipiridil.
22. Uso de acordo com a reivindicação 7, caracterizada pelo fato de que os polipeptídeos são isolados de um Staphylococcus aureus quando incubados em meios compreendendo 1600 μM de 2,2’-dipiridil e não são isolados quando crescidos nos meios sem 1600 μM de 2,2’-dipiridil.
23. Uso de acordo com a reivindicação 11, caracterizada pelo fato de que os polipeptídeos são isolados de um Staphylococcus aureus quando incubados em meios compreendendo 1600 μM de 2,2’-dipiridil e não são isolados quando crescidos nos meios sem 1600 μM de 2,2’-dipiridil.
24.Composição de acordo com a reivindicação 17, caracterizada pelo fato de que os polipeptídeos são isolados de um Staphylococcus aureus quando incubados em meios compreendendo 1600 μM de 2,2’-dipiridil e não são isolados quando crescidos nos meios sem 1600 μM de 2,2’-dipiridil.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US65284305P | 2005-02-14 | 2005-02-14 | |
| US60/652,843 | 2005-02-14 | ||
| PCT/US2006/005058 WO2006088803A2 (en) | 2005-02-14 | 2006-02-14 | Polypeptides from staphylococcus aureus and methods of use |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0607323A2 BRPI0607323A2 (pt) | 2009-09-01 |
| BRPI0607323B1 true BRPI0607323B1 (pt) | 2020-12-22 |
| BRPI0607323B8 BRPI0607323B8 (pt) | 2021-05-25 |
Family
ID=36694403
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0607323A BRPI0607323B8 (pt) | 2005-02-14 | 2006-02-14 | composições, usos de polipeptídeos e de anticorpos, bem como kits para a detecção de anticorpo que se liga especificamente a um polipeptídeo |
Country Status (12)
| Country | Link |
|---|---|
| US (13) | US8007811B2 (pt) |
| EP (1) | EP1853306B1 (pt) |
| JP (3) | JP2008532935A (pt) |
| CN (2) | CN101119744B (pt) |
| AU (1) | AU2006214534B2 (pt) |
| BR (1) | BRPI0607323B8 (pt) |
| CA (1) | CA2597263C (pt) |
| DK (1) | DK1853306T3 (pt) |
| ES (1) | ES2586125T3 (pt) |
| MX (1) | MX2007009828A (pt) |
| NZ (4) | NZ560612A (pt) |
| WO (1) | WO2006088803A2 (pt) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5830479A (en) * | 1994-02-09 | 1998-11-03 | Willmar Poultry Company, Inc. | Active immunization using a siderophore receptor protein |
| WO1995021627A1 (en) * | 1994-02-09 | 1995-08-17 | Willmar Poultry Company, Inc. | Active immunization using a siderophore receptor protein |
| DE19962924A1 (de) | 1999-12-24 | 2001-07-05 | Bayer Ag | Substituierte Oxazolidinone und ihre Verwendung |
| CA2433561C (en) * | 2001-01-03 | 2014-04-01 | Willmar Poultry Company, Inc. | Compositions including gram negative siderophore receptor proteins and methods of use |
| EP1678316B1 (en) | 2003-09-19 | 2011-08-17 | Epitopix, LLC | Campylobacter polypeptides and methods of use |
| NZ560612A (en) * | 2005-02-14 | 2011-01-28 | Epitopix Llc | Polypeptides from staphylococcus aureus and methods of use |
| AU2007221321B2 (en) * | 2006-02-22 | 2012-06-28 | The Texas A & M University System | Antibodies recognizing a highly expressed putative antigen of CA-MRSA and methods of use |
| JP5564249B2 (ja) * | 2006-06-23 | 2014-07-30 | アレシア・バイオセラピューティクス・インコーポレーテッド | 癌に関与するポリヌクレオチド配列およびポリペプチド配列 |
| WO2010060186A1 (en) | 2008-11-03 | 2010-06-03 | Alethia Biotherapeutics Inc. | Antibodies that specifically block the biological activity of a tumor antigen |
| EP2411046B1 (en) * | 2009-03-23 | 2017-12-06 | Epitopix, LLC | Polypeptides and immunizing compositions containing gram positive polypeptides and methods of use |
| JP6294221B2 (ja) | 2011-03-31 | 2018-03-14 | アー・デー・ツェー・セラピューティクス・エス・アー | 腎臓関連抗原1に対する抗体およびその抗原結合性フラグメント |
| TR201908872T4 (tr) | 2012-01-09 | 2019-07-22 | Adc Therapeutics Sa | Üçlü negatif meme kanserini tedavi etmek için ajanlar. |
| US9169477B2 (en) | 2012-01-27 | 2015-10-27 | Los Angeles Biomedical Research Institute At Harbor-Ucla Medical Center | Compositions and methods for immunization against bacteria expressing a carbapenemase |
| US10100093B2 (en) | 2013-12-31 | 2018-10-16 | Epitopix Llc | Polypeptides and immunizing compositions containing Burkholderia polypeptides and methods of use |
| US11000582B2 (en) | 2015-07-10 | 2021-05-11 | Epitopix, Llc | Proteins and immunizing compositions containing klebsiella proteins and methods of use |
| WO2017024038A1 (en) * | 2015-08-03 | 2017-02-09 | The Arizona Board Of Regents On Behalf Of The University Of Arizona | Solar concentrator for a tower-mounted central receiver |
| US10166280B2 (en) | 2016-06-08 | 2019-01-01 | Epitopix, Llc | Polypeptides and immunizing compositions containing Bacillus polypeptides and methods of use |
| US10738338B2 (en) | 2016-10-18 | 2020-08-11 | The Research Foundation for the State University | Method and composition for biocatalytic protein-oligonucleotide conjugation and protein-oligonucleotide conjugate |
| TWI733412B (zh) * | 2020-04-13 | 2021-07-11 | 華邦電子股份有限公司 | 具有氣隙之半導體元件及其製造方法 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4981685A (en) | 1986-03-07 | 1991-01-01 | Utah State University Foundation | Bacterial extract vaccines for veterinary application |
| US5554372A (en) | 1986-09-22 | 1996-09-10 | Emory University | Methods and vaccines comprising surface-active copolymers |
| US5292869A (en) | 1989-04-27 | 1994-03-08 | The Board Of Governors Of The University | Method for isolating and purifying transferrin and lactoferrin receptor proteins from bacteria and the preparation of vaccines containing the same |
| WO1995021627A1 (en) | 1994-02-09 | 1995-08-17 | Willmar Poultry Company, Inc. | Active immunization using a siderophore receptor protein |
| US5830479A (en) | 1994-02-09 | 1998-11-03 | Willmar Poultry Company, Inc. | Active immunization using a siderophore receptor protein |
| US5538733A (en) | 1994-07-07 | 1996-07-23 | Willmar Poultry Company, Inc. | Method of priming an immune response in a one-day old animal |
| US6403337B1 (en) * | 1996-01-05 | 2002-06-11 | Human Genome Sciences, Inc. | Staphylococcus aureus genes and polypeptides |
| EP0950068B1 (en) * | 1996-05-16 | 2005-11-09 | THE TEXAS A&M UNIVERSITY SYSTEM | Collagen binding protein compositions and methods of use |
| US6680195B1 (en) | 1997-11-26 | 2004-01-20 | Inhibitex, Inc. | Extracellular matrix-binding proteins from staphylococcus aureus |
| US6692739B1 (en) | 1998-08-31 | 2004-02-17 | Inhibitex, Inc. | Staphylococcal immunotherapeutics via donor selection and donor stimulation |
| US6703025B1 (en) | 1998-08-31 | 2004-03-09 | Inhibitex, Inc. | Multicomponent vaccines |
| US6682754B2 (en) | 1999-11-24 | 2004-01-27 | Willmar Poultry Company, Inc. | Ovo delivery of an immunogen containing implant |
| WO2001070955A2 (en) | 2000-03-21 | 2001-09-27 | Elitra Pharmaceuticals, Inc. | Identification of essential genes in prokaryotes |
| AT410173B (de) | 2000-06-08 | 2003-02-25 | Cistem Biotechnologies Gmbh | Antigene zusammensetzung |
| CA2433561C (en) * | 2001-01-03 | 2014-04-01 | Willmar Poultry Company, Inc. | Compositions including gram negative siderophore receptor proteins and methods of use |
| AT410798B (de) | 2001-01-26 | 2003-07-25 | Cistem Biotechnologies Gmbh | Verfahren zur identifizierung, isolierung und herstellung von antigenen gegen ein spezifisches pathogen |
| GB0107661D0 (en) | 2001-03-27 | 2001-05-16 | Chiron Spa | Staphylococcus aureus |
| CA2450939C (en) | 2001-06-15 | 2012-11-06 | The Provost Fellows And Scholars Of The College Of The Holy And Undivided Trinity Of Queen Elizabeth Near Dublin | Cross-reactive monoclonal and polyclonal antibodies which recognize surface proteins from coagulase-negative staphylococci and staphylococcus aureus |
| WO2003020875A2 (en) * | 2001-06-17 | 2003-03-13 | D-Squared Biotechnologies, Inc. | Staphylococci surface-exposed immunogenic polypeptides |
| US6720160B2 (en) | 2001-10-11 | 2004-04-13 | Helica Biosystems, Inc. | Method for simultaneous detection of multiple microbial antigens in biological specimens from mastitic animals |
| AU2003254555A1 (en) | 2002-07-26 | 2004-02-23 | Intercell Ag | S. aureus antigene |
| US6947260B2 (en) * | 2002-11-18 | 2005-09-20 | Hitachi Global Storage Technologies Netherlands B.V. | System and method of damping vibration on coil supports in high performance disk drives with rotary actuators |
| EP1678316B1 (en) | 2003-09-19 | 2011-08-17 | Epitopix, LLC | Campylobacter polypeptides and methods of use |
| US20070128183A1 (en) | 2004-04-27 | 2007-06-07 | Intercell Ag | Td antigens |
| EP1784220B1 (en) | 2004-08-26 | 2017-12-20 | The University Of Western Ontario | Bacterial iron acquisition targets |
| CA2581746A1 (en) | 2004-10-25 | 2006-06-08 | The University Of Western Ontario | Staphylococcus aureus isd protein-based anti-infectives |
| NZ560612A (en) | 2005-02-14 | 2011-01-28 | Epitopix Llc | Polypeptides from staphylococcus aureus and methods of use |
| EP2411046B1 (en) | 2009-03-23 | 2017-12-06 | Epitopix, LLC | Polypeptides and immunizing compositions containing gram positive polypeptides and methods of use |
-
2006
- 2006-02-14 NZ NZ560612A patent/NZ560612A/en not_active IP Right Cessation
- 2006-02-14 US US11/353,459 patent/US8007811B2/en not_active Expired - Lifetime
- 2006-02-14 NZ NZ597997A patent/NZ597997A/xx not_active IP Right Cessation
- 2006-02-14 NZ NZ589238A patent/NZ589238A/en not_active IP Right Cessation
- 2006-02-14 NZ NZ613923A patent/NZ613923A/en not_active IP Right Cessation
- 2006-02-14 AU AU2006214534A patent/AU2006214534B2/en not_active Ceased
- 2006-02-14 MX MX2007009828A patent/MX2007009828A/es active IP Right Grant
- 2006-02-14 WO PCT/US2006/005058 patent/WO2006088803A2/en not_active Ceased
- 2006-02-14 CN CN2006800049030A patent/CN101119744B/zh not_active Expired - Fee Related
- 2006-02-14 CN CN201310020750.0A patent/CN103143006B/zh not_active Expired - Fee Related
- 2006-02-14 CA CA2597263A patent/CA2597263C/en not_active Expired - Lifetime
- 2006-02-14 EP EP06734951.4A patent/EP1853306B1/en not_active Expired - Lifetime
- 2006-02-14 JP JP2007555321A patent/JP2008532935A/ja not_active Withdrawn
- 2006-02-14 BR BRPI0607323A patent/BRPI0607323B8/pt not_active IP Right Cessation
- 2006-02-14 DK DK06734951.4T patent/DK1853306T3/en active
- 2006-02-14 ES ES06734951.4T patent/ES2586125T3/es not_active Expired - Lifetime
- 2006-09-11 US US11/518,727 patent/US8025885B2/en active Active
- 2006-09-11 US US11/518,689 patent/US8007803B2/en active Active
-
2008
- 2008-03-18 US US12/077,268 patent/US8709436B2/en active Active
- 2008-11-17 US US12/272,021 patent/US8709760B2/en active Active
-
2012
- 2012-01-31 US US13/362,992 patent/US8961979B2/en not_active Expired - Lifetime
- 2012-12-05 JP JP2012266189A patent/JP2013053155A/ja not_active Withdrawn
-
2013
- 2013-07-01 US US13/932,875 patent/US20130287813A1/en not_active Abandoned
- 2013-07-01 US US13/932,870 patent/US20130288952A1/en not_active Abandoned
- 2013-07-01 US US13/932,863 patent/US20130280300A1/en not_active Abandoned
- 2013-07-01 US US13/932,877 patent/US20140005360A1/en not_active Abandoned
-
2015
- 2015-01-29 US US14/608,493 patent/US9266944B2/en not_active Expired - Lifetime
- 2015-05-01 JP JP2015094191A patent/JP6100826B2/ja not_active Expired - Fee Related
-
2016
- 2016-02-15 US US15/043,740 patent/US9623076B2/en not_active Expired - Lifetime
-
2017
- 2017-03-09 US US15/454,197 patent/US9981028B2/en not_active Expired - Lifetime
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9981028B2 (en) | Polypeptides and immunizing compositions containing gram positive polypeptides and methods of use | |
| AU2015258239B2 (en) | Polypeptides from staphylococcus aureus and methods of use | |
| AU2012244060B2 (en) | Polypeptides from staphylococcus aureus and methods of use | |
| HK1186126A (en) | Polypeptides from staphylococcus aureus and methods of use | |
| HK1117746B (en) | Polypeptides and immunizing compositions containing gram positive polypeptides and methods of use | |
| HK1186126B (en) | Polypeptides from staphylococcus aureus and methods of use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] |
Free format text: NOTIFICACAO DE ANUENCIA RELACIONADA COM O ART 229 DA LPI |
|
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09B | Patent application refused [chapter 9.2 patent gazette] | ||
| B12B | Appeal against refusal [chapter 12.2 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 22/12/2020, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 14/02/2006 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 20A ANUIDADE. |