BRPI0611765B1 - Anticorpo ou fragmento de anticorpo estável e solúvel que se liga especificamente ao tnf-alfa seus usos e composição diagnóstica ou terapêutica - Google Patents
Anticorpo ou fragmento de anticorpo estável e solúvel que se liga especificamente ao tnf-alfa seus usos e composição diagnóstica ou terapêutica Download PDFInfo
- Publication number
- BRPI0611765B1 BRPI0611765B1 BRPI0611765-1A BRPI0611765A BRPI0611765B1 BR PI0611765 B1 BRPI0611765 B1 BR PI0611765B1 BR PI0611765 A BRPI0611765 A BR PI0611765A BR PI0611765 B1 BRPI0611765 B1 BR PI0611765B1
- Authority
- BR
- Brazil
- Prior art keywords
- antibody
- seq
- tnfα
- antibodies
- scfv
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/241—Tumor Necrosis Factors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/522—CH1 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/567—Framework region [FR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Cardiology (AREA)
- Rheumatology (AREA)
- Pulmonology (AREA)
- Neurosurgery (AREA)
- Microbiology (AREA)
- Physical Education & Sports Medicine (AREA)
- Pain & Pain Management (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Ophthalmology & Optometry (AREA)
- Heart & Thoracic Surgery (AREA)
- Hospice & Palliative Care (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Mycology (AREA)
- Epidemiology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
ANTICORPOS ESTÁVEIS E SOLÚVEIS QUE INIBEM TNFALFA. A presente invenção refere-se a anticorpos scFv e fragmentos Fab particularmente estáveis e solúveis, específicos para TNF(Alfa), que compreendem seqüências com cadeia leve e cadeia pesada específicas, que são otimizadas quanto à estabilidade, solubilidade ligação in vitro e in vivo, e baixa imunogenicidade. Os ditos anticorpos são desenhados para o diagnóstico e/ou tratamento de distúrbios relacionados a TNF(Alfa). Os ácidos nucléicos, vetores e células hospedeiras para a expressão dos anticorpos recombinantes da invenção, os métodos para isolá-los e o uso dos ditos anticorpos em medicina, também são descritos.
Description
[0001] A presente invenção refere-se a anticorpos otimizados e derivados de anticorpos otimizados que se ligam ao fator alfa de necrose tumoral (TNFα) e bloqueiam sua função, e são úteis para o diagnóstico e/ou tratamento, prevenção ou melhora de doenças associadas ao TNFα; suas sequências codificadoras, produção e uso em composições farmacologicamente apropriadas.
[0002] O fator de necrose tumoral alfa (TNFα, também conhecido como caquectina) é uma citocina de ocorrência natural em mamíferos, produzida por inúmeros tipos de células, incluindo monócitos e macrófagos, em resposta a endotoxinas ou outros estímulos. TNFα é um mediador importante de reações inflamatórias, imunológicas e patofisiológicas (Grell, M. et al., Cell 83:793-802 (1995)).
[0003] O TNFα solúvel é formado pela clivagem de uma proteína transmembrana precursora (Kriegler et al., Cell 53:45-53 (1988)), e os polipeptídeos de 17 kDa secretados montam complexos homotriméricos solúveis (Smith et al., J. Biol. Chem. 262:6951-6954 (1987); para obter revisões vide Butler et al., Nature 320:584 (1986); Old, Science 230:630 (1986)). Estes complexos, então, se ligam a receptores encontrados em uma série de células. A ligação produz um arranjo de efeitos pró- inflamatórios, incluindo (i) liberação de outras citocinas pró- inflamatórias, tais como interleucina IL-6, IL-8 e IL-1, (ii) liberação de metaloproteinases de matriz, e (iii) regulação ascendente da expressão de moléculas de adesão endotelial, ampliando ainda mais a cascata inflamatória e imunológica por atrair leucócitos para dentro de tecidos extravasculares.
[0004] Inúmeros distúrbios estão associados a níveis elevados de TNFα, muitos deles de importância médica significativa. TNFα demonstrou estar regulado de forma ascendente em inúmeras doenças humanas, incluindo doenças crônicas tais como artrite reumatoide, distúrbios inflamatórios dos intestinos, incluindo doença de Crohn e colite ulcerativa, sepse, insuficiência cardíaca congestiva, asma brônquica, e esclerose múltipla. Os camundongos transgênicos quanto ao TNFα humano produzem altos níveis de TNFα constitutivamente e desenvolvem uma poliartrite espontânea destrutiva semelhante à artrite reumatoide (Keffer et al., EMBO J.10:4025-4031 (1991)). TNFα é, portanto, referido como uma citocina pró-inflamatória.
[0005] TNFα está agora bem estabelecido como um fator importante na patogênese de artrite reumatoide, que é uma doença crônica, progressiva e incapacitante, distinguida por inflamação e destruição poliarticular, com sintomas sistêmicos de febre, mal-estar e fadiga. A artrite reumatoide leva também à inflamação sinovial crônica, com frequente progressão para destruição das cartilagens e ossos articulares. Níveis aumentados de TNFα são encontrados no líquido sinovial e no sangue periférico de pacientes que sofrem de artrite reumatoide. Quando agentes bloqueadores de TNFα são administrados a pacientes que sofrem de artrite reumatoide, eles reduzem a inflamação, melhorar os sintomas e retardam a danificação das articulações (McKown et al., Arthritis Rheum. 42:1204-1208 (1999)).
[0006] Fisiologicamente, TNFα está associado também à proteção contra infecções específicas (Cerami et al., Immunol. Today 9:28 (1988)). TNFα é liberado por macrófagos que foram ativados por lipopolissacarídeos de bactérias gram-negativas. Assim sendo, TNFα parece ser um mediador endógeno de importância fundamental, envolvido no desenvolvimento e patogênese de choque endotóxico associado com sepse bacteriana (Michie et al., Br. J. Surg. 76:670-671 (1989); Debets et al., "Second Vienna Shock Forum", páginas 463-466 (1989); Simpson et al., Crit. Care Clin. 5:27-47 (1989); Waage et al., Lancet 1:355-357 (1987); Hammerle et al., "Second Vienna Shock Forum", páginas 715-718 (1989); Debets et al., Crit. Care Med. 17:489497 (1989); Calandra et al., J. Infect. Dis. 161:982-987 (1990); Revhaug et al. Arch. Surg. 123:162-170 (1988)).
[0007] Da mesma forma que em outros sistemas orgânicos, TNFα demonstrou também desempenhar um papel importante no sistema nervoso central, particularmente em distúrbios inflamatórios e autoimunes do sistema nervoso, incluindo esclerose múltipla, síndrome de Guillain-Barré e miastenia grave, e em distúrbios neurodegenerativos do sistema nervoso, incluindo doença de Alzheimer, doença de Parkinson e doença de Huntington. TNF α está envolvido também em distúrbios de sistemas afins da retina e do músculo, incluindo neurite óptica, degeneração macular, retinopatia diabética, dermatomiosite, esclerose lateral amiotrófica, bem como em lesões ao sistema nervoso, incluindo lesão cerebral traumática, lesão aguda do cordão espinhal, e acidente vascular cerebral.
[0008] A hepatite é outro distúrbio inflamatório relacionado ao TNFα, que, dentre outros disparadores, pode ser causada por infecções virais, incluindo Epstein-Barr, citomegalovírus, e vírus das hepatites A- E. A hepatite causa inflamação aguda do fígado na região portal e lobular, e em seguida, fibrose e progressão de tumores.
[0009] TNFα pode mediar a caquexia em câncer, que causa a maior parte da morbidade e morbidez de câncer (Tisdale, M.J., Langenbecks Arch. Surg. 389:299-305 (2004)).
[00010] O papel importante desempenhado por TNFα em inflamação, em respostas celulares imunes e na patologia de muitas doenças, levou à busca por antagonistas de TNFα.
[00011] TNFα é uma citocina importante, cujo bloqueio sistêmico porta o risco de maior frequência e gravidade de infecções clinicamente manifestadas, particularmente a reativação de tuberculose latente e possivelmente outros riscos que incluem indução de linfomas, doenças desmielinizantes e insuficiência cardíaca.
[00012] Uma classe de antagonistas de TNFα, desenhada para o tratamento de doenças mediadas por TNFα, são anticorpos ou fragmentos de anticorpos que se ligam especificamente ao TNFα, e desta forma, bloqueiam sua função. O uso de anticorpos anti-TNFα demonstrou que um bloqueio de TNFα pode reverter efeitos atribuídos ao TNFα, incluindo decréscimos em IL-1, GM-CSF, IL-6, IL-8, moléculas de adesão e destruição tecidual (Feldmann et al. Adv. Immunol. 1997:283-350 (1997)).
[00013] Os anticorpos direcionados contra TNFα foram propostos para a profilaxia e tratamento de choque endotóxico (Beutler et al., Science 234:470-474 (1985)). O uso de anticorpos anti-TNFα no tratamento de choque séptico está discutido em Bodmer et al., Crit. Care Med. 21:441-446 (1993); Wherry et al., Crit. Care Med. 21:436-440 (1993); e Kirschenbaum et al., Crit. Care Med. 26:1625-1626 (1998).
[00014] Um método para tratar uma doença neurodegenerativa em um humano administrando um anticorpo monoclonal anti-TNFα ou um seu fragmento ligante de TNFα foi descrito no documento no US 2003/147.891.
[00015] O documento no WO 0149321 enuncia o uso de bloqueadores de TNFα, incluindo anticorpos anti-TNFα, para tratar distúrbios neurológicos e afins causados por TNFα. O documento fornece um método para tratar os ditos distúrbios administrando um antagonista de TNFα.
[00016] O documento no WO 03047510 descreve vários tipos de anticorpos monoclonais e manipulados, direcionados contra TNFα, sua produção, compostos que os compreendem e o uso em medicina.
[00017] Os anticorpos úteis para terapias de doenças mediadas por TNFα são usualmente anticorpos monoclonais (mAb) produzidos por tecnologia com hibridomas a partir de uma fonte natural, usualmente um camundongo, ou anticorpos obtidos por bioengenharia. Estes últimos correspondem a anticorpos de ocorrência natural pelo fato de que eles compreendem cadeias pesadas e leves de comprimento inteiro, ou aos fragmentos Fab que também podem ser gerados a partir de anticorpos naturais por clivagem proteolítica, ou a anticorpos scFv de cadeia única, onde os fragmentos das regiões variáveis das cadeias pesadas e leves são ligadas por um ligante peptídico.
[00018] As cadeias pesadas e leves de um anticorpo compreendem domínios constantes e variáveis. Como os anticorpos não-humanos são imunogênicos, a quantidade de sequências semelhantes às humanas em um anticorpo é frequentemente aumentada em um anticorpo assim denominado "híbrido", que compreende regiões constantes de uma IgG humana, e regiões variáveis equivalentes às sequências de um anticorpo de animal, na maioria dos casos anticorpos murinos com a especificidade desejada. Estas regiões variáveis podem ser então adaptadas adicionalmente para se tornarem mais similares a um anticorpo humano típico por mutagênese, levando a um anticorpo "humanizado". Em ainda mais uma modalidade alternativa, apenas as partes ligantes de antígenos, isto é, as regiões determinantes complementares (CDRs) das regiões variáveis de um anticorpo de camundongo são combinadas com a estrutura de um anticorpo humano, resultando em um anticorpo "enxertado com CDR".
[00019] Os anticorpos monoclonais contra TNFα foram descritos nas técnicas anteriores. Meager et al., Hybridoma 6:305-311 (1987), descrevem anticorpos monoclonais murinos contra TNFα recombinante. Shimamoto et al., Immunol. Lett. 17:311-318 (1988), descrevem o uso de anticorpos monoclonais murinos contra TNF α na prevenção de choque endotóxico em camundongos.
[00020] A patente no US 5.919.452 descreve anticorpos quiméricos anti-TNFα e seu uso no tratamento de patologias associadas à presença de TNFα.
[00021] O uso de anticorpos anti-TNFα no tratamento de artrite reumatoide e doença de Crohn está discutido em Feldman et al., Transplantation Proceedings 30:4126-4127 (1998); Adorini et al., Trends in Immunology Today 18:209-211 (1997); e Feldman et al., Advanced Immunology 64:283-350 (1997). Os anticorpos para TNFα usados nesses tratamentos são geralmente anticorpos quiméricos, tais como aqueles descritos na patente no US 5.919.452.
[00022] O documento no US 2003/3187231 descreve anticorpos anti- TNFα humanizados com pelo menos uma região CDR não-humana que tem melhores características de ligação. Além disso, no pedido de patente internacional no WO 92/11383, estão descritos anticorpos recombinantes, incluindo anticorpos enxertados com CDR, específicos para TNFα. Rankin et al., Br. J. Rheumatol. 34:334-342 (1995), descrevem o uso desses anticorpos enxertados com CDR no tratamento de artrite reumatoide.
[00023] O documento no WO 9211383 descreve um anticorpo recombinante humanizado enxertado com CDR específico para TNFα, que é derivado a partir de um anticorpo monoclonal murino 61E7, hTNF1, hTNF3 ou 101.4, e ele enuncia a produção e uso dos ditos anticorpos no diagnóstico e/ou terapia de distúrbios associados ao TNFα.
[00024] Dentre os inibidores de TNFα específicos que se tornaram comercialmente disponíveis apenas recentemente, um anticorpo monoclonal, quimérico murino-humano, direcionado contra TNFα (infliximab, Remicade®; Centocor Corporation/Johnson & Johnson), demonstrou eficácia clínica no tratamento do distúrbio inflamatório do intestino, doença de Crohn (Baert et al., Gastroenterology 116:22-28 (1999)).
[00025] O documento no US 22002037934 descreve o tratamento de hepatite pela administração de um anticorpo anti-TNFa, tal como in infliximab.
[00026] A patente no US 6.428.787 enuncia o tratamento de doenças neurológicas e associadas ao TNF com anticorpos anti-TNFa, incluindo infliximab, CDP571 e D2E7.
[00027] D2E7 (adalimumab), um anticorpo monoclonal humano anti- TNFa (Abbott), foi desenvolvido para tratar artrite reumatoide e doença de Crohn (documento no WO 9729131). Celltech está desenvolvendo CDP571 (documento no EP 0626389), um anticorpo de IgG4 monoclonal anti-TNFa humanizado, para tratar doença de Crohn, e CDP870, um fragmento de anticorpo monoclonal anti-TNFa humanizado, para tratar artrite reumatoide. A administração local dos ditos anticorpos está descrita no documento no US 20033185826.
[00028] Muitos anticorpos de cadeia única (scFv's) foram gerados contra uma série de antígenos diferentes, particularmente porque eles podem ser selecionados facilmente quanto a uma alta capacidade de ligação, usando técnicas tais como, por exemplo, apresentação de fagos ou apresentação de ribossomas. Além disso, podem ser produzidos anticorpos scFv podem em sistemas microbianos, que estão associados com menores custos em comparação com a produção de anticorpos terapêuticos de comprimento inteiro.
[00029] Além de aplicações convencionais extracelulares e in vitro, os scFvs têm sido usados também com êxito para aplicações intracelulares (Worn et al., JBC 28;275(4):2795-2803 (2000); Auf der Maur et al., JBC 22;277(47):45075-45085 (2002); Stocks, M.R., Drug Discovery Today 15;9(22):960-966 (2004)); assim sendo, foram desenvolvidos scFv's direcionados contra antígenos intracelulares. Geralmente, a expressão intracelular de scFvs funcional está limitada por sua instabilidade, insolubilidade, e tendência a formar agregados. Por esta razão, sistemas de triagem in vivo para anticorpos scFvs, que são particularmente solúveis e estáveis sob condições redutoras típicas para o ambiente intracelular (por exemplo, núcleo, citoplasma), foram desenvolvidos com êxito usando uma assim denominada triagem por "Controle de Qualidade" (documento no WO 03097697). Além disso, essas estruturas apresentam níveis de expressão convencionais e melhores propriedades de estabilidade e solubilidade também sob condições naturais oxidantes no ambiente extracelular. Assim sendo, propriedades biofísicas e bioquímicas favoráveis se traduzem em altos volumes de produção favoráveis e permitem que esses fragmentos de anticorpos, uma vez direcionados contra antígenos específicos, sejam aplicados localmente e/ou por via sistêmica como terapias protéicas em áreas terapêuticas específicas. Como os anticorpos scFv e fragmentos Fab, em contraste com anticorpos de comprimento inteiro, carecem da parte Fc que é reconhecida pelo receptor de Fc de monócitos, tais como, por exemplo, células exterminadoras naturais, eles não evocam citotoxicidade mediada por células, dependente de anticorpos (ADCC), e assim sendo, não provocam toxicidade inespecífica devido à ligação a receptores de Fc em células não-alvo.
[00030] Assim sendo, há uma necessidade de se obter novas formas eficazes de anticorpos para o tratamento de distúrbios associados ao TNFα, tais como artrite reumatoide, particularmente tratamentos que podem proporcionar terapia prolongada controlada por administração local com um baixo grau de efeitos colaterais. A presente invenção fornece anticorpos, composições e métodos para o tratamento eficaz e contínuo de processos inflamatórios de artrite e outros distúrbios ou mecanismos patofisiológicos mediados por TNFα, particularmente várias formas de dor.
[00031] Todas publicações e referências aqui citadas são aqui incorporadas como referência em sua totalidade.
[00032] Assim sendo, é um objetivo geral da invenção fornecer um anticorpo ou derivado de anticorpo estável e solúvel, que se liga especificamente ao TNFα in vivo. Em uma modalidade preferida, o dito derivado de anticorpo é um anticorpo scFv ou um fragmento Fab.
[00033] Agora, para implementar estes e ainda outros objetos da invenção, que tornar-se-ão mais facilmente evidentes à medida que a descrição prossegue, o dito anticorpo ou derivado de anticorpo se manifesta pelas características que ele compreende um domínio variável de cadeia leve ou é derivado da sequência SEQ ID NO: 1 que é combinada com um domínio variável de cadeia pesada sendo ou não derivado da sequência SEQ ID NO: 2, onde no caso de uma sequência derivada, a dita sequência tem no máximo até 5 mudanças dentro da estrutura do dito domínio VL (variável leve) e/ou no máximo até 9 mudanças dentro da estrutura do dito VH (variável pesado).
[00034] Uma modalidade preferida da presente invenção é o dito anticorpo ou derivado de anticorpo, onde uma ou mais mudanças de aminoácidos são introduzidas em qualquer uma das posições selecionadas no grupo das posições 4, 46, 65, 67, 70 e 83 do domínio VL, e/ou em uma ou mais das posições selecionadas no grupo das posições 11, 16, 28, 43, 48, 68, 70, 71, 72, 73, 76, 77, 79, 93 e 112 do domínio VH. Mais preferivelmente, pelo menos uma das conversões leva a um aminoácido presente em SEQ ID NO: 3 para VL e/ou SEQ ID NO: 4 para VH, e ainda mais preferivelmente, no máximo 13 conversões no total estão presentes.
[00035] Mais preferivelmente, a dito anticorpo ou derivado de anticorpo compreende um domínio VL da sequência SEQ ID NO: 1 e/ou um domínio VH da sequência ou derivado da sequência SEQ ID NO: 2, ou um domínio VL da sequência SEQ ID NO: 11 e um domínio VH da sequência SEQ ID NO: 4. Caso o domínio VH do anticorpo da presente invenção compreenda um domínio VL de SEQ ID NO: 1, em uma modalidade preferida, a sequência VH é derivada de SEQ ID NO: 2, de tal modo que a fenilalanina na posição 68 seja mudada para alanina, leucina, isoleucina ou valina. Mudanças adicionais dentro de VH são opcionais. Os anticorpos scFv deste tipo estão fornecidos em SEQ ID NO: 31, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36 e SEQ ID NO: 37.
[00036] Em outra modalidade preferida da presente invenção, o dito anticorpo ou derivado de anticorpo é derivado do anticorpo com a sequência VL de SEQ ID NO: 1 e a sequência VH de SEQ ID NO: 2 e compreende pelo menos um resíduo de aminoácido que é convertido, em pelo menos uma das CDRs, em um resíduo presente na CDR correspondente da sequência VL de SEQ ID NO: 5 e/ou da sequência VH de SEQ ID NO: 6 ou SEQ ID NO: 25. Em uma modalidade mais preferida da presente invenção, no dito anticorpo ou derivado de anticorpo pelo menos uma das CDRs do grupo CDR2 de VL, CDR3 de VL, CDR2 de VH ou CDR3 de VH é convertida na CDR correspondente da sequência VL de SEQ ID NO: 5 e/ou da sequência VH de SEQ ID NO: 25 ou SEQ ID NO: 6.
[00037] Mais preferivelmente, o dito anticorpo ou derivado de anticorpo compreende as seguintes combinações de sequências VL/VH: SEQ ID NO: 7 de VL/SEQ ID NO: 2 de VH, SEQ ID NO: 8 de VL/SEQ ID NO: 2 de VH, SEQ ID NO: 1 de VL/SEQ ID NO: 9 de VH, SEQ ID NO: 1 de VL/SEQ ID NO: 25 de VH, SEQ ID NO: 1 de VL/SEQ ID NO: 28 de VH, SEQ ID NO: 1 de VL/SEQ ID NO: 29 de VH, SEQ ID NO: 26 de VL/SEQ ID NO: 30 de VH, SEQ ID NO: 27 de VL/SEQ ID NO: 30 de VH.
[00038] Em outra modalidade preferida, o anticorpo ou derivado de anticorpo da presente invenção tem especificidade para TNFα humano. De preferência, a ligação do antígeno se distingue por uma Kd «100 nM ou menos. Mais preferivelmente, é um anticorpo com uma Kd 10 nM ou menos, e mais preferivelmente ainda, é um anticorpo com uma Kd 1 nM ou menos.
[00039] Os derivados de anticorpos de acordo com a presente invenção são, por exemplo, fusões de Fcs, fusões de toxinas, fusões a atividades enzimáticas, diferentes formatos tais como anticorpos, diacorpos, anticorpos lineares, anticorpos de cadeia única, fragmentos de anticorpos biespecíficos, particularmente fragmentos scFv e Fab.
[00040] Outro objeto preferido da presente invenção é um anticorpo scFv cujos domínio VL e VH estão ligados por um ligante, de preferência em um arranjo de sequências VL-ligante-VH. Mais preferivelmente, o dito ligante tem a sequência SEQ ID NO: 10.
[00041] Outro objeto preferido da presente invenção é um anticorpo scFv derivado de SEQ ID NO: 40 (TB-A). Esse anticorpo pode ser obtido por mutagênese, e compreende três ou menos mutações na estrutura, na CDR e/ou nas sequências ligantes. De preferência, o anticorpo tem a sequência SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 22, SEQ ID NO: 23, SEQ ID NO: 24, SEQ ID NO: 31, SEQ ID NO: 32, SEQ ID NO: 33, SEQ ID NO: 34, SEQ ID NO: 35, SEQ ID NO: 36, SEQ ID NO: 37, ou SEQ ID NO: 38.
[00042] Outro objeto preferido da presente invenção é o fragmento Fab que compreende um domínio VL que é fusionado à região constante de uma cadeia kapa de Ig humana, e um domínio VH que é fusionado ao domínio CH1 de IgG humana, com o que dois polipeptídeos de fusão estão ligados por uma ponte dissulfeto entre cadeias.
[00043] Em ainda outro aspecto, o anticorpo ou derivado de anticorpo, por exemplo, o fragmento de anticorpo da presente invenção é marcado ou quimicamente modificado.
[00044] A presente invenção fornece também uma sequência de DNA que codifica qualquer um dos anticorpos ou derivados de anticorpos da presente invenção, bem como um vetor de clonagem ou de expressão que contém a dita sequência de DNA. Além disso, fornece-se uma célula hospedeira apropriada transformada com a dita sequência de DNA, que de preferência é uma célula de E. coli, de levedura ou de mamífero.
[00045] Além disso, fornece-se um método para a produção dos anticorpos ou derivados de anticorpos da presente invenção, compreendendo cultivar a célula hospedeira transformada com o DNA que codifica qualquer um dos ditos anticorpos ou derivados de anticorpos, sob condições que permitem a síntese do dito anticorpo ou derivado de anticorpo, e recuperar a dita molécula a partir da dita cultura. De preferência, o dito método fornece um anticorpo scFv ou fragmento Fab purificado a partir de E. coli.
[00046] Outro aspecto da presente invenção é o uso dos anticorpos ou derivados de anticorpos fornecidos pela presente invenção como uma ferramenta diagnóstica para diagnósticos in vitro, e/ou como um produto farmacêutico. Este uso é particularmente preferido no contexto de qualquer condição relacionada ao TNFα.
[00047] A presente invenção engloba também uma composição que compreende um anticorpo ou derivado de anticorpo da presente invenção em combinação com um veículo, diluente ou excipiente farmaceuticamente aceitável, a dita composição a ser usada como um medicamento para o tratamento de doenças associadas ao TNFα.
[00048] Em um outro aspecto, a presente invenção fornece uma preparação combinada que compreende um anticorpo ou derivado de anticorpo da presente invenção, de preferência com um segundo composto que não é um anticorpo ou derivado de anticorpo específico para TNFα.
[00049] Em ainda outro aspecto da presente invenção, o vetor que compreende a sequência de DNA que codifica um anticorpo scFv da presente invenção é usado para terapia gênica.
[00050] O tratamento de doenças associadas ao TNFα é realizado bloqueando TNFα devido a uma forte interação de TNFα com o anticorpo ou derivado de anticorpo. De preferência, visa-se um tratamento de doenças autoimunes, condições agudas ou crônicas de inflamação, doenças relacionadas a câncer, dor, distúrbios neurológicos e neurodegenerativos, doenças infecciosas e doenças cardiovasculares.
[00051] A invenção será mais bem entendida e os objetos diferentes daqueles enunciados acima tornar-se-ão evidentes ao se considerar a sua descrição detalhada que se segue. Esta descrição faz referência aos desenhos anexos, onde:
[00052] A Figura 1 ilustra um esquema dos anticorpos scFv com as sequências de TB-A e TB-B delimitando a faixa das variações mais frequentes. Os asteriscos designam as posições nas quais mudanças de aminoácidos na estrutura dos anticorpos da presente invenção são toleradas. Os aminoácidos indicados embaixo das CDRs (estando as CDRs enfatizadas com um fundo cinza) podem ser usados nas respectivas CDRs;
[00053] A Figura 2 ilustra um esquema exemplificativo para a expressão de um fragmento Fab;
[00054] A Figura 3 ilustra o rendimento da produção de scFv's quando expressados em E. coli. (A) Eletroforese em SDS-gel de poliacrilamida de proteínas expressadas. (B) Filtração analítica em gel de TB-A e TB-wt, ilustrando a excelente solubilidade de TB-A;
[00055] A Figura 4 ilustra uma comparação da afinidade de diferentes anticorpos scFv por TNFα, determinada por ELISA;
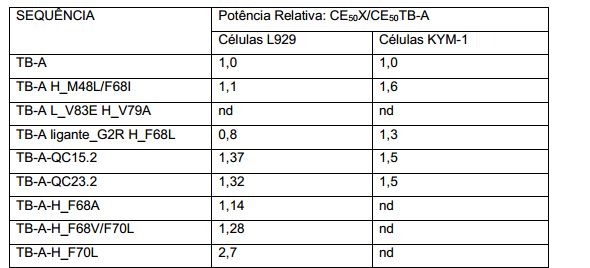
[00056] A Figura 5 ilustra a inibição da citotoxicidade induzida por TNFα humano em fibroblastos L929 do camundongo. (A) Inibição dependente da concentração de TB-A em comparação com TB-wt e infliximab com valores de CI50. (B) Comparação de derivados de TB-A para bloquear a citotoxicidade induzida por TNFα. (C) Comparação de formatos scFv e Fab de TB-A.
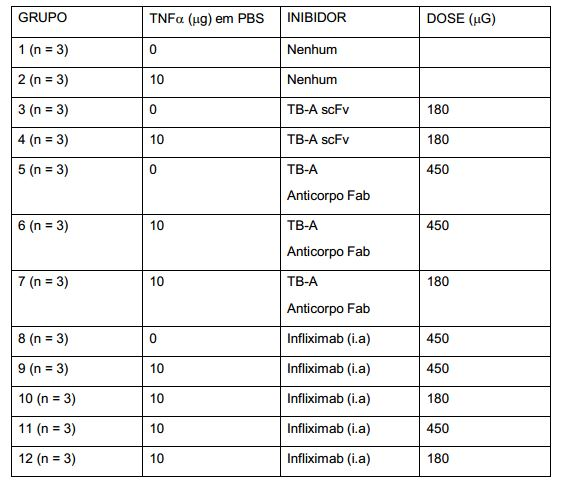
[00057] A Figura 6 ilustra o efeito do tratamento com anticorpo do inchaço das articulações induzido por TNFα humano no rato (Experimento: 5.3, Experimento 1).
[00058] A Figura 7 ilustra o esquema de pontuações para pontuação de inflamação histopatológica.
[00059] A Figura 8 ilustra o efeito do tratamento com anticorpo sobre a inflamação de articulações induzida por TNFα humano no rato Experimento 5.3, Experimento 1).
[00060] A Figura 9 ilustra o efeito do tratamento com anticorpo sobre o inchaço de articulações induzido por TNFα humano no rato Experimento 5.3, Experimento 2).
[00061] A Figura 10 ilustra o efeito do tratamento com anticorpo sobre a inflamação de articulações induzida por TNFα humano no rato Experimento 5.3, Experimento 2).
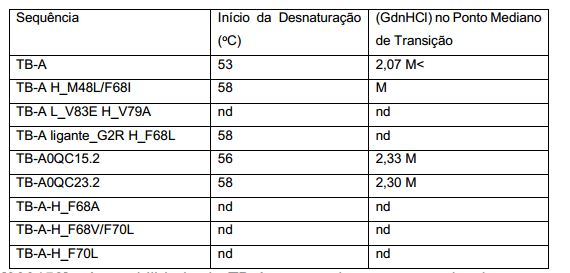
[00062] A Figura 11 ilustra a estabilidade de TB-A em diferentes fluidos corporais. MODOS PARA CONDUZIR A INVENÇÃO
[00063] Descobriu-se que os anticorpos ou derivados de anticorpos que compreendem as estruturas identificadas na assim denominada triagem com "controle de qualidade" (documento no WO 0148017) distinguem-se por uma estabilidade e/ou solubilidade geralmente alta, e assim sendo, podem ser úteis também no contexto de aplicações extracelulares tais como a neutralização de TNFα. A presente invenção fornece anticorpos ou derivados de anticorpos distinguidos por maior estabilidade e solubilidade, que reconhecem e se ligam especificamente ao TNFα, e assim sendo, são apropriados para bloquear a função de TNFα in vivo. Os ditos anticorpos ou derivados de anticorpos distinguem-se por uma estrutura especial derivada a partir de triagem com "controle de qualidade" para anticorpos com estruturas particularmente estáveis e solúveis independentemente do seu sítio de ligação a antígeno que foi descrito no documento no EP 1479694. Caso as estruturas usadas na triagem sejam estruturas de anticorpos humanos, elas podem ser consideradas como estruturas não- imunogênicas para aplicações humanas. As CDRs dos anticorpos da presente invenção são idênticas ou derivadas das CDRs do anticorpo monoclonal murino Di62 (Doring et al., 1994) que se liga especificamente ao TNFα humano com uma alta afinidade (Kd = 0,4 nM) e pode bloquear a ligação de TNFα ao seu receptor. Além disso, Di62 inibe a citotoxicidade induzido por TNFα humano em células L929 do camundongo. A etapa óbvia de enxertar CDRs do anticorpo do camundongo na estrutura do aceptor humano aparentemente mais apropriado com propriedades indefinidas de ligação de antígeno, a dita estrutura tendo a sequência de VL SEQ ID NO: 5 e a sequência de VH SEQ ID NO: 6, as ditas sequências sendo ligadas por um ligante (GGGGS)4 (SEQ ID NO: 10), resultou em um anticorpo scFv da sequência DIVLTQSPSSLSASVGDRVTLTCTASQSVSNDVVWYQQRPGKAPKR LIYSAFNRYTGVPSRFSGSGSGTEFTLTISSLQPEDVAVYYCQQDYN SPRTFGQGTKLEVRRGGGGSGGGGSGGGGSGGGGSQVQLVQSG AEVKKPGASVKVSCTASGYSFTHYGMNWVRQAPGQGLEWMGWINT YTGEPTYADKFKDRVTLTRDTSIGTVYMELTSLTSDDTAVYYCARER GDAMDYWGQGTLVTVSS (SEQ ID NO: 3 + SEQ ID NO: 10 + SEQ ID NO: 4) o dito anticorpo sendo denominado TB-B. TB-B deu bons rendimentos na expressão de proteínas (Figura 3a), mas foi incapaz de se ligar especificamente ao TNFα (Figura 4a).
[00064] Assim sendo, para obter um anticorpo ou derivado de anticorpo que é (i) suficientemente específico para se ligar ao TNFα, (ii) suficientemente solúvel para permitir a produção e purificação eficientes e para bloquear TNFα in vivo, (iii) suficientemente estável para ser útil como um produto farmacêutico sem sofrer uma degradação rápida, e (iv) suficientemente não-imunogênico, buscou-se um compromisso entre a melhor solubilidade e as melhores características de ligação a antígenos, variando a estrutura e as CDRs. A presente invenção fornece uma sequência para VL e VH que é otimizada para combinação dos critérios (i-iv). Um anticorpo scFv que compreende o dito VL (SEQ ID NO: 1 ligada por um ligante (GGGGS)4 ao dito VH (SEQ ID NO: 2) é denominado TB-A. A sequência de TB-A é fornecida por SEQ ID NO: 40. Este anticorpo é ainda razoavelmente estável e solúvel para dar rendimentos satisfatórios quando expressado e purificado a partir de E. coli (Figura 3A), e ele não se agrega (Figura 3B). Suas características de ligação ao TNFα são excelentes, com uma Kd 0,8 nM.
[00065] A presente invenção descreve também sequências de VL e VH derivadas da sequência presente em TB-A de várias maneiras. Primeiramente, mutações pontuais em até cinco posições na estrutura de VL e/ou em até nove posições na estrutura de VH demonstraram ser aceitáveis, especialmente as mutações pontuais que tornam as estruturas mais semelhantes a TB-B, isto é, mais semelhante a SEQ ID NO: 3 para VL ou SEQ ID NO: 4 para VH. Um anticorpo scFv que compreende um domínio VL com a sequência SEQ ID NO: 11 e um domínio VH com a sequência SEQ ID NO: 4, ligadas pelo ligante (GGGGS)4, é denominado TB-B R46L porque ele difere de TB-B apenas na posição 46 de VL. Em contraste com TB-B, este anticorpo ainda tem boas propriedades de ligação ao TNFα (Kd « 100 nM). Isto sugere que o número de mudanças em TB-B R46L em relação a TB-A representa aproximadamente o limite superior para mudanças na estrutura do domínio variável.
[00066] Em uma modalidade preferida da presente invenção, apenas mutações pontuais singulares ou duplas são introduzidas nas estruturas de VL e/ou VH de TB-A. Os resíduos preferidos das estruturas para mutações são nas posições 4, 46, 65, 67, 70 e/ou 83 para VL, e nas posições 11, 16, 28, 43, 48, 68, 70, 71, 72, 73, 76, 77, 79, 93 e/ou 112 para VH. As posições são numeradas de acordo com a numeração nas listagens de sequências. As substituições de aminoácidos são, de preferência, "conservativas", ou de tal modo que os aminoácidos substituintes sejam mais similares ou de preferência mesmo idênticos aos aminoácidos correspondentes presentes na sequência de TB-B. Por exemplo, A76 de VH em TB-A pode ser mudado para I76 como ele está presente em TB-B, mas ele pode ser trocado também por outro aminoácido com uma cadeia lateral similar, isto é, uma cadeia lateral apolar, tal como V ou L. Este é um exemplo de uma substituição "conservativa" de aminoácido. As famílias de resíduos de aminoácidos que têm cadeias laterais similares apropriadas para substituições "conservativas", como aqui utilizadas, foram definidas nessas técnicas, incluindo cadeias laterais básicas (K, R, H), cadeias laterais ácidas (D, E), cadeias laterais polares sem carga (Q, N, S, T, Y, C), cadeias laterais apolares (G, A, V, L, I, P, F, M, W), cadeias laterais ramificadas em beta (T, V, I) e cadeias laterais aromáticas (Y, F, W, H). Uma mudança conservativa preferida é aquela de VL na posição 83, pelo fato de que V é mudada para F (SEQ ID NO 26) ou para A (SEQ ID NO: 27). Entretanto, em SEQ ID NO: 32, uma mudança não-conservativa em VL é V83E, que é combinada com uma mudança em CDR1, isto é, N31D, e em VH com V79A. Outra variante extraordinária de TB-A é aquela de SEQ ID NO: 33, com uma troca conservativa de F68L em VH ligada a VL por um ligante que porta um R na posição 2, substituindo G.
[00067] As trocas de aminoácidos singulares mais preferidas são R65S ou Y67L em VL e K43Q ou F68 por V, L ou A em VH. As mudanças duplas muito mais preferidas são F70L/L72R ou A76I/S77G em VH. Os anticorpos scFv que compreendem sequências de TB-A com as ditas alterações apresentam inibição da toxicidade induzida por TNFα em células L929. Os resultados de algumas delas estão indicados na Figura 5B. Suas sequências são as seguintes: SEQ ID NO: 18 = TB-A H_K43Q (TB-A H43) SEQ ID NO: 19 = TB-A H_F68V (TB-A H68) SEQ ID NO: 20 = TB-A H_F70L/L72R (TB-A H70/72) SEQ ID NO: 21 = TB-A H_A76I/S77G (TB-A H 76/77) SEQ ID NO: 22 = TB-A L_46R (TB-A L46) SEQ ID NO: 23 = TB-A L_R65S (TB-A L65) SEQ ID NO: 24 = TB-A L_Y67S (TB-A L67)
[00068] Em uma modalidade preferida, qualquer um dos domínios VH supramencionados pode ser combinado com qualquer um dos domínios VL supramencionados.
[00069] Em outra modalidade preferida da presente invenção, os domínios VL e VH de TB-A e TB-B são embaralhados, de tal modo que o domínio VL de TB-A (SEQ ID NO: 1) seja combinado com o domínio VH de TB-B (SEQ ID NO: 4), ou o domínio VL de TB-B (SEQ ID NO: 4) é combinado com o domínio VH de TB-A (SEQ ID NO: 2). Em uma modalidade muito mais preferida, as versões embaralhadas obtidas em um scFv estão ligadas com o ligante (GGGGS)4 da sequência SEQ ID NO: 10, resultando nos anticorpos scFv TB-AB (SEQ ID NO: 12) ou TB- BA (SEQ ID NO: 13), respectivamente. O dito ligante (GGGGS)4 pode ter uma troca de aminoácidos de uma glicina por um aminoácido mais hidrofílico, isto é, polar ou mesmo carregado, que pode tornar o anticorpo mais solúvel. Dentre estas variações, aquela com a sequência GRGGS-(GGGGS)3 (SEQ ID NO: 39) é preferida.
[00070] Está também dentro do âmbito da presente invenção combinar os domínios VL ou VH de sequências semelhantes a TB-B com os domínios VH ou VL de sequências semelhantes a TB-A, onde semelhante a TB-B/TB-A significa que as sequências são mais iguais a uma do que à outra.
[00071] Em ainda outra modalidade preferida da presente invenção, um ou mais aminoácidos são mudados nas regiões CDR das sequências de VL e/ou VH de TB-A para equivaler aos aminoácidos correspondentes presentes nas sequências selecionadas SEQ ID NO: 5 de VL e/ou SEQ ID NO: 6 ou SEQ ID NO: 25 de VH. São mais preferidas as mudanças em uma das CDRs de VL (CDR2 de VL ou CDR3 de VL) e/ou das CDRs de VH (CDR2 ou CDR3), sendo que as mudanças mais preferidas levam às sequências de VL SEQ ID NO: 7 ou SEQ ID NO: 8 e/ou às sequências de VH SEQ ID NO: 25 ou SEQ ID NO: 9, respectivamente.
[00072] Em outra modalidade preferida da presente invenção, as sequências de VL SEQ ID NO: 26 ou SEQ ID NO: 27 são combinadas com a sequência de VH SEQ ID NO: 30. Em ainda outra modalidade preferida da presente invenção, a sequência de VL SEQ ID NO: 1 é combinada com as sequências de VH SEQ ID NO: 28 ou SEQ ID NO: 29.
[00073] Geralmente, qualquer uma das sequências de VL descritas pode ser combinada com qualquer uma das sequências de VH descritas.
[00074] Os objetos da presente invenção são anticorpos e fragmentos de anticorpos, particularmente polipeptídeos VL ou VH, anticorpos de cadeia única (scFv) ou fragmentos Fab. No caso de anticorpos scFv, um domínio VL selecionado pode ser ligado a um domínio VH selecionado na orientação por um ligante flexível. Um ligante apropriado do estado da técnica consiste em sequências de aminoácidos GGGGS repetidas ou suas variantes. Em uma modalidade preferida da presente invenção, usa-se um ligante (GGGGS)4 com a sequência SEQ ID NO: 10 ou seu derivado SEQ ID NO: 39, mas as variantes com 1 a 3 repetições também são possíveis (Holliger et al., Proc. Natl. Acad. Sci. USA 90:6444-6448 (1993)). Outros ligantes que podem ser usados na presente invenção estão descritos por Alfthan et al., Protein Eng. 8:725-731 (2001); Choi et al. Eur. J. Immunol. 31:94106 (2001); Hu et al., Cancer Res. 56:3055-3061 (1996); Kipriyanov et al., J. Mol. Biol. 293:41-56 (1999); e Roovers et al., Cancer Immunol. Immunother. 50:51-59 (2001). O arranjo pode ser VL-ligante-VH ou VH- ligante-VL, sendo preferida a primeira orientação.
[00075] No caso de fragmentos Fab, os domínios variáveis com cadeia leve VL selecionados são fusionados à região constante de uma cadeia kapa de Ig humana, enquanto que os domínios variáveis com cadeia pesada VH apropriados são fusionados ao primeiro domínio constante (N-terminal) CH1 de uma IgG humana. Em uma modalidade exemplificativa da presente invenção, o domínio CK humano tem a sequência SEQ ID NO: 14 e o domínio CH1 usado para construir os fragmentos Fab tem a sequência SEQ ID NO: 15. A Figura 2 ilustra um exemplo de um fragmento Fab no qual os domínios VL e VH de TB-A são usados de tal modo que o domínio VL esteja ligado diretamente ao domínio constante kapa humano, resultando na sequência DIVMTQSPSSLSASVGDRVTLTCTASQSVSNDVVWYQQRPGKAPKL LIYSAFNRYTGVPSRFSGRGYGTDFTLTISSLQPEDVAVYYCQQDYN SPRTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYP REAKVQWVDNALQSGNSQESVTEEQDSKDSTYSLSSTLTLSKADYE KHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID NO: 1 + SEQ ID NO: 14) e o domínio VH está fusionado ao primeiro domínio constante (CH1), resultando na sequência QVQLVQSGAEVKKPGASVKVSCTASGYTFTHYGMNWVRQAAPGKG LEWMGWINTYTGEPTYADKFKDRFTFSLETSASTVYMELTSLTSDDT AVYYCARERGDAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSG GTAALGCLVKDYFSEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSS VVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCTS (SEQ ID NO: 2 + SEQ ID NO: 15).
[00076] No C-terminal, uma ponte dissulfeto entre cadeias é formada entre os dois domínios constantes.
[00077] Os anticorpos ou derivados de anticorpos da presente invenção podem ter afinidades por TNFα humano com constantes de dissociação em uma faixa entre 0,8-10.000 nM. Em uma modalidade preferida da presente invenção, a Kd é < 10 nM. A afinidade de um anticorpo por um antígeno pode ser determinada experimentalmente usando um método apropriado (Berzofsky et al., "Antibody-Antigen Interactions", em "Fundamental Immunology", Paul, W.E., editor, Raven Press, New York, NY (1992); Ruby, J., "Immunology", W.H. Freeman and Company, New York, NY), e os métodos lá descritos.
[00078] Em um aspecto da presente invenção, os anticorpos ou derivados de anticorpos, especialmente os fragmentos scFv ou Fab, são marcados. A marcação detectável de um anticorpo ou derivado de anticorpo específico de TNFα pode ser realizada ligando-o a uma enzima para uso em um imunoensaio de enzima (EIA) ou ensaio imunoabsorvente ligado à enzima (ELISA), que são métodos bem conhecidos pelos versados nessas técnicas (por exemplo, "Current Protocols in Immunology", Coligan et al., editores, John Wiley & Sons, 2005).
[00079] Marcando de forma radioativa os anticorpos ou derivados de anticorpos específicos de TNFα, é possível detectar TNFα através do uso de radioimunoensaio (RIA) (vide, por exemplo, Work et al., "Laboratory Techniques and Biochemistry in Molecular Biology", North Holland Publishing Company, NY (1978). O radioisótopo pode ser detectado pelo uso de um contador gama ou um contador de cintilação ou por autorradiografia. Os isótopos particularmente úteis são 3H, 131I, 35S, 14C, e de preferência, 125I.
[00080] Os anticorpos ou derivados de anticorpos da presente invenção podem ser marcados também com compostos fluorescentes de marcação, tais como fluoresceína, isotiocianato, rodamina, ficoeritrina, ficocianina, aloficocianina, o-ftaldeído e fluorescamina, ou com compostos quimioluminescentes tais como luminol, éster teromático de acridínio, sal de imidazol-acridínio e éster oxalato.
[00081] Os protocolos de marcação e detecção são bem conhecidos pelos versados nessas técnicas. Por exemplo, eles estão disponíveis em "Using Antibodies: A Laboratory Manual: Portable Protocol No. 1 (Harlow, E. e Lane, D., 1998).
[00082] Os anticorpos ou derivados de anticorpos marcados da presente invenção são úteis para propósitos diagnósticos, particularmente a detecção de TNFα em uma amostra biológica removida de um paciente. Qualquer amostra que contém TNFα pode ser usada, como por exemplo, fluidos biológicos tais como sangue, soro, linfa, urina, exsudato inflamatório, líquido cerebroespinhal, líquido amniótico, extrato ou homogeneizado tecidual, e similares, ou espécimes histológicos para detecção in situ.
[00083] O termo "formulação farmacêutica" refere-se a preparações que estão em uma forma tal que permite a atividade biológica do anticorpo ou derivado de anticorpo seja inequivocamente eficaz, e que não contêm quaisquer componentes adicionais que são tóxicos para os indivíduos aos quais a formulação seria administrada. Excipientes (veículos, diluentes) "farmaceuticamente aceitáveis" são aqueles que podem ser administrados razoavelmente a um indivíduo mamífero para fornecer uma dose eficaz do ingrediente ativo a ser empregado.
[00084] Uma formulação "estável" é uma na qual o anticorpo ou derivado de anticorpo dentro dela retém essencialmente sua estabilidade física e/ou sua estabilidade química e/ou atividade biológica depois da estocagem. Várias técnicas analíticas para medir a estabilidade de proteínas estão disponíveis nessas técnicas e estão revisadas em "Peptide and Protein Drug Delivery", 247-301, Vincent Lee, editor, Marcel Dekker, Inc., New York, NY, editora (1991); e Jones, A., Adv. Drug Delivery Rev. 10:29-90 (1993), por exemplo. A estabilidade pode ser medida em uma temperatura selecionada por um período de tempo selecionado. De preferência, a formulação é estável à temperatura ambiente (cerca de 30 oC) ou a 40 oC por pelo menos 1 mês e/ou estável a cerca de 2-8 oC por pelo menos 1 ano ou pelo menos 2 anos. Além disso, a formulação é, de preferência, estável após congelamento (até, por exemplo, -70 oC) e descongelamento da formulação.
[00085] Um anticorpo ou derivado de anticorpo "retém sua estabilidade física" em uma formulação farmacêutica, caso ele não apresente quaisquer sinais de agregação, precipitação e/ou desnaturação após exame visual de cor e/ou limpidez, ou como medida por dispersão de luz UV ou por cromatografia por exclusão de tamanho.
[00086] Um anticorpo ou derivado de anticorpo "retém sua estabilidade química" em uma formulação farmacêutica, caso a estabilidade química em um dado tempo seja tal que a proteína seja considerada como ainda retendo sua atividade biológica, como definido abaixo. A estabilidade química pode ser avaliada detectando e quantificando formas quimicamente alteradas da proteína. A alteração química pode envolver modificação de tamanho (por exemplo, recorte) que pode ser avaliada usando SDS-PAGE e/ou espectrometria de massas por ionização/tempo de vôo e dessorção a laser auxiliada com matriz (MS MALDI/TOF), por exemplo. Outros tipos de alterações químicas incluem alteração de carga elétrica (por exemplo, ocorrendo como resultado de desamidação) que pode ser avaliada por cromatografia por troca iônica, por exemplo.
[00087] Um anticorpo ou derivado de anticorpo "retém sua atividade biológica" em uma formulação farmacêutica, caso a atividade biológica do anticorpo em um dado tempo fique dentro de cerca de 10% (dentro dos erros do ensaio) da atividade biológica apresentada na hora em que a formulação farmacêutica foi preparada, determinada em m ensaio de ligação de antígeno, por exemplo. Outros ensaios de "atividade biológica" para anticorpos estão elaborados abaixo neste relatório descritivo.
[00088] O termo "isotônica" significa que a formulação de interesse tem essencialmente a mesma pressão osmótica que o sangue humano. As formulações isotônicas devem ter geralmente uma pressão osmótica entre cerca de 250 e 350 mOsm. A isotonicidade pode ser medida usando um osmômetro do tipo pressão de vapor ou congelamento em gelo, por exemplo.
[00089] Um "poliol" é uma substância com múltiplos grupos hidroxila, e inclui açúcares (açúcares redutores e não-redutores), álcoois de açúcares e ácidos de açúcares. Os polióis preferidos neste caso têm um peso molecular menor do que cerca de 600 kD (por exemplo, na faixa entre cerca de 120 e cerca de 400 kD). Um "açúcar redutor" é um que contém um grupo hemiacetal que pode reduzir íons metálicos ou reagir de forma covalente com lisina ou outros grupos amínicos em proteínas, e um "açúcar não-redutor" é um que não tem estas propriedades de um açúcar redutor. Os exemplos de açúcares redutores são frutose, manose, maltose, lactose, arabinose, xilose, ribose, ramnose, galactose e glicose. Os açúcares não-redutores incluem sacarose, trealose, sorbose, melezitose e rafinose. Manitol, xilitol, eritritol, treitol, sorbitol e glicerina são exemplos de álcoois de açúcares. Quanto aos ácidos de açúcares, eles incluem L-gliconato e seus sais metálicos. Quando for desejado que a formulação seja estável após congelamento/descongelamento, o poliol é, de preferência, um que não cristalize nas temperaturas de congelamento (por exemplo, -20 oC), de tal modo que ele desestabilize o anticorpo na formulação. Os açúcares não-redutores tais como sacarose e trealose são os polióis preferidos neste caso, sendo que a trealose é preferida em detrimento de sacarose por causa da estabilidade excelente em solução da trealose.
[00090] Como aqui utilizado, o termo "tampão" refere-se a uma solução tamponada que resiste a mudanças no pH pela ação dos seus componentes conjugados ácidos/básicos. O tampão desta invenção tem um pH na faixa entre cerca de 4,5 e cerca de 6,0; de preferência, entre cerca de 4,8 e cerca de 5,5; e mais preferivelmente, tem um pH de cerca de 5,0. Os exemplos de tampões que controlarão o pH nesta faixa incluem acetato (por exemplo, acetato de sódio), succinato (tal como succinato de sódio), gliconato, histidina, citrato e outros tampões de ácidos orgânicos. Quando uma formulação estável após congelamento/descongelamento for desejada, o tampão não é de preferência fosfato.
[00091] Em um sentido farmacológico, no contexto da presente invenção, uma "quantidade terapeuticamente eficaz" de um anticorpo ou derivado de anticorpo refere-se a uma quantidade eficaz na prevenção ou tratamento de um distúrbio para cujo tratamento o anticorpo ou derivado de anticorpo é eficaz. Uma "doença/distúrbio é qualquer condição que se beneficiará do tratamento com o anticorpo ou derivado de anticorpo. Isto inclui distúrbios ou doenças crônicas e agudas, incluindo aquelas condições patológicas que predispõem o mamífero ao distúrbio em questão.
[00092] Um "conservante" é um composto que pode ser incluído na formulação para reduzir essencialmente a ação bacteriana nela, possibilitando assim a produção de uma formulação para múltiplos usos, por exemplo. Os exemplos de conservantes potenciais incluem cloreto de octadecil-dimetil-benzil-amônio, cloreto de hexametônio, cloreto de benzalcônio (uma mistura de cloretos de alquil-benzil-dimetil-amônio na qual os grupos alquila são compostos de cadeia longa), e cloreto de benzetônio. Outros tipos de conservantes incluem álcoois aromáticos, tais como fenol, álcool butílico e benzílico, alquil-parabens tais como metil- ou propil-parabeno, catecol, resorcinol, ciclo-hexanol, 3-pentanol, e m-cresol. O conservante mais preferido neste caso é álcool benzílico.
[00093] A presente invenção fornece também composições farmacêuticas que compreendem um ou mais anticorpos ou compostos derivados de anticorpos, junto com pelo menos um veículo ou excipiente fisiologicamente aceitável. As composições farmacêuticas podem compreender, por exemplo, uma ou mais entre água, tampões (por exemplo, solução salina tamponada neutra ou solução salina tamponada com fosfato), etanol, óleo mineral, óleo vegetal, sulfóxido de dimetila, carboidratos (por exemplo, glicose, manose, sacarose ou dextranos), manitol, proteínas, adjuvantes, polipeptídeos ou aminoácidos tais com glicina, antioxidantes agentes quelantes tais como EDTA ou glutationa e/ou conservantes. Como assinalado acima, outros ingredientes ativos podem, porém não necessariamente, ser incluídos nas composições farmacêuticas aqui fornecidas.
[00094] Um veículo é uma substância que pode ser associada com um anticorpo ou derivado de anticorpo antes da administração a um paciente, frequentemente com o propósito de controlar a estabilidade ou biodisponibilidade do composto. Os veículos para uso em tais formulações são geralmente biocompatíveis, e podem ser também biodegradáveis. Os veículos incluem, por exemplo, moléculas monovalentes ou multivalentes tais como albumina sérica (por exemplo, humana ou bovina), albumina do ovo, peptídeos, polilisina, e polissacarídeos tais como aminodextrano e poliamidoaminas. Os veículos incluem também materiais de suporte sólidos tais como pérolas e micropartículas que compreendem, por exemplo, polilactato, poliglicolato, poli(lactídeo-co-glicolídeo), poliacrilato, látex, amido, celulose ou dextrano. Um veículo pode portar os compostos de uma série de maneiras, incluindo ligação covalente (diretamente ou por intermédio de um grupo ligante), interação não-covalente, ou mistura.
[00095] As composições farmacêuticas podem ser formuladas para qualquer maneira de administração, incluindo, por exemplo, administração tópica, oral, nasal, retal ou parenteral. Em certas modalidades, as composições em uma forma apropriada para uso oral são preferidas. Essas formas incluem, por exemplo, pílulas, comprimidos, trociscos, pastilhas, suspensões aquosas ou oleosas, pós ou grânulos dispersáveis, emulsões, cápsulas de gelatina duras ou moles, ou xaropes ou elixires. Em ainda outras modalidades, as composições aqui fornecidas podem ser formuladas como um liofilizado. O termo "parenteral", como aqui utilizado, inclui injeção subcutânea, intradérmica, intravascular (por exemplo, intravenosa), intramuscular, espinhal, intracraniana, intratecal e intraperitoneal, bem como qualquer injeção similar ou técnica de infusão.
[00096] As composições pretendidas para uso oral podem ser preparadas de acordo com qualquer método conhecido para a fabricação de composições farmacêuticas e podem conter um ou mais agentes, tais como agentes edulcorantes, sabores, agente colorante, e agentes conservantes, para produzir preparações atraentes e palatáveis. Os comprimidos contêm o ingrediente ativo em mistura com excipientes fisiologicamente aceitáveis apropriados para a fabricação de comprimidos. Tais excipientes incluem, por exemplo, diluentes inertes (por exemplo, carbonato de cálcio, carbonato de sódio, lactose, fosfato de cálcio ou fosfato de sódio), agentes granuladores e desintegradores (por exemplo, amido de milho ou ácido algínico), agentes aglutinantes (por exemplo, amido, gelatina ou acácia) e agentes lubrificantes (por exemplo, estearato de magnésio, ácido esteárico ou talco). Os comprimidos podem ser não-revestidos ou eles podem ser revestidos por técnicas conhecidas para retardar a desintegração e absorção no trato gastrointestinal, e desta forma, proporcionar uma ação prolongada durante um período mais longo. Por exemplo, um material retardador, tais como monoestearato de glicerila ou diestearato de glicerila, podem ser empregados.
[00097] As formulações para uso oral podem ser apresentadas também com cápsulas de gelatina duras, onde o ingrediente ativo é misturado com um diluente sólido inerte (por exemplo, carbonato de cálcio, fosfato de cálcio ou caulim), ou como cápsulas de gelatina moles, onde o ingrediente ativo é misturado com água ou um meio oleoso (por exemplo, óleo de amendoim, parafina líquida ou óleo de oliva). As suspensões aquosas contêm o anticorpo ou derivado de anticorpo em mistura com excipientes apropriados para a fabricação de suspensões aquosas. Tais excipientes incluem auxiliares de suspensão (por exemplo, carbóxi-metil-celulose sódica, metil-celulose, hidróxi-propil- metil-celulose, alginato de sódio, poli(vinil-pirrolidona), goma de tragacanto, e goma de acácia); e agentes dispersantes ou umectantes (por exemplo, fosfatídeos de ocorrência natural tais como lecitina, produtos da condensação de um óxido de alquileno com ácidos graxos, tais como estearato de polioxietileno, produtos da condensação de óxido de etileno com álcoois alifáticos de cadeia longa, tais como heptadecaetilenóxi-cetanol, produtos da condensação de óxido de etileno com ésteres parciais derivados de ácidos graxos e hexitol, tais como monooleato de sorbitol com polioxietileno, ou produtos da condensação de óxido de etileno com ésteres parciais derivados de ácidos graxos e anidridos de hexitol tais como monooleato de sorbitano com polietileno). As suspensões aquosas podem compreender também um ou mais conservantes, como por exemplo, p-hidróxi-benzoato de etila ou n-propila, um ou mais agentes adoçantes um ou mais sabores, e um ou mais agentes edulcorantes tais como sacarose ou sacarina. Os xaropes e elixires podem ser formulados com agentes adoçantes, tais como glicerol, propilenoglicol, sorbitol ou sacarose. Tais formulações podem compreender também um ou mais demulcentes, conservantes, aromatizantes e/ou colorantes.
[00098] As suspensões oleosas podem ser formuladas colocando os ingredientes ativos em suspensão em um óleo vegetal (por exemplo, óleo de amendoim, óleo de oliva, óleo de gergelim ou óleo de coco), ou em um óleo mineral tal como parafina líquida. As suspensões oleosas podem conter um agente espessante, tal como cera de abelha, parafina dura ou álcool cetílico. Agentes adoçantes, tais como aqueles enunciados acima, e/ou aromatizantes podem ser adicionados para produzir preparações orais palatáveis. Tais suspensões podem ser conservadas pela adição de um antioxidante tal como ácido ascórbico.
[00099] Os pós e grânulos dispersáveis apropriados para a preparação de uma suspensão aquosa pela adição de água proporcionam o ingrediente ativo em mistura com um agente dispersante ou umectante, um agente auxiliar de suspensão e um ou mais conservantes. Os agentes dispersantes ou umectantes e os agentes auxiliares de suspensão são exemplificados pelos já mencionados acima. Excipientes adicionais, por exemplo, sabores e colorantes, também podem estar presentes.
[000100] As composições farmacêuticas podem estar também na forma de emulsões de óleo em água. A fase oleosa pode ser um óleo vegetal (por exemplo, óleo de oliva ou óleo de amendoim), um óleo mineral (por exemplo, parafina líquida), ou uma mistura deles. Os agentes emulsificantes apropriados incluem gomas de ocorrência natural (por exemplo, goma de acácia ou goma de tragacanto), fosfatídeos de ocorrência natural (por exemplo, soja, lecitina e ésteres ou ésteres parciais derivados de ácidos graxos e hexitol), anidridos (por exemplo, monooleato de sorbitano), e produtos da condensação de ésteres parciais derivados de ácidos graxos e hexitol com óxido de etileno (por exemplo, monooleato de sorbitano com polioxietileno). Uma emulsão pode compreender também um ou mais adoçantes e/ou sabores.
[000101] A composição farmacêutica pode ser preparada como uma suspensão aquosa ou oleaginosa injetável estéril na qual o modulador, dependendo do veículo e da concentração usada, está em suspensão ou dissolvido no veículo. Tal composição pode ser formulada de acordo com as técnicas conhecidas, usando agentes dispersantes, umectantes apropriados e/ou auxiliares de suspensão tais como aqueles mencionados acima. Dentre os veículos e solventes aceitáveis, que podem ser empregados, estão a água, 1,3-butanodiol, solução de Ringer e solução isotônica de cloreto de sódio. Além disso, óleos fixos estéreis podem ser empregados como um solvente ou meio de suspensão. Com este propósito, qualquer óleo fixo brando pode ser empregado, incluindo monoglicerídeos ou diglicerídeos sintéticos. Além disso, ácidos graxos, tal como ácido oléico, podem ser usados na preparação de composições injetáveis, e adjuvantes tais como anestésicos locais, conservantes e/ou tampões podem ser dissolvidos no veículo.
[000102] As composições farmacêuticas podem ser formuladas como formulações com liberação prolongada (isto é, uma formulação tal como uma cápsula que efetua a liberação lenta do modulador após a administração). Tais formulações podem ser preparadas geralmente usando tecnologia conhecida e administradas, por exemplo, por administração oral, retal ou implante subcutâneo, ou por implante no local-alvo desejado. Os veículos para uso nessas formulações são biocompatíveis, e podem ser também biodegradáveis; de preferência, a formulação proporciona um nível relativamente constante de liberação do modulador. A quantidade de um anticorpo ou derivado de anticorpo contida dentro de uma formulação com liberação prolongada depende, por exemplo, do local do implante, da taxa e da duração esperada da liberação e da natureza da doença/distúrbio a ser tratado ou prevenido.
[000103] Os anticorpos ou derivados de anticorpos aqui fornecidos são administrados geralmente em uma quantidade que atinge uma concentração em um fluido corporal (por exemplo, sangue, plasma, soro, líquido cerebrospinal, líquido sinovial, linfa, líquido intersticial celular, lágrimas ou urina), que é suficiente para se ligar de forma detectável ao TNFα e prevenir ou inibir doenças/distúrbios associados ao TNFα. Uma dose é considerada como sendo eficaz se ela resulta em benefício discernível para o paciente, como aqui descrito. As doses sistêmicas preferidas ficam na faixa entre cerca de 0,1 mg e cerca de 140 mg por quilograma de peso corporal por dia (cerca de 0,5 mg a cerca de 7 g por paciente por dia), sendo as doses orais cerca de 5-20 vezes mais altas do que as doses intravenosas. A quantidade de anticorpo ou derivado de anticorpo, que pode ser combinada com os materiais veículos para produzir uma forma de dosagem unitária, pode variar dependendo do hospedeiro tratado e do modo específico de administração. As formas de dosagem unitárias devem conter geralmente entre cerca de 1 mg e cerca de 500 mg de um ingrediente ativo.
[000104] As composições farmacêuticas podem ser embaladas para tratar condições responsivas a um anticorpo ou derivado de anticorpo direcionado para TNFα. As composições farmacêuticas embaladas podem incluir um recipiente para conter uma quantidade eficaz de pelo menos um anticorpo ou derivado de anticorpo como aqui descrito e instruções (por exemplo, um rótulo) indicando que a composição contida é para ser usada para tratar uma doença/distúrbio responsivo a um anticorpo ou derivado de anticorpo após administração ao paciente.
[000105] Os anticorpos ou derivados de anticorpos da presente invenção podem ser também quimicamente modificados. Os grupos modificadores preferidos são polímeros, por exemplo, um polímero de polialqueno, polialquenileno, ou polioxialquileno com cadeia linear ou ramificada, opcionalmente substituída, ou um polissacarídeo ramificado ou não-ramificado. Tal grupo efetor pode aumentar a meia-vida do anticorpo in vivo. Os exemplos específicos de polímeros sintéticos incluem polietilenoglicol (PEG) com cadeia linear ou ramificada opcionalmente substituída, polipropilenoglicol, poli(álcool vinílico), ou derivados deles. Os polímeros de ocorrência natural específicos incluem lactose, amilose, dextrano, glicogênio ou derivados deles. O tamanho do polímero pode ser variado conforme desejado, mas geralmente deve ficar na faixa de peso molecular entre 500 Da e 50.000 Da. Para aplicação local, quando o anticorpo é projetado para penetrar no tecido, um peso molecular preferido do polímero é de cerca de 5.000 Da. A molécula do polímero pode ser afixada ao anticorpo, particularmente à extremidade do C-terminal da cadeia pesada do fragmento Fab por intermédio de um peptídeo articulador ligado de forma covalente, como descrito no documento no WO 0194585. Quanto à anexação de grupamentos PEG, faz-se referência a "Poly(ethyleneglycol) Chemistry, Biotechnological and Biomedical Applications", 1992, J. Milton Harris (editor), Plenum Press, New York; e "Bioconjugation Protein Coupling Techniques for the Biomedical Sciences", 1998, M. Aslam e A. Dent, Grove Publishers, New York. Preparação da Formulação
[000106] Depois da preparação do anticorpo ou derivado de anticorpo, como descrito acima, a formulação farmacêutica que o compreende é preparada. O anticorpo a ser formulado não foi submetido a uma prévia liofilização, e a formulação de interesse neste caso é uma formulação aquosa. De preferência, o anticorpo ou derivado de anticorpo na formulação é um fragmento de anticorpo, tal como um scFv. A quantidade terapeuticamente eficaz do anticorpo, presente na formulação, é determinada levando em consideração os volumes desejados da dose e o(s) modo(s) de administração, por exemplo. Entre cerca de 0,1 mg/mL e cerca de 50 mg/mL, de preferência entre cerca de 0,5 mg/mL e cerca de 25 mg/mL, e mais preferivelmente, entre cerca de 2 mg/mL e cerca de 10 mg/mL, é uma concentração exemplificativa do anticorpo na formulação.
[000107] É preparada uma formulação aquosa que compreende o anticorpo ou derivado de anticorpo em uma solução com pH tamponado. O tampão desta invenção tem um pH na faixa entre cerca de 4,5 e cerca de 6,0, de preferência entre cerca de 4,8 e cerca de 5,5, e mais preferivelmente, a formulação tem um pH de cerca de 5,0. Os exemplos de tampões que controlarão o pH dentro desta faixa incluem acetato (por exemplo, acetato de sódio), succinato (por exemplo, succinato de sódio), gliconato, histidina, citrato e outros tampões ácidos orgânicos. A concentração do tampão pode ficar entre cerca de 1 mM e cerca de 50 mM, de preferência entre cerca de 5 mM e cerca de 30 mM, dependendo, por exemplo, do tampão e da isotonicidade desejada da formulação. O tampão preferido é acetato de sódio (cerca de 10 mM), pH 5,0.
[000108] Um poliol que atua como um agente para tonicidade é incluído na formulação. Em modalidades preferidas, a formulação não contém uma quantidade para tonicidade de um sal tal como cloreto de sódio, pois isto pode fazer com que o anticorpo ou derivado de anticorpo precipite e/ou pode resultar na oxidação em pH baixo. Em modalidades preferidas, o poliol é um açúcar não-redutor, tal como sacarose ou trealose. O poliol é adicionado à formulação em uma quantidade que pode variar com relação à isotonicidade desejada da formulação. De preferência, a formulação aquosa é isotônica, em cujo caso as concentrações apropriadas do poliol na formulação ficam na faixa entre cerca de 1% e cerca de 15% p/v, de preferência na faixa entre cerca de 2% e cerca de 10% p/v, por exemplo. Entretanto, formulações hipertônicas ou hipotônicas também podem ser apropriadas. A quantidade de poliol adicionada pode se alterar também com relação ao peso molecular do poliol. Por exemplo, uma quantidade mais baixa de um monossacarídeo (por exemplo, manitol) pode ser adicionada em comparação com um dissacarídeo (tal como trealose).
[000109] Um tensoativo também é adicionado à formulação do anticorpo ou derivado de anticorpo. Os tensoativos exemplificativos incluem tensoativos não-iônicos tais como Polissorbatos (por exmeplo, Polissorbatos 20, 80, etc.) ou Poloxâmeros (por exemplo, Poloxâmero 188). A quantidade de tensoativo adicionada é tal que ele reduza a agregação do anticorpo/derivado de anticorpo formulado e/ou minimize a formação de particulados na formulação e/ou reduza a adsorção. Por exemplo, o tensoativo pode estar presente na formulação em uma quantidade entre cerca de 0,001% e cerca de 0,5%, de preferência entre cerca de 0,005% e cerca de 0,2%, e mais preferivelmente, entre cerca de 0,01% e cerca de 0,1%.
[000110] Em uma modalidade, a formulação contém os agentes identificados acima (isto é, anticorpo ou derivado de anticorpo, tampão, poliol e tensoativo) e é essencialmente isenta de um ou mais conservantes, tais como álcool benzílico, fenol, m-cresol, cloro-butanol e cloreto de benzetônio. Em outra modalidade, um conservante pode ser incluído na formulação, particularmente quando a formulação é uma formulação para múltiplas doses. A concentração do conservante pode ficar na faixa entre cerca de 0,1% e cerca de 2%, mais preferivelmente entre cerca de 0,5% e cerca de 1%. Um ou mais outros veículos, excipientes ou estabilizadores farmaceuticamente aceitáveis, tais como aqueles descritos em "Remington's Pharmaceutical Sciences", 21a edição (2006), Osol, A. (editor), podem ser incluídos na formulação, desde que eles não afetem adversamente as características desejadas da formulação. Os veículos, excipientes, ou estabilizadores apropriados são atóxicos para os recebedores nas dosagens e concentrações empregadas e incluem: tampões adicionais; co-solventes; antioxidantes, incluindo ácido ascórbico e metionina; agentes quelantes tais como EDTA; complexos metálicos (por exemplo, complexos Zn/proteína), polímeros biodegradáveis tais como poliésteres; e/ou contra-íons formadores de sais, tal como sódio.
[000111] As formulações a serem usadas para administração in vivo devem ser estéreis. Isso é realizado facilmente por filtração através de membranas de filtração estéreis, antes ou depois da preparação da formulação.
[000112] A formulação é administrada a um mamífero que necessita de tratamento com o anticorpo, de preferência um ser humano, de acordo com métodos conhecidos, tais como administração intravenosa como uma injeção maciça ou por infusão contínua durante um período de tempo, por injeção intramuscular, intraperitoneal, intracerebrospinhal, subcutânea, intra-articular, intra-sinovial, intratecal, por via oral, tópica ou inalação. Em modalidades preferidas, a formulação é administrada a um mamífero por administração intravenosa. Com este propósito, a formulação pode ser injetada usando uma seringa ou por intermédio de uma linha IV, por exemplo.
[000113] A dosagem apropriada ("quantidade terapeuticamente eficaz") do anticorpo dependerá, por exemplo, da condição a ser tratada, da gravidade e curso da condição, se o anticorpo é administrado com propósitos preventivos ou terapêuticos, terapia anterior, história clínica do paciente e resposta ao anticorpo, do tipo de anticorpo usado, e do julgamento do médico atendente. O anticorpo ou derivado de anticorpo é administrado adequadamente ao paciente em uma vez ou durante uma série de tratamentos e pode ser administrado ao paciente em qualquer hora a partir do diagnóstico em diante. O anticorpo ou derivado de anticorpo pode ser administrado como o único tratamento ou em conjunto com outros fármacos ou terapias úteis no tratamento da condição em questão.
[000114] Como uma proposta geral, a quantidade terápeuticamente eficaz do anticorpo ou derivado de anticorpo administrada deve ficar na faixa entre cerca de 0,1 e cerca de 50 mg/kg do peso corporal do paciente, seja em uma ou mais administrações, sendo que a faixa típica da quantidade do anticorpo fica entre cerca de 0,3 e cerca de 20 mg/kg, mais preferivelmente entre cerca de 0,3 e cerca de 15 mg/kg, administrada diariamente, por exemplo. Entretanto, outros esquemas de dosagem podem ser úteis. A progressão desta terapia é monitorada facilmente por técnicas convencionais.
[000115] Em outra modalidade da invenção, fornece-se um artigo fabricado que compreende um recipiente que mantém a formulação farmacêutica aquosa da presente invenção e, opcionalmente, fornece instruções para seu uso. Os recipientes apropriados incluem, por exemplo, vidros, frascos e seringas. O recipiente pode ser formado a partir de uma série de materiais, tais como vidro ou plástico. Um recipiente exemplificativo é um frasco de vidro de 3-20 cm3 para uso único. Alternativamente, para uma formulação com múltiplas doses, o recipiente pode ser um frasco de vidro de 3-100 cm3. O recipiente mantém a formulação, e o rótulo sobre ele ou associado com o recipiente pode indicar orientações para uso. O artigo fabricado pode incluir ainda outros materiais desejáveis de um ponto de vista comercial ou do usuário, incluindo outros tampões, diluentes, filtros, agulhas, seringas e bulas com instruções para uso. Geração dos Anticorpos da Presente Invenção
[000116] Os anticorpos ou derivados de anticorpos da presente invenção podem ser gerados usando técnicas de rotina no campo da genética recombinante. Conhecendo as sequências dos polipeptídeos, os cDNAs que as codificam pode ser gerados por síntese gênica (www.genscript.com). Estes cDNAs podem ser clonados em vetores plasmidiais apropriados. Uma vez obtido o DNA que codifica um domínio VL e/ou VH, uma mutagênese direcionada a sítio, por exemplo, por PCR, usando iniciadores mutagênicos, pode ser realizada para obter vários derivados. A melhor sequência "de partida" pode ser escolhida dependendo do número de alterações desejado nas sequências de VL e/ou VH. Uma sequência preferida é a sequência de TB-A e seus derivados, por exemplo, sequências de scFv ou sequências do peptídeo de fusão, podem ser escolhidas como modelos para a mutagênese acionada por PCR e/ou clonagem.
[000117] As técnicas usuais de clonagem e mutagênese bem conhecidas pelos versados nessas técnicas podem ser usadas para anexar ligantes, domínios embaralhados ou fusões de constructos para a produção de fragmentos Fab. Os protocolos básicos que descrevem os métodos genéricos desta invenção estão descritos em "Molecular Cloning, A Laboratory Manual" (Sambrook & Russell, 3a edição, 2001) e em "Current Protocols in Molecular Biology" (Ausubel et al., 1999).
[000118] A sequência de DNA portadora de um gene que codifica um polipeptídeo scFv, ou no caso de fragmentos Fab, que codificam dois genes separados ou um operon bicistrônico, compreendendo dois genes para as fusões VL-CK e VH-CH1 (Figura 2), são clonados em um vetor de expressão apropriado, de preferência um com um promotor induzível. Deve-se tomar cuidado para que esteja na frente de cada gene um sítio de ligação de ribossoma (RBS na Figura 2) que assegura a tradução. Deve-se entender que os anticorpos da presente invenção compreendem as sequências descritas em vez de eles consistirem nelas. Por exemplo, as estratégias de clonagem podem requerer que seja produzida um construto a partir da qual um anticorpo com um ou alguns resíduos adicionais na extremidade do N-terminal estejam presentes. Especificamente, a metionina derivada do códon de iniciação pode estar presente na proteína final nos casos em que ela foi clivada depois da tradução. A maioria dos construtos para anticorpos scFv gera uma alanina adicional na extremidade do N-terminal. Em uma modalidade preferida da presente invenção, um vetor de expressão para a expressão periplasmática em E. coli é escolhido (Krebber, 1997). O dito vetor compreende um vetor na frente de uma sequência de sinais clivável. A sequência codificadora para o peptídeo do anticorpo é então fundida à sequência de sinais clivável. Isto permite o assestar o polipeptídeo expressado para o periplasma bacteriano, onde a sequência de sinais é clivada. O anticorpo é então dobrado. No caso dos fragmentos Fab, os peptídeos de fusão VL-Ck e VH-CH1 devem ser ligados a um sinal de exportação. A ligação S-S covalente é formada nas cisteínas do C-terminal depois que os peptídeos atingiram o periplasma. Caso a expressão citoplasmática de anticorpos seja preferida, os ditos anticorpos usualmente podem ser obtidos com altos rendimentos a partir de corpos de inclusão, que podem ser separados facilmente a partir de outros fragmentos celulares e proteínas. Neste caso, os corpos de inclusão são solubilizados em um agente desnaturador, tal como, por exemplo, cloridrato de guanidina (GdnHCl), e depois redobrados por procedimentos de renaturação bem conhecidos pelos versados nessas técnicas.
[000119] Os plasmídeos que expressam os polipeptídeos de scFv ou Fab são introduzidos em um hospedeiro apropriado, de preferência uma célula bacteriana, de levedura ou de mamífero, mais preferivelmente uma cepa de E. coli apropriada, tal como, por exemplo, JM83, para a expressão periplasmática de BL21 para expressão em corpos de inclusão. O polipeptídeo pode ser colhido a partir do periplasma ou a partir de corpos de inclusão, e purificado usando técnicas usuais, tais como cromatografia de troca iônica, cromatografia em fase reversa, cromatografia de afinidade e/ou filtração em gel, conhecidas pelos versados nessas técnicas.
[000120] Os anticorpos ou derivados de anticorpos da presente invenção podem ser distinguidos com relação ao rendimento, solubilidade e estabilidade in vitro. As capacidades de ligação ao TNFα, preferência TNFα humano, podem ser testadas in vitro por ELISA ou ressonância de plasmon de superfície (BIACore), usando TNFα humano recombinante, como descrito no documento no WO 9729131, sendo que este último método permite também determinar a constante da taxa koff, que deveria ser de preferência menor do que 10-3 s-1. Os valores de Kd < 10 nM são preferidos.
[000121] A atividade neutralizadora in vivo de um anticorpo ou derivado de anticorpo da presente invenção pode ser estimada usando o ensaio de citotoxicidade em L929. O TNFα humano recombinante exerce um efeito citotóxico contra células de fibroblastos L929 do camundongo cultivadas, de uma maneira dependente da concentração. Esta citotoxicidade induzida por TNFα pode ser inibida por anticorpos neutralizadores de TNFα (Doring, 1994). Um valor de CI50 preferido correspondente à concentração meia-máxima do inibidor é < 100 mg/mL.
[000122] Como TNFα tem um papel patofisiológico comprovado em várias doenças humanas, particularmente distúrbios inflamatórios, distúrbio autoimunes regulados imunologicamente, infecções causadoras de choque séptico, endotóxico e cardiovascular, doenças neurodegenerativas, e doenças malignas. Como TNFα é suspeito de desempenhar um papel relevante para doenças de um número constantemente crescente de doenças humanas adicionais, é difícil fornecer uma lista abrangente de indicações que assegure também uma representação completa do espectro de aplicações clínicas para inibidores de TNFα no futuro. Portanto, os anticorpos ou derivados de anticorpos da presente invenção podem ser aplicados para tratar as doenças listadas no catálogo que se segue, que não é considerado como uma lista completa ou excludente. Outras doenças não mencionadas especificamente, que sejam direta ou indiretamente influenciadas por TNFα, também estão incluídas. Inflamação Autoimune ou Crônica
[000123] Os estados crônicos e/ou autoimunes de inflamação em geral, distúrbios inflamatórios regulados imunologicamente em geral, doenças inflamatórias do sistema nervoso central, que afetam os olhos, articulações, pele, membranas mucosas, sistema nervoso central, trato gastrointestinal, trato urinário ou pulmões, estados de uveíte em geral, retinite, uveíte HLA-B27+, doença de Behcet, síndrome do olho seco, glaucoma, síndrome de Sjogren, diabetes melito (incluindo neuropatia diabética), resistência à insulina, estados de artrite em geral, artrite reumatoide, osteoartrite, artrite reativa e síndrome de Reiter, artrite juvenil, espondilite ancilosante, esclerose múltipla, síndrome de Guillain-Barré, miastenia grave, esclerose lateral amiotrófica, sarcoidose, glomerulonefrite, doença crônica dos rins, cistite, psoríase (incluindo artrite psoríaca), hidradenite supurativa, paniculite, piodermia gangrenosa, síndrome SAPHO (sinovite, acne, pustulose, hiperosteose, e osteíte), acne, síndrome de Sweet, pênfigo, doença de Crohn (incluindo manifestações extra-intestinais), colite ulcerativa, asma brônquica, pneumonite de hipersensibilidade, alergias gerais, rinite alérgica, sinusite alérgica, doença pulmonar obstrutiva crônica (COPD), fibrose pulmonar, granulomatose de Wegener, síndrome de Kawasaki, arterite de células gigantes, vasculite de Churg-Strauss, poliarterite nodosa, queimaduras, doença de enxerto versus hospedeiro, reações de hospedeiro versus enxerto, episódios de rejeição após transplante de órgão ou medula óssea, estados sistêmicos e locais de vasculite em geral, lúpus eritematoso sistêmico ou discóide, polimiosite e dermatomiosite, esclerodermia, pré-eclampse, pancreatite aguda e crônica, hepatite viral, hepatite alcoólica. Inflamação Aguda e/ou Prevenção de Inflamação de Dor Pós-cirúrgica ou Pós-traumática
[000124] Prevenção de inflamação pós-cirúrgica em geral, cirurgia ocular (por exemplo, catarata (substituição de lente ocular) ou cirurgia de glaucoma), cirurgia das articulações (incluindo cirurgia artroscópica), cirurgia em estruturas relacionadas a articulações (por exemplo, ligamentos), cirurgia oral e/ou dental, procedimentos cardiovasculares minimamente invasivos (por exemplo, PTCA, aterectomia, colocação de sondas), procedimentos laparoscópicos e/ou endoscópicos intra- abdominais e ginecológicos, procedimentos urológicos endoscópicos (por exemplo, cirurgia da próstata, ureteroscopia, cistoscopia, cistite intersticial), inflamação perioperatória (prevenção) em geral. Doenças Neurológicas e Neurodegenerativas
[000125] Doença de Alzheimer, doença de Parkinson, doença de Huntington, paralisia de Bell, doença de Creutzfeldt-Jakob.
[000126] Osteólise relacionada a câncer, inflamação relacionada a câncer, dor relacionada a câncer, caquexia relacionada a câncer, metástases ósseas.
[000127] Formas agudas e crônicas de dor, independentemente se elas são causadas por efeitos centrais ou periféricos de TNFα e se elas são classificadas como inflamatórias, formas nociceptivas ou neuropáticas de dor, ciática, dor do dorso inferior, síndrome do túnel do carpo, síndrome de dor regional complexa (CRPS), gota, neuralgia pós- herpética, fibromialgia, estados de dor local, síndromes de dor crônica devido a tumor metastático, dismenorréia.
[000128] Sepse bacteriana, viral ou fúngica, tuberculose, AIDS.
[000129] Aterosclerose, doença de artéria coronária, hipertensão, dislipidemia, insuficiência cardíaca e insuficiência cardíaca crônica.
[000130] Em uma modalidade preferida da presente invenção, o tratamento de osteoartrite ou uveíte ou doença inflamatória do intestino, pode ser realizado com os anticorpos ou derivados de anticorpos da presente invenção.
[000131] A presente invenção fornece também uma composição farmacêutica que compreende uma molécula de anticorpo ou derivado de anticorpo da presente invenção em combinação com um excipiente, diluente ou veículo farmaceuticamente aceitável.
[000132] A composição farmacêutica deve compreender, de preferência, uma quantidade terapeuticamente eficaz do anticorpo da presente invenção, isto é, uma quantidade do dito anticorpo, que é necessária para tratar, melhorar ou prevenir a doença ou condição relacionada ao TNFα, ou para apresentar um efeito terapêutico ou preventivo detectável. A dose terapeuticamente eficaz pode ser estimada em ensaios de cultura de células ou em modelos animais, usualmente em roedores, coelhos, cães, porcos ou primatas. O modelo animal pode ser usado também para determinar a faixa de concentração e a via de administração apropriadas. Um modelo animal apropriado para observar um efeito do anticorpo ou derivado de anticorpo da presente invenção é um modelo com ratos para monoartrite aguda (Bolon et al., Vet. Pathol. 41:235-243 (2004). O TNFα humano é injetado por via intra-articular dentro da articulação do joelho de um rato, levando a uma monoartrite aguda autolimitativa na articulação que recebeu a injeção. A bioatividade de um anticorpo (ou derivado) anti-TNFα pode ser quantificada pela redução do inchaço da articulação do joelho, induzido por TNFα, ou pela redução dos parâmetros histológicos da inflamação.
[000133] Como os anticorpos ou derivados de anticorpos da presente invenção são altamente solúveis, as altas concentrações do anticorpo (60 mg/mL ou mais) permitem o uso de pequenos volumes de aplicação.
[000134] O anticorpo ou derivado de anticorpo da presente invenção pode ser utilizado em qualquer terapia na qual se deseja reduzir o nível de TNFα biológico ativo no corpo humano ou animal. O TNFα pode estar circulando no corpo ou estar presente em um nível indesejavelmente alto localizado em um local específico do corpo. A presente invenção fornece modos para aplicações sistêmicas, bem como locais, em geral, que incluem, porém sem limitações, os seguintes: aplicação peroral, injeção intravenosa, subcutânea, intramuscular, intra-articular, intravítrea, intradérmica ou intraparenquimatosa, inalação de aerossol, aplicação tópica sobre a pele, membranas mucosas ou sobre os olhos, liberação sistêmica ou local por intermédio de minibomba implantável, ou liberação local por intermédio de formulação/dispositivo implantável para liberação retardada, aplicação tópica sobre superfícies serosas, aplicação intratecal ou intraventricular, aplicação oral em formulações que permitem a liberação controlada dentro do lúmen em partes selecionadas do trato gastrointestinal, liberação localizada dentro de vasos a partir de formulações/dispositivos adequados (por exemplo, sondas), distribuição local para cisto urinário liberação localizada dentro do lúmen (por exemplo, trato biliar, ureter), ou liberação a partir de lentes de contato. Uma aplicação preferida é uma local, tal como injeção intraarticular ou aplicação tópica, por exemplo, dentro do olho. Para ambas aplicações preferidas, o anticorpo da presente invenção precisa estar em solução.
[000135] A presente invenção revela também o uso do anticorpo ou derivado de anticorpo da presente invenção para a produção de um medicamento para o tratamento de doenças associadas ao TNFα. Neste caso, o anticorpo ou derivado de anticorpo está incluído em uma composição terapêutica. A dita composição é usada como um medicamento, de preferência para a prevenção ou terapia de doenças relacionadas ao TNFα.
[000136] Em outro aspecto, os anticorpos scFv da presente invenção são usados em terapia gênica, particularmente em terapia gênica celular adotiva. Os distúrbios autoimunes representam respostas imunes inadequadas direcionadas em próprio tecido. As células T CD4+ específicas de antígeno e as células dendríticas apresentadoras de antígenos (DCs) são mediadores importantes na patogênese de doenças autoimunes, e assim sendo, são candidatos ideais para terapia gênica celular adotiva, uma abordagem ex vivo para transferência de genes terapêuticos. Usando células transduzidas de forma retroviral e bioluminescência com luciferase, Tarner et al., Ann. N. Y. Acad. Sci. 998:512-519 (2003), demonstraram que células T primárias, hibridomas de células T, e DCs se alojam rapidamente e preferencialmente em sítios de inflamação em modelos animais de esclerose múltipla, artrite e diabetes. Estas células, transduzidas com vetores retrovirais que acionam a expressão de várias "proteínas reguladoras", tais como interleucinas e scFv anti-TNF, distribuem essas proteínas imunorreguladoras para lesões inflamadas, proporcionando terapia para encefalite autoimune experimental, artrite induzida por colágeno, e camundongos diabéticos não-obesos. As estruturas estáveis e solúveis dos anticorpos ou derivados de anticorpos da presente invenção são particularmente apropriadas para a distribuição intracelular do antígeno, por exemplo, quando o anticorpo ou derivado de anticorpo é expressado a partir de um transgene transportado por um vetor retroviral apropriado. A terapia gênica celular adotiva leva à expressão e secreção localizada do scFv anti-TNFa. Smith et al. (2003) demonstraram que os scFvs derivados de um anticorpo monoclonal neutralizador de TNFα (i) podem neutralizar TNFa in vitro e (ii) mudar o padrão de expressão de citocinas em camundongos que sofrem de artrite induzida por colágeno localmente nas articulações, mas não de forma sistêmica. Alternativamente, a injeção sistêmica ou local direta de vetores apropriados (por exemplo, vírus), que permite a expressão contínua de um anticorpo scFv anti-TNFa, é considerada como outra abordagem de terapia gênica possível.
[000137] As sequências da presente invenção são as seguintes: SEQ ID NO:1 VL of TB-A DIVMTQSPSSLSASVGDRVTLTCTASQSVSNDWWYQQRPGKAPK LLIYSAFNRYTGVPSRFSGRGYGTDFTLTISSLQPEDVAVYYCQQDYNSPRTFGQGT KLEVKR ' SEQ ID NO:2 VH of TB-A QVQLVQSGAEVKKPGASVKVSCTASGYTFTHYGMNWVRQAPGKGL EWMGWINTYTGEPTYADKFKDRFTFSLETSASTVYMELTSLTSDDTAVYYCARERGD AMDYWGQGTLVTVSS . . SEQ ID NO:3 VL of TB~B DIVLTQSPSSLSASVGDRVTLTCTASQSVSNDVWYQQRPGKAPK RLIYSAFNRYTGVPSRFSGSGSGTEFTLTISSLQPEDVAVYYCQQDYNSPRTFGQGT KLEVKR . . SEQ ID NO:4 VH of TB-B QVQLVQS GAEVKKPGASVKVSCT AS GY S FTHYGMNWVRQAPGQGL EWMGWINTYTGEPTYADKFKDRVTLTRDTSIGTVYMELTSLTSDDTAVYYCARERGD AMDYWGQGTLVTVSS - . . • SEQ ∑D N0;5 VL OF FW2.3 . DIVLTQSPSSLSASVGDRVTLTCRASQGIRNELAWYQQRPGKAPK RLIYAGSIEQSGVPSRFSGSGSGTE-FTLTISSLQPEDVAVYYCQQYYSLPYMFGQGT KLEVKR SEQ ID NO:6 VH of FW2.3 QVQLVQSGAEVKKPGASVKVSCTASGYSFTGYFLHWVRQAPGQGL EWMGRINPDSGDTIYAQKFQDRVTLTRDTSIGTVYMELTSLTSDDTAVYYCARVPRG TYLDPWDYFDYWGQGTLVTVSS ' SEQ ID NO:7 VL of TB_L2 DIVMTQSPSSLSASVGDRVTLTCTASQSVSNDWWYQQRPGKAPK LLIYAGSILQSGVP SRPSGRGYGT DFTLTIS SLQPE DVAVYYCQQDYN S PRT FGQGT KLEVKR SEQ ID NO:8 VL of TB_L3 DIVMTQSPSSLSASVGDRVTLTCTASQSVSNDWWYQQRPGKAPK LLIYSAFNRYTGVPSRFSGRGYGTDFTLTISSLQPEDVAVYYCQQYYSLPYMFGQGT KLEVKR . SEQ ID NO:9 VH of TB_H2 QVQLVQSGAEVKKPGASVKVSCTASGYTFTHYGMNWRQAPGKGL EWMGRINPDSGDTIYAQKFQDRFTFSLETSASTVYMELTSLTSDDTAVYYCARERGD AMDYWGQGTLVTVSS SEQ ID NO:10 Linker GGGGSGGGGSGGGGSGGGGS SEQ ID NO:11 VL of TB-B R46L DIVLTQSPSSLSASVGDRVTLTCTASQSVSNDWWYQQRPGKAPK LLIYSAFNRYTGVPS RFSG S GS GTE FTLTIS SLQPE DVAVYYCQQDYN S PRT FGQGT KLEVKR - SEQ ID NO:12 TB-AB ' ' " DIVMTQSPSSLSASVGDRVTLTCTASQSVSNDWWYQQRPGKAPK LLIYSÁFNRYTGVPSRESGRGY.GTDETLTISSLQPEDVAVYYCQQDYNSPRTFGQGT KLEVKRGGGGSGGGGSGGGGSGGGGSQVQLVQSGAEVKKPGASVKVSCTASGYSFTH YGMNWVRQAPGQGLEWMGWINTYTGEPTYADKFKDRVTLTRDTSIGTVYMELTSLTS DDTAVYYCARERGDAMDYWGQGTLVTVSS SEQ ID NO:13 TB-BA DIVLTQSPSSLSASVGDRVTLTCTASQSVSNDVWYQQRPGKAPK RLIYSAFNRYTGVPSRFSGSGSGTEFTLTISSLQPEDVAVYYCQQDYNSPRTFGQGT KLEVKRGGGGSGGGGSGGGGSGGGGSQVQLVQSGAEVKKPGASVKVSCTASGYTFTH YGMNWVRQAPGKGLEWMGWINTYTGEPTYADKFKDRFTFSLETSASTVYMELTSLTS DDTAVYYCARERGDAMDYWGQGTLVTVS S SEQ ID NO: 14 CK of Fab TVAAPSVFIFPPSDEQLKSGTASWCLLNNFYPREAKVQWKVDNA LQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFN RGEC • SEQ ID NO:15 CHI of Fab ' AS TKGPSVFPLAP S SKST SGGTAALGCLVKDYFSE PVTVSWN S GA LTSGVHTFPAVLQSSGLYSLSSWTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKS CTS - SEQ ID NO : 16 VL’ of TB-wt • DIVMTQTPKFLLVSAGDRVTITCTASQSVSNDWWYQQKPGQSPK MLMYSAFNRYTGVPDRFTGRGYGTDFTFTISSVQAEDLAVYFCQQDYNSPRTFGGGT KLEIKR SEQ ID NO:17 VH of TB-wt QIQLVQSGPELKKPGETVKISCKASGYTFTHYGMNWVKQAPGKGL KWMGWINTYTGEPTYADDFKEHFAFSLETSASTVFLQINNLKNEDTATYFCARERGD AMDYWGQGTSVTVSS SEQ ID NO?18 TB-A H_K43Qr also named TB-A H43 . DIVMTQSPSSLSASVGDRVTLTCTASQSVSNDWWYQQRPGKAPK LLIYSAFNRYTGVPSRFSGRGYGTDFTLTISSLQPEDVAVYYCQQDYNSPRTFGQGT KLEVKRGGGGSGGGGSGGGGSGGGGSQVQLVQSGAEVKKPGASVKVSCTASGYTFTH YGMNWVRQAPGQGLEWMGWINTYTGEPTYADKFKDRFTFSLETSASTVYMELTSLTS DDTAVYYCARERGDAMDYWGQGTLVTVSS . . . ' SEQ ID NO:19 TB-A H_F68Vf also named TB-A H68 DIVMTQSPSSLSASVGDRVTLTCTASQSVSNDWWYQQRPGKAPK 1LIYSAFNRYTGVPSRFSGRGYGTDFTLTISSLQPEDVAVYYCQQDYNSPRTFGQGT KLEVKRGGGGSGGGGSGGGGSGGGGSQVQLVQSGAEVKKPGASVKVSCTASGYTFTH YGMNWVRQAPGKGLEWMGWINTYTGE PTYADKFKDRVT FSLET SASTVYMELT S LT S . DDTAVYYCARERGDAMDYWGQGTLVTVSS : KLEVKRGGGGSGGGGSGGGGSGGGGSQVQLVQSGAEVKKPGASVKVSCTASGYTFTH YGMNWVRQAPGKGLEWMGWINTYTGEPTYADKFKDRFTFSLETSASTVYMELTSLTS DDTAVYYCARERGDAMDYWGQGTLVTVSS
[000138] A invenção será mais plenamente entendida fazendo referência aos exemplos que se seguem. Entretanto, eles não devem ser interpretados como limitativos do âmbito da invenção. Todas citações de literaturas e patentes são aqui incorporadas como referência. Experimento 1: Construção de Anticorpos scFv
[000139] O material de partida para a geração de anticorpos ou derivados de anticorpos anti-TNFa humano, humanizados, tais como fragmentos de cadeia única (scFv) ou fragmentos Fab, foi o anticorpo monoclonal murino Di62. As sequências da região variável da cadeia leve e da cadeia pesada estão descritas em Doring et al., Mol. Immunol. 31:1059-1067 (1994). As propriedades deste anticorpo monoclonal também estão discutidas na mesma publicação. Resumidamente, Di62 se liga especificamente ao TNFa humano de uma maneira dependente da concentração. Ele é um anticorpo de alta afinidade (Kd = 0,4 nM) e pode bloquear a ligação de TNFa ao seu receptor. Além disso, Di62 inibe a citotoxicidade induzida por TNFa humano em células L929 do camundongo.
[000140] Baseado na sua sequência publicada, Di62 foi construído na forma de um derivado de anticorpo de cadeia única (scFv) na orientação VL-ligante-VH, na qual a sequência do ligante é constituída de quatro repetições de quatro resíduos de glicina e um de serina (Gly4Ser)4. Neste caso, este scFv é referido como TB-wt, com uma VL de SEQ ID NO:16 e uma VH de SEQ ID NO: 17.
[000141] Para humanizar este derivado de anticorpo com o propósito de (a) torná-lo mais similar às sequências humanas a fim de minimizar a imunogenicidade potencial, e (b) torná-lo mais estável e mais solúvel, as sequências da CDR de TB-wt foram enxertadas em estruturas humanas estáveis e solúveis (Auf der Maur et al.,FEBS Lett. 508:407412 (2001); Auf der Maur et al., Methods 34:215-224 (2004)). O subgrupo I de VL-kapa e o subgrupo I de VH humanos foram identificados como a subfamília mais próxima da humana. A estrutura apropriada do aceptor foi escolhida a partir de uma coleção de sequências de VL e VH humanas, selecionadas quanto às propriedades bioquímicas e biofísicas vantajosas, tais como, por exemplo, as propriedades de estabilidade, solubilidade, e expressão (Auf der Maur et al.,FEBS Lett. 508:407-412 (2001); Auf der Maur et al., Methods 34:215-224 (2004)). O isolamento e as propriedades destas estruturas de anticorpo estão descritas nos documentos nos WO 03097697 e EP 1506236. A partir desta coleção, uma estrutura de anticorpo de cadeia única com propriedades indefinidas de ligação a antígeno foi identificada com um aceptor apropriado. Este aceptor consiste em um domínio V-kapa I humano (SEQ ID NO: 14) em combinação com um domínio VH I humano (SEQ ID NO: 15). Dentre 81 resíduos de estruturas VH, TB-wt e FW2.3 têm 55 resíduos idênticos, correspondendo a 63% de identidade. Ambos derivados de anticorpos de cadeia única têm comprimentos de CDRs idênticos, além da VH- CDR3, que é mais longa em FW2.3. A composição de aminoácidos dentro dos resíduos de CDRs é diferente para ambos scFv's. Vários métodos para a humanização de domínios variáveis de anticorpos são descritos (Riechmann et al., Nature 332:323-327 (1998); Padlan, E.A., Mol. Immunol. 28:489-498 (1991); Roguska et al., Proc. Natl. Acad. Sci. USA 91:969-973 (1994); Gonzales et al., Tumor Biol. 26:31-43 (2005); Ewert, S. et al., Methods 34:184-199 (2004). A abordagem mínima, a saber, a transferência conservativa de todas alças de CDRs do camundongo de YB-wt para FW2.3 foi conduzida em primeiro lugar. O scFv resultante é referido como TB-B e tem a sequência de VL SEQ ID NO: 3 e a sequência de VH SEQ ID NO: 4. As alças de CDRs em TB- wt foram definidas de acordo com o esquema de numeração de Kabat (Kabat et AL., "Sequences of Proteins of Immunological Interest", 5a Edição (1991), National Institutes of Health, Bethesda, MD, EUA) e confinam os seguintes resíduos (vide Figura 1): VL CDR1: L24-L34 (mesma numeração Kabat) CDR2: L50-L56 (mesma numeração Kabat) CDR3: L89-L97 (mesma numeração Kabat) VH CDR1: H31-H35 (mesma numeração Kabat) CDR2: H50-H66 (mesma numeração Kabat) CDR3: H99-H106 (mesma numeração Kabat)
[000142] Este anticorpo foi incapaz de se ligar ao TNFα eficientemente (Figura 4a). A próxima etapa foi determinar qual resíduo ou quais resíduos entre estes componentes devem ser substituídos para otimizar as propriedades do anticorpo humanizado resultante.
[000143] Como a substituição de resíduos de aminoácidos humanos por outros aminoácidos deve ser minimizada porque a introdução de sequências de aminoácidos estranhas aumenta o risco de imunogenicidade do anticorpo ou derivado de anticorpo em humanos (Gonzales et al., Tumor Biol. 26:31-43 (2005)), várias variantes foram construídas. Uma das ditas variantes - aqui referida como TB-B L46 (VL SEQ ID NO: 11; VH SEQ ID NO: 4) - foi construída com a meta de minimizar o risco de ser imunogênica, mas ainda apresentando atividade de ligação suficiente. Esta variante baseia-se em TB-B e contém uma única mudança de aminoácido na posição 46 em VL, a saber R^L. Este aminoácido fica localizado dentro do núcleo superior da cadeia leve e faz parte da interface dimérica. Ele está envolvido na definição da conformação de L-CDR1 e tem uma influência sobre o empacotamento de VH/VL. Relatou-se que um resíduo de leucina é favorecido nesta posição específica (documento no PCT/US03/19333). Em contraste com TB-B, o scFv L46 retém alguma ligação de TNFα (Figura 4A; Kd « 100 nM).
[000144] Para melhorar ainda mais a atividade de ligação ao TNFα, uma ou mais trocas adicionais foram feitas em um ou mais dos resíduos de VL 4, 46, 65, 67, 70 e/ou dos resíduos de VH 28, 43, 68, 70, 71, 72, 73, 76, 77. Neste caso, a variante com mudanças em todas posições é referido como TB-A (VL SEQ ID NO: 1; VH SEQ ID NO: 2).
[000145] Além disso, quanto aos anticorpos anti-TNFα específicos da presente invenção, ensaios de competição com peptídeos derivados de L-CDR1 e L-CDR2 indicaram que ambas alças de CDRs são importantes para a ligação do scFv ao antígeno (Doring et al., Mol. Immunol. 31:1059-1067 (1994)).
[000146] Em outros experimentos que visavam a minimizar o número de resíduos não-humanos necessários para reter a ligação e a otimizar as propriedades biofísicas (estabilidade e solubilidade), aplicou-se mutagênese sistemática e embaralhamento de domínios, permitindo elucidar as diferenças funcionais entre os domínios VL e VH murinos e humanizados.
[000147] Duas variantes foram obtidas pelo embaralhamento de domínios. A primeira variante é composta do domínio VL de TB-A ligado por intermédio de um ligante de glicina serina (SEQ ID NO: 10) com o domínio VH de TB-B, resultando em TB-AB (SEQ ID NO: 12). A segunda variante, TB-BA, é o inverso da primeira variante, a saber, o domínio VL de TB-B em combinação com o domínio VH de TB-A (SEQ ID NO: 13).
[000148] Variantes adicionais foram geradas por mutagênese sistemática de TB-A. A Figura 1 ilustra uma comparação de sequências das sequências de VL e VH de TB-A e TB-B. Um total de 14 resíduos de estruturas difere entre TB-A e TB-B (asteriscos). Apenas cinco deles, resíduos de VL 4 e 70, e os resíduos de VH 28, 71 e 73 apresentam apenas diferenças mínimas em tamanho e propriedade, e portanto, não foram considerados para mutagênese neste ponto. As seguintes posições nas estruturas foram trocadas pelo aminoácido correspondente de TB-B. Estes mutantes singulares e duplos de TB-A são os seguintes: TB-A H43 K >Q interface (SEQ ID NO: 18) TB-A H68 F >V alça externa VH (SEQ ID NO: 19) TB-A H70/72 F>L, L>R alça externa VH (SEQ ID NO: 20) TB-A H76/77 A>I, S>G alça externa VH (SEQ ID NO: 21) TB-A L46 L>R interface (SEQ ID NO: 22) TB-A L65 R>S alça externa VL (SEQ ID NO: 23) TB-A L67 Y>S alça externa VL (SEQ ID NO: 24)
[000149] Muitos fatores podem influenciar a imunogenicidade de um anticorpo ou derivado de anticorpo (Gonzales et al., Tumor Biol. 26:3143 (2005)). Para reduzir ainda mais o teor não-humano das regiões variáveis do scFv de TB-A humanizado, as alças de CDR2 e CDR3 murinas de VL e a alça de CDR2 murina de VH foram trocadas pelas alças de CDRs humanas correspondentes de FW2.3. Os constructos resultantes neste caso são referidos como TB_L2 (SEQ ID NO: 7), TB_L3 (SEQ ID NO: 8), e TB_H2 (SEQ ID NO: 9), respectivamente.
[000150] Os cDNAs que codificam a versão de cadeia única murina do anticorpo monoclonal Di62, e as duas versões humanizadas TB-B e TB-A, foram geradas por síntese gênica (www.genscript.cm). Todas mutações pontuais nas outras variantes (TB-B L46, TB-A H43, TB-A H67, TB-A H69/71, TB-A H75/76, TB-A L46, TB-A L65, TB-A L67, TB-A V83F, TB-A V83A, TB-A D66G) foram introduzidas por mutagênese direcionada a sódios acionada por PCR, após procedimentos de clonagem usuais. A troca das alças de CDRs murinas de TB-A pelas alças de CDRs humanas de FW2.3 foi realizada usando PCR procedimentos de clonagem do estado da arte. O cDNA que codifica todas as variações de VH TB-A, como descritas em SEQ ID NO: 28, SEQ ID NO: 29 e SEQ ID NO: 30, foram realizadas por síntese gênica completa.
[000151] Alguns outros TB-A preferidos estão descritos em SEQ ID NO: 31 a SEQ ID NO: 38. Estes anticorpos demonstraram ser particularmente estáveis e solúveis, como indicado abaixo na Tabela I.
[000152] Todos os fragmentos scFv foram clonados em um vetor de expressão para a produção periplasmática em E. coli (Krebber et al., J. Immunol. Methods 201:35-55 (1997)).
[000153] Além dos derivados de anticorpos de cadeia única (scFvs) descritos acima, os fragmentos Fab correspondentes foram gerados como se segue. Os domínios variáveis de cadeia leve (VL) selecionados foram fusionados à região constante de uma cadeia kapa de Ig humana, enquanto que os domínios variáveis de cadeia pesada (VH) apropriados foram fusionados ao primeiro domínio constante (CH1) (N-terminal) de uma IgG humana. Ambos domínios constantes humanos foram ampliados por PCR a partir de uma biblioteca de cDNA do baço humano e resultou na sequência SEQ ID NO: 14 para CK e SEQ ID NO: 15 para CH1. Experimento 2: Expressão, Produção e Estabilidade de Anticorpos scFv ou Fab Humanizados
[000154] Os plasmídeos que codificam TB-wt, seus derivados humanizados, ou fragmentos Fab foram introduzidos em uma cepa de E. coli apropriada (por exemplo, JM83) para expressão periplasmática. As variantes de scFv também foram expressadas como corpos de inclusão, por exemplo, na cepa BL21 de E. coli. Os anticorpos de cadeia única funcionais foram obtidos por redobra de corpos de inclusão e subsequente purificação, por exemplo, por filtração em gel.
[000155] Os rendimentos da expressão após a expressão periplasmática dos scFv's ficaram na faixa entre 0,5 mg até 12 mg por litro de cultura sob condições de cultura laboratoriais usuais (meio dYT, com aproximadamente 3 horas de tempo de indução a 30 oC, agitação a 200 rpm) com frascos para agitação convencionais. Geralmente, observou-se que, conforme esperado a partir de análise anterior das estruturas selecionadas quanto à estabilidade e solubilidade (Auf der Maur et al., Methods 34:215-224 (2004)), quanto mais parecida a sequência de um derivado humanizado for com a sequência da estrutura do aceptor (FW2.3), mais alto é o rendimento obtido após a expressão em bactérias. Por exemplo, o rendimento obtido a partir de TB-B é muito melhor do que aquele obtido a partir da expressão de TB-A. De acordo com estas descobertas, reduzir o número de resíduos de aminoácidos diferentes presentes em TB-A teve um efeito positivo sobre os rendimentos da expressão (Figura 3A).
[000156] Outra característica importante dos anticorpos ou derivados de anticorpos da presente invenção é sua solubilidade. A Figura 3B ilustra a superioridade da estrutura TB-A sobre a estrutura do doador (TB-wt) em termos de solubilidade em solução salina tamponada com fosfato. Na filtração em gel analítica, TB-A migra predominantemente em um estado monomérico (pico em 70 mL), enquanto que TB-wt apresente uma forte tendência a formar agregados (pico em 50 mL). Além disso, a solubilidade máxima de TB-A e certos derivados dele foi avaliada por precipitação em PEG (Athat, D.H. et al., JBC 256(23):12108-12117 (1981). Resumidamente, a solubilidade aparente de proteínas em teste foi medida na presença de polietilenoglicol 3000 (PEG 3000). As curvas de solubilidade foram determinadas medindo a concentração de proteína no sobrenadante de misturas de proteína/PEG300 centrifugadas. Todas curvas apresentaram uma dependência linear de log S (mg/mL) em concentração de PEG 3000 (%, p/v). A solubilidade máxima (Smax) de uma proteína em teste foi estimada por extrapolação da regressão linear até 0% de PEG (Tabela I). Para TB-A, a Smax foi calculada como sendo 70 mg/mL. Todas proteínas em teste apresentaram solubilidade excepcionalmente boa. Em uma segunda abordagem, foi aplicado um método denominado cromatografia de auto-interação (SIC) para avaliar a atração e a repulsão intermolecular de TB-A (SEQ ID NO: 40), TB-A Ligante _G2R H_F68L (SEQ ID NO: 33), TB-A H_K43R/F68I (SEQ ID NO: 34) e TB-A H_F68L (SEQ ID NO: 35) em uma concentração de 1 mg/mL em PBS (fosfato 50 mm, pH 6,5, NaCl 150 mM). Neste método, a proteína de interesse é imobilizada sobre uma fase estacionária porosa e recheada em uma coluna. As interações entre a proteína livre (fase móvel) e imobilizada são detectadas como deslocamentos no volume de retenção. O segundo coeficiente de vírion osmótico da proteína, B22, que é uma medida da atração/repulsão intermolecular, foi calculado de acordo com Tessier, P.M. et al., Biophys. J. 82:1620-1632 (2002) (Tabela I). Quanto mais positivo o B22, mais baixa é a atração intermolecular da proteína em teste, e portanto, mais alta é a sua solubilidade. Devido à alta similaridade das sequências das proteínas em teste, presumiu-se que os valores de B22 das diferentes proteínas podem ser comparados diretamente entre si. Tabela I Características de Solubilidade de Derivados de TB-A
[000157] Ainda outra característica relevante dos anticorpos ou derivados de anticorpos da presente invenção é sua alta estabilidade. A estabilidade de proteínas de TB-A, TB-A H_M48LF681 (SEQ ID NO: 31), TB-A Ligante _G2R H_F68L (SEQ ID NO: 33), TB-A H_K43R/F68I (SEQ ID NO: 34) e TB-A H_F68L (SEQ ID NO: 35) foi avaliado determinando a temperatura para o início da desdobra por dicroísmo circular e dispersão da luz a 218 e 292 nm (Tabela II). Neste experimento, TB-A iniciou a desdobrar em uma temperatura de 53 oC, enquanto que seus derivados TB-A H_M48LF681 (SEQ ID NO: 31), TB-A Ligante _G2R H_F68L (SEQ ID NO: 33), TB-A H_K43R/F68I (SEQ ID NO: 34) e TB-A H_F68L (SEQ ID NO: 35) apresentaram estabilidade térmica aumentada (56 e 58 oC). Todas proteínas em teste apresentaram desnaturação irreversível e precipitaram depois de desdobrar, tornando impossível determinar o ponto mediano de transição em um processo reversível, a desdobra foi induzida com cloridrato de guanidina (GdnHCl), para manter as proteínas desdobradas em solução. Nesta abordagem, as máximas de emissões de fluorescência foram determinadas por fluorimetria após a desdobra. Nesta instalação, TB-A apresentou novamente boa estabilidade com um ponto mediano de transição a 2,07 M de GdnHCl. Em linha com os resultados a partir da desdobra térmica, os derivados TB-A Ligante _G2R H_F68L (SEQ ID NO: 33) e TB-A H_K43R/F68I (SEQ ID NO: 34) apresentaram estabilidade aumentada conforme exibida com pontos medianos de transição mais altos, 2,33 e 2,3 M de GdnHCl, respectivamente. Tabela II Características de Estabilidade de Derivados de TB-A
[000158] A estabilidade d e TB-A no soro humano, na urina humana, no líquido corporal vítreo suíno, e no líquido da câmara anterior suína, foi avaliada medindo a atividade de ligação ao TNFα de TB-A depois da incubação por 3 dias a 37 oC no fluido corporal respectivo ou em tampão de ensaio (TBSTM) como um controle positivo. TB-A foi diluído em fluidos corporais até uma concentração final 10 μM. Depois do período de incubação, diluições seriais das amostras foram testadas por ELISA para determinar a constante de ligação Kd de TB-A (Figura 11). Quando se compara as amostras de fluidos corporais com as amostras de TBDTM do controle, um deslocamento da Kd na direção de concentrações mais altas indicaria um decréscimo de proteína ativa durante o período de incubação. Nestes experimentos, entretanto, nenhum deslocamento foi detectável, indicando que a quantidade de TB-A completamente ativo permaneceu constante em cada ensaio com fluido corporal devido a uma alta estabilidade do anticorpo. Experimento 3: Características de Ligação de Derivados de Anticorpos Humanizados
[000159] As propriedades de ligação de todas variantes de scFv humanizadas foram testadas por ELISA em TNFα humano recombinante. As constantes de dissociação Kd para todas variantes ficam dentro de uma faixa entre 0,8 e mais do que 10.000 nM. Parece existir uma correlação inversa entre o grau de homologia à estrutura do aceptor humano e a afinidade do respectivo ligante (Figura 4A). Contudo, algumas variantes de TB-A que contêm mutações na direção da sequência de TB-B apresentam níveis de afinidade por TNFα, que são comparáveis àqueles de TB-A. A Figura 4B ilustra dois derivados com melhor rendimento de expressão de TB-A (comparar com Figura 3A) que apresentam afinidades similares a TB-A quando se compara em ELISA.
[000160] TB-A representa um bom compromisso entre as opções de rendimento da expressão e afinidade. Em termos de afinidade, nenhuma diferença significativa entre cadeia única e formato de fragmento Fab e TB-A foi detectável (dados não ilustrados).
[000161] A afinidade por TNFα e a cinética de ligação também foram determinada para TB-A por ressonância de plasmon de superfície (BIACore), resultando em uma constante de dissociação Kd = 0,8 nM, uma taxa "off" de koff = 4,4 x 10-4/s e uma taxa "on" kon = 5 x 105 s-1M-1. Experimento 4: Ensaio de Citotoxicidade de L929
[000162] A função dos anticorpos ou derivados de anticorpos em neutralizar TNFα in vivo pode ser testada medindo a inibição da citotoxicidade de TNFα contra fibroblastos L929 do camundongo cultivados ou alternativamente contra células de mielossarcoma KYM-1 humano (Tabela III). Os derivados scFv humanizados de Di62 apresentam diferentes eficácias no ensaio com L929, como ilustrado na Figura 5B. Alguns derivados de scFv apresentam valores de CI50 (concentração inibitória para atingir 50% de inibição) na faixa de 5 ng/mL, enquanto que outros não tiveram qualquer efeito nos ensaios com L929. Os dados de ELISA e os resultados do ensaio com L929 nem sempre se correlacionam. Os dados com KYM-1 e os resultados com L929, entretanto, se correlacionaram muito bem, sendo a única diferença que concentrações muito mais altas de TNF humano recombinante e consequentemente também do antagonista foram necessárias para observar um efeito. KYM-1 foi, portanto, usado principalmente para confirmar os resultados com L929. Para uma comparação direta das proteínas em teste, a potência é expressa como um valor relativo normalizado para TB-A (CE50X/CE50TB-A). Em geral, entretanto, os valores de CI50 tornam-se novamente mais altos quanto mais a sequência de um ligante é semelhante à estrutura do aceptor humano (FW2.3). A Figura 5 compara a potência de diferentes derivados de TB-A para bloquear a citoxicidade induzida por TNFα contra células de fibroblastos do camundongo L929. A absorção a 450 nm se correlaciona com a sobrevivência das células.
[000163] TB-A e a IgG anti-hTNFα Infliximab® apresentam um valor de CI50 similar no ensaio com L929, enquanto que a potência de TB-wt para bloquear a citotoxicidade induzida por TNFα humano é significativamente mais baixa (Figura 5A). Quando os derivados de TB- A são comparados com TB-A quanto ao seu potencial para bloquear a citotoxicidade induzida por TNFα, a maioria destes derivados, exceto TB-H43, têm uma eficácia reduzida em L929 (Figura 9B). Tabela III Propriedades Funcionais de Derivados de TB-A
[000164] Em linha com os dados de ELISA, não há qualquer diferença significativa na capacidade de bloquear a citotoxicidade induzida por TNFα entre scFv e o formato Fab de TB-A (Figura 5C). O valor de CI50 do formato Fab de TB-A fica quase um fator de dois acima do valor de CI50 do formato scFv de TB-A (Figura 5B), muito provavelmente como resultado da massa molecular mais ata do fragmento Fab. Experimento 5: Experimentos Animais com Derivados do Anticorpo Anti- TNFα 5.1 Descrição do Experimento
[000165] Para testar a eficácia dos derivados de anticorpos da ESBATech (scFv e Fab) na bioatividade de TNFα humano funcionalmente neutralizadora em uma situação in vivo, foi usado um modelo de rato recém-publicado para monoartrite. Este modelo foi descrito extensivamente por Bolon e outros (vide Bolon et al., Vet. Pathol. 41:235-243 (2004)). Resumidamente, neste modelo animal de artrite, TNFα humano é injetado por via intra-articular dentro da articulação do joelho de ratos Lewis machos. A injeção de TNFα humano leva a uma monoartrite aguda autolimitativa na articulação do joelho. A artrite pode ser quantificada medindo o inchaço da articulação e a pontuação histológica. Consequentemente, a bioatividade dos respectivos antagonistas de TNFα pode ser quantificada pela redução do inchaço da articulação induzido por TNFα e/ou pela redução de parâmetros histológicos da inflamação. 5.2 Materiais e Métodos
[000166] Os atuais estudos foram desenhados para examinar o respectivo potencial de um anticorpo scFv representativo e de um anticorpo Fab representativo da série descrita acima em comparação com o anticorpo comercializado Infliximab (Remicade®) para inibir a bioatividade do TNFα humano em um modelo animal de artrite apropriado. Bolon e outros tinham demonstrado anteriormente que a aplicação intra-articular de 10 microgramas de TNFα humano recombinante dentro da articulação do joelho do rato provoca uma monoartrite aguda autolimitativa que pode ser quantificada por análise macroscópica e microscópica padronizada. Assim sendo, este modelo animal serviu como um sistema ideal para avaliar o efeito terapêutico de derivados de anticorpos aplicados localmente. Dois experimentos foram completados em série (Tabelas IV e V). (1) um estudo básico de eficácia para avaliar o potencial global dos anticorpos para bloquear a monoartrite induzida por TNFα humano; e (2) um estudo de resposta à dose para avaliar a eficácia relativa dos derivados de anticorpos entre 51. As citocinas e os derivados de anticorpos foram aplicados uma vez por injeções separadas, como descrito abaixo. A dose de citocina usada baseou-se na publicação de Bolon e outros, enquanto que a faixa das doses dos derivados de anticorpos baseou-se em dados de cultura de células disponíveis e em conjectura criteriosa. Os experimentos foram conduzidos de acordo com as orientações gerais de cuidados com cobaias.
[000167] Ratos Lewis machos adultos jovens (6-7 semanas de idade e 175-200 g) foram designados aleatoriamente a grupos de tratamento (n = 3/coorte) e alojados de acordo com Bolon et al., Vet. Pathol. 41:235243 (2004).
[000168] As injeções de anestesia e citocina foram realizadas como descrito por Bolon e outros. Para não exceder um volume total injetado por via intra-articular de 50 microlitros, as citocinas e os derivados de anticorpos foram instilados em duas injeções intra-articulares separadas, com o que os 10 microgramas de TNFα humano recombinante foram injetados em 10 microlitros de solução salina tamponada com fosfato (PBS) esterilizada por filtração, e a respectiva dose do respectivo anticorpo foi injetada em 40 microlitros de solução salina tamponada com fosfato (PBS) esterilizada por filtração. Os animais tratados por via intraperitoneal com Infliximab (Remicade®) receberam injeção intraperitoneal com os derivados de anticorpos 3 horas antes da injeção intra-articular de TNFα humano. Em todos animais tratados com anticorpo aplicado por via intra-articular, a respectiva dose de anticorpo foi injetada 5 minutos antes da injeção de TNFα humano. Os animais do controle receberam injeção de 10 microlitros de PBS sem TNFα humano.
[000169] Infliximab (Remicade® usado nos experimentos foi adquirido em uma farmácia suíça oficial. Os anticorpos scFv e Fab (TB-A) específicos para TNFα anti-humano, bem como uma estrutura de anticorpo scFv nulo usada como anticorpo de controle inespecífico no experimento de resposta à dose, foram expressados em E. coli e purificados por métodos usuais. A contaminação com endotoxinas foi mantida abaixo de 10 UE por miligrama de proteína em todas as preparações porque o componente lipossacarídeo é um indutor potente de TNFα.
[000170] O TNFα humano recombinante foi adquirido na PeproTech EC Ltd.
[000171] Momentos antes da injeção do respectivo derivado de anticorpo aplicado por via intraperitoneal ou intra-articular, ou, no caso dos animais de controle, antes da injeção de PBS ou TNFα, o diâmetro da articulação do joelho a receber a injeção foi determinado por meio de um paquímetro-padrão. 48 horas depois da injeção de TNFα (ou PBS nos animais do controle) e momentos antes do sacrifício dos animais, o diâmetro da articulação do joelho que recebeu a injeção foi determinado novamente e o inchaço da articulação foi calculado subtraindo o valor da segunda medição do diâmetro do valor da primeira medição do diâmetro (Figuras 6 e 9).
[000172] 48 horas depois da injeção de TNFα (ou PBS no caso dos animais do controle), os animais foram sacrificados. Na necropsia, os joelhos que receberam a injeção foram separados da pata e da coxa, fixados por imersão em etanol a 70% e prosseguiram para coloração- padrão com hematoxilina e eosina (HE), como descrito por Bolon e outros.
[000173] A análise de pontuação histológica para edição da inflamação da articulação foi realizada como descrito por Bolon e outros. Os critérios da pontuação histológica para avaliação da inflamação da articulação foram aplicados de acordo com Bolon e outros (Figuras 7, 8 e 9).
[000174] Em um primeiro conjunto de experimentos, um anticorpo scFv ESBATech representativo aplicado por via intra-articular, TB-A, e o anticorpo Fab ESBATech aplicado por via intra-articular correspondente, foram comparados quanto à sua capacidade de bloquear a indução da monoartrite aguda com Infliximab (Remicade®) aplicado por via intra-articular e intraperitoneal, de acordo com a Tabela IV: Tabela IV Esquema de Injeção do Experimento 1
[000175] Os resultados obtidos quanto aos efeitos do tratamento sobre a mudança do diâmetro do joelho (como um indicador dos efeitos sobre o inchaço da articulação induzido por TNFα) estão representados na Figura 6. Todos anticorpos bloquearam completamente o inchaço da articulação induzido por TNFα.
[000176] Para avaliação dos efeitos do tratamento sobre a inflamação da articulação, a pontuação histológica das lâminas de tecido corado com HE foi realizada. A inflamação da articulação foi pontuada pelos seguintes critérios (vide Figura 7 para obter exemplos de pontuação representativos): Pontuação 0: normal Pontuação 1: Espessamento brando do revestimento sinovial Pontuação 2: Espessamento do revestimento sinovial e inflamação branda do subrevestimento Pontuação 3: Espessamento do revestimento sinovial e inflamação moderada do subrevestimento
[000177] Os resultados obtidos quanto aos efeitos do tratamento sobre as pontuações de inflamação histopatológica estão ilustrados na Figura 8.
[000178] Foram observados efeitos comparáveis de todos tratamentos sobre as pontuações da inflamação histopatológica.
[000179] Em um segundo conjunto de experimentos, a resposta à dose relativa para os derivados de anticorpos avaliados foi comparada. O anticorpo TB-A scFv ESBATech representativo aplicado por via intraarticular e o anticorpo Fab correspondente do Experimento 1 aplicado por via intra-articular foram comparados com Infliximab (Remicade®) aplicado por via intra-articular e intraperitoneal e um anticorpo scFv não- relacionado carente de qualquer atividade de ligação ao TNFα humano em uma faixa de dose mais ampla e diferente, em comparação com o Experimento 1, de acordo com a Tabela V. Tabela V Esquema de Injeção do Experimento 2
[000180] Os resultados obtidos quanto aos efeitos do tratamento sobre a mudança do diâmetro do joelho (como um indicador dos efeitos sobre o inchaço da articulação induzido por TNFα estão representados na Figura 9.
[000181] Os resultados obtidos quanto aos efeitos do tratamento sobre as pontuações de inflamação histopatológica estão ilustrados na Figura 10.
[000182] Resumindo, o scFv ESBATech anti-TNFα representativo e o anticorpo Fab ESBATech anti-TNFα representativo foram altamente eficientes em bloquear a monoartrite induzida pelo TNFα humano após administração local (intra-articular).
[000183] Embora as modalidades atualmente preferidas da invenção tenham sido ilustradas e descritas, deve-se entender distintamente que a invenção não está limitada a elas, mas pode ter várias modalidades diferentes e praticadas dentro do âmbito as reivindicações que se seguem.
Claims (10)
1. Anticorpo ou fragmento de anticorpo estável e solúvel que se liga especificamente ao TNFα, caracterizado pelo fato de que compreende um domínio variável de cadeia leve (VL) de SEQ ID NO: 1 que é combinada com um domínio variável de cadeia pesada (VH) de SEQ ID NO: 2
2. Anticorpo ou fragmento de anticorpo, de acordo com a reivindicação 1, caracterizado pelo fato de que é um anticorpo scFv, em que os domínios VL e VH são conectados por um ligante.
3. Anticorpo scFv, de acordo com a reivindicação 2, caracterizado pelo fato de que compreende um arranjo de sequências VL-ligante-VH.
4. Anticorpo scFv, de acordo com a reivindicação 2 ou 3, caracterizado pelo fato de que o ligante apresenta a sequência de SEQ ID NO: 10.
5. Fragmento de anticorpo, de acordo com a reivindicação 1, caracterizado pelo fato de que é um fragmento Fab, em que o domínio VL está fusionado à região constante de uma cadeia kapa de Ig humana, o domínio VH está fusionado ao domínio CH1 de uma IgG humana, e os dois polipeptídeos de fusão estão ligados por uma ponte dissulfeto entre as cadeias.
6. Anticorpo ou fragmento de anticorpo, de acordo com qualquer uma das reivindicações 1 a 5, caracterizado pelo fato de que é marcado ou quimicamente modificado.
7. Anticorpo ou fragmento de anticorpo, de acordo com qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de que é como um produto farmacêutico.
8. Uso de um anticorpo ou fragmento de anticorpo como definido em qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de que é para o preparo de um medicamento para o tratamento de doenças associadas ao TNFα ou como diagnóstico in vitro para detecção de doenças associadas ao TNFα.
9. Uso, de acordo com a reivindicação 7, caracterizado pelo fato de que a doença associada ao TNFα é osteoartrite, síndrome do olho seco, uveíte, doenças inflamatórias que afetam a pele, psoríase ou doença inflamatória intestinal.
10. Composição diagnóstica ou terapêutica, caracterizada pelo fato de que compreende um anticorpo como definido em qualquer uma das reivindicações 1 a 6, em combinação com um veículo, diluente ou excipiente farmaceuticamente aceitável.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US68797105P | 2005-06-07 | 2005-06-07 | |
| US60/687,971 | 2005-06-07 | ||
| US78535306P | 2006-03-23 | 2006-03-23 | |
| US60/785,353 | 2006-03-23 | ||
| PCT/CH2006/000300 WO2006131013A2 (en) | 2005-06-07 | 2006-06-06 | STABLE AND SOLUBLE ANTIBODIES INHIBITING TNFα |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0611765A2 BRPI0611765A2 (pt) | 2011-12-20 |
| BRPI0611765B1 true BRPI0611765B1 (pt) | 2022-09-27 |
Family
ID=37193351
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0611765-1A BRPI0611765B1 (pt) | 2005-06-07 | 2006-06-06 | Anticorpo ou fragmento de anticorpo estável e solúvel que se liga especificamente ao tnf-alfa seus usos e composição diagnóstica ou terapêutica |
Country Status (21)
| Country | Link |
|---|---|
| US (5) | US8067547B2 (pt) |
| EP (3) | EP2390267B1 (pt) |
| JP (2) | JP5089582B2 (pt) |
| KR (2) | KR101457223B1 (pt) |
| CN (2) | CN102924597A (pt) |
| AU (1) | AU2006255415B2 (pt) |
| BR (1) | BRPI0611765B1 (pt) |
| CA (1) | CA2609999C (pt) |
| DK (1) | DK2390267T3 (pt) |
| ES (1) | ES2424042T3 (pt) |
| HK (1) | HK1218653A1 (pt) |
| HR (1) | HRP20130632T1 (pt) |
| IL (2) | IL187503A0 (pt) |
| MX (1) | MX2007015280A (pt) |
| NZ (1) | NZ563580A (pt) |
| PH (1) | PH12012500758B1 (pt) |
| PL (1) | PL2390267T3 (pt) |
| PT (1) | PT2390267E (pt) |
| RS (1) | RS52861B (pt) |
| RU (1) | RU2415151C2 (pt) |
| WO (1) | WO2006131013A2 (pt) |
Families Citing this family (95)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7538195B2 (en) * | 2002-06-14 | 2009-05-26 | Immunogen Inc. | Anti-IGF-I receptor antibody |
| NZ563580A (en) | 2005-06-07 | 2010-09-30 | Esbatech An Alcon Biomedical R | Stable and soluble antibodies inhibiting TNFaplha |
| AU2016200367B2 (en) * | 2006-07-10 | 2017-10-12 | Novartis Ag | scFv antibodies which pass epithelial and/or endothelial layers |
| JP2009542232A (ja) * | 2006-07-10 | 2009-12-03 | エスバテック・アーゲー | 上皮および/または内皮層を通過するscFv抗体 |
| IN2009DN05758A (pt) | 2007-03-12 | 2015-07-24 | Esbatech Ag | |
| CA2682292A1 (en) * | 2007-03-30 | 2008-10-09 | Medimmune, Llc | Aqueous formulation comprising an anti-human interferon alpha antibody |
| US20090074780A1 (en) * | 2007-06-25 | 2009-03-19 | David Urech | Methods of modifying antibodies, and modified antibodies with improved functional properties |
| KR101530723B1 (ko) | 2007-06-25 | 2015-06-22 | 에스바테크 - 어 노바티스 컴파니 엘엘씨 | 단일 쇄 항체의 서열에 기초한 공학처리 및 최적화 |
| KR20100084623A (ko) * | 2007-09-25 | 2010-07-27 | 인터벳 인터내셔널 비.브이. | 골관절염 치료용 백신 |
| AU2008323206B2 (en) * | 2007-11-12 | 2014-08-14 | U3 Pharma Gmbh | AXL antibodies |
| EP2243031B1 (en) * | 2008-01-21 | 2012-05-30 | Janssen Biotech, Inc. | Methods of predicting antibody solubility |
| RU2010136988A (ru) * | 2008-02-05 | 2012-03-20 | Деленекс Терапьютикс Аг (Ch) | Антигенсвязывающие полипептиды против дегенерации хряща |
| AU2016273957C1 (en) * | 2008-06-25 | 2019-04-18 | Novartis Ag | STABLE AND SOLUBLE ANTIBODIES INHIBITING TNFa |
| MX345039B (es) * | 2008-06-25 | 2017-01-16 | Esbatech Alcon Biomed Res Unit | Anticuerpos estables y solubles que inhiben el tnfa. |
| PL3241843T3 (pl) | 2008-06-25 | 2021-12-27 | Novartis Ag | Optymalizacja rozpuszczalności cząsteczek immunowiążących |
| PT2752428T (pt) * | 2008-06-25 | 2020-02-14 | Novartis Ag | Humanização de anticorpos de coelho com utilização de um framework de anticorpos universal |
| CN104004094B (zh) * | 2008-06-25 | 2017-09-22 | 艾斯巴技术-诺华有限责任公司 | 使用通用抗体构架进行的兔抗体的人源化 |
| WO2010006454A2 (en) | 2008-06-30 | 2010-01-21 | Esbatech, An Alcon Biomedical Research Unit Llc | Functionalized polypeptides |
| MX2011000009A (es) | 2008-07-10 | 2011-08-15 | Esbatech Alcon Biomed Res Unit | Metodos y composiciones para la administracion mejorada de macromoleculas. |
| BRPI1013428A2 (pt) | 2009-05-11 | 2019-07-02 | U3 Pharma Gmbh | anticorpos humanizados para axl |
| EP2270053A1 (en) * | 2009-05-11 | 2011-01-05 | U3 Pharma GmbH | Humanized AXL antibodies |
| WO2011127141A1 (en) * | 2010-04-07 | 2011-10-13 | Abbott Laboratories | TNF-α BINDING PROTEINS |
| AR083495A1 (es) | 2010-10-22 | 2013-02-27 | Esbatech Alcon Biomed Res Unit | Anticuerpos estables y solubles |
| ES2866674T3 (es) | 2010-11-12 | 2021-10-19 | Nektar Therapeutics | Conjugados de una fracción de IL-2 y un polímero |
| AR084210A1 (es) * | 2010-12-08 | 2013-05-02 | Abbott Lab | PROTEINAS DE UNION AL TNF-a |
| US12466897B2 (en) | 2011-10-10 | 2025-11-11 | Xencor, Inc. | Heterodimeric human IgG1 polypeptides with isoelectric point modifications |
| SG10201604104PA (en) | 2011-10-25 | 2016-07-28 | Prothena Therapeutics Ltd | Antibody formulations and methods |
| CA2888583C (en) | 2012-11-05 | 2022-03-29 | Delenex Therapeutics Ag | Binding members to il-1 beta |
| UA117466C2 (uk) | 2012-12-13 | 2018-08-10 | Мерк Шарп Енд Доме Корп. | СТАБІЛЬНИЙ СКЛАД У ВИГЛЯДІ РОЗЧИНУ АНТИТІЛА ДО IL-23p19 |
| PL2934582T3 (pl) * | 2012-12-21 | 2020-08-10 | Ichnos Sciences SA | Formulacja przeciwciała anty-her2 |
| US9605084B2 (en) | 2013-03-15 | 2017-03-28 | Xencor, Inc. | Heterodimeric proteins |
| CA2898100C (en) | 2013-01-14 | 2023-10-10 | Xencor, Inc. | Novel heterodimeric proteins |
| US11053316B2 (en) | 2013-01-14 | 2021-07-06 | Xencor, Inc. | Optimized antibody variable regions |
| CN105263476A (zh) | 2013-03-13 | 2016-01-20 | 库尔制药开发公司 | 用于治疗炎症的免疫修饰性颗粒 |
| CA2902739C (en) * | 2013-03-15 | 2022-11-22 | Xencor, Inc. | Heterodimeric proteins |
| US10858417B2 (en) | 2013-03-15 | 2020-12-08 | Xencor, Inc. | Heterodimeric proteins |
| EP3052132B1 (en) | 2013-09-30 | 2020-07-29 | Beth Israel Deaconess Medical Center, Inc. | Antibody therapies for human immunodeficiency virus (hiv) |
| WO2015057910A1 (en) | 2013-10-16 | 2015-04-23 | Oncobiologics, Inc. | Buffer formulations for enhanced antibody stability |
| JP6620094B2 (ja) * | 2013-11-26 | 2019-12-11 | ザ ブリガム アンド ウィメンズ ホスピタル インコーポレイテッドThe Brigham and Women’s Hospital, Inc. | 免疫応答を調節するための組成物および方法 |
| JP6618912B2 (ja) | 2013-12-20 | 2019-12-11 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 改良された、組換えポリペプチド作製方法 |
| MX373485B (es) | 2014-03-26 | 2020-04-27 | Cell Medica Switzerland Ag | Miembros de unión al factor de necrosis tumoral (tnf) alfa. |
| JP6775422B2 (ja) | 2014-03-28 | 2020-10-28 | ゼンコー・インコーポレイテッドXencor、 Inc. | Cd38及びcd3に結合する二重特異性抗体 |
| EP2946767B1 (en) | 2014-05-23 | 2016-10-05 | Ares Trading S.A. | Liquid pharmaceutical composition |
| EP3050557A1 (en) | 2014-05-23 | 2016-08-03 | Ares Trading S.A. | Liquid pharmaceutical composition |
| ES2572919T3 (es) | 2014-05-23 | 2016-06-03 | Ares Trading S.A. | Composición farmacéutica líquida |
| BR112017011166A2 (pt) | 2014-11-26 | 2018-02-27 | Xencor, Inc. | anticorpos heterodiméricos que se ligam a cd3 e cd38 |
| US10259887B2 (en) | 2014-11-26 | 2019-04-16 | Xencor, Inc. | Heterodimeric antibodies that bind CD3 and tumor antigens |
| CN110894240B (zh) | 2014-11-26 | 2022-04-15 | 森科股份有限公司 | 结合cd3和肿瘤抗原的异二聚体抗体 |
| EP3247718B1 (en) | 2015-01-21 | 2021-09-01 | Outlook Therapeutics, Inc. | Modulation of charge variants in a monoclonal antibody composition |
| MX391086B (es) | 2015-06-24 | 2025-03-21 | Hoffmann La Roche | Anticuerpos anti-receptor de transferrina con afinidad diseñada. |
| AR106189A1 (es) | 2015-10-02 | 2017-12-20 | Hoffmann La Roche | ANTICUERPOS BIESPECÍFICOS CONTRA EL A-b HUMANO Y EL RECEPTOR DE TRANSFERRINA HUMANO Y MÉTODOS DE USO |
| NZ741067A (en) | 2015-10-02 | 2023-07-28 | Hoffmann La Roche | Bispecific anti-human cd20/human transferrin receptor antibodies and methods of use |
| AU2016335860B2 (en) | 2015-10-08 | 2023-08-10 | Nektar Therapeutics | Combination of an IL-2Rbeta-selective agonist and a long-acting IL-15 agonist |
| US11229702B1 (en) | 2015-10-28 | 2022-01-25 | Coherus Biosciences, Inc. | High concentration formulations of adalimumab |
| ES2815224T3 (es) | 2015-11-06 | 2021-03-29 | Promise Proteomics | Un método para cuantificar anticuerpos terapéuticos |
| ES2716900T3 (es) * | 2015-11-06 | 2019-06-17 | Promise Advanced Proteomics | Un método para cuantificar anticuerpos anti-TNF |
| JP7058219B2 (ja) | 2015-12-07 | 2022-04-21 | ゼンコア インコーポレイテッド | Cd3及びpsmaに結合するヘテロ二量体抗体 |
| CN109563161A (zh) | 2016-02-03 | 2019-04-02 | 安口生物公司 | 用于提高抗体稳定性的缓冲制剂 |
| SMT202000706T1 (it) | 2016-03-17 | 2021-01-05 | Tillotts Pharma Ag | Anticorpi anti-tnf alfa e frammenti funzionali di essi |
| JP6978427B2 (ja) | 2016-03-17 | 2021-12-08 | ヌマブ セラピューティクス アクチェンゲゼルシャフト | 抗TNFα抗体とその機能性フラグメント |
| WO2017158084A1 (en) | 2016-03-17 | 2017-09-21 | Numab Innovation Ag | ANTI-TNFα-ANTIBODIES AND FUNCTIONAL FRAGMENTS THEREOF |
| CN108884156B (zh) | 2016-03-17 | 2021-10-01 | 努玛创新有限公司 | 抗TNFα抗体及其功能片段 |
| EP3219727B1 (en) | 2016-03-17 | 2020-12-16 | Tillotts Pharma AG | Anti-tnf alpha-antibodies and functional fragments thereof |
| SI3468586T1 (sl) | 2016-06-14 | 2025-01-31 | Xencor, Inc. | Bispecifična protitelesa za zaviralce kontrolnih točk |
| WO2018005706A1 (en) | 2016-06-28 | 2018-01-04 | Xencor, Inc. | Heterodimeric antibodies that bind somatostatin receptor 2 |
| EP3554485B9 (en) | 2016-12-14 | 2023-09-27 | Biora Therapeutics, Inc. | Treatment of a disease of the gastrointestinal tract with a jak inhibitor and devices |
| EP3554346B1 (en) | 2016-12-14 | 2024-01-31 | Biora Therapeutics, Inc. | Treatment of a disease of the gastrointestinal tract with an immunosuppressant |
| CA3046019A1 (en) | 2016-12-14 | 2018-06-21 | Progenity Inc. | Treatment of a disease of the gastrointestinal tract with a tlr modulator |
| WO2018112232A1 (en) | 2016-12-14 | 2018-06-21 | Progenity Inc. | Treatment of a disease of the gastrointestinal tract with an il-12/il-23 inhibitor released using an ingestible device |
| EP3600414A1 (en) | 2017-03-30 | 2020-02-05 | Progenity Inc. | Treatment of a disease of the gastrointestinal tract with il-10 or an il-10 agonist |
| AU2018263868A1 (en) | 2017-05-02 | 2019-12-12 | Merck Sharp & Dohme Llc | Formulations of anti-LAG3 antibodies and co-formulations of anti-LAG3 antibodies and anti-PD-1 antibodies |
| JOP20190260A1 (ar) | 2017-05-02 | 2019-10-31 | Merck Sharp & Dohme | صيغ ثابتة لأجسام مضادة لمستقبل الموت المبرمج 1 (pd-1) وطرق استخدامها |
| EP3409688A1 (en) | 2017-05-31 | 2018-12-05 | Tillotts Pharma Ag | Topical treatment of inflammatory bowel disease using anti-tnf-alpha antibodies and fragments thereof |
| EP3456739A1 (en) | 2017-09-19 | 2019-03-20 | Tillotts Pharma Ag | Use of anti-tnfalpha antibodies for treating wounds |
| EP3459529A1 (en) | 2017-09-20 | 2019-03-27 | Tillotts Pharma Ag | Preparation of sustained release solid dosage forms comprising antibodies by spray drying |
| ES2938608T3 (es) | 2017-09-20 | 2023-04-13 | Tillotts Pharma Ag | Método para preparar una forma farmacéutica sólida que comprende anticuerpos mediante granulación en húmedo, extrusión y esferonización |
| ES2938609T3 (es) | 2017-09-20 | 2023-04-13 | Tillotts Pharma Ag | Preparación de formas farmacéuticas sólidas que comprenden anticuerpos mediante estratificación de solución/suspensión |
| JP2021502100A (ja) | 2017-11-08 | 2021-01-28 | ゼンコア インコーポレイテッド | 新規抗pd−1配列を用いた二重特異性および単一特異性抗体 |
| US12582809B2 (en) | 2018-01-26 | 2026-03-24 | Bt Bidco, Inc. | Treatment of a disease of the gastrointestinal tract with a PDE4 inhibitor |
| WO2019195623A2 (en) | 2018-04-04 | 2019-10-10 | Xencor, Inc. | Heterodimeric antibodies that bind fibroblast activation protein |
| US11845788B2 (en) | 2018-05-22 | 2023-12-19 | Beth Israel Deaconess Medical Center, Inc. | Antibody therapies for human immunodeficiency virus (HIV) |
| KR102885113B1 (ko) | 2018-10-18 | 2025-11-13 | 머크 샤프 앤드 돔 엘엘씨 | 항-rsv 항체의 제제 및 그의 사용 방법 |
| CN120842406A (zh) | 2018-10-31 | 2025-10-28 | 默沙东有限责任公司 | 抗人pd-1抗体晶体及其使用方法 |
| CN113316458B (zh) | 2018-11-07 | 2024-08-02 | 默沙东有限责任公司 | 抗lag3抗体和抗pd-1抗体的共制剂 |
| WO2020106713A1 (en) * | 2018-11-21 | 2020-05-28 | Beth Israel Deaconess Medical Center, Inc. | Antibody therapies for human immunodeficiency virus (hiv) |
| WO2020114616A1 (en) | 2018-12-07 | 2020-06-11 | Tillotts Pharma Ag | Topical treatment of immune checkpoint inhibitor induced diarrhoea, colitis or enterocolitis using antibodies and fragments thereof |
| JP7525499B2 (ja) | 2019-01-31 | 2024-07-30 | ヌマブ セラピューティクス アクチェンゲゼルシャフト | TNFα及びIL-17Aに対する特異性を有する多重特異性抗体、IL-17Aを標的とする抗体、及びそれらの使用方法 |
| KR102735988B1 (ko) | 2019-02-18 | 2024-12-03 | 일라이 릴리 앤드 캄파니 | 치료 항체 제제 |
| UA128825C2 (uk) | 2019-03-01 | 2024-10-30 | Ксенкор, Інк. | Гетеродимерні антитіла, що зв'язують enpp3 та cd3 |
| CN111909267B (zh) * | 2019-05-07 | 2022-03-25 | 北京天成新脉生物技术有限公司 | 低免疫原性抗TNF-α人源化单克隆抗体TCX063及其应用 |
| WO2021231976A1 (en) | 2020-05-14 | 2021-11-18 | Xencor, Inc. | Heterodimeric antibodies that bind prostate specific membrane antigen (psma) and cd3 |
| CA3192204A1 (en) | 2020-08-19 | 2022-02-24 | Xencor, Inc. | Anti-cd28 and/or anti-b7h3 compositions |
| JP2024511319A (ja) | 2021-03-09 | 2024-03-13 | ゼンコア インコーポレイテッド | Cd3及びcldn6に結合するヘテロ二量体抗体 |
| JP2024509274A (ja) | 2021-03-10 | 2024-02-29 | ゼンコア インコーポレイテッド | Cd3及びgpc3に結合するヘテロ二量体抗体 |
| AU2024241638A1 (en) | 2023-03-28 | 2025-10-09 | Tillotts Pharma Ag | Solid oral dosage form comprising antibodies for sustained release in the lower gastrointestinal tract |
Family Cites Families (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2000318A (en) | 1933-05-22 | 1935-05-07 | James H Cannon | Cord connecter |
| US2200203A (en) | 1938-12-16 | 1940-05-07 | William W Heintz | Legend sheet and method of application |
| US5672347A (en) * | 1984-07-05 | 1997-09-30 | Genentech, Inc. | Tumor necrosis factor antagonists and their use |
| US5225539A (en) * | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| US6548640B1 (en) * | 1986-03-27 | 2003-04-15 | Btg International Limited | Altered antibodies |
| US5530101A (en) * | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US20030225254A1 (en) * | 1989-08-07 | 2003-12-04 | Rathjen Deborah Ann | Tumour necrosis factor binding ligands |
| US5644034A (en) * | 1989-08-07 | 1997-07-01 | Peptide Technology Ltd. | Tumour necrosis factor binding ligands |
| GB8928874D0 (en) * | 1989-12-21 | 1990-02-28 | Celltech Ltd | Humanised antibodies |
| US5859205A (en) * | 1989-12-21 | 1999-01-12 | Celltech Limited | Humanised antibodies |
| GB9109645D0 (en) | 1991-05-03 | 1991-06-26 | Celltech Ltd | Recombinant antibodies |
| US6277969B1 (en) | 1991-03-18 | 2001-08-21 | New York University | Anti-TNF antibodies and peptides of human tumor necrosis factor |
| US5919452A (en) | 1991-03-18 | 1999-07-06 | New York University | Methods of treating TNFα-mediated disease using chimeric anti-TNF antibodies |
| EP1400536A1 (en) * | 1991-06-14 | 2004-03-24 | Genentech Inc. | Method for making humanized antibodies |
| US5198030A (en) | 1991-06-18 | 1993-03-30 | E. I. Du Pont De Nemours And Company | Bead edge guide for use in slide-bead coating |
| ES2159529T5 (es) * | 1993-03-05 | 2011-03-09 | Bayer Corporation | Anticuerpos monoclonales humanos anti-tnf alfa. |
| US6090382A (en) * | 1996-02-09 | 2000-07-18 | Basf Aktiengesellschaft | Human antibodies that bind human TNFα |
| DK0929578T3 (da) | 1996-02-09 | 2003-08-25 | Abbott Lab Bermuda Ltd | Humane antistoffer, der binder human TNFalfa |
| US6171586B1 (en) * | 1997-06-13 | 2001-01-09 | Genentech, Inc. | Antibody formulation |
| EP0999853B1 (en) * | 1997-06-13 | 2003-01-02 | Genentech, Inc. | Stabilized antibody formulation |
| US6177077B1 (en) | 1999-02-24 | 2001-01-23 | Edward L. Tobinick | TNT inhibitors for the treatment of neurological disorders |
| US20030185826A1 (en) | 1999-02-24 | 2003-10-02 | Tobinick Edward L. | Cytokine antagonists for the treatment of localized disorders |
| EP2392596A3 (en) | 1999-12-28 | 2013-11-27 | ESBATech, an Alcon Biomedical Research Unit LLC | Intrabodies with defined framework that is stable in a reducing environment and applications thereof |
| GB0013810D0 (en) * | 2000-06-06 | 2000-07-26 | Celltech Chiroscience Ltd | Biological products |
| US6406863B1 (en) * | 2000-06-23 | 2002-06-18 | Genetastix Corporation | High throughput generation and screening of fully human antibody repertoire in yeast |
| SG97908A1 (en) * | 2000-08-03 | 2003-08-20 | Inst Data Storage | A method and apparatus for load/unload testing of disk drives |
| US6881407B2 (en) | 2000-08-11 | 2005-04-19 | Ashok Amin | Method for treating hepatitis |
| AU2002359495A1 (en) | 2001-11-30 | 2003-06-17 | Centocor, Inc. | Anti-tnf antibodies, compositions, methods and uses |
| SI2332989T1 (sl) | 2002-05-22 | 2015-06-30 | Esbatech, An Alcon Biomedical Research Unit Llc | Imunoglobulinski bralni okvirji, ki kaĺ˝ejo izboljĺ ano stabilnost v intraceliäśnem okolju, in postopki za njihovo identifikacijo |
| HRP20150037T4 (hr) * | 2003-04-08 | 2022-09-02 | Progenics Pharmaceuticals, Inc. | Farmaceutske formulacije koje sadrže metilnaltrekson |
| NZ563580A (en) * | 2005-06-07 | 2010-09-30 | Esbatech An Alcon Biomedical R | Stable and soluble antibodies inhibiting TNFaplha |
| ZA200710109B (en) * | 2005-06-07 | 2009-10-28 | Esbatech Ag | Stable and soluble antibodies inhibiting TNFALPHA |
| KR101530723B1 (ko) * | 2007-06-25 | 2015-06-22 | 에스바테크 - 어 노바티스 컴파니 엘엘씨 | 단일 쇄 항체의 서열에 기초한 공학처리 및 최적화 |
-
2006
- 2006-06-06 NZ NZ563580A patent/NZ563580A/en not_active IP Right Cessation
- 2006-06-06 JP JP2008515021A patent/JP5089582B2/ja not_active Expired - Fee Related
- 2006-06-06 KR KR1020087000199A patent/KR101457223B1/ko not_active Expired - Fee Related
- 2006-06-06 EP EP11002906.3A patent/EP2390267B1/en active Active
- 2006-06-06 CN CN2012103990292A patent/CN102924597A/zh active Pending
- 2006-06-06 BR BRPI0611765-1A patent/BRPI0611765B1/pt not_active IP Right Cessation
- 2006-06-06 CA CA2609999A patent/CA2609999C/en active Active
- 2006-06-06 RS RS20130309A patent/RS52861B/sr unknown
- 2006-06-06 EP EP06741625A patent/EP1891110A2/en not_active Ceased
- 2006-06-06 EP EP17167592.9A patent/EP3260465A1/en not_active Withdrawn
- 2006-06-06 DK DK11002906.3T patent/DK2390267T3/da active
- 2006-06-06 PT PT110029063T patent/PT2390267E/pt unknown
- 2006-06-06 WO PCT/CH2006/000300 patent/WO2006131013A2/en not_active Ceased
- 2006-06-06 RU RU2007149255/10A patent/RU2415151C2/ru active
- 2006-06-06 KR KR1020147011105A patent/KR101539545B1/ko not_active Expired - Fee Related
- 2006-06-06 PL PL11002906T patent/PL2390267T3/pl unknown
- 2006-06-06 MX MX2007015280A patent/MX2007015280A/es active IP Right Grant
- 2006-06-06 ES ES11002906T patent/ES2424042T3/es active Active
- 2006-06-06 CN CN201510565842.6A patent/CN105153306B/zh not_active Expired - Fee Related
- 2006-06-06 AU AU2006255415A patent/AU2006255415B2/en not_active Ceased
- 2006-06-06 US US11/916,793 patent/US8067547B2/en not_active Expired - Fee Related
-
2007
- 2007-11-20 IL IL187503A patent/IL187503A0/en active IP Right Grant
-
2011
- 2011-09-26 US US13/245,420 patent/US8389693B2/en not_active Expired - Fee Related
-
2012
- 2012-04-18 PH PH12012500758A patent/PH12012500758B1/en unknown
- 2012-07-20 JP JP2012161794A patent/JP5645890B2/ja not_active Expired - Fee Related
- 2012-12-07 US US13/708,500 patent/US8691228B2/en active Active
-
2013
- 2013-07-04 HR HRP20130632TT patent/HRP20130632T1/hr unknown
-
2014
- 2014-02-20 US US14/185,783 patent/US9315572B2/en not_active Expired - Fee Related
-
2015
- 2015-12-21 IL IL243270A patent/IL243270B/en active IP Right Grant
-
2016
- 2016-03-08 US US15/064,067 patent/US9683034B2/en not_active Expired - Fee Related
- 2016-06-24 HK HK16106662.6A patent/HK1218653A1/zh unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0611765B1 (pt) | Anticorpo ou fragmento de anticorpo estável e solúvel que se liga especificamente ao tnf-alfa seus usos e composição diagnóstica ou terapêutica | |
| JP6100463B2 (ja) | TNFαを阻害する安定かつ可溶性の抗体 | |
| CN101233154B (zh) | 抑制TNFα的稳定和可溶的抗体 | |
| AU2016204739C1 (en) | Stable and soluble antibodies inhibiting TNFalpha | |
| AU2013207650B2 (en) | Stable and soluble antibodies inhibiting TNFalpha | |
| AU2011265593B2 (en) | Stable and soluble antibodies inhibiting TNFalpha | |
| HK1164891B (en) | Stable and soluble antibodies inhibiting tnf(alpha) | |
| BR122019023673B1 (pt) | Uso de um anticorpo ou composição compreendendo um imunoligante que se liga especificamente ao tnfalfa humano para o tratamento de uma doença mediada por tnfalfa humano |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09B | Patent application refused [chapter 9.2 patent gazette] | ||
| B12B | Appeal against refusal [chapter 12.2 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 06/06/2006, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 18A ANUIDADE. |
|
| B24J | Lapse because of non-payment of annual fees (definitively: art 78 iv lpi, resolution 113/2013 art. 12) |
Free format text: EM VIRTUDE DA EXTINCAO PUBLICADA NA RPI 2778 DE 02-04-2024 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDA A EXTINCAO DA PATENTE E SEUS CERTIFICADOS, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |