BRPI0707040B1 - Método in vitro de seleção de um composto, método in vitro de previsão da presença de câncer, método de determinação in vitro da eficiência de um tratamento anticancerígeno e uso de um composto - Google Patents
Método in vitro de seleção de um composto, método in vitro de previsão da presença de câncer, método de determinação in vitro da eficiência de um tratamento anticancerígeno e uso de um composto Download PDFInfo
- Publication number
- BRPI0707040B1 BRPI0707040B1 BRPI0707040-3A BRPI0707040A BRPI0707040B1 BR PI0707040 B1 BRPI0707040 B1 BR PI0707040B1 BR PI0707040 A BRPI0707040 A BR PI0707040A BR PI0707040 B1 BRPI0707040 B1 BR PI0707040B1
- Authority
- BR
- Brazil
- Prior art keywords
- netrin
- cancer
- receptor
- dcc
- adenocarcinoma
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/18—Testing for antimicrobial activity of a material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/566—Immunoassay; Biospecific binding assay; Materials therefor using specific carrier or receptor proteins as ligand binding reagents where possible specific carrier or receptor proteins are classified with their target compounds
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/475—Assays involving growth factors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/02—Screening involving studying the effect of compounds C on the interaction between interacting molecules A and B (e.g. A = enzyme and B = substrate for A, or A = receptor and B = ligand for the receptor)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/52—Predicting or monitoring the response to treatment, e.g. for selection of therapy based on assay results in personalised medicine; Prognosis
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- Medicinal Chemistry (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Food Science & Technology (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Cell Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Toxicology (AREA)
- General Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
MÉTODO DE SELEÇÃO DE UM COMPOSTO, MÉTODO IN VITRO DE PREVISÃO DA PRESENÇA DE CÂNCER METASTÁTICO OU CÂNCER AGRESSIVO, MÉTODO DE DETERMINAÇÃO IN VITRO DA EFICIÊNCIA DE UM TRATAMENTO ANTICANCERÍGENO, KIT DE SELEÇÃO, COMPOSTO, MÉTODO DE TRATAMENTO, MÉTODO DE PREVENÇÃO OU DE TRATAMENTO, USO DE UM COMPOSTO, MÉTODO OU USO E USO DO NÍVEL DE EXPRESSÃO DE NETRINA-1. O objeto da presente invenção refere-se a um método in vitro de seleção de compostos anticancerígenos com base na capacidade de interação desses compostos com receptor de netrina-1 e/ou de inibir a dimerização do domínio intracelular do receptor de netrina- 1 expresso em células de tumores. A presente invenção também se refere a um método de previsão da presença de câncer agressivo ou metastático ou de determinação da eficiência de um tratamento anticancerígeno com base na medição do nível de expressão de netrina-1. A presente invenção compreende ainda kits e compostos como medicamento para o tratamento de câncer tal como câncer de mama metastático, com relação à sobreexpressão de netrina-1 pelas células de tumores.
Description
[001] O objeto da presente invenção refere-se a um método in vitro de seleção de compostos anticancerígenos com base na capacidade de interação desses compostos com o receptor de netrina-1 e/ou de inibir a dimerização do domínio intracelular do receptor de netrina-1 expresso em células tumorais. A presente invenção também se refere a um método de previsão da presença de câncer metastático ou de determinação da eficiência de um tratamento anticancerígeno com base na medição do nível de expressão de netrina-1. A presente invenção compreende ainda kits e compostos como medicamento para o tratamento de câncer metastático tal como câncer de mama, com relação à superexpressão de netrina-1 pelas células tumorais.
[002] Demonstrou-se que a netrina-1, uma proteína relativa a laminina difundível, desempenha um papel importante no controle da navegação neuronal durante o desenvolvimento do sistema nervoso 31, por meio de interação com os seus receptores principais, DCC (Excluído em Câncer Colo-Retal) 1, 2, 3e UNC5H 4, 5. Mais recentemente, entretanto, a netrina-1 surgiu como uma molécula completamente diferente que regula a sobrevivência celular. De fato, os receptores de netrina-1 DCC e UNC5H, ou seja, UNC5H1, UNC5H2 e UNC5H3, pertencem à chamada família de dependência de receptores 6, 7. Receptores de dependência formam um grupo de receptores que compartilham a capacidade de indução da morte celular quando expressos em configurações nas quais o seu ligante não está disponível 44. Esses receptores, que também incluem RET 8, β-integrinas 9, Patched 10, neogenina 11, p75NTR 12e o receptor andrógeno 40, compartilham a propriedade funcional de indução da morte celular quando desengatados dos seus ligantes, enquanto a presença do seu ligante bloqueia esta atividade pró- apoptótica. Estes receptores criam, desta forma, estados celulares de dependência sobre os seus ligantes correspondentes 13, 14.
[003] Sugeriu-se que este efeito de dependência age como mecanismo para eliminar células tumorais que se desenvolveriam em ambientes de indisponibilidade de ligantes: proliferação de células tumorais em ambiente celular com presença de ligantes constante e limitada ou migração de células tumorais metastáticas em direção a tecidos em que o ligante não é expresso. Uma vantagem seletiva de uma célula tumoral seria, portanto, a perda da atividade pró-apoptótica dos seus receptores de dependência. Previu- se a partir de telas genéticas que a netrina-1 de C. elegans -UNC6- interagiu com UNC40 e com UNC5 42. Quatro ortólogos de UNC5 foram identificados em mamíferos: concluiu-se que UNC5H1, H2, H3, H4 e UNC40 são o ortólogo do DCC (Excluído em Câncer Colo-Retal) de vertebrados 39. Ao longo desta linha, propôs-se no início dos anos 1990 que DCC é um gene supressor de tumores, cuja expressão é perdida na ampla maioria de cânceres humanos 15, 16. Esta hipótese também se enquadra na recente observação de que genes UNC5H são regulados para baixo na ampla maioria de tumores colo-retais, de forma a sugerir que a perda de genes UNC5H representa uma vantagem seletiva para o desenvolvimento de tumores 17. De forma interessante, em camundongos, tanto a desativação de UNC5H3 quando a superexpressão de netrina-1 no trato gastrointestinal são associadas ao progresso de tumores intestinais 18, 19, de forma a demonstrar intrinsecamente que a perda de receptores de dependência de netrina-1 na patologia humana é um fator causal do progresso de tumores. Embora uma série inicial de relatórios sustentasse o fato de que DCC agiu como supressor de tumores (para análise, vide 29), surgiram dúvidas, principalmente devido à raridade de mutações pontuais na seqüência de codificação de DCC e devido à falta de pré-disposição de tumores em camundongos hemizigóticos DCC 41.
[004] O modelo descrito acima prevê, entretanto, que tanto a perda dos receptores de netrina-1 quanto o ganho de expressão de ligantes (ou seja, expressão autócrina) deverão ser observados em cânceres humanos, pois eles deverão representar vantagens seletivas similares. Esta questão é importante não apenas para conhecimento básico, mas é crucial para a terapia; de fato, inibir a interação extracelular entre receptores de dependência de netrina-1 e netrina-1 poderá representar uma estratégia importante para acionar a regressão de tumores.
[005] É particularmente desejável fornecer meios simples e consistentes de identificação e caracterização de compostos novos que possam ser utilizados para o tratamento de câncer.
[006] Surpreendentemente, os inventores demonstraram em primeiro lugar que, em vez de perder receptores de dependência de netrina-1, a maior parte de tumores de mama metastáticos exibe maior expressão de netrina-1, uma característica que pode ser utilizada em terapia para acionar a morte de tumor metastático.
[007] Caso a sinalização pró-apoptótica de DCC e/ou UNC5H esteja começando a ser documentada, uma questão importante nesta assinatura de morte/vida ditada por DCC, UNC5H e, mais geralmente, pelos outros receptores de dependência conhecidos, é como a presença do ligante inibe a sua atividade pró-apoptótica 50.
[008] Em um segundo momento, os inventores analisaram se a multimerização de DCC e/ou UNC5H induzida por netrina-1 poderia ser a etapa fundamental que inibe a atividade apoptótica de DCC e/ou UNC5H. Surpreendentemente, eles demonstraram que um receptor de netrina-1, tal como DCC e/ou UNC5H, multimeriza-se em resposta a netrina-1, um processo suficiente para inibir a apoptose.
[009] Em um primeiro aspecto, a presente invenção refere-se a um método in vitro de seleção de um composto para a prevenção ou o tratamento de câncer, em que o mencionado método compreende as etapas a seguir de: (a) ter um meio que contenha netrina-1, ou um de seus fragmentos, e um receptor de netrina-1, ou um de seus fragmentos, em que: - a mencionada netrina-1, ou um de seus fragmentos, e o mencionado receptor de netrina-1, ou um de seus fragmentos, são capazes de interagir especificamente juntos para formar um par de ligação; e/ou - a mencionada netrina-1, ou um de seus fragmentos, é capaz de induzir a dimerização ou a multimerização do mencionado receptor de netrina-1, ou um de seus fragmentos, particularmente o domínio intracelular do mencionado receptor de netrina-1; (b) contato do mencionado meio com o composto a ser testado; (c) medição da inibição da interação entre a netrina-1, ou um de seus fragmentos, e o mencionado receptor de netrina-1, ou um de seus fragmentos; e/ou - determinação de se o mencionado composto inibe a dimerização ou multimerização do mencionado receptor de netrina-1, ou um de seus fragmentos, particularmente a dimerização do domínio intracelular do mencionado receptor de netrina-1; e (d) seleção do mencionado composto se: - a medição da etapa (c) demonstrar uma inibição significativa da interação entre a netrina-1, ou um de seus fragmentos, e o receptor de netrina-1, ou um de seus fragmentos, na presença do mencionado composto; e/ou - a determinação na etapa (c) demonstrar uma inibição significativa da dimerização ou multimerização do mencionado receptor de netrina-1, ou um de seus fragmentos, na presença do mencionado composto, particularmente a dimerização do domínio intracelular do mencionado receptor de netrina-1.
[010] Pelas expressões interação entre netrina-1 e o seu receptor de netrina-1, pretende-se designar no presente pedido a interação que resulta na vantagem seletiva para células tumorais de escapar de receptores de dependência de netrina-1 que induziram apoptose, preferencialmente devido ao nível elevado de netrina-1.
[011] Desta forma, a inibição desta interação pode ser obtida, por exemplo, por meio da inibição completa ou parcial da ligação de netrina-1 ao seu receptor, notadamente na presença de um ligante competitivo (tal como um anticorpo que é dirigido a esse domínio de membrana extracelular do mencionado receptor de netrina-1) ou na presença de um composto capaz de formar um complexo específico com a netrina-1 (tal como um domínio de membrana extracelular solúvel do seu receptor de netrina-1, ou uma de suas partes).
[012] Em uma realização preferida, o método de acordo com a presente invenção é caracterizado pelo fato de que o mencionado câncer a ser evitado ou tratado é um câncer em que as células tumorais expressam ou superexpressam netrina-1.
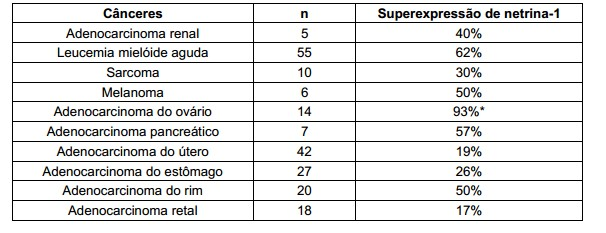
[013] Em outra realização preferida, o método de acordo com a presente invenção é caracterizado pelo fato de que o mencionado câncer a ser evitado ou tratado é selecionado a partir do grupo que consiste de câncer de mama, câncer colo-retal, câncer de pulmão, neuroblastoma, glioma, leucemia mielóide aguda, sarcoma, melanoma, adenocarcinoma do ovário, adenocarcinoma renal, adenocarcinoma pancreático, adenocarcinoma do útero, adenocarcinoma do estômago, adenocarcinoma do rim e adenocarcinoma retal.
[014] Em outra realização preferida, o método de acordo com a presente invenção é caracterizado pelo fato de que o mencionado câncer a ser evitado ou tratado é um câncer metastático ou agressivo.
[015] No método de acordo com a presente invenção, o mencionado receptor de netrina-1 é preferencialmente selecionado a partir do grupo de DCC, UNC5H (particularmente UNC5H1, UNC5H2 e UNC5H3), neogenina e a adenosina A2b, de maior preferência selecionado a partir do grupo de DCC, UNC5H1, UNC5H2 e UNC5H3.
[016] Em outra realização preferida, o método de acordo com a presente invenção é caracterizado pelo fato de que, na etapa (a): - o mencionado fragmento receptor de netrina-1 compreende ou é o domínio extracelular do receptor de netrina-1, ou uma de suas partes capaz de interagir com netrina-1; e/ou - o mencionado fragmento receptor de netrina-1 compreende ou é o domínio intracelular do receptor de netrina-1, ou uma de suas partes capaz de dimerizar-se ou multimerizar-se na presença de netrina-1.
[017] Em outra realização preferida, o método de acordo com a presente invenção é caracterizado pelo fato de que a mencionada netrina-1 e/ou o mencionado receptor de netrina-1 são de mamífero, particularmente de camundongo, rato ou ser humano.
[018] Em um aspecto adicional do método de acordo com a presente invenção, na etapa (a), a mencionada netrina-1 é de galinha.
[019] Em outra realização preferida, o método de acordo com a presente invenção é caracterizado pelo fato de que a mencionada netrina-1 e/ou o mencionado receptor de netrina-1 e/ou o composto a ser testado é marcado por um marcador capaz de ser medido direta ou indiretamente.
[020] Em outra realização preferida, o método de acordo com a presente invenção é caracterizado pelo fato de que, na etapa (c): - a medição da inibição da interação entre netrina-1, ou um de seus fragmentos, e o mencionado receptor de netrina-1, ou um de seus fragmentos, é conduzida por meio de imunoteste (particularmente por meio de ELISA ou de Teste Imunorradiométrico (IRMA)), por meio de Teste de Proximidade de Cintilação (SPA) ou Transferência de Energia de Ressonância por Fluorescência (FRET); e/ou - a dimerização ou multimerização, ou sua inibição, do mencionado receptor de netrina-1, ou um de seus fragmentos, particularmente do domínio intracelular, é conduzida por meio de imunoprecipitação ou FRET.
[021] Em outra realização preferida específica, o método, de acordo com a presente invenção, é caracterizado pelo fato de que, na etapa (a), o mencionado meio contém células que expressam na sua membrana de superfície um receptor de netrina-1 endógeno ou recombinante, particularmente um domínio extracelular recombinante do mencionado receptor de netrina-1.
[022] Em uma realização preferida, o mencionado receptor de netrina-1 recombinante também compreende o domínio intracelular do mencionado receptor de netrina-1.
[023] Em outra realização preferida específica, o método de acordo com a presente invenção é caracterizado pelo fato de que, na etapa (a), o mencionado meio contém células tumorais, preferencialmente células tumorais metastáticas, que expressam de forma endógena o mencionado receptor de netrina-1 na sua superfície de membrana e que expressam ou superexpressam a netrina-1, e em que, na etapa (c), a inibição da interação entre a netrina-1 e o seu receptor de netrina-1 na presença do composto a ser testado é medida por meio da apoptose ou morte celular induzida pela presença do composto a ser testado, preferencialmente analisada utilizando o método de manchas de azul de tripano conforme indicado nos exemplos abaixo.
[024] Em uma realização preferida, as mencionadas células tumorais são selecionadas a partir do grupo que consiste de células 4T1, células CAL51, células T47D, células SKBR7, células IMR32, células GL26 e células H358, notadamente linhagens de células CAL51, tais como linhagem de células CAL51-36, que são muito mais suscetíveis à morte celular em resposta à presença de DCC-EC-Fc.
[025] A presente invenção também se refere a um método in vitro de seleção de um composto para a prevenção ou o tratamento de câncer, em que o mencionado método compreende as etapas a seguir de: (a) ter um meio que contém uma célula de mamífero que expressa um receptor de netrina-1 endógeno ou recombinante, ou um de seus fragmentos que compreende pelo menos o seu domínio intracelular, preferencialmente uma célula tumoral, de maior preferência uma célula que apresente dimerização ou multimerização do seu domínio intracelular de receptor de netrina-1 ou uma célula em que o seu domínio intracelular de receptor de netrina-1 é capaz de dimerizar-se ou multimerizar-se na presença de netrina-1; (b) contato do mencionado meio com o composto a ser testado, em que o meio opcionalmente contém ainda netrina-1, ou um de seus fragmentos capaz de interagir com o domínio extracelular do receptor de netrina-1; (c) determinar se a dimerização ou multimerização do mencionado domínio intracelular de receptor de netrina-1 é inibida na presença do mencionado composto a ser testado; (d) opcionalmente, determinar (por meio do método de azul de tripano, por exemplo) se a presença do composto a ser testado induz a morte celular da mencionada célula de mamífero; e (e) seleção do mencionado composto caso a determinação na etapa (c) demonstre uma inibição significativa da dimerização ou multimerização do domínio intracelular do mencionado receptor de netrina-1 e/ou se a determinação na etapa (d) demonstrar a morte celular da mencionada célula de mamífero.
[026] Em segundo aspecto, a presente invenção refere-se a um método in vitro de previsão da presença de câncer metastático ou câncer agressivo (tal como neuroblastoma) em um paciente que possui um tumor primário a partir de uma biópsia do mencionado paciente que contém células de tumores primários, em que o mencionado método compreende a etapa a seguir de: (a) medição do nível de expressão de netrina-1 na mencionada biópsia.
[027] Em uma realização preferida, o método de previsão de acordo com a presente invenção é caracterizado pelo fato de que, na etapa (a), um aumento do nível de expressão de netrina-1 na mencionada biópsia, em comparação com a expressão de netrina-1 em biópsias de tumores primários não metastáticos ou em biópsias de câncer não agressivas, é indicativa da presença de um câncer metastático ou um câncer agressivo.
[028] Em uma realização preferida, o método de previsão de acordo com a presente invenção é caracterizado pelo fato de que uma razão superior a 2, preferencialmente a 2,5, a 3, a 3,5, a 4, a 4,5 e a 5, entre a expressão de netrina-1 na biópsia a ser testada e na biópsia de referência não metastática ou não agressiva é indicativa da presença de um câncer metastático ou agressivo.
[029] Em um terceiro aspecto, a presente invenção refere-se a um método de determinação in vitro da eficiência de um tratamento anticancerígeno para um paciente ou para selecionar pacientes que reajam a um tratamento anticancerígeno específico, em que o mencionado método compreende as etapas a seguir de: (a) obtenção de uma biópsia de tumor primária do mencionado paciente tratado; e (b) medição do nível de expressão de netrina-1 na mencionada biópsia; em que a eficiência do mencionado tratamento anticancerígeno é correlacionada com a redução da quantidade do nível de expressão de netrina- 1 medido na mencionada biópsia; ou em que os pacientes selecionados que reagem a um tratamento anticancerígeno específico são pacientes em que a quantidade do nível de expressão de netrina-1 medida na sua biópsia caiu após o mencionado tratamento específico.
[030] Em uma realização preferida, o método de determinação in vitro da eficiência de um tratamento anticancerígeno para um paciente ou para selecionar pacientes que reajam a um tratamento anticancerígeno específico é caracterizado pelo fato de que o mencionado câncer induziu a superexpressão de netrina-1 e/ou é um câncer metastático ou agressivo.
[031] Em uma realização preferida, o método de previsão ou de determinação in vitro da eficiência de um tratamento anticancerígeno para um paciente é caracterizado pelo fato de que o produto de expressão de netrina-1 medido é a netrina-1 que codifica RNA, particularmente medida por meio de um método de PCR reversa em tempo real quantitativa, ou pelo fato de que o nível de expressão de netrina-1 que é medido é a medida do nível de proteína de netrina-1, particularmente por meio de método que utiliza anticorpos específicos capazes de reconhecer especificamente a mencionada proteína de netrina-1.
[032] Em uma realização preferida, o método de previsão ou de determinação in vitro da eficiência de um tratamento anticancerígeno para um paciente é caracterizado pelo fato de que o tumor primário é um tumor primário de um câncer selecionado a partir do grupo que consiste de câncer de mama, câncer colo-retal, câncer do pulmão, neuroblastoma, glioma, leucemia mielóide aguda, sarcoma, melanoma, adenocarcinoma do ovário, adenocarcinoma renal, adenocarcinoma pancreático, adenocarcinoma do útero, adenocarcinoma do estômago, adenocarcinoma do rim e adenocarcinoma retal.
[033] Em um outro aspecto, a presente invenção refere-se a um kit de seleção de um composto de prevenção ou tratamento de câncer, em que o mencionado kit compreende: - uma proteína receptora de netrina-1, ou um de seus fragmentos capaz de interagir especificamente com a proteína de netrina-1 para formar um par de ligação, preferencialmente uma proteína recombinante; e - uma proteína de netrina-1, ou um de seus fragmentos capaz de interagir especificamente com a mencionada proteína receptora de netrina-1 para formar um par de ligação, preferencialmente uma proteína recombinante.
[034] O mencionado receptor de netrina-1 também é preferencialmente selecionado a partir do grupo que consiste de DCC, UNC5H (particularmente UNC5H1, UNC5H2 e UNC5H3), neogenina e a adenosina A2b, de maior preferência selecionado a partir do grupo que consiste de DCC, UNC5H1, UNC5H2 e UNC5H3, de maior preferência de mamífero tal como camundongo, rato ou ser humano.
[035] Em uma realização preferida, o mencionado kit compreende células tumorais que expressam o receptor de netrina-1 e que expressam ou superexpressam a netrina-1, particularmente células de linhagem de células tumorais metastáticas, preferencialmente selecionadas a partir do grupo que consiste de células 4T1, células CAL51, células T47D, células SKBR7, células IMR32, células GL26 e células H358, notadamente linhagens de células CAL51, tais como linhagem de células CAL51-36, que são muito mais suscetíveis a morte celular em resposta à presença de DCC-EC-Fc.
[036] Em um outro aspecto, a presente invenção compreende um composto selecionado a partir do grupo que consiste de: - um composto que compreende um domínio extracelular de receptor de netrina-1 ou seu fragmento capaz de inibir especificamente a interação entre a netrina-1 e o mencionado receptor de netrina-1 e/ou capaz de inibir a dimerização ou multimerização do mencionado receptor de netrina-1, ou um de seus fragmentos, particularmente para inibir o domínio intracelular do mencionado receptor de netrina-1; e - um anticorpo monoclonal ou policlonal dirigido especificamente contra netrina-1 ou receptor de netrina-1, particularmente dirigido ao domínio extracelular do mencionado receptor de netrina-1 ou ao fragmento de netrina-1 capaz de interagir com o domínio extracelular do mencionado receptor de netrina-1, como medicamento.
[037] A seqüência de aminoácidos de netrina-1 humana ou receptor de netrina humano tal como UNC5H1, UNC5H2 e UNC5H3 (homólogo de UNC-5 1, 2 e 3 equivalente ao homólogo de UNC-5 A, B e C) é bem conhecida dos técnicos no assunto. Um exemplo destas seqüências de aminoácidos com a localização do seu domínio específico pode ser encontrado no Genbank com o número de acesso AAD09221 ou NP_004813 para netrina-1 humana, NP_588610 para homólogo 1 de receptor de netrina humana UNC-5, Q8IZJ1 para homólogo 2 de receptor de netrina UNC-5 e O95185 para homólogo 3 de UNC-5.
[038] Preferencialmente, nos compostos de acordo com a presente invenção, o mencionado domínio extracelular de receptor de netrina-1 ou seu fragmento é selecionado a partir do grupo de DCC, UNC5H (particularmente UNC5H1, UNC5H2 e UNC5H3), neogenina e a adenosina A2b, selecionada de maior preferência a partir do grupo que consiste de DCC, UNC5H1, UNC5H2 e UNC5H3, de maior preferência a partir de mamífero tal como camundongo, rato ou ser humano.
[039] Em realização de maior preferência, o mencionado composto de acordo com a presente invenção compreende um domínio extracelular de receptor de netrina-1 de DCC e, preferencialmente, o mencionado composto é DCC-EC-Fc ou DCC-5Fbn.
[040] Em outro aspecto, a presente invenção refere-se ao uso do nível de expressão de netrina-1 como marcador para a identificação de câncer metastático em um paciente, preferencialmente de câncer colo-retal ou de mama metastático, em que o de maior preferência é o câncer de mama metastático.
[041] Em outro aspecto, a presente invenção refere-se a um método de tratamento para indução da apoptose ou da morte celular de células tumorais que tenham adquirido a vantagem seletiva de escapar de apoptose induzida por receptores de dependência de netrina-1, preferencialmente por nível elevado de netrina-1, em um paciente que compreende a administração de um composto capaz de inibir a interação entre netrina-1 e o seu receptor de netrina-1, um composto capaz de inibir a dimerização ou a multimerização do receptor de netrina-1, um composto de acordo com a presente invenção ou selecionado por meio do método de acordo com a presente invenção, no mencionado paciente dele necessitado.
[042] Em outro aspecto, a presente invenção refere-se a um método de prevenção ou de tratamento de câncer em pacientes que compreende a administração de um composto de acordo com a presente invenção, ou selecionado por meio do método de acordo com a presente invenção, no mencionado paciente dele necessitado.
[043] A presente invenção também compreende o uso de um composto de acordo com a presente invenção, ou selecionado por meio do método de acordo com a presente invenção, para a fabricação de um medicamento para a prevenção ou o tratamento de câncer em mamíferos, incluindo seres humanos. Preferencialmente, o mencionado câncer é um câncer metastático ou agressivo.
[044] De maior preferência, no método de tratamento ou no uso de um composto de acordo com a presente invenção, o mencionado câncer é selecionado a partir do grupo que consiste de câncer de mama, câncer colo- retal, câncer do pulmão, neuroblastoma, glioma, leucemia mielóide aguda, sarcoma, melanoma, adenocarcinoma do ovário, adenocarcinoma renal, adenocarcinoma pancreático, adenocarcinoma do útero, adenocarcinoma do estômago, adenocarcinoma do rim e adenocarcinoma retal.
[045] De maior preferência, no método de tratamento ou no uso de um composto de acordo com a presente invenção, as células tumorais primárias do mencionado câncer expressam ou superexpressam a netrina-1.
[046] O termo “anticorpo”, da forma utilizada no presente, indica moléculas de imunoglobulina e porções imunologicamente ativas de moléculas de imunoglobulina, ou seja, moléculas que contêm um local de ligação de antígenos que une especificamente (imunorreage com) a proteína de netrina-1 ou o seu receptor.
[047] O termo “anticorpo” compreende anticorpos monoclonais ou policlonais, mas também anticorpos quiméricos ou humanizados.
[048] Uma proteína de netrina-1 isolada ou proteína receptora de netrina-1, ou um de seus fragmentos específicos, pode ser utilizada como imunogene para gerar anticorpos que unem essa proteína utilizando métodos padrão para a preparação de anticorpos monoclonais e policlonais. Pode também ser possível utilizar qualquer fragmento dessas proteínas que contenha pelo menos um determinante antigênico para gerar estes anticorpos específicos.
[049] Um imunogene de proteína é tipicamente utilizado para preparar anticorpos por meio da imunização de um paciente apropriado (tal como coelho, cabra, camundongo ou outro mamífero) com o imunogene. Uma preparação imunogênica apropriada pode conter a mencionada proteína, ou seu fragmento, e pode incluir adicionalmente um adjuvante, tal como adjuvante completo ou incompleto de Freund, ou agente imunoestimulante similar.
[050] Desta forma, anticorpo para uso de acordo com a presente invenção inclui anticorpos policlonais, monoclonais, quiméricos ou humanizados, anticorpos capazes de unir seletivamente ou que se unem seletivamente a um epítopo que contém um polipeptídeo que compreende um espaço contíguo de pelo menos oito a dez aminoácidos de uma seqüência de aminoácidos da proteína de netrina-1 ou seu receptor.
[051] Um agente preferido para detectar e quantificar mRNA ou cDNA que codifica a proteína de netrina-1 é uma sonda de ácido nucleico marcada ou primers capazes de hibridizar este mRNA ou cDNA. A sonda de ácido nucleico pode ser um oligonucleotídeo com pelo menos 10, 15, 30, 50 ou 100 nucleotídeos de comprimento e suficiente para hibridização específica sob condições estringentes no mRNA ou cDNA. O primer de ácido nucleico pode ser um oligonucleotídeo com pelo menos 10, 15 ou 20 nucleotídeos de comprimento e suficiente para hibridizar-se especificamente sob condições estringentes no mRNA ou cDNA, ou sua seqüência complementar.
[052] Um agente preferido para detectar e quantificar a proteína de netrina-1 é um anticorpo capaz de unir-se especificamente a essa proteína, preferencialmente um anticorpo com uma marca detectável. Anticorpos podem ser policlonais ou, de maior preferência, monoclonais. Pode ser utilizado um anticorpo intacto, ou um de seus fragmentos (tal como Fab ou F(ab’)2). O termo “marcado”, com relação à sonda ou anticorpo, destina-se a englobar marcação direta da sonda ou anticorpo por meio de acoplamento (ou seja, ligação física) de substância detectável à sonda ou anticorpo, bem como marcação indireta da sonda ou anticorpo por meio de reatividade com outro reagente que é marcado diretamente. Exemplos de marcação indireta incluem a detecção de um anticorpo primário utilizando um anticorpo secundário marcado de forma fluorescente e marcação final de uma sonda de DNA com biotina, de forma que possa ser detectado com estreptavidina marcada de forma fluorescente.
[053] Métodos in vitro de detecção de possível mRNA incluem, por exemplo, hibridizações Northern e hibridizações in situ. Métodos in vitro de detecção da possível proteína incluem testes imunossorventes ligados por enzimas (ELISAs), Western Blots, imunoprecipitações e imunofluorescência. Os métodos in vitro para detecção de possível cDNA incluem hibridizações Southern.
[054] Quando a presente invenção englobar kits para quantificar o nível de proteína de netrina-1, o kit pode compreender um agente ou composto marcado capaz de quantificar estas proteínas. Os mencionados agentes podem ser embalados em um recipiente apropriado. O kit pode compreender ainda instruções de uso do kit para quantificar o nível da proteína de netrina-1 ou do transcrito de netrina-1.
[055] Em certas realizações do método de acordo com a presente invenção, a determinação dos transcritos de netrina-1 envolve o uso de uma sonda/primer em uma reação em cadeia de polimerase (PCR), tal como PCR âncora ou PCR RACE ou, alternativamente, em uma reação de cadeia de ligação (LCR) (vide, por exemplo, Landegran et al, 1988, Science 241: 23-1080; e Nakazawa et al, 1994, Proc. Natl. Acad. Sci. U. S. A. 91: 360364) ou, alternativamente, PCR RT em tempo real quantitativa. Este método pode incluir as etapas de coleta de uma amostra de células de um paciente, isolamento de ácido nucleico (tal como mRNA) das células da amostra, transformação opcional de mRNA em cDNA correspondente, contato da amostra de ácido nucleico com um ou mais primers que se hibridizam especificamente na netrina-1, mRNA ou seu cDNA correspondente sob condições tais que ocorra a hibridização e a amplificação de cDNA ou mRNA de netrina-1 e a quantificação da presença dos produtos de amplificação. Antecipa-se que PCR e/ou LCR pode ser desejável para uso como uma etapa de amplificação em conjunto com qualquer dos métodos utilizados para quantificar a detecção de ácido nucleico.
[056] Os métodos descritos no presente podem ser realizados, por exemplo, utilizando kits de diagnóstico previamente embalados que compreendem pelo menos uma sonda de ácido nucleico ou conjunto de primer ou reagente de anticorpo descrito no presente, que podem ser convenientemente utilizados, por exemplo, em ambientes clínicos para acompanhamento ou diagnóstico de pacientes.
[057] Por fim, a presente invenção refere-se ao uso de oligonucleotídeos sem sentido ou de iRNA (RNA interferente) específicos do ácido nucleico que codifica a proteína de netrina-1 para a fabricação de um medicamento destinado a evitar ou tratar câncer metastático ou agressivo, em que o mencionado câncer é preferencialmente selecionado a partir do grupo que consiste de câncer de mama, câncer colo-retal, câncer do pulmão, neuroblastoma, glioma, leucemia mielóide aguda, sarcoma, melanoma, adenocarcinoma do ovário, adenocarcinoma renal, adenocarcinoma pancreático, adenocarcinoma do útero, adenocarcinoma do estômago, adenocarcinoma do rim e adenocarcinoma retal.
[058] RNA interferente (iRNA) é um fenômeno no qual um RNA de fita dupla (dsRNA) suprime especificamente a expressão de um gene que contém a sua seqüência de complementaridade. iRNA tornou-se desde então uma ferramenta de pesquisa útil para muitos organismos. Embora o mecanismo por meio do qual dsRNA suprime a expressão genética não seja completamente compreendido, dados experimentais fornecem indicações importantes. Esta tecnologia possui grande potencial como ferramenta de estudo da função genética em células de mamíferos e pode gerar o desenvolvimento de agentes farmacológicos com base em siRNA (RNA interferente pequeno).
[059] Quando administrado a um paciente, um composto de acordo com a presente invenção é preferencialmente administrado como componente de uma composição que compreende opcionalmente um veículo farmaceuticamente aceitável. A composição pode ser administrada oralmente ou por qualquer outra via conveniente e pode ser administrada junto com outro agente biologicamente ativo. A administração pode ser sistêmica ou local. Vários sistemas de fornecimento são conhecidos, tais como encapsulação em lipossomos, micropartículas, microcápsulas, cápsulas etc., e podem ser utilizados para administrar o composto selecionado de acordo com a presente invenção ou seus sais farmaceuticamente aceitáveis.
[060] Os métodos de administração incluem, mas sem limitar-se a intradérmico, intramuscular, intraperitoneal, intravenoso, subcutâneo, intranasal, epidural, oral, sublingual, intranasal, intracerebral, intravaginal, transdérmico, retal, por inalação ou tópico. O modo de administração é deixado a critério do praticante. Na maior parte dos casos, a administração resultará na liberação do composto para o fluxo sangüíneo ou diretamente para o tumor primário.
[061] As composições que compreendem o composto de acordo com a presente invenção ou selecionadas por meio dos métodos de acordo com a presente invenção também fazem parte da presente invenção. Estas composições podem compreender adicionalmente uma quantidade apropriada de um veículo farmaceuticamente aceitável, para fornecer a forma para administração apropriada ao paciente. A expressão “farmaceuticamente aceitável” indica aprovado por uma agência reguladora ou relacionado por uma farmacopéia nacional ou reconhecida para uso em animais, mamíferos e, mais particularmente, em seres humanos. O termo “veículo” designa diluente, adjuvante, excipiente ou veículo com o qual é administrado um composto de acordo com a presente invenção. Esses veículos farmacêuticos podem ser líquidos, tais como água e óleos, incluindo os de petróleo, origem animal, vegetal ou sintética, tais como óleo de amendoim, óleo de soja, óleo mineral, óleo de gergelim e similares. Os veículos farmacêuticos podem ser solução salina, gelatina, amido e similares. Além disso, podem ser utilizados agentes auxiliares, estabilizantes, espessantes, lubrificantes e corantes. As soluções salinas e soluções aquosas de dextrose e glicerol podem também ser empregadas como veículos líquidos, particularmente para soluções injetáveis. Veículos farmacêuticos apropriados também incluem excipientes tais como amido, glicose, lactose, sacarose, gelatina, estearato de sódio, monoestearato de glicerol, cloreto de sódio, leite desnatado seco, glicerol, propileno, glicol, água e similares. Composições de compostos de teste, se desejado, podem também conter pequenas quantidades de agentes umectantes ou emulsificantes, ou agentes tamponadores do pH. As composições de acordo com a presente invenção podem assumir a forma de soluções, suspensões, emulsões, pastilhas, pílulas, comprimidos, cápsulas, cápsulas que contêm líquidos, pós, formulações para liberação sustentada, supositórios, emulsões, aerossóis, pulverizações, suspensões ou qualquer outra forma apropriada para uso. A mencionada composição geralmente é formulada de acordo com procedimentos de rotina na forma de composição farmacêutica adaptada a seres humanos para administração oral ou para administração intravenosa. A quantidade do composto ativo ou aquela que será eficaz no tratamento pode ser determinada por meio de métodos clínicos padrão. Além disso, testes in vitro ou in vivo podem ser opcionalmente empregados para ajudar a identificar faixas de dosagem ideais. A dose precisa a ser empregada também dependerá da via de administração e da seriedade da doença e deve ser decidida de acordo com o julgamento do praticante e com as circunstâncias de cada paciente. Faixas de dosagem apropriadas para administração oral, intranasal, intradérmica ou intravenosa, entretanto, são geralmente de cerca de 0,01 miligramas a cerca de 75 miligramas por quilograma de peso do corpo por dia, de maior preferência cerca de 0,5 miligramas a 5 miligramas por quilograma de peso do corpo por dia.
[062] Deve-se compreender que, embora a presente invenção tenha sido descrita em conjunto com as realizações acima, a descrição abaixo e os exemplos a seguir destinam-se a ilustrar e não a limitar o escopo da presente invenção. Outros aspectos, vantagens e modificações dentro do escopo da presente invenção serão evidentes para os técnicos no assunto ao qual pertence a presente invenção.
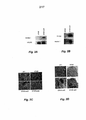
[063] Figura 1A: perfil de expressão de netrina-1 examinado com PCR de transcrição reversa em tempo real quantitativa. PCR Q-RT foi realizada utilizando RNA total extraído de quinze biópsias de tumores primários metastáticos (barra sólida) e quinze não metastáticos (barra aberta) com primers de netrina-1 humana específicos 26e primers correspondentes ao gene TBP humano (Proteína de Ligação TATA). TBP foi utilizado como controle no presente, pois ele exibe fraca variabilidade no nível de mRNA entre tecidos tumorais normais e de mama, conforme descrito em 25. A expressão de netrina- 1 é fornecida como a razão entre a expressão de netrina-1 em cada amostra e a média da expressão de netrina-1 nas amostras não metastáticas.
[064] Figura 1B: realizou-se PCR Q-RT utilizando RNA total extraído de linhagens de células de camundongo 67NR e 4T1 com primers de netrina-1 de camundongo específicos e o gene RPLP0 de camundongo como padrão.
[065] Figuras 2A e 2B: imitações de células 67NR transfectadas ou células 67NR transfectadas de forma estável com netrina-1 (67NR-net) foram submetidas a análise de expressão de netrina-1. A Figura 2A, PCR RT que utiliza primers de netrina-1 de galinha específicos, foi realizada utilizando RNA total extraído de 67NR-net1 e 67NR-imitação. Na Figura 2B, realizou-se Western Blot utilizando anticorpos anti-myc (netrina-1 de galinha) e anti-netrina-1.
[066] Figura 2C: microfotografias dos dois clones 67NR-net1 e 67NR-net2 em comparação com 67NR parental e linhagem celular 4T1.
[067] Figura 2D: células 4T1 metastáticas, dois clones de células controle que possuem resistência a puromicina (67NR1 e 67NR2) e dois clones de células que expressam netrina-1 (67NRnet1 e 67NRnet2) foram injetados em almofada de gordura de dezesseis camundongos (quatro camundongos por tipo de célula) e a metástase foi analisada no ambiente de pulmão. Microfotografias representativas de nódulos subplêuricos e intraparenquimatosos após a injeção dos clones de células correspondentes (4T1, 67NR1, 67NRnet1, 67NRnet2). IPL: lesão intraparenquimatosa, UPL: lesões subplêuricas.
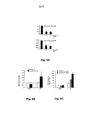
[068] Figura 3A: esquema que representa netrina-1 e seus receptores, DCC e UNC5H.
[069] Figuras 3B, 3C e 3D: análise quantitativa da morte celular em células 67NR e 4T1 utilizando DCC-EC-Fc e IL3-EC-Fc não específico como controle (Figura 3B) em concentrações diferentes (Figura 3C) ou o domínio DCC-5Fbn mais restrito (Figura 3D) como competidor para interação entre netrina-1 e receptor. A morte celular foi quantificada por meio do teste de exclusão de azul tripano (Figuras 3B e 3D) ou por meio de teste de atividade de caspase (Figura 3C). Os desvios padrão são indicados (n = 3).
[070] Figura 4A: medição quantitativa da morte de células CAL51 tratadas com concentração diferente de DCC-EC-Fc por meio do teste de exclusão de azul de tripano.
[071] Figura 4B: análise quantitativa da morte celular monitorada por meio de exclusão de azul de tripano na linhagem de células parentais CAL51 ou na linhagem de células clonais CAL51-36, tratadas ou não com o competidor DCC-EC-Fc em meios de cultivo.
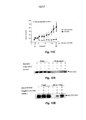
[072] Perfil de expressão de netrina-1 examinada com PCR de transcrição reversa em tempo real quantitativa. PCR Q-RT foi realizada utilizando RNA total extraído de 51 biópsias de tumor. Elas foram obtidas de um paciente com tumores localizados na mama (N0, barra vazia); com envolvimento apenas de nó axilar (N+, barra cinza) e com metástases distantes em diagnóstico (M+, barra sólida). Foram utilizados primers de netrina-1 humanos específicos 39e primers correspondentes ao gene PBGD humano (Proteína de Ligação TATA). PBGD foi utilizado como referência no presente, pois exibe variabilidade fraca em nível de mRNA entre tecidos de tumores de mama e normais, conforme descrito em 38. O outro TBP de referência também foi utilizado com resultados similares (não exibidos). A expressão de netrina-1 é fornecida como a razão entre a expressão de netrina-1 em cada amostra e a média da expressão de netrina-1 nas amostras N0. Foi utilizado teste de significação estatística não paramétrico (Mann-Whitney) e o valor p é indicado.
[073] Figura 6A: DCC-EC-Fc desloca a interação DCC/netrina-1 e UNC5H2/netrina-1. Teste ELISA com DCC-EC-Fc (painel superior) ou UNC5H2-EC-Fc (painel inferior) revestidos e a quantificação de netrina-1 unida utilizando anticorpo anti-netrina-1 na presença de concentração crescente de DCC-EC-Fc.
[074] Figuras 6B e 6C: análise quantitativa da morte celular em células 67NR e 4T1 utilizando DCC-EC-Fc e IL3-EC-Fc não específica como controle. A morte celular foi quantificada pelo teste de exclusão de azul de tripano (Figura 6B) ou por meio de teste de atividade de caspase (Figura 6C). São indicados os desvios padrão (n = 3).
[075] Figura 7A: análise quantitativa da morte celular em células 67NR e 4T1 tratadas com DCC-5Fbn. Teste MTT foi realizado sobre células 67NR ou 4T1 após o tratamento com doses crescentes de DCC-5Fbn (μg/ml). É apresentado o percentual de sobrevivência celular. São indicados desvios padrão (n = 3).
[076] Figuras 7B e 7C: células 4T1-luc foram injetadas por via intravenosa em camundongos BALB/c no dia 0 e PBS ou DCC-5Fbn foram injetados a cada dois dias, uma vez por via intravenosa, uma vez por via intraperitoneal a partir do dia 0. Após treze dias, o desenvolvimento de metástase foi estudado por meio de registro de luminescência (Figuras 7B e 7C) ou de exame de pulmões em um instrumento.
[077] Figura 7B: imagem representativa de registro de luminescência de camundongos tratados com PBS (direita) ou tratados com DCC-5Fbn (esquerda).
[078] Figura 7C: quantificação do sinal luminescente medido por meio do sistema NightOwLB. O número de fótons/pixel/seg foi quantificado em cada animal e um índice de sinal luminescente é fornecido na razão entre o fóton/camundongo médio em camundongos tratados com PBS e o sinal médio detectado em camundongos tratados com DCC-5Fbn. São apresentados dois experimentos independentes (vinte camundongos foram analisados no experimento 1 e oito camundongos no experimento 2).
[079] Foi tirada uma fotografia macroscópica representativa de um pulmão de camundongo tratado com PBS ou de camundongo tratado com DCC-5Fbn (não exibida) e pode ser demonstrada no pulmão de camundongos tratados com PBS.
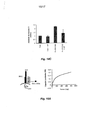
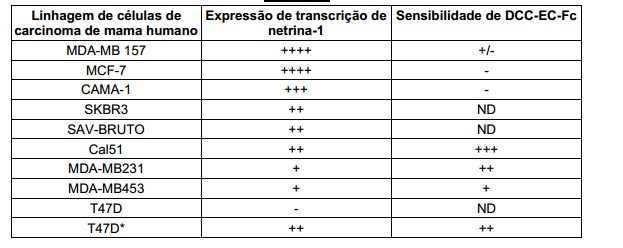
[080] Figura 8A: expressão de netrina-1 examinada por meio de PCR Q-RT utilizando RNA total extraído de 48 linhagens de células tumorais de mama diferentes. A expressão de netrina-1 é fornecida como a razão entre a expressão de netrina-1 e a expressão de HMBS do gene doméstico (hidroximetilbilano sintase) em cada amostra. TBP também foi utilizado como controle no presente e gerou resultados similares. As duas linhagens celulares que foram selecionadas pelo seu alto nível de netrina-1 são indicadas por estrelas.
[081] Figura 8B: indução da morte celular por DCC-5Fbn em linhagens de células SKBR7 e T47D. A morte celular foi quantificada por meio de teste MTT conforme descrito na Figura 4A (painel direito) ou por medição da atividade de caspase, conforme descrito na Figura 3D (painel esquerdo). São indicados os desvios padrão (n = 3).
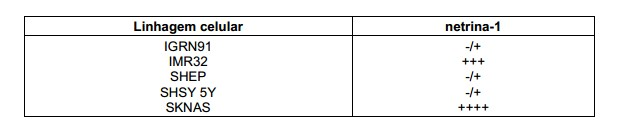
[082] Figura 9A: netrina-1 é um marcador da agressividade em neuroblastoma humano. O perfil de expressão de netrina-1 foi examinado com PCR de transcrição reversa em tempo real quantitativa. PCR Q-RT foi realizada utilizando RNA total extraído de 101 na etapa 4 ou biópsias de neuroblastoma 4s. Os tumores foram de estágio 4 diagnosticado em pacientes que tinham menos de um ano de idade (4 <1 ano) ou estágio 4 diagnosticado em pacientes que tinham mais de um ano de idade (4 >1 ano). Pode-se observar que cânceres com mau prognóstico (estágio 4 >1 ano) exibem superexpressão significativa de netrina-1. Testes de estudantes t foram utilizados e os valores p são indicados.
[083] Figura 9B: células IMR32 que produzem de forma endógena netrina-1 foram tratadas ou não com DCC-5Fbn ou como ILR3 controle (o ectodomínio receptor de interleucina-3) e foram analisadas para determinar a morte celular por meio de medição da atividade de caspase (acima) ou da medição da sobrevivência celular por meio de teste MTT (abaixo). Observe-se que, embora IL3R não possua efeito sobre a morte de células IMR32, DCC-5Fbn induz morte de células IMR32 significativa. Os desvios padrão são indicados (n = 3).
[084] Figura 10A: netrina-1 é superexpressa em uma grande fração de glioma. O perfil de expressão de netrina-1 foi examinado com PCR de transcrição reversa em tempo real quantitativa. Q-RT PCR foi realizada utilizando RNA total extraído de biópsias de oligodendroglioma do estágio II e estágio III e glioblastoma do estágio IV e foi comparado com cérebro humano normal.
[085] Figura 10B: células GL26 que produzem netrina-1 de forma endógena (não exibido) foram tratadas ou não com DCC-5Fbn na presença ou não de quantidade excessiva de netrina-1 recombinante e foram analisadas para determinar a morte celular seja por meio da medição da atividade de caspase (acima) ou por meio de medição da sobrevivência celular por meio de teste MTT (abaixo). Observe-se que DCC-5Fbn induz morte de células GL26 significativa e que este efeito é totalmente inibido pela adição de netrina-1, de forma a demonstrar que o efeito de DCC-5Fbn é diretamente relacionado com a inibição de netrina-1 endógena. Os desvios padrão são indicados (n = 3).
[086] Figura 11A: netrina-1 é superexpressa em uma fração dimensionável de câncer do pulmão humano. O perfil de expressão de netrina- 1 foi examinado com PCR de transcrição reversa em tempo real quantitativa. Q-RT PCR foi realizado utilizando RNA total extraído de biópsias de câncer do pulmão e foi comparado com tecido normal.
[087] Figura 11B: H358 e H460, duas linhagens de células NSCLC, foram adicionalmente utilizadas para testes de morte celular. Células H358 que expressam netrina-1 de forma endógena e células H460 que deixam de exibir expressão de netrina-1 detectável foram tratadas ou não com DCC- 5Fbn na presença ou não de quantidade excessiva de netrina-1 recombinante e foram analisadas para determinar a morte celular por meio de medição da atividade de caspase (acima) ou de medição da sobrevivência celular por meio de teste MTT (abaixo). Observe-se que DCC-5Fbn induz morte de células H358 significativa, mas deixa de exibir efeito sobre células H460. Além disso, o efeito de morte observado em células H358 é totalmente inibido pela adição de netrina-1. Junto com o fato de que as células H460 não são sensíveis a DCC- 5Fbn, estes dados sustentam que células tumorais de pulmão que expressam netrina-1 sofrem apoptose em resposta a DCC-5Fbn. Os desvios padrão são indicados (n = 3).
[088] Figura 11C: DCC-5Fbn inibe o crescimento de tumor H358 xenoenxertado em camundongos brutos. Fêmeas de camundongos nu/nu atímicos com cinco semanas de idade (20 a 22 g de peso do corpo) foram obtidas de Charles River. Os camundongos foram abrigados em gaiolas cobertas com filtro esterilizadas e mantidos em uma instalação de animais livre de patógenos. Células H358 foram implantadas por meio de injeção subcutânea de 5 x 106 células em 200 μl de PBS no flanco esquerdo dos camundongos. Quando os tumores foram estabelecidos, PBS ou 20 μg de DCC-5Fbn foram administrados ao tumor (it) todos os dias (a duração do tratamento é indicada por setas). Os tamanhos de tumores foram medidos por um calibrador durante 41 dias. O volume do tumor foi calculado com a fórmula v = (0,5 * (comprimento*largura2)) ± desvio padrão, *) em seis camundongos tratados com DCC-5Fbn e quatro camundongos tratados com PBS. Observe-se que, embora se tenha demonstrado que tumores tratados com PBS crescem, tumores tratados com DCC-5Fbn exibiram regressão massiva.
[089] Figura 12A: multimerização de DCC na presença de netrina-1 em células HEK293T. Lisatos de células HEK293T transfectadas transitoriamente com construções que expressam HA-DCC e/ou c-myc-DCC junto com construção que expressa netrina-1 ou não foram submetidos a retirada de myc (IP a-myc). A presença de DCC-HA foi revelada com um anticorpo anti-HA.
[090] Figura 12B: dimerização de UNC5H2 na presença de netrina-1 em células HEK293T. A transfecção das células e a preparação de lisato celular foram realizadas como em (A), mas com construções que expressam HA-Unc5H2 e/ou Marca M2-UNC5H2. Lisatos celulares foram submetidos a retirada de Marca M2 (IP a-Marca). A presença de HA-UNC5H2 foi revelada com um anticorpo anti-HA. Total: Western Blot sobre o lisato antes da retirada.
[091] Figura 13A: representação esquemática de construções de fusão de Fv2e-UNC5H2 que exibem as duas construções (um HA marcado, o outro c-myc marcado) utilizadas para validar o sistema de dimerização artificial.
[092] Figura 13B: lisatos de células HEK293T transfectadas transitoriamente com HA marcado por Fv2E-UNC5H2 ou c-myc com ou sem a droga de dimerização (AP20187) foram submetidos a retirada de c-myc (IP a- myc). Total: Western Blot sobre lisato antes da retirada. A presença de HA- Fv2E-UNC5H2 foi revelada com anticorpo anti-HA.
[093] Figura 14A: a morte celular induzida por DCC é inibida por meio de dimerização induzida por AP20187, conforme medido por meio de exclusão de azul de tripano. Células HEK293T foram transfectadas com imitação de plasmídeo (Cont.), Fv2E (Fv), Fv2E-DCC-IC (Fv-DCC) com ou sem AP20187 (AP). Em todas as condições, as células também foram transfectadas com o marcador de superfície pKk. Células transfectadas que expressam o marcador foram marcadas magneticamente com Microesferas MACSelect e separadas utilizando um Separador MACS e Colunas de Separação. A exclusão de azul de tripano foi testada sobre estas células purificadas.
[094] Figura 14B: a morte celular induzida por UNC5H2 é inibida por meio de dimerização induzida por AP20187, conforme medido por meio de exclusão de azul de tripano como em (A). As células foram transfectadas com pMACSKk e Fv2E (Fv), Fv2E-UNC5H2-IC (Fv-UNC5H2) com ou sem AP20187 (AP).
[095] Figura 14C: a ativação de caspase induzida por UNC5H2 é inibida por meio de dimerização induzida por AP20187, conforme medido pela atividade relativa de caspase-3. Células HEK293T foram transfectadas com imitação de vetor pCMV (Cont.), Fv2E (Fv), Fv2E-UNC5H2-IC (Fv-UNC5H2) com ou sem AP20187 (AP). O índice de atividade relativa de caspase é apresentado como a razão entre a atividade de caspase da amostra e aquela medida em células HEK293T transfectadas com pCMV. Os desvios padrão são indicados (n = 3).
[096] Figura 15A: curva de afinidade de netrina-1 sobre DCC- 5Fbn medida por meio de teste ELISA demonstra que DCC-5Fbn é capaz de unir netrina-1. DCC-5Fbn (100 ng) ou IL3-R (600 ng) foi revestido e foram adicionadas doses crescentes de netrina-1 (0 a 800 ng). Os valores IL3 foram subtraídos dos valores DCC-5Fbn. Kd aproximado de DCC-5Fbn/netrina-1 foi estimado em 5 nM.
[097] Figura 15B: teste de competição. Como em (A), mas o domínio extracelular completo de DCC (DCC-EC, 125 ng) foi revestido no lugar de DCC-5Fbn e adicionou-se netrina-1 (50 ng) na presença de DCC-5Fbn (625 ng) ou o DCC-EC completo (125 ng). Observe-se que DCC-5Fbn deixa de competir com a interação de DCC/netrina-1.
[098] Figura 15C: multimerização de DCC induzida por netrina-1 é inibida por DCC-5Fbn. Lisatos de células HEK293T transfectadas transitoriamente com construções que expressam HA-DCC e/ou c-myc-DCC com ou sem netrina-1 (300 ng/ml) e/ou DCC-5Fbn (900 ng/ml) foram submetidos a retirada de HA (IP α-HA). A presença de c-myc-DCC foi revelada com anticorpo anti-c-myc. Total: Western Blot sobre lisato antes da retirada.
[099] Figura 16A: células HEK293T foram transfectadas transitoriamente com imitação (Cont.) ou uma construção DCC de comprimento total e incubadas ou não com netrina-1 (300 ng/ml) e/ou DCC-5Fbn (800 ng/ml). A morte celular foi determinada por meio de manchas de azul tripano.
[0100] Figura 16B: células de câncer de mama metastático 4T1 foram cultivadas na presença (+ DCC-5Fbn) ou ausência (- DCC-5Fbn) de DCC-5Fbn (300 ng/ml) por 24 horas e a morte celular também foi medida por meio de teste de exclusão de azul tripano. Os desvios padrão são indicados (n = 3).
[0101] Células 4T1 e 67NR foram recebidas por gentileza de F. Miller (Detroit MI, Estados Unidos). Cal51, MCF7, MDA-MB231, 453, 361, 157, SK-BR3, CAMA-1, T47D foram cultivados utilizando procedimento padrão. Linhagens de células de mama humanas relacionadas na Figura 8B e, mais especificamente, linhagens de células T47D e SKB7 foram obtidas por meio de D. Birnbaun. Células 67NR foram transfectadas de forma estável utilizando o reagente lipofectamina (Invitrogen) e seleção de puromicina (Sigma). Transfecções transitórias de células de Rim Embriônico Humano 293T (HEK293T) foram realizadas conforme descrito anteriormente 10de acordo com um procedimento de fosfato de cálcio modificado ou utilizando Lipofectamina de acordo com as instruções do fabricante (Invitrogen). A linhagem de células de câncer de mama 4T1 foi descrita anteriormente 20. Células 4T1-luc foram obtidas por meio de transfecção estável de vetor CMV-luciferase que possui resistência a higromicina. Clones foram selecionados por meio de intensidade de luminescência utilizando a Estação Luminoskan Ascent (Labsystems). Imunomanchas foram realizadas conforme descrito anteriormente 6utilizando anti-c-myc (Sigma; 1/200) anti-Marca M2 (Sigma, 1/200) ou anti-HA (Sigma, 1/500). O agente de dimerização artificial AP20187 foi da Ariad Pharmaceuticals. O domínio extracelular completo de DCC (DCC-EC), DCC- EC-Fc, foi obtido por meio da R&D Systems e Netrina-1 da Apotech Corp. Para análise da morte celular, medição da atividade de caspase e imunoprecipitação, AP20187 foi utilizado em concentração final de 10 nM e netrina-1 foi utilizada em concentração final de 300 ng/ml.
[0102] Foram fornecidas 51 amostras de câncer de mama humano pelo banco de tumores do Centre Léon Bérard. Tecido novo do tumor foi obtido durante cirurgia da mama antes de qualquer terapia sistêmica e congelado rapidamente em nitrogênio líquido.
[0103] pGNET-1 pCMV e pGNET-1 que codifica netrina-1 de galinha foi conforme descrito anteriormente 6. pKk foi descrito 22. Os mutantes negativos dominantes para DCC (pCR-DCC-IC-D1290N) e para UNC5H (pCR- UNC5H2-IC-D412N) foram descritos anteriormente 6, 27, 7. HA-DCC foi obtido por meio da introdução de uma marca HA no modelo pCMV-DCC 6pelo sistema de mutagênese dirigida a local QuikChange (Stratagene) utilizando os primers a seguir: DCC-HA F: 5’- CACAGGCTCAGCCTTTTATCCATATGATGTACCGGATTATGCATAACATGT ATTTCTGAATG-3’ (SEQ ID N° 1); DCC-HA R: 5’- CATTCAGAAATACATGTTATGCATAATCCGGTACATCATATGGATAAAAGGC TGAGCCTGTG-3’ (SEQ ID N° 2).
[0104] c-myc-DCC também foi obtido por meio da introdução de uma marca c-myc no modelo pCMV-DCC por meio de QuikChange utilizando os primers a seguir: DCC-myc F: 5’- CACAGGCTCAGCCTTTGAGCAGAAGTTGATAAGTGAGGAAGATCTGTAAC ATGTATTTCTGAATG-3’ (SEQ ID N° 3). DCC-myc R: 5’- CATTCAGAAATACATGTTACAGATCTTCCTCACTTCTCAACTTCTGCTCAAA GGCTGAGCCTGTG-3’ (SEQ ID N° 4).
[0105] Vetor de expressão que codifica HA-Fv2E (em pC4M) do kit de Homodimerização Regulada Argent é da Ariad Pharmaceuticals. A partir deste plasmídeo, foi construído o plasmídeo HA-Fv2E-DCC-IC. Um fragmento de PCR do domínio intracelular de DCC (1122-1447) foi obtido com os primers: F 5’-TATGTCGACCGACGCTCTTCAGCCCAGCAGAGA-3‘ (SEQ ID N° 5) e R 5’- TATGAATTCTTAGTCGAGTGCGTAGTCTGGTACGTCGTACGGATAAAAGGC TGAGCCTGTGATGGCATTAAG-3’ (SEQ ID N° 6).
[0106] O primer reverso fundiu-se à marca HA para a extremidade C-terminal de DCC. O fragmento de PCR foi subclonado em HA-Fv2E por meio de digestão de restrição de SalI e EcoRI. O c-myc-Fv2E-DCC-IC foi obtido utilizando o sistema de mutagênese dirigido por local QuikChange (Stratagen) com pC4M-Fv2E-DCC-IC-HA como modelo e os primers a seguir: primer F: 5’- CTTAATGCCATCACAGGCTCAGCCTTTGAACAGAAACTCATCTCTGAAGAG GATCTGTAAGAATTCATAAAGGGCAAT-3’ (SEQ ID N° 7) e o primer R: 5’- ATTGCCCTTTATGAATTCTTACAGATCCTCTTCAGAGATGAGTTTCTGTTCA AAGGCTGAGCCTGTGATGGCATTAAG-3’ (SEQ ID N° 8).
[0107] HA-UNC5H2 (em pcDNA3.1) já foi descrito 7. As construções que codificam Marca M2-UNC5H2 foram geradas por meio de clonagem em p3xMarca-CMVTM-7.1 (Sigma) do fragmento de NotI-EcoRI PCR derivado de HA-UNC5H2 como modelo e os primers a seguir: primer F 5’- GCGCGGCCGCAGGGCCCGGAGCGGG-3’ (SEQ ID N° 9) e primer R 5’- CGGAATTCTCAGCAATCGCCATCAGTGGTC-3’ (SEQ ID N° 10).
[0108] HA-Fv2E-UNC5H2-IC e c-myc-Fv2E-UNC5H2-IC em pC4M foram gerados por meio de amplificação por PCR do domínio intracelular de UNC5H2 utilizando os primers a seguir: UNC5H2-HA F 5’- CGGTCGACGTGTACCGGAGAAACTGC-3’ (SEQ ID N° 11) e UNC5H2-HA R 5’- GCGAATTCTCATGCATAATCCGGCACATCATACGGATAGCAATCGCCATCAGT GGTC-3’ (SEQ ID N° 12) e UNC5H2-myc F 5’- CGGTCGACGTGTACCGGAGAAACTGC-3’ (SEQ ID N° 13) e UNC5H2-myc R 5’- GCGAATTCTCACAGATCCTCTTCTGAGATGAGTTTTTGTTCGCAATCGCCATC AGTGGTC-3’ (SEQ ID N° 14), respectivamente. Os fragmentos de PCR foram clonados em HA-Fv2E por meio de digestão de restrição de SalI e EcoRI.
[0109] O cDNA que codifica as proteínas de fusão HA-Fv2E- UNC5H2-IC e c-myc-Fv2E-UNC5H2-IC foi subclonado em seguida em pcDNA3.1-TOPO por meio de PCR utilizando os primers a seguir: Fv2E F 5’- CCACCATGGGGAGTAGCA-3’ (SEQ ID N° 15) e UNC5H2-HA R 5’- TCATGCATAATCCGGCACATCATACGGATAGCAATCGCCATCAGTGGTC-3’ (SEQ ID N° 16) e Fv2E F 5’-CCACCATGGGGAGTAGCA-3’ (SEQ ID N° 15) e UNC5H2-myc R 5’- TCACAGATCCTCTTCTGAGATGAGTTTTTGTTCGCAATCGCCATCAGTGGT C-3’ (SEQ ID N° 17), respectivamente, e HA-Fv2E-UNC5H2-IC e c-myc-Fv2E- UNC5H2-IC em pC4M como modelos correspondentes.
[0110] Ps974-DCC-5Fbn que permite a expressão bacteriana do quinto domínio de fibronectina tipo III de DCC foi obtido por meio da inserção de um fragmento de DNA de Pst1/BamHI gerado por meio de PCR utilizando pDCC-CMV-S como modelo.
[0111] A produção de DCC-5Fbn foi realizada utilizando um procedimento padrão. Resumidamente, células BL21 foram forçadas a expressar DCC-5Fbn em resposta a imidazol e o lisato de BL21 foi submetido a cromatografia de afinidade utilizando Marca-agarose (Sigma).
[0112] Foram conduzidas coimunoprecipitações sobre células HEK293T transfectadas com várias construções marcadas conforme descrito anteriormente 27. Resumidamente, células HEK293T foram lisadas em 50 mM de HEPES, pH 7,6, 125 mM de NaCl, 5 mM de EDTA e 0,1% NP-40 na presença de inibidor de protease e incubadas adicionalmente com anti-HA (Sigma), anticorpo anti-c-myc (Sigma), anti-Marca M2 (Sigma) e proteína A Sepharose (Sigma). Lavagens foram realizadas em 50 mM de HEPES, pH 7,6, 125 mM de NaCl, 5 mM de EDTA.
[0113] DCC-5Fbn (100 ng) ou IL3-R (R&D Systems, 600 ng) foram revestidos sobre placa Maxisorp (Nunc) e foram adicionadas doses crescentes de netrina-1 (Apotech) (0 a 800 ng) para teste de ligação.
[0114] DCC-EC (R&D Systems, 125 ng) foi revestido sobre placa Maxisorp para teste de competição ELISA. Netrina-1-Marca M2 (50 ng) e competidor DCC-EC (125 ng) ou DCC-5Fbn (625 ng) foram adicionados em seguida simultaneamente. Após as lavagens, para o teste de ligação ou teste de competição ELISA, netrina-1-Marca M2 residual ainda fixo foi revelado com um anticorpo anti-Marca M2.
[0115] DCC-EC-Fc (1,25 ng/ml) ou UNC5H2-EC-Fc (0,5 ng/ml) foi adsorvido sobre placas maxisorp de 96 cavidades (Nunc) de acordo com instruções do fabricante. Netrina-1 marcada com Marca (0,5 ng/ml) foi adicionada em seguida junto com concentrações crescentes de DCC-EC-Fc. Após incubação por uma hora, as placas foram extensamente lavadas e netrina-1 unida foi detectada por meio de imunomarcação utilizando um anticorpo anti-marca M2 (Sigma) e anti-camundongo de cabra HRP (Jackson). Medição colorimétrica foi realizada sobre a estação Victor multimarcas (Wallac).
[0116] 67NR, 4T1, CAL51, T47D e SKBR7 foram cultivados em meio pobre em soro e foram tratados (ou não) com DCC-EC-Fc ou DCC-5Fbn por 24 horas. A morte celular foi analisada utilizando procedimentos de mancha de azul tripano conforme descrito anteriormente 6. A extensão da morte celular é apresentada como o percentual de células positivas para azul de tripano nas diferentes populações celulares. Para selecionar células transfectadas, as células foram cotransfectadas com o marcador de superfície pKk e o plasmídeo que codifica genes de interesse. As células transfectadas que expressam o marcador foram marcadas magneticamente com Microesferas MACSelect e separadas utilizando Separador de MACS e Colunas de Separação (Miltenyi Biotec). A exclusão de azul de tripano foi testada sobre essas células purificadas. A sobrevivência celular também foi medida por meio de teste MTT utilizando kit de teste MTT Vybrant (Molecular Probes) de acordo com os procedimentos do fabricante.
[0117] A atividade de caspase relativa foi determinada por meio de análise citométrica de fluxo conforme segue: 2 x 105células tratadas foram colhidas, lavadas uma vez em 1 ml de PBS e novamente suspensas em 200 μl de solução de manchas contendo FITC-VAD-fmk (CaspACE, Promega). Após incubação por sessenta minutos a 37 °C, as células foram lavadas em 1 ml de PBS e novamente suspensas em 200 μl de PBS para análise por citometria de fluxo. Células manchadas foram contadas utilizando software de análise CellQuest e FACS Calibur (Becton Dickinson) com excitação e configurações de emissão de 488 nm e 525-550 nm (filtro FL1), respectivamente. A atividade de caspase-3 foi medida utilizando o teste Caspase-3 da BioVision. A atividade de caspase é apresentada como a razão entre a atividade de caspase da amostra e aquela medida em células HEK293T transfectadas com pCMV. Para análise da morte celular e medição da atividade de caspase, AP20187 e/ou netrina-1 e/ou DCC-5Fbn foram adicionados em meio de cultivo celular vinte horas e uma hora antes de recolher as células.
[0118] Para testar a expressão de netrina-1 em tumores de mama humanos, RNA total foi extraído de biópsias de pacientes que passam por cirurgia de câncer de mama utilizando kit Nucleospin RNAII (Macherey-Nagel) e 1 μg sofreu transcrição reversa utilizando o kit de Síntese de cDNA iScript (BioRad). RT-PCR quantitativo em tempo real foi realizado sobre um aparelho LightCycler 2.0 (Roche) utilizando o kit Light Cycler FastStart DNA Master SYBERGreen I (Roche). As condições de reação para toda a amplificação ideal, bem como seleção de primers de netrina-1, foram determinadas conforme já descrito 18. Os genes PBGD, TBP humanos e RPLP0 de camundongo onipresentemente expressos que exibem a menor variabilidade de expressão entre tecidos de tumores de mama e normais 25, 28foram utilizados como controles internos. Foram utilizados os primers a seguir: PBGD: - FOR: 5’-CTGGAGTTCAGGAGTATTCGGGG-3’ (SEQ ID N° 18); - REV: 5’-CAGATCCAAGATGTCCTGGTCCTT-3‘ (SEQ ID N° 19); TBP: - FOR: 5’-CACGAACCACGGCACTGATT-3’ (SEQ ID N° 20); - REV: 5’-TTTTCTTGCTGCCAGTCTGGAC-3’ (SEQ ID N° 21); Netrina-1 humana - NTN1: - FOR: 5’-TGCAAGAAGGACTATGCCGTC-3’ (SEQ ID N° 22); - REV: 5’-GCTCGTGCCCTGCTTATACAC-3’ (SEQ ID N° 23); UNC5B: - FOR: 5’-TGCAGGAGAACCTCATGGTC-3’ (SEQ ID N° 24); - REV: 5’-GGGCTGGAGGATTACTGGTG-3’ (SEQ ID N° 25); DCC: - FOR: 5’-AGCCAATGGGAAAATTACTGCTTAC-3’ (SEQ ID N° 26); - REV: 5’-AGGTTGAGATCCATGATTTGATGAG-3’ (SEQ ID N° 27); UNC5C: - FOR: 5’-GCAAATTGCTGGCTAAATATCAGGAA-3’ (SEQ ID N° 28); - REV: 5’-GCTCCACTGTGTTCAGGCTAAATCTT-3’ (SEQ ID N° 29).
[0119]Modelo de camundongos singênicos: fêmeas de camundongos BALB/cByJ com oito a onze semanas de idade do Jackson Laboratory foram utilizadas para cirurgia. Para injeção em glândulas mamárias de células 67NR, camundongos foram anestesiados com 2,2,2- tribromoetanol, 106 células em 50 μl de PBS foram injetadas na glândula mamária e camundongos foram sacrificados quando o tumor excedeu 1,5 cm e causou impedimento do movimento do animal. Para injeção intravenosa, 105células 4T1-luc de tumores em 150 μl de PBS foram injetadas em uma veia da cauda e os camundongos foram sacrificados no dia 13-15 (após a injeção de células 4T1) ou no dia 20-23 (após a injeção de células 67NR), ou analisados utilizando registro de luminescência. Quando os animais foram sacrificados, os pulmões foram removidos, pesados, comparados com o peso total do animal e os nódulos metastáticos foram contados.
[0120] Fêmeas de camundongos nu/nu atímicos com cinco semanas de idade (peso do corpo de 20 a 22 g) foram obtidas por meio da Charles River. Os camundongos foram abrigados em gaiolas com filtro no topo esterilizadas e mantidas em instalação de animais livre de patógenos. Linhagens de células de câncer de mama humano (SKBR7, T47D e H358) foram implantadas por meio de injeção subcutânea de 5 x 106células em 200 μl de PBS no flanco esquerdo dos camundongos. Quando tumores foram estabelecidos (cinco semanas para T47D, duas semanas para SKBR7 e cinco dias para H358), PBS ou 20 μg de DCC-5Fbn foram administrados ao tumor (it) todos os dias durante quatorze dias. Os tamanhos de tumores foram medidos por um calibrador. O volume do tumor foi calculado com a fórmula v = 0,5 * (comprimento * largura2).
[0121] Seções de pulmão com 4 μm de espessura foram preparadas e manchadas com hematoxilina-eosina-safron. A classificação histológica e graduação de lesões neoplásticas foi realizada de forma cega e de acordo com procedimentos padrão. Para formação de imagens in vivo de metástase utilizando células 4T1-luc, a luz resultante da oxidação bioluminescente da luciferina livre de endotoxina injetada por via intraperitoneal (Promega) (120 mg/kg de peso do corpo) foi detectada e quantificada (dez minutos após a injeção) com sistema NightOWL LB 981 NC 100 da Berthold Technologies, utilizando sistema de anestesia com isoflurano gasoso da TEM SEGA.
[0122] Analisamos em primeiro lugar netrina-1 e os seus receptores de dependência, ou seja, expressão de DCC e UNC5H por Q-RT- PCR em um quadro de trinta tumores primários de mama, quinze dos quais não apresentaram evolução metastática conhecida e quinze deles foram metastáticos no diagnóstico. Embora DCC fosse pouco detectável e UNC5H tenha deixado de exibir alterações significativas entre os dois tipos de tumores, netrina-1 aparentemente é significativamente mais expressa em tumores de mama metastáticos que em tumores de mama não metastáticos (Figura 1A).
[0123] 60% dos tumores de mama metastáticos testados exibiram superexpressa de netrina-1 (faixa de 1,4 a 9,6 vezes, p < 0,015) (Tabela 1). TABELA 1 PERCENTUAL DE AMOSTRAS QUE EXIBEM EXPRESSÃO DE NETRINA-1 SUPERIOR À EXPRESSÃO MÉDIA EM BIÓPSIAS NÃO METASTÁTICAS E FAIXA DE SUPEREXPRESSÃO
[0124] Em camundongos, Miller e seus colegas desenvolveram um modelo poderoso para estudar a biologia de tumores metastáticos contra não metastáticos: de um único tumor mamário primário que ocorreu naturalmente em um camundongo BALB/c, foi obtida uma série de linhagens celulares que exibiram diferentes potenciais metastáticos quando injetadas em camundongos singênicos. Particularmente, embora células 67NR formem tumores mamários primários mas sem metástase, células 4T1 de tumores primários e metástase, especialmente no pulmão, na medula óssea e no fígado 20. De forma interessante, embora netrina-1 não tenha sido detectada em células 67NR, netrina-1 foi altamente expressa em células 4T1 (Figura 1B).
[0125] Para determinar se o potencial metastático de células 4T1, em comparação com o de células 67NR, era relacionado à expressão de netrina-1, células 67NR foram forçadas a expressar de forma estável netrina-1. Imitações de células 67NR transfectadas ou células 67NR-net que expressam netrina-1 (Figuras 2A e 2B) foram injetadas em glândulas de mamíferos ou por via intravenosa e a metástase foi monitorada quando injetada em almofadas de gordura, o que sugere que a presença de netrina-1 em 67NR não é suficiente para permitir a formação de metástase de pulmão a partir do local primário. Quando as células recebem injeção intravenosa, entretanto, foi detectado aumento significativo de metástase nos pulmões no 67NR que expressa netrina-1 (Figura 2C).
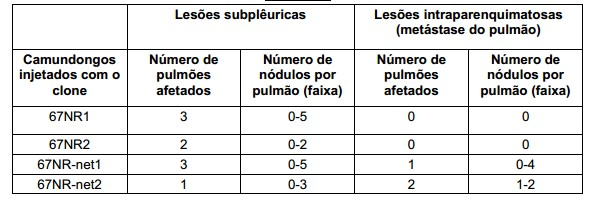
[0126] Vide a Tabela 2 que exibe a quantidade de nódulos subplêuricos (metástase fora do pulmão) e nódulos intraparenquimatosos (metástase no pulmão). TABELA 2
[0127] Desta forma, a expressão de netrina-1 aparentemente é um evento fundamental que sustenta a formação de metástase, provavelmente favorecendo células tumorais após a encravação.
[0128]Como netrina-1 aparentemente é suficiente para o potencial metastático de células 67NR após a encravação e como se demonstrou que netrina-1 inibe a morte celular induzida por receptores com dependência de netrina-1 6, 7, 18, investigamos em seguida se a produção autócrina de netrina-1 fornece vantagem seletiva para células 4T1 por meio da inibição da morte celular induzida por DCC/UNC5H nessas células. Um domínio localizado no terminal N de netrina-1 (o chamado domínio laminina-VI) interage com receptores de DCC e UNC5H (Figura 3A; 21), de forma que um domínio extracelular solúvel de DCC (DCC-EC-Fc) pode inibir a interação de DCC/netrina-1 e UNC5H/netrina-1 (não exibido). DCC-EC-Fc foi adicionado em seguida a um cultivo de células 4T1 e a morte celular foi monitorada por meio de teste de exclusão de azul de tripano (Figura 3B) ou da medição da atividade de caspase (Figura 3C). Conforme exibido na Figura 3C, a adição da proteína concorrente no meio de cultivo aciona a morte de células 4T1 de forma dependente de dosagem. Além disso, este efeito é específico, pois DCC- EC-Fc não apresentou efeito sobre a morte de células 67NR e IL3R-EC-Fc (o domínio extracelular de receptor IL3) deixou de acionar a morte de células 4T1 (Figuras 3B e 3C). Este efeito se deve à inibição de netrina-1, pois a adição de quantidade excessiva de netrina-1, junto com DCC-EC-Fc, inibiu a atividade pró-apoptótica de DCC-EC-Fc sobre células 4T1 (não exibido). Para restringir a concorrência a um domínio menor, produzimos o quinto domínio de fibronectina tipo III de DCC, que é conhecido por interagir com netrina-1 21. A adição deste domínio -DCC-5Fbn- apresentou atividade pró-apoptótica similar sobre células 4T1 (Figura 3D). Desta forma, embora netrina-1 aparentemente confira potencial metastático a células tumorais em camundongos, estas células tumorais metastáticos que expressam netrina-1 podem ser encaixadas para apoptose por meio de inibição da interação entre receptores e netrina-1.
[0129] Para analisar adicionalmente se isso permanece verdade em células tumorais de mama humano, a expressão de netrina-1 foi analisada em um quadro de linhagens de células de câncer de mama metastático humano (vide a Tabela 3). TABELA 3 Conduzido em outra linhagem de células T47D.
[0130] A Tabela 3 exibe as diferentes linhagens de células de mama metastáticas humanas analisadas para a expressão de netrina-1 por Q- RT PCR como nas Figuras 1A e 1B e a sua sensibilidade a DCC-EC-Fc por meio de medição da morte celular por meio de exclusão de azul tripano. A quantidade relativa de expressão de netrina-1 e sensibilidade a DCC-EC-Fc são indicadas por (+), enquanto a ausência destes critérios é indicada por (-). Em algumas linhagens celulares, o DCC-EC-Fc não foi determinado (ND).
[0131] Conforme o esperado, netrina-1 é expressa em grande quantidade de linhagens de células metastáticas e algumas delas sofrem apoptose quando cultivadas na presença de DCC-EC-Fc. Células CAL51 sofreram apoptose de forma dependente de dosagem, por exemplo, em resposta a DCC-Ec-Fc. Conforme o acima, a adição de netrina-1 em excesso reverte o efeito de DCC-EC-Fc, sustentando a opinião de que as proteínas concorrentes matam estas linhagens de células humanas inibindo a interação entre netrina-1 e receptores de netrina-1. Além disso, seleção clonal de células CAL51 permitiu o estabelecimento de uma linhagem de células CAL51-36, que é muito mais suscetível a morte celular em resposta a DCC-EC-Fc (Figura 4B). DCC-EC-Fc ou DCC-5Fbn podem conseqüentemente representar boas ferramentas para acionar apoptose seletiva de células tumorais metastáticos humanos.
[0132] Demonstramos aqui que a expressão de netrina-1 pode ser considerada marcador da disseminação de tumores de mama. Mais da metade dos tumores de mama com propensão à metástase obteve elevada expressão de netrina-1. Tanto o modelo de camundongo descrito acima quanto os dados obtidos sobre linhagens de célula de câncer de mama humano sustentam a visão de que este nível elevado de netrina-1 é uma vantagem seletiva obtida pela célula cancerosa para escapar de apoptose induzida por receptores com dependência de netrina-1 e, conseqüentemente, sobreviver independentemente da disponibilidade de netrina-1. Do ponto de vista mecânico, esta expressão autócrina de netrina-1 inibe a morte celular induzida por UNC5H. De fato, DCC era pouco detectável nos dois grupos (metastático e não metastático) de cânceres de mama estudados, de forma a sugerir que DCC é regulado para baixo cedo durante tumorigênese de mama ou é apenas fracamente expresso em tecido de mama. Além disso, a inibição de apoptose induzida por UNC5H por meio de coexpressão de forma mutante negativa dominante da atividade pró-apoptótica de UNC5H inibe a morte de células CAL51 em resposta a DCC-EC-Fc (não exibido). Isso pode corresponder à observação recente de que parte da atividade pró-apoptótica de UNC5H2 passa através da ativação da serina/treonina DAPK 22, proteína envolvida na regulagem de metástase 23.
[0133] Estas observações não apenas fornecem evidência da importância do par de receptores ligantes/de dependência na regulagem do desenvolvimento de tumores, mas também esclarecem uma nova estratégia terapêutica. De fato, atualmente, não há tratamento eficiente de pacientes com câncer de mama metastático, falta de tratamento que leva à morte 400.000 mulheres por ano em todo o mundo 24. Propomos no presente que um tratamento com base na inibição da interação entre netrina-1 e seus receptores de dependência poderá afetar positivamente a metade dos pacientes que sofrem de câncer de mama metastático. Estes tratamentos poderão incluir drogas químicas, anticorpos monoclonais ou a proteína DCC-5Fbn apresentada no presente. Permanece a ser demonstrado se isso deve ser considerado estratégia para evitar a formação de metástase, o que geraria tratamento preventivo a longo prazo de mulheres diagnosticadas com câncer de mama primário, ou como estratégia que poderá ser utilizada para induzir a regressão de metástase. Testes clínicos futuros deverão também responder esta questão.
[0134] Descrevemos no presente que, ao contrário de tumores de mama não metastáticos humanos, a maior parte dos cânceres de mama metastáticos exibe superexpressão de netrina-1. Em um modelo de camundongos, demonstramos que, em células de tumores mamários não metastáticos, a expressão forçada de netrina-1 é associada à metástase nos pulmões. Além disso, camundongos ou linhagens de células tumorais metastáticas humanas que se demonstrou expressarem altamente netrina-1 sofrem apoptose quando a interação entre netrina-1 e receptores é inibida por uma proteína concorrente. Desta forma, netrina-1 é um marcador para câncer metastático humano tal como mama metastática e inibição da interação entre netrina-1 e receptores representa uma abordagem terapêutico para induzir a morte de células metastáticas.
[0135] Netrina-1 e seus receptores de dependência, ou seja, expressão de DCC, UNC5H2 e UNC5H3, foram analisados por meio de Q-RT- PCR em um quadro de 51 tumores de mama. Ele inclui pacientes cujos tumores foram localizados para a mama (N0, 16 pacientes), apresentaram envolvimento de nódulos (N+, 19 pacientes) ou possuíam doença metastática distante no momento do diagnóstico (M+, 16 pacientes). Embora DCC fosse pouco detectável e a expressão de UNC5H deixasse de exibir alterações significativas entre os diferentes tipos de tumores (não exibidos), netrina-1 é significativamente mais expressa em tumores N+ que em tumores N0 (média: 1,8 contra 0,5, p = 0,007) com faixa de expressão de netrina-1 mais alta em tumores N+ (Figura 5 e Tabela 4). TABELA 4 PERCENTUAL DE AMOSTRAS QUE EXIBEM EXPRESSÃO DE NETRINA-1 SUPERIOR À EXPRESSÃO MÉDIA EM BIÓPSIASN0, CINCO VEZES MAIOR OU QUINZE VEZES MAIOR E A FAIXA DA SUPEREXPRESSÃO
[0136] 31,5% dos tumores N+ exibem aumento de pelo menos cinco vezes na expressão de netrina-1 enquanto nenhum aumento foi detectado em qualquer tumor N0 testado (Figura 5 e Tabela 4). Diferença ainda mais notável é observada ao comparar a expressão de netrina-1 em M+ com tumores N0 (média: 7,8 contra 0,5, p < 0,0001). Ao longo desta linha, 62,5% de tumores M+ exibem aumento de pelo menos cinco vezes da expressão de netrina-1. Diferença significativa da expressão de netrina-1 também existe entre tumores N+ e M+ (média: 1,8 contra 7,8, p = 0,009). Além disso, a superexpressão de netrina-1 é mais alta em tumores M+ que em tumores N+, pois 37,5% de tumores M+ exibem aumento de mais de quinze vezes no nível de netrina-1, enquanto esse aumento não é detectado em tumores N+ (Figura 5 e Tabela 4). Desta forma, a regulagem para cima de netrina-1 é um marcador do envolvimento nodal e da doença metastática distante em câncer de mama humano.
[0137] Em camundongos, Miller e seus colegas desenvolveram modelo poderoso para estudar a biologia de tumores metastáticos contra não metastáticos: a partir de um único tumor mamário primário que ocorreu naturalmente em um camundongo BALB/c, foi obtida uma série de linhagens celulares que exibiram diferentes potenciais metastáticos quando injetadas em camundongos singênicos. Particularmente, enquanto células 67NR formam tumores mamários primários, mas sem metástase, células 4T1 formam tumores primários e metástase, especialmente no pulmão, no fígado e na medula óssea 20. De forma interessante, enquanto netrina-1 deixava de ser detectada em células 67NR, netrina-1 era altamente expressa em células 4T1 (Figura 1B).
[0138] Para determinar em primeiro lugar se o potencial metastático de células 4T1, em comparação com o de células 67NR, era relacionado à expressão de netrina-1, células 67NR foram forçadas a expressar netrina-1 de forma estável. Imitações de células 67NR transfectadas ou células 67NR que expressam netrina-1 (Figuras 2A e 2B) foram injetadas em glândulas mamárias e a metástase foi monitorada por meio de exame anatômico-patológico. As duas linhagens celulares deixaram de formar eficientemente metástase no fígado ou em pulmões quando injetadas em almofadas de gordura de camundongos (19 camundongos receberam injeção de células 67NR que expressam netrina-1 e apenas duas suspeitas de micrometástases, uma no pulmão e outra no fígado, foram detectadas) (Tabela 5). TABELA 5 METÁSTASE DO PULMÃO E DO FÍGADO DE67NR INJETADO EM ALMOFADA DE GORDURA CONTRA CÉLULAS QUE EXPRESSAM NETRINA-1
[0139] Um clone de célula controle que possui resistência a puromicina (imitação de 67NR), um clone de célula que expressa netrina-1 (67NRnet1) e uma população policlonal de 67NR transfectada de forma estável de netrina-1 (67NR-net1-policlonal) foram injetados em almofada de gordura de camundongos e a metástase foi analisada no ambiente do pulmão ou do fígado.
[0140] Desta forma, a expressão de netrina-1 em células tumorais não é suficiente para permitir a formação de metástase a partir do local primário.
[0141] Como se demonstrou que netrina-1 inibe a morte celular induzida por receptores com dependência de netrina-1 6, 7, 18, investigamos a seguir se a produção autócrina de netrina-1 detectada em células 4T1 metastáticas confere vantagem seletiva para estas células, por meio da inibição da morte celular induzida por DCC/UNC5H. Para testar isso, observamos um composto que pode titular netrina-1. Relatou-se que um domínio localizado no terminal N de netrina-1 (o chamado domínio de laminina-VI) interage com os receptores de DCC e UNC5H (Figura 3A; 21). Demonstramos que um domínio extracelular solúvel de DCC (DCC-EC-Fc) pode inibir a interação de DCC/netrina-1 e UNC5H2/netrina-1, conforme medido por meio de teste ELISA (Figura 6A). DCC-EC-Fc foi adicionado em seguida a um cultivo de células 4T1 e a morte celular foi monitorada, seja por meio de teste de exclusão de azul de tripano (Figuras 3B e 6B) ou medindo-se a atividade de caspase por meio de citometria de fluxo (Figuras 3C e 6C). Conforme exibido nas Figuras 3B, 3C, 6B e 6C, a adição da proteína concorrente no meio de cultivo aciona a morte de células 4T1 de forma dependente da dose. Este efeito é específico, pois DCC- EC-Fc não apresentou efeito sobre a morte de células 67NR (Figuras 3B, 3C, 6B e 6C) e IL3R-EC-Fc (o domínio extracelular do receptor IL3) deixou de acionar a morte de células 4T1 (Figura 3D). Desta forma, as células 4T1 sobrevivem por meio da produção autócrina de netrina-1, que bloqueia a morte celular induzida por receptores de netrina-1.
[0142] Como o domínio extracelular completo de DCC aparece com interesse apenas modesto para uso in vivo e em terapia (DCC-EC-Fc possui tamanho de cerca de 1100 aminoácidos), procuramos um polipeptídeo alternativo a partir do domínio extracelular de DCC, que pudesse acionar a apoptose em células 4T1. Conseqüentemente, produzimos o quinto domínio tipo III de fibronectina de DCC, DCC-5Fbn, que é conhecido por interagir com netrina-1 21(Figura 3A). De forma interessante, essa proteína com cem aminoácidos não interfere com a ligação de DCC/netrina-1 ou UNC5H/netrina- 1, mas afeta a capacidade de netrina-1 de acionar a multimerização desses receptores (vide Exemplo 4). Como a multimerização de DCC e UNC5H é requisito prévio para a atividade inibidora de netrina-1 sobre a morte celular induzida por DCC/UNC5H, a adição de DCC-5Fbn aciona a apoptose em células que expressam DCC cultivadas na presença de netrina-1 22e aciona a morte dos dois 4T1 (Figura 7A).
[0143] Investigamos a seguir se o efeito de morte celular observado in vitro pode ser estendido in vivo. Para fazê-lo, células 4T1 foram transfectadas de forma estável com vetor com base em luciferase e células 4T1-luc foram injetadas por via intravenosa (iv) em camundongos BALB/c singênicos. Os camundongos receberam em seguida injeção intraperitoneal (ip) e intravenosa (uma injeção a cada dois dias, uma intravenosa e uma intraperitoneal) do dia 0 ao dia 13 com tampão PBS ou DCC-5Fbn marcado com Flag (1,25 μg/g de camundongo/injeção). A formação de metástase foi analisada em seguida utilizando registro de luminescência. Conforme exibido nas Figuras 7B e 7C, quando injetado por via intravenosa, células 4T1-luc colonizam pulmões eficientemente. Por outro lado, camundongos tratados com DCC-5Fbn exibem redução dramática da metástase de pulmão (Figuras 7B e 7C). Esta inibição da formação de metástase foi confirmada em seguida por meio de exame anatômico-patológico de pulmões (não exibido, vide Tabela 6). TABELA 6 NÚMERO TOTAL DE NÓDULOS METASTÁTICOS DO PULMÃO EM CAMUNDONGOS INDIVIDUAIS CONTADOS SOB INSTRUMENTO DE DISSECAÇÃO NAS DUAS POPULAÇÕES TRATADAS (+PBS, +DCC-5-FBN)
[0144] Foram obtidos resultados similares ao realizarmos diariamente injeção intraperitoneal de DCC-5Fbn marcado com GST no lugar de DCC-5Fbn marcado com Flag e GST-FADD em vez de PBS (não exibido). Desta forma, em camundongos, a inibição por DCC-5Fbn da atividade pró- sobrevivência conferida pela expressão autócrina de netrina-1 é associada à prevenção de metástase.
[0145] A vantagem de sobrevivência obtida por meio da expressão autócrina de netrina-1 não é restrita a células tumorais murinas, como é detectado em linhagens de células de câncer de mama humano. Na verdade, demonstrou-se que netrina-1 é expressa em fração dimensionável de linhagens de câncer de mama humano (Figura 8A) e a adição de DCC-EC-Fc ou DCC- 5Fbn a cultivos de células T47D ou SKBR7 de adenocarcinoma de mama humana que expressam netrina-1 naturalmente aciona a indução da morte celular medida por meio de teste de atividade de caspase-3 ou teste MTT (Figura 8B e não exibido). Este efeito deve-se à inibição de netrina-1, como adição de quantidade em excesso de netrina-1, que inibiu a atividade pró- apoptótica de DCC-EC-Fc/DCC-5Fbn (não exibida). Para monitorar o efeito antitumoral de DCC-5Fbn, xenoenxertos de células T47D foram implantados em camundongos brutos. Quando os tumores atingiram tamanho palpável, os camundongos foram tratados diariamente com PBS ou DCC-5Fbn e o volume de tumor foi determinado por dezoito dias. De forma similar aos dados obtidos no modelo singênico acima, DCC-5Fbn inibe completamente o crescimento de tumores (Tabela 7). TABELA 7 NÚMERO E COMPORTAMENTO DE TUMORES T47D XENOENXERTADOS QUE FORAM TRATADOS COM PBS OU DCC-5FBN
[0146] São indicados o número de tumores que cresceu de tamanho em mais de 40% e o número de tumores que apresentaram tamanho reduzido (mais de 30%).
[0147] Demonstramos no presente que a expressão de netrina-1 pode ser considerada um marcador da capacidade de disseminação de tumores de mama. A maior parte dos tumores de mama com propensão à metástase demonstrou elevada expressão de netrina-1. Os dados obtidos em linhagens de células de câncer de mama de camundongos/humano e os modelos de camundongos de xenoenxerto humano/singênico descritos acima sustentam a observação de que este nível elevado de netrina-1 é uma vantagem seletiva obtida pela célula de câncer para escapar da apoptose induzida por receptores com dependência de netrina-1 e, conseqüentemente, sobreviver independentemente da disponibilidade de netrina-1. Do ponto de vista mecânico, na patologia humana, esta expressão autócrina de netrina-1 provavelmente inibe a morte celular induzida por UNC5H. De fato, DCC era pouco detectável nos diferentes grupos (N0, N+, M+) de cânceres de mama estudados, de forma a sugerir que DCC é regulado para baixo cedo durante tumorigênese de mama ou somente é expresso fracamente em tecido de mama. Além disso, a inibição de apoptose induzida por UNC5H por meio de coexpressão de uma forma mutante negativa dominante da atividade pró- apoptótica de UNC5H inibe a morte de células de câncer de mama humano em resposta a DCC-EC-Fc (não exibido).
[0148] Desta forma, conforme previsto pelo modelo de receptor de dependência, demonstramos agora que uma célula tumoral pode escapar da dependência de receptor de dependência em pelo menos três maneiras. Primeiro, a expressão do receptor de dependência pode ser regulada para baixo, conforme descrito extensamente para DCC e, mais recentemente, para UNC5H 15, 17, 19, 29. Segundo, a sinalização de morte abaixo no fluxo pode ser desligada. Ao longo desta linha, demonstramos recentemente que a atividade pró-apoptótica de UNC5H2 depende da ligação de UNC5H2 à serina/treonina DAPK 22, uma proteína que se demonstrou estar envolvida na regulagem de metástase e regulada para baixo em malignidade humana 23. De forma similar, um relatório recente de Stupack e colegas demonstra que, no caso de algumas integrinas que agem como receptores de dependência, caspase-8, que aciona a morte celular mediada por estas integrinas, é fundamental para a metástase de neuroblastoma 30. Demonstramos no presente que terceira vantagem seletiva para a célula tumoral é a autoprodução do ligante de dependência. Permanece uma questão intrigante sobre como tumores de mama com propensão metastática parecem ter autoprodução de netrina-1 preferencialmente selecionada em vez de perda do receptor, enquanto tumores colo-retais possuem principalmente perda selecionada dos receptores em vez de ganho da expressão de netrina-1; de fato, apenas 7% de cânceres colo- retais exibem aumento da expressão de netrina-1 18. Uma possível explicação é que a expressão de netrina-1 não apenas confere um ganho de sobrevivência para as células migratórias, mas também possivelmente um ganho na sinalização positiva/não apoptótica de receptores de netrina-1. Ao longo desta linha, é importante observar que netrina-1 foi originalmente descrita como guia de orientação 31que, muito embora absolutamente não comprovada, poderia desempenhar papel no tropismo de células metastáticas. Outros papéis propostos de netrina-1 incluem regulagem da morfogênese e adesão 32-34, dois mecanismos que podem ser importantes para o desenvolvimento de metástase. De forma similar, propôs-se recentemente que netrina-1 desempenha papel durante a angiogênese embriônica e, muito embora tenham sido publicados resultados conflitantes 36-38, não podemos atualmente descartar o papel de netrina-1 como fator angiogênico que, de alguma forma, poderá favorecer o desenvolvimento de metástase no local secundário. Entretanto, o ganho de sinalização “positiva” por meio de expressão autócrina de netrina-1 provavelmente não é intrinsecamente suficiente para promover a metástase, como expressão forçada de netrina-1 em células não metastáticas que deixaram de ser associadas à formação de metástase.
[0149] Estas observações não apenas fornecem evidência para a importância de pares de ligante e receptores de dependência na regulagem do desenvolvimento de tumores, mas também ilustram uma nova estratégia terapêutica. De fato, atualmente, não há tratamento eficiente para pacientes com câncer de mama metastático, falta de tratamento que leva à morte 400.000 mulheres por ano em todo o mundo 24. Propomos no presente que tratamento com base na inibição da interação entre netrina-1 e os seus receptores de dependência poderá afetar positivamente uma parcela grande dos pacientes que sofrem de câncer metastático, tal como câncer de mama (ou seja, pacientes que exibiriam alta expressão de netrina-1 em tumores primários). Estes tratamentos poderão incluir drogas químicas, anticorpos monoclonais ou a proteína DCC-5Fbn apresentada no presente.
[0150] A. Netrina-1 é um marcador da agressividade em neuroblastoma humano (vide a Figura 9A, sua legenda e a Tabela 8) e a inibição da atividade de netrina-1 promove a morte de células de neuroblastoma (vide a Figura 10B e a sua legenda).
[0151] 26 linhagens de células de neuroblastoma (seja obtidas diretamente a partir de tumores de pacientes no Centre Léon Bérard (CLB-X) ou linhagens de células de neuroblastoma clássicas (IMR32, SHEP, SHSY ou SKNAS)) foram testadas como em (a) para determinar a expressão de netrina- 1 por meio de Q-RT-PCR. O nível de netrina-1 é indicado como (-) sem netrina- 1, (+, ++, +++) nível de netrina-1 baixo a alto. Pode-se observar que uma fração significativa de linhagens celulares possui alta expressão de netrina-1.
[0152] B. Netrina-1 é superexpressa em uma fração grande de glioma (vide Figura 10A e sua legenda) e a inibição da atividade de netrina-1 promove a morte de células de glioma (vide a Figura 10B e sua legenda).
[0153] C. Netrina-1 é superexpressa em câncer pulmonar humano (vide a Figura 11A, sua legenda e a Tabela 9) e a inibição da atividade de netrina-1 promove a morte de células de câncer do pulmão e evita o desenvolvimento de câncer do pulmão (vide as Figuras 12C e 12D e suas legendas).
[0154] Linhagens de células de câncer do pulmão derivadas de câncer do pulmão de células pequenas (SCLC) ou câncer do pulmão não de células pequenas (NSCLC) foram testadas como em (a) para determinar a expressão de netrina-1 por meio de Q-RT-PCR. O nível de netrina-1 é indicado como (-) sem netrina, (+, ++) baixo a alto nível de netrina-1. Pode-se observar que uma fração significativa de linhagens celulares possui alta expressão de netrina-1.
[0155] A expressão de netrina-1 examinada por meio de Q-RT PCR utilizando RNA total extraído de diferentes tumores humanos como nas Figuras 10A a 10B, 11A a 11C, 12A e 12B. A Tabela 10 indica (n) o número de tumores testados e o percentual de tumores que exibem superexpressão de netrina-1 em cada patologia. TABELA 10 100% das sete amostras metastáticas.
[0156] Para analisar se DCC estava sob sua forma monomérica a menos que netrina-1 estivesse presente, coexpressamos transitoriamente um DCC de comprimento total marcado com HA junto com DCC de comprimento total marcado com c-myc em células HEK293T. Imunoprecipitação foi realizada em seguida utilizando um anticorpo anti-c-myc e, conforme exibido na Figura 12A, apesar de boa expressão de HA e DCC marcado com c-myc, HA-DCC foi apenas modestamente incluído na retirada de c-myc-DCC na ausência de ligante, o que sugere que DCC estava principalmente presente na forma de monômero quando expresso em HEK293T na ausência de netrina-1. Nas mesmas condições experimentais, quando netrina-1 foi adicionada ao meio de cultivo (não exibido e Figura 15C) ou quando uma construção de expressão de netrina-1 foi coexpressa com as construções que expressam DCC (Figura 11A), HA-DCC foi claramente incluído na retirada de c-myc DCC, de forma a demonstrar que netrina-1 aciona a dimerização ou multimerização de DCC. Este resultado encontra-se de acordo com dados de Tessier-Lavigne e colegas que relataram pela primeira vez multimerização induzida por netrina-1 46, muito embora na nossa cultura e condições de imunoprecipitação, DCC exibe um nível modesto mas detectável de multimerização na ausência de netrina-1. Este baixo nível de multimerização constitutivo poderá ser atribuído à baixa afinidade de receptores DCC por si próprios na ausência de ligante ou para o sistema utilizado, que é baseado na expressão forçada de altos níveis de receptores transmembrana.
[0157] Investigamos em seguida se os outros receptores de netrina-1 UNC5H compartilham comportamento similar. Células HEK293T foram transfectadas transitoriamente com um UNC5H2 de comprimento total marcado com HA junto com UNC5H2 de comprimento total marcado com Flag na presença ou ausência de netrina-1. Imunoprecipitação foi realizada em seguida utilizando um anticorpo anti-Flag M2. Conforme exibido na Figura 11B, a presença de netrina-1 aciona imunoprecipitação eficiente de HA-UNC5H2 com Flag-UNC5H2. Desta forma, embora na ausência de netrina-1, DCC e UNC5H2 encontrem-se principalmente em formas monoméricas, DCC e UNC5H2 exibem maior propensão à multimerização na presença de netrina-1.
[0158] Para determinar se a multimerização induzida por netrina-1 é a etapa crucial de inibição da morte de células pró-apoptóticas DCC/UNC5H2, desenvolvemos um sistema quimérico no qual a dimerização de proteína pode ser induzida por um agente químico. Este sistema foi utilizado com sucesso para exibir o papel de dimerização de caspase-8 em ativação de caspase-8 49e a importância de multimerização de p75ntr em atividade pró- apoptótica de p75ntr 48. Este sistema é derivado da capacidade do composto Fk1012 de dimerização cruzada do motivo de FkBP. Domínios intracelulares de DCC e UNC5H2 foram fundidos no seu terminal N para motivos Fv2e FkBP derivados e a dimerização foi induzida utilizando o composto químico AP20187 (Figura 13A). Analisamos em primeiro lugar se o sistema desenvolvido recapitula multimerização induzida por netrina-1 do domínio intracelular UNC5H2. Células HEK293T foram cotransfectadas com Fv2e-UNC5H2-IC marcada com HA junto com Fv2e-UNC5H2-IC marcada com c-myc e coimunoprecipitações foram realizadas utilizando um anticorpo anti-c-myc. Conforme exibido na Figura 13B, sem adição de AP20187, HA-Fv2e-UNC5H2- IC foi pouco detectável na retirada de c-myc-Fv2e-UNC5H2-IC, de forma a sustentar que Fv2e-UNC5H2-IC é expresso em células HEK293T principalmente como monômero. Conforme esperado, a adição de AP20187 gerou a retirada eficiente de HA-Fv2e-UNC5H2-IC com c-myc-Fv2e-UNC5H2- IC. Resultados similares foram obtidos com Fv2e-DCC-IC (não exibido). Desta forma, este sistema de dimerização recapitula a dimerização do domínio intracelular dos receptores de netrina-1 DCC e UNC5H2.
[0159] Como este sistema de dimerização de DCC/UNC5H2 quimicamente indutível aparentemente trabalha adequadamente para imitar a multimerização de DCC/UNC5H2 induzida por netrina-1, determinamos em seguida se a dimerização de DCC/UNC5H2 era suficiente para inibir a atividade pró-apoptótica de DCC/UNC5H2. Células HEK293T foram forçadas a expressar Fv2e-DCC-IC na presença ou ausência de AP20187 e a morte celular foi determinada por manchas de azul de tripano, conforme descrito anteriormente, para medir a morte celular induzida por DCC 6, 27. Conforme exibido na Figura 14A, a expressão de Fv2e-DCC-IC foi associada a maior morte celular em comparação com a expressão dos motivos Fv2e sem a fusão de DCC-IC. De forma interessante, ao adicionar-se AP20187, a morte celular induzida por Fv2e-DCC-IC foi dramaticamente reduzida (Figura 14A). De forma similar, embora Fv2e-UNC5H2-IC acione a morte celular (Figura 14B) ou ativação de caspase (Figura 14C) quando expresso em HEK293T na ausência de AP20187, a adição da droga de dimerização é suficiente para reduzir significativamente a morte celular induzida por Fv2e-UNC5H2-IC (Figura 14B) ou ativação de caspase (Figura 14C). Desta forma, embora DCC-IC e UNC5H2-IC monoméricos sejam pró-apoptóticos, as formas multiméricas de DCC-IC ou UNC5H2-IC não exibem mais atividade pró-apoptótica. A capacidade de netrina-1 de inibir a atividade pró-apoptótica de DCC/UNC5H2, portanto, está intrinsecamente ligada à capacidade de netrina-1 de multimerizar DCC ou UNC5H2, pois este processo de multimerização é suficiente para desligar a atividade pró-apoptótica de DCC e UNC5H2.
[0160] Um modelo tentador seria aquele em que a forma monomérica de DCC ou UNC5H2 possui conformação espacial que é facilmente submetida à divisão de caspase inicial do domínio intracelular do receptor. Por outro lado, a presença do ligante geraria multimerização do domínio intracelular, que às vezes torna-se menos acessível à divisão de caspase. Ao longo desta linha, Arakawa e colegas demonstraram que a divisão de caspase de UNC5H2 é inibida pela presença de netrina-1 47. Ainda assim, devido a limitações técnicas, deixamos de detectar a divisão de DCC ou UNC5H2 em células forçadas a expressar as proteínas de fusão Fv2e. Um modelo alternativo de inibição da divisão seria aquele em que a multimerização de receptor induzida por netrina-1 aciona um sinal de sobrevivência, que de alguma forma inibe atividade pró-apoptótica constitutiva de DCC ou UNC5H2 relativa à divisão de caspase constitutiva. Deixamos de exibir, entretanto, que os processos de sinalização positiva conhecidos ativados por meio de DCC mediante ligação de netrina-1 estão envolvidos na atividade inibidora de netrina-1 sobre a atividade pró-apoptótica de DCC. Netrina-1 induz, por exemplo, a ativação mediada por DCC de ERK-1/2 3, quinases conhecidas por exibirem efeito anti-apoptótico. Inibidores clássicos do processo de ERK-1/2, entretanto, embora afetem a fosforilação de ERK-1/2 induzida por netrina-1, deixaram de bloquear o efeito inibidor de netrina-1 sobre a atividade pró- apoptótica de DCC (Forcet e Mehlen, não publicado). Desta forma, é provável que a multimerização de DCC induzida por netrina-1 afete a acessibilidade intracelular de DCC. Segue por ser demonstrado, entretanto, se esta é uma questão de estequiometria simples, ou se trazer mais perto os domínios extracelulares induz alteração de conformação dentro dos compartimentos intracelulares.
[0161] Caso os mecanismos subjacentes à multimerização do receptor induzida por netrina-1 ainda estejam por ser descritos, a observação de que a multimerização de DCC/UNC5H2 induzida por netrina-1 é suficiente para inibir a morte celular induzida por DCC/UNC5H2 pode representar uma ferramenta interessante para ligar a atividade pró-apoptótica de DCC ou UNC5H in vivo, em tumores nos quais netrina-1 é expressa de forma autócrina. Na verdade, demonstramos que a superexpressão de netrina-1 em intestino de camundongos está associada ao desenvolvimento de tumor intestinal devido à inibição da apoptose 18e observamos recentemente que netrina-1 é superexpressa na maior parte dos cânceres de mama metastáticos humanos. Além disso, o mecanismo de superexpressão de netrina-1 aparentemente é uma vantagem seletiva de células de tumores metastáticos para sobrevivência em configurações de ausência de netrina-1 no ambiente (vide Exemplos 2 e 3). Desta forma, a inibição da dimerização de DCC/UNC5H supostamente representaria uma forma interessante de acionar a apoptose de células tumorais.
[0162] Ao longo desta linha, demonstrou-se que o quinto domínio de fibronectina de DCC é um domínio de interação com netrina-1 (Figura 15A e 21), muito embora tenham também sido relatados dados conflitantes 43. Determinamos em primeiro lugar, portanto, se quinto domínio de fibronectina solúvel recombinante de DCC (DCC-5Fbn) poderia unir-se a netrina-1 recombinante. Teste ELISA demonstra que DCC-5Fbn une-se especificamente a netrina-1, e não ao domínio extracelular de um receptor não relacionado, IL3- R (Figura 15A). O Kd aproximado para DCC-5Fbn/netrina-1 foi estimado em aproximadamente 5 nM, mantendo a ordem de magnitude do Kd de DCC/netrina-1 descrito. Investigamos em seguida se este domínio foi suficiente para deslocar a interação de DCC/netrina-1. Conforme exibido na Figura 15B, utilizando um teste ELISA no qual o domínio extracelular de DCC foi revestido e a interação entre netrina-1 e DCC foi detectada por meio de imunorreatividade de netrina-1, observamos que, embora como controle positivo o domínio extracelular completo de DCC (DCC-EC) fosse suficiente para deslocar a interação entre DCC e netrina-1, DCC-5Fbn deixou de interferir. Desta forma, DCC-5Fbn interage com netrina-1, mas não é suficiente para inibir a interação entre DCC e netrina-1. Investigamos em seguida se DCC-5Fbn poderia influenciar a multimerização de DCC. Realizamos coimunoprecipitação em HEK293T transfectado de forma transitória com DCC de comprimento total marcado com HA junto com DCC de comprimento total marcado com c-myc na presença ou ausência de netrina-1. Também conforme descrito na Figura 1A, a presença de netrina-1 aciona a imunoprecipitação de HA-DCC com c-myc-DCC, o que demonstra multimerização de DCC induzida por netrina-1 (Figura 15C). Quando as células incubadas com netrina-1 também foram tratadas simultaneamente com DCC-5Fbn, entretanto, a interação entre DCC e c-myc retorna aos níveis não tratados de netrina-1. Desta forma, DCC-5Fbn interage com netrina-1 em uma região responsável pela aproximação mediada por netrina-1 de duas ou mais moléculas de DCC e é capaz de inibir a multimerização de DCC induzida por netrina-1.
[0163] Testamos em seguida se DCC-5Fbn poderia, conseqüentemente, acionar a morte celular induzida por receptores de netrina- 1. Com este propósito, células HEK293T foram forçadas a expressar DCC na presença ou ausência de netrina-1, com ou sem DCC-5Fbn, e a morte celular foi determinada por meio de teste de exclusão de azul de tripano (Figura 16A). Conforme exibido na Figura 16A, embora DCC acione a apoptose na ausência de netrina-1, atividade pró-apoptótica bloqueada pela presença de netrina-1, a presença de DCC-5Fbn é suficiente para bloquear a atividade inibidora de netrina-1, de forma a gerar a morte celular induzida por DCC. Como o sistema de células HEK293T utiliza expressão ectópica de netrina-1, testamos em seguida DCC-5Fbn em um modelo biologicamente mais relevante. Demonstramos recentemente que, em comparação com cânceres de mama não metastáticos, a maior parte dos cânceres de mama metastáticos humanos superexpressa netrina-1. Também demonstramos que a titulação de netrina-1 superexpressa aciona a apoptose de células tumorais in vitro e a inibição de metástase em camundongos (vide Exemplos 2 e 3). Muitas linhagens de células tumorais de mama aparentemente expressam netrina-1 e demonstramos que a titulação de netrina-1 em células 4T1 de carcinoma de mama de camundongos aciona a apoptose (vide Exemplos 2 e 3). Conforme exibido na Figura 16B, a adição de DCC-5Fbn a um cultivo de células 4T1 é associada a maior morte celular.
[0164] Em resumo, demonstramos no presente que a multimerização dos receptores de dependência DCC e UNC5H é um mecanismo suficiente para bloquear a sua atividade pró-apoptótica. De forma interessante, este mecanismo inibidor aparentemente espelha o que é observado com receptores de morte. De fato, sabe-se que TNFr ou Fas necessita de trimerização para induzir a apoptose 45. Esta diferença intrínseca pode representar, portanto, valor agregado para estratégias terapêuticas utilizando receptores de dependência. De fato, a busca de moléculas terapêuticas no passado gerou principalmente acertos que agem sobre a inibição de processos celulares (tais como inibidores de quinases, inibidores de IAP) e não ativadores. Conseqüentemente, a inibição da multimerização de receptores de netrina-1 utilizando DCC-5Fbn recombinante ou por meio de qualquer composto selecionado para interferir com a multimerização de receptores aparece como estratégia tentadora para o tratamento de cânceres nos quais foi adquirida a expressão de autócrina de netrina-1.
[0165] Demonstramos no presente que netrina-1 aciona a multimerização de receptores de DCC e UNC5H. Utilizando um sistema no qual a dimerização é induzida quimicamente, demonstramos que a multimerização do domínio intracelular de receptores de netrina-1, tais como DCC e UNC5H2, é a etapa fundamental para inibir a sua atividade pró-apoptótica. Propomos, portanto, um modelo no qual receptores com dependência de netrina-1 monoméricos são pró-apoptóticos, enquanto a sua multimerização, induzida por netrina-1, abole a sua atividade pró-apoptótica. Utilizando esta propriedade, propomos o uso de um domínio específico recombinante da região extracelular de DCC que (i) interage com netrina-1 e (ii) inibe a multimerização induzida por netrina-1, a fim de acionar a apoptose de células tumorais. REFERÊNCIAS 1. Serafini, T. et al. Netrin-1 is required for commissural axon guidance in the developing vertebrate nervous system. Cell 87, 1001-14 (1996). 2. Keino-Masu, K. et al. Deleted in Colorectal Cancer (DCC) encodes a netrin receptor. Cell 87, 175-85 (1996). 3. Forcet, C. et al. Netrin-1-mediated axon outgrowth requires deleted in colorectal cancer-dependent MAPK activation. Nature 417, 443-7 (2002). 4. Ackerman, S. L. et al. The mouse rostral cerebellar malformation gene encodes an UNC-5-like protein. Nature 386, 838-42 (1997). 5. Hong, K. et al. A ligand-gated association between cytoplasmic domains of UNC5 and DCC family receptors converts netrin- induced growth cone attraction to repulsion. Cell 97, 927-41 (1999). 6. Mehlen, P. et al. The DCC gene product induces apoptosis by a mechanism requiring receptor proteolysis. Nature 395, 801-4 (1998). 7. Llambi, F., Causeret, F., Bloch-Gallego, E. e Mehlen, P. Netrin-1 acts as a survival factor via its receptors UNC5H and DCC. Embo J. 20, 2715-22 (2001). 8. Bordeaux, M. C. et al. The RET proto-oncogene induces apoptosis: a novel mechanism for Hirschsprung disease. Embo J. 19, 4056-63 (2000). 9. Stupack, D. G., Puente, X. S., Boutsaboualoy, S., Storgard, C. M. e Cheresh, D. A. Apoptosis of adherent cells by recruitment of caspase-8 to unligated integrins. J. Cell Biol. 155, 459-70 (2001). 10. Thibert, C. et al. Inhibition of neuroepithelial patched- induced apoptosis by sonic hedgehog. Science 301, 843-6 (2003). 11. Matsunaga, E. et al. RGM and its receptor neogenin regulate neuronal survival. Nat. Cell Biol. 6, 749-55 (2004). 12. Rabizadeh, S. et al. Induction of apoptosis by the low- affinity NGF receptor. Science 261, 345-8 (1993). 13. Mehlen, P. e Thibert, C. Dependence receptors: between life and death. Cell Mol. Life Sci. 61, 1854-66 (2004). 14. Bredesen, D. E., Mehlen, P. e Rabizadeh, S. Receptors that mediate cellular dependence. Cell Death Differ 12, 1031-43 (2005). 15. Fearon, E. R. et al. Identification of a chromosome 18q gene that is altered in colorectal cancers. Science 247, 49-56 (1990). 16. Kinzler, K. W. e Vogelstein, B. Lessons from hereditary colorectal cancer. Cell 87, 159-70 (1996). 17. Thiebault, K. et al. The netrin-1 receptors UNC5H are putative tumor suppressors controlling cell death commitment. Proc. Natl. Acad. Sci. U. S. A. 100, 4173-4178 (2003). 18. Mazelin, L. et al. Netrin-1 controls colorectal tumorigenesis by regulating apoptosis. Nature 431, 80-4 (2004). 19. Bernet, A. et al. The netrin-1 receptor UNC5H3 is a tumor suppressor in colorectal malignancies submitted (2007). 20. Aslakson, C. J. e Miller, F. R. Selective events in the metastatic process defined by analysis of the sequential dissemination of subpopulations of a mouse mammary tumor. Cancer Res. 52, 1399-405 (1992). 21. Geisbrecht, B. V., Dowd, K. A., Barfield, R. W., Longo, P. A. e Leahy, D. J. Netrin binds discrete subdomains of DCC and UNC5 and mediates interactions between DCC and heparin. J. Biol. Chem. 278, 32561-8 (2003). 22. Llambi, F. et al. The dependence receptor UNC5H2 mediates apoptosis through DAP-kinase. Embo J. 24, 1192-201 (2005). 23. Inbal, B. et al. DAP kinase links the control of apoptosis to metastasis. Nature 390, 180-4 (1997). 24. Andre, F. et al. Breast cancer with synchronous metastases: trends in survival during a 14-year period. J. Clin. Oncol. 22, 33028 (2004). 25. de Cremoux, P. et al. Inter-laboratory quality control for hormone-dependent gene expression in human breast tumors using real-time reverse transcription-polymerase chain reaction. Endocr. Relat. Cancer 11, 48995 (2004). 26. Latil, A. et al. Quantification of expression of netrins, slits and their receptors in human prostate tumors. Int. J. Cancer 103, 306-15 (2003). 27. Forcet, C., Ye, X., Granger, L., Corset, V., Shin, H., Bredesen, D. E. e Mehlen, P. (2001). The dependence receptor DCC (deleted in colorectal cancer) defines an alternative mechanism for caspase activation. Proc. Natl. Acad. Sci. U. S. A., 98, 3416-3421. 28. de Kok, J. B. et al. Normalization of gene expression measurements in tumor tissues: comparison of 13 endogenous control genes. Lab. Invest. 85, 154-9 (2005). 29. Mehlen, P. e Fearon, E. R. Role of the dependence receptor DCC in colorectal cancer pathogenesis. J. Clin. Oncol. 22, 3420-8 (2004). 30. Stupack, D. G. et al. Potentiation of neuroblastoma metastasis by loss of caspase-8. Nature 439, 95-9 (2006). 31. Serafini, T. et al. The netrins define a family of axon outgrowth-promoting proteins homologous to C. elegans UNC-6. Cell 78, 40924 (1994). 32. Yebra, M. et al. Recognition of the neural chemoattractant Netrin-1 by integrins alpha6beta4 and alpha3beta1 regulates epithelial cell adhesion and migration. Dev. Cell 5, 695-707 (2003). 33. Srinivasan, K., Strickland, P., Valdes, A., Shin, G. C. e Hinck, L. Netrin-1/neogenin interaction stabilizes multipotent progenitor cap cells during mammary gland morphogenesis. Dev. Cell 4, 371-82 (2003). 34. Liu, Y. et al. Novel role for Netrins in regulating epithelial behavior during lung branching morphogenesis. Curr. Biol. 14, 897-905 (2004). 35. Park, K. W. et al. The axonal attractant Netrin-1 is an angiogenic factor. Proc. Natl. Acad. Sci. U. S. A. 101, 16210-5 (2004). 36. Lu, X. et al. The netrin receptor UNC5B mediates guidance events controlling morphogenesis of the vascular system. Nature 432, 179-86 (2004). 37. Nguyen, A. e Cai, H. Netrin-1 induces angiogenesis via a DCC-dependent ERK1/2-eNOS feed-forward mechanism. Proc. Natl. Acad. Sci. U. S. A. 103, 6530-5 (2006). 38. Wilson, B. D. et al, Netrins Promote Development and Therapeutic Angiogenesis. Science (2006). 39. Chan, S. S., Zheng, H., Su, M. W., Wilk, R., Killeen, M. T., Hedgecock, E. M. e Culotti, J. G. (1996). UNC-40, a C. elegans homolog of DCC (Deleted in Colorectal Cancer), is required in motile cells responding to UNC-6 netrin cues. Cell, 87, 187-195. 40. Ellerby, L. M., Hackam, A. S., Propp, S. S., Ellerby, H. M., Rabizadeh, S., Cashman, N. R., Trifiro, M. A., Pinsky, L., Wellington, C. L., Salvesen, G. S., Hayden, M. R. e Bredesen, D. E. (1999). Kennedy’s disease: caspage cleavage of the androgen receptor is a crucial event in cytotoxicity. J. Neurochem., 72, 185-195. 41. Fazeli, A., Dickinson, S. L., Hermiston, M. L., Tighe, R. V., Steen, R. G., Small, C. G., Stoeckli, E. T., Keino-Masu, K., Masu, M., Rayburn, H., Simons, J., Bronson, R. T., Gordon, J. I., Tessier-Lavigne, M. e Weinberg, R. A. (1997). Phenotype of mice lacking functional Deleted in Colorectal Cancer (DCC) gene. Nature, 386, 796-804. 42. Hedgecock, E. M., Culotti, J. G. e Hall, D. H. (1990). The unc-5, unc-6 and unc-40 genes guide circumferential migrations of pioneer axons and mesodermal cells on the epidermis in C. elegans. Neuron, 4, 61-85. 43. Kruger, R. P., Lee, J., Li, W. e Guan, K. L. (2004). Mapping netrin receptor binding reveals domains of Unc5 regulating its tyrosine phosphorylation. J. Neurosci., 24, 10826-10834. 44. Mehlen, P. e Bredesen, D. E. (2004). The dependence receptor hypothesis. Apoptosis, 9, 37-49. 45. Muppidi, J. R., Tschopp, J. e Siegel, R. M. (2004). Life and death decisions: secondary complexes and lipid rafts in TNF receptor family signal transduction. Immunity, 21, 461-465. 46. Stein, E., Zou, Y., Poo, M. e Tessier-Lavigne, M. (2001), Binding of DCC by netrin-1 to mediate axon guidance independent of adenosine A2B receptor activation. Science, 291, 1976-1982. 47. Tanikawa, C., Matsuda, K., Fukuda, S., Nakamura, Y. e Arakawa, H. (2003), p53RDL1 regulates p53-dependent apoptosis. Nat. Cell Biol., 5, 216-223. 48. Wang, J. J., Rabizadeh, S., Tasinato, A., Sperandio, S., Ye, X., Green, M., Assa-Munt, N., Spencer, D. e Bredesen, D. E. (2000), Dimerization-dependent block of the proapoptotic effect of p75 (NTR). J. Neurosci. Res., 60, 587-593. 49. Yang, X., Chang, H. Y. e Baltimore, D. (1998). Autoproteolytic activation of pro-caspases by oligomerization. Mol. Cell, 1, 319325. 50. Mehlen, P. e C. Furne (2005). Netrin-1: when a neuronal guidance cue turns out to be a regulator of tumorigenesis. Cell Mol. Life Sci. 62: 2599-616.
Claims (34)
1. MÉTODO IN VITRO DE SELEÇÃO DE UM COMPOSTO, para a prevenção ou tratamento de câncer, o mencionado câncer a ser evitado ou tratado é selecionado a partir do grupo que consiste em câncer de mama, câncer do pulmão, neuroblastoma, glioma, leucemia, sarcoma, melanoma e adenocarcinoma, em que o mencionado câncer a ser prevenido ou tratado é um câncer em que as células tumorais expressam ou superexpressam netrina- 1, caracterizado pelo fato de que o mencionado método compreende as etapas de: (a) ter um meio que contenha netrina-1, ou um de seus fragmentos, e um receptor de netrina-1, ou um de seus fragmentos, em que: - a mencionada netrina-1, ou um de seus fragmentos, e o mencionado receptor de netrina-1, ou um de seus fragmentos, são capazes de interagir especificamente juntos para formar um par de ligação; e/ou - a mencionada netrina-1, ou um de seus fragmentos, é capaz de induzir a dimerização ou a multimerização do domínio intracelular do mencionado receptor de netrina-1; (b) contato do mencionado meio com o composto a ser testado; (c) - medição da inibição da interação entre a netrina-1, ou um de seus fragmentos, e o mencionado receptor de netrina-1, ou um de seus fragmentos; e/ou - determinação de se o mencionado composto inibe a dimerização ou multimerização do mencionado receptor de netrina-1, ou um de seus fragmentos, particularmente a dimerização do domínio intracelular do mencionado receptor de netrina-1; e (d) seleção do mencionado composto se: - a medição da etapa (c) demonstrar uma inibição significativa da interação entre a netrina-1, ou um de seus fragmentos, e o receptor de netrina-1, ou um de seus fragmentos, na presença do mencionado composto; e/ou - a determinação na etapa (c) demonstrar uma inibição significativa da dimerização ou multimerização, na presença do mencionado composto, do domínio intracelular do mencionado receptor de netrina-1.
2. MÉTODO IN VITRO, de acordo com a reivindicação 1, caracterizado pelo fato de que o mencionado câncer a ser evitado ou tratado é selecionado a partir do grupo que consiste em adenocarcinoma do ovário, adenocarcinoma renal, adenocarcinoma pancreático, adenocarcinoma do útero, adenocarcinoma do estômago, adenocarcinoma do rim e adenocarcinoma retal.
3. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 2, caracterizado pelo fato de que o mencionado câncer a ser evitado ou tratado é um câncer metastático.
4. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 3, caracterizado pelo fato de que, na etapa (a), o mencionado receptor de netrina-1 é selecionado a partir do grupo que consiste em Excluído em Câncer Colo-Retal (DCC), homólogo de Unc-5 (UNC5H), neogenina e adenosina A2b.
5. MÉTODO IN VITRO, de acordo com a reivindicação 4, caracterizado pelo fato de que, na etapa (a), o mencionado receptor de netrina- 1 é selecionado a partir do grupo que consiste de DCC, UNC5H1, UNC5H2 e UNC5H3.
6. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 5, caracterizado pelo fato de que, na etapa (a): - o mencionado fragmento receptor de netrina-1 compreende ou é o domínio extracelular do receptor de netrina-1, ou uma de suas partes capaz de interagir com netrina-1; e/ou - o mencionado fragmento receptor de netrina-1 compreende ou é o domínio intracelular do receptor de netrina-1, ou uma de suas partes capaz de dimerizar-se ou multimerizar-se na presença de netrina-1.
7. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 6, caracterizado pelo fato de que, na etapa (a), a mencionada netrina-1 e/ou o mencionado receptor de netrina-1 são de mamíferos.
8. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 7, caracterizado pelo fato de que, na etapa (a), a mencionada netrina-1 é de galinha.
9. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 8, caracterizado pelo fato de que a mencionada netrina-1 e/ou o mencionado receptor de netrina-1 e/ou o composto a ser testado é marcado por um marcador capaz de ser medido direta ou indiretamente.
10. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 9, caracterizado pelo fato de que, na etapa (c): - a medição da inibição da interação entre a netrina-1, ou um de seus fragmentos, e o mencionado receptor de netrina-1, ou um de seus fragmentos, é conduzida por meio de imunoteste (particularmente por meio de ELISA ou de Teste Imunorradiométrico (IRMA)), por meio de Teste de Proximidade de Cintilação (SPA) ou Transferência de Energia de Ressonância de Fluorescência (FRET); e/ou - a dimerização ou multimerização, ou sua inibição, do mencionado receptor de netrina-1, ou um de seus fragmentos, particularmente do domínio intracelular, é conduzida por meio de imunoprecipitação ou FRET.
11. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 10, caracterizado pelo fato de que, na etapa (a), o mencionado meio contém células que expressam, na sua membrana de superfície, um receptor de netrina-1 endógeno ou recombinante, particularmente pelo menos o domínio extracelular de um receptor de netrina-1 recombinante.
12. MÉTODO IN VITRO, de acordo com a reivindicação 11, caracterizado pelo fato de que, na etapa (a), o mencionado meio contém células que expressam o receptor de netrina-1 recombinante.
13. MÉTODO IN VITRO, de acordo com a reivindicação 11, caracterizado pelo fato de que, na etapa (a), o mencionado meio contém células tumorais que expressam de forma endógena o mencionado receptor de netrina-1 na sua superfície de membrana e que expressam ou superexpressam a netrina-1, e em que, na etapa (c), a inibição da interação entre a netrina-1 e seu receptor de netrina-1 na presença do composto a ser testado é medida por meio da apoptose ou morte celular induzida pela presença do composto a ser testado.
14. MÉTODO IN VITRO, de acordo com a reivindicação 13, caracterizado pelo fato de que, na etapa (a), o mencionado meio contém células tumorais metastáticas.
15. MÉTODO IN VITRO, de acordo com uma das reivindicações 1 a 14, caracterizado pelo fato de ser para a seleção de um composto para a prevenção ou o tratamento de câncer, em que o mencionado método compreende as etapas a seguir de: (a) ter um meio que contém uma célula de mamífero que expressa um receptor de netrina-1 endógeno ou recombinante, ou um de seus fragmentos que compreende pelo menos o seu domínio intracelular,; (b) contato do mencionado meio com o composto a ser testado; (c) determinar se a dimerização ou multimerização do mencionado domínio intracelular de receptor de netrina-1 é inibida na presença do mencionado composto a ser testado; e (d) seleção do mencionado composto caso a determinação na etapa (c) demonstre uma inibição significativa da dimerização ou multimerização do domínio intracelular do mencionado receptor de netrina-1.
16. MÉTODO IN VITRO, de acordo com a reivindicação 15, caracterizado pelo fato de que a mencionada célula da etapa (a) é uma célula tumoral.
17. MÉTODO IN VITRO, de acordo com a reivindicação 15, caracterizado pelo fato de que a mencionada célula da etapa (a) é uma célula que apresenta dimerização ou multimerização de seu domínio intracelular de receptor de netrina-1 ou uma célula em que seu domínio intracelular de receptor de netrina-1 é capaz de dimerizar ou multimerizar na presença de netrina-1.
18. MÉTODO IN VITRO, de acordo com qualquer uma das reivindicações 15 a 17, caracterizado pelo fato de que, na etapa (b), o meio ainda contém netrina-1, ou um de seus fragmentos capaz de se ligar ao domínio extracelular do receptor de netrina-1.
19. MÉTODO IN VITRO, de acordo com qualquer uma das reivindicações 15 a 18, caracterizado pelo fato de que compreende ainda determinar se a presença do composto a ser testado induz a morte celular da referida célula de mamífero; e em que a etapa (d) compreende a determinação da morte celular da referida célula de mamífero.
20. MÉTODO IN VITRO DE PREVISÃO DA PRESENÇA DE CÂNCER metastático ou câncer agressivo em um paciente que possui um tumor primário, a partir de uma biópsia do mencionado paciente que contém células tumorais primárias, o mencionado câncer a ser evitado ou tratado é selecionado a partir do grupo que consiste em câncer de mama, câncer do pulmão, neuroblastoma, glioma, leucemia, sarcoma, melanoma e adenocarcinoma, em que o mencionado câncer a ser prevenido ou tratado é um câncer em que as células tumorais expressam ou superexpressam netrina- 1, caracterizado pelo fato de que o mencionado método compreende a etapa a seguir de: (a) medição do nível de produto de expressão de netrina-1 na mencionada biópsia, em que o referido produto é (i) RNA que codifica netrina-1 ou (ii) proteína de netrina-1; e (b) comparação do referido nível de produto de expressão com a expressão do nível de produto de expressão de netrina-1 em uma biópsia de tumor primário não metastático ou em uma biópsia de câncer não agressivo; em que um aumento com uma razão superior a 2 entre os níveis do produto de expressão de netrina-1 na biópsia a ser testada e na biópsia de referência não metastática ou não agressiva é indicativo da presença de um câncer metastático ou um câncer agressivo.
21. MÉTODO DE DETERMINAÇÃO IN VITRO DA EFICIÊNCIA DE UM TRATAMENTO ANTICANCERÍGENO, para um paciente ou para selecionar in vitro pacientes que reajam a um tratamento anticancerígeno específico, o mencionado câncer a ser evitado ou tratado é selecionado a partir do grupo que consiste em câncer de mama, câncer do pulmão, neuroblastoma, glioma, leucemia, sarcoma, melanoma e adenocarcinoma, em que o mencionado câncer a ser prevenido ou tratado é um câncer em que as células tumorais expressam ou superexpressam netrina-1, caracterizado pelo fato de que o mencionado método compreende as etapas a seguir de: - medição do nível de produto de expressão de netrina-1 na mencionada biópsia, em que o referido produto é (i) RNA que codifica netrina-1 ou (ii) proteína de netrina-1; em que a eficiência do mencionado tratamento anticancerígeno é correlacionada com a redução em uma razão de pelo menos 2 da quantidade do nível do produto de expressão de netrina-1 medido na mencionada biópsia; ou em que os pacientes selecionados que reagem a um tratamento anticancerígeno específico são pacientes em que a quantidade do nível do produto de expressão de netrina-1 medida na sua biópsia foi diminuída em uma proporção de pelo menos 2 após o mencionado tratamento específico.
22. MÉTODO, de acordo com a reivindicação 21, caracterizado pelo fato de que o mencionado câncer induziu uma superexpressão de netrina- 1 e/ou é um câncer metastático.
23. MÉTODO, de acordo com qualquer uma das reivindicações a 22, caracterizado pelo fato de que o mencionado RNA que codifica netrina-1 é medido por meio de um método de reação em cadeia de polimerase (PCR) reversa em tempo real quantitativo.
24. MÉTODO, de acordo com qualquer uma das reivindicações a 22, caracterizado pelo fato de que a proteína de netrina-1 é medida usando anticorpos específicos capazes de reconhecer especificamente a mencionada proteína de netrina-1.
25. MÉTODO, de acordo com uma das reivindicações 20 a 24, caracterizado pelo fato de que o tumor primário é um tumor primário de um câncer selecionado a partir do grupo que consiste de câncer de mama, câncer do pulmão, neuroblastoma, glioma, leucemia, sarcoma, melanoma e adenocarcinoma.
26. MÉTODO, de acordo com a reivindicação 25, caracterizado pelo fato de que o mencionado adenocarcinoma é selecionado a partir do grupo que consiste em adenocarcinoma do ovário, adenocarcinoma renal, adenocarcinoma pancreático, adenocarcinoma do útero, adenocarcinoma do estômago, adenocarcinoma do rim e adenocarcinoma retal.
27. USO DE UM COMPOSTO, selecionado a partir do grupo que consiste em: - um composto que compreende um domínio extracelular de receptor de netrina-1 ou seu fragmento capaz de inibir especificamente a interação entre a netrina-1 e o mencionado receptor de netrina-1, e/ou capaz de inibir a dimerização ou multimerização do domínio intracelular do mencionado receptor de netrina-1; e - um anticorpo monoclonal ou policlonal dirigido especificamente contra a netrina-1 ou o domínio extracelular do receptor de netrina-1 ou ao fragmento de netrina-1 capaz de interagir com o domínio extracelular do mencionado receptor de netrina-1, caracterizado pelo fato de ser para a fabricação de um medicamento para a prevenção ou o tratamento de câncer em mamíferos, incluindo seres humanos.
28. USO, de acordo com a reivindicação 27, caracterizado pelo fato de que o mencionado domínio extracelular de receptor de netrina-1 ou um de seus fragmentos é selecionado a partir do grupo que consiste de DCC, UNC5H , neogenina e adenosina A2b.
29. USO, de acordo com a reivindicação 27, caracterizado pelo fato de que o mencionado composto compreende um domínio extracelular de receptor de netrina-1 de DCC.
30. USO, de acordo com a reivindicação 27, caracterizado pelo fato de que o mencionado composto é DCC-EC-Fc ou DCC-5Fbn.
31. USO, acordo com qualquer uma das reivindicações 27 a 30, caracterizado pelo fato de que o mencionado câncer é selecionado a partir do grupo que consiste em câncer de mama, câncer do pulmão, neuroblastoma, glioma, leucemia, sarcoma, melanoma e adenocarcinoma, em que o mencionado câncer a ser prevenido ou tratado é um câncer em que as células tumorais expressam ou superexpressam netrina-1.
32. USO, de acordo com qualquer uma das reivindicações 27 a 31, caracterizado pelo fato de que o mencionado câncer é um câncer metastático.
33. USO, de acordo com qualquer uma das reivindicações 27 a 32, caracterizado pelo fato de que o mencionado adenocarcinoma é selecionado a partir do grupo que consiste em adenocarcinoma do ovário, adenocarcinoma renal, adenocarcinoma pancreático, adenocarcinoma do útero, adenocarcinoma do estômago, adenocarcinoma do rim e adenocarcinoma retal.
34. USO, de acordo com qualquer uma das reivindicações 27 a 33, caracterizado pelo fato de que as células tumorais primárias do mencionado câncer expressam ou superexpressam netrina-1.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US77692606P | 2006-02-28 | 2006-02-28 | |
| US60/776,926 | 2006-02-28 | ||
| PCT/EP2007/051920 WO2007099133A1 (en) | 2006-02-28 | 2007-02-28 | Screening for anti-cancer compounds using netrin-1 activity |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0707040A2 BRPI0707040A2 (pt) | 2011-04-12 |
| BRPI0707040B1 true BRPI0707040B1 (pt) | 2021-11-23 |
| BRPI0707040B8 BRPI0707040B8 (pt) | 2022-03-08 |
Family
ID=38051332
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0707040A BRPI0707040B8 (pt) | 2006-02-28 | 2007-02-28 | Método in vitro de seleção de um composto, método in vitro de previsão da presença de câncer, método de determinação in vitro da eficiência de um tratamento anticancerígeno e uso de um composto |
Country Status (21)
| Country | Link |
|---|---|
| US (3) | US20090226458A1 (pt) |
| EP (1) | EP1989546B1 (pt) |
| JP (1) | JP5602368B2 (pt) |
| KR (2) | KR20080113368A (pt) |
| CN (1) | CN101389958B (pt) |
| AU (1) | AU2007220515B2 (pt) |
| BR (1) | BRPI0707040B8 (pt) |
| CA (1) | CA2638974C (pt) |
| CY (1) | CY1118325T1 (pt) |
| DK (1) | DK1989546T3 (pt) |
| ES (1) | ES2601352T3 (pt) |
| HU (1) | HUE030738T2 (pt) |
| IL (1) | IL193580A (pt) |
| LT (1) | LT1989546T (pt) |
| MX (1) | MX336675B (pt) |
| PL (1) | PL1989546T3 (pt) |
| PT (1) | PT1989546T (pt) |
| SG (1) | SG172645A1 (pt) |
| SI (1) | SI1989546T1 (pt) |
| WO (1) | WO2007099133A1 (pt) |
| ZA (1) | ZA200806913B (pt) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2724830A1 (en) * | 2008-05-21 | 2009-11-26 | Centre Leon Berard | Inhibition of the nt-3:trkc bound and its application to the treatment of cancer such as neuroblastoma |
| WO2009141440A1 (en) * | 2008-05-21 | 2009-11-26 | Centre National De La Recherche Scientifique (Cnrs) | Netrin-1 overexpression as a biological marker and a survival factor for aggressive neuroblastoma |
| EP2208738A1 (en) * | 2009-01-09 | 2010-07-21 | Centre National pour la Recherche Scientifique (CNRS) | Method for the selection of endothelial cells death inducers via netrin-1 and its applications |
| US8052960B2 (en) | 2009-01-20 | 2011-11-08 | The Penn State Research Foundation | Netrin-1 as a biomarker of injury and disease |
| EP2267153A1 (en) * | 2009-05-26 | 2010-12-29 | Université Claude Bernard Lyon 1 | Identification of netrin-1 receptor unc5c gene mutation in solid cancers |
| US9050298B2 (en) | 2010-05-28 | 2015-06-09 | The Regents Of The University Of California | Method of treating ischemia/reperfusion injuries to a heart with netrin-1 |
| US20130336972A1 (en) * | 2010-08-26 | 2013-12-19 | Christian Klein | Recombinant fc-fusion protein of the fifth fibronectin type iii domain of dcc |
| JP2015504510A (ja) * | 2011-11-04 | 2015-02-12 | インヴィヴィス,エスエーエス | 抗エストロゲン剤の効果予測バイオマーカーのアッセイ |
| EP2708241A1 (en) | 2012-09-12 | 2014-03-19 | Netris Pharma | Recombinant Fc-fusion protein of the two Immunoglobulin domains of UNC5 |
| EP2708231A1 (en) * | 2012-09-12 | 2014-03-19 | Netris Pharma | Combined treatment with netrin-1 interfering drug and chemotherapeutic drug |
| EP2893939A1 (en) * | 2014-01-10 | 2015-07-15 | Netris Pharma | Anti-netrin-1 antibody |
| CN105031611B (zh) * | 2015-06-18 | 2018-02-09 | 中国医学科学院基础医学研究所 | netrin‑1蛋白在制备用于肿瘤治疗的药物中的用途 |
| TW201720459A (zh) | 2015-11-02 | 2017-06-16 | 妮翠斯製藥公司 | Ntn1中和劑與抑制後生控制之藥物之組合治療 |
| US10379534B2 (en) * | 2016-01-28 | 2019-08-13 | Qualcomm Incorporated | Drone flight control |
| CN107011444B (zh) * | 2016-01-28 | 2021-11-16 | 中国科学院脑科学与智能技术卓越创新中心 | 一种筛选hERG钾离子通道激动剂和毒性检测方法 |
| CN105925578A (zh) * | 2016-05-30 | 2016-09-07 | 东北师范大学 | 靶向沉默Neogenin的shRNA |
| AU2018205730B2 (en) | 2017-01-05 | 2024-05-30 | Centre Leon Berard | Combined treatment with netrin-1 interfering drug and immune checkpoint inhibitors drugs |
| US20230204565A1 (en) * | 2020-01-02 | 2023-06-29 | The Regents Of The University Of California | Methods for Culturing Cancer Cells and for Inhibiting Invasion of Cancer |
| CN112812167B (zh) * | 2021-01-06 | 2023-04-11 | 东北师范大学 | 一种促进细胞存活的Netrin-1模拟肽、Netrin-1截短多肽及其应用 |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3611194A1 (de) * | 1986-04-04 | 1987-10-08 | Bayer Ag | Cancerostatisches mittel |
| US5565331A (en) | 1993-11-12 | 1996-10-15 | The Regents Of The University Of California | Nucleic acids encoding neural axon outgrowth modulators |
| US6028173A (en) | 1995-06-30 | 2000-02-22 | Genzyme Corporation | Human chromosome 16 genes, compositions, methods of making and using same |
| US6030806A (en) | 1995-06-30 | 2000-02-29 | Landes; Gregory M. | Human chromosome 16 genes, compositions, methods of making and using same |
| US5824775A (en) * | 1996-04-19 | 1998-10-20 | The Regents Of The University Of California | Human netrin-1 |
| JPH11335398A (ja) * | 1998-05-22 | 1999-12-07 | Hoechst Marion Roussel Kk | 新規な骨誘導活性を有する単量体蛋白質およびそれらからなる軟骨・骨疾患の予防および治療薬 |
| US5939271A (en) | 1997-02-19 | 1999-08-17 | The Regents Of The University Of California | Netrin receptor |
| WO2005074556A2 (en) * | 2004-01-30 | 2005-08-18 | The General Hospital Corporation | Netrin compositions and methods of use thereof |
| US20080038255A1 (en) * | 2004-06-04 | 2008-02-14 | Aplied Research Systems Ars Holding N.V. | Splice Variant of Unc5h2 |
| AU2005275062A1 (en) | 2004-07-14 | 2006-02-23 | University Of Utah Research Foundation | Netrin-related compositions and uses |
| EP1814579B1 (fr) | 2004-11-22 | 2014-01-08 | Centre National de la Recherche Scientifique | Netrine 4 mutee, ses fragments et leur utilisation comme medicaments |
| US20060153840A1 (en) * | 2005-01-12 | 2006-07-13 | Anne Eichmann | Methods for preventing or treating a condition or a disease associated with angiogenesis |
| CA2489780A1 (en) | 2005-01-12 | 2006-07-12 | Inserm | Methods for preventing or treating a condition or a disease associated with angiogenesis |
| JP4677376B2 (ja) | 2006-07-07 | 2011-04-27 | キヤノン株式会社 | 画像処理装置、画像処理方法、画像処理プログラム及び記憶媒体 |
| WO2009141440A1 (en) * | 2008-05-21 | 2009-11-26 | Centre National De La Recherche Scientifique (Cnrs) | Netrin-1 overexpression as a biological marker and a survival factor for aggressive neuroblastoma |
-
2007
- 2007-02-28 HU HUE07726556A patent/HUE030738T2/en unknown
- 2007-02-28 BR BRPI0707040A patent/BRPI0707040B8/pt active IP Right Grant
- 2007-02-28 ES ES07726556.9T patent/ES2601352T3/es active Active
- 2007-02-28 SI SI200731865A patent/SI1989546T1/sl unknown
- 2007-02-28 CN CN200780006936.3A patent/CN101389958B/zh active Active
- 2007-02-28 PT PT77265569T patent/PT1989546T/pt unknown
- 2007-02-28 EP EP07726556.9A patent/EP1989546B1/en active Active
- 2007-02-28 WO PCT/EP2007/051920 patent/WO2007099133A1/en not_active Ceased
- 2007-02-28 AU AU2007220515A patent/AU2007220515B2/en active Active
- 2007-02-28 SG SG2011038783A patent/SG172645A1/en unknown
- 2007-02-28 KR KR1020087022051A patent/KR20080113368A/ko not_active Ceased
- 2007-02-28 CA CA2638974A patent/CA2638974C/en active Active
- 2007-02-28 DK DK07726556.9T patent/DK1989546T3/en active
- 2007-02-28 MX MX2008011067A patent/MX336675B/es unknown
- 2007-02-28 JP JP2008556779A patent/JP5602368B2/ja active Active
- 2007-02-28 KR KR1020147029279A patent/KR101587932B1/ko active Active
- 2007-02-28 US US12/224,384 patent/US20090226458A1/en not_active Abandoned
- 2007-02-28 LT LTEP07726556.9T patent/LT1989546T/lt unknown
- 2007-02-28 PL PL07726556T patent/PL1989546T3/pl unknown
-
2008
- 2008-08-12 ZA ZA200806913A patent/ZA200806913B/xx unknown
- 2008-08-20 IL IL193580A patent/IL193580A/en active IP Right Grant
-
2014
- 2014-09-15 US US14/486,124 patent/US20150004159A1/en not_active Abandoned
-
2016
- 2016-10-26 CY CY20161101087T patent/CY1118325T1/el unknown
-
2018
- 2018-06-21 US US16/014,529 patent/US11203641B2/en active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11203641B2 (en) | Screening for anti-cancer compounds using netrin-1 activity | |
| EP2452948B1 (en) | New tumor marker | |
| WO2007123274A1 (ja) | スルホンアミド化合物の新規感受性マーカー | |
| KR102074559B1 (ko) | 위암의 항암제 내성 진단용 바이오마커 및 이의 용도 | |
| WO2009141440A1 (en) | Netrin-1 overexpression as a biological marker and a survival factor for aggressive neuroblastoma | |
| AU2020278977B2 (en) | GPCR heteromer inhibitors and uses thereof | |
| US8975030B2 (en) | Method for cancer detection | |
| JP5885243B2 (ja) | 胆管細胞癌の検出方法および予防・治療剤のスクリーニング方法 | |
| WO2009120039A2 (en) | Use of cd9 for a target protein to develop anticancer drug of solid cancers that overexpress cd9 | |
| WO2012129395A2 (en) | Diagnosis and treatment of prostate cancer | |
| Annala | FR900359, an inhibitor of guanine nucleotide dissociation, effectively blunts signaling of GTPase-deficient Gq | |
| AU2014203702B2 (en) | New tumor marker | |
| HK1166329B (en) | New tumor marker | |
| HK1166329A (en) | New tumor marker | |
| WO2007037532A9 (ja) | Srms遺伝子の治療的又は診断的用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B06G | Technical and formal requirements: other requirements [chapter 6.7 patent gazette] |
Free format text: O CODIGO ALFANUMERICO APRESENTADO NAO CORRESPONDE AO CODIGO ALFANUMERICO DOS ARQUIVOS DA LISTAGEM DE SEQUENCIA APRESENTADOS NO CDS/DVDS. |
|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NO 10196/2001 |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 28/02/2007, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: REF. RPI 2655 DE 23/11/2021 QUANTO AO TITULAR E AO ENDERECO. |