BRPI0707579B1 - Sistema de expressão de polinucleotídeos, métodos de controle da população de um organismo em um meio ambiente natural para o mesmo, de controle biológico, e de separação de sexos, e, método ou controle biológico ou da população - Google Patents
Sistema de expressão de polinucleotídeos, métodos de controle da população de um organismo em um meio ambiente natural para o mesmo, de controle biológico, e de separação de sexos, e, método ou controle biológico ou da população Download PDFInfo
- Publication number
- BRPI0707579B1 BRPI0707579B1 BRPI0707579-0A BRPI0707579A BRPI0707579B1 BR PI0707579 B1 BRPI0707579 B1 BR PI0707579B1 BR PI0707579 A BRPI0707579 A BR PI0707579A BR PI0707579 B1 BRPI0707579 B1 BR PI0707579B1
- Authority
- BR
- Brazil
- Prior art keywords
- seq
- sequence
- expression system
- gene
- sex
- Prior art date
Links
- 230000014509 gene expression Effects 0.000 title claims abstract description 137
- 102000040430 polynucleotide Human genes 0.000 title claims abstract description 99
- 108091033319 polynucleotide Proteins 0.000 title claims abstract description 99
- 239000002157 polynucleotide Substances 0.000 title claims abstract description 99
- 238000000034 method Methods 0.000 title claims abstract description 34
- 238000000926 separation method Methods 0.000 title claims abstract description 11
- 108090000623 proteins and genes Proteins 0.000 claims description 204
- 102000004169 proteins and genes Human genes 0.000 claims description 125
- 239000002773 nucleotide Substances 0.000 claims description 85
- 125000003729 nucleotide group Chemical group 0.000 claims description 85
- 108091026890 Coding region Proteins 0.000 claims description 69
- 108091032973 (ribonucleotides)n+m Proteins 0.000 claims description 64
- 241000256118 Aedes aegypti Species 0.000 claims description 55
- 108020004705 Codon Proteins 0.000 claims description 53
- 230000009261 transgenic effect Effects 0.000 claims description 52
- 230000001665 lethal effect Effects 0.000 claims description 46
- 108700024394 Exon Proteins 0.000 claims description 39
- 239000013612 plasmid Substances 0.000 claims description 38
- 108091081024 Start codon Proteins 0.000 claims description 36
- 241000255925 Diptera Species 0.000 claims description 33
- 108700026244 Open Reading Frames Proteins 0.000 claims description 27
- 108020004999 messenger RNA Proteins 0.000 claims description 27
- 241000255581 Drosophila <fruit fly, genus> Species 0.000 claims description 26
- 241000255789 Bombyx mori Species 0.000 claims description 25
- 231100000225 lethality Toxicity 0.000 claims description 25
- 241000256182 Anopheles gambiae Species 0.000 claims description 24
- 241000238631 Hexapoda Species 0.000 claims description 24
- 241001136525 Anastrepha ludens Species 0.000 claims description 23
- 102100029450 M1-specific T cell receptor alpha chain Human genes 0.000 claims description 23
- 239000004098 Tetracycline Substances 0.000 claims description 23
- 230000000694 effects Effects 0.000 claims description 23
- 231100000518 lethal Toxicity 0.000 claims description 23
- 229960002180 tetracycline Drugs 0.000 claims description 23
- 229930101283 tetracycline Natural products 0.000 claims description 23
- 235000019364 tetracycline Nutrition 0.000 claims description 23
- 150000003522 tetracyclines Chemical class 0.000 claims description 21
- 238000012228 RNA interference-mediated gene silencing Methods 0.000 claims description 20
- 230000009368 gene silencing by RNA Effects 0.000 claims description 20
- 239000003623 enhancer Substances 0.000 claims description 19
- 210000001519 tissue Anatomy 0.000 claims description 19
- 101150058668 tra2 gene Proteins 0.000 claims description 19
- 239000003550 marker Substances 0.000 claims description 18
- 101710197635 Actin-4 Proteins 0.000 claims description 17
- 241000721451 Pectinophora gossypiella Species 0.000 claims description 17
- 241000256111 Aedes <genus> Species 0.000 claims description 16
- 241000557724 Ceratitis rosa Species 0.000 claims description 14
- 108700005090 Lethal Genes Proteins 0.000 claims description 14
- 108091035707 Consensus sequence Proteins 0.000 claims description 13
- 108091027974 Mature messenger RNA Proteins 0.000 claims description 13
- 230000002068 genetic effect Effects 0.000 claims description 13
- 210000004602 germ cell Anatomy 0.000 claims description 13
- 241000967809 Bactrocera zonata Species 0.000 claims description 12
- 235000014443 Pyrus communis Nutrition 0.000 claims description 12
- 241000255588 Tephritidae Species 0.000 claims description 10
- 241001490249 Bactrocera oleae Species 0.000 claims description 9
- 150000001413 amino acids Chemical class 0.000 claims description 9
- 238000012217 deletion Methods 0.000 claims description 9
- 230000037430 deletion Effects 0.000 claims description 9
- 230000002028 premature Effects 0.000 claims description 9
- 101100478296 Arabidopsis thaliana SR45A gene Proteins 0.000 claims description 8
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical class O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 claims description 8
- 230000001404 mediated effect Effects 0.000 claims description 8
- 210000001324 spliceosome Anatomy 0.000 claims description 8
- 241001124183 Bactrocera <genus> Species 0.000 claims description 7
- 241001635274 Cydia pomonella Species 0.000 claims description 7
- 241001646398 Pseudomonas chlororaphis Species 0.000 claims description 7
- 241000256186 Anopheles <genus> Species 0.000 claims description 6
- 241000254173 Coleoptera Species 0.000 claims description 6
- 108091023040 Transcription factor Proteins 0.000 claims description 6
- 230000001954 sterilising effect Effects 0.000 claims description 6
- 230000004083 survival effect Effects 0.000 claims description 6
- 102000040945 Transcription factor Human genes 0.000 claims description 5
- 210000001161 mammalian embryo Anatomy 0.000 claims description 5
- 239000000126 substance Substances 0.000 claims description 5
- 241001136523 Anastrepha Species 0.000 claims description 4
- 241000370909 Anastrepha obliqua Species 0.000 claims description 4
- 102000007272 Apoptosis Inducing Factor Human genes 0.000 claims description 4
- 108010033604 Apoptosis Inducing Factor Proteins 0.000 claims description 4
- 241000983417 Chrysomya bezziana Species 0.000 claims description 4
- 241000202814 Cochliomyia hominivorax Species 0.000 claims description 4
- 241000124008 Mammalia Species 0.000 claims description 4
- 241001249129 Scirpophaga incertulas Species 0.000 claims description 4
- 241000521243 Stegomyia Species 0.000 claims description 4
- 241001136529 Zeugodacus cucurbitae Species 0.000 claims description 4
- 230000002939 deleterious effect Effects 0.000 claims description 4
- 238000011161 development Methods 0.000 claims description 4
- 230000001568 sexual effect Effects 0.000 claims description 4
- 101150024821 tetO gene Proteins 0.000 claims description 4
- 241000256173 Aedes albopictus Species 0.000 claims description 3
- 241001124181 Bactrocera dorsalis Species 0.000 claims description 3
- 241000196324 Embryophyta Species 0.000 claims description 3
- 241000257166 Lucilia cuprina Species 0.000 claims description 3
- 241000721703 Lymantria dispar Species 0.000 claims description 3
- 241000500437 Plutella xylostella Species 0.000 claims description 3
- 230000034994 death Effects 0.000 claims description 3
- 230000004481 post-translational protein modification Effects 0.000 claims description 3
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 claims description 3
- 238000004659 sterilization and disinfection Methods 0.000 claims description 3
- 241001259789 Amyelois transitella Species 0.000 claims description 2
- 244000144730 Amygdalus persica Species 0.000 claims description 2
- 241001198505 Anarsia lineatella Species 0.000 claims description 2
- 241001136527 Anastrepha suspensa Species 0.000 claims description 2
- 241000256187 Anopheles albimanus Species 0.000 claims description 2
- 241000238421 Arthropoda Species 0.000 claims description 2
- 241000167854 Bourreria succulenta Species 0.000 claims description 2
- 241001249699 Capitata Species 0.000 claims description 2
- 229920000742 Cotton Polymers 0.000 claims description 2
- 241000256054 Culex <genus> Species 0.000 claims description 2
- 241000254171 Curculionidae Species 0.000 claims description 2
- 241000489975 Diabrotica Species 0.000 claims description 2
- 241000255777 Lepidoptera Species 0.000 claims description 2
- 241000258916 Leptinotarsa decemlineata Species 0.000 claims description 2
- 241001581015 Lyonetia clerkella Species 0.000 claims description 2
- 241000254101 Popillia japonica Species 0.000 claims description 2
- 101710150451 Protein Bel-1 Proteins 0.000 claims description 2
- 235000006040 Prunus persica var persica Nutrition 0.000 claims description 2
- 244000184734 Pyrus japonica Species 0.000 claims description 2
- 241000157279 Rhagoletis cerasi Species 0.000 claims description 2
- 244000061456 Solanum tuberosum Species 0.000 claims description 2
- 235000002595 Solanum tuberosum Nutrition 0.000 claims description 2
- 240000008042 Zea mays Species 0.000 claims description 2
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 claims description 2
- 235000002017 Zea mays subsp mays Nutrition 0.000 claims description 2
- 235000019693 cherries Nutrition 0.000 claims description 2
- 235000005822 corn Nutrition 0.000 claims description 2
- 230000007613 environmental effect Effects 0.000 claims description 2
- 230000009024 positive feedback mechanism Effects 0.000 claims description 2
- 230000000754 repressing effect Effects 0.000 claims description 2
- 241000255967 Helicoverpa zea Species 0.000 claims 2
- 241000251468 Actinopterygii Species 0.000 claims 1
- 240000007124 Brassica oleracea Species 0.000 claims 1
- 235000003899 Brassica oleracea var acephala Nutrition 0.000 claims 1
- 235000011301 Brassica oleracea var capitata Nutrition 0.000 claims 1
- 235000001169 Brassica oleracea var oleracea Nutrition 0.000 claims 1
- 240000007532 Butia capitata Species 0.000 claims 1
- -1 ange Species 0.000 claims 1
- 235000013379 molasses Nutrition 0.000 claims 1
- 101150069263 tra gene Proteins 0.000 description 75
- 239000012634 fragment Substances 0.000 description 65
- 230000002441 reversible effect Effects 0.000 description 59
- 108090000848 Ubiquitin Proteins 0.000 description 41
- 102000044159 Ubiquitin Human genes 0.000 description 41
- 241000255579 Ceratitis capitata Species 0.000 description 33
- 101100125027 Dictyostelium discoideum mhsp70 gene Proteins 0.000 description 32
- 101150031823 HSP70 gene Proteins 0.000 description 32
- 101150052825 dnaK gene Proteins 0.000 description 32
- 238000012340 reverse transcriptase PCR Methods 0.000 description 31
- 108020004414 DNA Proteins 0.000 description 23
- 101150108027 dsx gene Proteins 0.000 description 23
- 108091092195 Intron Proteins 0.000 description 22
- 230000006870 function Effects 0.000 description 20
- 238000010276 construction Methods 0.000 description 19
- 239000000499 gel Substances 0.000 description 19
- 244000003484 Molineria capitulata Species 0.000 description 17
- 230000004927 fusion Effects 0.000 description 16
- 230000000875 corresponding effect Effects 0.000 description 15
- 229920001184 polypeptide Polymers 0.000 description 15
- 102000004196 processed proteins & peptides Human genes 0.000 description 15
- 108090000765 processed proteins & peptides Proteins 0.000 description 15
- 230000001105 regulatory effect Effects 0.000 description 15
- 241000894007 species Species 0.000 description 14
- 239000000370 acceptor Substances 0.000 description 13
- 238000013519 translation Methods 0.000 description 13
- 108020003589 5' Untranslated Regions Proteins 0.000 description 12
- 101000732632 Homo sapiens Anillin Proteins 0.000 description 12
- 241000220225 Malus Species 0.000 description 12
- 108091028043 Nucleic acid sequence Proteins 0.000 description 12
- 241000220324 Pyrus Species 0.000 description 12
- 230000007246 mechanism Effects 0.000 description 12
- 241000701447 unidentified baculovirus Species 0.000 description 11
- 238000011144 upstream manufacturing Methods 0.000 description 11
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 10
- 238000012163 sequencing technique Methods 0.000 description 10
- 241000255601 Drosophila melanogaster Species 0.000 description 9
- 210000002257 embryonic structure Anatomy 0.000 description 9
- 108020005345 3' Untranslated Regions Proteins 0.000 description 8
- 108020005067 RNA Splice Sites Proteins 0.000 description 8
- 238000006243 chemical reaction Methods 0.000 description 8
- 230000002452 interceptive effect Effects 0.000 description 8
- 239000011159 matrix material Substances 0.000 description 8
- 241000201370 Autographa californica nucleopolyhedrovirus Species 0.000 description 7
- 108010029485 Protein Isoforms Proteins 0.000 description 7
- 102000001708 Protein Isoforms Human genes 0.000 description 7
- 238000010240 RT-PCR analysis Methods 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- 238000010586 diagram Methods 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 102100033393 Anillin Human genes 0.000 description 6
- 108010068250 Herpes Simplex Virus Protein Vmw65 Proteins 0.000 description 6
- 102100034343 Integrase Human genes 0.000 description 6
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 6
- 101150028940 SXL gene Proteins 0.000 description 6
- 210000004027 cell Anatomy 0.000 description 6
- 239000012636 effector Substances 0.000 description 6
- 238000003780 insertion Methods 0.000 description 6
- 230000037431 insertion Effects 0.000 description 6
- 230000002147 killing effect Effects 0.000 description 6
- 210000003205 muscle Anatomy 0.000 description 6
- 230000036961 partial effect Effects 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 241000255580 Ceratitis <genus> Species 0.000 description 5
- 239000000284 extract Substances 0.000 description 5
- 230000035772 mutation Effects 0.000 description 5
- 238000007500 overflow downdraw method Methods 0.000 description 5
- 238000002864 sequence alignment Methods 0.000 description 5
- 239000004055 small Interfering RNA Substances 0.000 description 5
- 238000013518 transcription Methods 0.000 description 5
- 230000010474 transient expression Effects 0.000 description 5
- 108020004459 Small interfering RNA Proteins 0.000 description 4
- 101150067366 adh gene Proteins 0.000 description 4
- 230000003321 amplification Effects 0.000 description 4
- 230000003466 anti-cipated effect Effects 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 108010021843 fluorescent protein 583 Proteins 0.000 description 4
- 108091006047 fluorescent proteins Proteins 0.000 description 4
- 102000034287 fluorescent proteins Human genes 0.000 description 4
- 238000003199 nucleic acid amplification method Methods 0.000 description 4
- 230000035897 transcription Effects 0.000 description 4
- 108020004491 Antisense DNA Proteins 0.000 description 3
- 108700036765 Drosophila Tra Proteins 0.000 description 3
- 101001006093 Escherichia coli (strain K12) Protein HemX Proteins 0.000 description 3
- 101000811817 Galdieria sulphuraria UPF0051 protein in atpA 3'region Proteins 0.000 description 3
- 101000907904 Homo sapiens Endoribonuclease Dicer Proteins 0.000 description 3
- 101000708525 Klebsiella aerogenes Uncharacterized protein in nac 5'region Proteins 0.000 description 3
- 101000786192 Klebsiella pneumoniae Uncharacterized protein in pqqA 5'region Proteins 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 241000382353 Pupa Species 0.000 description 3
- 101000746447 Pyrococcus woesei Uncharacterized protein in gap 3'region Proteins 0.000 description 3
- 101000819558 Salmonella typhimurium (strain LT2 / SGSC1412 / ATCC 700720) Inner membrane protein YjgN Proteins 0.000 description 3
- 108091081021 Sense strand Proteins 0.000 description 3
- 108091023045 Untranslated Region Proteins 0.000 description 3
- 241000700605 Viruses Species 0.000 description 3
- 239000003816 antisense DNA Substances 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 210000000038 chest Anatomy 0.000 description 3
- 230000000295 complement effect Effects 0.000 description 3
- 230000001276 controlling effect Effects 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 230000001965 increasing effect Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 230000020509 sex determination Effects 0.000 description 3
- 230000011664 signaling Effects 0.000 description 3
- 108020005029 5' Flanking Region Proteins 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- 101150026450 Act5C gene Proteins 0.000 description 2
- 101100064323 Arabidopsis thaliana DTX47 gene Proteins 0.000 description 2
- 102000051819 Baculoviral IAP Repeat-Containing 3 Human genes 0.000 description 2
- 108700003785 Baculoviral IAP Repeat-Containing 3 Proteins 0.000 description 2
- 241000255791 Bombyx Species 0.000 description 2
- 108700022579 Drosophila DSX Proteins 0.000 description 2
- 101100499270 Drosophila melanogaster Diap1 gene Proteins 0.000 description 2
- 101500025669 Drosophila melanogaster Ubiquitin Proteins 0.000 description 2
- 101500027496 Drosophila melanogaster Ubiquitin Proteins 0.000 description 2
- 101500028992 Drosophila melanogaster Ubiquitin Proteins 0.000 description 2
- 102100023387 Endoribonuclease Dicer Human genes 0.000 description 2
- 101100272587 Gallus gallus ITA gene Proteins 0.000 description 2
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 2
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 2
- 101150032161 IAP1 gene Proteins 0.000 description 2
- 241001599018 Melanogaster Species 0.000 description 2
- 241000244206 Nematoda Species 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 102000015097 RNA Splicing Factors Human genes 0.000 description 2
- 108010039259 RNA Splicing Factors Proteins 0.000 description 2
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 2
- 108091027967 Small hairpin RNA Proteins 0.000 description 2
- 101150048337 Sry-alpha gene Proteins 0.000 description 2
- 108700019146 Transgenes Proteins 0.000 description 2
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 2
- 210000001015 abdomen Anatomy 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 230000000692 anti-sense effect Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000010367 cloning Methods 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 230000007547 defect Effects 0.000 description 2
- 239000005547 deoxyribonucleotide Substances 0.000 description 2
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 235000005911 diet Nutrition 0.000 description 2
- 230000037213 diet Effects 0.000 description 2
- 230000009699 differential effect Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 238000004520 electroporation Methods 0.000 description 2
- 230000035558 fertility Effects 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 239000005090 green fluorescent protein Substances 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000010354 integration Effects 0.000 description 2
- 230000001418 larval effect Effects 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 230000013011 mating Effects 0.000 description 2
- 238000000520 microinjection Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 238000007857 nested PCR Methods 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- OFVLGDICTFRJMM-WESIUVDSSA-N tetracycline Chemical compound C1=CC=C2[C@](O)(C)[C@H]3C[C@H]4[C@H](N(C)C)C(O)=C(C(N)=O)C(=O)[C@@]4(O)C(O)=C3C(=O)C2=C1O OFVLGDICTFRJMM-WESIUVDSSA-N 0.000 description 2
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 2
- 230000002103 transcriptional effect Effects 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 230000001131 transforming effect Effects 0.000 description 2
- 108020005065 3' Flanking Region Proteins 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 241001520752 Anopheles sp. Species 0.000 description 1
- 241001414900 Anopheles stephensi Species 0.000 description 1
- 102000010565 Apoptosis Regulatory Proteins Human genes 0.000 description 1
- 108010063104 Apoptosis Regulatory Proteins Proteins 0.000 description 1
- 241000972773 Aulopiformes Species 0.000 description 1
- 241000611432 Bactrocera tryoni Species 0.000 description 1
- 201000004569 Blindness Diseases 0.000 description 1
- 241000409811 Bombyx mori nucleopolyhedrovirus Species 0.000 description 1
- 101100161935 Caenorhabditis elegans act-4 gene Proteins 0.000 description 1
- 101100440271 Caenorhabditis elegans ccf-1 gene Proteins 0.000 description 1
- 241000257161 Calliphoridae Species 0.000 description 1
- 102100024246 Caspase activity and apoptosis inhibitor 1 Human genes 0.000 description 1
- 101710196418 Caspase activity and apoptosis inhibitor 1 Proteins 0.000 description 1
- 235000005976 Citrus sinensis Nutrition 0.000 description 1
- 240000002319 Citrus sinensis Species 0.000 description 1
- 108700006604 Drosophila Slam Proteins 0.000 description 1
- 108700039668 Drosophila fru Proteins 0.000 description 1
- 101100532034 Drosophila melanogaster RTase gene Proteins 0.000 description 1
- 108700007861 Drosophila rpr Proteins 0.000 description 1
- 108700024070 Drosophila tra2 Proteins 0.000 description 1
- 101150013191 E gene Proteins 0.000 description 1
- 108010000912 Egg Proteins Proteins 0.000 description 1
- 108010022894 Euchromatin Proteins 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 108700039691 Genetic Promoter Regions Proteins 0.000 description 1
- 244000060234 Gmelina philippensis Species 0.000 description 1
- 108010034791 Heterochromatin Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 101710173438 Late L2 mu core protein Proteins 0.000 description 1
- 108091026898 Leader sequence (mRNA) Proteins 0.000 description 1
- 108060004795 Methyltransferase Proteins 0.000 description 1
- 108700011259 MicroRNAs Proteins 0.000 description 1
- 101710145242 Minor capsid protein P3-RTD Proteins 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 241001477931 Mythimna unipuncta Species 0.000 description 1
- 241001222956 Naupactus leucoloma Species 0.000 description 1
- 108091092724 Noncoding DNA Proteins 0.000 description 1
- 108010089610 Nuclear Proteins Proteins 0.000 description 1
- 102000043141 Nuclear RNA Human genes 0.000 description 1
- 108020003217 Nuclear RNA Proteins 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 101710188315 Protein X Proteins 0.000 description 1
- 108090000506 Protein phosphatase inhibitor 1 Proteins 0.000 description 1
- 102000004097 Protein phosphatase inhibitor 1 Human genes 0.000 description 1
- 108010026552 Proteome Proteins 0.000 description 1
- 238000002123 RNA extraction Methods 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108700008625 Reporter Genes Proteins 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- 241000277331 Salmonidae Species 0.000 description 1
- 241000190070 Sarracenia purpurea Species 0.000 description 1
- 238000012300 Sequence Analysis Methods 0.000 description 1
- 241000700584 Simplexvirus Species 0.000 description 1
- 102000039471 Small Nuclear RNA Human genes 0.000 description 1
- 108700009124 Transcription Initiation Site Proteins 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- 108700005077 Viral Genes Proteins 0.000 description 1
- 102000013814 Wnt Human genes 0.000 description 1
- 108050003627 Wnt Proteins 0.000 description 1
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 101150111846 aif gene Proteins 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 235000021016 apples Nutrition 0.000 description 1
- 230000003542 behavioural effect Effects 0.000 description 1
- 102000005936 beta-Galactosidase Human genes 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000022131 cell cycle Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000009274 differential gene expression Effects 0.000 description 1
- 238000002224 dissection Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 108010048367 enhanced green fluorescent protein Proteins 0.000 description 1
- 210000000632 euchromatin Anatomy 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 235000019688 fish Nutrition 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 230000028518 head involution Effects 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000004458 heterochromatin Anatomy 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000007901 in situ hybridization Methods 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 230000005865 ionizing radiation Effects 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 231100001160 nonlethal Toxicity 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 235000021017 pears Nutrition 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 239000002574 poison Substances 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 230000008488 polyadenylation Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000014493 regulation of gene expression Effects 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 238000010839 reverse transcription Methods 0.000 description 1
- 210000003705 ribosome Anatomy 0.000 description 1
- 235000019515 salmon Nutrition 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 238000010187 selection method Methods 0.000 description 1
- 230000035939 shock Effects 0.000 description 1
- 108091029842 small nuclear ribonucleic acid Proteins 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 230000004960 subcellular localization Effects 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 229940113082 thymine Drugs 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000014621 translational initiation Effects 0.000 description 1
- 229940035893 uracil Drugs 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/8509—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells for producing genetically modified animals, e.g. transgenic
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/60—New or modified breeds of invertebrates
- A01K67/61—Genetically modified invertebrates, e.g. transgenic or polyploid
- A01K67/63—Genetically modified worms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/60—New or modified breeds of invertebrates
- A01K67/61—Genetically modified invertebrates, e.g. transgenic or polyploid
- A01K67/65—Genetically modified arthropods
- A01K67/68—Genetically modified insects
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/05—Animals comprising random inserted nucleic acids (transgenic)
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/70—Invertebrates
- A01K2227/703—Worms, e.g. Caenorhabdities elegans
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/70—Invertebrates
- A01K2227/706—Insects, e.g. Drosophila melanogaster, medfly
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/02—Animal zootechnically ameliorated
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/001—Vector systems having a special element relevant for transcription controllable enhancer/promoter combination
- C12N2830/002—Vector systems having a special element relevant for transcription controllable enhancer/promoter combination inducible enhancer/promoter combination, e.g. hypoxia, iron, transcription factor
- C12N2830/003—Vector systems having a special element relevant for transcription controllable enhancer/promoter combination inducible enhancer/promoter combination, e.g. hypoxia, iron, transcription factor tet inducible
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/008—Vector systems having a special element relevant for transcription cell type or tissue specific enhancer/promoter combination
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/42—Vector systems having a special element relevant for transcription being an intron or intervening sequence for splicing and/or stability of RNA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/75—Vector systems having a special element relevant for transcription from invertebrates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2840/00—Vectors comprising a special translation-regulating system
- C12N2840/44—Vectors comprising a special translation-regulating system being a specific part of the splice mechanism, e.g. donor, acceptor
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Wood Science & Technology (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Organic Chemistry (AREA)
- Environmental Sciences (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- General Health & Medical Sciences (AREA)
- Biophysics (AREA)
- Animal Husbandry (AREA)
- Biodiversity & Conservation Biology (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
SISTEMA DE EXPRESSÃO DE POLINUCLEOTÍDEOS, MÉTODOS DE CONTROLE DA POPULAÇÃO DE UM ORGANISMO EM UM MEIO AMBIENTE NATURAL PARA O MESMO, DE CONTROLE BIOLÓGICO, E DE SEPARAÇÃO DE SEXOS, E, METODO OU CONTROLE BIOLÓGICO OU DA POPULAÇÃO. Um sistema de expressão de polinueleotídeos é provido, o qual é capaz de emendar alternativamente os transcritos de RNA de uma sequência polinucleotídica a ser expressada em um organismo.
Description
A presente invenção refere-se a um sistema de expressão de genes, em combinação com sequências de controle de splice, referidas sequências de controle provendo um mecanismo para splicing alternativo.
Splicing alternativo envolve a remoção de um ou mais íntrons e ligação dos éxons de flanqueamento. Esta reação é catalisada pela espliceossoma, uma máquina macromolecular composta de cinco RNAs e centenas de proteínas (Jurica, M. S. & Moore, M. J. (2003) Mol. Cell 12, 514). Splicing alternativo gera mRNAs múltiplos a partir de um gene único, deste modo aumentando a diversidade de proteomas (Graveley, B. R. (2001) Trends Genet. 17, 100-107).
Splicing alternativo também desempenha um papel chave na regulação de expressão de genes em muitos processos relativos ao desenvolvimento variando de determinação de sexo a apoptose (Black, D. L. (2003) Annu. Rev. Biochem. 72, 291-336), e defeitos no splicing alternativo foram ligados a muitos distúrbios humanos (Cáceres, J. F. & Kornblihtt, A. R. (2002) Trends Genet. 18, 186-193). Geralmente, splicing alternativo é regulado por proteínas que se associam com pré-mRNA e funcionam ou para aumentar ou reprimir a capacidade do espliceossoma de reconhecer o(s) sítio(s) de splice flanqueando o éxon regulado (Smith, C. W. & Valcarcel, J. (2000) Trends Biochem. Sci. 25, 381-388).
Se um éxon alternativo particular será incluído ou excluído de um RNA maduro em cada célula é determinado, como se pensa, pela concentração relativa de um número de reguladores de splicing positivos e negativos e as interações destes fatores com o pré-mRNA e componentes do espliceossoma (Smith, C. W. & Valcarcel, J. (2000) Trends Biochem. Sci. 25, 381-388).
Espliceossomas são complexos grandes de RNA nuclear pequeno e partículas de proteína (snRNPs) que se juntam com pré-mRNA para realizar o splicing de RNA, removendo os íntrons dos RNAs nucleares eucarióticos, assim produzindo mRNA que é então traduzido para proteína em ribossomas.
Apesar de pelo menos 74% de genes humanos codificarem mRNAs alternativamente spliced (Johnson, J. M., Castle, J., Garrett-Engele, P., Kan, Z., Loerch, P. M., Armour C. D., Santos, R., Schadt, E. E., Stoughton, R. & Shoemaker, D. D. (2003) Science 302, 2141-2144), relativamente poucos reguladores de splicing foram identificados.
Assim, em um primeiro aspecto, a presente invenção provê um sistema de expressão de polinucleotídeos compreendendo: pelo menos uma sequência polinucleotídica heteróloga codificando uma proteína funcional, definida entre um códon de partida e um códon de parada, e/ou polinucleotídeos para RNA interferência (RNAi), a ser expressada em um organismo; ligado operativamente pelo menos um promotor ligado operativamente ao mesmo; e pelo menos uma sequência de controle de splice que, em cooperação com um espliceossoma, é capaz de (i) mediar o splicing de um transcrito de RNA da sequência de codificação para produzir um primeiro produto de RNA mensageiro (mRNA) spliced, e (ii) mediar pelo menos um splicing alternativo de referido transcrito de RNA para produzir um produto de mRNA spliced alternativo; em que, quando pelo menos uma sequência polinucleotídica heteróloga codifica uma proteína funcional, pelo menos um dos produtos de mRNA maduro compreendendo uma Matriz de Leitura Aberta (ORF) contínua estendendo-se a partir de referido códon de partida para referido códon de parada, assim definindo uma proteína, que é a referida proteína funcional, ou está relacionada com a referida proteína funcional por pelo menos uma deleção de aminoácido, e que é funcional quando traduzida, e, opcionalmente, sofreu uma modificação pós-traducional; a mediação sendo selecionada dentre o grupo consistindo de: mediação específica de sexo, mediação específica de estágio, mediação específica de linhagem germinal, mediação específica de tecido, e combinações das mesmas.
O sistema de expressão pode ser DNA ou RNA ou um híbrido ou combinação de ambos. Visa-se que o sistema compreenda ambos ribo- e desoxirribonucleotídeos, isto é, porções de DNA e porções de RNA. Estes poderiam correspondem a elementos genéticos diferentes, tal que o sistema é um híbrido de DNA/RNA, com alguns elementos funcionais providos por DNA e outros por RNA.
Preferivelmente, a mediação é em um modo específico de sexo, específica de estágio, específica de linhagem germinal ou específica de tecido. Em particular, a mediação específica de sexo é particularmente preferida. No entanto, também se prefere que uma combinação destes quatro modos de mediação possa ser utilizada. Prefere-se particularmente que, quando uma combinação destes modos é usada, que isto inclua a mediação específica de sexo. Um exemplo particularmente preferido de tal combinação é uma combinação de mediação específica de sexo, específica de tecido e específica de estágio de splicing alternativo.
O sistema pode ser adaptado para expressão de um gene. Preferivelmente, a sequência polinucleotídica a ser expressada compreende uma sequência de codificação para uma proteína ou polipeptídeo, isto é pelo menos um éxon, e preferivelmente 2 ou mais éxons, capazes de codificar um polipeptídeo, tal como uma proteína ou fragmento da mesma.
Será entendido que um éxon é qualquer região de DNA dentro de um gene, que está presente em uma molécula de RNA maduro derivado deste gene, em vez de ser retirado (spliced out) da molécula de RNA transcrito. Para genes de codificações de proteína, moléculas de RNA maduro correspondem a moléculas de mRNA maduro, que podem codificar uma ou mais proteínas ou polipeptídeos. Éxons de muitos genes eucarióticos intercalam-se com segmentos de DNA não de codificação.
A pelo menos uma sequência polinucleotídica heteróloga pode codificar uma proteína funcional, definida entre um códon de partida e um códon de parada a ser expressada em um organismo. Alternativamente, ou em adição, a pelo menos uma sequência polinucleotídica heteróloga codifica ou compreende polinucleotídeos para RNA interferência (RNAi), a ser expressado em um organismo.
Estas sequências, a serem expressadas no organismo, também podem ser referidas como as sequências cuja expressão deve ser regulada no referido organismo.
Preferivelmente, a sequência polinucleotídica a ser expressada compreende dois ou mais éxons de codificação, sendo segmentos ou sequências polinucleotídicas que codificam aminoácidos quando traduzidas do mRNA. Preferivelmente, os éxons diferentes são diferencialmente spliced juntos para prover mRNAs alternativos. Preferivelmente, referidos mRNAs que sofreram splicing alternativos têm potenciais de codificação diferentes, isto é codificam proteínas diferentes ou sequências de polipeptídeos. Assim, a expressão da sequência de codificação é regulada pelo splicing alternativo nos modos acima mencionados de mediação.
A sequência polinucleotídica a ser expressada pode compreender polinucleotídeos de RNA interferência (RNAi). Tais sequências são capazes de prover, por exemplo, uma ou mais extensões de RNA filamento duplo (dsRNA), preferivelmente na forma de um transcrito primário, que por sua vez é capaz de processar pela enzima de tipo RNA Pol III "Dicer." Tais extensões incluem, por exemplo, extensões de RNA filamento único que podem formar laços, tais como os encontrados em RNA grampo de cabelo curto (shRNA), ou com regiões mais longas que são substancialmente auto-complementares.
Assim, onde o sistema é DNA, os polinucleotídeos para RNA interferência são desoxirribonucleotídeos que, quando transcritos nos ribonucleotídeos pré-RNA, provêem uma extensão de dsRNA, como discutido acima.
Polinucleotídeos para RNA interferência são particularmente preferidos quando referidos polinucleotídeos estão posicionados para minimizar a interferência com splicing alternativo. Isto pode ser realizado por posicionamento distal destes polinucleotídeos das sequências de controle de splicing alternativo, preferivelmente 3' para as sequências de controle. Em outra forma de realização preferida, regiões substancialmente auto- complementares podem ser separadas de cada por uma ou mais sequências de controle de splice, tais como um íntron, que media splicing alternativo. Preferivelmente, as regiões auto-complementares são arranjadas como uma série de duas ou mais repetições invertidas, cada repetição invertida separada por sequência de controle de splice, preferivelmente um íntron, como definido em outra parte.
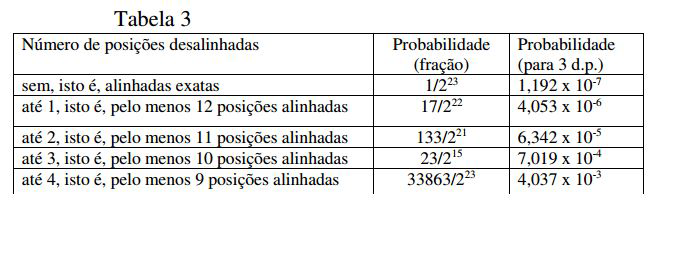
Nesta configuração, diferentes transcritos que foram spliced alternativamente podem ter suas regiões auto-complementares substancialmente separadas por diferentes comprimentos de sequência não auto-complementar no transcrito maduro (splicing pós alternativo). Será notado que regiões que são substancialmente auto-complementares são aqueles que são capazes de formar grampos de cabelo, por exemplo, como porções da sequência são capazes de formar pares de bases com outras porções da sequência. Estas duas porções não têm de ser exatamente complementares mutuamente, porque podem ocorrer alguns desalinhamentos ou tolerância de extensões em cada porção que não forma pares de base umas com as outras. Tais extensões podem não ter um equivalente em outra porção, tal que a simetria é perdida e "protuberâncias" se formam, como é conhecido com complementação de pares de base geralmente.
Em outra forma de realização preferida, um ou mais segmentos de sequência substancialmente complementares a outra seção do transcrito primário é posicionado, relativo à pelo menos uma sequência de controle de splice, de modo que isto não está incluído em todos dos transcritos produzidos por splicing alternativo do transcrito primário. Por esse método, alguns transcritos são produzidos que tendem a produzir dsRNAs enquanto outros não; por mediação do splicing alternativo, por exemplo mediação específica de sexo, mediação específica de estágio, mediação específica de linhagem germinal, mediação específica de tecido, e combinações das mesmas, dsRNA pode ser produzido em um modo específico de sexo, específica de estágio, específica de linhagem germinal ou específica de tecido, ou combinações das mesmas.
O sistema é preferivelmente capaz de expressar pelo menos uma proteína de interesse, isto é referida proteína funcional a ser expressada em um organismo. Referida pelo menos uma proteína de interesse pode ter um efeito terapêutico ou pode, preferivelmente, ser um marcador, por exemplo DsRed, proteína fluorescente verde (GFP) ou um ou mais de seus mutantes ou variantes, ou outros marcadores que são bem conhecidos na técnica.
O mais preferivelmente, a proteína funcional a ser expressada em um organismo tem um efeito letal, deletério ou esterilizante. Onde referência é feita aqui para um efeito letal, será notado que ela abrange um efeito deletério e esterilizante, tal como um efeito capaz de matar o organismo per se ou sua descendência, ou capaz de reduzir ou destruir a função de determinados tecidos do mesmo, dos quais os tecidos reprodutivos são particularmente preferidos, de modo que o organismo ou sua descendência são estéreis. Assim, alguns efeitos letais, tais como venenos, matarão o organismo ou tecido em uma matriz de tempo curto relativo a seu tempo de vida, enquanto outros podem simplesmente reduzir a capacidade do organismo de funcionar, por exemplo reprodutivamente.
Um efeito letal resultante em esterilização é particularmente preferido, como isto permite ao organismo competir no ambiente natural ("no estado selvagem") com organismo de tipo selvagem, mas o inseto estéril não pode então produzir uma descendência viável. Desta forma, a presente invenção realiza um resultado similar às técnicas tais como técnica de inseto estéril (SIT) em insetos, sem os problemas associados com SIT, tal como o custo, perigo ao usuário, e reduzida competitividade do organismo irradiado.
Preferivelmente, o sistema compreende pelo menos um mecanismo de retro-alimentação positiva, isto é, pelo menos proteína funcional a ser diferencialmente expressada, através de splicing alternativo, e pelo menos um promotor para o mesmo, onde um produto de um gene a ser expressado serve como um fator de controle transcripcional positivo para o pelo menos um promotor, e pelo qual o produto, ou a expressão do produto, é controlável. Preferivelmente, um melhorador é associado com o promotor, o produto de gene servindo para melhorar a atividade do promotor através do melhorador. Preferivelmente, o fator de controle é o produto do gene de tTA ou um análogo do mesmo, e onde uma ou mais unidades de operador de tetO é ligada operativamente como promotor e é o melhorador, tTA ou seu análogo servindo para melhorar atividade do promotor via tetO. Prefere-se que proteína funcional codifique o produto de tTAV ou tTAF e preferivelmente, o promotor está substancialmente inativo na ausência do fator de controle transcripcional positivo. Os promotores apropriados, preferivelmente mínimos, para esse sistema podem ser selecionados dentre: hsp70, um promotor mínimo de P, um promotor mínimo de CMV, um promotor mínimo baseado de Act5C, um fragmento de promotor de BmA3, um fragmento de promotor de hunchback, um promotor de núcleo de Adh, e um promotor mínimo de Act5C, ou combinações dos mesmos.
Em uma forma de realização, a proteína funcional é preferivelmente um fator de indução de apoptose, tal como a proteína de AIF descrita por exemplo em Cande et al (Journal of Cell Science 115, 4727-4734 (2002)) ou homólogos da mesma. Homólogos de AIF são encontrados em mamíferos e até mesmo em invertebrados, incluindo insetos, nematóides, fungos, e plantas, significando que o gene de AIF foi conservado ao longo de todo o reino eucariótico. Também preferido é Hid, o produto de proteína do gene defeituoso de involução de cabeça de Drosophila melanogaster, ou Reaper (Rpr), o produto do gene Reaper de Drosophila, ou mutantes dos mesmos. Uso de Hid foi descrito por Heinrich e Scott (Proc. Natl Acad. Sci USA 97, 8229-8232 (2000). Uso de um derivado mutante, HidAla5 foi descrito por Horn e Wimmer (Nature Biotechnology 21, 64-70 (2003)). Uso de um derivado mutante de Rpr, RprKR, é descrito aqui (ver também White et al 1996, Wing et al., 2001, e Olson et al., 2003). Ambos, Rpr e Hid são proteínas pró-apoptóticas, que se ligam a IAP1, como se pensa. IAP1 é uma proteína anti-apoptótica bem conservada. Hid e Rpr são, portanto, esperados como trabalhando através de uma extensa faixa filogenética (Huang et al., 2002, Vernooy et al., 2000) apesar de sua própria sequência não ser bem conservada.
Também é preferido Nipp1Dm, o homólogo de Drosophila de Nipp1 de mamífero (Parker et al Biochemical Journal 368, 789-797 (2002); Bennett et al, Genetics 164, 235-245 (2003)). Nipp1Dm é outro exemplo de uma proteína com efeito letal se expressada a um nível apropriado, como seria entendido pelo versado. De fato, muitos outros exemplos de proteínas com um efeito letal serão conhecidos pelo versado na técnica.
Também se prefere que a proteína funcional seja, ela mesma, um transativador transcripcional, tal como o sistema tTAV descrito acima.
Prefere-se que o promotor possa ser ativado por condições ambientais, por exemplo a presença ou ausência de um fator particular tal como tetraciclina no sistema tet descrito aqui, tal que a expressão do gene de interesse possa ser facilmente manipulada pelo versado. Alternativamente, um exemplo preferido de promotor apropriado é o promotor de choque térmico hsp 70, permitindo ao usuário controlar a expressão por variação da temperatura ambiente para a qual os hospedeiros estão expostos em um laboratório ou no campo, por exemplo. Outro exemplo preferido de controle de temperatura está descrito em Fryxell e Miller (Journal of Economic Entomology 88, 1221-1232 (1995)).
Também preferido como um promotor é o promotor específico de embrião syra (Horn & Wirnmer (2003) de Drosophila melanogaster, ou seus homólogos, ou promotores de outros genes específicos de embrião ou ativos de embrião, tais como os do gene de Drosophila slow as molasses (slam), ou seus homólogos de outras espécies.
Também se prefere que o sistema compreenda outros fatores a montante, 5', e/ou fatores a jusante, 3', para controlar a expressão. Exemplos incluem melhoradores tais como os melhoradores de gordura corporal dos genes de proteína yolk de Drosophila, e os melhoradores de região de homologia (hr) de baculovírus, por exemplo Ac MNPV. Também será notado que os produtos de RNA irão incluir UTRs 5' e 3' apropriados, por exemplo.
A sequência de controle de splice permite um nível adicional de controle de expressão de proteína, em adição ao promotor e/ou melhorador do gene. Por exemplo, a expressão específica de sexo ou de tecido em embriões de inseto apenas seria extremamente difícil por métodos convencionais. Promotores com esta especificidade são desconhecidos, mesmo em Drosophila. No entanto, usando controle combinatorial de acordo com a presente invenção, um promotor específico de embrião, por exemplo srya, pode ser combinado com um sistema de splicing alternativo apropriado.
Prefere-se que qualquer combinação de promotor e mecanismo de splicing alternativo seja considerada. O promotor é preferivelmente específico para uma proteína particular tendo um efeito temporal pequeno ou especial confinado, por exemplo um efeito autônomo celular.
Alternativamente, prefere-se que o promotor possa ser específico para uma classe de proteínas ou uma proteína específica que tem um efeito a longo prazo e/ou sistema extenso, tais como um hormônio, fator de crescimento positivo ou negativo, morfogene ou outra molécula secretada ou sinalizando superfície celular. Isto irá permitir, por exemplo, um padrão de expressão mais amplo de modo que uma combinação de um promotor de morfogene com um mecanismo de splicing alternativo específico de estágio poderia resultar no morfogene sendo expressado apenas uma vez que foi alcançada uma determinada fase do ciclo da vida, mas o efeito do morfogene ainda seria sentido (isto é o morfogene pode ainda agir e ter um efeito) para além desta etapa do ciclo da vida. Exemplos preferidos seriam moléculas de morfogene/sinalização Hedgehog, Wingless/WNTs, TGFβ/BMPs, EGF e seus homólogos, moléculas de sinalização conservadas evolucionariamente bem conhecidas.
Prevê-se também que um promotor que é ativado por uma faixa de fatores de proteína, por exemplo transativadores, ou que tem um amplo efeito sistêmico, tais como um hormônio ou morfogene, poderia ser usado em combinação com um mecanismo de splicing alternativo para realizar um controle específico de tecido ou sexo ou controle específico de sexo ou estágio, ou outras combinações de controle específico de estágio, tecido, linhagem germinal e sexo.
Prevê-se também que mais de um promotor, e opcionalmente um melhorador para o mesmo, pode ser usado no presente sistema, quer como meios alternativos para iniciar a transcrição da mesma proteína ou por virtude do fato de que o sistema genético compreende mais de um sistema de expressão de gene (isto é mais de um gene e seu promotor acompanhante).
Em um outro aspecto, a presente invenção provê um método de transformação, compreendendo expressar duas ou mais moléculas de RNA, derivadas de um transcrito primário simples, ou transcritos primários substancialmente similares, por splicing alternativo, referidas duas ou mais moléculas de RNA preferivelmente codificando diferentes proteínas ou polipeptídeos, em um organismo contatando o organismo com o sistema de expressão e preferivelmente induzindo a expressão do sistema de expressão. Métodos de introdução ou transformação do sistema de gene e indução de expressão são bem conhecidos na técnica com relação ao organismo relevante. Também são providos organismos (isto é transformantes) transformados pelo presente sistema.
Onde referência a um nucleotídeo ou sequência de proteína particular é feita, será entendido que isto inclui referência a qualquer mutante ou variante dos mesmos, tendo atividade biológica substancialmente equivalente ao mesmo. Preferivelmente, o mutante ou variante tem pelo menos 85%, preferivelmente pelo menos 90%, preferivelmente pelo menos 95%, preferivelmente pelo menos 99%, preferivelmente pelo menos 99,9%, e o mais preferível pelo menos 99,99% de identidade de sequência com as sequências de referência.
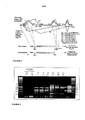
As sequências providas podem tolerar alguma variação de sequência e ainda splice corretamente. Existem alguns nucleotídeos conhecidos por serem importantes. Estes são aqueles requeridos para todos os splicings, por exemplo como mostrado na Figura 34 abaixo. O GU inicial e o AG final do íntron são particularmente importantes e, por isso, preferidos, como discutido em outra parte, embora ~5% de íntrons iniciam GC, ao contrário. Esta sequência de consenso é preferida, embora se aplique para todos os splicings, não especificamente o splicing alternativo. Na Figura 34, Pu = A ou G; Py = C ou U.
Preferivelmente, o sistema é ou compreende um plasmídeo. Como mencionado acima, isto pode ser quer DNA, RNA ou uma mistura de ambos. Se o sistema compreende RNA, então pode ser preferível traduzir de modo reverso o RNA em DNA por meio de uma transcriptase reversa. Se transcrição reversa é requerida, então o sistema pode também compreender uma sequência de codificação para a proteína RT e um promotor apropriado para a mesma. Alternativamente, a RTase e promotor assim pode ser provido em um sistema separado, tais como um vírus. Neste caso, o sistema apenas seria ativado seguindo a infecção com aquele vírus. A necessidade de incluir sequências cis-atuantes apropriadas para a transcriptase reversa ou RNA polimerase dependente de RNA seria evidente para o versado na técnica.
No entanto, é particularmente preferido que o sistema seja predominantemente DNA e mais preferivelmente consista apenas de DNA, pelo menos com relação às sequências a serem expressadas no organismo.
Enquanto em algumas formas de realização a pelo menos uma sequência polinucleotídica heteróloga a ser expressada em um organismo é uma sequência polinucleotídica de RNA interferência (RNAi), é particularmente preferido que esta seja uma sequência polinucleotídica capaz de codificar uma proteína funcional. A descrição irá focalizar predominantemente as sequências polinucleotídicas codificando uma proteína funcional, mas será entendido que ela também refere-se a polinucleotídeos de RNA interferência (RNAi), salvo especificado em contrário.
Será entendido que referência é feita à códons de partida e de parada entre os quais a sequência polinucleotídica a ser expressada em um organismo é definida, mas que esta não exclui posicionamento de pelo menos uma sequência de controle de splice, elementos da mesma, ou outras sequências, tais como íntrons, nesta região. De fato, será evidente da presente descrição que a sequência de controle de splice, pode, em algumas formas de realização, estar posicionada nesta região.
Ademais, a sequência de controle de splice, por exemplo, pode sobrepor com o códon de partida pelo menos, no sentido que o G de ATG pode ser, em algumas formas de realização, o 5' G inicial da sequência de controle de splice. Assim, o termo "entre" pode ser considerado como referindo a partir do início (3' para o nucleotídeo inicial, isto é A) do códon de partida, preferivelmente 3' para o segundo nucleotídeo do códon de partida (isto é T), até o lado 5' do primeiro nucleotídeo do códon de parada. Alternativamente, como será evidente por uma simples leitura de uma sequência polinucleotídica, o códon de parada pode também ser incluído.
A pelo menos uma sequência polinucleotídica heteróloga a ser expressada em um organismo é uma sequência heteróloga. Por "heterólogo", seria entendido que ele refere-se a uma sequência que não seria, no tipo selvagem, normalmente encontrada em associação com, ou ligada a, pelo menos um elemento ou componente da pelo menos uma sequência de controle de splice. Por exemplo, onde a sequência de controle de splice é derivada de um organismo particular, e o polinucleotídeo heterólogo é uma sequência de codificação de uma proteína ou polipeptídeo, isto é, é uma sequência polinucleotídica codificando uma proteína funcional, então a sequência de codificação poderia ser derivada, em parte ou completamente, de um gene do mesmo organismo, desde que a origem de pelo menos alguma parte da sequência polinucleotídica transcrita não foi a mesma como a origem da pelo menos uma sequência de controle de splice. Alternativamente, a sequência de codificação poderia ser de um organismo diferente e, nesse contexto, poderia ser pensado como "exógeno". O polinucleotídeo heterólogo poderia também ser pensado como "recombinante", em que a sequência de codificação para uma proteína ou polipeptídeo é derivada de locais diferentes, ou dentro do mesmo genoma (isto é o genoma de uma espécie simples ou subespécie) ou de genomas diferentes (isto é genomas de diferentes espécies ou subespécies).
Heterólogo pode referir-se à sequência diferente da sequência de controle de splice e pode, assim, referir-se ao fato de o promotor, e outras sequências tais como 5' UTR e/ou 3' UTR poderem ser heterólogas à sequência polinucleotídica a ser expressada no organismo, desde que a referida sequência polinucleotídica não é encontrada em associação com ou ligada operativamente ao promotor, 5' UTR e/ou 3 'UTR, no tipo selvagem, isto é o contexto natural de referida sequência polinucleotídica, se presente.
Será entendido que heterólogo também aplica-se a sequências "designer" ou híbridas que não são derivadas de um organismo particular mas são baseadas em um número de componentes de organismos diferentes, como isto iria atender à exigência de que a sequência e pelo menos um componente da sequência de controle de splice não estão ligados ou encontrados em associação no tipo selvagem, mesmo se uma parte ou elemento da sequência híbrida for assim encontrada, enquanto pelo menos uma parte ou elemento não é. Preferivelmente, uma porção de pelo menos 50 nucleotídeos da sequência híbrida não é encontrada em associação com pelo menos um componente da sequência de controle de splice, mais preferivelmente 200 nucleotídeos e o mais preferível, 500 nucleotídeos.
Também será entendido que versões sintéticas de sequências de ocorrência natural são visadas. Tais sequências sintéticas são também consideradas como heterólogas, a menos que elas sejam de sequência idêntica a uma sequência que seria, no tipo selvagem ou contexto natural, normalmente encontrada em associação com, ou ligada a, pelo menos um elemento ou componente da pelo menos uma sequência de controle de splice. Isto aplica-se igualmente para onde o polinucleotídeo heterólogo é um polinucleotídeo de RNA interferência.
Em uma forma de realização, onde a sequência polinucleotídica a ser expressada compreende uma sequência de codificação de uma proteína ou polipeptídeo, será entendido que referência a expressão em um organismo refere-se à provisão de uma ou mais sequências de RNAs transcritos, preferivelmente mRNAs maduros, mas isto pode, preferivelmente, também referir-se aos polipeptídeos traduzidos no referido organismo.
RT-PCR, que demonstra a presença de um transcrito, não de uma proteína, pode ser usado para identificar as sequências de RNAs transcritos. Isto também é particularmente útil quando a própria proteína não é traduzida ou não é funcional ou não identificável por anticorpos criados contra a proteína de ocorrência natural ou de tipo selvagem, devido a RNAi, modificação pós-translacional ou duplicação distorcida.
Em outra forma de realização, onde a sequência polinucleotídica a ser expressada compreende polinucleotídeos de RNA interferência, também será entendido que a referência à expressão em um organismo refere-se à interação dos polinucleotídeos de RNA interferência, ou transcritos do mesmo, na via de RNAi, por exemplo ligação de Dicer ou formação de RNA interferência pequeno (siRNA). De fato, é particularmente preferido que os polinucleotídeos de RNA interferência compreendam sequências de siRNA e são, por esta razão, preferivelmente de 20-25 nucleotídeos de comprimento, especialmente onde o organismo é mamífero.
Em insetos e nematóides especialmente, prevê-se prover porção de dsRNA, por exemplo por formação de grampo de cabelo, que pode então ser processada pelo Sistema Dicer. Células de mamíferos geralmente produzem uma retro-alimentação de interferon contra as sequências de dsRNA longas, assim para células de mamíferos é mais comum prover sequências menores, tais como siRNAs. Sequências anti-sentido ou sequências tendo homologia a microRNAs que são moléculas de RNA de ocorrência natural marcando os 3' UTRs de proteína são também visadas como sequências de RNAi de acordo com uma forma de realização da presente invenção.
Cada sequência de controle de splice no sistema compreende pelo menos um sítio aceitador de splice e pelo menos um sítio doador de splice. O número de sítios doadores e aceitadores pode variar, dependendo do número de segmentos da sequência que devem ser spliced juntos. Preferivelmente, sítios de ramificação estão incluídos em cada sequência de controle de splice. Um sítio de ramificação é a sequência em que o doador de splice está inicialmente ligado, ver figura 32, que mostra que splicing ocorrendo em dois estágios, em que o éxon 5' é separado e então ligado ao éxon 3'.
Referindo-se à referida figura, o A é o único nucleotídeo essencial, e está, por esta razão, preferivelmente incluído. Sem estar limitado pela teoria, acredita-se que o splicing de pré-mRNA prossegue através de um intermediário lariat, como é feito na auto-splicing de grupo II. Primeiro, clivagem ocorre na junção 5' - algumas vezes chamada de sítio doador de splice. O fosfato na extremidade 5' do íntron então torna-se ligado ao 2' OH de uma adenina de aproximadamente 25 nucleotídeos a montante da extremidade 3' do íntron, que é algumas vezes chamado de sítio aceitador. Este resíduo A é chamado de ponto de ramificação. A próxima etapa é que a clivagem ocorre na junção de splice 3' e o fosfato 5' do éxon a jusante é ligado ao 3'OH do éxon a montante.
Prefere-se particularmente que a maneira ou mecanismo de splicing alternativo seja específico de sexo. Preferivelmente, a sequência de controle de splice é derivada de um íntron tra. No entanto, é particularmente preferido que o mecanismo de splicing alternativo seja derivado do gene transformer Cctra de mosca-do-mediterrâneo, ou de outro ortólogo ou homólogo do gene transformer de Drosophila, preferivelmente de C. rosa, ou B. zonata especialmente um derivado de uma mosca tefrítida da fruta.
Também se prefere que a sequência de controle de splice seja derivada do mecanismo de splicing alternativo do gene Actin-4, em particular que de Aedes spp. e mais preferível de AaActin-4, que é um gene de Aedes/Stegomyia aegypti que mostra splicing específica de tecido, estágio e de sexo.
Preferivelmente, splicing alternativo, particularmente a mediada por Actin-4, pode adicionar sequências que influenciam a tradução ou estabilidade de RNA, por exemplo.
Também se prefere que o mecanismo de splicing compreenda pelo menos um fragmento do gene doublesex (dsx), preferivelmente o derivado de Drosophila, B. mori, lagarta-rosada, traça das maçãs e pêras, ou um mosquito, em particular A. gambiae ou especialmente A. aegypti.
Prefere-se que a sequência de controle de splice e a sequência polinucleotídica heteróloga codificando uma proteína funcional, definidas entre um códon de partida e um códon de parada, e/ou polinucleotídeos para RNA interferência (RNAi), a serem expressadas em um organismo, sejam providas na forma de uma construção de minigene ou um éxon de cassete.
Isto é particularmente preferido quando a sequência de controle de splice é derivada de dsx (preferivelmente minigene 1 como descrito nos exemplos e representado em SEQ ID NO. 149 (éxons estão presentes nas posições 1-135, 1311-2446 e 3900-4389 de SEQ ID NO. 149) que foi incluída na construção LA3491) ou Actin-4.
Os exemplos particularmente preferidos da presente invenção são providos nos exemplos, e podem ser selecionados dentre o grupo consistindo dos plasmídeos ou construções, em particular qualquer um dos de acordo com qualquer uma das figuras 19-31, especialmente qualquer um dos plasmídeos mostrados nas Figuras 16-18, 22- 24, 26-32, 49, 52-55, e 61-69, e/ou SEQ ID NOs 46-48, 50-56, 143-145 e 151-162. Preferivelmente, a proteína funcional a ser expressada em um organismo é tTAV, tTAV2 ou tTAV3.
Outras proteínas a serem expressadas no organismo são, ou como evidente previstas, em combinação com a referida proteína funcional, preferivelmente um gene letal como discutido em outra parte.
Um ORF contínuo pode também ser pensado como um ORF ininterrupto, isto é uma sequência polinucleotídica em mRNA maduro, que não inclui nucleotídeos não de codificação, por exemplo aqueles tendo o potencial para serem traduzidos em aminoácidos. Nesta definição, prefere-se que o códon de parada não seja incluído.
Em algumas formas de realização, a pelo menos uma sequência de controle de splice regula o splicing alternativo por meio de ambos, nucleotídeos intrônicos e exônicos. No entanto, em uma forma de realização, é particularmente preferido que a pelo menos uma sequência de controle de splice seja uma sequência de controle de splice intrônica. Em outras palavras, prefere-se que a pelo menos uma sequência de controle de splice seja substancialmente derivada de polinucleotídeos que formam parte de um íntron e são deste modo excisados do transcrito primário por splicing, de modo que estes nucleotídeos não são conservados na sequência de mRNA maduro.
Assim, sequências intrônicas podem ser pensadas como distintas de sequências "exônicas", que são conservadas na molécula de RNA (pós splicing) processada. Onde a molécula de RNA processada codifica uma sequência de proteína ou polipeptídeo, e é capaz de ser traduzida, isto é, tem a estrutura correta e modificações tais como uma terminação, e um sinal de poliadenilação, por exemplo, é conhecido como mRNA maduro ou processado e algumas das sequências exônicas então codificam para aminoácidos, quando traduzidos.
Será entendido que em splicing alternativo, sequências podem ser intrônicas sob algumas circunstâncias (isto é em algumas de splicing alternativo), mas exônicas sob outras circunstâncias (isto é em outras variantes). Assim, a pelo menos uma sequência de controle de splice da presente invenção é preferivelmente substancialmente derivada de polinucleotídeos que formam parte de um íntron em pelo menos uma variante de splicing alternativo, isto é, ou no primeiro produto de mRNA spliced ou em pelo menos um produto de mRNA alternativamente spliced. Assim, íntrons ou sequências intrônicas podem ser vistos como spliced out em pelo menos um transcrito ou tipo de transcrito.
Por exemplo, considerando o íntron tra de C. capitata (íntron Cctra), que é um exemplo particularmente preferido de uma pelo menos uma sequência de controle de splice de acordo com a presente invenção. De acordo com figura 2 A de Pane et al, reproduzida como figura 33, todos os 8 dos sítios de ligação de Tra/Tra2 putativos realçados estão na sequência intrônica no sentido que eles estão em porções da sequência spliced no F1 de transcrito mas por outro lado 6 dentre os 8 são exônicos no sentido que eles estão em éxons que estão incluídos ou retidos em quer M1 ou M2 de transcrito, ou ambos. Assim, estes sítios de ligação de Tra/Tra2 são intrônicos no presente sentido como eles são capazes de controlar o splicing alternativo, mas são spliced out, isto é não presentes, em pelo menos uma variante de splicing alternativo, isto é, pelo menos um mRNA que foi spliced em uma maneira alternativa de pré-RNA.
Em splicing "normal" (não alternativa) e em splicing alternativo, íntrons são geralmente removidos do pré-RNA para formar um mRNA spliced, que pode então ser traduzido em um polipeptídeo, tais como uma proteína ou fragmento de proteína, tendo uma sequência de aminoácido. Assim, será prontamente evidente para um versado como determinar aquelas sequências do presente sistema que devem ser considerados intrônicas, em vez de exônicas.
Será, como evidente, notado que somente uma parte de um mRNA é de fato traduzida, isto é, tipicamente a parte entre o códon de partida e o códon de parada, embora será entendido que algumas vezes múltiplas partidas e paradas estão presentes. Assim, quando a referência é feita aqui para a tradução de uma sequência de mRNA, será notado que isto é referente à tradução da porção partindo no primeiro nucleotídeo do códon de partida e terminando após o último nucleotídeo antes da partida do códon de parada, que pode ser considerado como a porção de codificação.
Como mencionado acima, sequências exônicas podem estar envolvidas na mediação do controle de splicing alternativo, mas prefere-se que pelo menos algumas sequências intrônicas de controle estejam envolvidas na mediação do splicing alternativo. Em outras palavras, o sistema de expressão de gene da presente invenção pode também incluir sequências de controle de splice presentes em éxons, enquanto ocorre algum envolvimento intrônico de controle. Exemplos particularmente preferidos destes são as sequências de controle de splice derivadas de ou contendo elementos do gene dsx, onde, sem estar vinculado pela teoria, pensa-se que as sequências exônicas auxiliam no mecanismo de splicing alternativo.
Assim, em algumas formas de realização, a pelo menos uma sequência de controle de splice não compreende sequência exônica e será entendido que isto é previsto por definições usadas para descrever a presente invenção. Assim, como será evidente, é possível para alguns nucleotídeos serem englobados dentro da definição de pelo menos uma sequência de controle de splice e também dentro da definição de uma sequência polinucleotídica codificando uma proteína funcional. Em outras palavras, a definição destes elementos pode se sobrepor, tal que determinados nucleotídeos podem ser cobertos pela definição de mais de um elemento.
No entanto, o versado reconhecerá que isto não é incomum em biologia molecular, como nucleotídeos podem frequentemente realizar mais de um papel. Por exemplo, na presente invenção, um nucleotídeo pode formar parte de uma sequência de codificação de uma proteína funcional, mas poderia também formar parte de uma sequência reconhecida e ligada por um fator de splicing, um exemplo de que a proteína TRA ou complexo TRA/TRA, como discutido em outra parte. Não é incomum que, por exemplo, alguns vírus terem um genoma altamente concentrado onde a mesma extensão de polinucleotídeos pode codificar para duas ou mesmo três proteínas diferentes, cada lida em uma matriz diferente.
Como evidente, pode também ser que a sequência de controle de splice ou sequências sejam unicamente intrônicas, isto é, sem nenhuma influência exônica. De fato, isto é particularmente preferido.
Em algumas formas de realização, prefere-se que a pelo menos uma sequência de controle de splice seja capaz de ser removida do pré-RNA, por splicing. Preferivelmente, a pelo menos uma sequência de controle de splice não resulta em uma armação em pelo menos uma variante de splice. Preferivelmente isto é uma variante de splice codificando uma proteína funcional de comprimento completo. Em outras palavras, pelo menos a uma sequência de controle de splice preferivelmente não media a remoção de nucleotídeos que formam parte, ou foram planejados para formar parte de, uma sequência polinucleotídica codificando uma proteína funcional, definida entre um códon de partida e um códon de parada, e/ou polinucleotídeos de RNA interferência (RNAi), a serem expressados em um organismo. Por isso, entende-se que nucleotídeos que são excisados por splicing, em pelo menos uma variante de splice, não são nucleotídeos que codificam aminoácidos na forma de tipo selvagem da proteína ou gene. Uma ou mais variantes de splice podem ter referidos nucleotídeos excisados, mas pelo menos uma variante deve reter estes nucleotídeos, de modo que uma armação não induzida em pelo menos uma variante. Estes nucleotídeos removidos são aqueles que são removidos em adição às sequências que são normalmente spliced tais como o íntron.
No entanto, em vista do acima, prevê-se também que as variantes de splicing diferentes podem resultar na mesma sequência sendo lida em matrizes diferentes.
Interação da pelo menos uma sequência de controle de splice com maquinário de splicing celular, por exemplo o espliceossoma, conduz a ou media a remoção de uma série de, preferivelmente, pelo menos 50 nucleotídeos consecutivos do transcrito primário e ligação (splicing) junto de sequências nucleotídicas que não foram consecutivas no transcrito primário (porque elas, ou seu complemento se a sequência anti-sentido for considerada, não foram consecutivas na sequência de modelo original do qual o transcrito primário foi transcrito). Referida série de pelo menos 50 nucleotídeos consecutivos compreende um íntron. Esta mediação atua preferivelmente em um modo específico de sexo, específica de estágio, específica de linhagem germinal ou específica de tecido, ou combinação das mesmas, tal que os transcritos primários equivalentes em sexos, estágios, tipos de tecido, diferentes etc, tendem a remover íntrons de diferente tamanho ou sequência, ou em alguns casos podem remover um íntron em um caso mas não no outro. Este fenômeno, a remoção de íntrons de tamanho diferente ou sequência em circunstâncias diferentes, ou a remoção diferencial de íntrons de um tamanho ou sequência dado, em circunstâncias diferentes, é conhecido como splicing alternativo. Splicing alternativo é um fenômeno bem conhecido na natureza, e muitos exemplos são conhecidos, ver acima.
Em algumas formas de realização, a pelo menos uma sequência de controle de splice é associada com uma matriz de leitura aberta heteróloga tal que, em pelo menos uma variante de splice, a matriz de leitura aberta heteróloga é separada, por exemplo por um códon de parada ou armação, enquanto em pelo menos uma variante de splicing alternativo a matriz de leitura aberta heteróloga não é separada. Transcritos do segundo tipo codificam ou potencialmente codificam uma proteína funcional, considerando que aqueles do primeiro tipo codificam uma proteína com função alterada, separada ou mesmo sem função, atividade ou estabilidade relativa àqueles de segundo tipo.
Geralmente, será evidente para o versado na técnica que a matriz de leitura aberta heteróloga pode ser, ela mesma, um compósito ou fusão de sequências de várias fontes. Splicing para produzir uma proteína funcional pode ainda produzir uma proteína alterada relativa à matriz de leitura aberta heteróloga de protótipo, por exemplo se o íntron spliced alternativamente inserido incluir sequência que é exônica em todas as formas de splicing alternativo, e por esta razão conservada em mRNAs maduros do segundo tipo. No entanto, é particularmente preferido que pelo menos um transcrito remova todas, ou substancialmente todas, das sequências spliced alternativamente inseridas, tal que a matriz de leitura aberta heteróloga seja restaurada, ou substancialmente restaurada, para a forma intacta, com poucas ou nenhuma sequência endogenamente associada com o íntron restante no mRNA maduro. Endógeno é usado aqui em contraste a heterólogo, então será entendido que este refere-se a uma sequência que seria, no tipo selvagem, normalmente encontrada em associação com, ou ligada a, pelo menos um elemento ou componente da pelo menos uma sequência de controle de splice.
Alternativamente, um ou mais transcritos podem remover nucleotídeos adicionais, de modo que a matriz de leitura aberta heteróloga é separada, não pela inserção de nucleotídeos extras (por exemplo códon de parada ou armação, mas também sequência potencialmente de codificação que separa a função), mas sim por deleção de nucleotídeos da matriz de leitura aberta heteróloga, por exemplo de tal forma a induzir uma armação. Uma ou mais variantes de splice podem ter nucleotídeos excisados, mas pelo menos uma variante precisa conservar estes nucleotídeos, de modo que uma armação não é induzida em pelo menos uma variante. Estes nucleotídeos removidos são aqueles que são removidos em adição às sequências que são normalmente retiradas por splicing tais como o íntron, onde uma sequência intrônica pode ser considerada como uma que forma parte de um íntron em pelo menos uma variante de splicing alternativo do análogo natural.
Quando nucleotídeos exônicos devem ser removidos, então estes devem ser removidos em múltiplos de três, se é desejado evitar uma armação, mas como um nucleotídeo único ou múltiplos de dois (que não são também múltiplos de três) se é desejado induzir uma armação. Será notado que se apenas um ou alguns múltiplos de dois nucleotídeos são removidos, então isto poderia conduzir a uma sequência de proteína completamente diferente sendo codificada em ou em torno da junção de splice do mRNA.
Este é particularmente o caso em uma forma de realização do sistema onde éxon de cassetes são usados para interromper uma matriz de leitura aberta em algumas variantes de splice mas não outras, tais como em, por exemplo, tra, especialmente Cctra.
Em outra forma de realização preferida da presente invenção, toda ou parte de uma matriz de leitura aberta está em um éxon de cassete, por exemplo algumas formas de realização de Dsx derivadas de Aedes, são providas com, por exemplo, uma região de codificação de tTAV em um éxon de cassete que está apenas presente em variantes de splice específicas de fêmeas.
Onde a mediação de splicing alternativo é específica de sexo, prefere-se que a variante de splice codificando uma proteína funcional a ser expressada em um organismo seja a variante de splice F1, isto é uma variante de splice encontrada apenas ou predominantemente em fêmeas, e preferivelmente é a variante a mais abundante encontrada em fêmeas, apesar da mesma não ser essencial. Correspondentemente para configurações onde toda ou parte de uma matriz de leitura aberta funcional está em um éxon de cassete, prefere-se que este éxon de cassete esteja incluído em transcritos encontrados apenas ou predominantemente em fêmeas, e preferivelmente tais transcritos são, individualmente ou em combinação, as variantes as mais abundantes encontras em fêmeas, apesar disto não ser essencial.
Em uma forma de realização preferida, sequências são incluídas em uma sequência híbrida ou recombinante ou construção que são derivadas de sequências intrônicas de ocorrência natural que são elas próprias sujeitas a splicing alternativo, em seu contexto nativo ou original. Por esta razão, uma sequência intrônica pode ser considerada como uma que forma parte de íntron em pelo menos uma variante de splicing alternativo do análogo natural. Assim, sequências correspondentes a extensões contíguas únicas de sequência intrônica de ocorrência natural são previstas, mas também híbridos de tais sequências, incluindo híbridos de duas sequências intrônicas de ocorrência natural diferentes, e também sequências com deleções ou inserções relativas a extensões contíguas únicas de sequência intrônica de ocorrência natural, e híbridos das mesmas. Referidas sequências derivadas de sequências intrônicas de ocorrência natural poderão ser associadas, na invenção, com sequências não fazendo parte, elas mesmas, de qualquer íntron de ocorrência natural. Se tais sequências forem transcritas, e preferivelmente retidas no RNA maduro em pelo menos uma variante de splice, elas podem ser então consideradas exônicas.
Também será notado que a referência a uma "armação" poderia também referir-se a uma codificação direta de um códon de parada, que também é provável de conduzir a uma proteína não funcionando como seria uma ruptura da sequência de mRNA spliced causada por inserção ou deleção de nucleotídeos. Produção de variantes de splice diferentes de duas ou mais proteínas diferentes ou sequências de polipeptídeo de função diferencial é também prevista, em adição à produção de duas ou mais proteínas diferentes ou sequências de polipeptídeo das quais uma ou mais não tem função prevista ou discernível. Também é prevista a produção de variantes de splice diferentes de duas ou mais proteínas diferentes ou sequências de polipeptídeo de função similar, mas diferindo a localização subcelular, estabilidade ou capacidade de se ligar a ou se associar com outras proteínas ou ácidos nucléicos.
Preferivelmente, a pelo menos uma sequência de controle de splice é intrônica e compreende em sua extremidade 5' um nucleotídeo de guanina (G). Em outras palavras, nucleotídeo 5' da sequência de controle de splice, 3' para o sítio doador de splice, e preferivelmente na superfície ou junção do éxon com sequência de controle de splice, é Guanina (G), no pré- RNA, ou C em uma sequência de DNA anti-sentido correspondendo à mesma.
Além disso, o nucleotídeo adjacente (3' para referida G) é preferivelmente Citosina (C) no pré-RNA, ou uma G correspondente em uma sequência de DNA, mas é mais preferível Uracila (U) no pré-RNA,ou um A correspondente na sequência anti-sentido de DNA. Assim, os dois nucleotídeos 5' da sequência de controle de splice são preferivelmente 5'GT com relação ao filamento sentido de DNA, 5'-GU no transcrito primário.
Preferivelmente, pelo menos uma sequência de controle de splice intrônica também compreende em sua extremidade 3' um nucleotídeo de guanina 3' e preferivelmente AG-3' na junção do sítio aceitador de splice com éxon, por exemplo, ver figura 34.
Preferivelmente, a sequência de flanqueamento 5' para o sítio doador de splice no sistema compreende 5'-TG, de modo que a sequência pode ser representada 3' de sequência de controle de splice-** de 5 '-TG-*, onde * representa o sítio doador de splice e ** representa o sítio aceitador de splice.
Preferivelmente, a sequência de controle de splice é também flanqueada em seu lado 3' por um nucleotídeo de G, e mais preferível por nucleotídeos de GT, tal que a sequência poderia ser representada como: 5'- TG- *- sequência de controle de splice ** -GT-3' *. Será notado que esta é a sequência de DNA de filamento sentido (TG). Assim, o pré-RNA transcrito irá ler UG por exemplo, onde U substitui T.
Derivados de Guanina ou Timina tendo a mesma função são também visados. Prefere-se particularmente que o splicing seja específico de sexo e ainda mediado ou controlado ligando a proteína TRA ou complexo de proteína TRA/TRA2, ou homólogos da mesma. Em insetos, por exemplo, a proteína TRA é diferencialmente expressada em sexos diferentes. Em particular, a proteína TRA é conhecida como estando presente basicamente em fêmeas, por esta razão, media o splicing alternativo de tal forma que uma sequência de codificação é expressada em um modo específico de sexo, isto é, que em alguns casos uma proteína é expressada apenas em fêmeas ou em um nível muito maior em fêmeas do que em machos ou, alternativamente, em outros casos uma proteína é expressada apenas em machos, ou em um nível muito maior em machos do que em fêmeas. Enquanto prefere-se que a proteína seja expressada apenas em machos, é particularmente preferido que a proteína seja expressada apenas em fêmeas. No entanto, o mecanismo para realizar este splicing alternativo específica de sexo mediada pela proteína TRA ou pelo complexo TRA/TRA2 é conhecido e é discutido, por exemplo, em Pane et al (Development 129, 3715-3725 (2002)).
Preferivelmente, a pelo menos uma sequência de controle de splice compreende, e mais preferivelmente consiste de, o íntron tra derivado do gene tra de Ceratitis capitata (Cctrd), que tem uma região alternativamente spliced. No transcrito F1, como ilustrado pela figura 33 (figura 2A de Pane et al (2002) supra), este é o primeiro íntron. Homólogos do gene tra em outras espécies, tais como Bactrocera oleae, Ceratitis rosa, Bactrocera zonata e Drosophila melanogaster também tem região alternativamente spliced em um local similar dentro da sequência de codificação de tra. Íntrons tras derivados destes insetos também são particularmente preferidos.
O padrão de splicing em Cctra em particular é bem conservado, com aqueles transcritos encontrados em machos contendo material exônico adicional relativo ao transcrito de F1, tal que estes transcritos não codificam proteína funcional de comprimento completo. Por contraste, o transcrito de F1 não codifica proteína Tra de comprimento completo; este transcrito é substancialmente específico de fêmea na maior parte dos estágios do ciclo da vida, ainda que seja especulado que embriões muito prematuros de ambos os sexos podem conter uma quantidade pequena deste transcrito. Os requerentes descreveram a sequência spliced do transcrito de F1, mas não os transcritos específicos de machos ou não específicos de sexo, como o íntron tra, ou mesmo o íntron F1 de tra. Assim a versão desta sequência encontrada no gene CCtra é o íntron Cctra.
Assim o gene tra é regulado em parte por splicing alternativo específica de sexo, enquanto seu produto chave, a proteína Tra, é ela própria envolvida em splicing alternativo. Em insetos, splicing alternativo específico de sexo mediada pela proteína Tra, ou um complexo compreendendo as proteínas TRA e TRA2, incluem sequências de controle de splice de Dípteros derivadas do gene doublesex (dsx) e também o próprio íntron tra, embora o mesmo excluiria o íntron tra de Drosophila (Dmtra), que é principalmente mediado pelo produto de gene Sxl em Drosophila, em vez de TRA ou complexo TRA/TRA2.
Fora de Drosophila, o produto de gene Sxl não é diferencialmente expressado em sexos diferentes. Não se pensa que Sxl atue na mediação de splicing alternativo específica de sexo em insetos não drosófilos.
Exemplos da proteína TRA que liga aos sítios de proteína de ligação (as sequências nucleotídicas especificamente reconhecidas pela proteína Tra) no íntron tra são preferivelmente de Díptera, preferivelmente da família Tephritidae, mais preferivelmente dos gêneros Ceratitis, Anastrepha ou Bactrocera. No entanto, prevê-se também que outros dípteros, tais como drosófilos ou mosquitos de várias formas discutidas acima, também são capazes de prover a proteína TRA ou homólogas da mesma, que são capazes de se ligar aos sítios apropriados nas sequências de controle de splice derivadas do gene dsx, o gene tra ou o íntron tra, isto é o íntron tra spliced alternativamente completamente removido no transcrito de F1, mesmo naqueles casos, tais como Drosophila, onde o gene tra natural (Dmtra) não é, ele mesmo, regulado por proteína TRA. Em algumas formas de realização, o "íntron tra" pode ser definido como uma sequência de controle de splice onde splicing alternativo do transcrito de RNA é regulado por TRA, por exemplo sua ligação, sozinha ou em combinação (isto é quando complexada) com TRA2. Isto exclui o íntron tra de Drosophila.
Prefere-se particularmente que as sequências de controle de splice sejam derivadas do íntron tra. Referido íntron tra pode ser derivado, como discutido em outra parte, de Ceratitis, Anastrepha ou Bactrocera. O íntron tra de Ceratitis capilala do gene transformer foi inicialmente caracterizado por Pane et al (2002), supra. No entanto, será notado que homólogos existem em outras espécies, e podem ser facilmente identificados em referidas espécies e também em seus vários gêneros. Assim, quando referência é feita a tra será notado que isto também se refere aos homólogos de tra em outras espécies, especialmente em espécies de Ceratitis, Anastrapha ou Bactrocera.
Por "derivado" será entendido que, usando a referência ao íntron tra, isto refere-se a sequências que se aproximam a ou replicam exatamente o íntron tra, como descrito na técnica, nesse caso por Pane et al (2002), supra. No entanto, será notado que, como estas são sequências intrônicas, alguns nucleotídeos podem ser adicionados ou substituídos sem uma perda substancial na função.
Exemplos preferidos disso incluem o íntron dsx, preferivelmente provido na forma de um minigene. Nesse exemplo, pode ser preferível deletar, como feito nos exemplos, quantidades relativamente grandes de íntrons spliced alternativamente spliced, por exemplo 90% ou mais de um íntron em alguns casos, enquanto ainda conservando a função de splicing alternativo. Assim, apesar de deleções grandes estarem previstas, prevê-se também que inserções, substituições ou deleções mesmo menores, por exemplo de nucleotídeo único, também são preferidas.
O comprimento exato da sequência de controle de splice derivado do íntron tra não é essencial, desde que seja capaz de mediar a splicing alternativo. A este respeito, pensa-se que cerca de 55 a 60 nucleotídeos é o comprimento mínimo de um íntron tra modificado, embora o íntron tra de tipo selvagem (variante de splice F1) de C. capitata é na região de 1345 nucleotídeos de comprimento. Prefere-se particularmente que a sequência de 1345 ntd de comprimento completo de Cctra seja usada.
Como com todas as sequências nucleotídicas discutidas aqui, prefere-se que um certo grau de homologia de sequência seja prevista, salvo de outra forma evidente. Assim, prefere-se que a sequência de controle de splice tenha pelo menos 80% de homologia de sequência com a referência SEQ ID NO., preferivelmente pelo menos 80% de homologia de sequência com a referência SEQ ID NO., preferivelmente pelo menos 80% de homologia de sequência com a referência SEQ ID NO., mais preferivelmente pelo menos 90% de homologia de sequência com a referência SEQ ID NO., mais preferivelmente pelo menos 95% de homologia de sequência com a referência SEQ ID NO., ainda mais preferivelmente pelo menos 99% homologia de sequência com a referência SEQ ID NO., e a mais preferível, pelo menos 99.9% de homologia de sequência com a referência SEQ ID NO.
Um algoritmo apropriado tal como BLAST pode ser usado para determinar homologia de sequência. Se quantidades grandes de sequência são deletadas do tipo selvagem, então a comparação de sequência pode ser sobre o comprimento completo do tipo selvagem ou sobre sequências alinhadas de homologia similar.
No entanto, será entendido que apesar da homologia de sequência acima, determinados elementos, em particular os nucleotídeos de flanqueamento e sítio de ramificação de splice devem ser conservados, para funcionamento eficiente do sistema. Em outras palavras, enquanto porções podem ser deletadas ou, de outro modo, alteradas, funcionalidade ou atividade de splicing alternativo, a pelo menos 30%, preferivelmente 50%, preferivelmente 70%, mais preferivelmente 90%, e, a mais preferível, 95% comparada ao tipo selvagem deve ser conservada. Isto pode ser aumentado do tipo selvagem, bem como, por engenharia apropriada dos sítios que ligam fatores de splicing alternativo ou interagem com espliceossoma, por exemplo.
Em particular, prefere-se que onde a sequência de controle de splice compreende um íntron tra modificado, ela compreenda pelo menos 20 a 40 pares de base de 5' e, preferivelmente, assim a extremidade 3' de referido íntron. Além disso, prefere-se que pelo menos 3 ou 4 e, mais preferido, pelo menos 5, preferivelmente 6, mais preferivelmente 7 e, mais preferido, todos os 8 dos 8 domínios de ligação de TRA putativos do íntron tra de C. capitata, como ensinado por Pane et al (2002), ou homólogos disso, sejam providos. Como evidente, se mais de tais sítios forem descobertos em devido curso, então é visado que a sequência de controle de splice poderia incluir mais do que 8 sítios. De fato, é previsto que mais do que 8 sítios possam ser engenheirados na sequência de controle de splice e que o splicing alternativo possa ser regulado desta forma, especialmente se alguns sítios estiverem ligados com afinidades diferentes levando um resultado de splicing alternativos diferentes.
Uma sequência de consenso para os domínios de ligação de TRA putativos do íntron tra de C. capitata é dada abaixo como SEQ ID NO 1, uma sequência de DNA, embora o RNA correspondente equivalente é também preferido. As sequências de consenso preferidas são 1: TCWWCRATCAACA (SEQ ID NO. 1), onde W = A ou T e R = A ou G.
Considerações similares aplicam-se a doublesex, onde a sequência de consenso da proteína TRA é também aquela dada em SEQ ID NO. 1 como um complexo de proteína compreendendo as proteínas Tra e TRA2 é um regulador chave de splicing alternativo de doublesex , como é de homólogos tra (embora não sejam os homólogos tra encontrados em drosofilídeos).
Como mencionado acima, as sequências de controle de splice são preferivelmente derivadas do íntron tra, preferivelmente da família Tephritidae. Prefere-se particularmente que o íntron tra seja derivado de B. zonata ou, preferivelmente, de outras moscas de frutas não drosofilídeos. No entanto, é particularmente preferido que o íntron tra seja derivado dos gêneros de Ceratitis, em particular C. rosa e, o mais preferível, C. capitata. Estes são mais vastamente conhecidos como as moscas-de-natal e do-mediterrâneo, respectivamente.
Com relação ao íntron tra derivado de B. zonata, os requerentes demonstraram que isto pode levar a um splicing alternativo específico de sexo em mosca mexicana das frutas transgênica (Anastrapha ludens) e em mosca-do-mediterrâneo transgênica (C capitata). Os requerentes também demonstraram que uma variedade de proteínas pode ser expressada em um modo específico de sexo através de splicing alternativo, incluindo tTAV 3 e Rpr.
Em relação ao íntron tra derivado de C. rosa, os requerentes demonstraram com sucesso splicing alternativo em um modo específico de sexo de um transgene em mosca-do-mediterrâneo.
Com relação ao íntron tra derivado de C. capitata (mosca-do- mediterrâneo), os requerentes demonstraram que este pode mediar o splicing específico de sexo em mosca-do-mediterrâneo transgênica, e outras tefrítidas, e outras tefrítidas tais como A. ludens (mosca mexicana das frutas). Não apenas isso, os requerentes demonstraram que este íntron pode trabalhar com sucesso através de toda faixa de insetos e, em particular, dípteros. De fato, os requerentes demonstraram que o íntron tra de C. capitata (referido como Cctra) pode prover splicing alternativo específico de sexo em Drosophila transgênica, que não é uma tefrítida, e também no mosquito Aedes aegypti. Embora mosquitos sejam dípteros, eles divergiram de drosófilos e tefrítidos cerca de 250 milhões de anos atrás e, por esta razão, são parentes bem mais distantes que os drosofilídeos são para as tefrítidas, para os quais o tempo de divergência foi estimado como 120-150 milhões de anos. Assim, isto mostra uma ampla aplicabilidade da presente invenção através de uma extensa faixa de insetos.
No que diz relação a sequências de controle de splice derivadas do íntron dsx, também os requerentes demonstraram que isto pode ser usado para splice alternativamente, em um modo específico de sexo, em uma ampla faixa de insetos. Consequentemente, é particularmente preferido que o dsx seja derivado de Bombyx mori (bicho da seda), Pectinophora gossypiella (lagarta rosada) Pectinophora gossypiella, Cydia pomonella (traça das maças e pêras), Drosophila, e mosquitos tais como Anopheles sp., por exemplo A. gambiae. Mosquitos particularmente preferidos incluem Stegomyia spp., particularmente S. aegypti (também conhecido como Aedes aegypti).
De fato, em A. aegypti, os requerentes demonstraram um número considerável de construções de DNA, que são capazes de prover splicing alternativo específico de sexo.
Será notado que o sistema ou construção seja preferivelmente administrado como um plasmídeo, mas geralmente testado após integrar no genoma. Administração pode ocorrer por métodos conhecidos na técnica, tais como parenteral, intravenosa, intramuscular, oral, transdérmica, liberada através de uma membrana mucosa, e assim por diante. Injeção em embriões é particularmente preferida. O plasmídeo pode ser linearizado antes ou durante administração, e nem todos dentre os plasmídeos podem ser integrados no genoma. Onde apenas parte do plasmídeo é integrada no genoma, prefere-se que esta parte inclua a pelo menos uma sequência de controle de splice capaz de mediar o splicing alternativo.
Preferivelmente, o sistema de expressão de polinucleotídeos é um sistema genético letal dominante recombinante, cujo efeito letal é condicional. Condições apropriadas incluem temperatura, de modo que o sistema é expressado a uma temperatura mas não, ou em menor grau, em outra temperatura, por exemplo. O sistema genético letal pode atuar em células ou tecidos específicos ou impor seu efeito em todo o organismo. Sistemas que não são estritamente letais mas impõem um custo substancial à aptidão física são também previstos, por exemplo levando à a cegueira, aptidão ao vôo (para organismos que poderiam normalmente voar), ou esterilidade. Sistemas que interferem com a determinação de sexo são também previstos, por exemplo transformando ou tendendo a transformar todo ou parte de organismo de um tipo sexual a outro. Será entendido que todos tais sistemas e consequências são englobados pelo termo letal como usado aqui. Similarmente, "matar", e termos similares referem-se à expressão efetiva do sistema letal e assim a imposição de um fenótipo deletério ou de deformidade sexual, por exemplo morte.
Mais preferivelmente, o sistema de expressão de polinucleotídeo é um sistema genético letal dominante recombinante, cujo efeito letal é condicional e não é expressado sobre condições permissivas requerendo a presença de uma substância que está ausente do ambiente natural do organismo, tal que o efeito letal do sistema letal ocorre no ambiente natural do organismo.
Em outras palavras, as sequências de codificações codificam um ligado letal a um sistema tal como o sistema tet descrito em WO 01/39599 e/ou WO2005/012534.
De fato, prefere-se que a expressão de referido gene letal ocorra sob o controle de uma proteína de transativador reprimível. Também prefere-se que o gene cuja expressão é regulada por splicing alternativo codifique um proteína de transativador tal como tTA. Isto não é incompatível com a proteína regulada ser uma letal. De fato, é particularmente preferido que ela seja os dois. A este respeito, os requerentes preferem particularmente que o sistema inclua um sistema de retro-alimentação positivo como ensinado em WO2005/012534.
Preferivelmente, o efeito letal do sistema letal dominante é condicionalmente supressivo. Organismos apropriados sobre os quais o presente sistema pode ser usado incluem mamíferos tais como camundongos, ratos e animais de criação. Também são preferidos peixes, tais como salmão e truta. Plantas também são preferidas, mas é particularmente preferido que o organismo hospedeiro seja um inseto, preferivelmente um díptero ou tefrítidos. Preferivelmente, o organismo não é um humano, preferivelmente não é um mamífero, preferivelmente não é um pássaro, preferivelmente é um invertebrado, preferivelmente é um artrópode.
Em particular, prefere-se que o inseto seja da Ordem Díptera, especialmente dípteros superiores e particularmente ele é uma mosca tefrítida das frutas, preferivelmente mosca-do-mediterrâneo (Ceratitis capitata), preferivelmente mosca mexicana das frutas (Anastrepha ludens), preferivelmente mosca oriental das frutas (Bactrocera dorsalis), mosca da azeitona (Bactrocera oleae), mosca do melão (Bactrocera cucurbitae), mosca-de-natal (Ceratitis rosa), mosca da cereja (Rhagoletis cerasi), mosca das frutas de Queensland (Bactrocera tyroni), mosca do pêssego (Bactrocera zonata), mosca das frutas do Caribe (Anastrepha suspensa) ou mosca das frutas da Índia Ocidental (Anastrepha obliqua). Também é particularmente preferido que o organismo hospedeiro seja um mosquito, preferivelmente dos gêneros Stegomyia, Aedes, Anopheles ou Culex. São particularmente preferidos Stegomyia aegyptae, também conhecidos como Aedes aegypti, Stegomyia albopicta (também conhecidos como Aedes albopictus), Anopheles stephensi, Anopheles albimanus e Anopheles gambiae.
Dentro dos Dípteros, outro grupo preferido é Calliphoridae, particularmente o verme-parafuso do Novo Mundo (Cochliomyia hominivorax), verme-parafuso do Velho Mundo (Chrysomya bezziana) e mosca australiana da ovelha (Lucilia cuprina). Lepidópteros e Coleópteros também são preferidos, especialmente traças, incluindo traça das maçãs e pêras (Cydia pomonella), e o bicho da seda (Bombyx mori), a lagarta rosada (Pectinophora gossypiella), a lagarta da couve (Plutella xylostella), a mariposa (Lymantria dispar), a traça de laranja-da-baía (Amyelois transitella), a lagarta mineira do pessegueiro (Anarsia lineatella), e a broca da haste do arroz (Tryporyza incertulas), as traças noctuídas, especialmente Heliothiane. Dentre os Coleópteros, o besouro japonês (Popilla japonica), o besouro franjado branco (Graphognatus spp.), o gorgulho do algodão (Anthonomous grandis), a lagarta da raiz do milho (Diabrotica spp), e escaravelho da batateira (Leptinotarsa decemlineata) são particularmente preferidos.
Preferivelmente, o inseto não é um drosofilídeo, especialmente Dm. Assim, em algumas formas de realização, expressão em drosofilídeos, especialmente Dm é excluída. Em outras formas de realização, a sequência de controle de splice não é derivada do íntron tra de um drosofilídeo, especialmente Dm.
Prefere-se que a expressão da sequência polinucleotídica heteróloga conduza a uma consequência fenotípica no organismo. Prefere-se particularmente que a proteína funcional não seja beta-galactosidase, mas possa estar associada com marcadores visíveis (incluindo fluorescência), viabilidade, fertilidade, fecundidade, conveniência, aptidão ao vôo, visão, e diferenças comportamentais. Será notado, como evidente, que, em algumas formas de realização, os sistemas de expressão são tipicamente condicionais, com o fenótipo sendo expressado apenas sobre algumas condições, por exemplo restritivas.
Em um outro aspecto, provê-se também um método de controle populacional de um organismo em um ambiente natural para o mesmo, compreendendo: i) reproduzir um lote do organismo, o organismo transportando um sistema de expressão de gene compreendendo um sistema de acordo com a presente invenção que é um sistema genético letal dominante, ii) distribuir os referidos animais de lote no meio ambiente em um local para controle populacional; e iii) obter um controle da população através da letalidade em estágio prematuro por expressão do sistema letal na descendência que resulta da inter-reprodução dos referidos indivíduos no lote com os indivíduos do sexo oposto da população selvagem.
Preferivelmente, a letalidade de estágio prematuro é embriônica ou antes de maturidade sexual, preferivelmente no início de desenvolvimento, mais preferível, nos estágios prematuros da vida larval ou embriônica.
Preferivelmente, o efeito letal do sistema letal é condicional e ocorre no referido ambiente natural através da expressão de um gene letal, a expressão de referido gene letal estando sob controle de uma proteína de transativados reprimível, a referida reprodução ocorrendo sob condições permissivas na presença de uma substância, a substância estando ausente do referido ambiente natural e capaz de reprimir referido transativador.
Preferivelmente, o efeito letal é expressado nos embriões de referida descendência. Preferivelmente, o organismo é um animal multicelular invertebrado ou é como discutido em outra parte.
Também provê-se um método de controle biológico, compreendendo: i) reproduzir um lote de organismos machos e fêmeas transformados com o sistema de expressão de acordo com a presente invenção sob condições permissivas, permitindo a sobrevivência dos machos e fêmeas, para dar um agente de controle biológico de sexo dual; ii) opcionalmente antes da próxima etapa impor ou permitir condições restritivas para causar a morte de indivíduos de um sexo e, assim, prover um agente de controle biológico de sexo único compreendendo indivíduos do outro sexo transportando o sistema genético letal condicional; iii) liberar o agente de controle biológico de sexo dual ou de sexo único no meio ambiente em um locus para controle biológico; e iv) obter controle biológico através da expressão do sistema genético na descendência resultante de inter-reprodução dos indivíduos do agente de controle biológico com indivíduos do sexo oposto da população selvagem.
Preferivelmente, ocorre separação de sexos antes da distribuição de organismo por expressão de um sistema genético letal específico de sexo.
Preferivelmente, o efeito letal resulta em matar mais de 90% da classe alvo da progênie de acasalamentos entre os organismo liberados e a população selvagem.
Também provê-se um método de separação de sexos compreendendo: i) reproduzir um lote de organismos machos e fêmeas transformados com o sistema de expressão de gene sob condições permissivas ou restritivas, permitindo a sobrevivência dos machos e fêmeas; e ii) remover as condições permissivas ou restritivas para induzir o efeito letal do gene letal em um sexo e não em outro por splicing alternativo específico de sexo do gene letal.
Preferivelmente, o efeito letal resulta em matar mais do que 90% da classe alvo da progênie de acasalamentos entre organismos liberados e a população selvagem.
Também provê-se um método de controle biológico ou populacional compreendendo; i) reproduzir um lote de organismo machos e fêmeas transformados com o sistema de expressão de genes sob condições permissivas ou restritivas, permitindo a sobrevivência dos machos e fêmeas; ii) remover as condições permissivas ou restritivas para induzir o efeito letal do gene letal em um sexo e não em outro por splicing alternativo específico de sexo do gene letal para obter uma separação de sexos; iii) esterilizar ou parcialmente esterilizar os indivíduos separados e iv) realizar referido controle através de da liberação dos indivíduos estéreis ou parcialmente estéreis separados no meio ambiente natural do organismo.
Preferivelmente, a esterilização é realizada através do uso e radiação ionizante. Geralmente, no entanto, métodos evitando irradiação, como usado na técnica de inseto estéril (SIT) são especialmente preferidos e têm muitas vantagens de custo e saúde sobre os métodos associados com ou seguidos pelo uso de radiação.
Também provê-se um método para eliminar seletivamente fêmeas de uma população. O equivalente para machos também é previsto.
Métodos de separação de sexo são enormemente importantes comercialmente em, por exemplo, bichos da seda, onde os machos produzem seda em maior e melhor quantidade do que as fêmeas. Assim, métodos de separação de sexo que eliminam as fêmeas e, em particular bichos da seda fêmeas são particularmente preferidos.
Prevê-se também que a proteína funcional pode ser uma expressada diferencialmente, mas detectável em mais de um variante de splice e preferivelmente, por esta razão, em ambos sexos, por exemplo. Tais exemplos incluem uma proteína fluorescente, tais como eGFP, CopGFP e DsRed2. Esta pode ser usada em um método de separação ou escolha de sexo não letal, de modo que se pode separar os dois tipos sem matar qualquer um deles.
Os requerentes verificaram surpreendentemente que o posicionamento da sequência de controle de splice pode ser alterado e melhores resultados obtidos. Preferivelmente, a sequência de controle de splice é a "primeira" sequência de controle de splice, quando lida a partir do promotor, na direção de 5' a 3'. Os requerentes verificaram que em determinadas construções com um íntron em 5' UTR do sistema este fato conduzida a reduzidos níveis ou expressão de proteína alternativamente spliced mediada pela sequência de controle de splice da presente invenção.
Preferivelmente, a sequência de controle de splice é 3' para o códon de partida. Preferivelmente, a sequência de controle de splice está inserida dentro do primeiro éxon, isto é a extensão de sequência imediatamente 3' para o sítio de partida de transcrição. Será entendido que tais termos podem referir-se à sequência de DNA que codifica o transcrito, ou para o próprio transcrito de RNA.
Onde a sequência de controle de splice é 3' para o códon de partida, prefere-se que seja também 5' para o primeiro códon de parada na matriz (que é 3' para e em matriz com o códon de partida), de modo que o splicing alternativo produz transcritos que codificam proteína ou sequências de polipeptídeos diferentes. Assim em uma forma de realização preferida, a construção ou sequência polinucleotídica compreende os seguintes elementos em ordem de 5' a 3', com relação ao filamento sentido ou transcrito primário: partida de transcrição, partida de tradução, íntron capaz de splicing alternativo, sequência de codificação de toda ou parte de uma proteína, códon de parada.
A sequência de controle de splice pode ser definida como preferivelmente até e incluindo 5' G (GT/C) seu equivalente 3' G, especialmente em tra, mas, como mencionado acima, pode incluir algumas sequências exônicas e, por esta razão, poderia incluir o nucleotídeo o mais 3' (último) do éxon (isto é G).
Prefere-se particularmente que a sequência de controle de splice seja imediatamente adjacente, na direção de 3', do códon de partida, de modo que G de ATG está 5' para partida (extremidade 5') da sequência de controle de splice. Isto é particularmente vantajoso como permite a G do códon de partida de ATG ser a sequência de flanqueamento de 5' G para a sequência de controle de splice.
Alternativamente, a sequência de controle de splice é 3' para o códon de partida mas dentro de 1000 bp exônico, preferivelmente 500 bp exônico, preferivelmente 300 bp exônico, preferivelmente 200 bp exônico, preferivelmente 150 bp exônico, preferivelmente 100 bp exônico, mais preferivelmente 75 bp exônico, mais preferivelmente 50 bp exônico, mais preferivelmente 30 bp exônico, mais preferivelmente 20 bp exônico, e, o mais preferível, 10 ou mesmo 5, 4, 3, 2, ou 1 bp exônico.
A presente invenção é um aperfeiçoamento no sistema definido como LA1188 em WO2005/012534. Esse plasmídeo tem um número de defeitos, sendo o principal que os nucleotídeos exônicos foram excisados com o íntron Cctra usado aí, assim resultando em uma armação induzida no transcrito.
Especificamente, em adição a sequência derivada de Cctra (o íntron Cctra), 4 nucleotídeos de sequência de tTAV foram removidos no transcrito específico de fêmea. Por esta razão, embora vários transcritos spliced alternativamente foram produzidos, incluindo um transcrito específico de fêmea, nenhum foi capaz de codificar a proteína tTAV funcional. Por esta razão, esta construção não foi capaz de prover expressão específica de sexo de proteína tTAV funcional.
Desde que splicing não foi direcionado à sequência de doador de splice (5'-GT...) normalmente usada no íntron Cctra, claramente esta construção não conteve todas das sequências regulatórias necessárias para direcionar splicing na forma do íntron Cctra em "seu contexto nativo" No entanto, isto realça outro tecido. Provavelmente a única coisa faltando foi o TG...GT de flanqueamento, do qual é possível que apenas importava 5' G.
Um benefício chave da presente invenção é, em particular em relação a tra, que as exigências das sequências exônicas são tão mínimas (por exemplo 2 nucleotídeos em cada extremidade) que elas podem facilmente ser projetadas em maiores sequências de codificação, usando a redundância no código genético. Assim, os nucleotídeos exônicos "extras" podem ser tanto parte de sequência de proteína heteróloga como a sequência de flanqueamento do íntron em seu contexto nativo ao mesmo tempo.
Consequentemente, o íntron Ccfra em LA1118 foi +132bp 3' para o G do Códon de partida ATG (para o último nucleotídeo exônico). De fato, embora o íntron Cctra em LA1118 seja o primeiro íntron lido na direção de 5' a 3' do códon de partida ATG, ele não é o "primeiro" íntron quando lido na direção de 5' a 3' do promotor. De fato, é o segundo íntron, como não há mais um íntron (derivado de gene Adh de Drosophila melanogaster) a montante do Códon de partida de ATG. Esta informação está incluída na Tabela 3.
Será entendido que onde referência é feita a códon de partida de ATGs ou G de flanqueamento, ou sequências de 5'- TG...GT-3', que isto está relacionado com a sequência de DNA, mas isto também abrange a sequência de DNA anti-sentido correspondente e, igualmente, a sequência de RNA correspondente.
Descrição das Sequências da presente invenção SEQ ID NO. 1 sequência de consenso tra SEQ ID NO. 2 sequência de flanqueamento 5' de LA3097 SEQ ED NO. 3 sequência de flanqueamento 3' de LA3097 SEQ ID NO. 4 iniciador 688 iel-transcr SEQ ID NO. 5 iniciador 790 Aedsx-m-r2 SEQ ID NO. 6 iniciador 761 Aedsx-fem-r SEQ ID NO. 7 iniciador AedsxRl SEQ ID NO. 8 sequência de consenso de Pane et al SEQ ID NO. 9 sequência de consenso de Scali et al 2005 SEQ ID NOS. 10 - 33 e 107 - 138 sequências de consenso de sítios de ligação Tra/Tra2 putativos deduzidos de Drosophila (ver Tabela 2). SEQ ID NO. 34: Matriz de leitura aberta de tTAV SEQ ID NO. 35: Sequência de proteína de tTAV SEQ ID NO. 36: Matriz de leitura aberta de tTAV2 SEQ ID NO. 37: Sequência de proteína de tTAV2 SEQ ID NO. 38: Matriz de leitura aberta de tTAV3 SEQ ID NO. 39: Sequência de proteína de tTAV3 SEQ ID NO. 40: Fragmento 1 de sequência específica de fêmea dsx de lagarta rosada SEQ ID NO. 41: fragmento 2 de sequência específica de fêmea dsx de lagarta rosada (PBW, Pectinophora gossypiella) SEQ ID NO. 42: sequência específica de macho de dsx de lagarta rosada (PBW, Pectinophora gossypiella) SEQ ID NO. 43: Sequência de gene parcial dsx de Aedes aegypti. Toda sequência exônica é incluída, mas apenas sequência intrônica parcial- ver figuras 47 e 48 para anotação. SEQ ID NO. 44: sequência de gene de fêmea dsx de traça das maçãs e pêras (Cydia pomonella): inclui uma extensão de nucleotídeos desconhecidos, preferivelmente além de 100, preferivelmente inferior a 50, mais preferivelmente inferior a 20, mais preferivelmente inferior 10, e, o mais preferível, inferior a 5. SEQ ID NO. 45: sequência de macho dsx de traça das maçãs e pêras (Cydia pomonella). SEQ ID NO. 46: sequência de construção de pLA3435/plasmídeo dsx de Bombyx mori . SEQ ID NO. 47: sequência de construção de pLA3359 dsx de Anopheles gambiae. SEQ ID NO. 48: sequência de construção de pLA3433 Agdsx (Anopheles gambiae) com éxon 2 incluído. SEQ ID NO. 49: sequência de construção de pLA1118 - íntron Cctra SEQ ID NO. 50: sequência de construção de pLA3077 - íntron Cctra-tTAV. SEQ ID NO. 51 : sequência de construção de pLA3097 - íntron Cctra-tTAV. SEQ ID NO. 52: sequência de pLA3233 - íntron Cctra - tTAV2. SEQ ID NO 53: sequência de construção de pLA3014 - íntron Cctra - ubiquitina - ReaperKR. SEQ ID NO. 54: sequência de construção de pLA3166 - íntron Cctra -ubiquitina - ReaperKR. SEQ BD NO. 55: sequência de pLA3376 - íntron Bztra - ReaperKR -- íntron Bztra - tTAV3. SEQ ED NO. 56: sequência de construção de pLA3242 - íntron Crtra - ReaperKR. SEQ ID NO. 57: Sequência parcial de um transcrito de macho gerado em Drosophila melanogaster de transformantes de LA3077 que diferem para a sequência gerada em linhagens de LA3077 de mosca-do- mediterrâneo. Esta sequência corresponde ao transcrito M3 representado na figura 36. SEQ ID NO. 58: Sequência parcial de homólogo tra de Bactrocera zonata. Sequência de íntron prevista para ser spliced em um transcrito específico de fêmea tra de B. zonata (+3 a +970bp em sequência). Nucleotídeo exônicos de flanqueamento estão nas posições 1-2 e 971-972, isto é nas extremidades de 5' e 3' da sequência intrônica. De fato, deve-se observar que a sequência intrônica é flanqueada em sua extremidade 5' por um nucleotídeo de guanina, que se pensa ser crítico de uma saída limpa do íntron. SEQ ID NO 59: Sequência parcial de homólogo tra de Ceratitis rosa. Sequência de íntron prevista para ser spliced em um transcrito específico de fêmea tra de C. rosa (+3 a 1311 bp em sequência). Nucleotídeo exônicos de flanqueamento são apresentados nas posições 1-2 e 1312-3. Novamente, observa-se que sequência intrônica é flanqueada em sua extremidade de 5' por um nucleotídeo de guanina, que se pensa ser crítico de uma saída limpa do íntron. SEQ ID NOS. 60-70: Iniciadores como referido nas figuras 44-46 e 50-51. SEQ ID NO. 71 : fragmento 3 específico de fêmea dsx de lagarta rosada (PBW, Pectinophora gossypiella). SEQ ID NO. 72: Matriz de leitura aberta de ubiquitina de Drosophila melanogaster. SEQ ID NO. 73: Sequência de proteína de ubiquitina de Drosophila melanogaster. SEQ ID NOS. 74-105 são iniciadores como discutido acima nos exemplos. SEQ ID NO. 106 é sequência nucleotídica de LA1172, incluindo espinha dorsal de plasmídeo. SEQ ID NOs 107-138 estão descritas acima. SEQ ID NO. 139 iniciador de HSP SEQ ID NO. 140 iniciador de VP 16 SEQ ID NO.141 iniciador de Agéxon1F SEQ ID NO. 142 iniciador TETRR1 SEQ ID NO. 143 sequência de plasmídeo LA3576 SEQ ID NO. 144 sequência de plasmídeo LA3582 SEQ ID NO. 145 sequência de plasmídeo LA3596 SEQ ID NO. 146 PBW - dsx (Fig 6) SEQ ID NO. 147 bombyx - dsx (Fig 6) SEQ ID NO. 148 traça das maçãs e pêras - dsx (Fig 6) SEQ ID NO. 149 DSX Minigene 1 de construção LA3491 SEQ ID NO. 150 DSX Minigene 2 de construção LA3534 SEQ ID NO. 151 sequência completa de plasmídeo LA3619 SEQ ID NO. 152 sequência completa de plasmídeo LA3612 SEQ ID NO. 153 sequência de plasmídeo LA3491 SEQ ID NO. 154 sequência de plasmídeo LA3515 SEQ ID NO. 155 sequência de plasmídeo LA3545 SEQ ID NO. 156 sequência de plasmídeo LA3604 SEQ ID NO. 157 sequência de plasmídeo LA3646 SEQ ID NO. 158 sequência de plasmídeo LA3054 SEQ ID NO. 159 sequência de plasmídeo LA3056 SEQ ID NO. 160 sequência de plasmídeo LA3488 SEQ ID NO. 162 sequência de plasmídeo LA3570
A invenção será agora descrita por referência aos seguintes, exemplos não limitantes.
Os requerentes prepararam uma inserção de um cassete de íntron Cctra em uma matriz de leitura aberta sintética (ORP). Duas versões deste splice corretamente em mosca-do-mediterrâneo, em outras palavras o splicing do cassete de íntron Cctra fielmente recapitula o que seria normalmente feito no contexto do gene de Cctra endógeno. Isto foi para produzir 3 variantes de splice (principais ou sozinhas) em fêmeas, uma das quais é específica de fêmea (chamada F1), enquanto as outras duas de ambos, machos e fêmeas (chamadas M1 e M2). Uma vez que cada um dos transcritos não específicos de sexo contém material exônico adicional com códons de parada, os requerentes também realizaram isto de modo que apenas a variante de splice de fêmea produz proteína funcional.
Cada uma destas construções (LA3077 e LA3097) tem o íntron Cctra flanqueado por TG e GT (para dar 5'...TG\íntron\GT...3'. Uma construção antiga, que não funciona perfeitamente, é LA1188. LA1118 é completamente bem caracterizada - splicing é exatamente como acima exceto que 4 nucleotídeos adicionais são removidos. O íntron está no contexto 5'...TGGCAC|íntron|GT...3'; splicing remove 4 bases adicionais, isto é 5'...TG|GCACíntron|G7...3' (figura 33).
Em todos os casos o íntron é invariável, e é simplesmente a sequência de íntron Cctra completa. Como é normal para íntrons, ele começa com GT e termina com AG. Quase todos os íntrons começam com GT, assim, o uso de GC alternativo raro em LA1118 é surpreendente [íntrons GC-AG são uma alternativa conhecida - em um estudo em grande escala, 0,5% de todos íntrons foram notificados para uso de GC-AG (Burset et al., 2001), embora isto possa ser subestimado, particularmente de íntrons spliced alternativamente, dos quais talvez 5% poderiam utilizar GC-AG (Thanaraj e Clark, 2001)] .
Análise de RT-PCR foi efetuada em LA3077, (uma construção de retro-alimentação positiva com o íntron Cctra na matriz de leitura aberta de tTAV). Moscas adultas transformadas de ambos os sexos foram criadas em dieta substancialmente livre de tetraciclina ("sem tetraciclina") por 7 dias. Moscas foram então coletadas para extração de RNA e RT PCR usando iniciadores (HSP- SEQ ID NO. 104 e VP16 SEQ ID NO. 105) foram usados para analisar o padrão de splicing do íntron CcTRA (Figura 34). Em duas amostras de fêmea os requerentes encontraram o padrão de splice correto do Cctra (776 bp, correspondendo a remoção precisa do íntron Cctra) e não notaram tal banda em machos.
Os requerentes encontraram que LA3077 e LA3097 correspondentemente deram uma letalidade específica de fêmea repressível. LA3077 foi testado fenotipicamente através de cruzamento de moscas heterozigóticas de LA3077 para tipo selvagem, com e sem tetraciclina. Letalidade de fêmea variou de 50 a 70%. LA3097 (uma versão modificada de LA3077 por meio da qual o íntron Cctra imediatamente segue o códon de partida em tTAV ORF), demonstrou um nível muito maior de letalidade específica de fêmea, atingindo um máximo de 100% (Figura 35). O íntron Cctra foi também inserido em tTAV2 na mesma posição como LA3097, na construção LA3233, e isto deu um resultado fenotípico similar como LA3097 (Figura 35).
Os requerentes também prepararam transformantes de LA3077 em Drosophila. Fenotipicamente, a construção funciona perfeitamente, isto é, que ela é letal específica de fêmea altamente efetiva. No entanto, sequenciamento das variantes de splice de uma destas inserções demonstrou que o splicing desta construção em Drosophila não é igual como é na moscado-mediterrâneo (SEQ ID NO. 57). O transcrito crítico, aquele específico de fêmea, é o mesmo em ambos, mas em pelo menos um dos transcritos não específicos de sexo é diferente. Ele incorpora ainda sequência exônica extra, com códons de parada, mas a junção de splice não são exatamente iguais (Figura 36). Esta observação é extremamente importante na medida em que demonstra que esse método (regulação de expressão de gene por uso de íntrons spliced alternativamente) pode ser bastante utilizado em toda uma faixa filogenética.
Um teste simples para determinar se um regulador de splice exônica ainda não caracterizado (tais como melhoradores e supressores) pode estar modificando a função do íntron spliced alternativamente, poderiam incluir a realização da construção e introdução no tecido alvo, e então examinar seu padrão de splice. Em muitos casos isto não vai requerer a transformação de linhagem germinal, assim, o teste pode ser bastante rápido, por exemplo por expressão transiente em células de cultura de tecido apropriadas ou in vivo. Por exemplo, teste in vivo em insetos poderia ser realizado liberando o DNA por microinjeção. No entanto, como o versado apreciará, microinjeção junto com eletroporação, ou eletroporação, transformação química, métodos balísticos, por exemplo, foram todos utilizados em vários contextos e tais métodos de introdução de plasmídeo e expressão de proteína a partir dos mesmos são bem conhecidos na técnica.
Os requerentes também realizaram recentemente e obtiveram transgênicos com, o íntron Cctra em um gene diferente (LA3014) (todos os exemplos acima são tTAV). LA3014 contém uma fusão ubiquitina - ReaperKR a jusante de um íntron Cctra. Dados fenotípicos (Figura 35) mostram que LA3014 mosca-do-mediterrâneo transgênica resultou em letalidade específica de fêmea repressível. Análise de RT-PCR em RNA extraído de machos e fêmeas adultos criados sem tetraciclina, usando iniciadores (HSP, SEQ ID NO 74) e ReaperKR (SEQ ID NO. 75), demonstra que splicing correto estava ocorrendo em fêmeas (banda de 508bp) e nenhuma destas bandas foi encontrada em machos (Figura 37). LA3166 é outra construção com o íntron Cctra localizado dentro da região de codificação de ubiquitina fusionada ao ReaperKR, mas localizada em uma posição diferente em ubiquitina. LA3166 também produz um efeito letal específico de fêmea repressível dominante na mosca-do-mediterrâneo (Figura 35).
Os requerentes também realizaram recentemente e obtiveram transgênicos com construções baseadas em Cctra com "apenas íntron" com íntron em um gene diferente (todos os exemplos acima estão em tTAV ou uma de suas variantes, isto é tTAV2 ou tTAV3). Estas construções funcionam como previsto. Este é um resultado importante, deste modo mostrando que não ocorrem sequências exônicas essenciais em Cctra que os requerentes simplesmente duplicaram (em função, se não necessariamente em sequência) por acaso, em tTAV. Também os requerentes realizaram construções ubi- rprKR deste tipo (LA3014 e LA3166), o que também valida o método de fusão de ubiquitina descrito acima.
A fim de demonstrar a faixa filogenética do íntron Cctra, os requerentes geraram LA3097 e LA3233 de Anastrepha ludens transgênico. LA3097 e LA3233 foram selecionados para injeção em Anastrepha ludens como demonstraram a melhor letalidade específica de fêmea em Ceratitis capitata (ver exemplo 13). Dados fenotípicos foram gerados de 4 linhagens de LA3097 independentes e 1 linhagem de LA3233 (ver figura 38). Letalidade específica de fêmea foi geralmente pouco menor em Anastrepha ludens quando comparada a C. capitata mas atingiu 100% em uma linhagem.
Anastrepha ludens transformada com LA3097 e criada com tetraciclina até eclosão foram isolados e mantidos sem tetraciclina durante 7 51 dias. RNA foi então extraído e análise de RT-PCR foi realizada usando iniciadores HSP (SEQ ID NO. 76) e TETRRl (SEQ ID NO. 77). O padrão correto de splice específico de fêmea (como F1) foi observado a partir de RNA isolado em fêmeas (348bp) mas não de machos demonstrando a função do íntron Cctra em uma espécie diferente (figura 39)
A banda do macho mais brilhante e banda específica de fêmea foram purificadas e precipitadas para sequenciamento. O transcrito específico de fêmea foi verificado como sendo spliced corretamente nas fêmeas de mosca mexicana das frutas como esperado para LA3097: LA3097: AGCCACCATG|GT...íntron...AG | GTCAGCCGCC
As duas sequências de flanqueamento acima são SEQ ID NOS. 2 e 3, respectivamente.
Os requerentes isolaram o íntron tra de Bactocera zonata (B. zonata) (SEQ ID NO. 58) usando iniciadores ROSA1 (SEQ ID NO. 78), ROSA2 (SEQ ID NO. 79), e ROSA3 (SEQ ID NO. 80).
Estas sequências de iniciadores foram designadas com base em sequência de codificação conservada de Ceratitis capitata e homólogos tra de Bactrocera oleae. Usando ROSA2 e ROSA3 ou ROSAl e ROSA3 como iniciadores, o íntron tra e sua região de codificação de flanqueamento foram amplificados de DNA genômico de Bactrocera zonata. Então os requerentes usaram estes produtos de PCR como um modelo e amplificaram o fragmento de íntron tra para fazer a construção LA3376 (figura 31 e SEQ ID NO. 55). Os iniciadores (BZNHE- SEQ ID NO. 81 e BZR-SEQ ID NO. 82) foram usados para fazer as construções; estes iniciadores contêm sequências adicionais para propósitos de clonagem. O íntron Bztra em LA3376 é clonado em ORF de tTAV3 e também de ReaperKR. Transformantes de mosca-do- mediterrâneo foram gerados e RNA extraído das moscas macho e fêmea. RT-PCR foi então realizado em ambos splice ReaperKR (HB- SEQ ID NO. 83) e ReaperKR SEQ ID NO. 84) e tTAV3 (SRY- SEQ ID NO. 85) e AV3F- SEQ ID NO. 86). Os fragmentos esperados de 200bp para ReaperKR e 670 bp para tTAV3, correspondendo a splicing em um padrão equivalente ao transcrito de F1 de Cctra (Pane et al, 2002), foram gerados em fêmeas (figura 40).
Iniciadores ROSA2 (SEQ ID NO. 87) e ROSA3 (SEQ ID NO. 88) foram projetados baseados na sequência de codificação conservada de Ceratitis capitata e Bactrocera oleae. Usando ROSA2 e ROSA3 como iniciadores, o íntron tra e sua região de codificação de flanqueamento foram amplificados de DNA genômico de Ceratitis rosa (SEQ ID NO. 59). Então os requerentes usaram os produtos de PCR como um modelo e amplificaram o fragmento de íntron tra para fazer as construções. Os iniciadores (CRNHE- SEQ ID NO 89 e CRR SEQ ID NO 90) foram usados durante a construção de LA3242 (SEQ ID NO. 56 e figura 32. LA3242 contém íntron de C. rosa na extremidade 5' de ORF de ReaperKR. Embriões de Ceratitis capitata foram injetados com DNA de LA3242, embriões injetados foram criados até idade adulta em uma dieta substancialmente livre de tetraciclina. RNA foi extraído de machos e fêmeas adultos; isto foi usado como um modelo de RT PCR usando iniciadores HB (SEQ ID NO. 91) e ReaperKR (SEQ ID NO. 92). A banda de splice específico de fêmea esperada (200bp), correspondendo a splicing no padrão equivalente ao do transcrito F1de Cctra, foi observada em fêmeas e não em machos (figura 41). Doublesex
A sequência de um homólogo de Bombyx mori (bicho-da-seda) de Dsx de Drosophila (Bmdsx) foi previamente descrita e um produto de splice específico de macho e de fêmea foi identificado (Suzuki et al, 2001).
Ambos machos e fêmeas usaram o mesmo 3' polyA, e há dois éxons específicos de fêmea. Um trabalho sugeriu que o splicing específico de sexo não é dependente em tra/tra2, em outras palavras mesmo se o padrão parece o mesmo, o mecanismo subjacente pode ser diferente (Suzuki et al., 2001), embora seus dados, principalmente a falta de sítios de ligação tra-tra2 reconhecíveis, no entanto, não sejam atraentes. Além disso, uma construção de minigene dsx de B. mori (contendo sequência exônica e sequência intrônica truncada) foi transformada no B. mori e os transformantes de linhagem germinal mostram splicing específico de sexo (Funaguma et al., 2005).
Os requerentes geraram um minigene de Bmdsx com base na sequência usada no trabalho de Funaguma et al, com algumas mudanças significantes, e o injetaram na lagarta rosada para averiguar se se poderia obter splicing específico de sexo em uma espécie divergente. A construção de minigene, gerada pelos requerentes, não incluía éxon 1, que está presente em ambos, machos e fêmeas. Além disso, os requerentes removeram o íntron entre éxon 3 e 4 (os dois éxons específicos de fêmea), incluíram uma sequência heteróloga (contendo sítios de clonagem múltiplos, MCS), usaram a sequência de melhorador/promotor de Hr5-IE1 do baculovírus AcNPV e usaram uma sequência de terminação transcripcional de 3' derivada de SV40 (ver figura 42 para um esquema). Os fragmentos de éxon / íntron de flanqueamento individuais usados foram amplificados e recombinados juntos por PCR e ligados em uma construção transportando um fragmento de promotor melhorador Hr5/ IE1 e SV40 3' UTR (figura 22 e SEQ ID NO. 22). LA3435 foi injetado nos embriões da lagarta rosada (Pectinophora gossypiella). As larvas do primeiro instar foram coletadas após 5-7 dias e analisadas individualmente por RT-PCR (usando iniciadores IEl transcr- SEQ ID NO. 93 e SV40-RT-P2- SEQ ID NO. 94) para determinar se BMdsx pode sofrer splicing específico de macho e fêmea (figura 43). A análise dos requerentes detectou a banda específica de macho (prevista para ser 442bp) em 4 amostras (Trilhas 1, 2, 3 e 4) e a banda específica de fêmea (prevista para ser 612bp) em 1 amostra (Trilha 5).
O splicing correto de dsx B. mori em PBW demonstra que os requerentes podem realizar (de fato realizaram) a expressão específica de sexo de uma sequência heteróloga (aqui, MCS) em um lepidóptero utilizando um sistema de splicing alternativo. Além disso, uma vez que este sistema de splicing foi derivado de uma espécie heteróloga, isto sugere que tais construções poderiam funcionar sobre uma extensa faixa filogenética. No entanto, a identificação de sistemas de splicing alternativo nas espécies de interesse é também prevista, e métodos para identificar tais sistemas de splicing alternativo são providos aqui ou serão conhecidos do versado na técnica. Ao prover um MCS no exemplo dos requerentes (ver figura 42), a expressão de uma sequência de interesse, por exemplo uma região de codificação de uma proteína de interesse poderia prontamente ser conseguida inserindo-se a referida sequência. Se a referida sequência codificou uma proteína apropriada, um fenótipo específico de sexo, por exemplo letalidade específica de sexo condicional, poderia assim ser introduzido, por exemplo em uma lagarta rosada.
O gene dsx da traça das maçãs e pêras (Cydia pomonella) foi isolado efetuando 3' RACE usando iniciadores que foram baseados em alinhamentos de sequência de B. oleae, B. tyroni, C. capitata, D. melanogaster, B. mori, e A. gambiae. RNA foi isolado de uma traça das maçãs e pêras, macho e fêmea, e 3' RACE, para gerar cDNA, foi realizado usando o iniciador de TT7T25 (SEQ ID NO. 95). PCR foi realizado usando os iniciadores ds1c (SEQ ID NO. 96) e TT7 (SEQ ID NO. 97). Dois ciclos de nested PCR foram então realizados no produto do primeiro PCR usando os iniciadores codling2a (SEQ ID NO. 98) e TT7 (SEQ ID NO. 99) e o produto do segundo ciclo de PCR usando Codling2b (SEQ ID NO. 100) e TT7. As sequências específicas de macho e fêmea isoladas compartilham a similaridade de sequência a homólogos dsx previamente isolados (Macho-SEQ ID NO. 43 e Fêmea- SEQ ID NO. 42).
O gene dsx da lagarta rosada foi isolado realizando 3' RACE usando iniciadores que foram baseados em alinhamentos de sequência de B. oleae, B. tyroni, C. capitata, D. melanogaster, B. mori, e A. gambiae. RNA foi isolado de uma traça das maçãs e pêras, macho e fêmea, e 3' RACE, para gerar cDNA, foi realizado usando TT7T25 (sequência definida aqui). PCR foi realizado usando os iniciadores Pbwdsx2 (SEQ ID NO. 101) e TT7 (SEQ ID NO. 102). Nested PCR foi então realizado no produto do primeiro PCR usando os iniciadores Pbwdsx3 (SEQ ID NO. 103) e TT7. Três sequências específicas de fêmea foram isoladas: PBWdsx-F1 (SEQ ID NO. 40), PBWdsx-F2 (figura 10), e PBWdsx-F3 (SEQ ID NO. 71) e uma sequência específica de macho (SEQ ID NO. 42). As sequências específicas de macho e fêmea isoladas compartilham similaridade de sequência a homólogos dsx isolados previamente.
A sequência do gene dsx de Anopheles gambiae foi previamente descrita (Scali et al 2005). No entanto, quando os requerentes tentaram repetir o trabalho descrito, eles verificaram que existiam algumas diferenças no splicing que ocorre. Quando os requerentes tentaram repetir a amplificação do transcrito específico de fêmea usando iniciadores projetados da sequência de mRNA (Acesso; AY903308 de sequência de codificação de fêmea e AY903307 de sequência de codificação de macho), a amplificação falhou. No entanto, quando Scali e colaboradores mostraram que havia um éxon compartilhado, o que não tinha sido previamente descrito, os requerentes projetaram iniciadores para amplificar o transcrito e gene dsx completo. Usando estes iniciadores e iniciadores projetados a partir da sequência de DNA genômico (Acesso; GI: 19611767) os requerentes verificaram que o splicing do transcrito de fêmea é diferente daquele descrito por Scali et al 2005 (figura 44). O transcrito mostrou que o éxon de fêmea estava em uma posição diferente. Há várias explicações para estas diferenças, mas as mais prováveis são ou algum tipo de diferença de cepa nos Anopheles, que os requerentes usaram para obter dados, ou a sequência publicada não é de Anopheles gambiae, ou se tem mais de uma isoforma de fêmea, como mostrado para Stegomyia aegypti no Exemplo 20.
Os requerentes também usaram com sucesso iniciadores, projetados em torno de sua versão do scipling de dsx de Anopheles gambiae, que são capazes de distinguir entre machos e fêmeas de Anopheles gambiae (figura 45). Isto fornece uma boa evidência de que o sistema será funcional como um mecanismo de splicing específico de sexo quando fusionado a uma proteína de interesse, como tTAV ou uma matadora.
O gene dsx de Anopheles gambiae que os requerentes isolaram do DNA genômico, que tem várias mudanças na sequência nucleotídica comparada com a sequência genômica relatada, foi clonado em LA3359 (SEQ ID NO. 47) e LA3433 (SEQ ID NO. 48), cujos esquemas podem ser encontrados nas figuras 23 e figura 24, respectivamente.
O splicing do gene parece ser similar a dsx de Anopheles gambiae (Scali et al 2005). O gene dsx de Stegomyia aegypti está ilustrado diagramaticamente na figura 47 ou 48. O transcrito específico de macho (M1) é produzido que não inclui éxons 5a ou 5b. Duas variantes de splice específicas de fêmea (F1 e F2) têm a seguinte estrutura; F1 compreende éxons 1-4, 5a, 6 e 7 mas não 5b, F2 compreende éxons 1-4 e 5b (figura 46). Além disso, mais um transcrito (C1) está presente em ambos, machos e fêmeas; isto compreende éxons 1-4 e 7, mas não éxons 5 a, 5b ou 6.
O splicing do gene parece ser similar a dsx de Anopheles gambiae (Scali et al 2005). O gene dsx de Stegomyia aegypti é ilustrado diagramaticamente na figura 47 ou 48. Actin 4
Uma forma de obter expressão específica de sexo, de tecido e de estágio de um gene de interesse é ligá-lo ao gene Actin-4 de Stegomyia aegypti (AeAct-4). Esse gene é apenas expressado no desenvolvimento de músculos aptos a voar de Stegomyia aegypti fêmea (Munoz et al 2004). Eles foram usados em hibridização in-situ para um RNA detectar o perfil de expressão de AeAct-4. Tomou-se um fragmento do gene Actin-4 de Stegomyia aegypti, compreendendo uma região de promotor putativa, um íntron spliced alternativamente, e uma seção de região não traduzida 5' (UTR) e colocou-se na frente da sequência codificando para tTAV (figura 49) para testar a função do splicing específico de sexo quando fusionada a tTAV.
Os requerentes integraram LA1172 no genoma de Stegomyia aegypti usando piggyBac. Duas linhagens independentes foram geradas (linhagens 2 e 8). Ambas as linhagens mostraram o splicing correto do gene Actin-4-tTAV (figuras 50 e 51). O promotor de Actin-4 e íntron spliced alternativamente podem, por esta razão, ser usados com sucesso para prover o splicing específico de sexo, de tecido e de estágio de um gene de interesse em Stegomyia aegypti.
Figura 19: Um uso do elemento P na geração de expressão específica de linhagem germinal de um gene de interesse (Gene E). Inserção do elemento P IVS3 e sequências de flanqueamento exônicas a montante de uma fusão de ubiquitina - gene E que permite a expressão específica de linhagem germinal de gene E sob um promotor ativo de linhagem germinal. A - Promotor ativo de linhagem germinal; B - Matriz de leitura aberta de elemento P; C - P íntron 'IVS3'; D - Ubiquitina; E - Região de codificação de proteína de interesse por exemplo tTAV.
Figura 20: Expressão específica de sexo usando dsx. A: Íntron usado como íntron Cctra acima, mas dando expressão específica de macho. Um fragmento de dsx (aqui a versão de Anopheles) é inserido em uma região de codificação heteróloga (caixas sombreadas). O íntron está completamente removido em machos, mas em fêmeas a região de codificação é prematuramente terminada. B: Uma abordagem alternativa a expressão específica de macho, no qual uma região de codificação heteróloga é fusionada a um fragmento de dsx. C: Expressão específica de fêmea: a região de codificação heteróloga está inserida no éxon específico de fêmea, ou como uma fusão na matriz para um fragmento de Dsx, ou com seus próprios códons de partida e parada. D: Expressão diferencial: projetos B e C podem ser combinados para resultar na expressão de gene a em fêmeas e b em machos.
Figura 21: Splicing alternativo específico de sexo de Cctra A: Cctra é spliced em fêmeas para produzir três transcritos: F1, que codifica proteína Tra, e M1 e M2, que não codificam, porque eles incluem éxons adicionais com códons de parada (re-escrito de Pane et al. 2002). Machos produzem apenas transcritos M1 e M2 e assim não produzem proteína Tra funcional de todo. B: Se esse íntron for para funcionar similarmente em uma região de codificação heteróloga, isto similarmente permitiria às fêmeas, mas não aos machos, produzir proteína funcional X. Figura 22: Representação diagramática de construção pLA3435/ plasmídeo (SEQ ID NO.46).
Figura 23: Mapa de plasmídeo de pLA3359 do gene dsx de Anopheles gambiae colocado sob o controle de um promotor Hr5-IE1 para avaliar splicing via expressão transiente .
Figura 24: pLA3433 - gene dsx de Anopheles gambiae colocado sob o controle de promotor Hr5-IE1, com adição de éxon 2, para avaliar splicing através de expressão transiente .
Figura 25: Representação esquemática de construção pLA1188. Figura 26: Representação esquemática de construção pLA3077. Figura 27: Representação esquemática de construção pLA3097. Figura 28: Representação esquemática de construção pLA3233. Figura 29: Representação esquemática de construção pLA3014. Figura 30: Representação esquemática de construção pLA3166. Figura 31: Representação esquemática de construção pLA3376. Figura 32: Representação esquemática de construção pLA3242.
Figura 33: Sequência de flanqueamento de Cctra Splicing do íntron Cctra em LA3077 e LA3097 é exatamente como seria visto no íntron Cctra nativo. Splicing em LA1118 resulta na remoção de 4 nucleotídeos adicionais. Em todos os casos os íntrons são flanqueados por éxon TG exônico 5' e 3' GT.
Figura 34: Gel mostrando splicing específico de sexo correto de íntron(s) derivado (s) de CcTra (banda de 776 bp em fêmeas) em Ceratitis capitata transformada com LA3077. Trilha 1: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,8, 1,0 e 1,5kb são indicadas); Trilhas 2 e 3: Ceratitis capitata LA3077 /+ machos; Trilhas 4 e 5: Ceratitis capitata LA3077 /+ fêmeas.
Figura 35: Dados fenotípicos de construções específicas de fêmea transformadas em Ceratitis capitata. Coluna 1: Designação de construção LA#, por exemplo LA3077, LA3097, LA3233, etc, é indicada pelo número, com linhas de inserção independentes referidas por letra; Colunas 2 e 3: Resultados sem tetraciclina (NT) resulta de cada linhagem transformada obtida nos machos totais (2) e fêmeas totais (3). Colunas 4 e 5: Tetraciclina (TET) resulta de cada linhagem transformada dada em machos totais (4) e fêmeas totais (5).
Figura 36: transcritos de construções de íntron Cctra em Drosophila e Ceratitis capitata. A linha de topo representa o DNA de construção contendo íntron tra flanqueado por gene desejado (a caixa aberta). A caixa vermelha representa os éxons específicos de macho. Íntrons são representados por linhas sólidas. A seta acima da primeira linha representa as posições dos oligonucleotídeos usados nos experimentos de RT-PCR. A barra indica a escala da figura.
Figura 37: Gel mostrando splicing específico de fêmea correto de sequência derivada de CcTRA (banda de 508bp) em Ceratitis capitata de fêmea transformada com LA3014. Trilha 1: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,4 e 1,0kb são indicadas); Trilha 2: Ceratitis capitata LA3014 /+ macho; Trilha 4: Ceratitis capitata LA3014 /+ fêmea; Trilhas 3 e 5: sem controles negativos de transcriptase reversa (banda de fundo, provavelmente de DNA genômico, pode ser vista nas trilhas 2 e 4).
Figura 38: Dados fenotípicos de Anastrepha ludens transgênico transformado com LA3097 ou LA3233. Coluna 1: Construção La# (LA3097 ou LA3233) indicou, com linhas de inserção independentes referidas por letra; Colunas 2 e 3: não tetraciclina (NT) resulta de cada linhagem transformada obtida em machos totais (2) e fêmeas totais (3). Colunas 4 e 5: Tetraciclina (TET) resulta para cada linhagem transformada dada em machos totais (4) e fêmeas totais (5).
Figura 39: Gel mostrando splicing específico de sexo correto de CcTRA (banda de 348bp em fêmeas) em Anastrepha ludens transformada com LA3097. Trilha 1 : Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,4 e 1,0kb são indicadas); Trilhas 2, 3 e 4: A. ludens LA3097 /+ machos; Trilhas 5, 6 e 7: A. ludens LA3097 /+ fêmeas.
Figura 40: Gel mostrando splicing específico de sexo correto de BzTRA em ReaperKR (banda de 200 bp em fêmeas) e tTAV3 (banda de 670 bp em fêmeas) regiões de LA3376, em Ceratitis capitata transformada com LA3376. Trilha 1: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,2, 0,6 e 1,0kb são indicadas); Trilhas 2 e 3: C. capitata LA3376 /+ machos testadas para splicing em ReaperKR; Trilhas 4 e 5: C. capitata LA3376 /+ fêmeas testadas para splicing em ReaperKR; Trilha 6: SmartLadder™; Trilhas 7 e 8: C. capitata LA3376 /+ machos testada para splicing em tTAV; Trilhas 9 e 10: C. capitata LA3376 /+ fêmeas testadas para splicing e, tTAV; Trilha 11: SmartLadder™.
Figura 41: Gel mostrando splicing de CrTRA específico de sexo correto em CrTRA - ReaperKR (banda de 200 bp em fêmeas) em Ceratitis capitata injetada com LA3242. Trilha 1: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,2, 0,6 e 1,0kb são indicadas); Trilhas 2-7: C. capitata machos de tipo selvagem injetados com LA3242; Trilha 8: SmartLadder™; Trilhas 9-14: C. capitata fêmeas de tipo selvagem injetadas com LA3242; Trilha 15: SmartLadder™.
Figura 42: Representação esquemática de construção de minigene Bmdsx. Duas construções de minigenes derivadas do gene dsx de Bombyx mori são ilustradas diagramaticamente, junto com o splicing alternativo previsto destas construções (padrão de fêmea mostrado acima da construção, padrão de macho abaixo). (A) é a construção de minigene dsx de Bombyx mori usada em Funaguma et al., 2005) (B) é pLA3435. A e B diferem entre si de várias formas: (i) Éxon 1 é excluído de pLA3435, (ii) o íntron entre éxons específicos de fêmea 3 e 4 foi removido e uma sequência heteróloga pequena foi inserida em pLA3435 (iii) Funaguma et al., usam o promotor iel do baculovírus BmNPV e um BmA 33' UTR comparado com pLA3435 que usa melhorador/promoter hr5-IE1 do baculovírus AcNPV de e um 3' SV40 3' UTR. (iv) pLA3435 usa as sequências de íntron ligeiramente mais longas quando comparadas com (A) (ver figura 15 para sequência). Duas construções de minigenes derivadas do gene dsx de Bombyx mori são ilustradas diagramaticamente, junto com o splicing alternativo previsto destas construções (padrão de fêmea mostrado acima da construção, padrão de macho abaixo).
Figura 43: Splicing específico de sexo de construção de minigene BMdsx em PBW. Análise de expressão transiente de pLA3435 usando RT-PCR mostra a presença de um fragmento de 442 bp (Trilhas 1,2,3 e 4) em machos e um fragmento de 612 bp em fêmeas (Trilha 5), mostrando que o minigene BMdsx com um fragmento heterólogo inserido entre éxon 3 e 4 é capaz de splice corretamente na traça divergente, PBW. Marcadores são SmartLadder™ de Eurogentec; bandas de aproximadamente 0,2, 0,4 e 0,6 kb são indicadas
Figura 44: Splicing específico de sexo de dsx Anopheles gambiae. Anófelos (A) mostram o splicing que foi relatado por Scali et al 2005. No entanto, quando RT- PCR foi realizado usando os iniciadores dos requerentes (spl-agdsx-e3 (SEQ ID NO. 60) e spl-agdsx-m (SEQ ID NO. 61)) um padrão de splicing diferente para fêmeas foi revelado, representado por Anófelos (B).
Figura 45: Identificação de Anopheles gambiae macho e fêmea usando iniciadores dsx. RNA foi extraído da Anopheles gambiae macho e fêmea e os transcritos de dsx foram amplificados por RT-PCR usando os iniciadores spl- agdsx-e3 (SEQ ID NO. 62) e spl-agdsx-m (SEQ ID NO. 63); o padrão de banda resultante é mostrado no gel acima. As bandas esperadas para os transcritos de macho e fêmea. são indicadas por setas brancas, as bandas foram clonadas e sequenciadas e são idênticas à sequência prevista da versão dos requerentes de transcrito de dsx (ver SEQ ID NO. 47 (LA3359) e SEQ ID NO. 48 (LA3433)). Os marcadores de peso molecular são mostrados em kb (SmartLadder™ de Eurogentec; tamanhos são aproximados). Figura 46; Identificação de Stegomyia aegypti macho e fêmea usando iniciadores dsx.
Os iniciadores para o RT-PCR de Stegomyia aegypti de A e B foram AedesxFl (SEQ ID NO. 64) e AedesxR5 (SEQ ID NO. 65) e foram testados em pupas, um estágio de vida de Stegomyia aegypti que pode ser sexuado convenientemente e corretamente; a amplificação de RT-PCR resultante é mostrada na imagem em gel (A). As pupas, macho e fêmea, mostram uma banda específica de sexo distintiva. Então os iniciadores foram testados em extrações de RNA de larvas, que não podem ser prontamente sexuadas por sua morfologia e a amplificação de RT-PCR resultante mostrada em imagem em gel (B). As larvas mostram um padrão de banda claro que distingue machos de fêmeas sem ambiguidade. Imagem em gel (C) mostra uma banda de aproximadamente 600 bp de RT-PCR usando os iniciadores
Aedes sxF1 e Aedes xR2 (SEQ ID NO. 66) de pupas de indivíduos machos e fêmeas. O sequenciamento desta banda mostrou uma variante de splice específica de fêmea a qual parece não possuir o éxon compartilhado de macho para o qual Aedes xR5 é previsto se recombinar (éxon 7, ver figura 56). Os marcadores de peso molecular são mostrados em kb (SmartLadder™ de Eurogentec; tamanhos são aproximados). Figura 47: Representação diagramática de parte do gene dsx de Stegomyia aegypti (fora de escala).
Um fragmento do gene dsx de Stegomyia aegypti é representado acima. Éxons 5a e 5b são específicos de fêmea e éxon 6 é um éxon específico de macho. Duas variantes de splice específicas de fêmea foram encontradas (Fl e F2) as quais compreendem éxons l-4,5b,6 e 7 (F1) ou l-4,5a (F2); transcritos em machos (M1) compreendem éxons 1-4,6 e 7 mas não éxon 5 a ou 5b e um transcrito (C1) de 1-4 e 7 mas não éxons 5 a, 5b ou 6 é mostrado em machos e fêmeas. O número para cada um dos éxons após # refere-se a contig 1.370 (http://www.broad.mit.edu/annotation/disease vetor/Aedes aegypti/), que se lêem orientação oposta, e após * refere-se à sequência nucleotídica mostrada em SEQ ID NO. 43.
Figura 48: Representação diagramática do gene dsx de Stegomyia aegypti. O gene dsx completo de Stegomyia aegypti é representado acima Éxon 5 é o éxon específico de fêmea e éxon 6 é um éxon putativo específico de macho. Em princípio, transcritos em fêmeas compreendem éxons 1,2,3,4,5 e 7, e machos compreendem éxons 1,2,3,4,6 e 7. O número de cada um dos éxons após # refere-se ao contig 1.370 (http://www.broad.mit.edu/annotation/disease vector/Aedes aegypti/) que se lê na orientação oposto, e após * refere-se à figura 12. Figura 49: Mapa de Plasmídeo de pLA 1172.
A região de codificação para tTAV foi colocada sob o controle de um fragmento do gene Actin-4 de Stegomyia aegypti (Munoz et al 2005) que inclui o 5' UTR, primeiro íntron, e sequências a montante (promotor putativo). A construção também contém sequência tetO Nipper. A construção tem extremidades de tipo piggyBac e um marcador de DsRed2 para integração estável em um genoma.
Figura 50: Splicing específico de sexo de tTAV em transformantes LA1172. Imagem em gel de RT-PCR de RNA extraído de pupas machos e fêmeas de LA 1172 linhagem 2 . Os iniciadores usados foram Agexonl (SEQ ID NO. 67) e Tra (tTAV) seq+ (SEQ ID NO. 68). Sequenciamento das bandas de RT-PCR mostrou o splicing esperado ocorrendo em machos e fêmeas. Os dados mostrados no diagrama acima são de LA1172 linhagem 2, a linhagem 8 mostrou exatamente os mesmos resultados (dados não mostrados). Marcadores são SmartLadder™ de Eurogentec; tamanhos aproximados são indicados, em kb).
Figura 51: RT-PCR de amostras de tipo selvagem, mostrando variantes de splice específicas de sexo do gene Actin-4 de Stegomyia aegypti. Imagem em gel de RT-PCR de RNA extraída de diferentes estágios de desenvolvimento, e dissecações de adultos, de LA1172 linhagem 8 . Os iniciadores usados foram Agexon1 (SEQ ID NO. 69) e Éxon 3 (SEQ ID NO. 70). A imagem em gel mostra que a expressão forte do gene Actin-4 apenas ocorre no estágio de pupa, e que a expressão de adulto é geralmente limitada para o tórax de fêmea onde os músculos de vôo são encontrados. Tabela 17, abaixo mostra os conteúdos de cada trilha. Tabela 1. E = conjunto de ~ 100 embriões MH = cabeça de macho adulto L4 = larva no quarto instar MT = tórax de macho adulto ME = pupa de macho precoce (<4 MA = abdome de adulto macho horas de vida) FE = pupa de fêmea precoce (<4 ) FH = cabeça de fêmea adulta MP = pupa de macho FT = tórax de fêmea adulta FP = pupas de fêmea FA = abdome de fêmea adulta - vê = controle de água OUTROS EXEMPLOS
Os requerentes realizaram recentemente construções baseadas em seus dados de expressão transiente usando uma construção de minigene recombinante derivada de Bombyx mori. Isto ainda é discutido abaixo na seção intitulada " alinhamento de sequência dsx de traça e motivos conservados"
Os requerentes realizaram recentemente duas construções baseadas em Bztra, expressadas na mosca mexicana das frutas (LA3376). LA3376 concede letalidade específica de fêmea repressível. Os requerentes previamente mostraram que LA3376 funciona e splice corretamente em mosca-do-mediterrâneo. Transformantes em mosca mexicana das frutas (Anastrepha ludens) também foram gerados com LA3376. Estes foram analisados para splicing correto do íntron Bztra a fim de demonstrar a faixa filogenética do íntron Bztra por RT-PCR usando iniciadores SRY e AV3F (figura 15 e "géis de RT-PCR de mosca-do-mediterrâneo " seção acima). Isto mostra splicing correto do íntron Bztra em mosca mexicana das frutas.
Os requerentes também obtiveram recentemente dados em uma construção de Dmdsx em mosca-do-mediterrâneo. A construção usou um fragmento do gene doublesex em Drosophila melanogaster para dar expressão específica de sexo de um fragmento de gene Nipp1Dm de Drosophila melanogaster (os requerentes chamam este fragmento "nipper"). Os requerentes não notaram splicing específico de sexo claro. No entanto, os dados fenotípicos mostram alguma especificidade de sexo; os requerentes notaram a letalidade aumentada de fêmeas, a cerca de 75% de penetração. Como evidente, esta penetrância incompleta poderia ser devido a nível de expressão, falta de toxicidade de nipper em mosca-do-mediterrâneo, etc. Os requerentes também notaram uma significante redução no número de machos, mas a fonte de tTA, LA670, usada neste experimento poderia ela própria matar alguns dos machos.
Os requerentes testaram três linhagens transgênicas de moscado-mediterrâneo independentes que transportam uma fusão de nipper para sequência DmDsx que se destinava a ser expressada especificamente em fêmeas. Esta construção pode não ter funcionado perfeitamente possivelmente devido à sequência essencial de splicing alternativo correto e/ou os sítios de ligação Sxl requeridos por DmDsx, e uma vez que a mosca-do-mediterrâneo não usa Sxl na via de determinação de sexo, DmDsx pode estar incapaz de splice completamente esta fusão na forma correta em mosca-do-mediterrâneo. No entanto, os requerentes alcançaram sucesso em causar de modo reprodutível uma letalidade aumentada em fêmeas comparada aos machos através de três linhagens em uma eficiência muito similar (aproximadamente 75% mais letalidade observada em fêmeas do que em machos). Isto demonstra que o sistema dsx pode funcionar através de espécies de parentesco bastante distante (separação evolucionária é em torno de 120-150 milhões de anos), e se a sequência Ccdsx foi usada, pode ter bem funcionado devido à exigência de Sxl de Dmdsx .
Os resultados de 797 são mostrados abaixo, usando um sistema nipper de splice Tet014 dsx (Pub EGFP). Eles mostram que este sistema é letal em um estágio larval ( ~50%), e é provável ser atuante com maior sucesso em fêmeas (~75%). 797 é marcado com verde (G), 670 com vermelho (R). 670 é uma fonte de tTAV, assim, espera-se ver um fenótipo nas moscas R+G; G (e R) são apenas controles. NF não fluorescente (isto é tipo selvagem) é também um controle onde incluído. Toda a progênie criada em meio livre de tet. Todas as três linhagens independentes vistas como atuando de maneira similar.
Média de todas as 3 linhagens: número de fêmeas R+G = 21% do número de machos R+G, assim, a mortalidade em excesso substancial em fêmeas R+G com relação a machos. Esse efeito não é visto em fêmeas de 10 controle R apenas ou G apenas, nem em tipo selvagem.
Os requerentes demonstraram recentemente: (5) splicing específico de sexo em construções de minigene baseadas em Aadsx recombinante ; 15 (6) fenótipo específico de sexo de uma construção baseada em Cctra; e (7) splicing específico de sexo em construções baseadas em Aedes - Actin4.
Pelo menos alguns de cada um destes exemplos não apenas mostram minigenes, mas realmente mostram splicing para gerar tTAV/tTAV2 ou ubi tTAV2
Ver também seção intitulada Sítios de ligação dsx Tra2 de Aedes. Os requerentes isolaram o gene dsx de Aedes aegypti (Aadsx) e identificaram 6 transcritos desta região (figura 1). Estes são: 2 transcritos específicos de machos (M1 e M2), 3 transcritos específicos de fêmeas (F1, F2 e F3) e um transcrito encontrado em ambos, machos e fêmeas (MF). Os requerentes realizaram duas construções de minigenes. Nestas construções, a grande maioria da sequência intrônica foi deletada. Por exemplo, minigene 1 de DSX é aproximadamente 4,4kb em comprimento, considerando que suas sequências terminais são separadas por aproximadamente 26kb em seu contexto natural, isto é, no DNA genômico de Aedes aegypti.
O splicing em minigene 2 da figura 1 é ilustrativo como splicing ocorre na forma de "fêmea" em ambos, machos e fêmeas. Isto pode significar que esse sistema depende de uso de aceitador de splicing alternativo. Nesse modelo, ocorre competição entre aceitadores de splicing alternativo, com algum fator específico de sexo influenciando isso, o fator específico de sexo provavelmente sendo Tra. Mas a deleção dos aceitadores de splice 3' de M1 e M2 força o splicing nas formas F, por remoção da alternativa.
Assim, prefere-se que um ou mais dos aceitadores de splice 3' específicos de fêmea (Fl e/ou F2) sejam providos junto com um aceitador de splice 3' adicional. O mais preferível, referido aceitador de splice adicional é o aceitador de splice 3' de variante de splice de M1 ou M2 (ou ambos), embora seja previsto que isto não é essencial pois outros aceitadores de splice 3' conhecidos irão provavelmente funcionar.
Figura 1 ilustra os vários transcritos produzidos por splicing alternativo do gene doublesex de Aedes aegypti (Aadsx). Será notado que
Aedes aegypti é também conhecido como Stegomyia aegypti. A figura mostra o gene Aadsx do quarto éxon, que não é spliced alternativamente, isto é, está presente em todos os transcritos discutidos aqui. Numeração é do primeiro nucleotídeo do quarto éxon (acgacgaact...). Note-se que o diagrama está fora de escala — os íntrons são muito mais longos que os éxons. A região total spliced alternativamente compreende acima de 43kb.
Este fragmento de minigene foi incluído em uma construção de expressão (LA3515). Aedes aegypti transgênicos foram gerados por recombinação específica de sítio no sítio de attP, usando o método de Nimmo et al (2006 : Nimmo, D.D., Alphey, L. Meredith, J.M. e Eggleston, P (2006). High efficiency site-specific genetic engineering of the mosquito genoma. Insecto Molecular Biology, 15: 129-136)
Um segundo minigene, menor, foi construído similarmente (minigene 2 de DSX) e uma construção de expressão para este foi inserida no mesmo sítio de atfP como minigene 1 de DSX, para permitir comparação direta (LA3534). Minigene 2 de DSX não mostrou splicing específico de sexo. Isto indica que as sequências presentes em minigene 1 de DSX mas não em minigene 2 de DSX (aproximadamente 2029bp, ver Fig 1 e SEQ ID NO. 150, onde éxons são encontrados nas posições 29-163 e 1535-2572) são essenciais para o splicing alternativo correto, mesmo se o primeiro íntron spliced alternativamente, e a sequência exônica imediatamente flanqueando o mesmo, estiverem presentes em ambas construções.
Os requerentes produziram duas linhagens transgênicas (LA3491 e LA3534) usando construções de minigenes de gene dsx de Aedes aegypti. LA3491 é uma fusão de éxon 4 compartilhado, éxons de cassete específicos de fêmea, e parte do primeiro éxon 3' compartilhado (éxon 5 em M1 transcrito).
Transcritos da região de minigene LA3491 foram analisados por PCR de transcriptase reversa (RT-PCR) e sequenciamento. Transcritos correspondendo ao splicing alternativo na forma de F2 foram encontrados em fêmeas mas não em machos (Fig 2 e 3) e na forma F1 ocorreu alguma expressão de macho mas ela foi muito baixa (Fig 4). Enquanto transcritos correspondendo à forma de M1 foram detectados em machos mas não em fêmeas (Fig 2). Uma vez que o minigene não continha o aceitador de splice de 3' da variante M2, este transcrito não foi possível a partir desta construção. Esse minigene não contém qualquer sequência exógena, embora o mesmo demonstre claramente splicing específico de sexo de um fragmento de Aadsx, de fato um fragmento de "minigene" altamente deletado.
Será evidente que algumas sequências são importantes para controlar splicing e devem ser, assim, conservadas, como discutido em outra parte. Isto pode ser facilmente estabelecido por deleção de algumas porções e teste para splicing alternativo por RT-PCR por exemplo.
Figura 2 mostra RT-PCR de machos e fêmeas de linhagem transgênica de Aedes aegypti LA3491 usando os iniciadores 688 - iel-transcr (SEQ ID NO. 4) e 790 - Aedsx-m-r2 (SEQ ID NO. 5). Usando estes iniciadores, splicing no padrão de F2 iria dar uma banda de aproximadamente 985bp enquanto splicing no padrão de M1 iria dar uma banda de aproximadamente 516bp. Uma banda de aproximadamente 985bp (F2) apareceu apenas em trilhas representando fêmeas e uma banda de aproximadamente 516bp de transcrito 1 específico de macho (M1) apareceu apenas em machos. Estes bandas foram sequenciadas e mostraram que o splicing correto tinha ocorrido, isto é tipo F2 e tipo M1 respectivamente. A ausência de bandas nos controles de RT (-RT CON) mostra que não houve contaminação de DNA genômico mas amostras. Trilhas 1 e 11 são marcadores (SmartLadder™ de Eurogentec, bandas de 1,5kb a 0,2kb são indicadas). Trilhas 2 e 3 são controles negativos (sem transcriptase reversa) e trilhas 2-9 representam reações realizadas em extratos dos machos e fêmeas, como marcado.
Figura 3 mostra RT-PCR dos machos e fêmeas de linhagens transgênicas de Aedes aegypti LA3491 usando os iniciadores 688 - iel-transcr (SEQ ID NO. 4) e 761 - Aedsx-fem-r (SEQ ID NO. 6). Usando estes iniciadores, splicing no padrão de F2 iria dar uma banda de aproximadamente 525bp. Uma banda de aproximadamente 525bp estava presente nas reações em extratos de fêmeas, mas não de reações correspondentes em extratos de machos. Sequenciamento desta banda de 525bp confirmou estar correto, isto é o splicing de tipo F2 ocorreu. Marcador (SmartLadder™ de Eurogentec, bandas de 1,5kb a 0,2kb são indicadas).
Figura 4 mostra RT-PCR dos machos e fêmeas de linhagens transgênicas de Aedes aegypti de LA3491 usando os iniciadores 688 - iel- transcr (SEQ ID NO. 4) e AedsxRl (SEQ ID NO. 4). Usando estes iniciadores, splicing no padrão F1 iria dar uma banda de 283bp. A banda de aproximadamente 283bp está predominantemente presente em fêmeas, embora haja evidência de uma quantidade pequena de splicing em machos. Sequenciamento confirmou que esta banda de fato corresponde ao splicing no padrão F1. Marcador (SmartLadder™ de Eurogentec, bandas de 1,5kb a 0,2kb são indicadas). LA3534 é idêntico a LA3491 exceto para uma deleção 3' de aproximadamente 2kb. Esta construção não mostrou nenhum splicing diferencial entre machos e fêmeas (Fig 1, minigene 2). Géis de RT-PCR não foram mostrados para este caso. Com base nestes resultados, várias construções foram projetadas para incorporar o splicing específico de sexo de LA3491 (Fig 1, minigene 1) em um sistema de retro-alimentação positivo. LA3612 (Fig 5), que incorpora uma fusão de ubiquitina e tTAV2 na região de codificação dsx, é engenheirado de modo que quando o transcrito de fêmea F2 é produzido, a ubiquitina é clivada e o tTAV2 é liberado para iniciar e sustentar o sistema de retro-alimentação positiva. LA3619 (Fig 5) tem tTAV2 sem ubiquitina e usando seu próprio códon de partida de tradução. LA3646 (Fig 5) é idêntico a LA3619 exceto os códons de partida para o gene de dsx foi mudado; isto deve melhorar a quantidade de tTAV2 produzida removendo a tradução não específica.
Figura 5 é uma representação diagramática de plasmídeos com base em splicing em minigene dsx de Aedes aegypti. Para maior certeza, será entendido que o primeiro íntron de fêmea representa qualquer splicing F1, F2 ou F3, e tTAV no diagrama refere-se a tTAV2 (será notado que outras proteínas ou outras versões de tTA ou tTAV poderiam alternativamente ser usadas). Em cada um destes plasmídeos, além de LA3491, a sequência heteróloga foi adicionada ao éxon F2. "ATG putativo" representa qualquer sequência de tripleto ATG em sequência exônica localizada 5' com relação ao DNA heterólogo. Em LA3646, estes códons de partida de tradução putativos ("ATG putativo") foram removidos ou modificados. No caso de construção LA3612, tradução de um ATG a montante (5') que está em matriz com a região de codificação de ubi-tTAV irá ainda (assumindo nenhuma intervenção de códon de parada) produzir tTAV funcional, seguindo separação das porções de ubiquitina e tTAV por ação de protease. Os vários cassetes de splicing alternativo estão ligados operativamente a um promotor apropriado, terminador transcripcional e outras sequências regulatórias.
Esse exemplo mostra splicing específico de sexo de um fragmento de "minigene" altamente comprimido em um contexto heterólogo (isto é promotor heterólogo, 5' UTR e 3' UTR). Embora não mostre expressão diferencial de uma sequência não Aedes, como os éxons spliced alternativamente são derivados do gene Aadsx e não contêm material adicional, isto ilustra claramente a possibilidade desta abordagem. Em qualquer caso, os promotores, 5' UTR e 3' UTR, são heterólogos. Os requerentes realizaram construções adicionais que ilustram vários métodos diferentes para obter expressão diferencial (específica de sexo) de uma proteína heteróloga por este dsx .
Pane et al. (2002) sugeriram que determinadas sequências relacionadas a sítios de ligação conhecidos do complexo TRA/TRA2 em Drosophila poderiam ser importantes na regulação do splicing de Cctra, e isto também era conhecido para dsx de Drosophila e foi também sugerido para dsx de Anopheles gambiae (Scali et al 2005). A sequência de consenso é diferentemente descrita como UC(U/A)(U/A)C(A/G)AUCAACA (Pane et al), SEQ ID NO. 8, ou UC(U/A)(U/A)CAAUCAACA (Scali et al 2005), SEQ ID NO. 9.
É notável que estas definições sejam extremamente similares. Pane et al identificam 8 alinhamentos parciais para esse consenso na sequência de Cctra (7 ou mais nucleotídeos alinhando as 13 sequências nucleotídicas de consenso). Scali et al identificam 6 alinhamentos em Agdsx (9/13 ou melhor). Tais sequências são também conhecidas para regular o splicing alternativo do gene fruitless de Drosophila; Scali et al reviram 3 alinhamentos naquela sequência (12/13 ou melhor). Splicing correto de dsx pode também requerer uma região rica em purina, como discutido por Scali et al.
Como pode ser visto da Tabela 2 e figura 7, os requerentes identificaram o que se pensa ser agrupamentos significantes de sítios de ligação para Tra/Tra2 em minigene 1 dsx de Aedes aegypti dos requerentes.
Figura 6 mostra um alinhamento dos segundos éxons específicos de fêmea e sequências de flanqueamento de gene dsxs da lagarta rosada (Pectinophora gossypiella, PBW - dsx, SEQ ID NO. 146), bicho-da- seda (Bombyx rnori, bombyx-dsx, SEQ DD NO. 147) e traça das maçãs e pêras (Cydia pomonella, traça das maças e pêras- dsx, SEQ ED NO. 148). O segundo éxon específico de fêmea é mostrado em negrito. Os requerentes identificaram múltiplas cópias de uma sequência nucleotídica curta, repetida, conservada em sequência e localização aproximada entre estas traças de parentesco relativamente distante; estas estão localizadas apenas 5' para o éxon específico de fêmea. As repetições AGTGAC/T conservadas estão sublinhadas. Asteriscos (*) representam nucleotídeos idênticos, traços (-) representam intervalos para melhor alinhamento. Os éxons estão representados na SEQ ID NOS. pela seguinte numeração de nucleotídeos: SEQ ID NO. 146289-439; SEQ ID NO. 147 339-492; e SEQ ID NO. 148 285-439. Sítios de ligação Tra2 Aedes dsx.
Em fêmeas de Drosophila melanogaster, Tra e um produto do gene tra2 constitutivamente ativo, atuam como reguladores de splicing por ligação dos sítios de melhorador de splicing no pré-mRNA de dsx, que ativa o sítio do aceitador 3' fraco do éxon específico de fêmea (Scali et al). Em machos não há expressão de TRA e sítio do aceitador 3' fraco não é reconhecido e o splicing ocorre no éxon de macho. Para buscar por sítios de ligação Tra/Tra2 putativos, os requerentes usaram a sequência de consenso destes sítios de ligação deduzidas para Drosophila Tra/Tra2 e procuraram a distribuição destes na sequência de gene dsx de Aedes aegypti. Isto é mostrado na Tabela 2, abaixo.
Tabela 2: * = em 3491, apenas 9/13 mas 6/6 no núcleo. Esta tabela não inclui 9/13 de identidades além daquelas em 3491 com identidade de 6/6 com sequência de núcleo de wwcrat. Esta sequência de núcleo de consenso (WWCRAT) é particularmente preferida. Figura 7 é uma representação diagramática de sítios de ligação Tra/Tra2 putativos na região de codificação dsx de plasmídeo LA3491. Esse diagrama está aproximadamente em escala e representa uma sequência de aproximadamente 4kb. Os requerentes puderam calcular a possibilidade de 5 um alinhamento aleatório para a sequência de consenso Tra/Tra2.
Considerando que todos os 4 nucleotídeos ocorrem em uma freqüência igual, as chances de qualquer dado nucleotídeo em uma sequência aleatória ser o primeiro nucleotídeo de um alinhamento 10/13 ou melhor para o consenso são de aproximadamente 7x10-4. Assim, seria de se esperar um pouco menos do que um tal alinhamento por 1000 nucleotídeos de tal sequência aleatória. O cálculo para isto é apresentado abaixo:
Uma sequência de consenso de sítio de ligação consiste de 13 bases. Dez daquelas posições (fixas) (chamado conjunto X) deve ser cada uma base específica. As outras três (chamado de conjunto Y) pode ser cada de duas bases específicas. Considerando que cada base possível A, G, C e T é igualmente provável e que a base de cada posição é independente das bases em outras posições, qual é a probabilidade de uma sequência de 13 bases selecionada aleatoriamente exatamente alinhar esta sequência? Quais são as probabilidades de tal sequência ser um desalinhamento próximo (permitindo até uma, duas, três ou quatro diferenças)? As respostas são dadas na Tabela 2 abaixo e os aspectos operacionais são mostrados a seguir. Respostas
Os requerentes possuem uma linhagem de LA3097 (LA3097A) que mostra expressão muito boa de seu marcador fluorescente; é desconhecido se esta linhagem é um evento de integração simples. Esta linhagem mostra evidência de splicing específico de sexo, quando criadas sem tetraciclina todas as fêmeas morreram como embriões, e quando administrados com 30μg/ml de tetraciclina ambos, machos e fêmeas, sobrevivem.
Esse exemplo é importante. Ele mostra que Cctra provê splicing alternativo específico de sexo em Aedes, e que isto pode ser usado para resultar em letalidade específica de sexo. Assim, por esta razão, ele fornece uma evidência da faixa filogenética de splicing CcTRA. Assim, é inteiramente plausível que a presente invenção possa ser aplicada para todos dípteros, como os requerentes demonstraram que Cctra trabalha em Drosophila, tefrítidas e mosquitos, que essencialmente estendem-se sobre toda ordem de Dípteros. É surpreendente que Cctra funcione em Aedes, dado a rápida evolução de sequência de tra.
Os requerentes transformaram Aedes aegypti com construção LA3097. Machos heterozigóticos da linhagem transgênica resultante foram cruzados com tipo selvagem e a progênie criada em meio de cultura aquoso suplementado com tetraciclina para uma concentração final de 30 μg/ml. Adultos foram recuperados como segue: 14 machos e uma fêmea, deste modo mostrando letalidade específica de fêmea resultante.
Esta espécie e cepa têm normalmente uma relação de sexo de aproximadamente 1:1, por esta razão esta construção resultou em letalidade específica de fêmea em Aedes aegypti. Construções equivalentes que não continham a sequência intrônica de Cctra resultaram em letalidade não específica de sexo. Por esta razão, o íntron Cctra pode ser usado para prover regulação (isto é, específica de sexo) de expressão de gene diferencial em mosquitos, e isto pode ainda ser usado para prover letalidade específica de sexo e um método para eliminação seletiva de fêmeas de uma população.
Em maiores detalhes: em 0 μg/ml de tetraciclina, machos sobrevivem apenas para pupas, isto é não se tornam adultos. Fêmeas morrem tão prematuramente que não foram vistas, provavelmente como embriões, assim, ainda há um efeito diferencial entre os sexos. No entanto, a letalidade pupal em machos sugere que o sistema não é completamente desligado em machos. A linhagem de inserção única que os requerentes recuperaram é incomum, em que ela mostra expressão extremamente forte do marcador; outras inserções com níveis de expressão mais típicos poderiam bem não mostrar letalidade para machos.
Análise de splicing de LA3097 de mosquitos transgênicos de LA3097A por RT-PCR mostrou que machos e fêmeas compartilharam dois transcritos, uma banda de aproximadamente 950 bp e uma banda fraca de aproximadamente 800 bp (figura 59). Sequenciamento destas bandas mostraram que banda de 900 bp corresponde a uma variante de splice não específica de sexo (AeM2, -920 bp), e a banda fraca foi uma mistura de uma variante de splice não específica de sexo (AeM1, ~804bp) e a forma de fêmea (AeF1, ~765bp), ver figura 60. O splicing do transcrito de AeF1 foi idêntico ao mostrado para esta construção em mosca-do-mediterrâneo (figura 33). O splicing dos transcritos de M diferem um pouco da vista no contexto nativo (Splicing de CcTRA em mosca-do-mediterrâneo, que o gene nativo ou como observado pelos requerentes de LA3097 em mosca-do-mediterrâneo transgênica); em AeM1, o segundo éxon spliced alternativamente (ME1b) não está incluído no transcrito de AeM1 maduro e, em AeM2, o segundo éxon de splicing alternativo (ME2b) está similarmente não incluído no transcrito AeM2 maduro. Em outras palavras, para cada um destes transcritos o primeiro, mas não o segundo, éxon de cassete está presente, relativo ao protótipo de mosca-do-mediterrâneo. Note-se que, como uma consequência da ausência do segundo éxon de cassete em AeM1, e a matriz de leitura de tTAV2 relativa ao primeiro éxon de cassete nesta construção, splicing no padrão de AeM1 não conduz a interrupção da matriz de leitura aberta de tTAV2, mas sim à adição de 39 nucleotídeos (correspondendo a 13 aminoácidos) entre a ATG e o resto da matriz de leitura aberta de tTAV2. É provável que esta variante de tTAV2 possa reter alguma atividade, relativa ao tTAV2 normal ou prototípico (como codificado pela variante de splice de F1). Na ausência de tetraciclina, um efeito fenotípico foi observado em machos bem como em fêmeas, embora mais fraco em machos do que em fêmeas. Produção de uma variante parcialmente ativa de tTAV2 a partir do transcrito de AeM1 em machos (e fêmeas) pode explicar isso.
Figura 59 mostra RT-PCR dos machos e fêmeas de linhagem transgênica de Aedes aegypti LA3097A usando os iniciadores HSP (SEQ ID NO. 139) e VP16 (SEQ ID NO. 140). Usando estes iniciadores, splicing no padrão de CcF1 (isto é correspondendo à variante de F1 de Ceratitis capitata) resultaria em uma banda de aproximadamente 765bp e splicing na CcMl 1005bp e CcM2 1094bp. Em ambos, machos e fêmeas, uma banda forte de aproximadamente 950bp (1)foi observada junto com uma banda fraca de aproximadamente 800bp (2). Marcador (SmartLadder™ de Eurogentec, bandas de 1,5kb a 0,4kb são indicadas).
Análise de sequência de vários clones de banda 2 (isto é variantes de splice de AeMl/Ae F1) de machos e fêmeas mostraram que um dentre cinco clones de fêmeas mostraram splicing de AeM2 (20%), enquanto em machos, três dos quatro clones mostraram splicing de AeM2 (75%); todos os outros clones mostraram splicing de AeF1. Isto indica que há mais transcrito de AeF1 presente em fêmeas que em machos e isto explicaria o efeito de morte diferencial visto entre os mesmos.
Figura 60 ilustra os vários transcritos produzidos por splicing alternativo de Cctra de linhagem transgênica de Aedes aegypti LA3Q91A. 3097 representa a sequência de DNA de Cctra e os número referem-se a figura descrita em outra parte. Sombreamento e caixas também se referem à figura 33. Nota-se que o diagrama está fora de escala.
Os requerentes obtiveram onze linhagens de LA3545, que usam o gene actin-4 de Aedes (AeAct-4 ou AaAct4) para dirigir a expressão de tTAV2. Em construção LA3545, uma sequência codificando tTAV2 foi inserida no segundo éxon de AaAct4 (fig 10). Para transcritos spliced no padrão característico de splicing AaAct4 em fêmeas, o ATG da região de codificação de tTAV2 será o primeiro ATG (o mais a 5') do transcrito. O splicing no padrão característico de splicing AaAct4 em machos introduz um arranjo de códons de partida e de parada antes da sequência de tTAV2 que tende a inibir ou interferir com a tradução do ATG da região de codificação de tTAV2. Estas linhagens devem apenas expressar tTAV2 em pupas de fêmeas. O splicing é mostrado na figura 8, abaixo.
Figura 8 mostra RT-PCR de adultos machos e fêmeas de linhagem transgênica de Aedes aegypti LA3545AeC usando os iniciadores Agéxon1F (SEQ ID NO. 141) e TETRRl (SEQ ID NO. 142). Usando estes iniciadores, splicing em um padrão equivalente àquele do gene AaAct4 nativo iria dar bandas de aproximadamente 347bp para a variante de splice de tipo fêmea e de aproximadamente 595bp para a variante de splice de tipo macho. Uma banda de aproximadamente 347 bp (F) foi encontrada apenas em reações em extratos de fêmeas; uma banda de aproximadamente 595bp (M) foi encontrada em ambos, machos e fêmeas. Sequenciamento confirmou que o splicing correto ocorreu tanto em machos como em fêmeas. Marcador (SmartLadder™ de Eurogentec, bandas de 1,5kb a 0,2kb são indicadas).
Os requerentes também obtiveram Aedes aegypti transgênico portando construção LA3604, que é similar a LA3545 exceto que este tem um códon de partida engenheirado na porção de éxon 1 que está presente em ambos, transcritos de tipo macho e de tipo fêmea (Fig 10). Isto está disposto para ser o primeiro ATG em qualquer tipo de transcrito. LA3604 codifica tTAV2 fusionado a ubiquitina (LA3545 codifica tTAV, enquanto LA3604 codifica ubi-tTAV2). Esta construção deve produzir proteína de tTAV2 completamente funcional em fêmeas apenas, mesmo se a forma de macho for expressada em fêmeas o éxon de macho extra contém vários códons de partida e de parada que poderiam prevenir a tradução da proteína de fusão ubi-tTAV2.
O splicing alternativo de AaAct4 ocorre no 5' UTR (do gene nativo). Ela pode ou não ter uma parte regulatória no gene nativo. Uma possibilidade é como a seguir: na variante de splice específico de fêmea, o códon de partida da região de codificação de AaAct4 é o primeiro ATG do transcrito. No entanto, na variante de splice específica específico de macho, existem várias sequências de ATG adicionais a 5' para o códon de partida da região de codificação de AaAct4; a maior destes tem códons de parada na matriz em uma distância pequena 3'. Esta arrumação de sequência pode interferir com a tradução eficiente da proteína AaAct4 e assim reduzir expressão da proteína em machos como comparado com fêmeas. Esta é a arrumação em LA3545.
No entanto, um efeito diferencial maior entre machos e fêmeas seria esperado se o íntron fosse incluído na região de codificação (em vez de 5' UTR), isto é, inserido entre os códons de partida e parada do polinucleotídeo para expressão no organismo. Nesse caso, o éxon de cassete específico de macho mudaria o potencial de codificação do transcrito, em vez de simplesmente interferir com tradução.
Isso é obtido na construção LA3604. Os requerentes modificaram o primeiro éxon compartilhado para incluir uma sequência de ATG em um contexto de sequência apropriado para uma iniciação translacional. Nesta sequência modificada, esse é o primeiro ATG em ou as variantes de splice de tipo macho (M) ou de tipo fêmea (F). Seguindo o splicing na forma de F, esse (projetado) ATG de 5' está na matriz com a região de codificação de ubi-tTAV. Transcritos de tipo F codificariam, por esta razão, uma proteína de fusão, compreendendo seções codificadas por (i) parte de qual é normalmente 5' UTR de Act4 (mas aqui obviamente traduzida, e assim, não UTR em todas), (ii) região de codificação de ubiquitina e (iii) região de codificação de tTAV2.
Atividade de ubiquitina proteases celulares irão liberar a proteína de tTAV2. Tradução do ATG 5' engenheirado seria terminada por códons de parada em matriz na sequência adicional (éxon de cassete) presente em transcritos spliced na forma M. Isto poderia, assim, evitar a expressão de tTAV2 funcional em machos, assim dando expressão específica de sexo de tTAV2. Obviamente, isto proporcionaria um método geral de expressão específica de sexo de uma proteína, substituindo-se o segmento tTAV2 com outra proteína ou sequência de interesse. Usando esta estratégia os requerentes proveram transgênicos e mostraram o splicing específico de sexo (Fig 9).
Figura 9 mostra RT-PCR dos machos e fêmeas de linhagem transgênica de Aedes aegypti LA3604AeA usando os iniciadores AgexonlF (SEQ ID NO. 141) e TETRRl (SEQ ID NO. 142).Usando estes iniciadores, splicing na forma de fêmea iria dar uma banda de aproximadamente 575 bp, enquanto inclusão do éxon de cassete específico de macho aumentaria o mesmo a aproximadamente 823bp. Uma banda de aproximadamente 575bp foi vista em cada fêmea analisada, enquanto uma banda de aproximadamente 823bp foi vista em cada macho analisado. Estas bandas parecem ser substancialmente específicas para os respectivos sexos. Sequenciamento destas bandas mostrou que o splicing correto ocorreu em machos e fêmeas. Marcador: SmartLadder™ de Eurogentec, bandas de 1,5 kb a 0,2 kb são indicadas.
Figura 10, abaixo, é uma representação diagramática de LA3545 e LA3604 de plasmídeos. S1: éxon 1 compartilhado; M1: sequência adicional incluída em éxon 1 específico de macho; S2: éxon 2 compartilhado (extremidade de 5' apenas); ubi: sequência codificando ubiquitina; tTAV2: sequência codificando tTAV2.
Em várias das linhagens transgênicas LA3545, um efeito específico de sexo e tecido foi observado: fêmeas não são aptas a voar. Duas das linhagens mostraram 90-100% de um fenótipo de inaptidão ao vôo de fêmeas, uma linhagem mostra 70% sem a aptidão ao vôo e outros 50%. Este fenótipo é provavelmente devido à expressão específica de fêmea de tTAV2 no desenvolvimento de músculos aptos a voar. A diferença nos fenótipos entre as linhagens é devido aos efeitos posicionais na expressão do promotor AaAct4. Devido a uma posição de genes na expressão de genoma poder ser influenciada pelo número de fatores (regiões de heterocromatina ou eucromatina, elementos melhoradores e supressores, proximidade de outros genes) que podem ser vistos prontamente nos marcadores fluorescentes usados para identificar transgênicos. Todas as onze linhagens de LA3545 foram identificadas porque elas têm perfis fluorescentes diferentes, mesmo se elas têm os mesmos promotores e marcador. Esta variação é devido aos efeitos posicionais. Isto poderia então significar que os requerentes esperaram que algumas linhagens de LA3545 expressassem mais tTAV2 do que outras, devido aos efeitos posicionais, e as linhagens que expressam mais irão dar um fenótipo de inaptidão ao vôo específico de fêmea.
Para testar esta hipótese, os requerentes desenvolveram uma linhagem separada de Aedes aegypti com um gene repórter tetO-DsRed2 (LA3576 ver Fig 17 e SEQ ID NO. 143), quando cruzados com linhagens LA3545 diferentes isto iria permitir a visualização de onde e quando Actin4- tTAV2 estava sendo expressado. Dentre as 8 linhagens de LA3545 cruzadas para LA3576 todas mostraram fluorescência de músculo de vôo indireto específico de fêmeas em larvas L4 tardias, pupas e adultos. Em quatro das linhagens, a expressão de DsRed2 pareceu ser específica (isto é exclusiva) para os músculos aptos ao vôo indiretos de fêmeas; em outros, quatro tecidos adicionais mostraram expressão de DsRed2. Este fenômeno, onde expressão de um transgene depende, em parte, da região ou ponto no genoma em que está inserido, é chamado efeito de posição, e será bem conhecido e entendido pela pessoa versada na técnica.
Usando LA3576, provou-se que a expressão de tTAV2 em LA3604 foi específica de fêmea, ocorre principalmente nos músculos de vôo indiretos e é específica de estágio. Várias construções de efetuador tetO foram então construídas para analisar seus efeitos. Os transgênicos tetO- MichelobX (LA3582, ver Fig 15 e SEQ ID NO. 144) quando cruzados para LA3545 demonstraram todos fenótipos de inaptidão ao vôo específicos de fêmea que poderiam ser reprimidos por tetraciclina. Isto prova que Actin4 pode ser usada para dirigir um gene efetuador em um modo específico de estágio, tecido e sexo.
Porque algumas linhagens de LA3545 têm um fenótipo de inaptidão ao vôo específico de fêmea sem a presença de um gene efetuador induzido, isto mostrou que tTAV2 poderia atuar como uma molécula de efetuador. tTAV2 é composto de um tTA, um domínio de ligação de tetO e VP16, uma proteína de vírus de herpes simplex. VP16 ativa a transcrição de genes virais prematuros imediatos usando suas sequências amino-terminais para fixar a uma ou mais proteínas codificadas de hospedeiro que reconhecem sequências de DNA em seus promotores. Em LA3604, um efetuador de tetO - VP16 foi adicionado para melhorar o efeito de tTAV2. Em três linhagens transgênicas de LA3604 isto levou a um fenótipo de inaptidão ao vôo específico de fêmeas de 100% quando criadas sem tetraciclina, mostrando que VP16 é uma molécula efetuadora efetiva. Nota-se que LA3604 tem um códon de partida potencial (ATG) engenheirado a 5' de para o íntron spliced alternativamente. Assim, nesta construção, o éxon específico de macho é esperado para interromper a matriz de leitura aberta codificando tTAV (ubi- tTAV); uma vez que a sequência específica de macho contém vários códons de parada, isto tenderá a reduzir ou eliminar a produção de tTAV funcional em machos. Por meio de comparação, o éxon específico de macho 5' para o códon de partida de tTAV em LA3545. No entanto, inserindo um número de códons de partida 5' para o códon de partida de tTAV (que é o primeiro ATG do transcrito de fêmea mas não do transcrito de macho), nenhum destes códons de partida adicionais sendo apropriados para a produção eficiente de tTAV funcional devido a estar fora da matriz ou ter códons de parada intervindo, esta arrumação também irá tender a reduzir ou eliminar a produção de tTAV funcional em machos, consistente com dados fenotípicos acima.
Os requerentes realizaram recentemente construções baseadas em Cctra com o íntron de cassete de Cctra em uma variedade de contextos diferentes, isto é flanqueado por sequências diferentes. Várias linhagens de mosca-do-mediterrâneo transgênicas transportando estes foram construídas. Isto mostra que o sistema é geral e robusto, isto é, que vai funcionar para uma extensa faixa de sequências de interesse heterólogas.
Os requerentes também obtiveram pelo menos um exemplo feito recentemente de uma fusão Cctra -ubi-tTAV dando um splicing correto (DsRed- Cctra - ubi-tTAV).
Exemplos preferidos da proteína funcional colocam a sequência de codificação para ou ubiquitina ou tTA, ou seus mutantes funcionais e ou variantes tais como tTAV, tTAV2 ou tTAV3, 3' para o íntron. Estes estão dispostos de modo que estes elementos estão substancialmente adjacentes à extremidade 3' do íntron, mais preferivelmente de modo que a região de codificação inicia dentro de 20 nucleotídeos ou menos do limite do íntron 3'), e, o mais preferivelmente, imediatamente adjacente à extremidade 3' do íntron, embora isto seja menos relevante se o sistema de ubiquitina for usado.
Exemplos preferidos de construções de acordo com a presente invenção estão listados na Tabela 4, abaixo. Será notado que LA1118 não está dentro do escopo da presente invenção, como ele não codifica uma proteína funcional, isto é não funciona propriamente. Pensa-se que isto é devido ao uso inesperado de um doador de splice 5' de 4bp para a junção com sequência de íntron Cctra, conduzindo a uma armação que é induzida em todas os splices. Assim, isto é incluído apenas com a finalidade de informação. Tabela 4 mostra construções que contêm uma sequência de controle de splice que é derivada de um íntron tra. Os íntrons foram derivados de C. capitata (mosca-do-mediterrâneo), B. zonata ou C. rosa (ver coluna 2). Referido íntron foi inserido dentro da região de codificação tal que a distância entre ATG de iniciador putativo e o último nucleotídeo do éxon imediatamente precedendo o íntron tra foi como deve estar indicado na coluna 3. Íntron é inserido em ou adjacente à região de codificação para ubiquitina, tTAV, ReaperKR, nipper ou ubiquitina- DsRed como mostrado na coluna 4. Estes foram gerados e mostrados como splice com sucesso, por RT-PCR ou 89 fenotipicamente em mosca-do-mediterrâneo em, em alguns casos, também quer em Drosophila melanogaster (LA3077) ou Anastrepha ludens (LA3097, LA3233, LA3376). Além disso, a distância entre o ATG e a extremidade do éxon imediatamente precedendo o íntron tra (assumindo splicing em forma de tipo F1) pode variar de 0bp a pelo menos +949bp sem consequências adversas para splicing (ver Tabela 4, coluna 3). Assim, é razoável assumir que esta distância pode ser até pelo menos 900 e preferivelmente até pelo menos 949 bp.
Mais informação nestes exemplos está sumarizada na Tabela 5. A opção preferida é usar nenhuma sequência endógena para obter o controle de splicing alternativo correto de expressão (+0bp na tabela 4). Os requerentes preferiram inserir o íntron tra entre os dinucleotídeos de flanqueamento TG... GT na região de codificação da proteína de interesse para ser spliced alternativamente de modo a assegurar splicing correto como isto pode ser importante, no entanto os requerentes não irão se limitar a isto, se necessário, como outros nucleotídeos de flanqueamento podem funcionar corretamente também. Exemplos LA1038, LA3054 e LA3056 inclui alguma sequência exônica de flanqueamento endógena do gene CCtra natural. Na tabela 5, se 6 nucleotídeos ou menos (incluindo o códon de partida ATG) estão incluídos de fusões particulares para 3' ou 5' da junção de splice, para os propósitos de sumário desta tabela estes não serão considerados como fazendo parte da fusão. Tabela 4 pode estar correlacionada com a tabela 3 para encontrar qual íntron tra (Cctra, Bztra ou Crtra) é usado em cada exemplo. Novamente, LA1118 está apenas incluído para os fins de informação e está fora do escopo da presente invenção.
Como mencionado acima quando um íntron é colocado 5' para uma região de codificação de proteína (ORF-X), prefere-se posicionar ou usar ubiquitina 3' para o íntron, 5' para ORP-X, assim, e provendo regulação específica de fêmea de ORF-X, enquanto introduzindo separação física entre 5 esta sequência e o íntron tra, assim reduzindo a possibilidade de que sequências dentro de ORF-X irão interferir com o splicing do íntron tra.
Construções e sequências compostas também são previstas, por exemplo da forma: X-ubi-Y 10 com o íntron alternativamente spliced inserido entre a região de codificação X e a região codificando ubiquitina (ubi), ou dentro da região de codificação de ubiquitina, ou entre a região codificando ubiquitina e região de codificação Y. Assim X será expressado independentemente de splicing do íntron, enquanto Y será apenas expressado quando o íntron é spliced em uma 15 forma apropriada. Mais configurações e arrumações deste tipo geral serão evidentes para o versado na técnica. Alguns exemplos dos mesmos são LA3014, LA3054, LA3056, LA3166, LA3488 e LA3596, sendo que todos usam fusões de ubiquitina, desta forma demonstrando a capacidade desta idéia ser aplicada com sucesso em mosca-do-mediterrâneo transgênica. Exemplos alternativos em mosquitos transgênicos incluem LA3604 e LA3612, mostrando a extensa aplicabilidade filogenética deste sistema em não apenas espécies diferentes (mosquitos e mosca-do-mediterrâneo), mas também em diferentes contextos incluindo AaActin4, Aadsx e Cctra. LA3596 (ver Fig 67 e SEQ ID NO. 145) é de projeto similar a LA3488, planejado para gerar fluorescência verde (por expressão de proteína fluorescente TurboGreen localizada nuclear) em ambos sexos, mas fluorescência vermelha apenas em fêmeas (por expressão de proteína fluorescente DsRed2 localizada nuclear). Isto é obtido pela fusão destas duas proteínas, dirigida por cassete de melhorador/promotor de Hr5-Iel, ligado junto com um ligador de 11 aminoácidos curto (ligador de SG4) e a região de codificação compreendendo ubiquitina (com uma mutação em pontos planejada para estabilizar a proteína resultante reduzindo sua propensão à degradação mediada por ubiquitina) e o íntron Cctra para limitar expressão de DsRed2 para fêmeas. Moscas-do-mediterrâneo transgênicas foram geradas com esta construção. Fluorescência vermelha foi limitada a fêmeas nesta linhagem como esperado, enquanto fluorescência verde foi observada em ambos, machos e fêmeas. Isto poderia ser usado para separação de sexos por triagem de fluorescência para uma particular proteína fluorescente, nesse caso fluorescência vermelha representando expressão de DsRed2.
Referência também é feita a LA3014 e LA3166 e dados fenotípicos dos mesmos em outros exemplos.
Os requerentes previamente realizaram e obtiveram transgênicos com o íntron Cctra em uma proteína funcional diferente de tTAV, ver LA3014 e LA3166. LA3014 contém uma fusão de ubiquitina - reaperKR a jusante de um íntron Cctra. Dados fenotípicos mostram que moscado-mediterrâneo transgênica LA3014 concedeu letalidade específica de fêmea repressível. Análise de RT-PCR em RNA extraído de machos e fêmeas adultos criados sem tetraciclina, usando iniciadores e ReaperKR, demonstram que splicing correto estava ocorrendo em fêmeas (banda de 508 bp) e nenhuma desta banda foi encontrada em machos (figura 37). LA3166 é outra construção com o íntron Cctra colocado dentro da região de codificação de ubiquitina fusionado a reaperKR, mas colocado em uma posição diferente em ubiquitina. LA3166 também produz um efeito letal específico de fêmea repressível dominante em mosca-do-mediterrâneo. LA1038 é um novo exemplo do uso do íntron Cctra em um contexto de sequência diferente, aqui colocado em um fragmento de Nipp1Dm chamado 'nipper' que também splice corretamente em mosca-do- mediterrâneo transgênica quando analisada por RT-PCR (figura 12). LA670 foi requerido como uma fonte de tTAV para dirigir a expressão de nipper alternativamente spliced.
Os requerentes também realizaram recentemente e obtiveram transgênicos com construções baseadas em Cctra "somente íntron" com o íntron em um gene diferente (muitos dos exemplos acima, salvo especificado em contrário, estão em tTAV ou uma de suas variantes, isto é tTAV2 ou tTAV3). Estas construções funcionam como previsto. Isto é um resultado importante, deste modo mostrando que existem sequências exônicas não essenciais em Cctra que os requerentes simplesmente duplicaram (em função, se não necessariamente em sequência) por acaso, em tTAV. Também os requerentes realizaram construções de ubi - rprKR deste tipo (LA3014 e LA3166), que também validam o método de fusão de ubiquitina descrito acima. O método de fusão de ubiquitina é ainda exemplificado por análise RT-PCR de LA3054, LA3056 e LA3488 (figuras 11, 13, 14), como descrito no Exemplo 16, acima.
Referência também é feita a LA3014 e LA3166 e dados fenotípicos a partir dos mesmos em outros exemplos.
Os requerentes previamente realizaram e obtiveram transgênicos com o íntron Cctra em uma proteína funcional diferente de tTAV, ver LA3014 e LA3166. LA3014 contém uma fusão de ubiquitina - ReaperKR a jusante de um íntron Cctra. Dados fenotípicos mostram que mosca-do-mediterrâneo transgênica de LA3014 concedeu letalidade específica de fêmea repressível. Análise de RT-PCR em RNA extraído de adultos machos e fêmeas criados sem tetraciclina, usando iniciadores e ReaperKR, demonstram que o splicing correto estava ocorrendo em fêmeas (banda de 508bp) e nenhuma desta banda foi encontrada em machos (figura 37). LA3166 é outra construção com o íntron Cctra substituído dentro da região de codificação de ubiquitina fusionada ao ReaperKR, mas substituído em uma posição diferente em ubiquitina. LA3166 também produz um efeito letal específico de fêmea repressível dominante em mosca-do-mediterrâneo. LA1038 é um novo exemplo do uso do íntron Cctra em um contexto de sequência diferente, aqui substituído em um fragmento de Nipp1Dm chamado 'nipper' que também splice corretamente e, mosca-do-mediterrâneo transgênica quando analisada por RT-PCR (figura 12). LA670 foi requerida como uma fonte de tTAV para conduzir expressão nipper alternativamente spliced.
Os requerentes realizaram recentemente e obtiveram transgênicos com construções baseadas em Cctra apenas de íntron com o íntron em um gene diferente (muitos dos exemplos acima, salvo aparente, ocorrem em tTAV ou uma das suas variantes, isto é tTAV2 ou tTAV3). Estas construções funcionam como previsto. Isto é um resultado importante, deste modo mostrando que existem sequências exônicas não essenciais em Cctra que os requerentes simplesmente duplicaram (em função, se não necessariamente em sequência) aleatoriamente, em tTAV. Também os requerentes notaram construções de ubi - rprKR deste tipo (LA3014 e LA3166), que também validam o método de fusão de ubiquitina descrito acima. O método de fusão de ubiquitina é ainda exemplificado por análise de RT-PCR de LA3054, LA3056 e LA3488 (figuras 11, 13, 14), e como descrito no Exemplo 16, acima. Figura 11: Gel mostrando splicing específico de sexo de íntron(s) derivados de Cctra (banda de 780bp em fêmeas) em Ceratitis capitata transformadas com LA3488. Splicing na forma de Fl poderia dar um produto de aproximadamente 780bp. Uma banda deste tamanho é claramente visível de fêmeas (trilha 4), mas não de machos, nem em trilhas com reações das quais a enzima de transcriptase reversa foi omitida ("sem RT"). Por esta razão, o íntron derivado de Cctra é capaz de splicing alternativo específico de sexo nesse contexto de sequência novo. Trilha 1: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,8, 1,0 e 1,5kb são indicadas); Trilhas 2 e 3: LA3488 de Ceratitis capitata /+ machos (controle de RT e sem controle RT, respectivamente); Trilhas 4 e 5: LA3488 de Ceratitis capitata /+ fêmeas (controle de RT e sem controle de RT, respectivamente). Figura 12: Gel mostrando splicing específico de sexo de íntron(s) derivados de Cctra em Ceratitis capitata transformada com LA1038. Splicing na forma de F1 poderia dar um produto de aproximadamente 230bp. Uma banda deste tamanho é claramente visível de fêmeas (trilhas 1, 2, 7, 8, 9 e 10), mas não de machos. Por esta razão, o íntron derivado de Cctra é capaz de splicing alternativo específico de sexo nesse contexto de sequência nova. Trilha 15: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,2, 0,4 e 0,6kb são indicadas); Trilhas 1, 2, 7, 8, 9 e 10: LA670 Ceratitis capitata; fêmeas de LA1038; Trilhas 3, 4, 5, 6, 11, 12, 13 e 14: LA670 de Ceratitis capitata; machos de LA1038. Figura 13: Gel mostrando splicing específico de sexo de íntron(s) derivados de Cctra em Ceratitis capitata transformada com LA3054. Splicing na forma de F1 poderia dar um produto de aproximadamente 340 bp. Uma banda deste tamanho é claramente visível na trilha 7, mas não de machos. Por esta razão, o íntron derivado de Cctra é capaz de splicing alternativo específico de sexo nesse contexto de sequência nova. Trilha 1 : Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,4, 0,6, 0,8 e 1,0kb são indicadas); Trilhas 2-5: machos de LA3054 de Ceratitis capitata; Trilha 7: fêmea de LA3054 Ceratitis capitata. Figura 14: Gel mostrando splicing específico de sexo de íntron(s) derivados de Cctra e, Ceratitis capitata transformada com LA3056. Splicing na forma de F1 poderia dar um produto de aproximadamente 200 bp. Uma banda deste tamanho é claramente visível de uma fêmea (trilha 6), mas não de machos (trilhas 2-4). Por esta razão, o íntron derivado de Cctra é capaz de splicing alternativo específico de sexo nesse contexto de sequência nova. Trilha 1: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,2, 0,4, 0,6 e 0,8kb são indicadas); Trilhas 2-5: LA3056 de Ceratitis capitata /+ machos; Trilhas 6-7: LA3056 Ceratitis capitata /+ fêmeas. Figura 15: Gel mostrando splicing específico de sexo de íntron(s) derivados de BzTra em Anastrepha ludens transformada com LA3376. Splicing na forma F1 poderia dar um produto de aproximadamente 672 bp. Uma banda deste tamanho é claramente visível de fêmeas (trilha 4), mas não de machos, nem em trilhas com reações de que enzima de transcriptase reversa foi omitida ("sem RT"), iniciadores usados foram SRY e AV3F. Por esta razão, o íntron derivados de Bztra é capaz de splicing alternativo específico de sexo nesse contexto de sequência novo e espécie. Trilha 1: Marcador (SmartLadder™ de Eurogentec, bandas de aproximadamente 0,6, 0,8, e 1,0kb são indicadas); Trilhas 2 e 3: LA3376 Anastrepha ludens /+ machos (controle de RT e sem controle RT, respectivamente); Trilhas 4 e 5: LA3376 de Anastrepha ludens /+ fêmeas (controle de RT e sem controle de RT, respectivamente). Figura 18 e SE ID NOs 149 e 150 mostra sequências de minigene1 de DSX, minigene2 de DSX e mapa de plasmídeo de LA3619. Figuras 19-51 são como por Exemplos 1-9 acima. Figuras 52-58, 68 e 69 mostram vários diagramas e sequências de plasmídeo. Figuras 59-60 estão descritas acima e Figuras 61-66 mostram vários diagramas e sequências de plasmídeo. Fig 67 é pLA3596, como discutido em outra parte.
Allen ML, Christensen BM. Related 2004 Flight muscle-specific expression of act88F: GFP in transgenic Culex quinquefasciatus Say (Diptera: Culicidae). Parasitol Int. 55 (4): 307- 14. Bennett D5 Szoor B, Gross S, VereshchaginaN, Alphey L. 2003 Ectopic expression of inhibitors of protein phosphatase type 1 (PPl) can be used to analyze roles of PPl in Drosophila development. Genetics. 164(1) :235-45. Black, D. (2003). Mechanisms of alternative pre-messenger RNA splicing. Annu Rev Biochem 72, 291-336. Burset, M., Seledtsov, L, and Solovyev, V. (2001). SpliceDB: database of canonical and non- canonical splice sites in mammalian genomes. Nucleic Acids Research 2Ps 255-259. Caceres JF, Kornblihtt AR. 2002 Alternative splicing: multiple control mechanisms and involvement in human disease. Trends Genet. 18(4): 186-93. Cande C, Cecconi F, Dessen P, Kroemer G. 2002 Apoptosis-inducing factor (AIF): key to the conserved caspase-independent pathways of cell death? J Cell Sci. 115(24):4727-34. Cartegni, L., Chew, S., and Krainer, A. (2002). Listening to silence and understanding nonsense: éxonic mutations that affect splicing. Nature Reviews Genetics 3, 285-298. Clark, F., and Thanaraj, T. (2002). Categorization and characterization of transcript-confirmed constitutively and alternatively spliced introns and exóns from human. Human Molecular Genetics 11, 451-464. Funaguma, S., Suzuki, M., Tamura, T., and Shimada, T. (2005). The Bmdsx transgene including trimmed introns is sex-specifically spliced in tissues of the silkworm, Bombyx mori. J Insect Sci 5, 17. George, EX., Ober, M.B. and Emerson Jr, CP. (1989). Functional domains of the Drosophila melanogaster muscle myosin heavy chain gene are encoded by alternatively spliced éxons. MoL Cell Biol. P:2957-2974. Graveley BR. 2001 Alternative splicing: increasing diversity in the proteomic world. Trends Genet. 17(2): 100-7. Hammes, A.5 Guo, J.K., Lutsch, G., Leheste, J.R., Landrock, D., Zeigler, U., Gubler, M.C. and Schedl, A. (2001). Two splice variants of the Wilms' Tumour 1 gene have distinct functions during sex determination and nephron formation. Cell 106:319-329. Hastings, G.A. and Emerson Jrs CP (1991). Myosin functional domains encoded by alternative éxons are expressed in specific thoracic muscles of Drosophila. J. Cell Biol. 114: 263-276. Hedley, MX. and Maniatis (1991). Sex-specific splicing and polyadenylation of dsx pre-mRNA requires a sequence that binds specifically to a tra-2 protein in vivo. Cell 65:579-586. Heinrich J. C. and Scott MJ. 2000 A repressible female-specific lethal genetic system for making transgenic insect strains suitable for a sterile-release program PNAS 97 (15): 8229-8232 Horn C, Wimmer EA. 2003 A transgene-based, embryo-specific lethality system for insect pest management. Nat Biotechnol. 2i(%): 64-70. Hoshijima, K.K, Inoue, L., Higuchi, L, Sakamoto, H. and Shimura, Y. (1991). Control of doublesex alternative splicing by transformer and transformer-2 in Drosophila. Science 252:833-836. Huang, Q., Deveraux, Q.L., Maeda, S., Salvesen, G.S., Stennicke, H.R., Hammock, B.D. e Reed, J.C. (2002). Evolutionary conservation of apoptosis mechanisms: Lepidopteran and baculoviral inhibitor of apoptosis proteins are inhibitor of mammalian caspase- 9.Agricultural Sciences 97(4): 1427-1432. Ito, Y., Hirochicka, H. and Kurata, N. (2002). Organ-specific alternative transcripts of KNOX family class 2 homeobox genes of rice. Gene 288:41-47. Johnson JM, Castle J5 Garrett-Engele P, Kan Z5 Loerch PM5 Armour CD5 Santos R, Schadt EE, Stoughton R, Shoemaker DD. 2003 Genome-wide survey of human alternative pre-mRNA splicing with éxon junction microarrays. Science. 302(5653):214l-4. Jurica MS, Moore MJ. 2003 Pre-mRNA splicing: awash in a sea of proteins. Mol Cell. 12(1):5- 14. Kazzaz JA, Rozek CE. 1989 Tissue-specific expression of the alternately processed Drosophila myosin heavy-chain messenger RNAs. Dev Biol. 133 (2): 550-61. Maniatis, T., e Tasic, B. (2002). Alternative pre-mRNA splicing and proteome expansion in metazoans. Nature 418, 236-243. Munoz, D., Jimenez, A., Marinotti, O, and James, A. (2004). Yhe.AeAct-4 gene is expressed in the developing flight muscles of females Aedes aegypti. Insect Molecular Biology 13, 563-568. Nishiyama, R., Mizuno, H., Okada, S., Yamaguchi, T., Takenaka, M., Fukuzawa, H. e Ohyama, K. (1999). Two mRNA species encoding calcium-dependent protein kinases are differentially expressed in sexual organs of Marchantia polymorpha through alternative splicing. Plant Cell Physiol.40(2J:205-212. Nishiyama, R.,Yamato, K.T., Miura, K., Sakida, M., Okada, S.5 Kono, K., Takahama, M., Sone, T., Takenaka, M., Fukuzawa, H. e Ohyama, K. (2000). Comparison of expressed sequence tags from male and female sexual organs of Marchantia polymorpha. DNA Res. 7:165-174. Olson, M.R., Holley, C.L., Ji Yoo, S., Huh, J.R, Hay, B.A. and Kornbluth, S. (2003). Reaper is regulated by IAP-mediated Ubiquitination. J.Biol.Chem., 27Sf<5;:4028-4034. Olson, M.R., Holley, CX., Gan, E.C., Colon-Ramos, D.A., Kaplan, B. and Kornbluth, S. (2003). A GH3-like domain in reaper is required for mitochondrial localization and induction of IAP degradation. J. Biol. Chem. 218(45). -44758-44768. Pan, Q., Shai, O., Misquitta, C, Zhang, W., Saltzman, A., Mohammad, N., Babak, T., Siu, H., Hughes, T., Morris, Q., et al. (2004). Revealing global regulatory features of mammalian alternative splicing using a quantitative microarray platform. Mol Cell 16, 929-941. Pane, A., Salvemini, M., Delli Bovi, P., Polito, C, and Saccone, G. (2002). The transformer gene in Ceratitis capitata provides a genetic basis for selecting and remembering the sexual fate. Development 129, 3715-3725. Park, J., Parisky, K., Celotto, A., Reenan, R., and Graveley, B. (2004). Identification of alternative splicing regulators by RNA interference in Drosophila. Proc Nat'l Acad Sci (USA) 101, 15974-15979. Parker L, Gross S, Beullens M, Bollen M, Bennett D, Alphey L. 2002 Functional interaction between nuclear inhibitor of protein phosphatase type 1 (NIPPl) and protein phosphatase type 1 (PPl) in Drosophila: consequences of over-expression of NIPPl in flies and suppression by co- expression of PPl. Biochem J. 368 (3) :1 '89-97. Raphael, K.A., Whyard, S., Shearman, D., An, X. e Frommer, M. (2004). Bactrocera tyroni and closely related pest-tephritids-molecular analysis and prospects for transgenic control strategies. Insect Biochem. MoI. Biol. 34:167-176. Ryner, L. and Baker, B. S. (1991). Regulation of doublesex pre-mRNA processing occurs by 3'- splice site activation. Genes Dev. 5:20712085. Saccone, G., Pane, A., e Polito, C. (2002). Sex determination in flies, fruit flies and butterflies. Genetica 116, 15-23. Scali, C, Catteruccia, F., Li, Q., e Crisanti, A. (2005). Identification of sex-specific transcripts of the Anopheles gambiae doublesex gene. J Exp Biol 208, 3701-3709. Scott, M., Heinrich, J., and Li, X. (2004). Progress towards the development of a transgenic strain of the Australian sheep blowfly (Lucilia cuprina) suitable for a male-only sterile release program. Insect Biochem MoI Biol 34, 185-192. Seo, S-J., Cheon, H-M., Sun, J., Sappington, T. W. and Raikhel, A.S. (2003). Tissue- and stage- specific expression of two lipophorin receptor variants with seven and eight ligand-binding repeats in the adult mosquito. J. Biol. Chem. 275(¥5j:41954-41962. Siebel CW, Fresco LD, Rio DC. 1992 The mechanism of somatic inhibition of Drosophila P- element pre-mRNA splicing: multiprotein complexes at an éxon pseudo-5' splice site control Ul snRNP binding. Genes Dev. (5:1386-401. Shivikrupa, Singh., R e Swarup, G. (1999). Identification of a novel splice variant of C3G which shows tissue-specific expression. DNA Cell Biol. /5: 701-708. Smith, C, and Valcarcel, J. (2000). Alternative pre-mRNA splicing: the logic of combinatorial control. Trends Biochem Sci 25, 381-388. Stoss, O., Stoilov, P., Hartmann, A. M., Nayler, O., and Stamm, S. (1999). The in vivo minigene approach to analyze tissue-specific splicing. Brain Research Protocols 4, 383-394. Stoss, O., Olbrich, M, Hartmann, A. M., Konig, H., Memmott, J., Andreadis, A and Stamm, S. (2001). The STAR/GSG family protein rSLM-2 regulates the selection of alternative splice sites. J. Biol. Chem. 276(12):8665-8673. Streuli, M. and Saito, H. (1989). Regulation of tissue-specific alternative splicing: exon-specific cis-elements govern the splicing of leukocyte common antigen pre-mRNA. EMBO J. 8(3): 787-796. Suzuki, M., Ohbayashi, F., Mita, K., and Shimada, T. (2001). The mechanism of sex-specific splicing at the doublesex gene is different between Drosophila melanogaster and Bombyx mori. Insect Biochem MoI Biol 31, 1201-1211. Thanaraj, T., and Clark, F. (2001). Human GC-AG alternative intron isoforms with weak donor sites show enhanced consensus at acceptor exon positions. Nucleic Acids Research 29, 2581-2593. Thanaraj, T., Stamm, S., Clark, F., Reithoven, J., Le Texier, V., and Muilu, J. (2004). ASD: the Alternative Splicing Database. Nucleic Acids Research 32, D64-D69. Varshavsky, A. (2000). Ubiquitin fusion technique and its descendants. Meth Enz 327. Venables, J. (2002). Alternative splicing in the testes. Curr Opin Genet Dev 12, 615-619. Venables JP. 2004 Aberrant and alternative splicing in cancer. Cancer Res. 64(21): 7647-54. Vernooy, S.Y., Copeland, J., Ghaboosi, N., Griffin, E.E., Yoo, SJ. and Hay, BA. (2000). J. Cell Biol. 150(2):F69-¥75. White, K., Tahoaglu, E. and Steller, H. (1996). Cell killing by the Drosophila gene reaper. Science 271 (5250): 805-807. Wing, J.P., Zhou, L., Schwartz, L.M. e Nambu, J.R. (2001) Distinct cell killing properties of the Drosophila reaper, head involution defective, and grim genes. Cell Death Diffn 5(11): 930-939 YaIi Chiu A., e Pin Ouyang, A.B.,(2006).Loss of Pnn expression attenuates expression levels of SR family splicing factors and modulates alternative pre-mRNA splicing in vivo. Bioch. Biophys.Res. Comm. W:663-671. Yoshimura, K., Yabuta, Y., Ishikawa, T. e Shigeoka, S. (2002). Idenitification of a cis element for tissue-specific alternative splicing of chloroplast Ascorbate Peroxidase pre-mENA in higher plants. J. Biol.Chem 277 (43,1:40623-40632.
O seguinte refere-se aos vários plasmídeos do presente e enfatiza a posição de certos elementos aqui preferidos. <223> Sequência de pLA3359 (SEQ ID NO. 47). <***> Aspectos chaves incluem: 1. Mini-gene de Anopheles gambiae dsx (Agdsx), [um mini-gene é uma sequência recombinante derivado de um gene particular (o gene Agdsx neste exemplo) por ligação junta de segmentos não contíguos enquanto retendo a ordem 5’-3’ original; isto é equivalente para deleção de alguns segmentos internos de um fragmento mais longo de sequência genômica derivado do gene], (1-3135): incluindo parte de Agdsx de éxon3, éxon 4a (fêmea), éxon 4b (fêmea) e parte do éxon5 (macho e fêmea). < ***> éxons derivados de Agdsx de posições 426 a 560 (parte do éxon 3); 1068 a 2755 (incluindo parte do éxon 4, encontrado em fêmeas); 1809 a 2755 (incluindo parte do éxon 4, encontrado em fêmeas); e 2914 a 3135 (incluindo parte do éxon 5, encontrado em machos). < ***> Transcrito alternativamente spliced começa no segmento derivado de baculovírus AcMNPV Ie1 (prematuro imediato 1) em posição ~8031 (fragmento Ie1 é da posição 7431 a 8060). < ***> Aspecto incluído: 1. íntron adicional derivado de gene "scraps" de Drosophila (“íntron 'scraps'”) a montante da sequência Agdsx de posição 8075 a 8137. <223> Sequência de pLA3433 (SEQ ID NO. 48). <***> Aspectos chaves incluem: 1. Mini-gene de Agdsx (778-4623): incluindo parte de Agdsx do éxon 2, éxon3, éxon 4a (fêmea), éxon 4b (fêmea) e parte do éxon5 (macho e fêmea). < ***> éxons derivados de Agdsx de posição 778 a 908 (parte do éxon 2); 1913 a 2048 (parte do éxon 3); 2556 a 2642 (parte do éxon 4a); 3297 a 4243 (parte do éxon 4b) e 4402 a 4623 (parte do éxon 5). < ***> Transcrito alternativamente spliced começa no segmento derivado de baculovírus AcMNPV Ie1 (prematuro imediato 1) em posição ~606 (fragmento Ie1 é da posição 6 a 635). < ***> Aspecto incluído: 1. íntron adicional derivado de gene "scraps" de Drosophila(“íntron 'scraps'”) a montante da sequência Agdsx de posição 650 a 712. <223> Sequência de pLA3491. <***> Aspectos chaves incluem: 1. Mini-gene de Aedes aegypti dsx (Aadsx): incluindo parte de Aadsx éxon 4, éxon 5a (fêmea), éxon 5b (fêmea), e parte do éxon6 (macho e fêmea). < ***> éxons derivados de Aadsx de posição 1316 a 1450 (parte do éxon 4); 2626 a 3761 (parte do éxon 5a); 3293 a 3761 (parte do éxon 5b); e 5215 a 5704 (parte do éxon 6). < ***> Parte do transcrito F1 é previsto como compreendendo nucleotídeos ~1174-1450, 2626-3761, 5215~5850. < ***> Parte do transcrito F2 é previsto como compreendendo nucleotídeos ~1174-1450, 3293-3761, 5215-~5850. < ***> Parte do transcrito F3 é previsto como compreendendo nucleotídeos ~1174-1450, 2626-3083, 3293-3761, 5215-~5850. < ***> Parte do transcrito M1 é previsto como compreendendo nucleotídeos ~1174-1450, 5215-~5850. < ***> O transcrito alternativamente spliced começa em segmento derivado de baculovírus AcMNPV Ie1 (prematuro imediato 1) em posição ~1174 (fragmento Ie1 é de posição 574 a 1203). < ***> Aspecto incluído: 1. íntron adicional derivado de gene "scraps" de Drosophila (“íntron 'scraps'”) a montante para sequência Aadsx de posição 1218 a 1280. <223> Sequência de pLA3646. <***> Aspectos chaves incluem: 1. Mini-gene de Aadsx (17218-11707): incluindo parte de Aadsx éxon 4 de posição 17113 a 16979, éxon 5a de posição 15803 a 15025 + 14010 a 13650, éxon 5b de posição 15136 a 15025 + 14010 a 13650 e éxon 6 de posição 12196 a 11707 (nota: orientação reversa). < ***> parte do éxon 4 contém mutações de 4 pontos com relação ao tipo selvagem em posições 17087 (ATG-ACG), 17053 (ATG- ACG), 17050 (ATG-ACG) e 17041 (ATG-ACG) (nota: orientação reversa); parte do éxon 5a e 5b contém mutações de 3 pontos com relação ao tipo selvagem em posições 15129 (ATG-ATA), 15116 (ATG-ATA) e 15113 (ATG-ATA) (nota: orientação reversa). Todas destas mutações são para eliminar sequências de ATG. < ***> tTAV2 é inserido nos éxons de sobreposição 5a e 5b da posição 15024 a 14011 (nota: orientação reversa). < ***> O transcrito alternativamente spliced começa em fragmento derivado de hsp70 de posição ~17312 (fragmento hsp70 é de posição 17354 a 17225); (nota: orientação reversa). < ***> Aspecto incluído: 1. íntron adicional derivado de gene "scraps" de Drosophila (“íntron 'scraps'”) a montante da sequência Aadsx de posição 1107 a 1045 (nota: orientação reversa) Sequência de pLA3435 (SEQ ID NO. 46). <223> Aspectos chaves incluem: 1. Mini-gene de dsx Bombyx mori (Bmdsx) (1411-3161) com um ligador exógeno entre éxons 3 e 4 de fêmea fusionados. < ***> Fragmento de éxons dois compartilhados (1411bp- 1554bp) < ***> Parte de éxon três específico de fêmea (2121bp-2202) fusionado para parte de éxon 4 específico de fêmea (2225bp-2290bp) usando um ligador exógeno (2203bp-2224bp) < ***> Fragmento de éxon cinco compartilhado (3007bp- 3161bp) < ***> Produto de splicing de minigene dsx fêmea é codificado por 1411-1554 + 2121-2290 + 3007-3161. < ***> Produto de splicing de minigene dsx macho é codificado por 1411-1554 + 3007-3161. < ***> Transcrição é prevista para começar em aproximadamente posição ~1239 dentro do segmento derivado de baculovírus AcMNPV Ie1 (prematuro imediato 1) promotor (639bp-1268bp). < 223> Sequência de pLA3534. < ***> Aspectos chaves incluem: 1. Mini-gene de Aadsx (6996-4425): contendo Aadsx éxon 4, parte de éxon 5a (fêmea) e parte de éxon 5b (fêmea), inclusive de fragmentos de íntron Aadsx. < ***> éxons derivados de Aadsx de posição 6968 a 6834 (parte de éxon 4), 5462 a 4425 (parte de éxon 5a) e 4795 a 4425 (parte de éxon 5b); (nota: orientação reversa). < ***> Parte do transcrito F1 é prevista como compreendendo nucleotídeos ~7146-6834, 5462-~4300 (nota: orientação reversa). < ***> Parte do transcrito F2 é prevista como compreendendo nucleotídeos ~7146-6834, 4795-~4300 (nota: orientação reversa). < ***> Parte do transcrito F3 é prevista como compreendendo nucleotídeos ~7146-6834, 5462-5005, 4795-~4300 (nota: orientação reversa). < ***> O transcrito alternativamente spliced começa em segmento derivado de baculovírus AcMNPV Ie1 (prematuro imediato 1) em posição ~7146 (fragmento Ie1 é de posição 7746 a 7117, orientação reversa). < 223> Sequência de pLA3612. < ***> Aspectos chaves incluem: 1. Região de codificação de ubiquitina-tTAV2 inserida em um éxon fêmea de gene Aadsx. < ***> Ubiquitina-tTAV2 é de posição 15185-16429 em Aadsx (ubiquitina é de 15185-15412; tTAV2 é de 15413-16429), inclusive de códon de partida e de parada. < ***> Sequência derivada de Aadsx: 13150-15184, 16438-18805. < ***> Transcrito alternativamente spliced Aadsx-ubiquitina- tTAV2 começa em segmento derivado de hsp70 (fragmento hsp70 é de 13014-13143). < 223> Sequência de pLA3619. < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV2 inserida em um éxon fêmea de gene Aadsx. < ***> Sequência derivada de Aadsx: 5635-3641, 2610-243 (nota: orientação reversa). < ***> Transcrito alternativamente spliced Aadsx-tTAV2 começa em segmento derivado de hsp70 de 5642-5771 (nota: orientação reversa). < ***> O transcrito tTAV2 é previsto como sendo traduzido entre 2619-3635, inclusive de códon de partida e de parada (nota: orientação reversa). < 223> Sequência de pLA3545. < ***> Aspectos chaves incluem: 1. Promotor AaActin4 e 5’ UTR incluindo primeiro intron regula a expressão de tTAV. < ***> Sequência derivada de AaActin4 é de posição 923- < ***> O transcrito alternativamente spliced é previsto para começar em aproximadamente ~2366. < ***> O primeiro íntron de AaActin4 (variante de splicing fêmea) é de 2458-4259. < ***> tTAV é previsto como sendo traduzido entre 4300-5316, inclusive de códon de partida e de parada. < 223> Sequência de pLA3604. < ***> Aspectos chaves incluem: 1. Promotor AaActin4 e 5’ UTR regula expressão ubiquitina- tTAV2. < ***> Sequência derivada de AaActin4 é de posição 5795-2407 (nota: orientação reversa). < ***> O transcrito alternativamente spliced é previsto para começar em aproximadamente ~4353 (nota: orientação reversa). < ***> O primeiro íntron de AaActin4 (variante de splicing fêmea) é de 2455-4254 (nota: orientação reversa). < ***> O transcrito ubiquitina-tTAV2 é previsto como sendo traduzido a partir do códon de partida engenheirado no primeiro éxon do gene AaAct4 a 4299-4297 (ubiquitina é de 2406-2179; tTAV2 é de 2178-1162); (nota: orientação reversa). < 223> Sequência de pLA3641. < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV inserida em um éxon fêmea de gene CodlingDsx. < ***> tTAV é de posição 2731-3747 no gene CodlingDsx. < ***> Transcrito alternativamente spliced Dsx-tTAV começa em segmento derivado de hsp70 (fragmento hsp70 é de 4811-4940). < ***> O transcrito tTAV é previsto como sendo traduzido entre 2731-3747, inclusive do códon de partida e de parada (nota: orientação reversa). < 223> Sequência de pLA3570 < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV inserida em um éxon fêmea de gene PBW-Dsx. < ***> Região de codificação de tTAV é de 2336-3352. < ***> Transcrito alternativamente spliced Dsx-tTAV começa em segmento derivado de hsp70 (fragmento hsp70 é de 4683-4812). < ***> O transcrito tTAV é previsto como sendo traduzido entre 2336-3352, inclusive do códon de partida e de parada (nota: orientação reversa). < 223> Sequência de pLA1188 (SEQ ID NO. 49) < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV com íntron Cctra inserido. < ***> Íntron Cctra é de posição 3905-2561 em tTAV (nota: orientação reversa). < ***> Transcrito alternativamente spliced tTAV começa em segmento derivado de hsp70 de posição 4217 (fragmento hsp70 é de 4260-4131); (nota: orientação reversa). < ***> O transcrito tTAV F1 é previsto como sendo traduzido entre 4040-1679 (nota: orientação reversa). < ***> Aspecto incluído: 1. Íntron Adh dentro do transcrito F1 previsto de posição 4118-4049 (nota: orientação reversa). <223> Sequência de pLA3077 (SEQ ID NO. 50). <***> Aspectos chaves incluem: 1. Região de codificação de tTAV com íntron Cctra inserido. <***> Íntron Cctra é de posição 3975-2631 em tTAV (nota: orientação reversa). < ***> Transcrito alternativamente spliced tTAV começa em segmento derivado de hsp70 de posição ~4217 (fragmento hsp70 é de 4260-4131); (nota: orientação reversa). < ***> O transcrito tTAV F1 é previsto como sendo traduzido entre 4039-1678, inclusive de códon de partida e de parada (nota: orientação reversa). < ***> Aspecto incluído: 1. Íntron Adh dentro do transcrito F1 previsto de posição 4117-4048 (nota: orientação reversa). <223> Sequência de pLA3097 (SEQ ID NO. 51). <***> Aspectos chaves incluem: 1. Região de codificação de tTAV com íntron Cctra inserido. < ***> Íntron Cctra é de posição 3282-1938 em tTAV (nota: orientação reversa). < ***> Transcrito alternativamente spliced tTAV começa em segmento derivado de hsp70 de posição ~3382 (fragmento hsp70 é de 3425-3296); (nota: orientação reversa). < ***> O transcrito tTAV F1 é previsto como sendo traduzido entre 3285-924, inclusive de códon de partida e de parada (nota: orientação reversa). < 223> Sequência de pLA3233 (SEQ ID NO. 52). < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV2 com íntron Cctra inserido. < ***> Íntron Cctra é de posição 3289-1945 em tTAV2 (nota: orientação reversa). < ***> Transcrito alternativamente spliced tTAV2 começa em segmento derivado de hsp70 de posição ~3389 (fragmento hsp70 é de 34323303); (nota: orientação reversa). < ***> O transcrito tTAV2 F1 é previsto como sendo traduzido entre 3292-931, inclusive de códon de partida e de parada (nota: orientação reversa). < 223> Sequência de pLA3014 (SEQ ID NO. 53). < ***> Aspectos chaves incluem: 1. Região de codificação de ubi-reaper[KR] com íntron Cctra inserido. < ***> Íntron Cctra é de posição 3356-4700 em ubi- reaper[KR]. < ***> Transcrito alternativamente spliced ubi-reaper[KR] começa em segmento derivado de hsp70 de posição ~3234 (fragmento hsp70 é de 3191-3320). < ***> O transcrito ubi-reaper[KR] F1 é previsto como sendo traduzido entre 3331-5143, inclusive de códon de partida e de parada (ubiquitina é de 3331-3355, 4701-4948; reaper[KR] é de 4949-5143). < 223> Sequência de pLA3166 (SEQ ID NO. 54). < ***> Aspectos chaves incluem: 1. Região de codificação de ubi-reaper[KR] com íntron Cctra inserido. < ***> Íntron Cctra é de posição 9987-8643 em ubi- reaper[KR] (nota: orientação reversa). < ***> Transcrito alternativamente spliced ubi-reaper[KR] começa em segmento derivado de hsp70 de posição ~10227 (fragmento hsp70 é de 10270-10141); (nota: orientação reversa). < ***> O transcrito ubi-reaper[KR] F1 é previsto como sendo traduzido entre 10126-8359, inclusive de códon de partida e de parada (ubiquitina é de 10126-9988, 8642-8554; reaper[KR] é de 8553-8359); (nota: orientação reversa). < 223> Sequência de pLA3376 (SEQ ID NO. 55). < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV2 com íntron Cctra inserido. 2. Região de codificação de tTAV3 com íntron Bztra inserido. 3. Região de codificação de reaper[KR] com íntron Bztra inserido. < ***> Íntron Cctra é de posição 3289-1945 em tTAV2 (nota: orientação reversa). < ***> Íntron Bztra é de posição 5981-5014 em tTAV3 (nota: orientação reversa). < ***> Íntron Bztra é de posição 16391-17358 em reaper[KR]. < ***> Transcrito alternativamente spliced tTAV2 começa em segmento derivado de hsp70 de posição ~3389 (fragmento hsp70 é de 34323303); (nota: orientação reversa). < ***> Transcrito alternativamente spliced tTAV3 começa em segmento derivado de sry-alfa de posição ~6019 (fragmento sry-alfa é de 6243-5999); (nota: orientação reversa). < ***> Transcrito alternativamente spliced reaper[KR] começa em segmento derivado de hunchback de posição ~16339 (fragmento hunchback é de 16289-16372). < ***> O transcrito tTAV2 F1 é previsto como sendo traduzido entre 3292-931, inclusive de códon de partida e de parada (nota: orientação reversa). < ***> O transcrito tTAV3 F1 é previsto como sendo traduzido entre 5984-4006, inclusive de códon de partida e de parada (nota: orientação reversa). < ***> O transcrito reaper[KR] é previsto como sendo traduzido entre 16385-17550, inclusive de códon de partida e de parada. < 223> Sequência de pLA3242 (SEQ ID NO. 56). < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV com íntron Cctra inserido. < ***> Região de codificação de reaper[KR] com íntron Crtra inserido. < ***> Íntron Cctra é de posição 3282-1938 em tTAV (nota: orientação reversa). < ***> Íntron Crtra é de posição 5488-4180 em reaperKR (nota: orientação reversa). < ***> Transcrito alternativamente spliced reaperKR começa em segmento derivado de hunchback de posição ~5540 (fragmento hunchback é de 5590-5507); (nota: orientação reversa). < ***> Transcrito alternativamente spliced tTAV começa em segmento derivado de hsp70 de posição ~3382 (fragmento hsp70 é de 3425-3296); (nota: orientação reversa). < ***> O transcrito reaperKR F1 é previsto como sendo principalmente traduzido entre 4088-5494, inclusive de códon de partida e de parada (nota: orientação reversa). < ***> O transcrito tTAV F1 é previsto como sendo principalmente traduzido entre 924-3285, inclusive de códon de partida e de parada (nota: orientação reversa). < 223> Sequência de pLA1172 (SEQ ID NO. 106). < ***> Aspectos chaves incluem: 1. Região de codificação de tTAV entre fragmentos derivados de AaActin4. < ***> Fragmentos derivados de AaActin4 são de 7868-11257 e 12366-13100. < ***> O transcrito tTAV é previsto como sendo traduzido entre 11342-12358, inclusive de códon de partida e de parada. < ***> O transcrito AaActin4-tTAV é previsto para começar na posição ~9312. < ***> AaActin4 contém um íntron (variante de splice tipo fêmea) de posição 9403-11204. < 223> Sequência de pLA1038 (Fig. 12). < ***> Aspectos chaves incluem: 1. Fragmento de região de codificação de Nipp1Dm (‘nipper’) com íntron Cctra inserido com sequência exônica tra de flanqueamento. < ***> Íntron Cctra é de posição 3365-4709 em nipper. < ***> Íntron Cctra é flanqueado por sequência exônica Cctra de posições 3343-3364 e 4710-4729. < ***> Transcrito alternativamente spliced nipper começa em segmento derivado de hsp70 de posição ~3243 (fragmento hsp70 é de 3200-3329). < ***> O transcrito nipper F1 é previsto como sendo traduzido entre 3340-5014, inclusive de códon de partida e de parada. < 223> Sequência de pLA3054 (SEQ ID NO. 158). < ***> Aspectos chaves incluem: 1. Região de codificação de DsRed-ubi-tTAV com íntron Cctra inserido com sequência exônica tra de flanqueamento. < ***> Íntron Cctra é de posição 3509-2165 em DsRed-ubi- tTAV (nota: orientação reversa). < ***> Íntron Cctra é flanqueado por sequência exônica Cctra de posições 3531-3510 e 2164-2145 (nota: orientação reversa). < ***> Transcrito alternativamente spliced DsRed-ubi-tTAV começa ou em segmento derivado de hsp70 de posição ~3243 (fragmento hsp70 é de 4930-4801) ou segmento derivado de Opie2 de posição ~4353 (fragmento Opie2 é de 4795-4255); (nota: orientação reversa). < ***> O transcrito DsRed-ubi-tTAV F1 é previsto como sendo traduzido entre 4320-888, inclusive de códon de partida e de parada (DsRed é de 4212-3538; ubiquitina é de 2135-1908; tTAV é de 1907-888); (nota: orientação reversa). < 223> Sequência de pLA3056 (SEQ ID NO. 159). < ***> Aspectos chaves incluem: 1. Região de codificação de DsRed-ubi-tTAV com íntron Cctra inserido com sequência exônica tra de flanqueamento. < ***> Íntron Cctra é de posição 3731-2387 em DsRed-ubi- tTAV (nota: orientação reversa). < ***> Íntron Cctra é flanqueado por sequência exônica Cctra de posições 3753-3732 e 2386-2145 (nota: orientação reversa). < ***> Transcrito alternativamente spliced DsRed-ubi-tTAV começa ou em segmento derivado de hsp70 de posição ~5109 (fragmento hsp70 é de 5152-5023) ou segmento derivado de Opie2 de posição ~4575 (fragmento Opie2 é de 5017-4477); (nota: orientação reversa). < ***> O transcrito DsRed-ubi-tTAV F1 é previsto como sendo traduzido entre 4542-888, inclusive de códon de partida e de parada (DsRed é de 4434-3760; ubiquitina é de 2135-1908; tTAV é de 1907-888); (nota: orientação reversa). < ***> Aspecto incluído: 1. Íntron adicional derivado de gene Cctra (segundo íntron de transcrito Cctra F1) dentro do transcrito F1 previsto de posição 2222-2168 (nota: orientação reversa). <223> Sequência de pLA3488 (SEQ ID NO. 160). <***> Aspectos chaves incluem: 1. Região de codificação de TurboGreen-ubi-DsRed com íntron Cctra inserido. < ***> Íntron Cctra é de posição 2263-3607 em TurboGreen- ubi-DsRed. < ***> Transcrito alternativamente spliced TurboGreen-ubi- DsRed começa no segmento derivado de baculovírus de AcMNPV Ie1 (prematuro imediato 1) em posição ~1180 (fragmento Ie1 é de 580-1209). < ***> O transcrito TurboGreen-ubi-DsRed F1 é previsto como sendo traduzido entre 1311-4467, inclusive de códon de partida e de parada (TurboGreen é de 1311-2093; ligador SG4 é de 2094-2123; ubiquitina é de 2124-3696, inclusive de íntron Cctra; DsRed é de 3697-4467). < ***> Aspecto incluído: 1. Íntron adicional derivado de gene "scraps" de Drosophila (“íntron 'scraps'”) dentro do transcrito F1 previsto de posição 1224-1286. <223> Sequência de pLA3596 (SEQ ID NO. 145). <***> Aspectos chaves incluem: 1. Região de codificação de TurboGreen-ubi-DsRed2 com íntron Cctra inserido. < ***> Íntron Cctra é de posição 5947-7291 em TurboGreen- ubi-DsRed2. < ***> TurboGreen-ubi-DsRed2 o transcrito alternativamente spliced começa no segmento derivado de baculovírus AcMNPV Ie1 (prematuro imediato 1) em posição ~4864 (fragmento Ie1 é de 4264-4893). < ***> O transcrito TurboGreen-ubi-DsRed2 F1 é previsto como sendo traduzido entre 4995-8148, inclusive de códon de partida e de parada (TurboGreen é de 4995-5777; ligador SG4 é de 5778-5807; ubiquitina é de 5808-7380, inclusive de íntron Cctra; DsRed2 é de 7381-8151). < ***> Aspecto incluído: 1. Íntron adicional derivado de gene "scraps" de Drosophila (“intron 'scraps'”) dentro do transcrito F1 previsto de posição 4908-4970. 2. Mutação de aminoácido destinada para comparar a LA3488 de posição 7294-7296.
Claims (42)
1. Sistema de expressão de polinucleotídeos, caracterizado pelo fato de compreender: pelo menos uma sequência polinucleotídica heteróloga codificando uma proteína funcional, definida entre um códon de partida e um códon de parada, e/ou polinucleotídeos para RNA interferência (RNAi), a ser expressado em um organismo; pelo menos um promotor ligado operativamente à sequência polinucleotídica heteróloga; e pelo menos uma sequência de controle de splice que, em cooperação com um espliceossoma, é capaz de (i) mediar splicing de um transcrito de RNA da sequência de codificação para produzir um primeiro produto de RNA mensageiro (mRNA) spliced, e (ii) mediar pelo menos um splicing alternativo de referido transcrito de RNA para produzir um produto de mRNA spliced alternativamente; em que, quando a pelo menos uma sequência polinucleotídica heteróloga codifica uma proteína funcional, pelo menos um dentre os produtos de mRNA maduros compreendendo uma matriz de leitura aberta contínua (ORF) se estendendo a partir do referido códon de partida para referido códon de parada, assim definindo uma proteína, que é referida proteína funcional, ou está relacionada com referida proteína funcional por, pelo menos, uma deleção de aminoácido e que é funcional quando traduzida e, opcionalmente, sofreu uma modificação pós-translacional; em que a mediação é selecionada dentre o grupo consistindo de: mediação específica de sexo, mediação específica de estágio, mediação específica de linhagem germinal, mediação específica de tecido, e combinações das mesmas; e em que a sequência de controle de splice é derivada de um gene selecionado do grupo que consiste do gene transformer Cctra de C. capitata, o gene transformer Bztra de B. zonata, o gene transformer Crtra de C. rosa, o gene doublesex Bmdsx de B. mori, o gene doublesex Aedsx de A. aegypti, o gene doublesex Agdsx de A. gambiae, e o gene Actin-4 AeActin-4 de A. aegypti.
2. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 1, caracterizado pelo fato de que a mediação é específica do sexo.
3. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 1 ou 2, caracterizado pelo fato de que a sequência polinucleotídica a ser expressada compreende dois ou mais éxons de codificação para a proteína funcional.
4. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de que a proteína é um marcador, ou tem um efeito letal, deletério ou esterilizante.
5. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 4, caracterizado pelo fato de que a proteína tem um efeito letal resultando em esterilização.
6. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 5, caracterizado pelo fato de que o efeito letal da proteína é condicionalmente suprimível.
7. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 4, caracterizado pelo fato de que a proteína é selecionada dentre o grupo consistindo de um fator indutor de apoptose, Hid, Reaper (Rpr) e Nipp1Dm.
8. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 7, caracterizado pelo fato de que o sistema compreende pelo menos um mecanismo de retro-alimentação positivo, sendo pelo menos uma proteína funcional a ser diferencialmente expressada, via splicing alternativo, e pelo menos um promotor para o mesmo, em que um produto de um gene a ser expressado serve como um fator de controle transcricional positivo para pelo menos um promotor, e assim o produto, ou a expressão do produto, é controlável.
9. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 8, caracterizado pelo fato de que um melhorador está associado com o promotor, o produto de gene servindo para melhorar a atividade do promotor via o melhorador.
10. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 9, caracterizado pelo fato de que o fator de controle é o produto de gene tTA ou um análogo do mesmo, e em que uma ou mais das unidades de operador tetO é ligada operativamente com o promotor e é o melhorador, tTA ou seu análogo servindo para melhorar a atividade do promotor via tetO.
11. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 10, caracterizado pelo fato de que a proteína funcional é, ela mesma, um transativador transcricional, como o tTAV, tTAV2, ou tTAV3.
12. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 11, caracterizado pelo fato de que o promotor é ativado por condições ambientais, por exemplo a presença ou ausência de um fator particular como tetraciclina no sistema tet ou por variação da temperatura ambiental.
13. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 11, caracterizado pelo fato de que o promotor é selecionado dentre o grupo consistindo de promotor específico de embrião srya, ou seus homólogos, o gene de Drosophila "slow as molasses" (slam) ou seus homólogos.
14. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 13, caracterizado pelo fato de ainda compreender um melhorador.
15. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 14, caracterizado pelo fato de que a mediação de splicing alternativo é específica de sexo e a sequência de controle de splice é derivada de Cctra, Bztra, ou Crtra.
16. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 15, caracterizado pelo fato de que a sequência de controle de splice é derivada do gene transformer Cctra de mosca-do-mediterrâneo.
17. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 15, caracterizado pelo fato de que de que a sequência de controle de splice é derivada de Crtra ou Bztra.
18. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 14, caracterizado pelo fato de que a sequência de controle de splice é derivada de AeActin-4.
19. Sistema de exprssão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 14, caracterizado pelo fato de que a sequência de controle de splice é derivada de Bmdsx ou Aedsx.
20. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 18 ou 19, caracterizado pelo fato de que a sequência de controle de splice e a sequência polinucleotídica heteróloga codificando uma proteína funcional, definida entre um códon de partida e um códon de parada, e/ou polinucleotídeos para RNA interferência (RNAi), a ser expressado em um organismo, são providas na forma de uma construção de minigene ou um éxon de cassete.
21. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 4, caracterizado pelo fato de que o sistema é um plasmídeo ou construção selecionado dentre o grupo consistindo de LA3435 (SEQ ID NO: 46), LA3077 (SEQ ID NO: 50), LA3097 (SEQ ID NO: 51), LA3233 (SEQ ID NO: 52), LA3014 (SEQ ID NO: 53), LA3166 (SEQ ID NO: 54), LA3376 (SEQ ID NO: 55), LA3242 (SEQ ID NO: 56), LA3596 (SEQ ID NO: 145), LA3612 (SEQ ID NO: 152), LA3491 (SEQ ID NO: 153), LA3545 (SEQ ID NO: 155), e LA3604 (SEQ ID NO: 156).
22. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 1, caracterizado pelo fato de que o sistema compreende uma sequência de controle de splice de um plasmídeo ou construção selecionado dentre o grupo consistindo de LA3435 (SEQ ID NO: 46), LA3077 (SEQ ID NO: 50), LA3097 (SEQ ID NO: 51), LA3233 (SEQ ID NO: 52), LA3014 (SEQ ID NO: 53), LA3166 (SEQ ID NO: 54), LA3376 (SEQ ID NO: 55), LA3242 (SEQ ID NO: 56), LA3596 (SEQ ID NO: 145), LA3612 (SEQ ID NO: 152), LA3491 (SEQ ID NO: 153), LA3545 (SEQ ID NO: 155), e LA3604 (SEQ ID NO: 156).
23. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 22, caracterizado pelo fato de que o sistema é um plasmídeo ou construção selecionado dentre o grupo consistindo de LA3435 (SEQ ID NO: 46), LA3077 (SEQ ID NO: 50), LA3097 (SEQ ID NO: 51), LA3233 (SEQ ID NO: 52), LA3014 (SEQ ID NO: 53), LA3166 (SEQ ID NO: 54), LA3376 (SEQ ID NO: 55), e LA3242 (SEQ ID NO: 56).
24. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 23, caracterizado pelo fato de que pelo menos uma sequência de controle de splice é intrônica e compreende em sua extremidade 5' nucleotídeo guanina (G), em RNA.
25. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 24, caracterizado pelo fato de que pelo menos uma sequência de controle de splice é intrônica e apresenta nucleotídeos UG flanqueando sua extremidade 5' e GU flanqueando sua extremidade 3', em RNA.
26. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 25, caracterizado pelo fato de que a mediação é específica de sexo e ainda mediada ou controlada por ligação da proteína TRA ou complexo de proteína TRA/TRA2, ou homólogos das mesmas.
27. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 26, caracterizado pelo fato de que o sistema compreende a sequência de consenso: TCWWCRATCAACA (SEQ ID NO: 138), em que W = A ou T e R = A ou G.
28. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 27, caracterizado pelo fato de que o organismo é um mamífero, um peixe, um invertebrado, um artrópode, um inseto ou uma planta.
29. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 28, caracterizado pelo fato de que o organismo é um inseto da Ordem Díptera, Lepidoptera, ou Coleoptera.
30. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 29, caracterizado pelo fato de que o inseto é uma mosca tefrítida das frutas selecionada dentre o grupo consistindo de: mosca-do- mediterrâneo (Ceratis capitata), mosca mexicana das frutas (Anastrepha ludens), mosca oriental das frutas (Bactrocera dorsalis), mosca da azeitona (Bactrocera oleae), mosca do melão (Bactrocera cucurbitae), mosca das frutas do natal (Ceratitis rosa), mosca da cereja (Rhagoletis cerasi), mosca- de-queensland (Bactrocera tyroni), mosca-do-pêssego (Bactrocera zonata), mosca das frutas do Caribe (Anastrepha suspensa) e mosca das frutas da índia ocidental (Anastrepha obliqua).
31. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 29, caracterizado pelo fato de que o inseto é um mosquito dos gêneros Stegomyia, Aedes, Anopheles ou Culex.
32. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 31, caracterizado pelo fato de que o mosquito é selecionado do grupo que consiste de Aedes aegypti, Aedes albopictus, Anopheles stephenst, Anopheles albimanus e Anopheles gambiae.
33. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 29, caracterizado pelo fato de que o inseto é selecionado dentre o grupo consistindo de: verme-parafuso do Novo Mundo (Cochliomyia hominivorax), verme-parafuso do Velho Mundo (Chrysomya bezziana), mosca varejeira da ovelha australiana (Lucilia cuprina), traça das maçãs e pêras (Cydia pomonella), o bicho-da-seda (Bombyx mori), a lagarta-rosada (Pectinophora gossypiella), a lagarta da couve (Plutella xylostella), a mariposa-cigana (Lymantria díspar), a lagarta da laranja-da-baía (Amyelois transitella), a lagarta mineira do pessegueiro (Anarsia lineatella), e a broca da haste do arroz (Tryporyza incertulas), as traças noctuídas, especialmente Heliothiane, o besouro japonês (Popilla japonica), o besouro branco (Graphognatus spp.), o gorgulho do algodão (Anthonomous grandis), a lagarta da raiz do milho (Diabrotica spp), e escaravelho da batateira (Leptinotarsa decemlineata).
34. Sistema de expressão de polinucleotídeos de acordo com a reivindicação 29, caracterizado pelo fato de que o inseto não é uma drosófila.
35. Sistema de expressão de polinucleotídeos de acordo com qualquer uma das reivindicações 1 a 34, caracterizado pelo fato de que a expressão da sequência polinucleotídica heteróloga leva a uma consequência fenotípica no organismo.
36. Método de controle da população de um organismo em um meio ambiente natural para o mesmo, caracterizado pelo fato de compreender: i) reproduzir um lote de um organismo transgênico compreendendo o sistema de expressão de polinucleotídeos como definido em qualquer uma das reivindicações 1-35, que é um sistema genético letal dominante, ii) distribuir os referidos organismos transgênicos do lote no meio ambiente em um locus para controle da população; e iii) obter um controle da população através da letalidade em estágio prematuro por expressão do sistema letal na descendência que resulta da inter-reprodução dos referidos indivíduos no lote com os indivíduos do sexo oposto da população selvagem.
37. Método de acordo com a reivindicação 36, caracterizado pelo fato de que a letalidade em estágio prematuro é embriônica ou antes da maturidade sexual.
38. Método de acordo com a reivindicação 37, caracterizado pelo fato de que a letalidade em estágio prematuro ocorre de modo prematuro no desenvolvimento.
39. Método de acordo com a reivindicação 36 ou 37, caracterizado pelo fato de que o efeito letal do sistema letal é condicional e ocorre no referido meio ambiente natural via a expressão de um gene letal, a expressão de referido gene letal estando sob o controle de uma proteína de transativador reprimível, a referida reprodução ocorrendo sob condições permissivas na presença de uma substância, a substância estando ausente do referido meio ambiente natural e capaz de reprimir referido transativador.
40. Método de controle biológico, caracterizado pelo fato de compreender: i) reproduzir um lote de organismos transgênicos machos e fêmeas transformados com o sistema de expressão de polinucleotídeos como definido em qualquer uma das reivindicações 1-35, sob condições permissivas, permitindo a sobrevivência de machos transgênicos e fêmeas transgênicas, para produzir um agente de controle biológico de sexo dual; ii) opcionalmente antes da próxima etapa impor ou permitir condições restritivas para causar a morte de indivíduos transgênicos de um sexo e, assim, prover um agente de controle biológico de sexo único compreendendo indivíduos do outro sexo transportando o sistema genético letal condicional; iii) liberar o agente de controle biológico de sexo dual ou de sexo único no meio ambiente em um locus para controle biológico; e iv) obter controle biológico através da expressão do sistema genético na descendência resultante de inter-reprodução dos indivíduos transgênicos do agente de controle biológico com indivíduos do sexo oposto da população selvagem.
41. Método de separação de sexos, caracterizado pelo fato de compreender: i) reproduzir um lote de organismos transgênicos machos e fêmeas transformados com o sistema de expressão de polinucleotídeo como definido em qualquer uma das reivindicações 1 a 35 sob condições permissivas ou restritivas, permitindo a sobrevivência de machos transgênicos e fêmeas transgênicas; e ii) remover as condições permissivas ou restritivas para induzir o efeito letal do gene letal em um sexo e não no outro por splicing alternativo específico de sexo do gene letal.
42. Método ou controle biológico ou da população, caracterizado pelo fato de compreender: i) reproduzir um lote de organismos transgênicos machos e fêmeas transformados com o sistema de expressão de polinucleotídeos como definido em qualquer uma das reivindicações 1 a 35, sob condições permissivas ou restritivas, permitindo a sobrevivência de machos e fêmeas; ii) remover as condições permissivas ou restritivas para induzir o efeito letal do gene letal em um sexo e não no outro por splicing alternativo específico do sexo do gene letal para obter separação de sexos; iii) esterilizar ou parcialmente esterilizar os indivíduos transgênicos separados, e iv) obter referido controle através da liberação de indivíduos transgênicos estéreis ou parcialmente estéreis separados no meio ambiente natural do organismo.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/352,177 US9133477B2 (en) | 2003-07-28 | 2006-02-10 | Expression systems |
| US11/352177 | 2006-02-10 | ||
| GB0621234A GB2443186A (en) | 2006-10-25 | 2006-10-25 | Expression system for mediating alternative splicing |
| GB0621234.4 | 2006-10-25 | ||
| PCT/GB2007/000488 WO2007091099A1 (en) | 2006-02-10 | 2007-02-12 | Gene expression system using alternative splicing in insects |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0707579A2 BRPI0707579A2 (pt) | 2011-05-10 |
| BRPI0707579B1 true BRPI0707579B1 (pt) | 2023-01-24 |
Family
ID=37545968
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0707579-0A BRPI0707579B1 (pt) | 2006-02-10 | 2007-02-12 | Sistema de expressão de polinucleotídeos, métodos de controle da população de um organismo em um meio ambiente natural para o mesmo, de controle biológico, e de separação de sexos, e, método ou controle biológico ou da população |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US9970025B2 (pt) |
| BR (1) | BRPI0707579B1 (pt) |
| CU (1) | CU23936B1 (pt) |
| ES (1) | ES2618405T3 (pt) |
| GB (1) | GB2443186A (pt) |
| MY (1) | MY162738A (pt) |
| PT (1) | PT1984512T (pt) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2404382B (en) | 2003-07-28 | 2008-01-30 | Oxitec Ltd | Pest control |
| GB2443186A (en) | 2006-10-25 | 2008-04-30 | Oxitec Ltd | Expression system for mediating alternative splicing |
| GB2500113A (en) | 2012-03-05 | 2013-09-11 | Oxitec Ltd | Arthropod male germline gene expression system |
| GB201303932D0 (en) | 2013-03-05 | 2013-04-17 | Oxitec Ltd | Muscle actin promoter |
| GB2526867A (en) * | 2014-06-05 | 2015-12-09 | Oxitec Ltd | Gene expression system |
| JP6937309B2 (ja) | 2016-01-27 | 2021-09-22 | ジャスト−エヴォテック バイオロジックス、インコーポレイテッド | ハイブリッドプロモーターおよびその使用 |
| US11261462B2 (en) | 2016-01-27 | 2022-03-01 | Just-Evotec Biologics, Inc. | Inducible expression from transposon-based vectors and uses |
| US11098310B2 (en) | 2016-01-27 | 2021-08-24 | Just-Evotec Biologics, Inc. | Expression from transposon-based vectors and uses |
| US10494175B2 (en) | 2016-03-03 | 2019-12-03 | Simplehuman, Llc | Receptacle assemblies with motion dampers |
| US11827876B2 (en) | 2016-08-12 | 2023-11-28 | Oxitec Ltd. | Self-limiting, sex-specific gene and methods of using |
| AR117409A1 (es) | 2018-03-29 | 2021-08-04 | Oxitec Ltd | Noctuidas autolimitantes |
| CN112805009A (zh) * | 2018-08-07 | 2021-05-14 | 费城儿童医院 | 基因表达的选择性剪接调控及治疗方法 |
| MX2021001708A (es) * | 2018-08-14 | 2021-04-19 | Oxitec Ltd | Autoseleccion de artropodos machos esteriles. |
| AU2019418154B2 (en) | 2019-01-01 | 2026-01-22 | Geneneer Ltd | Gene expression elements and systems and use thereof |
| EP4103717A4 (en) * | 2020-02-12 | 2024-02-28 | The Children's Hospital of Philadelphia | COMPOSITIONS AND METHODS FOR INDUCIBLE ALTERNATIVE SPLICING REGULATION OF GENE EXPRESSION |
Family Cites Families (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5180873A (en) | 1985-04-16 | 1993-01-19 | Dna Plant Technology Corporation | Transformation of plants to introduce closely linked markers |
| GB8901677D0 (en) | 1989-01-26 | 1989-03-15 | Ici Plc | Hybrid seed production |
| US5643776A (en) | 1988-11-01 | 1997-07-01 | The Regents Of The University Of California | Insect diagnostic and control compositions |
| US5254801A (en) | 1990-12-03 | 1993-10-19 | Monsanto Company | Heterologous dominant conditional lethal gene which is a phosphonate monoester hydrolase and use thereof in plants |
| GB9216151D0 (en) | 1992-07-29 | 1992-09-09 | Ici Plc | Containment of plant germplasm |
| US6225121B1 (en) | 1992-09-14 | 2001-05-01 | Institute Of Molecular Biology And Biotechnology/Forth | Eukaryotic transposable element |
| GB9313975D0 (en) | 1993-07-06 | 1993-08-18 | Sandoz Ltd | Improvements in or relating to organic compounds |
| EG23907A (en) | 1994-08-01 | 2007-12-30 | Delta & Pine Land Co | Control of plant gene expression |
| US5670353A (en) | 1994-08-25 | 1997-09-23 | Mycogen Plant Science, Inc. | Subgenomic promoter |
| US5753434A (en) | 1995-02-10 | 1998-05-19 | The Board Of Trustees Of The Leland Stanford Junior University | Methods and compositions for altering sexual behavior |
| US5851796A (en) | 1995-06-07 | 1998-12-22 | Yale University | Autoregulatory tetracycline-regulated system for inducible gene expression in eucaryotes |
| FR2737731B1 (fr) | 1995-08-07 | 1997-10-10 | Pasteur Institut | Sequence de retroelements naturels ou synthetiques ayant pour fonction de permettre l'insertion de sequences nucleotidiques dans une cellule eucaryote |
| AUPN816196A0 (en) | 1996-02-19 | 1996-03-14 | Forbio Research Pty Ltd | Regulation of eukaryotic gene expression |
| US5773697A (en) | 1996-04-23 | 1998-06-30 | Pioneer Hi-Bred International, Inc. | Genetic constructs and methods for producing fruits with very little or diminished seed |
| EP0920521A1 (en) | 1996-08-26 | 1999-06-09 | Genencor International, Inc. | IDENTIFICATION OF AND CLONING A MOBILE TRANSPOSON FROM $i(ASPERGILLUS) |
| BR9711840A (pt) | 1996-10-01 | 1999-08-24 | Univ Georgia Res Found | Agentes de controle de insetos biolÄgico expressando os genes para toxinas de caro especificas para insetos m-todos e composi-{es |
| US7135608B1 (en) | 1997-08-28 | 2006-11-14 | The Salk Institute For Biological Studies | Site-specific recombination in eukaryotes and constructs useful therefor |
| US6338040B1 (en) | 1999-02-12 | 2002-01-08 | Agren, Inc. | Method for delaying the development in pest species of resistance to control techniques, using insurance to encourage correct uses of refuges |
| ATE532872T1 (de) | 1999-06-01 | 2011-11-15 | Univ Utah Res Found | Methode zur expression von transgene in der keimbahn von caenorhabditis elegans |
| GB2355459B (en) | 1999-11-29 | 2001-09-26 | Isis Innovation | A dominant conditional lethal genetic system |
| EP1257657A2 (en) | 2000-02-11 | 2002-11-20 | QUEEN MARY & WESTFIELD COLLEGE | Autoregulatory expression vector for gene therapy |
| AU2001265187A1 (en) | 2000-05-30 | 2001-12-11 | Baylor College Of Medicine | Chimeric viral vectors for gene therapy |
| US6962810B2 (en) | 2000-10-31 | 2005-11-08 | University Of Notre Dame Du Lac | Methods and compositions for transposition using minimal segments of the eukaryotic transformation vector piggyBac |
| US7067644B2 (en) | 2000-12-05 | 2006-06-27 | Wisconsin Alumni Research Foundation | Double transposition methods for manipulating nucleic acids |
| ITRM20010120A1 (it) | 2001-03-08 | 2002-09-08 | Univ Napoli Federico Ii | Gene cctra come strumento per produrre progenie di soli maschi nella mosca mediterranea ceratitis capitata. |
| FR2825579B1 (fr) | 2001-06-11 | 2004-07-23 | Rhobio | Methode d'obtention de plante monocotyledone contenant un gene d'interet sans sequence auxiliaire etrangere |
| US6854302B2 (en) | 2001-07-10 | 2005-02-15 | Master Lock Company | Pneumatic tool lock |
| DE10251918A1 (de) | 2002-11-08 | 2004-05-19 | Horn, Carsten, Dipl.-Biochem. Dr. | Systeme zur Erzeugung stabiler genomischer Transgen-Insertionen |
| GB2402675B (en) | 2003-05-12 | 2008-02-20 | Oxitec Ltd | Resistance dilution |
| JP4719147B2 (ja) | 2003-06-10 | 2011-07-06 | ナショナル リサーチ カウンシル オブ カナダ | クメルマイシン/ノボビオシン調節遺伝子発現系 |
| GB2403475B (en) | 2003-07-01 | 2008-02-06 | Oxitec Ltd | Stable integrands |
| GB2404382B (en) | 2003-07-28 | 2008-01-30 | Oxitec Ltd | Pest control |
| JP2007529223A (ja) * | 2004-03-15 | 2007-10-25 | バイオジェン・アイデック・エムエイ・インコーポレイテッド | 選択的スプライシングを用いて真核細胞においてポリペプチドマルチマーを発現するための方法および構築物 |
| US7563601B1 (en) | 2005-06-01 | 2009-07-21 | City Of Hope | Artificial riboswitch for controlling pre-mRNA splicing |
| GB2443186A (en) | 2006-10-25 | 2008-04-30 | Oxitec Ltd | Expression system for mediating alternative splicing |
| WO2007091099A1 (en) | 2006-02-10 | 2007-08-16 | Oxitec Limited | Gene expression system using alternative splicing in insects |
| JP2008067678A (ja) | 2006-09-15 | 2008-03-27 | Kyushu Institute Of Technology | 昆虫の減数分裂期における染色体標的組換え誘導方法 |
| CN101688246B (zh) | 2007-04-26 | 2013-09-25 | 默沙东公司 | 用于昆虫细胞的合成的表达载体 |
| EP2183277A1 (en) | 2007-07-30 | 2010-05-12 | Yissum Research Development Company Of The Hebrew University Of Jerusalem | Sex-peptides resistant to proteolytic degradation and their use in biological control of insects |
| US20110088105A1 (en) | 2008-03-20 | 2011-04-14 | Wimmer Ernst A | Development stage-specific lethality system for insect population control |
| DK3456192T3 (da) | 2008-06-27 | 2025-11-24 | Merus Nv | Anvendelse af antistof-producerende murine pattedyr for at generere antistoffer med høj affinitet |
| US8704041B2 (en) | 2009-12-30 | 2014-04-22 | Pioneer Hi Bred International Inc | Methods and compositions for targeted polynucleotide modification |
| GB2500113A (en) | 2012-03-05 | 2013-09-11 | Oxitec Ltd | Arthropod male germline gene expression system |
-
2006
- 2006-10-25 GB GB0621234A patent/GB2443186A/en not_active Withdrawn
-
2007
- 2007-02-12 MY MYPI20083026A patent/MY162738A/en unknown
- 2007-02-12 BR BRPI0707579-0A patent/BRPI0707579B1/pt active IP Right Grant
- 2007-02-12 ES ES07712717.3T patent/ES2618405T3/es active Active
- 2007-02-12 PT PT77127173T patent/PT1984512T/pt unknown
-
2008
- 2008-08-08 CU CU2008000150A patent/CU23936B1/es active IP Right Grant
-
2016
- 2016-01-08 US US14/991,825 patent/US9970025B2/en not_active Expired - Lifetime
-
2018
- 2018-05-01 US US15/968,629 patent/US10941416B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| CU23936B1 (es) | 2013-08-29 |
| US20160122780A1 (en) | 2016-05-05 |
| PT1984512T (pt) | 2017-03-13 |
| US20180251785A1 (en) | 2018-09-06 |
| BRPI0707579A2 (pt) | 2011-05-10 |
| ES2618405T3 (es) | 2017-06-21 |
| MY162738A (en) | 2017-07-14 |
| GB0621234D0 (en) | 2006-12-06 |
| US9970025B2 (en) | 2018-05-15 |
| GB2443186A (en) | 2008-04-30 |
| CU20080150A7 (es) | 2012-06-21 |
| US10941416B2 (en) | 2021-03-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2007213444B2 (en) | Gene expression system using alternative splicing in insects | |
| US10941416B2 (en) | Gene expression system using alternative splicing in insects | |
| US10844402B2 (en) | Expression systems | |
| Eckermann et al. | Hyperactive piggyBac transposase improves transformation efficiency in diverse insect species | |
| Anderson et al. | Validation of novel promoter sequences derived from two endogenous ubiquitin genes in transgenic Aedes aegypti | |
| Schetelig et al. | Male only progeny in Anastrepha suspensa by RNAi-induced sex reversion of chromosomal females | |
| BR112014021922B1 (pt) | Sistema de expressão de gene de linhagem germinativa de artrópode macho adequado, e, métodos para expressar uma proteína efetora em uma gônada ou espermatozoide, para controle da população, para administração de resistência, para controle de qualidade, e para determinar o estágio de acasalamento de um artrópode fêmea | |
| US12492404B2 (en) | Self-limiting noctuids | |
| Navarro-Payá et al. | Targeting female flight for genetic control of mosquitoes | |
| Takasu et al. | Precise genome editing in the silkworm Bombyx mori using TALENs and ds-and ssDNA donors–A practical approach | |
| Xin et al. | Transcription factor Bmsage plays a crucial role in silk gland generation in silkworm, Bombyx mori | |
| Williamson et al. | Conditional knockdown of transformer in sheep blow fly suggests a role in repression of dosage compensation and potential for population suppression | |
| BR112016028197B1 (pt) | Sequência de polinucleotídeo, construto genético para transformar um artrópode, método para gerar um artrópode transformado, método para detectar um artrópode, iniciador ou par de iniciadores, sonda para uso em um método e método de controle de uma população de artrópodes | |
| Chen et al. | Hyperactive piggyBac transposase-mediated germline transformation in the fall armyworm, Spodoptera frugiperda | |
| Strobl et al. | A universal vector concept for a direct genotyping of transgenic organisms and a systematic creation of homozygous lines | |
| BR112021002776A2 (pt) | artrópodes macho estéril de auto-seleção | |
| Warren et al. | Germline transformation of the stalk-eyed fly, Teleopsis dalmanni | |
| US20090105170A1 (en) | Multiple Heat Shock Elements | |
| HK1236990A1 (en) | Expression system | |
| Yu et al. | Mutation of a palmitoyltransferase ZDHHC18-like gene is responsible for the minute wing mutation in the silkworm (Bombyx mori) | |
| Takeda et al. | Introduction of diapause trait into the muga silkmoth, Antheraea assamensis: a scientific collaboration over the Himalayas | |
| McLaughlin | Post-transcriptional regulation of the Drosophila anterior determinant, Bicoid | |
| Hackett et al. | Functional genomics | |
| Saccone et al. | Genomics, transcriptomics and CRISPR/CAS9 gene editing approaches to investigate embryonic sex determination in insect pest Ceratitis capitata. | |
| Young | Histone Deacetylase 7 and Transcriptional Regulatory Networks of the Vascular Endothelium |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B08F | Application dismissed because of non-payment of annual fees [chapter 8.6 patent gazette] |
Free format text: REFERENTE A 3A ANUIDADE. |
|
| B08G | Application fees: restoration [chapter 8.7 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09B | Patent application refused [chapter 9.2 patent gazette] | ||
| B12B | Appeal against refusal [chapter 12.2 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 12/02/2007, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |