BRPI0807864B1 - complexo cristalino, processos de pasta fluida e de cisalhamento para a preparação do complexo cristalino e composição agrícola - Google Patents
complexo cristalino, processos de pasta fluida e de cisalhamento para a preparação do complexo cristalino e composição agrícola Download PDFInfo
- Publication number
- BRPI0807864B1 BRPI0807864B1 BRPI0807864-5A BRPI0807864A BRPI0807864B1 BR PI0807864 B1 BRPI0807864 B1 BR PI0807864B1 BR PI0807864 A BRPI0807864 A BR PI0807864A BR PI0807864 B1 BRPI0807864 B1 BR PI0807864B1
- Authority
- BR
- Brazil
- Prior art keywords
- methyl
- thiophanate
- crystalline
- crystalline complex
- compound
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 110
- 238000000034 method Methods 0.000 title claims abstract description 25
- 230000008569 process Effects 0.000 title claims abstract description 15
- 238000002360 preparation method Methods 0.000 title claims abstract description 9
- 239000002002 slurry Substances 0.000 title description 11
- 229940126062 Compound A Drugs 0.000 claims abstract description 66
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 claims abstract description 66
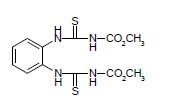
- 239000005842 Thiophanate-methyl Substances 0.000 claims abstract description 27
- 150000002894 organic compounds Chemical class 0.000 claims abstract description 19
- QGHREAKMXXNCOA-UHFFFAOYSA-N thiophanate-methyl Chemical compound COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC QGHREAKMXXNCOA-UHFFFAOYSA-N 0.000 claims description 125
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 45
- 239000007788 liquid Substances 0.000 claims description 35
- ZMYFCFLJBGAQRS-IRXDYDNUSA-N (2R,3S)-epoxiconazole Chemical compound C1=CC(F)=CC=C1[C@@]1(CN2N=CN=C2)[C@H](C=2C(=CC=CC=2)Cl)O1 ZMYFCFLJBGAQRS-IRXDYDNUSA-N 0.000 claims description 34
- 239000002245 particle Substances 0.000 claims description 34
- 239000005767 Epoxiconazole Substances 0.000 claims description 33
- 239000005869 Pyraclostrobin Substances 0.000 claims description 33
- HZRSNVGNWUDEFX-UHFFFAOYSA-N pyraclostrobin Chemical compound COC(=O)N(OC)C1=CC=CC=C1COC1=NN(C=2C=CC(Cl)=CC=2)C=C1 HZRSNVGNWUDEFX-UHFFFAOYSA-N 0.000 claims description 33
- 239000005868 Metconazole Substances 0.000 claims description 25
- XWPZUHJBOLQNMN-UHFFFAOYSA-N metconazole Chemical compound C1=NC=NN1CC1(O)C(C)(C)CCC1CC1=CC=C(Cl)C=C1 XWPZUHJBOLQNMN-UHFFFAOYSA-N 0.000 claims description 25
- 239000002904 solvent Substances 0.000 claims description 20
- 239000000843 powder Substances 0.000 claims description 19
- 239000003960 organic solvent Substances 0.000 claims description 17
- 229910052799 carbon Inorganic materials 0.000 claims description 14
- 230000015572 biosynthetic process Effects 0.000 claims description 12
- 239000000725 suspension Substances 0.000 claims description 6
- 239000007900 aqueous suspension Substances 0.000 claims description 5
- 230000005855 radiation Effects 0.000 claims description 5
- 239000000470 constituent Substances 0.000 claims description 3
- 239000012530 fluid Substances 0.000 claims description 3
- 239000001257 hydrogen Substances 0.000 abstract description 34
- 229910052739 hydrogen Inorganic materials 0.000 abstract description 34
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 abstract description 14
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 78
- -1 sprinkles Substances 0.000 description 73
- 238000009472 formulation Methods 0.000 description 44
- 150000001875 compounds Chemical class 0.000 description 41
- 239000013078 crystal Substances 0.000 description 37
- 235000013339 cereals Nutrition 0.000 description 32
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 28
- 239000004546 suspension concentrate Substances 0.000 description 28
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 27
- 240000007594 Oryza sativa Species 0.000 description 27
- 235000007164 Oryza sativa Nutrition 0.000 description 27
- 235000009566 rice Nutrition 0.000 description 27
- 235000010469 Glycine max Nutrition 0.000 description 25
- 150000003254 radicals Chemical class 0.000 description 25
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 24
- 239000007787 solid Substances 0.000 description 23
- 229920000742 Cotton Polymers 0.000 description 21
- 241000219146 Gossypium Species 0.000 description 21
- 239000002270 dispersing agent Substances 0.000 description 21
- 244000068988 Glycine max Species 0.000 description 20
- 241000196324 Embryophyta Species 0.000 description 19
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 17
- 240000008042 Zea mays Species 0.000 description 15
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 15
- 239000000049 pigment Substances 0.000 description 15
- 238000000634 powder X-ray diffraction Methods 0.000 description 15
- 239000002609 medium Substances 0.000 description 14
- 239000000654 additive Substances 0.000 description 13
- 235000014113 dietary fatty acids Nutrition 0.000 description 13
- 239000000194 fatty acid Substances 0.000 description 13
- 229930195729 fatty acid Natural products 0.000 description 13
- 238000000227 grinding Methods 0.000 description 13
- 229910052736 halogen Inorganic materials 0.000 description 13
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 12
- 150000002367 halogens Chemical class 0.000 description 12
- 239000000126 substance Substances 0.000 description 12
- 239000004094 surface-active agent Substances 0.000 description 12
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 11
- 239000002178 crystalline material Substances 0.000 description 11
- 239000006185 dispersion Substances 0.000 description 11
- 239000000417 fungicide Substances 0.000 description 11
- 235000011187 glycerol Nutrition 0.000 description 11
- 125000005843 halogen group Chemical group 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 10
- 239000000975 dye Substances 0.000 description 10
- 238000002844 melting Methods 0.000 description 10
- 230000008018 melting Effects 0.000 description 10
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 description 9
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 9
- 210000004027 cell Anatomy 0.000 description 9
- 235000005822 corn Nutrition 0.000 description 9
- 229920001223 polyethylene glycol Polymers 0.000 description 9
- 239000000523 sample Substances 0.000 description 9
- 239000000230 xanthan gum Substances 0.000 description 9
- 229920001285 xanthan gum Polymers 0.000 description 9
- 235000010493 xanthan gum Nutrition 0.000 description 9
- 229940082509 xanthan gum Drugs 0.000 description 9
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 8
- 229920001577 copolymer Polymers 0.000 description 8
- 229920001451 polypropylene glycol Polymers 0.000 description 8
- 125000004767 (C1-C4) haloalkoxy group Chemical group 0.000 description 7
- 241000219310 Beta vulgaris subsp. vulgaris Species 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- 241000233866 Fungi Species 0.000 description 7
- 241000238631 Hexapoda Species 0.000 description 7
- 239000002202 Polyethylene glycol Substances 0.000 description 7
- 235000021536 Sugar beet Nutrition 0.000 description 7
- 239000000853 adhesive Substances 0.000 description 7
- 230000001070 adhesive effect Effects 0.000 description 7
- 239000007798 antifreeze agent Substances 0.000 description 7
- 235000013877 carbamide Nutrition 0.000 description 7
- 239000000084 colloidal system Substances 0.000 description 7
- 239000012141 concentrate Substances 0.000 description 7
- 238000005384 cross polarization magic-angle spinning Methods 0.000 description 7
- 150000004665 fatty acids Chemical class 0.000 description 7
- 125000000623 heterocyclic group Chemical group 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 238000005259 measurement Methods 0.000 description 7
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 7
- YFNCATAIYKQPOO-UHFFFAOYSA-N thiophanate Chemical compound CCOC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OCC YFNCATAIYKQPOO-UHFFFAOYSA-N 0.000 description 7
- 235000013311 vegetables Nutrition 0.000 description 7
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 6
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 241000244206 Nematoda Species 0.000 description 6
- 229910019142 PO4 Inorganic materials 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 241000209140 Triticum Species 0.000 description 6
- 235000021307 Triticum Nutrition 0.000 description 6
- 235000016383 Zea mays subsp huehuetenangensis Nutrition 0.000 description 6
- 239000002253 acid Substances 0.000 description 6
- 125000000129 anionic group Chemical group 0.000 description 6
- 239000004202 carbamide Substances 0.000 description 6
- 238000010790 dilution Methods 0.000 description 6
- 239000012895 dilution Substances 0.000 description 6
- 238000001035 drying Methods 0.000 description 6
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 6
- 235000009973 maize Nutrition 0.000 description 6
- 235000021317 phosphate Nutrition 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- 238000003860 storage Methods 0.000 description 6
- PPDBOQMNKNNODG-NTEUORMPSA-N (5E)-5-(4-chlorobenzylidene)-2,2-dimethyl-1-(1,2,4-triazol-1-ylmethyl)cyclopentanol Chemical compound C1=NC=NN1CC1(O)C(C)(C)CC\C1=C/C1=CC=C(Cl)C=C1 PPDBOQMNKNNODG-NTEUORMPSA-N 0.000 description 5
- 239000004375 Dextrin Substances 0.000 description 5
- 229920001353 Dextrin Polymers 0.000 description 5
- 239000004372 Polyvinyl alcohol Substances 0.000 description 5
- 244000061456 Solanum tuberosum Species 0.000 description 5
- 235000002595 Solanum tuberosum Nutrition 0.000 description 5
- 238000002441 X-ray diffraction Methods 0.000 description 5
- 230000000895 acaricidal effect Effects 0.000 description 5
- 239000000642 acaricide Substances 0.000 description 5
- 229910052783 alkali metal Inorganic materials 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 239000002518 antifoaming agent Substances 0.000 description 5
- 125000004429 atom Chemical group 0.000 description 5
- 125000004432 carbon atom Chemical group C* 0.000 description 5
- 229920002678 cellulose Polymers 0.000 description 5
- 239000004927 clay Substances 0.000 description 5
- 239000013530 defoamer Substances 0.000 description 5
- 235000019425 dextrin Nutrition 0.000 description 5
- 238000000113 differential scanning calorimetry Methods 0.000 description 5
- NALBLJLOBICXRH-UHFFFAOYSA-N dinitrogen monohydride Chemical group N=[N] NALBLJLOBICXRH-UHFFFAOYSA-N 0.000 description 5
- 235000019441 ethanol Nutrition 0.000 description 5
- 239000000945 filler Substances 0.000 description 5
- 239000002917 insecticide Substances 0.000 description 5
- 239000002736 nonionic surfactant Substances 0.000 description 5
- 229920002451 polyvinyl alcohol Polymers 0.000 description 5
- 235000012015 potatoes Nutrition 0.000 description 5
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 5
- 238000001228 spectrum Methods 0.000 description 5
- 238000002411 thermogravimetry Methods 0.000 description 5
- 239000000080 wetting agent Substances 0.000 description 5
- WHOZNOZYMBRCBL-OUKQBFOZSA-N (2E)-2-Tetradecenal Chemical compound CCCCCCCCCCC\C=C\C=O WHOZNOZYMBRCBL-OUKQBFOZSA-N 0.000 description 4
- 240000002791 Brassica napus Species 0.000 description 4
- 235000004977 Brassica sinapistrum Nutrition 0.000 description 4
- 241000489975 Diabrotica Species 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- 239000001692 EU approved anti-caking agent Substances 0.000 description 4
- 241000208818 Helianthus Species 0.000 description 4
- 235000003222 Helianthus annuus Nutrition 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 241000460671 Promecops Species 0.000 description 4
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 4
- 241000950030 Sternechus Species 0.000 description 4
- 239000005859 Triticonazole Substances 0.000 description 4
- 150000001340 alkali metals Chemical class 0.000 description 4
- 150000005215 alkyl ethers Chemical class 0.000 description 4
- 125000000217 alkyl group Chemical group 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 239000003945 anionic surfactant Substances 0.000 description 4
- 239000003139 biocide Substances 0.000 description 4
- 229920001400 block copolymer Polymers 0.000 description 4
- 235000010980 cellulose Nutrition 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- XCJYREBRNVKWGJ-UHFFFAOYSA-N copper(II) phthalocyanine Chemical compound [Cu+2].C12=CC=CC=C2C(N=C2[N-]C(C3=CC=CC=C32)=N2)=NC1=NC([C]1C=CC=CC1=1)=NC=1N=C1[C]3C=CC=CC3=C2[N-]1 XCJYREBRNVKWGJ-UHFFFAOYSA-N 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 239000003995 emulsifying agent Substances 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 235000013312 flour Nutrition 0.000 description 4
- 238000002329 infrared spectrum Methods 0.000 description 4
- 239000012669 liquid formulation Substances 0.000 description 4
- 239000006194 liquid suspension Substances 0.000 description 4
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 4
- 125000004430 oxygen atom Chemical group O* 0.000 description 4
- 229940044654 phenolsulfonic acid Drugs 0.000 description 4
- 239000004014 plasticizer Substances 0.000 description 4
- 229920000151 polyglycol Polymers 0.000 description 4
- 239000010695 polyglycol Substances 0.000 description 4
- 239000003755 preservative agent Substances 0.000 description 4
- 230000001681 protective effect Effects 0.000 description 4
- 235000018102 proteins Nutrition 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 239000002562 thickening agent Substances 0.000 description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 3
- 125000003626 1,2,4-triazol-1-yl group Chemical group [*]N1N=C([H])N=C1[H] 0.000 description 3
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 3
- ZOCSXAVNDGMNBV-UHFFFAOYSA-N 5-amino-1-[2,6-dichloro-4-(trifluoromethyl)phenyl]-4-[(trifluoromethyl)sulfinyl]-1H-pyrazole-3-carbonitrile Chemical compound NC1=C(S(=O)C(F)(F)F)C(C#N)=NN1C1=C(Cl)C=C(C(F)(F)F)C=C1Cl ZOCSXAVNDGMNBV-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- 241000238421 Arthropoda Species 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- 229920000089 Cyclic olefin copolymer Polymers 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- 239000005899 Fipronil Substances 0.000 description 3
- 239000005785 Fluquinconazole Substances 0.000 description 3
- 239000004166 Lanolin Substances 0.000 description 3
- 244000070406 Malus silvestris Species 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 229920000881 Modified starch Polymers 0.000 description 3
- 240000005561 Musa balbisiana Species 0.000 description 3
- 235000018290 Musa x paradisiaca Nutrition 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 208000002193 Pain Diseases 0.000 description 3
- 239000005820 Prochloraz Substances 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- 241000228453 Pyrenophora Species 0.000 description 3
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 3
- 229920002125 Sokalan® Polymers 0.000 description 3
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 3
- 241000722133 Tilletia Species 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 235000021016 apples Nutrition 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 239000004359 castor oil Substances 0.000 description 3
- 235000019438 castor oil Nutrition 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 238000005388 cross polarization Methods 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 229940013764 fipronil Drugs 0.000 description 3
- IJJVMEJXYNJXOJ-UHFFFAOYSA-N fluquinconazole Chemical compound C=1C=C(Cl)C=C(Cl)C=1N1C(=O)C2=CC(F)=CC=C2N=C1N1C=NC=N1 IJJVMEJXYNJXOJ-UHFFFAOYSA-N 0.000 description 3
- 230000004927 fusion Effects 0.000 description 3
- 150000004676 glycans Chemical class 0.000 description 3
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 3
- 239000004519 grease Substances 0.000 description 3
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 3
- 235000019388 lanolin Nutrition 0.000 description 3
- 229940039717 lanolin Drugs 0.000 description 3
- 239000007791 liquid phase Substances 0.000 description 3
- 239000011976 maleic acid Substances 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- WSFSSNUMVMOOMR-NJFSPNSNSA-N methanone Chemical compound O=[14CH2] WSFSSNUMVMOOMR-NJFSPNSNSA-N 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 235000019426 modified starch Nutrition 0.000 description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 description 3
- 239000003002 pH adjusting agent Substances 0.000 description 3
- 238000004806 packaging method and process Methods 0.000 description 3
- 230000010287 polarization Effects 0.000 description 3
- 229920000058 polyacrylate Polymers 0.000 description 3
- 229920001282 polysaccharide Polymers 0.000 description 3
- 239000005017 polysaccharide Substances 0.000 description 3
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 3
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 3
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 3
- TVLSRXXIMLFWEO-UHFFFAOYSA-N prochloraz Chemical compound C1=CN=CN1C(=O)N(CCC)CCOC1=C(Cl)C=C(Cl)C=C1Cl TVLSRXXIMLFWEO-UHFFFAOYSA-N 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 229910052710 silicon Inorganic materials 0.000 description 3
- 239000010703 silicon Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 239000003381 stabilizer Substances 0.000 description 3
- 150000003852 triazoles Chemical group 0.000 description 3
- 238000009736 wetting Methods 0.000 description 3
- KAATUXNTWXVJKI-NSHGMRRFSA-N (1R)-cis-(alphaS)-cypermethrin Chemical compound CC1(C)[C@@H](C=C(Cl)Cl)[C@H]1C(=O)O[C@H](C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 KAATUXNTWXVJKI-NSHGMRRFSA-N 0.000 description 2
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 2
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 description 2
- PGOOBECODWQEAB-UHFFFAOYSA-N (E)-clothianidin Chemical compound [O-][N+](=O)\N=C(/NC)NCC1=CN=C(Cl)S1 PGOOBECODWQEAB-UHFFFAOYSA-N 0.000 description 2
- 125000001305 1,2,4-triazol-3-yl group Chemical group [H]N1N=C([*])N=C1[H] 0.000 description 2
- PXMNMQRDXWABCY-UHFFFAOYSA-N 1-(4-chlorophenyl)-4,4-dimethyl-3-(1H-1,2,4-triazol-1-ylmethyl)pentan-3-ol Chemical compound C1=NC=NN1CC(O)(C(C)(C)C)CCC1=CC=C(Cl)C=C1 PXMNMQRDXWABCY-UHFFFAOYSA-N 0.000 description 2
- PZBPKYOVPCNPJY-UHFFFAOYSA-N 1-[2-(allyloxy)-2-(2,4-dichlorophenyl)ethyl]imidazole Chemical compound ClC1=CC(Cl)=CC=C1C(OCC=C)CN1C=NC=C1 PZBPKYOVPCNPJY-UHFFFAOYSA-N 0.000 description 2
- FXNDIJDIPNCZQJ-UHFFFAOYSA-N 2,4,4-trimethylpent-1-ene Chemical compound CC(=C)CC(C)(C)C FXNDIJDIPNCZQJ-UHFFFAOYSA-N 0.000 description 2
- OVSKIKFHRZPJSS-UHFFFAOYSA-N 2,4-D Chemical compound OC(=O)COC1=CC=C(Cl)C=C1Cl OVSKIKFHRZPJSS-UHFFFAOYSA-N 0.000 description 2
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 2
- 239000003148 4 aminobutyric acid receptor blocking agent Substances 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- 229920002126 Acrylic acid copolymer Polymers 0.000 description 2
- 239000005995 Aluminium silicate Substances 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- 101100097467 Arabidopsis thaliana SYD gene Proteins 0.000 description 2
- 241001373565 Ascochyta sp. Species 0.000 description 2
- 244000003416 Asparagus officinalis Species 0.000 description 2
- 235000005340 Asparagus officinalis Nutrition 0.000 description 2
- 235000000832 Ayote Nutrition 0.000 description 2
- 239000005730 Azoxystrobin Substances 0.000 description 2
- 125000003830 C1- C4 alkylcarbonylamino group Chemical group 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- TWFZGCMQGLPBSX-UHFFFAOYSA-N Carbendazim Natural products C1=CC=C2NC(NC(=O)OC)=NC2=C1 TWFZGCMQGLPBSX-UHFFFAOYSA-N 0.000 description 2
- 102000011632 Caseins Human genes 0.000 description 2
- 108010076119 Caseins Proteins 0.000 description 2
- 241000252254 Catostomidae Species 0.000 description 2
- 241001157813 Cercospora Species 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- 239000005888 Clothianidin Substances 0.000 description 2
- 241000254173 Coleoptera Species 0.000 description 2
- 241000617784 Corynespora sp. Species 0.000 description 2
- 240000008067 Cucumis sativus Species 0.000 description 2
- 241000219122 Cucurbita Species 0.000 description 2
- 235000009854 Cucurbita moschata Nutrition 0.000 description 2
- 235000009804 Cucurbita pepo subsp pepo Nutrition 0.000 description 2
- 241001558166 Curvularia sp. Species 0.000 description 2
- 239000005946 Cypermethrin Substances 0.000 description 2
- 241000916723 Diabrotica longicornis Species 0.000 description 2
- 241000916731 Diabrotica speciosa Species 0.000 description 2
- 241000489977 Diabrotica virgifera Species 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 241000839434 Diplodia sp. Species 0.000 description 2
- 241000400699 Elasmopalpus Species 0.000 description 2
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 241000223218 Fusarium Species 0.000 description 2
- 240000005979 Hordeum vulgare Species 0.000 description 2
- 235000007340 Hordeum vulgare Nutrition 0.000 description 2
- 239000005795 Imazalil Substances 0.000 description 2
- 239000005906 Imidacloprid Substances 0.000 description 2
- 239000005909 Kieselgur Substances 0.000 description 2
- 241000255777 Lepidoptera Species 0.000 description 2
- 229920001732 Lignosulfonate Polymers 0.000 description 2
- 235000007688 Lycopersicon esculentum Nutrition 0.000 description 2
- 241001143352 Meloidogyne Species 0.000 description 2
- 239000005807 Metalaxyl Substances 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- 241001207509 Phoma sp. Species 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 241001640279 Phyllophaga Species 0.000 description 2
- 241001281803 Plasmopara viticola Species 0.000 description 2
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 101100495925 Schizosaccharomyces pombe (strain 972 / ATCC 24843) chr3 gene Proteins 0.000 description 2
- 241001207471 Septoria sp. Species 0.000 description 2
- 240000003768 Solanum lycopersicum Species 0.000 description 2
- 239000005839 Tebuconazole Substances 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 239000005941 Thiamethoxam Substances 0.000 description 2
- 241000743436 Ustilago sp. Species 0.000 description 2
- 229920004482 WACKER® Polymers 0.000 description 2
- 241000607479 Yersinia pestis Species 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- 241001360088 Zymoseptoria tritici Species 0.000 description 2
- ORILYTVJVMAKLC-UHFFFAOYSA-N adamantane Chemical compound C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 150000001342 alkaline earth metals Chemical class 0.000 description 2
- 125000003545 alkoxy group Chemical group 0.000 description 2
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 2
- 235000012211 aluminium silicate Nutrition 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 150000003863 ammonium salts Chemical class 0.000 description 2
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 2
- 239000001166 ammonium sulphate Substances 0.000 description 2
- 235000011130 ammonium sulphate Nutrition 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- WFDXOXNFNRHQEC-GHRIWEEISA-N azoxystrobin Chemical compound CO\C=C(\C(=O)OC)C1=CC=CC=C1OC1=CC(OC=2C(=CC=CC=2)C#N)=NC=N1 WFDXOXNFNRHQEC-GHRIWEEISA-N 0.000 description 2
- 235000012216 bentonite Nutrition 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- 125000003739 carbamimidoyl group Chemical group C(N)(=N)* 0.000 description 2
- 239000006013 carbendazim Substances 0.000 description 2
- JNPZQRQPIHJYNM-UHFFFAOYSA-N carbendazim Chemical compound C1=C[CH]C2=NC(NC(=O)OC)=NC2=C1 JNPZQRQPIHJYNM-UHFFFAOYSA-N 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 125000005518 carboxamido group Chemical group 0.000 description 2
- 239000005018 casein Substances 0.000 description 2
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 2
- 235000021240 caseins Nutrition 0.000 description 2
- 229920003086 cellulose ether Polymers 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000002447 crystallographic data Methods 0.000 description 2
- 125000004093 cyano group Chemical group *C#N 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- BGTOWKSIORTVQH-UHFFFAOYSA-N cyclopentanone Chemical compound O=C1CCCC1 BGTOWKSIORTVQH-UHFFFAOYSA-N 0.000 description 2
- 229960005424 cypermethrin Drugs 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 239000000539 dimer Substances 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 238000002296 dynamic light scattering Methods 0.000 description 2
- 235000013399 edible fruits Nutrition 0.000 description 2
- 229960002125 enilconazole Drugs 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 239000003925 fat Substances 0.000 description 2
- 150000002191 fatty alcohols Chemical class 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 230000000855 fungicidal effect Effects 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 239000004009 herbicide Substances 0.000 description 2
- 238000000265 homogenisation Methods 0.000 description 2
- 150000002431 hydrogen Chemical class 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 229940056881 imidacloprid Drugs 0.000 description 2
- YWTYJOPNNQFBPC-UHFFFAOYSA-N imidacloprid Chemical compound [O-][N+](=O)\N=C1/NCCN1CC1=CC=C(Cl)N=C1 YWTYJOPNNQFBPC-UHFFFAOYSA-N 0.000 description 2
- 125000003037 imidazol-2-yl group Chemical group [H]N1C([*])=NC([H])=C1[H] 0.000 description 2
- MTNDZQHUAFNZQY-UHFFFAOYSA-N imidazoline Chemical compound C1CN=CN1 MTNDZQHUAFNZQY-UHFFFAOYSA-N 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 229910052500 inorganic mineral Inorganic materials 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 2
- 239000006028 limestone Substances 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- ZQEIXNIJLIKNTD-UHFFFAOYSA-N methyl N-(2,6-dimethylphenyl)-N-(methoxyacetyl)alaninate Chemical compound COCC(=O)N(C(C)C(=O)OC)C1=C(C)C=CC=C1C ZQEIXNIJLIKNTD-UHFFFAOYSA-N 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 239000011707 mineral Substances 0.000 description 2
- PSZYNBSKGUBXEH-UHFFFAOYSA-N naphthalene-1-sulfonic acid Chemical class C1=CC=C2C(S(=O)(=O)O)=CC=CC2=C1 PSZYNBSKGUBXEH-UHFFFAOYSA-N 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 235000019198 oils Nutrition 0.000 description 2
- 239000000575 pesticide Substances 0.000 description 2
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 2
- 229940099800 pigment red 48 Drugs 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920005646 polycarboxylate Polymers 0.000 description 2
- 229920005862 polyol Polymers 0.000 description 2
- 150000003077 polyols Chemical class 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- ULWHHBHJGPPBCO-UHFFFAOYSA-N propane-1,1-diol Chemical compound CCC(O)O ULWHHBHJGPPBCO-UHFFFAOYSA-N 0.000 description 2
- 235000015136 pumpkin Nutrition 0.000 description 2
- 125000004353 pyrazol-1-yl group Chemical group [H]C1=NN(*)C([H])=C1[H] 0.000 description 2
- 125000004289 pyrazol-3-yl group Chemical group [H]N1N=C(*)C([H])=C1[H] 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 238000010008 shearing Methods 0.000 description 2
- 239000000377 silicon dioxide Substances 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N succinic acid Chemical compound OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- 150000003871 sulfonates Chemical class 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 229920001169 thermoplastic Polymers 0.000 description 2
- NWWZPOKUUAIXIW-FLIBITNWSA-N thiamethoxam Chemical compound [O-][N+](=O)\N=C/1N(C)COCN\1CC1=CN=C(Cl)S1 NWWZPOKUUAIXIW-FLIBITNWSA-N 0.000 description 2
- 125000001425 triazolyl group Chemical group 0.000 description 2
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000008158 vegetable oil Chemical class 0.000 description 2
- 238000001238 wet grinding Methods 0.000 description 2
- SNICXCGAKADSCV-JTQLQIEISA-N (-)-Nicotine Chemical compound CN1CCC[C@H]1C1=CC=CN=C1 SNICXCGAKADSCV-JTQLQIEISA-N 0.000 description 1
- CXBMCYHAMVGWJQ-CABCVRRESA-N (1,3-dioxo-4,5,6,7-tetrahydroisoindol-2-yl)methyl (1r,3r)-2,2-dimethyl-3-(2-methylprop-1-enyl)cyclopropane-1-carboxylate Chemical compound CC1(C)[C@H](C=C(C)C)[C@H]1C(=O)OCN1C(=O)C(CCCC2)=C2C1=O CXBMCYHAMVGWJQ-CABCVRRESA-N 0.000 description 1
- FJDPATXIBIBRIM-QFMSAKRMSA-N (1R)-trans-cyphenothrin Chemical compound CC1(C)[C@H](C=C(C)C)[C@H]1C(=O)OC(C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 FJDPATXIBIBRIM-QFMSAKRMSA-N 0.000 description 1
- SBNFWQZLDJGRLK-RTWAWAEBSA-N (1R)-trans-phenothrin Chemical compound CC1(C)[C@H](C=C(C)C)[C@H]1C(=O)OCC1=CC=CC(OC=2C=CC=CC=2)=C1 SBNFWQZLDJGRLK-RTWAWAEBSA-N 0.000 description 1
- ZXQYGBMAQZUVMI-RDDWSQKMSA-N (1S)-cis-(alphaR)-cyhalothrin Chemical compound CC1(C)[C@H](\C=C(/Cl)C(F)(F)F)[C@@H]1C(=O)O[C@@H](C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 ZXQYGBMAQZUVMI-RDDWSQKMSA-N 0.000 description 1
- NHOWDZOIZKMVAI-UHFFFAOYSA-N (2-chlorophenyl)(4-chlorophenyl)pyrimidin-5-ylmethanol Chemical compound C=1N=CN=CC=1C(C=1C(=CC=CC=1)Cl)(O)C1=CC=C(Cl)C=C1 NHOWDZOIZKMVAI-UHFFFAOYSA-N 0.000 description 1
- SAPGTCDSBGMXCD-UHFFFAOYSA-N (2-chlorophenyl)-(4-fluorophenyl)-pyrimidin-5-ylmethanol Chemical compound C=1N=CN=CC=1C(C=1C(=CC=CC=1)Cl)(O)C1=CC=C(F)C=C1 SAPGTCDSBGMXCD-UHFFFAOYSA-N 0.000 description 1
- WCXDHFDTOYPNIE-RIYZIHGNSA-N (E)-acetamiprid Chemical compound N#C/N=C(\C)N(C)CC1=CC=C(Cl)N=C1 WCXDHFDTOYPNIE-RIYZIHGNSA-N 0.000 description 1
- HOKKPVIRMVDYPB-UVTDQMKNSA-N (Z)-thiacloprid Chemical compound C1=NC(Cl)=CC=C1CN1C(=N/C#N)/SCC1 HOKKPVIRMVDYPB-UVTDQMKNSA-N 0.000 description 1
- CKPCAYZTYMHQEX-NBVRZTHBSA-N (e)-1-(2,4-dichlorophenyl)-n-methoxy-2-pyridin-3-ylethanimine Chemical compound C=1C=C(Cl)C=C(Cl)C=1C(=N/OC)/CC1=CC=CN=C1 CKPCAYZTYMHQEX-NBVRZTHBSA-N 0.000 description 1
- JLHMJWHSBYZWJJ-UHFFFAOYSA-N 1,2-thiazole 1-oxide Chemical class O=S1C=CC=N1 JLHMJWHSBYZWJJ-UHFFFAOYSA-N 0.000 description 1
- BGJSXRVXTHVRSN-UHFFFAOYSA-N 1,3,5-trioxane Chemical compound C1OCOCO1 BGJSXRVXTHVRSN-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- JWUCHKBSVLQQCO-UHFFFAOYSA-N 1-(2-fluorophenyl)-1-(4-fluorophenyl)-2-(1H-1,2,4-triazol-1-yl)ethanol Chemical compound C=1C=C(F)C=CC=1C(C=1C(=CC=CC=1)F)(O)CN1C=NC=N1 JWUCHKBSVLQQCO-UHFFFAOYSA-N 0.000 description 1
- WDQFELCEOPFLCZ-UHFFFAOYSA-N 1-(2-hydroxyethyl)pyrrolidin-2-one Chemical compound OCCN1CCCC1=O WDQFELCEOPFLCZ-UHFFFAOYSA-N 0.000 description 1
- WURBVZBTWMNKQT-UHFFFAOYSA-N 1-(4-chlorophenoxy)-3,3-dimethyl-1-(1,2,4-triazol-1-yl)butan-2-one Chemical compound C1=NC=NN1C(C(=O)C(C)(C)C)OC1=CC=C(Cl)C=C1 WURBVZBTWMNKQT-UHFFFAOYSA-N 0.000 description 1
- VGPIBGGRCVEHQZ-UHFFFAOYSA-N 1-(biphenyl-4-yloxy)-3,3-dimethyl-1-(1,2,4-triazol-1-yl)butan-2-ol Chemical compound C1=NC=NN1C(C(O)C(C)(C)C)OC(C=C1)=CC=C1C1=CC=CC=C1 VGPIBGGRCVEHQZ-UHFFFAOYSA-N 0.000 description 1
- ZFPGARUNNKGOBB-UHFFFAOYSA-N 1-Ethyl-2-pyrrolidinone Chemical compound CCN1CCCC1=O ZFPGARUNNKGOBB-UHFFFAOYSA-N 0.000 description 1
- LQDARGUHUSPFNL-UHFFFAOYSA-N 1-[2-(2,4-dichlorophenyl)-3-(1,1,2,2-tetrafluoroethoxy)propyl]1,2,4-triazole Chemical compound C=1C=C(Cl)C=C(Cl)C=1C(COC(F)(F)C(F)F)CN1C=NC=N1 LQDARGUHUSPFNL-UHFFFAOYSA-N 0.000 description 1
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 1
- GHELJWBGTIKZQW-UHFFFAOYSA-N 1-propan-2-ylpyrrolidin-2-one Chemical compound CC(C)N1CCCC1=O GHELJWBGTIKZQW-UHFFFAOYSA-N 0.000 description 1
- ZMYFCFLJBGAQRS-UHFFFAOYSA-N 1-{[3-(2-chlorophenyl)-2-(4-fluorophenyl)oxiran-2-yl]methyl}-1H-1,2,4-triazole Chemical compound C1=CC(F)=CC=C1C1(CN2N=CN=C2)C(C=2C(=CC=CC=2)Cl)O1 ZMYFCFLJBGAQRS-UHFFFAOYSA-N 0.000 description 1
- XUJLWPFSUCHPQL-UHFFFAOYSA-N 11-methyldodecan-1-ol Chemical compound CC(C)CCCCCCCCCCO XUJLWPFSUCHPQL-UHFFFAOYSA-N 0.000 description 1
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical group C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- KAESVJOAVNADME-UHFFFAOYSA-N 1H-pyrrole Natural products C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 1
- NSPMIYGKQJPBQR-CVMUNTFWSA-N 1h-1,2,4-triazole Chemical group [13CH]=1[15N]=[13CH][15NH][15N]=1 NSPMIYGKQJPBQR-CVMUNTFWSA-N 0.000 description 1
- FFMBYMANYCDCMK-UHFFFAOYSA-N 2,5-dihydro-1h-imidazole Chemical compound C1NCN=C1 FFMBYMANYCDCMK-UHFFFAOYSA-N 0.000 description 1
- STMIIPIFODONDC-UHFFFAOYSA-N 2-(2,4-dichlorophenyl)-1-(1H-1,2,4-triazol-1-yl)hexan-2-ol Chemical compound C=1C=C(Cl)C=C(Cl)C=1C(O)(CCCC)CN1C=NC=N1 STMIIPIFODONDC-UHFFFAOYSA-N 0.000 description 1
- PAWQVTBBRAZDMG-UHFFFAOYSA-N 2-(3-bromo-2-fluorophenyl)acetic acid Chemical compound OC(=O)CC1=CC=CC(Br)=C1F PAWQVTBBRAZDMG-UHFFFAOYSA-N 0.000 description 1
- UFNOUKDBUJZYDE-UHFFFAOYSA-N 2-(4-chlorophenyl)-3-cyclopropyl-1-(1H-1,2,4-triazol-1-yl)butan-2-ol Chemical compound C1=NC=NN1CC(O)(C=1C=CC(Cl)=CC=1)C(C)C1CC1 UFNOUKDBUJZYDE-UHFFFAOYSA-N 0.000 description 1
- KWLVWJPJKJMCSH-UHFFFAOYSA-N 2-(4-chlorophenyl)-N-{2-[3-methoxy-4-(prop-2-yn-1-yloxy)phenyl]ethyl}-2-(prop-2-yn-1-yloxy)acetamide Chemical compound C1=C(OCC#C)C(OC)=CC(CCNC(=O)C(OCC#C)C=2C=CC(Cl)=CC=2)=C1 KWLVWJPJKJMCSH-UHFFFAOYSA-N 0.000 description 1
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 1
- XNWFRZJHXBZDAG-UHFFFAOYSA-N 2-METHOXYETHANOL Chemical compound COCCO XNWFRZJHXBZDAG-UHFFFAOYSA-N 0.000 description 1
- ZQMRDENWZKMOTM-UHFFFAOYSA-N 2-butoxy-6-iodo-3-propylchromen-4-one Chemical compound C1=C(I)C=C2C(=O)C(CCC)=C(OCCCC)OC2=C1 ZQMRDENWZKMOTM-UHFFFAOYSA-N 0.000 description 1
- OWDLFBLNMPCXSD-UHFFFAOYSA-N 2-chloro-N-(2,6-dimethylphenyl)-N-(2-oxotetrahydrofuran-3-yl)acetamide Chemical compound CC1=CC=CC(C)=C1N(C(=O)CCl)C1C(=O)OCC1 OWDLFBLNMPCXSD-UHFFFAOYSA-N 0.000 description 1
- ZDOOQPFIGYHZFV-UHFFFAOYSA-N 2-ethyl-4-[(4-phenoxyphenoxy)methyl]-1,3-dioxolane Chemical compound O1C(CC)OCC1COC(C=C1)=CC=C1OC1=CC=CC=C1 ZDOOQPFIGYHZFV-UHFFFAOYSA-N 0.000 description 1
- IULJSGIJJZZUMF-UHFFFAOYSA-N 2-hydroxybenzenesulfonic acid Chemical compound OC1=CC=CC=C1S(O)(=O)=O IULJSGIJJZZUMF-UHFFFAOYSA-N 0.000 description 1
- ACVSHQGHCWUJFU-UHFFFAOYSA-N 2h-imidazole Chemical compound C1N=CC=N1 ACVSHQGHCWUJFU-UHFFFAOYSA-N 0.000 description 1
- ACNUVXZPCIABEX-UHFFFAOYSA-N 3',6'-diaminospiro[2-benzofuran-3,9'-xanthene]-1-one Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(N)C=C1OC1=CC(N)=CC=C21 ACNUVXZPCIABEX-UHFFFAOYSA-N 0.000 description 1
- SOUGWDPPRBKJEX-UHFFFAOYSA-N 3,5-dichloro-N-(1-chloro-3-methyl-2-oxopentan-3-yl)-4-methylbenzamide Chemical compound ClCC(=O)C(C)(CC)NC(=O)C1=CC(Cl)=C(C)C(Cl)=C1 SOUGWDPPRBKJEX-UHFFFAOYSA-N 0.000 description 1
- UMVOQQDNEYOJOK-UHFFFAOYSA-N 3,5-dimethylbenzoic acid Chemical compound CC1=CC(C)=CC(C(O)=O)=C1 UMVOQQDNEYOJOK-UHFFFAOYSA-N 0.000 description 1
- FSCWZHGZWWDELK-UHFFFAOYSA-N 3-(3,5-dichlorophenyl)-5-ethenyl-5-methyl-2,4-oxazolidinedione Chemical compound O=C1C(C)(C=C)OC(=O)N1C1=CC(Cl)=CC(Cl)=C1 FSCWZHGZWWDELK-UHFFFAOYSA-N 0.000 description 1
- DHTJFQWHCVTNRY-UHFFFAOYSA-N 3-[5-(4-chlorophenyl)-2,3-dimethyl-1,2-oxazolidin-3-yl]pyridine Chemical compound CN1OC(C=2C=CC(Cl)=CC=2)CC1(C)C1=CC=CN=C1 DHTJFQWHCVTNRY-UHFFFAOYSA-N 0.000 description 1
- MCGBIXXDQFWVDW-UHFFFAOYSA-N 4,5-dihydro-1h-pyrazole Chemical compound C1CC=NN1 MCGBIXXDQFWVDW-UHFFFAOYSA-N 0.000 description 1
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 1
- UHPMCKVQTMMPCG-UHFFFAOYSA-N 5,8-dihydroxy-2-methoxy-6-methyl-7-(2-oxopropyl)naphthalene-1,4-dione Chemical compound CC1=C(CC(C)=O)C(O)=C2C(=O)C(OC)=CC(=O)C2=C1O UHPMCKVQTMMPCG-UHFFFAOYSA-N 0.000 description 1
- ASMNSUBMNZQTTG-UHFFFAOYSA-N 5-chloro-7-(4-methylpiperidin-1-yl)-6-(2,4,6-trifluorophenyl)-[1,2,4]triazolo[1,5-a]pyrimidine Chemical compound C1CC(C)CCN1C1=C(C=2C(=CC(F)=CC=2F)F)C(Cl)=NC2=NC=NN12 ASMNSUBMNZQTTG-UHFFFAOYSA-N 0.000 description 1
- 125000004008 6 membered carbocyclic group Chemical group 0.000 description 1
- 239000005875 Acetamiprid Substances 0.000 description 1
- 239000005877 Alpha-Cypermethrin Substances 0.000 description 1
- 241000223600 Alternaria Species 0.000 description 1
- 241000223602 Alternaria alternata Species 0.000 description 1
- 241000213004 Alternaria solani Species 0.000 description 1
- 241001558165 Alternaria sp. Species 0.000 description 1
- 239000004254 Ammonium phosphate Substances 0.000 description 1
- 241000380490 Anguina Species 0.000 description 1
- 241001444083 Aphanomyces Species 0.000 description 1
- 241000294569 Aphelenchoides Species 0.000 description 1
- 244000105624 Arachis hypogaea Species 0.000 description 1
- 235000007319 Avena orientalis Nutrition 0.000 description 1
- 244000075850 Avena orientalis Species 0.000 description 1
- 239000005734 Benalaxyl Substances 0.000 description 1
- 239000005884 Beta-Cyfluthrin Substances 0.000 description 1
- 241001465178 Bipolaris Species 0.000 description 1
- 241001450781 Bipolaris oryzae Species 0.000 description 1
- 241000190150 Bipolaris sorokiniana Species 0.000 description 1
- 241001480061 Blumeria graminis Species 0.000 description 1
- 241000123650 Botrytis cinerea Species 0.000 description 1
- 241000233685 Bremia lactucae Species 0.000 description 1
- 239000005741 Bromuconazole Substances 0.000 description 1
- 239000005742 Bupirimate Substances 0.000 description 1
- 239000005885 Buprofezin Substances 0.000 description 1
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 1
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 1
- WIUBYSTZBMEDEJ-UHFFFAOYSA-N CC1=CC(=C(C=C1)C)OC=C2C(C=CC=C2C)C(=COC)C(=O)O Chemical compound CC1=CC(=C(C=C1)C)OC=C2C(C=CC=C2C)C(=COC)C(=O)O WIUBYSTZBMEDEJ-UHFFFAOYSA-N 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical class NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- 235000008733 Citrus aurantifolia Nutrition 0.000 description 1
- 239000005654 Clofentezine Substances 0.000 description 1
- 241000228437 Cochliobolus Species 0.000 description 1
- 241000222199 Colletotrichum Species 0.000 description 1
- 241001123536 Colletotrichum acutatum Species 0.000 description 1
- 235000009849 Cucumis sativus Nutrition 0.000 description 1
- 235000010799 Cucumis sativus var sativus Nutrition 0.000 description 1
- 241000371644 Curvularia ravenelii Species 0.000 description 1
- 239000005757 Cyproconazole Substances 0.000 description 1
- 239000005758 Cyprodinil Substances 0.000 description 1
- 206010011732 Cyst Diseases 0.000 description 1
- 241001259996 Dalbulus maidis Species 0.000 description 1
- 239000005892 Deltamethrin Substances 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- RUPBZQFQVRMKDG-UHFFFAOYSA-M Didecyldimethylammonium chloride Chemical compound [Cl-].CCCCCCCCCC[N+](C)(C)CCCCCCCCCC RUPBZQFQVRMKDG-UHFFFAOYSA-M 0.000 description 1
- 239000005893 Diflubenzuron Substances 0.000 description 1
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 1
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical class CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 1
- 239000005762 Dimoxystrobin Substances 0.000 description 1
- 241000947843 Drechslera sp. Species 0.000 description 1
- 241000591358 Eballistra oryzae Species 0.000 description 1
- UPEZCKBFRMILAV-JNEQICEOSA-N Ecdysone Natural products O=C1[C@H]2[C@@](C)([C@@H]3C([C@@]4(O)[C@@](C)([C@H]([C@H]([C@@H](O)CCC(O)(C)C)C)CC4)CC3)=C1)C[C@H](O)[C@H](O)C2 UPEZCKBFRMILAV-JNEQICEOSA-N 0.000 description 1
- HMEKVHWROSNWPD-UHFFFAOYSA-N Erioglaucine A Chemical compound [NH4+].[NH4+].C=1C=C(C(=C2C=CC(C=C2)=[N+](CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=2C(=CC=CC=2)S([O-])(=O)=O)C=CC=1N(CC)CC1=CC=CC(S([O-])(=O)=O)=C1 HMEKVHWROSNWPD-UHFFFAOYSA-N 0.000 description 1
- 241000221787 Erysiphe Species 0.000 description 1
- 239000005895 Esfenvalerate Substances 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 1
- 239000005896 Etofenprox Substances 0.000 description 1
- 239000005769 Etridiazole Substances 0.000 description 1
- 240000002989 Euphorbia neriifolia Species 0.000 description 1
- 241000306559 Exserohilum Species 0.000 description 1
- 239000005780 Fluazinam Substances 0.000 description 1
- 239000005781 Fludioxonil Substances 0.000 description 1
- 239000005782 Fluopicolide Substances 0.000 description 1
- 239000005784 Fluoxastrobin Substances 0.000 description 1
- 239000005786 Flutolanil Substances 0.000 description 1
- 239000005787 Flutriafol Substances 0.000 description 1
- 240000009088 Fragaria x ananassa Species 0.000 description 1
- 239000005791 Fuberidazole Substances 0.000 description 1
- 241000221778 Fusarium fujikuroi Species 0.000 description 1
- 241000223195 Fusarium graminearum Species 0.000 description 1
- 241001149959 Fusarium sp. Species 0.000 description 1
- 239000005903 Gamma-cyhalothrin Substances 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 241001442498 Globodera Species 0.000 description 1
- 241001442497 Globodera rostochiensis Species 0.000 description 1
- 241000896246 Golovinomyces cichoracearum Species 0.000 description 1
- 241000560010 Harpophora graminicola Species 0.000 description 1
- 241000258937 Hemiptera Species 0.000 description 1
- 241001480224 Heterodera Species 0.000 description 1
- 241001481225 Heterodera avenae Species 0.000 description 1
- 241000498254 Heterodera glycines Species 0.000 description 1
- 241000379510 Heterodera schachtii Species 0.000 description 1
- 241000040487 Heterodera trifolii Species 0.000 description 1
- 235000008694 Humulus lupulus Nutrition 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- 239000005867 Iprodione Substances 0.000 description 1
- 241000256602 Isoptera Species 0.000 description 1
- 240000008415 Lactuca sativa Species 0.000 description 1
- 235000003228 Lactuca sativa Nutrition 0.000 description 1
- 235000019738 Limestone Nutrition 0.000 description 1
- 239000005912 Lufenuron Substances 0.000 description 1
- 241001373592 Macrophomina sp. Species 0.000 description 1
- 241001344131 Magnaporthe grisea Species 0.000 description 1
- 241001330975 Magnaporthe oryzae Species 0.000 description 1
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 1
- 241000243787 Meloidogyne hapla Species 0.000 description 1
- 241000243786 Meloidogyne incognita Species 0.000 description 1
- 241000243785 Meloidogyne javanica Species 0.000 description 1
- 239000005805 Mepanipyrim Substances 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- 239000005917 Methoxyfenozide Substances 0.000 description 1
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical class NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 1
- 239000005810 Metrafenone Substances 0.000 description 1
- 241001335049 Microdochium sp. Species 0.000 description 1
- 239000004368 Modified starch Substances 0.000 description 1
- 241001459558 Monographella nivalis Species 0.000 description 1
- 101100365384 Mus musculus Eefsec gene Proteins 0.000 description 1
- 241000131448 Mycosphaerella Species 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- XFOXDUJCOHBXRC-UHFFFAOYSA-N N-Ethyl-N-methyl-4-(trifluoromethyl)-2-(3,4-dimethoxyphenyl)benzamide Chemical compound CCN(C)C(=O)C1=CC=C(C(F)(F)F)C=C1C1=CC=C(OC)C(OC)=C1 XFOXDUJCOHBXRC-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- 241000498271 Necator Species 0.000 description 1
- 229940123925 Nicotinic receptor agonist Drugs 0.000 description 1
- 229940123859 Nicotinic receptor antagonist Drugs 0.000 description 1
- 241001668536 Oculimacula yallundae Species 0.000 description 1
- 241000736122 Parastagonospora nodorum Species 0.000 description 1
- 241000682645 Phakopsora pachyrhizi Species 0.000 description 1
- 235000010627 Phaseolus vulgaris Nutrition 0.000 description 1
- 244000046052 Phaseolus vulgaris Species 0.000 description 1
- 241001480007 Phomopsis Species 0.000 description 1
- 241001557902 Phomopsis sp. Species 0.000 description 1
- 241000233622 Phytophthora infestans Species 0.000 description 1
- 239000005818 Picoxystrobin Substances 0.000 description 1
- 241000317981 Podosphaera fuliginea Species 0.000 description 1
- 241001337928 Podosphaera leucotricha Species 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 229920002367 Polyisobutene Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000005824 Proquinazid Substances 0.000 description 1
- 241001281802 Pseudoperonospora Species 0.000 description 1
- 241000221300 Puccinia Species 0.000 description 1
- 241000601159 Puccinia asparagi Species 0.000 description 1
- 241000540505 Puccinia dispersa f. sp. tritici Species 0.000 description 1
- 241000520648 Pyrenophora teres Species 0.000 description 1
- VQXSOUPNOZTNAI-UHFFFAOYSA-N Pyrethrin I Natural products CC(=CC1CC1C(=O)OC2CC(=O)C(=C2C)CC=C/C=C)C VQXSOUPNOZTNAI-UHFFFAOYSA-N 0.000 description 1
- VMORCWYWLVLMDG-YZGWKJHDSA-N Pyrethrin-II Natural products CC(=O)OC(=C[C@@H]1[C@H](C(=O)O[C@H]2CC(=O)C(=C2C)CC=CC=C)C1(C)C)C VMORCWYWLVLMDG-YZGWKJHDSA-N 0.000 description 1
- 241000619663 Pyricularia sp. Species 0.000 description 1
- 239000005828 Pyrimethanil Substances 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 241000220324 Pyrus Species 0.000 description 1
- 241000233639 Pythium Species 0.000 description 1
- 241001385948 Pythium sp. Species 0.000 description 1
- 241001361634 Rhizoctonia Species 0.000 description 1
- 241000813090 Rhizoctonia solani Species 0.000 description 1
- 241000684075 Rhizoctonia sp. Species 0.000 description 1
- 241001203381 Rhynchosporium sp. Species 0.000 description 1
- 240000000111 Saccharum officinarum Species 0.000 description 1
- 235000007201 Saccharum officinarum Nutrition 0.000 description 1
- 241000800292 Sarocladium attenuatum Species 0.000 description 1
- 241000800294 Sarocladium oryzae Species 0.000 description 1
- 206010039509 Scab Diseases 0.000 description 1
- 241000221662 Sclerotinia Species 0.000 description 1
- 244000082988 Secale cereale Species 0.000 description 1
- 235000007238 Secale cereale Nutrition 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- 241001250060 Sphacelotheca Species 0.000 description 1
- 241001203355 Sphacelotheca sp. Species 0.000 description 1
- 239000005664 Spirodiclofen Substances 0.000 description 1
- 239000005665 Spiromesifen Substances 0.000 description 1
- 239000005931 Spirotetramat Substances 0.000 description 1
- 229930182692 Strobilurin Natural products 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 239000005937 Tebufenozide Substances 0.000 description 1
- 239000005938 Teflubenzuron Substances 0.000 description 1
- 239000005840 Tetraconazole Substances 0.000 description 1
- 241001617088 Thanatephorus sasakii Species 0.000 description 1
- 239000005940 Thiacloprid Substances 0.000 description 1
- 235000011941 Tilia x europaea Nutrition 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- 239000005846 Triadimenol Substances 0.000 description 1
- 239000005857 Trifloxystrobin Substances 0.000 description 1
- 239000005858 Triflumizole Substances 0.000 description 1
- 239000005942 Triflumuron Substances 0.000 description 1
- 235000019714 Triticale Nutrition 0.000 description 1
- 241000510929 Uncinula Species 0.000 description 1
- 241000221566 Ustilago Species 0.000 description 1
- 241000317942 Venturia <ichneumonid wasp> Species 0.000 description 1
- 241000228452 Venturia inaequalis Species 0.000 description 1
- 241000082085 Verticillium <Phyllachorales> Species 0.000 description 1
- BUHNCQOJJZAOMJ-UHFFFAOYSA-N ZXI 8901 Chemical compound C=1C=C(OC(F)F)C=CC=1C(C(C)C)C(=O)OC(C#N)C(C=1)=CC=CC=1OC1=CC=C(Br)C=C1 BUHNCQOJJZAOMJ-UHFFFAOYSA-N 0.000 description 1
- 108010055615 Zein Proteins 0.000 description 1
- 229920002494 Zein Polymers 0.000 description 1
- 239000005863 Zoxamide Substances 0.000 description 1
- QQODLKZGRKWIFG-RUTXASTPSA-N [(R)-cyano-(4-fluoro-3-phenoxyphenyl)methyl] (1S)-3-(2,2-dichloroethenyl)-2,2-dimethylcyclopropane-1-carboxylate Chemical compound CC1(C)C(C=C(Cl)Cl)[C@@H]1C(=O)O[C@@H](C#N)C1=CC=C(F)C(OC=2C=CC=CC=2)=C1 QQODLKZGRKWIFG-RUTXASTPSA-N 0.000 description 1
- KAATUXNTWXVJKI-QPIRBTGLSA-N [(s)-cyano-(3-phenoxyphenyl)methyl] 3-(2,2-dichloroethenyl)-2,2-dimethylcyclopropane-1-carboxylate Chemical compound CC1(C)C(C=C(Cl)Cl)C1C(=O)O[C@H](C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 KAATUXNTWXVJKI-QPIRBTGLSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 235000011054 acetic acid Nutrition 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000011149 active material Substances 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 125000006177 alkyl benzyl group Chemical group 0.000 description 1
- UPEZCKBFRMILAV-UHFFFAOYSA-N alpha-Ecdysone Natural products C1C(O)C(O)CC2(C)C(CCC3(C(C(C(O)CCC(C)(C)O)C)CCC33O)C)C3=CC(=O)C21 UPEZCKBFRMILAV-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229910000148 ammonium phosphate Inorganic materials 0.000 description 1
- 235000019289 ammonium phosphates Nutrition 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229940051881 anilide analgesics and antipyretics Drugs 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000002528 anti-freeze Effects 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 230000003416 augmentation Effects 0.000 description 1
- 235000012733 azorubine Nutrition 0.000 description 1
- 239000003899 bactericide agent Substances 0.000 description 1
- LJOZMWRYMKECFF-UHFFFAOYSA-N benodanil Chemical compound IC1=CC=CC=C1C(=O)NC1=CC=CC=C1 LJOZMWRYMKECFF-UHFFFAOYSA-N 0.000 description 1
- YFXPPSKYMBTNAV-UHFFFAOYSA-N bensultap Chemical compound C=1C=CC=CC=1S(=O)(=O)SCC(N(C)C)CSS(=O)(=O)C1=CC=CC=C1 YFXPPSKYMBTNAV-UHFFFAOYSA-N 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical class OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- DMSMPAJRVJJAGA-UHFFFAOYSA-N benzo[d]isothiazol-3-one Chemical compound C1=CC=C2C(=O)NSC2=C1 DMSMPAJRVJJAGA-UHFFFAOYSA-N 0.000 description 1
- 150000008047 benzoylureas Chemical class 0.000 description 1
- OMFRMAHOUUJSGP-IRHGGOMRSA-N bifenthrin Chemical compound C1=CC=C(C=2C=CC=CC=2)C(C)=C1COC(=O)[C@@H]1[C@H](\C=C(/Cl)C(F)(F)F)C1(C)C OMFRMAHOUUJSGP-IRHGGOMRSA-N 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 239000002981 blocking agent Substances 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 1
- 239000004327 boric acid Substances 0.000 description 1
- 235000010338 boric acid Nutrition 0.000 description 1
- 235000012745 brilliant blue FCF Nutrition 0.000 description 1
- 239000004161 brilliant blue FCF Substances 0.000 description 1
- HJJVPARKXDDIQD-UHFFFAOYSA-N bromuconazole Chemical compound ClC1=CC(Cl)=CC=C1C1(CN2N=CN=C2)OCC(Br)C1 HJJVPARKXDDIQD-UHFFFAOYSA-N 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- DSKJPMWIHSOYEA-UHFFFAOYSA-N bupirimate Chemical compound CCCCC1=C(C)N=C(NCC)N=C1OS(=O)(=O)N(C)C DSKJPMWIHSOYEA-UHFFFAOYSA-N 0.000 description 1
- PRLVTUNWOQKEAI-VKAVYKQESA-N buprofezin Chemical compound O=C1N(C(C)C)\C(=N\C(C)(C)C)SCN1C1=CC=CC=C1 PRLVTUNWOQKEAI-VKAVYKQESA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- GTCAXTIRRLKXRU-UHFFFAOYSA-N carbamic acid methyl ester Natural products COC(N)=O GTCAXTIRRLKXRU-UHFFFAOYSA-N 0.000 description 1
- GYSSRZJIHXQEHQ-UHFFFAOYSA-N carboxin Chemical compound S1CCOC(C)=C1C(=O)NC1=CC=CC=C1 GYSSRZJIHXQEHQ-UHFFFAOYSA-N 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- RXDMAYSSBPYBFW-PKFCDNJMSA-N carpropamide Chemical compound N([C@@H](C)C=1C=CC(Cl)=CC=1)C(=O)[C@@]1(CC)[C@H](C)C1(Cl)Cl RXDMAYSSBPYBFW-PKFCDNJMSA-N 0.000 description 1
- 239000012876 carrier material Substances 0.000 description 1
- 229920006317 cationic polymer Polymers 0.000 description 1
- ALLOLPOYFRLCCX-UHFFFAOYSA-N chembl1986529 Chemical compound COC1=CC=CC=C1N=NC1=C(O)C=CC2=CC=CC=C12 ALLOLPOYFRLCCX-UHFFFAOYSA-N 0.000 description 1
- 230000001055 chewing effect Effects 0.000 description 1
- UISUNVFOGSJSKD-UHFFFAOYSA-N chlorfluazuron Chemical compound FC1=CC=CC(F)=C1C(=O)NC(=O)NC(C=C1Cl)=CC(Cl)=C1OC1=NC=C(C(F)(F)F)C=C1Cl UISUNVFOGSJSKD-UHFFFAOYSA-N 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- UXADOQPNKNTIHB-UHFFFAOYSA-N clofentezine Chemical compound ClC1=CC=CC=C1C1=NN=C(C=2C(=CC=CC=2)Cl)N=N1 UXADOQPNKNTIHB-UHFFFAOYSA-N 0.000 description 1
- 238000002288 cocrystallisation Methods 0.000 description 1
- 235000016213 coffee Nutrition 0.000 description 1
- 235000013353 coffee beverage Nutrition 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000007859 condensation product Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000013256 coordination polymer Substances 0.000 description 1
- 229910052593 corundum Inorganic materials 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 150000005676 cyclic carbonates Chemical class 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 229960001591 cyfluthrin Drugs 0.000 description 1
- QQODLKZGRKWIFG-QSFXBCCZSA-N cyfluthrin Chemical compound CC1(C)[C@@H](C=C(Cl)Cl)[C@H]1C(=O)O[C@@H](C#N)C1=CC=C(F)C(OC=2C=CC=CC=2)=C1 QQODLKZGRKWIFG-QSFXBCCZSA-N 0.000 description 1
- KAATUXNTWXVJKI-UHFFFAOYSA-N cypermethrin Chemical compound CC1(C)C(C=C(Cl)Cl)C1C(=O)OC(C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 KAATUXNTWXVJKI-UHFFFAOYSA-N 0.000 description 1
- HAORKNGNJCEJBX-UHFFFAOYSA-N cyprodinil Chemical compound N=1C(C)=CC(C2CC2)=NC=1NC1=CC=CC=C1 HAORKNGNJCEJBX-UHFFFAOYSA-N 0.000 description 1
- 208000031513 cyst Diseases 0.000 description 1
- 229960002483 decamethrin Drugs 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- OWZREIFADZCYQD-NSHGMRRFSA-N deltamethrin Chemical compound CC1(C)[C@@H](C=C(Br)Br)[C@H]1C(=O)O[C@H](C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 OWZREIFADZCYQD-NSHGMRRFSA-N 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- GUJOJGAPFQRJSV-UHFFFAOYSA-N dialuminum;dioxosilane;oxygen(2-);hydrate Chemical compound O.[O-2].[O-2].[O-2].[Al+3].[Al+3].O=[Si]=O.O=[Si]=O.O=[Si]=O.O=[Si]=O GUJOJGAPFQRJSV-UHFFFAOYSA-N 0.000 description 1
- MNNHAPBLZZVQHP-UHFFFAOYSA-N diammonium hydrogen phosphate Chemical compound [NH4+].[NH4+].OP([O-])([O-])=O MNNHAPBLZZVQHP-UHFFFAOYSA-N 0.000 description 1
- 238000002050 diffraction method Methods 0.000 description 1
- QQQYTWIFVNKMRW-UHFFFAOYSA-N diflubenzuron Chemical compound FC1=CC=CC(F)=C1C(=O)NC(=O)NC1=CC=C(Cl)C=C1 QQQYTWIFVNKMRW-UHFFFAOYSA-N 0.000 description 1
- 229940019503 diflubenzuron Drugs 0.000 description 1
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- WXUZAHCNPWONDH-DYTRJAOYSA-N dimoxystrobin Chemical compound CNC(=O)C(=N\OC)\C1=CC=CC=C1COC1=CC(C)=CC=C1C WXUZAHCNPWONDH-DYTRJAOYSA-N 0.000 description 1
- FBOUIAKEJMZPQG-BLXFFLACSA-N diniconazole-M Chemical compound C1=NC=NN1/C([C@H](O)C(C)(C)C)=C/C1=CC=C(Cl)C=C1Cl FBOUIAKEJMZPQG-BLXFFLACSA-N 0.000 description 1
- YKBZOVFACRVRJN-UHFFFAOYSA-N dinotefuran Chemical compound [O-][N+](=O)\N=C(/NC)NCC1CCOC1 YKBZOVFACRVRJN-UHFFFAOYSA-N 0.000 description 1
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 1
- YSVBPNGJESBVRM-UHFFFAOYSA-L disodium;4-[(1-oxido-4-sulfonaphthalen-2-yl)diazenyl]naphthalene-1-sulfonate Chemical compound [Na+].[Na+].C1=CC=C2C(N=NC3=C(C4=CC=CC=C4C(=C3)S([O-])(=O)=O)O)=CC=C(S([O-])(=O)=O)C2=C1 YSVBPNGJESBVRM-UHFFFAOYSA-L 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000010459 dolomite Substances 0.000 description 1
- 229910000514 dolomite Inorganic materials 0.000 description 1
- UPEZCKBFRMILAV-JMZLNJERSA-N ecdysone Chemical compound C1[C@@H](O)[C@@H](O)C[C@]2(C)[C@@H](CC[C@@]3([C@@H]([C@@H]([C@H](O)CCC(C)(C)O)C)CC[C@]33O)C)C3=CC(=O)[C@@H]21 UPEZCKBFRMILAV-JMZLNJERSA-N 0.000 description 1
- RDYMFSUJUZBWLH-SVWSLYAFSA-N endosulfan Chemical compound C([C@@H]12)OS(=O)OC[C@@H]1[C@]1(Cl)C(Cl)=C(Cl)[C@@]2(Cl)C1(Cl)Cl RDYMFSUJUZBWLH-SVWSLYAFSA-N 0.000 description 1
- VMNULHCTRPXWFJ-UJSVPXBISA-N enoxastrobin Chemical compound CO\C=C(\C(=O)OC)C1=CC=CC=C1CO\N=C(/C)\C=C\C1=CC=C(Cl)C=C1 VMNULHCTRPXWFJ-UJSVPXBISA-N 0.000 description 1
- IINNWAYUJNWZRM-UHFFFAOYSA-L erythrosin B Chemical compound [Na+].[Na+].[O-]C(=O)C1=CC=CC=C1C1=C2C=C(I)C(=O)C(I)=C2OC2=C(I)C([O-])=C(I)C=C21 IINNWAYUJNWZRM-UHFFFAOYSA-L 0.000 description 1
- NYPJDWWKZLNGGM-RPWUZVMVSA-N esfenvalerate Chemical compound C=1C([C@@H](C#N)OC(=O)[C@@H](C(C)C)C=2C=CC(Cl)=CC=2)=CC=CC=1OC1=CC=CC=C1 NYPJDWWKZLNGGM-RPWUZVMVSA-N 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- YREQHYQNNWYQCJ-UHFFFAOYSA-N etofenprox Chemical compound C1=CC(OCC)=CC=C1C(C)(C)COCC1=CC=CC(OC=2C=CC=CC=2)=C1 YREQHYQNNWYQCJ-UHFFFAOYSA-N 0.000 description 1
- 229950005085 etofenprox Drugs 0.000 description 1
- KQTVWCSONPJJPE-UHFFFAOYSA-N etridiazole Chemical compound CCOC1=NC(C(Cl)(Cl)Cl)=NS1 KQTVWCSONPJJPE-UHFFFAOYSA-N 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 150000002193 fatty amides Chemical class 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- JFSPBVWPKOEZCB-UHFFFAOYSA-N fenfuram Chemical compound O1C=CC(C(=O)NC=2C=CC=CC=2)=C1C JFSPBVWPKOEZCB-UHFFFAOYSA-N 0.000 description 1
- HJUFTIJOISQSKQ-UHFFFAOYSA-N fenoxycarb Chemical compound C1=CC(OCCNC(=O)OCC)=CC=C1OC1=CC=CC=C1 HJUFTIJOISQSKQ-UHFFFAOYSA-N 0.000 description 1
- FKLFBQCQQYDUAM-UHFFFAOYSA-N fenpiclonil Chemical compound ClC1=CC=CC(C=2C(=CNC=2)C#N)=C1Cl FKLFBQCQQYDUAM-UHFFFAOYSA-N 0.000 description 1
- NYPJDWWKZLNGGM-UHFFFAOYSA-N fenvalerate Aalpha Natural products C=1C=C(Cl)C=CC=1C(C(C)C)C(=O)OC(C#N)C(C=1)=CC=CC=1OC1=CC=CC=C1 NYPJDWWKZLNGGM-UHFFFAOYSA-N 0.000 description 1
- 239000003337 fertilizer Substances 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- UZCGKGPEKUCDTF-UHFFFAOYSA-N fluazinam Chemical compound [O-][N+](=O)C1=CC(C(F)(F)F)=C(Cl)C([N+]([O-])=O)=C1NC1=NC=C(C(F)(F)F)C=C1Cl UZCGKGPEKUCDTF-UHFFFAOYSA-N 0.000 description 1
- MUJOIMFVNIBMKC-UHFFFAOYSA-N fludioxonil Chemical compound C=12OC(F)(F)OC2=CC=CC=1C1=CNC=C1C#N MUJOIMFVNIBMKC-UHFFFAOYSA-N 0.000 description 1
- RYLHNOVXKPXDIP-UHFFFAOYSA-N flufenoxuron Chemical compound C=1C=C(NC(=O)NC(=O)C=2C(=CC=CC=2F)F)C(F)=CC=1OC1=CC=C(C(F)(F)F)C=C1Cl RYLHNOVXKPXDIP-UHFFFAOYSA-N 0.000 description 1
- GBOYJIHYACSLGN-UHFFFAOYSA-N fluopicolide Chemical compound ClC1=CC(C(F)(F)F)=CN=C1CNC(=O)C1=C(Cl)C=CC=C1Cl GBOYJIHYACSLGN-UHFFFAOYSA-N 0.000 description 1
- UFEODZBUAFNAEU-NLRVBDNBSA-N fluoxastrobin Chemical compound C=1C=CC=C(OC=2C(=C(OC=3C(=CC=CC=3)Cl)N=CN=2)F)C=1C(=N/OC)\C1=NOCCO1 UFEODZBUAFNAEU-NLRVBDNBSA-N 0.000 description 1
- FQKUGOMFVDPBIZ-UHFFFAOYSA-N flusilazole Chemical compound C=1C=C(F)C=CC=1[Si](C=1C=CC(F)=CC=1)(C)CN1C=NC=N1 FQKUGOMFVDPBIZ-UHFFFAOYSA-N 0.000 description 1
- PTCGDEVVHUXTMP-UHFFFAOYSA-N flutolanil Chemical compound CC(C)OC1=CC=CC(NC(=O)C=2C(=CC=CC=2)C(F)(F)F)=C1 PTCGDEVVHUXTMP-UHFFFAOYSA-N 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- ZEYJIQLVKGBLEM-UHFFFAOYSA-N fuberidazole Chemical compound C1=COC(C=2N=C3[CH]C=CC=C3N=2)=C1 ZEYJIQLVKGBLEM-UHFFFAOYSA-N 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 229910021485 fumed silica Inorganic materials 0.000 description 1
- 244000053095 fungal pathogen Species 0.000 description 1
- ZXQYGBMAQZUVMI-GCMPRSNUSA-N gamma-cyhalothrin Chemical compound CC1(C)[C@@H](\C=C(/Cl)C(F)(F)F)[C@H]1C(=O)O[C@H](C#N)C1=CC=CC(OC=2C=CC=CC=2)=C1 ZXQYGBMAQZUVMI-GCMPRSNUSA-N 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 229920000578 graft copolymer Polymers 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 239000003630 growth substance Substances 0.000 description 1
- CNKHSLKYRMDDNQ-UHFFFAOYSA-N halofenozide Chemical compound C=1C=CC=CC=1C(=O)N(C(C)(C)C)NC(=O)C1=CC=C(Cl)C=C1 CNKHSLKYRMDDNQ-UHFFFAOYSA-N 0.000 description 1
- 230000002363 herbicidal effect Effects 0.000 description 1
- RGNPBRKPHBKNKX-UHFFFAOYSA-N hexaflumuron Chemical compound C1=C(Cl)C(OC(F)(F)C(F)F)=C(Cl)C=C1NC(=O)NC(=O)C1=C(F)C=CC=C1F RGNPBRKPHBKNKX-UHFFFAOYSA-N 0.000 description 1
- 229920001903 high density polyethylene Polymers 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 239000004700 high-density polyethylene Substances 0.000 description 1
- 239000000852 hydrogen donor Substances 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- FYQGBXGJFWXIPP-UHFFFAOYSA-N hydroprene Chemical compound CCOC(=O)C=C(C)C=CCC(C)CCCC(C)C FYQGBXGJFWXIPP-UHFFFAOYSA-N 0.000 description 1
- 229930000073 hydroprene Natural products 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 229920003063 hydroxymethyl cellulose Polymers 0.000 description 1
- 229940031574 hydroxymethyl cellulose Drugs 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- AGKSTYPVMZODRV-UHFFFAOYSA-N imibenconazole Chemical compound C1=CC(Cl)=CC=C1CSC(CN1N=CN=C1)=NC1=CC=C(Cl)C=C1Cl AGKSTYPVMZODRV-UHFFFAOYSA-N 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- VPRAQYXPZIFIOH-UHFFFAOYSA-N imiprothrin Chemical compound CC1(C)C(C=C(C)C)C1C(=O)OCN1C(=O)N(CC#C)CC1=O VPRAQYXPZIFIOH-UHFFFAOYSA-N 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- ONUFESLQCSAYKA-UHFFFAOYSA-N iprodione Chemical compound O=C1N(C(=O)NC(C)C)CC(=O)N1C1=CC(Cl)=CC(Cl)=C1 ONUFESLQCSAYKA-UHFFFAOYSA-N 0.000 description 1
- UGWALRUNBSBTGI-ZKMZRDRYSA-N kadethrin Chemical compound C(/[C@@H]1C([C@@H]1C(=O)OCC=1C=C(CC=2C=CC=CC=2)OC=1)(C)C)=C1/CCSC1=O UGWALRUNBSBTGI-ZKMZRDRYSA-N 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 150000003951 lactams Chemical class 0.000 description 1
- 150000002596 lactones Chemical class 0.000 description 1
- 239000005910 lambda-Cyhalothrin Substances 0.000 description 1
- 239000004571 lime Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- SXQCTESRRZBPHJ-UHFFFAOYSA-M lissamine rhodamine Chemical compound [Na+].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=C(S([O-])(=O)=O)C=C1S([O-])(=O)=O SXQCTESRRZBPHJ-UHFFFAOYSA-M 0.000 description 1
- PWPJGUXAGUPAHP-UHFFFAOYSA-N lufenuron Chemical compound C1=C(Cl)C(OC(F)(F)C(C(F)(F)F)F)=CC(Cl)=C1NC(=O)NC(=O)C1=C(F)C=CC=C1F PWPJGUXAGUPAHP-UHFFFAOYSA-N 0.000 description 1
- 229960000521 lufenuron Drugs 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- CIFWZNRJIBNXRE-UHFFFAOYSA-N mepanipyrim Chemical compound CC#CC1=CC(C)=NC(NC=2C=CC=CC=2)=N1 CIFWZNRJIBNXRE-UHFFFAOYSA-N 0.000 description 1
- BCTQJXQXJVLSIG-UHFFFAOYSA-N mepronil Chemical compound CC(C)OC1=CC=CC(NC(=O)C=2C(=CC=CC=2)C)=C1 BCTQJXQXJVLSIG-UHFFFAOYSA-N 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229930002897 methoprene Natural products 0.000 description 1
- 229950003442 methoprene Drugs 0.000 description 1
- QCAWEPFNJXQPAN-UHFFFAOYSA-N methoxyfenozide Chemical compound COC1=CC=CC(C(=O)NN(C(=O)C=2C=C(C)C=C(C)C=2)C(C)(C)C)=C1C QCAWEPFNJXQPAN-UHFFFAOYSA-N 0.000 description 1
- WCYWZMWISLQXQU-UHFFFAOYSA-N methyl Chemical class [CH3] WCYWZMWISLQXQU-UHFFFAOYSA-N 0.000 description 1
- CRFYLQMIDWBKRT-UHFFFAOYSA-N methyl (2-chloro-5-{N-[(6-methylpyridin-2-yl)methoxy]ethanimidoyl}benzyl)carbamate Chemical compound C1=C(Cl)C(CNC(=O)OC)=CC(C(C)=NOCC=2N=C(C)C=CC=2)=C1 CRFYLQMIDWBKRT-UHFFFAOYSA-N 0.000 description 1
- CJPQIRJHIZUAQP-UHFFFAOYSA-N methyl N-(2,6-dimethylphenyl)-N-(phenylacetyl)alaninate Chemical compound CC=1C=CC=C(C)C=1N(C(C)C(=O)OC)C(=O)CC1=CC=CC=C1 CJPQIRJHIZUAQP-UHFFFAOYSA-N 0.000 description 1
- YLGXILFCIXHCMC-JHGZEJCSSA-N methyl cellulose Chemical compound COC1C(OC)C(OC)C(COC)O[C@H]1O[C@H]1C(OC)C(OC)C(OC)OC1COC YLGXILFCIXHCMC-JHGZEJCSSA-N 0.000 description 1
- HIIRDDUVRXCDBN-OBGWFSINSA-N metominostrobin Chemical compound CNC(=O)C(=N\OC)\C1=CC=CC=C1OC1=CC=CC=C1 HIIRDDUVRXCDBN-OBGWFSINSA-N 0.000 description 1
- AMSPWOYQQAWRRM-UHFFFAOYSA-N metrafenone Chemical compound COC1=CC=C(Br)C(C)=C1C(=O)C1=C(C)C=C(OC)C(OC)=C1OC AMSPWOYQQAWRRM-UHFFFAOYSA-N 0.000 description 1
- 239000010445 mica Substances 0.000 description 1
- 229910052618 mica group Inorganic materials 0.000 description 1
- 238000003801 milling Methods 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 229910052901 montmorillonite Inorganic materials 0.000 description 1
- JCPCLLBVKYTARN-UHFFFAOYSA-N n-[2-[4-[3-(4-chlorophenyl)prop-2-ynoxy]-3-methoxyphenyl]ethyl]-2-(ethylsulfonylamino)-3-methylbutanamide Chemical compound COC1=CC(CCNC(=O)C(C(C)C)NS(=O)(=O)CC)=CC=C1OCC#CC1=CC=C(Cl)C=C1 JCPCLLBVKYTARN-UHFFFAOYSA-N 0.000 description 1
- YNKFZRGTXAPYFD-UHFFFAOYSA-N n-[[2-chloro-3,5-bis(trifluoromethyl)phenyl]carbamoyl]-2,6-difluorobenzamide Chemical compound FC1=CC=CC(F)=C1C(=O)NC(=O)NC1=CC(C(F)(F)F)=CC(C(F)(F)F)=C1Cl YNKFZRGTXAPYFD-UHFFFAOYSA-N 0.000 description 1
- 150000002790 naphthalenes Chemical class 0.000 description 1
- 229960002715 nicotine Drugs 0.000 description 1
- SNICXCGAKADSCV-UHFFFAOYSA-N nicotine Natural products CN1CCCC1C1=CC=CN=C1 SNICXCGAKADSCV-UHFFFAOYSA-N 0.000 description 1
- 239000000181 nicotinic agonist Substances 0.000 description 1
- 239000003367 nicotinic antagonist Substances 0.000 description 1
- LJDZFAPLPVPTBD-UHFFFAOYSA-N nitroformic acid Chemical compound OC(=O)[N+]([O-])=O LJDZFAPLPVPTBD-UHFFFAOYSA-N 0.000 description 1
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- ODUCDPQEXGNKDN-UHFFFAOYSA-N nitroxyl Chemical group O=N ODUCDPQEXGNKDN-UHFFFAOYSA-N 0.000 description 1
- 239000000346 nonvolatile oil Substances 0.000 description 1
- NJPPVKZQTLUDBO-UHFFFAOYSA-N novaluron Chemical compound C1=C(Cl)C(OC(F)(F)C(OC(F)(F)F)F)=CC=C1NC(=O)NC(=O)C1=C(F)C=CC=C1F NJPPVKZQTLUDBO-UHFFFAOYSA-N 0.000 description 1
- YTYGAJLZOJPJGH-UHFFFAOYSA-N noviflumuron Chemical compound FC1=C(Cl)C(OC(F)(F)C(C(F)(F)F)F)=C(Cl)C=C1NC(=O)NC(=O)C1=C(F)C=CC=C1F YTYGAJLZOJPJGH-UHFFFAOYSA-N 0.000 description 1
- JPMIIZHYYWMHDT-UHFFFAOYSA-N octhilinone Chemical compound CCCCCCCCN1SC=CC1=O JPMIIZHYYWMHDT-UHFFFAOYSA-N 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- UWVQIROCRJWDKL-UHFFFAOYSA-N oxadixyl Chemical compound CC=1C=CC=C(C)C=1N(C(=O)COC)N1CCOC1=O UWVQIROCRJWDKL-UHFFFAOYSA-N 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 125000005646 oximino group Chemical group 0.000 description 1
- 125000000466 oxiranyl group Chemical group 0.000 description 1
- AMEKQAFGQBKLKX-UHFFFAOYSA-N oxycarboxin Chemical compound O=S1(=O)CCOC(C)=C1C(=O)NC1=CC=CC=C1 AMEKQAFGQBKLKX-UHFFFAOYSA-N 0.000 description 1
- 125000006353 oxyethylene group Chemical group 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 235000020232 peanut Nutrition 0.000 description 1
- 235000021017 pears Nutrition 0.000 description 1
- WBTYBAGIHOISOQ-UHFFFAOYSA-N pent-4-en-1-yl 2-[(2-furylmethyl)(imidazol-1-ylcarbonyl)amino]butanoate Chemical compound C1=CN=CN1C(=O)N(C(CC)C(=O)OCCCC=C)CC1=CC=CO1 WBTYBAGIHOISOQ-UHFFFAOYSA-N 0.000 description 1
- 239000010451 perlite Substances 0.000 description 1
- 235000019362 perlite Nutrition 0.000 description 1
- 229960000490 permethrin Drugs 0.000 description 1
- RLLPVAHGXHCWKJ-UHFFFAOYSA-N permethrin Chemical compound CC1(C)C(C=C(Cl)Cl)C1C(=O)OCC1=CC=CC(OC=2C=CC=CC=2)=C1 RLLPVAHGXHCWKJ-UHFFFAOYSA-N 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- 229960003536 phenothrin Drugs 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 125000005498 phthalate group Chemical class 0.000 description 1
- 239000006069 physical mixture Substances 0.000 description 1
- 230000003032 phytopathogenic effect Effects 0.000 description 1
- 230000000885 phytotoxic effect Effects 0.000 description 1
- IBSNKSODLGJUMQ-SDNWHVSQSA-N picoxystrobin Chemical compound CO\C=C(\C(=O)OC)C1=CC=CC=C1COC1=CC=CC(C(F)(F)F)=N1 IBSNKSODLGJUMQ-SDNWHVSQSA-N 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920001281 polyalkylene Polymers 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 229920001083 polybutene Polymers 0.000 description 1
- 229920006149 polyester-amide block copolymer Polymers 0.000 description 1
- 229920001522 polyglycol ester Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 238000001144 powder X-ray diffraction data Methods 0.000 description 1
- 238000000079 presaturation Methods 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- QXJKBPAVAHBARF-BETUJISGSA-N procymidone Chemical compound O=C([C@]1(C)C[C@@]1(C1=O)C)N1C1=CC(Cl)=CC(Cl)=C1 QXJKBPAVAHBARF-BETUJISGSA-N 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- FLVBXVXXXMLMOX-UHFFFAOYSA-N proquinazid Chemical compound C1=C(I)C=C2C(=O)N(CCC)C(OCCC)=NC2=C1 FLVBXVXXXMLMOX-UHFFFAOYSA-N 0.000 description 1
- 239000011814 protection agent Substances 0.000 description 1
- DNXIASIHZYFFRO-UHFFFAOYSA-N pyrazoline Chemical compound C1CN=NC1 DNXIASIHZYFFRO-UHFFFAOYSA-N 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- ROVGZAWFACYCSP-VUMXUWRFSA-N pyrethrin I Chemical compound CC1(C)[C@H](C=C(C)C)[C@H]1C(=O)O[C@@H]1C(C)=C(C\C=C/C=C)C(=O)C1 ROVGZAWFACYCSP-VUMXUWRFSA-N 0.000 description 1
- VJFUPGQZSXIULQ-XIGJTORUSA-N pyrethrin II Chemical compound CC1(C)[C@H](/C=C(\C)C(=O)OC)[C@H]1C(=O)O[C@@H]1C(C)=C(C\C=C/C=C)C(=O)C1 VJFUPGQZSXIULQ-XIGJTORUSA-N 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- ZLIBICFPKPWGIZ-UHFFFAOYSA-N pyrimethanil Chemical compound CC1=CC(C)=NC(NC=2C=CC=CC=2)=N1 ZLIBICFPKPWGIZ-UHFFFAOYSA-N 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- NHDHVHZZCFYRSB-UHFFFAOYSA-N pyriproxyfen Chemical compound C=1C=CC=NC=1OC(C)COC(C=C1)=CC=C1OC1=CC=CC=C1 NHDHVHZZCFYRSB-UHFFFAOYSA-N 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 229940108410 resmethrin Drugs 0.000 description 1
- VEMKTZHHVJILDY-FIWHBWSRSA-N resmethrin Chemical compound CC1(C)[C@H](C=C(C)C)C1C(=O)OCC1=COC(CC=2C=CC=CC=2)=C1 VEMKTZHHVJILDY-FIWHBWSRSA-N 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- MSHXTAQSSIEBQS-UHFFFAOYSA-N s-[3-carbamoylsulfanyl-2-(dimethylamino)propyl] carbamothioate;hydron;chloride Chemical compound [Cl-].NC(=O)SCC([NH+](C)C)CSC(N)=O MSHXTAQSSIEBQS-UHFFFAOYSA-N 0.000 description 1
- 239000004576 sand Substances 0.000 description 1
- 125000000467 secondary amino group Chemical group [H]N([*:1])[*:2] 0.000 description 1
- 239000013049 sediment Substances 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- HPYNBECUCCGGPA-UHFFFAOYSA-N silafluofen Chemical compound C1=CC(OCC)=CC=C1[Si](C)(C)CCCC1=CC=C(F)C(OC=2C=CC=CC=2)=C1 HPYNBECUCCGGPA-UHFFFAOYSA-N 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- DTDSAWVUFPGDMX-UHFFFAOYSA-N spirodiclofen Chemical compound CCC(C)(C)C(=O)OC1=C(C=2C(=CC(Cl)=CC=2)Cl)C(=O)OC11CCCCC1 DTDSAWVUFPGDMX-UHFFFAOYSA-N 0.000 description 1
- GOLXNESZZPUPJE-UHFFFAOYSA-N spiromesifen Chemical compound CC1=CC(C)=CC(C)=C1C(C(O1)=O)=C(OC(=O)CC(C)(C)C)C11CCCC1 GOLXNESZZPUPJE-UHFFFAOYSA-N 0.000 description 1
- CLSVJBIHYWPGQY-GGYDESQDSA-N spirotetramat Chemical compound CCOC(=O)OC1=C(C=2C(=CC=C(C)C=2)C)C(=O)N[C@@]11CC[C@H](OC)CC1 CLSVJBIHYWPGQY-GGYDESQDSA-N 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 235000021012 strawberries Nutrition 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 239000001384 succinic acid Substances 0.000 description 1
- 235000011044 succinic acid Nutrition 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 125000001273 sulfonato group Chemical group [O-]S(*)(=O)=O 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000004548 suspo-emulsion Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229920002994 synthetic fiber Polymers 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- UJMBCXLDXJUMFB-GLCFPVLVSA-K tartrazine Chemical compound [Na+].[Na+].[Na+].[O-]C(=O)C1=NN(C=2C=CC(=CC=2)S([O-])(=O)=O)C(=O)C1\N=N\C1=CC=C(S([O-])(=O)=O)C=C1 UJMBCXLDXJUMFB-GLCFPVLVSA-K 0.000 description 1
- 235000012756 tartrazine Nutrition 0.000 description 1
- 239000004149 tartrazine Substances 0.000 description 1
- QYPNKSZPJQQLRK-UHFFFAOYSA-N tebufenozide Chemical compound C1=CC(CC)=CC=C1C(=O)NN(C(C)(C)C)C(=O)C1=CC(C)=CC(C)=C1 QYPNKSZPJQQLRK-UHFFFAOYSA-N 0.000 description 1
- CJDWRQLODFKPEL-UHFFFAOYSA-N teflubenzuron Chemical compound FC1=CC=CC(F)=C1C(=O)NC(=O)NC1=CC(Cl)=C(F)C(Cl)=C1F CJDWRQLODFKPEL-UHFFFAOYSA-N 0.000 description 1
- 125000001302 tertiary amino group Chemical group 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 229960005199 tetramethrin Drugs 0.000 description 1
- 239000004416 thermosoftening plastic Substances 0.000 description 1
- 239000004308 thiabendazole Substances 0.000 description 1
- 235000010296 thiabendazole Nutrition 0.000 description 1
- WJCNZQLZVWNLKY-UHFFFAOYSA-N thiabendazole Chemical compound S1C=NC(C=2NC3=CC=CC=C3N=2)=C1 WJCNZQLZVWNLKY-UHFFFAOYSA-N 0.000 description 1
- 229960004546 thiabendazole Drugs 0.000 description 1
- DNVLJEWNNDHELH-UHFFFAOYSA-N thiocyclam Chemical compound CN(C)C1CSSSC1 DNVLJEWNNDHELH-UHFFFAOYSA-N 0.000 description 1
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea group Chemical group NC(=S)N UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 description 1
- 235000010215 titanium dioxide Nutrition 0.000 description 1
- BAZVSMNPJJMILC-UHFFFAOYSA-N triadimenol Chemical compound C1=NC=NN1C(C(O)C(C)(C)C)OC1=CC=C(Cl)C=C1 BAZVSMNPJJMILC-UHFFFAOYSA-N 0.000 description 1
- DQJCHOQLCLEDLL-UHFFFAOYSA-N tricyclazole Chemical compound CC1=CC=CC2=C1N1C=NN=C1S2 DQJCHOQLCLEDLL-UHFFFAOYSA-N 0.000 description 1
- ONCZDRURRATYFI-TVJDWZFNSA-N trifloxystrobin Chemical compound CO\N=C(\C(=O)OC)C1=CC=CC=C1CO\N=C(/C)C1=CC=CC(C(F)(F)F)=C1 ONCZDRURRATYFI-TVJDWZFNSA-N 0.000 description 1
- HSMVPDGQOIQYSR-KGENOOAVSA-N triflumizole Chemical compound C1=CN=CN1C(/COCCC)=N/C1=CC=C(Cl)C=C1C(F)(F)F HSMVPDGQOIQYSR-KGENOOAVSA-N 0.000 description 1
- XAIPTRIXGHTTNT-UHFFFAOYSA-N triflumuron Chemical compound C1=CC(OC(F)(F)F)=CC=C1NC(=O)NC(=O)C1=CC=CC=C1Cl XAIPTRIXGHTTNT-UHFFFAOYSA-N 0.000 description 1
- RROQIUMZODEXOR-UHFFFAOYSA-N triforine Chemical compound O=CNC(C(Cl)(Cl)Cl)N1CCN(C(NC=O)C(Cl)(Cl)Cl)CC1 RROQIUMZODEXOR-UHFFFAOYSA-N 0.000 description 1
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical compound COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 description 1
- 238000001622 two pulse phase modulation pulse sequence Methods 0.000 description 1
- 150000003672 ureas Chemical class 0.000 description 1
- 230000017260 vegetative to reproductive phase transition of meristem Effects 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 241000228158 x Triticosecale Species 0.000 description 1
- 229910001845 yogo sapphire Inorganic materials 0.000 description 1
- 239000005943 zeta-Cypermethrin Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/08—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having one or more single bonds to nitrogen atoms
- A01N47/28—Ureas or thioureas containing the groups >N—CO—N< or >N—CS—N<
- A01N47/34—Ureas or thioureas containing the groups >N—CO—N< or >N—CS—N< containing the groups, e.g. biuret; Thio analogues thereof; Urea-aldehyde condensation products
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N25/00—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/02—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms
- A01N43/04—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom
- A01N43/20—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with one or more oxygen or sulfur atoms as the only ring hetero atoms with one hetero atom three- or four-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/56—1,2-Diazoles; Hydrogenated 1,2-diazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D231/18—One oxygen or sulfur atom
- C07D231/20—One oxygen atom attached in position 3 or 5
- C07D231/22—One oxygen atom attached in position 3 or 5 with aryl radicals attached to ring nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D249/00—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms
- C07D249/02—Heterocyclic compounds containing five-membered rings having three nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D249/08—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/06—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/64—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with three nitrogen atoms as the only ring hetero atoms
- A01N43/647—Triazoles; Hydrogenated triazoles
- A01N43/653—1,2,4-Triazoles; Hydrogenated 1,2,4-triazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/08—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having one or more single bonds to nitrogen atoms
- A01N47/10—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof
- A01N47/24—Carbamic acid derivatives, i.e. containing the group —O—CO—N<; Thio analogues thereof containing the groups, or; Thio analogues thereof
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Dentistry (AREA)
- Plant Pathology (AREA)
- Engineering & Computer Science (AREA)
- Pest Control & Pesticides (AREA)
- Agronomy & Crop Science (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Toxicology (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
Abstract
COMPLEXO CRISTALINO, PROCESSO PARA A PREPARAÇÃO DO COMPLEXO CRISTALINO, E, COMPOSIÇÃO AGRÍCOLA. A presente invenção refere-se aos complexos cristalinos compreendendo pelo menos um composto orgânico agricolamente ativo A tendo pelo menos um componente funcional que é capaz de ser servir como um aceptor de hidrogênio e uma ligação de hidrogênio e tiofanato-metila.
Description
[001] A presente invenção diz respeito aos complexos cristalinos de pelo menos um composto orgânico agricolamente ativo A tendo pelo menos um componente funcional que é capaz de servir como um aceptor de hidrogênio em uma ligação de hidrogênio.
[002] Os compostos orgânicos agricolamente ativos tais como fungicidas, herbicidas e inseticidas ou acaricidas são geralmente negociados como formulações líquidas ou sólidas que compreendem um ou mais compostos orgânicos agricolamente ativos e aditivos de formulação adequados. Por várias razões, os tipos de formulação são preferidos, em que o composto orgânico agricolamente ativo (A) está presente no estado sólido, exemplos incluindo formulações sólidas tais como polvilhos, pós ou grânulos e formulações líquidas tais como concentrados de suspensão, isto é, formulações líquidas contendo partículas sólidas do composto orgânico ativo colocado em suspensão em um meio de suspensão líquido.
[003] Para propósitos de formulação o composto orgânico agricolamente ativo deve ser um material cristalino tendo um ponto de fusão suficientemente elevado. Infelizmente, um grande número de tais compostos orgânicos são materiais amorfos e/ou possuem pontos de fusão baixos. Tais compostos são difíceis de formular como concentrados de suspensão (SC) em uma maneira convencional, visto que o mecanismo de trituração ficará preso durante a trituração como um resultado da pegajosidade do composto ativo. As formulações de compostos orgânicos sólidos amorfos são freqüentemente instáveis com referência à separação de fase. Por exemplo, os concentrados de suspensão de ativos sólidos amorfos tendem a se tornarem não homogêneos mediante a separação do composto orgânico ativo como um resultado da agregação de partículas ou aumento de partículas.
[004] Os complexos cristalinos de compostos orgânicos, também denominados como co-cristais são cristais de múltiplos componentes ou material cristalino que consiste de pelo menos dois compostos orgânicos diferentes que são geralmente sólidos a 25 oC ou pelo menos um óleo não volátil (pressão de vapor menor do que 1 mbar a 25 oC). Nos complexos cristalinos (ou co-cristais) pelo menos dois compostos orgânicos diferentes formam um material cristalino tendo uma estrutura cristalina definida, isto é, o pelo menos dois compostos orgânicos possuem uma disposição espacial relativa definida dentro da estrutura cristalina, desse modo formando uma estrutura supra-molecular.
[005] Nos co-cristais o pelo menos dois compostos diferentes interagem através da ligação não covalente tal como ligações de hidrogênio e, possivelmente, outras forças intermoleculares não covalentes, incluindo empilhamento π e interação van der Waals. A ligação de hidrogênio é uma interação direcional e relativamente forte e devido a estas duas propriedades, é freqüentemente a força dominante também no reconhecimento molecular em toda a natureza, por exemplo, na formação do DNA, dobradura das proteínas em geral, receptores, etc. Assim, a ligação de hidrogênio é a força considerada nos métodos onde novos materiais de múltiplos componentes ou co-cristais estão sendo designados e descritos na literatura (ver, por exemplo, D. Braga et al., Chem. Commun., 2005, pp. 2635-3645 e O. Almarsson et al., Chem. Commun., 2004, pp. 1889-1896). No entanto, outras forças intermoleculares também podem ser responsáveis pelo reconhecimento molecular.
[006] Embora o acondicionamento na treliça cristalina não possa ser designada ou predita, vários synthons supramoleculares podem ser com sucesso reconhecidos nos co-cristais. O termo “ligação supramolecular” deve ser compreendido como uma entidade geralmente de dois compostos que são de hidrogênio ligados entre si. Nos co-cristais estas ligações ainda no acondicionamento da treliça cristalina formam um cristal molecular. O reconhecimento molecular é uma condição da formação de ligação. No entanto, o co-cristal também deve ser energicamente favorável, isto é, uma energia ganha na formação dos co-cristais também é requerida, como moléculas tipicamente podem acondicionar muito eficientemente como cristais de componentes puros, desse modo impedindo a formação de co-cristal.
[007] Nos co-cristais, geralmente um dos compostos orgânicos serve como uma matriz de co-cristal, isto é, um composto que em si facilmente forma um material cristalino e que é capaz de formar co-cristais com vários outros compostos orgânicos que eles próprios podem não necessariamente formar uma fase cristalina.
[008] Os complexos cristalinos de compostos farmacêuticos ativos foram descritos na técnica em várias ocasiões, por exemplo, nas US 2003/224006, WO 03/074474, WO 2005/08951 1, EP 1608339, EP 1631260 e WO 2006/007448.
[009] Tiofanato metila é um composto fungicida cristalino bem conhecido de formula que funde acima de 172 oC sob decomposição. Q tiofanato metila possui ação protetora e curativa contra uma ampla faixa de patógenos fúngicos. A molécula de tiofanato é degradada no vegetal por carbendazime e, portanto, pertence ao grupo de fungicidas de benzimidazol.
[010] Qs inventores da presente invenção surpreendentemente descobriram que o tiofanato-metila é uma matriz de co-cristal adequada que forma complexos cristalinos com um grande número de compostos orgânicos agricolamente ativos tendo pelo menos um componente funcional que é capaz de servir como um aceptor de hidrogênio em uma ligação de hidrogênio.
[011] Portanto, a presente invenção diz respeito aos complexos cristalinos compreendendo pelo menos um composto orgânico agricolamente ativo A tendo pelo menos um componente funcional que é capaz de servir como um aceptor de hidrogênio em uma ligação de hidrogênio e tiofanato-metila.
[012] Os complexos cristalinos de acordo com a presente invenção possuem uma estrutura cristalina definida e possuem um ponto de fusão elevado razoável que facilita a incorporação de tais complexos nas formulações sólidas ou líquidas em que o material ativo está presente no estado sólido. Além do mais, as formulações de tais complexos cristalinos apresentam estabilidade aumentada, em particular em comparação com as formulações contendo uma mistura de tiofanato metila e composto A como compostos sólidos individuais.
[013] Presume-se que a formação dos complexos cristalinos de acordo com a presente invenção resulta da incapacidade do tiofanato metila em alcançar ligações de hidrogênio eficazes para todos os doadores de hidrogênio e acondicionamento eficaz das moléculas no estado cristalino ao mesmo tempo. Portanto, pelo menos um dos átomos de hidrogênio ligados a N da unidade de tiouréia na molécula de tiofanato forma uma ligação de hidrogênio com pelo menos um componente aceptor de hidrogênio no composto agricolamente ativo A e/ou as moléculas de tiofanato formam uma estrutura semelhante a grade com cavidades, em que as moléculas de composto ativo A são incluídas.
[014] Os grupos ou componentes funcionais, que são capazes de ser um aceptor de hidrogênio em uma ligação de hidrogênio incluem átomos de oxigênio, tais como átomos de oxigênio em um componente de éter, em particular um grupo de oxirano, em um grupo de hidroxila, em um grupo de carbonila, em um grupo de carboxila, em um grupo de carboxiamido, e átomos de nitrogênio, em particular na forma de grupos de amino primários, secundários ou terciários ou com átomos de imino-nitrogênio, isto é, =N-.
[015] Preferivelmente, o composto A compreende pelo menos um, por exemplo, 1, 2, 3 ou 4 átomos de imino-nitrogênio como grupos ou componentes funcionais, que são capazes de ser um aceptor de hidrogênio em uma ligação de hidrogênio. O átomo de imino-nitrogênio pode ser parte de um componente cíclico ou acíclico tal como um anel heterocíclico, um componente de oximino ou um componente de amidino. Naturalmente, o composto A pode carregar um ou mais átomos ou componentes, que são capazes de atuar como um aceptor de hidrogênio em uma ligação de hidrogênio.
[016] Em particular, o composto A compreende pelo menos um componente funcional sendo capaz de ser um aceptor de hidrogênio em uma ligação de hidrogênio que contém pelo menos um imino-hidrogenio que é um membro do anel em um anel heterocíclico aromático ou parcialmente insaturado de 5 ou 6 membros, tal como piridina, pirimidina, imidazol ou imidazolina tal como 1H-imidazol, 2H-imidazol, 4,5-diidro-1H-imidazol, 2,5- diidro-1H-imidazol, pirazol ou pirazolina tal como 1H-pirazol, 4,5-diidro-1H- pirazol e anéis de triazol tais como anéis de 1H-1,2,4-triazol, 1H-1,3,4-triazol e 1H-1,2,3-triazol, em particular anel de pirazol ou triazol. O anel heterocíclico pode ser não substituído ou substituído, por exemplo, por 1, 2 ou 3 radicais substituintes. Os radicais substituintes adequados são em particular aqueles que não exercem um efeito mesomérico de retirada de elétron (-M) tal como nitro, carboxilato, sulfonila ou ciano. Os radicais substituintes adequados incluem halogênio, C1-C6-alcóxi, C1-C4-haloalquila, C1-C4-haloalcóxi ou fenila, que por si mesmo pode ser substituído ou substituído por 1, 2, 3 ou 4 radicais selecionados de C1-C6-alquila, halogênio, C1-C6-alcóxi, C1-C4- haloalquila e C1- C4-haloalcóxi, e C1-C6-alquila, que podem ser não substituídos ou substituídos por um radical selecionado de alcóxi, ciano, fenila, C1-C4-alquilcarbonila, C1-C4- alcoxicarbonila, carboxila, carboxamido, C1-C4-alquilaminocarbonila, C1-C4- dialquilamino-carbonila e C1-C4-alquilcarbonilamino. Deve ficar entendido que o próprio anel heterocíclico aromático ou parcialmente insaturado de 5 ou 6 membros substituído ou não substituído pode ser parte de uma molécula maior.
[017] Da mesma forma preferivelmente, o imino-nitrogênio pode ser parte de um componente de oximino acíclico tal como um grupo de imino- éter =N-O-R ou um grupo de amidino C(N=R)NR'2, em que R e R' independentemente um do outro são selecionados de hidrogênio, C1-C6-alquila, C2-C6-alquenila ou C2-C6-alquinila.
[018] Preferivelmente o composto A compreende um componente funcional que é selecionado de um radical heterocíclico aromático de 5 ou 6 membros, tal como piridinila, pirimidinila, 1H-imidazolila, 1H-pirazol, 4,5-diidro-1H-pirazolila, e triazolila, tal como anéis de 1H-1,2,4- triazolila, 4H- 1,2,4-triazolila (= 1H-1,3,4-triazolila), 1H-1,2,3-triazolila e 2H-1,2,3-triazolila, preferivelmente um radical de pirazolila ou triazolila, em particular uma 1H- pirazolila ou um radical de 1H-1,3,4-triazolila, que pode ser substituído ou substituído como definido acima. Os radicais de substituinte preferidos incluem halogênio, C1-C6-alquila, C1-C6-alcóxi, C1-C4-haloalquila, C1-C4-haloalcóxi ou fenila, que em si podem ser substituídos ou substituídos por 1,2,3 ou 4 radicais selecionados de C1-C6-alquila, halogênio, C1-C6-alcóxi, C1-C4-haloalquila e C1- C4-haloalcóxi, em particular de halogênio ou metila. Em particular o composto A compreende um componente funcional, que é selecionado de imidazol-2-ila, pirazol-1-ila, pirazol-3-ila, 1,2,4-triazol-3-ila ou 1,2,4-triazol-1-ila, em que Het é não substituído ou pode carregar 1 ou 2 radicais selecionados de átomos de halogênio e C1-C4-alquila e/ou 1 grupo de fenila, que pode carregar 1, 2 ou 3 átomos de halogênio.
[019] Em uma forma de realização preferida da invenção o composto A carrega um anel de fenila opcionalmente substituída, além do componente funcional, que é capaz de ser um aceptor de hidrogênio em uma ligação de hidrogênio. Sem ser limitado a uma teoria, os inventores acreditam que nos complexos cristalinos da presente invenção o anel de fenila possui uma pi- interação com a molécula de tiofanato. Preferivelmente o anel de fenila é não substituído ou transporta 1, 2 ou 3 radicais selecionados de halogênio, C1-C6-alcóxi, C1-C4-haloalquila, C1-C4-haloalcóxi, fenila, que em si podem ser substituídos ou substituídos por 1, 2, 3 ou 4 radicais selecionados de C1-C6-alquila, halogênio, C1- C6-alcóxi, C1-C4-haloalquila e C1-C4-haloalcóxi, e C1-C6-alquila, que pode ser não substituído ou substituído por um radical selecionado de alcóxi, ciano, fenila, C1-C4- alquilcarbonila, C1-C4-alcoxicarbonila, carboxila, carboxamido, C1-C4-alquilaminocarbonila, C1-C4-dialquilaminocarbonila e C1-C4-alquilcarbonilamino. Os radicais adequados no anel de fenila também incluem os seguintes grupos: N(OCH3)(C(O)OCH3), C(=CH-OCH3)(C(O)OCH3), C(=CH-OCH3)(C(O)NHCH3), C(=N-OCH3)(C(O)OCH3) e C(=N-OCH3)(C(O)OCH3). Preferência é dada à fenila não substituída ou fenila, que carrega 1, 2 ou 3 radicais selecionados de C1-C6- alquila, halogênio, C1-C6-alcóxi, C1-C4-haloalquila e C1-C4-haloalcóxi, em particular de halogênio e metila, e fenila que carrega um dos seguintes radicais: N(OCH3)(C(O)OCH3), C(=CH-OCH3)(C(O)OCH3), C(=CH-OCH3)(C(O)NHCH3), C(=N-OCH3)(C(O)OCH3) ou C(=N-OCH3)(C(O)OCH3).
[020] Preferivelmente, o anel de fenila opcionalmente substituído é ligado a um heterociclo de nitrogênio aromático não substituído ou substituído que carrega pelo menos um átomo de imino nitrogênio como membro do anel através de uma ligação química ou uma cadeia de 1 a 5 membros de átomos, preferivelmente através de uma cadeia de 2 a 3 membros de átomos. Geralmente a cadeia é formada por átomos de carbono. No entanto, um dos átomos de carbono da cadeia pode ser substituído por oxigênio ou silício. A cadeia pode ser não substituída ou carregar 1, 2 ou 3 substituintes tais como ciano, OH, =O, C1-C4- alquila, que podem carregar 1 ou 2 radicais selecionados de OH, C1-C2-alcóxi, C1- C2-haloalcóxi, C1-C2-haloalquila, trimetilsilila, C3-C6-cicloalquila e fenila, que por sua vez podem carregar 1, 2 ou 3 radicais selecionados de átomos de halogênio e C1- C4-alquila, ou fenila, que pode carregar 1, 2 ou 3 radicais selecionados de átomos de halogênio e C1-C4-alquila, ou dois radicais que são ligados ao mesmo átomo da cadeia ou a dois átomos adjacentes da cadeia podem formar um carbociclo ou heterociclo saturado de 3 a 6 membros, que carrega 1 ou 2 átomos de oxigênio como membros do anel, o carbociclo e o heterociclo sendo não substituídos ou que carregam um radical selecionado de halogênio, C1-C4-alquila, C1-C4-haloalquila, C1- C4-alcóxi, halo-C1-C4-alcóxi e fenila, que em si podem carregar 1, 2 ou 3 radicais selecionados de átomos de halogênio e C1-C4-alquila.
[021] Os compostos A adequados possuem um peso molecular, variando de 150 a 500 Dalton.
[022] Os compostos A adequados podem ser selecionados de herbicida, fungicida e inseticidas/acaricidas. Exemplos de compostos A adequados incluem: Fungicidas das classes de - Estrobilurinas, tais como azoxistrobina, dimoxistrobina, enestroburina, fluoxastrobina, cresoxim-metila, metominostrobina,picoxistrobina, piraclostrobina, trifloxistrobina, orisastrobina, (2-cloro-5-[1-(3- metil-benziloxiimino)-etil]-benzil)-carbamato de metila, (2-cloro-5-[1-(6-metil- piridin-2-ilmetoxiimino)-etil]-benzil)-carbamato de metila, 2-(orto-(2,5-dimetil- fenil-oximetilen)fenil)-3-metóxi-acrilato de metila; - Anilidas tais como benalaxila, benodanila, boscalide, carboxina, mepronil, fenfuram, fenexamida, flutolanil, furametpir, metalaxila, ofurace, oxadixila, oxicarboxina, pentiopirad, tifluzamida, tiadinila, 4-difluorometil-2-metil- tiazol-5-[N-(4'-bromo-bifenil-2-il)]-carboxamida, 4-difluorometil-2-metil-tiazol-5- [N-(4'-trifluorometil-bifenil-2-il)]-carboxamida, 4-difluorometil-2-metil-tiazol-5-[N- (4'-cloro-3'-fluoro-bifenil-2-il)]-carboxamida, 3-difluorometil-1-metil-pirazol-4-[N- (3',4'-dicloro-4-fluoro-bifenil-2-il)]-carboxamida, 3-difluorometil-1-metil-pirazol-4- [N-(3’,4’-dicloro-5-flúor-bifenil-2-il)]-carboxamida, 3,4-dicloroisotiazol-5-[N-(2-ciano-fenil)]carboxamida; - Morfolidas tais como dimetomorf, flumorf; - Amidas de ácido benzóico tais como flumetover, fluopicolide (picobenzamida), zoxamida; - Outras carboxiamidas, tais como carpropamida, diclocimet, mandipropamida, N-(2-(4-[3-(4-Clor-fenil)-prop-2-inilóxi]-3-metóxi-fenil)-etil)-2-metansulfonilamino-3-metil-butiramida, N-(2-(4-[3-(4-Clor-fenil)-prop-2-inilóxi]-3-metóxi-fenil)-etil)-2-etanossulfonilamino-3-metil-butiramida; - Fungicidas de azol, em particular: - Triazóis: bitertanol, bromuconazol, ciproconazol, difenoconazol, diniconazol, enilconazol, epoxiconazol, fembuconazol, flusilazol, fluquinconazol, flutriafol, hexaconazol, imibenconazol, ipconazol, metconazol, miclobutanila, penconazol, propiconazol, protioconazol, simeconazol, tebuconazol, tetraconazol, triadimenol, triadimefon, triticonazol; - imidazóis: ciazofamida, imazalil, pefurazoato, procloraz,triflumizol; - benzimidazol: benomila, carbendazim, fuberidazol, tiabendazol; - outros: etaboxam, etridiazol, mimexazol; - piridinas: fluazinam, pirifenox, 3-[5-(4-cloro-fenil)-2,3-dimetil-isoxazolidin-3-il]-piridina; - pirimidinas: bupirimato, ciprodinil, ferinzona, fenarimol,mepanipirim, nuarimol, pirimetanil; - piperazinas: triforina; - pirróis: fludioxonila, fenpiclonil; - dicarboximidas: Iprodiona, procimidona, vinclozolina; e - outros fungicidas: proquinazid, piroquilon, quinoxifen, triciclazol, 5-cloro-7-(4-metil-piperidin-1-il)-6-(2,4,6-trifluorofenil)-[1,2,4]triazolo[1,5-a]piri- midina, 2-butóxi-6-iodo-3-propil-cromen-4-ona, ácido 3-(3-bromo-6-fluoro-2-metilindol-1-sulfonil)-[1,2,4]triazol-1-sulfônico dimetilamida e metrafenona.
[023] Inseticida/Acaricida das classes de: - Piretróides: acrinatrina, aletrina, d-cis-trans aletrina, d-trans aletrina, bifentrina, bioaletrina, bioaletrina S-ciclopentenila, biorresmetrina, cicloprotrina, ciflutrina, beta-ciflutrina, cialotrina, lambda-cialotrina, gama- cialotrina, cifenotrina, cipermetrina, alfa-cipermetrina, beta-cipermetrina, teta- cipermetrina, zeta-cipermetrina, deltametrina, empentrina, esfenvalerato, etofenprox, fenpropatrina, fenvalerato, flucitrinato, flumetrina, tau-fluvalinato, halfenprox, imiprotrina, permetrina, fenotrina, praletrina, proflutrina, piretrin I e II, resmetrina, RU 15525, silafluofen, tau- fluvalinato, teflutrina, tetrametrina, tralometrina, transflutrina, dimeflutrina, ZXI 8901; - Reguladores do crescimento: a) inibidores da síntese de quitina: benzoiluréias; bistrifluron, clorfluazuron, diflubenzuron, flucicloxuron, flufenoxuron, hexaflumuron, lufenuron, novaluron, noviflumuron, teflubenzuron, triflumuron; buprofezin, diofenolan, hexitiazox, etoxazol, clofentezina; b) antagonistas de ecdisona: clormafenozida, halofenozida, metoxifenozida, tebufenozida, azadiraquitina; c) juvenóides: piriproxifen, hidropreno, quinopreno, metopreno, fenoxicarb; d) inibidores da biossintese de lipídeo: espirodiclofen, espiromesifen, espirotetramat; - Compostos agonistas/antagonistas do receptor nicotínico: acetamiprid, clotianidin, dinotefuran, imidacloprid, nitenpiram, tiacloprid, tiametoxam, nicotina, bensultap, cloridreto de cartap, tiociclam, tiossultap-sódio; - o composto de tiazol de formula (r1) - Compostos antagonistas de GABA: acetoprol, etiprol,), fipronil,vaniliprol, pirafluprol, piriprol, vaniliprol.
[024] Os compostos A preferidos incluem fungicidas, selecionados de azoxistrobina, piraclostrobina, orisastrobina, epoxiconazol, tebuconazol, difenconazol, protioconazol, procloraz, triticonazol, fluquinconazol, metconazol, metalaxila, mefenoxam e boscalid, e insecticidas/acaricidas selecionados de fipronil, acetamiprid, imidacloprid, tiametoxam e clotianidina.
[025] Preferência particular é dada a um complexo cristalino, emque o composto A é de o formula I em que Het é imidazol-2-ila, pirazol-1-ila, pirazol-3-ila, 1,2,4-triazol-3-ila ou 1,2,4-triazol-1-ila, em particular pirazol-3-ila ou 1,2,4-triazol-1-ila, em que Het é não substituído ou pode carregar 1 ou 2 radicais selecionados de átomos de halogênio e C1-C4-alquila e/ou 1 grupo de fenila, que pode carregar 1, 2 ou 3 átomos de halogênio; X é O ou um radical CHR3; Y é CR4R5 ou SiR4aR5a, Y também pode ser O, se X for um radical CHR3; ou X e Y juntos são uma ligação química ou uma radical bivalente das formulas k é 0, 1 ou 2; m é 0 ou 1; n é 0, 1, 2 ou 3; R1é halogênio, C1-C4-alquila, metóxi, ou fenila; R2 selecionado de N(OCH3)(C(O)OCH3), C(=CH-OCH3)(C(O)OCH3), C(=CH-OCH3)(C(O)NHCH3), C(=N-OCH3)(C(O)OCH3) e C(=N-OCH3)(C(O)OCH3); R3é hidrogênio ou C1-C6-alquila, que pode carregar 1, 2, 3, 4 ou 5 átomos de halogênio e/ou 1 grupo funcional selecionado de OH e um grupo de carbonila; R4é hidrogênio, CN, OH ou C1-C4-alquila ou juntamente com R3 forma uma ligação; R5é C1-C4-alquila, que pode carregar 1 ou 2 radicais selecionados de OH, C1-C2-alcóxi, C1-C2-haloalcóxi, C1-C2-haloalquila, trimetilsilila, C3-C6-cicloalquila e fenila, que pode carregar 1, 2 ou 3 radicais selecionados de átomos de halogênio e C1-C4-alquila, ou fenila, que pode carregar 1, 2 ou 3 radicais selecionados de átomos de halogênio e C1-C4- alquila, ou R4 e R5 juntos formam um heterociclo saturado de 3 a 6 membros, que carrega 1 ou 2 átomos de oxigênio como membros do anel e que pode carregar um radical selecionado de halogênio, C1-C4-alquila, C1-C4-haloalquila, C1-C4-alcóxi, halo-C1-C4-alcóxi e fenila, que pode carregar 1, 2 ou 3 radicais selecionados de átomos de halogênio e C1-C4-alquila, em particular flúor, cloro ou metila; R4aé C1-C4-alquila ou C1-C4-alcóxi, em particular metila ou metóxi; R5aé C1-C4-alquila, C1-C4-alcóxi ou fenila, que pode carregar 1, 2 ou 3 radicais selecionados de átomos de halogênio e C1-C4-alquila, em particular flúor, cloro ou metila; R6é independentemente selecionado de OH e C1-C4-alquila, em particular OH ou metila; R6aé selecionado de hidrogênio e C1-C4-alquila, eQ é (CH2)p ou (CH2)qO com p sendo 1, 2, 3 ou 4 e q sendo 1, 2 ou 3.
[026] Os compostos A preferidos particulares incluem piraclostrobina, orisastrobina, epoxiconazol, procloraz, triticonazol, fluquinconazol, metconazol, boscalide e fipronil.
[027] Os compostos mais preferidos são selecionados de epoxiconazol, triticonazol, metconazol e piraclrostrobina.
[028] Uma forma de realização muito preferida da invenção refere-se a um complexo cristalino, em que o composto A é epoxiconazol (IUPAC: (2RS,3SR)-1-[3-(2-clorofenil)-2,3-epóxi-2-(4-fluorofenil)propil]-1H-1,2,4-triazol).
[029] Uma outra forma de realização muito preferida da invenção diz respeito a um complexo cristalino, em que o composto A é piraclostrobina (IUPAC: {2-[1-(4-clorofenil)pirazol-3-iloximetil]fenil}(metóxi)carbamato demetila).
[030] Outra forma de realização muito preferida da invenção refere-se a um complexo cristalino, em que o composto A é metconazol (IUPAC: (1RS,5RS;1RS,5SR)-5-(4-clorobenzil)-2,2-dimetil-1-(1H-1,2,4-triazol-1- ilmetil)ciclopentanol).
[031] Uma outra forma de realização muito preferível da invenção se refere a um complexo cristalino, em que o composto A é tritconazol (IUPAC: (RS)-(E)-5-(4-clorobenzilidene)-2,2-dimetil-1-(1H-1,2,4-triazol-1- ilmetil)ciclopentanol).
[032] Nos complexos cristalinos de acordo com a presente invenção, a relação molar de tiofanato metila e o composto A é de pelo menos 0,5:1 e pode variar de 0,5:1 a 3:1 e é preferivelmente de 0,8:1 a 2,5:1 ou 0,9:1 a 2,1:1. Em particular, a relação molar é de 1:1 a 2:1, no entanto, divergências são possíveis, embora elas geralmente não excedem a 20 % molar epreferivelmente 10 %.
[033] Os complexos cristalinos podem ser distintos a partir de simples misturas de tiofanato metila cristalino e composto cristalino A por meios analíticos padrão usados para a análise do material cristalino, incluindo a difractometria em pó de raio X (PXRD), espectrometria de IR, em particular a falta de faixas de absorção estreitas em 3350 cm-1 e 3305 cm-1, característica para tiofanato metila, estado sólido 13C-NMR (13C-CP/MAS: polarização cruzada - rotação de ângulo mágico) e análise termoquímica tal como termogravimetria (TGA) e calorimetria de varredura diferencial (DSC). Quantidades relativas de tiofanato metila e composto A podem ser determinadas, por exemplo, por HPLC ou por 1H-NMR- espectroscopia.
[034] Por exemplo, o complexo cristalino de tiofanato metila e epoxiconazol apresenta um difractograma em pó de raio X a 25 °C (Cu-Ka- radiação, 1,54178 A) em que os reflexos característicos dos compostos puros estão ausentes. Em particular, o complexo cristalino de tiofanato metila e epoxiconazol apresenta pelo menos 4, preferivelmente pelo menos 6, em particular pelo menos 8 e mais preferivelmente todos os seguintes reflexos, fornecidos na seguinte tabela 1 como valores 2θ ou como espaçamentos de treliça d: TABELA 1: PXRD DO COMPLEXO CRISTALINO DE TIOFANATO METILA E EPOXICONAZOL (25 °C, Cu-Ka-RADIAÇÃO, 1.54178 A)
[035] No complexo cristalino de acordo com dita forma derealização da presente invenção, a relação molar de tiofanato metila e epoxiconazol é de 0,9:1 a 1,1:1 e em particular ao redor de 1:1.
[036] Estudos de cristais isolados do complexo cristalino de tiofanato metila e epoxiconazol mostram que a estrutura básica de cristal é triclínica e possui o grupo de espaço P-c. A análise da estrutura revela que o complexo cristalino é uma mistura de 1:1 de tiofanato metila e epoxiconazol, a célula assimétrica contendo uma molécula de tiofanato metila e epoxiconazol, cada. No cristal, duas moléculas de tiofanato metila formam um dímero através das ligações de hidrogênio intermoleculares entre os grupos N-H e C=O de duas moléculas de tiofanato metila adjacentes. O dímero parece formar duas bolsas que atuam como um receptor para duas moléculas de epoxiconazol. Parece que existem ligações de hidrogênio entre o átomo de nitrogênio do anel de triazol da molécula de epoxiconazol e os grupos de NH das moléculas de tiofanato metila. Além do mais, parece existir uma pi-interação entre o anel de fenila da molécula de tiofanato metila e o anel de fenila fluorada da molécula de epoxiconazol. Este complexo de duas moléculas de tiofanato metila e duas moléculas de epoxiconazol forma um synthon supramolecular que é depois acondicionado na treliça cristalina para formar o co-cristal. Os dados característicos da estrutura cristalina do complexo são mostrados na tabela 2: TABELA 2: DADOS CRISTALOGRÁFICOS DO COMPLEXO CRISTALINO DE TIOFANATOMETILA E EPOXICONAZOL a,b,c = Comprimento das bordas da célula unitária α,β,Y = Ângulos da célula unitária Z = Número de moléculas na célula unitária
[037] A análise termogravimétrico mostra que a fusão do complexo cristalino de epoxiconazol e tiofanato metila começa em 148 °C seguida pela decomposição de tiofanato metila.
[038] Por exemplo, o complexo cristalino de tiofanato metila e piraclostrobina apresenta um difractograma em pó de raio X em 25 °C (Cu-Ka- radiação, 1,54178 A) em que os reflexos característicos dos compostos puros estão ausentes. Em particular, o complexo cristalino de tiofanato metila e piraclostrobina apresenta em um difractograma em pó de raio X em 25 °C (Cu- Ka-radiação, 1,54178 A) pelo menos 4, preferivelmente pelo menos 6, em particular pelo menos 8 e mais preferivelmente todos os seguintes reflexos, fornecidos na tabela 3 que segue como valores 2θ ou como espaçamentos de treliça d. TABELA 3: PXRD DO COMPLEXO CRISTALINO DE TIOFANATO METILA EPIRACLOSTROBINA (25 °C, CU-Ka-RADIAÇÃO, 1,54178 A)
[039] 13C-CP/MAS confirma a presença de um complexocristalino em vez da presença de uma mistura simples de tiofanato metila sólido e piraclostrobina sólida. Em particular, o 13C-CP/MAS dos complexos cristalinos (CP = 3 ms, D1 = 30 s, 25 °C, RO 5700 Hz) apresenta mudanças químicas em δ 182,0, 180,8, 178,7, 177,7, 164,3, 158,8, 154,9, 154,0, 152,1 139,4, 137,9, 134,3, 131,2, 130,2, 127,6, 125,9, 123,8, 117,7, 115,6, 94,3, 65,7, 63,0, 58,8, 54,3, 53,6 e 52,6. As mudanças 164,3, 158,8 ppmsão mais características e falta nos 13C-CP/MAS de tiofanato metila e piraclostrobina. Experiências de transferência da polarização dos prótons para 13C confirmar que o tiofanato metila e piraclostrobina estão presentes como um co-cristal e não como uma mistura de material cristalino dos compostos puros.
[040] No complexo cristalino de acordo com dita forma de realização da presente invenção, a relação molar de tiofanato metila e piraclostrobina pode variar de 1,1:1 a 2,5:1, e é em particular de 1,9:1 a 2,1:1, especialmente ao redor de 2:1.
[041] A análise termogravimétrica mostra que o ponto de fusão do complexo cristalino de piraclostrobina e tiofanato metila está ao redor de 150 °C.
[042] Por exemplo, o complexo cristalino de tiofanato metila e metconazol apresenta um difractograma em pó de raio X a 25 °C (Cu-Kα- radiação, 1,54178 A) em que os reflexos característicos dos compostos puros estão ausentes. Em particular, o complexo cristalino de tiofanato metila e epoxiconazol apresenta pelo menos 4, preferivelmente pelo menos 6, em particular pelo menos 8 e mais preferivelmente todos os seguintes reflexos, fornecidos n tabela 4 que segue como valores 2θ ou como espaçamentos de treliça d: TABELA 4: PXRD DO COMPLEXO CRISTALINO DE TIOFANATO METILA E METCONAZOL (25 °C, CU-KA-RADIAÇÃO, 1,54178 A)
[043] No complexo cristalino de acordo com dita forma derealização da presente invenção, a relação molar de tiofanato metila e metconazol é de 0,9:1 a 1,1:1 e em particular ao redor de 1:1.
[044] Os estudos de cristais isolados do complexo cristalino de tiofanato metila e metconazol mostram que a estrutura básica de cristal é monoclínica e possui o grupo de espaço P2(1)/c. A análise de estrutura revela que o complexo cristalino é uma mistura de 1:1 de tiofanato metila e metconazol, a célula assimétrica contendo uma molécula de tiofanato metila e metconazol, cada. Parece que existem ligações de hidrogênio entre os átomos de nitrogênio do anel de triazol da molécula de metconazol e os grupos de NH das moléculas de tiofanato metila. Os dados característicos da estrutura cristalina do complexo são mostrados na tabela 5: TABELA 5: DADOS CRISTALOGRÁFICOS DO COMPLEXO CRISTALINO DE TIOFANATO METILA E METCONAZOL (-170 °C) a,b,c = Comprimento das bordas da célula unitária α,β,Y = Ângulos da célula unitária Z = Número de moléculas na célula unitária
[045] A medição de DSC do complexo cristalino de metconazol e tiofanato metila mostra um pico de fusão endotérmica com início em 155 a 158 °C e pico máximo em 160 a 168 °C. Isto é ao redor de 60 graus mais elevado do que o metconazol cristalino puro (100 °C, como relatado em Pesticide Manual) e ao redor de 10 a 20 °C mais baixo do que o ponto de fusão do tiofanato-metila.
[046] Os complexos cristalinos da presente invenção podem ser preparados pela co-cristalização de tiofanato-metila e pelo menos um composto A de uma solução ou pasta fluida ou de uma fusão contendo tiofanato-metila e pelo menos um composto A. Da mesma maneira, é possível preparar os complexos cristalinos da presente invenção, mediante a trituração de uma mistura do composto A e tiofanato metila em temperatura elevada, por exemplo, acima de 30 °C, preferivelmente em uma temperatura de pelo menos 40 °C, em particular de pelo menos 50 °C, mais preferivelmente de pelo menos 55 °C, por exemplo, de >30 °C a 110 °C, preferivelmente de 40 °C a 100 °C, em particular de 50 °C a 90 °C ou de 55 °C a 90 °C. O composto A pode ser sólido na temperatura de trituração. No entanto, isto não é necessário e pode ser vantajoso se a temperatura estiver próxima ou acima do ponto de fusão do composto A.
[047] Em uma forma de realização preferida do complexo cristalino é tiofanato-metila e pelo menos um composto A é obtido de uma pasta fluida de tiofanato-metila e o pelo menos um composto A em um solvente orgânico ou em uma mistura de água e solvente orgânico. Conseqüentemente, este método compreende a suspensão de tiofanato-metila e o composto ativo A em um solvente orgânico ou em uma mistura de água e um solvente orgânico (Processo de pasta fluida).
[048] Os solventes orgânicos para o processo de pasta fluida são aqueles que são pelo menos parcialmente miscíveis em água, isto é, que possuem miscibilidade com água de pelo menos 10 % v/v, mais preferivelmente pelo menos 20 % v/v em temperatura ambiente, misturas destes e misturas de ditos solventes miscíveis em água com solventes orgânicos que possuem miscibilidae com água de menos do que 10 % v/v em temperatura ambiente. Preferivelmente o solvente orgânico compreende pelo menos 80 % v/v, com base na quantidade total de solvente orgânico, do pelo menos um solvente miscível em água.
[049] Os solventes adequados tendo uma miscibilidade em água de pelo menos 10 % em temperatura ambiente incluem, mas não são limitados a eles: 1. C1-C4-Alcanóis tais como metanol, etanol, n-propanol ou isopropanol; 2. Amidas, N-metilamidas e N,N-dimetilamidas de ácidos C1-C3- carboxílicos tais como formamida, dimetilformamida (DMF), acetamida e N,N- dimetilacetamida; 3. Lactamas de 5 ou 6 membros com um total de 7 átomos de carbono tais como pirrolidona, N-metilpirrolidona, N-etilpirrolidona, N- isopropilpirrolidona, N-hidroxietilpirrolidona; 4. Dimetilsulfóxido e sulfolano; 5. Cetonas com 3 a 6 átomos de carbono tais como acetona, 2- butanona, ciclopentanona e ciclohexanona; 6. Acetonitrila; 7. Lactonas de 5 ou 6 membros tais como Y-butirolactona; 8. Polióis e polieteróis tais como glicol, glicerina, dimetoxietano, etilenodiglicol, etilenoglicolmonometiléter, etc; 9. Carbonatos cíclicos tendo de 3 a 5 átomos de carbono incluindo carbonato de propileno e carbonato de etileno; e 10. Éteres cíclicos tais como tetraidrofurano, dioxano e trioxano, dimetil (poli)C2-C3-alquileneglicol éteres tais comodimetoxietano, dietilenoglicoldimetiléter, trietilenoglicoldimetiléter,dipropilenoglicoldimetiléter, polietilenoglicóis de peso molecular baixo e polipropilenoglicóis de peso molecular baixo (MW <400).
[050] Mais preferência é dada aos solventes orgânicos dos grupos 1, 6, 8 e 9, e a suas misturas com água. Nas misturas com água a quantidade relativa de solvente orgânico e água pode variar de 10:1 a 1:10, em particular de 2:1 a 1:5.
[051] O processo de pasta fluida pode ser simplesmente executado mediante a suspensão de tiofanato metila e o pelo menos um composto A no solvente orgânico ou mistura de solvente/água. As quantidades relativas de tiofanato metila, o pelo menos um composto A e o solvente ou mistura de solvente/água serão selecionadas para obter uma suspensão na temperatura fornecida. A dissolução completa de tiofanato metila e o pelo menos um composto A deve ser evitada. Em particular tiofanato metila e o pelo menos um composto A são colocados em suspensão em uma quantidade de 50 a 800 g, mais preferivelmente de 100 a 600 g per litro de solvente ou mistura de solvente/água.
[052] A quantidade molar relativa de tiofanato metila e o pelo menos um composto A pode variar de 1:2 a 20:1, preferivelmente de 1:1 a 15:1. Se um dos componentes estiver em excesso com referência à estequiometria do complexo cristalino, uma mistura do complexo cristalino e do composto estando em excesso pode ser obtida, embora um excesso menor pode permanecer dissolvido na substância líquida mãe. Para propósitos de formulação, a presença de um excesso de composto A ou tiofanato metila pode ser aceitável. Em particular a presença de um excesso de tiofanato metila não causa problemas de estabilidade. Para a preparação do complexo cristalino puro, tiofanato metila e composto A serão usados em uma quantidade molar relativa que é próxima à estequiometria do complexo a ser formado e que geralmente não se desviará mais do que 50 % molar, com base na quantidade estequiometricamente requerida.
[053] O processo de pasta fluida é geralmente executado em uma temperatura de pelo menos 10 °C, preferivelmente pelo menos 20 °C e em particular pelo menos 30 °C, por exemplo, de 20 a 90 °C, preferivelmente de 30 a 85 °C, em particular de 40 a 70 °C.
[054] O tempo requerido para a formação do complexo cristalino pelo processo de pasta fluida depende da temperatura, do tipo de solvente e é geralmente pelo menos 12 h. Em qualquer caso, a conversão completa é alcançada após uma semana, no entanto, a conversão completa geralmente não exigirá mais do que 24 h.
[055] Em uma outra forma de realização preferida da invenção o complexo cristalino é preparado mediante a aplicação de forças de cisalhamento a um líquido que contém partículas em suspensão de tiofanato- metila e composto A ativo em uma temperatura de pelo menos 30 °C até que o complexo cristalino tenha se formado (processo de cisalhamento).
[056] No líquido, o tiofanato metila e o pelo menos um composto A estão presentes como partículas, que são colocadas em suspensão em um meio líquido. Após aplicação de forças de cisalhamento ao líquido em temperaturas elevadas, a formação do complexo cristalino ocorre.
[057] O principal constituinte do meio líquido é água ou um solvente orgânico, em que tiofanato metila e o composto A são praticamente insolúveis, isto é, a solubilidade a 25 °C é menor do que 5 g/l, em particular menor do que 1 g/l. Os solventes orgânicos adequados incluem hidrocarbonetos alifáticos, álcoois minerais, óleos vegetais e ésteres de óleo vegetal. Em uma forma de realização preferida, o meio líquido contém água ou uma mistura de água com até 20 % v/v de um solvente miscível em água, em particular um solvente do grupo 1 ou 9, como constituinte principal. Além disso, o meio líquido também pode conter aditivos que estão geralmente presentes em um concentrado de suspensão líquida.
[058] O meio líquido pode conter tiofanato metila e o composto A cristalino em uma quantidade de 5 a 70 % em peso, em particular de 10 a 60 % em peso e mais preferivelmente de 15 a 50 % em peso, com base no peso total do meio líquido, do composto A e do tiofanato metila.
[059] O meio líquido pode conter tiofanato metila e o composto A cristalino em uma quantidade molar relativa de tiofanato metila e o pelo menos um composto A variando de 1:2 a 20:1, preferivelmente de 1:1 a 15:1. Se um dos componentes estiver em excesso com referência à estequiometria do complexo cristalino, uma mistura do complexo cristalino e do composto estando em excesso será obtida. Para os propósitos de formulação, a presença de um excesso de composto A ou tiofanato metila pode ser aceitável. Em particular a presença de um excesso de tiofanato metila não causa problemas de estabilidade. Da mesma maneira, a presença de um excesso de composto A geralmente não causa problemas de estabilidade. Entretanto, é preferível que uma formulação não contenha nem tiofanato metila não complexo nem composto A não complexo em quantidades de mais do que 20 % em peso cada, nem em particular em quantidades de mais do que 10 % em peso cada, com base na quantidade de composto A e tiofanato presente na forma do complexo cristalino, de modo a evitar a formação descontrolada do complexo na formulação. Portanto, a presente invenção refere-se em particular às formulações contendo o complexo cristalino da presente invenção, contanto que, se ambos os compostos A e tiofanato estiverem presentes na formulação na forma não complexa, a quantidade do composto A não excede a 20 % em peso, em particular 10 % em peso, com base na quantidade de complexo na formulação, e ao mesmo tempo, a quantidade de tiofanato metila não excede a 20 % em peso, em particular 10 % em peso, com base na quantidade de complexo na formulação.
[060] O meio líquido pode incluir aditivos que estão geralmente presentes em um concentrado de suspensão líquida. Os aditivos adequados são descritos em seguida e incluem tensoativos, em particular emulsificantes aniônicos ou não iônicos, agentes umectantes e dispersantes geralmente empregados nas composições de proteção de lavouras, além disso agentes antiespumantes, agentes anticongelantes, agentes para o ajuste do pH, estabilizantes, agentes antiaglomerante, corantes e biocidas (conservantes). Preferivelmente, o meio líquido não contém aditivos de modificação da viscosidade (espessantes). A quantidade de tensoativos geralmente será de 0,5 a 20 % em peso, em particular de 1 a 15 % em peso e particularmente preferível de 1 a 10 % em peso, com base no peso total do meio líquido, do composto A e do tiofanato metila. A quantidade de agentes anticongelantes pode ser de até 10 % em peso, em particular até 20 % em peso, por exemplo, de 0,5 a 20 % em peso, em particular de 1 a 10 % em peso, com base no peso total do meio líquido, o composto A e tiofanato metila. Outros aditivos, além dos agentes anticongelantes e tensoativos, podem estar presentes em quantidades de 0 a 5 % em peso, com base no peso total do meio líquido, do composto A e do tiofanato metila.
[061] A temperatura requerida para a formação do complexo cristalino é geralmente pelo menos 30 °C, preferivelmente pelo menos 35 °C e em particular pelo menos 40 °C, mais preferivelmente pelo menos 50 °C, especialmente pelo menos 55 °C, por exemplo, de 30 a 100 °C, preferivelmente de 35 a 100 °C, em particular de 40 a 100 °C, mais preferivelmente de 50 a 90°C e especialmente de 55 a 80 °C.
[062] O tempo requerido para a formação do complexo cristalino depende de uma maneira conhecida per se sobre o tipo de processo de cisalhamento e a temperatura e pode ser determinado pela pessoa versada na técnica em experiências padrão. Os tempos de cisalhamento na faixa de, por exemplo, 30 min. a 48 horas foram observados de serem adequados, embora um período de tempo mais longo também é concebível. Um tempo de cisalhamento de 1 a 24 horas é preferível.
[063] As forças de cisalhamento podem ser aplicadas por técnicas adequadas, que são capazes de fornecer cisalhamento suficiente para levar as partículas de tiofanato metila e o pelo menos um composto A a um contato íntimo. As técnicas adequadas incluem trituração, compressão ou moagem, em particular mediante a trituração úmida ou moagem úmida, incluindo, por exemplo, a moagem de glóbulos incluindo ou mediante o uso de um moinho colóide. Os dispositivos de cisalhamento adequados incluem em particular moinhos de bolas ou moinhos de glóbulos, moinhos de bolas com agitador, moinhos circulantes (moinhos de bolas com agitador com sistema de moagem de pinos), moinhos de disco, moinhos de câmara anular, moinhos de cone duplo, moinhos de rolo triplo, moinhos de batelada, moinhos colóides e moinhos de membrana, tais como moinhos de areia. Para dissipar a energia térmica introduzida durante o processo de trituração, as câmaras de trituração são preferivelmente adaptadas com sistemas de esfriamento. Particularmente adequado é o moinho de bolas Drais Superflow DCP SF 12 da DRAISWERKE, INC.40 Whitney Road. Mahwah, NJ 07430 USA, um Drais Perl Mill PMC da DRAISWERKE, INC., o sistema de moinho circulante ZETA da Netzsch- Feinmahltechnik GmbH, o moinho de disco da Netzsch Feinmahltechnik GmbH, Selb, Germany, o moinho de glóbulos Eiger Mini 50 da Eiger Machinery, Inc., 888 East Belvidere Rd., Grayslake, IL 60030 USA e o moinho de glóbulos DYNO-Mill KDL da WA Bachofen AG, Switzerland. No entanto, outros equipamentos de homogeneização também podem ser adequados, incluindo os agitadores de alto cisalhamento, mecanismo Ultra-Turrax, misturadores estáticos, por exemplo, sistemas tendo bicos de mistura e outros equipamentos de homogeneização tais como moinhos colóides.
[064] Em uma forma de realização preferida da invenção, o cisalhamento é aplicado pela moagem de glóbulos. Em particular, as dimensões dos glóbulos na faixa de 0,05 a 5 mm, mais particularmente de 0,2 a 2,5 mm, e o mais particularmente de 0,5 a 1,5 mm foram observados de serem adequados. Em general, as cargas de glóbulo na faixa de 40 a 99 %, particularmente de 70 a 97 %, e mais particularmente de 65 a 95 % podem ser usadas.
[065] Após a aplicação de forças de cisalhamento suficientes,uma suspensão do complexo cristalino, opcionalmente em mistura com excesso de tiofanato metila ou composto ativo A, é obtida, em que 90 % em peso das partículas colocadas em suspensão possuem o tamanho de partícula de não mais do que 30 μm, preferivelmente não mais do que 20 μm, em particular não mais do que 10 μm, especialmente não mais do que 5 μm, como determinado pela dispersão luminosa dinâmica.
[066] A suspensão líquida assim obtida do complexo cristalino pode, após, ou em particular antes de uma formulação com aditivos, ser convertida por métodos de secagem costumeiros, em particular pela secagem por pulverização ou secagem por congelamento, nas composições em pó.Antes ou durante a secagem, um auxiliar de secagem ou de pulverização pode ser adicionado. Os auxiliares de secagem ou pulverização adequados para a secagem de dispersões aquosas são conhecidos. Estes incluem colóides de proteção, tais como álcool polivinílico, em particular álcool polivinílico tendo um grau de hidrólise de > 70 %, álcool polivinílico carboxilado, condensados deácido fenolsulfônico/formaldeído, condensados de ácidofenolsulfônico/uréia/formaldeído, condensados de ácidonaftalenossulfônico/formaldeído, condensados de ácidonaftalenossulfônico/formaldeído/uréia, polivinilpirrolidona, copolímeros de ácido maleico (ou anidrido maleico) e vinilaromáticos tais como estireno e seus derivados etoxilados, copolímeros de ácido maleico ou anidrido maleico com C2-C10-olefinas, tais como diisobuteno, e seus derivados etoxilados, polímeros catiônicos, por exemplo, homo- e copolímeros de compostos de N-alquil- N-vinilimidazolínio com lactamas de N-vinila e outros mais, e também agentes anti-bloqueio inorgânicos (às vezes também denominados com agentes antiaglomerantes), tais como ácido silícico, em particular, sílica pirogênica, alumina, carbonato de cálcio e outros mais. Os auxiliares de secagem são geralmente empregados em uma quantidade de 0,1 a 20 % em peso, com base no peso das partículas de composto ativo na composição líquida de pesticida da presente invenção.
[067] Como já mencionado acima, os complexos cristalinos como aqui definidos são adequados para a preparação de concentrados de suspensão para a preparação de concentrados de suspensão aquosa. Conseqüentemente, a invenção também fornece uma composição para a proteção da lavoura, que compreende um complexo cristalino como aqui definido, se apropriado uma fase líquida e também, se apropriado, veículos e/ou auxiliares costumeiros, geralmente sólidos.
[068] Os veículos adequados são, em princípio, todas substâncias sólidas geralmente usados em composições de proteção de lavouras, em particular em fungicidas. Os veículos sólidos são, por exemplo, terras minerais, tais como géis de sílica, silicatos, talco, caulim, attaclay, calcário, cal, giz, argila, limo argilo-calcário, argila, dolomita, terra diatomácea, sulfato de cálcio e sulfato de magnésio, óxido de magnésio, materiais sintéticos moídos, fertilizantes, tais como, por exemplo, sulfato de amônio, fosfato de amônio, nitrato de amônio, uréias e produtos de origem vegetal, tais como farinha de cereal, farinha de casca de árvore, serragem e farinha de casca de noz, pós de celulose e outros veículos sólidos.
[069] No caso de formulações líquidas dos complexos cristalinos, as composições possuem uma fase líquida. As fases líquidas adequadas são, em princípio, água e também solventes orgânicos em que a piraclostrobina possui baixa ou nenhuma solubilidade, por exemplo, aqueles em que a solubilidade de piraclostrobina a 25 °C e 1013 mbar não é mais do que 1 % em peso, em particular não mais do que 0,1 % em peso e especialmente não mais do que 0,01 % em peso.
[070] Os auxiliares típicos compreendem tensoativos, em particular os agentes umectantes e dispersantes geralmente empregados nas composições de proteção de lavouras, além disso aditivos de modificação da viscosidade (espessantes), agentes antiespumantes, agentes anticongelantes, agentes para o ajuste do pH, estabilizantes, agentes antiaglomerantes e biocidas (conservantes).
[071] A invenção refere-se em particular às composições para a proteção de lavouras na forma de concentrado de suspensão, em particular, um concentrado de suspensão aquosa (SC). Tais concentrados de suspensão compreendem o complexo cristalino em uma forma particulada finamente dividida, onde as partículas do complexo cristalino são colocadas em suspensão em um meio líquido, preferivelmente em um meio aquoso. O tamanho das partículas de composto ativo, isto é, o tamanho que não é excedido em 90 % em peso das partículas de composto ativo, é tipicamente não mais do que 30 μm, preferivelmente não mais do que 20 μm, em particular não mais do que 10 μm, especialmente não mais do que 5 μm, como determinado pela dispersão luminosa dinâmica. Vantajosamente, pelo menos 40 % em peso e em particular pelo menos 60 % em peso das partículas nos SCs de acordo com a invenção possuem diâmetros abaixo de 2 μm.
[072] Os concentrados de suspensão, em particular concentrados de suspensão aquosa, podem ser preparados mediante a suspensão do complexo cristalino em um portador líquido adequado, que pode conter aditivos de formulação convencionais como descrito mais abaixo. No entanto, é preferível preparar o concentrado de suspensão pelo processo de cisalhamento como aqui descrito, isto é, mediante a aplicação de forças de cisalhamento à um líquido que contém partículas colocadas em suspensão de tiofanato-metila e composto ativo A e opcionalmente outros aditivos em uma temperatura de pelo menos 30 °C até que o complexo cristalino tenha sido formado.
[073] Além do composto ativo, os concentrados de suspensão tipicamente compreendem tensoativos, e também, se apropriado, agentes antiespumantes, espessantes, agentes anticongelantes, estabilizantes (biocidas), agentes para o ajuste do pH e agentes antiaglomerantes.
[074] Em tais SCs, a quantidade de composto ativo, isto é, a quantidade total do complexo cristalino e, se apropriado, outros compostos ativos, está geralmente na faixa de 10 a 70 % em peso, em particular na faixa de 15 a 50 % em peso, com base no peso total do concentrado de suspensão.
[075] Os tensoativos preferidos são tensoativos aniônicos e não iônicos (emulsificantes). Os tensoativos adequados também são colóides de proteção. A quantidade de tensoativos geralmente será de 0,5 a 20 % em peso, em particular de 1 a 15 % em peso e particularmente preferível de 1 a 10 % em peso, com base no peso total dos SCs de acordo com a invenção. Preferivelmente, os tensoativos compreendem pelo menos um tensoativo aniônico e pelo menos um tensoativo não iônico, a relação de tensoativo aniônico para não iônico tipicamente estando na faixa de 10:1 a 1:10.
[076] Exemplos de tensoativos aniônicos (tensoativos, emulsificantes e dispersantes aniônicos) incluem sulfonatos de alquilarila, sulfonatos de fenila, sulfatos de alquila, sulfonatos de alquila, sulfatos de éter alquílico, sulfatos de éter alquilarílico, fosfatos de alquil poliglicol éter, fosfatos de éter poliaril fenílico, sulfossuccinatos de alquila, sulfonatos de olefina, sulfonatos de parafina, sulfonatos de petróleo, tauridas, sarcosídeos, ácidos graxos, ácidos alquilnaftalenossulfônicos, ácidos snaftalenossulfônicos, ácidos lignossulfônicos, condensados de naftalenos sulfonados com formaldeído ou com formaldeído e fenol e, se apropriado, uréia, e também condensados de ácido fenolsulfônico, formaldeído e uréia, substâncias líquidas residuais de lignossulfito e lignossulfonatos, fosfatos de alquila, fosfatos de alquilarila, por exemplo, fosfatos de triestirila, e o metal alcalino, metal terroso alcalino, sais de amônio e amina das substâncias mencionadas acima. Os tensoativos aniônicos preferidos são aqueles que carregam pelo menos um grupo de sulfonato, e em particular seu metal alcalino e seus sais de amônio.
[077] Exemplos de tensoativos não iônicos (emulsificantes e dispersantes não iônicos) compreendem alcoxilados de alquilfenol, alcoxilados de álcool, alcoxilados de amina graxos, ésteres de ácido graxo de polioxietileno glicerol, alcoxilados de óleo de mamona, alcoxilados de ácido graxo, alcoxilados de amida graxa, polidietanolamidas graxas, etoxilados de lanolina, ésteres poliglicol de ácido graxo, álcool isotridecílico, amidas graxas, metilcelulose, ésteres de ácido graxo, poliglicosídeos de alquila, ésteres de ácido graxo de glicerol, polietileno glicol, polipropileno glicol, copolímeros de bloco de polietileno glicol/polipropileno glicol, éteres alquílicos de polietileno glicol, éteres alquílicos de polipropileno glicol, copolímeros de bloco de éter de polietileno glicol/polipropileno glicol (copolímeros de bloco de óxido de polietileno/óxido de polipropileno) e misturas destes. Os tensoativos não iônicos preferidos são etoxilados de álcool graxo, alquil poliglicosídeos, ésteres de glicerol ácido graxo, alcoxilados de óleo de mamona, alcoxilados de ácido graxo, alcoxilados de amida graxa, etoxilados de lanolina, ésteres de ácido graxo poliglicol e copolímeros de bloco de óxido de etileno/óxido de propileno e misturas destes.
[078] Os colóides de proteção são tipicamente polímeros anfifílicos solúveis em água. Exemplos incluem proteínas e proteínas desnaturadas tais como caseína, polissacarídeos tais como derivados de amido e derivados de celulose solúveis em água, em particular amidos e celuloses modificados hidrofóbicos, além disso policarboxilatos tais como ácido poliacrílico (poliacrilatos), copolímeros de ácido acrílico ou ácido metacrílico ou copolímeros de ácido maleico tais como copolímeros de ácido acrílico/olefina, ácido acrílico, copolímeros de estireno, copolímeros de anidrido maleico/olefina (por exemplo, Sokalan® CP9, BASF) e os produtos de esterificação de ditos copolímeros com polietileno glicóis, polivinilálcool, polivinilpirrolidona, copolímeros de vinilpirrolidona, polivinilaminas, polietileniminas e éteres de polialquileno.
[079] Em particular, os SCs de acordo com a invenção compreendem pelo menos um tensoativo que melhora a umectação das partes do vegetal mediante a forma de aplicação aquosa (agente umectante) e pelo menos um tensoativo que estabiliza a dispersão das partículas de composto ativo no SC (dispersante). A quantidade de agente umectante está tipicamente na faixa de 0,5 a 10 % em peso, em particular de 0,5 a 5 % em peso e especialmente de 0,5 a 3 % em peso, com base no peso total do SC. A quantidade de dispersante é tipicamente de 0,5 a 10 % em peso e em particular de 0,5 a 5 % em peso, com base no peso total do SC.
[080] Os agentes umectantes preferidos são de natureza aniônica ou não iônica e selecionados, por exemplo, de ácidosnaftalenossulfônicos incluindo seus sais de metal alcalino, metal terrosoalcalino, amônio e amina, além disso, etoxilados de álcool graxo, alquil poliglicosídeos, ésters de ácido graxo de glicerol, alcoxilados de óleo de mamona, alcoxilados de ácido graxo, alcoxilados de amida graxa, polidietanolamidas graxas, etoxilados de lanolina e ésteres de ácido graxo de poliglicol.
[081] Os dispersantes preferidos são de natureza aniônica ou não iônica e selecionados, por exemplo, de copolímeros de bloco de polietileno glicol/polipropileno glicol, éteres alquílicos de polietileno glicol, éteres alquílicos de polipropileno glicol, copolímeros de éter de polietileno glicol/polipropileno glicol, fosfatos de alquilarila, por exemplo, fosfatos de triestirila, ácidos lignossulfônicos, condensados de naftalenos sulfonados com formaldeído ou com formaldeído e fenol e, se apropriado, uréia, e também condensados de ácido fenolsulfônico, formaldeído e uréia, substâncias líquidas residuais de lignossulfito e lignossulfonatos, policarboxilatos, tais como, por exemplo, poliacrilatos, copolímeros de anidrido maleico/olefina (por exemplo Sokalan® CP9, BASF), incluindo os sais de metal alcalino, metal alcalino terroso, amônio e amina das substâncias mencionadas acima.
[082] Os aditivos de modificação da viscosidade (espessantes) adequados para os SCs de acordo com a invenção são em particular compostos que se aplicam após as propriedades de fluxo pseudoplásticas da formulação, isto é, viscosidade elevada no estado em repouso e viscosidade baixa no estado agitado. Adequados são, em princípio, todos os compostos usados para este propósito em concentrados de suspensão. Menção pode ser feita, por exemplo, de substâncias inorgânicas, tais como bentonitas ou atapulgitas (por exemplo Attaclay®da Engelhardt), e substâncias orgânicas, tais como polissacarídeos e heteropolissacarídeos, tais como Xantan Gum® (Kelzan®da Kelco), Rhodopol®23 (Rhone Poulenc) ou Veegum®(da R.T. Vanderbilt), e preferência é dada ao uso de Xantan-Gum®. Freqüentemente, a quantidade de aditivos de modificação da viscosidade é de 0,1 a 5 % em peso, com base no peso total do SC.
[083] Os agentes antiespumantes adequados para os SCs de acordo com a invenção são, por exemplo, emulsões de silicona conhecidas para este propósito (Silikon®SRE, da Wacker, ou Rhodorsil®da Rhodia), álcoois de cadeia longa, ácidos graxos, desespumantes do tipo de dispersões aquosas de cera, desespumantes sólidos (assim chamados compostos), compostos de organoflúor e misturas destes. A quantidade de agente antiespumante é tipicamente de 0,1 a 1 % em peso, com base no peso total do SC.
[084] Conservantes podem ser adicionados para a estabilização dos concentrados de suspensão de acordo com a invenção. Os conservantes adequados são aqueles baseados em isotiazolonas, por exemplo, Proxel®da ICI ou Acticide® RS da Thor Chemie ou Kathon® MK da Rohm & Haas. A quantidade de bactericidas é tipicamente de 0,05 a 0,5 % em peso, com base no peso total do SC.
[085] Os agentes anticongelantes adequados são polióis líquidos, por exemplo, etileno glicol, propileno glicol ou glicerol. A quantidade de agentes anticongelantes é geralmente de 1 a 20 % em peso, em particular de 5 a 10 % em peso, com base no peso total do concentrado de suspensão.
[086] Se apropriado, os SCs de acordo com a invenção podem compreender tamponantes para a regulação do pH. Exemplos de tamponantes são sais de metal alcalino de ácidos inorgânicos ou orgânicos fracos, tais como, por exemplo, ácido fosfórico, ácido bórico, ácido acético, ácido propiônico, ácido cítrico, ácido fumárico, ácido tartárico, ácido oxálico e ácido succínico.
[087] Se as formulações dos complexos cristalinos forem usadas para o tratamento de sementes, elas podem compreender outros componentes costumeiros como empregados no tratamento de sementes, por exemplo, em corretivos ou revestimentos. Exemplos são em particular colorantes, adesivos, cargas e plastificantes além dos componentes acima mencionados.
[088] Os colorantes são todos corantes e pigmentos que são costumeiros para tais propósitos. Neste contexto, tanto os pigmentos, que são moderadamente solúveis em água, quanto os corantes, que são solúveis em água, podem ser usados. Exemplos que podem ser mencionados são as corantes e os pigmentos conhecidos sob os nomes Rhodamin B, C. I. Pigment Red 112 e C. I. Solvent Red 1, Pigment blue 15:4, Pigment blue 15:3, Pigment blue 15:2, Pigment blue 15:1, Pigment blue 80, Pigment yellow 1, Pigment yellow 13, Pigment red 48:2, Pigment red 48:1, Pigment red 57:1, Pigment red 53:1, Pigment orange 43, Pigment orange 34, Pigment orange 5, Pigment green 36, Pigment green 7, Pigment white 6, Pigment brown 25, Basic violet 10, Basic violet 49, Acid red 51, Acid red 52, Acid red 14, Acid blue 9, Acid yellow 23, Basic red 10, Basic red 108. A quantidade de colorantes geralmente não excederá a 20 % em peso da formulação e preferivelmente varia de 0,1 a 15 % em peso, com base no peso total da formulação.
[089] Os adesivos são todos aglutinantes costumeiros que podem ser empregados nos produtos curativos. Exemplos de aglutinantes adequados compreendem polímeros termoplásticos tais como polivinilpirrolidona, acetato de polivinila, álcool polivinílico e tilose, além disso, poliacrilatos, polimetacrilatos, polibutenos, poliisobutenos, poliestireno, polietilenominas, polietilenoamidas, os colóides de proteção anteriormente mencionados, poliésteres, polieterésteres, polianidridos, poliesteruretanos, poliesteramidas, polissacarídeos termoplásticos, por exemplo, derivados de celulose tais como ésteres de celulose, éteres de celulose, éter éster de celulose incluindo metilcelulose, etilcelulose, hidroximetilcelulose, carboximetilcelulose, hidroxipropilcelulose e derivado de amido e amidos modificados, dextrinas, maltodextrinas, alginatos e quitosanos, além do mais gorduras, óleos, proteínas, incluindo caseína, gelatina e zeínas, gomas arábicas, goma-laca. Os adesivos preferidos são biocompatíveis, isto é, eles não possuem uma atividade fitotóxica perceptível. Preferivelmente os adesivos são biodegradáveis. Preferivelmente o adesivo é selecionado de modo que atue como uma matriz para os ingredientes ativos da formulação. A quantidade de adesivos geralmente não excederá a 40 % em peso da formulação e preferivelmente varia de 1 a 40 % em peso, e em particular na faixa de 5 a 30 % em peso, com base no peso total da formulação.
[090] Além do adesivo a formulação também pode conter cargas inertes. Exemplos para estes incluem os materiais veículos sólidos anteriormente mencionados, especialmente os materiais inorgânicos particulados finos tais como argilas, giz, bentonita, caulim, talco, perlita, mica, sílica, terra diatomácea, pó de quartzo, montmorilonita, mas também materiais orgânicos particulados finos tais como serragens, farinhas de cereal, carvão ativado e outros mais. A quantidade de carga é preferivelmente selecionada em que a quantidade total da carga não exceda a 75 % em peso, com base no peso total de todos os componentes não voláteis da formulação. Comumente, a quantidade de carga varia de 1 a 50 % em peso, com base no peso total de todos os componentes não voláteis da formulação.
[091] Além disso, a formulação também pode conter um plastificante, que aumenta a flexibilidade do revestimento. Exemplos de plastificantes incluem polialquilenoglicóis oligoméricos, glicerol, ftalatos de dialquila, ftalatos de alquilbenzila, benzoatos de glicola e compostos relacionados. A quantidade de plastificante no revestimento freqüentemente varia de 0,1 a 20 % em peso, com base no peso total da formulação.
[092] Os complexos cristalinos da invenção podem ser usados em uma maneira conhecida per se para o controle de fungos fitopatogênicos ou pestes de insetos, dependendo do composto A. Em particular, os complexos cristalinos podem ser formulados juntamente com outros compostos ativos, para aumentar a atividade e/ou para ampliar o espectro de atividade. Estes incluem, em princípio, todos os inseticidas e fungicidas que são tipicamente usados juntamente com piraclostrobina. Os novos complexos cristalinos da invenção podem ser usados na proteção de plantas como fungicidas foliares, curativos e de solo.
[093] Eles são particularmente importantes para o combate de uma multiplicidade de fungos em várias plantas cultivadas, tais como trigo, centeio, cevada, triticale, aveia, arroz, milho, grama, banana, algodão, soja, café, cana de açúcar, parreiras, frutas e plantas ornamentais, e vegetais, tais como pepinos, feijão, tomate, batata e abóboras, e nas sementes destas plantas.
[094] Os complexos cristalinos da invenção são particularmente adequados para a formulação de união como concentrados de suspensão com compostos ativos que por sua vez podem ser formulados como concentrados de suspensão. Conseqüentemente, uma forma de realização preferida da invenção diz respeito aos concentrados de suspensão que, além do complexo cristalino, compreendem pelo menos um outro composto ativo na forma particulada finamente dividida. Com respeito aos tamanhos de partícula, a quantidade de composto ativo e auxiliares, que foi dita acima, se aplica.
[095] Outros pares de mistura típicos dos complexos cristalinos incluem os compostos A anteriormente mencionados, em particular os fungicidas e inseticidas/acaricidas anteriormente mencionados.
[096] Em princípio, as formulações dos complexos cristalinos de acordo com a presente invenção podem ser usadas para o combate de todas as doenças de plantas causadas por fungos nocivos ou outras pestes, que podem ser combatidas com as formulações convencionais de uma combinação do tiofanato metila e do composto ativo A. Dependendo do composto A ou o outro par de mistura, por exemplo, é uma das seguintes doenças de planta: • Espécies Alternaria em vegetais, semente de colza,beterraba açucareira, soja, cereais, algodão, fruta e arroz, (por exemplo, A. solani ou A. alternata em batata e várias plantas) • Espécies Aphanomyces em beterraba açucareira evegetais, • Ascochyta sp. em algodão e arroz, • Bipolaris e Drechslera species em milho, cereais, arroz egramados, (por exemplo, D. teres em cevada, D. tritci-repentis em trigo) • Blumeria graminis (mofo pulverulento) em cereais, • Botrytis cinerea (mofo cinza) em morangos, vegetais, florese parreiras, Botryodiplodia sp. em algodão, Bremia lactucae em alface, • Espécies Cercospora em milho, feijão de soja, arroz ebeterraba açucareira, (por exemplo C. beticula em beterrabas açucareiras), • Espécies Cochliobolus em milho, cereais, arroz (porexemplo, Cochliobolus sativus em cereais, Cochliobolus miyabeanus em arroz), • Corynespora sp. em feijão de soja, algodão e váriasplantas, • Espécies Colletotricum em feijão de soja, algodão, e váriasplantas, (por exemplo, C. acutatum em várias plantas) • Curvularia sp. em cereais e arroz, • Diplodia sp. em cereais e milho, • Exserohilum species em milho, • Erysiphe cichoracearum e Sphaerotheca fuliginea emabóboras, • Espécies Fusarium e Verticillium (por exemplo, V dahliae)em várias plantas, (por exemplo, F. graminearum em trigo) • Gaeumanomyces graminis em cereais, • Espécies Gibberella em cereais e arroz (por exemplo,Gibberella fujikuroi em arroz), • Grainstaining complex em arroz, • Espécies Helminthosporium (por exemplo, H. graminicola)em milho e arroz, • Macrophomina sp. em soja e algodão, • Michrodochium sp, por exemplo, M. nivale, em cereais, • Espécies Mycosphaerella em cereais, banana e amendoim,(M. graminicola em trigo, M. fijiesis em banana), • Phaeoisaripsis sp. em feijão de soja Phakopsara sp, por exemplo, P. pachyrhizi e Phakopsarameibomiae em feijão de soja, • Phoma sp. em feijão de soja • Espécies Phomopsis em feijão de soja, girassóis eparreiras, (P. viticola em parreiras, P. helianthii em girassóis), • Phytophthora infestans em batata e tomate, • Plasmopara viticola em parreiras, • Penecilium sp. em feijão de soja e algodão, • Podosphaera leucotricha em maças, • Pseudocercosporella herpotrichoides em cereais, • Espécies Pseudoperonospora em lúpulo e abóboras, (porexemplo, P. cubenis em cucumber), • Espécies Puccinia em cereais, milho e aspargo (P. triticinae P. striformis em trigo, P. asparagi em aspargo), • Pyrenophora species em cereais, • Pyricularia oryzae, Corticium sasakii, Sarocladium oryzae,S. attenuatum, Entyloma oryzae em arroz, - Pyricularia grisea em gramados e cereais, - Pythium spp. em gramados, arroz, milho, algodão, sementede colza, girassóis, beterraba açucareira, vegetais e várias plantas, - Rhizoctonia species (por exemplo, R. solani) em algodão,arroz, batata, gramados, milho, semente de colza, batata, beterraba açucareira, vegetais e várias plantas, - Rynchosporium sp. (por exemplo, R secalis) em arroz ecereais, - Espécies Sclerotinia em semente de colza, girassóis, evárias plantas, - Septoria tritici e Stagonospora nodorum em trigo, - Erysiphe (syn. Uncinula) necator em parreiras, - Setospaeria species em milho e gramados, - Sphacelotheca reilinia em milho, - Espécies Thievaliopsis em feijão de soja e algodão, - Espécies Tilletia em cereais, - Espécies Ustilago em cereais, milho e beterrabaaçucareira, e - Espécies Venturia (scab) em maças e pêras (por exemplo,(z.B. V. inaequalis em maças).
[097] Os complexos de acordo com a presente invenção podem ser formulados com outros compostos que apresentam uma atividade contra insetos, acaricidas ou nematóides em uma maneira conhecida per se. Além disso, tem comprovado ser particularmente vantajoso fornecer um complexo cristalino de tiofanato metila com um composto A que é ativo contra insetos de ferrão, mastigadores, cortantes ou sugadores e outros artrópodes, ou para formular um complexo cristalino juntamente com pelo menos um tal outro ingrediente ativo que é ativo contra insetos de ferrão, mastigadores, cortantes ou sugadores e outros artrópodes. Os insetos de ferrão, mastigadores, cortantes ou sugadores e outros artrópodes, incluem, por exemplo, insetos da ordem das - Coleoptera, em particular Phyllophaga sp. tal comoPhyllophaga cuyabana, Sternechus sp. tal como Sternechus pingusi, Sternechuns subsignatus, Promecops sp. tal como Promecops carinicollis, Aracanthus sp. tal como Aracanthus morei, e Diabrotica sp. tal como Diabrotica speciosa, Diabrotica longicornis, Diabrotica 12-punctata, Diabrotica virgifera, - Lepidoptera, em particular Elasmopalpus sp. tal comoElasmopalpus lignosellus, Diloboderus sp., - Isoptera, em particular Rhinotermitida, - Homoptera, em particular Dalbulus maidis, e nematóides, incluindo nematóides do nó da raiz, por exemplo Meloidogyne spp. tal como Meloidogyne hapla, Meloidogyne incognita, Meloidogyne javanica e outras espécies Meloidogyne species; nematóides de formação de cisto tais como Globodera rostochiensis e outras espécies Globodera; Heterodera avenae, Heterodera glycines, Heterodera schachtii, Heterodera trifolii e outras espécies Heterodera; nematóides Gall, por exemplo, espécies Anguina; anguilulas do caule e nematóides foliares tais como espécies Aphelenchoides.
[098] Por exemplo, uma formulação compreendendo um complexo cristalino de piraclostrobina e tiofanato-metila pode ser usada para o combate dos seguintes fungos nocivos: - Alternaria sp. cereais, algodão e arroz, - Ascochyta sp. em algodão e arroz, - Botryodiplodia sp. em algodão, - Cercospora species em milho, feijão de soja, arroz e váriasplantas, - Corynespora sp. em feijão de soja, algodão e váriasplantas, - Colletotrichum species em feijão de soja, algodão e váriasplantas, - Curvularia sp. em cereais e arroz, - Diplodia sp. em cereais e arroz, - Drechslera sp. em cereais e arroz, - Fusarium sp. em cereais, feijão de soja e algodão, - Giberella sp. em cereais e arroz, - Macrophomia sp. feijão de soja e algodão, - Penecilium sp. em feijão de soja e algodão - Phaeoisaripsis sp. em feijão de soja, - Phoma sp. em feijão de soja, - Phomopsis sp. em feijão de soja, - Pythium sp. em feijão de soja e algodão, - Pyrenophora sp. - Pyricularia sp. em arroz, - Rhizoctonia sp. em soja, arroz e algodão, - Rhychosporium sp. em arroz, - Septoria sp. em soja, - Tilletia sp. em cereais e arroz, - Ustilago sp. em cereais.
[099] Por exemplo, uma formulação compreendendo complexo cristalino de piraclostrobina e tiofanato-metila juntamente com fipronila ou um outro antagonista de GABA tal como acetoprol, endosulfan, etiprol, vaniliprol, pirafluprol ou piriprol como um outro ingrediente, pode ser usada para o combate de um dos seguintes fungos nocivos como mencionado acima e ao mesmo tempo para o combate de insetos, por exemplo, - Coleoptera, em particular Phyllophaga sp. tal comoPhyllophaga cuyabana, Sternechus sp. tal como Sternechus pingusi, Sternechuns subsignatus, Promecops sp. tal como Promecops carinicollis, Aracanthus sp. tal como Aracanthus morei, e Diabrotica sp. tal como Diabrotica speciosa, Diabrotica longicornis, Diabrotica 12-punctata, Diabrotica virgifera, Oryzophagus sp., e - Lepidoptera, em particular Elasmopalpus sp. tal comoElasmopalpus lignosellus, Diloboderus sp.
[0100] Uma formulação, compreendendo tiofanato metila e epoxiconazol, pode ser usada, por exemplo, para o combate dos seguintes fungos nocivos: - Microdochium sp. em cereais. - Tilletia sp. em cereais e arroz, - Ustilago sp. em cereais.
[0101] Uma formulação, compreendendo tiofanato metila e metconazol, pode especialmente ser usada, por exemplo, para o combate dos seguintes fungos nocivos: - Rhynchosporium sp. em cereais. - Sphacelotheca sp. em milho, - Septoria sp. em soja.
[0102] Os novos complexos cristalinos permitem a preparação de concentrados de suspensão aquosa com pouco solvente ou livre de solvente tanto de complexo cristalino por si mesmos quanto dos complexos cristalinos com outros agentes de proteção da lavoura, em particular os pares de mistura indicados acima. O teor de solvente, em particular o teor de hidrocarbonetos aromáticos, sem qualquer agente anticongelante, é geralmente não mais do que 2 % em peso do concentrado de suspensão e está freqüentemente abaixo de 2 % em peso. Os concentrados de suspensão de acordo com a invenção são distintos, em particular, com estabilidade de armazenagem superior comparado como os concentrados de suspensão conhecidos e concentrados de suspoemulsão contendo um composto A ou uma mistura de composto A com tiofanato metila.
[0103] As figuras e exemplos abaixo servem para ilustrar a invenção e não devem ser compreendidas como limitativas dela.
[0104] Figura 1: difractograma em pó de raio X de tiofanato metila.
[0105] Figura 2: difractograma em pó de raio X de epoxiconazol.
[0106] Figura 3: difractograma em pó de raio X de piraclostrobina.
[0107] Figura 4: difractograma em pó de raio X do complexocristalino de tiofanato metila e epoxiconazol.
[0108] Figura 5a: Estrutura do complexo cristalino de tiofanato metila e epoxiconazol de acordo com a análise de raio X dos cristais isolados, com ligações potenciais de hidrogênio indicadas.
[0109] Figura 5b: Disposição espacial das moléculas de tiofanato metila no complexo cristalino de tiofanato metila e epoxiconazol de acordo com a análise de raio X dos cristais isolados, com ligações potenciais de hidrogênio.
[0110] Figura 6: difractograma em pó de raio X do complexo cristalino de tiofanato metila e piraclostrobina.
[0111] Figura 7: Espectros 13C-CP/MAS de piraclostrobina (acima), tiofanato metila (central) e o complexo cristalino de tiofanato metila e piraclostrobina (abaixo).
[0112] Figura 8: difractograma em pó de raio X do complexo cristalino de tiofanato metila e metconazol.
[0113] Figura 9: Espectro de IR do complexo cristalino de piraclostrobina e tiofanato metila.
[0114] Figura 10: Espectro de IR do complexo cristalino de metconazol e tiofanato metila.
[0115] Análise:
[0116] As imagens dos difractogramas em pó de raio X (PXRD) foram tiradas usando um difractômetro D-5000 da Siemens em geometria de reflexão na faixa de 2θ = 4° - 35° com aumentos de 0,02° usando radiação Cu- Kα em 25 °C. Os valores 2θ encontrados foram usados para calcular o espaçamento interplanar mencionado d.
[0117] Difração de raio X do cristal isolado. Os dados foram coletados em 103(2) K em um Bruker AXS CCD Detector, usando uma radiação CuKα monocromada por grafita (À = 1,54178 A). A estrutura foisolucionada com métodos diretos, refinada e expandida mediante o uso de técnicas de Fourier com o pacote de software SHELX-97.
[0118] As análises térmicas termogravimétricas/diferenciais foram realizadas com um Mettler Toledo TGA/SDTA 851 usando Al2O3 como referência. As amostras (8-22 mg) foram colocadas em copos de amostra de platina para a medição. Um programa de temperatura de 30 a 605 °C em 10 °C/min e fluxo de gás de N2 foi usado.
[0119] As determinações calorimétricas de varredura diferenciais (DSC) foram feitas em um Mettler Toledo DSC 823e com TS0801RO Sample Robot e TS08006C1 Gas Control. As medições foram feitas com taxas de aquecimento de 5 °C/min de 30 a 185°C usando cadinhos de alumínio com orifícios.
[0120] As medições 13C-CP/MAS foram operadas em um instrumento BRUKER Avance 300 ligado a um ímã de furo grande 7T, freqüência de ressonância 13C foi de 75,47 MHz. Uma sonda Bruker MAS com 7 mm o.d. ZrO2 rotores, movimento giratório em 5700 Hz foi usada (isto produz faixas laterais de movimento giratório espaçadas 75,5 ppm do sinal isotrópico). Os espectros 13C foram gerados pela polarização cruzada (Hartmann-Hahn contact 3ms, B1= 45 kHz), tempo de aquisição 35 ms, desacoplamento modulado TPPM (B1=45 kHz) durante a aquisição, tempo de espera 2s até 120s, dependendo do tempo de relaxamento longitudinal suspeito (ou medido) T1(H) dos prótons; número de varreduras de 500 a 10.000, dependendo do tempo de espera usado. A escala de ppm foi externamente calibrada, fixação do sinal de campo baixo de adamantano em 38,066 ppm. Uma medição típica, no “cristal misturado”, por exemplo, envolveu 500 varreduras com um tempo de espera de 120 s entre as verreduras, assim usando um tempo de medição total de 17 hrs.
[0121] Os espectros de IR das amostras foram medidos a partir das tabelas KBr em um espectrômetro Thermo Nicolet Nexus 470 IR com um detector DTGS KBr.
[0122] Os tamanhos de partícula nos concentrados de suspensão foram determinados usando um Mastersizer 2000 da Malvern Instruments GmbH.
[0123] Epoxiconazol foi usado como uma mistura racêmica. É sabido de existir na forma cristalina monoclínica I que é termodinamicamente estável a 22 °C. Uma estrutura cristalina isolada de Forma I foi determinada (monoclínica, grupo de espaço P21/n, a = 5,396 A, b = 17,304 A, c = 16,568 A, β = 91,742°). Os dados de PXRD experimental são fornecidos na figura 2. A Forma I possui uma faixa de fusão de 130 a 140 °C.
[0124] Tiofanato metila é conhecido de existir na forma cristalina monoclínica que é termodinamicamente estável a 22 °C. A análise de raio X de cristal isolado revela uma célula única monoclínica (grupo de espaço P21/n) com dimensões a = 10,715 A, b = 11,548 A, c = 11,548 A e β = 90,49°. Tiofanato-M se decompõe diretamente após a fusão (p.f ~180 °C para a Forma I).
[0125] Piraclostrobina é conhecida de existir em polimorfos diferentes como descrito na WO 2006/136357. Para as seguintes experiências, polimorfo IV foi usado (ver PXRD na figura 3).
[0126] Exemplo 1: 1 g de tiofanato metila e 1,13 g de epoxiconazol (1:1 relação molar) foram fornecidos em um frasco de fundo redondo juntamente com 20 ml de mistura de propanodiol e água (1:3 v/v). A pasta fluida obtida foi agitada durante uma semana a 50 °C, após o que a mistura foi esfriada para 22 °C, filtrada e secada a 22 °C em uma placa de argila. Um PXRD revelou que o material cristalino obtido foi um co-cristal de tiofanato metila e epoxiconazol (figura 4). A fusão do complexo cristalino começa em 148
[0127] Exemplos de 2 a 6: O processo do exemplo 1 foi repetido mediante o uso de diferentes solventes ou misturas de solvente e água e aplicação de diferentes temperaturas como fornecido abaixo: Exp. 2: 1:3 glicerina:água (50 °C) Exp. 3: 1:3 carbonato de propileno:água (50 °C) Exp. 4: 1:3 carbonato de propileno:água (22 °C) Exp. 5: 1:3 isopropanol:água (50 °C) Exp. 6: Etanol (22 °C)
[0128] Em qualquer um dos exemplos de 2 a 6 um material cristalino foi obtido, que foi identificado por PXRD como sendo o complexo cristalino de tiofanato metila e epoxiconazol.
[0129] Exemplo 7: 2 g de tiofanato metila e 0,96 g depiraclostrobina (2:1 relação molar) foram fornecidos em um frasco de fundo redondo juntamente com 20 ml de mistura de propanodiol e água (1:3 v/v). A pasta fluida fornecida foi agitada durante uma semana em 50 °C, após o que mistura foi esfriada para 22 °C, filtrada e secada em 22 °C em uma placa de argila. Um PXRD revelou que o material cristalino obtido foi um co-cristal de tiofanato metila e piraclostrobina (figura 5). O material obtido foi identificado por PXRD como sendo o complexo cristalino de tiofanato metila e piraclostrobina.
[0130] Exemplos de 8 a 10: O processo do exemplo 7 foi repetido mediante o uso de diferentes solventes ou misturas de solvente e água e aplicação de diferentes temperaturas como fornecidas abaixo: Exp. 8: 1:3 glicerina:água (50 °C) Exp. 9: 1:3 carbonato de propileno:água (50 °C) Exp. 10: 1:3 carbonato de propileno:água (22 °C)
[0131] Em qualquer um dos exemplos de 8 a 10 um material cristalino foi obtido, que foi identificado por PXRD como sendo o complexo cristalino de tiofanato metila e piraclostrobina.
[0132] 13C-CP/MAS do material obtido dos exemplos de 7 a 10 confirmou a presença de um co-cristal em vez de uma mistura dos materiais cristalinos individuais. Em particular, piraclostrobina e metiltiofanato repousam com o mesmo T1(H): Uma pré-saturação do 1H seguido por um atraso de espera variável leva em conta o relaxamento parcial dos prótons. Esta polarização foi transferida de 1H para 13C através da polarização cruzada. As amplitudes dos sinais 13C de piraclostrobina e de metiltiofanato depois refletem o desenvolvimento da polarização do reservatório de 1H observado por cada um dos dois tipos de moléculas. Piraclostrobina e metiltiofanato apresentaram indicação de relaxamento de 1H idêntica que ambos foram acoplados no mesmo reservatório de 1H e assim devem ser vizinhos. Os sinais de ambos os componentes diminuíram identicamente, isto é, as escalas de espectro total como o reservatório de 1H diminuem. Os espectros tomados em diferentes atrasos (20s e 120 s res.) foram diferentes por um fator de dois em intensidade absoluta, mas completamente adaptados um ao outro após a representação em escala. O relaxamento de T1 dos prótons foi de 34,4 s (tiofanato metila puro 28,6 s, piraclostrobina pura 7,0 s).
[0133] Os seguintes aditivos de formulação foram usados.
[0134] Dispersante 1: Copolímero de bloco de óxido de etileno/óxido de propileno (Pluronic PE 10500 da BASF Aktiengesellschaft).
[0135] Dispersante 2: Copolímero de enxerto acrílico (Atlox 4913 da Uniquema).
[0136] Dispersante 3: Sulfato de amônio triestirilfenol etoxilado tendo 16 unidades de oxietileno: Soprophor 4D384 da Rhodia.
[0137] Dispersante 4: Sal de sódio do produto de condensação de ácido fenolsulfônico e formaldeído.
[0138] Desespumante: Desespumante de silício comercial (emulsão aquosa, 20 % em peso de ativos - Silfoam SRE obtido da Wacker Chemie AG.
[0139] Formulação de corante: Disperse Green
[0140] Exemplo 11 (comparativo): Uma amostra de 5 kg foi preparada de acordo com a receita fornecida na seguinte tabela (Todas as quantidades são fornecidas em g/kg). Todos os componentes exceto a solução de goma xantana aquosa e dispersão verde foram misturados em um recipiente e depois triturados por duas passagens consecutivas em 8 kg/h através de um moinho de glóbulos de 600 ml operando em uma velocidade de ponta de 6,7 m/s, enquanto mantém a mistura em 20 °C. À mistura obtida, a solução a 2 % de goma xantana e a formulação de corante foram fornecidas com agitação. Um líquido opaco verde homogêneo levemente viscoso foi obtido. O tamanho de partícula desta dispersão foi determinado pela difração de laser em uma diluição de 100 vezes em água para apresentar 90 % das partículas tendo um tamanho abaixo de 3,9 μm (valor D90). Piraclostrobina 42 Tiofanato-metila 378 Glicerol 70 Dispersante 1 30 Dispersante 2 19 Dispersante 3 6 Desespumante 5 Goma Xantana (2 % solução em água) 55 Formulação de corante 100 Água 295
[0141] Exemplo 12: Uma amostra de 5 kg foi preparada de acordo com a receita fornecida no exemplo 11. Todos os componentes exceto a solução de goma xantana e dispersão verde foram misturados em um recipiente. Esta mistura foi circulada em 20 kg/h durante 8 horas através de moinho de glóbulos de 600 ml operando em 6,8 m/s, enquanto mantém a mistura em 40 °C. À mistura obtida a solução a 2 % de goma xantana e a formulação de corante foram fornecidas com agitação. Um líquido opaco verde homogêneo levemente viscoso foi obtido. O tamanho de partícula desta dispersão foi determinado de acordo com o exemplo 11 para mostrar um valor D90 de 1,3 μm.
[0142] Uma amostra foi evaporada para secura. Um PXRD do material obtido revelou a presença do complexo cristalino de piraclostrobina e tiofanato metila além de excesso de tiofanato metila.
[0143] Exemplo 13 (comparativo): Uma amostra de 2 kg foi preparada de acordo com a receita fornecida na seguinte tabela (Todas as quantidades são fornecidas em g/kg). Todos os componentes exceto a solução de goma xantana aquosa foram misturados em um recipiente. Esta mistura é girada em 8 kg/h durante 4 horas através de um moinho de glóbulos de 600 ml operando em 6,8 m/s, enquanto mantém a mistura em 20 °C. À mistura obtida, a solução a 2 % de goma xantana foi fornecida com agitação. Um líquido opaco incolor homogêneo levemente viscoso foi obtido. O tamanho de partícula desta dispersão foi determinado de acordo com o exemplo 11 para apresentar um valor D90 de 1,4 μm. Piraclostrobina 42 Tiofanato-metila 378 Glicerol 70 Dispersante 1 30 Dispersante 2 19 Dispersante 3 6 Desespumante 5 Goma Xantana (2 % solução em água) 55 Água 295
[0144] Exemplo 14: Uma amostra de 2 kg foi preparada de acordo com a mesma receita e o mesmo procedimento como no exemplo 3, exceto que a mistura foi aquecida para 45 °C antes da moagem ter sido iniciada em mantida nesta temperatura durante a moagem por 4 horas. Um líquido opaco incolor homogêneo levemente viscoso foi obtido. O tamanho de partícula desta dispersão foi determinado de acordo com o exemplo 11 para apresentar um valor D90 de 1,5 μm.
[0145] A estabilidade das amostras produzidas nos exemplos 1, 2, 3 e 4 foi determinada mediante o armazenamento de uma sub-amostra de 100 ml em uma garrafa de HDPE durante um período definido em uma temperatura definida. Um teste de armazenagem típico deve ser para 8 semanas a 40 °C. Após a armazenagem, o tamanho de partícula foi determinado tanto por difração de laser em uma diluição de ~100 vezes quanto pela determinação do resíduo em uma peneira úmida de 150 μm.
[0146] Tipicamente uma boa qualidade de suspensão écaracterizada por um D90 < 10 μm e um resíduo de peneira úmida que é < 0,5 %.
[0147] Exemplo 15 (comparativo): Cerca de 350 g de água desmineralizada foram colocados em um recipiente. A este, 100 g de propileno glicol, 20 g de um dispersante 1, 30 g de dispersante 4, 2 g de um auxiliar de trituração (sílica amorfa) e 2 g de um desespumante (emulsão aq. de um óleo de silício) foram adicionados. A mistura foi agitada em 25 °C durante 15 min. com uma velocidade de agitação de 1000 rpm. Depois, 200 g de epoxiconazol e 300 g de tiofanato metila foram adicionados com agitação em 1000 rpm. A mistura foi depois triturada em um moinho de glóbulos como descrito no exemplo 11 até que pelo menos 80 % em peso das partículas tenha um diâmetro abaixo de 2 μm, enquanto mantém a mistura em 10 °C. À mistura obtida uma solução aquosa a 2 % de goma xantana e 2 g de uma formulação de biocida foram adicionados. Um líquido homogêneo levemente viscoso foi obtido. O tamanho de partícula desta dispersão foi determinado pela difração a laser de uma diluição de 100 vezes em água para apresentar 80 % das partículas tendo um tamanho abaixo de 2 μm (valor D90). Um PXRD do sólido mostrou uma mistura física de epoxiconazol e tiofanato metila.
[0148] Após 1 semana de armazenagem a 60 °C, a mistura se tornou altamente viscosa e a difração a laser de uma diluição de 100 vezes do líquido espesso em água mostrou que menos do que 25 % das partículas possui um tamanho de partícula abaixo de 2 μm (valor D90).
[0149] Exemplo 16: Uma formulação de epoxiconazol e tiofanato metila foi preparada de acordo com a receita geral e similar ao procedimento descrito no exemplo 15, mas executando a moagem em 50 °C em lugar de 10 °C. O tamanho de partícula desta dispersão foi determinado pela difração a laser de uma diluição de 100 vezes em água para apresentar 90 % das partículas tendo um tamanho abaixo de 2 μm (valor D90). Um PXRD dos sólidos mostrou que o material era o complexo cristalino de epoxiconazol e tiofanato metila.
[0150] Após 1 semana de armazenagem a 60 °C, a misturaviscosa era similar à viscosidade do líquido recentemente preparado e a difração a laser de uma diluição de 100 vezes do líquido espesso em água mostrou que 90 % das partículas possui um tamanho de partícula abaixo de 2 μm (valor D90).
[0151] Exemplo 17: 1 g de uma mistura de metconazol e tiofanato- metila (1:1 relação molar) foi colocado em um frasco de fundo redondo e transformado em substância líquida em 20 ml de glicerina a 50 °C durante 2 dias. A mistura foi esfriada lentamente para a temperatura ambiente, filtrada e deixada secar em uma placa de argila durante algumas horas. O sólido foi analisado por PXRD (ver a Figura 8) de ser > 95 - % de co-cristais puros de metconazol e tiofanato-metila. A medição de DSC do material mostrou um pico de fusão endotérmica com início em 155 a 158 °C e pico máximo em 160 a 168 °C. O espectro de IR é mostrado na figura 10.
[0152] Exemplo 18: 2 g de uma mistura de metconazol e tiofanato- metila (1:1 relação molar) foram dissolvidos em 50 ml de acetonitrila por aquecimento e agitação suaves. A solução foi filtrada e o filtrado foi deixado evaporar em um frasco aberto. Após 1 dia cristais em forma quadrada grandes o bastante para análise de raio X de cristal isolado foram obtidos. A solução de estrutura revelou um co-cristal de metconazol e tiofanato-metila 1:1. A experiência foi repetida em acetato de etila e nitrometano com resultados similares.
[0153] Exemplo 19: 32 partes em peso de tiofanato-metila e 6 partes em peso de metconazol foram transformados em pasta fluida em uma mistura de 50 partes em peso de água, 8 partes em peso de glicerina, 2 partes em peso de dispersante 1 e 2 partes em peso de dispersante 2. Esta mistura foi mecanicamente triturada em um moinho colóide durante 4 horas a 65 °C. A pasta fluida foi deixada esfriar e após a sedimentação do material sólido o sobrenadante foi decantado. O sedimento foi secado e analisado por IR para mostrar a presença de co-cristal de tiofanato metila e metconazol.
Claims (4)
1. COMPLEXO CRISTALINO, caracterizado por compreender pelo menos um composto orgânico A agricolamente ativo selecionado a partir de piraclostrobina, epoxiconazol e metconazol; e tiofanato-metila, em que o complexo cristalino compreende priraclostrobina e tiofanato-metila, em um difractograma em pó de raio X a 25 °C e Cu-Kα radiação, apresenta pelo menos quatro dos seguintes reflexos, fornecidos como valores 2θ: 4,9 ± 0,2°, 6,8 ± 0,2°, 8,5 ± 0,2°, 12,0 ± 0,2°, 14,5 ± 0,2°, 16,9 ± 0,2°, 20,4 ± 0,2°, 22,9 ± 0,2°, 25,5 ± 0,2°, 29,3 ± 0,2°; e em que o complexo cristalino compreende epoxiconazol e tiofanato-metila, em um difractograma em pó de raio X a 25 °C e Cu-Kα radiação, apresenta pelo menos quatro dos seguintes reflexos, fornecidos como valores 2θ: 6,2 ± 0,2°, 9,0 ± 0,2°, 9,8 ± 0,2°, 12,4 ± 0,2°, 15,1 ± 0,2°, 18,0 ± 0,2°, 21,9 ± 0,2°, 23,5 ± 0,2°, 24,7 ± 0,2°, 30,9 ± 0,2°; e em que o complexo cristalino compreende metconazol e tiofanato-metila, em um difractograma em pó de raio X a 25 °C e Cu-Kα radiação, apresenta pelo menos quatro dos seguintes reflexos, fornecidos como valores 2θ: 5,0 ± 0,2°, 9,9 ± 0,2°, 11,3 ± 0,2°, 12,0 ± 0,2°, 15,0 ± 0,2°, 16,7 ± 0,2°, 18,1 ± 0,2°, 21,6 ± 0,2°, 27,8 ± 0,2°.
2. PROCESSO DE PASTA FLUIDA PARA A PREPARAÇÃO DO COMPLEXO CRISTALINO, conforme definido na reivindicação 1, caracterizado por compreender a suspensão de tiofanato-metila e o composto A ativo em uma temperatura de pelo menos 30 °C em um solvente orgânico, possuindo uma miscibilidade com água de pelo menos 10% em temperatura ambiente, ou em uma mistura de água e um solvente orgânico possuindo uma miscibilidade com água de pelo menos 10% em temperatura ambiente, em que se obtém uma suspensão em pasta fluida, onde o tiofanato de metila e o composto A, em uma proporção de 1:2 a 20:1, são colocados em suspensão, em um uma quantidade de 50 a 800 g, mais preferivelmente de 100 a 600 g por litro de solvente ou uma mistura de solvente/água, em que o tempo de formação do complexo cristalino é de até uma semana, ou mais preferivelmente de 12 a 24 h.
3. PROCESSO DE CISALHAMENTO PARA A PREPARAÇÃO DO COMPLEXO CRISTALINO, conforme definido na reivindicação 1, caracterizado por compreender a aplicação de forças de cisalhamento capazes de fornecer cisalhamento suficiente para levar as partículas de tiofanato de metila e o composto A a um contato íntimo, a uma suspensão aquosa, que contém tiofanato-metila e composto A ativo na forma de partículas colocadas em suspensão no líquido aquoso, onde o principal constituinte do meio líquido é água ou um solvente orgânico, em que o tiofanato de metila e composto A estão na proporção de 1:2 a 20:1, e são praticamente insolúveis neste solvente, e a temperatura é de 35 a 100 ° C, mais preferivelmente de 50 a 90 °C, com um tempo de cisalhamento de 30 min a 48 horas, ou mais preferivelmente de 1 a 24 horas.
4. COMPOSIÇÃO AGRÍCOLA, caracterizada por compreender um complexo cristalino de tiofanato-metila e o composto agricolamente ativo A, conforme definido na reivindicação 1.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP07102083 | 2007-02-09 | ||
| EP07102083.8 | 2007-02-09 | ||
| PCT/EP2008/051562 WO2008096005A1 (en) | 2007-02-09 | 2008-02-08 | Crystalline complexes of agriculturally active organic compounds |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0807864A2 BRPI0807864A2 (pt) | 2014-06-17 |
| BRPI0807864A8 BRPI0807864A8 (pt) | 2016-03-08 |
| BRPI0807864B1 true BRPI0807864B1 (pt) | 2021-02-02 |
Family
ID=39186845
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0807864-5A BRPI0807864B1 (pt) | 2007-02-09 | 2008-02-08 | complexo cristalino, processos de pasta fluida e de cisalhamento para a preparação do complexo cristalino e composição agrícola |
Country Status (27)
| Country | Link |
|---|---|
| US (1) | US8859607B2 (pt) |
| EP (1) | EP2117297B1 (pt) |
| JP (1) | JP5523838B2 (pt) |
| KR (1) | KR101488034B1 (pt) |
| AR (1) | AR065288A1 (pt) |
| AT (1) | ATE542421T1 (pt) |
| AU (1) | AU2008212764B2 (pt) |
| BR (1) | BRPI0807864B1 (pt) |
| CA (1) | CA2675627C (pt) |
| CL (1) | CL2008000395A1 (pt) |
| CR (1) | CR10984A (pt) |
| CY (1) | CY1112576T1 (pt) |
| DK (1) | DK2117297T3 (pt) |
| EA (1) | EA017040B1 (pt) |
| EC (1) | ECSP099615A (pt) |
| ES (1) | ES2378909T3 (pt) |
| HR (1) | HRP20120198T1 (pt) |
| MX (1) | MX2009007733A (pt) |
| PE (1) | PE20081754A1 (pt) |
| PL (1) | PL2117297T3 (pt) |
| PT (1) | PT2117297E (pt) |
| RS (1) | RS52230B (pt) |
| SI (1) | SI2117297T1 (pt) |
| TW (1) | TW200901889A (pt) |
| UA (1) | UA97973C2 (pt) |
| WO (1) | WO2008096005A1 (pt) |
| ZA (1) | ZA200906209B (pt) |
Families Citing this family (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102160207A (zh) * | 2008-09-19 | 2011-08-17 | 巴斯夫欧洲公司 | 二苯并四苯基二茚并(1,2,3-cd:1’,2’,3’-lm)苝在有机太阳能电池中的用途 |
| GB0817513D0 (en) * | 2008-09-24 | 2008-10-29 | Syngenta Ltd | Co-crystals |
| GB0817976D0 (en) * | 2008-10-01 | 2008-11-05 | Syngenta Ltd | Co-crystals |
| WO2010118833A1 (de) | 2009-04-16 | 2010-10-21 | Bayer Technology Services Gmbh | Co-kristall umfassend imidacloprid und verfahren zu dessen herstellung |
| MX2012000421A (es) | 2009-07-28 | 2012-02-08 | Basf Se | Composiciones plaguicidas de suspo - emulsiones. |
| WO2011051242A1 (de) | 2009-10-27 | 2011-05-05 | Bayer Technology Services Gmbh | Co-kristall von 4- { [ (6-chlorpyrid-3-yl) methyl] (2,2-difluorethyl) amino} furan-2 (5h) -on mit salizylsäure und dessen verwendung als pestizid |
| US20120283294A1 (en) | 2009-10-27 | 2012-11-08 | Bayer Technology Services Gmbh | Co-crystal of 4-furan-2(5h)-one with benzoic acid and use thereof as pesticide |
| WO2011051241A1 (de) | 2009-10-27 | 2011-05-05 | Bayer Technology Services Gmbh | Co-kristall von 4-{[(6-chlorpyrid-3yl)methyl](2,2-difluorethyl)amino}furan-2(5h)-on mit oxalsäure und dessen verwendung als pestizid |
| KR20120115492A (ko) | 2009-11-06 | 2012-10-18 | 바스프 에스이 | 4―히드록시 벤조산 및 선택된 살충제의 결정질 복합체 |
| BRPI1000361B1 (pt) | 2010-02-05 | 2017-04-11 | Rotam Agrochem Int Co Ltd | composição fungicida, seu uso e métodos de prevenção e/ou combate a dano patogênio ou dano por pragas em uma planta |
| GB201006326D0 (en) * | 2010-04-15 | 2010-06-02 | Syngenta Ltd | Formulation |
| DE102010039687A1 (de) | 2010-08-24 | 2012-03-01 | Bayer Technology Services Gmbh | Pulverformulierung umfassend Imidacloprid und Oxalsäure, sowie Verfahren zur Herstellung von Co-Kristallen umfassend Imidacloprid und Oxalsäure durch Kompaktieren |
| US9161542B2 (en) | 2011-05-26 | 2015-10-20 | Dow Agrosciences Llc | Pesticidal compositions and related methods |
| WO2013162725A1 (en) * | 2012-04-25 | 2013-10-31 | Bayer Cropscience Lp | Metalaxyl and prothioconazole cocrystals and methods of making and using |
| GB201222287D0 (en) * | 2012-12-11 | 2013-01-23 | Ct For Process Innovation Ltd | Methods for making active crystalline materials |
| US9648879B2 (en) * | 2013-11-13 | 2017-05-16 | Nippon Soda Co., Ltd. | Co-crystal and method for producing same |
| US9635856B2 (en) | 2013-12-19 | 2017-05-02 | Nippon Soda Co., Ltd. | Co-crystal production method |
| RU2601603C1 (ru) * | 2015-09-11 | 2016-11-10 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Чувашский государственный педагогический университет им. И.Я. Яковлева" | Способ получения стимулятора зерновых культур |
| CN108503665A (zh) * | 2018-06-15 | 2018-09-07 | 天津大学 | 一种氟硅唑与甲基托布津农药共晶及其制备方法 |
| CA3166630A1 (en) | 2020-01-03 | 2021-07-08 | Berg Llc | Polycyclic amides as ube2k modulators for treating cancer |
| DE102022104759A1 (de) | 2022-02-28 | 2023-08-31 | SCi Kontor GmbH | Co-Kristall-Screening Verfahren, insbesondere zur Herstellung von Co-Kristallen |
| EP4660184A1 (en) * | 2023-01-30 | 2025-12-10 | Eurofarma Laboratórios S.A. | Nav1.7- and/or nav1.8-inhibiting hydroxamates, processes for the preparation thereof, compositions, uses, methods for treatment using same, and kits |
| AR131715A1 (es) * | 2023-01-30 | 2025-04-23 | Eurofarma Laboratorios S A | AMIDAS BLOQUEADORAS DE Nav 1.7 Y/O Nav 1.8, SUS PROCESOS DE OBTENCIÓN, COMPOSICIONES, USOS, MÉTODOS DE TRATAMIENTO DE LOS MISMOS Y KITS |
| CN116569919B (zh) * | 2023-04-26 | 2025-01-14 | 天津大学 | 一种响应型纳米农药递送系统及其制备方法和应用 |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5394036A (en) * | 1977-01-25 | 1978-08-17 | Hokko Chem Ind Co Ltd | Fungicides composition for agriculture and horticulture |
| JPS5681506A (en) * | 1979-12-07 | 1981-07-03 | Nippon Soda Co Ltd | Fungicidal composition for agricultural and horticultural use |
| JPS5916808A (ja) * | 1982-07-20 | 1984-01-28 | Hokko Chem Ind Co Ltd | 農園芸用殺菌剤 |
| IL78175A (en) * | 1985-03-29 | 1989-10-31 | Basf Ag | Azolylmethyloxiranes,their preparation and their use as fungicide crop protection agents |
| JPH07121842B2 (ja) * | 1986-09-09 | 1995-12-25 | 有恒薬品工業株式会社 | 水性懸濁状殺生剤組成物 |
| FR2663195A1 (fr) * | 1990-06-13 | 1991-12-20 | Rhone Poulenc Agrochimie | Procede de traitement fongicide foliaire au moyen d'un triazole et composition fongicide pour mettre en óoeuvre le procede. |
| JPH04261106A (ja) * | 1991-02-13 | 1992-09-17 | Hokko Chem Ind Co Ltd | 農園芸用殺菌剤 |
| JP3417995B2 (ja) | 1994-04-12 | 2003-06-16 | 呉羽化学工業株式会社 | 殺菌剤組成物 |
| DE4423612A1 (de) * | 1994-07-06 | 1996-01-11 | Basf Ag | 2-[(Dihydro)pyrazolyl-3'-oxymethylen]-anilide, Verfahren zu ihrer Herstelung und ihre Verwendung |
| US5968964A (en) * | 1998-07-01 | 1999-10-19 | American Cyanamid Company | Fungicidal liquid formulation |
| JP2001302420A (ja) * | 2000-04-28 | 2001-10-31 | Nippon Soda Co Ltd | 農園芸用殺菌剤組成物 |
| DE50200540D1 (de) * | 2001-12-17 | 2004-07-29 | Basf Ag | Verfahren zur Herstellung lösungsmittelfreier Suspensionen |
| WO2004078163A2 (en) | 2003-02-28 | 2004-09-16 | Transform Pharmaceuticals, Inc. | Pharmaceutical co-crystal compositions of drugs such as carbamazepine, celecoxib, olanzapine, itraconazole, topiramate, modafinil, 5-fluorouracil, hydrochlorothiazide, acetaminophen, aspirin, flurbiprofen, phenytoin and ibuprofen |
| CA2477923C (en) * | 2002-03-01 | 2021-02-23 | University Of South Florida | Multiple-component solid phases containing at least one active pharmaceutical ingredient |
| US6889914B2 (en) * | 2003-01-31 | 2005-05-10 | Nlb Corp. | Shroud assembly for high pressure fluid cleaning lance |
| ATE550022T1 (de) | 2003-02-28 | 2012-04-15 | Mcneil Ppc Inc | Pharmazeutische mischkristalle von celecoxib- nicotinamid |
| WO2005089511A2 (en) | 2004-03-19 | 2005-09-29 | Transform Pharmaceuticals, Inc. | Novel pharmaceutical forms, and methods of making and using the same |
| WO2006007448A2 (en) | 2004-06-17 | 2006-01-19 | Transform Pharmaceuticals, Inc. | Pharmaceutical co-crystal compositions and related methods of use |
| AR054777A1 (es) * | 2005-06-20 | 2007-07-18 | Basf Ag | Modificaciones cristalinas de piraclostrobina |
-
2008
- 2008-02-04 TW TW097104280A patent/TW200901889A/zh unknown
- 2008-02-07 CL CL200800395A patent/CL2008000395A1/es unknown
- 2008-02-08 AU AU2008212764A patent/AU2008212764B2/en not_active Ceased
- 2008-02-08 AT AT08708832T patent/ATE542421T1/de active
- 2008-02-08 EA EA200901081A patent/EA017040B1/ru not_active IP Right Cessation
- 2008-02-08 US US12/526,351 patent/US8859607B2/en not_active Expired - Fee Related
- 2008-02-08 DK DK08708832.4T patent/DK2117297T3/da active
- 2008-02-08 RS RS20120080A patent/RS52230B/sr unknown
- 2008-02-08 MX MX2009007733A patent/MX2009007733A/es active IP Right Grant
- 2008-02-08 PT PT08708832T patent/PT2117297E/pt unknown
- 2008-02-08 AR ARP080100572A patent/AR065288A1/es active IP Right Grant
- 2008-02-08 CA CA2675627A patent/CA2675627C/en not_active Expired - Fee Related
- 2008-02-08 HR HR20120198T patent/HRP20120198T1/hr unknown
- 2008-02-08 KR KR1020097018787A patent/KR101488034B1/ko not_active Expired - Fee Related
- 2008-02-08 SI SI200830534T patent/SI2117297T1/sl unknown
- 2008-02-08 UA UAA200909063A patent/UA97973C2/ru unknown
- 2008-02-08 WO PCT/EP2008/051562 patent/WO2008096005A1/en not_active Ceased
- 2008-02-08 PL PL08708832T patent/PL2117297T3/pl unknown
- 2008-02-08 EP EP08708832A patent/EP2117297B1/en active Active
- 2008-02-08 JP JP2009548695A patent/JP5523838B2/ja not_active Expired - Fee Related
- 2008-02-08 BR BRPI0807864-5A patent/BRPI0807864B1/pt active IP Right Grant
- 2008-02-08 PE PE2008000292A patent/PE20081754A1/es not_active Application Discontinuation
- 2008-02-08 ES ES08708832T patent/ES2378909T3/es active Active
-
2009
- 2009-08-21 CR CR10984A patent/CR10984A/es unknown
- 2009-09-08 EC EC2009009615A patent/ECSP099615A/es unknown
- 2009-09-08 ZA ZA2009/06209A patent/ZA200906209B/en unknown
-
2012
- 2012-03-12 CY CY20121100248T patent/CY1112576T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8859607B2 (en) | Crystalline complexes of agriculturally active organic compounds | |
| CN101203136B (zh) | 唑菌胺酯的晶型 | |
| PT2176229E (pt) | Nova forma cristalina de 3-(difluorometil)-1-metil-n-(3',4',5'-trifluoro[1,1'-bifenil]-2-il)-1h-pirazole-4-carboxamida | |
| EA021068B1 (ru) | Способ обработки семян, препаративная форма для дражирования семян и набор | |
| CN114007421A (zh) | 促进吸收的ulv制剂 | |
| AU2017100047A4 (en) | An aqueous suspoemulsion containing lambda-cyhalothrin and methods for making and using the same | |
| KR20100061719A (ko) | 피리메타닐 및 디티아논의 공결정 | |
| EA018640B1 (ru) | Кристаллические комплексы пендиметалина и метазахлора | |
| TWI652011B (zh) | 新穎之水性濃懸乳劑及其製備方法 | |
| EA025318B1 (ru) | Сокристаллы ципродинила и дитианона | |
| JP4958304B2 (ja) | 殺虫剤としてのn−フェニルピラゾール誘導体 | |
| CA2681024C (en) | Fungicidal compositions comprising a carboxamide derivative, cyprodinil and an unsaturated fatty acid | |
| KR20110018948A (ko) | 네오니코티노이드 내성 곤충의 방제 방법 | |
| JP4873650B2 (ja) | 殺虫剤としてのn−フェニルピラゾール誘導 | |
| JP2001233705A (ja) | 農薬粉剤の製造方法 | |
| JP2008519777A (ja) | 有害生物防除剤としてのビニルアミノピラゾール誘導体 | |
| CN110810419A (zh) | 一种含有氟苯醚酰胺与氟菌唑的杀菌组合物 | |
| BR102012012559A2 (pt) | composição inseticida em grânulos; processo para a preparação dos grânulos da composição, e seu uso |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B15K | Others concerning applications: alteration of classification |
Free format text: AS CLASSIFICACOES ANTERIORES ERAM: A01N 25/00 , A01N 47/34 Ipc: A01N 47/34 (2006.01), A01N 47/24 (2006.01), A01N 4 |
|
| B09B | Patent application refused [chapter 9.2 patent gazette] | ||
| B12B | Appeal against refusal [chapter 12.2 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 02/02/2021, OBSERVADAS AS CONDICOES LEGAIS. |