Campo técnico
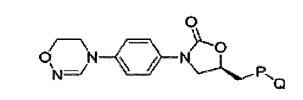
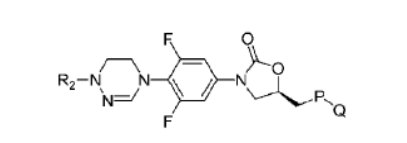
A presente invenção relaciona-se a novos derivados de oxazolidinona representados pela fórmula química 1, particularmente a novos derivados de oxazolidinona que têm uma amidoxima cíclica ou um grupo amidrazona cíclica. Fórmula Química 1
A presente invenção também se relaciona a composições farmacêuticas de antibiótico que incluem novos derivados de oxazolidinona representados pela Fórmula Química 1, pró- fármacos destes, hidratos destes, solvatos destes, isômeros destes ou sais farmaceuticamente aceitáveis destes como um ingrediente eficaz.
Técnica de fundamento
Desde a descoberta da penicilina, numerosos antibióticos têm sido desenvolvidos pelas companhias farmacêuticas por todo o mundo, incluindo antibióticos de p-lactama contra infecções bacterianas, sulfonamidas, tetraciclinas, aminoglicosídeos, macrolídeos, quinolonas, glicopeptídeos, e outros. E mesmo assim, novas bactérias resistentes a antibióticos ou bactérias resistentes a multidrogas surgem incessantemente devido ao mau uso ou abuso de antibióticos. Por causa disso, as preocupações são crescentes por todo o mundo. A comunidade microbiológica internacional se preocupa que, com a evolução de resistência aos antibióticos, novas bactérias resistentes que não são afetadas por quaisquer antibióticos atualmente usados devem ser desenfreadas no futuro próximo.
Em geral, os patógenos bacterianos podem ser classificados em bactérias gram-positivas ou gram- negativas. Em particular, as bactérias gram-positivas, por exemplo Staphylococcus, Enterococcus, Streptococcus e bactérias álcool-ácido-resitente, são muito importantes. Isso é porque, uma vez que ocorrem em um ambiente hospitalar, elas são difíceis de ser erradicadas e tendem a se desenvolver em bactérias resistentes intratáveis. Tais bactérias resistentes incluem Staphylococcus resistente à meticilina (MRSA), Staphylococcus coagulase-negativo resistente à meticilina (MRCNS), Streptococcus pneumoniae resistente à penicilina, Enterococcus faecium de múltipla- resistência, ou outros.
Para o tratamento clinicamente eficaz das bactérias gram-positivas, vancomicina, um antibiótico, é frequentemente usada. No entanto, vancomicina está relacionada a uma variedade de toxicidades e, desde o surgimento de Enterococcus resistente à vancomicina (VRE) em 1990, têm surgido bactérias resistentes à vancomicina e a outros antibióticos com base em glicopeptídeo.
E, para antibióticos como JS-lactama, quinolona e macrolídeo usados para tratar infecções do trato respiratório superior causadas por bactérias específicas Gram-negativas que incluem Haemophilus influenzae (H. influenzae) e Moraxella catarrhalis (M. catarrhalis), surgem bactérias resistentes como Staphylococcus aureus resistente à quinolina (QRSA). Portanto, os pesquisadores em novos antibióticos estão em seu caminho.
Portanto, para solucionar fundamentalmente o problema de resistência aos antibióticos, é urgente o desenvolvimento de antibióticos com nova estrutura química e mecanismo antibacteriano. Com relação a isso, uma vez que um antibiótico de oxazolidinona com uma nova estrutura química foi primeiramente relatado em 1984 por DuPont (Publicação de Patente Européia No. 127,902), vários derivados de oxazolidinona foram designados e sintetizados por várias companhias farmacêuticas.
Aqueles derivados de oxazolidinona são novos antibióticos sintéticos e devem ser administrados por via oral. Os antibióticos de oxazolidinona têm uma estrutura química totalmente diferente dos antibióticos clássicos. Uma vez que eles inibem o estágio inicial de síntese de proteína, eles exibem atividade antibacteriana superior contra bactérias resistentes aos antibióticos, particularmente bactérias gram-positivas, como Staphylococcus aureus resistente à meticilina (MRSA), Staphylococcus epidermidis resistente à meticilina (MRSE), Staphylococcus aureus resistente à quinolona (QRSA), Enterococcus resistente à vancomicina (VRE) e Mycobacterium tuberculosis resistente à multidrogas (MDRTB).
Como exemplos de compostos de oxazolidinona que incluem um anel de oxazolidinona, derivados de 3-fenil-2- oxazolidinona que têm um ou dois substituinte(s) são descritos nas Patentes US Nos. 4,948.801, 4,461,773, 4,340,606, 4,476,136, 4,250,318 e 4,128,654, e derivados de 3- [ (mono-substituído)fenil]-2-oxazolidinona representados pela Fórmula Química A são descritos em EP 0312000, J. Med. Chem. 32, 1673(1989), J. Med. Chem. 33, 2569 (1990), Tetrahedron Lett. 45,123(1989), e outros. Formula química A
E, derivados de oxazolidinona representados pela Formula Química B e Fórmula química C foram sintetizados por Pharmacia & Upjohn (WO 93/23384, WO 95/14684 e WO 95/07271). O composto de Fórmula química B, "linezolida", é o primeiro antibiótico de oxazolidinona e é comercializado sob o nome comercial "zyvox" para administração oral e injeção, aprovado pala "U.S. Food and Drug Administration" (FDA). No entanto, a maioria dos compostos de oxazolidinona sintéticos está associada com algumas limitações, como toxicidade, baixa eficácia in vivo e baixa solubilidade. Como para linezolida, a solubilidade em água é apenas cerca de 3 mg/ml, o que torna limitado seu uso como injeção. Fórmula química B
Fórmula química C
WO 93/09103 revela derivados de fenil oxazolidinona que têm um anel heterocíclico, que inclui piridina, tiazol, indol, oxazol, quinol etc., na posição 4 do grupo fenil. Porém, os substituintes do anel heterocíclico são meramente grupo alquil ou amino simples, e as atividades não são assim excelentes.
Para solucionar esses problemas, WO 01/94342 revela derivados de feniloxazolidinona que têm vários derivados de piridina ou fenil na posição 4 do grupo fenil. Os compostos sintéticos têm amplo espectro antibacteriano e excelente atividade antibacteriana. Embora os compostos de oxazolidinona que têm vários derivados de piridina na posição 4 do grupo fenil de oxazolidinona tenham espectro antibacteriano mais amplo e excelente atividade antibacteriana quando comparados a linezolida, a maior parte deles tem solubilidade aquosa de 30 μg/ml ou menos, e assim tem limitação na preparação de injeções.
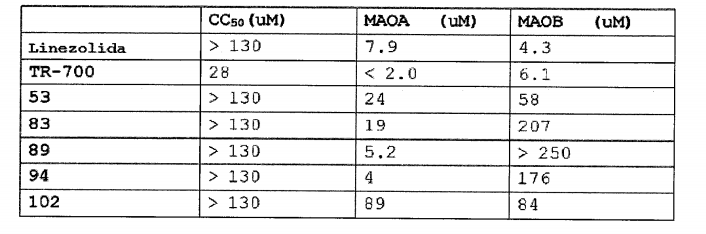
TR-700 e TR-701, representados pela Fórmula Química D, são desenvolvidos por Dong-A Pharmaceutical e recentemente licenciados para Trius Therapeutics. TR-701 é um pró- fármaco de TR-700 e ele está na fase II de experimento clínico. TR-701 soluciona o problema de solubilidade por meio da formação de pró-fármaco a partir de TR-700, exibe uma atividade antibacteriana superior àquela de linezolida. No entanto, o composto mostra maiores toxicidades (citotoxicidade, perfil de MAO, mielossupressão etc.) que linezolida, e, portanto, acredita-se que tenha várias limitações.
TR-700 ( R = OH ) TR-701 ( R = OPO3Na2 )
Como acima descrito, um composto que tem atividade antibacteriana superior, solubilidade satisfatória e menor toxicidade ainda está para ser descoberto.
Revelação da Invenção
Problema técnico
Os inventores da presente invenção sintetizaram novos derivados de oxazolidinona para desenvolver antibióticos que têm atividade antibacteriana superior quando comparados aos antibióticos existentes e que têm maior solubilidade para uma preparação mais fácil em formulações de administração oral e injeção. Foi confirmado que os novos derivados de oxazolidinona de acordo com a presente invenção têm atividade antibacteriana superior e espectro antibacteriano significativamente melhorado.
Especialmente, o composto de amidoxima cíclica ou amidrazona cíclica apresentado pela presente invenção não foi estudado antes. Embora a amidoxima ou amidrazona acíclica seja relativamente bem conhecida, o composto de amidoxima cíclica ou amidrazona cíclica como aqueles revelados na presente invenção é pouco conhecida. A introdução da forma cíclica resulta em absorção marcadamente melhorada e permite a formação de um sal que tem uma basicidade adequada, assim aumentando muito a solubilidade em água. A solubilidade em água aumentada torna possível a preparação de injeções sem o uso de um pró-fármaco e com pouca toxicidade.
Portanto, um objetivo da presente invenção é o fornecimento de novos derivados de oxazolidinona, particularmente novos compostos de oxazolidinona com um grupo de amidoxima cíclica ou amidrazona cíclica de modo a melhorar a solubilidade, e métodos para a preparação dos mesmos.
Outro objetivo da presente invenção é o fornecimento de composições farmacêuticas de antibiótico que incluem novos derivados de oxazolidinona, pró-fármacos destes, hidratos destes, solvatos destes, isômeros destes, ou sais farmaceuticamente aceitáveis destes como um ingrediente eficaz.
Os novos derivados de oxazolidinona de acordo com a presente invenção podem ser usados para o tratamento de pneumonia adquirida em hospital, pneumonia adquirida socialmente, infecções cutâneas e da estrutura da pele complicadas, infecções cutâneas e da estrutura da pele não complicadas, ou infecções causadas por bactérias resistentes aos antibióticos, particularmente septicemia causada por Enterococcus faecium resistente à vancomicina (VRE) ou Enterococcus faecalis resistente à linezolida, ou para uma terapia de combinação para doenças associadas a bactérias gram-negativas.
Solução do problema
A seguir, as modalidades da presente invenção serão descritas em detalhes. A presente invenção relaciona-se a novos derivados de oxazolidinona representados pela Fórmula Química 1, particularmente novos compostos de oxazolidinona com um grupo de amidoxima cíclica ou um grupo de amidrazona cíclica. A presente invenção também se relaciona a composições farmacêuticas de antibiótico que compreendem um novo derivado de oxazolidinona representado pela Fórmula
Química 1, um pró-fármaco deste, um hidrato deste, um solvato deste, um isômero deste, ou um sal farmaceuticamente aceitável deste como um ingrediente eficaz. Fórmula química 1
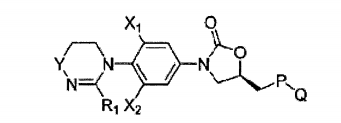
Na Fórmula química 1, Ri representa hidrogênio, (Ci-C6) alquil ou (C3_ C6) cicloalquil ; Y representa -O- ou -N(R2)-;
R2 representa hidrogênio, ciano, (Ci-C6) alquil, (C3. C6) cicloalquil, - (CH2) mOC (=0) Rn, - (CH2) mC (=0) Rn, (CH2)mC (=S) R12 OU -SO2RÍ3, em que o alquil de R2 pode ser também substituído por um ou mais substituintes selecionados de um grupo que consiste em (C2_C6 )alquenil, (C2.CS) alquinil, halogênio, halo (Ci_C6) alquil, (Ci- C6) alquil (C2.C6) alquinil, hidroxil, (C3.C6) cicloalquil e ciano;
Rn até R33 representam independentemente hidrogênio, (Ci-Cs) alquil, (Ci-Cs) alcoxi, amino, (C3.C6) cicloalquil, (C2_ C6)alquenil, (C2_C6) alquinil ou (Ci-C6) alquilcarbonil, em que o alquil, alcoxi ou amino de Rn até Ri3 pode ser também substituído por um ou mais substituintes selecionados de halogênio, amino, hidroxil, ciano, (Ci-C6 )alquil, (Ci- Ce) alquilcarboniloxi e hidroxi (Ci-C6) alquil ; m representa um número inteiro de 0 a 2;
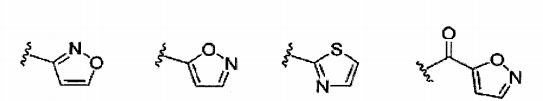
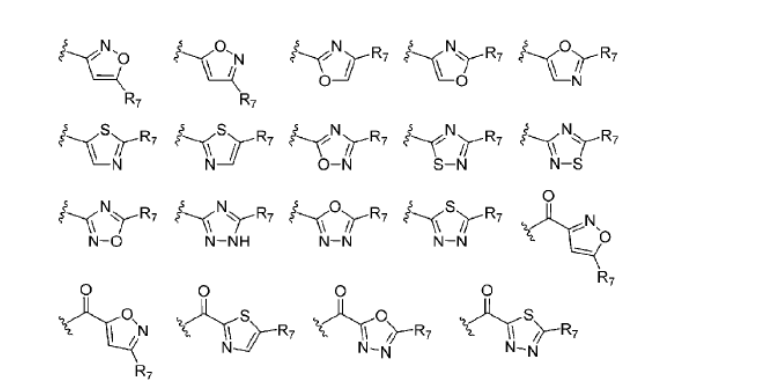
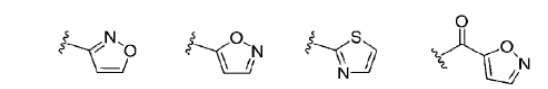
X1 e X2 representam independentemente hidrogênio ou flúor; P representa -0-, -NH- ou um heterociclo aromático de cinco membros com a seguinte estrutura
Q representa hidrogênio, -C(=O)R3, -C(=S)R4, C(=O)NR5R6, -C(=S)NR5R6, OU um heterociclo aromático de cinco membros com a estrutura selecionada das seguintes:
R3 e R4 representam independentemente hidrogênio, (Ci- C6) alquil, (Ci-Cg) alcoxi, (C3_C6) cicloalquil, (C2_CS) alquenil ou (C2-C6) alquinil;
R5 e R6 representam independentemente hidrogênio, (Ci- C6) alquil, (C3_C6) cicloalquil ou (C2-C6) alquenil ;
R7 representa hidrogênio, halogênio, (Ci-C6) alquil ou (C3-C6) cicloalquil; e o alquil de R3 até R7 pode ser também substituído por um ou mais substituintes selecionados de um grupo que consiste em hidroxil, ciano, halogênio, (Ci- C6)alquilcarboniloxi e amino.
Como aqui usado, o termo "alquil" inclui estruturas lineares e ramificadas. Por exemplo, o termo " (Ci-C6) alquil" inclui todos os possíveis isômeros posicionais e geométricos, como metil, etil, propil, isopropil, butil, isobutil, terc-butil, pentil, hexil, e outros.
O termo " (C3_C6) cicloalquil" inclui todos os possíveis isômeros posicionais e geométricos, como ciclopropil, ciclobutil, ciclopentil, ciclohexil, ciclopropilmetil, e outros.
O termo " (C2-C6) alquenil" inclui todos os possíveis isômeros posicionais e geométricos, como vinil, propenil, 1- e 2-butenil, pentenil e outros.
O termo " (C2_C6) alquinil" inclui todos os possíveis isômeros posicionais e geométricos, como acetilenil, propargil, 1-propinil, 2-pentinil3 e outros.
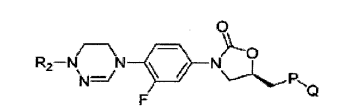
Os derivados de oxazolidinona de acordo com a presente invenção podem ser representados pela Fórmula Química 2 ou 3 : Fórmula química 2
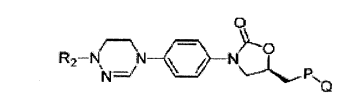
Fórmula química 3
Nas Fórmulas químicas 2 e 3, R2, Xi, X2, P e Q são o mesmo como definido na Fórmula química 1.
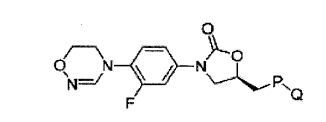
Mais preferivelmente, os derivados de oxazolidinona de acordo com a presente invenção incluem os compostos representados pelas Fórmulas Químicas 4 a 9: Fórmula química 4
Fórmula química 5
Fórmula química 6
Fórmula química 7
Fórmula química 8
Fórmula química 9
Nas Fórmulas químicas 4 a 9, R2 representa hidrogênio, ciano, (Cx-C6) alquil, (C3_ C6) cicloalquil, - (CH2) mOC (=0) Rllz - (CH2) mC (=0) R12, (CH2) mC (=S) R12 OU -SO2Ri3, em que o alquil de R2 pode ser também substituído por um ou mais substituintes selecionados de um grupo que consiste em (C2_CS )alquenil, (C2_C6) alquinil, halogênio, halo (Ci-Cδ) alquil, (Ci- C6) alquil (C2_C6) alquinil, hidroxil, (C3-C6) cicloalquil e ciano; Rn até Ria representam independentemente hidrogênio, (Ci-C6) alquil, (Ci-C6) alcoxi, amino, (C3_C6) cicloalquil, ou (Ci-C6) alquilcarbonil, em que o alquil, alcoxi ou amino de Rn até R13 pode ser também substituído por um ou mais substituintes selecionados de halogênio, amino, hidroxil, ciano, (Ci-C6) alquil, (Ci-Ce) alquilcarboniloxi e hidroxi (Ci- C6) alquil ; m representa um número inteiro de 0 a 2; P representa -O-, -NH- ou um heterociclo aromático de cinco membros com a seguinte estrutura

Q representa hidrogênio, -C(=O)R3, -C(=S)R4, C(=O)NR5R6, -C(=S)NR5R6, OU um heterociclo aromático de cinco membros com a estrutura selecionada das seguintes
R3 e R4 representam independentemente hidrogênio, (Ci- Cs) alquil ou (Ci-Cs) alcoxi ; R5 e R6 representam independentemente hidrogênio ou (Ci-C6) alquil; e
O alquil de R3 até R6 pode ser também substituído por um ou mais substituintes selecionados de um grupo que consiste em hidroxil, ciano, halogênio, (Ci- C6)alquilcarboniloxi e amino.
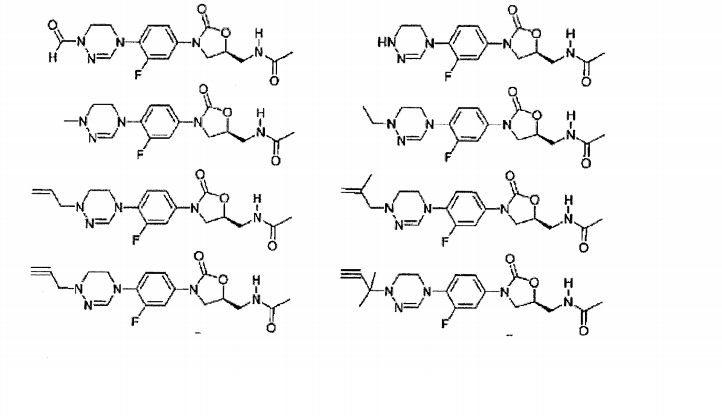
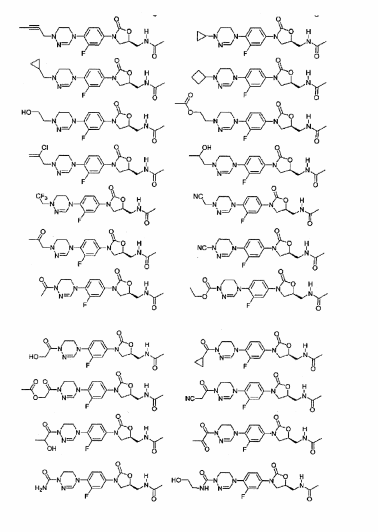
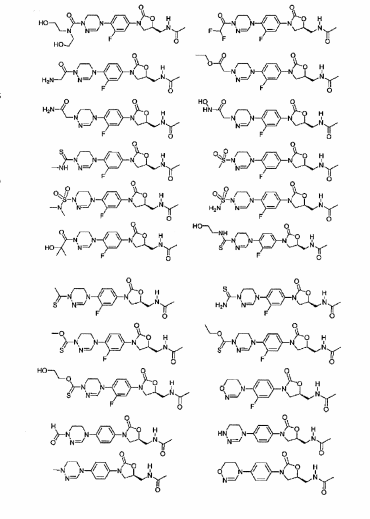
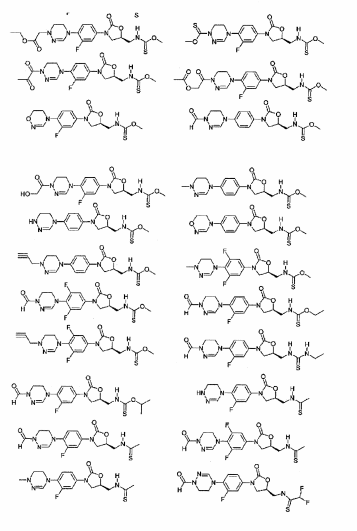
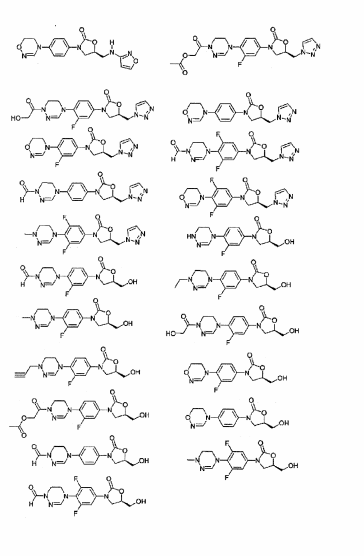
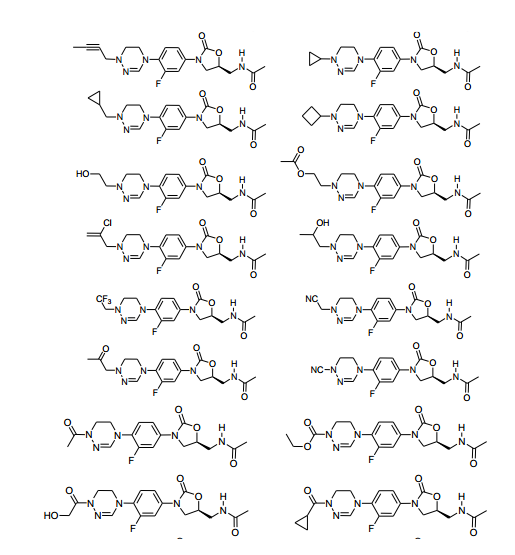
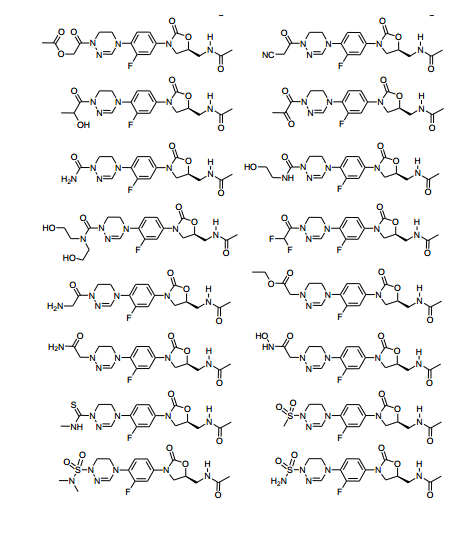
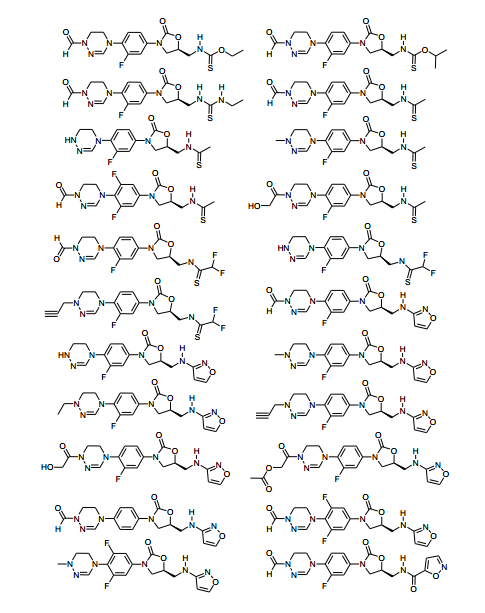
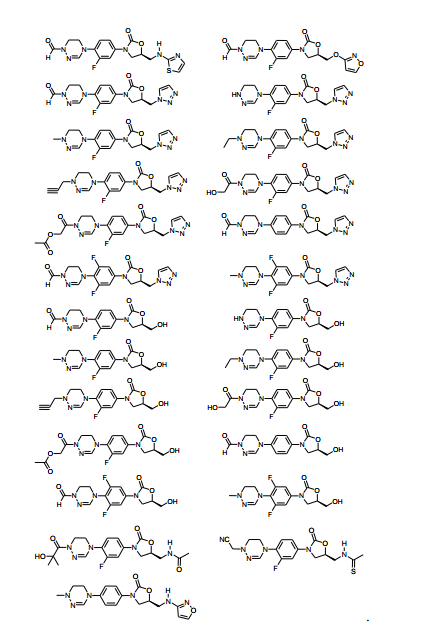
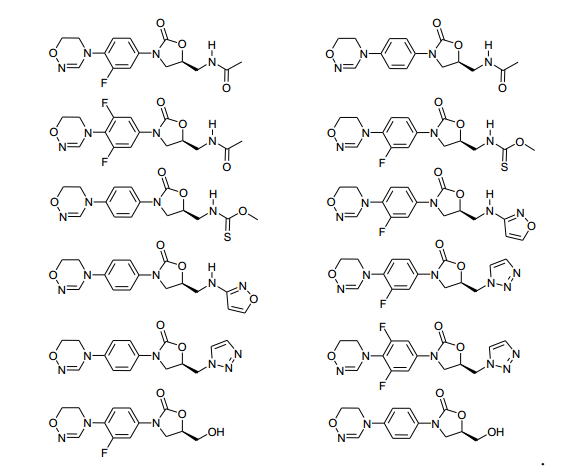
Exemplos dos novos derivados de oxazolidinona de acordo com a presente invenção incluem os seguintes compostos, mas o escopo da presente invenção não é limitado a eles:
Os novos derivados de oxazolidinona de acordo com a presente invenção têm um grupo de amidoxima cíclica ou um grupo amidrazona cíclica e podem ser preparados em pró- fármacos, hidratos, solvatos, isômeros ou sais farmaceuticamente aceitáveis para melhorar a absorção no corpo ou para melhorar a solubilidade. Portanto, os pró- fármacos, hidratos, solvatos, isômeros ou sais farmaceuticamente aceitáveis também estão dentro do escopo da presente invenção.
Os novos derivados de oxazolidinona de acordo com a presente invenção podem ser convertidos a sais farmaceuticamente aceitáveis. O termo "sais farmaceuticamente aceitáveis referem-se a sais de adição ácida" úteis para administração dos compostos desta invenção, e inclui metanossulfonato, etanossulfonato, fumarato, succinato, cloridrato, citrato, malato, tartrato e (menos preferivelmente) hidrobrometo, fosfato, sulfato, e outros. Além disso, um sal básico adequado inclui, por exemplo, um sal de metal alcalino (por exemplo, sal de sódio) ou um sal de metal alcalino terroso (por exemplo, sal de cálcio ou magnésio) , um sal de amina orgânica (por exemplo, trietilamina, morfolino, N-metilpiperidina, N- etilpiperidina, dibenzilamina, N,N-dibenziletilamina e tris(2-hidroxietil)amina), ou um aminoácido (por exemplo, N-metil-d-glutamina e lisina).
Os sais podem incluir um ou mais cátions ou ânions dependendo do número de grupo(s) e da valência do cátion ou ânion correspondente. Um sal básico farmaceuticamente aceitável preferido é um sal de sódio. No entanto, para facilitar a liberação do sal durante a preparação, um sal menos solúvel no solvente selecionado pode ser preferido.
O derivado de oxazolidinona da presente invenção pode estar presente em uma forma solvatada, por exemplo, como um hidrato, ou em uma forma não solvatada. Os solvatos dos derivados de oxazolidinona de acordo com a presente invenção incluem todas as formas solvatadas farmaceuticamente ativas.
Os derivados de oxazolidinona da presente invenção podem ser administrados em uma forma de pró-fármaco, que é transformada no corpo de humano ou animal para fornecer o ingrediente ativo da presente invenção. O pró-fármaco pode ser formado por introdução de um grupo ou substituinte adequado capaz de modificar ou melhorar o perfil físico e/ou farmacológico do composto parente. Exemplos do pró- fármaco incluem ésteres dos compostos da presente invenção e sais farmaceuticamente aceitáveis destes que podem ser hidrolisados in vivo.
Vários tipos de formas de pró-fármaco são conhecidos na técnica relacionada. Por exemplo, referência a: a) Design of Prodrugs, editado por H. Bundgaard, (Elsevier, 1985) e Methods in Enzymology, Vol. 42, p.309- 396, editado por K. Widder, e cols. (Academic press, 1985); b) A Textbook of Drug Design and Development, editado por Krogsgaard-Larsen e H. Bundgaard, capítulo 5 "Design and Application of Prodrugs", by H. Bundgaard p. 113-191 (1991); c) H. Bundgaard, Advanced Drug Delivery Reviews, 8, 1- 38 (1992); d) H. Bundgaard, e cols., Journal of Pharmaceutical Sciences, 77, 285 (1988); e e) N. Kakeya, e cols., Chem. Pharm. Bull., 32, 692 (1984) .
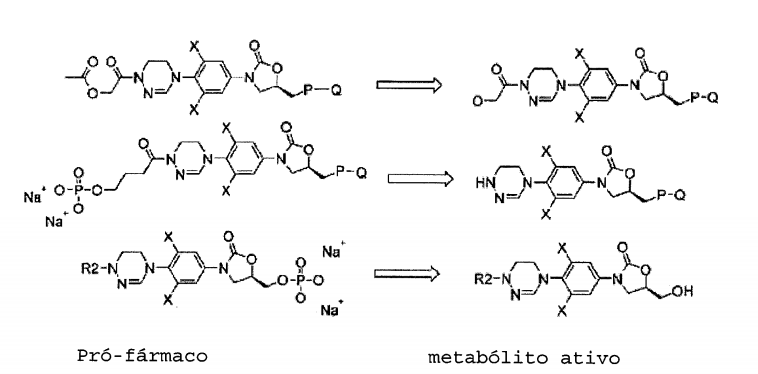
Exemplos do pró-fármaco de acordo com a presente invenção incluem os seguintes compostos.
Como nos exemplos anteriores, um grupo fosfonato ou acetil pode ser anexado no grupo hidroxil, de modo que o pró-fármaco é transformado a uma forma ativa depois da administração. Alternativamente, um aminoácido pode ser anexado ou uma forma de carbonato pode ser preparada. A forma de pró-fármaco é usada principalmente quando a solubilidade é relativamente baixa ou a absorção é baixa. O uso do pró-fármaco pode levar à melhoria do perfil de absorção, distribuição, metabolismo e excreção (ADME) e PK, além da melhoria da solubilidade e capacidade de absorção.
O composto da presente invenção tem um centro quiral na posição C-5 do anel oxazolidinona. Um diastereômero preferido do composto derivado de oxazolidinona de acordo com a presente invenção é representado pela Fórmula Química 1. Comparado ao epímero representado pela Fórmula Química lb, ele exibe um melhor perfil de MAO. Fórmula química lb
Quando uma mistura de epímeros com relação ao centro quiral de oxazolidinona é usada, a quantidade pode ser controlada em consideração à proporção dos enantiômeros (ou diastereômeros) para adquirir um efeito farmacológico 10 comparável quando comparado com quando o isômero de imagem em espelho é usado isoladamente.
Além disso, alguns compostos da presente invenção podem ter um diferente centro quiral dependendo de seus substituintes. Todos os isômeros óticos, diastereômeros e 15 misturas que tenham atividade antibacteriana são incluídos no escopo da presente invenção. O método para a preparação de formas oticamente ativas (por exemplo, recristalização, síntese quiral, resolução enzimática, biotransformação, ou separação de misturas por cromatografia) e os métodos para 20 medição da atividade antibacteriana são conhecidos na técnica relacionada.
Como os compostos representados pela Fórmula Química 1 ou os sais destes podem tautomerizar, embora apenas um dos possíveis tautômeros seja descrito nas Fórmulas químicas ou 25 esquemas de reação na descrição, a presente invenção engloba todos os tautômeros que têm atividade antibacteriana, e não é limitada à forma de tautômero descrita nas Fórmulas químicas ou esquemas de reação.
Além disso, o composto da presente invenção pode 30 exibir polimorfismo. Assim, todos os compostos polimórficos que têm atividade antibacteriana são incluídos na presente invenção.
Os novos derivados de oxazolidinona de acordo com a presente invenção podem ser preparados através de métodos alternativos dependendo de seus substituintes. Por exemplo, eles podem ser preparados de acordo com os métodos exemplificados pelos esquemas 1 a 6. Os métodos de preparação descritos nos Esquemas 1 a 6 são apenas exemplos e podem ser facilmente modificados por aqueles habilitados na técnica dependendo dos substituintes particulares. Portanto, os métodos exemplificados nos Esquemas 1 a 6 não limitam o método para a preparação dos compostos de oxazolidinona da presente invenção. A menos que especificado em contrário, as definições para os substituintes nos esquemas de reação são as mesmas como na Fórmula química 1.
Os derivados de oxazolidinona de Fórmula química 1 de acordo com a presente invenção podem ser sintetizados por meio de diferentes vias sintéticas, dependendo de X±, X2, Y, P e Q. Métodos de síntese representativos no caso em que Xj. é um átomo de flúor (F) e X2 é átomo de hidrogênio (H) são exemplificados nos Esquemas 1 a 5. E, o caso em que ambos X2 e X2 são H ou F é exemplificado no Esquema 6.
Para preparações de compostos de amidrazona cíclica, com Y sendo átomo de nitrogênio (N-R2) , os métodos de síntese no caso em que P é NH são exemplificados nos Esquemas 1 e 2, um método de síntese no caso em que P é um heterociclo aromático (por exemplo, Triazol) é exemplificado no Esquema 3, e o caso em que P é um átomo de oxigênio (O) é exemplificado no Esquema 4. Além disso, um método de síntese de compostos de amidoxima cíclica, com Y sendo O, é exemplificado no Esquema 5.
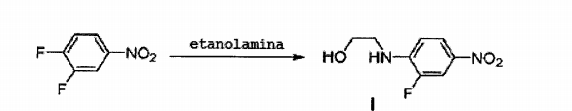
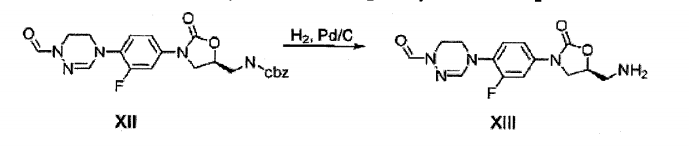
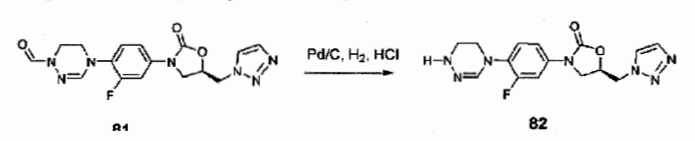
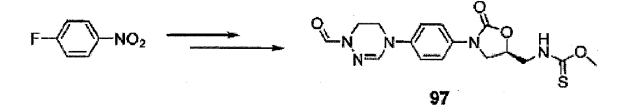
Em referência ao Esquema 1, 3, 4-difluornitrobenzeno reage com etanolamina para gerar o Composto I. Depois de proteção do álcool e grupos amina com (t- butildimetilsilil (TBS) e terc-butiloxicarbonil (boc) seqüencialmente (Composto II) , o grupo nitro é reduzido a amina com o uso de Pd/C (Composto III) . O grupo benziloxicarbonil (cbz) é anexado com o uso de benzil clorofórmioato (Cbz-Cl) para sintetizar o Composto IV. O composto IV reage com (R)- glicidil butirato e n-butillítio (n-BuLi) para sintetizar Composto quiral V. 0 composto V reage com metanossulfonil cloreto (Ms-Cl) (Composto VI) , e então com sódio azida (NaN3) (Composto VII) . Depois da conversão do grupo azida na amina com o uso de Pd/C sob gás hidrogênio, um grupo cbz é anexado com o uso de Cbz-Cl para sintetizar Composto VIII. O composto VIII é tratado com ácido clorídrico para remover os grupos de proteção (boc e tbs) para gerar Composto IX, que reage com metanossulfonil cloreto (Ms-Cl) para sintetizar o Composto X. A reação de composto X com hidrazina seguido por reação com trimetil ortoformato gera uma composto de amidrazona cíclica XII. Depois da remoção do grupo cbz do Composto XII (Composto XIII), vários grupos Q podem ser introduzidos. Além disso, depois da remoção do grupo formil, vários grupos R2 podem ser introduzidos. Exemplos específicos são descritos na preparação de compostos. Esquema 1

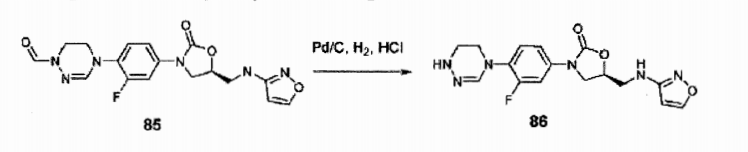
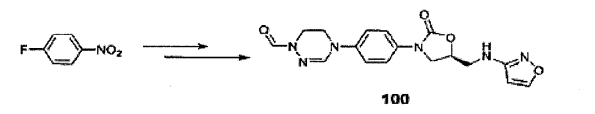
Em referência ao Esquema 2, no caso em que Q é um heterociclo aromático sem grupo carbonil, os grupos P e Q são primeiramente introduzidos ao Composto VI. Uma reação com aminoisoxazol é exemplificada no Esquema 2. Composto VI reage com aminoisoxazol com o grupo amina protegido por boc para sintetizar Composto XIV. Remoção de grupos boc e tbs que usam ácido clorídrico gera Composto XV, por mesilação seguido por reação com hidrazina gerou o Composto XVII, que reage com trimetil ortoformato para sintetizar um composto de amidrazona cíclica. Depois da remoção do grupo formil, vários grupos R2 são introduzidos. Exemplos específicos são descritos na preparação de compostos. Esquema 2
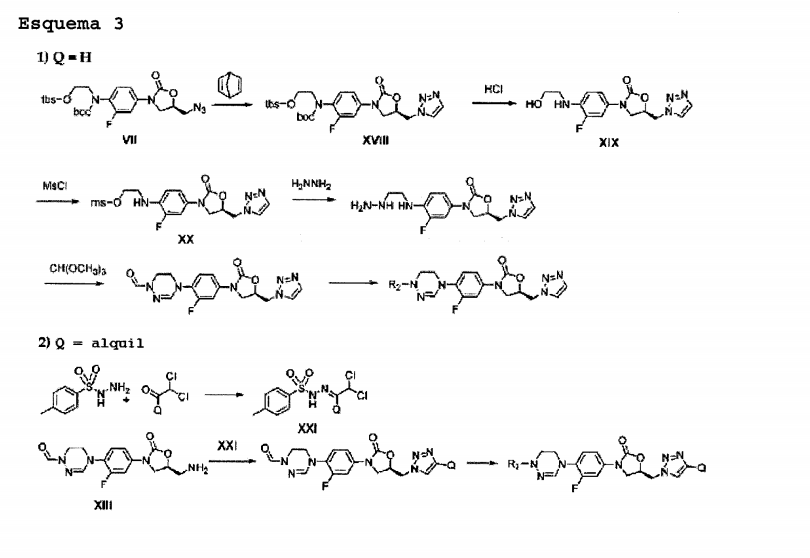
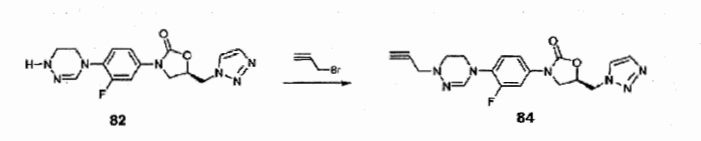
Em referência ao Esquema 3, o caso em que P é um heterociclo aromático é subdividido em 1) em que Q é H e 2) em que Q é um substituinte diferente de H. Primeiro, para um composto em que Q é H, um composto de azido (Composto VII) reage com 2,5-norbornadieno para sintetizar um composto de triazol (Composto XVIII). Remoção de grupos boc e tbs com o uso de ácido clorídrico gera o Composto XIX. Mesilação (Composto XX) , tratamento com hidrazina seguido por trimetil ortoformato gera um composto de amidrazona cíclica. Compostos em que Q é um substituinte diferente de
H podem ser preparados como se segue; uma diclorotosilhidrazona, composto XXI, é preparada por reação de tosilhidrazida e cloreto ácido como mostrado. A reação da amina Xlll e tosilhidrazona XXI gera intermediário de amidrazona cíclica, que depois da remoção de grupo formil é derivatizada com vários grupos R2. Exemplos específicos são descritos na preparação de compostos. Esquema 3
O caso em que P é átomo de oxigênio (O) e Q é H é exemplificado no Esquema 4. Um composto com P sendo O e Q sendo um heterociclo aromático pode ser sintetizado de acordo com o Esquema 2. Para um composto com Q sendo H, 5 proteção do grupo álcool do Composto V com benzoil gera Composto XXII. Remoção dos grupos de proteção boc e tbs com o uso de ácido clorídrico (Composto XXIII) e mesilação gera Composto XXIV, que reage com hidrazina para gerar Composto XXV. Durante uma reação com hidrazina, o grupo benzoil é 10 removido. O composto de hidrazina reage com trimetil ortoformato para sintetizar um composto de amidrazona cíclica. Depois da remoção do grupo formil, vários grupos R2 são introduzidos. Exemplos específicos são descritos na preparação de compostos. Esquema 4
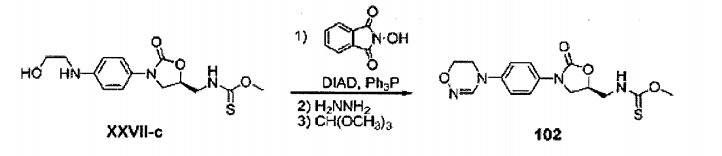
Um método de síntese de um composto de amidoxima cíclica com Y sendo 0 é exemplificado no Esquema 5. 25 Dependendo de se P-Q é OH ou não, os casos são subdivididos em 1) e 2) . 1) A menos que P-Q seja OH, os grupos P e Q são introduzidos no Composto VI de acordo com os Esquemas 1 a 4 para sintetizar o Composto XXVI, que é tratado com ácido 30 clorídrico para remover grupos boc e tbs gerando o Composto XXVII. O composto XXVII é submetido a condição de Mitsunobu com hidroxiftalimida para obter o Composto XXVIII. A remoção de ftalimida com o uso de hidrazina seguida por reação com trimetil ortoformato gera um composto de amidoxima cíclica.
2) Quando P-Q é OH, o grupo álcool de oxazolidinona deve ser protegido com grupo benzoil (Composto XXIII) . A reação de Mitsunobu com hidroxiftalimida gera o Composto XXIX. A remoção de ftalimida com o uso de hidrazina seguida por reação com trimetil ortoformato gera um composto de amidoxima cíclica. Novamente, o grupo benzoil é removido durante a reação de hidrazina. Um composto de amidoxima cíclica também pode ser obtido por reação com trimetil ortoformato. Esquema 5
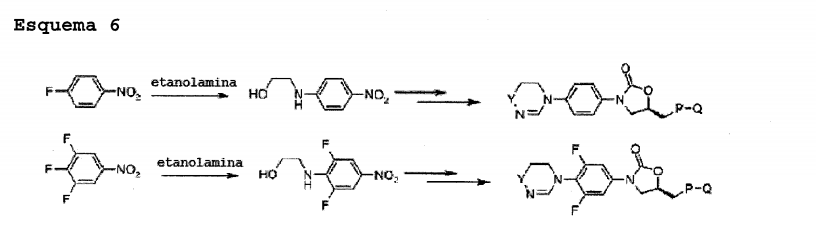
Os casos em que Xx é F e X2 é H foram descritos nos Esquemas 1 a 5. Em referência ao Esquema 6, um composto com Xi e X2 sendo H ou F pode ser sintetizado da mesma forma que nos Esquemas 1 a 5, a única diferença é que 4- fluornitrobenzeno ou 3,4,5-trifluornitrobenzeno é usado como um material de iniciação. Esquema 6
As composições da presente invenção podem estar em uma forma adequada para administração oral (por exemplo, comprimido, losango, cápsula rígida ou macia, suspensão aquosa ou oleosa, emulsão, pó ou granulo dispersível, xarope ou elixir), em uma forma adequada para aplicação tópica (por exemplo, creme, pomada, gel, solução ou suspensão aquosa ou oleosa) , em uma forma adequada para administração ocular, em uma forma adequada para administração por inalação (por exemplo, pó finamente dividido ou aerossol líquido), em uma forma adequada para administração por insuflação (por exemplo, pó finamente dividido), ou em uma forma adequada para administração parenteral (por exemplo, solução estéril aquosa ou oleosa para injeção intravenosa, subcutânea, sublingual ou intramuscular, ou supositório retal).
Além dos compostos da presente invenção, as composições farmacêuticas da presente invenção também podem compreender (ou seja, formuladas junto com) um ou mais fármacos conhecidos selecionados dos agentes antibacterianos clinicamente úteis (por exemplo, p-lactama, macrolídeo, quinolona ou aminoglicosídeo) e agentes antiinflamatórios (por exemplo, triazol antifúngico ou anfotericina), ou podem ser administrados em combinação com um ou mais dos fármacos conhecidos. As composições também podem compreender carbapenem, por exemplo, meropenem ou imipenem, para melhorar o efeito terapêutico. Além disso, os compostos da presente invenção podem ser formulados junto com ou administrados em combinação com um produto de proteína bactericida/de aumento de permeabilidade (BPI) ou um inibidor de bomba de efluxo, para aumentar a atividade contra bactérias gram-negativas e bactérias resistentes a antibióticos.
Os compostos da presente invenção podem ser formulados junto com ou administrados em combinação com vitamina, por exemplo, vitamina B, como vitamina B2, vitamina B6 ou vitamina B12, e ácido fólico. Além disso, os compostos da presente invenção podem ser formulados junto com ou administrados em combinação com um inibidor de ciclooxigenase (COX), particularmente inibidor de COX-2. Em adição, os compostos da presente invenção podem ser formulados junto com ou administrados em combinação com um agente antibacteriano ativo contra bactérias gram-positivas ou bactérias gram-negativas.
As composições da presente invenção podem ser preparadas com o uso de um excipiente farmacêutico conhecido comumente usado. Conseqüentemente, uma composição para administração oral pode compreender, por exemplo, um ou mais agentes colorantes, agentes adoçantes, agentes flavorizantes e/ou antissépticos. Preferivelmente, uma composição farmacêutica para administração intravenosa pode compreender (por exemplo, para melhorar a estabilidade) bactericida, antioxidante, agente redutor ou seqüestrante adequado.
Uma composição para administração oral pode estar na forma de cápsula de gelatina rígida preparada por mistura do ingrediente ativo com um diluente solido inerte, por exemplo, carbonato de cálcio, fosfato de cálcio ou caolin, ou na forma de cápsula de gelatina macia preparada por mistura do ingrediente ativo com água ou óleo, por exemplo, óleo de amendoim, parafina líquida ou óleo de oliva.
Uma suspensão aquosa geralmente compreende um ou mais agentes de suspensão, por exemplo, carboximetilcelulose de sódio, metilcelulose, hidroxipropilmetilcelulose, alginato de sódio, polivinilpirrolidona, goma tragacanto ou goma acácia, ou agentes de dispersão ou umectantes, por exemplo, lecitina, produto da condensação de óxido de alquileno com ácido graxo (por exemplo, polioxietileno estearato), produto da condensação de óxido de etileno com álcool alifático de cadeia longa, por exemplo, heptadecaetilenooxicetanol, produto da condensação de óxido de etileno com derivado de éster parcial de ácido graxo e hexitol, por exemplo, polioxietileno sorbitol monooleato, produto da condensação de óxido de etileno com derivado de éster parcial de ácido graxo e anidrido de hexitol, por exemplo, polietileno sorbitano monooleato, além do ingrediente ativo na forma de pó finamente dividido. A suspensão aquosa também pode compreender um ou mais antissépticos (por exemplo, etil ou propil p- hidroxibenzoato), antioxidantes (por exemplo, ácido ascórbico), agentes colorantes, agentes flavorizantes, e/ou agentes adoçantes (por exemplo, sacarose, sacarina ou aspartame).
Uma suspensão oleosa pode ser preparada por suspensão do ingrediente ativo em óleo vegetal (por exemplo, óleo de arachis, óleo de oliva, óleo de gergelim ou óleo de coco) ou óleo mineral (por exemplo, parafina líquida). A suspensão oleosa também pode compreender um espessante, por exemplo, cera de abelha, cerca de parafina ou cetil álcool. Além disso, o agente adoçante anteriormente mencionado ou agente flavorizante pode ser adicionado para fornecer uma composição de administração oral saborosa. A composição pode ser conservada por adição de um antioxidante como ácido ascórbico.
Pó dispersível ou grânulo adequado para a preparação de uma suspensão aquosa por adição de água compreende um agente de dispersão ou umectante, um agente de suspensão e um ou mais antissépticos, além do ingrediente ativo. Exemplos de agentes de dispersão ou umectantes e agentes de suspensão adequados são descritos anteriormente. Também pode compreender um excipiente adicional como um agente adoçante, um agente flavorizante e um agente colorante.
Além disso, informações a respeito de formulações podem ser encontradas no capítulo 25,2 no Volume 5 de "Comprehensive Medicinal Chemistry" (Corwin Hansch; Chairman of Editorial Board), Pergamon Press, 1990.
A quantidade do ingrediente ativo misturado com um ou mais excipientes para preparar uma formulação de dose unitária pode variar, de fato, dependendo da pessoa que dela necessita e da via de administração particular. Por exemplo, uma formulação para administração oral a um ser humano pode compreender, em geral, 50 mg a 5 g do ingrediente ativo junto com uma quantidade adequada de excipiente (o teor pode variar de cerca de 5 a cerca de 98% com base no peso total da composição) . Em geral, uma formulação de dose unitária compreenderá de cerca de 200 mg a cerca de 2 g do ingrediente ativo. Informações adicionais sobre via de administração e regime de administração podem ser encontradas no capítulo 25,3 no Volume 5 de "Comprehensive Medicinal Chemistry" (Corwin Hansch; Chairman of Editorial Board), Pergamon Press, 1990.
Uma composição farmacêutica adequada da presente invenção é uma formulação de dose unitária para administração oral, por exemplo, um comprimido ou cápsula que compreende 0,1 mg a 1 g, preferivelmente 100 mg a 1 g, do composto da presente invenção. Especialmente, um comprimido ou cápsula que compreende 5 0 mg a 800 mg do composto da presente invenção é preferível.
Além disso, as composições farmacêuticas da presente invenção podem ser uma formulação adequada para injeção intravenosa, subcutânea ou intramuscular, por exemplo, uma injeção que compreende 0,1% w/v a 50% w/v (1 mg/ml a 500 mg/ml) do composto da presente invenção.
A cada paciente, o composto da presente invenção pode ser administrado por via intravenosa, subcutânea ou intramuscular, por exemplo, em uma dose de 0,1 mg/kg a 20 mg/kg por dia. A composição correspondente é administrada uma a quatro vezes ao dia. Em outra modalidade, o composto da presente invenção é administrado em uma dose de 1 mg/kg a 20 mg/kg por dia. Uma dose para administração intravenosa, subcutânea ou intramuscular pode ser fornecida por injeção em bolo. Alternativamente, uma dose para administração intravenosa pode ser injeção contínua por um período de tempo. Além disso, uma dose única diária para administração oral, que pode ser aproximadamente equivalente a uma dose única por dia para administração parenteral, pode ser administrada a cada paciente. A composição correspondente é administrada uma a quatro vezes ao dia.
Quando comparados à linezolida atualmente comercializada por Pfizer, os derivados de oxazolidinona da presente invenção exibem atividade antibacteriana contra várias bactérias resistentes aos antibióticos pré- existentes, incluindo bactérias gram-positivas como Staphylococcus aureus, Enterococcus faecalis etc., e bactérias gram-negativas como Haemophilus influenzae, Moraxella catarrhalis etc., particularmente atividade antibacteriana excelente com Enterococcus faecalis resistente à linezolida, em concentrações muito menores.
Modo para realizar a invenção
Ós exemplos e experimentos serão agora descritos. No entanto, os exemplos e experimentos a seguir são para objetivos de ilustração apenas, e não pretendem limitar o escopo da presente invenção. Exemplo de preparação 1 - Preparação do composto I
Depois da dissolução de 3,4-difluornitrobenzeno (158 g, 0,99 mol) em acetonitrila (800 ml) e adição de etanolamina (117 g, 1,9 mol), a mistura foi agitada por 4 horas sob refluxo. A solução da reação foi resfriada até a temperatura ambiente, concentrada sob pressão reduzida, triturada com éter dietílico, e filtrada para obter um Composto I amarelo (199 g, 0,99 mol, 100%).
1H RMN (400 MHz, clorofórmio-di) δ 7,97 (d, 1H, J = 8,8 Hz), 7,87 (dd, 1H, 11,6 Hz, J2 = 2,4 Hz), 6,65 (t, 1H, J = 8,8 Hz), 5,10-4,87 (bs, 1H), 3,97-3,83 (m, 2H), 3,43- 3,37 (m, 2H). Exemplo de preparação 2 - Preparação do composto II
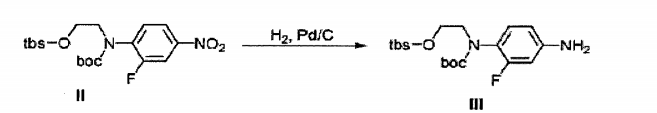
Composto I (100 g, 0,5 mol), t-butildimetilsilil cloreto (TBS-C1, 97 g, 0,65 mol) e imidazol (51 g, 0,75 mol) foram dissolvidos em diclorometano (700 ml) a 0 °C e agitados de um dia para o outro depois de aquecimento lento até a temperatura ambiente. A solução da reação foi concentrada sob pressão reduzida, dissolvida em acetato de etila e lavada com 0,5 N HC1, lavada sequencialmente com solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, e concentrada sob pressão reduzida para obter quantitativamente um composto com um grupo tbs anexado ao álcool. Esse composto foi dissolvido em THF (500 ml) e 1,2 equivalente de Boc20 e 0,1 equivalente de 4- dimetilaminopiridina (DMAP) foram adicionados. Depois de agitação por 3 horas em temperatura ambiente, amónia aquosa (30 ml) foi adicionada. Depois de agitação por mais 2 0 minutos, a solução foi concentrada sob pressão reduzida. O concentrado foi dissolvido novamente em acetato de etila, sequencialmente lavado com 0,5 N HC1, solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seco com sulfato do sódio anidro, e concentrado sob pressão reduzida para obter quantitativamente Composto II.
1H RMN (600 MHz, clorof órmio-di) δ 8,06-7,98 (m, 1H) , 7,95 (dd, 1H, Jx = 10,2 Hz, J2 = 2,4 Hz), 7,57 (t, 1H, J = 7,8 Hz), 3,80 (t, 2H, J = 5,4 Hz), 3,73 (t, 2H, J = 4,8 Hz), 1,42 (s, 9H), 0,81 (s, 9H), 0,01 (s, 6H). Exemplo de preparação 3 - Preparação do composto III
Composto II (92 g, 0,22 mol) foi dissolvido em metanol (600 ml) e agitado por 4 horas sob balão de hidrogênio depois da adição de Pd/C (6 g) . A mistura da reação foi filtrada com o uso de celite e concentrada sob pressão reduzida para obter quantitativamente Composto III (86 g) como um óleo incolor.
1H RMN (400 MHz, clorofórmio-di) δ 6,99 (t, 1H, J = 12,0 Hz), 6,44-6,30 (m, 2H), 3,81-3,63 (m, 4H), 3,63-3,52 (m, 2H), 1,50 (s, 3H), 1,35 (s, 6H), 0,86 (s, 9H), 0,03 (s, 6H) . 4 - Preparação do composto IV
Composto III (86 g, 0,22 mol) foi dissolvido em diclorometano (3 00 ml) . Depois da adição de 1 N de solução aquosa de NaOH (300 ml), benzil cloroformato (Cbz-Cl, 38 ml, 0,27 mol) foi lentamente adicionado em gotas com agitação. Depois de agitação por 1 hora em temperatura ambiente, a camada orgânica foi separada, lavada duas vezes com água, seca com sulfato do sódio anidro, e concentrada sob pressão reduzida para obter quantitativamente Composto IV (116 g) como um óleo amarelo.
1H RMN (600 MHz, clorofórmio-di) δ 7,44-7,32 (m, 6H) , 7,18 (t, 1H, J = 8,1 Hz), 6,96 (d, 1H, J = 8,4 Hz), 6,84- 6,66 (bs, 1H), 5,20 (s, 2H), 3,82-3,63 (m, 2H), 3,63-3,58 (m, 2H), 1,51 (s, 3H), 1,35 (s, 6H), 0,86 (s, 9H), 0,02 (s, 6H) . Exemplo de preparação 5 - Preparação do composto V
Composto IV (116 g, 0,22 mol) foi dissolvido em THF (400 ml) e agitado por 20 minutos depois da adição lenta de n-butillítio (2,5 M solução em n-hexano, 90 ml, 0,23 mol) e gotas a -78 °C. Depois da adição de (R)-glicidil butirato (31,5 ml, 0,23 mol), seguida por agitação por 3 horas com aquecimento lento até a temperatura ambiente, a solução foi ajustada ao pH —6 com solução aquosa de cloreto de amónio, e concentrada sob pressão reduzida. O concentrado foi dissolvido em 80% acetato de etila/solução de hexano, sequencialmente lavado com água e solução de cloreto de sódio aquosa saturada (salmoura), seco com sulfato do sódio anidro, e concentrado sob pressão reduzida. O concentrado foi separado por cromatografia em coluna com o uso de 4 0% acetato de etila/solução de hexano para obter Composto V (45 g, 0,093 mol, 42%) como um óleo incolor.
XH RMN (600 MHz, CDCI3) 6 7,50-7,48 (m, 1H), 7,30-7,28 (m, 1H) , 7,17-7,16 (m, 1H) , 4,74-4,70 (m, 1H) , 4,03-4,02 (m, 1H), 3,98 (m, 2H), 3,75 (m, 3H), 3,65 (m, 2H), 1,51 (s, 3H), 1,36 (s, 6H), 0,85 (s, 9H), 0,02 (s, 6H). Exemplo de preparação 6 - Preparação do composto VI
Composto V (45 g, 0,093 mol) foi dissolvido em diclorometano (300 ml) e agitado por 20 minutos depois de adição sequencialmente de trietilamina (26 ml, 0,186 mol) e metanossulfonil cloreto (MsCl, 10,9 ml, 0,14 mol) em gotas a 0 °C. Depois de aquecimento até a temperatura ambiente, seguida por agitação por 1 hora, a solução foi concentrada sob pressão reduzida. O concentrado foi dissolvido em acetato de etila, sequencialmente lavado com 0,5 N HC1, solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seco com sulfato do sódio anidro, e concentrado sob pressão reduzida para obter Composto VI (50 g, 0,089 mol, 96%) como um óleo amarelo.
TH RMN (400 MHz, CDC13) δ 7,46 (dd, 1H, Jx = 11,6 Hz, J2=2,4 Hz), 7,29 (m, 1H) , 7,13 (m, 1H), 4,94-4,88 (m, 1H) , 4,50-4,39 (m, 2H) , 4,12 (m, 1H) , 3,92 (m, 1H) , 3,72 (m, 2H) , 3,64-3,62 (m, 2H) , 3,08 (s, 3H) , 1,49 (s, 3H) , 1,34 (s, 6H), 0,83 (s, 9H), 0,00 (s, 6H). Exemplo de preparação 7 - Preparação do composto VII
Composto VI (50 g, 0,089 mol) foi dissolvido em DMF (200 ml) e agitado por 3 horas a 80 °C depois da adição de NaN3 (7,16 g, 0,11 mol). A solução foi resfriada até a temperatura ambiente, diluída com acetato de etila, sequencialmente lavada com água, solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, e concentrada sob pressão reduzida para obter quantitativamente Composto VII (47 g, 0,089 mol) como um sólido oleoso incolor.
XH RMN (600 MHz, CDC13) δ 7,48 (dd, J3 = 8,2 Hz, J2 = 1,4 Hz) 7,30 (m, 1H) , 7,16 (m, 1H) , 4,81-4,79 (m, 1H) , 4,09-4,08 (m, 1H) , 3,86 (m, 1H) , 3,74 (m, 2H) , 3,62-3,59 (m, 1H), 1,51 (s, 3H), 1,36 (s, 6H), 0,85 (s, 9H), 0,02 (s, 6H) . Exemplo de preparação 8 - Preparação do composto VIII
Composto VII (47 g, 0,089 mol) foi dissolvido em metanol (4 00 ml) e agitado por 4 horas sob balão de hidrogênio depois da adição de Pd/C (3,5 g) . A solução foi filtrada com celite e concentrada sob pressão reduzida. O concentrado foi dissolvido em diclorometano (130 ml) e, depois da adição de 1 N de solução aquosa de NaOH (130 ml),
Cbz-Cl (15,5 ml, 0,11 mol) foi lentamente adicionado em gotas com agitação. Depois de agitação por 2 horas em temperatura ambiente, a camada orgânica foi separada, lavada com água e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, concentrada sob pressão reduzida, e separada por cromatograf ia em coluna com o uso de 2 0% acetato de etila/solução de hexano para obter Composto VIII (50,5 g, 0,082 mol, 92%) como um óleo amarelo claro.
XH RMN (400 MHz, CDC13) δ 7,46-7,43 (m, 1H) , 7,36-7,35 (m, 1H), 7,31 (s, 6H), 7,11 (m, 1H), 5,09 (s, 2H), 4,75 (m, 1H) , 4,01 (t, 1H, J = 8,4 Hz), 3,76-3,50 (m, 1H) , 1,49 (s, 3H), 1,34 (s, 6H), 0,83 (s, 9H), 0,01 (s, 6H). Exemplo de preparação 9 - Preparação do composto IX
Composto VIII (50,5 g, 0,082 mol) foi dissolvido em diclorometano (100 ml), agitado por 3 horas em temperatura ambiente depois da adição de 4 N de solução de HCI em dioxano (13 0 ml) , e concentrado sob pressão reduzida para obter quantitativamente Composto IX (36 g, 0,082 mol) como um sólido branco.
1H RMN (400 MHz, DMSO-d6) δ 7,69 (t, 1H, J = 6,0 Hz), 7,44-7,40 (m, 1H) , 7,32 (s, 6H) , 7,09-7,07 (m, 1H) , 6,88 (t, 1H, J = 9,2 Hz), 5,03 (s, 2H), 4,71-4,68 (m, 1H), 4,08- 4,03 (m, 2H), 3,73-3,69 (m, 1H), 3,60-3,57 (m, 3H), 3,39- 3,34 (m, 2H) , 3,18-3,15 (m, 2H) . Exemplo de preparação 10 - Preparação do composto XII
Composto IX (36 g, 0,082 mol) foi dissolvido em diclorometano (300 ml) e agitado por 10 minutos depois da adição lenta de trietilamina (34,5 ml, 0,245 mol) e metanossulfonil cloreto (MsCl, 9,5 ml, 0,123 mol) sequencialmente a 0 °C em gotas. A solução foi aquecida até a temperatura ambiente, agitada por 2 horas, diluída com diclorometano, sequencialmente lavada com água, solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, e concentrada sob pressão reduzida. 0 sólido resultante foi triturado com solvente de éter dietílico e filtrado para obter Composto X (30,5 g, 0,063 mol, 77%) como um sólido branco.
Composto X (20 g, 0,042 mol) foi adicionado a etanol (100 ml) e agitado por 2 horas a 60 °C depois da adição de hidrazina monohidrato (H2NNH2-H2O, 50 ml) . A solução foi concentrada sob pressão reduzida para obter Composto XI (17,4 g, 0,042 mol) como um óleo.
Composto XI (17,4 g, 0,042 mol) foi adicionado a ácido acético (200 ml) e refluído por 8 horas depois da adição de trimetil ortoformato (100 ml) . A solução foi destilada sob pressão reduzida, dissolvida em diclorometano, sequencialmente lavada com solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, e concentrada sob pressão reduzida. O concentrado foi separado por cromatograf ia em coluna com o uso de 5% metanol/diclorometano solução para obter Composto XII (5,8 g, 0,013 mol, 31%) como um sólido branco.
1H RMN (600 MHz, CDC13) δ = 8,52 (s, 1H) , 7,55-7,53 (m, 1H) , 7,30-7,28 (m, 6H) , 7,19-7,18 (m, 1H) , 7,11-7,08 (m, 1H) , 6,86 (s, 1H) , 5,27 (t, J = 6 Hz, 1H) , 5,08 (s, 2H) , 4,77 (m, 1H) , 4,03-4,00 (m, 1H) , 3,97 (t, J = 4,8 Hz, 2H) , 3,81-3,76 (m, 1H) , 3,70 (t, J = 5,1 Hz, 2H) , 3,65-3,60 (m, 1H), 3,59-3,54 (m, 1H). Exemplo de preparação 11 - Preparação do composto XIII
Composto XII (5 g, 0,011 mol) foi dissolvido em metanol (100 ml) e agitado por 4 horas sob balão de hidrogênio depois da adição de Pd/C (0,5 g) . A solução foi filtrada com celite e concentrada sob pressão reduzida para obter Composto XIII (3,2 g, 0,010 mol, 91%) como um sólido oleoso.
XH RMN (600 MHz, DMSO-ds) δ = 8,43 (s, 1H) , 7,65-7,63 (m, 1H) , 7,40-7,36 (m, 2H) , 7,12 (s, 1H) , 4,65-4,62 (m, 1H), 4,09-4,06 (m, 1H), 3,89-3,86 (m, 1H), 3,85 (t, J = 5,1 Hz, 2H), 3,70 (t, J = 4,8 Hz, 2H), 2,88-2,85 (m, 1H), 2,82- 2,79 (m, 1H). Exemplo de preparação 12 - Preparação do composto XV
Boc-3-aminoisoxazol (1,22g, 6,6 mmol) foi dissolvido em DMF (40 ml) e agitado por 30 minutos depois da adição de 50% NaH (0,32 g, 6,6 mmol) . Depois da adição lenta de Composto VI (3,6 g, 6,6 mmol) dissolvido em DMF (10 ml) em gotas, a solução foi agitada a 80 °C por 4 horas. A solução foi resfriada até a temperatura ambiente, diluída com acetato de etila, lavada duas vezes com água, seca com sulfato do sódio anidro, e concentrada sob pressão reduzida para obter Composto XIV (4,16 g, 6,4 mmol).
Composto XIV (4,16 g, 6,4 mmol) foi dissolvido em diclorometano (2 0 ml) , agitado de um dia para o outro em temperatura ambiente depois da adição de 4 N de solução de HC1 em dioxano (20 ml), concentrada sob pressão reduzida, e triturada com solvente de éter dietílico para obter Composto XV (2,2 g, 6,2 mmol, 94%) como um sólido branco.
RMN (600 MHz, DMSO-d6) δ 8,39 (d, J = 2,2 Hz, 1H) , 7,52 (dd, Ji = 13,8 Hz, J2 = 2,4 Hz, 1H) , 7,18 (dd, J, = 8,4 Hz, J2 = 1,8 Hz, 1H) , 7,10 (t, J = 9,3 Hz, 1H) , 6,00 (d, J = 2,2 Hz, 1H) , 4,86 (m, 1H) , 4,11 (t, J = 9 Hz, 1H) , 3,80-3,19 (m, 7H).
Exemplo de preparação 13 - Preparação do composto XIX
Composto VII (0,613 g, 1,2 mmol) foi dissolvido em dioxano (10 ml), agitado por 4 horas sob refluxo depois da adição de 2,5-norbornadieno (0,6 ml, 6 mmol), e resfriado até a temperatura ambiente. A solução foi concentrada sob pressão reduzida, dissolvido em diclorometano, lavada com água, e seca com sulfato de sódio para obter Composto XVIII (triazol, 98%), que foi tratado com ácido clorídrico como no Exemplo de Preparação 9 para obter Composto XIX (0,35 g, 1,1 mmol, 92 %).
TH RMN (600 MHz, DMSO-d6) δ = 8,18 (s, 1H) , 7,77 (s, 1H) , 7,39 (dd, Ji = 13 Hz, J2 = 2,4 Hz, 1H) , 7,09-7,00 (m, 2H) , 5,11 (m, 1H) , 4,82 (d, J = 4,8 Hz, 2H) , 4,18 (t, J = 9,0 Hz, 1H) , 3,84 (m, 1H) , 3,59 (t, J = 6,0 Hz, 2H) , 3,19 (t, J = 6,0 Hz, 2H). Exemplo de preparação 14 - Preparação do composto XXVII-b
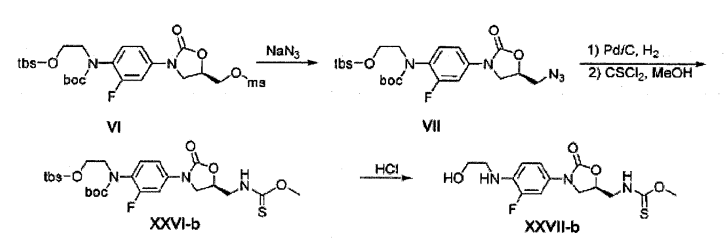
Composto VI (12 g, 21 mmol) foi dissolvido em DMF (100 ml) e agitado a 80 °C por 3 horas depois da adição de NaN3 (1,65 g, 26 mmol) . A solução foi resfriada até a temperatura ambiente, diluída com acetato de etila/hexano (150 ml/30 ml), lavada 3 vezes com água destilada (200 ml), seca com sulfato do sódio anidro, concentrada sob pressão reduzida, e separada por cromatografia em coluna com o uso de 30% acetato de etila/solução de hexano para obter Composto VII (9,6 g, 19 mmol, 89%).
Composto VII (9,6 g, 19 mmol) foi dissolvido em metanol (120 ml), agitado por 4 horas sob balão de hidrogênio depois da adição de Pd/C (1 g) , e filtrado com celite para obter um composto de amina (8,6 g, 95%) . O composto de amina (8,6 g) foi dissolvido em diclorometano (120 ml) e, depois da adição de solução saturada aquosa de NaHCO3 (40 ml) e então adição de tiofosgeno (1,6 ml, 21 mmol) a 0o C, foi agitada por 2 horas. A camada orgânica foi seca com sulfato de sódio, destilada sob pressão reduzida, dissolvida em metanol (150 ml), agitada de um dia para o outro sob refluxo, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto XXVI-b (2,6 g, 7,6 mmol) , que foi tratado com ácido clorídrico como no Exemplo de Preparação 9 para obter quantitativamente Composto XXVII-b.
RMN (600 MHz, CDC13) δ = 7,35 (dd, Jx = 13 Hz, J2 = 2,4 Hz, 1H) , 6,99-6,89 (m, 2H) , 6,70 (t, J = 9,2 Hz, 1H) , 4,93 (m, 1H) , 4,10-3,91 (m, 6H) , 3,88-3,78 (m, 3H) , 3,32 (t, J = 5,2 Hz, 2H). Exemplo de preparação 15 - Preparação do composto XXVII-a
Um cloridrato do Composto XXVII-a (3,4 g, 9,8 mmol, 85 %) foi obtido a partir do Composto VI como no Exemplo de Preparação 14, com o uso de Ac2O em vez de tiofosgeno.
1H RMN (600 MHz, DMSO-d6) δ 7,69 (t, 1H, J = 6,0 Hz), 7,46 (dd, 1H, Ji = 13,8 Hz, J2 = 2,4 Hz), 7,41-7,26 (m, 5H), 7,18-7,11 (m, 1H), 7,00 (t, 1H, J = 9,6 Hz), 6,21-5,73 (m, 2H) , 5,03 (s, 2H), 4,74-4,66 (m, 1H) , 4,07 (t, 1H, J = 9,0 Hz), 3,76-3,70 (m, 1H), 3,60 (t, 2H, J = 5,7 Hz), 3,42- 3,33 (m, 2H), 3,19 (t, 2H, J = 5,7 Hz). Exemplo de preparação 16 - Preparação do composto XXVIII-a
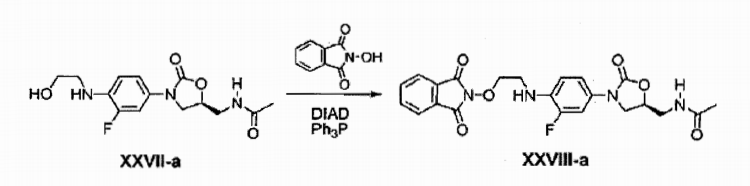
Um cloridrato do Composto XXV-a (1,69 g, 4,86 mmol), hidroxiftalimida (0,83 g, 5,11 mmol), trifenilfosfino (1,34 g, 5,11 mmol) e trietilamina (0,7 ml, 4,87 mmol) foram adicionados a THF (20 ml) . Depois da adição lenta de diisopropil azodicarboxilato (DIAD, 1,15 ml, 5,84 mmol) em gotas com agitação, a solução foi agitada por 3 horas em temperatura ambiente. Depois da filtração, o filtrado foi concentrado sob pressão reduzida e separado por cromatografia em coluna para obter Composto XXVIII-a (1,49 g, 3,26 mmol, 88%).
XH RMN (400 MHz, CDC13) δ = 7,86 (m, 2H) , 7,76 (m, 2H), 7,38 (dd, J = 8,8, 1,6 Hz, 1H), 7,00 (dd, J = 8,8, 1,6 Hz, 1H) , 6,69 (t, J = 6,0 Hz, 1H) , 6,13 (t, J = 4,0 Hz), 4,92 (br, s, 1H) , 4,75 (m, 1H) , 4,42 (t, J = 3,6 Hz, 1H) , 4,00 (t, J = 6 Hz, 1H) , 3,70 (m, 2H) , 3,60 (m, 1H) , 3,50 (br, s, 2H), 2,03 (s, 3H). LCMS: 457 (M + H+) para C22H21FN4O6.
Exemplo de preparação 17 - Preparação do composto XXIII
Composto V (26 g, 0,053 mol) foi dissolvido emdiclorometano (180 ml) e agitado por 10 minutos depois da adição lenta de diisopropiletilamina (DIPEA, 13 ml, 0,079 mol) e benzoil cloreto (Bz-Cl, 7,4 ml, 0,064 mol) sequencialmente em gotas a 0 °C. Depois de aquecimento ate a temperatura ambiente, seguido por adição de uma pequena quantidade de DMAP, a solução foi agitada por 2 horas. A solução foi concentrada sob pressão reduzida, dissolvida em acetato de etila, sequencialmente lavada com solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, e concentrada sob pressão reduzida para obter quantitativamente Composto XXII (31 g, 0,053 mol), que foi tratado com ácido clorídrico como no Exemplo de Preparação 9 para obter quantitativamente Composto XXIII
2H RMN (600 MHz, DMSO-d6) δ 7,88 (d, J = 7,8 Hz, 2H) , 7,63 (t, 1H, J = 7,2 Hz), 7,46 (t, 2H, J = 7,2 Hz), 7,41 (dd, 1H, Ji = 13,8 Hz, J2 = 2,4 Hz), 7,11 (d, 1H, J = 9,0 Hz), 6,88 (t, 1H, J = 9,0 Hz), 5,02 (m, 1H), 4,54-4,45 (m, 2H), 4,16 (t, 1H, J = 9,0 Hz), 3,88 (m, 1H), 3,54 (t, 2H, J = 6,0 Hz), 3,13 (t, 2H, J = 6,0 Hz).
Métodos para a síntese de compostos alvo a partir do intermediário preparado nos Exemplos de Preparação 1 a 17 são exemplificados pelos exemplos a seguir. Exemplo 1- Preparação do composto 1
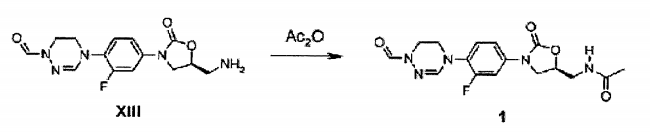
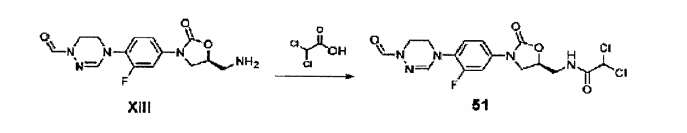
Composto XIII (0,1 g, 0,31 mmol) obtido no Exemplo de Preparação 11 foi dissolvido em diclorometano (3 ml) , agitado por 2 horas em temperatura ambiente depois de adição seqüencial de DIPEA (0,1 ml, 0,6 mmol) e Ac20 (0,06 ml, 0,6 mmol) em gotas, concentrado sob pressão reduzida, e separado por cromatografia em coluna para obter Composto 1 (0,098 g, 0,27 mmol, 87%) como um sólido branco.
RMN (400 MHz, clorofórmio-d4) δ = 8,54 (s, 1H) , 7,59 (dd, J = 13,6, 2,4 Hz, 1H) , 7,20 (dd, J = 13,6, 2,4 Hz, 1H), 7,13 (t, J = 8,8, Hz, 1H), 6,88 (s, 1H), 6,19 (t, J = 6,0 Hz, 1H) , 4,81 (m, 1H) , 4,05 (t, J = 8 Hz, 1H) , 3,99 (t, J = 4,8 Hz, 2H) , 3,80 (dd, J = 8,8, 6,8 Hz, 1H) , 3,73 (t, J = 4,8 Hz, 2H), 3,69 (m, 2H), 2,03 (s, 3H). LCMS: 364 (M + H+) para C16H18FN5O4 . Exemplo 2- Preparação do composto 2
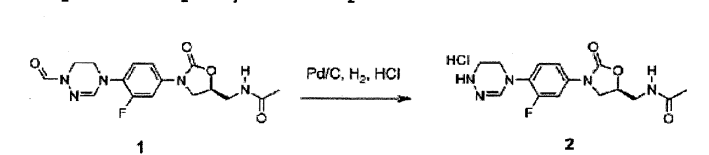
Composto 1 (0,7 g, 1,93 mmol), 4 N ácido clorídrico dissolvido em 1,4-dioxano (3 ml, 12 mmol) e Pd/C (70 mg) foram adicionados a THF (20 ml), e agitados por 2 horas sob gás hidrogênio. A solução foi filtrada com celite e concentrada sob pressão reduzida para obter Composto 2 (0,72 g, 1,93 mmol, 100%) como um sólido branco.
1H RMN (400 MHz, DMSO-d6) δ = 8,34-8,31 (m, 2H), 7,68 (dd, J = 13,6, 2,4 Hz, 1H) , 7,56 (t, J = 8,8 Hz, 1H) , 7,41 (dd, J = 13,6, 2,4 Hz, 1H), 4,76 (m, 1H), 4,15 (t, J = 8,8 Hz, 1H) , 3,78 (m, 3H) , 3,46 (m, 2H) , 3,35 (t, J = 8,4 Hz, 2H), 1,83 (s, 3H). LCMS: 33 6 (M + H+) para CI5H18FN5O3 . Exemplo 3- Preparação do composto 3
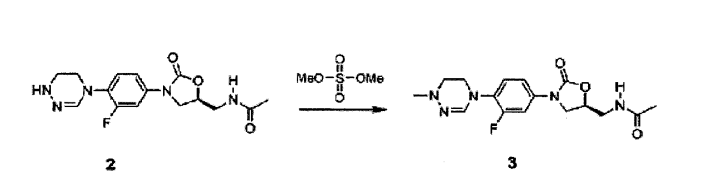
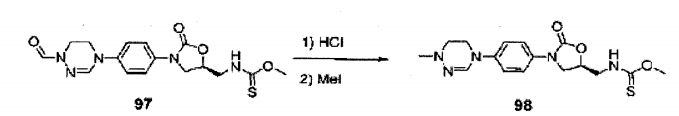
Composto 2 (0,11 g, 0,34 mmol) foi dissolvido em metanol (3 ml), agitado por 6 horas em temperatura ambiente depois da adição de DIPEA (0,17 ml, 1 mmol) e dimetil sulfato (52 mg, 0,41 mmol), e separado por cromatografia em coluna para obter Composto 3 (29 mg, 0,083 mmol, 24%) como um sólido branco.
RMN (600 MHz, clorofórmio-dl) δ 7,52 (dd, 1H, Jx = 13,8 Hz, J2 = 2,4 Hz), 7,18-7,62 (m, 1H) , 7,10 (t, 1H, 8,4 Hz), 6,90 (s, 1H), 6,70 (t, 1H, J = 6,0 Hz), 4,82-4,75 (m, 1H) , 4,04 (t, 1H, J = 9,0 Hz), 3,85 (t, 2H, J = 4,8 Hz), 3,82 (t, 1H, 4,8 Hz), 3,74-3,60 (m, 2H), 2,99 (t, 2H, J = 4,8 Hz), 2,79 (s, 3H), 2,02 (s, 3H). LCMS: 350 (M + H+) para C16H20F-1-N5O3. Exemplo 4- Preparação do composto 4
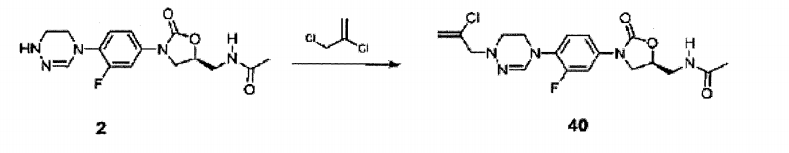
Composto 2 (0,21 g, 0,63 mmol) foi dissolvido em DMF (3 ml), agitado por 6 horas em temperatura ambiente depois da adição de DIPEA (0,17 ml, 1 mmol) e alil brometo (0,1 g, 0,8 mmol), e separado por cromatografia em coluna para obter Composto 4 (80 mg, 0,21 mmol, 33%) como um sólido branco.
TH RMN (600 MHz, CDC13) δ = 7,51 (dd, Jx = 13 Hz, J2 = 2,4 Hz, 1H), 7,15-7,09 (m, 2H), 6,92 (s, 1H), 6,18 (br, t, 1H) , 6,02 (m, 1H) , 5.30-5,22 (m, 2H) , 4,79 (m, 1H) , 4,05 (t, J = 9 Hz, 1H), 3,82 (t, J = 4,8 Hz, 2H), 3,79-3,58 (m, 6H) , 3,00 (t, J = 4,8 Hz, 2H) , 2,03 (s, 3H) . LCMS: 376 (M + H+) para C18H22F-1-N5O3. Exemplo 5- Preparação do composto 5
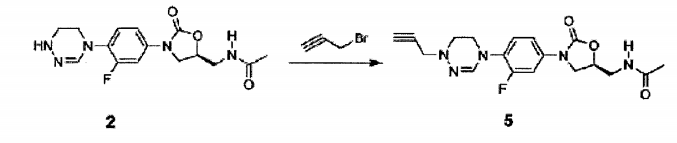
Composto 5 (34 mg, 0,091 mmol, 43%) foi obtido a partir do Composto 2 como no Exemplo 4, com o uso de propargil brometo.
TH RMN (60 0 MHz, CDC13) δ = 7,51 (dd , Jj. = 13 Hz, J2 = 2,4 Hz, 1H), 7,16-7,11 (m, 2H) , 6,95 (s, 1H) , 6,00 (br, t, 1H) , 4,79 (m, 1H) , 4,04 (t, J = 9 Hz, 1H) , 3,85 (t, J = 4,8 Hz, 2H), 3,82 (d, J = 2,4 Hz, 2H), 3,79- 3,62 (m, 3H), 3,13 (t, J = 4,8 Hz, 2H) , 2,31 (t, J = 2,4 Hz, 1H) , 2,03 (s, 3H) . LCMS: 3 74 (M + H+) para C^oF-i-NgOa . Exemplo 6- Preparação do composto 6
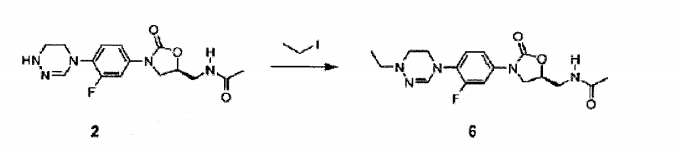
Composto 2 (30 mg, 0,08 mmol), DIPEA (66 uL, 0,40 mmol) e iodeto de etila (2 0 uL, 0,24 mmol) foram sequencialmente adicionados a diclorometano (2 ml) a 0 °C e agitados por 8 horas sob refluxo. A solução foi concentrada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 6 (5 mg, 0,01 mmol, 13%) como uma espuma amarela.
XH RMN (400 MHz, clorofórmio-d4) δ = 7,57 (dd, J = 15 Hz, 1H) , 7,18 (s, 2H) , 7,08 (s, 1H) , 6,31 (t, J = 6,0 Hz, 1H) , 4,83 (m, 1H) , 4,07 (t, J = 8,0 Hz, 1H) , 3,90 (t, J = 4,2 Hz, 2H) , 3,83 (dd, J = 8,0, 7,2 Hz, 1H) , 3,74-3,65 (m, 2H) , 3,12 (t, J = 5,4 Hz, 3H) , 3,05 (q, J = 6,6 Hz, 2H) , 2,06 (s, 3H), 1,31 (t, J = 6,6 Hz, 3H). LCMS: 364 (M + H+) para CI7H22FN5O3 . Exemplo 7- Preparação do composto 7
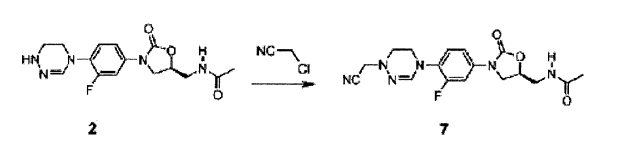
Composto 2 (0,1 g, 0,3 mmol) foi dissolvido em DMF (3 ml) , aquecido por 6 horas a 80 °C depois da adição de 1 equivalente de K2CO3, 2 equivalentes de cloroacetonitrila e uma quantidade catalítica de Kl, e separado por cromatografia em coluna para obter Composto 7 (107 mg, 0,287 mmol, 96%) como um sólido branco.
XH RMN (600 MHz, clorofórmio-dl) δ 7,40 (dd, 1H, Ji = 13,2 Hz, J2 = 2,4 Hz), 7,01 (dd, 1H, Jx = 8,4 Hz, J2 = 1,2 Hz), 6,69 (t, 1H, J = 9,3 Hz), 6,14 (d, 1H, J = 5,4 Hz), 4,78-4,72 (m 1H), 4,40 (t, 2H, J = 5,4 Hz), 4,00 (t, 1H, J = 9,0 Hz), 3,76-3,66 (m, 2H) , 3,61 (t, 1H, J = 6,0 Hz), 3,55 (t, 2H, J = 5,4 Hz), 3,03 (s, 3H), 2,03 (s, 3H). LCMS: 3 74 (M + H+) pata CI7HI9FN6O3 . Exemplo 8- Preparação do composto 8
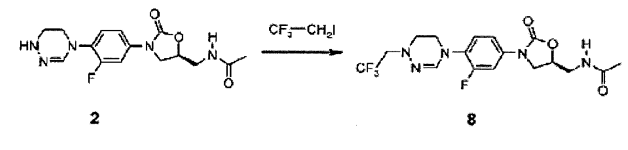
Composto 2 (0,1 g, 0,3 mmol) foi dissolvido em DMF (3 ml) por 6 horas a 200 °C depois da adição de 1 equivalente de K2CO3 e 2 equivalentes de 1,1,1-triflúor-2-iodoetano, e separado por cromatografia em coluna para obter Composto 8 (11 mg, 0,026 mmol, 9%) como um sólido branco.
1H RMN (600 MHz, clorofórmio-dl) δ 7,52 (dd, 1H, Ji = 13,8 Hz, J2 = 2,4 Hz), 7,18-7,07 (m, 2H) , 6,86 (s, 1H) , 6,32-6,24 (m, 1H) , 4,90-4.76 (m, 1H) , 4,04 (t, J = 8,7 Hz), 3,84 (t, 2H, J = 4,5 Hz), 3,81-3,76 (m, 1H), 3,62-3,52 (m, 2H) , 3,24 (t, 4,5 Hz), 2,02 (s, 3H) . LCMS: 418 (M + H+) para Ci7Hi9F4N5O3 . Exemplo 9- Preparação do composto 9
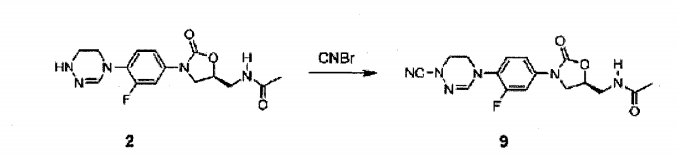
Composto 2 (150 mg, 0,40 mmol), DIPEA (200 uL, 1,20 mmol) e brometo de cianogênio (63 mg, 0,60 mmol) foram sequencialmente adicionados ao diclorometano (2 ml) a 0 °C e agitados por 0,5 hora. A solução foi concentrada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 9 (25 mg, 0,07 mmol, 17%) como um sólido branco.
1H RMN (400 MHz, clorof Órmio-d4) δ = 7,60 (dd, J = 13,2, 2,4 Hz, 1H) , 7,20 (dd, J = 13,2, 2,4 Hz, 1H) , 7,13 (t, J = 8,8, Hz, 1H), 6,89 (s, 1H), 4,80 (m, 1H), 4,05 (t, J = 9,2 Hz, 1H) , 3,85-3,61 (m, 2H) , 2,03 (s, 3H) . LCMS: 3 61 (M + H+) para C16H17FN6O3. Exemplo 10- Preparação do composto 10
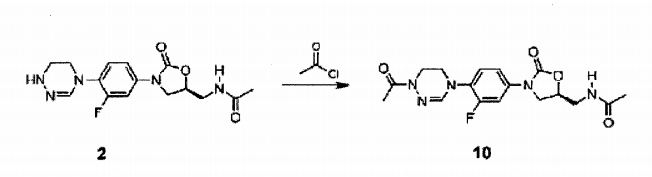
Composto 2 (5 mg, 0,013 mmol), DIPEA (4 uL, 0,026 mmol) e acetil cloreto (1,5 uL, 0,02 mmol) foram sequencialmente adicionados a diclorometano (2 ml) a 0 °C e agitados por 1,5 hora. Depois da adição de diclorometano (30 ml), a solução foi lavada com solução de bicarbonato de sódio aquosa saturada (15 ml) , seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 10 (2 mg, 0,004 mmol, 30%) como um sólido branco.
1H RMN (600 MHz, clorof órmio-d4) δ = 7,57 (dd, J = 13,2, 2,4 Hz, 1H), 7,20 (dd, J = 9,6, 2,4 Hz, 1H), 7,13 (t, J = 9,6, Hz, 1H) , 6,85 (s, 1H) , 6,03 (t, J = 6,0 Hz, 1H) , 4,80 (m, 1H), 4,06 (m, 2H), 3,79 (dd, J = 9,0, 6,6 Hz, 2H), 3,71 (m, 2H), 3,62 (m, 1H) 2,03 (s, 3H). LCMS: 3 78 (M + H+) para C17H20FN5O4. Exemplo 11- Preparação do composto 11
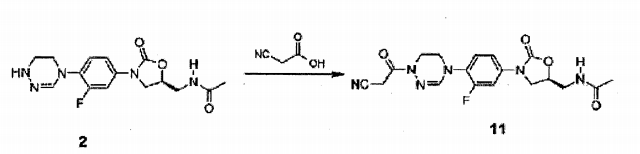
Composto 2 (30 mg, 0,08 mmol), (IH-benzotriazol-l- iloxi)tripirrolidinofosfônio hexafluorfosfato (PyB OP, 105 mg, 0,20 mmol), ácido cianoacético (14 mg, 0,16 mmol) e DIPEA (40 uL, 0,24 mmol) foram sequencialmente adicionados a DMF (2 ml) a 0 °C e agitados por 1,5 hora em temperatura ambiente. Depois da adição de diclorometano (30 ml), a solução foi lavada 3 vezes com solução de bicarbonato de sódio aquosa saturada, seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 11 (5 mg, 0,01 5 mmol, 13%) como um sólido branco.
1H RMN (400 MHz, clorof órmio-d4) δ = 7,61 (dd, J = 13,2, 2,8 Hz, 1H) , 7,25 (dd, J = 13,2, 2,8 Hz, 1H) , 7,13 (t, J = 8,8, Hz, 1H) , 6,85 (s, 1H) , 6,19 (t, J = 6,0 Hz, 1H), 4,81 (m, 1H), 4,07 (m, 2H), 3,85 (m, 3H), 3,75 (t, J = 10 6,0 Hz, 2H), 3,68 (m, 2H), 2,03 (s, 3H). LCMS: 403 (M + H+) para C18H19FN6O4. Exemplo 12- Preparação do composto 12
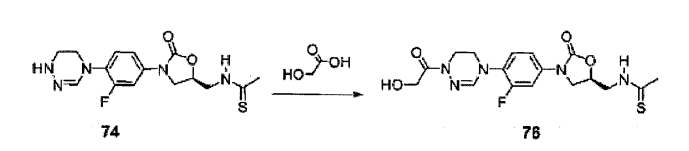
Composto 2 (200 mg, 0,54 mmol), PyBOP (700 mg, 1,34 mmol), ácido glicólico (82 mg, 1,07 mmol) e DIPEA (266 uL, 1,61 mmol) foram sequencialmente adicionados a DMF (2 ml) a 20 0 °C e agitados por 2 horas em temperatura ambiente. Depois da adição de diclorometano (100 ml), a solução foi lavada 3 vezes com água destilada, seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 12 (83 mg, 0,21 25 mmol, 39%) como um sólido branco.
TH RMN (400 MHz, DMSO-d6) δ = 8,25 (t, J = 6 Hz, 1H) , 7,62 (dd, J = 8,8, 2,4 Hz, 1H) , 7,37 (t, J = 8,8 Hz, 1H) , 7,32 (dd, J = 8,8, 2,4 Hz, 1H) , 7,07 (t, J = 2,0 Hz, 1H) , 4,74 (m, 1H) , 4,53 (t, J = 6,0 Hz, 1H) , 4,32 (d, J = 6 Hz, 30 2H) , 4,12 (t, J = 8,8 Hz, 1H) , 3,89 (t, J = 4,6 Hz, 2H) , 3,75-3,69 (m, 3H), 3,40 (m, 2H), 1,83 (s, 3H). LCMS: 394 (M + H+) para C17H20FN5O5. Exemplo 13- Preparação do composto 13
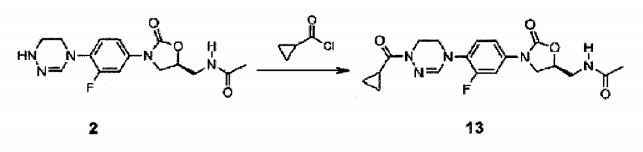
Composto 2 (35 mg, 0,09 mmol), DIPEA (45 uL, 0,28 mmol) e ciclopropanocarbonil cloreto (13 uL, 0,14 mmol) foram sequencialmente adicionados a diclorometano (3 ml) a 0 °C e agitados por 1 hora em temperatura ambiente. A solução foi concentrada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 13 (13 mg, 0,03 mmol, 33%) como um sólido branco. XH RMN (600 MHz, DMSO-d6) δ = 8,25 (t, J = 6 Hz, 1H) , 7,6 (d, J = 13,8 Hz, 1H) , 7,39 (t, J = 9,0 Hz, 1H) , 7,32 (d, J = 13,8 Hz, 1H), 7,10 (m, 1H), 4,75 (m, 1H), 4,12 (t, J = 9,0 Hz, 1H) , 3,90 (s, 2H) , 3,74 (t, J = 6,6 Hz, 1H) , 3,70 (s, 2H) , 3,42 (t, J = 5,4 Hz, 2H) , 2,69 (t, J = 6,0 Hz, 1H), 1,83 (s, 3H), 0,85 (d, J = 6,0 Hz, 3H). LCMS: 404 (M + H+) para CI9H22FN5O4 . Exemplo 14- Preparação do composto 14
Composto 2 (30 mg, 0,08 mmol), trietilamina (23 uL, 0,16 mmol) e trimetilsilil isocianato (63 uL, 0,40 mmol) foram sequencialmente adicionados a diclorometano (3 ml) a 0 °C e agitados por 2 horas em temperatura ambiente. Depois da adição de diclorometano (3 0 ml) , a solução foi lavada duas vezes com solução de bicarbonato de sódio aquosa saturada, seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 14 (8 mg, 0,02 mmol, 26%) como um sólido branco.
XH RMN (400 MHz, DMSO-d6) δ = 8,26 (t, J = 6,0 Hz, 1H) , 7,60 (dd, J = 15,0,2,4 Hz, 1H) , 7,37-7,30 (m, 2H) , 6,96 (d, J = 2,0 Hz, 1H), 6,32 (s, 2H), 4,74 (m, 1H), 4,12 (t, J = 8,8 Hz, 1H) , 3,78-3,67 (m, 4H) , 3,40-3,28 (m, 3H) , 1,83 (s, 3H). LCMS: 379 (M + H+) para CI6H19FN6O4 . Exemplo 15- Preparação do composto 15
Composto 15 (25 mg, 0,059 mmol, 42%) foi obtido a partir do Composto 2 como no Exemplo 6, com o uso de carbonildiimidazol (437 mg, 2,7 mmol) e etanolamina. 1H RMN (600 MHz, clorofórmio-dl) δ 7,69 (s, 1H), 7,54 (dd, 1H, Ji = 13,2 Hz, J2 = 2,4 Hz), 7,16 (dd, 1H, Jx = 9,0 Hz, J2 = 1,8 Hz), 7,10-7,08 (m, 1H) , 6,87 (t, 1H, J = 6,0 Hz), 6,78 (s, 1H), 6,72 (t, 1H, J = 6,0 Hz), 4,83-7,49 (m, 1H) , 4,04 (t, 1H, J = 9,0 Hz), 3,95 (t, 2H, J = 4,8 Hz), 3,84-3,78 (m, 1H), 3,76 (t, 2H, J = 5,4 Hz), 3,72 (t, 2H, J = 4,8 Hz), 3,67 (dd, 2H, Jx = 6,0 Hz, J2 = 4,8 Hz), 2,03 (s, 3H). LCMS: 423 (M + H+) para Ci8H23FN6O5. Exemplo 16- Preparação do composto 16
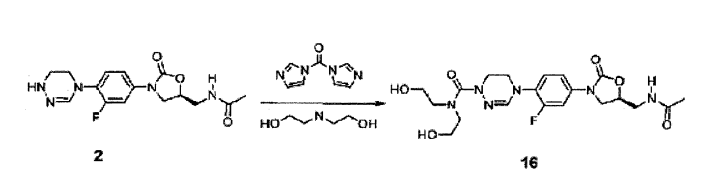
Composto 16 (15 mg, 0,032 mmol, 25%) foi obtido a partir do Composto 2 como no Exemplo 15, com o uso carbonildiimidazol e dietanolamina.
RMN (600 MHz, DMSO-d6) δ 7,70-7,62 (m, 1H) , 7,37- 7,30 (m, 2H), 7,1 (s, 1H), 4,81-4,76 (m, 1H), 4,45-4,40 (m, 10 2H), 4,14 (t, 1H, J = 9,0 Hz), 4,01-3,94 (m, 2H), 3,82-3,78 (m, 4H), 3,55 (d, 2H, J = 4,8 Hz), 3,48-3,42 (m, 1H), 3,42- 3,38 (m, 2H), 3,20-3,16 (m, 2H), 1,94 (s, 3H), 1,29 (t, 2H, J = 7,2 Hz). LCMS: 467 (M + H+) para C2oH27FN606. Exemplo 17- Preparação do composto 17
Composto 17 (31 mg, 0,075 mmol, 88%) foi obtido a partir do Composto 2 como no Exemplo 11, com o uso de ácido difluoracético. 1H RMN (600 MHz, clorofórmio-dl) δ 7,61 (dd, 1H, J, = 13,2 Hz, J2 = 3,0 Hz), 7,22 (dd, 1H, Jx = 9,0 Hz, J2 = 2,4 25 Hz), 7,14 (t, 1H, J = 9,0 Hz), 6,90 (s, 1H), 6,77 (t, 1H, J = 53,4 Hz), 6,04 (t, 1H, J = 6,3 Hz), 4,83-4,79 (m, 1H) , 4,08 (t, 2H, J = 4,8 Hz), 4,05 (t, 1H, J = 9,0 Hz), 3,88- 3,80 (m, 1H), 3,78 (t, 2H, J = 4,8 Hz), 3,75-3,69 (m, 1H) , 3,69-3,60 (m, 1H) , 2,03 (s, 3H) . LCMS: 414 (M + H+) para CI7HI8F3N5O4 . Exemplo 18- Preparação do composto 18
Composto 2 (35 mg, 0,09 mmol), DIPEA (45 uL, 0,28 mmol) e metanossulfonil cloreto (11 uL, 0,14 mmol) foram sequencialmente adicionados a diclorometano (3 ml) a 0 °C e agitados por 1 hora em temperatura ambiente. A solução foi concentrada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 18 (13 mg, 0,03 mmol, 33%) como um sólido branco. XH RMN (600 MHz, DMSO-d6) δ = 8,26 (t, J = 5,4 Hz, 2H) , 7,61 (d, J = 13,8 Hz, 1H) , 7,43 (t, J = 9,6 Hz, 1H) , 7,33 (d, J = 9,6 Hz, 1H), 7,21 (s, 1H), 4,75 (m, 1H), 4,13 (t, J = 8,4 Hz, 1H) , 3,84 (s, 1H) , 3,74 (t, J = 8,4 Hz, 1H) , 3,56 (s, 2H) , 3,41 (t, J = 5,4 Hz, 2H) , 2,98 (s, 3H) , 1,83 (s, 3H). LCMS: 414 (M + H+) para CISHSQFNSOSS . Exemplo 19 Preparação do composto 19
Composto 2 (30 mg, 0,08 mmol), DIPEA (66 uL, 0,40 mmol) e metil isotiocianeto (6 uL, 0,24 mmol) foram sequencialmente adicionados a diclorometano (2 ml) a 0 °C e agitados por 12 horas. A solução foi concentrada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 19 (17 mg, 0,03 mmol, 38%) como um sólido branco. 1H RMN (600 MHz, clorofórmio-d4) Ô = 7,78 (s, 1H) , 7,58 (dd, J = 13,2, 2,4 Hz, 1H) , 7,21 (dd, J = 13,2, 2,4 Hz, 1H), 7,13 (t, J = 8,4, Hz, 1H), 6,86 (s, 1H), 5,96 (t, J = 6,0 Hz, 1H) , 4,80 (m, 1H) , 4,59 (t, J = 5,4 Hz, 2H) , 4,05 (t, J = 7,5 Hz, 1H), 3,81-3,77 (m, 3H), 3,71 (m, 1H), 3,65 (m, 1H), 3,20 (d, J = 4,8 Hz, 1H), 2,03 (s, 3H). LCMS: 409 (M + H+) para C17H21FN6O3S. Exemplo 20- Preparação do composto 20
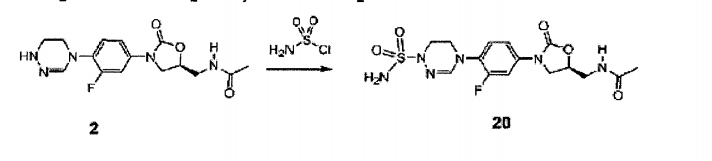
Composto 2 (50 mg, 0,13 mmol), trietilamina (55 uL, 0,39 mmol) e amidosulf onil cloreto (145 uL, 0,26 mmol) foram sequencialmente adicionados a diclorometano (3 ml) a 0 °C e agitados por 12 horas em temperatura ambiente. Depois da adição de diclorometano (30 ml) , a solução foi lavada duas vezes com solução de bicarbonato de sódio aquosa saturada, seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 20 (5 mg, 0,01 mmol, 10%) como um sólido branco. XH RMN (400 MHz, DMSO-d6) δ = 8,26 (t, J = 4,8 Hz, 1H) 7,60 (dd, J = 13,2, 2,4 Hz, 1H) , 7,42 (t, J = 8,8 Hz, 1H) , 7,32 (dd, J = 13,2, 2,4 Hz, 1H) , 7,12 (s, 1H) , 7,05 (s, 2H) , 4,74 (m, 1H) , 4,12 (t, J = 9,2 Hz, 1H) , 3,81 (t, J = 5,2 Hz, 2H) , 3,73 (dd, J = 9,2, 6,4 Hz, 1H) , 3,50-3,38 (m, 4H), 1,83 (s, 3H). LCMS: 414 (M + H+) para C15H19FN6O5S. Exemplo 21- Preparação do composto 21
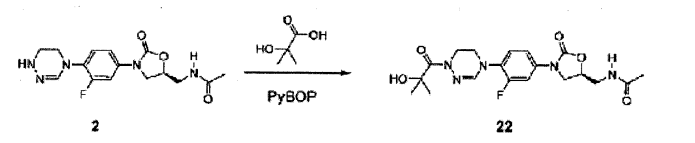
Composto 2 (50 mg, 0,13 mmol), trietilamina (36 uL, 0,26 mmol) e dimetilaminosulfonil cloreto (16 uL, 0,15 mmol) foram sequencialmente adicionados a DMF (1 ml) a 0 °C e agitados por 12 horas em temperatura ambiente. Depois da adição de diclorometano (30 ml), a solução foi lavada duas vezes com solução de bicarbonato de sódio aquosa saturada (10 ml) , seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 21 (6 mg, 0,01 mmol, 10%) como um sólido branco. RMN (400 MHz, DMSO-d6) δ = 7,62 (dd, J = 13,2, 2,4 Hz, 1H) , 7,19 (dd, J = 13,2, 2,0 Hz, 1H) , 7,12 (t, J = 8,8 Hz, 1H) , 6,94 (s, 1H) , 6,00 (t, J = 6,0 Hz, 1H) , 4,80 (m, 1H) , 4,05 (t, J = 8,8 Hz, 1H) , 3,85 (t, J = 4,4 Hz, 2H) , 3,79 (dd, J = 8,8, 6,8 Hz, 1H), 3,71-3,60 (m, 4H), 3,03 (s, 6H), 2,03 (s, 3H). LCMS: 443 (M + H+) para C17H23FN6O5. Exemplo 22- Preparação do composto 22
Composto 22 (36 mg, 0,085 mmol, 78%) foi obtido a partir do Composto 2 como no Exemplo 11. TH RMN (400 MHz, DMSO-d6) δ = 8,26 (t, J = 6,0 Hz, 1H) , 7,50 (d, J = 13,8 Hz, 1H) , 7,37 (t, J = 9,0 Hz, 1H) , 7,24 (d, J = 9,0 Hz, 1H), 5,86 (s, 1H) , 5,61 (m, 1H) , 4,72 (m, 1H) , 4,11 (m, 1H) , 3,72 (m, 1H) , 3,41-3,35 (tn, 2H) , 3,08 (m, 2H) , 2,86 (m, 2H) , 1,83 (s, 3H) , 1,31 (s, 3H) , 1,24 (s, 3H). LCMS: 422 (M + H+) para Cx^FNsOs. Exemplo 23- Preparação do composto 23
Composto 2 (30 mg, 0,08 mmol), PyBOP (105 mg, 0,20 mmol), Boc-Gly-OH (28 mg, 0,16 mmol) e DIPEA (40 uL, 0,24 mmol) foram sequencialmente adicionados a DMF (2 ml) 0 °C e agitados por 1,5 horas em temperatura ambiente. Depois da adição de diclorometano (30 ml), a solução foi lavada 3 vezes com água destilada (10 ml) , seca com sulfato de magnésio, concentrada sob pressão reduzida, separada por cromatografia em coluna, e agitada por 0,5 hora depois da adição de 4 N ácido clorídrico dissolvido em 1,4-dioxano (3 ml) . O produto foi concentrado sob pressão reduzida para obter Composto 23 (10 mg, 0,02 mmol, 29%). 1H RMN (400 MHz, DMSO-d6) δ = 8,29 (t, J = 6 Hz, 1H) , 8.10 (s, 3H), 7,62 (dd, J = 15,0, 2,4 Hz, 1H), 7,40 (t, J = 8,8 Hz, 1H), 7,34 (dd, J = 15,0, 2,4 Hz, 1H), 7,20 (s, 1H), 4,74 (m, 1H) , 4,13 (t, J = 8,8 Hz, 1H) , 3,99-3,94 (m, 3H) , 3,74 (t, J = 4,0 Hz, 2H) , 3,42 (t, J = 4,8 Hz, 2H) , 1,83 (s, 3H). LCMS: 393 (M + H+) para CI7H2IFN6O4 . Exemplo 24- Preparação do composto 24
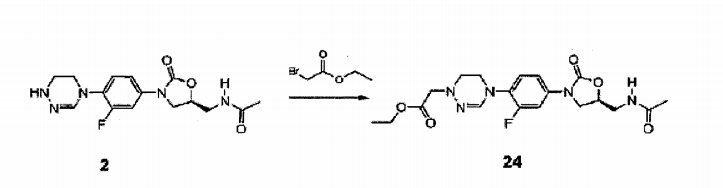
Composto 24 (200 mg, 0,48 mmol, 34%) foi obtido a partir do Composto 2 como no Exemplo 7, com o uso de bromoacetato de etila. 1H RMN (600 MHz, clorofórmio-di) δ 7,50 (dd, 1H, J, = 13,8 Hz, J2 = 2,4 Hz), 7,13 (dd, 1H, Jx = 9,0 Hz, J2 = 2,4 Hz), 7,10 (t, 1H, J = 8,4 Hz), 6,89 (s, 1H) , 6,70 (t, 1H, J = 6,0 Hz), 4,82-4,79 (m, 1H), 4,25-4,21 (m, 2H), 4,04 (t, 1H, J = 9,0 Hz), 3,84 (t, 2H, J = 4,2 Hz), 3,82-3,80 (m, 1H), 3,77 (s, 2H) , 3,66 (t, 2H, J = 4,2 Hz), 3,24 (t, 2H, J = 4,2 Hz), 2,02 (s, 3H). LCMS: 422 (M + H+) para CigH^FNgOg. Exemplo 25- Preparação do composto 25
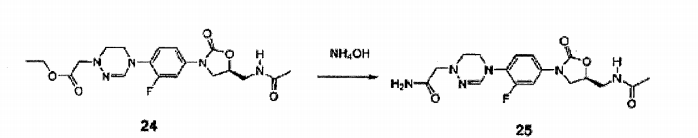
Composto 24 (100 mg, 0,24 mmol) foi dissolvido em metanol (2 mL) , agitado de um dia para o outro a 100 °C em um tubo selado depois da adição de água amoniacal (0,5 mL) , concentrado sob pressão reduzida, e separado por cromatografia em coluna para obter Composto 25 (20 mg, 0,051 mmol, 21%). XH RMN (400 MHz, DMSO-d6) δ 8,25 (t, 1H, J = 5,6 Hz), 7,56 (d, 1H, 14,0 Hz), 7,83-7,26 (m, 2H) , 7,21-7,08 (m, 2H) , 6,91 (S, 1H) , 4,75-4,71 (m, 1H) , 4,11 (t, 1H, J = 9,0 Hz), 3,82-3,69 (m, 3H) , 3,50-3,40 (m, 2H) , 3,31 (s, 2H) , 3,03 (t, 2H, J = 4,4 Hz), 1,83 (s, 3H). LCMS: 393 (M + H+) para C17H22FN6O4. Exemplo 26- Preparação do composto 26
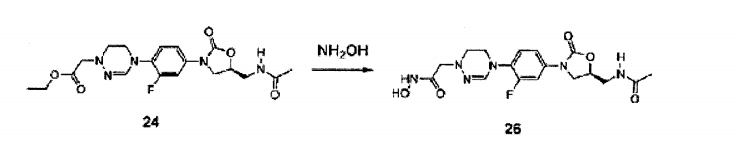
Composto 24 (100 mg, 0,24 mmol) foi dissolvido em metanol (20 mL) , agitado de um dia para o outro em temperatura ambiente depois da adição de solução de hidroxilamina (obtida por adição de 2,4 g de KOH a 2,4 g de NH2OH-HCI e então filtragem) dissolvida em metanol (20 mL), concentrado sob pressão reduzida, e separado por cromatografia em coluna para obter Composto 26 (22 mg, 0,054 mmol, 23%). 1H RMN (600 MHz, DMSO-d6) δ 8,30-8,20 (m, 1H) , 7,35- 7,25 (m, 1H) , 7,10-7,00 (m, 1H) , 6,87 (s, 1H) , 5,33-5,28 (m, 1H) , 4,71-7,64 (m, 1H) , 4,11 (t, 2H, J = 9,0 Hz), 4,04 (t, 2H, J = 8,4 Hz), 3,17 (s, 2H) , 2,91 (t, 2H, J = 6,6 Hz), 1,83 (s, 1H). LCMS: 4 09 (M + H+) para CI7H22FN6O5 . Exemplo 27- Preparação do composto 27
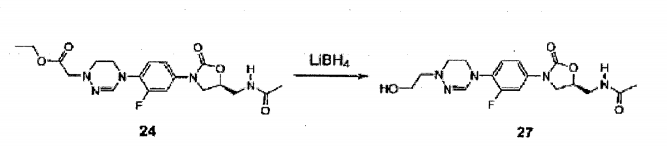
Composto 24 (110 mg, 0,26 mmol) foi dissolvido em THF (10 mL) e agitado por 3 horas em temperatura ambiente depois da adição de 2M de solução de LiBH4 (0,2 mL, 0,4 mmol) . Depois da adição de uma pequena quantidade de água, a solução foi separada por cromatografia em coluna para obter Composto 27 (24 mg, 0,063 mmol, 29%) como um sólido amarelo claro.
XH RMN (600 MHz, clorofórmio-dl) δ 7,54 (dd, 1H, J, = 13,8 Hz, J2 = 2,4 Hz), 7,16 (dd, 1H, J, = 9,0 Hz, J2 = 2,4 Hz), 7,12 (t, 1H, J = 8,4 Hz), 6,90 (s, 1H), 5,98 (t, 1H, J = 6,0 Hz), 4,87 (m, 1H), 4,05 (t, 1H, J = 9,0 Hz), 3,97 (m, 2H) , 3,85 (t, 2H, J = 4,2 Hz), 3,82-3,6 (m, 3H), 3,07 (t, 2H, J = 4,2 Hz), 3,00 (m, 2H), 2,04 (s, 3H). LCMS: 380 (M + H+) para CI7H22FNSO4 . Exemplo 28- Preparação do composto 28
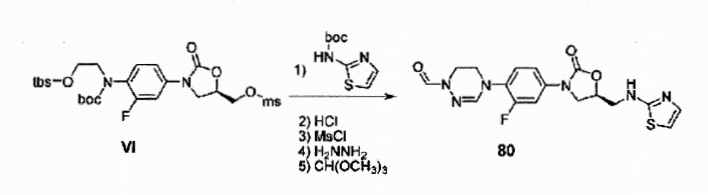
Composto XXVIII-a (0,22 g, 0,49 mmol) e hidrazina (monohidrato, 1 mL) foram dissolvidos em metanol (10 mL) , agitados por 2 horas sob refluxo, concentrados sob pressão reduzida, e agitados por 4 horas sob refluxo depois da adição de trimetil ortoformato (5 mL) e ácido acético (5 mL) . A solução foi concentrada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 28 (32 mg, 0,10 mmol, 20%) como um sólido branco.
XH RMN (400 MHz, DMSO-d6) δ = 8,25 (t, J = 6 Hz, 1H) , 7,60 (dd, J = 14,0, 2,4 Hz, 1H), 7,46 (s, 1H), 7,38 (t, J = 8,8 Hz, 1H) , 7,31 (dd, J = 9,2, 2,0 Hz, 1H) , 4,74 (m, 1H) , 4,12 (t, J = 9,2 Hz, 1H) , 4,04 (t, J = 3,6 Hz, 2H) , 3,75- 3,67 (m, 3H), 3,41 (t, J = 5,6 Hz, 2H), 1,83 (s, 3H). LCMS: 337 (M + H+) para C15H17FN4O4. Exemplo 29- Preparação do composto 29
Composto 2 (100 mg, 0,27 mmol) foi dissolvido em clorofórmio (3 mL) e agitado por 30 minutos depois da adição de solução saturada aquosa de NaHCO3 (3 mL) e então adição de tiofosgeno (0,021 mL) a 0 °C. A camada orgânica foi separada e água amoniacal (1 mL) foi adicionada. A solução foi diluída com THF (10 mL) e destilada sob pressão reduzida para remover a quantidade do solvente ao meio. Depois de adição adicional de água amoniacal (2 mL), a solução foi agitada de um dia para o outro em temperatura ambiente. A solução foi destilada sob pressão reduzida e triturada com éter etílico para obter Composto 29 (80 mg, 0,20 mmol, 74%) como um sólido branco.
XH RMN (600 MHz, DMSO-d6) δ 8,27 (t, 1H, J = 4,8 Hz), 7,98 (s, 1H) , 7,62 (dd, 1H, = 13,8 Hz, J2 = 2,4 Hz), 7,59-7,46 (m, 1H), 7,42 (t, 1H, J = 9,0 Hz), 7,34 (d, 1H, J = 9,0 Hz), 7,16 (s, 1H), 7,51-6,89 (bs, 2H), 4,79-4,69 (m, 1H) , 4,37 (t, 2H, J = 4,2 Hz), 4,13 (t, 1H, J = 9,6 Hz), 3,79-3,70 (m, 3H), 3,42 (t, 2H, J = 4,8 Hz), 3,38-3,29 (m, 1H), 1,83 (s, 3H). LCMS: 3 95 (M + H+) para CI6H19FNSO3S . Exemplo 30- Preparação
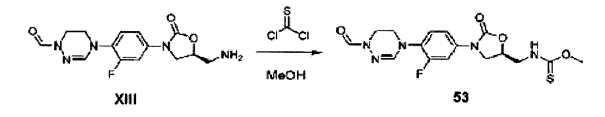
Composto 2 (100 clorofórmio (3 mL), agitado por 30 minutos depois da adição de solução saturada aquosa de NaHCO3 (3 mL) , e então adição de tiofosgeno (0,021 mL) a 0 °C. A camada orgânica foi separada, destilada sob pressão reduzida, e agitada de um dia para o outro em temperatura ambiente depois da adição de metanol (5 mL) . A solução foi destilada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 30 (31 mg, 0,20 mmol, 74%) como um sólido branco. TH RMN (600 MHz, DMSO-d6) δ 7,60 (dd, 1H, J, = 13,2 Hz, J2 = 1,2 Hz), 7,25-7,18 (m, 1H) , 7,16 (t, 1H, J = 8,4 Hz), 6,96 (s, 1H), 6,51 (bs, 1H), 4,86-4,79 (m, 1H), 4,64- 4,54 (m, 2H), 4,19 (s, 3H), 4,06 (t, 1H, J = 9,0 Hz), 3,88- 3,76 (m, 3H), 3,74-3,66 (m, 2H), 2,03 (s, 3H). LCMS: 410 (M + H+) para C17H20FN5O4S. Exemplo 31- Preparação do composto 31
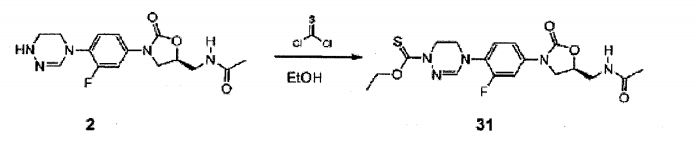
Composto 31 (26 mg, 0,061 mmol, 32%) foi obtido a partir do Composto 2 como no Exemplo 30, com o uso de etanol em vez de metanol. 1H RMN (600 MHz, DMSO-d6) δ 7,60 (d, J = 12,0 Hz), 7,24-7,18 (m, 1H), 7,15 (t, 1H, J = 8,4 Hz), 6,97 (s, 1H), 6,32 (bs, 1H), 4,88-4,76 (m, 1H), 4,75-4,64 (m, 2H), 4,64- 4,53 (m, 2H) , 4,06 (t, 1H, J = 8,4 Hz), 3,88-3,77 (m, 3H) , 3,74-3,60 (m, 2H), 2,03 (s, 3H), 1,46 (t, 3H, J = 6,6 Hz). LCMS: 424 (M + H+) para C18H22FN5O4S . Exemplo 32- Preparação do composto 32
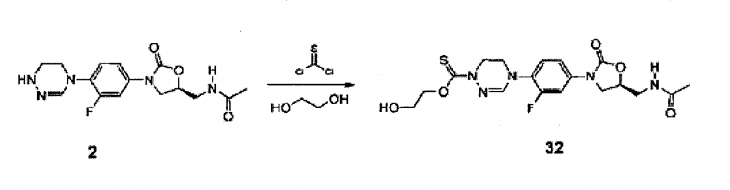
Composto 32 (23 mg, 0,052 mmol, 22%) foi obtido a partir do Composto 2 como no Exemplo 30, com o uso de etileno glicol em vez de metanol.
1H RMN (600 MHz, clorofórmio-dl) δ 7,62 (dd, 1H, Jx = 12,6 Hz, J2 = 1,8 Hz), 7,23-7,19 (m, 1H), 7,18 (t, 1H, 9,0 Hz), 7,06 (s, 1H) , 6,42 (t, 1H, J = 6,6 Hz), 4,96-4,86 (bs, 1H), 4,86-4,77 (m, 1H), 4,65 (t, 2H, J = 3,6 Hz), 4,59 (t, 2H, J = 4,8 Hz), 4,07 (t, 1H, 9,0 Hz), 3,98-3,89 (m, 2H), 3,88-3,79 (m, 3H), 3,72-3,65 (m, 2H), 2,03 (s, 3H). LCMS: 44 0 (M + H+) para C18H22FN5O5S.
Exemplo 33- Preparação do composto 33
Composto 33 (16 mg, 0,036 mmol, 35%) foi obtido a partir do Composto 2 como no Exemplo 30, com o uso de aminoetanol em vez de metanol.
XH RMN (600 MHz, DMSO-d6) δ 8,28 (t, 1H, J = 5,4 Hz), 7,67-7,58 (m, 1H), 7,43 (t, 1H, J = 9,0 Hz), 7,38-7,31 (m, 1H) , 7,20 (s, 1H) , 4,08 (t, 1H, J = 5,4 Hz), 4,78-4,70 (m, 1H) , 4,39 (t, 2H, J = 4,8 Hz), 4,13 (t, 1H, J = 9,0 Hz), 3,81-3,75 (m, 2H), 3,58 (t, 2H, J = 4,2 Hz), 3,53 (t, 2H, J = 5,7 Hz), 3,42 (t, 2H, J = 5,4 Hz), 1,83 (s, 3H). LCMS: 439 (M + H+) para CI8H23FN6O4S .
Exemplo 24- Preparação do composto 34
Composto 2 (50 mg, 0,13 mmol) foi dissolvido em etanol (5 mL) e agitado de um dia para o outro em temperatura ambiente depois da adição de DIPEA (0,03 mL, 0,2 mmol), NaF (7 mg, 0,17 mmol) e etil ditioacetato (0,019 mL, 0,16 mmol) . A solução foi destilada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 34 (10 mg, 0,025 mmol, 19%) como um sólido branco.
XH RMN (600 MHz, CDC13) δ = 7,62 (dd, Ji = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,25-7,21 (m, 2H), 7,16 (t, J = 8,4 Hz, 1H), 6,94 (s, 1H), 5,93 (br, t, 1H), 4,81 (m, 1H), 4,73 (t, J = 5,2 Hz, 2H), 4,06 (t, J = 8,8 Hz, 1H), 3,83-3,62 (m, 5H), 2,81 (s, 3H), 2,03 (s, 3H). LCMS: 3 94 (M + H+) para CI7H2OFN503S . Exemplo 35- Preparação do composto 35
Composto 35 (35 mg, 0,086 mmol, 65%) foi obtido a partir do Composto 2 como no Exemplo 6, com o uso de carbonildiimidazol e etanol.
XH RMN (600 MHz, CDC13) δ = 7,58-7,56 (m, 1H) , 7,19- 7,18 (m, 1H) , 7,13-7,10 (m, 1H ), 6,92 (s, 1H) , 6,21 (m, 1H) , 4,80 (m, 1H) , 4,33-4,32 (m, 2H) , 4,06-4,03 (m, 1H) , 3,99 (m, 2H) , 3,81-3,77 (m, 3H) , 3,71-3,66 (m, 2H) , 2,03 (s, 3H), 1,38 (t, J = 6,3 Hz, 3H). LCMS: 4 07 (M + H+) para C18H22FN5O5.
Exemplo 36- Preparação do composto 36
Composto 36 mg, 0,034 mmol, 74%) foi obtido a partir do Composto 2 como no Exemplo 11, com o uso de ácido pirúvico.
RMN (600 MHz, DMSO-d6) δ 8,27 (t, J = 6,0 Hz, 1H) 7,61 (dd, J, = 13,2 Hz, J2 = 3,0 Hz, 1H) , 7,40 (t, J = 9,0 Hz, 1H) , 7,33 (dd, Jx = 9,0 Hz, J2 = 2,4 Hz, 1H) , 7,18 (s, 1H), 4,74 (m, 1H), 4,13 (t, J = 9 Hz, 1H), 3,90 (t, J = 4,8 Hz, 2H) , 3,77-3,72 (m, 3H) , 3,42-3,30 (m, 2H) , 2,33 (s, 3H), 1,83 (s, 3H). LCMS: 4 06 (M + H+) para Ci8H20FN5O5. Exemplo 37- Preparação do composto 37
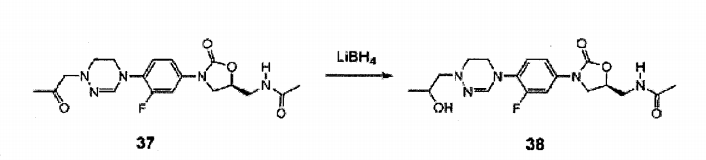
Composto 37 (13 mg, 0,033 mmol, 65%) foi obtido a partir do Composto 2 como no Exemplo 4, com o uso de cloroacetona.
XH RMN (600 MHz, CDC13) δ = 7,52 (dd, Jx = 13,8 Hz, J2 = 2,4 Hz, 1H) , 7,15 (dd, Jx = 8,4 Hz, J2 = 2,4 Hz, 1H) , 7,11 (t, J = 8,4 Hz, 1H) , 6,89 (s, 1H) , 6,09 (br, t, 1H) , 4,79 (m, 1H), 4,04 (t, J = 9 Hz, 1H), 3,85 (t, J = 4,8 Hz, 2H) , 3,79-3,62 (m, 5H), 3,12 (t, J = 4,8 Hz, 2H) , 2,26 (s, 3H), 2,03 (s, 3H). LCMS: 3 92 (M + H+) para CI8H22FN5O4 .
Exemplo 38- Preparação do composto 38
Composto 37 (7 mg, 0,018 mmol) foi dissolvido em diclorometano (2 mL) e agitado por 2 horas em temperatura ambiente depois da adição de 2M de solução de LiBH4. Depois da adição de uma pequena quantidade de água, a solução foi separada por cromatografia em coluna para obter Composto 38 (3,6 mg, 0,009 mmol, 50%) como um sólido branco.
XH RMN (600 MHz, CDC13) δ = 7,54 (dd, Jx = 13,8 Hz, J2 = 2,4 Hz, 1H) , 7,15 (dd, J, = 8,4 Hz, J2 = 2,4 Hz, 1H) , 7,11 (t, J = 8,4 Hz, 1H) , 6,89 (s, 1H) , 6,09 (br, t, 1H) , 4,79 (m, 1H), 4,04 (t, J = 9 Hz, 1H), 3,85 (t, J = 4,8 Hz, 2H) , 3,79-3,62 (m, 5H) , 3,12 (t, J = 4,8 Hz, 2H) , 2,26 (s, 3H), 2,03 (s, 3H). LCMS: 3 94 (M + H+) para CI8H24FN5O4 .
Exemplo 39- Preparação do composto 39
Composto 39 (15 mg, 0,039 mmol, 74%) foi obtido a partir do Composto 2 como no Exemplo 4, com o uso de 3- cloro-2-metilpropeno.
XH RMN (600 MHz, CDC13) δ = 7,51 (dd, Jx = 13 Hz, J2 = 2,4 Hz, 1H) , 7,15-7,09 (m, 2H) , 6,91 (s, 1H) , 6,06 (br, t, 1H) , 4,97 (s, 1H) , 4,93 (s, 1H) , 4,79 (m, 1H) , 4,04 (t, J = 9 Hz, 1H) , 3,81 (t, J = 4,8 Hz, 2H) , 3,78-3,61 (m, 3H) , 3,48 (s, 2H) , 2,94 (t, J = 4,8 Hz, 2H) , 2,03 (s, 3H) , 1,83 (s, 3H). LCMS: 3 90 (M + H+) para CI9H24FN5O3 .
Exemplo 40- Preparação do composto 40
Composto 40 (11 mg, 0,027 mmol, 34%) foi obtido a partir do Composto 2 como no Exemplo 4, com o uso de 2,3- dicloro-l-propeno.
TH RMN (600 MHz, CDC13) δ = 7,52 (dd, Jx = 13 Hz, J2 = 2,4 Hz, 1H), 7,15-7,09 (m, 2H), 6,91 (s, 1H), 6,23 (br, t, 1H) , 5,49 (s, 1H) , 5,42 (s, 1H) , 4,79 (m, 1H) , 4,04 (t, J = 9 Hz, 1H) , 3,85 (t, J = 4,8 Hz, 2H) , 3,79-3,62 (m, 5H) , 3,08 (t, J = 4,8 Hz, 2H), 2,03 (s, 3H). LCMS: 410 (M + H+) para CI8H2IC1FN5O3 .
Exemplo 41- Preparação do composto 41
Composto 2 (228 mg, 0,68 mmol), ciclobutanona (0,076 mL, 1,02 mmol) e NaBH(OAc)3 (187 mg, 0,88 mmol) foram dissolvidos em diclorometano (20 mL) e agitados por 2 horas em temperatura ambiente depois da adição de ácido acético (1 mL) . A solução foi diluída com diclorometano, sequencialmente lavada com solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, e concentrada sob pressão reduzida para obter Composto 41 (200 mg, 0,51 mmol, 75%) como um sólido branco.
RMN (600 MHz, CDC13) δ = 7,51 (dd, Ji = 13 Hz, J2 = 5 2,4 Hz, 1H), 7,15-7,09 (m, 2H), 6,95 (s, 1H), 6,09 (br, t, 1H) , 4,79 (m, 1H) , 4,03 (t, J = 9 Hz, 1H) , 3,82 (t, J = 4,8 Hz, 2H) , 3,78-3,61 (m, 3H) , 3,41 (m, 1H) , 2,91 (t, J = 4,8 Hz, 2H) , 2,21-2,11 (m, 4H) , 2,03 (s, 3H) , 1,81-1,72 (m, 2H) . 10 LCMS: 390 (M + H+) para C19H24FN5O3.
Exemplo 42- Preparação do composto 42
Composto 42 (15 mg, 0,039 mmol, 79%) foi obtido a partir do Composto XIII como no Exemplo 11.
TH RMN (400 MHz, DMSO-d6) δ = 8,64 (t, J = 5,6 Hz, 1H) , 8,42 (s, 1H) , 7,61 (dd, J∑ = 14 Hz, J2 = 2,0 Hz, 1H) , 20 7,38 (t, J = 8,8 Hz, 1H) , 7,33 (dd, Ji = 8,8 Hz, J2 = 2,0 Hz, 1H) , 7,12 (s, 1H) , 4,78 (m, 1H) , 4,14 (t, J = 9,2 Hz, 1H) , 3,84 (t, J = 4,8 Hz, 2H) , 3,75-3,47 (m, 7H) . LCMS: 389 (M + H+) para C17H17FN6O4.
Exemplo 43- Preparação do composto 43
Composto XIII (190 mg, 0,6 mmol) e carbonildiimidazol 30 (143 mg, 0,9 mmol) foram dissolvidos em diclorometano (5 mL) e agitados por 6 horas em temperatura ambiente depois da adição de trietilamina (0,25 mL, 1,8 mmol). Depois, 1/3 da solução foi destilada sob pressão reduzida, dissolvida em diclorometano (5 mL) e etanol (10 mL), e agitada por 36 horas em temperatura ambiente. A solução foi lavada com água destilada, seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 43 (23 mg, 0,058 mmol, 29%).
1H RMN (600 MHz, DMSO-d6) δ = 8,38 (s, 1H) , 7,56 (dd, Ji = 14 Hz, J2 = 2,0 Hz, 1H) , 7,45 (br, t, 1H) , 7,35-7,28 (m, 2H) , 7,01 (s, 1H) , 4,69 (m, 1H) , 4,10 (t, J = 9,2 Hz, 1H), 3,95 (q, J = 6,6 Hz, 2H), 3,80-3,3 (m, 7H), 1,09 (t, J = 6,6 Hz, 3H) . LCMS: 394 (M + H+) para C17H2oFN505.
Exemplo 44- Preparação do composto 44
Composto XIII (190 mg, 0,6 mmol) e carbonildiimidazol (143 mg, 0,9 mmol) foram dissolvidos em diclorometano (5 mL) e agitados por 6 horas em temperatura ambiente depois da adição de trietilamina (0,25 mL, 1,8 mmol). Depois, 1/3 da solução foi destilada sob pressão reduzida, dissolvida em THF (5 mL) e etilamina (50 mg), agitada por 36 horas em temperatura ambiente, e refluída por 2 horas. A solução foi lavada com água destilada, seca com sulfato de magnésio, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 44 (35 mg, 0,089 mmol, 45%).
XH RMN (600 MHz, CDC13) δ = 8,53 (s, 1H) , 7,59 (d, J = 13 Hz, 1H), 7,19 (d, J = 9 Hz, 1H), 7,13 (d, J = 9 Hz, 1H), 6,88 (s, 1H) , 5,75 (br, s, 1H) , 5,28 (br, s, 1H) , 4,81 (m, 1H), 4,04 (t, J = 8,2 Hz, 1H), 3,98-3,15 (m, 9H), 1,08 (t, J = 6,6 Hz, 3H). LCMS: 393 (M + H+) para CI7H21FN6O4 .
Exemplo 45- Preparação do composto 45
Composto 45 (840 mg, 2,1 mmol, 95%) foi obtido a partir do Composto XIII como no Exemplo 11, com o uso de ácido difluoracético.
1H RMN (400 MHz, DMSO-d6) δ = 9,18 (t, J = 5,6 Hz, 1H) , 8,42 (s, 1H) , 7,61 (dd, J = 14 Hz, J2 = 2,0 Hz, 1H) , 7,38 (t, J = 8,8 Hz, 1H) , 7,32 (dd, Jx = 8,8 Hz, J2 = 2,0 Hz, 1H) , 7,12 (s, 1H) , 6,26 (t, J = 53 Hz, 1H) 4,82 (m, 1H) , 4,16 (t, J = 8,8 Hz, 1H) , 3,84 (t, J = 4,8 Hz, 2H) , 3,80-3,53 (m, 5H). LCMS: 400 (M + H+) para C16H16F3N5O4.
Exemplo 46- Preparação do composto 46
Composto 46 (750 mg, 1,8 mmol, 84%) foi obtido a partir do Composto 45 como no Exemplo 2.
1H RMN (600 MHz, DMSO-d6) δ 9,17-9,30 (m, 1H) , 8,43- 8,28 (m, 1H) , 7,67 9dd, 1H, Jx = 13,8 Hz, J2 = 2,4 Hz), 7,61 (t, 1H, J = 9,0 Hz), 7,44-7,36 (m, 1H) , 6,27 (9t, 1H, J = 53,4 Hz), 4,85-4,80 (m, 1H), 4,19 (t, 1H, J = 9,0 Hz), 3,81-3,75 (m, 2H), 3,38-3,32 (m, 2H). LCMS: 3 72 (M + H+) para CisHi^NsCU.
Exemplo 47- Preparação do composto 47
Composto 47 (16 mg, 0,037 mmol, 25%) foi obtido a partir do Composto 46 como no Exemplo 12.
TH RMN (600 MHz, clorofórmio-dl) δ 7,57 (dd, 1H, J, = 13,8 Hz, J2 = 2,4 Hz), 7,21 (dd, 1H, J, = 9,0 Hz, J2 = 2,4 Hz), 7,13 (t, 1H, J = 9,0 Hz), 6,96-6,90 (m, 1H), 6,86 (s, 1H) , 5,94 (t, 1H, J = 54,0 Hz), 4,88-4,83 (m, 1H) , 4,12 (t, 1H, J = 9,0 Hz), 4,06 (t, 2H, J = 5,4 Hz), 3,90-3,81 (m, 1H), 3,80-3,74 (m, 3H), 3,74-3,66 (m, 1H), 3,64 (s, 2H). LCMS: 43 0 (M + H+) para C17H18F_3.N5O5.
Exemplo 48- Preparação do composto 48
Composto 48 (16 mg, 0,04 mmol, 61%) foi obtido a partir do Composto 46 como no Exemplo 6.
1H RMN (600 MHz, clorofórmio-dl) Ô 7,48 (dd, 1H, J, = 13,2 Hz, J2 = 2,4 Hz), 7,23 (t, 1H, J = 5,4 Hz), 7,16-7,08 (m, 2H), 6,94 (s, 1H), 5,94 (t, 1H, J = 54,0 Hz), 4,86-4,82 (m, 1H), 4,10 (t, 1H, J = 9,0 Hz), 3,88-3,84 (m, 1H), 3,83 (t, 2H, J = 4,8 Hz), 3,78-3,73 (m, 1H) , 3,73-3,64 (m, 1H) , 3,02 (t, 2H, J = 4,8 Hz), 3,00-2,94 (m, 3H), 1,23 (t, 2H, LCMS: 4 00 (M + H+) para CI7H20F-3.N5O3 .
Exemplo 49- Preparação do composto 49
Composto 49 (15 mg, 0,037 mmol, 57%) foi obtido a partir do Composto 46 como no Exemplo 5. RMN (600 MHz, CDC13) δ 7,51 (dd, J, = 13,8 Hz, J2 = 2,4 Hz, 1H) , 7,16-7,11 (m, 2H) , 6,96 (s, 1H) , 6,89 (br, t, 1H) , 5,94 (t, J = 54,0 Hz, 1H) , 4,84 (m, 1H) , 4,11 (t, J = 9,0 Hz, 1H) , 3,89-3,64 (m, 7H) , 3,13 (t, J = 4,8 Hz, 2H) , 2,31 (t, J = 2,4 Hz, 1H) . LCMS: 410 (M + H+) para CI8HI8F.3.N5O3 .
Exemplo 50- Preparação do composto 50
Composto 50 (15 mg, 0,037 mmol, 68%) foi obtido a partir do Composto 46 como no Exemplo 7.
XH RMN (600 MHz, CDC13) δ 7,53 (dd, J3 = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,17-7,13 (m, 2H), 7,01 (br, t, 1H), 6,96 (s, 1H), 5,94 (t, J = 54,0 Hz, 1H), 4,85 (m, 1H), 4,11 (t, J = 9,0 Hz, 1H), 3,98 (s, 2H) 3,89-3,66 (m, 5H), 3,15 (t, J = 4,8 Hz, 2H). LCMS: 411 (M + H+) para C17Hi7F_3_N6O3 .
Exemplo 51- Preparação do composto 51
Composto 51 (155 mg, 0,36 mmol, 86%) foi obtido a partir do Composto XIII como no Exemplo 11, com o uso de ácido dicloroacético.
RMN (400 MHz, DMSO-d6) δ = 8,99 (t, J = 6,0 Hz, 1H) , 8,42 (S, 1H) , 7,61 (d, J = 12 Hz, 1H) , 7,38 (t, J = 9,0 Hz, 1H), 7,31 (d, J = 9Hz, 1H), 7,12 (s, 1H), 6,49 (s, 1H) , 4,81 (m, 1H) , 4,16 (t, J = 8,8 Hz, 1H) , 3,84 (t, J = 4,8 Hz, 2H), 3,74-3,66 (m, 3H), 3,55 (t, J = 5,2 Hz, 2H). LCMS: 432 (M + H+) para C16H16Cl-2-FN5O4. Exemplo 52- Preparação do composto 52
Composto 52 (250 mg, 0,6 mmol, 92%) foi obtido a partir do Composto XIII como no Exemplo 11, com o uso de isoxazol ácido.
TH RMN (400 MHz, DMSO-d6) δ = 9,32 (t, J = 5,6 Hz, 1H) , 8.75 (d, J = 1,2 Hz, 1H) 8,42 (s, 1H) , 7,60 (dd, Jx = 14 Hz, J2 = 2,0 Hz, 1H) , 7,38 (t, J = 8,8 Hz, 1H) , 7,33 (dd, = 8,8 Hz, J2 = 2,0 Hz, 1H) , 7,11 (d, J = 1,2 Hz, 1H) , 4,88 (m, 1H) , 4,18 (t, J = 9,2 Hz, 1H), 3,88-3,82 (m, 3H) , 3,69 (t, J = 5,2 Hz, 2H), 3,64 (t, J = 5,6 Hz, 2H). LCMS: 417 (M + H+) para Ci8Hi7-FN6O5. Exemplo 53- Preparação do composto 53
Composto XIII (4,5 g, 14 mmol) foi dissolvido em diclorometano (75 mL) e agitado por 1 hora depois da adição de solução saturada aquosa de NaHCO3 (75 mL) e tio-fosgeno (1,1 mL, 14 mmol) a 0 °C. A camada orgânica foi seca com sulfato de sódio, destilada sob pressão reduzida, dissolvida em metanol (120 mL) , agitada de um dia para o outro sob refluxo, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 53 (3,18 g, 8,05 mmol, 58%) como um sólido branco.
1H RMN (600 MHz, CDC13) δ = 8,55 (s, 1H) , 7,58 (dd, Jx = 13 Hz, J2 = 2,4 Hz, 1H) , 7,21 (dd, Jx = 9,0 Hz, J2 = 2,7 Hz, 1H), 7,13 (t, J = 8,4 Hz, 1H), 6,89 (s, 1H), 6,71 (t, J = 6,3 Hz, 1H) , 4,93 (m, 1H) , 4,13-4,08 (m, 2H) , 4,05 (m, 1H), 4,01 (s, 3H), 3,99 (t, J = 5,0 Hz, 2H), 3,90 (m, 1H), 3,74 (t, J = 5,0 HZ, 2H) . LCMS: 3 96 (M + H+) para CI6HI8FN5O4S .
Exemplo 54- Preparação do composto 54
Composto 54 (210 mg, 0,51 mmol, 65%) foi obtido a partir do Composto XIII como no Exemplo 53, com o uso de etanol em vez de metanol.
TH RMN (600 MHz, CDC13) δ = 8,54 (s, 1H) , 7,58 (dd, Jx = 14 Hz, J2 = 2,8 Hz, 1H) , 7,21 (dd, Jx = 14 Hz, J2 = 3,8 Hz, 1H), 7,13 (t, J = 8,4 Hz, 1H), 6,88 (s, 1H), 6,75 (t, J = 6,3 Hz, 1H), 4,96 (m, 1H), 4,54-4,44 (m, 2H), 4,09-4,02 (m, 3H), 3,98 (t, J = 4,8 Hz, 2H), 3,92 (m, 1H), 3,73 (t, J = 4,8 Hz, 2H), 1,31 (t, J = 7 Hz, 3H). LCMS: 410 (M + H+) para CI7H2OFN504S .
Exemplo 55- Preparação do composto 55
Composto 55 (52 mg, 0,12 mmol, 52%) foi obtido a partir do Composto XIII como no Exemplo 53, com o uso de isopropanol em vez de metanol.
RMN (600 MHz, CDC13) δ = 8,55 <S, 1H) , 7,58 (dd, J/ = 13 Hz, J2 = 2,4 Hz, 1H) , 7,22 (dd, Jx = 9,0 Hz, J2 = 2,7 Hz, 1H), 7,13 (t, J = 8,4 Hz, 1H), 6,88 (s, 1H), 6,57 (t, J = 6,3 Hz, 1H) , 5,54 (m, 1H) , 4,93 (m, 1H) , 4,12-4,06 (m, 2H), 4,02 (m, 1H), 3,99 (t, J = 4,8 Hz, 2H), 3,92 (m, 1H), 3,73 (t, J = 4,8 Hz, 2H) , 1,32 (d, J = 6 Hz, 3H) , 1,27 (d, J = 6 Hz, 3H). LCMS: 424 (M + H+) para CI8H22FN5O4S .
Exemplo 56- Preparação do composto 56
Composto 56 (36 mg, 0,088 mmol, 57%) foi obtido a partir do Composto XIII como no Exemplo 53, com o uso de etilamina em vez de metanol.
TH RMN (600 MHz, CDC13) δ = 8,54 (s, 1H) , 7,58 (dd, 1H, Ji = 13,2 Hz, J2=2,4 HZ), 7,20-7,19 (m, 1H) , 7,13 (t, 1H, J = 9,0 Hz), 6,88 (s, 1H), 4,92-4,96 (m, 1H), 4,10-4,06 (m, 3H), 3,99 (t, 2H, J = 4,8 Hz), 1,44-1,43 (m, 2H), 1,21 (t, 3H, J = 7,2 Hz). LCMS: 409 (M + H+) para CI7H21FN6O3S .
Exemplo 57- Preparação do composto 57
Composto XXVII-b preparado no Exemplo de Preparação 14 foi submetido a reação de Mitsunobu como no Exemplo 16. Então, o composto 57 (84 mg, 0,23 mmol, 31%) foi obtido como no Exemplo 28.
1H RMN (600 MHz, CDC13) δ = 8,25 (s, 1H) , 7,62 (dd, Jx = 13 Hz, J2 = 2,0 Hz, 1H) , 7,30 (t, J = 9 Hz, 1H) , 7,24 (dd, Jx = 9 Hz, J2 = 2,0 Hz, 1H), 6,73 (br, t, 1H), 4,94 (m, 1H) , 4,21-4,04 (m, 4H) , 4,01 (s, 3H) , 3,90 (t, J = 4,8 Hz, 2H) , 3,80 (t, J = 4,8 Hz, 2H) . LCMS: 369 (M + H+) para CI5HI7FN4O4S .
Exemplo 58- Preparação do composto 58 metanol (20 mL) , agitado por 2 horas sob balão de hidrogênio depois da adição de 4N de solução de HC1 dioxano (2 mL) e 10% Pd/C (50 mg), filtrado com celite, e destilado sob pressão reduzida para obter quantitativamente Composto 58 como um sólido branco.
1H RMN (600 MHz, CDC13) δ = 7,51 (dd, Jx = 14 Hz, J2 = 1,8 Hz, 1H) , 7,16-7,10 (m, 2H) , 6,89 (s, 1H) , 6,78 (br, t, 1H) , 4,93 (m, 1H) , 4,10-3,98 (m, 6H) , 3,88-3,81 (m, 3H) , 3,32 (t, J = 4,8 Hz, 2H). LCMS: 3 68 (M + H+) para CX5H18FN5O3S.
Exemplo 59- Preparação do composto 59
Composto 58 (150 mg, 0,41 mmol) foi dissolvido em diclorometano (5 mL), agitado em temperatura ambiente por 6 horas depois da adição de DIPEA (0,14 mL, 0,82 mmol) e acetoxiacetil cloreto (0,066 mL, 0,61 mmol) a 0 °C. A solução foi destilada sob pressão reduzida e separada por cromatografia em coluna para obter Composto 59 (31 mg, 0,066 mmol, 16%) como um sólido branco.
TH RMN (600 MHz, CDC13) δ 7,58 (dd, J, = 13,8 Hz, J2 = 2,4 Hz, 1H) , 7,22-7,11 (m, 2H) , 6,83 (s, 1H), 6,69 (t, J = 6,0 Hz, 1H) , 5,08 (s, 2H), 4,96 (m, 1H) , 4,10-3,89 (m, 9H) , 3,74 (t, J = 4,8 Hz, 2H), 2,20 (s, 3H). LCMS: 468 (M + H+) para C19H22FN5OeS.
Exemplo 60- Preparação do composto 60
Composto 58 (0,013 mg, 0,035 mmol) foi dissolvido em DMF (2 mL) , agitado de um dia para o outro em temperatura ambiente depois da adição de DIPEA (0,01 mL, 0,07 mmol) e iodometano (0,003 mL, 0,035 mmol), e separado por cromatografia em coluna para obter Composto 60 (3,1 mg, 0,0081 mmol, 23%) como um sólido branco.
TH RMN (600 MHz, CDC13) δ = 7,52 (dd, J3 = 14 Hz, J2 = 2,0 Hz, 1H) , 7,15 (dd, J3 = 9 Hz, J2 = 2,0 Hz, 1H) , 7,11 (t, J = 9 Hz, 1H), 6,90 (s, 1H), 6,76 (br, t, 1H), 4,94 (m, 1H), 4,10-3,85 (m, 7H), 3,82 (t, Ji = 4,8 Hz, 2H), 2,99 (t, Jx = 4,8 Hz, 2H), 2,79 (s, 3H). LCMS: 382 (M + H+) para C16H2oFN5θ3S.
Exemplo 61- Preparação do composto 61
Composto 61 (15 mg, 0,038 mmol, 45%) foi obtido a partir do Composto 58 como no Exemplo 60, com o uso de iodoetano em vez de iodometano.
XH RMN (600 MHz, CDC13) δ = 7,51 (dd, Jx = 14 Hz, J2 = 1,8 Hz, 1H), 7,15 (dd, Jx = 8,4 Hz, J2 = 2,4 Hz, 1H), 7,11 (m, 1H) , 6,92 (s, 1H) , 6,77 (br, t, 1H) , 4,93 (m, 1H) , 4,11-4,02 (m, 3H) , 4,01 (s, 3H) , 3,88-3,85 (m, 1H) , 3,83 (t, J = 4,8 Hz, 2H) , 3,02 (t, J = 4,8 Hz, 2H) , 2,98-2,94 (m, 2H), 1,24 (t, J = 7,2 Hz, 3H). LCMS: 3 96 (M + H+) para CI7H22FNSO3S .
Exemplo 62- Preparação do composto 62
Composto 62 (15 mg, 0,037 mmol, 67%) foi obtido a partir do Composto 58 como no Exemplo 60, com o uso de alil brometo em vez de iodometano.
XH RMN (600 MHz, clorofórmio-dl) δ 7,51 (dd, 1H, Jx = 13,2 Hz, J2 = 1,8 Hz), 7,15 (dd, 1H, Jx = 9,0 Hz, J2 = 2,4 Hz), 7,11 (t, 1H, 8,4 Hz), 6,92 (s, 1H) , 6,68 (t, 1H, J = 6,0 Hz), 6,08-5,96 (m, 1H) , 5,29 (dd, 1H, Jx = 10,2 Hz, J2 = 1,8 Hz), 5,24 (dd, 1H, Ji = 10,2 Hz, J2 = 1,8 Hz), 4,98- 4,88 (m, 1H) , 4,12-4,04 (m, 2H) , 4,02-3,98 (m, 1H) , 4,01 (s, 3H), 3,86 (dd, 1H, Jx = 9,6 Hz, J2 = 7,2 Hz), 3,82 (t, 2H, J = 4,2 Hz), 3,58 (d, 2H, J = 6,0 Hz), 3,00 (t, 2H, J = 4,8 Hz). LCMS: 4 08 (M + H+) para C18H22FN5O3S.
Exemplo 63- Preparação do composto 63
partir do Composto 58 como no Exemplo 60, com o uso de propargil brometo em vez de iodometano. XH RMN (600 MHz, clorofórmio-dl) δ 7,53 (dd, 1H, J, = 13,8 Hz, J2 = 2,4 Hz), 7,16 (dd, 1H, Jx = 9,0 Hz, J2 = 2,4 Hz), 7,13 (t, 1H, 8,4 Hz), 6,96 (s, 1H) , 6,69 (t, 1H, J = 6,0 Hz), 4,98-4,90 (m, 1H) , 4,14-3,98 (m, 3H) , 4,01 (s, 3H) , 3,90-3,82 (m, 1H) , 3,85 (t, 2H, J = 6,6 Hz), 3,83 (d, 2H, J = 2,4 Hz), 3,13 (t, 2H, J = 5,4 Hz), 2,31 (t, 1H, J = 2,4 Hz). LCMS: 406 (M + H+) para Cx8H20FN5O3S.
Exemplo 64- Preparação do composto 64
TH RMN (600 MHz, CDC13) δ 7,52 (dd, J, = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,16 (dd, J, = 9,0 Hz, J2 = 2,4 Hz, 1H), 7,12 (t, 8,4 Hz, 1H) , 6,95 (s, 1H) , 6,70 (t, J = 6,0 Hz, 1H) , 4,94 (m, 1H), 4,13-3,75 (m, 11H), 3,12 (t, J = 5,4 Hz, 2H), 1,87 (t, J = 2,4 Hz, 3H). LCMS: 420 (M + H+) para C19H22FN5O3S.
Exemplo 65- Preparação do composto 65
Composto 65 (22 mg, 0,054 mmol, 64%) foi obtido a partir do Composto 58 como no Exemplo 60, com o uso de bromoacetonitrila em vez de iodometano. TH RMN (600 MHz, CDC13) δ 7,56 (dd, Jx = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,17 (dd, Ji = 9,0 Hz, J2 = 2,4 Hz, 1H), 7,14 (t, 8,4 Hz, 1H) , 6,96 (s, 1H) , 6,68 (t, J = 6,0 Hz, 1H) , 4,95 (m, 1H), 4,12-3,86 (m, 11H), 3,15 (t, J = 5,4 Hz, 2H). LCMS : 407 (M + H+) para CI7H19FNSÒ3S .
Exemplo 66- Preparação do composto 66
Composto 66 (15 mg, 0,034 mmol, 54%) foi obtido a partir do Composto 58 como no Exemplo 60, com o uso de 2,3- dicloropropeno em vez de iodometano. XH RMN (600 MHz, CDC13) δ 7,52 (dd, J, = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,16 (dd, Ji = 9,0 Hz, J2 = 2,4 Hz, 1H), 7,11 (t, 8,4 Hz, 1H) , 6,92 (s, 1H) , 6,73 (t, J = 6,0 Hz, 1H) , 5,49 (s, 1H) , 5,42 (s, 1H) , 4,94 (m, 1H) , 4,12-3,84 (m, 9H), 3,72 (s, 2H), 3,08 (t, J = 5,4 Hz, 2H). LCMS: 442 (M + H+) para C18H21C1FN5O3S.
Exemplo 67 - Preparação do composto 67
Composto 67 (18 mg, 0,043 mmol, 84%) foi obtido a partir do Composto 58 como no Exemplo 41, com o uso de ciclopropanocarboxaldeído.
1H RMN (600 MHz, CDC13) δ 7,51 (dd, Ji = 13,8 Hz, J2 = 2,4 Hz, 1H) , 7,18 (dd, Ji = 9,0 Hz, J2 = 2,4 Hz, 1H) , 7,11 (t, 8,4 Hz, 1H) , 7,01 (t, J = 6,0 Hz, 1H) , 6,91 (s, 1H) , 4,95 (m, 1H) , 4,12-3,83 (m, 9H) , 3,13 (t, J = 4,8 Hz, 2H), 2,82 (d, J = 7,2 Hz, 2H) , 1,08 (m, 1H) , 0,57 (m, 2H) , 0,21 (m, 2H) . LCMS: 422 (M + H+) para Ci9H24FN5O3S.
Exemplo 68- Preparação do composto 68
Composto 68 (19 mg, 0,045 mmol, 76%) foi obtido a partir do Composto 58 como no Exemplo 41, com o uso de ciclobutanona.
XH RMN (600 MHz, CDC13) Ô 7,51 (dd, J3 = 13,8 Hz, J2 = 2,4 Hz, 1H) , 7,16-7,09 (m, 2H) , 6,95 (s, 1H) , 6,64 (br, t, 1H) , 4,94 (m, 1H) , 4,11-3,98 (m, 6H) , 3,87 (m, 1H) , 3,82 (t, J = 4,8 Hz, 2H) , 3,42 (m, 1H) , 2,91 (t, J = 4,8 Hz, 2H), 2,23-2,12 (m, 4H), 1,81-1,73 (m, 2H). LCMS: 422 (M + H+) para Ci9H24FN5O3S Ci9H24FN503S.
Exemplo 69- Preparação do composto 69
Composto 69 (24 mg, 0,053 mmol, 47%) foi obtido a partir do Composto 58 como no Exemplo 60, com o uso de etil bromoacetato em vez de iodometano.
1H RMN (600 MHz, clorofórmio-dl) δ 7,52 (dd, 1H, J, = 13,2 Hz, J2 = 1,8 Hz), 7,15 (dd, 1H, Jx = 9,0 Hz, J2 = 2,4 Hz), 7,11 (t, 1H, 8,4 Hz), 6,91 (s, 1H) , 6,83 (t, 1H, J = 6,6 Hz), 4,98-4,90 (m, 1H) , 4,26-4,21 (m, 2H) , 4,13-3,97 (m, 3H) , 4,01 (s, 3H) , 3,85 (t, 2H, J = 4,2 Hz), 3,78 (s, 2H), 3,24 (t, 2H, J = 4,8 Hz), 1,03 (t, 3H, J = 7,2 Hz). LCMS: 454 (M + H+) para CX9H24FN5O5S.
Exemplo 70- Preparação do composto 70
Composto 69 (17 mg, 0,037 mmol) foi dissolvido em THF (2 mL) e agitado em temperatura ambiente por 3 horas depois da adição de 2M de solução de LiBH4 (1 mL) . Depois da adição de uma pequena quantidade de água, a solução foi separada por cromatografia em coluna para obter Composto 70 (6,5 mg, 0,016 mmol, 43%) como um sólido branco.
XH RMN (600 MHz, clorofórmio-dl) δ 7,53 (dd, 1H, Jx = 13,2 Hz, J2 = 1,8 Hz), 7,17 (dd, 1H, Jx = 8,4 Hz, J2 = 2,4 Hz), 7,12 (t, 1H, 9,0 Hz), 6,90 (s, 1H) , 6,73 (t, 1H, J = 6,0 Hz), 4,98-4,90 (m, 1H) , 4,18-4,04 (m, 2H) , 4,04-3,98 (m, 1H), 4,01 (s, 3H) , 3,96 (t, 2H, J = 4,8 Hz), 3,87 (dd, 1H, Jx = 9,0 Hz, J2 = 7,2 Hz), 3,84 (t, 2H, J = 4,8 Hz), 3,07 (t, 2H, J = 4,8 Hz), 3,00 (t, 2H, J = 4,8 Hz). LCMS: 412 (M + H+) para CI7H22FN5O4S . Exemplo 71- Preparação do composto 71
Composto 71 (84 mg, 0,19 mmol, 76%) foi obtido a partir do Composto 58 como no Exemplo 60, com o uso de bromoacetato de etila em vez de iodometano.
TH RMN (600 MHz, CDC13) δ 7,51 (dd, Jx = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,16-7,07 (m, 2H), 6,91-6,89 (m, 2H), 4,95 (m, 1H), 4,40 (t, J = 5,4 Hz, 2H) 4,13-3,86 (m, 7H), 3,83 (t, J = 4,8 Hz, 2H), 3,15 (t, J = 5,4 Hz, 2H), 3,09 (t, J = 4,8 Hz, 2H), 2,10 (s, 3H). LCMS: 454 (M + H+) para CI9H24FN5O5S .
Exemplo 72- Preparação do composto 72
Composto 72 (54 mg, 0,12 mmol, 61%) foi obtido a partir do Composto 58 como no Exemplo 53.
2H RMN (600 MHz, DMSO-d6) δ = 9,56 (t, J = 6 Hz, 1H) , 7,62 (dd, Ji = 14 Hz, J2 = 2,0 Hz, 1H) , 7,43 (t, J = 9 Hz, 1H) , 7,34 (dd, Ji = 9 Hz, J2 = 2,0 Hz, 1H) , 7,17 (s, 1H) , 4,92 (m, 1H) , 4,41 (br, t, 2H) , 4,17 (t, Jx = 9 Hz, 1H) , 3,99 (s, 3H), 3,88 (s, 3H), 3,85-3,76 (m, 5H). LCMS : 442 (M + H+) para C17H20FN5O4S2. Exemplo 73- Preparação do composto 73
Composto XIII (223 mg, 0,69 mmol) e NaF (38 mg, 1,3 equivalentes) foram dissolvidos em etanol (10 mL) e agitados de urn dia para o outro em temperatura ambiente depois da adição de etil ditioacetato (0,1 mL, 1,2 equivalente). Depois de destilação sob pressão reduzida, a mistura foi dissolvida em acetato de etila, lavada com salmoura, seca com sulfato de sódio, e separada por cromatografia em coluna para obter Composto 73 (220 mg, 0,58 mmol, 84%) como um sólido branco.
TH RMN (600 MHz, CDC13) Ô = 8,52 (s, 1H) 7,91 (br, t, 1H) , 7,56 (dd, Ji = 13 Hz, J2 = 2,4 Hz, 1H) , 7,17 (dd, Jx = 9,0 Hz, J2 = 2,7 Hz, 1H) , 7,11 (t, J = 8,4 Hz, 1H) , 6,87 (S, 1H) , 4,98 (m, 1H) , 4,28-4,24 (m, 1H) , 4,12-4,07 (m 2H) , 3,97 (t, J = 4,8 Hz, 2H), 3,86-3,84 (m, 1H), 3,71 (t, J = 4,8 Hz, 2H) , 2,58 (s, 3H) . LCMS: 38 0 (M + H+) para CI6HI8-FN5O3S .
Exemplo 74- Preparação do composto 74
sal cloridrato. XH RMN (400 MHz, DMSO-d6) δ = 10,5 (br, t, 1H) , 7,70 (d, J = 14 Hz, 1H) , 7,61 (t, J = 8,8 Hz, 1H) , 7,42 (d, J = 8,8 Hz, 1H) , 5,00 (m, 1H) , 4,20 (m, 1H) , 3,94-3,78 (m, 5H) , 3,62 (br, t, 2H), 2,45 (s, 3H). LCMS: 352 (M + H+) para CI5HI8-FN5O2S .
Exemplo 75- Preparação do composto 75
Composto 75 (35 mg, 0,090 mmol, 42%) foi obtido a partir do Composto 74 como no Exemplo 7. 1H RMN (600 MHz, CDC13) δ = 7,74 (br, t, 1H) , 7,55 (dd, Ji = 14 Hz, J2 = 1,8 Hz, 1H) , 7,18-7,12 (m, 2H) , 6,96 (s, 1H) , 5,01 (m, 1H) , 4,32 (m, 1H) , 4,12-4,04 (m, 2H) , 3,96 (s, 2H) , 3,88-3,83 (m, 3H) , 3,15 (t, J = 4. Hz, 2H) , 2,98-2,94 (m, 2H), 1,24 (t, J = 4,2 Hz, 2H), 2,61 (s, 3H). LCMS: 391 (M + H+) para Ci7Hi9-FNeO2S.
Exemplo 76- Preparação do composto 76
Composto 76 (35 mg, 0,086 mmol, 36%) foi obtido a partir do Composto 74 como no Exemplo 12.
1H RMN (600 MHz, CDC13) δ = 7,80 (m, 1H) , 7,56 (dd, Jx = 13 Hz, J2 = 2,4 Hz), 7,19-7,17 (m, 1H) , 7,13-7,10 (m, 1H), 5,00-4,96 (m, 1H), 4,48 (d, J = 4,2 Hz, 2H), 4,29-4,25 (m, 1H) , 4,10-4,07 (m, 2H) , 4,05 (t, J = 4,8 Hz, 2H) , 3,86- 3,83 (m, 1H) , 3,74 (t, J = 4,8 Hz, 2H) , 3,27 (t, J = 4,8 Hz, 1H), 2,58 (s, 3H).
LCMS: 410 (M + H+) para Ci7H2oFN504S. Exemplo 77- Preparação do composto 77
Composto 77 (350 mg, 0,84 mmol, 79%) foi obtido por reação do Composto XIII com Ph2CHCH2CH2OC (S) CHF2 de um dia para o outro em temperatura ambiente como em Bioorg. Med. Cheiti. Lett. 2006, 16, 3.475-3.478.
1H RMN (400 MHz, CDC13) δ = 8,55 (s, 1H) , 8,48 (br, t, 1H) , 7,56 (dd, Ji = 14 Hz, J2 = 2,0 Hz, 1H) , 7,20 (dd, Jx = 8,8 Hz, J2 = 2,0 Hz, 1H) , 7,14 (t, J = 8,8 Hz, 1H) , 6,89 (s, 1H) , 6,22 (t, J = 56 Hz, 1H) , 5,03 (m, 1H) , 4,34 (m, 1H) , 4,16 (t, J = 8,8 Hz, 1H) , 4,06 (m, 1H) , 3,99 (t, J = 4,8 Hz, 2H), 3,82-3,73 (m, 3H). *LCMS: 416 (M + H+) para CISHI6F3N5O3S. Exemplo 78- Preparação do composto 78
Composto 77 reagiu como no Exemplo 74. Então, o composto 78 (26 mg, 0,061 mmol, 35%) foi obtido como no Exemplo 5.
XH RMN (600 MHz, CDC13) δ = 8,65 (br, t, 1H) , 7,49 (dd, Ji = 14 Hz, J2 = 2,0 Hz, 1H) , 7,14-7,13 (m, 2H) , 6,96 (s, 1H) , 6,22 (t, J = 56 Hz, 1H) , 5,03 (m, 1H) , 4,34 (m, Exemplo 79- Preparação do composto 79
Composto VI reagiu como no Exemplo de Preparação 12, com o uso de boc-aminotiazol em vez de boc-aminoisoxazol. Então, composto 80 (26 mg, 0,064 mmol, 16%) foi obtido como no Exemplo de Preparação 10.
XH RMN (400 MHz, DMS0-d6) ô = 8,71 d II 2 Hz, 8,42 (s, , 1H), 7,65 (dd, Jx = 14 Hz, , J2 = 2,0 Hz, 1H), 7,37 (m, 2H), 7, ,07 (s, 1H), 6,39 (d, J = 2 Hz, 1H), (m, 1H), 4,81 (m, 1H), 4,49 (m, 1H), 4,21 (t, J = 9,2 Hz, 1H), 3,93 (m, 1H), 3,84 (t, J = 5,6 Hz, 2H), 3,70 (t, J = 4,8 Hz, 2H). LCMS: 390 (M + H+) para Ci7H16-FN505.
Exemplo 80- Preparação do composto 80
Composto VI reagiu como no Exemplo de Preparação 12, com o uso de boc-aminotiazol em vez de boc-aminoisoxazol. Então, composto 80 (26 mg, 0,064 mmol, 16%) foi obtido como no Exemplo de Preparação 10.
1H RMN (400 MHz, CDC13) δ = 8,55 (s, 1H) , 7,57 (dd, Ji = 13 Hz, J2 = 2,4 Hz, 1H) , 7,21 (dd, J3 = 9,0 Hz, J2 = 2,7 Hz, 1H), 7,13-7,08 (m, 2H), 6,84 (s, 1H), 6,55 (d, J = 3,6 Hz, 1H) , 5,34 (br, s, 1H) , 4,97 (m, 1H) , 4,10 (t, J = 8,8 Hz, 1H) , 3,99 (t, J = 5,4 Hz, 2H) , 3,92-3,79 (m, 3H) , 3,73 (t, J = 5,4 Hz, 2H). LCMS: 405 (M + H+) para CI7H17-FN6O3S .
Exemplo 81- Preparação do composto 81
Composto 81 (35 mg, 0,094 mmol, 25%) foi obtido a partir do Composto XIX como no Exemplo de Preparação 10.
XH RMN (400 MHz, CDC13) δ = 8,49 (s, 1H) , 7,77 (d, J = 1 Hz, 1H), 7,71 (s, 1H), 7,41 (dd, J3 = 13 Hz, J2 = 2,4 Hz, 1H) , 7,08-7,04 (m, 2H) , 6,84 (d, J = 1 Hz, 1H) , 6,86 (s, 1H), 5,06 (m, 1H), 4,78 (d, J = 4 Hz, 2H), 4,14 (t, J = 8,8 Hz, 1H), 3,94-3,64 (m, 7H). LCMS: 374 (M + H+) para C16H16-FN7O3.
Exemplo 82- Preparação do composto 82
Composto 82 (84 mg, 0,24 mmol, 73%) foi obtido a partir do Composto 81 como no Exemplo 2.
XH RMN (400 MHz, DMSO-d6) δ = 8,37 (s, 1H) , 8.19 (s, 1H) , 7,77 (s, 1H) , 7,64-7,56 (m, 2H) , 7,35 (dd, J, = 9,0 Hz, J2 = 2,4 Hz, 1H), 7,08-7,04 (m, 2H), 5,18 (m, 1H), 4,85 (d, J = 5,2 Hz, 2H) , 4,27 (t, J = 9,2 Hz, 1H) , 3,93 (m, 1H), 3,78 (br, t, 2H), 3,35 (br, t, 2H). LCMS: 346 (M + H+) para CISHI6-FN7O2 .
Exemplo 83- Preparação do composto 83
Composto 82 (62 mg, 0,16 mmol) foi dissolvido em metanol (5 mL) e reagiu por 2 horas em temperatura ambiente sob balão de hidrogênio depois da adição de 4 M de solução de HCI dioxano (0,1 mL), formalina (0,2 mL) e Pd/C (6 mg) . A solução foi filtrada com celite, dissolvida em água destilada (10 mL) , neutralizada, extraída com diclorometano, seca com sulfato de sódio, e concentrada sob pressão reduzida para obter Composto 83 (34 mg, 0,086 mmol, 54%) .
1H RMN (400 MHz, CDC13) δ = 7,78 (s, 1H) , 7,75 (s, 1H) , 7,39-7,00 (m, 3H) , 6,88 (s, 1H) , 5,08 (m, 1H) , 4,80 (d, J = 4,4 Hz, 2H) , 4,15 (t, J = 9,2 Hz, 1H) , 3,95 (m, 1H) , 3,80 (t, J = 4,6 Hz, 2H) , 2,98 (t, J = 4,6 Hz, 2H) 2,79 (s, 3H). LCMS: 360 (M + H+) para CieHi8-FN7O2 .
Exemplo 84- Preparação do composto 84
Composto 84 (26 mg, 0,068 mmol, 74%) foi obtido a partir do Composto 82 como no Exemplo 5.
1H RMN (400 MHz, CDC13) δ = 7,79 (s, 1H) , 7,76 (s, 1H) , 7,39-7,03 (m, 3H) , 6,94 (s, 1H) , 5,08 (m, 1H) , 4,80 (d, J = 3,6 Hz, 2H) , 4,15 (t, J = 9,2 Hz, 1H) , 3,95 (m, 1H), 3,84-3,82 (m, 4H), 3,12 (br, t, 2H), 2,34 (s, 1H). LCMS: 384 (M + H+) para CI8HI8-FN7O2 .
Exemplo 85- Preparação do composto 85
Composto 85 (81 mg, 0,21 mmol, 31%) foi obtido a partir do Composto XV como no Exemplo de Preparação 10.
1H RMN (400 MHz, CDC13) δ = 8,49 (s, 1H) , 8,02 (d, J = 2,0 Hz, 1H) , 7,54 (dd, 13 Hz, J2 = 2,4 Hz, 1H) , 7,17 (dd, .11, 9,0 Hz, J2 = 2,7 Hz, 1H) , 7,08 (t, J = 8,4 Hz, 1H) , 6,86 (s, 1H), 5,86 (d, J = 2,0 Hz, 1H), 4,93 (m, 1H), 4,06 (t, J = 8,8 Hz, 1H) , 3,94 (t, J = 5,0 Hz, 2H) , 3,87-3,57 (m, 5H). LCMS: 389 (M + H+) para C17HI7-FN6O4 .
Exemplo 86- Preparação do composto 86
Composto 86 (35 mg, 0,097 mmol, 71%) foi obtido a partir do Composto 85 como no Exemplo 2.
XH RMN (600 MHz, DMSO-d6) δ = 8,40 (s, 1H) , 8,30 (s, 1H) , 7,70 (d, J = 13 Hz, 1H) , 7,60 (t, J= 8,4 Hz, 1H) , 7,41 (d, J = 8,4 Hz, 1H) , 6,03 (s, 1H) , 5,86 (d, J = 2,0 Hz, 1H) , 4,92 (m, 1H), 4,20 (t, J = 7,8 Hz, 1H), 3,89-3,36 (m, 7H) . LCMS: 361 (M + H+) para CieHi7-FN6O3.
Exemplo 87- Preparação do composto 87
Composto 87 (15 mg, 0,036 mmol, 35%) foi obtido a partir do Composto 86 como no Exemplo 12.
XH RMN (600 MHz, DMSO-d6) δ = 8,39 (d, J = 1,2 Hz, 1H) , 7,62 (dd, Ji = 14 Hz, J2 = 2,4 Hz, 1H) , 7,38-7,33 (m, 1H), 7,07 (s, 1H), 6,56 (t, J = 6 Hz, 1H), 6,00 (d, J = 1,2 Hz, 1H), 4,91-4,87 (m, 1H), 4,54-4,52 (m, 1H), 4,32 (d, J = 6,0 Hz, 2H) , 4,18-4,15 (m, 1H) , 3,89 (t, J = 4,8 Hz, 2H) , 3,83-3,80 (m, 1H), 3,70 (t, J = 4,8 Hz, 2H), 3,46-3,43 (m, 2H) . LCMS: 419 (M + H+) para CI8HI9-FN6O5 .
Exemplo 88- Preparação do composto 88
Composto 88 (210 mg, 0,46 mmol, 42%) foi obtido a partir do Composto 86 como no Exemplo 59.
1H RMN (600 MHz, CDC13) δ = 8,07 (d, 1H, J = 1,8 Hz), 7,58 (dd, 1H, Ji = 13,2 Hz, J2 = 3,0 Hz), 7,21 (dd, 1H J3 = 8,4 Hz, J2 = 2,4 Hz), 7,11 (t, 1H, J = 8,4 Hz), 6,82 (s, 1H), 5,88 (d, 1H, J = 1,8 Hz), 5,08 (s, 2H), 4,96-5,00 (m, 1H) , 4,40 (t, 1H, J = 6,6 Hz), 4,09 (t, 1H, J = 9,0 Hz), 4,02 (t, 2H, J = 4,8 Hz), 3,77-3,78 (m, 1H), 3,74-3,76 (m, 1H), 3,66-3,62 (m, 1H). LCMS: 461 (M + H+) para C20H2I-FN6O6.
Exemplo 89- Preparação do composto 89
Composto 89 (36 mg, 0,096 mmol, 68%) foi obtido a partir do Composto 86 como no Exemplo 3.
1H RMN (600 MHz, CDC13) δ 8,07 (d, J = 1,2 Hz, 1H) , 7,51 (dd, Ji = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,15 (dd, Jx = 9,0 Hz, J2 = 2,4 Hz, 1H) , 7,09 (t, 8,4 Hz, 1H) , 6,89 (s, 1H) , 5,87 (d, J = 1,2 Hz 1H) , 4,97 (m, 1H) , 4,42 (t, J = 6 Hz, 1H), 4,08 (t, J = 8,4 Hz, 1H), 3,87-3,60 (m, 5H), 2,98 (t, J = 4,8 Hz, 2H) , 2,79 (s, 3H) . LCMS: 375 (M + H+) para CI7HI9-FN6O3 . Exemplo 90- Preparação do composto 90
Composto 90 (15 mg, 0,039 mmol, 45%) foi obtido a partir do Composto 86 como no Exemplo 6. XH RMN (400 MHz, CDC13) δ= 8,07 (d, 1H, J = 1,6 Hz), 7,51 (dd, 1H, Ji = 13,6 Hz, J2= 2,4 Hz), 7,15 (dd, 1H, Jx = 9,2 Hz, J2= 2,4 Hz), 7,09 (t, 1H, J = 8,8 Hz), 6,91 (s, 1H), 5,87 (dd, 1H, J = 1,6 Hz), 4,99-4,93 (m, 1H), 4,40 (t, 1H, J = 6,4 Hz), 4,07 (t, 1H, J = 9,0 Hz), 3,86-3,81 (m, 3H), 3,78-3,72 (m, 1H), 3,64 (t, 1H, J = 3,2 Hz), 3,62-3,58 (m, 1H) , 3,01 (t, 2H, J = 4,8 Hz), 2,95 (t, 2H, J = 7,07 Hz), 1,23 (t, 3H, J = 7,0 Hz). LCMS: 389 (M + H+) para C18H21- FN6O3 .
Exemplo 91- Preparação do composto 91
Composto 91 (25 mg, 0,063 mmol, 64%) foi obtido a partir do Composto 86 como no Exemplo 5. TH RMN (600 MHz, CDC13) δ 8,07 (d, J = 1,8 Hz, 1H) , 7,53 (dd, Ji = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,16 (dd, Jx = 9,0 Hz, J2 = 2,4 Hz, 1H) , 7,11 (t, 8,4 Hz, 1H) , 6,95 (s, 1H) , 5,87 (d, J = 1,8 Hz 1H), 4,96 (m, 1H), 4,35 (t, J = 6,6 Hz, 1H) , 4,08 (t, J = 9 Hz, 1H) , 3,87-3,60 (m, 7H) , 3,13 (t, J = 4,8 Hz, 2H), 2,31 (t, J = 2,4 Hz, 1H). LCMS: 3 99 (M + H+) para Ci9Hi9-FNeO3 .
Exemplo 92- Preparação do composto 92
Composto 92 (240 mg, 0,75 mmol, 32%) foi obtido a partir do Composto XXIII como no Exemplo de Preparação 10. TH RMN (600 MHz, CDC13) Ô = 8,55 (s, 1H) , 7,61 (dd, = 13 Hz, J2 = 2,4 Hz, 1H) , 7,25 (dd, Jx = 9,0 Hz, J2 = 2,7 Hz, 1H) , 7,14 (t, J = 8,4 Hz, 1H) , 6,90 (s, 1H) , 4,79 (m, 1H) , 4,04-3,99 (m, 5H) , 3,79-3,73 (m, 3H) , 2,58 (br, s, 1H) . LCMS: 323 (M + H+) para CI4H15-FN4O4 .
Exemplo 93- Preparação do composto 93
Composto 93 (190 mg, 0,65 mmol, 74%) foi obtido a partir do Composto 92 como no Exemplo 2. XH RMN (600 MHz, DMSO-d6) δ = 7,73 (dd, Jx = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,60 (t, J = 9 Hz, 1H), 7,45 (dd, Jx = 9,0 Hz, J2 = 2,4 Hz, 1H) , 4,75 (m, 1H) , 4,11 (t, J = 9,0 Hz, 1H), 3,88 (m, 1H), 3,78 (t, J = 4,8 Hz, 2H), 3,70-3,55 (m, 2H) , 3,36 (t, J = 4,8 Hz, 2H) . LCMS: 295 (M + H+) para CX3HX5-FN4O3 .
Exemplo 94- Preparação do composto 94
Composto 93 (150 mg, 0,51 mmol) foi dissolvido em metanol (5 mL) , formaldeído (37% solução aquosa, 0,21 mL, 2,55 mmol), e agitado por 1 hora em temperatura ambiente depois da adição de ácido acético (0,03 mL, 0,51 mmol) e NaBH3CN (48 mg, 0,77 mmol). A solução foi destilada sob pressão reduzida, dissolvida em diclorometano (100 mL) , sequencialmente lavada com solução de bicarbonato de sódio aquosa saturada e solução de cloreto de sódio aquosa saturada (salmoura), seca com sulfato do sódio anidro, concentrada sob pressão reduzida, e separada por cromatografia em coluna para obter Composto 94 (71 mg, 0,23 mmol, 45%) . XH RMN (600 MHz, DMSO-d6) δ = 7,59 (dd, J3 = 13,8 Hz, J2 = 2,4 Hz, 1H), 7,33-7,30 (m, 2H), 6,84 (s, 1H), 5,23 (t, J = 5,4 Hz, 1H) , 4,70 (m, 1H) , 4,07 (t, J = 9,0 Hz, 1H) , 3,82 (m, 1H), 3,71 (t, J = 4,8 Hz, 2H), 3,69-3,54 (m, 2H), 5 2,87 (t, J = 4,8 Hz, 2H) , 2,61 (s, 3H) . LCMS: 309 (M + H+) para Ci4H17-FN4O3.
Exemplo 95- Preparação do composto 95
Composto 95 (300 mg, 0,86 mmol) foi obtido a partir de 4-fluornitrobenzeno de acordo com o Esquema 6, como na síntese do Composto 1. 1H RMN (600 MHz, CDC13) δ = 8,56 (s, 1H) , 7,55 (m, 15 2H), 7,11 (s, 1H), 7,07 (m, 2H), 6,00 (br, t, 1H), 4,79 (m, 1H) , 4,07 (t, J = 9,6 Hz, 1H) , 4,02 (t, J = 4,8 Hz, 2H) , 3,81 (m, 1H), 3,76 (t, J = 4,8 Hz, 2H), 3,72-3,61 (m, 2H), 2,03 (s, 3H). LCMS: 346 (M + H+) para CI6HI9N5O4.
Exemplo 96- Preparação do composto 96
Composto 96 (42 mg, 0,13 mmol, 48%) foi obtido a partir do Composto 95 como no Exemplo 3. 1H RMN (600 MHz, CDC13) δ = 7,48 (d, J = 9,0 Hz, 2H) , 7,22 (s, 1H) , 7,02 (d, J = 9,0 Hz, 2H) , 5,93 (br, t, 1H) , 4,77 (m, 1H) , 4,05 (t, J = 9,6 Hz, 1H) , 3,81 (t, J = 4,8 30 Hz, 2H) , 3,79-3,58 (m, 3H) , 3,01 (t, J = 4,8 Hz, 2H) , 2,80 (s, 3H), 2,03 (s, 3H). LCMS: 332 (M + H+) para CieH2iN5O3.
Exemplo 97- Preparação do composto 97 O
Composto 97 (540 mg, 1,4 mmol) foi obtido a partir de 4-fluornitrobenzeno de acordo com o Esquema 6, como na síntese do Composto 53.
1H RMN (600 MHz, CDC13) δ = 8,56 (s, 1H) , 7,55 (d, J = 9,0 Hz, 2H) , 7,11 (s, 1H) , 7,07 (d, J = 9,0 Hz, 2H) , 6,69 (br, t, 1H), 4,94 (m, 1H), 4,13-4,05 (m, 3H), 4,04-3,99 (m, 5H), 3,90 (m, 1H), 3,76 (t, J = 4,8 Hz, 2H). LCMS: 378 (M + H+) para CI6HI9N5O4S .
Exemplo 98- Preparação do composto 98
Composto 98 (160 mg, 0,44 mmol, 62%) foi obtido a partir do Composto 97 como no Exemplo 60.
XH RMN (600 MHz, CDC13) δ = 7,48 (d, J = 9,0 Hz, 2H) , 7,21 (s, 1H) , 7,02 (d, J = 9,0 Hz, 2H) , 6,69 (br, t, 1H) , 4,92 (m, 1H) , 4,13-4,08 (m, 2H) , 4,01-3,95 (m, 4H) , 3,86 (m, 1H) , 3,81 (t, J = 4,8 Hz, 2H) , 3,01 (t, J = 4,8 Hz, 2H), 2,80 (s, 3H). LCMS: 364 (M + H+) para C16H2iN5O3S.
Exemplo 99- Preparação do composto 99
Composto 99 (340 mg, 0,96 mmol) foi obtido a partir de 4-fluornitrobenzeno de acordo com Esquema 6, como na síntese do Composto 81.
TH RMN (600 MHz, CDC13) δ = 8,55 (s, 1H) , 7,80 (d, J = 1 Hz, 1H) , 7,75 (d, J = 1 Hz, 1H) , 7,40 (d, J = 9,0 Hz, 2H), 7,09 (s, 1H), 7,03 (d, J = 9,0 Hz, 2H), 5,08 (m, 1H), 4,81 (d, J = 4 Hz, 2H), 4,17 (t, J = 8,4 Hz, 1H), 4,00-3,97 (m, 4H), 3,73 (t, J = 4,8 Hz, 2H). LCMS: 356 (M + H+) para CI6HI7-N7O3.
Exemplo 100- Preparação do composto 100
Composto 100 (280 mg, 0,76 mmol) foi obtido a partir de 4-fluornitrobenzeno de acordo com Esquema 6, como na síntese do Composto 85.
TH RMN (600 MHz, CDC13) δ = 8,55 (s, 1H) , 8,06 (d, J = 1,8 Hz, 1H), 7,54 (d, J = 9 Hz, 2H), 7,10 (s, 1H), 7,06 (d, J = 9 Hz, 2H), 5,89 (d, J = 1,8 Hz, 1H), 4,96 (m, 1H), 4,10 (t, J = 9 Hz, 1H), 3,99 (t, J = 4,8 Hz, 2H), 3,89 (m, 1H), 3,75-3,72 (m, 3H), 3,62 (m, 1H) . LCMS: 371 (M + H+) para C17Hi8-N6O4.
Exemplo 101- Preparação do composto 101
Composto 101 (37 mg, 0,10 mmol, 68%) foi obtido a partir do Composto 100 como no Exemplo 89.
TH RMN (600 MHz, CDC13) δ = 8,07 (s, 1H) , 7,48 (d, J = 9 Hz, 2H) , 7,21 (s, 1H) , 7,01 (d, J = 9 Hz, 2H) , 5,87 (s,
Exemplo 102- Preparação do composto 102
Composto 102 (24 mg, 0,069 mmol, 37%) foi obtido a partir do Composto XXVII-c, que foi preparado a partir de 4-fluornitrobenzeno de acordo com o Esquema 6 como no
Exemplo de Preparação 14, como no Exemplo 57. TH RMN (600 MHz, CDC13) δ = 7,56 (s, 1H) , 7,54 (d, J = 9 Hz, 2H) , 7,06 (d, J = 9 Hz, 2H) , 6,67 (br, t, 1H) , 4,93 (m, 1H), 4,21 (t, J = 4,8 Hz, 2H), 4,13-4,07 (m, 3H), 4,01 (s, 3H) , 3,88 (t, J = 9 Hz, 1H) , 3,77 (t, J = 4,8 Hz, 2H) . LCMS: 351 (M + H+) para Ci5Hi8-N4O4S.
Exemplo 103- Preparação do composto 103
Composto 103 (350 mg, 0,90 mmol) foi obtido a partir de 3,4,5-trifluornitrobenzeno de acordo com o Esquema 6, como na síntese do Composto 81.
TH RMN (600 MHz, CDC13) δ = 8,54 (s, 1H) , 7,77 (d, J = 1 Hz, 1H) , 7,75 (d, J = 1 Hz, 1H) , 7,15 (s, 1H) , 7,13 (s, 1H) , 6,69 (s, 1H) , 5,11 (m, 1H) , 4,81 (d, J = 4 Hz, 2H) , 4,15 (t, J = 8,8 Hz, 1H) , 4,02-3,98 (m, 3H) , 3,65 (t, J = 4,8 Hz, 2H) . LCMS: 3 92 (M + H+) para CieH15-F2N7θ3.
Exemplo 104- Preparação do composto 104
Composto 104 (23 mg, 0,061 mmol, partir do Composto 103 como no Exemplo 83.
XH RMN (400 MHz, CDC13) δ = 7,79 (s, 1H) , 7,74 (s, 1H) , 7,11 (s, 1H) , 7,09 (s, 1H) , 6,65 (s, 1H) , 5,11 (m, 1H) , 4,81 (d, J = 4 Hz, 2H) , 4,16 (t, J = 9 Hz, 1H) , 3,95 (m, 1H) , 3,73 (t, J = 4,8 Hz, 2H) , 2,99 (t, J = 4,8 Hz, 2H) . LCMS: 378 (M + H+) para ClsHi7-F2N7θ2.
Exemplo 105- Preparação do composto 105
Composto 105 (640 mg, 1 6 mmol) foi obtido a partir de 3,4,5-trifluornitrobenzeno de acordo com o Esquema 6, como na síntese do Composto 85.
TH RMN (400 MHz, CDC13) δ = 8,54 (s, 1H) , 8,08 (d, J = 1,6 Hz, 1H) , 7,29 (s, 1H) , 7,27 (s, 1H), 6,71 (s, 1H) , 5,89 (d, J = 1,6 Hz, 1H), 4,99 (m, 1H) , 4,54 (t, J = 6,4 Hz, 1H) , 4,08 (t, J = 9 Hz, 1H) , 4,00 (t, J = 4,8 Hz, 2H) , 3,90-3,73 (m, 2H), 3,69-3,62 (m, 3H). LCMS: 407 (M + H+) para Ci7Hie-F2N6O4.
Exemplo 106- Preparação do composto 106
Composto 106 (24 mg, 0,061 mmol, 74%) foi obtido a partir do Composto 105 como no Exemplo 89.
XH RMN (400 MHz, CDC13) δ = 8,06 (d, J = 1,6 Hz, 1H) , 7,23 (s, 1H) , 7,18 (s, 1H) , 6,65 (s, 1H) , 5,90 (d, J = 1,6 Hz, 1H) , 4,99 (m, 1H) , 4,92 (t, J = 6,4 Hz, 1H) , 4,06 (t, J = 8,8 Hz, 1H), 3,89-3,61 (m, 5H), 3,00 (t, J = 4,8 Hz, 2H). LCMS: 393 (M + H+) para CI7H18-F2N6O3 .
Exemplo de Teste 1- Medição da atividade antibacteriana in vitro
Para testar a atividade antibacteriana dos derivados de oxazolidinona sintetizados nos Exemplos 1 a 106, foi realizado um teste de atividade in vitro como se segue.
A atividade antibacteriana in vitro dos derivados de oxazolidinona dos Exemplos 1 a 106 foi avaliada por método de microdiluição de caldo, como comparado ao crescimento bacteriano no grupo de controle não tratado. A concentração inibidora mínima de um antibiótico em que o crescimento de bactérias pode ser inibido em até 90% (MIC90, ug/ml) foi medida. A medição de MIC90 foi feita de acordo com o método de microdiluição de caldo com base no documento CLSI [Clinical and Laboratory Standards Institute Document. (2000) "Methods for Dilution Antimicrobial Susceptibility Test for Bacteria that Grow Aerobically" - quinta edição: M7-A5. CLSI, Villanova, PA]. 1) Bactérias de teste - a atividade antibacteriana foi medida contra 14 espécies bacterianas que incluem Staphylococcus aureus suscetível à meticilina (MSSA), Staphylococcus aureus resistente à meticilina (MRSA), Enterococcus resistente à vancomicina (VRE), Enterococcus faecalis resistente à linezolida e vancomicina (LYRE), Haemophilus influenzae e Moraxellacatarrhalis (S. aureus, S. aureusmR, S. epidermidis, S. epiderrnidismR, E. faecalis, E. faecalisVanA, E. faecalis73^ LR, E. faeciumvanA, E. faecium, E. coli, P. aeruginosa, K. pneumoniae, H. influenzae e M. catarrhalis) . O resultado de MIC90 contra as duas bactérias mais importantes, MRSA e LYRE, é dado na Tabela 1. 2) Preparação do composto de teste
Os compostos de teste (Compostos 1 a 106, ou seja, os derivados de oxazolidinona sintetizados nos Exemplos 1 a 106) foram dissolvidos em DMSO na concentração de 10.240 ug/ml e submetidos a diluição de duas vezes em série com DMSO. Os compostos de teste em solução de DMSO foram também diluídos 20 vezes com água destilada estéril. A concentração final do composto de teste em incubações antibacterianas foi de 0,0625 a 128 ug/ ml. A concentração final de DMSO, que foi usado como um excipiente, foi 2,5% (v/v) . Linezolida (Fórmula química B) foi usada como um composto de comparação. Os resultados da atividade antibacteriana dos compostos de teste são sumarizados na Tabela 1. Fórmula química B
Tabela 1- Atividade antibacteriana (MIC90, ug/ml) de compostos representados pela Fórmula Química 1
1. Staphylococcus aureus resistente à meticilina 2. Enterococcus faecalis resistente à linezolida e vancomicina
Como observado a partir da Tabela 1, os derivados de oxazolidinona da presente invenção mostraram potente atividade antibacteriana contra algumas bactérias gram- positivas resistentes aos antibióticos existentes, como Staphylococcus aureus resistente à meticilina e Enterococcus faecalis resistente à vancomicina, em concentrações muito menores quando comparados ao composto de comparação linezolida. Embora não mostrado na Tabela 1, eles também foram eficazes contra várias bactérias gram- positivas, e alguns deles foram eficazes contra bactérias gram-negativas, como Haemophilus influenzae, Moraxella catarrhalis. Especialmente, uma vez que eles mostram excelente atividade antibacteriana contra Enterococcus faecalis resistente à linezolida, eles podem ser usados de forma útil contra bactérias resistentes à linezolida, que se disseminam atualmente.
Portanto, percebe-se que os derivados de oxazolidinona da presente invenção podem ser usados como antibióticos que têm um amplo espectro antibacteriano contra bactérias gram- positivas .
Exemplo de Teste 2- Medição de solubilidade em água
As solubilidades em água de metanossulfonatos (MSA) de compostos representativos entre os derivados de oxazolidinona de Fórmula química 1 foram medidas. Linezolida de Fórmula química B foi usada como um material de referência. Os resultados são dados na Tabela 2.
A medição da solubilidade foi feita por XH RMN de acordo com o seguinte método. Primeiramente, um metanossulfonato (100 mg) do composto foi adicionado a D20 (0,5 ml). Depois da preparação de uma solução saturada por agitação vigorosa por 30 minutos, a solução foi filtrada e 0,3 ml foi retirado dela. Uma solução do composto de referência (0,3 ml) (neste exemplo de teste, DMSO diluído com D2O foi usado) com uma concentração exatamente conhecida foi adicionada a ela. A partir do espectro de 1H RMN da solução, a proporção integral do pico da amostra para o pico de referência (DMSO) foi calculada. Uma vez que a concentração da solução de referência é conhecida, os mols da amostra podem ser calculados a partir da proporção integral. Então, a solubilidade da amostra foi calculada. Tabela 2- Solubilidade de metanossúlfonato em água
Como observado a partir da tabela, as solubilidades dos compostos representados pela Fórmula Química 1 em água são maiores que 10%, porque eles podem ser preparados como sais. Em contraste, a solubilidade da linezolida em água é apenas 0,3%. Ou seja, as solubilidades dos compostos da presente invenção em água são até 50 vezes maiores que aquela da linezolida. Essa vantagem permite o desenvolvimento dos compostos da presente invenção em antibióticos que podem ser administrados por via oral ou por via intravenosa como bolo, o que não é realizável para linezolida. Além disso, uma vez que eles são eficazes contra bactérias resistentes à linezolida, bem como MRSA e VRE, eles podem ser desenvolvidos em antibióticos notáveis capazes de substituir a linezolida.
Exemplo de Teste 3- Citotoxicidade e inibição de MAO (monoamina oxidase)
1) Medição da citotoxicidade por ensaio MTT O ensaio MTT é um ensaio qualitativo, colorimétrico, para sobrevivência de célula de mamífero e proliferação celular. Ele depende da redução de MTT de sal tetrazólio pela succinato desidrogenase mitocondrial de células viáveis para formar um produto de azul formazan. 0 ensaio mede a respiração celular e a quantidade de produto formazan para o número de células vivas presentes em cultura. Nesse teste, células ovarianas de hamster da China (CHO-K1) foram adquiridas de ATCC (USA). As células CHO subcultivadas foram destacadas do frasco de cultura por tratamento com solução de tripsina-EDTA, e semeadas em uma microplaca de 96 cavidades, com 5.000 células por cada cavidade. Depois da cultura por 24 horas em um incubador a 5% CO2 a 37 °C, as células foram tratadas com os derivados de oxazolidinona de acordo com a presente invenção sintetizados nos exemplos acima, em 7 diferentes concentrações. Depois de cultivo adicional por 48 horas em um incubador a 5% C02 a 37 °C, 15 uL de solução a 5 ug/ml MTT foram adicionados a cada cavidade. As células foram também incubadas no incubador a 5% CO2 a 37 °C por cerca de 2 horas. Então, o meio de cultura foi descartado e 100 uL de solução de DMSO foram adicionados a cada cavidade. Depois de agitação da microplaca por 30 minutos, a absorvência foi medida a 550 nm com o uso de um leitor de placa "Spectramax plus 190" (Molecular Devices, USA) . A diminuição da absorvência dos grupos tratados com composto comparada ao grupo de controle não tratado é uma indicação da diminuição de células sobreviventes, que permite a medição da citotoxicidade dos compostos. O valor de CC50, ou seja, a concentração em que a proliferação celular é reduzida a 50%, dos compostos de acordo com a presente invenção foi computada com o uso do programa de análise estatística GraFit (versão 5.0.12) adquirido de Erithacus Software depois do cálculo das percentagens da absorvência em várias concentrações quando comparado ao grupo de controle.
2) Inibição de MAO
Linezolida é conhecida por agir como um inibidor não seletivo, reversível de monoamina oxidases, e pode interagir possivelmente com fármacos adrenérgicos ou serotonérgicos. Os derivados de oxazolidinona de acordo com a presente invenção sintetizados nos exemplos foram testados para inibição de monoamina oxidase A (MAO A) e monoamina oxidase B (MAO B) . O kit de ensaio MAO-GLO foi adquirido de Promega (USA) e as enzimas MAO A e MAO B foram adquiridas de Sigma-Aldrich (USA). A partir do produto de aldeído que resulta da ação da enzima MAO sobre o grupo amina do substrato, luciferina metil éster é produzido. O reagente de detecção de luciferina é então adicionado para inativar a enzima MAO. A esterase e a luciferase incluídas no reagente oxidam luciferina, assim emitindo luz. A emissão de luz é detectada para medir a atividade de MAO. A emissão de luz foi detectada com o uso de "LEADseeker" (Amershan Bioscience, Sweden). A atividade de MAO foi medida na presença dos compostos de acordo com a presente invenção a 3,9-500 uM e comparada com o grupo controle não comparação. Para a medição da atividade de inibição de MAO dos compostos representados pela Fórmula Química 1, o valor de IC50, ou seja, a concentração dos compostos em que a atividade enzimática é inibida em 50% (esse valor está relacionado com a constante de inibição Ki) pode ser determinada. A concentração do inibidor em que a taxa de hidrólise do substrato é reduzida em 50% (ou seja, o valor de IC50) pode ser determinada a partir de um gráfico de log da taxa relativa de hidrólise (quando comparada ao grupo controle não inibido) versus a concentração dos compostos de Fórmula química 1. O efeito de inibição de MAO dos compostos de Fórmula química 1 foi medido por determinação da constante de inibição Ki. Equação 1
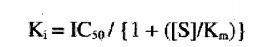
Na Equação 1, Km é a constante de Michaelis-Menten, ou seja, a concentração do substrato em que a taxa de reação enzimática é metade da máxima, e IC50 é a concentração do inibidor em que a taxa da hidrólise do substrato é reduzida em 50%. O valor de IC50 foi medido por tabulação de log da taxa relativa de hidrólise (quando comparado ao grupo de controle não inibido) versus a concentração dos compostos de Fórmula química 1. 0 programa de análise estatística GraFit (versão 5.0.12), adquirido de Erithacus Software, foi usado.
Os resultados de teste de citotoxicidade e de inibição de MAO para compostos representativos entre os derivados de oxazolidinona de Fórmula química 1 são dados na Tabela 3.
Uma vez que o composto de comparação linezolida exibe ação inibidora significativa contra enzimas MAO e tem a possibilidade de causar toxicidade ou outros efeitos colaterais, tem sido feito um grande esforço para descobrir um composto sem efeito de inibição da MAO. Em geral, compostos à base de oxazolidinona mostram tal efeito forte de inibição de MAO de modo a serem usados como inibidores da MAO. No entanto, embora o inibidor da MAO possa fornecer um efeito terapêutico para aqueles que dele necessitam, ele pode resultar em toxicidade ou outros efeitos colaterais quando ele é usado como um antibiótico. Portanto, a determinação do efeito de inibição de MAO dos antibióticos de oxazolidinona é absolutamente necessária, e um com menos de tal efeito é favorável.
Linezolida e TR-700 de Fórmula química D, desenvolvidos por Trius Therapeutics, foram usados como compostos de comparação. Uma vez que TR-701 é um pró- fármaco de TR-700, TR-700 foi usado. Tabela 3- Testes de citotoxicidade e inibição de MAO
Como observado a partir da tabela 3, TR-700 exibe quantidade substancial de efeito citotóxico e potente efeito inibidor contra MAO A e MAO B também. Em contraste, a maior parte dos compostos da presente invenção é segura em termos de citotoxicidade e exibe menos efeito inibidor que TR-700 em 1/10.
Pelo fato de os compostos da presente invenção exibirem alta solubilidade e boa atividade antibacteriana com menos toxicidade, eles são altamente promissores como prováveis antibióticos da próxima geração.
O presente pedido contém material relacionado ao Pedido de Patente Coreana No. 10-2008-0093712, depositado no "Korean Intellectual Property Office" em 24 de setembro de 2008, cujo conteúdo é aqui incorporado por referência.
Embora a presente invenção tenha sido descrita com relação às modalidades específicas, será aparente para aqueles habilitados na técnica que várias alterações e modificações podem ser feitas sem fugir do espírito e escopo da invenção, como definido nas reivindicações a seguir.
Aplicabilidade Industrial
Como acima descrito, os novos derivados de oxazolidinona da presente invenção exibem um espectro antibacteriano contra bactérias resistentes, que incluem Staphylococcus resistente à meticilina (MRSA), uma baixa toxicidade, e uma forte atividade antibacteriana contra as bactérias resistentes aos antibióticos existentes, como Staphylococcus aureus e Enterococcus faecalis, especialmente uma excelente atividade antibacteriana contra Enterococcus faecalis resistente à linezolida. Portanto, eles podem ser usados, de modo útil, como os antibióticos de oxazolidinona de segunda geração. Além disso, os derivados de oxazolidinona com um grupo de amidoxima cíclica ou amidrazona cíclica de acordo com a presente invenção podem ser facilmente preparados em formulação para administração oral ou injeção porque eles têm solubilidade mais alta em água que outros compostos de oxazolidinona que já existem.