BRPI0919065B1 - Anticorpos monoclonais anti-claudin-i para a inibição de infecção por vírus de hepatite c - Google Patents
Anticorpos monoclonais anti-claudin-i para a inibição de infecção por vírus de hepatite c Download PDFInfo
- Publication number
- BRPI0919065B1 BRPI0919065B1 BRPI0919065-1A BRPI0919065A BRPI0919065B1 BR PI0919065 B1 BRPI0919065 B1 BR PI0919065B1 BR PI0919065 A BRPI0919065 A BR PI0919065A BR PI0919065 B1 BRPI0919065 B1 BR PI0919065B1
- Authority
- BR
- Brazil
- Prior art keywords
- hcv
- antibody
- antibodies
- cells
- cldn1
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/29—Hepatitis virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
- C12N5/12—Fused cells, e.g. hybridomas
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Virology (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Biomedical Technology (AREA)
- Zoology (AREA)
- Communicable Diseases (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Biotechnology (AREA)
- Mycology (AREA)
- General Chemical & Material Sciences (AREA)
- Wood Science & Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Engineering & Computer Science (AREA)
- Cell Biology (AREA)
- Oncology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
anticorpos monoclonais anti-claudin-1 para a inibição de infecção por vírus de hepatite c. a presente invenção provê anticorpos monoclonais que se ligam especificamente ao domínio extracelular de claudin-1 humano na superfície de célula, desse modo inibindo entrada de hcv em células suscetíveis e evitando infecção por hcv dessas células; e linhagens de célula de hibridoma que produzem tais anticorpos monoclonais. são também fornecidos reagentes que compreendem tais anticorpos, e composições farmacêuticas ou evitar infecção por hcv por administração de um anticorpo monoclonal invertido, ou uma administração farmacêutica do mesmo são também descritos.
Description
O presente pedido reivindica prioridade ao pedido de patente européia número EP 08 305 597.0 depositado em 25 de setembro de 2008. 0 pedido de patente européia é incorporado aqui a título de referência na íntegra.
O vírus de hepatite C (HCV) é um principal problema de saúde global, com uma estimativa de 150-200 milhões de pessoas infectadas no mundo inteiro, incluindo pelo menos 5 milhões de indivíduos infectados na União Européia (Pawkotskty, 2004). De acordo com a Organização mundial da Saúde, 3 a 4 milhões de novas infecções ocorrem anualmente. A infecção é frequentemente assintomática; entretanto, a maioria dos indivíduos infectados com HCV desenvolve infecção crônica (Hoofnagle, 2002; Lauer, 2001; e Seeff, 1995). A infecção crônica por HCV resulta freqüentemente em doença grave do fígado, incluindo fibrose e esteatose (Chisari, 2005). Aproximadamente 20% dos pacientes com infecção crônica por HCV desenvolvem cirrose do fígado, o que avança para carcinoma hepatocelular em 5% dos casos (Hoofnagle, 2002).
Infecção Crônica por HCV é a indicação principal para transplantes de figado (Seeff, 2002) . Infelizmente, o transplante de figado não é uma cura para hepatite C; recorrência virai é um problema invariável e causa principal de perda de enxerto (Brown, 2005). Nenhuma vacina que protege contra HCV está disponível. Terapias atuais incluem administração de ribaviridina e/ou interferon-alfa (IFN-cc) , dois agentes antivirais não específicos. Utilizando um tratamento de combinação de IFN-a peguilada e ribavirina, depuração persistente é obtida em aproximadamente 50% de pacientes com hepatite Crônica C., entretanto, um grande número de pacientes têm contra- indicações a um dos componentes da combinação, não podem tolerar o tratamento, não respondem à terapia com IFN ou experimentam um relapso quando a administração é interrompida. Além de eficácia limitada e efeitos colaterais substanciais como neutropenia, anemia hemolítica e depressão severa, terapias antivirais atuais são também caracterizadas por custo elevado.
Até recentemente, o desenvolvimento de terapias mais eficazes para combater infecção por HCV foi dificultado pela ausência de um sistema de cultura de células que suporta replicação de HCV. A produção robusta de HCV infeccioso em cultura de célula foi obtida agora utilizando um genoma de HCV exclusivo derivado do sangue de um paciente japonês com hepatite C fulminante (HFH-1) (Wakita, 2005; Lindenbach, 2005; Zhong, 2005). A capacidade da cepa 5 HFH-1 de HCV liberar partículas infecciosas em cultura de célula (HCVcc) e o desenvolvimento de pseudopartículas HCV retrovirais (HCVpp) (Bartosch, 2003; Hsu, 2003) permitiram estudos sobre o mecanismo de entrada e replicação de HCV, que levaram à identificação de biomoléculas alvo 10 terapêuticas em potencial.
HCV é um virus de RNA de fita positiva classificado no gênero Hepacivitus, na família Flaviviridae. A translação do quadro de leitura aberto principal do genoma HCV resulta na produção de uma poliproteína com 15 aproximadamente 3000 aminoácidos de comprimento, que é clivada co- e pós-translação pela ação coordenada de proteases virais e celulares em pelo menos 10 proteínas maturas, incluindo duas glicoproteínas envelope (El e E2) . HCV inicia infecção por ligar-se a moléculas ou receptores 20 na superfície de hepatócitos. A evidência atual sugere que pelo menos quatro moléculas de célula hospedeiras são importantes para entrada de HCV in vitro; a tetraspanina CD81 (Pileri, 1998), o receptor expurgador classe B tipo I (SB-RI) (Zeisel, 2007; Bartosch, 2003; Grove, 2007; Kapadia, 2007; Scarselli, 2002), Occludin (Ploss, 2009) e Claudin-1 (CLDN1), urtia proteina de membrana integral e urn componente de fitas de junção apertada (Evans, 2007) . Glicoproteinas de HCV foram reportadas como interagindo 5 diretamente com CD81 e SR-BI (Cocquerel, 2006) . Estudos de bloqueio de anticorpo e mutagênese com versões etiquetadas de CLDN1 sugerem que o primeiro loop extracelular está envolvido em interações com HCV (Evans, 2007) . Entretanto, o papel exato desempenhado por cada dos receptores não é 10 claro.
A identificação desses receptores ou co-receptores para HCV abriu novos caminhos para o desenvolvimento de agentes terapêuticos e prolifáticos como candidatos de droga para a prevenção e/ou tratamento de infecção por HCV.
Desse modo, por exemplo, Nicosia e co-trabalhadores geraram anticorpos monoclonais contra SR-BI humano nativo que inibem ligação de HCV E2 a SR-BI e bloqueiam eficientemente infecção por HCVcc de células de hepatoma em um modo dependente de dose (Catanese, 2007; WO 2006/005465) . O 20 pedido de patente européia No. EP 1 256 348 revela substâncias com efeitos antivirais (por exemplo, anticorpos, proteinas, polissacarideos sulfatados e compostos de baixo teor de moléculas) que inibem ligação de HCV E2 e. CD81. O pedido de patente internacional WO 2007/130646 descreve ensaios baseados em célula e in vitro para identificar agentes que interferem nas interações de HCV com Claudin-1 desse modo evitando infecção por HCV. Uma vez que o desenvolvimento de abordagens terapêuticas novas contra HCV permanece um objetivo de alta prioridade, esses estudos são encorajadores visto que demonstram que agentes que afetam a entrada de HCV em células suscetíveis podem constituir uma alternativa eficaz e segura para terapias de HCV atuais.
A presente invenção refere-se a sistemas alvejados e estratégias para a prevenção e/ou tratamento de infecção por HCV e doenças relacionadas à HCV. Em particular, a presente invenção é dirigida a anticorpos que interferem em interações de células hospedeiras-HCV por ligação ao dominio extracelular de Claudin-1, um receptor conhecido de HCV. Sem desejar ser limitado por teoria, acredita-se que a ligação de tal anticorpo ao dominio extracelular de Claudin-1 em uma superfície de célula iniba ou bloqueie a entrada de HCV na célula e desse modo evite infecção por HCV da célula. Os requerentes mostraram que anticorpos anti-Claudin inibem a ligação de glicoproteína de envelope E2 e virions a linhagens de célula permissiva de HCV na ausência de interação de Claudin-E2 detectável. Os requerentes demonstraram que os anticorpos neutralizam infectividade por HCV por reduzir a associação de glicoproteina de envelope E2 com a superficie de célula e romper as interações de CD81-Claudin-1. Os anticorpos podem ser utilizados no tratamento profilático ou terapêutico de infecção por HCV (infecção por HCV aguda ou crônica) e doenças ou distúrbios relacionados à HCV (por exemplo, inflamação de figado, cirrose, e carcinoma hepatocelular e transplante de figado). Anticorpos como aqueles fornecidos aqui que inibem a entrada de HCV em células são particularmente atraentes como terapêutica antiviral. Um inibidor de entrada de HCV não necessita cruzar a membrana de plasma ou ser modificado intracelularmente. Além disso, como a entrada virai é mediada por estruturas conservadas das membranas virai e celular, inibidores de anticorpo de entrada virai podem ser muito potentes e menos suscetíveis ao desenvolvimento de resistência virai.
Mais especificamente, em um aspecto, a presente invenção provê linhagens de células de hibridoma que secretam anticorpos monoclonais que se ligam especificamente ao domínio extracelular de Claudin-1 humano. Em particular, os presentes requerentes depositaram oito de tais linhagens de células de hibridoma no DSMZ Zellkuturen GmbH, InhoffenstraBe 7 B, 38124 Braunschweig, Alemanha) em 29 de julho de 2008. Receberam os números de acessão DSM ACC2931, DSM ACC2932, DSM ACC2933, DSM ACC2934, DSM ACC2935, DSM ACC2936, DSM ACC2937 e DSM ACC2938. 0 depósito foi feito de acordo com as disposições do Tratado de Budapeste sobre Reconhecimento internacional do depósito de microorganismos para fins de proteção de patente (Tratado de Budapeste).
Em outro aspecto, a presente invenção provê um anticorpo monoclonal que é secretado por uma das linhagens de células de hibridoma depositadas sob os números de acessão DSM ACC2931, DSM ACC2932, DSM ACC2933, DSM ACC2934, DSM ACC2935, DSM ACC2936, DSM ACC2937 e DSM ACC2938. O anticorpo monoclonal pode ou não ser isolado e/ou purificado de culturas de hibridoma. Em certas modalidades, o anticorpo monoclonal é uma imunoglobulina do isotipo de cadeia leve (L) kappa e cadeia pesada (H) r!gG2a. em outras modalidades, o anticorpo monoclonal é uma imunoglobulina do isotipo de cadeia leve (L) kappa e cadeia pesada (H) r!gG2b.
Como demonstrado pelos requerentes, anticorpos monoclonais secretados pelas linhagens de células de hibridoma depositadas se ligam especificamente ao domínio extracelular de Claudin-1 humano e inibem eficientemente infecção por HCV in vitro. A presente invenção também abrange qualquer fragmento biologicamente ativo dos anticorpos monoclonais inventivos, isto é, qualquer fragmento ou porção que retenha a capacidade do anticorpo 5 monoclonal interferir em interações de células hospedeiras- HCV, e/ou ligar especificamente ao dominio extracelular de Claudin-1 humano, e/ou inibir ou bloquear entrada de HCV em células suscetíveis a HCV, e/ou reduzir ou evitar infecção por HCV de células suscetíveis.
Mais genericamente, a presente invenção abrange qualquer molécula que compreenda um anticorpo monoclonal anti-Claudin-1 inventivo ou um fragmento do mesmo, incluindo anticorpos quiméricos, anticorpos humanizados, anticorpos desimunizados e moléculas derivadas de anticorpo 15 compreendendo pelo menos uma região de determinação complementar (CDR) de uma região variável de cadeia pesada ou cadeia leve de um anticorpo monoclonal anti-Claudin-1 inventivo como secretado por uma linhagem de célula de hibridoma, incluindo moléculas como fragmentos Fab, fragmentos F(ab')2z fragmentos Fd, anticorpos Sc (anticorpos de cadeia única), diacorpos, cadeias únicas leves de anticorpo individuais, cadeias pesadas de anticorpo individuais, fusões quiméricas entre cadeias de anticorpo e outras moléculas, e conjugados de anticorpo como anticorpos conjugados com um agente de diagnóstico (fração detectável) ou agente terapêutico, desde que essas moléculas relacionadas a anticorpo retenham pelo menos uma propriedade biologicamente relevante do anticorpo monoclonal inventivo a partir do qual é "derivado". A propriedade biologicamente relevante pode ser a capacidade de interferir com interações de células hospedeiras-HCV, para ligar-se especificamente ao dominio extracelular de Claudin-1 humano, inibir ou bloquear entrada de HCV em células suscetíveis a HCV, e/ou reduzir ou evitar infecção por HCV de células suscetíveis. Em certas modalidades preferidas, um fragmento biologicamente ativo de um anticorpo monoclonal da invenção se liga especificamente ao domínio extracelular de Claudin-1 humano.
Os requerentes mostraram que anticorpos monoclonais secretados pelas linhagens de células de hibridoma depositadas reconhecem um epítopo que é fortemente afetado por mutações no motivo conservado no primeiro loop extracelular de Claudin-1 humano. Esse motivo é: W(30)- GLW(51)-C(54)-C(64) . Consequentemente, em certas modalidades um anticorpo monoclonal de acordo com a presente invenção, ou um fragmento biologicamente ativo do mesmo, reconhece um epítopo que é dependente da estrutura de motivo conservado W (30)-GLW (51)-C (54 )-C (64) no primeiro loop extracelular de Claudin-1.
Similarmente, os requerentes mostraram que anticorpos monoclonais secretados pelas linhagens de células de hibridoma depositadas não reagem de forma cruzada com Claudin-1 de murino, porém reagem de forma cruzada com seu ortólogo no macaco cinomolgus primata não humano (Macaca fascicularis) . Portanto, em certas modalidades, um anticorpo monoclonal de acordo com a presente invenção, ou um fragmento biologicamente ativo do mesmo, não se liga a Claudin-1 de roedor, porém se liga a Claüdin-1 de primata não humano.
Genericamente, um anticorpo da presente invenção inibe a ligação de glicoproteína de envelope E2 ou virions infecciosos a linhagens de células permissivas de HCV; e inibe associação(ões) de CD81-Claudin-1.
Os anticorpos monoclonais e moléculas relacionadas a anticorpos da presente invenção podem encontrar aplicação em uma variedade de tratamentos terapêuticos e profiláticos. Por conseguinte, em outro aspecto, as moléculas relacionadas a anticorpo e monoclonais inventivos são fornecidas para evitar infecção por HCV de uma célula (por exemplo, uma célula suscetível ou uma população de células suscetíveis); para evitar ou tratar infecção por HCV ou uma doença relacionada à HCV em um sujeito; para controlar infecção Crônica por HCV; e para evitar recorrência de HCV em um paciente com transplante de figado. A infecção por HCV pode ser devido a HCV de um genótipo selecionado do grupo que consiste em genótipo 1, genótipo 2, genótipo 3, genótipo 4, genótipo 5, e genótipo ou mais especificamente de um subtipo selecionado do grupo que consiste em subtipo la, subtipo lb, subtipo 2a, subtipo 2b, subtipo 2c, subtipo 3a, subtipo 4a-f, subtipo 5a, e subtipo 6a.
Em um aspecto relacionado, a presente invenção provê um método de reduzir a probabilidade de uma célula suscetível de se tornar infectada com HCV como resultado de contato com HCV, que compreende contatar a célula suscetível com uma quantidade eficaz de um anticorpo inventivo ou molécula relacionada a anticorpo. Também é fornecido um método de reduzir a probabilidade de células suscetíveis de um sujeito de se tornarem infectadas com HCV como resultado de contato com HCV, que compreende administrar ao sujeito uma quantidade eficaz de uma molécula relacionada a anticorpo ou anticorpo inventivo. A presente invenção também provê um método de tratar ou evitar infecção por HCV ou uma doença associada à HCV (por exemplo, uma patologia ou doença de figado) em um sujeito necessitando do mesmo que compreende administrar ao sujeito uma quantidade eficaz de uma molécula relacionada a anticorpo ou anticorpo monoclonal inventivo. A invenção também provê um método para controlar infecção crônica por HCV em um sujeito necessitando do mesmo que compreende administrar ao sujeito uma quantidade eficaz de uma molécula relacionada a anticorpo ou anticorpo monoclonal inventivo.
Também é fornecido um método de evitar recorrência de HCV em um paciente de transplante de figado, que compreende administrar ao paciente uma quantidade eficaz de uma molécula relacionada a anticorpo ou anticorpo monoclonal inventivo. A administração de uma molécula relacionada a anticorpo ou anticorpo inventivo a um sujeito pode ser por qualquer via, incluindo, por exemplo, vias parenteral, aerossol, oral e tópica. A molécula relacionada a anticorpo ou anticorpo monoclonal inventivo pode ser administrada individualmente ou em combinação com um agente terapêutico, como um agente antiviral.
As moléculas relacionadas a anticorpo e anticorpos monoclonais inventivos podem ser administradas por si ou como composições farmacêuticas. Por conseguinte, em outro aspecto, a presente invenção provê o uso de uma molécula relacionada a anticorpo ou anticorpo monoclonal inventivo para a fabricação de medicamentos, composições farmacêuticas, ou kits farmacêuticos para o tratamento e/ou prevenção de infecção por HCV e doenças associadas à HCV.
Em um aspecto relacionado, a presente invenção provê uma composição farmacêutica que compreende uma quantidade eficaz de uma molécula relacionada a anticorpo ou anticorpo monoclonal inventivo e pelo menos um excipiente ou veiculo farmaceuticamente aceitável. Em certas modalidades, a composição farmacêutica é adaptada para administração em combinação com um agente terapêutico adicional, como um agente antiviral. Em outras modalidades, a composição farmacêutica compreende ainda um agente terapêutico adicional, como um agente antiviral, agentes antivirais apropriados para uso em métodos e composições farmacêuticas da presente invenção incluem, porém não são limitadas a interferons (por exemplo, interferon-alfa, interferon-alfa peguilado), ribavirina, anticorpos anti-HCV (monoclonal ou policlonal), inibidores de polimerase RNA, inibidores de protease, inibidores de IRES, inibidores de helicase, compostos anti-sentido, ribozimas e qualquer combinação dos mesmos.
Quando conjugado com uma fração detectável, uma molécula relacionada a anticorpo ou anticorpo monoclonal da invenção pode encontrar aplicações em uma variedade de métodos não terapêuticos, por exemplo, no diagnóstico e/ou prognóstico de certas doenças como cânceres. Realmente, o nível de expressão de claudin-1 foi demonstrado como sendo um marcador de diagnóstico ou prognóstico útil para cânceres diferentes. Por conseguinte, em outro aspecto, a presente invenção provê o uso de uma molécula relacionada a anticorpo ou anticorpo monoclonal inventivo para a fabricação de composições ou kits para o diagnóstico e/ou prognostico de certos cânceres.
Em um aspecto relacionado, a presente invenção provê um método para detectar Claudin-1 em uma amostra biológica que compreende contatar a amostra biológica com um anticorpo inventivo por um tempo e sob condições que permitem que um complexo Claudin-lanticorpo forme entre o anticorpo e claudin-1 presente na amostra biológica; e detectar (e/ou quantificar) a presença de qualquer complexo Claudin-l-anticorpo formado. O anticorpo inventivo (ou molécula relacionada a anticorpo utilizado em tal método é preferivelmente conjugado com uma fração detectável. Em certas modalidades, a amostra biológica é obtida de um sujeito, por exemplo, um sujeito com suspeita de ter câncer. 0 diagnóstico ou prognóstico pode ser fornecido com base na presença, ausência ou quantidade de complexo de anticorpo-Claudin-1 formado, por exemplo, após comparação com resultados obtidos sob condições idênticas para uma amostra biológica obtida de um sujeito saudável.
Esses e outros objetivos, vantagens e características da presente invenção se tornarão evidentes para aqueles com conhecimentos comuns na técnica tendo lido a seguinte descrição detalhada das modalidades preferidas.
A figura 1 é um conjunto de dois gráficos que ilustram a ligação especifica de soro CLDN-1 anti-humano de rato a CLDN-1 expresso em células CHO. O soro policlonal anti-CLDN-1 dirigido contra o loop de ectodominio de CLDN-1 foi criado por imunização genética de ratos Wistar utilizando um plasmideo que abriga cDNA de CLDN-1 humano (vide exemplo 1). Células CHO foram transfectadas com pcDNA-CLDN-1 ou um vetor de controle (pcDNA). Citometria de fluxo de CLDN-1 ou células CHO não permeabilizadas transfectadas de controle incubadas com soro policlonal CLDN-1 anti-humano de rato e IgG anti-rato conjugado com PE demonstrou interação especifica de anticorpos anti-CLDN-1 com CLDN-1 humano (figura 1B). ao contrário, nenhuma interação foi observada em células CHO transfectadas com o vetor de controle e incubadas com soro anti-CLDN-1 (figura IA) .
A figura 2 é um conjunto de três gráficos que demonstra a interação de anticorpos anti-CLDN-1 com o ectodominio de CLDN-1 em células de hepatoma humanas Huh7.5.1 (figura 2A) , hepatócitos humanos (figura 2B) . a expressão de superficie de célula de CLDN-1 foi determinada por citometria de fluxo utilizando soro de CLDN-1 anti- 5 humano de rato ou soro pré-imune de controle (vide o exemplo 1). Histogramas correspondendo à expressão de superficie de célula das moléculas de superficie de célula respectivas (curvas abertas) são sobrepostas com histogramas de células incubadas com o controle de isotipo 10 apropriado (curvas sombreadas cinza). O soro de CLDN-1 anti-humano de rato detectou especificamente CLDN-1 na superficie de célula de células Huh7.5.1 de hepatoma humano, e hepatócitos primários humanos.
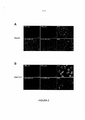
A figura 3 é um conjunto de imagens de imunofluorescência que mostram expressão de CLDN1 em células CaCo2 (A) e Huh7.5.1 (B) . os painéis inferiores da figura 3A e da figura 3B mostram células Caco2 e Huh7.5.1, respectivamente, que foram coloridas para CLDN1 utilizando anticorpos policlonais anti-CLDNl dirigidos contra os 20 ectodominios de CLDNl ("pAb anti-CLDNl") e um anticorpo anti-CLDNl comercial dirigido contra o dominio de terminal- C intracelular ("anti-CLDNl mAb") e para o núcleo utilizando DAPI, como descrito no exemplo 1. Os controles são mostrados nos painéis superiores da figura 3A e figura 3B, onde células Caco2 e células Huh7.5.1, respectivamente, foram incubadas com IgG policlonal de rato ("pAb de controle"), IgG monoclonal de camundongo ("mAb de controle") e DAPI. As barras de escala representam 10 μm.
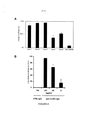
A figura 4 é um conjunto de dois gráficos que mostram a inibição de infecção por HCV (infecção por HCVcc Jcl) por anticorpos anti-CLDN-1 (antisoro anti-CLDN-1 policlonal de rato) . A figura 4A mostra os resultados obtidos para células Huh7.5.1 que foram pré-incubadas por 1 hora a 37 °C com soro de rato anti-CLDN-1 (diluição 1/50) ou soro de controle ("rato pan") antes da infecção com HC1 HCVcc por 3 horas a 37 °C. a infecção por HCV foi avaliada por quantização de RNA HCV em lisados de células Huh7.5.1 infectadas 72 horas após infecção. 0 RNA total foi isolado e RNA HCV foi quantificado por pRT-PCR. A figura 4B mostra a inibição de infecção por HCVcc Jcl por imunoglobulina anti-CLDN-1 purificada. IgG anti-CLDN-1 foi purificada de soro no. 2 e adicionada a células Huh7.5.1 como descrito no exemplo 1 (CTRL - IgG de controle). A infecção por HCV foi avaliada por quantificação de RNA HCV como descrito acima. Os resultados são expressos como % média de infectividade por HCVcc ± SD de determinações duplicatas de um entre pelo menos dois experimentos independentes.
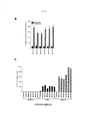
A figura 5(A) mostra a inibição de dependência de dose de infecção por HCVcc Luc-Jcl por anticorpos anti-SR- BI, anti-CD81 e anti-CLDNl. O uso de concentrações de anticorpo que bloquearam de for sub-máxima infecção por HCV permitiu a observação de efeitos aditivos ou sinergistas. Células Huh7.5.1 foram pré-incubadas por 1 hora a 37°C com mAn anti-CD81 (0,1 e 0,05 μg/mL) , mAb de camundongo de controle (mlgG: 0,1 e 0,05 μg/mL), soro de rato-anti-SR-BI (1/200, 1/400 e 1/800), soro de anti-CLDNl de rato (1/100, 1/200, 1/400) ou soro pré-imune de rato de controle (CTRL: 1/200) antes da infecção com Luc-Jcl HCVcc por 4 horas a 37°C. a infecção por HCV foi avaliada por medição de atividade de luciferase 48 horas pós-infecção. Os dados são expressos como percentagem de infectividade por HCVcc Luc- Jcl na ausência de anticorpo. Médias ± SD de quatro experimentos independentes executados em duplicata são mostrados. A figura 5(B)-(D) é um conjunto de quatro gráficos que mostram o efeito aditivo de anticorpos anti- SR-BI, anti-CD81 e anti-CLDNl na inibição de entrada de HCVcc. Células Huh7.5.1 foram pré-incubadas por 1 hora a 37°C com anti-SR-BI de rato (1/400, 1/800), anti-CLDNl de rato (1/200, 1/400) e anti-CD81 de camundongo (0,05, 0,1 μg/mL), quer individualmente (barras pretas) ou em combinação (barras cinza) antes da infecção com Luc-JCl HCVcc por 4horas a 37°C. a infecção por HCVcc foi avaliada como descrito em (A) . os dados são expressos como percentagem de infectividade por Luc-Jcl HCVcc n ausência de anticorpo. Médias ± SD de quatro experimentos independentes executados em duplicata são mostrados.
A figura 6(B) mostra a cinética de inibição de entrada de HCVcc em células de hepatoma humano por mAb anti-CD81 (■), soro anti-SR-BI de rato (♦), soro anti-CLDNl (À) OU soro de rato de controle (Δ). A inibição de entrada de HCVcc Luc-JCl nas células HJuh7.5.1 por soro anti-CLDNl de rato (1/100), soro anti-SR-BI de rato (1/100), soro de controle de rato (1/100) ou anticorpo monoclonal anti-CD81 (5 μg/mL) foi executado como mostrado no desenho esquemático da montagem experimental apresentada na figura 6(A). após ligação de virus a células alvo, células foram lavadas, e inibidores foram adicionados a cada 20 minutos por 120 minutos a 37 °C para permitir que a entrada prossiga. Linhas tracejadas indicam os intervalos de tempo onde inibidores estavam presentes. A atividade de luciferase foi determinada 48 horas após e é expressa em relação a infecções de controle executadas do mesmo modo porém sem adição de inibidores. Os resultados em (B) São expressos como percentagem de infectividade por HCVcc Luc- Jcl na ausência de anticorpo. Médias + SD de um de três experimentos executados em duplicata são mostradas.
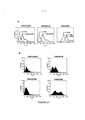
A figura 7 é um conjunto de cinco gráficos que mostram os resultados de análise de citometria de fluxo para soros obtidos de 5 ratos imunizados contra Claudin-1 humano (como descrito no exemplo 2} , As curvas pretas mostram resultados em células de mamíferos (BOSC23) transfectadas de forma transiente com um vetor de expressão Claudin-1 humano e as curvas vermelhas com um cDNA irrelevante. Um deslocamento da curva preta para a direita indica positividade. Anticorpos foram detectados com um anticorpo IgG anti-rato rotulado com PE (FL2).
A figura 8 é um gráfico que mostra resultados da análise de inibição de infecção com HCV infeccioso recombinante (HCVcc Luc-Jcl) com sobrenadantes de hibridoma contendo anticorpos anti-CLDN-1 (cujos nomes são indicados no eixo geométrico-x) . os sobrenadantes de hibridoma foram obtidos como descrito no exemplo 2. Os resultados são expressos como percentagem de infecção por HCVcc Luc-Jcl na presença ou ausência de sobrenadante de hibridoma (com infecção na presença de PBS=100%). OM-3E5, OM-6D9, OM-7C11, OM-4A4, OM-6E1, OM-7D3, OM-7D4, OM-7C8 e OM-8A9 mostraram uma inibição marcada de infecção por HCV, enquanto OM-5A1, OM-6G10, e OM-5A8 não mostraram efeito. 0 controle negativo corresponde a células não infectadas.
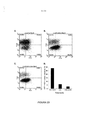
A figura 9(A) é um conjunto de oito gráficos que mostra os resultados de análise de citometria de fluxo para sobrenadantes de anticorpo monoclonal obtidos de linfóçitos agrupados de ratos imunizados contra Claudin-1 humano (como descrito no exemplo 2), As curvas pretas mostram resultados em células de mamifero transfectadas de forma transiente com um vetor de expressão de Claudin-1 humano (pCMV-SPORTβ- CLDN1) e as curvas vermelhas com um cDNA irrelevante (pCMV- SPORT6) . Um deslocamento da curva preta para a direita indica positividade. Os anticorpos foram detectados com um anticorpo IgG anti-rato rotulado por PE (FL2.). Os eixos geométricos x e y mostram intensidades de fluorescência média e números relativos de células coloridas, respectivamente. Ã figura 9(B) é um gráfico que mostra a ligação especifica de seis anticorpos CLDN1 anti-humanos monoclonais a CLDN1 expresso na superfície de célula de células CHO transfectadas estudadas por citometria de fluxo. Células CHO foram transfectadas com pCMV-SPORTβ- CLDN1 (barras listradas) ou vetor de controle (pCMV-SPORTβ; barras pretas). A figura 9(C) é um gráfico que mostra a ligação dos seis anticorpos monoclonais à CLDN1 expresso em superfície de célula, em células de hepatoma Huh 7.5.1 e negativo em células BOSC23. Os resultados são mostrados como as unidades fluorescentes relativas médias (RFU) calculadas para cada experimento executado em duplicata, A figura 9(D) mostra o imageamento de CLDN1 de superfície de célula em células Huh7.5.1 não permeabilizados vivos por um anticorpo monoclonal anti-CLDNl. As células Huh7.5.1 foram incubadas com controle de isotipo de rato ou anticorpos 0M- 7D3-A3 anti-CLDNl (10 μg/mL), um anticorpo secundário antiratoconjugado com Cy5 e analisado como descrito no exemplo 2. Núcleos de células foram coloridos com DAPI. A figura 9(E) é um gráfico que mostra a ligação dos seis anticorpos monoclonais a CLDN1 expresso em superfície de célula em hepatócitos cinomolgos primários estudados por citometria de fluxo.
A figura 10 é um conjunto de dois gráficos que mostram as propriedades de ligação de mAbs anti-CLDNl a linhagens de células permissivas de HCV Huh7.5.1. células Huh7.5.1 foram incubadas com concentrações crescentes de Mabs anti-CLDNl como descrito no exemplo 2. A ligação de 20 mAb foi relevada por citometria de fluxo utilizando mAb de IgG anti-rato conjugado com PE. Como controle, um IgG2 humano casado com. isotipo foi utilizado.
A figura 11 é um gráfico que mostra a inibição dependente de dose de infecção por HCVcc por anticorpos anti-CLDNl utilizando virions infecciosos contendo as proteinas estruturas da cepa J6 de genótipo 2a HCV (Luc- Jcl) e a cepa Conl de genótipo lb (Luc-Conl) . (A) células Huh7.5.1 foram pré-incubadas com concentrações crescentes de anti-CLDNl de rato ou anticorpos de controle de isotipo (CTRL Igl) por 1 hora a 37°C antes de infecção com Luc-Jcl HCVcc (genótipo 2a), (B) células Huh7.5.1 foram pré- incubadas com anti-CLDNl de rato (10 μg/μL de anticorpos OM6E1-B5; OM-7D3-B3; OM-8A9-A3), anti-CD81 (10 μg/μL) ou anticorpos de controle de isotipo (CTRL IgG; 10 (μg/μL) ou na ausência de anticorpo (CTRL) antes da incubação com HCVcc Luc-Conl por 4 horas a 37°C. HCVcc Luc-Con 1 contém as proteinas estruturais de HCV da cepa de genótipo lb.Conl. a infecção por HCV foi avaliada por medição de atividade de luciferase 48 horas após infecção como descrito no exemplo 2. Média ± SD a partir de um experimento representativo executado em triplicata é mostrado.
A figura 12 é um conjunto de gráficos que mostra que anticorpos monoclonais anti-CLDNl neutralizam de forma cruzada glicoproteinas de envelope contendo HCVpp derivadas dos genótipos de HCV principais. Cepas diferentes de glicoproteinas de envelope contendo HCVpp à base de MLV de cepas H77 (genótipo la) , HCV-J (genótipo lb) , JFH1 (genótipo 2a), UKN3a 1.28 (genótipo 3), UKN4a 21.16 (genótipo 4), UKN 5.14.4 (genótipo 5), e UKN 6.5.340 (genótipo 6) . Pseudo-particulas VSV foram utilizadas como controle. HCVpp e VSVpp foram produzidas como descrito no exemplo 2. Células Huh7 foram pré-incubadas com concentrações crescentes de anti-CLDNl de rato ou anticorpos de controle de isotipo de rato por 1 hora a 37°C antes da infecção com HCVpp ou VSVpp por 4 horas a 37°C. a infecção por HCVpp e VSV foi avaliada por medição de atividade de luciferase 72 horas após infecção como descrito no exemplo 2. Médias ± SD de um experimento representativo executado em triplicata são mostradas.
A figura 13 é um conjunto de gráficos que mostra a inibição de infecção por HCVpp em hepatócitos humanos primários. Glicoproteinas de envelope que contém HCVpp a base de HIV de cepas HCV H77 (genótipo la), HCV-J (genótipo lb) , JFH-1 (genótipo 2a), UKN3A.1.28 (genótipo 3) foram produzidos como descrito no exemplo 2. Hepatócitos humanos primários foram pré-incubados com anti-CLDNl de rato ou anticorpos de controle de isotipo de rato (10 μg/mL) por 1 hora a 37°C antes da infecção com HCVpp por 4 horas a 37°C. a infecção por HCVpp foi avaliada por medição de atividade de luciferase 72 horas após infecção como descrito no exemplo 2. Médias i SD de um experimento representativo executado em triplicate são mostradas.
A figura 14 mostra que anticorpos monoclonais anti- CLDNl neutralizam de forma cruzada a infecção por quasiespécie de HCV em dois pacientes individuais com infecção crônica por HCV (vide o exemplo 2). A figura 14(A) mostra a distribuição relativa das três variantes denominadas VJ, VI, VK (subtipo lb) no primeiro paciente infectado com HCV com base em alinhamento de sequências de HVR1. Aminoácido deduzido de domínios selecionados de glicoproteínas de envelope é mostrado à direita. Alterações de aminoácido são indicadas em letras em negrito vermelho. As figuras 14(B)-(C) são um conjunto de dois gráficos que mostram a inibição de infecção de glicoproteínas de envelope contendo HCVpp de quasiespécie virai nesse paciente por anti-CLDNl OM-7D3 (25 μg/mL) em células Huh7.5.1 (B) e hepatócitos humanos primários (C) . a figura 14 (D) mostra a distribuição relativa das variantes (denominadas VA-VY; subtipo 1b) em um segundo paciente com infecção crônica por HCV com base em alinhamento de seqüências E1E2 completas. A figura 14(E)-(F) é um conjunto de dois gráficos que mostra infecção de células Huh7.5.1 por glicoproteínas de envelope contendo HCVpp de quasiespécie viral do segundo paciente com hepatite crônica C (D) esua neutralização por anti-CLDNl OM-7D3 (25 μg/mL) (E) . a infecção de HCVpp foi analisada como descrito no exemplo 2. A neutralização por anticorpo anti-CLDNl foi somente avaliada para HCVpp derivada de quasiespécie com infectivida.dedetectável. Variantes virais contendo um códon de parada são indicados por um asterisco. Médias ± SD de um experimento representativo executado em triplicate são mostradas. ND - não feito; CTRL IgG - anticorpo de controle de isotipo de rato.
A figura 15 é um conjunto de dois gráficos que mostram a prevenção de infecção por HCV de glicoproteinas de envelope contendo HCVpp de pacientes com escapamento de respostas de neutralizar hospedeiro e reinfecção do enxerto de figado. Glicoproteinas de envelope contendo HCVpp (cepas denominadas VD, VH, VK) de três pacientes diferentes com escapamento de respostas de neutralização de hospedeiro e reinfecção do enxerto de figado (HCV subtipo lb) foram produzidos como descrito no exemplo 2. A prevenção de infecção por HCVpp foi avaliada por pré-incubar hepatócitos humanos primários com anticorpo anti-CLDNl OM-7D3 (25 μg/ml) ou anti-CD81 ou anticorpos de controle de isotipo (CTRL) (25 μg/ml) por 1 hora a 37QC antes da infecção com HCVpp por 4 horas a 37°C. a infecção foi analisada como descrito no exemplo 2. Médias ± SD de um experimento representativo executado em triplicata são mostradas.
A figura 16 é um conjunto de gráficos que mostra a falta de toxicidade de anticorpos monoclonais anti-CLDNl em células Huh7.5.1 e hepatócitos humanos primários (PHH). Os efeitos citotóxicos em células foram avaliados em triplicatas por metabolização de MTT. As células Huh7.5.1 (A) e hepatócitos humanos primários de três doadores diferentes (B-D) foram incubadas com anticorpo monoclonal de rato, anti-CLDNl OM-7D3-B3 (10 μg/ml), flavopiridol (10 μM) ou composto C (20 μM) por 48horas e analisadas por metabolização MTT. A viabilidade relativa de células foi avaliada em comparação com hepatócitos humanos primários incubados simulados ou células Huh7.5.1 (=100%) (D) composto C (0,01 - 100 μM) , anti-CLDNl anticorpo OM-7D3 (0.01 - 100 μM) ou anticorpo de controle de isotipo foram adicionados a hepatócitos humanos primários em doses crescentes e toxicidade avaliada como descrito nos painéis (B) e (C) .
A figura 17 é um conjunto de gráficos que mostra a competição cruzada de dois anticorpos monoclonais anti- CLDNl em estudos de infecção e ligação. Figura 17(A): competição entre mAbs anti-CLDNl foi medida utilizando um ELISA baseado em célula. Células Huh7.5.1 foram incubadas com 0,1 ug/mL de mAb anti-CLDNl biotinilado (0M-8A9-A3 - painel superior ou OM-7D3-B3- painel inferior) juntamente com concentrações crescentes de mAbs anti-CLDNl não rotulados como concorrentes, após lavagem de células em PBS, a ligação de anticorpo biotinilado foi detectada por incubação com estreptavidina rotulada com peroxidase de raiz forte. A ligação foi medida como unidades de fluorescência relativa (RED). As curvas determinadas por medição de ligação na presença de um controle casado de isotipo (mAb de controle negativo) foram comparadas com aquelas determinadas na presença do anticorpo concorrente. Figura 17(B): a competição cruzada entre o painel inteiro de anticorpos monoclonais anti-CLDNl. A competição cruzada foi analisada como mostrado no painel A utilizando 0,1 μg/mL de mAb anti-CLDNl biotinilado (mostrado no eixo geométrico x) e 10 μg/ml do anti-CLDNl não rotulado concorrente ou um mAb de controle de isotipo (irr anticorpo de controle) (mostrado no eixo geométrico y) . a ligação de mAb anti-CLDNl biotinilado ocorreu somente na presença de anticorpo de controle de isotipo. Figura 17(C): a competição cruzada de anticorpos em estudos de infecção. Células Huh7.5.1 foram pré-incubadas com anti-CLDNl de rato ou anticorpos de controle de isotipo por 1 hora a 37°C antes de infecção com HCVcc Luc-Jcl como descrito no exemplo 2. Para estudar competição cruzada, baixas concentrações de rnAbs anti-CLDNl (0,5 μg/ml) foram adicionados simultaneamente antes da infecção por HCV. O uso de concentrações de anticorpo que bloquearam de forma sub-máxima infecção por HCV permitiu observação de efeitos aditivos ou sinergistas. O efeito de combinações de anticorpo ê indicado por um "+" (concentração final 1 ug/ml) (barras listradas).
A figura 18 é um conjunto de gráficos que mostram que anticorpos anti-CLDNl monoclonais se ligam a um epitopo que é fortemente dependente da conservação do motivo claudin altamente conservado: W(30)-GLW(51)-C(54)-C(64). A ligação de anticorpo foi realizada como descrito no exemplo 2 utilizando plasmideos pQCXIN-hClaudin-1 codificando para CLDN1 do tipo selvagem ou CLDNl contendo mutações definidas indicadas no eixo geométrico x. a ligação de anticorpos anti-CLDNl monoclonais (OM-7D3-B3 (A) e OM-8A9-A3 (B) ) a CLDNl mutante em relação à ligação a CLDN1 do tipo selvagem é mostrada (barras pretas). A expressão adequada do CLDNl mutante e do tipo selvagem em células Bosc transfectadas de forma transiente foi confirmada por análise citométrica de fluxo de niveis de expressão HA-tag e anticorpo anti-HA (barras abertas) exceto para I32A mutante onde o tag HA estava ausente e a expressão de CLDN1 foi avaliada. A ligação de anticorpo anti- HA a HA de CLDN1 mutante em relação a HA de CLDN1 do tipo selvagem é mostrada como controle interno para a expressão de CLDN1 mutante (barras abertas).
A figura 19 é um gráfico que mostra a ligação dos seis anticorpos monoclonais à expressão de superfície de célula de CLDN1 em células de hepatoma Huh7.5.1 humanas e células de hepatoma Hepa 1.6 de camundongo estudadas por citometria de fluxo. Os resultado são mostrados como a média fluorescente relativa e cada experimento foi executado em duplicata. Um anticorpo monoclonal anti-CD81 foi utilizado como controle positivo.
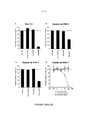
A figura 20 é um conjunto de gráficos que mostram a inibição dependente de dose de ligação E2 a linhagens de células permissivas por anticorpos anti-CLDNl. (A) ligação de glicoproteína E2 recombinante a células Huh7.5.1 permissivas. Células Huh7.5.1 foram pré-incubadas com soro pré-imune de rato de controle (CTRL: painel esquerdo) ou anticorpos anti-CLDNl de rato (painel direito) diluído 1/100 por 1 hora em temperatura ambiente. A ligação de E2 foi detectada por citometria de fluxo. As células incubadas na ausência de anticorpo e E2 (PBS) serviram como controle negativo (NC - histogramas .sombreados claros) . Um experimento representativo é mostrado. (B) ligação de glicoproteína E2 recombinante a células Huh7.5.1 permissivas. Células Huh7.5.1 foram pré-incubadas com anticorpos anti-CD81 de rato, anti-SR-BI de rato e anti- CLDNl de rato ou soro pré-imune de rato de controle (todos diluídos 1/100) por 1 hora em temperatura ambiente. A ligação a E2 foi detectada por citometria de fluxo. Os resultados são expressos como percentagem de ligação de E2 na ausência de anticorpo (BBS). Médias ± SD de quatro experimentos independentes executados em duplicata são mostrados. (C) inibição dependente de dose de ligação E2 a células Huh7.5.1 por anti-CLDNl. Células Huh7.5.1 foram pré-incubadas com diluições diferentes de anticorpos anti- CLDNl de rato policlonal (quadrados cinza) ou soro pré- imune de rato de controle (losangos pretos). Os resultados são expressos como percentagem de ligação de E2 na ausência de anticorpo. Médias ± SD de quatro experimentos independentes executados em duplicata são mostrados. (D) ligação de glicoproteína El recombinante a células Huh7.5.1 permissivas. Células Huh7.5.1 foram pré-incubadas com heparina, anti-CD81 de camundongo (JS-81; 5 μg/mL), IgG de camundongo de controle (CTRL) (5 μg/mL), anti-CLDNl de rato (1/100), soro pré-imune de rato (1/100) por 1 hora em temperatura ambiente. A ligação de El foi detectada por citometria de fluxo. Os resultados são expressos como percentagem de ligação El na ausência de anticorpo (PBS)- Médias ± SD de dois experimentos independentes executados em duplicata são mostrados. Os resultados são expressos como percentagem de ligação E2 na ausência de anticorpo (PBS) . Médias ± SD de dois experimentos independentes executados em duplicata são mostrados. ***P<0,0001 (teste 10 t) . (E) Ligação de HCVcc a células Huh7.5.1 permissivas. Células Huh7.5.1 foram pré-incubadas com heparina, anti- CLDNl de rato, anti-SR-BI de rato ou soro pré-imune de rato de controle (PI) (todos diluídos 1/100) por 1 hora em temperatura ambiente antes da incubação com HCVcc (cepa 15 JC1) que tinha sido parcialmente purificado de sobrenadantes de cultura de célula utilizando ultra centrifugação de gradiente. Após incubação com HCVcc, HCVcc não ligado foi removido por lavagem de células com PBS. A ligação de HCVcc foi então quantificada por RT-PCR de RNA 20 HCV ligado por célula, que é indicado no eixo geométrico y.
A figura 21 é um conjunto de gráficos que mostra ligação celular de glicoproteína de envelope E2 a células CHO expressando CD81 e SR-BI porém não células que expressam CLDNl. (A) expressão de fatores de entrada humana em células CHO transfectadas. Células CHO foram transfectadas com plasmideos de expressão que codificam CLDNI humano, SR-BI ou CD81 como descrito no exemplo 3. Células CHO transfectadas foram analisadas por citometria de fluxo utilizando controle de rato (CTRL), anti-CLDNl de rato (painel esquerdo), anti-SR-BI de rato (painel médio) ou IgG de controle de camundongo e anti-CD81 (JS-81; painel direito). (B) ligação de glicoproteina de envelope E2 a células CHO que expressam fatores de entrada de HCV humano. Células CHO foram transfectadas com plasmideo de expressão individuais codificando CLDN1 humano, SR-BI ou CD81 como indicado. A ligação E2 celular foi analisada por citometria de fluxo. Um experimento representativo executado em duplicata é mostrado.
A figura 22 é um conjunto de dois gráficos que mostram inibição anti-CLDNl de associação de co-receptor CD81-CLDN1 utilizando análise FRET. Células HEK293T co- transfectadas para expressar AcGFP, CD81 e DsRED.CDδl, AcGFP.CLDN1 e DsRED.CD81, ou AcGFP.CLDN1 e DsRED.CLDNl foram semeadas sobre laminulas de vidro e tratadas com soros anti-CLDNl ou pré-imune por 1 hora. As células foram fixas, imageadas por microscopia confocal de varredura laser e FRET entre proteínas doadoras AcGFP e aceptoras DsRED foi medido. A percentagem de FRET é definida como a frequência de pixels que demonstram FRET relativo ao número total de pixels analisados na membrana de plasma de dez células. ***P<0.0001, **P<0.01 (teste t) . AcGFP.CLDNl e DsRED.CLDNl em locais intracelulares (pretos) e de membrana de plasma (brancos) em células tratadas com anti-CLDNl e não tratadas foram quantificados e a percentagem de CLDN1 em cada local determinada.
A figura 23 é um conjunto de gráficos que mostra a inibição de transmissão de célula para célula de HCV por um anticorpo monocolonal anti-CLDNl. Células produtoras de Huh7.5.1 eletroporadas Hcl foram cultivadas em conjunto por 24 horas com células receptoras Huh7.5 GFP+ na ausência de anticorpos (A) ou na presença de anticorpo anti-CD81 (10 mg/ml) para bloquear transmissão livre de células HCV (B) ou na presença de anti-CD81 e anti-CLDNl para bloquear célula HCV livre e transmissão de célula para célula (C) . em cada painel, os quadrantes inferiores contêm células não infectadas (esquerdo inferior representa células GFP- HCV-, direita inferior representa células HCV- GFP+); esquerdo superior representa células produtoras infectadas por GFP- HCV+; e direito superior representa células receptoras GFP+ HCV+ recentemente infectadas. No gráfico em pontos, FL1- altura (FL1-H) representa a intensidade de fluorescência de GFP e FL2-altura (FL2-0H) representa a intensidade de fluorescência de anticorpos anti-núcleo/PE (A-C). a freqüência relativa de células receptoras GFP+ HCV+ sob os diferentes tratamentos é representada em (D). os resultados de um experimento representativo são mostrados. A incubação de células com anticorpos de controle de isotipo de rato foi mostrada como não tendo efeito sobre o nivel de infecção por HCV (dados não mostrados).
A figura 24 é um gráfico que mostra a inibição de infecção por HCV por um anticorpo monoclonal anti-CLDNl (7D3) adicionado pós-infecção. Células Huh7.5.1 foram infectadas com HCVcc Luc-Jcl. Quatro horas após infecção, o anticorpo monoclonal anti-CLDNl (7D3) ou um anticorpo monoclonal de controle de isotipo de rato (50 μg/mL) foram adicionados a células. A infecção por HCV foi quantificada por expressão repórter de luciferase nos dias 3, 5, 7 e 9 pós-infecção e é representada como carga viral (Logio RLU) . O meio foi alterado a cada 2 dias com substituição de anticorpos novos (50 μg/mL). O limite para detecção positiva de carga viral nesse ensaio é de 800 RLU (linha pontilhada). Os resultados de um experimento representativo são mostrados. Os valores são médias de duplicatas. Abreviaturas: RLU - unidades light relativas.
Em todo relatório descritivo, vários termos são empregados que são definidos nos seguintes parágrafos.
Como utilizado aqui, o termo "sujeito" se refere a um ser humano ou outro mamifero (por exemplo, primata, cão, gato, cabra, cavalo, porco, camundongo, rato, coelho e similar) que pode ser o hospedeiro do virus de hepatite C (HCV) porém pode estar infectado ou não com o virus, e/ou pode sofre ou não de uma doença relacionada à HCV. Sujeitos não humanos podem ser transgênicos ou animais de outro modo modificados. Em muitas modalidades da presente invenção, o sujeito é um ser humano. Em tais modalidades, o sujeito é frequentemente mencionado como "individuo". O termo "indivíduo" não indica idade específica, e desse modo abrange recém-nascidos, crianças, adolescentes e adultos.
Como utilizado aqui, o termo "HCV" se refere a qualquer genótipo, subtipo, isolado e/ou quasiespécie de HCV. Genótipos de HCV incluem, porém não são limitados a, genótipos 1, 2, 3, 4, 5 e 6; subtipos de HCV incluem, porém não são limitados a subtipos la, lb, 2a, 2b, 2c, 3a, 4a-f, 5a e 6a.
Os termos "afligido com HCV" ou "infectado com HCV" são utilizados aqui de modo intercambiável. Quando utilizados em referência a um sujeito, se referem a um sujeito que pelo menos uma célula que é infectada por HCV.
O termo "infecção por HCV" se refere à introdução de informações genéticas de HCV em uma célula alvo, como por fusão da membrana de célula alvo com HCV ou uma célula positiva de glicoproteína de envelope HCV.
Os termos"doença relacionada à HCV" e "doença associada à HCV" são aqui utilizadas de modo intercambiável. Refere-se a qualquer doença ou distúrbio conhecido ou que se suspeita estar associado a e/ou causado, direta ou indiretamente, por HCV. Doenças relacionadas à HCV (ou associadas à HCV) incluem, porém não são limitadas a, uma ampla variedade de doenças de fígado, como estado de veículo subclínico de hepatite aguda, hepatite crônica, cirrose e carcinoma hepatocelular. O termo inclui sintomas e efeitos colaterais de qualquer infecção por HCV, incluindo infecções latentes, persistentes e subclínicas, quer a infecção seja clinicamente aparente ou não.
O termo "tratamento" é utilizado aqui para caracterizar um método ou processo que é direcionado a (1) retardar ou evitar o início de uma doença ou condição (por exemplo, infecção por HCV ou doença relacionada à HCV); (2) diminuir ou parar o avanço, agravação ou deterioração dos sintomas da doença ou condição; (3) ocasionar melhora dos sintomas da doença ou condição; ou (4) curar a doença ou condição. Um tratamento pode ser administrado antes do inicio da doença ou condição, para uma ação profilática ou preventiva. Alternativamente ou adicionalmente, um tratamento pode ser administrado após inicio da doença ou 5 condição para uma ação terapêutica.
Uma "composição farmacêutica" é definida aqui como compreendendo uma quantidade eficaz de pelo menos um anticorpo (ou um fragmento do mesmo) da invenção e pelo menos um excipiente ou veiculo farmaceuticamente aceitável.
Como utilizado aqui, o termo "quantidade eficaz" se refere a qualquer quantidade de um composto,a gente, anticorpo ou composição que seja suficiente para atender sua(s) finalidade(s) pretendida (s) , por exemplo, uma resposta medicinal ou biológica desejada em uma célula, 15 tecido, sistema ou sujeito. Por exemplo, em certas modalidades da presente invenção, a(s) finalidade(s) pode(m) ser: evitar infecção por HCV, evitar o inicio de uma doença relacionada à HCV, diminuir, aliviar ou parar o avanço, agravação ou deterioração dos sintomas de uma 20 doença relacionada à HCV (por exemplo hepatite crônica C, cirrose, e similar) ; ocasionar melhora dos sintomas da doença, ou curar a doença relacionada à HCV.
O termo "excipiente ou veículo farmaceuticamente aceitável" se refere a um meio de veículo que não interfere não eficácia da atividade biológica do(s) ingrediente (s) ativo(s) e que não é excessivamente tóxico para o hospedeiro na concentração na qual é administrado. 0 termo inclui solventes, dispersão, meios, revestimentos, agentes antibacterianos e antifúngicos, agentes isotônicos, e agentes retardadores de adsorção e similares. O uso de tais meios e agentes para substâncias farmaceuticamente ativas é bem conhecido na arte (vide, por exemplo, "Remington's Pharmaceutical Sciences", E.W. Martin, 18 Ed. , 1990, Mack Publishing Co.: Easton, PA, que é incorporado aqui a titulo de referência na integra).
O termo "anticorpo", como utilizado aqui, se refere a qualquer imunoglobulina (isto é, uma molécula de imunoglobulina intacta, uma porção ativa de uma molécula de imunoglobulina, etc.) que se liga a um epitopo especifico. O termo abrange anticorpos monoclonais e anticorpos policlonais. Todos os derivados e fragmentos dos mesmos, que mantêm capacidade de ligação especifica, são também incluidos no termo. O termo também cobre qualquer proteina tendo um dominio de ligação, que seja homólogo ou largamente homólogo a um dominio de ligação de imunoglobulina. Essas proteinas podem ser derivadas de fontes naturais, ou parcial ou totalmente sinteticamente produzidas.
O termo "ligação específica", quando utilizado com referência a um anticorpo, se refere a um anticorpo se ligando a um antígeno predeterminado. Tipicamente, o anticorpo se liga a uma afinidade de pelo menos 1 x 107 M’1, e se liga ao antígeno predeterminado com uma afinidade que é pelo menos duas vezes maior do que a afinidade para ligação a um antígeno não específico (por exemplo, BSA, caseína).
O termo "Claudin-1 humano ou CLDN1 humano" se refere a uma proteína tendo a sequência mostrada em NCBI número de acessão NP_066924, ou quaisquer variantes de ocorrência natural comumente encontrados em populações humanas permissivas de HCV. O termo "domínio extracelular" ou "ectodomínio" de Claudin-1 se refere à região da sequência de Claudin-1 que estende para dentro do espaço extracelular (isto é, o espaço fora de uma célula).
Os termos "célula suscetível" e "célula suscetível a HCV" são utilizados de forma intercambiável. Referem-se a qualquer célula que possa estar infectada com HCV. Células suscetíveis incluem,não são limitadas a, células hepáticas ou de fígado, células primárias, células de hepatoma, células CaCo2, células dendríticas, células placentais, células endometriais, células de linfonodo, células linfóides (células B e T) , células mononucleares de sangue periférico e monócitos/macrófagos.
O termo "evitar, inibir ou bloquear infecção por HCV" quando utilizado com referência a uma molécula relacionada a anticorpo ou anticorpo inventivo, significa reduzir a 5 quantidade de informações genéticas de HCV introduzidas em uma célula suscetível ou população de células suscetíveis em comparação com a quantidade que seria introduzida na ausência do anticorpo ou molécula relacionada a anticorpo.
O termo "isolado", como utilizado aqui em referência 10 a uma proteína ou polipeptídio, significa uma proteína ou polipeptídio, que em virtude de sua origem ou manipulação é separado de pelo menos alguns dos componentes com os quais é naturalmente associado ou com os quais ê associado quando inicialmente obtido. Por "isolado" ê alternativamente ou adicionalmente significado que a proteína ou polipeptídio de interesse é produzida ou sintetizada pela mão do homem.
Os termos "proteína", "polipeptídio" e "peptídeo" são utilizados aqui de forma intercambiável, e se referem a sequências de aminoácidos de uma variedade de comprimentos, 20 em suas formas neutras (não carregadas) ou como sais, e não modificadas ou modificadas por glicosilação, oxidação de cadeia lateral ou fosforilação. Em certas modalidades, a sequência de aminoácidos é uma proteína nativa de comprimento total. Em outras modalidades, a sequência de aminoácidos é um fragmento menor da proteína de comprimento total. Ainda em outras modalidades, a sequência de aminoácido é modificada por substituintes adicionais ligados às cadeias laterais de aminoácidos, como unidades de glicosila, lipídeos, ou íons inorgânicos como fosfates, bem como modificações referentes a conversões químicas das cadeias como oxidação de grupos de sulfidrila. Desse modo, o termo "proteína" (ou seus termos equivalentes) pretende incluir a sequência de aminoácidos da proteína nativa de comprimento total ou um fragmento da mesma, sujeito àquelas modificações que não mudam significativamente suas propriedades específicas. Em particular, o termo "proteína" abrange isoformas de proteína, isto é, variantes que são codificadas pelo mesmo gene, porém que diferem em seu PI ou MW, ou ambos. Tais isoformas podem diferir em sua seqüência de aminoácidos (Por exemplo, como resultado de variação alélica, junção alternativa ou proteólise limitada) ou na alternativa, podem se originar de modificação pós- translação diferencial (por exemplo, glicosilação, acilação, fosforilação) .
O termo "análogo", como utilizado aqui em referência a uma proteína se refere a um polipeptídio que possui uma função similar ou idêntica à da proteína porém não precisa necessariamente compreender uma seqüência de aminoácido que seja similar ou idêntica à seqüência de aminoácido da proteína ou uma estrutura que seja similar ou idêntica àquela da proteína. Preferivelmente, no contexto da presente invenção, um análogo de proteína tem uma seqüência 5 de aminoácidos que é pelo menos 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% ou 99% idêntico à seqüência de aminoácidos da proteína.
O termo "fragmento" ou o termo "porção", como utilizado aqui em referência a uma proteína, se refere a um 10 polipeptídio que compreende uma seqüência de aminoácidos de pelo menos 5 resíduos de aminoácidos consecutivos (preferivelmente, pelo menos aproximadamente: 10, 15, 20, 25, 30, 35, 40, 50, 60, 70, 80, 90, 100, 125, 150, 175, 200, 250 ou mais resíduos de aminoácidos) da seqüência de 15 aminoácidos de uma proteína. O fragmento de uma proteína pode possuir ou não uma atividade funcional da proteína.
O termo "biologicamente ativo", como utilizado aqui para caracterizar uma variante de proteína, análogo ou fragmento, se refere a uma molécula que partilha identidade 20 de seqüência de aminoácidos ou homologia suficiente com a proteína para apresentar propriedades similares ou idênticas à proteína. Por exemplo, em muitas modalidades da presente invenção, um fragmento biologicamente ativo de um anticorpo inventivo é um fragmento que retém a capacidade do anticorpo de se ligar ao domínio extracelular de Claudin-1.
O termo "homólogo" (ou "homologia") como utilizado aqui, é sinônimo do termo "identidade" e se refere à similaridade de sequência entre duas moléculas de polipeptídio ou entre duas moléculas de ácido nucléico. Quando uma posição nas duas sequências comparadas é ocupada pela mesma base ou mesmo resíduo de aminoácido, as moléculas respectivas são então homólogas naquela posição. A percentagem de homologia entre duas sequências corresponde ao número de posições homólogas ou casadas partilhadas pelas sequências divididas pelo número de posições comparadas e multiplicado por 100. Genericamente, uma comparação é feita quando duas sequências são alinhadas para fornecer homologia máxima. Sequências de aminoácidos homólogos compartilham de sequências de aminoácidos idênticas ou similares. Resíduos similares são substituições conservativas para, ou "mutações de ponto permitido" de, resíduos de aminoácidos correspondentes em uma sequência de referência. "Substituições conservativas" de um resíduo em uma sequência de referência são substituições que são física ou funcionalmente similares ao resíduo de referência correspondente, por exemplo, que têm um tamanho, formato, carga elétrica, propriedades químicas similares, incluindo a capacidade de formar ligações de hidrogênio ou covalentes, ou similares. substituições conservativas particularmente preferidas são aquelas que atendem os critérios definidos para uma "mutação de ponto aceito" como descrito por Dayhoff e outros ("Atlas of Protein Sequence and Structure", 1978, Nat. Biomed. Res. Foundation, Washington, DC, Suppl. 3, 22: 354-352).
Os termos "rotulado", "rotulado com um agente detectável" e "rotulado com uma fração detectável" são utilizados aqui de forma intercambiável. Esses termos são utilizados para especificar que uma entidade (por exemplo, um anticorpo) pode ser visualizado, por exemplo, após ligação a outra entidade (por exemplo, um antígeno). Preferivelmente, uma fração ou agente detectável é selecionado de tal modo que gere um sinal que possa ser medido e cuja intensidade está relacionada à quantidade de entidade ligada. Os métodos para rotular proteínas e polipeptídios, incluindo anticorpos, são bem conhecidos na técnica. Polipeptídios rotulados podem ser preparados por incorporação de ou conjugação com um rótulo, que é direta ou indiretamente detectável por meio espectroscópico, fotoquímico, bioquímico, imunoquímico, elétrico, óptico ou químico ou qualquer outro meio apropriado. Agentes detectáveis apropriados incluem porém não são limitados a, vários ligandos, radionuclides, corantes fluorescentes, agentes quimiluminescentes, microparticulas, enzimas, rótulos colorimétricos, rótulos magnéticos e haptenos.
Os termos "aproximadamente"e "cerca de" como utilizado aqui em referência a um número incluem genericamente números que estão compreendidos em uma faixa de 10% em qualquer direção do número (maior ou menor do que o número) a menos que de outro modo mencionado ou de outro modo evidente a partir do contexto (exceto onde tal número excederia 100% de um valor possível).
Como mencionado acima, a presente invenção provê anticorpos monoclonais que evitam infecção por HCV por interferir em interações de células hospedeiras-HCV e linhagens de células de hibridoma que secretam tais anticorpos monoclonais. I - Hibridomas e anticorpos monoclonais anti-Claudin- 1
Como mostrado na seção Exemplos abaixo, os presentes requerentes produziram anticorpos policlonais dirigidos contra o dominio extracelular de Claudin-1 humano por imunização genética utilizando um vetor de expressão que contém o gene CLDN 1 de comprimento total. Verificou-se que os anticorpos policlonais desse modo produzidos inibem eficientemente infecção por HCV utilizando sistemas baseados em HCVcc e HCVpp (vide o exemplo 1) . Em vistas desses resultados encorajadores, os requerentes utilizaram imunização genética de ratos e métodos de triagem para 5 gerar linhagens de células de hibridoma que secretam anticorpos monoclonais que se ligam especificamente ao domínio extracelular de Claudin-1 humano e inibem eficientemente infecção por HCV (vide exemplo 2).
Por conseguinte, a presente invenção provê linhagens de células de hibridoma que secretam anticorpos monoclonais que se ligam especificamente ao domínio extracelular de Claudin-1 humano, e em particular, a W(30)-GLW(51)-C(54)- 15 C(64), um motivo conservado localizado no primeiro loop extracelular de Claudin-1. Mais especificamente, a presente invenção prove oito de tais linhagens de células de hibridoma, geradas por imunização genética como descrito no exemplo 2 (Lohrmann, 2003). Essas linhagens de células de 20 hibridoma que são denominadas OM-4A4-D4, OM-7C8-A8, OM-6D9- A6, OM-7D4-C1, OM-6E1-B5, OM-3E5-B6, OM-8A9-A3 e OM-7D3-B3, foram depositadas em 29 de julho de 2008 no DSMZ (Deutsche Sammlung von Mikro-organismen und Zellkuturen GmbH, InhoffenstraBe 7 B, 38124 Braunschweig, Alemanha) sob os números de Acessão DSM ACC2931, DSM ÃCC2932, DSM ACC2933, DSM ACC2934, DSM ACC2935, DSM ACC2936, DSM ACC2937, e DSM ACC2938, respectivamente.
São também fornecidos pela presente invenção anticorpos monoclonais secretados por quaisquer dessas linhagens de células de hibridomas. Os métodos para a produção e isolamento de anticorpos monoclonais a partir de culturas de hibridoma são bem conhecidos na arte. Células de hibridoma são cultivadas utilizando métodos padrão, em meios de cultura apropriados como, por exemplo, D-MEM e meio RPMI-1640. Um anticorpo monoclonal anti-Claudin-1 pode ser recuperado e purificado de culturas de células de hibridoma por purificação de proteína A, precipitação de etanol ou sulfato de amónio, extração de ácido, cromatografia de permuta de cátion ou ânion, cromatografia de fosfocelulose, cromatografia de interação hidrofóbica, cromatografia de afinidade, como coluna de proteína A, cromatografia hidroxilapatita, cromatografia de lectina, ou qualquer combinação apropriada desses métodos. A cromatografia de líquido de desempenho elevado (HPLC) pode ser também empregada para purificação.
Cada dos anticorpos monoclonais anti-Claudin-1 secretados pelas linhagens de células de hibridoma da invenção foi determinado como sendo uma imunoglobulina do isotipo de cadeia pesada (H) r!gG2b e cadeia leve kappa (L) . entretanto, anticorpos monoclonais da presente invenção compreendem mais genericamente qualquer anticorpo monoclonal (ou fragmento do mesmo), que é secretado por uma 5 linhagem de células de hibridoma inventiva (ou uma linhagem de célula derivatizada) e que especificamente se liga ao dominio extracelular de Claudin-1 humano. Sem desejar ser limitado por qualquer teoria, acredita-se que a ligação de um anticorpo monoclonal ao dominio extracelular de Claudin- 10 1 em uma célula suscetível interfira em interações de células hospedeiras-HCV, e desse modo evita, inibe ou bloqueia HCV de entrar na célula e de infectar a célula.
Em vez de utilizar as hibridomas descritas aqui como uma fonte dos anticorpos, os anticorpos monoclonais podem 15 ser preparados por qualquer outro método adequado conhecido na arte. Por exemplo, um anticorpo monoclonal anti-Claudin- 1 inventivo pode ser preparado por métodos de DNA recombinantes. Esses métodos envolvem genericamente isolamento dos genes que codificam o anticorpo desejado, 20 transferência dos genes para um vetor apropriado, e expressão de volume em um sistema de cultura de células. Os genes ou DNA que codificam o anticorpo monoclonal desejado podem ser facilmente isolados e seqüenciados utilizando procedimentos convencionais (por exemplo, utilizando sondas de oligonucleotldeo que são capazes de ligar especificamente a genes que codificam as cadeias pesadas e leves de anticorpos de murino). As linhagens de células de hibridoma fornecidas aqui servem como uma fonte preferida desse DNA. Células hospedeiras apropriadas para produção recombinante de anticorpos monoclonais incluem, porém não são limitadas a, células hospedeiras de mamíferos apropriadas, como CHO, HeLa, ou CV1. Plasmídeos de expressão apropriados incluem, sem limitação, pcDNA3.1 Zeo, pIND(SPl), pREP8 (todos comercialmente disponíveis da Invitrogen, Carlsboad, CA, EUA), e similares. Os genes de anticorpo podem ser expressos através de vetores virais ou retrovirais, incluindo vetores baseados em MLV, vetores baseados em vírus de vacinia e similares. Anticorpos da presente invenção podem ser expressos como anticorpos de cadeia única. O isolamento e purificação de anticorpos monoclonais recombinantemente produzidos podem ser executados como descrito acima.
Em certas modalidades, um anticorpo monoclonal inventivo é utilizado em sua forma nativa. Em outras modalidades, pode ser truncado (por exemplo, através de divagem enzimática ou outro método apropriado) para fornecer fragmentos ou porções de imunoglobulina, em particular fragmentos ou porções que são biologicamente ativas. Fragmentos ou porções biologicamente ativos de um anticorpo monoclonal inventivo incluem fragmentos ou porções que retêm a capacidade do anticorpo monoclonal de 5 interferir nas interações de células hospedeiras-HCV, e/ou ligar especificamente ao dominio extracelular de Claudin-1 humano, e/ou inibir ou bloquear entrada de HCV em células suscetíveis, e/ou reduzir ou evitar infecção por HCV de células suscetíveis. Fragmentos ou porções biologicamente 10 ativos de anticorpos monoclonais inventivos descritos aqui são abrangidos pela presente invenção.
Um fragmento ou porções biologicamente ativas de um anticorpo monoclonal inventivo pode ser um fragmento ou porção Fab, uma porção ou fragmento F(ab')z, um dominio 15 variável, ou uma ou mais CDRs (regiões de determinação complementar) do anticorpo. Alternativamente, uma porção ou fragmento biologicamente ativo de um anticorpo monoclonal inventivo pode ser derivado da extremidade ou porção carboxila da proteina de anticorpo e pode compreender um 20 fragmento Fc, um fragmento Fd ou um fragmento Fv.
Fragmentos de anticorpo da presente invenção podem ser produzidos por qualquer método apropriado conhecido na arte que inclui, porém não é limitado a, clivagem anticorpos intactos) ou por técnicas recombinantes ou sintéticas. Fragmentos de anticorpo F(ab')s, Fab, Fv e ScFv (Fv de cadeia única) podem, por exemplo, ser expressos em e secretados a partir de células hospedeiras de mamifero ou de E. coli. Anticorpos também podem ser produzidos em uma variedade de formas truncadas utilizando genes de anticorpo nos quais um ou mais códons de parada foram introduzidos a montante do sitio de parada natural. As várias porções de anticorpos podem ser unidas quimicamente por técnicas convencionais, ou podem ser preparadas como uma proteina contigua utilizando técnicas de engenharia genética.
Anticorpos da presente invenção (ou fragmentos dos mesmos) podem ser produzidos em um a forma modificada, como uma proteína de fusão (isto é, uma molécula de imunoglobulina ou porção ligada a uma entidade de polipeptídio). preferivelmente, proteínas de fusão da invenção retêm a capacidade de ligação do anticorpo monoclonal em direção ao domínio extracelular de Claudin-1 humano. Uma entidade de polipeptídio a ser fundida a um anticorpo monoclonal inventivo, ou um fragmentos do mesmo, pode ser selecionada para conferir qualquer de diversas propriedades vantajosas à proteína de fusão resultante. Por exemplo, a entidade de polipeptídio pode ser selecionada para fornecer expressão aumentada da proteina d efusão recombinante. Alternativamente ou adicionalmente, a entidade de polipeptídio pode facilitar a purificação da proteina de fusão, por exemplo, por atuar como um ligando em purificação de afinidade. Um sitio de clivagem proteolitico pode se adicionado à proteina recombinante de modo que a sequência desejada possa finalmente ser separada da entidade de polipeptídio após purificação. A entidade de polipeptídio pode ser também selecionada para conferir uma estabilidade aperfeiçoada à proteína de fusão, quando a estabilidade é um objetivo. Os exemplos de entidades de polipeptídio apropriadas incluem, por exemplo, tags de poliistidina, que permitem â purificação fácil da proteína de fusão resultante em uma coluna de quelação de níquel. Glutatiiona-S-transferase (GTS), proteína de ligação de maltose B, ou proteína A são outros exemplos de entidades de polipeptídios apropriados.
Dependendo do uso pretendido, um anticorpo da invenção pode ser reconstruído de modo a otimizar estabilidade, solubilidade, meia-vida in vivo, ou capacidade de ligar alvos adicionais. Abordagens de engenharia genética bem como modificações químicas para realizar todas ou quaisquer dessas alterações são bem conhecidas na arte. Por exemplo, a adição, remoção e/ou modificação das regiões constantes de um. anticorpo são conhecidas por desempenhar um papel particularmente importante na biodisponibilidade, distribuição e meia-vida de anticorpos terapeuticamente administrados. A classe e sub-classe de anticorpo, determinada pela Fc ou região constante do anticorpo (que media funções efetoras), quando presentes, transmite propriedades adicionais importantes. Desse modo, anticorpos anti-Claudin-1 com domínios constantes reconfigurados, reprojetados ou de outro modo alterados são abrangidos pela presente invenção.
Proteínas de fusão adicionais da invenção podem ser geradas através das técnicas de shuffling DNA bem conhecidas na arte (vide, por exemplo, patentes US números 5.605.793; 5.811.238; 5.830.721; 5.834.252; e 5.837.458). shuffling de DNA pode ser empregado para modular a atividade de anticorpos, ou fragmentos dos mesmos, por exemplo, para obter anticorpos com afinidade mais elevada e taxas de dissociação mais baixas. Em tais métodos, polinucleotídeos codificando anticorpos da invenção podem ser alterados através de mutagênese aleatória por PCR propenso a erro, inserção de nucleotídeo aleatório ou outros métodos antes da recombinação. alternativamente, uma ou mais porções de um polinucleotídeo codificando um anticorpo inventivo podem ser recombinadas com um ou mais componentes, motivos, seções, partes, domínios fragmentos etc. de uma ou mais moléculas heterólogas.
Alternativamente, um anticorpo inventivo pode ser ligado a outro anticorpo, por exemplo, para produzir um anticorpo biespecífico ou multiespecifico. Por exemplo, um anticorpo monoclonal anti-Claudin-1 da presente invenção, ou um fragmento biologicamente ativo do mesmo, pode ser ligado a um anticorpo (ou um fragmento do mesmo) que especificamente se liga a outro receptor de HCV em células suscetíveis, como CD81 e SR-BI. Os métodos para produzir anticorpos biespecíficos e multiespecíficos são conhecidos na arte e incluem, por exemplo, síntese química envolvendo ret.iculação através de ligações de dissulfeto redutíveis ou ligações de tioéter não redutíveis, e métodos de recombinação.
Anticorpos monoclonais anti-Claudin-1 da presente invenção também podem ser humanizados : diferenças de seqüência entre anticorpos de roedor e sequências humanas 20 podem ser minimizadas por substituir resíduos que diferem daqueles nas seqüências humanas por mutagênese dirigida a sítio de resíduos individuais ou por enxerto de regiões inteiras ou por síntese química. Anticorpos humanizados também podem ser produzidos utilizando métodos recombinantes. Na forma humanizada do anticorpo, alguns, a maioria ou todos os aminoácidos fora das regiões de CDR são substituídos com aminoácidos a partir de moléculas de imunoglobulina humanas, enquanto, alguns, a maioria ou todos os aminoácidos em uma ou mais regiões CDR são inalteradas. Pequenas adições, deleçoes, inserções, substituições ou modificações de aminoácidos são permissíveis desde qué não anule a capacidade do anticorpo resultante em ligar-se ao domínio extracelular de Claudin-1 humano. Moléculas de imunoglobulina de "substituição" humanas apropriadas incluem moléculas de IgGl, IgG2, IgG2a, IgG2b, IgG3, IgG4, IgA, IgM, IgD ou IgE, e fragmentos dos mesmos, alternativamente, os epítopos de célula T presentes em anticorpos de roedor podem ser modificados por mutação (desimunização) para gerar anticorpos de roedor não imunogênicos que podem ser aplicados para fins terapêuticos em seres humanos (vide www.accurobio.com).
Um anticorpo monoclonal da invenção, ou uma variante biologicamente ativa ou fragmento do mesmo, pode ser funcionalmente ligado (por exemplo, por acoplamento químico, fusão genética, associação não covalente ou de outro modo) a uma ou mais outras entidades moleculares. Os métodos para a preparação de tais anticorpos modificados (ou anticorpos conjugados) são conhecidos na arte, (vide, por exemplo, "Affinity Techniques. Enzyme Purification: Part 5", Methods in Enzymol, 1974, Vol. 34, W.B. Jakoby e M. Wilneck (Eds.), Academic Press: New York, NY; e M. Wilchek e E.A. Bayer, Anal. Biochem., 1988, 171: 1-32). Preferivelmente, entidades moleculares são ligadas nas posições na molécula de anticorpo que não interferem nas propriedades de ligação do conjugado resultante, isto é, posições que não participam na ligação especifica do anticorpo ao dominio extracelular de Claudin-1 humano.
Em certas modalidades, a molécula de anticorpo e entidade molecular são ligadas covalentemente, diretamente entre si. A ligação covalente direta pode ser através de uma ligação como uma amida, éster, carbono-carbono, dissulfeto, carbamato, éter, tioéter, uréia, amina ou ligação de carbonato. A ligação covalente pode ser obtida por tirar proveito de grupos funcionais presentes no anticorpo e entidade molecular. Um agente de ativação, como um carbodiimida, pode ser utilizado para formar uma ligação direta. Em outras modalidades, a molécula de anticorpo e a entidade molecular são covalentemente ligadas entre si através de um grupo ligador. Isso pode ser realizado utilizando qualquer de uma ampla variedade de agents bifuncionais estáveis bem conhecidos na arte, incluindo ligadores homofuncionais e heterofuncionais.
Em certas modalidades, um anticorpo da presente invenção (ou um fragmento biologicamente ativo do mesmo) é conjugado com uma fração terapêutica. Qualquer de uma ampla variedade de frações terapêuticas pode ser apropriada para uso na prática da presente invenção incluindo, sem limitação citotoxinas (por exemplo, agentes citostáticos ou citocidas), agentes terapêuticos, e ions de metal radioativo (por exemplo, alfa-emissores e alfa-emissores ligados a queladores macrociclicos como DOTA). Citotoxinas ou agentes citotóxicos incluem qualquer agente que é prejudicial a células. Os exemplos incluem, porém não são limitados a, paclitaxol, citocalasina B, gramicidina D, brometo de etidio, emetine, mitomicina, etoposide, tenoposide, vincristina, vinblastina, colchicina, doxorubicina, daunorubicina, diidróxi antracin diona, mitoxantrona, mitramicina, actinomicina D, 1- desidrotestosterona, glicocorticóides, procaína, tetracaina, lidocaina, propranolol, timidina cinase, endonuclease, RNAse, e puromicina e fragmentos, variantes ou homólogos dos mesmos. Agentes terapêuticos incluem, porém não são limitados a, antimetabólitos (por exemplo, metotrexato, 6-mercaptopurina, 6-tioguanina, alquilação (por exemplo, mecloretamina, tioepa clorambucil, melfalan, carmustina (BSNU) e lomustina (CCNU), ciclotosfamide, busulfan, dibromomanitol, estreptozotocina, mitomicina C, e cisdiclorodiamina platina (II) (DDP) 5 cisplatina), antraciclinas (por exemplo, daunorubicina e doxorubicina) , antibióticos (por exemplo, dactinomicina, bleomicina, mitramicina e antramicina), e agentes anti- mitóticos (por exemplo, vincristina e vinblastina). Os conjugados de anticorpo resultantes podem encontrar 10 aplicação no tratamento de câncer de figado associado à infecção por HCV (vide abaixo),
Outras frações terapêuticas incluem proteinas ou polipeptídios que possuem uma atividade biológica desejada. Tais proteinas incluem, porém não são limitadas a, toxinas (por exemplo, abrin, ricina A, toxina alfa, pseudomonas exotocina, toxina de difteria, saporina, momordina, gelonina, proteina antiviral de caruru-de-cacho, alfa- sarcina e toxina de cólera); proteínas como fator de necrose de tumor, alfa-interferon, beta-interferon, fator de crescimento de nervo, fator de crescimento derivado de plaqueta, ativador de plasminogeno de tecido; agentes apoptóticos (por exemplo, INF-oc, TNF-β) ou modificadores de resposta biológica (por exemplo, linfocinas, interleucina-1 (IL-1), interleucina-2 (IL-2), interleucina-6 (IL-6), fator de estimular colônia de macrófago granulócito (GM-CSF) , fator de estimular colônia de granulócito (G-CSF) ou outros fatores de crescimento).
Alternativamente ou adicionalmente, um anticorpo da presente invenção (ou um fragmento biologicamente ativo do mesmo) pode ser conjugado com um agente detectável. Qualquer de uma ampla variedade de agentes detectáveis pode ser utilizado na prática da presente invenção, incluindo, sem limitação, vários ligandos, radionuclides (por exemplo, 3H, :L25I, 131I, e similar), corantes fluorescentes (por exemplo, isotiocianato de fluoresceina, rodamina, ficoeriterina, ficocianina, aloficocianina, o-ftalaldeido e fluorescamina), agentes quimiluminescentes (por exemplo, luciferina, luciferase e aequorina), microparticuias (como, por exemplo, pontos de quantum, nanocristais,fósforos e similares), enzimas (como, por exemplo, aquelas utilizadas em uma ELISA, isto é, peroxidase de raiz forte, beta- galactosidase, luciferase, fosfatase alcalina), rótulos colorimétricos, rótulos magnéticos, e biotina, dioxigenina ou outros haptenos e proteinas para os quais anticorpos ou anticorpos monoclonais são disponíveis. Os anticorpos detectáveis resultantes podem ser utilizados em métodos de diagnóstico e/ou prognóstico (vide abaixo).
Outras entidades moleculares que podem ser conjugadas com um anticorpo da presente invenção (ou um fragmento biologicamente ativo do mesmo) incluem, porém não são limitados a, grupos poliméricos hidrofilicos lineares ou ramificados, grupos de ácido graxo, ou grupos de éster graxo.
Desse modo, além de anticorpos monoclonais anti- Claudin-1 secretados pelas linhagens de células de hibridoma descritas aqui, e quaisquer variantes biologicamente ativos ou fragmentos dos mesmos, a presente invenção também abrange anticorpos quiméricos, anticorpos humanizados, e moléculas derivadas de anticorpo compreendendo pelo menos uma região de determinação complementar (CDR) a partir de uma região variável de cadeia pesada ou cadeia leve de um anticorpo monoclonal anti-Claudin-1 inventivo, incluindo moléculas como fragmentos Fab, fragmentos F(ab')2, fragmentos Fd, fragmentos Fabc, anticorpos Sc (anticorpos de cadeia única), diacorpos, cadeias únicas leves de anticorpo individual, cadeias pesadas de anticorpo individual, fusões quiméricas entre cadeias de anticorpo e outras moléculas, e conjugados de anticorpo, como anticorpos conjugados com uma gente de diagnóstico ou terapêutico. Todos esses anticorpos e moléculas relacionadas a anticorpo abrangidas pela presente invenção retêm especificamente se ligam ao domínio extracelular de Claudin-1 humano.
cada dos anticorpos monoclonais anti-Claudin-1 inventivos descritos no Exemplo 2 foi produzido de uma linhagem de célula de hibridoma fornecida aqui e foi selecionada por sua capacidade de inibir infecção de HCVcc de células Huh7.5.1. como será reconhecido por aqueles versados na técnica, o efeito inibidor de infecção por HCV 10 de outros anticorpos e moléculas relacionadas a anticorpo da invenção pode ser também avaliado utilizando um sistema de infecção por HCVcc. O efeito inibidor de anticorpos e moléculas relacionadas a anticorpo sobre infecção por HCV podem, alternativamente ou adicionalmente, ser avaliado 15 utilizando partículas pseudotipadas de HCV retroviral (HCVpp) como conhecido na técnica, preferivelmente, um anticorpo ou molécula relacionada a anticorpo da presente invenção será mostrado como inibindo infecção por HCV de células suscetíveis por HCVcc ou HCVpp em um modo 20 dependente de dose.
Outros métodos que podem ser utilizados para testar a especificidade de anticorpos e reagentes da presente invenção incluem, porém não são limitados a, análise de citometria de fluxo. A análise Western blot, ELISA e ensaios de ligação de inibição envolvendo ligação de receptor/ligando pelo anticorpo. Esses métodos podem ser utilizados para testar sobrenadantes a partir de hibridomas que produzem anticorpos, para testar a atividade de anticorpos purificados/isolados, e/ou para testar a atividade de anticorpos modificados (moléculas relacionadas a anticorpo). 0 teste de especificidade de ligação pode ser executado utilizando o anticorpo ou molécula relacionada a anticorpo contra um painel de células, por exemplo, células humanas, incluindo, sem limitação, linhagens de células de figado (como, por exemplo, Huh7, Hep3b ou HepG2), células de rim embriônico (293T), fibroblastos (HeLa), células B, células T (por exemplo, Molt-4, Sup-TI, ou Hut-78), células monociticas (THP-I), células astrociticas (U87), células de hepatoma (PLC/PRF:5) ou outros tipos de célula de figado, por exemplo, o adenocarcinoma de figado SkHepl, células de sangue periférico humano e vários subtipos fracionados das mesmas incluindo linfócitos e monócitos ou outras linhagens de células incluindo células CaCo2. A análise de citometria de fluxo pode revelar especificidade de ligação do anticorpo ou molécula relacionada a anticorpo para Claudin- 1 em vários tipos de células. Células de mamíferos não humanos podem ser também utilizadas em tais ensaios.
Utilizando tais ensaios, valores IC50 podem ser determinados para os anticorpos e moléculas relacionadas a anticorpo da presente invenção. Esses valores, que fornecem uma indicação da concentração de anticorpo ou molécula relacionada a anticorpo exigida para 50% de inibição de infectividade virai, fornecem critérios quantitativos significativos e permitem comparação da atividade de inibir infecção de diferentes anticorpos e moléculas relacionadas a anticorpo.
Verificou-se que os anticorpos monoclonais antiClaudin-1 inventivos descritos no exemplo 2 neutralizam de forma cruzada potentemente infecção por HCV a partir de todos os genótipos principais bem como todos os isolados da população de quasiespécie inteira a partir de dois pacientes infectados cronicamente por HCV. A capacidade de outros anticorpos e moléculas relacionadas a anticorpo da invenção neutralizar de forma cruzada infecção por HCV a partir de genótipos de HCV principais e de isolados de quasiespécie de pacientes individuais pode ser avaliada utilizando qualquer método apropriado como pelo uso de partículas pseudotipadas HCV (HCVpp) contendo glicoproteinas de envelope de HCV a partir de um genótipo HCV especifico, um HCVpp contendo glicoproteinas de envelope de HCV a partir de um paciente individual infectado cronicamente com HCV, como descrito no exemplo 2. preferivelmente, um anticorpo ou molécula relacionada a anticorpo da presente invenção será mostrado como inibindo infecção por HCV a partir de genótipos de HCV principais e de quasiespécie de um paciente infectado por HCV em um modo 5 dependente de dose.
Similarmente, um anticorpo ou molécula relacionada a anticorpo da presente invenção foi mostrado como não reagindo de forma cruzada com Claudin-1 de roedor (como Claudin-1 de murino) porém ligando especificamente a 10 Claudin-1 de primata não humano (como Claudin-1 de macaco cinomolgo) .
Anticorpos anti-Claudin-1 da presente invenção podem ser utilizados em métodos terapêuticos e profiláticos para tratar e/ou evidente infecção por HCV, ou tratar e/ou evitar uma doença de figado ou uma condição patológica que afeta células suscetíveis a HCV, como células de fígado, 20 células linfóides ou monócitos/macrófagos. Um anticorpo anti-Claudin-1 inventivo interfere em interações de células de hospedeiro-HCV por ligação com o domínio extracelular de Claudin-1 em uma superfície de célula, desse modo, reduzindo, inibindo, bloqueando ou evitando entrada de HCV na célula e/ou infecção por HCV da célula.
Os métodos de tratamento da presente invenção podem ser realizados utilizando um anticorpo inventivo ou uma composição farmacêutica compreendendo um anticorpo inventivo (vide abaixo). Esses métodos compreendem genericamente administração de uma quantidade eficaz de pelo menos um anticorpo anti-Claudin-1 inventivo, ou uma composição farmacêutica do mesmo a um sujeito necessitando do mesmo. A administração pode ser executada utilizando qualquer dos métodos conhecidos por uma pessoa versada na arte. Em particular, o anticorpo ou composição pode ser administrado por várias vias incluindo, porém não limitado a aerossol, parenteral, oral ou via tópica.
Em geral, um anticorpo inventivo ou composição será administrado em uma quantidade eficaz, isto é, uma quantidade que é suficiente para atender a sua finalidade pretendida. A quantidade exata de anticorpo ou composição f armacêutica a ser administrada variará de sujeito para sujeito, dependendo da idade, sexo, peso e condição de saúde em geral do sujeito a ser tratado, da resposta biológica ou médica desejada (por exemplo, prevenção de infecção por HCV ou tratamento de doença de fígado associada à HCV) e similar. Em muitas modalidades, uma quantidade eficaz é uma que inibe ou evita que HCV entre nas células suscetíveis de um sujeito e/ou infecte as células de um sujeito, de modo a evitar desse modo infecção por HCV, tratar ou evitar doença de figa ou outra patologia associada à HCV no sujeito.
Anticorpos e composições da presente invenção podem ser utilizadas em uma variedade de métodos terapêuticos ou profiláticos. Em particular, a presente invenção provê um método para tratar ou evitar uma doença ou patologia de fígado em um sujeito, que compreende administrar ao sujeito 10 uma quantidade eficaz de um anticorpo inventivo (ou composição do mesmo) que inibe que HCV entre ou infecte as células do sujeito, de modo a tratar ou evitar desse modo a doença ou patologia de fígado no sujeito. A doença ou patologia de fígado pode ser inflamação do fígado, fibrose 15 do figado, cirrose e/ou carcinoma hepatocelular (isto é, câncer do figado) associado à infecção por HCV.
A presente invenção também provê um método para tratar ou evitar uma condição ou doença associada à HCV (incluindo uma doença de fígado) em um sujeito, que 20 compreende administrar ao sujeito uma quantidade eficaz de um anticorpo inventivo (ou composição do mesmo) que inibe HCV de entrar ou infectar as células do sujeito, de modo a tratar desse modo ou evitar a doença ou condição associada à HCV no sujeito. Em certas modalidades da presente invenção, o anticorpo ou composição é administrado a um sujeito diagnosticado com hepatite aguda C. em outras modalidades da invenção, o anticorpo ou composição é administrado a um sujeito diagnosticado com hepatite crônica Ç.
A administração de uma composição ou anticorpo inventivo de acordo com tais métodos pode resultar em melhora de pelo menos um dos sintomas experimentados pelo individuo incluindo, porém não limitado a, sintomas de hepatite aguda C como diminuição de apetite, fadiga, dor abdominal, ictericia, coceira e sintomas semelhantes a resfriado; sintomas de hepatite crônica C como fadiga, perda acentuada de peso, sintomas semelhantes a resfriado, dor muscular, dor nas articulações, febres de grau baixo intermitentes, coceira, distúrbios de sono, dor abdominal, alterações de apetite, náusea, diarréia, dispepsia, alterações cognitivas, depressão, dores de cabeça, e oscilações de humor; sintomas de cirrose como ascites, tendência a machucadura e sangramento, dor nos ossos, varizes (especialmente no estômago e esôfago), esteatorreia, icterícia e encefalopatia hepática; e sintomas de manifestações extra-hepáticas associadas à HCV como tireoidite, porfíria cutânea tardia, crioglobulinemia, glomerulonefrite, síndrome seca, trombocitopenia, líquen plano, diabetes mellitus e distúrbios linfoproliferativos de célula-B.
Alternativamente ou adicionalmente, a administração de uma composição ou anticorpo inventivo de acordo com tais métodos pode diminuir, reduzir, parar ou aliviar o avanço de infecção por HCV ou uma doença associada à HCV, ou reverter o avanço até o ponto de eliminar a infecção ou doença. A administração de uma composição ou anticorpo inventivo de acordo com tais métodos também pode resultar em uma redução do número de infecções virais, redução do número de partículas virais infecciosas, e/ou redução no número de células viralmente infectadas.
Os efeitos de um tratamento de acordo com a invenção podem ser monitorados utilizando quaisquer dos ensaios conhecidos na arte para o diagnóstico de infecção por HCV e/ou doença de figado. Tais ensaios incluem, porém não são limitados a, testes de sangue sorológicos, testes de função do figado para medir um ou mais de albumina, alanina transaminase (ALT), fosfatase alcalina (ALP), transaminase de aspartato (AST), e transpeptidase de gama glutaminal (GGT) e testes de ácido nucléico molecular utilizando técnicas diferentes como reação de cadeia de polimerase (PCR) , amplificação mediada por transcrição (TMA) ou DNA ramificada (bDNA).
Anticorpos e composições da presente invenção também podem ser utilizados em terapias de imunização. Por conseguinte, a presente invenção provê um método de reduzir a probabilidade de células suscetíveis de se tornarem 5 infectadas com HCV como resultado de contato com HCV. O método compreende contatar as células suscetíveis com uma quantidade eficaz de uma composição ou anticorpo inventivo que inibe HCV de entrar ou infectar as células suscetíveis, de modo a reduzir a probabilidade das células se tornarem 10 infectadas com HCV como resultado de contato com HCV. A presente invenção também provê um método de reduzir a probabilidade das células suscetíveis de um sujeito de se tornarem infectadas com HCV como resultado de contato com HCV. Nesse método, o contato das células suscetíveis com a 15 composição ou anticorpo inventivo pode ser executado por administrar o anticorpo ou composição ao sujeito.
A redução da probabilidade de células suscetíveis ou de um sujeito de se tornar infectada com HCV significa diminuir a probabilidade de células suscetíveis ou um 20 sujeito de se tornar infectado com HCV como resultado de contato com HCV. A diminuição pode ser de qualquer quantidade significativa, por exemplo, pelo menos uma diminuição de 2 vezes, uma diminuição superior a 2 vezes, uma diminuição de pelo menos 10 vezes, uma diminuição maior do que 10 vezes, uma diminuição de pelo menos 100 vezes, ou uma diminuição maior do que 100 vezes.
Em certas modalidades, o sujeito está infectado com HCV antes da administração da composição ou anticorpo inventivo. Em outras modalidades, o sujeito não está infectado com HCV antes da administração do anticorpo ou composição inventiva. Ainda em outras modalidades, o sujeito não está infectado com, porém foi exposto a, HCV. Em certas modalidades, o sujeito pode ser infectado com. HIV ou HBV.
Por exemplo, os métodos da presente invenção podem ser utilizados para reduzir a probabilidade das células suscetíveis de um sujeito de se tornarem infectadas com HCV como resultado de transplante de figado. Como já mencionado acima, quando um fígado doente é removido de um paciente infectado com HCV, níveis virais de soro caem verticalmente. Entretanto, após receber um transplante de fígado saudável, os níveis de vírus ressaltam e podem ultrapassar os níveis pré-transplante em alguns dias (Powers, 2006). Os pacientes de transplante de fígado podem beneficiar da administração de um anticorpo inventivo que se liga ao ectodomínio de Claudin-1 na superfície de hepatócitos e desse modo reduzem, inibem, bloqueiam ou evitam entrada de HCV nas células. A administração pode ser executada antes do transplante de figado, durante transplante de fígado e/ou após transplante de figado.
Outros sujeitos que podem se beneficiar da administração de uma composição ou anticorpo inventive incluem, porém não são limitados a, bebês nascidos de mães infectadas com HCV, em particular se a mãe também é HIV positiva; trabalhadores de cuidados da saúde que estiveram em contato com sangue contaminado por HCV ou instrumentos médicos contaminados de sangue; usuários de drogas que foram expostos a HCV por compartilhar equipamentos para injetar ou de outro modo administrar drogas; e pessoas que foram expostas a HCV através de tatuagem, perfuração de corpo/orelha e acupuntura com procedimentos insuficiente de controle de infecção.
Outros sujeitos que podem beneficiar da administração de uma composição ou anticorpo inventivo incluem, porém não são limitados a, sujeitos que apresentam um ou mais fatores que são conhecidos por aumentarem a taxa de avanço de doença de HCV. Tais fatores incluem, em particular, idade sexo (os homens apresentam genericamente avanço mais rápido da doença do que as mulheres), consumo de álcool, co- infecção de HIV (associado a uma taxa acentuadamente aumentada de avanço de doença) e fígado gorduroso.
Em certas modalidades, uma composição ou anticorpo inventivo é administrado individualmente de acordo com um método de tratamento da presente invenção. Em outras modalidades, uma composição ou anticorpo inventivo é administrado em combinação com pelo menos um agente terapêutico adicional. A composição ou anticorpo inventivo pode ser administrado antes da administração do agente terapêutico, simultaneamente com o agente terapêutico, e/ou após administração do agente terapêutico.
Agentes terapêuticos que podem ser administrados em combinação com uma composição ou anticorpo inventivo podem ser selecionados entre uma grande variedade de compostos biologicamente ativos que são conhecidos por ter um efeito benéfico no tratamento ou prevenção de infecção por HCV, ou uma condição ou doença associada à HCV. Tais agents incluem, em particular, agentes antivirais incluindo, porém não limitados a, interferons (por exemplo, interferon-alfa, interferon-alfa peguilado), ribavirina, anticorpos anti-HCV (monoclonal ou policlonal), inibidores de polimerase de RNA, inibidores de protease, inibidores de IRES, inibidores de helicase, compostos anti-sentido, ribozimas e qualquer combinação dos mesmos.
Um. anticorpo inventivo, (opcionalmente após a farmaceuticamente aceitáveis apropriados) , em uma dosagem desejada pode ser administrado a um sujeito necessitando do mesmo por qualquer via apropriada. Vários sistemas de distribuição são conhecidos e podem ser utilizados para administrar anticorpos da presente invenção, incluindo tabletes, cápsulas, soluções injetáveis, encapsulação em lipossomas, micropartículas, microcápsulas, etc. os métodos de administração incluem, porém não são limitados a, vias dérmica, intradérmica, intramuscular, intraperitoneal, intralesional, intravenosa, subcutânea, intranasal, pulmonar, epidural, ocular e oral. Uma composição ou anticorpo inventivo pode ser administrado por qualquer via apropriada conveniente ou outra, por exemplo, por infusão ou injeção de bolo, por absorção através de revestimentos epiteliais ou mucocutâneos (por exemplo, oral, mucosa, retal e mucosa intestinal, etc.), a administração pode ser sistêmica ou local. A administração parenteral pode ser preferencialmente dirigida ao fígado do paciente, como por cateterização em artérias hepáticas ou em um duto de bílis. Como será reconhecido por aqueles com conhecimentos comuns na técnica, em modalidades onde um anticorpo inventivo é administrado em combinação com um agente terapêutico adicional, o anticorpo e agente terapêutico pode ser intravenoso) ou por vias diferentes (por exemplo, por meio intravenoso e oral).
A administração de um anticorpo inventivo (ou composição) da presente invenção será em uma dosagem de tal modo que a quantidade fornecida seja eficaz para a finalidade pretendida. A via de administração, formulação e dosagem administrada dependerá do efeito terapêutico desejado, da gravidade da condição relacionada à HCV a ser 10 tratada se já presente, a presença de qualquer infecção, idade, sexo, peso, e condição de saúde em geral do paciente bem como da potência, biodisponibilidade, e meia-vida in vivo do anticorpo ou composição utilizada, o uso (ou não) de terapias concomitantes, e outros fatores clínicos. Esses 15 fatores são facilmente determináveis pelo médico atendente no curso da terapia. Alternativamente ou adicionalmente, a dosagem a ser administrada pode ser determinada de estudos utilizando modelos de animais (por exemplo, chimpanzé ou camundongos). O ajuste da dose para obter eficácia máxima 20 com base nesses ou em outros métodos é bem conhecido na técnica e está compreendido nas capacidades dos médicos treinados. Como estudos são realizados utilizando os anticorpos monoclonais inventivos, informações adicionais surgirão em relação aos níveis de dosagem e duração de tratamento apropriados.
Um tratamento de acordo com a presente invenção pode consistir em uma dose única ou múltiplas doses. Desse modo, a administração de um corpo inventivo, ou composição do 5 mesmo, pode ser constante por certo período de tempo ou periódico e em intervalos específicos, por exemplo, de hora em hora, diariamente, semanalmente (ou em algum outro intervalo de múltiplos dias), mensalmente, anualmente (por exemplo, em uma forma de liberação de tempo).
Alternativamente, a distribuição pode ocorrer em múltiplos tempos durante um dado período de tempo, por exemplo, duas ou mais vezes por semana; duas ou mais vezes por mês, e similares. A distribuição pode ser distribuição contínua por um período de tempo, por exemplo, distribuição 15 intravenosa.
Em geral, a quantidade de anticorpo monoclonal administrado será preferivelmente na faixa de aproximadamente 1 ng/kg a aproximadamente 100 mg/kg de peso corpóreo do sujeito, por exemplo, entre aproximadamente 100 20 ng/kg e aproximadamente 50 mg/kg de peso corpóreo do sujeito; ou entre aproximadamente 1 μg/kg e aproximadamente 10 mg/kg de peso corpóreo do sujeito, ou entre aproximadamente 100 μg/kg e aproximadamente 1 mg/kg de peso corpóreo do sujeito.
Como mencionado acima, anticorpos anti-Claudin-1 (e moléculas relacionadas) da invenção podem ser administrados por si ou como uma composição farmacêutica. Por conseguinte, a presente invenção provê composições farmacêuticas que compreendem uma quantidade eficaz de um anticorpo inventivo descrito aqui e pelo menos um excipiente ou veiculo farmaceuticamente aceitável. Em algumas modalidades, a composição compreende ainda um ou mais agentes biologicamente ativos adicionais.
Anticorpos inventivos e composições farmacêuticas podem ser administrados em qualquer quantidade e utilizando quando via de administração eficaz para obter o efeito profilático e/ou terapêutico desejado. A formulação farmacêutica ótima pode ser variada dependendo da via de administração e dosagem desejada. Tais formulações podem influenciar o estado fisico, estabilidade, taxa de liberação in vivo, e taxa de depuração in vivo do ingrediente ativo administrado.
As composições farmacêuticas da presente invenção podem ser formulações em forma de unidade de dosagem para facilidade de administração e uniformidade de dosagem. A expressão "forma de dosagem unitária", como utilizado aqui se refere a uma unidade fisicamente discreta de um anticorpo anti-Claudin-1 inventivo para o paciente a ser tratado. Será entendido, entretanto, que a dosagem diária total das composições será decidida pelo médico atendente 5 no escopo de decisão médica acertada.
Preparados injetáveis, por exemplo suspensões oleaginosas ou aquosas injetáveis estéreis podem ser formuladas de acordo com a técnica conhecida utilizando 10 agentes umectantes ou de dispersão apropriados, e agentes de suspensão. O preparado injetável estéril também pode ser uma solução injetável estéril, suspensão ou emulsão em um diluente ou solvente parenteralmente aceitável não tóxico, por exemplo, como um solução em 2,3-butanodiol. Entre os 15 veiculos e solventes aceitáveis que podem ser empregados estão água, solução de Ringer, U.S.P. e solução de cloreto de sódio isotônico. Além disso, óleos fixos estéreis são convencionalmente empregados como solução ou meio de suspensão. Para essa finalidade qualquer óleo fixo suave 20 pode ser empregado incluindo mono- ou diglicerideos sintéticos. Ácidos graxos como ácido oléico também podem ser utilizados na preparação de formulações injetáveis. Veiculos líquidos estéreis são úteis em composições de forma líquida estéreis para administração parenteral.
Formulações injetáveis podem ser esterilizadas, por exemplo, por filtração através de um filtro que retém bactéria, ou por incorporar agentes de esterilização na forma de composições sólidas estéreis que podem ser 5 dissolvidas ou dispersas em água estéril ou outro meio injetável estéril antes do uso. Composições farmacêuticas líquidas que são soluções ou suspensões estéreis podem ser administradas, por exemplo, por injeção intravenosa, intramuscular, intraperitoneal ou subcutânea. A injeção 10 pode ser através de empurrão único ou por infusão gradual.
Onde necessário ou desejado, a composição pode incluir um anestésico local para diminuir a dor no local de injeção.
Para prolongar o efeito de um ingrediente ativo (aqui um anticorpo anti-Claudin-1 inventivo), é frequentemente 15 desejável diminuir a absorção do ingrediente a partir de injeção subcutânea ou intramuscular. O retardamento de absorção de um ingrediente ativo administrado por via parenteral pode ser realizado por dissolver ou suspender o ingrediente em um veículo de óleo. Formas de depósito 20 injetáveis são feitas por formar matrizes micro- encapsuladas do ingrediente ativo em polímeros biodegradáveis como polilactide-poliglicolide. dependendo da razão de ingrediente ativo para polímero e a natureza do polímero específico empregado, a taxa de liberação de ingrediente pode ser controlada. Os exemplos de outros polimeros biodegradáveis incluem poli(ortoésteres) e poli(anidridos) . Formulações injetáveis de depósito também podem ser preparadas por reter o ingrediente ativo em lipossomas ou microemulsões que são compatíveis com tecidos do corpo.
Formas de dosagem líquida para administração oral incluem, porém não são limitadas a, emulsões farmaceuticamente aceitáveis, microemulsões, soluções, suspensões, xaropes, elixires, e composições pressurizadas. Além do anticorpo anti-Claudin-1, a forma de dosagem líquida pode conter diluentes inertes comumente utilizados na técnica como, por exemplo, água ou outro solvente, agentes de solubilização e emulsificantes como álcool de etila, álcool de isopropila, carbonato de etila, acetato de etila, álcool de benzila, benzoato de benzila, propileno glicol, 1,3-butileno glicol, dimetil formamida, óleos (em particular, semente de algodão, amendoim, milho, germe, azeite, mamona e óleos de gergelim), glicerol, álcool tetraidrofurfurila, polietileno glicóis e ésteres de ácido graxo de sorbitano e misturas dos mesmos. Além de diluentes inertes, as composições orais podem incluir também adjuvantes como agentes umectantes, agentes de suspensão, preservativos, agentes adoçantes, aromatizantes e de perfumar, agentes espessantes, cores, reguladores de viscosidade, estabilizadores ou osmorreguladores. Os exemplos de veículos líquidos apropriados para administração oral incluem água (contendo potencialmente aditivos como acima, por exemplo, derivados de celulose, como solução de carbóxi metil celulose de sódio), alcoóis (incluindo alcoóis monoídricos e alcoóis poliídricos como glicóis) e seus derivados, e óleos (por exemplo, óleo de côco fracionado e óleo de amendoim) . Para composições pressurizadas, o veículo líquido pode ser hidrocarboneto halogenado ou outro propelente farmaceuticamente aceitável.
Formas de dosagem sólidas para administração oral incluem, por exemplo, cápsulas, tabletes, pílulas, pós e grânulos. Em tais formas de dosagem sólida, um anticorpo anti-Claudin-1 inventivo pode ser misturado com pelo menos um inerte, excipiente ou veículo fisiologicamente aceitável como citrato de sódio ou fosfato de dicalcio e um ou mais de: (a) cargas ou diluentes como amidos, lactose, sacarose, glicose, manitol e ácido silícico; (b) aglutinantes como, por exemplo, carboxi metil celulose, alginatos, gelatina, polivinil pirrolidona, sacarose e acácia; (c) umectantes como glicerol; (d) agentes desintegrantes como Agar-agar, carbonato de cálcio, amido de tapioca ou batata, ácido algínico, certos silicatos, e carbonato de sódio; (e) agentes de retardar solução como parafina; aceleradores de absorção como compostos de amónio quaternário; (g) agentes umectantes como, por exemplo, álcool de cetila e monoestearato de glicerol; (h) absorventes como caulim e argila bentonita; e (i) lubrificantes como talco, estearato de cálcio, estearato de magnésio, polietileno glicóis sólidos, sulfato de laurila de sódio, e misturas dos mesmos. Outros excipientes apropriados para formulações sólidas incluem agentes modificadores de superficies como agentes modificadores de superficie não iônicos e aniônicos. Exemplos representativos de agentes modificadores de superficie incluem, porém não são limitados a poloxâmero 188, cloreto de benzalcônio, estearato de cálcio, álcool de cetoestearila, cera emulsificante de cetomacrogol, ésteres de sorbitol, dióxido de silicio coloidal, fosfatos, dodecil sulfato de sódio, silicato de alumínio magnésio, e trietanol amina. No caso de cápsulas, tabletes e pílulas, a forma de dosagem pode compreender também agentes de tamponamento.
Composições sólidas de um tipo similar também podem ser empregadas como cargas em cápsulas de gelatina cheias macias e duras utilizando tais excipientes como lactose ou açúcar de leite bem como polietileno glicóis de peso molecular elevado e similar. As formas de dosagem sólida de tablete, drágeas, cápsulas, pílulas e grânulos podem ser preparadas com revestimentos e invólucros como revestimentos entéricos, revestimentos para controlar liberação e outros revestimentos bem conhecidos na técnica de formulação farmacêutica. Podem conter opcionalmente agentes de opacificação e também podem ser uma composição de tal modo que liberem o(s) ingrediente(s) ativo(s) somente, ou preferivelmente em certa parte do trato intestinal, opcionalmente em um modo retardador. Os exemplos de composições de incorporação que podem ser utilizados incluem ceras e substâncias poliméricas.
Em certas modalidades, pode ser desejável administrar uma composição inventiva localmente em uma área necessitando de tratamento (por exemplo, o figado). Isso pode ser obtido, por exemplo, e não como limitação, por infusão local durante cirurgia (por exemplo, transplante de figado), aplicação tópica, por injeção, por intermédio de um cateter, por meio de supositório, ou por intermédio de um adesivo de pele ou stent ou outro implante.
Para administração tópica, a composição é preferivelmente formulada como um gel, um ungüento, uma loção, ou um creme que pode incluir veículos como água, glicerol, álcool, propileno glicol, alcoóis graxos, triglicerídeos, ésteres de ácido graxo, ou óleo mineral.
Outros veículos tópicos incluem petróleo líquido, palmitato de isopropila, polietileno glicol, etanol (95%), polioxietileno monolaurat (5%) em água, ou sulfato de laurila de soído (5%) em água. Outros materiais como antioxidantes, umectantes, estabilizadores de viscosidade e agentes similares podem ser adicionados como necessário.
Além disso, em certos casos, espera-se que as composições inventivas possam ser dispostas em dispositivos transdermicos colocados sobre, na ou sob a pele. Tais dispositivos incluem adesivos, implantes e injeções que liberam o ingrediente ativo por mecanismos de liberação passiva ou ativa, administrações transdérmicas incluem toda administração através da superfície do corpo e revestimentos internos de passagem corpórea incluindo tecidos epiteliais e de mucosa. Tais administrações podem ser realizadas utilizando as presentes composições em loções, cremes, espumas, adesivos, suspensões, soluções e supositórios (retal e vaginal).
A administração transdérmica pode ser realizada através do uso de um adesivo transdérmico contendo um ingrediente ativo (isto é, um anticorpo anti-Claudin-1 inventivo) e um veículo que é não tóxico à pele, e permite a distribuição do ingrediente para absorção sistêmica na corrente sanguínea através da pele. 0 veículo pode assumir qualquer número de formas como cremes e unguentos, pastas, géis e dispositivos oclusivos. Os cremes e unguentos podem ser emulsões liquidas ou semi-sólidas viscosas do tipo óleo em água ou água em óleo. Pastas compreendidas de pós absortivos dispersos em petróleo ou petróleo hidrofilico contendo o ingrediente ativo podem ser apropriadas. Uma variedade de dispositivos oclusivos pode ser utilizada para liberar o ingrediente ativo na corrente sanguinea como uma membrana semi-permeável cobrindo um reservatório que contém o ingrediente ativo com ou sem um veiculo, ou uma matriz contendo o ingrediente ativo.
Formulações de supositório podem ser feitas de materiais tradicionais, incluindo manteiga de cacau, com ou sem a adição de ceras para alterar o ponto de fusão do supositório, e glicerina. Bases de supositório solúveis em água, como polietileno glicóis de vários pesos moleculares, também podem ser utilizadas.
Quando uma composição farmacêutica da presente invenção é utilizada como "vacina" para evita que células suscetíveis a HCV se tornem infectadas com HCV, a composição farmacêutica pode compreender ainda veículos de vacina conhecidos na técnica como, por exemplo, tiroglobulina, albumina, tétano toxoide, e poliamino ácidos como polímeros de D-lisina e D-glutamato. A vacina também pode incluir qualquer de uma variedade de adjuvantes bem conhecidos como, por exemplo, adjuvante de Freund incompleto, alum, fosfato de alumínio, hidróxido de alumínio, lipídeo monofosforila A (MPL, GlaxoSmithKline), 5 uma saponina, oligonucleotídeos CpG, montanide, vitamina A e várias emulsões de água em óleo preparadas de óleos biodegradáveis como squarelene e/ou tocoferol, Quil A, Ribi Detox, CRL-1005, L-121 e combinações dos mesmos.
Materiais e métodos para produzir várias formulações são conhecidos na técnica e podem ser adaptados para pôr em prática a presente invenção. Formulações apropriadas para a distribuição de anticorpos podem ser encontradas, pro exemplo, em "Remington's Pharmaceutical Sciences", E.W. Martin, 18th Ed., 1990, Mack Publishing Co.: Easton, PA.
Em certas modalidades, um anticorpo anti-Claudin-1 inventivo é o único ingrediente ativo em uma composição farmacêutica da presente invenção. Em outras modalidades, a composição farmacêutica compreende ainda um ou mais agents biologicamente ativos. Os exemplos de agentes biologicamente ativos apropriados incluem, porém não são limitados a, adjuvantes de vacina e agentes terapêuticos como agentes antivirais (como descrito acima), agents antiinflamatórios, agentes imunomoduladores, analgésicos, agentes antimicrobianos, agentes antibacterianos, antibióticos, antioxidantes, agentes anti-sépticos e combinações dos mesmos.
Em tais composições farmacêuticas, o anticorpo anti- Claudin-1 e agente(s) terapêutico(s) adicional(is) podem ser combinados em um ou mais preparados para administração simultânea, separada ou seqüencial do anticorpo anti- Claudin-1 e agente(s) terapêutico(s). mais especificamente, uma composição inventiva pode ser formulada de tal modo que o anticorpo e agente(s) terapêutico(s) possam ser administrados juntos ou independentemente entre si. Por exemplo, um anticorpo anti-Claudin-1 e um agente terapêutico podem ser formulados juntos em uma composição única. Alternativamente, podem ser mantidos (por exemplo, em composições e/ou recipientes diferentes) e administrados separadamente.
Em outro aspecto, a presente invenção provê um Pacote farmacêutico ou kit compreendendo um ou mais recipientes 20 (por exemplo, fracos, ampolas, tubos de teste, frascos ou garrafas) contendo um ou mais ingredientes de uma composição farmacêutica inventiva, permitindo administração de um anticorpo anti-Claudin-1 da presente invenção.
Ingredientes diferentes de um Pacote farmacêutico ou kit podem ser fornecidos em uma forma líquida ou sólida (por exemplo, liofilizada). Cada ingrediente será genericamente apropriada como formada em alíquota em seu recipiente respectivo ou fornecido em uma forma concentrada. Pacotes farmacêuticos ou kits podem incluir meios para a reconstituição de ingredientes liofilizados. Recipientes individuais dos kits serão preferivelmente mantidos em confinamento estreito para venda comercial.
Em certas modalidades, um pacote farmacêutico ou kit inclui um ou mais agente(s) terapêutico(s) adicional(is) (por exemplo, um ou mais agentes anti-virais, como descrito acima). Opcionalmente associado ao(s) recipiente(s) pode haver um aviso ou inserção de embalagem na forma determinada por um órgão governamental que regula a fabricação, uso ou venda de produtos biológicos ou farmacêuticos, cujo aviso reflete a aprovação pelo órgão de fabricação, uso ou venda para administração humana. 0 aviso de inserção de embalagem pode conter instruções para uso de uma composição farmacêutica de acordo com métodos de tratamento revelados aqui.
Um identificador, por exemplo, um código de barra, radiofrequência, etiquetas de ID, etc., podem estar presentes em ou no kit. 0 identificador pode ser utilizado, por exemplo, para identificar exclusivamente o kit para fins de controle de qualidade, controle de inventário, movimento de rastreamento entre estações de trabalho, etc.
Anticorpos da presente invenção, por exemplo, um anticorpo monoclonal anti-claudin-1 produzido por uma linhagem de células de hibridoma fornecida aqui, podem ser empregados em uma variedade de aplicações não terapêuticas, como métodos de purificação, triagem e diagnóstico.
Desse modo, anticorpos da invenção podem ser utilizados como agentes de purificação por afinidade. Nesse pedido, um anticorpo inventivo é imobilizado em uma fase sólida como resina Sephadex ou papel filtro, utilizando 15 métodos bem conhecidos na arte. 0 anticorpo imobilizado é contatado com uma amostra que contém Claudin-1 humano (ou um fragmento do mesmo) a ser purificado, e posteriormente o suporte é lavado com um solvente apropriado que removerá substancialmente todo material na amostra exceto a proteína 20 de Claudin-1, que é ligada ao anticorpo imobilizado. Finalmente, o suporte é lavado com outro solvente apropriado que liberará a proteína Claudin-1 do anticorpo.
Anticorpos anti-Claudin-1 da presente invenção também podem ser utilizados em métodos de triagem de drogas com base em ensaios de ligação competitivos. Tais métodos podem envolver as etapas de permitir ligação competitiva entre um composto de teste (por exemplo, um anticorpo de teste) em 5 uma amostra e uma quantidade conhecida de um anticorpo monoclonal anti-Claudin-1 inventivo, para ligar-se a células as quais o anticorpo inventivo se liga, e medir a quantidade do anticorpo monoclonal conhecido ligado. O anticorpo monoclonal inventivo é apropriadamente rotulado, 10 por exemplo, com um rótulo enzimático, quimiluminescente ou fluorescente.
Anticorpos anti-Claudin-1 da presente invenção também podem ser úteis em ensaios de diagnóstico e/ou prognóstico, 15 em particular para o diagnóstico e/ou prognóstico de cânceres diferentes, por exemplo, por detectar a expressão de Claudin-1 em células especificas, tecidos ou soro. Desse modo, por exemplo, a expressão diminuída de claudin-1 tem sido mostrada como sendo um forte preditor de recorrência 20 de câncer de cólon e sobrevivência inferior de paciente no câncer de cólon estágio II (Resnick, 2005); expressão aumentada de Claudin-1 é um bom marcador de diagnóstico para a detecção de neoplasia intra-epitelial cervical (Sobel, 2005) e foi relatado como sendo um marcador útil para transformação maligna de células escamosas cervicais (Lee, 2005); expressão diminuída de Claudin-1 correlaciona com tipo de tumor elevado e recorrência de doença bioquímica em adenocarcinoma prostática (Sheeban, 2007); expressão diminuída de Claudin-1 foi demonstrada como correlacionando com status de recorrência e potencial maligno de câncer de mama (Morohashi, 2007).
Ensaios de diagnóstico e/ou prognóstico da presente invenção compreendem genericamente contatar uma amostra biológica obtida de um paciente com um anticorpo anticlaudin 1 inventivo por um tempo e sob condições que permitem que um complexo anticorpo-Claudin-1 forme entre o anticorpo e claudin-1 presente na amostra biológica; e detectar (e/ou quantificar) a presença ou ausência de qualquer complexo anticorpo-Claduinl formado. A presença ou quantidade determinada pode ser utilizada como uma indicação da presença de uma condição dada (por exemplo, um câncer). Em certos métodos, a quantidade medida é comparada com a quantidade de complexo de anticorpo-Claudin-1 formado sob as mesmas condições para uma amostra biológica obtida de um sujeito saudável (ou de uma série de amostras biológicas obtidas de um número significativo de sujeitos saudáveis).
Esses métodos podem ser aplicados ao estudo de qualquer tipo de amostras biológicas. Os exemplos de amostras biológicas incluem, porém não são limitadas a, sangue integral, urina, soro, plasma, saliva, fluido sinovial, fluido seminal, fluido linfático, fluido cérebro- 5 espinhal, fluido peritoneal, bem como amostras endocervical, uretral, retal e vaginal. Amostras biológicas podem incluir seções de tecido (por exemplo, amostras de biópsia de mama), seções congeladas, e amostras de arquivo com diagnóstico conhecido, tratamento e/ou histórico de resultado. Amostras biológicas podem ser coletadas por qualquer meio não invasivo, como, por exemplo, por tirar sangue de um sujeito, ou utilizar aspiração por agulha fina ou biópsia.
Os métodos de diagnóstico podem ser executados na própria amostra biológica sem, ou com processamento limitado da amostra. Alternativamente, podem ser executados após processamento da amostra biológica. O processamento de uma amostra biológica pode envolver um ou mais de: filtração, destilação, centrifugação, extração, concentração, diluição, purificação, inativação de componentes interferentes, adição de reagentes e similares. Por exemplo, o método de diagnóstico pode ser executado em um extrato de proteina da amostra biológica, métodos de extração de proteína são bem conhecidos na técnica.
Nos métodos de diagnóstico descritos acima, a detecção de um complexo de anticorpo-Claudin-1 pode ser realizada por qualquer método apropriado (vide, por exemplo, E. Harlow and A. Lane, "Antibodies: A Laboratories Manual", 1988, Cold Spring Harbor Laboratory: Cold Spring Harbor, NY) . Por exemplo, a detecção de um complexo de anticorpo-Claudin-1 pode ser executada utilizando urn imunoensaio. Uma ampla gama de técnicas de imunoensaio é disponível, incluindo radioimunoensaio, imunoensaios de enzima (EIA), ensaios imunossorventes ligados por enzima (ELISA) e imunoprecipitação de imunofluorescência. Imunoensaios são bem conhecidos na técnica. Os métodos para realizar tais ensaios bem como aplicações práticas e procedimentos são resumidos em livros (vide, por exemplo, P. Tijssen, In: Practice and theory of enzyme immunoassays, eds. R.H. Burdon e v. P.H. Knippenberg, Elsevier, Amsterdam (1990), pág. 221-278 e vários volumes de Methods in Enzymology, Eds. S.P. Colowick e outros, Academic Press, lidando com métodos de detecção imunológica, especialmente volumes 70, 73, 74, 84, 92 el21) . Os imunoensaios podem ser competitivos ou não competitivos.
Em certas modalidades, o anticorpo inventivo é imobilizado por ser covalentemente ou passivamente ligado à superficie de veiculo ou suporte sólido, o suporte sólido é qualquer suporte sólido conhecido na técnica a qual o anticorpo pode ser operativamente afixado; operativamente afixado se refere ao anticorpo sendo afixado em um modo que permite a formação de um complexo entre o anticorpo afixado e o dominio extracelular de Claudin-1. Os exemplos de materiais de suporte ou veiculo apropriados incluem, porém não são limitados a agarose, celulose, nitrocelulose, dextrano, Sefadex, Sefarose, carboxi metil celulose, poliacrilamidas, poliestireno, cloreto de polivinila, polipropileno, gabbros, magnético, resina de permuta de ions, copolimero de ácido maléico-éter-vinil-metila- poliamida, copolimero de aminoácido, copolimero de ácido maléico-etileno, náilon, seda e similar. A imobilização de um anticorpo na superficie de um suporte ou veiculo sólido pode envolver a reticulação, ligação covalente ou adsorção fisica, utilizando métodos bem conhecidos na arte. O suporte ou veiculo sólido pode estar na forma de uma conta, uma particula, uma cavidade de microplaca, um conjunto uma cubeta, um tubo, uma membrana ou qualquer outro formato apropriado para condição de um imunoensaio. Em certas modalidades, a imobilização de um antigeno para um suporte ou veiculo sólido inclui eletroforese de gel seguido por transferência para uma membrana (tipicamente nitrocelulose ou PVDF) em um processo denominado western blotting (ou imunoblot) bem conhecido na arte.
A presente invenção também provê kits que compreendem materiais, incluindo pelo menos um anticorpo monoclonal anti-Claudin-1 inventivo, útil para realizar os métodos de diagnóstico ou triagem descritos acima. Preferivelmente, o kit compreende uma combinação de reagentes em quantidades predeterminadas com instruções para executar um dos métodos. Em modalidades onde o anticorpo é rotulado com uma enzima, o kit incluirá substratos e co-fatores exigidos pela enzima (por exemplo, um precursor de substrato que provê o cromóforo ou fluóforo detectável). Além disso, outros aditivos podem ser incluidos como estabilizadores, tampões (por exemplo, um tampão de bloco ou tampão de lise) e similar. As quantidades relativas dos vários reagentes podem ser variadas amplamente para fornecer concentrações em solução dos reagentes que substancialmente otimizam a sensibilidade do ensaio, particularmente, os reagents podem ser fornecidos como pós secos, normalmente liofilizados, incluindo excipientes que mediante dissolução fornecerão uma solução reagente tendo a concentração apropriada. O anticorpo pode ser imobilizado ou não em uma superficie de substrato (por exemplo, contas, conjunto e similar) . Os kits podem conter também um aviso na forma determinada por um órgão governamental regulando a fabricação, uso ou venda de produtos farmacêuticos ou produtos biológicos.
Os seguintes exemplos descrevem alguns dos modos preferidos de fazer e pôr em prática a presente invenção, entretanto, deve ser entendido que os exemplos são para fins ilustrativos e não pretendem limitar o escopo da invenção. Além disso, a menos que a descrição em um exemplo seja apresentada no passado, o texto, como o resto do relatório descritivo, não pretende sugerir que experimentos foram na realidade executados ou dados são na realidade obtidos.
Alguns dos resultados relatados abaixo para antisoro policlonal foram apresentados no International Symposium on Hepatitis C Virus and Related Viruses (San Antonio, Texas, USA, 5-9 de outubro de 2008) e são resumidos em um Resume intitulado "Production of anti-claudinl antibodies potently inhibiting HCV infection reveals that Claudin-1 is required for an entry step closely linked to SR-BI and CD81" de S. Krieger e outros. Outros resultados são apresentados em S. Krieger e outros, "Inhibition of hepatitis C virus infection by anti-Claudin antibodies is mediated by inhibition of E2-CD81-CLDN1 association", que foi submetido para publicação em agosto de 2009 bem como S. Krieger e outros, "Monoclonal anti-claudin-1 antibodies for prevention and treatment of hepatitis C virus infection", que será submetido para publicação em outubro de 2009.
Células. Células de ovário de hamster chinês (CHO), células BOSC23, e células de hepatoma Huh7.5.1 utilizados nos presentes estudos foram descritos (Barth, 2005; Barth, 20 2003; Bartosch, 2003; Blight, 2002). Células BOSC23 são células de embalagem ecotrópica derivadas de HEK293 que não expressam CLDN1 endógeno (Pear, 1993). Hepatócitos humanos primários foram isolados e cultivados como descrito por David, 1998 (que é incorporado aqui a titulo de referência na integra).
Produção de anticorpos policlonais anti-CLDNl. anticorpos dirigidos contra o loop extracelular de Claudin- 1 humano foram criados por imunização genética de ratos Wistar utilizando um vetor de expressão pcCMVSport-6 contendo o cDNA de CLDN-1 humano de comprimento total (pcDNA CLDN-1). Em resumo, animais receberam cinco aplicações de pcDNA CLDN-1 por via intradérmica em intervalos de 2 semanas. 0 soro de controle pré-imune foi coletado do mesmo animal sangrado antes da imunização. Para analisar a especificidade do soro policlonal anti-CLDN-1 produzido, células BOSC23 ou CHO foram transfectadas com pcDNA (vetor de controle) ou pcDNA CLDN-1 utilizando transferência de gene mediada por lipossoma ((Lipofectamine; Invitrogen, Karlsruhe, Alemanha) de acordo com o protocolo do fabricante. Células BOSC23 ou CHO foram então incubadas com soro policlonal anti-CLDN-1 ou soro de controle pré-imune e analisadas para expressão de CLDN-1 de superficie de célula por citometria de fluxo como anteriormente descrito (Barth, 2005).
Caracterização de anticorpos policlonais anti-CLDNl por imunofluorescència. Células Caco2 e células Huh7.5.1 foram semeadas sobre laminulas de vidro, fixadas com 3% de paraformaldeido em PBS por 20 minutos, e coloridas por CLDNl utilizando anticorpos anti-CLDNl dirigidos contra os ectodominios de CLDNl (isto é, antiporos policlonais inventivos, "anti-CLDNl pAb", 50 μg/mL de IgG anti-CLDNl de rato), um anticorpo anti-CLDNl dirigido contra o dominio terminal-C intracelular ("anti-CLDNl mAb", clone IC5-D9, Abnova), e para o núcleo utilizando DAPI (4 ' , 6'-diamidino- 2-fenilindol). IgG policlonal de rato de controle ("pAb de controle") e IgG monoclonal de camundongo ("mAb de controle") foram utilizados como controles. Anticorpos primários ligados foram visualizados utilizando anticorpos secundários anti-rato-Cy5 e anti-camundongo Alexa Fluor® 488 e um microscópio Zeiss Axio Observer (Carl Zeiss S.A.S, Le Pecq, France).
Produção de ensaios de infecção e HCV recombinante. Plasmideos pFK-Jcl (Pietschmann, 2006) codificam o HCV JFH1 CDNA de comprimento total ou o genoma HCV quimérico designado Jcl que consiste em segmentos H6CF e JFH1. Sintese de RNA HCV in vitro e transfecção de RNA foram realizados como descrito (Wakita, 2005). Sobrenadantes de cultura a partir de células transfectadas foram depurados e concentrados como anteriormente descrito utilizando Amicon Ultra 15 (Millipore, Billerica, MA, EUA) e utilizados diretamente ou foram armazenadas a 4 °C ou -80 °C. os virus foram titulados utilizando o ensaio de diluição de limitação em células Huh7.5.1 com algumas modificações menores e TCID50 (a dose infectiva de cultura de tecido de 50%) foi calculada com. base no método descrito por Lindenbach, 2005. Células Huh7.5.1 foram misturadas cora soro de controle ou anti-CLDN-1 (iniciando em uma concentração de 5 ug/mL a 100 ug/mL) e pré-incubadas por 1 hora a 37°C. HCVcc foram adicionados e incubados por 16 horas a 37 °C. os sobrenadantes foram removidos e células incubadas em meio regular por 72 horas a 37 °C e infecção por HCV foi determinada por qRT-PCR. de RNA HCV intracelular como descrito. A neutralização mediada por anticorpo foi avaliada pela infectividade especifica.
Produção de pseudoparticulas de HCV retrovirais e inibição mediada por anticorpo de infecção por HCVpp. HCVpp contendo proteinas de envelope a partir da cepa H77 ou outras cepas e VSVpp foram geradas como descrito (Bartosch, 2003). HCVpp sem glicoproteinas de envelope (PP de controle) serviram como controle negativo. Para o estudo de neutralização mediada por anticorpo, células Huh7.5.1 foram semeadas no dia antes dos ensaios de infecção em placas com 96 cavidades em uma densidade de 0,5 x 104 células/cavidade. Células Huh7.5.1 foram misturadas com anti-CLDN-1 ou soro de controle (iniciando em uma diluição de 1/20) e pré-incubadas por 1 hora a 37°C. os sobrenadantes foram removidos e as células incubadas em meio regular por 72 horas a 37°C. a entrada de HCV foi determinada por análise de expressão de gene repórter de Luciferase como descrito. A neutralização mediada por anticorpo foi avaliada pela infectividade especifica de HCVpp na presença de soro anti-claudinl ou soro pré-imune.
Produção de anticorpos policlonais dirigidos contra o loop extracelular de Claudin-1 expresso em células BOSC23 ou CHO que expressam Claudin-1.
Para avaliar o papel de função de CLDN-1 na iniciação de infecção por HCV, soros anti-CLDN-1 policlonais de ratos dirigidos contra o loop extracelular de CLDN-1 foram primeiramente gerados por imunização genética como descrito acima. Após conclusão de imunização, anticorpos foram selecionados por sua capacidade em ligar-se a CLDN-1 humano expresso na superfície de célula de células CHO ou BOSC23 transfectadas não permeabilizadas, Como mostrado na figura 1, a incubação de células CHO que expressam CLDN-1 humano com anticorpos anti-CLDN-1 policlonais de ratos resultou em interação específica do soro com o ectodominio extracelular de CLDN-1 (figura 1B) . ao contrário, nenhuma interação foi vista em células CHO transfectadas com o vetor de controle pcDNA3.1 e incubadas com soro anti-CLDN-1 de rato ou nas células CHO incubadas com CLDN-1 humano que expressam cDNA e incubadas com soro pré-imune de rato (figura IA) ..
Para estudar se CLDN-1 anti-humano reconhece CLDN-1 em células suscetíveis a infecção por HCV, hepatócitos humanos em células de hepatoma Huh7.5.1 foram incubadas com os soros e analisadas por citometria de fluxo. Como mostrado na figura 2, a incubação de células Huh7.5.1 humanas (figura 2A) e hepatócitos humanos (figura 2B) com anticorpo anti-CLDN-1 policlonal de rato demonstrou que o anticorpo reconheceu CLDN-1 expresso em células alvo HCV incluindo hepatócitos humanos. Tomados juntos, esses dados demonstram que anticorpos policlonais anti-CLDNl produzidos por imunização genética se ligam ao ectodominio de CLDN1 humano expresso em hepatócitos humanos bem como células de hepatoma humano.
Caracterização de anticorpos policlonais anti-CLDN-1 por imunofluorescência. Os resultados obtidos por imunofluorescência são apresentados na figura 3. Demonstram que, como esperado, anticorpos policlonais anti-CLDNl ligados são localizados na superficie de célula.
Inibição de infecção por HCV por anticorpos policlonais anti-CLDN-1. Para avaliar o papel de CLDN-1 por infecção por HCV, a infecção JCVcc JFH1 de células Huh7.5.1 foi estudada na presença de anticorpos anti-CLDN-1 dirigidos contra epitopos dos loops extracelulares CLDN-1. A figura 4A mostra que soro de rato anti-CLDN-1 inibiu infecção HCVcc JC1 em mais de 80% em uma concentração de 100 ug/mL. ao contrário, o soro pré-imune de controle não teve efeito sobre infecção por HCVcc (figura 4A) . tomados juntos, esses dados demonstram que anticorpos dirigidos contra o ectodominio CLDN1 inibem eficientemente infecção por HCV.
Para confirmar que a inibição de infecção por HCVcc JFH1 foi realmente mediada por anticorpos anti-CLDN-1, IgG foi purificado de soro anti-CLDN-1 de rato e de soro de controle. Como mostrado na figura 4B, IgG purificado anti- claudin-1 inibiu acentuadamente infecção por HCVcc de células Huh7.5.1 em um modo similar a soro anti-CLDN-1. Ao contrário IgG de controle (100 ug/mL) purificado de soro pré-imune não inibiu infecção por HCVcc (figura 4B) . esses dados demonstram claramente que o efeito inibidor de soro anti-CLDNl é mediado por anticorpo anti-CLDNl e não por outras substâncias presentes no soro (como ligandos de CLDN-1 potencialmente interferindo na função de CLDN-1).
Além disso, o efeito inibidor de anticorpos anti- claudin-1 purificados sobre a infecção por HCV foi confirmado utilizando particulas pseudotipadas HCV retrovirais (HCVpp). Anticorpos anti-claudin-1, porém não anticorpos de controle, inibiram a infecção de células Huh7 por HCVpp em um modo dependente de dose (dados não mostrados).
Em conclusão, esses resultados demonstram que anticorpos policlonais anti-claudin-1 inibem eficientemente infecção por HCV.
Utilizando um anticorpo monoclonal anti-CD81, soro anti-SR-BI de rato, e soro anti-CLDNl de rato obtido como descrito acima, os requerentes mostraram que o bloqueio de CLDNl e CD81, ou CLDNl e SR-BI, ou CLDNl, CD81 e SR-BIT inibiu a infecção por HCVcc mais potentemente do que o bloqueio de cada fator de entrada individualmente (vide a figura 5(A)-(D)). tomados juntos, esses dados sugerem que CLDNl media entrada de HCV em cooperação com CD81 e SR-BI. O anticorpo monoclonal anti-CD81, soro anti-SR-BI de rato, e soro anti-CLDNIl de rato foram também verificados como inibindo infecção por HCVcc de células Huh7.5.1 com cinética similar, sugerindo que CLDNl, SR-BI e CD81 atuam quase simultaneamente durante o processo de entrada de HCV em células Huh7.5.1 (vide a figura 6).
Linhagens de células e hepatócitos primários. A cultura de Huh7 humano (Steinmann, 2004), Huh7.5.1 (Zhong, 2005), 293T (Pestka, 2007), BOSC23 (Pear, 1993), CHO de hamster (Barth, 2005) e células Hepal.6 de murino (Steinmann, 2004) foram descritas anteriormente. Hepatócitos de camundongo e humanos primários foram isolados e cultivados como descrito (Codran, 2006; Lan, 2008; Zeisel, 2007). Hepatócitos cinomolgos primários foram adquiridos de PRIMACYT Cell Culture Technology GmbH, Alemanha.
Ligação de Mabs anti-CLDNl a hepatócitos humanos primários e análise de competição cruzada.
Células Huh7.5.1 ou hepatócitos humanos ou cinomolgos primários (2 x 10b de células/cavidade) foram incubadas por 30 minutos em temperatura ambiente com concentrações crescentes de mAbs anti-CLDNl em solução salina tamponada com fosfato (PBS)-3% de soro de vitelo fetal (FCS). A ligação de mAb foi revelada por incubação com mAb de IgG anti-rato conjugado com PE (Southern Biotechnology Associates). Como controle, IgG2b de rato de isotipo casado (Genovac) foi utilizado. As aquisições de FACS e análise foram realizadas com um FACScan (Beckton Dickinson) e software CellQuest. A competição entre MAbs anti-CLDNl foi medida por um ELISA baseado em célula. Células de hepatoma humano Huh7.5.1 (2 x IO5 células/cavidade) foram semeadas em placas de 96 cavidades. Após bloquear as cavidades, as células foram incubadas por 60 minutos com 0,1 ug/mL de MAb anti-CLDNl biotinilado juntamente com concentrações crescentes de MAbs anti-CLDNl não rotulado como concorrentes. Após lavagem das células em PBS ligação de anticorpo biotinilado foi detectada por incubação com estreptavidina rotulada com peroxidase de raiz forte (BD) . A ligação foi medida como unidades de fluorescência relativa (590 nm) após lavagem e desenvolvimento com reagente Amplex Red. Curvas determinadas por medição de ligação na presença de um controle de isotipo casado foram comparadas com aqueles determinadas na presença do anticorpo concorrente. Rotulação de biotina foi executada utilizando Sulfo-NHS-LC-Biotina (Thermo Scientific) de acordo com as recomendações do fabricante.
Estudos de imageamento de CLDN1 de superficie de célula. Células Huh7.5.1 vivas foram incubadas com controle de isotipo de rato ou OM-7D3-B3 anti-CLDNl de rato (10 ug/mL) e um anticorpo secundário anti-rato conjugado com Cy5 (1/300; Jackson Immunoresearch) na ausência de reagentes de permeabilização. Após coloração, as células foram fixadas, montadas e observadas utilizando Leica LSR2 CLSM (IGBMC Imaging Center, Illkirch, França).
Mapeamento de epitopos alvejados por MAbs anti-CLDNl. Mapeamento de epitopo foi executado utilizando plasmideos pQCXIN-hClaudinl codificando para CLDN1 do tipo selvagem ou CLDN1 contendo mutações definidas introduzidas por mutagênese dirigida ao sitio (Cukierman, 2009). Esses plasmideos mutantes CLDN-1 foram gentilmente fornecidos por Dr. Tanya Dragic (Department of Microbiology and Immunology, Albert Einstein College of Medicine, Bronx, Nova York) . CLDN1 do tipo selvagem e mutante contêm uma hemaglutinina terminal-N citoplásmica (HA)-Tag, permitindo quantificação de eficiência de transfecçao e expressão de proteina (Cukierman, 2009). Para estudar a ligação de MAbs anti-CLDNl a CLDNl mutante, células BOS23 negativas-CLDNl foram transfectadas de forma transiente com construções de expressão CLDNl (0,05 ug DNA; Lipofectamina). 48 horas após, a ligação de anticorpo monoclonal OM-7D3-B3 ou OM- 8A9-A3 a células BOSC23 transfectadas de forma transiente com plasmideos pQCXUIN-hClaudinl foi determinada por citometria de fluxo. A quantificação de citometria de fluxo de expressão de HA-tag utilizando um anticorpo anti-HA serviu como controle interno. As células transfectadas foram permeabilizadas com Cytoperm/Cytofix (BD) para análise de expressão HA-Tag citoplásmico ou não tratadas para análise de interações de CLDNl mutante-anti-CLDNl. Para análise de FACS, células transfectadas foram incubadas com mAb anti-CLDNl ou anti-HA (Covance) por 30 minutos, seguido por incubação com 10 ug/mL mAb IgG anti-rato (para anti-CLDNl) ou 10 ug/mL de mAb IgG anti-camundongo rotulado com ficoeritrina (para anti-HA).
Produção e infecção por HCVcc. HCVcc (cepas Jcl, Luc- Jcl, Luc-Conl) foram geradas como descrito anteriormente (Haberstroh, 2008; Koutsoudakis, 2006; Pietschmann, 2006; Wakita, 2005; e Zeisel, 2007). Para experimentos de infecção, células Huh7.5.1 foram semeadas em placas de cultura de tecido de 48 cavidades em uma densidade de 2 x 105células/cavidade. As células foram pré-incubadas na presença ou ausência de anticorpos por 1 hora a 37 °C e então infectadas a 37°C por 4 horas com Jcl HCVcc ou Luc- Jcl HCVcc. 48 horas após, a infecção por HCV foi analisada em lisados de célula por quantificação de RNA HCV intracelular utilizando RT-PCR ou atividade de luciferase como descrito anteriormente (Haberstroh, 2008; Koutsoudakis, 2005; Tscherne, 2006; e Zeisel, 2007).
Produção e infecção de pseudoparticulas de HCV (HCVpp). HCVpp baseada em HIV ou MLV (cepas H77, HCV-J, JFH-1, UKN3A.1.28, UKN4A.21.16, UKN5.14.4, UKN6.5.340, VI, VJ, VD, VH, VK e VA-VY) e VSVpp foram produzidas como descrito (Lavilette, 2005; Bartosch, 2003; Pietschmann, 2006; Zeisel, 15 2007; Fafi-Kremer, 2009). Para experimentos de infecção, HEK293T, 293T/CLDN1+ e células Huh7.5 foram revestidas em placas de 24 cavidades no dia antes aos experimentos cinéticos como descrito anteriormente (Haberstroh, 2008). 72 horas após, as células foram lisadas e a entrada de HCVpp foi analisada por quantização de expressão de gene repórter de luciferase como descrito (Koutsoudakis, 2006).
Ensaios de toxicidade. Efeitos citotóxicos sobre células foram ensaiados em triplicata por análise da capacidade de metabolizar 3-(4,5-dimetil tiazoila-2-ila)- 2,5-difenil-brometo de tetrazólio (MTT) (Mosmann, 1983). Células Huh7.5.1 e hepatócitos humanos primários de três doadores diferentes foram incubados com anticorpo monoclonal de rato, anti-CLDNl OM-7D3-B3 (0.01-100 ug/mL), flavopiridol (10 (uM, Sigma) ou composto C (0.01-100 uM, Sigma). A concentração final de MTT foi de 0,6 mg/mL. Cristais de formazan produzidos pelas células foram solubilizados e medidos como descrito (Mosmann, 1983) .
Análise estatística. Os resultados foram expressos como a média ± desvio padrão (SD) . Análises estatísticas foram realizadas utilizando teste t de Student com um valor P de <0,05 sendo considerado estatisticamente significativo.
Produção de anticorpos monoclonais específicos para os domínios extracelulares de CLDN1 de superfície de célula. Cinco ratos foram imunizados com um cDNA de Claudin-1 humano de comprimento total (número de acessão NCBI : NM_021101) em um vetor de expressão de mamífero que aplica protocolos de imunização genética padrão utilizados por Genovac GmbH como resumido em outro lugar (Lohrmann, 2003, que é incorporado aqui a título de referência na com triagem baseada em um sistema Genovac descrito na patente alemã número DE 198 52 800 (que é incorporada aqui a titulo de referência na integra.) . Resumidamente, para essa triagem, soros e sobrenadantes de hibridoma são testados contra células de mamiferos transfectadas com construções de cDNA etiquetada que expressam os alvos contra os quais os anticorpos estão sendo gerados. Os vetores de DNA são de tal modo projetados que a proteina resultado é secretada e temporariamente ligada à membrana de plasma. Isso permite um ensaio de triagem baseado em células utilizando citometria de fluxo ou um ELISA baseado em célula.
Após vários reforços de DNA, os animais foram sacrificados, e soros e linfócitos foram coletados dos animais individuais. Soros de cada animal foram testados por citometria de fluxo para reconhecimento da proteina Claudin-1 humana, após transfecção transiente do cDNA de Claudin-1 em células de mamiferos (figura 7).
Os linfócitos a partir do rato 3 foram removidos e fundidos com células de mieloma de camundongo SP2/0/Agl4 (Número de ATCC: CRL-1581) utilizando condições PEG padrão e as hibridomas resultantes foram revestidas sobre placas de 96 cavidades sob condições de seleção padrão (vide, por exemplo, E. Harlow e D. Lane, in "Antibodies, A Laboratory capitulo 6, 1988, Cold Spring Harbor). Após duas Ill semanas, os sobrenadantes de hibridoma foram testados em um ELISA baseado em células contra células de mamíferos que tinham sido transfectadas de forma transiente com o cDNA Claudin-1 e as células transfectadas com um cDNA irrelevante como um controle de expressão negativo. Essa pré-seleção permitiu a identificação de hibridomas positivos que foram transferidos para expansão sobre placas de 24 cavidades seguido por placas de 6 cavidades e seus sobrenadantes foram testados novamente por citometria de fluxo contra células de mamíferos que tinham sido transfectadas de foram transiente com as mesmas construções de cDNA positivas e negativas como utilizado para ELIAS baseado em célula.
Uma análise da inibição de infecção com HCV infeccioso recombinante (HCVcc Luc-Jcl) por sobrenadantes de hibridoma contendo anticorpos anti-CLDN-1 foi então executada. Mais especificamente, células Huh7 foram incubadas com 100 μL de sobrenadante de hibridoma contendo anticorpos por 1 hora a 37°C. a seguir, HCVcc infeccioso (TCID 105/mL; derivado da cepa Luc-Jcl contendo um elemento repórter de luciferase) foram adicionados por 3 horas a 37°C. o sobrenadante foi então removido e substituído por meio novo (DMEM, 10% FBS) . Dois ou três dias após, a infecção virai foi quantificada por expressão de gene repórter de luciferase em Usados de célula (Zeisel, 2007) . Os resultados obtidos expressos como percentagem de infecção por HCVcc Luc-Jcl na presença ou ausência de sobrenadante de hibridoma (infecção na presença de PBS = 100%) são apresentados na figura 8. Como pode ser visto nessa figura, OM-3E5, OM-6D9, 10 OM-7C11, OM-4A4, OM-6E1, OM-7D3, OM-7D4, OM-7C8 e OM-8A9 mostraram uma iniciação acentuada de infecção por HCV, ao passo que 0M-5A1, OM-6G10 e OM-5A8 não mostraram efeito.
Após análise de sua atividade de bloqueio, os clones mães OM-3E5, OM-6D9, 0M-7C11, QM-4A4, OM-6E1, OM-7D3, OM- 7D4, OM-7C8 e OM-8A9 foram subclonados por revestir os mesmos em um meio semi-sólido, pegando as colônias de subclone resultantes e transferindo as mesmas para placas de 96 cavidades (OM7C11 revelou atividade de bloqueio porém como esse era um produtor ineficiente de anticorpos não foi subclonado). Os subclones resultantes foram pegos e testados novamente em relação a sua capacidade de ligar-se a CLDN1 humano expresso na superficie de célula de BOSC23 humano não permeabilizado, transfectado bem como células CHO de hamster transfectado. Células BOSC23 humanas são células de embalagem ecotrópica derivadas de HEK293 (Pear, 1993) que não expressam CLDN1 endógeno (dados não mostrados) . Os resultados dessas análises são apresentados na figura 9. Os seguintes subclones foram selecionados: 0M- 3E5-B6, OM-6D9-A6, OM-4A4-D4, OM-6E1-B5, OM-7D3-B3, OM-7D4- Cl, OM-7C8-A8 e OM-8A9-A3.
A incubação de células BOSC23 e CHO que expressam CLDNl humano com anticorpos CLDNl anti-humanos monoclonais resultou em uma interação específica com CLDNl humano (figura 9A e figura 9B).
Para estudar se os anticorpos CLDNl anti-humanos se ligam aos loops extracelulares de CLDNl na superfície de célula das células Huh7.5,l permissivas de HCV e hepatócitos humanos primários, as células foram incubadas com anticorpos anti-CLDNl e analisadas por citometria de fluxo na ausência de reagentes de permeabilização, A coloração positiva de células de hepatoma Huh7.5.1 humanas nativas e hepatócitos humanos com anticorpos anti-CLDNl demonstrou que esses anticorpos se ligam a CLDNl expresso na superfície da célula de hepatócitos primários e linhagens de células permissivas de HCV (figura 9C) . ao contrário, nenhuma coloração foi observada para células BOSC23 deficientes de CLDNl humanas (figura 9A) incubadas com mAbs anti-CLDN ou células Huh7.5.1, CHO/CLDN-i- ou hepatócitos humanos primários incubados com anticorpos de controle de isotipo (figura 9B) . a coloração de CLDNl de superfície de célula nativa por anticorpos monoclonais foi também confirmada por imunofluorescência em células Huh7.5.1 não permeabilizadas vivas (figura 9D) . tomados juntos, esses dados demonstram que anticorpos anti-CLDNl monoclonais produzidos por imunização genética se ligam especificamente aos loops extracelulares de CLDN1 nativo expresso na superfície de célula de linhagens de células permissivas de HCV e hepatócitos humanos.
Para investigar se anticorpos CLDN1 anti-humanos reagem de forma cruzada com CLDN1 de murino, a ligação de mAbs a CLDN1 de murino expresso em linhagens de células derivadas de fígado de murino foi estudada. De forma interessante, anticorpos anti-CLDNl monoclonais não interagiram com CLDN1 de murino expresso na linhagem de célula de hepatoma de camundongo Hepal.6. além disso, como mostrado na figura 9 anticorpos anti-CLDNl não coloriram linhagem de célula de hamster CHO. essas descobertas sugerem nenhuma reatividade cruzada de anticorpos de CLDN1 anti-humano com os loops extracelulares de CLDN1 de hamster ou de murino (figura 9 e figura 19) . Ao contrário, anti- CLDNl monoclonal de rato mostrou reatividade cruzada com hepatócitos primários do macaco cinomolgo primata não humano (Macaca fascicularis) (figura 9E). esses dados sugerem que o(s) epítopo(s) alvejados pelos anticorpos são conservados entre os primatas porém diferentes em roedores como camundongo ou hamster.
Cada subclone foi congelado e uma porção expandida em meio ISF-1 isento de soro (Biochrom AG, número do catálogo*. 9061-01). Os anticorpos foram purificados em uma coluna G 5 de proteina e suas concentrações foram determinadas em tampa PBS. Os isotipos foram determinados para cada clone utilizando um teste de ELISA comercial a partir de BD- Pharmingem (Número do catálogo 557081). A natureza das cadeias leves também foi determinada utilizando o mesmo kit ELISA comercial. Os resultados dessas análises são mostrados na tabela 1 abaixo. Tabela 1. Características dos anticorpos monoclonais secretados pelas linhagens de célula de hibridoma selecionadas
Caracterização de propriedades de ligação de mAbs anti-CLDNl a células permissivas de HCV e hepatócitos humanos primários. As propriedades de ligação de mAbs anti- CLDNl a células permissivas de HCV e hepatócitos humanos primários foram caracterizadas por citometria de fluxo. Como mostrado na figura 10, as concentrações de meia- saturação medidas para ligação a células Huh7.5.1 - que corresponde ao KD aparente dos anticorpos foram como a seguir: 7D3-B3 4 nM; 7D4-C1 5 nM; 8A9-A3 2 nM; 4A4-D4 9 nM, 6D9-A6 8 nM, 6E1-B5 3 nM, 7C8-A8 7 nM (Fig. 10A). concentrações de meia-saturação similares e KD aparente dos anticorpos foram obtidos para ligação de anticorpo a hepatócitos humanos primários (dados não mostrados). Esses resultados demonstram que anticorpos anti-CDLNl se ligam a linhagens de células permissivas de HCV e hepatócitos humanos com elevada afinidade.
Neutralização cruzada de Isolados de HCV de todos os genótipos principais e quasiespécie individual por anticorpos anti-CLDNl. Para investigar se os anticorpos produzidos por imunização genética eram capazes de inibir infecção por HCV, células Huh7.5.1 foram infectadas com virus repórter de luciferase de pirilampo J6/CF-HFH1 Luc-Jl (Koutsoudakis, 2006) na presença de anticorpos de controle de isotipo ou anti- CLDN1.
A figura 11 mostra que anticorpos anti-CLDNl monoclonais inibiram infecção por HCV de células Huh7,5.1 por virus Luc-Jcl e Luc-Conl em um modo dependente de dose ao passo que anticorpos de controle de isotipo não tiveram efeito inibidor. Tomados juntos, esses dados demonstram que anticorpos dirigidos contra os loops extracelulares de CLDN1 inibem infecção por HCV. Para tratar se os anticorpos anti-CLDNl eram capazes de neutralizar cruzado infecção por HCV de todos os principais genótipos, o impacto de anticorpos sobre a entrada de partículas pseudotipadas HCV (HCVpp) contendo glicoproteínas de envelope de HCV de genótipos HCV 1-6 foi analisada. Como mostrado na figura 12, anticorpos anti-CLDNl monoclonais inibiram eficientemente e dependentemente da dose infecção de células Huh7.5.1 com HCVpp de genótipos 1-6 com um IC50 para inibição de infecção por HCV que varia de 0,1 a 5 μg/mL. resultados similares foram encontrados em infecção de hepatócitos humanos primários (figura 13).
Um desafio principal para o desenvolvimento de antivirais e estratégias imunossupressoras é a elevada variabilidade do virus. HCV tem uma taxa de replicação muito elevada e a polimerase virai altamente propensa a erro permitem produção rápida de variantes virais secundárias denominadas "quasiespécies" que podem tomar a dianteira de respostas imunes celulares e humorais (Aurora, 2009; Farei, 2006; Ray, 2005; Uebelhoer, 2008). Essas variantes estão sob pressão imune constante no hospedeiro infectado, e processos de seleção levam à dominação das quasiespécies virais pelo vírus mais apto que pode evadir reconhecimento imune ou conferir resistência a terapias antivirais.
Para tratar de se anticorpos anti-CLDNl inibiram eficientemente a população de quasiespécies em pacientes individuais, as glicoproteinas de envelope de dois pacientes individuais infectados cronicamente com HCV foram clonados, seqüenciados e expressos. Como mostrado na figura 14, anticorpos anti-CLDNl neutralizaram amplamente infecção por HCV de glicoproteinas de envelope contendo HCVpp de quasiespécies de dois pacientes individuais. Esses dados demonstram que anticorpos anti-CLDNl neutralizam de forma cruzada infecção por HCV de todos os principais genótipos bem como isolados da população de quasiespécie de um paciente individual.
Neutralização de quasiespécies de HCV e cepas virais tendo anticorpos de neutralização de hospedeiro escapado e reinfecção do enxerto de fígado. A doença de fígado no estágio final devido à infecção crônica por HCV é uma causa principal para transplante de figado. Devido à evasão virai das respostas imunes de hospedeiro e a ausência de estratégias antivirais preventivas, a reinfecção do enxerto é universal e caracterizada por avanço acelerado de doença de fígado. Utilizando hepatócitos humanos primários e pseudotipos de HCV retroviral contendo glicoproteínas de envelope virais derivadas de pacientes infectados com HC sendo submetidos a transplante de fígado. Os requerentes demonstraram anteriormente que a entrada e escapamento virai aumentado de neutralização mediada por anticorpo são determinantes chave para seleção de variantes virais durante reinfecção por HCV do enxerto de fígado (Fafi- Kremer, 2009, submetido para publicação).
No presente estudo, glicoproteínas de envelope que exibem HCVpp de pacientes sendo submetidos a transplante de fígado e reinfecção por HCV foram utilizados para avaliar se anticorpos anti-CLDNl são capazes de inibir infecção de hepatócitos humanos primários com isolados virais que tinham respostas de neutralização de hospedeiro escapado e tinham resultado em reinfecção do enxerto de fígado. Para obter esse objetivo, os requerentes estudaram o efeito de anticorpos anti-CLDNl na entrada de glicoproteínas de envelope contendo HCVpp a partir de cepas HCV selecionadas durante transplante e reinfecção do enxerto de fígado (cepas HCV VD, VH, VK). como mostrado na figura 15, a pré- incubação de células com anticorpo anti-CLDNl inibiu acentuadamente a entrada de HCVpp derivado de paciente em hepatócitos humanos primários. Esses dados demonstram claramente que anti-CLDNl inibe especificamente entrada de HCV de isolados derivados de paciente reinfectando o enxerto de fígado.
As análises de viabilidade de células com base em teste MTT foram realizadas para tratar de efeitos tóxicos em potencial de anticorpos anti-CLDNl. Nenhum efeito tóxico foi detectado em uma análise lado a lado de viabilidade de células com base em teste de MTT mesmo em doses elevadas de anti-CLDNl (figura 16) . Ao contrário, o composto C - um inibidor de AMPK bem caracterizado com toxicidade conhecida - resultou em toxicidade facilmente detectável (figura 16) .
Ligação de anticorpos anti-CLDNl monoclonais depende de conservação do motivo altamente conservado W(30)- GLW(51)-C(64) em loops extracelulares de CLDN1. Finalmente, os requerentes se dirigiram para mapear o(s) epítopo(s) alvejados por anticorpos anti-CDLNl monoclonais. Experimentos de competição cruzada foram realizados utilizando os seis anticorpos monoclonais para pesquisar se MAbs anti-CLDNl reconhecem epitopos não relacionados, similares ou diferentes. A ligação de OM8A9-A3 ou OM-7D3-B3 rotulado a células Huh7.5.1 foi medida após pré-incubação com concentrações crescentes de um IgG casado com isotipo de controle ou o mAbs anti-CLDNl. A co-incubação com todo mAb anti-CLDN2 reduziu a ligação de 8A9-A3 para anti-CLDNl exibido em superficie de célula em quase 80%, enquanto o IgG de controle não prejudicou o reconhecimento de células Huh7.5.1 (figura 17A). Resultados similares foram obtidos não somente para OM-8A9-A3 ou OM-7D3-B3 como para todos mAbs OM demonstrados utilizando concentrações saturadas de inibir mAbs (figura 17B). os resultados obtidos no ensaio de ligação foram confirmados por executar estudos de competição cruzada em experimentos de infecção. Como mostrado na figura 17C, a combinação de anticorpos anti- CLDNl diferentes não mostrou um efeito aditivo ou sinergista acentuado na magnitude de inibição de infecção por HCV. Além de confirmar os resultados obtidos em estudos de ligação, esses resultados sugerem que todos os seis anticorpos anti-CDLNl reconhecem um motivo estreitamente relacionado ou similar nos loops extracelulares de CLDN1. Dados de seqüenciamento provisional, entretanto em dois dos anticorpos monoclonais indicam que variam em seqüência para as cadeias pesadas e leves (dados não mostrados).
As interações dos seis anticorpos monoclonais com urn painel de mutantes de CLDNl descrito por Cukierman e co- trabalhadores (Cukierman, 2009) foram estudados para definir adicionalmente o motivo alvejado pelos anticorpos. Utilizando uma abordagem de mutagênese de varredura de alanina, Cukierman e co-trabalhadores tinham identificado sete resíduos no primeiro loop extracelular CLDNl que são críticos para entrada de isolados de HCV tirados de seis subtipos diferentes, grande parte dos resíduos críticos pertencem ao motivo W(30)-GLW(51)-C(54)-C(64), que é altamente conservado entre todos os claudins humanos (Cukierman, 2009). Utilizando células BOSC23 transfectados de forma transiente que expressam moléculas de CLDNl do tipo selvagem e mutantes, os requerentes demonstraram que a substituição de resíduos de aminoácido por alanina nas posições 30, 35, 49, 50, 51, 54 e 64 de CLDNl reduziu drasticamente a ligação de anticorpo monoclonal OM-7D3-B3, ao passo que as outras mutações não afetaram a interação de anticorpos (figura ISA).
Estudos anteriores mostraram que o resíduo 132 é importante para entrada (Evans, 2007) e o resíduo D38 próximo (Cukierman, 2009) foi igualmente importante para entrada virai. De forma interessante, mutagênese desses resíduos ainda permitiu ligação parcial de anticorpos anti- CLDN1 (figura 18) sugerindo que esses residues desempenham um papel menos importante para interação CLDN-l-anti-CLDNl. Além disso, a análise de ligação anti-CLDNl a CLDN1 mutante demonstram que o residuo Y35 parece ser reconhecido por 5 anticorpos anti-CLDNl monoclonais (figura 18A e B) . a expressão adequada De CLDN1 mutante e do tipo selvagem em células BOSC23 transfectadas de forma transiente foi confirmada por análise de citometria de fluxo de niveis de expressão HA-tag e anticorpo anti-HA (figura 18AB) exceto 10 por I32A mutante onde o HA tag estava ausente (figura 18AB) e expressão de CLDN1 foi avaliada por análise FACS utilizando um anticorpo não relacionado dirigido contra o dominio de terminal-C CLDN1 não mudado (I32A mutante; dados não mostrados). Um padrão similar foi observado para 15 anticorpo OM-8A9-A3 (figura 18B). esses resultados sugerem que mAbs reconhecem epitopos dependentes de conformação afetados pelo motivo W (30)-GLW (51)-C (54)-C (64) que foram identificados como co-residuos essenciais para entrada de HCV (Cukierman, 2009).
pela primeira vez, anticorpos monoclonais foram gerados contra os loops extracelulares de Claudin 1 que neutralizam de forma cruzada de forma potente infecção por HCV a partir de todos os genótipos principais. O reconhecimento depende fortemente da conservação do motivo W (30)-GLW(51)-C(54)-C(64) de loop extracelular de CLDN1 humano 1. O fato de se esse motivo representa o epítõpo, ou se as mutações que afetam o reconhecimento causam alterações de conformação que levam à perda de ou mascaramento desse epitopo permanece a ser determinado, anticorpos anti-CLDNl inibem de forma cruzada entrada de isolados HCV em pacientes individuais bem como entrada de variantes HCV principais selecionadas durante transplante de figado utilizando glicoproteinas de envelope derivadas de paciente com HCVpp de quatro pacientes com reinfecção por HCV durante transplante de figado.
Uma principal limitação de terapias antivirais atuais e em desenvolvimento que alvejam o virus é o desenvolvimento rápido de resistência virai. Um desafio principal para o desenvolvimento de antivirais e estratégias imunopreventivas é a alta variabilidade do virus. HCV tem uma taxa de replicação muito elevada e a polimerase virai altamente propensa a erro permite produção rápida de variantes virais secundários denominados "quasiespécie" que podem tomar a dianteira de resposta imune humoral e celular e resultam em isolados virais que conferem resistência viral a terapia antiviral convencional (Aurora, 2009). Alvejar fatores hospedeiros essenciais pode representar uma alternativa complementar. Se escapamento virai ocorrer, consistirá em mecanismos diferentes e fatores virais. 0 fato de que anticorpos anti-CLDNl inibem similarmente infecção por HCV de isolados virais de todos 5 os genótipos e quasiespécies em pacientes individuais sugere a ausência de variantes preexistentes ou genótipos resistentes a anticorpos anti-CLDNl.
Por desenvolver anticorpos anti-CLDNl neutralizando de forma cruzada eficientemente infecção por HCV, os 10 requerentes demonstraram uma prova de conceito para CLDNl como alvo para estratégias antivirals novas. Uma vez que a entrada de HCV é a primeira etapa de interações de hospedeiro-virus e um alvo principal de respostas de neutralização de hospedeiro, representa um alvo promissor 15 para terapias antivirais que podem complementar esforços continuos para bloquear eventos de replicação intracelular com inibidores das protease HCV e polimerase (Stamataki, 2008; Timpe e McKeating, 2008; Zeisel, 2008). O desenvolvimento clinico bem sucedido de inibidores de 20 entrada para outras infecções virais como HIV (Este e Telenti, 2007) destaca a relevância da etapa de entrada virai como um alvo terapêutico ou preventivo.
Uma aplicação importante de anticorpos monoclonais pode ser a prevenção de reinfecção por HCV após transplante de fígado. Uma limitação atual principal de transplante de fígado (LI) é a reinfecção por HCV universal do enxerto seguido por um curso acelerado de doença de figado induzida por HCV (Brown, 2005). Uma estratégia profilática para 5 prevenção de reinfecção não existe e terapias antivirais a base de interferon têm eficácia limitada e tolerabilidade em receptores de LT (*Brown, 2005). Devido à evasão virai de respostas imunes hospedeiras e a ausência de estratégias antivirais preventivas, a reinfecção do enxerto é universal 10 e caracterizada por avanço acelerado de doença de fígado (Brown, 2005). utilizando hepatócitos humanos primários e pseudotipos de HCV retrovirais contendo glicoproteínas de envelope virais derivadas de pacientes infectados por HCV sendo submetidos a transplante de fígado, a equipe de um 15 dos requerentes demonstrou anteriormente que a entrada virai aumentada e escapamento de neutralização mediada por anticorpo são determinantes principais para seleção de variantes virais durante reinfecção por HCV do enxerto de fígado (Fafi-Kremer, 2009, submetida para publicação).
No presente estudo, os requerentes mostraram que anticorpos monoclonais anti-CLDNl inibiram eficientemente infecção por HCV de hepatócitos humanos primários com isolados tendo resposta imune de célula hospedeira escapade durante transplante de fígado. A neutralização eficiente de variantes variais tendo escapado das respostas de neutralização de paciente por um anticorpo anti-CLDNl de neutralização cruzada demonstra que a entrada de HCV é um alvo viável para estratégias antivirais que evitam reinfecção do enxerto. Essa descoberta é adicionalmente apoiada por estudos recentes em um modelo de camundongo humanizado para infecção por HCV, demonstrando que anticorpos anti-E2 e anti-CD81 monoclonais foram capazes de neutralizar isolados de HCV geneticamente diversos e protegem controla desafio de quasiespécie de HCV heterólogo (Meuleman, 2008; Law, 2008). Desse modo, a administração de anticorpos anti-CLDNl de neutralização cruzada monoclonais, com ou sem terapia antiviral concomitante, pode oferecer uma opção viável e promissora para evitar reinfecção de HCV do fígado transplantado.
Uma limitação em potencial para o uso de anticorpos anti-receptores para prevenção ou tratamento de infecção por HCV poderia ser toxicidade. Fatores de célula hospedeira têm funções importantes que podem ser ligadas a mecanismo de entrada virai. Desse modo, anticorpos que ligam a fatores de entrada de HCV podem alterar a função ou expressão de receptores resultando em efeitos colaterais. De forma interessante, nenhum efeito tóxico foi detectado em uma análise lado a lado de viabilidade de célula com base em teste MTT mesmo em doses elevadas de anti-CLDNl (figura 16) . A esse respeito, é de interesse observar que os requerentes demonstraram anteriormente que antisoro anti-CLDNl policlonal não teve efeito sobre a 5 permeabilidade de junção apertada e integridade em células de hepatoma HepG2 polarizadas (Krieger, 2009, manuscrito submetido). Embora estudos adicionais sejam necessários para tratar de toxicidade in vivo, os estudos de toxicidade piloto executados pelos requerentes em células permissivas 10 de HCV e hepatócitos humanos sugerem que anticorpos anti- CLDNl podem ser bem tolerados.
O que é o mecanismo de neutralização de infecção por HCV por anticorpos anti-CLDNl monoclonais? CLDNs são componentes críticos de junções apertadas e têm uma 15 topologia de tetraspanina com quatro domínios de transmembrana, dois loops extracelulares e um intracelular, e domínios citoplásmicos de terminal C e N (Van Itallie e Anderson, 2006). O loop extracelular CLDNl (ELI) foi mostrado como sendo exigido para entrada de HCV (Evans, 20 2007) e está envolvido em função de barreira e contribui para formação de poro entre células polarizadas (Krause, 2008). Os estudos de mutagênese em células HEK293T não polarizadas demonstraram que o enriquecimento de CLDNl em contatos de célula-célula pode ser importante para entrada de HCV (Cukierman, 2009) . Utilizando uma variedade de técnicas de imageamento e bioquímica, vários laboratórios reportaram que CLDN1 associa com CD81. Dados mais recentes do laboratório dos requerentes, mostraram que CLDN1 media entrada de HCV por formar um complexo de vírus/co-receptor incluindo HCV E2, CD81 e CLDN1, que é exigido para entrada viral (vide o exemplo 3). Os requerentes demonstraram ainda que anticorpos anti-CLDNl neutralizam infectividade por HCV por reduzir associação de E2 com a superfície de célula e romper interações de CD81-CLDN1 (vide o exemplo 3).
De forma interessante, embora a magnitude de inibição parecesse ser similar para infecção de células Huh7.5.1 com HCVcc (figura 1) e HCVpp (figura 12), a magnitude de inibição de infecção por HCVpp pareceu ser mais acentuada em hepatócitos humanos primários em comparação com células Huh7.5.1 (figura 13-15 e dados não mostrados). Isso pode ser devido ao fato de que a expressão de receptores ou complexos de co-receptor pode ser diferente em hepatócitos humanos primários parcialmente polarizados em comparação com linhagens de células de hepatoma huh7 não polarizadas.
Os estudos de infecção e ligação de anticorpo de competição cruzada mostraram claramente que anticorpos monoclonais alvejaram um domínio de epítopo estreitamente relacionado (figura 17). Utilizando um painel de mutantes de CLDN1 bem caracterizados, os requerentes demonstraram que a substituição de aminoácidos nas posições 30, 35, 49, 50, 51, 54 e 64 de CLDNl ELI por alanina reduziu drasticamente a ligação de anticorpo monoclonal OM-7D3-B3 a CLDN1, ao passo que a interação de anticorpos com outros mutantes não foi afetada ou foi afetada a um ponto menor (figura 19).
Esses dados sugerem que mAbs reconhecem um epitopo presente no cluster de resíduos de aminoácidos compreendendo W(30)-GLW(51)-C(54)-C (64) do CLDNl ELI ou um epitopo que pode se tornar perdido ou mascarado através de alterações estruturais. No caso anterior, como esses aminoácidos conservados não são estruturalmente agrupados juntos, é provável que os epítopos reconhecidos sejam dependentes de conformação. Essa hipótese é adicionalmente apoiada pela descoberta de que a pré-incubação de anticorpos com peptídeos lineares codificando aminoácidos do CLDNl ELI não foi capaz de reverter inibição de infecção mediada por anticorpo (dados não mostrados). Além disso, anticorpos anti-CLDNl produzidos por imunização genética não mostraram uma interação facilmente detectável com peptídeos CLDNl lineares como antígenos em um ELISA (dados não mostrados). extracelular CLDNl e alvejados pelos anticorpos monoclonais foram mostrados como sendo criticos para entrada de isolados de HCV tirados de seis subtipos diferentes (Cukierman, 2009). O fato de que anticorpos anti-CLDNl monoclonais alvejando esse epitopo neutralizam de forma cruzada eficientemente a entrada de isolados de HCV a partir de seis isolados diferentes destaca adicionalmente a relevância desses residuos de CLDNl para entrada de HCV. É de interesse observar que as substituições de alanina desses residuos não prejudicaram a expressão de superficie de célula CLDNl (Cukierman, 2009) . Uma vez que anticorpos policlonais produzidos pela mesma abordagem foram mostrados como rompendo o complexo de co-receptor/virus incluindo HCV E2, CD81 e CLDNl (exemplo 3) , é concebivel que os residuos de aminoácidos alvejados em ELI desempenham um papel importante para a formação de complexo de co-receptor CLDN1-CD81-E2 que é essencial para entrada virai. Estudos adicionais estão em andamento para tratar dessa questão.
Em conclusão, anticorpos monoclonais que são dependentes da conservação do motivo W(30)-GLW(51)-C(54)- C(64) em CLDNl ELI foram produzidos que neutralizam de forma cruzada a infecção por HCV. Esses resultados definem residuos em CLDNl ELI que são cruciais para a entrada de HCV e são acessíveis para anticorpos que bloqueiam infecção por HCV. Finalmente, os dados sugerem que alvejar CLDN1 ELI utilizando anticorpos anti-CLDNl monoclonais constitui uma abordagem antiviral nova para evitar infecção por HCV primaria, como após transplante de figado e poderia também refrear a difusão de virus em pacientes cronicamente infectados.
Linhagens de células. Como descrito no exemplo 2. Células HEK293T/CLDN1+ (clone IIIA6) foram obtidas por transfecção estável de células HEK293T com um vetor pcDNA3.1 que codifica cDNA CLDN1. Anticorpos. Como descrito no exemplo 2. Além disso, anticorpos anti-SR-BI ou CD81 de rato policlonais foram obtidos por imunização genética como descrito (Zeisel, 2007). IgG anti-rato de cabra conjugado com ficoeritrina-R era de Jackson ImmunoResearch Laboratories, IgG de camundongo de Caltag, anti-CD81 de camundongo (JS-81) de BD Biosciences.
Ligação celular de glicoproteínas de envelope de HCV e virions infecciosos. A produção e ligação de glicoproteínas de envelope truncadas terminalmente-C El e E2 para células alvo foram descritas (Haberstroh, Dreux, 2009) . Para o estudo de interação de fator de entrada-E2, células CHO foram transfectadas de forma transiente com vetores de expressão baseados em pcDNA3 codificando SR-BI; CD81 ou CLDNl (Barth, 2005). A expressão de fatores de entrada foi avaliada por citometria de fluxo utilizando anticorpos anti-receptores como descrito anteriormente (Barth, 2005). Para o estudo de ligação de glicoproteína de envelope na presença de anticorpos anti- receptores, células Huh7.5.1 (Zhong, 2005) foram pré- incubadas por 1 hora em temperatura ambiente com anti-SR-BI de rato, anti-CLDNl e soro anti-CD81 (1/100) ou CD81 anti- humano de camundongo (JS-81, 5 ug/mL) ou anticorpos de controle (1/100 ou 5 ug/mL). E2 recombinante (30 uL de sobrenadante de cultura de célula concentrada) ou El (10 ug/mL) foi adicionado a células por 1 hora em temperatura ambiente. Após lavagem com PBS, glicoproteinas de envelope ligadas foram detectadas utilizando citometria de fluxo e anti-El humano (IGH526; Haberstroh, 2008) ou anti-His de camundongo (RGS-His, Qiagen) e anticorpos secundários conjugados de PE (Dreux, 2009; Barth, 2008). Para o estudo de ligação de células Huh7.5.1 permissivas a HCVcc, células Huh7.5.1 foram pré-incubadas com heparina, anti- CLDNl de rato, anti-SR-BI de rato ou soro pré-imune de rato de controle (PI) (todos diluidos 1/100) por 1 hora em temperatura ambiente antes da incubação com HCVcc (cepa Jcl) que tinha sido parcialmente purificado de sobrenadantes de cultura de célula utilizando ultracentrifugação de gradiente. Após incubação com HCVcc, HCVcc não ligado foi removido por lavagem de células com PBS. A ligação de HCVcc foi então quantificada por RT-PCR ou HCV-RNA ligado por célula como descrito por Ploss e outros (2009).
Associação de receptor utilizando transferência de energia de ressonância de fluorescência. Interações homotipicas e heterotipicas de CD81 e CLDNl foram analisadas como descrito (Harris, 2008; Mee, 2009) . Resumidamente, células HEK293T transduzidas para expressar AcGFP e CD81 etiquetada DsRED e CLDNl foram cultivadas em laminulas de vidro e fixadas em metanol gelado. As células foram imageadas em um LSCM de cabeça meta Zeiss, com ajustes de microscópio otimizados para cada proteina fluorescente para obter a razão mais elevada de sinal para ruido. Para análise FRET, o método de fotoalvejamento de aceptor gradual de FRET foi utilizado, que abrangeu fotoalvejar o fluóforo DsRED gradualmente com o passar do tempo enquanto monitora a intensidade fluorescente AcGFP (Harris, 2008). Após correção de diafonia e background, qualquer aumento em intensidade de AcGFP após fotoalvejamento de DsRED é devido a FRET entre proteínas, indicando uma distância menor do que 10 nm. A percentagem de FRET é definida como o número de pixels que exibem FRET sobre o número total de pixels analisados na membrana de 5 plasma das células (Harris, 2008). A intensidade de AcGFP e CD81 etiquetada DsRED e CLDN1 (unidades de fluorescência arbitrárias/pixel) na membrana de plasma provê 500 a 1000 medições por célula. Os dados de 10 células foram normalizados e a expressão localizada foi calculada.
anti-CLDNl inibe ligação de glicoproteína de envelope E2 e virions infecciosos a células permissivas de GCV na ausência de interação de CLDN1-E2. Para investigar se anticorpos anti-CLDNl poderiam interferir em ligação E2 15 para linhagens de células permissivas, estudos de ligação foram realizados utilizando glicoproteínas El e E2 recombinantes na presença de anticorpos de controle ou anti-receptor. Como mostrado na figura 20B, anticorpos anti-CD81, anti-CD81, e anti-SR-BI e anti-CLDNl inibiram a 20 ligação de E2 a células Huh7.5.1. ao contrário, soro de controle não relacionado ou pré-imune não teve efeito (figura 20A-C). de forma interessante, a magnitude de inibição de ligação de E2 a células Huh7.5.1 (figura 20C) correlacionou com a magnitude de inibição de infecção por HCV, sugerindo que a inibição de ligação de interações de superficie de célula E2 provê um mecanismo de ação para a atividade de neutralização dos anticorpos anti-CLDNl. A relevância dessas observações para virions infecciosos foi adicionalmente confirmada por estudos de ligação utilizando HCVcc (figura 20E) . ao contrário, a ligação El não foi afetada por anti-CLDNl (figura 20D) . para estudar se a inibição de anticorpo de ligação de E2 a linhagens de células permissivas era atribuivel a interações de CLDNl com E2, os requerentes investigaram se CLDNl era capaz de ligar glicoproteína truncada recombinante E2. para tratar dessa questão, células CHO foram construídas para expressa CLDNl humano, SR-BI ou CD81 (figura 21A) . a expressão de superficie de célula de CD81 humano ou SR-BI humano conferiu ligação E2 a células CHO (figura 21B), ao passo que a expressão CLDNl não teve efeito (figura 21B) . esses dados sugerem que CLDNl não interage diretamente com glicoproteína de envelope HCV E2 e que o bloqueio de anticorpo de interações de superficie de célula-E2 pode ser mediado por mecanismos indiretos.
Anticorpos anti-CLDNl inibem associação (ões) de coreceptorde CD81-CLDN1. Uma vez que anticorpos anti-CLDNl inibem a ligação de E2 a células permissivas de HCV na ausência de uma interação de E2-CLDN1 direta (figura 21B) , os requerentes levantaram a hipótese de que anticorpos anti-CLDNl podem interferir nos complexos co-receptores CD81-CLDN1. Para avaliar se anticorpos anti-CLDNl alteram a associação CLDN1-CD81, células HEK293T foram transfectadas para expressar Ac-GFP-CD81 e DsRED-CD81 ou AcGFP-CLDNl e DsRED-CD81 ou AcGFP-CLDNl e DsRED-CLDNl, incubados com soro pré imune e anti-CLDNl (1/100 e 1/400) e interação(ões) co-receptora(s) analisadas por FRET. Como mostrado na figura 22, anticorpos anti-CLDNl reduziram signif icat ivamente FRET entre CD81 e CLDNl em um modo dependente de dose. A pré-incubação de células com soro de controle não modificou interação(ões) de co-receptor CD812- CLDN1. A inibição de interação de co-receptor CD81-CLDN1 foi específica como mostrado pelo FRET inalterado entre CD81-CD81 e CLDN1-CLDN1 após pré-incubação com soro anti- CLDNl. Tomados juntos, esses dados sugerem que anticorpos anti-CLDN12 interferem na associação de heterodimero CD81- CLDN1.
CLDNl é um co-fator essencial que confere entrada de HCV. Entretanto, o papel preciso de CLDNl no processo de entrada de múltiplas etapas permanece pouco entendido, utilizando células CHO transfectadas que expressam fatores de entrada de HCV humano, os requerentes demonstraram que em contraste com CD81 e SR-BI, CLDN1 não interage diretamente com glicoproteina de envelope E2 na superfície de célula, utilizando um sistema à base de FRET para estudar associação de cor-receptor CD81-CLDN1, anticorpos 5 anti-CLDNl de neutralização da invenção foram mostrados como especificamente rompendo CD81-CLDN1 FRET (figura 22).
Esses dados sugerem que anticorpos que alvejam CLDN1 neutralizam infectividade de HCV por reduzir associações de E2 com a superfície de célula e reduzir interações de 10 CDE81-CLDN1. Os complexos de co-receptor CD81-CLDN1 são críticos para entrada de HCV e CLDN1 pode potenciar associação de CD81 cora partículas de HCV através de interações de E2. Também fornecem um novo caminho para estratégias antivirais que alvejam interações E2-CD81- 15 CLDN1.
Ensaio de transmissão de célula-célula. Células Huh7.5.1 foram fornecidas por F. Chisari (The Scripps Research institute, EUA; Zhong, 2005) e foram cultivadas como descrito (Zeisel, 2007; Barth, 2008; Dimitrova, 2008). células GFP Huh7 foram fornecidas por Dr. Patel (University of Glasgow, RU; Witteveldt, 2009). Linhagens de células derivadas de Huh7 tinham sido obtidas por transdução com um vetor retrovirus que carrega proteina fluorescente verde intensificada (EGFP), seguido por seleção em meio suplementado com 300 ug de G418/mL (Witteveldt, 2009) . Para detectar transmissão de célula-célula de HCV, células Huh7.5.1 recentemente submetidas a eletroporação foram semeadas e incubadas por um periodo de 24 horas, e então lavadas com meio para remover HCV ligado por superficie de célula residual antes de adicionar as células receptoras que expressam EGFP com 10 ug/mL de anticorpos anti-CLDNl. As células co-cultivadas foram crescidas até confluência, tripsinizadas, fixas com 1% de paraformaldeido e permeabilizadas com 0,1% de saponina para análise FACS. As células foram coloridas utilizando anticorpo anti-núcleo de camundongos seguido por um anticorpo secundário conjugado de ficoeritrina (PE) para análise FACS como descrito anteriormente para SR-BI (Barth, 2006; Barth, 2008).
Em geral, virus podem disseminar em um hospedeiro por dois mecanismos incluindo liberação de virions livres de células e passagem direta entre células infectadas e não infectadas. A transferência direta de célula-célula é considerada como sendo mais rápida e eficiente do que a difusão livre de células porque evita etapas iniciais de limitação de taxa no ciclo de vida do virus, como fixação de virion. Além disso, a transferência de célula-célula de infectividade virai pode permitir que virus escapem de elementos da resposta imune, como anticorpos de neutralização.
Estudos recentes mostraram que a infecção por HCV de células de hepatoma resulta em áreas focais de infecção que são potenciadas por contato de célula-célula, sugerindo transmissão localizada entre células adjacentes. Realmente, com o uso de células receptoras ou produtoras rotuladas, dois laboratórios demonstraram que HCV pode ser transmitido in vitro por infecção de virus tanto livre de células como transferência direta entre células, a última oferecendo uma via nova para evadir anticorpos de neutralização (Timpe, 2008; Witteveldt, 2009).
Para avaliar a capacidade de anticorpos monoclonais anti-CLDNl inibirem transmissão de célula para célula, um ensaio de transmissão de célula para célula foi estabelecido com base em células receptoras rotuladas que expressam proteina de fluorescência verde (GFP). Nesse ensaio, células produtoras de HCV são co-cultivadas com células receptoras rotuladas com GFP na presença ou ausência de anticorpos anti-receptores. Por bloquear a transmissão de vírus livre de células com anticorpos anti- CD81 (Timpe, 2008; Witteveldt, 2009) esse ensaio permite estudar o efeito específico de antivirais sobre a transmissão de célula-célula por quantificar células receptoras HCV+, GFP+ em análise de FACS.
Após uma co-cultura de 24 horas de células produtoras e receptoras na ausência de anticorpos (ou anticorpos de controle), 43,6% de todas as células correspondem células receptoras HCV+ GFP+ (figura 23A) . ao bloquear transmissão livre de células por anticorpos anti-CD81 (figura 23B), o número de células receptoras HCV GFP+ diminuiu para 6,20%. Essas células correspondem a células exclusivamente infectadas por transmissão de célula para célula como mostrado anteriormente por dois outros laboratórios (Timpe, 2008; Witteveltd, 2009) e o laboratório dos requerentes (Baurmert, observações não publicadas). Como mostrado na figura 23C, anticorpos monoclonais anti-CLDNl reduziram acentuadamente o número de células receptoras HCV+, GFP+. A adição de anticorpo monoclonal anti-CLDNl 7D3 reduziu a percentagem de células receptoras GFP+ infectadas por HCV de 6,20% para 2,98%, sugerindo que o anticorpo monoclonal anti-CLDNl foi capaz de reduzir infecção por transmissão de célula-célula em mais de 50%. Ao contrário, anticorpos de controle de isotipo não tiveram efeito (dados não mostrados) . Esses resultados indicam que anticorpos monoclonais anti-CLDNl inibem transmissão de célula para célula de HCV.
Para confirmar a relevância dessa descoberta para 5 difusão virai em um sistema de cultura de tecido infeccioso, os requerentes realizaram experimentos de curso de tempo em células Huh7.5.1. para estudar o efeito de anticorpos anti-CLDNl monoclonais em difusão virai, o anticorpo monoclonal anti-CLDNl OM-7D3 foi adicionado 4 10 horas após infecção de células com virus livre de célula.
Como mostrado na figura 24, o anticorpo monoclonal anti- CLDNl inibiu eficientemente a difusão virai. Embora a incubação de células Huh7.5.1 pós-infecção com anticorpos de controle de isotipo resultasse em um aumento dependente 15 de tempo de carga viral durante um periodo de tempo de 7 dias (> 10° de unidades leves relativas), a adição de anti- CLDNl pós infecção resultou em niveis baixos de carga viral próximos ao limite de detecção (aproximadamente 103 unidades leves relativas) . Esses dados indicam ainda a 20 relevância do efeito de anticorpos anti-CLDNl ou transmissão de célula-célula de difusão virai em um sistema de cultura de célula infecciosa e sugerem que os anticorpos monoclonais anti-CLDNl inventivos podem não somente ser úteis na prevenção de infecção por HCV como também no controle de infecção viral crônica. Referências R. Aurora e outros, J.Clin. Invest., 2009, 119: 225- 236. 5 H. Barth e outros, J. Biol. Chem., 2003, 278: 41003- 41012. H. Barth e outros, J. Virol, 2005, 79: 5774-5785. H. Barth e outros, J. Virol, 2008, 82: 3466-3479. B. Bartosch e outros, J. Exp. Med. , 2003, 197: 633- 10 642. K.J. Blight e outros, J. Virol, 2002, 76: 13001- 13014. R.S; Brown, Nature, 2005, 436: 973-978 M.T. Catanese e outros, J. Virol, 2007, 81: 8063-8071 15 F.V. Chisari, Nature, 2005, 435: 930-932 L. Cocquerel e outros, J: Gen. Virol, 2006, 87: 1075- 1084 A. Codran e outros, J. Gen. Virol, 2006, 87: 2583- 2593. 20 L. Cukierman e outros, J. Virol, 2009, 83: 5477-5484. P. David e outros, Hum. Exp. Toxicol, 1998, 17: 544- 553. M.C. Dimitrova e outros, Proc. Natl. Acad. Sei. USA, 2008, 105: 16320-16325. M. Dreux e outros, PLoS Pathog 2009; 5:el000310. JA. Este e A. Telenti, Lancet, 2007, 370: 81-88. M.J. Evans e outros, Nature, 2007, 446: 801-805 S. Fafi-Kremer e outros, "Escape from antibody- mediated neutralization and viral entry are key determinants for hepatitis C virus re-infection in liver transplantation", 2009, submetido para publicação. P. Farci e ouros, Proc. Natl. Acad. Sci. USA, 2006, 103: 8475-5480. J.J. Feld e outros, Nature, 2005, 436: 967-972 J.T. Grove e outros, J. Virol, 2007, 81: 3162-3169 A. Haberstroh e outros, Gastroenterology, 2008, 135: 1719-1728. H.J. Harris e outros, J. Virol., 2008, 82: 5007-5020. J.H. Hoofnagle, Hepatology, 2002, 36: S21-S29 M. Hsu e outros, Proc. Natl. Acad. Sci. USA, 2003, 100: 7271-727 S.B. Kapadia e outros, J. Virol, 2007, 81: 374-383 T. Kato e outros, J. Virol, 2007, 81: 4405-4411 G. Koutsoudakis e outros, J. Virol, 2006, 80: 5308- 5320. G. Krause e outros, Biochim. Biophys. Acta, 2008, 1778: 631-645. Inhibition of hepatitis C virus infection by anti-claudin antibodies is mediated by neutralization of E2-CD81-Claudin 1 association(s, 2009, submetido para publicação. L. Lan e outros, J. Immunol, 2008, 181: 4926-4935. G.M. Lauer e outros, N. Engl. J. Med., 2001, 345: 41- 52 D. Lavillette e outros, Hepatology, 2005, 41: 265- 274. M. Law e outros, Nature Med., 2008, 14: 25-27. J.W. Lee e outros, Gynecol Oncol, 2005, 97: 53-59 B.D. Lindenbach e outros, Science, 2005, 309: 623- 626. B.D. Lindenbach e outros, Proc. Natl. Acad. Sci. USA, 2006, 103: 3805-3809 J. Lorhmann e outros, Curr. Drug Disc, 2003, 17-21 de outubro. C.J. Mee e outros, J, Virol, 2009, 83: 6211-6221. P. Meuleman e outros, Hepatology, 2008, 48: 1761- 1768. S. Morohashi e outros, Int. J. Mol. Med., 2007, 20: 139-143 T. Mosmann, J. Immunol., 1983, 65: 55-63. Pawlotsky, Trends Microbiol, 2004, 12: 96-102 WS. Pear e outros, Proc. Natl. Acad. Sci. USA., 1993 90: 8392-8396. JM. Pestka e outros, Proc. Natl. Acad. Sci. USA., 2007, 104: 6026-6030. T. Pietschmann e outros, Proc. Natl. Acad. Sci. USA, 2006, 103: 7408-7413. P. Pileri e outros, Science, 1998, 282: 938-941 A. Ploss e outros, Nature, 2009, 457: 882-886 K.A. Powers e outros, Liver Transpl, 2006, 12: 207- 216 SC. Ray e outros, J. Exp. Med., 2005, 201: 1753-1759. M.B. Resnick e outers, Mod. Pathol., 2005, 18: 511- 518 L.B. Seeff, Semin. Gastrointest, 1995, 6: 20-27. L.B. Seeff e J.H. Hoofnagle, Hepatology, 2002, 36: 1- 2 E. Scarselli e outros, EMBO J., 2002, 21: 5017-5025 G.M. Sheehan e outros, Hum. Pathol, 2007, 38: 564-569 G. Sobel e outros, Hum. Pathol, 2005, 36: 162-169 Z. Stamataki e outros, Clin. Liver Dis., 2008, 12: 693-712. D. Steinmann e outros, J. Virol, 2004, 78: 9030-9040. M. Timpe e JA. McKeating, Gut, 2008, 57: 1728-1727. J.M. Timpe e outros, Hepatology, 2008, 47: 17-24. DM. Tscherne e outros, J. Virol, 2006, 80: 1734-1741. L. Uebelhoer e outros, PLoS Pathog, 2008, 4: el000143. CM. Van Itallie e JM. Anderson, Annu. Rev. Physiol, 2006, 68: 403-429. 5 T. Wakita e outros, Nat. Med., 2005, 11: 791-796. J. Witteveldt e outros, J. Gen. Virol, 2009, 90(Pt 1) : 48-58. M. Yi e outros, Proc. Natl. Acad. Sci. USA, 2006, 103: 2310-2315 10 M.B. Zeisel e outros, Hepatology, 2007, 46: 1722- 1731. MB. Zeisel e outros, "Hepatology, 2008, 48: 299-307. J. Zhong e outros, Proc. Natl. Acad. Sci. USA, 2005, 102: 9294-9299.
Outras modalidades da invenção serão evidentes para um técnico versado no assunto a partir de uma consideração do relatório descritivo ou prática da invenção revelada aqui. Pretende-se que o relatório descritivo e exemplos 20 sejam considerados como exemplares somente, com o escopo verdadeiro da invenção sendo indicado pelas seguintes reivindicações.
Claims (18)
1. Linhagem de célula de hibridoma caracterizada pelo de ser depositada no DSMZ em 29 de julho de 2008 sob um número de acesso selecionado do grupo que consiste em DSM ACC2931, DSM ACC2932, DSM ACC2933, DSM ACC2934, DSM ACC2935, DSM ACC2936, DSM ACC2937 e DSM ACC2938.
2. Anticorpo monoclonal secretado por uma linhagem de célula de hibridoma caracterizada pelo fato de estar depositada no DSMZ em 29 de julho de 2008, sob um número de acesso selecionado do grupo que consiste em DSM ACC2931, DSM ACC2932, DSM ACC2933, DSM ACC2934, DSM ACC2935, DSM ACC2936, DSM ACC2937, e DSM ACC2938, ou um fragmento biologicamente ativo do mesmo que liga domínio extracelular Claudin 1.
3. Anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, de acordo com a reivindicação 2, caracterizado pelo fato de que o anticorpo monoclonal ou fragmento biologicamente ativo se liga a um epítopo que é fortemente dependente da conservação do motivo conservado W(30)-GLW(51)-C(54)-C(64) no primeiro loop extracelular Claudin 1.
4. Anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, de acordo com a reivindicação 2 ou 3, caracterizado pelo fato de que o anticorpo monoclonal ou fragmento biologicamente ativo do mesmo não se liga a Claudin1 de roedor, porém se liga a Claudin 1 de primata não humano.
5. Anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, de acordo com qualquer uma das reivindicações 2 a 4, caracterizado pelo fato de que o anticorpo monoclonal é humanizado, deimunizado ou quimérico.
6. Anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, de acordo com a reivindicação 5, caracterizado pelo fato de que o anticorpo monoclonal compreende as seis regiões de determinação complementar (CDRs) de um anticorpo monoclonal secretado por uma linhagem celular de hibridoma depositada no DSMZ em 29 de julho de 2008 sob um número de acesso selecionado do grupo que consiste em DSM ACC2931, DSM ACC2932, DSM ACC2933, DSM ACC2934, DSM ACC2935, DSM ACC2936, DSM ACC2937 e DSM ACC2938.
7. Anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, de acordo com qualquer uma das reivindicações 2 a 6, caracterizado pelo fato de que o anticorpo monoclonal ou fragmento do mesmo inibe: - ligação de glicoproteína E2 de envelope de HCV ou virionsinfecciosos a linhagens de células permissivas de HCV.
8. Anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, de acordo com qualquer uma das reivindicações 2 a 7, caracterizado pelo fato de que o anticorpo monoclonal ou fragmento do mesmo inibe associação ou associações CD81- Claudin-1.
9. Anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, de acordo com qualquer uma das reivindicações 2 a 8, caracterizado pelo fato de que o anticorpo monoclonal ou fragmento do mesmo inibe a transmissão de célula para célula de HCV e disseminação viral.
10. Molécula caracterizada pelo fato de que compreende um anticorpo monoclonal ou fragmento biologicamente ativo do mesmo, conforme definido por qualquer uma das reivindicações 2 a 9.
11. Molécula, de acordo com a reivindicação 10, caracterizada pelo fato de que o anticorpo monoclonal, ou fragmento do mesmo está ligado a uma porção detectável ou a um agente terapêutico.
12. Composição farmacêutica caracterizada pelo fato de compreender uma quantidade eficaz de um anticorpo monoclonal ou fragmento biologicamente ativo do mesmo de conforme definido por qualquer uma das reivindicações 2 a 9 ou uma molécula, conforme definido pela reivindicação 10 ou 11, e pelo menos um excipiente ou veículo farmaceuticamente aceitável.
13. Composição farmacêutica, de acordo com a reivindicação 12, caracterizada pelo fato de também compreender pelo menos um agente antiviral.
14. Composição farmacêutica, de acordo com a reivindicação 13, caracterizada pelo fato de que o agente antiviral é selecionado do grupo que consiste em interferons, rabivirina, anticorpos monoclonais de vírus de anti-hepatite C, anticorpos policlonais de vírus anti-hepatite C, inibidores de polimerase de RNA, inibidores de protease, inibidores de IRES, inibidores de helicase, compostos anti- sentido, ribozimas e qualquer combinação dos mesmos.
15. Kit farmacêutico caracterizado pelo fato de compreender um anticorpo monoclonal ou fragmento biologicamente ativo do mesmo conforme definido pelas reivindicações 2 a 9 ou a molécula conforme definida pela reivindicação 10 ou 11.
16. kit farmacêutico, de acordo com a reivindicação 15, caracterizado pelo fato de que compreende ainda pelo menos um agente antiviral selecionado do grupo que consiste em interferons, rabivirina, anticorpos monoclonais anti-vírus da hepatite C, anticorpos policlonais anti-vírus da hepatite C, inibidores de RNA polimerase, inibidores de protease, inibidores de IRES, inibidores de helicase, compostos antissenso, ribozimas e qualquer combinação dos mesmos
17. Kit para a detecção de Claudin-1 em uma amostra biológica caracterizado pelo fato de compreender um anticorpo monoclonal, um fragmento biologicamente ativo do mesmo, conforme definido por qualquer uma das reivindicações 2 a 9, em que o anticorpo monoclonal ou fragmento do mesmo é ligado a uma fração detectável.
18. Kit para detectar Claudin-1 em uma amostra biológica caracterizado pelo fato de compreender uma molécula conforme definido pela reivindicação 10 ou 11, em que o anticorpo monoclonal ou fragmento do mesmo é ligado a uma fração detectável.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08305597 | 2008-09-25 | ||
| EP08305597.0 | 2008-09-25 | ||
| PCT/EP2009/062449 WO2010034812A1 (en) | 2008-09-25 | 2009-09-25 | Monoclonal anti-claudin 1 antibodies for the inhibition of hepatitis c virus infection |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0919065A2 BRPI0919065A2 (pt) | 2015-12-15 |
| BRPI0919065B1 true BRPI0919065B1 (pt) | 2021-09-21 |
Family
ID=40352777
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0919065-1A BRPI0919065B1 (pt) | 2008-09-25 | 2009-09-25 | Anticorpos monoclonais anti-claudin-i para a inibição de infecção por vírus de hepatite c |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US8518408B2 (pt) |
| EP (1) | EP2328933B1 (pt) |
| JP (1) | JP5698137B2 (pt) |
| KR (1) | KR101698015B1 (pt) |
| CN (1) | CN102224171B (pt) |
| BR (1) | BRPI0919065B1 (pt) |
| CA (1) | CA2738027C (pt) |
| ES (1) | ES2529511T3 (pt) |
| WO (1) | WO2010034812A1 (pt) |
| ZA (1) | ZA201102112B (pt) |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2007248493B2 (en) | 2006-05-04 | 2010-09-30 | The Rockefeller University | HCV coreceptor and methods of use thereof |
| EP2575885A1 (en) | 2010-05-25 | 2013-04-10 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Combination of anti-envelope antibodies and anti-receptor antibodies for the treatment and prevention of hcv infection |
| WO2013024157A2 (en) | 2011-08-17 | 2013-02-21 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Combinations of host targeting agents for the treatment and the prevention of hcv infection |
| WO2013024158A1 (en) | 2011-08-17 | 2013-02-21 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Combinations of protein kinase inhibitors and interferons or of protein kinase inhibitors and direct acting antivirals for the treatment and the prevention of hcv infection |
| WO2013024155A1 (en) | 2011-08-17 | 2013-02-21 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Combinations of anti-hcv-entry factor antibodies and direct acting antivirals for the treatment and the prevention of hcv infection |
| WO2013024156A2 (en) | 2011-08-17 | 2013-02-21 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Combinations of anti-hcv-entry factor antibodies and interferons for the treatment and the prevention of hcv infection |
| WO2014033266A1 (en) | 2012-08-31 | 2014-03-06 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Anti-sr-bi antibodies for the inhibition of hepatitis c virus infection |
| JP6393875B2 (ja) * | 2013-02-28 | 2018-09-26 | 公益財団法人ヒューマンサイエンス振興財団 | 抗体 |
| EP2778126A1 (en) | 2013-03-15 | 2014-09-17 | Clariant International Ltd. | Lithium transition metal phosphate secondary agglomerates and process for its manufacture |
| WO2014179716A2 (en) * | 2013-05-03 | 2014-11-06 | Emmetrope Ophthalmics Llc | IDENTIFICATION AND ISOLATION OF HUMAN CORNEAL ENDOTHELIAL CELLS (HCECs) |
| JP2016525558A (ja) * | 2013-08-02 | 2016-08-25 | アンスティチュ ナショナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシュ メディカル | 結腸直腸ガンの処置に使用するための抗クローディン1抗体 |
| EP3027648A1 (en) * | 2013-08-02 | 2016-06-08 | Institut National de la Santé et de la Recherche Médicale (INSERM) | Anti-claudin 1 antibodies and uses thereof |
| US10746738B2 (en) * | 2015-02-27 | 2020-08-18 | The Regents Of The University Of Michigan | Claudin-1 peptide reagents and methods |
| EP3070103A1 (en) * | 2015-03-19 | 2016-09-21 | Institut Hospitalier Universitaire De Strasbourg | Anti-Claudin 1 monoclonal antibodies for the prevention and treatment of hepatocellular carcinoma |
| CN114907483B (zh) * | 2016-03-22 | 2024-07-26 | 国家医疗保健研究所 | 人源化抗claudin-1抗体及其用途 |
| US11170872B2 (en) | 2019-11-05 | 2021-11-09 | Apeel Technology, Inc. | Prediction of latent infection in plant products |
| EP3821946A1 (en) * | 2019-11-12 | 2021-05-19 | Université de Strasbourg | Anti-claudin-1 monoclonal antibodies for the prevention and treatment of fibrotic diseases |
| EP4433042A4 (en) * | 2021-11-18 | 2025-10-15 | Univ Nebraska | NOVEL CLAUDIN-1 INHIBITORS FOR THERAPEUTIC INTERVENTION |
| US20250179170A1 (en) | 2022-03-08 | 2025-06-05 | Alentis Therapeutics Ag | Use of anti-claudin-1 antibodies to increase t cell availability |
| EP4532550A1 (en) | 2022-06-01 | 2025-04-09 | Alentis Therapeutics AG | Use of anti-claudin-1 antibodies to treat cholangiocarcinoma |
| CN120076826A (zh) | 2022-06-01 | 2025-05-30 | 阿伦蒂斯治疗股份公司 | 抗紧密连接蛋白-1抗体治疗胆管病的用途 |
| CN115850502A (zh) * | 2022-07-14 | 2023-03-28 | 清华-伯克利深圳学院筹备办公室 | 蛋白酶响应的gpcr受体及其应用 |
| JP2025533015A (ja) | 2022-09-30 | 2025-10-03 | アレンティス セラピューティクス アクチェンゲゼルシャフト | 薬物抵抗性肝細胞癌の処置 |
| CN121605309A (zh) | 2023-03-23 | 2026-03-03 | 阿伦蒂斯治疗股份公司 | 使用抗紧密连接蛋白-1抗体的癌症治疗的生物标志物 |
| WO2025224337A1 (en) | 2024-04-26 | 2025-10-30 | Alentis Therapeutics Ag | Anti-cldn1 antibody-drug conjugates comprising exatecan and methods of use thereof |
| WO2025224335A1 (en) | 2024-04-26 | 2025-10-30 | Alentis Therapeutics Ag | Anti-cldn1 antibody-drug conjugates comprising mmae and methods of use thereof |
| WO2026057702A1 (en) | 2024-09-12 | 2026-03-19 | Alentis Therapeutics Ag | Claudin-1/egfr bispecific antibodies |
| WO2026057723A1 (en) | 2024-09-12 | 2026-03-19 | Alentis Therapeutics Ag | Claudin-1/egfr bispecific antibodies for targeted degradation |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1044384C (zh) * | 1994-08-25 | 1999-07-28 | 中国药品生物制品检定所 | 抗丙型肝炎病毒抗原单克隆抗体细胞株建立及其单克隆抗体 |
| CN1089802C (zh) * | 1998-07-31 | 2002-08-28 | 中国药品生物制品检定所 | 抗丙型肝炎病毒非结构区4抗原的单克隆抗体细胞株及其单克隆抗体 |
| EP1167387A1 (en) | 2000-06-23 | 2002-01-02 | F. Hoffmann-La Roche Ag | Antibodies against SEMP1, methods for their production and uses thereof |
| AU750296B2 (en) * | 2000-06-23 | 2002-07-11 | F. Hoffmann-La Roche Ag | Antibodies against SEMP1, methods for their production and uses thereof |
| AU2007248493B2 (en) * | 2006-05-04 | 2010-09-30 | The Rockefeller University | HCV coreceptor and methods of use thereof |
-
2009
- 2009-09-25 ES ES09783424.6T patent/ES2529511T3/es active Active
- 2009-09-25 WO PCT/EP2009/062449 patent/WO2010034812A1/en not_active Ceased
- 2009-09-25 CA CA2738027A patent/CA2738027C/en active Active
- 2009-09-25 US US13/119,233 patent/US8518408B2/en active Active
- 2009-09-25 BR BRPI0919065-1A patent/BRPI0919065B1/pt active IP Right Grant
- 2009-09-25 JP JP2011528342A patent/JP5698137B2/ja active Active
- 2009-09-25 CN CN200980147935.XA patent/CN102224171B/zh active Active
- 2009-09-25 EP EP09783424.6A patent/EP2328933B1/en active Active
- 2009-09-25 KR KR1020117009324A patent/KR101698015B1/ko active Active
-
2011
- 2011-03-22 ZA ZA2011/02112A patent/ZA201102112B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| WO2010034812A1 (en) | 2010-04-01 |
| JP2012503632A (ja) | 2012-02-09 |
| CA2738027C (en) | 2018-12-04 |
| KR20110061634A (ko) | 2011-06-09 |
| US20110236347A1 (en) | 2011-09-29 |
| ZA201102112B (en) | 2012-07-25 |
| CA2738027A1 (en) | 2010-04-01 |
| CN102224171A (zh) | 2011-10-19 |
| US8518408B2 (en) | 2013-08-27 |
| JP5698137B2 (ja) | 2015-04-08 |
| CN102224171B (zh) | 2015-03-11 |
| ES2529511T3 (es) | 2015-02-20 |
| KR101698015B1 (ko) | 2017-01-19 |
| EP2328933A1 (en) | 2011-06-08 |
| EP2328933B1 (en) | 2014-11-05 |
| BRPI0919065A2 (pt) | 2015-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2529511T3 (es) | Anticuerpos monoclonales anti-claudina 1 para la inhibición de la infección por virus de la hepatitis C | |
| Hashimoto et al. | Claudin-5-binders enhance permeation of solutes across the blood-brain barrier in a mammalian model | |
| US7507408B2 (en) | Anti hepatitis C virus antibody and uses thereof | |
| US20100291545A1 (en) | Antibody having inhibitory activity on infection with hepatitis c virus (hcv) and use thereof | |
| US20090110685A1 (en) | Treatment and prevention of viral infections | |
| JP2012504602A (ja) | C型肝炎抗体およびその使用 | |
| PT1835937E (pt) | Composições e métodos para tratar infeção viral | |
| WO2009025759A1 (en) | Tight junction proteins associated with infection and entry of hepatitis c virus (hcv), methods and uses thereof | |
| JP2022507836A (ja) | 新規の抗ジカウイルス抗体及びその使用 | |
| JP5756757B2 (ja) | C型肝炎ウイルス(hcv)に対して感染阻害活性を有する抗体及びその用途 | |
| WO2022044573A1 (ja) | コロナウイルススパイク蛋白に対するヒト抗体またはその抗原結合断片 | |
| CN103429265A (zh) | 用于治疗和预防hcv感染的抗包膜抗体和抗受体抗体组合物 | |
| US10435463B2 (en) | Hepatitis C virus specific antibody | |
| TWI432211B (zh) | 與登革病毒相關之胜肽及抗體以及其用途 | |
| CN104119436B (zh) | 抗丙型肝炎病毒的中和性全人单克隆抗体 | |
| TW201620931A (zh) | 具有抗c型肝炎病毒的感染抑制活性的抗體 | |
| JPWO2016139941A1 (ja) | 抗体、フラグメント、分子及び抗hcv治療剤 | |
| CN107011435A (zh) | 抗丙型肝炎病毒的全人单克隆抗体8d6 | |
| HK1241897A (en) | A novel neutralizing human monoclonal antibody 8d6 against hcv infection | |
| HK1241897A1 (en) | A novel neutralizing human monoclonal antibody 8d6 against hcv infection | |
| AU2012254920A1 (en) | Improvements in or relating to treatment and prevention of viral infections |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NAO 10196/2001, QUE MODIFICOU A LEI NAO 9279/96, A CONCESSAO DA PATENTE ESTA CONDICIONADA A ANUAANCIA PRA VIA DA ANVISA. CONSIDERANDO A APROVAA AO DOS TERMOS DO PARECER NAO 337/PGF/EA/2010, BEM COMO A PORTARIA INTERMINISTERIAL NAO 1065 DE 24/05/2012, ENCAMINHA-SE O PRESENTE PEDIDO PARA AS PROVIDAANCIAS CABA-VEIS. |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 25/09/2009, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |