BRPI1014371B1 - Coaglomerado de manitol e de amido granular, uso e processo para a preparação deste, comprimido composto de coaglomerados de manitol e de amido granular e cápsula rígida de gelatina, composta de coaglomerados de manitol e de amido granular - Google Patents
Coaglomerado de manitol e de amido granular, uso e processo para a preparação deste, comprimido composto de coaglomerados de manitol e de amido granular e cápsula rígida de gelatina, composta de coaglomerados de manitol e de amido granular Download PDFInfo
- Publication number
- BRPI1014371B1 BRPI1014371B1 BRPI1014371-8A BRPI1014371A BRPI1014371B1 BR PI1014371 B1 BRPI1014371 B1 BR PI1014371B1 BR PI1014371 A BRPI1014371 A BR PI1014371A BR PI1014371 B1 BRPI1014371 B1 BR PI1014371B1
- Authority
- BR
- Brazil
- Prior art keywords
- mannitol
- starch
- coagglomerates
- fact
- dry
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4365—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system having sulfur as a ring hetero atom, e.g. ticlopidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4866—Organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Organic Chemistry (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Preparation (AREA)
- General Preparation And Processing Of Foods (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Polysaccharides And Polysaccharide Derivatives (AREA)
Abstract
coaglomerados de manitol e de amido granular comprimíveis e com escoamento livre. a invenção tem por objeto coaglomerados de manitol cristalino e de granular, caracterizados pelo fato de apresentarem uma capacidade de compressão, determinada seguindo um teste a, superior a 120 n, de preferência, compreendida entre 200 e 450 n, e uma escala de escoamento, determinada segundo um teste b, compreendida entre 3 e 15 segundos de preferência, compreendida entre 4 e 8 segundos.
Description
[001]A presente invenção tem por objeto coaglomerados de manitol cristalino e de amido granular que apresentam uma capacidade de compressão notavelmente elevada, o que os destina particularmente ao preparo de comprimidos.
[002]A invenção é também relativa à coaglomerados de manitol cristalino e de amido granular, apresentando uma excelente aptidão ao fluxo, o que os destina também a serem utilizados para o enchimento de cápsulas rígidas de gelatina.
[003]A invenção é, enfim, relativa ao processo, permitindo obter esses coa- glomerados.
[004]No domínio da utilização de polióis no que se refere ao domínio pelo qual se interessará especificamente na presente invenção, a saber, os excipientes farmacêuticos e os edulcorantes mássicos utilizados na indústria alimentícia, vários polióis pulverulentos são de uso corrente. Trata-se do sorbitol, do xilitol e, sobretudo do manitol.
[005]A indústria farmacêutica é consumidora de toneladas consideráveis de manitol. Este é notadamente utilizado como excipiente nas formas secas que são, por exemplo, os pós de enchimento das cápsulas rígidas de gelatina, os pós para sachê a dispersar ou a dissolver extemporaneamente na água, as formas sólidas orais e os comprimidos.
[006]Com efeito, o manitol, em razão de seu sabor e da fraca higroscopici- dade de sua forma cristalina, constitui um excelente excipiente, notadamente para sua grande inércia química face os princípios ativos.
[007]Infelizmente, o produto obtido por cristalização na água, a partir de uma solução supersaturada, não é naturalmente compressível.
[008]Para prevenir essa situação, é conhecido pelos especialistas do domí nio o acréscimo de um ligante para aumentar sua capacidade de compressão.
[009]A patente US 3.145.146 descreve, por exemplo, um processo que con-siste em utilizar a parafina, a goma ou um derivado da celulose como ligante, antes da etapa de pulverização a seco, que leva ao preparo do pó de manitol.
[0010]Essa solução técnica não é, todavia, considerada pelo usuário.
[0011]Para o preparo das cápsulas rígidas de gelatina, é conhecido do técni co que as misturas sucessíveis capazes de servir ao preenchimento das cápsulas rígidas de gelatina devem poder se prestar para o preenchimento automático, a fim de garantir uma dosagem uniforme.
[0012]É evidente que um trabalho de formulação de doses farmacêuticas é necessário para certas substâncias, a fim de assegurar um preenchimento uniforme e precisa sobre máquinas de velocidade muito elevada.
[0013]Convém, em particular, fiscalizar os seguintes parâmetros: - forma e tamanho das partículas, - granulometria uniforme, - homogeneidade da mistura, - propriedade de fluxo do pó, - taxa de umidade, - boa aglomeração sob pressão.
[0014]Ora, ao lado de sua não capacidade de compressão, é preciso acres-centar outro inconveniente do manitol obtido por cristalização na água, que é o fato de apresentar propriedades de fluxo medíocres, em razão da estrutura orto-rômbica de seus cristais, e, sobretudo em razão de sua friabilidade excessiva.
[0015]Essa friabilidade leva à formação de finas partículas que prejudica par-ticularmente suas propriedades de fluxo, em particular quando do enchimento e do esvaziamento das moegas e dos condutos de alimentação dos dispositivos utiliza dos para fabricar comprimidos, ou preencher as cápsulas rígidas de gelatina.
[0016]Dessa forma, o manitol cristalizado na água não é absolutamente um excipiente de escolha utilizável para o preenchimento de cápsulas rígidas de gelati na.
[0017]Ainda, é necessário acrescentar um agente ligante.
[0018]Na patente US 3.145.146, o acréscimo de agente ligante não impede, todavia, que pelo menos 50% das partículas do pó tenham ainda um tamanho inferi or a 75 μm, o que está longe de ser ideal para se obter um bom fluxo.
[0019]No domínio dos comprimidos, o amido pode ser vantajosamente utili-zado como ligante, quando se faz com que sofra um cozimento prévio, e pode tam bém servir de diluente.
[0020]Ele possui, por outro lado, boas propriedades desintegrantes devido à sua hidrofilia na água quando é empregado o estado de grânulo.
[0021]Ele deve, todavia, ser incorporado em quantidade elevada, geralmente superior a 15% da formulação final.
[0022]Ao contrário, ele apresenta devido ao seu pequeno tamanho de suas partículas e de sua pequena densidade, o inconveniente de não escoar.
[0023]A alta elasticidade de seus granulados lhe confere, por outro lado, uma fraca capacidade de compressão que não permite a fabricação de comprimidos de dureza satisfatória.
[0024]Não pode, portanto, ser considerado pelo técnico associar o manitol e o amido granular, a fim de aproveitar as propriedades ligantes do amido para forne cer ao manitol as propriedades de capacidade de compressão ou de fluxo que lhe constitui um defeito.
[0025]Na realidade, se a associação do amido e do manitol tiver sido traba-lhada,será antes de tudo no domínio da fabricação dos comprimidos orodispersí- veis, nos quais é, sobretudo, tratado aproveitar as propriedades desintegrantes e diluentes do amido.
[0026]Por exemplo, no pedido de patente WO 00/47233, é descrito um pre paro para comprimidos que compreendem a mistura física de um princípio ativo, um amido, com notadamente o manitol. Ora, é muito recomendado nesse pedido de pa tente acrescentar a essa mistura física um ou vários lubrificantes escolhidos dentre o estearato de magnésio, o estearato de cálcio, o estearil fumarato de sódio e o ani- drido silícico leve para facilitar o fluxo dessas misturas nos equipamentos de fabrica-ção de comprimidos.
[0027]No pedido de patente JP 09.1077669, é descrito uma mistura física contendo o manitol, o amido e a vitamina C. Essa mistura física é secada por um processo de pulverização a seco clássico, isto é, uma pulverização a seco de tipo simples e feito sem reciclagem das finas. Resulta daí um pó pouco compressível e apresentando um mau escoamento.
[0028]Parece assim difícil propor uma solução única, que permita conciliar, ao mesmo tempo, as propriedades de capacidade de compressão e a aptidão ao fluxo, de um pó de manitol cristalino, e é ir ao encontro de um pré-julgado técnico do que propor uma solução que consiste em utilizar um aglomerado de manitol e de amido granular.
[0029]É assim que, mesmo a sociedade requerente em sua patente EP 1.138.661, conseguia conferir a um manitol cristalino de fina granulometria uma ex-celenteaptidão ao fluxo, mas fracassava ao lhe atribuir propriedades de capacidade de compressão.
[0030]O manitol pulverulento, obtido segundo essa patente EP 1.138.661, ti-nha assim exemplificado na formulação de um pó de enchimento de cápsulas rígidas de gelatina, mas o enchimento devera ser simulado sobre um aparelho especialmen te concebido para a experiência.
[0031]A invenção tem, portanto, por finalidade prevenir esses inconvenientes e a sociedade requerente teve o mérito de encontrar, após numerosos trabalhos, que essa finalidade podia ser alcançada, desde quando se utilizam coaglomerados à base de amido granular e de manitol.
[0032]Por amido granular, entendem-se os amidos nativos de quaisquer ori-gens, naturais ou híbridos, de tipo granular, e todos os amidos modificados quimi-camente que mantiveram uma forma granular.
[0033]Utilizar-se-á, de preferência, um amido de milho, tal como aquele co-mercializado pela sociedade requerente sob a denominação “amido extra-branco” que permite obter grânulos de uma brancura inteiramente satisfatória.
[0034]A invenção tem também por objeto coaglomerados de manitol cristali no e de amido granular, caracterizados pelo fato de permitirem: - o preparo, por compressão direta, de comprimidos que apresentam notá veis propriedades de dureza, - o enchimento de cápsulas rígidas de gelatina para o preparo das quais é necessário utilizar grandes quantidades de lubrificante e de agente de fluxo para fa-cilitar o enchimento e o esvaziamento das moegas e dos condutos de alimentação dos dispositivos utilizados.
[0035]A invenção tem assim por objeto a utilização dos coaglomerados de manitol cristalino e de amido granular nos quais o amido granular participa da capa-cidade de compressão desse aglomerado e facilita a lubrificação, como de proprie-dades do amido granular que o técnico não espera encontrar.
[0036]A invenção tem enfim por objeto: - comprimidos; - cápsulas rígidas de gelatina contendo coaglomerados de manitol cristalino e de amido granular nos quais o amido granular age, ao mesmo tempo, como agente ligante e como agente lubrifi- cante.
[0037]A invenção tem mais particularmente por objeto coaglomerados de manitol cristalino e de amido granular, caracterizados pelo fato de apresentarem: - uma capacidade de compressão, determinada segundo um teste A superior a 120 N, de preferência, compreendida entre 200 e 450 N, e, mais preferencialmente ainda compreendida entre 220 e 400 N, - uma escala de fluxo, determinada segundo o teste B, compreendida entre 3 e 15 segundos, de preferência, compreendida entre 4 e 8 segundos e mais prefe-rencialmente ainda compreendida entre 4 e 6 segundos.
[0038]Os coaglomerados, de acordo com a invenção, são caracterizados por seu comportamento em compressão, determinado segundo um teste A.
[0039]O teste A consiste em medir a força, expressa em Newtons, que é ne-cessária para provocar a compressão de um comprimido preparado com o auxílio de uma prensa alternativa de laboratório FROGERAIS AM comercializado pela socie dade SVIAC (FRANÇA) a partir desse coaglomerado lubrificado com 1,2% de estea- rato de magnésio (lubrificação realizada pela mistura durante 5 minutos do coaglo- merado e do estearato de magnésio em um misturador TURBULA T2C de WILLY A. BACHOFEN), traduzindo, portanto, a resistência a compressão do comprimido que é cilíndrico com faces convexas de um diâmetro de 13 mm, de uma espessura de 6 mm e de um peso de 0,734 g, isto é, de uma densidade aparente de 1,3 g/ml. Essa força, que expressa a dureza do comprimido e, por conseguinte, a capacidade de compressão do pó, é medida sobre um durômetro ERWEKA TBH 30 GMD. O valor dado em Newtons corresponde a uma média realizada em 10 medidas.
[0040]Os coaglomerados, de acordo com a invenção, apresentam então uma capacidade de compressão, determinada segundo um teste A superior a 120 N, de preferência, compreendida entre 200 e 450 N.
[0041]O amido, possuindo uma capacidade de compressão ruim, é surpre- endente constatar que esses coaglomerados de manitol e de amido apresentam uma capacidade de compressão elevada. O que permite realizar comprimidos que, embora contendo além dos ativos farmacêuticos, veterinários ou nutracêuticos ou produtos alimentícios ou excipientes, aromas, corantes, conservarão uma dureza suficiente para a sua manipulação posterior, quer seja de revestimento com película, acondicionamento em blister, em tubo, até mesmo em vácuo.
[0042]Uma capacidade de compressão importante assim é também buscada para o preenchimento das cápsulas rígidas de gelatina, notadamente sobre as en- capsuladoras industriais, utilizando os princípios do compressor-dosador ou do disco dosador.
[0043]Os coaglomerados, de acordo com a invenção, são também caracteri-zados por sua aptidão ao fluxo, determinada segundo um teste B.
[0044]O teste B consiste em determinar o tempo necessário ao fluxo de 100 g de pó, segundo o método de medida preconizada pela Farmacopéia Européia (PE 5.0 tomo 1, 01/2005: 20916, parágrafo 2.9.1.6; equipamento, segundo a figura 2.9.16.-2).
[0045]Os coaglomerados, de acordo com a invenção, apresentam, então, uma escala de fluxo, determinada segundo o teste B, compreendida entre 3 e 15 segundos, de preferência, compreendida entre 4 e 8 segundos.
[0046]Os coaglomerados apresentam um excelente fluxo livre, enquanto que o amido granular não escoa livremente e que as misturas físicas de manitol e de amido não escoam ou escoam muito pouco.
[0047]Os coaglomerados, de acordo com a invenção, apresentam um diâ-metromédio volumétrico laser D4, 3 compreendido entre 60 e 500 μm, de preferên cia, compreendido entre 100 e 250 μm.
[0048]Os valores de repartição granulométrica são determinados sobre um granulômetro com difração LASER tipo LS 200 da sociedade BECKMAN-COULTER, equipado com seu módulo de dispersão pó (via seca) seguindo o manual técnico e as especificações do construtor.
[0049]As condições operacionais de velocidade de parafuso sob moega e de intensidade de vibração do conduto de dispersão são determinadas de maneira que a concentração óptica esteja compreendida entre 4% e 12%, idealmente de 8%.
[0050]A gama de medida do granulômetro com difração LASER tipo LS 200 é de 0,04 μm a 2.000 μm. Os resultados são calculados em % volumétrica, e ex pressos em μm.
[0051]A curva de distribuição granulométrica permite também determinar o valor do diâmetro médio volumétrico (média aritmética) D4, 3.
[0052]Nos comprimidos e nas cápsulas rígidas de gelatina contendo ativos, a homogeneidade da dosagem em ativos é obtida, otimizando o diâmetro médio dos excipientes em relação ao diâmetro médio dos ativos, geralmente, sem que seja sis-temático, aproximando esses diâmetros médios.
[0053]Os coaglomerados, de acordo com a invenção, dão acesso a diâme-trosmédios correspondentes à maioria dos ativos, de 60 a 500 μm, tanto para a rea-lização de comprimidos quanto para o preenchimento de cápsulas rígidas de gelati na.
[0054]Os coaglomerados, de acordo com a invenção, são também caracteri-zados pelo fato de a razão manitol / amido estar compreendida entre 99,5 / 0,5 e 50 / 50, e, de preferência, entre 95/5 e 70/30.
[0055]Além de 99,5% de manitol ou aquém de 50% de manitol, a sociedade requerente constatou que esses coaglomerados não possuíam propriedades de ca-pacidade de compressão ou de fluxo satisfatórios.
[0056]De preferência, escolhe-se uma razão de manitol e de amido compre-endida entre 95/5 e 70/30.
[0057]De acordo com outro modo de realização da invenção, os coaglome- rados compreendem manitol e amido e podem, além disso, conter qualquer aditivo apropriado, desde que não prejudique as propriedades buscadas dos granulados finais, como, em particular aromas, corantes, agentes estabilizantes, ligantes, lubrifi cantes, conservantes.
[0058]Pode tratar-se também de princípios ativos farmacêuticos ou fito- sanitários, detergentes.
[0059]Os coaglomerados, de acordo com a invenção, apresentam: - uma densidade aerada compreendida entre 0,400 e 0,750 g/ml, de prefe-rência, compreendida entre 0,450 e 0,650 g/ml, e - uma densidade compactada entre 0,500 e 0,850 g/ml, de preferência, com-preendida entre 0,550 e 0,750 g/ml.
[0060]As densidades aeradas e compactadas dos coaglomerados conforme a invenção são as densidades aparentes aeradas e compactadas determinadas se-gundo o método de medida preconizada pela Farmacopéia Européia (PE 5.1 tome 1, 01/2005: 20915 parágrafo 2-9-15; equipamento segundo a figura 2-9-15-1), a densi-dade aparente compactada sendo obtida após 1.250 empilhamentos.
[0061]Para diminuir o volume dos comprimidos e das cápsulas rígidas de ge-latina a ingerir, e, portanto, melhorar a observância medicamentosa dos pacientes, densidades compactadas elevadas são buscadas.
[0062]Todavia, uma homogeneidade de mistura entre o coaglomerado e o pó de ativos necessita frequentemente de uma similaridade nas densidades aera- das. É preciso, portanto, que o coaglomerado seja mais ou menos denso em função do ativo a incorporar.
[0063]Os coaglomerados, de acordo com a invenção, podem apresentar densidades sobre uma faixa importante, adaptando-se à maioria dos casos.
[0064]Os coaglomerados de manitol cristalino e de amido granular, de acor do com a invenção, são, enfim, caracterizados pelo fato de o manitol se apresentar, ao mesmo tempo, sob as formas cristalinas alfa e beta.
[0065]O manitol é classicamente comercializado sob três formas cristalinas: alfa, beta e delta, a forma beta sendo a forma a mais comumente utilizada, pois de maior estabilidade.
[0066]Com efeito, é conhecido em toda generalidade que o manitol de forma cristalina alfa ou delta, colocado em presença de uma pequena quantidade de água era instável, pois se dissolvia, depois se recristalizava sob a forma beta.
[0067]A sociedade requerente foi, portanto, ao encontro de um pré-julgado técnico que considera ser preciso preferir a forma cristalina beta à forma alfa, nota- damente em aplicações nas quais o risco de uma recristalização da forma alfa em forma beta é nociva, por exemplo, pela aptidão à desintegração em boca de com-primidos que os contêm, ou para tentar otimizar as propriedades de capacidade de compressão, ou a aptidão ao fluxo, do manitol.
[0068]A determinação da co-existência das duas formas cristalinas alfa e be ta do manitol pode ser realizada classicamente por qualquer método conhecido, por outro lado, do técnico, isto é, por espectrometria infravermelho ou por difração X.
[0069]Por espectrometria infravermelha, o método comumente aplicado é di-topélete ao brometo de potássio. As duas formas cristalinas do manitol apresentam, então, um perfil diferente.
[0070]Localmente, as diferenças são mais ou menos marcadas; a zona es-pectral estudada fica assim localizada entre 2850 e 3050 cm-1; a forma alfa se ca-racteriza pela presença de uma banda de adsorção a aproximadamente 2885 cm-1, a forma beta se caracteriza por aquelas a cerca de 2985 e 2900 cm-1.
[0071]As misturas dessas duas formas mostraram então diferenças mais ou menos pronunciadas segundo as proporções das duas formas e a zona espectral estudada.
[0072]Graças a medidas feitas sobre misturas amostras de formas cristalinas alfa e beta, é relativamente fácil quantificar as proporções de formas cristalinas nos coaglomerados de manitol cristalino e de amido granular, de acordo com a invenção, conforme será exemplificado a seguir.
[0073]Uma confirmação desses valores pode ser realizada por espectrome- tria de difração dos raios X.
[0074]O técnico sabe, com efeito, que a quantificação relativa é tornada pos-sível por meio da relação de intensidade dos sulcos de difração: a altura do sulco a 27°2 correspondente à forma cristalina beta em relação à altura do sulco a 20°1 cor-respondente à forma alfa.
[0075]Uma mistura que apresenta, por exemplo, 25% de forma cristalina alfa e 75% de forma cristalina beta dá uma relação de altura dos sulcos de 21, enquanto que uma mistura de 50% dá um valor de relações de sulcos de 5.
[0076]Os coaglomerados, de acordo com a invenção, que possuem caracte-rísticas mencionadas acima são capazes de serem obtidos particularmente segundo um processo que compreende uma etapa de pulverização a seco ou de granulação de uma mistura de manitol e de amido.
[0077]Essa finalidade não tinha sido alcançada até então por meio dos pro-cessos conhecidos do técnico, e aplicáveis ao mesmo tempo ao manitol e ao amido. Este apresenta, com efeito, o inconveniente, quando se aplicam processos térmicos em meio aquoso, cozer e perder assim seu caráter granular.
[0078]Em um primeiro modo preferencial de realização do processo, de acordo com a invenção, os coaglomerados de manitol cristalino e de amido são pre parados por pulverização a seco ou por granulação de uma mistura de uma solução de manitol e de amido, o amido sendo colocado em suspensão na solução de mani- tol.
[0079]Em um segundo modo preferencial de realização do processo confor me a invenção, os coaglomerados de manitol cristalino e de amido são preparados por pulverização a seco ou por granulação de uma mistura de uma solução de mani- tol e de amido seco, o amido sendo incorporado sob a forma seca no pulverizador ou quando da etapa de granulação.
[0080]De acordo com um primeiro modo preferencial, pode-se proceder con-forme as seguintes etapas: a) preparar a uma temperatura compreendida entre 45 e 65 °C uma “solu ção” de manitol e de amido granular, na qual: - a razão manitol / amido está compreendida entre 99,5 / 0,5 e 50 / 50, e, de preferência, entre 95 / 5 e 70 / 30; - a matéria seca está compreendida entre 25 e 45% em peso seco; b) manter essa solução de manitol e de amido a uma temperatura compre-endida entre 45 e 65 °C; c) pulverizar a seco essa solução em um pulverizador de tipo MSD equipado com um bocal de pulverização a seco de alta pressão com reciclagem das finas par-tículas no topo do pulverizador; d) recuperar os coaglomerados de manitol e de amido assim obtidos. A primeira etapa consiste, portanto, em preparar a uma temperatura com-preendida entre 45 e 65 °C uma solução de manitol e de amido granular, na qual: - a razão manitol/amido está compreendida entre 99,5 / 0,5 e 50 / 50, e, de preferência, entre 95 / 5 e 70 / 30; - a matéria seca está compreendida entre 25 e 45% em peso seco.
[0081]Se a granulometria inicial dos cristais de manitol não for uma caracte-rística essencial, o teor em amido é, ao contrário, um parâmetro importante, assim como sua relação com o manitol.
[0082]É, então, escolhida uma razão manitol / amido compreendida entre 99,5 / 0,5 e 50 / 50, e, de preferência, entre 95 / 5 e 70/30.
[0083]A segunda etapa consiste em manter essa solução de cristais de ma- nitol e de amido à temperatura compreendida entre 45 e 65 °C.
[0084]A manutenção a essa temperatura permite conservar o manitol no es-tado dissolvido ou sob as formas de cristais de pequena granulometria. A temperatu ra é escolhida, de modo a conservar o amido sob a forma granular.
[0085]A terceira etapa consiste então em pulverizar a seco essa solução em um pulverizador de tipo MSD (isto é, Multi Stage Dryer) equipado com um bocal de pulverização a seco de alta pressão com reciclagem das partículas finas no topo do pulverizador.
[0086]Conforme será exemplificado a seguir, a sociedade Requerente reco-menda utilizar um pulverizador de tipo MSD 20 comercializado pela sociedade NIRO.
[0087]O bocal de pulverização é escolhido, de maneira a se obter uma pres são compreendida entre 20 e 250 bárias, para uma vazão compreendida entre 50 e 170 l/h, de preferência, da ordem de 120 l/h.
[0088]A temperatura dos ares de entrada é regulada da seguinte maneira: - para o ar de entrada a montante no topo do pulverizador: temperatura compreendida entre 120 °C e 240 °C; - para o leito fluidizado estático: temperatura compreendida entre 50 e 120 °C; - para o leito fluidizado vibrado: temperatura da ordem de 20 °C.
[0089]A temperatura de saída do pulverizador está então compreendida en tre 50 e 120 °C.
[0090]Os coaglomerados, de acordo com a invenção, são enfim recuperados na saída do pulverizador.
[0091]De acordo com um segundo modo preferencial, pode-se proceder, conforme as seguintes etapas: a) preparar a uma temperatura compreendida entre 45 e 90 °C uma solução de manitol, na qual a matéria seca está compreendida entre 25 e 50% em peso se co; b) manter essa solução de manitol a uma temperatura compreendida entre 45 e 90 °C; c) pulverizar a seco essa solução em um pulverizador de tipo MSD equipado com um bocal de pulverização a seco de alta pressão com reciclagem das finas par-tículas no topo do pulverizador, injetando via um dosador ponderal o amido seco no sistema de reciclagem das finas em uma razão manitol / amido compreendida entre 99,5 / 0,5 e 50 / 50, e, de preferência, entre 95 / 5 e 70 / 30; d) recuperar os coaglomerados de manitol e de amido assim obtidos.
[0092]A sociedade requerente observou assim que a injeção do amido no sistema de reciclagem permite uma mistura íntima com o manitol, quando da seca gem.
[0093]A solução é pulverizada a seco, conforme no modo preferencial pre-cedente, em um pulverizador de tipo MSD (isto é, Multi Stage Dryer) equipada com um bocal de pulverização a seco com alta pressão com reciclagem das finas partícu las no topo do pulverizador.
[0094]Conforme será exemplificado a seguir, a sociedade requerente reco-menda utilizar um pulverizador de tipo MSD 20 comercializado pela sociedade NIRO.
[0095]O bocal de pulverização é escolhido de maneira a se obter uma pres são compreendida entre 20 e 250 bárias para uma vazão compreendida entre 50 e 170 l/h, de preferência, da ordem de 120 l/h.
[0096]As temperaturas dos ares de entrada são reguladas da seguinte ma-neira: - para o ar de entrada a montante no topo do pulverizador: temperatura compreendida entre 120 °C e 240 °C; - para o leito fluidizado estático: temperatura compreendida entre 50 e 120 °C; - para o leito fluidizado vibrado: temperatura da ordem de 20 °C.
[0097]A temperatura de saída do pulverizador está então compreendida en tre 50 e 120 °C.
[0098]Os coaglomerados, de acordo com a invenção, são enfim recuperados na saída do pulverizador.
[0099]De acordo com um terceiro modo preferencial, pode-se proceder, con-forme as seguintes etapas: a) preparar a uma temperatura compreendida entre 45 e 65 °C uma solução de manitol e de amido granular, na qual: - a razão manitol / amido está compreendida entre 99,5 / 0,5 e 50 / 50, e, de preferência, entre 95 / 5 e 70 / 30; - a matéria seca está compreendida entre 25 e 45% em peso seco; b) manter essa solução de manitol e de amido a uma temperatura compre-endida entre 45 e 65 °C; c) granular por pulverização dessa solução em um granulador com leito de ar fluidizado; d) recuperar os coaglomerados de manitol e de amido assim obtidos.
[00100]Para proceder à granulação, pode-se empregar, por exemplo, um granulador com leito de ar fluidizado contínuo.
[00101]Pode ser escolhido vantajosamente um granulador com leito de ar fluidizado contínuo circular com tubo de descarregamento ou contínua retangular com fluxo pistão.
[00102]Como será exemplificado a seguir, a sociedade requerente escolheu empregar um granulador com leito de ar fluidizado contínuo com classificador de tipo AGT comercializado pela sociedade GLATT.
[00103]A invenção será mais bem compreendida com o auxílio dos exem plos que se seguem, os quais são ilustrativos e não limitativos.
[00104]Exemplo 1: Preparo de coaglomerados, de acordo com a invenção, por pulverização a seco da mistura de uma solução de manitol, na qual o amido gra nular é colocado em suspensão.
[00105]Preparam-se por pulverização a seco, de acordo com a invenção, di-ferentescomposições de coaglomerados que consistem em manitol e em amido granular a razões respectivamente de 99 / 1, 95 / 5, 90 / 10, 85 / 15 e 80 / 20.
[00106]Utiliza-se manitol cristalizado, comercializado pela sociedade reque rente pelo nome de PEARLITOL® 50C que apresenta um diâmetro médio volumétri co laser de aproximadamente 50 μm e amido de milho “extra-branco”.
[00107]Prepara-se uma solução de manitol e de amido na matéria seca de-sejada, dissolvendo o manitol cristalizado na água desmineralizada a 55 °C, aí colo cando em suspensão o amido de milho “extra branco”.
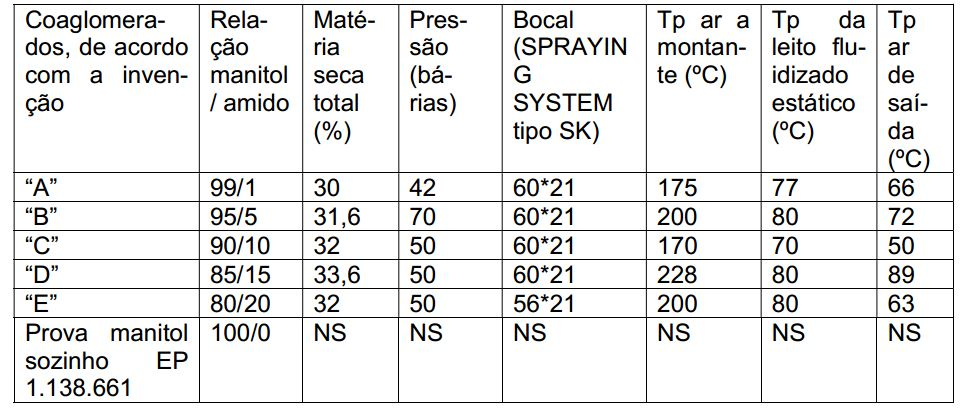
[00108]A agitação deve permitir obter uma solução fluida, homogênea e sem embolotamentos. As condições operacionais de fabricação desses coaglomerados no pulverizador de tipo MSD 20 comercializado pela sociedade NIRO são representadas na tabela 1 a seguir. Tabela 1
[00109]Durante a modificação da taxa de amido, o preparo dos coaglomera- dos, de acordo com a invenção, necessita mais particularmente dos ajustes na esco lha do bocal, da pressão de pulverização a seco e das temperaturas de ar para se obter uma granulometria média similar.
[00110]As características dos coaglomerados de manitol e de amido, de acordo com a invenção, são apresentadas na tabela 2 seguinte. Tabela 2
[00111]O comportamento dos coaglomerados de manitol, de acordo com a invenção, é inteiramente satisfatório em termos de capacidade de compressão e de fluxo.
[00112]Com teores em amido baixos (1%) ou mais elevado (20%), o coa- glomerado, de acordo com a invenção, apresenta uma capacidade de compressão elevada.
[00113]Essa capacidade de compressão elevada permite formular dois com-primidos que conservam uma dureza e, portanto, uma coesão suficiente, após incor-poração de um teor elevado em princípio ativo.
[00114]Portanto, é uma característica essencial e buscada para um excipien- te farmacêutico dedicado aos comprimidos e cápsulas rígidas de gelatina. Além dis so, os tempos de fluxo medidos são muito curtos, o que permitirá uma utilização in dustrial à cadência muito alta sobre prensas a comprimir e encapsuladoras.
[00115]Exemplo 2: Preparo de coaglomerados, de acordo com a invenção, por pulverização a seco de uma solução de manitol e incorporação de amido granu lar sob a forma seca no pulverizador.
[00116]Preparam-se por pulverização a seco, de acordo com a invenção, di-ferentescomposições de coaglomerados que consistem em manitol e em amido com razões respectivamente de 80/20, 70/30 e 50/50.
[00117]Utiliza-se manitol cristalizado, comercializado pela sociedade reque rente pelo nome de PEARLITOL® 50C que apresenta um diâmetro médio volumétri co laser de aproximadamente 50 μm e amido de milho “extra-branco”.
[00118]Prepara-se uma solução de manitol na matéria seca desejada, dis-solvendo o manitol cristalizado na água desmineralizada a 70 °C.
[00119]O amido é introduzido sob a forma seca na reciclagem das finas, via um dosador ponderal comercializado pela sociedade K-TRON.
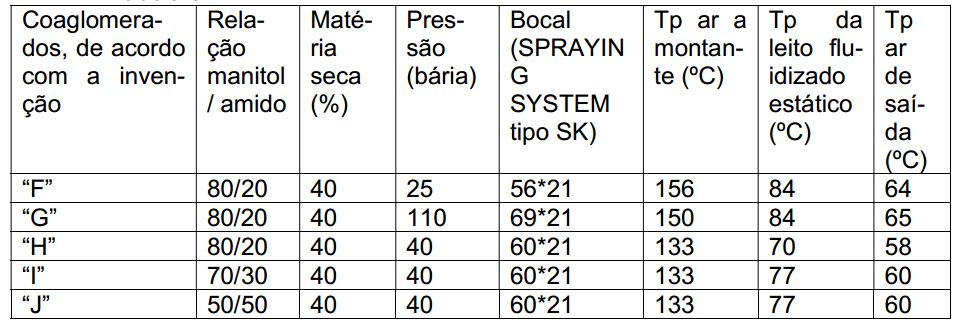
[00120]As condições operacionais de fabricação desses coaglomerados no pulverizador de tipo MSD 20 comercializado pela sociedade NIRO estão representa das na tabela 3 a seguir. Tabela 3
[00121]As condições de preparo dos coaglomerados H, I, J, de acordo com a invenção, mostram que, nos mesmos parâmetros, o aumento da taxa de amido faz diminuir a granulometria média.
[00122]Aquelas relativas ao preparo dos coaglomerados F e G mostram que quanto mais considerável for a pressão de pulverização a seco, mais a granulome- tria média diminuirá.
[00123]As características dos coaglomerados de manitol e de amido, de acordo com a invenção, são apresentadas na tabela 4 a seguir, em comparação com duas misturas físicas P1 e P2: - a mistura P1 sendo constituída de 80% de PEARLITOL® 50C e 20% de amido “extra-branco”, - a mistura P2 sendo constituída de 80% de PEARLITOL® 200SD (comer-cializado pela sociedade requerente) e 20% de amido “extra-branco”. Tabela 4
[00124]O comportamento dos coaglomerados de manitol, de acordo com a invenção, é inteiramente satisfatório, em termos de fluxo e de capacidade de com pressão.
[00125]É possível fazer variar os parâmetros de produção, para ajustar a granulometria e a densidade do pó.
[00126]A homogeneidade de mistura de um excipiente e de um ativo depen de do processo de mistura utilizado, mas também da similitude das características dos dois pós.
[00127]É mais fácil misturar um pó de princípio ativo e um pó de excipiente, quando apresentam a mesma granulometria e a mesma densidade.
[00128]Daí o interesse de fazer variar essas características e dispor de uma faixa de pós de propriedades diferentes para se adaptar aos diferentes pós de prin cípios ativos. Além disso, é possível fazer variar o teor em amido do coaglomerado para ajustar a capacidade de compressão ao produto a formular sem perturbar as notáveis propriedades de fluxo do pó.
[00129]Uma simples mistura física de pós (P1 e P2) não permite obter os comprimidos buscados.
[00130]Exemplo 3: Preparo de coaglomerados, de acordo com a invenção, por granulação da mistura de uma solução de manitol e de amido, o amido sendo colocado em suspensão na solução de manitol.
[00131]Preparam-se por granulação, de acordo com a invenção, diferentes composições de coaglomerados que consistem em manitol e em amido com razões respectivamente de 85/15, 70/30 e 50/50.
[00132]Utiliza-se o manitol cristalizado, comercializado pela sociedade re-querente pelo nome PEARLITOL® 50C que apresenta um diâmetro médio volumé trico laser de aproximadamente 50 μm e amido de milho “extra-branco”.
[00133]Prepara-se uma solução de manitol e de amido na matéria seca de-sejada, dissolvendo o manitol cristalizado na água desmineralizada a 55 °C e colo cando em suspensão o amido de milho “extra branco”.
[00134]A agitação deve permitir obter uma solução fluida, homogênea e sem embolotamentos.
[00135]As condições operacionais de fabricação desses coaglomerados no granulador com leito de ar fluidizado contínuo de tipo AGT 150 comercializado pela Sociedade GLATT estão representadas na tabela 5 a seguir.
[00137]As características dos coaglomerados de manitol e de amido, de acordo com a invenção, são apresentadas na tabela 6 seguinte. Tabela 6
[00138]Os resultados obtidos demonstram que se obtiveram, por granula- ção, coaglomerados, de acordo com a invenção, equivalentes àqueles obtidos por pulverização a seco.
[00139]Exemplo 4: Preparo de coaglomerados, de acordo com a invenção, por pulverização a seco da mistura de uma solução de manitol e de amido granular introduzido sob a forma seca no pulverizador.
[00140]Prepara-se por pulverização a seco, de acordo com a invenção, três coaglomerados que consistem em manitol e em amido a uma razão de 80/20 com o manitol cristalizado e três amidos granulares diferentes, o amido de milho “extra branco”, a fécula de batata, e um amido de milho ceroso hidróxipropilado estabiliza do e de ligações transversais de fosfato, comercializado pela sociedade requerente sob a denominação CLEARAM® CR 20/10.
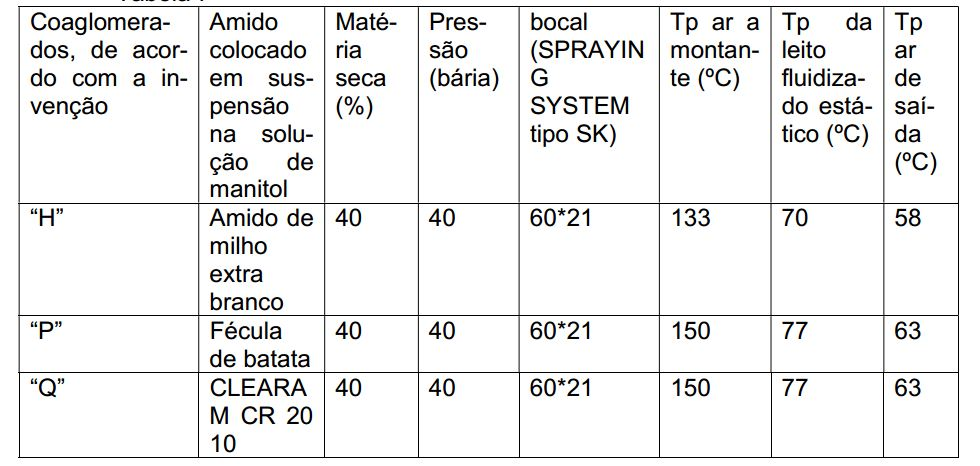
[00141]As condições operacionais de fabricação desses coaglomerados es tão representadas na tabela 7 a seguir. Tabela 7
[00142]As características dos coaglomerados de manitol e de amido, de acordo com a invenção, são apresentadas na tabela 8 a seguir. Tabela 8
[00143]O comportamento dos coaglomerados de manitol, de acordo com a invenção, é inteiramente satisfatório em capacidade de compressão e em fluxo.
[00144]A substituição do amido de milho “extra branco” por qualquer outro tipo de amido granular é possível, preservando-se as características essenciais do produto, de acordo com a invenção.
[00145]Portanto, é possível realizar esse aglomerado independentemente do amido granular em sua disposição, e, portanto, se livrar dos problemas de disponibi-lidade, de cultura regional, mas também considerar o desejo ou problemas dos con-sumidores(ausência de organismo geneticamente modificado) ou dos pacientes (amido de trigo que causa o mal celíaco).
[00146]Uma modificação química do amido para modular suas propriedades é também realizável, desde que este permaneça granular.
[00147]Exemplo 5: Enchimento de cápsulas rígidas de gelatina sobre uma encapsuladora automática de tipo disco dosadora, com um coaglomerado, de acor do com a invenção, e em comparação, com dois pós de manitol comercializados pe la sociedade requerente.
[00148]O objetivo desses testes é de determinar a taxa mínima de lubrifican-tenecessário a um funcionamento correto da encapsuladora.
[00149]Para isto, utiliza-se o estearato de magnésio que o lubrificante mais utilizado em farmácia.
[00150]Uma mistura homogênea do pó de teste e de estearato de magnésio Pharma Veg de BARLOCHER (Alemanha) é preparada. Em um pote com conteúdo de um litro, colocam-se as quantidades de produto a testar e de estearato de mag nésio, de maneira a atingir uma massa final para as duas quantidades de 300 g.
[00151]Os dois produtos são em seguida misturados durante cinco minutos com o auxílio de um misturador epicicloidal Turbula T2F de WILLY A. BACHOFEN (Suíça). A mistura assim realizada é dita lubrificada.
[00152]O material utilizado para encher essas cápsulas rígidas de gelatina é uma encapsuladora In-Cap de DOTT. BONAPACE (Italie).
[00153]O tamanho das cápsulas rígidas de gelatina escolhido é o formato “2” e todas as peças correspondentes a esse formato são instaladas sobre a encapsu- ladora In-Cap.
[00154]Dois formatos de tambor dosador são possíveis sobre a encapsula- dora In-Cap. Utiliza-se o grande modelo.
[00155]Regulam-se as agulhas de compressão da seguinte forma: agulha 1 = 27,5 mm, agulha 2 = 29 mm, agulha 3 = 32 mm e agulha 4 = 35 mm.
[00156]A distância expressa é aquela medida entre a face superior da porca de fixação de cada agulha e a face inferior da porca de regulagem de cada agulha.
[00157]A agulha 1 é a primeira agulha a entrar em ação. A agulha 1 penetra mais profundamente no disco dosador e a agulha 4 penetra menos profundamente no disco dosador. O disco dosador e o contra-disco têm uma espessura de 14,5 mm.
[00158]Os envoltórios de cápsulas rígidas de gelatina utilizados são Coni- Snap de CAPSUGEL (referência 2Cs Natural Tr. Código 43.000).
[00159]Regula-se a espessura da camada de pó no tambor dosador, a fim de serem obtidas cápsulas rígidas de gelatina cheias com a mistura lubrificada e com uma massa final de 310 mg.
[00160]O teste é considerado como satisfatório, caso a produção de uma sé-riecontínua de 300 cápsulas rígidas de gelatina seja possível.
[00161]Nenhuma interrupção de nenhum modo é tolerada durante a produ ção dessas 300 cápsulas rígidas de gelatina.
[00162]As cápsulas rígidas de gelatina não são fechadas definitivamente, a fim de poder abri-las de novo e assim fazer uma observação das tampas que elas contêm. Tabela 9
[00163]Com uma taxa de estearato de magnésio inferior a 3% para o PEARLITOL® 200SD e o PEARLITOL® 300DC (duas qualidades de manitol comer-cializadas pela sociedade requerente), ou inferior a 1,5% para os coaglomerados, de acordo com a invenção, a encapsuladora In-Cap não pode funcionar corretamente.
[00164]Produz-se um bloqueio das tampas no disco dosador e a agulha de ejeção deve exercer uma força anormalmente elevada para empurrá-las no corpo das cápsulas rígidas de gelatina.
[00165]O que ocasiona problemas que vão de uma irregularidade de peso das cápsulas rígidas de gelatina a paradas frequentes de produção, até a quebra da encapsuladora.
[00166]O acréscimo de um teor elevado - 3 % - de estearato de magnésio permite resolver o problema em todos os casos, mas ela cria um retardo na dissolu ção da cápsula rígida de gelatina e, portanto, da biodisponibilidade do princípio ativo. E, detrimento do cuidado levado ao paciente.
[00167]Com efeito, o estearato de magnésio é insolúvel na água, e a essa concentração elevada de 3 %, gera uma camada de barreira insolúvel que diminui muito a dissolução da cápsula rígida de gelatina.
[00168]Os coaglomerados, de acordo com a invenção, necessitam apenas de uma baixa taxa de estearato de magnésio; a metade da taxa precedente. A ca mada de barreira insolúvel não pode se criar ou é muito frágil para limitar a dissolu ção e a biodisponibilidade do princípio ativo.
[00169]Exemplo 6: Enchimento de cápsulas rígidas de gelatina com coaglo- merados, de acordo com a invenção, e um princípio ativo, o paracetamol.
[00170]O material utilizado para encher as cápsulas rígidas de gelatina é um simulador montado sobre uma máquina universal de tração-compressão INSTRON (EUA). O simulador é um bloco de metal atravessado por um orifício vertical cilíndri co fechado na parte inferior por uma cauda de andorinha móvel.
[00171]O diâmetro interno desse orifício é ligeiramente inferior ao diâmetro interno de um envoltório de cápsula rígida de gelatina de formato “0”. A parte inferior do bloco metálico é prevista para receber um suporte que mantém a parte inferior do envoltório da cápsula rígida de gelatina no eixo do orifício vertical.
[00172]Um cilindro metálico, denominado pistão, de um diâmetro ligeiramen te inferior àquele do orifício vertical é utilizado para comprimir o pó lubrificado no bloco metálico e assim formar a tampa.
[00173]Uma mistura homogênea do coaglomerado, do paracetamol (RHODAPAP® cristalizado fino de RHODIA) e de estearato de magnésio Pharma Veg de BARLOCHER (Alemanha) é preparado.
[00174]Em um pote com conteúdo de um litro, colocam-se 147,75 g (49,25%) de coaglomerado e 147,75g (49,25%) de paracetamol. Os dois produtos são misturados durante cinco minutos com o auxílio de um misturador epicicloidal Turbula T2F de WILLY A. BACHOFEN (Suíça).
[00175]São acrescentados 4,5 g de (1,5 %) de estearato de magnésio e mis tura-se de novo durante 5 minutos. A mistura assim realizada é dita lubrificada.
[00176]Os envoltórios de cápsulas rígidas de gelatina de formato “0” utiliza dos são provenientes do laboratório LGA (Bandol France).
[00177]São introduzidos 500 mg de mistura lubrificada no simulador. O pis tão encarregado de comprimir o pó desce a uma velocidade vertical constante de 20 mm por minuto até que a força aplicada sobre a mistura lubrificada para formar a tampa seja de 600 N.
[00178]A tampa, uma vez formada, e, após retirada da cauda de andorinha móvel, é empurrada pelo pistão na parte inferior do envoltório da cápsula rígida de gelatina.
[00179]As cápsulas rígidas de gelatina são em seguida fechadas manual mente.
[00180]O tempo de desagregação das cápsulas rígidas de gelatina assim preparadas é medido segundo o método preconizado pela Farmacopéia Européia (P.E. 6.0, 01/2008: 20901, 2.9.1. Desagregação dos comprimidos e das cápsulas), medida feita em doze cápsulas rígidas de gelatina.Tabela 10
[00181]As cápsulas rígidas de gelatina de paracetamol assim preparadas apresentam um tempo de desintegração na água muito pequeno, inferior a 3 minu tos. Esse tempo é muito inferior aos 15 minutos, tempo de desagregação imposto pela Farmacopéia Européia para as cápsulas rígidas de gelatina.
[00182]Esses testes confirmam que os coaglomerados, de acordo com a in-venção, permitem atingir tempos de desintegração muito curtos.
[00183]Exemplo 7: Realização de comprimidos com coaglomerados, de acordo com a invenção, e em comparação com um pó de manitol comercializado pela sociedade requerente.
[00184]O objetivo desses testes é de determinar a taxa mínima de lubrifican-tenecessária a um funcionamento correto da prensa para comprimir. Para isso, utili za-se o estearato de magnésio que é o lubrificante mais usado em farmácia.
[00185]Uma mistura homogênea do pó a testar e de estearato de magnésio Pharma Vegl de BARLOCHER (Alemanha) é preparada.
[00186]Em um pote com conteúdo de um litro, colocam-se as quantidades de produto a testar e de estearato de magnésio, de maneira a atingir uma massa final para as duas quantidades de 300 g.
[00187]Os dois produtos são em seguida misturados durante cinco minutos com o auxílio de um misturador epicicloidal Turbula T2F de WILLY A. BACHOFEN (Suíça). A mistura assim realizada é dita lubrificada.
[00188]Os comprimidos são preparados com o auxílio de uma prensa alter nativa de laboratório FROGERAIS AM comercializado pela sociedade SVIAC (Fran ça) equipada com dois punções côncavos de diâmetro 13 mm. Os comprimidos com faces convexas e com diâmetro de 13 mm têm uma espessura de 6 mm e um peso de 0,734 g.
[00189]Teores decrescentes em estearato de magnésio foram testados: 1,2%; 1,0%; 0,8%; 0,6%; 0,4%; (% expresso em relação à mistura dos dois pós).
[00190]A presença de colagem (uma parte do pó permanece colada na su-perfície do punção após ejeção do comprimido) e de bloqueio (o corte dos compri midos apresenta estrias) é observada. O teor mínimo em lubrificantes corresponde ao teor no qual nenhum desses dois defeitos foi observado.
[00191]Para o PEARLITOL® 200SD, pó de manitol comercializado pela so-ciedade requerente, esse teor é de 1,2%. Para os coaglomerados, de acordo com a invenção, ele é de 0,6%.
[00192]Um teor mais baixo em lubrificante é favorável à dissolução e à bio- disponibilidade dos ativos, além disso, ele pressagia maior facilidade em produzir industrialmente os comprimidos.
[00193]Uma lubrificação simples e facilitada permite atingir cadências de produção muito elevadas sem risco de desclassificação ou parada, em consequên cia dos problemas de colagem ou de bloqueio.
[00194]Exemplo 8: Comparação de coaglomerados, de acordo com a inven ção, e de aglomerados de manitol e de amido realizados em um pulverizador de simples efeito.
[00195]Preparam-se aglomerados de manitol cristalino e de amido granular, com razões manitol/amido respectivamente de 80/20 e 50/50, em um pulverizador de simples efeito.
[00196]Para isso, utiliza-se o manitol cristalizado, comercializado pela socie dade requerente pelo nome de PEARLITOL® 50C apresentando um diâmetro médio volumétrico laser de aproximadamente 50 μm e do amido de milho “extra-branco”.
[00197]Prepara-se uma solução de manitol e de amido na matéria seca de-sejada, dissolvendo o manitol cristalizado na água desmineralizada a 55 °C e colo cando aí em suspensão o amido de milho “extra-branco”.
[00198]A agitação deve permitir obter uma solução fluida, homogênea e sem embolotamento. As condições operacionais de fabricação desses aglomerados no pulverizador de simples efeito comercializado pela sociedade NIRO (atomizador NIRO Minor) são apresentadas na tabela 11 a seguir. Tabela 11
[00199]As características dos aglomerados de manitol e de amido assim preparados em um pulverizador de simples efeito são apresentadas na tabela 12 a seguir. Tabela 12 * O fluxo no funil foi facilitado graças a uma haste, a fim de se obter o volu- me aerado.
[00200]Em relação ao comportamento dos coaglomerados, de acordo com a invenção, o comportamento dos aglomerados de manitol e de amido realizados em um pulverizador de simples efeito não é absolutamente satisfatório em termos de capacidade de compressão e de fluxo.
[00201]A capacidade de compressão fraca (aglomerado “R”) até mesmo ine-xistente (aglomerado “S”) não permite formular comprimidos que conservam uma dureza e, portanto, uma coesão suficiente após incorporação de um teor elevado em princípio ativo.
[00202]Além disso, as propriedades de fluxo dos aglomerados “R” e “S” são tão más que elas não permitem medir um tempo de fluxo (tempo infinito segundo o teste B).
Claims (12)
1. Coaglomerado de manitol cristalino e de amido granular, CARACTERIZADO pelo fato de que: - a capacidade de compressão, determinada de acordo com o teste A, é maior que 120 N, de preferência, entre 200 e 450 N, - a escala de fluxo, determinada de acordo com o teste B, é entre 3 e 15 se-gundos, de preferência, entre 4 e 8 segundos, em que a razão manitol/amido é entre 99,5/0,5 e 50/50, e, de preferência, entre 95/5 e 70/30.
2. Coaglomerado, de acordo com a reivindicação 1, CARACTERIZADO pelo fato de que o diâmetro médio de volume de laser D4, 3 é entre 60 e 500 μm, de pre-ferência, entre 100 e 250 μm.
3. Coaglomerado, de acordo com a reivindicação 1 ou 2, CARACTERIZADO pelo fato de que: - a densidade aerada é entre 0,400 e 0,750 g/mL, de preferência, entre 0,450 e 0,650 g/mL, e - a densidade compactada é entre 0,500 e 0,850 g/mL, de preferência, entre 0,550 e 0,750 g/mL.
4. Coaglomerado, de acordo com qualquer uma das reivindicações 1 a 3, CARACTERIZADO pelo fato de que o amido é escolhido do grupo consistindo em amido de milho padrão, amido de milho extra branco e a amido de batata, conside rados sozinhos ou em combinação.
5. Coaglomerado, de acordo com qualquer uma das reivindicações 1 a 4, CARACTERIZADO pelo fato de que o manitol é fornecido em ambas as formas cris-talinas alfa e beta.
6. Processo para a preparação de um coaglomerado de manitol cristalino e de amido, conforme definido em qualquer uma das reivindicações 1 a 5, CARACTERIZADO pelo fato de que compreende as seguintes etapas: a) preparar a uma temperatura entre 45 e 65 °C, uma solução de manitol e de amido granular, na qual: - a razão manitol/amido é entre 99,5/0,5 e 50/50, e, de preferência, entre 95/5 e 70/30; - o teor de sólidos é entre 25 e 45% em peso seco; b) manter a dita solução de manitol e de amido a uma temperatura entre 45 e 65 °C; c) pulverizar a seco a dita solução em um pulverizador a seco de tipo MSD equipado com um bocal de pulverização a seco de alta pressão com reciclagem das partículas finas no topo do pulverizador a seco, d) recuperar os coaglomerados de manitol e de amido assim obtidos.
7. Processo para a preparação de um coaglomerado de manitol cristalino e de amido, conforme definido em qualquer uma das reivindicações 1 a 5, CARACTERIZADO pelo fato de que compreende as seguintes etapas: a) preparar a uma temperatura entre 45 e 90 °C uma solução de manitol, na qual o teor de sólidos é entre 25 e 50% em peso seco, b) manter a dita solução de manitol a uma temperatura entre 45 e 90 °C, c) pulverizar a seco a dita solução em um pulverizador a seco de tipo MSD equipado com um bocal de pulverização a seco de alta pressão com reciclagem das partículas finas no topo do pulverizador a seco, o amido seco sendo injetado via um dispositivo dosador em peso no sistema para reciclagem das partículas finas em uma razão manitol/amido entre 99,5/0,5 e 50/50, e, de preferência, entre 95/5 e 70/30, d) recuperar os coaglomerados de manitol e de amido assim obtidos.
8. Processo, conforme definido em qualquer uma das reivindicações 1 a 5, CARACTERIZADO pelo fato de que compreende as seguintes etapas: a) preparar a uma temperatura entre 45 e 65 °C, uma solução de manitol e de amido granular, na qual: - a razão manitol/amido é entre 99,5/0,5 e 50/50, e, de preferência, entre 95/5 e 70/30; - o teor de sólidos é entre 25 e 45% em peso seco; b) manter a dita solução de manitol e de amido a uma temperatura entre 45 e 65 °C; c) granular a dita solução por pulverização em um granulador com leito flui- dizado por ar; d) recuperar os coaglomerados de manitol e de amido assim obtidos.
9. Uso dos coaglomerados, conforme definidos em qualquer uma das reivin-dicações 1 a 5, ou preparados de acordo com o processo, conforme definido em qualquer uma das reivindicações 6 a 8, CARACTERIZADO pelo fato de que é para a fabricação de comprimidos destinados aos campos alimentícios, farmacêuticos, proteção de plantas e detergentes.
10. Comprimido composto de coaglomerados de manitol e de amido granu lar, conforme definidos em qualquer uma das reivindicações 1 a 5, CARACTERIZADO pelo fato de que é obtido de acordo com o processo conforme definido em qualquer uma das reivindicações 6 a 8.
11. Uso dos coaglomerados, conforme definidos em qualquer uma das rei-vindicações 1 a 5, ou preparados conforme definidos em qualquer uma das reivindi-cações 6 a 8, CARACTERIZADO pelo fato de que é para a fabricação de cápsulas rígidas de gelatina destinadas aos campos alimentícios e farmacêuticos.
12. Cápsula rígida de gelatina, composta de coaglomerados de manitol e de amido granular, conforme definidos em qualquer uma das reivindicações 1 a 5, CARACTERIZADA pelo fato de que é obtida de acordo com o processo, conforme definido em qualquer uma das reivindicações 6 a 8.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0952894 | 2009-04-30 | ||
| FR0952894A FR2944971B1 (fr) | 2009-04-30 | 2009-04-30 | Coagglomerats de mannitol et d'amidon granulaire comprimables et a ecoulement libre |
| PCT/FR2010/050813 WO2010125313A1 (fr) | 2009-04-30 | 2010-04-28 | Coagglomerats de mannitol et d'amidon granulaire comprimables et a ecoulement libre |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI1014371A2 BRPI1014371A2 (pt) | 2020-09-24 |
| BRPI1014371B1 true BRPI1014371B1 (pt) | 2021-07-27 |
Family
ID=41402540
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI1014371-8A BRPI1014371B1 (pt) | 2009-04-30 | 2010-04-28 | Coaglomerado de manitol e de amido granular, uso e processo para a preparação deste, comprimido composto de coaglomerados de manitol e de amido granular e cápsula rígida de gelatina, composta de coaglomerados de manitol e de amido granular |
Country Status (13)
| Country | Link |
|---|---|
| US (4) | US9937131B2 (pt) |
| EP (1) | EP2424508B1 (pt) |
| JP (1) | JP5676566B2 (pt) |
| KR (2) | KR20170012593A (pt) |
| CN (1) | CN102413819B (pt) |
| AR (2) | AR076519A1 (pt) |
| BR (1) | BRPI1014371B1 (pt) |
| CA (1) | CA2755992C (pt) |
| ES (1) | ES2795824T3 (pt) |
| FR (1) | FR2944971B1 (pt) |
| MX (1) | MX358382B (pt) |
| RU (1) | RU2540914C2 (pt) |
| WO (1) | WO2010125313A1 (pt) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2944971B1 (fr) * | 2009-04-30 | 2012-09-07 | Roquette Freres | Coagglomerats de mannitol et d'amidon granulaire comprimables et a ecoulement libre |
| CN104770694B (zh) * | 2015-04-15 | 2020-09-15 | 中国农业科学院农产品加工研究所 | 利用马铃薯冲调粉造粒设备进行造粒的方法 |
| FR3038836B1 (fr) | 2015-07-17 | 2017-07-14 | Roquette Freres | Granules de mannitol pour compression directe |
| CA2916077C (en) * | 2015-12-22 | 2023-06-20 | Euro-Pharm International Canada Inc. | Nicotine-containing solid oral formulations and uses thereof |
| JP2017158534A (ja) * | 2016-03-07 | 2017-09-14 | 焼津水産化学工業株式会社 | チップ状食品の製造方法及びチップ状食品 |
| KR102151268B1 (ko) | 2018-08-24 | 2020-09-02 | 주식회사 산하이앤씨 | 지하수정호 결합 복합 지열시스템 및 그 성능 평가방법 |
| KR102191122B1 (ko) | 2019-01-18 | 2020-12-16 | 엘지전자 주식회사 | 전동식 압축기 |
| IT201900002857A1 (it) * | 2019-02-27 | 2020-08-27 | Ntc S R L | Procedimento di riempimento di contenitori con una polvere |
| CN120076787A (zh) | 2022-10-28 | 2025-05-30 | 罗盖特公司 | 用于配制湿气敏感性活性成分的化合物 |
| CN116617406A (zh) * | 2023-06-16 | 2023-08-22 | 齐鲁理工学院 | 一种微晶甘露醇药用辅料、硬胶囊及其制备方法 |
| CN116509807B (zh) * | 2023-07-04 | 2023-09-19 | 山东天力药业有限公司 | 一种甘露醇颗粒的制备方法 |
| CN117503938B (zh) * | 2023-11-24 | 2024-09-13 | 江苏西典药用辅料有限公司 | 直压型甘露醇的制备方法 |
| CN117860688B (zh) * | 2024-03-12 | 2024-05-31 | 山东天力药业有限公司 | 一种直压级甘露醇颗粒及其制备方法 |
| CN118453884B (zh) * | 2024-07-12 | 2024-09-27 | 山东天力药业有限公司 | 一种含甘露醇的药用辅料及其制备方法 |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3145146A (en) | 1961-10-31 | 1964-08-18 | Warner Lambert Pharmaceutical | Modified mannitol for pharmaceutical tablets |
| JPS6185331A (ja) * | 1984-10-04 | 1986-04-30 | Fuji Kagaku Kogyo Kk | 直打用賦形薬の製造法 |
| FR2640876B1 (pt) * | 1988-12-28 | 1993-09-24 | Jouveinal Sa | |
| DE3903217A1 (de) * | 1989-02-03 | 1990-08-09 | Boehringer Ingelheim Vetmed | Verfahren zur herstellung fester pharmazeutischer zubereitungen |
| JPH0977669A (ja) * | 1995-09-19 | 1997-03-25 | Takeda Chem Ind Ltd | ビタミンb群顆粒品の組成物およびその製造方法 |
| US6235947B1 (en) * | 1997-04-14 | 2001-05-22 | Takeda Chemical Industries, Ltd. | D-mannitol and its preparation |
| JPH10158153A (ja) * | 1996-11-25 | 1998-06-16 | Nippon Eranko Kk | 医薬用硬質ゼラチンカプセル及びその製造方法 |
| GB9802201D0 (en) * | 1998-02-03 | 1998-04-01 | Cerestar Holding Bv | Free-flowable directly compressible starch as binder,disintegrant and filler for compresion tablets and hard gelatine capsules |
| ATE283708T1 (de) * | 1999-02-15 | 2004-12-15 | Sumitomo Pharma | Im mundraum schnellzerfallende tabletten |
| US6740339B1 (en) * | 1999-06-18 | 2004-05-25 | Takeda Chemical Industries, Ltd. | Quickly disintegrating solid preparations |
| US6664389B1 (en) * | 1999-10-01 | 2003-12-16 | National Starch And Chemical Investment Holding Coporation | Highly resistant granular starch |
| CA2342121C (fr) | 2000-03-29 | 2010-05-25 | Roquette Freres | Mannitol pulverulent et son procede de preparation |
| FR2807034B1 (fr) * | 2000-03-29 | 2002-06-14 | Roquette Freres | Mannitol pulverulent et son procede de fabrication |
| DE60036205T2 (de) * | 2000-07-27 | 2008-05-21 | Roquette Frères | Granulat bestehend aus Stärke und Laktose |
| US6544552B2 (en) * | 2001-01-11 | 2003-04-08 | Particle And Coating Technologies, Inc. | Method of producing porous tablets with improved dissolution properties |
| DE10161402A1 (de) * | 2001-12-13 | 2003-06-18 | Merck Patent Gmbh | Verfahren zur Herstellung von direkt tablettierbarem beta-Mannit |
| JP2004175795A (ja) * | 2002-11-13 | 2004-06-24 | Takeda Chem Ind Ltd | 薬物の放出性に優れた医薬組成物 |
| KR100535228B1 (ko) * | 2003-03-11 | 2005-12-08 | 한국유나이티드제약 주식회사 | 란소프라졸함유 경질캅셀제의 제조방법 |
| SE0301880D0 (sv) * | 2003-06-25 | 2003-06-25 | Astrazeneca Uk Ltd | New drug delivery composition |
| CN101269055B (zh) * | 2007-03-21 | 2011-12-14 | 北京德众万全药物技术开发有限公司 | 盐酸氨溴索口腔崩解片及其制备方法 |
| CN101181404A (zh) * | 2007-11-28 | 2008-05-21 | 南京海陵中药制药工艺技术研究有限公司 | 一种治疗咽部疾病的口含片及制备方法 |
| FR2933299B1 (fr) * | 2008-07-04 | 2012-02-03 | Roquette Freres | Mannitol orodispersible |
| FR2944971B1 (fr) * | 2009-04-30 | 2012-09-07 | Roquette Freres | Coagglomerats de mannitol et d'amidon granulaire comprimables et a ecoulement libre |
-
2009
- 2009-04-30 FR FR0952894A patent/FR2944971B1/fr active Active
-
2010
- 2010-04-28 US US13/318,211 patent/US9937131B2/en active Active
- 2010-04-28 CA CA2755992A patent/CA2755992C/fr active Active
- 2010-04-28 KR KR1020177002042A patent/KR20170012593A/ko not_active Ceased
- 2010-04-28 KR KR1020117025617A patent/KR101867621B1/ko active Active
- 2010-04-28 ES ES10727061T patent/ES2795824T3/es active Active
- 2010-04-28 RU RU2011148600/15A patent/RU2540914C2/ru active
- 2010-04-28 EP EP10727061.3A patent/EP2424508B1/fr active Active
- 2010-04-28 JP JP2012507804A patent/JP5676566B2/ja active Active
- 2010-04-28 WO PCT/FR2010/050813 patent/WO2010125313A1/fr not_active Ceased
- 2010-04-28 MX MX2011011497A patent/MX358382B/es active IP Right Grant
- 2010-04-28 BR BRPI1014371-8A patent/BRPI1014371B1/pt active IP Right Grant
- 2010-04-28 CN CN201080019380.3A patent/CN102413819B/zh active Active
- 2010-04-30 AR ARP100101479A patent/AR076519A1/es not_active Application Discontinuation
-
2017
- 2017-06-12 US US15/620,399 patent/US20170281550A1/en not_active Abandoned
-
2020
- 2020-01-21 US US16/748,222 patent/US11364204B2/en active Active
- 2020-04-23 AR ARP200101143A patent/AR118760A2/es unknown
-
2021
- 2021-09-24 US US17/483,990 patent/US20220008343A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| KR101867621B1 (ko) | 2018-06-15 |
| WO2010125313A1 (fr) | 2010-11-04 |
| JP5676566B2 (ja) | 2015-02-25 |
| US20220008343A1 (en) | 2022-01-13 |
| AR076519A1 (es) | 2011-06-15 |
| CN102413819A (zh) | 2012-04-11 |
| US20200155460A1 (en) | 2020-05-21 |
| RU2011148600A (ru) | 2013-06-10 |
| EP2424508B1 (fr) | 2020-03-11 |
| FR2944971A1 (fr) | 2010-11-05 |
| KR20170012593A (ko) | 2017-02-02 |
| US11364204B2 (en) | 2022-06-21 |
| US20120053249A1 (en) | 2012-03-01 |
| JP2012525361A (ja) | 2012-10-22 |
| ES2795824T3 (es) | 2020-11-24 |
| AR118760A2 (es) | 2021-10-27 |
| CA2755992A1 (fr) | 2010-11-04 |
| EP2424508A1 (fr) | 2012-03-07 |
| RU2540914C2 (ru) | 2015-02-10 |
| CN102413819B (zh) | 2015-09-09 |
| BRPI1014371A2 (pt) | 2020-09-24 |
| MX2011011497A (es) | 2011-11-18 |
| US9937131B2 (en) | 2018-04-10 |
| KR20120016075A (ko) | 2012-02-22 |
| MX358382B (es) | 2018-08-15 |
| FR2944971B1 (fr) | 2012-09-07 |
| US20170281550A1 (en) | 2017-10-05 |
| CA2755992C (fr) | 2018-04-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI1014371B1 (pt) | Coaglomerado de manitol e de amido granular, uso e processo para a preparação deste, comprimido composto de coaglomerados de manitol e de amido granular e cápsula rígida de gelatina, composta de coaglomerados de manitol e de amido granular | |
| ES2218346T5 (es) | Manitol en polvo y procedimiento para la preparación del mismo | |
| US10105314B2 (en) | Orodispersible mannitol | |
| CN106998720A (zh) | 压缩固体奶片及其制备方法 | |
| CA2643054A1 (en) | Granules, tablets and method of producing the same | |
| Chauhan et al. | Fast dissolving tablets: a promising approach for drug delivery | |
| MX2007016072A (es) | Formulaciones de diclofenac y metodos para usarlas. | |
| UA114412C2 (uk) | Тверда дозована форма гіпурату (s)-2-аміно-3-(4-(2-аміно-6-((r)-1-(4-хлор-2-(3-метил-1h-піразол-1-іл)феніл)-2,2,2-трифторетокси)піримідин-4-іл)феніл)пропаноату | |
| UA129276C2 (uk) | Багатоодинична пероральна лікарська форма з модифікованим вивільненням доксиламіну сукцинату і піридоксину гідрохлориду і спосіб її отримання | |
| JP2020059660A (ja) | マンニトール造粒物 | |
| EP2913049B1 (en) | Stable pharmaceutical compositions | |
| Deshmukh et al. | Formulation and evaluation of fast dissolving tablets of chlorpromazine hydrochloride using novel co-processed superdisintegrants | |
| US20240115600A1 (en) | Oral granules with combination of extended-release and quick-release magnesium, and production methods | |
| JP4573542B2 (ja) | ビタミンb1誘導体組成物 | |
| EP2796130A2 (en) | Immediate release tablets of rasagiline hemitartrate | |
| Bhatjire et al. | Hot melt extrusion technique for solid oral dosage form-a review | |
| JP6451310B2 (ja) | 固形医薬組成物及びその製造方法 | |
| WO2011135106A1 (es) | Granulado altamente dispersable para la preparación de formulaciones de sustancias activas de altas dosis y procedimiento de obtención del mismo | |
| JP2011073972A (ja) | 混合粉体およびその製造方法、固形製剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NO 10196/2001, QUE MODIFICOU A LEI NO 9279/96, A CONCESSAO DA PATENTE ESTA CONDICIONADA A ANUENCIA PREVIA DA ANVISA. CONSIDERANDO A APROVACAO DOS TERMOS DO PARECER NO 337/PGF/EA/2010, BEM COMO A PORTARIA INTERMINISTERIAL NO 1065 DE 24/05/2012, ENCAMINHA-SE O PRESENTE PEDIDO PARA AS PROVIDENCIAS CABIVEIS. |
|
| B07G | Grant request does not fulfill article 229-c lpi (prior consent of anvisa) [chapter 7.7 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 28/04/2010, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |