一种新型含三唑的烯丙基苯甲酸酯类化合物及其制备方法和
应用
技术领域
本发明涉及一种新型含三唑的烯丙基苯甲酸酯类化合物及其制备方法和应用。
背景技术
含氮杂环化合物具有广泛的生物活性,因此在农药创制过程中意义重大。三唑类杀菌剂属于有机杂环氮类化合物,是麦角甾醇合成抑制剂,对危害作物生长的多数真菌病害均有良好防治效果。近几十年以来,三唑类杀菌剂以其高效、广谱、低毒等优势占据了极大市场,由于多数三唑类杀菌剂同时还具有植物生长调节功能,所以三唑类抗真菌药物类型的研究备受关注。迄今为止,数万个三唑类化合物先后被合成发现,而其中1,2,4-三氮唑类化合物占据了大部分,其中已经商品化的品种达到40多种,例如三唑酮(triadimefon)、三唑醇(triadimenol)、丙环唑(propiconazole)、多效唑(Paclobutrazol)等等。随着三唑类杀菌剂在农业上的频繁使用,一些缺点也随之暴露出来,其单一的活性位点,由于频繁使用使得真菌的抗药性越来越强从而使其失去了高效性。
设计合成新型的三唑类杀菌剂对我们开发高效、低毒、低残留的新型农药具有重要意义。
发明内容
针对现有技术存在的上述技术问题,本发明的目的在于提供一种新型含三唑的烯丙基苯甲酸酯类化合物及其制备方法和应用。本发明是基于烯效唑结构为母体,保持烯效唑的苯环、三唑环和碳碳双键不变,用氢与三氟甲基取代苯环上的氯,用苯环替代烯效唑的叔丁基,羟基上引入酯基、芳环合成酯类化合物以考察对化合物生物活性的影响,设计合成了三唑类系列化合物。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物,其特征在于其结构式如式(Ⅰ)所示:
式(Ⅰ)中:取代基R1为苯基或取代苯基,所述取代苯基的苯环上的取代基数量为一个或多个,各个取代基各自独立地选自H、卤素、C1-C4烷基、甲氧基或硝基;取代基R2为氢或三氟甲基。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物,其特征在于式(Ⅰ)中R1为下列之一:苯基、2-甲基苯基、2-氯苯基、2,4-二氯苯基、3-甲氧基苯基、2,6-二氯苯基、2-氟苯基、3-氟苯基、4-甲基苯基、2,3-二氯苯基、4-叔丁基苯基、4-正丙基苯基、4-甲氧基苯基、3-甲基苯基、4-氟苯基、3-硝基苯基、3-氯苯基。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物的制备方法,其特征在于包括以下步骤:
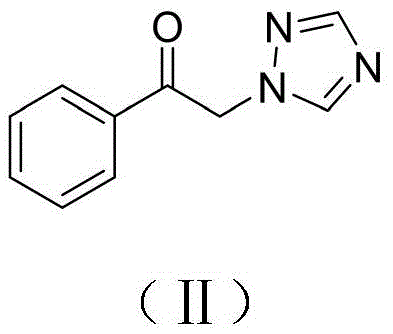
1)ɑ-溴代苯乙酮和1,2,4-三氮唑混合在有机溶剂A中,控温至0℃以下,滴加三乙胺后,于室温下搅拌反应,TLC跟踪反应进程;反应结束后抽滤除去反应生成的三乙胺盐酸盐,滤液经脱溶后,用有机溶剂B重结晶处理制得如式(Ⅱ)所示1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮;
2)将步骤1)所得式(Ⅱ)所示1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮、苯甲醛或对三氟甲基苯甲醛、哌啶在有机试剂C中加热回流反应,TLC跟踪反应进程;待反应结束后,冷却至室温,将反应液转移至分液漏斗内,水洗后分层,有机相再用饱和食盐水洗涤1-3次后,经无水硫酸钠干燥,过滤,滤液浓缩除去溶剂,浓缩物经柱层析分离提纯处理制得如式(Ⅲ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-酮类化合物;
3)步骤2)所得式(Ⅲ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-酮类化合物分散在有机试剂D中,加入PEG 600和硼氢化钠,在0℃冰浴条件下搅拌反应,TLC跟踪反应进程;待反应结束后,将反应液脱溶,脱溶浓缩物中滴加0.5~2N盐酸溶液,用有机试剂E萃取并合并有机相,随后经无水硫酸钠干燥,过滤,旋干溶剂处理制得如式(Ⅳ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-醇类化合物;
4)将步骤3)所得如式(Ⅳ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-醇类化合物分散在有机试剂F中,并加入DMAP、EDC和取代苯甲酸,室温下搅拌反应,TLC跟踪反应进程;待反应结束后,水洗,再用饱和食盐水洗涤,无水硫酸钠干燥,过滤,经柱层析分离提纯处理制得如式(Ⅰ)所示的一种新型含三唑的烯丙基苯甲酸酯类化合物;
其中,所述R1为苯基或取代苯基,所述取代苯基的苯环上的取代基数量为一个或多个,各个取代基各自独立地选自H、卤素、C1-C4烷基、甲氧基或硝基;取代基R2为氢或三氟甲基。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物的制备方法,其特征在于步骤1)中的有机溶剂A为酮类溶剂,优选为丙酮;有机溶剂B为醇类溶剂,优选为异丙醇;步骤2)中的有机溶剂C为苯类溶剂,优选为甲苯;步骤3)中的有机试剂D为醇类溶剂,优选为甲醇;步骤3)中的有机试剂E和步骤4)中的有机溶剂F均为二氯甲烷。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物的制备方法,其特征在于步骤1)中,所述ɑ-溴代苯乙酮和1,2,4-三氮唑的投料摩尔比为1:1.1~1.5;步骤2)中,式(Ⅱ)所示的1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮和(对三氟甲基)苯甲醛的投料摩尔比为1:1.1~1.5;步骤3)中,式(Ⅲ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-酮类化合物和硼氢化钠的投料摩尔比为1:1.1~1.5;步骤4)中,式(Ⅳ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-醇类化合物和取代苯甲酸的投料摩尔比为1:1.1~1.5。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物的制备方法,其特征在于步骤1)中有机溶剂A的体积用量以ɑ-溴代苯乙酮的物质的量计为1~2mL/mmol,步骤2)中有机溶剂C的体积用量以式(Ⅱ)所示的1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮的物质的量计为1~1.5mL/mmol,步骤3)中有机溶剂D的体积用量以式(Ⅲ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-酮类化合物的物质的量计为2~3mL/mmol,步骤4)中有机溶剂F的体积用量以式(Ⅳ)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-醇类化合物的物质的量计为6~8mL/mmol。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物的制备方法,其特征在于步骤2)和步骤4)中柱层析分离的洗脱剂均采用体积比1:0.5~2的乙酸乙酯和石油醚混合液。
所述的一种新型含三唑的烯丙基苯甲酸酯类化合物在制备杀菌剂中的应用。
进一步地,所述新型含三唑的烯丙基苯甲酸酯类化合物用于制备抑制油菜菌核病菌的杀菌剂。
本发明新型含三唑的烯丙基苯甲酸酯类化合物的合成工艺路线如下:
与现有技术相比,本发明的有益效果主要体现在:本发明提供了一种新型含三唑的烯丙基苯甲酸酯类化合物及其制备方法与其制备杀菌剂中的应用,其制备方法简单、操作方便,得到的化合物在50ppm有效浓度下对油菜菌核病菌抑制活性最好,抑制率达到了71.4%,本发明所述化合物为具有杀菌活性的新化合物,为新农药的研发提供了基础。
具体实施方式
下面结合具体实施例对本发明作进一步说明,但本发明的保护范围并不限于此。
实施例1(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基苯甲酸酯的制备
1)1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮(Ⅱ)的合成:
在500mL三口烧瓶中依次加入ɑ-溴代苯乙酮(19.90g,0.10mol)、1,2,4-三氮唑(7.60g,0.11mol),加入150mL丙酮作溶剂,用冰盐浴控温在0℃以下,通过恒压滴液漏斗逐滴缓慢滴加三乙胺(11.13g,0.11mol)。滴加完毕后,继续反应1h,去冰浴,室温下继续搅拌1h,TLC(VEA/VPE=1/1,v/v)跟踪反应进程。待反应结束后,抽滤除去反应生成的三乙胺盐酸盐,三乙胺盐酸盐用丙酮淋洗,合并淋洗液和滤液后,经脱溶得到红色油状物,冷却固化,用20mL异丙醇重结晶制得式(Ⅱ)所示的1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮;
2)(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-酮(Ⅲ-1)的合成:
在装有分水器、温度计、冷凝管的100mL三口烧瓶中一次加入式(Ⅱ)所示的1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮(5.62g,30.00mmol),苯甲醛(3.50g,33.00mmol),加入30mL甲苯作溶剂,滴加哌啶(0.20g,2.35mmol)作为催化剂,加热回流反应6h,TLC(VEA/VPE=1/1,v/v)跟踪反应进程。待反应结束后,冷却至室温,将反应液转移至分液漏斗内,水洗后分层,有机相再用饱和食盐水洗涤两次(每次洗涤采用的饱和食盐水体积20mL),无水硫酸钠干燥,过滤,滤液浓缩除去溶剂,浓缩残留物经柱层析分离提纯(洗脱剂为体积比1:1石油醚和乙酸乙酯)制得式(Ⅲ-1)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-酮;
3)(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-醇(Ⅳ-1)的合成:
将式(Ⅲ-1)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-酮(1.93g,7.00mmol)加入到50mL圆底烧瓶中,加入15mL甲醇作溶剂,冰浴控温在0℃,加入PEG600(0.50g,0.83mmol),然后在搅拌下分批加入硼氢化钠(0.42g,11.00mmol),在0℃冰浴下反应4h,TLC(VEA/VPE=1/2,v/v)跟踪反应进程。待反应结束后,将反应液脱溶,脱溶浓缩物中滴加1N盐酸溶液,用二氯甲烷萃取三次(每次萃取用二氯甲烷15mL),合并有机相,随后经无水硫酸钠干燥,过滤,旋干溶剂制得式(Ⅳ-1)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-醇;
4)(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基苯甲酸酯(C1)的合成:
将式(Ⅳ-1)所示的(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)丙-2-烯-1-醇(0.20g,0.72mmol)、苯甲酸(0.10g,0.80mmol)、DMAP(0.09g,0.72mmol)、EDC(0.28g,1.44mmol)加入到5mL二氯甲烷中,室温下反应4h,随后将反应液转移至分液漏斗内,经水洗(3×5mL),再用饱和食盐水洗涤(2×5mL),无水硫酸钠干燥,过滤,滤液浓缩除去溶剂,浓缩残留物经柱层析分离提纯(洗脱剂为体积比1:1石油醚和乙酸乙酯)制得(C1)化合物。
其中式(Ⅲ)和式(Ⅳ)结构式中的取代基R2均为氢,分别形成了式(Ⅲ-1)和式(Ⅳ-1)的分子结构。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基苯甲酸酯:黄色油状物,收率52.36%;1H NMR(500MHz,CDCl3)δ:8.08(s,1H,triazole-H),7.68(s,1H,triazole-H),7.60-7.56(m,1H,ArH),7.48-7.42(m,5H,ArH),7.38-7.33(m,4H,ArH),7.21-7.17(m,3H,ArH),7.03(s,1H,CH),6.95(s,1H,=CH),6.84-6.79(m,2H,ArH).HRMS(ESI)for C24H19N3O2m/z:Calculated,382.1550,Found,382.1556[M+H]+.
实施例2(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2-甲基苯甲酸酯(C2)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的2-甲基苯甲酸,其他操作同实施例1,制得(C2)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2-甲基苯甲酸酯:黄色油状物,收率42.62%;1H NMR(500MHz,CDCl3)δ:8.09(s,1H,triazole-H),7.98(d,J=7.8Hz,1H,ArH),7.66(s,1H,triazole-H),7.45-7.42(m,2H,ArH),7.41-7.31(m,4H,ArH),7.27-7.21(m,2H,ArH),7.20-7.15(m,3H,ArH),7.02(s,1H,CH),6.93(s,1H,=CH),6.82-6.79(m,2H,ArH),2.56(s,3H,CH3).HRMS(ESI)for C25H21N3O2 m/z:Calculated,396.1707,Found,396.1712[M+H]+.
实施例3(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2-氯苯甲酸酯(C3)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的2-氯苯甲酸,其他操作同实施例1,制得(C3)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2-氯苯甲酸酯:黄色油状物,收率60.21%;1H NMR(500MHz,CDCl3)δ:8.09(s,1H,triazole-H),7.87(dd,J=7.8,1.3Hz,1H,ArH),7.67(s,1H,triazole-H),7.48-7.41(m,4H,ArH),7.38-7.31(m,4H,ArH),7.23-7.17(m,3H,ArH),7.03(s,1H,CH),6.98(s,1H,=CH),6.84-6.77(m,2H,ArH).HRMS(ESI)forC24H18ClN3O2m/z:Calculated,416.1160,Found,416.1166[M+H]+.
实施例4(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2,4-二氯苯甲酸酯(C4)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的2,4-二氯苯甲酸,其他操作同实施例1,制得(C4)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2,4-二氯苯甲酸酯:白色油状物,收率42.17%;1H NMR(500MHz,CDCl3)δ:8.09(s,1H,triazole-H),7.85(d,J=8.5Hz,1H,ArH),7.64(s,1H,triazole-H),7.48(d,J=2.0Hz,1H,ArH),7.44-7.40(m,2H,ArH),7.39-7.33(m,3H,ArH),7.32(dd,J=8.5,2.0Hz,1H,ArH),7.23-7.17(m,3H,ArH),7.02(s,1H,CH),6.96(s,1H,=CH),6.84-6.77(m,2H,ArH).HRMS(ESI)for C24H17Cl2N3O2 m/z:Calculated,450.0771,Found,450.0776[M+H]+.
实施例5(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-甲氧基苯甲酸酯(C5)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的3-甲氧基苯甲酸,其他操作同实施例1,制得(C5)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-甲氧基苯甲酸酯:白色蜡状物,收率25.35%;1H NMR(500MHz,CDCl3)δ:8.07(s,1H,triazole-H),8.06-8.02(m,2H,ArH),7.69(s,1H,triazole-H),7.44-7.40(m,2H,ArH),7.37-7.31(m,3H,ArH),7.21-7.16(m,3H,ArH),7.00(s,1H,CH),6.95(s,1H,=CH),6.94-6.91(m,2H,ArH),6.83-6.79(m,2H,ArH),3.83(s,3H,OCH3).HRMS(ESI)for C25H21N3O3 m/z:Calculated,412.1656,Found,412.1661[M+H]+.
实施例6(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2,6-二氯苯甲酸酯(C6)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的2,6-二氯苯甲酸,其他操作同实施例1,制得(C6)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2,6-二氯苯甲酸酯:黄色油状物,收率47.66%;1H NMR(500MHz,CDCl3)δ:8.08(s,1H,triazole-H),7.78(s,1H,triazole-H),7.52-7.49(m,2H,ArH),7.46-7.41(m,1H,ArH),7.39-7.35(m,3H,ArH),7.30-7.25(m,2H,ArH),7.21-7.17(m,3H,ArH),7.12(s,1H,CH),6.87(s,1H,=CH),6.82-6.78(m,2H,ArH).HRMS(ESI)for C24H17Cl2N3O2 m/z:Calculated,450.0771,Found,450.0776[M+H]+.
实施例7(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2-氟苯甲酸酯(C7)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的2-氟苯甲酸,其他操作同实施例1,制得(C7)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2-氟苯甲酸酯:黄色油状物,收率56.35%;1HNMR(500MHz,CDCl3)δ:8.07(s,1H,triazole-H),8.00-7.92(m,1H,ArH),7.72(s,1H,triazole-H),7.55-7.47(m,1H,ArH),7.46-7.40(m,2H,ArH),7.38-7.29(m,3H,ArH),7.22-7.10(m,5H,ArH),7.04(s,1H,CH),7.02(s,1H,=CH),6.86-6.78(m,2H,ArH).HRMS(ESI)for C24H18FN3O2 m/z:Calculated,400.1456,Found,400.1461[M+H]+.
实施例8(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-氟苯甲酸酯(C8)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的3-氟苯甲酸,其他操作同实施例1,制得(C8)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-氟苯甲酸酯:黄色油状物,收率58.34%;1H NMR(500MHz,CDCl3)δ:8.09(s,1H,triazole-H),7.90-7.85(m,1H,ArH),7.79-7.74(m,1H,ArH),7.65(s,1H,triazole-H),7.46-7.40(m,3H,ArH),7.39-7.33(m,3H,ArH),7.31-7.26(m,1H,ArH),7.23-7.17(m,3H,ArH),7.02(s,1H,CH),6.94(s,1H,=CH),6.88-6.78(m,2H,ArH).HRMS(ESI)for C24H18FN3O2 m/z:Calculated,400.1456,Found,400.1461[M+H]+.
实施例9(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-甲基苯甲酸酯(C9)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的4-甲基苯甲酸,其他操作同实施例1,制得(C9)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-甲基苯甲酸酯:白色油状物,收率44.72%;1H NMR(500MHz,CDCl3)δ:8.07(s,1H,triazole-H),7.97(d,J=8.2Hz,2H,ArH),7.69(s,1H,triazole-H),7.45-7.40(m,3H,ArH),7.36-7.32(m,4H,ArH),7.22-7.16(m,3H,ArH),7.01(s,1H,CH),6.95(s,1H,=CH),6.84-6.78(m,2H,ArH),2.40(s,3H,CH3).HRMS(ESI)for C25H21N3O2 m/z:Calculated,396.1707,Found,396.1712[M+H]+.
实施例10(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2,3-二氯苯甲酸酯(C10)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的2,3-二氯苯甲酸,其他操作同实施例1,制得(C10)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基2,3-二氯苯甲酸酯:黄色油状物,收率30.33%;1H NMR(500MHz,CDCl3)δ:8.08(s,1H,triazole-H),8.03(d,J=8.3Hz,2H,ArH),7.71(s,1H,triazole-H),7.50-7.45(m,3H,ArH),7.35-7.31(m,3H,ArH),7.21-7.15(m,3H,ArH),7.02(s,1H,CH),6.95(s,1H,=CH),6.84-6.78(m,2H,ArH).HRMS(ESI)forC24H17Cl2N3O2 m/z:Calculated,450.0771,Found,450.0776[M+H]+.
实施例11(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-叔丁基苯甲酸酯(C11)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的4-叔丁基苯甲酸,其他操作同实施例1,制得(C11)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-叔丁基苯甲酸酯:白色蜡状物,收率44.20%;1H NMR(500MHz,CDCl3)δ:8.10(s,1H,triazole-H),7.67(dd,J=7.8,1.5Hz,1H,ArH),7.64(s,1H,triazole-H),7.62(dd,J=8.0,1.5Hz,1H,ArH),7.44-7.41(m,2H,ArH),7.41-7.32(m,4H,ArH),7.29(d,J=7.9Hz,1H,ArH),7.24-7.20(m,3H,ArH),7.02(s,1H,CH),6.94(s,1H,=CH),6.83-6.80(m,2H,ArH),1.56(s,9H,t-Bu).HRMS(ESI)forC28H27N3O2 m/z:Calculated,438.2176,Found,438.2182[M+H]+.
实施例12(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-正丙基苯甲酸酯(C12)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的4-正丙基苯甲酸,其他操作同实施例1,制得(C12)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-正丙基苯甲酸酯:白色蜡状物,收率48.96%;1H NMR(500MHz,CDCl3)δ:8.07(s,1H,triazole-H),8.00(d,J=8.2Hz,2H,ArH),7.69(s,1H,triazole-H),7.45-7.41(m,2H,ArH),7.36-7.31(m,3H,ArH),7.26(d,J=8.4Hz,2H,ArH),7.22-7.17(m,3H,ArH),7.01(s,1H,CH),6.95(s,1H,=CH),6.81(dd,J=7.8,1.4Hz,2H,ArH),2.65(t,J=7.5Hz,2H,CH2),1.71-1.59(m,2H,CH2),0.94(t,J=7.3Hz,3H,CH3).HRMS(ESI)for C27H25N3O2 m/z:Calculated,424.2020,Found,424.2025[M+H]+.
实施例13(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-甲氧基苯甲酸酯(C13)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的4-甲氧基苯甲酸,其他操作同实施例1,制得(C13)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-甲氧基苯甲酸酯:白色蜡状物,收率27.43%;1H NMR(500MHz,CDCl3)δ:8.07(s,1H,triazole-H),8.06-8.02(m,2H,ArH),7.69(s,1H,triazole-H),7.42(d,J=7.0Hz,2H,ArH),7.36-7.29(m,3H,ArH),7.20-7.15(m,3H,ArH),7.00(s,1H,CH),6.95(s,1H,=CH),6.92(d,J=8.9Hz,2H,ArH),6.83-6.79(m,2H,ArH),3.82(s,3H,OCH3).HRMS(ESI)for C25H21N3O3 m/z:Calculated,412.1656,Found,412.1661[M+H]+.
实施例14(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-甲基苯甲酸酯(C14)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的3-甲基苯甲酸,其他操作同实施例1,制得(C14)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-甲基苯甲酸酯:白色油状物,收率55.64%;1H NMR(500MHz,CDCl3)δ:8.07(s,1H,triazole-H),7.89(d,J=7.6Hz,2H,ArH),7.70(s,1H,triazole-H),7.46-7.41(m,2H,ArH),7.36-7.30(m,5H,ArH),7.20-7.15(m,3H,ArH),7.03(s,1H,CH),6.95(s,1H,=CH),6.83-6.78(m,2H,ArH),2.38(s,3H,CH3).HRMS(ESI)for C25H21N3O2 m/z:Calculated,396.1707,Found,396.1712[M+H]+.
实施例15(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-氟苯甲酸酯(C15)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的4-氟苯甲酸,其他操作同实施例1,制得(C15)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基4-氟苯甲酸酯:黄色油状物,收率47.25%;1H NMR(500MHz,CDCl3)δ:8.08(s,1H,triazole-H),7.66(s,1H,triazole-H),7.44-7.39(m,3H,ArH),7.38-7.31(m,4H,ArH),7.21-7.15(m,3H,ArH),7.13-7.09(m,2H,ArH),7.02(s,1H,CH),6.95(s,1H,=CH),6.83-6.79(m,2H,ArH).HRMS(ESI)for C24H18FN3O2m/z:Calculated,400.1456,Found,400.1461[M+H]+.
实施例16(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-硝基苯甲酸酯(C16)的制备
将实施例1步骤4)中的苯甲酸替换为同等摩尔量的3-硝基苯甲酸,其他操作同实施例1,制得(C16)化合物。
(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-硝基苯甲酸酯:黄色蜡状物,收率15.16%;1H NMR(500MHz,CDCl3)δ:8.95-8.89(m,1H,ArH),8.47-8.43(m,1H,ArH),8.41-8.38(m,1H,ArH),8.11(s,1H,triazole-H),7.68(t,J=8.0Hz,1H,ArH),7.63(s,1H,triazole-H),7.44-7.37(m,5H,ArH),7.25-7.20(m,3H,ArH),7.07(s,1H,CH),6.94(s,1H,=CH),6.84-6.81(m,2H,ArH).HRMS(ESI)for C24H18N4O4 m/z:Calculated,427.1401,Found,427.1406[M+H]+.
实施例17(E)-1,3-二苯基-2-(1H-1,2,4-三唑-1-基)烯丙基3-硝基苯甲酸酯的制备
1)1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮(Ⅱ)的合成:
在500mL三口烧瓶中依次加入ɑ-溴代苯乙酮(19.90g,0.10mol)、1,2,4-三氮唑(7.60g,0.11mol),加入150mL丙酮作溶剂,用冰盐浴控温在0℃以下,通过恒压滴液漏斗逐滴缓慢滴加三乙胺(11.1g,0.11mol)。滴加完毕后,继续反应1h,去冰浴,室温下继续搅拌1h,TLC(VEA/VPE=1/1,v/v)跟踪反应进程。待反应结束后,抽滤除去反应生成的三乙胺盐酸盐,三乙胺盐酸盐用丙酮淋洗,合并淋洗液和滤液后,经脱溶得到红色油状物,冷却固化,用20mL异丙醇重结晶制得式(Ⅱ)所示的1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮;
2)(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)丙-2-烯-1-酮(Ⅲ-2)的合成:
在装有分水器、温度计、冷凝管的100mL三口烧瓶中依次加入式(Ⅱ)所示的1-苯基-2-(1H-1,2,4-三唑-1-基)乙-1-酮(5.62g,30.00mol),对三氟甲基苯甲醛(5.75g,33.00mmol),加入30mL甲苯作溶剂,滴加哌啶(0.20g,2.35mmol)作为催化剂,加热回流反应7h,TLC(VEA/VPE=1/1,v/v)跟踪反应进程。待反应结束后,冷却至室温,将反应液转移至分液漏斗内,水洗后分层,有机相再用饱和食盐水洗涤两次(每次洗涤采用的饱和食盐水体积20mL),无水硫酸钠干燥,过滤,滤液浓缩除去溶剂,浓缩残留物经柱层析分离提纯(洗脱剂为体积比1:1石油醚和乙酸乙酯)制得式(Ⅲ-2)所示的(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)丙-2-烯-1-酮;
3)(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)丙-2-烯-1-醇(Ⅳ-2)的合成:
将式(Ⅲ-2)所示的(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)丙-2-烯-1-酮(2.40g,7.00mmol)加入到50mL圆底烧瓶中,加入15mL甲醇作溶剂,冰浴控温在0℃,加入PEG 600(0.50g,0.83mmol),然后在搅拌下分批加入硼氢化钠(0.42g,11.0mmol),在0℃冰浴下反应4h,TLC(VEA/VPE=1/2,v/v)跟踪反应进程。待反应结束后,将反应液脱溶,脱溶浓缩物中滴加1N盐酸溶液,用二氯甲烷萃取三次(每次萃取用二氯甲烷15mL),合并有机相,经无水硫酸钠干燥,过滤,旋干溶剂制得式(Ⅳ-2)所示的(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)丙-2-烯-1-醇;
4)(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基苯甲酸酯(B1)的合成:
将式(Ⅳ-2)所示的(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)丙-2-烯-1-醇(0.25g,0.72mmol)、苯甲酸(0.10g,0.80mmol)、DMAP(0.09g,0.72mmol)、EDC(0.28g,1.44mmol)加入到5mL二氯甲烷中,室温下反应4h,随后将反应液转移至分液漏斗内,经水洗(3×5mL),再用饱和食盐水洗涤(2×5mL),无水硫酸钠干燥,过滤,滤液浓缩除去溶剂,浓缩残留物经柱层析分离提纯(洗脱剂为体积比1:1石油醚和乙酸乙酯)制得式(B1)化合物。
其中式(Ⅲ)和式(Ⅳ)结构式中的取代基R2均为三氟甲基,分别形成了式(Ⅲ-2)和式(Ⅳ-2)的分子结构。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基苯甲酸酯:黄色油状物,收率46.37%;1H NMR(500MHz,CDCl3)δ:8.10(s,1H,triazole-H),8.09-8.07(m,2H,ArH),7.67(s,1H,triazole-H),7.59(t,J=7.5Hz,1H,ArH),7.49-7.42(m,6H,ArH),7.40-7.33(m,3H,ArH),7.04(s,1H,CH),6.99(s,1H,=CH),6.96(d,J=8.3Hz,2H,ArH).HRMS(ESI)for C25H18F3N3O2 m/z:Calculated,450.1424,Found,450.1423[M+H]+.
实施例18(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2-甲基苯甲酸酯(B2)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的2-甲基苯甲酸,其他操作同实施例17,制得(B2)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2-甲基苯甲酸酯:黄色油状物,收率58.38%;1H NMR(500MHz,CDCl3)δ:8.10(s,1H,triazole-H),8.01-7.94(m,1H,ArH),7.65(s,1H,triazole-H),7.48-7.42(m,5H,ArH),7.39-7.33(m,3H,ArH),7.26(t,J=7.4Hz,2H,ArH),7.03(s,1H,CH),6.96(s,2H,ArH),6.94(s,1H,=CH),2.57(s,3H,CH3).HRMS(ESI)for C26H20F3N3O2 m/z:Calculated,464.1580,Found,464.1577[M+H]+.
实施例19(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2-氟苯甲酸酯(B3)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的2-氟苯甲酸,其他操作同实施例17,制得(B3)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2-氟苯甲酸酯:黄色油状物,收率72.35%;1H NMR(500MHz,CDCl3)δ:8.08(s,1H,triazole-H),8.01-7.94(m,1H,ArH),7.69(s,1H,triazole-H),7.61-7.52(m,1H,ArH),7.48-7.42(m,4H,ArH),7.38-7.32(m,3H,ArH),7.23(t,J=7.6Hz,1H,ArH),7.20-7.14(m,1H,ArH),7.07(s,1H,CH),7.04(s,1H,=CH),6.96(d,J=8.2Hz,2H,ArH).HRMS(ESI)for C25H17F4N3O2 m/z:Calculated,468.1330,Found,468.1327[M+H]+.
实施例20(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基4-叔丁基苯甲酸酯(B4)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的4-叔丁基苯甲酸,其他操作同实施例17,制得(B4)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基4-叔丁基苯甲酸酯:白色蜡状物,收率55.16%;1H NMR(500MHz,CDCl3)δ:8.08(s,1H,triazole-H),8.05-8.01(m,2H,ArH),7.68(s,1H,triazole-H),7.50-7.48(m,2H,ArH),7.47-7.42(m,4H,ArH),7.38-7.32(m,3H,ArH),7.03(s,1H,CH),6.98(s,1H,=CH),6.95(d,J=8.3Hz,2H,ArH),1.34(s,9H,t-Bu).HRMS(ESI)for C29H26F3N3O2 m/z:Calculated,506.2050,Found,506.2061[M+H]+.
实施例21(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基3-氯苯甲酸酯(B5)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的3-氯苯甲酸,其他操作同实施例17,制得(B5)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基3-氯苯甲酸酯:黄色油状物,收率48.75%;1H NMR(500MHz,CDCl3)δ:8.10(s,1H,triazole-H),8.04(t,J=1.8Hz,1H,ArH),7.98-7.94(m,1H,ArH),7.64(s,1H,triazole-H),7.59-7.55(m,1H,ArH),7.46(d,J=8.3Hz,2H,ArH),7.43-7.36(m,6H,ArH),7.04(s,1H,CH),6.97(s,2H,ArH),6.95(s,1H,=CH).HRMS(ESI)for C25H17ClF3N3O2 m/z:Calculated,484.1034,Found,484.1028[M+H]+.
实施例22(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基4-正丙基苯甲酸酯(B6)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的4-正丙基苯甲酸,其他操作同实施例17,制得(B6)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基4-正丙基苯甲酸酯:白色蜡状物,收率55.32%;1H NMR(500MHz,CDCl3)δ:8.10(s,1H,triazole-H),8.00(d,J=8.2Hz,2H,ArH),7.72(s,1H,triazole-H),7.58(t,J=7.4Hz,2H,ArH),7.45-7.41(m,3H,ArH),7.40-7.32(m,4H,ArH),7.02(s,1H,CH),6.99(s,1H,=CH),6.96(d,J=8.2Hz,2H,ArH),2.65(t,J=7.5Hz,2H,CH2),1.70-1.61(m,2H,CH2),0.94(t,J=7.3Hz,3H,CH3).HRMS(ESI)for C28H24F3N3O2 m/z:Calculated,492.1893,Found,492.1861[M+H]+.
实施例23(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基4-甲氧基苯甲酸酯(B7)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的4-甲氧基苯甲酸,其他操作同实施例17,制得(B7)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基4-甲氧基苯甲酸酯:白色蜡状物,收率44.10%;1H NMR(500MHz,CDCl3)δ:8.08(s,1H,triazole-H),8.06-8.03(m,2H,ArH),7.67(s,1H,triazole-H),7.46(d,J=8.3Hz,2H,ArH),7.43-7.40(m,2H,ArH),7.38-7.33(m,3H,ArH),7.00(s,1H,CH),6.98(s,1H,=CH),6.97-6.94(m,4H,ArH),3.86(s,3H,OCH3).HRMS(ESI)for C26H20F3N3O3 m/z:Calculated,480.1530,Found,480.1530[M+H]+.
实施例24(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2,4-二氯苯甲酸酯(B8)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的2,4-二氯苯甲酸,其他操作同实施例17,制得(B8)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2,4-二氯苯甲酸酯:黄色油状物,收率66.16%;1H NMR(500MHz,CDCl3)δ:8.10(s,1H,triazole-H),7.85(d,J=8.5Hz,1H,ArH),7.63(s,1H,triazole-H),7.49-7.45(m,3H,ArH),7.39-7.35(m,4H,ArH),7.34-7.31(m,2H,ArH),7.04(s,1H,CH),7.01(s,1H,=CH),6.95(d,J=8.2Hz,2H,ArH).
实施例25(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基3-硝基苯甲酸酯(B9)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的3-硝基苯甲酸,其他操作同实施例17,制得(B9)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基3-硝基苯甲酸酯:白色蜡状物,收率23.17%;1H NMR(500MHz,CDCl3)δ:8.93-8.89(m,1H,ArH),8.48-8.43(m,1H,ArH),8.40(d,J=7.9Hz,1H,ArH),8.13(s,1H,triazole-H),7.70(t,J=8.0Hz,1H,ArH),7.67(s,1H,triazole-H),7.49-7.39(m,7H,ArH),7.09(s,1H,CH),6.99(s,1H,=CH),6.98(d,J=8.3Hz,2H,ArH).HRMS(ESI)for C25H17F3N4O4 m/z:Calculated,495.1275,Found,495.1271[M+H]+.
实施例26(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2,3-二氯苯甲酸酯(B10)的制备
将实施例17步骤4)中的苯甲酸替换为同等摩尔量的2,3-二氯苯甲酸,其他操作同实施例17,制得(B10)化合物。
(E)-1-苯基-2-(1H-1,2,4-三唑-1-基)-3-(4-(三氟甲基)苯基)烯丙基2,3-二氯苯甲酸酯:黄色油状物,收率33.25%;1H NMR(500MHz,CDCl3)δ:8.11(s,1H,triazole-H),7.67(dd,J=7.8,1.6Hz,1H,ArH),7.64(s,1H,triazole-H),7.47(d,J=8.3Hz,2H,ArH),7.45-7.42(m,2H,ArH),7.41-7.36(m,3H,ArH),7.31-7.27(m,2H,ArH),7.04(s,1H,CH),6.99(s,1H,=CH),6.95(d,J=8.3Hz,2H,ArH).HRMS(ESI)for C25H16Cl2F3N3O2 m/z:Calculated,518.0644,Found,518.0644[M+H]+.
实施例27杀菌活性测试
试验对象:番茄早疫病菌(Alternari asolani)、小麦赤霉病菌(Gibberellazeae)、马铃薯晚疫病菌(Phytophthora infestans)、辣椒疫霉病菌(Phytophthoracapsici)、油菜菌核(Sclerotinia sclerotiorum)、黄瓜灰霉病菌(Botrytis cinerea)、水稻纹枯病菌(Rhizoctonia solani)、黄瓜枯萎病菌(Fusarium oxysporum)、花生褐斑病菌(Cercospora arachidicola)、苹果轮纹病菌(Physalosporapiricola)。
将实施例1~16制备的式(C1)~式(C16)所示化合物,将实施例17~26制备的式(B1)~式(B10)所示化合物分别标记为待测化合物,并按以下方式进行杀菌活性测试:
试验处理:各待测化合物用DMSO溶解成1%EC母液备用。采用抑菌圈法,评价待测化合物在50ppm剂量下对试验靶标的室内杀菌活性,另设溶剂清水对照(QCK),另设有效含量为50ppm的氟唑菌酰胺对照(YCK)。
试验方法:用移液枪吸取150微升上述配置的EC母液,溶于2.85mL的吐温水中,配成待测化合物的有效浓度为500ppm的药液。用移液枪吸取1mL药液放入已灭菌的培养皿中,再放入9mL的PDA培养基,摇匀,冷却。用打孔器打取圆形菌饼后用接种针挑至培养皿中央,然后将培养皿置于培养箱27℃中培养,48~72h后测量菌落直径。菌落纯生长量为菌落平均直径与菌饼直径的差值,抑菌率(%)计算方法参照如下公式进行计算。
上述计算公式中的对照菌落纯生长量,是指清水对照(QCK)测试下的菌落纯生长量。
杀菌活性测试结果如表1所示。
表1 50ppm下各化合物的杀菌活性(%防效)
由表可知,C系列化合物对油菜菌核表现出了不错的抑制率,大部分化合物抑菌率都超过了60%,其中C1、C7、C14对油菜菌核的抑菌率超过了70%,C8、C13对水稻纹枯的抑菌率也超过了60%,C7、C11、C13、C16对苹果轮纹的抑菌率都达到了58.3%,但均不及对照药剂氟唑菌酰胺。
由表可知,B系列各化合物均表现出一定的活性,其中B1、B2、B3、B5、B6、B7、B8、B9化合物对于油菜菌核的抑制率均超过了50%,B7对小麦赤霉的抑制率超过了50%,B1、B3、B6、B7对于水稻纹枯的防治率超过了50%,总体来说B系列的杀菌活性不是非常理想,与对照药剂氟唑菌酰胺相比,对辣椒疫霉的防治率高于氟唑菌酰胺,部分化合物对小麦赤霉的防治率也要高于氟唑菌酰胺。
本说明书所述的内容仅仅是对发明构思实现形式的列举,本发明的保护范围不应当被视为仅限于实施例所陈述的具体形式。