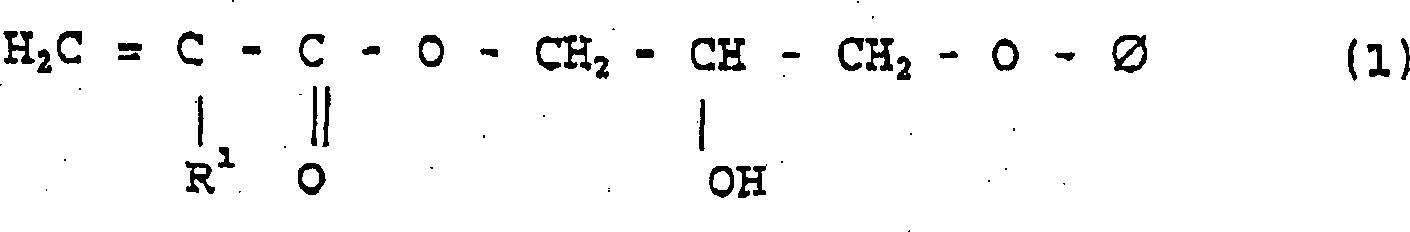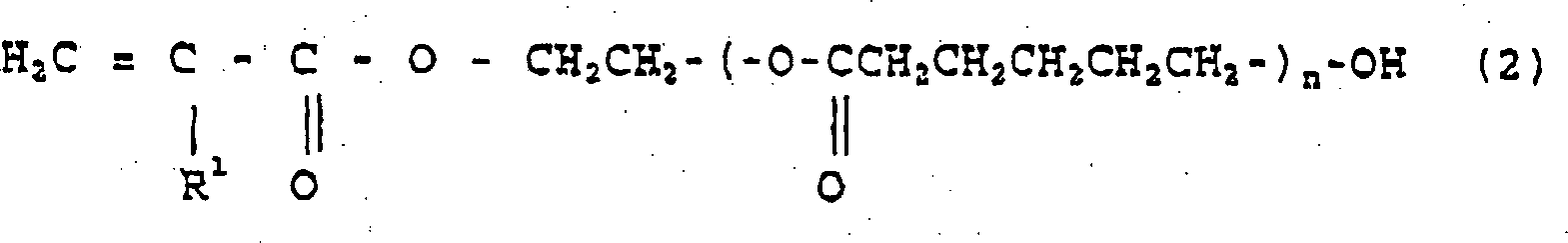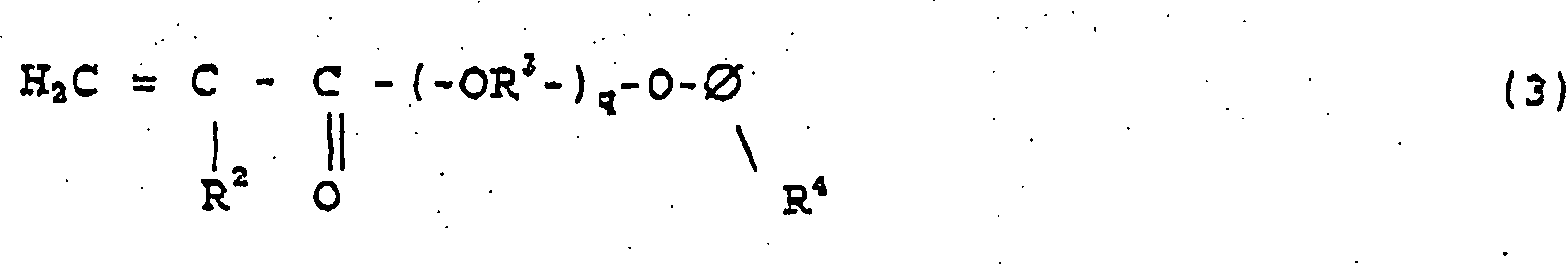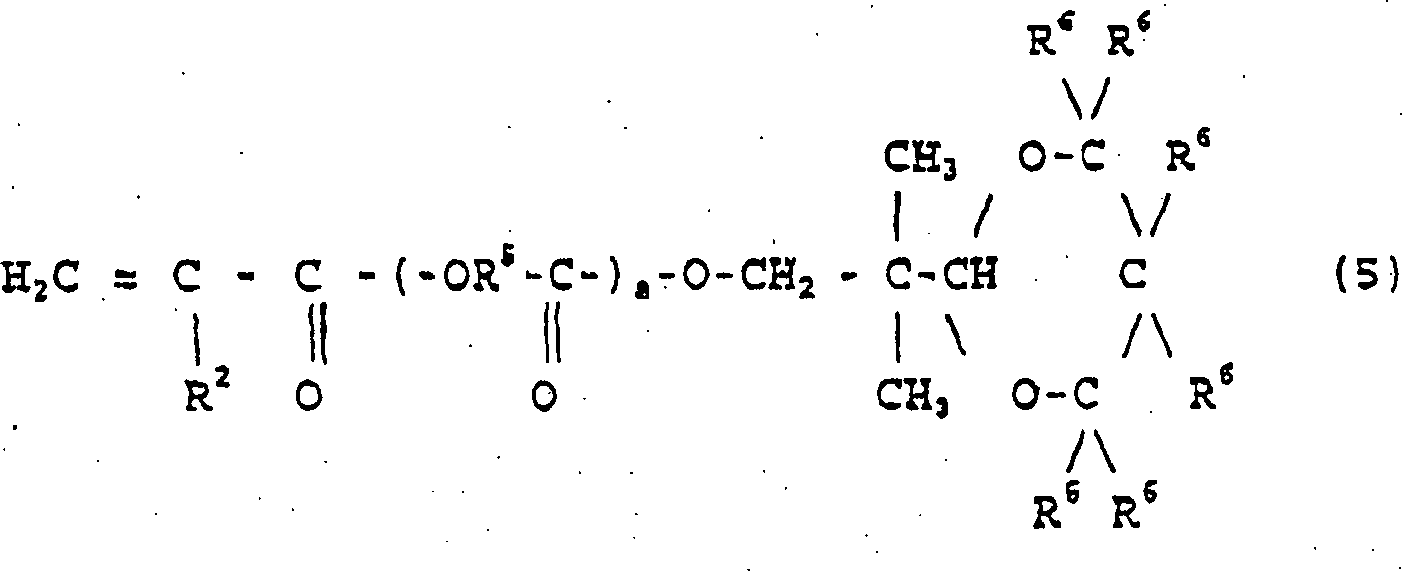DE69827807T2 - Beschichtete optische faser und strahlungshärtbare harzzusammensetzung - Google Patents
Beschichtete optische faser und strahlungshärtbare harzzusammensetzung Download PDFInfo
- Publication number
- DE69827807T2 DE69827807T2 DE69827807T DE69827807T DE69827807T2 DE 69827807 T2 DE69827807 T2 DE 69827807T2 DE 69827807 T DE69827807 T DE 69827807T DE 69827807 T DE69827807 T DE 69827807T DE 69827807 T2 DE69827807 T2 DE 69827807T2
- Authority
- DE
- Germany
- Prior art keywords
- composition
- meth
- radiation
- acrylate
- optical fiber
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000013307 optical fiber Substances 0.000 title claims description 36
- 230000005855 radiation Effects 0.000 title claims description 8
- 239000011342 resin composition Substances 0.000 title claims description 7
- 239000000203 mixture Substances 0.000 claims description 66
- 229920000642 polymer Polymers 0.000 claims description 44
- 238000000576 coating method Methods 0.000 claims description 41
- 239000011248 coating agent Substances 0.000 claims description 38
- 239000000178 monomer Substances 0.000 claims description 26
- 239000004721 Polyphenylene oxide Substances 0.000 claims description 20
- 229920000570 polyether Polymers 0.000 claims description 20
- 239000004814 polyurethane Substances 0.000 claims description 12
- 229920002635 polyurethane Polymers 0.000 claims description 12
- 229920005862 polyol Polymers 0.000 claims description 9
- 150000003077 polyols Chemical class 0.000 claims description 9
- 239000003999 initiator Substances 0.000 claims description 7
- 239000008199 coating composition Substances 0.000 claims description 5
- 239000000758 substrate Substances 0.000 claims description 4
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims description 4
- 230000001464 adherent effect Effects 0.000 claims description 2
- 239000011521 glass Substances 0.000 claims description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 89
- -1 methacryloyl group Chemical group 0.000 description 29
- 150000001875 compounds Chemical class 0.000 description 24
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 22
- 239000000463 material Substances 0.000 description 20
- 150000002009 diols Chemical class 0.000 description 17
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 14
- WERYXYBDKMZEQL-UHFFFAOYSA-N butane-1,4-diol Chemical compound OCCCCO WERYXYBDKMZEQL-UHFFFAOYSA-N 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 8
- 239000007788 liquid Substances 0.000 description 8
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical group NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 7
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 7
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 7
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 239000003963 antioxidant agent Substances 0.000 description 6
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 6
- 239000005056 polyisocyanate Substances 0.000 description 6
- 229920001228 polyisocyanate Polymers 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- JWYVGKFDLWWQJX-UHFFFAOYSA-N 1-ethenylazepan-2-one Chemical compound C=CN1CCCCCC1=O JWYVGKFDLWWQJX-UHFFFAOYSA-N 0.000 description 5
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 5
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 5
- 230000005540 biological transmission Effects 0.000 description 5
- 150000001923 cyclic compounds Chemical class 0.000 description 5
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 5
- 239000004417 polycarbonate Substances 0.000 description 5
- 229920000515 polycarbonate Polymers 0.000 description 5
- IGFHQQFPSIBGKE-UHFFFAOYSA-N Nonylphenol Natural products CCCCCCCCCC1=CC=C(O)C=C1 IGFHQQFPSIBGKE-UHFFFAOYSA-N 0.000 description 4
- 239000006096 absorbing agent Substances 0.000 description 4
- 125000002723 alicyclic group Chemical group 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 239000004611 light stabiliser Substances 0.000 description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 4
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- SNQQPOLDUKLAAF-UHFFFAOYSA-N nonylphenol Chemical compound CCCCCCCCCC1=CC=CC=C1O SNQQPOLDUKLAAF-UHFFFAOYSA-N 0.000 description 4
- 229920001223 polyethylene glycol Polymers 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- DTGKSKDOIYIVQL-WEDXCCLWSA-N (+)-borneol Chemical group C1C[C@@]2(C)[C@@H](O)C[C@@H]1C2(C)C DTGKSKDOIYIVQL-WEDXCCLWSA-N 0.000 description 3
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 3
- 239000006087 Silane Coupling Agent Substances 0.000 description 3
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 3
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical class C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 3
- 125000002947 alkylene group Chemical group 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 150000004985 diamines Chemical class 0.000 description 3
- VFHVQBAGLAREND-UHFFFAOYSA-N diphenylphosphoryl-(2,4,6-trimethylphenyl)methanone Chemical compound CC1=CC(C)=CC(C)=C1C(=O)P(=O)(C=1C=CC=CC=1)C1=CC=CC=C1 VFHVQBAGLAREND-UHFFFAOYSA-N 0.000 description 3
- 239000000835 fiber Substances 0.000 description 3
- 229920000728 polyester Polymers 0.000 description 3
- 229920001451 polypropylene glycol Polymers 0.000 description 3
- 229920001296 polysiloxane Polymers 0.000 description 3
- 238000007142 ring opening reaction Methods 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- BPXVHIRIPLPOPT-UHFFFAOYSA-N 1,3,5-tris(2-hydroxyethyl)-1,3,5-triazinane-2,4,6-trione Chemical compound OCCN1C(=O)N(CCO)C(=O)N(CCO)C1=O BPXVHIRIPLPOPT-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- INQDDHNZXOAFFD-UHFFFAOYSA-N 2-[2-(2-prop-2-enoyloxyethoxy)ethoxy]ethyl prop-2-enoate Chemical compound C=CC(=O)OCCOCCOCCOC(=O)C=C INQDDHNZXOAFFD-UHFFFAOYSA-N 0.000 description 2
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 2
- LJPCNSSTRWGCMZ-UHFFFAOYSA-N 3-methyloxolane Chemical compound CC1CCOC1 LJPCNSSTRWGCMZ-UHFFFAOYSA-N 0.000 description 2
- UUEWCQRISZBELL-UHFFFAOYSA-N 3-trimethoxysilylpropane-1-thiol Chemical compound CO[Si](OC)(OC)CCCS UUEWCQRISZBELL-UHFFFAOYSA-N 0.000 description 2
- VVBLNCFGVYUYGU-UHFFFAOYSA-N 4,4'-Bis(dimethylamino)benzophenone Chemical compound C1=CC(N(C)C)=CC=C1C(=O)C1=CC=C(N(C)C)C=C1 VVBLNCFGVYUYGU-UHFFFAOYSA-N 0.000 description 2
- FIHBHSQYSYVZQE-UHFFFAOYSA-N 6-prop-2-enoyloxyhexyl prop-2-enoate Chemical compound C=CC(=O)OCCCCCCOC(=O)C=C FIHBHSQYSYVZQE-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- VVJKKWFAADXIJK-UHFFFAOYSA-N Allylamine Chemical compound NCC=C VVJKKWFAADXIJK-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 2
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical group C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 2
- LFOXEOLGJPJZAA-UHFFFAOYSA-N [(2,6-dimethoxybenzoyl)-(2,4,4-trimethylpentyl)phosphoryl]-(2,6-dimethoxyphenyl)methanone Chemical compound COC1=CC=CC(OC)=C1C(=O)P(=O)(CC(C)CC(C)(C)C)C(=O)C1=C(OC)C=CC=C1OC LFOXEOLGJPJZAA-UHFFFAOYSA-N 0.000 description 2
- UKLDJPRMSDWDSL-UHFFFAOYSA-L [dibutyl(dodecanoyloxy)stannyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)O[Sn](CCCC)(CCCC)OC(=O)CCCCCCCCCCC UKLDJPRMSDWDSL-UHFFFAOYSA-L 0.000 description 2
- VEBCLRKUSAGCDF-UHFFFAOYSA-N ac1mi23b Chemical compound C1C2C3C(COC(=O)C=C)CCC3C1C(COC(=O)C=C)C2 VEBCLRKUSAGCDF-UHFFFAOYSA-N 0.000 description 2
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- 230000003712 anti-aging effect Effects 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- XITRBUPOXXBIJN-UHFFFAOYSA-N bis(2,2,6,6-tetramethylpiperidin-4-yl) decanedioate Chemical compound C1C(C)(C)NC(C)(C)CC1OC(=O)CCCCCCCCC(=O)OC1CC(C)(C)NC(C)(C)C1 XITRBUPOXXBIJN-UHFFFAOYSA-N 0.000 description 2
- MQDJYUACMFCOFT-UHFFFAOYSA-N bis[2-(1-hydroxycyclohexyl)phenyl]methanone Chemical compound C=1C=CC=C(C(=O)C=2C(=CC=CC=2)C2(O)CCCCC2)C=1C1(O)CCCCC1 MQDJYUACMFCOFT-UHFFFAOYSA-N 0.000 description 2
- 150000004292 cyclic ethers Chemical class 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 239000012975 dibutyltin dilaurate Substances 0.000 description 2
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 2
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- IQPQWNKOIGAROB-UHFFFAOYSA-N isocyanate group Chemical group [N-]=C=O IQPQWNKOIGAROB-UHFFFAOYSA-N 0.000 description 2
- QQVIHTHCMHWDBS-UHFFFAOYSA-N isophthalic acid Chemical compound OC(=O)C1=CC=CC(C(O)=O)=C1 QQVIHTHCMHWDBS-UHFFFAOYSA-N 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- OTLDLKLSNZMTTA-UHFFFAOYSA-N octahydro-1h-4,7-methanoindene-1,5-diyldimethanol Chemical compound C1C2C3C(CO)CCC3C1C(CO)C2 OTLDLKLSNZMTTA-UHFFFAOYSA-N 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- 229920001610 polycaprolactone Polymers 0.000 description 2
- 239000004632 polycaprolactone Substances 0.000 description 2
- KIDHWZJUCRJVML-UHFFFAOYSA-N putrescine Chemical compound NCCCCN KIDHWZJUCRJVML-UHFFFAOYSA-N 0.000 description 2
- 238000007151 ring opening polymerisation reaction Methods 0.000 description 2
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- DVKJHBMWWAPEIU-UHFFFAOYSA-N toluene 2,4-diisocyanate Chemical compound CC1=CC=C(N=C=O)C=C1N=C=O DVKJHBMWWAPEIU-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 229920002554 vinyl polymer Polymers 0.000 description 2
- 229940042596 viscoat Drugs 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- JNELGWHKGNBSMD-UHFFFAOYSA-N xanthone Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3OC2=C1 JNELGWHKGNBSMD-UHFFFAOYSA-N 0.000 description 2
- QNODIIQQMGDSEF-UHFFFAOYSA-N (1-hydroxycyclohexyl)-phenylmethanone Chemical compound C=1C=CC=CC=1C(=O)C1(O)CCCCC1 QNODIIQQMGDSEF-UHFFFAOYSA-N 0.000 description 1
- BJZYYSAMLOBSDY-QMMMGPOBSA-N (2s)-2-butoxybutan-1-ol Chemical compound CCCCO[C@@H](CC)CO BJZYYSAMLOBSDY-QMMMGPOBSA-N 0.000 description 1
- WYTZZXDRDKSJID-UHFFFAOYSA-N (3-aminopropyl)triethoxysilane Chemical compound CCO[Si](OCC)(OCC)CCCN WYTZZXDRDKSJID-UHFFFAOYSA-N 0.000 description 1
- IQGIEMYBDGDBMR-UHFFFAOYSA-N (3-methyl-5-prop-2-enoyloxypentyl) prop-2-enoate Chemical compound C=CC(=O)OCCC(C)CCOC(=O)C=C IQGIEMYBDGDBMR-UHFFFAOYSA-N 0.000 description 1
- PSGCQDPCAWOCSH-UHFFFAOYSA-N (4,7,7-trimethyl-3-bicyclo[2.2.1]heptanyl) prop-2-enoate Chemical compound C1CC2(C)C(OC(=O)C=C)CC1C2(C)C PSGCQDPCAWOCSH-UHFFFAOYSA-N 0.000 description 1
- UYVWNPAMKCDKRB-UHFFFAOYSA-N 1,2,4,5-tetraoxane Chemical compound C1OOCOO1 UYVWNPAMKCDKRB-UHFFFAOYSA-N 0.000 description 1
- GJZFGDYLJLCGHT-UHFFFAOYSA-N 1,2-diethylthioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=C(CC)C(CC)=CC=C3SC2=C1 GJZFGDYLJLCGHT-UHFFFAOYSA-N 0.000 description 1
- QWQFVUQPHUKAMY-UHFFFAOYSA-N 1,2-diphenyl-2-propoxyethanone Chemical compound C=1C=CC=CC=1C(OCCC)C(=O)C1=CC=CC=C1 QWQFVUQPHUKAMY-UHFFFAOYSA-N 0.000 description 1
- BGJSXRVXTHVRSN-UHFFFAOYSA-N 1,3,5-trioxane Chemical compound C1OCOCO1 BGJSXRVXTHVRSN-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- ALQLPWJFHRMHIU-UHFFFAOYSA-N 1,4-diisocyanatobenzene Chemical compound O=C=NC1=CC=C(N=C=O)C=C1 ALQLPWJFHRMHIU-UHFFFAOYSA-N 0.000 description 1
- CBCKQZAAMUWICA-UHFFFAOYSA-N 1,4-phenylenediamine Chemical compound NC1=CC=C(N)C=C1 CBCKQZAAMUWICA-UHFFFAOYSA-N 0.000 description 1
- SBJCUZQNHOLYMD-UHFFFAOYSA-N 1,5-Naphthalene diisocyanate Chemical compound C1=CC=C2C(N=C=O)=CC=CC2=C1N=C=O SBJCUZQNHOLYMD-UHFFFAOYSA-N 0.000 description 1
- ATOUXIOKEJWULN-UHFFFAOYSA-N 1,6-diisocyanato-2,2,4-trimethylhexane Chemical compound O=C=NCCC(C)CC(C)(C)CN=C=O ATOUXIOKEJWULN-UHFFFAOYSA-N 0.000 description 1
- ALVZNPYWJMLXKV-UHFFFAOYSA-N 1,9-Nonanediol Chemical compound OCCCCCCCCCO ALVZNPYWJMLXKV-UHFFFAOYSA-N 0.000 description 1
- LAYAKLSFVAPMEL-UHFFFAOYSA-N 1-ethenoxydodecane Chemical compound CCCCCCCCCCCCOC=C LAYAKLSFVAPMEL-UHFFFAOYSA-N 0.000 description 1
- UKDKWYQGLUUPBF-UHFFFAOYSA-N 1-ethenoxyhexadecane Chemical compound CCCCCCCCCCCCCCCCOC=C UKDKWYQGLUUPBF-UHFFFAOYSA-N 0.000 description 1
- SDXHBDVTZNMBEW-UHFFFAOYSA-N 1-ethoxy-2-(2-hydroxyethoxy)ethanol Chemical compound CCOC(O)COCCO SDXHBDVTZNMBEW-UHFFFAOYSA-N 0.000 description 1
- 239000012956 1-hydroxycyclohexylphenyl-ketone Substances 0.000 description 1
- CSCSROFYRUZJJH-UHFFFAOYSA-N 1-methoxyethane-1,2-diol Chemical compound COC(O)CO CSCSROFYRUZJJH-UHFFFAOYSA-N 0.000 description 1
- XLPJNCYCZORXHG-UHFFFAOYSA-N 1-morpholin-4-ylprop-2-en-1-one Chemical compound C=CC(=O)N1CCOCC1 XLPJNCYCZORXHG-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- GELKGHVAFRCJNA-UHFFFAOYSA-N 2,2-Dimethyloxirane Chemical compound CC1(C)CO1 GELKGHVAFRCJNA-UHFFFAOYSA-N 0.000 description 1
- KWVGIHKZDCUPEU-UHFFFAOYSA-N 2,2-dimethoxy-2-phenylacetophenone Chemical compound C=1C=CC=CC=1C(OC)(OC)C(=O)C1=CC=CC=C1 KWVGIHKZDCUPEU-UHFFFAOYSA-N 0.000 description 1
- STMDPCBYJCIZOD-UHFFFAOYSA-N 2-(2,4-dinitroanilino)-4-methylpentanoic acid Chemical compound CC(C)CC(C(O)=O)NC1=CC=C([N+]([O-])=O)C=C1[N+]([O-])=O STMDPCBYJCIZOD-UHFFFAOYSA-N 0.000 description 1
- WAVKEPUFQMUGBP-UHFFFAOYSA-N 2-(3-nitrophenyl)acetonitrile Chemical compound [O-][N+](=O)C1=CC=CC(CC#N)=C1 WAVKEPUFQMUGBP-UHFFFAOYSA-N 0.000 description 1
- YSUQLAYJZDEMOT-UHFFFAOYSA-N 2-(butoxymethyl)oxirane Chemical compound CCCCOCC1CO1 YSUQLAYJZDEMOT-UHFFFAOYSA-N 0.000 description 1
- VFBJXXJYHWLXRM-UHFFFAOYSA-N 2-[2-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxy]ethylsulfanyl]ethyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)OCCSCCOC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 VFBJXXJYHWLXRM-UHFFFAOYSA-N 0.000 description 1
- TXBCBTDQIULDIA-UHFFFAOYSA-N 2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)(CO)COCC(CO)(CO)CO TXBCBTDQIULDIA-UHFFFAOYSA-N 0.000 description 1
- ZCDADJXRUCOCJE-UHFFFAOYSA-N 2-chlorothioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=CC(Cl)=CC=C3SC2=C1 ZCDADJXRUCOCJE-UHFFFAOYSA-N 0.000 description 1
- UFAKDGLOFJXMEN-UHFFFAOYSA-N 2-ethenyloxetane Chemical compound C=CC1CCO1 UFAKDGLOFJXMEN-UHFFFAOYSA-N 0.000 description 1
- XIXWTBLGKIRXOP-UHFFFAOYSA-N 2-ethenyloxolane Chemical compound C=CC1CCCO1 XIXWTBLGKIRXOP-UHFFFAOYSA-N 0.000 description 1
- KMNCBSZOIQAUFX-UHFFFAOYSA-N 2-ethoxy-1,2-diphenylethanone Chemical compound C=1C=CC=CC=1C(OCC)C(=O)C1=CC=CC=C1 KMNCBSZOIQAUFX-UHFFFAOYSA-N 0.000 description 1
- QPXVRLXJHPTCPW-UHFFFAOYSA-N 2-hydroxy-2-methyl-1-(4-propan-2-ylphenyl)propan-1-one Chemical compound CC(C)C1=CC=C(C(=O)C(C)(C)O)C=C1 QPXVRLXJHPTCPW-UHFFFAOYSA-N 0.000 description 1
- XMLYCEVDHLAQEL-UHFFFAOYSA-N 2-hydroxy-2-methyl-1-phenylpropan-1-one Chemical compound CC(C)(O)C(=O)C1=CC=CC=C1 XMLYCEVDHLAQEL-UHFFFAOYSA-N 0.000 description 1
- OMIGHNLMNHATMP-UHFFFAOYSA-N 2-hydroxyethyl prop-2-enoate Chemical compound OCCOC(=O)C=C OMIGHNLMNHATMP-UHFFFAOYSA-N 0.000 description 1
- LWRBVKNFOYUCNP-UHFFFAOYSA-N 2-methyl-1-(4-methylsulfanylphenyl)-2-morpholin-4-ylpropan-1-one Chemical compound C1=CC(SC)=CC=C1C(=O)C(C)(C)N1CCOCC1 LWRBVKNFOYUCNP-UHFFFAOYSA-N 0.000 description 1
- KTALPKYXQZGAEG-UHFFFAOYSA-N 2-propan-2-ylthioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=CC(C(C)C)=CC=C3SC2=C1 KTALPKYXQZGAEG-UHFFFAOYSA-N 0.000 description 1
- CXURGFRDGROIKG-UHFFFAOYSA-N 3,3-bis(chloromethyl)oxetane Chemical compound ClCC1(CCl)COC1 CXURGFRDGROIKG-UHFFFAOYSA-N 0.000 description 1
- FIMAGFSGWNAHTD-UHFFFAOYSA-N 3,5,8-trimethyl-1,4-diazabicyclo[2.2.2]octane Chemical compound C1C(C)N2C(C)CN1CC2C FIMAGFSGWNAHTD-UHFFFAOYSA-N 0.000 description 1
- DSSAWHFZNWVJEC-UHFFFAOYSA-N 3-(ethenoxymethyl)heptane Chemical compound CCCCC(CC)COC=C DSSAWHFZNWVJEC-UHFFFAOYSA-N 0.000 description 1
- XDLMVUHYZWKMMD-UHFFFAOYSA-N 3-trimethoxysilylpropyl 2-methylprop-2-enoate Chemical compound CO[Si](OC)(OC)CCCOC(=O)C(C)=C XDLMVUHYZWKMMD-UHFFFAOYSA-N 0.000 description 1
- UPMLOUAZCHDJJD-UHFFFAOYSA-N 4,4'-Diphenylmethane Diisocyanate Chemical compound C1=CC(N=C=O)=CC=C1CC1=CC=C(N=C=O)C=C1 UPMLOUAZCHDJJD-UHFFFAOYSA-N 0.000 description 1
- YBRVSVVVWCFQMG-UHFFFAOYSA-N 4,4'-diaminodiphenylmethane Chemical compound C1=CC(N)=CC=C1CC1=CC=C(N)C=C1 YBRVSVVVWCFQMG-UHFFFAOYSA-N 0.000 description 1
- YDIYEOMDOWUDTJ-UHFFFAOYSA-N 4-(dimethylamino)benzoic acid Chemical compound CN(C)C1=CC=C(C(O)=O)C=C1 YDIYEOMDOWUDTJ-UHFFFAOYSA-N 0.000 description 1
- UGVRJVHOJNYEHR-UHFFFAOYSA-N 4-chlorobenzophenone Chemical compound C1=CC(Cl)=CC=C1C(=O)C1=CC=CC=C1 UGVRJVHOJNYEHR-UHFFFAOYSA-N 0.000 description 1
- HMBNQNDUEFFFNZ-UHFFFAOYSA-N 4-ethenoxybutan-1-ol Chemical compound OCCCCOC=C HMBNQNDUEFFFNZ-UHFFFAOYSA-N 0.000 description 1
- IZSHZLKNFQAAKX-UHFFFAOYSA-N 5-cyclopenta-2,4-dien-1-ylcyclopenta-1,3-diene Chemical group C1=CC=CC1C1C=CC=C1 IZSHZLKNFQAAKX-UHFFFAOYSA-N 0.000 description 1
- XAYDWGMOPRHLEP-UHFFFAOYSA-N 6-ethenyl-7-oxabicyclo[4.1.0]heptane Chemical compound C1CCCC2OC21C=C XAYDWGMOPRHLEP-UHFFFAOYSA-N 0.000 description 1
- PGDIJTMOHORACQ-UHFFFAOYSA-N 9-prop-2-enoyloxynonyl prop-2-enoate Chemical compound C=CC(=O)OCCCCCCCCCOC(=O)C=C PGDIJTMOHORACQ-UHFFFAOYSA-N 0.000 description 1
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical compound C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004593 Epoxy Substances 0.000 description 1
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 239000005057 Hexamethylene diisocyanate Substances 0.000 description 1
- 239000005058 Isophorone diisocyanate Substances 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 1
- GWGWXYUPRTXVSY-UHFFFAOYSA-N N=C=O.N=C=O.CC1=CC=C(C)C=C1 Chemical compound N=C=O.N=C=O.CC1=CC=C(C)C=C1 GWGWXYUPRTXVSY-UHFFFAOYSA-N 0.000 description 1
- UQBRAHLFLCMLBA-UHFFFAOYSA-N N=C=O.N=C=O.CC1=CC=CC(C)=C1 Chemical compound N=C=O.N=C=O.CC1=CC=CC(C)=C1 UQBRAHLFLCMLBA-UHFFFAOYSA-N 0.000 description 1
- OFSAUHSCHWRZKM-UHFFFAOYSA-N Padimate A Chemical compound CC(C)CCOC(=O)C1=CC=C(N(C)C)C=C1 OFSAUHSCHWRZKM-UHFFFAOYSA-N 0.000 description 1
- FQYUMYWMJTYZTK-UHFFFAOYSA-N Phenyl glycidyl ether Chemical compound C1OC1COC1=CC=CC=C1 FQYUMYWMJTYZTK-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- AWMVMTVKBNGEAK-UHFFFAOYSA-N Styrene oxide Chemical compound C1OC1C1=CC=CC=C1 AWMVMTVKBNGEAK-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- BGYHLZZASRKEJE-UHFFFAOYSA-N [3-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxy]-2,2-bis[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxymethyl]propyl] 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)OCC(COC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)(COC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)COC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 BGYHLZZASRKEJE-UHFFFAOYSA-N 0.000 description 1
- YIMQCDZDWXUDCA-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCC(CO)CC1 YIMQCDZDWXUDCA-UHFFFAOYSA-N 0.000 description 1
- YNTQTLGBCMXNFX-UHFFFAOYSA-N [5-ethyl-2-(2-methyl-1-prop-2-enoyloxypropan-2-yl)-1,3-dioxan-5-yl]methyl prop-2-enoate Chemical compound C=CC(=O)OCC1(CC)COC(C(C)(C)COC(=O)C=C)OC1 YNTQTLGBCMXNFX-UHFFFAOYSA-N 0.000 description 1
- MZVQCMJNVPIDEA-UHFFFAOYSA-N [CH2]CN(CC)CC Chemical group [CH2]CN(CC)CC MZVQCMJNVPIDEA-UHFFFAOYSA-N 0.000 description 1
- KXBFLNPZHXDQLV-UHFFFAOYSA-N [cyclohexyl(diisocyanato)methyl]cyclohexane Chemical compound C1CCCCC1C(N=C=O)(N=C=O)C1CCCCC1 KXBFLNPZHXDQLV-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000001361 adipic acid Substances 0.000 description 1
- 235000011037 adipic acid Nutrition 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- PYKYMHQGRFAEBM-UHFFFAOYSA-N anthraquinone Natural products CCC(=O)c1c(O)c2C(=O)C3C(C=CC=C3O)C(=O)c2cc1CC(=O)OC PYKYMHQGRFAEBM-UHFFFAOYSA-N 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 230000000712 assembly Effects 0.000 description 1
- 238000000429 assembly Methods 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- HIFVAOIJYDXIJG-UHFFFAOYSA-N benzylbenzene;isocyanic acid Chemical class N=C=O.N=C=O.C=1C=CC=CC=1CC1=CC=CC=C1 HIFVAOIJYDXIJG-UHFFFAOYSA-N 0.000 description 1
- RSOILICUEWXSLA-UHFFFAOYSA-N bis(1,2,2,6,6-pentamethylpiperidin-4-yl) decanedioate Chemical compound C1C(C)(C)N(C)C(C)(C)CC1OC(=O)CCCCCCCCC(=O)OC1CC(C)(C)N(C)C(C)(C)C1 RSOILICUEWXSLA-UHFFFAOYSA-N 0.000 description 1
- VBIAXKVXACZQFW-OWOJBTEDSA-N bis(2-isocyanatoethyl) (e)-but-2-enedioate Chemical compound O=C=NCCOC(=O)\C=C\C(=O)OCCN=C=O VBIAXKVXACZQFW-OWOJBTEDSA-N 0.000 description 1
- ZLSMCQSGRWNEGX-UHFFFAOYSA-N bis(4-aminophenyl)methanone Chemical compound C1=CC(N)=CC=C1C(=O)C1=CC=C(N)C=C1 ZLSMCQSGRWNEGX-UHFFFAOYSA-N 0.000 description 1
- RFVHVYKVRGKLNK-UHFFFAOYSA-N bis(4-methoxyphenyl)methanone Chemical compound C1=CC(OC)=CC=C1C(=O)C1=CC=C(OC)C=C1 RFVHVYKVRGKLNK-UHFFFAOYSA-N 0.000 description 1
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 1
- 125000006226 butoxyethyl group Chemical group 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 238000010073 coating (rubber) Methods 0.000 description 1
- 239000011247 coating layer Substances 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- ZWAJLVLEBYIOTI-UHFFFAOYSA-N cyclohexene oxide Chemical compound C1CCCC2OC21 ZWAJLVLEBYIOTI-UHFFFAOYSA-N 0.000 description 1
- FWFSEYBSWVRWGL-UHFFFAOYSA-N cyclohexene oxide Natural products O=C1CCCC=C1 FWFSEYBSWVRWGL-UHFFFAOYSA-N 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- SWXVUIWOUIDPGS-UHFFFAOYSA-N diacetone alcohol Chemical compound CC(=O)CC(C)(C)O SWXVUIWOUIDPGS-UHFFFAOYSA-N 0.000 description 1
- KORSJDCBLAPZEQ-UHFFFAOYSA-N dicyclohexylmethane-4,4'-diisocyanate Chemical compound C1CC(N=C=O)CCC1CC1CCC(N=C=O)CC1 KORSJDCBLAPZEQ-UHFFFAOYSA-N 0.000 description 1
- GYZLOYUZLJXAJU-UHFFFAOYSA-N diglycidyl ether Chemical compound C1OC1COCC1CO1 GYZLOYUZLJXAJU-UHFFFAOYSA-N 0.000 description 1
- 125000005442 diisocyanate group Chemical group 0.000 description 1
- MCPKSFINULVDNX-UHFFFAOYSA-N drometrizole Chemical compound CC1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 MCPKSFINULVDNX-UHFFFAOYSA-N 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 125000005448 ethoxyethyl group Chemical group [H]C([H])([H])C([H])([H])OC([H])([H])C([H])([H])* 0.000 description 1
- UHESRSKEBRADOO-UHFFFAOYSA-N ethyl carbamate;prop-2-enoic acid Chemical compound OC(=O)C=C.CCOC(N)=O UHESRSKEBRADOO-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- YLQWCDOCJODRMT-UHFFFAOYSA-N fluoren-9-one Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3C2=C1 YLQWCDOCJODRMT-UHFFFAOYSA-N 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- 238000005755 formation reaction Methods 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-L fumarate(2-) Chemical class [O-]C(=O)\C=C\C([O-])=O VZCYOOQTPOCHFL-OWOJBTEDSA-L 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- VOZRXNHHFUQHIL-UHFFFAOYSA-N glycidyl methacrylate Chemical compound CC(=C)C(=O)OCC1CO1 VOZRXNHHFUQHIL-UHFFFAOYSA-N 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- RRAMGCGOFNQTLD-UHFFFAOYSA-N hexamethylene diisocyanate Chemical compound O=C=NCCCCCCN=C=O RRAMGCGOFNQTLD-UHFFFAOYSA-N 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- NIMLQBUJDJZYEJ-UHFFFAOYSA-N isophorone diisocyanate Chemical compound CC1(C)CC(N=C=O)CC(C)(CN=C=O)C1 NIMLQBUJDJZYEJ-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- JJTUDXZGHPGLLC-UHFFFAOYSA-N lactide Chemical compound CC1OC(=O)C(C)OC1=O JJTUDXZGHPGLLC-UHFFFAOYSA-N 0.000 description 1
- PBOSTUDLECTMNL-UHFFFAOYSA-N lauryl acrylate Chemical compound CCCCCCCCCCCCOC(=O)C=C PBOSTUDLECTMNL-UHFFFAOYSA-N 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- FSPSELPMWGWDRY-UHFFFAOYSA-N m-Methylacetophenone Chemical compound CC(=O)C1=CC=CC(C)=C1 FSPSELPMWGWDRY-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 150000002688 maleic acid derivatives Chemical class 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 229910001507 metal halide Inorganic materials 0.000 description 1
- 150000005309 metal halides Chemical class 0.000 description 1
- 238000000034 method Methods 0.000 description 1
- AYLRODJJLADBOB-QMMMGPOBSA-N methyl (2s)-2,6-diisocyanatohexanoate Chemical compound COC(=O)[C@@H](N=C=O)CCCCN=C=O AYLRODJJLADBOB-QMMMGPOBSA-N 0.000 description 1
- CRVGTESFCCXCTH-UHFFFAOYSA-N methyl diethanolamine Chemical compound OCCN(C)CCO CRVGTESFCCXCTH-UHFFFAOYSA-N 0.000 description 1
- UCAOGXRUJFKQAP-UHFFFAOYSA-N n,n-dimethyl-5-nitropyridin-2-amine Chemical compound CN(C)C1=CC=C([N+]([O-])=O)C=N1 UCAOGXRUJFKQAP-UHFFFAOYSA-N 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- ZDHCZVWCTKTBRY-UHFFFAOYSA-N omega-Hydroxydodecanoic acid Natural products OCCCCCCCCCCCC(O)=O ZDHCZVWCTKTBRY-UHFFFAOYSA-N 0.000 description 1
- 239000005304 optical glass Substances 0.000 description 1
- 125000001741 organic sulfur group Chemical group 0.000 description 1
- XRQKARZTFMEBBY-UHFFFAOYSA-N oxiran-2-ylmethyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1CO1 XRQKARZTFMEBBY-UHFFFAOYSA-N 0.000 description 1
- RPQRDASANLAFCM-UHFFFAOYSA-N oxiran-2-ylmethyl prop-2-enoate Chemical compound C=CC(=O)OCC1CO1 RPQRDASANLAFCM-UHFFFAOYSA-N 0.000 description 1
- WEVYNWIJRMVEMS-UHFFFAOYSA-N oxiran-2-ylmethyl prop-2-enyl carbonate Chemical compound C=CCOC(=O)OCC1CO1 WEVYNWIJRMVEMS-UHFFFAOYSA-N 0.000 description 1
- 239000003973 paint Substances 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- FZUGPQWGEGAKET-UHFFFAOYSA-N parbenate Chemical compound CCOC(=O)C1=CC=C(N(C)C)C=C1 FZUGPQWGEGAKET-UHFFFAOYSA-N 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920001281 polyalkylene Polymers 0.000 description 1
- 229920005906 polyester polyol Polymers 0.000 description 1
- 229920002523 polyethylene Glycol 1000 Polymers 0.000 description 1
- 229920000151 polyglycol Polymers 0.000 description 1
- 239000010695 polyglycol Substances 0.000 description 1
- 150000007519 polyprotic acids Polymers 0.000 description 1
- 229920000909 polytetrahydrofuran Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 229960000380 propiolactone Drugs 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- UWHCKJMYHZGTIT-UHFFFAOYSA-N tetraethylene glycol Chemical compound OCCOCCOCCOCCO UWHCKJMYHZGTIT-UHFFFAOYSA-N 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 238000012719 thermal polymerization Methods 0.000 description 1
- YRHRIQCWCFGUEQ-UHFFFAOYSA-N thioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3SC2=C1 YRHRIQCWCFGUEQ-UHFFFAOYSA-N 0.000 description 1
- RUELTTOHQODFPA-UHFFFAOYSA-N toluene 2,6-diisocyanate Chemical compound CC1=C(N=C=O)C=CC=C1N=C=O RUELTTOHQODFPA-UHFFFAOYSA-N 0.000 description 1
- IMNIMPAHZVJRPE-UHFFFAOYSA-N triethylenediamine Chemical compound C1CN2CCN1CC2 IMNIMPAHZVJRPE-UHFFFAOYSA-N 0.000 description 1
- QXJQHYBHAIHNGG-UHFFFAOYSA-N trimethylolethane Chemical compound OCC(C)(CO)CO QXJQHYBHAIHNGG-UHFFFAOYSA-N 0.000 description 1
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229920001567 vinyl ester resin Polymers 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- PAPBSGBWRJIAAV-UHFFFAOYSA-N ε-Caprolactone Chemical compound O=C1CCCCCO1 PAPBSGBWRJIAAV-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C03—GLASS; MINERAL OR SLAG WOOL
- C03C—CHEMICAL COMPOSITION OF GLASSES, GLAZES OR VITREOUS ENAMELS; SURFACE TREATMENT OF GLASS; SURFACE TREATMENT OF FIBRES OR FILAMENTS MADE FROM GLASS, MINERALS OR SLAGS; JOINING GLASS TO GLASS OR OTHER MATERIALS
- C03C25/00—Surface treatment of fibres or filaments made from glass, minerals or slags
- C03C25/10—Coating
- C03C25/104—Coating to obtain optical fibres
- C03C25/106—Single coatings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D4/00—Coating compositions, e.g. paints, varnishes or lacquers, based on organic non-macromolecular compounds having at least one polymerisable carbon-to-carbon unsaturated bond ; Coating compositions, based on monomers of macromolecular compounds of groups C09D183/00 - C09D183/16
- C09D4/06—Organic non-macromolecular compounds having at least one polymerisable carbon-to-carbon unsaturated bond in combination with a macromolecular compound other than an unsaturated polymer of groups C09D159/00 - C09D187/00
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Wood Science & Technology (AREA)
- General Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Geochemistry & Mineralogy (AREA)
- Macromonomer-Based Addition Polymer (AREA)
- Optical Fibers, Optical Fiber Cores, And Optical Fiber Bundles (AREA)
Description
- Die vorliegende Erfindung betrifft eine strahlungshärtbare Harzzusammensetzung und insbesondere eine strahlungshärtbare Harzzusammensetzung, die als Beschichtungsmaterial für Substrate, insbesondere optische Fasern, geeignet ist.
- Optische Fasern, insbesondere optische Glasfasern, sind zerbrechlich und werden leicht beschädigt und deshalb werden diese mit einem Beschichtungsmaterial beschichtet. Im Stand der Technik wurden verschiedene Arten von Beschichtungen als Beschichtungsmaterial beschrieben. Im Allgemeinen werden zur Beschichtung optischer Fasermaterialien zwei Beschichtungen angewandt: Eine relativ weiche Primärbeschichtung und eine vergleichsweise harte Sekundärbeschichtung. Beispielsweise beschreiben die WO 96/17000, die
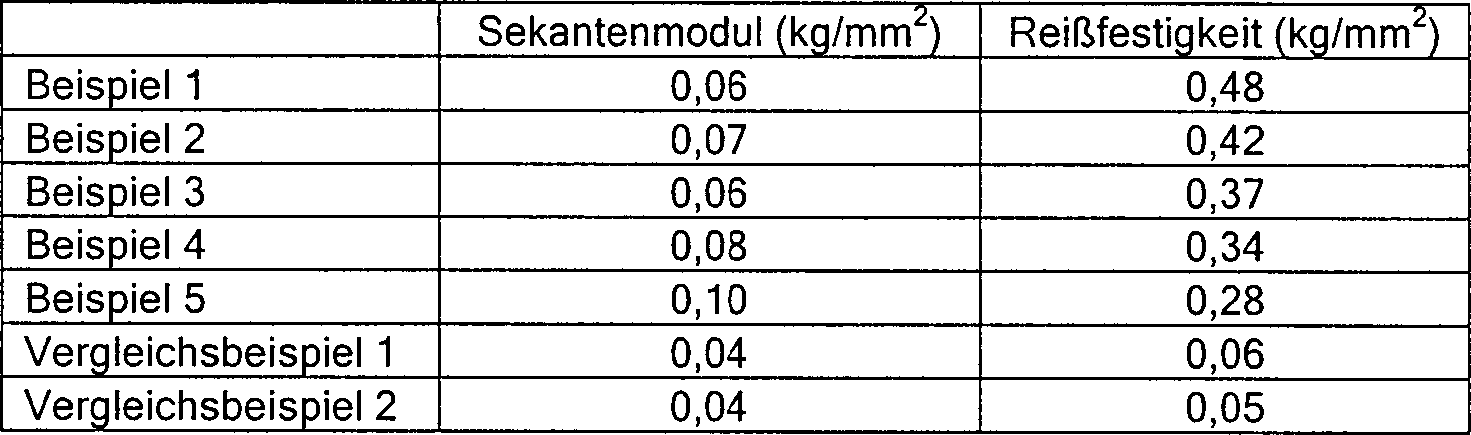
EP 0 336 653 A2 und die GB 2163755 Primärbeschichtungszusammensetzungen, während dieEP 0 301 733 A1 eine Sekundärbeschichtung beschreibt. Alternativ beschreibt dieEP 0 111 280 A1 eine Beschichtung, welche die Eigenschaften einer Primär- und einer Sekundärbeschichtung in einer einzigen Beschichtung zu vereinigen versucht. Darüber hinaus sind häufig in einer zusätzlichen Matrix- oder Gummibeschichtung Faseranordnungen enthalten. Solche Beschichtungen wurden in der WO 97/19898 und der WO 98/32780 beschrieben. - Die Eigenschaften, insbesondere der Elastizitätsmodul und dergleichen, eines Beschichtungsfilms, der z.B. aus einem UV-härtbaren Harz hergestellt ist, haben einen großen Einfluss auf die Übertragungsleistungen optischer Fasern. Wenn die optischen Fasern mit einem Primärbeschichtungsmaterial beschichtet sind, das einen hohen Elastizitätsmodul aufweist, nimmt der Übertragungsverlust der optischen Fasern aufgrund eines hohen Lateraldrucks zu. Ein Material mit einem niedrigen Elastizitätsmodul ist deshalb als Primärbeschichtungsmaterial bevorzugt. Herkömmliche Beschichtungsmaterialien mit einem niedrigen Elastizitätsmodul weisen jedoch die Nachteile auf, dass diese Materialien im Allgemeinen eine geringe Reißfestigkeit aufweisen und daher brüchig sind. Insbesondere ist es bevorzugt, dass der Elastizitätsmodul des Primärbeschichtungsmaterials für optische Fasern 0,15 kg/mm2 oder weniger beträgt, angegeben als Sekantenmodul gemäß JIS K7127, um einen hohen Lateraldruck zu absorbieren. Die Reißfestigkeit gehärteter Produkte mit einem solchen niedrigen Elastizitätsmodul weist jedoch einen niedrigen Wert von 0,15 kg/mm2 oder weniger, angegeben als Reißfestigkeit gemäß JIS K7127, auf. Diese Produkte weisen folglich nur eine schlechte Praxiseignung auf.
- Eine Aufgabe der vorliegenden Erfindung ist die Bereitstellung einer strahlungshärtbaren Harzzusammensetzung, die zur Verwendung als Substratbeschichtungsmaterial, insbesondere als Beschichtungsmaterial für optische Fasern, geeignet ist, und insbesondere als Primärbeschichtungsmaterial für optische Fasern, das eine hohe Reißfestigkeit aufweist, während es einen niedrigen Elastizitätsmodul zeigt.
- Demgemäß stellt die vorliegende Erfindung eine beschichtete optische Faser bereit, die eine Beschichtung mit einer Reißfestigkeit von mehr als 0,15 kg/mm2 und einen Sekantenmodul von 0,15 kg/mm2 oder weniger aufweist.
- Ferner stellt die vorliegende Erfindung eine strahlungshärtbare Harzzusammensetzung bereit, umfassend:
- (A) Eine Polymerzusammensetzung, weiche ein oder mehrere Polyetherpolyolurethanbasierende Polymere mit im Durchschnitt 1,2 oder mehr polymerisationsfähigen ungesättigten Gruppen in einem Molekül und einem Molekulargewichts-Zahlenmittel von 3000 bis 30000 aufweist,
- (B) ein polyfunktionelles Monomer mit zwei oder mehr polymerisationsfähigen ungesättigten Gruppen,
- (C) ein Monomer mit einer polymerisationsfähigen ungesättigten Gruppe und
- (D) einen strahlungsaktiven Initiator, wobei die strahlungshärtbare Zusammensetzung mit
- Ultraviolettstrahlung an Luft bei einer Dosis von 1 J/cm2 bestrahlt wird, so dass ein gehärtetes Produkt mit einer Dicke von 200 μm, einem Sekantenmodul von 0,15 kg/mm2 oder weniger und einer Reißfestigkeit von mehr als 0,15 kg/mm2 bereitgestellt wird.
- Die erfindungsgemäße Zusammensetzung wird nachstehend mittels einer bevorzugten Ausführungsform detailliert erläutert. In dieser Beschreibung beziehen sich bestimmte Begriffe, falls nichts anderes angegeben ist, auf bestimmte chemische Gruppen und Verbindungen. Diese Begriffe sind nachstehend definiert.
- „(Meth)acrylsäure" bezieht sich auf substituierte und unsubstituierte Acrylsäure, Methacrylsäure und Gemische davon, wobei unsubstituierte (Meth)acrylsäure bevorzugt ist.
- „(Meth)acryloylgruppe" bezieht sich auf eine substituierte und unsubstituierte Acryloylgruppe, Methacryloylgruppe und Gemische davon, wobei eine unsubstituierte (Meth)acryloylgruppe bevorzugt ist.
- „(Meth)acrylat" bezieht sich auf substituiertes und unsubstituiertes Acrylat, Methacrylat und Gemische davon, wobei unsubstituiertes (Meth)acrylat bevorzugt ist.
- Komponente (A)
- Die Komponente (A) ist eine Polymerzusammensetzung, die ein oder mehrere Polyetherpolyolurethan-basierende Polymere (mit einem Molekulargewichts-Zahlenmittel von 3000 bis 30000) derart aufweist, dass die gesamten vorliegenden Polymere im Durchschnitt 1,2 oder mehr polymerisationsfähige ungesättigte Gruppen pro Molekül aufweisen. Die polymerisationsfähige ungesättigte Gruppe in der vorliegenden Beschreibung ist eine radikalisch polymerisierbare ethylenisch ungesättigte Gruppe, die z.B. (Meth)acryloyl- und (Meth)acrylatgruppen umfasst. Die durchschnittliche Anzahl polymerisierbarer ungesättigter Gruppen pro Polymermolekül in der Polymerzusammensetzung, die für die Komponente (A) ausgewählt wird, beträgt 1,2 oder mehr, vorzugsweise 1,2 bis 4 und insbesondere 1,5 bis 2,5. Die Anzahl der polymerisierbaren ungesättigten Gruppen, die in jedem Molekül des Polymers enthalten sein kann, beträgt 1 oder zwei oder mehr. Es ist jedoch erforderlich, dass die durchschnittliche Anzahl der polymerisierbaren ungesättigten Gruppen in der gesamten Komponente (A) 1,2 oder mehr pro Molekül beträgt. Wenn die durchschnittliche Anzahl der polymerisierbaren ungesättigten Gruppen weniger als 1,2 pro Molekül beträgt, wird nur eine unzureichende Härtung der Zusammensetzung erhalten. Wenn die durchschnittliche Anzahl andererseits zu hoch ist, wird eine übermäßige Vernetzung verursacht, wodurch das gehärtete Produkt zur Brüchigkeit neigt.
- Das Molekulargewichts-Zahlenmittel des Polymers beträgt 3000 bis 30000 und vorzugsweise 5000 bis 20000. Wenn das Molekulargewichts-Zahlenmittel weniger als 3000 beträgt, nimmt die Dehnung des resultierenden gehärteten Produkts ab, wodurch die Zähigkeit leicht abnehmen kann und eine Tendenz dahingehend besteht, dass ein Übertragungsverlust einer optischen Faser erzeugt wird, wenn die Zusammensetzung als Beschichtungsmaterial für optische Fasern verwendet wird. Wenn das Molekulargewichts-Zahlenmittel andererseits 30000 übersteigt, wird die Viskosität der resultierenden Zusammensetzung zu hoch, was eine einfache Handhabung der Zusammensetzung schwierig macht.
- Die Polymere, die in der Polymerzusammensetzung der Komponente (A) enthalten sind, umfassen diejenigen, die zwei oder mehr Urethanbindungen und vorzugsweise 2 bis 10 Urethanbindungen enthalten. Wenn die Anzahl der Urethanbindungen weniger als 2 beträgt, nimmt die Zähigkeit des resultierenden gehärteten Produkts ab, was zu einer Tendenz da hingehend führt, dass ein Übertragungsverlust einer optischen Faser erzeugt wird, wenn die Zusammensetzung als Beschichtungsmaterial für optische Fasern verwendet wird.
- In der Polymerzusammensetzung, welche die Komponente (A) ist, gelten bezüglich der Anzahl der polymerisierbaren ungesättigten Gruppen, der Anzahl der Urethanbindungen und des Molekulargewichts-Zahlenmittels die vorstehend genannten Beschränkungen. Die Hauptkette geeigneter Polymere sollte jedoch mindestens ein Polyetherpolyol umfassen. Das Polyetherpolyolurethan-basierende Polymer kann entweder einzeln oder in einer Kombination mit vielen verschiedenen Polymergrundgerüsten verwendet werden, einschließlich einem Polyesterpolyolurethan-basierenden Polymer, einem Polycaprolactonpolyolurethan-basierenden Polymer oder dergleichen. Entweder die gesamte Komponente (A) oder ein Teil der Komponente (A) kann ein Polyetherpolyolurethan-basierendes Polymer sein.
- Das Polymer, das als Komponente (A) verwendet wird, welche aus einem Polyetherpolyolurethan-basierenden Polymer als Grundstruktur zusammengesetzt ist, wird durch Umsetzen von (a) einem Polyetherpolyol (nachstehend als „Polyetherpolyol (a)" bezeichnet), das durch eine Ringöffnungsreaktion eines Alkylenoxids erhalten wird, (b) einem Polyisocyanat (nachstehend als „Polyisocyanat (b)" bezeichnet) und (c) einer Verbindung (nachstehend als „Verbindung (c)" bezeichnet), die sowohl aktiven Wasserstoff, der mit der Isocyanatgruppe reagieren kann, als auch eine polymerisationsfähige ungesättigte Gruppe enthält, erzeugt.
- Das vorstehend genannte Polyetherpolyol (a) ist ein Polyol, das eine Polyoxyalkylenstruktur aufweist, die aus einer Polyoxyalkylengruppe mit 2 bis 10 Kohlenstoffatomen als Wiederholungseinheit zusammengesetzt ist, wobei es sich vorzugsweise um ein Diol handelt.
- Beispiele für Diole, welche die vorstehend genannte Polyoxyalkylenstruktur aufweisen, sind Polyglykolverbindungen wie z.B. Polyethylenglykol, Polypropylenglykol, Polytetramethylenglykol, Polyheptamethylenglykol, Polyhexamethylenglykol, Polydecamethylenglykol und dergleichen, sowie Polyetherdiole, die durch eine Ringöffnungscopolymerisation von zwei oder mehr ionisch polymerisierbaren cyclischen Verbindungen erhalten werden.
- Beispiele für ionisch polymerisierbare cyclische Verbindungen umfassen cyclische Ether wie z.B. Ethylenoxid, Propylenoxid, Buten-1-oxid, Isobutenoxid, 3,3-Bischlormethyloxetan, Tetrahydrofuran, 2-Methyltetrahydrofuran, 3-Methyltetrahydrofuran, Dioxan, Trioxan, Tetraoxan, Cyclohexenoxid, Styroloxid, Epichlorhydrin, Glycidylmethacrylat, Glycidylacrylat, Allylglycidylether, Allylglycidylcarbonat, Butadienmonoxid, Isoprenmonoxid, Vinyloxetan, Vinyltetrahydro furan, Vinylcyclohexenoxid, Phenylglycidylether, Butylglycidylether und Glycidylbenzoat, mit cyclischen Ethern wie z.B. Ethylenoxid und Tetrahydrofuran.
- Auch Polyetherdiole, die durch eine Ringöffnungscopolymerisation der vorstehend genannten ionisch polymerisierbaren cyclischen Verbindung mit einem cyclischen Imin wie z.B. Ethylenimin oder dergleichen erzeugt werden, ein cyclisches Lacton wie z.B. p-Propiolacton oder Glycolsäurelactid oder dergleichen, oder ein cyclisches Siloxan wie z.B. Dimethylcyclopolysiloxan oder dergleichen können verwendet werden.
- Beispiele für die spezifischen Kombinationen von zwei oder mehr ionisch polymerisierbaren cyclischen Verbindungen umfassen Kombinationen von Tetrahydrofuran und Propylenoxid, Tetrahydrofuran und 2-Methyltetrahydrofuran, Tetrahydrofuran und 3-Methyltetrahydrofuran, Tetrahydrofuran und Ethylenoxid, und Propylenoxid und Ethylenoxid. Zwei oder mehr ionisch polymerisierbare cyclische Verbindungen können in dem resultierenden Ringöffnungspolymer statistisch kombiniert sein.
- Die vorstehend genannten Diole mit einer Polyoxyalkylenstruktur sind beispielsweise unter den Marken PTMG1000, PTMG2000 (von Mitsubishi Chemical Corp. hergestellt), PPG1000, PPG2000, EXCENOL2020, EXCENOL1020 (von Asahi Oline Co., Ltd. hergestellt), PEG1000, Unisafe DC1100, Unisafe DC1800 (von Nippon Oil and Fats Co., Ltd. hergestellt), PPTG2000, PPTG1000, PTG400, PTGL2000 (von Hodogaya Chemical Co., Ltd. hergestellt) und dergleichen erhältlich.
- Bei der vorstehend genannten Herstellung kann bzw. können ein Diol ohne Polyoxyalkylenstruktur und/oder ein Diamin in einer Kombination mit dem Polyetherpolyol (a) verwendet werden. Beispiele für ein Diol ohne Polyoxyalkylenstruktur sind ein Polyesterdiol, ein Polycaprolactondiol, ein Polycarbonatdiol und dergleichen. Beispiele für ein Polyesterdiol umfassen Polyesterdiole, die durch Umsetzen eines mehrwertigen Alkohols wie z.B. Ethylenglykol, Propylenglykol, Tetramethylenglykol, 1,6-Hexandiol, Neopentylglykol oder 1,4-Cyclohexandimethanol mit einer mehrbasigen Säure wie z.B. Phthalsäure, Isophthalsäure, Terephthalsäure, Maleinsäure, Fumarsäure, Adipinsäure, Sebacinsäure oder dergleichen erhalten werden. Beispiele für ein Polycaprolactondiol umfassen Polycaprolactondiole, die durch Umsetzen eines ε-Caprolactondiols mit einem Diol wie z.B. Ethylenglykol, Tetramethylenglykol, 1,6-Hexandiol, Neopentylglykol, 1,4-Butandiol oder dergleichen erhalten werden. Beispiele für das Polycarbonatdiol sind ein Polycarbonatdiol von Polytetrahydrofuran, ein Polycarbonat von 1,6-Hexandiol oder dergleichen. Diese Polycarbonatdiole sind unter den Marken DN-980, DN-981, DN-982, DN-983 (von Nippon Polyurethane Industry Co., Ltd. hergestellt), PC- 8000 (von PPG in den USA hergestellt) und dergleichen erhältlich. Beispiele für das Diamin sind Diamine wie z.B. Ethylendiamin, Tetramethylendiamin, Hexamethylendiamin, p-Phenylendiamin, 4,4'-Diaminodiphenylmethan, Diamine, die ein Heteroatom umfassen, und Polyetherdiamine.
- Das vorstehend genannte Polyisocyanat (b) ist eine Verbindung, die 2 bis 6 Isocyanatgruppen enthält, wobei Diisocyanate bevorzugt sind. Spezifische Beispiele des Polyisocyanats (b) umfassen 2,4-Toluylendiisocyanat, 2,6-Toluylendiisocyanat, 1,3-Xyloldiisocyanat, 1,4-Xyloldiisocyanat, 1,5-Naphthalindiisocyanat, p-Phenylendiisocyanat, 3,3'-Dimethyl-4,4'-diphenylmethandiisocyanat, 4,4'-Diphenylmethandiisocyanat, 3,3'-Dimethylphenylendiisocyanat, 4,4'-Biphenylendiisocyanat, Hexamethylendiisocyanat, Isophorondiisocyanat, Dicyclohexylmethandiisocyanat, Methylenbis(4-cyclohexylisocyanat), hydriertes Diphenylmethandiisocyanat, 2,2,4-Trimethylhexamethylendiisocyanat, Bis(2-isocyanatoethyl)fumarat, 6-Isopropyl-l,3-phenyldiisocyanat, 4-Diphenylpropandiisocyanat und Lysindiisocyanat.
- Die vorstehend genannte Verbindung (c) mit einem aktiven Wasserstoff und einer polymerisierbaren ungesättigten Gruppe kann z.B. Verbindungen des (Meth)acryl-Typs mit mindestens einer Hydroxylgruppe umfassen. Spezielle Beispiele der Verbindung (c) umfassen 2-Hydroxyethyl(meth)acrylat, 2-Hydroxypropyl(meth)acrylat, 2-Hydroxyoctyl(meth)acrylat, Pentaerythrittri(meth)acrylat, Glycerindi(meth)acrylat, Dipentaerythritmonohydroxypenta(meth)acrylat, 1,4-Butandiolmono(meth)acrylat, 4-Hydroxycyclohexyl(meth)acrylat, 1,6-Hexandiolmono(meth)acrylat, Neopentylglykolmono(meth)acrylat, Trimethylolpropandi(meth)acrylat, Trimethylolethandi(meth)acrylat und (Meth)acrylate der folgenden Formeln (1) und (2): worin R1 ein Wasserstoffatom oder eine Methylgruppe darstellt, worin R1 die vorstehend angegebene Bedeutung hat und n eine ganze Zahl von 1 bis 5 ist. Ein bevorzugtes Beispiel für diese Gruppen ist 2-Hydroxyethyl(meth)acrylat.
- Das Polymer (A) kann durch Umsetzen mindestens eines Polyether-basierenden Polyols (a) mit mindestens einem Polyisocyanat (b) und mindestens einer Verbindung (c) gemäß Verfahren und in Anteilen hergestellt werden, die für die Durchführung solcher Reaktionen bekannt sind. Bezüglich der Polymer (A)-Bildungsreaktion des Polyetherpolyols (a) mit dem Polyisocyanat (b) und der Verbindung (c) ist es beispielsweise, wenn eine Diolverbindung mit einer Diisocyanatverbindung und einer Verbindung mit einer ethylenisch ungesättigten Gruppe umgesetzt wird, bevorzugt, einen Urethanisierungskatalysator wie z.B. Kupfernaphthanat, Cobaltnaphthanat, Zinknaphthanat, Dibutylzinndilaurat, Triethylamin, 1,4-Diazabicyclo[2.2.2]octan, 2,6,7-Trimethyl-l,4-diazabicyclo[2.2.2]octan oder dergleichen in einer Menge von 0,01 bis 1 Gewichtsteil pro 100 Teile der Gesamtmenge der Reaktionskomponenten zu verwenden. Diese Reaktion kann bei einer beliebigen geeigneten Temperatur durchgeführt werden, wobei diese Reaktion typischerweise bei einer Temperatur von 10 bis 90°C und vorzugsweise von 30 bis 80°C durchgeführt wird.
- Die Komponente (A) kann entweder vollständig aus Polyetherpolyolurethan-basierenden Polymeren zusammengesetzt sein oder Polyetherpolyolurethan-basierende Polymere als Hauptkomponente sowie andere Polymere, die der Komponente (A) entsprechen, umfassen. Beispiele für diese anderen Polymere, die in die Kategorie der Komponente (A) fallen, umfassen Polyesterpolyolurethan-basierende Polymere, Polycaprolactonpolyolurethanbasierende Polymere und dergleichen. Wenn das Polyetherpolyolurethan-basierende Polymer in einer Kombination mit den anderen Polymeren verwendet wird, beträgt der Anteil der Polyalkylenstruktur in der Komponente (A) vorzugsweise mindestens 50, jedoch nicht mehr als 98 Gew.-%, mehr bevorzugt mindestens 60, jedoch nicht mehr als 93 Gew.-% und insbesondere mindestens 70, jedoch nicht mehr als 90 Gew.-%. Wenn der Anteil der Polyoxyalkylenstruktur in der Komponente (A) zu klein ist, nimmt der Elastizitätsmodul des resultierenden gehärteten Produkts bei einer niedrigeren Temperatur wie z.B. 0°C oder weniger zu, was zu einer Tendenz dahingehend führt, dass ein Übertragungsverlust einer optischen Faser verursacht wird, wenn die Zusammensetzung als Beschichtungsmaterial für optische Fasern verwendet wird.
- Die Anteilsmenge des Polymers der Komponente (A) in der erfindungsgemäßen Zusammensetzung beträgt im Allgemeinen 25 bis 75 Gew.-% und vorzugsweise 40 bis 70 Gew.-%. Wenn der Anteil der Komponente (A) zu klein ist, nimmt die Dehnung des resultierenden gehärteten Produkts aus der Zusammensetzung ab, wohingegen dann, wenn der Anteil zu groß ist, die Viskosität der Zusammensetzung zunimmt, wodurch eine Tendenz dahingehend besteht, dass die Handhabungseigenschaften beeinträchtigt werden.
- Komponente (B)
- Das polyfunktionelle Monomer, das als Komponente (B) in der vorliegenden Erfindung verwendet wird, enthält zwei oder mehr, im Allgemeinen 2 bis 10 und vorzugsweise 2 bis 6 polymerisierbare ungesättigte Gruppen. Es ist bevorzugt, als polymerisierbare ungesättigte Gruppe eine (Meth)acryloylgruppe zu verwenden.
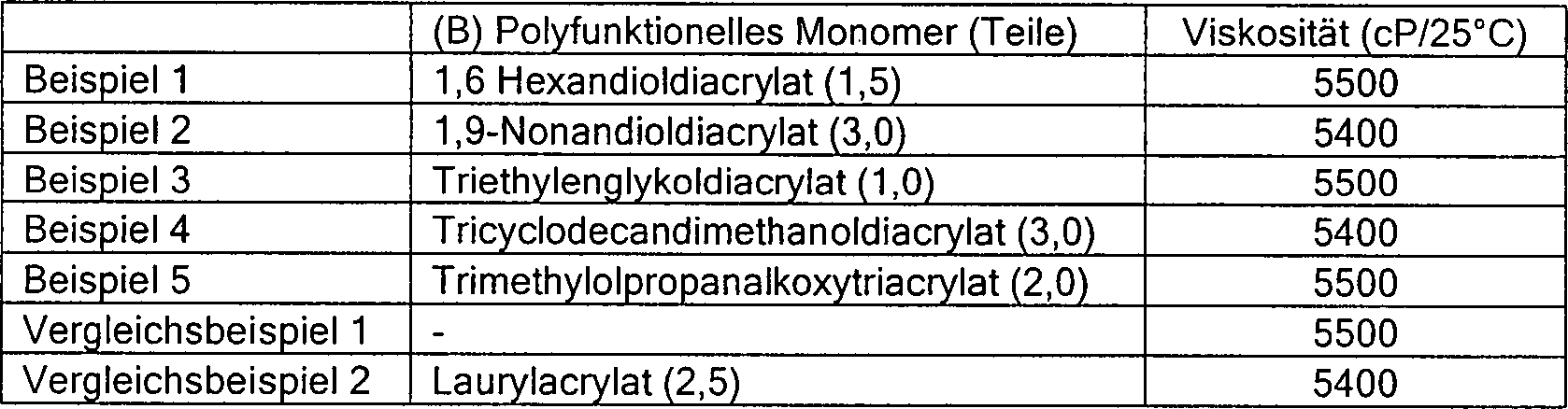
- Um zu ermöglichen, dass die gehärtete Beschichtungszusammensetzung eine hohe Reißfestigkeit erreicht, während ein niedriger Elastizitätsmodul beibehalten wird, wird das polyfunktionelle Monomer vorzugsweise ein vergleichsweise niedriges Molekulargewicht aufweisen, insbesondere 800 oder weniger, vorzugsweise 100 bis 800 und mehr bevorzugt 150 bis 600. Bevorzugte Beispiele eines solchen polyfunktionellen Monomers umfassen Di-, Tri- und Tetra(meth)acrylate, wobei Di- und Tri(meth)acrylate bevorzugt sind und diejenigen mit einem Mw von 800 oder weniger ganz besonders bevorzugt sind, wie z.B. Trimethylolpropantri(meth)acrylat, Pentaerythrit(meth)acrylat, Ethylenglykoldi(meth)acrylat, Tetraethylenglykoldi(meth)acrylat, Polyethylenglykoldi(meth)acrylat, 1,4-Butandioldi(meth)acrylat, 1,6-Hexandioldi(meth)acrylat, 1,9-Nonandioldi(meth)acrylat, Neopentylglykoldi(meth)acrylat, Trimethylolpropantrioxyethyl(meth)acrylat, Tris(2-hydroxyethyl)isocyanurattri(meth)acrylat, Tris(2-hydroxyethyl)isocyanuratdi(meth)acrylat, Tricyclodecandimethanoldi(meth)acrylat, Epoxy(meth)acrylat, das durch Zugeben eines (Meth)acrylats zu dem Diglycidylether von Bisphenol A erzeugt wird, und 3-Methyl-l,5-pentandioldiacrylat. Von diesen Verbindungen umfassen ganz besonders bevorzugte polyfunktionelle Monomere 1,6-Hexandioldiacrylat, 1,9-Nonandioldiacrylat, Triethylenglykoldiacrylat, Trimethylolpropanalkoxytriacrylat und Tricyclodecandimethanoldiacrylat. Diese Monomere als Komponente (B) können entweder einzeln oder in Kombinationen von zwei oder mehr verwendet werden.
- Diese polyfunktionellen Monomere sind z.B. unter den Marken HDDA, L-C9A (von Daiichi Kogyo Seiyaku Co., Ltd. hergestellt), Yupimer UV, SA1002, SA2007 (von Mitsubishi Chemical Corp. hergestellt), 3-EGA, 14-EGA (von Kyoeisha Co., Ltd. hergestellt), PHOTOMER4149 (Sun Nopco Co., Ltd.), Viscoat 700 (von Osaka Organic Chemical Industry Co., Ltd. hergestellt), KAYARAD R-604, DPCA-20, 30, 60, 120, HX-620, D-310, 330 (von Nippon Kayaku Co., Ltd. hergestellt), Aronix M-210, 215, 315, 325 (von Toagosei Co., Ltd. hergestellt), A-MPD (Shin-Nakamura Chemical Co., Ltd.) und dergleichen erhältlich.
- Es ist bevorzugt, dass die polyfunktionellen Monomere der Komponente (B) in der erfindungsgemäßen Zusammensetzung in einer Menge von 0,1 bis 10 Gew.-% und insbesondere von 0,5 bis 5 Gew.-% vorliegen. Wenn die Menge der Komponente (B) zu klein ist, nimmt die Reißfestigkeit des resultierenden gehärteten Produkts ab, wohingegen dann, wenn die Menge zu groß ist, der Elastizitätsmodul des gehärteten Produkts übermäßig hoch ist und die Dehnung des gehärteten Produkts abnimmt, was zeigt, dass eine solche Zusammensetzung als Primärbeschichtungsmaterial für optische Fasern nicht geeignet ist.
- Komponente (C)
- Monomere, die eine polymerisierbare ungesättigte Gruppe enthalten und die als Komponente (C) in der erfindungsgemäßen Beschichtungszusammensetzung geeignet sind, umfassen z.B. Monomere, die nur eine polymerisierbare ungesättigte Gruppe enthalten, wie z.B. eine Vinylgruppe, und ein Molekulargewicht von 1000 oder weniger und vorzugsweise von 70 bis 800 aufweisen. Obwohl es bezüglich der Art der polymerisierbaren Vinylgruppe keine speziellen Beschränkungen gibt, ist es bevorzugt, dass als polymerisierbare Vinylgruppe eine (Meth)acryloylgruppe, eine N-Vinylgruppe, eine (Meth)acrylamidgruppe, eine Vinylethergruppe, eine Vinylestergruppe oder dergleichen enthalten ist. Von diesen Gruppen ist eine (Meth)acryloylgruppe bevorzugt.
- Die Komponente (C) wirkt in der erfindungsgemäßen Zusammensetzung als reaktives Verdünnungsmittel und es ist daher bevorzugt, dass die Komponente (C) bei 25°C flüssig ist. Die Arten und Mengen der Verbindungen, die als Komponente (C) verwendet werden, werden so eingestellt, dass die Viskosität der Zusammensetzung und der Elastizitätsmodul des resultierenden gehärteten Produkts gesteuert werden. Wenn die Komponente (C) aus einer Mehrzahl von Verbindungen zusammengesetzt ist, sind die ausgewählten Verbindungen vorzugsweise Flüssigkeiten, wenn sie gemischt werden, und führen zu einem Gemisch, das bei 25°C flüssig ist.
- Spezielle Beispiele geeigneter Monomere zur Verwendung als Komponente (C) umfassen 2-Hydroxyethyl(meth)acrylat, 2-Hydroxypropyl(meth)acrylat, 2-Hydroxybutyl(meth)acrylat, Methyl(meth)acrylat, Ethyl(meth)acrylat, Propyl(meth)acrylat, Isopropyl(meth)acrylat, Butyl(meth)acrylat, Amyl(meth)acrylat, Isobutyl(meth)acrylat, t-Butyl(meth)acrylat, Pentyl(meth)acrylat, Isoamyl(meth)acrylat, Hexyl(meth)acrylat, Heptyl(meth)acrylat, Octyl(meth)acrylat, Isooctyl(meth)acrylat, 2-Ethylhexyl(meth)acrylat, Nonyl(meth)acrylat, Decyl(meth)acrylat, Isodecyl(meth)acrylat, Undecyl(meth)acrylat, Dodecyl(meth)acrylat, Lauryl(meth)acrylat, Octadecyl(meth)acrylat, Stearyl(meth)acrylat, Tetrahydrofurfuryl(meth)acrylat, Butoxyethyl(meth)acrylat, Ethoxydiethylenglykol(meth)acrylat, Benzyl(meth)acrylat, Cyclohexyl(meth)acrylat, Phenoxyethyl(meth)acrylat, Polyethylenglykolmono(meth)acrylat, Polypropylenglykolmono(meth)acrylat, Methoxyethylenglykol(meth)acrylat, Ethoxy ethyl(meth)acrylat, Methoxypolyethylenglykol(meth)acrylat, Methoxypolypropylenglykol(meth)acrylat, Dicyclopentadienyl(meth)acrylat, Dicyclopentanyl(meth)acrylat, Dicyclopentenyl(meth)acrylat, Tricyclodecanyl(meth)acrylat, Isobornyl(meth)acrylat, Bornyl(meth)acrylat, Diaceton(meth)acrylamid, Isobutoxymethyl(meth)acrylamid, N-Vinylpyrrolidon, N-Vinylcaprolactam, N-Vinylformaldehyd, N,N-Dimethyl(meth)acrylamid, t-Octyl(meth)acrylamid, Dimethylaminoethyl(meth)acrylat, Diethylaminoethyl(meth)acrylat, 7-Amino-3,7-dimethyloctyl(meth)acrylat, N,N-Diethyl(meth)acrylamid, N,N'-Dimethylaminopropyl(meth)acrylamid, (Meth)acryloylmorpholin, Hydroxybutylvinylether, Laurylvinylether, Cetylvinylether, Vinylether wie z.B. 2-Ethylhexylvinylether, Maleate, Fumarate und die Verbindungen der nachstehenden Formeln (3) bis (5): worin R2 ein Wasserstoffatom oder eine Methylgruppe darstellt, R3 unabhängig eine Alkylengruppe mit 2 bis 6 und vorzugsweise 2 bis 4 Kohlenstoffatomen darstellt, R4 an den aromatischen Ring (Ø) gebunden ist und ein Wasserstoffatom oder eine Alkylgruppe mit 1 bis 12 und vorzugsweise 1 bis 9 Kohlenstoffatomen darstellt und q eine ganze Zahl von 0 bis 12 und vorzugsweise 1 bis 8 ist, worin R2 die vorstehend angegebene Bedeutung hat, R5 unabhängig eine Alkylengruppe mit 2 bis 8 und vorzugsweise 2 bis 5 Kohlenstoffatomen darstellt und r eine ganze Zahl von 1 bis 8 und vorzugsweise 1 bis 4 ist und R7 eine Tetrahydrofurylgruppe darstellt, worin R2 und R5 die vorstehend angegebene Bedeutung haben, s eine ganze Zahl von 1 bis 15 ist und jedes R6 unabhängig ein Wasserstoffatom oder eine Methylgruppe darstellt.
- Beispiele für Verbindungen der Formel (3) sind Nonylphenol-EO-modifiziertes (8 mol) Acrylat, Phenol-EO-modifiziertes (4 mol) Acrylat, Nonylphenol-EO-modifiziertes (4 mol) Acrylat, Nonylphenol-PO-modifiziertes (2,5 mol) Acrylat, Nonylphenol-EO-modifiziertes (1 mol) Acrylat und Phenol-EO-modifiziertes (2 mol) Acrylat.
- Die vorstehend als Beispiele genannten Verbindungen können unabhängig oder in Kombinationen von zwei oder mehr verwendet werden.
- Von den vorstehend als Beispiele angegebenen Verbindungen umfassen bevorzugte Verbindungen zur Verwendung als Komponente (C) N-Vinyllactame wie z.B. N-Vinylpyrrolidon, N-Vinyl-ε-caprolactam (nachstehend als „N-Vinylcaprolactam" bezeichnet) und dergleichen. Es ist bevorzugt, dass die Komponente (C), bezogen auf die Komponente (C), N-Vinylcaprolactam im Bereich von 3 bis 20 Gew.-% und vorzugsweise von 3 bis 15 Gew.-% umfasst.
- Es ist bevorzugt, dass die Komponente (C) eine Verbindung mit einer alicyclischen Struktur enthält, da das resultierende gehärtete Produkt dann eine Wasserbeständigkeit, Heißwasserbeständigkeit, Säurebeständigkeit, Alkalibeständigkeit und dergleichen sowie eine verbesserte Langzeitzuverlässigkeit aufweist. Beispiele für ein solches Monomer mit einer alicyclischen Struktur, insbesondere für alicyclische (Meth)acrylatverbindungen, umfassen Isobornyl(meth)acrylat, Dicyclopentenyl(meth)acrylat, Tricyclodecanyl(meth)acrylat, Cyclohexyl(meth)acrylat, Tricyclodecandimethanoldi(meth)acrylat und dergleichen. Von diesen Verbindungen sind Isobornylacrylat und Tricyclodecandimethanoldiacrylat bevorzugt.
- In einer bevorzugten Ausführungsform umfasst die Komponente (C) eine Kombination aus N-Vinyllactamen und einer Verbindung mit einer alicyclischen Struktur.
- Monomere, die zur Verwendung in der Komponente (C) geeignet sind, sind beispielsweise unter den Marken Aronix M-102, M-111, M-113, M-114, M-117 (von Toagosei Co., Ltd. hergestellt), KAYARAD TC110S, R629, R644 (von Nippon Kayaku Co., Ltd. hergestellt), Viscoat 3700 (Osaka Organic Chemical Industry Co., Ltd.) und dergleichen erhältlich.
- Es ist bevorzugt, dass die Komponente (C) in einer Menge von 20 bis 70 Gew.-% und vorzugsweise von 25 bis 55 Gew.-% bezogen auf die erfindungsgemäße Zusammensetzung vorliegt.
- Komponente (D)
- Beispiele für strahlungsaktive Initiatoren, die als Komponente (D) in der vorliegenden Erfindung geeignet sind, umfassen 1-Hydroxycyclohexylphenylketon, 2,2-Dimethoxy-2-phenylacetophenon, Xanthon, Fluorenon, Benzaldehyd, Fluoren, Anthrachinon, Triphenylamin, Carbazol, 3-Methylacetophenon, 4-Chlorbenzophenon, 4,4'-Dimethoxybenzophenon, 4,4'-Diaminobenzophenon, Michler's Keton, Benzoinpropylether, Benzoinethylether, Benzylmethylketal, 1-(4-Isopropylphenyl)-2-hydroxy-2-methylpropan-1-on, 2-Hydroxy-2-methyl-1-phenylpropan-1-on, Thioxanthon, Diethylthioxanthon, 2-Isopropylthioxanthon, 2-Chlorthioxanthon, 2-Methyl-1-[4-(methylthio)phenyl]-2-morpholinopropan-1-on, 2,4,6-Trimethylbenzoyldiphenylphosphinoxid, Bis(2,6-dimethoxybenzoyl)-2,4,4-trimethylpentylphosphinoxid und dergleichen. Diese Verbindungen können entweder einzeln oder in Kombinationen von zwei oder mehr verwendet werden. Von diesen Verbindungen sind 2,4,6-Trimethylbenzoyldiphenylphosphinoxid, Bis(2,6-dimethoxybenzoyl)-2,4,4-trimethylpentylphosphinoxid und 1-Hydroxycyclohexylphenylketon bevorzugt.
- Beispiele für käufliche Produkte, die zur Verwendung als Komponente (D) geeignet sind, umfassen Irgacure 184, 651, 500, 907 (von Ciba Specialty Chemicals Co., Ltd. hergestellt), Lucirin LR8728, Lucirin LR8953X (von BASF hergestellt), Darocur E1116, 1173 (von Ciba Specialty Chemicals Co., Ltd. hergestellt) und Ubecryl P36 (von UCB Co. hergestellt).
- Die Komponente (D) kann einen oder mehrere strahlungsaktive Initiatoren) umfassen. Der Anteil der Komponente (D) in der erfindungsgemäßen Zusammensetzung beträgt im Allgemeinen 0,1 bis 10 Gew.-% und vorzugsweise 1 bis 5 Gew.-%, bezogen auf das Gesamtgewicht der Zusammensetzung.
- Je nach den Anforderungen der jeweiligen Anwendung kann zusätzlich zu den strahlungsaktiven Initiatoren, die als Komponente (D) vorliegen, auch ein Photoinitiator verwendet werden. Geeignete Beispiele für Photoinitiatoren sind Triethylamin, Diethylamin, N-Methyldiethanolamin, Ethanolamin, 4-Dimethylaminobenzoesäure, Ethyl-4-dimethylaminobenzoat, Isoamyl-4-dimethylaminobenzoat und dergleichen. Diese Verbindungen sind z.B. unter den Marken Ubecryl P102, 103, 104, 105 (von UCB Co. hergestellt) und dergleichen erhältlich.
- Andere Komponenten
- Darüber hinaus kann es abhängig von den speziellen Anforderungen der Endanwendung der Zusammensetzung bevorzugt sein, Bestandteile zusätzlich zu den Komponenten (A) bis (D) zu verwenden. Typische Beispiele für solche zusätzlichen Bestandteile sind Antioxidationsmittel, UV-Absorptionsmittel, Lichtstabilisatoren, Silanhaftvermittler, Alterungsverhinderungsmittel, thermische Polymerisationsinhibitoren, Egalisiermittel, Farbmittel, oberflächenaktive Mittel, Konservierungsmittel, Weichmacher, Gleitmittel, Lösungsmittel, Füllstoffe, Benetzbarkeitsverbesserer, Beschichtungsoberflächenverbesserer und dergleichen. Beispiele für Antioxidationsmittel sind Antioxidationsmittel des Phenoltyps, Antioxidationsmittel des organischen Schwefeltyps und dergleichen. Diese Antioxidationsmittel sind z.B. unter den Marken Irganox 1010, 1035, 1076, 1222 (von Ciba Specialty Chemicals Co., Ltd. hergestellt) und dergleichen erhältlich.
- Beispiele für UV-Absorptionsmittel sind UV-Absorptionsmittel des Benzotriazol-Typs und dergleichen. Beispiele für käufliche Produkte, die als UV-Absorptionsmittel verwendet werden, umfassen Tinuvin P, 234, 320, 326, 327, 328, 213 (von Ciba-Geigy hergestellt), Sumisorb 110, 130, 140, 220, 250, 300, 320, 340, 350, 400 (von Sumitomo Chemical Industries Co., Ltd. hergestellt) und dergleichen.
- Beispiele für Lichtstabilisatoren sind Lichtstabilisatoren des gehinderten Amintyps und dergleichen. Beispiele für käufliche Lichtstabilisatorprodukte umfassen Tinuvin 292, 144, 622LD (von Ciba Specialty Chemicals Co., Ltd. hergestellt), Sanol LS-770, 765, 292, 2626, 1114, 744 (von Sankyo Chemical Co. hergestellt) und dergleichen.
- Beispiele für Verbindungen, die als Silanhaftvermittler verwendet werden, umfassen γ-Aminopropyltriethoxysilan, γ-Mercaptopropyltrimethoxysilan, γ-Methacryloyloxypropyltrimethoxysilan und käufliche Produkte wie z.B. SH6062, SZ6030 (von Toray-Dow Corning Silicone Co. hergestellt), KBE903, KBM803 (von Shin-Etsu Silicone Co., Ltd. hergestellt) und dergleichen. Beispiele für Alterungsverhinderungsmittel sind Alterungsverhinderungsmittel des Phenoltyps, des Allylamintyps und des Ketonamintyps. Beispiele für käufliche Alterungsverhinderungsmittelprodukte umfassen Antigene W, S, P, 3C, 6C, RD-G, FR, AW (von Sumitomo Chemical Industries Co., Ltd. hergestellt) und dergleichen.
- Die erfindungsgemäße Zusammensetzung kann durch Formulieren der vorstehend genannten Komponenten (A) bis (D) und der Komponenten, die gegebenenfalls zugesetzt werden, in den jeweiligen vorgeschriebenen erforderlichen Mengen hergestellt werden.
- Die Viskosität der resultierenden Zusammensetzung bei 25°C beträgt vorzugsweise 1000 bis 20000 cP und mehr bevorzugt 1500 bis 15000 cP, um ein hervorragendes Beschichtungsvermögen auf optischen Fasern sicherzustellen.
- Die erfindungsgemäße Zusammensetzung ist strahlungshärtbar, so dass sie durch Aussetzen gegenüber einer geeigneten Strahlung gehärtet werden kann. Dabei umfassen die Strahlungsquellen Infrarotlicht, sichtbare Strahlung, Ultraviolettlicht, α-Strahlen, β-Strahlen, γ-Strahlen und dergleichen. Wenn die Zusammensetzung gehärtet wird, wie z.B. durch Aussetzen gegenüber Ultraviolettlicht, kann sie bei einer Dosis von 2 bis 2000 mJ/cm2, vorzugsweise von 50 bis 200 mJ/cm2 gehärtet werden.
- Anwendungen
- Die erfindungsgemäße Zusammensetzung ist für viele Anwendungen geeignet, einschließlich z.B. als Anstrichmittel, Oberflächenerneuerungsmaterial, Druckfarbe und Beschichtungsmaterial für Substrate, insbesondere für optische Fasern.
- Von den gehärteten Produkten, die durch Bestrahlen mit ultraviolettem Licht bei einer Dosis von 1 J/cm2 an Luft erzeugt werden, werden diejenigen mit einer gehärteten Beschichtung mit einer Dicke von 200 μm mit einem Sekantenmodul (gemäß JIS K7127) von 0,15 kg/mm2 oder weniger, mehr bevorzugt von 0,1 bis 0,05 kg/mm2, und einer Reißfestigkeit (gemäß JIS K7127) von mehr als 0,15 kg/mm2, mehr bevorzugt von 0,25 kg/mm2 bis 0,50 kg/mm2, bevorzugt als Primärbeschichtung für optische Fasern verwendet, da diese Produkte einen geeigneten Elastizitätsmodul und eine hervorragende Reißfestigkeit aufweisen, wenn sie als Primärbeschichtung für optische Fasern verwendet werden. Um beschichtete optische Glasfasern mit guten Handhabungseigenschaften zu erhalten, ist es bevorzugt, die Glasfaser, die mit einer anhaftenden Primärbeschichtung beschichtet ist, weiter mit einer härteren Sekundärbeschichtung zu beschichten.
- Eine Beschichtungsschicht aus der erfindungsgemäßen Zusammensetzung kann eine Dicke im Bereich von 5 bis 500 μm, vorzugsweise von 15 bis 300 μm aufweisen. Eine Primärbeschichtung für optische Glasfasern weist im Allgemeinen eine Dicke von etwa 30 μm (15 bis 50 μm) auf.
- In einer bevorzugten Form der erfindungsgemäßen Zusammensetzung umfasst die Zusammensetzung die Komponenten (A), (B), (C) und (D) in Bereichen, bezogen auf das Gesamtgewicht der Zusammensetzung, von 25 bis 75 Gew.-%, von 0,1 bis 10 Gew.-%, von 20 bis 70 Gew.-% bzw. von 0,1 bis 10 Gew.-%. Bevorzugte erfindungsgemäße Zusammensetzungen umfassen diejenigen mit einer Viskosität von 1000 bis 20000 bei 25°C. Die erfindungsgemäße Zusammensetzung wird vorzugsweise zur Verwendung als Primärbeschichtung für optische Fasern angepasst.
- Beispiele
- Die vorliegende Erfindung wird detaillierter mittels Beispielen beschrieben, die nicht beschränkend aufzufassen sind. In den nachstehenden Beispielen steht „Teil(e)" für „Gewichtsteil(e)", falls nichts anderes angegeben ist.
- Synthesebeispiel 1
- Synthese eines Polymers für die Komponente (A)
- 4,07 g Toluylendiisocyanat (das 97,5 Gew.-% oder mehr eines 2,4-Derivats und 2,5 Gew.-% oder weniger eines 2,6-Derivats umfasst), 59,3 g eines Ringöffnungscopolymers von Ethylenoxid und Tetrahydrofuran mit einem Molekulargewichts-Zahlenmittel (nachstehend als „Mn" abgekürzt) von 4000, 0,02 g 2,6-Di-t-butyl-p-kresol und 0,007 g Phenothiazin wurden in einen mit einem Rührer ausgestatteten Reaktionsbehälter eingebracht. Dieses Gemisch wurde unter Rühren mit Eis gekühlt, bis die Temperatur des Gemischs 10°C oder weniger betrug. Wenn die Temperatur 10°C oder weniger betrug, wurden dem Gemisch 0,08 g Dibutylzinndilaurat zugesetzt, worauf 2 Stunden gerührt wurde, während die Flüssigkeitstemperatur bei 20 bis 30°C gehalten wurde. Dann wurden 0,33 g γ-Mercaptopropyltrimethoxysilan (Marke: SH6062, von Toray-Dow Corning Silicone Co., Ltd. hergestellt), bei dem es sich um einen Silanhaftvermittler handelt, zugesetzt und das Gemisch wurde eine Stunde bei 40 bis 50°C gerührt. Nach beendetem Rühren wurden 1,15 g 2-Hydroxyethylacrylat zugesetzt und das resultierende Gemisch wurde 30 min bei einer Flüssigkeitstemperatur von 45 bis 55°C gerührt.
- Als nächstes wurden 0,13 g Methanol der Reaktionslösung zugesetzt, die vier Stunden kontinuierlich bei 55 bis 60°C gerührt wurde. Die Reaktion wurde beendet, wenn die Menge des restlichen Isocyanats 0,1 Gew.-% oder weniger betrug, wobei ein flüssiges Urethanacrylatpolymer mit einem Mn von 8327 erhalten wurde, das der Komponente (A) entsprach.
- Beispiele 1 bis 5 und Vergleichsbeispiele 1 und 2
- 10 g Laurylacrylat, 17 g Polyoxyethylennonylphenyletheracrylat (Marke: M113, von Toagosei Co., Ltd. hergestellt), 5 g N-Vinylcaprolactam, 0,8 g Irganox 1035 als Antioxidationsmittel, 2 g 2,4,6-Trimethylbenzoyldiphenylphosphinoxid und 0,15 g Diethylamin wurden 65 g des im Synthesebeispiel 1 hergestellten flüssigen Urethanacrylatpolymers zugesetzt. Das Gemisch wurde gerührt, während die Temperatur bei 50 bis 60°C gehalten wurde, bis eine einheitliche und transparente Flüssigkeit hergestellt wurde, um eine Harzlösung l zu erhalten.
- In den Beispielen 1 bis 5 wurden 100 Teile der Harzlösung l und jedes der in der Tabelle 1 gezeigten polyfunktionellen Monomere in der in der Tabelle 1 gezeigten Menge in einen mit einem Rührer ausgestatteten Reaktionsbehälter eingebracht, um eine Zusammensetzung herzustellen. Das Gemisch wurde 3 Stunden gerührt, während die Temperatur bei 50 bis 60°C gehalten wurde. Die Viskosität jeder der resultierenden Zusammensetzungen wurde mit einem Viskosimeter des B-Typs bei 25°C gemessen. Die Ergebnisse sind in der Tabelle 2 gezeigt. Die Viskosität aller Zusammensetzungen lag in einem Bereich von 5000 bis 6000 cP. Im Vergleichsbeispiel 1 wurde die Harzlösung l als solche ohne die Verwendung eines polyfunktionellen Monomers eingesetzt. Tabelle 1
- Jede der Zusammensetzungen, die auf diese Weise hergestellt worden ist, wurde unter Verwendung einer Auftragungsvorrichtung in einer Dicke von 250 μm auf die Oberfläche einer Glasplatte aufgebracht und mit Ultraviolettlicht bei einer Dosis von 1,0 J/cm2 an Luft unter Verwendung einer 3,5 kW-Metallhalogenidlampe (SMX-3500/F-OS, von ORC Co., Ltd. hergestellt) bestrahlt, so dass ein gehärteter Film mit einer Dicke von 200 μm erhalten wurde. Der gehärtete Film wurde dann in Streifenprüfkörper mit einer Breite von 0,6 cm geschnitten, um eine Testprobe herzustellen. Die Bedingungen für die Testprobe wurden in geeigneter Weise bei 23°C und einer Feuchtigkeit von 50 % für 12 Stunden oder mehr eingestellt und die Testprobe wurde dann Messungen des Elastizitätsmoduls und der Reißfestigkeit unterworfen, die nachstehend veranschaulicht sind. Die Ergebnisse sind in der Tabelle 2 gezeigt.
- Messung des Elastizitätsmoduls
- Der Sekantenmodul wurde unter den Bedingungen einer Zuggeschwindigkeit von 1 mm/min und einem Intervall zwischen Fixpunkten von 25 mm gemäß JIS K7127 gemessen.
- Messung der Reißfestigkeit
-
- Wie es aus den Tabellen 1 und 2 ersichtlich ist, wies jede der Zusammensetzungen der Beispiele 1 bis 5 eine Viskosität in einem zum Beschichten optischer Fasern angemessenen Bereich auf und das resultierende gehärtete Produkt zeigte eine hohe Reißfestigkeit von 0,26 bis 0,42 kg/mm2, während dessen Sekantenmodul einen niedrigen Wert von 0,06 bis 0,11 kg/mm2 aufwies. Andererseits wies der gehärtete Film, der aus den Zusammensetzungen der Vergleichsbeispiele 1 und 2, die das polyfunktionelle Monomer nicht enthielten, hergestellt worden ist, eine niedrige Reißfestigkeit auf.
- Aus den vorstehenden Erläuterungen wird deutlich, dass die erfindungsgemäße strahlungshärtbare Zusammensetzung dadurch gekennzeichnet ist, dass das gehärtete Produkt eine hohe Reißfestigkeit aufweist, während dessen Elastizitätsmodul niedrig ist. Wenn die strahlungshärtbare Zusammensetzung als Beschichtungsmaterial für optische Fasern verwendet wird, kann sie somit optische Fasern für einen langen Zeitraum in einer sicheren und stabilen Weise schützen, während eine hervorragende optische Übertragungsleistung beibehalten wird.
Claims (12)
- Beschichtete optische Faser, wobei die Primärbeschichtung aus einer strahlungshärtbaren Zusammensetzung gebildet ist, umfassend: (A) eine Polymerzusammensetzung, welche ein oder mehrere Polyetherpolyolurethan-basierende Polymere mit einem Molekulargewichts-Zahlenmittel von 3.000 bis 30.000 umfaßt, wobei die Zusammensetzung im Durchschnitt 1,2 oder mehr polymerisationsfähige ungesättigte Gruppen pro Polymermolekül aufweist, (B) ein polyfunktionelles Monomer mit zwei oder mehr polymerisationsfähigen ungesättigten Gruppen, (C) ein Monomer mit einer polymerisationsfähigen ungesättigten Gruppe und (D) einen strahlungsaktiven Initiator, wobei die Beschichtung eine Reißfestigkeit von mehr als 0,15 kg/mm2 und einen Sekantenmodul von 0,15 kg/mm2 oder weniger aufweist.
- Beschichtete optische Faser nach Anspruch 1, wobei die Polymerzusammensetzung (A) ein aus einem Polyoxyalkylenpolyetherpolyol abgeleitetes Polymer umfaßt.
- Beschichtete optische Faser nach einem der Ansprüche 1 bis 2, wobei die Polymerzusammensetzung mindestens ein Polymer mit 2 bis 10 Urethanbindungen einschließt.
- Beschichtete optische Faser nach einem der Ansprüche 1 bis 3, wobei die strahlungshärtbare Zusammensetzung, bezüglich der gesamten strahlungshärtbaren Zusammensetzung, zwischen 40 und 70 Gew.% der Polymerzusammensetzung (A) umfaßt.
- Beschichtete optische Faser nach einem der Ansprüche 1 bis 4, wobei das polyfunktionelle Monomer (B) ein Molekulargewicht von 800 oder weniger aufweist.
- Beschichtete optische Faser nach einem der Ansprüche 1 bis 5, wobei die strahlungshärtbare Zusammensetzung, bezüglich der gesamten strahlungshärtbaren Zusammensetzung, zwischen 0,1 und 10 Gew.% polyfunktionelles Monomer (B) umfaßt.
- Beschichtete optische Faser nach einem der Ansprüche 1 bis 6, wobei das Monomer (C) eine polymerisationsfähige Vinylgruppe umfaßt.
- Strahlungshärtbare Harzzusammensetzung, umfassend: (A) eine Polyetherpolyolurethan-basierende Polymerzusammensetzung, welche 1,2 oder mehr polymerisationsfähige ungesättigte Gruppen im Durchschnitt in einem Molekül und ein Molekulargewichts-Zahlenmittel von 3.000 bis 30.000 aufweist, (B) ein polyfunktionelles Monomer mit zwei oder mehr polymerisationsfähigen ungesättigten Gruppen, (C) ein Monomer mit einer polymerisationsfähigen ungesättigten Gruppe und (D) einen strahlungsaktiven Initiator, wobei die strahlungshärtbare Harzzusammensetzung (bei einer Dicke von 200 μm), wenn sie mit Ultraviolettstrahlung an Luft bei einer Dosis von 1 J/cm2 bestrahlt wird, ein gehärtetes Produkt mit einem Sekantenmodul von 0,15 kg/mm2 oder weniger und einer Reißfestigkeit von mehr als 0,15 kg/mm2 bereitstellt.
- Beschichtungszusammensetzung nach Anspruch 8, wobei die strahlungshärtbare Zusammensetzung bei 25°C eine Viskosität von 1.000 bis 20.000 cP aufweist.
- Beschichtungszusammensetzung nach einem der Ansprüche 8 bis 9, wobei das gehärtete Produkt einen Sekantenmodul von 0,05 bis 0,1 kg/mm2 und eine Reißfestigkeit von 0,25 bis 0,5 kg/mm2 aufweist.
- Beschichtete optische Faser mit einer Primärbeschichtung nach einem der Ansprüche 1 bis 7, welche an das Glassubstrat anhaftet.
- Beschichtete optische Faser nach Anspruch 11, welche weiter eine an die Primärbeschichtung anhaftende Sekundärbeschichtung aufweist.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP23544997 | 1997-08-15 | ||
| JP23544997 | 1997-08-15 | ||
| PCT/NL1998/000464 WO1999008975A1 (en) | 1997-08-15 | 1998-08-14 | Radiation-curable resin composition |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE69827807D1 DE69827807D1 (de) | 2004-12-30 |
| DE69827807T2 true DE69827807T2 (de) | 2005-11-03 |
Family
ID=16986282
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE69827807T Expired - Fee Related DE69827807T2 (de) | 1997-08-15 | 1998-08-14 | Beschichtete optische faser und strahlungshärtbare harzzusammensetzung |
Country Status (5)
| Country | Link |
|---|---|
| EP (1) | EP1007490B1 (de) |
| KR (1) | KR100508714B1 (de) |
| CN (1) | CN1208275C (de) |
| DE (1) | DE69827807T2 (de) |
| WO (1) | WO1999008975A1 (de) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6579618B1 (en) | 1997-08-15 | 2003-06-17 | Dsm N.V. | Coated optical fiber and radiation curable resin composition |
| KR20010042636A (ko) * | 1998-04-15 | 2001-05-25 | 윌리암 로엘프 드 보에르 | 방사선 경화성 수지조성물 |
| KR20020067056A (ko) | 1999-12-30 | 2002-08-21 | 코닝 인코포레이티드 | 1차 광섬유 코팅의 급속 경화방법 |
| AU1582701A (en) | 1999-12-30 | 2001-07-16 | Corning Incorporated | Optical fibers prepared with a primary coating composition including a monomer with a pendant hydroxyl functional group |
| US7706659B2 (en) | 2000-11-22 | 2010-04-27 | Dsm Ip Assets B.V. | Coated optical fibers |
| US7067564B2 (en) | 2000-11-22 | 2006-06-27 | Dsm Ip Assets B.V. | Coated optical fibers |
| US6916855B2 (en) | 2000-11-22 | 2005-07-12 | Dsm Ip Assets B.V. | Radiation curable compositions |
| EP1209132A1 (de) * | 2000-11-22 | 2002-05-29 | Dsm N.V. | Beschichtete optische Fasern, primäre Beschichtungszusammensetzung, Härtungsverfahren, sowie ein Messungsgerät und ein Messungsverfahren |
| AU2002230259A1 (en) * | 2001-01-12 | 2002-07-24 | Dsm Ip Assets B.V. | Radiation curable compositions comprising alkoxylated aliphatic reactive diluents |
| EP1358276A2 (de) * | 2001-01-12 | 2003-11-05 | DSM IP Assets B.V. | Durch strahlung härtbare zusammensetzung und damit beschichtete produkte |
| US20030123839A1 (en) * | 2001-07-27 | 2003-07-03 | Chou Kevin Y. | Low modulus, high tensile strength optical fiber coating |
| EP1323784B1 (de) * | 2001-12-26 | 2005-02-16 | Dainippon Ink And Chemicals, Inc. | Harzzusammensetzung zur Beschichtung von optischem Glasfaser, beschichtete optische Faser, und dieses verwendende faseroptische Kabel |
| WO2005028570A2 (de) * | 2003-08-22 | 2005-03-31 | Basf Aktiengesellschaft | Formulierungen und ihre verwendung bei der beschichtung von substraten |
| US20060030634A1 (en) | 2004-08-04 | 2006-02-09 | Dean Roy E | Radiation curable, sprayable coating compositions |
| JP5220279B2 (ja) * | 2006-03-23 | 2013-06-26 | 古河電気工業株式会社 | 光ファイバ素線 |
| CN103468108B (zh) * | 2006-12-15 | 2016-03-02 | 科洛普拉斯特公司 | 涂料组合物 |
| US8460762B2 (en) * | 2009-12-16 | 2013-06-11 | Ideon Llc | Electron beam curable composition for curing in a vacuum chamber |
| CN114207063B (zh) | 2019-07-31 | 2023-07-25 | 科思创(荷兰)有限公司 | 具有多功能长臂低聚物的涂覆光纤用辐射固化组合物 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4932750A (en) * | 1982-12-09 | 1990-06-12 | Desoto, Inc. | Single-coated optical fiber |
| JPS6114210A (ja) * | 1984-06-30 | 1986-01-22 | Yokohama Rubber Co Ltd:The | 光ファイバユニット緩衝材用紫外線硬化型樹脂組成物 |
| JPS6424816A (en) * | 1987-07-21 | 1989-01-26 | Mitsui Toatsu Chemicals | Photo-setting resin composition |
| US4973611A (en) * | 1988-04-04 | 1990-11-27 | Uvexs Incorporated | Optical fiber buffer coating with Tg |
| DE69507335T2 (de) * | 1994-11-29 | 1999-09-09 | Dsm N.V. | Optische glasfaser, beschichtet mit einer strahlungshärtbaren beschichtungszusammensetzung |
| JPH09143233A (ja) * | 1995-11-28 | 1997-06-03 | Japan Synthetic Rubber Co Ltd | 光硬化性液状樹脂組成物 |
| JPH10204250A (ja) * | 1997-01-23 | 1998-08-04 | Jsr Corp | 液状硬化性樹脂組成物 |
-
1998
- 1998-08-14 DE DE69827807T patent/DE69827807T2/de not_active Expired - Fee Related
- 1998-08-14 CN CNB988081547A patent/CN1208275C/zh not_active Expired - Lifetime
- 1998-08-14 KR KR10-2000-7001399A patent/KR100508714B1/ko not_active Expired - Fee Related
- 1998-08-14 WO PCT/NL1998/000464 patent/WO1999008975A1/en not_active Ceased
- 1998-08-14 EP EP98939023A patent/EP1007490B1/de not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| EP1007490B1 (de) | 2004-11-24 |
| CN1267273A (zh) | 2000-09-20 |
| KR100508714B1 (ko) | 2005-08-17 |
| WO1999008975A1 (en) | 1999-02-25 |
| CN1208275C (zh) | 2005-06-29 |
| EP1007490A1 (de) | 2000-06-14 |
| KR20010022799A (ko) | 2001-03-26 |
| DE69827807D1 (de) | 2004-12-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69506577T2 (de) | Optische glasfaser-beschichtungszusammensetzung | |
| DE69827807T2 (de) | Beschichtete optische faser und strahlungshärtbare harzzusammensetzung | |
| DE69810287T3 (de) | Flüssige härtbare harzzusammensetzung | |
| DE69819336T2 (de) | Flüssige, härtbare harzzusammensetzung | |
| US20020132118A1 (en) | Photocurable resin composition | |
| DE69607855T2 (de) | Flüssige photohärtbare harzzusammensetzung | |
| AU705686B2 (en) | Optical glass fiber coating composition | |
| CA2499704A1 (en) | Optical fiber with cured polymeric coating | |
| DE60120941T2 (de) | Flüssige härtbare harzzusammensetzung und zweischichtiger film | |
| US5913004A (en) | Optical glass fiber coating composition | |
| US6579618B1 (en) | Coated optical fiber and radiation curable resin composition | |
| KR20010042636A (ko) | 방사선 경화성 수지조성물 | |
| DE60125201T2 (de) | Flüssige, härtbare harzzusammensetzungen und gehärtete produkte | |
| JP4025852B2 (ja) | 放射線硬化性樹脂組成物 | |
| WO1997014737A1 (en) | Liquid curable resin composition | |
| WO1998041483A1 (en) | Liquid curable resin composition for fat fibre | |
| DE69502186T2 (de) | Flüssige härtbare harzzusammensetzung für optische fasern | |
| EP1476487B1 (de) | Härtbare flüssige harzzusammensetzung | |
| JP2002544351A (ja) | 均一に一貫した放射線硬化可能な組成物の製造法 | |
| JPH11116642A (ja) | 放射線硬化性樹脂組成物 | |
| DE69817234T2 (de) | Flüssige, härtbare Harzzusammensetzung | |
| JP3324710B2 (ja) | 液状硬化性樹脂組成物 | |
| JP3607748B2 (ja) | 多層被覆 | |
| JP5307317B2 (ja) | 液状硬化性樹脂組成物 | |
| DE69331201T2 (de) | Flüssige, härtbare harzzusammensetzung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8339 | Ceased/non-payment of the annual fee |