EP0014982A2 - Zweikomponenten-Diazotypiematerial - Google Patents
Zweikomponenten-Diazotypiematerial Download PDFInfo
- Publication number
- EP0014982A2 EP0014982A2 EP80100807A EP80100807A EP0014982A2 EP 0014982 A2 EP0014982 A2 EP 0014982A2 EP 80100807 A EP80100807 A EP 80100807A EP 80100807 A EP80100807 A EP 80100807A EP 0014982 A2 EP0014982 A2 EP 0014982A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- hydroxy
- diazonium salt
- material according
- naphthalene
- sulfonic acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 239000000463 material Substances 0.000 title claims abstract description 26
- CIZVQWNPBGYCGK-UHFFFAOYSA-N benzenediazonium Chemical class N#[N+]C1=CC=CC=C1 CIZVQWNPBGYCGK-UHFFFAOYSA-N 0.000 claims abstract description 6
- 125000000217 alkyl group Chemical group 0.000 claims description 8
- UIAFKZKHHVMJGS-UHFFFAOYSA-N beta-resorcylic acid Natural products OC(=O)C1=CC=C(O)C=C1O UIAFKZKHHVMJGS-UHFFFAOYSA-N 0.000 claims description 8
- 150000001875 compounds Chemical class 0.000 claims description 8
- 125000003342 alkenyl group Chemical group 0.000 claims description 7
- 150000001412 amines Chemical class 0.000 claims description 7
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 7
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 7
- 125000004432 carbon atom Chemical group C* 0.000 claims description 6
- GLDQAMYCGOIJDV-UHFFFAOYSA-N 2,3-dihydroxybenzoic acid Chemical compound OC(=O)C1=CC=CC(O)=C1O GLDQAMYCGOIJDV-UHFFFAOYSA-N 0.000 claims description 5
- 125000003118 aryl group Chemical group 0.000 claims description 4
- 229910052736 halogen Inorganic materials 0.000 claims description 4
- 150000002367 halogens Chemical class 0.000 claims description 4
- 125000003545 alkoxy group Chemical group 0.000 claims description 3
- 150000002989 phenols Chemical class 0.000 claims description 3
- LEVPVSDWYICRIN-UHFFFAOYSA-N 2,5-diethoxy-4-(4-methylphenyl)sulfanylbenzenediazonium Chemical class CCOC1=CC([N+]#N)=C(OCC)C=C1SC1=CC=C(C)C=C1 LEVPVSDWYICRIN-UHFFFAOYSA-N 0.000 claims description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 2
- 125000002252 acyl group Chemical group 0.000 claims description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 2
- 229910052794 bromium Inorganic materials 0.000 claims description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 2
- 229910052801 chlorine Inorganic materials 0.000 claims description 2
- 239000000460 chlorine Substances 0.000 claims description 2
- 229910052739 hydrogen Inorganic materials 0.000 claims description 2
- 239000001257 hydrogen Substances 0.000 claims description 2
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 2
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 2
- 125000003107 substituted aryl group Chemical group 0.000 claims description 2
- WPWHSFAFEBZWBB-UHFFFAOYSA-N 1-butyl radical Chemical compound [CH2]CCC WPWHSFAFEBZWBB-UHFFFAOYSA-N 0.000 claims 1
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical compound [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 claims 1
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 claims 1
- 230000008878 coupling Effects 0.000 abstract description 6
- 238000010168 coupling process Methods 0.000 abstract description 6
- 238000005859 coupling reaction Methods 0.000 abstract description 6
- 150000001408 amides Chemical class 0.000 abstract 1
- 239000000243 solution Substances 0.000 description 11
- QVOUKNHIWFHHPP-UHFFFAOYSA-O 4-sulfanylbenzenediazonium Chemical class SC1=CC=C([N+]#N)C=C1 QVOUKNHIWFHHPP-UHFFFAOYSA-O 0.000 description 8
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 8
- JDQOQWKEOLQHKB-UHFFFAOYSA-N 4-aminobenzenediazonium Chemical class NC1=CC=C([N+]#N)C=C1 JDQOQWKEOLQHKB-UHFFFAOYSA-N 0.000 description 7
- 239000000975 dye Substances 0.000 description 7
- HKWPUUYEGGDLJF-UHFFFAOYSA-N 4-hydroxynaphthalene-2-sulfonic acid Chemical compound C1=CC=C2C(O)=CC(S(O)(=O)=O)=CC2=C1 HKWPUUYEGGDLJF-UHFFFAOYSA-N 0.000 description 5
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 4
- 229910021529 ammonia Inorganic materials 0.000 description 4
- 239000001045 blue dye Substances 0.000 description 4
- 229920002678 cellulose Polymers 0.000 description 4
- 230000001808 coupling effect Effects 0.000 description 4
- 239000012954 diazonium Substances 0.000 description 4
- 229940124530 sulfonamide Drugs 0.000 description 4
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 4
- 239000002253 acid Substances 0.000 description 3
- HQABUPZFAYXKJW-UHFFFAOYSA-N butan-1-amine Chemical compound CCCCN HQABUPZFAYXKJW-UHFFFAOYSA-N 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- PAFZNILMFXTMIY-UHFFFAOYSA-N cyclohexylamine Chemical compound NC1CCCCC1 PAFZNILMFXTMIY-UHFFFAOYSA-N 0.000 description 3
- 150000001989 diazonium salts Chemical class 0.000 description 3
- 230000007935 neutral effect Effects 0.000 description 3
- 229920006267 polyester film Polymers 0.000 description 3
- NKTOLZVEWDHZMU-UHFFFAOYSA-N 2,5-xylenol Chemical compound CC1=CC=C(C)C(O)=C1 NKTOLZVEWDHZMU-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- JWAZRIHNYRIHIV-UHFFFAOYSA-N 2-naphthol Chemical class C1=CC=CC2=CC(O)=CC=C21 JWAZRIHNYRIHIV-UHFFFAOYSA-N 0.000 description 2
- FBLAHUMENIHUGG-UHFFFAOYSA-N 3-hydroxy-n-(2-methylphenyl)naphthalene-2-carboxamide Chemical compound CC1=CC=CC=C1NC(=O)C1=CC2=CC=CC=C2C=C1O FBLAHUMENIHUGG-UHFFFAOYSA-N 0.000 description 2
- NFTNTGFZYSCPSK-UHFFFAOYSA-N 3-hydroxynaphthalene-2-carboxamide Chemical class C1=CC=C2C=C(O)C(C(=O)N)=CC2=C1 NFTNTGFZYSCPSK-UHFFFAOYSA-N 0.000 description 2
- LVAOVTMXTCAMIG-UHFFFAOYSA-N 8-hydroxy-6-sulfamoylnaphthalene-1-sulfonic acid Chemical class OS(=O)(=O)C1=CC=CC2=CC(S(=O)(=O)N)=CC(O)=C21 LVAOVTMXTCAMIG-UHFFFAOYSA-N 0.000 description 2
- VVJKKWFAADXIJK-UHFFFAOYSA-N Allylamine Chemical compound NCC=C VVJKKWFAADXIJK-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- WGQKYBSKWIADBV-UHFFFAOYSA-N benzylamine Chemical compound NCC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 description 2
- 229940114055 beta-resorcylic acid Drugs 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 125000000664 diazo group Chemical group [N-]=[N+]=[*] 0.000 description 2
- BRDIPNLKURUXCU-UHFFFAOYSA-N ethyl 2,4-dihydroxybenzoate Chemical compound CCOC(=O)C1=CC=C(O)C=C1O BRDIPNLKURUXCU-UHFFFAOYSA-N 0.000 description 2
- MGJXBDMLVWIYOQ-UHFFFAOYSA-N methylazanide Chemical compound [NH-]C MGJXBDMLVWIYOQ-UHFFFAOYSA-N 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 235000005074 zinc chloride Nutrition 0.000 description 2
- 239000011592 zinc chloride Substances 0.000 description 2
- ZYECOAILUNWEAL-NUDFZHEQSA-N (4z)-4-[[2-methoxy-5-(phenylcarbamoyl)phenyl]hydrazinylidene]-n-(3-nitrophenyl)-3-oxonaphthalene-2-carboxamide Chemical compound COC1=CC=C(C(=O)NC=2C=CC=CC=2)C=C1N\N=C(C1=CC=CC=C1C=1)/C(=O)C=1C(=O)NC1=CC=CC([N+]([O-])=O)=C1 ZYECOAILUNWEAL-NUDFZHEQSA-N 0.000 description 1
- UNHOPMIDKWXFMF-UHFFFAOYSA-N 1-methylpyrrolidin-3-amine Chemical compound CN1CCC(N)C1 UNHOPMIDKWXFMF-UHFFFAOYSA-N 0.000 description 1
- KJCVRFUGPWSIIH-UHFFFAOYSA-N 1-naphthol Chemical class C1=CC=C2C(O)=CC=CC2=C1 KJCVRFUGPWSIIH-UHFFFAOYSA-N 0.000 description 1
- CDULGHZNHURECF-UHFFFAOYSA-N 2,3-dimethylaniline 2,4-dimethylaniline 2,5-dimethylaniline 2,6-dimethylaniline 3,4-dimethylaniline 3,5-dimethylaniline Chemical group CC1=CC=C(N)C(C)=C1.CC1=CC=C(C)C(N)=C1.CC1=CC(C)=CC(N)=C1.CC1=CC=C(N)C=C1C.CC1=CC=CC(N)=C1C.CC1=CC=CC(C)=C1N CDULGHZNHURECF-UHFFFAOYSA-N 0.000 description 1
- IIUJCQYKTGNRHH-UHFFFAOYSA-N 2,4-dihydroxybenzamide Chemical compound NC(=O)C1=CC=C(O)C=C1O IIUJCQYKTGNRHH-UHFFFAOYSA-N 0.000 description 1
- UPKAFSNUROXYDY-UHFFFAOYSA-N 2,5-dimethoxy-4-morpholin-4-ylaniline Chemical compound C1=C(N)C(OC)=CC(N2CCOCC2)=C1OC UPKAFSNUROXYDY-UHFFFAOYSA-N 0.000 description 1
- AMCOCUDBDKVWRZ-UHFFFAOYSA-N 2-(2-hydroxyethoxy)phenol Chemical compound OCCOC1=CC=CC=C1O AMCOCUDBDKVWRZ-UHFFFAOYSA-N 0.000 description 1
- HEQOJEGTZCTHCF-UHFFFAOYSA-N 2-amino-1-phenylethanone Chemical compound NCC(=O)C1=CC=CC=C1 HEQOJEGTZCTHCF-UHFFFAOYSA-N 0.000 description 1
- LTHNHFOGQMKPOV-UHFFFAOYSA-N 2-ethylhexan-1-amine Chemical compound CCCCC(CC)CN LTHNHFOGQMKPOV-UHFFFAOYSA-N 0.000 description 1
- IMLAIXAZMVDRGA-UHFFFAOYSA-N 2-phenoxyethanamine Chemical compound NCCOC1=CC=CC=C1 IMLAIXAZMVDRGA-UHFFFAOYSA-N 0.000 description 1
- WRXNJTBODVGDRY-UHFFFAOYSA-N 2-pyrrolidin-1-ylethanamine Chemical compound NCCN1CCCC1 WRXNJTBODVGDRY-UHFFFAOYSA-N 0.000 description 1
- WGTASENVNYJZBK-UHFFFAOYSA-N 3,4,5-trimethoxyamphetamine Chemical compound COC1=CC(CC(C)N)=CC(OC)=C1OC WGTASENVNYJZBK-UHFFFAOYSA-N 0.000 description 1
- LPUBRQWGZPPVBS-UHFFFAOYSA-N 3-butoxypropan-1-amine Chemical compound CCCCOCCCN LPUBRQWGZPPVBS-UHFFFAOYSA-N 0.000 description 1
- FAXDZWQIWUSWJH-UHFFFAOYSA-N 3-methoxypropan-1-amine Chemical compound COCCCN FAXDZWQIWUSWJH-UHFFFAOYSA-N 0.000 description 1
- UIKUBYKUYUSRSM-UHFFFAOYSA-N 3-morpholinopropylamine Chemical compound NCCCN1CCOCC1 UIKUBYKUYUSRSM-UHFFFAOYSA-N 0.000 description 1
- MVOHVYMORIMKGN-UHFFFAOYSA-N 4-hydroxynaphthalene-1,5-disulfonamide Chemical class OC1=CC=C(C2=CC=CC(=C12)S(=O)(=O)N)S(=O)(=O)N MVOHVYMORIMKGN-UHFFFAOYSA-N 0.000 description 1
- HGWQOFDAUWCQDA-UHFFFAOYSA-N 4-hydroxynaphthalene-1-sulfonic acid Chemical compound C1=CC=C2C(O)=CC=C(S(O)(=O)=O)C2=C1 HGWQOFDAUWCQDA-UHFFFAOYSA-N 0.000 description 1
- AGNFWIZBEATIAK-UHFFFAOYSA-N 4-phenylbutylamine Chemical compound NCCCCC1=CC=CC=C1 AGNFWIZBEATIAK-UHFFFAOYSA-N 0.000 description 1
- ACOXURKIHJSMAC-UHFFFAOYSA-N 4-piperidin-1-ylbutan-1-amine Chemical compound NCCCCN1CCCCC1 ACOXURKIHJSMAC-UHFFFAOYSA-N 0.000 description 1
- BGNLXETYTAAURD-UHFFFAOYSA-N 4-tert-butylcyclohexan-1-amine Chemical compound CC(C)(C)C1CCC(N)CC1 BGNLXETYTAAURD-UHFFFAOYSA-N 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- MHZGKXUYDGKKIU-UHFFFAOYSA-N Decylamine Chemical compound CCCCCCCCCCN MHZGKXUYDGKKIU-UHFFFAOYSA-N 0.000 description 1
- WUGQZFFCHPXWKQ-UHFFFAOYSA-N Propanolamine Chemical compound NCCCO WUGQZFFCHPXWKQ-UHFFFAOYSA-N 0.000 description 1
- SKZKKFZAGNVIMN-UHFFFAOYSA-N Salicilamide Chemical compound NC(=O)C1=CC=CC=C1O SKZKKFZAGNVIMN-UHFFFAOYSA-N 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 150000003931 anilides Chemical class 0.000 description 1
- 150000001448 anilines Chemical class 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 150000003974 aralkylamines Chemical class 0.000 description 1
- UCMIRNVEIXFBKS-UHFFFAOYSA-N beta-alanine Chemical compound NCCC(O)=O UCMIRNVEIXFBKS-UHFFFAOYSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- IMHDGJOMLMDPJN-UHFFFAOYSA-N biphenyl-2,2'-diol Chemical group OC1=CC=CC=C1C1=CC=CC=C1O IMHDGJOMLMDPJN-UHFFFAOYSA-N 0.000 description 1
- LLEMOWNGBBNAJR-UHFFFAOYSA-N biphenyl-2-ol Chemical group OC1=CC=CC=C1C1=CC=CC=C1 LLEMOWNGBBNAJR-UHFFFAOYSA-N 0.000 description 1
- MSZJEPVVQWJCIF-UHFFFAOYSA-N butylazanide Chemical compound CCCC[NH-] MSZJEPVVQWJCIF-UHFFFAOYSA-N 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- HSOHBWMXECKEKV-UHFFFAOYSA-N cyclooctanamine Chemical compound NC1CCCCCCC1 HSOHBWMXECKEKV-UHFFFAOYSA-N 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 239000004922 lacquer Substances 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- UDGSVBYJWHOHNN-UHFFFAOYSA-N n',n'-diethylethane-1,2-diamine Chemical compound CCN(CC)CCN UDGSVBYJWHOHNN-UHFFFAOYSA-N 0.000 description 1
- IMCCZKHIPVEUEI-UHFFFAOYSA-N n,n-difluoroaniline Chemical compound FN(F)C1=CC=CC=C1 IMCCZKHIPVEUEI-UHFFFAOYSA-N 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 238000010421 pencil drawing Methods 0.000 description 1
- 239000007793 ph indicator Substances 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 1
- ORFSSYGWXNGVFB-UHFFFAOYSA-N sodium 4-amino-6-[[4-[4-[(8-amino-1-hydroxy-5,7-disulfonaphthalen-2-yl)diazenyl]-3-methoxyphenyl]-2-methoxyphenyl]diazenyl]-5-hydroxynaphthalene-1,3-disulfonic acid Chemical compound COC1=C(C=CC(=C1)C2=CC(=C(C=C2)N=NC3=C(C4=C(C=C3)C(=CC(=C4N)S(=O)(=O)O)S(=O)(=O)O)O)OC)N=NC5=C(C6=C(C=C5)C(=CC(=C6N)S(=O)(=O)O)S(=O)(=O)O)O.[Na+] ORFSSYGWXNGVFB-UHFFFAOYSA-N 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 150000003456 sulfonamides Chemical class 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 150000008053 sultones Chemical group 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 150000004992 toluidines Chemical class 0.000 description 1
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03C—PHOTOSENSITIVE MATERIALS FOR PHOTOGRAPHIC PURPOSES; PHOTOGRAPHIC PROCESSES, e.g. CINE, X-RAY, COLOUR, STEREO-PHOTOGRAPHIC PROCESSES; AUXILIARY PROCESSES IN PHOTOGRAPHY
- G03C1/00—Photosensitive materials
- G03C1/52—Compositions containing diazo compounds as photosensitive substances
- G03C1/54—Diazonium salts or diazo anhydrides
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03C—PHOTOSENSITIVE MATERIALS FOR PHOTOGRAPHIC PURPOSES; PHOTOGRAPHIC PROCESSES, e.g. CINE, X-RAY, COLOUR, STEREO-PHOTOGRAPHIC PROCESSES; AUXILIARY PROCESSES IN PHOTOGRAPHY
- G03C1/00—Photosensitive materials
- G03C1/52—Compositions containing diazo compounds as photosensitive substances
- G03C1/58—Coupling substances therefor
Definitions
- the present invention relates to a two-component diazotype material, consisting of a support and a photosensitive layer applied thereon, comprising at least one photosensitive diazonium salt and a coupler.
- a two-component diazotype material consisting of a support and a photosensitive layer applied thereon, comprising at least one photosensitive diazonium salt and a coupler.
- Many compounds coupling to a blue dye have been described for use in two-component diazotype materials.
- the main part relates to 2-hydroxy-naphthalene derivatives, e.g. B. 2-hydroxy-naphthalene-3-carboxamides, which are used in combination with p-aminobenzene diazonium salts for blue and, in combination with other couplers, for black settings.
- 1-hydroxy-naphthalene-3,8-sulfonic acid amides are also known as blue couplers, for which, however, either no technical details are given or those that are not specific Let suitability conclude. They are characterized as lightfast, slowly coupling with pale blue or, in combination with a special p-amino-benzene diazonium salt (blue salt), with a beautiful blue color and as strongly basic.
- p-aminobenzene diazonium salts also have some serious disadvantages.
- the dyes With a pH shift, e.g. B. by acidic vapors, the dyes lose their contrast and turn, similar to pH indicator dyes, to burgundy to light yellow tones.
- light-sensitive p-amino Benzene diazonium salts also limit thermal stability, which leads to loss of contrast when storing unexposed material.
- Blacks are achieved in the diazo type by mixing two or more couplers (Kosar, Light-Sensitive Systems, Wiley & Sons, New York (1965), p. 303). For this it is usually necessary to use a little reddish blue coupler, the coupling speed of which is similar to that of the yellow and brown couplers added.
- DE-AS 20 00 819 describes 1-hydroxy-naphthalene-3-sulfonic acid-8-sulfonic acid amide derivatives as blue couplers, preferably in combination with p-aminobenzene diazonium salts. In combination with p-mercaptobenzene diazonium salts, these also form reddish, violet dyes which are neither useful for blue nor for black settings.
- DE-AS 12 29 844 1-Bydroxy-naphthalin-8-sulfonamides, which may be further substituted, are known as alkali donors in diazotype materials.
- the invention thus relates to a two-component diazotype material, consisting of a support and a photosensitive layer applied thereon, which contains at least one benzene diazonium salt and at least one coupler as the photosensitive component, characterized by the combination of at least one 2,5-dialkoxy-4-mercaptobenzene diazonium salt and at least one compound of the general formula wherein R 1 and R 2 are the same or different and are hydrogen, alkyl, alkenyl, aralkyl, aryl or cycloalkyl, which may be further substituted.
- a 2,5-dialkoxy-4-arylmercaptobenzene diazonium salt in particular 2,5-diethoxy-4-p-tolylmercaptobenzene diazonium salt, is preferably used as the benzene diazonium salt.
- R 1 and R 2 are preferably alkyl or alkenyl, aryl, aralkyl or cycloalkyl having up to 10 carbon atoms, which are substituted by alkyl or alkoxyl up to 4 carbon atoms, by carboxyl, by acyl having up to 3 carbon atoms, by pbenoxy, by halogen, in particular chlorine or bromine, by hydroxyl or by optionally alkyl-substituted amine.
- R 1 is an optionally substituted aryl and R 2 is an optionally substituted alkyl, alkenyl, aralkyl or cycloalkyl have proven particularly useful.
- naphthosultone-3-sulfochloride reacts Room temperature with excess aniline quantitatively to naphthosultone-3-sulfonic acid anilide, and this in turn reacts quickly and quantitatively at room temperature with methylamine to 1-hydroxy-naphthalene-3-sulfonic acid anilide-8-sulfonic acid methylamide.
- the solubility in aqueous or organic solvents is strongly dependent on the type of radicals R 1 and R 2.
- the radicals also have a certain influence on the coupling rate and the color.
- the 1-hydroxy-naphthalene-3,8-di (alkyl, aralkyl, alkenyl or cycloalkyl) sulfonamides couple somewhat faster and are more reddish than the 1-hydroxy-naphthalene-3-arylsulfonamido-8-alkylsulfonamides.
- the 1-hydroxy-naphthalene-3,8-di (N-arylsulfonamides) are even more greenish. The latter are less resistant to light and tend to yellow slightly.
- 1-Hydroxy-naphthalene-3-arylsulfonamido-8-alkylsulfonamides such as 1-hydroxy-naphthalene-3-p-tolylsulfonamido-8-h-butylsulfonamide are particularly suitable for black adjustments.
- Amines which are suitable for the reaction are, in addition to ammonia, alkylamines, for. B. methylamine, ethylamine, n or iso propylamine, butylamine, 2-ethylhexylamine or decylamine, alkenylamines, e.g. B. allylamine, aralkylamines, e.g. B. benzylamine, phenethylamine, phenylbutylamine, cycloalkylamines, e.g. B.
- cyclohexylamine, cyclooctylamine, 4-t-butylcyclohexylamine, and aniline derivatives which may be substituted by amine, alkyl, alkoxy or halogen, for.
- aniline derivatives which may be substituted by amine, alkyl, alkoxy or halogen, for.
- the aliphatic residues can also be without Disadvantage to be substituted.
- inexpensive technical amines z. B.
- ethanolamine hydroxypropylamine, diethylaminoethylamine, morpholinopropylamine, pyrrolidinoethylamine, 4-amino- (N-methylpyrrolidine), piperidinobutylamine, butoxypropylamine, phenoxyethylamine or aminopropionic acid.
- the blueprint layer preferably in a lacquer layer of cellulose ester, for. B. cellulose acetobutyrate is dispersed.
- Simple phenol derivatives e.g. B. 2-hydroxydiphenyl, 2,2'-dihydroxydiphenyl, 2-hydroxyethoxyphenol, 2-hydroxybenzoic acid amide, 3,6-dimethylphenol as Mannich base or resorcylic acid with their derivatives, e.g. B. 2,4-dihydroxybenzoic acid, 2,4-dihydroxybenzoic acid amide, 2,4-dihydroxybenzoic acid ethanolamide or 2,4-dihydroxybenzoic acid ethyl ester into consideration.
- each 100 ml of a solution are in the form of their double salts with zinc chloride solved.
- the solutions are made on polyester film with a Wet weight of approx. 100 g / m 2 applied and dried.
- the amount of diazo is dimensioned so that the contrast of the different patterns is approximately the same.
- TD-205 with Wratten 106 filter
- the density is aged after fresh (I) and after two, four and seven (II, III, IV) days in the forced storage test at 60 ° C (hot box) the development following the exposure under a template with ammonia measured.
- the values included in the following table show that the density drop for the p-mercaptobenzene diazonium salts is very much lower than for the p-aminobenzene diazonium salts.
- the compounds according to the invention produce neutral blue tones as desired. It is noteworthy that the replacement of a sulfonic acid amide group with a sulfonic acid group reduces the amount of red in the dye even further.
- Solutions a) to h) are coated in the first case immediately (A), in the second case after 6 hours (B) and in the third case after 24 hours (C) in each case a polyester film coated with cellulose acetopropionate.
- a polyester film coated with cellulose acetopropionate already the fresh solutions a - e are considerably darker than the solutions f - h and accordingly the base of the break is darker from the beginning after imagewise exposure and development with the materials a - e.
- Material a is basically blue, materials b - e blue-gray, and materials f - h light to light gray.
- Transparent paper coated with cellulose acetobutyrate is coated with a solution of the following composition and dried:
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Non-Silver Salt Photosensitive Materials And Non-Silver Salt Photography (AREA)
- Heat Sensitive Colour Forming Recording (AREA)
- Prostheses (AREA)
- Radiation-Therapy Devices (AREA)
- Liquid Developers In Electrophotography (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
- Die vorliegende-Erfindung bezieht sich auf ein Zweikomponenten-Diazotypiematerial, bestehend aus einem Schichtträger und einer darauf aufgebrachten lichtempfindlichen Schicht aus mindestens einem lichtempfindlichen Diazoniumsalz und einem Kuppler. Zur Verwendung in Zweikomponenten-Diazotypiematerialien wurden bereits viele zu einem blauen Farbstoff kuppelnde Verbindungen beschrieben. Der wesentliche Teil bezieht sich auf 2-Hydroxy-naphthalinderivate, z. B. 2-Hydroxy-naphthalin-3-carbonsäureamide, die in Kombination mit p-Aminobenzoldiazoniumsalzen für Blau- und, in Kombination mit anderen Kupplern, für Schwarzeinstellungen technisch eingesetzt werden. Aus dem Landau-Bericht, 9-17, Seite 49 (1962), sind auch 1-Hydroxy-naphthalin-3,8-sulfonsäureamide als Blaukuppler bekannt, für die jedoch entweder keine technischen Angaben gemacht werden oder solche, die nicht auf eine besondere Eignung schließen lassen. So werden sie als lichtbeständig, langsam kuppelnd mit blaß-blauer oder, in Kombination mit einem speziellen p-Amino-benzoldiazoniumsalz (Blausalz), mit schön blauer Farbe sowie als stark basisch charakterisiert.
- p-Aminobenzoldiazoniumsalze haben neben vielen Vorteilen auch einige gravierende Nachteile. So verfärbt sich bei der Aktenlagerung mit der Zeit der Hintergrund der Pausen, er vergilbt. Bei einer pH-Verschiebung, z. B. durch saure Dämpfe, verlieren die Farbstoffe ihren Kontrast und schlagen, ähnlich wie pH-Indikator-Farbstoffe, nach weinrot bis hellgelben Farbtönen um. Gerade bei den vielverwendeten, lichtempfindlichen p-Aminobenzoldiazoniumsalzen ist auch die thermische Stabilität begrenzt, was zu Kontrastverlusten bei der Lagerung von unbelichtetem Material führt.
- Es ist auch bekannt (US-PS 2,286,701), vornehmlich für Einkomponenten-Diazotypiematerialien p-Mercapto-2,5-di- alkoxy-benzoldiazoniumsalze zu verwenden. Aufgrund ihrer relativ hohen Kupplungsaktivität und der damit verbundenen unvorteilhaften Lagerfähigkeit, hat man sie lange Zeit als für Zweikomponenten-Materialien nicht geeignet angesehen. Kürzlich wurden Zweikomponenten-Diazotypiematerialien mit p-Mercapto-2,5-dialkoxybenzoldiazoniumsalzen bekannt, welche mit Phenolen als Gelbkupplern und Resorcylsäure oder Resorcylsäureamiden als Rotbraunkupplern zu interessanten, kontrastreichen Braunmarken mit besonders aktenfestem, hellem Pausengrund führen. Es war bisher aber nicht möglich, auch entsprechende Blau- oder Schwarzmarken zu entwickeln. Die üb- lichen Blaukuppler bilden mit p-Mercaptobenzoldiazoniumsalzen nur rotviolette bis violettblaue Farbstoffe und nicht die von den p-Aminobenzoldiazoniumsalzen her bekannten neutral blauen Farbtöne. Dabei ist die hohe Kupplungsaktivität und die Rotverschiebung der Farbstoffe typisch für p-Mercaptobenzoldiazoniumsalze.
- Schwarzeinstellungen werden in der Diazotypie durch Mischen von zwei oder mehr Kupplern erreicht (Kosar, Light-Sensitive Systems, Wiley & Sons, New York (1965), Seite 303). Hierfür ist es in der Regel nötig, einen wenig rotstichigen Blaukuppler einzusetzen, dessen Kupplungsgeschwindigkeit in einer ähnlichen Größenordnung liegt, wie die der beigemischten Gelb- und Braunkuppler.
- Es zeigte sich, daß keines der bekannten 2-Hydroxy-naphthalin-Derivate für Schwarzeinstellungen mit p-Mercaptobenzoldiazoniumsalzen geeignet ist. Die vielverwendeten 2-Hydroxy-naphthalin-3-carbonsäureamide zum Beispiel kuppeln zu schnell und bilden rotstichige Farbstoffe. Auch die als Kuppler bekannten 1-Hydroxy-naphthalin-Derivate, z. B. aus der DE-AS 10 68 555, kuppeln mit p-Mercaptobenzoldiazoniuasalzen zu weinroten Farbstoffen. Schließlich sind aus DE-AS 12 40 738 1-Hydroxy-4-alkyl-naphthalin-8-sulfonamid-Derivate als kontrastreiche Kuppler bekannt. Diese zeigen jedoch eine so hohe Kupplungsaktivität, daß mit p-Mercaptobenzoldiazoniumsalzen keine lagerfähigen, stabilen Diazotypiematerialien hergestellt werden können. In der DE-AS 20 00 819 werden 1-Hydroxy-naphthalin-3-sulfonsäure-8-sulfonsäureamidderivate als Blaukuppler, bevorzugt in Kombination mit p-Aminobenzoldiazoniumsalzen,beschrieben. In Kombination mit p-Mercaptobenzoldiazoniumsalzen bilden auch diese rotstichige, violette Farbstoffe, die weder für Blau- noch für Schwarzeinstellungen brauchbar sind. AusDE-AS 12 29 844 sind 1-Bydroxy-naphthalin-8-sulfonsäureamide, die weiter substituiert sein können, als Alkalispender in Diazotypiematerialien bekannt. Daß sie als Kuppler geeignet sind, läßt sich daraus keineswegs entnehmen. Streichlösungen mit den dort beschriebenen 1-Hydroxy-naphthalin-4,8-disulfonsäurediamiden dunkeln beim Stehen rasch und sind wenig-brauchbar. Ähnliches gilt für die in der DE-OS 17 72 697 beschriebenen 1-Hydroxy-naphthalin-4-sulfonsäure-8-sulfonamide.
- Aufgabe war es daher, Blaukuppler mit angepaßter Kupplungsaktivität zu finden, die mit p-Mercaptobenzoldiazoniumsalzen neutral-blaue Farbstoffe bilden, welche aufgrund dieser Eigenschaften auch für Schwarzeinstellungen geeignet sind.
- Gegenstand der Erfindung ist damit ein Zweikomponenten-Diazotypiematerial, bestehend aus einem Schichtträger und einer darauf aufgebrachten lichtempfindlichen Schicht, die als lichtempfindliche Komponente mindestens ein Benzoldiazoniumsalz und mindestens einen Kuppler enthält, gekennzeichnet durch die Kombination von mindestens einem 2,5-Dialkoxy-4-mercaptobenzoldiazoniumsalz und mindestens einer Verbindung der allgemeinen Formel
- Als Benzoldiazoniumsalz wird vorzugsweise ein 2,5-Dialkoxy-4-arylmercaptobenzoldiazoniumsalz, insbesondere 2,5-Diethoxy-4-p-tolylmercaptobenzoldiazoniumsalz eingesetzt, das in Form seines Tetrafluoborats, Sulfats oder Chlorids als Doppelsalz, z. B. mit Zinkchlorid, Verwendung findet.
- In der allgemeinen Formel bedeuten R1 und R2 vorzugsweise Alkyl oder Alkenyl, Aryl, Aralkyl oder Cycloalkyl mit bis zu 10 Kohlenstoffatomen, welche durch Alkyl oder Alkoxyl mit bis zu 4 Kohlenstoffatomen, durch Carboxyl, durch Acyl mit bis zu 3 Kohlenstoffatomen, durch Pbenoxy, durch Halogen, insbesondere Chlor oder Brom, durch Hydroxyl oder durch gegebenenfalls alkyl-substituiertes Amin substituiert sein können.
- Ganz besonders bewährt haben sich Verbindungen nach der allgemeinen Formel, in der R1 ein gegebenenfalls substituiertes Aryl und R2 ein gegebenenfalls substituiertes Alkyl, Alkenyl, Aralkyl oder Cycloalkyl darstellen..
- Überraschenderweise wurde gefunden, daß gerade die erfindungsgemäßen 1-Hydroxy-naphthalin-3,8-disulfonsäureamide in Kombination mit den p-Mercaptobenzoldiazoniumsalzen neutral-blaue Farbstoffe liefern. Außerdem wurde gefunden, daß die Kupplungsgeschwindigkeit dieser Verbindungen in ähnlicher Größenordnüng liegt wie die von Phenol- oder Res orcylsäurederivaten. Sie können damit in Kombination mit diesen Kupplern vorteilhaft zu Schwarzeinstellungen herangezogen werden.
- Die Synthese dieser Verbindungen erfolgt über das Naphtho- sulton-3-sulfochlorid, das in Friedländer, Fortschritte der Teerfarbenfabrikation, Berlin (1923), Teil 13, Seite 1108, beschrieben ist. Dieses setzt sich mit Ammoniak oder Aminen zu 1-Hydroxy-naphthalin-3,8-disulfonsäureamiden um. Da die 3-ständige Sulfonsäurechlorid-Gruppe aber reaktionsfähiger ist als die Sultongruppierung, können auch nacheinander Umsetzungen mit zwei verschiedenen Aminen durchgeführt werden. Zum Beispiel reagiert Naphthosulton-3-sulfochlorid bei Raumtemperatur mit überschüssigem Anilin quantitativ zu Naphthosulton-3-sulfonsäureanilid, und dieses reagiert wiederum bei Raumtemperatur mit Methylamin rasch und quantitativ zu 1-Hydroxy-naphthalin-3-sulfonsäureanilid-8-sulfonsäuremethylamid.
- Von der Art der Reste R1 und R2 ist die Löslichkeit in wäßrigen oder organischen Lösungsmitteln stark abhängig Einen gewissen Einfluß haben die Reste auch auf die Kupplungsgeschwindigkeit und den Farbton. So kuppeln zum Beispiel die 1-Hydroxy-naphthalin-3,8-di-(alkyl, aralkyl, alkenyl oder cycloalkyl)-sulfonamide etwas schneller und sind rotstichiger als die 1-Hydroxy-naphthalin-3-arylsulfonamido-8-alkylsulfonamide. Noch grünstichiger sind die 1-Hydroxy-naphthalin-3,8-di-(N-arylsulfonamide). Letztere sind weniger lichtbeständig und neigen etwas zur Lichtgilbung. Für Schwarzeinstellungen besonders geeignet sind 1-Hydroxy-naphthalin-3-arylsulfonamido-8-alkylsulfonamide wie 1-Hydroxy-naphthalin-3-p-tolylsulfonamido-8-h-butylsulfonamid.
- Amine, die für die Umsetzung geeignet sind, sind neben Ammoniak Alkylamine, z. B. Methylamine, Ethylamin, n oder iso Propylamin, Butylamin, 2-Ethylhexylamin oder Dezylamin, Alkenylamine, z. B. Allylamin, Aralkylamine, z. B. Benzylamin, Phenethylamin, Phenylbutylamin, Cycloalkylamine, z. B. Cyclohexylamin, Cyclooctylamin, 4-t-Butylcyclohexylamin, sowie Anilinderivate, die durch Amin, Alkyl, Alkoxy oder Halogen substituiert sein können, z. B. Toluidin, Xylidin, Difluoranilin, Tribromanilin, 4-Morpholino-2,5-dimethoxyanilin oder Aminoacetophenon. Auch die aliphatischen Reste können ohne Nachteil substituiert sein. Als preiswerte technische Amine bieten sich z. B. Ethanolamin, Hydroxypropylamin, Diethylaminoethylamin, Morpholinopropylamin, Pyrrolidinoethylamin, 4-Amino-(N-methylpyrrolidin), Piperidinobutylamin, Butoxypropylamin, Phenoxyethylamin oder Aminopropionsäure an.
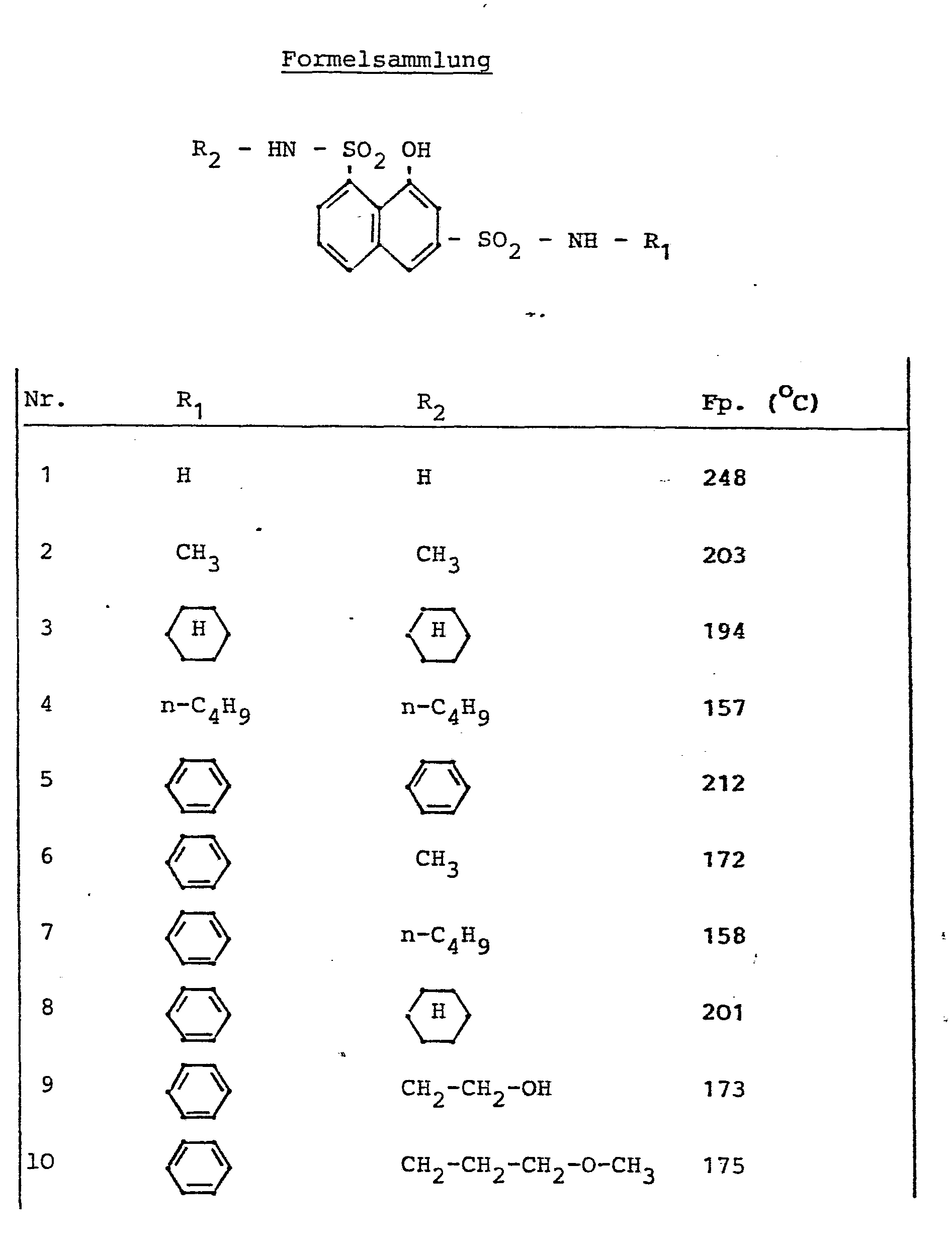
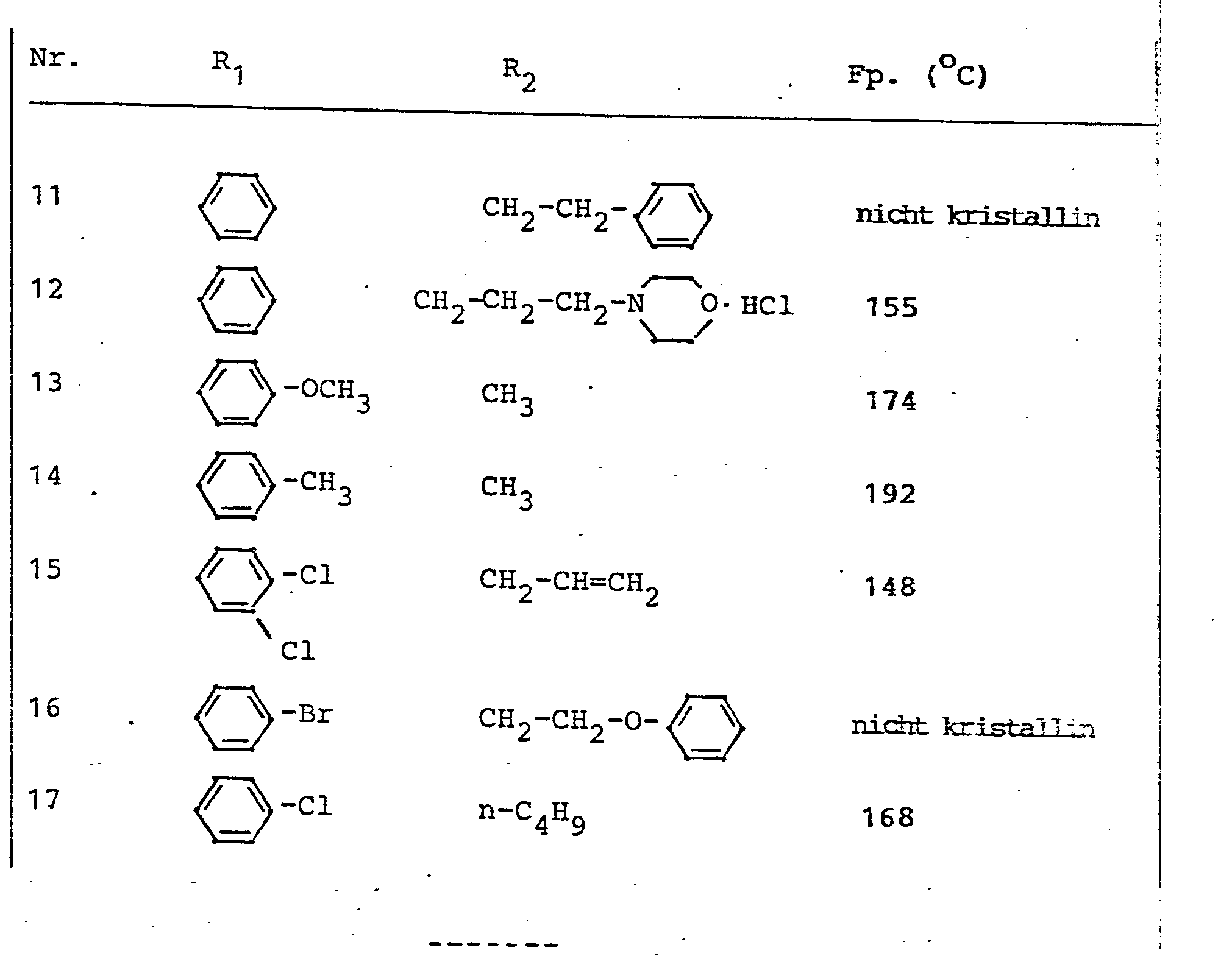
- Erfindungsgemäße Verbindungen sind beispielsweise der beigefügten Formelsammlung zu entnehmen.
- Als Träger kann z. B. Papier oder Folie verwendet werden, wobei die Lichtpausschicht bevorzugt in einer Lackschicht aus Celluloseester, z. B. Celluloseacetobutyrat dispergiert wird.
- Für Schwarzeinstellungen kommen zusätzlich einfache Phenolderivate, z. B. 2-Hydroxydiphenyl, 2,2'-Dihydroxydiphenyl, 2-Hydroxyethoxyphenol, 2-Hydroxybenzoesäureamid, 3,6-Dimethylphenol als Mannichbase oder Resorcylsäure mit ihren Derivaten, z. B. 2,4-Dihydroxybenzoesäure, 2,4-Dihydroxybenzoesäureamid, 2,4-Dihydroxybenzoesäureethanolamid oder 2,4-Dihydroxybenzoesäureethylester in Betracht.
- Die folgenden Beispiele dienen der weiteren Erläuterung der Erfindung, ohne den Erfindungsbereich hierauf zu begrenzen.
-
- Die Diazomenge ist so bemessen, daß der Kontrast bei den verschiedenen Mustern etwa gleich hoch ist. Mit einem Macbeth Quantalog-Densitometer TD-205 mit Wratten 106 Filter wird die Dichte bei frischem (I) und bei zwei, vier und sieben (II, III, IV) Tagen im forcierten Lagertest bei 60°C (Hot Box) gealtertem Material nach der der Belichtung unter einer Vorlage folgenden Entwicklung mit Ammoniak gemessen. Die in die folgende Tabelle aufgenommenen Werte zeigen, daß der Dichteabfall bei den p-Mercaptobenzoldiazoniumsalzen sehr viel geringer ist als bei den p-Aminobenzoldiazoniumsalzen.
-
- a) -2-Hydroxy-3-naiphthoesäure-toluidid (Naphthol AS-D)
- b) 2-Hydroxy-3-naphthoesäure-N-morpholinopregylamid (HCl-Salz)
- c) 1-Hydroxy-naphthalin-3-sulfonsäureethanolamid (entsprechend DE-AS 10 68 555)
- d) 1-Hydroxy-naphthalin-3-sulfonsäure-8-sulfcnsäure- amid (entsprechend DE-AS 20 00 819)
- e) 1-Hydroxy-naphthalin-3-sulfonsäure-8-sulfonsäuren-butylamid (entsprechend DE-AS 20 00 819)
- f) 1-Hydroxy-naphthalin-3,8-di(sulfonsäure-n-butylamid) (Formel 4)
- g) 1-Hydroxy-naphthalin-3-sulfonsäureanilid-8-sulfon- säurecyclohexylamid (Formel 8)
- h) 1-Hydroxy-naphthalin-3,8-di(suifonsäureanilid) (Formel 5)
- i) 1-Hydroxy-naphthalin-3-sulfonsäureanilid-8-sulfonsäure-γ-methoxypropylamid (Formel 10)
- Die Lösungen werden mit ca. 100 g Naßgewicht pro m2 auf Polyesterfolie aufgebracht und getrocknet. Dann werden die Folien unter einem Stufenkeil belichtet und anschließend mit Ammoniak entwickelt. Mit einem Hunterlab Color Difference-Meter D 25/D 28 mit Halogenlampe wird die Farbsättigung im Durchlicht gemessen. Bei konstantem L (Farbtiefe) = 44,0 wird das Verhältnis von Blau (-b) und Rot (+a) rechnerisch ermittelt, das für ein reines Blau mit wenig Rotanteil möglichst hoch liegen soll. Im folgenden sind für die Versuche a) .bis i) die Beschreibung des Farbtons und anschließend der -b/+a - Wert angegeben.
- Die erfindungsgemäßen Verbindungen ergeben wunschgemäße neutrale Blautöne. Beachtenswert ist, daß der Ersatz von einer Sulfonsäureamid- durch eine Sulfonsäureaniliägruppierung den Rotanteil im Farbstoff noch weiter reduziert.
-
- a) 1-Hydroxy-naphthalin-4-methyl-8-sulfonsäure-N-n-butylamid (entsprechend DE-AS 12 40 738)
- b) 1-Hydroxy-naphthalin-4-sulfonsäureanilid-8-sulfonsäure-N-methylamid (entsprechend DE-AS 12 29 844)
- c) 1-Hydroxy.-naphthalin-4,8-di(sulfonsäure-N-cyclo- hexylamid)
- d) 1-Hydroxy-naphthalin-4-sulfonsäure-8-sulfonsäureN-(ß-diethylaminoethylamid) (entsprechend DE-OS 17 72 697)
- e) 2-Hydroxy-naphthalin-4-sulfonsäure-8-sulfonsäureN-n-butylamid (entsprechend DE-AS 20 00 819)
- f) 1-Hydroxy-naphthalin-3-sulfonsäure-3',4'-dichlor- anilid-8-sulfonsäure-N-allylamid (Formel 15)
- g) 1-Hydroxy-naphthalin-3-sulfonsäure-p-anisidid-8-sulfonsäure-N-methylamid (Formel 13)
- h) 1-Hydroxy-naphthalin-3-sulfonsäure-p-toluidid-8-sulfonsäure-N-methylamid (Formel 14)
- Mit den Lösungen a) bis h) werden im ersten Fall sofort (A), im zweiten Fall nach 6 Stunden (B) und im dritten Fall nach 24 Stunden (C) je eine mit Celluloseacetopropionat lackierte Polyesterfolie beschichtet. Bereits die frischen Lösungen a - e sind erheblich dunkler als die Lösungen f - h und entsprechend ist der Pausengrund nach bildmäßiger Belichtung und Entwicklung bei den Materialien a - e von Anfang an dunkler. Nach in der Technik durchaus üblichem 6-stündigeni Stehen (B) werden mit den 1-Hydroxy-nachthalin-4,8-Derivaten keine brauchbaren Lichtpausfolien mehr erhalten. Der Pausengrund ist deutlich dunkel.
- Um dies in Zahlen auszudrücken; werden mit einem Hunterlab Modell D 25 die Helligkeit (L-Wert, maximal = 100) in Remission gemessen und in der folgenden Tabelle zusammengestellt:
- Nur die erfindungsgemäßen Materialien f - h sind bezüglich der Haltbarkeit und auch in bezug auf den Farbton als Schwarzmarken brauchbar.
-
- Nach bildmäßigem Belichten des fertigen Materials unter einer Bleistiftzeichnung auf Transparentpapier erhält man eine Kopie mit dunklen Linien auf hellgrauem Grund.
-
Claims (8)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AT80100807T ATE1398T1 (de) | 1979-02-26 | 1980-02-18 | Zweikomponenten-diazotypiematerial. |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19792907446 DE2907446A1 (de) | 1979-02-26 | 1979-02-26 | Zweikomponenten-diazotypiematerial |
| DE2907446 | 1979-02-26 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| EP0014982A2 true EP0014982A2 (de) | 1980-09-03 |
| EP0014982A3 EP0014982A3 (en) | 1981-01-21 |
| EP0014982B1 EP0014982B1 (de) | 1982-07-28 |
Family
ID=6063930
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP80100807A Expired EP0014982B1 (de) | 1979-02-26 | 1980-02-18 | Zweikomponenten-Diazotypiematerial |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US4273850A (de) |
| EP (1) | EP0014982B1 (de) |
| JP (1) | JPS55129338A (de) |
| AT (1) | ATE1398T1 (de) |
| DE (2) | DE2907446A1 (de) |
| DK (1) | DK79980A (de) |
| ES (1) | ES488914A0 (de) |
| FI (1) | FI68733C (de) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0161655A3 (en) * | 1984-05-18 | 1987-05-27 | Hoechst Aktiengesellschaft | Light-sensitive composition and two-component diazotype material prepared therefrom |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2903342A1 (de) * | 1979-01-29 | 1980-07-31 | Hoechst Ag | Derivate des 2-hydroxy-naphthalins |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NL51536C (de) * | 1939-06-08 | |||
| US2537098A (en) * | 1946-04-12 | 1951-01-09 | Gen Aniline & Film Corp | Sulfonamide azo coupling components used in diazo types |
| US2560137A (en) * | 1948-12-21 | 1951-07-10 | Gen Aniline & Film Corp | Diazotype photoprinting material |
| DE1068555B (de) * | 1957-02-04 | 1959-11-05 | ||
| GB1052977A (de) * | 1963-09-14 | |||
| GB1052978A (de) * | 1963-11-26 | |||
| GB1217294A (en) * | 1968-04-17 | 1970-12-31 | Ricoh Kk | Improvements in and relating to photosensitised materials |
| JPS4814255B1 (de) * | 1968-06-01 | 1973-05-04 | ||
| GB1278640A (en) * | 1969-01-09 | 1972-06-21 | Ricoh Kk | Improvements in and relating to photosensitive materials |
| US3761263A (en) * | 1971-11-03 | 1973-09-25 | Eastman Kodak Co | Diazotype compositions and photographic processes |
-
1979
- 1979-02-26 DE DE19792907446 patent/DE2907446A1/de not_active Withdrawn
-
1980
- 1980-02-18 DE DE8080100807T patent/DE3060684D1/de not_active Expired
- 1980-02-18 EP EP80100807A patent/EP0014982B1/de not_active Expired
- 1980-02-18 AT AT80100807T patent/ATE1398T1/de active
- 1980-02-22 FI FI800532A patent/FI68733C/fi not_active IP Right Cessation
- 1980-02-25 ES ES488914A patent/ES488914A0/es active Granted
- 1980-02-25 DK DK79980A patent/DK79980A/da not_active Application Discontinuation
- 1980-02-25 US US06/124,575 patent/US4273850A/en not_active Expired - Lifetime
- 1980-02-26 JP JP2231580A patent/JPS55129338A/ja active Granted
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0161655A3 (en) * | 1984-05-18 | 1987-05-27 | Hoechst Aktiengesellschaft | Light-sensitive composition and two-component diazotype material prepared therefrom |
Also Published As
| Publication number | Publication date |
|---|---|
| DE3060684D1 (de) | 1982-09-16 |
| ES8101784A1 (es) | 1980-12-16 |
| FI800532A7 (fi) | 1980-08-27 |
| EP0014982B1 (de) | 1982-07-28 |
| JPS55129338A (en) | 1980-10-07 |
| ES488914A0 (es) | 1980-12-16 |
| JPS6239727B2 (de) | 1987-08-25 |
| EP0014982A3 (en) | 1981-01-21 |
| FI68733B (fi) | 1985-06-28 |
| FI68733C (fi) | 1985-10-10 |
| US4273850A (en) | 1981-06-16 |
| DE2907446A1 (de) | 1980-09-04 |
| DK79980A (da) | 1980-08-27 |
| ATE1398T1 (de) | 1982-08-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE825204C (de) | Lichtempfindliches Material fuer das Diazotypieverfahren | |
| EP0014982B1 (de) | Zweikomponenten-Diazotypiematerial | |
| EP0004574B1 (de) | 2-Hydroxy-3-naphthoesäureamide und deren Verwendung als Kupplungskomponenten in Diazotypiematerialien | |
| DE1256065B (de) | Lichtempfindliches Material, das eine o-Aminobenzoldiazoverbindung enthaelt | |
| DE1174612B (de) | Diazotypiematerial | |
| DE2031602A1 (de) | Verfahren zum Stabilisieren photo graphischer Bilder | |
| DE815301C (de) | Verfahren zur Herstellung von Kopien auf Diazotypiematerial | |
| DE68923463T2 (de) | Wärmeempfindliche Aufzeichnungsmaterialien. | |
| DE1772017A1 (de) | Diazotypie-Materialien | |
| DE2123282A1 (de) | Wärmeempfindliches Kopiermaterial | |
| DE1962391C2 (de) | Benzoldiazoniumverbindungen und deren Verwendung | |
| DE1572088C3 (de) | Zweikomponenten-Diazotypiematerial für die Herstellung von Zwischenoriginalen | |
| DE2411825A1 (de) | Diazotypiematerial | |
| DE2021583C3 (de) | Photopolymerisierbares Gemisch | |
| DE3938763C1 (de) | ||
| DE2433072A1 (de) | Lichtempfindliches photographisches material | |
| EP0008472B1 (de) | Lichtempfindliche Benzoldiazoniumsalze und Diazotypiematerial unter Verwendung derselben | |
| DE694078C (de) | Lichtempfindliche Schichten | |
| DE881754C (de) | Lichtempfindliche Schichten | |
| DE1255486B (de) | Zweikomponenten-Diazotypiematerial | |
| DE2353470C2 (de) | ||
| AT229132B (de) | ||
| DE2202251A1 (de) | Diazoniumsalze | |
| AT225528B (de) | Lichtempfindliches Material | |
| CH513428A (de) | Strahlungsempfindliche Zusammensetzung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Designated state(s): AT BE CH DE FR GB IT NL SE |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Designated state(s): AT BE CH DE FR GB IT NL SE |
|
| 17P | Request for examination filed |
Effective date: 19810716 |
|
| ITF | It: translation for a ep patent filed | ||
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Designated state(s): AT BE CH DE FR GB IT NL SE |
|
| REF | Corresponds to: |
Ref document number: 1398 Country of ref document: AT Date of ref document: 19820815 Kind code of ref document: T |
|
| REF | Corresponds to: |
Ref document number: 3060684 Country of ref document: DE Date of ref document: 19820916 |
|
| PLBI | Opposition filed |
Free format text: ORIGINAL CODE: 0009260 |
|
| 26 | Opposition filed |
Opponent name: RENKER GMBH & CO. KG Effective date: 19830425 |
|
| PLBN | Opposition rejected |
Free format text: ORIGINAL CODE: 0009273 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: OPPOSITION REJECTED |
|
| 27O | Opposition rejected |
Effective date: 19840416 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19920115 Year of fee payment: 13 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: CH Payment date: 19920117 Year of fee payment: 13 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: SE Payment date: 19920120 Year of fee payment: 13 Ref country code: GB Payment date: 19920120 Year of fee payment: 13 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: AT Payment date: 19920122 Year of fee payment: 13 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: BE Payment date: 19920203 Year of fee payment: 13 |
|
| ITTA | It: last paid annual fee | ||
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: NL Payment date: 19920229 Year of fee payment: 13 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19920409 Year of fee payment: 13 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Effective date: 19930218 Ref country code: AT Effective date: 19930218 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Effective date: 19930219 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CH Effective date: 19930228 Ref country code: BE Effective date: 19930228 |
|
| BERE | Be: lapsed |
Owner name: HOECHST A.G. Effective date: 19930228 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19930901 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 19930218 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee | ||
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Effective date: 19931029 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19931103 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| EUG | Se: european patent has lapsed |
Ref document number: 80100807.9 Effective date: 19930912 |