EP0307836A2 - Wärmeempfindliches Aufzeichnungsmaterial - Google Patents
Wärmeempfindliches Aufzeichnungsmaterial Download PDFInfo
- Publication number
- EP0307836A2 EP0307836A2 EP88114852A EP88114852A EP0307836A2 EP 0307836 A2 EP0307836 A2 EP 0307836A2 EP 88114852 A EP88114852 A EP 88114852A EP 88114852 A EP88114852 A EP 88114852A EP 0307836 A2 EP0307836 A2 EP 0307836A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- group
- heat
- bis
- sensitive recording
- atom
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41M—PRINTING, DUPLICATING, MARKING, OR COPYING PROCESSES; COLOUR PRINTING
- B41M5/00—Duplicating or marking methods; Sheet materials for use therein
- B41M5/26—Thermography ; Marking by high energetic means, e.g. laser otherwise than by burning, and characterised by the material used
- B41M5/30—Thermography ; Marking by high energetic means, e.g. laser otherwise than by burning, and characterised by the material used using chemical colour formers
- B41M5/323—Organic colour formers, e.g. leuco dyes
- B41M5/327—Organic colour formers, e.g. leuco dyes with a lactone or lactam ring
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41M—PRINTING, DUPLICATING, MARKING, OR COPYING PROCESSES; COLOUR PRINTING
- B41M5/00—Duplicating or marking methods; Sheet materials for use therein
- B41M5/26—Thermography ; Marking by high energetic means, e.g. laser otherwise than by burning, and characterised by the material used
- B41M5/30—Thermography ; Marking by high energetic means, e.g. laser otherwise than by burning, and characterised by the material used using chemical colour formers
- B41M5/337—Additives; Binders
- B41M5/3377—Inorganic compounds, e.g. metal salts of organic acids
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B41—PRINTING; LINING MACHINES; TYPEWRITERS; STAMPS
- B41M—PRINTING, DUPLICATING, MARKING, OR COPYING PROCESSES; COLOUR PRINTING
- B41M5/00—Duplicating or marking methods; Sheet materials for use therein
- B41M5/26—Thermography ; Marking by high energetic means, e.g. laser otherwise than by burning, and characterised by the material used
- B41M5/30—Thermography ; Marking by high energetic means, e.g. laser otherwise than by burning, and characterised by the material used using chemical colour formers
- B41M5/323—Organic colour formers, e.g. leuco dyes
- B41M5/327—Organic colour formers, e.g. leuco dyes with a lactone or lactam ring
- B41M5/3275—Fluoran compounds
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S428/00—Stock material or miscellaneous articles
- Y10S428/913—Material designed to be responsive to temperature, light, moisture
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S428/00—Stock material or miscellaneous articles
- Y10S428/914—Transfer or decalcomania
Definitions
- the invention relates to a heat-sensitive recording material which has superior resistance to the effects of light, climate and oils and has better optical readability in the near infrared range.
- a heat-sensitive recording sheet is generally prepared by applying a coating composition to the surface of a support such as paper, synthetic paper, film, plastic, etc., which is obtained by finely grinding and dispersing a colorless chromogenic substance and a color developing material, mixing the dispersions obtained and Addition of a binder, filler, sensitizer, lubricant and other auxiliaries. Under the influence of heat from the thermal spring, thermal head, thermal stamp, laser beam, etc., an instantaneous chemical conversion takes place, which leads to the recording.
- a coating composition to the surface of a support such as paper, synthetic paper, film, plastic, etc.
- heat sensitive recording sheets include use in technical recording equipment, computer terminal printers, facsimile machine printers, ticket machines, bar code printer printers and the like. Recently, much higher and more diverse requirements have been placed on recording devices, which is why a high quality of the recording sheet is required.
- the rapid recording of the heat-sensitive recording sheet is said to have a clear high-density recording image even with little heat input, and it is also said to have superior resistance to the effects of light, climate and oils, that is, good durability.
- heat-sensitive recording sheets are used for heat-sensitive notes in which the color formation is restricted to the visible range. Therefore, when using a semiconductor laser as a bar code scanner of POS systems, etc., they were unsuitable for reading in the near infrared range.
- JA-OS 59-199757 and JA-OS 60-22681 have proposed heat-sensitive recording sheets in which a known color developing agent (acidic clay, phenolic resin, hydroxybenzoic acid ester, bisphenol-A) and a fluoranleuco dye are combined with superior color formation in the near IR range are.
- a known color developing agent acidic clay, phenolic resin, hydroxybenzoic acid ester, bisphenol-A
- fluoranleuco dye are combined with superior color formation in the near IR range are.
- JA-OS 62-243652, JA-OS 62-243653 and JA-OS 62-257970 describe heat-sensitive recording sheets in which a known color developing agent and a divinyl compound are combined with superior near-infrared color formation.
- the invention has for its object to provide a heat-sensitive recording material which is improved in the resistance to the action of light, climate and oils, and in the optical readability in the near infrared range, especially in bar code recordings.
- the dyes of the following general formula (IV) are preferred: wherein R1, R2, R3, R4, R5, R7, R8, R9, T1, T2, T3 and R4 have the meaning given above.
- R1, R2, R3, R4, R5, R7, R8, R9, T1, T2, T3 and R4 have the meaning given above.
- an alkyl group preferably has 1-8 carbon atoms and a cycloalkyl group 5-8 ring atoms.
- Aryl is preferably phenyl and naphthyl.
- fluorine leuco dyes is not particularly limited; you can use the following, for example: 2-methyl-6-p- (p-dimethylaminophenyl) aminoaniline fluoran, 2-methoxy-6-p- (p-dimethylaminophenyl) aminoanilinofluoran, 2-chloro-6-p- (p-dimethylaminophenyl) aminoanilinofluoran, p-nitro-6-p- (p-di ethylaminophenyl) amino-anilinofluoran, 2- Amino-6-p- (p-dimethylaminophenyl) aminoanilinofluoran, 2-diethylamino-6-p- (p-dimethylaminophenyl) aminoanilinofluoran, 2-phenyl-6-p- (p-phenylaminophenyl) aminoanilinofluoran, 2-benzyl-6-p - (p-phenyl) aminoaniline flu
- a C1-C12 alkyl group and a C1-C12 alkoxy group can be a straight or branched radical.
- Typical examples of an alkyl group with 1-12 carbon atoms and an alkoxy group with 1-12 carbon atoms are methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, sec-butyl -, hexyl, octyl, nonyl, dodecyl, methoxy, ethoxy, tert-butoxy group and the like.
- Typical examples of a C3-C10 cycloalkyl group are a cyclohexyl, 2-ethylcyclohexyl, p-tert-butylcyclohexyl group and the like.
- Halogen-substituted zinc benzoate derivatives which can be used according to the invention are colorless substances with high melting points and can be prepared by reacting a halogen-substituted sodium benzoate derivative with zinc sulfate.
- the stabilizer that can be used according to the invention is selected from several organic carboxylic acid metal salts.
- Benzoic acid zinc salts with 1 - 2 halogen atoms on the benzene ring show greater resistance to light, oils and climatic influences than organic carboxylic acids and their polyvalent metal salts.
- Halogen-substituted zinc benzoate derivatives which can be used according to the invention are, for example:
- Preferred examples of the organic color developing agent which can be used according to the invention are bisphenol A types, 4-hydroxybenzoic acid esters, 4-hydroxyphthalic diesters, phthalic acid monoesters, bis (hydroxyphenyl) sulfides, 4-hydroxyphenylarylsulfones, 4-hydroxyphenylarylsulfonates, 1,3-di- [2- (hydroxyphenyl) -2-propyl] benzene, 4-hydroxybenzoyloxybenzoic acid ester, bisphenolsulfones, etc.
- suitable compounds of this type are as follows:
- the above color developing agents can be used either alone or in combination.
- the fluoranleuco dye according to the invention can be used to further improve the optical readability in the near infrared range in combination with at least one substance from the group of the fluorene leuco dyes, divinylphthalide derivatives [in addition to those of the general formula (II)], sulfonylmethane derivatives, etc.
- the divinyl compounds according to the invention can of course also be used in combination with at least one substance from the group of the fluorene leuco dyes, fluoranleuco dyes [in addition to those of the general formula (I)], sulfonylmethane derivatives, etc.
- Preferred fluorene leuco dyes are the following near infrared absorbing leuco dyes of the general formula (VII): wherein R21, R22, R23, R24, R25 and R26 are the same or different and each represents a hydrogen atom, a C1-C8 alkyl group, a C5-C8 cycloalkyl group, a C3-C8 alkoxyalkyl group, a C3-C9 unsaturated alkyl group, one Tetrahydrofurfuryl group, a tetrahydropyran-2-methyl group, an alkyl group which can be substituted by a halogen atom, a C1-C4 alkyl group and / or a C1-C4 alkoxy group, an aryl group which by a halogen atom, a C1-C4 alkyl group and / or a C1-C4 alkoxy group can be substituted, or a C2-C8 alkyl group
- the selection of the leuco dye of the formula (VII) used according to the invention is not subject to any particular restrictions; you can use the following, for example: 3,6-bis (dimethylamino) fluorene-9-spiro-3 ′ - (6′-dimethylamino) phthalide and 3,6-bis (diethylamino) fluorene-9-spiro-3 ′ - (6 ′ -diethylamino) -phthalide.
- Preferred divinylphthalide derivatives are the following leuco dyes of the general formula (VIII) which absorb in the near infrared range: wherein R27, R28, R29 and R30 are the same or different and each have a C1-C8 alkyl group, a C5-C8 cycloalkyl group, a C3-C8 alkoxyalkyl group, a halogen atom, an aryl group, which is replaced by a halogen atom, a C1-C4- Alkyl group and / or a C1-C4-alkoxy group may be substituted, or a C1-C8-alkyl group which may be substituted by a halogen atom, a C1-C4-alkyl group and / or a C1-C4-alkoxy group; R27 and R28 or R29 and R30 optionally together or with an adjacent benzene ring a heterocyclic Can form a ring; and R31 and
- Preferred sulfonylmethane derivatives are the following leuco dyes of the general formula (IX) which absorb in the near infrared range: wherein R41, R42, R43 and R44 are the same or different and each represents a hydrogen atom or a substituted or unsubstituted alkyl group; R45 and R46 are the same or different and each represents a hydrogen atom or a substituted or unsubstituted one Represent phenyl group; and R47 represents a substituted or unsubstituted alkyl group, or a substituted or unsubstituted phenyl group.
- R41, R42, R43 and R44 are the same or different and each represents a hydrogen atom or a substituted or unsubstituted alkyl group
- R45 and R46 are the same or different and each represents a hydrogen atom or a substituted or unsubstituted one Represent phenyl group
- R47 represents a substituted or un
- sulfonylmethane derivatives which can be used according to the invention is not subject to any particular restrictions, for example the following can be used: Bis- (p-dimethylaminostyryl) -p-methylphenylsulfonylmethane, Bis- (p-diethylaminostyryl) -p-methylphenylmethane, Bis (p-dimethylaminostyryl) benzenesulfonylmethane.
- a sensitizer can be added to the color development layer according to the invention.
- Typical examples of such sensitizers are fatty acid amides, such as stearic acid amide, palmitic acid amide, etc., ethylene bisamide, montan wax, polyethylene wax, dibenzyl terephthalate, benzyl p-benzyloxybenzoate, di-p-tolyl carbonate, p-benzylbiphenyl, phenylnaphthoxynyl carbonate, 1,4-phenyl-1-phthalyl-1,4-phthalate -naphthoic acid phenyl ester etc.
- Binders according to the invention are, for example, completely saponified polyvinyl alcohol, degree of polymerization: 200-1900, partially saponified polyvinyl alcohol, carboxylated polyvinyl alcohol, amide-modified polyvinyl alcohol, sulfonic acid-modified polyvinyl alcohol, butyral-modified polyvinyl alcohol, other modified polyvinyl alcohols, hydroxyethyl cellulose, methyl cellulose styrene, methyl cellulose acid, carboxy Copolymers, cellulose derivatives such as ethyl cellulose and acetyl cellulose, polyvinyl chloride, polyvinyl acetate, polyacrylamide, polyacrylic acid ester, polyvinyl butyral, polystyrene, copolymers of the above compounds, polyamide resin, silicone resin, petroleum resin, terpene resin, ketone resin and coumarone resin.
- These high molecular weight Binders can be used after being dissolved in a solvent such
- the type and amount of the organic color developing agent according to the invention, the basic colorless chromogenic dye, the other additives which are determined depending on the desired effect and the suitability for recording purposes are not restricted.
- the heat-sensitive material according to the invention is produced by applying the coating composition to a base material such as paper, synthetic paper, film, plastic, etc.
- the organic color developing agent according to the invention, iron salt of a saturated higher fatty acid, the basic colorless chromogenic dye and optionally the other additives are ground to a particle size of several microns or smaller by means of a grinding device such as a ball mill, attritor, sand grinder, etc., or by means of a suitable emulsifying machine .
- a grinding device such as a ball mill, attritor, sand grinder, etc.
- Various additives are added to produce the coating composition of the invention.
- the additives which can be used according to the invention are, for example, the following: fillers; Release agents for preventing sheet sticking, such as metal salts of fatty acids; lubricant for mottling prevention such as fatty acid amide, ethylene bisamide, montan wax, polyethylene wax, etc .; Dispersants such as sodium dioctylsulfosuccinic acid, sodium dodecylbenzenesulfonate, sodium lauryl alcohol sulfate, sodium alginate, etc .; UV absorbers of the benzophenone and triazole series; Anti-foaming agents; Fluorescent dyes; water repellant, etc.
- both inorganic and organic fillers which are used in the paper processing industry can be used as the fillers according to the invention.
- the fillers according to the invention are alumina, talc, silicon dioxide, magnesium carbonate, aluminum hydroxide, magnesium hydroxide, barium sulfate, kaolin, titanium dioxide, zinc oxide, calcium carbonate, aluminum oxide, urea-formaldehyde resin, polystyrene resin, phenolic resin, etc.
- a cover layer e.g. be applied from a polymer.
- the reason for the superior optical readability of the heat-sensitive recording sheet according to the invention in the near infrared range is probably the following:
- the colored image of the recording sheet when using conventional, electron-donating color developing agents do not take up any light in the near infrared range.
- the fluoranleuco dyes of the general formula (I) according to the invention or the divinyl compounds of the general formula (II) according to the invention absorb during color development in the heat-melting reaction in the presence of an electron acceptor particularly strong in the near infrared range (especially in the range of 700 - 1500 nm).
- a heat sensitive recording sheet consists of a basic colorless dye as an electron donor and an organic acidic substance, e.g. a phenolic compound, aromatic carboxylic acid, organic sulfonic acid, etc.
- the heat-melting reaction is a kind of acid-base reaction based on electron donation and uptake, thereby forming a metastable charge transfer complex, which leads to the colored image .
- each of the halogen atoms is bonded directly to a benzene nucleus and, because of its strong electron attraction, leads to a decrease in the electron density on the metal via the mediation of the ⁇ electrons of the benzene ring.
- zinc is a transition metal atom with an empty d-orbital and, in contrast to other polyvalent metals (magnesium, aluminum, calcium, titanium, manganese, tin and nickel), takes up electrons more easily.
- the halogen-substituted zinc benzoate derivative therefore leads to the strengthening of the chemical bond between an organic color developing agent and the fluoranleuco dye according to the invention or the divinyl compound according to the invention. Therefore, it is believed that the chemical bond even under the influence of light, heat Moisture etc. is not dissolved for a long time, so that the recording image is very stable and the optical readability in the near infrared region is not reduced.
- the reason for the better thermal responsiveness is based on the fact that halogen-substituted zinc benzoate derivatives have a superior color development ability and, because of their synergism with another color development agent, lead to an increase in color development sensitivity.
- Stabilizer (see Table I) 4.0 parts 10% aqueous solution of polyvinyl alcohol 9.2 parts Water 5.2 parts
- a heat-sensitive coating composition is obtained:
- Solution A (dye dispersion) 9.2 parts
- Solution B (color developing agent dispersion) 36.0 parts
- Solution C (stabilizer dispersion) 18.4 parts Kaolin clay (50% aqueous dispersion) 12.0 parts.
- This coating composition was applied in a coating amount of 6.0 g / m 2 on a base paper with a weight of 50 g / m 2, dried and supercalendered in order to achieve a smoothness of 200-600 s.
- a heat sensitive recording sheet was obtained.
- Solution A (dye dispersion 1) 4.6 parts Solution D (dye dispersion 2) 4.6 parts Solution C (stabilizer dispersion) 18.4 parts Solution B (color developing agent dispersion) 36.0 parts Kaolin clay (50% aqueous dispersion) 12.0 parts
- This coating composition was applied in a coating amount of 6.0 g / m2 on a base paper with a weight of 50 g / m2, dried and supercalendered to achieve a smoothness of 200-600 s.
- a heat sensitive recording sheet was obtained.
- a heat-sensitive recording sheet was obtained in the same manner as in Example 1, except that Solution C was not used.
- Color developing agent (see Table III) 6.0 parts 10% aqueous solution of polyvinyl alcohol 18.8 parts Water 11.2 parts
- Stabilizer (see Table III) 4.0 parts 10% aqueous solution of polyvinyl alcohol 9.2 parts Water 5.2 parts
- the solutions of the above compositions were individually milled in a attritor to a particle size of 1 ⁇ m.
- the solutions were mixed together in the following proportions; a heat-sensitive coating composition is obtained.
- Solution A (dye dispersion) 9.2 parts
- Solution B (color developing agent dispersion) 36.0 parts
- Solution C (stabilizer dispersion) 18.4 parts Kaolin clay (50% aqueous dispersion) 12.0 parts
- This coating composition was applied in a coating amount of 6.0 g / m2 on a base paper with a weight of 50 g / m2, dried and supercalendered to achieve a smoothness of 200-600 s.
- a heat sensitive recording sheet was obtained.
- a heat-sensitive recording sheet was obtained in the same manner as in Example 3, except that Solution C was not used.
- Example 3 10th 4,4'-isopropylidenediphenol Z-salt of p-chlorobenzoic acid 3,3-bis [2- (p-dimethylaminophenyl) -2- (p-methoxyphenyl) ethenyl] -4,5,6,7-tetrabromophthalide 1.50 1.19 11 4,4'-isopropylidenediphenol Zinc salt of m-chlorobenzoic acid 3,3-bis [2- (p-dimethylaminophenyl) -2- (p-methoxyphenyl) ethenyl] -4,5,6,7-tetrabromophthalide 1.49 1.18 12 1,7-di (4-hydroxyphenylthio) 3,5-dioxaheptane Z
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Inorganic Chemistry (AREA)
- Heat Sensitive Colour Forming Recording (AREA)
Abstract
Description
- Die Erfindung betrifft ein wärmeempfindliches Aufzeichnungsmaterial, das überlegene Beständigkeit gegenüber den Einwirkungen von Licht, Klima und Ölen aufweist sowie bessere optische Lesbarkeit im nahen Infrarot-Bereich besitzt.
- Ein wärmeempfindliches Aufzeichnungsblatt wird im allgemeinen hergestellt, indem man auf die Oberfläche eines Trägers, wie Paier, synthetisches Papier, Film, Kunststoff usw. eine Beschichtungsmasse aufbringt, die man durch Feinvermahlen und Dispergieren eines farblosen chromogenen Stoffes und eines Farbentwicklungsmaterials, Vermischen der erhaltenen Dispersionen und Zugabe eines Bindemittels, Füllstoffs, Sensibilisators, Gleitmittels und anderer Hilfsmittel erhält. Unter der Wärmeeinwirkung von Thermofeder, Thermokopf, Thermostempel, Laserstrahl usw. erfolgt eine augenblickliche chemische Umsetzung, die zur Aufzeichnung führt.
- Die vielfältigen praktischen Verwendungen dieser wärmeempfindlichen Aufzeichnungsblätter umfassen die Anwendung bei technischen Aufzeichnungsgeräten, Terminaldruckern von Computern, Druckern von Faksimiliermaschinen, Fahrscheinautomaten, Druckern für Strichcode-Zettel und dergleichen. In letzter Zeit werden wesentlich höhere und vielfältigere Anforderungen an Aufzeichnungsvorrichtungen gestellt, deshalb ist eine hohe Qualität des Aufzeichnungsblattes erforderlich. Beispielsweise soll bei der raschen Aufzeichnung des wärmeempfindlichen Aufzeichnungsblattes ein deutliches Aufzeichnungsbild mit hoher Dichte sogar bei geringer Wärmezufuhr haben, und es soll weiter überlegene Beständigkeit gegenüber Einwirkungen von Licht, Klima und Ölen, d.h. gute Haltbarkeit haben.
- Diese wärmeempfindlichen Aufzeichnungsblätter werden für wärmeempfindliche Zettel verwendet, bei denen die Farbbildung auf dem sichtbaren Bereich beschränkt ist. Daher waren sie bei der Verwendung eines Halbleiter-Lasers als Strichcode-Scanner von POS-Systemen usw. ungeeignet für das Lesen im nahen Infrarot-Bereich.
- Dagegen sind in JA-OS 59-199757 und JA-OS 60-22681 wärmeempfindliche Aufzeichnungsblätter vorgeschlagen worden, bei denen ein bekanntes Farbentwicklungsmittel (saurer Ton, Phenolharz, Hydroxybenzoesäureester, Bisphenol-A) und ein Fluoranleukofarbstoff mit überlegener Farbbildung im nahen IR-Bereich kombiniert sind.
- Die JA-OS 62-243652, JA-OS 62-243653 und JA-OS 62-257970 beschreiben wärmeempfindliche Aufzeichnungsblätter, bei denen ein bekanntes Farbentwicklungsmittel und eine Divinylverbindung mit überlegener Farbbildung im nahen Infrarot-Bereich kombiniert sind.
- Da diese wärmeempfindlichen Aufzeichnungsblätter jedoch zu Aufzeichnungen schlechter Haltbarkeit (schlechter Beständigkeit gegenüber Licht, Klima und Ölen) führen, verfärbt sich das Bild, die Bilddichte nimmt ab oder das Bild verlöscht. Die optische Lesbarkeit im Infrarot-Bereich nimmt daher erheblich ab, wenn man die Blätter lange Zeit unter der Einwirkung von Licht, Hitze, Feuchtigkeit usw. aufbewahrt.
- Auch wenn Hautabsonderungen am Aufzeichnungsbild haften, oder Weichmacher (DOP, DOA usw.) aus einer Verpackungsfolie, wie Polyvinylchloridfolien, damit in Berührung kommen, wird die Bilddichte erheblich verringert oder das Bild verlöscht. Daher wird die optische Lesbarkeit im nahen Infrarot-Bereich beträchtlich erniedrigt. Die obigen Nach teile machen die praktische Verwendung der wärmeempfindlichen Aufzeichnungsblätter schwierig.
- Der Erfindung liegt die Aufgabe zugrunde, ein wärmeempfindliches Aufzeichnungsmaterial zu schaffen, das in der Beständigkeit gegenüber der Einwirkung von Licht, Klima und Ölen, und in der optischen Lesbarkeit im nahen Infrarot-Bereich, insbesondere bei Strichcode-Aufzeichnungen, verbessert ist.
- Diese Aufgabe wird erfindungsgemäß wie folgt gelöst. Ein wärmeempfindliches Aufzeichnungsmaterial wird hergestellt, indem man eine wärmeempfindliche Farbentwicklungsschicht auf einen Träger aufbringt, wobei die wärmeempfindliche Farbentwicklungsschicht einen basischen farblosen oder schwach farbigen chromogenen Farbstoff und ein organisches Farbentwicklungsmittel enthält, das dadurch gekennzeichnet ist, daß die wärmeempfindliche Farbentwicklungsschicht als basischen farblosen chromogenen Farbstoff mindestens einen Farbstoff aus der Gruppe:
- a) der Fluoranleukofarbstoffe der folgenden allgemeinen Formel (I):
die anderen Reste unter R₁, R₂, R₃, R₄, R₅, R₆, R₇, R₈ und R₉ gleich oder verschieden sind, und jeweils ein Wasserstoff- oder Halogenatom, eine Alkyl-, Alkoxy-, Cycloalkyl-, Nitro-, Hydroxy-, Amino-, substituierte Amino-, Aralkyl-, substituierte Aralkyl-, Aryl- oder substituierte Arylgruppe bedeuten;
T₁, T₂ und T₃ gleich oder verschieden sind und jeweils ein Wasserstoffatom, eine C₁-C₈ Alkyl-, C₃-C₉-Alkenyl- oder C₃-C₉-Alkinylgruppe bedeuten;
T₄ ein Wasserstoffatom, eine C₁-C₈-Alkyl-, C₃-C₉-Alkenyl-, C₃-C₉-Alkinyl oder Phenylgruppe bedeutet; oder
T₃ und T₄ mit einem benachbarten Stickstoffatom verbunden sein können und dabei eine Morpholino-, Pyrrolidino-, Piperidino- oder Hexamethyleniminogruppe bilden; und
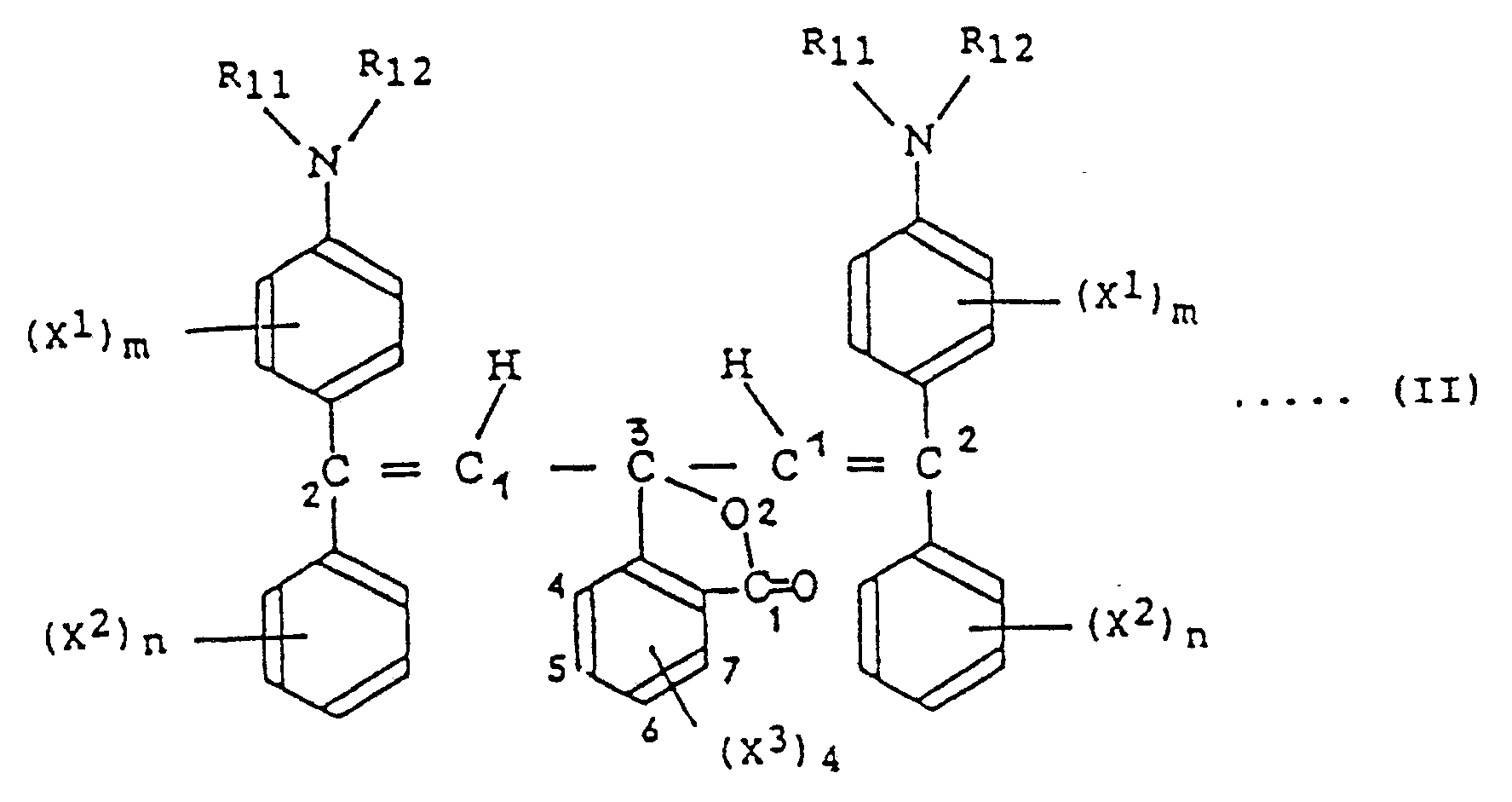
n eine ganze Zahl von 0 bis 4 bedeutet; - b) und/oder der Divinylverbindungen der folgenden allgemeinen Formel (II):
R₁₁ eine Alkylgruppe mit 8 oder weniger C-Atomen bedeutet;
R₁₂ eine Alkylgruppe mit 8 oder weniger C-Atomen, eine C₅-C₇. Cycloalkylgruppe oder eine Benzyl- oder Phenylgruppe, die gegebenenfalls durch ein Chlor- oder Bromatom oder ein C₁-C₄-Alkyl substituiert werden kann,
bedeutet;
X¹ und X² gleich oder verschieden sind und jeweils eine Alkylgruppe mit 8 oder weniger C-Atomen, eine Alkoxygruppe mit 8 oder weniger C-Atomen, ein Fluor-, Chlor- oder Bromatom bedeuten;
m und n gleich oder verschieden sind und jeweils eine ganze Zahl 0, 1, 2 oder 3 bedeuten;
jedes X¹ in (X¹)m gleich oder verschieden ist;
jedes X² in (X²)n gleich oder verschieden ist;
und jedes X³ in (X³)₄ gleich oder verschieden ist, und ein Chlor- oder Bromatom bedeutet, wobei mindestens ein X³ ein Bromatom bedeutet;
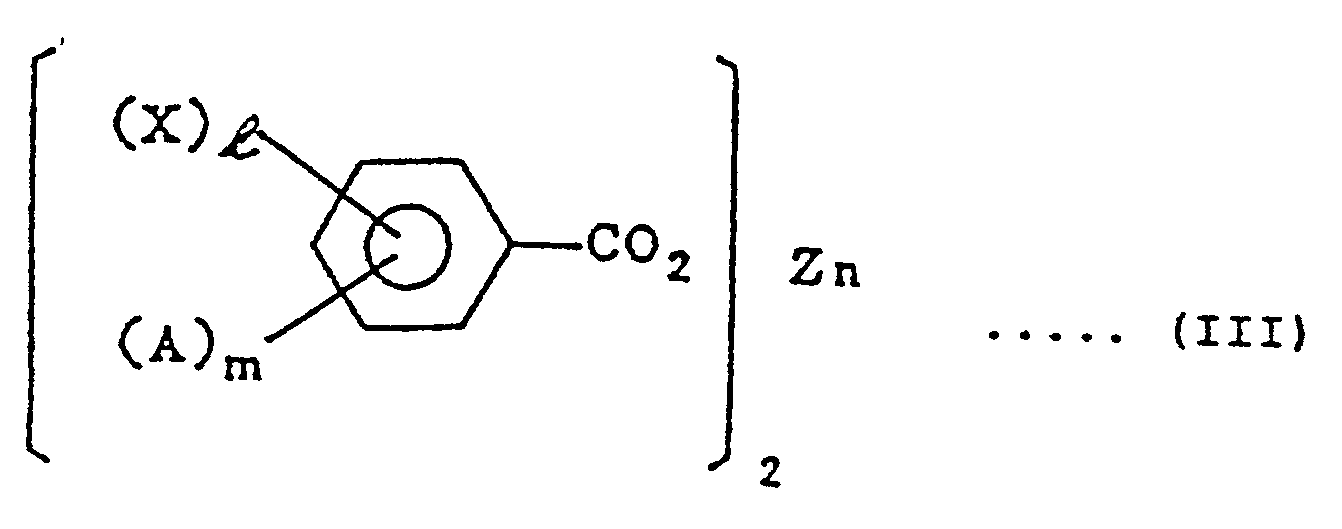
und als Stabilisator ein halogensubstituiertes Zinkbenzoat der folgenden allgemeinen Formel (III):
X ein Halogenatom bedeutet;
A ein Wasserstoffatom, eine Nitro-, C₁-C₁₂-Alkyl-, C₁-C₁₂-Alkoxy-, C₃-C₁₀-Cycloalkyl-, Cyano- oder Hydroxygruppe bedeutet;
l eine ganze Zahl 1 oder 2 bedeutet; und
m eine ganze Zahl von 0 bis 5 bedeutet,
enthält. - Von den Fluoranleukofarbstoffen der allgemeinen Formel (I) sind die Farbstoffe der folgenden allgemeinen Formel (IV) bevorzugt:
Soweit nicht anders angegeben, weist in den hierin angegebenen Formeln eine Alkylgruppe vorzugsweise 1 - 8 Kohlenstoffatome und eine Cycloalkylgruppe 5 - 8 Ringatome auf. Aryl steht vorzugsweise für Phenyl und Naphthyl. Unter Berücksichtigung der Produktivität, Kosten und Leistungsfähigkeit sind 2-Methyl-6-p-(p-dimethylaminophenyl)-aminoanilinofluoran (Schmelzpunkt: 197- 203°C) der folgenden Formel (V) und 2-Chlor-3-methyl-6-p-(p-phenylaminophenyl)-aminoanilinofluoran (Schmelzpunkt: 191,5 - 196°C) der folgenden Formel (VI) am stärksten bevorzugt: - Die Wahl der erfindungsgemäßen Fluoranleukofarbstoffe ist nicht besonders beschränkt; man kann z.B. folgende verwenden:
2-Methyl-6-p-(p-dimethylaminophenyl)-aminoanilinfluoran, 2-Methoxy-6-p-(p-dimethylaminophenyl)aminoanilinofluoran, 2-Chlor-6-p-(p-dimethylaminophenyl)aminoanilinofluoran, p-Nitro-6-p-(p-di äthylaminophenyl)amino-anilinofluoran, 2-Amino-6-p-(p-dimäthylaminophenyl)aminoanilinofluoran, 2-Diäthylamino-6-p-(p-dimäthylaminophenyl)aminoanilinofluoran, 2-Phenyl-6-p-(p-phenylaminophenyl)aminoanilinofluoran, 2-Benzyl-6-p-(p-phenylaminophenyl)aminoanilinofluoran, 2-Hydroxy-6-p-(p-phenylaminophenyl)aminoanilinofluoran, 3-Methyl-6-p-(p-dimethylaminophenyl)aminoanilinofluoran, 3-Diäthylamino-6-p-(p-diäthylaminophenyl)aminoanilinofluoran, 3-Diäthylamino-6-p-(p-dibutylaminophenyl)aminoanilino-fluoran, 3-Methyl-7-p-(p-dimethylaminophenyl)aminoanilinofluoran, 3-Methoxy-7-p-(p-dimethylaminophenyl)aminoanilinofluoran, 3-Chlor-7-p-(p-dimethylaminophenyl)aminoanilinofluoran, 3-Nitro-7-p-(p-diäthylaminophenyl)aminoanilinofluoran 3-Amino-7-p-(p-diäthylaminophenyl)aminoanilinofluoran, 3-Diäthylamino-7-p-(p-diäthylaminophenyl)aminoanilino-fluoran, 3-Phenyl-7-p-(p-phenylaminophenyl)aminoanilinofluoran, 3-Benzyl-7-p-(p-phenylaminophenyl)aminoanilinofluoran, 3-Hydroxy-7-p-(p-phenylaminophenyl)aminoanilinofluoran, 2-Methyl-7-p-(p-dimethylaminophenyl)aminoanilinofluoran, 2-Diäthylamino-7-p-(p-diäthyl aminophenyl)aminoanilinofluoran, 2-Diäthylamino-7-p-(p-dibutylaminophenyl)aminoanilinofluoran, 2-p-(p-dimethylaminophenyl)aminoanilino-6-methylfluoran, 2-p-(p-Dimethylaminophenyl)aminoanilino-6-methoxyfluoran, 2-p-(p-Dimethylaminophenyl)aminoanilino-6-chlorfluoran, 2-p-(p-diäthylaminophenyl)aminoanilino-6-nitrofluoran, 2-p-(p-diäthylaminophenyl)aminoanilino-6-aminofluoran, 2-p-(p-diäthylaminophenyl)aminoanilino-6-diäthylaminofluoran,
2-p-(p-Phenylaminophenyl)aminoanilino-6-phenylfluoran, 2-p-(p-Phenylaminophenyl)aminoanilino-6-benzylfluoran, 2-p-(p-Phenylaminophenyl)aminoanilino-6-hydroxyfluoran, 2-p-(p-Dimethylaminophenyl)aminoanilino-6-methylfluoran, 2-p-(p-Diäthylaminophenyl)aminoanilino-6-diäthylfluoran, 2-p-(p-Phenylaminophenyl)aminoanilino-6-diäthylaminofluoran,
3-p-(p-Dimethylaminophenyl)aminoanilino-7-methylfluoran, 3-p-(p-Dimethylaminophenyl)aminoanilino-7-methoxyfluoran, 3-p-(p-Dimethylaminophenyl)aminoanilino-7-chlorfluoran, 3-p-(p-Diäthylaminophenyl)aminoanilino-7-nitrofluoran, 3-p-(p-Diäthylaminophenyl)aminoanilino-7-aminofluoran, 3-p-(p-Diäthylaminophenyl)aminoanilino-7-diäthylaminofluoran,
3-p-(p-Phenylaminophenyl)aminoanilino-7-phenylfluoran, 3-p-(p-Phenylaminophenyl)aminoanilino-7-benzylfluoran, 3-p-(p-Phenylaminophenyl)aminoanilino-7-hydroxyfluoran, 3-p-(p-Dimethylaminophenyl)aminoanilino-7-methylfluoran, 3-p-(p-Diäthylaminophenyl)aminoanilino-7-diäthylaminofluoran, und
3-p-(p-Phenylaminophenyl)aminoanilino-7-diäthylaminofluoran. -
- Unter Berücksichtigung der Produktivität, Kosten und Leistungsfähigkeit sind von den Divinylverbindungen der allgemeinen Formel (II) 3,3-Bis-[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl)-ethenyl]-4,5,6,7-tetrabromphthalid (Schmelzpunkt: 133 - 135°C) am stärksten bevorzugt.
- In der allgemeinen Formel (III) können eine C₁ -C₁₂-Alkylgruppe und eine C₁-C₁₂-Alkoxygruppe ein gerader oder verzweigter Rest sein. Typische Beispiele für eine Alkylgruppe mit 1 - 12 C-Atomen und eine Alkoxygruppe mit 1 - 12 C-Atomen sind eine Methyl-, Ethyl-, n-Propyl-, Isopropyl-, n-Butyl-, Isobutyl-, sek.-Butyl-, Hexyl-, Octyl-, Nonyl-, Dodecyl-, Methoxy-, Ethoxy-, tert.-Butoxygruppe und dergleichen. Typische Beispiele für eine C₃-C₁₀-Cycloalkylgruppe sind eine Cyclohexyl-, 2-Ethylcyclohexyl-, p-tert.-Butylcyclohexylgruppe und dergleichen.
- Erfindungsgemäß anwendbare halogensubstituierte Zinkbenzoatderivate sind farblose Substanzen mit hohen Schmelzpunkten und können durch Umsetzung eines halogensubstituierten Natriumbenzoatderivates mit Zinksulfat hergestellt werden.
- Der erfindungsgemäß anwendbare Stabilisator ist aus mehreren organischen Carbonsäuremetallsalzen ausgewählt. Benzoesäurezinksalze, mit 1 - 2 Halogenatomen am Benzolring zeigen größere Beständigkeit gegenüber Licht, Ölen und Klimaeinflüssen als organische Carbonsäuren und ihre mehrwertigen Metallsalze.
-
- Bevorzugte Beispiele für das erfindungsgemäß anwendbare organische Farbentwicklungsmittel sind Bisphenol-A-Typen, 4-Hydroxybenzoesäureester, 4-Hydroxyphthalsäurediester, Phthalsäuremonoester, Bis- (hydroxyphenyl)-sulfide, 4-Hydroxyphenylarylsulfone, 4-Hydroxyphenylarylsulfonate, 1,3-Di-[2-(hydroxyphenyl)-2-propyl]-benzol, 4-Hydroxybenzoyloxybenzoesäureester, Bisphenolsulfone usw.. Beispiele für geeignete Verbindungen dieser Art sind folgende:
- 4,4′-Isopropylidendiphenol
4,4′-Cyclohexylidendiphenol
p,p′-(1-Methyl-normalhexyliden)diphenol
1,7-Di(4-hydroxyphenylthio)-3,5-Dioxaheptan
- 4-Hydroxybenzoesäurebenzylester
4-Hydroxybenzoesäureäthylester
4-Hydroxybenzoesäurepropylester
4-Hydroxybenzoesäureisopropylester
4-Hydroxybenzoesäurebutylester
4-Hydroxybenzoesäureisobutylester
4-Hydroxybenzoesäuremethylbenzylester
- 4-Hydroxyphthalsäuredimethylester
4-Hydroxyphthalsäurediisopropylester
4-Hydroxyphthalsäuredibenzylester
4-Hydroxyphthalsäuredihexylester
- Phthalsäuremonobenzylester
Phthalsäuremonocyclohexylester
Phthalsäuremonophenylester
Phthalsäuremonomethylphenylester
Phthalsäuremonoethylphenylester
Phthalsäuremonoalkylbenzylester
Phthalsäuremonohalogenbenzylester
Phthalsäuremonoalkoxybenzylester
- Bis-(4-hydroxy-3-tert.-butyl-6-methylphenyl)sulfid
Bis-(4-Hydroxy-2,5-dimethylphenyl)sulfid
Bis-(4-hydroxy-2-methyl-5-ethylphenyl)sulfid
Bis-(4-hydroxy-2-methyl-5-isopropylphenyl)sulfid
Bis-(4-hydroxy-2,3-dimethylphenyl)sulfid
Bis-(4-hydroxy-2,5-diethylphenyl)sulfid
Bis-(4-hydroxy-2,5-diisopropylphenyl)sulfid
Bis-(4-hydroxy-2,3,6-trimethylphenyl)sulfid
Bis-(2,4,5-trihydroxyphenyl)sulfid
Bis-(4-hydroxy-2-cyclohexyl-5-methylphenyl)sulfid
Bis-(2,3,4-trihydroxyphenyl)sulfid
Bis-(4,5-dihydroxy-2-tert-butylphenyl)sulfid
Bis-(4-hydroxy-2,5-diphenylphenyl)sulfid
Bis-(4 hydroxy-2-tert.-octyl-5-methylphenyl)sulfid
- 4-Hydroxy-4′-isopropoxydiphenylsulfon
4-Hydroxy-4′-methyldiphenylsulfon
4-Hydroxy-4′-n-butyloxydiphenlysulfon
- 4-Hydroxyphenylbenzolsulfonat
4-Hydroxyphenyl-p-tolylsulfonat
4-Hydroxyphenylmethylensulfonat
4-Hydroxyphenyl-p-chlorbenzolsulfonat
4-Hydroxyphenyl-p-tert-butylbenzolsulfonat
4-Hydroxyphenyl-p-isopropoxybenzolsulfonat
4-Hydroxyphenyl-1′-naphthalinsulfonat
4-Hydroxyphenyl-2′-naphthalinsulfonat
- 1,3-Di(2-(4-hydroxyphenyl)-2-propyl)-benzol
1,3-Di(2-(4-hydroxy-3-alkylphenyl)-2-propyl)-benzol
1,3-Di(2-(2,4′-dihydroxyphenyl)-2-propyl)-benzol
1,3-Di(2-(2-hydroxy-5-methylphenyl)-2-propyl)-benzol
- 1,3-Dihdroxy-6(α,α-dimethylbenzyl)-benzol
- 4-Hydroxybenzoyloxybenzoesäure-Benzylester
4-Hydroxybenzoyloxybenzoesäure-Methylester
4-Hydroxybenzoyloxybenzoesäure-Äthylester
4-Hydroxybenzoyloxybenzoesäure-Propylester
4-Hydroxybenzoyloxybenzoesäure-Butylester
4-Hydroxybenzoyloxybenzoesäure-Isopropylester
4-Hydroxybenzoyloxybenzoesäure-tert-Butylester
4-Hydroxybenzoyloxybenzoesäure-Hexylester
4-Hydroxybenzoyloxybenzoesäure-Octylester
4-Hydroxybenzoyloxybenzoesäure-Nonylester
4-Hydroxybenzoyloxybenzoesäure-Cyclohexylester
4-Hydroxybenzoyloxybenzoesäure-β-Phenäthylester
4-Hydroxybenzoyloxybenzoesäure-Phenylester
4-Hydroxybenzoyloxybenzoesäure-α-Naphtylester
4-Hydroxybenzoyloxybenzoesäure-β-Naphtylester
4-Hydroxybenzoyloxybenzoesäure-sec-Butylester
- Bis-(3-1-butyl-4-hydroxy-6-mehtylphenyl)sulfon
Bis-(3-äthyl-4-hydroxyphenyl)sulfon
Bis-(3-propyl-4-hydroxyphenyl)sulfon
Bis-(3-methyl-4-hydroxyphenyl)sulfon
Bis-(2-isopropyl-4-hydroxyphenyl)sulfon
Bis-(2-äthyl-4-hydroxyphenyl)sulfon
Bis-(3-chlor-4-hydroxyphenyl)sulfon
Bis-(2,3-dimethyl-4-hydroxyphenyl)sulfon
Bis-(2,5-dimethyl-4-hydroxyphenyl)sulfon
Bis-(3-methoxy-4-hydroxyphenyl)sulfon
4-Hydroxyphenyl-2′-äthyl-4′-hydroxyphenylsulfon
4-Hydroxyphenyl-2′-isopropyl-4′-hydroxyphenylsulfon
4-Hydroxyphenyl-3′-isopropyl-4′-hydroxyphenylsulfon
4-Hydroxyphenyl-3′-sec-butyl-4′-hydroxyphenylsulfon
3-Chlor-4-hydroxyphenyl-3′-isopropyl-hydroxyphenylsulfon
2-Hydroxy-5-t-butylphenyl-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-aminophenyl-4′-hydroxyphenylsulfon
2-Hydroxy-5-isopropylphenyl-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-octylphenyl-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-butylphenyl-3′-chlor-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-butylphenyl-3′-methyl-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-butylphenyl-3′-isopropyl-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-butylphenyl-3′-chlor-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-butylphenyl-3′-methyl-4′-hydroxyphenylsulfon 2-Hydroxy-5-t-butylphenyl-3′-isopropyl-4′-hydroxyphenylsulfon
2-Hydroxy-5-t-butylphenyl-2′-methyl-4′-hydroxyphenylsulfon
- 4,4′-Sulfonyldiphenol
2,4′-Sulfonyldiphenol
3,3′-Dichlor-4,4′-sulfonyldiphenol
3,3′-Dibromo-4,4′-sulfonyldiphenol
3,3′;5,5′-Tetrabromo-4,4′-sulfonyldiphenol
3,3′-Diamino-4,4′-sulfonyldiphenol
- p-tert.-Butylphenol
2,4-Dihydroxybenzophenon
Novolak-Phenolharz
4-Hydroxyphenylacetat
p-Phenylphenol
Benzyl-4-hydroxyphenylacetat
p-Benzylphenol.
- Die vorstehenden Farbentwicklungsmittel können entweder allein oder in Kombination verwendet werden.
- Der erfindungsgemäße Fluoranleukofarbstoff kann zur weiteren Verbesserung der optischen Lesbarkeit im nahen Infrarot-Bereich in Kombination mit mindestens einer Substanz aus der Gruppe der Fluorenleukofarbstoffe, Divinylphthalidderivate [zusätzlich zu denen der allgemeinen Formel (II)], Sulfonylmethanderivate usw. verwendet werden. Natürlich können auch die erfindungsgemäßen Divinylverbindungen in Kombination mit mindestens einer Substanz aus der Gruppe der Fluorenleukofarbstoffe, Fluoranleukofarbstoffe [zusätzlich zu denen der allgemeinen Formel (I)], Sulfonylmethanderivate, usw. verwendet werden.
- Bevorzugte Fluorenleukofarbstoffe sind folgende im nahen Infrarot absorbierende Leukofarbstoffe der allgemeinen Formel (VII):
R₂₁, R₂₂, R₂₃, R₂₄, R₂₅ und R₂₆ gleich oder verschieden sind und jeweils ein Wasserstoffatom, eine C₁-C₈-Alkylgruppe, eine C₅-C₈-Cycloalkylgruppe, eine C₃-C₈-Alkoxyalkylgruppe, eine C₃-C₉-ungesättigte Alkylgruppe, eine Tetrahydrofurfurylgruppe, eine Tetrahydropyran-2-methylgruppe, eine Alkylgruppe, die durch ein Halogenatom, eine C₁-C₄-Alkylgruppe und/oder eine C₁-C₄-Alkoxygruppe substituiert werden kann, eine Arylgruppe, die durch ein Halogenatom, eine C₁-C₄-Alkylgruppe und/oder eine C₁-C₄-Alkoxygruppe substituiert werden kann, oder eine C₂-C₈-Alkylgruppe mit einer Phenoxygruppe, die durch ein Halogenatom, eine C₁-C₄-Alkylgruppe und/oder eine C₁-C₄-Alkoxygruppe substituiert werden kann, bedeuten;
und wobei
R₂₁ und R₂₂, R₂₃ und R₂₄ oder R₂₅ und R₂₆ gegebenenfalls miteinander oder mit einem benachbarten Benzolring einen heterocyclischen Ring bilden können. - Die Auswahl des erfindungsgemäß verwendeten Leukofarbstoffs der Formel (VII) unterliegt keinen besonderen Einschränkungen; man kann z.B. folgende verwenden:
3,6-Bis-(dimethylamino)-fluoren-9-spiro-3′-(6′-dimethylamino)-phthalid und 3,6-Bis-(diethylamino)-fluoren-9-spiro-3′-(6′-diethylamino)-phthalid. - Bevorzugte Divinylphthalidderivate sind folgende im nahen Infrarot-Bereich absorbierende Leukofarbstoffe der allgemeinen Formel (VIII):
R₂₇, R₂₈, R₂₉ und R₃₀ gleich oder verschieden sind und jeweils eine C₁-C₈-Alkylgruppe, eine C₅-C₈-Cycloalkylgruppe, eine C₃-C₈-Alkoxyalkylgruppe, ein Halogenatom, eine Arylgruppe, die durch ein Halogenatom, eine C₁-C₄-Alkylgruppe und/oder eine C₁-C₄-Alkoxygruppe substituiert sein kann, oder eine C₁-C₈-Alkylgruppe, die durch ein Halogenatom, eine C₁-C₄-Alkylgruppe und/oder eine C₁-C₄-Alkoxygruppe substituiert sein kann, bedeuten;
R₂₇ und R₂₈ oder R₂₉ und R₃₀ gegebenenfalls miteinander oder mit einem benachbarten Benzolring einen heterocyclischen Ring bilden können; und
R₃₁ und R₃₂ gleich oder verschieden sind und jeweils ein Wasserstoffatom, ein Halogenatom, eine C₁-C₄-Alkylgruppe, eine C₁-C₄-Alkoxygruppe, oder eine Acyloxygruppe bedeuten; R₃₃ ein Wasserstoffatom oder eine C₁-C₄-Alkylgruppe bedeutet;
a, b, c und/oder d jeweils ein Kohlenstoffatom bedeuten können, wobei ein oder zwei der Kohlenstoffatome durch ein Stickstoffatom ersetzt sein können; jedes dieser Kohlenstoffatome mit einem Wasserstoffatom, einem Halogenatom, einer C₁-C₈-Alkylgruppe, einer C₁-C₄ Alkoxygruppe, einer C₂-C₁₆-Dialkylaminogruppe oder einer Nitrogruppe verbunden sein kann; und eine Bindung von a-b, b-c oder c-d Bestandteil eines anderen aromatischen Ringes sein kann. - Bevorzugte Sulfonylmethanderivate sind folgende im nahen Infrarot-Bereich absorbierenden Leukofarbstoffe der allgemeinen Formel (IX):
R₄₁, R₄₂, R₄₃ und R₄₄ gleich oder verschieden sind und jeweils ein Wasserstoffatom oder eine substituierte oder unsubstituierte Alkylgruppe bedeuten;
R₄₅ und R₄₆ gleich oder verschieden sind und jeweils ein Wasserstoffatom oder eine substituierte oder unsubstituierte Phenylgruppe bedeuten; und
R₄₇ eine substituierte oder unsubstituierte Alkylgruppe, oder eine substituierte oder unsubstituierte Phenylgruppe bedeutet. - Die Auswahl der erfindungsgemäß verwendbaren Sulfonylmethanderivate unterliegt keinen besonderen Einschränkungen, man kann z.B. folgende verwenden:
Bis-(p-dimethylaminostyryl)-p-methylphenylsulfonylmethan,
Bis-(p-diethylaminostyryl)-p-methylphenylmethan,
Bis-(p-dimethylaminostyryl)-benzolsulfonylmethan. - Weiterhin kann ein Sensibilisator zur erfindungsgemäßen Farbentwicklungsschicht zugegeben werden. Typische Beispiele für solche Sensibilisatoren sind Fettsäureamide, wie Stearinsäureamid, Palmitinsäureamid usw., Ethylenbisamid, Montanwachs, Polyethylenwachs, Terephthalsäuredibenzylester, p-Benzyloxybenzoesäurebenzylester, Di-p-tolylcarbonat, p-Benzylbiphenyl, Phenylnaphthylcarbonat, 1,4-Diethoxynaphthalin, 1-Hydroxy-2-naphthoesäurephenylester usw.
- Erfindungsgemäße Bindemittel sind z.B. vollständig verseifter Polyvinylalkohol, Polymerisationsgrad: 200 - 1900, teilweise verseifter Polyvinylalkohol, carboxylierter Polyvinylalkohol, amidmodifizierter Polyvinylalkohol, sulfonsäuremodifizierter Polyvinylalkohol, butyralmodifizierter Polyvinylalkohol, andere modifizierte Polyvinylalkohole, Hydroxyethylcellulose, Methylcellulose, Carboxymethylcellulose, Styrol-Maleinsäureanhydrid-Copolymere, Styrol-Butadien-Copolymere, Cellulosederivate, wie Ethylcellulose und Acetylcellulose, Polyvinylchlorid, Polyvinylacetat, Polyacrylamid, Polyacrylsäureester, Polyvinylbutyral, Polystyrol, Copolymere von obigen Verbindungen, Polyamidharz, Silikonharz, Petroleumkunstharz, Terpenharz, Ketonharz und Cumaronharz. Diese hochmolekularen Bindemittel können verwendet werden, nachdem sie in einem Lösungsmittel, wie Wasser, Alkohol, Keton, Ester, Kohlenwasserstoff usw. gelöst oder in Wasser oder Lösungsmittel emulgiert oder dispergiert wurden.
- Die Art und Menge des erfindungsgemäßen organischen Farbentwicklungsmittels, des basischen farblosen chromogenen Farbstoffs, der anderen Additive, die je nach dem gewünschten Effekt und der Eignung für Aufzeichnungszwecke bestimmt werden, sind nicht beschränkt. Im allgemeinen ist es vorteilhaft, 1 - 8 Gew.-Teile des erfindungsgemäßen organischen Farbentwicklungsmittels, 0,1 - 5 Gew.-Teile Stabilisator und 1 - 20 Gew.-Teile Füllstoff, bezogen auf 1 Gew.-Teil des basischen farblosen chromogenen Farbstoffs, und 10 - 25 Gew.-Teile Bindemittel, bezogen auf den Gesamtfeststoffgehalt, zu verwenden.
- Das erfindungsgemäße wärmeempfindliche Material wird hergestellt, indem man die Beschichtungsmasse auf ein Basismaterial, wie Papier, synthetisches Papier, Film, Kunststoff usw. aufträgt.
- Das erfindungsgemäße organische Farbentwicklungsmittel, Eisensalz einer gesättigten höheren Fettsäure, der basische farblose chromogene Farbstoff und gegebenenfalls die anderen Additive werden mittels einer Mahlvorrichtung, wie Kugelmühle, Reibmühle, Sandschleifmaschine usw., oder mittels einer geeigneten Emulgiermaschine bis zu einer Teilchengröße von mehreren Mikron oder kleiner zermahlen. Hierzu gibt man verschiedene Additive, um die erfindungsgemäße Beschichtungsmasse herzustellen.
- Die erfindungsgemäß anwendbaren Additive sind z.B. folgende: Füllstoffe; Trennmittel für die Verhütung des Anhaftens eines Blattes, wie Metallsalze von Fettsäuren; Gleitmittel zur Mottling-Verhinderung, wie Fettsäureamid, Ethylenbisamid, Montanwachs, Polyethylenwachs usw.; Dispergiermittel, wie Dioctylsulfobernsteinsäurenatriumsalz, Natriumdodecylbenzolsulfonat, Natriumlaurylalkoholsulfat, Natriumalginat usw.; UV-Absorptionsmittel der Benzophenon- und Triazolreihe; Antischaummittel; Fluoreszenzfarbstoffe; wasserabweisende Mittel usw..
- Als die erfindungsgemäßen Füllstoffe können sowohl anorganische als auch organische Füllstoffe, die in der Papierverarbeitungsindustrie angewendet werden, verwendet werden. Beispiele für die erfindungsgemäßen Füller sind Tonerde, Talkum, Siliziumdioxid, Magnesiumcarbonat, Aluminiumhydroxid, Magnesiumhydroxid, Bariumsulfat, Kaolin, Titandioxid, Zinkoxid, Calciumcarbonat, Aluminiumoxid, Harnstoff-Formaldehydharz, Polystyrolharz, Phenolharz usw..
- Zur weiteren Verbesserung der Haltbarkeit kann eine Deckschicht Z.B. aus einem Polymerisat aufgebracht werden.
- Die Ursache für die überlegene optische Lesbarkeit des erfindungsgemäßen wärmeempfindlichen Aufzeichnungsblattes im nahen Infrarot-Bereich ist wahrscheinlich folgende:
- Das gefärbte Bild des Aufzeichnungsblattes bei Verwendung herkömmlicher, Elektronen abgebender Farbentwicklungsmittel, z.B. aus der Fluoranreihe, nehmen kein Licht im nahen Infrarot-Bereich auf. Die erfindungsgemäßen Fluoranleukofarbstoffe der allgemeinen Formel (I) oder die erfindungsgemäßen Divinylverbindungen der allgemeinen Formel (II) absorbieren jedoch bei der Farbentwicklung bei der Hitzeschmelzreaktion in Gegenwart eines Elektronenakzeptors im nahen Infrarot-Bereich (besonders im Bereich von 700 - 1500 nm) besonders stark.
- Die Ursache für die überlegene Beständigkeit gegenüber Licht, Öl und Klimaeinflüssen ist wahrscheinlich folgende:
- Im allgemeinen besteht ein wärmeempfindliches Aufzeichnungsblatt aus einem basischen farblosen Farbstoff als Elektronendonator und einer organischen sauren Substanz, z.B. einer phenolischen Verbindung, aromatischen Carbonsäure, organischen Sulfonsäure usw.. Die Hitzeschmelzreaktion ist eine Art von Säure-Base-Reaktion, die sich auf eine Elektronenabgabe und -aufnahme gründet, wodurch ein metastabiler Charge-Transfer-Komplex gebildet wird, was zum gefärbten Bild führt.
- Andererseits ist die chemische Bindung bei der obigen chemischen Reaktion zwischen einem organischen Farbentwicklungsmittel und dem erfindungsgemäßen Fluoranleukofarbstoff sehr schwach. Bei dem erfindungsgemäßen halogensubstituierten Zinkbenzoatderivat ist jedes der Halogenatome unmittelbar mit einem Benzolkern gebunden und führt wegen seiner starken Elektronenanziehungskraft zur Abnahme der Elektronendichte am Metall über die Vermittlung der π-Elektronen des Benzolrings. Weiter ist Zink ein Übergangsmetallatom mit einem leeren d-Orbital und nimmt dadurch im Gegensatz zu anderen mehrwertigen Metallen (Magnesium, Aluminium, Calcium, Titan, Mangan, Zinn und Nickel) Elektronen leichter auf. Bei der Hitzereaktion führt das halogensubstituierte Zinkbenzoatderivat deshalb zur Verstärkung der chemischen Bindung zwischen einem organischen Farbentwicklungsmittel und dem erfindungsgemäßen Fluoranleukofarbstoff oder der erfindungsgemäßen Divinylverbindung. Daher wird vermutet, daß die chemische Bindung sogar unter Einwirkung von Licht, Hitze Feuchtigkeit usw. lange Zeit nicht gelöst wird, so daß das Aufzeichnungsbild sehr stabil ist, und die optische Lesbarkeit im nahen Infrarot-Bereich nicht verringert wird.
- Die Ursache für die bessere thermische Ansprechbarkeit gründet sich darauf, daß halogensubstituierte Zinkbenzoatderivate eine überlegene Farbentwicklungsfähigkeit besitzt und aufgrund ihres Synergismus mit einem anderen Farbentwicklungsmittel zur Erhöhung der Farbentwicklungssensibilität führt.
- Die Erfindung wird durch folgende Beispiele erläutert. Als Abkürzung für Gewichtsteile wird "Teile" verwendet.
- Basischer, farbloser chromogener Farbstoff (s. Tabelle I) 2,0 Teile
10%ige wäßrige Lösung von Polyvinylalkohol 4,6 Teile
Wasser 2,6 Teile
- 4,4′-Isopropylidendiphenol 6,0 Teile
10%ige wäßrige Lösung von Polyvinylalkohol 18,8 Teile
Wasser 11,2 Teile
- Stabilisator (s. Tabelle I) 4,0 Teile
10%ige wäßrige Lösung von Polyvinylalkohol 9,2 Teile
Wasser 5,2 Teile
- Die Lösungen der obigen Zusammensetzungen wurden in einer Reibmühle einzeln bis zur Teilchengröße von 1 µm vermahlen. Die Lösungen wurden im folgenden Verhältnis miteinander vermischt. Man erhält dabei eine wärmeempfindliche Beschichtungsmasse:
- Lösung A (Farbstoffdispersion) 9,2 Teile
Lösung B (Farbentwicklungsmitteldispersion) 36,0 Teile
Lösung C (Stabilisatordispersion) 18,4 Teile
Kaolinton (50%ige wäßrige Dispersion) 12,0 Teile.
- Diese Beschichtungsmasse wurde in einer Beschichtungsmenge von 6,0 g/m² auf ein Basispapier mit einem GEwicht von 50 g/m² aufgetragen, getrocknet und superkalandriert, um eine Glätte von 200 - 600 s einzustellen. Man erhielt ein wärmeempfindliches Aufzeichnungsblatt.
- Basischer, farbloser chromogener Farbstoff 1 (s. Tabelle I) 1,0 Teil
10%ige wäßrige Lösung von Polyvinylalkohol 2,3 Teile
Wasser 1,3 Teile
- Basischer, farbloser chromogener Farbstoff 1 (s. Tabelle I) 1,0 Teil
10%ige wäßrige Lösung von Polyvinylalkohol 2,3 Teile
Wasser 1,3 Teile.
Die Lösungen der obigen Zusammensetzungen wurden in einer Reibmühle einzeln bis zur Teilchengröße von 1 µm vermahlen. Die Lösungen wurden im folgenden Verhältnis miteinander vermischt; man erhält dabei eine wärmeempfindliche Beschichtungsmasse. - Lösung A (Farbstoffdispersion 1) 4,6 Teile
Lösung D (Farbstoffdispersion 2) 4,6 Teile
Lösung C (Stabilisatordispersion) 18,4 Teile
Lösung B (Farbentwicklungsmitteldispersion) 36,0 Teile
Kaolinton (50%ige wäßrige Dispersion) 12,0 Teile
- Diese Beschichtungsmasse wurde in einer Beschichtungsmenge von 6,0 g/m² auf ein Basispapier mit einem Gewicht von 50 g/m² aufgetragen, getrocknet und superkalandriert, um eine Glätte von 200 - 600 s einzustellen. Man erhielt ein wärmeempfindliches Aufzeichnungsblatt.
- Man erhielt in der gleichen Weise wie im Beispiel 1 ein wärmeempfindliches Aufzeichnungsblatt, wobei man jedoch Lösung C nicht verwendet.
- Die in den Beispielen und Vergleichsbeispielen erhaltenen Aufzeichnungsblätter wurden hinsichtlich der Qualität überprüft. Die Ergebnisse sind in den Tabellen I und II zusammengefaßt.
TABELLE I Prüfungsergebnisse Versuch Nr. Stabilisator Basischer farbloser chromogener Farbstoff 1 Basischer farbloser chromogener Farbstoff 2 Bilddichte statisch (1) dynamisch (2) Beispiel 1 1 Zinksalz der p-Chlorbenzoesäure 2-Chlor-3-methyl-6-p-(p-phenylaminophenyl)aminoanilinofluoran --- 1.38 0.74 2 Zinksalz der p-Chlorbenzoesäure 2-Methyl-6-p-(p-dimethylaminophenyl)aminoanilinofluoran --- 1.37 0.75 Beispiel 2 3 Zinksalz der p-Chlorbenzoesäure 2-Chlor-3-methyl-6-p-(p-phenylaminophenyl)aminoanilinofluoran 3,6-Bis(dimethylamino)fluoren-9-spiro-3′-(6′-dimethylamio)phthalid 1.30 0.72 4 Zinksalz der m-Chlorbenzoesäure 2-Methyl-6-p-(p-dimethylamiophenyl)aminoanilinofluoran 3,6-Bis(dimethylamino)fluoren-9-spiro-3′-(6′-dimethylamio)phthalid 1.31 0.73 5 Zinksalz der 3,4-di-Chlorbenzoesäure 2-Chlor-3-methyl-6-p-(p-phenylaminophenyl)aminoanilinofluoran 3,3-Bis(1,1-bis(4-pyrrolidinophenyl)äthylen-2-yl]-4,5,6,7-tetrachlorphthalid 1.29 0.71 6 Zinksalz der 3,4-di-Chlorbenzoesäure 2-Methyl-6-p-(p-dimethylaminophenyl)aminoanilinofluoran 3,3-Bis(1,1-bis(4-pyrrolidinophenyl)äthylen-2-yl]-4,5,6,7-tetrachlorphthalid 1.29 0.72 Vergleichsbeispiel 1 7 --- 2-Chlor-3-methyl-6-p-(p-phenylaminophenyl)aminoanilinofluoran --- 1.25 0.74 8 --- 2-Methyl-6-p-(p-dimethylaminophenyl)aminoanilinofluoran --- 1.24 0.73 9 --- 3,6-Bis(dimethylamino)fluoren-9-spiro-3′-(6′-dimethylamino)phthalid --- 1.13 0.71 TABELLE II Prüfungsergebnisse Versuch Nr. Reflexionsgrad des infraroten Lichtes (%) (3) Beständigkeit gegenüber Licht (4) Beständigkeit gegenüber Ölen (5) Beständigkeit gegenüber Klimaeinflüssen (6) Vor Behandlung Nach Behandlung Restprozent (%) Reflexionsgrad des infraroten Lichtes (%) Vor Behandlung Nach Behandlung Restprozent (%) Reflexionsgrad des infraroten Lichtes (%) Vor Behandlung Nach Behandlung Restprozent (%) Reflexionsgrad des infraroten Lichtes (%) Beispiel 1 1 25 0.74 0.74 100 25 0.74 0.72 97 28 0.74 0.73 99 26 2 26 0.75 0.7 100 26 0.75 0.74 99 27 0.75 0.73 97 27 Beispiel 2 3 22 0.72 0.72 100 22 0.72 0.70 98 24 0.72 0.71 99 23 4 22 0.73 0.73 100 22 0.73 0.71 97 24 0.73 0.71 97 24 5 21 0.71 0.70 99 21 0.71 0.70 99 23 0.71 0.70 99 23 6 21 0.72 0.71 99 21 0.72 0.71 99 23 0.72 0.70 98 23 Vergleichsbeispiel 1 7 35 0.74 0.65 88 49 0.74 0.36 49 75 0.74 0.58 78 57 8 34 0.73 0.64 87 50 0.73 0.36 49 74 0.73 0.57 78 55 9 35 0.71 0.30 42 80 0.71 0.10 14 99 0.71 0.40 56 73 -
- (1) Statische Bilddichte: Ein wärmeempfindliches Aufzeichnungsblatt wird 5 s unter einem Druck von 10 g/cm² gegen eine auf 135°C erhitzte Platte gepreßt. Die statische Bilddichte wird mit einem Macbeth-Dichtemesser (RD-914, Verwendung des Amber-Filters, unten gelten die gleichen Bedingungen) bestimmt.
- (2) Dynamische Bilddichte: Ein wärmeempfindliches Aufzeichnungsblatt wird bei einer angelegten Spannung von 18,03 V und einer Pulsbreite von 3,2 Millisekunden unter Verwendung einer Faksimiliermaschine KB-4800 (von TOSHIBA CORPORATION) aufgezeichnet und mit einem Macbeth-Dichtemesser bestimmt.
- (3) Reflexionsgrad des infraroten Lichtes (%): Der Reflexionsgrad des durch die obige Anmerkung (1) aufgezeichneten Teils wird mit einem Spektrophotometer bei einer Wellenlänge von 940 nm gemessen.
- (4) Beständigkeit gegenüber Licht: Das gemäß obiger Anmerkung (2) aufgezeichnete Bild wird als Bilddichte vor der Behandlung bezeichnet. Die Aufzeichnung wird 2 Stunden mit dem Licht eines Fade-O-Meters bestrahlt.
- (5) Beständigkeit gegenüber Ölen: Die gemäß obiger Anmerkung (2) aufgezeichnete Bilddichte wird als Bilddichte vor der Behandlung definiert. Ein Tropfen Rizinusöl wird auf die Aufzeichnung getröpfelt, nach 10 s mit einem Filterpapier abgewischt und 24 h stehengelassen. Danach wird die Bilddichte (nach der Ölbehandlung) gemessen. Der Restprozentsatz wird nach folgender Formel berechnet:
- (6) Beständigkeit gegenüber Klimaeinflüssen: Das gemäß obiger Anmerkung (2) behandelte wärmeempfindliche Blatt wird 1 Woche lang bei 40°C und 90% relativer Luftfeuchtigkeit stehengelassen und dann mit einem Macbeth-Dichtemesser gemessen. Der Restprozentsatz wird nach folgender Formel berechnet:
- Basischer farbloser chromogener Farbstoff (s. Tabelle III) 2,0 Teile
10%ige wäßrige Lösung von Polyvinylalkohol 4,6 Teile
Wasser 2,6 Teile
- Farbentwicklungsmittel (s. Tabelle III) 6,0 Teile
10%ige wäßrige Lösung von Polyvinylalkohol 18,8 Teile
Wasser 11,2 Teile
- Stabilisator (s. Tabelle III) 4,0 Teile
10%ige wäßrige Lösung von Polyvinylalkohol 9,2 Teile
Wasser 5,2 Teile
- Die Lösungen der obigen Zusammensetzungen wurden in einer Reibmühle einzeln bis zur Teilchengröße von 1 µm vermahlen. Die Lösungen wurden in folgenden Verhältnissen miteinander vermischt; man erhält dabei eine wärmeempfindliche Beschichtungsmasse.
- Lösung A (Farbstoffdispersion) 9,2 Teile
Lösung B (Farbentwicklungsmitteldispersion) 36,0 Teile
Lösung C (Stabilisatordispersion) 18,4 Teile
Kaolinton (50%ige wäßrige Dispersion) 12,0 Teile
- Diese Beschichtungsmasse wurde in einer Beschichtungsmenge von 6,0 g/m² auf ein Basispapier mit einem Gewicht von 50 g/m² aufgetragen, getrocknet und superkalandriert, um eine Glätte von 200 - 600 s einzustellen. Man erhielt ein wärmeempfindliches Aufzeichnungsblatt.
- Man erhielt in der gleichen Weise wie im Beispiel 3 ein wärmeempfindliches Aufzeichnungsblatt, wobei man jedoch Lösung C nicht verwendet.
- Die in dem Beispiel 3 und Vergleichsbeispiel 2 erhaltenen Aufzeichnungsblätter wurden hinsichtlich der Qualität geprüft, die Ergebnisse sind in den Tabellen III und IV zusammengefaßt.
TABELLE III Prüfungsergebnisse Versuch Nr. Farbentwicklungsmittel Stabilisator Basischer farbloser Farbstoff Bilddichte Statisch (1) Dynamisch (2) Beispiel 3 10 4,4′-Isopropylidendiphenol Zinksalz der p-Chlorbenzoesäure 3,3-Bis[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl) äthenyl]-4,5,6,7-tetrabromphthalid 1.50 1.19 11 4,4′-Isopropylidendiphenol Zinksalz der m-Chlorbenzoesäure 3,3-Bis[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl)äthenyl]-4,5,6,7-tetrabromphthalid 1.49 1.18 12 1,7-Di(4-hydroxyphenylthio)3,5-dioxaheptan Zinksalz der p-Chlorbenzoesäure 3,3-Bis[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl)äthenyl]-4,5,6,7-tetrabromphthalid 1.51 1.19 13 1,8-Di-(4-hydroxyphenylthio)3,6-dioxaoctan Zinksalz der m-Chlorbenzoesäure 3,3-Bis[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl)äthenyl]-4,5,6,7-tetrabromphthalid 1.50 1.18 14 4-Hydroxy-4′-isopropoxydiphenylsulfon Zinksalz der 3,4-dichlorbenzoesäure 3,3-Bis[2-(p-dimethylaminophenyl)-2-(m,p-dimethoxyphenyl)äthenyl]4,5,6,7-tetrabromphthalid 1.48 1.19 15 4-Hydroxy-4′-isopropoxydiphenylsulfon Zinksalz der 3,4-dichlorbenzoesäure 3,3-Bis[2-(p-dimethylaminophenyl)-2-(m,p-dimethoxyphenyl)äthenyl]4,5,6,7-tetrabromphthalid 1.50 1.18 Vergleichsbeispiel 2 16 4,4′-Isopropylidendiphenol --- 3,3-Bis[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl)äthenyl]-4,5,6,7-tetrabromphthalid 1.11 1.03 17 1,7-Di(4-hydroxyphenylthio)3,5-dioxaheptan --- 3,3-Bis[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl)äthenyl]-4,5,6,7-tetrabromphthalid 1.10 1.01 18 4-Hydroxy-4′-isopropoxydiphenylsulfon --- 3,3-Bis[2-(p-dimethylaminophenyl)-2-(p-methoxyphenyl)äthenyl]-4,5,6,7-tetrabromphthalid 1.11 1.00 TABELLE IV Prüfungsergebnisse Versuch Nr. Reflexionsgrad des infraroten Lichtes (%) (3) Beständigkeit gegenüber Licht (4) Beständigkeit gegenüber Ölen (5) Beständigkeit gegenüber Klimaeinflüssen (6) Vor Behandlung Nach Behandlung Restprozent (%) Reflexionsgrad des infraroten Lichtes (%) Vor Behandlung Nach Behandlung Restprozent (%) Reflexionsgrad des infraroten Lichtes (%) Vor Behandlung Nach Behandlung Restprozent (%) Reflexionsgrad des infraroten Lichtes (%) Beispiel 3 10 11 1.19 1.09 92 25 1.19 1.15 97 13 1.19 1.03 87 28 11 11 1.18 1.07 91 24 1.18 1.16 98 14 1.18 1.00 85 27 12 12 1.19 1.09 92 27 1.19 1.16 97 15 1.19 1.02 86 29 13 11 1.18 1.08 92 25 1.18 1.14 97 14 1.18 1.02 86 27 14 12 1.19 1.08 91 26 1.19 1.17 98 15 1.19 1.02 86 28 15 11 1.18 1.06 90 25 1.18 1.16 98 15 1.18 1.00 85 27 Vergleichsbeispiel 2 16 17 1.03 0.62 60 70 1.03 0.50 49 80 1.03 0.41 40 90 17 18 1.01 0.61 60 72 1.01 0.49 49 82 1.01 0.39 39 91 18 20 1.00 0.60 60 71 1.00 0.48 48 85 1.00 0.38 38 92 -
- (1) Statische Bilddichte: Ein wärmeempfindliches Aufzeichnungsblatt wird 5 s unter einem Druck von 10 g/cm² gegen eine auf 135°C erhitzte Platte gepreßt. Die statische Bilddichte wird mit einem Macbeth-Dichtemesser (RD-914, Verwendung des Amber-Filters, unten gelten die gleichen Bedingungen) bestimmt.
- (2) Dynamische Bilddichte: Ein wärmeempfindliches Aufzeichnungsblatt wird bei einer angelegten Spannung von 18,03 V und einer Pulsbreite von 3,2 Millisekunden unter Verwendung einer Faksimiliermaschine KB-4800 (von TOSHIBA CORPORATION) aufgezeichnet und mit einem Macbeth-Dichtemesser bestimmt.
- (3) Reflexionsgrad des infraroten Lichtes (%): Der Reflexionsgrad des durch die obige Anmeldung (2) aufgezeichneten Teils wird mit einem Spektrophotometer bei einer Wellenlänge von 1000 nm gemessen.
- (4) Beständigkeit gegenüber Licht: Das gemäß obiger Anmerkung (2) aufgezeichnete Bild wird als Bilddichte vor der Behandlung bezeichnet. Die Aufzeichnung wird 4 Stunden mit dem Licht eines Fade-O-Meters bestrahlt.
- (5) Beständigkeit gegenüber Ölen: Die gemäß obiger Anmerkung (2) aufgezeichnete Bilddichte wird als Bilddichte vor der Behandlung definiert. Ein Tropfen Rizinusöl wird auf die Aufzeichnung getröpfelt, nach 10 s mit einem Filterpapier abgewischt und 24 h stehengelassen. Danach wird die Bilddichte (nach der Ölbehandlung) gemessen. Der Restprozentsatz wird nach folgender Formel berechnet:
- (6) Beständigkeit gegenüber Klimaeinflüssen: Das gemäß obiger Anmerkung (2) behandelte wärmeempfindliche Blatt wird 24 Stunden lang bei 40°C und 90% relativer Luftfeuchtigkeit stehengelassen und dann mit einem Macbeth-Dichtemesser gemessen. Der Restprozentsatz wird nach folgender Formel berechnet:
- Das erfindungsgemäße Aufzeichnungsmaterial weist folgende Vorteile auf:
- (1) Höhere thermische Ansprechbarkeit.
- (2) Überlegene optische Lesbarkeit im nahen Infrarot-Bereich.
- (3) Überlegene Beständigkeit gegenüber Licht, Ölen und Klimaeinflüssen und dadurch gute Haltbarkeit und
- (4) Verwendbarkeit unter schwierigen Bedingungen bei Strichcode-Zettel usw. wegen des obigen Effekts (3).
Claims (8)
die anderen der Reste R₁, R₂, R₃, R₄, R₅, R₆, R₇, R₈ und R₉ gleich oder verschieden sind, und jeweils ein Wasserstoff- oder Halogenatom, eine Alkyl-, Alkoxy-, Cycloalkyl-, Nitro-, Hydroxy-, Amino-, substituierte Amino-, Aralkyl-, substituierte Aralkyl-, Aryl- oder substituierte Arylgruppe bedeuten;
T₁, T₂ und T₃ gleich oder verschieden sind und jeweils ein Wasserstoffatom, eine C₁-C₈-Alkyl-, C₃-C₉-Alkenyl- oder C₃-C₉-Alkinylgruppe bedeuten;
T₄ ein Wasserstoffatom, eine C₁-C₈-Alkyl-, C₃-C₉-Alkenyl-, C₃-C₉-Alkinyl- oder Phenylgruppe bedeutet; oder
T₃ und T₄ mit einem benachbarten Stickstoffatom verbunden sein können und dabei eine Morpholino-, Pyrrolidino-, Piperidino- oder Hexamethyleniminogruppe bilden; und
n eine ganze Zahl von 0 bis 4 bedeutet;
R₁₁ eine Alkylgruppe mit 8 oder weniger C-Atomen bedeutet;
R₁₂ eine Alkylgruppe mit 8 oder weniger C-Atomen, eine C₅-C₇-Cycloalkylgruppe oder eine Benzyl- oder Phenylgruppe, die gegebenenfalls durch ein Chlor- oder Bromatom oder ein C₁-C₄-Alkyl substituiert werden kann,
bedeutet;
X¹ und X² gleich oder verschieden sind und jeweils eine Alkylgruppe mit 8 oder weniger C-Atomen, eine Alkoxygruppe mit 8 oder weniger C-Atomen, ein Fluor-, Chlor- oder Bromatom bedeuten;
m und n gleich oder verschieden sind und jeweils eine ganze Zahl 0, 1, 2 oder 3 bedeuten;
jedes X¹ in (X¹)m gleich oder verschieden ist;
jedes X² in (X²)n gleich oder verschieden ist;
und jedes X³ in (X³)₄ gleich oder verschieden ist, und ein Chlor- oder Bromatom bedeutet, wobei mindestens ein X³ ein Bromatom bedeutet;
und als Stabilisator ein halogensubstituiertes Zinkbenzoat der folgenden allgemeinen Formel (III):
X ein Halogenatom bedeutet;
A ein Wasserstoffatom, eine Nitro-, C₁-C₁₂ Alkyl-, C₁-C₁₂-Alkoxy-, C₃-C₁₀-Cycloalkyl-, Cyano- oder Hydroxygruppe bedeutet;
l eine ganze Zahl 1 oder 2 bedeutet; und
m eine ganze Zahl von 0 bis 5 bedeutet, enthält.
R₂₇, R₂₈, R₂₉ und R₃₀ gleich oder verschieden sind und jeweils eine C₁-C₈-Alkylgruppe, eine C₅-C₈-Cycloalkylgruppe, eine C₃-C₈-Alkoxyalkylgruppe, ein Halogenatom, eine Arylgruppe, die durch ein Halogenatom, eine C₁-C₄-Alkylgruppe und/oder eine C₁-C₄-Alkoxygruppe substituiert sein kann, oder eine C₁-C₈-Alkylgruppe, die durch ein Halogenatom, eine C₁-C₄-Alkylgruppe und/oder eine C₁-C₄-Alkoxygruppe substituiert sein kann, bedeuten;
R₂₇ und R₂₈ oder R₂₉ und R₃₀ gegebenenfalls miteinander oder mit einem benachbarten Benzolring einen heterocyclischen Ring bilden können; und
R₃₁ und R₃₂ gleich oder verschieden sind und jeweils ein Wasserstoffatom, ein Halogenatom, eine C₁-C₄-Alkylgruppe, eine C₁-C₄-Alkoxygruppe, oder eine Acyloxygruppe bedeuten;
R₃₃ ein Wasserstoffatom oder eine C₁-C₄ Alkylgruppe bedeutet;
a, b, c und/oder d jeweils ein Kohlenstoffatom bedeuten können, wobei ein oder zwei der Kohlenstoffatome durch ein Stickstoffatom ersetzt sein können; jedes dieser Kohlenstoffatome mit einem Wasserstoffatom, einem Halogenatom, einer C₁-C₈-Alkylgruppe, einer C₁-C₄ Alkoxygruppe, einer C₂-C₁₆-Dialkylaminogruppe oder einer Nitrogruppe verbunden sein kann; und eine Bindung von a-b, b-c oder c-d Bestandteil eines anderen aromatischen Ringes sein kann, enthält.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP230774/87 | 1987-09-14 | ||
| JP62230774A JPH068072B2 (ja) | 1987-09-14 | 1987-09-14 | 感熱記録材料 |
| JP333939/87 | 1987-12-28 | ||
| JP62333939A JPH01171980A (ja) | 1987-12-28 | 1987-12-28 | 感熱記録材料 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| EP0307836A2 true EP0307836A2 (de) | 1989-03-22 |
| EP0307836A3 EP0307836A3 (en) | 1990-09-19 |
| EP0307836B1 EP0307836B1 (de) | 1993-04-28 |
Family
ID=26529528
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP88114852A Expired - Lifetime EP0307836B1 (de) | 1987-09-14 | 1988-09-12 | Wärmeempfindliches Aufzeichnungsmaterial |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US4853362A (de) |
| EP (1) | EP0307836B1 (de) |
| CA (1) | CA1296896C (de) |
| DE (1) | DE3880599D1 (de) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1990014235A1 (en) * | 1989-05-18 | 1990-11-29 | Smith & Mclaurin Limited | Heat-sensitive record material |
| EP0545525A1 (de) * | 1991-11-12 | 1993-06-09 | Appleton Papers Inc. | Wärmeempfindliches Aufzeichnungsmaterial |
| EP0325231B1 (de) * | 1988-01-20 | 1994-06-22 | Nippon Paper Industries Co., Ltd. | Wärmeempfindliches Aufzeichnungsmaterial |
| US5348930A (en) * | 1993-03-31 | 1994-09-20 | Nicca Chemical Co., Ltd. | Heat sensitive recording material |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69032232T2 (de) * | 1989-02-03 | 1998-08-06 | Jujo Paper Co Ltd | Optisches Aufzeichnungsmaterial, optisches Aufzeichnungsverfahren und optische Aufzeichnungsvorrichtung für dieses Verfahren |
| US5200947A (en) * | 1989-02-03 | 1993-04-06 | Jujo Paper Co., Ltd. | Optical recording medium, optical recording method, and optical recording device used in method |
| JP2536917B2 (ja) * | 1989-02-06 | 1996-09-25 | 日本製紙株式会社 | 光記録体 |
| US5146087A (en) * | 1991-07-23 | 1992-09-08 | Xerox Corporation | Imaging process with infrared sensitive transparent receiver sheets |
| US5441418A (en) * | 1993-05-20 | 1995-08-15 | Binney & Smith Inc. | Thermochromic drawing device |
| US5514635A (en) * | 1993-12-29 | 1996-05-07 | Optum Corporation | Thermal writing surface and method for making the same |
| US7993807B2 (en) * | 2004-04-28 | 2011-08-09 | Hewlett-Packard Development Company, L.P. | Compositions, systems, and methods for imaging |
| US20060153608A1 (en) * | 2005-01-10 | 2006-07-13 | Xerox Corporation | System and method for determining printing media is appropriate for use in a printer/copier |
| US7198834B2 (en) * | 2005-03-22 | 2007-04-03 | Hewlett-Packard Development Company, L.P. | Imaging media including interference layer for generating human-readable marking on optical media |
| US20070065749A1 (en) * | 2005-09-21 | 2007-03-22 | Vladek Kasperchik | Radiation-markable coatings for printing and imaging |
| US20070065623A1 (en) * | 2005-09-21 | 2007-03-22 | Vladek Kasperchik | Laser-imageable coating based on exothermic decomposition |
| US20070086308A1 (en) * | 2005-10-13 | 2007-04-19 | Gore Makarand P | Systems and methods for imaging |
| CN118834546B (zh) * | 2024-06-25 | 2026-01-27 | 吉林大学 | 一种电致变色器件及其制备方法 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS59199757A (ja) * | 1983-04-28 | 1984-11-12 | Yamamoto Kagaku Gosei Kk | フルオレン化合物、その製造法およびそれを用いる記録材料 |
| US4721701A (en) * | 1985-01-09 | 1988-01-26 | Jujo Paper Co., Ltd. | Thermosensitive recording sheet |
| JPS62148287A (ja) * | 1985-12-24 | 1987-07-02 | Kanzaki Paper Mfg Co Ltd | 記録体 |
| US4761396A (en) * | 1986-02-12 | 1988-08-02 | Kanzaki Paper Manufacturing Co., Ltd. | Heat-sensitive recording material |
| JPH0815813B2 (ja) * | 1986-06-09 | 1996-02-21 | 山田化学工業株式会社 | 感熱記録材料 |
| US4835291A (en) * | 1986-04-16 | 1989-05-30 | Yamada Chemical Co., Ltd. | Divinyl compounds and chromogenic recording-material prepared by using thereof |
| US4826806A (en) * | 1986-07-31 | 1989-05-02 | Shin Nisso Kako Co., Ltd. | Fluoran compounds and color forming recording materials using same |
| JPH066392B2 (ja) * | 1987-04-09 | 1994-01-26 | 日本製紙株式会社 | 感熱記録体 |
| JP2778701B2 (ja) * | 1988-09-12 | 1998-07-23 | マナック株式会社 | ブリーチ加工用脱色促進剤 |
-
1988
- 1988-08-19 US US07/234,463 patent/US4853362A/en not_active Expired - Fee Related
- 1988-09-12 EP EP88114852A patent/EP0307836B1/de not_active Expired - Lifetime
- 1988-09-12 CA CA000577088A patent/CA1296896C/en not_active Expired - Lifetime
- 1988-09-12 DE DE8888114852T patent/DE3880599D1/de not_active Expired - Fee Related
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0325231B1 (de) * | 1988-01-20 | 1994-06-22 | Nippon Paper Industries Co., Ltd. | Wärmeempfindliches Aufzeichnungsmaterial |
| WO1990014235A1 (en) * | 1989-05-18 | 1990-11-29 | Smith & Mclaurin Limited | Heat-sensitive record material |
| EP0545525A1 (de) * | 1991-11-12 | 1993-06-09 | Appleton Papers Inc. | Wärmeempfindliches Aufzeichnungsmaterial |
| US5348930A (en) * | 1993-03-31 | 1994-09-20 | Nicca Chemical Co., Ltd. | Heat sensitive recording material |
| EP0618082A1 (de) * | 1993-03-31 | 1994-10-05 | NICCA CHEMICAL CO., Ltd. | Wärmeempfindliches Aufzeichnungsmaterial |
Also Published As
| Publication number | Publication date |
|---|---|
| CA1296896C (en) | 1992-03-10 |
| EP0307836A3 (en) | 1990-09-19 |
| DE3880599D1 (de) | 1993-06-03 |
| US4853362A (en) | 1989-08-01 |
| EP0307836B1 (de) | 1993-04-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0307836B1 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| DE112015000518B4 (de) | Thermisches Aufzeichnungsmaterial | |
| EP0171810B1 (de) | Wärmeempfindliches Aufzeichnungsblatt | |
| DE60006196T2 (de) | Selbstklebendes Etikett für Aufzeichnung durch Wärme | |
| DE69301527T2 (de) | Wärmeempfindliches Aufzeichnungsblatt | |
| DE3818354C2 (de) | ||
| EP0211263B1 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| DE69915962T2 (de) | Wärmeempfindliches Aufzeichnungsmedium | |
| EP0251209B1 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| DE3801837A1 (de) | Waermeempfindliche aufzeichnungsmaterialien | |
| DE69505475T2 (de) | Harnstoff- oder Thioharnstoff-Derivat und wärmeempfindliche Aufzeichnungsschicht | |
| EP0248405B1 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| EP0181646B1 (de) | Wärmeempfindliches Aufzeichnungsblatt | |
| EP0287121B1 (de) | Wärme- und lichtempfindliches Aufzeichnungsmaterial und Aufzeichnungsverfahren | |
| EP0224075B1 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| EP0286116B1 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| EP0081228A1 (de) | Druckempfindliche Aufzeichnungsblätter | |
| DE69605725T2 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| EP0325231B1 (de) | Wärmeempfindliches Aufzeichnungsmaterial | |
| DE3879539T2 (de) | Waermeempfindliches aufzeichnungsblatt. | |
| EP0135901B1 (de) | Wärmeempfindliches Aufzeichnungsblatt | |
| DE69113850T2 (de) | Wärmeempfindliches Aufzeichnungsblatt. | |
| EP0421278B1 (de) | Wärmeempfindliches Aufzeichnungsblatt | |
| EP0422680B1 (de) | Wärmeempfindliches Aufzeichnungsblatt | |
| DE69315915T2 (de) | Wärmeempfindliche Aufzeichnungsschicht |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): BE DE FR GB IT SE |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): BE DE FR GB IT SE |
|
| 17P | Request for examination filed |
Effective date: 19901015 |
|
| 17Q | First examination report despatched |
Effective date: 19920810 |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): BE DE FR GB IT SE |
|
| REF | Corresponds to: |
Ref document number: 3880599 Country of ref document: DE Date of ref document: 19930603 |
|
| ET | Fr: translation filed | ||
| GBT | Gb: translation of ep patent filed (gb section 77(6)(a)/1977) |
Effective date: 19930510 |
|
| ITF | It: translation for a ep patent filed | ||
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed | ||
| EAL | Se: european patent in force in sweden |
Ref document number: 88114852.2 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: CD |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: SE Payment date: 19950918 Year of fee payment: 8 Ref country code: DE Payment date: 19950918 Year of fee payment: 8 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GB Payment date: 19960903 Year of fee payment: 9 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19960910 Year of fee payment: 9 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Effective date: 19960913 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: BE Payment date: 19961118 Year of fee payment: 9 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19970603 |
|
| EUG | Se: european patent has lapsed |
Ref document number: 88114852.2 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19970912 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: THE PATENT HAS BEEN ANNULLED BY A DECISION OF A NATIONAL AUTHORITY Effective date: 19970930 Ref country code: BE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19970930 |
|
| BERE | Be: lapsed |
Owner name: NIPPON PAPER INDUSTRIES CO. LTD Effective date: 19970930 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 19970912 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: IT Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES;WARNING: LAPSES OF ITALIAN PATENTS WITH EFFECTIVE DATE BEFORE 2007 MAY HAVE OCCURRED AT ANY TIME BEFORE 2007. THE CORRECT EFFECTIVE DATE MAY BE DIFFERENT FROM THE ONE RECORDED. Effective date: 20050912 |