ES2733643T3 - Esteroides 5.beta.-6-alquil-7-hidroxi-3-ona como intermedios para la producción de moduladores FXR de esteroides - Google Patents
Esteroides 5.beta.-6-alquil-7-hidroxi-3-ona como intermedios para la producción de moduladores FXR de esteroides Download PDFInfo
- Publication number
- ES2733643T3 ES2733643T3 ES15800910T ES15800910T ES2733643T3 ES 2733643 T3 ES2733643 T3 ES 2733643T3 ES 15800910 T ES15800910 T ES 15800910T ES 15800910 T ES15800910 T ES 15800910T ES 2733643 T3 ES2733643 T3 ES 2733643T3
- Authority
- ES
- Spain
- Prior art keywords
- general formula
- compound
- alkyl
- halo
- optionally substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 C[C@](**)[C@@](C(*)CC1C2[C@](C3*)O)[C@@]1(C)C(*)CC2[C@@](C)(CC1)C3=CC1=O Chemical compound C[C@](**)[C@@](C(*)CC1C2[C@](C3*)O)[C@@]1(C)C(*)CC2[C@@](C)(CC1)C3=CC1=O 0.000 description 2
- MPXMCHHSSMKXMF-ARWAOWQXSA-N CCOC(/C=C/[C@@H](C)[C@@H](CC1)[C@@](C)(CCC2[C@@]3(C)CC4)C1C2C=CC3=CC4=O)=O Chemical compound CCOC(/C=C/[C@@H](C)[C@@H](CC1)[C@@](C)(CCC2[C@@]3(C)CC4)C1C2C=CC3=CC4=O)=O MPXMCHHSSMKXMF-ARWAOWQXSA-N 0.000 description 1
- QNPQVQZTQRRFMQ-MVXJCBDQSA-N CC[C@@H]([C@H](CC(CC1)=O)[C@@]1(C)C(CC1)C2C(CC3)[C@@]1(C)[C@H]3[C@H](C)CCC(OCC)=O)C2=O Chemical compound CC[C@@H]([C@H](CC(CC1)=O)[C@@]1(C)C(CC1)C2C(CC3)[C@@]1(C)[C@H]3[C@H](C)CCC(OCC)=O)C2=O QNPQVQZTQRRFMQ-MVXJCBDQSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J9/00—Normal steroids containing carbon, hydrogen, halogen or oxygen substituted in position 17 beta by a chain of more than two carbon atoms, e.g. cholane, cholestane, coprostane
- C07J9/005—Normal steroids containing carbon, hydrogen, halogen or oxygen substituted in position 17 beta by a chain of more than two carbon atoms, e.g. cholane, cholestane, coprostane containing a carboxylic function directly attached or attached by a chain containing only carbon atoms to the cyclopenta[a]hydrophenanthrene skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J71/00—Steroids in which the cyclopenta(a)hydrophenanthrene skeleton is condensed with a heterocyclic ring
- C07J71/0005—Oxygen-containing hetero ring
- C07J71/001—Oxiranes
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Steroid Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Un compuesto de fórmula general (I):**Fórmula** en donde: R1 es alquilo C1-4 opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, OR6 o NR6R7; donde cada uno de R6 y R7 está seleccionado independientemente de H o alquilo C1-4; R2 es H, halo u OH o un OH protegido; Y1 es un enlace o un grupo enlazador alquileno que tiene de 1 a 20 átomos de carbono y opcionalmente sustituido con uno o más grupos R3; cada R3 es independientemente halo, OR8 o NR8R9; donde cada uno de R8 y R9 está seleccionado independientemente de H o alquilo C1-4; y R4 es C(O)OR10, OC(O)R10, C(O)NR10R11, OR10, OSi(R13)3, S(O)R10, SO2R10, OSO2R10, SO3R10 o OSO3R10; donde cada R10 y R11 es independientemente: a. hidrógeno o b. alquilo C1-20, alquenilo C2-20, alquinilo C2-20, -O-alquilo C1-20, -O-alquenilo C2-20 u -O-alquinilo C2-20, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2, o un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con alquilo C1-6, haloalquilo C1-6, halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2; o c. un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes seleccionados de alquilo C1-6, haloalquilo C1-6, halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2; o d. un residuo de polietilenglicol;
Description
DESCRIPCIÓN
Esteroides 5.beta.-6-alquil-7-hidroxi-3-ona como intermedios para la producción de moduladores FXR de esteroides La presente invención se refiere a compuestos que son intermedios en la síntesis de derivados de ácidos biliares con actividad farmacológica. En particular, la invención se refiere a intermedios en la síntesis de ácido obeticólico y sus análogos. Además, la invención se refiere a un método para sintetizar estos intermedios y a un método para preparar ácido obeticólico y análogos de ácido obeticólico a partir de los compuestos de la invención.
Los ácidos biliares son ácidos esteroides que se encuentran en las bilis de mamíferos e incluyen compuestos tales como ácido cólico, ácido quenodesoxicólico, ácido litocólico y ácido desoxicólico, los cuales se encuentran todos en seres humanos. Muchos ácidos biliares son ligandos naturales del receptor farnesoide X (FXR) que es expresado en el hígado e intestino de mamíferos, incluyendo seres humanos.
Los ácidos biliares son derivados de esteroides y están numerados del siguiente modo. A continuación se muestra el sistema de numeración general para esteroides y la numeración de átomos de carbono en el ácido quenodesoxicólico.
Numeración general para esteroides Numeración CDCA
Se ha encontrado que agonistas de FXR son de uso en el tratamiento de trastornos colestásicos hepáticos incluyendo cirrosis biliar primaria y esteatohepatitis no alcohólica (véase la revisión de Jonker et al, in Journal of Steroid Biochemistry & Molecular Biology, 2012, 130, 147-158).
El ácido ursodesoxicólico (UDCA), un ácido biliar aislado originalmente de la vesícula biliar de los osos, se usa actualmente en el tratamiento de trastornos colestásicos hepáticos, aunque parece ser inactivo en el FXR.
Además de su acción en FXR, los ácidos biliares y sus derivados son también moduladores del receptor acoplado a proteína G TGR5. Este es un miembro de la superfamilia tipo rodopsina de receptores acoplados a proteína G y tiene una importante función en la red de señalización de los ácidos biliares, que complementa la función del FXR.
Debido a la importancia de agonistas de FXR y TGF5 en el tratamiento de trastornos colestásicos hepáticos, se han realizado esfuerzos por desarrollar nuevos compuestos que tengan actividad agonista en estos receptores. Un compuesto particularmente activo es el ácido obeticólico, que es un potente agonista de FXR y TGR5. El ácido obeticólico se describe en los documentos WO 02/072598 y EP1568706, los cuales describen ambos un proceso para la preparación de ácido obeticólico a partir de ácido 7-ceto litocólico, que se deriva del ácido cólico. Otros procesos para la producción de ácido obeticólico y sus derivados se describen en los documentos WO 2006/122977, US 2009/0062256 y WO 2013/192097 y todos estos procesos parten también de ácido 7-ceto litocólico.
Es evidente a partir del número de publicaciones de patente dirigidas a procesos para la producción de ácido obeticólico que, en absoluto es sencillo sintetizar este compuesto y, de hecho, el proceso que se usa actualmente parte de ácido cólico, tiene 12 etapas y un bajo rendimiento global.
Además de la ineficiencia y alto coste de este proceso, también hay problemas con el coste y disponibilidad de los materiales de partida. El ácido cólico, el actual material de partida para la producción de ácido obeticólico, es un ácido biliar natural que normalmente se obtiene del sacrificio de reses y otros animales. Esto significa que la disponibilidad de ácido cólico y otros ácidos biliares está limitada por el número de reses bovinas disponibles para el sacrificio. Puesto que la incidencia de la enfermedad colestásica hepática aumenta a nivel mundial, la demanda de ácidos biliares sintéticos tales como el ácido obeticólico también es probable que aumente y es cuestionable si el suministro de ácidos biliares de origen natural continuará siendo suficiente para satisfacer la demanda.
Además, el uso de un material de partida derivado de animales significa que existe la posibilidad de contaminación del material con agentes infecciosos tales como virus o priones, que pueden no solo ser peligrosos para los trabajadores sino que podrían contaminar potencialmente los productos finales si no se adoptan etapas para prevenir esto.
Aunque algunos pacientes con enfermedad colestásica hepática pueden tratarse con ácido ursodesoxicólico, este también es un ácido biliar natural y se enfrenta a los mismos problemas de disponibilidad limitada y alto coste.
En un intento de solucionar los problemas asociados con el uso de ácido biliares como materiales de partida, los autores de la presente invención han ideado un proceso para la síntesis de derivados de ácidos biliares sintéticos, tales como ácido obeticólico, que usa esteroles vegetales como materiales de partida.
Los autores de la invención han desarrollado un proceso para la producción de ácidos biliares sintéticos que transcurre a través de intermedios novedosos y que proporciona el producto final con un rendimiento significativamente mayor que los procesos actuales. El proceso es flexible y puede usar una diversidad de materiales de partida diferentes incluyendo esteroles animales, fúngicos y vegetales.
Esteroles animales adecuados que pueden usarse como materiales de partida incluyen ácido desoxicólico, ácido cólico, mientras que los esteroles fúngicos incluyen ergosterol.
Los esteroles vegetales están ampliamente disponibles a coste significativamente menor y, de hecho, son con frecuencia productos de desecho de otros procesos. Esteroles vegetales y derivados de esteroles vegetales que pueden usarse como materiales de partida incluyen bis-norcolenol (también conocido como 20-hidroximetilpregn-4-en-3-ona), androstenodiona, androstenodienodiona, deshidroepiandrosterona, estigmasterol, brassicasterol, campesterol y P-sitosterol.
La presente invención se refiere a intermedios en el proceso novedoso así como a procesos para preparar los intermedios y procesos para convertir los mismos en los productos deseados.
Por tanto, en la presente invención se proporciona un compuesto de fórmula general (I):
donde:
R1 es alquilo C1-4 opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, OR6 o NR6R7; donde cada uno de R6 y R7 está seleccionado independientemente de H o alquilo C1-4;
R2 es H, halo u OH o un OH protegido;
Y1 es un enlace o un grupo enlazador alquileno que tiene de 1 a 20 átomos de carbono y opcionalmente sustituido con uno o más grupos R3;
cada R3 es independientemente halo, OR8 o NR8R9;
donde cada uno de R8 y R9 está seleccionado independientemente de H o alquilo C1-4;
y
R4 es C(O)OR10, OC(O)R10, C(O)NR10R11, OR10, OSi(R13)3, S(O)R10, SO2R10, OSO2R10, SO3R10, o OSO3R10; donde cada R10 y R11 es independientemente:
a. hidrógeno o
b. alquilo C1-20, alquenilo C2-20, alquinilo C2-20, -O-alquilo C1-20, -O-alquenilo C2-20 u -O-alquinilo C2-20, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 , o grupo un arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con alquilo C1-6, haloalquilo C1-6, halo, NO2 , CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 ; o
c. un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente
sustituido con uno o más sustituyentes seleccionados de alquilo C1-6, haloalquilo C1-6, halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 ;
d. un residuo de polietilenglicol;
cada R19 está seleccionado independientemente de H, alquilo C1-6, haloalquilo C1-6, o un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con halo, alquilo C1-6 o haloalquilo C1-6;
cada R13 es independientemente
a. alquilo C1-20, alquenilo C2-20 o alquinilo C2-20 opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2, un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con alquilo C1-6, haloalquilo C1-6, halo, NO2 , CN, OR19, SO2R19, SO3R19 o N(R19)2 ; o
b. un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros opcionalmente sustituido con uno o más sustituyentes seleccionados de alquilo C1-6, haloalquilo C1-6, halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 ; cada R19 está seleccionado independientemente de H, alquilo C1-6 o haloalquilo C1-6;
R5 es H u OH o un OH protegido;
o una sal o una variante isotópica del mismo.
Compuestos de fórmula general (I) son intermedios en la síntesis de compuestos farmacéuticamente activos tales como ácido obeticólico y sus derivados.
En la presente memoria descriptiva, salvo cuando el contexto lo requiera de otro modo debido a un texto expreso o una necesaria implicación, la palabra “comprende” o variaciones tales como “comprende” o “que comprende” se usan en un sentido inclusivo, es decir, para especificar la presencia de las características afirmadas y no para excluir la presencia o adición de otras características en diversas formas de realización de la invención.
En la presente solicitud, el término “alquilo C1-20” se refiere a un grupo hidrocarbonado totalmente saturado lineal o ramificado que tiene de 1 a 20 átomos de carbono. El término abarca metilo, etilo, n-propilo, isopropilo, n-butilo, isobutilo y t-butilo. Otros grupos alquilo, por ejemplo, alquilo C1-20, alquilo C1-6 o alquilo C1-3 son como se definen antes pero contienen diferente número de átomos de carbono.
El término “haloalquilo C1-6” se refiere a un grupo hidrocarbonado lineal o ramificado que tiene de 1 a 6 átomos de carbono y está sustituido con uno o más átomos halo, hasta sustitución perhalo. Ejemplos incluyen trifluorometilo, cloroetilo y 1 ,1 -difluoroetilo.
El término “alquenilo C2-20” se refiere a un grupo hidrocarbonado lineal o ramificado que tiene de 2 a 20 átomos de carbono y al menos un doble enlace carbono-carbono. Ejemplos incluyen etenilo, prop-1-enilo, hex-2-enilo etc. El término “alquinilo C2-20” se refiere a un grupo hidrocarbonado lineal o ramificado que tiene de 2 a 20 átomos de carbono y al menos un triple enlace carbono-carbono. Ejemplos incluyen etinilo, prop-1 -inilo, hex-2-inilo etc.
El término “alquileno” se refiere a una cadena hidrocarbonada totalmente saturada lineal o ramificada. Ejemplos de grupos alquileno incluyen -CH2-, -CH2CH2-, CH(CH3)-CH2-, CH2CH(CH3)-, -CH2CH2CH2-, -CH2CH(CH2CH3)- y -CH2CH(CH2CH3)CH2-.
El término “alquenileno” se refiere a una cadena hidrocarbonada lineal o ramificada que contiene al menos un doble enlace carbono-carbono. Ejemplos de grupos alquenileno incluyen -CH=CH-, -CH=C(CH3)-, -CH2CH=CH-, -CH=CHCH2-, CH2CH2CH=CH-, CH2CH=C(CH3)-y-CH2CH=C(CH2CH3)-.
El término “alquinileno” se refiere a una cadena hidrocarbonada lineal o ramificada que contiene al menos un triple enlace carbono-carbono. Ejemplos de grupos alquinileno incluyen -C=C-, -CH2CEC-, -CEC-CH2-, CH2CH2CEC-, CH2CECCH2- y -CH2CHEC-CH2CH2-.
Los términos “arilo” y “aromático” se refieren a un grupo cíclico con carácter aromático que tiene de 6 a 14 átomos de carbono (a no ser que se especifique otro) y que contiene hasta tres anillos. Cuando un grupo arilo contiene más de un anillo, no todos los anillos deben ser de carácter aromático. Ejemplos incluyen fenilo, naftilo y antracenilo así como sistemas parcialmente saturados tales como tetrahidronaftilo, indanilo e indenilo.
Los términos “heteroarilo” y “heteroaromático” se refieren a un grupo cíclico con carácter aromático que tiene de 5 a 14 átomos de carbono (a no ser que se especifique otro), al menos uno de los cuales es un heteroátomo seleccionado de N, O y S y que contiene hasta tres anillos. Cuando un grupo heteroarilo contiene más de un anillo, no todos los anillos deben ser de carácter aromático. Ejemplos de grupos heteroarilo incluyen piridina, pirimidina, indol,
benzofurano, benzimidazol y indoleno.
El término “halógeno” se refiere a flúor, cloro, bromo o yodo y el término “halo” a grupos fluoro, cloro, bromo o yodo.
El término “variante isotópica” se refiere a compuestos isotópicamente marcados que son idénticos a los citados en la fórmula (I) salvo por el hecho de que uno o más átomos están reemplazados por un átomo que tiene una masa atómica o número másico diferentes de la masa atómica o número másico encontrados más comúnmente en la naturaleza, o en el que la proporción de un átomo que tiene una masa atómica o número másico encontrado menos comúnmente en la naturaleza ha sido aumentado (haciéndose referencia al último concepto como “enriquecimiento isotópico”). Ejemplos de isótopos que pueden incorporarse en compuestos de la invención incluyen isótopos de hidrógeno, carbono, nitrógeno, oxígeno, flúor, yodo y cloro tales como 2H (deuterio), 3H, 11C, 13C, 14C, 18F, 123I o 125I (por ejemplo, 3H, 11C, 14C, 18F, 123I o 125I), que pueden encontrarse de forma natural o isótopos que no se encuentran de forma natural.
Polietilenglicol (PEG) es un compuesto poliéter, que en forma lineal tiene la fórmula genera1H-[OCH2-CH2]n-OH. Un residuo de polietilenglicol es un PEG en el que el extremo H está reemplazado por un enlace que une el mismo al resto de la molécula.
Versiones ramificadas, incluyendo versiones hiperramificadas y dendríticas también están contempladas y son generalmente conocidas en la técnica. Típicamente, un polímero ramificado tiene un resto de núcleo de ramificación central y una pluralidad de cadenas de polímero lineal unidas al núcleo de ramificación central. PEG se usa habitualmente en formas ramificadas que pueden prepararse por adición de óxido de etileno a diversos polioles, tales como glicerol, oligómeros de glicerol, pentaeritritol y sorbitol. El resto de ramificación central puede también obtenerse de varios aminoácidos, tales como lisina. El poli(etilenglicol) ramificado puede representarse en forma general como R(-PEG-OH)m en el que R se deriva de un resto central, tal como glicerol, oligómeros de glicerol o pentaeritritol, y m representa el número de brazos. También pueden usarse moléculas de PEG multibrazo, tales como las descritas en los documentos US 5,932,462; US 5,643,575; US 5,229,490; US 4,289,872; US 2003/0143596; WO 96/21469; y WO 93/21259.
Los polímeros de PEG pueden tener un peso molecular promedio en número de, por ejemplo, 600-2.000.000 Da, 60.000-2.000.000 Da, 40.000-2.000.000 Da, 400.000-1.600.000 Da, 800-1.200.000 Da, 600-40.000 Da, 600-20.000 Da, 4.000-16.000 Da, o 8.000-12.000 Da.
El término “OH protegido” se refiere a un grupo OH protegido con cualquier grupo protector adecuado. Por ejemplo, el OH protegido puede ser un grupo R4 como se define antes.
Grupos protectores adecuados incluyen ésteres tal que, por ejemplo, cuando R2 y/o R5 es un OH protegido, R2 y/o R5 pueden ser independientemente un grupo OC(O)R14, donde R14 es un grupo R10 como se define antes. También son adecuados éteres sililo, y en este caso, R2 y/o R5 pueden ser independientemente un grupo OSi(R16)3 , donde cada R16 es independientemente un grupo R13 como se define antes.
Otros grupos protectores adecuados para OH son bien conocidos por los expertos en la técnica (véase Wuts, PGM and Greene, TW (2006) “Greene's Protective Groups in Organic Synthesis”, 4a Edition, John Wiley & Sons, Inc., Hoboken, NJ, Estados Unidos de América).
Referencias a un grupo protector que es estable en condiciones básicas significa que el grupo protector no puede retirarse por tratamiento con una base.
Sales apropiadas de los compuestos de fórmula general (I) incluyen sales de adición de bases tales como de sodio, potasio, calcio, aluminio, cinc, magnesio y otras sales de metales así como de colina, dietanolamina, etanolamina, etil diamina, meglumina y otras sales de adición de bases bien conocidas como se resume en Paulekuhn et al., J. Med. Chem. 2007, 50, 6665-6672 y/o son conocidas por los expertos en la técnica.
En algunos compuestos adecuados de fórmula general (I):
R1 es alquilo C1-4 opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, OR6 o NR6R7;
donde cada uno de R6 y R7 está seleccionado independientemente de H o alquilo C1-4;
R2 es H, halo u OH;
Y1 es un enlace o un grupo enlazador alquileno que tiene de 1 a 6 átomos de carbono y opcionalmente sustituido con uno o más grupos R3;
cada R3 es independientemente halo, OR8 o NR8R9;
donde cada uno de R8 y R9 está seleccionado independientemente de H o alquilo C1-4;
R4 es C(O)OR10, C(O)NR10R11, S(O)R10, SO2R10, OSO2R10, SO3R10 o OSO3R10;
donde cada R10 es hidrógeno o alquilo C1-6 o bencilo, cualquiera de los cuales puede estar opcionalmente sustituido con uno o más sustituyentes halo y R11 es hidrógeno o alquilo C1-6 , bencilo, -alquileno C1-4-SO3H o -alquileno C1-4-SO3(alquilo C1-4), cualquiera de los cuales puede estar opcionalmente sustituido con uno o más sustituyentes halo; y
R5b es H u OH;
o una sal de los mismos.
En compuestos adecuados de fórmula general (I), R1 puede ser alquilo C1-4 opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, OR6 o NR6R7, donde R6 y R7 son cada uno independientemente H, metilo o etilo, especialmente H o metilo.
Más adecuadamente, R1 es alquilo C1-4 no sustituido.
En compuestos particularmente adecuados, R1 es etilo.
En algunos compuestos de fórmula general (I), Y1 es un enlace.
Adecuadamente en compuestos de fórmula general (I), Y1 es un grupo enlazador alquileno que tiene de 1 a 15 átomos de carbono, más adecuadamente 1 a 1 2 , 1 a 10 o 1 a 8 átomos de carbono y opcionalmente sustituido con uno o más grupos R3 como se define antes. Típicamente cada R3 es independientemente halo, OR8 o NR8R9; donde cada uno de R8 y R9 está seleccionado independientemente de H, metilo o etilo, especialmente H o metilo.
En algunos compuestos adecuados, Y1 es un enlazador alquileno no sustituido que tiene de 1 a 15 átomos de carbono, más adecuadamente 1 a 1 2 , 1 a 10 o 1 a 8 átomos de carbono.
En algunos compuestos adecuados de fórmula general (I), R2 es H.
En otros compuestos adecuados de fórmula general (I), R2 es OH.
Aún en otros compuestos adecuados de fórmula general (I), R2 es un grupo OH protegido. Cuando R2 es un grupo OH protegido, este puede ser un grupo que no es estable en un entorno básico tal que el tratamiento con una base convierte el grupo OH protegido en OH. Ejemplos de tales grupos son bien conocidos en la técnica e incluyen un grupo OC(O)R14 como se define antes en el que R14 es un grupo R10 como se define antes para la fórmula general (I). Grupos R14 particularmente adecuados son como se definen para R10 más adelante.
De forma alternativa, R2 puede ser un grupo OH protegido que es estable en un entorno básico. Ejemplos de tales grupos incluyen OSi(R16)3 , donde cada R16 es independientemente un grupo R13 como se define antes.
Grupos R16 particularmente adecuados son como se definen para R13 más adelante
En los compuestos de fórmula general (I), R4 es C(O)OR10, OC(O)R10, C(O)NR10R11, OR10, OSi(R13)3 , S(O)R10, SO2R10, OSO2R10, SO3R10 o OSO3R10.
Adecuadamente, es C(O)OR10, OR10, SO3R10 o OSO3R10
Más adecuadamente, R4 es C(O)OR10, SO3R10 o OSO3R10
Adecuadamente, cada R10 y R11 es independientemente:
a. hidrógeno o
b. alquilo C1-10, alquenilo C2-10, alquinilo C2-10, -O-alquilo C1-10, -O-alquenilo C2-10 u -O-alquinilo C2-10, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes como se describe antes; o
c. un grupo arilo de 6 a 10 miembros o heteroarilo de 5 a 10 miembros opcionalmente sustituido con uno o más sustituyentes como se describe antes.
d. un residuo de polietilenglicol.
Más adecuadamente, cada R10 y R11 es independientemente
a. hidrógeno o
b. alquilo C1-10, alquenilo C2-10, alquinilo C2-10 u -O-alquilo C1-10 opcionalmente sustituido con uno o más sustituyentes como se describe antes o
c. un grupo arilo de 6 a 10 miembros opcionalmente sustituido con uno o más sustituyentes como se describe antes.
Adecuadamente cada R13 está seleccionado independientemente de:
a. alquilo C1-10, alquenilo C2-10 o alquinilo C2-10 opcionalmente sustituido con uno o más sustituyentes como se describe antes; o
b. un grupo arilo de 6 a 10 miembros o heteroarilo de 5 a 10 miembros opcionalmente sustituido con uno o más sustituyentes como se describe antes.
Más adecuadamente, cada R13 está seleccionado independientemente de:
a. alquilo C1-10, alquenilo C2-10 o alquinilo C2-10 opcionalmente sustituido con uno o más sustituyentes como se describe antes; o
b. un grupo arilo de 6 a 10 miembros opcionalmente sustituido con uno o más sustituyentes como se describe antes. Aún más adecuadamente, cada R13 está seleccionado independientemente de alquilo C1-10 o fenilo, cualquiera de los cuales está opcionalmente sustituido como se describe antes.
Sustituyentes adecuados para grupos R10 y R11 alquilo, alquenilo, alquinilo, alcoxi, alqueniloxi y alquiniloxi y grupos R13 alquilo, alquenilo y alquinilo incluyen halo, NO2, CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 , o un grupo arilo de 6 a 10 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con alquilo C1-6 , haloalquilo C1-6, halo, NO2, CN, OR19, SO2R19, SO3R19 o N(R19)2 ; donde R19 es como se define antes.
Sustituyentes más adecuados para estos grupos R10, R11 y R13 incluyen halo, OR19, N(R19)2 o un grupo arilo de 6 a 10 miembros opcionalmente sustituido como se describe antes, más adecuadamente, opcionalmente sustituido con halo, alquilo C1-4, haloalquilo C1-4 , -O-alquilo C1-4 , -O-haloalquilo C1-4 , -NH(alquilo C1-4) o -N(alquilo C1-4)2 ; por ejemplo, fluoro, cloro, metilo, etilo, trifluorometilo, metoxi, etoxi, trifluorometoxi, amino, metilo amino y dimetilamino.
Sustituyentes adecuados para grupos R10, R11 y R13 arilo y heteroarilo incluyen alquilo C1-6, haloalquilo C1-6 , halo, NO2 , CN, OR19, SR19oN(R19)2.
Sustituyentes más adecuados para estos grupos R10, R11 y R13 incluyen alquilo C1-4, haloalquilo C1.4, halo, OR19 o N(R19)2; en particular, halo, alquilo C1-4 , haloalquilo C1.4 , -O-alquilo C1-4 ,-O-haloalquilo C1.4, -NH(alquilo C1.4) o -N(alquilo C1-4)2.
Ejemplos específicos para sustituyentes para grupos R10, R11 y R13 arilo y heteroarilo incluyen fluoro, cloro, metilo, etilo, trifluorometilo, metoxi, etoxi, trifluorometoxi, amino, metilo amino y dimetilamino.
Como se ha expuesto antes, cada R19 está seleccionado independientemente de H, alquilo C1-6, haloalquilo C1-6, o un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes halo, alquilo C1-6 o haloalquilo C1-6.
Adecuadamente, R19 es H, alquilo C1-6 , haloalquilo C1-6 , o un grupo arilo de 6 a 10 miembros o heteroarilo de 5 a 10 miembros opcionalmente sustituido con uno o más sustituyentes halo, alquilo C1-4 o haloalquilo C1-4.
Más adecuadamente, R19 es H, alquilo C1-6 , haloalquilo C1-6 o fenilo opcionalmente sustituido con uno o más sustituyentes halo, alquilo C1-4 o haloalquilo C1.4.
Ejemplos específicos de R19 incluyen H, metilo, etilo, trifluorometilo o fenilo opcionalmente sustituidos con uno o más grupos fluoro, cloro, metilo, etilo o trifluorometilo.
En algunos compuestos adecuados de fórmula general (I), R5 es H.
En otros compuestos adecuados de fórmula general (I), R5 es OH.
Aún en otros compuestos adecuados de fórmula general (I), R5 es un grupo OH protegido.
Aún en otros compuestos adecuados de fórmula general (I), R5 es un grupo OH protegido. Cuando R5 es un grupo OH protegido, este puede ser un grupo que no es estable en un entorno básico tal que el tratamiento con una base convierte el grupo OH protegido en OH. Ejemplos de tales grupos son bien conocidos en la técnica e incluyen un grupo OC(O)R14 como se define antes en el que R14 es un grupo R10 como se define antes para la fórmula general (I). Grupos R14 particularmente adecuados son como se definen antes para R10.
De forma alternativa, R5 puede ser un grupo OH protegido que es estable en un entorno básico.
Ejemplos de tales grupos incluyen OSi(R16)3, donde cada R16 es independientemente un grupo R13 como se define antes.
Grupos R16 particularmente adecuados son como se definen antes para R13.
En algunos compuestos adecuados de fórmula general (I), independientemente o en cualquier combinación:
Y1 es un enlace o un grupo alquileno que tiene 1 a 3 átomos de carbono y está opcionalmente sustituido con uno o dos grupos R3;
R4 es C(O)OR10, SO3R10 o OSO3R10, donde R10 es como se define antes pero es más adecuadamente H, alquilo C1-6 o bencilo;
R5 e s H u OH.
En algunos compuestos más adecuados, independientemente o en cualquier combinación:
R1 es etilo; y/o
R2 es H; y/o
Y1 es un enlace, -CH2- o -CH2CH2-; y/o
R4 es C(O)OR10, donde R10 es H, alquilo C1-6 o bencilo; y/o
R5 es H.
Un compuesto particularmente adecuado de la presente invención es
ácido (6 p, 5P, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico
y ásteres de alquilo C1-6 y bencilo del mismo y sales del mismo, especialmente los ásteres metílico y etílico.
Compuestos de fórmula general (I) pueden prepararse a partir de compuestos de fórmula general (II):
donde R1, R2, R4 y R5 son como se definen para la fórmula general (I); y
Y es un enlace o grupo enlazador alquileno, alquenileno o alquinileno que tiene de 1 a 20 átomos de carbono y opcionalmente sustituido con uno o más grupos R3, donde R3 es como se define para la fórmula general (I); por reducción.
En algunos compuestos de fórmula general (II), Y es un enlace.
Adecuadamente en compuestos de fórmula general (II), Y es un grupo enlazador alquileno o alquenileno que tiene de 1 a 15 átomos de carbono, más adecuadamente 1 a12, 1 a10 o1 a 8 átomos de carbono y opcionalmente sustituido con uno o más grupos R3 como se define antes. Típicamente cada R3 es independientemente halo, OR8 o NR8R9; donde cada uno de R8 y R9 está seleccionado independientemente de H, metilo o etilo, especialmente H o metilo. En algunos compuestos adecuados de fórmula general (II), Y es un grupo enlazador alquileno o alquenileno no sustituido que tiene de 1 a 15 átomos de carbono, más adecuadamente 1 a12, 1 a10 o1 a 8 átomos de carbono. Ejemplos específicos de grupos Y incluyen un enlace, -CH2-, -CH2CH2-, -CH=CH- o-CH=C(CH3)-.
La conversión del compuesto de fórmula general (II) en el compuesto de fórmula general (I) puede llevarse a cabo por hidrogenación, normalmente hidrogenación catalítica. Catalizadores adecuados para la hidrogenación catalítica incluyen un catalizador de paladio/carbono, paladio/carbonato de calcio, paladio/óxido de aluminio, platino/paladio o níquel Raney. La reacción puede llevarse a cabo en un disolvente orgánico, que puede ser un disolvente alcohol tal como metanol, etanol o isopropanol; acetato de etilo; piridina; ácido acético; ciclopentil metil éter (CPME) o N,N-dimetilformamida (DMF). El disolvente orgánico puede mezclarse opcionalmente con un disolvente común tal como acetona o agua y/o también puede añadirse una base tal como trietilamina.
La elección del catalizador y disolvente afecta a la relación del producto requerido de fórmula general (I):
También afecta la velocidad de conversión del intermedio de fórmula (XXXI):
en el producto.
Más adecuadamente, se usa un catalizador de paladio/carbono o paladio/carbonato de calcio. Típicamente, en el catalizador el paladio está presente en una cantidad de 5-10% en peso con respecto al peso de la matriz (donde la matriz es el carbono, carbonato de calcio etc.).
Disolventes que proporcionan relaciones superiores de (I):(XXX) incluyen metanol, etanol y DMF, particularmente metanol y DMF.
Cuando se usa metanol como disolvente, este puede usarse solo o en presencia de una base tal como trietilamina. Adecuadamente, la cantidad de trietilamina usada es una cantidad subestequiométrica. Típicamente 0,1 a 0,5 equivalentes con respecto a la cantidad de material de partida de fórmula general (II).
Metanol en presencia de trietilamina proporciona una relación particularmente alta de producto requerido de fórmula general (I) respecto a isómero de fórmula general (XXX).
Reacciones llevadas a cabo con metanol como disolvente pueden llevarse a cabo a una temperatura de aproximadamente -30 a 25°C y la temperatura tiene poco efecto sobre la relación de (I):(XXX).
Cuando se usa DMF como disolvente, este puede estar mezclado con un disolvente común como acetona, tBME, THF, acetonitrilo o acetona/agua. Opcionalmente, el disolvente contiene una base tal como trietilamina en una cantidad subestequiométrica. Típicamente 0,1 a 0,5 equivalentes con respecto a la cantidad de material de partida de fórmula general (II).
Reacciones llevadas a cabo usando DMF como disolvente parecen ser más sensibles a la temperatura que reacciones llevadas a cabo en metanol y la relación de (I):(XXX) disminuye con el aumento de la temperatura. Adecuadamente,
por tanto la reacción se lleva a cabo a una temperatura de -30 a 0°C, más adecuadamente -20 a -10°C.
Se ha encontrado que la presión de hidrógeno tiene poco efecto sobre la selectividad y por tanto la presión de hidrógeno es adecuadamente aproximadamente 101,33 kPa.
Igualmente, la dilución no parece tener un impacto importante sobre la selectividad y por tanto el disolvente puede usarse en cualquier cantidad conveniente.
La hidrogenación de un compuesto de fórmula (II) también reducirá las uniones alqueno, si están presentes, en el enlazador Y.
El proceso para preparar un compuesto de fórmula (I) a partir de un compuesto de fórmula (II) forma otro aspecto de la invención.
El método es particularmente adecuado para la preparación de compuestos de fórmula general (I) en la que R4 es C(O)OR10 a partir de compuestos de fórmula general (II) donde R4 también es C(O)OR10, donde R10 es como se define antes pero es especialmente H, alquilo C1-6 o bencilo.
De forma alternativa, pueden prepararse compuestos de fórmula (I) a partir de otros compuestos de fórmula general (I). Por ejemplo, compuesto de fórmula general (I) en el que R4 es C(O)OR10 puede convertirse en un compuesto de fórmula general (I) en el que R4 es C(O)NR10R11, S(O)R10, SO2R10, OSO2R10, SO3R10 o OSO3R10.
Compuestos de fórmula general (I) en la que R4 es SO3R10 pueden sintetizarse a partir de compuestos de fórmula general (I) en la que R4 es C(O)OH por los métodos dados a conocer en los documentos WO2008/002573, WO2010/014836 y WO2014/066819.
Así, un compuesto de fórmula (I) en la que R4 es C(O)OH puede hacerse reaccionar con un alcanoilo C1-6 o cloruro de benzoilo o con un anhídrido alcanoico C1-6 para proteger los grupos OH.
El compuesto protegido puede hacerse reaccionar entonces con un agente reductor tal como un hidruro, adecuadamente hidruro de litio y aluminio o borohidruro de sodio con el fin de reducir el grupo ácido carboxílico a OH. El grupo alcohol puede reemplazarse por un halógeno, por ejemplo, bromo o yodo, usando el método de trifenilfosfina/imidazol/halógeno descrito por Classon et al, J. Org. Chem., 1988, 53, 6126-6130. El compuesto halogenado puede hacerse reaccionar entonces con sulfito de sodio en un disolvente alcohol para dar un compuesto con un sustituyente SO3" Na+.
Un compuesto de fórmula general (I) en la que R4 es OSO3R10 puede obtenerse haciendo reaccionar el alcohol obtenido a partir de la reducción del ácido carboxílico protegido como se describe antes con ácido clorosulfúrico en presencia de una base tal como trietilamina para proporcionar la sal de trietilamonio protegida. Los grupos protectores pueden retirarse usando hidrólisis con base como se describe antes. La reducción del ácido carboxílico seguida de reacción del alcohol resultante con ácido clorusulfuroso proporciona un compuesto de fórmula general (I) en la que R4 es OSO2R10.
Compuestos de fórmula general (I) en la que R4 es C(O)NR10R11 pueden prepararse a partir del ácido carboxílico por reacción con una amina de fórmula H-NR10R11 en un disolvente adecuado con calentamiento. Compuestos de fórmula general (I) en la que R4 es C(O)NR10R11 o OSO3R10 también pueden prepararse por métodos similares a los descritos por Festa et al, J. Med. Chem., 2014, 57, 8477-8495.
Compuestos de fórmula general (I) con otros grupos R4 pueden prepararse a partir los compuestos anteriores de fórmula general (I) por métodos que son familiares para los expertos en la técnica. Estos métodos también forman un aspecto de la invención.
Compuestos de fórmula general (II) pueden prepararse a partir de compuestos de fórmula general (III):
donde R2, R4 y R5 son como se definen para la fórmula general (I) e Y es como se define para la fórmula general (II);
por alquilación selectiva con un reaccionante organometálico.
Reaccionantes organometálicos adecuados incluyen reactivos de Gilman formados por reacción de un compuesto de alquil litio de fórmula (XXIV):
R1-Li (XXIV)
donde R1 es como se define para la fórmula general (I);
y una sal de cobre (I), particularmente un haluro de cobre (I) tal como yoduro de cobre (I).
La reacción puede llevarse a cabo en un disolvente orgánico tal como tetrahidrofurano, otros éteres tales como dietiléter o una mezcla de los mismos.
De forma alternativa, la adición puede llevarse a cabo usando reactivos de Grignard R1MgX, donde R1 es como se define para la fórmula general (I) y X es un haluro, por ejemplo, bromuro de etilmagnesio y la reacción se lleva a cabo adecuadamente en presencia de una sal de cinc (II) tal como cloruro de cinc y una cantidad catalítica de una sal o complejo de cobre (I) o cobre (II), por ejemplo, cloruro de cobre (I), cloruro de cobre (II) o un complejo de acetilacetonato de cobre (I) o cobre (II) (acac).
La reacción puede llevarse a cabo en un disolvente orgánico, por ejemplo, un éter tal como THF, 2-metil THF, metil terc-butil éter (tBME), dietil éter. De forma sorprendente, la temperatura de la reacción no es particularmente significativa y aunque en algunos casos la reacción puede llevarse a cabo a temperatura reducida, por ejemplo, a aproximadamente -25 a 0°C, se ha llevado a cabo con éxito a mayores temperaturas de hasta aproximadamente 55°C. El proceso para preparar un compuesto de fórmula (II) a partir de un compuesto de fórmula (III) se describe en el presente documento.
El método es particularmente adecuado para la preparación de compuestos de fórmula general (II) en la que R4 es C(O)OR10 a partir de compuestos de fórmula general (III) donde R4 también es C(O)OR10, donde R10 es como se define antes pero es especialmente H, alquilo C1-6 o bencilo. Compuestos de fórmula general (III) pueden prepararse a partir de compuestos de fórmula (IV):
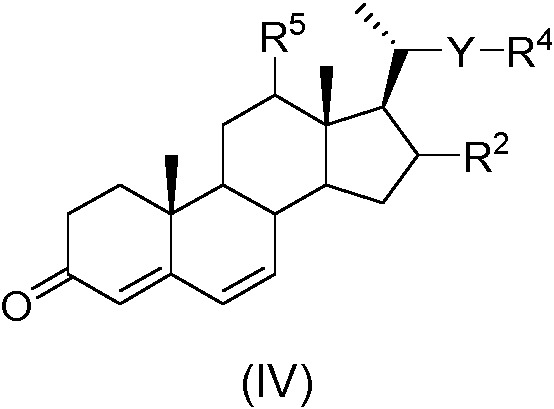
donde R2, R4 y R5 son como se definen para la fórmula general (I) e Y es como se define para la fórmula general (II); por oxidación, por ejemplo, usando monoperoxiftalato (MMPP) o ácido 3-cloroperoxibenzoico, (mCPBA).
La reacción usando MMPP puede llevarse a cabo en un disolvente orgánico tal como acetato de etilo y si se usa mCPBA, la reacción puede llevarse a cabo en un disolvente tal como diclorometano o tolueno. Adecuadamente, la reacción se lleva a cabo a, o justo por debajo de la temperatura de reflujo del disolvente.
Compuestos de fórmula general (IV) pueden prepararse a partir de compuestos de fórmula general (V):
donde R2, R4 y R5 son como se definen para la fórmula general (I) e Y es como se define para la fórmula general (II); por reacción con un agente oxidante tal como cloranilo.
La reacción puede llevarse a cabo bajo condiciones ácidas, por ejemplo, en presencia de ácido acético, y en un disolvente orgánico como tolueno.
Algunos compuestos de fórmulas generales (III), (IV) y (V) son conocidos y, por ejemplo, Uekawa et al en Biosci. Biotechnol. Biochem., 2004, 68, 1332-1337 describen la síntesis de éster etílico de ácido (22E)-3-oxo-4,22-coladien-24-oico a partir de estigmasterol seguido de su conversión a éster etílico de ácido (22E)-3-oxo-4,6,22-colatrien-24-oico, que tiene la fórmula:
Uekawa et al luego siguieron describiendo la conversión de este compuesto en éster etílico del ácido (6a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24-oico, un compuesto de fórmula general (III) en la que R2 y R5 son H, Y es -CH=CH-, y R4 es C(O)OCH2CH3.
Otros compuestos de fórmulas generales (III), (IV) y (V) pueden prepararse por métodos análogos a partir de fitoesteroles similares a estigmasterol.
Estigmasterol y otros fitoesteroles son esteroles vegetales y están fácilmente disponibles o pueden prepararse por rutas conocidas.
Compuestos de fórmula general (V) también pueden prepararse a partir de fórmula general (VIa):
donde R2, R4 y R5 son como se definen para la fórmula general (I) e Y es como se define para la fórmula general (II); por reacción con bromuro de litio y una base tal como carbonato de litio. La reacción puede llevarse a cabo en un disolvente tal como W,W-dimetilformamida (DMF) y a una temperatura de aproximadamente 120°C a 180°C.
Compuestos de fórmula general (VIa) pueden obtenerse por bromación de un compuesto de fórmula general (VI):
donde R2, R4 y R5 son como se definen para la fórmula general (I) e Y es como se define para la fórmula general (II); usando, por ejemplo, bromo en ácido acético.
Compuestos de fórmula general (VI) pueden prepararse a partir de compuestos de fórmula general (VII):
donde R2, R4 y R5 son como se definen para la fórmula general (I) e Y es como se define para la fórmula general (II); por oxidación, típicamente con un agente oxidante a base de cromo o con hipoclorito de sodio.
Compuestos de fórmula general (VII) en la que R4 es C(O)OR10, donde R10 es alquilo C1-6 o bencilo pueden prepararse a partir de compuestos de fórmula general (VII) en la que R4 es C(O)OH por esterificación, típicamente por reacción con un alcohol apropiado en condiciones ácidas.
Compuestos de fórmula general (VII) en la que R4 es C(O)OH y R5 es H pueden prepararse a partir de compuestos de fórmula general (VIII):
donde R2 es como se define en la fórmula general (I) e Y es como se define en la fórmula general (II);
R4 es C(O)OR10, donde R10 es alquilo C1-6 o bencilo; y
R12 es un OH protegido;
por reacción con un agente reductor, típicamente hidrazina en condiciones básicas y en un disolvente a base de alcohol o glicol, por ejemplo, dietilenglicol.
Cuando R12 es un grupo OH protegido que es estable en condiciones básicas, la reacción puede estar seguida de una reacción para retirar el grupo protector R12 dejando un grupo OH.
Grupos protectores para OH se describen antes y, por ejemplo, R12 puede ser un grupo C(O)R14, donde R14 es como se define antes, en particular, alquilo C1-6 o bencilo. También son adecuados silil éteres y, en este caso, R2 y/o R5 pueden ser independientemente un grupo Si(R16)3, donde R16 es como se define antes pero es especialmente alquilo C1-6 o fenilo. Otros grupos protectores adecuados para OH son bien conocidos por los expertos en la técnica (véase Wuts, PGM and Greene, TW (2006) “Greene's Protective Groups in Organic Synthesis”, 4a Edición, John Wiley & Sons, Inc., Hoboken, NJ, Estados Unidos de América).
Grupos R12 particularmente adecuados incluyen grupos que no son estables en presencia de una base puesto que esto elimina la necesidad de una etapa adicional para retirar el grupo protector. Un ejemplo de un grupo R12 que no es estable en condiciones básicas es un grupo C(O)R14, donde R14 es como se define antes, y es particularmente alquilo C1-6 o bencilo.
De forma alternativa, la reacción puede llevarse a cabo en 2 etapas tal que el compuesto de fórmula general (VIII) se hace reaccionar con un compuesto de fórmula general (XXXII):
R20-NH-NH2 (XXXII)
donde R20 es un grupo lábil tal como toluenosulfonilo o metanosulfonilo;
para dar un compuesto de fórmula general (XXXIII):
seguido de reducción con un agente reductor adecuado. Ejemplos de agentes reductores que pueden usarse en esta reacción incluyen hidruros tales como borohidruro de sodio, cianoborohidruro de calcio, hidruro de litio y aluminio, etc. Compuestos de fórmula general (VIII) pueden prepararse a partir de compuestos de fórmula general (IX):
donde R2 es como se define en la fórmula general (I) e Y es como se define en la fórmula general (II);
R4 es C(O)OR10, donde R10 es alquilo C1-6 o bencilo; y
R12 es como se define antes, especialmente -C(O)alquilo C1-3;
por reacción con un agente oxidante, por ejemplo, hipoclorito de sodio.
La reacción puede llevarse a cabo en condiciones ácidas, por ejemplo, en presencia de ácido acético, y en un disolvente orgánico tal como acetato de etilo.
Compuestos de fórmula general (IX) pueden prepararse a partir de compuestos de fórmula general (X):
donde R2 es como se define en la fórmula general (I) e Y es como se define en la fórmula general (II);
R4 es C(O)OR10, donde R10 es alquilo C1-6 o bencilo;
por reacción con un agente adecuado para introducir el grupo protector R12. Por ejemplo, cuando R12 es C(O)R14, el compuesto de fórmula general (X) puede hacerse reaccionar con un anhídrido de ácido carboxílico o un cloruro de ácido en presencia de una base débil tal como piridina, adecuadamente catalizada por4-dimetilaminopiridina (DMAP). La reacción puede llevarse a cabo en un disolvente tal como acetato de etilo.
Compuestos de fórmula general (X) pueden prepararse mediante la esterificación de compuestos de fórmula general (XI):
donde R2 es como se define en la fórmula general (I) e Y es como se define en la fórmula general (II).
La reacción puede llevarse a cabo haciendo reaccionar el ácido de fórmula general (XI) con un alcohol adecuado en condiciones ácidas.
Compuestos de fórmula general (XI) son conocidos. Por ejemplo, el compuesto de fórmula general (XI) en la que Y es -CH2CH2- y R2 es H es ácido desoxicólico, que es fácilmente asequible de una serie de suministradores.
Otros ácidos biliares con diferentes valores para Y y R2 pueden usarse como materiales de partida alternativos. Una ruta alternativa para compuestos de fórmula general (V) es como la mostrada en el Esquema 1 en el que se convierte androstenodiona en un compuesto de fórmula general (V) en la que R2 y R5 son H; R4 es -C(O)OCH3 e Y es -CH2CH2-o-CH=CH-.
Esquema 1
Una ruta alternativa para compuestos de fórmula general (IV) en la que Y es un grupo alquenileno es mediante el uso de una reacción de olefinación, por ejemplo, una olefinación de Horner-Wadsworth-Emmons (HWE) de un compuesto de fórmula general (XII):
donde R2 y R5 son como se definen para la fórmula general (I);
usando un compuesto de fórmula general (XIII):
donde R10 es como se define para la fórmula general (I).
La reacción puede llevarse a cabo en condiciones de HWE convencionales, por ejemplo, usando una base tal como hidruro de sodio.
Compuestos de fórmula general (XIII) son fácilmente asequibles o pueden prepararse por métodos conocidos por expertos en la técnica.
Otras reacciones de olefinación tales como olefinación de Tebbe, una reacción de Wittig o una olefinación de Julia-Kocienski también darían lugar a compuestos de fórmula general (IV) en la que Y es un grupo alquenileno. Estas reacciones de olefinación son familiares para un químico experto en la técnica.
Compuestos de fórmula general (XII) pueden prepararse por reacción de un compuesto de fórmula general (XIV) con ozono 15
donde R2 y R5 son como se definen para la fórmula general (I) y R15 es alquilo C1-6.
Un ejemplo de una reacción de este tipo se presenta en el documento US 2,624,748.
Compuestos de fórmula general (XIV) pueden prepararse por reacción de un compuesto de fórmula general (XV):
donde R2 y R5 son como se definen para la fórmula general (I) y R15 es alquilo C1-6
con un ácido en un disolvente tal como metanol.
Compuestos de fórmula general (XV) pueden prepararse por oxidación de un compuesto de fórmula general (XVI):
donde R2 y R5 son como se definen para la fórmula general (I) y R15 es alquilo C1-6 usando una oxidación de Oppenauer.
Ejemplos de la conversión de compuestos de fórmula general (XVI) en compuestos de fórmula general (XIV) se dan a conocer por Shepherd et al, J. Am. Chem. Soc. 1955, 77, 1212-1215 y Goldstein, J. Med. Chem. 1996, 39, 5092-5099. Un ejemplo de un compuesto de fórmula general (XVI) es ergosterol, que es un esterol fúngico y el Esquema 2 siguiente muestra la conversión de ergosterol en un compuesto de fórmula general (IV) en la que ambos R2 y R5 son H, Y es CH=CH2 y R4 es C(O)OR10, donde R10 es etilo.
Esquema 2
Como con los compuestos de fórmula general (I), los compuestos de fórmulas generales (II) a (XI), (VIa) y (XXXIII) en la que R4 es C(O)R10, C(O)NR10R11, S(O)R10, SO3R10 o OSO3R10 pueden prepararse a partir de los compuestos correspondientes en los que R4 es C(O)OR10 por reacción con un reaccionante apropiado usando métodos bien conocidos por los expertos en la técnica. Por ejemplo, los métodos descritos en los documentos WO2008/002573 y WO2010/014836 o métodos similares a los descritos por Classon et al, J. Org. Chem., 1988, 53, 6126-6130 y Festa et al, J. Med. Chem., 2014, 57, 8477-8495.
Compuestos de fórmula general (I) son intermedios en la síntesis de compuestos de fórmula general (XIX):
donde Y1, R1 y R4 son como se definen en la fórmula general (I);
R2 es H, halo u OH;
R5a es H u OH; y
Los compuestos de fórmula general (I) pueden convertirse en compuestos de fórmula general (XIX) en un proceso en 3 etapas a través de intermedios de fórmulas generales, (XX) y (XXI) como se describe más adelante.
Por tanto, en otro aspecto de la invención se proporciona un proceso para la preparación de un compuesto de fórmula general (XIX), comprendiendo el proceso:
i. oxidación del compuesto de fórmula general (I) usando un agente oxidante adecuado para dar un compuesto de fórmula general (XX):
donde Y1, R1, R2, R4 y R5 son como se definen en la fórmula general (I);
ii. epimerización del compuesto de fórmula general (XX) para dar un compuesto de fórmula general (XXI):
donde Y1, R1 y R4 son como se definen en la fórmula general (I);
R2 es H, halo u OH o un grupo OH protegido que es estable en condiciones básicas; y
R5b es H u OH o un grupo OH protegido que es estable en condiciones básicas; y
(iii) reducción del compuesto de fórmula general (XXI) usando un agente reductor adecuado y, cuando R2 y/o R5b es un OH protegido, retirada del grupo o grupos protectores para dar un compuesto de fórmula general (XIX) como se define antes, donde la retirada del grupo protector puede tener lugar antes o después de la reducción; y opcionalmente
(iv) conversión de un compuesto de fórmula general (XIX) en otro compuesto de fórmula general (XIX).
Los compuestos de fórmula general (XIX) son potentes agonistas de FXR y TGR5 e incluyen ácido obeticólico, que es un compuesto de fórmula (XIX) en la que R1 es etilo, R2 y R5a son ambos H, Y1 es -CH2CH2-, y R4 es C(O)OH.
En los compuestos de fórmulas generales (XIX) a (XXI), valores más adecuados para Y1, R1 y R4 son como se definen para la fórmula general (I).
En la etapa (i) del proceso expuesto antes, la reacción de oxidación puede llevarse a cabo usando cualquier método adecuado. Un método adecuado es una oxidación con peryodinano de Dess-Martin (1,1,1 -triacetoxi-1,1 -dihidro-1,2-benziodoxol), que puede llevarse a cabo en un disolvente clorado tal como cloroformo o diclorometano a una temperatura de aproximadamente 15 a 25°C, adecuadamente a temperatura ambiente.
Un método de oxidación alternativo es oxidación usando hipoclorito, por ejemplo, hipoclorito de sodio, en condiciones ácidas, por ejemplo, proporcionadas por ácido acético. La reacción puede llevarse a cabo en un disolvente acuoso y a una temperatura de 0 a 15°C, más normalmente a aproximadamente 0 a 10°C.
Otros métodos de oxidación incluyen una reacción de Jones usando dicromato de sodio o, más normalmente, trióxido crómico en ácido sulfúrico diluido. Este proceso es conocido por ser seguro para la conversión limpia de grupos hidroxilo de ácido biliares a los correspondientes derivados ceto (Bortolini et al, J. Org. Chem., 2002, 67, 5802). Puede llevarse a cabo una oxidación alternativa usando TEMPO ((2,2,6,6-Tetrametil-piperidin-1-il)oxi) o un derivado del mismo.
La reacción de epimerización de la etapa (ii) comprende adecuadamente tratar el compuesto de fórmula general (XX) con una base. El compuesto de fórmula general (XX) puede disolverse en un disolvente alcohol, mezclarse opcionalmente con agua y ponerse en contacto con una base, por ejemplo, hidróxido de sodio o potasio o un alcóxido de sodio o potasio, típicamente un etóxido.
En el caso de compuestos de fórmula general (XX) en la que R4 es C(O)OR10, donde R10 es alquilo C1-6 o bencilo y donde se usa una base fuerte tal como hidróxido de sodio o potasio, la reacción de epimerización de la etapa (ii) puede llevarse a cabo por hidrólisis para dar un compuesto de fórmula general (XXI) en la que R4 es C(O)OH.
Si en el compuesto de fórmula general (XX), R2 y/o R5 es un OH protegido, por ejemplo, un grupo OC(O)OR14, donde R14 es como se define antes pero es especialmente alquilo C1-6 o bencilo, este puede retirarse durante la etapa de epimerización para dar un compuesto de fórmula general (XXI) en la que R2 y/o R5b es OH. Otros grupos OH protegidos que son estables en condiciones básicas (por ejemplo un grupo OSi(R16)3 donde cada R16 es independientemente como se define antes pero es especialmente alquilo C1-6 o fenilo) pueden retirarse antes o después de la etapa (iii).
En la etapa (iii), el agente reductor es típicamente un hidruro, tal como borohidruro de sodio que puede usarse en un disolvente tal como una mezcla de tetrahidrofurano y agua. Típicamente, esta reacción se lleva a cabo en condiciones básicas, por ejemplo, en presencia de una base fuerte tal como hidróxido de sodio o potasio y a una temperatura de aproximadamente 0 a 110°C, más normalmente 60 a 100°C. Puede producirse un compuesto de fórmula general (XIX) en la que R4 es C(O)OH mediante la reducción de un compuesto de fórmula general (XXI) en la que R4 es C(O)OH.
Compuestos de fórmulas generales (XIX) a (XXI) en la que R4 es C(O)R10, C(O)NR10R11, S(O)R10, SO2R10 o OSO2R10 pueden prepararse a partir de los compuestos correspondientes en los que R4 es C(O)OR10 por reacción con reaccionantes apropiados usando métodos bien conocidos por los expertos en la técnica.
Compuestos de fórmulas generales (XIX) a (XXI) en la que R4 es SO3R10 pueden sintetizarse a partir de compuestos de fórmulas generales (XVIII) a (XXI) en las que R4 es C(O)OH por los métodos dados a conocer en los documentos WO2008/002573, WO2010/014836 y WO2014/066819.
Así, un compuesto de fórmula general (XIX) a (XXI) en la que R4 es C(O)OH puede hacerse reaccionar con un cloruro de alcanoilo C1-6 o benzoilo o con un anhídrido alcanoico C1-6 para proteger los grupos OH. El compuesto protegido puede hacerse reaccionar entonces con un agente reductor tal como un hidruro, adecuadamente borohidruro de sodio con el fin de reducir el grupo ácido carboxílico a OH. El grupo alcohol puede reemplazarse por un halógeno, por ejemplo, bromo o yodo, usando el método de trifenil fosfina/imidazol/halógeno descrito por Classon et al, J. Org. Chem., 1988, 53, 6126-6130. El compuesto halogenado puede hacerse reaccionar entonces con sulfito de sodio en un disolvente alcohol para dar un compuesto con un sustituyente SO3'Na+.
Compuestos de fórmulas generales (XIX) a (XXI) en las que R4 es OSO3R10 pueden obtenerse haciendo reaccionar el alcohol obtenido de la reducción del ácido carboxílico protegido con ácido clorosulfúrico en presencia de una base tal como trietilamina para proporcionar la sal trietilamonio protegida. Los grupos protectores pueden retirarse usando hidrólisis con base como se describe antes. La reducción del ácido carboxílico seguida de reacción del alcohol resultante con ácido clorusulfuroso proporciona un compuesto de fórmulas generales (XIX) a (XXI) en las que R4 es OSO2R10.
Compuestos de fórmulas generales (XIX) a (XXI) en las que R4 es C(O)NR10R11 pueden prepararse a partir del ácido carboxílico por reacción con una amina de fórmula H-NR10R11 en un disolvente adecuado con calentamiento. Los compuestos de fórmulas generales (XIX) a (XXI) en las que R4 es C(O)NR10R11 o OSO3R10también pueden prepararse
por métodos similares a los descritos por Festa et al, J. Med. Chem., 2014, 57 (20), 8477-8495. Estos métodos también forman un aspecto de la invención.
Un compuesto de fórmula general (XIX) a (XXI) en la que R4 es C(O)R10 puede obtenerse por reducción de un compuesto en el que R4 es C(O)OR10 usando un equivalente de hidruro de diisobutil aluminio (DIBAL) para obtener un aldehído en el que R4 es c (O)H (véase, por ejemplo, el documento WO2011/014661).
De forma alternativa, el aldehído puede prepararse por oxidación de un compuesto protegido en el que R4 es OH preparado como se describe antes. La oxidación puede ser una oxidación de Swern llevada a cabo usando cloruro de oxalilo y dimetil sulfóxido seguido de trimetilamina (véase, por ejemplo, Xiang-Dong Zhou et al, Tetrahedron, 2002, 58, 10293-10299). De forma alternativa, la oxidación puede llevarse a cabo usando un agente oxidante tal como cloroformiato de piridinio (PCC) como se describe por Carnell et al (J. Med. Chem., 2007, 50, 2700-2707).
Un compuesto de fórmula general (I) en la que R4 es C(O)R10 donde R10 es distinto de hidrógeno puede obtenerse por métodos conocidos, por ejemplo, por reacción del aldehído en el que R4 es C(O)H con un reactivo de Grignard adecuado, seguido de oxidación. Tales métodos son bien conocidos por los expertos en la técnica.
La invención se describirá ahora con más detalle con referencia a los ejemplos.
En los ejemplos, se usaron las siguientes abreviaturas:
AcOH Ácido acético
CPME Ciclopentil metil éter
DMF W,W-dimetilformamida
EtOAc Acetato de etilo
EtOH Etanol
IPA Alcohol isopropílico
MeOH Metanol
NEt3 Trietilamina
nBuOAc Acetato de n-butilo
TBME t-butil metil éter
THF Tetrahidrofurano
TLC Cromatografía en película delgada
Ejemplos 1 a 4 - Síntesis de (éster etílico del ácido 6p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico a partir de estigmasterol.
Ejemplo 1 - Síntesis de éster etílico del ácido (22E)-3-oxo-4,6,22-colatrien-24-oico
El material de partida, éster etílico del ácido (22E)-3-oxo-4,22-coladien-24-oico, se preparó a partir de estigmasterol según el método descrito por Uekawa et al in Biosci, Biotechnol, Biochem., 2004, 68, 1332-1337.
Se cargó éster etílico del ácido (22E)-3-oxo-4,22-coladien-24-oico (1,00 kg, 2,509 mol; 1 eq) en un recipiente de reacción, seguido de AcOH (3 vol, 3,0 l) y tolueno (1 vol, 1,0 l) con agitación. Se cargó entonces cloranilo (0,68 kg, 2,766 mol; 1,1 eq) y la mezcla de reacción se calentó hasta 100°C y se mantuvo a esta temperatura durante 1-2 h (IPC por TLC sobre sílice, eluyente EtOAc :heptano 3:7; Material de partida: Rf 0,50, Producto: Rf 0,46; se visualiza con tinción con anisaldehído). La mezcla se enfrió seguidamente en un baño de hielo/agua hasta 10°C y el sólido resultante se separó por filtración. La torta del filtro se lavó con AcOH :tolueno 3:1 premezclado (4 x 0,5 vol) a 5°C ± 4°C y el filtrado se concentró a vacío hasta 70°C. El residuo se disolvió en acetona (3 vol), luego se cargó NaOH acuoso al 3% p/p (10 vol) gota a gota con agitación, manteniendo la temperatura por debajo de 30°C (exotérmica). La
suspensión resultante se enfrió hasta 10-15°C y se agitó durante 30 minutos. Los sólidos se recogieron por filtración y la torta del filtro se lavó con acetona:agua 1:1 premezclada (1 x 2 vol luego 3 x 1 vol). La torta del filtro (sólido color castaño) se secó bajo vacío a 70-75°C, 672 g (6 8 % de rendimiento). La caracterización del compuesto coincide con los datos publicados en la bibliografía.
Ejemplo 2 - Éster etílico del ácido (6 a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24-oico
A una solución de éster etílico del ácido (22E)-3-oxo-4,6,22-colatrien-24-oico (58,0 g, 146,3 mmol) en EtOAc (1,0 l) a reflujo se añadió MMPP al 80% (bis(monoperoxiftalato) de magnesio hexahidratado, 197,0 g, aproximadamente 318,6 mmol) en cuatro porciones iguales a intervalos de 30 minutos. La suspensión se agitó vigorosamente a reflujo durante 5 h y a temperatura ambiente durante otras 16 h. La reacción se calentó entonces hasta reflujo y se agitó otras 6 horas. La mezcla se enfrió hasta aproximadamente 50°C y los sólidos se filtraron y aclararon con EtOAc caliente (200 ml). El filtrado se lavó seguidamente con NaHSO3 ac. al 20% (100 ml), NaOH ac. 1M (100 ml luego 200 ml) y NaCl ac. al 10% (250 ml), se secó sobre Na2SO4 , se filtró y concentró a vacío. El residuo (sólido amarillo) se cristalizó en un volumen mínimo de EtOAc a 60°C dando el epóxido producto como cristales blanquecinos/amarillo pálido (25,7 g, 43% de rendimiento, prismas). La caracterización del compuesto coincide con los datos publicados en la bibliografía.
Ejemplo 3 - Síntesis de éster etílico del ácido (6 p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico
Método 1:
En una suspensión de Cul (1,40 g, 7,35 mmol) en éter dietílico (10 ml), enfriada hasta -78°C bajo una manta de argón se cargó EtLi (28,8 ml, 14,4 mmol, solución 0,5 M en benceno/ciclohexano). La suspensión blanca espesa formada se dejó calentar hasta 0°C, se agitó durante 5 minutos (formando una solución oscura) y se enfrió hasta -78°C. Se preparó una solución de éster etílico del ácido (6 a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24-oico (1,00 g, 2,42 mmol) en éter dietílico / THF (24 ml, 3:1) y se cargó en el recipiente de reacción que contenía el organocuprato. Se usó THF (1 ml) para aclarar el recipiente que contenía la solución del epóxido y este se cargó también en el organocuprato. La mezcla de reacción se dejó calentar hasta -4°C durante 30 minutos, tiempo después del cual la reacción era completa por TLC (sílice, 1:1 EtOAc :heptano). Después de otros 30 minutos de agitación a aproximadamente -4°C se cargó una solución de NH4O ac. saturada y la mezcla se agitó durante 30 minutos. La mezcla se transfirió a un embudo de separación y la fase acuosa se separó, junto con material sólido presente en la interfase. La fase orgánica se lavó con NaHCO3 acuoso al 5% en peso (2 x 50 ml,) y agua (1 x 50 ml). Se usó TBME (50 ml) para extraer la fase acuosa original de la reacción y los lavados reunidos. Las fases orgánicas reunidas se concentraron y el residuo se purificó y por cromatografía usando sílice (25 g) como la fase estacionaria (elución con gradiente con EtOAc al 0-30% en heptano) dando éster etílico del ácido (6 p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico (0,63 g, 59 %).
RMN de 1H (400 MHz, CDCI3): 5 = 6,82 (1H, dd, J = 15,6, 8,9, C22H), 5,75 (1H, s, C4H), 5,74 (1H, d, J = 15,6, C23H), 4,17 (2H, q, J = 7,1, OCH2CH3), 3,72 (1H, s ancho, C7H), 2,52-2,25 (5H, m), 2,05-1,98 (2H, m), 1,82-1,10 (23H, m), 0,91 (3H, t, J = 7,4, CH3), 0,77 (3H, s, CH3). RMN de 13C (100 MHz, CDCh): 5 = 199,2, 171,2, 167,1, 154,5, 128,4, 119,0, 71,9, 60,1,55,3, 54,9, 49,9, 44,3, 42,7, 39,6, 39,1,38,3, 37,4, 35,6, 34,0, 28,0, 26,3, 23,6, 20,8, 19,7, 19,2, 14,2, 12,8, 12,0; (IR) vmax(cm-1): 3467, 2939, 2870, 1716, 1651, 1457, 1268, 1229, 1034; HRMS (ESI-TOF) (Espectro de Masas de Alta Resolución (Ionización por Electronebulización-Tiempo de Vuelo)) m/z: (M+H)+ calculado para C28H43O4 443,3161; encontrado: 443,3156. p.f. = 59,4 - 62,9°C
Método 2
Se secó ZnCl2 (32,84 g, 240,9 mmol) bajo vacío con agitación lenta a 180°C durante 2 h. El matraz se enfrió hasta temperatura ambiente bajo una atmósfera de argón y el residuo se disolvió en THF (520 ml) y se transfirió mediante una cánula a un matraz de reacción de tres bocas equipado con agitador mecánico y sonda de temperatura. La solución se enfrió en un baño de hielo hasta 0-3°C y se añadió gota a gota durante 20 minutos una solución 3M de EtMgBr en Et2O (80 ml, 240,0 mmol), manteniendo la temperatura interna por debajo de 10°C. Se observó formación de un precipitado blanco (especies de cincato activas) después de la adición de aproximadamente 1/3 de la solución de Grignard. La mezcla se agitó durante 1,2 h a 0°C antes de que se añadiera gota a gota una solución del epóxido éster etílico del ácido (6 a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24-oico (43,0 g, 104,2 mmol) en THF (300 ml), manteniendo la temperatura interna por debajo de 10°C. Se añadió entonces CuCI sólido (1,03 g, 0,104 mmol) en dos porciones iguales con agitación vigorosa. Después de 10 minutos, se retiró el baño de enfriamiento y se continuó agitando a temperatura ambiente durante otras 1,2 horas. La reacción se inactivó mediante la adición gota a gota de NH4Cl acuoso saturado (800 ml) a < 15°C y se agitó durante 0,5 h. La mezcla se filtró y el sólido se aclaró con TBME (150 ml). Las fases se separaron y la fase acuosa se extrajo con TBME 2^250 ml. Los extractos orgánicos reunidos se lavaron con NaCl acuoso al 10% (2x200 ml), se secaron sobre Na2SO4 , se filtraron y se concentraron a vacío dando 43,7 g del éster etílico del ácido (6 p, 7a, 22É)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico bruto como una espuma amarilla.
Método 3
En una solución de ZnCl2 en THF (0,5 M, 8,7 ml, 4,85 mmol, 0,9 eq) se cargó THF anhidro (8,0 ml) y los contenidos se enfriaron entonces hasta -25°C. Se añadió una solución de EtMgBr en TBME (1,0 M, 8,7 ml, 8,70 mmol, 1,8 eq) durante 30 minutos y la mezcla se agitó durante 45 minutos a -25°C. Se añadió CuCl sólido (24 mg, 0,49 mmol, 0,05 eq) en una porción y se añadió una solución de éster etílico del ácido (6 a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24-oico (2,0 g, 4,85 mmol) en THF (8,0 ml) gota a gota durante 30 minutos. El CuCl sólido que quedaba (24 mg, 0,49 mmol, 0,05 eq) se añadió a medio camino mediante la adición de éster etílico del ácido (6 a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24-oico. La reacción se agitó durante 1 h a -25°C, (TLC 1:1 heptano:EtOAc, visualizado por UV y revelado usando tinción con molibdato cérico amónico) y luego se añadió más EtMgBr durante 10 minutos en TBME (1,0 M, 2,9 ml, 2,91 mmol, 0,6 eq). La reacción se agitó durante 0,5 h a -25°C y luego se inactivó mediante la adición de NH4Cl acuoso saturado (5 ml), manteniendo la temperatura por debajo de -5°C. Las sales inorgánicas se separaron por filtración, se aclararon con TBME y las fases filtradas se separaron. La capa acuosa se extrajo con TBME y luego se lavaron los extractos orgánicos reunidos con NH4Cl acuoso saturado (3 x 5 ml) y salmuera al 10% (3 x 6 ml). La fase orgánica se concentró a vacío a 40°C dando éster etílico del ácido (6 p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico bruto como una espuma amarilla (1,91 g).
Método 4
En una solución de ZnCl2 en THF (0,5 M, 8,7 ml, 4,85 mmol, 0,9 eq) se cargó THF anhidro (8,0 ml) y los contenidos se calentaron entonces hasta 40°C. Se añadió una solución de EtMgBr en TBME (1,0 M, 8,7 ml, 8,70 mmol, 1,8 eq) durante 30 minutos y la mezcla se agitó durante 45 minutos a 40°C. Se añadió CuCl sólido (24 mg, 0,49 mmol, 0,05 eq) en una porción y se añadió una solución de éster etílico del ácido (6 a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24
oico (2,0 g, 4,85 mmol) en THF (8,0 ml) gota a gota durante 30 minutos. El CuCI sólido que quedaba (24 mg, 0,49 mmol, 0,05 eq) se añadió a medio camino mediante la adición de éster etílico del ácido (6a, 7a, 22E)-6,7-epoxi-3-oxo-4.22- coladien-24-oico. La reacción se agitó durante 1 h a 40°C, (TLC 1:1 Heptano:EtOAc, visualizado por UV y revelado usando tinción con molibdato cérico amónico) y luego se inactivó mediante la adición gota a gota de NH4O acuoso saturado (5 ml). Las sales inorgánicas se separaron por filtración, se aclararon con TBME y las fases filtradas se separaron. La capa acuosa se extrajo con TBME y luego se lavaron los extractos orgánicos reunidos con NH4Cl acuoso saturado (3 x 5 ml) y salmuera al 10% (3 x 6 ml). La fase orgánica se concentró a vacío a 40°C dando éster etílico del ácido (6p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico bruto como una espuma amarilla (2,08 g).
Método 5
En una solución de ZnCl2 en THF (0,5 M, 8,7 ml, 4,85 mmol, 0,9 eq) se cargó THF anhidro (8,0 ml) y los contenidos se enfriaron entonces hasta -15°C. Se añadió una solución de EtMgBr en THF (1,0 M, 8,7 ml, 8,70 mmol, 1,8 eq) durante 30 minutos y la mezcla se agitó durante 45 minutos a -15°C. Se añadió CuCl sólido (24 mg, 0,49 mmol, 0,05 eq) en una porción y se añadió una solución de éster etílico del ácido (6a, 7a, 22E)-6,7-epoxi-3-oxo-4,22-coladien-24-oico (2,0 g, 4,85 mmol) en THF (8,0 ml) gota a gota durante 30 minutos. El CuCl sólido que quedaba (24 mg, 0,49 mmol, 0,05 eq) se añadió a medio camino mediante la adición de éster etílico del ácido (6a, 7a, 22E)-6,7-epoxi-3-oxo-4.22- coladien-24-oico. La reacción se agitó durante 1 h a -15°C, (TLC 1:1 heptano:EtOAc, visualizado por UV y revelado usando tinción con molibdato cérico amónico) y luego se añadió más EtMgBr en THF (1,0 M, 4,35 ml, 4,36 mmol, 0,9 eq) durante 15 minutos y luego se inactivó mediante la adición gota a gota de NH4Cl acuoso saturado (5 ml). Las sales inorgánicas se separaron por filtración, se aclararon con TBME y las fases filtradas se separaron. La fase acuosa se extrajo con TBME y luego se lavaron los extractos orgánicos reunidos con NH4Cl acuoso saturado (3 x 5 ml) y salmuera al 10% (3 x 6 ml). La fase orgánica se concentró a vacío a 40°C dando éster etílico del ácido (6p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico bruto como una espuma amarilla (1,94 g).
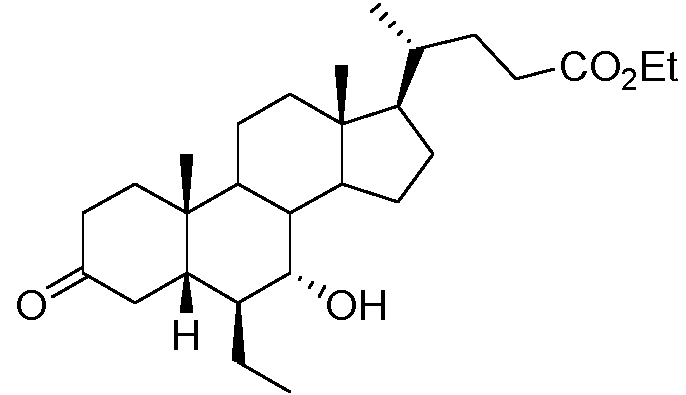
Ejemplo 4 - Síntesis de éster etílico del ácido (6p, 5P, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico
Método 1
A una suspensión de Pd al 10% peso/C (50% húmedo, 20 mg, 8,6 mol%) en DMF (2 ml) se añadió una solución de éster etílico del ácido (6p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico (50 mg, 0,11 mmol) en DMF (3 ml) y la mezcla de reacción se enfrió hasta 0°C. El matraz se evacuó y luego se llenó con hidrógeno tres veces con agitación vigorosa. Después de 3 h el matraz se evacuó y luego se llenó con argon y la mezcla se filtró mediante un filtro de jeringa. La mezcla se repartió entre TBME (30 ml) y H2O (20 ml). La fase orgánica se secó (Na2SO4) y se concentró a vacío. El producto bruto (50 mg) era una mezcla 14:1 de isómeros 5P a 5a (analizado por RMN de 1H) de éster etílico del ácido (6p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico, rendimiento 92%.
RMN de 1H (700 MHz, CDCh): 5 = 4,12 (2H, q, J = 7,1, OCH2CH3), 3,71 (1H, s ancho, C7H), 3,34 (1H, dd, J = 15,5, 13,6, C4H), 2,39-2,32 (2H, m), 2,24-2,20 (1H, m), 2,14-2,09 (2H, m), 2,03-1,91 (4H, m), 1,83-1,79 (2H, m), 1,68-1,63 (2H, m), 1,58 (1H, s), 1,55-1,12 (19H, m), 1,04 (3H, s), 0,95-0,93 (6H, m), 0,88 (1H, J = 7,0), 0,71 (3H, s). RMN de 13C (100 MHz, CDCl3): 5 = 213,5, 174,2, 72,1, 60,2, 55,9, 50,2, 49,8, 47,0, 46,7, 42,7, 39,5, 37,7, 36,3, 36,0, 35,7, 35,3, 34,2, 31,3, 31,0, 28,1, 27,7, 24,4, 23,8, 20,8, 18,3, 14,2, 13,9, 11,8. (IR) vmax(cm-1):3514, 2939, 2870, 1710, 1462, 1377, 1159, 1099, 1032; HRMS (ESI-TOF) m/z: (M-H2O+H)+ calculado para C28H45O3 429,3369; encontrado: 429,3363.
Método 2
Se disolvió éster etílico del ácido (6p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico (20,0 g) en DMF (400 ml) y se añadió bajo argón a Pd al 10% peso/C sólido (50% húmedo, 10,0 g). La mezcla se enfrió en un baño de hielo-sal hasta aproximadamente -15°C y el matraz se evacuó y luego se llenó con hidrógeno tres veces con agitación vigorosa. La mezcla se agitó bajo una atmósfera de hidrógeno durante 6 h y luego se evacuó el matraz, se llenó con argón y se filtró a través de un lecho de Celite. El catalizador se aclaró con 400 ml de TBME. El filtrado se lavó con NaCl acuoso al 10% (400 ml) y la fase acuosa se extrajo con TBME (400 ml). Las fases orgánicas reunidas se lavaron con NaCl acuoso al 10% (3 x 200 ml), se secaron sobre Na2SO4 , se filtraron y se concentraron a vacío dando éster etílico del ácido (6p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico bruto (20,0 g, relación aproximadamente 28:1 de 5Hp:5Ha) como aceite amarillo pálido.
Método 3
Se cargó Pd al 10%/C en un recipiente de reacción encamisado de acero inoxidable bajo una atmósfera de argón; se añadió DMF (20 ml), seguido de una solución de éster etílico del ácido (6 p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico bruto del Ejemplo 3 (aproximadamente 72,6 mmol) en DMF (130 ml). La mezcla de reacción se enfrió hasta -25°C (durante aproximadamente 40 minutos) con agitación vigorosa (1200 rpm). El recipiente de reacción se evacuó y se cargó con hidrógeno (10-12 bar) tres veces. La mezcla se agitó durante 16 h bajo una atmósfera de hidrógeno (1000-1200 kPa). El recipiente se evacuó, se purgó con argón y se calentó hasta 20°C con agitación. La TLC de la mezcla de reacción (heptano:EtOAc 1:1, revelado usando molibdato cérico amónico o baño de vainillina, valores Rf: Material de partida = 0,42, producto = 0,67) indicó el consumo completo del material de partida. La suspensión se diluyó con CH3CN (120 ml) y H2O (30 ml) y la suspensión se filtró a través de un papel de filtro GFA y la torta del filtro se aclaró con CH3CN (60 ml). La mezcla se lleva a la etapa siguiente sin purificación posterior. La mezcla contenía aproximadamente 5% del isómero 5H-a.
Optimización
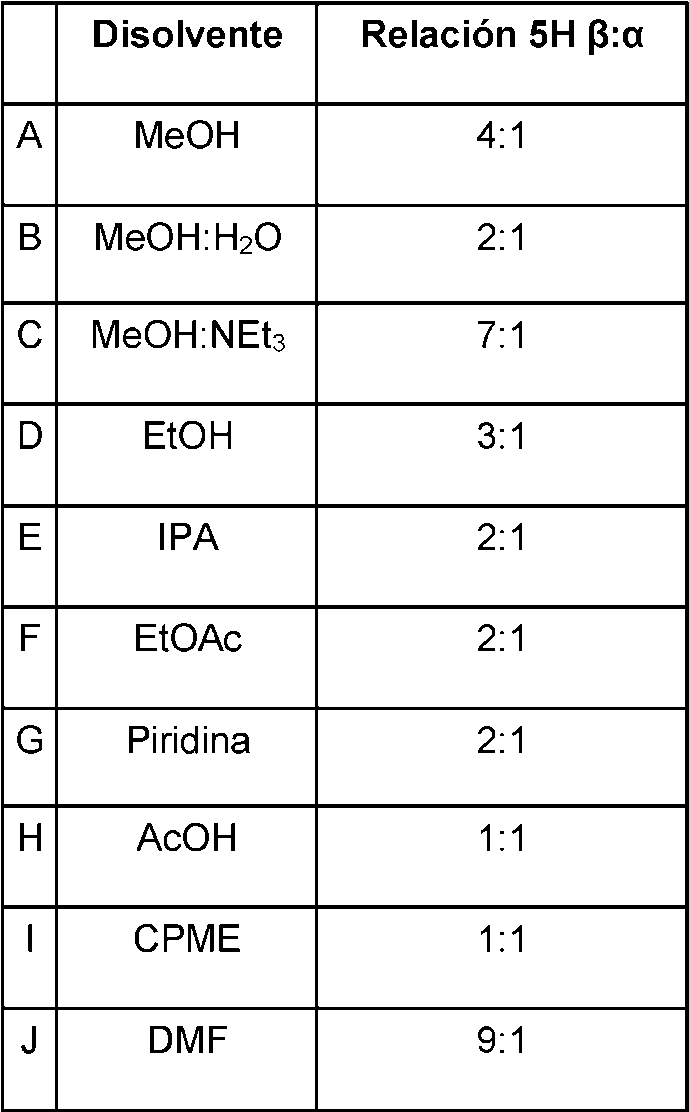
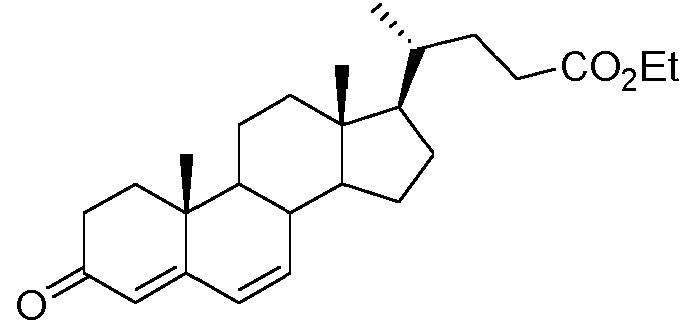
La reacción de hidrogenación de este ejemplo transcurre a través del intermedio mostrado a continuación y produce tanto el compuesto requerido 5Hp como su isómero 5Ha. Se llevó a cabo una prueba con disolvente y catalizador para determinar las condiciones de reacción que conducen al mayor rendimiento y las mayores relaciones de isómero 5Hp a isómero 5Ha.
La prueba de disolvente se llevó a cabo usando catalizador de Pd al 10% en peso/C y las reacciones se realizaron a temperatura ambiente bajo presión atmosférica de hidrógeno. La reacción realizada en MeOH en presencia de NEt3 fue más selectiva que la realizada en MeOH puro, mientras que la adición de 10% de H2O redujo la selectividad por 5pH. La reacción en DMF proporcionó la mejor relación p:a. La reacción en piridina dio baja conversión al producto requerido fundamentalmente con material de partida e intermedio presente en la mezcla.
Se probaron reacciones en DMF y MeOH en un intervalo de temperaturas. Para las reacciones realizadas en DMF la temperatura tiene un impacto sustancial sobre la selectividad (la selectividad disminuye al aumentar la temperatura),
mientras que se observó poca diferencia para reacciones en MeOH.
Las reacciones en DMF y MeOH se probaron en una gama de catalizadores de Pd al 5 y 10% disponibles comercialmente, sobre soporte de carbón, carbonato de calcio, sulfato de bario y óxido de aluminio.
Las reacciones se realizaron en 10 volúmenes de disolvente a -15°C bajo presión atmosférica de hidrógeno gas. Para reacciones realizadas en DMF la presión tiene menor impacto sobre la selectividad que la temperatura. El efecto de la dilución sobre la selectividad es insignificante.
Ejemplos 5 a 14 - Síntesis de éster etílico del ácido (6p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico a partir de ácido desoxicólico
Ejemplo 5 - Síntesis de éster metílico del ácido (3a, 5p)-3-acetoxi-12-oxo-colan-24-oico
En una solución de ácido desoxicólico (500 g, 1,27 mol) en MeOH (1,5 l) se cargó H2SO4 (0,68 ml, 12,7 mmol) y la reacción se calentó hasta 64°C hasta finalización. La reacción se enfrió hasta 55°C y se cargó piridina (2,06 ml, 25,4 mmol). Se eliminó el MeOH (800 ml) por destilación y la reacción se enfrió hasta 50°C. Se cargó EtOAc (500 ml) y continuó la destilación. Esta coevaporación se repitió hasta que el contenido en MeOH era <0,5%. La reacción se enfrió hasta 40°Cy se cargó EtOAc (1,01) seguido de piridina (134 ml, 1,65 mol) y DMAP (1,1 g, 8,89 mmol). Se añadió anhídrido acético (150 ml, 1,58 mmol) gota a gota y el recipiente de reacción se agitó a 40°C hasta finalización. La reacción se enfrió hasta 22°C y se añadió H2SO4 acuoso 2M (1500 ml) manteniendo la temperatura por debajo de 25°C. La fase acuosa se separó y la fase orgánica se lavó con agua (1,2 l), solución acuosa saturada de NaHCO3 (1,2 l x 2) y agua (1,2 l). Se cargó AcOH (1,0 l) en la capa orgánica, seguido de NaBr (6 , 6 g, 63,5 mmol). Se cargó solución acuosa al 16,4% de NaOCI (958 ml, 2,54 mol) gota a gota manteniendo la temperatura de reacción por debajo de 25°C. La reacción se agitó hasta finalización, luego se enfrió hasta 10°C y se agitó durante 90 minutos. Los sólidos resultantes se recogieron por filtración, se lavaron con agua (3 x 500 ml) y la torta del filtro se secó bajo vacío a 40°C. Los sólidos se cristalizaron en MeOH (10 vol) dado éster metílico del ácido (3a, 5p)-3-acetoxi-12-oxo-colan-24-oico como un sólido blanquecino (268 g).
Ejemplo 6 - Síntesis de éster metílico del ácido (3a, 5P)-3-acetoxi-colan-24-oico
Se cargó éster metílico del ácido (3a, 5P)-3-acetoxi-12-oxo-colan-24-oico (268 g, 0,6 mol) en el recipiente de reacción bajo argón, seguido de AcOH (1,8 l). Se añadió entonces tosil hidrazina (190 g, 1,02 mol) manteniendo la temperatura de reacción a 25°C. La reacción se agitó hasta finalización y luego se cargó NaBH4 (113,5 g, 3,00 mol) en varias porciones manteniendo la temperatura por debajo de 25°C. La mezcla de reacción se agitó hasta finalización y luego se enfrió mediante la adición gota a gota de agua (1,34 l) manteniendo la temperatura por debajo de 25°C. La mezcla de reacción se agitó durante 30 minutos, los sólidos resultantes se recogieron por filtración, se lavaron con agua (3 x 270 ml) y el sólido se secó bajo vacío a 40°C. Los sólidos se cristalizaron en MeOH (3 vol) dando éster metílico del ácido (3a, 5p)-3-acetoxi-colan-24-oico como un sólido blanquecino (214,5 g).
En una solución de éster metílico del ácido (3a, 5p)-3-acetoxi-colan-24-oico (214,5 g, 0,50 mol) en IPA (536 ml) se cargó agua (536 ml) y 50% p/p de NaOH (99 g, 1,24 mol). La reacción se calentó hasta 50°C y se agitó hasta finalización. Se cargó H2SO42M lentamente con agitación vigorosa hasta que se obtuvo un pH 2-3 y luego se enfrió la reacción hasta 20°C. Los sólidos resultantes se recogieron por filtración, se lavaron con agua (3 x 215 ml) y el sólido resultante se secó bajo vacío a 40°C dando ácido (3a, 5p)-3-hidroxi-colan-24-oico (176,53 g)
Ejemplo 8 - Síntesis de éster etílico del ácido (5p)-3-oxocolan-24-oico
En una solución de ácido (3a, 5p)-3-hidroxi-colan-24-oico (10 g, 26,5 mmol) en EtOH (50 ml) se cargó H2SO496% (14 |jl, 0,27 mmol) y la mezcla de reacción se calentó entonces hasta reflujo durante 16 h. Se cargó entonces piridina, la mezcla se agitó durante 30 minutos y se concentró a vacío a 40°C. El residuo se disolvió en EtOAc (30 ml) y luego se cargó AcOH (10 ml) y NaBr (136 mg, 1,33 mmol). La solución se enfrió hasta 5°C y se cargó NaOCI 9% (27 ml, 39,8 mmol) gota a gota manteniendo la temperatura por debajo de 10°C. La suspensión resultante se calentó hasta temperatura ambiente y se agitó durante 1 h. La mezcla de reacción se enfrió hasta 0°C durante 10 minutos, los sólidos se recogieron por filtración y se lavaron con agua (3 x 3 vol). El sólido resultante se secó bajo vacío a 40°C dando éster etílico del ácido (5P)-3-oxocolan-24-oico (7,83 g).
Ejemplo 9 - Síntesis de éster etílico del ácido (4a, 5P)-3-oxo-4-bromo-colan-24-oico
A una solución de éster etílico del ácido (5p)-3-oxocolan-24-oico (8,0 g, 19,9 mmol) en AcOH (84 ml) se añadió Br2 en AcOH (16 ml, 21,9 mmol) gota a gota durante 15 minutos. La mezcla de reacción se agitó durante 10 minutos, luego se diluyó con EtOAc (250 ml), se lavó con agua (2 x 200 ml) y se concentró a vacío a 40°C. El material bruto se purificó por cromatografía en columna (30% de Heptano: EtOAc) y se concentró a vacío a 40°C dando éster etílico del ácido (4a, 5p)-3-oxo-4-bromo-colan-24-oico como un sólido cristalino pálido (7,49 g).
Ejemplo 10 - Síntesis de éster etílico del ácido 3-oxo-4-colen-24-oico
En una solución de éster etílico del ácido (4a, 5p)-3-oxo-4-bromo-colan-24-oico (4,0 g, 8,33 mmol) en DMF (40 ml) se cargó U2CO3 (4,0 g, 1 eq masa) y LiBr (2,0 g, 0,5 eq masa). La mezcla se calentó hasta 150°C durante 2 h luego se
dejó enfriar hasta temperatura ambiente y se vertió en una mezcla de agua y hielo (200 g, 50 volúmenes) y AcOH ( 8 ml). La suspensión resultante se agitó durante 15 minutos, los sólidos se recogieron por filtración y luego se purificaron por cromatografía en columna (30% de Heptano: EtOAc) dando éster etílico del ácido 3-oxo-4-colen-24-oico como un sólido cristalino pálido (1 , 68 g).
Ejemplo 11 - Síntesis de éster etílico del ácido 3-oxo-4,6-coladien-24-oico.
Se cargó éster etílico del ácido 3-oxo-4-colen-24-oico (2,23 g, 5,57 mmol) en un recipiente de reacción, seguido de AcOH (6,7 ml) y tolueno (2,23 ml). Se cargó cloranilo (1,5 g, 6,13 mmol) y la mezcla de reacción se calentó hasta 100°C durante 2 h (IPC por TLC, EtOAc: Heptano 3:7; visualizado por tinción con anisaldehído). La mezcla de reacción se enfrió hasta 10°C durante 10 minutos y el sólido resultante se separó por filtración. La torta del filtro se lavó con DCM (9 vol) y el filtrado resultante se concentró luego a vacío a 40°C. El residuo se disolvió en acetona (9 vol) luego se añadió NaOH acuoso al 3% p/p (27 vol) gota a gota manteniendo la temperatura por debajo de 30°C. La mezcla resultante se enfrió en un baño de hielo durante 10 minutos y los sólidos se recogieron por filtración. La torta del filtro se lavó con agua (2 x 9 vol) y acetona: agua 2:1 (4 vol). La purificación por cromatografía en columna (0-30% de Heptano: EtOAc) dio éster etílico del ácido 3-oxo-4,6-coladien-24-oico como un sólido cristalino pálido (1,45 g)
Ejemplo 12 - Síntesis éster etílico del ácido de (6 a, 7a)-6,7-epoxi-3-oxo-4-colen-24-oico
Se cargó éster etílico del ácido 3-oxo-4,6-coladien-24-oico (1,37 g, 4,27 mmol) en un recipiente de reacción, seguido de BHT (23 mg, 0,13 mmol), EtOAc (11 ml) y agua (3,4 ml) con agitación. La solución se calentó hasta 80°C y luego se añadió, gota a gota durante 15 minutos una solución de mCPBA 70% (1,5 g, 7,51 mmol) en EtOAc (7,5 ml). La mezcla de reacción se agitó a 70°C durante 2 h (IPC por TLC, EtOAc: Heptano 3:7; visualizado con tinción con anisaldehído), se enfrió hasta temperatura ambiente y luego se lavó con NaOH acuoso 1 M ( 2 x 2 0 ml) seguido de NaS2O3 acuoso al 10%: NaHCO3 al 2% (3 x 20 ml). Las fases orgánicas se secaron sobre Na2SO4 y se concentraron a vacío a 40°C. Los sólidos brutos se cristalizaron en EtOAc (3 vol) a 60°C dando un sólido blanquecino que se secó bajo vacío a 40°C dando éster etílico del ácido (6 a, 7a)-6,7-epoxi-3-oxo-4-colen-24-oico (0,90 g).
Ejemplo 13 - Síntesis de éster etílico del ácido (6p,7a)-6-etil-7-hidroxi-3-oxo-4-colen-24-oico
Se cargó ZnCl2 (600 mg, 4,25 mmol) en un recipiente de reacción y se secó bajo vacío a 180°C durante 1 h. El recipiente de reacción se enfrió hasta temperatura ambiente, se cargó THF (15 ml) y los contenidos del recipiente de reacción se enfriaron hasta 3°C. Se cargó una solución de EtMgBr 3M en Et2O (1,5 ml, 4,25 mmol) en el recipiente de reacción durante 40 minutos manteniendo la temperatura por debajo de 5°C. La mezcla de reacción se agitó luego durante 1 hora. Se cargó éster etílico del ácido (6 a, 7a)-6,7-epoxi-3-oxo-4-colen-24-oico (0,80 g, 1,93 mmol) en THF ( 6 ml) en el recipiente de reacción durante 40 minutos, manteniendo la temperatura por debajo de 5°C. Se cargó CuCl (20 mg, 0,19 mmol) en una porción y la reacción se agitó a temperatura ambiente durante 16 h (IPC por TLC, EtOAc: Heptano 3:7; visualizado con tinción con anisaldehído). La mezcla de reacción se enfrió en un baño de hielo y se
añadió NH4CI acuoso saturado gota a gota, manteniendo la temperatura por debajo de 10°C. La mezcla de reacción se filtró y la torta del filtro se lavó con TBME (12,5 vol). La fase orgánica del filtrado se separó y la fase acuosa se extrajo con TBME (2 x 12,5 vol). Las fases orgánicas reunidas se lavaron con NaCl al 5% (3 x 12,5 vol) y se concentraron a vacío a 40°C.
Ejemplo 14 - Síntesis de éster etílico del ácido (6 P, 5P, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico
Se cargó Pd al 10%/C (70 mg) en un recipiente de reacción bajo una atmósfera de argón seguido del material bruto del Ejemplo 13 en DMF (14,6 ml). La mezcla se enfrió hasta -10°C y el recipiente de reacción se evacuó y luego se llenó con hidrógeno tres veces con agitación vigorosa. La mezcla se agitó bajo una atmósfera de hidrógeno durante 24 h mientras se mantenía la temperatura a -10°C (IPC por TLC, eluyente EtOAc: Heptano 1:1; visualizado con tinción con anisaldehído) luego se evacuó el matraz, se llenó con argón y se filtró a través de una almohadilla de Celite y se aclaró con DMF ( 7 ml). Se volvió a cargar Pd al 10%/C (70 mg) en el recipiente de reacción bajo una atmósfera de argón seguido de mezcla de reacción en DMF. La mezcla se enfrió hasta aproximadamente -10°C y el recipiente de reacción se evacuó y luego se llenó con hidrógeno tres veces con agitación vigorosa. La mezcla se agitó bajo una atmósfera de hidrógeno durante 24 h a -10°C (IPC por TLC, EtOAc 1:1: Heptano; visualizado con tinción con anisaldehído) luego se evacuó el matraz, se llenó con argón y se filtró a través de una almohadilla de Celite y se lavó con TBME (62,5 vol, 50 ml). El filtrado se lavó con NaCl acuoso al 10% (4 x 25 vol), se secó sobre Na2SO4 , se filtró y se concentró a vacío a 40°C. La purificación por cromatografía en columna (SiO2 , 0-30% de Heptano: EtOAc) dio éster etílico del ácido (6P, 5P, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico (0,17 g). El producto era idéntico al material obtenido de éster etílico del ácido (6p, 7a, 22E)-6-etil-7-hidroxi-3-oxo-4,22-coladien-24-oico de origen vegetal (véase Ejemplo 4).
Ejemplos 15 a 17 - Conversión de éster etílico del ácido (6p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico en ácido (3a, 5p, 6a, 7a)-6-etil-3,7-dihidroxi-colan-24-oico
Ejemplo 15 - Síntesis de éster etílico del ácido (6p, 5P)-3,7-dioxo-6-etil-colan-24-oico
Método 1
Una solución de reactivo de Jones preparado a partir de CrO3 (1,10 g, 11 mmol) en H2SO4 (1,4 ml) y diluida hasta 5 ml con agua se cargó gota a gota en una solución de éster etílico del ácido (6P, 5P, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico (0,18 g, 0,40 mmol) en acetona (10 ml) hasta persistencia de un color naranja. La mezcla de reacción se enfrió con IPA (1 ml), se filtró a través de un filtro de jeringa de nailon de 0,45 pm y el filtro se lavó con acetona (10 ml). El filtrado reunido y el lavado se concentraron, el residuo se disolvió en EtOAc (20 ml) y se lavó con agua (2 x 10 ml). La fase acuosa se extrajo con EtOAc (20 ml), las fases de EtOAc reunidas se concentraron y el residuo se disolvió y concentró en tolueno (20 ml) y luego acetona (20 ml) dando un aceite trasparente que contenía éster etílico del ácido (6P, 5P, 7a)-6-etil-7-hidroxi-3,7-dioxo-colan-24-oico (185 mg).
RMN de 1H (700 MHz, CDCh): 5 = 4,12 (2H, q, J = 7,1), 2,42 (1H, t, J = 11,4), 2,38-2,17 (6H, m), 2,09-1,74 (9H, m), 1,68-1,11 (17H, m), 0,93 (3H, d, J = 6,5), 0,85 (3H, t, J =7,4), 0,72 (3H, s). RMN de 13C (100 MHz, CDCh): 5 = 214,5, 211,4, 174,0, 60,1, 57,1, 55,1, 50,3, 48,4, 47,3, 44,9, 43,6, 43,1, 39,2, 35,8, 35,2 (x2), 34,9, 31,3, 30,9, 28,1, 24,6, 23,7, 23,4, 21,7, 18,3, 14,2, 12,6, 12,2. (IR) vmax(cm-1): 2950, 2872, 1709, 1461, 1377, 1304, 1250, 1177, 1097, 1034; HRMS (ESI-TOF) m/z: (M+H)+ calculado para C28H45O4445,3318; encontrado: 445,3312;
Método 2
A una solución de éster etílico del ácido (6 p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico (41,0 g masa en bruto) en CH2CI2 anhidro (600 ml) a 0°C se añadió DMP sólido (34,0 g, 80,2 mmol) en varias porciones durante 20 minutos (exotérmica). La mezcla se agitó a 0-5°C durante 2 h, luego se añadió una porción más de DMP (4,0 g, 9,4 mmol) y la reacción se agitó a 0-5°C durante 1 h. La mezcla se filtró a través de un filtro GFA y el sólido se aclaró con CH2O 2 (50 ml), el filtrado se agitó vigorosamente con Na2S2O3 acuoso al 10 % y NaHCO3 acuoso al 2 % ( 1 0 0 ml) durante 20 minutos. Las fases se separaron y la acuosa se extrajo con CH2Cl2 (2 x 100 ml). Los extractos orgánicos reunidos se lavaron con NaOH 1M (100 ml). La mezcla se diluyó con CH2O 2 (300 ml) y se separaron las fases. La capa orgánica se concentró a presión reducida y el residuo (aceite pardo turbio) se disolvió en TBME (600 ml) y se lavó con NaOH 1M (100 ml) y NaCl (3 x 100 ml). La fase orgánica se concentró a vacío dando un aceite fluido amarillo oscuro, masa en bruto 38,1 g. El aceite se disolvió en EtOH (400 ml) y se agitó con carbón activado (10 g) a 50°C, la mezcla se filtró seguidamente, el carbón se aclaró con EtOH (200 ml) y el filtrado se concentró a vacío dando éster etílico del ácido (6 p, 5p)-3,7-dioxo-6-etil-colan-24-oico como un aceite amarillo (35,9 g).
Método 3
Una solución de éster etílico del ácido (6 p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico (218 mmol) en DMF (450 ml), CH3CN (540 ml) y H2O (90 ml) se cargó en un recipiente de 2 l y se enfrió hasta 9°C, luego se cargó AcOH (180 ml), seguido de NaBr (4,1 g). Se añadió una solución de hipoclorito de sodio (-10,5% p/v, 450 ml) gota a gota durante 1,5 h, manteniendo la temperatura interna a 5-6°C, luego se agitó la mezcla durante 5 h a 7°C. La TLC de la mezcla de reacción indicó consumo total del material de partida (IPC por TLC, eluyente EtOAc/heptano 3:7, Rf para éster etílico del ácido (6 p, 5p, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico = 0,34; éster etílico del ácido (6 p, 5P)-3,7-dioxo-6-etil-colan-24-oico = 0,45). Se cargó una solución de Na2SO3 acuoso al 10% p/v (360 ml) gota a gota con agitación vigorosa, manteniendo la temperatura interna a 8-10°C, luego se añadió H2O (270 ml) gota a gota y la mezcla se agitó a 5°C durante 16 h. El sólido se filtró y se lavó con H2O (720 ml). El sólido se disolvió entonces en TBME (1,1 l) y seguidamente se lavó con NaHCO3 acuoso (300 ml) y salmuera al 10% (300 ml). La fase orgánica se agitó entonces con carbón activado ( 1 0 g) durante 2 0 minutos a 40°C, se trató con MgSO4 anhidro (5 g) y se filtró a través de papel de filtro GFA, la torta del filtro se aclaró con TBME (50 ml) y el filtrado se concentró a vacío dando éster etílico del ácido (6 p, 5p)-3,7-dioxo-6-etil-colan-24-oico como aceite marrón claro que solidifica en reposo (82,7 g).
Ejemplo 16 - Síntesis de ácido (6 a, 5p)-3,7-dioxo-6-etil-colan-24-oico
En un matraz de 500 ml se cargaron 0,5 vol de NaOH 0,5 M (9 ml) seguido de éster etílico del ácido (6 p, 5p)-3,7-dioxo-6-etil-colan-24-oico del Ejemplo 15 (18,00 g, 1 eq) y luego IPA ( 1 8 0 ml, 10 vol) (la carga inicial de NaOH fue para evitar la posibilidad de formación del cetal C3). La mezcla se calentó hasta 60 ± 2°C y se mantuvo hasta que se obtuvo una solución (10-15 minutos). El resto de la solución de NaOH 0,5 M (171 ml, 9,5 vol) se cargó durante 20 minutos y luego se agitó la reacción durante otras 3,5 horas a 60 ± 2°C. Se eliminó IPA bajo vacío a 60°C y luego se cargó HCl 2M ( 8 ml) hasta pH 9. Se cargó EtOAc (90 ml, 5 vol) seguido de HCl 2M (54 ml) hasta pH 1. La mezcla vigorosa fue seguida de separación de fases. La fase acuosa se volvió a extraer con más EtOAc (90 ml, 5 vol) y luego se lavaron las fases orgánicas reunidas con agua (54 ml, 3 vol), seguido por tres porciones de NaCl acuoso al 10% (3 x 54 ml, 3 x 3 vol). La fase orgánica se trató con carbón activado (polvo de 100 mallas, 3,37 g, -0,20 equivalente en masa) durante 12 minutos y luego se filtró a través de GF/B. La concentración a 50°C a vacío dio ácido (6 a, 5p)-3,7-dioxo-6-etil-colan-24-oico como una espuma amarilla con rendimiento cuantitativo.
RMN de 1H (700 MHz, CDCI3): 5 = 2,74 (1H, dd, J = 12,8, 5,4), 2,47 (1H, t, J = 12,5), 2,43-0,90 (32H, m), 0,81 (3H, t, J = 7,4), 0,70 (3H, s). RMN de 13C (100 MHz, CDCI3): 5 = 212,1,210,6, 179,4, 54,9, 52,4, 52,3, 50,0, 48,9, 43,7, 42,7, 38,9, 38,3, 36,7, 36,0, 35,5, 35,2, 30,9, 30,7, 28,2, 24,6, 22,9, 22,3, 18,6, 18,3, 12,1, 11,8. (IR) Vmax(cm-1): 2939, 2873, 1706, 1458, 1382, 1284,8. HRMS (ESI-TOF) m/z: (M+H)+ calculado para C26H41O4417,3005; encontrado: 417,2997; p.f. = 71,2-75,9°C
Ejemplo 17 - Síntesis de ácido (3a, 5P, 6a, 7a)-6-etil-3,7-dihidroxi-colan-24-oico
A una solución de ácido (6a, 5P)-6-etil-3,7-dioxo-colan-24-oico (21,7 g masa en bruto) en H2O (260 ml) y NaOH al 50% (15,2 ml) a 90°C se añadió, gota a gota, una solución de NaBH4 (4,4 g, 116,3 mmol) en NaOH acuoso (preparado a partir de 25 ml de H2O y 0,8 ml de NaOH al 50%). La mezcla se calentó hasta reflujo y se agitó durante 3 h. La mezcla se enfrió entonces hasta 60°C y se añadió una solución 2M de HCl (200 ml) gota a gota con agitación vigorosa. Se cargó entonces nBuOAc (100 ml) en el matraz de reacción y la mezcla se agitó durante otros 20 minutos. Las fases se separaron y la fase acuosa (pH = 1/2) se extrajo con nBuOAc (100 ml). Las fases orgánicas reunidas se lavaron con HCl 2M (50 ml) y NaCl acuoso al 10% (100 ml). El disolvente orgánico se eliminó por destilación bajo presión reducida a 70-80°C. El residuo (aceite denso) se disolvió en nBuOAc (60 ml) a 70°C y se dejó enfriar gradualmente hasta temperatura ambiente, luego se almacenó a 6°C durante 2 h. El sólido se recogió por filtración, se aclaró con nBuOAc frío (20 ml), luego se secó bajo vacío a 70°C durante 5h dando ácido (3a, 5P, 6a, 7a)-6-etil-3,7-dihidroxicolan-24-oico como un sólido blanco (8,2 g).
Claims (1)
- REIVINDICACIONES1. Un compuesto de fórmula general (I):en donde:R1 es alquilo C1-4 opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, OR6 o NR6R7; donde cada uno de R6 y R7 está seleccionado independientemente de H o alquilo C1-4;R2 es H, halo u OH o un OH protegido;Y1 es un enlace o un grupo enlazador alquileno que tiene de 1 a 20 átomos de carbono y opcionalmente sustituido con uno o más grupos R3;cada R3 es independientemente halo, OR8 o NR8R9;donde cada uno de R8 y R9 está seleccionado independientemente de H o alquilo C1-4;yR4 es C(O)OR10, OC(O)R10, C(O)NR10R11, OR10, OSi(R13)3, S(O)R10, SO2R10, OSO2R10, SO3R10 o OSO3R10; donde cada R10 y R11 es independientemente:a. hidrógeno ob. alquilo C1-20, alquenilo C2-20, alquinilo C2-20, -O-alquilo C1-20, -O-alquenilo C2-20 u -O-alquinilo C2-20, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, NO2 , CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 , o un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con alquilo C1-6, haloalquilo C1-6, halo, NO2 , CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 ; oc. un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes seleccionados de alquilo C1-6, haloalquilo C1-6, halo, NO2 , CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 ; od. un residuo de polietilenglicol;cada R19 está seleccionado independientemente de H, alquilo C1-6, haloalquilo C1-6, o un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con halo, alquilo C1-6 o haloalquilo C1-6;cada R13 es independientementea. alquilo C1-20, alquenilo C2-20 o alquinilo C2-20 opcionalmente sustituido con uno o más sustituyentes seleccionados de halo, NO2 , CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 , un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con alquilo C1-6, haloalquilo C1-6, halo, NO2 , CN, OR19, SO2R19, SO3R19 o N(R19)2 ; ob. un grupo arilo de 6 a 14 miembros o heteroarilo de 5 a 14 miembros, cualquiera de los cuales está opcionalmente sustituido con uno o más sustituyentes seleccionados de alquilo C1-6, haloalquilo C1-6, halo, NO2 , CN, OR19, SR19, SO2R19, SO3R19 o N(R19)2 ;cada R19 está seleccionado independientemente de H, alquilo C1-6 o haloalquilo C1-6;R5 es H u OH o un OH protegido;o una sal o una variante isotópica del mismo.2. Un compuesto según la reivindicación 1, donde, independientemente o en cualquier combinación: Y1 es un grupo enlazador alquileno que tiene de 1 a 8 átomos de carbono y opcionalmente sustituido con uno o más grupos R3, donde R3 es como se define en la reivindicación 1;R5 es H u OH.3. Un compuesto según la reivindicación 1, donde, independientemente o en cualquier combinación:R1 es etilo; y/oR2 es H; y/oY1 es un enlace, -CH2- o -CH2CH2-, y/oR4 es C(O)OR10, donde R10 es H, alquilo C1-6 o bencilo; y/oR5 es H.4. Un compuesto según la reivindicación 1 que es ácido (6 p, 5P, 7a)-6-etil-7-hidroxi-3-oxo-colan-24-oico o los ásteres de alquilo C1-6 y bencilo del mismo y sales del mismo, especialmente los ásteres metílico y etílico.5. Un proceso para la preparación de un compuesto de fórmula general (I) según una cualquiera de las reivindicaciones 1 a 4 que comprende, o bien:A. reducir un compuesto de fórmula general (II):donde R1, R2, R4 y R5 son como se definen en la reivindicación 1; yY es un enlace o un grupo enlazador alquileno, alquenileno o alquinileno que tiene de 1 a 20 átomos de carbono y opcionalmente sustituido con uno o más grupos R3, donde R3 es como se define en la reivindicación 1; o B. convertir un compuesto de fórmula general (I) en la que R4 es C(O)OR10 en un compuesto de fórmula general (I) en la que R4 es C(O)NR10R11, S(O)R10, SO2R10, OSO2R10, SO3R10 u OSO3R10; donde R10 y R11 son como se definen en la reivindicación 1.6. Un proceso según la reivindicación 5 donde la reducción se lleva a cabo por hidrogenación catalítica.7. Un proceso según la reivindicación 6 donde la hidrogenación catalítica se lleva a cabo usando un catalizador seleccionado de un catalizador de paladio/carbono, paladio/carbonato de calcio, paladio/óxido de aluminio, platino/paladio o níquel Raney.8. Un proceso según la reivindicación 6 o la reivindicación 7 donde el catalizador es un catalizador de paladio/carbono o paladio/carbonato de calcio y en el catalizador el paladio está presente en una cantidad de 5-10% en peso con respecto al peso de la matriz (donde la matriz es el carbono, carbonato de calcio, etc.).9. Un proceso según una cualquiera de las reivindicaciones 6 a 8 donde la hidrogenación catalítica se lleva a cabo en un disolvente seleccionado de disolventes alcohol tales como metanol, etanol o isopropanol; acetato de etilo; piridina; ácido acético; ciclopentil metil éter (CPME) o W,W-dimetilformamida (DMF), cualquiera de los cuales puede estar opcionalmente mezclado con un disolvente común tal como acetona o agua y/o una base tal como trietilamina. 10. Un proceso según la reivindicación 9 donde el disolvente es metanol que opcionalmente comprende una cantidad subestequiomátrica de una base tal como trimetilamina.11. Un proceso según la reivindicación 9 donde el disolvente es DMF opcionalmente mezclado con un disolvente común tal como acetona, TBME, THF, acetonitrilo o acetona/agua y que opcionalmente comprende una cantidad subestequiométrica de una base tal como trietilamina.12. Un proceso para la preparación de un compuesto de fórmula general (XIX):donde Y1, R1 y R4 son como se definen en la fórmula general (I) en la reivindicación 1;R2 es H, halo u OH;R5a es H u OH;comprendiendo el proceso:i. oxidación del compuesto de fórmula general (I) según una cualquiera de las reivindicaciones 1 a 4 usando un agente oxidante adecuado para dar un compuesto de fórmula general (XX):ii. epimerización del compuesto de fórmula general (XX) para dar un compuesto de fórmula general (XXI):donde Y1, R1 y R4 son como se definen en la fórmula general (I);R2 es H, halo u OH o un grupo OH protegido que es estable en condiciones básicas; yR5b es H u OH o un grupo OH protegido que es estable en condiciones básicas; yiii. reducción del compuesto de fórmula general (XXI) usando un agente reductor adecuado, y cuando R2 y/o R5b es un OH protegido, retirada del grupo o grupos protectores, para dar un compuesto de fórmula general (XIX) como se define antes, donde la retirada del grupo protector puede tener lugar antes o después de la reducción; y opcionalmenteiv. conversión de un compuesto de fórmula general (XIX) en la que R4 es C(O)OR10 en un compuesto de fórmula general (XIX) en la que R4 es C(O)R10, C(O)NR10R11, S(O)R10, SO2R10 y OSO2R10, donde R10 y R11 son como se definen en la reivindicación 1.13. Un proceso según la reivindicación 12 donde, en la etapa i la reacción de oxidación se lleva a cabo usando un peryodinano de Dess-Martin (1,1,1-triacetoxi-1,1-dihidro-1,2-benziodoxol); un hipoclorito, por ejemplo, hipoclorito de sodio, en condiciones ácidas; una reacción de Jones usando dicromato de sodio o, más normalmente, trióxido crómico en ácido sulfúrico diluido; o TEMPO ((2,2,6,6-Tetrametil-piperidin-1-il)oxi) o un derivado del mismo; y/oen la reacción de epimerización de la etapa ii, el compuesto de fórmula general (XX) se disuelve en un disolvente alcohol, opcionalmente mezclado con agua y se pone en contacto con una base, por ejemplo, hidróxido de sodio o potasio, o un alcóxido de sodio o potasio, típicamente un etóxido; y/oen la etapa iii, el agente reductor es un hidruro tal como borohidruro de sodio.14. Un proceso según la reivindicación 12 o la reivindicación 13 donde, en el compuesto de fórmula general (XX), R4 es C(O)OR10, y en la etapa ii la base es hidróxido de sodio o potasio y la epimerización se lleva a cabo por hidrólisis para dar un compuesto de fórmula general (XXI) en la que R4 es C(O)OH; y/oen el compuesto de fórmula general (XX), R2 y/o R5 es un grupo OC(O)OR14, donde R14 es alquilo C1-6 o bencilo; y donde la etapa de epimerización proporciona un compuesto de fórmula general (XXI) en la que R2 y/o R5b es OH; oen el compuesto de fórmula general (XX), R2 y/o R5 es un OH protegido que es estable en condiciones básicas y el proceso comprende además la etapa de retirar el grupo protector antes o después de la etapa iii.15. Un proceso según una cualquiera de las reivindicaciones 12 a 14 para la preparación de un compuesto de fórmula general (XIX) donde R1 es etilo, R2 y R5a son ambos H, Y1 es -CH2CH2-, y R4 es C(O)OH.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1420593.4A GB201420593D0 (en) | 2014-11-19 | 2014-11-19 | Compounds |
| GBGB1420594.2A GB201420594D0 (en) | 2014-11-19 | 2014-11-19 | Compounds |
| GBGB1505674.0A GB201505674D0 (en) | 2015-04-01 | 2015-04-01 | Compounds |
| PCT/GB2015/053517 WO2016079518A1 (en) | 2014-11-19 | 2015-11-19 | 5.beta.-6-alkyl-7-hydroxy-3-one steroids as intermediates for the production of steroidal fxr modulators |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2733643T3 true ES2733643T3 (es) | 2019-12-02 |
Family
ID=54704020
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15800910T Active ES2733643T3 (es) | 2014-11-19 | 2015-11-19 | Esteroides 5.beta.-6-alquil-7-hidroxi-3-ona como intermedios para la producción de moduladores FXR de esteroides |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US10131688B2 (es) |
| EP (1) | EP3221332B1 (es) |
| JP (1) | JP6724004B2 (es) |
| KR (1) | KR102526632B1 (es) |
| CN (1) | CN107108687B (es) |
| CA (1) | CA2968301C (es) |
| DK (1) | DK3221332T3 (es) |
| EA (1) | EA033445B1 (es) |
| ES (1) | ES2733643T3 (es) |
| HK (1) | HK1244285B (es) |
| MX (1) | MX375864B (es) |
| PL (1) | PL3221332T3 (es) |
| TW (1) | TWI686400B (es) |
| WO (1) | WO2016079518A1 (es) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6700274B2 (ja) | 2014-11-19 | 2020-05-27 | エヌゼットピー ユーケー リミテッド | ステロイドfxrモジュレーター製造のための中間体としての6−アルキル−7−ヒドロキシ−4−エン−3−オンステロイド |
| JP6698085B2 (ja) | 2014-11-19 | 2020-05-27 | エヌゼットピー ユーケー リミテッド | ステロイドFXRモジュレーター製造のための中間体としての6α−アルキル−6,7−ジオン−ステロイド |
| PL3221333T3 (pl) | 2014-11-19 | 2020-01-31 | NZP UK Limited | Steroidy, 6.alfa-alkilo-3,7-diony jako związki pośrednie do wytwarzania steroidowych modulatorów fxr |
| CN108495858A (zh) * | 2015-12-22 | 2018-09-04 | 英特塞普特医药品公司 | 奥贝胆酸的多晶结晶形式 |
| GB201608779D0 (en) * | 2016-05-18 | 2016-06-29 | Dextra Lab Ltd | Methods and compounds |
| GB201608776D0 (en) | 2016-05-18 | 2016-06-29 | Dextra Lab Ltd | Methods and compounds |
| GB201608777D0 (en) | 2016-05-18 | 2016-06-29 | Dextra Lab Ltd | Compounds |
| CN106279331B (zh) * | 2016-07-27 | 2019-06-14 | 宋火良 | 胆酸类肝病治疗药物 |
| EP3431486A1 (en) | 2017-07-18 | 2019-01-23 | Bionice, S.L.U. | Process and intermediates for the synthesis of obeticholic acid and derivatives thereof |
| GB201812382D0 (en) | 2018-07-30 | 2018-09-12 | Nzp Uk Ltd | Compounds |
| CN111138509B (zh) * | 2018-11-02 | 2022-12-06 | 东莞东阳光药物研发有限公司 | 奥贝胆酸的制备方法 |
| CN113135970B (zh) * | 2020-01-20 | 2024-11-22 | 成都贝诺科成生物科技有限公司 | 一种具有抗芽孢活性的化合物及其药用组合物 |
Family Cites Families (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2624748A (en) | 1950-09-09 | 1953-01-06 | Upjohn Co | Bisnorchola-4, 6-dien-3-one-22-al |
| US4289872A (en) | 1979-04-06 | 1981-09-15 | Allied Corporation | Macromolecular highly branched homogeneous compound based on lysine units |
| US5229490A (en) | 1987-05-06 | 1993-07-20 | The Rockefeller University | Multiple antigen peptide system |
| CA2118130A1 (en) | 1992-04-14 | 1993-10-28 | Jean M. J. Frechet | Dendritic based macromolecules and method of production |
| AU6392894A (en) | 1993-02-26 | 1994-09-14 | Magainin Pharmaceuticals, Inc. | Chemical synthesis of squalamine |
| US5643575A (en) | 1993-10-27 | 1997-07-01 | Enzon, Inc. | Non-antigenic branched polymer conjugates |
| US5932462A (en) | 1995-01-10 | 1999-08-03 | Shearwater Polymers, Inc. | Multiarmed, monofunctional, polymer for coupling to molecules and surfaces |
| USRE48286E1 (en) | 2001-03-12 | 2020-10-27 | Intercept Pharmaceuticals, Inc. | Steroids as agonists for FXR |
| US20090062256A1 (en) | 2001-06-01 | 2009-03-05 | Bristol-Myers Squibb Pharma Company | LACTAMS SUBSTITUTED BY CYCLIC SUCCINATES AS INHIBITORS OF Abeta PROTEIN PRODUCTION |
| MXPA04004336A (es) | 2001-11-07 | 2005-05-16 | Nektar Therapeutics Al Corp | Polimeros ramificados y sus conjugados. |
| EP1568706A1 (en) | 2004-02-26 | 2005-08-31 | Intercept Pharmaceuticals, Inc. | Novel steroid agonist for FXR |
| ITMI20050912A1 (it) * | 2005-05-19 | 2006-11-20 | Erregierre Spa | Processo di preparazione di acidi 3-a-ya(b)-diidrossi-6-a(b)-alchil-5b-colanici |
| JP2007210888A (ja) * | 2006-01-12 | 2007-08-23 | Mitsubishi Chemicals Corp | ステロイド化合物の製造方法 |
| CN101395170A (zh) | 2006-02-14 | 2009-03-25 | 英特塞普特药品公司 | 用于预防或治疗fxr介导的疾病或状态的作为fxr配体的胆汁酸衍生物 |
| CN101522703B (zh) | 2006-06-27 | 2013-04-17 | 英特塞普特医药品公司 | 胆酸派生物及其在制备预防或治疗fxr介导的疾病或状况的药物中的应用 |
| ES2438271T3 (es) | 2007-01-19 | 2014-01-16 | Intercept Pharmaceuticals, Inc. | Ácidos biliares 23-sustituidos como moduladores de TGR5 y métodos de uso de los mismos |
| CN102164940B (zh) * | 2008-07-30 | 2015-08-19 | 英特塞普特医药品公司 | Tgr5调节剂及其使用方法 |
| PL2698375T3 (pl) | 2008-11-19 | 2018-08-31 | Intercept Pharmaceuticals, Inc. | Modulatory TGR5 i sposób ich zastosowania |
| JP5639073B2 (ja) * | 2008-11-19 | 2014-12-10 | インターセプト ファーマシューティカルズ, インコーポレイテッド | Tgr5モジュレーターおよびその使用方法 |
| US8829213B2 (en) | 2009-07-29 | 2014-09-09 | The University Of Chicago | Liver X receptor agonists |
| NZ703072A (en) | 2012-06-19 | 2016-06-24 | Intercept Pharmaceuticals Inc | Preparation, uses and solid forms of obeticholic acid |
| PT2912013T (pt) | 2012-10-26 | 2018-01-03 | Intercept Pharmaceuticals Inc | Processo de preparação de derivados de ácidos biliares |
| MY170802A (en) | 2012-11-28 | 2019-08-28 | Intercept Pharmaceuticals Inc | Treatment of pulmonary disease |
| US20140206657A1 (en) * | 2013-01-18 | 2014-07-24 | City Of Hope | Bile acid analog tgr5 agonists |
| DK3848038T3 (da) | 2013-05-14 | 2023-02-06 | Intercept Pharmaceuticals Inc | 11-Hydroxyl-6substituerede-derivater af galdesyrer og aminosyrerkonjugater heraf som farnesoid X receptor modulerer. |
| SG11201509370UA (en) | 2013-05-24 | 2015-12-30 | Nestec Sa | Pathway specific assays for predicting irritable bowel syndrome diagnosis |
| WO2015183794A1 (en) | 2014-05-27 | 2015-12-03 | City Of Hope | Tgr5 agonist complexes for treating diabetes and cancer |
| RS59910B1 (sr) | 2014-05-29 | 2020-03-31 | Bar Pharmaceuticals S R L | Derivati holana za upotrebu u lečenju i/ili prevenciji fxr i tgr5/gpbar1 posredovanih bolesti |
| HK1243930A1 (zh) | 2014-11-06 | 2018-07-27 | 英安塔制药有限公司 | 作爲fxr/tgr5激动剂的胆汁酸类似物和其使用方法 |
| PL3221333T3 (pl) | 2014-11-19 | 2020-01-31 | NZP UK Limited | Steroidy, 6.alfa-alkilo-3,7-diony jako związki pośrednie do wytwarzania steroidowych modulatorów fxr |
| JP6698085B2 (ja) | 2014-11-19 | 2020-05-27 | エヌゼットピー ユーケー リミテッド | ステロイドFXRモジュレーター製造のための中間体としての6α−アルキル−6,7−ジオン−ステロイド |
| WO2016079527A1 (en) | 2014-11-19 | 2016-05-26 | Tetralogic Birinapant Uk Ltd | Combination therapy |
| JP6700274B2 (ja) | 2014-11-19 | 2020-05-27 | エヌゼットピー ユーケー リミテッド | ステロイドfxrモジュレーター製造のための中間体としての6−アルキル−7−ヒドロキシ−4−エン−3−オンステロイド |
| WO2016086134A1 (en) | 2014-11-26 | 2016-06-02 | Enanta Pharmaceuticals, Inc. | Bile acid derivatives as fxr/tgr5 agonists and methods of use thereof |
| AU2015353473A1 (en) | 2014-11-26 | 2017-06-08 | Enanta Pharmaceuticals, Inc. | Bile acid analogs as FXR/TGR5 agonists and methods of use thereof |
| WO2016086115A1 (en) | 2014-11-26 | 2016-06-02 | Enanta Pharmaceuticals, Inc. | Tetrazole derivatives of bile acids as fxr/tgr5 agonists and methods of use thereof |
| US10208081B2 (en) | 2014-11-26 | 2019-02-19 | Enanta Pharmaceuticals, Inc. | Bile acid derivatives as FXR/TGR5 agonists and methods of use thereof |
| CN106279328A (zh) | 2015-05-20 | 2017-01-04 | 重庆药友制药有限责任公司 | 一种制备6α-烷基鹅去氧胆酸的方法 |
| KR20180043247A (ko) | 2015-06-19 | 2018-04-27 | 인터셉트 파마슈티컬즈, 인크. | Tgr5 조절제 및 이를 사용하는 방법 |
| CN106397522A (zh) | 2015-07-31 | 2017-02-15 | 中国人民解放军军事医学科学院毒物药物研究所 | 3,7‑二(叔丁基二甲基硅基氧基)‑6‑烯‑5β‑胆烷‑24‑酸甲酯 |
| CN106478759A (zh) | 2015-08-31 | 2017-03-08 | 陕西合成药业股份有限公司 | 奥贝胆酸衍生物及其制备方法和用途 |
| CN106478756A (zh) | 2015-09-02 | 2017-03-08 | 中美华世通生物医药科技(武汉)有限公司 | Oca-e单晶及其制备方法和用途 |
| CN106518946A (zh) | 2015-09-10 | 2017-03-22 | 上海迪诺医药科技有限公司 | 磺酰脲衍生物、其药物组合物及应用 |
-
2015
- 2015-11-19 KR KR1020177016856A patent/KR102526632B1/ko active Active
- 2015-11-19 HK HK18103791.5A patent/HK1244285B/en unknown
- 2015-11-19 CN CN201580062893.5A patent/CN107108687B/zh active Active
- 2015-11-19 MX MX2017006564A patent/MX375864B/es active IP Right Grant
- 2015-11-19 PL PL15800910T patent/PL3221332T3/pl unknown
- 2015-11-19 DK DK15800910.0T patent/DK3221332T3/da active
- 2015-11-19 JP JP2017527816A patent/JP6724004B2/ja active Active
- 2015-11-19 TW TW104138184A patent/TWI686400B/zh not_active IP Right Cessation
- 2015-11-19 US US15/528,220 patent/US10131688B2/en active Active
- 2015-11-19 EA EA201790881A patent/EA033445B1/ru unknown
- 2015-11-19 EP EP15800910.0A patent/EP3221332B1/en active Active
- 2015-11-19 CA CA2968301A patent/CA2968301C/en active Active
- 2015-11-19 WO PCT/GB2015/053517 patent/WO2016079518A1/en not_active Ceased
- 2015-11-19 ES ES15800910T patent/ES2733643T3/es active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20170320907A1 (en) | 2017-11-09 |
| CA2968301C (en) | 2023-05-16 |
| TW201629081A (zh) | 2016-08-16 |
| CN107108687A (zh) | 2017-08-29 |
| EP3221332B1 (en) | 2019-04-24 |
| JP2017538691A (ja) | 2017-12-28 |
| US10131688B2 (en) | 2018-11-20 |
| CN107108687B (zh) | 2019-10-29 |
| HK1244285B (en) | 2020-06-05 |
| EA201790881A8 (ru) | 2019-07-31 |
| MX2017006564A (es) | 2018-01-26 |
| KR102526632B1 (ko) | 2023-04-27 |
| EA201790881A1 (ru) | 2017-11-30 |
| MX375864B (es) | 2025-03-07 |
| TWI686400B (zh) | 2020-03-01 |
| EP3221332A1 (en) | 2017-09-27 |
| PL3221332T3 (pl) | 2019-10-31 |
| EA033445B1 (ru) | 2019-10-31 |
| WO2016079518A1 (en) | 2016-05-26 |
| KR20170099895A (ko) | 2017-09-01 |
| JP6724004B2 (ja) | 2020-07-15 |
| CA2968301A1 (en) | 2016-05-26 |
| DK3221332T3 (da) | 2019-07-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2733643T3 (es) | Esteroides 5.beta.-6-alquil-7-hidroxi-3-ona como intermedios para la producción de moduladores FXR de esteroides | |
| ES2748692T3 (es) | Esteroides 6.alfa.-alquil-3,7-diona como intermedios para la producción de moduladores FXR de esteroides | |
| ES2759725T3 (es) | Esteroides 6-alquil-7-hidroxi-4-en-3-ona como intermediarios para la producción de moduladores de FXR esteroideo | |
| KR102527821B1 (ko) | 스테로이드 FXR 조절인자를 제조하기 위한 중간체로서의 6α-알킬-6,7-다이온 스테로이드 | |
| HK1244285A1 (en) | 5.beta -6-alkyl-7-hydroxy-3-one steroids as intermediates for the production of steroidal fxr modulators | |
| ES2878577T3 (es) | Intermedios para la síntesis de derivados del ácido biliar, en particular del ácido obeticólico | |
| ES2857869T3 (es) | 6,7-beta-epóxidos de esteroides como compuestos intermedios químicos | |
| ES2841324T3 (es) | Proceso para la 6,7-alfa-epoxidación de 4,6-dienos esteroideos | |
| HK1246801B (en) | 6-alkyl-7-hydroxy-4-en-3-one steroids as intermediates for the production of steroidal fxr modulators | |
| HK1244287B (en) | 6.alpha.-alkyl-3,7-dione steroids as intermediates for the production of steroidal fxr modulators | |
| HK1244286B (en) | 6.alpha.-alkyl-6,7-dione steroids as intermediates for the production of steroidal fxr modulators | |
| NZ731924B2 (en) | 6-alkyl-7-hydroxy-4-en-3-one steroids as intermediates for the production of steroidal fxr modulators |