ES2807849T3 - Derivados de oxadiazol microbicidas - Google Patents
Derivados de oxadiazol microbicidas Download PDFInfo
- Publication number
- ES2807849T3 ES2807849T3 ES16774508T ES16774508T ES2807849T3 ES 2807849 T3 ES2807849 T3 ES 2807849T3 ES 16774508 T ES16774508 T ES 16774508T ES 16774508 T ES16774508 T ES 16774508T ES 2807849 T3 ES2807849 T3 ES 2807849T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- cycloalkyl
- heterocyclyl
- alkoxy
- phenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- IWXYNYIUPQSMPY-UHFFFAOYSA-N CCC(N(Cc(cc1)ccc1-c1n[o]c(C(F)(F)F)n1)C1COC1)=O Chemical compound CCC(N(Cc(cc1)ccc1-c1n[o]c(C(F)(F)F)n1)C1COC1)=O IWXYNYIUPQSMPY-UHFFFAOYSA-N 0.000 description 1
- XTOIORALOUPBKN-UHFFFAOYSA-N Cc1ccc(-c2n[o]c(C(F)(F)F)n2)c(F)c1 Chemical compound Cc1ccc(-c2n[o]c(C(F)(F)F)n2)c(F)c1 XTOIORALOUPBKN-UHFFFAOYSA-N 0.000 description 1
- JHPJHMHUZVPBQE-UHFFFAOYSA-N FC(c1nc(-c2ccc(CCBr)cc2)n[o]1)(F)F Chemical compound FC(c1nc(-c2ccc(CCBr)cc2)n[o]1)(F)F JHPJHMHUZVPBQE-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D271/00—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms
- C07D271/02—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms not condensed with other rings
- C07D271/06—1,2,4-Oxadiazoles; Hydrogenated 1,2,4-oxadiazoles
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/82—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms five-membered rings with three ring hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Agronomy & Crop Science (AREA)
- Pest Control & Pesticides (AREA)
- Plant Pathology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Dentistry (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Plural Heterocyclic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Enzymes And Modification Thereof (AREA)
Abstract
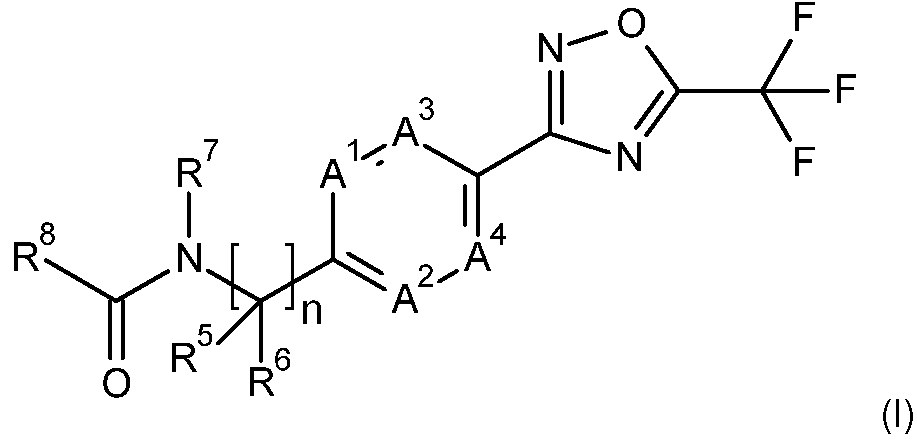
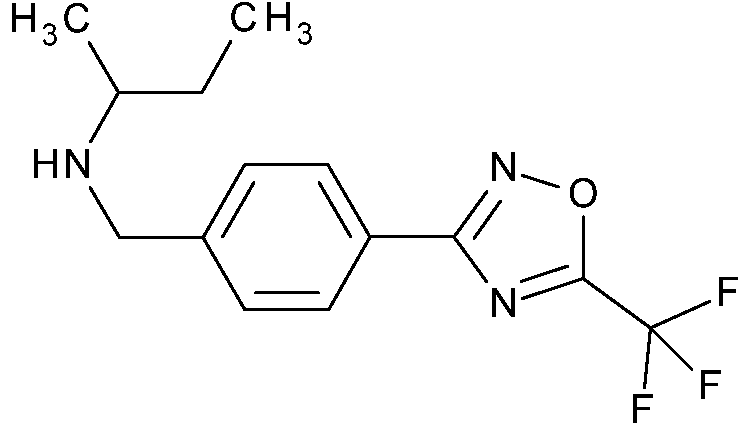
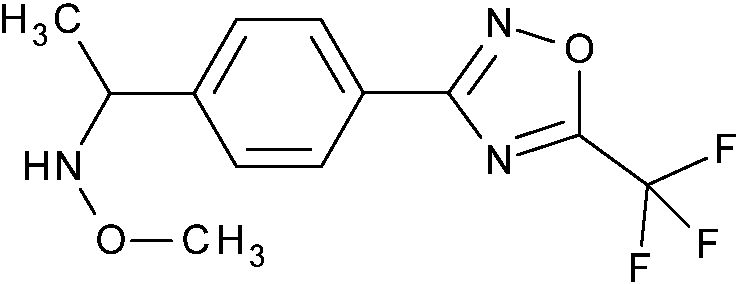
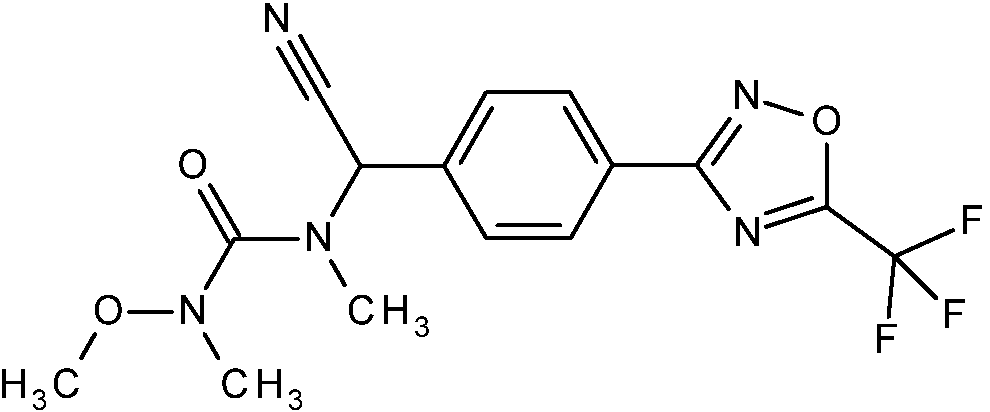
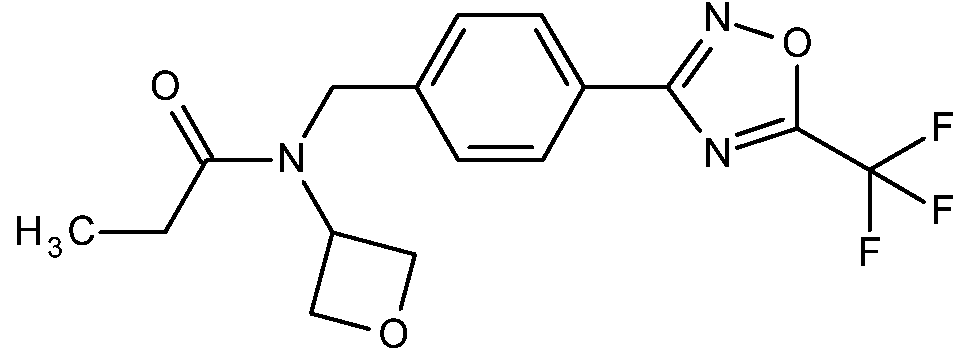
Un compuesto de fórmula (I): **(Ver fórmula)** donde n es 1 o 2 A1 representa N o CR1, donde R1 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi; A2 representa N o CR2, en el que R2 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi; A3 representa N o CR3, donde R3 es hidrógeno o halógeno; A4 representa N o CR4, donde R4 es hidrógeno o halógeno; y donde 0, 1 o 2 de A1, A2, A3 y A4 son N; R5 y R6 se seleccionan independientemente de hidrógeno, alquilo C1-4, halógeno, ciano, trifluorometilo y difluorometilo, o R5 y R6, junto con el átomo de carbono que comparten, forman un ciclopropilo; R7 es hidroxi, alquilo C1-4, haloalquilo C1-4, alcoxi C1-4, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, haloalcoxi C1-2alquilo C1-4, alquenilo C3-6, alquinilo C3-4, alqueniloxi C3-6, alquiniloxi C3-6, haloalquenilo C3-6, haloalqueniloxi C3-6, alquilcarboniloxi C1-4, haloalquilcarboniloxi C1-4, alcoxicarboniloxi C1-4, alquilcarboniloxi C1-4alquilo C1-4, haloalquilcarboniloxi C1-4alquilo C1-4 o alcoxicarboniloxi C1-4alquilo C1-4; o R7 es cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, cicloalquil C3-6alcoxi C1-2, fenilo, fenilalquilo C1-2, fenilalcoxi C1-2, heteroarilo, heteroarilalquilo C1-2, heteroarilalcoxi C1-2, heterociclilo, heterociclilalquilo C1-2, heterociclilalcoxi C1-2, cicloalquilcarboniloxi C3-6, heterociclilcarboniloxi, fenilcarboniloxi, cicloalquilcarboniloxi C3-6alquilo C1-4, heterociclilcarboniloxialquilo C1-4 o fenilcarboniloxialquilo C1-4, en donde el resto heteroarilo es un anillo aromático monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente de N, O y S, el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente de N, O y S, y en el que cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados de ciano, flúor, cloro, bromo, metilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi; R8 es hidrógeno, alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C2-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, alquiniloxi C2- 4alquilo C1-6, aminoalquilo C1-6, N-alquilamino C1-4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1- 6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, Nalquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1-4alquilo C1-6, alquilsulfanil C1-6alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6, alquilsulfonilamino C1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6, alquiniloxicarbonilamino C2-6alquilo C1-6, alquilcarbonilamino C1-4alquilo C1-6 o alcoxicarbonilamino C1-4alquilo C1-6; o R8 es cicloalquilo C3-8, cicloalquilo C3-8alquilo C1-6, donde el resto cicloalquilo está opcionalmente insaturado parcialmente, fenilo, fenilalquilo C1-6, fenilalquenilo C2-6, naftilo, naftiloalquilo C1-6, heteroarilo, heteroarilalquilo C1-6, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterodiarilo, heterodiarilalquilo C1-6 donde el resto heterodiarilo es un sistema aromático, bicíclico, de 9 a 10 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S o cicloalquilcarbonilamino C3-6alquilo C1-6, donde para R8, cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo o heterociclilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9; o, adicionalmente, cuando R8 es ciclopropilo, el resto ciclopropilo está sustituido con 4 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9, con la condición de que al menos 2 sustituyentes R9 sean los mismos; donde R9 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C1- 4, haloalcoxi C1-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, cicloalquilcarbonil o C3-6, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 o alcoxicarbonilamino C1-4, y donde cuando R8 es cicloalquil C3-8alquilo C1-6, heterociclilo, heterociclilalquilo C1-6 o cicloalquilo C3-8 sustituido, R9 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo; o donde para R8, cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo o heterociclilo está opcionalmente sustituido con 1 sustituyente seleccionado entre R10 y además opcionalmente sustituido con 1 o 2 sustituyentes seleccionados entre R9; donde R10 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-2, fenilo, fenilalquilo C1-2, heteroarilo, heteroarilalquilo C1-2 donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo o heterociclilalquilo C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R11; donde R11 es hidrógeno, ciano, flúor, cloro, bromo, metilo, trifluorometilo, metoxi y etoxi; o R8 representa -OR12, donde R12 es hidrógeno, alquilo C1-6, alquenilo C3-6, alquinilo C3-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C3-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, aminoalquilo C1-6, N-alquilamino C1-4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1-4alquilo C1-6, alquilsulfanil C1-4alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6 o alquilsulfonilamino C1-6alquilo C1-6; o R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, donde el resto cicloalquilo es fenilo, fenilalquilo C1-6, heteroarilo, heteroarilalquilo C1-6 opcionalmente insaturado parcialmente, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo o heterociclilalquilo C1-6, donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S, donde para R12, cualquier resto cicloalquilo, fenilo, heteroarilo o heterociclilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R13; donde R13 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C1- 4, haloalcoxi C1-4, alqueniloxi C3-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 o alcoxicarbonilamino C1-4; y donde cuando R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, heterociclilo o heterociclilalquilo C1-6 sustituido, R13 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo; o R8 representa -NR14R15, donde R14 es hidrógeno, ciano, alquilo C1-6, alcoxi C1-6, alquenilo C2-6, alquinilo C2-6, alqueniloxi C3-6, alquiniloxi C3-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C1-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquil C1-6, aminoalquil C1-6, N-alquilamino C1-4alquilo C1-6, N,Ndialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1-4alquilo C1- 6, alquilsulfanil C1-4alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6 o alquilsulfonilamino C1-6alquilo C1-6; o R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, cicloalquil C3-8alcoxi C1-6, cicloalquiloxi C3-6, donde el resto cicloalquilo es fenilo, fenilalquilo C1-6, fenilalcoxi C1-6, heteroarilo, heteroarilalquilo C1-6, heteroarilalcoxi C1-6 opcionalmente insaturado parcialmente, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C1-6 o heterociclilalcoxi C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S, donde para R14, cualquier resto cicloalquilo, fenilo, heteroarilo, heterociclilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R17; donde R16 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C1- 4, alcoxi C1-2alquilo C1-2, haloalcoxi C1-4, alqueniloxi C3-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 y alcoxicarbonilamino C1-4; y donde cuando R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, cicloalquil C3-8alcoxi C1-5 6, heterociclilo, heterociclilalquilo C1-6 o heterociclilalcoxi C1-6 sustituido, R16 también puede representar oxo en el resto cicloalquilo C3- 8 o heterociclilo; R15 es hidrógeno, alquilo C1-4, alquinilo C3-4, alcoxi C1-4alquilo C1-4, cianoalquilo C1-4, cicloalquilo C3-6, cicloalquil C3- 6alquilo C1-2; o R14 y R15, junto con el átomo de nitrógeno al que están unidos, forman un ciclo de 4, 5 o 6 miembros que contiene opcionalmente un heteroátomo adicional o grupo seleccionado entre O, S, S(O)2, oxo (=O) y NR17; donde R17 es hidrógeno, metilo, metoxi, formilo o acilo; o una de sus sales o N-óxidos.
Description
DESCRIPCIÓN
Derivados de oxadiazol microbicidas
La presente invención se refiere a derivados de oxadiazol microbicidas, por ejemplo, como principios activos, que tienen actividad microbicida, en particular actividad fungicida. La invención se refiere además a composiciones agroquímicas que comprenden al menos uno de los derivados de oxadiazol, a procesos de preparación de estos compuestos y a los usos de los derivados de oxadiazol o las composiciones en agricultura u horticultura para controlar o prevenir la infestación de plantas, cultivos alimentarios recolectados, semillas o materiales inertes por parte de microorganismos fitopatógenos, preferentemente hongos.
Se ha publicado que los derivados de oxadiazol microbicidas son agentes insecticidas y acaricidas, por ejemplo, en el documento CN 1927860. Los documentos WO 2013/064079, EP 0276 432 y WO 2015/185485 describen el uso de oxadiazoles sustituidos para combatir hongos fitopatógenos.
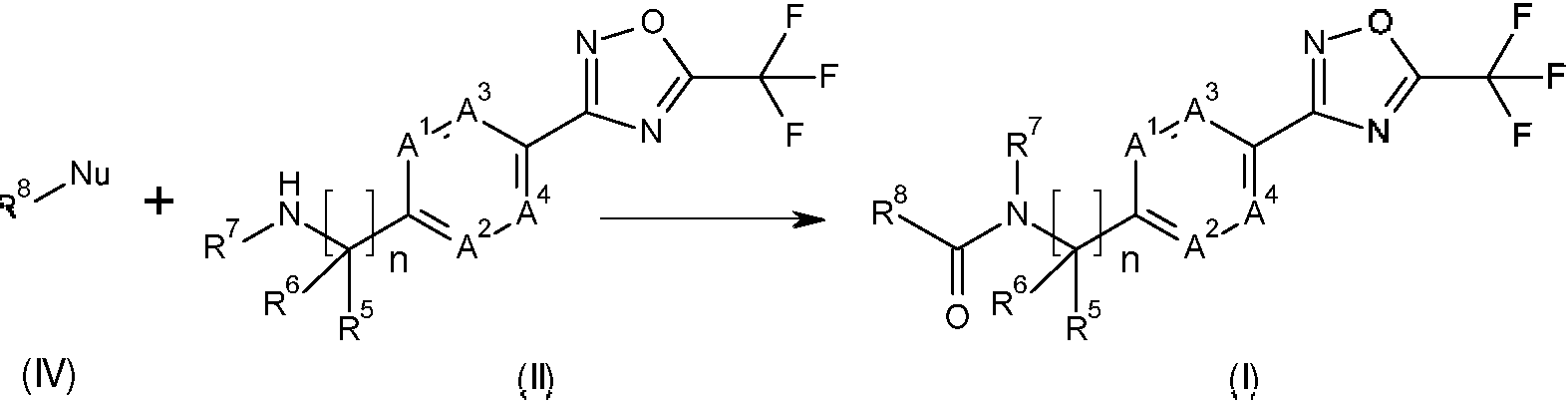
De acuerdo con la presente invención se proporciona un compuesto de fórmula (I):
donde
n es 1 o 2
A1 representa N o CR1, donde R1 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi;
A2 representa N o CR2, donde R2 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi;
A3 representa N o CR3 , donde R3 es hidrógeno o halógeno;
A4 representa N o CR4 , donde R4 es hidrógeno o halógeno; y
donde 0, 1 o 2 de A1, A2 , A3 y A4 son N;
R5 y R6 se seleccionan independientemente de hidrógeno, alquilo C1-4, halógeno, ciano, trifluorometilo y difluorometilo, o R5 y R6 , junto con el átomo de carbono que comparten, forman un ciclopropilo;
R7 es hidroxi, alquilo C1-4, haloalquilo C1-4, alcoxi C1-4, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, haloalcoxi C1-2alquilo C1-4, alquenilo C3-6, alquinilo C3-4, alqueniloxi C3-6, alquiniloxi C3-6, haloalquenilo C3-6, haloalqueniloxi C3-6, alquilcarboniloxi C1-4, haloalquilcarboniloxi C1-4, alcoxicarboniloxi C1-4, alquilcarboniloxi C1-4alquilo C1-4, haloalquilcarboniloxi C1-4alquilo C1-4 o alcoxicarboniloxi C1 -4alquilo C1-4; o
R7 es cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, cicloalquil C3-6alcoxi C1-2, fenilo, fenilalquilo C1-2, fenilalcoxi C 1-2, heteroarilo, heteroarilalquilo C1-2, heteroarilalcoxi C1-2, heterociclilo, heterociclilalquilo C1-2, heterociclilalcoxi C1-2, cicloalquilcarboniloxi C3-6, heterociclilcarboniloxi, fenilcarboniloxi, cicloalquilcarboniloxi C3-6alquilo C1-4, heterociclilcarboniloxialquilo C1-4 o fenilcarboniloxialquilo C1-4,
donde el resto heteroarilo es un anillo aromático, monocíclico, de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre ciano, flúor, cloro, bromo, metilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi; R8 es hidrógeno, alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C2-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, alquiniloxi C2-4alquilo C1-6, aminoalquilo C1-6, N-alquilamino C1-4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C 1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1 -4alquilo C1-6, alquilsulfanil C1-6alquilo C1-6,
alquilsulfonil C i -6 alquilo C i -6, alquiisulfonilamino C i -6alquilo C i -6, alquiisulfonilamino C i -6alqu¡n¡lo C2-6, alquiniloxicarbonilamino C2-6alquilo C i -6, alquilcarbonilamino C i -4alquilo C i -6, o alcoxicarbonilamino C i -4alquilo C i -6 ; o
R8 es cicloalquilo C3-8, cicloalquilo C3-8alquilo C i -6, donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C i-6 , fenilalquenilo C2-6, naftilo, naftiloalquilo C i -6,heteroarilo, heteroarilalquilo C i -6, parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende i , 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterodiarilo, heterodiarilalquilo C i -6 donde el resto heterodiarilo es un sistema aromático, bicíclico, de 9 a i0 miembros que comprende i , 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C i -6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende i , 2 o 3 heteroátomos seleccionados individualmente entre N, O y S o cicloalquilcarbonilamino C3-6alquilo C i -6,
donde para R8 , cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo o heterociclilo está opcionalmente sustituido con i , 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; o, adicionalmente, cuando R8 es ciclopropilo, el resto ciclopropilo está sustituido con 4 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 , con la condición de que al menos 2 sustituyentes R9 sean los mismos; donde
R9 es ciano, halógeno, hidroxi, alquilo C i -4, alquenilo C2-4, alquinilo C2-4, haloalquilo Ci -4, haloalquenilo C2-4, alcoxi C i-4 , haloalcoxi C i -4, alquiniloxi C3-4, N-alquilamino C i -4, N,N-dialquilamino C i -4, alquilcarbonilo C i -4, cicloalquilcarbonilo C3-6, alcoxicarbonilo C i -4, carbonilamino, N-alquilaminocarbonilo C i -4, N,N-dialquilaminocarbonilo C i -4 o alcoxicarbonilamino C i -4, y donde cuando R8 es cicloalquil C3-8alquilo C i -6, heterociclilo, heterociclilalquilo C i -6 o cicloalquilo C3-8 sustituido, R9 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo; o
donde para R8 , cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo o heterociclilo está opcionalmente sustituido con i sustituyente seleccionado entre Ri0 y además opcionalmente sustituido con i o 2 sustituyentes seleccionados entre R9 ; donde
Ri0 es cicloalquilo C3-8, cicloalquil C3-8alquilo C i-2 , fenilo, fenilalquilo Ci-2 , heteroarilo, heteroarilalquilo C i-2 donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende i , 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo o heterociclilalquilo Ci -6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende i , 2 o 3 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con i , 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R11; donde
R11 es hidrógeno, ciano, flúor, cloro, bromo, metilo, trifluorometilo, metoxi y etoxi;
o
R8 representa -OR12, donde R12 es hidrógeno, alquilo C i -6, alquenilo C3-6, alquinilo C3-6, cianoalquilo C i -6, haloalquilo C i -6, haloalquenilo C3-6, hidroxialquilo C i -6, alcoxi C i -4alquilo Ci -6, haloalcoxi Ci -4alquilo C i -6, alcoxi C i -4alcoxi C i -4alquilo Ci -6, aminoalquilo C i -6, N-alquilamino C i -4alquilo C i -6, N,N-dialquilamino C i -4alquilo C i -6, alquilcarbonil C i -6alquilo C i -6, alquilcarbonil C i -6alquenilo C2-6, alcoxicarbonil C i -6alquilo Ci -6, alquilcarboniloxi C i -6alquilo Ci -6, N-alquilaminocarbonil C i -4alquilo C i -6, N,N-dialquilaminocarbonil C i -4alquilo C i -6, alquilsulfanil C i -4alquilo C i -6, alquilsulfonil Ci -6 alquilo C i -6 o alquilsulfonilamino C i -6alquilo C i -6 ; o
R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C i -6, donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C i-6, heteroarilo, heteroarilalquilo C i -6, parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y 5, heterociclilo o heterociclilalquilo C i -6, donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S;
donde para R12, cualquier resto cicloalquilo, fenilo, heteroarilo o heterociclilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R13; donde
R13 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C i-4 , haloalcoxi C1-4, alqueniloxi C3-4, alquiniloxi C3-4, N-alquilamino C 1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 o alcoxicarbonilamino C i -4 ;
y donde cuando R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C i -6, heterociclilo o heterociclilalquilo C i -6 sustituido, R13 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo;
o
R8 representa -NR14R15, donde R14 es hidrógeno, ciano, alquilo C i -6, alcoxi C i -6, alquenilo C2-6, alquinilo C2-6, alqueniloxi C3-6, alquiniloxi C3-6, cianoalquilo C i -6, haloalquilo C i -6, haloalquenilo Ci -6, hidroxialquilo C i -6, alcoxi C i -4alquilo C i -6, haloalcoxi C i -4alquilo C i -6, alcoxi C i -4alcoxi C i -4alquil C i -6, aminoalquil C i -6, N-alquilamino C i -4alquilo Ci -6, N,Ndialquilamino C i -4alquilo C i -6, alquilcarbonil C i -6alquilo Ci -6, alquilcarbonil C i -6alquenilo C2-6, alcoxicarbonil C i -6alquilo C1-6, alquilcarboniloxi C i -6alquilo C1-6, N-alquilaminocarbonil C i -4alquilo C1-6, N,N-dialquilaminocarbonil C i -4alquilo C i-6 , alquilsulfanil C i -4alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6 o alquilsulfonilamino Ci -6alquilo C1-6 ; o
R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, cicloalquil C3-8alcoxi C1-6, cicloalquiloxi C3-6, donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C1-6, fenilalcoxi C1-6, heteroarilo, heteroarilalquilo C1-6, heteroarilalcoxi C1-6 parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1,2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C i-6 o heterociclilalcoxi C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S;
donde para R14, cualquier resto cicloalquilo, fenilo, heteroarilo, heterociclilo está opcionalmente sustituido con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R16; donde
R16 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C i-4 , alcoxi C i-2alquilo C1-2, haloalcoxi C1-4, alqueniloxi C3-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 y alcoxicarbonilamino C1-4;
y donde cuando R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, cicloalquil C3-8alcoxi C1-6, heterociclilo, heterociclilalquilo C1-6 o heterociclilalcoxi C1-6 sustituido, R16 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo;
R15 es hidrógeno, alquilo C1-4, alquinilo C3-4, alcoxi C i -4alquilo C1-4, cianoalquilo C1-4, cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2 ; o
R14 y R15, junto con el átomo de nitrógeno al que están unidos, forman un ciclo de 4, 5 o 6 miembros que contiene opcionalmente un heteroátomo adicional o grupo seleccionado entre O, S, S(O)2 , oxo (=O) y NR17; donde
R17 es hidrógeno, metilo, metoxi, formilo o acilo; o
una de sus sales o N-óxidos.
Sorprendentemente, se ha descubierto que los compuestos novedosos de fórmula (I) tienen, a efectos prácticos, un nivel muy ventajoso de actividad biológica para la protección de plantas contra enfermedades provocadas por hongos. De acuerdo con un segundo aspecto de la invención, se proporciona una composición agroquímica que comprende una cantidad eficaz como fungicida de un compuesto de fórmula (I). La composición puede comprender además al menos un principio activo adicional y/o un diluyente o portador agroquímicamente aceptable.
De acuerdo con un tercer aspecto de la invención, se proporciona un método para controlar o prevenir la infestación de plantas útiles por parte de microorganismos fitopatógenos, donde una cantidad eficaz como fungicida de un compuesto de fórmula (I), o una composición que comprende este compuesto como principio activo, se aplica a las plantas o sus partes o su emplazamiento.
De acuerdo con un cuarto aspecto de la presente invención, se proporciona el uso de un compuesto de fórmula (I) como un fungicida, con la condición de que dicho uso excluya métodos para el tratamiento del cuerpo humano o animal por cirugía o terapia.
Como se usa en el presente documento, el término "halógeno" o "halo" se refiere a flúor (fluoro), cloro (cloro), bromo (bromo) o yodo (yodo), preferentemente flúor, cloro o bromo.
Como se usa en el presente documento, ciano, se refiere a un grupo -CN.
Como se usa en el presente documento, amino, se refiere a un grupo -NH2.
Como se usa en el presente documento, hidroxi se refiere a un grupo -OH.
Como se usa en el presente documento, carbonilamino se refiere a un grupo -N(H)C(O)H.
Como se usa en el presente documento, formilo se refiere un grupo -C(O)H.
Como se usa en el presente documento, acilo se refiere un grupo -C(O)CH3.
Como se usa en el presente documento, la expresión "alquilo C1-6" se refiere a un radical de cadena de hidrocarburo lineal o ramificada que consiste solamente de átomos de carbono e hidrógeno, que no contienen insaturación, que tienen de uno a seis átomos de carbono, y que se une al resto de la molécula mediante un enlace sencillo. Las expresiones "alquilo C1-4" y “alquilo C1-2” se deben interpretar con el mismo sentido. Los ejemplos de alquilo C1-6 incluyen, pero sin limitarse a, metilo, etilo, n-propilo, 1 -metiletilo (iso-propilo), n-butilo,1, 1 -dimetiletil (tert-butilo) y npentilo. Un grupo "alquileno C1-C6" se refiere a la definición correspondiente de alquilo C1-C6 (y alquilo C1-4 y alquilo
C1-2), excepto que tal radical está unido al resto de la molécula por dos enlaces sencillos. Ejemplos de alquileno C i -C6 , incluyen, pero no se limitan a -CH2-, -CH2CH2- y -(CH2)3.
Como se usa en el presente documento, la expresión "alquenilo C2-6", se refiere a un grupo radical que es una cadena hidrocarbonada lineal o ramificada constituida únicamente por átomos de carbono y de hidrógeno, que contiene al menos un doble enlace que puede tener la configuración (£)- o (Z), que tiene entre dos y seis átomos de carbono y que está unida al resto de la molécula por un enlace sencillo. La expresión "alquenilo C3-6" se debe interpretar con el mismo sentido. Los ejemplos de alquenilo C2-6 incluyen, pero sin limitarse a, etenilo, prop-1-enilo y but-1-enilo.
Como se usa en el presente documento, la expresión "alquinilo C2-6", se refiere a un grupo radical de cadena hidrocarburo lineal o ramificada que consiste solamente de átomos de carbono y de hidrógeno, que contiene al menos un triple enlace, que tiene entre dos a seis átomos de carbono y que está unida al resto de la molécula por un enlace sencillo. La expresión "alquinilo C3-4" se debe interpretar con el mismo sentido. Los ejemplos de alquinilo C2-6 incluyen, pero sin limitarse a, etinilo, prop-1-inilo y but-1-inilo.
Como se usa en el presente documento, oxo significa un grupo =O, por ejemplo, un cetonilo (-C(O)-), sulfinilo (-S(O)-) u oxígeno sulfonilo (-S(O)2-).
Como se usa en el presente documento, la expresión "N-alquilamino C1-4", se refiere a un radical de fórmula -NH-Ra donde Ra es un radical alquilo C1-4 como se ha definido anteriormente.
Como se usa en el presente documento, la expresión "N,N-di-alquilamino C1-4" se refiere a un radical de fórmula -N(Ra)-Ra donde cada Ra es un radical alquilo C1-4, que puede ser idéntico o diferente, como se ha definido anteriormente.
Como se usa en el presente documento, la expresión "alcoxi C1-6", se refiere a un radical de fórmula -ORa donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. Las expresiones "alcoxi C1-4" y "alcoxi C1-2" se deben interpretar con el mismo sentido. Los ejemplos de alcoxi C1-6 incluyen, pero sin limitarse a, metoxi, etoxi, propoxi, isopropoxi y butoxi.
Como se usa en el presente documento, la expresión "alcoxicarboniloxi C1-4" se refiere a un radical de la fórmula -OC(O)Ra donde Ra es un radical alcoxi C1-4 como se define en general anteriormente.
Como se usa en este documento, la expresión "alcoxicarboniloxi C1 -4-alquilo C1-4" se refiere a un radical alquilo C1-4 como se define en general anteriormente sustituido con un radical alcoxicarboniloxi C1-4 como se define en general anteriormente.
Como se usa en el presente documento, la expresión "hidroxialquilo C1-4", se refiere a un radical alquilo C1-4, como se ha definido de manera general anteriormente, sustituido con uno o más grupos hidroxi como se han definido anteriormente.
Como se usa en el presente documento, la expresión "alquilcarbonilo C1-6", se refiere a un radical de fórmula -C(O)Ra donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. La expresión "(alquil C1-4)carbonilo" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alcoxicarbonilo C1-6", se refiere a un radical de fórmula -C(O)ORa donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. La expresión "alcoxicarbonilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilcarboniloxi C1-6", se refiere a un radical de fórmula -OC(O)Ra donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. La expresión "alquilcarboniloxi C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "N-alquilaminocarbonilo C1-4", se refiere a un radical de fórmula -C(O)NHRa donde Ra es un radical alquilo C1-4 como se ha definido de manera general anteriormente.
Como se usa en el presente documento, la expresión "N,N-dialquilaminocarbonilo C1-4" se refiere a radical de la fórmula -C(O)NRa (Ra) donde cada Ra es un radical alquilo C1-4 como se ha definido de manera general anteriormente.
Como se usa en el presente documento, la expresión "alquilcarbonilamino C1-4" se refiere a un radical de la fórmula -NHC(O)Ra donde Ra es un radical alquilo C1-4 como se define en general anteriormente.
Como se usa en el presente documento, la expresión "alquilcarbonilamino C1-4 alquilo C1-6" se refiere a un radical alquilo C1-6 como se define en general anteriormente sustituido con un grupo alquilcarbonilamino C1-4 como se definió anteriormente.
Como se usa en el presente documento, la expresión "alcoxicarbonilamino C1-4" se refiere a un radical de la fórmula -NHC(O)ORa donde Ra es un radical alquilo C1-4 como se define en general anteriormente.
Como se usa en este documento, la expresión "alcoxicarbonilamino C i -4-alquilo C i -6" se refiere a un radical alquilo C i-6 como se define en general anteriormente sustituido con un grupo alcoxicarbonilamino C1-4 como se define anteriormente.
Como se usa en el presente documento, la expresión "alquilsulfanilo C1-6", se refiere a un radical de fórmula -SRa donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. La expresión "alquilsulfanilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilsulfinilo C1-6" se refiere a un radical de la fórmula -S(O)Ra donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. La expresión "(alquil C1-4)sulfonilo" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilsulfonilo C1-6", se refiere a un radical de fórmula -S(O)2 Ra donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. La expresión "(alquil C1-4)sulfonilo" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilsulfonilamino C1-6", se refiere a un radical de fórmula -NHS(O)2 Ra donde Ra es un radical alquilo C1-6 como se ha definido de manera general anteriormente. La expresión "alquilsulfonilamino C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alqueniloxi C3-6" se refiere a un radical de la fórmula -ORa donde Ra es un radical alquenilo C3-6 como se ha definido de manera general anteriormente.
Como se usa en el presente documento, la expresión "alquiniloxi C2-6" se refiere a un radical de la fórmula -ORa donde Ra es un radical alquinilo C2-6como se ha definido de manera general anteriormente. Las expresiones "alquiniloxi C2-4" y "alquiniloxi C3-6" deben interpretarse en consecuencia.
Como se usa en el presente documento, la expresión "haloalqueniloxi C3-6" se refiere a un radical alqueniloxi C3-6 como se ha definido de manera general anteriormente sustituido con uno o más de los mismos o diferentes átomos halógenos.
Como se usa en el presente documento, la expresión "alquiniloxicarbonilamino C2-6" se refiere a un radical de la fórmula -NHC(O)ORa donde Ra es un radical alquinilo C2-6 como se ha definido de manera general anteriormente. La expresión "alquiniloxicarbonilamino C2-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "haloalcoxi C1-4" se refiere a un grupo alcoxi C1-4 como se ha definido anteriormente, sustituido con uno o más de los mismos o diferentes átomos de halógeno. Los ejemplos de haloalcoxi C1-4 incluyen, pero sin limitarse a, fluorometoxi, fluoroetoxi, trifluorometoxi, trifluoroetoxi.
Como se usa en el presente documento, la expresión "cianoalquilo C1-6", se refiere a un radical alquilo C1-6, como se ha definido de manera general anteriormente sustituido, con uno o más grupos ciano como se han definido anteriormente. La expresión "cianoalquilo C1-4" se debe interpretar con el mismo sentido. Los ejemplos de cianoalquilo C1-6 incluyen, pero sin limitarse a, cianometilo, cianoetilo.
Como se usa en el presente documento, la expresión "haloalquilo C1-6", se refiere a un radical alquilo C1-6, como se ha definido de manera general anteriormente, sustituido con uno o más átomos halógenos idénticos o diferentes. La expresión "haloalquilo C1-4" se debe interpretar con el mismo sentido. Los ejemplos de haloalquilo C1-6 incluyen, pero sin limitarse a, fluorometilo, fluoroetilo, trifluorometilo, 2,2,2-trifluoroetilo.
Como se usa en el presente documento, la expresión "haloalquenilo C2-6", se refiere a un radical alquenilo C2-6, como se ha definido de manera general anteriormente, sustituido con uno o más átomos halógenos idénticos o diferentes. Las expresiones "haloalquenilo C2-4" y "haloalquenilo C3-6" se deben interpretar en el mismo sentido.
Como se usa en el presente documento, la expresión "haloalquilcarboniloxi C1-4" se refiere a un radical de la fórmula -OC (O)Ra en la que Ra es un radical haloalquilo C1-4 como se ha definido en general anteriormente.
Como se usa en este documento, la expresión "haloalquilcarboniloxi C1-4 alquilo C1-4" se refiere a un radical alquilo C1-4 como se define en general anteriormente sustituido con un radical haloalquilcarboniloxi C1-4como se ha definido en general anteriormente.
Como se usa en el presente documento, la expresión "hidroxialquilo C1-6", se refiere a un radical alquilo C1-6, como se ha definido de manera general anteriormente, sustituido con uno o más grupos hidroxi como se han definido anteriormente. La expresión "hidroxialquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alcoxi C1-4alquilo C1-6" se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alcoxi C1-4 como se han definido anteriormente. Las expresiones "alcoxi C1-4alquilo C1-4" y "alcoxi C1-2alquilo C1-4" se deben interpretar con el mismo sentido. Los ejemplos de alcoxi C1-4alquilo C1-6 incluyen, pero sin limitarse a, metoximetilo, 2-metoxietilo.
Como se usa en el presente documento, la expresión "haloalcoxi C i -4alquilo C i -6" se refiere a un radical alquilo C i -6 como se ha definido de manera general anteriormente, sustituido con un grupo haloalcoxi C1-4 como se han definido anteriormente. Las expresiones "haloalcoxi C1-4alquilo C1-4" y "haloalcoxi C 1-2alquilo C1-4" se deben interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alcoxi C1-4alcoxi C1-4alquilo C1-6" se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alcoxi C1-4 como se ha definido anteriormente, estando el propio grupo alcoxi C1-4sustituido con un grupo alcoxi C1-4como se ha definido anteriormente.
Como se usa en el presente documento, la expresión "alquiniloxi C2-6alquilo C1-6", se refiere a un radical alquilo C1-6, como se ha definido de manera general anteriormente, sustituido con un grupo alquiniloxi C2-6 tal como se han definido anteriormente.
Como se usa en el presente documento, la expresión "aminoalquilo C1-6", se refiere a un radical alquilo C1-6, como se ha definido de manera general anteriormente, sustituido con uno o más grupos amino tal como se han definido anteriormente. La expresión "amino(alquilo C1-4)" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "N-alquilamino C1-4alquilo C1-6" se refiere a un radical alquilo C 1-6 como se ha definido de manera general anteriormente, sustituido con un grupo N-alquilamino C1-4 como se han definido anteriormente. La expresión "N-(alquil C1-4)amino(alquilo C1-4)" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "N,N-dialquilamino C1-4alquilo C1-6" se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo N,N-dialquilamino C1-4 como se han definido anteriormente. La expresión "N,N-dialquilamino C1-4alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilcarbonilo C1-6alquilo C1-6" se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alquilcarbonilo C1-6 como se han definido anteriormente. La expresión "alquilcarbonil C1 -6alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilcarbonilo C1-6alquenilo C2-6" se refiere a un radical alquenilo C2-6 como se ha definido de manera general anteriormente, sustituido con un grupo alquilcarbonilo C 1-6 como se han definido anteriormente. La expresión "alquilcarbonil C1-6alquenilo C2-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alcoxicarbonilo C1-6alquilo C1-6" se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alcoxicarbonilo C1-6 como se han definido anteriormente. La expresión "alcoxicarbonil C1-6alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilcarboniloxi C1-6alquilo C1-6" se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alquilcarboniloxi C1-6 como se han definido anteriormente. La expresión "alquilcarboniloxi C1-6alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "N-alquilaminocarbonil C1-4alquilo C1-6" se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo N-alquilaminocarbonilo C 1-4 como se han definido anteriormente. La expresión "N-alquilaminocarbonil C1-4alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "N,N-dialquilaminocarbonil C1-4alquilo C1-6", se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo N,N-dialquilaminocarbonil C1-4alquilo C1-6 como se ha definido anteriormente. La expresión "N,N-dialquilaminocarbonil C1-4 alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilsulfanil C1-6alquilo C1-6", se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alquilsulfanilo C1-6 como se ha definido anteriormente. La expresión "alquilsulfanil C1-6alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilsulfonil C1-6alquilo C1-6", se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alquilsulfonilo C1-6 como se ha definido anteriormente. La expresión "alquilsulfonil C1-6alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilsulfonilamino C1-6alquilo C1-6", se refiere a un radical alquilo C1-6 como se ha definido de manera general anteriormente, sustituido con un grupo alquilsulfonilamino C1-6 como se han definido anteriormente. La expresión "alquilsulfonilamino C1-6alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "alquilsulfonilamino C1-6alquinilo C2-6", se refiere a un radical alquinilo C2-6 como se ha definido de manera general anteriormente, sustituido con un grupo alquilsulfonilamino C1-6 como se han definido anteriormente. La expresión "alquilsulfonilamino C1-6alquinilo C2-4" se debe interpretar en el mismo sentido.
Como se usa en el presente documento, alquiniloxicarbonilamino C2-6alquilo C i -6, se refiere a un radical alquilo C i -6 como se ha definido de manera general anteriormente, sustituido con un grupo alquiniloxicarbonilamino C2-6 como se han definido anteriormente. La expresión "alquiniloxicarbonilamino C2-4alquilo C1-4" se debe interpretar con el mismo sentido.
Como se usa en el presente documento, la expresión "cicloalquilo C3-8" puede ser mono o bicíclica y contener de 3 a 8 átomos de carbono. "Cicloalquilo C3-6" se debe interpretar con el mismo sentido. Los ejemplos de cicloalquilo C3-8 incluyen, pero sin limitarse a, ciclopropilo, 1 -metilciclopropilo, 2-metilciclopropilo, ciclobutilo, ciclopentilo y ciclohexilo.
Como se usa en el presente documento, el término "arilo" se refiere a un sistema anular aromático constituido únicamente por átomos de hidrógeno de carbono que podrá ser mono-, bi- o tricíclico. Los ejemplos de tales sistemas anulares incluyen fenilo, naftalenilo, antracenilo, indenilo o fenantrenilo.
Como se usa en el presente documento, el término "heteroarilo" se refiere a un radical anular monocíclico aromático de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre nitrógeno, oxígeno y azufre. El radical heteroarilo puede unirse mediante un átomo de carbono o un heteroátomo. Los ejemplos de heteroarilo incluyen, pero sin limitarse a, furilo, pirrolilo, tienilo, pirazolilo, imidazolilo, tiazolilo, isotiazolilo, oxazolilo, isoxazolilo, triazolilo, tetrazolilo, pirazinilo, piridazinilo, pirimidilo o piridilo.
Como se usa en el presente documento, el término "heterodiarilo" se refiere a un sistema de anillo, aromático, bicíclico de 9 o 10 miembros estable, que comprende 1,2, 3 o 4 heteroátomos seleccionados individualmente entre nitrógeno, oxígeno y azufre. El radical heteroarilo puede unirse mediante un átomo de carbono o un heteroátomo.
Como se usa en el presente documento, el término "heterociclilo" o "heterocíclico" se refiere a un radical de anillo no aromático, de 4, 5 o 6 miembros, estable que comprende 1,2 o 3, heteroátomos seleccionados individualmente entre nitrógeno, oxígeno y azufre. El radical heterociclilo puede unirse al resto de la molécula mediante un átomo de carbono o un heteroátomo. Los ejemplos de heterociclilo incluyen, pero sin limitarse a, azetidinilo, oxetanilo, pirrolinilo, pirrolidilo, tietanilo, tetrahidrofurilo, tetrahidrotienilo, tetrahidrotiopiranilo, piperidilo, piperazinilo, tetrahidropiranilo, morfolinilo o perhidroazepinilo.
Como se usa en el presente documento, la expresión "cicloalquil C3 -8alquilo C0-6" se refiere a un anillo cicloalquilo C3 -8 como se ha definido anteriormente, unido al resto de la molécula mediante un enlace sencillo o mediante un radical alquileno C1-6 como se ha definido anteriormente. "Cicloalquil C3-6alquilo C1-2" se debe interpretar con el mismo sentido. Los ejemplos de cicloalquil C3-8alquilo C0-6 incluyen, pero sin limitarse a, ciclopropilo, ciclopropilmetilo, ciclopropiletilo, ciclobutilo, ciclopentilo o ciclohexilo.
Como se usa en el presente documento, la expresión "cicloalquil C3-6alcoxi C1-2" se refiere a un radical C1-2 alcoxi como se defien en general anteriormente sustituido con un anillo cicloalquilo C3-6 como se ha definido anteriormente.
Como se usa en el presente documento, la expresión "cicloalquil C3-6 carbonilo" se refiere a un radical -C(O)Ra , en el que Ra es un anillo de cicloalquilo C3-6 como se definió anteriormente.
Como se usa en el presente documento, la expresión "cicloalquil C3-6 carboniloxi" se refiere a un radical -OC(O)Ra en el que Ra es un anillo de cicloalquilo C3-6 como se describió anteriormente.
Como se usa en el presente documento, la expresión "cicloalquil carboniloxi C3-6 alquilo C1-4" se refiere a un grupo cicloalquilcarboniloxi C3-6 como se describió anteriormente unido al resto de la molécula por un radical alquileno C1-4 como se definió anteriormente.
Como se usa en el presente documento, la expresión "fenilalquilo C0-6" se refiere a un anillo fenilo unido al resto de la molécula mediante un enlace sencillo o mediante un radical alquileno C1-6 como se ha definido anteriormente. "Fenilalquilo C1-6" y "fenilalquilo C1-2" se deben interpretar en consecuencia. Los ejemplos de fenilalquilo C0-6 incluyen, pero sin limitarse a, fenilo, bencilo o 2-feniletilo.
Como se usa en el presente documento, el término "fenilalcoxi C1-2" se refiere a un radical alcoxi C1-2 como se define generalmente anteriormente sustituido por un anillo de fenilo.
Como se usa en el presente documento, la expresión "fenilalquenilo C2-6" se refiere a un radical alquenilo C2-6 como se define generalmente más arriba sustituido por un anillo de fenilo.
Como se usa en el presente documento, el término "fenilcarboniloxi" se refiere a un radical -OC(O)Ra en el que Ra es un anillo de fenilo.
Como se usa en el presente documento, la expresión "fenilcarboniloxi alquilo C1-4" se refiere a un grupo fenilcarboniloxi como se describió anteriormente unido al resto de la molécula mediante un radical alquileno C1-4 como se ha definido anteriormente.
Como se usa en el presente documento, la expresión "naftilalquilo C0-6" se refiere a un anillo naftaleno unido al resto de la molécula mediante un enlace sencillo o mediante un radical alquileno C1-6 como se ha definido anteriormente.
Como se usa en el presente documento, la expresión "heteroarilalquilo C0-6" se refiere a un anillo heteroarilo como se ha descrito anteriormente unido al resto de la molécula mediante un enlace sencillo o mediante un radical alquileno C1-6 radical como se ha definido anteriormente. "Heteroarilalquilo C1-6" y "heteroarilalquilo C1-2" se deben interpretar en consecuencia.
Como se usa en el presente documento, la expresión "heteroarilalcoxi C1-6" se refiere a un radical alcoxi C1-6como se define en general anteriormente sustituido por un grupo heteroarilo como se ha definido en general anteriormente. Heteroarilalcoxi C 1-2" se debe interpretar en consecuencia.
Como se usa en el presente documento, la expresión "heterodiaralquilo C0-6" se refiere a un anillo heterodiarilo como se ha descrito anteriormente unido al resto de la molécula mediante un enlace sencillo o mediante un radical alquileno C1-6 radical como se ha definido anteriormente. "Heterodiarilalquilo C1-6" y "heterodiarilalquilo C1-2" se deben interpretar en consecuencia
Como se usa en el presente documento, la expresión "heterociclilalquilo C0-6" se refiere a un anillo heterociclilo como se ha descrito anteriormente unido al resto de la molécula mediante un enlace sencillo o mediante un radical alquileno C1-6 como se ha definido anteriormente. "Heterociclilalquilo C1-6" y "heterociclilalquil C1-2" se deben interpretar en consecuencia.
Como se usa en este documento, el término "heterociclilalcoxi C1-6" se refiere a un radical alcoxi C1-6 como se define en general anteriormente sustituido por un grupo heterociclilo como se define en general anteriormente. "Heterociclilalcoxi C1-2" se debe interpretar en consecuencia.
Como se usa en el presente documento, el término "heterociclilcarboniloxi" se refiere a un radical -OC(O)Ra en el que Ra es un anillo de heteroarilo como se describió anteriormente.
Como se usa en este documento, el término "heterociclilcarboniloxialquilo C1-4" se refiere a un grupo heterociclilcarboniloxi como se describió anteriormente unido al resto de la molécula por un radical alquileno C1-4 como se definió anteriormente.
Como se usa en el presente documento, la expresión "cicloalquilcarbonilamino C3-6alquilo C1-6" se refiere a un radical de la fórmula -Ra NHC(O)Rb , donde Ra es un radical alquilo C^com o se ha definido anteriormente y Rb es un anillo cicloalquilo C3-6 como se ha descrito anteriormente.
La presencia de uno o más átomos de carbono asimétricos posibles en un compuesto de fórmula (I) se refiere a que los compuestos pueden existir en formas isoméricas quirales, es decir, formas enantioméricas o diastereoméricas. También pueden existir atropoisómeros como resultado de la rotación restringida alrededor de un enlace sencillo. Se pretende que la fórmula (I) incluya todas estas formas isoméricas posibles y sus mezclas. La presente invención incluye todas aquellas formas isoméricas posibles y sus mezclas para un compuesto de fórmula (I). Asimismo, se pretende que la fórmula (I) incluya todos los tautómeros posibles (incluido el tautomerismo lactama-lactima y el tautomerismo ceto-enol) cuando estén presentes. La presente invención incluye todas las posibles formas tautoméricas para un compuesto de fórmula (I).
En cada caso, los compuestos de fórmula (I) de acuerdo con la invención se encuentran en forma libre, en forma covalentemente hidratada, en forma oxidada en forma de un N-óxido o en forma de sal, por ejemplo, una forma de sal útil desde el punto de vista agrícola o agroquímicamente aceptable.
Los N-óxidos son formas oxidadas de aminas terciarias o formas oxidadas de compuestos heteroaromáticos que contienen nitrógeno. Se describen, por ejemplo, en el libro "Heterociclic N-oxides" de A. Albini y S. Pietra, CRC Press, Boca Raton 1991.
La siguiente lista proporciona definiciones, que incluyen definiciones preferidas, para sustituyentes n, A1, A2 , A3 , A4 , R1, R2 , R3 , R4 , R5 , R6 , R7 , R8 , R9 , R10, R11, R12, R13, R14, R15, R16, y R17 en referencia a los compuestos de fórmula (I). Para cualquiera de estos sustituyentes, se puede combinar cualquiera de las definiciones que se indican a continuación con cualquier definición de cualquier otro sustituyente que se indique a continuación o en otra sección de este documento.
n representa 1 o 2. En algunas realizaciones de la invención, n es 1. En otras realizaciones de la invención, n es 2. Preferentemente, n es 1.
A1 representa N o CR1, donde R1 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi.
A2 representa N o CR2 , donde R2 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi.
A3 representa N o CR3 , donde R3 es hidrógeno o halógeno.
A4 representa N o CR4 , donde R4 es hidrógeno o halógeno. y
donde 0, 1 o 2 de A1, A2 , A3 y A4 son N;
R1 y R2 se seleccionan independientemente entre hidrógeno, halógeno, metilo, etilo. difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi. Preferentemente, R1 y R2 se seleccionan independientemente entre hidrógeno y halógeno. Más preferentemente, R1 y R2 son hidrógeno.
R3 y R4 se seleccionan independientemente entre hidrógeno y halógeno. Preferentemente, R3 y R4 se seleccionan independientemente entre hidrógeno y flúor. Más preferentemente, R3 y R4 son hidrógeno.
A3 puede representar CR3 , donde R3 es hidrógeno o halógeno.
A4 puede representar CR4 , donde R4 es hidrógeno o halógeno.
En los compuestos de acuerdo con la Fórmula (I), al menos dos de los grupos R1, R2 , R3 y R4 puede ser hidrógeno.
Preferentemente, tres de R1, R2 , R3 y R4 pueden ser hidrógeno, donde más preferentemente R2 , R3 y R4 son hidrógeno.
En algunas realizaciones de la invención, el anillo de 6 miembros que comprende de A1 to A4 es un grupo fenilo (donde de A1 a A4 son C-H), piridinilo (donde A1 o A3 es N y las otras posiciones A son C-H), pirimidinilo (donde A1 y A3 son N y las otras posiciones A son C-H), fluorofenilo (donde A 1 o A3 son C-F (preferentemente A3 es C-F) y las otras posiciones A son C-H) o difluorofenilo (donde A1 y A3 son C-F y las posiciones A2 y A4 son C-H).
En los compuestos de acuerdo con la Formula (I), cuando R8 no es OR12 o NR14R15, preferentemente A1, A2 , A3 y A4 son C-H; A2 , A3 y A4 son C-H y A1 es N; A1, A2 y A4 son C-H y A3 es N; A1, A2 y A4 son C-H y A3 es C-halógeno (preferentemente flúor); A2 , A3 y A4 son C-H y A1 es C-halógeno (preferentemente flúor) o A2 , A3 y A4 son C-H y A1 es
C-halógeno (preferentemente flúor); A2 y A4 son C-H y A1 y A3 son C-halógeno (preferentemente flúor); o A3 y A4 son
C-H y A1 y A2 son C-halógeno (preferentemente flúor). Más preferentemente, A1, A2 , A3 y A4 son C-H.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 es -OR12, preferentemente A1, A2 , A3 y A4 son C-H.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 es -NR14R15, preferentemente A1, A2 , A3 y A4 son C-H;
A1, A2 y A4 son C-H y A3 es C-halógeno (preferentemente flúor); o A2 , A3 y A4 son C-H y A1 (preferentemente flúor). Más preferentemente, A1, A2 , A3 y A4 son C-H.
R5 y R6 representan independientemente hidrógeno, alquilo C1-4, halógeno, ciano, trifluorometilo y difluorometilo, o R5 y R6 , junto con el átomo de carbono que comparten, forman un ciclopropilo. Preferentemente R5 y R6 pueden seleccionarse independientemente entre hidrógeno, alquilo C 1-4, halógeno, ciano, trifluorometilo y difluorometilo, o R5 y R6 , junto con el átomo de carbono que comparten, forman un ciclopropilo. Más preferentemente, R5 y R6 se seleccionan independientemente entre hidrógeno, alquilo C1-4 (en particular metilo) y ciano.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 no es -OR12 o -NR14R15, preferentemente R5 y R6 son hidrógeno; R5 es hidrógeno y R6 es metilo; o R5 es hidrógeno y R6 es ciano. Más preferentemente, R5 y R6 son hidrógeno y n es 1.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 es -OR12, preferentemente R5 y R6 son hidrógeno y n es
1.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 es -NR14R15, preferentemente R5 y R6 son hidrógeno y n es 1.
R7 es hidroxi, alquilo C1-4, haloalquilo C2-4, alcoxi C1-4, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, haloalcoxi C1-2alquilo
C1-4, alquinilo C3-4, alquenilo C3-6, alqueniloxi C3-6, alquiniloxi C3-6, haloalquenilo C3-6, haloalqueniloxi C3-6, alquilcarboniloxi C1-4, haloalquilcarboniloxi C1-4, alcoxicarboniloxi C1-4, alquilcarboniloxi C1-4alquilo C1-4, haloalquilcarboniloxi C1-4alquilo C1-4, alcoxicarboniloxi C1-4alquilo C1-4; o R7 es cicloalquilo C3-6, cicloalquil C3-6alquilo
C1-2, cicloalquil C3-6alcoxi C1-2, fenilo, fenilalquilo C1-2, fenilalcoxi C1-2, heteroarilo, heteroarilalquilo C1-2, heteroarilalcoxi
C1-2, heterociclilo, heterociclilalquilo C1-2, heterociclilalcoxi C1-2, cicloalquilcarboniloxi C3-6, heterociclilcarboniloxi, fenilcarboniloxi, cicloalquilcarboniloxi C3-6alquilo C1-4, heterociclilcarboniloxialquilo C1-4 o fenilcarboniloxialquilo C1-4; donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre ciano, flúor, cloro, bromo, metilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi.
Preferentemente, R7 es alquilo C1-4, alcoxi C1-4, alcoxi C1-2alquilo C1-4, haloalcoxi C1-2alquilo C1-4, alquenilo C3-6, alquinilo C3-4, alqueniloxi C3-6, alquiniloxi C3-6, haloalquenilo C3-6, haloalqueniloxi C3-6, cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, cicloalquil C3-6alcoxi C1-2, fenilo, fenilalquilo C1-2, fenilalcoxi C1-2, heteroarilo, heteroarilalquilo C1-2, heteroarilalcoxi C1-2, heterociclilo, heterociclilalquilo C1-2 o heterociclilalcoxi C1-2.
Más preferentemente, R7 es alquilo C1-4, alcoxi C1-4, alcoxi C i-2alqu¡lo C1-4, alquenilo C3-6, alquinilo C3-4, alqueniloxi C3-6 , haloalquenilo C3-6, haloalqueniloxi C3-6, cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, fenilalcoxi C1-2, heteroarilalquilo C1-2, o heterociclilalquilo C1-2.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 no es -OR12 o -NR14R15, preferentemente R7 es hidoxi, alquilo C1-4, haloalquilo C2-4, alcoxi C1-4, hidroxialquilo C1-4, alcoxi C1 -2alquilo C1-4, alquenilo C3-6, alquinilo C3-4, haloalqueniloxi C3-6, cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, fenilalcoxi C1-2, heterociclilo, heterociclilalquilo C1-2, heteroarilo o heteroarilalquilo C1-2, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente entre N, O y S, el resto heterociclilo es un anillo no aromático de 5 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre ciano, flúor, cloro, bromo, metilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi. Más preferentemente, R7 es hidoxi, alquilo C1-4, fluoroalquilo C2-4, alcoxi C1-4, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, alquenilo C3-4, alquinilo C3-4, haloalqueniloxi C3-6, ciclopropilo, (ciclopropil)metilo, fenilalcoxi C1-2, (tetrahidrofuran-2-il)metilo o (2-furil)metilo, donde cualquiera de dichos restos ciclopropilo, fenilo, tetrahidrofuran-2-ilo y 2-furilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre ciano, flúor, cloro, bromo, metilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 no es -OR12 o -NR14R15, aún más preferentemente R7 es alquilo C1-4, haloalquilo C2-4, alcoxi C1-4 o cicloalquilo C3-6. Además, más preferentemente, R7 es alquilo C1-4, fluoroalquilo C2-4, metoxi, etoxi o ciclopropilo. Más preferentemente, R7 es metilo, etilo, n-propilo, iso-propilo, 2,2,2-fluoroetilo, metoxi, etoxi o ciclopropilo.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 es -OR12, preferentemente R7 es hidoxi, alquilo C1-4, haloalquilo C2-4, alcoxi C1-4, alquenilo C3-6, alquinilo C3-4, alcoxicarboniloxi C1-4. Más preferentemente, R7 es hidoxi, alquilo C1-4, haloalquilo C2-4, alcoxi C1-4, alquenilo C3-4, alquinilo C3-4, alcoxicarboniloxi C1-4. Incluso más preferentemente, R7 es alcoxi C1-4, en particular, metoxi.
En los compuestos de acuerdo con la Fórmula (I), cuando R8 es -NR14R15, preferentemente R7 es hidoxi, alquilo C1-4, haloalquilo C2-4, alcoxi C1-4, alquenilo C3-6, alquinilo C3-4, cicloalquilo C3-6. Más preferentemente, R7 es hidoxi, alquilo C1-4, haloalquilo C2 , alcoxi C1-2, alquenilo C3-4, alquinilo C3-4, ciclopropilo. Incluso más preferentemente, R7 es alquilo C1-4 o alcoxi C1-4, y en particular, metilo, etilo o metoxi.
R8 es hidrógeno, alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C2-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C^alcoxi C1-4alquilo C1-6, alquiniloxi C2-4alquilo C1-6, aminoalquilo C1-6, N-alquilamino C^alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C 1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C^alquilo C1-6, N,N-dialquilaminocarbonil C1 -4alquilo C1-6, alquilsulfanil C1-6alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6, alquilsulfonilamino C1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6, alquiniloxicarbonilamino C2-6alquilo C1-6, alquilcarbonilamino C1-4alquilo C1-6, alcoxicarbonilamino C^alquilo C1-6 ; o
R8 es cicloalquilo C3-8, cicloalquilo C3-8alquilo C1-6, donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C 1-6 , fenilalquenilo C2-6, naftilo, naftiloalquilo C1-6, heteroarilo, heteroarilalquilo C1-6 parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterodiarilo, heterodiarilalquilo C1-6 donde el resto heterodiarilo es un sistema aromático, bicíclico, de 9 a 10 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S o cicloalquilcarbonilamino C3-6alquilo C1-6,
donde para R8 , cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo, heterociclilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; o, adicionalmente, cuando R8 es ciclopropilo, el resto ciclopropilo está sustituido con 4 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 , con la condición de que al menos 2 sustituyentes R9 sean los mismos; donde
R9 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C 1-4 , haloalcoxi C1-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, cicloalquilcarbonilo C3-6, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C 1-4 o alcoxicarbonilamino C1-4, y donde cuando R8 es cicloalquil C3-8alquilo C1-6, heterociclilo, heterociclilalquilo C1-6 o cicloalquilo C3-8 sustituido, R9 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo; o
donde para R8 , cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo, heterociclilo está opcionalmente sustituido con 1 sustituyente seleccionado entre R10 y además opcionalmente sustituido con 1 o 2 sustituyentes seleccionados entre R9 ; donde
R10 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-2, fenilo, fenilalquilo C1-2, heteroarilo, heteroarilalquilo C1-2 donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos
seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo Ci -6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N,
O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R11; donde
R11 es hidrógeno, ciano, flúor, cloro, bromo, metilo, trifluorometilo, metoxi y etoxi.
En algunas realizaciones de los compuestos de acuerdo con la Fórmula (I), R8 es hidrógeno, alquilo C1-6, alquenilo C2-6 , alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C1-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C 1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, alquiniloxi C2-4alquilo C1-6, aminoalquilo C1-6, N-alquilamino
C1-4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1-4alquilo C1-6, alquilsulfanil C1 -6alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6, alquilsulfonilamino C 1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6 o alquiniloxicarbonilamino C2-6alquilo C1-6.
En algunas realizaciones de los compuestos de acuerdo con la Fórmula (I), R8 es cicloalquilo C3-8, cicloalquilo C3-8alquilo C1-6, donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C1-6, fenilalquenilo C2-6, naftilo, naftiloalquilo C1-6, heteroarilo, heteroarilalquilo C1-6 parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterodiarilo, heterodiarilalquilo C1-6 donde el resto heterodiarilo es un sistema aromático, bicíclico, de
9 a 10 miembros que comprende 1,2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o
3 heteroátomos seleccionados individualmente entre N, O y S y cicloalquilcarbonilamino C3-6alquilo C1-6. Al menos uno de los restos cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, fenilo, fenilalquilo C1-6, fenilalquenilo C2-6, naftilo, naftilalquilo
C1-6, heteroarilo, heteroarilalquilo C1-6, heterodiarilo, heterodiarilalquilo C1-6, heterociclilo, heterociclilalquilo C1-6 y cicloalquilcarbonilamino C3-6alquilo C1-6 puede estar sustituido con 1, 2 o 3 sustituyentes seleccionados entre ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C1-4, haloalcoxi
C1-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 y alcoxicarbonilamino C1-4.
Preferentemente, R8 es hidrógeno, alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C2-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alco 6, alquiniloxi C2-4alquilo C1-6, aminoalquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alquilcarboniloxi C1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6, alquiniloxicarbonilamino C2-6alquilo C1-6, alquilcarbonilamino C1-4alquilo C1-6, alcoxicarbonilamino C1-4alquilo C1-6; o R8 es cicloalquilo C3-8, cicloalquil C3-8alquilo
C1-6, donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C1-6, fenilalquenilo C2-6, naftilo, heteroarilo, heteroarilalquilo C1-6 parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o
3 heteroátomos seleccionados individualmente entre N, O y S o cicloalquilcarbonilamino C3-6alquilo C1-6, donde para
R8 , cualquier resto de cicloalquilo C3-8, cicloalquilo C3-8alquilo C1-6, fenilo, fenilalquilo C1-6, fenilalquenilo C2-6, heteroarilo, heteroarilalquilo C1-6, heterociclilo y heterociclilalquilo C1-6 están opcionalmente sustituidos con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde R9 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C1-4, haloalcoxi C1-4, alquiniloxi C3-4, alquilcarbonilo C1-4, cicloalquilcarbonilo C3-6, alcoxicarbonilo C1-4, carbonilamino; o donde para R8 , cualquier resto de cicloalquilo C3-8, fenilo están opcionalmente sustituidos con 1 sustituyente seleccionado entre R10 y además están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre R9 ; donde R10 es fenilo, heteroarilo donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos fenilo y heteroarilo están opcionalmente sustituidos con unos sustituyentes individuales seleccionados entre R11; donde R11 es ciano, flúor, cloro, bromo, metilo, trifluorometilo, metoxi y etoxi.
Más preferentemente, R8 es alquilo C1-6, alquenilo C2-4, alquinilo C2-4, cianoalquilo C1-4, haloalquilo C1-5, haloalquenilo
C2-4, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, haloalcoxi C1-2alquilo C1-4, alcoxi C1-2alcoxi C1-2alquilo C1-4, alquiniloxi
C2-4alquilo C1-4, aminoalquilo C1-4, alquilcarbonil C1 -4alquilo C1-4, alquilcarbonil C1-4alquenilo C2-4, alquilcarboniloxi C1-4alquilo C1-4, alquilsulfonilamino C1-4alquinilo C2-4, alquiniloxicarbonilamino C2-4alquilo C1-4, alquilcarbonilamino C1-2alquilo C1-4, alcoxicarbonilamino C1-2alquilo C1-4; o R8 es cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C1-4, fenilalquenilo C2-4, naftilo, heteroarilo, heteroarilalquilo C1-2 parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros comprende
1, 2 o 3 heteroátomos seleccionados entre N, O y S, heterocicliclo, heterociclilalquilo C1-2 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S, o cicloalquilcarbonilamino C3-6alquilo C1-4, donde para R8 , cualquier resto de cicloalquilo C3-6, cicloalquil
C3-6alquilo C1-2, fenilo, fenilalquilo C1-2, fenilalquenilo C2-4, naftilo, heteroarilo, heteroarilalquilo C1-2, heterocicliclo y heterociclilalquilo C1-2 están opcionalmente sustituidos con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde R9 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, haloalquenilo
C2-4, alcoxi C1-4, haloalcoxi C1-4, alquiniloxi C3-4, alquilcarbonilo C1-4, cicloalquilcarbonil C3-6, alcoxicarbonilo C1-4, carbonilamino; o donde para R8 , cualquier resto de cicloalquilo C3-6, fenilo están opcionalmente sustituidos con 1
sustituyente seleccionado entre R10 y están además opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre R9 ; donde R10 es fenilo, heteroarilo donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1,2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos fenilo y heteroarilo están opcionalmente sustituidos con un sustituyente solo seleccionado entre R11; donde R11 es ciano, flúor, cloro, bromo, metilo, trifluorometilo, metoxi y etoxi.
Incluso más preferentemente, R8 es alquilo C1-6, alquenilo C2-4, alquinilo C2-4, cianoalquilo C1-4, haloalquilo C1-5, haloalquenilo C2-4, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, haloalcoxi C1-2alquilo C1-4, alcoxi C1-2alcoxi C1-2alquilo C1-4, aminoalquilo C1-4, alquilcarbonil C1-2alquilo C1-4, alquilcarbonil C1-4alquenilo C2-4, alquilcarboniloxi C1-4alquilo C1-4, alquilsulfonilamino C1-4alquinilo C2-4, alquilcarbonilamino C1-2alquilo C1-4, alquiniloxicarbonilamino C2-4alquilo C1-4, alcoxicarbonilamino C1-2alquilo C1-4 ; o
R8 es cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, fenilo, fenilalquilo C1-4, fenilalquenilo C2-4, naftilo, un resto que contiene heteroarilo seleccionado entre furanilo (que incluye furan-2-ilo, furan-3-ilo), pirazolilo (que incluye pirazol-1-ilo, pirazol-3-ilo, pirazol-4-ilo, pirazol-5-ilo), imidazolilo (que incluye imidazol-1-ilo, imidazol-2-ilo, imidazol-4-ilo, imidazol-5-ilo), triazolilo (que incluye 1,2,3-triazol-1 -ilo), 1,2,3-benzotiadiazol, (piridinil)metilo (que incluye piridin-2-metilo, piridin-3-metilo, piridin-4-metilo), o un resto que contiene heterociclilo seleccionado entre oxetanilo (que incluye oxetan-2-ilo, oxetan-3-ilo), pirrolidinilo (que incluye pirrolidin-2-ilo, pirrolidin-3-ilo), azetidinilo (que incluye azetidin-2-ilo, azetidin-3-ilo), tetrahidrofuranilo (que incluye tetrahidrofuran-2-ilo, tetrahidrofuran-3-ilo), 1,3-dioxolanilo (que incluye 1,3-dioxolan-2-ilo), tietanilo (que incluye tietan-2-ilo, tietan-3-ilo), 1-oxo-tietan-3-ilo, 1,1-dioxo-tietan-3-ilo, tetrahidropiranilo (que incluye tetrahidropiran-2-ilo, tetrahidropiran-3-ilo, tetrahidropiran-4-il), tetrahidrotiopiranilo (que incluye tetrahidrotiopiran-2-ilo, tetrahidrotiopiran-3-ilo, tetrahidrotiopiran-4-ilo), cicloalquilcarbonilamino C3-6alquilo C 1-4 ,
donde el ciclo de cada resto que contiene heteroarilo o el resto que contiene heterociclilo está opcionalmente sustituido con 1 o 2 o 3 sustituyentes, que pueden ser los mismo o diferentes, seleccionados entre R9 ; donde
R9 es ciano, metilo, cloro, flúor, hidroxilo, metoxi, trifluorometilo, haloalquenilo C2-, metilcarbonilo, etilcarbonilo, carbonilamino; o
donde el ciclo de cada resto que contiene heteroarilo o el resto que contiene heterociclilo está opcionalmente sustituido con 1 sustituyente seleccionado entre R10 y además opcionalmente sustituido con 1 o 2 sustituyentes seleccionados entre R9 , donde
R10 es fenilo o piridinilo (que incluye piridin-2-ilo), donde fenilo o piridinilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R11; donde
R11 es flúor, cloro, bromo y metoxi.
En algunas realizaciones de los compuestos de acuerdo con la Fórmula (I), preferentemente R8 es alquilo C1-6, haloalquilo C1-2, hidroxialquilo C1-6, alcoxi C1-2alquilo C1-4, cicloalquilo C3-6 o heterociclilo, donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente entre N y O, donde el cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde R9 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4 o alcoxi C1-4.
Más preferentemente, R8 es alquilo C1-4, haloalquilo C1-2, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, cicloalquilo C3-6 o heterociclilo, donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos que son oxígeno, donde cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde R9 es ciano, flúor, cloro, hidroxi, metilo, etilo, trifluorometilo y metoxi.
Incluso más preferentemente, R8 es alquilo C1-4, haloalquilo C1-2, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-2, cicloalquilo C3-6 o heterociclilo, donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos que son oxígeno, donde cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde R9 es flúor, cloro, metilo.
Aún más preferentemente, R8 es alquilo C1-4 (metilo, etilo, n-propilo, iso-propilo, n-butilo, sec-butilo, iso-butilo, t-butilo), 2,2,2-trifluoroetilo, hidroxialquilo C1-4, alcoxi C1 -2alquilo C1-2, ciclopropilo o heterociclilo, donde el resto heterociclilo es tetrahidrofuran-2-ilo, oxetan-3-ilo o 1,3-dioxolan-2-ilo, donde ciclopropilo y heterociclilo están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre R9, donde R9 es flúor, cloro, metilo.
R8 puede representar -OR12, donde R12 es hidrógeno, alquilo C 1-6, alquenilo C3-6, alquinilo C3-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C3-6, hidroxialquilo C 1-6, alcoxi C1 -4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C 1-4alcoxi C1-4alquilo C1-6, aminoalquilo C1-6, N-alquilamino C1 -4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1-4alquilo C1-6, alquilsulfanil C1-4alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6, alquilsulfonilamino C1-6alquilo C1-6 ; o
R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6 , donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo Ci-6, heteroarilo, heteroarilalquilo C1-6 parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y 5, heterociclilo, heterociclilalquilo C1-6 , donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S;
donde para R12, cualquier resto cicloalquilo, fenilo, heteroarilo, heterociclilo está opcionalmente sustituido con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R13; donde
R13 es ciano, halógeno, hidroxi, alquilo C1-4 , alquenilo C2-4 , alquinilo C2-4 , haloalquilo C1-4, haloalquenilo C2-4 , alcoxi C1-4 , haloalcoxi C1-4, alqueniloxi C3-4, alquiniloxi C3-4 , N-alquilamino C 1-4, N,N-dialquilamino C1-4 , alquilcarbonilo C1-4 , alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4 , N,N-dialquilaminocarbonilo C1-4 o alcoxicarbonilamino C1-4;
y donde cuando R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6 , heterociclilo o heterociclilalquilo C1-6 sustituido, R13 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo;
Preferentemente, R12 es hidrógeno, alquilo C1-6 , alquenilo C3-6, alquinilo C3-6 , cianoalquilo C1-6 , haloalquilo C1-6 , haloalquenilo C3-6, hidroxialquilo C1-6 , alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6 , alcoxi C1-4alcoxi C1-4alquilo C1-6, aminoalquilo C1-6 , N-alquilamino C1-4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6 , alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6 , alcoxicarbonil C1-6alquilo C1-6 , alquilcarboniloxi C1-6alquilo C1-6 , N-alquilaminocarbonil C1-4alquilo C1-6 , N,N-dialquilaminocarbonil C1-4alquilo C1-6 , alquilsulfanil C1-4alquilo C1-6 , alquilsulfonil C1-6 alquilo C1-6, alquilsulfonilamino C1-6alquilo C1-6 , fenilalquilo C1-6 , cicloalquilo C3-8 o cicloalquil C3-8alquil C1-6. Más preferentemente, R12 es hidrógeno, alquilo C1-6 , alquenilo C3-6, alquinilo C3-6 , haloalquilo C1-6, alcoxi C1 -4alquilo C1-6 , fenilo o fenilalquilo C1-6. Incluso más preferentemente, R12 es alquilo C1-6 , alquenilo C3-4, alquinilo C3-4 , haloalquilo C1-4 , alcoxi C1 -2alquilo C1-4 , fenilo o fenilalquilo C1-2. Incluso más preferentemente, R12 es alquilo C1-6 , alquenilo C3-4 , alquinilo C3-4 , fluoroalquilo C1-4 , cloroalquilo C1-4 , alcoxi C1-2alquilo C1-2 , fenilo, bencilo.
R8 representa -NR14R15, donde R14 es hidrógeno, ciano, alquilo C1-6 , alcoxi C1-6 , alquenilo C2-6 , alquinilo C2-6 , alqueniloxi C3-6 , alquiniloxi C3-6, cianoalquilo C1-6, haloalquilo C1-6 , haloalquenilo C1-6, hidroxialquilo C1-6, alcoxi C1 -4alquilo C1-6 , haloalcoxi C1-4alquilo C1-6 , alcoxi C1-4alcoxi C1-4alquil C1-6 , aminoalquil C1-6 , N-alquilamino C1-4alquilo C1-6 , N,N-dialquilamino C1-4alquilo C1-6 , alquilcarbonil C1-6alquilo C1-6 , alquilcarbonil C1-6alquenilo C2-6 , alcoxicarbonil C1-6alquilo C1-6 , alquilcarboniloxi C1-6alquilo C1-6 , N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1-4alquilo C 1-6, alquilsulfanil C1-4alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6 , alquilsulfonilamino C1-6alquilo C1-6 ; o
R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6 , cicloalquil C3-8alcoxi C1-6 , cicloalquiloxi C3-6 , donde el resto cicloalquilo es, opcionalmente, fenilo, fenilalquilo C1-6, fenilalcoxi C1-6 , heteroarilo, heteroarilalquilo C1-6, heteroarilalcoxi C1-6 parcialmente insaturados donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1,2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C 1-6, heterociclilalcoxi C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S;
donde para R14, cualquier resto cicloalquilo, fenilo, heteroarilo, heterociclilo está opcionalmente sustituido con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R16; donde
R16 es ciano, halógeno, hidroxi, alquilo C1-4 , alquenilo C2-4 , alquinilo C2-4 , haloalquilo C1-4, haloalquenilo C2-4 , alcoxi C1-4 , alcoxi C1-2alquilo C1-2 , haloalcoxi C1-4 , alqueniloxi C3-4 , alquiniloxi C3-4 , N-alquilamino C1-4 , N,N-dialquilamino C1-4 , alquilcarbonilo C1-4 , alcoxicarbonilo C1-4 , carbonilamino, N-alquilaminocarbonilo C1-4 , N,N-dialquilaminocarbonilo C 1-4 o alcoxicarbonilamino C1-4 ;
y donde cuando R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6 , cicloalquil C3-8alcoxi C1-6 , heterociclilo, heterociclilalquilo C1-6 , heterociclilalcoxi C1-6 sustituido, R16 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo;
R15 es hidrógeno, alquilo C1-4 , alquinilo C3-4 , alcoxi C1-4alquilo C1-4 , cianoalquilo C1-4 , cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2 ; o
R14 y R15, junto con el átomo de nitrógeno al que están unidos, forman un ciclo de 4, 5 o 6 miembros que contiene opcionalmente un heteroátomo adicional seleccionado entre O, S y NR17; donde
R17 es hidrógeno, metilo, metoxi, formilo o acilo.
Preferentemente, R8 representa -NR14R15, donde R14 es hidrógeno, alquilo C1-6, alcoxi C1-6 , alquenilo C2-6 , alquinilo C2-6, cianoalquilo C1-6 , haloalquilo C1-6, haloalquenilo C1-6, hidroxialquilo C1-6 , alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6 , alcoxi C1-4alcoxi C1-4alquilo C1-6 , aminoalquilo C1-6 , N-alquilamino C1 -4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6 , C1-6alquilcarbonil C1-6alquilo C1-6 , alquilcarbonil C1-6alquenilo C2-6 , alcoxicarbonil C1-6alquilo C1-6 , alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6 , N,N-dialquilaminocarbonil C1-4alquilo C1-6 , alquilsulfanil C1
4alquilo C i -6, alquilsulfonil C i -6alquilo C i -6, alquiisulfonilamino C i -6alquilo C i -6 o cicloalquilo C3-8 y R15 es hidrógeno, alquilo C1-4, alcoxi C i -4alquilo C1-4 o cianoalquilo C1-4.
Mas preferentemente, R14 es hidrógeno, ciano, alquilo C1-6, alcoxi C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, alcoxi C i -4alquilo C1-6, alcoxicarbonil C i -6alquilo C1-6, o cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, fenilo o heteroarilalquilo C1-6, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, donde cualquiera de cicloalquilo
C3-8, fenilo o heteroarilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre R16, donde R16 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, alcoxi C1-4, haloalcoxi C1-4 o alcoxicarbonilo C1-4. Incluso más preferentemente, R14 es hidrógeno, alquilo C1-6, alcoxi C1-6, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-2, cicloal C3-6. Aún más preferentemente, R14 es hidrógeno, metilo, etilo, propilo, iso-propilo, sec-butilo, metoxi, etoxi, alilo, propin-2-ilo, 2,2,2-trifluorometilo, ciclopropilo o ciclobutilo.
Preferentemente, R15 es hidrógeno, metilo, etilo, alquinilo C3-4 o metoxietilo. Más preferentemente, R15 es hidrógeno, metilo o etilo, en particular, hidrógeno.
En otras realizaciones, R15 puede ser hidrógeno, alquilo C1-4, alcoxi C1-4 alquilo C1-4 o cianoalquilo C1-4.
R14 y R15, junto con el átomo de nitrógeno al que están unidos, pueden forman un ciclo de 5 o 6 miembros que contiene opcionalmente un heteroátomo adicional que es oxígeno.
En algunas realizaciones, para los compuestos de Fórmula (I), preferiblemente n es 1;
A1 a A4 son C-H, A1 es C-F y A2 a A4 son C-H, A1 y A2 son C-F y A3 y A4 son C-H, y A2 y o A1 es N y A2 son A4 C-H;
R5 y R6 se seleccionan independientemente de hidrógeno, alquilo C1-4 y ciano;
R7 es hidroxi, alquilo C1-4, fluoroalquilo C2-4, alcoxi C 1-4, hidroxialquilo C1-4, alcoxi C i-2alquilo C1-4, alquenilo C3-4, alquinilo C3-4, haloalqueniloxi C3-6, ciclopropilo, (ciclopropil) metilo, fenilC i-2alcoxi, (tetrahidrofuran-2-il) metilo o (2-furil) metilo, donde cualquiera de dichos restos ciclopropilo, fenilo, tetrahidrofuran-2-ilo y 2-furilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre ciano, fluoro, cloro, bromo, metilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi;
R8 es C i -6alquilo, C i-2haloalquilo, hidroxiCi -6alquilo, C i -2alcoxiCi -4alquilo, C3-6cicloalquilo o heterociclilo, en donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente de N y O, en donde cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1, 2 o 3 sustituyentes, que pueden ser iguales o diferentes, seleccionados de R9 ; y
R9 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1 -4 o alcoxi C1-4.
Más preferiblemente en los compuestos de Fórmula (I), n es 1;
A1 a A4 son C-H;
R5 y R6 se seleccionan independientemente entre hidrógeno y alquilo C1-4;
R7 es C i -4alquilo, C2-4fluoroalquilo, metoxi, etoxi o ciclopropilo;
R8 es C i -6alquilo, C i-2haloalquilo, hidroxiCi -6alquilo, C i -2alcoxiCi -4alquilo, C3-6cicloalquilo o heterociclilo, en donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente de N y O, en donde cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1, 2 o 3 sustituyentes, que pueden ser iguales o diferentes, seleccionados de R9 ; y
R9 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1 -4 o alcoxi C1-4.
Incluso más preferiblemente en los compuestos de Fórmula (I), n es 1;
A1 a A4 son C-H;
R5 y R6 se seleccionan independientemente de hidrógeno y metilo, preferiblemente hidrógeno;
R7 es metilo, etilo, n-propilo, iso-propilo, 2,2,2-fluoroetilo, metoxi, etoxi o ciclopropilo;
R8 es C i -4alquilo, C i-2haloalquilo, hidroxiCi -4alquilo, C i-2alcoxiCi-2alquilo, C3-6cicloalquilo o heterociclilo, en donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos que son oxígeno, en el que cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes, que pueden ser iguales o diferentes, seleccionados de R9 ; y
R9 es fluoro, cloro, metilo.
En otras realizaciones, para los compuestos de Fórmula (I), preferiblemente n es 1;
A1 a A4 son C-H;
R5 y R6 se seleccionan independientemente entre hidrógeno y metilo;
R7 es hidroxi, C1-4alquilo, C2-4haloalquilo, C1-4alcoxi, C3-6alquenilo, C3-4alquinilo o C1-4alcoxicarboniloxi;
R8 es -OR12; y
R12 es hidrógeno, C1-6alquilo, C3-6alquenilo, C3-6alquinilo, C1-6haloalquilo, C1-4alcoxic 1-6alquilo, fenilo, fenilC1-6alquilo. Más preferiblemente en los compuestos de Fórmula (I), n es 1;
A1 a A4 son C-H;
R5 y R6 son hidrógeno;
R7 es metoxi;
R8 es -OR12; y
R12 es hidrógeno, C1-6alquilo, C3-6alquenilo, C3-6alquinilo, C1-6haloalquilo, C1-4alcoxiC1-6alquilo, fenilo, fenilC1-6alquilo. En aún otras realizaciones, para los compuestos de Fórmula (I), preferiblemente n es 1;
A1 a A4 son C-H o A1, A2 y A4 son C-H y A3 son C-F;
R5 y R6 son hidrógeno;
R7 es hidroxi, C1-4alquilo, C2-4haloalquilo, C1-4alcoxi, C3-6alquenilo, C3-4alquinilo, C3-6cicloalquilo; R8 es -NR14R15; R14 es hidrógeno, ciano, C1-6alquilo, C1-6alcoxi, C2-6alquenilo, C2-6alquinilo, cianoC1-6alquilo, C1-6haloalquilo, C 1-4alcoxiC1-6alquilo, C1-6alcoxicarbonilC1-6alquilo, o C3-8cicloalquilo, C3-8cicloalquilC1-6alquilo, fenilo o heteroarilC1-6alquilo, donde el resto heteroarilo es un anillo aromático monocíclico de 5 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente de N, O y S, en donde cualquiera de C3-8 cicloalquilo, fenilo o heteroarilo, están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados entre R16, en donde R16 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, alcoxi C1-4, haloalcoxi C1-4 o alcoxicarbonilo C1-4; y
R15 es hidrógeno, metilo, etilo, alquinilo C3-4 o metoxietilo.
Más preferiblemente en los compuestos de Fórmula (I), n es 1;
A1 a A4 son C-H;
R5 y R6 son hidrógeno;
R7 es hidroxi, C1-4alquilo, C2-4 haloalquilo, C1-2alcoxi, C3-4alquenilo, C3-4alquinilo o ciclopropilo;
R8 es -NR14R15;
R14 es hidrógeno, metilo, etilo, propilo, iso-propilo, sec-butilo, metoxi, etoxi, alilo, propin-2-ilo, 2,2,2-trifluorometilo, ciclopropilo o ciclobutilo; y
R15 es hidrógeno, metilo o etilo.
Incluso más preferiblemente en los compuestos de Fórmula (I), n es 1;
A1 a A4 son C-H;
R5 y R6 son hidrógeno;
R7 es alquilo C1-4 o alcoxi C1-2 ;
R8 es -NR14R15;
R14 es hidrógeno, metilo, etilo, propilo, iso-propilo, sec-butilo, metoxi, etoxi, alilo, propin-2-ilo, ,2,2,2-trifluorometilo, ciclopropilo o ciclobutilo; y R15 es hidrógeno.
El compuesto de acuerdo con la Fórmula (I) puede seleccionarse a partir del compuesto 1.1 a 1.811 enumerados en la Tabla T1 a continuación, a partir del compuesto 2.1 al 2.26 enumerados en la Tabla T2 a continuación, y a partir del compuesto 3.1 al 3.140 enumerados en la Tabla T3 a continuación.
El compuesto de Fórmula (I) puede ser un compuesto de acuerdo con la Fórmula (IA):
donde
R1 y R2 se seleccionan independientemente entre hidrógeno, cloro, flúor, metilo, metoxi y trifluorometilo; y
R3 y R4 se seleccionan independientemente entre hidrógeno y halógeno;
donde al menos dos de los grupos R1, R2 , R3 y R4 son hidrógeno;
R5 y R6 se seleccionan independientemente entre hidrógeno y alquilo C1-4;
R7 es alquilo C1-4 o alcoxi C1-4; y
R8 es hidrógeno, alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C2-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, alquiniloxi C2-4alquilo C1-6, aminoalquilo C1-6, N-alquilamino C1-4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C 1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1 -4alquilo C1-6, alquilsulfanil C1-6alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6, alquilsulfonilamino C1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6, alquiniloxicarbonilamino C2-6alquilo C1-6 ; o
R8 es cicloalquilo C3-8alquilo C0-6, donde el resto cicloalquilo está opcionalmente insaturado parcialmente, fenilalquilo C0-6, fenilalquenilo C2-6,naftiloalquilo C0-6, heteroarilalquilo C0-6, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterodiarilalquilo C0-6 donde el resto heterodiarilo es un sistema aromático, bicíclico, de 9 a 10 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilalquilo C0-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S o cicloalquilcarbonilamino C3-6alquilo C1-6,
donde para R8 , cualquier resto de cicloalquil C3-8alquilo C0-6, fenilalquilo C0-6, fenilalquenilo C2-6, naftilalquilo C0-6, heteroarilalquilo C0-6, heterodiarilalquilo C0-6, heterociclilalquilo C0-6 y cicloalquilcarbonilamino C3-6alquilo C1-6 están opcionalmente sustituidos con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde
R9 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C 1-4 , haloalcoxi C1-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 o alcoxicarbonilamino C1-4, y donde R8 es cicloalquil C3-8alquilo C0-6 o heterociclilalquilo C0-6 sustituido, R9 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo; o
donde para R8 , cualquier resto de cicloalquil C3-8alquilo C0-6, fenilalquilo C0-6, fenilalquenilo C2-6, naftilalquilo C0-6, heteroarilalquilo C0-6, heterodiarilalquilo C0-6, heterociclilalquilo C0-6 y cicloalquilcarbonilamino C3-6alquilo C1-6 están opcionalmente sustituidos con 1 sustituyente, seleccionado entre R10; donde
R10 es cicloalquil C3-8alquilo C0-2, fenilalquilo C0-2, heteroarilalquilo C0-2 donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y 5, heterociclilalquilo C0-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R11; donde
R11 es hidrógeno, ciano, flúor, cloro, bromo, metilo, trifluorometilo, metoxi y etoxi; o
una de sus sales o N-óxidos.
Para los compuestos de Fórmula (IA), cuando R8 como un cicloalquil C3-8alquilo C0-6, fenilalquilo C0-6, fenilalquenilo C2-6, naftilalquilo C0-6, heteroarilalquilo C0-6, heterodiarilalquilo C0-6, heterociclilalquilo C0-6 o cicloalquilcarbonilamino C3-6alquilo C1-6 se indican como opcionalmente sustituidos con R9 o R10, los fragmentos cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo, heterociclilo solo pueden sustituirse.
En los compuestos de Fórmula (IA), preferentemente, R1 y R2 se seleccionan independientemente entre hidrógeno y flúor. Más preferentemente, R1 y R2 son hidrógeno.
En los compuestos de Fórmula (IA), preferentemente, R3 y R4 se seleccionan independientemente entre hidrógeno y flúor. Más preferentemente, R3 y R4 son hidrógeno.
En los compuestos de Fórmula (IA), preferentemente tres de los grupos R1, R2, R3 y R4 son hidrógeno, donde más preferentemente R2 , R3 y R4 son hidrógeno.
En los compuestos de Fórmula (IA), preferentemente, R5 y R6 son hidrógeno o R5 es hidrógeno y R6 es alquilo C1-4, preferentemente metilo o etilo. De la manera más preferida, R5 y R6 son hidrógeno.
En los compuestos de la Fórmula (IA), preferentemente R7 es metilo, etilo, propilo, isopropilo, butilo, sec-butilo, metoxi, etoxi, propoxi, isopropoxi, butoxi o sec-butoxi. Más preferentemente, R7 es metilo, etilo, sec-butilo, metoxi, etoxi o propoxi. Más preferentemente, R7 es sec-butilo, metoxi o propoxi.
En los compuestos de Fórmula (IA), preferentemente R8 es hidrógeno, alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C2-6, hidroxialquilo C1-6, alcoxi C1 -4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, alquiniloxi C2-4alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alquilcarboniloxi C 1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6, alquiniloxicarbonilamino C2-6alquilo C1-6 ; o cicloalquil C3-8alquilo C0-2 , donde el resto cicloalquilo está opcionalmente insaturado parcialmente, fenilalquilo C0-2, heteroarilalquilo C0-2 donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, o heterociclilalquilo C0-2 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S; donde cualquiera de dichos restos cicloalquil C3-8alquilo C0-2, fenilalquilo C0-2, heteroarilalquilo C0-2 y heterociclilalquilo C0-2 están opcionalmente sustituidos con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; y R9 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, alcoxi C1-4, haloalquenilo C2-4, alquiniloxi C3-4, alquilcarbonilo C1-4 y alcoxicarbonilo C1-4.
Más preferentemente, R8 es alquilo C1-6, alquenilo C2-6, alquinilo C2-6, fluoroalquilo C1-6, cloroalquilo C1-6, alcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alquilcarboniloxi C1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6 o alquiniloxicarbonilamino C2-6alquilo C1-6 ; cicloalquil C3-8alquilo C0-6, fenilalquilo C0-6, o heterociclilalquilo C0-6, donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1, 2 o 3 sustituyentes que pueden ser los mismos o diferentes, seleccionados entre R9 , donde R9 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, haloalquenilo C2-4, alquiniloxi C3-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4; o donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1 sustituyente seleccionado entre R10 que es un fenilo.
Incluso más preferentemente, R8 es alquilo C1-6, alquenilo C2-4, alquinilo C2-4, fluoroalquilo C1-6, cloroalquilo C1-4, alcoxi C1-4alquilo C1-4, alcoxi C1-4alcoxi C1-2alquilo C1-4, alquilcarbonil C1-4alquenilo C2-4, alquilcarboniloxi C1-2alquilo C1-4, alquilsulfonilamino C1-4alquinilo C2-4 o alquiniloxicarbonilamino C2-4alquilo C1-4 ; cicloalquil C3-6alquilo C0-1, fenilalquilo C0 -1, o heterociclilalquilo C0-1, donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1, 2 o 3 sustituyentes que pueden ser los mismos o diferentes, seleccionados entre R9 , donde R9 es ciano, flúor, cloro, hidroxi, metilo, etilo, trifluorometilo, 2,2-dicloroetenilo, propiniloxi, acetilo, metoxicarbonilo; o donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1 sustituyente seleccionado entre R10 que es un fenilo.
En algunas realizaciones de la invención de acuerdo con la Fórmula (IA) donde R8 es un grupo seleccionado entre cicloalquil C3-8alquilo C0-6, fenilalquilo C0-6, fenilalquenilo C2-6, naftilalquilo C0-6, heteroarilalquilo C0-6, heterodiarilalquilo C0-6, heterociclilalquilo C0-6, preferentemente R8 es cicloalquil C3-8alquilo C0-2, fenilalquilo C0-2, fenilalquenilo C2-4, naftilalquilo C0-2, heteroarilalquilo C0-2, heterodiarilalquilo C0-2 o heterociclilalquilo C0-2.
En algunas realizaciones de la invención de acuerdo con la Fórmula (IA) donde R8 es un grupo seleccionado entre cicloalquil C3-8alquilo C0-6, preferentemente cicloalquilo C3-8 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo.
En algunas realizaciones de la invención de acuerdo con la Fórmula (IA) donde R8 es un grupo seleccionado entre fenilalquilo C0-6, preferentemente, R8 es fenilo o bencilo.
En algunas realizaciones de la invención de acuerdo con la Fórmula (IA) donde R8 es un grupo seleccionado entre heterociclilalquilo C0-6, preferentemente el grupo heterociclilo tiene 1 o 2 heteroátomos seleccionados entre N, O y S. Más preferentemente, el grupo heterociclilo tiene un heteroátomo solo seleccionado entre O y S. Lo más preferentemente para R8 como un heterociclilalquilo C0-6 son oxetanilo, tetrahidrofuranilo, tetrahidropiranilo, tietanilo o tetrahidrotiopiranilo.
En los compuestos de Fórmula (IA), preferentemente, R1 y R2 se seleccionan independientemente entre hidrógeno y flúor;
R3 y R4 se seleccionan independientemente entre hidrógeno y flúor;
donde al menos dos de R1, R2, R3 y R4 son hidrógeno,
R5 y R6 son hidrógeno, o R5 es hidrógeno y R6 es metilo;
R7 es alquilo C1-4 o alcoxi C1-4; y
R8 es alquilo C1-6, alquenilo C2-6, alquinilo C2-6, fluoroalquilo C1-6, cloroalquilo C1-6, alcoxi C1-4alquilo C1-6, alcoxi C 1-4alcoxi C1-4alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alquilcarboniloxi C1-6alquilo C1-6, alquilsulfonilamino C 1-6alquinilo C2-6 o alquiniloxicarbonilamino C2-6alquilo C1-6; cicloalquil C3-8alquilo C0-6, fenilalquilo C0-6, o heterociclilalquilo C0-6, donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes que pueden ser los mismos o diferentes, seleccionados entre R9 , donde R9 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, haloalquenilo C2-4, alquiniloxi C3-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4; o donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1 sustituyente seleccionado entre R10 que es un fenilo.
En los compuestos de Fórmula (IA), más preferentemente, R1 y R2 se seleccionan independientemente entre hidrógeno y flúor;
R3 y R4 se seleccionan independientemente entre hidrógeno y flúor;
donde al menos dos de R1, R2, R3 y R4 son hidrógeno
R5 y R6 son hidrógeno, o R5 es hidrógeno y R6 es metilo;
R7 es metoxi, propoxi o sec-butilo; y
R8 es alquilo C1-6, alquenilo C2-4, alquinilo C2-4, fluoroalquilo C1-6, cloroalquilo C1-4, alcoxi C1-4alquilo C1-4, alcoxi C 1-4alcoxi C1-2alquilo C1-4, alquilcarbonil C1-4alquenilo C2-4, alquilcarboniloxi C1-2alquilo C1-4, alquilsulfonilamino C 1-4alquinilo C2-4 o alquiniloxicarbonilamino C2-4alquilo C1-4; cicloalquil C3-6alquilo C0-1, fenilalquilo C0-1, o heterociclilalquilo C0 -1, donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes que pueden ser los mismos o diferentes, seleccionados entre R9 , donde R9 es ciano, flúor, cloro, hidroxi, metilo, etilo, trifluorometilo, 2,2-dicloroetenilo, propiniloxi, acetilo, metoxicarbonilo; o donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1 sustituyente seleccionado entre R10 que es un fenilo.
En los compuestos de Fórmula (IA), aún más preferentemente, R1 y R2 son hidrógeno;
R3 y R4 son hidrógeno;
R5 y R6 son hidrógeno;
R7 es metoxi, propoxi o sec-butilo; y
R8 es alquilo C1-6, alquenilo C2-4, alquinilo C2-4, fluoroalquilo C1-6, cloroalquilo C1-4, alcoxi C1-4alquilo C1-4, alcoxi C 1-4alcoxi C1-2alquilo C1-4, alquilcarbonil C1-4alquenilo C2-4, alquilcarboniloxi C1-2alquilo C1-4, alquilsulfonilamino C 1-4alquinilo C2-4 o alquiniloxicarbonilamino C2-4alquilo C1-4; cicloalquil C3-6alquilo C0-1, fenilalquilo C0-1, o heterociclilalquilo C0 -1, donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes que pueden ser los mismos o diferentes, seleccionados entre R9 , donde R9 es ciano, flúor, cloro, hidroxi, metilo, etilo, trifluorometilo, 2,2-dicloroetenilo, propiniloxi, acetilo, metoxicarbonilo; o donde cualquiera de dichos restos cicloalquilo, fenilo y heterociclilo están opcionalmente sustituidos con 1 sustituyente seleccionado entre R10 que es un fenilo.
Los compuestos de la presente invención pueden ser enantiómeros del compuesto de Fórmula (I) según los representan la Fórmula (Ia) o la Fórmula (Ib) cuando n es 1, donde R5 y R6 son diferentes (véase más adelante) o, ciertamente, cuando n es 2 y únicamente una de las dos posiciones de los carbonos unidos a R5 y R6 , R5 y R6 son diferentes.
(Ib)
Asimismo, los compuestos de la presente invención pueden ser diastereómeros del compuesto de Fórmula (I) cuando n es 2 y donde en cada una de las dos posiciones de los carbonos unidos a R5 y R6 , R5 y R6 son diferentes.
Se sobreentiende que cuando están en un medio acuoso, los compuestos de fórmula (I) de acuerdo con la invención pueden estar presentes en un equilibrio reversible con las correspondientes formas hidratadas covalentemente (es decir, los compuestos de fórmula (I-I) y fórmula (I-II) tal como se muestran a continuación) en el motivo CF3-oxadiazol.
Este equilibrio dinámico puede ser importante para la actividad biológica de los compuestos de Fórmula (I). Las designaciones de n, A1, A2 , A3 , A4 , R1, R2 , R3 , R4 , R5 , R6 , R7 , R8 , R9 , R10, R11, R12, R13, R14, R15, a los compuestos de fórmula (I) de la presente invención se aplican, generalmente, a los compuestos de Fórmula (I-I) y Fórmula (I-II), así como también a las divulgaciones específicas de las combinaciones de n, A1, A2 , A3 , A4 , R1, R2 ,
R3 , R4 , R5 , R6 , R7 , R8 , R9 , R10, R11, R12, R13, R14, R15, R16, y R17 como se representa en las Tablas Tables 1.1 a 1.29,
2.1 a 2.5, 3.1 a 3.14 y 4.1 a 4.4 a continuación o los compuestos 1.1 a 1.811 descritos en la Tabla T1 (a continuación), los compuestos 2.1 a 2.26 descritos en la Tabla T2 (a continuación) y los compuestos 3.1 a 3.140 descritos en la Tabla
T3 (a continuación).
Los compuestos de la presente invención se pueden preparar como se muestra en los siguientes esquemas 1 a 14, en los que, a menos que se indique lo contrario, la definición de cada variable es como se ha definido anteriormente para un compuesto de fórmula (I).
Los compuestos de fórmula (I) pueden obtenerse mediante una transformación de acoplamiento de amida con compuestos de fórmula (II) y compuestos de fórmula (III), activando la función ácido carboxílico de los compuestos de fórmula (III), un proceso que normalmente tiene lugar convirtiendo el -OH del ácido carboxílico en un buen grupo saliente, tal como un grupo cloruro, por ejemplo, usando (COCl)2 o SOCl2 , antes del tratamiento con los compuestos de fórmula (II), preferentemente en un disolvente adecuado (por ejemplo, dimetilformamida, diclorometano o tetrahidrofurano), preferentemente a una temperatura entre 25 °C y 100 °C y, opcionalmente, en presencia de una base tal como trietilamina o W,W-diisopropiletilamina o en condiciones descritas en la bibliografía para un acoplamiento de amida. Para consultar ejemplos, remítase al documento WO 2003/028729. Los compuestos de fórmula (III) están comercializados o se preparan utilizando métodos conocidos. Para consultar ejemplos relacionados, remítase a: Nelson, T. D et al Tetrahedron Lett. (2004), 45, 8917; Senthil, K. et al Pest. Res. Journal (2009), 21, 133; y Crich, D., Zou, Y. J. Org. Chem. (2005), 70, 3309. Esta reacción se muestra en el Esquema 1.
(III) (II) (I)
Esquema 1
Como alternativa, los compuestos de fórmula (I) pueden prepararse a partir de compuestos de fórmula (II) mediante el tratamiento con trifosgeno en un disolvente adecuado (por ejemplo, acetato de etilo, CHCl3 o tolueno) calentando entre 65 °C y 100 °C, seguido de la adición de nucleófilos adecuados de fórmula (IV), donde R8-Nu es un reactivo organometálico(por ejemplo, organomagnesio, organocinc u organolitio) en un disolvente adecuado (por ejemplo, tolueno, éter dietílico o tetrahidrofurano) a una temperatura entre -78 °C y 25 °C. Para ejemplos relacionados, véase Charalambides, Y. C., Moratti, S. C. Synth. Commun. (2007), 37, 1037; Schaefer, G. et al Angew. Chem., Int. Ed. (2012) 51, 9173; Lengyel, I. et al Heterocicles (2007), 73, 349; y Benalil, A et al Synthesis (1991), 9, 787. Además, los
compuestos de fórmula (I) pueden prepararse a partir de compuestos de fórmula (II) mediante el tratamiento con trifosgeno en un disolvente adecuado (por ejemplo, 1,2-dicloroetano, CHCI3 o tolueno), seguido de la adición de nucleófilos adecuados de fórmula (IV), donde R8-Nu representa HOR10 o HN(R11)R12 en presencia de una base adecuada tal como trietilamina. Esta reacción se muestra en el Esquema 2
Esquema 2
Adicionalmente, los compuestos de fórmula (I) pueden prepararse a partir de compuestos de fórmula (V) mediante el tratamiento con anhídrido trifluoroacético en presencia de una base (por ejemplo, piridina o 4-dimetilaminopiridina) en un disolvente adecuado, tal como tetrahidrofurano o etanol, a una temperatura entre 25 °C y 75 °C. Para ejemplos relacionados, véase los documentos WO 2003/028729 y WO 2010/045251. Esta reacción se muestra en el Esquema 3.
Esquema 3
Los compuestos de fórmula (V) pueden prepararse a partir de compuestos de fórmula (VI) mediante el tratamiento con la sal clorhídrica de hidroxilamina en presencia de una base tal como trietilamina, en un disolvente adecuado, tal como metanol, a una temperatura entre 0 °C y 100 °C. Para ejemplos relacionados, véase Kitamura, S. et al Chem. Pharm. Bull. (2001), 49, 268 y el documento WO 2013/066838. Esta reacción se muestra en el Esquema 4.
Esquema 4
Los compuestos de fórmula (VI) pueden prepararse a partir de compuestos de fórmula (VII), donde Z es Br o I, mediante una reacción con un metal como promotor con un reactivo de tipo cianuro adecuado, tal como Pd(0)/Zn(CN)2 o CuCN, en un disolvente adecuado (por ejemplo, dimetilformamida o N-metilpirrolidona) a una temperatura elevada entre 100 °C y 120 °C. Para ejemplos relacionados, véase los documentos Us 2007/0155739 y WO 2009/022746. Esta reacción se muestra en el Esquema 5.
Esquema 5
Los compuestos de fórmula (VII), donde el enlace N-R7 contiene un segmento -CH2 directamente vinculado, pueden prepararse a partir de compuestos de fórmula (VIII), donde Z es Br o I, mediante una reacción con una base como promotora (por ejemplo, hidruro de sodio) con un reactivo de alquilación adecuado (por ejemplo, yoduro de metilo o yoduro de propilo), en un disolvente adecuado (por ejemplo, dimetilformamida o N-metilpirrolidona) a temperatura elevada entre 100 °C y 120 °C. Esta reacción se muestra en el Esquema 6.
Esquema 6
Los compuestos de fórmula (II), donde n es preferentemente 0 y R6 es hidrógeno, pueden prepararse a partir de compuestos carbonilo de fórmula (IX), comenzando con el tratamiento de los compuestos de fórmula (X), donde RPG es terc-butilsulfinamida, opcionalmente en presencia de un reactivo activante (por ejemplo, Ti(OEt)4), en un disolvente adecuado (por ejemplo, tetrahidrofurano) a una temperatura entre 60 °C y 75 °C y seguido de la adición de un reactivo de fórmula (XI), tal como reactivo alquílico de Grignard (por ejemplo, alquilMgBr), MeaSiCN o un hidruro metálico (por ejemplo, NaBH4, NaBHaCN o LiAlH4), en un disolvente adecuado (por ejemplo, tetrahidrofurano o etanol) a temperaturas entre 0 °C y 25 °C. La retirada del grupo terc-butanosulfinilo con la consiguiente liberación de compuestos de amina de fórmula (II) tiene lugar tras el tratamiento con HCl metanólico. Para consultar ejemplos relacionados, remítase a Cogan, D., Ellman J. A. J. Am. Chem. Soc. (1999), 121, 268. Esta reacción se muestra en el Esquema 7.
Esquema 7
De manera alternativa, los compuestos de fórmula (II), donde n es preferentemente 1, pueden prepararse a partir de compuestos de fórmula (XIII), donde X es Cl o Br, mediante el tratamiento con aminas de fórmula (XII), donde Y es terc-butilcarboxilato, en un disolvente adecuado (por ejemplo, tetrahidrofurano) a una temperatura entre 25 °C y 60 °C. La retirada de los grupos terc-butilcarboxilato con la consiguiente liberación de bencilaminas de fórmula (II) tiene lugar tras el tratamiento con HCl o ácido trifluoroacético en un disolvente adecuado (por ejemplo, dioxano o MeOH). Para ejemplos relacionados, véase Miyawaki, K. et al Heterocicles (2001), 54, 887, el documento WO 2003/028729 y el documento WO 2013/066839. Esta reacción se muestra en el Esquema 8.
Esquema 8
Los compuestos de fórmula (XIII), donde n es 1, pueden prepararse a partir de los compuestos de fórmula (XIV), donde X es Cl o Br, mediante el tratamiento con una fuente de halógeno (por ejemplo, N-bromosuccinimida (NBS) o N-clorosuccinimida (NCS)) y un iniciador radicalario (por ejemplo, (PhCO2)2 o azobisisobutironitrilo (AIBN)) en un disolvente adecuado, tal como tetraclorometano, a temperaturas entre 55 °C y 100 °C en presencia de luz ultravioleta. Para ejemplos relacionados, véase Liu, S. et al Synthesis (2001), 14, 2078 y Kompella, A. et al Org. Proc. Res. Dev. (2012), 16, 1794. Esta reacción se muestra en el Esquema 9.
Esquema 9
Los compuestos de fórmula (VII) pueden obtenerse mediante una transformación de acoplamiento de amida con compuestos de fórmula (XV) y compuestos de fórmula (III), activando la función ácido carboxílico de los compuestos de fórmula (III), un proceso que normalmente tiene lugar convirtiendo el -OH del ácido carboxílico en un buen grupo saliente, tal como un grupo cloruro, por ejemplo, usando (COCl)2 o SOCl2 , antes del tratamiento con los compuestos de fórmula (XV), preferentemente en un disolvente adecuado (por ejemplo, dimetilformamida, diclorometano o tetrahidrofurano), preferentemente a una temperatura entre 25 °C y 100 °C y, opcionalmente, en presencia de una base tal como trietilamina o W,W-diisopropiletilamina o en condiciones descritas en la bibliografía para un acoplamiento de amida. Para consultar ejemplos, remítase al documento WO 2003/028729. Los compuestos de fórmula (III) están comercializados o se preparan utilizando métodos conocidos. Para consultar ejemplos relacionados, remítase a: Nelson, T. D et al Tetrahedron Lett. (2004), 45, 8917; Senthil, K. et al Pest. Res. Journal (2009), 21, 133; y Crich, D., Zou, Y. J. Org. Chem. (2005), 70, 3309. Esta reacción se muestra en el Esquema 10.
Esquema 10
Además, los compuestos de fórmula (VII), donde Z es Br, I, o CN y R8 también pueden ser OR10 *2 *o NR14R15 *20donde R15 no es hidrógeno y n es preferentemente 1, pueden prepararse a partir de compuestos de fórmula (XVIII), donde X es Cl, Br o I, mediante tratamiento con amidas de fórmula (XVII), donde Y es terc-butilcarboxilato, en presencia de una base adecuada, tal como NaH, en un disolvente adecuado, tal como dimetilformamida, a una temperatura entre 0 °C y 100 °C. En algunos casos, puede conseguirse un mayor rendimiento de la reacción a partir del uso de un catalizador (por ejemplo, NaI o 4-dimetilaminopiridina) y con irradiación de microondas. La retirada de los grupos terc
butilcarboxilato con la consiguiente liberación de bencilamidas de fórmula (VIII) tiene lugar tras el tratamiento con HCl o ácido trifluoroacético en un disolvente adecuado (por ejemplo, dioxano, diclorometano o MeOH). Para ejemplos relacionados, véase Miyawaki, K. et al Heterocicles (2001), 54, 887. Esta reacción se muestra en el Esquema 11.
Esquema 11
Los compuestos de fórmula (XVIII), donde Z es Br, I o CN y X es Cl o Br y en n es preferentemente 1, están disponibles en el mercado o pueden prepararse a partir de compuestos de fórmula (XIX), mediante el tratamiento con una fuente de halógeno (por ejemplo, N-bromosuccinimida (NBS) o N-clorosuccinimida (NCS)) y un iniciador radicalario, tal como (PhCO2)2 o azobisisobutironitrilo (AIBN), en presencia de luz ultravioleta, en un disolvente adecuado, tal como tetraclorometano, a temperaturas entre 55 °C y 100 °C. Para ejemplos relacionados, véase Liu, S. et al Synthesis (2001), 14, 2078 y Kompella, A. et al Org. Proc. Res. Dev. (2012), 16, 1794. Esta reacción se muestra en el Esquema 12.
Esquema 12
Como alternativa, los compuestos de fórmula (XVIII), donde X es Cl, Br, I u OSO2Me y Z es Br, I y n es preferentemente 1, están disponibles en el mercado o pueden prepararse a partir de compuestos de fórmula (XX) mediante el tratamiento con una fuente de halógeno (por ejemplo, CBr4, CCU o I2) en presencia de trifenilfosfina o con cloruro de metanosulfonilo (ClSO2Me), en un disolvente adecuado (por ejemplo, diclorometano) a una temperatura entre 0 °C y 100 °C. Para ejemplos relacionados, véase Liu, H. et al Bioorg. Med. Chem. (2008), 16, 10013, el documento w O 2014/020350 y Kompella, A. et al Bioorg. Med. Chem. Lett. (2001), 1, 3161. Los compuestos de fórmula (XIX) están disponibles en el mercado. Esta reacción se muestra en el Esquema 13.
(XVIII)
(XX)
Esquema 13
Los compuestos de fórmula (XV), donde n es preferentemete 0 o 1 y R6 es preferentemente hidrógeno, pueden prepararse a partir de compuestos carbonilo de fórmula (XXI), comenzando con el tratamiento de los compuestos de fórmula (X), donde RPG es una terc-butilsulfinamida o hidrógeno, opcionalmente en presencia de un reactivo activante (por ejemplo, Ti(OEt)4), en un disolvente adecuado (por ejemplo, tetrahidrofurano) a una temperatura entre 60 °C y 75 °C y seguido de la adición de un compuesto organometálico de fórmula (XI), tal como reactivo alquílico de Grignard
(por ejemplo, alquilMgBr), Me3SiCN o un hidruro metálico de fórmula (XI), donde el metal es B o Al (por ejemplo, NaBH4, NaBH3CN o LiAlhU), en un disolvente adecuado (por ejemplo, tetrahidrofurano o etanol) a temperaturas entre 0 °C y 25 °C. La retirada del grupo terc-butanosulfinilo con la consiguiente liberación de compuestos de bencilaminas de fórmula (XV) tiene lugar tras el tratamiento con HCl metanólico. Para consultar ejemplos relacionados, remítase a Cogan, D., Ellman J. A. J. Am. Chem. Soc. (1999), 121, 268. Esta reacción se muestra en el Esquema 14.
Esquema 14
Como ya se ha indicado, sorprendentemente, se acaba de descubrir que compuestos novedosos de fórmula (I) de acuerdo con la invención tienen, a efectos prácticos, un nivel muy ventajoso de actividad biológica para proteger plantas contra enfermedades que están provocadas por hongos.
Los compuestos de fórmula (I) pueden usarse en el sector agrícola y campos de uso relacionados, por ejemplo, como principios activos para controlar plagas en plantas, o en materiales inertes para controlar microorganismos responsables de su descomposición u organismos potencialmente dañinos para el ser humano. Los compuestos novedosos se diferencian por su excelente actividad en tasas de aplicación bajas, al ser bien tolerados por plantas y al ser ecológicos. Tienen unas propiedades curativas, preventivas y sistémicas muy útiles, y pueden usarse para proteger numerosas plantas de cultivo. Los compuestos de fórmula (I) pueden usarse para inhibir o exterminar las plagas que aparecen en plantas o partes de plantas (frutos, flores, hojas, tallos, tubérculos, raíces) de diferentes cultivos de plantas útiles, a la vez que también protegen las partes de las plantas que crecen más tarde, por ejemplo, de los microorganismos fitopatógenos.
La presente invención se refiere además a un método para controlar o prevenir la infestación de plantas o material de propagación vegetal y/o cultivos alimentarios recolectados susceptibles de ser atacados por microbios mediante el tratamiento de las plantas o material de propagación vegetal y/o cultivos alimentarios recolectados donde se aplica una cantidad eficaz de un compuesto de fórmula (I) a las plantas, a partes de los mismos o al emplazamiento del mismo.
También es posible usar compuestos de fórmula (I) como fungicidas. El término "fungicida", como se usa en el presente documento, se refiere a un compuesto que controla, modifica o previene el crecimiento de hongos. La expresión "cantidad eficaz como fungicida" se refiere a la cantidad de un compuesto de este tipo o combinación de compuestos de este tipo que es capaz de producir un efecto sobre el crecimiento de los hongos. Los efectos de control o modificación incluyen toda desviación del desarrollo natural, tal como su exterminación, ralentización y similares, y la prevención incluye una barrera u otra formación defensiva en o sobre una planta para prevenir la infección fúngica.
También puede ser posible usar los compuestos de fórmula (I) como agentes de revestimiento para tratar el material de propagación vegetal, por ejemplo, semillas tales como frutos, tubérculos o granos, o esquejes vegetales, para protegerlo contra infecciones fúngicas, así como también contra hongos fitopatógenos presentes en el suelo. El material de propagación se puede tratar con una composición que comprende un compuesto de fórmula (I) antes de plantarlo, por ejemplo, las semillas se pueden revestir antes de ser sembradas. Los compuestos activos de fórmula (I) también pueden aplicarse a granos (recubrimiento), ya sea impregnando las semillas en una formulación líquida o recubriéndolas con una formulación sólida. La composición también se puede aplicar al sitio de siembra cuando el material de propagación está siendo plantado, por ejemplo, al surco de la semilla durante la siembra. La invención se refiere también a tales métodos de tratamiento del material de propagación vegetal y al material de propagación vegetal tratado de tal modo.
Además, los compuestos de fórmula (I) se pueden emplear para controlar hongos en áreas relacionadas, por ejemplo, en la protección de materiales técnicos, que incluyen la madera y productos técnicos relacionados con la madera, en el almacenamiento de alimentos y en la gestión sanitaria.
Además, la invención se podría utilizar para proteger materiales inertes contra ataques fúngicos, por ejemplo, madera, paneles para tabicar y pintura.
Los compuestos de fórmula I son eficaces, por ejemplo, contra hongos y vectores fúngicos de enfermedades, así como también bacterias y virus fitopatógenos. Estos hongos y vectores fúngicos de enfermedades, así como también las bacterias y virus fitopatógenos, son, por ejemplo:
Absidia corymbifera, Alternaria spp, Aphanomyces spp, Ascochyta spp, Aspergillus spp. que incluye A. flavus, A. fumigatus, A. nidulans, A. niger, A. terrus, Aureobasidium spp. que incluye A. pullulans, Blastomyces dermatitidis, Blumeria graminis, Bremia lactucae, Botryosphaeria spp. que incluye B. dothidea, B. obtusa, Botrytis spp. inclusing B. cinerea, Candida spp. que incluye C. albicans, C. glabrata, C. krusei, C. lusitaniae, C. parapsilosis, C. tropicalis, Cephaloascus fragrans, Ceratocystis spp, Cercospora spp. que incluye C. arachidicola, Cercosporidium personatum, Cladosporium spp, Claviceps purpurea, Coccidioides immitis, Cochliobolus spp, Colletotrichum spp. que incluye C. musae, Cryptococcus neoformans, Diaporthe spp, Didymella spp, Drechslera spp, Elsinoe spp,Epidermophyton spp, Erwinia amylovora, Erysiphe spp. que incluye E. cichoracearum, Eutypa lata, Fusarium spp. que incluye F. culmorum, F. graminearum, F. langsetiae, F. moniliforme, F. oxisporum, F. proliferatum, F. subglutinans, F. solani, Gaeumannomyces graminis, Gibberella fujikuroi, Gloeodes pomigena, Gloeosporium musarum, Glomerella cingulato, Guignardia bidwellii, Gymnosporangium juniperi-virginianae, Helminthosporium spp, Hemileia spp, Histoplasma spp. que incluye H. capsulatum, Laetisaria fuciformis, Leptographium lindbergi, Leveillula taurica, Lophodermium seditiosum, Microdochium nivale, Microsporum spp, Monilinia spp, Mucor spp, Mycosphaerella spp. que incluye M. graminicola, M. pomi, Oncobasidium theobromaeon, Ophiostoma piceae, Paracoccidioides spp, Penicillium spp. que incluye P. digitatum, P. italicum, Petriellidium spp, Peronosclerospora spp. Including P. maydis, P. philippinensis y P. sorghi, Peronospora spp, Phaeosphaeria nodorum, Phakopsora pachyrhizi, Phellinus igniarus, Phialophora spp, Phoma spp, Phomopsis viticola, Phytophthora spp. que incluye P. infestans, Plasmopara spp. que incluye P. halstedii, P. viticola, Pleospora spp., Podosphaera spp. que incluye P. leucotricha, Polymyxa graminis, Polymyxa betae, Pseudocercosporella herpotrichoides, Pseudomonas spp, Pseudoperonospora spp. que incluye P. cubensis, P. humuli, Pseudopeziza tracheiphila, Puccinia Spp. que incluye P. hordei, P. recondita, P. striiformis, P. triticina, Pyrenopeziza spp, Pyrenophora spp, Pyricularia spp. que incluye P. oryzae, Pythium spp. que incluye P. ultimum, Ramularia spp, Rhizoctonia spp, Rhizomucor pusillus, Rhizopus arrhizus, Rhynchosporium spp, Scedosporium spp. que incluye S. apiospermum y S. prolificans, Schizothyrium pomi, Sclerotinia spp, Sclerotium spp, Septoria spp, que incluye S. nodorum, S. tritici, Sphaerotheca macularis, Sphaerotheca fusca (Sphaerotheca fuliginea), Sporothorix spp, Stagonospora nodorum, Stemphylium spp,. Stereum hirsutum, Thanatephorus cucumeris, Thielaviopsis basicola, Tilletia spp, Trichoderma spp. que incluye T. harzianum, T. pseudokoningii, T. viride, Trichophyton spp, Typhula spp, Uncinula necator, Urocystis spp, Ustilago spp, Venturia spp. que incluye V. inaequalis, Verticillium spp y Xanthomonas spp.
Los compuestos de fórmula (I) pueden usarse, por ejemplo, en el césped, en plantas ornamentales, tales como flores, arbustos, árboles latifolios o perennifolios, por ejemplo, coníferas, así como también para la inyección de árboles, gestión de plagas y similares.
Dentro del alcance de la presente invención, los cultivos diana y/o plantas útiles que se han de proteger comprenden normalmente cultivos perennes y anuales tales como plantas de bayas, por ejemplo, moras, arándanos azules, zarzamoras, arándanos rojos y frutillas; cereales, por ejemplo, cebada, maíz, mijo, avena, arroz, centeno, sorgo, triticale y trigo; plantas que producen fibra, por ejemplo, algodón, lino, cáñamo, yute y sisal; cultivos de campo, por ejemplo, azúcar y remolacha forrajera, café, lúpulos, mostaza, colza oleaginosa (canola), amapola, caña de azúcar, girasol, té y tabaco; árboles frutales, por ejemplo, los que producen manzana, damasco, palta, plátano, cereza, cítricos, nectarina, durazno, pera y ciruela; pastos, por ejemplo, grama común, pasto azul, agróstide, Eremocloa ophiuroides, festuca, Lolium, pasto de San Agustín y pasto Zoysia; hierbas tales como albahaca, borraja, cebolletas, cilantro, lavanda, apio de monte, menta, orégano, perejil, romero, salvia y tomillo; legumbres, por ejemplo, porotos, lentejas, arvejas y soja; frutos secos, por ejemplo, almendra, anacardo, cacahuete, avellana, maní, pacana, pistacho y nuez; palmeras, por ejemplo, palmera oleaginosa; plantas ornamentales, por ejemplo, flores, arbustos y árboles; otros árboles, por ejemplo, de cacao, coco, oliva y caucho; hortalizas, por ejemplo, espárragos, berenjena, brócoli, col, zanahoria, pepino, ajo, lechuga, tuétano, melón, quingombó, cebolla, pimiento, papa, calabaza, ruibarbo, espinaca y tomate; y vides, por ejemplo, uvas.
Se debe entender que la expresión "plantas útiles" también incluye las plantas útiles que se han modificado para que sean tolerantes a herbicidas, tales como bromoxinilo, o a clases de herbicidas (tales como, por ejemplo, inhibidores de HPPD, inhibidores de ALS, por ejemplo, primisulfurón, prosulfurón y trifloxisulfurón, inhibidores de EPSPS (5-enolpirovil-shikimato-3-fosfato-sintasa), inhibidores de GS (glutamina-sintetasa) o inhibidores de PPO (protoporfirinógeno-oxidasa)) como resultado de métodos convencionales de cultivo selectivo o de ingeniería genética. Un ejemplo de un cultivo que ha sido modificado para que sea tolerante a imidazolinonas, por ejemplo, imazamox, mediante métodos convencionales de cultivo selectivo (mutagénesis) es la colza de verano Clearfield® (canola). Los ejemplos de cultivos que se han modificado para que sean tolerantes a herbicidas o clases de herbicidas mediante métodos de ingeniería genética incluyen las variedades de maíz resistentes a glifosato y glufosinato comercializadas con los nombres comerciales RoundupReady®, Herculex I® y LibertyLink®.
Se debe entender que la expresión "plantas útiles" también incluye plantas útiles que han sido transformadas utilizando técnicas de ADN recombinante, las cuales son capaces de sintetizar una o más toxinas que actúan selectivamente
tales como, por ejemplo, las conocidas que proceden de bacterias que producen toxinas, especialmente las del género Bacillus.
Algunos ejemplos de estas plantas son: YieldGard® (variedad del maíz que expresa una toxina CryIA(b)); YieldGard Rootworm® (variedad del maíz que expresa una toxina CryMIB(b1)); YieldGard Plus® (variedad del maíz que expresa una toxina CryIA(b) y una toxina CryIIIB(b1)); Starlink® (variedad del maíz que expresa una toxina Cry9(c)); Herculex I® (variedad del maíz que expresa una toxina CryIF(a2) y la enzima fosfinotricina-N-acetiltransferasa (PAT) para conseguir tolerancia al herbicida glufosinato de amonio); NuCOTN 33B® (variedad del algodón que expresa una toxina CryIA(c)); Bollgard I® (variedad del algodón que expresa una toxina CryIA(c)); Bollgard II® (variedad del algodón que expresa una toxina CryIA(c) y una toxina CryIIA(b)); VIPCOT® (variedad del algodón que expresa una toxina VIP); NewLeaf® (variedad de la papa que expresa una toxina CryIIIA); NatureGard® Agrisure® GT Advantage (rasgo de tolerancia a glifosato GA21), Agrisure® CB Advantage (rasgo de barrenador del maíz (CB) Bt11), Agrisure® RW (rasgo del gusano del maíz) y Protecta®.
Se debe entender que el término "cultivos" también incluye las plantas de cultivo que han sido transformadas mediante el uso de técnicas de ADN recombinante de tal forma que sean capaces de sintetizar una o más toxinas que actúan selectivamente, tales como, por ejemplo, las conocidas que proceden de bacterias que producen toxinas, especialmente las del género Bacillus.
Las toxinas que pueden expresarse por tales plantas transgénicas incluyen, por ejemplo, proteínas insecticidas de Bacillus cereus o Bacillus popilliae; o proteínas insecticidas de Bacillus thuringiensis tales como 8-endotoxinas, por ejemplo, Cry1Ab, Cry1Ac, Cry1F, Cry1Fa2, Cry2Ab, Cry3A, Cry3Bb1 o Cry9C, o proteínas insecticidas vegetativas (Vip), por ejemplo, Vip1, Vip2, Vip3 o Vip3A; o proteínas insecticidas de bacterias que colonizan nematodos, por ejemplo, Photorhabdus spp. o Xenorhabdus spp., tales como Photorhabdus luminescens, Xenorhabdus nematophilus; toxinas producidas por animales tales como toxinas de escorpiones, toxinas de arácnidos, toxinas de avispas y otras neurotoxinas específicas de insectos; toxinas producidas por hongos tales como toxinas de estreptomicetos, lectinas de plantas tales como lectinas de arvejas, lectinas de cebada o lectinas de la campanilla de invierno; aglutininas; inhibidores de proteinasas tales como inhibidores de la tripsina, inhibidores de la serín proteasa, inhibidores de la patatina, cistatina, papaína; proteínas que desactivan ribosomas (RIP, por sus siglas en inglés) tales como ricina, RIP del maíz, abrina, lufina, saporina o briodina; enzimas que participan en el metabolismo de esteroides tales como 3-hidroxiesteroidoxidasa, ecdiesteroide-UDP-glicosiltransferasa, colesterol-oxidasas, inhibidores de la ecdisona, HMG-COA-reductasa, bloqueadores de los canales iónicos tales como los bloqueadores de los canales del sodio o el calcio, esterasa de la hormona juvenil, receptores de hormonas diuréticas, estilbeno-sintasa, bibencilo-sintasa, quitinasas y glucanasas.
Además, en el contexto de la presente invención, se sobreentenderá que las 8-endotoxinas son, por ejemplo, Cry1 Ab, Cry1Ac, Cry1F, Cry1Fa2, Cry2Ab, Cry3A, Cry3Bb1 o Cry9C, o proteínas insecticidas vegetativas (Vip), por ejemplo, Vip1, Vip2, Vip3 o Vip3A, expresamente también toxinas híbridas, toxinas truncadas y toxinas modificadas. Las toxinas híbridas se producen por recombinación mediante una combinación nueva de diferentes dominios de estas proteínas (véase, por ejemplo, el documento WO 02/15701). Existe constancia de toxinas truncadas, por ejemplo, una toxina Cry1Ab truncada. En el caso de las toxinas modificadas, se reemplazan uno o más aminoácidos de la toxina de origen natural. En tales reemplazos de aminoácidos, preferentemente se insertan secuencias de reconocimiento de proteasas que no están presentes de forma natural en la toxina, como, por ejemplo, en el caso de Cry3A055, en el que se inserta una secuencia de reconocimiento de catepsina-G en una toxina Cry3A (remítase al documento WO 03/018810).
Se describen ejemplos de estas toxinas o plantas transgénicas capaces de sintetizar estas toxinas, por ejemplo, en EP-A-0 374 753, WO93/07278, WO95/34656, EP-A-0427 529, EP-A-451 878 y WO 03/052073.
Los procesos para preparar estas plantas transgénicas son generalmente conocidos por los expertos en la técnica y se describen, por ejemplo, en las publicaciones mencionadas previamente. Los ácidos desoxirribonucleicos de tipo CryI y su preparación se describen, por ejemplo, en los documentos WO 95/34656, EP-A-0367474, EP-A-0401 979 y WO 90/13651.
La toxina contenida en las plantas transgénicas les confiere a las plantas tolerancia a insectos dañinos. Estos insectos pueden pertenecer a cualquier grupo taxonómico de insectos, pero de forma habitual pertenecen especialmente al grupo de los escarabajos (coleópteros), insectos con dos alas (dípteros) y mariposas (lepidópteros).
Se conocen plantas transgénicas que contienen uno o más genes que codifican para la resistencia a un insecticida y expresan una o más toxinas, y algunas de ellas pueden adquirirse de proveedores comerciales. Algunos ejemplos de estas plantas son: YieldGard® (variedad del maíz que expresa una toxina Cry1Ab); YieldGard Rootworm® (variedad del maíz que expresa una toxina Cry3Bb1); YieldGard Plus® (variedad del maíz que expresa una toxina Cry1Ab y una toxina Cry3Bb1); Starlink® (variedad del maíz que expresa una toxina Cry9C); Herculex I® (variedad del maíz que expresa una toxina Cry1 Fa2 y la enzima fosfinotricina-N-acetiltransferasa (PAT, por sus siglas en inglés) para
obtener tolerancia al herbicida glufosinato de amonio); NuCOTN 33B® (variedad del algodón que expresa una toxina CrylAc); Bollgard I® (variedad del algodón que expresa una toxina Cry1Ac); Bollgard II® (variedad del algodón que expresa una toxina Cry1Ac y una toxina Cry2Ab); VipCot® (variedad del algodón que expresa una toxina Vip3A y una toxina Cry1Ab); NewLeaf® (variedad de la papa que expresa una toxina Cry3A); NatureGard®, Agrisure® GT Advantage (rasgo de tolerancia al glifosato GA21), Agrisure® CB Advantage (rasgo del gusano barrenador del maíz (CB, por sus siglas en inglés) Bt11) y Protecta®.
Ejemplos adicionales de tales cultivos transgénicos son:
1. Maíz Bt11 de Syngenta Seeds SAS, Chemin de l'Hobit 27, F-31 790 St. Sauveur, Francia, número de registro C/FR/96/05/10. Consiste en Zea mays que se ha modificado genéticamente para que sea resistente al ataque del gusano barrenador del maíz europeo (Ostrinia nubilalis y Sesamia nonagrioides) mediante la expresión transgénica de una toxina Cry1 Ab truncada. El maíz Bt11 también expresa transgénicamente la enzima PAT para lograr tolerancia al herbicida glufosinato de amonio.
2. Maíz Bt176 de Syngenta Seeds SAS, Chemin de l'Hobit 27, F-31 790 St. Sauveur, Francia, número de registro C/FR/96/05/10. Consiste en Zea mays que se ha modificado genéticamente para que sea resistente al ataque del gusano barrenador del maíz europeo (Ostrinia nubilalis y Sesamia nonagrioides) mediante la expresión transgénica de una toxina Cry1Ab. El maíz Bt176 también expresa transgénicamente la enzima PAT para lograr tolerancia al herbicida glufosinato de amonio.
3. Maíz MIR604 de Syngenta Seeds SAS, Chemin de l'Hobit 27, F-31 790 St. Sauveur, Francia, número de registro C/FR/96/05/10. Consiste en maíz que se ha modificado para que sea resistente a insectos mediante la expresión transgénica de una toxina Cry3A modificada. Esta toxina es Cry3A055 modificada mediante la inserción de una secuencia de reconocimiento de la proteasa catepsina G. La preparación de estas plantas de maíz transgénicas se describe en el documento WO 03/018810.
4. Maíz MON 863 de Monsanto Europe S.A. 270-272 Avenue de Tervuren, B-1150 Bruselas, Bélgica, número de registro C/DE/02/9. MON 863 expresa una toxina Cry3Bb1 y tiene resistencia a ciertos insectos coleópteros.
5. Algodón IPC 531 de Monsanto Europe S.A. 270-272 Avenue de Tervuren, B-1150 Bruselas, Bélgica, número de registro C/ES/96/02.
6. Maíz 1507 de Pioneer Overseas Corporation, Avenue Tedesco, 7 B-1160 Bruselas, Bélgica, número de registro C/NL/00/10. Consiste en maíz modificado genéticamente para que exprese la proteína Cry1F, con el fin de obtener resistencia a ciertos insectos lepidópteros, y para que exprese la proteína PAT, con el fin de lograr tolerancia al herbicida glufosinato de amonio.
7. Maíz NK603 x MON 810 de Monsanto Europe S.A. 270-272 Avenue de Tervuren, B-1150 Bruselas, Bélgica, número de registro C/GB/02/M3/03. Consiste en variedades de maíz híbridas cultivadas de forma convencional mediante el cruce de las variedades modificadas genéticamente NK603 y MON 810. El maíz NK603 x MON 810 expresa transgénicamente la proteína CP4 EPSPS, obtenida de la cepa CP4 de Agrobacterium sp., la cual confiere tolerancia al herbicida Roundup® (contiene glifosato), y también expresa una toxina Cry1Ab obtenida a partir de Bacillus thuringiensis subsp. kurstaki, la cual proporciona tolerancia a ciertos lepidópteros, incluido el gusano barrenador del maíz europeo.
El término “emplazamiento”, como se usa en el presente documento, se refiere a campos en o sobre los cuales crecen las plantas, o en los cuales se siembran semillas de plantas cultivadas o en los que se colocarán semillas en el suelo. Este término incluye el suelo, las semillas y las plántulas, así como también la vegetación establecida.
El término “plantas” se refiere a todas las partes físicas de una planta, incluidas las semillas, plántulas, briznas, raíces, tubérculos, tallos, espigas, follaje y frutos.
Se sobreentenderá que la expresión "material de propagación vegetal" se refiere a partes generativas de la planta, tales como las semillas, las cuales se pueden emplear para la multiplicación de esta última, y a material vegetativo, tal como esquejes o tubérculos, por ejemplo, patatas. Cabe mencionar, por ejemplo, semillas (en el sentido estricto), raíces, frutos, tubérculos, bulbos, rizomas y partes de plantas. También se pueden mencionar plantas germinadas y plantas jóvenes que se van a trasplantar después de que germinen o después de que emerjan del suelo. Estas plantas jóvenes pueden protegerse antes de trasplantarlas mediante un tratamiento total o parcial de inmersión. Preferentemente, se entenderá que el "material de propagación vegetal" se refiere a las semillas.
Los compuestos de fórmula I se pueden emplear en una forma no modificada o, preferentemente, junto con adyuvantes empleados convencionalmente en el campo de la formulación. Con este fin, se pueden formular convenientemente de una forma conocida para obtener concentrados emulsionables, pastas que se pueden aplicar como recubrimiento, soluciones o suspensiones diluibles o que se pueden pulverizar directamente, emulsiones diluidas, polvos humectables, polvos solubles, polvos finos, materiales granulados y también encapsulaciones, por ejemplo, en sustancias poliméricas. Al igual que para el tipo de composiciones, los métodos de aplicación, tales como
pulverización, atomización, espolvoreo, dispersión, recubrimiento o vertido, se seleccionan de acuerdo con los objetivos deseados y las circunstancias particulares. Las composiciones también pueden contener otros adyuvantes tales como estabilizantes, antiespumantes, reguladores de la viscosidad, aglutinantes o adherentes, así como fertilizantes, dadores de micronutrientes u otras formulaciones para obtener efectos especiales.
Los adyuvantes y portadores adecuados, por ejemplo, para uso agrícola, pueden ser sólidos o líquidos y son sustancias útiles en la tecnología de la formulación, por ejemplo, sustancias minerales naturales o regeneradas, disolventes, dispersantes, agentes humectantes, adherentes, espesantes, aglutinantes o fertilizantes. Estos portadores se describen, por ejemplo, en el documento WO 97/33890.
Los concentrados en suspensión son formulaciones acuosas en las que se suspenden partículas sólidas finamente divididas del compuesto activo. Estas formulaciones incluyen agentes antisedimentación y agentes dispersantes y pueden incluir, además, un agente humectante para mejorar la actividad, así como también un antiespumante y un inhibidor del crecimiento cristalino. Cuando se utilizan, estos concentrados se diluyen en agua y se aplican normalmente como un aerosol a la zona que se desee tratar. La cantidad de ingrediente activo puede variar entre un 0.5% y un 95% del concentrado.
Los polvos humectables se presentan en forma de partículas finamente divididas que se dispersan fácilmente en agua u otros portadores líquidos. Las partículas contienen el principio activo retenido en una matriz sólida. Las matrices sólidas típicas incluyen tierra de batán, arcillas de caolín, sílices y otros sólidos orgánicos o inorgánicos fácilmente humectables. Los polvos humectables normalmente contienen entre un 5% y un 95% del principio activo más una pequeña cantidad del agente humectante, dispersante o emulsionante.
Los concentrados emulsionables son composiciones líquidas homogéneas dispersables en agua u otro líquido, y pueden constar únicamente del compuesto activo con un agente emulsionante líquido o sólido, o también pueden contener un portador líquido, tal como xileno, naftas aromáticas pesadas, isoforona y otros disolventes orgánicos no volátiles. Cuando se utilizan, estos concentrados se dispersan en agua u otro líquido y se aplican normalmente como un aerosol a la zona que se desee tratar. La cantidad de ingrediente activo puede variar entre un 0.5% y un 95% del concentrado.
Las formulaciones granulares incluyen tanto extrudados como partículas relativamente gruesas y se aplican comúnmente sin dilución al área en la que se requiere el tratamiento. Los portadores típicos para formulaciones granulares incluyen arena, tierra de batán, arcilla de atapulgita, arcillas de bentonita, arcilla de montmorillonita, vermiculita, perlita, carbonato de calcio, ladrillo, piedra pómez, pirofilita, caolín, dolomita, yeso, harina de madera, mazorcas de maíz molidas, cáscara de maíz molida, azúcares, cloruro de sodio, sulfato de sodio, silicato de sodio, borato de sodio, magnesia, mica, óxido de hierro, óxido de zinc, óxido de titanio, óxido de antimonio, criolita, yeso, tierra de diatomeas, sulfato de calcio y otros materiales orgánicos o inorgánicos que absorben o que pueden recubrirse con el compuesto activo. Las formulaciones granulares normalmente contienen de un 5% a un 25% de principios activos que pueden incluir agentes tensioactivos tales como naftas aromáticas pesadas, queroseno y otras fracciones de petróleo o aceites vegetales; y/o adhesivos tales como dextrinas, pegamento o resinas sintéticas.
Los polvos finos son mezclas no aglomeradas del principio activo con sólidos finamente divididos tales como talco, arcillas, harinas y otros sólidos orgánicos e inorgánicos que actúan como agentes dispersantes y portadores.
Las microcápsulas son normalmente microgotas o gránulos del principio activo envueltos en una carcasa porosa inerte que permite la salida del material envuelto hacia su entorno en tasas controladas. Las microgotas encapsuladas tienen normalmente de 1 a 50 micrómetros de diámetro. El líquido envuelto normalmente constituye entre un 50 y un 95% del peso de la cápsula y puede incluir disolvente además del compuesto activo. Los gránulos encapsulados son generalmente gránulos porosos con membranas porosas que sellan las aberturas de los poros de los gránulos, de este modo se retienen las especies activas en forma líquida dentro de los poros de los gránulos. Los gránulos tienen normalmente un diámetro de 1 milímetro a 1 centímetro y, preferentemente, de 1 a 2 milímetros de diámetro. Los gránulos se forman por extrusión, aglomeración o perlado, o son de origen natural. Los ejemplos de tales materiales son vermiculita, arcilla sinterizada, caolín, arcilla atapulgítica, serrín y carbón granular. Los materiales de la membrana o la carcasa incluyen cauchos naturales y sintéticos, materiales celulósicos, copolímeros de estireno-butadieno, poliacrilonitrilos, poliacrilatos, poliésteres, poliamidas, poliureas, poliuretanos y xantatos de almidón.
Otras formulaciones útiles para aplicaciones agroquímicas incluyen simples soluciones del principio activo en un disolvente en el que sea completamente soluble para la concentración deseada, tal como acetona, naftalenos alquilados, xileno y otros disolventes orgánicos. Se pueden utilizar también pulverizadores presurizados, en los que el principio activo se dispersa de forma finamente dividida como resultado de la vaporización de un portador del disolvente dispersante de bajo punto de ebullición.
Los expertos en la técnica estarán familiarizados con los adyuvantes y portadores agrícolas adecuados que son útiles para formular las composiciones de la invención en los tipos de formulaciones descritos anteriormente.
Los portadores líquidos que se pueden utilizar incluyen, por ejemplo, agua, tolueno, xileno, nafta de petróleo crudo, aceite de cultivos, acetona, cetona etil metílica, ciclohexanona, anhídrido de ácido, acetonitrilo, acetofenona, acetato de amilo, 2-butanona, clorobenceno, ciclohexano, ciclohexanol, acetatos alquílicos, diacetonoalcohol, 1,2dicloropropano, dietanolamina, p-dietilbenceno, dietilenglicol, abietato de dietilenglicol, éter butílico de dietilenglicol, éter etílico de dietilenglicol, éter metílico de dietilenglicol, N,N-dimetilformamida, sulfóxido de dimetilo, 1,4-dioxano, dipropilenglicol, éter metílico de dipropilenglicol, dibenzoato de dipropilenglicol, diproxitol, alquilpirrolidona, acetato de etilo, 2-etilhexanol, carbonato de etileno, 1,1,1-tricloroetano, 2-heptanona, alfa-pineno, d-limoneno, etilenglicol, éter butílico de etilenglicol, éter metílico de etilenglicol, gamma-butirolactona, glicerol, diacetato de glicerol, monoacetato de glicerol, triacetato de glicerol, hexadecano, hexilenglicol, acetato de isoamilo, acetato de isobornilo, isooctano, isoforona, isopropilbenceno, miristato de isopropilo, ácido láctico, laurilamina, óxido de mesitilo, metoxipropanol, cetona isoamil metílica, cetona isobutil metílica, laurato de metilo, octanoato de metilo, oleato de metilo, cloruro de metileno, m-xileno, n-hexano, n-octilamina, ácido octadecanoico, acetato de octilamina, ácido oleico, oleilamina, oxileno, fenol, polietilenglicol (PEG400), ácido propiónico, propilenglicol, éter monometílico de propilenglicol, p-xileno, tolueno, fosfato de trietilo, trietilenglicol, ácido xilenosulfónico, parafina, aceite mineral, tricloroetileno, percloroetileno, acetato de etilo, acetato de amilo, acetato de butilo, metanol, etanol, isopropanol y alcoholes de peso molecular superior tales como el alcohol amílico, alcohol tetrahidrofurfurílico, hexanol, octanol, etc., etilenglicol, propilenglicol, glicerina y N-metil-2-pirrolidinona. Generalmente el portador elegido para la dilución de los concentrados es agua.
Los portadores sólidos adecuados incluyen, por ejemplo, talco, dióxido de titanio, arcilla pirofilita, sílice, arcilla de atapulgita, diatomita, tiza, tierra de diatomeas, cal, carbonato de calcio, arcilla de bentonita, tierra de batán, vainas de algodón, harina de trigo, harina de soja, piedra pómez, harina de madera, harina de la cáscara de la nuez y lignina.
Se emplea convenientemente una amplia gama de agentes tensioactivos tanto en dichas composiciones líquidas como sólidas, especialmente en las diseñadas para ser diluidas con un portador antes de su aplicación. Estos agentes, cuando se utilizan, normalmente comprenden entre un 0.1% y un 15% en peso de la formulación. Estos pueden ser de naturaleza aniónica, catiónica, no iónica o polimérica y se pueden emplear como agentes emulsionantes, agentes humectantes, agentes de suspensión o con otros fines. Los agentes tensioactivos habituales incluyen sales de alquilsulfatos tales como laurilsulfato de dietanolamonio; sales de alquilarilsulfonato tales como dodecilbencenosulfonato de calcio; productos de la adición de alquilfenol y óxido de alquileno, tales como nonilfenol etoxilado C sub18 productos de la adición de alcohol y óxido de alquileno, tales como alcohol tridecílico etoxilado C16 jabones, tales como estearato de sodio; sales de alquilnaftalenosulfonato, tales como dibutilnaftalenosulfonato de sodio; ésteres dialquílicos de sales de sulfosuccinato, tales como sulfosuccinato sódico de di(2-etilhexilo); ésteres de sorbitol, tales como oleato de sorbitol; aminas cuaternarias, tales como cloruro de lauriltrimetilamonio; ésteres polietilenglicólicos de ácidos grasos, tales como estearato de polietilenglicol; copolímeros en bloque de óxido de etileno y óxido de propileno; y sales de ésteres de fosfato mono y dialquílico.
Otros adyuvantes utilizados comúnmente en composiciones agrícolas incluyen inhibidores de la cristalización, modificadores de la viscosidad, agentes de suspensión, modificadores de las microgotas de los aerosoles, pigmentos, antioxidantes, agentes espumantes, agentes antiespumantes, agentes bloqueadores de la luz, agentes compatibilizantes, agentes antiespumantes, agentes secuestrantes, tampones y agentes neutralizantes, inhibidores de la corrosión, tintes, odorizantes, agentes de dispersión, potenciadores de la penetración, micronutrientes, emolientes, lubricantes y agentes de adhesivos.
Asimismo, pueden combinarse otros ingredientes o composiciones adicionales activos como biocidas con las composiciones de la invención y utilizarse en los métodos de la invención y aplicarse simultánea o secuencialmente con las composiciones de la invención. Cuando se aplican simultáneamente, estos ingredientes activos adicionales podrán formularse junto con las composiciones de la invención o mezclarse, por ejemplo, en el tanque de pulverización. Estos ingredientes adicionales activos como biocidas pueden ser fungicidas, herbicidas, insecticidas, bactericidas, acaricidas, nematicidas y/o reguladores del crecimiento de plantas.
Los agentes pesticidas se mencionan en el presente documento usando su nombre común y se describen, por ejemplo, en "The Pesticide Manual", 15.a Ed., Consejo Británico para la Protección de Cultivos, 2009.
Además, las composiciones de la invención también pueden aplicarse con uno o más inductores de resistencia adquirida sistémicamente (inductores "SAR"). Los inductores SAR son conocidos y se describen en, por ejemplo, la Patente de Estados Unidos n.° US 6 919 298 e incluyen, por ejemplo, salicilatos y el inductor SAR comercializado acibenzolar-S-metilo.
Los compuestos de fórmula (I) se usan normalmente en forma de composiciones agroquímicas y pueden aplicarse al área de cultivo o a la planta que se desee tratar, simultánea o sucesivamente, con otros compuestos. Estos otros compuestos pueden ser, por ejemplo, fertilizantes o dadores de micronutrientes u otros preparados que fomenten el crecimiento de las plantas. También pueden ser herbicidas selectivos o herbicidas no selectivos, así como insecticidas, fungicidas, bactericidas, nematicidas, molusquicidas o mezclas de varios de estos preparados, si se desea junto con otros portadores, tensioactivos o adyuvantes que faciliten la aplicación empleados habitualmente en el campo de la formulación.
Los compuestos de fórmula (I) pueden usarse en forma de composiciones (fungicidas) para el control o la protección contra microorganismos fitopatógenos, que comprenden como principio activo al menos un compuesto de fórmula (I) o al menos un compuesto individual preferido como se definen en el presente documento, en forma libre o en forma salina útil desde un punto de vista agroquímico, y al menos uno de los adyuvantes mencionados anteriormente.
Por lo tanto, la invención proporciona una composición, preferentemente una composición fungicida, que comprende al menos un compuesto de fórmula (I), un portador aceptable en agricultura y opcionalmente un adyuvante. Un portador agrícola aceptable es, por ejemplo, un portador que sea adecuado para el uso agrícola. Los portadores agrícolas son muy conocidos en la técnica. Preferentemente, dicha composición puede comprender al menos uno o más compuestos activos como pesticidas, por ejemplo, un principio activo fungicida adicional además del compuesto de fórmula (I).
El compuesto de fórmula (I) puede ser el único principio activo de una composición o puede estar mezclado con uno o más principios activos adicionales tales como un pesticida, fungicida, sinergista, herbicida o regulador del crecimiento vegetal, cuando proceda. En algunos casos, un principio activo adicional puede producir actividades sinérgicas inesperadas.
Los ejemplos de principios activos adicionales adecuados incluyen los siguientes: fungicidas aminoacídicos acíclicos, fungicidas alifáticos nitrogenados, fungicidas de tipo amida, fungicidas de tipo anilida, fungicidas antibióticos, fungicidas aromáticos, fungicidas que contienen arsénico, fungicidas de tipo cetona aril fenílica, fungicidas de tipo benzamida, fungicidas de tipo benzanilida, fungicidas de tipo bencimidazol, fungicidas de tipo benzotiazol, fungicidas botánicos, fungicidas difenílicos con puente, fungicidas de tipo carbamato, fungicidas de tipo carbanilato, fungicidas de tipo conazol, fungicidas que contienen cobre, fungicidas de tipo dicarboximida, fungicidas de tipo dinitrofenol, fungicidas de tipo ditiocarbamato, fungicidas de tipo ditiolano, fungicidas de tipo furamida, fungicidas de tipo furanilida, fungicidas de tipo hidrazida, fungicidas de tipo imidazol, fungicidas que contienen mercurio, fungicidas morfolínicos, fungicidas organofosforados, fungicidas de organoestaño, fungicidas de tipo oxatiino, fungicidas de tipo oxazol, fungicidas de tipo fenilsulfamida, fungicidas de tipo polisulfuro, fungicidas de tipo pirazol, fungicidas de tipo piridina, fungicidas de tipo pirimidina, fungicidas de tipo pirrol, fungicidas de tipo amonio cuaternario, fungicidas de tipo quinolina, fungicidas de tipo quinona, fungicidas de tipo quinoxalina, fungicidas de tipo estrobilurina, fungicidas de tipo sulfonanilida, fungicidas de tipo tiadiazol, fungicidas de tipo tiazol, fungicidas de tipo tiazolidina, fungicidas de tipo tiocarbamato, fungicidas de tipo tiofeno, fungicidas de tipo triazina, fungicidas de tipo triazol, fungicidas de tipo triazolopirimidina, fungicidas de tipo urea, fungicidas de tipo valinamida y fungicidas que contienen zinc.
Los ejemplos de principios activos adicionales adecuados también incluyen los siguientes: (9-diclorometileno-1,2,3,4-tetrahidro-1,4-metano-naftalen-5-il)-amida del ácido 3-difluorometil-1 -metil-1 H-pirazol-4-carboxílico, metoxi-[1 -metil-2-(2,4,6-triclorofenil)-etil]-amida del ácido 3-difluorometil-1-metil-1H-pirazol-4-carboxílico, (2-diclorometileno-3-etil-1-metil-indan-4-il)-amida del ácido 1-metil-3-difluorometil-1H-pirazol-4-carboxílico (1072957-71-1), (4'-metilsulfanilbifenil-2-il)-amida del ácido 1 -metil-3-difluorometil-1 H-pirazol-4-carboxílico, [2-(2,4-dicloro-fenil)-2-metoxi-1 -metil-etil]-amida del ácido 1-metil-3-difluorometil-4H-pirazol-4-carboxílico, (5-cloro-2,4-dimetil-piridin-3-il)-(2,3,4-trimetoxi-6-metil-fenil)-metanona, (5-bromo-4-cloro-2-metoxi-piridin-3-il)-(2,3,4-trimetoxi-6-metil-fenil)-metanona, 2-{2-[(E)-3-(2,6-dicloro-fenil)-1-metil-prop-2-en-(E)-ilidenoaminooximetil]-fenil}-2-[(Z)-metoxiimino]-N-metil-acetamida, 3-[5-(4-clorofenil)-2,3-dimetil-isoxazolidin-3-il]-piridina, (E)-N-metil-2-[2-(2, 5-dimetilfenoximetil)fenil]-2-metoxi-iminoacetamida, 4-bromo-2-ciano-N, N-dimetil-6-trifluorometilbenzoimidazol-1 -sulfonamida, a-[N-(3-cloro-2, 6-xilil)-2-metoxiacetamido]-ybutirolactona, 4-cloro-2-ciano-N-dimetil-5-p-tolilimidazol-1-sulfonamida, N-alil-4,5,-dimetil-2-trimetilsililtiofeno-3-carboxamida, N- (1 -ciano-1,2-dimetilpropil)-2-(2,4-diclorofenoxi)propionamida, N-(2-metoxi-5-piridil)-ciclopropanocarboxamida, (.+-.)-cis-1 -(4-clorofenil)-2-(1 H-1,2,4-triazol-1 -il)-cicloheptanol, 2-(1 -ferc-butyl)-1 -(2-clorofenil)-3-(1,2,4-triazol-1 -il)-propan-2-ol, 2',6'-dibromo-2-metil-4-trifluorometoxi-4'-trifluorometil-1,3-tiazol-5-carboxanilida, 1-imidazolil-1-(4'-clorofenoxi)-3,3-dimetilbutan-2-ona, (E)-2-[2-[6-(2-cianofenoxi)pirimidin-4-iloxi]fenil]3-metoxiacrilato de metilo, (E)-2-[2-[6-(2-tioamidofenoxi)pirimidin-4-iloxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[6-(2-fluorofenoxi)pirimidin-4-iloxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[6-(2,6-difluorofenoxi)pirimidin-4-iloxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[3-(pirimidin-2-iloxi)fenoxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[3-(5-metilpirimidin-2-iloxi)-fenoxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[3-(fenil-sulfoniloxi)fenoxi]fenil-3-metoxiacrilato de metilo, (E)-2-[2-[3-(4-nitrofenoxi)fenoxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-fenoxifenil]-3-metoxiacrilato de metilo, (E)-2-[2-(3,5-dimetil-benzoil)pirrol-1-il]-3-metoxiacrilato de metilo, (E)-2-[2-(3-metoxifenoxi)fenil]-3-metoxiacrilato de metilo, (E)-2[2-(2-fenileten-1-il)-fenil]-3-metoxiacrilato de metilo, (E)-2-[2-(3,5-diclorofenoxi)piridin-3-il]-3-metoxiacrilato de metilo, (E)-2-(2-(3-(1,1,2,2-tetrafluoroetoxi)fenoxi)fenil)-3-metoxiacrilato de metilo, (E)-2-(2-[3-(alfa-hidroxibencil)fenoxi]fenil)-3-metoxiacrilato de metilo, (E)-2-(2-(4-fenoxipiridin-2-iloxi)fenil)-3-metoxiacrilato de metilo, (E)-2-[2-(3-n-propiloxi-fenoxi)fenil]3-metoxiacrilato de metilo, (E)-2-[2-(3-isopropiloxifenoxi)fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[3-(2-fluorofenoxi)fenoxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-(3-etoxifenoxi)fenil]-3-metoxiacrilato de metilo, (E)-2-[2-(4-ferc-butyl-piridin-2-iloxi)fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[3-(3-cianofenoxi)fenoxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[(3-metil-piridin-2-iloximetil)fenil]-3-metoxiacrilato de metilo, (E)-2-[2-[6-(2-metil-fenoxi)pirimidin-4-iloxi]fenil]-3-metoxiacrilato de metilo, (E)-2-[2-(5-bromo-piridin-2-iloximetil)fenil]-3-metoxiacrilato de metilo, (E)-2-[2-(3-(3-yodopiridin-2-iloxi)fenoxi)fenil]-3-metoxiacrilato de metilo, (E)-2- [2-[6-(2-cloropiridin-3-iloxi)pirimidin-4-iloxi]fenil]-3-metoxiacrilato de metilo, (E),(E)-2-[2-(5,6-dimetilpirazin-2-ilmetiloximinometil)fenil]-3-metoxiacrilato de metilo, (E)-2-{2-[6-(6-metilpiridin-2-iloxi)pirimidin-4-iloxi]fenil}-3-metoxiacrilato de metilo, (E),(E)-2-{2-(3-metoxifenil)metiloximinometil]-fenil}-3-metoxiacrilato de metilo, (E)-2-{2-(6-(2-azidofenoxi)-pirimidin-4-iloxi]fenil}-3-metoxiacrilato de metilo, (E),(E)-2-{2-[6-fenilpirimidin-4-il)-metiloximinometil]fenil}-3- metoxiacrilato de metilo, (E),(E)-2-{2-[(4-clorofenil)-metiloximinometil]-fenil}-3-metoxiacrilato de metilo, (E)-2-{2-[6-(2-n-propilfenoxi)-1,3,5-triazin-4-iloxi]fenil}-3-metoxiacrilato de metilo, (E),(E)-2-{2-[(3-nitrofenil)metiloximinometil]fenil}-3-metoxiacrilato, 3-cloro-7-(2-aza-2,7,7-trimetil-oct-3-en-5-ina), 2,6-dicloro-N-(4-trifluorometilbencil)-benzamida, alcohol 3-yodo-2-propinílico, 4-clorofenil-3-yodopropargil formal, etilcarbamato de 3-bromo-2,3-diyodo-2-propenilo, alcohol 2,3,3-triiodoalílico, alcohol 3-bromo-2,3-diyodo-2-propenílico, n-butilcarbamato
de 3-yodo-2-propinilo, n-hexilcarbamato de 3-yodo-2-propinilo, ciclohexil-carbamato de 3-yodo-2-propinilo, fenilcarbamato de 3-yodo-2-propinil; derivados de fenol, tal como tribromofenol, tetraclorofenol, 3-metil-4-clorofenol, 3,5-dimetil-4-clorofenol, fenoxietanol, diclorofeno, o-fenilfenol, m-fenilfenol, p-fenilfenol, 2-bencil-4-clorofenol, 5-hidroxi-2(5H)-furanona; 4,5-dicloroditiazolinona, 4,5-benzoditiazolinona, 4,5-trimetilenoditiazolinona, 4,5-dicloro-(3H)-1,2-ditiol-3-ona, 3,5-dimetil-tetrahidro-1,3,5-tiadiazina-2-tiona, cloruro de N-(2-p-clorobenzoiletil)-hexaminio, acibenzolar, acipetacs, alanicarb, albendazol, aldimorph, allicin,alcohol alílico, ametoctradin, amisulbrom, amobam, ampropilfos, anilazina, asomato, aureofungin, azaconazol, azafendin, azithiram, azoxistrobin, polisulfuro de bario, benalaxilo, benalaxil-M, benodanilo, benomilo, benquinox, bentaluron, bentiavalicarb, bentiazol, cloruro de benzalconio, benzamacrilo, benzamorf, ácido benzohidroxámico, benzovindiflupir, berberine, betoxazin, biloxazol, binapacrilo, bifenilo, bitertanol, bitionol, bixafen, blasticidin-S, boscalid, bromothalonilo, bromuconazol, bupirimato, butiobato, butilamina polisulfuro de calcio, captafol, captan, carbamorph, carbendazim, clorhidrato de carbendazim, carboxin, carpropamid, carvone, CGA41396, CGA41397, cinometionato, citosan, clobentiazona, cloraniformetan, cloranilo, clorfenazol, cloroneb, cloropicrin, clorotalonilo, clorozolinato, clozolinato, climbazol, clotrimazol, clozilacon, compuestos que contienen cobre, tales como acetato de cobre, carbonato de cobre, hidróxido de cobre, naftenato de cobre, oleato de cobre, oxicloruro de cobre, oxiquinolato de cobre, silicato de cobre, sulfato de cobre, tallato de cobre, cinc cromato de cobrey mezcla de Bordeaux, cresol, cufraneb, cuprobam, óxido cuproso, ciazofamid, ciclafuramid, cicloheximida, ciflufenamid, cimoxanilo, cipendazol, ciproconazol, ciprodinilo, dazomet, debacarb, decafentin, ácido dehidroacético, 1,1 '-dióxido de di-2-piridil disulfuro, diclofluanid, diclomezina, diclona, dicloran, diclorofen, diclozolina, diclobutrazol, diclocimet, dietofencarb, difenoconazol, difenzoquat, diflumetorim, tiofosfato de O,O-di-iso-propil-S-bencilo, dimefluazol, dimetaclona, dimetconazol, dimethomorph, dimethirimol, diniconazol, diniconazol-M, dinobuton, dinocap, dinocton, dinopenton, dinosulfon, dinoterbon, difenilamina, dipiritione, disulfiram, ditalimfos, ditianon, ditioéter, dodecil dimetil cloruro de amonio, dodemorph, dodicin, dodina, doguadina, drazoxolon, edifenfos, enestroburin, epoxiconazol, etaconazol, etem, ethaboxam, ethirimol, etoxiquin, etilicin, (Z)-N-bencil-N([metil(metil-tioetilidenoaminooxicarbonil) amino]tio)-B-alaninato de etilo, etridiazol, famoxadona, fenamidona, fenaminosulf, fenapanilo, fenarimol, fenbuconazol, fenfuram, fenhexamid, fenitropan, fenoxanilo, fenpiclonilo, fenpropidin, fenpropimorph, fenpirazamina, acetato de fentín, hidróxido de fentín, ferbam, ferimzona, fluazinam, fludioxonilo, flumetover, flumorph, flupicolida, fluopiram, fluoroimida, fluotrimazol, fluoxastrobin, fluquinconazol, flusilazol, flusulfamida, flutanilo, flutolanilo, flutriafol, fluxapiroxad, folpet, formaldehído, fosetilo, fuberidazol, furalaxilo, furametpir, furcarbanilo, furconazol, furfural, furmeciclox, furofanato, gliodin, griseofulvin, guazatina, halacrinata, hexaclorobenceno, hexaclorobutadieno, hexaclorofeno, hexaconazol, hexiltiofos, hidrargafen, hidroxiisoxazol, himexazol, imazalilo, sulfato de imazalilo, imibenconazol, iminoctadina, triacetato de iminoctadina, inezin, yodocarb, ipconazol, ipfentrifluconazol, iprobenfos, iprodiona, iprovalicarb, butilcarbamato de isopropanil, isoprotiolano, isopirazam, isotianilo, isovalediona, izopamfos, kasugamycin, kresoxim-metilo, LY186054, LY211795, LY248908, mancozeb, mandipropamid, maneb, mebenilo, mecarbinzid, mefenoxam, mefentrifluconazol, mepanipirim, mepronilo, cloruro de mercúrico, cloruro mercuroso, meptildinocap, metalaxilo, metalaxil-M, metam, metazoxolon, metconazol, methasulfocarb, methfuroxam, bromuro de metilo, yoduro de metilo, isotiocianato de metilo, metiram, metiram-cinc, metominostrobin, metrafenona, metsulfovax, milneb, moroxidina, miclobutanilo, miclozolin, nabam, natamicin, neoasozin, dimetilditiocarbamato de níquel, nitroestireno, nitrotal-iso-propilo, nuarimol, octilinona, ofurace, compuestos organomercúricos, orisastrobina, ostol, oxadixilo, oxasulfuron, oxina-cobre, ácido oxolínico, oxpoconazol, oxicarboxin, parinol, pefurazoato, penconazol, pencicuron, penflufen, pentaclorofenol, pentiopirad, fenamacrilo, óxido de fenazina, fosdifen, fosetil-Al, ácidos fosforosos, ftalida, picoxistrobin, piperalin, policarbamato, polioxin D, polioxrim, poliram, probenazol, procloraz, procymidone, propamidina, propamocarb, propiconazol, propineb, ácido propiónico, proquinazid, protiocarb, protioconazol, pidiflumetofen, piracarbolid, piraclostrobin, pirametrostrobin, piraoxistrobin, pirazophos, piribencarb, piridinitrilo, pirifenox, pirimetanilo, piriofenona, piroquilon, piroxiclor, piroxifur, pirrolnitrin, compuestos de amonio cuaternario, quinacetol, quinazamid, quinconazol, quinometionato, quinoxifen, quintozeno, rabenzazol, santonin, sedaxano, siltiofam, simeconazol, sipconazol, pentaclorofenato de sodio, solatenol, espiroxamina, streptomycin, azufre, sultropen, tebuconazol, tebfloquin, tecloftalam, tecnazeno, tecoram, tetraconazol, tiabendazol, tiadiflúor, ticiofen, thifluzamida, 2-(tiocianometiltio)benzotiazol, tiophanato-metilo, tioquinox, tiram, tiadinilo, timibenconazol, tioximid, tolclofos-metilo, tolilfluanid, triadimefon, triadimenol, triamifos, triarimol, triazbutilo, triazóxido, triciclazol, tridemorph, trifloxistrobin, triflumazol, triforina, triflumizol, triticonazol, uniconazol, urbacida, validamicin, valifenalato, vapam, vinclozolin, zarilamid, zineb, ziram y zoxamida.
Los compuestos de la invención también se pueden utilizar combinados con agentes antihelmínticos. Tales agentes antihelmínticos incluyen compuestos seleccionados entre la clase de compuestos lactónicos macrocíclicos tales como derivados de ivermectina, avermectina, abamectina, emamectina, eprinomectina, doramectina, selamectina, moxidectina, nemadectina y milbemicina como los descritos en los documentos EP-357460, EP-444964 y EP-594291. Otros agentes antihelmínticos incluyen derivados de avermectina/milbemicina semisintéticos y biosintéticos tales como los descritos en los documentos US-5015630, WO-9415944 y WO-9522552. Otros agentes antihelmínticos incluyen bencimidazoles tales como albendazol, cambendazol, fenbendazol, flubendazol, mebendazol, oxfendazol, oxibendazol, parbendazol y otros miembros de la clase. Otros agentes antihelmínticos incluyen imidazotiazoles y tetrahidropirimidinas tales como tetramisol, levamisol, pamoato de pirantel, oxantel o morantel. Otros agentes antihelmínticos incluyen fluquicidas, tales como triclabendazol y clorsulón, y cestocidas tales como praziquantel y epsiprantel.
Los compuestos de la invención se pueden utilizar combinados con derivados y análogos de la clase paraherquamida/marcfortina de agentes antihelmínticos así como también oxazolinas antiparasitarias tales como las descritas en los documentos US-5478855, US-4639771 y DE-19520936.
Los compuestos de la invención pueden emplearse en combinación con derivados y análogos de la clase general de agentes antiparasitarios dioxomorfolínicos como los descritos en el documento WO 96/15121 y también con depsipéptidos antihelmínticos cíclicos activos tales como los descritos en los documentos WO 96/11945, WO 93/19053, WO 93/25543, EP 0626 375, EP 0382 173, WO 94/19334, EP 0382 173 y EP 0503 538.
Los compuestos de la invención se pueden emplear combinados con otros ectoparasiticidas, por ejemplo, fipronilo, piretroides, organofosfatos, reguladores del crecimiento de insectos tales como lufenurón, agonistas de la ecdisona tales como tebufenocida y similares, neonicotinoides tales como imidacloprid y similares.
Los compuestos de la invención pueden usarse combinados con alcaloides terpénicos, por ejemplo, los descritos en las Publicaciones de Solicitud de Patente Internacional con números WO 95/19363 o WO 04/72086, particularmente los compuestos descritos en dichos documentos.
Otros ejemplos de este tipo de compuestos biológicamente activos que se pueden emplear combinados con los compuestos de la invención incluyen, sin carácter limitante, los siguientes:
Organofosfatos: acefato, azametifós, azinfós etílico, azinfós metílico, bromofós, bromofós etílico, cadusafós, cloretoxifós, clorpirifós, clorfenvinfós, clormefós, demetón, demetón-S-metilo, demetón-S-metilsulfona, dialifós, diacinona, diclorvós, dicrotofós, dimetoato, disulfotón, etión, etoprofós, etrimfós, famfur, fenamifós, fenitrotión, fensulfotión, fentión, flupirazofós, fonofós, formotión, fostiazato, heptenofós, isazofós, isotioato, isoxatión, malatión, metacrifós, metamidofós, metidatión, paratión metílico, mevinfós, monocrotofós, naled, ometoato, oxidemetón metílico, paraoxona, paratión, paratión metílico, fentoato, fosalona, fosfolán, fosfocarb, fosmet, fosfamidón, forato, foxima, pirimifós, pirimifós metílico, profenofós, propafós, proetamfós, protiofós, piraclofós, piridapentión, quinalfós, sulprofós, temefós, terbufós, tebupirimfós, tetraclorvinfós, timetón, triazofós, triclorfón, vamidotión.
Carbamatos: alanicarb, aldicarb, metilcarbamato de 2-sec-butilfenilo, benfuracarb, carbarilo, carbofurano, carbosulfán, cloetocarb, etiofencarb, fenoxicarb, fentiocarb, furatiocarb, HCN-801, isoprocarb, indoxacarb, metiocarb, metomilo, (metil)carbamato de 5-metil-m-cumenilbutirilo, oxamilo, pirimicarb, propoxur, tiodicarb, tiofanox, triazamato, UC-51717.
Piretroides: acrinatina, aletrina, alfametrina, (1 R)-cis-2,2-dimetil-3-(2-oxotiolan-3-ilidenometil)ciclopropanocarboxilato de 5-bencil-3-furilmetilo, bifentrina, beta-ciflutrina, ciflutrina, a-cipermetrina, beta-cipermetrina, bioaletrina, bioaletrina (isómero S ciclopentílico), biorresmetrina, bifentrina, NCI-85193, cicloprotrina, cihalotrina, cititrina, cifenotrina, deltametrina, empentrina, esfenvalerato, etofenprox, fenflutrina, fenpropatrina, fenvalerato, flucitrinato, flumetrina, fluvalinato (isómero D), imiprotrina, cihalotrina, lambda-cihalotrina, permetrina, fenotrina, praletrina, piretrinas (productos naturales), resmetrina, tetrametrina, transflutrina, theta-cipermetrina, silafluofeno, t-fluvalinato, teflutrina, tralometrina, Zeta-cipermetrina.
Reguladores del crecimiento de artrópodos: a) inhibidores de la síntesis de la quitina: benzoilureas: clorfluazurón, diflubenzurón, fluazurón, flucicloxurón, flufenoxurón, hexaflumurón, lufenurón, novalurón, teflubenzurón, triflumurón, buprofecina, diofenolano, hexitiazox, etoxazol, clorfentacina; b) antagonistas de la ecdisona: halofenocida, metoxifenocida, tebufenocida; c) juvenoides: piriproxifeno, metopreno (incluido el S-metopreno), fenoxicarb; d) inhibidores de la biosíntesis de lípidos: espirodiclofeno.
Otros antiparasitarios: acequinocilo, amitraz, AKD-1022, ANS-118, azadiractina, Bacillus thuringiensis, bensultap, bifenazato, binapacrilo, bromopropilato, BTG-504, BTG-505, camfeclor, cartap, clorobencilato, clordimeform, clorfenapir, cromafenocida, clotianidina, ciromacina, diaclodeno, diafentiurón, DBI-3204, dinactina, dihidroximetildihidroxipirrolidina, dinobutón, dinocap, endosulfán, etiprol, etofenprox, fenazaquín, flumite, MTI-800, fenpiroximato, fluacripirim, flubencimina, flubrocitrinato, flufencina, flufenprox, fluproxifeno, halofenprox, hidrametilnona, IKI-220, kanemite, NC-196, protector de nim, nidinorterfurano, nitenpiram, SD-35651, WL-108477, piridarilo, propargita, protrifenbute, pimetrocina, piridabeno, pirimidifeno, NC-1111, R-195, RH-0345, RH-2485, RYI-210, S-1283, S-1833, SI-8601, silafluofeno, silomadina, espinosad, tebufenpirad, tetradifón, tetranactina, tiacloprid, tiociclam, tiametoxam, tolfenpirad, triazamato, trietoxiespinosina, trinactina, verbutina, vertalec, YI-5301.
Agentes biológicos: las subespecies aizawai, kurstaki, delta endotoxina de Bacillus thuringiensis, baculovirus, bacterias, virus y hongos entomopatógenos.
Bactericidas: clortetraciclina, oxitetraciclina, estreptomicina.
Otros agentes biológicos: enrofloxacina, febantel, penetamato, moloxicam, cefalexina, kanamicina, pimobendano, clenbuterol, omeprazol, tiamulina, benazeprilo, piriprol, cefquinoma, florfenicol, buserelina, cefovecina, tulatromicina, ceftiofur, carprofeno, metaflumizona, praziquarantel, triclabendazol.
Otro aspecto de la invención se refiere al uso de un compuesto de fórmula (I) o de un compuesto individual preferido como se definen en el presente documento, de una composición que comprende al menos un compuesto de fórmula
(I) o al menos un compuesto individual preferido como los definidos anteriormente, o de una mezcla fungicida o insecticida que comprende al menos un compuesto de fórmula (I) o al menos un compuesto individual preferido como se han definido, mezclado con otros fungicidas o insecticidas, como los descritos anteriormente, para controlar o prevenir la infestación de plantas, por ejemplo, plantas útiles tales como plantas de cultivo, su material de propagación, por ejemplo, semillas, cultivos recolectados, por ejemplo, cultivos alimentarios recolectados, o materiales inertes por parte de insectos o microorganismos fitopatógenos, preferentemente organismos fúngicos.
Un aspecto adicional de la invención se refiere a un método para controlar o prevenir una infestación de plantas, por ejemplo, de plantas útiles tales como plantas de cultivo, su material de propagación, por ejemplo, semillas, cultivos recolectados, por ejemplo, cultivos alimentarios recolectados, o de materiales inertes por parte de insectos o microorganismos fitopatógenos o responsables de la descomposición, u organismos potencialmente dañinos para el ser humano, especialmente organismos fúngicos, que comprende la aplicación de un compuesto de fórmula (I) o un compuesto individual preferido como los definidos anteriormente como principio activo a las plantas, a partes de las plantas o a su emplazamiento, a su material de propagación o a cualquier parte de los materiales inertes.
Controlar o prevenir quiere decir reducir la infestación por parte de microorganismos fitopatógenos o responsables de la descomposición, u organismos potencialmente dañinos para el ser humano, especialmente organismos fúngicos, hasta un nivel tal que se demuestra una mejora.
Un método preferido para controlar o prevenir una infestación de plantas de cultivo por parte de microorganismos fitopatógenos, especialmente organismos fúngicos, o insectos que comprende aplicar un compuesto de fórmula (I) o una composición agroquímica que contenga al menos uno de dichos compuestos, es la aplicación foliar. La frecuencia de aplicación y la tasa de aplicación dependerán del riesgo de infestación por parte del patógeno o insecto correspondiente. Sin embargo, los compuestos de fórmula (I) también se pueden infiltrar en la planta a través de las raíces mediante la tierra (acción sistémica) empapando el emplazamiento de la planta con una formulación líquida o aplicando los compuestos en forma sólida a la tierra, por ejemplo, en forma granular (aplicación en la tierra). En cultivos de arrozales, estos materiales granulados se pueden aplicar al campo de arroz inundado. Los compuestos de fórmula I también se pueden aplicar a las semillas (recubrimiento) impregnando las semillas o los tubérculos con una formulación líquida del fungicida o recubriéndolos con una formulación sólida.
Una formulación, por ejemplo, una composición que contiene el compuesto de fórmula (I) y, si se desea, un adyuvante sólido o líquido, o monómeros para encapsular el compuesto de fórmula (I), se puede preparar empleando un método conocido, habitualmente mezclando y/o moliendo íntimamente el compuesto con diluyentes, por ejemplo, disolventes, portadores sólidos y, opcionalmente, compuestos tensioactivos (tensioactivos).
Las tasas de aplicación convenientes son normalmente de 5 g a 2 kg de principio activo (p.a.) por hectárea (ha), preferentemente de 10 g a 1 kg de p.a./ha y más preferentemente de 20 g a 600 g de p.a./ha. Cuando se emplea como un agente para empapar las semillas, las dosis convenientes son de 10 mg a 1 g de sustancia activa por kg de semillas.
Cuando las combinaciones de la presente invención se usan para el tratamiento de semillas, en general, son suficientes tasas de 0.001 a 50 g de un compuesto de fórmula I por kg de semillas, preferentemente de 0.01 a 10 g por kg de semillas.
Convenientemente, una composición que comprende un compuesto de fórmula (I) de acuerdo con la presente invención se aplica ya sea de manera preventiva, que se refiere a antes del desarrollo de la enfermedad, o curativa, que se refiere a después del desarrollo de la enfermedad.
Las composiciones de la invención se pueden emplear en cualquier forma convencional, por ejemplo, en forma de un paquete doble, un polvo para el tratamiento de semillas en seco (SS), una emulsión para el tratamiento de semillas (ES), un concentrado fluido para el tratamiento de semillas (CF), una solución para el tratamiento de semillas (LS), un polvo dispersable en agua para el tratamiento de semillas (DS), una suspensión de cápsulas para el tratamiento de semillas (CF), un gel para el tratamiento de semillas (GF), un concentrado emulsionable (CE), un concentrado en suspensión (CS), una suspoemulsión (SE), una suspensión de cápsulas (SC), un gránulo dispersable en agua (GD), un gránulo emulsionable (GE), una emulsión de agua en aceite (EAc), una emulsión de aceite en agua (EAg), una microemulsión (ME), una dispersión oleosa (DO), un fluido miscible en aceite (FAc), un líquido miscible en aceite (LAc), un concentrado soluble (SL), una suspensión de volumen ultrabajo (SU), un líquido de volumen ultrabajo (LU), un concentrado técnico (CT), un concentrado dispersable (CD), un polvo humectable (PH) o cualquier formulación técnicamente factible combinada con adyuvantes aceptables en agricultura.
Estas composiciones se pueden producir empleando métodos convencionales, por ejemplo, mezclando los principios activos con materiales inertes de formulación adecuados (diluyentes, disolventes, rellenos y opcionalmente otros ingredientes de formulación tales como tensioactivos, biocidas, anticongelantes, adherentes, espesantes y compuestos que proporcionen efectos adyuvantes). Cuando se desee obtener una eficacia de duración prolongada, también se pueden emplear formulaciones de liberación lenta convencionales. En particular, las formulaciones que se van a aplicar en formas de pulverización, tales como los concentrados dispersables en agua (por ejemplo, CE, CS, CD, DO, SE, EAg, EAc y similares), polvos humectables y gránulos, pueden contener tensioactivos tales como agentes humectantes y dispersantes y otros compuestos que proporcionen efectos adyuvantes, por ejemplo, el producto de
condensación del formaldehído con sulfonato de naftaleno, un alquilarilsulfonato, un ligninosulfonato, un sulfato de alquilo graso, alquilfenol etoxilado y un alcohol graso etoxilado.
Una formulación para el revestimiento de semillas se aplica con métodos conocidos por sí mismos a las semillas, empleando la combinación de la invención y un diluyente en una forma de formulación para el revestimiento de semillas adecuada, por ejemplo, como una suspensión acuosa o en una forma de polvo seco que tenga una adherencia satisfactoria a las semillas. Estas formulaciones para el revestimiento de semillas son de uso común en la técnica. Las formulaciones para el revestimiento de semillas pueden contener los principios activos individuales o la combinación
de principios activos en forma encapsulada, por ejemplo, como cápsulas o microcápsulas de liberación lenta.
En general, las formulaciones incluyen entre un 0.01 y un 90% en peso de agente activo, entre un 0 y un 20% de tensioactivo aceptable en agricultura y entre un 10 y un 99.99% de un adyuvantes o adyuvantes y componentes inertes
de formulación sólidos o líquidos, estando constituido el agente activo por al menos el compuesto de fórmula (I) junto
con, opcionalmente, otros agentes activos, particularmente microbicidas, conservantes o similares. Las formas concentradas de las composiciones contienen generalmente entre aproximadamente un 2 y un 80%, preferentemente
entre aproximadamente un 5 y un 70% en peso de agente activo. Las formas de aplicación de la formulación pueden contener, por ejemplo, entre un 0.01 y un 20% en peso, preferentemente entre un 0.01 y un 5% en peso de agente
activo. Aunque los productos comerciales se formularán preferentemente como concentrados, el usuario final normalmente empleará formulaciones diluidas.
Aunque se prefiere formular los productos comerciales como concentrados, el usuario final normalmente usará formulaciones diluidas.
Tabla 1.1: Esta tabla describe los 149 compuestos específicos de fórmula (T-1):
(T-1)
donde R5 y R6 son hi R8 es como se define a continuación en la Tabla 1.
Cada una de las Tablas 1.2 a 1.29 (que siguen a la Tabla 1.1) proporcionan 149 compuestos individuales de fórmula
(T-1) en los cuales n, A1, A2, A3, A4, R1, R2, R3, R4, R5, R6 y R7son como se definen específicamente en las Tablas 1.2
a 1.29, que hacen referencia a la Tabla 1 donde R8 se define específicamente.
Tabla 1
Tabla 1.2: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R2, R3, R4, R5 y R6 son hidrógeno, R7 es metoxi, R1 es flúor y anteriormente en la Tabla 1.
T a b la 1.3: E sta ta b la d e s c rib e 149 c o m p u e s to s e s p e c ífic o s de fó rm u la (T -1) d o n d e n es 1, A 1 es C -R 1, A 2 es C -R 2, A 3 es C -R 3, A 4 es C -R 4 y R2, R3, R4, R5 y R6 son h id ró g e n o , R7 es m etoxi, R 1 es c lo ro y R8 es co m o se ha de fin id o a n te rio rm e n te en la T a b la 1.
T a b la 1.4: E sta ta b la d e s c rib e 149 c o m p u e s to s e s p e c ífic o s de fó rm u la (T -1) d o n d e n es 1, A 1 es C -R 1, A 2 es C -R 2, A 3 es C -R 3, A 4 es C -R 4 y R2, R 3, R4, R5 y R6 son h id ró g e n o , R7 es m etoxi, R 1 es m etilo y R8 es co m o se ha de fin id o a n te rio rm e n te en la T a b la 1.
Tabla 1.5: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es N, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R2, R3, R4, R5 y R6 son hidrógeno, R7 es metoxi y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.6: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R4, R5 y R6 son hidrógeno, R7 es metoxi, R3 es flúor y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.7: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R2, R4, R5 y R6 son hidrógeno, R7 es metoxi, R1 y R3 son flúor y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.8: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R3, R4, R5 y R6 son hidrógeno, R7 es metoxi, R1 y R2 son flúor y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.9: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 2, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es metoxi y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.10: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4 y R5 son hidrógeno, R7 es metoxi, R6 es metilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.11: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4 y R5 son hidrógeno, R7 es metilo, R6 es ciano y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.13: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es metilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.14: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es etilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.15: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es propilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.16: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es isopropilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.17: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es alilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.18: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es isobutilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.19: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es 2-metoxietilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.20: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es propiloxi y R8 es como se ha definido anteriormente en la Tabla 1.
T a b la 1.21: E sta ta b la d e sc rib e 149 c o m p u e s to s e s p e c ífic o s de fó rm u la (T -1) d o n d e n es 1, A 1 es C -R 1, A 2 es C -R 2, A 3 es C -R 3, A 4 es C -R 4 y R 1, R2, R3, R4, R5 y R 6 son h id róg en o , R7 es 2 -p ro p in ilo y R8 es co m o se ha de fin id o a n te rio rm e n te en la T a b la 1.
T a b la 1.22: E sta ta b la d e s c rib e 149 c o m p u e s to s e s p e c ífic o s de fó rm u la (T -1) d o n d e n es 1, A 1 es C -R 1, A 2 es C -R 2,
A 3 es C -R 3, A 4 es C -R 4 y R 1, R2, R3, R4, R5 y R6 son h id ró g e n o , R7 es 2 -fu rilm e tilo y R8 es co m o se ha de fin id o a n te rio rm e n te en la T a b la 1.
Tabla 1.23: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2,
A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es tetrahidrofiran-2-ilm definido anteriormente en la Tabla 1.
Tabla 1.24: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2,
A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es ciclopropilmetilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.25: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2,
A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es ciclopropilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.26: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2,
A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es etoxi y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.27: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2,
A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es hidroxi y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.28: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2,
A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es 2,2,2-trifluoroetilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 1.29: Esta tabla describe 149 compuestos específicos de fórmula (T-1) donde n es 1, A1 es C-R1, A2 es C-R2,
A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es 2-hidroxietilo y R8 es como se ha definido anteriormente en la Tabla 1.
Tabla 2.1: Esta tabla describe los 26 compuestos específicos de fórmula (T-2):
(T-2)
donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 R4, R5 y R12 es como se define a continuación en la Tabla 2.
Cada una de las Tablas 2.2 a 2.5 (que siguen a la Tabla 2.1) proporcionan 26 compuestos individuales de fórmula (T-2) en los cuales n, A1, A2, A3, A4, R1, R2, R3, R4, R5, R6 y R7son como se definen específicamente en las Tablas 2.2 a
2.5, que hacen referencia a la Tabla 2 donde R12 se define específicamente.
Tabla 2
Tabla 2.2: Esta tabla describe 26 compuestos específicos de fórmula (T-2) donde n es 1, A1 es C-R1, A2 es C-R2, A3
es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es alilo y R12 es como se ha definido anteriormente en
la Tabla 2.
Tabla 2.3: Esta tabla describe 26 compuestos específicos de fórmula (T-2) donde n es 1, A1 es C-R1, A2 es C-R2, A3
es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es etoxi y R12 es como se ha definido anteriormente
en la Tabla 2.
Tabla 2.4: Esta tabla describe 26 compuestos específicos de fórmula (T-2) donde n es 1, A1 es C-R1, A2 es C-R2, A3
es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es hidroxi y R12 es como se ha definido anteriormente
en la Tabla 2.
Tabla 2.5: Esta tabla describe 26 compuestos específicos de fórmula (T-2) donde n es 1, A1 es C-R1, A2 es C-R2, A3
es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es 2,2,2-trifluoroetilo y R12 anteriormente en la Tabla 2.
Tabla 3.1: Esta tabla describe los 100 compuestos específicos de fórmula (T-3):
(T-3)
donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2 R3, R4, R5, R6 y R16 son hidrógeno, R7 es metoxi
y R14 es como se define a continuación en la Tabla 3.
Cada una de las Tablas 3.2 a 3.14 (que siguen a la Tabla 3.1) proporcionan 100 compuestos individuales de fórmula
(T-3) en los cuales n, A1, A2, A3, A4, R1, R2, R3, R4, R5, R6, R7 y R15 son como se definen específicamente en las Tablas
3.2 a 3.14, que hacen referencia a la Tabla 3 donde R14 se define específicamente.
Tabla 3
Tabla 3.2: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R2, R3, R4, R5, R6 y R15 son hidrógeno, R7 es metoxi, R1 es flúor, n es 1 y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.3: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es N, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R2, R3, R4, R5, R6 y R15 son hidrógeno, R7 es metoxi, n es 1, y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.4: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R4, R5, R6 y R15 son hidrógeno, R7 es metoxi, R3 es flúor, n es 1 y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.5: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R3, R4, R5, R6, y R15 son hidrógeno, R7 es metoxi, R1 y R2 son flúor, n es 1 y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.6: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5, R6 y R15 son hidrógeno, R7 es isopropilo, n es 2 y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.7: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es metoxi, R15 es metilo, n es 1 y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.8: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R2, R3, R4, R5, y R6 son hidrógeno, R7 es metoxi, R1 es flúor, R15 es metilo,n es 1 y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.9: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R4, R5, y R6 son hidrógeno, R7 es metoxi, R3 es flúor, R15 es metilo, n es 1 y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.10: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5, R6 y R15 son hidrógeno, R7 es metilo, n es 1, y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.11: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5, R6 y R15 son hidrógeno, R7 es etilo, n es 1, y R14 es como se ha definido anteriormente en la Tabla 3.
Tabla 3.12: Esta tabla describe 100 compuestos específicos de fórmula (T-3) donde A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1, R2, R3, R4, R5, R6 y R15 son hidrógeno, R7 es isopropilo, n es 1 y R14 es como se ha definido anteriormente en la Tabla 3.
T a b la 3.13 : E sta ta b la d e s c rib e 100 c o m p u e s to s e s p e c ífic o s de fó rm u la (T -3) d o n d e A 1 es C -R 1, A 2 es C -R 2, A 3 es C-R3, A 4 es C -R 4 y R 1, R2, R3, R4, R5, R6 y R 15 son h id róg en o , R7 es c ic lo p ro p ilo , n es 1 y R 14 es co m o se ha de fin id o a n te rio rm e n te en la T a b la 3.
T a b la 3.14 : E sta ta b la d e s c rib e 100 c o m p u e s to s e s p e c ífic o s de fó rm u la (T -3) d o n d e A 1 es C -R 1, A 2 es C -R 2, A 3 es C-R3, A 4 es C -R 4 y R 1, R2, R3, R4, R5, R6 y R 15 son h id róg en o , R7 es h idroxi, n es 1 y R 14 es co m o se ha de fin id o a n te rio rm e n te en la T a b la 3.
Tabla 4.1: Esta tabla describe los 4 compuestos específicos de fórmula (T-4):
(T-4)
donde n es 1, A1 es C-R1, A2 es C-R2, A3 es C-R3, A4 es C-R4 y R1 R2, R3, R4, R5 y R6 son hidrógeno, R7 es metoxi y
R14-N-R15 es como se define a continuación en la Tabla 4.
Cada una de las Tablas 4.2 a 4.4 (que siguen a la Tabla 4.1) proporcionan 4 compuestos individuales de fórmula (T-4) en los cuales n, A1, A2, A3, A4, R1, R2, R3, R4, R5, R6 y R7son como se definen específi 4.4, que hacen referencia a la Tabla 4.1 donde R14-N-R15 se define específicamente.
Tabla 4
Tabla 4.2: Esta tabla describe 4 compuestos específicos de fórmula (T-4) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es
C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es metilo y R14-N-R15 es como se ha definido anteriormente en la Tabla 4.
Tabla 4.3: Esta tabla describe 4 compuestos específicos de fórmula (T-4) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es
C-R3, A4 es C-R4 y R1, R2, R3, R4, R5 y R6 son hidrógeno, R7 es etilo y R14-N-R15 es como se ha definido anteriormente
en la Tabla 4.
Tabla 4.4: Esta tabla describe 4 compuestos específicos de fórmula (T-4) donde n es 1, A1 es C-R1, A2 es C-R2, A3 es
C-R3, A4 es C-R4 y R1, R2, R3, R4, R5, R6 son hidrógeno, R7 es isopropilo y R14-N-R15 es como se ha definido anteriormente en la Tabla 4.
EJEMPLOS
Los siguientes Ejemplos sirven para ilustrar la invención. Los compuestos de la invención se pueden diferenciar de los compuestos conocidos debido a su mayor eficacia con tasas de aplicación bajas, que puede ser verificada por un experto en la técnica utilizando los procedimientos experimentales que se exponen en los Ejemplos, usando tasas de aplicación más bajas, cuando proceda, por ejemplo, 50 ppm, 12.5 ppm, 6 ppm, 3 ppm, 1.5 ppm o 0.2 ppm.
Los compuestos de Fórmula (I) (que incluyen aquellos de acuerdo con la invención) pueden presentar varios beneficios que incluyen, entre otros, unos niveles favorables de actividad biológica para proteger las plantas contra enfermedades que están provocadas por hongos o unas propiedades idóneas para su uso como principios activos agroquímicos (por ejemplo, una actividad biológica mayor, un espectro de actividad favorable, un perfil de seguridad más amplio (que incluye una mejor tolerancia del cultivo), unas propiedades fisicoquímicas mejores o una mayor biodegradabilidad).
A lo largo de esta memoria descripción, las temperaturas se dan en grados Celsius (°C) y "pf" quiere decir punto de fusión. LC/MS quiere decir cromatografía de líquidos/espectroscopía de masas, y la descripción del equipo y el método (Métodos A y B) es la siguiente:
La descripción del aparato de LC/MS y el método A es:
Detector SQ 2 de Waters
Método de ionización: Electronebulización
Polaridad: iones positivos y negativos
Capilaridad (kV) 3.0, Cono (V) 30.00, Extractor (V) 2.00, Temperatura de fuente (°C) 150, Temperatura de desolvatación (°C) 350, Flujo del gas del cono (l/h) 0, Flujo del gas de desolvatación (l/h) 650
Intervalo de masa: 100-900 Da
Intervalo de longitudes de onda del DAD (nm): 210-500
Método ACQUITY UPLC de Waters con las siguientes condiciones de gradiente de HPLC:
(Disolvente A: Agua/Metanol a 20:1 ácido fórmico al 0.05%, y Disolvente B: Acetonitrilo+ ácido fórmico al 0.05%) Tiempo (minutos) A (%) B (%) Caudal (ml/min)
0 100 0 0.85
1.2 0 100 0.85
1.5 0 100 0.85
Tipo de columna: ACQUITY UPLC HSS T3 de Waters; longitud de la columna: 30 mm; diámetro interno de la columna: 2.1 mm; tamaño de partícula: 1.8 micras; temperatura: 60 °C.
La descripción del aparato de LC/MS y el método B es:
Detector SQ 2 de Waters
Método de ionización: Electronebulización
Polaridad: iones positivos
Capilaridad (kV) 3.5, Cono (V) 30.00, Extractor (V) 3.00, Temperatura de fuente (°C) 150, Temperatura de desolvatación (°C) 400, Flujo del gas del cono (l/h) 60, Flujo del gas de desolvatación (l/h) 700
Intervalo de masa: 140-800 Da
Intervalo de longitudes de onda del DAD (nm): 210 a 400
Método ACQUITY UPLC de Waters con las siguientes condiciones de gradiente de HPLC
(Disolvente A: Agua/Metanol a 9:1 ácido fórmico al 0.1%, y Disolvente B: Acetonitrilo ácido fórmico al 0.1%) Tiempo (minutos) A (%) B (%) Caudal (ml/min)
0 100 0 0.75
2.5 0 100 0.75
2.8 0 100 0.75
3.0 100 0 0.75
Tipo de columna: ACQUITY UPLC HSS T3 de Waters; longitud de la columna: 30 mm; diámetro interno de la columna: 2.1 mm; tamaño de partícula: 1.8 micras; temperatura: 60 °C.
Cuando sea necesario, pueden obtenerse los compuestos finales enantioméricamente puros a partir de los materiales racémicos según proceda mediante técnicas de separación físicas habituales tales como cromatografía quiral de fase inversa o mediante técnicas sintéticas estereoselectivas, por ejemplo, usando materiales de partida quirales Ejemplos de formulaciones
Polvos humectables a) b) c)
principio activo [compuesto de fórmula (I)] 25 % 50 % 75 %
lignosulfonato de sodio 5 % 5 % -laurilsulfato de sodio 3 % - 5 % diisobutilnaftaleno sulfato de sodio - 6 % 10 %
éter de fenol y polietilenglicol - 2 %
(7-8 mol de óxido de etileno)
ácido silícico sumamente dispersado 5 % 10 % 10 %
Caolín 62 % 27 % -El principio activo se mezcla completamente con los adyuvantes y la mezcla se muele completamente en un molino adecuado para obtener polvos humectables que se pueden diluir con agua para obtener suspensiones de la concentración deseada.
Polvos para el tratamiento de semillas en seco a) b) c)
principio activo [compuesto de fórmula (I)] 25 % 50 % 75 %
aceite mineral ligero 5 % 5 % 5 %
ácido silícico sumamente dispersado 5 % 5 % -Caolín 65 % 40 % -Talco - 20%
El ingrediente activo se mezcla detenidamente con los adyuvantes y la mezcla se muele cuidadosamente en un molino adecuado, proporcionando polvos que pueden utilizarse directamente para el tratamiento de semillas.
Concentrado emulsionable
principio activo [compuesto de fórmula (I)] 10 %
éter de octilfenol y polietilenglicol 3 %
(4-5 mol de óxido de etileno)
dodecilbencenosulfonato de calcio 3 %
éter de poliglicol y aceite de ricino (35 mol de óxido de etileno) 4 %
Ciclohexanona 30 %
mezcla de xilenos 50 %
Pueden obtenerse emulsiones de cualquier dilución requerida, que pueden utilizarse en la protección de plantas, a partir del mismo concentrado diluyendo con agua.
Polvos a) b) c)
Principio activo [compuesto de fórmula (I)] 5 % 6 % 4 %
Talco 95 % - -Caolín - 94 % -carga mineral - - 96 %
Los polvos listos para usar se obtienen mezclando el principio activo con el portador y moliendo la mezcla en un molino adecuado. Tales polvos también pueden usarse en tratamientos en seco para semillas.
Gránulos extrusores
Principio activo [compuesto de fórmula (I)] 15 %
lignosulfonato de sodio 2 %
Carboximetilcelulosa 1 %
Caolín 82 %
El ingrediente activo se mezcla y muele con los adyuvantes, y la mezcla se humedece con agua. Se extruye la mezcla y después se seca en una corriente de aire.
Gránulos recubiertos
Principio activo [compuesto de fórmula (I)] 8 %
polietilenglicol (peso molecular 200) 3 %
Caolín 89 %
El principio activo finamente molido se aplica uniformemente, en una mezcladora, sobre el caolín humedecido con polietilenglicol. De esta forma se obtienen los gránulos recubiertos que no generan polvo.
Concentrado en suspensión
principio activo [compuesto de fórmula (I)] 40 %
propilenglicol 10 %
nonilfenol éter de polietilenglicol (15 moles de óxido de etileno) 6 %
Lignosulfonato de sodio 10 %
Carboximetilcelulosa 1 %
aceite de silicona (en forma de una emulsión al 75 % en agua) 1 %
Agua 32 %
Se crea una mezcla íntima entre el principio activo finamente molido y los adyuvantes para obtener un concentrado en suspensión a partir del cual se pueden obtener suspensiones de cualquier dilución deseada por dilución con agua. Utilizando tales diluciones, pueden tratarse tanto plantas vivas como material de propagación de plantas y pueden protegerse contra la infestación por microorganismos mediante pulverización, vertido o inmersión.
Concentrado fluido para el tratamiento de semillas
principio activo [compuesto de fórmula (I)] 40 %
propilenglicol 5 %
copolímero de butanol PO/EO 2 %
triestirenofenol con 10-20 moles de OE 2 %
1,2-bencisotiazolin-3-ona (en forma de una disolución al 20% en agua) 0.5 %
sal de calcio de pigmento monoazo 5 %
Aceite de silicona (en forma de una emulsión al 75 % en agua) 0.2 %
Agua 45.3 %
Se crea una mezcla íntima entre el principio activo finamente molido y los adyuvantes para obtener un concentrado en suspensión a partir del cual se pueden obtener suspensiones de cualquier dilución deseada por dilución con agua. Utilizando tales diluciones, pueden tratarse tanto plantas vivas como material de propagación de plantas y pueden protegerse contra la infestación por microorganismos mediante pulverización, vertido o inmersión.
Suspensión de cápsulas de liberación lenta
Se mezclan 28 partes de una combinación del compuesto de fórmula I con 2 partes de un disolvente aromático y 7 partes de una mezcla de diisocianato de tolueno/polifenilisocianato de polimetileno (8:1). Se emulsiona esta mezcla en una mezcla de 1.2 partes de polivinilalcohol, 0.05 partes de un desespumante y 51.6 partes de agua, hasta que se obtiene el tamaño de partícula deseado. Se añade a esta emulsión una mezcla de 2.8 partes de 1,6-diaminohexano en 5.3 partes de agua. Se agita la mezcla hasta que finaliza la reacción de polimerización.
Se estabiliza la suspensión de cápsulas obtenida añadiendo 0.25 partes de un espesante y 3 partes de un agente dispersante. La formulación de suspensión de cápsulas contiene un 28% de los principios activos. El diámetro medio de cápsula es de 8-15 micrómetros.
Se aplica la formulación resultante a semillas como una suspensión acuosa en un aparato adecuado para dicho fin. Lista de abreviaturas:
AIBN = azobisisobutironitrilo
BOP-Cl = cloruro de ácido bis(2-oxooxazolidido)fosfórico
CDI = carbonildiimidazol
DCE = 1,2-dicloroetano
DCM = diclorometano
DIBAL-H = hidruro de diisobutilaluminio
DIPEA = N,N-diisopropiletilamina
DMA = dimetilacetamida
DMF = dimetilformamida
EdCl = 3-(etiliminometilenoamino)-A/,W-dimetilpropan-1-amina
EtOAc = acetato de etilo
EtOH = alcohol etílico
HCl = ácido clorhídrico
HOAt = 1-hidroxi-7-azabenzotriazol
HATU = 3-oxid-hexafluorofosfato de 1 -[bis(dimetilamino)metileno]-1 H-1,2,3-triazolo[4,5-b]piridinio Min = minutos
pf = punto de fusión
MeOH = alcohol metílico
NaOH = hidróxido de sodio
NBS = N-bromosuccinimida
TFAA = anhídrido del ácido trifluoroacético
THF = tetrahidrofurano
Ejemplos de preparación
Por consiguiente, los compuestos de fórmula (I) pueden prepararse usando las técnicas sintéticas descritas tanto anteriormente como a continuación.
Ejemplo 1: Este ejemplo ilustra la preparación de N-metoxi-N-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]-acetamida (Compuesto 1.1 d la Tabla T1 a continuación).
Paso 1: Preparación de cloruro de 4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1benzoílo
Se suspendió ácido 4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzoico (4.00 g, 15.0 mmol) en diclorometano (90 ml), se añadió DMF (0.01 ml, 0.150 mmol) seguido de cloruro de oxalilo (1.46 ml, 16.5 mmol). La mezcla se calentó a reflujo durante 2 horas. La mezcla se evaporó a presión reducida para proporcionar 4.15 g de cloruro de 4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzoílo en forma de un sólido de color amarillo.
Paso 2: Preparación de N-metoxi-N-metil-4-[5-(trifluorometil)-1,2.4-oxadiazol-3-il1benzamida
Se añadió gota a gota una solución de cloruro de 4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzoílo del Paso 1 (4.15 g, 14.6 mmol) en diclorometano (20 ml) a temperatura ambiente a una solución en agitación de N-metoximetanamina (1.10 g, 17.5 mmol) y trietilamina (3.10 ml, 21.8 mmol) en diclorometano (80 ml). La mezcla se agitó a temperatura ambiente durante 18 horas. La mezcla de reacción se vertió en agua, se extrajo dos veces con diclorometano. Las fases orgánicas combinadas se lavaron con salmuera, se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el residuo en bruto resultante se sometió a cromatografía ultrarrápida sobre gel de sílice (heptano: EtOAc gradiente de elución 9:1 a 65:35) para proporcionar 4.12 g de N-metoxi-N-metil-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzamida en forma de un sólido. LC/MS (Método A) tiempo de retención = 0.97 minutos, 302 (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 8.18 (d, 2H), 7.84 (d, 2H), 3.56 (s,3H), 3.40 (s,3H).
Paso 3: Preparación de 4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzaldehído
En un matraz de múltiples bocas equipado de 75 ml equipado con un agitador, el termómetro a -78°C en argón, se añadió gota a gota DIBAL-H, 1.0M en tolueno (16 ml, 16.0 mmol) a una solución de N-metoxi-N-metil-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzamida (4.10 g, 13.3 mmol) en 2-metiltetrahidrofurano (90 ml). La mezcla se agitó dos horas a -78°C y durante una hora la temperatura se dejó incrementar a 0°C. La conversión completa se observó mediante LC-MS. La mezcla se inactivo añadiendo gota a gota una solución sat. de cloruro de amonio. Se produjo la precipitación de un sólido de color blanco. Se añadió HCl 4 M hasta la solubilización completa. La mezcla se extrajo tres veces con acetato de etilo. Los orgánicos combinados se secaron sobre sulfato de magnesio y se evaporaron para proporcionar el material en bruto en forma de un sólido de color beis. El material en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (hepatano: EtOAc gradiente de elución de 99:1 a 90:10) para proporcionar 2.93 g de 4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzaldehído en forma de un sólido de color blanco, pf: 40-50 2C.
1H RMN (400 MHz, CDCls) 5 ppm: 10.12 (s, 1H), 8.31 (d, 2H), 8.05 (d, 2H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.29 (s).
Paso 4: Preparación de N-metoxi-1-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-infenil]metanimina
Una solución de 4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzaldehído (0.30 g, 1.1 mmol) en metanol (11 ml) se trató a temperatura ambiente con piridina (0.15 ml, 1.9 mmol) seguido de adición de clorhidrato de O-metilhidroxilamina (0.15 g, 1.8 mmol). La mezcla se agitó a temperatura ambiente durante el fin de semana, se vertió en agua, se acidificó con HCl 1M y se extrajo tres veces con acetato de etilo. Los orgánicos combinados se lavaron con agua, se secaron sobre sulfato de magnesio y se evaporaron para proporcionar una resina. El material en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (hepatano: EtOAc gradiente de elución de 100:0 a 95:5) para proporcionar el compuesto del título en forma de un sólido de color blanco, pf: 55-65 °C.
1H RMN (400 MHz, CDCla) 5 ppm: 8.14 (s, 1H), 8.11 (d, 2H), 7.73 (d, 2H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.40 (s).
Paso 5: Preparación de N-metoxi-1-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1metanamina
Una solución de N-metoxi-1-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metanimina (0.81 g, 2.89 mmol) en ácido acético (11 ml) se trató a 15 °C ciano borohidruro de sodio (0.4 g, 6.1 mmol). La mezcla se agitó a 22 °C durante 18 horas hasta que se observó el consumo completo del material de partida. La mezcla de reacción se vertió cuidadosamente en una solución 0.1 M de NaOH. Mediante la adición de NaOH 1 M, el pH se ajustó a 12-13. La mezcla se extrajo cuatro veces con TBME. Los orgánicos combinados se lavaron dos veces con agua y una vez con salmuera, después se secaron sobre sulfato de magnesio y se concentraron a presión reducida. El aceite de color verde resultante se purificó mediante cromatografía ultrarrápida sobre gel de sílice (hepatano: EtOAc gradiente de elución de 99:1 a 70:30) para dar 0.60 g del compuesto del título en forma de un aceite.
1H RMN (400 MHz, CDCla) 5 ppm: 8.09 (d, 2H), 7.53 (d, 2H), 5.33 (Sa ,1H), 4.12 (s,2H), 3.50 (s,3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.32 (s).
Paso 6: Preparación de N-metoxi-N-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il1fenil1metil]-acetamida
A una solución en agitación de ácido acético (0.03 g, 0.49 mmol), EDCI (0.15 g, 0.76 mmol), HOAt (0.03 g, 0.19 mmol) y triethilamina (0.16 ml, 1.14 mmol) en diclorometano seco (2.9 ml) en una atmósfera de nitrógeno a temperatura ambiente, se le añadió N-metoxi-1-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metanamina (0.11 g, 0.38 mmol). La mezcla de reacción se agitó a temperatura ambiente durante 18 horas y después se añadieron HCl 1 M y diclorometano. La mezcla resultante se agitó y las fases se separaron. La fase acuosa se extrajo tres veces con diclorometano y las fases orgánicas combinadas se lavaron con salmuera, se sulfato de sodio, se filtraron y se evaporaron a sequedad. El aceite en bruto se purificó mediante cromatografía ultrarrápida sobre gel de sílice
(hepatano: EtOAc gradiente de elución de 99:1 a 80:20) para dar 0.08 g del compuesto del título en forma de un aceite transparente.
LC/MS (Método A) tiempo de retención = 0.98 minutos, 316.3 (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 8.09 (d, 2H), 7.47 (d, 2H), 4.86 (s, 2H), 3.68 (s,3H).
9F RMN (400 MHz, CDCla) 5 ppm: -65.34 (s).
Ejemplo 2 : Este ejemplo ilustra la preparación del intermedio 3-[4-(bromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol
Paso 1: Preparación de N'-hidroxi-4-metil-benzamidina
A una suspensión en agitación de 4-metilbenzonitrilo (35 g, 0.29 mol) en etanol (220 ml) y agua (440 ml) se la añadieron a temperatura ambiente clorhidrato de hidroxilamina (41.1 g, 0.58 mol), carbonato de potasio (65.4 g, 0.47 mol) y 8-hidroxiquinolina (0.22 g, 1.5 mmol). La mezcla de reacción se calentó a 80 °C durante 4 horas. La mezcla se enfrió a temperatura ambiente y se diluyó con HCl 2 N hasta pH 8. El etanol se evaporó a presión reducida. La mezcla se filtró, se lavó con agua y se secó al vacío para proporcionar 39.1 g del compuesto del título. LC/MS (Método A) tiempo de retención = 0.23 minutos, 151.0 (M+H).
Paso 2: Preparación de 3-(p-tolil)-5-(trifluorometil)-1,2,4-oxadiazol
A una solución en agitación de N'-hidroxi-4-metilbenzamidina (38.7 g, 0.25 mol) en 2-metiltetrahidrofurano (750 ml) se le añadió TFAA a 0 °C. La mezcla de reacción se agitó a 15 °C durante dos horas y se diluyó con agua. La fase orgánica se separó, se lavó sucesivamente con una solución de bicarbonato de sodio, una solución de cloruro de amonio y agua, se secó sobre sulfato de sodio, se filtró y se evaporó a sequedad. El producto en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (750 g de columna preempaquetada) con heptano/EtOAc de 99:1 a 90:10 para proporcionar 54.1 g del compuesto del título como un aceite transparente, el cual solidificó después de almacenarse.
LC/MS (Método A) tiempo de retención = 1.15 minutos, masa no detectada.
1H RMN (400 MHz, CDCls) 5 ppm: 8.00 (d, 2H), 7.32 (d, 2H), 2.45 (s,3H).
19F RMN (400 MHz, CDCls) 5 ppm: -65.41 (s).
Paso 3a: Preparación de 3-[4-(bromometil)fenil1-5-(trifluorometil)-1.2.4-oxadiazol
Una mezcla agitada de 3-(p-tolil)-5-(trifluorometil)-1,2,4-oxadiazol (56.0 g, 0.24 mol) y NBS (45.4 g, 0.25 mol) en tetraclorometano (480 ml) en argón se calentó hasta 70 °C. Se añadió AIBN (4.03 g, 24 mmol) y la mezcla de reacción se agitó a 65 °C durante 18 horas. La mezcla se enfrió a temperatura ambiente y se diluyó con diclorometano y agua. Las fases se separaron. Las fase orgánica se lavó con una solución de bicarbonato de sodio, se secó sobre sulfato de sodio, se filtró y se evaporó al vacío. El producto en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (columna preempaquetada de 750 g) con ciclohexano/EtOAc de 100:0 a 95:5 para proporcionar 44.7 g del compuesto del título como un sólido blanco, pf: 58-63 °C
1H RMN (400 MHz, CDCh) 5 ppm: 8.11 (d, 2H), 7.55 (d, 2H), 4.53 (s,2H).
19F RMN (400 MHz, CDCls) 5 ppm: -65.32 (s).
Se aisló 3-[4-(dibromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol como un subproduto en forma de un sólido de color blanco, pf: 61-66 °C.
1H RMN (400 MHz, CDCls) 5 ppm: 8.15 (d, 2H), 7.73 (d, 2H), 6.68 (s,1H).
19F RMN (400 MHz, CDCh) 5 ppm: -65.34 (s).
Paso 3b: Preparación de 3-[4-(bromometil)fenil1-5-(trifluorometil)-1.2.4-oxadiazol a partir de 3-[4-(dibromometil)fenil]-5-(trifluorometil)-1.2.4-oxadiazol
A una mezcla de 3-[4-(bromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol y 3-[4-(dibromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol (10.2 g), relación 1:9, en acetonitrilo (95 ml), agua (1.9 ml) y DlPEA (6.20 ml, 35.7 mol) se le añadió fosfito de dietilo (4.7 ml, 35.7 mmol) a 5 °C. La mezcla se agitó a 5-10 °C durante dos horas, se añadieron agua y HCl 1 M, y el acetonitrilo se evaporó a presión reducida. La suspensión de color blanco se extrajo tres veces con diclorometano. Las fases orgánicas combinadas se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el producto en bruto resultante se sometió a cromatografía ultrarrápida sobre gel de sílice (columna preempaquetada de 40 g) con ciclohexano/EtOAc de 99:1 a 9:1 para proporcionar 7.10 g de 3-[4-(bromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol.
1H RMN (400 MHz, CDCla) 5 ppm: 8.11 (d, 2H), 7.55 (d, 2H), 4.53 (s,2H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.32 (s).
Ejemplo 3 : Este ejemplo ilustra la preparación del intermedio N-propoxi-1-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metanamina
Una solución de 3-[4-(bromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol (1.30 g, 4.06 mmol) en diclorometano (10 ml), se añadió gota a gota a temperatura ambiente a una solución en agitación de clorhidrato de O-propilhidroxilamina (3.74 g, 32.5 mmol) y DIEA (6.40 ml, 36.6 mmol) en diclorometano (6 ml). La mezcla se agitó a temperatura ambiente durante 24 horas. La mezcla de reacción se vertió en agua y las fases se separaron. La fase acuosa se extrajo tres veces con diclorometano. Las fases orgánicas combinadas se lavaron con salmuera, se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el producto en bruto resultante se purificó mediante a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución de 1:0 a 1:1) para dar 0.92 g del compuesto del título en forma de un aceite transparente. LC/MS (Método A) tiempo de retención = 1.12 minutos, 302 (M+H).
1H RMN (400 MHz, CDCh) 5 ppm: 8.09 (d, 2H), 7.02 (d, 2H), 5.70 (sa ,1H), 4.11 (s,2H), 3.59 (m,2H), 1.52 (m,2H), 0.86 (s,3H).
19F RMN (400 MHz, CDCls ) 5 ppm: -65.33 (s).
Ejemplo 4 : Este ejemplo ilustra la preparación del intermedio N-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]etanamina.
Una solución de 3-[4-(bromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol (1.50 g, 4.69 mmol) en diclorometano (9.4 ml) se añadió gota a gota a temperatura ambiente a una solución en agitación de etilamina 2 M en MeOH (12 ml, 24.0 mmol). La mezcla se agitó a temperatura ambiente durante 24 horas. La mezcla de reacción se vertió en agua y las fases se separaron. La fase acuosa se extrajo tres veces con diclorometano. Las fases orgánicas combinadas se lavaron con salmuera, se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el producto en bruto resultante se purificó mediante a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución 1:0 a 1:1) para dar 0.92 g del compuesto del título en forma de un sólido de color blanco, pf: 102 112 °C, LC/MS (Método A) tiempo de retención = 0.66 minutos, 272 (M+H).
1H RMN (400 MHz, DMSO) 5 ppm: 8.01 (d, 2H), 7.57 (d, 2H), 3.86 (q,2H), 3.29 (sa ,1 H), 2.53 (q,2H), 1.05 (t,3H).
19F RMN (400 MHz, CDCls ) 5 ppm: -64.77 (s).
Ejemplo 5 : Este ejemplo ilustra la preparación del intermedio N-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]etanamina.
Una solución de 3-[4-(bromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol (1.50 g, 4.69 mmol) en diclorometano (9.4 ml) se añadió gota a gota a temperatura ambiente a una solución en agitación de sec-butilamina (2.4 ml, 23.4 mmol) en diclorometano (5 ml). La mezcla se agitó a temperatura ambiente durante 24 horas. La mezcla de reacción se vertió en agua y se extrajo tres veces con diclorometano. Las fases orgánicas combinadas se lavaron con salmuera, se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el residuo en bruto resultante se purificó mediante a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución 1:0 a 1:1) para dar 1.18 g del compuesto del título en forma de un aceite transparente, LC/MS (Método A) tiempo de retención = 0.71 minutos, 300 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 8.06 (d, 2H), 7.49 (d, 2H), 3.86 (q,2H), 2.62 (m,1 H), 1.53 (m,1 H), 1.49 (m,1 H), 1.09 (d,3H), 0.91 (m,3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.39 (s).
Ejemplo 6 : Este ejemplo ilustra la preparación del intermedio N-metoxi-1-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]etanamina.
Paso 1: Preparación de 4-[(E)-N-metoxi-C-metil-carbonimidoil1benzonitrilo
h 3c
Una solución de benzonitrilo de 4-acetilo (5.0 g, 33.8 mmol) en EtOH (270 ml) se trató a temperatura ambiente con clorhidrato de O-metilhidroxilamina (4.32 g, 50.6 mmol). La mezcla se agitó a temperatura ambiente durante 70 horas, se vertió en agua y se extrajo tres veces con diclorometano. Los orgánicos combinados se lavaron con agua, se secaron sobre sulfato de magnesio y se evaporaron para proporcionar 5.95 g del compuesto del título en forma de un aceite de color transparente. No se requirió purificación adicional. LC/MS (Método A) tiempo de retención = 0.93 minutos, 175 (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 7.78 (d, 2H), 7.65 (d, 2H), 4.03 (s, 3H), 2.22 (s, 3H).
Paso 2: Preparación de N'-hidroxi-4-[(E)-N-metoxi-C-metil-carbonimidoil1benzamidina
A una suspensión en agitación de 4-[(E)-N-metoxi-C-metil-carbonimidoil1benzonitrilo (5.95 g, 33.5 mmol) en etanol (50 ml) y agua (100 ml), se le añadió a temperatura ambiente clorhidrato de hidroxilamina (4.7 g, 66.9 mmol), carbonato de potasio (7.48 g, 53.6 mmol) y 8-hidroxiquinolina (0.025 g, 0.17mmol). La mezcla de reacción se calentó a 80°C durante 3 horas. La mezcla se enfrió a temperatura ambiente y se añadió HCl 1 M hasta pH 8-9. El etanol se retiró a presión reducida a 50 °C. La mezcla se agitó 30 minutos a 5 °C, se filtró, se lavó con agua y se secó al vacío para proporcionar 6.6 g del compuesto del título en forma de un sólido de color blanco, pf: 134-139 °C, LC/MS (Método A) tiempo de retención = 0.43 minutos, 208 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 8.23(sa ,1 H), 7.69 (d, 2H), 7.62 (d, 2H), 4.88 (sa, 2H), 4.00 (s, 3H), 2.23 (s, 3H).
Paso 3: Preparación de N-metoxi-1-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1etanimina
A una solución en agitación de N'-hidroxi-4-[(E)-N-metoxi-C-metil-carbonimidoil]benzamidina (6.46 g, 31.2 mmol) en 2-metiltetrahidrofurano (93 ml) se le añadió TFAA (6.24 ml, 43.7 mmol) a 15 °C. La mezcla de reacción se agitó a 15 °C durante dos horas y se diluyó con agua. La fase orgánica se separó y se lavó sucesivamente con una solución de bicarbonato de sodio, una solución de cloruro de amonio y agua, se secó sobre sulfato de sodio, se filtró y se evaporó
a sequedad para proporcionar 8.9 g del compuesto del título en forma de un sólido de color beis, pf: 56-61 °C, LC/MS (Método A) tiempo de retención = 1.19 minutos, 286 (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 8.13 (d, 2H), 7.81 (d, 2H), 4.03 (s, 3H), 2.25 (s, 3H).
19F RMN (400 MHz, CDCls) 5 ppm: -65.34 (s).
Paso 4: Preparación de N-metoxi-1-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1etanamina
Una solución de N-metoxi-1 -[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]etanimina (8.9 g, 29.6 mmol) en ácido acético (119 ml) se trató a 15°C en porciones con cianoborohidruro de sodio (4.12 g, 62.3 mmol). La mezcla se agitó a 23 °C durante 18 horas. Se observó el consumo parcial del material de partida. Se añadió en porciones cianoborohidruro adicional (4.12 g, 62.3 mmol). La mezcla de reacción se vertió cuidadosamente en una solución 0.1 M de hidróxido de sodio. Mediante la adición de NaOH 4 M se ajustó el pH a 9-12. La mezcla se extrajo cuatro veces con TBME. Los orgánicos combinados se lavaron dos veces con agua y una vez con salmuera, después se secaron sobre sulfato de magnesio y se concentraron a presión reducida. El aceite de color verde resultante se purificó mediante cromatografía ultrarrápida sobre gel de sílice (hepatano: EtOAc gradiente de elución de 99:1 a 70:30) para dar 5.0 g del compuesto del título en forma de un aceite. LC/MS tiempo de retención = 1.05 minutos, 288 (M+H).
1H RMN (400 MHz, CDCls ) 5 ppm: 8.10 (d, 2H), 7.51 (d, 2H), 5.65 (Sa ,1H), 4.22 (q,1H), 3.47 (s,3H), 1.38 (d,3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.37 (s).
Ejemplo 7 : Este ejemplo ilustra la preparación de la 1-[ciano-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]-3-metoxi-1,3-dimetil-urea (Compuesto 3.31 de la Tabla T3)
Paso 1: Preparación de 2-(metilamino)-2-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1acetonitrilo
A una solución en agitación de 4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]benzaldehído (2.5 g, 10.3 mmol) en THF (16 ml) se le añadió, se le añadió a temperatura ambiente, metilamina (0.38 g, 12.4 mmol). Después de 10 minutos se añadieron agua (51.6 ml) y cianhidrina de acetona (0. 8 g, 10.3 mmol). La mezcla se agitó durante toda la noche, se vertió en agua y se extrajo dos veces con acetato de etilo. Las fase orgánica se lavó sucesivamente con salmuera, se secó sobre sulfato de sodio, se filtró y se evaporó a sequedad. El producto en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice con ciclohexano/t-butilmetiléter 9:1 para proporcionar 2.1 g del compuesto del título en forma de un sólido de color blanco.
1H RMN (400 MHz, CDCls ) 5 ppm: 8.17 (d, 2H), 7.72 (d, 2H), 4.87 (s,1H), 2.61 (s,3H), 1.62 (Sa ,1 H).
Paso 2: Preparación de 1-[ciano-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-illfenillmetill-3-metoxi-1.3-dimetil-urea
A una solución en agitación de 2-(met¡lam¡no)-2-[4-[5-(tr¡fluoromet¡l)-1,2,4-oxad¡azol-3-¡l]fen¡l]acetonitr¡lo (0.17 g. 0.60 mmol) en diclorometano (5 ml) en una atmósfera de nitrógeno. se le añadieron a 0 °C. trietilamina (0.17 ml. 1.20 mmol). N.N-dimetilpiridin-4-amina (0.07 g. 0.60 mmol) seguido de cloruro de N.N-dimetilcarbamoilo (0.09 g. 0.72 mmol). La mezcla de reacción se agitó durante 18 horas a temperatura ambiente. se vertió en una solución 1 M de HCl y se extrajo con diclorometano. Las fases orgánicas combinadas se lavaron con NAOH 1 M. se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el residuo crudo resultante se sometió a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución de 7:1 a 5:1) para proporcionar 0.085 g de 1-[ciano-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il]fenillmetill-3-metoxi-1.3-dimetil-urea en forma de un sólido de color blanco. pf: 106-107 2C.
1H RMN (400 MHz. CDCla) 5 ppm: 8.20 (d. 2H). 7.67 (d. 2H). 6.57 (s.1H). 3.67 (s.3H). 3.11 (s.3H). 2.86 (s.3H).
Ejemplo 8 : Preparación de N-(oxetan-3-il)-N-[[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-illfenillmetillpropanamida (Compuesto 1.604 de la Tabla T1)
Paso 1: Preparación de N-[[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-illfenillmetilloxetan-3-amina
A una solución en agitación de 3-[4-(bromometil)fenill-5-(trifluorometil)-1.2.4-oxadiazol (2.0 g. 6.25 mmol) en diclorometano (13 ml). se le añadió gota a gota a temperatura ambiente N-etil-N-isopropil-propan-2-amina (1.1 ml) seguido de la adición de oxetan-3-amina (3.5 g. 50 mmol). La mezcla se agitó a temperatura ambiente durante 24 horas. La mezcla de reacción se vertió en agua y se extrajo tres veces con diclorometano. Las fases orgánicas combinadas se lavaron con salmuera. se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el residuo en bruto resultante se purificó mediante a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución de 1:0 a 0:1) para dar el compuesto del título en forma de un aceite transparente.
1H RMN (400 MHz. CDCla) 5 ppm: 8.08 (d. 2H). 7.48 (d. 2H). 4.80 (t.2H). 4.44 (t.2H). 4.04 (m.1H). 3.83 (s.2H). 2.01 (s.1H).
Paso 2: Preparación de N-(oxetan-3-il)-N-[[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-illfenillmetill propanamida
A una suspensión en agitación de N-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-illfenillmetilloxetan-3-amina (0.10 g. 0.33 mmol) en diclorometano (6 ml) en una atmósfera de nitrógeno. se le añadió trietilamina (0.09 ml. 0.66 mmol) a 0 °C seguido de cloruro de propanoílo (0.03 ml. 0.35 mmol). La mezcla de reacción se evaporó a presión reducida y el
residuo en bruto resultante se sometió a cromatografía ultrarrápida sobre gel de sílice (hepatano: EtOAc gradiente de elución de 9:1 a 1:9) para proporcionar el producto deseado forma de un sólido de color blanco, pf: 88.8 °C-93.5 °C.
Ejemplo 8 : N-(2,2,2-trifluoroetil)-N-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]tetrahidrofuran-2-carboxamida (Compuesto 1.587 de la Tabla T1)
Paso 1: Preparación de 2.2.2-trifluoro-N-[[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1metil1etanamina
A una solución en agitación de 3-[4-(bromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol (1.5 g. 4.69 mmol) en diclorometano (10 ml). se le añadió gota a gota a temperatura ambiente N-etil-N-isopropil-propan-2-amina (0.82 ml.
4.69 mmol) seguido de la adición de 2.2.2-trifluoroetanamina (2.94 g. 37.5 mmol). La mezcla se agitó a temperatura ambiente durante 24 horas. La mezcla de reacción se vertió en agua y se extrajo tres veces con diclorometano. Las fases orgánicas combinadas se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el residuo en bruto resultante se purificó mediante a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución de 1:0 a 0:1) para dar el compuesto del título en forma de un aceite transparente.
1H RMN (400 MHz. CDCla) 5 ppm: 8.09 (d. 2H). 7.51 (d. 2H). 4.00 (s.2H). 3.22 (q.2H). 1.71 (s.1H).
Paso 2: Preparación de N-(2.2.2-trifluoroetil)-N-[[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1metil1tetrahidrofuran-2-carboxamida
A una suspensión en agitación de 2.2.2-trifluoro-N-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1metil1etanamina (0.09 g. 0.27 mmol) en diclorometano (6 ml) en una atmósfera de nitrógeno. se le añadió trietilamina (0.08 mL. 0.55 mmol) a 0 °C seguido de cloruro de tetrahidrofuran-2-carbonilo (0.04 ml. 0.29 mmol). La mezcla de reacción se evaporó a presión reducida y el residuo en bruto resultante se sometió a cromatografía ultrarrápida sobre 12 g de gel de sílice preempaquetados (hepatano: EtOAc gradiente de elución de 9:1 a 1:9) para proporcionar el producto deseado en forma de un aceite de color amarillento transparente. LC/MS (Método A) tiempo de retención = 1.14 minutos. 424.3 (M+H).
Ejemplo 9: Este ejemplo ilustra la preparación N-[[3-fluoro-4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1metil1-N.2-dimetoxi-propanamida (Compuesto 1.783 de la Tabla T1)
Paso 1: Preparación de 2-fluoro-N'-hidroxi-4-metil-benzamidina
A una suspensión de 2-fluoro-4-metilbenzonitrilo (5 g, 37.0 mmol) en etanol (125 ml) a 25 °C se le añadió clorhidrato de hidroxilamina (7.7 g, 111 mmol). La mezcla de reacción se calentó a 80 °C durante 2 h. Después de enfriarse a temperatura ambiente, los volátiles se retiraron a presión reducida, proporcionando por lo tanto un sólido de color blanco que se usó en el siguiente paso sin ninguna purificación. LC/MS (Método A) tiempo de retención = 1.14 minutos, 169.2 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 7.96 (t, 1H), 7.11 (m, 2H), 2.45 (s, 3H).
Paso 2: Preparación de 3-(2-fluoro-4-metil-fenil)-5-(trifluorometil)-1.2.4-oxadiazol
A una solución de 2-fluoro-N'-hidroxi-4-metil-benzamidina (37 mmol) en tetrahidrofurano (122 ml) enfriada mediante un baño con hielo, se le añadió TFAA (7.71 ml, 55.5 mmol). La mezcla de reacción se agitó a 25 °C durante toda la noche y después se diluyó con agua. La fase orgánica se separó, se lavó sucesivamente con una solución de bicarbonato de sodio, una solución de cloruro de amonio y agua, se secó sobre sulfato de sodio, se filtró y se evaporó a sequedad. El producto en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice con ciclohexano/EtOAc de 99:1 a 1:1 para proporcionar el compuesto del título (6.6 g, rendimiento del 72%) en forma de un sólido amorfo de color blanco . LC/MS (Método A) tiempo de retención = 1.14 minutos, 247 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 8.00 (d, 1H), 7.32 (d, 2H), 2.45 (s, 3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.3 (s), 108.1 (s).
Paso 3a: Preparación de 3-[4-(bromometil)fenil1-5-(trifluorometil)-1.2.4-oxadiazol
Una mezcla agitada de 3-(2-fluoro-4-metil-fenil)-5-(trifluorometil)-1,2,4-oxadiazol (4.2 g, 17.1 mmol) y NBS (3.11 g, 17.1 mmol) en tetraclorometano (34.3 ml) en argón se calentó a 70 °C. Se añadió AIBN (0.29 g, 1.71 mmol) y la mezcla de reacción se agitó a 65 °C durante 18 h. La mezcla se enfrió a 25°C, después se diluyó con diclorometano y agua, después de lo cual las fases se separaron. El subproducto de succinimida se retiró por filtración, y el disolvente se retiró a presión reducida para proporcionar una goma de color pardo. Este residuo en bruto se sometió a cromatografía
ultrarrápida sobre gel de sílice (con cicIohexano/EtOAc de 100:0 a 4:1 para proporcionar el compuesto del título en forma de un sólido de color blanco (1.7 g, rendimiento del 31%. LC/MS (Método A) tiempo de retención = 1.13 minutos, no detectada (M+H).
1H RMN (400 MHz, CDCls ) 5 ppm: 8.09 (t, 1H), 7.34 (m, 2H), 4.49 (s, 2H).
9F RMN (400 MHz, CDCls ) 5 ppm: -65.18 (s), -106.2 (s).
Se aislaron 3-[4-(dibromometil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol en forma de un subproducto en la forma de un sólido de color beis (4.0 g, rendimiento del 58%) LC/MS (Método A) tiempo de retención = 1.20 minutos, no detectado (M+H).
1H RMN (400 MHz, CDCls ) 5 ppm: 8.14 (d, 1H), 7.52 (dd, 2H), 6.63 (s, 1H).
Paso 3b: Preparación de 3-[4-(bromometil)-2-fluoro-fenil1-5-(trifluorometil)-1,2,4-oxadiazol a partir de 33-[4-(dibromometil)-2-fluoro-fenil1-5-(trifluorometil)-1.2.4-oxadiazol
A una mezcla de 3-[4-(bromometil)-2-fluoro-fenil]-5-(trifluorometil)-1,2,4-oxadiazol y 3-[4-(dibromometil)-2-fluoro-fenil]-5-(trifluorometil)-1,2,4-oxadiazol (4.0 g, 9.9 mmol), relación 1:20, en acetonitrilo (37 ml), agua (0.8 ml) y DIPEA (2.59 ml, 14.8 mmol) a 5 °C se le añadió fosfito de dietilo (2.0 ml, 14.8 mmol). La mezcla se agitó a 5-10 °C durante 2 h, se añadieron agua y HCl 1 M y los volátiles se retiraron a presión reducida. La suspensión de color blanco se extrajo tres veces con diclorometano y las fases orgánicas combinadas se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el residuo en bruto de color naranja claro resultante se sometió a cromatografía ultrarrápida sobre gel de sílice con ciclohexano/EtOAc de 99:1 a 1:1 para proporcionar 3-[4-(bromometil)-2-fluoro-fenil]-5-(trifluorometil)-1,2,4-oxadiazol (2.2 g, rendimiento del 68%). LC/MS (Método A) tiempo de retención = 1.13 minutos, no detectada (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 8.09 (t, 1H), 7.34 (m, 2H), 4.49 (s, 2H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.18 (s), -106.2 (s).
Paso 4: Preparación de 1-[3-fluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il1fenil1-N-metoxi-metanamina
Una solución de clorhidrato de O-metilhidroxilamina (4.9 g, 59mmol) en diclorometano (15mL) se trató gota a gota con DIPEA (12 ml, 66 mmol) seguido de una solución de 3-[4-(bromometil)-2-flurorfenil]-5-(trifluorometil)-1,2,4-oxadiazol (1.2 g, 3.7 mmol) en diclorometano (5 ml). Después de 18h, se introdujo agua (10 ml) y los contenidos de la reacción se extrajeron dos veces con diclorometano y las fases orgánicas combinadas se secaron sobre sulfato de sodio y se filtraron. El residuo resultante se purificó mediante cromatografía ultrarrápida sobre gel de sílice (ciclohexano/EtOAc gradiente de elución de 1:0 a 1:1) para proporcionar 1 -[3-fluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]-N-metoximetanamina en forma de un aceite incoloro (410 mg, rendimiento del 38%). LC/MS (Método A) tiempo de retención = 1.01 minutos, no detectada (M+H).
1H RMN (400 MHz, CDCls ) 5 ppm: 8.05 (t, 1H), 7.45 (m, 2H), 5.85 (s a, 1H), 4.12 (s, 2H), 3.50 (s, 3H).
19F RMN (400 MHz, CDCls ) 5 ppm: -65.21 (s), -107.33 (s).
Paso 4: Preparación de N-[[3-fIuoro-4-[5-(trifIuorometiI)-1.2.4-oxadiazoI-3-iI1feniI1metiI1-N.2-dimetoxi-propanamida
A una solución en agitación de ácido 2-metoxi propanóico (0.01 g, 0.08 mmol) y HATU (0.03 g, 0.08 mmol en DMF (0.35 ml) en una atmósfera de nitrógeno a temperatura ambiente, se le introdujo N-etil-N-isopropil-propan-2-amina (0.2 ml, 1.03 mmol). Después de 5 minutos, se añadió 1-[3-fluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]-N-metoximetanamina (0.02 g, 0.07 mmol). Después de 2 horas, se introdujeron acetato de etilo y agua y las fases se separaron. La fase acuosa se extrajo con EtOAc y la fase orgánica combinada se lavó con salmuera, se secó sobre sulfato de sodio, se filtró y se evaporó a sequedad. Una goma de color blanco en bruto se purificó mediante cromatografía ultrarrápida sobre gel de sílice (cicloheptano: EtOAc gradiente de elución de 99:1 a 1:1) para dar N-[[3-fluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]-N,2-dimetoxi-propanamida (0.08 g, 35%) en forma de un aceite transparente. LC/MS (Método A) tiempo de retención = 1.02 minutos, 378 (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 8.06 (t, 1H), 7.25 (m, 2H), 4.96 (m, 1H), 4.83 (m, 1H), 4.28 (q, 1H), 3.71 (s, 3H), 3.38 (s, 3H), 1.26 (d, 3H).
19F RMN (400 MHz, CDCls) 5 ppm: -65.21 (s), -106.58 (s).
Ejemplo 10: Este ejemplo ilustra la preparación 1-[[3-fluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]-1-metoxi-3-metil-urea (Compuesto 3.45 de la Tabla T1)
A una solución de 1-[3-fluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]-N-metoxi-metanamina (20mg, 0.07 mmol) en DCM (0.23 ml, 0.07 mmol), se le añadió cloruro de N-metilcarbamoílo (0.012 g, 0.14 mmol) seguido de trietilamina (0.02 ml, 0.02 mmol). Después de 1 hora, la mezcla de reacción se concentró a presión reducida y el residuo se purificó mediante cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución de 99:1 a 1:1) para proporcionar 1-[[3-fluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]-1-metoxi-3-metil-urea (12 mg, rendimiento del 50%) en forma de una goma. LC/MS (Método A) tiempo de retención = 0.97 minutos, 349 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 8.04 (t, 1H), 7.31 (m, 2H), 5.81 (m, 1H), 4.71 (s, 2H), 3.60 (s, 3H), 2.87 (d, 3H).
19F RMN (400 MHz, CDCh) 5 ppm: -65.17 (s), -107.10 (s).
Ejemplo 11: Este ejemplo ilustra la preparación de 2-cloro-N-[[2,3-difluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]-N-metoxi-benzamida (Compuesto 1.576 de la Tabla T1)
Paso 1: Preparación de 2,3-difluoro-N'-hidroxi-4-metil-benzamidina
A una suspensión de 2,3-difluoro-4-metilbenzonitrilo (5.0 g, 32.6 mmol) en etanol (111 ml) a 25 °C, se le añadió clorhidrato de hidroxilamina (4.5 g, 65.3 mmol). La mezcla de reacción se calentó a 80 °C durante 2 h. Después de enfriarse a temperatura ambiente, los volátiles se retiraron a presión reducida, proporcionando por lo tanto un sólido de color blanco que se usó en el siguiente paso sin purificación.
1H RMN (400 MHz, CDCh) 5 ppm: 7.30 (m, 1H), 6.95 (m, 1H), 6.50 (s a, 1H), 5.05 (s a, 2H), 2.30 (s, 3H).
Paso 2: Preparación de 3-(2,3-difluoro-4-metil-fenil)-5-(trifluorometil)-1,2,4-oxadiazol
A una solución de 2,3-difluoro-N'-hidroxi-4-metil-benzamidina (2.6 mmol) en tetrahidrofurano (108 ml) enfriada usando un baño con hielo, se le añadió TFAA (6.9 ml, 49 mmol). La mezcla de reacción se agitó a 25 °C durante toda la noche y después se diluyó con agua. La fase orgánica se separó, se lavó sucesivamente con una solución de bicarbonato de sodio, una solución de cloruro de amonio y agua, se secó sobre sulfato de sodio, se filtró y se evaporó a sequedad. El compuesto del título en bruto (6.6 g, rendimiento del 72%) se aisló en forma de un sólido de color pardo claro que se usó en la siguiente transformación sin purificación adicional. LC/MS (Método A) tiempo de retención = 1.16 minutos, 265 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 7.76 (d, 1H), 7.12 (d, 1H), 2.41 (s, 3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.41 (s), -133.3 (s), -140.1 (s).
Paso 3: Preparación de 3-[4-(bromometil)-2.3-difluoro-fenil1-5-(trifluorometil)-1.2.4-oxadiazol
Una mezcla de 3-(2,3-difluoro-4-metil-fenil)-5-(trifluorometil)-1,2,4-oxadiazol (6.0 g, 22.6 mmol) y NBS (7.17 g, 10.0 mmol) en tetraclorometano (79 ml) en argón se calentó a 70 °C. Se añadió AIBN (0.68 g, 3.95 mmol) y la mezcla de reacción se agitó a 65 °C durante 36 h. La mezcla se enfrió a 25 °C, se diluyó con diclorometano y agua y las fases se separaron. El subproducto de succinimida se retiró por filtración, y el disolvente se retiró al vacío ,para proporcionar
una goma de color pardo. Este residuo en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (cicIohexano/EtOAc gradiente de elución de 100:0 a 4:1 para proporcionar el compuesto del título en forma de un sólido de color blanco (4.8 g, rendimiento del 72%. LC/MS (Método A) tiempo de retención = 1.16 minutos, 344 (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 7.80 (m, 1H), 7.37 (m, 1H), 4.55 (s, 2H).
9F RMN (400 MHz, CDCls) 5 ppm: -65.1 (s), -131.2 (s), -139.1 (s).
Paso 4: Preparación de 1-[2.3-difluoro-4-[5-(trifluorometin-1.2.4-oxadiazol-3-il1fenil1-N-metoxi-metanamina
Una solución de clorhidrato de O-metilhidroxilamina (3.5g, 42 mmol) en diclorometano (8 ml) se trató gota a gota con DIPEA (8.3 ml, 47 mmol) seguido de una solución de 3-[4-(bromometil)-2,3-difluoro-fenil]-5-(trifluorometil)-1,2,4-oxadiazol (2 g, 5.2 mmol) en diclorometano (5 ml). Después de 18h, se introdujo agua (10 ml) y los contenidos de la reacción se extrajeron dos veces con diclorometano y las fases orgánicas combinadas se secaron sobre sulfato de sodio y se filtraron. El residuo resultante se purificó mediante cromatografía ultrarrápida sobre gel de sílice (ciclohexano/EtOAc gradiente de elución de 1:0 a 1:1) para proporcionar 1-[2,3-difluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il1fenil1-N-metoxi-metanamina en forma de un aceite de color amarillo pálido (1.1 g, rendimiento del 68%). LC/MS (Método A) tiempo de retención = 1.03 minutos, 310 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 7.84 (t, 1H), 7.38 (t, 1H), 5.87 (s a, 1H), 4.20 (s, 2H), 3.52 (s, 3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.21 (s), -132.53 (s), -147.50 (s).
Paso 5: Preparación de 2-cloro-N-[[2,3-difluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il1fenil1metil1-N-metoxibenzamida
Una solución transparente de 1-[2,3-difluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il1fenil1-N-metoxi-metanamina (0.150 g, 0.485 mmol) y DCM (3 ml) se trató con trietilamina (0.13 ml, 0.970 mmol) seguido de cloruro de 2-clorobenzoílo (80 mg, 0.51 mmol). Después de 2 h, se añadió soluto a la mezcla de reacción y los volátiles se retiraron a presión reducida. El producto en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice con ciclohexano/EtOAc de 99:1 a 1:1 para proporcionar 2-cloro-N-[[2,3-difluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il1fenil1metil1-N-metoxi-benzamida (212mg, rendimiento del 98%) en forma de un aceite incoloro. LC/MS (Método A) tiempo de retención = 1.16 minutos, 448 (M+H).
1H RMN (400 MHz, CDCh) 5 ppm: 7.88 (m, 1H), 7.54 (m, 1H), 7.40 (m, 4H), 5.14 (s a, 2H), 3.52 (s a, 3H).
19F RMN (400 MHz, CDCh) 5 ppm: -65.21 (s), -131.98 (s), -141.10 (s).
Ejemplo 12: Este ejemplo ilustra la preparación de N-metoxi-N-[[5-[5-(trifluorometil)-1,2,4-oxadiazol-3-il1-2-piridil1metil1ciclopropanocarboxamida (Compuesto 1.570 de la Tabla T1).
Paso 1: Preparación de N'-hidroxi-6-metil-piridin-3-carboxamidina
A una suspensión de 5-ciano-2-picolina (3 g, 25.0 mmol) en etanol (86 ml) a 25 °C, se le añadió clorhidrato de hidroxilamina (5.3 g, 76 mmol). La mezcla de reacción se calentó a 80 °C durante 2 h. Después de enfriarse a temperatura ambiente, los volátiles se retiraron a presión reducida, proporcionando por lo tanto un sólido de color blanco que se usó en el siguiente paso sin ninguna purificación. LC/MS (Método A) tiempo de retención = 0.17 minutos, 152 (M+H).
1H RMN (400 MHz, CDCh) 5 ppm: 8.75 (s, 1H), 7.83 (d, 1H), 7.19 (d, 1H), 4.86 (s a, 2H), 2.63 (s, 3H).
Paso 2: Preparación de 3-(6-metil-3-piridil)-5-(trifluorometil)-1.2.4-oxadiazol
A una solución de N'-hidroxi-6-metil-piridin-3-carboxamidina (25 mmol) en tetrahidrofurano (84 ml) enfriada mediante un baño con hielo, se le añadió TFAA (5.28 ml, 38.0 mmol). La mezcla de reacción se agitó a 25 °C durante toda la noche y después se diluyó con agua. La fase orgánica se separó, se lavó sucesivamente con una solución de bicarbonato de sodio, una solución de cloruro de sodio y agua, después se secó sobre sulfato de sodio, se filtró y se evaporó a sequedad para proporcionar 3-(6-metil-3-piridil)-5-(trifluorometil)-1,2,4-oxadiazol (5.8 g, rendimiento del 84%) en forma de un sólido de color blanco amorfo. LC/MS (Método A) tiempo de retención = 1.14 minutos, 247 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 9.23 (d, 1H), 8.27 (dd, 1H), 7.33 (d, 1H), 2.63 (s, 3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.3 (s).
Paso 3: Preparación de 3-[6-(bromometil)-3-piridil1-5-(trifluorometil)-1.2.4-oxadiazol
Una solución de 3-(6-metil-3-piridil)-5-(trifluorometil)-1,2,4-oxadiazol (4.4 g, 19 mmol), AIBN (0.32 g, 1.9 mmol) y tetraclorometano (38 ml) en argón, se calentó a 65 °C. Se añadió en porciones NBS (3.11 g, 17.1 mmol) y la mezcla de reacción se agitó a 65 °C durante 5 h y después un segundo equivalente de NBS (3.11 g, 17.1 mmol) y se continuó agitando durante toda una noche. La mezcla se enfrió a 25 °C, después se diluyó con diclorometano y agua, después de lo cual las fases se separaron. El subproducto de succinimida se retiró por filtración, y el disolvente se retiró a presión reducida para proporcionar una goma de color pardo. Este residuo en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (ciclohexano/EtOAc gradiente de elución de 100:0 a 4:1 para proporcionar 3-[6
(bromometil)-3-piridil]-5-(trifluorometil)-1,2,4-oxadiazol en forma de un sólido de color blanco (5.9 g, rendimiento del 37%. LC/MS (Método A) tiempo de retención = 1.01 minutos, 308 (M+H).
1H RMN (400 MHz, CDCls) 5 ppm: 9.30 (d, 1H), 8.40 (dd, 1H), 7.63 (d, 1H), 4.62 (s, 2H).
19F RMN (400 MHz, CDCls) 5 ppm: -65.2 (s).
Paso 4: Preparación de N-metoxi-1-[5-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1-2-piridil1metanamina
Una solución de clorhidrato de O-metilhidroxilamina (4.4 g, 52 mmol) en diclorometano (26 ml) se trató gota a gota con DIPEA (10.3 ml, 58 mmol) seguido de una solución de 33-[6-(bromometil)-3-piridil]-5-(trifluorometil)-1,2,4-oxadiazol (2 g, 6.5 mmol) en diclorometano (10 ml). Después de 18 h, se introdujeron equivalentes adicionales de clorhidrato de O-metilhidroxilamina (4.4 g, 52 mmol) y DIPEA (10.3 ml, 58 mmol) y la reacción se calentó a 40 °C durante 48 h. Se introdujo agua (50 ml) y los contenidos de la reacción se extrajeron dos veces con diclorometano y las fases orgánicas combinadas se secaron sobre sulfato de sodio y se filtraron. El residuo resultante se purificó mediante cromatografía ultrarrápida sobre gel de sílice (ciclohexano/EtOAc gradiente de elución de 1:0 a 1:1) para proporcionar 1 -[2,3-difluoro-4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]-N-metoxi-metanamina en forma de un sólido de color amarillo pálido (1.4 mg, rendimiento del 79%). LC/MS (Método A) tiempo de retención = 0.87 minutos, 275 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 9.31 (s, 1H), 8.37 (d, 1H), 7.52 (d, 1H), 6.42 (s a, 1H), 4.24 (s, 2H), 3.56 (s, 3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.25 (s).
Paso 5: Preparación de ciclopropanocarboxamida de N-metoxi-N-[[5-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]-2-piridil]metilo]
Una solución transparente de N-metoxi-1-[5-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]-2-piridil]metanamina (0.10 g, 0.36 mmol) y DCM (2 ml) se enfrió a 0 °C, se trató con trietilamina (0.10 ml, 0.73 mmol) seguido de cloruro de ciclopropanocarbonilo (38 mg, 0.36 mmol). Después de 2 h, se añadió soluto a la mezcla de reacción y los volátiles se retiraron a presión reducida. El producto en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (ciclohexano/EtOAc gradiente de elución de 99:1 a 1:1) para proporcionar N-metoxi-N-[[5-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]-2-piridil]metil]ciclopropanocarboxamida (212 mg, rendimiento del 98%) en forma de un aceite incoloro. LC/MS (Método A) tiempo de retención = 1.16 minutos, 448 (M+H).
1H RMN (400 MHz, CDCh) 5 ppm: 7.88 (m, 1H), 7.54 (m, 1H), 7.40 (m, 4H), 5.14 (s a, 2H), 3.52 (s a, 3H).
19F RMN (400 MHz, CDCh) 5 ppm: -65.21 (s), -131.98 (s), -141.10 (s).
Ejemplo 13: Este ejemplo ilustra la preparación de N-metoxi-N-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]carbamato de metilo (Compuesto 2.3 de la Tabla T2)
A una solución de N-metoxi-1-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metanamina (0.10 g, 0.37 mmol) en DCM (1.2 ml) se le añadió cloroformiato de metilo (0.06 ml, 0.732 mmol) y trietilamina (0.10 ml, 0.73 mmol). La mezcla de reacción se agitó durante 1 h 30 min a temperatura ambiente, tiempo después del cual el disolvente se retiró a presión reducida y el residuo en bruto resultante se purificó mediante cromatografía combiflash sobre gel de sílice (ciclohexano/EtOAc gradiente de elución de 1:0 a 1:1) para dar N-metoxi-N-[[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]metil]carbamato de metilo (0.105 g, rendimiento del 87%) en forma de un aceite de color amarillo. LC/MS (Método A) tiempo de retención = 1.06 minutos, 332 (M+H).
1H RMN (400 MHz, CDCh) 5 ppm: 8.04 (d, 2H), 7.42 (d, 2H), 4.64 (s, 2H), 3.75 (s, 3H), 3.57 (s, 3H).
19F RMN (400 MHz, CDCla) 5 ppm: -65.33 (s).
Ejemplo________14: Preparación de N-isopropil-N-[2-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]etil]ciclopropanocarboxamida (Compuesto 1.810 de la Tabla T1)
Paso 1: Preparación de 4-(2-bromoetil)-N'-hidroxi-benzamidina
A una solución en agitación de 4-(2-bromoetil)benzonitrilo (5 g, 24 mmol) en etanol (80 ml), se le añadieron a temperatura ambiente, trietilamina (15 ml, 110 mmol) y clorhidrato de hidroxilamina (3.3 g, 48 mmol). Después de 6 horas, el disolvente se evaporó a presión reducida para proporcionar el compuesto del título en forma de un sólido que se usó sin purificación adicional.
Paso 2: Preparación de 3-[4-(2-bromoetil)fenil1-5-(trifluorometil)-1.2.4-oxadiazol
A una suspensión en agitación de 4-(2-bromoetil)-N'-hidroxi-benzamidina en bruto (24 mmol) en 2-metiltetrahidrofurano (150 ml), se le añadió TFAA (10 ml, 71 mmol) a 0 °C. La mezcla de reacción se agitó a 25 °C durante 15 horas y después se diluyó con agua (100 ml), seguido de extracción con EtOAc. Las fases orgánicas se separaron, se lavaron sucesivamente con una solución acuosa saturada de bicarbonato de sodio y agua, se secaron sobre sulfato de sodio, se filtraron y se evaporaron a sequedad a presión reducida. El residuo en bruto se sometió a cromatografía ultrarrápida sobre gel de sílice (ciclohexano/EtOAc gradiente de elución de 95:5) para proporcionar 3
[4-(2-bromoetil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol (4.93 g, rendimiento del 65%) en forma de un sólido de color blanco p.f 39-40 °C. LC/MS (Método A) tiempo de retención = 1.19 minutos, masa no detectada.
1H RMN (400 MHz, CDCls) 5 ppm: 8.07 (d, 2H), 7.37 (d, 2H), 3.61 (t, 2H), 3.25 (t, 2H).
Paso 3: Preparación de N-[2-[4-[5-(trifluorometil)-1.2.4-oxadiazol-3-il1fenil1etil]propan-2-amina
A una solución en agitación de 3-[4-(2-bromoetil)fenil]-5-(trifluorometil)-1,2,4-oxadiazol (1.5 g, 4.40 mmol) en diclorometano (10 ml), se le añadió gota a gota a temperatura ambiente N-etil-N-isopropil-propan-2-amina (0.76 ml, 4.40 mmol) seguido de la adición de isopropilamina (9.2 ml, 110 mmol). La mezcla se agitó a temperatura ambiente durante 37 horas, después se vertió en agua y se extrajo tres veces con EtOAc. Las fases orgánicas combinadas se lavaron con salmuera, se secaron sobre sulfato de sodio y se filtraron. El disolvente se retiró a presión reducida y el residuo en bruto resultante se purificó mediante a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución de 98:2 a 95:5) para dar N-[2-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]etil]propan-2-amina (530 mg, rendimiento del 44%) en forma de un aceite transparente. LC/MS (Método A) tiempo de retención = 0.75 minutos, 300.5 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 8.05 (d, 2H), 7.37 (d, 2H), 2.91 (m, 4H), 2.85 (m, 1H), 1.06 (d, 6H).
Paso 4: Preparación de N-isopropil-N-[2-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-infeninetinciclopropanocarboxamida
A una suspensión en agitación de N-[2-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]etil]propan-2-amina (0.075 g, 0.25 mmol) en diclorometano (5 ml) en una atmósfera de nitrógeno, se le añadió trietilamina (0.04 mL, 0.30 mmol) a 0 °C seguido de cloruro de ciclopropanocarbonilo (0.024 ml, 0.26 mmol). La mezcla de reacción se agitó a temperatura ambiente durante 17 horas, se vertió en agua y se extrajo dos veces con EtOAc. Las fases orgánicas combinadas se lavaron con salmuera, se secaron sobre sulfato de sodio y se filtraron. El disolvente se evaporó a presión reducida y el residuo crudo resultante se sometió a cromatografía ultrarrápida sobre gel de sílice (ciclohexano: EtOAc gradiente de elución de 3:1 a 2:1) para proporcionar N-isopropil-N-[2-[4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]fenil]etil]ciclopropanocarboxamida (89mg, rendimiento del 96%) en forma de un sólido de color blanco. LC/MS (Método A) tiempo de retención = 1.17 minutos, 368.5 (M+H).
1H RMN (400 MHz, CDCla) 5 ppm: 8.06 (m, 2H), 7.38 (m, 2H), 4.79 (m, 0.5H), 4.47 (m, 0.5H), 3.58 (m, 1H), 3.40 (m, 1H), 3.05 (m, 1H), 2.95( m, 1H), 1.76 (m, 1H), 1.29 (m, 3H), 1.13 (d, 3H), 1.04 (m, 1H), 0.83 (m, 2H).
El siguiente procedimiento se utilizó de manera combinatoria utilizando los componentes básicos apropiados (compuestos (II) y (III)) para proporcionar los compuestos de Fórmula (I) donde R8 es -C(O)R9. Los compuestos preparados mediante el siguiente protocolo combinatorio se analizaron usando el Método B de LC/MS.
A modo de ejemplo, los derivados de ácido de fórmula (III) (0.0375 mmol en 375 pl de DMA) se transfirieron a una placa con pocillos profundos con 96 ranuras (DWP96) que contenía el derivado de tipo [4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]aril]metanamina de fórmula (II) (0.03 mmol) y DIPEA (0.09 mmol) en 250 pl de DMA y acto seguido se añadió BOP-Cl (0.06 mmol) disuelto en d Ma (250 pl). La DWP se selló herméticamente y se agitó a 50 °C durante 18 horas. El disolvente se retiró con una corriente de nitrógeno. Los residuos en bruto resultantes se solubilizaron en una mezcla de MeOH (250 pl) y DMA (500 pl) y se sometieron directamente a la purificación por LC/MS preparativa que proporcionó los compuestos de fórmula (I) con rendimientos de un 10-85%.
Como alternativa, los siguientes procedimientos (protocolo A y protocolo B) se usaron de manera combinatoria usando los componentes básicos apropiados (compuestos (II) y (IV)) para proporcionar los compuestos de Fórmula (I) donde R8 es -C(O)OR10 o -C(O)NR11R12. Los compuestos preparados mediante el siguiente protocolo combinatorio se analizaron usando el Método B de LC/MS.
Protocolo A : Se transfirieron porciones de trifosgeno (6 mg) en DCE (0.3 ml) a 0 °C a una placa de pocillos profundos con 96 ranuras (DWP96) que contenía el derivado de tipo alcohol [HOR10] o el derivado de tipo amina [HN(R11)R12] de fórmula (IV) (0.05 mmol) y trietilamina (0.12 mmol) en 200 pl de DMA. Las mezclas de reacción se agitaron a temperatura ambiente durante 30 minutos. Se añadieron los derivados de tipo [4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]aril]metanamina de fórmula (II) (0.05 mmol) y trietilamina (0.12 mmol) en 200 pl de DMA. La DWP se selló herméticamente y se agitó a temperatura ambiente durante 18 horas. El DCE se retiró en la estación Barkey. Los residuos en bruto se solubilizaron en una mezcla de MeOH (200 pl) y DMA (600 pl) y se sometieron directamente a la purificación por LC/MS preparativa que proporcionó los compuestos de fórmula (I) con rendimientos de un 3-45%.
Protocolo B : El derivado de tipo alcohol [HOR10] o el derivado de tipo amina [HNR11R12] de fórmula (IV) (0.05 mmol) y DIPEA (0.25 mmol) en 300 pl de DMA se transfirieron a temperatura ambiente a una placa con pocillos profundos con 96 ranuras (DWP96). Se añadió CDI (0.10 mmol) en DMA (300 pl) y se agitó hasta que se logró la solubilización. Se añadieron los derivados de tipo [4-[5-(trifluorometil)-1,2,4-oxadiazol-3-il]aril]metanamina de fórmula (II) (0.05 mmol) y trietilamina (0.12 mmol) en 200 pl de DMA. La DWP se selló herméticamente y se agitó a temperatura ambiente durante 18 horas. El DCE se retiró en la estación Barkey. Los residuos en bruto se solubilizaron en una mezcla de MeOH (200 pl) y DMA (600 pl) y se sometieron directamente a la purificación por LC/MS preparativa que proporcionó los compuestos de fórmula (I) con rendimientos de un 5-47%.
Cuando sea necesario, pueden obtenerse los compuestos finales enantioméricamente puros a partir de los materiales racémicos según proceda mediante técnicas de separación físicas habituales tales como cromatografía quiral de fase inversa o mediante técnicas sintéticas estereoselectivas, (por ejemplo, utilizando materiales de partida quirales).
Tabla T1: Datos de puntos de fusión (pf) y/o tiempos de retención (TR) para compuestos de acuerdo con la Fórmula UL
Tabla T2: Datos de puntos de fusión (pf) y/o tiempos de retención (TR) para compuestos de acuerdo con la Fórmula rn¡
Tabla T3: Datos de puntos de fusión (pf) y/o tiempos de retención (TR) para compuestos de acuerdo con la Fórmula rn¡
EJEMPLOS BIOLÓGICOS:
Ejemplos generales de pruebas en disco foliar en placas de pocilios:
A partir de plantas cultivadas en un invernadero, se cortan discos foliares o segmentos foliares de varias especies vegetales. Los discos o segmentos foliares cortados se colocan en placas de múltiples pocillos (formato de 24 pocillos) sobre agua-agar. Se pulveriza una solución de prueba sobre los discos foliares antes (prevención) o después (curación) de la inoculación. Los compuestos que se van a probar se preparan como soluciones en DMSO (máx. de 10 mg/mL), que se diluyen hasta la concentración apropiada con Tween20 al 0.025% justo antes de la pulverización. Los discos o segmentos foliares inoculados se incuban en condiciones definidas (temperatura, humedad relativa, luz, etc.) de acuerdo con el sistema de prueba respectivo. Se realiza una única evaluación del nivel de la enfermedad de 3 a 14 días después de la inoculación, dependiendo del patosistema. A continuación, se calcula el porcentaje de control de la enfermedad respecto a los discos o segmentos foliares de muestras de referencia no tratadas.
Ejemplos generales de pruebas en cultivo líquido en placas de pocillos:
En un caldo de nutrientes se mezclan directamente fragmentos de Mycelia o suspensiones de conidios de un hongo, recién preparados a partir de cultivos líquidos del hongo o preparados a partir de un depósito criogénico. Las soluciones del compuesto de prueba en DMSO (máx. de 10 mg/ml) se diluyen con Tween20 al 0.025% en un factor de 50 y se pipetean 10 pl de esta solución a una placa de microvaloración (formato de 96 pocillos). A continuación, se añade el caldo de nutrientes que contiene las esporas/fragmentos de micelios fúngicos para obtener la concentración final del compuesto de prueba. Las placas de prueba se incuban en la oscuridad a 24 °C y un 96% de humedad relativa. La inhibición del crecimiento fúngico se determina fotométricamente después de 2 a 7 días, dependiendo del patosistema, y se calcula el porcentaje de actividad antifúngica respecto a la muestra de referencia no tratada.
Actividad fungicida contra Puccinia recondita f. sp. tritic i/ trigo / prevención en disco foliares (roya parda)
Se colocan segmentos de hojas de trigo cv. Kanzler sobre agar en placas de múltiples pocillos (formato de 24 pocillos) y se pulverizó el compuesto de prueba formulado diluido en agua sobre estos. Los discos de hoja fueron inoculados con una suspensión de esporas del hongo 1 día después de la aplicación. Los segmentos foliares inoculados se incubaron a 19 °C y un 75% de humedad relativa (HR) con un régimen de luz de 12 h de luz / 12 h de oscuridad en una cámara climática, y se determinó la actividad de un compuesto como el porcentaje de control de la enfermedad, en comparación con los segmentos foliares no tratados, cuando aparece un nivel apropiado de daños debidos a la enfermedad en segmentos foliares de control no tratados (de 7 a 9 días después de la aplicación).
Los siguientes compuestos proporcionan al menos un 80% de control de la enfermedad en esta prueba a 200 ppm en la formulación aplicada, cuando se comparan con los discos foliares de control no tratados en las mismas condiciones, los cuales presentan un desarrollo considerable de la enfermedad.
Compuestos (de la Tabla T1) 1.1, 1.2, 1.3, 1.4, 1.6, 1.8,, 1.10, 1.11, 1.12, 1.15, 1.16 , 1.17, 1.19, 1.20, 1.22, 1.24, 1.25, 1.26, 1.27, 1.28, 1.29, 1.30, 1.31, 1.32, 1.33, 1.34, 1.35 , 1.36, 1.38, 1.40, 1.41, 1.42 , 1.43, 1.44, 1.45, 1.46, 1.47, 1.48, 1.49, 1.50, 1.51, 1.52, 1.53, 1.54, 1.57, 1.59, 1.60, 1.62 , 1.64, 1.67, 1.69, 1.77, 1.81 , 1.83, 1.86, 1.87, 1.89, 1.90, 1.91, 1.92, 1.93, 1.!95, 1.97, 1.99, 1.100, 1.101, 1.102, 1.103, 1.104, 1.105, 1.106, 1.107, 1.109, 1.110, 1.111, 1.112, 1.113, 1.114, 1.115, 1.117, 1.118, 1.119, 1.120, 1.121, 1.122, 1.123, 1.124, 1.125, 1.126, 1.127, 1.128, 1.129, 1.130, 1.132, 1.133, 1.134, 1.135, 1.136, 1.138, 1.139, 1.140, 1.141, 1.142, 1.143, 1.144, 1.145, 1.146, 1.147, 1.149, 1.150, 1.151, 1.152, 1.154, 1.155, 1.157, 1.158, 1.159, 1.161, 1.162, 1.164, 1.165, 1.167, 1.168, 1.169, 1.170, 1.171, 1.172, 1.173, 1.175, 1.176, 1.177, 1.178, 1.180, 1.181, 1.182, 1.183, 1.184, 1.185, 1.186, 1.187, 1.188, 1.189, 1.190, 1.191, 1.192, 1.193, 1.194, 1.196, 1.198, 1.199, 1.200, 1.201, 1.202, 1.205, 1.206, 1.209, 1.212, 1.214, 1.215, 1.216, 1.217, 1.218, 1.219, 1.221, 1.222, 1.223, 1.225, 1.226, 1.227, 1.229, 1.230, 1.233, 1.234, 1.235, 1.237, 1.238, 1.242, 1.243, 1.244, 1.245, 1.247, 1.248, 1.249, 1.250, 1.251, 1.252, 1.253, 1.258, 1.259, 1.260, 1.264, 1.266, 1.270, 1.273, 1.274, 1.275, 1.276, 1.279, 1.280, 1.283, 1.287, 1.298, 1.305, 1.306, 1.308, 1.309, 1.312, 1.313, 1.314, 1.315, 1.316, 1.320, 1.323, 1.324, 1.325, 1.326, 1.327, 1.328, 1.329, 1.330, 1.331, 1.332, 1.333, 1.334, 1.335, 1.336, 1.337, 1.338, 1.339, 1.340, 1.341, 1.342, 1.344, 1.345, 1.346, 1.347, 1.348, 1.350, 1.351, 1.352, 1.353, 1.354, 1.355, 1.356, 1.357, 1.358, 1.359, 1.360, 1.361, 1.362, 1.363, 1.364, 1.365, 1.366, 1.367, 1.368, 1.369, 1.370, 1.371, 1.372, 1.373, 1.374, 1.375, 1.376, 1.378, 1.379, 1.383, 1.384, 1.387, 1.388, 1.389, 1.390, 1.391, 1.392, 1.395, 1.396, 1.398, 1.399, 1.400, 1.401, 1.402, 1.403, 1.404, 1.405, 1.406, 1.407, 1.408, 1.410, 1.411, 1.412, 1.413, 1.414, 1.415, 1.416, 1.417, 1.418, 1.421, 1.422, 1.423, 1.424, 1.426, 1.427, 1.430, 1.431, 1.432, 1.433, 1.434, 1.435, 1.436, 1.437, 1.438, 1.440, 1.441, 1 .4 4 2 , 1 .443, 1.446, 1.447, 1.448, 1.449, 1.450, 1.451, 1.452, 1.453, 1.456, 1.457, 1.458, 1.459, 1.460, 1.461, 1.462, 1.463, 1.464, 1.465, 1.466, 1.467, 1.468, 1.469, 1.471, 1.472, 1.473, 1.474, 1.475, 1.476, 1.477, 1.478, 1.479, 1.480, 1.481, 1.482, 1.483, 1.484, 1.485, 1.486, 1.487, 1.488, 1.489, 1.490, 1.491, 1.492, 1.493, 1.494, 1.495, 1.496, 1.497, 1.498, 1.499, 1.500, 1.501, 1.502, 1.503, 1.504, 1.505, 1.506, 1.507, 1.508, 1.509, 1.510, 1.511, 1.512, 1.513, 1.514, 1.515, 1.516, 1.517, 1.518, 1.519, 1.520, 1.521, 1.522, 1.523, 1.524, 1.525, 1.526, 1.527, 1.528, 1.529, 1.530, 1.531, 1.532, 1.537, 1.550, 1.552, 1.562, 1.563, 1.564, 1.565, 1.566, 1.567, 1.569, 1.570, 1.572, 1.573, 1.574, 1.575, 1.576, 1.577, 1.578, 1.579, 1.580, 1.581, 1.582, 1.583, 1.584, 1.585, 1.587, 1.589, 1.590, 1.591, 1.592, 1.593, 1.594, 1.595, 1.596, 1.597, 1.598, 1.599, 1.600, 1.602, 1.603, 1.604, 1.605, 1.606, 1.607, 1.608, 1.609, 1.610, 1.611, 1.612, 1.613, 1.614, 1.615, 1.617, 1.618, 1.619, 1.620, 1.621, 1.622, 1.623, 1.624, 1.625, 1.626, 1.627, 1.628, 1.629, 1.631, 1.636, 1.640, 1.647, 1.651, 1.652, 1.654, 1.655, 1.656, 1.658, 1.659, 1.660, 1.661, 1.662, 1.663, 1.664, 1.665, 1.666, 1.668, 1.669, 1.670,
1.671, 1.672, 1.673, 1.674, 1.675, 1.676, 1.677, 1.678, 1.679, 1.680, 1.681, 1.682, 1.683, 1.684, 1.685, 1.686, 1.687, 1.688, 1.689, 1.690, 1.692, 1.696, 1.698, 1.701, 1.702, 1.703, 1.704, 1.705, 1.707, 1.708, 1.709, 1.711, 1.712, 1.713, 1.714, 1.715, 1.716, 1.717, 1.718, 1.720, 1.721, 1.722, 1.723, 1.724, 1.725, 1.726, 1.727, 1.728, 1.729, 1.731, 1.732, 1.733, 1.734, 1.735, 1.736, 1.737, 1.738, 1.739, 1.740, 1.741, 1.742, 1.743, 1.744, 1.745, 1.747, 1.748, 1.749, 1.751, 1.752, 1.753, 1.754, 1.756, 1.757, 1.758, 1.759, 1.760, 1.761, 1.762, 1.763, 1.764, 1.765, 1.766, 1.767, 1.768, 1.769, 1.770, 1.771, 1.772, 1.773, 1.774, 1.775, 1.776, 1.777, 1.778, 1.779, 1.781, 1.782, 1.783, 1.784, 1.785, 1.786, 1.787, 1.788, 1.789, 1.790, 1.791, 1.792, 1.793, 1.794, 1.795 y 1.810.
Compuestos (de la Tabla T2) 2.1,2.4, 2.6, 2.7, 2.14, 2.16, 2.21,2.22, 2.24, y 2.25.
Compuestos (de la Tabla T3) 3.11, 3.2, 3.3, 3.4, 3.5, 3.6, 3.7, 3.8, 3.9, 3.10, 3.11, 3.12, 3.13, 3.14, 3.15, 3.16, 3.17,
3.18, 3.19, 3.20, 3.21,3.22, 3.23, 3.24, 3.25, 3.26, 3.28, 3.29, 3.30, 3.31,3.32, 3.33, 3.34, 3.35, 3.36, 3.37, 3.3 3.40, 3.41, 3.42, 3.43, 3.44, 3.45, 3.46, 3.47, 3.48, 3.49, 3.50, 3.51,3.52, 3.53, 3.54, 3.55, 3.56, 3.57, 3.58, 3.5 3.61,3.62, 3.63, 3.64, 3.65, 3.66, 3.67, 3.68, 3.69, 3.70, 3.71, 3.72, 3.73, 3.74, 3.75, 3.76, 3.77, 3.78 3.82, 3.83, 3.84, 3.85, 3.86, 3.87, 3.88, 3.89, 3.90, 3.91,3.92, 3.93, 3.94, 3.95, 3.96, 3.97, 3.98, 3.99, 3.101,3.102, y
3.103.
Actividad fungicida contra Puccinia recóndita f. sp. tritic i/ trigo / prevención en discos foliares (roya parda)
Se colocan segmentos de hojas de trigo cv. Kanzler sobre agar en placas de múltiples pocillos (formato de 24 pocillos).
A continuación, los segmentos foliares se inoculan con una suspensión de esporas del hongo. Las placas se almacenaron en la oscuridad a 19 °C y un 75% de humedad relativa. El compuesto formulado del ensayo diluido en agua se aplicó 1 día después de la inoculación. Los segmentos foliares se incubaron a 19 °C y un 75% de humedad relativa con un régimen de luz de 12 h de luz / 12 h de oscuridad en una cámara climática, y se determinó la actividad de un compuesto como el porcentaje de control de la enfermedad, en comparación con los segmentos foliares no tratados, cuando aparece un nivel apropiado de daños debidos a la enfermedad en segmentos foliares de control no tratados (de 6 a 8 días después de la aplicación).
Los siguientes compuestos proporcionan al menos un 80% de control de la enfermedad en esta prueba a 200 ppm en la formulación aplicada, cuando se comparan con los discos foliares de control no tratados en las mismas condiciones, los cuales presentan un desarrollo considerable de la enfermedad.
Compuestos (de la Tabla T1) 1.1, 1.2, 1.3, 1.4, 1.6, 1.8, 1.10, 1.11, 1.12, 1.13, 1.14, 1.15, 1.16, 1.17, 1.19, 1.20, 1.22,
1.23, 1.24, 1.25, 1.26, 1.27, 1.28, 1.29, 1.30, 1.31, 1.32, 1.34, 1.35, 1.36, 1.37, 1.38, 1.40, 1.41, 1.42, 1.43, 1.44, 1.45,
1.46, 1.47, 1.48, 1.49, 1.50, 1.52, 1.53, 1.54, 1.57, 1.59, 1.64, 1.71, 1.77, 1.81, 1.83, 1.86, 1.87, 1.89, 1.91, 1.92, 1.95,
1.97, 1.99, 1.100, 1.1 0 1 , 1 .102, 1.103, 1.104, 1.106, 1.109, 1.1 1 0 , -1.1 1 1 , 1 .1 1 2 , 1 .114, 1.115, 1.117, 1.118, 1 .119,
1 .1 2 1 , 1.122, 1.123, 1 .124, 1.125, 1.126, 1 .127, 1.128, 1.129, 1 .130, 1.131, 1.132, 1 .134, 1 .136, 1.137, 1.138, 1 .139, 1.145, 1.146, 1.147, 1 .149, 1.150, 1.151, 1 .153, 1.154, 1.155, 1 .157, 1.159, 1.160, 1 .161, 1 .162, 1.164, 1.165, 1 .167, 1.168, 1.169, 1.170, 1 .171, 1.172, 1.173, 1 .175, 1.176, 1.177, 1 .178, 1.180, 1.181, 1 .182, 1 .183, 1.185, 1.187, 1 .188, 1.189, 1.191, 1.192, 1 .194, 1.196, 1.199, 1 .2 0 0 , 1 .2 0 1 , 1 .2 0 2 , 1 .204, 1.206, 1.207, 1 .2 1 0 , 1 .215, 1.216, 1.217, 1 .223, 1.225, 1.226, 1.227, 1 .229, 1.230, 1.233, 1 .235, 1.237, 1.242, 1 .243, 1.244, 1.245, 1 .248, 1 .249, 1.253, 1.259, 1 .260, 1.264, 1.266, 1.270, 1 .273, 1.275, 1.276, 1 .279, 1.280, 1.308, 1 .309, 1.314, 1.315, 1 .316, 1 .317, 1.323, 1.324, 1 .325, 1.326, 1.327, 1.328, 1 .329, 1.330, 1.331, 1 .332, 1.333, 1.334, 1 .335, 1.336, 1.337, 1 .339, 1 .340, 1.341, 1.344, 1 .345, 1.346, 1.347, 1.348, 1 .349, 1.350, 1.351, 1 .353, 1.355, 1.356, 1 .357, 1.358, 1.359, 1 .360, 1 .361, 1.362, 1.363, 1 .364, 1.365, 1.366, 1.368, 1 .369, 1.370, 1.371, 1 .372, 1.373, 1.374, 1 .375, 1.377, 1.378, 1 .379, 1 .383, 1.384, 1.387, 1 .388, 1.389, 1.390, 1.391, 1 .392, 1.395, 1.396, 1 .398, 1.399, 1.400, 1 .401, 1.402, 1.403, 1 .404, 1 .406, 1.407, 1.408, 1 .411, 1.412, 1.415, 1.417, 1 .421, 1.422, 1.426, 1 .427, 1.431, 1.432, 1 .433, 1.434, 1.435, 1 .438, 1 .442, 1.443, 1.444, 1 .445, 1.446, 1 .4 4 7 , 1 .4 4 8 , 1 .450, 1.451, 1.452, 1 .455, 1.456, 1.457, 1 .458, 1.459, 1.460, 1 .463, 1 .465, 1.466, 1.467, 1 .468, 1.469, 1.472, 1.473, 1 .474, 1.476, 1.477, 1 .478, 1.479, 1.480, 1 .481, 1.483, 1.484, 1 .485, 1 .486, 1.487, 1.488, 1 .489, 1.490, 1.491, 1.492, 1 .493, 1.494, 1.495, 1 .496, 1.497, 1.498, 1 .499, 1.500, 1.501, 1 .502, 1 .503, 1.504, 1.505, 1 .506, 1.507, 1.508, 1.509, 1 .510, 1.511, 1.512, 1 .513, 1.514, 1.515, 1 .516, 1.517, 1.518, 1 .519, 1 .520, 1.521, 1.522, 1 .523, 1.524, 1.525, 1.526, 1 .527, 1.528, 1.529, 1 .530, 1.531, 1.532, 1 .563, 1.564, 1.566, 1 .567, 1 .568, 1.569, 1.570, 1 .571, 1.573, 1.574, 1.575, 1 .577, 1.578, 1.579, 1 .580, 1.582, 1.583, 1 .584, 1.585, 1.586, 1 .587, 1 .589, 1.590, 1.591, 1 .592, 1.593, 1.594, 1.595, 1 .596, 1.597, 1.599, 1 .600, 1.603, 1.604, 1 .605, 1.606, 1.607, 1 .608, 1 .609, 1.610, 1.611, 1 .612, 1.613, 1.614, 1.615, 1 .617, 1.618, 1.620, 1 .621, 1.622, 1.623, 1 .624, 1.625, 1.626, 1 .629, 1 .631, 1.640, 1.651, 1 .652, 1.654, 1.655, 1.656, 1 .658, 1.659, 1.660, 1 .661, 1.662, 1.663, 1 .664, 1.665, 1.666, 1 .667, 1 .6 6 8 , 1.669, 1.670, 1 .671, 1.673, 1.674, 1.675, 1 .676, 1.677, 1.678, 1 .679, 1.680, 1.681, 1 .682, 1.683, 1.684, 1 .685, 1 .6 8 6 , 1.687, 1 .6 8 8 , 1 .689, 1.690, 1.692, 1.693, 1 .696, 1.698, 1.701, 1 .702, 1.703, 1.705, 1 .707, 1.711, 1.712, 1 .713, 1 .714, 1.717, 1.718, 1 .721, 1.722, 1.723, 1.724, 1 .725, 1.726, 1.727, 1 .731, 1.732, 1.738, 1 .739, 1.740, 1.741, 1 .742, 1 .743, 1.744, 1.745, 1 .747, 1.748, 1.749, 1.750, 1 .751, 1.752, 1.753, 1 .756, 1.757, 1.758, 1 .759, 1.760, 1.761, 1 .762, 1 .763, 1.764, 1.765, 1 .766, 1.767, 1.768, 1.769, 1 .770, 1.771, 1.772, 1 .773, 1.774, 1.775, 1 .776, 1.777, 1.778, 1 .779, 1 .781, 1.782, 1.783, 1 .784, 1.785, 1.786, 1.787, 1 .788, 1.789, 1.790, 1 .791, 1.792, 1.793, 1 .794, 1.795 y 1.810
Compuestos (de la Tabla T2) 2.1,2.2, 2.3, 2.4, 2.5, 2.6, 2.11, 2.14, 2.15, 2.16, 2.17, 2.20, 2.22, 2.24, y 2.25.
Compuestos (de la Tabla T3) 3.1, 3.2, 3.3, 3.4, 3.5, 3.6, 3.7, 3.8, 3.9, 3.10, 3.12, 3.13, 3.14, 3.15, 3.16, 3.17, 3.18,
3.19, 3.20, 3.21,3.22, 3.23, 3.24, 3.25, 3.26, 3.28, 3.29, 3.30, 3.31, 3.32, 3.33, 3.34, 3.36, 3.37, 3.38, 3.39, 3.40, 3.41,
3.42 , 3.43, 3.44, 3.45, 3.46, 3.47, 3.48, 3.49, 3.50, 3.51 ,3.52 , 3.53, 3.54, 3.55, 3.56, 3.57 , 3.58, 3.59, 3.60, 3.61 ,3.63 , 3.64 , 3.65, 3.67, 3.68, 3.69, 3.70, 3.71 ,3.72 , 3.73, 3.74, 3.75, 3.76, 3.77, 3.78, 3.79, 3.80 , 3.81 ,3.82 , 3.83, 3.84, 3.85, 3.86 , 3.87, 3.88, 3.89, 3.90, 3.91 ,3.92 , 3.93 , 3.94, 3.95, 3.97, 3.98, 3.99, 3.100 , 3.101 ,3.102 , y 3.103.
Actividad fungicida contra Phakopsora pachyrhizi/ soja / prevención en discos foliares (roya asiática de la soja)
Se colocan discos foliares de soja en agar-agua en placas de múltiples pocillos (formato de 24 pocillos) y se pulveriza el compuesto de ensayo formulado diluido en agua sobre estos. Un día después de la aplicación los discos foliares se inoculan pulverizando una suspensión de esporas sobre su superficie foliar más baja. Tras un periodo de incubación en una cámara climática de 24-36 horas en la oscuridad a 20 °C y un 75% de HR, los discos foliares se mantienen a 20 °C con 12 h de luz/día y un 75% de HR. La actividad de un compuesto se determina como el porcentaje de control de la enfermedad en comparación con los discos foliares no tratados cuando aparece un nivel apropiado de daños debidos a la enfermedad en los discos foliares de control no tratados (de 12 a 14 días después de la aplicación).
Los siguientes compuestos proporcionan al menos un 80% de control de la enfermedad en esta prueba a 200 ppm en la formulación aplicada, cuando se comparan con los discos foliares de control no tratados en las mismas condiciones, los cuales presentan un desarrollo considerable de la enfermedad.
Compuestos (de la Tabla T1) 1.1, 1.2, 1.3, 1.4, 1.5, 1.6, 1.8, 1.11, 1.12, 1.14, 1.15, 1.16, 1.17, 1.19, 1.20, 1.22, 1.23, 1.24, 1.26, 1.27, 1.28, 1.29, 1.30, 1.31, 1.32, 1.33, 1.34, 1.35, 1.36, 1.38, 1.40, 1.41, 1.42, 1.43, 1.44, 1.45, 1.46, 1.47, 1.48, 1.49, 1.50, 1.51, 1.53, 1.54, 1.57, 1.58, 1.59, 1.60, 1.64, 1.71, 1.77, 1.81, 1.82, 1.83, 1.84, 1.86, 1.87, 1.89, 1.90, 1.91, 1.92, 1.93, 1.95, 1.97, 1.99, 1.100, 1.101, 1.102, 1.103, 1.104, 1.106, 1.109, 1.110, 1.111, 1.112, 1.114, 1.115, 1.117, 1.118, 1.119, 1.121, 1.122, 1.123, 1.124, 1.125, 1.126, 1.128, 1.130, 1.132, 1.134, 1.135, 1.136, 1.138, 1.144, 1.145, 1.146, 1.147, 1.149, 1.150, 1.151, 1.154, 1.155, 1.157, 1.158, 1.159, 1.164, 1.165, 1.166, 1.167, 1.168, 1.169, 1.170, 1.171, 1.172, 1.173, 1.175, 1.176, 1.177, 1.178, 1.180, 1.181, 1.182, 1.183, 1.185, 1.187, 1.189, 1.190, 1.191, 1.192, 1.193, 1.194, 1.195, 1.196, 1.197, 1.199, 1.200, 1.201, 1.202, 1.206, 1.207, 1.209, 1.210, 1.212, 1.215, 1.216, 1.217, 1.218, 1.220, 1.221, 1.222, 1.223, 1.224, 1.226, 1.227, 1.229, 1.230, 1.233, 1.235, 1.238, 1.241, 1.242, 1.243, 1.244, 1.245, 1.246, 1.253, 1.264, 1.273, 1.274, 1.275, 1.309, 1.312, 1.314, 1.315, 1.316, 1.324, 1.325, 1.327, 1.329, 1.331, 1.335, 1.337, 1.339, 1.341, 1.342, 1.344, 1.345, 1.346, 1.350, 1.351, 1.355, 1.356, 1.358, 1.359, 1.360, 1.361, 1.363, 1.365, 1.368, 1.369, 1.372, 1.379, 1.383, 1.384, 1.387, 1.389, 1.390, 1.392, 1.395, 1.398, 1.399, 1.401, 1.402, 1.403, 1.404, 1.407, 1.408, 1.412, 1.416, 1.418, 1.432, 1.457, 1.466, 1.471, 1.472, 1.475, 1.476, 1.477, 1.478, 1.479, 1.480, 1.483, 1.484, 1.485, 1.486, 1.487, 1.488, 1.489, 1.491, 1.492, 1.493, 1.494, 1.495, 1.496, 1.497, 1.498, 1.499, 1.500, 1.503, 1.504, 1.505, 1.506, 1.507, 1.508, 1.509, 1.510, 1.511, 1.512, 1.513, 1.514, 1.515, 1.516, 1.517, 1.518, 1.519, 1.520, 1.521, 1.523, 1.524, 1.525, 1.526, 1.527, 1.528, 1.529, 1.531, 1.532, 1.562, 1.563, 1.564, 1.566, 1.567, 1.568, 1.569, 1.570, 1.571, 1.573, 1.574, 1.575, 1.576, 1.577, 1.578, 1.579, 1.580, 1.581, 1.582, 1.583, 1.584, 1.585, 1.586, 1.587, 1.589, 1.590, 1.591, 1.592, 1.594, 1.595, 1.596, 1.597, 1.599, 1.600, 1.603, 1.604, 1.605, 1.606, 1.607, 1.608, 1.610, 1.611, 1.612, 1.613, 1.614, 1.615, 1.616, 1.617, 1.618, 1.619, 1.620, 1.621, 1.622, 1.623, 1.624, 1.625, 1.626, 1.627, 1.628, 1.629, 1.630, 1.631, 1.632, 1.634, 1.636, 1.637, 1.639, 1.640, 1.641, 1.642, 1.643, 1.644, 1.645, 1.646, 1.647, 1.648, 1.649, 1.651, 1.652, 1.653, 1.654, 1.655, 1.656, 1.657, 1.658, 1.659, 1.660, 1.661, 1.662, 1.663, 1.664, 1.665, 1.666, 1.667, 1.668, 1.669, 1.670, 1.671, 1.672, 1.673, 1.674, 1.675, 1.676, 1.677, 1.678, 1.679, 1.680, 1.681, 1.682, 1.683, 1.684, 1.685, 1.686, 1.687, 1.688, 1.689, 1.690, 1.691, 1.692, 1.693, 1.694, 1.695, 1.696, 1.697, 1.698, 1.699, 1.700, 1.701, 1.702, 1.703, 1.704, 1.705, 1.706, 1.707, 1.708, 1.709, 1.710, 1.711, 1.712, 1.714, 1.715, 1.716, 1.717, 1.718, 1.720, 1.721, 1.722, 1.723, 1.724, 1.725, 1.726, 1.727, 1.728, 1.729, 1.730, 1.731, 1.732, 1.733, 1.734, 1.735, 1.736, 1.737, 1.738, 1.739, 1.740, 1.741, 1.742, 1.743, 1.744, 1.745, 1.746, 1.747, 1.748, 1.749, 1.750, 1.751, 1.752, 1.753, 1.754, 1.755, 1.756, 1.757, 1.758, 1.759, 1.760, 1.761, 1.762, 1.763, 1.764, 1.765, 1.766, 1.767, 1.768, 1.769, 1.770, 1.771, 1.772, 1.773, 1.774, 1.775, 1.776, 1.777, 1.778, 1.779, 1.781, 1.782, 1.783, 1.784, 1.786 y 1.810.
Los Compuestos (de la Tabla T2) 2.2, 2.3, 2.4, 2.5, 2.21,2.24 y 2.25.
Compuestos (de la Tabla T3) 3.1, 3.2, 3.3, 3.4, 3.5, 3.6, 3.7, 3.8, 3.9, 3.11, 3.12, 3.13, 3.14, 3.15, 3.16, 3.17, 3.18, 3.19, 3.20, 3.21,3.22, 3.23, 3.24, 3.25, 3.26, 3.28, 3.29, 3.30, 3.31,3.32, 3.33, 3.34, 3.36, 3.37, 3.38, 3.39, 3.40, 3.41, 3.42, 3.43, 3.44, 3.45, 3.46, 3.47, 3.48, 3.51,3.52, 3.53, 3.55, 3.56, 3.57, 3.58, 3.59, 3.60, 3.61, y 3.62.
Actividad fungicida contra Glomerella lagenarium (Colletrotrichum lagenarium) en cultivo líquido / pepino / prevención (antracnosis)
Se mezclan conidios del hongo procedentes de un depósito criogénico directamente en un caldo de nutrientes (PDB -caldo de dextrosa de papa). Después de colocar una solución (DMSO) del compuesto de prueba en una placa de microtitulación (formato de 96 pocillos), se añade el caldo nutritivo que contiene las esporas fúngicas. Las placas de prueba se incuban a 24 oC y la inhibición del crecimiento se mide fotométricamente de 3 a 4 días después de la aplicación.
Los s ig u ie n te s c o m p u e s to s p ro p o rc io n a n al m en os un 80 % de c o n tro l de la e n fe rm e d a d en e s ta p ru e b a a 20 ppm en la fo rm u la c ió n ap lica da , c u a n d o se c o m p a ra n con las m u e s tra s de con tro l no tra ta d a s en las m ism a s c o n d ic io n e s , las c u a le s p re se n ta n un d e sa rro llo c o n s id e ra b le de la e n fe rm e d a d .
Compuestos (de la Tabla T1) 1.1, 1.2, 1.3, 1.4, 1.5, 1.6, 1.7, 1.8, 1.9, 1.10, 1.11, 1.12, 1.13, 1.15, 1.16, 1.17, 1.18, 1.19, 1.20, 1.22, 1.23, 1.24, 1.25, 1.26, 1.27, 1.28, 1.29, 1.30, 1.31, 1.32, 1.33 1.34, 1.35, 1.36, 1.37, 1.38, 1.40, 1.41, 1.42, 1.43, 1.44, 1.45, 1.46, 1.47, 1.48, 1.49, 1.50, 1.51, 1.53, 1.54, 1.55, 1.57 1.58, 1.59, 1.61, 1.64, 1.67, 1.68, 1.69, 1.71, 1.72, 1.74, 1.77, 1.81, 1.82, 1.83, 1.84, 1.85, 1.86, 1.87, 1.88, 1.89, 1.90 1.91, 1.92, 1.93, 1.94, 1.95, 1.96, 1.97, .98, 1.99, 1 101, 1102, 1 103, 1.104, 1.105, 1.106, .107, 1.109, 1.110, 1.111, 1.112, 1.113, 1.114, .115, 1.116, 1.117, 1.118, 1.119, 1.120, 1.121, 1.122, 1.123, 1.124, 1.125, 1.126, 1.127, 1.128, 1.129, 1.130, 1.131, .132, 1.133, 1.134, 1.135, 1.136, 1.138, 1.139, 1.142, 1.144, 1.145, 1.146, 1.147, 1.148, 1.149, 1.150, 1.151, 1.152, .153, 1.154, 1.155, 1.157, 1.158, 1.159, 1.161, 1.162, 1.163, 1.164, 1.165, 1.166, 1.167, 1.168, 1.169, 1.170, 1.171, .173, 1.174, 1.175, 1.176, 1.177, 1.178, 1.179, 1.180, 1.181, 1.182, 1.183, 1.184, 1.185, 1.187, 1.189, 1.190, 1.191, .192, 1.193, 1.194, 1.195, 1.196, 1.199, 1.201, 1.202, 1.203, 1.205, 1.206, 1.207, 1.208, 1.209, 1.210, 1.211, 1.212, .213, 1.214, 1.215, 1.216, 1.217, 1.218, 1.219, 1.220, 1.221, 1.222, 1.223, 1.224, 1.225, 1.226, 1.227, 1.228, 1.229, .230, 1.231, 1.232, 1.233, 1.235, 1.236, 1.237, 1.238, 1.239, 1.240, 1.242, 1.243, 1.244, 1.245, 1.246, 1.247, 1.248, .249, 1.250, 1.251, 1.252, 1.253, 1.254, 1.255, 1.256, 1.257, 1.258, 1.259, 1.260, 1.261, 1.262, 1.264, 1.265, 1.266, .268, 1.269, 1.270, 1.271, 1.272, 1.273, 1.274, 1.275, 1.276, 1.277, 1.278, 1.279, 1.280, 1.281, 1.282, 1.283, 1.284, .285, 1.286, 1.287, 1.288, 1.289, 1.290, 1.291, 1.292, 1.293, 1.294, 1.295, 1.297, 1.298, 1.299, 1.301, 1.302, 1.303, .304, 1.305, 1.306, 1.307, 1.308, 1.309, 1.310, 1.311, 1.312, 1.313, 1.314, 1.315, 1.316, 1.317, 1.318, 1.319, 1.320, .321, 1.322, 1.323, 1.324, 1.325, 1.326, 1.327, 1.328, 1.329, 1.330, 1.331, 1.332, 1.333, 1.334, 1.335, 1.336, 1.337, .338, 1.339, 1.340, 1.341, 1.342, 1.343, 1.344, 1.345, 1.346, 1.347, 1.348, 1.349, 1.350, 1.351, 1.352, 1.355, 1.356, .358, 1.359, 1.360, 1.361, 1.362, 1.363, 1.364, 1.365, 1.366, 1.367, 1.368, 1.369, 1.370, 1.371, 1.372, 1.373, 1.374, .375, 1.376, 1.377, 1.378, 1.379, 1.380, 1.381, 1.382, 1.384, 1.385, 1.387, 1.388, 1.389, 1.390, 1.391, 1.392, 1.393, .394, 1.395, 1.396, 1.397, 1.398, 1.399, 1.400, 1.401, 1.402, 1.403, 1.404, 1.405, 1.406, 1.407, 1.408, 1.409, 1.410, .411, 1.412, 1.413, 1.414, 1.415, 1.416, 1.417, 1.418, 1.419, 1.420, 1.421, 1.422, 1.423, 1.424, 1.425, 1.426, 1.427, .428, 1.429, 1.430, 1.431, 1.432, 1.433, 1.434, 1.435, 1.436, 1.437, 1.438, 1.439, 1.440, 1.442, 1.443, 1.445, 1.446, .447, 1.448, 1.449, 1.450, 1.451, 1.452, 1.453, 1.455, 1.456, 1.457, 1.458, 1.459, 1.460, 1.461, 1.462, 1.463, 1.464, .465, 1.466, 1.467, 1.468, 1.469, 1.470, 1.471, 1.472, 1.473, 1.474, 1.475, 1.476, 1.477, 1.478, 1.479, 1.480, 1.481, .482, 1.483, 1.484, 1.485, 1.486, 1.487, 1.488, 1.489, 1.490, 1.491, 1.492, 1.493, 1.494, 1.495, 1.496, 1.497, 1.498, .499, 1.500, 1.501, 1.502, 1.503, 1.504, 1.505, 1.506, 1.507, 1.508, 1.509, 1.510, 1.511, 1.512, 1.513, 1.514, 1.515, .516, 1.517, 1.518, 1.519, 1.520, 1.521, 1.522, 1.523, 1.524, 1.525, 1.526, 1.527, 1.528, 1.529, 1.530, 1.531, 1.532, .533, 1.534, 1.535, 1.536, 1.537, 1.538, 1.539, 1.540, 1.541, 1.542, 1.543, 1.544, 1.545, 1.546, 1.547, 1.548, 1.549, .550, 1.551, 1.553, 1.554, 1.555, 1.556, 1.557, 1.558, 1.559, 1.560, 1.561, 1.562, 1.563, 1.564, 1.565, 1.566, 1.567, .568, 1.569, 1.570, 1.571, 1.572, 1.573, 1.574, 1.575, 1.576, 1.577, 1.578, 1.579, 1.580, 1.581, 1.582, 1.583, 1.584, .585, 1.586, 1.587, 1.588, 1.589, 1.590, 1.591, 1.592, 1.593, 1.594, 1.595, 1.596, 1.597, 1.598, 1.599, 1.600, 1.601, .602, 1.603, 1.604, 1.605, 1.606, 1.607, 1.608, 1.609, 1.610, 1.611, 1.612, 1.613, 1.614, 1.615, 1.616, 1.617, 1.618, .619, 1.620, 1.621, 1.622, 1.623, 1.624, 1.625, 1.626, 1.627, 1.628, 1.629, 1.630, 1.631, 1.632, 1.633, 1.634, 1.636, .637, 1.638, 1.639, 1.641, 1.642, 1.643, 1.644, 1.645, 1.646, 1.647, 1.648, 1.649, 1.650, 1.651, 1.652, 1.653, 1.654, .655, 1.656, 1.657, 1.658, 1.659, 1.660, 1.661, 1.662, 1.663, 1.664, 1.665, 1.666, 1.667, 1.668, 1.669, 1.670, 1.671, .672, 1.673, 1.674, 1.675, 1.676, 1.677, 1.678, 1.679, 1.680, 1.681, 1.682, 1.683, 1.684, 1.685, 1.686, 1.687, 1.688, .689, 1.690, 1.691, 1.692, 1.693, 1.694, 1.695, 1.696, 1.697, 1.698, 1.699, 1.700, 1.701, 1.702, 1.703, 1.704, 1.705, .706, 1.707, 1.708, 1.709, 1.713, 1.714, 1.715, 1.716, 1.717, 1.718, 1.720, 1.723, 1.724, 1.725, 1.726, 1.727, 1.729, .730, 1.733, 1.734, 1.735, 1.736, 1.737, 1.738, 1.739, 1.740, 1.741, 1.742, 1.743, 1.745, 1.749, 1.751, 1.752, 1.753, .754, 1.755, 1.756, 1.757, 1.758, 1.759, 1.760, 1.761, 1.762, 1.763, 1.764, 1.765, 1.766, 1.768, 1.769, 1.770, 1.771, .772, 1.773, 1.774, 1.775, 1.776, 1.777, 1.778, 1.779, 1.780, 1.781, 1.782, 1.783, 1.784, 1.785, 1.786, 1.787, 1.790, .791, 1.793, 1.794, 1.795, 1.810 y 1.811
Los Compuestos (de la Tabla T2) 2.1,2.2, 2.3, 2.4, 2.5, 2.6, 2.7, 2.8, 2.9, 2.10, 2.11,2.12, 2.13, 2.14, 2.15, 2.16, 2.17, 2.18, 2.19, 2.20, 2.21,2.22, 2.24 y 2.25.
Compuestos (de la Tabla T3) 3.1, 3.2, 3.3, 3.4, 3.5, 3.6, 3.7, 3.8, 3.9, 3.10, 3.11, 3.12, 3.13, 3.14, 3.15, 3.16, 3.17, 3.18, 3.19, 3.20, 3.21,3.22, 3.23, 3.24, 3.25, 3.26, 3.28, 3.29, 3.30, 3.31,3.32, 3.33, 3.34, 3.35, 3.36, 3.37, 3.38, 3.39, 3.40, 3.41, 3.42, 3.43, 3.44, 3.45, 3.46, 3.47, 3.48, 3.49, 3.51, 3.52, 3.53, 3.54, 3.55, 3.56, 3.57, 3.58, 3.59, 3.60, 3.61, 3.62, 3.63, 3.64, 3.65, 3.66, 3.67, 3.69, 3.70, 3.71,3.72, 3.73, 3.74, 3.75, 3.76, 3.77, 3.78, 3.79, 3.80, 3.81,3.82, 3.83, 3.84, 3.85, 3.87, 3.88, 3.89, 3.90, 3.91,3.92, 3.93, 3.94, 3.95, 3.96, 3.97, 3.98, 3.99, 3.100, 3.101,3.102, y 3.103.
Claims (16)
1. Un compuesto de fórmula (I):
donde
n es 1 o 2
A1 representa N o CR1, donde R1 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi;
A2 representa N o CR2 , en el que R2 es hidrógeno, halógeno, metilo, etilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi;
A3 representa N o CR3 , donde R3 es hidrógeno o halógeno;
A4 representa N o CR4 , donde R4 es hidrógeno o halógeno; y
donde 0, 1 o 2 de A1, A2 , A3 y A4 son N;
R5 y R6 se seleccionan independientemente de hidrógeno, alquilo C1-4, halógeno, ciano, trifluorometilo y difluorometilo, o R5 y R6 , junto con el átomo de carbono que comparten, forman un ciclopropilo;
R7 es hidroxi, alquilo C1-4, haloalquilo C1-4, alcoxi C1-4, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, haloalcoxi C1 -2alquilo C1-4, alquenilo C3-6, alquinilo C3-4, alqueniloxi C3-6, alquiniloxi C3-6, haloalquenilo C3-6, haloalqueniloxi C3-6, alquilcarboniloxi C1-4, haloalquilcarboniloxi C1-4, alcoxicarboniloxi C1-4, alquilcarboniloxi C1-4alquilo C1-4, haloalquilcarboniloxi C1-4alquilo C1-4 o alcoxicarboniloxi C1 -4alquilo C1-4; o
R7 es cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, cicloalquil C3-6alcoxi C1-2, fenilo, fenilalquilo C1-2, fenilalcoxi C 1-2, heteroarilo, heteroarilalquilo C1-2, heteroarilalcoxi C1-2, heterociclilo, heterociclilalquilo C1-2, heterociclilalcoxi C1-2, cicloalquilcarboniloxi C3-6, heterociclilcarboniloxi, fenilcarboniloxi, cicloalquilcarboniloxi C3-6alquilo C1-4, heterociclilcarboniloxialquilo C1-4 o fenilcarboniloxialquilo C1-4, en donde el resto heteroarilo es un anillo aromático monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente de N, O y S, el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente de N, O y S, y en el que cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes seleccionados de ciano, flúor, cloro, bromo, metilo, difluorometilo, trifluorometilo, metoxi, etoxi o difluorometoxi;
R8 es hidrógeno, alquilo C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C1-6, haloalquilo C1-6, haloalquenilo C2-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6, haloalcoxi C1-4alquilo C1-6, alcoxi C1-4alcoxi C1-4alquilo C1-6, alquiniloxi C2-4alquilo C1-6, aminoalquilo C1-6, N-alquilamino C1-4alquilo C1-6, N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6, alcoxicarbonil C 1-6alquilo C1-6, alquilcarboniloxi C1-6alquilo C1-6, N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1 -4alquilo C1-6, alquilsulfanil C1-6alquilo C1-6, alquilsulfonil C1-6 alquilo C1-6, alquilsulfonilamino C1-6alquilo C1-6, alquilsulfonilamino C1-6alquinilo C2-6, alquiniloxicarbonilamino C2-6alquilo C1-6, alquilcarbonilamino C1-4alquilo C1-6 o alcoxicarbonilamino C1-4alquilo C1-6; o
R8 es cicloalquilo C3-8, cicloalquilo C3-8alquilo C1-6, donde el resto cicloalquilo está opcionalmente insaturado parcialmente, fenilo, fenilalquilo C1-6, fenilalquenilo C2-6, naftilo, naftiloalquilo C1-6, heteroarilo, heteroarilalquilo C1-6, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterodiarilo, heterodiarilalquilo C1-6 donde el resto heterodiarilo es un sistema aromático, bicíclico, de 9 a 10 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1, 2 o 3 heteroátomos seleccionados individualmente entre N, O y S o cicloalquilcarbonilamino C3-6alquilo C1-6,
donde para R8 , cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo o heterociclilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; o,
a d ic io n a lm e n te , c u a n d o R8 es c ic lo p ro p ilo , e l resto c ic lo p ro p ilo e s tá su s titu id o con 4 s u s titu ye n te s , q u e p u e d e n s e r los m ism o s o d ife re n te s , se le c c io n a d o s e n tre R9, con la c o n d ic ió n de q u e al m en os 2 s u s titu y e n te s R9 sea n los m ism o s; d o n d e
R9 es ciano, halógeno, hidroxi, alquilo C1-4 , alquenilo C2-4 , alquinilo C2-4 , haloalquilo C1-4 , haloalquenilo C2-4 , alcoxi C 1-4 , haloalcoxi C1-4 , alquiniloxi C3-4 , N-alquilamino C1-4 , N,N-dialquilamino C1-4 , alquilcarbonilo C1-4, cicloalquilcarbonilo C3-6 , alcoxicarbonilo C1-4 , carbonilamino, N-alquilaminocarbonilo C1-4 , N,N-dialquilaminocarbonilo C 1-4 o alcoxicarbonilamino C1-4 , y donde cuando R8 es cicloalquil C3-8alquilo C 1-6, heterociclilo, heterociclilalquilo C1-6 o cicloalquilo C3-8 sustituido, R9 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo; o
donde para R8, cualquier resto cicloalquilo, fenilo, naftilo, heteroarilo, heterodiarilo o heterociclilo está opcionalmente sustituido con 1 sustituyente seleccionado entre R10 y además opcionalmente sustituido con 1 o 2 sustituyentes seleccionados entre R9; donde
R10 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-2 , fenilo, fenilalquilo C1-2 , heteroarilo, heteroarilalquilo C1-2 donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo o heterociclilalquilo C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S, y donde cualquiera de dichos restos cicloalquilo, fenilo, heteroarilo y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R11; donde
R11 es hidrógeno, ciano, flúor, cloro, bromo, metilo, trifluorometilo, metoxi y etoxi;
o
R8 representa -OR12, donde R12 es hidrógeno, alquilo C1-6, alquenilo C3-6 , alquinilo C3-6 , cianoalquilo C1-6 , haloalquilo C1-6 , haloalquenilo C3-6, hidroxialquilo C1-6, alcoxi C1-4alquilo C1-6 , haloalcoxi C1-4alquilo C1-6 , alcoxi C1-4alcoxi C1-4alquilo C1-6 , aminoalquilo C 1-6 , N-alquilamino C1-4alquilo C1-6 , N,N-dialquilamino C1-4alquilo C1-6, alquilcarbonil C1-6alquilo C1-6, alquilcarbonil C1-6alquenilo C2-6 , alcoxicarbonil C1-6alquilo C1-6 , alquilcarboniloxi C1-6alquilo C1-6 , N-alquilaminocarbonil C1-4alquilo C1-6 , N,N-dialquilaminocarbonil C1-4alquilo C1-6 , alquilsulfanil C1-4alquilo C1-6 , alquilsulfonil C1-6 alquilo C1-6 o alquilsulfonilamino C1-6alquilo C1-6 ; o
R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6 , donde el resto cicloalquilo es fenilo, fenilalquilo C1-6 , heteroarilo, heteroarilalquilo C1-6 opcionalmente insaturado parcialmente, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y 5, heterociclilo o heterociclilalquilo C1-6 , donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S,
donde para R12, cualquier resto cicloalquilo, fenilo, heteroarilo o heterociclilo está opcionalmente sustituido con 1, 2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R13; donde
R13 es ciano, halógeno, hidroxi, alquilo C1-4 , alquenilo C2-4 , alquinilo C2-4 , haloalquilo C1-4, haloalquenilo C2-4 , alcoxi C1-4 , haloalcoxi C1-4, alqueniloxi C3-4, alquiniloxi C3-4 , N-alquilamino C 1-4, N,N-dialquilamino C1-4 , alquilcarbonilo C1-4 , alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4 , N,N-dialquilaminocarbonilo C1-4 o alcoxicarbonilamino C1-4 ;
y donde cuando R12 es cicloalquilo C3-8, cicloalquil C3-8alquilo C 1-6 , heterociclilo o heterociclilalquilo C1-6 sustituido, R13 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo;
o
R8 representa -NR14R15, donde R14 es hidrógeno, ciano, alquilo C1-6 , alcoxi C1-6 , alquenilo C2-6 , alquinilo C2-6 , alqueniloxi C3-6 , alquiniloxi C3-6, cianoalquilo C1-6, haloalquilo C 1-6 , haloalquenilo C1-6, hidroxialquilo C1-6, alcoxi C1 -4alquilo C1-6 , haloalcoxi C1-4alquilo C1-6 , alcoxi C1-4alcoxi C1-4alquil C1-6 , aminoalquil C1-6 , N-alquilamino C1-4alquilo C1-6 , N,N-dialquilamino C1-4alquilo C1-6 , alquilcarbonil C1-6alquilo C1-6 , alquilcarbonil C1-6alquenilo C2-6 , alcoxicarbonil C1-6alquilo C1-6 , alquilcarboniloxi C1-6alquilo C1-6 , N-alquilaminocarbonil C1-4alquilo C1-6, N,N-dialquilaminocarbonil C1-4alquilo C 1-6, alquilsulfanil C1-4alquilo C1-6, alquilsulfonil C1-6 alquilo C 1-6 o alquilsulfonilamino C1 -6alquilo C1-6 ; o
R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6 , cicloalquil C3-8alcoxi C1-6 , cicloalquiloxi C3-6 , donde el resto cicloalquilo es fenilo, fenilalquilo C1-6, fenilalcoxi C1-6 , heteroarilo, heteroarilalquilo C1-6, heteroarilalcoxi C1-6 opcionalmente insaturado parcialmente, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 o 6 miembros que comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, heterociclilo, heterociclilalquilo C1-6 o heterociclilalcoxi C1-6 donde el resto heterociclilo es un anillo no aromático de 4 a 6 miembros que comprende 1,2 o 3 heteroátomos seleccionados individualmente entre N, O y S,
donde para R14, cualquier resto cicloalquilo, fenilo, heteroarilo, heterociclilo está opcionalmente sustituido con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R17; donde
R16 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4, haloalquenilo C2-4, alcoxi C i-4 , alcoxi C1-2alquilo C1-2, haloalcoxi C1-4, alqueniloxi C3-4, alquiniloxi C3-4, N-alquilamino C1-4, N,N-dialquilamino C1-4, alquilcarbonilo C1-4, alcoxicarbonilo C1-4, carbonilamino, N-alquilaminocarbonilo C1-4, N,N-dialquilaminocarbonilo C1-4 y alcoxicarbonilamino C1-4;
y donde cuando R14 es cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, cicloalquil C3-8alcoxi C1-6, heterociclilo, heterociclilalquilo C1-6 o heterociclilalcoxi C1-6 sustituido, R16 también puede representar oxo en el resto cicloalquilo C3-8 o heterociclilo;
R15 es hidrógeno, alquilo C1-4, alquinilo C3-4, alcoxi C1-4alquilo C1-4, cianoalquilo C1-4, cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2 ; o
R14 y R15, junto con el átomo de nitrógeno al que están unidos, forman un ciclo de 4, 5 o 6 miembros que contiene opcionalmente un heteroátomo adicional o grupo seleccionado entre O, S, S(O)2 , oxo (=O) y NR17; donde
R17 es hidrógeno, metilo, metoxi, formilo o acilo; o
una de sus sales o N-óxidos.
2. Un compuesto de acuerdo con la reivindicación 1, donde A1, A2 , A3 y A4 son C-H.
3. Un compuesto de acuerdo con la reivindicación 1 o la reivindicación 2, donde R5 y R6 son hidrógeno y n es 1.
4. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 3, donde:
cuando R8 no es OR12 o NR14R15, R7 es alquilo C1-4, haloalquilo C2-4, alcoxi C1-4 o cicloalquilo C3-6; o
cuando R8 es OR12, R7 es hidoxi, alquilo C1-4, haloalquilo C2-4, alcoxi C1-4, alquenilo C3-4, alquinilo C3-4 o alcoxicarboniloxi C1-4; o
cuando R8 es NR14R15, R7 es hidoxi, alquilo C1-4, haloalquilo C2 , alcoxi C1-2, alquenilo C3-4, alquinilo C3-4 o ciclopropilo.
5. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 4, donde:
R8 es alquilo C1-6, alquenilo C2-4, alquinilo C2-4, cianoalquilo C1-4, haloalquilo C1-5, haloalquenilo C2-4, hidroxialquilo C 1-4 , alcoxi C1-2alquilo C1-4, haloalcoxi C1-2alquilo C1-4, alcoxi C1-2alcoxi C1 -2alquilo C1-4, aminoalquilo C1-4, alquilcarbonil C1-2alquilo C1-4, alquilcarbonil C1-4alquenilo C2-4, alquilcarboniloxi C1-4alquilo C1-4, alquilsulfonilamino C1 -4alquinilo C2-4, alquilcarbonilamino C1-2alquilo C1-4, alquiniloxicarbonilamino C2-4alquilo C1-4 o alcoxicarbonilamino C1-2alquilo C1-4; o R8 es cicloalquilo C3-6, cicloalquil C3-6alquilo C1-2, fenilo, fenilalquilo C1-4, fenilalquenilo C2-4, naftilo, un resto que contiene heteroarilo seleccionado entre furanilo, pirazolilo, imidazolilo, triazolilo, 1,2,3-benzotiadiazol, (piridinil)metilo o un resto que contiene heterociclilo seleccionado entre oxetanilo, pirrolidinilo, azetidinilo, tetrahidrofuranilo, 1,3-dioxolanilo, tietanilo, 1-oxo-tietan-3-ilo, 1,1-dioxo-tietan-3-ilo, tetrahidropiranilo, tetrahidrotiopiranilo o cicloalquilcarbonilamino C3-6alquilo C1-4,
donde el ciclo de cada resto que contiene heteroarilo o el resto que contiene heterociclilo está opcionalmente sustituido con 1,2 o 3 sustituyentes, que pueden ser los mismo o diferentes, seleccionados entre R9 o
donde el ciclo de cada resto que contiene heteroarilo o el resto que contiene heterociclilo está opcionalmente sustituido con 1 sustituyente seleccionado entre R10 y además opcionalmente sustituido con 1 o 2 sustituyentes seleccionados entre R9 ;
R9 es ciano, metilo, cloro, flúor, hidroxilo, metoxi, trifluorometilo, haloalquenilo C2 , metilcarbonilo, etilcarbonilo y carbonilamino;
R10 es fenilo o piridinilo, donde fenilo o piridinilo está opcionalmente sustituido con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R11; donde
R11 es flúor, cloro, bromo y metoxi;
o
cuando R8 es -OR12, R12 es hidrógeno, alquilo C1-6, alquenilo C3-6, alquinilo C3-6, haloalquilo C1-6, alcoxi C1 -4alquilo C1-6. fenilo o fenilalquilo C1-6 ;
o
cuando R8 es NR14R15, R14 es hidrógeno, ciano, alquilo C1-6, alcoxi C1-6, alquenilo C2-6, alquinilo C2-6, cianoalquilo C 1-6 , haloalquilo C1-6, alcoxi C1-4alquilo C1-6, alcoxicarbonil C1-6alquilo C1-6, o cicloalquilo C3-8, cicloalquil C3-8alquilo C1-6, fenilo o heteroarilalquilo C1-6, donde el resto heteroarilo es un anillo aromático, monocíclico de 5 miembros que
comprende 1, 2, 3 o 4 heteroátomos seleccionados individualmente entre N, O y S, donde cualquier resto de cicloalquilo, fenilo o heteroarilo está opcionalmente sustituido con 1 o 2 sustituyentes que pueden ser iguales o diferentes seleccionados entre R16, donde R16 es ciano, halógeno, hidroxi, alquilo C1-4, haloalquilo C1-4, alcoxi C1-4, haloalcoxi C1-4 y alcoxicarbonilo C1-4; y
R15 es hidrógeno, metilo, etilo, alquinilo C3-4 o metoxietilo.
6. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 4, donde R8 es alquilo C1-6, haloalquilo C 1-2 , hidroxialquilo C 1-6, alcoxi C1-2alquilo C1-4, cicloalquilo C3-6 o heterociclilo, donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos seleccionados individualmente entre N y O, donde el cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1,2 o 3 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde R9 es ciano, halógeno, hidroxi, alquilo C1-4, alquenilo C2-4, alquinilo C2-4, haloalquilo C1-4 y alcoxi C1-4.
7. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 4 o 6, donde R8 es alquilo C1-4, haloalquilo C1-2, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-4, cicloalquilo C3-6 o heterociclilo, donde el resto heterociclilo es un anillo no aromático de 4 o 5 miembros que comprende 1 o 2 heteroátomos que son oxígeno, donde cicloalquilo C3-6 y heterociclilo están opcionalmente sustituidos con 1 o 2 sustituyentes, que pueden ser los mismos o diferentes, seleccionados entre R9 ; donde R9 representa ciano, flúor, cloro, hidroxi, metilo, etilo, trifluorometilo y metoxi.
8. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 4, 6 o 7, donde R8 es alquilo C1-4, 2,2,2-trifluoroetilo, hidroxialquilo C1-4, alcoxi C1-2alquilo C1-2, ciclopropilo o heterociclilo, donde el resto heterociclilo es tetrahidrofuran-2-ilo, oxetan-3-ilo o 1,3-dioxolan-2-ilo, donde ciclopropilo y heterociclilo están cada uno opcionalmente sustituidos con 1 o 2 sustituyentes, que pueden ser iguales o diferentes, seleccionados entre R9 , donde R9 es flúor, cloro y metilo.
9. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 5, donde R12 es alquilo C1-6, alquenilo C3-4 , alquinilo C3-4, fluoroalquilo C1-4, cloroalquilo C1-4, alcoxi C1-2alquilo C1-2, fenilo o bencilo.
10. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 5, donde R15 es hidrógeno, alquilo C1-6, alcoxi C1-6, alquenilo C2-4, alquinilo C2-4 o haloalquilo C1-2, cicloalquilo C3-6.
11. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 5 o 10, donde R15 es hidrógeno, metilo o etilo.
12. Una composición agroquímica que comprende una cantidad eficaz como fungicida de un compuesto de fórmula (I) de acuerdo con cualquiera de las reivindicaciones 1 a 11.
13. Una composición de acuerdo con la reivindicación 12, que además comprende al menos un principio activo adicional y/o un diluyente o portador agroquímicamente aceptable.
14. Un método para controlar o prevenir la infestación de plantas útiles por parte de microorganismos fitopatógenos, donde una cantidad eficaz como fungicida de un compuesto de fórmula (I) de acuerdo con cualquiera de las reivindicaciones 1 a 11, o una composición que comprende este compuesto como principio activo, se aplica a las plantas, a sus partes o a su emplazamiento.
15. Uso de un compuesto de fórmula (I) de acuerdo con una cualquiera de las reivindicaciones 1 a 11 como un fungicida, con la condición de que dicho uso excluya métodos de tratamiento del cuerpo humano o animal mediante cirugía o terapia.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15188238 | 2015-10-02 | ||
| EP16150491 | 2016-01-07 | ||
| PCT/EP2016/073295 WO2017055473A1 (en) | 2015-10-02 | 2016-09-29 | Microbiocidal oxadiazole derivatives |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2807849T3 true ES2807849T3 (es) | 2021-02-24 |
Family
ID=57018148
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16774508T Active ES2807849T3 (es) | 2015-10-02 | 2016-09-29 | Derivados de oxadiazol microbicidas |
Country Status (17)
| Country | Link |
|---|---|
| US (3) | US10899724B2 (es) |
| EP (1) | EP3356358B1 (es) |
| JP (1) | JP6864675B2 (es) |
| CN (1) | CN108137570B (es) |
| BR (1) | BR112018006623B1 (es) |
| CL (1) | CL2018000834A1 (es) |
| CO (1) | CO2018003840A2 (es) |
| DK (1) | DK3356358T3 (es) |
| ES (1) | ES2807849T3 (es) |
| HU (1) | HUE050030T2 (es) |
| IL (1) | IL258012B (es) |
| MX (1) | MX2018004038A (es) |
| PL (1) | PL3356358T3 (es) |
| SI (1) | SI3356358T1 (es) |
| UY (1) | UY36925A (es) |
| WO (1) | WO2017055473A1 (es) |
| ZA (1) | ZA201801828B (es) |
Families Citing this family (297)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108137517B (zh) | 2015-10-02 | 2022-04-12 | 先正达参股股份有限公司 | 杀微生物的噁二唑衍生物 |
| BR112018008608B1 (pt) | 2015-11-05 | 2022-05-17 | Basf Se | Uso de compostos de fórmula i, compostos de fórmula i, compostos, composição agroquímica e método para combater fungos nocivos fitopatogênicos |
| AU2016355949A1 (en) | 2015-11-19 | 2018-05-10 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| AU2016354902A1 (en) | 2015-11-19 | 2018-05-10 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| JP6930972B2 (ja) * | 2015-12-02 | 2021-09-01 | シンジェンタ パーティシペーションズ アーゲー | 殺微生物性オキサジアゾール誘導体 |
| AU2017250397A1 (en) * | 2016-04-11 | 2018-10-11 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| WO2017211652A1 (en) | 2016-06-09 | 2017-12-14 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| EP3468958B1 (en) | 2016-06-09 | 2020-12-16 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| WO2017211650A1 (en) | 2016-06-09 | 2017-12-14 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| AR108745A1 (es) | 2016-06-21 | 2018-09-19 | Syngenta Participations Ag | Derivados de oxadiazol microbiocidas |
| AR109304A1 (es) * | 2016-08-10 | 2018-11-21 | Sumitomo Chemical Co | Compuesto de oxadiazol y su uso |
| JP2020023442A (ja) * | 2016-12-19 | 2020-02-13 | 住友化学株式会社 | オキサジアゾール化合物及び植物病害防除方法 |
| UY37623A (es) | 2017-03-03 | 2018-09-28 | Syngenta Participations Ag | Derivados de oxadiazol tiofeno fungicidas |
| CA3055680A1 (en) * | 2017-03-31 | 2018-10-04 | Syngenta Participations Ag | Fungicidal compositions |
| WO2018177880A1 (en) | 2017-03-31 | 2018-10-04 | Syngenta Participations Ag | Fungicidal compositions |
| BR112019020734B1 (pt) | 2017-04-05 | 2023-12-05 | Syngenta Participations Ag | Compostos derivados de oxadiazol, composição agroquímica, método para controlar ou prevenir a infestação de plantas úteis por microrganismos fitopatogênicos e uso dos referidos compostos |
| WO2018184987A1 (en) | 2017-04-05 | 2018-10-11 | Syngenta Participations Ag | Microbiocidal oxadiazole derivatives |
| WO2018184982A1 (en) | 2017-04-05 | 2018-10-11 | Syngenta Participations Ag | Microbiocidal oxadiazole derivatives |
| BR112019020739B1 (pt) | 2017-04-05 | 2023-12-19 | Syngenta Participations Ag | Compostos derivados de oxadiazol microbiocidas e seu uso, composição agroquímica, método para controlar ou prevenir a infestação de plantas úteis por microrganismos fitopatogênicos |
| WO2018184984A1 (en) | 2017-04-05 | 2018-10-11 | Syngenta Participations Ag | Microbiocidal oxadiazole derivatives |
| WO2018184988A1 (en) | 2017-04-05 | 2018-10-11 | Syngenta Participations Ag | Microbiocidal oxadiazole derivatives |
| TWI886480B (zh) * | 2017-04-06 | 2025-06-11 | 美商富曼西公司 | 殺真菌之噁二唑 |
| EP3606912A1 (en) | 2017-04-07 | 2020-02-12 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| WO2018188962A1 (en) | 2017-04-11 | 2018-10-18 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| JP7160487B2 (ja) | 2017-05-04 | 2022-10-25 | ビーエーエスエフ ソシエタス・ヨーロピア | 植物病原菌を駆除するための置換5-(ハロアルキル)-5-ヒドロキシ-イソオキサゾール |
| WO2018202491A1 (en) | 2017-05-04 | 2018-11-08 | Basf Se | Substituted trifluoromethyloxadiazoles for combating phytopathogenic fungi |
| WO2018219773A1 (en) | 2017-06-02 | 2018-12-06 | Syngenta Participations Ag | Fungicidal compositions |
| WO2018219797A1 (en) | 2017-06-02 | 2018-12-06 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| WO2018228896A1 (en) | 2017-06-14 | 2018-12-20 | Syngenta Participations Ag | Fungicidal compositions |
| JP7171634B2 (ja) | 2017-06-28 | 2022-11-15 | シンジェンタ パーティシペーションズ アーゲー | 殺菌性組成物 |
| AR112221A1 (es) * | 2017-07-05 | 2019-10-02 | Fmc Corp | Oxadiazoles fungicidas, composición que los comprende y un método para controlar fitoenfermedades que los emplea |
| EP3658543A1 (en) | 2017-07-28 | 2020-06-03 | Basf Se | Preparation of substituted 3-aryl-5-trifluoromethyl-1,2,4-oxadiazoles |
| WO2019025250A1 (en) * | 2017-08-04 | 2019-02-07 | Basf Se | SUBSTITUTED TRIFLUOROMETHYLOXADIAZOLES FOR COMBATING PHYTOPATHOGENIC FUNGI |
| WO2019131867A1 (ja) | 2017-12-28 | 2019-07-04 | 日本農薬株式会社 | オキサジアゾール化合物又はその塩類及び該化合物を含有する農園芸用殺菌剤並びにその使用方法 |
| US11286242B2 (en) | 2018-01-30 | 2022-03-29 | Pi Industries Ltd. | Oxadiazoles for use in controlling phytopathogenic fungi |
| EP3762367A1 (en) | 2018-03-09 | 2021-01-13 | PI Industries Ltd. | Heterocyclic compounds as fungicides |
| CN112041317A (zh) * | 2018-04-26 | 2020-12-04 | 先正达参股股份有限公司 | 杀微生物的噁二唑衍生物 |
| WO2019207062A1 (en) | 2018-04-26 | 2019-10-31 | Syngenta Participations Ag | Microbiocidal oxadiazole derivatives |
| BR112020023915A2 (pt) | 2018-05-25 | 2021-02-09 | Syngenta Participations Ag | derivados de picolinamida microbiocidas |
| CN112351981A (zh) | 2018-06-29 | 2021-02-09 | 先正达农作物保护股份公司 | 杀微生物的噁二唑衍生物 |
| EP3818058A1 (en) | 2018-07-02 | 2021-05-12 | Syngenta Crop Protection AG | 3-(2-thienyl)-5-(trifluoromethyl)-1,2,4-oxadiazole derivatives as agrochemical fungicides |
| EP3823966A1 (en) | 2018-07-16 | 2021-05-26 | Syngenta Crop Protection AG | Microbiocidal oxadiazole derivatives |
| GB201812692D0 (en) | 2018-08-03 | 2018-09-19 | Syngenta Participations Ag | Microbiocidal compounds |
| WO2020032071A1 (ja) | 2018-08-08 | 2020-02-13 | 日本農薬株式会社 | オキサジアゾリン化合物又はその塩類及び該化合物を含有する農園芸用殺菌剤並びにその使用方法 |
| PY1974248A (es) | 2018-09-13 | 2020-08-21 | Syngenta Participations Ag | Compuestos de azol-amida pesticidamente activos |
| PY1974629A (es) | 2018-09-13 | 2021-01-11 | Syngenta Participations Ag | Compuestos de azol-amida pesticidamente activos |
| PY1981411A (es) | 2018-10-01 | 2020-04-09 | Pi Industries Ltd | Nuevos oxadiazoles |
| CN113195461A (zh) | 2018-10-01 | 2021-07-30 | Pi工业有限公司 | 新型恶二唑类化合物 |
| AR116628A1 (es) | 2018-10-18 | 2021-05-26 | Syngenta Crop Protection Ag | Compuestos microbiocidas |
| PY1986700A (es) | 2018-10-19 | 2020-08-28 | Syngenta Participations Ag | Compuestos de azol-amida pesticidamente activos |
| EP3877380A1 (en) | 2018-11-05 | 2021-09-15 | Syngenta Participations Ag | Pesticidally active azole-amide compounds |
| PY1999867A (es) | 2018-11-30 | 2020-10-19 | Syngenta Crop Protection Ag | Derivados de tiazol microbiocidas |
| AR117200A1 (es) | 2018-11-30 | 2021-07-21 | Syngenta Participations Ag | Derivados de tiazol microbiocidas |
| CN109651183A (zh) * | 2019-01-18 | 2019-04-19 | 广东工业大学 | 一种新型酰胺菊酯类化学修饰物及其制备方法和应用 |
| WO2020165403A1 (en) | 2019-02-15 | 2020-08-20 | Syngenta Crop Protection Ag | Phenyl substituted thiazole derivatives as microbiocidal compounds |
| WO2020169526A1 (en) | 2019-02-18 | 2020-08-27 | Syngenta Crop Protection Ag | Pesticidally-active cyanamide heterocyclic compounds |
| EP3696175A1 (en) | 2019-02-18 | 2020-08-19 | Syngenta Crop Protection AG | Pesticidally active azole-amide compounds |
| US20220167618A1 (en) | 2019-03-08 | 2022-06-02 | Syngenta Crop Protection Ag | Pesticidally active azole-amide compounds |
| BR112021018501A2 (pt) | 2019-03-20 | 2021-11-30 | Syngenta Crop Protection Ag | Compostos de azolamida ativos em termos pesticidas |
| CN113597424B (zh) | 2019-03-20 | 2025-04-18 | 先正达农作物保护股份公司 | 杀有害生物活性的唑酰胺化合物 |
| BR112021018822A2 (pt) | 2019-03-22 | 2021-11-23 | Syngenta Crop Protection Ag | Derivados de n-[1-(5-bromo-2-pirimidin-2-il-1,2,4-triazol-3-il)etil]-2-ciclopropil-6-(trifluorometil)piridina-4-carboxamida e compostos relacionados como inseticidas |
| GB201903942D0 (en) | 2019-03-22 | 2019-05-08 | Syngenta Crop Protection Ag | Microbiocidal compounds |
| EP3947371B1 (en) | 2019-03-27 | 2023-11-22 | Syngenta Crop Protection AG | Microbiocidal thiazole derivatives |
| TWI853009B (zh) | 2019-03-29 | 2024-08-21 | 瑞士商先正達農作物保護公司 | 殺有害生物活性之二-醯胺化合物 |
| MA55500A (fr) | 2019-04-05 | 2022-02-09 | Syngenta Crop Protection Ag | Composés de diazine-amide à action pesticide |
| WO2020208095A1 (en) | 2019-04-10 | 2020-10-15 | Syngenta Crop Protection Ag | Microbiocidal picolinamide derivatives |
| MX2021012352A (es) | 2019-04-10 | 2022-01-18 | Syngenta Crop Protection Ag | Composiciones fungicidas. |
| BR112021020386A2 (pt) | 2019-04-11 | 2021-12-07 | Syngenta Crop Protection Ag | Compostos de diazina-amida ativos pesticidamente |
| AR118673A1 (es) * | 2019-04-18 | 2021-10-20 | Syngenta Crop Protection Ag | Procedimiento para la preparación de derivados de oxadiazol microbiocidas |
| US12528778B2 (en) | 2019-05-29 | 2026-01-20 | Syngenta Crop Protection Ag | Microbiocidal derivatives |
| WO2020239855A1 (en) | 2019-05-29 | 2020-12-03 | Syngenta Crop Protection Ag | Microbiocidal derivatives |
| AR119009A1 (es) | 2019-05-29 | 2021-11-17 | Syngenta Crop Protection Ag | Derivados de alcoxipiridina y alcoxipirimidina microbicidas |
| AR119011A1 (es) | 2019-05-29 | 2021-11-17 | Syngenta Crop Protection Ag | DERIVADOS DE [1,3]DIOXOLO[4,5-c]PIRIDIN-4-CARBOXAMIDA, COMPOSICIONES AGROQUÍMICAS QUE LOS COMPRENDEN Y SU EMPLEO COMO FUNGICIDA PARA CONTROLAR O PREVENIR LA INFESTACIÓN DE PLANTAS ÚTILES |
| WO2020254530A1 (en) | 2019-06-18 | 2020-12-24 | Syngenta Crop Protection Ag | 7-sulfonyl-n-(1,3,4-thiadiazol-2-yl)-quinoxaline-6-carboxamide derivatives and the respective -benzimidazole-5-, -imidazo[4,5-b]pyridine-5-, -3h-furo[3,2b]pyridine-5-, -quinoline-2-, and -naphthalene-2-carboxamide derivatives as pesticides |
| WO2020256113A1 (ja) | 2019-06-21 | 2020-12-24 | 日本農薬株式会社 | オキサジアゾール化合物又はその塩類及び該化合物を含有する農園芸用殺菌剤並びにその使用方法 |
| WO2023061838A1 (en) | 2021-10-14 | 2023-04-20 | Syngenta Crop Protection Ag | Imidazo[1,2-a]pyridine derivatives |
| WO2021004968A1 (en) | 2019-07-05 | 2021-01-14 | Syngenta Crop Protection Ag | Microbiocidal picolinamide derivatives |
| GB201910037D0 (en) | 2019-07-12 | 2019-08-28 | Syngenta Crop Protection Ag | Microbiocidal compounds |
| US12376512B2 (en) | 2019-08-21 | 2025-08-05 | Syngenta Crop Protection Ag | Precision treatment and sowing or planting method and device |
| CA3147089A1 (en) | 2019-08-21 | 2021-02-25 | Jamie RICKARD | Sowing device and method for treating seeds during planting |
| WO2021032634A1 (en) | 2019-08-21 | 2021-02-25 | Syngenta Participations Ag | Apparatus and method for reducing dust development in precision drill sowing |
| BR112022003060A2 (pt) | 2019-08-21 | 2022-05-10 | Syngenta Participations Ag | Aparelho e método para conversão de equipamentos de semeadura existentes |
| EP4017243A1 (en) | 2019-08-21 | 2022-06-29 | Syngenta Participations Ag | High precision greenhouse seed and seedling treatment |
| BR112022003375A2 (pt) | 2019-08-23 | 2022-05-17 | Syngenta Crop Protection Ag | Compostos de pirazina-amida pesticidamente ativos |
| GB201912595D0 (en) | 2019-09-02 | 2019-10-16 | Syngenta Crop Protection Ag | Plant growth regulator compounds |
| UY38885A (es) | 2019-09-20 | 2021-04-30 | Syngenta Crop Protection Ag | Compuestos de azetidinil-, pirrolidinil-,piperdinil- o piperazinil-piridinil carbonilo pesticidamente activos |
| ES2979156T3 (es) | 2019-09-20 | 2024-09-24 | Syngenta Crop Protection Ag | Derivados heterocíclicos plaguicidamente activos con sustituyentes que contienen azufre y sulfoximina |
| CN114630825B (zh) | 2019-11-01 | 2025-05-16 | 先正达农作物保护股份公司 | 杀有害生物活性的稠合二环杂芳香族化合物 |
| US12336535B2 (en) | 2019-11-07 | 2025-06-24 | Nihon Nohyaku Co., Ltd. | Oxadiazoline compound or salts thereof, agricultural and horticultural fungicide containing said compound, and method for using same |
| US20230053607A1 (en) | 2019-12-04 | 2023-02-23 | Syngenta Crop Protection Ag | Pesticidally active fused bicyclic heteroaromatic amino compounds |
| WO2021122645A1 (en) | 2019-12-20 | 2021-06-24 | Syngenta Crop Protection Ag | Pesticidally active azole-amide compounds |
| JP2023510175A (ja) | 2019-12-31 | 2023-03-13 | シンジェンタ クロップ プロテクション アクチェンゲゼルシャフト | 硫黄含有置換基を有する殺有害生物的に活性な複素環式誘導体 |
| TW202132300A (zh) | 2020-01-06 | 2021-09-01 | 瑞士商先正達農作物保護公司 | 具有含硫取代基的殺有害生物活性雜環衍生物 |
| WO2021144354A1 (en) | 2020-01-15 | 2021-07-22 | Syngenta Crop Protection Ag | Pesticidally-active bicyclic heteroaromatic compounds |
| BR112022014313A2 (pt) | 2020-01-24 | 2022-09-20 | Syngenta Crop Protection Ag | Compostos heteroaromáticos bicíclicos fundidos ativos em termos pesticidas |
| WO2021151926A1 (en) | 2020-01-30 | 2021-08-05 | Syngenta Crop Protection Ag | Pesticidally active fused bicyclic heteroaromatic amino compounds |
| US20230146180A1 (en) | 2020-02-11 | 2023-05-11 | Syngenta Crop Protection Ag | Pesticidally active cyclic amine compounds |
| JP2023515979A (ja) | 2020-02-27 | 2023-04-17 | シンジェンタ クロップ プロテクション アクチェンゲゼルシャフト | 殺有害生物的に活性なジアジン-ビスアミド化合物 |
| WO2021175822A1 (en) | 2020-03-02 | 2021-09-10 | Syngenta Crop Protection Ag | Pesticidally amidine-substituted benzoic acid amide compounds |
| UY39114A (es) | 2020-03-05 | 2021-10-29 | Syngenta Crop Protection Ag | Mezclas fungicidas de derivados de arilo metoxiacrilato |
| UY39115A (es) | 2020-03-05 | 2021-10-29 | Syngenta Crop Protection Ag | Mezclas fungicidas de derivados de arilo metoxiacrilato |
| EP4117433A1 (en) | 2020-03-13 | 2023-01-18 | Syngenta Crop Protection AG | Methods of controlling or preventing infestation of plants by the phytopathogenic microorganism corynespora cassiicola |
| EP4117438A1 (en) | 2020-03-13 | 2023-01-18 | Syngenta Crop Protection AG | Methods of controlling or preventing infestation of plants by the phytopathogenic microorganism corynespora cassiicola |
| CN115334885B (zh) | 2020-03-13 | 2025-04-18 | 先正达农作物保护股份公司 | 控制或预防植物被植物病原性微生物多主棒孢菌、大豆灰斑病菌和/或大豆紫斑病菌侵染的方法 |
| JP2023516796A (ja) | 2020-03-13 | 2023-04-20 | シンジェンタ クロップ プロテクション アクチェンゲゼルシャフト | 植物病原性微生物コリネスポラ・カッシコーラ(Corynespora cassiicola)による植物の被害を防除又は防止する方法 |
| BR112022018267A2 (pt) | 2020-03-13 | 2022-10-25 | Syngenta Crop Protection Ag | Métodos de controle ou prevenção de infestação de plantas pelo microrganismo fitopatogênico corynespora cassiicola |
| EP4117437A1 (en) | 2020-03-13 | 2023-01-18 | Syngenta Crop Protection AG | Methods of controlling or preventing infestation of plants by the phytopathogenic microorganism corynespora cassiicola |
| CN115443273A (zh) | 2020-04-08 | 2022-12-06 | 先正达农作物保护股份公司 | 杀微生物喹啉二氢-(噻嗪)噁嗪衍生物 |
| AR121733A1 (es) | 2020-04-08 | 2022-07-06 | Syngenta Crop Protection Ag | Derivados microbiocidas de tipo dihidro-(tiazina)oxazina de quinolina |
| AR121734A1 (es) | 2020-04-08 | 2022-07-06 | Syngenta Crop Protection Ag | Derivados microbicidas de tipo dihidropirrolopirazina de quinolina |
| WO2021213929A1 (en) | 2020-04-20 | 2021-10-28 | Syngenta Crop Protection Ag | Pesticidally active substituted 1,3-dihydro-2h-imidazo[4,5-c]pyridin-2-one derivatives with sulfur containing substituents |
| GB202006386D0 (en) | 2020-04-30 | 2020-06-17 | Syngenta Crop Protection Ag | Microbiocidal Compounds |
| GB202006399D0 (en) | 2020-04-30 | 2020-06-17 | Syngenta Crop Protection Ag | Microbiocidal compounds |
| BR112022021895A2 (pt) | 2020-04-30 | 2023-01-24 | Syngenta Crop Protection Ag | Derivados heterocíclicos com substituintes contendo enxofre ativos em termos pesticidas |
| GB202006480D0 (en) | 2020-05-01 | 2020-06-17 | Syngenta Crop Protection Ag | Microbiocidal compounds |
| GB202006606D0 (en) | 2020-05-05 | 2020-06-17 | Syngenta Crop Protection Ag | Microbiocidal compounds |
| WO2021224409A1 (en) | 2020-05-06 | 2021-11-11 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| MX2022015065A (es) | 2020-06-03 | 2023-01-11 | Syngenta Crop Protection Ag | Composiciones fungicidas. |
| BR112022024661A2 (pt) | 2020-06-03 | 2022-12-27 | Syngenta Crop Protection Ag | Derivados microbiocidas |
| GEP20257723B (en) | 2020-06-03 | 2025-01-27 | Syngenta Crop Protection Ag | Fungicidal compositions |
| WO2022013417A1 (en) | 2020-07-17 | 2022-01-20 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| WO2022017975A1 (en) | 2020-07-18 | 2022-01-27 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| CN116018344B (zh) | 2020-08-31 | 2026-03-03 | 先正达农作物保护股份公司 | 具有含硫取代基的杀有害生物活性的杂环衍生物 |
| EP4208463A1 (en) | 2020-09-01 | 2023-07-12 | Syngenta Crop Protection AG | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| WO2022049146A1 (en) | 2020-09-02 | 2022-03-10 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| GB202013756D0 (en) | 2020-09-02 | 2020-10-14 | Syngenta Crop Protection Ag | Plant growth regulator compounds |
| WO2022049144A1 (en) | 2020-09-02 | 2022-03-10 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| UY39411A (es) | 2020-09-09 | 2022-04-29 | Syngenta Crop Protection Ag | Derivados de indazolil pirazolo[3,4-c] piridina pesticídicamente activos con sustituyentes que contienen azufre |
| GB202014840D0 (en) | 2020-09-21 | 2020-11-04 | Syngenta Crop Protection Ag | Microbiocidal compounds |
| EP4232440A1 (en) | 2020-10-22 | 2023-08-30 | Syngenta Crop Protection AG | Zealactone derivatives as plant growth regulators |
| WO2022101265A1 (en) | 2020-11-13 | 2022-05-19 | Syngenta Crop Protection Ag | Pesticidally active fused bicyclic heteroaromatic compounds |
| WO2022117650A1 (en) | 2020-12-02 | 2022-06-09 | Syngenta Crop Protection Ag | Fungicidal compositions |
| PY21103556A (es) * | 2020-12-02 | 2023-05-03 | Syngenta Crop Protection Ag | Composiciones fungicidas |
| WO2022128554A1 (en) * | 2020-12-15 | 2022-06-23 | Basf Se | Mixtures containing n-methoxy-n-[[4-[5-(trifluoromethyl)-1,2,4-oxadiazol-3-yl]phenyl]methyl]cyclopropanecarboxamide |
| PY2203251A (es) | 2021-01-21 | 2023-01-18 | Syngenta Crop Protection Ag | Derivados heterocíclicos activos como plaguicidas con sustituyentes que contienen azufre |
| US20240397947A1 (en) | 2021-01-22 | 2024-12-05 | Syngenta Crop Protection Ag | Method for the control or suppression of phytopathogenic bacteria |
| WO2022157188A2 (en) | 2021-01-23 | 2022-07-28 | Syngenta Crop Protection Ag | Pesticidally active heteroaromatic compounds |
| BR112023019532A2 (pt) | 2021-03-27 | 2023-10-31 | Syngenta Crop Protection Ag | Derivados de amida isonicotínicos microbicidas |
| US20240217950A1 (en) | 2021-03-30 | 2024-07-04 | Syngenta Crop Protection Ag | Pesticidally active cyclic amine compounds |
| WO2022207496A1 (en) * | 2021-03-30 | 2022-10-06 | Bayer Aktiengesellschaft | 3-(hetero)aryl-5-chlorodifluoromethyl-1,2,4-oxadiazole as fungicide |
| PY2222114A (es) | 2021-03-31 | 2023-01-19 | Syngenta Crop Protection Ag | Derivados microbiocidas de quinolin/quinoxalin-benzotiazina |
| AR125342A1 (es) | 2021-04-16 | 2023-07-05 | Syngenta Crop Protection Ag | Compuestos de amina cíclica activos como plaguicidas |
| AU2022260028A1 (en) | 2021-04-20 | 2023-10-12 | Syngenta Crop Protection Ag | Microbiocidal quinoline/quinoxaline isoquinoline derivatives |
| BR112023022979A2 (pt) | 2021-05-04 | 2024-01-23 | Syngenta Crop Protection Ag | Uso de cletodim para controle de insetos |
| CR20230559A (es) | 2021-06-01 | 2024-01-22 | Syngenta Crop Protection Ag | Derivados de tetrahidroisoquinolina microbiocida |
| WO2022253841A1 (en) | 2021-06-02 | 2022-12-08 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfoximine containing substituents |
| WO2022258481A1 (en) | 2021-06-09 | 2022-12-15 | Syngenta Crop Protection Ag | Pesticidally active diazine-amide compounds |
| EP4359408A1 (en) | 2021-06-24 | 2024-05-01 | Syngenta Crop Protection AG | 2-[3-[1 [(quinazolin-4-yl)amino]ethyl]pyrazin-2-yl]thiazole-5-carbonitrile derivatives and similar compounds as pesticides |
| US20240306639A1 (en) | 2021-07-02 | 2024-09-19 | Syngenta Crop Protection Ag | Use of fluazifop-p-butyl for insect control |
| JP2024528002A (ja) | 2021-07-27 | 2024-07-26 | シンジェンタ クロップ プロテクション アクチェンゲゼルシャフト | ジアミド耐性有害生物の防除のための方法及びそのための化合物 |
| US20240327397A1 (en) | 2021-07-29 | 2024-10-03 | Syngenta Crop Protection Ag | Pesticidally Active Fused Bicyclic Heteroaromatic Compounds |
| BR112024001979A2 (pt) | 2021-08-02 | 2024-04-30 | Syngenta Crop Protection Ag | Derivados de pirazol microbicidas |
| WO2023012081A1 (en) | 2021-08-05 | 2023-02-09 | Syngenta Crop Protection Ag | Method for controlling diamide resistant pests & compounds therefor |
| AR126729A1 (es) | 2021-08-10 | 2023-11-08 | Syngenta Crop Protection Ag | Mezcla fungicida |
| US20250145640A1 (en) | 2021-08-10 | 2025-05-08 | Syngenta Crop Protection Ag | 2,2-difluoro-5h-[1,3]dioxolo[4,5-f]isoindol-7-one derivatives as pesticides |
| AR126789A1 (es) | 2021-08-19 | 2023-11-15 | Syngenta Crop Protection Ag | Método para controlar plagas resistentes a diamidas y compuestos para esto |
| UY39992A (es) | 2021-10-25 | 2023-05-15 | Syngenta Crop Protection Ag | Derivados heterocíclicos activos como plaguicidas con sustituyentes que contienen azufre |
| WO2023072849A1 (en) | 2021-10-27 | 2023-05-04 | Syngenta Crop Protection Ag | Pesticidally active pyridazinone compounds |
| MX2024004741A (es) | 2021-10-29 | 2024-05-14 | Syngenta Crop Protection Ag | Composiciones fungicidas que comprenden fludioxonil. |
| CN118368985A (zh) | 2021-10-29 | 2024-07-19 | 先正达农作物保护股份公司 | 杀真菌组合物 |
| CN118265702A (zh) | 2021-11-19 | 2024-06-28 | 先正达农作物保护股份公司 | 杀微生物的异烟酰胺衍生物 |
| WO2023094304A1 (en) | 2021-11-25 | 2023-06-01 | Syngenta Crop Protection Ag | Microbiocidal heterobiaryl amide derivatives |
| WO2023094303A1 (en) | 2021-11-25 | 2023-06-01 | Syngenta Crop Protection Ag | Microbiocidal heterobiaryl amide derivatives |
| WO2023099460A1 (en) | 2021-12-02 | 2023-06-08 | Syngenta Crop Protection Ag | Fungicidal compositions |
| US20250049033A1 (en) | 2021-12-10 | 2025-02-13 | Syngenta Crop Protection Ag | Pesticidally active pyridazinone compounds |
| WO2023110710A1 (en) | 2021-12-13 | 2023-06-22 | Syngenta Crop Protection Ag | Method for controlling diamide resistant pests & compounds therefor |
| AR127922A1 (es) | 2021-12-15 | 2024-03-13 | Syngenta Crop Protection Ag | Derivados heterocíclicos bicíclicos microbiocidas |
| EP4197333A1 (en) | 2021-12-15 | 2023-06-21 | Syngenta Crop Protection AG | Method for controlling diamide resistant pests & compounds therefor |
| WO2023111215A1 (en) | 2021-12-17 | 2023-06-22 | Syngenta Crop Protection Ag | Microbiocidal pyridine-substituted benzothiazine derivatives |
| JP2024546902A (ja) | 2021-12-17 | 2024-12-26 | シンジェンタ クロップ プロテクション アクチェンゲゼルシャフト | 殺菌性組成物 |
| WO2023110871A1 (en) | 2021-12-17 | 2023-06-22 | Syngenta Crop Protection Ag | Microbiocidal pyrazole derivatives |
| WO2023118434A1 (en) | 2021-12-22 | 2023-06-29 | Globachem Nv | Pesticidally active amide compounds |
| AU2022423908A1 (en) | 2021-12-22 | 2024-06-20 | Syngenta Crop Protection Ag | Fungicidal compositions |
| WO2023118011A1 (en) | 2021-12-22 | 2023-06-29 | Syngenta Crop Protection Ag | Microbiocidal aza-heterobiaryl derivatives |
| WO2023139166A1 (en) | 2022-01-19 | 2023-07-27 | Syngenta Crop Protection Ag | Methods for controlling plant pathogens |
| WO2023148206A1 (en) | 2022-02-02 | 2023-08-10 | Syngenta Crop Protection Ag | Microbiocidal n-amide derivatives |
| WO2023148368A1 (en) | 2022-02-07 | 2023-08-10 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| UY40139A (es) | 2022-02-07 | 2023-08-31 | Syngenta Crop Protection Ag | Derivados de imidazo[1,2-a]piridin-2-il]-1-pirazolo[3,4-c]piridina activos como pesticidas con susti |
| WO2023166067A1 (en) | 2022-03-02 | 2023-09-07 | Syngenta Crop Protection Ag | Microbiocidal pyridazinone amide derivatives |
| UY40202A (es) | 2022-04-01 | 2023-10-31 | Syngenta Crop Protection Ag | Derivados de pirazolopiridina activos como pesticidas con sustituyentes que contienen azufre |
| PY2331003A (es) | 2022-04-29 | 2024-08-28 | Syngenta Crop Protection Ag | Composiciones fungicidas |
| AR129265A1 (es) | 2022-05-12 | 2024-08-07 | Syngenta Crop Protection Ag | Compuestos de alcoxi-heteroaril-carboxamida o tioamida |
| AR129535A1 (es) | 2022-06-21 | 2024-09-04 | Syngenta Crop Protection Ag | Derivados de carboxamida heterocíclicos bicíclicos microbiocidas |
| CN119421880A (zh) | 2022-06-21 | 2025-02-11 | 先正达农作物保护股份公司 | 杀有害生物活性的稠合二环杂芳香族化合物 |
| AU2023303685A1 (en) | 2022-07-07 | 2024-12-12 | Syngenta Crop Protection Ag | Precision application devices and compositions |
| WO2024018016A1 (en) | 2022-07-21 | 2024-01-25 | Syngenta Crop Protection Ag | Crystalline forms of 1,2,4-oxadiazole fungicides |
| WO2024017788A1 (en) | 2022-07-22 | 2024-01-25 | Syngenta Crop Protection Ag | Solid form of a heterocyclic amide derivative |
| WO2024022910A1 (en) | 2022-07-26 | 2024-02-01 | Syngenta Crop Protection Ag | 1-[1-[2-(pyrimidin-4-yl)-1,2,4-triazol-3-yl]ethyl]-3-[2,4-dichloro-5-phenyl]urea derivatives and similar compounds as pesticides |
| WO2024033374A1 (en) | 2022-08-11 | 2024-02-15 | Syngenta Crop Protection Ag | Novel arylcarboxamide or arylthioamide compounds |
| TW202412626A (zh) | 2022-08-16 | 2024-04-01 | 瑞士商先正達農作物保護股份公司 | 新用途 |
| EP4587430A1 (en) | 2022-09-16 | 2025-07-23 | Syngenta Crop Protection AG | Pesticidally active cyclic amine compounds |
| EP4295688A1 (en) * | 2022-09-28 | 2023-12-27 | Bayer Aktiengesellschaft | Active compound combination |
| WO2024068518A1 (en) | 2022-09-28 | 2024-04-04 | Bayer Aktiengesellschaft | 3-heteroaryl-5-chlorodifluoromethyl-1,2,4-oxadiazole as fungicide |
| AR130569A1 (es) | 2022-09-28 | 2024-12-18 | Syngenta Crop Protection Ag | Composiciones fungicidas |
| WO2024068655A1 (en) | 2022-09-28 | 2024-04-04 | Syngenta Crop Protection Ag | Fungicidal compositions |
| GB202214203D0 (en) | 2022-09-28 | 2022-11-09 | Syngenta Crop Protection Ag | Fungicidal compositions |
| TW202430031A (zh) | 2022-09-30 | 2024-08-01 | 瑞士商先正達農作物保護股份公司 | 殺微生物之吡唑衍生物 |
| TW202430514A (zh) | 2022-09-30 | 2024-08-01 | 瑞士商先正達農作物保護股份公司 | 殺微生物之吡唑衍生物 |
| CN120112521A (zh) | 2022-10-25 | 2025-06-06 | 先正达农作物保护股份公司 | 具有含硫取代基的杀有害生物活性的杂环衍生物 |
| WO2024089216A1 (en) | 2022-10-27 | 2024-05-02 | Syngenta Crop Protection Ag | Novel sulfur-containing heteroaryl carboxamide compounds |
| CN120476119A (zh) | 2022-10-27 | 2025-08-12 | 先正达农作物保护股份公司 | 杀微生物的杂双环二氢噁二嗪衍生物 |
| CN120112528A (zh) | 2022-10-31 | 2025-06-06 | 先正达农作物保护股份公司 | 具有含硫取代基的杀有害生物活性的杂环衍生物 |
| WO2024100069A1 (en) | 2022-11-08 | 2024-05-16 | Syngenta Crop Protection Ag | Microbiocidal pyridine derivatives |
| PY2389146A (es) | 2022-11-09 | 2025-06-23 | Syngenta Crop Protection Ag | Derivados de pirazol microbiocidas |
| TW202434579A (zh) | 2022-11-16 | 2024-09-01 | 瑞士商先正達農作物保護股份公司 | 殺微生物的四氫異喹啉衍生物 |
| CN120344511A (zh) | 2022-11-29 | 2025-07-18 | 先正达农作物保护股份公司 | 杀微生物的四氢异喹啉衍生物 |
| TW202439972A (zh) | 2022-11-30 | 2024-10-16 | 瑞士商先正達農作物保護股份公司 | 殺真菌組成物 |
| EP4626882A1 (en) | 2022-11-30 | 2025-10-08 | Syngenta Crop Protection AG | Microbiocidal tetrahydroisoquinoline derivatives |
| WO2024126388A1 (en) | 2022-12-12 | 2024-06-20 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| EP4634178A1 (en) | 2022-12-14 | 2025-10-22 | Syngenta Crop Protection AG | Imidazo[1,2-a]pyridine derivatives |
| WO2024126650A1 (en) | 2022-12-15 | 2024-06-20 | Syngenta Crop Protection Ag | Novel bicyclic-carboxamide compounds useful as pesticides |
| CN120359205A (zh) | 2022-12-16 | 2025-07-22 | 先正达农作物保护股份公司 | 苯并咪唑衍生物 |
| WO2024132901A1 (en) | 2022-12-19 | 2024-06-27 | Syngenta Crop Protection Ag | Microbiocidal pyridazine dihydrooxadiazine derivatives |
| WO2024132895A1 (en) | 2022-12-19 | 2024-06-27 | Syngenta Crop Protection Ag | Microbiocidal dihydrooxadiazinyl pyridazinone compounds |
| WO2024133426A1 (en) | 2022-12-21 | 2024-06-27 | Syngenta Crop Protection Ag | Method for controlling diamide resistant pests and compounds therefor |
| WO2024133551A1 (en) | 2022-12-21 | 2024-06-27 | Syngenta Crop Protection Ag | Pesticidally active pyridazine compounds |
| AR131541A1 (es) | 2023-01-07 | 2025-04-09 | Syngenta Crop Protection Ag | Compuestos de carboxamida novedosos |
| WO2024156664A1 (en) | 2023-01-23 | 2024-08-02 | Syngenta Crop Protection Ag | Pesticidally active heterocyclic derivatives with sulfur containing substituents |
| PY2403614A (es) | 2023-01-27 | 2025-09-11 | Syngenta Crop Protection Ag | Derivados de pirazol microbiocidas |
| AR131665A1 (es) | 2023-02-01 | 2025-04-16 | Syngenta Crop Protection Ag | Composiciones fungicidas |
| WO2024170339A1 (en) | 2023-02-13 | 2024-08-22 | Syngenta Crop Protection Ag | Pesticidally active bicyclic compounds |
| WO2024170484A1 (en) | 2023-02-13 | 2024-08-22 | Globachem Nv | Pesticidally active amide compounds |
| WO2024170365A1 (en) | 2023-02-14 | 2024-08-22 | Syngenta Crop Protection Ag | Composition comprising cyprodinil and lactose-based filler |
| WO2025201636A1 (en) | 2023-03-31 | 2025-10-02 | Syngenta Crop Protection Ag | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2024213651A1 (en) | 2023-04-13 | 2024-10-17 | Syngenta Crop Protection Ag | Imidazo[1,2-a]pyridine derivatives |
| PY2427467A (es) | 2023-04-13 | 2025-10-14 | Syngenta Crop Protection Ag | Derivados de pirazolo [1,5-a]piridina |
| PY2426847A (es) | 2023-04-13 | 2025-03-20 | Syngenta Crop Protection Ag | Derivados bicíclicos de imidazo |
| CN121002016A (zh) | 2023-04-13 | 2025-11-21 | 先正达农作物保护股份公司 | 咪唑并[1,2-a]吡啶衍生物 |
| AR132352A1 (es) | 2023-04-13 | 2025-06-18 | Syngenta Crop Protection Ag | Derivados de imidazo[1,2-a]pirazina |
| AR132354A1 (es) | 2023-04-13 | 2025-06-18 | Syngenta Crop Protection Ag | Derivados de pirazolo[1,5-a]piridina |
| WO2024213650A1 (en) | 2023-04-13 | 2024-10-17 | Syngenta Crop Protection Ag | Imidazo[1,2-a]pyridine derivatives |
| AR132351A1 (es) | 2023-04-13 | 2025-06-18 | Syngenta Crop Protection Ag | Derivados de imidazo[1,2-a]pirazina |
| TW202446263A (zh) | 2023-04-13 | 2024-12-01 | 瑞士商先正達農作物保護股份公司 | 殺真菌組成物 |
| WO2025214612A1 (en) | 2023-04-14 | 2025-10-16 | Syngenta Crop Protection Ag | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2024217995A1 (en) | 2023-04-20 | 2024-10-24 | Syngenta Crop Protection Ag | Pesticidally active dihydropyridinone derivatives |
| PY2447478A (es) | 2023-06-14 | 2025-03-18 | Syngenta Crop Protection Ag | Composiciones fungicidas |
| CN121311114A (zh) | 2023-06-14 | 2026-01-09 | 先正达农作物保护股份公司 | 杀真菌组合物 |
| WO2025261608A1 (en) | 2023-06-29 | 2025-12-26 | Syngenta Crop Protection Ag | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2026002399A1 (en) | 2023-07-07 | 2026-01-02 | Syngenta Crop Protection Ag | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| PY2457454A (es) | 2023-07-21 | 2025-04-22 | Syngenta Crop Protection Ag | Derivados de bencimidazol |
| WO2025022008A1 (en) | 2023-07-27 | 2025-01-30 | Syngenta Crop Protection Ag | Pesticidally active quinazoline compounds |
| WO2025022007A1 (en) | 2023-07-27 | 2025-01-30 | Syngenta Crop Protection Ag | Pesticidally active quinazoline compounds |
| WO2026017247A1 (en) | 2023-07-28 | 2026-01-22 | Syngenta Crop Protection Ag | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2025031913A1 (en) | 2023-08-04 | 2025-02-13 | Syngenta Crop Protection Ag | Methods of controlling or preventing infestation of plants by the phytopathogenic microorganism corynespora cassiicola |
| WO2025031990A1 (en) | 2023-08-04 | 2025-02-13 | Syngenta Crop Protection Ag | Methods of controlling or preventing infestation of soybean plants by the phytopathogenic microorganism corynespora cassiicola |
| WO2025031989A1 (en) | 2023-08-04 | 2025-02-13 | Syngenta Crop Protection Ag | Methods of controlling or preventing infestation of plants by the phytopathogenic microorganism corynespora cassiicola |
| PY2467000A (es) | 2023-08-07 | 2025-05-23 | Syngenta Crop Protection Ag | Composiciones fungicidas |
| WO2025032129A1 (en) | 2023-08-08 | 2025-02-13 | Syngenta Crop Protection Ag | Novel aminoindane and aminotetraline compounds |
| AU2024334603A1 (en) | 2023-08-30 | 2026-02-19 | Syngenta Crop Protection Ag | Pesticidally active oxoindole compounds |
| WO2025045838A2 (en) | 2023-08-31 | 2025-03-06 | Syngenta Crop Protection Ag | Pesticidally active benzisothiazole compounds |
| WO2025045837A1 (en) | 2023-08-31 | 2025-03-06 | Syngenta Crop Protection Ag | Pesticidally active indazole compounds |
| TW202513532A (zh) | 2023-09-15 | 2025-04-01 | 瑞士商先正達農作物保護股份公司 | 用於製備鏡像異構物富集的脂肪族胺之方法 |
| WO2025078263A1 (en) | 2023-10-11 | 2025-04-17 | Syngenta Crop Protection Ag | Microbiocidal pyridyl pyrazole derivatives |
| WO2025087761A1 (en) | 2023-10-27 | 2025-05-01 | Syngenta Crop Protection Ag | Pesticidally active cyclic amine compounds |
| WO2025104032A1 (en) | 2023-11-14 | 2025-05-22 | Syngenta Crop Protection Ag | Novel carboxamide compounds |
| WO2025104152A1 (en) | 2023-11-15 | 2025-05-22 | Syngenta Crop Protection Ag | Microbiocidal tetrahydroisoquinoline derivatives |
| WO2025109114A1 (en) | 2023-11-24 | 2025-05-30 | Syngenta Crop Protection Ag | Novel carboxamide compounds |
| WO2025114167A1 (en) | 2023-11-28 | 2025-06-05 | Syngenta Crop Protection Ag | Microbiocidal pyrazole derivatives |
| PY24108853A (es) | 2023-12-08 | 2025-10-06 | Syngenta Crop Protection Ag | Polimorfos |
| WO2025125639A1 (en) | 2023-12-13 | 2025-06-19 | Syngenta Crop Protection Ag | Method of pathogen control in soybean |
| WO2025132349A1 (en) | 2023-12-19 | 2025-06-26 | Syngenta Crop Protection Ag | Pesticidally active quinazoline compounds |
| WO2025132758A1 (en) | 2023-12-21 | 2025-06-26 | Syngenta Crop Protection Ag | Pesticidally active quinazoline compounds |
| WO2025132754A1 (en) | 2023-12-21 | 2025-06-26 | Syngenta Crop Protection Ag | Pesticidally active quinazoline compounds |
| WO2025149637A1 (en) | 2024-01-12 | 2025-07-17 | Syngenta Crop Protection Ag | Novel carboxamide compounds |
| PY2501648A (es) | 2024-01-12 | 2025-10-31 | Syngenta Crop Prot Ag | Nuevos compuestos de carboxamida |
| WO2025163143A1 (en) | 2024-02-02 | 2025-08-07 | Syngenta Crop Protection Ag | Microbiocidal pyrazole derivatives |
| TW202545918A (zh) | 2024-02-02 | 2025-12-01 | 瑞士商先正達農作物保護股份公司 | 用於製備殺微生物的二唑衍生物之方法 |
| WO2025172374A1 (en) | 2024-02-13 | 2025-08-21 | Syngenta Crop Protection Ag | Microbiocidal pyrazole derivatives |
| WO2025172368A1 (en) | 2024-02-13 | 2025-08-21 | Syngenta Crop Protection Ag | (5-isoxazol-3-yl)-[4-(pyrazol-4-yl)-3,4-dihydro-1h-isoquinolin-2-yl]methanone derivatives for use as fungicides |
| WO2025191053A1 (en) | 2024-03-14 | 2025-09-18 | Syngenta Crop Protection Ag | Microbiocidal pyrazole derivatives |
| WO2025202482A1 (en) | 2024-03-28 | 2025-10-02 | Syngenta Crop Protection Ag | Fungicidal compositions |
| WO2025202499A1 (en) | 2024-03-28 | 2025-10-02 | Syngenta Crop Protection Ag | Fungicidal compositions |
| WO2025210095A1 (en) | 2024-04-03 | 2025-10-09 | Syngenta Crop Protection Ag | Microbiocidal tetrahydroisoquinoline compounds |
| WO2025210096A1 (en) | 2024-04-03 | 2025-10-09 | Syngenta Crop Protection Ag | Fungicidal compositions |
| WO2025210149A1 (en) | 2024-04-04 | 2025-10-09 | Syngenta Crop Protection Ag | Fungicidal composition |
| WO2025233384A1 (en) | 2024-05-08 | 2025-11-13 | Syngenta Crop Protection Ag | Microbiocidal pyrazole compounds |
| TW202547357A (zh) | 2024-05-15 | 2025-12-16 | 瑞士商先正達農作物保護股份公司 | 殺真菌組成物 |
| WO2025247783A1 (en) | 2024-05-29 | 2025-12-04 | Syngenta Crop Protection Ag | Pesticidally active dihydro-benzoxazinone compounds |
| WO2025248032A1 (en) | 2024-05-31 | 2025-12-04 | Syngenta Crop Protection Ag | Pesticidally active indazole compounds |
| WO2025252553A1 (en) | 2024-06-04 | 2025-12-11 | Syngenta Crop Protection Ag | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2025252556A1 (en) | 2024-06-05 | 2025-12-11 | Syngenta Crop Protection Ag | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2025252655A1 (en) | 2024-06-06 | 2025-12-11 | Syngenta Crop Protection Ag | Pesticidally active pyridopyrimidone compounds |
| WO2025257342A1 (en) | 2024-06-12 | 2025-12-18 | Syngenta Crop Protection Ag | Microbiocidal bicyclic heterocyclic compounds |
| WO2025257023A1 (en) | 2024-06-12 | 2025-12-18 | Syngenta Crop Protection Ag | Fungicidal compositions |
| WO2025257024A1 (en) | 2024-06-12 | 2025-12-18 | Syngenta Crop Protection Ag | Fungicidal compositions |
| WO2025256333A1 (en) | 2024-06-13 | 2025-12-18 | Syngenta Crop Protection Ag | Pesticidally active aminoheterocycle derivatives |
| WO2025257413A1 (en) | 2024-06-13 | 2025-12-18 | Syngenta Crop Protection Ag | Pecticidally active dihydroazole derivatives |
| WO2025257072A1 (en) | 2024-06-14 | 2025-12-18 | Syngenta Crop Protection Ag | Pesticidally active 2-oxobenzimidazole compounds |
| EP4667451A1 (en) | 2024-06-21 | 2025-12-24 | Syngenta Crop Protection AG | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2026008511A1 (en) | 2024-07-02 | 2026-01-08 | Syngenta Crop Protection Ag | Microbiocidal quinoline-amide compounds |
| WO2026008750A1 (en) | 2024-07-05 | 2026-01-08 | Syngenta Crop Protection Ag | Novel carboxamide compounds |
| WO2026022188A1 (en) | 2024-07-23 | 2026-01-29 | Syngenta Crop Protection Ag | Microbiocidal quinoline compounds |
| WO2026022173A1 (en) | 2024-07-26 | 2026-01-29 | Syngenta Crop Protection Ag | Microbiocidal pyrazole compounds |
| EP4692056A1 (en) | 2024-08-06 | 2026-02-11 | Syngenta Crop Protection AG | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| EP4691242A1 (en) | 2024-08-06 | 2026-02-11 | Syngenta Crop Protection AG | Pesticidally-active 2,2-dihalocyclopropyl compounds |
| WO2026047037A1 (en) | 2024-08-28 | 2026-03-05 | Syngenta Crop Protection Ag | Microbiocidal quinoline-amide compounds |
| EP4703353A1 (en) | 2024-09-03 | 2026-03-04 | Syngenta Crop Protection AG | Pesticidally-active 2,2-dihalocyclopropyl compounds |
Family Cites Families (90)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS61107392A (ja) | 1984-10-31 | 1986-05-26 | 株式会社東芝 | 画像処理システム |
| BR8600161A (pt) | 1985-01-18 | 1986-09-23 | Plant Genetic Systems Nv | Gene quimerico,vetores de plasmidio hibrido,intermediario,processo para controlar insetos em agricultura ou horticultura,composicao inseticida,processo para transformar celulas de plantas para expressar uma toxina de polipeptideo produzida por bacillus thuringiensis,planta,semente de planta,cultura de celulas e plasmidio |
| EP0276432A3 (de) | 1986-12-12 | 1988-10-26 | Ciba-Geigy Ag | Schädlingsbekämpfungsmittel |
| AU613521B2 (en) | 1988-09-02 | 1991-08-01 | Sankyo Company Limited | 13-substituted milbemycin derivatives, their preparation and use |
| US5169629A (en) | 1988-11-01 | 1992-12-08 | Mycogen Corporation | Process of controlling lepidopteran pests, using bacillus thuringiensis isolate denoted b.t ps81gg |
| NZ231804A (en) | 1988-12-19 | 1993-03-26 | Ciba Geigy Ag | Insecticidal toxin from leiurus quinquestriatus hebraeus |
| US5015630A (en) | 1989-01-19 | 1991-05-14 | Merck & Co., Inc. | 5-oxime avermectin derivatives |
| NO176766C (no) | 1989-02-07 | 1995-05-24 | Meiji Seika Kaisha | Fremgangsmåte for fremstilling av en forbindelse med anthelmintaktivitet |
| GB8910624D0 (en) | 1989-05-09 | 1989-06-21 | Ici Plc | Bacterial strains |
| CA2015951A1 (en) | 1989-05-18 | 1990-11-18 | Mycogen Corporation | Novel bacillus thuringiensis isolates active against lepidopteran pests, and genes encoding novel lepidopteran-active toxins |
| ES2074547T3 (es) | 1989-11-07 | 1995-09-16 | Pioneer Hi Bred Int | Lectinas larvicidas, y resistencia inducida de las plantas a los insectos. |
| JPH085894B2 (ja) | 1990-03-01 | 1996-01-24 | 三共株式会社 | ミルベマイシンエーテル誘導体 |
| JPH0570366A (ja) | 1991-03-08 | 1993-03-23 | Meiji Seika Kaisha Ltd | 薬用組成物 |
| UA48104C2 (uk) | 1991-10-04 | 2002-08-15 | Новартіс Аг | Фрагмент днк, який містить послідовність,що кодує інсектицидний протеїн, оптимізовану для кукурудзи,фрагмент днк, який забезпечує направлену бажану для серцевини стебла експресію зв'язаного з нею структурного гена в рослині, фрагмент днк, який забезпечує специфічну для пилку експресію зв`язаного з нею структурного гена в рослині, рекомбінантна молекула днк, спосіб одержання оптимізованої для кукурудзи кодуючої послідовності інсектицидного протеїну, спосіб захисту рослин кукурудзи щонайменше від однієї комахи-шкідника |
| DE122005000058I1 (de) | 1992-03-17 | 2006-04-27 | Astellas Pharma Inc | Depsipeptide, Herstellung und Anwendung |
| DE69226449T2 (de) | 1992-04-28 | 1998-12-10 | Yashima Chemical Industrial Co., Ltd., Kawasaki, Kanagawa | 2-(2,6-difluorphenyl)-4-(2-ethoxy-4-tert-butylphenyl)-2-axazoline |
| DE4317458A1 (de) | 1992-06-11 | 1993-12-16 | Bayer Ag | Verwendung von cyclischen Depsipeptiden mit 18 Ringatomen zur Bekämpfung von Endoparasiten, neue cyclische Depsipeptide mit 18 Ringatomen und Verfahren zu ihrer Herstellung |
| US5461168A (en) | 1992-09-01 | 1995-10-24 | Sankyo Company, Limited | Processes for the production of 13-ether derivatives of milbemycins, and intermediates therefor |
| GB9300883D0 (en) | 1993-01-18 | 1993-03-10 | Pfizer Ltd | Antiparasitic agents |
| NZ261630A (en) | 1993-02-19 | 1998-05-27 | Meiji Seika Kaisha | Heteromacrocyclic compound and use as an assthelmintie |
| DE4317457A1 (de) | 1993-05-26 | 1994-12-01 | Bayer Ag | Octacyclodepsipeptide mit endoparasitizider Wirkung |
| US5801023A (en) | 1994-01-14 | 1998-09-01 | Pfizer Inc. | Antiparasitic pyrrolobenzoxazine compounds |
| GB9402916D0 (en) | 1994-02-16 | 1994-04-06 | Pfizer Ltd | Antiparasitic agents |
| US5530195A (en) | 1994-06-10 | 1996-06-25 | Ciba-Geigy Corporation | Bacillus thuringiensis gene encoding a toxin active against insects |
| DE4437198A1 (de) | 1994-10-18 | 1996-04-25 | Bayer Ag | Verfahren zur Sulfonylierung, Sulfenylierung und Phosphorylierung von cyclischen Depsipeptiden |
| DE4440193A1 (de) | 1994-11-10 | 1996-05-15 | Bayer Ag | Verwendung von Dioxomorpholinen zur Bekämpfung von Endoparasiten, neue Dioxomorpholine und Verfahren zur ihrer Herstellung |
| DE19520936A1 (de) | 1995-06-08 | 1996-12-12 | Bayer Ag | Ektoparasitizide Mittel |
| DE69712331T2 (de) | 1996-03-11 | 2002-11-28 | Syngenta Participations Ag, Basel | Pyrimidin-4-on derivate als pestizidesmittel |
| BR0113500A (pt) | 2000-08-25 | 2003-07-01 | Syngenta Participations Ag | Toxinas inseticidas derivadas de proteìnas de cristais inseticidas de bacillus thuringiensis |
| US7230167B2 (en) | 2001-08-31 | 2007-06-12 | Syngenta Participations Ag | Modified Cry3A toxins and nucleic acid sequences coding therefor |
| MXPA04003169A (es) | 2001-10-03 | 2004-07-08 | Pharmacia Corp | Profarmacos de compuestos policiclicos sustituidos utiles para inhibicion selectiva de la cascada de coagulacion. |
| AU2002361696A1 (en) | 2001-12-17 | 2003-06-30 | Syngenta Participations Ag | Novel corn event |
| AU2002361831B2 (en) | 2002-04-04 | 2007-07-19 | Valent Biosciences, Corp | Enhanced herbicide composition |
| GB0303439D0 (en) | 2003-02-14 | 2003-03-19 | Pfizer Ltd | Antiparasitic terpene alkaloids |
| CN100556905C (zh) * | 2005-09-08 | 2009-11-04 | 国家南方农药创制中心江苏基地 | 吡唑酰胺类化合物及其中间体和以该类化合物为活性成分的有害生物防治剂 |
| US20070155739A1 (en) | 2005-12-30 | 2007-07-05 | Alantos Pharmaceuticals, Inc. | Substituted bis-amide metalloprotease inhibitors |
| CL2007002787A1 (es) * | 2006-09-29 | 2008-05-30 | Bayer Cropscience Sa | Compuestos derivados de n-cicloalquil-carboxamida, n-cicloalquil-tiocarboxamida y n-cicloalquil-carboxamidamida n-sustituida; composicion fungicida que comprende dichos compuestos; y metodo para combatir hongos fitopatogenos de cultivos que comprende |
| US8288393B2 (en) | 2007-08-10 | 2012-10-16 | Nippon Soda Co., Ltd. | Nitrogen-containing heterocyclic compound and pest control agent |
| JP5554337B2 (ja) | 2008-10-17 | 2014-07-23 | ゼノン・ファーマシューティカルズ・インコーポレイテッド | 治療剤としてのスピロオキシインドール化合物およびそれらの使用 |
| US8981084B2 (en) | 2010-01-13 | 2015-03-17 | Tempero Pharmaceuticals, Inc. | Oxadiazole HDAC inhibitors |
| AU2011205283B2 (en) | 2010-01-13 | 2014-07-10 | Tempero Pharmaceuticals, Inc. | Compounds and methods |
| EP2630125B1 (en) * | 2010-10-21 | 2016-08-24 | Bayer Intellectual Property GmbH | N-benzyl heterocyclic carboxamides |
| JP6007417B2 (ja) * | 2011-05-31 | 2016-10-12 | レセプトス エルエルシー | 新規glp−1受容体安定剤および調節剤 |
| WO2013006408A1 (en) | 2011-07-01 | 2013-01-10 | Tempero Pharmaceuticals, Inc. | Compounds and methods |
| CA2841113A1 (en) | 2011-07-08 | 2013-01-17 | Novartis Ag | Novel trifluoromethyl-oxadiazole derivatives and their use in the treatment of disease |
| WO2013009830A1 (en) | 2011-07-13 | 2013-01-17 | Tempero Pharmaceuticals, Inc. | Methods of treatment |
| WO2013009827A1 (en) | 2011-07-13 | 2013-01-17 | Tempero Pharmaceuticals, Inc. | Methods of treatment |
| WO2013009810A1 (en) | 2011-07-13 | 2013-01-17 | Tempero Pharmaceuticals, Inc. | Methods of treatment |
| WO2013066835A2 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066839A2 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| WO2013066838A1 (en) | 2011-10-31 | 2013-05-10 | Glaxosmithkline Llc | Compounds and methods |
| CN103081916B (zh) * | 2011-11-02 | 2014-08-06 | 中国中化股份有限公司 | 吡唑酰胺类化合物作为农用杀菌剂的用途 |
| CA2856334A1 (en) | 2011-11-28 | 2013-06-06 | Christina Hebach | Novel trifluoromethyl-oxadiazole derivatives and their use in the treatment of disease |
| GB201213700D0 (en) | 2012-08-01 | 2012-09-12 | Proximagen Ltd | Receptor antagnists II |
| MX2016004533A (es) * | 2013-10-16 | 2016-07-22 | Bayer Cropscience Ag | Derivados de n-cicloalquil-n-(biheterociclilmetilen)-(tio)carboxam ida. |
| FR3021902B1 (fr) | 2014-06-05 | 2016-07-22 | Inria Inst Nat Rech Informatique & Automatique | Procede de determination des points a supporter pour un objet fabrique au moyen d'un procede de fabrication additive ; support d'enregistrement d'informations et structure de support associes |
| PL3151669T3 (pl) | 2014-06-06 | 2021-04-19 | Basf Se | Zastosowanie podstawionych oksadiazoli do zwalczania fitopatogennych grzybów |
| US10081624B2 (en) | 2014-08-26 | 2018-09-25 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| WO2017033946A1 (ja) | 2015-08-25 | 2017-03-02 | 武田薬品工業株式会社 | 複素環化合物 |
| WO2017076757A1 (en) | 2015-11-02 | 2017-05-11 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| EP3165094A1 (en) | 2015-11-03 | 2017-05-10 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| EP3371155A1 (en) | 2015-11-03 | 2018-09-12 | Basf Se | Use of substituted oxadiazoles for combating phytopathogenic fungi |
| EP3371178A1 (en) | 2015-11-04 | 2018-09-12 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| EP3370525A1 (en) | 2015-11-04 | 2018-09-12 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| EP3165093A1 (en) | 2015-11-05 | 2017-05-10 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| BR112018008608B1 (pt) | 2015-11-05 | 2022-05-17 | Basf Se | Uso de compostos de fórmula i, compostos de fórmula i, compostos, composição agroquímica e método para combater fungos nocivos fitopatogênicos |
| EP3373735A1 (en) | 2015-11-13 | 2018-09-19 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| AR106679A1 (es) | 2015-11-13 | 2018-02-07 | Basf Se | Oxadiazoles sustituidos para combatir hongos fitopatógenos |
| US20180354921A1 (en) | 2015-11-13 | 2018-12-13 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| BR112018009566A2 (pt) | 2015-11-13 | 2018-11-06 | Basf Se | compostos, mistura, composição agroquímica, uso de compostos e método para combater fungos nocivos fitopatogênicos |
| AU2016355949A1 (en) | 2015-11-19 | 2018-05-10 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| AU2016354902A1 (en) | 2015-11-19 | 2018-05-10 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| KR20180088449A (ko) | 2015-12-03 | 2018-08-03 | 바스프 에스이 | 식물병원성 진균을 퇴치하기 위한 치환 옥사디아졸 |
| US20180368410A1 (en) * | 2015-12-17 | 2018-12-27 | Syngenta Participations Ag | Microbiocidal oxadiazole derivatives |
| JP2019504019A (ja) * | 2015-12-18 | 2019-02-14 | シンジェンタ パーティシペーションズ アーゲー | 殺微生物性オキサジアゾール誘導体 |
| CN108430980B (zh) * | 2015-12-22 | 2022-09-02 | 先正达参股股份有限公司 | 杀微生物的噁二唑衍生物 |
| BR112018012954B1 (pt) | 2015-12-25 | 2022-04-26 | Sumitomo Chemical Company, Limited | Compostos de oxadiazol, uso dos mesmos, agente e método para controle de doenças de planta e composição que os compreende |
| WO2017110862A1 (ja) | 2015-12-25 | 2017-06-29 | 住友化学株式会社 | オキサジアゾール化合物及びその用途 |
| WO2017110861A1 (ja) | 2015-12-25 | 2017-06-29 | 住友化学株式会社 | オキサジアゾール化合物を含有する植物病害防除剤 |
| WO2017110864A1 (ja) | 2015-12-25 | 2017-06-29 | 住友化学株式会社 | 植物病害防除組成物およびその用途 |
| WO2017111152A1 (ja) | 2015-12-25 | 2017-06-29 | 住友化学株式会社 | オキサジアゾール化合物及びその用途 |
| WO2017169893A1 (ja) | 2016-03-31 | 2017-10-05 | 住友化学株式会社 | オキサジアゾール化合物及びその用途 |
| AU2017250397A1 (en) | 2016-04-11 | 2018-10-11 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| JP2017190296A (ja) | 2016-04-13 | 2017-10-19 | 住友化学株式会社 | 有害生物防除組成物およびその用途 |
| EP3468958B1 (en) | 2016-06-09 | 2020-12-16 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| WO2017211650A1 (en) | 2016-06-09 | 2017-12-14 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| WO2017211652A1 (en) | 2016-06-09 | 2017-12-14 | Basf Se | Substituted oxadiazoles for combating phytopathogenic fungi |
| WO2017213252A1 (en) | 2016-06-10 | 2017-12-14 | Sumitomo Chemical Company, Limited | Oxadiazole compound and use as pesticide |
| EP3475275B1 (en) * | 2016-06-23 | 2024-04-10 | Merck Sharp & Dohme LLC | 3-aryl and heteroaryl substituted 5-trifluoromethyl oxadiazoles as histone deacetylase 6 (hdac6) inhibitors |
| AR109304A1 (es) | 2016-08-10 | 2018-11-21 | Sumitomo Chemical Co | Compuesto de oxadiazol y su uso |
-
2016
- 2016-09-29 DK DK16774508.2T patent/DK3356358T3/da active
- 2016-09-29 HU HUE16774508A patent/HUE050030T2/hu unknown
- 2016-09-29 SI SI201630854T patent/SI3356358T1/sl unknown
- 2016-09-29 US US15/765,138 patent/US10899724B2/en active Active
- 2016-09-29 CN CN201680058005.7A patent/CN108137570B/zh active Active
- 2016-09-29 EP EP16774508.2A patent/EP3356358B1/en active Active
- 2016-09-29 BR BR112018006623-0A patent/BR112018006623B1/pt active IP Right Grant
- 2016-09-29 JP JP2018516818A patent/JP6864675B2/ja active Active
- 2016-09-29 MX MX2018004038A patent/MX2018004038A/es unknown
- 2016-09-29 ES ES16774508T patent/ES2807849T3/es active Active
- 2016-09-29 PL PL16774508T patent/PL3356358T3/pl unknown
- 2016-09-29 WO PCT/EP2016/073295 patent/WO2017055473A1/en not_active Ceased
- 2016-09-30 UY UY0001036925A patent/UY36925A/es active IP Right Grant
-
2018
- 2018-03-11 IL IL258012A patent/IL258012B/en active IP Right Grant
- 2018-03-19 ZA ZA2018/01828A patent/ZA201801828B/en unknown
- 2018-03-29 CL CL2018000834A patent/CL2018000834A1/es unknown
- 2018-04-11 CO CONC2018/0003840A patent/CO2018003840A2/es unknown
-
2020
- 2020-02-10 US US16/786,672 patent/US11066375B2/en active Active
- 2020-02-10 US US16/786,688 patent/US11180462B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20200172498A1 (en) | 2020-06-04 |
| BR112018006623A2 (pt) | 2018-10-23 |
| ZA201801828B (en) | 2019-01-30 |
| CN108137570A (zh) | 2018-06-08 |
| DK3356358T3 (da) | 2020-08-03 |
| US20200181100A1 (en) | 2020-06-11 |
| IL258012B (en) | 2021-02-28 |
| EP3356358A1 (en) | 2018-08-08 |
| CO2018003840A2 (es) | 2018-07-10 |
| BR112018006623B1 (pt) | 2022-04-26 |
| US11180462B2 (en) | 2021-11-23 |
| EP3356358B1 (en) | 2020-05-06 |
| UY36925A (es) | 2017-04-28 |
| US20180273494A1 (en) | 2018-09-27 |
| US11066375B2 (en) | 2021-07-20 |
| PL3356358T3 (pl) | 2020-11-02 |
| CN108137570B (zh) | 2022-01-28 |
| HUE050030T2 (hu) | 2020-11-30 |
| JP2018531246A (ja) | 2018-10-25 |
| IL258012A (en) | 2018-05-31 |
| US10899724B2 (en) | 2021-01-26 |
| MX2018004038A (es) | 2019-07-18 |
| JP6864675B2 (ja) | 2021-04-28 |
| WO2017055473A1 (en) | 2017-04-06 |
| CL2018000834A1 (es) | 2018-07-06 |
| SI3356358T1 (sl) | 2020-09-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2807849T3 (es) | Derivados de oxadiazol microbicidas | |
| ES2842550T3 (es) | Derivados de tiazol microbiocidas | |
| US10501425B2 (en) | Microbiocidal oxadiazole derivatives | |
| US10640497B2 (en) | Microbiocidal oxadiazole derivatives | |
| BR112018013821B1 (pt) | Compostos derivados de oxadiazol microbiocidas, composição agroquímica compreendendo os referidos compostos, método de controle ou prevenção de infestação de plantas úteis por microrganismos fitopatogênicos e uso dos referidos compostos | |
| JP2018531246A6 (ja) | 殺微生物オキサジアゾール誘導体 | |
| WO2015010832A1 (en) | Microbiocidal heterocyclic derivatives | |
| EP3356335B1 (en) | Microbiocidal oxadiazole derivatives | |
| ES2810752T3 (es) | Derivados de oxadiazol microbicidas |