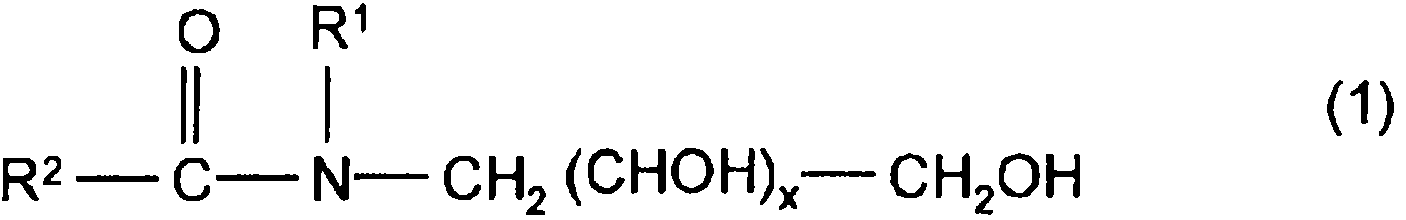ES2818799T3 - Proceso continuo para la preparación de un tensioactivo en un reactor tubular - Google Patents
Proceso continuo para la preparación de un tensioactivo en un reactor tubular Download PDFInfo
- Publication number
- ES2818799T3 ES2818799T3 ES15790990T ES15790990T ES2818799T3 ES 2818799 T3 ES2818799 T3 ES 2818799T3 ES 15790990 T ES15790990 T ES 15790990T ES 15790990 T ES15790990 T ES 15790990T ES 2818799 T3 ES2818799 T3 ES 2818799T3
- Authority
- ES
- Spain
- Prior art keywords
- process according
- range
- temperature
- aqueous solution
- fatty acids
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C231/00—Preparation of carboxylic acid amides
- C07C231/02—Preparation of carboxylic acid amides from carboxylic acids or from esters, anhydrides, or halides thereof by reaction with ammonia or amines
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J19/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J19/18—Stationary reactors having moving elements inside
- B01J19/1812—Tubular reactors
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J19/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J19/24—Stationary reactors without moving elements inside
- B01J19/2415—Tubular reactors
- B01J19/242—Tubular reactors in series
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C231/00—Preparation of carboxylic acid amides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/24—Stationary reactors without moving elements inside
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Detergent Compositions (AREA)
Abstract
Procedimiento continuo para la preparación de un tensioactivo que comprende un compuesto de la fórmula (1), en donde R2 es el resto alquilo de un ácido graso y R1 es un resto hidrocarbilo C1 a C12 de cadena lineal o ramificada, y x está en el intervalo de 1 a 15, **(Ver fórmula)** mediante la reacción de ésteres alquílicos de ácidos grasos o triglicéridos de ácidos grasos con un compuesto polihidroxilado N-n-alquilado, en presencia de un catalizador alcalino o un catalizador elegido de entre hidróxidos o alcóxidos de elementos de transición de los grupos 2 y 4 de la Tabla Periódica, a una temperatura en el intervalo de 40 a 300°C, en donde el procedimiento comprende las etapas siguientes: 1. mezclar la disolución acuosa de materias primas que comprende una o varias N-alquilglucaminas con el catalizador; 2. secar la disolución acuosa, en donde el contenido de agua después del secado se encuentra en el intervalo del 0-5 % en peso; 3. calentar la mezcla seca a una temperatura en el intervalo de 60 a 180°C y mezclar la masa fundida con ésteres alquílicos de ácidos grasos o triglicéridos; 4. opcionalmente, almacenar temporalmente y mezclar la mezcla de reacción en una caldera de agitación en funcionamiento continuo; 5. hacer reaccionar en un reactor tubular; y 6. opcionalmente, retirar los subproductos.
Description
DESCRIPCIÓN
Proceso continuo para la preparación de un tensioactivo en un reactor tubular
La siguiente invención se refiere a un proceso continuo para la preparación de tensioactivos, en particular, de amidas de ácidos grasos polihidroxilados (p. ej., W-metilglucamidas), en un reactor tubular. Los tensioactivos pueden emplearse, por ejemplo, como sustancias con actividad superficial, por ejemplo, en formulaciones de detergentes. El procedimiento según la invención permite producir tensioactivos de forma continua con gran rendimiento y pureza.
Antecedentes de la invención
Existe una gran diversidad de tensioactivos no iónicos para su empleo en formulaciones de detergentes, productos de cuidado personal y en protección vegetal. Una alternativa a muchos de los tensioactivos convencionales son las amidas de ácidos grasos polihidroxilados, que son valiosos compuestos con actividad superficial para aplicaciones muy diversas.
Así, estas pueden emplearse, por ejemplo, como tales o mezcladas con tensioactivos aniónicos, catiónicos y/o no iónicos, como productos de limpieza, detergentes, productos de tratamiento textil o similares, en forma de productos sólidos (por ejemplo, como polvos, granos, gránulos o escamas), disoluciones, dispersiones, emulsiones, pastas y similares. Dado que las amidas de ácidos grasos polihidroxilados son también fácilmente biodegradables y pueden prepararse a partir de materias primas renovables, su importancia ha aumentado en los últimos tiempos.
Por consiguiente, podría presumirse que estos compuestos han encontrado aplicación en diversas formulaciones. Sin embargo, esta presunción no puede confirmarse. Como motivo, se asume que la preparación de estas amidas de ácidos grasos polihidroxilados, sobre todo en la calidad y la pureza deseadas, es muy compleja. Aunque la preparación de amidas de ácidos grasos polihidroxilados mediante procedimientos por lotes se ha descrito en numerosas ocasiones, la calidad resultante de estos procedimientos no ha sido satisfactoria. En particular, para el empleo en el ámbito del cuidado personal, ha de cumplirse una estricta especificación, p. ej., con respecto al color, el contenido de disolventes y los componentes secundarios. Ello no es posible de una forma económica con los procedimientos descritos en la bibliografía. En particular, los largos tiempos de permanencia con gran carga térmica, un mezclado insuficiente y la intensa formación de espuma pueden causar problemas en un procedimiento de funcionamiento discontinuo.
La preparación en un procedimiento por lotes permite ocuparse específicamente de los distintos requisitos durante la reacción. Así pues, pueden surgir formas reológicas diferentes que, según el producto, tienen distinta duración. Un procedimiento continuo debe hacer frente a estos desafíos y esto es un motivo por el que hasta ahora no se ha descrito ningún procedimiento continuo que satisfaga los requisitos de calidad mencionados.
El documento EP 0633244 A2 describe el funcionamiento de una cascada de calderas de agitación para la preparación de amidas de ácidos grasos polihidroxilados. Sin embargo, este proceso tiene la desventaja de una amplia distribución de tiempos de permanencia, lo aumenta la formación de productos secundarios no deseados. Debido a los grandes volúmenes de reacción y a la distribución desfavorable de temperaturas en el sistema de reacción que esto conlleva, el estrés térmico es demasiado elevado, lo que tiene un efecto negativo sobre el color del producto.
Además, este procedimiento presenta la desventaja de la intensa formación de espuma que tiene lugar al retirar los subproductos. La formación de espuma hace que no se alcance la baja presión deseada para poder retirar por completo los subproductos. Para asegurar la retirada de los subproductos, debe usarse una temperatura más elevada o un menor caudal, lo que conduce a una mayor carga térmica del producto final. Sin embargo, una mayor carga térmica conlleva un mayor contenido de productos secundarios y peor color.
Para superar los problemas mencionados anteriormente, se ha desarrollado un procedimiento continuo nuevo, mediante el cual, gracias al reducido tiempo de permanencia y al optimizado control de la temperatura, pueden prepararse amidas de ácidos grasos polihidroxilados con mejor calidad y mayores rendimientos. La mejor calidad se manifiesta, en particular, por una disminución de las sustancias colorantes y una reducción de los componentes secundarios (número de color de Gardner <3, componentes cíclicos <0,1 %). Además, con el nuevo procedimiento es posible garantizar un contenido de MeOH <0,3 % en el producto final).
Descripción de la invención
Sorprendentemente, se ha encontrado ahora que la preparación de tensioactivos, en particular, de amidas de ácidos grasos polihidroxilados, es posible de manera más económica y con una mayor calidad de producto con el procedimiento continuo según la invención. Dado que el producto es muy sensible a la temperatura, sobre todo en lo que se refiere al contenido de amidas cíclicas y al color del producto, un procedimiento de preparación continuo en un reactor tubular con un tiempo de permanencia reducido es una alternativa considerablemente mejor para obtener una calidad de producto excelente. Además, de este modo pueden reducirse los costes de producción.
La presente invención se refiere a un proceso continuo para la preparación de un tensioactivo, que comprende un compuesto de la fórmula (1), en donde R2 es el resto alquilo de un ácido graso y R1 representa un resto hidrocarbilo
Ci a C12 de cadena lineal o ramificada, preferentemente Ci a Cs, en particular Ci a C6, por ejemplo, un resto metilo, etilo, propanilo, isopropilo, n-butanilo o iso-butilo. Se prefieren en particular metilo y etilo; en especial metilo. X está en el intervalo de 1 a 15, en particular de 2 a 6.
A este respecto, la preparación del tensioactivo tiene lugar mediante la reacción de ásteres alquílicos de ácidos grasos o triglicáridos de ácidos grasos con un compuesto polihidroxilado W-n-alquilado, en presencia de un catalizador alcalino o un catalizador elegido de entre hidróxidos o alcóxidos de elementos de transición de los grupos 2 y 4 de la Tabla Periódica, a una temperatura en el intervalo de 40 a 300°C, en donde el procedimiento comprende las etapas siguientes:
1. mezclar la disolución acuosa de materias primas que comprende una o varias W-alquilglucaminas con el catalizador;
2. secado de la disolución acuosa, en donde el contenido de agua despuás del secado se encuentra en el intervalo del 0-5 % en peso;
3. calentar la mezcla seca a una temperatura en el intervalo de 60 a 1 S0°C y mezclar la masa fundida con ásteres alquílicos de ácidos grasos o triglicáridos;
4. opcionalmente, almacenar temporalmente y mezclar la mezcla de reacción en una caldera de agitación en funcionamiento continuo;
5. reacción en un reactor tubular; y
6. opcionalmente, retirada de los subproductos.
La proporción del compuesto (1) en el tensioactivo está normalmente en el intervalo del 15 al 100 % en peso, preferentemente en el intervalo del 30 al 100 % en peso.
El proceso incluye la reacción de ásteres alquílicos de ácidos grasos o triglicáridos de ácidos grasos con una longitud de cadena de C4 a C50, preferentemente de C6 a C28, en particular de C6 a C20, y W-alquilglucaminas, en presencia de catalizadores alcalinos, preferentemente hidróxidos alcalinos y alcóxidos alcalinos, en particular hidróxido de sodio, metanolato de sodio, etanolato de sodio, hidróxido de potasio, metanolato de potasio o etanolato de potasio como catalizador, en un reactor tubular continuo. Además, pueden usarse como catalizadores hidróxidos o alcóxidos de elementos de transición de los grupos 2 y 4 de la Tabla Periódica como, por ejemplo, tetraisopropilato de titanio.
El proceso según la invención convierte W-alquilglucaminas, p. ej., W-metil-D-glucaminas, en tensioactivos lineales de glucamida de gran calidad, que son adecuados para uso en el ámbito del cuidado personal aún sin una etapa de procesamiento posterior (p. ej., recristalización).
El procedimiento según la invención incluye 4 a 7 etapas de proceso:
1. Mezclar la disolución acuosa de materias primas con W-alquilglucamina (concentración del 30-90 % en peso de amina en agua) con el 0,01 -5 % en peso, preferentemente el 0,05-4 % en peso, en particular el 1 -3 % en peso de catalizador, en donde el mezclado es posible en cualquier orden.
La temperatura durante el mezclado debe ser de 40-120°C, preferentemente de 50-100°C, en particular de 50-90°C, en donde dicho mezclado tiene lugar a una presión de 0-6.000 hPa (0-6 bar), aunque normalmente a presión normal.
2. Secado de la disolución acuosa: el secado debe ser lo más eficaz posible y el contenido de agua despuás de dicho secado no debe superar el 0-5 % en peso, preferentemente el 0-3 % en peso y en particular el 0-1 % en peso.
La temperatura durante el secado (2) es de 80-1 S0°C, preferentemente de 90-160°C, en particular de 100-150°C, en donde puede trabajarse tanto a presión normal como en vacío. Normalmente, la presión en esta etapa se encuentra en el intervalo de 0-2.000 hPa (0-2 bar), preferentemente 0-1.000 hPa (0-1 bar), en particular 10-1.000 hPa (0,01-1 bar).
3. Calentar la mezcla seca de W-alquilglucamina a una temperatura en el intervalo de 60-180°C, preferentemente 70-160°C, en particular 80-150°C, a una presión en el intervalo de 0-6.000 hPa (0-6 bar) y mezclar la masa fundida de W-alquilglucamina con ásteres alquílicos de ácidos grasos en una relación molar entre la masa fundida
de W-alquilglucamina y el éster alquílico de ácido graso de 1:0,85 a 1:1,2, preferentemente de 1:0,9 a 1,15, con preferencia especial de 1:0,95 a 1:1,1, o respectivamente, en caso de usar triglicéridos, en una relación molar entre la masa fundida de W-alquilglucamina y la triglicerina de 0,25:1 a 0,45:1, preferentemente de 0,3:1 a 0.4:1, en particular de 0,33:1 a 0,37:1. En ello, el tiempo de permanencia medio está normalmente en el intervalo de 1 min a 2 h, preferentemente de 2 min a 1 h, en particular de 5 a 45 min.
4. (Opcional) Almacenar temporalmente y mezclar la mezcla de reacción en una caldera de agitación en funcionamiento continuo. En este caso, la temperatura en la caldera de agitación es normalmente de 60-300°C, preferentemente 70-200°C, en particular de 80-150°C, a presiones de 0-200.000 hPa (0-200 bar), preferentemente 500-80.000 hPa (0,5-80 bar), en particular a 1.000-5.000 hPa (1 -5 bar).
5. La reacción en el reactor tubular tiene lugar a una temperatura en el intervalo de 60-300°C, preferentemente 70-200°C, en particular a 80-150°C, a presiones de 0-200.000 hPa (0-200 bar), preferentemente 500-80.000 hPa (0,5-80 bar), en particular a 1.000-20.000 hPa (1-20 bar). En ello, el tiempo de permanencia medio está normalmente en el intervalo de 2 min a 2 h, preferentemente de 2 min a 1 h, en particular de 5 a 45 min, y opcionalmente:
6. Retirada de los subproductos. La retirada de los subproductos es opcional y se realiza a una temperatura en el intervalo de 50-180°C, preferentemente a 60-160°C, en particular a 70-150°C. En ello, la presión aplicada puede oscilar entre la presión normal y el vacío y normalmente es de 0-2.000 hPa (0-2 bar), preferentemente de 0-1.000 hPa (0-1 bar), en particular de 10-1.000 hPa (0,01-1 bar). Normalmente, la retirada de los subproductos se realiza por procedimientos conocidos por el experto en la técnica, p. ej., por destilación continua o mediante un evaporador de capa delgada (o también, evaporador de corto recorrido o evaporador de película descendente).
7. (Opcional) Formulación del producto: para una operación más sencilla en las etapas del procesamiento posterior, los productos de la fórmula (1) obtenidos mediante el proceso según la invención pueden mezclarse (formularse) con distintos disolventes como agua, alcoholes (p. ej., etanol, isopropanol, alcohol cetearílico), glicoles (etilenglicol, propilenglicol, polipropilenglicoles, polietilenglicoles) y sus mezclas, así como con aditivos y conservantes (p. ej., metilisotiazolinona, ácido benzoico, ácido sórbico) y sustancias para ajuste del pH (p. ej., ácido cítrico, ácido láctico, ácido benzoico y otros). Esto tiene lugar normalmente a temperaturas en el intervalo de 10 a 130°C, preferentemente de 20 a 110°C, a presión normal.
Se ha demostrado que en los reactores correspondientes existe una diferencia de temperatura entre la pared del reactor y el flujo del núcleo <20°C. Preferentemente, esta diferencia de temperatura debe ser <10°C, en particular <5°C, para garantizar la alta calidad y pureza del producto deseadas.
El alcohol que se genera durante la reacción puede separarse mediante un evaporador de capa delgada en funcionamiento continuo u otros dispositivos conocidos por el experto en la técnica. Una de las ventajas del procedimiento según la invención es que se produce muy poca o ninguna espuma durante la totalidad del proceso. En las reacciones en las que se hace reaccionar W-alquilglucamina con triglicéridos, la última etapa de la reacción no es necesaria. En este caso se genera glicerina como subproducto, la cual puede permanecer en el producto final. En caso de que las W-alquilglucaminas estén presentes como disolución acuosa, se prepara una masa fundida mediante un procedimiento de secado continuo (p. ej., con un evaporador de capa delgada).
El diseño del mezclador debe permitir una gran superficie interfásica y/o debe garantizarse un buen intercambio de fases a través de la adición de pequeñas cantidades (0-10 %) de agentes de transferencia de fase. Los agentes de transferencia de fase pueden añadirse según la invención en las tres primeras etapas, es decir, 1,2 o 3. Como agentes de transferencia de fase son posibles, por ejemplo, agua y/o alcoholes (etanol, metanol, propanol, isopropanol, butanol, isobutanol), glicoles (propilenglicol, monoetilenglicol), W-alquilglucamidas, polialquilglicoles, éteres de corona o glicerina. La concentración de los agentes de transferencia de fase en el producto final es normalmente de entre el 0 y el 30 %, preferentemente del 0-20 % y en particular del 0-10 %.
El procedimiento continuo según la invención presenta varias ventajas en comparación con los procedimientos descritos en el estado de la técnica: la capacidad de la instalación aumenta debido a la supresión de la ejecución secuencial de las etapas de operación individuales (llenado, reacción, separación de metanol, vaciado, calentamiento, enfriamiento).
De este modo, el proceso según la invención puede automatizarse fácilmente y puede hacerse funcionar con menores necesidades de personal. Además, el rendimiento espacio-temporal aumenta y los tiempos de reacción se acortan, lo que conduce a una distribución más estrecha de los tiempos de permanencia, en comparación con el proceso por lotes. Además, la calidad del producto es más reproducible y menos variable, lo que se demuestra, en particular, por la alta pureza del producto obtenido. Así pues, los compuestos de la fórmula (1) obtenidos según la invención presentan unos números de color de Gardner de 0 a 3, preferentemente de 0,1 a 2,5, en particular de 0,3 a 2,0, lo que representa una mejora considerable con respecto a los productos obtenidos en el procedimiento por lotes, como muestran también los ejemplos siguientes. La cantidad de los componentes secundarios cíclicos, con una proporción <0,05 % en peso, preferentemente <0,03 %, en particular <0,02 % en peso, también es considerablemente inferior a
la de los procedimientos conocidos. De este modo, los productos obtenidos pueden usarse sin purificación posterior incluso en aplicaciones con altas exigencias (p. ej., cuidado personal).
Ejemplos
Ejemplo 1: Cocoilglucamida a partir de una disolución acuosa de N-metilglucamina y aceite de coco
A partir de una disolución acuosa de N-metilglucamina con hidróxido de sodio, se prepara una masa fundida de N-metilglucamina caliente a 135°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. Esta masa fundida y una masa fundida de aceite de coco caliente a 40°C (Gustavheess (n.° de material: 204403) se mezclan a 130°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 35 min y en el reactor tubular de 11 min. La temperatura en el recipiente de agitación es de 130°C y la temperatura en el reactor tubular es de 100°C. El producto puede envasarse a la salida del reactor tubular sin procesamiento posterior.
Ejemplo 2: Cocoilglucamida a partir de una disolución acuosa de N-metilglucamina y aceite de coco con el uso de un agente de transferencia de fase
A partir de una disolución acuosa de N-metilglucamina con hidróxido de sodio, se prepara una masa fundida de N-metilglucamina caliente a 135°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. La masa fundida, propilenglicol y una masa fundida de aceite de coco caliente a 40°C (Gustavheess (n.° de material: 204403) se mezclan a 130°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 25 min y en el reactor tubular de 8 min. La temperatura en el recipiente de agitación es de 100°C y la temperatura en el reactor tubular es de 95°C. El producto puede envasarse a la salida del reactor tubular sin procesamiento posterior.
Ejemplo 3: Oleilglucamida a partir de una disolución acuosa de N-metilglucamina y aceite de girasol
A partir de una disolución acuosa de N-metilglucamina con hidróxido de sodio, se prepara una masa fundida de N-metilglucamina seca por medio de una cascada de calderas de agitación de dos etapas en funcionamiento continuo a 135°C. Esta masa fundida se mezcla, con la adición de propilenglicol y aceite de girasol caliente a 80°C (Cargill (Agripur AP88, número de material: 233301)), a 120°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 55 min y en el reactor tubular de 21 min. La temperatura en el recipiente de agitación es de 110°C y la temperatura en el reactor tubular es de 100°C. El producto puede envasarse a la salida del reactor tubular sin procesamiento posterior.
Ejemplo 4: Octanoil/decanoilglucamida a partir de una disolución acuosa de N-metilglucamina y éster metílico de ocatonoilo/decanoilo con el uso de un agente de transferencia de fase
A partir de una disolución acuosa de N-metilglucamina con hidróxido de sodio, se prepara una masa fundida de N-metilglucamina caliente a 135°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. Esta masa fundida de N-metilglucamina caliente a 135°C y el éster metílico de octanoilo/decanoilo se mezclan, con la adición de propilenglicol, a 120°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 10 min y en el reactor tubular de 3 min. La temperatura en el recipiente de agitación es de 85°C y la temperatura en el reactor tubular es de 75°C. En la reacción se genera metanol, que se separa a 120°C, mediante un evaporador de capa delgada en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 5: Octanoil/decanoilglucamida a partir de una disolución acuosa de N-metilglucamina y éster metílico de ocatonoilo/decanoilo
A partir de una disolución acuosa de N-metilglucamina con hidróxido de sodio, se prepara una masa fundida de N-metilglucamina caliente a 135°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. Esta masa fundida de N-metilglucamina caliente a 135°C y el éster metílico de octanoilo/decanoilo se mezclan a 120°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 17 min y en el reactor tubular de 4 min. La temperatura en el recipiente de agitación es de 95°C y la temperatura en el reactor tubular es de 85°C. En la reacción se genera metanol, que se separa a 135°C, mediante un evaporador de corto recorrido en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 6: n-Lauroil/n-miristoil-N-metil-N-glucamida a partir de una disolución acuosa de N-metilglucamina y éster metílico de ácido láurico/mirístico con el uso de un agente de transferencia de fase
A partir de una disolución acuosa de N-metilglucamina con hidróxido de sodio, se prepara una masa fundida de N-metilglucamina caliente a 135°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. Esta masa fundida de N-metilglucamina caliente a 135°C y el éster metílico de ácido láurico/mirístico se mezclan, con
la adición de etanol como agente de transferencia de fase, a 120°C mediante un mezclador estático. La mezcla se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor tubular es de 45 min. La temperatura en el reactor tubular es de 155°C. En la reacción se genera metanol, que se separa a 135°C, mediante una columna en funcionamiento continuo, colocada a la salida del reactor tubular.
Ejemplo 7: n-Lauroil/n-miristoil-W-metil-W-glucamida a partir de una disolución acuosa de W-metilglucamina y éster metílico de ácido láurico/mirístico
A partir de una disolución acuosa de W-metilglucamina con hidróxido de sodio, se prepara una masa fundida de W-metilglucamina caliente a 130°C por medio de un evaporador de capa delgada en funcionamiento continuo a 140°C. Esta masa fundida de W-metilglucamina caliente a 130°C y el éster metílico de ácido láurico/mirístico se mezclan a 130°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 33 min y en el reactor tubular de 13 min. La temperatura en el recipiente de agitación es de 100°C y la temperatura en el reactor tubular es de 95°C. En la reacción se genera metanol, que se separa a 145°C, mediante un evaporador de corto recorrido en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 8: Hexadecanoil/octadecanoil-W-metil-W-glucamida a partir de una disolución acuosa de W-metilglucamina y éster metílico de hexadecanoilo/octadecanoilo con el uso de un agente de transferencia de fase.
A partir de una disolución acuosa de W-metilglucamina con hidróxido de potasio, se prepara una masa fundida de W-metilglucamina caliente a 135°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. Esta masa fundida de W-metilglucamina caliente a 135°C y el éster metílico de hexadecanoilo/octadecanoilo se mezclan, con la adición de hexadecanoil/octadecanoil-W-metil-W-glucamida como agente de transferencia de fase, a 120°C mediante un mezclador estático. La mezcla se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor tubular es de 28 min. La temperatura en el reactor tubular es de 105°C. En la reacción se genera metanol, que se separa a 135°C, mediante un evaporador de capa delgada en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 9: Hexadecanoil/octadecanoil-W-metil-W-glucamida a partir de una disolución acuosa de W-metilglucamina y éster metílico de hexadecanoilo/octadecanoilo.
A partir de una disolución acuosa de W-metilglucamina con hidróxido de sodio, se prepara una masa fundida de W-metilglucamina caliente a 140°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. Esta masa fundida de W-metilglucamina caliente a 140°C y el éster metílico de hexadecanoilo/octadecanoilo se mezclan, con la adición de propilenglicol como agente de transferencia de fase, a 130°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 17 min y en el reactor tubular de 5 min. La temperatura en el recipiente de agitación es de 95°C y la temperatura en el reactor tubular es de 85°C. En la reacción se genera metanol, que se separa a 135°C, mediante un evaporador de capa delgada en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 10: n-Dodecanoil/n-docosanoil-W-metil-W-glucamida a partir de una disolución acuosa de W-metilglucamina y éster metílico de n-dodecanoilo/n-docosanoilo
A partir de una disolución acuosa de W-metilglucamina con hidróxido de sodio, se prepara una masa fundida de W-metilglucamina caliente a 135°C por medio de un evaporador de capa delgada en funcionamiento continuo a 145°C. Esta masa fundida de W-metilglucamina caliente a 135°C se mezcla, con la adición de propilenglicol y éster metílico de n-dodecanoilo/n-docosanoilo, a 120°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 20 min y en el reactor tubular de 9 min. La temperatura en el recipiente de agitación es de 88°C y la temperatura en el reactor tubular es de 78°C. En la reacción se genera metanol, que se separa a 135°C, mediante un evaporador de capa delgada en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 11: n-Dodecanoil-W-etil-W-glucamida a partir de una disolución acuosa de W-etilglucamina y éster metílico de n-dodecanoilo
A partir de una disolución acuosa de W-etilglucamina con hidróxido de sodio, se prepara una masa fundida de W-etilglucamina caliente a 145°C por medio de un evaporador de capa delgada en funcionamiento continuo a 155°C. Esta masa fundida de W-etilglucamina caliente a 145°C y el éster metílico de n-dodecanoilo se mezclan, con la adición de propilenglicol, a 120°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 44 min y en el reactor tubular de 28 min. La temperatura en el recipiente de agitación es de 105°C y la temperatura en el reactor tubular es de 95°C. En la reacción se genera metanol, que se separa a 135°C, mediante un evaporador de capa delgada en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 12: n-Dodecanoil-W-octil-W-glucamida a partir de una disolución acuosa de W-octilglucamina y éster metílico de n-dodecanoilo
A partir de una disolución acuosa de W-octilglucamina con hidróxido de sodio, se prepara una masa fundida de W-octilglucamina caliente a 145°C por medio de un evaporador de capa delgada en funcionamiento continuo a 155°C. Esta masa fundida de W-octilglucamina caliente a 145°C y el éster metílico de n-dodecanoilo se mezclan, con la adición de propilenglicol, a 120°C mediante un mezclador estático. La mezcla se acumula en un reactor de agitación continuo y a continuación se hace reaccionar en un reactor tubular. El tiempo de permanencia en el reactor de agitación es de 44 min y en el reactor tubular de 28 min. La temperatura en el recipiente de agitación es de 105°C y la temperatura en el reactor tubular es de 95°C. En la reacción se genera metanol, que se separa a 135°C, mediante un evaporador de capa delgada en funcionamiento continuo, colocado a la salida del reactor tubular.
Ejemplo 13: Preparación por lotes: octanoil/decanoilglucamida a partir de una disolución acuosa de W-metilglucamina y éster metílico de octanoilo/decanoilo
Una disolución acuosa de W-metilglucamina con hidróxido de sodio se deshidrata a 130-135°C y a una presión de 25 30 hPa (25-30 mbar) hasta un contenido de agua inferior al 1 %. A la masa fundida de W-metilglucamina se le añade propilenglicol. Después se añade el éster metílico de octanoilo/decanoilo a 120°C. La mezcla se hace reaccionar en un reactor de agitación en funcionamiento discontinuo en condiciones de reflujo. A continuación, el metanol generado se elimina por destilación a una presión de entre 25 hPa (25 mbar) y 1.000 hPa (1 bar) y la reacción posterior se lleva a cabo a 75-85°C. El tiempo de permanencia de la reacción en total es de entre 3 y 8 h, dependiendo del tamaño de la preparación.
Sobre los ejemplos 1 a 13:
Los ejemplos 1 a 5, 10 y 13 se formulan a continuación con agua, ácido cítrico y un conservante. Los ejemplos 6 y 7 se formulan a continuación con agua, ácido cítrico y etanol. Los ejemplos 8 y 9 se formulan con alcohol cetearílico. En comparación con un experimento en funcionamiento discontinuo, pudo observarse una clara mejora del color del producto. En el experimento en funcionamiento discontinuo, el número de color de Gardner (según la norma EN 1557) fue superior a 3,5. El producto obtenido en funcionamiento continuo presenta un número de color de Gardner por debajo de 3,5. En cuanto al componente secundario (glucamida cíclica), se observó una proporción inferior al 0,1 % en peso. En el proceso por lotes, el valor es superior al 0,1 % en peso. Los números de color APHA se midieron según la norma EN 1557.
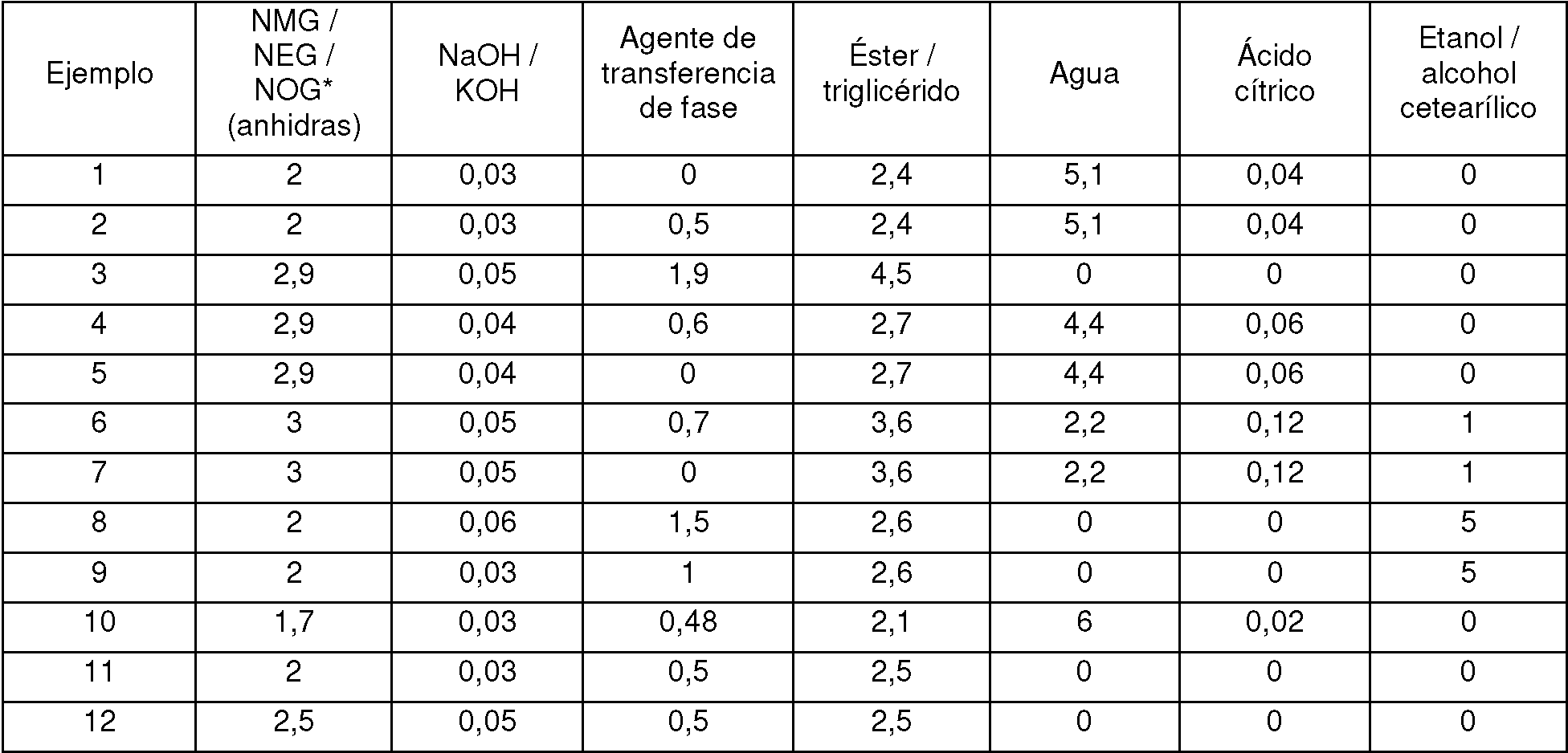
Tablas sobre las condiciones de proceso de los ejemplos 1 a 12:
Temperaturas en °C:
Presión (absoluta) en hPa (bar):
Flujos de cantidades en kg/h:
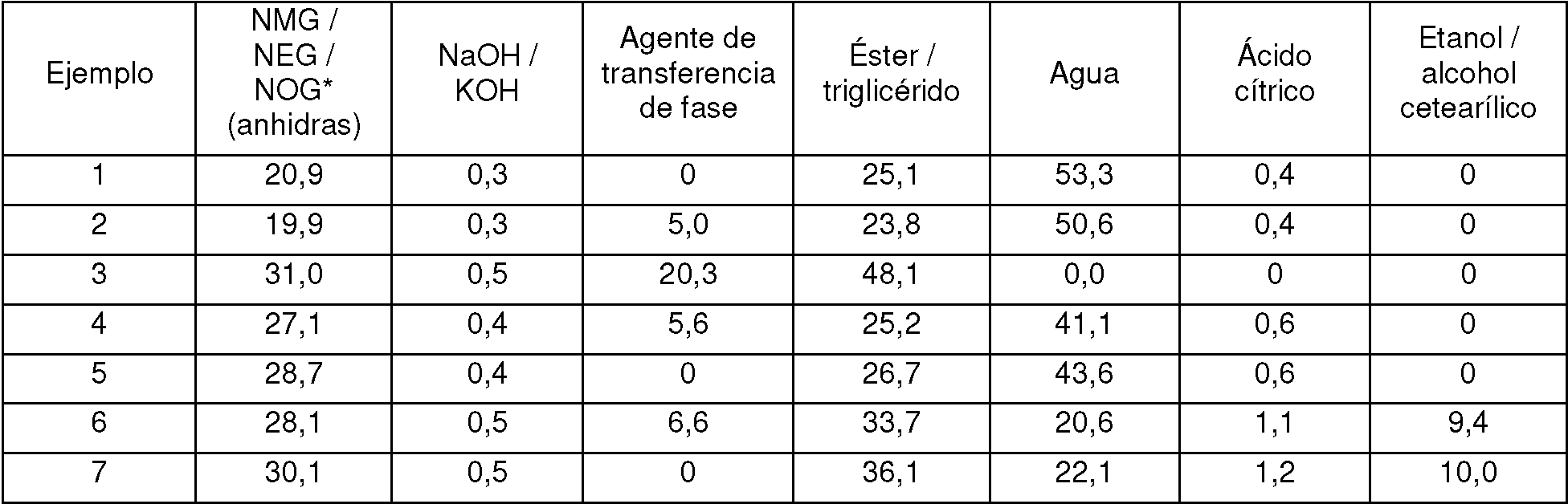
* NMG = W-metilglucamina; NEG = /V-etilglucamina; NOG = W-octilglucamina Flujos de cantidades en % en peso:
* NMG = W-metilglucamina; NEG = W-etilglucamina; NOG = W-octilglucamina
Proporciones másicas para el experimento por lotes (en % en peso):
Resultados:
* NMG = W-metilglucamina; NEG = W-etilglucamina; NOG = W-octilglucamina
Claims (15)
1. Procedimiento continuo para la preparación de un tensioactivo que comprende un compuesto de la fórmula (1), en donde R2 es el resto alquilo de un ácido graso y R1 es un resto hidrocarbilo C1 a C12 de cadena lineal o ramificada, y x está en el intervalo de 1 a 15,
mediante la reacción de ésteres alquílicos de ácidos grasos o triglicéridos de ácidos grasos con un compuesto polihidroxilado N-n-alquilado, en presencia de un catalizador alcalino o un catalizador elegido de entre hidróxidos o alcóxidos de elementos de transición de los grupos 2 y 4 de la Tabla Periódica, a una temperatura en el intervalo de 40 a 300°C, en donde el procedimiento comprende las etapas siguientes:
1. mezclar la disolución acuosa de materias primas que comprende una o varias N-alquilglucaminas con el catalizador;
2. secar la disolución acuosa, en donde el contenido de agua después del secado se encuentra en el intervalo del 0-5 % en peso;
3. calentar la mezcla seca a una temperatura en el intervalo de 60 a 180°C y mezclar la masa fundida con ésteres alquílicos de ácidos grasos o triglicéridos;
4. opcionalmente, almacenar temporalmente y mezclar la mezcla de reacción en una caldera de agitación en funcionamiento continuo;
5. hacer reaccionar en un reactor tubular; y
6. opcionalmente, retirar los subproductos.
2. Procedimiento según la reivindicación 1, en donde los ésteres alquílicos de ácidos grasos o triglicéridos de ácidos grasos presentan una longitud de cadena de C4 a C50.
3. Procedimiento según la reivindicación 1 o 2, en donde se usan N-alquilglucaminas C5 a C26.
4. Procedimiento según una o varias de las reivindicaciones 1 a 3, en donde la concentración de las N-alquilglucaminas en la disolución acuosa en la primera etapa del procedimiento está en el intervalo del 30-90 % en peso.
5. Procedimiento según una o varias de las reivindicaciones 1 a 4, en donde el catalizador se emplea en una concentración del 0,01-5 % en peso.
6. Procedimiento según una o varias de las reivindicaciones 1 a 5, en donde la relación molar entre la N-alquilglucamina y el éster alquílico de ácido graso es de 1:0,85 a 1:1,2, o la relación molar entre la N-alquilglucamina y la triglicerina es de 0,25:1 a 0,45:1.
7. Procedimiento según una o varias de las reivindicaciones 1 a 6, en donde el mezclado de la disolución de materias primas de glucamina en la primera etapa tiene lugar a una temperatura en el intervalo de 40-120°C.
8. Procedimiento según una o varias de las reivindicaciones 1 a 7, en donde la reacción de los componentes en el reactor tubular tiene lugar a una temperatura en el intervalo de 60-300°C y a una presión de 0 a 200.000 hPa (0 a 200 bar).
9. Procedimiento según una o varias de las reivindicaciones 1 a 8, en donde la diferencia de temperatura entre la pared del reactor y el flujo del núcleo en los reactores correspondientes es <20°C.
10. Procedimiento según una o varias de las reivindicaciones 1 a 9, en donde se añaden agentes de transferencia de fase a la mezcla de reacción en una o varias de las primeras tres etapas del procedimiento.
11. Procedimiento según la reivindicación 10, en donde como agentes de transferencia de fase se emplean agua, alcoholes, glicoles, N-alquilglucamidas, polialquilglicoles, éteres de corona y/o glicerina.
12. Procedimiento según una o varias de las reivindicaciones 1 a 11, en donde las amidas de ácidos grasos polihidroxilados de la fórmula (1) presentan un número de color (Gardner) en el intervalo de 0 a 3.
13. Procedimiento según una o varias de las reivindicaciones 1 a 12, en donde la proporción de productos secundarios cíclicos en las amidas de ácidos grasos polihidroxilados de la fórmula (1) obtenidas es <0,05 % en peso.
14. Procedimiento según una o varias de las reivindicaciones 1 a 13, en donde la proporción del compuesto (1) en el tensioactivo está en el intervalo del 15 al 100 % en peso.
15. Procedimiento según una o varias de las reivindicaciones 1 a 14, en donde los compuestos de la fórmula (1) obtenidos se mezclan en una etapa final del procedimiento con disolventes o mezclas de disolventes que opcionalmente pueden contener otros aditivos.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102014016841 | 2014-11-13 | ||
| DE102015006119 | 2015-05-11 | ||
| PCT/EP2015/076072 WO2016075080A1 (de) | 2014-11-13 | 2015-11-09 | Kontinuierlicher prozess zur herstellung eines tensids in einem rohrreaktor |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2818799T3 true ES2818799T3 (es) | 2021-04-14 |
Family
ID=54476994
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15790990T Active ES2818799T3 (es) | 2014-11-13 | 2015-11-09 | Proceso continuo para la preparación de un tensioactivo en un reactor tubular |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US10112889B2 (es) |
| EP (1) | EP3218353B1 (es) |
| CN (2) | CN107001239B (es) |
| ES (1) | ES2818799T3 (es) |
| WO (1) | WO2016075080A1 (es) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2855650B1 (de) | 2012-05-30 | 2016-12-28 | Clariant International Ltd | N-methyl-n-acylglucamin enthaltende zusammensetzung |
| US10172774B2 (en) | 2012-05-30 | 2019-01-08 | Clariant International Ltd. | Use of N-methyl-N-acylglucamines as thickening agents in surfactant solutions |
| ES2599504T3 (es) | 2012-05-30 | 2017-02-02 | Clariant International Ltd | Utilización de N-metil-N-acil-glucaminas como agentes solubilizantes |
| IN2014DN09937A (es) | 2012-05-30 | 2015-08-14 | Clariant Int Ltd | |
| DE102012021647A1 (de) | 2012-11-03 | 2014-05-08 | Clariant International Ltd. | Wässrige Adjuvant-Zusammensetzungen |
| US9949909B2 (en) | 2013-06-28 | 2018-04-24 | Clariant International Ltd. | Use of special N-alkyl-N-acylglucamines for conditioning hair in hair washing agents |
| DE102014003215A1 (de) | 2014-03-06 | 2015-05-28 | Clariant International Ltd. | Korrosionsinhibierende Zusammensetzungen |
| DE102014005771A1 (de) | 2014-04-23 | 2015-10-29 | Clariant International Ltd. | Verwendung von wässrigen driftreduzierenden Zusammensetzungen |
| DE102015219651A1 (de) | 2015-10-09 | 2017-04-13 | Clariant International Ltd. | Zusammensetzungen enthaltend Zuckeramin und Fettsäure |
| DE102015219608B4 (de) | 2015-10-09 | 2018-05-03 | Clariant International Ltd | Universelle Pigmentdispersionen auf Basis von N-Alkylglukaminen |
| DE102016207877A1 (de) | 2016-05-09 | 2017-11-09 | Clariant International Ltd | Stabilisatoren für Silikatfarben |
| CN106278922B (zh) * | 2016-08-15 | 2019-01-18 | 广州天赐高新材料股份有限公司 | 一种脂肪酸酰胺丙基叔胺的制备方法 |
| US11572499B2 (en) | 2019-12-11 | 2023-02-07 | Clariant International Ltd | Method of and a composition for controlling gas hydrate blockage through the addition of a synergistically acting blend with a quaternary benzyl ammonium compound |
| EP3858961A1 (en) | 2020-01-28 | 2021-08-04 | The Procter & Gamble Company | Cleaning product |
| EP3858965B1 (en) | 2020-01-28 | 2022-05-11 | The Procter & Gamble Company | Cleaning product |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3244522A1 (de) * | 1982-12-02 | 1984-06-07 | Basf Ag, 6700 Ludwigshafen | Verfahren zur herstellung von nicotinsaeureamid |
| US5194639A (en) * | 1990-09-28 | 1993-03-16 | The Procter & Gamble Company | Preparation of polyhydroxy fatty acid amides in the presence of solvents |
| JP3345005B2 (ja) * | 1991-07-26 | 2002-11-18 | ザ、プロクター、エンド、ギャンブル、カンパニー | 水性/ヒドロキシ溶媒中でのn−アルキルポリヒドロキシアルキルアミンの製造法 |
| DE4235783A1 (de) * | 1992-10-23 | 1994-04-28 | Basf Ag | Verfahren zur Herstellung von N-Alkanoyl-polyhydroxyalkylaminen |
| DE4322874C2 (de) * | 1993-07-09 | 1995-07-20 | Hoechst Ag | Verfahren zur kontinuierlichen Herstellung von Polyhydroxyfettsäureamiden aus N-Alkylpolyhydroxyaminen und Fettsäurealkylestern |
| US5777165A (en) * | 1995-06-07 | 1998-07-07 | The Procter & Gamble Company | Process for preparing amides of N-alkyl polyhydroxyalkyl amines |
| DE19962999A1 (de) * | 1999-12-24 | 2001-07-05 | Clariant Gmbh | Verfahren zur Herstellung von Fettsäure-N-Alkylpolyhydroxyamiden |
-
2015
- 2015-11-09 CN CN201580068307.8A patent/CN107001239B/zh active Active
- 2015-11-09 EP EP15790990.4A patent/EP3218353B1/de active Active
- 2015-11-09 CN CN202010098121.XA patent/CN111217717A/zh active Pending
- 2015-11-09 ES ES15790990T patent/ES2818799T3/es active Active
- 2015-11-09 WO PCT/EP2015/076072 patent/WO2016075080A1/de not_active Ceased
- 2015-11-09 US US15/526,464 patent/US10112889B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2016075080A1 (de) | 2016-05-19 |
| US20170305838A1 (en) | 2017-10-26 |
| CN107001239B (zh) | 2020-02-21 |
| CN111217717A (zh) | 2020-06-02 |
| US10112889B2 (en) | 2018-10-30 |
| CN107001239A (zh) | 2017-08-01 |
| EP3218353A1 (de) | 2017-09-20 |
| EP3218353B1 (de) | 2020-08-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2818799T3 (es) | Proceso continuo para la preparación de un tensioactivo en un reactor tubular | |
| CN103201369B (zh) | 基于天然油复分解生成的组合物的衣物洗涤剂 | |
| CN108699097B (zh) | 鼠李糖脂酯作为非离子表面活性剂用于化妆品用途 | |
| ES2551910T3 (es) | 17alfa propionato de cortexolona en la forma cristalina I | |
| WO2015026538A1 (en) | Process for preparing n-acyl amino acid salts | |
| EP3204365A1 (de) | Langkettige mono- und diester des 2,5-di(hydroxymethyl)tetrahydrofurans, deren herstellung und verwendung | |
| EP2144987B1 (de) | Verfärbungsinhibition von wasch- und reinigungsmitteln und/oder kosmetischen mitteln | |
| CN104023836B (zh) | 表面活性剂组合物 | |
| CN116601139A (zh) | N-酰基氨基酸表面活性剂及其衍生物 | |
| ES2807631T3 (es) | Alcoxilatos de alcohol de intervalo estrecho y derivados de los mismos | |
| EP2810935B1 (de) | Sulfatierte Ester von Oligohydroxycarbonsäuren und deren Verwendung | |
| CN105001127A (zh) | 一种格尔伯特醇磺基琥珀酸单酯二钠盐及其制备方法 | |
| JP7695359B2 (ja) | 炭素/窒素結合を有するプロ有益剤化合物 | |
| CN102482289B (zh) | 异山梨醇甘油醚衍生物以及它们在家庭应用中的用途 | |
| CN101514217B (zh) | 一种辛酸蔗糖酯的超声合成方法 | |
| JP5925001B2 (ja) | 脂肪酸アルカノールアミドの製造方法 | |
| US10829498B2 (en) | Composition comprising precursor for volatiles | |
| CN101554569B (zh) | 一种阴离子型Gemini表面活性剂的合成方法 | |
| JPWO2002002510A1 (ja) | ポリオキシプロピレン脂肪酸イソプロパノールアミド界面活性剤精製物、その製造方法及びそれを含む洗浄剤組成物 | |
| ES2636866T3 (es) | Procedimiento de producción de óxido de rosa deshidro | |
| JP5912899B2 (ja) | アニオン界面活性剤組成物の製造方法 | |
| KR101918074B1 (ko) | 당류계 계면활성제의 제조방법 | |
| CN101511769A (zh) | 乳酰乳酸烷基酯及其制备方法 | |
| US20240209282A1 (en) | N-acyl aminoalkane sulfonate surfactants and derivatives thereof | |
| CN116634998A (zh) | 具有碳/氮键的助益剂化合物 |