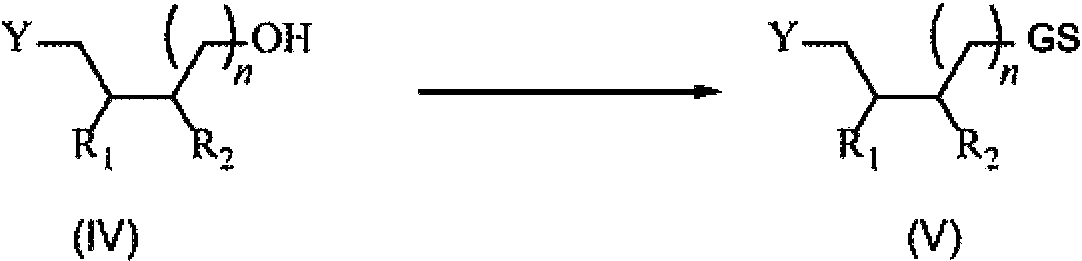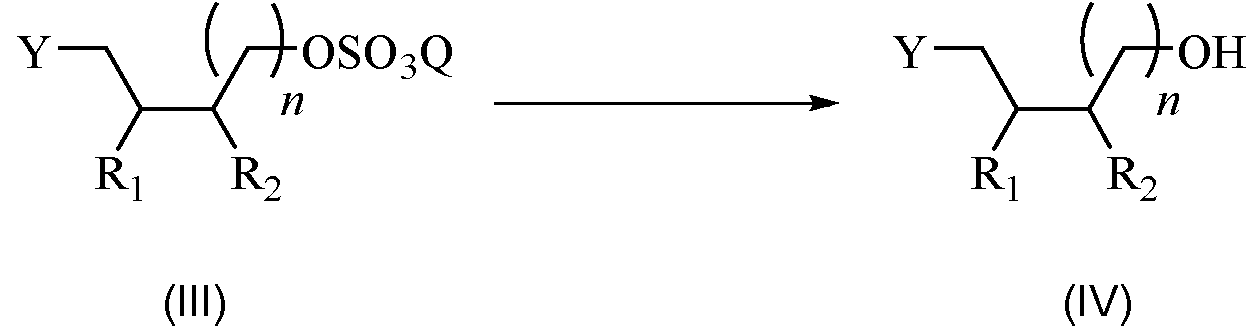ES2826603T3 - Procesos para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada que incluyen productos intermedios novedosos - Google Patents
Procesos para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada que incluyen productos intermedios novedosos Download PDFInfo
- Publication number
- ES2826603T3 ES2826603T3 ES15731459T ES15731459T ES2826603T3 ES 2826603 T3 ES2826603 T3 ES 2826603T3 ES 15731459 T ES15731459 T ES 15731459T ES 15731459 T ES15731459 T ES 15731459T ES 2826603 T3 ES2826603 T3 ES 2826603T3
- Authority
- ES
- Spain
- Prior art keywords
- formula
- compound
- group
- aryl
- methyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 72
- 238000000034 method Methods 0.000 title claims abstract description 46
- 238000002360 preparation method Methods 0.000 title claims abstract description 29
- 239000000543 intermediate Substances 0.000 title description 8
- -1 piperazine compound Chemical class 0.000 claims abstract description 51
- 125000003118 aryl group Chemical group 0.000 claims abstract description 50
- 125000001072 heteroaryl group Chemical group 0.000 claims abstract description 46
- 125000000623 heterocyclic group Chemical group 0.000 claims abstract description 40
- 125000004122 cyclic group Chemical group 0.000 claims abstract description 33
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 19
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims abstract description 15
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 14
- 239000001257 hydrogen Substances 0.000 claims abstract description 14
- 125000002619 bicyclic group Chemical group 0.000 claims abstract description 11
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 claims abstract description 10
- 239000002168 alkylating agent Substances 0.000 claims abstract description 10
- 125000002252 acyl group Chemical group 0.000 claims abstract description 9
- 229940100198 alkylating agent Drugs 0.000 claims abstract description 9
- 150000003863 ammonium salts Chemical class 0.000 claims abstract description 9
- 230000002152 alkylating effect Effects 0.000 claims abstract description 7
- GLUUGHFHXGJENI-UHFFFAOYSA-N diethylenediamine Natural products C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 claims abstract description 7
- 229910052751 metal Inorganic materials 0.000 claims abstract description 7
- 239000002184 metal Substances 0.000 claims abstract description 7
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims abstract description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims abstract description 5
- 125000000547 substituted alkyl group Chemical group 0.000 claims abstract description 5
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 claims description 24
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 15
- 125000001424 substituent group Chemical group 0.000 claims description 14
- 229910000027 potassium carbonate Inorganic materials 0.000 claims description 12
- 229960001432 lurasidone Drugs 0.000 claims description 11
- PQXKDMSYBGKCJA-CVTJIBDQSA-N lurasidone Chemical compound C1=CC=C2C(N3CCN(CC3)C[C@@H]3CCCC[C@H]3CN3C(=O)[C@@H]4[C@H]5CC[C@H](C5)[C@@H]4C3=O)=NSC2=C1 PQXKDMSYBGKCJA-CVTJIBDQSA-N 0.000 claims description 11
- TZJUVVIWVWFLCD-UHFFFAOYSA-N 1,1-dioxo-2-[4-[4-(2-pyrimidinyl)-1-piperazinyl]butyl]-1,2-benzothiazol-3-one Chemical compound O=S1(=O)C2=CC=CC=C2C(=O)N1CCCCN(CC1)CCN1C1=NC=CC=N1 TZJUVVIWVWFLCD-UHFFFAOYSA-N 0.000 claims description 8
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 claims description 8
- 229910052799 carbon Inorganic materials 0.000 claims description 8
- 229950003599 ipsapirone Drugs 0.000 claims description 8
- 125000003545 alkoxy group Chemical group 0.000 claims description 7
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 6
- 229910052736 halogen Inorganic materials 0.000 claims description 5
- 150000002367 halogens Chemical class 0.000 claims description 5
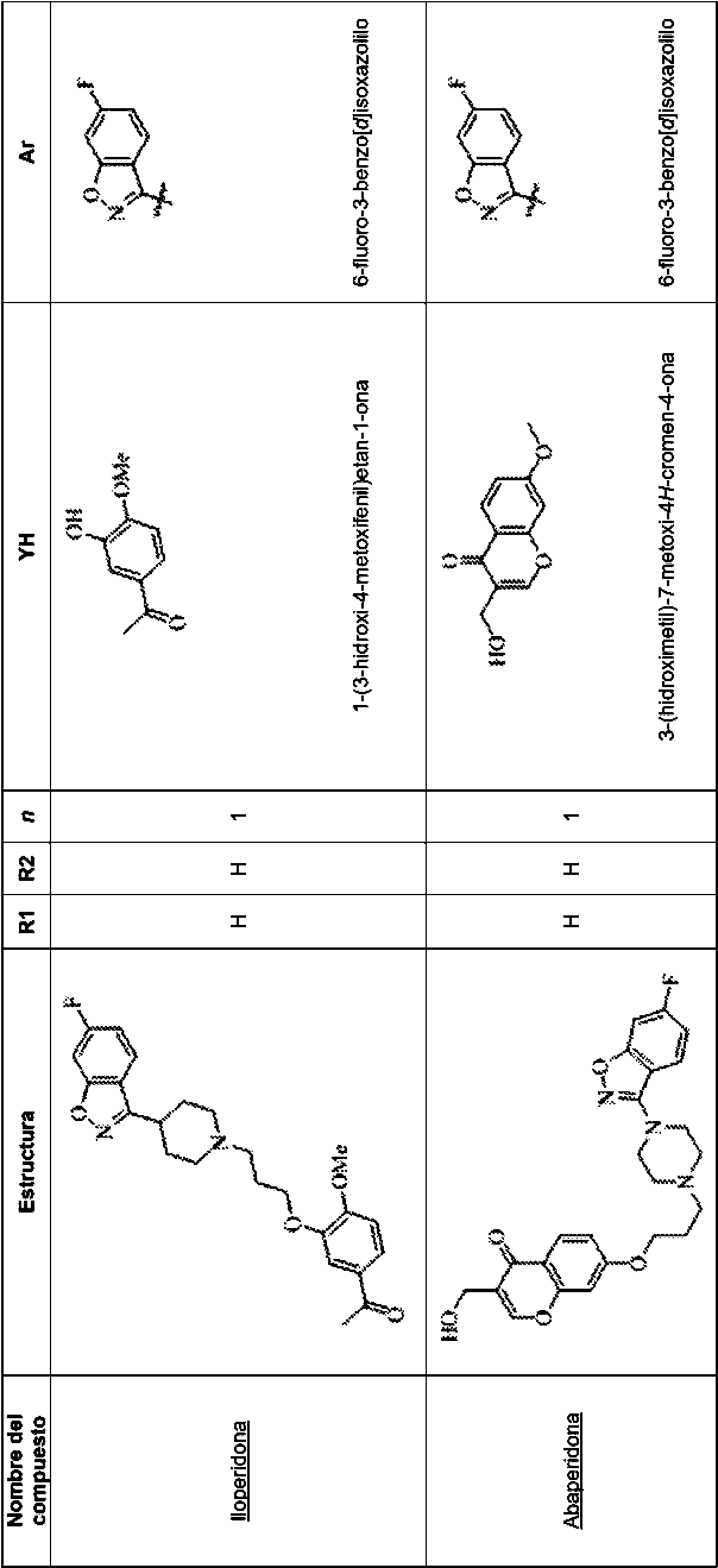
- 229960003162 iloperidone Drugs 0.000 claims description 5
- XMXHEBAFVSFQEX-UHFFFAOYSA-N iloperidone Chemical compound COC1=CC(C(C)=O)=CC=C1OCCCN1CCC(C=2C3=CC=C(F)C=C3ON=2)CC1 XMXHEBAFVSFQEX-UHFFFAOYSA-N 0.000 claims description 5
- 239000011591 potassium Substances 0.000 claims description 5
- 229910052700 potassium Inorganic materials 0.000 claims description 5
- CEUORZQYGODEFX-UHFFFAOYSA-N Aripirazole Chemical compound ClC1=CC=CC(N2CCN(CCCCOC=3C=C4NC(=O)CCC4=CC=3)CC2)=C1Cl CEUORZQYGODEFX-UHFFFAOYSA-N 0.000 claims description 4
- WOGUGQPVSGXHBK-YUMQZZPRSA-N C(CC1)C[C@@H]2[C@@H]1COSOC2 Chemical compound C(CC1)C[C@@H]2[C@@H]1COSOC2 WOGUGQPVSGXHBK-YUMQZZPRSA-N 0.000 claims description 4
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 claims description 4
- 229960004372 aripiprazole Drugs 0.000 claims description 4
- 235000015320 potassium carbonate Nutrition 0.000 claims description 4
- MSZUCXVGSQLRIL-HGPDSQILSA-N (1S,2R,6S,7R)-4-[[(1R,2R)-2-(hydroxymethyl)cyclohexyl]methyl]-4-azatricyclo[5.2.1.02,6]decane-3,5-dione Chemical compound O=C([C@H]1[C@@H](C2=O)[C@]3([H])CC[C@]1(C3)[H])N2C[C@@H]1CCCC[C@H]1CO MSZUCXVGSQLRIL-HGPDSQILSA-N 0.000 claims description 3
- 239000012359 Methanesulfonyl chloride Substances 0.000 claims description 3
- 229910019142 PO4 Inorganic materials 0.000 claims description 3
- 150000008052 alkyl sulfonates Chemical class 0.000 claims description 3
- 125000005228 aryl sulfonate group Chemical group 0.000 claims description 3
- 229960002495 buspirone Drugs 0.000 claims description 3
- QWCRAEMEVRGPNT-UHFFFAOYSA-N buspirone Chemical compound C1C(=O)N(CCCCN2CCN(CC2)C=2N=CC=CN=2)C(=O)CC21CCCC2 QWCRAEMEVRGPNT-UHFFFAOYSA-N 0.000 claims description 3
- 229960000647 gepirone Drugs 0.000 claims description 3
- QOIGKGMMAGJZNZ-UHFFFAOYSA-N gepirone Chemical compound O=C1CC(C)(C)CC(=O)N1CCCCN1CCN(C=2N=CC=CN=2)CC1 QOIGKGMMAGJZNZ-UHFFFAOYSA-N 0.000 claims description 3
- 230000003301 hydrolyzing effect Effects 0.000 claims description 3
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 claims description 3
- 229950004193 perospirone Drugs 0.000 claims description 3
- GTAIPSDXDDTGBZ-OYRHEFFESA-N perospirone Chemical compound C1=CC=C2C(N3CCN(CC3)CCCCN3C(=O)[C@@H]4CCCC[C@@H]4C3=O)=NSCC2=C1 GTAIPSDXDDTGBZ-OYRHEFFESA-N 0.000 claims description 3
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 claims description 3
- 239000010452 phosphate Substances 0.000 claims description 3
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 claims description 3
- 125000003107 substituted aryl group Chemical group 0.000 claims description 3
- CEIJFEGBUDEYSX-FZDBZEDMSA-N tandospirone Chemical compound O=C([C@@H]1[C@H]2CC[C@H](C2)[C@@H]1C1=O)N1CCCCN(CC1)CCN1C1=NC=CC=N1 CEIJFEGBUDEYSX-FZDBZEDMSA-N 0.000 claims description 3
- 229950000505 tandospirone Drugs 0.000 claims description 3
- AERLHOTUXIJQFV-RCPZPFRWSA-N zalospirone Chemical compound O=C([C@@H]1[C@@H]([C@@H]2C=C[C@H]1[C@H]1C=C[C@H]12)C1=O)N1CCCCN(CC1)CCN1C1=NC=CC=N1 AERLHOTUXIJQFV-RCPZPFRWSA-N 0.000 claims description 3
- 229950005255 zalospirone Drugs 0.000 claims description 3
- BXNRTMZZILHVNJ-ZRZAMGCNSA-N (1s,5r)-7-butyl-3-[4-[4-(2-methoxyphenyl)piperazin-1-yl]butyl]-9,9-dimethyl-3,7-diazabicyclo[3.3.1]nonane-2,4,6,8-tetrone Chemical compound O=C([C@@H]1C(=O)N(C([C@H](C2=O)C1(C)C)=O)CCCC)N2CCCCN(CC1)CCN1C1=CC=CC=C1OC BXNRTMZZILHVNJ-ZRZAMGCNSA-N 0.000 claims description 2
- MPLTZRTXQLNGED-UHFFFAOYSA-N 1,1-dioxo-2-[3-(4-pyrimidin-2-ylpiperazin-1-yl)propyl]-1,2-benzothiazol-3-one Chemical compound O=S1(=O)C2=CC=CC=C2C(=O)N1CCCN(CC1)CCN1C1=NC=CC=N1 MPLTZRTXQLNGED-UHFFFAOYSA-N 0.000 claims description 2
- RIVOBMOBWMOLDJ-UHFFFAOYSA-N 6713-41-3 Chemical compound C1CC2C3C(=O)NC(=O)C3C1C2 RIVOBMOBWMOLDJ-UHFFFAOYSA-N 0.000 claims description 2
- ICAXEUYZCLRXKY-UHFFFAOYSA-N 7-[3-[4-(6-fluoro-1,2-benzoxazol-3-yl)piperidin-1-yl]propoxy]-3-(hydroxymethyl)chromen-4-one Chemical compound FC1=CC=C2C(C3CCN(CC3)CCCOC=3C=C4OC=C(C(C4=CC=3)=O)CO)=NOC2=C1 ICAXEUYZCLRXKY-UHFFFAOYSA-N 0.000 claims description 2
- NMYAHEULKSYAPP-UHFFFAOYSA-N Eptapirone Chemical compound O=C1N(C)C(=O)C=NN1CCCCN1CCN(C=2N=CC=CN=2)CC1 NMYAHEULKSYAPP-UHFFFAOYSA-N 0.000 claims description 2
- KRDOFMHJLWKXIU-UHFFFAOYSA-N ID11614 Chemical compound C1CNCCN1C1=NSC2=CC=CC=C12 KRDOFMHJLWKXIU-UHFFFAOYSA-N 0.000 claims description 2
- 229950007013 abaperidone Drugs 0.000 claims description 2
- 125000004104 aryloxy group Chemical group 0.000 claims description 2
- 125000005605 benzo group Chemical group 0.000 claims description 2
- 150000001720 carbohydrates Chemical class 0.000 claims description 2
- 229950002850 eptapirone Drugs 0.000 claims description 2
- JZMJDSHXVKJFKW-UHFFFAOYSA-M methyl sulfate(1-) Chemical compound COS([O-])(=O)=O JZMJDSHXVKJFKW-UHFFFAOYSA-M 0.000 claims description 2
- 229950000275 revospirone Drugs 0.000 claims description 2
- 229950011472 umespirone Drugs 0.000 claims description 2
- RIVOBMOBWMOLDJ-RNGGSSJXSA-N (3ar,4s,7r,7as)-hexahydro-1h-4,7-methanoisoindole-1,3(2h)-dione Chemical compound O=C1NC(=O)[C@@H]2[C@H]1[C@]1([H])C[C@@]2([H])CC1 RIVOBMOBWMOLDJ-RNGGSSJXSA-N 0.000 claims 1
- LYXKFNHUJJDTIA-UHFFFAOYSA-N 2-[4-[4-(7-chloro-2,3-dihydro-1,4-benzodioxin-5-yl)piperazin-1-yl]butyl]-1,1-dioxo-1,2-benzothiazol-3-one Chemical compound O=C1C2=CC=CC=C2S(=O)(=O)N1CCCCN(CC1)CCN1C1=CC(Cl)=CC2=C1OCCO2 LYXKFNHUJJDTIA-UHFFFAOYSA-N 0.000 claims 1
- RRLWEQBPSAFVAS-UHFFFAOYSA-N 7-[3-[4-(2,3-dimethylphenyl)piperazin-1-yl]propoxy]-1h-quinolin-2-one Chemical compound CC1=CC=CC(N2CCN(CCCOC=3C=C4NC(=O)C=CC4=CC=3)CC2)=C1C RRLWEQBPSAFVAS-UHFFFAOYSA-N 0.000 claims 1
- VGIGHGMPMUCLIQ-UHFFFAOYSA-N LSM-2183 Chemical compound C1=CC(F)=CC=C1N1CCN(CCCN2S(C=3C=CC=C4C=CC=C2C=34)(=O)=O)CC1 VGIGHGMPMUCLIQ-UHFFFAOYSA-N 0.000 claims 1
- 229950002951 fananserin Drugs 0.000 claims 1
- 125000001793 isothiazol-3-yl group Chemical group [H]C1=C([H])C(*)=NS1 0.000 claims 1
- 229950007918 mafoprazine Drugs 0.000 claims 1
- PHOCQBYGUQPMIB-UHFFFAOYSA-N n-[4-[3-[4-(2-fluorophenyl)piperazin-1-yl]propoxy]-3-methoxyphenyl]acetamide Chemical compound COC1=CC(NC(C)=O)=CC=C1OCCCN1CCN(C=2C(=CC=CC=2)F)CC1 PHOCQBYGUQPMIB-UHFFFAOYSA-N 0.000 claims 1
- WPKPLSFHHBBLRY-UHFFFAOYSA-N pelanserin Chemical compound O=C1NC2=CC=CC=C2C(=O)N1CCCN(CC1)CCN1C1=CC=CC=C1 WPKPLSFHHBBLRY-UHFFFAOYSA-N 0.000 claims 1
- 229950005867 pelanserin Drugs 0.000 claims 1
- 125000004194 piperazin-1-yl group Chemical group [H]N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 claims 1
- WBGWGHYJIFOATF-UHFFFAOYSA-M potassium;methyl sulfate Chemical compound [K+].COS([O-])(=O)=O WBGWGHYJIFOATF-UHFFFAOYSA-M 0.000 claims 1
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 48
- 125000005842 heteroatom Chemical group 0.000 description 48
- 239000000203 mixture Substances 0.000 description 41
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical group CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 39
- 238000006243 chemical reaction Methods 0.000 description 34
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 32
- 239000000243 solution Substances 0.000 description 32
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 23
- 238000004128 high performance liquid chromatography Methods 0.000 description 21
- 229910001868 water Inorganic materials 0.000 description 21
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 20
- 239000002585 base Substances 0.000 description 20
- 125000004432 carbon atom Chemical group C* 0.000 description 20
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 18
- 229910052757 nitrogen Inorganic materials 0.000 description 18
- 235000019439 ethyl acetate Nutrition 0.000 description 17
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 16
- 239000007787 solid Substances 0.000 description 16
- 239000002904 solvent Substances 0.000 description 16
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 14
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 14
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 14
- 229910052760 oxygen Inorganic materials 0.000 description 14
- 239000001301 oxygen Chemical group 0.000 description 14
- 229910052717 sulfur Chemical group 0.000 description 14
- 239000011593 sulfur Chemical group 0.000 description 14
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 12
- 239000010410 layer Substances 0.000 description 11
- 239000012044 organic layer Substances 0.000 description 11
- 239000012458 free base Substances 0.000 description 10
- 239000012074 organic phase Substances 0.000 description 10
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- 235000015497 potassium bicarbonate Nutrition 0.000 description 8
- 229910000028 potassium bicarbonate Inorganic materials 0.000 description 8
- 239000011736 potassium bicarbonate Substances 0.000 description 8
- 235000011181 potassium carbonates Nutrition 0.000 description 8
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 8
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 7
- 230000015572 biosynthetic process Effects 0.000 description 7
- 150000003254 radicals Chemical class 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 7
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 125000002837 carbocyclic group Chemical group 0.000 description 6
- 239000003208 petroleum Substances 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 5
- 238000005804 alkylation reaction Methods 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- 150000007529 inorganic bases Chemical class 0.000 description 5
- 125000004433 nitrogen atom Chemical group N* 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 238000010992 reflux Methods 0.000 description 5
- 239000000741 silica gel Substances 0.000 description 5
- 229910002027 silica gel Inorganic materials 0.000 description 5
- 125000002373 5 membered heterocyclic group Chemical group 0.000 description 4
- 125000006163 5-membered heteroaryl group Chemical group 0.000 description 4
- 125000004070 6 membered heterocyclic group Chemical group 0.000 description 4
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- 229910000288 alkali metal carbonate Inorganic materials 0.000 description 4
- 150000008041 alkali metal carbonates Chemical class 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- 125000006574 non-aromatic ring group Chemical group 0.000 description 4
- 239000002244 precipitate Substances 0.000 description 4
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 4
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 4
- XUEIXBTXKMJFLK-UHFFFAOYSA-N 1-[3-(3-hydroxypropoxy)-4-methoxyphenyl]ethanone Chemical compound OCCCOC=1C=C(C=CC=1OC)C(C)=O XUEIXBTXKMJFLK-UHFFFAOYSA-N 0.000 description 3
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Chemical compound C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 3
- JBMFHJZAZFFGGM-UHFFFAOYSA-N 3-(5-acetyl-2-methoxyphenoxy)propyl methanesulfonate Chemical compound CS(=O)(=O)OCCCOC1=C(C=CC(=C1)C(C)=O)OC JBMFHJZAZFFGGM-UHFFFAOYSA-N 0.000 description 3
- 125000006164 6-membered heteroaryl group Chemical group 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- ZTHQBROSBNNGPU-UHFFFAOYSA-N Butyl hydrogen sulfate Chemical compound CCCCOS(O)(=O)=O ZTHQBROSBNNGPU-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- 230000029936 alkylation Effects 0.000 description 3
- 239000012296 anti-solvent Substances 0.000 description 3
- 239000008346 aqueous phase Substances 0.000 description 3
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000004440 column chromatography Methods 0.000 description 3
- 238000002425 crystallisation Methods 0.000 description 3
- 230000008025 crystallization Effects 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- 150000002170 ethers Chemical class 0.000 description 3
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthene Chemical compound C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 3
- 150000008282 halocarbons Chemical class 0.000 description 3
- 229930195733 hydrocarbon Natural products 0.000 description 3
- 238000006460 hydrolysis reaction Methods 0.000 description 3
- 150000002576 ketones Chemical class 0.000 description 3
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 3
- 125000002950 monocyclic group Chemical group 0.000 description 3
- 150000002825 nitriles Chemical class 0.000 description 3
- 125000004193 piperazinyl group Chemical group 0.000 description 3
- 229930195734 saturated hydrocarbon Natural products 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 229910052938 sodium sulfate Inorganic materials 0.000 description 3
- 235000011152 sodium sulphate Nutrition 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 235000011149 sulphuric acid Nutrition 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 2
- 125000006708 (C5-C14) heteroaryl group Chemical group 0.000 description 2
- LBHHODMHAKLELL-UHFFFAOYSA-N 2-(4-hydroxybutyl)-1,1-dioxo-1,2-benzothiazol-3-one Chemical compound C1=CC=C2S(=O)(=O)N(CCCCO)C(=O)C2=C1 LBHHODMHAKLELL-UHFFFAOYSA-N 0.000 description 2
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical group [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- 125000005915 C6-C14 aryl group Chemical group 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- XADCESSVHJOZHK-UHFFFAOYSA-N Meperidine Chemical compound C=1C=CC=CC=1C1(C(=O)OCC)CCN(C)CC1 XADCESSVHJOZHK-UHFFFAOYSA-N 0.000 description 2
- 239000007832 Na2SO4 Substances 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical group [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- 125000003158 alcohol group Chemical group 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 2
- 229910000318 alkali metal phosphate Inorganic materials 0.000 description 2
- 125000000304 alkynyl group Chemical group 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 239000000164 antipsychotic agent Substances 0.000 description 2
- 229940005529 antipsychotics Drugs 0.000 description 2
- 239000011260 aqueous acid Substances 0.000 description 2
- CUFNKYGDVFVPHO-UHFFFAOYSA-N azulene Chemical compound C1=CC=CC2=CC=CC2=C1 CUFNKYGDVFVPHO-UHFFFAOYSA-N 0.000 description 2
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 2
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 2
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- LFLBHTZRLVHUQC-UHFFFAOYSA-N butyl methanesulfonate Chemical compound CCCCOS(C)(=O)=O LFLBHTZRLVHUQC-UHFFFAOYSA-N 0.000 description 2
- 229910000019 calcium carbonate Inorganic materials 0.000 description 2
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 2
- 239000000920 calcium hydroxide Substances 0.000 description 2
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- VPUGDVKSAQVFFS-UHFFFAOYSA-N coronene Chemical compound C1=C(C2=C34)C=CC3=CC=C(C=C3)C4=C4C3=CC=C(C=C3)C4=C2C3=C1 VPUGDVKSAQVFFS-UHFFFAOYSA-N 0.000 description 2
- 239000013058 crude material Substances 0.000 description 2
- 239000008367 deionised water Substances 0.000 description 2
- 229910021641 deionized water Inorganic materials 0.000 description 2
- 238000006073 displacement reaction Methods 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 238000004817 gas chromatography Methods 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- PQNFLJBBNBOBRQ-UHFFFAOYSA-N indane Chemical compound C1=CC=C2CCCC2=C1 PQNFLJBBNBOBRQ-UHFFFAOYSA-N 0.000 description 2
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 2
- 125000001041 indolyl group Chemical group 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- NEKCRUIRPWNMLK-SCIYSFAVSA-N lurasidone hydrochloride Chemical compound Cl.C1=CC=C2C(N3CCN(CC3)C[C@@H]3CCCC[C@H]3CN3C(=O)[C@@H]4[C@H]5CC[C@H](C5)[C@@H]4C3=O)=NSC2=C1 NEKCRUIRPWNMLK-SCIYSFAVSA-N 0.000 description 2
- 229960002863 lurasidone hydrochloride Drugs 0.000 description 2
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 2
- 239000001095 magnesium carbonate Substances 0.000 description 2
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 2
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 description 2
- 239000000347 magnesium hydroxide Substances 0.000 description 2
- 229910001862 magnesium hydroxide Inorganic materials 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- IZDROVVXIHRYMH-UHFFFAOYSA-N methanesulfonic anhydride Chemical compound CS(=O)(=O)OS(C)(=O)=O IZDROVVXIHRYMH-UHFFFAOYSA-N 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 239000013618 particulate matter Substances 0.000 description 2
- 229960000482 pethidine Drugs 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 239000011574 phosphorus Chemical group 0.000 description 2
- JJRDAUHFDQNQIA-UHFFFAOYSA-M potassium 3-(5-acetyl-2-methoxyphenoxy)propyl sulfate Chemical compound S(=O)(=O)(OCCCOC1=C(C=CC(=C1)C(C)=O)OC)[O-].[K+] JJRDAUHFDQNQIA-UHFFFAOYSA-M 0.000 description 2
- 229910000160 potassium phosphate Inorganic materials 0.000 description 2
- 235000011009 potassium phosphates Nutrition 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 2
- 229940095743 selective estrogen receptor modulator Drugs 0.000 description 2
- 239000000333 selective estrogen receptor modulator Substances 0.000 description 2
- 229940124834 selective serotonin reuptake inhibitor Drugs 0.000 description 2
- 239000012896 selective serotonin reuptake inhibitor Substances 0.000 description 2
- BNRNXUUZRGQAQC-UHFFFAOYSA-N sildenafil Chemical compound CCCC1=NN(C)C(C(N2)=O)=C1N=C2C(C(=CC=1)OCC)=CC=1S(=O)(=O)N1CCN(C)CC1 BNRNXUUZRGQAQC-UHFFFAOYSA-N 0.000 description 2
- 229910052710 silicon Chemical group 0.000 description 2
- 239000010703 silicon Chemical group 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 239000001488 sodium phosphate Substances 0.000 description 2
- 229910000162 sodium phosphate Inorganic materials 0.000 description 2
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- AHOUBRCZNHFOSL-YOEHRIQHSA-N (+)-Casbol Chemical compound C1=CC(F)=CC=C1[C@H]1[C@H](COC=2C=C3OCOC3=CC=2)CNCC1 AHOUBRCZNHFOSL-YOEHRIQHSA-N 0.000 description 1
- ZCVIMNDSJRRGRK-YUMQZZPRSA-N (5aR,9aR)-1,5,5a,6,7,8,9,9a-octahydrobenzo[e][1,3,2]dioxathiepine 3-oxide Chemical compound C1OS(OC[C@H]2[C@H]1CCCC2)=O ZCVIMNDSJRRGRK-YUMQZZPRSA-N 0.000 description 1
- JJIBEXZGSXIQBV-UHFFFAOYSA-N 1,1-dioxo-1,2-thiazol-3-one Chemical compound O=C1NS(=O)(=O)C=C1 JJIBEXZGSXIQBV-UHFFFAOYSA-N 0.000 description 1
- 125000005926 1,2-dimethylbutyloxy group Chemical group 0.000 description 1
- OQYOVYWFXHQYOP-UHFFFAOYSA-N 1,3,2-dioxathiane 2,2-dioxide Chemical compound O=S1(=O)OCCCO1 OQYOVYWFXHQYOP-UHFFFAOYSA-N 0.000 description 1
- MRBFGEHILMYPTF-UHFFFAOYSA-N 1-(2-Pyrimidyl)piperazine Chemical compound C1CNCCN1C1=NC=CC=N1 MRBFGEHILMYPTF-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- IZXIZTKNFFYFOF-UHFFFAOYSA-N 2-Oxazolidone Chemical compound O=C1NCCO1 IZXIZTKNFFYFOF-UHFFFAOYSA-N 0.000 description 1
- ZKLPARSLTMPFCP-OAQYLSRUSA-N 2-[2-[4-[(R)-(4-chlorophenyl)-phenylmethyl]-1-piperazinyl]ethoxy]acetic acid Chemical compound C1CN(CCOCC(=O)O)CCN1[C@@H](C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-OAQYLSRUSA-N 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000001627 3 membered heterocyclic group Chemical group 0.000 description 1
- 125000001963 4 membered heterocyclic group Chemical group 0.000 description 1
- SXIFAEWFOJETOA-UHFFFAOYSA-N 4-hydroxy-butyl Chemical group [CH2]CCCO SXIFAEWFOJETOA-UHFFFAOYSA-N 0.000 description 1
- MRMGJMGHPJZSAE-UHFFFAOYSA-N 6-fluoro-3-piperidin-4-yl-1,2-benzoxazole Chemical compound N=1OC2=CC(F)=CC=C2C=1C1CCNCC1 MRMGJMGHPJZSAE-UHFFFAOYSA-N 0.000 description 1
- 125000003341 7 membered heterocyclic group Chemical group 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 125000005330 8 membered heterocyclic group Chemical group 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 125000000041 C6-C10 aryl group Chemical group 0.000 description 1
- ZKLPARSLTMPFCP-UHFFFAOYSA-N Cetirizine Chemical compound C1CN(CCOCC(=O)O)CCN1C(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-UHFFFAOYSA-N 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- PLDUPXSUYLZYBN-UHFFFAOYSA-N Fluphenazine Chemical compound C1CN(CCO)CCN1CCCN1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C21 PLDUPXSUYLZYBN-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- OCJYIGYOJCODJL-UHFFFAOYSA-N Meclizine Chemical compound CC1=CC=CC(CN2CCN(CC2)C(C=2C=CC=CC=2)C=2C=CC(Cl)=CC=2)=C1 OCJYIGYOJCODJL-UHFFFAOYSA-N 0.000 description 1
- DUGOZIWVEXMGBE-UHFFFAOYSA-N Methylphenidate Chemical compound C=1C=CC=CC=1C(C(=O)OC)C1CCCCN1 DUGOZIWVEXMGBE-UHFFFAOYSA-N 0.000 description 1
- ZFMITUMMTDLWHR-UHFFFAOYSA-N Minoxidil Chemical compound NC1=[N+]([O-])C(N)=CC(N2CCCCC2)=N1 ZFMITUMMTDLWHR-UHFFFAOYSA-N 0.000 description 1
- XKLMZUWKNUAPSZ-UHFFFAOYSA-N N-(2,6-dimethylphenyl)-2-{4-[2-hydroxy-3-(2-methoxyphenoxy)propyl]piperazin-1-yl}acetamide Chemical compound COC1=CC=CC=C1OCC(O)CN1CCN(CC(=O)NC=2C(=CC=CC=2C)C)CC1 XKLMZUWKNUAPSZ-UHFFFAOYSA-N 0.000 description 1
- XWURZHGKODQZMK-UHFFFAOYSA-N O.[Ru]=O Chemical compound O.[Ru]=O XWURZHGKODQZMK-UHFFFAOYSA-N 0.000 description 1
- AHOUBRCZNHFOSL-UHFFFAOYSA-N Paroxetine hydrochloride Natural products C1=CC(F)=CC=C1C1C(COC=2C=C3OCOC3=CC=2)CNCC1 AHOUBRCZNHFOSL-UHFFFAOYSA-N 0.000 description 1
- RGCVKNLCSQQDEP-UHFFFAOYSA-N Perphenazine Chemical compound C1CN(CCO)CCN1CCCN1C2=CC(Cl)=CC=C2SC2=CC=CC=C21 RGCVKNLCSQQDEP-UHFFFAOYSA-N 0.000 description 1
- YILKCZCSLWVTFP-UHFFFAOYSA-N S1N=CC=C1.[K] Chemical compound S1N=CC=C1.[K] YILKCZCSLWVTFP-UHFFFAOYSA-N 0.000 description 1
- KLBQZWRITKRQQV-UHFFFAOYSA-N Thioridazine Chemical compound C12=CC(SC)=CC=C2SC2=CC=CC=C2N1CCC1CCCCN1C KLBQZWRITKRQQV-UHFFFAOYSA-N 0.000 description 1
- GFBKORZTTCHDGY-UWVJOHFNSA-N Thiothixene Chemical compound C12=CC(S(=O)(=O)N(C)C)=CC=C2SC2=CC=CC=C2\C1=C\CCN1CCN(C)CC1 GFBKORZTTCHDGY-UWVJOHFNSA-N 0.000 description 1
- UHWVSEOVJBQKBE-UHFFFAOYSA-N Trimetazidine Chemical compound COC1=C(OC)C(OC)=CC=C1CN1CCNCC1 UHWVSEOVJBQKBE-UHFFFAOYSA-N 0.000 description 1
- SLGBZMMZGDRARJ-UHFFFAOYSA-N Triphenylene Natural products C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 description 1
- SECKRCOLJRRGGV-UHFFFAOYSA-N Vardenafil Chemical compound CCCC1=NC(C)=C(C(N=2)=O)N1NC=2C(C(=CC=1)OCC)=CC=1S(=O)(=O)N1CCN(CC)CC1 SECKRCOLJRRGGV-UHFFFAOYSA-N 0.000 description 1
- XDODWINGEHBYRT-YUMQZZPRSA-N [(1r,2r)-2-(hydroxymethyl)cyclohexyl]methanol Chemical compound OC[C@@H]1CCCC[C@H]1CO XDODWINGEHBYRT-YUMQZZPRSA-N 0.000 description 1
- QVXFGVVYTKZLJN-KHPPLWFESA-N [(z)-hexadec-7-enyl] acetate Chemical compound CCCCCCCC\C=C/CCCCCCOC(C)=O QVXFGVVYTKZLJN-KHPPLWFESA-N 0.000 description 1
- 125000004054 acenaphthylenyl group Chemical group C1(=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- SQFPKRNUGBRTAR-UHFFFAOYSA-N acephenanthrylene Chemical group C1=CC(C=C2)=C3C2=CC2=CC=CC=C2C3=C1 SQFPKRNUGBRTAR-UHFFFAOYSA-N 0.000 description 1
- HXGDTGSAIMULJN-UHFFFAOYSA-N acetnaphthylene Natural products C1=CC(C=C2)=C3C2=CC=CC3=C1 HXGDTGSAIMULJN-UHFFFAOYSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 125000004423 acyloxy group Chemical group 0.000 description 1
- 150000001335 aliphatic alkanes Chemical group 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical group 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- QWGDMFLQWFTERH-UHFFFAOYSA-N amoxapine Chemical compound C12=CC(Cl)=CC=C2OC2=CC=CC=C2N=C1N1CCNCC1 QWGDMFLQWFTERH-UHFFFAOYSA-N 0.000 description 1
- 229960002519 amoxapine Drugs 0.000 description 1
- 229950000388 amperozide Drugs 0.000 description 1
- NNAIYOXJNVGUOM-UHFFFAOYSA-N amperozide Chemical compound C1CN(C(=O)NCC)CCN1CCCC(C=1C=CC(F)=CC=1)C1=CC=C(F)C=C1 NNAIYOXJNVGUOM-UHFFFAOYSA-N 0.000 description 1
- 239000002269 analeptic agent Substances 0.000 description 1
- 230000003555 analeptic effect Effects 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 230000003257 anti-anginal effect Effects 0.000 description 1
- 229940124345 antianginal agent Drugs 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 229940125715 antihistaminic agent Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- KNNXFYIMEYKHBZ-UHFFFAOYSA-N as-indacene Chemical compound C1=CC2=CC=CC2=C2C=CC=C21 KNNXFYIMEYKHBZ-UHFFFAOYSA-N 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 125000003725 azepanyl group Chemical group 0.000 description 1
- 125000002785 azepinyl group Chemical group 0.000 description 1
- 125000002393 azetidinyl group Chemical group 0.000 description 1
- FXCHUJDUNXTHRW-UHFFFAOYSA-N benzenesulfonyloxy-(4-methylphenyl)sulfonyloxymethanesulfonic acid Chemical compound CC1=CC=C(C=C1)S(=O)(=O)OC(OS(=O)(=O)C2=CC=CC=C2)S(=O)(=O)O FXCHUJDUNXTHRW-UHFFFAOYSA-N 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000002618 bicyclic heterocycle group Chemical group 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 229960001705 buclizine Drugs 0.000 description 1
- MOYGZHXDRJNJEP-UHFFFAOYSA-N buclizine Chemical compound C1=CC(C(C)(C)C)=CC=C1CN1CCN(C(C=2C=CC=CC=2)C=2C=CC(Cl)=CC=2)CC1 MOYGZHXDRJNJEP-UHFFFAOYSA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 229960001803 cetirizine Drugs 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 1
- DERZBLKQOCDDDZ-JLHYYAGUSA-N cinnarizine Chemical compound C1CN(C(C=2C=CC=CC=2)C=2C=CC=CC=2)CCN1C\C=C\C1=CC=CC=C1 DERZBLKQOCDDDZ-JLHYYAGUSA-N 0.000 description 1
- 229960000876 cinnarizine Drugs 0.000 description 1
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 1
- NJMYODHXAKYRHW-DVZOWYKESA-N cis-flupenthixol Chemical compound C1CN(CCO)CCN1CC\C=C\1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C2/1 NJMYODHXAKYRHW-DVZOWYKESA-N 0.000 description 1
- 229960004170 clozapine Drugs 0.000 description 1
- QZUDBNBUXVUHMW-UHFFFAOYSA-N clozapine Chemical compound C1CN(C)CCN1C1=NC2=CC(Cl)=CC=C2NC2=CC=CC=C12 QZUDBNBUXVUHMW-UHFFFAOYSA-N 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 150000003950 cyclic amides Chemical class 0.000 description 1
- 229960003564 cyclizine Drugs 0.000 description 1
- UVKZSORBKUEBAZ-UHFFFAOYSA-N cyclizine Chemical compound C1CN(C)CCN1C(C=1C=CC=CC=1)C1=CC=CC=C1 UVKZSORBKUEBAZ-UHFFFAOYSA-N 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000006639 cyclohexyl carbonyl group Chemical group 0.000 description 1
- 125000000723 dihydrobenzofuranyl group Chemical group O1C(CC2=C1C=CC=C2)* 0.000 description 1
- 125000004582 dihydrobenzothienyl group Chemical group S1C(CC2=C1C=CC=C2)* 0.000 description 1
- 125000004852 dihydrofuranyl group Chemical group O1C(CC=C1)* 0.000 description 1
- 125000004655 dihydropyridinyl group Chemical group N1(CC=CC=C1)* 0.000 description 1
- 125000005054 dihydropyrrolyl group Chemical group [H]C1=C([H])C([H])([H])C([H])([H])N1* 0.000 description 1
- 125000005057 dihydrothienyl group Chemical group S1C(CC=C1)* 0.000 description 1
- 125000000532 dioxanyl group Chemical group 0.000 description 1
- WOMOXMDBLOIJIX-UHFFFAOYSA-N dioxathiepine Chemical compound C=1C=CSOOC=1 WOMOXMDBLOIJIX-UHFFFAOYSA-N 0.000 description 1
- 125000005879 dioxolanyl group Chemical group 0.000 description 1
- 125000005883 dithianyl group Chemical group 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- RMEDXOLNCUSCGS-UHFFFAOYSA-N droperidol Chemical compound C1=CC(F)=CC=C1C(=O)CCCN1CC=C(N2C(NC3=CC=CC=C32)=O)CC1 RMEDXOLNCUSCGS-UHFFFAOYSA-N 0.000 description 1
- 229960000394 droperidol Drugs 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- AIVSIRYZIBXTMM-UHFFFAOYSA-N ethylphenidate Chemical compound C=1C=CC=CC=1C(C(=O)OCC)C1CCCCN1 AIVSIRYZIBXTMM-UHFFFAOYSA-N 0.000 description 1
- 239000012065 filter cake Substances 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 229960002419 flupentixol Drugs 0.000 description 1
- 229960002690 fluphenazine Drugs 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 229960003878 haloperidol Drugs 0.000 description 1
- QSQIGGCOCHABAP-UHFFFAOYSA-N hexacene Chemical compound C1=CC=CC2=CC3=CC4=CC5=CC6=CC=CC=C6C=C5C=C4C=C3C=C21 QSQIGGCOCHABAP-UHFFFAOYSA-N 0.000 description 1
- PKIFBGYEEVFWTJ-UHFFFAOYSA-N hexaphene Chemical compound C1=CC=C2C=C3C4=CC5=CC6=CC=CC=C6C=C5C=C4C=CC3=CC2=C1 PKIFBGYEEVFWTJ-UHFFFAOYSA-N 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- ZQDWXGKKHFNSQK-UHFFFAOYSA-N hydroxyzine Chemical compound C1CN(CCOCCO)CCN1C(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZQDWXGKKHFNSQK-UHFFFAOYSA-N 0.000 description 1
- 229960000930 hydroxyzine Drugs 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- YLTGFGDODHXMFB-UHFFFAOYSA-N isoacetovanillone Chemical compound COC1=CC=C(C(C)=O)C=C1O YLTGFGDODHXMFB-UHFFFAOYSA-N 0.000 description 1
- 125000004594 isoindolinyl group Chemical group C1(NCC2=CC=CC=C12)* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- MGIYRDNGCNKGJU-UHFFFAOYSA-N isothiazolinone Chemical compound O=C1C=CSN1 MGIYRDNGCNKGJU-UHFFFAOYSA-N 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 229960001508 levocetirizine Drugs 0.000 description 1
- RDOIQAHITMMDAJ-UHFFFAOYSA-N loperamide Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(C(=O)N(C)C)CCN(CC1)CCC1(O)C1=CC=C(Cl)C=C1 RDOIQAHITMMDAJ-UHFFFAOYSA-N 0.000 description 1
- 229960001571 loperamide Drugs 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 229960001474 meclozine Drugs 0.000 description 1
- SLVMESMUVMCQIY-UHFFFAOYSA-N mesoridazine Chemical compound CN1CCCCC1CCN1C2=CC(S(C)=O)=CC=C2SC2=CC=CC=C21 SLVMESMUVMCQIY-UHFFFAOYSA-N 0.000 description 1
- 229960000300 mesoridazine Drugs 0.000 description 1
- 229960001344 methylphenidate Drugs 0.000 description 1
- 229960003632 minoxidil Drugs 0.000 description 1
- 125000002757 morpholinyl group Chemical group 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- VRBKIVRKKCLPHA-UHFFFAOYSA-N nefazodone Chemical compound O=C1N(CCOC=2C=CC=CC=2)C(CC)=NN1CCCN(CC1)CCN1C1=CC=CC(Cl)=C1 VRBKIVRKKCLPHA-UHFFFAOYSA-N 0.000 description 1
- 229960001800 nefazodone Drugs 0.000 description 1
- 229960002686 niaprazine Drugs 0.000 description 1
- RSKQGBFMNPDPLR-UHFFFAOYSA-N niaprazine Chemical compound C=1C=CN=CC=1C(=O)NC(C)CCN(CC1)CCN1C1=CC=C(F)C=C1 RSKQGBFMNPDPLR-UHFFFAOYSA-N 0.000 description 1
- 239000002664 nootropic agent Substances 0.000 description 1
- 230000001777 nootropic effect Effects 0.000 description 1
- 239000012038 nucleophile Substances 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- PFTXKXWAXWAZBP-UHFFFAOYSA-N octacene Chemical compound C1=CC=CC2=CC3=CC4=CC5=CC6=CC7=CC8=CC=CC=C8C=C7C=C6C=C5C=C4C=C3C=C21 PFTXKXWAXWAZBP-UHFFFAOYSA-N 0.000 description 1
- OVPVGJFDFSJUIG-UHFFFAOYSA-N octalene Chemical compound C1=CC=CC=C2C=CC=CC=CC2=C1 OVPVGJFDFSJUIG-UHFFFAOYSA-N 0.000 description 1
- WTFQBTLMPISHTA-UHFFFAOYSA-N octaphene Chemical compound C1=CC=C2C=C(C=C3C4=CC5=CC6=CC7=CC=CC=C7C=C6C=C5C=C4C=CC3=C3)C3=CC2=C1 WTFQBTLMPISHTA-UHFFFAOYSA-N 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 229960005017 olanzapine Drugs 0.000 description 1
- KVWDHTXUZHCGIO-UHFFFAOYSA-N olanzapine Chemical compound C1CN(C)CCN1C1=NC2=CC=CC=C2NC2=C1C=C(C)S2 KVWDHTXUZHCGIO-UHFFFAOYSA-N 0.000 description 1
- 229940005483 opioid analgesics Drugs 0.000 description 1
- LSQODMMMSXHVCN-UHFFFAOYSA-N ovalene Chemical compound C1=C(C2=C34)C=CC3=CC=C(C=C3C5=C6C(C=C3)=CC=C3C6=C6C(C=C3)=C3)C4=C5C6=C2C3=C1 LSQODMMMSXHVCN-UHFFFAOYSA-N 0.000 description 1
- 125000005882 oxadiazolinyl group Chemical group 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 125000003551 oxepanyl group Chemical group 0.000 description 1
- 125000003585 oxepinyl group Chemical group 0.000 description 1
- 125000003566 oxetanyl group Chemical group 0.000 description 1
- 125000000466 oxiranyl group Chemical group 0.000 description 1
- 229960002296 paroxetine Drugs 0.000 description 1
- PMJHHCWVYXUKFD-UHFFFAOYSA-N penta-1,3-diene Chemical compound CC=CC=C PMJHHCWVYXUKFD-UHFFFAOYSA-N 0.000 description 1
- SLIUAWYAILUBJU-UHFFFAOYSA-N pentacene Chemical compound C1=CC=CC2=CC3=CC4=CC5=CC=CC=C5C=C4C=C3C=C21 SLIUAWYAILUBJU-UHFFFAOYSA-N 0.000 description 1
- GUVXZFRDPCKWEM-UHFFFAOYSA-N pentalene Chemical compound C1=CC2=CC=CC2=C1 GUVXZFRDPCKWEM-UHFFFAOYSA-N 0.000 description 1
- JQQSUOJIMKJQHS-UHFFFAOYSA-N pentaphene Chemical compound C1=CC=C2C=C3C4=CC5=CC=CC=C5C=C4C=CC3=CC2=C1 JQQSUOJIMKJQHS-UHFFFAOYSA-N 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 229960000762 perphenazine Drugs 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- NQFOGDIWKQWFMN-UHFFFAOYSA-N phenalene Chemical compound C1=CC([CH]C=C2)=C3C2=CC=CC3=C1 NQFOGDIWKQWFMN-UHFFFAOYSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- 150000004885 piperazines Chemical class 0.000 description 1
- 150000003053 piperidines Chemical class 0.000 description 1
- 125000003386 piperidinyl group Chemical group 0.000 description 1
- XSWHNYGMWWVAIE-UHFFFAOYSA-N pipradrol Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(O)C1CCCCN1 XSWHNYGMWWVAIE-UHFFFAOYSA-N 0.000 description 1
- 229960000753 pipradrol Drugs 0.000 description 1
- 125000003367 polycyclic group Chemical group 0.000 description 1
- WIKYUJGCLQQFNW-UHFFFAOYSA-N prochlorperazine Chemical compound C1CN(C)CCN1CCCN1C2=CC(Cl)=CC=C2SC2=CC=CC=C21 WIKYUJGCLQQFNW-UHFFFAOYSA-N 0.000 description 1
- 229960003111 prochlorperazine Drugs 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001042 pteridinyl group Chemical group N1=C(N=CC2=NC=CN=C12)* 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- GZUITABIAKMVPG-UHFFFAOYSA-N raloxifene Chemical compound C1=CC(O)=CC=C1C1=C(C(=O)C=2C=CC(OCCN3CCCCC3)=CC=2)C2=CC=C(O)C=C2S1 GZUITABIAKMVPG-UHFFFAOYSA-N 0.000 description 1
- 229960004622 raloxifene Drugs 0.000 description 1
- 229960000213 ranolazine Drugs 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 229960001534 risperidone Drugs 0.000 description 1
- RAPZEAPATHNIPO-UHFFFAOYSA-N risperidone Chemical compound FC1=CC=C2C(C3CCN(CC3)CCC=3C(=O)N4CCCCC4=NC=3C)=NOC2=C1 RAPZEAPATHNIPO-UHFFFAOYSA-N 0.000 description 1
- FMKFBRKHHLWKDB-UHFFFAOYSA-N rubicene Chemical compound C12=CC=CC=C2C2=CC=CC3=C2C1=C1C=CC=C2C4=CC=CC=C4C3=C21 FMKFBRKHHLWKDB-UHFFFAOYSA-N 0.000 description 1
- 229910001925 ruthenium oxide Inorganic materials 0.000 description 1
- WOCIAKWEIIZHES-UHFFFAOYSA-N ruthenium(iv) oxide Chemical compound O=[Ru]=O WOCIAKWEIIZHES-UHFFFAOYSA-N 0.000 description 1
- WEMQMWWWCBYPOV-UHFFFAOYSA-N s-indacene Chemical compound C=1C2=CC=CC2=CC2=CC=CC2=1 WEMQMWWWCBYPOV-UHFFFAOYSA-N 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229960003310 sildenafil Drugs 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000003039 tetrahydroisoquinolinyl group Chemical group C1(NCCC2=CC=CC=C12)* 0.000 description 1
- 125000001712 tetrahydronaphthyl group Chemical group C1(CCCC2=CC=CC=C12)* 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- 125000000147 tetrahydroquinolinyl group Chemical group N1(CCCC2=CC=CC=C12)* 0.000 description 1
- 125000003507 tetrahydrothiofenyl group Chemical group 0.000 description 1
- 125000005247 tetrazinyl group Chemical group N1=NN=NC(=C1)* 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 125000005305 thiadiazolinyl group Chemical group 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000005458 thianyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000005297 thienyloxy group Chemical group S1C(=CC=C1)O* 0.000 description 1
- 125000001583 thiepanyl group Chemical group 0.000 description 1
- 125000003777 thiepinyl group Chemical group 0.000 description 1
- 229960002784 thioridazine Drugs 0.000 description 1
- 229960005013 tiotixene Drugs 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 229960003991 trazodone Drugs 0.000 description 1
- PHLBKPHSAVXXEF-UHFFFAOYSA-N trazodone Chemical compound ClC1=CC=CC(N2CCN(CCCN3C(N4C=CC=CC4=N3)=O)CC2)=C1 PHLBKPHSAVXXEF-UHFFFAOYSA-N 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000005881 triazolinyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- ZEWQUBUPAILYHI-UHFFFAOYSA-N trifluoperazine Chemical compound C1CN(C)CCN1CCCN1C2=CC(C(F)(F)F)=CC=C2SC2=CC=CC=C21 ZEWQUBUPAILYHI-UHFFFAOYSA-N 0.000 description 1
- 229960002324 trifluoperazine Drugs 0.000 description 1
- 229960001177 trimetazidine Drugs 0.000 description 1
- 125000005580 triphenylene group Chemical group 0.000 description 1
- 229960004847 urologicals Drugs 0.000 description 1
- 238000005292 vacuum distillation Methods 0.000 description 1
- 229960002381 vardenafil Drugs 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- UXDQRXUZPXSLJK-UHFFFAOYSA-N vilazodone Chemical compound C1=CC(C#N)=C[C]2C(CCCCN3CCN(CC3)C=3C=C4C=C(OC4=CC=3)C(=O)N)=CN=C21 UXDQRXUZPXSLJK-UHFFFAOYSA-N 0.000 description 1
- 229960003740 vilazodone Drugs 0.000 description 1
- 229960000607 ziprasidone Drugs 0.000 description 1
- MVWVFYHBGMAFLY-UHFFFAOYSA-N ziprasidone Chemical compound C1=CC=C2C(N3CCN(CC3)CCC3=CC=4CC(=O)NC=4C=C3Cl)=NSC2=C1 MVWVFYHBGMAFLY-UHFFFAOYSA-N 0.000 description 1
- WFPIAZLQTJBIFN-DVZOWYKESA-N zuclopenthixol Chemical compound C1CN(CCO)CCN1CC\C=C\1C2=CC(Cl)=CC=C2SC2=CC=CC=C2/1 WFPIAZLQTJBIFN-DVZOWYKESA-N 0.000 description 1
- 229960004141 zuclopenthixol Drugs 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C39/00—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/52—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring condensed with a ring other than six-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/16—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D215/20—Oxygen atoms
- C07D215/22—Oxygen atoms attached in position 2 or 4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/16—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D215/20—Oxygen atoms
- C07D215/22—Oxygen atoms attached in position 2 or 4
- C07D215/227—Oxygen atoms attached in position 2 or 4 only one oxygen atom which is attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
- C07D239/72—Quinazolines; Hydrogenated quinazolines
- C07D239/86—Quinazolines; Hydrogenated quinazolines with hetero atoms directly attached in position 4
- C07D239/88—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D241/00—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings
- C07D241/02—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings
- C07D241/04—Heterocyclic compounds containing 1,4-diazine or hydrogenated 1,4-diazine rings not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D261/00—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings
- C07D261/20—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D275/00—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings
- C07D275/04—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings condensed with carbocyclic rings or ring systems
- C07D275/06—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings condensed with carbocyclic rings or ring systems with hetero atoms directly attached to the ring sulfur atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/06—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/06—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2
- C07D311/20—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2 hydrogenated in the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/08—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing alicyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains three hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Thiazole And Isothizaole Compounds (AREA)
- Indole Compounds (AREA)
- Hydrogenated Pyridines (AREA)
Abstract
Un proceso para la preparación de un compuesto de arilpiperazina alquilada de Fórmula (I): **(Ver fórmula)** en donde, R1 y R2 se seleccionan individualmente de hidrógeno, alquilo no sustituido y alquilo sustituido o R1 y R2 se conectan para formar un anillo cíclico de 5 a 8 carbonos; n es 0, 1 o 2; Y es NR3R4, OR5 o SR5, donde R3 y R4 se seleccionan individualmente de acilo o sulfonilo, en donde R3 y R4 se pueden conectar para formar un anillo cíclico o bicíclico sustituido o no sustituido y en donde R5 es arilo o heteroarilo, o heterocíclico; y Ar es un grupo arilo o heteroarilo; comprendiendo dicho proceso las etapas de: (i) alquilar YH con un sulfato cíclico de Fórmula (II) en presencia de una base para formar un compuesto de Fórmula (III), en donde Q es hidrógeno, un metal o una sal de amonio; **(Ver fórmula)** (ii) hidrolizar el compuesto de Fórmula (III) para formar un alcohol de Fórmula (IV); **(Ver fórmula)** (iii) convertir el compuesto de Fórmula (IV) para formar un agente alquilante de Fórmula (V) en donde GS es un grupo saliente; y **(Ver fórmula)** (iv) alquilar un compuesto de piperazina de Fórmula (VI) con el agente alquilante de Fórmula (V) para proporcionar la arilpiperazina alquilada de Fórmula (I) **(Ver fórmula)**
Description
DESCRIPCIÓN
Procesos para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada que incluyen productos intermedios novedosos
Referencia cruzada a solicitudes relacionadas
Campo de la invención
La presente divulgación proporciona procesos para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada, así como compuestos intermedios novedosos formados durante esos procesos.
Antecedentes de la invención
Las piperazinas son una amplia clase de compuestos químicos, muchos con importantes propiedades farmacológicas, que contienen un grupo funcional piperazina de núcleo. Muchos medicamentos actualmente destacados contienen un anillo de piperazina como parte de su estructura molecular. Los ejemplos incluyen: antianginosos (ranolazina, trimetazidina); antidepresivos (amoxapina, befuralina, buspirona, flesinoxano, gepirona, ipsapirona, nefazodona, piberalina, tandospirona, trazodona, vilazodona, zalospirona); antihistamínicos (buclizina, meclozina, cinarizina, ciclizina, hidroxizina, cetirizina, levocetirizina, niaprazina); antipsicóticos (flufenazina, perfenazina, trifluoperazina, proclorperazina, tiotixeno, flupentixol, zuclopentixol, amperozida, aripiprazol, lurasidona, clozapina, olanzapina, perospirona, ziprasidona); urológicos (sildenafil, vardenafil).
La piperidina también es un componente básico y un reactivo químico ampliamente usado en la síntesis de compuestos orgánicos, incluyendo los productos farmacéuticos. Al igual que la piperazina, la piperidina y sus derivados son componentes básicos ubicuos en la síntesis de productos farmacéuticos y productos químicos refinados. Por ejemplo, la estructura de la piperidina se halla en las siguientes clases de productos farmacéuticos: ISRS (inhibidores selectivos de la recaptación de serotonina) (paroxetina); analépticos/nootrópicos (estimulantes) (metilfenidato, etilfenidato, pipradrol, desoxipipradrol); MSRE (moduladores selectivos de los receptores de estrógenos) (raloxifeno); vasodilatadores (minoxidil); neurolépticos (antipsicóticos) (risperidona, tioridazina, haloperidol, droperidol, mesoridazina); opioides (petidina, meperidina, loperamida).
Teniendo en cuenta su prevalencia en la formación de una diversidad de compuestos farmacéuticos importantes, existe la necesidad de procesos nuevos y mejorados para la preparación de compuestos tanto de piperazina como de piperidina, incluyendo los productos intermedios y derivados de los mismos, que minimicen la formación de subproductos no deseados y eliminen la necesidad de etapas de purificación adicionales en caso de pérdida del producto. También se hace referencia al documento WO2013/014665.
Sumario de la invención
La presente divulgación proporciona procesos para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada, incluyendo los productos intermedios y derivados de los mismos. De manera más específica, la presente invención proporciona procesos para la preparación de una diversidad de compuestos de arilpiperazina alquilada y arilpiperidina alquilada de Fórmulas (I) y (VII) generales, respectivamente,
en donde R1 y R2 se seleccionan individualmente de hidrógeno, alquilo no sustituido y alquilo sustituido o R1 y R2 se conectan para formar un anillo cíclico de 5 a 8 carbonos; n es 0, 1 o 2; Y es NR3R4, OR5 o SR5, donde R3 y R4 se seleccionan individualmente de acilo o sulfonilo, en donde R3 y R4 se pueden conectar para formar un anillo cíclico o bicíclico sustituido o no sustituido y en donde R5 es arilo o heteroarilo, o heterocíclico; y Ar es un grupo arilo o heteroarilo.
Los compuestos intermedios novedosos, preparados durante los procesos descritos y reivindicados en el presente documento, también se desvelan.
Breve descripción de los dibujos
Sin dibujos.
Descripción detallada de la invención
Definiciones
A menos que se indique de otro modo, los siguientes términos usados en la presente Solicitud, incluyendo la memoria descriptiva y las reivindicaciones, tienen las definiciones proporcionadas a continuación. Cabe señalar que, tal como se usa en la memoria descriptiva y las reivindicaciones adjuntas, las formas en singular "un", "una", "el" y "la" incluyen referentes en plural, a menos que el contexto indique claramente otra cosa.
Todas las designaciones numéricas, tales como, el peso, el pH, la temperatura, el tiempo, la concentración y el peso molecular, incluyendo los intervalos, son aproximaciones que varían en el 10 %. También se ha de entender, aunque no siempre se indique explícitamente, que los reactivos descritos en el presente documento son simplemente ilustrativos y que los equivalentes de los mismos se conocen en la técnica.
En referencia a la presente divulgación, los términos técnicos y científicos usados en las descripciones del presente documento tendrán los significados comúnmente entendidos por un experto habitual en la materia, a menos que se defina específicamente de otro modo. Por consiguiente, los siguientes términos están destinados a tener los siguientes significados.
Los compuestos descritos en el presente documento pueden comprender uno o más centros asimétricos y, por tanto, pueden existir en diversas formas isoméricas, por ejemplo, enantiómeros y/o diastereómeros. Por ejemplo, los compuestos descritos en el presente documento pueden estar en forma de un enantiómero, diastereómero o isómero geométrico individual o pueden estar en forma de una mezcla de estereoisómeros, incluyendo mezclas racémicas y mezclas enriquecidas con uno o más estereoisómeros. Los isómeros se pueden aislar a partir de mezclas mediante métodos conocidos por aquellos expertos en la materia, incluyendo la cromatografía líquida de alta presión (HPLC en inglés) quiral y la formación y cristalización de sales quirales; o se pueden preparar isómeros preferidos mediante síntesis asimétricas. La invención abarca, de manera adicional, los compuestos descritos en el presente documento como isómeros individuales sustancialmente libres de otros isómeros y, como alternativa, como mezclas de diversos isómeros.
Cuando se enumera un intervalo de valores, este está destinado a abarcar cada valor y subintervalo dentro del intervalo. Por ejemplo, el alquilo C1-6 está destinado a abarcar alquilo C1, C2, C3, C4, C5, C6, C1-6, C1-5, C1-4, C1-3, C1-2, C2-6, C2-5, C2-4, C2-3, C3-4, C4-6, C4-5 y C5-13.
Tal como se usa en el presente documento, el término "alquilo" significa el resto de hidrocarburo saturado lineal o ramificado monovalente, que consiste únicamente en átomos de carbono e hidrógeno, que tiene de uno a doce átomos de carbono. El término "alquilo inferior" se refiere a un grupo alquilo de uno a seis átomos de carbono, es decir, alquilo C1-C6. Los ejemplos de grupos alquilo incluyen, pero sin limitación, metilo, etilo, propilo, isopropilo, isobutilo, sec-butilo, ferc-butilo, pentilo, n-hexilo, octilo, dodecilo y similares. El término "alquilo ramificado" significa, por ejemplo, isopropilo, isobutilo y ferc-butilo. Dentro de la definición de "alquilo", se incluyen específicamente aquellas cadenas de hidrocarburo alifático que están opcionalmente sustituidas.
Tal como se usa en el presente documento, el término "alquileno" significa un radical de hidrocarburo saturado lineal divalente de uno a seis átomos de carbono o un radical de hidrocarburo saturado ramificado divalente de tres a seis átomos de carbono, por ejemplo, metileno, etileno, 2,2-dimetiletileno, propileno, 2-metilpropileno, butileno, pentileno y similares.
Tal como se usa en el presente documento, el término "arilo" se refiere a un radical de un sistema de anillo aromático monocíclico o policíclico (por ejemplo, bicíclico o tricíclico) 4n+2 (por ejemplo, que tiene 6, 10 o 14 electrones n compartidos en una disposición cíclica) que tiene 6-14 átomos de carbono en el anillo y cero heteroátomos proporcionados en el sistema de anillo aromático ("arilo C6-14"). En algunas realizaciones, un grupo arilo tiene seis átomos de carbono en el anillo ("arilo C6"; por ejemplo, fenilo), en algunas realizaciones, un grupo arilo tiene diez átomos de carbono en el anillo ("arilo C10"; por ejemplo, naftilo, tal como 1-naftilo y 2-naftilo). En algunas realizaciones, un grupo arilo tiene catorce átomos de carbono en el anillo ("arilo C14"; por ejemplo, antracilo). El término "arilo" también incluye sistemas de anillo en donde el anillo de arilo, tal como se ha definido anteriormente, está condensado con uno o más grupos carbocíclicos o heterocíclicos, en donde el radical o punto de unión está en el anillo de arilo y, en tales casos, el número de átomos de carbono sigue designando el número de átomos de carbono en el sistema de anillo de arilo. Los grupos arilo típicos incluyen, pero sin limitación, grupos derivados de aceantrileno, acenaftileno, acefenantrileno, antraceno, azuleno, benceno, criseno, coroneno, fluoranteno, fluoreno, hexaceno, hexafeno, hexaleno, as-indaceno, s-indaceno, indano, indeno, naftaleno, octaceno, octafeno, octaleno, ovaleno, penta-2,4-dieno, pentaceno, pentaleno, pentafeno, perileno, fenaleno, fenantreno, piceno, pleyadeno, pireno, pirantreno, rubiceno, trifenileno y trinaftaleno. Particularmente, los grupos arilo incluyen fenilo, naftilo, indenilo y tetrahidronaftilo. A menos que se especifique de otro modo, cada caso de un grupo arilo independientemente está opcionalmente sustituido, es decir, no sustituido (un "arilo no sustituido") o sustituido (un "arilo sustituido") con uno o más sustituyentes. En
determinadas realizaciones, el grupo arilo es arilo C6-14 no sustituido. En determinadas realizaciones, el grupo arilo es arilo C6-14 sustituido.
Tal como se usa en el presente documento, el término "heteroarilo" se refiere a un radical de un sistema de anillo aromático monocíclico o bicíclico 4n+2 de 5-10 elementos (por ejemplo, que tiene 6 o 10 electrones n compartidos en una disposición cíclica) que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema de anillo aromático, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-10 elementos"). En los grupos heteroarilo que contienen uno o más átomos de nitrógeno, el punto de unión puede ser un átomo de carbono o nitrógeno, según lo permita la valencia. Los sistemas de anillo bicíclico de heteroarilo pueden incluir uno o más heteroátomos en uno o ambos anillos. El término "heteroarilo" incluye sistemas de anillo en donde el anillo de heteroarilo, tal como se ha definido anteriormente, está condensado con uno o más grupos carbocíclicos o heterocíclicos en donde el punto de unión está en el anillo de heteroarilo y, en tales casos, el número de elementos en el anillo sigue designando el número de elementos en el anillo en el sistema de anillo de heteroarilo. El término "heteroarilo" también incluye sistemas de anillo en donde el anillo de heteroarilo, tal como se ha definido anteriormente, está condensado con uno o más grupos arilo en donde el punto de unión está en el anillo de arilo o heteroarilo y, en tales casos, el número de elementos en el anillo designa el número de elementos en el anillo en el sistema de anillo (de arilo/heteroarilo) condensado. En los grupos heteroarilo bicíclico en donde un anillo no contiene un heteroátomo (por ejemplo, indolilo, quinolinilo, carbazolilo y similares), el punto de unión puede estar en cualquiera de los anillos, es decir, ya sea el anillo que lleva un heteroátomo (por ejemplo, 2-indolilo) o el anillo que no contiene un heteroátomo (por ejemplo, 5-indolilo).
En algunas realizaciones, un grupo heteroarilo es un sistema de anillo aromático de 5-10 elementos que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema de anillo aromático, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-10 elementos"). En algunas realizaciones, un grupo heteroarilo es un sistema de anillo aromático de 5-8 elementos que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema de anillo aromático, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-8 elementos"). En algunas realizaciones, un grupo heteroarilo es un sistema de anillo aromático de 5-6 elementos que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo proporcionados en el sistema de anillo aromático, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heteroarilo de 5-6 elementos"). En algunas realizaciones, el heteroarilo de 5-6 elementos tiene 1-3 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heteroarilo de 5-6 elementos tiene 1-2 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heteroarilo de 5-6 elementos tiene 1 heteroátomo en el anillo seleccionado de nitrógeno, oxígeno y azufre. A menos que se especifique de otro modo, cada caso de un grupo heteroarilo independientemente está opcionalmente sustituido, es decir, no sustituido (un "heteroarilo no sustituido") o sustituido (un "heteroarilo sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo heteroarilo es heteroarilo de 5-14 elementos no sustituido. En determinadas realizaciones, el grupo heteroarilo es heteroarilo de 5-14 elementos sustituido.
Los grupos heteroarilo de 5 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, pirrolilo, furanilo y tiofenilo. Los grupos heteroarilo de 5 elementos de ejemplo que contienen dos heteroátomos incluyen, sin limitación, imidazolilo, pirazolilo, oxazolilo, isoxazolilo, tiazolilo e isotiazolilo. Los grupos heteroarilo de 5 elementos de ejemplo que contienen tres heteroátomos incluyen, sin limitación, triazolilo, oxadiazolilo y tiadiazolilo. Los grupos heteroarilo de 5 elementos de ejemplo que contienen cuatro heteroátomos incluyen, sin limitación, tetrazolilo. Los grupos heteroarilo de 6 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, piridinilo. Los grupos heteroarilo de 6 elementos de ejemplo que contienen dos heteroátomos incluyen, sin limitación, piridazinilo, pirimidinilo y pirazinilo. Los grupos heteroarilo de 6 elementos de ejemplo que contienen tres o cuatro heteroátomos incluyen, sin limitación, triazinilo y tetrazinilo, respectivamente. Los grupos heteroarilo de 7 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, azepinilo, oxepinilo y tiepinilo. Los grupos heteroarilo 5,6-bicíclico de ejemplo incluyen, sin limitación, indolilo, isoindolilo, indazolilo, benzotriazolilo, benzotiofenilo, isobenzotiofenilo, benzofuranilo, benzoisofuranilo, bencimidazolilo, benzoxazolilo, bencisoxazolilo, benzoxadiazolilo, benzotiazolilo, bencisotiazolilo, benzotiadiazolilo, indolizinilo y purinilo. Los grupos heteroarilo 6,6-bicíclico de ejemplo incluyen, sin limitación, naftiridinilo, pteridinilo, quinolinilo, isoquinolinilo, cinolinilo, quinoxalinilo, ftalazinilo y quinazolinilo.
Tal como se usa en el presente documento, el término "heterocíclico" se refiere a un radical de un sistema de anillo no aromático de 3 a 10 elementos que tiene átomos de carbono en el anillo y de 1 a 4 heteroátomos en el anillo, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno, azufre, boro, fósforo y silicio ("heterocíclico de 3-10 elementos"). En los grupos heterocíclicos que contienen uno o más átomos de nitrógeno, el punto de unión puede ser un átomo de carbono o nitrógeno, según lo permita la valencia. Un grupo heterocíclico puede ser un sistema de anillo monocíclico ("heterocíclico monocíclico") o condensado, puenteado o espiro, tal como un sistema bicíclico ("heterocíclico bicíclico"), y puede estar saturado o puede estar parcialmente insaturado. Los sistemas de anillo bicíclico heterocíclico pueden incluir uno o más heteroátomos en uno o ambos anillos. El término "heterocíclico" también incluye sistemas de anillo en donde el anillo heterocíclico, tal como se ha definido anteriormente, está condensado con uno o más grupos carbocíclicos, en donde el punto de unión está en el anillo carbocíclico o heterocíclico, o sistemas de anillo en donde el anillo heterocíclico, tal como se ha definido anteriormente,
está condensado con uno o más grupos arilo o heteroarilo, en donde el punto de unión está en el anillo heterocíclico y, en tales casos, el número de elementos en el anillo sigue designando el número de elementos en el anillo en el sistema de anillo heterocíclico. A menos que se especifique de otro modo, cada caso de heterocíclico independientemente está opcionalmente sustituido, es decir, no sustituido (un "heterocíclico no sustituido") o sustituido (un "heterocíclico sustituido") con uno o más sustituyentes. En determinadas realizaciones, el grupo heterocíclico es heterocíclico de 3-10 elementos no sustituido. En determinadas realizaciones, el grupo heterocíclico es heterocíclico de 3-10 elementos sustituido.
En algunas realizaciones, un grupo heterocíclico es un sistema de anillo no aromático de 5-10 elementos que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno, azufre, boro, fósforo y silicio ("heterocíclico de 5-10 elementos"). En algunas realizaciones, un grupo heterocíclico es un sistema de anillo no aromático de 5-8 elementos que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heterocíclico de 5-8 elementos"). En algunas realizaciones, un grupo heterocíclico es un sistema de anillo no aromático de 5-6 elementos que tiene átomos de carbono en el anillo y 1-4 heteroátomos en el anillo, en donde cada heteroátomo se selecciona independientemente de nitrógeno, oxígeno y azufre ("heterocíclico de 5-6 elementos"). En algunas realizaciones, el heterocíclico de 5-6 elementos tiene 1-3 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heterocíclico de 5-6 elementos tiene 1-2 heteroátomos en el anillo seleccionados de nitrógeno, oxígeno y azufre. En algunas realizaciones, el heterocíclico de 5-6 elementos tiene un heteroátomo en el anillo seleccionado de nitrógeno, oxígeno y azufre.
Los grupos heterocíclicos de 3 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, azirdinilo, oxiranilo y tiiranilo. Los grupos heterocíclicos de 4 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, azetidinilo, oxetanilo y tietanilo. Los grupos heterocíclicos de 5 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, tetrahidrofuranilo, dihidrofuranilo, tetrahidrotiofenilo, dihidrotiofenilo, pirrolidinilo, dihidropirrolilo y pirrolil-2,5-diona. Los grupos heterocíclicos de 5 elementos de ejemplo que contienen dos heteroátomos incluyen, sin limitación, dioxolanilo, oxasulfuranilo, disulfuranilo y oxazolidin-2-ona. Los grupos heterocíclicos de 5 elementos de ejemplo que contienen tres heteroátomos incluyen, sin limitación, triazolinilo, oxadiazolinilo y tiadiazolinilo. Los grupos heterocíclicos de 6 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, piperidinilo, tetrahidropiranilo, dihidropiridinilo y tianilo. Los grupos heterocíclicos de 6 elementos de ejemplo que contienen dos heteroátomos incluyen, sin limitación, piperazinilo, morfolinilo, ditianilo, dioxanilo. Los grupos heterocíclicos de 6 elementos de ejemplo que contienen dos heteroátomos incluyen, sin limitación, triazinanilo. Los grupos heterocíclicos de 7 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, azepanilo, oxepanilo y tiepanilo. Los grupos heterocíclicos de 8 elementos de ejemplo que contienen un heteroátomo incluyen, sin limitación, azocanilo, oxecanilo y tiocanilo. Los grupos heterocíclicos de 5 elementos de ejemplo condensados con un anillo de arilo C6 (también denominado en el presente documento anillo heterocíclico 5,6-bicíclico) incluyen, sin limitación, indolinilo, isoindolinilo, dihidrobenzofuranilo, dihidrobenzotienilo, benzoxazolinonilo y similares. Los grupos heterocíclicos de 6 elementos de ejemplo condensados con un anillo de arilo (también denominado en el presente documento anillo heterocíclico 6,6-bicíclico) incluyen, sin limitación, tetrahidroquinolinilo, tetrahidroisoquinolinilo y similares.
Tal como se usa en el presente documento, el término "acilo" se refiere a un radical --C(O)Ra, donde Ra es hidrógeno, alquilo sustituido o no sustituido, alquenilo sustituido o no sustituido, alquinilo sustituido o no sustituido, carbocíclico sustituido o no sustituido, heterocíclico sustituido o no sustituido, arilo sustituido o no sustituido o heteroarilo sustituido o no sustituido, tal como se define en el presente documento. Los grupos acilo representativos incluyen, pero sin limitación, formilo (-CHO), acetilo (--C(=O)CH3), ciclohexilcarbonilo, ciclohexilmetilcarbonilo, benzoílo (-C(=O)Ph), bencilcarbonilo (--C(=O)CH2Ph), --C(O)--alquilo C1-C8, --C(O)--(CH2)t(arilo C6-C10), -C(O)-(CH2)t(heteroarilo de 5-10 elementos), -C(O)--(CH2)t(cicloalquilo C3-C10) y -C(O)-(CH2)t(heterocíclico de 4-10 elementos), en donde t es un número entero de 0 a 4.
Tal como se usa en el presente documento, el término "alcoxi" se refiere al grupo -ORb, donde Rb es alquilo sustituido o no sustituido, alquenilo sustituido o no sustituido, alquinilo sustituido o no sustituido, carbocíclico sustituido o no sustituido, heterocíclico sustituido o no sustituido, arilo sustituido o no sustituido o heteroarilo sustituido o no sustituido. Los grupos alcoxi particulares son metoxi, etoxi, n-propoxi, isopropoxi, n-butoxi, terc-butoxi, sec-butoxi, n-pentoxi, nhexoxi y 1,2-dimetilbutoxi. Los grupos alcoxi particulares son alcoxi inferior, es decir, con entre 1 y 6 átomos de carbono. Los grupos alcoxi particulares adicionales tienen entre 1 y 4 átomos de carbono.
Tal como se usa en el presente documento, el término "halo" o "halógeno" se refiere a fluoro (F), cloro (CI), bromo (Br) y yodo (I).
Los grupos alquilo, heterocíclico, arilo y heteroarilo, tal como se definen en el presente documento, están opcionalmente sustituidos (por ejemplo, grupo alquilo "sustituido" o "no sustituido", heterocíclico "sustituido" o "no sustituido", arilo "sustituido" o "no sustituido" o heteroarilo "sustituido" o "no sustituido"). En general, el término "sustituido", ya esté precedido o no por el término "opcionalmente", significa que al menos un hidrógeno presente en un grupo (por ejemplo, un átomo de carbono o nitrógeno) se reemplaza con un sustituyente admisible, por ejemplo,
un sustituyente que, tras la sustitución, da como resultado un compuesto estable, por ejemplo, un compuesto que no experimenta espontáneamente una transformación, tal como mediante reorganización, ciclación, eliminación u otra reacción. A menos que se indique de otro modo, un grupo "sustituido" tiene un sustituyente en una o más posiciones sustituibles del grupo y, cuando está sustituida más de una posición en cualquier estructura dada, el sustituyente es el mismo o diferente en cada posición. Se contempla que el término "sustituido" incluya la sustitución con todos los sustituyentes admisibles de compuestos orgánicos, cualquiera de los sustituyentes descritos en el presente documento que dé como resultado la formación de un compuesto estable. La presente invención contempla cualquiera y la totalidad de tales combinaciones con el fin de llegar a un compuesto estable. Para los fines de la presente invención, los heteroátomos, tales como nitrógeno, pueden tener sustituyentes de hidrógeno y/o cualquier sustituyente adecuado, tal como se describe en el presente documento, que satisfaga las valencias de los heteroátomos y dé como resultado la formación de un resto estable.
Aquellos expertos en la materia conocen bien los sustituyentes opcionales de los grupos alquilo, alquenilo, arilo, heteroarilo o heterociclo. Estos sustituyentes incluyen alquilo, alcoxi, ariloxi, hidroxi, acetilo, ciano, nitro, glicerilo y carbohidrato o dos sustituyentes tomados en conjunto se pueden unir como grupo -alquileno para formar un anillo.
Tal como se usa en el presente documento, el término "grupo saliente" o "GS" significa el grupo con el significado asociado convencionalmente al mismo en la química orgánica sintética, es decir, un átomo o grupo desplazable en condiciones de reacción de sustitución. Los ejemplos de grupos salientes incluyen, pero sin limitación, halógeno, alcano o arilenosulfoniloxi, tal como metanosulfoniloxi, etanosulfoniloxi, tiometilo, bencenosulfoniloxi, tosiloxi, mesilato, y tieniloxi, dihalofosfinoiloxi, benciloxi opcionalmente sustituido, isopropiloxi, aciloxi y similares.
Realizaciones preferidas del proceso de la invención
La presente invención proporciona procesos para la preparación de compuestos de arilpiperazina y arilpiperidina, incluyendo los productos intermedios y derivados de los mismos. De manera más específica, la presente invención proporciona procesos o métodos para la preparación de una diversidad de compuestos de arilpiperazina alquilada y arilpiperidina alquilada de Fórmulas (I) y (VII) generales, respectivamente.
en donde R1 y R2 se seleccionan individualmente de hidrógeno, alquilo no sustituido y alquilo sustituido o R1 y R2 se conectan para formar un anillo cíclico de 5 a 8 carbonos; n es 0, 1 o 2; Y es NR3R4, OR5 o SR5, donde R3 y R4 se seleccionan individualmente de acilo o sulfonilo, en donde R3 y R4 se pueden conectar para formar un anillo cíclico o bicíclico sustituido o no sustituido y en donde R5 es arilo o heteroarilo, o heterocíclico; y Ar es un grupo arilo o heteroarilo.
Los compuestos de arilpiperazina de Fórmula (I) incluyen, por ejemplo, lurasidona, tiospirona, revospirona, perospirona, brexipirazol, aripiprazol, buspirona, gepirona, ipsapirona, eptapirona, umespirona, tandospirona y zalospirona.
Los compuestos de arilpiperidina de Fórmula (VII) incluyen, por ejemplo, iloperidona y abaperidona.
Los procesos para la preparación de los compuestos de arilpiperazina alquilada y arilpiperidina alquilada desvelados en el presente documento tienen determinadas características y etapas de proceso comunes. Por ejemplo, tal como se muestran, los procesos para la preparación de los compuestos de arilpiperazina alquilada y arilpiperidina alquilada comprenden la etapa de alquilación del compuesto YH con un sulfato cíclico de Fórmula (II) en presencia de una base para formar un compuesto de Fórmula (III), en donde Q es hidrógeno, un metal o una sal de amonio.
En las realizaciones preferidas, R1 y R2 en las Fórmulas (II) y (III) se conectan para formar un anillo cíclico de 5 a 8 carbonos. Preferentemente, R1 y R2 se conectan para formar un anillo cíclico de 5 o 6 carbonos y, lo más
preferentemente, un anillo alifático cíclico de 6 carbonos.
En las realizaciones preferidas, el compuesto YH es una imida cíclica o amida cíclica, de tal manera que Y es NR3R4, donde R3 y/o R4 son acilo y en donde R3 y R4 se conectan para formar un anillo cíclico o bicíclico. Los compuestos preferidos que cumplen con los requisitos de YH incluyen, por ejemplo:
Tabla 1: compuestos representativos de Fórmula YH
(continuación)
En una realización preferida de la presente invención, YH es:
En la reacción entre el compuesto YH y el sulfato cíclico de Fórmula (II) en la presente invención, el compuesto YH está presente, preferentemente, en la mezcla de reacción en una cantidad de aproximadamente 1,0 a 2,0 equivalentes y, más preferentemente, de aproximadamente 1,1 a 1,2 equivalentes basándose en la cantidad del sulfato cíclico de Fórmula (II).
La reacción de alquilación de acuerdo con la presente invención se lleva a cabo preferentemente en un disolvente adecuado a una temperatura de aproximadamente 20 °C a aproximadamente 120 °C en presencia de una base. Los disolventes adecuados en esta etapa incluyen, pero sin limitación, hidrocarburos, hidrocarburos halogenados, hidrocarburos aromáticos, ésteres, éteres, nitrilos, cetonas y mezclas de los mismos. En las realizaciones preferidas, el disolvente es acetonitrilo.
Las bases adecuadas en esta etapa incluyen carbonatos de metales alcalinos, tales como carbonato de potasio, carbonato de sodio, carbonato de calcio y carbonato de magnesio; bicarbonatos de metales alcalinos, tales como bicarbonato de sodio y bicarbonato de potasio; preferentemente, un carbonato de metal alcalino, en particular, carbonato de potasio; hidróxidos de metales alcalinos, tales como hidróxido de sodio, hidróxido de potasio, hidróxido de magnesio o hidróxido de calcio; fosfatos de metales alcalinos, tales como fosfato de sodio o fosfato de potasio; y bases de amina orgánica, tales como trietilamina, diisopropiletilamina y piridina. También son adecuadas las sales de amonio de las bases anteriores. Las bases inorgánicas sólidas se pueden usar de manera individual o en forma de una mezcla de dos o más tipos de bases y pueden ser una forma anhidra o un hidrato de la misma. En las realizaciones preferidas, la base empleada en esta etapa es carbonato de potasio, K2CO3.
La cantidad de la base usada en el presente documento es generalmente de aproximadamente 0,7 mol o más, preferentemente 1,0 mol o más, por mol de la cantidad total de compuesto YH. La cantidad límite superior de la base inorgánica sólida usada en el presente documento no está limitada, pero una cantidad en exceso de base puede aumentar los costes del proceso. Por consiguiente, una cantidad práctica de la base inorgánica sólida es de 10 mol o
menos, preferentemente 2,0 mol o menos, por mol de la cantidad total de compuesto YH.
La evolución de la reacción de alquilación en la presente invención se puede controlar mediante cualquier medio conocido por aquellos expertos en la materia, tal como, por ejemplo, cromatografía de gases (GC en inglés) o cromatografía líquida de alto rendimiento (HPLC en inglés).
El compuesto de Fórmula (III) se puede aislar mediante cualquier método conocido por aquellos expertos en la materia. Sin embargo, en las realizaciones preferidas, el compuesto de Fórmula (III) no se aísla de la mezcla de reacción en la que este se formó, sino que, más bien, se amplía. En este sentido, el compuesto de Fórmula (III) se puede preparar para una etapa de hidrólisis mediante la adición de agua, que genera una fase limpia dividida con, por ejemplo, acetonitrilo debido a la base solubilizada, tal como, por ejemplo, carbonato de potasio, sin una pérdida de producto significativa. A continuación, la capa de disolvente orgánico se lava preferentemente con NaCl acuoso en un proceso de extracción convencional para retirar cualquier carbonato residual antes de una reacción de hidrólisis.
Un beneficio inesperado del empleo de un sulfato cíclico de Fórmula (II) en el proceso de la presente invención es que este conduce a la monoalquilación selectiva ventajosa del sulfato cíclico sin la posibilidad de una alquilación doble. El sulfato de anillo abierto aniónico (después de la alquilación inicial) no es propenso a un desplazamiento adicional por parte de los nucleófilos. Por tanto, después de la conversión del alcohol en un grupo saliente adecuado, se emplea una química de desplazamiento sencilla para proporcionar el producto final. En otras palabras, el proceso de la presente invención produce compuestos de arilpiperazina alquilada y arilpiperidina alquilada en donde no se detecta ningún producto de bis-imida en la alquilación del sulfato cíclico.
El proceso para la preparación de los compuestos derivados de arilpiperazina y arilpiperidina alquilada de acuerdo con la presente invención también comprende la etapa de hidrolización de un compuesto de Fórmula (III) para formar un alcohol de Fórmula (IV), tal como se muestra en el presente documento.
En esta etapa de reacción, se añade ácido acuoso a una capa de disolvente orgánico lavada que contiene el compuesto de Fórmula (III) y la mezcla se agita a una temperatura de aproximadamente 20 °C a aproximadamente 100 °C. Durante esta etapa, el resto de éster de sulfato del compuesto de Fórmula (III) se hidroliza a un grupo alcohol (-OH). En algunas realizaciones, un disolvente adicional, tal como, por ejemplo, tolueno, se puede añadir a la mezcla antes del ácido acuoso.
La evolución de la reacción de hidrólisis en la presente invención se puede controlar mediante cualquier medio conocido por aquellos expertos en la materia, tal como, por ejemplo, cromatografía líquida de alto rendimiento (HPLC).
Preferentemente, una vez que se completa la reacción, la fase orgánica se enfría y la fase orgánica se prepara para otra etapa en el proceso de la presente invención. Esta preparación implica, típicamente, lavar varias veces con agua empleando un proceso de extracción convencional. La fase orgánica también se puede destilar al vacío, seguido de la adición del disolvente deseado para la siguiente etapa del proceso. Un ejemplo de tal disolvente es el tolueno.
El proceso de la presente invención para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada también comprende una etapa de conversión del compuesto de Fórmula (IV) en un agente alquilante de Fórmula (V), en donde GS es un grupo saliente.
En el compuesto de Fórmula (V), preferentemente, el GS se selecciona del grupo que consiste en un sulfonato de arilo, sulfonato de alquilo, fosfato, fosfonato, proazafosfatrano y un halógeno. En las realizaciones preferidas, el GS es un mesilato.
La conversión del grupo hidroxilo en uno de los grupos salientes citados se puede efectuar mediante cualquier medio conocido por un experto en la materia. En las realizaciones preferidas donde el GS es un mesilato, por ejemplo, se halló que la conversión se puede producir rápida y eficazmente en una mezcla de tolueno y una base, tal como, por ejemplo, trietilamina. En esta realización, se añaden a la mezcla aproximadamente 1,2 equivalentes de cloruro de metanosulfonilo respecto al alcohol para iniciar la reacción. Otros disolventes adecuados en esta etapa incluyen, por ejemplo, hidrocarburos, hidrocarburos halogenados, hidrocarburos aromáticos, ésteres, éteres, nitrilos, cetonas y mezclas de los mismos.
La evolución de la reacción de conversión en la presente invención se puede controlar mediante cualquier medio conocido por aquellos expertos en la materia, tal como, por ejemplo, HPLC. Tal reacción requiere, típicamente, de aproximadamente 0,5 horas a aproximadamente 12 horas para completarse, dependiendo de variables, tales como, por ejemplo, la temperatura, los equivalentes de agente activador y la concentración de los reactivos. Por ejemplo, cuanto menos disolvente se emplee, más rápido es probable que avance la reacción.
Una vez que se completa la reacción, la mezcla se lava, preferentemente, con agua. A continuación, la capa acuosa se puede separar y retirar después del lavado. La preparación de la fase orgánica para la siguiente etapa en el proceso de la presente invención se puede realizar mediante destilación al vacío hasta que se alcance el volumen deseado.
El proceso de preparación de compuestos de arilpiperazina alquilada de acuerdo con la presente invención comprende una etapa de alquilación de un compuesto de piperazina de Fórmula (VI) con un agente alquilante de Fórmula (V) para proporcionar la arilpiperazina alquilada de Fórmula (I).
En la reacción entre los compuestos de Fórmula (V) y (VI) en la presente invención, el compuesto de Fórmula (VI) está presente, preferentemente, en la mezcla de reacción en una cantidad de 1,0 a 10,0 equivalentes y, más preferentemente, de 1,1 a 1,2 equivalentes basándose en la cantidad del compuesto de Fórmula (V). En la reacción, también están presentes aproximadamente 1,5 equivalentes de una base. Las bases adecuadas en esta etapa incluyen carbonatos de metales alcalinos, tales como carbonato de potasio, carbonato de sodio, carbonato de calcio y carbonato de magnesio; bicarbonatos de metales alcalinos, tales como bicarbonato de sodio y bicarbonato de potasio; preferentemente, un carbonato de metal alcalino, en particular, carbonato de potasio; hidróxidos de metales alcalinos, tales como hidróxido de sodio, hidróxido de potasio, hidróxido de magnesio o hidróxido de calcio; fosfatos de metales alcalinos, tales como fosfato de sodio o fosfato de potasio; y bases de amina orgánica, tales como trietilamina, diisopropiletilamina y piridina. También son adecuadas las sales de amonio de las bases anteriores. Las bases inorgánicas sólidas se pueden usar de manera individual o en forma de una mezcla de dos o más tipos de bases y pueden ser una forma anhidra o un hidrato de la misma. En las realizaciones preferidas, la base empleada en esta etapa es carbonato de potasio, K2CO3. La cantidad de la base usada en el presente documento es generalmente de aproximadamente 0,7 mol o más, preferentemente 1,0 mol o más, por mol de la cantidad total de compuesto de Fórmula (VI). La cantidad límite superior de la base inorgánica sólida usada en el presente documento no está limitada, pero, en caso de que la cantidad sea demasiado grande, el coste del proceso aumenta. Por consiguiente, una cantidad práctica de la base es de 3 mol o menos, preferentemente 2,0 mol o menos, por mol de la cantidad total de compuesto de Fórmula (VI).
La evolución de la reacción se puede controlar mediante cualquier medio conocido por aquellos expertos en la materia, tal como, por ejemplo, HPLC.
Una vez completa, la mezcla de reacción, preferentemente, se enfría, seguido de la adición de disolvente. La capa acuosa se retira, seguido de lavados adicionales de la fase orgánica con agua. Una vez que se separa la capa acuosa, la capa orgánica, preferentemente, se destila al vacío y se añade un antidisolvente. Los antidisolventes adecuados en esta etapa incluyen, pero sin limitación, hidrocarburos, hidrocarburos halogenados, hidrocarburos aromáticos, ésteres, éteres, nitrilos, cetonas y mezclas de los mismos. A fin de efectuar la cristalización de la arilpiperazina de Fórmula (I), la mezcla, preferentemente, se calienta y enfría sucesivamente en la mezcla de disolvente y antidisolvente.
El proceso de preparación de compuestos de arilpiperidina alquilada de acuerdo con la presente invención comprende una etapa de alquilación de un compuesto de arilpiperidina de Fórmula (VIII) con un agente alquilante de Fórmula (V) para proporcionar la arilpiperidina alquilada de Fórmula (VII).
Las condiciones de reacción y separación del producto son aproximadamente las mismas que aquellas descritas anteriormente con respecto a los compuestos de arilpiperazina alquilada.
Tal como entenderán aquellos expertos habituales en la materia, se pueden emplear los procesos descritos anteriormente y en el presente documento para producir una diversidad de compuestos. Por ejemplo, tal como se muestra a continuación en la Tabla 2, se pueden preparar los siguientes compuestos mediante el proceso descrito en el presente documento para la preparación de los compuestos de arilpiperazina alquilada de Fórmula (I).
De manera similar, tal como se muestra a continuación en la Tabla 3, se pueden preparar los siguientes compuestos mediante el proceso descrito en el presente documento para la preparación de los compuestos de arilpiperidina alquilada de Fórmula (VII).
En el proceso de preparación de los compuestos de arilpiperazina alquilada y arilpiperidina alquilada desvelados en el presente documento, se producen numerosos compuestos intermedios.
Los siguientes Ejemplos ilustran diversos aspectos de la presente invención.
Ejemplos
Ejemplo 1: preparación ampliada de 3,3-dióxido de (5aR,9aR)-octahidrobenzo[e][1,3,2]dioxatiepina
Se añade [(1R,2R)-ciclohexano-1,2-diil]dimetanol (peso molecular de 144,21) a acetonitrilo proporcionando una mezcla de reacción en forma de una suspensión. La mezcla se agita y enfría hasta 0-5 °C. Se añade cloruro de tionilo a la mezcla a una temperatura de 0-10 °C que da como resultado una solución transparente. La solución se agita a 0 5 °C y se analiza periódicamente para confirmar la finalización de la reacción.
En un recipiente separado, se añade una solución acuosa de bicarbonato de potasio (2,5 equiv.) preparada y, a continuación, se enfría hasta 0-5 °C. La solución de reacción completada anterior se interrumpe, a continuación, en la solución acuosa de bicarbonato de potasio. A continuación, el lote se calienta hasta 20-25 °C y la capa superior de acetonitrilo se separa y se recoge. La capa acuosa se extrae con acetonitrilo y las capas orgánicas se combinan dando como resultado una solución de 3-óxido de (5aR,9aR)-octahidrobenzo[e][1,13,2]dioxatiepina (peso molecular de 190,26).
En un recipiente separado, se suspenden hidrato de óxido de rutenio al 50 % (0,1 % en peso) y peryodato de sodio (1,1 equiv.) en agua y EtOAc a 20-25 °C. La solución de 3-óxido de (5aR,9aR)-octahidrobenzo[e][1,3,2]dioxatiepina anterior se añade, a continuación, a la suspensión de peryodato de sodio/óxido de rutenio, al tiempo que se mantiene la temperatura a <30 °C. Después de completarse la reacción, a continuación, se filtra el lote, tras lo que se lava la torta de filtro con EtOAc. La capa orgánica superior se recoge y se lava con cloruro de sodio acuoso al 20 %. La capa orgánica se destila hasta un volumen mínimo, tras lo que se añade isopropanol al destilado. La suspensión resultante se calienta hasta 40-45 °C, tras lo que esta se enfría hasta 0-5 °C y, a continuación, se filtra. Los sólidos se lavan con isopropanol y se secan en un horno de vacío dando como resultado 3,3-dióxido de (5aR,9aR)-octahidrobenzo[e][1,3,2]dioxatiepina (peso molecular de 206,26).
Ejemplo 2: preparación ampliada de base libre de lurasidona
Se añade acetonitrilo a una mezcla de 3,3-dióxido de (5aR,9aR)-octahidrobenzo[e][1,3,2]dioxatiepina (peso molecular de 206,26, 1 equiv.), (3aR,4s,7R,7aS-hexahidro-1H-7,4-metanoisoindol-1,3(2H)-diona (peso molecular de 165,19, 1,2 equiv.) y carbonato de potasio (2 equiv.) y la mezcla se calienta hasta aproximadamente 75 °C.
Una vez que se completa la reacción, la mezcla se enfría hasta 20-25 °C y se añade agua a la mezcla. A continuación, se retira una fase acuosa inferior y se lava una fase orgánica superior con cloruro de sodio acuoso.
Las fases acuosas se combinan y extraen con acetonitrilo. Las fases orgánicas se combinan para formar una solución de ((1R,2R)-2(((3aR,4S,7R,7aS)-1,3-dioxooctahidro-2H-4,7-metanoisoindol-2-il)metil)ciclohexil)metil sulfato de potasio (peso molecular de 409,54) en acetonitrilo, que se destila a continuación hasta aproximadamente 5 volúmenes. Se añade tolueno al lote y, por separado, se prepara una solución de ácido sulfúrico (0,5 equiv.) y agua (0,6 volúmenes). La solución de ácido sulfúrico se añade al lote. A continuación, esta mezcla se calienta hasta aproximadamente 75 °C y la reacción se controla mediante HPLC.
Una vez que se completa la reacción, esta se enfría hasta aproximadamente 45 °C y se lava dos veces con agua (4 volúmenes). A continuación, la capa acuosa se retira y la capa orgánica se lava con KHCO3 acuoso al 5 % (4 volúmenes), seguido de dos lavados con agua adicionales (4 volúmenes). La solución orgánica que comprende (3aR,4S,7R,7aS)-2-(((1R,2R)-2-(hidroximetil)ciclohexil)metil)hexahidro-1H-4,7-metanoisoindol-1,3(2H)-diona (peso molecular de 291,39) se destila al vacío hasta aproximadamente 4 volúmenes y se añade tolueno al lote. Esta solución se destila hasta aproximadamente 4 volúmenes y se añade tolueno. Este lote se enfría hasta aproximadamente 0 5 °C y se añade trietilamina (1,5 equiv.), tras lo que se añade cloruro de metanosulfonilo (1,2 equiv.). La evolución de esta reacción se controla mediante HPLC.
Una vez que se completa la reacción, se añade agua (3 volúmenes). Se retira la capa acuosa y se lava la capa orgánica con agua (2 x 3 volúmenes).
La solución en tolueno de metanosulfonato de ((1R,2R)-2-(((3aR,4S,7R,7aS)-1,3-dioxooctahidro-2H-4,7-metanoisoindol-2-il)metil)ciclohexil)metilo se destila hasta aproximadamente 4 volúmenes al vacío y esta solución se añade a una mezcla de 3-(piperazin-1-il)benzo[d]isotiazol (1,1 equiv.) y KHCO3 (1,5 equiv.). Se añade agua (1,8 volúmenes) y la mezcla se calienta hasta aproximadamente 90 °C. La evolución de la reacción se controla mediante HPLC.
Una vez que se completa la reacción, el lote se enfría hasta 45 ± 5 °C y se añaden tolueno (4,5 volúmenes), agua (3,25 volúmenes) e IPA (1,75 volúmenes). Se retira la capa acuosa y se lava la capa orgánica con agua (2 x 2,5 volúmenes) a 40 ± 5 °C. La capa orgánica se destila a presión reducida hasta 3,5 volúmenes a 50-60 °C y, a continuación, se añade isopropanol (8 volúmenes). El lote se destila hasta 3,5 volúmenes y, a continuación, se añade IPA (2,5 volúmenes). La suspensión se calienta hasta 80 ± 5 °C durante 1-2 horas, a continuación se enfría hasta 0 5 °C y se filtra. Los sólidos se lavan con IPA y se secan para aislar la (3aR,4S,7R,7aS)-2-(((1R,2R)-2-((4-(benzo[d]isotiazol-3-il)piperazin-1-il)metilciclohexil)metil)hexahidro-1H-4,7-metanoisoindol-1,3(2H)-diona (base libre de lurasidona, peso molecular de 492,68).
Ejemplo 3: cristalización de base libre de lurasidona
La base libre de lurasidona en bruto del Ejemplo 2 se suspende en acetato de etilo (10 volúmenes) y se calienta hasta que se obtiene una solución transparente. La solución se enfría hasta 50-55 °C y se filtra para retirar cualquier material en forma de partículas en la solución. La solución se destila adicionalmente hasta aproximadamente 4-5 volúmenes y, a continuación, se enfría hasta aproximadamente 0-5 °C. El precipitado sólido resultante se filtra, se enjuaga con acetato de etilo y, a continuación, se seca al vacío para proporcionar una base libre de lurasidona cristalina.
Ejemplo 4: preparación de clorhidrato de lurasidona
La base libre de lurasidona del Ejemplo 3 se suspende en isopropanol (1 equiv. de base hasta 15 volúmenes de isopropanol). A continuación, la suspensión se calienta hasta que se obtiene una solución transparente. La solución se filtra para retirar cualquier material en forma de partículas en la solución. A continuación, se añade una solución filtrada previamente de HCl acuoso al 10 % y el lote se enfría lentamente hasta aproximadamente 45-70 °C hasta que los cristales comienzan a precipitar. El lote se mantiene en este punto durante varias horas y, a continuación, se enfría adicionalmente hasta aproximadamente 0 °C. El precipitado sólido resultante se filtra y, a continuación, se lava con isopropanol (3 x 2 volúmenes). El precipitado se seca para proporcionar clorhidrato de lurasidona.
Ejemplo 5: preparación ampliada de metanosulfonato de (3-(5-acetil-2-metoxifenoxi)propilo hacia iloperidona
Una mezcla de 2,2-dióxido de 1,3,2-dioxatiano (22,4 g, 160 mmol, 1 equiv.), 1-(3-hidroxi-4-metoxifenil)etan-1-ona (26,9 g, 160 mmol, 1 equiv.) y carbonato de potasio (44,8 g, 320 mmol, 2 equiv.) en acetonitrilo (220 ml) se calienta a aproximadamente temperatura de reflujo. La reacción se controla mediante HPLC. Tras completarse, el lote se enfría hasta aproximadamente 20-25 °C. La mezcla de reacción se filtra a través de una almohadilla de Celite y la almohadilla se lava con acetonitrilo (180 ml) para dar una solución de 3-(5-acetil-2-metoxifenoxi)propil sulfato de potasio en acetonitrilo, que se usa en la siguiente etapa.
Una solución de H2SO4 (10 ml de H2SO4 en 90 ml de agua) se añade lentamente a la solución de acetonitrilo anterior. A continuación, el lote se calienta hasta aproximadamente reflujo; la reacción se controla mediante HPLC. Tras completarse, la mezcla de reacción se enfría hasta aproximadamente 20-25 °C y las fases resultantes se separan. La fase orgánica se lava con salmuera (2 x 100 ml) y se divide en 2 partes (80 ml y 320 ml).
La parte de 80 ml de la reacción anterior se trata para proporcionar un marcador de referencia de 1-(3-(3-hidroxipropoxi)-4-metoxifenil)etan-1-ona de la siguiente manera. El disolvente se retira a presión reducida para dar el producto en bruto, que se purifica mediante cromatografía en columna sobre gel de sílice (10 x gel de sílice con respecto al producto en bruto, éter de petróleo:acetato de etilo [2:1] respecto a éter de petróleo:acetato de etilo [1:1]), para dar 1-(3-(3-hidroxipropoxi)-4-metoxifenil)etan-1-ona del 99 % de pureza (2,3 g, sólido de color blanco).
Una gran parte de la solución en acetonitrilo de 3-(5-acetil-2-metoxifenoxi)propil sulfato de potasio (320 ml) evoluciona de la siguiente manera. Se retira aproximadamente el 80 % del disolvente y, a continuación, se añade acetato de etilo (200 ml). Aproximadamente el 80 % del disolvente se retira de nuevo para dar una solución concentrada de 1-(3-(3-hidroxipropoxi)-4-metoxifenil)etan-1-ona en acetato de etilo para la siguiente etapa.
Se añaden trietilamina (75 g) y acetato de etilo (200 ml) a la solución anterior y, a continuación, se añade gota a gota una solución de Ms2O (40 g) en acetato de etilo (200 ml) a menos de 15 °C. La mezcla se agita a aproximadamente 10 °C durante una noche. La reacción se controla mediante HPLC. Se añade hidróxido de sodio acuoso (15 %, 250 ml) cuando se completa la reacción y la mezcla se agita a aproximadamente 20-25 °C durante 15 min. La capa orgánica separada se lava, a continuación, con HCl 2 M (200 ml) y salmuera (200 ml). El disolvente se retira a presión reducida para dar el producto en bruto metanosulfonato de (3-(5-acetil-2-metoxifenoxi)propilo en forma de un sólido de color blanquecino (15 g, 90 % de AUC mediante HPLC).
Ejemplo 6: preparación de base libre de iloperidona
Una mezcla de metanosulfonato de 3-(5-acetil-2-metoxifenoxi)propilo (3 g, 10 mmol, 1 equiv.), 6-fluoro-3-(piperidin-4-il)benzo[d]isoxazol (2,42 g, 11 mmol, 1,1 equiv.), KHCO3 (1,5 g, 15 mmol, 1,5 equiv.), H2O (6 g) y tolueno (15 ml) se
calienta a temperatura de reflujo durante 12-16 h. Una vez que se completa la reacción, el lote se enfría hasta aproximadamente 20-25 °C y, a continuación, se añaden tolueno (15 ml), IPA (10 ml) y agua (10 ml). La solución bifásica se agita durante aproximadamente 15 min a aproximadamente 20-25 °C. La capa orgánica se separa y se lava con agua (2 x 10 ml). El lote se concentra a aproximadamente 3-4 volúmenes al vacío a <50 °C para precipitar un sólido de color blanquecino. Se añade isopropanol (20 ml), el lote se concentra hasta 3-4 volúmenes al vacío a < 50 °C. Se añade isopropanol (20 ml) de nuevo y el lote se concentra hasta 3-4 volúmenes al vacío a < 50 °C. Se añade isopropanol (10 ml) una vez de nuevo y el lote se calienta a temperatura de reflujo durante 1 h y, a continuación, la mezcla se enfría hasta 5-8 °C durante 4 h. La mezcla se filtra; la torta se lava con isopropanol (2 x 5 ml) y se seca para dar una base libre de iloperidona (3,1 g, 74 % de rendimiento, 98 % de AUC mediante HPLC).
Ejemplo 7: preparación de 4-(1,1-dióxido-3-oxobenzo[d]isotiazol-2(3ft)-il)butil sulfato de potasio hacia ipsapirona
Una mezcla de 1, 1 -dióxido de benzo[d]isotiazol-3(2H)-ona (16,0 g, 87,3 mmol, 1,0 equiv.), 2,2-dióxido de 1,3,2-dioxatiepano (15,3 g, 100,5 mmol, 1,2 equiv.), K2CO3 (24,1 g, 174,6 mmol, 2,0 equiv.) y Ac N (240 ml) se calienta a temperatura de reflujo durante 20 h. Después de completarse la reacción, la mezcla se filtra y se concentra al vacío para dar un producto oleoso. Al residuo se le añade a Cn (200 ml) y se precipita inmediatamente un sólido. La mezcla se agita durante 1 h a 20-25 °C y, a continuación, se filtra. Se recoge 4-(1,1-dióxido-3-oxobenzo[d]isotiazol-2(3H)-il)butil sulfato de potasio en forma de un sólido de color blanco (11,4 g, 35 % de rendimiento, 98,5 % de AUC mediante HPLC); CL-EM, M+: 335,6 (ácido sulfónico).
Ejemplo 8: preparación de 1,1-dióxido de 2-(4-hidroxibutil)benzo[d]isotiazol-3(2H)-ona hacia ipsapirona
Una solución de H2SO4 (0,8 g, 8,2 mmol, 0,5 equiv.) en H2O (2 ml) se añade a una mezcla de 4-( 1, 1 -dióxido-3-oxobenzo[d]isotiazol-2(3H)-il)butil sulfato de potasio (6,1 g, 16,3 mmol, 1,0 equiv.) en ACN (90 ml) y H2O (5 ml) gota a gota. La mezcla resultante se calienta a 75-80 °C hasta que la reacción se considera completa mediante análisis de HPLC. La mezcla se filtra y el filtrado se concentra hasta aproximadamente 10 ml. Al residuo se le añaden diclorometano y agua desionizada. Las capas se separan y la capa orgánica se lava con una solución saturada de NaHCO3, se seca sobre sulfato de sodio y, a continuación, se concentra para dar el producto en bruto del 94 % de pureza mediante HPLC. El material en bruto se purifica adicionalmente mediante cromatografía en columna sobre gel de sílice (4:1 a 3:1 de éter de petróleo:acetato de etilo) para proporcionar 1,1-dióxido de 2-(4-hidroxibutil)benzo[d]isotiazol-3(2H)-ona en forma de un aceite de color amarillo claro (2,3 g, 55 % de rendimiento, 99 % de AUC mediante HPLC); CL-EM, M+: 255,8.
Ejemplo 9: preparación de metanosulfonato de 4-(1,1-dióxido-3-oxobenzo|d]isotiazol-2(3H)-il)butilo hacia ipsapirona
A una mezcla de 1,1-dióxido de 2-(4-hidroxibutil)benzo[d]isotiazol-3(2H)-ona (17,2 g, 67,4 mmol, 1,0 equiv.) en acetato de etilo (172 ml, 10 volúmenes) se le añade trietilamina (13,6 g, 134,7 mmol, 2,0 equiv.) a < 5 °C, seguido de la adición gota a gota de Ms2O (12,9 g, 74,1 mmol, 1,1 equiv.) en acetato de etilo (20 ml) a 5-15 °C. La mezcla se agita a 20 25 °C durante 20 h y la reacción se considera completa mediante HPLC. La mezcla se lava con H2O dos veces y, a continuación, se seca sobre Na2SO4. El disolvente se retira a presión reducida para obtener el material en bruto. El producto en bruto se purifica mediante cromatografía en columna sobre gel de sílice (30 x gel de sílice, éter de petróleo:acetato de etilo [10:1] respecto a éter de petróleo:acetato de etilo [4:1]) que da metanosulfonato de 4-(1,1-dióxido-3-oxobenzo[d]isotiazol-2(3H)-il)butilo en forma de un sólido de color blanco (8,5 g, 38 % de rendimiento, 96 % de AUC mediante HPLC); CL-EM, M+: 355,6.
Ejemplo 10: preparación de base libre de ipsapirona
Una suspensión de metanosulfonato de (1,1-dióxido-3-oxobenzo[d]isotiazol-2(3H)-il)butilo (4,6 g, 13,8 mmol, 1,0 equiv.), 2-(piperazin-1-il)pirimidina (2,9 g, 17,9 mmol, 1,3 equiv.), KHCO3 (2,1 g, 20,7 mmol, 1,5 equiv.) y tolueno (46 ml) se calienta a 95-100 °C durante 22 h. Se añade agua desionizada (35 ml) y la fase orgánica se separa. La fase acuosa se extrae con acetato de etilo (2x30 ml). Las fases orgánicas se combinan y secan sobre Na2SO4. El disolvente se retira a presión reducida para dar el producto en bruto, que se purifica mediante cromatografía en columna sobre gel de sílice mediante elución con EtOAc al 17-33 %/éter de petróleo para ofrecer una base libre de ipsapirona en forma de un sólido de color blanquecino (2 g, 27 % de rendimiento, 96 % de AUC mediante HPLC).
Los ejemplos anteriores y la descripción de las realizaciones preferidas se deben considerar como ilustrativos, en lugar de limitantes, de la presente invención, tal como se define en las reivindicaciones. Tal como se apreciará fácilmente, se pueden utilizar numerosas variaciones y combinaciones de lo expuesto anteriormente sin apartarse de la presente invención, tal como se expone en las reivindicaciones.
Claims (14)
1. Un proceso para la preparación de un compuesto de arilpiperazina alquilada de Fórmula (I):
en donde,
R1 y R2 se seleccionan individualmente de hidrógeno, alquilo no sustituido y alquilo sustituido o R1 y R2 se conectan para formar un anillo cíclico de 5 a 8 carbonos;
n es 0, 1 o 2;
Y es NR3R4, OR5 o SR5, donde R3 y R4 se seleccionan individualmente de acilo o sulfonilo, en donde R3 y R4 se pueden conectar para formar un anillo cíclico o bicíclico sustituido o no sustituido y en donde R5 es arilo o heteroarilo, o heterocíclico; y
Ar es un grupo arilo o heteroarilo;
comprendiendo dicho proceso las etapas de:
(i) alquilar YH con un sulfato cíclico de Fórmula (II) en presencia de una base para formar un compuesto de Fórmula (III), en donde Q es hidrógeno, un metal o una sal de amonio;
(ii) hidrolizaerl compuesto de Fórmula (III) para formar un alcohol de Fórmula (IV);
(iii) convertir el compuesto de Fórmula (IV) para formar un agente alquilante de Fórmula (V) en donde GS es un grupo saliente; y
(iv) alquilar un compuesto de piperazina de Fórmula (VI) con el agente alquilante de Fórmula (V) para proporcionar la arilpiperazina alquilada de Fórmula (I)
2. El proceso de la reivindicación 1, en donde Ri y R2 forman parte individualmente de un anillo cíclico C5, C6 o C7.
3. El proceso de la reivindicación 1, en donde R3 y R4 forman parte individualmente de un anillo cíclico C5, C6 o C7.
4. El proceso de la reivindicación 1, en donde el grupo saliente GS se selecciona del grupo que consiste en un sulfonato de arilo, sulfonato de alquilo, fosfato, fosfonato, proazafosfatrano y un halógeno.
5. El proceso de la reivindicación 1, en donde el compuesto de Fórmula (I) se selecciona del grupo que consiste en lurasidona, tiospirona, revospirona, perospirona, brexipirazol, aripiprazol, lauroxil de aripiprazol, buspirona, gepirona, ipsapirona, eptapirona, umespirona, tandospirona, zalospirona, pelanserina, fananserina, piricapirón, DU-125530, OPC-4392, mafoprazina y enasculina.
6. Un proceso para la preparación de un compuesto de arilpiperidina alquilada de Fórmula (VII):
en donde,
R1 y R2 se seleccionan individualmente de hidrógeno, alquilo no sustituido y alquilo sustituido o R1 y R2 se conectan para formar un anillo cíclico de 5 a 8 carbonos;
n = 0, 1 o 2;
Y es NR3R4, OR5 o SR5, donde R3 y R4 se seleccionan individualmente de acilo o sulfonilo, en donde R3 y R4 se pueden conectar para formar un anillo cíclico o bicíclico sustituido o no sustituido y en donde R5 es arilo o heteroarilo, o heterocíclico; y
Ar es un grupo arilo o heteroarilo,
comprendiendo dicho método:
(i) alquilar YH con un sulfato cíclico de Fórmula (II) en presencia de una base para formar un compuesto de Fórmula (III), en donde Q es hidrógeno, un metal o una sal de amonio;
(ii) hidrolizar el compuesto de Fórmula (III) para formar un alcohol de Fórmula (IV);
(iii) convertir el compuesto de Fórmula (IV) para formar un agente alquilante de Fórmula (V), en donde GS es un grupo saliente; y
(iv) alquilar una piperidina de Fórmula (VIII) con el agente alquilante de Fórmula (V) para proporcionar un compuesto de arilpiperidina alquilada de Fórmula (VII)
7. El proceso de la reivindicación 6, en donde R1 y R2 forman parte individualmente de un grupo cíclico C5, C6 o C7.
8. El proceso de la reivindicación 6, en donde R3 y R4 forman parte individualmente de un grupo cíclico C5, C6 o C7.
9. El proceso de la reivindicación 6, en donde el grupo saliente GS se selecciona del grupo que consiste en un sulfonato de arilo, un sulfonato de alquilo, fosfato, fosfonato, proazafosfatrano y un halógeno.
10. El proceso de la reivindicación 6, en donde el compuesto de arilpiperidina alquilada de Fórmula (VII) es iloperidona o abaperidona.
11. Un compuesto de Fórmula (III):
en donde,
R1 y R2 se conectan para formar un anillo cíclico de 5 a 8 carbonos;
n = 0, 1 o 2;
Y es NR3R4, OR5 o SR5, donde R3 y R4 se seleccionan individualmente de acilo o sulfonilo, en donde R3 y R4 se pueden conectar para formar un anillo cíclico o bicíclico sustituido o no sustituido y en donde los sustituyentes se seleccionan del grupo que consiste en alquilo, alcoxi, ariloxi, hidroxi, acetilo, ciano, nitro, glicerilo y carbohidrato o dos sustituyentes tomados en conjunto se pueden unir como grupo -alquileno para formar un anillo y en donde R5 es arilo o heteroarilo, o heterocíclico; y
Q es hidrógeno, un metal o una sal de amonio.
12. Un compuesto que tiene la estructura:
en donde Q es hidrógeno, un metal o una sal de amonio.
14. Un proceso de acuerdo con la reivindicación 1, comprendiendo el proceso para la preparación de lurasidona las etapas de:
(i) alquilar (3aR,4S,7R,7aS)-hexahidro-1H-4,7-metanoisoindol-1,3(2H)-diona mediante la reacción de la misma con 3,3-dióxido de (5aR,9aR)-octahidrobenzo[e][1,3,2]dioxatiepina en presencia de K2CO3 para formar ((1R,2R)-2-(((3aR,4S,7R,7aS)-1,3-dioxooctahidro-2H-4,7-metanoisoindol-2-il)metil)ciclohexil)metil sulfato de potasio;
(ii) hidrolizar ((1R,2R)-2-(((3aR,4S,7R,7aS)-1,3-dioxooctahidro-2H-4,7-metanoisoindol-2-il)metil)ciclohexil)metil sulfato de potasio para formar (3aR,4S,7R,7aS)-2-(((1R,2R)-2-(hidroximetil)ciclohexil)metil)hexahidro-1H-4,7-metanoisoindol-1,3(2H)-diona;
(iii) hacer reaccionar (3aR,4S,7R,7aS)-2-(((1R,2R)-2-(hidroximetil)ciclohexil)metil)hexahidro-1H-4,7-metanoisoindol-1,3(2H)-diona con cloruro de metanosulfonilo para formar metanosulfonato de ((1R,2R)-2-(((3aR,4S,7R,7aS)-1,3-dioxooctahidro-2H-4,7-metanoisoindol-2-il)metil)ciclohexil)metilo; y
(iv) hacer reaccionar 3-(piperazin-1-il)benzo[d]isotiazol con metanosulfonato de ((1 R,2R)-2-(((3aR,4S,7R,7aS)-1,3-dioxooctahidro-2H-4,7-metanoisoindol-2-il)metil)ciclohexil)metilo para formar (3aR,4S,7R,7aS)-2-(((1R,2R)-2-((4-(benzo[d]isotiazol-3-il)piperazin-1-il)metil)ciclohexil)metil)hexahidro-1H-4,7-metanoisoindol-1,3(2H)-diona (Lurasidona).
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462012701P | 2014-06-16 | 2014-06-16 | |
| PCT/US2015/035558 WO2015195478A1 (en) | 2014-06-16 | 2015-06-12 | Processes for making alkylated arylpiperazine and alkylated arylpiperidine compounds including novel intermediates |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2826603T3 true ES2826603T3 (es) | 2021-05-18 |
Family
ID=54835598
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15731459T Active ES2826603T3 (es) | 2014-06-16 | 2015-06-12 | Procesos para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada que incluyen productos intermedios novedosos |
Country Status (10)
| Country | Link |
|---|---|
| US (3) | US9790237B2 (es) |
| EP (1) | EP3154967B1 (es) |
| JP (1) | JP6594351B2 (es) |
| CA (1) | CA2951917C (es) |
| ES (1) | ES2826603T3 (es) |
| HR (1) | HRP20201638T1 (es) |
| HU (1) | HUE052277T2 (es) |
| PL (1) | PL3154967T3 (es) |
| SI (1) | SI3154967T1 (es) |
| WO (1) | WO2015195478A1 (es) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL233778B1 (pl) | 2016-07-19 | 2019-11-29 | Adamed Spolka Z Ograniczona Odpowiedzialnoscia | Sposob wytwarzania brekspiprazolu oraz zastosowanie zwiazkow posrednich w sposobie wytwarzania brekspiprazolu |
| WO2020087031A1 (en) | 2018-10-26 | 2020-04-30 | The Research Foundation For The State University Of New York | Combination serotonin specific reuptake inhibitor and serotonin 1a receptor partial agonist for reducing l-dopa-induced dyskinesia |
| EP4317156A1 (en) * | 2021-03-31 | 2024-02-07 | Sichuan Kelun Pharmaceutical Research Institute Co., Ltd. | Injectable lurasidone suspension and preparation method therefor |
| CN115073444A (zh) * | 2022-08-05 | 2022-09-20 | 山东科源制药股份有限公司 | 一种盐酸鲁拉西酮环氧杂质的精制去除方法 |
Family Cites Families (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE967826C (de) | 1954-06-14 | 1957-12-19 | Henkel & Cie Gmbh | Verfahren zur Herstellung von Aryloxyalkanol-schwefelsaeurehalbestersalzen |
| GB1511159A (en) * | 1975-07-10 | 1978-05-17 | Leo A | Amines preparation |
| US5153206A (en) | 1988-12-02 | 1992-10-06 | Pfizer Inc. | Arylpiperidine derivatives |
| JP2800953B2 (ja) | 1990-07-06 | 1998-09-21 | 住友製薬株式会社 | 新規なイミド誘導体 |
| US5159100A (en) | 1990-12-19 | 1992-10-27 | Lonza Ltd. | Process for the production of cyclopropanenitrile derivatives |
| US6467121B1 (en) | 2000-08-15 | 2002-10-22 | Goodway Technologies Corporation | Rotary tube scrubber |
| UA79300C2 (en) | 2002-08-12 | 2007-06-11 | Janssen Pharmaceutica Nv | N-aryl piperidine substituted biphenylcarboxamides as inhibitors of apolipoprotein b secretion |
| ES2685780T3 (es) | 2002-08-22 | 2018-10-11 | Sumitomo Dainippon Pharma Co., Ltd. | Agente para el tratamiento de esquizofrenia |
| USRE45573E1 (en) | 2003-07-29 | 2015-06-23 | Sumitomo Dainippon Pharma Co., Ltd. | Process for producing imide compound |
| JP2007502815A (ja) * | 2003-08-20 | 2007-02-15 | イーライ リリー アンド カンパニー | Ppar調節因子 |
| CA2536461A1 (en) | 2003-08-27 | 2005-03-10 | Janssen Pharmaceutica, N.V. | Aryl piperidine amides |
| US20070160537A1 (en) | 2004-02-20 | 2007-07-12 | Takeo Ishiyama | In vivo screening method of therapeutic agent for memory/learning dysfunctions by schizophrenia |
| WO2006134864A1 (ja) | 2005-06-13 | 2006-12-21 | Dainippon Sumitomo Pharma Co., Ltd. | 可溶化型製剤 |
| ATE492539T1 (de) | 2006-08-17 | 2011-01-15 | Hoffmann La Roche | Arylpiperazinderivate und anwendungen davon |
| US20090076027A1 (en) | 2007-09-17 | 2009-03-19 | Protia, Llc | Deuterium-enriched lurasidone |
| JP5409382B2 (ja) | 2007-11-21 | 2014-02-05 | 大日本住友製薬株式会社 | 口腔内崩壊錠 |
| US8735397B2 (en) | 2010-03-29 | 2014-05-27 | Vanderbilt University | Method for treating schizophrenia and related diseases |
| ES2594709T3 (es) | 2010-04-26 | 2016-12-22 | Sumitomo Dainippon Pharma Co., Ltd. | Un proceso de preparación de una sal de amonio cuaternario |
| JP5820822B2 (ja) | 2010-04-26 | 2015-11-24 | 大日本住友製薬株式会社 | リン酸塩を用いる第四級アンモニウム塩の製造法 |
| US8258139B2 (en) | 2010-11-08 | 2012-09-04 | Dainippon Sumitomo Pharma Co., Ltd. | Method of treatment for mental disorders |
| WO2012063246A1 (en) | 2010-11-11 | 2012-05-18 | Mapi Pharma Ltd. | Amorphous form of lurasidone hydrochloride |
| WO2012107890A2 (en) | 2011-02-10 | 2012-08-16 | Ranbaxy Laboratories Limited | Crystalline forms of lurasidone hydrochloride |
| WO2012123858A1 (en) | 2011-03-14 | 2012-09-20 | Ranbaxy Laboratories Limited | Amorphous lurasidone hydrochloride |
| EP2694499A1 (en) | 2011-04-01 | 2014-02-12 | Ranbaxy Laboratories Limited | Process for the preparation of an antipsychotic agent |
| US20140113912A1 (en) | 2011-05-13 | 2014-04-24 | Dainippon Sumitomo Pharma Co., Ltd. | Treatment and management of cns disorders |
| WO2013014665A1 (en) | 2011-07-28 | 2013-01-31 | Mapi Pharma Ltd. | Intermediate compounds and process for the preparation of lurasidone and salts thereof |
| WO2013030722A1 (en) | 2011-08-26 | 2013-03-07 | Ranbaxy Laboratories Limited | Crystalline lurasidone hydrochloride |
-
2015
- 2015-06-12 CA CA2951917A patent/CA2951917C/en active Active
- 2015-06-12 HR HRP20201638TT patent/HRP20201638T1/hr unknown
- 2015-06-12 HU HUE15731459A patent/HUE052277T2/hu unknown
- 2015-06-12 EP EP15731459.2A patent/EP3154967B1/en active Active
- 2015-06-12 ES ES15731459T patent/ES2826603T3/es active Active
- 2015-06-12 JP JP2016572799A patent/JP6594351B2/ja active Active
- 2015-06-12 US US14/737,599 patent/US9790237B2/en active Active
- 2015-06-12 PL PL15731459T patent/PL3154967T3/pl unknown
- 2015-06-12 WO PCT/US2015/035558 patent/WO2015195478A1/en not_active Ceased
- 2015-06-12 SI SI201531384T patent/SI3154967T1/sl unknown
-
2017
- 2017-10-16 US US15/784,585 patent/US9957283B1/en active Active
-
2018
- 2018-04-20 US US15/958,645 patent/US20180312530A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| HUE052277T2 (hu) | 2021-04-28 |
| JP2017522284A (ja) | 2017-08-10 |
| US9957283B1 (en) | 2018-05-01 |
| CA2951917A1 (en) | 2015-12-23 |
| US20180312530A1 (en) | 2018-11-01 |
| US20150361099A1 (en) | 2015-12-17 |
| PL3154967T3 (pl) | 2021-01-11 |
| HRP20201638T1 (hr) | 2021-03-05 |
| EP3154967A1 (en) | 2017-04-19 |
| EP3154967B1 (en) | 2020-07-29 |
| US20180099982A1 (en) | 2018-04-12 |
| JP6594351B2 (ja) | 2019-10-23 |
| WO2015195478A1 (en) | 2015-12-23 |
| US9790237B2 (en) | 2017-10-17 |
| SI3154967T1 (sl) | 2020-11-30 |
| CA2951917C (en) | 2019-09-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7307144B2 (ja) | 1,4-置換ピペリジン誘導体 | |
| ES2347987T3 (es) | Proceso para preparar (s)-4-fluorometil-dihidro-furan-2-ona. | |
| ES2930305T3 (es) | Inhibidores del bromodominio | |
| ES2625945T3 (es) | Tieno[3,2-c]piridin-4(5H)-onas como inhibidores de bet | |
| ES2826603T3 (es) | Procesos para la preparación de compuestos de arilpiperazina alquilada y arilpiperidina alquilada que incluyen productos intermedios novedosos | |
| ES2861648T3 (es) | Compuestos de espirociclo y procedimientos de fabricación y uso de los mismos | |
| CN107001289B (zh) | N-酰基-(3-取代的)-(8-取代的)-5,6-二氢-[1,2,4]三唑并[4,3-a]吡嗪的新手性合成 | |
| CA2975605A1 (en) | 3-alkyl-4-amido-bicyclic [4,5,0] hydroxamic acids as hdac inhibitors | |
| PT1260512E (pt) | ''novos derivados de amida cíclicos'' | |
| ES2849951T3 (es) | Derivados de piperidina 4-bencil y 4-benzoil sustituidos | |
| KR20230142529A (ko) | Mk2 억제제, 이의 합성, 및 이의 중간체 | |
| JP2010111684A (ja) | キラル2−メチル−4−保護化ピペラジンの立体選択的アルキル化 | |
| CA2879256A1 (en) | Substituted carbamate compounds and their use as transient receptor potential (trp) channel antagonists | |
| ES2592154T3 (es) | Derivado de N-hidroxiformamida y medicamento que contiene el mismo | |
| CA2885417A1 (en) | Substituted phenylcarbamate compounds | |
| ES2893793T3 (es) | Posaconazol, composición, producto intermedio, método de preparación para el mismo y usos del mismo | |
| ES2992926T3 (en) | Process for the preparation of a substituted imidazoquinoline | |
| WO2016023522A2 (en) | Substituted phosphoramidate compounds and uses thereof | |
| WO1999054297A1 (en) | Process for preparing chloro alcohol derivatives and intermediates | |
| ES2759650T3 (es) | Compuestos quinoxalina y sus usos | |
| CN107922426B (zh) | 四氢噁庚英吡啶化合物 | |
| WO2023288253A1 (en) | Small molecules inhibitors of cyclic gmp-amp synthase (cgas) | |
| KR101346555B1 (ko) | 9-히드록시-3-(2-클로로에틸)-2-메틸-6,7,8,9-테트라히드로-4H-피리도[1,2-a]피리미딘-4-온의 제조방법 | |
| BR112020011901A2 (pt) | processo para preparar derivados anti-helminticos de 4-amino-quinolina-3-carboxamida | |
| BR112020011901B1 (pt) | Processo para preparar derivados anti-helminticos de 4-aminoquinolina-3-carboxamida |