ES2833251T3 - Procedimiento para producir derivados de 2-(3,6-dihalopiridin-2-il)-3h-imidazol[4,5-c]piridina y compuestos relacionados por reacción del derivado de piridina 3h-imidazol[4,5-c] con una base organometálica de zinc-amina - Google Patents
Procedimiento para producir derivados de 2-(3,6-dihalopiridin-2-il)-3h-imidazol[4,5-c]piridina y compuestos relacionados por reacción del derivado de piridina 3h-imidazol[4,5-c] con una base organometálica de zinc-amina Download PDFInfo
- Publication number
- ES2833251T3 ES2833251T3 ES17746524T ES17746524T ES2833251T3 ES 2833251 T3 ES2833251 T3 ES 2833251T3 ES 17746524 T ES17746524 T ES 17746524T ES 17746524 T ES17746524 T ES 17746524T ES 2833251 T3 ES2833251 T3 ES 2833251T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- cycloalkyl
- halo
- alkoxy
- alkynyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 88
- 238000000034 method Methods 0.000 title claims abstract description 55
- 230000008569 process Effects 0.000 title claims description 35
- 150000003222 pyridines Chemical class 0.000 title description 17
- 125000002524 organometallic group Chemical group 0.000 title description 4
- RAXXELZNTBOGNW-UHFFFAOYSA-N 1H-imidazole Chemical compound C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 title description 2
- 125000005843 halogen group Chemical group 0.000 claims abstract description 117
- -1 halo (C1-C4) alkoxy Chemical group 0.000 claims abstract description 58
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims abstract description 49
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 48
- 125000000304 alkynyl group Chemical group 0.000 claims abstract description 43
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 42
- 229910052799 carbon Inorganic materials 0.000 claims abstract description 40
- 229910052736 halogen Inorganic materials 0.000 claims abstract description 37
- 150000002367 halogens Chemical class 0.000 claims abstract description 37
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 29
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims abstract description 28
- 125000004448 alkyl carbonyl group Chemical group 0.000 claims abstract description 28
- 125000004414 alkyl thio group Chemical group 0.000 claims abstract description 26
- 125000004963 sulfonylalkyl group Chemical group 0.000 claims abstract description 22
- 125000000262 haloalkenyl group Chemical group 0.000 claims abstract description 21
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 19
- 125000003342 alkenyl group Chemical group 0.000 claims abstract description 18
- 125000003282 alkyl amino group Chemical group 0.000 claims abstract description 18
- 239000001257 hydrogen Substances 0.000 claims abstract description 18
- 125000004093 cyano group Chemical group *C#N 0.000 claims abstract description 17
- 125000003302 alkenyloxy group Chemical group 0.000 claims abstract description 16
- 125000005291 haloalkenyloxy group Chemical group 0.000 claims abstract description 16
- 125000001188 haloalkyl group Chemical group 0.000 claims abstract description 16
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 claims abstract description 13
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims abstract description 12
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 11
- 125000006650 (C2-C4) alkynyl group Chemical group 0.000 claims abstract description 10
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims abstract description 10
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 claims abstract description 10
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 claims abstract description 10
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims abstract description 10
- 150000001721 carbon Chemical group 0.000 claims abstract description 10
- 229910052717 sulfur Inorganic materials 0.000 claims abstract description 10
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 9
- 125000004768 (C1-C4) alkylsulfinyl group Chemical group 0.000 claims abstract description 8
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 claims abstract description 8
- 125000004663 dialkyl amino group Chemical group 0.000 claims abstract description 7
- 125000004966 cyanoalkyl group Chemical group 0.000 claims abstract description 6
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims abstract description 6
- 125000004758 (C1-C4) alkoxyimino group Chemical group 0.000 claims abstract description 3
- 125000004441 haloalkylsulfonyl group Chemical group 0.000 claims abstract 2
- 150000002431 hydrogen Chemical class 0.000 claims abstract 2
- 125000000217 alkyl group Chemical group 0.000 claims description 84
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 58
- UOCLXMDMGBRAIB-UHFFFAOYSA-N 1,1,1-trichloroethane Chemical compound CC(Cl)(Cl)Cl UOCLXMDMGBRAIB-UHFFFAOYSA-N 0.000 claims description 53
- 239000000460 chlorine Substances 0.000 claims description 42
- 229910052801 chlorine Inorganic materials 0.000 claims description 42
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 40
- 229910052794 bromium Inorganic materials 0.000 claims description 40
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 39
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 39
- 229910052731 fluorine Inorganic materials 0.000 claims description 34
- 239000011737 fluorine Substances 0.000 claims description 34
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 claims description 32
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 29
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 27
- 239000002585 base Substances 0.000 claims description 24
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 22
- 125000004399 C1-C4 alkenyl group Chemical group 0.000 claims description 19
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 claims description 19
- 125000005133 alkynyloxy group Chemical group 0.000 claims description 18
- 125000006001 difluoroethyl group Chemical group 0.000 claims description 18
- 125000003784 fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 claims description 18
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 claims description 18
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 claims description 17
- 239000002904 solvent Substances 0.000 claims description 17
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical group [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 claims description 16
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 claims description 16
- 125000006337 tetrafluoro ethyl group Chemical group 0.000 claims description 16
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 claims description 14
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 claims description 14
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 12
- 125000004644 alkyl sulfinyl group Chemical group 0.000 claims description 12
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 claims description 12
- 125000005119 alkyl cycloalkyl group Chemical group 0.000 claims description 11
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 11
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims description 10
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims description 10
- 239000011630 iodine Substances 0.000 claims description 10
- 229910052740 iodine Inorganic materials 0.000 claims description 10
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 10
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 10
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 claims description 10
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 9
- 125000005243 carbonyl alkyl group Chemical group 0.000 claims description 9
- 239000003054 catalyst Substances 0.000 claims description 9
- 125000001153 fluoro group Chemical group F* 0.000 claims description 9
- 229910052725 zinc Inorganic materials 0.000 claims description 9
- RKMGAJGJIURJSJ-UHFFFAOYSA-N 2,2,6,6-Tetramethylpiperidine Substances CC1(C)CCCC(C)(C)N1 RKMGAJGJIURJSJ-UHFFFAOYSA-N 0.000 claims description 8
- HVZJRWJGKQPSFL-UHFFFAOYSA-N tert-Amyl methyl ether Chemical compound CCC(C)(C)OC HVZJRWJGKQPSFL-UHFFFAOYSA-N 0.000 claims description 8
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 7
- 125000000676 alkoxyimino group Chemical group 0.000 claims description 7
- 150000004820 halides Chemical class 0.000 claims description 7
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 claims description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 6
- 125000004656 alkyl sulfonylamino group Chemical group 0.000 claims description 6
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 claims description 6
- 229910052727 yttrium Chemical group 0.000 claims description 6
- 125000004471 alkyl aminosulfonyl group Chemical group 0.000 claims description 5
- 125000006350 alkyl thio alkyl group Chemical group 0.000 claims description 5
- 239000000203 mixture Substances 0.000 claims description 5
- 229910052721 tungsten Chemical group 0.000 claims description 5
- QPFMBZIOSGYJDE-UHFFFAOYSA-N 1,1,2,2-tetrachloroethane Chemical compound ClC(Cl)C(Cl)Cl QPFMBZIOSGYJDE-UHFFFAOYSA-N 0.000 claims description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 claims description 4
- ZFPGARUNNKGOBB-UHFFFAOYSA-N 1-Ethyl-2-pyrrolidinone Chemical compound CCN1CCCC1=O ZFPGARUNNKGOBB-UHFFFAOYSA-N 0.000 claims description 4
- BNXZHVUCNYMNOS-UHFFFAOYSA-N 1-butylpyrrolidin-2-one Chemical compound CCCCN1CCCC1=O BNXZHVUCNYMNOS-UHFFFAOYSA-N 0.000 claims description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 4
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 claims description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 claims description 4
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical compound BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 claims description 4
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 claims description 4
- 150000002941 palladium compounds Chemical group 0.000 claims description 4
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 claims description 4
- 125000001931 aliphatic group Chemical group 0.000 claims description 3
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 claims description 3
- AUHZEENZYGFFBQ-UHFFFAOYSA-N mesitylene Substances CC1=CC(C)=CC(C)=C1 AUHZEENZYGFFBQ-UHFFFAOYSA-N 0.000 claims description 3
- 125000001827 mesitylenyl group Chemical group [H]C1=C(C(*)=C(C([H])=C1C([H])([H])[H])C([H])([H])[H])C([H])([H])[H] 0.000 claims description 3
- 239000008096 xylene Substances 0.000 claims description 3
- 150000003738 xylenes Chemical class 0.000 claims description 3
- GETTZEONDQJALK-UHFFFAOYSA-N (trifluoromethyl)benzene Chemical compound FC(F)(F)C1=CC=CC=C1 GETTZEONDQJALK-UHFFFAOYSA-N 0.000 claims description 2
- BOSAWIQFTJIYIS-UHFFFAOYSA-N 1,1,1-trichloro-2,2,2-trifluoroethane Chemical compound FC(F)(F)C(Cl)(Cl)Cl BOSAWIQFTJIYIS-UHFFFAOYSA-N 0.000 claims description 2
- SEQRDAAUNCRFIT-UHFFFAOYSA-N 1,1-dichlorobutane Chemical compound CCCC(Cl)Cl SEQRDAAUNCRFIT-UHFFFAOYSA-N 0.000 claims description 2
- KNKRKFALVUDBJE-UHFFFAOYSA-N 1,2-dichloropropane Chemical compound CC(Cl)CCl KNKRKFALVUDBJE-UHFFFAOYSA-N 0.000 claims description 2
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 claims description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 claims description 2
- CYTYCFOTNPOANT-UHFFFAOYSA-N Perchloroethylene Chemical group ClC(Cl)=C(Cl)Cl CYTYCFOTNPOANT-UHFFFAOYSA-N 0.000 claims description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 claims description 2
- 229940117389 dichlorobenzene Drugs 0.000 claims description 2
- GUVUOGQBMYCBQP-UHFFFAOYSA-N dmpu Chemical compound CN1CCCN(C)C1=O GUVUOGQBMYCBQP-UHFFFAOYSA-N 0.000 claims description 2
- 150000005826 halohydrocarbons Chemical class 0.000 claims description 2
- 229910001629 magnesium chloride Inorganic materials 0.000 claims description 2
- QULYNCCPRWKEMF-UHFFFAOYSA-N parachlorobenzotrifluoride Chemical compound FC(F)(F)C1=CC=C(Cl)C=C1 QULYNCCPRWKEMF-UHFFFAOYSA-N 0.000 claims description 2
- 229950011008 tetrachloroethylene Drugs 0.000 claims description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims 5
- 125000001309 chloro group Chemical group Cl* 0.000 claims 3
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 claims 2
- RELMFMZEBKVZJC-UHFFFAOYSA-N 1,2,3-trichlorobenzene Chemical compound ClC1=CC=CC(Cl)=C1Cl RELMFMZEBKVZJC-UHFFFAOYSA-N 0.000 claims 1
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 claims 1
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 claims 1
- 229910001508 alkali metal halide Inorganic materials 0.000 claims 1
- 150000008045 alkali metal halides Chemical class 0.000 claims 1
- 125000003118 aryl group Chemical group 0.000 claims 1
- KCXMKQUNVWSEMD-UHFFFAOYSA-N benzyl chloride Chemical compound ClCC1=CC=CC=C1 KCXMKQUNVWSEMD-UHFFFAOYSA-N 0.000 claims 1
- 125000001246 bromo group Chemical group Br* 0.000 claims 1
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 claims 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 abstract 1
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 abstract 1
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 48
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 21
- 150000003254 radicals Chemical group 0.000 description 21
- 238000006243 chemical reaction Methods 0.000 description 20
- 239000000243 solution Substances 0.000 description 20
- 238000003786 synthesis reaction Methods 0.000 description 13
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 12
- 230000015572 biosynthetic process Effects 0.000 description 11
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 10
- 125000004433 nitrogen atom Chemical group N* 0.000 description 10
- 239000000543 intermediate Substances 0.000 description 9
- 239000011701 zinc Substances 0.000 description 9
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 8
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N DMSO Substances CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 8
- 238000004440 column chromatography Methods 0.000 description 8
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethyl cyclohexane Natural products CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 8
- 239000012074 organic phase Substances 0.000 description 8
- 238000000746 purification Methods 0.000 description 8
- 239000007787 solid Substances 0.000 description 8
- 238000010626 work up procedure Methods 0.000 description 8
- YAXWOADCWUUUNX-UHFFFAOYSA-N 1,2,2,3-tetramethylpiperidine Chemical compound CC1CCCN(C)C1(C)C YAXWOADCWUUUNX-UHFFFAOYSA-N 0.000 description 7
- 238000005160 1H NMR spectroscopy Methods 0.000 description 7
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 7
- 239000012528 membrane Substances 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 7
- 239000011734 sodium Substances 0.000 description 7
- 229910052786 argon Inorganic materials 0.000 description 6
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 6
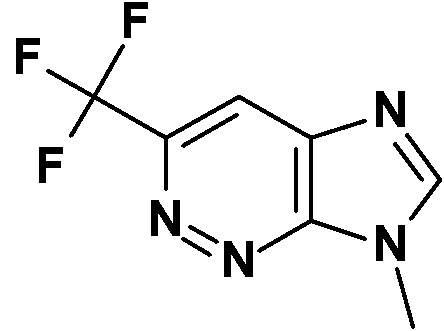
- ZJDIQHDHACZBRJ-UHFFFAOYSA-N 7-methyl-3-(trifluoromethyl)imidazo[4,5-c]pyridazine Chemical compound CN1C=NC2=C1N=NC(=C2)C(F)(F)F ZJDIQHDHACZBRJ-UHFFFAOYSA-N 0.000 description 5
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 5
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 5
- 125000004438 haloalkoxy group Chemical group 0.000 description 5
- PYRYQBSOOMBRKH-UHFFFAOYSA-N 3-methyl-6-(trifluoromethyl)imidazo[4,5-c]pyridine Chemical compound CN1C=NC2=C1C=NC(=C2)C(F)(F)F PYRYQBSOOMBRKH-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 239000003513 alkali Substances 0.000 description 4
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 4
- 238000009833 condensation Methods 0.000 description 4
- 230000005494 condensation Effects 0.000 description 4
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 4
- 238000006411 Negishi coupling reaction Methods 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 125000004769 (C1-C4) alkylsulfonyl group Chemical group 0.000 description 2
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 2
- YQTCQNIPQMJNTI-UHFFFAOYSA-N 2,2-dimethylpropan-1-one Chemical group CC(C)(C)[C]=O YQTCQNIPQMJNTI-UHFFFAOYSA-N 0.000 description 2
- VJZSIGSBEMWLCS-UHFFFAOYSA-N 2-(6-bromo-3-fluoropyridin-2-yl)-3-methyl-6-(trifluoromethyl)imidazo[4,5-c]pyridine Chemical compound BrC1=CC=C(C(=N1)C1=NC2=C(C=NC(=C2)C(F)(F)F)N1C)F VJZSIGSBEMWLCS-UHFFFAOYSA-N 0.000 description 2
- LSMZRMAVVUNNDO-UHFFFAOYSA-N 2-(6-chloro-3-fluoropyridin-2-yl)-3-methyl-6-(trifluoromethyl)imidazo[4,5-c]pyridine Chemical compound ClC1=CC=C(C(=N1)C1=NC2=C(C=NC(=C2)C(F)(F)F)N1C)F LSMZRMAVVUNNDO-UHFFFAOYSA-N 0.000 description 2
- UBOOKRVGOBKDMM-UHFFFAOYSA-N 3h-imidazo[4,5-c]pyridine Chemical compound C1=NC=C2NC=NC2=C1 UBOOKRVGOBKDMM-UHFFFAOYSA-N 0.000 description 2
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 2
- YYZLJLKIFNHVQI-UHFFFAOYSA-N 6-(6-bromo-3-fluoropyridin-2-yl)-7-methyl-3-(trifluoromethyl)imidazo[4,5-c]pyridazine Chemical compound BrC1=CC=C(C(=N1)C1=NC2=C(N=NC(=C2)C(F)(F)F)N1C)F YYZLJLKIFNHVQI-UHFFFAOYSA-N 0.000 description 2
- HLFVDGPBZNIAAD-UHFFFAOYSA-N 6-bromo-3-fluoro-2-iodopyridine Chemical compound BrC1=CC=C(C(=N1)I)F HLFVDGPBZNIAAD-UHFFFAOYSA-N 0.000 description 2
- MINXERMPCQJEFL-UHFFFAOYSA-N 6-chloro-3-fluoro-2-iodopyridine Chemical compound FC1=CC=C(Cl)N=C1I MINXERMPCQJEFL-UHFFFAOYSA-N 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 238000006880 cross-coupling reaction Methods 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 150000008040 ionic compounds Chemical class 0.000 description 2
- JMWYSMBTMNOYFN-UHFFFAOYSA-N methyl 5-fluoro-6-iodopyridine-2-carboxylate Chemical compound COC(=O)C1=NC(=C(C=C1)F)I JMWYSMBTMNOYFN-UHFFFAOYSA-N 0.000 description 2
- SIOXPEMLGUPBBT-UHFFFAOYSA-M picolinate Chemical compound [O-]C(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-M 0.000 description 2
- 239000000376 reactant Substances 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 2
- 125000004760 (C1-C4) alkylsulfonylamino group Chemical group 0.000 description 1
- 125000006529 (C3-C6) alkyl group Chemical group 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000006039 1-hexenyl group Chemical group 0.000 description 1
- BLRHMMGNCXNXJL-UHFFFAOYSA-N 1-methylindole Chemical compound C1=CC=C2N(C)C=CC2=C1 BLRHMMGNCXNXJL-UHFFFAOYSA-N 0.000 description 1
- 125000006023 1-pentenyl group Chemical group 0.000 description 1
- 125000006017 1-propenyl group Chemical group 0.000 description 1
- 125000000530 1-propynyl group Chemical group [H]C([H])([H])C#C* 0.000 description 1
- KAESVJOAVNADME-UHFFFAOYSA-N 1H-pyrrole Natural products C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 1
- YWIWMGNLWAKIRE-UHFFFAOYSA-N 2-(3-fluoro-6-nitropyridin-2-yl)-3-methyl-6-(trifluoromethyl)imidazo[4,5-c]pyridine Chemical compound FC=1C(=NC(=CC=1)[N+](=O)[O-])C1=NC2=C(C=NC(=C2)C(F)(F)F)N1C YWIWMGNLWAKIRE-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000006040 2-hexenyl group Chemical group 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- 125000006024 2-pentenyl group Chemical group 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- NESRSFKZZDFADT-UHFFFAOYSA-N 3-N-methyl-6-(trifluoromethyl)pyridazine-3,4-diamine Chemical compound CNC=1N=NC(=CC=1N)C(F)(F)F NESRSFKZZDFADT-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000006041 3-hexenyl group Chemical group 0.000 description 1
- 125000003542 3-methylbutan-2-yl group Chemical group [H]C([H])([H])C([H])(*)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- GAMYYCRTACQSBR-UHFFFAOYSA-N 4-azabenzimidazole Chemical compound C1=CC=C2NC=NC2=N1 GAMYYCRTACQSBR-UHFFFAOYSA-N 0.000 description 1
- 125000006042 4-hexenyl group Chemical group 0.000 description 1
- 125000006043 5-hexenyl group Chemical group 0.000 description 1
- RURRCFZATBARET-UHFFFAOYSA-N 6-(6-chloro-3-fluoropyridin-2-yl)-7-methyl-3-(trifluoromethyl)imidazo[4,5-c]pyridazine Chemical compound ClC1=CC=C(C(=N1)C1=NC2=C(N=NC(=C2)C(F)(F)F)N1C)F RURRCFZATBARET-UHFFFAOYSA-N 0.000 description 1
- ZHRWOPMANBDMSZ-UHFFFAOYSA-N CNc1cnc(cc1N)C(F)(F)F Chemical compound CNc1cnc(cc1N)C(F)(F)F ZHRWOPMANBDMSZ-UHFFFAOYSA-N 0.000 description 1
- RNNSKVCDHWXZJR-UHFFFAOYSA-N C[n]1c(-c(nc(cc2)C(OC)=O)c2F)nc2cc(C(F)(F)F)ncc12 Chemical compound C[n]1c(-c(nc(cc2)C(OC)=O)c2F)nc2cc(C(F)(F)F)ncc12 RNNSKVCDHWXZJR-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 239000007832 Na2SO4 Substances 0.000 description 1
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 238000006619 Stille reaction Methods 0.000 description 1
- 238000006069 Suzuki reaction reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000003905 agrochemical Substances 0.000 description 1
- 150000001347 alkyl bromides Chemical class 0.000 description 1
- 125000005278 alkyl sulfonyloxy group Chemical group 0.000 description 1
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 230000009435 amidation Effects 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 125000002619 bicyclic group Chemical group 0.000 description 1
- 229910052793 cadmium Inorganic materials 0.000 description 1
- BDOSMKKIYDKNTQ-UHFFFAOYSA-N cadmium atom Chemical compound [Cd] BDOSMKKIYDKNTQ-UHFFFAOYSA-N 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- BGXNDODUJKVDJK-UHFFFAOYSA-N carbonic acid;4-methyl-1,3-dioxepan-2-one Chemical compound OC(O)=O.CC1CCCOC(=O)O1 BGXNDODUJKVDJK-UHFFFAOYSA-N 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 238000010960 commercial process Methods 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 238000009795 derivation Methods 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 150000002148 esters Chemical group 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 150000005233 imidazopyridazines Chemical class 0.000 description 1
- 239000013067 intermediate product Substances 0.000 description 1
- 150000004694 iodide salts Chemical class 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 238000006263 metalation reaction Methods 0.000 description 1
- 238000001465 metallisation Methods 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000002816 nickel compounds Chemical class 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 238000010651 palladium-catalyzed cross coupling reaction Methods 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- SIOXPEMLGUPBBT-UHFFFAOYSA-N picolinic acid Chemical class OC(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-N 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- ZZYXNRREDYWPLN-UHFFFAOYSA-N pyridine-2,3-diamine Chemical class NC1=CC=CN=C1N ZZYXNRREDYWPLN-UHFFFAOYSA-N 0.000 description 1
- 238000006798 ring closing metathesis reaction Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000003396 thiol group Chemical class [H]S* 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 150000003624 transition metals Chemical class 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000011592 zinc chloride Substances 0.000 description 1
- 235000005074 zinc chloride Nutrition 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/90—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having two or more relevant hetero rings, condensed among themselves or with a common carbocyclic ring system
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/24—Phosphines, i.e. phosphorus bonded to only carbon atoms, or to both carbon and hydrogen atoms, including e.g. sp2-hybridised phosphorus compounds such as phosphabenzene, phosphole or anionic phospholide ligands
- B01J31/2404—Cyclic ligands, including e.g. non-condensed polycyclic ligands, the phosphine-P atom being a ring member or a substituent on the ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/056—Ortho-condensed systems with two or more oxygen atoms as ring hetero atoms in the oxygen-containing ring
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/82—Metals of the platinum group
- B01J2531/824—Palladium
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Inorganic Chemistry (AREA)
- Materials Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Zoology (AREA)
- Plant Pathology (AREA)
- Agronomy & Crop Science (AREA)
- Dentistry (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Pest Control & Pesticides (AREA)
- Environmental Sciences (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Pyridine Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Procedimiento para producir compuestos de la Fórmula (II) **(Ver fórmula)** en la que Q es un elemento estructural **(Ver fórmula)** en donde el símbolo indica el enlace con el resto de la molécula y Q1 es N o CR6, Q2 es N o CR6, Q3 es N o C, Q4 es O, S, N o NR7, Q5 es N o C, Q6 es N o CH, R6 es hidrógeno, alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)- alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2- C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1- C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1- C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4), R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)- alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3- C6), halo(cicloalquilo(C3-C6)) alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1- 25 C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4) y A es hidrógeno, ciano, halógeno, alquilo(C1-C4), haloalquilo(C1-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)- cicloalquilo(C3-C6), alcoxi(C1-C4), halo(alcoxi(C1-C4)), alcoxiimino(C1-C4), alquiltio(C1-C4), halo(alquiltio(C1-C4)), alquilsulfinilo(C1-C4), halo(alquilsulfinilo(C1-C4)), sulfonilalquilo(C1-C4), haloalquilsulfonilo(C1-C4), sulfonilalquiloxi(C1-C4), alquilcarbonilo(C1-C4), halo(alquilcarbonilo(C1-C4)), aminocarbonilo, alquilaminocarbonilo(C1-C4), di-alquilo(C1-C4)-aminocarbonilo, alquilamino(C1-C4)sulfonilo, alquilamino(C1-C4), dialquilamino( C1-C4), aminosulfonilo, alquilamino(C1-C4)sulfonilo o di-alquilamino(C1-C4)sulfonilo, o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros, en donde Q1 es carbono, W es halógeno, Y es halógeno, CO2R1 o NO2, en donde R1 es alquilo(C1-C6) o haloalquilo(C1-C6),
Description
DESCRIPCIÓN
Procedimiento para producir derivados de 2-(3,6-dihalopiridin-2-il)-3h-imidazol[4,5-c]piridina y compuestos relacionados por reacción del derivado de piridina 3h-imidazol[4,5-c] con una base organometálica de zinc-amina La presente invención se refiere a un procedimiento para producir derivados de piridina halogenados de la Fórmula (II)
(II)
partiendo de compuestos Q-H a través de intermediarios de la Fórmula (IIIa) o (IIIb)
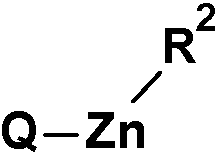
r2
/
Q -Zn Q—Zn— Q
(Illa) (IIIb),
en las que los elementos estructurales indicados en las Fórmulas (II), (IIIa) y (IIIb) tienen los significados indicados a continuación. La invención se refiere, además, a derivados de piridina halogenados e intermediarios de este tipo. Los derivados de piridina halogenados de la Fórmula (II) son de gran importancia para la industria farmacéutica y agroquímica y son un intermediario importante, entre otros, en la preparación de compuestos que son efectivos como pesticidas, por ejemplo.
En la literatura se describe que los compuestos de la Fórmula (II) se pueden producir, por ejemplo, en una primera etapa por condensación de derivados de ácido piridina-2-carboxílico con derivados de bis(amina) orto-sustituida, alcohol amina o amina tiol (hetero)arilo, en presencia de un agente de condensación (véanse los documentos US2003/69257 o WO2006/65703) y luego, en una segunda etapa, por condensación adicional, como se describe en el documento WO2012/86848. Por medio de doble condensación se representan en el documento WO2011/027249 nuevos derivados de bencidimazol, en el documento WO2016/124557 derivados de heterocicleno bicíclicos. Asimismo, se pueden sintetizar de manera no catalítica también 1,3,5-triazaindeno (G. B. Barlin et al., J. Chem. Soc. B, 1966, 285-291) y se puede acoplar ribosa protegida con sales de magnesio, cadmio y zinc de heterociclos aromáticos (H. Togo et al., J. Chem. Soc. Perkin Trans. 1997, 1,29-33).
En el documento WO2007/075561 se desvelan procedimientos de preparación de nuevas triazolpiridinas por medio de catálisis de metales de transición (acoplamientos de Suzuki, Stille o Negishi). Las 2-arilvinolaciones de 1-metilindol son posibles con la ayuda del acoplamiento cruzado catalizado por paladio (G. Maas et al., Synthesis 1999, 6, 1013-1016). Los reactivos de (hetero)arilzinc se pueden hacer reaccionar con bromuros y yoduros de alquilo en acoplamientos Negishi catalizados por cobalto (P. Knochel et al., Angew. Chem. Int. Ed. 2015, 54, 4478 4481). Con ayuda de amidaciones catalizadas por cobre y paladio se pueden representar imidazo[4,5-c]piridinas (R. J. Wilson et al., J. Org. Chem. 2014, 79, 2203-2212).
Sin embargo, los procedimientos de síntesis química descritos hasta ahora en el estado de la técnica de tales derivados de piridina halogenados hacen uso con mucha frecuencia de procedimientos que no son económicamente implementables desde el punto de vista industrial o presentan otras desventajas.
Las desventajas son los bajos rendimientos químicos, la realización a temperaturas muy altas (aproximadamente de 150 a 250°C) y la posible regio- y quimioselectividad difíciles de la condensación, en particular en el caso de los derivados de imidazopiridina e imidazopiridazina. Por lo tanto, la preparación es muy costosa e inadecuada para procedimientos comerciales a escala industrial. Además, los compuestos correspondientes apenas están disponibles comercialmente. Esto es en particular cierto para derivados del ácido 3,6-dihalopiridina-2-carboxílico.
Con respecto a las desventajas descritas anteriormente, existe una necesidad urgente de un procedimiento simplificado, industrial y económicamente realizable para producir derivados de piridina halogenados, en particular derivados de piridina halogenados de la Fórmula (II). Los derivados de piridina halogenados obtenibles mediante este procedimiento buscado deben obtenerse a este respecto con preferencia con buen rendimiento, alta pureza y de manera económica.
Se ha encontrado que, sorprendentemente, los derivados de piridina halogenados de la Fórmula (II) se pueden producir ventajosamente en un procedimiento con el uso de una base de organozinc.
En consecuencia, el objeto de la presente invención es un procedimiento para producir compuestos de la Fórmula (II)
(II),
en donde (configuración 1)
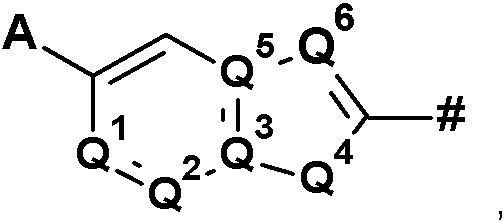
Q es un elemento estructural
en donde el símbolo # indica el enlace con el resto de la molécula,
Q1 es N o CR6,
Q2 es N o CR6,
Q3 es N o C,
Q4 es O, S, N o NR7,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo (C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4) y
A es hidrógeno, ciano, halógeno, alquilo(C1-C4), haloalquilo(C1-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), alcoxi(C1-C4), halo(alcoxi(C1-C4)), alcoxiimino(C1-C4), alquiltio(C1-C4), halo(alquiltio(C1-C4)), alquilsulfinilo(C1 -c4), halo(alquilsulfinilo(C1-C4)), sulfonilalquilo(C1-C4), halo(alquilsulfonilo(C1-C4)), alquilsulfoniloxi(C1-C4), alquilcarbonilo(C1-C4), halo(alquilcarbonilo(C1-C4)), aminocarbonilo, alquilamino(C1-C4)-carbonilo, di-alquilo(C1-C4)-aminocarbonilo, alquilsulfonilamino(C1-C4), alquilamino(C1-C4), di-alquilamino(C1-C4), aminosulfonilo, alquilaminosulfonilo(C1-C4) o di-alquilaminosulfonilo(C1-C4),
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros donde Q1 es carbono,
W es halógeno e
Y es halógeno, CO2R1 o NO2 , en donde R1 es alquilo(Ci-C6) o haloalquilo(Ci-C6),
caracterizado porque, en una primera etapa del procedimiento a), un compuesto Q-H, en el que Q tiene el significado mencionado anteriormente,
se hace reaccionar con una base de organozinc de la estructura (NR3R4)-Zn-R2 o (NR3R4 )2-Zn, en la que
R2 es halógeno o -O-pivaloilo y
R3 y R4 juntos forman un grupo -(CH2)4-, -(CH2)5- o -(CH2)2- o -(CH2)2-, donde cada uno de estos grupos puede estar opcionalmente sustituido por los radicales R51, 2, 3 o 4 y R5 se selecciona del grupo que consiste en metilo, etilo, npropilo e i-propilo,
hasta dar un compuesto de la Fórmula (Illa) o la Fórmula (IlIb),
(Illa)
Q-Zn-Q (IlIb),
en la que Q y R2 tienen en cada caso los significados indicadoslos significados mencionados anteriormente, y este compuesto de la Fórmula (Illa) o (IlIb) se hace reaccionar en una segunda etapa de procedimiento b) con un compuesto de la Fórmula (I)
en la que X es halógeno y W e Y tienen en cada caso los significados mencionados anteriormentelos significados indicados, en presencia de un catalizador hasta dar el compuesto de la Fórmula (II).
Con preferencia, Q1, Q2, Q3, Q4, Q5 y Q6 representan no más de cinco átomos de nitrógeno en total y, además, preferentemente, no más de cuatro átomos de nitrógeno en total.
Las definiciones preferentes y especialmente preferentes de los restos Q, W, R1, R2, X e Y, incluidos en las Fórmulas (I), (II), (Illa) y (IlIb) mencionadas anteriormente se explican a continuación, en donde la base de organozinc se describe más abajo más exactamente, pde modo que las configuraciones preferentes de la base se indican en ese punto.
(Configuración 2)
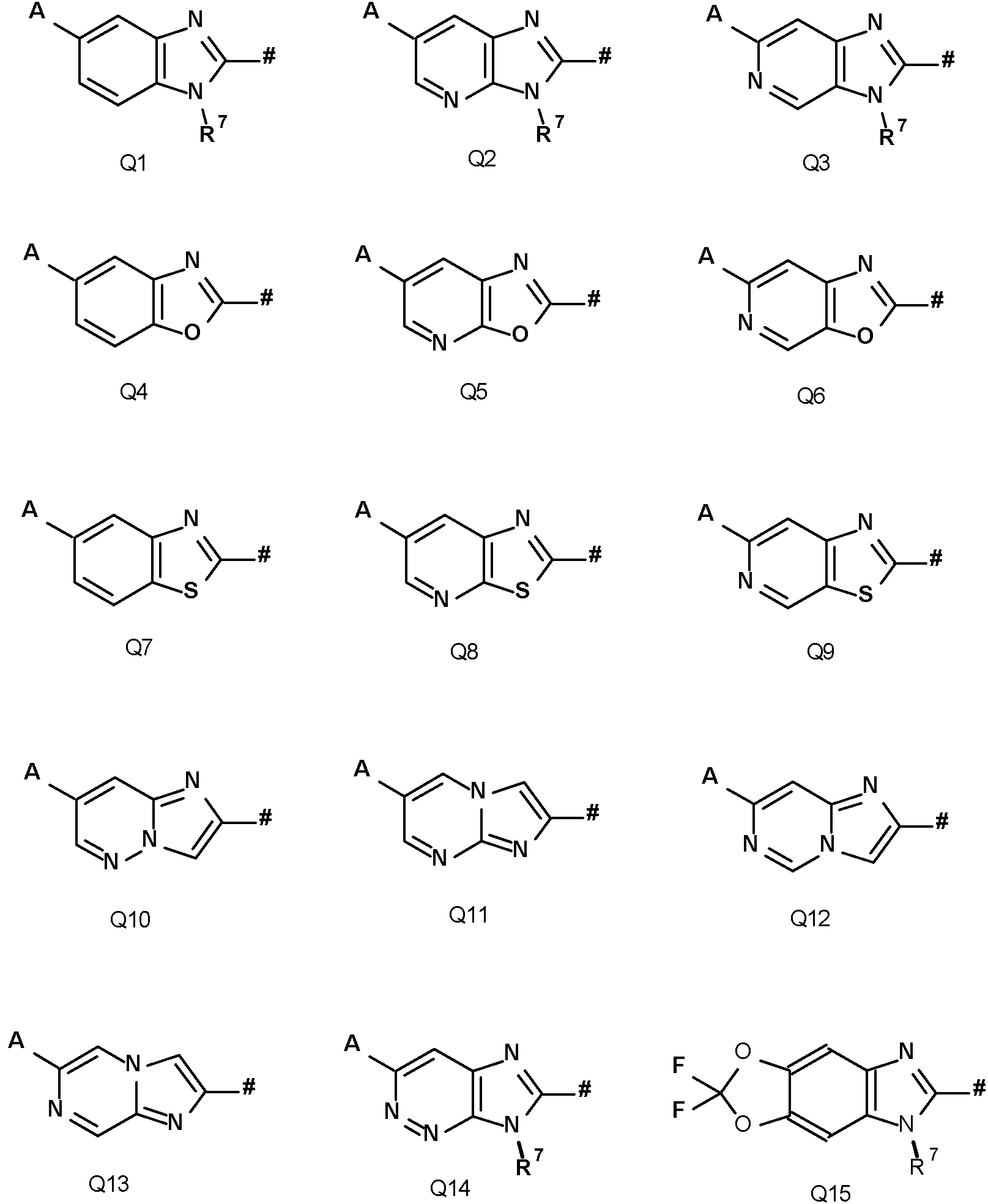
Q es preferentemente un elemento estructural de la serie de Q1 a Q15.
R7 es preferentemente alquilo(Ci -C4), haloalquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(Ci -C4))-alquilo(Ci -C4), alquiltio(Ci -C4)-alquilo(Ci -C4), sulfonilalquilo(Ci -C4)-alquilo(Ci -C4), sulfonilalquilo(Ci -C4)-alquilo(Ci -C4) o carbonilalquilo(Ci -C4)-alquilo(Ci -C4).
A es preferentemente flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es preferentemente flúor, cloro o bromo,
R2 es preferentemente halógeno, en particular cloro, bromo o yodo,
X es preferentemente halógeno, en particular bromo o yodo e
Y es preferentemente flúor, cloro, bromo, CO2R1 o NO2, en donde R1 es alquilo(C1-C4).
(Configuración 3)
Q es de manera especialmente preferente un elemento estructural de la serie de Q2, Q3, Q10, Q12, Q14 y Q15, R7 es de manera especialmente preferente alquilo(C1-C4) o alcoxi(C1-C4)-alquilo(C1-C4),
A es de manera especialmente preferente trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2 , CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es de manera especialmente preferente flúor o cloro, en particular flúor,
R2 es de manera especialmente preferente cloro,
X es de manera especialmente preferente bromo o yodo, en particular yodo, e
Y es de manera especialmente preferente cloro, bromo, CO2R1 o NO2, en donde R1 es alquilo(C1-C4).
(Configuración 4)
Q es de manera especialmente preferente el elemento estructural Q3 o Q14,
R7 es de manera especialmente preferente metilo, etilo, n-propilo o isopropilo, en particular metilo,
A es de manera especialmente preferente trifluorometilo,
W es de manera especialmente preferente flúor,
R2 es de manera especialmente preferente cloro,
X es de manera especialmente preferente yodo e
Y es de manera especialmente preferente cloro, bromo, CO2R1 o NO2, en donde R1 es metilo.
Las definiciones de radicales o explicaciones dadas anteriormente se aplican tanto a los productos finales y productos intermediarios, como a los materiales de partida de una manera correspondiente. Estas definiciones de radicales pueden combinarse entre sí de manera discrecional, es decir, incluyendo combinaciones entre los respectivos índices de preferencia.
De acuerdo con la invención, se prefieren aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como preferentes.
De acuerdo con la invención se prefieren especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como especialmente preferentes.
De acuerdo con la invención, se prefieren muy especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como muy especialmente preferentes.
En una forma de realización preferente adicional de la invención, Q es Q1 y R7 , A, W, R2 , X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 5).
En una forma de realización preferente adicional de la invención, Q es Q2 y R7 , A, W, R2 , X e Y tienen los significados indicadoslos significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 6).
En una forma de realización preferente adicional de la invención, Q es Q3 y R7 , A, W, R2 , X e Y tienen los significados indicadoslos significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 7).
En una forma de realización preferente adicional de la invención, Q es Q4 y R7 , A, W, R2 , X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 8).
En una forma de realización preferente adicional de la invención, Q es Q5 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 9).
En una forma de realización preferente adicional de la invención, Q es Q6 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 10).
En una forma de realización preferente adicional de la invención, Q es Q7 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 11).
En una forma de realización preferente adicional de la invención, Q es Q8 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 12).
En una forma de realización preferente adicional de la invención, Q es Q9 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 13).
En una forma de realización preferente adicional de la invención, Q es Q10 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 14).
En una forma de realización preferente adicional de la invención, Q es Q11 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 15).
En una forma de realización preferente adicional de la invención, Q es Q12 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 16).
En una forma de realización preferente adicional de la invención, Q es Q13 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 17).
En una forma de realización preferente adicional de la invención, Q es Q14 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 18).
En una forma de realización preferente adicional de la invención, Q es Q15 y R7, A, W, R2, X e Y tienen los significados indicados en la configuración 1 o los indicados en la configuración 2 o los indicados en la configuración 3 o los indicados en la configuración 4 (configuración 19).
Ventajosamente, los derivados de piridina halogenados de la Fórmula (II) se pueden producir con el procedimiento de acuerdo con la invención con buenos rendimientos y en alta pureza. Una gran ventaja del procedimiento de acuerdo con la invención es su la regioselectividad. Debido a la muy buena tolerancia de los reactivos de zinc al grupo funcional, las bases de zinc son muy atractivas. Especialmente ventajosa es además la posibilidad de poder conducir acoplamientos Negishi incluso a temperaturas claramente más bajas, en donde en procedimientos de acuerdo con la invención se toleran incluso a temperaturas más altas grupos funcionales sensibles como los ésteres o los átomos de flúor, sin perjudicar la presente regioselectividad. Existen, además, los acoplamientos cruzados de Negishi dentro del contexto de un procedimiento de acuerdo con la invención también en presencia de orto sustituyentes en la estructura de piridina dan como resultado buenos rendimientos de producto diana, aunque tales acoplamientos con derivados de piridina sustituidos en la posición 2 son, hasta la fecha, conocidos por dar bajos rendimientos. De este modo, son posibles derivaciones adicionales y/o más flexibles del reactante y del producto, sin tener que alterar o adaptar constantemente las rutas de síntesis.
El procedimiento de acuerdo con la invención se puede explicar mediante el siguiente Esquema (I):
Esquema (I)
En este esquema, Q, W, R2, X e Y, así como los elementos estructurales adicionales presentes dado el caso dentro de las definiciones respectivas, tienen en cada caso los significados indicados anteriormente. Los compuestos indicados entre paréntesis son los intermediarios (Fórmula IIIa o IIIb), que se hacen reaccionar adicionalmente con un compuesto de la Fórmula (I) hasta dar el compuesto de la Fórmula (II). Por consiguiente, el procedimiento de acuerdo con la invención se puede dividir en las dos etapas de procedimiento a) y b), siendo la etapa a) la conversión del compuesto Q-H en el intermediario respectivo y, la etapa b), la conversión adicional del intermediario hasta dar el compuesto de la Fórmula (II).
Definiciones generales
En el contexto de la presente invención, el término halógeno (Hal), a menos que se defina de otro modo, abarca aquellos elementos que están seleccionados del grupo que consiste en flúor, cloro, bromo y yodo.
El término “haluros” describe compuestos en relación con la presente invención entre halógenos y elementos de otros grupos de la tabla periódica, que pueden dar lugar a sales de haluros (compuestos iónicos (sales) que consisten en aniones y cationes debido a la gran diferencia en electronegatividad entre los elementos involucrados y se mantienen unidos por interacciones electrostáticas) o haluros covalentes (compuestos covalentes en los que la diferencia en la electronegatividad no es tan grande como en los compuestos iónicos mencionados anteriormente, pero los enlaces pueden presentar una polaridad de carga), dependiendo del tipo de enlace químico. De acuerdo con la invención son especialmente preferentes las sales de haluro.
El término “pivaloilo” describe en el contexto de la presente invención el radical desprotonado del ácido piválico (X) que tiene la fórmula empírica (CH3)3CCO2H.
“O-pivaloilo” significa correspondientemente que el enlace del radical pivaloilo se efectúa a través del átomo de oxígeno desprotonado del grupo ácido.
A menos que se defina de manera diferente en otra parte, se entiende por el término “alquilo”, ya sea por sí solo o en combinación con otros términos, tal como por ejemplo haloalquilo, en el contexto de la presente invención un radical de un grupo hidrocarburo alifático saturado con 1 a 12 átomos de carbono, que puede estar ramificado o no ramificado. Son ejemplos de radicales alquilo C1-C12 metilo, etilo, n-propilo, isopropilo, n-butilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, iso-pentilo, neopentilo, terc-pentilo, 1-metilbutilo, 2-metilbutilo, 1 -etilpropilo, 1,2-dimetilpropilo, hexilo, n-heptilo, n-octilo, n-nonilo, n-decilo, n-undecilo y n-dodecilo. Entre estos radicales alquilo son especialmente preferentes los radicales alquilo C1-C6. En particular son preferentes los radicales alquilo C1-C4.
A menos que se defina de manera diferente en otra parte, se entiende por el término “alquenilo”, ya sea solo o en combinación con otros términos, de acuerdo con la invención un radical alquenilo C2-C12 de cadena lineal o ramificado, que presenta al menos un doble enlace, por ejemplo vinilo, alilo, 1-propenilo, isopropenilo, 1-butenilo, 2-butenilo, 3-butenilo, 1,3-butadienilo, 1-pentenilo, 2-pentenilo, 3-pentenilo, 4-pentenilo, 1,3-pentadienilo, 1-hexenilo, 2-hexenilo, 3-hexenilo, 4-hexenilo, 5-hexenilo y 1,4-hexadienilo. Entre estos, son preferentes los radicales alquenilo C2-C6 y son especialmente preferentes los radicales alquenilo C2-C4.
A menos que se defina de manera diferente en otra parte, se entiende por el término “alquinilo”, ya sea por sí solo o en combinación con otros términos, de acuerdo con la invención un radical alquinilo C2-C12 de cadena lineal o ramificado, que presenta al menos un triple enlace, por ejemplo etinilo, 1 -propinilo y propargilo. Entre estos, son preferentes los radicales alquinilo C3-C6 y son especialmente preferentes los radicales alquinilo C3-C4. El radical
alquinilo puede contener a este respecto también al menos un doble enlace.
A menos que se defina de manera diferente en otra parte, se entiende por el término “cidoalquilo”, ya sea por sí solo o en combinación con otros términos, de acuerdo con la invención un radical cicloalquilo C3-C8 , por ejemplo ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, cicloheptilo y ciclooctilo. Entre estos, son preferentes los radicales cicloalquilo C3-C6.
Por el término “alcoxi”, ya sea solo o en combinación con otros términos, por ejemplo haloalcoxi, se entiende en el presente caso un radical O-alquilo, en donde el término “alquilo” presenta el significado anterior.
Los radicales sustituidos con halógeno, por ejemplo haloalquilo, son mono- o polihalogenados hasta el número máximo de posibles sustituyentes. En el caso de la polihalogenación, los átomos de halógeno pueden ser idénticos o diferentes. A menos que se defina de manera diferente, a este respecto, el halógeno es flúor, cloro, bromo o yodo, en particular es flúor, cloro o bromo. Los grupos alquilo sustituidos con uno o más átomos de halógeno (-Hal) están, por ejemplo, seleccionados entre trifluorometilo (CF3), difluorometilo (CHF2), CF3CH2, ClCH2 o CF3CCh .
A menos que se indique lo contrario, los radicales dado el caso sustituidos pueden estar mono- o polisustituidos, en donde en el caso de las polisustituciones los sustituyentes pueden ser iguales o diferentes.
La síntesis de los compuestos Q-H como reactantes de un procedimiento de acuerdo con la invención es conocida en principio por el experto en la materia. Por ejemplo, los compuestos Q-H con Q = Q1, Q2, Q3, Q14 o Q15 pueden obtenerse a partir de los correspondientes derivados de piridindiamina por cierre de anillo hasta dar el compuesto de azol respectivo, como se describe, por ejemplo, en los documentos WO2014/100065 o WO2015/017610, preferentemente bajo condiciones ácidas. Las síntesis alternativas también son posibles, pero son más complejas y, como resultado, generalmente más desventajosas desde el punto de vista económico.
La conversión de los compuestos Q-H en compuestos de la Fórmula (IIIa) o (IIIb) en la primera etapa de procedimiento (etapa a)) se efectúa en presencia de una base de organozinc de la estructura (NR3R4)-Zn-R2 o (NR3R4)2-Zn, en la cual (configuración B-1)
R2 es como se definió anteriormente (configuración 1) (por lo tanto es halógeno u -O-pivaloilo),
R3 y R4 juntos forman un grupo -(CH2)5-, -(CH2)5- o -(CH2)2O(CH2)2 , en donde cada uno de estos grupos puede estar opcionalmente sustituido por 1,2, 3 o 4 radicales R5 y
R5 se selecciona del grupo que consiste en metilo, etilo, n-propilo e i-propilo.
Se prefiere que (configuración B-2)
R2 esté definido como antes como preferente (configuración 2) (por lo tanto sea halógeno, en particular cloro, bromo o yodo),
R3 y R4 juntos formen un grupo -(CH2)5-, en donde cada uno de estos grupos puede estar opcionalmente sustituido con 1, 2, 3 o 4 radicales R5 y
R5 se seleccione del grupo que consiste en metilo y etilo.
Es especialmente preferente que (configuración B-3)
R2 esté definido como antes como especialmente preferente (configuración 3) o como muy especialmente preferente (configuración 4) (y por lo tanto sea cloro) y
R3 y R4 juntos formen un grupo -(CH2)5-, que está sustituido con 4 grupos metilo.
Las definiciones de los radicales dadas anteriormente pueden combinarse entre sí de manera discrecional, es decir, entre los respectivos índices de preferencia.
En una configuración muy especialmente preferente de la base de acuerdo con la invención, el elemento estructural (NR3R4) es tetrametilpiperidina (TMP) de la Fórmula (IV).
(IV)
Las bases de organozinc muy especialmente preferentes de acuerdo con la invención se caracterizan, como resultado, porque el zinc está unido a TMP, en particular como haluro de zinc y de manera muy especialmente preferente como cloruro de zinc. Las bases de este tipo presentan la siguiente estructura de la Fórmula (V) (configuración B-4)
(V) (TMP)x ZnCh-x,
en donde x es el número 1 o 2. Entre estos, son preferentes a su vez bases con x = 1 (configuración B-5) de acuerdo con la Fórmula (VI):
En una forma de realización preferente adicional del procedimiento de acuerdo con la invención, la base de organozinc está presente junto con haluros alcalinos o alcalinotérreos. Esto se aplica en particular para bases de las Fórmulas (V) y (VI). Los haluros alcalinos o alcalinotérreos especialmente preferentes de este tipo son el cloruro de litio y el cloruro de magnesio, muy especialmente preferente es el cloruro de litio. Las bases de organozinc muy especialmente preferentes de acuerdo con la invención son TMP ZnClLiCl o (TMP)2 Zn2LiCl (configuración B-6). El más preferente es TMP ZnClLiCl (VII; configuración B-7).
Las combinaciones específicas de compuestos de las Fórmulas (I), (II) y (IIIa) o (IIIb) con bases de acuerdo con la invención se citan a continuación a modo de ejemplo en la Tabla 1, pudiendo emplearse en un procedimiento de acuerdo con la invención. Dado que, en algunas configuraciones, el elemento estructural R2 está presente tanto en la base de acuerdo con la invención como en el compuesto de la Fórmula (IIIa), la definición más estrecha se aplica a R2 en cada caso.
Tabla 1:
Con preferencia, la base de organozinc se usa en el procedimiento de acuerdo con la invención en una cantidad total de 0,5 a 5 equivalentes, preferentemente de 0,8 a 2 equivalentes, más preferentemente de 1 a 1,5 equivalentes y de manera especialmente preferente de 1,0 a 1,2 equivalentes, con respecto al compuesto Q-H. Una ventaja del procedimiento de acuerdo con la invención es, a este respecto, que la base organometálica se puede usar en cantidades aproximadamente estequiométricas.
Dependiendo de si el elemento estructural (NR3R4) está presente una o dos veces en la base organometálica utilizada, los compuestos intermediarios de la Fórmula (IIIa) o de la Fórmula (IIIb) se forman en la etapa de procedimiento a).
La conversión de los compuestos de la Fórmula (IIIa) o (IIIb) en compuestos de la Fórmula (II) en la segunda etapa de procedimiento (paso b)) se efectúa en presencia de un compuesto de la Fórmula (I)
en la que X, W e Y tienen los significados indicados anteriormente.
Durante el acoplamiento cruzado de Negishi, la reacción tiene lugar casi exclusivamente en la posición 2, ya que el yodo es el mejor grupo saliente en la estructura de piridina. De esta manera, se proporciona regioselectivamente el correspondiente derivado de piridina de la Fórmula (II).
Los compuestos de la Fórmula (I) se pueden obtener, por ejemplo, mediante la sustitución de un compuesto precursor correspondiente, es decir, un derivado de piridina con los radicales W e Y, con el radical X. Una sustitución de este tipo puede efectuarse, por ejemplo, mediante la metalación del compuesto precursor en presencia de bases de zinc y la reacción subsiguiente con halógeno elemental. Las metalizaciones de este tipo están descritas, por ejemplo, con piridinas sustituidas en la posición 4 en Angewandte Chemie 2007 (46), pág. 7685 y ss. u Organic Letters 2009 (11), pág. 1837 y ss.
Con preferencia, el compuesto de la Fórmula (I) se usa en el procedimiento de acuerdo con la invención en una cantidad total de 0,5 a 10,0 equivalentes, con preferencia de 0,8 a 5 equivalentes, más preferentemente de 1 a 2,5 equivalentes y de manera especialmente preferente de 1,0 a 1,5 equivalentes o de manera especialmente preferente de 1,5 a 2,0 equivalentes o de manera especialmente preferente de 1,0 a 2,0 equivalentes, con respecto al compuesto Q-H.
La conversión en la etapa de procedimiento b) se efectúa adicionalmente en presencia de un catalizador. Con preferencia, el catalizador es un compuesto de paladio o un compuesto de níquel. De manera especialmente preferente, el catalizador es un compuesto de paladio. De manera muy especialmente preferente se trata de tetrakis(trifenilfosfina)paladio(0), abreviado como Pd(PPh3)4, de la Fórmula (IX).
en moles de catalizador.
La conversión de acuerdo con la invención de los compuestos Q-H hasta dar compuestos de la Fórmula (IIIa) o (IIIb) y adicionalmente hasta dar compuestos de la Fórmula (II), se efectúa preferentemente en presencia de un disolvente orgánico en cada caso. Los disolventes útiles en principio incluyen todos los disolventes orgánicos que son inertes en las condiciones de reacción empleadas y en los que los compuestos que se van a convertir tienen una solubilidad suficiente. Los disolventes adecuados incluyen en particular: tetrahidrofurano (THF), 1,4-dioxano, dietil éter, diglime, metil terc-butil éter (MTBE), terc-amil metil éter (TAME), 2-metil-THF, tolueno, xilenos, mesitileno, carbonato de
etileno, carbonato de propileno, N,N-dimetilacetamida, N,N-dimetilformamida (DMF), N-metilpirrolidona (NMP), N-etil-2-pirrolidona (NEP), N-butil-2-pirrolidona (NBP); N,N'-dimetilpropilenurea (DMPU), halohidrocarburos e hidrocarburos aromáticos, en particular clorhidrocarburos tales como tetracloroetileno, tetracloroetano, dicloropropano, cloruro de metileno, diclorobutano, cloroformo, tetracloruro de carbono, tricloroetano, tricloroetileno, pentacloroetano, difluorobenceno, 1,2-dicloroetano, clorobenceno, bromobenceno, diclorobenceno, en particular 1,2-diclorobenceno, clorobenceno; 4-metoxibenceno, alifáticos fluorados y aromáticos tales como triclorotrifluoroetano, benzotrifluoruro y 4-clorobenzotrifluoruro. También es posible utilizar mezclas de disolventes, con preferencia mezclas de los disolventes mencionados anteriormente, tales como tetrahidrofurano (THF), 1,4-dioxano, dietil éter, diglime, metil terc-butil éter (MTBE), terc-amil metil éter (TAME), 2-metil-THF, tolueno, xilenos, mesitileno, dimetilformamida (DMF).
Los disolventes preferentes son THF, N,N-dimetilformamida (DMF), 1,4-dioxano, diglime, metil terc-butil éter (MTBE), terc-amil metil éter (TAME), 2-metil-THF, tolueno y 4-metoxibenceno.
Los disolventes especialmente preferentes son THF y N,N-dimetilformamida (DMF), muy especialmente preferente es THF.
El disolvente también puede estar desgasificado (libre de oxígeno).
Con preferencia se usa el mismo disolvente para ambas etapas de procedimiento a) y b). No obstante, son igualmente posibles configuraciones alternativas de acuerdo con la invención, en las que se utilizan diferentes disolventes para las etapas del procedimiento a) y b), en donde los disolventes se seleccionan entonces igualmente con preferencia de entre los disolventes mencionados anteriormente, y los disolventes respectivos especificados como preferentes, especialmente preferentes y muy especialmente preferentes son aplicables a la respectiva etapa de procedimiento a) o b).
La conversión en la etapa de procedimiento a) se realiza generalmente a una temperatura de entre 0°C y 80°C y de manera más preferente de entre 10°C y 70°C, de entre 15°C y 60°C, de entre 20°C y 50°C, de entre 20°C y 40°C, y aún de manera muy especialmente preferente de entre 20°C y 35°C, por ejemplo, a una temperatura ambiente o a 25°C.
La conversión en el procedimiento de la etapa b) se realiza generalmente a una temperatura de entre 40°C y 90°C y de manera más preferente de entre 50°C y 85°C, de entre 55°C y 80°C, de entre 60°C y 80°C y de manera muy especialmente preferente de entre 65°C y 75°C, por ejemplo a 65°C.
La reacción se realiza habitualmente a presión normal, pero también puede realizarse a presión elevada o reducida. El aislamiento de los compuestos deseados de la Fórmula (II) se puede efectuar, por ejemplo, mediante tratamiento acuoso en presencia de soluciones saturadas de cloruro de amonio o tiosulfato de sodio y/o cromatografía posterior. Dichos procedimientos son conocidos por el experto en la materia y también incluyen una cristalización a partir de un disolvente orgánico o mezcla de disolventes.
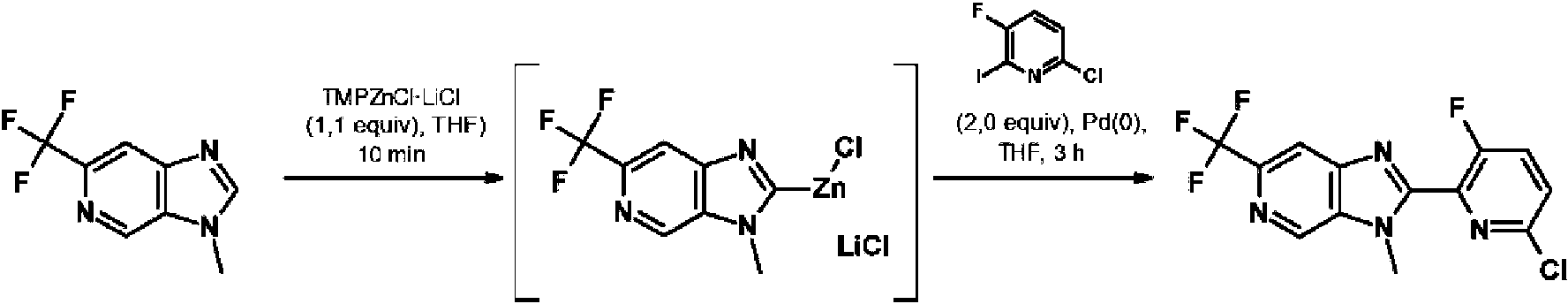
Un ejemplo de una forma de realización especialmente preferente del procedimiento de acuerdo con la invención se puede explicar mediante el siguiente esquema (II):
Esquema II:
En este esquema, A, W e Y tienen los significados indicados anteriormente. El compuesto indicado entre paréntesis representa el intermediario correspondiente de la Fórmula IIIa, el cual se convierte adicionalmente en el producto, un compuesto de la Fórmula (II). Ambas reacciones tienen lugar en THF como disolvente. “Equiv.” se refiere a la cantidad usada de equivalentes de TMPZnCl LiCl o compuesto de la Fórmula (I). Pd(0) es un compuesto de paladio como catalizador, con preferencia Pd(PPh3)4.
Un objeto adicional de la presente invención son compuestos de la estructura (configuración Q-H-1-1)
en donde
Q1 es N o CR6 ,
Q2 es N o CR6 ,
Q3 es N o C,
Q4 es O, S, N o NR7 ,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(Ci -C4), haloalquilo(Ci -C4), cianoalquilo(Ci -C4), hidroxialquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Cr C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltioalquilo(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4), o alquilcarbonilo(C1-C4)-alquilo(C1-C4) y
A es hidrógeno, ciano, halógeno, alquilo(Ci -C4), haloalquilo(Ci -C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), alcoxi(Ci -C4), halo(alcoxi(Ci -C4)), alcoxiimino(Ci -C4), alquiltio(Ci -C4), halo(alquiltio(Ci -C4)), sulfinilalquilo(Ci -C4), halo(alquilsulfinilo(Ci -C4)), sulfonilalquilo(Ci -C4), halo(sulfonilalquilo(Ci -C4)), sulfonilalquiloxi(Ci -C4), alquilcarbonilo(Ci -C4), halo(alquilcarbonilo(Ci -C4)), aminocarbonilo, alquilaminocarbonilo(Ci -C4), di-alquilo(Ci -C4)-aminocarbonilo, sulfonilalquilamino(Ci -C4), alquilamino(Ci -C4), dialquilamino(Ci -C4), aminosulfonilo, alquilo(Ci -C4)-aminosulfonilo o di-alquilamino(Ci -C4)-sulfonilo,
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros, en donde Q1 es carbono.
Una forma de realización alternativa son compuestos de la estructura (configuración Q-H-1-2)
en donde
Q1 es N o CR6,
Q2 es N o CR6,
Q3 es N o C,
Q4 es O, S, N o NR7,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(Ci -C4), haloalquilo(Ci -C4), cianoalquilo(Ci -C4), hidroxialquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(Ci -C4))-alquilo(Ci -C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(Ci -C4), haloalqueniloxi(C2-C4)-alquilo(Ci -C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(Ci -C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(Ci -C4)-alquilo(Ci -C4), sulfinilalquilo(Ci -C4)-alquilo(Ci -C4), sulfonilalquilo(Ci -C4)-alquilo(Ci -C4) o alquilcarbonilo(Ci -C4)-alquilo(Ci -C4),
R7 es alquilo(Ci -C4), haloalquilo(Ci -C4), cianoalquilo(Ci -C4), hidroxialquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(Ci -C4))-alquilo(Ci -C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(Ci -C4), haloalqueniloxi(C2-C4)-alquilo(Ci -C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(Ci -C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(Ci -C4)-alquilo(Ci -C4) o alquilcarbonilo(Ci -C4)-alquilo(Ci -C4) y
A es ciano, alquilo(Ci -C4), haloalquilo(Ci -C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), alcoxi(Ci -C4), halo(alcoxi(Ci -C4)), alcoxiimino(Ci -C4), alquiltio(Ci -C4), halo(alquiltio(Ci -C4)), sulfinilalquilo(Ci -C4), halo(alquilsulfinilo(Ci -C4)), sulfonilalquilo(Ci -C4), halo(alquilsulfonilo(Ci -C4)), alquiloxi(Ci -C4)-sulfonilo, alquilcarbonilo(Ci -C4), halo(alquilcarbonilo(Ci -C4)), aminocarbonilo, alquilaminocarbonilo(Ci -C4), di-alquilo(Ci -C4)aminocarbonilo, alquilsulfonilamino(Ci -C4), alquilamino(Ci -C4), di-alquilamino(Ci -C4), aminosulfonilo, alquilaminosulfonilo(Ci -C4) o di-alquilaminosulfonilo(Ci -C4).
o A es -O-CF2-O- y, junto con Qi y el átomo de carbono al que está unido, forma un anillo de cinco miembros, en donde Qi es carbono.
Con preferencia, Qi , Q2, Q3, Q4, Q5 y Q6 en la configuración Q-H-i-i y la configuración Q-H-i-2, representan no más de cinco átomos de nitrógeno en total y más preferentemente no más de cuatro átomos de nitrógeno en total.
Se explican a continuación los significados preferentes (configuración Q-H-2-i y Q-H-2-2), especialmente preferentes (configuración Q-H-3-i) y muy especialmente preferentes (configuración Q-H-4-i), de los radicales incluidos en los compuestos Q-H mencionados en las configuraciones anteriores Q-H-i-i y Q-H-i-2.
Configuración Q-H-2-i:
Q es preferentemente un elemento estructural de la serie de Qi a Qi5.
R7 es preferentemente alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), haloalcoxi(Ci-C4)-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), sulfinilalquilo(Ci-C4)-alquilo(Ci-C4), sulfonilalquilo(ci-C4)-alquilo(ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4) y
A es preferentemente flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo.
Configuración Q-H-2-2:
Q es preferentemente un elemento estructural de la serie de Qi a Qi5,
R7 es preferentemente alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), haloalcoxi(Ci-C4)-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), sulfinilalquilo(Ci-C4)-alquilo(Ci-C4), sulfonilalquilo(Ci-C4)-alquilo(Ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4),
A es preferentemente fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo.
Configuración Q-H-3-i:
Q es de manera especialmente preferente un elemento estructural de la serie de Q2, Q3, Qi0, Qi2, Q i4 y Qi5, R7 es de manera especialmente preferente alquilo(Ci -C4) o alcoxi(Ci -C4)-alquilo(Ci -C4) y
i8
A es de manera especialmente preferente trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2 , CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo.
Configuración Q-H-4-1:
Q es de manera especialmente preferente el elemento estructural Q3 o Q14,
R7 es de manera especialmente preferente metilo, etilo, n-propilo o isopropilo, en particular metilo y
A es de manera muy especialmente preferente trifluorometilo.
Las definiciones de los radicales dadas anteriormente pueden combinarse entre sí de manera discrecional, es decir, también entre los respectivos índices de preferencia.
De acuerdo con la invención, se prefieren aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como preferentes.
De acuerdo con la invención, se prefieren especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como especialmente preferentes.
De acuerdo con la invención, se prefieren muy especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como muy especialmente preferentes.
Un ejemplo de un compuesto muy especialmente preferente de este tipo es:
Q-X-1:
3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina
Q-X-2:
7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina
Un objeto adicional de la presente invención son compuestos de la Fórmula (IIIa)
en la que
Q es un elemento estructural
en donde el símbolo # indica el enlace con el resto de la molécula y
Q1 es N o CR6 ,
Q2 es N o CR6 ,
Q3 es N o C,
Q4 es O, S, N o NR7 ,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Cr C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)) alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
A es hidrógeno, ciano, halógeno, alquilo(C1-C4), haloalquilo(C1-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), alcoxi(C1-C4), halo(alcoxi(C1-C4)), alcoxiimino(C1-C4), alquiltio(C1-C4), halo(alquiltio(C1-C4)), alquilsulfinilo(C1-C4), halo(alquilsulfinilo(C1-C4)), sulfonilalquilo(C1-C4), halo(sulfonilalquilo(C1-C4)), sulfonilalquiloxi(C1-C4), alquilcarbonilo(C1-C4), halo(alquilcarbonilo(C1-C4)), aminocarbonilo, alquilaminocarbonilo(C1-C4), di-alquilo(C1-C4)-aminocarbonilo, alquilsulfonilamino(C1-C4), alquilamino(C1-C4), dialquilamino(C1-C4), aminosulfonilo, alquilaminosulfonilo(C1-C4) o di-alquilaminosulfonilo(C1-C4),
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros, en donde Q1 es carbono y
R2 es halógeno o -O-pivaloilo.
Con preferencia, Q1, Q2, Q3 , Q4, Q5 y Q6 representan no más de cinco átomos de nitrógeno en total y más preferentemente no más de cuatro átomos de nitrógeno en total.
Los significados preferentes, especialmente preferentes y muy especialmente preferentes de los radicales incluidos en los compuestos mencionados anteriormente de la Fórmula (IIIa) se explican a continuación.
Q es preferentemente un elemento estructural de la serie de Q1 a Q15,
R7 es preferentemente alquilo(C1-C4), haloalquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), haloalcoxi(C1-C4)-alquilo(C1-C4), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o carbonilalquilo(C1-C4)-alquilo(C1-C4),
A es preferentemente flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3 , CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo y
R2 es preferentemente halógeno, en particular cloro, bromo o yodo.
Q es de manera especialmente preferente un elemento estructural de la serie de Q2, Q3, Q10, Q12, Q14 y Q15, R7 es de manera especialmente preferente alquilo(Ci -C4) o alcoxi(Ci -C4)-alquilo(Ci -C4),
A es de manera especialmente preferente trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2 , CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo y
R2 es de manera especialmente preferente cloro.
Q es de manera muy especialmente preferente el elemento estructural Q3 o Q14,
R7 es de manera muy especialmente preferente metilo, etilo, n-propilo o isopropilo, en particular metilo,
A es de manera muy especialmente preferente trifluorometilo y
R2 es de manera muy especialmente preferente cloro.
Las definiciones de los radicales dadas anteriormente pueden combinarse entre sí de manera discrecional, es decir, también entre los respectivos índices de preferencia.
De acuerdo con la invención, se prefieren aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como preferentes.
De acuerdo con la invención, se prefieren especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como especialmente preferentes.
De acuerdo con la invención, se prefieren muy especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como muy especialmente preferentes.
Los compuestos de la Fórmula (IIIa) también pueden estar presentes por sí solos o como complejo de haluro alcalino o alcalinotérreo, con preferencia como complejo de cloruro de litio.
Son ejemplos de tales compuestos muy especialmente preferentes:
Un objeto adicional de la presente invención son compuestos de la Fórmula (IIIb)
Q-Zn-Q (IIIb)
en la que
Q es un elemento estructural
en donde el símbolo # indica el enlace con el resto de la molécula y
Q1 es N o CR6 ,
Q2 es N o CR6 ,
Q3 es N o C,
Q4 es O, S, N o NR7 ,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Cr C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)) alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4) y
A es hidrógeno, ciano, halógeno, alquilo(C1-C4), haloalquilo(C1-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), alcoxi(C1-C4), halo(alcoxi(C1-C4)), alcoxiimino(C1-C4), alquiltio(C1-C4), halo(alquiltio(C1-C4)), alquilsulfinilo(C1-C4), halo(alquilsulfinilo(C1-C4)), sulfonilalquilo(C1-C4), halo(alquilsulfonilo(C1-C4)), sulfonilalquiloxi(C1-C4), alquilcarbonilo(C1-C4), halo(alquilcarbonilo(C1-C4)), aminocarbonilo, alquilaminocarbonilo(C1-C4), di-alquilo(C1-C4)-aminocarbonilo, alquilsulfonilamino(C1-C4), alquilamino(C1-C4), dialquilamino(C1-C4), aminosulfonilo, alquilamino(C1-C4)sulfonilo o di-alquilamino(C1-C4)sulfonilo,
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros donde Q1 es carbono.
Con preferencia, Q1, Q2, Q3 , Q4, Q5 y Q6 representan no más de cinco átomos de nitrógeno en total y más preferentemente no más de cuatro átomos de nitrógeno en total.
Los significados preferentes, especialmente preferentes y muy especialmente preferentes de los radicales incluidos en los compuestos mencionados antes de la Fórmula (IIIb) se explican a continuación.
Q es preferentemente un elemento estructural de la serie de Q1 a Q15,
R7 es preferentemente alquilo(C1-C4), haloalquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), haloalcoxi(C1-C4)-alquilo(C1-C4), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o carbonilalquilo(C1-C4)-alquilo(C1-C4) y
A es preferentemente flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3 , CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo.
Q es de manera especialmente preferente un elemento estructural de la serie de Q2, Q3, Q10, Q12, Q14 o Q15, R7 es de manera especialmente preferente alquilo(C-i-C4) o alcoxi(C1-C4)-alquilo(C-i-C4) y
A es de manera especialmente preferente trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2 , CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo.
Q es de manera especialmente preferente el elemento estructural Q3 o Q14,
R7 es de manera especialmente preferente metilo, etilo, n-propilo o isopropilo, en particular metilo y
A es de manera especialmente preferente trifluorometilo.
Las definiciones de los radicales dadas anteriormente pueden combinarse entre sí de manera discrecional, es decir, también entre los respectivos índices de preferencia.
De acuerdo con la invención, se prefieren aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como preferentes.
De acuerdo con la invención, se prefieren especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como especialmente preferentes.
De acuerdo con la invención, se prefieren muy especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como muy especialmente preferentes.
Los compuestos de la Fórmula (IIIb) también pueden estar presentes solos o como complejo de haluro alcalino o alcalinotérreo, con preferencia como complejo de cloruro de litio.
Un objeto adicional de la presente invención son compuestos de la Fórmula (II)
(II)
en la que (configuración II-1-1):
Q es un elemento estructural
en donde el símbolo # indica el enlace con el resto de la molécula y
Q1 es N o CR6,
Q2 es N o CR6,
Q3 es N o C,
Q4 es O, S, N o NR7,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(Ci -C4), haloalquilo(Ci -C4), cianoalquilo(Ci -C4), hidroxialquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(Ci -C4))-alquilo(Ci -C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(Ci -C4), haloalqueniloxi(C2-C4)-alquilo(Ci -C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(Ci -C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(Ci -C4)-alquilo(Ci -C4), sulfinilalquilo(Ci -C4)-alquilo(Ci -C4), sulfonilalquilo(Ci -C4)-alquilo(Ci -C4) o alquilcarbonilo(Ci -C4)-alquilo(Ci -C4),
R7 es alquilo(Ci -C4), haloalquilo(Ci -C4), cianoalquilo(Ci -C4), hidroxialquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(Ci -C4))-alquilo(Ci -C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(Ci -C4), haloalqueniloxi(C2-C4)-alquilo(Ci -C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(Ci -C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(Ci -C4)-alquilo(Ci -C4), sulfinilalquilo(Ci -C4)-alquilo(Ci -C4), sulfonilalquilo(Ci -C4)-alquilo(Ci -C4) o alquilcarbonilo(Ci -C4)-alquilo(Ci -C4),
A es hidrógeno, ciano, halógeno, alquilo(Ci -C4), haloalquilo(Ci -C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), alcoxi(Ci -C4), halo(alcoxi(Ci -C4)), alcoxiimino(Ci -C4), alquiltio(Ci -C4), halo(alquiltio(Ci -C4)), alquilsulfinilo(Ci -C4), halo(alquilsulfinilo(Ci -C4)), sulfonilalquilo(Ci -C4), halo(alquilsulfonilo) (C1-C4)), sulfonilalquiloxi(Ci -C4), alquilcarbonilo(Ci -C4), halo(alquilcarbonilo(Ci -C4)), aminocarbonilo, alquilaminocarbonilo(Ci -C4), di-alquilo(Ci -C4)-aminocarbonilo, alquilsulfonilamino(Ci -C4), alquilamino(Ci -C4), dialquilamino(Ci -C4), aminosulfonilo, alquilamino(Ci -C4)-sulfonilo o di-alquilamino(Ci -C4)sulfonilo,
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros donde Q1 es carbono,
W es halógeno,
Y es halógeno, CO2R1 o NO2, en donde R1 es alquilo(Ci -C6) o haloalquilo(Ci -C6).
Una forma de realización alternativa (configuración II-1-2) son compuestos de la Fórmula (II) en la que:
Q es un elemento estructural
en donde el símbolo # indica el enlace con el resto de la molécula y
Q1 es N o CR6 ,
Q2 es N o CR6 ,
Q3 es N o C,
Q4 es O, S, N o NR7 ,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(Ci -C4), haloalquilo(Ci -C4), cianoalquilo(Ci -C4), hidroxialquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(Ci -C4))-alquilo(Ci -C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(Ci -C4), haloalqueniloxi(C2-C4)-alquilo(Ci -C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(Ci -C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(Ci -C4)-alquilo(Ci -C4), sulfinilalquilo(Ci -C4)-alquilo(Ci -C4), sulfonilalquilo(Ci -C4)-alquilo(Ci -C4) o alquilcarbonilo(Ci -C4)-alquilo(Ci -C4),
R7 es alquilo(Ci -C4), haloalquilo(Ci -C4), cianoalquilo(Ci -C4), hidroxialquilo(Ci -C4), alcoxi(Ci -C4)-alquilo(Ci -C4), halo(alcoxi(Ci -C4))-alquilo(Ci -C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(Ci -C4), haloalqueniloxi(C2-C4)
alquilo(Ci-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(Ci-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cidoalquilo(C3-C6)-cidoalquilo(C3-C6), alquilo(Ci-C4)-cicloalquilo(C3- Cq), halo(cicloalquilo(C3-C6)), alquiltio(Ci-C4)-alquilo(Ci-C4), sulfinilalquilo(Ci-C4)-alquilo(Ci-C4), sulfonilalquilo(Ci-C4)-alquilo(Ci-C4) o alquilcarbonilo(Ci-C4)-alquilo(Ci-C4),
A es hidrógeno, ciano, halógeno, alquilo(Ci-C4), haloalquilo(Ci-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-CQ), cidoalquilo(C3-CQ)-cidoalquilo(C3-CQ), alquilo(Ci-C4)-cicloalquilo(C3-CQ), alcoxi(Ci-C4), halo(alcoxi(Ci-C4)), alcoxiimino(Ci-C4), alquiltio(Ci-C4), halo(alquiltio(Ci-C4)), alquilsulfinilo(Ci-C4), halo(alquilsulfinilo(Ci-C4)), sulfonilalquilo(Ci-C4), halo(alquilsulfonilo(Ci-C4)), sulfonilalquiloxi(Ci-C4), alquilcarbonilo(Ci-C4), halo(alquilcarbonilo(Ci-C4)), aminocarbonilo, alquilaminocarbonilo(Ci-C4), di-alquilo(Ci-C4)-aminocarbonilo, alquilsulfonilamino(Ci-C4), alquilamino(Ci-C4), dialquilamino(Ci-C4), aminosulfonilo, alquilamino(Ci-C4)sulfonilo o di-alquilamino(Ci-C4)sulfonilo,
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros, en donde Q1 es carbono,
W es flúor o bromo,
Y es halógeno, CO2R1 o NO2, en donde R1 es alquilo(Ci-CQ) o haloalquilo(Ci-CQ).
Con preferencia, Q1, Q2, Q3, Q4, Q5 y Qq en la configuración II-1-1 y la configuración II-1-2 representan no más de cinco átomos de nitrógeno en total y más preferentemente no más de cuatro átomos de nitrógeno en total.
Los significados de los radicales preferentes (configuraciones II-2-1 y II-2-2), especialmente preferentes (configuraciones II-3-1 y II-3-2) y muy especialmente preferentes (configuración II-4-1), incluidos en la fórmula (II) mencionada anteriormente, se explican a continuación.
Configuración II-2-1:
Q es preferentemente un elemento estructural de la serie de Q1 a Q15,
R7 es preferentemente alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), haloalcoxi(Ci-C4)-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), sulfinilalquilo(Ci-C4)-alquilo(Ci-C4), sulfonilalquilo(Ci-C4)-alquilo(Ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4),
A es preferentemente flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es preferentemente flúor o bromo y
Y es preferentemente flúor, cloro, bromo, CO2R1 o NO2, en donde R1 es alquilo(Ci-C4).
Configuración II-2-2:
Q es preferentemente un elemento estructural de la serie de Q1 a Q15,
R7 es preferentemente alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), haloalcoxi(Ci-C4)-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), sulfinilalquilo(Ci-C4)-alquilo(Ci-C4), sulfonilalquilo(Ci-C4)-alquilo(Ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4),
A es preferentemente flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es preferentemente flúor o bromo y
Y es preferentemente flúor, cloro, bromo, CO2R1 o NO2, en donde R1 es alquilo(Ci-C4).
Configuración II-3-1:
Q es de manera especialmente preferente un elemento estructural de la serie de Q2, Q3, Q10, Q12, Q14 o Q15, R7 es de manera especialmente preferente alquilo(Ci-C4) o alcoxi(Ci-C4)-alquilo(Ci-C4),
A es de manera especialmente preferente trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2 , CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es de manera especialmente preferente flúor o cloro, en particular flúor y
Y es de manera especialmente preferente cloro, bromo, CO2R1 o NO2, donde R1 es alquilo(C-i-C4).
Configuración II-3-2:
Q es de manera especialmente preferente un elemento estructural de la serie de Q2, Q3, Q10, Q12, Q14 o Q15, R7 es de manera especialmente preferente alquilo(C1-C4) o alcoxi(C1-C4)-alquilo(C1-C4),
A es de manera especialmente preferente trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2 , CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es de manera especialmente preferente flúor e
Y es de manera especialmente preferente cloro, bromo, CO2R1 o NO2, en donde R1 es alquilo(C1-C4).
Configuración II-4-1:
Q es de manera especialmente preferente el elemento estructural Q3 o Q14,
R7 es de manera especialmente preferente metilo, etilo, n-propilo o isopropilo, en particular metilo,
A es de manera especialmente preferente trifluorometilo,
W es de manera especialmente preferente flúor e
Y es de manera especialmente preferente cloro, bromo, CO2R1 o NO2, en donde R1 es metilo.
Las definiciones de los radicales dadas anteriormente pueden combinarse entre sí de manera discrecional, es decir, entre los respectivos índices de preferencia.
De acuerdo con la invención, se prefieren aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como preferentes.
De acuerdo con la invención, se prefieren especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como especialmente preferentes.
De acuerdo con la invención, se prefieren muy especialmente aquellos compuestos en los que existe una combinación de los significados enumerados anteriormente como muy especialmente preferentes.
Son ejemplos de compuestos muy especialmente preferentes de este tipo:
2-(6-cloro-3-fluoropiridin-2-il)-3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina
2-(6-bromo-3-fluoropiridin-2-il)-3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina
Metil-5-fluoro-6-[3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridin-2-il]piridina-2-carboxilato
2-(3-fluoro-6-nitropiridin-2-il)-3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina
6-(6-doro-3-fluoropiridin-2-il)-7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina
Metil-5-fluoro-6-[7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazin-6-il]piridina-2-carboxilato
6-(6-Bromo-3-fluoropiridin-2-il)-7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina
La presente invención se explica en detalle mediante los ejemplos que siguen, aunque los ejemplos no deben interpretarse de tal manera que limiten la invención.
Ejemplo 1
Síntesis de 3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazor4.5-clp¡r¡d¡na
La N3-metil-6-(trifluorometil)piridina-3,4-diamina (500 mg, 2,6 mmol), disuelta en ácido fórmico (4 ml, 106 mmol), se calentó con microondas durante 1 hora a 150°C. Después del tratamiento habitual mediante la adición de una solución de cloruro de amonio saturada, la mezcla de reacción se extrajo con acetato de etilo, las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo 3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina (480 mg, 91 %) como sólido blanco. HPLC-MS: logP=1,09; masa (m/z+1): 202,0; RMN de 1H (D6-DMSO): 89,14 (s, 1H), 8,61 (s, 1H), 8,19 (s, 1H), 4,02 (s, 3H).
Ejemplo 2
Síntesis de 2-(6-cloro-3-fluorop¡r¡d¡n-2-¡n-3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazor4.5-clp¡r¡d¡na:
La3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina (201 mg, 1,0 mmol), disuelta en THF (2 ml) se mezcló con TMPZnClLiCl (1,31 M en THF, 0,84 ml, 1,1 mmol) a 25°C en argón; esta solución de reacción se agitó durante 10 min. Posteriormente, se agregaron 6-cloro-3-fluoro-2-yodopiridina (515 mg, 2 mmol en 4 ml de THF) y tetrakis(trifenilfosfina)paladio(0) (115 mg, 0,1 mmol) a 25°C y la solución se siguió agitando durante 3 horas a 65°C. Después del tratamiento habitual mediante la adición de solución de cloruro de amonio saturada, la mezcla de reacción se extrajo con acetato de etilo, las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo 2-(6-cloro-3-fluoropiridin-2-il)-3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina (177 mg, 52 %) como sólido blanco. Hp Lc-MS: logP = 2,38; masa (m/z): 331,0; RMN de 1H (D6-DMSO): 8 9,29 (s, 1H), 8,32 (s, 1H), 8,19 (t, 1H), 7,91 (dd, 1H), 4,14 (s, 3H).
Ejemplo 3
Síntesis de met¡l-5-fluoro-6-r3-met¡l-6-(tr¡fluoromet¡n-3H-¡m¡dazor4.5-clp¡r¡d¡n-2-¡llp¡r¡d¡na-2-carbox¡lato
La 3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina (201 mg, 1,0 mmol) disuelta en THF (2 ml) se mezcló con TMPZnClLiCl (1,31 M en THF, 0,84 ml, 1,1 mmol) a 25°C en argón; esta solución de reacción se agitó durante 10 min. Posteriormente, se agregaron metil-5-fluoro-6-yodopiridina-2-carboxilato (562 mg, 2 mmol en 4 ml de THF) y tetrakis(trifenilfosfina)paladio(0) (115 mg, 0,1 mmol) a 25°C y la solución se siguió agitando durante 3 horas a 65°C. Después del tratamiento habitual mediante la adición de una solución de cloruro de amonio saturada, la mezcla de reacción se extrajo con acetato de etilo, las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo metil-5-fluoro-6-[3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridin-2-il]piridina-2-carboxilato (160 mg, 45 %) como sólido blanco. HPLC-MS: logP = = 2,03; masa (m/z+1): 355,1; RMN de 1H (D6-DMSO): 9,30 (s, 1H), 8,38 (dd, 1H), 8,34 (s, 1H), 8,24 (dd, 1H), 4,19 (s, 3H), 3,93 (s, 3H).
Ejemplo 4
Síntesis de 2-(6-bromo-3-fluorop¡r¡d¡n-2-¡n-3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazor4.5-clp¡r¡d¡na:
La 3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina (100 mg, 0,5 mmol), disuelta en THF (2 ml), se mezcló con TMPZnClLiCl (1,31 M en THF, 0,52 ml, 0,55 mmol) a 25°C en argón; esta solución de reacción se agitó durante 10 min. Posteriormente, se agregaron 6-bromo-3-fluoro-2-yodopiridina (301 mg, 1 mmol en 2 ml de THF) y tetrakis(trifenilfosfina)paladio(0) (58 mg, 0,05 mmol) a 25°C y la solución se siguió agitando durante 3 horas a 65°C. Después del tratamiento habitual mediante la adición de una solución de cloruro de amonio saturada, la mezcla de reacción se extrajo con acetato de etilo, las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo 2-(6-bromo-3-fluoropiridin-2-il)-3-metil-6-(trifluorometil)-3H-imidazo[4,5-c]piridina (101 mg, 54%) como sólido blanco. HPLC-MS: logP = 2,51; masa (m/z+1): 376,9; RMN de 1H (D6-DMSO): 89,29 (s, 1H), 8,33 (s, 1H), 8,05 (m, 2H), 4,13 (s, 3H).
Ejemplo 5
Síntesis de 7-met¡l-3-(tr¡fluoromet¡l)-7H-¡m¡dazor4.5-clp¡r¡daz¡na
La N3-metil-6-(trifluorometil)piridazina-3,4-diamina (192 mg, 1,0 mmol), disuelta en ácido fórmico (0,4 ml, 106 mmol), se calentó con microondas durante 2 horas a 150°C. Después del tratamiento habitual mediante la adición de una solución de cloruro de amonio saturada, la mezcla de reacción se extrajo con acetato de etilo, las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo 7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina (149 mg, 74 %) como sólido blanco. HPLC-MS: logP = 0,95; masa (m/z+1): 203,1; RMN de 1H (D6-DMSO): 88,97 (s, 1H), 8,62 (s, 1H), 4,08 (s, 3H).
Ejemplo 6
Síntesis de 6-(6-cloro-3-fluorop¡r¡d¡n-2-¡n-7-met¡l-3-(tr¡fluoromet¡l)-7H-¡m¡dazor4.5-clp¡r¡daz¡na:
La 7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina (202 mg, 1,0 mmol), disuelta en THF (2 ml), se mezcló con TMPZnClLiCl (1,31 M en THF, 0,84 ml, 1,1 mmol) a 25°C en argón; esta solución de reacción se agitó durante 10 min. Posteriormente, se agregaron 6-cloro-3-fluoro-2-yodopiridina (515 mg, 2 mmol en 4 ml de THF) y tetrakis(trifenilfosfina)paladio(0) (115 mg, 0,1 mmol) a 25°C y la solución se siguió agitando durante 3 horas a 65°C. Después del tratamiento habitual mediante la adición de una solución de cloruro de amonio saturada, la mezcla de reacción se extrajo con acetato de etilo y las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo 6-(6-cloro-3-fluoropiridin-2-il)-7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina (125 mg, 38%) como sólido blanco. HPLC-MS: logP = 2,46; masa (m/z+1): 332,0; Rm N de 1H (D6-DMSO): 88,77 (s, 1H), 8,23 (t, 1H), 7,98 (dd, 1H), 4,25 (s, 3H).
Ejemplo 7
Síntesis de met¡l-5-fluoro-6-r7-met¡l-3-(tr¡fluoromet¡n-7H-¡m¡dazor4.5-clp¡r¡daz¡n-6-¡llp¡r¡d¡n-2-carboxilato La 7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina (202 mg, 1,0 mmol), disuelta en THF (2 ml), se mezcló con TMPZnCl LiCl (1,31 M en THF, 0,84 ml, 1,1 mmol) a 25°C en argón; esta solución de reacción se agitó durante 10 min. Posteriormente, se agregó metil-5-fluoro-6-yodopiridina-2-carboxilato (562 mg, 2 mmol en 4 ml de THF) y tetrakis(trifenilfosfina)paladio(0) (115 mg, 0,1 mmol) a 25°C y la solución se siguió agitando durante 3 a 65°C horas. Después del tratamiento habitual mediante la adición de una solución de cloruro de amonio saturada, la mezcla de reacción se extrajo con acetato de etilo, las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo metil-5-fluoro-6-[7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazin-6-il]piridina-2-carboxilato (208 mg, 59 %) como sólido blanco. Hp Lc -MS: logP = = 2,09; masa (m/z+1): 356,0; RMN 1H (D6-DMSO): 8,78 (s, 1H), 8,43 (dd, 1H), 8,28 (t, 1H), 4,32 (s, 3H), 3,96 (s, 3H).
Ejemplo 8
Síntesis de 6-(6-bromo-3-fluorop¡r¡d¡n-2-¡n-7-met¡l-3-(tr¡fluoromet¡l)-7H-¡m¡dazor4.5-clp¡r¡daz¡na:
La 7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina (340 mg, 1,7 mmol), disuelto en THF (2 ml) se mezcló con TMPZnClLiCl (1,31 M en THF, 1,41 ml, 1,85 mmol) a 25°C en argón; esta solución de reacción se agitó durante 10 min. Posteriormente, se agregaron 6-bromo-3-fluoro-2-yodopiridina (1,016 g, 3,36 mmol en 4 ml de THF) y tetrakis(trifenilfosfina)paladio(0) (195 mg, 0,16 mmol) a 25°C y la solución se siguió agitando durante 3 horas a 65°C. Después del tratamiento habitual mediante la adición de una solución de cloruro de amonio saturada, la mezcla de
reacción se extrajo con acetato de etilo, las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de la bomba de membrana. Después de la purificación por cromatografía en columna (acetato de etilo/ciclohexano), se obtuvo 6-(6-bromo-3-fluoropiridin-2-il)-7-metil-3-(trifluorometil)-7H-imidazo[4,5-c]piridazina (408 mg, 62%) como sólido blanco. HPLC-MS: logP = 2,58; masa (m/z+1): 375,9; RMN de 1H (D6-DMSO): 58,77 (s, 1H), 8,10 (m, 2H), 4,25 (s, 3H).
La presente invención se refiere a un procedimiento para producir derivados de piridina halogenados de la Fórmula (11) partiendo de compuestos de la estructura Q-H a través de intermediarios de la Fórmula (Illa) o (IlIb)
en las que
Q es un elemento estructural
en donde el símbolo # indica el enlace con el resto de la molécula y A, Q1, Q2, Q3, Q4, Q5 y Q6 tienen los significados indicados en la descripción,
W es halógeno,
Y es halógeno o CO2R1, en donde R1 es alquilo(C1-C6) o haloalquilo(C1-C6) y
R2 es halógeno.
Claims (18)
1. Procedimiento para producir compuestos de la Fórmula (II)
(II)
en la que
Q es un elemento estructural
en donde el símbolo # indica el enlace con el resto de la molécula y
Q1 es N o CR6 ,
Q2 es N o CR6 ,
Q3 es N o C,
Q4 es O, S, N o NR7 ,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Cr C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)) alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4) y
A es hidrógeno, ciano, halógeno, alquilo(Ci -C4), haloalquilo(Ci -C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Ci -C4)-cicloalquilo(C3-C6), alcoxi(Ci -C4), halo(alcoxi(Ci -C4)), alcoxiimino(Ci -C4), alquiltio(Ci -C4), halo(alquiltio(Ci -C4)), alquilsulfinilo(Ci -C4), halo(alquilsulfinilo(Ci -C4)), sulfonilalquilo(Ci -C4), haloalquilsulfonilo(Ci -C4), sulfonilalquiloxi(Ci -C4), alquilcarbonilo(Ci -C4), halo(alquilcarbonilo(Ci -C4)), aminocarbonilo, alquilaminocarbonilo(Ci -C4), di-alquilo(Ci -C4)-aminocarbonilo, alquilamino(Ci -C4)sulfonilo, alquilamino(Ci -C4), dialquilamino(Ci -C4), aminosulfonilo, alquilamino(Ci -C4)sulfonilo o di-alquilamino(Ci -C4)sulfonilo,
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros, en donde Q1 es carbono,
W es halógeno,
Y es halógeno, CO2R1 o NO2, en donde R1 es alquilo(C1-C6) o haloalquilo(C1-C6),
caracterizado porque, en una primera etapa de procedimiento a), un compuesto Q-H, en el que Q tiene el significado mencionado antes,
se hace reaccionar con una base de organozinc de la estructura (NR3R4)-Zn-R2 o (NR3R4)2-Zn, en la que:
R2 es halógeno o -O-pivaloilo y
R3 y R4 juntos forman un grupo -(CH2)4-, -(CH2)5- o -(CH2)2O(CH2)2-, en donde cada uno de estos grupos puede estar opcionalmente sustituido por 1,2, 3 o 4 radicales R5 y R5está seleccionado del grupo que consiste en metilo, etilo, n-propilo e i-propilo,
hasta dar un compuesto de la Fórmula (IIIa) o de la Fórmula (IIIb),
en la que Q y R2 tienen, en cada caso, los significados mencionados anteriormente,
y este compuesto de la Fórmula (IIIa) o (IIIb) se hace reaccionar en una segunda etapa de procedimiento b) con un compuesto de la Fórmula (I)
en la que X es halógeno y W e Y tienen en cada caso los significados mencionados anteriormente, en presencia de un catalizador hasta dar el compuesto de la Fórmula (II).
2. Procedimiento de acuerdo con la reivindicación 1, caracterizado porque
Q es un elemento estructural de la serie de Q1 a Q15,
R7 es alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), halo(alcoxi(Ci-C4)-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), alquilsulfinilo(Ci-C4)-alquilo(Ci-C4), alquilsulfonilo(Ci-C4)-alquilo(Ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4),
A es flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es flúor, cloro o bromo,
R2 es halógeno, en particular cloro, bromo o yodo,
X es halógeno, en particular bromo o yodo e
Y es flúor, cloro, bromo, CO2R1 o NO2 , en donde R1 es alquilo(Ci-C4).
3. Procedimiento de acuerdo con una de las reivindicaciones 1 o 2, caracterizado porque
Q es un elemento estructural de la serie de Q2, Q3, Q10, Q12, Q14 o Q15,
R7 es alquilo(Ci-C4) o alcoxi(Ci-C4)-alquilo(Ci-C4),
A es trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3 , CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es flúor o cloro, en particular flúor,
R2 es cloro,
X es bromo o yodo, en particular yodo e
Y es cloro, bromo, CO2R1 o NO2, en donde R1 es alquilo (C1-C4).
4. Procedimiento de acuerdo con una de las reivindicaciones 1 a 3, caracterizado porque
Q es el elemento estructural Q3 o Q14,
R7 es metilo, etilo, n-propilo o isopropilo, en particular metilo,
A es trifluorometilo,
W es flúor,
R2 es cloro,
X es yodo e
Y es cloro, bromo, CO2R1 o NO2, en donde R1 es metilo.
5. Procedimiento de acuerdo con una de las reivindicaciones 1 a 4, caracterizado porque
R3 y R4 juntos forman un grupo -(CH2)5-, que está sustituido con 4 grupos metilo.
6. Procedimiento de acuerdo con una de las reivindicaciones 1 a 5, caracterizado porque en el caso de la base de organozinc se trata de un compuesto de la Fórmula (V):
(V) (TMP)x ZnCl2-x,
en donde x es el número 1 o 2.
7. Procedimiento de acuerdo con una de las reivindicaciones 1 a 6, caracterizado porque la base de organozinc está presente unida con un haluro alcalino o haluro alcalinotérreo, con preferencia cloruro de litio o cloruro de magnesio.
8. Procedimiento de acuerdo con una de las reivindicaciones 1 a 7, caracterizado porque la base de organozinc se utiliza en una cantidad total de 0,5 a 5 equivalentes, con respecto al compuesto Q-H.
9. Procedimiento de acuerdo con una de las reivindicaciones 1 a 8, caracterizado porque el compuesto de la Fórmula (I) se utiliza en una cantidad total de 0,5 a 10,0 equivalentes, con respecto al compuesto Q-H.
10. Procedimiento de acuerdo con una de las reivindicaciones 1 a 9, caracterizado porque en el caso del catalizador se trata de un compuesto de paladio.
11. Procedimiento de acuerdo con una de las reivindicaciones 1 a 10, caracterizado porque en el caso del catalizador se trata de tetrakis(trifenilfosfina)paladio(0).
12. Procedimiento de acuerdo con una de las reivindicaciones 1 a 11, caracterizado porque se realiza en presencia de un disolvente, que está seleccionado del grupo que consiste en tetrahidrofurano (THF), 1,4-dioxano, dietil éter, diglime, metil terc-butil éter (MTBE), terc-amil metil éter (TAME), 2-metil-THF, tolueno, xilenos, mesitileno, carbonato de etileno, carbonato de propileno, N,N-dimetilacetamida, N,N-dimetilformamida (DMF), N-metilpirrolidona (NMP), N-etil-2-pirrolidona (NEP), N-butil-2-pirrolidona (NBP); N,N'-dimetilpropilenurea (DMPU), halohidrocarburo, hidrocarburo aromático, clorohidrocarbono, tetracloroetileno, tetracloroetano, dicloropropano, cloruro de metileno, diclorobutano, cloroformo, tetracloruro de carbono, tricloroetano, tricloroetileno, pentacloroetano, difluorobenceno, 1,2-dicloroetano, clorobenceno, bromobenceno, diclorobenceno, 1,2-diclorobenceno, clorotolueno, triclorobenceno, 4-metoxibenceno,
alifático fluorado, aromático fluorado, triclorotrifluoroetano, benzotrifluoruro y 4-clorobenzotrifluoruro, o una mezcla de al menos dos de estos disolventes entre sí.
13. Procedimiento de acuerdo con la reivindicación 12, caracterizado porque el disolvente es THF o N,N-dimetilformamida (DMF).
14. Procedimiento de acuerdo con una de las reivindicaciones 1 a 13, caracterizado porque la etapa de procedimiento a) se realiza a una temperatura de entre 0°C y 80°C.
15. Procedimiento de acuerdo con una de las reivindicaciones 1 a 13, caracterizado porque la etapa de procedimiento b) se realiza a una temperatura de entre 40°C y 90°C.
16. Compuesto de la estructura
en donde
Q1 es N o CR6,
Q2 es N o CR6,
Q3 es N o C,
Q4 es O, S, N o NR7,
Q5 es N o C,
Q6 es N o CH,
R6 es hidrógeno, alquilo(C-i-C4), haloalquilo(C1-C4), cianoalquilo(C-i-C4), hidroxialquilo(C1-C4), alcoxi(C-i-C4)-alquilo(C-i-C4), halo(alcoxi(C-i-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(Cr C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), halo(alcoxi(C1-C4))-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), halo(alqueniloxi(C2-C4))-alquilo(C1-C4), halo(alquenilo(C2-C4)), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halo(cicloalquilo(C3-C6)), alquiltio(C1-C4)-alquilo(C1-C4), sulfinilalquilo(C1-C4)-alquilo(C1-C4), sulfonilalquilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4) y
A es ciano, alquilo(C1-C4), haloalquilo(C1-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), halo(alquinilo(C2-C4)), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), alcoxi(C1-C4), halo(alcoxi(C1-C4)), alcoxiimino(C1-C4), alquiltio(C1-C4), halo(alquiltio(C1-C4)), alquilsulfinilo(C1-C4), halo(alquilsulfinilo(C1-C4)), sulfonilalquilo(C1-C4), halo(alquilo(C1-C4))sulfonilo, alquiloxi(C1-C4)sulfonilo, alquilcarbonilo(C1-C4), halo(alquilcarbonilo(C1-C4)), aminocarbonilo, alquilaminocarbonilo(C1-C4), di-alquilo(Cr C4)-aminocarbonilo, alquilsulfonilamino(C1-C4), alquilamino(C1-C4), di-alquilamino(C1-C4), aminosulfonilo, alquilaminosulfonilo(C1-C4) o di-alquilaminosulfonilo(C1-C4),
o A es -O-CF2-O- y, junto con Q1 y el átomo de carbono al que está unido, forma un anillo de cinco miembros, en donde Q1 es carbono.
17. Compuesto de la Fórmula (Illa)
(Illa)
en la que
Q es un elemento estructural de la serie de Q1 a Q15,
R7 es alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), halo(alcoxi(Ci-C4))-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), alquilsulfinilo(Ci-C4)-alquilo(Ci-C4), alquilsulfonilo(Ci-C4)-alquilo(Ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4),
A es flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo y
R2 es halógeno, en particular cloro, bromo o yodo.
18. Compuesto de la Fórmula (IIIb)
Q-Zn-Q (IIIb)
en la que
Q es un elemento estructural de la serie de Q1 a Q15,
R7 es alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), halo(alcoxi(Ci-C4))-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), alquilsulfinilo(Ci-C4)-alquilo(Ci-C4), alquilsulfonilo(Ci-C4)-alquilo(Ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4) y
A es flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo.
i9. Compuesto de la Fórmula (II)
(II)
en la que
Q es un elemento estructural de la serie de Qi a Qi5,
R7 es alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), halo(alcoxi(Ci-C4))-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), alquilsulfinilo(Ci-C4)-alquilo(Ci-C4), alquilsulfonilo(Ci-C4)-alquilo(Ci-C4) o carbonilalquilo(Ci-C4)-alquilo(Ci-C4),
A es flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
W es flúor o bromo e
Y es flúor, cloro, bromo, CO2R'1 o NO2 , en donde Ri es alquilo(Ci-C4).
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16184368 | 2016-08-16 | ||
| PCT/EP2017/070184 WO2018033448A1 (de) | 2016-08-16 | 2017-08-09 | Verfahren zur herstellung von 2-(3,6-dihalopyridin-2-yl)-3h-imidazol[4,5-c]pyridinderivaten und verwandten verbindungen durch umsetzung des 3h-imidazol[4,5-c]pyridinderivats mit einer metallorganischen zink-amin base |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2833251T3 true ES2833251T3 (es) | 2021-06-14 |
Family
ID=56737974
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17746524T Active ES2833251T3 (es) | 2016-08-16 | 2017-08-09 | Procedimiento para producir derivados de 2-(3,6-dihalopiridin-2-il)-3h-imidazol[4,5-c]piridina y compuestos relacionados por reacción del derivado de piridina 3h-imidazol[4,5-c] con una base organometálica de zinc-amina |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US10875858B2 (es) |
| EP (1) | EP3500568B1 (es) |
| JP (1) | JP7098600B2 (es) |
| KR (1) | KR102420235B1 (es) |
| CN (1) | CN109819653A (es) |
| BR (1) | BR112019003174B1 (es) |
| DK (1) | DK3500568T3 (es) |
| ES (1) | ES2833251T3 (es) |
| IL (1) | IL264780B (es) |
| MX (1) | MX2019001917A (es) |
| TW (1) | TWI743165B (es) |
| WO (1) | WO2018033448A1 (es) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI820231B (zh) | 2018-10-11 | 2023-11-01 | 德商拜耳廠股份有限公司 | 用於製備經取代咪唑衍生物之方法 |
| IL282036B2 (en) | 2018-10-11 | 2024-03-01 | Bayer Ag | Process for preparing imidazole derivatives |
| EP3636645A1 (de) * | 2018-10-11 | 2020-04-15 | Bayer Aktiengesellschaft | Verfahren zur herstellung schwefel-substituierter pyridinderivate |
| WO2025026738A1 (en) | 2023-07-31 | 2025-02-06 | Bayer Aktiengesellschaft | 6-[5-(ethylsulfonyl)-1-methyl-1h-imidazol-4-yl]-7-methyl-3-(pentafluoroethyl)-7h-imidazo[4,5-c]pyridazine derivatives as pesticides |
Family Cites Families (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2004911A1 (en) * | 1988-12-22 | 1990-06-22 | Mitsuaki Ohta | 4,5,6,7-tetrahydrobenzimidazole derivatives |
| AU705511B2 (en) * | 1995-08-10 | 1999-05-27 | Bayer Aktiengesellschaft | Halobenzimidazoles and their use as microbicides |
| PA8535601A1 (es) | 2000-12-21 | 2002-11-28 | Pfizer | Derivados benzimidazol y piridilimidazol como ligandos para gabaa |
| JP2008512438A (ja) * | 2004-09-10 | 2008-04-24 | ファイザー・プロダクツ・インク | 療法用ジフェニルエーテル系リガンド |
| WO2006065703A1 (en) | 2004-12-13 | 2006-06-22 | Sunesis Pharmaceuticals, Inc. | Pyrido pyrimidinones, dihydro pyrimido pyrimidinones and pteridinones useful as raf kinase inhibitors |
| PT1966214T (pt) | 2005-12-21 | 2017-02-03 | Janssen Pharmaceutica Nv | Triazolpiridazinas como moduladores de tirosina quinase |
| WO2011027249A2 (en) | 2009-09-01 | 2011-03-10 | Pfizer Inc. | Benzimidazole derivatives |
| WO2012088266A2 (en) * | 2010-12-22 | 2012-06-28 | Incyte Corporation | Substituted imidazopyridazines and benzimidazoles as inhibitors of fgfr3 |
| PH12013501178A1 (en) | 2010-12-24 | 2013-07-15 | Sumitomo Chemical Co | Fused heterocyclic compound and use for pest control thereof |
| BR112015010207A2 (pt) * | 2012-11-09 | 2017-07-11 | Sumitomo Chemical Co | método para promover o crescimento de plantas |
| ES2707305T3 (es) | 2012-12-20 | 2019-04-03 | Merck Sharp & Dohme | Imidazopiridinas sustituidas como inhibidores de HDM2 |
| CN105358555B (zh) * | 2013-07-01 | 2018-01-30 | 住友化学株式会社 | 稠合杂环化合物及其有害生物防除用途 |
| PT3027601T (pt) | 2013-07-31 | 2018-01-08 | Gilead Sciences Inc | Inibidores de syk |
| AR099677A1 (es) * | 2014-03-07 | 2016-08-10 | Sumitomo Chemical Co | Compuesto heterocíclico fusionado y su uso para el control de plagas |
| WO2015171951A1 (en) * | 2014-05-07 | 2015-11-12 | The Regents Of The University Of Colorado, A Body Corporate | 2-(4-aryl-1h-imidazol-1-yl)aniline compounds |
| WO2015198859A1 (ja) * | 2014-06-26 | 2015-12-30 | 住友化学株式会社 | 縮合複素環化合物 |
| UY36547A (es) * | 2015-02-05 | 2016-06-01 | Bayer Cropscience Ag | Derivados heterocíclicos condensados bicíclicos sustituidos por 2-(het)arilo como pesticidas |
| UY36548A (es) * | 2015-02-05 | 2016-06-01 | Bayer Cropscience Ag | Derivados heterocíclicos condensados bicíclicos sustituidos por 2-(het)arilo como pesticidas |
| JP2016102104A (ja) * | 2015-09-08 | 2016-06-02 | 住友化学株式会社 | 有害生物防除組成物およびその用途 |
| KR102471278B1 (ko) * | 2016-09-14 | 2022-11-25 | 바이엘 크롭사이언스 악티엔게젤샤프트 | 할로겐화 바이사이클릭 화합물의 제조 방법 |
| ES2884902T3 (es) * | 2017-05-02 | 2021-12-13 | Bayer Ag | Derivados de heterociclos condensados sustituidos con 2-(het)arilo como pesticidas |
-
2017
- 2017-08-09 EP EP17746524.2A patent/EP3500568B1/de active Active
- 2017-08-09 WO PCT/EP2017/070184 patent/WO2018033448A1/de not_active Ceased
- 2017-08-09 JP JP2019508264A patent/JP7098600B2/ja active Active
- 2017-08-09 MX MX2019001917A patent/MX2019001917A/es unknown
- 2017-08-09 CN CN201780061786.XA patent/CN109819653A/zh active Pending
- 2017-08-09 ES ES17746524T patent/ES2833251T3/es active Active
- 2017-08-09 KR KR1020197006835A patent/KR102420235B1/ko active Active
- 2017-08-09 US US16/325,666 patent/US10875858B2/en active Active
- 2017-08-09 DK DK17746524.2T patent/DK3500568T3/da active
- 2017-08-09 BR BR112019003174-0A patent/BR112019003174B1/pt active IP Right Grant
- 2017-08-14 TW TW106127424A patent/TWI743165B/zh active
-
2019
- 2019-02-11 IL IL264780A patent/IL264780B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| KR102420235B1 (ko) | 2022-07-12 |
| KR20190038890A (ko) | 2019-04-09 |
| JP7098600B2 (ja) | 2022-07-11 |
| IL264780B (en) | 2021-09-30 |
| CN109819653A (zh) | 2019-05-28 |
| JP2019524828A (ja) | 2019-09-05 |
| EP3500568A1 (de) | 2019-06-26 |
| WO2018033448A1 (de) | 2018-02-22 |
| BR112019003174A2 (pt) | 2019-06-18 |
| US10875858B2 (en) | 2020-12-29 |
| DK3500568T3 (da) | 2020-12-14 |
| BR112019003174B1 (pt) | 2022-10-25 |
| US20190202829A1 (en) | 2019-07-04 |
| EP3500568B1 (de) | 2020-09-23 |
| MX2019001917A (es) | 2019-07-15 |
| TWI743165B (zh) | 2021-10-21 |
| TW201819375A (zh) | 2018-06-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2833251T3 (es) | Procedimiento para producir derivados de 2-(3,6-dihalopiridin-2-il)-3h-imidazol[4,5-c]piridina y compuestos relacionados por reacción del derivado de piridina 3h-imidazol[4,5-c] con una base organometálica de zinc-amina | |
| US10961220B2 (en) | Method for preparing substituted imidazolyl carboxyamides | |
| ES2919558T3 (es) | Método para producir compuestos bicíclicos halogenados | |
| ES2951539T3 (es) | Procedimiento para la preparación de derivados de imidazol | |
| US11479565B2 (en) | Process for preparing substituted imidazole derivatives | |
| ES2906081T3 (es) | Procedimiento para preparar derivados de imidazopiridina halogenados | |
| JP2019521123A (ja) | ハロゲン化ピリジン誘導体の製造方法 | |
| TW202012373A (zh) | 製備經取代的n-芳基吡唑之方法 |