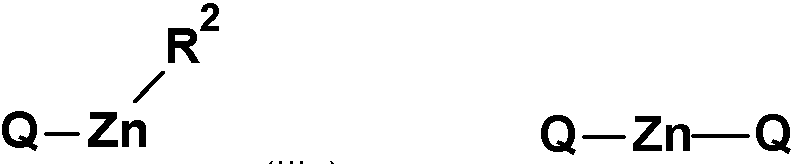ES2919558T3 - Método para producir compuestos bicíclicos halogenados - Google Patents
Método para producir compuestos bicíclicos halogenados Download PDFInfo
- Publication number
- ES2919558T3 ES2919558T3 ES17765149T ES17765149T ES2919558T3 ES 2919558 T3 ES2919558 T3 ES 2919558T3 ES 17765149 T ES17765149 T ES 17765149T ES 17765149 T ES17765149 T ES 17765149T ES 2919558 T3 ES2919558 T3 ES 2919558T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- hal
- cycloalkyl
- compound
- process according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 125000002619 bicyclic group Chemical group 0.000 title abstract description 13
- 238000004519 manufacturing process Methods 0.000 title abstract description 6
- 150000001875 compounds Chemical class 0.000 claims abstract description 70
- 229910052736 halogen Inorganic materials 0.000 claims abstract description 23
- 150000002367 halogens Chemical class 0.000 claims abstract description 22
- 238000000034 method Methods 0.000 claims description 48
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 42
- -1 (C2-C4)cyanoalkenyl Chemical group 0.000 claims description 37
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 34
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 claims description 34
- 229910052794 bromium Inorganic materials 0.000 claims description 26
- 229910052740 iodine Inorganic materials 0.000 claims description 24
- 239000002585 base Substances 0.000 claims description 23
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 22
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 22
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims description 21
- 125000000217 alkyl group Chemical group 0.000 claims description 21
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 21
- UOCLXMDMGBRAIB-UHFFFAOYSA-N 1,1,1-trichloroethane Chemical compound CC(Cl)(Cl)Cl UOCLXMDMGBRAIB-UHFFFAOYSA-N 0.000 claims description 20
- 239000011630 iodine Substances 0.000 claims description 20
- 239000002904 solvent Substances 0.000 claims description 17
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 claims description 16
- 239000000460 chlorine Substances 0.000 claims description 15
- 229910052801 chlorine Inorganic materials 0.000 claims description 15
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 13
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 13
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 12
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 11
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims description 9
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 8
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 8
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 claims description 8
- HVZJRWJGKQPSFL-UHFFFAOYSA-N tert-Amyl methyl ether Chemical compound CCC(C)(C)OC HVZJRWJGKQPSFL-UHFFFAOYSA-N 0.000 claims description 8
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 7
- 229910052731 fluorine Inorganic materials 0.000 claims description 7
- 239000011737 fluorine Substances 0.000 claims description 7
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 7
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 7
- 229910052757 nitrogen Inorganic materials 0.000 claims description 7
- 125000006650 (C2-C4) alkynyl group Chemical group 0.000 claims description 6
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 claims description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 6
- 125000006001 difluoroethyl group Chemical group 0.000 claims description 6
- 125000003784 fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 claims description 6
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 claims description 6
- 125000006337 tetrafluoro ethyl group Chemical group 0.000 claims description 6
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 claims description 6
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 claims description 6
- 125000004767 (C1-C4) haloalkoxy group Chemical group 0.000 claims description 5
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 claims description 5
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 5
- 125000004399 C1-C4 alkenyl group Chemical group 0.000 claims description 5
- 125000000262 haloalkenyl group Chemical group 0.000 claims description 5
- 125000001188 haloalkyl group Chemical group 0.000 claims description 5
- 125000000232 haloalkynyl group Chemical group 0.000 claims description 5
- QPFMBZIOSGYJDE-UHFFFAOYSA-N 1,1,2,2-tetrachloroethane Chemical compound ClC(Cl)C(Cl)Cl QPFMBZIOSGYJDE-UHFFFAOYSA-N 0.000 claims description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 claims description 4
- ZFPGARUNNKGOBB-UHFFFAOYSA-N 1-Ethyl-2-pyrrolidinone Chemical compound CCN1CCCC1=O ZFPGARUNNKGOBB-UHFFFAOYSA-N 0.000 claims description 4
- BNXZHVUCNYMNOS-UHFFFAOYSA-N 1-butylpyrrolidin-2-one Chemical compound CCCCN1CCCC1=O BNXZHVUCNYMNOS-UHFFFAOYSA-N 0.000 claims description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 4
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 claims description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 claims description 4
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical compound BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 claims description 4
- 229910052799 carbon Inorganic materials 0.000 claims description 4
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 claims description 4
- 125000004966 cyanoalkyl group Chemical group 0.000 claims description 4
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 claims description 4
- 125000004438 haloalkoxy group Chemical group 0.000 claims description 4
- 125000005347 halocycloalkyl group Chemical group 0.000 claims description 4
- 239000001257 hydrogen Substances 0.000 claims description 4
- 229910052739 hydrogen Inorganic materials 0.000 claims description 4
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims description 4
- 239000000203 mixture Chemical class 0.000 claims description 4
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 claims description 4
- 229910001508 alkali metal halide Inorganic materials 0.000 claims description 3
- 229910001615 alkaline earth metal halide Inorganic materials 0.000 claims description 3
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 claims description 3
- 125000003282 alkyl amino group Chemical group 0.000 claims description 3
- 125000004471 alkyl aminosulfonyl group Chemical group 0.000 claims description 3
- 125000004414 alkyl thio group Chemical group 0.000 claims description 3
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 claims description 3
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 3
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 claims description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 3
- AUHZEENZYGFFBQ-UHFFFAOYSA-N mesitylene Substances CC1=CC(C)=CC(C)=C1 AUHZEENZYGFFBQ-UHFFFAOYSA-N 0.000 claims description 3
- 125000001827 mesitylenyl group Chemical group [H]C1=C(C(*)=C(C([H])=C1C([H])([H])[H])C([H])([H])[H])C([H])([H])[H] 0.000 claims description 3
- 229910052760 oxygen Inorganic materials 0.000 claims description 3
- 238000002360 preparation method Methods 0.000 claims description 3
- 239000008096 xylene Substances 0.000 claims description 3
- 150000003738 xylenes Chemical class 0.000 claims description 3
- GETTZEONDQJALK-UHFFFAOYSA-N (trifluoromethyl)benzene Chemical class FC(F)(F)C1=CC=CC=C1 GETTZEONDQJALK-UHFFFAOYSA-N 0.000 claims description 2
- BOSAWIQFTJIYIS-UHFFFAOYSA-N 1,1,1-trichloro-2,2,2-trifluoroethane Chemical class FC(F)(F)C(Cl)(Cl)Cl BOSAWIQFTJIYIS-UHFFFAOYSA-N 0.000 claims description 2
- SEQRDAAUNCRFIT-UHFFFAOYSA-N 1,1-dichlorobutane Chemical compound CCCC(Cl)Cl SEQRDAAUNCRFIT-UHFFFAOYSA-N 0.000 claims description 2
- RELMFMZEBKVZJC-UHFFFAOYSA-N 1,2,3-trichlorobenzene Chemical compound ClC1=CC=CC(Cl)=C1Cl RELMFMZEBKVZJC-UHFFFAOYSA-N 0.000 claims description 2
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 claims description 2
- KNKRKFALVUDBJE-UHFFFAOYSA-N 1,2-dichloropropane Chemical compound CC(Cl)CCl KNKRKFALVUDBJE-UHFFFAOYSA-N 0.000 claims description 2
- GOYDNIKZWGIXJT-UHFFFAOYSA-N 1,2-difluorobenzene Chemical compound FC1=CC=CC=C1F GOYDNIKZWGIXJT-UHFFFAOYSA-N 0.000 claims description 2
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 claims description 2
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 claims description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 claims description 2
- CYTYCFOTNPOANT-UHFFFAOYSA-N Perchloroethylene Chemical group ClC(Cl)=C(Cl)Cl CYTYCFOTNPOANT-UHFFFAOYSA-N 0.000 claims description 2
- XSTXAVWGXDQKEL-UHFFFAOYSA-N Trichloroethylene Chemical group ClC=C(Cl)Cl XSTXAVWGXDQKEL-UHFFFAOYSA-N 0.000 claims description 2
- 150000007824 aliphatic compounds Chemical class 0.000 claims description 2
- 125000003545 alkoxy group Chemical group 0.000 claims description 2
- 125000004448 alkyl carbonyl group Chemical group 0.000 claims description 2
- 125000005278 alkyl sulfonyloxy group Chemical group 0.000 claims description 2
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 claims description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 claims description 2
- KCXMKQUNVWSEMD-UHFFFAOYSA-N benzyl chloride Chemical compound ClCC1=CC=CC=C1 KCXMKQUNVWSEMD-UHFFFAOYSA-N 0.000 claims description 2
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims description 2
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 2
- 229940117389 dichlorobenzene Drugs 0.000 claims description 2
- GUVUOGQBMYCBQP-UHFFFAOYSA-N dmpu Chemical compound CN1CCCN(C)C1=O GUVUOGQBMYCBQP-UHFFFAOYSA-N 0.000 claims description 2
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 claims description 2
- 125000004692 haloalkylcarbonyl group Chemical group 0.000 claims description 2
- 125000004441 haloalkylsulfonyl group Chemical group 0.000 claims description 2
- 125000004995 haloalkylthio group Chemical group 0.000 claims description 2
- 150000005826 halohydrocarbons Chemical class 0.000 claims description 2
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 claims description 2
- 229910001629 magnesium chloride Inorganic materials 0.000 claims description 2
- QULYNCCPRWKEMF-UHFFFAOYSA-N parachlorobenzotrifluoride Chemical class FC(F)(F)C1=CC=C(Cl)C=C1 QULYNCCPRWKEMF-UHFFFAOYSA-N 0.000 claims description 2
- BNIXVQGCZULYKV-UHFFFAOYSA-N pentachloroethane Chemical compound ClC(Cl)C(Cl)(Cl)Cl BNIXVQGCZULYKV-UHFFFAOYSA-N 0.000 claims description 2
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 claims description 2
- 229910052717 sulfur Inorganic materials 0.000 claims description 2
- 229950011008 tetrachloroethylene Drugs 0.000 claims description 2
- UBOXGVDOUJQMTN-UHFFFAOYSA-N trichloroethylene Natural products ClCC(Cl)Cl UBOXGVDOUJQMTN-UHFFFAOYSA-N 0.000 claims description 2
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 claims description 2
- 125000006656 (C2-C4) alkenyl group Chemical group 0.000 claims 1
- 150000008045 alkali metal halides Chemical class 0.000 claims 1
- 125000000676 alkoxyimino group Chemical group 0.000 claims 1
- 125000004644 alkyl sulfinyl group Chemical group 0.000 claims 1
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims 1
- 125000004656 alkyl sulfonylamino group Chemical group 0.000 claims 1
- 125000006350 alkyl thio alkyl group Chemical group 0.000 claims 1
- 125000005133 alkynyloxy group Chemical group 0.000 claims 1
- 150000001491 aromatic compounds Chemical class 0.000 claims 1
- 125000004473 dialkylaminocarbonyl group Chemical group 0.000 claims 1
- 125000005291 haloalkenyloxy group Chemical group 0.000 claims 1
- 125000004440 haloalkylsulfinyl group Chemical group 0.000 claims 1
- 150000002431 hydrogen Chemical class 0.000 claims 1
- 125000005843 halogen group Chemical group 0.000 abstract description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 42
- 238000006243 chemical reaction Methods 0.000 description 19
- 239000000243 solution Substances 0.000 description 14
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 12
- 150000003254 radicals Chemical group 0.000 description 12
- 238000003786 synthesis reaction Methods 0.000 description 10
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 8
- 230000015572 biosynthetic process Effects 0.000 description 8
- 238000010626 work up procedure Methods 0.000 description 8
- YAXWOADCWUUUNX-UHFFFAOYSA-N 1,2,2,3-tetramethylpiperidine Chemical compound CC1CCCN(C)C1(C)C YAXWOADCWUUUNX-UHFFFAOYSA-N 0.000 description 7
- 238000005160 1H NMR spectroscopy Methods 0.000 description 7
- RKMGAJGJIURJSJ-UHFFFAOYSA-N 2,2,6,6-Tetramethylpiperidine Substances CC1(C)CCCC(C)(C)N1 RKMGAJGJIURJSJ-UHFFFAOYSA-N 0.000 description 7
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 7
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N DMSO Substances CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 7
- 238000004440 column chromatography Methods 0.000 description 7
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethyl cyclohexane Natural products CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 7
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 7
- 239000012528 membrane Substances 0.000 description 7
- 239000012074 organic phase Substances 0.000 description 7
- 238000000746 purification Methods 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 7
- 239000011734 sodium Substances 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- 239000011701 zinc Substances 0.000 description 7
- 239000000543 intermediate Substances 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 5
- 235000019345 sodium thiosulphate Nutrition 0.000 description 5
- 229910052725 zinc Inorganic materials 0.000 description 5
- 235000019270 ammonium chloride Nutrition 0.000 description 4
- 229910052786 argon Inorganic materials 0.000 description 4
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 3
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical group [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 150000004820 halides Chemical class 0.000 description 3
- 239000013067 intermediate product Substances 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- YQTCQNIPQMJNTI-UHFFFAOYSA-N 2,2-dimethylpropan-1-one Chemical group CC(C)(C)[C]=O YQTCQNIPQMJNTI-UHFFFAOYSA-N 0.000 description 2
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 2
- LQZMLBORDGWNPD-UHFFFAOYSA-N N-iodosuccinimide Chemical compound IN1C(=O)CCC1=O LQZMLBORDGWNPD-UHFFFAOYSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 150000008040 ionic compounds Chemical class 0.000 description 2
- ZCSHNCUQKCANBX-UHFFFAOYSA-N lithium diisopropylamide Chemical compound [Li+].CC(C)[N-]C(C)C ZCSHNCUQKCANBX-UHFFFAOYSA-N 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 2
- 125000004758 (C1-C4) alkoxyimino group Chemical group 0.000 description 1
- 125000004768 (C1-C4) alkylsulfinyl group Chemical group 0.000 description 1
- 125000004769 (C1-C4) alkylsulfonyl group Chemical group 0.000 description 1
- 125000004760 (C1-C4) alkylsulfonylamino group Chemical group 0.000 description 1
- 125000004771 (C1-C4) haloalkylsulfinyl group Chemical group 0.000 description 1
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000006039 1-hexenyl group Chemical group 0.000 description 1
- 125000006023 1-pentenyl group Chemical group 0.000 description 1
- 125000006017 1-propenyl group Chemical group 0.000 description 1
- 125000000530 1-propynyl group Chemical group [H]C([H])([H])C#C* 0.000 description 1
- KAESVJOAVNADME-UHFFFAOYSA-N 1H-pyrrole Natural products C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000006040 2-hexenyl group Chemical group 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- RLRUNZFXEAZVIT-UHFFFAOYSA-N 2-n-methyl-5-(trifluoromethyl)pyridine-2,3-diamine Chemical compound CNC1=NC=C(C(F)(F)F)C=C1N RLRUNZFXEAZVIT-UHFFFAOYSA-N 0.000 description 1
- 125000006024 2-pentenyl group Chemical group 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- NESRSFKZZDFADT-UHFFFAOYSA-N 3-N-methyl-6-(trifluoromethyl)pyridazine-3,4-diamine Chemical compound CNC=1N=NC(=CC=1N)C(F)(F)F NESRSFKZZDFADT-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000006041 3-hexenyl group Chemical group 0.000 description 1
- 125000003542 3-methylbutan-2-yl group Chemical group [H]C([H])([H])C([H])(*)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- XAUBEYHIVLSHOG-UHFFFAOYSA-N 3-methylimidazo[4,5-b]pyridine Chemical compound C1=CN=C2N(C)C=NC2=C1 XAUBEYHIVLSHOG-UHFFFAOYSA-N 0.000 description 1
- GKVVKWNIYISLDO-UHFFFAOYSA-N 3-methylimidazo[4,5-c]pyridine Chemical compound C1=NC=C2N(C)C=NC2=C1 GKVVKWNIYISLDO-UHFFFAOYSA-N 0.000 description 1
- 125000006042 4-hexenyl group Chemical group 0.000 description 1
- 125000006043 5-hexenyl group Chemical group 0.000 description 1
- FSASFVDSKLAMQH-UHFFFAOYSA-N 7-methylimidazo[4,5-c]pyridazine Chemical compound C1=NN=C2N(C)C=NC2=C1 FSASFVDSKLAMQH-UHFFFAOYSA-N 0.000 description 1
- ZHRWOPMANBDMSZ-UHFFFAOYSA-N CNc1cnc(cc1N)C(F)(F)F Chemical compound CNc1cnc(cc1N)C(F)(F)F ZHRWOPMANBDMSZ-UHFFFAOYSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 239000003905 agrochemical Substances 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- 125000005119 alkyl cycloalkyl group Chemical group 0.000 description 1
- 125000004687 alkyl sulfinyl alkyl group Chemical group 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 238000010960 commercial process Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 125000006575 electron-withdrawing group Chemical group 0.000 description 1
- 230000009881 electrostatic interaction Effects 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 230000026030 halogenation Effects 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- VHHHONWQHHHLTI-UHFFFAOYSA-N hexachloroethane Chemical compound ClC(Cl)(Cl)C(Cl)(Cl)Cl VHHHONWQHHHLTI-UHFFFAOYSA-N 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- FAIAAWCVCHQXDN-UHFFFAOYSA-N phosphorus trichloride Chemical compound ClP(Cl)Cl FAIAAWCVCHQXDN-UHFFFAOYSA-N 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- ZZYXNRREDYWPLN-UHFFFAOYSA-N pyridine-2,3-diamine Chemical class NC1=CC=CN=C1N ZZYXNRREDYWPLN-UHFFFAOYSA-N 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 238000006798 ring closing metathesis reaction Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000011592 zinc chloride Substances 0.000 description 1
- 235000005074 zinc chloride Nutrition 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F3/00—Compounds containing elements of Groups 2 or 12 of the Periodic Table
- C07F3/06—Zinc compounds
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
La presente invención se refiere a un método para producir compuestos bicíclicos halogenados de fórmula (II) que comienzan a partir de compuestos de la estructura Q-H a través de pasos intermedios de fórmula (IIIA) o (IIIB) Q-Hal (II), (IIIA), (IIIB), en el que Q es un elemento estructural, el signo # que indica el enlace al radical de la molécula y A, Q1, Q2, Q3, Q4, Q5 y Q6 que tiene las designaciones proporcionadas en la descripción, Hal es halógeno y R2 es halógeno o -O -Pivaloyl. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Método para producir compuestos bicíclicos halogenados
La presente invención se relaciona con un procedimiento para preparar sistemas bicíclicos halogenados de fórmula (II)
Q-Hal (II), que procede de los compuestos Q-H a través de intermedios de fórmula (IIIa) o (IIIb)
a (IIIb),
en los que los elementos estructurales mostrados en las fórmulas Q-H, (II), (IIIa) y (IIIb) tienen las definiciones que se dan a continuación. La invención se relaciona además con sistemas bicíclicos halogenados y productos intermedios de este tipo.
Los sistemas bicíclicos halogenados de fórmula (II) son de gran importancia industrial para la industria farmacéutica y agroquímica y son un producto intermedio importante, entre otros, en la preparación de compuestos que son efectivos como pesticidas, por ejemplo.
La literatura divulga que los compuestos de la fórmula (II) se pueden preparar mediante, en un primer paso, la incorporación de metal en presencia de una base de litio muy reactiva, por ejemplo diisopropilamida de litio o n-butillitio y reacción posterior con una fuente de haluro, por ejemplo hexacloroetano o N-yodosuccinimida (como se describe en el Journal of Organic Chemistry 2014, 79, 2203-2212 y Tetrahedron Letters 2012, 53, 1036-1041). Asimismo, se sabe que los compuestos de fórmula (II) se pueden preparar por reacción de compuestos de hidroxilo bicíclicos con tricloruro de fósforo (como se describe en el documento WO 2013/180193). Sin embargo, los métodos de síntesis química que se han descrito en la técnica anterior hasta la fecha para tales sistemas bicíclicos halogenados hacen uso con mucha frecuencia de métodos que no son económicamente implementables desde un punto de vista industrial y/o tienen otras desventajas.
Las desventajas son los bajos rendimientos químicos, particularmente en el caso de los sistemas bicíclicos altamente sustituidos, el rendimiento a temperaturas muy bajas para las incorporaciones de metal (aproximadamente -80 ° C) y la generalmente difícil regio y quimioselectividad de la halogenación. Además, la introducción de átomos de bromo o más particularmente de átomos de yodo en dichos compuestos de hidroxilo bicíclicos es generalmente problemática o incluso no ha sido posible hasta la fecha. Por lo tanto, la preparación -si es posible- es muy costosa e inadecuada para procesos comerciales a escala industrial. Además, los compuestos correspondientes apenas están disponibles comercialmente. Esto es especialmente cierto de 7-metil-7H-imidazo[4,5-c]piridazina, 3-metil-3H-imidazo[4,5-c]piridina y 3-metil-3H-imidazo[4,5-b]piridina.
Respecto a las desventajas descritas anteriormente, existe una necesidad urgente de un proceso simplificado, industrialmente y económicamente realizable para preparar sistemas bicíclicos halogenados, especialmente sistemas bicíclicos halogenados de la fórmula (II). Los sistemas bicíclicos halogenados obtenibles mediante este proceso buscado deben obtenerse preferiblemente con buen rendimiento, alta pureza y de una manera económica.
Se ha encontrado que, sorprendentemente, se pueden preparar los sistemas bicíclicos halogenados de la fórmula (II) ventajosamente en un proceso usando una base de organozinc.
En consecuencia, la presente invención proporciona un proceso para preparar compuestos de fórmula (II)
Q-Hal (II),
en la cual (configuración 1)
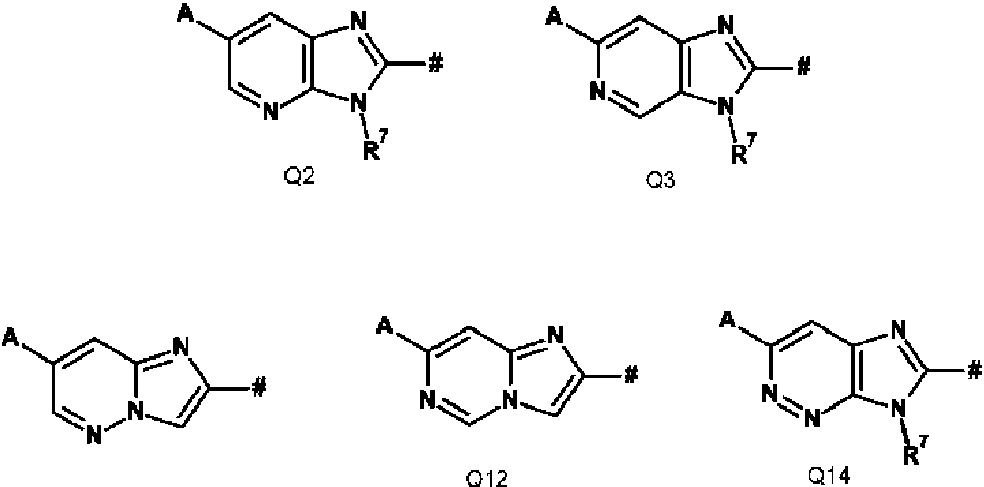
Q es un elemento structural
donde el símbolo # indica el enlace con Hal y
Q1 es N o CR6,
Q2 es N o CR6,
Q3 es N o C,
Q4 es O, S, N o NR7,
Q5 es N o C,
Q6 es N o CH,
y donde Q es un elemento estructural del grupo Q2, Q3, Q10, Q12 o Q14.
R6 es hidrógeno, alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), haloalcoxi(C1-C4),-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), haloalquinilo(C2-C4), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halocicloalquilo(C3-C6), alquiltio(C1-C4)-alquilo(C1-C4), alquilsulfinilo(C1-C4)-alquilo(C1-C4), alquilsulfonilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), haloalcoxi(C1-C4),-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), haloalquinilo(C2-C4), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halocicloalquilo(C3-C6), alquiltio(C1-C4)-alquilo(C1-C4), alquilsulfinilo(C1-C4)-alquilo(C1-C4), alquilsulfonilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4), y
A es hidrógeno, ciano, halógeno, alquilo(C1-C4), haloalquilo(C1-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), haloalquinilo(C2-C4), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), alcoxi(C1-C4), haloalcoxi(C1-C4),, alcoxiimino(C1-C4), alquiltio(C1-C4), haloalquiltio(C1-C4), alquilsulfinilo(C1-C4), haloalquilsulfinilo(C1-C4), alquilsulfonilo(C1-C4), haloalquilsulfonilo(C1-C4), alquilsulfoniloxi(C1-C4), alquilcarbonilo(C1-C4), haloalquilcarbonilo(C1-C4), aminocarbonilo, alquilaminocarbonilo(C1-C4), di-alquilaminocarbonilo(C1-C4), alquilsulfonilamino(C1-C4), alquilamino(C1-C4), dialquilamino(C1-C4), aminosulfonilo, alquilaminosulfonilo(C1-C4) o di-alquilaminosulfonilo(C1-C4),
Hal es halógeno,
caracterizado porque, en un primer paso del proceso a), un compuesto Q-H en el que Q es como se definió anteriormente
se hace reaccionar con una base organozinc de la estructura (NR3R4)-Zn-R2 o (NR3R4)2-Zn en la cual
R2 es halógeno o -O-pivaloilo y
R3 y R4juntos forman un grupo -(CH2)4-, -(CH2)5- o -(CH2)2O(CH2)2-, donde cada uno de estos grupos puede estar opcionalmente sustituido por radicales 1, 2, 3 o 4 R5 y R5 se selecciona del grupo que consiste en metilo, etilo, npropilo e i-propilo,
para dar un compuesto de la fórmula (IIIa) o la fórmula (IIIb)
a (IIIb),
en la que Q y R2 cada uno tiene las definiciones dadas arriba,
y este compuesto de la fórmula (IIIa) o (IIIb) se hace reaccionar en un segundo paso del proceso b) con un compuesto de la estructura X-Hal en la que X es halógeno y Hal tiene la definición antes mencionada para dar el compuesto de la fórmula ( II).
El compuesto X-Hal, como se desprende de las definiciones de X y Hal, es un compuesto interhalógeno, preferiblemente halógeno elemental.
Preferiblemente, Q1, Q2, Q3, Q4, Q5 y Q6 representan no más de cinco átomos de nitrógeno en general y, además, preferiblemente, no más de cuatro átomos de nitrógeno en general.
Las definiciones preferidas y particularmente preferidas de los radicales Q, X, Hal y R2 incluidos en las fórmulas QH, (II), (IIIa) y (IIIb) mencionadas anteriormente del proceso de la invención se explican a continuación, con una descripción más específica de la base organozinc más abajo, y así se especifican las configuraciones preferidas de la base en ese punto.
(Configuración 2)
Q es preferiblemente un elemento estructural del grupo de Q2, Q3, Q10, Q12 o Q14
R7 es preferiblemente alquilo(C-i-C4), haloalquilo(C-i-C4), alcoxi(C1-C4)-alquilo(C-i-C4), haloalcoxi(C-i-C4),-alquilo(C1-C4), alquiltio(C1-C4)-alquilo(C1-C4), alquilsulfinilo(C1-C4)-alquilo(C1-C4), alquilsulfonilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
A es preferiblemente flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3, CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
Hal y X tienen la misma definición y son preferiblemente flúor, cloro, yodo o bromo, y
R2 es preferiblemente halógeno, especialmente cloro, bromo o yodo.
(Configuración 3)
Q es más preferiblemente un elemento estructural del grupo de Q2, Q3, Q10, Q12 o Q14,
R7 es más preferiblemente alquilo(C1-C4) o alcoxi(C1-C4)-alquilo(C1-C4),
A es más preferiblemente trifluorometilo, fluoroetilo (CH2CFH2 , CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3 , CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
Hal y X tienen la misma definición y son más preferiblemente yodo o bromo, y
R2 es más preferiblemente cloro,
(Configuración 4)
Q es más preferiblemente el elemento estructural Q2, Q3, Q12 o Q14,
R7 es lo más preferiblemente metilo, etilo, n-propilo o isopropilo, especialmente metilo,
A es lo más preferiblemente trifluorometilo,
Hal y X tienen la misma definición y son lo más preferiblemente yodo o bromo, y
R2 es lo más preferiblemente cloro.
Las definiciones y explicaciones de radicales dadas anteriormente se aplican tanto a los productos finales e intermedios como a los materiales de partida de una manera correspondiente. Estas definiciones de radicales pueden combinarse entre sí según se desee, es decir, incluyendo combinaciones entre los respectivos intervalos de preferencia.
De acuerdo con la invención, se da preferencia a aquellos compuestos en los que existe una combinación de las definiciones enumeradas anteriormente como preferidas.
Se da preferencia particular de acuerdo con la invención a aquellos compuestos en los que existe una combinación de las definiciones enumeradas anteriormente como más preferidas.
De acuerdo con la invención, se da una preferencia muy particular a aquellos compuestos en los que existe una combinación de las definiciones enumeradas anteriormente como las más preferidas.
En una realización preferida adicional de la invención, Q es Q2 y R7, A, Hal, X y R2 tienen las definiciones dadas en la configuración 1 o las dadas en la configuración 2 o las dadas en la configuración 3 o las dadas en la configuración 4 (configuración 6).
En una realización preferida adicional de la invención, Q es Q3 y R7, A, Hal, X y R2 tienen las definiciones dadas en la configuración 1 o las dadas en la configuración 2 o las dadas en la configuración 3 o las dadas en la configuración 4 (configuración 7).
En una realización preferida adicional de la invención, Q es Q10 y R7, A, Hal, X y R2 tienen las definiciones dadas en la configuración 1 o las dadas en la configuración 2 o las dadas en la configuración 3 o las dadas en la configuración 4 (configuración 14).
En una realización preferida adicional de la invención, Q es Q12 y R7, A, Hal, X y R2 tienen las definiciones dadas en la configuración 1 o las dadas en la configuración 2 o las dadas en la configuración 3 o las dadas en la configuración 4 (configuración 16).
En una realización preferida adicional de la invención, Q es Q14 y R7, A, Hal, X y R2 tienen las definiciones dadas en la configuración 1 o las dadas en la configuración 2 o las dadas en la configuración 3 o las dadas en la configuración 4 (configuración 18).
Ventajosamente, los sistemas bicíclicos halogenados de la fórmula (II) pueden prepararse mediante el proceso de acuerdo con la invención con buenos rendimientos y en alta pureza. Una gran ventaja del proceso de acuerdo con la invención es su regioselectividad y las condiciones de reacción comparativamente suaves en las que se puede llevar a cabo, esencialmente como un resultado de su rendimiento a temperaturas claramente más altas en comparación con -80°C. La posibilidad de ser capaz de introducir halógenos a temperaturas claramente más altas también es muy atractiva, y los procesos de acuerdo con la invención, incluso a tales temperaturas más altas, toleran grupos funcionales como el trifluorometilo u otros grupos que halan electrones que activan las posiciones orto sin dañar la regioselectividad existente. Además, debido a la muy buena tolerancia del grupo funcional a los reactivos de zinc, las bases de zinc son muy atractivas. En general, así es posible preparar compuestos de fórmula (II) en poco tiempo y con muy buenos rendimientos.
El proceso de acuerdo con la invención se puede dilucidar mediante el siguiente esquema (I):
Esquema (I)
En este esquema, Q, X, Hal y R2 y, dentro de las definiciones respectivas, cualquier otro elemento estructural presente cada uno tiene las definiciones dadas arriba. Los compuestos mostrados entre paréntesis son el producto intermedio (fórmula IIIa o fórmula IIIb), que se hacen reaccionar adicionalmente con un compuesto X-Hal para dar el compuesto de fórmula (II). Por consiguiente, el proceso de acuerdo con la invención se puede dividir en los dos pasos a) y b) del proceso, siendo el paso a) la conversión del compuesto QH en el producto intermedio respectivo y siendo el paso b) la conversión adicional del producto intermedio al compuesto de la fórmula (II).
Definiciones generales
En el contexto de la presente invención, el término halógeno (Hal), a menos que se defina de otro modo, abarca aquellos elementos seleccionados del grupo que consiste en flúor, cloro, bromo y yodo.
El término "haluros" en relación con la presente invención describe compuestos entre halógenos y elementos de otros grupos de la Tabla Periódica, que pueden dar lugar a sales de haluros (compuestos iónicos (sales) que consisten en aniones y cationes debido a la gran diferencia en electronegatividad entre los elementos involucrados y se mantienen unidos por interacciones electrostáticas) o haluros covalentes (compuestos covalentes donde la diferencia en la electronegatividad no es tan grande como en los compuestos iónicos mencionados anteriormente, pero los enlaces tienen polaridad de carga), dependiendo de la naturaleza del enlace químico. Se da preferencia particular de acuerdo con la invención a las sales de haluro.
El término "pivaloilo" en el contexto de la presente invención describe el radical desprotonado de ácido pivalico (X) que tiene la fórmula empírica (CH3)3CCO2H.
"O-pivaloilo" significa correspondientemente que el enlace del radical pivaloilo es a través del átomo de oxígeno desprotonado del grupo ácido.
En el contexto de la presente invención, a menos que se defina de manera diferente en otra parte, el término "alquilo", ya sea por sí solo o en combinación con otros términos, por ejemplo haloalquilo, se entiende que indica un radical de un grupo hidrocarburo alifático saturado que tiene 1 a 12 átomos de carbono y puede ser ramificado o no ramificado. Ejemplos de radicales alquilo C1-C12 son metilo, etilo, n-propilo, isopropilo, n-butilo, isobutilo, sec-butilo, tert-butilo, npentilo, isopentilo, neopentilo, tert-pentilo, 1-metillbutilo, 2-metilbutilo, 1-etilpropilo, 1,2-dimetilpropilo, hexilo, n-heptilo, n-octilo, n-nonilo, n-decilo, n-undecilo y n-dodecilo. Entre estos radicales alquilo, se da particular preferencia a los radicales alquilo C1-C6. Se da especial preferencia a los radicales alquilo C1-C4.
De acuerdo con la invención, a menos que se defina de manera diferente en otro lugar, se entiende que el término
"alquenilo", ya sea solo o en combinación con otros términos, indica un radical alquenilo C2-C12 de cadena lineal o ramificada que tiene al menos un doble enlace, por ejemplo vinilo, alilo, 1-propenilo, isopropenilo, 1-butenilo, 2-butenilo, 3-butenilo, 1,3-butadienilo, 1-pentenilo, 2-pentenilo, 3-pentenilo, 4-pentenilo, 1,3-pentadienilo, 1-hexenilo, 2-hexenilo, 3-hexenilo, 4-hexenilo, 5-hexenilo y 1,4-hexadienilo. Entre estos, se da preferencia a los radicales alquenilo C2-C6 y en particular se prefiere a los radicales alquenilo C2-C4.
De acuerdo con la invención, a menos que se defina de manera diferente en otro lugar, se entiende que el término "alquinilo", ya sea por sí solo o en combinación con otros términos, indica un radical alquinilo C2-C12 de cadena lineal o ramificada que tiene al menos un triple enlace, por ejemplo, etinilo, 1 -propinilo y propargilo. Entre estos, se da preferencia a los radicales alquinilo C3-C6 y en particular preferencia a los radicales alquinilo C3-C4. El radical alquinilo también puede contener al menos un doble enlace.
De acuerdo con la invención, a menos que se defina de manera diferente en otra parte, se entiende que el término "cicloalquilo", ya sea por sí solo o en combinación con otros términos, indica un radical cicloalquilo C3-C8, por ejemplo ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo cicloheptilo y ciclooctilo. Entre estos, se da preferencia a los radicales cicloalquilo C3-C6.
El término "alcoxi", ya sea solo o en combinación con otros términos, por ejemplo haloalcoxi, se entiende en el presente caso que indica un radical O-alquilo, donde el término "alquilo" es como se define anteriormente.
Los radicales sustituidos con halógeno, por ejemplo haloalquilo, son mono- o polihalogenados, hasta el número máximo de posibles sustituyentes. En el caso de la polihalogenación, los átomos de halógeno pueden ser idénticos o diferentes. A menos que se defina de manera diferente, aquí el halógeno es flúor, cloro, bromo o yodo, especialmente flúor, cloro o bromo. Los grupos alquilo sustituidos con uno o más átomos de halógeno (-Hal) se seleccionan, por ejemplo, de trifluorometilo (CF3), difluorometilo (CHF2), CF3CH2 , ClCH2 o CF3CCh.
A menos que se indique lo contrario, los radicales opcionalmente sustituidos pueden estar mono- o polisustituidos, donde los sustituyentes en el caso de las polisustituciones pueden ser iguales o diferentes.
Se conoce la síntesis de los compuestos Q-H como reactivos de un proceso de acuerdo con la invención en principio por los expertos en la técnica. Por ejemplo, los compuestos QH con Q = Q1, Q2, Q3, Q14 o Q15 pueden obtenerse a partir de los correspondientes derivados de piridindiamina por cierre de anillo para dar el compuesto de azol respectivo, como se describe, por ejemplo, en los documentos WO2014/100065 o WO2015/017610, preferiblemente bajo condiciones ácidas. Las síntesis alternativas también son posibles, pero son más complejas y, como resultado generalmente menos ventajosas económicamente.
La conversión de los compuestos Q-H en compuestos de la fórmula (IIIa) o (IIIb) en el primer paso del proceso (paso a) se efectúa en presencia de una base de organozinc de la estructura (NR3R4)-Zn-R2 o (NR3R4)2-Zn, en la cual (configuración B-1)
R2 es como se definió anteriormente (Configuración 1) (y es por lo tanto halógeno o -O-pivaloilo),
R3 y R4 juntos forman un grupo -(CH2)4-, -(CH2)5- o -(CH2)2O(CH2)2-, donde cada uno de estos grupos puede ser sustituido opcionalmente por radicales 1, 2, 3 o 4 R5y
R5 es seleccionado del grupo que consiste en metilo, etilo, n-propilo e i-propilo.
Es preferible que (configuración B-2)
R2 es como se definió anteriormente como preferido (Configuración 2) (y es por lo tanto halógeno, especialmente cloro, bromo o yodo),
R3 y R4 juntos forman un grupo -(CH2)5-, donde cada uno de estos grupos puede ser sustituido opcionalmente por radicales 1, 2, 3 o 4 R5 y
R5 es seleccionado del grupo que consiste en metilo y etilo.
Es particularmente preferible que (configuración B-3)
R2 es como se definió anteriormente como más preferido (configuración 3) o como lo más preferido (configuración 4) (y es por lo tanto cloro) y
R3 y R4 juntos forman un grupo -(CH2)5- sustituido por 4 grupos metilo.
Las definiciones de radicales dadas anteriormente pueden combinarse entre sí según se desee, es decir, incluyendo combinaciones entre los respectivos intervalos de preferencia.
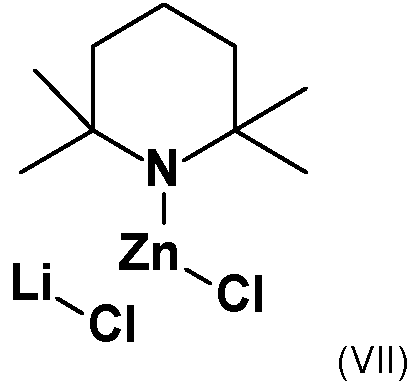
En una configuración muy particularmente preferida de la base de acuerdo la invención, el elemento estructural (NR3R4) es tetrametilpiperidina (TMP) de fórmula (IV).
Las bases de organozinc más preferidas de acuerdo con la invención se caracterizan en consecuencia porque el zinc está unido a TMP, especialmente en la forma de haluro de zinc y más preferiblemente en la forma de cloruro de zinc. Las bases de este tipo tienen la siguiente estructura de la fórmula (V) (configuración B-4)
(V) (TMP)x ZnCl2-x,
en la que x es el número 1 o 2. Entre estos, se da preferencia a su vez a las bases con x = 1 (configuración B-5) de fórmula (VI):
En una realización preferida adicional del proceso de acuerdo con la invención, la base de organozinc está presente junto con haluros de metales alcalinos o de metales alcalinotérreos. Esto es especialmente cierto de las bases de las fórmulas (V) y (VI). Los haluros de metales alcalinos o de metales alcalinotérreos particularmente preferidos de esta clase son el cloruro de litio y cloruro de magnesio, dando una preferencia muy particular al cloruro de litio. Las bases de organozinc que se prefieren muy particularmente de acuerdo con la invención son TMP ZnClLiCl o (TMP)2 Zn2LiCl (configuración B-6). El más preferido es TMP ZnClLiCl (VII; configuración B-7).
Las combinaciones específicas de compuestos de las fórmulas Q-H, (II) y (IIIa) o (IIIb) con bases de acuerdo con la invención se citan en la tabla 1 a continuación, pudiéndose emplear estas en un proceso de acuerdo con la invención. Dado que, en algunas configuraciones, el elemento estructural R2 está presente tanto en la base de acuerdo con la invención como en el compuesto de la fórmula (IIIa), la definición más estrecha se aplica a R2 en cada caso.
Tabla 1:
Preferiblemente, la base de organozinc se usa en el proceso de acuerdo con la invención en una cantidad total de 0,5 a 5 equivalentes, preferiblemente de 0,8 a 2 equivalentes, aún más preferiblemente de 1 a 1,5 equivalentes y más preferiblemente de 1,0 a 1,2 equivalentes, con base en un compuesto Q-H. Una ventaja del proceso de acuerdo con la invención a este respecto es que la base organometálica se puede usar en cantidades virtualmente estequiométricas.
Dependiendo de si el elemento estructural (NR3R4) está presente una o dos veces en la base organozinc utilizada, los compuestos intermedios de fórmula (IIIa) o de la fórmula (IIIb) se forman en el paso a) del proceso.
La conversión de los compuestos de la fórmula (IIIa) o (IIIb) en compuestos de la fórmula (II) en el segundo paso del proceso (paso b)) se efectúa en la presencia de un compuesto X-Hal en el que X y Hal cada uno tiene las definiciones dadas arriba.
Dado que tanto X como Hal son halógenos, el compuesto es un compuesto interhalógeno. X y Hal no necesariamente tienen que ser el mismo halógeno. Por ejemplo, X puede ser yodo o bromo y Hal puede ser cloro, bromo o yodo. Preferiblemente, el compuesto X-Hal, sin embargo, es halógeno elemental, especialmente F2, Ch, Br2 o I2. Se da preferencia particular a I2 o Br2 , preferencia muy particular a I2.
Preferiblemente, el compuesto X-Hal se usa en el proceso de acuerdo con la invención en una cantidad total de 0,5 a 10,0 equivalentes, preferiblemente de 0,8 a 5 equivalentes, aún más preferiblemente de 1 a 2,5 equivalentes y más preferiblemente de 1,0 a 2,0 equivalentes, con base en el compuesto Q-H.
La conversión inventiva de los compuestos Q-H en compuestos de la fórmula (IIIa) o (IIIb) y adicionalmente en compuestos de fórmula (II) se efectúa preferiblemente en la presencia de un solvente orgánico en cada caso. Los solventes útiles en principio incluyen todos los solventes orgánicos que son inertes bajo las condiciones de reacción empleadas y en los que los compuestos que se van a convertir tienen una solubilidad adecuada. Los solventes adecuados incluyen especialmente: tetrahidrofurano (THF), 1,4-dioxano, dietil eter, diglima, metil tert-butil eter(MTBE), tert-amil metil eter (TAME), 2-metil-THF, tolueno, xilenos, mesitileno, carbonato de etileno, carbonato de propileno, N,N-dimetilacetamida, N,N-dimetilformamida (DMF), N-metilpirrolidona (NMP), N-etil-2-pirrolidona (NEP), N-butil-2-pirrolidona (NBP); N,N'-dimetilpropolenurea (DMPU), halohidrocarburos e hidrocarburos aromáticos, especialmente clorohidrocarburos tal como tetracloroetileno, tetracloroetano, dicloropropano, cloruro de metileno, diclorobutano, cloroformo, tetracloruro de carbono, tricloroetano, tricloroetileno, pentacloroetano, difluorobenceno, 1,2-dicloroetano, clorobenceno, bromobenceno, diclorobenceno, especialmente 1,2-diclorobenceno, clorotolueno, triclorobenceno; 4-metoxibenceno, compuesto alifáticos fluorados y aromáticos, tal como triclorotrifluoroetano, benzotrifluoruro y 4-clorobenzotrifluoruro. También es posible utilizar mezclas de solventes, preferiblemente mezclas de los solventes mencionados anteriormente, tales como tetrahidrofurano (THF), 1,4-dioxano, dietil eter, diglima, metil tert-butil eter (MTBE), tert-amil metil eter (TAME), 2-metil-THF, tolueno, xilenos, mesitileno, dimetilformamida (DMF).
Los solventes preferidos son THF, N,N-dimetilformamida (DMF), 1,4-dioxano, diglima, metil tert-butil éter (MTBE), tertamil metil eter (TAME), 2-metil-THF, tolueno y 4- metoxibenceno.
Los solventes particularmente preferidos son THF y N,N-dimetilformamida (DMF), dando preferencia muy particular a THF.
El solvente también puede desgasificarse (libre de oxígeno).
Se da preferencia al uso del mismo solvente para ambos pasos del proceso a) y b). Sin embargo, también son posibles Configuraciones Alternativas de la invención en las que se utilizan diferentes solventes para los pasos de proceso a) y b), en cuyo caso los solventes se seleccionan igualmente de manera preferible entre los solventes mencionados anteriormente, y son aplicables los solventes respectivos especificados como preferidos, más preferidos y los más preferidos a los respectivos pasos a) o b) del proceso.
La conversión en el paso a) del proceso se realiza generalmente a una temperatura entre 0°C y 80°C y con preferencia creciente entre 10°C y 70°C, entre 15°C y 60°C, entre 20°C y 50°C, entre 20°C y 40°C, y lo más preferiblemente entre 20°C y 35°C, por ejemplo a temperatura ambiente o 25°C.
La conversión en el paso b) del proceso se realiza generalmente a una temperatura entre 0°C y 40°C y con preferencia creciente entre 0°C y 35°C, entre 0°C y 30°C, y lo más preferiblemente entre 0°C y 25°C, por ejemplo a temperatura ambiente o 25°C. Es particularmente ventajoso cuando las reacciones con bromo elemental (X y Hal son cada uno bromo) se efectúan a 0°C y las reacciones con yodo elemental (X y Hal son cada yodo) a temperatura ambiente o 25°C.
La reacción se realiza típicamente a presión estándar, pero también puede realizarse a presión elevada o reducida.
Los compuestos deseados de la fórmula (II) se pueden aislar, por ejemplo, mediante tratamiento acuoso en la presencia de soluciones saturadas de cloruro de amonio o tiosulfato de sodio y/o cromatografía posterior. Dichos procesos son conocidos por los expertos en la técnica y también incluyen la cristalización a partir de un solvente orgánico o mezcla de solventes.
Dos ejemplos de realizaciones particularmente preferidas del proceso de acuerdo con la invención se pueden aclarar con referencia a los siguientes esquemas (IIa) y (IIb):
Esquema IIa:
El esquema IIa y el esquema IIb difieren simplemente en que la reacción en el paso b) del proceso se efectúa con yodo elemental (IIa) o con bromo elemental (IIb). En ambos esquemas, A en cada caso tiene las definiciones dadas anteriormente. El compuesto mostrado entre paréntesis representa el producto intermedio correspondiente de la fórmula IIIa que se convierte adicionalmente en el producto, un compuesto de la fórmula (II). Ambas reacciones tienen lugar en THF como solvente. "equiv" denota la cantidad de equivalentes de TMPZnClLiCl o compuesto X-Hal utilizado, es decir, yodo elemental o bromo elemental aquí.
Se describen además compuestos de la estructura Q-H seleccionados de los siguientes compuestos:
Q-H-1:
Q-H-3:
Se describen además compuestos de la fórmula (Illa) seleccionados de los siguientes compuestos:
La presente invención proporciona además compuestos de la fórmula (II).
Q-Hal (II),
en la que (configuración Q-Hal-1-1)
Q es un elemento estructural del grupo Q2, Q3, Q10, Q12 o Q14
R7 es alquilo(C-i-C4) o alcoxi(C1-C4)-alquilo(C1-C4),
A es trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2 , CHFCFH2), trifluoroetilo, (CH2CF3 , CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3 , CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo, y
Hal es yodo o bromo.
(Configuración Q-Hal-4-1)
Q es lo más preferiblemente el elemento estructural Q2, Q3, Q12 o Q14,
R7 es lo más preferiblemente metilo, etilo, n-propilo o isopropilo, especialmente metilo,
A es lo más preferiblemente trifluorometilo, y
Hal es lo más preferiblemente yodo o bromo.
Las definiciones de radicales dadas anteriormente pueden combinarse entre sí según se desee, es decir, incluyendo combinaciones entre los respectivos intervalos de preferencia.
De acuerdo con la invención, se da preferencia a aquellos compuestos en los que existe una combinación de las definiciones enumeradas anteriormente como preferidas.
Se da preferencia particular de acuerdo con la invención a aquellos compuestos en los que existe una combinación de las definiciones enumeradas anteriormente como más preferidas.
De acuerdo con la invención, se da una preferencia muy particular a aquellos compuestos en los que existe una combinación de las definiciones enumeradas anteriormente como las más preferidas.
Ejemplos de tales compuestos particularmente preferidos son:
II-1:
con Y = I o Br
con Y = I o Br
con Y = I o Br
La presente invención se explica en detalle mediante los ejemplos que siguen, aunque los ejemplos no deben
interpretarse de tal manera que restrinjan la invención.
Ejemplo 1
Síntesis de 3-metil-6-(trifluorometil)-3H-imidazo[4.5-c1piridina (reactivo)
Se calentó N3-Metil-6-(trifluorometil)piridina-3.4-diamina (500 mg, 2.6 mmol). disuelto en ácido fórmico (4 ml, 106 mmol). con microondas a 150°C durante 1 hora. Después del tratamiento habitual mediante la adición de una solución acuosa saturada de cloruro de amonio. la mezcla de reacción se extrajo con acetato de etilo y se secaron las fases orgánicas combinadas sobre Na2SO4 y se concentraron en un vacío de bomba de membrana. Después de la purificación por cromatografía de columna (acetato de etilo/ciclohexano). se obtuvo 3-metil-6-(trifluorometil)-3H-imidazo[4.5-c1piridina (480 mg. 91%) como un sólido blanco. HPLC-MS: logP = 1.09; Masa (m/z+1): 202.0; 1HNMR (D6-DMSO): 89.14 (s. 1H). 8.61 (s. 1H). 8.19 (s. 1H). 4.02 (s. 3H).
Ejemplo 2
Síntesis de 2-yodo-3-met¡l-6-(tr¡fluorometil)-3H-¡m¡dazo[4.5-c1p¡r¡d¡na:
A 3-metil-6-(trifluorometil)-3H-imidazo[4.5-c1piridina (201 mg. 1.0 mmol). disuelto en THF (0.8 ml). se añadió TMPZnClLiCl (1.35 M en THF. 0.82 ml. 1.1 mmol) a 25°C bajo argón; esta solución de reacción se agitó durante 10 min. Posteriormente. se añadió bromo (224 mg. 1.4 mmol) a 0°C y la solución se agitó durante 20 min más. Después de la elaboración habitual por adición de soluciones saturadas de cloruro de amonio y tiosulfato de sodio. la mezcla de reacción se extrajo con acetato de etilo. y las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de bomba de membrana. Después de la purificación por cromatografía de columna (etil acetato/ciclohexano). se obtuvo 2-bromo-3-metil-6-(trifluorometil)-3H-imidazo[4.5-c1piridina (269 mg. 96%) como un sólido amarillo. HPLC-MS: logP = 1.71; Masa (m/z+1): 281.0; 1HNMR (D6-DMSO): 89.15 (s. 1H). 8.17 (s. 1H). 3.96 (s. 3H).
Ejemplo 3
Síntesis de 2-bromo-3-met¡l-6-(tr¡fluorometil)-3H-¡m¡dazo[4.5-c1p¡r¡d¡na:
A 3-metil-6-(trifluorometil)-3H-imidazo[4.5-c1piridina (201 mg. 1.0 mmol). disuelto en THF (0.8 ml). se añadió TMPZnClLiCl (1.35 M en THF. 0.82 ml. 1.1 mmol) a 25°C bajo argón; esta solución de reacción se agitó durante 10 min. Posteriormente. se añadió bromo (224 mg. 1.4 mmol) a 0°C y la solución se agitó durante 20 min más. Después de la elaboración habitual por adición de soluciones saturadas de cloruro de amonio y tiosulfato de sodio. la mezcla de reacción se extrajo con acetato de etilo. y las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de bomba de membrana. Después de la purificación por cromatografía de columna (etil acetato/ciclohexano). se obtuvo 2-bromo-3-metil-6-(trifluorometil)-3H-imidazo[4.5-c1piridina (269 mg. 96%) como un sólido amarillo. HPLC-MS: logP = 1.71; Masa (m/z+1): 281.0; 1HNMR (D6-DMSO): 89.15 (s. 1H). 8.17 (s. 1H). 3.96 (s. 3H).
Ejemplo 4
Síntesis de 7-met¡l-3-(tr¡fluorometil)-7H-¡m¡dazo[4.5-c1p¡r¡daz¡na (reactivo)
Se calentó N3-Metil-6-(trifluorometil)piridazina-3.4-diamina (1.0 g. 5.2 mmol). disuelto en ácido fórmico (5 ml. 132 mmol). con microondas a 150°C durante 1 hora. Después de la elaboración habitual por adición de solución acuosa saturada de cloruro de amonio. la mezcla de reacción se extrajo con acetato de etilo. y las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de bomba de membrana. Después de la purificación por cromatografía de columna (etil acetato/ciclohexano). se obtuvo 7-metil-3-(trifluorometil)-7H-imidazo[4.5-c1piridazina (758 mg. 73%) como un sólido blanco. HPLC-MS: logP = 0.91; Masa (m/z+1): 203.1; 1HNMR (D6-DMSO): 88.92 (s.
1H). 8.62 (s. 1H). 4.08 (s. 3H).
Ejemplo 5
Síntesis de 6-yodo-7-met¡l-3-(tr¡fluorometil)-7H-¡m¡dazo[4.5-c1p¡r¡daz¡na:
A 7-metil-3-(trifluorometil)-7H-imidazo[4.5-c1piridazina (203 mg. 1.0 mmol). disuelto en THF (0.8 ml). se añadió TMPZnClLiCl (1.35 M en THF. 0.82 ml. 1.1 mmol) a 25°C bajo argón; esta solución de reacción se agitó durante 10 min. Posteriormente. se añadió yodo (508 mg en 4 ml of THF) a 25°C y la solución se agitó durante 20 min más. Después de la elaboración habitual por adición de soluciones saturada de cloruro de amonio y tiosulfato de sodio. la mezcla de reacción se extrajo con acetato de etilo. y las fases orgánicas combinadas se secaron sobre Na2SO4 y se concentraron en un vacío de bomba de membrana. Después de la purificación por cromatografía de columna (etil acetato/cyclohexano). se obtuvo 6-iodo-7-metil-3-(trifluorometil)-7H-imidazo[4.5-c1piridazina (230 mg. 70%) como un sólido amarillo. HPLC-MS: logP = 1.66; Masa (m/z+1): 329.0; 1HNMR (D6-DMSO): 88.53 (s. 1H). 3.99 (s. 3H).
Ejemplo 6
Síntesis de 3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazo[4.5-b1p¡r¡d¡na (reactivo):
Se calentó N2-Met¡l-5-(tr¡fluoromet¡l)p¡r¡d¡na-2.3-d¡am¡na (500 mg, 2.61 mmol). d¡suelto en ác¡do fórm¡co (4 ml. 106 mmol). con m¡croondas a 150°C durante 1 hora. Después de la elaborac¡ón hab¡tual por ad¡c¡ón de soluc¡ón acuosa saturada de cloruro de amon¡o. la mezcla de reacc¡ón se extrajo con acetato de et¡lo. y las fases orgán¡cas comb¡nadas se secaron sobre Na2SO4 y se concentraron en un vacío de bomba de membrana. Después de la pur¡f¡cac¡ón por cromatografía de columna (et¡l acetato/c¡clohexano). se obtuvo 3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazo[4.5-c1p¡r¡d¡na (385 mg. 74%) como un sól¡do blanco. HPLC-MS: logP = 1.44; Masa (m/z+1): 202.1; 1HNMR (D6-DMSO): 88.77 (s. 1H).
8.67 (s. 1H). 8.52 (s. 1H). 3.90 (s. 3H).
Ejemplo 7
Síntes¡s de 2-yodo-3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazo[4.5-b1p¡r¡d¡na:
A 3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazo[4.5-b1p¡r¡d¡na (100 mg. 0.49 mmol). d¡suelto en THF (0.4 ml). se añad¡ó TMPZnCl-üCl (1.35 M en THF. 0.41 ml. 0.54 mmol) a 25°C bajo argón; esta soluc¡ón de reacc¡ón se ag¡tó durante 10 m¡n. Poster¡ormente. se añad¡ó yodo (252 mg en 1 ml de THF) a 25°C y la soluc¡ón se ag¡tó durante 20 m¡n más. Después de la elaborac¡ón hab¡tual por ad¡c¡ón de soluc¡ones saturadas de cloruro de amon¡o y t¡osulfato de sod¡o. la mezcla de reacc¡ón se extrajo con acetato de et¡lo. y las fases orgán¡cas comb¡nadas se secaron sobre Na2SO4 y se concentraron en un vacío de bomba de membrana. Después de la pur¡f¡cac¡ón por cromatografía de columna (et¡l acetato/cyclohexano). se obtuvo 2-¡odo-3-met¡l-6-(tr¡fluoromet¡l)-3H-¡m¡dazo[4.5-b1p¡r¡d¡na (111 mg. 69%) como un sól¡do amar¡llo. HPLC-MS: logP = 2.29; Masa (m/z+1): 328.0; 1HNMR (D6-DMSO): 88.71 (s. 1H). 8.47 (s. 1H). 3.82 (s. 3H).
Claims (15)
1. Proceso para la preparación de compuestos de la fórmula (II)
Q-Hal (II)
en la que
Q es un elemento estructural
donde el símbolo # indica el enlace con Hal y
Q1 es N o CR6,
Q2 es N o CR6,
Q3 es N o C,
Q4 es O, S, N o NR7,
Q5 es N o C,
Q6 es N o CH,
y donde Q es un elemento estructural del grupo Q2, Q3, Q10, Q12 o Q14,
R6 es hidrógeno, alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C-i-C4)-alquilo(C-i-C4), haloalcoxi(C1-C4),-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)-alquilo(C1-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(C1-C4), haloalquinilo(C2-C4), cicloalquilo(C3-C6), cicloalquilo(C3-C6)-cicloalquilo(C3-C6), alquilo(C1-C4)-cicloalquilo(C3-C6), halocicloalquilo(C3-C6), alquiltio(C1-C4)-alquilo(C1-C4), alquilsulfinilo(C1-C4)-alquilo(C1-C4), alquilsulfonilo(C1-C4)-alquilo(C1-C4) o alquilcarbonilo(C1-C4)-alquilo(C1-C4),
R7 es alquilo(C1-C4), haloalquilo(C1-C4), cianoalquilo(C1-C4), hidroxialquilo(C1-C4), alcoxi(C1-C4)-alquilo(C1-C4), haloalcoxi(C1-C4),-alquilo(C1-C4), alquenilo(C2-C4), alqueniloxi(C2-C4)-alquilo(C1-C4), haloalqueniloxi(C2-C4)
alquilo(Ci-C4), haloalquenilo(C2-C4), cianoalquenilo(C2-C4), alquinilo(C2-C4), alquiniloxi(C2-C4)-alquilo(Ci-C4), haloalquinilo(C2-C4), cicloalquilo(C3-C6), cidoalquilo(C3-C6)-cidoalquilo(C3-C6), alquilo(Ci-C4)-cidoalquilo(C3-C6), halocicloalquilo(C3-C6), alquiltio(Ci-C4)-alquilo(Ci-C4), alquilsulfinilo(Ci-C4)-alquilo(Ci-C4), alquilsulfonilo(Ci-C4)-alquilo(Ci-C4) o alquilcarbonilo(Ci-C4)-alquilo(Ci-C4), y
A es hidrógeno, ciano, halógeno, alquilo(Ci-C4), haloalquilo(Ci-C4), alquenilo(C2-C4), haloalquenilo(C2-C4), alquinilo(C2-C4), haloalquinilo(C2-C4), cicloalquilo(C3-C6), cidoalquilo(C3-C6)-cidoalquilo(C3-C6), alquilo(Ci-C4)-cicloalquilo(C3-C6), alcoxi(Ci-C4), haloalcoxi(Ci-C4), alcoxiimino(Ci-C4), alquiltio(Ci-C4), haloalquiltio(Ci-C4), alquilsulfinilo(Ci-C4), haloalquilsulfinilo(Ci-C4), alquilsulfonilo(Ci-C4), haloalquilsulfonilo(Ci-C4), alquilsulfoniloxi(Ci-C4), alquilcarbonilo(Ci-C4), haloalquilcarbonilo(Ci-C4), aminocarbonilo, alquilaminocarbonilo(Ci-C4), dialquilaminocarbonilo(Ci-C4), alquilsulfonilamino(Ci-C4), alquilamino(Ci-C4), di-alquilamino(Ci-C4), aminosulfonilo, alquilaminosulfonilo(Ci-C4) o di-alquilaminosulfonilo(Ci-C4),
Hal es halógeno,
caracterizado porque, en un primer paso a) del proceso, un compuesto Q-H en el que Q es como se definió anteriormente
se reacciona con una base de organozinc de la estructura (NR3R4)-Zn-R2 o (NR3R4)2-Zn en la que
R2 es halógeno o -O-pivaloilo y
R3 y R4 juntos forman un grupo -(CH2)4-, -(CH2)5- o -(CH2)2O(CH2)2-, donde cada uno de estos grupos puede ser sustituido opcionalmente por radicales i, 2, 3 o 4 R5 y R5 es seleccionado del grupo que consiste en metilo, etilo, n-propilo e i-propilo,
para dar un compuesto de la fórmula (Illa) o la fórmula (IIIb)
a (IIIb),
en las que Q y R2 cada uno tiene las definiciones dadas arriba,
y este compuesto de la fórmula (IIIa) o (IIIb) se hace reaccionar en un segundo paso b) del proceso con un compuesto de la estructura X-Hal en la que X es halógeno y Hal tiene la definición antes mencionada para dar el compuesto de fórmula (II).
2. Proceso de acuerdo con la reivindicación i, caracterizado porque
Q es un elemento estructural del grupo de Q2, Q3, Q i0, Q i2 o Qi4,
R7 es alquilo(Ci-C4), haloalquilo(Ci-C4), alcoxi(Ci-C4)-alquilo(Ci-C4), haloalcoxi(Ci-C4),-alquilo(Ci-C4), alquiltio(Ci-C4)-alquilo(Ci-C4), alquilsulfinilo(Ci-C4)-alquilo(Ci-C4), alquilsulfonilo(Ci-C4)-alquilo(Ci-C4) o alquilcarbonilo(Ci-C4)-alquilo(Ci-C4),
A es flúor, cloro, bromo, fluorometilo, difluorometilo, trifluorometilo, fluoroetilo (CH2CFH2, CHFCH3), difluoroetilo (CF2CH3 , CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3 , CHFCHF2 , CF2CFH2), tetrafluoroetilo (CHFCF3, CF2CHF2), pentafluoroetilo, trifluorometoxi, difluoroclorometoxi, diclorofluorometoxi, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
Hal y X tienen la misma definición y son flúor, cloro, yodo o bromo, y
R2 es halógeno, especialmente cloro, bromo o yodo.
3. Proceso de acuerdo con cualquiera de las reivindicaciones i o 2, caracterizado porque
Q es un elemento estructural del grupo de Q2, Q3, Q i0, Q i2 o Qi4,
R7 es alquilo(Ci-C4) o alcoxi(Ci-C4)-alquilo(Ci-C4),
A es trifluorometilo, fluoroetilo (CH2CFH2 , CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3 , CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3 , CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo,
Hal y X tienen la misma definición y son yodo o bromo, y
R2 es cloro.
4. Proceso de acuerdo con cualquiera de las reivindicaciones i a 3, caracterizado porque
Q es el elemento estructural Q2, Q3, Q i2 o Qi4,
R7 es metilo, etilo, n-propilo o isopropilo, especialmente metilo,
A es trifluorometilo,
Hal y X tienen la misma definición y son yodo o bromo, y
i8
R2 es cloro.
5. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 4, caracterizado porque R3 y R4 juntos forman un grupo -(CH2)5- sustituido por 4 grupos metilo.
6. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 5, caracterizado porque la base de organozinc es un compuesto de la fórmula (V)
(V) (TMP)x ZnCl2-x,
en la que x es el número 1 o 2.
7. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 6, caracterizado porque la base de organozinc está presente junto con un haluro de metal alcalino o haluro de metal alcalinotérreo, preferiblemente cloruro de litio o cloruro de magnesio.
8. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 7, caracterizado porque la base de organozinc se usa en una cantidad total de 0,5 a 5 equivalentes, con base en el compuesto Q-H.
9. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 8, caracterizado porque el compuesto X-Hal es un halógeno elemental, especialmente F2 , Ch, Br2 o I2.
10. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 9, caracterizado porque el compuesto X-Hal se usa en una cantidad total de 0,5 a 10,0 equivalentes, con base en el compuesto Q-H.
11. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 10, caracterizado porque se lleva a cabo en presencia de un solvente seleccionado del grupo que consiste en tetrahidrofurano (THF), 1,4-dioxano, dietil eter, diglima, metil tert-butil eter (MTBE), tert-amil metil eter (TAME), 2-metil-THF, tolueno, xilenos, mesitileno, carbonato de etileno, carbonato de propileno, N,N-dimetilacetamida, N,N-dimetilformamida (DMF), N-metilpirrolidona (NMP), N-etil-2-pirrolidona (NEP), N-butil-2-pirrolidona (NBP); N,N'-dimetilpropilenurea (DMPU), halohidrocarburo, hidrocarburo aromático, clorohidrocarburo, tetracloroetileno, tetracloroetano, dicloropropano, cloruro de metileno, diclorobutano, cloroformo, tetrachloruro de carbono, tricloroetano, tricloroetileno, pentacloroetano, difluorobenceno, 1,2-dicloroetano, clorobenceno, bromobenceno, diclorobenceno, 1,2-diclorobenceno, clorotolueno, triclorobenceno; 4-metoxibenceno, compuestos alifáticos fluorados, compuestos aromáticos fluorados, triclorotrifluoroetano, benzotrifluoruro y 4-clorobenzotrifluoruro, o una mezcla de al menos dos de estos solventes entre sí.
12. Proceso de acuerdo con la reivindicación 11, caracterizado porque el solvente es THF o N,N-dimetilformamida (DMF).
13. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 12, caracterizado porque el paso a) del proceso se realiza a una temperatura entre 0°C y 80°C.
14. Proceso de acuerdo con cualquiera de las reivindicaciones 1 a 13, caracterizado porque el paso b) del proceso se realiza a una temperatura entre 0°C y 40°C.
15. Compuesto de la fórmula (II)
Q-Hal (II),
en la que
Q es un elemento estructural del grupo Q2, Q3, Q10, Q12 o Q14 de acuerdo con la reivindicación 1,
R7 es alquilo(C-i-C4) o alcoxi(C1-C4)-alquilo(C-i-C4),
A es trifluorometilo, fluoroetilo (CH2CFH2 , CHFCH3), difluoroetilo (CF2CH3, CH2CHF2, CHFCFH2), trifluoroetilo, (CH2CF3 , CHFCHF2, CF2CFH2), tetrafluoroetilo (CHFCF3 , CF2CHF2), pentafluoroetilo, trifluorometiltio, trifluorometilsulfinilo o trifluorometilsulfonilo, y
Hal es yodo o bromo.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16188760 | 2016-09-14 | ||
| PCT/EP2017/072363 WO2018050515A1 (de) | 2016-09-14 | 2017-09-06 | Verfahren zur herstellung von halogenierten bizyklen |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2919558T3 true ES2919558T3 (es) | 2022-07-27 |
Family
ID=56943355
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17765149T Active ES2919558T3 (es) | 2016-09-14 | 2017-09-06 | Método para producir compuestos bicíclicos halogenados |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US20190375766A1 (es) |
| EP (1) | EP3512847B1 (es) |
| JP (1) | JP7066683B2 (es) |
| KR (1) | KR102471278B1 (es) |
| CN (1) | CN109715627A (es) |
| BR (1) | BR112019004946B1 (es) |
| DK (1) | DK3512847T3 (es) |
| ES (1) | ES2919558T3 (es) |
| IL (1) | IL265257B (es) |
| MX (1) | MX2019002937A (es) |
| TW (1) | TWI749060B (es) |
| WO (1) | WO2018050515A1 (es) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3500568B1 (de) * | 2016-08-16 | 2020-09-23 | Bayer CropScience Aktiengesellschaft | Verfahren zur herstellung von 2-(3,6-dihalopyridin-2-yl)-3h-imidazol[4,5-c]pyridinderivaten und verwandten verbindungen durch umsetzung des 3h-imidazol[4,5-c]pyridinderivats mit einer metallorganischen zink-amin base |
| TWI820231B (zh) | 2018-10-11 | 2023-11-01 | 德商拜耳廠股份有限公司 | 用於製備經取代咪唑衍生物之方法 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4472409A (en) * | 1981-11-05 | 1984-09-18 | Byk Gulden Lomberg Chemische Fabrik Gesellschaft Mit Beschrankter Haftung | 2-Pyridylmethyl thio(sulfinyl)benzimidazoles with gastric acid secretion inhibiting effects |
| JPS5910590A (ja) * | 1982-07-08 | 1984-01-20 | Ishihara Sangyo Kaisha Ltd | 置換酢酸アニリド系化合物およびそれらを含有する除草剤 |
| JPS61106563A (ja) * | 1984-10-30 | 1986-05-24 | Oouchi Shinko Kagaku Kogyo Kk | 2−クロルベンゾチアゾ−ル誘導体の製造方法 |
| GB0027561D0 (en) * | 2000-11-10 | 2000-12-27 | Merck Sharp & Dohme | Therapeutic agents |
| WO2006107784A1 (en) * | 2005-04-05 | 2006-10-12 | Eli Lilly And Company | Imidazopyridazine compounds |
| EP2680697B1 (en) * | 2011-03-03 | 2018-01-10 | Merck Sharp & Dohme Corp. | Process for the preparation of an orexin receptor antagonist |
| EP2857396B1 (en) * | 2012-05-31 | 2018-11-21 | Sumitomo Chemical Co., Ltd | Fused heterocyclic compounds for pest control |
| BR112015010207A2 (pt) * | 2012-11-09 | 2017-07-11 | Sumitomo Chemical Co | método para promover o crescimento de plantas |
| ES2707305T3 (es) | 2012-12-20 | 2019-04-03 | Merck Sharp & Dohme | Imidazopiridinas sustituidas como inhibidores de HDM2 |
| PT3027601T (pt) | 2013-07-31 | 2018-01-08 | Gilead Sciences Inc | Inibidores de syk |
| KR101698640B1 (ko) * | 2013-09-26 | 2017-01-20 | 주식회사 엘지화학 | 헤테로환 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102007796B1 (ko) * | 2013-11-18 | 2019-08-07 | 포르마 세라퓨틱스 인크. | Bet 브로모도메인 저해제로서 테트라하이드로퀴놀린 조성물 |
-
2017
- 2017-09-06 KR KR1020197010078A patent/KR102471278B1/ko active Active
- 2017-09-06 JP JP2019513945A patent/JP7066683B2/ja active Active
- 2017-09-06 ES ES17765149T patent/ES2919558T3/es active Active
- 2017-09-06 BR BR112019004946-0A patent/BR112019004946B1/pt active IP Right Grant
- 2017-09-06 CN CN201780054870.9A patent/CN109715627A/zh active Pending
- 2017-09-06 EP EP17765149.4A patent/EP3512847B1/de active Active
- 2017-09-06 MX MX2019002937A patent/MX2019002937A/es unknown
- 2017-09-06 WO PCT/EP2017/072363 patent/WO2018050515A1/de not_active Ceased
- 2017-09-06 US US16/331,843 patent/US20190375766A1/en not_active Abandoned
- 2017-09-06 DK DK17765149.4T patent/DK3512847T3/da active
- 2017-09-12 TW TW106131162A patent/TWI749060B/zh active
-
2019
- 2019-03-10 IL IL265257A patent/IL265257B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| TWI749060B (zh) | 2021-12-11 |
| TW201825485A (zh) | 2018-07-16 |
| DK3512847T3 (da) | 2022-06-27 |
| JP2019529405A (ja) | 2019-10-17 |
| KR102471278B1 (ko) | 2022-11-25 |
| MX2019002937A (es) | 2019-06-06 |
| IL265257B (en) | 2021-12-01 |
| WO2018050515A1 (de) | 2018-03-22 |
| BR112019004946B1 (pt) | 2023-01-10 |
| US20190375766A1 (en) | 2019-12-12 |
| IL265257A (en) | 2019-05-30 |
| KR20190045332A (ko) | 2019-05-02 |
| EP3512847B1 (de) | 2022-03-30 |
| EP3512847A1 (de) | 2019-07-24 |
| JP7066683B2 (ja) | 2022-05-13 |
| BR112019004946A2 (pt) | 2019-06-25 |
| CN109715627A (zh) | 2019-05-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2833251T3 (es) | Procedimiento para producir derivados de 2-(3,6-dihalopiridin-2-il)-3h-imidazol[4,5-c]piridina y compuestos relacionados por reacción del derivado de piridina 3h-imidazol[4,5-c] con una base organometálica de zinc-amina | |
| ES2919558T3 (es) | Método para producir compuestos bicíclicos halogenados | |
| US10961220B2 (en) | Method for preparing substituted imidazolyl carboxyamides | |
| ES2941903T3 (es) | Procedimiento para la preparación de derivados de piridina halogenada | |
| TWI820232B (zh) | 用於製備咪唑衍生物之方法 | |
| ES2930222T3 (es) | Procedimiento para la preparación de derivados de imidazol sustituidos | |
| ES2928370T3 (es) | Método para producir N-arilpirazoles halogenados |