ES2851602T3 - Derivados de 3-fenil-5-ureidoisotiazol-4-carboxamida como inhibidores de cinasa - Google Patents
Derivados de 3-fenil-5-ureidoisotiazol-4-carboxamida como inhibidores de cinasa Download PDFInfo
- Publication number
- ES2851602T3 ES2851602T3 ES17156014T ES17156014T ES2851602T3 ES 2851602 T3 ES2851602 T3 ES 2851602T3 ES 17156014 T ES17156014 T ES 17156014T ES 17156014 T ES17156014 T ES 17156014T ES 2851602 T3 ES2851602 T3 ES 2851602T3
- Authority
- ES
- Spain
- Prior art keywords
- amino
- phenyl
- ureido
- carbonyl
- isothiazole
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- PCJKQVZFZFRGSE-UHFFFAOYSA-N C1(=CC=CC=C1)C1=NSC(=C1C(=O)N)NC(=O)N Chemical class C1(=CC=CC=C1)C1=NSC(=C1C(=O)N)NC(=O)N PCJKQVZFZFRGSE-UHFFFAOYSA-N 0.000 title description 2
- 229940043355 kinase inhibitor Drugs 0.000 title description 2
- 239000003757 phosphotransferase inhibitor Substances 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 169
- -1 {[(2-fluoro-5-methylphenyl) amino] carbonyl} amino Chemical group 0.000 claims abstract description 117
- 150000003839 salts Chemical class 0.000 claims abstract description 37
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 22
- BEPMYBTTZSNHPS-UHFFFAOYSA-N 1,2-thiazole-4-carboxamide Chemical compound NC(=O)C=1C=NSC=1 BEPMYBTTZSNHPS-UHFFFAOYSA-N 0.000 claims abstract description 19
- 239000002253 acid Substances 0.000 claims abstract description 10
- VGXBEIFLGSBCSQ-UHFFFAOYSA-N 3-[4-[(4-methylphenyl)carbamoylamino]phenyl]-5-[(2-oxopyrrolidine-1-carbonyl)amino]-1,2-thiazole-4-carboxamide Chemical compound C1=CC(C)=CC=C1NC(=O)NC1=CC=C(C=2C(=C(NC(=O)N3C(CCC3)=O)SN=2)C(N)=O)C=C1 VGXBEIFLGSBCSQ-UHFFFAOYSA-N 0.000 claims abstract description 5
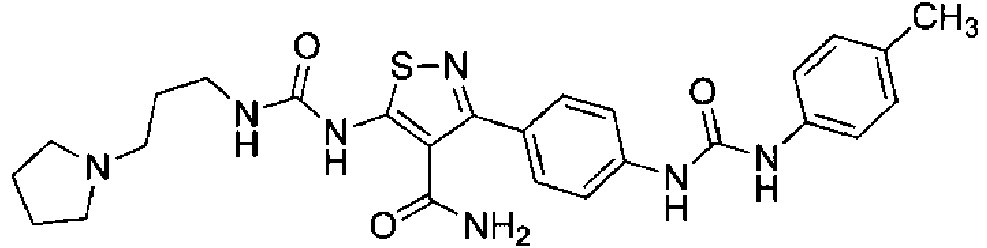
- RCHBURXYVZCGRM-UHFFFAOYSA-N 3-[4-[(4-methylphenyl)carbamoylamino]phenyl]-5-(3-pyrrolidin-1-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound C1=CC(C)=CC=C1NC(=O)NC1=CC=C(C=2C(=C(NC(=O)NCCCN3CCCC3)SN=2)C(N)=O)C=C1 RCHBURXYVZCGRM-UHFFFAOYSA-N 0.000 claims abstract description 4
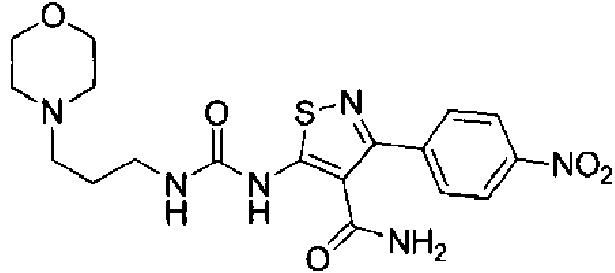
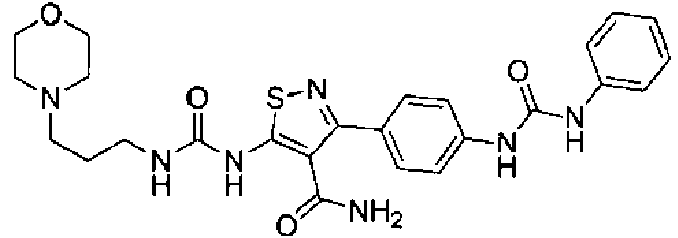
- DVMIIUOULRDNLG-UHFFFAOYSA-N 5-(3-morpholin-4-ylpropylcarbamoylamino)-3-[4-(phenylcarbamoylamino)phenyl]-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(NC(=O)NC=3C=CC=CC=3)=CC=2)C(C(=O)N)=C1NC(=O)NCCCN1CCOCC1 DVMIIUOULRDNLG-UHFFFAOYSA-N 0.000 claims abstract description 4
- JJKVPTCDYLGUKC-UHFFFAOYSA-N 5-(3-morpholin-4-ylpropylcarbamoylamino)-3-[4-[[3-(trifluoromethyl)benzoyl]amino]phenyl]-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(NC(=O)C=3C=C(C=CC=3)C(F)(F)F)=CC=2)C(C(=O)N)=C1NC(=O)NCCCN1CCOCC1 JJKVPTCDYLGUKC-UHFFFAOYSA-N 0.000 claims abstract description 4
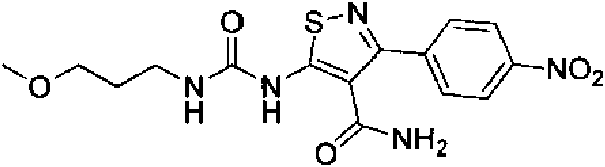
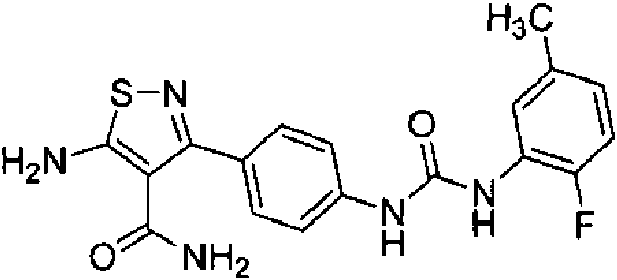
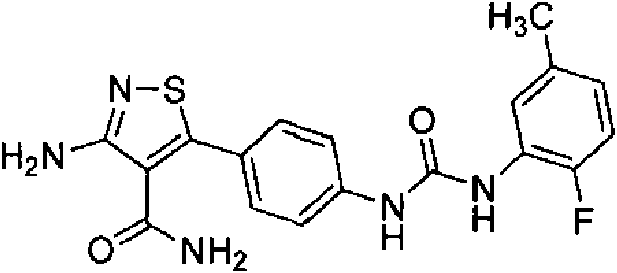
- VJYLJSYNDVZYLY-UHFFFAOYSA-N 5-amino-3-[4-[(2-fluoro-5-methylphenyl)carbamoylamino]phenyl]-1,2-thiazole-4-carboxamide Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C=2C(=C(N)SN=2)C(N)=O)=C1 VJYLJSYNDVZYLY-UHFFFAOYSA-N 0.000 claims abstract description 4
- ZJBJTRVSIRUZGZ-UHFFFAOYSA-N 5-amino-3-[4-[(4-methylphenyl)carbamoylamino]phenyl]-1,2-thiazole-4-carboxamide Chemical compound C1=CC(C)=CC=C1NC(=O)NC1=CC=C(C=2C(=C(N)SN=2)C(N)=O)C=C1 ZJBJTRVSIRUZGZ-UHFFFAOYSA-N 0.000 claims abstract description 4
- KJXMKVRWXYEKJV-UHFFFAOYSA-N 3-[2-methyl-4-(phenylcarbamoylamino)phenyl]-5-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound C=1C=C(C=2C(=C(NC(=O)NCCCN3CCOCC3)SN=2)C(N)=O)C(C)=CC=1NC(=O)NC1=CC=CC=C1 KJXMKVRWXYEKJV-UHFFFAOYSA-N 0.000 claims abstract description 3
- MWEYSKGHFYPKGD-UHFFFAOYSA-N 3-[2-methyl-4-[(3-methylphenyl)carbamoylamino]phenyl]-5-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound CC1=CC=CC(NC(=O)NC=2C=C(C)C(C=3C(=C(NC(=O)NCCCN4CCOCC4)SN=3)C(N)=O)=CC=2)=C1 MWEYSKGHFYPKGD-UHFFFAOYSA-N 0.000 claims abstract description 3
- SLHDRMBMCYTUQL-UHFFFAOYSA-N 3-[2-methyl-4-[(4-methylphenyl)carbamoylamino]phenyl]-5-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound C1=CC(C)=CC=C1NC(=O)NC(C=C1C)=CC=C1C1=NSC(NC(=O)NCCCN2CCOCC2)=C1C(N)=O SLHDRMBMCYTUQL-UHFFFAOYSA-N 0.000 claims abstract description 3
- IKAHITUCYMQCPQ-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[2-methyl-4-(phenylcarbamoylamino)phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound C=1C=C(C=2C(=C(NC(=O)NCCC(O)=O)SN=2)C(N)=O)C(C)=CC=1NC(=O)NC1=CC=CC=C1 IKAHITUCYMQCPQ-UHFFFAOYSA-N 0.000 claims abstract description 3
- JIGHQBLECILCFH-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[2-methyl-4-[(3-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound CC1=CC=CC(NC(=O)NC=2C=C(C)C(C=3C(=C(NC(=O)NCCC(O)=O)SN=3)C(N)=O)=CC=2)=C1 JIGHQBLECILCFH-UHFFFAOYSA-N 0.000 claims abstract description 3
- LMEJYASQKRQUBG-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[2-methyl-4-[(4-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound C1=CC(C)=CC=C1NC(=O)NC(C=C1C)=CC=C1C1=NSC(NC(=O)NCCC(O)=O)=C1C(N)=O LMEJYASQKRQUBG-UHFFFAOYSA-N 0.000 claims abstract description 3
- XEXJXFMENUEWSY-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[4-(phenylcarbamoylamino)phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound NC(=O)C1=C(NC(=O)NCCC(O)=O)SN=C1C(C=C1)=CC=C1NC(=O)NC1=CC=CC=C1 XEXJXFMENUEWSY-UHFFFAOYSA-N 0.000 claims abstract description 3
- ZQQRMBYSEJOEHH-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[4-[(2-fluoro-5-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C=2C(=C(NC(=O)NCCC(O)=O)SN=2)C(N)=O)=C1 ZQQRMBYSEJOEHH-UHFFFAOYSA-N 0.000 claims abstract description 3
- JRCFEYDZTOIQDM-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[4-[(3-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound CC1=CC=CC(NC(=O)NC=2C=CC(=CC=2)C=2C(=C(NC(=O)NCCC(O)=O)SN=2)C(N)=O)=C1 JRCFEYDZTOIQDM-UHFFFAOYSA-N 0.000 claims abstract description 3
- QKHGHVGCDZGVJM-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[4-[(4-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound C1=CC(C)=CC=C1NC(=O)NC1=CC=C(C=2C(=C(NC(=O)NCCC(O)=O)SN=2)C(N)=O)C=C1 QKHGHVGCDZGVJM-UHFFFAOYSA-N 0.000 claims abstract description 3
- FHUAOARWFLKDAW-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[4-[[2-fluoro-5-(trifluoromethyl)phenyl]carbamoylamino]-2-methylphenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound C=1C=C(C=2C(=C(NC(=O)NCCC(O)=O)SN=2)C(N)=O)C(C)=CC=1NC(=O)NC1=CC(C(F)(F)F)=CC=C1F FHUAOARWFLKDAW-UHFFFAOYSA-N 0.000 claims abstract description 3
- OPPWLAIYCXUKBY-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[4-[[2-fluoro-5-(trifluoromethyl)phenyl]carbamoylamino]phenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound NC(=O)C1=C(NC(=O)NCCC(O)=O)SN=C1C(C=C1)=CC=C1NC(=O)NC1=CC(C(F)(F)F)=CC=C1F OPPWLAIYCXUKBY-UHFFFAOYSA-N 0.000 claims abstract description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 33
- 208000035475 disorder Diseases 0.000 claims description 19
- 238000000034 method Methods 0.000 claims description 14
- 201000010099 disease Diseases 0.000 claims description 13
- 230000002062 proliferating effect Effects 0.000 claims description 12
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 10
- 210000004204 blood vessel Anatomy 0.000 claims description 8
- 208000002780 macular degeneration Diseases 0.000 claims description 8
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 8
- 206010012689 Diabetic retinopathy Diseases 0.000 claims description 7
- 206010028980 Neoplasm Diseases 0.000 claims description 7
- 201000011510 cancer Diseases 0.000 claims description 7
- 201000004681 Psoriasis Diseases 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 5
- 230000003176 fibrotic effect Effects 0.000 claims description 5
- 210000003584 mesangial cell Anatomy 0.000 claims description 5
- 208000030159 metabolic disease Diseases 0.000 claims description 5
- 206010064930 age-related macular degeneration Diseases 0.000 claims description 4
- 206010003246 arthritis Diseases 0.000 claims description 4
- 201000001320 Atherosclerosis Diseases 0.000 claims description 3
- 206010063209 Chronic allograft nephropathy Diseases 0.000 claims description 3
- 208000007342 Diabetic Nephropathies Diseases 0.000 claims description 3
- 206010018364 Glomerulonephritis Diseases 0.000 claims description 3
- 206010061218 Inflammation Diseases 0.000 claims description 3
- 201000002154 Pterygium Diseases 0.000 claims description 3
- 206010038933 Retinopathy of prematurity Diseases 0.000 claims description 3
- 208000034841 Thrombotic Microangiopathies Diseases 0.000 claims description 3
- 206010052779 Transplant rejections Diseases 0.000 claims description 3
- 208000019425 cirrhosis of liver Diseases 0.000 claims description 3
- 206010012601 diabetes mellitus Diseases 0.000 claims description 3
- 208000033679 diabetic kidney disease Diseases 0.000 claims description 3
- 230000004054 inflammatory process Effects 0.000 claims description 3
- 230000003211 malignant effect Effects 0.000 claims description 3
- 201000009925 nephrosclerosis Diseases 0.000 claims description 3
- 230000004770 neurodegeneration Effects 0.000 claims description 3
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 3
- 239000008194 pharmaceutical composition Substances 0.000 claims description 3
- 208000037803 restenosis Diseases 0.000 claims description 3
- 208000011580 syndromic disease Diseases 0.000 claims description 3
- 230000029663 wound healing Effects 0.000 claims description 3
- UUIQMZJEGPQKFD-UHFFFAOYSA-N n-butyric acid methyl ester Natural products CCCC(=O)OC UUIQMZJEGPQKFD-UHFFFAOYSA-N 0.000 claims 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 abstract description 23
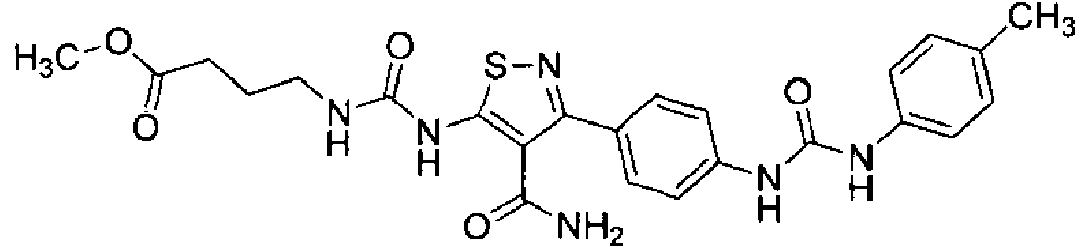
- LUIRMPBUMLMGFN-UHFFFAOYSA-N 4-[[4-carbamoyl-3-[4-[(4-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-5-yl]carbamoylamino]butanoic acid Chemical compound C1=CC(C)=CC=C1NC(=O)NC1=CC=C(C=2C(=C(NC(=O)NCCCC(O)=O)SN=2)C(N)=O)C=C1 LUIRMPBUMLMGFN-UHFFFAOYSA-N 0.000 abstract description 3
- FWBUUGDBUKHCQX-UHFFFAOYSA-N 3-[4-[[2-fluoro-5-(trifluoromethyl)phenyl]carbamoylamino]phenyl]-5-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(NC(=O)NC=3C(=CC=C(C=3)C(F)(F)F)F)=CC=2)C(C(=O)N)=C1NC(=O)NCCCN1CCOCC1 FWBUUGDBUKHCQX-UHFFFAOYSA-N 0.000 abstract description 2
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 135
- 239000007787 solid Substances 0.000 description 135
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical class OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 82
- 239000000203 mixture Substances 0.000 description 79
- 238000006243 chemical reaction Methods 0.000 description 64
- 235000019439 ethyl acetate Nutrition 0.000 description 64
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 54
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 52
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 43
- 238000002360 preparation method Methods 0.000 description 43
- 239000000243 solution Substances 0.000 description 43
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 39
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 38
- 239000011541 reaction mixture Substances 0.000 description 34
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 33
- 125000000217 alkyl group Chemical group 0.000 description 32
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 31
- 125000003118 aryl group Chemical group 0.000 description 31
- 125000004432 carbon atom Chemical group C* 0.000 description 29
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 28
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 27
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 27
- 238000005160 1H NMR spectroscopy Methods 0.000 description 26
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 26
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 25
- 239000012267 brine Substances 0.000 description 22
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 22
- 102000005962 receptors Human genes 0.000 description 21
- 230000019491 signal transduction Effects 0.000 description 21
- 239000012453 solvate Substances 0.000 description 21
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 20
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 20
- 239000000706 filtrate Substances 0.000 description 19
- 229910052739 hydrogen Inorganic materials 0.000 description 19
- 108020003175 receptors Proteins 0.000 description 19
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 18
- 229910052757 nitrogen Inorganic materials 0.000 description 17
- 125000001424 substituent group Chemical group 0.000 description 17
- 239000000725 suspension Substances 0.000 description 17
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 17
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 16
- 125000001072 heteroaryl group Chemical group 0.000 description 16
- 239000000651 prodrug Substances 0.000 description 16
- 229940002612 prodrug Drugs 0.000 description 16
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 15
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 15
- 125000006413 ring segment Chemical group 0.000 description 15
- 239000000758 substrate Substances 0.000 description 15
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 14
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 14
- 239000002904 solvent Substances 0.000 description 14
- 230000003197 catalytic effect Effects 0.000 description 13
- 125000000753 cycloalkyl group Chemical group 0.000 description 13
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 13
- 239000000463 material Substances 0.000 description 13
- 239000000047 product Substances 0.000 description 13
- 229910052717 sulfur Inorganic materials 0.000 description 13
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 12
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 12
- 125000004122 cyclic group Chemical group 0.000 description 12
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 12
- 229910052938 sodium sulfate Inorganic materials 0.000 description 12
- 235000011152 sodium sulphate Nutrition 0.000 description 12
- 210000004027 cell Anatomy 0.000 description 11
- 238000001914 filtration Methods 0.000 description 11
- 229910052760 oxygen Inorganic materials 0.000 description 11
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 10
- 125000000623 heterocyclic group Chemical group 0.000 description 10
- 239000001301 oxygen Substances 0.000 description 10
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 9
- 229910052799 carbon Inorganic materials 0.000 description 9
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 9
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 9
- 230000026731 phosphorylation Effects 0.000 description 9
- 238000006366 phosphorylation reaction Methods 0.000 description 9
- 239000000843 powder Substances 0.000 description 9
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 9
- IVEWVUMNGBFGMO-UHFFFAOYSA-N 3-(4-aminophenyl)-5-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(N)=CC=2)C(C(=O)N)=C1NC(=O)NCCCN1CCOCC1 IVEWVUMNGBFGMO-UHFFFAOYSA-N 0.000 description 8
- 101150065749 Churc1 gene Proteins 0.000 description 8
- 206010012812 Diffuse cutaneous mastocytosis Diseases 0.000 description 8
- 125000003710 aryl alkyl group Chemical group 0.000 description 8
- 150000002148 esters Chemical class 0.000 description 8
- 238000004128 high performance liquid chromatography Methods 0.000 description 8
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 8
- 230000005764 inhibitory process Effects 0.000 description 8
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 8
- 235000019341 magnesium sulphate Nutrition 0.000 description 8
- 235000017550 sodium carbonate Nutrition 0.000 description 8
- 229910000029 sodium carbonate Inorganic materials 0.000 description 8
- 125000004434 sulfur atom Chemical group 0.000 description 8
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 7
- MGYGFNQQGAQEON-UHFFFAOYSA-N 4-tolyl isocyanate Chemical compound CC1=CC=C(N=C=O)C=C1 MGYGFNQQGAQEON-UHFFFAOYSA-N 0.000 description 7
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 7
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 7
- CSCPPACGZOOCGX-WFGJKAKNSA-N acetone d6 Chemical compound [2H]C([2H])([2H])C(=O)C([2H])([2H])[2H] CSCPPACGZOOCGX-WFGJKAKNSA-N 0.000 description 7
- 125000003342 alkenyl group Chemical group 0.000 description 7
- 125000000304 alkynyl group Chemical group 0.000 description 7
- 125000004429 atom Chemical group 0.000 description 7
- 239000003814 drug Substances 0.000 description 7
- 239000001257 hydrogen Substances 0.000 description 7
- 230000004044 response Effects 0.000 description 7
- 229920006395 saturated elastomer Polymers 0.000 description 7
- 239000000741 silica gel Substances 0.000 description 7
- 229910002027 silica gel Inorganic materials 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- QGJOPFRUJISHPQ-UHFFFAOYSA-N Carbon disulfide Chemical compound S=C=S QGJOPFRUJISHPQ-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 6
- 101000727826 Homo sapiens Tyrosine-protein kinase RYK Proteins 0.000 description 6
- 238000005481 NMR spectroscopy Methods 0.000 description 6
- 239000007832 Na2SO4 Substances 0.000 description 6
- 102000014400 SH2 domains Human genes 0.000 description 6
- 108050003452 SH2 domains Proteins 0.000 description 6
- 102100029759 Tyrosine-protein kinase RYK Human genes 0.000 description 6
- 125000003545 alkoxy group Chemical group 0.000 description 6
- 239000011575 calcium Substances 0.000 description 6
- 239000012043 crude product Substances 0.000 description 6
- 229940079593 drug Drugs 0.000 description 6
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 6
- 239000000284 extract Substances 0.000 description 6
- 125000001153 fluoro group Chemical group F* 0.000 description 6
- 230000002401 inhibitory effect Effects 0.000 description 6
- 230000003834 intracellular effect Effects 0.000 description 6
- 239000003446 ligand Substances 0.000 description 6
- 230000002503 metabolic effect Effects 0.000 description 6
- 239000002953 phosphate buffered saline Substances 0.000 description 6
- 229910000027 potassium carbonate Inorganic materials 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 6
- 230000001225 therapeutic effect Effects 0.000 description 6
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 5
- NZECOPVCNLQMTG-UHFFFAOYSA-N 1-[4-[4-cyano-3-[(2,4-dimethoxyphenyl)methylamino]-1,2-thiazol-5-yl]phenyl]-3-(2-fluoro-5-methylphenyl)urea Chemical compound COC1=CC(OC)=CC=C1CNC1=NSC(C=2C=CC(NC(=O)NC=3C(=CC=C(C)C=3)F)=CC=2)=C1C#N NZECOPVCNLQMTG-UHFFFAOYSA-N 0.000 description 5
- GLSUJZPVKMKUPJ-UHFFFAOYSA-N 1-fluoro-2-isocyanato-4-methylbenzene Chemical compound CC1=CC=C(F)C(N=C=O)=C1 GLSUJZPVKMKUPJ-UHFFFAOYSA-N 0.000 description 5
- PSLKWTVUMXYPNR-UHFFFAOYSA-N 5-amino-3-(4-nitrophenyl)-1,2-thiazole-4-carbonitrile Chemical compound N#CC1=C(N)SN=C1C1=CC=C([N+]([O-])=O)C=C1 PSLKWTVUMXYPNR-UHFFFAOYSA-N 0.000 description 5
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 5
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 5
- 108091000080 Phosphotransferase Proteins 0.000 description 5
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 5
- 108091008605 VEGF receptors Proteins 0.000 description 5
- 235000019270 ammonium chloride Nutrition 0.000 description 5
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- 229910052791 calcium Inorganic materials 0.000 description 5
- 239000003054 catalyst Substances 0.000 description 5
- 230000004663 cell proliferation Effects 0.000 description 5
- 125000000392 cycloalkenyl group Chemical group 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 125000005843 halogen group Chemical group 0.000 description 5
- 239000005457 ice water Substances 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 229910052751 metal Inorganic materials 0.000 description 5
- 239000002184 metal Substances 0.000 description 5
- 102000020233 phosphotransferase Human genes 0.000 description 5
- 230000001105 regulatory effect Effects 0.000 description 5
- 230000011664 signaling Effects 0.000 description 5
- 230000000638 stimulation Effects 0.000 description 5
- 238000006467 substitution reaction Methods 0.000 description 5
- HYHMQFQMUKYBPI-UHFFFAOYSA-N tert-butyl n-[4-(3-chloro-4-cyano-1,2-thiazol-5-yl)phenyl]carbamate Chemical compound C1=CC(NC(=O)OC(C)(C)C)=CC=C1C1=C(C#N)C(Cl)=NS1 HYHMQFQMUKYBPI-UHFFFAOYSA-N 0.000 description 5
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 description 4
- NCOSUPYQFRQJTJ-UHFFFAOYSA-N 3-(4-nitrophenyl)-5-[(2-oxopyrrolidine-1-carbonyl)amino]-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(=CC=2)[N+]([O-])=O)C(C(=O)N)=C1NC(=O)N1CCCC1=O NCOSUPYQFRQJTJ-UHFFFAOYSA-N 0.000 description 4
- DWGDVSHUBRFDPV-UHFFFAOYSA-N 3-[[3-(4-aminophenyl)-4-carbamoyl-1,2-thiazol-5-yl]carbamoylamino]propyl acetate Chemical compound NC(=O)C1=C(NC(=O)NCCCOC(=O)C)SN=C1C1=CC=C(N)C=C1 DWGDVSHUBRFDPV-UHFFFAOYSA-N 0.000 description 4
- HFTYFHFQNRQHGR-UHFFFAOYSA-N 5-amino-3-(3-aminophenyl)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(N)SN=C1C1=CC=CC(N)=C1 HFTYFHFQNRQHGR-UHFFFAOYSA-N 0.000 description 4
- NLSJUCHHLFWKSS-UHFFFAOYSA-N 5-amino-3-(3-nitrophenyl)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(N)SN=C1C1=CC=CC([N+]([O-])=O)=C1 NLSJUCHHLFWKSS-UHFFFAOYSA-N 0.000 description 4
- MTVBLZKFCSNXFC-UHFFFAOYSA-N 5-amino-3-(4-aminophenyl)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(N)SN=C1C1=CC=C(N)C=C1 MTVBLZKFCSNXFC-UHFFFAOYSA-N 0.000 description 4
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 4
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 4
- 229920001213 Polysorbate 20 Polymers 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 4
- 125000002877 alkyl aryl group Chemical group 0.000 description 4
- 239000012300 argon atmosphere Substances 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 230000001086 cytosolic effect Effects 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 239000000839 emulsion Substances 0.000 description 4
- 230000014509 gene expression Effects 0.000 description 4
- 239000003102 growth factor Substances 0.000 description 4
- 229910052736 halogen Inorganic materials 0.000 description 4
- 150000002367 halogens Chemical group 0.000 description 4
- 239000012535 impurity Substances 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 230000003993 interaction Effects 0.000 description 4
- 238000000021 kinase assay Methods 0.000 description 4
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 4
- 235000011181 potassium carbonates Nutrition 0.000 description 4
- NROKBHXJSPEDAR-UHFFFAOYSA-M potassium fluoride Chemical compound [F-].[K+] NROKBHXJSPEDAR-UHFFFAOYSA-M 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000007858 starting material Substances 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 4
- 238000010626 work up procedure Methods 0.000 description 4
- YUKPVAPWXZMVME-UHFFFAOYSA-N 1-[4-(3-amino-4-cyano-1,2-thiazol-5-yl)phenyl]-3-(2-fluoro-5-methylphenyl)urea Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C2=C(C(N)=NS2)C#N)=C1 YUKPVAPWXZMVME-UHFFFAOYSA-N 0.000 description 3
- OTJPHAIMMGMIRL-UHFFFAOYSA-N 1-[4-cyano-3-(4-nitrophenyl)-1,2-thiazol-5-yl]-3-(3-morpholin-4-ylpropyl)urea Chemical compound C1=CC([N+](=O)[O-])=CC=C1C1=NSC(NC(=O)NCCCN2CCOCC2)=C1C#N OTJPHAIMMGMIRL-UHFFFAOYSA-N 0.000 description 3
- RUNARDFVMLWILC-UHFFFAOYSA-N 3,5-dichloro-1,2-thiazole-4-carbonitrile Chemical compound ClC1=NSC(Cl)=C1C#N RUNARDFVMLWILC-UHFFFAOYSA-N 0.000 description 3
- DCDCADZVJDJYNC-UHFFFAOYSA-N 3-(4-aminophenyl)-5-(3-pyrrolidin-1-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(N)=CC=2)C(C(=O)N)=C1NC(=O)NCCCN1CCCC1 DCDCADZVJDJYNC-UHFFFAOYSA-N 0.000 description 3
- BKYIRQVDTJNSKN-UHFFFAOYSA-N 3-(4-aminophenyl)-5-[(2-oxopyrrolidine-1-carbonyl)amino]-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(N)=CC=2)C(C(=O)N)=C1NC(=O)N1CCCC1=O BKYIRQVDTJNSKN-UHFFFAOYSA-N 0.000 description 3
- PRIWEOJZCKENRC-UHFFFAOYSA-N 3-(4-nitrophenyl)-5-(3-pyrrolidin-1-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(=CC=2)[N+]([O-])=O)C(C(=O)N)=C1NC(=O)NCCCN1CCCC1 PRIWEOJZCKENRC-UHFFFAOYSA-N 0.000 description 3
- RUJYJCANMOTJMO-UHFFFAOYSA-N 3-(trifluoromethyl)benzoyl chloride Chemical compound FC(F)(F)C1=CC=CC(C(Cl)=O)=C1 RUJYJCANMOTJMO-UHFFFAOYSA-N 0.000 description 3
- GCQYCMMQALQFHG-UHFFFAOYSA-N 3-[(2,4-dimethoxyphenyl)methylamino]-5-[4-[(2-fluoro-5-methylphenyl)carbamoylamino]phenyl]-1,2-thiazole-4-carboxamide Chemical compound COC1=CC(OC)=CC=C1CNC1=NSC(C=2C=CC(NC(=O)NC=3C(=CC=C(C)C=3)F)=CC=2)=C1C(N)=O GCQYCMMQALQFHG-UHFFFAOYSA-N 0.000 description 3
- FAPBVPAUCWORHN-UHFFFAOYSA-N 3-[[4-carbamoyl-3-(4-nitrophenyl)-1,2-thiazol-5-yl]carbamoylamino]propyl acetate Chemical compound NC(=O)C1=C(NC(=O)NCCCOC(=O)C)SN=C1C1=CC=C([N+]([O-])=O)C=C1 FAPBVPAUCWORHN-UHFFFAOYSA-N 0.000 description 3
- AEERMDZPXWNANY-UHFFFAOYSA-N 3-amino-5-[4-[(2-fluoro-5-methylphenyl)carbamoylamino]phenyl]-1,2-thiazole-4-carboxamide Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C2=C(C(N)=NS2)C(N)=O)=C1 AEERMDZPXWNANY-UHFFFAOYSA-N 0.000 description 3
- HUFBWESKARHDOZ-UHFFFAOYSA-N 4-[[4-carbamoyl-3-(4-nitrophenyl)-1,2-thiazol-5-yl]carbamoylamino]butanoic acid Chemical compound NC(=O)C1=C(NC(=O)NCCCC(O)=O)SN=C1C1=CC=C([N+]([O-])=O)C=C1 HUFBWESKARHDOZ-UHFFFAOYSA-N 0.000 description 3
- AHPOWMWRGUZUKU-UHFFFAOYSA-N 5-(3-hydroxypropylcarbamoylamino)-3-(4-nitrophenyl)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(NC(=O)NCCCO)SN=C1C1=CC=C([N+]([O-])=O)C=C1 AHPOWMWRGUZUKU-UHFFFAOYSA-N 0.000 description 3
- RBGLFBWVOYONGT-UHFFFAOYSA-N 5-(3-methoxypropylcarbamoylamino)-3-(4-nitrophenyl)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(NC(=O)NCCCOC)SN=C1C1=CC=C([N+]([O-])=O)C=C1 RBGLFBWVOYONGT-UHFFFAOYSA-N 0.000 description 3
- XLZMEASIFJCIPE-UHFFFAOYSA-N 5-(3-morpholin-4-ylpropylcarbamoylamino)-3-(4-nitrophenyl)-1,2-thiazole-4-carboxamide Chemical compound S1N=C(C=2C=CC(=CC=2)[N+]([O-])=O)C(C(=O)N)=C1NC(=O)NCCCN1CCOCC1 XLZMEASIFJCIPE-UHFFFAOYSA-N 0.000 description 3
- UCSCCPRUVOVKBL-UHFFFAOYSA-N 5-[4-[(2-fluoro-5-methylphenyl)carbamoylamino]phenyl]-3-(3-morpholin-4-ylpropylamino)-1,2-thiazole-4-carboxamide Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C2=C(C(NCCCN3CCOCC3)=NS2)C(N)=O)=C1 UCSCCPRUVOVKBL-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- FERIUCNNQQJTOY-UHFFFAOYSA-M Butyrate Chemical compound CCCC([O-])=O FERIUCNNQQJTOY-UHFFFAOYSA-M 0.000 description 3
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 3
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 3
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 3
- 241000282414 Homo sapiens Species 0.000 description 3
- 101000692455 Homo sapiens Platelet-derived growth factor receptor beta Proteins 0.000 description 3
- 101000851007 Homo sapiens Vascular endothelial growth factor receptor 2 Proteins 0.000 description 3
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 3
- 150000001204 N-oxides Chemical class 0.000 description 3
- 102100026547 Platelet-derived growth factor receptor beta Human genes 0.000 description 3
- 241000534944 Thia Species 0.000 description 3
- 230000002159 abnormal effect Effects 0.000 description 3
- 125000001931 aliphatic group Chemical group 0.000 description 3
- 150000001413 amino acids Chemical group 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical group 0.000 description 3
- 239000000969 carrier Substances 0.000 description 3
- 230000036755 cellular response Effects 0.000 description 3
- 229910052801 chlorine Inorganic materials 0.000 description 3
- 239000000460 chlorine Substances 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000004440 column chromatography Methods 0.000 description 3
- 239000006071 cream Substances 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 229910052805 deuterium Inorganic materials 0.000 description 3
- 230000004069 differentiation Effects 0.000 description 3
- 229920001971 elastomer Polymers 0.000 description 3
- 210000002889 endothelial cell Anatomy 0.000 description 3
- 229910052731 fluorine Inorganic materials 0.000 description 3
- 239000011737 fluorine Substances 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 239000012948 isocyanate Substances 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- CUONGYYJJVDODC-UHFFFAOYSA-N malononitrile Chemical compound N#CCC#N CUONGYYJJVDODC-UHFFFAOYSA-N 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 150000002825 nitriles Chemical class 0.000 description 3
- 230000003287 optical effect Effects 0.000 description 3
- MUMZUERVLWJKNR-UHFFFAOYSA-N oxoplatinum Chemical compound [Pt]=O MUMZUERVLWJKNR-UHFFFAOYSA-N 0.000 description 3
- 230000037361 pathway Effects 0.000 description 3
- ASWRNXKPCDWHLP-UHFFFAOYSA-N phenyl n-[4-cyano-3-(4-nitrophenyl)-1,2-thiazol-5-yl]carbamate Chemical compound C1=CC([N+](=O)[O-])=CC=C1C1=NSC(NC(=O)OC=2C=CC=CC=2)=C1C#N ASWRNXKPCDWHLP-UHFFFAOYSA-N 0.000 description 3
- 229910003446 platinum oxide Inorganic materials 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 3
- 235000017557 sodium bicarbonate Nutrition 0.000 description 3
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 3
- QOWBXWFYRXSBAS-UHFFFAOYSA-N (2,4-dimethoxyphenyl)methanamine Chemical compound COC1=CC=C(CN)C(OC)=C1 QOWBXWFYRXSBAS-UHFFFAOYSA-N 0.000 description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 2
- DIGYITSFWJORIL-UHFFFAOYSA-N 1-[4-(5-chloro-4-cyano-1,2-thiazol-3-yl)phenyl]-3-(2-fluoro-5-methylphenyl)urea Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C=2C(=C(Cl)SN=2)C#N)=C1 DIGYITSFWJORIL-UHFFFAOYSA-N 0.000 description 2
- CSFOTKSGYQNSRD-UHFFFAOYSA-N 1-[4-[4-cyano-3-(3-morpholin-4-ylpropylamino)-1,2-thiazol-5-yl]phenyl]-3-(2-fluoro-5-methylphenyl)urea Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C2=C(C(NCCCN3CCOCC3)=NS2)C#N)=C1 CSFOTKSGYQNSRD-UHFFFAOYSA-N 0.000 description 2
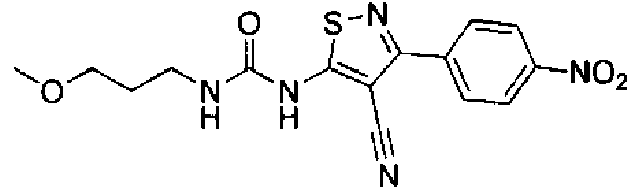
- WFWWKAUKRCZJJW-UHFFFAOYSA-N 1-[4-cyano-3-(4-nitrophenyl)-1,2-thiazol-5-yl]-3-(3-methoxypropyl)urea Chemical compound N#CC1=C(NC(=O)NCCCOC)SN=C1C1=CC=C([N+]([O-])=O)C=C1 WFWWKAUKRCZJJW-UHFFFAOYSA-N 0.000 description 2
- YKRRHBDQHSMKEF-UHFFFAOYSA-N 1-[4-cyano-3-(4-nitrophenyl)-1,2-thiazol-5-yl]-3-(3-pyrrolidin-1-ylpropyl)urea Chemical compound C1=CC([N+](=O)[O-])=CC=C1C1=NSC(NC(=O)NCCCN2CCCC2)=C1C#N YKRRHBDQHSMKEF-UHFFFAOYSA-N 0.000 description 2
- XEZNGIUYQVAUSS-UHFFFAOYSA-N 18-crown-6 Chemical compound C1COCCOCCOCCOCCOCCO1 XEZNGIUYQVAUSS-UHFFFAOYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- MVNOWNDWPWJXQR-UHFFFAOYSA-N 2-[amino-(4-nitrophenyl)methylidene]propanedinitrile Chemical compound N#CC(C#N)=C(N)C1=CC=C([N+]([O-])=O)C=C1 MVNOWNDWPWJXQR-UHFFFAOYSA-N 0.000 description 2
- RAWBQFHDJWAXKE-UHFFFAOYSA-N 2-[hydroxy-(4-nitrophenyl)methylidene]propanedinitrile Chemical compound N#CC(C#N)=C(O)C1=CC=C([N+]([O-])=O)C=C1 RAWBQFHDJWAXKE-UHFFFAOYSA-N 0.000 description 2
- VHQNWVNVMDJLTF-UHFFFAOYSA-N 2-[methoxy-(4-nitrophenyl)methylidene]propanedinitrile Chemical compound N#CC(C#N)=C(OC)C1=CC=C([N+]([O-])=O)C=C1 VHQNWVNVMDJLTF-UHFFFAOYSA-N 0.000 description 2
- TYQHNWWGKHTCBA-UHFFFAOYSA-N 3-(4-aminophenyl)-5-(3-hydroxypropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(NC(=O)NCCCO)SN=C1C1=CC=C(N)C=C1 TYQHNWWGKHTCBA-UHFFFAOYSA-N 0.000 description 2
- LDCQPCHMNOJESG-UHFFFAOYSA-N 3-(4-aminophenyl)-5-(3-methoxypropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(NC(=O)NCCCOC)SN=C1C1=CC=C(N)C=C1 LDCQPCHMNOJESG-UHFFFAOYSA-N 0.000 description 2
- AXHOLCUYAMMEGU-UHFFFAOYSA-N 3-(4-aminophenyl)-5-chloro-1,2-thiazole-4-carbonitrile Chemical compound C1=CC(N)=CC=C1C1=NSC(Cl)=C1C#N AXHOLCUYAMMEGU-UHFFFAOYSA-N 0.000 description 2
- UIKUBYKUYUSRSM-UHFFFAOYSA-N 3-morpholinopropylamine Chemical compound NCCCN1CCOCC1 UIKUBYKUYUSRSM-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- SVWJPCAFPRQWJF-UHFFFAOYSA-N 5-(4-aminophenyl)-3-chloro-1,2-thiazole-4-carbonitrile Chemical compound C1=CC(N)=CC=C1C1=C(C#N)C(Cl)=NS1 SVWJPCAFPRQWJF-UHFFFAOYSA-N 0.000 description 2
- TYBCFFQLXWWXJB-UHFFFAOYSA-N 5-amino-3-(3-nitrophenyl)-1,2-thiazole-4-carbonitrile Chemical compound N#CC1=C(N)SN=C1C1=CC=CC([N+]([O-])=O)=C1 TYBCFFQLXWWXJB-UHFFFAOYSA-N 0.000 description 2
- JOVJBGJVLBSCJW-UHFFFAOYSA-N 5-amino-3-[3-(hydroxyamino)phenyl]-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(N)SN=C1C1=CC=CC(NO)=C1 JOVJBGJVLBSCJW-UHFFFAOYSA-N 0.000 description 2
- FNYPNCJYDWZYCG-UHFFFAOYSA-N 5-amino-3-[3-(phenylcarbamoylamino)phenyl]-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(N)SN=C1C1=CC=CC(NC(=O)NC=2C=CC=CC=2)=C1 FNYPNCJYDWZYCG-UHFFFAOYSA-N 0.000 description 2
- WFUKOKLJQOUMRV-UHFFFAOYSA-N 5-amino-3-[3-[[3-(trifluoromethyl)benzoyl]amino]phenyl]-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(N)SN=C1C1=CC=CC(NC(=O)C=2C=C(C=CC=2)C(F)(F)F)=C1 WFUKOKLJQOUMRV-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- 108010081589 Becaplermin Proteins 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- 0 COC(CCCNC(NC(SN=*C1c(cc2)ccc2[N+]([O-])=O)=C1C#N)=O)=O Chemical compound COC(CCCNC(NC(SN=*C1c(cc2)ccc2[N+]([O-])=O)=C1C#N)=O)=O 0.000 description 2
- 201000009030 Carcinoma Diseases 0.000 description 2
- OKKJLVBELUTLKV-MZCSYVLQSA-N Deuterated methanol Chemical compound [2H]OC([2H])([2H])[2H] OKKJLVBELUTLKV-MZCSYVLQSA-N 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- 102000016359 Fibronectins Human genes 0.000 description 2
- 108010067306 Fibronectins Proteins 0.000 description 2
- OUVXYXNWSVIOSJ-UHFFFAOYSA-N Fluo-4 Chemical compound CC1=CC=C(N(CC(O)=O)CC(O)=O)C(OCCOC=2C(=CC=C(C=2)C2=C3C=C(F)C(=O)C=C3OC3=CC(O)=C(F)C=C32)N(CC(O)=O)CC(O)=O)=C1 OUVXYXNWSVIOSJ-UHFFFAOYSA-N 0.000 description 2
- YSWHPLCDIMUKFE-QWRGUYRKSA-N Glu-Tyr Chemical compound OC(=O)CC[C@H](N)C(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 YSWHPLCDIMUKFE-QWRGUYRKSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerol Natural products OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical class CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- UWHHODHRCAKPNA-UHFFFAOYSA-N N-[2-amino-1-cyano-2-(4-nitrophenyl)ethenyl]methanethioamide Chemical compound S=CNC(C#N)=C(N)C1=CC=C([N+]([O-])=O)C=C1 UWHHODHRCAKPNA-UHFFFAOYSA-N 0.000 description 2
- 102000003992 Peroxidases Human genes 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- 206010039491 Sarcoma Diseases 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 2
- UBVOLHQIEQVXGM-UHFFFAOYSA-N [4-[(2-methylpropan-2-yl)oxycarbonylamino]phenyl]boronic acid Chemical compound CC(C)(C)OC(=O)NC1=CC=C(B(O)O)C=C1 UBVOLHQIEQVXGM-UHFFFAOYSA-N 0.000 description 2
- UACPLQANRQVKHE-UHFFFAOYSA-N [amino-[(4-hydroxyphenyl)methyl]phosphanyl]formic acid Chemical group OC(=O)P(N)CC1=CC=C(O)C=C1 UACPLQANRQVKHE-UHFFFAOYSA-N 0.000 description 2
- 230000001594 aberrant effect Effects 0.000 description 2
- 125000004423 acyloxy group Chemical group 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 125000003158 alcohol group Chemical group 0.000 description 2
- 150000001447 alkali salts Chemical class 0.000 description 2
- 125000005206 alkoxycarbonyloxymethyl group Chemical group 0.000 description 2
- 125000004414 alkyl thio group Chemical group 0.000 description 2
- 125000000266 alpha-aminoacyl group Chemical group 0.000 description 2
- 125000000539 amino acid group Chemical group 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000002585 base Chemical class 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- RIIWUGSYXOBDMC-UHFFFAOYSA-N benzene-1,2-diamine;hydron;dichloride Chemical compound Cl.Cl.NC1=CC=CC=C1N RIIWUGSYXOBDMC-UHFFFAOYSA-N 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 150000001649 bromium compounds Chemical class 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 239000004202 carbamide Substances 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 230000024245 cell differentiation Effects 0.000 description 2
- 230000032823 cell division Effects 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000009918 complex formation Effects 0.000 description 2
- 125000004093 cyano group Chemical group *C#N 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- IRDLUHRVLVEUHA-UHFFFAOYSA-N diethyl dithiophosphate Chemical compound CCOP(S)(=S)OCC IRDLUHRVLVEUHA-UHFFFAOYSA-N 0.000 description 2
- 238000006471 dimerization reaction Methods 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- VHVPPDQPTYJSNO-UHFFFAOYSA-L disodium;2,2-dicyanoethene-1,1-dithiolate Chemical compound [Na]SC(S[Na])=C(C#N)C#N VHVPPDQPTYJSNO-UHFFFAOYSA-L 0.000 description 2
- 238000009510 drug design Methods 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 238000006345 epimerization reaction Methods 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- 239000003517 fume Substances 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 208000005017 glioblastoma Diseases 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 150000002431 hydrogen Chemical class 0.000 description 2
- RCCPEORTSYDPMB-UHFFFAOYSA-N hydroxy benzenecarboximidothioate Chemical compound OSC(=N)C1=CC=CC=C1 RCCPEORTSYDPMB-UHFFFAOYSA-N 0.000 description 2
- 238000003384 imaging method Methods 0.000 description 2
- 238000002329 infrared spectrum Methods 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 230000031146 intracellular signal transduction Effects 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 150000004694 iodide salts Chemical class 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 150000002513 isocyanates Chemical class 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 208000032839 leukemia Diseases 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
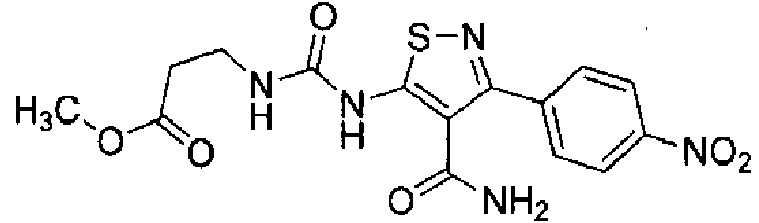
- KWSPUCFWCUSDPV-UHFFFAOYSA-N methyl 3-[[4-carbamoyl-3-(4-nitrophenyl)-1,2-thiazol-5-yl]carbamoylamino]propanoate Chemical compound NC(=O)C1=C(NC(=O)NCCC(=O)OC)SN=C1C1=CC=C([N+]([O-])=O)C=C1 KWSPUCFWCUSDPV-UHFFFAOYSA-N 0.000 description 2
- LCKXGYVHSANKEN-UHFFFAOYSA-N methyl 3-[[4-cyano-3-(4-nitrophenyl)-1,2-thiazol-5-yl]carbamoylamino]propanoate Chemical compound N#CC1=C(NC(=O)NCCC(=O)OC)SN=C1C1=CC=C([N+]([O-])=O)C=C1 LCKXGYVHSANKEN-UHFFFAOYSA-N 0.000 description 2
- HFLQZKRHQCDFCA-UHFFFAOYSA-N methyl 4-[[4-cyano-3-(4-nitrophenyl)-1,2-thiazol-5-yl]carbamoylamino]butanoate Chemical compound N#CC1=C(NC(=O)NCCCC(=O)OC)SN=C1C1=CC=C([N+]([O-])=O)C=C1 HFLQZKRHQCDFCA-UHFFFAOYSA-N 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 102000037979 non-receptor tyrosine kinases Human genes 0.000 description 2
- 108091008046 non-receptor tyrosine kinases Proteins 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 150000002923 oximes Chemical class 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 2
- 108040007629 peroxidase activity proteins Proteins 0.000 description 2
- 238000005191 phase separation Methods 0.000 description 2
- DCWXELXMIBXGTH-UHFFFAOYSA-N phosphotyrosine Chemical compound OC(=O)C(N)CC1=CC=C(OP(O)(O)=O)C=C1 DCWXELXMIBXGTH-UHFFFAOYSA-N 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 235000015320 potassium carbonate Nutrition 0.000 description 2
- 235000003270 potassium fluoride Nutrition 0.000 description 2
- 239000011698 potassium fluoride Substances 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- 125000003373 pyrazinyl group Chemical group 0.000 description 2
- 125000003226 pyrazolyl group Chemical group 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical group O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 2
- 150000003254 radicals Chemical class 0.000 description 2
- 238000002390 rotary evaporation Methods 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical class [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 235000011149 sulphuric acid Nutrition 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 238000004448 titration Methods 0.000 description 2
- 230000026683 transduction Effects 0.000 description 2
- 238000010361 transduction Methods 0.000 description 2
- 230000001052 transient effect Effects 0.000 description 2
- ONDSBJMLAHVLMI-UHFFFAOYSA-N trimethylsilyldiazomethane Chemical compound C[Si](C)(C)[CH-][N+]#N ONDSBJMLAHVLMI-UHFFFAOYSA-N 0.000 description 2
- 125000001493 tyrosinyl group Chemical group [H]OC1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 2
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical class CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- PAORVUMOXXAMPL-SECBINFHSA-N (2s)-3,3,3-trifluoro-2-methoxy-2-phenylpropanoyl chloride Chemical compound CO[C@](C(Cl)=O)(C(F)(F)F)C1=CC=CC=C1 PAORVUMOXXAMPL-SECBINFHSA-N 0.000 description 1
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 1
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 1
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 1
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 description 1
- 125000005845 (C2-C12)alkanoyloxymethyl group Chemical group 0.000 description 1
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 description 1
- 125000004514 1,2,4-thiadiazolyl group Chemical group 0.000 description 1
- 125000004530 1,2,4-triazinyl group Chemical group N1=NC(=NC=C1)* 0.000 description 1
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 1
- 125000005940 1,4-dioxanyl group Chemical group 0.000 description 1
- 125000005851 1-(N-(alkoxycarbonyl)amino)ethyl group Chemical group 0.000 description 1
- 125000005846 1-(alkanoyloxy)ethyl group Chemical group 0.000 description 1
- 125000005848 1-(alkoxycarbonyloxy)ethyl group Chemical group 0.000 description 1
- RWYOZJWQHMJWNT-UHFFFAOYSA-N 1-[4-(3-chloro-4-cyano-1,2-thiazol-5-yl)phenyl]-3-(2-fluoro-5-methylphenyl)urea Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C2=C(C(Cl)=NS2)C#N)=C1 RWYOZJWQHMJWNT-UHFFFAOYSA-N 0.000 description 1
- VFWCMGCRMGJXDK-UHFFFAOYSA-N 1-chlorobutane Chemical class CCCCCl VFWCMGCRMGJXDK-UHFFFAOYSA-N 0.000 description 1
- VUQPJRPDRDVQMN-UHFFFAOYSA-N 1-chlorooctadecane Chemical class CCCCCCCCCCCCCCCCCCCl VUQPJRPDRDVQMN-UHFFFAOYSA-N 0.000 description 1
- NAIKHCBDZGSGHH-UHFFFAOYSA-N 1-fluoro-2-isocyanato-4-(trifluoromethyl)benzene Chemical compound FC1=CC=C(C(F)(F)F)C=C1N=C=O NAIKHCBDZGSGHH-UHFFFAOYSA-N 0.000 description 1
- CPPGZWWUPFWALU-UHFFFAOYSA-N 1-isocyanato-3-methylbenzene Chemical compound CC1=CC=CC(N=C=O)=C1 CPPGZWWUPFWALU-UHFFFAOYSA-N 0.000 description 1
- 125000005847 1-methyl-1-(alkanoyloxy)-ethyl group Chemical group 0.000 description 1
- 125000005849 1-methyl-1-(alkoxycarbonyloxy)ethyl group Chemical group 0.000 description 1
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- WMPPDTMATNBGJN-UHFFFAOYSA-N 2-phenylethylbromide Chemical class BrCCC1=CC=CC=C1 WMPPDTMATNBGJN-UHFFFAOYSA-N 0.000 description 1
- NZASCBIBXNPDMH-UHFFFAOYSA-N 3,3-diethyl-1H-pyridine-2,4-dione Chemical compound CCC1(CC)C(=O)NC=CC1=O NZASCBIBXNPDMH-UHFFFAOYSA-N 0.000 description 1
- QHAMKFNWTSEZQB-UHFFFAOYSA-N 3-(3-morpholin-4-ylpropylcarbamoylamino)-5-[4-(phenylcarbamoylamino)phenyl]-1,2-thiazole-4-carboxamide Chemical compound N=1SC(C=2C=CC(NC(=O)NC=3C=CC=CC=3)=CC=2)=C(C(=O)N)C=1NC(=O)NCCCN1CCOCC1 QHAMKFNWTSEZQB-UHFFFAOYSA-N 0.000 description 1
- QZRYJTAZFJGFMM-UHFFFAOYSA-N 3-[(3-amino-3-oxopropyl)carbamoylamino]-5-[2-methyl-4-[(4-methylphenyl)carbamoylamino]phenyl]-1,2-thiazole-4-carboxamide Chemical compound C(N)(=O)C=1C(=NSC=1C1=C(C=C(C=C1)NC(=O)NC1=CC=C(C=C1)C)C)NC(NCCC(=O)N)=O QZRYJTAZFJGFMM-UHFFFAOYSA-N 0.000 description 1
- LLMLYJIDIGNFJG-UHFFFAOYSA-N 3-[[4-carbamoyl-3-[4-[(2-fluoro-5-methylphenyl)carbamoylamino]-2-methylphenyl]-1,2-thiazol-5-yl]carbamoylamino]propanoic acid Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=C(C)C(C=3C(=C(NC(=O)NCCC(O)=O)SN=3)C(N)=O)=CC=2)=C1 LLMLYJIDIGNFJG-UHFFFAOYSA-N 0.000 description 1
- KBOWBEYYMHTYOE-UHFFFAOYSA-N 3-[[4-carbamoyl-5-[2-methyl-4-(phenylcarbamoylamino)phenyl]-1,2-thiazol-3-yl]carbamoylamino]propanoic acid Chemical compound C=1C=C(C2=C(C(NC(=O)NCCC(O)=O)=NS2)C(N)=O)C(C)=CC=1NC(=O)NC1=CC=CC=C1 KBOWBEYYMHTYOE-UHFFFAOYSA-N 0.000 description 1
- BWKNOLACZZKDNT-UHFFFAOYSA-N 3-[[4-carbamoyl-5-[2-methyl-4-[(3-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-3-yl]carbamoylamino]propanoic acid Chemical compound CC1=CC=CC(NC(=O)NC=2C=C(C)C(C3=C(C(NC(=O)NCCC(O)=O)=NS3)C(N)=O)=CC=2)=C1 BWKNOLACZZKDNT-UHFFFAOYSA-N 0.000 description 1
- DMZJQZXITYXKCP-UHFFFAOYSA-N 3-[[4-carbamoyl-5-[4-(phenylcarbamoylamino)phenyl]-1,2-thiazol-3-yl]carbamoylamino]propanoic acid Chemical compound OC(=O)CCNC(=O)NC1=NSC(C=2C=CC(NC(=O)NC=3C=CC=CC=3)=CC=2)=C1C(=O)N DMZJQZXITYXKCP-UHFFFAOYSA-N 0.000 description 1
- JDRKQXYFBFTMLB-UHFFFAOYSA-N 3-[[4-carbamoyl-5-[4-[(2-fluoro-5-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-3-yl]carbamoylamino]propanoic acid Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C2=C(C(NC(=O)NCCC(O)=O)=NS2)C(N)=O)=C1 JDRKQXYFBFTMLB-UHFFFAOYSA-N 0.000 description 1
- KTRHIYMBAKQYDF-UHFFFAOYSA-N 3-[[4-carbamoyl-5-[4-[(3-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-3-yl]carbamoylamino]propanoic acid Chemical compound CC1=CC=CC(NC(=O)NC=2C=CC(=CC=2)C2=C(C(NC(=O)NCCC(O)=O)=NS2)C(N)=O)=C1 KTRHIYMBAKQYDF-UHFFFAOYSA-N 0.000 description 1
- JZIDESPIFOEXQB-UHFFFAOYSA-N 3-[[4-carbamoyl-5-[4-[(4-methylphenyl)carbamoylamino]phenyl]-1,2-thiazol-3-yl]carbamoylamino]propanoic acid Chemical compound C1=CC(C)=CC=C1NC(=O)NC1=CC=C(C2=C(C(NC(=O)NCCC(O)=O)=NS2)C(N)=O)C=C1 JZIDESPIFOEXQB-UHFFFAOYSA-N 0.000 description 1
- JUCILFMVOGZUTB-UHFFFAOYSA-N 3-[[4-carbamoyl-5-[4-[[2-fluoro-5-(trifluoromethyl)phenyl]carbamoylamino]phenyl]-1,2-thiazol-3-yl]carbamoylamino]propanoic acid Chemical compound OC(=O)CCNC(=O)NC1=NSC(C=2C=CC(NC(=O)NC=3C(=CC=C(C=3)C(F)(F)F)F)=CC=2)=C1C(=O)N JUCILFMVOGZUTB-UHFFFAOYSA-N 0.000 description 1
- FAXDZWQIWUSWJH-UHFFFAOYSA-N 3-methoxypropan-1-amine Chemical compound COCCCN FAXDZWQIWUSWJH-UHFFFAOYSA-N 0.000 description 1
- NXTNASSYJUXJDV-UHFFFAOYSA-N 3-nitrobenzoyl chloride Chemical compound [O-][N+](=O)C1=CC=CC(C(Cl)=O)=C1 NXTNASSYJUXJDV-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- VPBWZBGZWHDNKL-UHFFFAOYSA-N 3-pyrrolidin-1-ylpropan-1-amine Chemical compound NCCCN1CCCC1 VPBWZBGZWHDNKL-UHFFFAOYSA-N 0.000 description 1
- 125000004364 3-pyrrolinyl group Chemical group [H]C1=C([H])C([H])([H])N(*)C1([H])[H] 0.000 description 1
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 1
- SKDHHIUENRGTHK-UHFFFAOYSA-N 4-nitrobenzoyl chloride Chemical compound [O-][N+](=O)C1=CC=C(C(Cl)=O)C=C1 SKDHHIUENRGTHK-UHFFFAOYSA-N 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- ZUIVSEYJFYSYRR-UHFFFAOYSA-N 5-[2-methyl-4-[(3-methylphenyl)carbamoylamino]phenyl]-3-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound CC1=CC=CC(NC(=O)NC=2C=C(C)C(C3=C(C(NC(=O)NCCCN4CCOCC4)=NS3)C(N)=O)=CC=2)=C1 ZUIVSEYJFYSYRR-UHFFFAOYSA-N 0.000 description 1
- NQQBWNOXZCUHMK-UHFFFAOYSA-N 5-[2-methyl-4-[(4-methylphenyl)carbamoylamino]phenyl]-3-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound C1=CC(C)=CC=C1NC(=O)NC(C=C1C)=CC=C1C1=C(C(N)=O)C(NC(=O)NCCCN2CCOCC2)=NS1 NQQBWNOXZCUHMK-UHFFFAOYSA-N 0.000 description 1
- LUKXJGIEBWKELG-UHFFFAOYSA-N 5-[4-[(3-methylphenyl)carbamoylamino]phenyl]-3-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound CC1=CC=CC(NC(=O)NC=2C=CC(=CC=2)C2=C(C(NC(=O)NCCCN3CCOCC3)=NS2)C(N)=O)=C1 LUKXJGIEBWKELG-UHFFFAOYSA-N 0.000 description 1
- DWWPINGIURWDPB-UHFFFAOYSA-N 5-[4-[(4-methylphenyl)carbamoylamino]phenyl]-3-(3-morpholin-4-ylpropylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound C1=CC(C)=CC=C1NC(=O)NC1=CC=C(C2=C(C(NC(=O)NCCCN3CCOCC3)=NS2)C(N)=O)C=C1 DWWPINGIURWDPB-UHFFFAOYSA-N 0.000 description 1
- SSMRFHIWXNKLBZ-UHFFFAOYSA-N 5-amino-3-(4-nitrophenyl)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(N)SN=C1C1=CC=C([N+]([O-])=O)C=C1 SSMRFHIWXNKLBZ-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 206010003210 Arteriosclerosis Diseases 0.000 description 1
- 206010003571 Astrocytoma Diseases 0.000 description 1
- 125000006577 C1-C6 hydroxyalkyl group Chemical group 0.000 description 1
- OKTJSMMVPCPJKN-NJFSPNSNSA-N Carbon-14 Chemical compound [14C] OKTJSMMVPCPJKN-NJFSPNSNSA-N 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical class C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 108010009202 Growth Factor Receptors Proteins 0.000 description 1
- 102000009465 Growth Factor Receptors Human genes 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000808011 Homo sapiens Vascular endothelial growth factor A Proteins 0.000 description 1
- 101000851018 Homo sapiens Vascular endothelial growth factor receptor 1 Proteins 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical class Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- 150000008575 L-amino acids Chemical class 0.000 description 1
- 125000002061 L-isoleucyl group Chemical group [H]N([H])[C@]([H])(C(=O)[*])[C@](C([H])([H])[H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 125000003580 L-valyl group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(C([H])([H])[H])(C([H])([H])[H])[H] 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 208000007727 Muscle Tissue Neoplasms Diseases 0.000 description 1
- 125000005855 N,N-di(C1-C2)alkylcarbamoyl-(C1-C2)alkyl group Chemical group 0.000 description 1
- 125000005850 N-(alkoxycarbonyl)aminomethyl group Chemical group 0.000 description 1
- 229910020700 Na3VO4 Inorganic materials 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical class OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-N Propionic acid Chemical class CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 1
- 102000009484 Vascular Endothelial Growth Factor Receptors Human genes 0.000 description 1
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 1
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 1
- 102100033178 Vascular endothelial growth factor receptor 1 Human genes 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 150000008043 acidic salts Chemical class 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 125000005042 acyloxymethyl group Chemical group 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 108010081667 aflibercept Proteins 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- 125000005213 alkyl heteroaryl group Chemical group 0.000 description 1
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 230000003266 anti-allergic effect Effects 0.000 description 1
- 230000000879 anti-atherosclerotic effect Effects 0.000 description 1
- 230000000843 anti-fungal effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 125000005140 aralkylsulfonyl group Chemical group 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000003435 aroyl group Chemical group 0.000 description 1
- 208000011775 arteriosclerosis disease Diseases 0.000 description 1
- 125000005251 aryl acyl group Chemical group 0.000 description 1
- 125000004659 aryl alkyl thio group Chemical group 0.000 description 1
- 125000005160 aryl oxy alkyl group Chemical group 0.000 description 1
- 125000005161 aryl oxy carbonyl group Chemical group 0.000 description 1
- 125000004391 aryl sulfonyl group Chemical group 0.000 description 1
- 125000005110 aryl thio group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 125000003289 ascorbyl group Chemical class [H]O[C@@]([H])(C([H])([H])O*)[C@@]1([H])OC(=O)C(O*)=C1O* 0.000 description 1
- 229940120638 avastin Drugs 0.000 description 1
- 125000005334 azaindolyl group Chemical group N1N=C(C2=CC=CC=C12)* 0.000 description 1
- 208000021592 benign granular cell tumor Diseases 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical class OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000005513 benzoazaindolyl group Chemical group 0.000 description 1
- 125000004601 benzofurazanyl group Chemical group N1=C2C(=NO1)C(=CC=C2)* 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 150000005347 biaryls Chemical class 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M bisulphate group Chemical group S([O-])(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 150000004648 butanoic acid derivatives Chemical class 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical class C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 230000036952 cancer formation Effects 0.000 description 1
- 125000005242 carbamoyl alkyl group Chemical group 0.000 description 1
- 125000001589 carboacyl group Chemical group 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- QGJOPFRUJISHPQ-NJFSPNSNSA-N carbon disulfide-14c Chemical compound S=[14C]=S QGJOPFRUJISHPQ-NJFSPNSNSA-N 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical compound C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 150000001733 carboxylic acid esters Chemical class 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 230000019522 cellular metabolic process Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 238000004296 chiral HPLC Methods 0.000 description 1
- 150000001860 citric acid derivatives Chemical class 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- UKJLNMAFNRKWGR-UHFFFAOYSA-N cyclohexatrienamine Chemical group NC1=CC=C=C[CH]1 UKJLNMAFNRKWGR-UHFFFAOYSA-N 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 229940124569 cytoprotecting agent Drugs 0.000 description 1
- 125000003493 decenyl group Chemical group [H]C([*])=C([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 238000002059 diagnostic imaging Methods 0.000 description 1
- 150000008050 dialkyl sulfates Chemical class 0.000 description 1
- LMEDOLJKVASKTP-UHFFFAOYSA-N dibutyl sulfate Chemical class CCCCOS(=O)(=O)OCCCC LMEDOLJKVASKTP-UHFFFAOYSA-N 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000004852 dihydrofuranyl group Chemical group O1C(CC=C1)* 0.000 description 1
- 125000005047 dihydroimidazolyl group Chemical group N1(CNC=C1)* 0.000 description 1
- 125000005049 dihydrooxadiazolyl group Chemical group O1N(NC=C1)* 0.000 description 1
- 125000005050 dihydrooxazolyl group Chemical group O1C(NC=C1)* 0.000 description 1
- 125000005056 dihydrothiazolyl group Chemical group S1C(NC=C1)* 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- VAYGXNSJCAHWJZ-UHFFFAOYSA-N dimethyl sulfate Chemical compound COS(=O)(=O)OC VAYGXNSJCAHWJZ-UHFFFAOYSA-N 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000002500 effect on skin Effects 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- FCZCIXQGZOUIDN-UHFFFAOYSA-N ethyl 2-diethoxyphosphinothioyloxyacetate Chemical compound CCOC(=O)COP(=S)(OCC)OCC FCZCIXQGZOUIDN-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 208000030533 eye disease Diseases 0.000 description 1
- 229940051306 eylea Drugs 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- RFHAOTPXVQNOHP-UHFFFAOYSA-N fluconazole Chemical compound C1=NC=NN1CC(C=1C(=CC(F)=CC=1)F)(O)CN1C=NC=N1 RFHAOTPXVQNOHP-UHFFFAOYSA-N 0.000 description 1
- 229960004884 fluconazole Drugs 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-L fumarate(2-) Chemical class [O-]C(=O)\C=C\C([O-])=O VZCYOOQTPOCHFL-OWOJBTEDSA-L 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 125000003838 furazanyl group Chemical group 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 125000005643 gamma-butyrolacton-4-yl group Chemical group 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 125000002791 glucosyl group Chemical group C1([C@H](O)[C@@H](O)[C@H](O)[C@H](O1)CO)* 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 201000011066 hemangioma Diseases 0.000 description 1
- 150000002373 hemiacetals Chemical group 0.000 description 1
- 125000004475 heteroaralkyl group Chemical group 0.000 description 1
- 125000004447 heteroarylalkenyl group Chemical group 0.000 description 1
- 125000005312 heteroarylalkynyl group Chemical group 0.000 description 1
- 125000005143 heteroarylsulfonyl group Chemical group 0.000 description 1
- 125000005368 heteroarylthio group Chemical group 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 102000058223 human VEGFA Human genes 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical class I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 230000000521 hyperimmunizing effect Effects 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000005945 imidazopyridyl group Chemical group 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 230000000155 isotopic effect Effects 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 150000003951 lactams Chemical class 0.000 description 1
- 150000003903 lactic acid esters Chemical class 0.000 description 1
- 150000002596 lactones Chemical class 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 229940076783 lucentis Drugs 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 150000002688 maleic acid derivatives Chemical class 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 206010027191 meningioma Diseases 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M methanesulfonate group Chemical class CS(=O)(=O)[O-] AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- HRDXJKGNWSUIBT-UHFFFAOYSA-N methoxybenzene Chemical group [CH2]OC1=CC=CC=C1 HRDXJKGNWSUIBT-UHFFFAOYSA-N 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 125000005858 morpholino(C2-C3)alkyl group Chemical group 0.000 description 1
- 125000002757 morpholinyl group Chemical group 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 201000004130 myoblastoma Diseases 0.000 description 1
- 125000004370 n-butenyl group Chemical group [H]\C([H])=C(/[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000006606 n-butoxy group Chemical group 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- PSZYNBSKGUBXEH-UHFFFAOYSA-N naphthalene-1-sulfonic acid Chemical class C1=CC=C2C(S(=O)(=O)O)=CC=CC2=C1 PSZYNBSKGUBXEH-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 150000002823 nitrates Chemical class 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- ODUCDPQEXGNKDN-UHFFFAOYSA-N nitroxyl Chemical compound O=N ODUCDPQEXGNKDN-UHFFFAOYSA-N 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 125000004365 octenyl group Chemical group C(=CCCCCCC)* 0.000 description 1
- 239000003605 opacifier Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 150000003901 oxalic acid esters Chemical class 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 125000004095 oxindolyl group Chemical group N1(C(CC2=CC=CC=C12)=O)* 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- AHWALFGBDFAJAI-UHFFFAOYSA-N phenyl carbonochloridate Chemical compound ClC(=O)OC1=CC=CC=C1 AHWALFGBDFAJAI-UHFFFAOYSA-N 0.000 description 1
- DGTNSSLYPYDJGL-UHFFFAOYSA-N phenyl isocyanate Chemical compound O=C=NC1=CC=CC=C1 DGTNSSLYPYDJGL-UHFFFAOYSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 239000007981 phosphate-citrate buffer Substances 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 150000003014 phosphoric acid esters Chemical class 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 125000005856 piperidino(C2-C3)alkyl group Chemical group 0.000 description 1
- 125000005936 piperidyl group Chemical group 0.000 description 1
- 238000002600 positron emission tomography Methods 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- ALDITMKAAPLVJK-UHFFFAOYSA-N prop-1-ene;hydrate Chemical group O.CC=C ALDITMKAAPLVJK-UHFFFAOYSA-N 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- DNIAPMSPPWPWGF-UHFFFAOYSA-N propylene glycol Substances CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 230000004224 protection Effects 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000005857 pyrrolidino(C2-C3)alkyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000006085 pyrrolopyridyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 150000003902 salicylic acid esters Chemical class 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 238000002603 single-photon emission computed tomography Methods 0.000 description 1
- 229910000033 sodium borohydride Inorganic materials 0.000 description 1
- 239000012279 sodium borohydride Substances 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 238000013456 study Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 150000003900 succinic acid esters Chemical class 0.000 description 1
- 150000003871 sulfonates Chemical class 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000003507 tetrahydrothiofenyl group Chemical group 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000011287 therapeutic dose Methods 0.000 description 1
- 125000001984 thiazolidinyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 150000007944 thiolates Chemical class 0.000 description 1
- 125000004568 thiomorpholinyl group Chemical group 0.000 description 1
- 238000003354 tissue distribution assay Methods 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 238000003325 tomography Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 102000027257 transmembrane receptors Human genes 0.000 description 1
- 108091008578 transmembrane receptors Proteins 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical class OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 1
- IHIXIJGXTJIKRB-UHFFFAOYSA-N trisodium vanadate Chemical compound [Na+].[Na+].[Na+].[O-][V]([O-])([O-])=O IHIXIJGXTJIKRB-UHFFFAOYSA-N 0.000 description 1
- 238000001665 trituration Methods 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 210000003606 umbilical vein Anatomy 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 230000004862 vasculogenesis Effects 0.000 description 1
- 239000002525 vasculotropin inhibitor Substances 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D275/00—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings
- C07D275/02—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings not condensed with other rings
- C07D275/03—Heterocyclic compounds containing 1,2-thiazole or hydrogenated 1,2-thiazole rings not condensed with other rings with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/04—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms
- C07D295/12—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly or doubly bound nitrogen atoms
- C07D295/125—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly or doubly bound nitrogen atoms with the ring nitrogen atoms and the substituent nitrogen atoms attached to the same carbon chain, which is not interrupted by carbocyclic rings
- C07D295/13—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly or doubly bound nitrogen atoms with the ring nitrogen atoms and the substituent nitrogen atoms attached to the same carbon chain, which is not interrupted by carbocyclic rings to an acyclic saturated chain
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Compuesto seleccionado del grupo que consiste en: 3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-metoxipropil)amino]carbonil}amino)isotiazol- 4-carboxamida; {4-(aminocarbonil)-3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}carbamato de etilo; 3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4- ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida; amida de ácido 3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metil-fenil}-5-[3-(3-morfolin-4-il-propil)-ureido]- isotiazol-4-carboxílico; ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-fenil}-isotiazol-5-il)-ureido]-propiónico; ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metil-fenil}-isotiazol-5-il)-ureido]-propiónico; 3-[4-({[(3-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4- carboxamida; amida de ácido 3-[2-metil-4-(3-m-tolil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[4-(3-m-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico; ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-m-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico; 3-{4-[({[2-fluoro-5-(trifluorometil)fenil]amino}carbonil)amino]fenil}-5-({[(3-morfolin-4- ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida; amida de ácido 3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metil-fenil}-5-[3-(3-morfolin-4-il-propil)-ureido]- isotiazol-4-carboxílico; ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-fenil}-isotiazol-5-il)-ureido]-propiónico; ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metilfenil}-isotiazol-5-il)-ureido]- propiónico; 3-{4-[(anilinocarbonil)amino]fenil}-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida; amida de ácido 3-[2-metil-4-(3-fenil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[4-(3-fenil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico; ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-fenil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico; 3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4- carboxamida; amida de ácido 3-[2-metil-4-(3-p-tolil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-p-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico; ácido 3-(3-{4-carbamoil-3-[4-(3-p-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico; 5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)-3-(4-{[3-(trifluorometil)benzoil]amino}fenil)isotiazol-4- carboxamida; 3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4- carboxamida; ácido 4-{[({4-(aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5- il}amino)carbonil]amino}butanoico; 4-{[({4-(aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5- il}amino)carbonil]amino}butanoato de metilo; 5-({[(3-hidroxipropil)amino]carbonil}amino)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4- carboxamida; 5-amino-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida; 5-amino-3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida; y 3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4- carboxamida; o una sal farmacéuticamente aceptable del mismo.
Description
DESCRIPCIÓN
Derivados de 3-fenil-5-ureidoisotiazol-4-carboxamida como inhibidores de cinasa
Campo de la invención
La presente invención se refiere a nuevos compuestos capaces de modular, regular y/o inhibir la transducción de señales de tirosina cinasa tal como se define en las reivindicaciones. La presente invención también se refiere a métodos para regular, modular o inhibir las tirosina cinasas, o bien del tipo receptor o no receptor, para la prevención y/o el tratamiento de trastornos relacionados con la transducción de señales de tirosina cinasa no reguladas, incluido el crecimiento celular, trastornos proliferativos de los vasos sanguíneos y metabólicos.
Descripción de la técnica relacionada
Las proteína tirosina cinasas (PTK) comprenden una clase grande y diversa de proteínas que tienen actividad enzimática. Las PTK cumplen una función en el control del crecimiento y la diferenciación celular.
Por ejemplo, la transducción de señales mediadas por tirosina cinasas es iniciada por la interacción extracelular con un factor de crecimiento específico (ligando), seguida de dimerización de los receptores, estimulación transitoria de la actividad de la proteína tirosina cinasa intrínseca y fosforilación. Los sitios de unión se crean así para moléculas de transducción de señales intracelulares y llevan a la formación de complejos con un espectro de moléculas de señalización citoplásmicas que facilitan la respuesta celular apropiada (p. ej., división celular, homeostasis metabólica y respuestas al microentorno extracelular).
Con respecto a las tirosina cinasas de tipo receptor, se ha demostrado que los sitios de fosforilación de tirosinas funcionan como sitios de unión de gran afinidad hacia dominios SH2 (homología src) de moléculas de señalización. Se han identificado varias proteínas de sustrato intracelulares que se asocian con las tirosina cinasas de tipo receptor (RTK). Se pueden dividir en dos grupos principales: (1) sustratos que tienen un dominio catalítico; y (2) sustratos que carecen de dicho dominio pero que sirven como adaptadores y se asocian con moléculas catalíticamente activas. La especificidad de las interacciones entre receptores o proteínas y los dominios SH2 de sus sustratos es determinada por los residuos de aminoácidos que rodean inmediatamente al residuo tirosina fosforilado. Las diferencias en las afinidades de unión entre los dominios SH2 y las secuencias de aminoácidos que rodean a los residuos de fosfatirosina en receptores particulares concuerdan con las diferencias observadas en sus perfiles de fosforilación de sustratos. Estas observaciones sugieren que la función de cada tirosina cinasa de tipo receptor es determinada no solamente por su patrón de expresión y disponibilidad de ligandos, sino también por la gama de vías de transducción de señales en dirección 3' que son activadas por un receptor particular. Por lo tanto, la fosforilación proporciona un importante paso que determina la selectividad de las vías de señalización obtenidas por receptores de los factores de crecimiento específicos, además de los receptores de los factores de diferenciación.
Se ha demostrado que la expresión aberrante o las mutaciones en las PTK conducen a la proliferación celular descontrolada (p. ej., crecimiento de tumores malignos) o a defectos en proceso del desarrollo clave. En consecuencia, la comunidad biomédica ha expandido recursos importantes para descubrir la función biológica específica de los miembros de la familia de PTK, su función en los procesos de diferenciación, su implicancia en la tumorigénesis y otras enfermedades, los mecanismos bioquímicos que subyacen a sus vías de transducción de señales activadas tras la estimulación de los ligandos y el desarrollo de nuevos fármacos.
Las tirosina cinasas pueden ser del tipo receptor (que tiene dominios extracelulares, transmembrana e intracelulares) o del tipo no receptor (en donde son totalmente intracelulares).
Las tirosina cinasas de tipo receptor (RTK) comprenden una gran familia de receptores transmembrana con diversas actividades biológicas. La función intrínseca de las RTK se activa tras la unión al ligando, que resulta en la fosforilación del receptor y múltiples sustratos celulares, y posteriormente en una diversidad de respuestas celulares. Las tirosina cinasas de tipo no receptor representan un grupo de enzimas celulares que carecen de secuencias extracelulares y transmembrana. Se expone un análisis más detallado de tirosina cinasas de tipo receptor y no receptor en Cowan-Jacob Cell Mol. Life Sci., 2996, 63, 2608-2625.
Hay una serie de ejemplos en los que se ha hallado que las cinasas RTK están implicadas en vías de señalización celular que conducen a patologías, incluidas degeneración macular relacionada con la edad (Ni et al. Opthalmologica 2009 223 401-410; Chappelow et al. Drugs 2008 68 1029-1036), retinopatía diabética (Zhang et al Int. J. Biochem. Cell Biol. 2009 41 2368-2371), cáncer (Aora et al. J. Path. Exp. Ther. 2006, 315, 971), psoriasis (Heidenreich et al Drug News Perspective 2008 21 97-105) y respuesta hiperinmunitaria. En enfermedades oftálmicas tales como la degeneración macular neovascular relacionada con la edad y retinopatía diabética, la activación aberrante de receptores VEGF puede provocar el crecimiento anormal de los vasos sanguíneos. La importancia de la señalización de VEGFR en el proceso de la enfermedad de degeneración macular neovascular relacionada con la edad es evidente por el éxito clínico de múltiples agentes de direccionamiento anti-VEGF incluidos Lucentis®, Avastin® y EYLEA™ (Barakat et al. Expert Opin. Investig. Drugs 2009, 18, 637). Recientemente se ha sugerido que la inhibición de múltiples
vías de señalización de RTK puede proporcionar un mayor efecto terapéutico que dirigir una sola vía de señalización de RTK. Por ejemplo, en trastornos oculares neovasculares tales como la degeneración macular neovascular relacionada con la edad y la retinopatía diabética, la inhibición de VEGFR y PDGFRp puede proporcionar un mayor efecto terapéutico causando la regresión de los vasos sanguíneos neovasculares existentes presentes en la enfermedad (Adamis et al. Am. J. Pathol. 2006 168 2036-2053). En cáncer, se ha sugerido que la inhibición de múltiples vías de señalización de RTK tiene un mayor efecto que la inhibición de una sola vía de RTK (DePinho et al. Science 2007 318287-290; Bergers et al. J. Clin Invest. 2003 111 1287-1295).
Se desea entonces la identificación de pequeños compuestos eficaces que inhiben específicamente la transducción de señales modulando la actividad de tirosina cinasas de tipo receptor y no receptor para regular y modular la proliferación celular anormal o inapropiada y es un objeto de la presente invención.
Se describen determinados compuestos pequeños en la publicación PCT núm. WO/1999/062890, publicación PCT Núm. WO/2005/082001 y publicación Pc T núm. WO/2006/026034 como útiles para el tratamiento de enfermedades relacionadas con la transducción no regulada de TKS. Estas patentes divulgan materiales y métodos de partida para su preparación, estudios y ensayos para determinar la capacidad de los compuestos reivindicados de modular, regular y/o inhibir la proliferación celular, indicaciones que son tratables con dichos compuestos, formulaciones y rutas de administración, dosis eficaces, etc.
Resumen breve de la invención
La presente invención se refiere a moléculas orgánicas capaces de modular, regular y/o inhibir la transducción de señales de tirosina cinasatal como se define en las reivindicaciones. Dichos compuestos son útiles para el tratamiento de enfermedades relacionadas con la transducción desregulada de TKS, incluidas enfermedades proliferativas de las células tales como cáncer; trastornos proliferativos vasculares (vasos sanguíneos) tales como retinopatía diabética, degeneración macular relacionada con la edad, retinopatía de prematuridad, terigión, artritis y restenosis; trastornos fibróticos tales como cirrosis hepática y aterosclerosis; trastornos proliferativos de las células mesangiales tales como glomerulonefritis, nefropatía diabética, nefrosclerosis maligna, síndromes de microangiopatía trombótica, rechazo de trasplantes y glomerulopatías; trastornos metabólicos tales como psoriasis, diabetes mellitus, curación de heridas, inflamación y enfermedades neurodegenerativas.
En lo siguiente, las realizaciones no cubiertas por las reivindicaciones no pertenecen a la invención y se han clasificado como que pertenecen a la presente divulgación.
En una realización ilustrativa, los compuestos de la presente divulgación son de Fórmula I:
o una sal farmacéuticamente aceptable, en donde:
cada uno de X1 y X2 es independientemente N o S; con la condición de que X1 y X2 no sean simultáneamente S;
L1 se selecciona del grupo que consiste en -N(R)-, -N(R)-C(=O)-N(R)-, -O-C(=O)-N(R)-, -N(R)-C(=O)- y -C(=O)-N(R)-
L2 se selecciona del grupo que consiste en un enlace covalente, -N(R)-, -N(R)-C(=O)-, -C(=O)-N(R)- y -N(R)-C(=O)-N(R)-;
cada R es independientemente H o alquilo C1-6;
cada R1 se selecciona independientemente del grupo que consiste en alquilo C1-6, haloalquilo C1-6, halógeno y OR; o en donde dos grupos R1 adyacentes tomados junto con los átomos de carbono a los que están unidos forman un arilo de seis miembros o un heteroarilo de cinco o seis miembros;
n es 0, 1 o 2;
R2 se selecciona del grupo que consiste en: a) H; b) alquilo C1-6 no sustituido o sustituido con uno o dos sustituyentes
seleccionados del grupo que consiste en heterociclilo, -C(=O)OR, hidroxi, alcoxi C1-6 y arilo; y
R3 se selecciona del grupo que consiste en H, hidroxi, -NO2, arilo y heteroarilo, en donde dicho arilo o heteroarilo no está sustituido o está sustituido con uno a tres sustituyentes seleccionados del grupo que consiste en halo, haloalquilo C1-6 y alquilo C1-6.
En otra realización, en la fórmula I:
cada uno de X1 y X2 es independientemente N o S;
L1 se selecciona del grupo que consite en -N(R)-C(=O)-N(R)-, -OC(=O)-N(R)-, -N(R)-C(=O)- y -C(=O)-N(R)-;
L2 se selecciona del grupo que consiste en un enlace covalente, -N(R)-, -N(R)-C(=O)-, -C(=O)-N(R)- y -N(R)-C(=O)-N(R)-;
cada R es independientemente H o alquilo C1-6;
cada R1 se selecciona independientemente del grupo que consiste en alquilo C1-6, haloalquilo C1-6, halógeno y OR; o en donde dos grupos R1 adyacentes tomados junto con los átomos de carbono a los que están unidos forman un arilo de seis miembros o un heteroarilo de cinco o seis miembros;
n es 0, 1 o 2;
R2 es alquilo C1-6 que no está sustituido o está sustituido con uno o dos sustituyentes seleccionados del grupo que consiste en heterociclilo, -C(=O)OR, hidroxialquilo C1-6 y alcoxi C1-6; y
R3 se selecciona del grupo que consiste en H, -NO2, arilo y heteroarilo, en donde dicho arilo o heteroarilo no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados del grupo que consiste en halo, haloalquilo C1-6 y alquilo C1-6.
En otra realización, en la Fórmula I, X1 es N y X2 es S.
En otra realización, en la Fórmula I, X1 es S y X2 es N.
En otra realización, en la Fórmula I, L1 se selecciona del grupo que consiste en -N(H)-, -N(H)-C(=O)-, -N(H)-C(=O)-N(H)-, -O-C(=O)-N(H)-, -N(R)-C(=O)- y - C(=O)-N(R)-.
En otra realización, en la Fórmula I, L1 se selecciona del grupo que consiste en -N(H)-C(=O)-N(H)-, -O-C(=O)-N(H)-, -N(R)-C(=O)- y -C(=O)-N(R)-.
En otra realización, en la Fórmula I, L2 se selecciona del grupo que consiste en un enlace covalente, -N(H)-, -N(H)-C(=O)-, -C(=O)-N(R)- y -N(H)-C(=O)-N(H)-.
En otra realización, en la Fórmula I, n es 0 o 1.
En otra realización, en la Fórmula I, R2 se selecciona del grupo que consiste en H,
2,4-dimetoxibencilo, morfolinil-(CH2)3-, HO-C(=O)-(CH2)2-, HO-C(=O)-(CH2)3-, CHsO-C(=O)-(CH2)2-, CHsO-C(=O)-(CH2)3-, HO-(CH2)s-, CHsO-(CH2)s- y etilo.
En otra realización, en la Fórmula I, R2 se selecciona del grupo que consiste en morfolinil-(CH2)3-, HO-C(=O)-(CH2)2-, CH3O-(CH2)3- y etilo.
En otra realización, en la Fórmula I, R3 se selecciona del grupo que consiste en H, -NO2, hidroxi y arilo no sustituido o sustituido con uno a dos sustituyentes seleccionados del grupo que consiste en metilo, fluoro y trifluorometilo.
En otra realización, en la Fórmula I, R3se selecciona del grupo que consiste en H, -NO2y arilo no sustituido o sustituido con uno a dos sustituyentes seleccionados del grupo que consiste en metilo, fluoro y trifluorometilo.
En otra realización, el compuesto de Fórmula I se representa con la Fórmula IA:
en donde n, R1, R2, R3, L1 y L2 son como se expone en la Fórmula I.
En otra realización, el compuesto de Fórmula I se representa con la Fórmula IB:
en donde n es 0 o 1; y R1, R2, R3, L1 y L2 son como se expone para la Fórmula I.
En otra realización, el compuesto de Fórmula I se representa por la Fórmula IC:
en donde n es 0 o 1; y R1, R2, R3, L1 y L2 son como se expone para la Fórmula I.
En otra realización, en la Fórmula IB:
L1 se selecciona del grupo que consiste en -N(H)-, -N(H)-C(=O)-N(H)- y -O-C(=O)-N(H)-;
L2 se selecciona del grupo que consiste en un enlace covalente, -N(H)-, -N(H)-C(=O)- y -N(H)-C(=O)-N(H)-;
R1 es metilo;
R2 se selecciona del grupo que consiste en H, morfolinil-(CH2)3-, HO-C(=O)-(CH2)2-, CH3O-(CH2)3- y etilo; y R3 se selecciona del grupo que consiste en H, -NO2 y arilo no sustituido o sustituido con uno a dos sustituyentes
seleccionados del grupo que consiste en metilo, fluoro y trifluorometilo.
En otra realización, en la Fórmula IB:
L1 se selecciona del grupo que consiste en-N(H)-C(=O)-N(H)- y -O-C(=O)-N(H)-;
L2 se selecciona del grupo que consiste en un enlace covalente, -N(H)-, -N(H)-C(=O)- y -N(H)-C(=O)-N(H)-;
R1 es metilo;
R2 se selecciona del grupo que consiste en H, morfolinil-(CH2)3-, HO-C(=O)-(CH2)2-, CH3O-(CH2)3- y etilo; y R3 se selecciona del grupo que consiste en H, -NO2 y arilo no sustituido o sustituido con uno a dos sustituyentes seleccionados del grupo que consiste en metilo, fluoro y trifluorometilo.
En otra realización, en la Fórmula IC:
L1 se selecciona del grupo que consiste en -N(H)-, -N(H)-C(=O)-, -N(H)-C(=O)-N(H)- y -O-C(=O)-N(H)-;
L2 se selecciona del grupo que consiste en un enlace covalente, -N(H)-, -N(H)-C(=O)- y -N(H)-C(=O)-N(H)-;
R1 es metilo;
R2 se selecciona del grupo que consiste en H,
morfolinil-(CH2)3-, HO-C(=O)-(CH2)2-, HO-C(=O)-(CH2)3-, CH3O-C(=O)-(CH2)2-, CH3O-C(=O)-(CH2)3-, HO-(CH2)3-, CH3O-(CH2)3- y etilo; y
R3 se selecciona del grupo que consiste en H, hidroxi, -NO2 y arilo no sustituido o sustituido con uno o dos sustituyentes seleccionados del grupo que consiste en metilo, fluoro y trifluorometilo.
En otra realización, en la Fórmula IC:
L1 se selecciona del grupo que consiste en -N(H)-C(=O)-N(H)- y -O-C(=O)-N(H)-;
L2 se selecciona del grupo que consiste en un enlace covalente, -N(H)-, -N(H)-C(=O)- y -N(H)-C(=O)-N(H)-;
R1 es metilo;
R2 se selecciona del grupo que consiste en morfolinil-(CH2)3-, HO-C(=O)-(CH2)2-, CH3O-(CH2)3- y etilo; y
R3 se selecciona del grupo que consiste en H, -NO2 y arilo no sustituido o sustituido con uno o dos sustituyentes seleccionados del grupo que consiste en metilo, fluoro y trifluorometilo.
En otra realización, el compuesto de Fórmula IB se selecciona del grupo que consiste en:
amida del ácido 5-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-fenil}-3-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; amida de ácido 5-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metil-fenil}-3-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico;
ácido 3-[3-(4-carbamoil-5-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-fenil}-isotiazol-3-il)-ureido]-propiónico;
ácido 3-[3-(4-carbamoil-5-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metil-fenil}-isotiazol-3-il)-ureido]-propiónico; amida de ácido 3-[3-(3-morfolin-4-il-propil)-ureido]-5-[4-(3-m-tolil-ureido)-fenil]-isotiazol-4-carboxílico;
amida de ácido 5-[2-metil-4-(3-m-tolil-ureido)-fenil]-3-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico;
ácido 3-(3-{4-carbamoil-5-[4-(3-m-tolil-ureido)-fenil]-isotiazol-3-il}-ureido)-propiónico;
ácido 3-(3-{4-carbamoil-5-[2-metil-4-(3-m-tolil-ureido)-fenil]-isotiazol-3-il}-ureido)-propiónico;
amida de ácido 5-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-fenil}-3-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico;
amida de ácido 5-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metil-fenil}-3-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4- carboxílico;
ácido 3-[3-(4-carbamoil-5-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-fenil}-isotiazol-3-il)-ureido]-propiónico; ácido 3-[3-(4-carbamoil-5-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metil-fenil}-isotiazol-3-il)-ureido]-propiónico; amida de ácido 3-[3-(3-morfolin-4-il-propil)-ureido]-5-[4-(3-fenil-ureido)-fenil]-isotiazol-4-carboxílico;
ácido 3-(3-{4-carbamoil-5-[4-(3-fenil-ureido)-fenil]-isotiazol-3-il}-ureido)-propiónico;
ácido 3-(3-{4-carbamoil-5-[2-metil-4-(3-fenil-ureido)-fenil]-isotiazol-3-il}-ureido)-propiónico;
amida de ácido 3-[3-(3-morfolin-4-il-propil)-ureido]-5-[4-(3-p-tolil-ureido)-fenil]-isotiazol-4-carboxílico;
amida de ácido 5-[2-metil-4-(3-p-tolil-ureido)-fenil]-3-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; amida de ácido 3-(3-{4-Carbamoil-5-[2-metil-4-(3-p-tolil-ureido)-fenil]-isotiazol-3-il}-ureido)-propiónico;
ácido 3-(3-{4-carbamoil-5-[4-(3-p-tolil-ureido)-fenil]-isotiazol-3-il}-ureido)-propiónico;
3-amino-5-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida;
5- [4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-3-[(3-morfolin-4-ilpropil)amino]isotiazol-4-carboxamida; y 3-[(2,4-dimetoxibencil)amino]-5-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida; o una sal farmacéuticamente aceptable de éste. Las estructuras de los compuestos anteriores se exponen en las Tablas 2 y 3 a continuación.
En otra realización, el compuesto de fórmula IC se selecciona del grupo que consiste en:
5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)-3-(4-nitrofenil)isotiazol-4-carboxamida;
3-(4-aminofenil)-5-({[(3-metoxipropil)amino]carbonil}amino)isotiazol-4-carboxamida;
5-({[(3-metoxipropil)amino]carbonil}amino)-3-(4-nitrofenil)isotiazol-4-carboxamida;
3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-metoxipropil)amino]carbonil}amino)isotiazol-4-carboxamida;
{4-(aminocarbonil)-3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}carbamato de etilo;
3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
amida de ácido 3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metil-fenil}-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico;
ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-fenil}-isotiazol-5-il)-ureido]-propiónico;
ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metilfenil}-isotiazol-5-il)-ureido]-propiónico;
3-[4-({[(3-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
amida de ácido 3-[2-metil-4-(3-m-tolil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[4-(3-m-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;
ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-m-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;
3- {4-[({[2-fluoro-5-(trifluorometil)feml]amino}carbonil)amino]feml}-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
amida de ácido 3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metil-fenil}-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4- carboxílico;
ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-fenil}-isotiazol-5-il)-ureido]-propiónico; ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metilfenil}-isotiazol-5-il)-ureido]-propiónico; 3-{4-[(anilinocarbonil)amino]fenil}-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida; amida de ácido 3-[2-metil-4-(3-fenil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[4-(3-fenil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;
ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-fenil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;
3-(4-aminofenil)-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
amida de ácido 3-[2-metil-4-(3-p-tolil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-p-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;
ácido 3-(3-{4-carbamoil-3-[4-(3-p-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;
5- ({[(3-morfolin-4-ilpropil)amino]carbonil}amino)-3-(4-{[3-(trifluorometil)benzoil]amino}fenil)isotiazol-4-carboxamida; amida de ácido 3-(4-nitro-fenil)-5-[(2-oxo-pirrolidin-1-carbonil)-amino]-isotiazol-4-carboxílico;
3-(4-aminofenil)-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4-carboxamida;
3- [4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4-carboxamida; ácido 4-{[({4-(aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}amino)carbonil]amino}butanoico;
4- {[({4-(aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}amino)carbonil]amino}butanoato de metilo;
ácido 4-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]butanoico;
4- [({[4-(aminocarbonil)-3-(4-aminofenil)isotiazol-5-il]amino}carbonil)amino]butanoato de metilo;
3-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]propanoato de metilo;
5- ({[(3-hidroxipropil)amino]carbonil}amino)-3-(4-nitrofenil)isotiazol-4-carboxamida;
acetato de 3-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]propilo;
acetato de 3-[({[4-(aminocarbonil)-3-(4-aminofenil)isotiazol-5-il]amino}carbonil)amino]propilo;
5-({[(3-hidroxipropil)amino]carbonil}amino)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida; 3-(4-aminofenil)-5-({[(3-hidroxipropil)amino]carbonil}amino)isotiazol-4-carboxamida;
5-amino-3-(4-aminofenil)isotiazol-4-carboxamida;
5-amino-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida;
5-amino-3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida;
5-amino-3-(3-nitrofenil)isotiazol-4-carboxamida;
5-amino-3-(3-aminofenil)isotiazol-4-carboxamida;
5-amino-3-[3-(hidroxiamino)fenil]isotiazol-4-carboxamida;
5-amino-3-(3-{[3-(trifluorometil)benzoil]amino}fenil)isotiazol-4-carboxamida;
5-amino-3-{3-[(anilinocarbonil)amino]fenil}isotiazol-4-carboxamida;
3-(4-nitrofenil)-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
3-(4-aminofenil)-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;
3-amino-5-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida;
5-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-3-[(3-morfolin-4-ilpropil)amino]isotiazol-4-carboxamida; y 3-[(2,4-dimetoxibencil)amino]-5-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida; o una sal farmacéuticamente aceptable de éste. Las estructuras de estos compuestos anteriores se exponen en las Tablas 1 y 3 a continuación.
La presente invención se refiere además a composiciones farmacéuticas que comprenden una cantidad farmacéuticamente eficaz de los compuestos anteriormente descritos y a un vehículo o excipiente farmacéuticamente aceptable tal como se define en las reivindicaciones. Se cree que dicha composición modula la transducción de señales por una tirosina cinasa, o bien por la inhibición de actividad catalítica, afinidad hacia ATP o capacidad de interactuar con un sustrato.
Por consiguiente, la presente divulgación también proporciona un método para inhibir una tirosina cinasa de tipo receptor en un sujeto que lo necesita, que comprende administrar a dicho sujeto una cantidad terapéuticamente eficaz de por lo menos un compuesto de Fórmula I, o una sal farmacéuticamente aceptable del mismo.
En una realización, la cinasa de tipo receptor es una VEGFR cinasa.
En otra realización, la VEGFR cinasa es VEGFR1 o VEGFR2 cinasa.
En otra realización, la tirosina cinasa de tipo receptor es una PDGFR cinasa.
En otra realización, la PDGFR cinasa es una PDGFR cinasa de tipo beta (PDGFRb).
En otra realización, la presente divulgación proporciona un método para tratar una enfermedad relacionada con la transducción de señales de tirosina cinasa no regulada, que comprende administrar a un sujeto que lo necesita una cantidad terapéuticamente eficaz de por lo menos un compuesto de Fórmula I o una sal farmacéuticamente aceptable del mismo.
En otra realización, la enfermedad anterior es una enfermedad que se selecciona del grupo que consiste en cáncer, trastornos proliferativos de los vasos sanguíneos, trastornos fibróticos, trastornos proliferativos de las células mesangiales y enfermedades metabólicas.
En otra realización, el trastorno proliferativo de los vasos sanguíneos se selecciona del grupo que consiste en retinopatía diabética, degeneración macular relacionada con la edad, retinopatía de prematuridad, terigión, artritis y restenosis.
En otra realización, el trastorno fibrótico se selecciona del grupo que consiste en cirrosis hepática y aterosclerosis. En otra realización, el trastorno proliferativo de las células mesangiales se selecciona del grupo que consiste en glomerulonefritis, nefropatía diabética, nefrosclerosis maligna, síndromes de microangiopatía trombótica, rechazo de trasplantes y glomerulopatías.
En otra realización, las enfermedades metabólicas se seleccionan del grupo que consiste en psoriasis, diabetes mellitus, cicatrización de heridas, inflamación y enfermedades neurodegenerativas.
Descripción detallada de la invención
Tal como se emplearon anteriormente y se emplearán en toda la presente descripción, los siguientes términos y expresiones, a menos que se indique otra cosa, se entenderán con los siguientes significados:
“Paciente” incluye tanto seres humanos como animales.
“Mamífero” significa seres humanos y otros animales mamíferos.
“Alquilo” significa un grupo hidrocarbonado alifático que puede ser lineal o ramificado y que comprende aproximadamente 1 a aproximadamente 20 átomos de carbono en la cadena. Los grupos alquilo preferidos contienen aproximadamente 1 a aproximadamente 12 átomos de carbono en la cadena. Los grupos alquilo más preferidos contienen aproximadamente 1 a aproximadamente 6 átomos de carbono en la cadena. Ramificado significa que uno o más grupos alquilo inferior tales como metilo, etilo o propilo, están unidos a una cadena de alquilo lineal. “Alquilo inferior” significa un grupo que tiene aproximadamente 1 a aproximadamente 6 átomos de carbono en la cadena que puede ser lineal o ramificada. “Alquilo” puede no estar sustituido o estar sustituido con uno o más sustituyentes que son iguales o diferentes, en donde cada sustituyente se selecciona independientemente del grupo que consiste en halo, arilo, cicloalquilo, ciano, hidroxi, alcoxi, alquiltio, amino, oxima (p. ej., =N-OH), - NH(alquilo),
-NH(cicloalquilo), -N(alquilo)2, -O-C(O)-alquilo, -O-C(O)-arilo, -O-C(O)-cicloalquilo, -SF5, carboxi y -C(O)O-alquilo. Los ejemplos no limitativos de grupos alquilo adecuados incluyen metilo, etilo, n-propilo, isopropilo y t-butilo.
“Alquenilo” significa un grupo hidrocarbonado alifático que contiene por lo menos un doble enlace carbono-carbono y que puede ser lineal o ramificado y que comprende aproximadamente 2 a aproximadamente 15 átomos de carbono en la cadena. Los grupos alquenilo preferidos tienen aproximadamente 2 a aproximadamente 12 átomos de carbono en la cadena; y más preferiblemente aproximadamente 2 a aproximadamente 6 átomos de carbono en la cadena. Ramificado significa que uno o más grupos alquilo inferior tales como metilo, etilo o propilo, están unidos a una cadena de alquenilo lineal. “Alquenilo inferior” significa aproximadamente 2 a aproximadamente 6 átomos de carbono en la cadena que puede ser lineal o ramificada. “Alquenilo” puede estar sustituido u opcionalmente sustituido con uno o más sustituyentes que pueden ser iguales o diferentes, en donde cada uno se selecciona independientemente del grupo que consiste en halo, alquilo, arilo, cicloalquilo, ciano, alcoxi y -S(alquilo). Los ejemplos no limitativos de grupos alquenilo adecuados incluyen etenilo, propenilo, n-butenilo, 3-metilbut-2-enilo, n-pentenilo, octenilo y decenilo.
“Alquinilo” significa un grupo hidrocarbonado alifático que contiene por lo menos un triple enlace carbono-carbono y que puede ser lineal o ramificado y que comprende aproximadamente 2 a aproximadamente 15 átomos de carbono en la cadena. Los grupos alquinilo preferidos tienen aproximadamente 2 a aproximadamente 12 átomos de carbono en la cadena; y más preferiblemente aproximadamente 2 a aproximadamente 4 átomos de carbono en la cadena. Ramificado significa que uno o más grupos alquilo inferior tales como metilo, etilo o propilo, están unidos a una cadena de alquinilo lineal. “Alquinilo inferior” significa aproximadamente 2 a aproximadamente 6 átomos de carbono en la cadena que puede ser lineal o ramificada. Los ejemplos no limitativos de grupos alquinilo adecuados incluyen etinilo, propinilo, 2-butinilo y 3-metilbutinilo. “Alquinilo” puede estar sustituido u opcionalmente sustituido con uno o más sustituyentes que pueden ser iguales o diferentes, en donde cada uno se selecciona independientemente del grupo que consiste en alquilo, arilo y cicloalquilo.
“Arilo” significa un sistema de anillos monocíclico o multicíclico aromático que comprende aproximadamente 6 a aproximadamente 14 átomos de carbono, preferiblemente aproximadamente 6 a aproximadamente 10 átomos de carbono. El grupo arilo puede estar opcionalmente sustituido con uno o más “sustituyentes de sistemas de anillos” que pueden ser iguales o diferentes, y son como se definen en este documento. Los ejemplos no limitativos de grupos arilo adecuados incluyen fenilo y naftilo.
“Heteroarilo” significa un sistema de anillos monocíclico o multicíclico aromático que comprende aproximadamente 5 a aproximadamente 14 átomos del anillo, preferiblemente aproximadamente 5 a aproximadamente 10 átomos del anillo, en donde uno o más átomos del anillo consisten en un elemento distinto de carbono, por ejemplo nitrógeno, oxígeno o azufre, solos o combinados. Los heteroarilos preferidos contienen aproximadamente 5 a aproximadamente 6 átomos del anillo. El “heteroarilo” puede estar opcionalmente sustituido con uno o más “sustituyentes del sistema de anillos” que pueden ser iguales o diferentes y son como se definen en este documento. El prefijo aza, oxa o tia antes de la raíz de heteroarilo significa que por lo menos un átomo de nitrógeno, oxígeno o azufre respectivamente, está presente como el átomo del anillo. Un átomo de nitrógeno de un heteroarilo se puede oxidar opcionalmente al correspondiente N-óxido. “Heteroarilo” puede además incluir un heteroarilo como se definió anteriormente condensado a un arilo como se definió anteriormente. Los ejemplos no limitativos de heteroarilos adecuados incluyen piridilo, pirazinilo, furanilo, tienilo, pirimidinilo, piridiona (incluidas piridonas N-sustituidas), isoxazolilo, isotiazolilo, oxazolilo, tiazolilo, pirazolilo, furazanilo, pirrolilo, pirazolilo, triazolilo, 1,2,4-tiadiazolilo, pirazinilo, piridazinilo, quinoxalinilo, ftalazinilo, oxindolilo, imidazo[1,2-a]piridinilo, imidazo[2,1-b]tiazolilo, benzofurazanilo, indolilo, azaindolilo, bencimidazolilo, benzotienilo, quinolinilo, imidazolilo, tienopiridilo, quinazolinilo, tienopirimidilo, pirrolopiridilo, imidazopiridilo, isoquinolinilo, benzoazaindolilo, 1,2,4-triazinilo, benzotiazolilo y similares. El término “heteroarilo” también se refiere a restos parcialmente saturados tales como, por ejemplo, tetrahidroisoquinolilo, tetrahidroquinolilo y similares.
“Aralquilo” o “arilalquilo” significa un grupo aril-alquilo en el que el arilo y el alquilo son como se describió previamente. Los aralquilos preferidos comprenden un grupo alquilo inferior. Los ejemplos no limitativos de grupos aralquilo adecuados incluyen bencilo, 2-fenetilo y naftalenilmetilo. El enlace al resto madre es a través del alquilo.
“Alquilarilo” significa un grupo alquil-arilo en el que el alquilo y el arilo son como se describió previamente. Los alquilarilos preferidos comprenden un grupo alquilo inferior. Un ejemplo no limitativo de un grupo alquilarilo adecuado es tolilo. El enlace al resto madre es a través del arilo.
“Cicloalquilo” significa un sistema de anillos monocíclico o multicíclico no aromático que comprende aproximadamente 3 a aproximadamente 10 átomos de carbono, preferiblemente aproximadamente 5 a aproximadamente 10 átomos de carbono. Los anillos cicloalquilo preferidos contienen aproximadamente 5 a aproximadamente 7 átomos en el anillo. El cicloalquilo puede estar opcionalmente sustituido con uno o más “sustituyentes del sistema de anillos” que pueden ser iguales o diferentes y que son como se definieron anteriormente. Los ejemplos no limitativos de cicloalquilos mnonocíclicos adecuados incluyen ciclopropilo, ciclopentilo, ciclohexilo, cicloheptilo y similares. Los ejemplos no limitativos de cicloalquilos multicíclicos adecuados incluyen 1-decalinilo, norbornilo, adamantilo y similares.
“Cicloalquilo” significa un resto cicloalquilo como se definió anteriormente unido mediante un resto alquilo (definido anteriormente) a un núcleo principal. Los ejemplos no limitativos de cicloalquilos adecuados incluyen ciclohexilmetilo, adamantilmetilo y similares.
“Cicloalquenilo” significa un sistema de anillos mono o multicíclico no aromático que comprende aproximadamente 3 a aproximadamente 10 átomos de carbono, preferiblemente aproximadamente 5 a aproximadamente 10 átomos de carbono, que contiene por lo menos un doble enlace carbono-carbono. Los anillos cicloalquenilo preferidos contienen aproximadamente 5 a aproximadamente 7 átomos en el anillo. El cicloalquenilo puede estar opcionalmente sustituido con uno o más “sustituyentes del sistema de anillos” que pueden ser iguales o diferentes y que son como se definieron anteriormente. Los ejemplos no limitativos de cicloalquenilos monocíclicos adecuados incluyen ciclopentenilo, ciclohexenilo, ciclohepta-1,3-dienilo y similares. Un ejemplo no limitativo de un cicloalquenilo multicíclico adecuado es norbornilenilo.
“Cicloalquenilalquilo” significa un resto cicloalquenilo como se definió anteriormente unido mediante un resto alquilo (definido anteriormente) a un núcleo principal. Los ejemplos no limitativos de cicloalquenilalquilos adecuados incluyen ciclopentenilmetilo, ciclohexenilmetilo y similares.
“Halógeno” significa flúor, cloro, bromo o yodo. Se prefieren flúor, cloro y bromo.
“Sustituyente de sistema de anillos” significa un sustituyente acoplado a un sistema de anillos aromático o no aromático que, por ejemplo, reemplaza a un hidrógeno disponible en el sistema de anillos. Los sustituyentes de sistemas de anillos pueden ser iguales o diferentes, en donde cada uno se selecciona independientemente entre el grupo que consiste en alquilo, alquenilo, alquinilo, arilo, heteroarilo, aralquilo, acilarilo, heteroaralquilo, heteroarilalquenilo, heteroarilalquinilo, alquilheteroarilo, hidroxi, hidroxialquilo, alcoxi, ariloxi, aralcoxi, acilo, aroílo, halo, nitro, ciano, carboxi, alcoxicarbonilo, ariloxicarbonilo, aralcoxicarbonilo, alquilsulfonilo, arilsulfonilo, heteroarilsulfonilo, alquiltio, ariltio, heteroariltio, aralquiltio, heteroaralquiltio, cicloalquilo, heterociclilo, -SF5, -OSF5 (para arilo), -O-C(O)-alquilo, -O-C(O)-arilo, -O-C(O)-cicloalquilo, -C(=N-CN)-NH2, -C(=NH)-NH2, -C(=NH)-NH(alquilo), oxima (p. ej., =N-OH), -NY1Y2, -alquil-NY-iY2, -C(O)n Y-iY2, -SO2NY1Y2 y-SO2NY-iY2, en donde Y1 y Y2 pueden ser iguales o diferentes y se seleccionan independientemente entre el grupo que consiste en hidrógeno, alquilo, arilo, cicloalquilo y aralquilo. “Sustituyente de sistemas de anillos” puede también significar un solo resto que puede reemplazar simultáneamente a dos hidrógenos disponibles en dos átomos de carbono adyacentes (un H en cada carbono) en un sistema de anillos. Los ejemplos de dicho resto son metileno dioxi, etilendioxi, -C(CH3)2- y similares, que forman restos tales como por ejemplo:
“Heterociclilo” significa un sistema de anillos monocíclico o multicíclico saturado no aromático que comprende aproximadamente 3 a aproximadamente 10 átomos del anillo, preferiblemente aproximadamente 5 a aproximadamente 10 átomos del anillo, en donde uno o más de los átomos en el sistema de anillos es un elemento distinto de carbono, por ejemplo nitrógeno, oxígeno o azufre, solos o combinados. No hay átomos de oxígeno y/o azufre adyacentes presentes en el sistema de anillos. Los heterociclilos preferidos contienen aproximadamente 5 a aproximadamente 6 átomos del anillo. El prefijo aza, oxa o tia antes del nombre de raíz heterociclilo significa que por lo menos un átomo de nitrógeno, oxígeno o azufre respectivamente está presente como un átomo del anillo. Cualquier -NH en un anillo heterociclilo puede existir protegido tal como, por ejemplo, como un grupo -N(Boc), -N(CBz), -N(Tos)
y similar; dichas protecciones también se consideran parte de la presente invención. El “heterocidilo” puede estar opcionalmente sustituido con uno o más “sustituyentes del sistema de anillos” que pueden ser iguales o diferentes y son como se definen en este documento. El átomo de nitrógeno o azufre del heterociclilo puede opcionalmente oxidarse al correspondiente N-óxido, S-óxido o S,S-dióxido. Los ejemplos no limitativos de anillos heterociclilo monocíclicos adecuados incluyen piperidilo, pirrolidinilo, piperazinilo, morfolinilo, tiomorfolinilo, tiazolidinilo, 1,4-dioxanilo, tetrahidrofuranilo, tetrahidrotiofenilo, lactama, lactona y similares. “Heterociclilo” también incluye los anillos heterociclilo descritos anteriormente en donde =O reemplaza a dos hidrógenos disponibles en el mismo átomo de carbono del anillo. Un ejemplo de dicho resto es pirrolidona:
“Heterociclenilo” significa un sistema de anillos monocíclico o multicíclico no aromático que comprende aproximadamente 3 a aproximadamente 10 átomos del anillo, preferiblemente aproximadamente 5 a aproximadamente 10 átomos del anillo, en donde uno o más de los átomos en el sistema de anillos es un elemento distinto de carbono, por ejemplo, un átomo de nitrógeno, oxígeno o azufre, solo o combinado, y que contiene por lo menos un doble enlace carbono-carbono o un doble enlace carbono-nitrógeno. No hay átomos de oxígeno y/o azufre adyacentes en el sistema de anillos. Los anillos heterociclenilo preferidos contienen aproximadamente 5 a aproximadamente 6 átomos en el anillo. El prefijo aza, oxa o tia antes del nombre de raíz heterociclenilo significa que por lo menos un átomo de nitrógeno, oxígeno o azufre respectivamente está presente como un átomo del anillo. El heterociclenilo puede estar opcionalmente sustituido por uno o más sustituyentes del sistema de anillos, en donde el “sustituyente del sistema de anillos” es como se definió anteriormente. El átomo de nitrógeno o azufre del heterociclenilo puede opcionalmente oxidarse al correspondiente N-óxido, S-óxido o S,S-dióxido. Los ejemplos no limitativos de grupos heterociclenilo adecuados incluyen 1,2,3,4-tetrahidropiridinilo, 1,2-dihidropiridinilo, 1,4-dihidropiridinilo, 1,2,3,6-tetrahidropiridinilo, 1,4,5,6-tetrahidropirimidinilo, 2-pirrolinilo, 3-pirrolinilo, 2-imidazolinilo, 2-pirazolinilo, dihidroimidazolilo, dihidrooxazolilo, dihidrooxadiazolilo, dihidrotiazolilo, 3,4-dihidro-2H-piranilo, dihidrofuranilo, fluorodihidrofuranilo, 7-oxabiciclo[2.2.1]heptenilo, dihidrotiofenilo, dihidrotiopiranilo y similares. “Heterociclenilo” también incluye los anillos heterociclenilo descritos anteriormente en donde =O reemplaza a dos hidrógenos disponibles en el mismo átomo de carbono del anillo. Un ejemplo de dicho resto es pirrolidinona:
Se ha de entender que en los sistemas de anillos que contienen átomos de la presente invención, no hay grupos hidroxilo en los átomos de carbono adyacentes a un N, O o S, así como tampoco hay grupos N o S en el carbono adyacente a otro heteroátomo. Por lo tanto, por ejemplo, en el anillo:
no hay -OH directamente unido a los carbonos marcados 2 y 5.
Se ha de destacar que las formas tautoméricas tales como, por ejemplo, los restos:
se consideran equivalentes en ciertas realizaciones de la presente invención.
“Alcoxi” significa un grupo alquil-O- en el que el grupo alquilo es como se describió previamente. Los ejemplos no limitativos de grupos alcoxi adecuados incluyen metoxi, etoxi, n-propoxi, isopropoxi y n-butoxi. El enlace al resto madre es a través del oxígeno de éter.
El término “sustituido” significa que uno o más de los hidrógenos en el átomo designado se reemplazan con una selección del grupo indicado, siempre que no se exceda la valencia normal del átomo designado bajo circunstancias existentes y que la sustitución resulte en un compuesto estable. Las combinaciones de sustituyentes y/o variables son permisibles solamente si dichas combinaciones resultan en compuestos estables. Por “compuesto estable' o “estructura estable” se entiende un compuesto que es lo suficientemente robusto para sobrevivir al aislamiento hasta un grado de pureza útil a partir de la mezcla de reacción, y la formulación en un agente terapéutico eficaz.
La expresión “opcionalmente sustituido” significa la sustitución opcional con los grupos, radicales o restos especificados.
El término “purificado”, “en forma pura” o “en forma aislada y pura” para un compuesto se refiere al estado físico de dicho compuesto después de ser aislado a partir de un proceso sintético (p. ej., de una mezcla de reacción), o fuente natural o sus combinaciones. Por lo tanto, el término “purificado”, “en forma purificada” o “en forma aislada y purificada” para un compuesto hace referencia al estado físico de dicho compuesto después de obtenerse por un proceso o procesos de purificación descritos en este documento o conocidos por el experto en la técnica (p. ej., cromatografía, recristalización y similares) en pureza suficiente para ser caracterizable mediante técnicas analíticas estándar descritas en este documento o conocidas por el experto en la materia.
La presente divulgación incluye además el compuesto de fórmula I en todas sus formas aisladas. Por lo tanto, por ejemplo, el compuesto de Fórmula I está destinado a abarcar todas las formas del compuesto tales como, por ejemplo, cualquier solvato, hidrato, estereoisómero, tautómero, etc.
La presente divulgación incluye además el compuesto de fórmula I en su forma purificada.
Se ha de entender que se asume que cualquier carbono, así como también cualquier heteroátomo con valencias no satisfechas en el texto, los esquemas, ejemplos y Tablas de este documento tiene un número suficiente de átomo(s) de hidrógeno para satisfacer las valencias. Cualquiera de estos átomos de hidrógeno puede ser deuterio.
Cuando un grupo funcional en un compuesto se denomina “protegido”, esto significa que el grupo en forma modificada impide reacciones colaterales indeseables en el sitio protegido cuando el compuesto se somete a una reacción. Los grupos protectores adecuados serán reconocidos por los expertos en la técnica así como por referencia a libros de texto estándar tales como, por ejemplo, T. W. Greene et al, Protective Groups in Organic Synthesis (1991), Wiley, New York.
Cuando ocurra cualquier variable (p. ej., arilo, heterociclo, R2, etc.) más de una vez en cualquier constituyente o en la Fórmula I, su definición en cada caso será independiente de su definición en cualquier otro caso.
Tal como se emplea en la presente memoria, el término “composición” está destinado a abarcar un producto que comprende los ingredientes especificados en las cantidades especificadas, así como también cualquier producto que resulte, directa o indirectamente, de la combinación de los ingredientes especificados en las cantidades especificadas.
Los profármacos y solvatos de los compuestos de la invención también se contemplan en este documento. Se da a conocer un análisis de profármacos en T. Higuchi and V. Stella, Pro-drugs as Novel Delivery Systems (1987) 14 del A.C.S. Symposium Series, y en Bioreversible Carriers in Drug Design, (1987) Edward B. Roche, ed., American Pharmaceutical Association and Pergamon Press. El término “profármaco” significa un compuesto (p. ej., un precursor de fármacos) que se transforma in vivo para producir un compuesto de Fórmula (I) o su sal, hidrato o solvato farmacéuticamente aceptable del compuesto. La transformación puede ocurrir mediante distintos mecanismos (p. ej., por procesos metabólicos o químicos), tal como por ejemplo, a través de la hidrólisis en la sangre. Se expone un análisis del uso de profármacos en T. Higuchi and W. Stella, “Prodrugs as Novel Delivery Systems,” Vol. 14 del A.C.S. Symposium Series, y en Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987.
Por ejemplo, si un compuesto de Fórmula (I) o su sal, hidrato o solvato farmacéuticamente aceptable del compuesto contiene un grupo funcional de ácido carboxílico, un profármaco puede comprender un éster formado por el reemplazo del átomo de hidrógeno del grupo ácido con un grupo tal como, por ejemplo, alquilo (C1-C8)), alcanoiloximetilo (C2-C12), 1 -(alcanoiloxi)etilo que tiene entre 4 y 9 átomos de carbono, 1 -metil-1 -(alcanoiloxi)-etilo que tiene entre 5 y 10 átomos de carbono, alcoxicarboniloximetilo que tiene entre 3 y 6 átomos de carbono, 1-(alcoxicarboniloxi)etilo que tiene entre 4 y 7 átomos de carbono, 1-metil-1-(alcoxicarboniloxi)etilo que tiene entre 5 y 8 átomos de carbono, N-(alcoxicarbonil)aminometilo que tiene entre 3 y 9 átomos de carbono, 1-(N-(alcoxicarbonil)amino)etilo que tiene entre 4 y 10 átomos de carbono, 3-ftalidilo, 4-crotonolactonilo, gamma-butirolacton-4-ilo, di-N,N-alquilamino (C-i-C2)-alquilo (C2-C3) (tal como p-dimetilaminoetilo), carbamoil-alquilo (C1-C2), N,N-di-alquilcarbamoil (C1-C2)-alquilo (C1-C2 y piperidino-, pirrolidino- o morfolino-alquilo (C2-C3), y similares.
De modo similar, si un compuesto de Fórmula (I) contiene un grupo funcional alcohol, un profármaco se puede formar con el reemplazo del átomo de hidrógeno del grupo alcohol con un grupo tal como, por ejemplo, alcanoiloximetilo (C1-Ca), 1-(alcanoiloxi (C1-Ca))etilo, 1-metil-1-(alcanoiloxi (C1-Ce))etilo, alcoxicarboniloximetilo (C1-C6), N-alcoxicarbonilaminometilo (C1-Ca), succinoílo, alcanoílo (C1-Ca), a-amino-alcanilo (C1-C4), arilacilo y a-aminoacilo, o un a-aminoacil-a-aminoacilo, en donde cada grupo a-aminoacilo se selecciona independientemente de los L-aminoácidos naturales, P(O)(OH)2, -P(O)(O-alquilo (C1-Ca))2 o glucosilo (en donde el radical resulta de la eliminación de un grupo hidroxilo de la forma de hemiacetal de un carbohidrato), y similares.
Si un compuesto de Fórmula (I) incorpora un grupo funcional amina, un profármaco se puede formar por el reemplazo de un átomo de hidrógeno en el grupo amina con un grupo tal como, por ejemplo, R-carbonilo, RO-carbonilo, NRR'-carbonilo en donde R y R' son cada uno independientemente alquilo (C1-C10), cicloalquilo (C3-C7), bencilo, o R-carbonilo es un a-aminoacilo o a-aminoacilo natural, -C(OH)C(O)OY1 en donde Y1 es H, alquilo (C1-Ca) o bencilo, -C(OY2)Y3 en donde Y2 es alquilo (C1-C4) y Y3 es alquilo (C1-C6), carboxi-alquilo (C1-Ca), amino-alquilo (C1-C4) o mono-N-o di-N,N-alquilaminoalquilo (C1-Ca), -C(Y4)Y5 en donde Y4 es H o metilo y Y5 es mono-N- o di-N,N-alquilamino (C1-Ca) morfolino, piperidin-1-ilo o pirrolidin-1-ilo, y similares.
Uno o más de los compuestos de la invención pueden existir en formas no solvatadas como también en formas solvatadas con disolventes farmacéuticamente aceptables tales como agua, etanol y similares, y se pretende que la invención abarque ambas formas, solvatadas y no solvatadas. “Solvato” significa una asociación física de un compuesto de la presente invención con una o más moléculas de disolvente. Esta asociación física implica grados variables de enlaces iónicos y covalentes, incluido el enlace de hidrógeno. En ciertos casos, el solvato será capaz de aislamiento, por ejemplo cuando una o más moléculas de disolvente estén incorporadas en la red cristalina del sólido cristalino. “Solvato” abarca tanto solvatos en fase de disolución como aislables. Los ejemplos no limitativos de solvatos adecuados incluyen etanolatos, metanolatos y similares. “Hidrato” es un solvato en el que la molécula de disolvente es H2O.
Uno o más de los compuestos de la invención puede convertirse opcionalmente a un solvato. La preparación de solvatos en general se conoce. Por lo tanto, por ejemplo, M. Caira et al, J. Pharmaceutical Sci., 93(3), 601-611 (2004) describen la preparación de los solvatos de fluconazol antifúngico en acetato de etilo, así como también a partir de agua. Se describen preparaciones similares de solvatos, hemisolvatos, hidratos y similares en E. C. van Tonder et al, AAPS PharmSciTech., 5(1), artículo 12 (2004); y en A. L. Bingham et al, Chem. Commun., 603-604 (2001). Un procedimiento habitual, no limitativo, implica disolver el compuesto inventivo en cantidades deseadas del disolvente deseado (orgánico o agua o sus mezclas) a una temperatura mayor que ambiente, y enfriar la disolución a una velocidad suficiente como para formar cristales que luego se aíslan por métodos estándar. Las técnicas analíticas tales como, por ejemplo espectroscopia de I. R., demuestran la presencia del disolvente (o agua) en los cristales como un solvato (o hidrato).
“Cantidad eficaz” o “cantidad terapéuticamente eficaz” tiene como fin describir una cantidad del compuesto o composición de la presente invención eficaz para inhibir las enfermedades anteriormente mencionadas y producir entonces un efecto terapéutico, paliativo, inhibidor o preventivo deseado.
Los compuestos de Fórmula I pueden formar sales que también se encuentran dentro del alcance de la presente divulgación. Se entiende que la referencia a un compuesto de Fórmula I en este documento incluye la referencia a sus sales, a menos que se indique algo distinto. El término “sal(es)”, tal como se emplea en la presente memoria, indica sales ácidas formadas con ácidos inorgánicos y/u orgánicos, así como también sales básicas formadas con bases inorgánicas y/u orgánicas. Además, cuando un compuesto de Fórmula I contiene tanto un resto básico, tal como, aunque sin limitarse a ello, un resto piridina o imidazol, y un resto ácido, tal como, aunque sin limitarse a ello, un ácido carboxílico, se pueden formar zwitteriones (“sales internas”) y se incluyen dentro del término “sal(es)” tal como se emplea en este documento. Se prefieren las sales farmacéuticamente aceptables (es decir, no tóxicas, fisiológicamente aceptables), aunque son útiles otras sales. Las sales de dichos compuestos de la Fórmula I se pueden formar, por ejemplo, sometiendo a reacción un compuesto de Fórmula I con una cantidad equivalente, en un medio tal como uno en el que la sal precipita o en un medio acuoso seguido de liofilización.
Las sales de adición de ácido ilustrativas incluyen acetatos, ascorbatos, benzoatos, bencenosulfonatos, bisulfatos,
boratos, butiratos, citratos, alcanforatos, alcanforsulfonatos, fumaratos, hidrocloruros, hidrobromuros, hidroyoduros, lactatos, maleatos, metanosulfonatos, naftalenosulfonatos, nitratos, oxalatos, fosfatos, propionatos, salicilatos, succinatos, sulfatos, tartaratos, tiocianatos, toluenosulfonatos (también conocidos como tosilatos,) y similares. Además, los ácidos que en general se consideran adecuados para la formación de sales farmacéuticamente útiles a partir de compuestos farmacéuticos básicos se analizan, por ejemplo, en P. Stahl et al, Camille G. (eds.) Handbook of Pharmaceutical Salts. Properties, Selection and Use. (2002) Zurich: Wiley-VCH; S. Berge et al, Journal of Pharmaceutical Sciences (1977) 66(1) 1-19; P. Gould, International J. of Pharmaceutics (1986) 33201-217; Anderson et al, The Practice of Medicinal Chemistry (1996), Academic Press, New York; y en el sitio web de The Orange Book (Food & Drug Administration, Washington, D.C.).
Las sales básicas ilustrativas incluyen sales de amonio, sales de metal alcalino tales como sales de sodio, litio y potasio, sales de metales alcalino-térreos tales como calcio y magnesio, sales con bases orgánicas (por ejemplo, aminas orgánicas) tales como diciclohexilaminas, t-butil aminas, y sales con aminoácidos tales como arginina, lisina y similares. Los grupos básicos que contienen nitrógeno se pueden cuaternizar con agentes tales como haluros de alquilo inferior (p. ej., cloruros, bromuros y yoduros de metilo, etilo y butilo), dialquilsulfatos (p. ej., dimetil, dietil y dibutil sulfatos), haluros de cadena larga (p. ej., cloruros, bromuros y yoduros de decilo, laurilo y estearilo), haluros de aralquilo (p. ej., bromuros de bencilo y fenetilo), y otros.
Todas estas sales de ácido y sales de base están destinadas a ser sales farmacéuticamente aceptables dentro del alcance de la invención y todas las sales de ácido y base se consideran equivalentes a las formas libres de los correspondientes compuestos para los propósitos de la invención.
Los ésteres farmacéuticamente aceptables de los presentes compuestos incluyen los siguientes grupos: (1) ésteres de ácido carboxílico obtenidos por esterificación de los grupos hidroxi, en los que el resto no carbonilo de la porción de ácido carboxílico se selecciona entre alquilo de cadena ramiificada o lineal (por ejemplo, acetilo, n-propilo, t-butilo o n-butilo), alcoxialquilo (por ejemplo, metoximetilo), aralquilo (por ejemplo, bencilo), ariloxialquilo (por ejemplo, fenoximetilo), arilo (por ejemplo, fenilo opcionalmente sustituido con, por ejemplo, halógeno, alquilo C1-4 o alcoxi C1-4 o amino); (2) ésteres de sulfonato, tales como alquilo o aralquilsulfonilo (por ejemplo, metanosulfonilo); (3) ésteres de aminoácidos (por ejemplo, L-valilo o L-isoleucilo); (4) ésteres de fosfonato y (5) ésteres de mono-, di- o trifosfato. Los ésteres de fosfato pueden además esterificarse, por ejemplo, mediante un alcohol C1-20 o su derivado reactivo, o mediante un 2,3-di (C6-24)acil glicerol.
Los compuestos de Fórmula I, y sus sales, solvatos, ésteres y profármacos pueden existir en su forma tautomérica (por ejemplo, como una amida o imino éter). Todas estas formas tautoméricas se contemplan en este documento como parte de la presente divulgación.
Los compuestos de Fórmula (I) pueden contener centros asimétricos o quirales, y por lo tanto existir en diferentes formas estereoisoméricas. Se pretende que todas las formas estereoisoméricas de los compuestos de Fórmula (I), así como también sus mezclas, incluidas mezclas racémicas, formen parte de la presente divulgación. Además, la presente divulgación abarca todos los isómeros geométricos y de posición. Por ejemplo, si un compuesto de Fórmula (I) incorpora un doble enlace o un anillo condensado, ambas formas cis y trans, así como también sus mezclas, se abarcan dentro del alcance de la divulgación.
Las mezclas diastereoméricas se pueden separar en sus diastereómeros individuales en base a sus diferencias físicoquímicas por métodos conocidos por los expertos en la técnica, tales como por ejemplo, por cromatografía y/o cristalización fraccionada. Los enantiómeros se pueden separar convirtiendo la mezcla enantiomérica en una mezcla diastereomérica por reacción con un compuesto ópticamente activo apropiado (p. ej., auxiliar quiral tal como un alcohol quiral o un cloruro de ácido de Mosher), separando los diastereómeros y convirtiendo (p. ej., hidrolizando) los diastereómeros individuales a los enantiómeros puros correspondientes. Además, algunos de los compuestos de Fórmula (I) pueden ser atropisómeros (p. ej., biarilos sustituidos) y se consideran parte de la presente divulgación. Los enantiómeros también se pueden separar por uso de una columna HPLC quiral.
Es también posible que los compuestos de Fórmula (I) puedan existir en diferentes formas tautoméricas, y todas esas formas se incluyen dentro del alcance de la divulgación. Además, por ejemplo, todas las formas ceto-enol e iminaenamina de los compuestos se incluyen en la divulgación.
Todos los estereoisómeros (por ejemplo, isómeros geométricos, isómeros ópticos y similares) de los presentes compuestos (incluidos aquellos de las sales, solvatos, ésteres y profármacos de los compuestos, además de las sales, solvatos y ésteres de los profármacos), tales como aquellos que pueden existir debido a carbonos asimétricos en diversos sustituyentes, incluidas formas enantioméricas (que pueden existir incluso en ausencia de carbonos asimétricos), formas rotaméricas, atropisómeros y formas diastereoméricas, se contemplan dentro del alcance de la presente invención, ya que son isómeros de posición (tales como, por ejemplo, 4-piridilo y 3-piridilo). (Por ejemplo, si un compuesto de Fórmula (I) incorpora un doble enlace o un anillo condensado, ambas formas cis y trans, así como también sus mezclas, se abarcan dentro del alcance de la divulgación. Además, por ejemplo, todas las formas cetoenol e imina-enamina de los compuestos se incluyen en la divulgación). Los estereoisómeros individuales de los compuestos de la divulgación pueden, por ejemplo, estar sustancialmente libres de otros isómeros, o se pueden
mezclar, por ejemplo, como racematos o con todos los otros estereoisómeros u otros estereoisómeros seleccionados. Los centros quirales de la presente divulgación pueden tener la configuración S o R como lo definen las Recomendaciones IUPAC de 1974. El uso de los términos “sal”, “solvato”, “éster”, “profármaco” y similares, tiene como fin aplicarse de manera equivalente a la sal, solvato, éster y profármaco de enantiómeros, estereoisómeros, rotámeros, isómeros de posición, racematos o profármacos de los compuestos inventivos.
La presente invención también abarca compuestos de la presente invención marcados isotópicamente, que son idénticos a los enumerados en la presente memoria excepto por el hecho de que uno o más átomos han sido reemplazados por un átomo que tiene una masa atómica o número másico diferente de la masa atómica o número másico que se da habitualmente en la naturaleza. Los ejemplos de isótopos que se pueden incorporar a los compuestos de la invención incluyen isótopos de hidrógeno, carbono, nitrógeno, oxígeno, fósforo, flúor, cloro y yodo, tales como 2H, 3H, 11C, 13C, 14C, 15N, 18O, 17O, 31P, 32P, 35S, 18F, 36Cl y 123I, respectivamente.
Ciertos compuestos isotópicamente marcados de Fórmula (I) (p. ej., aquellos marcados con 3H y 14C) son útiles en ensayos de distribución de tejido de sustrato y/o compuestos. Los isótopos tritiados (es decir, 3H) y carbono-14 (es decir, 14C) se prefieren particularmente por su facilidad de preparación y detectabilidad. Ciertos compuestos isotópicamente marcados de Fórmula (I) pueden ser útiles para propósitos de imágenes médicas. P. ej., aquellos marcados con isótopos de emisión de positrones como 11C o 18F pueden ser útiles para aplicación en tomografía por emisión de positrones (PET) y aquellos marcados con isótopos que emiten rayos gamma como 123I pueden ser útiles para aplicación en una tomografía computada por emisión monofotónica (SPECT). A su vez, la sustitución con isótopos más pesados tales como deuterio (es decir, 2H) puede proporcionar ciertas ventajas terapéuticas que resultan de una mayor estabilidad metabólica (p. ej., mayor semivida in vivo o menores requerimientos de dosis) y por lo tanto se pueden preferir en algunas circunstancias. A su vez, la sustitución con isótopos más pesados tales como deuterio (es decir, 2H) puede proporcionar ciertas ventajas terapéuticas que resultan de una mayor estabilidad metabólica (p. ej., mayor semivida in vivo o menores requerimientos de dosis) y por lo tanto se pueden preferir en algunas circunstancias. Además, la sustitución isotópica en un sitio en el que ocurre la epimerización puede demorar o reducir el proceso de epimerización y retener de este modo la forma más activa o eficaz del compuesto por un periodo de tiempo mayor. Los compuestos isotópicamente marcados de Fórmula (I), en particular aquellos que contienen isótopos con mayores semividas (T1/2 >1 día), pueden en general prepararse siguiendo los procedimientos análogos a aquellos descritos en los Esquemas y/o en los Ejemplos que se exponen a continuación, sustituyendo un reactivo no isotópicamente marcado por un reactivo isotópicamente marcado apropiado.
Las formas polimórficas de los compuestos de Fórmula I, y de las sales, solvatos, ésteres y profármacos de los compuestos de Fórmula I, están destinadas a incluirse en la presente divulgación.
La presente invención se refiere a compuestos capaces de regular y/o modular la transducción de señales de tirosina cinasa y más particularmente la transducción de señales de tirosina cinasa de tipo no receptor.
La transducción de señales mediadas por tirosina cinasas es iniciada por la interacción extracelular con un factor de crecimiento específico (ligando), seguida de dimerización de los receptores, estimulación transitoria de la actividad de la proteína tirosina cinasa intrínseca y fosforilación. Los sitios de unión se crean así para moléculas de transducción de señales intracelulares y llevan a la formación de complejos con un espectro de moléculas de señalización citoplásmicas que facilitan la respuesta celular apropiada (p. ej., división celular, efectos metabólicos y respuestas al microentorno extracelular).
Se ha demostrado que los sitios de fosforilación de tirosinas en los receptores de los factores de crecimiento funcionan como sitios de unión de gran afinidad hacia dominios SH2 (homología src) de moléculas de señalización. Se han identificado varias proteínas de sustrato intracelulares que se asocian con las tirosina cinasas de tipo receptor. Se pueden dividir en dos grupos principales: (1) sustratos que tienen un dominio catalítico; y (2) sustratos que carecen de dicho dominio pero que sirven como adaptadores y se asocian con moléculas catalíticamente activas. La especificidad de las interacciones entre receptores y dominios SH2 de sus sustratos es determinada por los residuos de aminoácidos que rodean inmediatamente al residuo tirosina fosforilado. Las diferencias en las afinidades de unión entre los dominios SH2 y las secuencias de aminoácidos que rodean a los residuos de fosfatirosina en receptores particulares concuerdan con las diferencias observadas en sus perfiles de fosforilación de sustratos. Estas observaciones sugieren que la función de cada tirosina cinasa de tipo receptor es determinada no solamente por su patrón de expresión y disponibilidad de ligandos, sino también por la gama de vías de transducción de señales en dirección 3' que son activadas por un receptor particular. Por lo tanto, la fosforilación proporciona un importante paso que determina la selectividad de las vías de señalización obtenidas por receptores de los factores de crecimiento específicos, además de los receptores de los factores de diferenciación.
La transducción de señales de tirosina cinasa resulta en, entre otras respuestas, proliferación, diferenciación y metabolismo celular. La proliferación celular anormal puede resultar en una amplia gama de trastornos y enfermedades, incluidos el desarrollo de neoplasias tales como carcinoma, sarcoma, leucemia, glioblastoma, hemangioma, psoriasis, arteriosclerosis, artritis y retinopatía diabética (u otros trastornos relacionados con la angiogénesis y/o vasculogénesis descontrolada, p. ej., degeneración macular).
La presente invención se refiere por lo tanto a compuestos que regulan, modulan y/o inhiben la transducción de señales, afectando la actividad enzimática de las RTK y/o las tirosina cinasas de tipo no receptor e interfiriendo con la señal transducida por dichas proteínas. Más particularmente, la presente invención se refiere a compuestos que regulan, modulan y/o inhiben las vías de transducción de señales mediadas por RTK y/o tirosina cinasa de tipo no receptor como un planteamiento terapéutico para curar muchas clases de tumores sólidos, incluidos aunque sin limitarse a ellos, carcinoma, sarcoma, leucemia, eritroblastoma, glioblastoma, meningioma, astrocitoma, melanoma y mioblastoma. Las indicaciones pueden incluir, aunque sin limitarse a ello, tumores malignos de cerebro, vejiga, ovario, gástricos, de páncreas, de colon, de la sangre, de pulmón y de hueso.
Esquema 1
3-Hidroxi-3-(4-nitrofenil)-2-cianoacrilonitrilo
Se disolvieron cloruro de 4-nitrobenzoílo (93 g, 0,50 mol) y malononitrilo (33 g, 0,50 mol) en tolueno (400 ml) y THF (70 ml) en un matraz equipado con un embudo de adición, un termómetro, una varilla agitadora y una atmósfera de argón. El matraz se sumergió en un baño a -30°C. Cuando la temperatura interna alcanzó -10°C, DIPEA (129 g, 1,0 mol) en 300 ml de tolueno se le añadió gota a gota durante 40 min. Después de 1 hora más, el baño se eliminó. Después de aprox. 14 horas, la mezcla tenía 2 capas. La capa inferior se concentró al vacío, se disolvió en 400 ml de EtoAc, se lavó con ácido cítrico acuoso al 10% (2 X 250 ml), se secó sobre Na2SO4 y se concentró al vacío. El residuo se disolvió principalmente en THF (100 ml) y se dejó 30 min en un congelador. El sólido resultante se recogió con la ayuda de THF adicional enfriado en el congelador y se presionó bien con un dique de goma. El sólido aislado (60 g) se suspendió en H2SO41M, se recogió, se prensó y se lavó con agua. Después de secar, el sólido pesaba 36 g. Este sólido se disolvió en EtOAc (400 ml), se lavó con H2SO4 1 M (200 ml) y agua (200 ml), se filtró a través de un papel de separación de fases y se concentró. El residuo sólido se reconcentró sucesivamente a partir de diclorometano y tolueno, y se secó en alto vacío. En esta etapa, se aislaron 25 g. La pureza de1HPLC fue 94%. El análisis de un espectro de RMN de 60 MHz indicó aproximadamente 18% en mol de DIPEA. El material se usó en la siguiente etapa sin más purificación.
Eventualmente se aisló otra porción de 15 g de sólido con 95% pureza de HPLC pero que contenía 30% en mol de DIPEA, a partir del filtrado de THF. Este material se apartó. El rendimiento total estimado de la reacción fue aproximadamente 42% RMN (60 MHz) (CDCla) 8 ^8,0 (AB, 4 H)
Preparación 2
3-Metoxi-3-(4-nitrofenil)-2-cianoacrilonitrilo
Se disolvió 3-hidroxi-3-(4-nitrofenil)-2-cianoacrilonitrilo (21,5 g, 0,10 mol) en acetonitrilo (430 ml) y metanol (43 ml) en un matraz equipado con un embudo de goteo, un termómetro, una varilla agitadora y una atmósfera de argón. El matraz se sumergió en un baño a -15°C hasta el nivel en que la temperatura interna se mantuvo entre -5°C y 0°C. (75 ml de una disolución 2,0 M en éter dietílico, 0,15 mol) se añadió gota a gota en 20 min. El análisis de HPLC indicó una reacción incompleta, y se añadió una porción adicional (25 ml, 0,05 mol) de trimetilsilildiazometano. Esto se repitió con 35 ml (0,07 mol). Después de 20 min, la mezcla se vertió en una disolución de ácido acético agitada rápidamente (15 g, 0,25 mol) en EtOAc (1,8 l). La mezcla se extrajo con agua (3 X 1,5 l), se filtró a través de un papel para separación de fases y se concentró al vacío. El residuo sólido pesó 14,4 g y se utilizó en la siguiente etapa sin más purificación. RMN (60 MHz) (CDCla) 88,0 (AB, 4 H); 4,0 (s, 3 H).
Preparación 3
3-Amino-3-(4-nitrofenil)-2-cianoacrilonitrilo
Se suspendió 3-metoxi-3-(4-nitrofenil)-2-cianoacrilonitrilo (14,4 g, 0,063 mol) en etanol (1 l) en un matraz equipado con un agitador magnético. A la suspensión se le añadieron 60 ml (aprox. 0,20 mol) de una disolución al 10% (p/p) de amoniaco en metanol. La mezcla se agitó vigorosamente durante 15 min, momento en el cual el análisis HPLC demostró la ausencia de material de partida. La mezcla ahora homogénea se concentró al vacío hasta aprox. 80 ml. El sólido que se había formado se recogió con la ayuda de una pequeña cantidad de etanol adicional y se prensó bien con un dique de goma. La torta se lavó con etanol (2 X 5 ml) y se dejó secar en una campana de extracción. }El sólido seco pesaba 8,8 g. El filtrado se concentró y se mezcló con diclorometano (10 ml). El sólido resultante se recogió, se lavó con diclorometano (2 X 2 ml), se secó y se combinó con la primera cosecha para producir 9,9 g (46% en 2 etapas). El análisis HPLC indicó una pureza de 91%. RMN (60 MHz) (DMSO-d6) 88,8 (bs, 0,5 H); 8,0 (AB, 4 H); 3,2 (bs, 1 H); 2,8 (bs, 0,5 H). El espectro de IR exhibió extensiones de nitrilo a 2221 y 2207 cm-1.
Preparación 4
3-Amino-3-(4-nitrofenil)-2-tioformamidoacrilonitrilo
Se suspendieron 3-amino-3-(4-nitrofenil)-2-cianoacrilonitrilo (8,8 g, 0,052 mol) en etanol (60 ml) y agua (60 ml) en un matraz equipado con una varilla agitadora, un condensador de reflujo y una atmósfera de argón. Después de añadir ditiofosfato de dietilo (13,3 g, 0,083 mol), la mezcla se dispuso en un baño a 100°C durante aprox. 14 horas. El análisis de HPLC indicó una reacción incompleta, y se añadió una porción más de ditiofosfato de dietilo (2,6 g, 0,014 mol). Después de 4 h, la mezcla se vertió en 1,2 l de hielo/agua (agitación rápida).
Una vez que esta suspensión se había agitado durante 40 min, se recogió el sólido, se prensó con un dique de goma
y se lavó con agua (100 ml). El sólido seco pesó aprox. 8,8 g (aprox. 88%). La pureza de1HPLC fue 97%. RMN (60 MHz) (DMSO-d6) 88,6 (bs, 1 H); 8,0 (AB, 4 H); 8,2 (bs, 1 H); 7,8 (bs, 1 H); 3,3 (bs, 1 H); El espectro de IR exhibió una sola extensión de nitrilo a 2191 cm-1.
Preparación 5
5-Amino-3-(4-nitrofenil)isotiazol-4-carbonitrilo
3-Amino-3-(4-nitrofenil)-2-tioformamidoacrilonitrilo (10,0 g, 0,040 mol) y peróxido de hidrógeno al 30% (9,1 g, 0,08 mol) se mezclaron con etanol (50 ml) en un matraz equipado con una varilla agitadora y una atmósfera de argón. La mezcla se agitó vigorosamente sin salpicar material hacia los lados del matraz. Después de 14 horas, el análisis HPLC indicó solamente 50% de conversión, y se añadió una porción adicional de peróxido de hidrógeno (9,1 g, 0,08 mol) y etanol (30 ml). Después de 8 h, la mezcla se vertió agitando rápidamente en hielo/agua (250 ml). Después de que la suspensión se había agitado durante 20 min, se recogió el sólido. Este sólido se secó hasta peso constante en una campana de extracción para dar 9,3 g (95%). El análisis HPLC indicó una pureza de 97%. RMN (60 MHz) (DMSO-d6/CD3OD) 88,2 (AB, 4H); 4,1 (s, 2 H). La extensión de nitrilo se movió a 2216 cirr1
Preparación 6
[4-Ciano-3-(4-nitrofenil)isotiazol-5-il]carbamato de fenilo
A una mezcla de 5-amino-3-(4-nitrofenil)isotiazol-4-carbonitrilo (394 mg, 1,60 mmol), N, N-diisopropiletilamina (0,836 ml, 4,8 mmol) y DMAP catalítico en 20 ml de 1,2-dicloroetano a TA se le añadió cloroformiato de fenilo (0,301 ml, 2,40 mmol) gota a gota en 1 minuto. La mezcla de reacción se agitó a TA durante 22 horas, luego se añadió directamente a una columna de gel de sílice empaquetada seca eluyendo con CHCh, luego gradiente de 10% a 50% EtOAc en CHCl3. El compuesto del título se obtuvo como un sólido beis (131 mg, 22%) y se usó tal cual en la siguiente etapa.
1H RMN (DMSO D2O) 8: 8,33 - 8,39 (m, 2H), 8,12 - 8,17 (m, 2H), 7,36 - 7,44 (m, 2H), 7,14 - 7,25 (m, 3H) Preparación 7
1-[4-ciano-3-(4-nitrofenil)isotiazol-5-il]-3-(3-morfolin-4-ilpropil)urea
Una mezcla de (4-ciano-3-(4-nitrofenil)isotiazol-5-il)carbamato de fenilo (37 mg, 0,10 mmol) y 3-morfolinopropilamina (0,021 ml, 0,14 mmol) en 0,8 ml de dioxano se calentó a 80°C. Después de 2 horas, la mezcla de reacción se evaporó hasta una película oleosa amarilla. Este material se cromatografió luego eluyendo con EtOAc, luego gradiente de 2% a 6% MeOH en EtOAc para dar el compuesto del título en forma de un sólido amarillo pálido (33 mg, 80%).1H RMN (acetona) 8: 8,38 - 8,44 (m, 2H), 8,22 - 8,27 (m, 2H), 6,91 (t, J = 5,4 Hz, 1 H), 3,59 - 3,64 (m, 4H), 3,38 - 3,45 (m, 2H), 2,37 - 2,45 (m, 6H), 1,77 (quin, J = 6,8 Hz, 2H)
Ejemplo 1 (parte de la divulgación)
5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)-3-(4-nitrofenil)isotiazol-4-carboxamida
Una mezcla de 1-(4-ciano-3-(4-nitrofenil)isotiazol-5-il)-3-(3-morfolinopropil)urea (113 mg, 0,27 mmol) en 3,5 m1H2SO4 conc. se calentó a 45°C. Después de 1,5 horas, la reacción se inactivó en 100 ml de agua con hielo, proporcionando un sólido de tipo gel blanco. La disolución acuosa se tornó básica usando Na2CO3 y luego se extrajo con EtOAc, la capa de EtOAc se lavó con salmuera, se secó con Na2SO4 anhidro y evaporación rotatoria para dar el compuesto del título en forma de un sólido beis (118 mg, 100%).
1H RMN (acetona) 8: 10,58 (br. s., 1 H), 8,31 - 8,36 (m, 2H), 7,88 - 7,94 (m, 2H), 7,50 (br. s., 1 H), 3,59 - 3,64 (m, 4H), 3,39 (td, J = 6,7, 5,6 Hz, 2H), 2,41 - 2,45 (m, 2H), 2,37 - 2,41 (m, 4H), 1,76 (quin, J = 6,8 Hz, 2H)
Ejemplo 2 (parte de la invención)
3-(4-aminofenil)-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
Una mezcla de 5-(3-(3-morfolinopropil)ureido)-3-(4-nitrofenil)isotiazol-4-carboxamida (110 mg, 0,25 mmol) y óxido de platino (25 mg, 0,11 mmol) en 15 ml de MeOH se hidrogenó bajo 60 PSI de hidrógeno. Después de 16,5 horas, la mezcla se filtró y se efectuó la evaporación rotatoria hasta obtener un sólido blanquecino. Luego se combinaron 16 mg adicionales de producto impuro de otra reacción, y este material se cromatografió eluyendo con gradiente de 5% a 15% MeOH en CHCh para dar el compuesto del título en la forma de un sólido blanquecino (47 mg, 40%).
1H RMN (acetona) 8: 10,97 (br. s., 1 H), 7,47 (br. s., 1 H), 7,22 - 7,27 (m, 2H), 6,72 - 6,78 (m, 2H), 6,69 (br. s., 1 H), 5,86 (br. s,, 1 H), 5,00 (s, 2H), 3,59 - 3,63 (m, 4H), 3,37 (td, J = 6,7, 5,6 Hz, 2H), 2,41 - 2,45 (m, 2H), 2,36 - 2,41 (m, 4H), 1,75 (quin, J = 6,8 Hz, 2H)
Ejemplo 3
3-{4-[(anilinocarbonil)amino]fenil}-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
Una mezcla de 3-(4-aminofenil)-5-(3-(3-morfolinopropil)ureido)isotiazol-4-carboxamida (12 mg, 0,030 mmol), N,N-diisopropiletilamina (0,021 ml, 0,120 mmol) e isocianato de fenilo (0,0056 ml, 0,051 mmol) en 1,0 ml de THF se agitó a TA durante 19 horas. La reacción se inactivó con 0,2 ml de disolución acuosa de Na2CO3, se agitó 5 min a TA y luego se repartió entre EtOAc y disolución acuosa de Na2CO3, se lavó la capa de EtOAc con H2O, salmuera, se secó con Na2SO4 anhidro y evaporación rotatoria para obtener un sólido blanco. El sólido se cromatografió eluyendo con CHCl3, luego con un gradiente de 2,5% a 10% MeOH en CHCh. El sólido resultante se sometió a un tratamiento con EtOAc/NaHCO3 para eliminar la presencia de cualquier impureza del gel de sílice. Tras la evaporación de la capa de EtOAc, se obtuvo el compuesto del título en forma de un sólido blanco (12 mg, 77%).
1H RMN (acetona) 8: 10,89 (br. s., 1 H), 8,37 (s, 1 H), 8,21 (s, 1 H), 7,65 - 7,70 (m, 2H), 7,53 - 7,58 (m, 2H), 7,46 - 7,52 (m, 3H), 7,25 - 7,32 (m, 2H), 6,96 - 7,03 (m, 1 H), 6,66 - 6,83 (m, 1 H), 5,86 (br. s., 1 H), 3,59 - 3,64 (m, 4H), 3,34 -3,42 (m, 2H), 2,42 - 2,46 (m, 2H), 2,37 - 2,41 (m, 4H), 1,76 (quin, J = 6,8 Hz, 2H)
Ejemplo 4
3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
En un modo similar a aquel descrito para el Ejemplo 3, se usaron 3-(4-aminofenil)-5-(3-(3-morfolinopropil)ureido)isotiazol-4-carboxamida (8 mg, 0,020 mmol) e isocianato de 2-fluoro-5-metilfenilo (0,0029 ml, 0,022 mmol) para dar el compuesto del título en forma de un sólido blanco (6 mg, 58%).
1H RMN (acetona) 8: 10,88 (br. s., 1 H), 8,72 (s, 1 H), 8,14 (dd, J = 7,8, 2,2 Hz, 1 H), 8,02 (d, J = 2,9 Hz, 1 H), 7,66 -7,71 (m, 2H), 7,45 - 7,54 (m, 3H), 7,02 (dd, J = 11,3, 8,4 Hz, 1 H), 6,79 -6,86 (m, 1 H), 6,69 -6,79 (m, 1 H), 5,87 (br. s., 1 H), 3,59 - 3,64 (m, 4H), 3,34 - 3,42 (m, 2H), 2,41 - 2,46 (m, 2H), 2,37 - 2,41 (m, 4H), 2,32 (s, 3H), 1,76 (quin, J = 6,8 Hz, 2H)
Ejemplo 5
3- [4-({[(3-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
En un modo similar a aquel descrito para el Ejemplo 3, se usó 3-(4-aminofenil)-5-(3-(3-morfolinopropil)ureido)isotiazol-4- carboxamida (12 mg, 0,030 mmol), 3 gotas de N, N-diisopropiletilamina e isocianato de meta-tolilo (0,0056 ml, 0,045 mmol) para dar el compuesto del título en forma de un sólido blanco (13 mg, 83%).
1H RMN (acetona) 8: 10,89 (br. s., 1H), 8,35 (s, 1H), 8,14 (s, 1 H), 7,64 - 7,69 (m, 2H), 7,44 - 7,54 (m, 3H), 7,38 - 7,40 (m, 1 H), 7,31 - 7,36 (m, 1 H), 7,16 (t, J = 7,8 Hz, 1 H), 6,80 - 6,85 (m, 1 H), 6,68 - 6,79 (m, 1 H), 5,86 (br. s., 1 H), 3,60 - 3,64 (m, 4H), 3,34 - 3,42 (m, 2H), 2,42 - 2,47 (m, 2H), 2,38 - 2,43 (m, 4H), 2,30 (s, 3H), 1,76 (quin, J = 6,7 Hz, 2H)
Ejemplo 6
3- {4-[({[2-fluoro-5-(trifluorometil)fenil]amino}carbonil)amino]fenil}-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
En un modo similar a aquel descrito para el Ejemplo 3, se usó 3-(4-aminofenil)-5-(3-(3-morfolinopropil)ureido)isotiazol-4- carboxamida (12 mg, 0,030 mmol), 3 gotas de N, N-diisopropiletilamina e isocianato de 2-fluoro-5-(trifluorometilo)fenilo (0,0087 ml, 0,060 mmol) para dar el compuesto del título en forma de un sólido blanco (11 mg, 62%).
1H RMN (acetona) 8: 10,87 (br. s., 1 H), 8,89 (s, 1 H), 8,76 - 8,81 (m, 1 H), 8,45 (d, J = 2,6 Hz, 1 H), 7,66 - 7,72 (m, 2H), 7,47 - 7,56 (m, 3H), 7,36 - 7,45 (m, 2H), 6,66 - 6,83 (m, 1 H), 5,86 (br. s., 1 H), 3,59 - 3,64 (m, 4H), 3,34 - 3,42 (m, 2H), 2,41 -2,46 (m, 2H), 2,37 -2,41 (m, 4H), 1,76 (quin, J = 6,7 Hz, 2H)
Ejemplo 7
3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
En un modo similar a aquel descrito para el Ejemplo 3, se usó 3,3-(4-aminofenil)-5-(3-(3-morfolinopropil)ureido)isotiazol-4-carboxamida (12 mg, 0,030 mmol), N, N-diisopropiletilamina (0,021 ml, 0,120 mmol) e isocianato de para-tolilo (0,0068 ml, 0,054 mmol) para dar el compuesto del título en forma de un sólido blanco (11 mg, 70%).
1H RMN (acetona) 8: 7,55 - 7,60 (m, 2H), 7,47 - 7,52 (m, 2H), 7,28 - 7,34 (m, 2H), 7,09 - 7,14 (m, 2H), 3,67 - 3,73 (m, 4H), 3,30 -3,34 (m, 2H), 2,41 -2,52 (m, 6H), 2,30 (s, 3H), 1,78 (quin, J = 7,2 Hz, 2H)
Preparación 7
1-[4-ciano-3-(4-nitrofenil)isotiazol-5-il]-3-(3-metoxipropil)urea
Una mezcla de (4-ciano-3-(4-nitrofenil)isotiazol-5-il)carbamato de fenilo (37 mg, 0,10 mmol) y 3-metoxipropilamina (0,015 ml, 0,15 mmol) en 0,8 ml de dioxano se calentó a 80°C. Después de 2 horas, la mezcla de reacción se evaporó hasta una película sólida. El sólido se trituró con diclorometano y luego 10% EtOAc en hexano para dar un sólido amarillo-anaranjado. Este material se cromatografió luego, eluyendo con gradiente de 50% a 70% EtOAc en hexano. El filtrado de la trituración y el material de otra reacción se combinaron y cromatografiaron con EtOAc/hexano. Los lotes de producto limpio se combinaron para dar el compuesto del título en forma de un sólido blanquecino (27 mg).
1H RMN (acetona) 8: 10,04 (br. s. 1 H), 8,38 - 8,44 (m, 2H), 8,22 - 8,28 (m, 2H), 6,90 (s, 1 H), 3,47 (t, J = 6,0 Hz, 2H), 3,39 - 3,46 (m, 2H), 3,29 (s, 3H), 1,83 (quin, J = 6,3 Hz, 2H)
Ejemplo 8 (parte de la divulgación)
5-({[(3-metoxipropil)amino]carbonil}amino)-3-(4-nitrofenil)isotiazol-4-carboxamida
Una mezcla de 1-(4-ciano-3-(4-nitrofenil)isotiazol-5-il)-3-(3-metoxipropil)urea (12 mg, 0,032 mmol) en 0,8 m1H2SO4 conc. se calentó a 45°C. Después de 1,5 horas, la reacción se inactivó en 25 ml de agua que contenía salmuera. La disolución acuosa se ajustó hasta pH = 1 usando NaHCO3 saturado y luego se extrajo con EtOAc, la capa de EtOAc se lavó con salmuera, se secó con Na2SO4 anhidro y se sometió a evaporación rotatoria para obtener un sólido. El sólido se recristalizó a partir de acetonitrilo proporcionando el compuesto del título en forma de un sólido blanco (4 mg, 29%).
1H RMN (acetona) 8: 10,54 (br. s. 1H), 8,31 - 8,36 (m, 2H), 7,88 - 7,93 (m, 2H), 7,40 (br. s. 1 H), 3,45 (t, J = 6,2 Hz, 2H), 3,36 - 3,43 (m, 2H), 3,28 (s, 3H), 1,82 (quin, J = 6,4 Hz, 2H)
Ejemplo 9 (parte de la divulgación)
3-(4-aminofenil)-5-({[(3-methoxipropil)amino]carbonil}amino)isotiazol-4-carboxamida
Una mezcla de 5-(3-(3-methoxipropil)ureido)-3-(4-nitrofenil)isotiazol-4-carboxamida (4 mg, 0,009 mmol) y óxido de platino catalítico en 4 ml de MeOH se hidrogenó bajo 60 PSI de hidrógeno. Después de 17 horas, la mezcla se filtró y se efectuó la evaporación rotatoria hasta obtener un sólido blanco. El sólido se repartió entre EtOAc y disolución acuosa de NaHCOa, la capa de EtOAc se secó con Na2SO4 anhidro y se evaporó para dar el compuesto del título en forma de un sólido blanco (2 mg, 66%).
1H RMN (acetona) 8: 10,93 (br. s. 1 H), 7,36 (br. s. 1 H), 7,22 - 7,27 (m, 2H), 6,72 - 6,78 (m, 2H), 6,67 (br. s. 1 H), 5,86 (br. s. 1 H), 5,00 (br. s., 2H), 3,44 (t, J = 6,2 Hz, 2H), 3,33 - 3,41 (m, 2H), 3,27 (d, J = 0,6 Hz, 3H), 1,81 (quin, J = 6,4 Hz, 2H)
Ejemplo 10
3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-metoxipropil)amino]carbonil}amino)isotiazol-4-carboxamida
En un modo similar a aquel descrito para el Ejemplo 3, 3-(4-aminofenil)-5-(3-(3-methoxipropil)ureido)isotiazol-4-carboxamida e isocianato de 2-fluoro-5-metilfenilo se pueden convertir al compuesto del título.
Ejemplo 11
5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)-3-(4-{[3-(trifluorometil)benzoil]amino}fenil)isotiazol-4-carboxamida
A una mezcla de 3-(4-aminofenil)-5-(3-(3-morfolinopropil)ureido)isotiazol-4-carboxamida (6 mg, 0,015 mmol) y N,N-diisopropiletilamina (0,0078 ml, 0,045 mmol) en 0,8 ml de THF a TA se le añadió cloruro de 3-(trifluorometil)benzoílo (0,0024 ml, 0,017 mmol). La reacción se agitó a TA durante 2 horas, luego se inactivó con disolución acuosa de Na2CO3, se agitó 5 min a TA y luego se repartió entre EtOAc y disolución acuosa de Na2CO3, se lavó la capa de EtOAc con H2O, salmuera, se secó con Na2SO4 anhidro y se sometió a evaporación rotatoria para obtener un sólido blanco. El sólido se cromatografió eluyendo con CHCh, luego con un gradiente de 2,5% a 10% MeOH en CHCh. El sólido resultante se sometió a un tratamiento con EtOAc/NaHCO3 para eliminar la presencia de cualquier impureza del gel de sílice. Tras la evaporación de la capa de EtOAc, se obtuvo el compuesto del título en forma de un sólido blanco (7 mg, 76%).
1H RMN (acetona) 8: 10,86 (br. s,, 1 H), 9,99 (s, 1 H), 8,30 - 8,35 (m, 2H), 7,93 - 8,00 (m, 3H), 7,76 - 7,84 (m, 1 H), 7,52 - 7,63 (m, 3H), 6,82 (br. s., 1 H), 5,90 (br. s., 1 H), 3,59 - 3,64 (m, 4H), 3,34 - 3,42 (m, 2H), 2,41 - 2,45 (m, 2H), 2,36 -2,41 (m, 4H), 1,76 (quin, J = 6,7 Hz, 2H)
Preparación 8
2,2-Dicianoeteno-1,1-bis(tiolato) de sodio
Se añadió NaOH sólido (187,2 g, 4541 mmol) a EtOH (2000,0 ml, 34253 mmol) a TA y se agitó hasta disolver. La disolución se enfrió hasta 15°C y se añadió malononitrilo (150 g, 2300 mmol) en una porción, y la suspensión resultante se agitó hasta que el malononitrilo se había disuelto (la reacción es ligeramente endotérmica). La mezcla de reacción
se agitó durante 1 h y se añadió disulfuro de carbono (136,6 ml, 2271 mmol) mientras se mantenía a temperatura entre 10 y 20°C. Después de añadir aproximadamente la mitad del disulfuro de carbono, la mezcla de reacción comienza a solidificar y se torna muy difícil de agitar. La adición de disulfuro de carbono siguió, y la reacción se agitó mecánicamente con una espátula. Una vez completada la adición, la mezcla de reacción se calentó hasta 30°C y luego se enfrió hasta temperatura ambiente. El producto se filtró y secó al vacío a 82°C durante 2 días. El material sólido obtenido se trituró con un mortero y luego se secó al vacío para dar el compuesto del título (335 gramos, 79%).
Preparación 9
3,5-dicloroisotiazol-4-carbonitrilo
Una suspensión de 2,2-dicianoeteno-1,1-bis(tiolato) de sodio (40 gramos, 0.21 mol) se suspendió en CCU (250 ml) a TA. A la mezcla de reacción se le inyectó gas Cl2 (aproximadamente 2 equivalentes) que causó que la mezcla de reacción llegara a reflujo. La mezcla de reacción se filtró y se concentró. Este procedimiento se repitió cuatro veces más con 41, 44, 45 y 50 gramos de 2,2-dicianoeteno-1,1-bis(tiolato) sódico. Los productos de la reacción se combinaron y destilaron con kugelrohr. El destilado se recristalizó a partir de heptanos para dar el compuesto del título (50 gramos, 0,288 mol).
Preparación 10
4-(3-Cloro-4-cianoisotiazol-5-il)fenilcarbamato de terc-butilo
Una mezcla de 3,5-dicloroisotiazol-4-carbonitrilo (5,37 g, 30 mmol), ácido 4-(tercbutoxicarbonilamino)fenilborónico (14,22 g, 60 mmol), fluoruro de potasio (6,11 g, 105 mmol), 18-corona-6 (3,96 g, 15 mmol) y acetato de paladio (337 mg, 1,5 mmol) en tolueno (250 ml) se calentó a reflujo durante 6 horas. La reacción se enfrió hasta TA y la mezcla se diluyó con agua y EtOAc. Las capas se separaron y la capa acuosa se extrajo con EtOAcx3. Los extractos orgánicos combinados se lavaron con salmuera y se secaron con MgSO4, se filtraron y se concentraron. El producto bruto se purificó mediante columna de gel de sílice ultrarrápida, se eluyó con 5-15% EtOAc en hexanos para obtener el compuesto de arriba como un sólido blanco cristalino (8,55g, 85%). Los espectros de RMN y MS coinciden con la estructura. Pureza HPLC 97,6%.
Preparación 11
5-(4-Aminofenil)-3-cloroisotiazol-4-carbonitrilo
Una disolución de 4-(3-cloro-4-cianoisotiazol-5-il)fenilcarbamato de terc-butilo (4,76 g, 13,38 mmol) en DCM (100 ml) se trató con 10 ml de TFA. La mezcla de reacción se agitó a TA durante la noche. El disolvente se retiró al vacío. El residuo se diluyó con agua y DCM (100 ml). Las capas se separaron y la capa acuosa se extrajo con DCMx2. Los extractos orgánicos combinados se lavaron con salmuera y se secaron con MgSO4, se filtraron y se concentraron. El producto se enjuagó con Et2O/hexanos y se recogió por filtración en forma de un sólido amarillo brillante (3,15 g, 94%).
Preparación 12
1-[4-(3-doro-4-cianoisotiazol-5-il)fenil]-3-(2-fluoro-5-metilfenil)urea
Una disolución de 5-(4-Aminofenil)-3-cloroisotiazol-4-carbonitrilo (4,565 g, 19,4 mmol) e isocianato de 2-fluoro-5-metilfenilo (5,85 g, 38,7 mmol) en 100 ml de THF seco se sometió a reflujo durante una noche. La TLC se indicó la presencia de una cantidad considerable de material de partida. Se añadieron 2 g adicionales de isocianato de 2-fluoro-5-metilfenilo y la reacción continuó durante otras 24 h. La reacción se enfrió hasta TA. Se eliminó el THF al vacío y el sólido resultante se agitó en 200 ml de Et2O durante 1 h. El producto se recogió por filtración y se lavó con Et2O/hexanos para proporcionar un sólido amarillo ligero (6,78 g, 90%).
Preparación 13
1-(4-{4-Ciano-3-[(2,4-dimethoxibenzil)amino]isotiazol-5-il}fenil)-3-(2-fluoro-5-metilfenil)urea
Una suspensión de 1-[4-(3-cloro-4-cianoisotiazol-5-il)fenil]-3-(2-fluoro-5-metilfenil)urea (4,3 g, 11,1 mmol) en 15 ml de 2,4-dimethoxibencilamina se calentó a 73°C durante 24 h. La reacción se tornó clara después de ~3h. La reacción se enfrió hasta TA. El residuo se diluyó con 300 ml de DCM y se lavó dos veces con disolución al 10% de HCl, Na2S2O5 saturado dos veces y luego salmuera. La disolución orgánica se secó con MgSO4, se filtró y se concentró. El producto bruto se purificó en columna de gel de sílice ultrarrápida con 2-5% MTBE en DCM/hexanos (2:1) para obtener el compuesto del título en forma de un sólido amarillo ligero (1,19 g, 21%).
Preparación 14
1-[4-(3-amino-4-cianoisotiazol-5-il)fenil]-3-(2-fluoro-5-metilfenil)urea
Una suspensión de 1-(4-{4-ciano-3-[(2,4-dimethoxibenzil)amino]isotiazol-5-il}fenil)-3-(2-fluoro-5-metilfenil)urea (593 mg, 1,15 mmol) en 50 ml de DCM se trató con 1,5 ml de TFA. Se disolvió el sólido y la reacción se tornó amarilla y luego roja. La TLC indicó que la reacción se había completado en <30 min. Se añadió disolución saturada de Na2CO3 y la mezcla se agitó durante 30 min. Las capas se separaron y la capa acuosa se extrajo con DCMx3. Los extractos orgánicos combinados se lavaron con salmuera y se secaron con MgSO4, se filtraron y se concentraron. El producto bruto se redisolvió en 100 ml de EtOAc. La impureza insoluble se filtró a través de celite y se lavó con EtOAc. El filtrado se concentró al vacío para dar el producto en forma de un sólido color crema (398 mg, 94%).
Preparación 15
4-[({[4-Ciano-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]butanoato de metilo
Una disolución de 5-amino-3-(4-nitrofenil)isotiazol-4-carbonitrilo (25,0 g, 0,101 mol) en tetrahidrofurano (300 ml) dimetilsulfóxido (40 ml) a temperatura ambiente se trató con carbonato de potasio (35,0 g, 0,25 mol). La mezcla resultante se agitó a temperatura ambiente durante 15 min. La mezcla de reacción se trató con éster metílico de ácido 4-isocianato-butírico (21,8 g, 0,15 mol) a temperatura ambiente. Se agitó la mezcla a temperatura normal durante la noche. La mezcla de reacción se filtró a través de celite y el filtrado se concentró al vacío. El residuo se disolvió en EtOAc (600 ml) y se lavó con agua y salmuera, luego se secó (sulfato sódico), se filtró, y el disolvente se concentró al vacío. El residuo bruto se purificó por cromatografía en columna (20% acetato de etilo en diclorometano) para dar el compuesto del título en forma de un sólido de color pardo (31,5 g, 78%).
Ejemplo 45 (parte de la divulgación)
Ámida de ácido 3-(4-nitro-fenil)-5-[(2-oxo-pirrolidina-1-carbonil)-amino]-isotiazol-4-carboxílico
Se añadió 4-[({[4-ciano-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino] butanoato de metilo (10,0 g) en porciones a ácido sulfúrico concentrado (50,0 ml) a temperatura ambiente durante 20 min. La suspensión resultante se calentó a 45°C durante 90 min. La mezcla de reacción se enfrió hasta temperatura ambiente. La mezcla de reacción se vertió en agua con hielo (600 ml), se agitó durante 30 min. El sólido que se formó se recogió y lavó con agua, luego se secó al vacío para dar el compuesto del título en forma de un sólido blanquecino (10,2 g, 99%).
Ejemplo 46 (parte de la divulgación)
3-(4-Aminofenil)-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4-carboxamida
Amida de ácido 3-(4-nitro-fenil)-5-[(2-oxo-pirrolidina-1-carbonil)-amino]-isotiazol-4-carboxílico (10,2 g,) y paladio al 10% sobre carbono (2 g) en tetrahidrofurano (300 ml) y dimetilformamida (50 ml) se hidrogenaron a 80 psi en 24 h en una bomba de metal. El catalizador se eliminó por filtración a través de celite y se lavó con tetrahidrofurano. El filtrado se concentró al vacío para dar un sólido blanquecino que se agitó en éter (150 ml) y se filtró para dar el compuesto del título en forma de un sólido blanquecino (8,7 g, 94%).
Ejemplo 47
3-[4-({[(4-Metilfenil)amino]carbonil}amino)fenil]-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4-carboxamida
Una disolución de 3-(4-aminofenil)-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4-carboxamida (9,6 g, 0,027 mol), diisopropiletilamina (5,3 g, 0,046 mol) en dimetilformamida (150 ml) a temperatura ambiente se trató con isocianato de para-Tolilo (4,0 g 0,03 mol) en un periodo de 20 minutos . La mezcla resultante se agitó a temperatura ambiente durante 2 horas. La mezcla de reacción se concentró al vacío para dar un sólido blanquecino que se agitó en EtOAc (150 ml), el sólido se filtró y se lavó con EtOAc para dar el compuesto del título en forma de un sólido blanco (11,8 g,
88% ) .
Ejemplo 48
Ácido 4-{[({4-(aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}amino)carbonil]amino}butanoico
Se añadió 3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4-carboxamida (11,8 g,) a hidróxido sódico 1 N(100 ml) a temperatura ambiente. La mezcla resultante se agitó a temperatura ambiente durante toda la noche (la mezcla de reacción se convirtió en una disolución clara). La mezcla de reacción se acidificó con HCl 2 N. El sólido que se formó se recogió por filtración y se lavó con agua, luego se secó al vacío para dar el compuesto del título en forma de un sólido blanquecino (9,1 g, 75%).
EM-IES: Calc. para C23H25N6O52S (M H)+: 497,5, encontrado: 497,2
Ejemplo 49
4-{[({4-(Aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}amino)carbonil]amino}butanoato de metilo
Una mezcla de 4-[({[4-(aminocarbonil)-3-(4-aminofenil)isotiazol-5-il]amino}carbonil)amino]butanoato de metilo (121 mg, 0,321 mmol), N,N-diisopropiletilamina (0,14 ml, 0,80 mmol) e isocianato de para-tolilo (0,053 ml, 0,42 mmol) en 4,0 ml de dioxano se sometió a reacción a temperatura ambiente durante 21 horas. La reacción se inactivó con 1 ml de MeOH, se agitó 5 min a temperatura ambiente y luego se evaporó. El sólido resultante se trituró con EtOAc para dar 159 mg de un sólido blanquecino. A este material se le añadieron 51 mg de un lote impuro de otra reacción, y los lotes combinados se trituraron con acetonitrilo/MeOH, nuevamente se trituraron con acetonitrilo para dar un sólido blanco. Este material se recristalizó a partir de una mezcla de CHCh/MeOH/EtOAc para dar 89 mg de un sólido blanco. Los lotes del filtrado impuro se cromatografiaron luego eluyendo con CHCl3/EtOAc más 5% MeOH y el producto resultante se trituró con acetonitrilo para dar 56 mg adicionales de producto limpio. Los lotes se combinaron para dar el compuesto del título en forma de un sólido blanco (145 mg, 67% de rendimiento combinado).
1H RMN (DSMO-d6) 8: 10,23 (s, 1 H), 8,79 (s, 1 H), 8,60 (s, 1 H), 7,80 (t, J = 5,6 Hz, 1 H), 7,59 (br. s., 1 H), 7,47 -7,54 (m, 4H), 7,32 - 7,37 (m, 2H), 7,09 (d, J = 8,2 Hz, 2H), 6,71 (br. s., 1 H), 3,60 (s, 3H), 3,13 - 3,20 (m, 2H), 2,36 (t, J = 7,5 Hz, 2H), 2,25 (s, 3H), 1,72 (quin, J = 7,1 Hz, 2H)
Ejemplo 50 (parte de la divulgación)
Ácido 4-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]butanoico
Se añadieron amida de ácido 3-(4-nitro-fenil)-5-[(2-oxo-pirrolidina-1-carbonil)-amino]-isotiazol-4-carboxílico (12,5 g) a hidróxido sódico 1 N (250 ml) a temperatura ambiente. La mezcla resultante se agitó a temperatura ambiente durante toda la noche (la mezcla de reacción se convirtió en una disolución clara). La mezcla de reacción se acidificó con HCl 2 N. El sólido que se formó se recogió por filtración y se lavó con agua, luego se secó al vacío para dar el compuesto del título en forma de un sólido blanquecino (11,5 g, 88%).
Ejemplo 51 (parte de la divulgación)
4-[({[4-(Aminocarbonil)-3-(4-aminofenil)isotiazol-5-il]amino}carbonil)amino]butanoato de metilo
Se añadió dimetilsulfato (4,4 g, 0,035 mol) a una disolución de ácido 4-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]butanoico (11,5 g, 0,029 mol) y carbonato de potasio (6,0 g 0,043 mol) en dimetilformamida (250 ml) a temperatura ambiente durante 20 min. La mezcla resultante se agitó a temperatura ambiente durante la noche. La mezcla de reacción se filtró, el filtrado se concentró al vacío. El residuo se recogió en acetato de etilo (300 ml) y se lavó con agua y salmuera, se secó sobre sulfato de sodio. El disolvente se concentró al vacío para dar un sólido amarillo (10,4 g). El sólido bruto se usó en la etapa siguiente. El sólido bruto (9,5 g) y paladio al 10% sobre carbono (2 g) en tetrahidrofurano (300 ml) y dimetilformamida (50 ml) se hidrogenaron a 80 psi en 24 h en una bomba de metal. El catalizador se extrajo por filtración a través de celite y se lavó con tetrahidrofurano. El filtrado se concentró al vacío para dar un sólido blanquecino que se agitó en éter (150 ml) y se filtró para dar el compuesto del título en forma de un sólido blanquecino (8,5 g, 96%).
EM-IES: Calc. para C16H20N5O3S (M H)+: 378,4, encontrado: 378,2
Preparación 16
3-[({[4-Ciano-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]propanoato de metilo
Se añadió carbonato de potasio (35,0 g, 0,25 mol) a una disolución de 5-amino-3-(4-nitrofenil)isotiazol-4-carbonitrilo (25,0 g, 0,101 mol) en tetrahidrofurano (300 ml) dimetilsulfóxido (60 ml) a temperatura ambiente. La mezcla resultante se agitó a temperatura ambiente durante 15 min. Se añadió éster metílico de ácido 3-isocianato-propiónico (22,0 g, 0,15 mol) a temperatura ambiente. Se agitó la mezcla a temperatura normal durante la noche. La mezcla de reacción se filtró a través de celite y el filtrado se concentró al vacío. El residuo se disolvió en EtOAc (600 ml) y se lavó con agua y salmuera, luego se secó (sulfato sódico), se filtró, el disolvente se concentró al vacío. El residuo bruto se purificó por cromatografía en columna (20% EtOAc en diclorometano) para dar el compuesto del título en forma de un sólido de color pardo (36,0 g, 94%).
Ejemplo 52 (parte de la divulgación)
3-[({[4-(Aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino] propanoato de metilo
Se añadió 3-[({[4-ciano-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino] propanoato de metilo (36,0 g) en porciones a ácido sulfúrico concentrado (150,0 ml) a temperatura ambiente durante 20 min. La suspensión resultante se calentó a 45°C durante 90 min. La mezcla de reacción se enfrió hasta temperatura ambiente. La mezcla de reacción se vertió en agua con hielo (600 ml), se agitó durante 30 min. El sólido que se formó por filtración se recogió y lavó con agua, luego se secó al vacío para dar el compuesto del título en forma de un sólido blanquecino (28,0 g, 75%).
Ejemplo 53 (parte de la divulgación)
5-({[(3-Hidroxipropil)amino]carbonil}amino)-3-(4-nitrofenil)isotiazol-4-carboxamida
Se añadió borohidruro de sodio (24,0 g 0,636 mol) a una disolución de 3-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino] propanoato de metilo (25,0 g, 0,0636 mol) en tetrahidrofurano (1200 ml). La suspensión resultante se calentó a reflujo. Se añadió metanol (200 ml) gota a gota durante 1 h. y la reacción se sometió a reflujo durante 1 h. La mezcla de reacción se enfrió hasta temperatura ambiente y el disolvente se concentró al vacío. El residuo se recogió en EtOAc (600 ml) y se lavó con agua, HCl 2 N y salmuera, luego se secó (sulfato de sodio), se filtró, se concentró el disolvente al vacío para dar el compuesto del título en forma de un sólido amarillo (18,8 g, 80%). Ejemplo 54 (parte de la divulgación)
Acetato de 3-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]propilo
Se añadió anhídrido acético (4,2 g 0,041 mol) a una disolución de 5-({[(3-hidroxipropil)amino]carbonil}amino)-3-(4-nitrofenil)isotiazol-4-carboxamida (12,0 g, 0,032 mol) en piridina (120 ml) a temperatura ambiente durante 10 min. La mezcla resultante se agitó a temperatura ambiente durante 2 h. La mezcla de reacción se concentró al vacío. El residuo se recogió en EtOAc (500 ml) y se lavó con agua y salmuera, luego se secó (sulfato de sodio), se filtró, se concentró el disolvente al vacío para dar el compuesto del título en forma de un sólido amarillo (12,2 g, 92%).
Ejemplo 55 (parte de la divulgación)
Acetato de 3-[({[4-(aminocarbonil)-3-(4-aminofenil)isotiazol-5-il]amino}carbonil)amino]propilo
Acetato de 3-[({[4-(aminocarbonil)-3-(4-nitrofenil)isotiazol-5-il]amino}carbonil)amino]propilo (12,0 g,) y paladio al 10% sobre carbono (3 g) en tetrahidrofurano (400 ml) y dimetilformamida (100 ml) se hidrogenaron a 80 psi durante 24 h. en una bomba de metal. Se filtró el catalizador en celite y se lavó con tetrahidrofurano. El filtrado se concentró al vacío para dar un sólido blanquecino que se agitó en éter (100 ml) y se filtró para dar el compuesto del título en forma de un sólido blanquecino (8,5 g, 77%).
Ejemplo 56
5-({[(3-Hidroxipropil)amino]carbonil}amino)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida Se añadió isocianato de para-tolilo (3,2 g 0,024 mol) a una disolución de acetato de 3-[({[4-(aminocarbonil)-3-(4-aminofenil)isotiazol-5-il]amino}carbonil)amino]propilo (8,4 g, 0,022 mol), diisopropiletilamina (4,3 g, 0,046 mol) en tetrahidrofurano (250 ml) dimetilsulfóxido (20 ml) a temperatura ambiente. La mezcla resultante se agitó a temperatura ambiente por 2 horas. La mezcla de reacción se concentró al vacío para dar un sólido blanquecino que se agitó en éter (150 ml), se filtró el sólido y se lavó con éter para dar un sólido blanco (10,8 g, 95%). El sólido se recogió en una mezcla de metanol (100 ml) y tetrahidrofurano (100 ml), se añadió 25% metóxido de sodio en metanol (5 ml) a temperatura ambiente. La mezcla resultante se agitó a temperatura ambiente durante 2 horas. La mezcla de reacción se concentró al vacío para dar un sólido blanquecino, el sólido se agitó en agua y se acidificó con HCl 2 N y se filtró. Se lavó con agua y se secó para dar el compuesto del título en forma de un sólido blanquecino (8,7 g, 87%).
EM-IES: Calc. para C22H25N6O4S (M H)+: 469,5, encontrado: 469,1
Ejemplo 57 (parte de la divulgación)
3-(4-Aminofenil)-5-({[(3-hidroxipropil)amino]carbonil}amino)isotiazol-4-carboxamida
Acetato de 3-[({[4-(aminocarbonil)-3-(4-aminofenil)isotiazol-5-il]amino}carbonil)amino]propilo (10,0 g) y paladio al 10% sobre carbono (3 g) en tetrahidrofurano (400 ml) y dimetilformamida (100 ml) se hidrogenaron a 80 psi en 24 horas en una bomba de metal. El catalizador se extrajo por filtración a través de celite y se lavó con tetrahidrofurano. El filtrado se concentró al vacío para dar un sólido amarillo que se agitó en éter (100 ml) y se recogió por filtración para dar el compuesto del título en forma de un sólido amarillo ligero (8,8 g, 96%).
EM-IES: Calc. para C14H17N5O3S (M H)+: 336,3, encontrado: 336,2
Ejemplo 58 (parte de la divulgación)
5-Amino-3-(4-aminofenil)isotiazol-4-carboxamida
Una mezcla de 5-amino-3-(4-nitrofenil)isotiazol-4-carboxamida (63 mg, 0,24 mmol), 12 gotas de NH4Cl acuoso saturado y polvo de Zn catalítico en 4 ml de MeOH se agitó rápidamente a TA. Después de 1,5 horas, se añadieron más NH4Cl acuoso saturado (6 gotas) y polvo de Zn catalítico, y la reacción se calentó a 55°C. Luego se añadieron más NH4Cl sólido y polvo de Zn catalítico para impulsar a que la reacción se completara. Después de 4 horas, la reacción se filtró usando Celite y los sólidos se aclararon con MeOH y EtOAc, el filtrado se evaporó y se trató con tratamiento acuoso usando EtOAc y NaHCO3 saturado acuoso para dar un sólido gomoso amarillo. Este material se trituró con 20% EtOAc/hexano para dar el compuesto del título en forma de un sólido amarillo-beis (53 mg, 94%).
1H RMN (Acetona-d6) 8: 7,62 (br, s., 2H), 7,20 - 7,25 (m, 2H), 6,71 - 6,77 (m, 2H), 6,29 (br. s., 1 H), 5,53 (b. s., 1 H), 4,98 (br. s., 2H)
Ejemplo 59
5-Amino-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida
Una mezcla de 5-amino-3-(4-aminofenil)isotiazol-4-carboxamida (25 mg, 0,11 mmol), N,N-diisopropiletilamina (0,047 ml, 0,27 mmol) e isocianato de para-tolilo (0,016 ml, 0,13 mmol) en 0,9 ml de DCM se sometió a reacción a temperatura ambiente. Después de 1 hora, se añadió 0,006 ml adicional de isocianato de para-tolilo y luego 0,004 ml a las 3,5 horas. Después de 21 horas, la reacción se inactivó con 1 ml de MeOH, se agitó 10 min a TA y luego se evaporó. El residuo se trituró con EtOAc que proporcionó el compuesto del título en forma de un sólido amarillo pálido (28 mg, 72%).
1H RMN (Acetona-d6) 8: 8,28 (s, 1 H), 8,08 (s, 1 H), 7,61 - 7,68 (m, 4H), 7,40 - 7,48 (m, 4H), 7,10 (d, J = 8,2 Hz, 2H), 6,33 (br. s, 1 H), 5,49 (br. s, 1 H), 2,27 (s, 3H)
Ejemplo 60
5-Amino-3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida
Una mezcla de 5-amino-3-(4-aminofenil)isotiazol-4-carboxamida (18 mg, 0,079 mmol), N, N-diisopropiletilamina (0,034 ml, 0,20 mmol) e isocianato de 2-fluoro-5-metilfenilo (0,014 ml, 0,11 mmol) en 1,0 ml dioxano se sometió a reacción a temperatura ambiente durante 2,5 horas. La reacción se inactivó con 0.5 ml de MeOH, se agitó 5 min a temperatura ambiente y luego se evaporó. El residuo se recristalizó a partir de EtOAc/CHCh para dar el compuesto del título en forma de un sólido amarillo pálido (27 mg, 88%).
1H RMN (Acetona-d6) 8: 8,70 (s, 1 H), 8,15 (d, J = 7,6 Hz, 1 H), 8,01 (br, s., 1 H), 7,67 (d, J = 8,5 Hz, 2H), 7,63 (br. s., 2H), 7,48 (d, J = 8,5 Hz, 2H), 7,02 (dd, J = 11,4, 8,2 Hz, 1 H), 6,78 - 6,86 (m, 1 H), 2,32 (s, 3H)
Preparación 17
5-Amino-3-(3-nitrofenil)isotiazol-4-carbonitrilo
Se convirtió cloruro de 3-nitrobenzoílo al compuesto del título, usando una ruta similar a aquella descrita en las preparaciones 1-5.
Ejemplo 61 (parte de la divulgación)
5-Amino-3-(3-nitrofenil)isotiazol-4-carboxamida
Una mezcla de 5-amino-3-(3-nitrofenil)isotiazol-4-carbonitrilo (500 mg, 2,03 mmol) en 5 m1H2SO4 conc. se calentó a 65°C. Después de 4 horas, la mezcla se añadió lentamente a 75 ml de agua con hielo (incluida una reacción adicional ejecutada en una balanza de 0,50 mmol en 1,5 ml de H2SO4 conc.) La mezcla se agitó durante 10 min y después el precipitado se filtró y enjuagó con agua y 10% EtOAc/hexano para dar el compuesto del título en forma de un sólido beis claro (572 mg, 86% de rendimiento combinado).
1H RMN (DSMO-d6) 8: 8,34 (t, J = 1,9 Hz, 1 H), 8,27 (ddd, J = 8,2, 2,3, 0,9 Hz, 1 H), 7,97 (dt, J = 8,1, 1,2 Hz, 1 H), 7,68 -7,74 (m, 1 H), 7,37 (s, 2H)
Ejemplo 62 (parte de la divulgación)
5-Amino-3-(3-aminofenil)isotiazol-4-carboxamida
Una mezcla de 5-amino-3-(3-nitrofenil)isotiazol-4-carboxamida (150 mg, 0,57 mmol), 0,5 ml de NH4Cl acuoso saturado y polvo de Zn catalítico en 6 ml de MeOH se agitó rápidamente a TA. Después de 1,5 horas, se añadieron más NH4Cl saturado acuoso y polvo de Zn catalítico varias veces para impulsar a que la reacción se completara. Después de 20 horas, la reacción se calentó a 55°C durante 6 horas, luego se agitó a TA. La reacción se filtró usando Celite y los
sólidos se aclararon con MeOH, el filtrado se evaporó y se trató con un tratamiento acuoso usando EtOAc y Na2CO3 acuoso para dar un sólido amarillo pálido. El sólido se trituró con EtOAc/hexano para dar 94 mg de un sólido amarillo tenue. Luego el lote de filtrado y los 94 mg de sólido se cromatografiaron por separado, eluyendo con hexano/acetona, y se combinaron para dar el compuesto del título en forma de un sólido blanquecino (96 mg, 72%).
1H RMN (Acetona-d6) 8: 7,72 (br. s., 2H), 7,13 - 7,20 (m, 1 H), 6,75 - 6,80 (m, 2H), 6,68 (d, J = 7,3 Hz, 1 H), 6,28 (br. s., 1 H), 5,46 (br. s., 1 H), 4,87 (br. s., 2H)
Ejemplo 63 (parte de la divulgación)
5-Amino-3-[3-(hidroxiamino)fenil]isotiazol-4-carboxamida
Una mezcla de 5-amino-3-(3-nitrofenil)isotiazol-4-carboxamida (50 mg, 0,19 mmol) y óxido de platino (20 mg, 0,088 mmol) en 5 ml de MeOH se hidrogenó bajo 60 PSI de hidrógeno. Después de 5 horas se añadió una cantidad catalítica adicional y la reacción continuó por 67 horas. La mezcla de reacción se filtró usando Celite y el lecho de filtro se enjuagó con 40% MeOH/CHCh. El filtrado se evaporó para dar 32 mg de un sólido amarillo. Luego se sometieron a cromatografía 22 mg de este material eluyendo con CHCl3/MeOH para dar el compuesto del título en forma de un sólido amarillo pálido (10,2 mg).
1H RMN (DSMO-d6) 8: 8,42 (s, 1 H), 8,39 (d, J = 2,3 Hz, 1 H), 7,67 (s, 2H), 7,21 - 7,28 (m, 1 H), 7,15 (br. s., 1 H), 6,93 (s, 1 H), 6,90 (d, J = 7,9 Hz, 1 H), 6,83 (d, J = 7,3 Hz, 1 H), 5,64 (br. s., 1 H)
Ejemplo 64 (parte de la divulgación)
5-Amino-3-(3-{[3-(trifluorometil)benzoil]amino}fenil)isotiazol-4-carboxamida
A una mezcla de 5-amino-3-(3-aminofenil)isotiazol-4-carboxamida (13 mg, 0,056 mmol) y N,N-diisopropiletilamina (0,029 ml, 0,17 mmol) en 1,0 ml de CH2Cl2 a temperatura ambiente se le añadió cloruro de 3-(trifluorometil)benzoílo (0,008 ml, 0,056 mmol) y la reacción se agitó a temperatura ambiente. Después de 1 hora, se añadió más cloruro de 3-(trifluorometil)benzoílo (0,0015 ml), luego nuevamente a las 2 horas (0,002 ml) y a las 3 horas (0,0015 ml). Después de 4 horas, la reacción se evaporó y luego se trató hasta un tratamiento de Na2CO3 acuoso y EtOAc para proveer un sólido amarillo ligero. El sólido precipitó a partir de EtOAc/hexano para dar el compuesto del título en forma de un sólido blanquecino (16 mg, 68%).
1H RMN (Acetona-d6) 8: 9,93 (br. s., 1 H), 8,29 - 8,36 (m, 2H), 8,01 - 8,06 (m, 1 H), 7,98 - 8,00 (m, 1 H), 7,94 (d, J = 7,9 Hz, 1 H), 7,76 - 7,83 (m, 1 H), 7,68 (br. s., 2H), 7,50 (t, J = 7,8 Hz, 1 H), 7,29 - 7,34 (m, 1 H)
Ejemplo 65 (parte de la divulgación)
5-Amino-3-{3-[(anilinocarbonil)amino]fenil}isotiazol-4-carboxamida
Una mezcla de 5-amino-3-(3-aminofenil)isotiazol-4-carboxamida (21 mg, 0,090 mmol), N,N-diisopropiletilamina (0,039 ml, 0,23 mmol) e isocianato de fenilo (0,014 ml, 0,13 mmol) en 1,0 ml de dioxano se sometió a reacción a TA durante 1 hora. El precipitado se filtró y aclaró con 30% EtOAc/hexano para dar el compuesto del título en forma de un sólido blanco (31 mg, 96%).
1H RMN (DSMO-d6) 8: 8,81 (s, 1 H), 8,68 (s, 1 H), 7,62 (s, 1 H), 7,58 (s, 2H), 7,52 (d, J = 8,2 Hz, 1 H), 7,45 (d, J = 7,6 Hz, 2H), 7,35 (t, J = 7,9 Hz, 1 H), 7,28 (t, J = 7,8 Hz, 2H), 7,17 (br. s., 1H), 7,08 (d, J = 7,6 Hz, 1H), 6,93 - 7,01 (m, 1H), 5,88 (br. s., 1H)
Preparación 18
1-[4-Ciano-3-(4-nitrofenil)isotiazol-5-il]-3-(3-pirrolidin-1-ilpropil)urea
Se añadió carbonildiimidazol (24,7 g, 0,152 mol) a una disolución de 3-pirrolidin-1 -il-propilamina (19,5 g, 0,152 mol) en dimetilformamida (200 ml) a 0°C. La mezcla resultante se agitó a temperatura ambiente durante 1 hora.
Se añadió carbonato de potasio (35,0 g, 0,25 mol) a una disolución de 5-amino-3-(4-nitrofenil)isotiazol-4-carbonitrilo (25,0 g, 0,101 mol) en dimetilformamida (200 ml) a temperatura ambiente. La mezcla resultante se agitó a temperatura ambiente durante 15 min. La mezcla anterior se añadió a temperatura ambiente. La mezcla se agitó a temperatura ambiente durante la noche. La mezcla de reacción se concentró al vacío. El residuo se disolvió en acetato de etilo (600 ml) y se filtró a través de celite y se lavó con acetato de etilo. El filtrado se lavó con agua y salmuera, luego se secó (sulfato de sodio), se filtró y se concentró al vacío. El compuesto bruto se purificó por cromatografía en columna (10% metanol/diclorometano) para dar el compuesto del título en forma de un sólido amarillo (34,0 g, 85%).
Ejemplo 66 (parte de la divulgación)
3-(4-Nitrofenil)-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
Se añadió 1-[4-ciano-3-(4-nitrofenil)isotiazol-5-il]-3-(3-pirrolidin-1-ilpropil)urea (36,0 g) en porciones a ácido sulfúrico concentrado (180,0 ml) a temperatura ambiente durante 20 min. La suspensión resultante se calentó a 45°C durante 90 min. La mezcla de reacción se enfrió hasta temperatura ambiente. La mezcla de reacción se vertió en agua con hielo (2000 ml), se agitó durante 30 min. La mezcla resultante se tornó básica usando hidróxido de amonio, se filtró, el sólido se lavó con agua, luego se secó al vacío para dar el compuesto del título en forma de un sólido blanquecino (34,0 g, 90%).
Ejemplo 67 (parte de la divulgación)
3-(4-Aminofenil)-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
3-(4-nitrofenil)-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida (16,0 g,) y paladio al 10% sobre carbono (6 g) en tetrahidrofurano (1500 ml) se hidrogenaron a 80 psi en 24 horas en una bomba de metal. Se filtró el catalizador en celite y se lavó con tetrahidrofurano. El filtrado se concentró al vacío para dar un sólido blanquecino que se agitó en éter (200 ml) y se filtró para dar el compuesto del título en forma de un sólido blanquecino (13,8 g, 93%).
EM-IES: Calc. para C18H25N6O2S (M H)+: 389, encontrado: 389.1
Ejemplo 68
3-[4-({[(4-Metilfenil)amino]carbonil}amino)fenil]-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida
Se añadió isocianato de para-tolilo (4,5 g, 0,0339 mol) a una disolución de 3-(4-aminofenil)-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida (12,0 g, 0,0308 mol),diisopropiletilamina (6,0 g, 0,046 mol) en una mezcla de tetrahidrofurano (300 ml) y dimetilformamida (50 ml) a temperatura ambiente en 20 min. La mezcla resultante se agitó a temperatura ambiente durante 2 horas. La mezcla de reacción se concentró al vacío para dar un sólido blanquecino que se agitó en una mezcla de tetrahidrofurano al 20% y acetato de etilo (200 ml), el sólido se filtró y se lavó con acetato de etilo para dar el compuesto del título en forma de un sólido blanco (15,8 g, 98%).
EM-IES: Calc. para C26H32N7O3 (M H)+: 522, encontrado: 522,2
Preparación 19
[4-(3-Cloro-4-cianoisotiazol-5-il)fenil]carbamato de terc-butilo
Una mezcla de 3,5-dicloroisotiazol-4-carbonitrilo (5,37 g, 30 mmol), ácido 4-(terc-butoxicarbonilamino)fenilborónico (14,22 g, 60 mmol), fluoruro de potasio (6,11 g, 105 mmol), 18-corona-6 (3,96 g, 15 mmol) y acetato de paladio (337 mg, 1,5 mmol) en tolueno (250 ml) se calentó a reflujo durante 6 horas. La reacción se enfrió hasta temperatura ambiente y la mezcla se diluyó con agua y EtOAc. Las capas se separaron y la capa acuosa se extrajo con EtOAc (3x). Los extractos orgánicos combinados se lavaron con salmuera y se secaron con MgSO4, se filtraron y se concentraron. El producto bruto se purificó mediante columna de gel de sílice ultrarrápida, se eluyó con 5-15% EtOAc en hexanos para obtener el compuesto del título como un sólido blanco cristalino (8,55 g, 85%).
Preparación 20
3-(4-Amino-fenil)-5-cloro-isotiazol-4-carbonitrilo
Una disolución de [4-(3-cloro-4-cianoisotiazol-5-il)fenil]carbamato de terc-butilo (4,76 g, 13,38 mmol) en CH2Q2 (100 ml) se trató con 10 ml de ácido trifluoroacético. La mezcla de reacción se agitó a temperatura ambiente durante la noche. El disolvente se retiró a vacío. El residuo se diluyó con agua y CH2Q2 (100 ml). Las capas se separaron y la capa acuosa se extrajo con CH2Q2 (2x). Los extractos orgánicos combinados se lavaron con salmuera y se secaron con MgSO4, se filtraron y se concentraron. El producto se aclaró con Et2O/hexanos y se recogió por filtración para dar el compuesto del título en forma de un sólido amarillo brillante (3,15 g, 94%).
Preparación 21
1-[4-(5-Cloro-4-ciano-isotiazol-3-il)-fenil]-3-(2-fluoro-5-metil-fenil)-urea
Una disolución de 3-(4-amino-fenil)-5-cloro-isotiazol-4-carbonitrilo (4,565 g, 19,4 mmol) e isocianato de 2-fluoro-5-metilfenilo (5,85 g, 38,7 mmol) en 100 ml de THF seco se calentó a reflujo durante la noche. La TLC indicó la presencia de una cantidad considerable de material de partida. Se añadieron 2 g más de isocianato de 2-fluoro-5-metilfenilo, y la reacción continuó durante otras 24 h. La reacción se enfrió a temperatura ambiente. Se eliminó el THF al vacío y el sólido resultante se agitó en 200 ml de Et2O durante 1 h. El producto se recogió por filtración y se lavó con Et2O/hexanos para proporcionar el compuesto del título como un sólido amarillo ligero (6,78 g, 90%).
Preparación 22
1-(4-(3-Amino-4-cianoisotiazol-5-il)fenil)-3-(2-fluoro-5-metilfenil)urea,
Una suspensión de 1-(4-{4-ciano-3-[(2,4-dimethoxibenzil)amino]isotiazol-5-il}fenil)-3-(2-fluoro-5-metilfenil)urea (593 mg, 1,15 mmol) en 50 ml de CH2Cl2 se trató con 1,5 ml de ácido trifluoroacético. Se disolvió el sólido y la reacción se tornó amarilla y luego roja. La TLC indicó que la reacción se había completado en <30 min. Se añadió disolución saturada de Na2CO3 y la mezcla se agitó durante 30 min. Las capas se separaron y la capa acuosa se extrajo con CH2Cl2 (3x). Los extractos orgánicos combinados se lavaron con salmuera y se secaron con MgSO4, se filtraron y se concentraron. El producto bruto se redisolvió en 100 ml de EtOAc. La impureza insoluble se filtró a través de celite y se lavó con EtOAc. El filtrado se concentró al vacío para dar el compuesto del título en forma de un sólido color crema (398 mg, 94%).
Ejemplo 69 (parte de la divulgación)
3-Amino-5-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida
A una mezcla de 1-[4-(3-amino-4-cianoisotiazol-5-il)fenil]-3-(2-fluoro-5-metilfenil)urea (10,2 mg, 0,028 mmol) en 0,8 ml de EtOH a TA se le añadieron 15 gotas de NaOH acuoso 1,0 M, 7 gotas de peróxido de hidrógeno al 30%, y la reacción se agitó a TA durante 30 min, luego se calentó a 60°C. Después de 2,5 horas, se efectuó un tratamiento de HCl acuoso (dilución) y EtOAc para dar un sólido amarillo ligero. A este material se le añadió un lote impuro de otra reacción, y los lotes combinados se trituraron con EtOAc para dar el compuesto del título en forma de un sólido amarillo pálido (26 mg, 93% de rendimiento combinado).
1H RMN (DSMO-d6) 8: 9,32 (s, 1 H), 8,55 (d, J = 2,6 Hz, 1 H), 7,98 (dd, J = 7,9, 1,8 Hz, 1 H), 7,54 - 7,59 (m, 2H), 7,49 (br. s., 1 H), 7,39 - 7,44 (m, 2H), 7,06 - 7,15 (m, 2H), 6,78 - 6,85 (m, 1 H), 6,21 (s, 2H), 2,28 (s, 3H)
Preparación 23
1-(4-{4-Ciano-3-[(3-morfolin-4-ilpropil)amino]isotiazol-5-il}fenil)-3-(2-fluoro-5-metilfenil)urea
Una mezcla de 1-[4-(3-doro-4-cianoisotiazol-5-il)fenil]-3-(2-fluoro-5-metilfenil)urea (50 mg, 0,13 mmol) y 0,2 ml de 3-morfolinopropilamina se calentó a 70°C durante 18 horas. Luego se efectuó un tratamiento de una mezcla acuosa de Na2CO3/salmuera y EtOAc, y el material resultante se sometió a cromatografía eluyendo con CHCl3/MeOH. El sólido resultante se trituró luego con una mezcla 1:1/ CHCl3/hexano que proporcionó el compuesto del título en forma de un sólido amarillo pálido (10 mg, 16%).
1H RMN (Acetona-d6) 8: 8,88 (s, 1 H), 8,13 (dd, J = 7,8, 1,9 Hz, 1 H), 8,08 (d, J = 2,6 Hz, 1 H), 7,73 - 7,80 (m, 4H), 7,10 (t, J = 4,7 Hz, 1 H), 7,03 (dd, J = 11,4, 8,5 Hz, 1 H), 6,81 -6,87 (m, 1 H), 3,69 - 3,74 (m, 4H), 3,49 -3,57 (m, 2H), 2,50 - 2,55 (m, 2H), 2,46 (br. s., 4H), 2,32 (s, 3H), 1,87 (quin, J = 6,2 Hz, 2H)
Ejemplo 70 (parte de la divulgación)
5-[4-({[(2-Fluoro-5-metilfenil)amino]carbonil}amino)fenil]-3-[(3-morfolin-4-ilpropil)amino]isotiazol-4-carboxamida A una disolución de 1-(4-{4-ciano-3-[(3-morfolin-4-ilpropil)amino]isotiazol-5-il}fenil)-3-(2-fluoro-5-metilfenil)urea (5 mg, 0,011 mmol) en 0,8 ml de DMSO a TA se le añadió K2CO3 catalítico, 1 gota de peróxido de hidrógeno al 30%, y la reacción se agitó a TA durante 30 min. La reacción se añadió a una disolución de salmuera diluida y el precipitante se filtró y enjuagó con agua, luego 20% EtOAc/hexano. El producto se lavó a partir de papel de filtro usando 15% MeOH/CHCl3 y luego se evaporó para dar el compuesto del título en forma de un sólido blanco (5 mg, 85%).
1H RMN (Acetona-d6) 8: 8,80 (s, 1 H), 8,13 (dd, J = 7,8, 2,2 Hz, 1 H), 8,05 (d, J = 2,9 Hz, 1 H), 7,70 - 7,75 (m, 2H), 7,44 - 7,49 (m, 2H), 7,39 (t, J = 5,4 Hz, 1 H), 7,02 (dd, J = 11,4, 8,2 Hz, 1 H), 6,80 -6,86 (m, 1 H), 6.68 (br. s., 1 H), 6,10 (br. s., 1 H), 3,63 -3,67 (m, 4H), 3,46 -3,53 (m, 2H), 2,38 -2,47 (m, 6H), 2,32 (s, 3H), 1,82 (quin, J = 6,7 Hz, 2H) Preparación 24
1- (4-{4-Ciano-3-[(2,4-dimethoxibenzil)amino]isotiazol-5-il}fenil)-3-(2-fluoro-5-metilfenil)urea
Una suspensión de 1-[4-(5-Cloro-4-ciano-isotiazol-3-il)-fenil]-3-(2-fluoro-5-metil-fenil)-urea (véase Preparación 21 anterior; 4,3 g, 11,1 mmol) en 15 ml de 2,4-dimetoxibencilamina se calentó hasta 73°C durante 24 h. La reacción se tornó clara después de ~3h. La reacción se enfrió a temperatura ambiente. El residuo se diluyó con 300 ml de DCM y se lavó dos veces con disolución al 10% de HCl, Na2S2O5 saturado dos veces y luego salmuera. La disolución orgánica se secó con MgSO4, se filtró y se concentró. El producto bruto se purificó en columna de gel de sílice ultrarrápida con 2- 5% MTBE en DCM/hexanos (2:1) para obtener el compuesto del título en forma de un sólido amarillo ligero (1,19 g, 21%).
Ejemplo 71 (parte de la divulgación)
3-[(2,4-Dimetoxibencil)amino]-5-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida
A una disolución de 1-(4-{4-ciano-3-[(2,4-dimethoxibenzil)amino]isotiazol-5-il}fenil)-3-(2-fluoro-5-metilfenil)urea (26 mg, 0,050 mmol) en 0,8 ml de DMSO a TA se le añadió K2CO3 catalítico, 5 gotas de peróxido de hidrógeno al 30%, y la reacción se agitó a TA durante 30 min. La reacción se añadió a una disolución de salmuera diluida y el precipitante se filtró y aclaró con agua, luego 30% EtOAc/hexano para dar el compuesto del título en forma de un sólido amarillo pálido (24 mg, 91%).
1H RMN (DSMO-d6) 8: 9,31 (s, 1 H), 8,55 (d, J = 2,3 Hz, 1 H), 7,98 (dd, J = 7,8, 1,6 Hz, 1 H), 7,50 - 7,60 (m, 3H), 7,41 (d, J = 8,5 Hz, 2H), 7,17 (d, J = 8,5 Hz, 1 H), 7,11 (dd, J = 11,4, 8,2 Hz, 1 H), 6,95 (br. s., 1 H), 6,88 (t, J = 5,9 Hz, 1 H), 6,78 - 6,85 (m, 1 H), 6,57 (d, J = 2,3 Hz, 1 H), 6,47 (dd, J = 8,4, 2,2 Hz, 1 H), 4,39 (d, J = 5,9 Hz, 2H), 3,81 (s, 3H), 3,74 (s, 3H), 2,27 (s, 3H)
Los datos biológicos para los compuestos de la presente invención se generaron mediante el uso de los siguientes ensayos.
Ensayo de cinasa VEGFR2
Se efectuaron ensayos bioquímicos de cinasa KDR en placas de microtitulación de 96 pocillos recubiertas toda la noche con 75 |ig/pocillo de poly-Glu-Tyr (4:1) en disolución salina tamponada con fosfato (OBS) 10 mM, pH 7,4. Las placas recubiertas se lavaron con 2 ml por pocillo de PBS 0,05% Tween-20 (PBS-T), se bloquearon por incubación con PBS que contenía 1% BSA, luego se lavaron con 2 ml por pocillo de PBS-T antes de comenzar la reacción. Las reacciones se llevaron a cabo en volúmenes de reacción de 100 |il que contenían 2,7 |iM ATP en tampón de cinasa (tampón Hepes 50mM, pH 7,4, MgCh 20mM, MnCh 0,1 mM y Na3VO40,2 mM). Los compuestos de ensayo se reconstituyeron en 100% DMSO y se añadieron a la reacción para dar una concentración de DMSO final de 5%. Las reacciones se iniciaron con la adición de 20 ul por pocillo de tampón de cinasa que contenía 200-300 ng de proteína KDR de dominio citoplásmico purificada (BPS Bioscience, San Diego, CA). Después de una incubación de 15 minutos a 30°C., las reacciones se lavaron con 2 ml por pocillo de PBS-T. Se añadieron a los pocillos 100 |il de un conjugado de anticuerpo anti-fosfotirosina monoclonal-peroxidasa diluido 1:10,000 en PBS-T durante 30 minutos. Después de un lavado de 2 ml por pocillo con PBS-Tween-20, se añadieron 100 |il de dihidrocloruro de O-fenilendiamina en tampón de fosfato-citrato, que contenía peróxido de hidrógeno y urea, a los pocillos durante 7-10 minutos como sustrato colorimétrico para la peroxidasa. La reacción finalizó por adición de 100 |il de H2SO42,5N a cada pocillo y se leyó usando una lectora de microplacas ELISA configurada a 492 nm. Se calcularon los valores CI50 para la inhibición del compuesto directamente de los gráficos de densidad óptica (unidades arbitrarias) frente a la concentración de compuesto que le sigue a la sustracción de valores testigo.
Ensayo celular de VEGFR2
Se usó tecnología FLIPR automatizada (lectora de placa de imágenes fluorométricas) para valorar si los inhibidores de VEGF inducían incrementos en los niveles de calcio intracelular en células endoteliales cargadas con tinte fluorescente. Se sembraron HUVEC (células endoteliales de vena umbilical humana) (Clonetics) en placas de 384 pocillos con paredes negras recubiertas con fibronectina durante la noche @ 37°C/5% CO2. Las células se cargaron con el indicador de calcio Fluo-4 por 45 minutos a 37°C. Las células se lavaron 2 veces (EIx405, Biotek Instruments) para eliminar el tinte extracelular. Para valoración, las células se pre-incubaron con los agentes de prueba durante 30 minutos, en una sola concentración (10 uM) o a concentraciones que oscilan entre 0,0001 y 10,0 uM seguidas de estimulación con VEGF165 (10 ng/ml). Los cambios en fluorescencia a 516 nm se midieron simultáneamente en los 384 pocillos usando una cámara CCD enfriada. Los datos se generaron determinando los niveles de fluorescencia máx-mín para muestras no estimuladas, estimuladas y tratadas con el fármaco. Los valores CI50 para los compuestos de ensayo se calcularon a partir del % de inhibición de respuestas estimuladas con VEGF en ausencia de inhibidor.
Ensayo de cinasa PDGFRp
Se efectuaron ensayos bioquímicos de cinasa PDGFRp en placas de microtitulación de 96 pocillos recubiertas toda la noche con 75 |ig de poly-Glu-Tyr (4:1) en disolución salina tamponada con fosfato (OBS) 10 mM, pH 7,4. Las placas recubiertas se lavaron con 2 ml por pocillo de PBS 0,05% Tween-20 (PBS-T), se bloquearon por incubación con
PBS que contenía 1% BSA, luego se lavaron con 2 ml por pocilio de PBS-T antes de comenzar la reacción. Las reacciones se llevaron a cabo en volúmenes de reacción de 100 |il que contenían 36 |iM ATP en tampón de cinasa (tampón Hepes 50mM, pH 7,4, MgCh 20 mM, MnCh 0,1 mM y Na3VO4 0,2 mM). Los compuestos de ensayo se reconstituyeron en 100% DMSO y se añadieron a la reacción para dar una concentración de DMSO final de 5%. Las reacciones se iniciaron con la adición de 20 ul por pocillo de tampón de cinasa que contenía 200-300 ng de proteína PDGFR-b de dominio citoplásmico purificada (Millipore). Después de una incubación de 60 minutos a 30°C., las reacciones se lavaron con 2 ml por pocillo de PBS-T. Se añadieron a los pocillos 100 |il de un conjugado de anticuerpo anti-fosfotirosina monoclonal-peroxidasa diluido 1:10,000 en PBS-T durante 30 minutos. Después de un lavado de 2 ml por pocillo con PBS-Tween-20, se añadieron 100 |il de dihidrocloruro de O-fenilendiamina en tampón de fosfatocitrato, que contenía peróxido de hidrógeno y urea, a los pocillos durante 7-10 minutos como sustrato colorimétrico para la peroxidasa. La reacción finalizó por adición de 100 |il de H2SO42,5N a cada pocillo y se leyó usando una lectora de microplacas ELISA configurada a 492 nm. Se calcularon los valores CI50 para la inhibición del compuesto directamente de los gráficos de densidad óptica (unidades arbitrarias) frente a la concentración de compuesto que le sigue a la sustracción de valores testigo.
Ensayo celular de PDGFRp
Se usó tecnología FLIPR automatizada (lectora de placa de imágenes fluorométricas) para valorar inhibidores de incrementos inducidos por PDGF en los niveles de calcio intracelular en células endoteliales cargadas con tinte fluorescente. Se sembraron NHDF-Ad (fibroblastos dérmicos humanos normales, adultos; Lonza) en placas de 384 pocillos con paredes negras recubiertas con fibronectina durante la noche @ 37°C/5%CO2. Las células se cargaron con el indicador de calcio Fluo-4 por 45 minutos a 37°C. Las células se lavaron 2 veces (EIx405, Biotek Instruments) para eliminar el tinte extracelular. Para valoración, las células se pre-incubaron con los agentes de prueba durante 30 minutos, en una sola concentración(10 uM) o a concentraciones que oscilan entre 0,0001 y 10,0 uM seguidas de estimulación con PDGF-BB (30 ng/ml). Los cambios en fluorescencia a 516 nm se midieron simultáneamente en los 384 pocillos usando una cámara CCD enfriada. Los datos se generaron determinando los niveles de fluorescencia máx-mín para muestras no estimuladas, estimuladas y tratadas con el fármaco. Los valores CI50 para los compuestos de ensayo se calcularon a partir del % de inhibición de respuestas estimuladas con PDGF-BB en ausencia de inhibidor.
Los resultados biológicos para los distintos compuestos se exponen en las Tablas 1 y 2 a continuación.
Para preparar composiciones farmacéuticas de los compuestos descritos por la presente invención, los vehículos inertes farmacéuticamente aceptables pueden ser sólidos o líquidos. Las preparaciones en forma sólida incluyen polvos, comprimidos, gránulos dispersables, cápsulas, sellos y supositorios. Los polvos y comprimidos pueden comprender entre aproximadamente 5 y aproximadamente 95 por ciento de ingrediente activo. Los vehículos sólidos adecuados se conocen en la técnica, p. ej., carbonato de magnesio, estearato de magnesio, talco, azúcar o lactosa. Los comprimidos, polvos, sellos y cápsulas se pueden utilizar como presentaciones sólidas adecuadas para administración oral. Los ejemplos de vehículos y métodos farmacéuticamente aceptables de fabricación para diversas composiciones se pueden hallar en A. Gennaro (ed.), Remington's Pharmaceutical Sciences, 18va edición, (1990), Mack Publishing Co., Easton, Pennsilvania.
Las preparaciones en forma líquida incluyen disoluciones, suspensiones y emulsiones. Como ejemplo, se pueden mencionar disoluciones con agua o agua-propilenglicol para inyección parenteral o adición de edulcorantes y opacificadores para disoluciones, suspensiones y emulsiones orales. Las preparaciones en forma líquida pueden incluir disoluciones para administración intranasal.
Las preparaciones en aerosol para inhalación pueden incluir disoluciones y sólidos en forma de polvo, que pueden ser en combinación con vehículos farmacéuticamente aceptables, tales como gas comprimido inerte, p. ej., nitrógeno.
También se incluyen las presentaciones en forma sólida destinadas a ser convertidas, poco después del uso, en preparaciones en forma líquida para administración oral o parenteral. Dichas formas líquidas incluyen disoluciones, suspensiones y emulsiones.
Los compuestos de la invención también se pueden administrar por la ruta transdérmica. Las composiciones transdérmicas pueden adoptar la forma de cremas, lociones, aerosoles y/o emulsiones y pueden incluirse en un parche transdérmico de tipo matriz o reservorio, de la manera convencional de la técnica para este propósito.
Los compuestos de la presente invención pueden también administrarse por las vías oral, subcutánea, intravenosa, intratecal o algunas de sus combinaciones adecuadas.
Además de las presentaciones comunes expuestas anteriormente, los compuestos de la invención pueden también administrarse por medios de liberación controlada y/o dispositivos de administración tales como aquellos descritos en las patentes de EE. UU. núm. 3.845.770; 3.916.899; 3.536.809; 3.598.123; 3.630.200; 4.008.719; y 5.366.738.
Para uso en una composición para administración intravenosa, un intervalo de administración diaria adecuado para
uso anti-inflamatorio, anti-aterosclerótico o anti-alérgico es entre aproximadamente 0,001 mg y aproximadamente 25 mg (preferiblemente entre 0,01 mg y aproximadamente 1 mg) de un compuesto de la presente invención por kg de peso corporal por día y para uso citoprotector entre aproximadamente 0,1 mg y aproximadamente 100 mg (preferiblemente entre aproximadamente 1 mg y aproximadamente 100 mg y lo más preferiblemente entre aproximadamente 1 mg y aproximadamente 10 mg) de un compuesto de la presente invención por kg de peso corporal por día. Para el tratamiento de enfermedades del ojo, se pueden utilizar preparaciones oftálmicas para administración ocular que comprenden 0,001-1% en peso de disoluciones o suspensiones de los compuestos de la presente invención en una formulación oftálmica aceptable.
Preferiblemente, la preparación farmacéutica es una presentación unitaria. En dicha forma, la preparación se subdivide en dosis unitarias de tamaño adecuado que contienen cantidades apropiadas del componente activo, p. ej., una cantidad eficaz para lograr el propósito deseado.
La magnitud de la dosis profiláctica o terapéutica de un compuesto de la presente invención variará, por supuesto, dependiendo de la naturaleza de la gravedad de la afección que se ha de tratar y con el compuesto particular y su ruta de administración. También variará de acuerdo con la edad, el peso y la respuesta del paciente individual. Se ha de entender que una cantidad de dosis diaria específica puede ser simultáneamente una cantidad terapéuticamente eficaz, p. ej., para el tratamiento hasta una progresión lenta de una afección existente, y una cantidad profilácticamente eficaz, p. ej., para la prevención de una afección.
La cantidad de compuesto activo en una dosis unitaria de la preparación se puede variar o ajustar entre aproximadamente 0,001 mg y aproximadamente 500 mg. En una realización, la cantidad de compuesto activo en una preparación de dosis unitaria es entre aproximadamente 0,01 mg y aproximadamente 250 mg. En otra realización, la cantidad de compuesto activo en una preparación de dosis unitaria es entre aproximadamente 0,1 mg y aproximadamente 100 mg. En otra realización, la cantidad de compuesto activo en una preparación de dosis unitaria es entre aproximadamente 1,0 mg y aproximadamente 100 mg. En otra realización, la cantidad de compuesto activo en una preparación de dosis unitaria es entre aproximadamente 1,0 mg y aproximadamente 50 mg. Incluso en otra realización, la cantidad de compuesto activo en una preparación de dosis unitaria es entre aproximadamente 1,0 mg y aproximadamente 25 mg.
La dosis real empleada puede variará dependiendo de los requerimientos del paciente y de la gravedad de la afección que se esté tratando. La determinación del esquema de dosis correcto para una situación particular está dentro de la técnica. Para fines prácticos, la dosis diaria total se puede dividir y administrar en porciones durante el día, según se requiera.
La cantidad y frecuencia de administración de los compuestos de la invención y/o las sales farmacéuticamente aceptables se regularán de acuerdo con el criterio del médico, quien tendrá en cuenta factores tales como la edad, la afección y la talla del paciente, así como también la gravedad de los síntomas que se estén tratando. Un esquema de administración diaria recomendada típico para administración oral puede oscilar entre aproximadamente 0,01 mg/día y aproximadamente 2000 mg/día de los compuestos de la presente invención. En una realización, un esquema de dosis diario para administración oral es de aproximadamente 1 mg/día a 1000 mg/día. En otra realización, un esquema de dosis diario para administración oral es de aproximadamente 1 mg/día a 500 mg/día. En otra realización, un esquema de dosis diario para administración oral es de aproximadamente 100 mg/día a 500 mg/día. En otra realización, un esquema de dosis diario para administración oral es de aproximadamente 1 mg/día a 250 mg/día. En otra realización, un esquema de dosis diario para administración oral es de aproximadamente 100 mg/día a 250 mg/día. Incluso en otra realización, un esquema de dosis diario para administración oral es de aproximadamente 1 mg/día a 100 mg/día. Incluso en otra realización, un esquema de dosis diario para administración oral es de aproximadamente 50 mg/día a 100 mg/día. Incluso en otra realización, un esquema de dosis diario para administración oral es de aproximadamente 1 mg/día a 50 mg/día. En otra realización, un esquema de dosis diario para administración oral es de aproximadamente 25 mg/día a 50 mg/día. Incluso en otra realización, un esquema de dosis diario para administración oral es de aproximadamente 1 mg/día a 25 mg/día. La dosis diaria se puede administrar en una sola dosis o se puede dividir en dos a cuatro dosis.
En un aspecto, la presente invención proporciona un kit que comprende una cantidad terapéuticamente eficaz de por lo menos un compuesto de la presente invención, o una sal farmacéuticamente aceptable de dicho compuesto y un vehículo o diluyente farmacéuticamente aceptable, e instrucciones para uso de dicho kit. En lo siguiente, los ejemplos clasificados como representativos no están comprendidos en el alcance de la invención (ejemplos de referencia).
Claims (1)
- REIVINDICACIONESCompuesto seleccionado del grupo que consiste en:3- [4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-metoxipropil)amino]carbonil}amino)isotiazol-4- carboxamida;{4-(aminocarbonil)-3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}carbamato de etilo; 3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;amida de ácido 3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metil-fenil}-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico;ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-fenil}-isotiazol-5-il)-ureido]-propiónico; ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-metil-fenil)-ureido]-2-metil-fenil}-isotiazol-5-il)-ureido]-propiónico; 3-[4-({[(3-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;amida de ácido 3-[2-metil-4-(3-m-tolil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[4-(3-m-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-m-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;3-{4-[({[2-fluoro-5-(trifluorometil)feml]amino}carbonil)amino]feml}-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;amida de ácido 3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metil-fenil}-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico;ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-fenil}-isotiazol-5-il)-ureido]-propiónico; ácido 3-[3-(4-carbamoil-3-{4-[3-(2-fluoro-5-trifluorometil-fenil)-ureido]-2-metilfenil}-isotiazol-5-il)-ureido]-propiónico;3-{4-[(anilinocarbonil)amino]fenil}-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida; amida de ácido 3-[2-metil-4-(3-fenil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[4-(3-fenil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-fenil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-morfolin-4-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;amida de ácido 3-[2-metil-4-(3-p-tolil-ureido)-fenil]-5-[3-(3-morfolin-4-il-propil)-ureido]-isotiazol-4-carboxílico; ácido 3-(3-{4-carbamoil-3-[2-metil-4-(3-p-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;ácido 3-(3-{4-carbamoil-3-[4-(3-p-tolil-ureido)-fenil]-isotiazol-5-il}-ureido)-propiónico;5- ({[(3-morfolin-4-ilpropil)amino]carbonil}amino)-3-(4-{[3-(trifluorometil)benzoil]amino}fenil)isotiazol-4-carboxamida;3- [4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-{[(2-oxopirrolidin-1-il)carbonil]amino}isotiazol-4-carboxamida;ácido 4-{[({4-(aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5-il}amino)carbonil]amino}butanoico;4- {[({4-(aminocarbonil)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-5il}amino)carbonil]amino}butanoato de metilo;5-({[(3-hidroxipropil)amino]carbonil}amino)-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida;5-amino-3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida;5-amino-3-[4-({[(2-fluoro-5-metilfenil)amino]carbonil}amino)fenil]isotiazol-4-carboxamida; y3-[4-({[(4-metilfenil)amino]carbonil}amino)fenil]-5-({[(3-pirrolidin-1-ilpropil)amino]carbonil}amino)isotiazol-4-carboxamida;o una sal farmacéuticamente aceptable del mismo.Composición farmacéutica que comprende por lo menos un compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable, y un vehículo farmacéuticamente aceptable.Compuesto según la reivindicación 1, para uso en un método para tratar una enfermedad seleccionada del grupo que consiste en cáncer, trastornos proliferativos de los vasos sanguíneos, trastornos fibróticos, trastornos proliferativos de las células mesangiales y enfermedades metabólicas, comprendiendo el método administrar a un sujeto que lo necesita una cantidad terapéuticamente eficaz de por lo menos un compuesto según la reivindicación 1 o una sal farmacéuticamente aceptable del mismo.Compuesto para uso según la reivindicación 3, en el que el trastorno proliferativo de los vasos sanguíneos se selecciona del grupo que consiste en retinopatía diabética, degeneracíón macular relacionada con la edad, retinopatía de prematuridad, terigión, artritis y restenosis; el trastorno fibrótico se selecciona del grupo que consiste en cirrosis hepática y aterosclerosis; el trastorno proliferativo de las células mesangiales se selecciona del grupo que consiste en glomerulonefritis, nefropatía diabética, nefrosclerosis maligna, síndromes de microangiopatía trombótica, rechazo de trasplantes y glomerulopatías; y las enfermedades metabólicas se seleccionan del grupo que consiste en psoriasis, diabetes mellitus, cicatrización de heridas, inflamación y enfermedades neurodegenerativas.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161581031P | 2011-12-28 | 2011-12-28 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2851602T3 true ES2851602T3 (es) | 2021-09-08 |
Family
ID=47505371
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12810524.4T Active ES2623652T3 (es) | 2011-12-28 | 2012-12-27 | Derivados de 3-fenil-5-ureidoisotiazol-4-carboximida y 3-amino-5-fenilisotiazol como inhibidores de cinasa |
| ES17156014T Active ES2851602T3 (es) | 2011-12-28 | 2012-12-27 | Derivados de 3-fenil-5-ureidoisotiazol-4-carboxamida como inhibidores de cinasa |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12810524.4T Active ES2623652T3 (es) | 2011-12-28 | 2012-12-27 | Derivados de 3-fenil-5-ureidoisotiazol-4-carboximida y 3-amino-5-fenilisotiazol como inhibidores de cinasa |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8969583B2 (es) |
| EP (2) | EP2797916B1 (es) |
| ES (2) | ES2623652T3 (es) |
| WO (1) | WO2013101954A1 (es) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102339724B1 (ko) | 2013-11-28 | 2021-12-17 | 씨에스엘 리미티드 | 신장병증의 치료 방법 |
| WO2021115560A1 (en) * | 2019-12-09 | 2021-06-17 | Rottapharm Biotech S.R.L. | New fyn and vegfr2 kinase inhibitors |
| CN114366740B (zh) * | 2021-09-18 | 2023-08-22 | 江苏海洋大学 | 化合物a-6在制备广谱抗癌药物中的应用 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3536809A (en) | 1969-02-17 | 1970-10-27 | Alza Corp | Medication method |
| US3598123A (en) | 1969-04-01 | 1971-08-10 | Alza Corp | Bandage for administering drugs |
| US3630200A (en) | 1969-06-09 | 1971-12-28 | Alza Corp | Ocular insert |
| US3845770A (en) | 1972-06-05 | 1974-11-05 | Alza Corp | Osmatic dispensing device for releasing beneficial agent |
| US3916899A (en) | 1973-04-25 | 1975-11-04 | Alza Corp | Osmotic dispensing device with maximum and minimum sizes for the passageway |
| US4008719A (en) | 1976-02-02 | 1977-02-22 | Alza Corporation | Osmotic system having laminar arrangement for programming delivery of active agent |
| US5366738A (en) | 1982-07-29 | 1994-11-22 | Merck & Co., Inc. | Controlled release drug dispersion delivery device |
| DE4328425A1 (de) * | 1993-08-24 | 1995-03-02 | Basf Ag | Acylamino-substituierte Isoxazol- bzw. Isothiazolderivate, Verfahren zu deren Herstellung und ihre Verwendung |
| GB9608435D0 (en) | 1996-04-24 | 1996-06-26 | Celltech Therapeutics Ltd | Chemical compounds |
| UA60365C2 (uk) | 1998-06-04 | 2003-10-15 | Пфайзер Продактс Інк. | Похідні ізотіазолу, спосіб їх одержання, фармацевтична композиція та спосіб лікування гіперпроліферативного захворювання у ссавця |
| GB9823103D0 (en) * | 1998-10-23 | 1998-12-16 | Pfizer Ltd | Pharmaceutically active compounds |
| WO2003072541A2 (en) * | 2001-09-27 | 2003-09-04 | Smithkline Beecham Corporation | Chemical compounds |
| WO2005082001A2 (en) | 2004-02-20 | 2005-09-09 | The Scripps Research Institute | Advanced isothiazole based protein kinase inhibitors |
| ATE542533T1 (de) | 2004-08-26 | 2012-02-15 | Pfizer | Verfahren zur herstellung von isothiazol- derivaten |
-
2012
- 2012-12-27 ES ES12810524.4T patent/ES2623652T3/es active Active
- 2012-12-27 EP EP12810524.4A patent/EP2797916B1/en active Active
- 2012-12-27 US US13/728,502 patent/US8969583B2/en active Active
- 2012-12-27 ES ES17156014T patent/ES2851602T3/es active Active
- 2012-12-27 EP EP17156014.7A patent/EP3184525B1/en active Active
- 2012-12-27 WO PCT/US2012/071855 patent/WO2013101954A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| EP3184525A1 (en) | 2017-06-28 |
| EP3184525B1 (en) | 2020-10-28 |
| EP2797916B1 (en) | 2017-02-15 |
| US20130172353A1 (en) | 2013-07-04 |
| ES2623652T3 (es) | 2017-07-11 |
| US8969583B2 (en) | 2015-03-03 |
| WO2013101954A1 (en) | 2013-07-04 |
| EP2797916A1 (en) | 2014-11-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3080084B1 (en) | Substituted nicotinamide derivatives as kinase inhibitors | |
| ES2426951T3 (es) | Imidazopiridazinacarbonitrilos útiles como inhibidores de quinasa | |
| ES2878160T3 (es) | Derivados de 5,7-dihidro-pirrolo-piridina para el tratamiento de enfermedades neurológicas y neurodegenerativas | |
| ES2363269T3 (es) | Amidas sustituidas, procedimiento de preparación y procedimiento de utlización de las mismas. | |
| EP3133075B1 (en) | Fused heterocyclic compound | |
| KR102892275B1 (ko) | 이미다조피리디닐 화합물 및 신경퇴행성 장애의 치료를 위한 그의 용도 | |
| TWI434834B (zh) | 作為蛋白質激酶抑制劑之吡唑化合物及噻唑化合物、其醫藥組成物及用途 | |
| WO2013134298A1 (en) | Raf inhibitor compounds | |
| JP2016518316A (ja) | Mk2阻害剤およびそれらの使用 | |
| BRPI0618520A2 (pt) | imidazopirazinas como inibidores de proteìna cinase | |
| CA3171774A1 (en) | Substituted pyrimidine or pyridine amine derivative, composition thereof, and medical use thereof | |
| KR20100023040A (ko) | 폴리사이클릭 구아닌 유도체 및 이의 용도 | |
| JP2016037467A (ja) | スルホンアミド誘導体及びその医薬用途 | |
| ES2851602T3 (es) | Derivados de 3-fenil-5-ureidoisotiazol-4-carboxamida como inhibidores de cinasa | |
| ES2838448T3 (es) | Derivados de dialquil(óxido)-lambda4-sulfaniliden-nicotinamida sustituidos como inhibidores de cinasas | |
| KR20210120052A (ko) | 야누스 키나아제 jak 패밀리 억제제 및 이의 제조와 응용 | |
| WO2016127213A1 (en) | Inhibitors of necroptosis | |
| CN110437220B (zh) | 三氮唑类化合物及其应用 | |
| EP2825166A1 (en) | Method of treating ophthalmic conditions with kinase inhibitors | |
| KR20240024077A (ko) | Mglu7 수용체의 음성 다른 자리 입체성 조절제로서의 축합된 헤테로사이클 유도체 | |
| WO2013177053A1 (en) | Pyrimidino [1, 2 -c] quinazolinone derivatives as tyrosine kinases inhibitors | |
| JP2023503470A (ja) | ガラクトセレブロシダーゼの活性の変質に関連する状態におけるアリールおよびヘテロアリール化合物、ならびにそれらの治療的使用 | |
| HK40043779A (en) | Substituted dialkyl(oxido)-lambda4-sulfanylidene nicotinamide derivatives as kinase inhibitors | |
| HK40058868A (en) | Imidazopyridinyl compounds and use thereof for treatment of neurodegenerative disorders | |
| HK40047614A (en) | Dual atm and dna-pk inhibitors for use in anti-tumor therapy |